https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html



































https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
об’ємом 2–3 мл (Б). Поміркуйте, чи спостерігаємо
1. Виділення газу (CO₂) — видно бульбашки на зображенні В.
2.Утворення нових речовин — натрій ацетат (сіль), вода та вуглекислий газ.
3.Неможливість простим способом повернути початкові
відновляться самі знову).
Отже, це саме хімічна реакція.
Сторінка 11
Поміркуйте Хімічна
CH3COONa,
3COONa + CO2 + H2O = NaHCO3 + CH3COOH
наведене рівняння складене
Правильно: NaHCO3 + CH3COOH → CH3COONa + CO2↑ + H2O
Досліджуємо, моделюємо, проєктуємо Мідну пластинку
пальника. Поміркуйте, які
2.
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
1.
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
брязкальця.
231,0 19,25 = 211,75 г
2. Науковець обчислив об'єм
який було видано ювелірові. ■ Обчисліть об'єм бруска та
,c = 3,0 см. Об’єм: V = a ⋅ b ⋅ c = 2 2 3 = 12 см3 Густина: ρ = ���� ���� = 231 12 = 19,25
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
посуд. – Уникати вдихання або потрапляння речовин
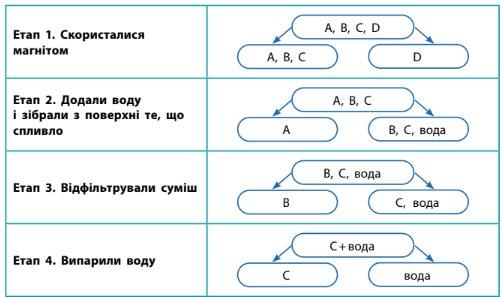
Визначте літери, якими позначено кожен компонент
A – деревна тирса (спливає на поверхні води).
B – глина (залишається нерозчиненою у воді).
C – кухонна сіль (розчиняється у воді). shkola.in.ua
D – залізні ошурки (відділяються магнітом).
Для кожного етапу зазначте суміш (однорідна
та Андрій.
– Етап 1 (Скористалися магнітом):
Суміш: (A, B, C, D)
Вилучили D (залізні ошурки).
Суміш після відділення: (A, B, C)
Характеристика: Неоднорідна суміш.
– Етап 2 (Додали воду, зібрали те, що спливло):
Суміш: (A, B, C, вода)
Вилучили A (деревна тирса), бо вона спливла.
Суміш після відділення: (B, C, вода)
Характеристика: Неоднорідна суміш.
– Етап 3 (Відфільтрували суміш):
Суміш: (C, D, вода)
Вилучили D (глина), бо вона не розчиняється. Суміш після відділення: (C + вода)
4 (Випарили воду):
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
shkola.in.ua
Сторінка
6.
папером. Порівняти кількість
хорошого горіння.
2. Вогонь кочерги не боїться. Це, скоріше,
Як перевірити: Наукова перевірка
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
shkola.in.ua
Як перевірити: Проаналізувати звіти екологічних
ГМО-культур на біорізноманіття, забруднення ґрунтів і використання
10. Срібло знезаражує воду. Іони срібла мають
Сторінка 18
елементами.
Наприклад: shkola.in.ua
NaCl — натрій хлорид
CaS — кальцій сульфід (кальцій + сульфур).
Отже, якщо
Сторінка 20
Пригадайте
Формули яких бінарних
H₂O — гідроген оксид (вода)
CO₂ — карбон(IV) оксид (вуглекислий газ)
NaCl — натрій хлорид (кухонна сіль)
HCl — гідроген хлорид (хлороводень,
CaO — кальцій оксид (негашене вапно)
MgO — магній оксид
FeS — ферум сульфід
KBr — калій
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
напівметали (Бор, Силіцій, Арсен, Стибій тощо). shkola.in.ua
Тобто:
Якщо елемент стоїть у 1-й або 2-й групі (крім Гідрогену) → це метал.
Якщо він у 15–17 групах (наприклад, N, O, F, Cl, S) → це неметал.
Якщо він у 13-й групі (Al, Ga) → це метал, але з особливостями. 18-та група — інертні гази (не утворюють йонів).
Сторінка 23
Досліджуємо, моделюємо, проєктуємо За матеріалом параграфа створіть алгоритми: - складання формули речовини за її назвою;
1. Записати символи катіона й аніона. shkola.in.ua
2. Визначити їхні заряди за періодичною таблицею.
3. Добрати індекси так, щоб сумарні заряди були рівні.
4. Записати формулу (спочатку катіон, потім аніон).
- визначення зарядів катіона й аніона в бінарній сполуці
1. Визначити, який елемент метал (катіон),
2. Заряд аніона відомий із таблиці.
3. Використати правило електронейтральності
Робота з інформацією
7. Із додаткових джерел дізнайтеся
8.
у CaCl₂: Ca²⁺ + 2Cl⁻ → (+2) + 2(–1) = 0. у Al₂S₃: 2Al³⁺ + 3S²⁻ → 6(+) + 6(
формулою речовини.
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
As → арсид shkola.in.ua
10. Латинською binarius — той, що складається з двох, подвійний (від bini — «по два» та bis — «двічі»). Поясніть значення термінів «бінарна сполука»,
виразу «зіграти щось на біс».
Бінарна сполука — речовина, утворена двома різними елементами.
Бінарний код — система кодування з двох символів (0 і 1).
«Зіграти на біс» — виконати ще раз «удруге» на прохання глядачів.
У всіх випадках слово «бінарний / біс» пов’язане з числом два.
11. Запишіть формули та систематичні назви сполук, утворених хімічними
а) H і S; б) K і S; в) Ba і F; г) Al і I; д) Mg і P;
а) H₂S – гідроген сульфід (сірководень)
б) K₂S – калій сульфід
в) BaF₂ – барій фторид
г) AlI₃ – алюміній йодид
д) Mg₃P₂ – магній фосфід
е) Na₃N – натрій нітрид
ж) Na₂O – натрій оксид
и) K₃P – калій фосфід shkola.in.ua
У
всіх формулах індекси підібрані
12. Запишіть систематичні
Cr2O3, PbCl4.
K₂O – калій оксид
Al₂S₃ – алюміній сульфід
Ca₃P₂
LiBr – літій бромід
NaI – натрій йодид shkola.in.ua
HBr – гідроген бромід
FeF₂ – ферум(II) фторид
Cr₂O₃
Сторінка
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Сторінка 29
Поміркуйте
Як можна
shkola.in.ua
Приклад:
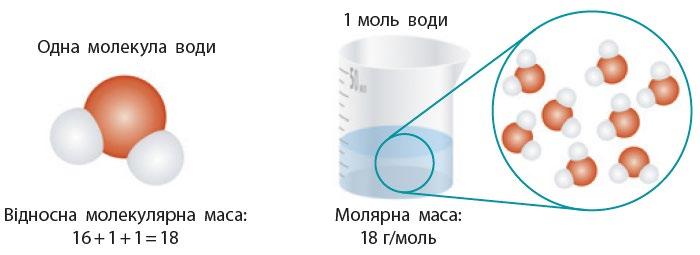
H₂O → 2×Ar(H) + 1×Ar(O) = 2×1 + 16 = 18.
Сторінка 30
Берковець ≈ 163,8 кг
Пуд = 16,38 кг
Гривня ≈ 409 г shkola.in.ua
Золотник ≈ 4,27 г
Ці стародавні міри ваги
стала кілограм.
Сторінка 31
16. Випишіть із періодичної
Al — Алюміній, Ar ≈ 27
F — Флуор, Ar ≈ 19
Zn — Цинк, Ar ≈ 65
Ag — Аргентум, Ar ≈ 108
Sn — Станум, Ar ≈ 119
17. Дізнайтеся,
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
а) Нітроген (14) – Гелій (4)
б) Оксиген (16) – Сульфур (32)
в) Ферум (56) – Силіцій (28)
г) Сульфур (32) – Купрум (64)
19. Обчисліть, скільки
Ar(O) = 16
Ar(Cu) = 64 shkola.in.ua
Обчислення: 64 : 16 = 4
20. Обчисліть
shkola.in.ua
H2SO4; в) сахарози C12H22O11;
CaCO3; ж) малахіту (CuOH)2CO3.
(H = 1, C = 12, O = 16, S = 32, Cl = 35, Ca = 40, Cu = 64):
а) Cl₂ = 2×35 = 70
б) H₂SO₄ = 2×1 + 32 + 4×16 = 2 + 32 + 64 = 98
в) C₁₂H₂₂O₁₁ = 12×12 + 22×1 + 11×16 = 144 + 22 + 176 = 342
г) Cu = 64 shkola.in.ua
д) CaSO₄ = 40 + 32 + 4×16 = 40 + 32 + 64 = 136
е) CaCO₃ = 40 + 12 + 3×16 = 40 + 12 + 48 = 100
ж) (CuOH)₂CO₃ = 2×(64 + 16 + 1) + (12 + 3×16) = 2×81 + (12 + 48) = 162 + 60 = 222.
Відповідь: а) 70; б) 98; в) 342; г) 64; д) 136; е) 100; ж) 222. 21. Запишіть формули й
натрій хлориду; б) кальцій
нітроген(ІІІ) оксиду.
H = 1, C = 12, O = 16, N = 14, Na = 23, Cl = 35, Ca = 40, Br = 80, Pb = 207, I = 127, Al = 27.
а) NaCl = 23 + 35 = 58
б) CaBr₂ = 40 + 2×80 = 40 + 160 = 200
в) PbI₂ = 207 + 2×127 = 207 + 254 = 461
г) Al₂O₃ = 2×27 + 3×16 = 54 + 48 = 102
д) N₂O₃ = 2×14 + 3×16 = 28 + 48 = 76 shkola.in.ua
Відповідь: а) 58; б) 200; в) 461; г) 102; д) 76.
22.
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Mr(H₂O₂) = 2 × 17 = 34.
34 : 17 = 2,
Відповідь: формула
1. У піриті є Ферум (Fe, Ar = 56) і Сульфур (S, Ar = 32).
2. Спробуємо скласти просту формулу.
FeS: Mr = 56 + 32 = 88 (замало). shkola.in.ua
FeS₂: Mr = 56 + 2×32 = 56 + 64 = 120.
Відповідь: формула піриту — FeS₂.
24. Формула жасмоналю, який зумовлює
Обчисліть його відносну молекулярну масу.
Підрахуємо кількість атомів: C = 14, H = 18, O = 1.
Mr = 14 × 12 + 18 × 1 + 16 = 168 + 18 + 16 = 202.
Відповідь: Mr(C₁₄H₁₈O) = 202.
Сторінка 32
Розуміння явищ природи (робота в
C6H5CHC(C5H11)CHO.
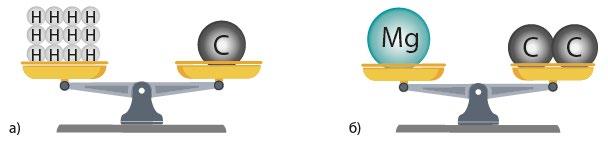
а) Ліворуч 12 атомів Гідрогену (Ar(H) = 1).
Сума: 12 × 1 = 12.
Праворуч 1 атом Карбону (Ar(C) = 12). 12 = 12 → терези врівноважені. shkola.in.ua
б) Ліворуч 1 атом Магнію (Ar(Mg) = 24).
Праворуч 2 атоми Карбону (2 × 12 = 24).
24 = 24 → терези врівноважені.
26. Визначте,

Mr(H₂O) = 2×1 + 16 = 18. 3×18 = 54.
H₂O.
Права шалька — 2 молекули CO₂.
Mr(CO₂) = 12 + 2×16 = 44.
2×44 = 88. shkola.in.ua 54 < 88,
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
формулою.
Сторінка 36
Робота з інформацією
27.
а) NO2;
Відомо: NO2 Розв’язання:
ω(����) ? ω(O) — ?
б) PbCl2;
Відомо: PbCl2
ω(Pb) ?
ω(Cl) — ?
в) Na2CO3;
Розв’язання: Обчислимо
Відомо: Na2CO3 Розв’язання:
ω(Na)— ?
ω(C) — ?
ω(O) — ? г) H2SO4;
�������� (Na2 CO3 ) =2 ⋅�������� (Na) + �������� (C) +3 ⋅�������� (O) = =2 ⋅ 23 + 12 +3 ⋅ 16 = 46 + 12 + 48 = 106 Обчислимо
ω(H) ?
ω(S) — ?
ω(O) — ?
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
�������� (H2 SO4 ) =2 ⋅�������� (H) + �������� (S) +4 ⋅�������� (O) = =2 ⋅ 1+ 32 +4 ⋅ 16 =2+ 32 + 64 = 98 Обчислимо масові частки: shkola.in.ua
д) Ba3(PO4)2.
Відомо:
Ba3(PO4)2
100% ≈ 65,3%
Відповідь: ω(H) = 2,0%; ω(S) = 32,7%; ω(O) = 65,3%.
Розв’язання: Обчислимо відносну
�������� (Ba3 (PO4 )2 ) =3 ⋅�������� (Ba) +2 ⋅ ��������� (P) +4 ⋅�������� (O)� = =3 ⋅ 137 +2 ⋅ (31 +4 ⋅ 16) = 411 + 190 = 601
Обчислимо масові частки: shkola.in.ua
(PO4 )2 ) ⋅ 100% =
(P)
(O) = 2 ⋅ 4 ⋅�������� (O)
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
амоніаку алхіміки. Відомо: ��������3 Розв’язання: 1. Обчислимо відносну молекулярну
�������� (��������3 ) = �������� (���� ) +3 ⋅�������� (���� ) = 14 +3 ⋅ 1= 17
2. Обчислимо масову частку Гідрогену: shkola.in.ua ω(���� ) = 3 ⋅�������� (���� ) �������� (��������3 ) = 3 ⋅ 1 17
3. Знайдемо масу Гідрогену в 10 г амоніаку: ����(���� ) = ω(���� ) ⋅����(��������3 ) =0,176 ⋅ 10
у 10 г NH₃
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
розписів, орнаментів
Відомо:
(�������� ) ?
Відомо:
Відомо: NH4 NO3
ω(����) ?
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
= 23 + 14 + 3 ⋅ 16 == 23 + 14 + 48 = 85 Обчислимо масову частку
shkola.in.ua
ω(����) = �������� (����) �������� (����������������3 ) = 14 85 ≈ 0,165 або 16,5%
Відповідь: ω(����) = 16,5%
Розв’язання: Обчислимо відносну
селітри: �������� (��������4 ��������3 ) = �������� (���� ) +4 ⋅�������� (���� ) + �������� (����) +3 ⋅�������� (���� ) = = 14 +4 ⋅ 1+ 14 + 48 = 14 +4+ 14 + 48 = 80
shkola.in.ua
ω(����) = 2 ⋅�������� (����) �������� (��������4 ��������3 ) = 28 80 =0,35 або 35%
Відповідь: ω(����) = 35%
Висновок: математично видно, що в амоніачній
обчислень
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
48 ∶ 16 =3
Відповідь: CrO3 .
б) Оксид Феруму
Відомо: ���� (Fe) = 70% =0,70.
Необхідно визначити: хімічну формулу сполуки. Fex Oy
1. Визначимо відносну формульну масу сполуки: �������� = ����(Fe) ⋅�������� (Fe) ���� (Fe) = 1 ⋅ 56 0,70 = 80
2. Маса Оксигену: 80 56 = 24
3. Число атомів Оксигену: shkola.in.ua 24 ∶ 16 =1,5
4. Домножуємо індекси на 2 → Fe2 O3
Відповідь: Fe2 O3 .
37. Визначте хімічну формулу сполуки: а) Нітрогену
і Оксиген
���� (O) = 63,2% =0,632. Необхідно визначити: хімічну формулу сполуки. Nx Oy
1. Визначимо відносну формульну масу сполуки: �������� = ����(O) ⋅�������� (O) ���� (O) = 1 ⋅ 16 0,632 = 25,32
2. Маса Нітрогену: 25,32 − 16 =9,32
3. Число атомів Нітрогену: shkola.in.ua
9,32 ∶ 14 =0,665 (дробове)
4. Домножуємо індекси на 3 → N2 O3 .
Відповідь: N2 O3 . б) Карбон і Гідроген
Відомо: ���� (C) = 81,82% =0,8182
Необхідно визначити: хімічну формулу сполуки. Cx Hy 1.
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Відомо:
���� (Cu) = 34,8% =0,348,
���� (Fe) = 30,4% =0,304, �������� = 184.
Необхідно визначити: хімічну формулу сполуки.
Cux Fey Sz
1. Для Купруму: shkola.in.ua
����(Cu) = �������� ⋅���� (Cu) �������� (Cu) = 184 ⋅ 0,348 64 = 64 64 =1
2. Для Феруму: ����(
3. Для Сульфуру: Спочатку визначимо масову частку: shkola.in.ua
���� (S) =1 −���� (Cu) −���� (Fe) =1 − 0,348 − 0,304 =0,348
Тепер:
Відповідь: формула халькопіриту CuFeS2 .
39. Поширений мінерал магнетит складається
Визначте хімічну формулу магнетиту,
Відомо:
���� (Fe) = 72,4% =0,724, �������� = 232.
Необхідно
1.
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
1 доба = 24 години
1 тиждень = 7 діб
1 рік = 365 діб shkola.in.ua 1
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Сторінка 52
41. Обчисліть
а) Cl2
Розв’язання: у молекулі 2 атоми Хлору, отже
����(Cl) =1 ⋅ 2= 2 моль.
Відповідь: ����(Cl) = 2 моль
б) H2 SO4
Розв’язання: shkola.in.ua
����(H) =1 ⋅ 2= 2 моль;
����(S) =1 ⋅ 1= 1 моль;
����(O) =1 ⋅ 4= 4 моль.
Відповідь: ����(H) = 2 моль,; ����(S) = 1 моль,; ����(O) = 4 моль.
в) H3 PO4
Розв’язання: shkola.in.ua
����(H) =1 ⋅ 3= 3 моль;
����(P) =1 ⋅ 1= 1 моль;
����(O) =1 ⋅ 4= 4 моль.
Відповідь: ����(H) = 3 моль,; ����(P) = 1 моль,; ����(O) = 4 моль.
г) Fe2 O3
Розв’язання: shkola.in.ua
����(Fe) =1 ⋅ 2= 2 моль;
����(O) =1 ⋅ 3= 3 моль.
Відповідь: ����(Fe) = 2 моль,; ����(O) = 3 моль.
д) Ca(OH)2
Розв’язання: shkola.in.ua
����(Ca) =1 ⋅ 1= 1 моль;
����(O) =1 ⋅ 2= 2 моль;
����(H) =1 ⋅ 2= 2 моль.
Відповідь: ����(Ca) = 1 моль,; ����(O) = 2 моль,; ����(H) = 2 моль
42. Обчисліть молярні маси речовин: а) H2S; б) NH3; в) F2; г) CaCO3; д) SO2; е) NaOH; ж) K2SO4; и) Fe(NO3)3; к) NaAl(OH)4.
а) Відомо: H2 S Розв’язання:
���� (H2 S)— ?
б) Відомо: NH3
���� (NH3 ) ?
в) Відомо: F2
���� (F2 ) ?
���� = �������� =2 ⋅�������� (H) +1 ⋅�������� (S) =2 ⋅ 1+ 32 = 34 г/моль Відповідь: ���� = 34 г/моль. shkola.in.ua
���� = �������� =1 ⋅�������� (N) +3 ⋅�������� (H) = 14 +3 ⋅ 1= 17 г/моль Відповідь: ���� = 17 г/моль. shkola.in.ua
���� = �������� =2 ⋅�������� (F) =2 ⋅ 19 = 38 г/моль Відповідь: ���� = 38 г/моль. shkola.in.ua
г)
Відомо: CaCO3
���� (CaCO3 ) ?
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Розв’язання: shkola.in.ua
Обчислимо відносну молекулярну масу:
���� = �������� =1 ⋅�������� (Ca) +1 ⋅�������� (C) +3 ⋅�������� (O) = = 40 + 12 +3 ⋅ 16 = 100 г/моль
Відповідь: ���� = 100 г/моль.
д)
Відомо: SO2
���� (SO2 ) ?
е) Відомо: NaOH
���� (NaOH) ?
ж) Відомо: K2 SO4
���� (K2 SO4 ) ?
и) Відомо:
Fe(NO3 )3
���� (Fe(NO3 )3 ) ?
Розв’язання: shkola.in.ua
Обчислимо відносну молекулярну масу:
���� = �������� =1 ⋅�������� (S) +2 ⋅�������� (O) = 32 +2 ⋅ 16 = 64 г/моль
Відповідь: ���� = 64 г/моль
Розв’язання: Обчислимо відносну молекулярну масу: shkola.in.ua ���� = �������� =1 ⋅�������� (Na) +1 ⋅�������� (O) +1 ⋅�������� (H) = = 23 + 16 +1= 40 г/моль
Відповідь: ���� = 40 г/моль.
Розв’язання: Обчислимо
���� = �������� =2 ⋅�������� (K) +1 ⋅�������� (S) +4 ⋅�������� (O) = =2 ⋅ 39 + 32 +4 ⋅ 16 = 174 г/моль
Відповідь: ���� = 174 г/моль. shkola.in.ua
Розв’язання: shkola.in.ua
Обчислимо
масу: M= �������� =1 ⋅�������� (Fe) +3 ⋅ ��������� (N) +3 ⋅�������� (O)� = = 56 +3 ⋅ (14 + 48) = 242 г/моль Відповідь: ���� = 242 г/моль.
к) Відомо:
NaAl(OH)4
(NaAl(OH)4 ) ?
(N2 ) ? shkola.in.ua
Розв’язання: shkola.in.ua
Обчислимо
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
����(CaCO3 ) = 500 г
Відповідь: ����(CaCO3 ) = 5 моль. shkola.in.ua ����(CaCO3 ) ? г) Відомо: ����(NaHCO3 ) = = 10 кг = 10000 г
����(NaHCO3 ) ?
shkola.in.ua
Розв’язання: �������� (CaCO3 ) =1 ⋅�������� (Ca) +1 ⋅�������� (C) +3 ⋅�������� (O) = = 40 + 12 +3 ⋅ 16 = 100 г/моль ���� = ���� ���� = 500 100 = 5 моль
Розв’язання: �������� (NaHCO3 ) =1 ⋅�������� (Na) +1 ⋅�������� (H) +1 ⋅�������� (���� ) +3 ⋅�������� (
Відповідь: ����(NaHCO3 ) ≈ 119.05 моль.
44. Обчисліть масу (г): а) водню
речовини 0,75 моль; д)
а) Відомо: ����(H2 ) = 2 моль
shkola.in.ua
Розв’язання:
���� (H2 ) =2 ⋅�������� (H) =2 ⋅
���� = ����⋅���� =2 ⋅ 2= 4 г.
����(H2 ) = 4 г. ����(H2 ) ?
б) Відомо: ����(O2 ) = 3 моль
(O2 ) ?
в) Відомо: ����(H2 O) = 2.5 моль
����(H2 O) ?
г) Відомо:
����(C12 H22 O11 ) = = 0.75 моль
����(C12 H22 O11 ) ?
Розв’язання: 1. Обчислимо
shkola.in.ua ���� (O2 ) =2 ⋅�������� (O) =2 ⋅ 16 = 32 г/моль
2. Обчислимо масу: ���� = ����⋅���� =3 ⋅ 32 = 96 г Відповідь: ����(O2 ) = 96 г.
Розв’язання: shkola.in.ua 1. Обчислимо молярну масу води: ���� (H2 O) =2 ⋅�������� (H) +1 ⋅�������� (O) =2 ⋅ 1+ 16 = 18 г/моль
2. Обчислимо масу: ���� = ����⋅���� =2.5 ⋅ 18 = 45 г
Відповідь: ����(H2 O) = 45 г.
Розв’язання: shkola.in.ua
1. Обчислимо молярну масу цукру: ���� (C12 H22 O11 ) = 12 ⋅�������� (C) + 22 ⋅�������� (H) + 11 ⋅�������� (O) = = 12 ⋅ 12 + 22 ⋅ 1+ 11 ⋅ 16 = 342 г/моль
2. Обчислимо масу: ���� = ����⋅���� =0.75 ⋅ 342 = 256.5 г
Відповідь: ����(C12 H22 O11 ) = 256.5 г.
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
якщо маса
кількістю речовини: а) 7 моль дорівнює 444,5 г; б) 3,5 моль дорівнює 84 г; в) 0,25 моль
дорівнює 8 г. а) Відомо: ���� = 7 моль, ���� = 444.5 г
���� ?
б) Відомо:
���� =3.5 моль, ���� = 84 г
���� ? shkola.in.ua
в) Відомо: ���� =0.25 моль, ���� = 8 г
Розв’язання: shkola.in.ua ���� = ���� ���� = 444.5 7 = 63.5 г/моль
Атомна маса ≈ 63.5 → це Купрум (Cu).
Відповідь: ���� = 63.5 г/моль, мідь.
Розв’язання: ���� =
= 84 3.5 = 24 г/моль
Атомна маса ≈ 24 → це
(Mg).
Відповідь: ���� = 24 г/моль, магній.
Розв’язання: shkola.in.ua ���� = ���� ���� = 8 0.25 = 32 г/моль
(O2 ) = 3 моль, ����(N2 ) = 2 моль. Розв’язання:
у якого зразка маса більша? shkola.in.ua
б) Відомо:
����(H2 O) = 5 моль, ����(Cl2 ) = 1.4 моль.
якого зразка маса більша? shkola.in.ua
Обчислимо маси:
(O2 ) = ����⋅���� =3 ⋅ 32 = 96 г
(N2 ) = ����⋅���� =2 ⋅ 28 = 56 г 3. Порівняння: 96 г > 56 г Відповідь: більша
кисню O2 .
1. Обчислимо молярні маси: ���� (H2 O) =2 ⋅�������� (H) +1 ⋅�������� (O) =2 ⋅ 1+ 16 = 18 г/моль ���� (Cl2 ) =2 ⋅�������� (Cl) =2 ⋅ 35.5= 71 г/моль 2. Обчислимо маси: ����(H2 O) = ����⋅���� =5 ⋅ 18 = 90 г ����(Cl2 ) = ���� ⋅ ���� = 1.4 ⋅ 71 = 99.4 г
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
3. Порівняння:
99.4 г > 90 г
Відповідь: більша маса
в) Відомо:
����(CaO) = 1 моль,
����(MgO) = 1.5 моль.
у якого зразка маса більша?
Розв’язання:
1. Обчислимо молярні маси:
���� (CaO) = �������� (Ca) + �������� (O) = 40 + 16 = 56 г/моль
���� (MgO) = �������� (Mg) + �������� (O) = 24 + 16 = 40 г/моль
2. Обчислимо маси: shkola.in.ua
����(CaO) = ����⋅���� =1 ⋅ 56 = 56 г
����(MgO) = ����⋅���� =1.5 ⋅ 40 = 60 г
3. Порівняння: 60 г > 56 г Відповідь: більша
47. Обчисліть кількість речовини
3 моль; б) мідній окалині CuO масою 40
а) Відомо: ����(SO2 ) = 3
Розв’язання: shkola.in.ua У молекулі SO2 міститься 2
Відповідь: ����(O) = 6 моль. ����(O) ? б)
Відомо:
����(CuO) = 40 г
(O) ? shkola.in.ua
����(O) = ����(SO2 ) ⋅ 2=3 ⋅ 2= 6 моль
Розв’язання: 1. Обчислимо
���� (CuO) = �������� (Cu) + �������� (O) = 64 + 16 = 80 г/моль
2. Обчислимо кількість речовини CuO: ����(CuO) = ���� ���� = 40 80 =0.5 моль
3. У 1 молекулі CuO є 1 атом
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
����(HNO3 ) = 126 г
а) ����(HNO3 ) ?
б) ����(N) — ?
в) ����(H) — ?
г) ����(O) — ? shkola.in.ua
���� (HNO3 ) =1+ 14 +3 ⋅ 16 = 63 г/моль
а) Кількість речовини молекул:
����(HNO3 ) = ���� ���� = 126 63 = 2 моль
б) У 1 молекулі HNO3 міститься 1 атом Нітрогену, тому
����(N) = ����(HNO3 ) ⋅ 1=2 ⋅ 1= 2 моль
в) У 1 молекулі HNO3 міститься 1 атом Гідрогену, тому
����(H) = ����(HNO3 ) ⋅ 1=2 ⋅ 1= 2 моль г) У 1 молекулі HNO3 міститься 3 атоми Оксигену, тому
(O) = ����(HNO3 ) ⋅ 3=2 ⋅ 3= 6 моль
Відповідь:
а) ����(HNO3 )
Сторінка 53
50. Кількість
моль.
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
років. shkola.in.ua 2. Якщо рахувати по одному числу
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
утворюється
б) масою 7 г.
Відомо:
а) ����(CaO) =0,5 моль б) ����(CaO) = 7 г shkola.in.ua
а) ����(Ca(OH)2 ) ?
б) ����(Ca(OH)2 ) — ?
Розв’язання:
Рівняння реакції: CaO + H2 O → Ca(OH)2 . За рівнянням: ���� (CaO)
����(Ca(OH)2 ) = 1 1 .
а) ����(Ca(OH)2 ) = ����(CaO) =0,5 моль. б) Знаходимо ����(CaO):
���� (CaO) = 40 + 16 = 56 г/моль,
����(CaO) = ���� ���� = 7 56 =0,125 моль
Отже, ����(Ca(OH)2 ) =0,125 моль
Відповідь: а) ����(Ca(OH)2 ) =0,5 моль;
б) ����(Ca(OH)2 ) = 0,125 моль.
����(O2 ) ?
����(N2 ) — ? ����(H2 O) — ?
shkola.in.ua
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
кількістю речовини 0,15 моль.
Відомо:
����(CO2 ) = 0,15 моль
Розв’язання: Рівняння реакції:
Відповідь: ����(NH4 HCO3 ) = 11,85 г. ����(NH4 HCO3 ) ?
Сторінка 60
CH4. Обчисліть,
NH4 HCO3 → NH3 ↑ + CO2 ↑ + H2 O
За рівнянням: 1 моль NH4 HCO3 розкладається з утворенням
1 моль CO2 .
Тобто: shkola.in.ua
����(NH4 HCO3 ) = ����(CO2 ) =0,15 моль
Знаходимо масу розпушувача: ���� (NH4 HCO3 ) = �������� (N) + �������� (H) ⋅ 5+ �������� (C) + �������� (O) ⋅ 3= = 14 + (1 ⋅ 4) +1+ 12 + (16 ⋅ 3) = 79 г/моль ����(NH4 HCO3 ) = ����⋅���� =0,15 ⋅ 79 = 11,85 г.
shkola.in.ua ����(C) = ����(CO2 ) =1,25 моль ���� (C) = �������� (C) = 12
CH4 дає 1 моль CO2
����(CH4 ) = ����(CO2 ) =1,25 моль ���� (CH4 ) = �������� (C) + �������� (H) ⋅
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
NH4NO3 =N2O + 2H2O
Відомо:
����(N2 O) = 5 г
����(NH4 NO3 ) ? shkola.in.ua
Розв’язання: 1. Знайдемо кількість речовини N2 O: ���� (N2 O) = �������� (N) ⋅ 2+ �������� (O) = 14 ⋅ 2+ 16 = 44 г/моль
����(N2 O) = ���� ���� = 5 44 =0,114 моль
2. За рівнянням реакції: NH4 NO3 → N2 O +2H2 O 1 моль амоній
N2 O.
����(NH4 NO3 ) = ����(N2 O) =0,114 моль 3. Знайдемо масу
нітрату: ���� (NH4 NO3 ) = �������� (N) ⋅ 2+ �������� (H) ⋅ 4+ �������� (O)
Відомо: ����(NaClO) = = 5 кг = 5000 г Розв’язання:
����(NaCl) — ?
2NaClO → 2NaCl + O2
2. Знайдемо кількість речовини NaClO:
���� (NaClO) = �������� (Na) + �������� (Cl) + �������� (O) = = 23 + 35,5+ 16 = 74,5 г/моль
����(NaClO) = ���� ���� = 5000 74,5 ≈ 67,11 моль
3. За рівнянням: 2����(NaClO) =2����(NaCl). Отже: shkola.in.ua
����(NaCl) = ����(NaClO) = 67,11 моль
4. Знаходимо масу NaCl:
���� (NaCl) = �������� (Na) + �������� (Cl) = 23 + 35,5= 58,5 г/моль
����(NaCl) = ����⋅���� = 67,11 ⋅ 58,5 ≈ 3927 г =3,93 кг
Відповідь: ����(NaCl) ≈ 3,93 кг.
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
����(Fe2 O3 ) = 54 г
����(Fe) ? shkola.in.ua
2Al + Fe2 O3 → 2Fe + Al2 O3 2. Знайдемо кількість речовини ферум(III) оксиду:
���� (Fe2 O3 ) = �������� (Fe) ⋅ 2+ �������� (O) ⋅ 3
���� (Fe2 O3 ) = 56 ⋅ 2+ 16 ⋅ 3= 112 + 48 = 160 г/моль
����(Fe2 O3 ) = ���� ���� = 54 160 =0,3375 моль
3. За рівнянням: 1 моль Fe2 O3 → 2 моль Fe.
����(Fe) =0,3375 ⋅ 2=0,675 моль
4. Обчислюємо масу заліза:
���� (Fe) = �������� (Fe) = 56 г/моль
����(Fe) = ����⋅���� =0,675 ⋅ 56 = 37,8 г Відповідь: ����(Fe) ≈ 37,8 г.
Розуміння явищ природи (робота в групах)
62. Створіть модель реакції
параграфі на с. 55.
Рівняння реакції горіння метану:
CH4 +2O2 → CO2 +2H2 O
Модель (у молях): shkola.in.ua - 1 моль метану реагує
����(FeS) = 1моль.
����(Fe) ?
����(S) — ?
����(Fe)
���� (S) —?
реакції: Fe + S → FeS
рівнянням: shkola.in.ua
(Fe) ∶����(S) =1 ∶ 1
����(FeS) =1
(Fe) = 1 моль
Поміркуйте
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
. shkola.in.ua
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
систему. � Коли це може статися:
• під час дихання
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
o Природне (атмосферне) —
o
3. За вологістю: shkola.in.ua
o Сухе повітря — без водяної пари.
o Вологе повітря
4. За складом:
o Атмосферне повітря — суміш газів: азоту (≈78%), кисню (≈21%), вуглекислого газу та домішок.
o Збагачене киснем або збагачене вуглекислим газом — використовується у медицині чи промисловості.
68. Чи можна використовувати термін «молекула
поясніть. Ні, використовувати термін «молекула повітря» неправильно. Пояснення: Повітря — це суміш різних газів (переважно
тощо).
• молекула азоту — N2,
• молекула кисню — O2, shkola.in.ua
• молекула вуглекислого газу — CO2. Тобто повітря не має єдиної спільної молекули
це те саме, що сказати «молекула
казати:
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
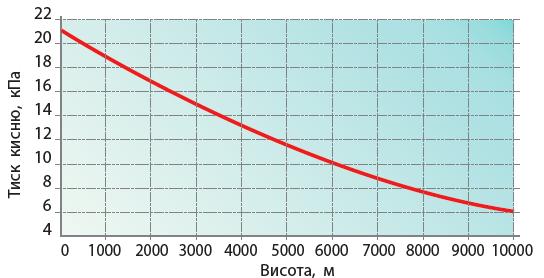
зростає, тому вода трохи опускається.
Сторінка
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
• Карл Вільгельм Шеєле (≈1772): нагрівав різні речовини
повітрям». Публікацію затримав, тому пріоритет поділив з іншими.
• Джозеф Прістлі (1774): сфокусував сонячне світло «палаючою лінзою» на червоному оксиді ртуті (HgO) й зібрав газ, у якому свічка горіла яскравіше, а мишеня жило довше. Назвав його «дефлогістованим повітрям».
• Антуан Лавуазьє (1775–1777): повторив досліди з HgO, правильно пояснив явище без «флогістону», показав роль
кисень (oxygen). Також встановив співвідношення складників повітря.
Чому це довело, що повітря — суміш
Висновок
Відкриття
shkola.in.ua
властивості: • Біла кристалічна
При нагріванні
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Каталізатор змінює шлях
• Платина, нікель — у
• Марган(IV) оксид (MnO₂) —
кисню.
• Ферменти — природні
ρ(����2 ) ρ(повітря) −? shkola.in.ua
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
shkola.in.ua а) ����(O2 ) = 25 г; б) ���� (H2 O2 ) ≈ 13,3%.
Сторінка 74
78. Порівняйте масові
Відомо:
KMnO4 (калій
перманганат) і
KClO3
(бертолетова сіль).
����O (KMnO4 ) ? ����O (KClO3 ) ? shkola.in.ua
Розв’язання:
1. Для KMnO4 : ���� (KMnO4 ) = �������� (K) + �������� (Mn) + �������� (O) ⋅ 4= = 39 + 55 + 16 ⋅ 4= 158 г/моль ����(O у KMnO4 ) = �������� (O) ⋅ 4= 16 ⋅ 4= 64 г ����O = 64 158
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
����0 = 1 кг = 1000 г.
(O2 ) — ?
(0∘ C, 1 атм) Що вигідніше для добування O2 ?
shkola.in.ua
2KClO3 → 2KCl +3O2 ↑, 2KMnO4 → K2 MnO4 + MnO2 + O2 ↑
а) Із бертолетової солі KClO3
Молярні маси:
���� (KClO3 ) = �������� (K) + �������� (Cl) + �������� (O) ⋅ 3= = 39 + 35,5+ 16 ⋅ 3= 122,5 г/моль
���� (O2 ) = �������� (O) ⋅ 2= 16 ⋅ 2= 32 г/моль
Кількість речовини: ����(KClO3 ) = ���� ���� = 1000 122,5 ≈ 8,163 моль
За рівнянням: ����(O2 ) ����(KClO3 ) = 3 2 ⇒����(O2 ) =8,163 ⋅ 3 2
Маса та об’єм кисню: ����(O2 ) = ����⋅���� =
б) Із калій перманганату
Молярні маси: shkola.in.ua ���� (KMnO4 ) = �������� (K) + �������� (Mn) + �������� (O) ⋅
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Лабораторний спосіб
- Отримують малі кількості речовини;
- Потрібні невеликі реактори, пробірки;
- Використовується для навчання і дослідів;
- Реакції короткотривалі, контроль простий.
Промисловий спосіб
- Відбуваються ті самі хімічні реакції;
- Потребують вихідних речовин і енергії;
- Обидва способи мають на меті одержати певну чисту речовину.
- Отримують великі обсяги речовини;
- Використовують великі установки, тиск, каталізатори;
- Використовується для виробництва;
- Реакції безперервні, контроль автоматичний.
Економічніше
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
в класі. Каталізатори: чому вони такі важливі?
1) Що таке каталізатор
• Речовина, яка прискорює
• Допомагає реакції йти
2) Промисловість (заводи)
• Майже
• Аміак (Haber–Bosch):
• Автомобілі: каталітичний
(NOx, CO, вуглеводні) на безпечніші (N₂, CO₂, H₂O).
• SCR у дизелях: додавання сечовини + каталізатор → значно менше NOx.
• Інші приклади:
пального з біомаси. 4) У живих організмах
•
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
2.
3. Далі скраплене повітря подають у ректифікаційну колону, де його поступово
нагрівають.
4. Різні гази випаровуються при різних
• спочатку азот (найлегше кипить),
• потім аргон,
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
випромінювання.
рідкий кисень довго залишається у скрапленому
Обмеження використання:
• скраплений кисень поступово
короткий час;
• посудина дуже крихка й дорога; •
підвищення тиску.
Поміркуйте
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
всередину). Якщо скіпка яскраво спалахує,
горіння.
Поміркуйте
Чи підтвердилася ваша думка?
Так, підтвердилася.
кисень, який підтримує горіння.
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Ознаки розкладу гідроген пероксиду:
• під час реакції виділяються бульбашки газу (кисню);
• утворюється піна, якщо реакція проходить швидко;
• пробірка може нагріватися, бо реакція екзотермічна.
Швидкість реакції можна оцінити за інтенсивністю
1.
час реакції каталізатор
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Поміркуйте
вогню”:
• зменшити температуру (охолодити водою);
• припинити доступ
вогнегасник);
• прибрати горючу речовину (припинити подачу газу чи пального).
Якщо хоча б одна з цих умов зникне — горіння припиниться.
Сторінка 88
Поміркуйте
Висловіть гіпотезу:
Сторінка 90
Робота з інформацією
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
оксиду, плюмбум(IV) оксиду.
• Барій оксид — BaO
• Купрум(І) оксид — Cu₂O
• Хром(ІІІ) оксид — Cr₂O₃
• Йод(V) оксид — I₂O₅
• Плюмбум(IV) оксид — PbO₂
97. Запишіть рівняння реакцій із киснем речовин: а) літію; б) кальцію; в) силіцію, якщо продуктом реакції є силіцій(IV) оксид.
а) 4Li + O₂ → 2Li₂O
б) 2Ca + O₂ → 2CaO в) Si + O₂ → SiO₂
98. Обчисліть масу (г) сірки, яка згоріла, якщо
Розв’язання:
(����) ? shkola.in.ua
2.Зарівняннямреакції
3. ����(����) = ����(����) × ���� (����) =0,35 × 32 = 11,2 г
Відповідь: 11,2 г
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
починається, хоча кисень і горючі речовини є поруч.
103. Схарактеризуйте ознаки горіння. Що таке полум’я? Звідки береться дим? Звідки
виникають теплота й світло?
Ознаки горіння: виділення теплоти,
shkola.in.ua
104. Прикладами
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Сторінка
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Сторінка 96
Утворення кисню
Поміркуйте
Уміст кисню в
Сторінка
ці зміни: • З’явилися організми (наприклад, ціанобактерії),
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
• Окиснення вуглецю: C + O2 → CO (утворюється
• Окиснення водню:
2H2 + O2 → 2H2O (утворюється
Під час вивержень вулканів у
— водяна пара (H2O), shkola.in.ua
— вуглекислий газ (CO2),
— сірчистий газ (SO2),
— сірководень (H2S),
— оксиди азоту (NO, NO2).
Отже, кисень під час вулканічних
що містяться в магмі, а
Розуміння явищ
цей
постійно переходить із одних форм у
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Сторінка 103
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Сторінка
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Так, це твердження

108
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
а) Азот N2
Відомо: n = 2 моль.
Розв’язання: V = n · Vm = 2 моль · 22,4 л/моль = 44,8 л.
Відповідь: 44,8 л. V – ?
shkola.in.ua
б) Кисень O2
Відомо: n = 0,5 моль.
Розв’язання: V = n · Vm = 0,5 моль · 22,4 л/моль = 11,2 л.
Відповідь: 11,2 л. V – ?
в) Фтор F2
Відомо: n = 0,25
моль.
Розв’язання: V = n · Vm = 0,25 моль · 22,4 л/моль = 5,6 л.
Відповідь: 5,6 л. V – ?
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
г) Сірководень H2S
Відомо: n = 2,9 моль.
Розв’язання: V = n · Vm = 2,9 моль · 22,4 л/моль = 64,96 л ≈ 65,0 л.
Відповідь: 65 л. V – ?
д) Амоніак NH3
Відомо: n = 4,2 моль.
Розв’язання: V = n · Vm = 4,2 моль · 22,4 л/моль = 94,08 л ≈ 94,1 л.
Відповідь: 94,1 л. shkola.in.ua V – ?
138. У чотирьох однакових посудинах містяться однакові об’єми газів: амоніаку NH3,
азоту N2, сірчистого газу SO2, кисню O2.Визначте, маса якої посудини з газом буде
найбільша, а якої найменша.
Відомо:
Однакові об’єми газів NH3, N2, SO2
однакова (за законом Авоґадро).
Розв’язання:
Знайдемо молярні маси газів:
NH3: M = 14 + 3·1 = 17 г/моль
N2: M = 2·14 = 28 г/моль
O2: M = 2·16 = 32 г/моль
SO2: M = 32 + 2·16 = 64 г/моль
Маса газу m = n·M, а n однакове, тому
масою, а найменшу — з найменшою.
Відповідь: найбільша
139. Обчисліть масу (г) сірководню H2S об’ємом 16,8 л (н. у.).
Відомо:
V(H2S) = 16,8 л Vm = 22,4 л/моль
m(H2S) – ?
shkola.in.ua
Сторінка 116
Розв’язання: n(H2S) = V(H2S) : Vm = 16,8 л : 22,4 л/моль = 0,75 моль
M(H2S) = 2 · 1 + 32 = 34 г/моль
m(H2S) = n(H2S) · M(H2S) = 0,75 моль · 34 г/моль = 25,5 г
Відповідь: m(H2S) = 25,5 г.
140. Обчисліть об’єм (н. у.) водню: а) масою 10 г; б) кількістю речовини 10 моль. а)
shkola.in.ua
Відомо:
m(H2) = 10 г.
V(H2) – ? б)
Відомо: n(H2) = 10 моль.
Розв’язання: M(H2) = 2 г/моль. n(H2) = m(H2) : M(H2) = 10 г : 2 г/моль = 5 моль.
V(H2) = n(H2) · Vm = 5 моль · 22,4 л/моль = 112 л.
Відповідь: V(H2) = 112 л.
Розв’язання: V(H2) = n(H2) · Vm = 10 моль · 22,4 л/моль = 224 л.
Відповідь: V(H2) = 224 л. V(H2) – ?
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Відомо:
V(CH4) = 10 л (н. у.)
V(Cl2) = 20 л (н. у.)
Знайти:
1.
2. У якому зразку більше атомів і в скільки разів.
Розв’язання:
Обчислимо кількість молекул (кількість речовини) у кожному зразку:
n(CH4) = V(CH4) : Vm = 10 л : 22,4 л/моль ≈ 0,446 моль;
n(Cl2) = V(Cl2) : Vm = 20 л : 22,4 л/моль ≈ 0,893 моль.
Більше молекул у зразку Cl2, бо кількість речовини більша:
n(Cl2) : n(CH4) = 0,893 : 0,446 ≈ 2 рази.
Обчислимо кількість атомів у кожному зразку:
CH4: 1 молекула містить 5 атомів (1 C + 4 H); n(атомів у CH4) = 0,446 · 5 ≈ 2,23 моль атомів.
Cl2: 1 молекула містить 2 атоми Cl; n(атомів у Cl2) = 0,893 · 2 ≈ 1,786 моль атомів. shkola.in.ua
Порівнюємо:
n(атомів у CH4) : n(атомів у Cl2) = 2,23 : 1,786 ≈ 1,25 рази.
Відповідь: більше молекул у зразку Cl2 у 2 рази;
у зразку CH4 у 1,25 раза. 142. Чи дорівнюють маси й об’єми (за
кількістю речовини по 1,5 моль?
Відомо:
n(CO2) = 1,5 моль; n(O2) = 1,5 моль; Vm = 22,4 л/моль.
m(CO2), m(O2), V(CO2), V(O2) – ? shkola.in.ua
Розв’язання:
1. Обчислимо маси газів.
M(CO2) = 12 + 2 · 16 = 44 г/моль.
M(O2) = 2 · 16 = 32 г/моль.
m(CO2) = n(CO2) · M(CO2) = 1,5 моль · 44 г/моль = 66 г.
m(O2) = n(O2) · M(O2) = 1,5 моль · 32 г/моль = 48 г.
Отже, маси не однакові: m(CO2) > m(O2).
2. Обчислимо об’єми газів за н. у.
V(CO2) = n(CO2) · Vm = 1,5 моль · 22,4 л/моль = 33,6 л.
V(O2) = n(O2) · Vm = 1,5 моль · 22,4 л/моль = 33,6 л.
V(CH4) = 100 л (н. у.); Vm = 22,4 л/моль.
V(NH3) – ?
по 33,6 л.
100 л (н. у.).
Розв’язання: n(CH4) = V(CH4) : Vm = 100 л : 22,4 л/моль ≈ 4,46 моль. n(NH3) = 3 · n(CH4) = 3 · 4,46 моль ≈ 13,38 моль.
V(NH3) = n(NH3) · Vm = 13,38 моль · 22,4 л/моль ≈ 300 л.
Відповідь: V(NH3) ≈ 300 л.
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
100 л (н. у.)?
Відомо:
m(NH3) = 100 г; V(NH3) = 100 л (н. у.); Vm = 22,4 л/моль
У якому зразку NH3
більше молекул?
Розуміння
учня.
Розв’язання:
M(NH3) = 14 + 3 · 1 = 17 г/моль. n1(NH3) = m(NH3) : M(NH3) = 100 г : 17 г/моль ≈ 5,88 моль. n2(NH3) = V(NH3) : Vm = 100 л : 22,4 л/моль ≈ 4,46 моль.
Оскільки 5,88 моль > 4,46 моль, то більше молекул
масою 100 г. shkola.in.ua Відповідь: більше молекул амоніаку в
Відповідь учня неправильна,
2 об’єми H2 + 1 об’єм O2 → 2
3 об’єми H2 + 1
2
N2 → 2
H2 + 1
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
слід урахувати: температуру
2. Умови здійснення експерименту
Температура в кабінеті: 20 °C
Атмосферний тиск: p = 101000 Па
Обладнання: кристалізатор, конічна
циліндри, ваги, фільтрувальний папір
Реактиви: H2O2 (3 %), CaCO3, оцтова кислота (6 %), розчин NaCl (10 %)
Сторінка 118
4. Визначення молярного
Маса розчину H2O2 (3 %): 5,5 мл
Приблизна кількість речовини
����(����2 ) ≈ 0,00275
(����2 ) = 58 мл =0,058
кисню (O2)
shkola.in.ua
����
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
н.у. (����2 ) = 0,058 ⋅ 101000 ⋅ 0,0027
20 + 273,15 ≈ 0,0539 л
Для CO2: shkola.in.ua
����
н.у. (��������2 ) = 0,072 ⋅ 101000 ⋅ 0,0027
Сторінка 119
20 + 273,15 ≈ 0,0670 л
7. Обчислення кількості речовини газів
����(����2 ) =0,00275 моль
����(��������2 ) =0,0032 моль
8. Обчислення молярних об’ємів газів
�������� = ����н.у. ����
Для O2: shkola.in.ua
�������� (����2 ) = 0,0539 0,00275 = 19,6 л/моль
Для CO2:
�������� (��������2 ) = 0,0670 0,0032 = 20,9 л/моль
Висновок:
ході дослідження я визначив молярний
нормальних умов.
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
результатами, тим точніше проведено дослідження.
На точність могли вплинути:
• часткові втрати газу;
• нещільні з’єднання приладу; shkola.in.ua
• неточне вимірювання маси або об’єму;
• температура й тиск, що відрізняються
• вологість газу або домішки. 7. Як ви вважаєте, навіщо
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
• Усі вони утворилися
Сторінка
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
є основними, а які кислотними?
• калій оксиду → K2O
• фосфор(ІІІ) оксиду → P2O3
• аргентум(1+) оксиду → Ag2O
• ферум(2+) оксиду → FeO
• хлор(IV) оксиду → ClO2
• нітроген(V) оксиду → N2O5
• сульфур(VI) оксиду → SO3
• ванадій(V) оксиду → V2O5
Класифікація:
• Основні оксиди (метали з невисоким ступенем окиснення): K2O, Ag2O, FeO
• Кислотні оксиди: P2O3, ClO2, N2O5, SO3, V2O5
148. Запишіть формули гідроксидів: Калію, Магнію, Стануму(2+),Хрому(3+), Купруму(2+), Барію. Підкресліть формули
• Калію – KOH shkola.in.ua
• Магнію – Mg(OH)2
• Стануму(2+) – Sn(OH)2
• Хрому(3+) – Cr(OH)3
• Купруму(2+) – Cu(OH)2
• Барію – Ba(OH)2
149. Випишіть окремо формули оксидів: а) кислотних; б) основних.
Na2O, P2O5, CO2, SO3, SO2, CrО, ВаО, Cu
Кислотні оксиди: P2O5, CO2, SO3, SO2, SiO2, Mn2O7, N2O5, SnO2, I2O5.
Основні оксиди: shkola.in.ua
Na2O, CrO, BaO, Cu2O, Li2O, MnO. Для оксидів, які можуть реагувати
кислот
оксиди → основи (луги):
основ.
• Na2O + H2O = 2NaOH
• Li2O + H2O = 2LiOH
• BaO + H2O = Ba(OH)2 Кислотні оксиди → кислоти: shkola.in.ua
• P2O5 + 3H2O = 2H3PO4
• CO2 + H2O = H2CO3
• SO3 + H2O = H2SO4
• SO2 + H2O = H2SO3
• Mn2O7 + H2O = 2HMnO4
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
• N2O5 + H2O = 2HNO3
• SnO2 + H2O = H2SnO3
• I2O5 + H2O = 2HIO3
• CrO → Cr(OH)2
• Cu2O → CuOH shkola.in.ua
• MnO → Mn(OH)2
• SiO2 → H2SiO3 (силікатна кислота)
150. Доповніть схеми
а) Li2O + H2O → 2LiOH – утворюється
(луг).
б) SO2 + H2O → H2SO3 – утворюється сульфітна (сірчиста) кислота.
в) BaO + H2O → Ba(OH)2 – утворюється
151. Унаслідок взаємодії
реакції: CaO + H2O → Ca(OH)2 Утворюється
(екзотермічна). shkola.in.ua
Розуміння явищ
152.
SO3 + H2O → H2SO4;
Na2O + H2O → 2NaOH; CaO + H2O → Ca(OH)2.
Сторінка128
153. Оксос
(робота
(луг).
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
• SO2 (сульфур(IV) оксид)
• SO3 (сульфур(VI)
• NO2 (нітроген(IV)
синіми/жовтими/рожевими.
Тому для склянки з екстрактом капусти:
• Верхня частина (фіолетово-рожева,
кисле. shkola.in.ua
• Нижня частина (зелена) → там є луг,
156. Висловіть
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Сторінка130
Кислота (оцет) червоний рожевий/червоний
Луг (питна сода) синій жовтий/помаранчевий
Вода (нейтральна)
Кухонна сіль (нейтр.) фіолетовий
Висновок: Індикатори
Рефлексуємо
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
навчальних хімічних
нейтральним
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html

https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
а) N2 + 3H2 → 2NH3
б) H2 + Cl2 → 2HCl
в) C + 2H2 → CH4
163.
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html


https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Відомо: shkola.in.ua
за 20°C в 1 л води розчиняється:
���� (����2 ) = 18,8 мл =0,0188 л; ���� (����2 ) =6,7 мл =0,0067 л;
густина: ρ(����2 ) =0,09 г/л, ρ(����2 ) =1,43 г/л;
маса води ����води = 1000 г.
Знайти: масові частки ���� (����2 ) і ���� (����2 ); зробити
Розв’язання
Маса розчиненого водню:
����(����2 ) = ρ(����2 ) ⋅���� (����2 ) =0,09 ⋅ 0,0188 =0,001692 г.
Масова частка: ���� (����2 ) =
0,001692 1000 ≈ 1,7 ⋅ 10−6 , ���� (����2 ) ≈ 1,7 ⋅ 10−4 %. Маса розчиненого кисню: ����(����2 ) = ρ(����2 ) ⋅���� (����2 ) =1,43 ⋅ 0,0067 =0,
(����2 )
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
ρ(Pd) = 12,02 г/см3; ρ(H2) = 0,09 г/л.
���� (����2 ) — ? shkola.in.ua
Розв’язання: У 1 см3
Візьмемо 1 см3 паладію:
����(�������� ) = ρ(�������� ) ⋅���� = 12,02 ⋅ 1= 12,02 г.
Об’єм водню: 850 см3 = 0,85 л.
����(����2 ) = ρ(����2 ) ⋅���� =0,09 ⋅ 0,85 =0,0765 г.
(н.у.);
Масова частка водню: ���� (����2 ) = ����(����2 ) ����(�������� ) + ����(����2 ) = 0,0765 12,02 +0,0765 ≈ 0,0063.
У відсотках: ���� (����2 ) ≈ 0,63%.
Відповідь: масова частка
Розуміння явищ природи (робота в групах) 168. Чому Гідроген є
є
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
���� (���� ) = 2 18 ≈ 11,1%,
���� (���� ) = 16 18 ≈ 88,9%.
shkola.in.ua
����балона (����2 ) = 40 л,
����
балона (����2 ) = 560 г
���� (�������� ) = 40 л = 40 000 см3
ρ(�������� ) = 12,02 г/см3
Розчинність: 850 об’ємів H2 на 1 об’єм Pd
ρ(����2 ) =0,09 г/л
Розв’язання
1. Маса паладієвого бруска: shkola.in.ua ����(�������� ) = ����⋅ρ = 40 000 см3 ⋅ 12,02 г/см3 =
2. Об’єм водню, який може розчинитися
Pd: ���� (����2 )в Pd =
3. Маса цього водню:
(����2 )в Pd = ρ(����2 ) ⋅����
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
(відносна
�������� (������������ ) = ��������(���� ) + ��������(�������� ) =1+ 35,5= 36,5
Якщо «мурієва»
�������� (������������ ) = ��������(���� ) + ��������(�������� ) = 36,5
��������(�������� ) = 36,5 1= 35,5
Отже, Мурій
2H2 + O2
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
відбувається та чи інша
З фтором:
H2 + F2 = 2HF.
хлором:
H2 + Cl2 = 2HCl.
Реакція
З киснем:
2H2 + O2 = 2H2O.
Потрібно
З сіркою:
H2 + S = H2S.
Реакція йде за
З азотом:
3H2 + N2 = 2NH3.
Потрібні висока
(сажею):
2H2 + C = CH4.
Реакція
2Li
2Al
CuO
Ag2
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Ag2O + H2 → 2Ag + H2O
MnO + H2 → Mn + H2O 180.
Відомо:
m(Fe2O3) = 160 кг = = 160000 г
V(H2) (н. у.) ? shkola.in.ua
Розв’язання:
1. Записуємо рівняння реакції: Fe2O3 + 3H2 → 2Fe + 3H2O
2. Обчислюємо кількість речовини ферум(3+) оксиду:
M(Fe2O3) = 2·56 + 3·16 = 160 г/моль
n(Fe2O3) = 160000 : 160 = 1000 моль
3. За рівнянням: з 1 моль Fe2O3 реагує 3 моль H2, отже
n(H2) = 3 · 1000 = 3000 моль
4. За н. у. Vм = 22,4 л/моль, тоді
V(H2) = n · Vм = 3000 · 22,4 = 67200 л = 67,2 м3 Відповідь: 67,2 м3 водню.
181. Реакція цинку з хлоридною
об’ємом 5,6 л (н. у.).
Відомо:
V(H2) = 5,6 л (н. у.)
Vм = 22,4 л/моль
m(Zn) ?
shkola.in.ua
m(СH4) = 44 г Vм = 22,4 л/моль
Розв’язання:
1. Записуємо рівняння реакції: Zn + 2HCl → ZnCl2 + H2
2. Обчислюємо кількість речовини водню: n(H2) = V : Vм = 5,6 : 22,4 = 0,25 моль
3. За рівнянням реакції: 1 моль Zn → 1 моль H2, тому n(Zn) = n(H2) = 0,25 моль
4. Обчислюємо
M(Zn) = 65 г/моль m(Zn) = n · M = 0,25 · 65 = 16,25 г
183. Під час
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Об’єм
V(H2) = n · Vм = 5,5 · 22,4 = 123,2 л
Відповідь: 123,2 л водню.
електролізу одержано 2 м3 водню (н. у.).
Відомо:
V(H2) = 2 м3 = = 2000 л (н. у.)
Vm = 22,4 л/моль
m(H2O) ?
V(O2) — ?
shkola.in.ua
Розв’язання:
1. Рівняння реакції електролізу води:
2H2O → 2H2 + O2
2. Знаходимо кількість речовини водню:
n(H2) = V : Vm = 2000 : 22,4 = 625/7 ≈ 89,3 моль
3. За рівнянням 2H2O → 2H2 видно, що кількості H2O і H2
однакові, тобто
n(H2O) = n(H2) = 89,3 моль
4. Обчислюємо масу води:
M(H2O) = 18 г/моль
m(H2O) = n · M = 89,3 · 18 ≈ 1607 г ≈ 1,6 кг
5. За рівнянням 2H2O → 2H2 + O2 об’єм газів
як 2 : 1, тобто V(O2) = V(H2) : 2 = 2000 : 2 = 1000 л = 1 м3 Відповідь: m(H2O) ≈ 1,6 кг, V(O2) = 1 м3 .
340 кг.
Відомо:
m(NH3) = 340 кг = = 340000 г
Vм = 22,4 л/моль
V(H2) (н. у.) ? shkola.in.ua
Розв’язання: Рівняння реакції:
N2 + 3H2 → 2NH3
M(NH3) = 14 + 3·1 = 17 г/моль
n(NH3) = 340000 : 17 = 20000 моль
За рівнянням: з 3
H2 утворюється 2 моль NH3, тобто n(H2) = 3 2·n(NH3) = 1,5·20000 = 30000 моль
тоді
V(H2) = n·Vм = 30000·22,4 = 672000 л = 672 м3
Відповідь: 672 м3 водню.
Деякі метали, зокрема, хром, використовують для захисту сталі від корозії (іржавіння). Обчисліть
відновити, використовуючи водень об’ємом 44,8 л (н. у.). Обчисліть масу утвореного хрому.
Відомо:
V(H2) = 44,8 л Vм = 22,4 л/моль
m(Cr2O3) ?
m(Cr) — ?
shkola.in.ua
Розв’язання: 1. Записуємо рівняння реакції: Cr2O3 + 3H2 → 2Cr + 3H2O
2. Обчислюємо кількість речовини водню: n(H2) = V : Vm = 44,8 : 22,4 = 2 моль
3. За рівнянням 3 моль H2 відповідають 1 моль Cr2O3, тому: n(Cr2O3) = 2 : 3 = 0,67 моль (приблизно)
4. Обчислюємо масу Cr2O3: M(Cr2O3) = 2·52 + 3·16 = 152 г/моль m(Cr2O3) = n·M = 0,67·152 ≈ 101 г
5. За рівнянням з 1 моль Cr2O3 утворюється 2 моль Cr: n(Cr) = 2·n(Cr2O3) = 2·0,67 ≈ 1,33 моль
Розуміння
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
парою. Щоб зробити
пропустити через речовину, яка поглинає воду.
Сторінка 144 187. Зважаючи
виділити, зокрема, такі: -сполучення: А + В → АВ; -розкладу: AВ → А + В; -обміну: АВ + CD → AD + CB; -заміщення: АВ + С → СВ + А.
Горіння водню:
2H2 + O2 → 2H2O. Це
CuO + H2 → Cu + H2O.
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Сторінка
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
3.
4.
5.
6.
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Сторінка 154
Робота з інформацією 194. Назвіть солі: а) K2SO4; б) Сr(NO3)3; в) MgCl2; г) CuSO4; д) SnCl2;е) AgNO3; ж) AlPO4; и) BaSO3; к) BaS; л) BaSO4; м) Na2SiO3; н) NaBr; п) MnSO4; р) Ag2S; с) Mg3(PO4)2
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
в) алюміній нітрат → Al(NO3 )3
г) натрій сульфат → Na2 SO4
д) кальцій силікат → CaSiO3
е)
аргентум(1+) хлорид → AgCl
ж) магній сульфіт → MgSO3
и) алюміній сульфід → Al2 S3
к) ферум(3+) сульфат → Fe2 (SO4 )3
л) хром(3+) ортофосфат → CrPO4
м) магній бромід → MgBr2
н)
кальцій йодид → CaI2
п)
кальцій ортофосфат → Ca3 (PO4 )2
р) меркурій(2+) нітрат → Hg(NO3 )2
с) купрум(1+) фторид → CuF
196. Назва «кальцинована сода»
карбонату прожарюванням, що на
кількість речовини
масовою часткою солі 4 %.
Відомо: m(розчину) = 120 г w(CuSO4) = 4 % = = 0,04
n(CuSO4) ? shkola.in.ua
Сторінка 155
Розв’язання:
1. Знайдемо масу купрум(2+) сульфату
розчині: m(CuSO4) = w · m(розчину) = 0,04 · 120 г = 4,8 г 2. Обчислимо кількість речовини: М(CuSO4) ≈ 160 г/моль n(CuSO4) = m / M = 4,8 г : 160 г/моль = 0,03 моль Відповідь: n(CuSO4) = 0,03 моль.
198. Обчисліть маси: а) хром(3+) сульфату кількістю речовини 0,35 моль; б) кальцій фториду кількістю речовини 0,7 моль; в) магній силікату кількістю речовини 1,2 моль.
Відомо:
а) n(Cr2(SO4)3) = 0,35 моль б) n(CaF2) = 0,7 моль в) n(MgSiO3) = 1,2 моль
m(Cr2(SO4)3) ?
m(CaF2) — ?
m(MgSiO3) — ?
shkola.in.ua
Розв’язання:
1. Формули солей і молярні маси:
– хром(3+) сульфат: Cr2(SO4)3
M(Cr2(SO4)3) = 2·52 + 3·(32 + 4·16) = 392 г/моль
– кальцій фторид: CaF2
M(CaF2) = 40 + 2·19 = 78 г/моль
– магній силікат: MgSiO3
M(MgSiO3) = 24 + 28 + 3·16 = 100 г/моль
2. Обчислюємо маси:
а) m(Cr2(SO4)3) = n · M = 0,35 моль · 392 г/моль = 137,2 г
б) m(CaF2) = 0,7 моль · 78 г/моль = 54,6 г
в) m(MgSiO3) = 1,2 моль · 100 г/моль = 120 г
Відповідь: а) 137,2 г; б) 54,6 г; в) 120 г.
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
0,9 %.
фізіологічного розчину об’ємом 5 л (густину розчину вважати 1 г/мл).
Відомо:
w(NaCl) = 0,9 % = 0,009
V(розчину) = 5 л
ρ(розчину) = 1 г/мл
m(NaCl) ? shkola.in.ua
201.
Відомо:
m(води) = 532,8 г n(CaCl2) = 0,2 моль
w(CaCl2) ?
shkola.in.ua
Розв’язання:
1. Знайдемо масу розчину: V = 5 л = 5000 мл, а ρ = 1 г/мл, тому m(розчину) = ρ·V = 1 г/мл · 5000 мл = 5000 г
2. Знайдемо масу натрій хлориду за масовою часткою: m(NaCl) = w·m(розчину) = 0,009 · 5000 г = 45 г
Відповідь: m(NaCl) = 45 г.
Розв’язання: 1. Обчислюємо
хлориду: M(CaCl2) = 40 + 2·35,5 = 111
2. Обчислюємо
хлориду: m(CaCl2) = n·M = 0,2 моль · 111 г/моль = 22,2 г
3. Обчислюємо масу розчину: m(розчину) = m(води) + m(CaCl2) = 532,8 г + 22,2 г = 555 г 4.
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
2.
3. Реакція металу з кислотою занадто
відступити назад.
4. Виділяється багато газу (водень) — не підносити
5. Розлили кислоту —
6. Розбилося скло — не збирати
Поміркуйте
(Mg)
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Цинк (Zn) реагує
Залізо (Fe) реагує
(Cu)
Хімічні рівняння реакцій:
Mg + 2HCl = MgCl2 + H2↑
Zn + 2HCl = ZnCl2 + H2↑
Fe + 2HCl = FeCl2 + H2↑
Cu + 2HCl = реакція не відбувається ■ Розташуйте символи
активного.
Найактивніший
За спостереженнями: Mg > Zn > Fe > Cu
Отже, ряд активності досліджених
Mg, Zn, Fe, Cu
Ряд активності
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Сторінка 165 Робота з інформацією 204.

https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Наприклад:
2Na + 2H2O → 2NaOH + H2
Ca + 2H2O → Ca(OH)2 + H2
б) Під час взаємодії
основи (луги).
Наприклади:
Na2O + H2O → 2NaOH
CaO + H2O → Ca(OH)2 в) Під час взаємодії
Наприклади:
SO3 + H2O → H2SO4 CO2 + H2O → H2CO3
Mg + H2SO4 → MgSO4
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
реакція можлива
Ni + H2SO4 → NiSO4 + H2
продукти: нікель(2) сульфат і водень
(Au
реакція можлива, але дуже повільно; практично
малорозчинного PbCl2 на поверхні
Pb + 2HCl → PbCl2↓ + H2
продукти: плюмбум(2) хлорид і водень
к) реакція можлива
Sn + H2SO4 → SnSO4 + H2
продукти: станум(2) сульфат і водень
л) реакція можлива
Zn + 2HBr → ZnBr2 + H2
продукти: цинк бромід і водень
м) реакція можлива
Mn + H2SO4 → MnSO4 + H2
продукти: манган(2) сульфат і водень
210. Визначте можливість
K реагує з водою:
2K + 2H2O → 2KOH + H2
продукти:
Sr реагує з водою:
Sr + 2H2O → Sr(OH)2 + H2
продукти:
Ba
Ba + 2H2O → Ba(OH)2 + H2
продукти:
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
д) Hg(NO3)2 і Cu
Cu + Hg(NO3)2 → Cu(NO3)2 + Hg
продукти: купрум(2) нітрат і ртуть
е) Hg(NO3)2 і Ag
2Ag + Hg(NO3)2 → 2AgNO3 + Hg
продукти: аргентум(1) нітрат і ртуть
ж) CrCl3 і Zn
3Zn + 2CrCl3 → 3ZnCl2 + 2Cr
продукти: цинк хлорид і хром
и) Al2(SO4)3 і Pb
реакція не відбувається (Pb менш активний за Al)
к) SnCl2 і Zn
Zn + SnCl2 → ZnCl2 + Sn
продукти: цинк хлорид і олово
л) FeCl2 і Zn
Zn + FeCl2 → ZnCl2 + Fe
продукти: цинк хлорид і залізо
м) NiSO4 і Fe
Fe + NiSO4 → FeSO4 + Ni
продукти: ферум(2) сульфат і нікель
н) CuBr2 і Al
2Al + 3CuBr2 → 2AlBr3 + 3Cu
продукти: алюміній бромід і мідь
п) Pb(NO3)2 і Ni
Ni + Pb(NO3)2 → Ni(NO3)2 + Pb
продукти: нікель(2) нітрат і свинець
Сторінка 166
212. Які з речовин реагують із водою: Na, Fe, Fe2O3, H2SO4, NaOH, CaO, ZnО?
підтвердьте рівняннями реакцій.
З наведених речовин з
2Na + 2H2O → 2NaOH + H2
CaO + H2O → Ca(OH)2
H2SO4 + H2O → H3O+ + HSO4
NaOH + H2O → Na+ + OH Fe з водою за
Al2O3 і
е) Cr2O3 і Zn
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
3Zn + Cr2O3 → 3ZnO + 2Cr
продукти:
PbO
Sn + PbO → SnO + Pb
продукти: станум(II) оксид і свинець
214. Після занурення цинкової пластини
виділилася мідь масою 3,2 г. Обчисліть масу цинку, що прореагував.
Відомо: m(Cu) = 3,2 г
m(Zn) ? shkola.in.ua
Розв’язання:
Реакція:
Zn + Cu(NO3)2 → Zn(NO3)2 + Cu За рівнянням реакції 1
Молярні маси:
M(Cu) = 64 г/моль
M(Zn) = 65 г/моль
Кількість речовини міді:
n(Cu) = m(Cu) / M(Cu) = 3,2 / 64 = 0,05 моль
Отже, n(Zn) = 0,05 моль
Маса цинку:
m(Zn) = n(Zn) · M(Zn) = 0,05 · 65 = 3,25 г
Відповідь: 3,25 г.
Cu.
масою 0,54 кг.
Відомо:
m(Al) = 0,54 кг = 540 г
m(Sn) ? shkola.in.ua 216.
m(Zn) = 97,5
Рівняння реакції:
3SnO + 2Al → Al2O3 + 3Sn
Розв’язання:
Молярні маси: M(Al) = 27 г/моль
M(Sn) = 119 г/моль
Кількість речовини алюмінію:
n(Al) = m(Al) / M(Al) = 540 / 27 = 20 моль За рівнянням реакції: 2 моль Al → 3 моль Sn Отже: n(Sn) = (3 / 2) · 20 = 30 моль Маса олова: m(Sn) = n(Sn) · M(Sn) = 30 · 119 = 3570 г = 3,57 кг
3,57 кг.
V(H2) ?
shkola.in.ua
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Розв’язання: M(Zn) = 65 г/моль
n(Zn) = m(Zn) / M(Zn) = 97,5 / 65 = 1,5 моль
рівнянням реакції: n(Zn) : n(H2) = 1 : 1, отже n(H2) = 1,5 моль
об’єм газу
н. у.: Vm = 22,4 л/моль V(H2) = n(H2) · Vm = 1,5 · 22,4 = 33,6 л Відповідь: 33,6 л
Відомо: m(Mg) = 12 г
n(H2SO4) ?
m(MgSO4) — ?
V(H2) — ?
shkola.in.ua
Рівняння реакції:
Mg + H2SO4 → MgSO4 + H2
Розв’язання:
M(Mg) = 24 г/моль
n(Mg) = m(Mg) / M(Mg) = 12 / 24 = 0,5 моль
За рівнянням:
n(H2SO4) = n(Mg) = 0,5 моль
n(MgSO4) = 0,5 моль
n(H2) = 0,5 моль
M(MgSO4) = 24 + 32 + 64 = 120 г/моль
m(MgSO4) = n(MgSO4) · M(MgSO4) = 0,5 · 120 = 60 г
Vm = 22,4 л/моль
V(H2) = n(H2) · Vm = 0,5 · 22,4 = 11,2 л
Відповідь:
n(H2SO4) = 0,5 моль; m(MgSO4) = 60 г; V(H2) = 11,2 л
218. Обчисліть кількість речовини
сульфату, що містить 32 г цієї солі.
Відомо:
m(CuSO4) = 32 г
n(Cu) ? shkola.in.ua
Розв’язання:
M(CuSO4) = 64 + 32 + 64 = 160 г/моль
n(CuSO4) = m(CuSO4) / M(CuSO4) = 32 / 160 = 0,2 моль
n(Cu) : n(CuSO4) = 1 : 1
Отже: n(Cu) = 0,2 моль
0,2 моль
Відомо: m(Mg) = 6,0
m(Fe) = 16,8
V(H2) ?
shkola.in.ua
Mg + H2SO4 → MgSO4 + H2
Fe + H2SO4 → FeSO4 + H2 Розв’язання:
M(Mg) = 24 г/моль, M(Fe) = 56 г/моль
n(Mg) = m/M = 6,0/24 = 0,25 моль
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
n(Fe) = m/M = 16,8/56 = 0,30 моль
n(H2) = 0,25 + 0,30 = 0,55 моль
Vm = 22,4 л/моль
V(H2) = n·Vm = 0,55·22,4 = 12,32 л
Відповідь:
V(H2) = 12,32 л 220. У розчин
реакції. Обчисліть, як зміниться
Відомо:
m(AgNO3) = 85 г
w(AgNO3) = 2%
m(Ag) ?
Δm — ?
shkola.in.ua
Рівняння реакцій:
Zn + 2AgNO3 → Zn(NO3)2 + 2Ag
Розв’язання:
m(AgNO3) = 0,02 · 85 = 1,7 г
M(AgNO3) = 108 + 14 + 48 = 170 г/моль
n(AgNO3) = m/M = 1,7/170 = 0,01 моль
За рівнянням реакції 2 моль AgNO3 утворюють 2 моль Ag,
отже
n(Ag) = n(AgNO3) = 0,01 моль
m(Ag) = n · M = 0,01 · 108 = 1,08 г
Цинку витратиться вдвічі
AgNO3):
n(Zn) = 0,01/2 = 0,005 моль
m(Zn) = 0,005 · 65 = 0,325 г
Зміна маси пластинки:
Δm = m(Ag) − m(Zn) = 1,08 − 0,325 = 0,755
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
твердому стані.
Рівняння реакції:
Сторінка 167
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
У 18 столітті люди навчилися
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
горіння етану:
2C2H6 + 7O2 = 4CO2 + 6H2O
Рівняння горіння пропану:
C3H8 + 5O2 = 3CO2 + 4H2O 231.
1. З магній оксидом: MgO + CO2 = MgCO3
2. З натрій оксидом:
Na2O + CO2 = Na2CO3
3. З натрій гідроксидом:
2NaOH + CO2 = Na2CO3 + H2O
4. З калій гідроксидом: 2KOH + CO2 = K2CO3 + H2O
5. З барій гідроксидом: Ba(OH)2 + CO2 = BaCO3 + H2O 233.
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
гідроген хлориду, який витрачається для
Відомо:
m(NaHCO3) = 10 г
m(HCl) ?
V(CO2) (н. у.) — ?
shkola.in.ua
Розв’язання:
NaHCO3 + HCl = NaCl + H2O + CO2
кількість речовини соди:
M(NaHCO3) = 23 + 1 + 12 + 16·3 = 84 г/моль
n(NaHCO3) = 10 / 84 ≈ 0,119
За рівнянням реакції:
n(HCl) = n(NaHCO3) = 0,119
n(CO2) = n(NaHCO3) = 0,119
Знайдемо масу гідроген хлориду: M(HCl) = 1 + 35,5 = 36,5 г/моль m(HCl) = 0,119 · 36,5 ≈ 4,34
V(CO2) = n · 22,4 = 0,119 · 22,4 ≈ 2,67
m(Ca(OH)2) ? shkola.in.ua
V(CO2) = 45000 · 0,00056 = 25,2
Ca(OH)2 + CO2 = CaCO3↓ + H2O
речовини CO2: n(CO2) = 25,2 / 22,4 = 1,125 моль
рівнянням реакції: n(Ca(OH)2) = n(CO2) = 1,125 моль
молярну масу Ca(OH)2: M(Ca(OH)2) = 40 + 16·2 + 1·2 = 74 г/моль
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
m(CO2) = 1 кг = = 1000 г
Поглинач: CaO
m(CaO) ?
shkola.in.ua
Розв’язання: Запишемо рівняння реакції:
CaO + CO2 = CaCO3
M(CO2) = 12 + 16·2 = 44 г/моль
n(CO2) = 1000 / 44 ≈ 22,73 моль
За рівнянням реакції: n(CaO) = n(CO2) = 22,73 моль
Знайдемо
M(CaO) = 40 + 16 = 56 г/моль
Знайдемо масу кальцій
m(CaO) = 22,73 · 56 ≈ 1273
Відомо: V(CH4) = 560 л (н. у.)
m(CaCO3) ? shkola.in.ua
метану: CH4 + 2O2 = CO2 + 2H2O
За рівнянням: з 1 моль CH4 утворюється 1 моль CO2
Знайдемо кількість речовини метану: n(CH4) = 560 / 22,4 = 25 моль
Отже, n(CO2) = 25 моль
2. Запишемо рівняння реакції одержання кальцій карбонату: Ca(OH)2 + CO2 = CaCO3↓ + H2O За рівнянням: 1 моль CO2 → 1 моль CaCO3 Отже, n(CaCO3) = 25 моль
3. Знайдемо молярну масу CaCO3: M(CaCO3) = 40 + 12 + 16·3 = 100 г/моль Знайдемо масу осаду: m(CaCO3) = n · M = 25 · 100 = 2500 г = 2,5 кг
2,5
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Пояснимо призначення
1. Посудина
кислотою: CaCO3 + 2HCl = CaCl2 + CO2↑ + H2O
цій частині
2. Пляшка з водою
3. Пляшка
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
4.
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
1. Механізм
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
2. Симптоми
(CO)
2.
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
кіптяви?
Етанол має формулу C2H5OH (C2H6O).
Молярна маса: 2·12 + 6·1 + 16 = 46.
Маса Карбону: 24.
Масова частка Карбону: 24/46 ≈ 0,52 (52%).
Пентанол має формулу C5H11OH (C5H12O).
Молярна маса: 5·12 + 12·1 + 16 = 88.
Маса Карбону: 60.
Масова частка Карбону: 60/88 ≈ 0,68 (68%).
Отже, у
CH4.
12 + 4·1 = 16.
12.
8·12 + 18·1 = 96 + 18 = 114.
96/114 ≈ 0,84 (84%).
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
m(Fe3O4) = 1 кг = = 1000 г
V(CO) ?
shkola.in.ua
Розв’язання:
Рівняння реакції:
Fe3O4 + 4CO = 3Fe + 4CO2
Молярна маса Fe3O4: 3·56 + 4·16 = 232 г/моль.
Кількість речовини Fe3O4: n = 1000 / 232 ≈ 4,31 моль.
За рівнянням реакції на 1 моль Fe3O4 потрібно 4 моль CO,
отже:
n(CO) = 4 · 4,31 ≈ 17,24 моль.
Об’єм за н. у.:
V = 17,24 · 22,4 ≈ 386 л.
Відповідь: приблизно 386 л чадного газу.
Відомо:
V(C8H18) = 1 л
ρ(C8H18) = 750 г/л
m(CO) = 200 г
ω(C8H18), % ? shkola.in.ua
Розв’язання:
М(CO) = 12 + 16 = 28 г/моль
n(CO) = 200 / 28 ≈ 7,14 моль
Рівняння (неповне згоряння):
2C8H18 + 17O2 = 16CO + 18H2O
З рівняння: 16 моль CO утворюються з 2 моль C8H18, тобто
1 моль C8H18 → 8 моль CO
n(C8H18) = 7,14 / 8 ≈ 0,893 моль
М(C8H18) = 8·12 + 18·1 = 114 г/моль
m(C8H18, що згорів з утворенням CO) = 0,893 · 114 ≈ 102 г Маса 1 л бензину: m(усього) = ρ · V = 750 · 1 = 750 г
Масова частка: ω = 102 / 750 ≈ 0,136 = 13,6 % Відповідь:
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
1. Утворення чадного газу: C + O2 = CO2 CO2 + C = 2CO
2. Відновлення
Fe2O3 + 3CO = 2Fe + 3CO
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
m(води) = 1000
m(CH4) = 0,04
m(CO2) = 3,5
m(O2) = 0,07
ω(CH4), ω(CO2), ω(O2) — ? shkola.in.ua
Розв’язання: Для метану: m(розчину) = 1000 + 0,04 = 1000,04 г ω(CH4) = 0,04 / 1000,04 · 100% ≈ 0,004 % Для вуглекислого газу: m(розчину) = 1000 + 3,5 = 1003,5 г
ω(CO2) = 3,5 / 1003,5 · 100% ≈ 0,349 %
Для кисню: m(розчину) = 1000 + 0,07 = 1000,07 г
ω(O2) = 0,07 / 1000,07 · 100% ≈ 0,007 %
Висновок:
ω(CO2) > ω(O2) > ω(CH4).
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
• без доступу кисню,
• у вологому середовищі,
• за участю бактерій,
• із гною, харчових відходів, рослинних решток, відходів сільського господарства. Для цього використовують спеціальні установки — біореактори або метантенки.
Біогаз використовують:
• як паливо для опалення і приготування їжі,
• для виробництва електроенергії,
0,04 г CH4.
1 000 000
m(CH4) = 0,04 · 1000 = 40 г М(CH4) = 16
= 40 / 16 = 2,5
Відомо:
S = 10 м2 h = 2,5 м
V(CH4) ?
shkola.in.ua
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Розв’язання: V(повітря) = S · h = 10 · 2,5 = 25 м3 Із параграфа:
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
1. Після
2.
3.
для одоризації газу.
New London (Техас, 1937)
4. Бувають і випадки, коли сильний “газовий” запах у місті виникав через
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Відомо:
m(Al4C3) = 360 г
V(CH4) ?
shkola.in.ua
Розв’язання:
М(Al4C3) = 4·27 + 3·12 = 108 + 36 = 144 г/моль
n(Al4C3) = 360 / 144 = 2,5 моль
Рівняння реакції: Al4C3 + 12H2O = 4Al(OH)3 + 3CH4
рівняння:
моль Al4C3 → 3 моль CH4
n(CH4) = 2,5 · 3 = 7,5 моль
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
можна стверджувати,
транспорт), там і утворюється CO2.
Сторінка 205
Поміркуйте Проаналізуйте малюнок 22.2 та
Землі, а яка — атмосферою.
Із 343 Вт/м2 сонячної енергії: • Поверхня Землі утримує 168 Вт/м2 (це приблизно
• Атмосфера утримує 72 Вт/м2 (бо
Сторінка 208
Робота з інформацією





https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html


• Лікувальні/фольклорні
оберігами.
Як відрізнити справжній перл
• Тест зубом: справжній
• Блиск: натуральні мають «глибинний» перламутровий блиск.
• Форма і поверхня: природні часто неправильні; ідеально круглі — цінніші
культивовані.
Догляд за перлами
• Берегти від кислот, косметики і парфумів.
• Зберігати окремо, щоб не подряпати.
• Чистити м'якою вологою тканиною.
Короткі факти
• Найдорожчі перли можуть коштувати
• Кольори: білі, кремові, рожеві,
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
пожежі, блискавки, біогенні випаровування)
частку.
Сторінка 209 Розуміння
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Неправильне. На Землю потрапляє 343
віддається менше, ніж приходить.
■ Земна поверхня поглинає 4/5 енергії,
Правильне. На поверхню
168 / 240 = 0,7 ≈ близько 4/5 (приблизно). ■
випромінювання.
■ Близько
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
• Парниковий ефект — це
тощо).
• Завдяки йому на Землі тепло, але
планета перегрівається. • Наслідки: спеки, посухи, повені, танення льодовиків, підняття рівня океану. Головна причина: спалювання вугілля, нафти і газу, транспорт, заводи, вирубка лісів. Чому це важливо? Клімат змінюється швидше, ніж природа і люди встигають
пристосуватися.
Листівка 2 (заклична)
ЩО МОЖЕ ЗРОБИТИ КОЖЕН?
• Економити електроенергію і тепло.
• Частіше ходити пішки або користуватися громадським транспортом.
• Менше користуватися одноразовими речами.
• Сортувати сміття.
• Саджати дерева і берегти природу.
Навіть маленькі дії багатьох людей дають великий результат!
Листівка 3 (коротка, для швидкого читання)
ЗЕМЛЯ ПЕРЕГРІВАЄТЬСЯ!
• Причина: надлишок парникових
• Наслідки: спеки, повені, посухи, танення
• Рішення:
людини.
Сторінка
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
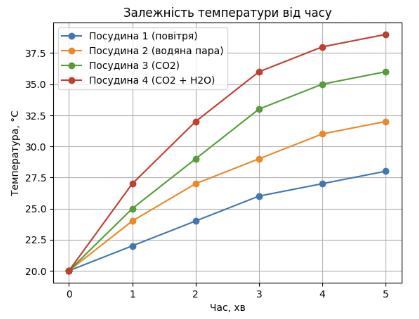
4.
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
CO2, CO2 + H2O, метан). Сторінка
те, як
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
велику користь людям, наприклад
несуть відповідальність за створення
бомб.
часто усвідомлюють
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Calcify (Carbon Footprint
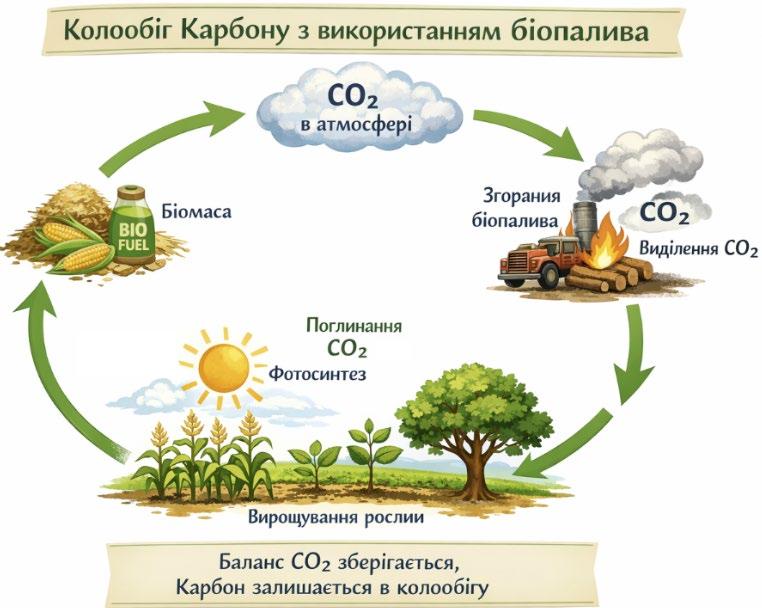
296.
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
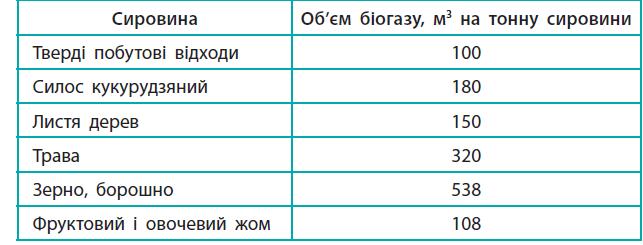
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
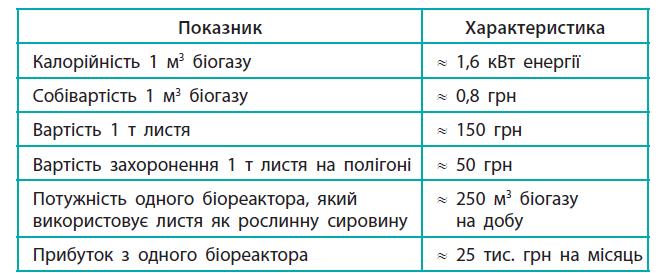
один біореактор.
За добу біореактор дає:
250 × 1,6 = 400
За місяць (≈ 30 діб):
400 × 30 =
•
• Не купуйте
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
• Сортуйте сміття.
• Саджайте дерева.
Листівка 3 (коротка, заклична)
ТВОЇ ЩОДЕННІ ДІЇ ВАЖЛИВІ
• Менше енергії — менше CO2.
• Менше відходів — чистіше довкілля.
• Почни з себе — і допоможеш планеті.
Сторінка 220 НАВЧАЛЬНЕ ДОСЛІДЖЕННЯ
посудині.
Сторінка 221
Що ми маємо зробити?
1. Для дослідження
групах).
2. Рівняння реакції:
CaCl2 + Na2CO3 → CaCO3↓ + 2NaCl
Молярна маса CaCl2 = 111 г/моль
Молярна маса CaCO3 = 100 г/моль Для повного перебігу
CaCl2.
3. До склянки
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
зробити?
Які висновки ми маємо зробити? Маса осаду CaCO3
Сторінка
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Сторінка
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
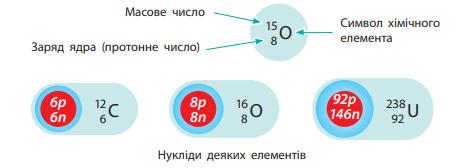
Тобто на рисунку: • А і В — один і той самий атом
• Б — другий атом
• Г — третій атом
Відповідь: зображено моделі 3 різних атомів.
Сторінка 229
Поміркуйте
Сторінка 230
Поміркуйте Запропонуйте
Сторінка
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Z = 43) у
році.
отримали в лабораторії Нові хімічні елементи ще можуть відкрити. Ученим уже вдалося синтезувати
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
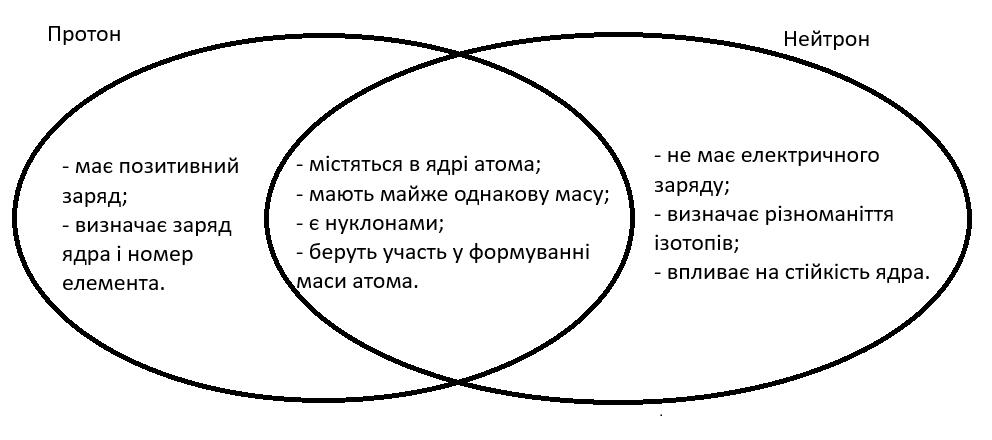
305.
б) ядра
Карбону? +6 (або +6e).
306. Запишіть
а) 2 протони й 1 нейтрон; p = 2, n = 1 ⇒ A = 2 × 1 = 3: б) 8 протонів і 9 нейтронів; P = 8, N = 9 ⇒ A = 8 × 9 = 17;
в) 15
протонів і 16 нейтронів; P = 15, N = 16 ⇒ A = 15 × 16 = 31;
г) 35
протонів і 45 нейтронів; P = 35, N = 45 ⇒ A = 35 × 45 = 80;
д) 25 протонів і 30 нейтронів; P = 25, N = 30 ⇒ A = 25 × 30 = 55; е) 89 протонів і 117 нейтронів. P = 89, N = 117 ⇒ A = 89 × 117 = 206;
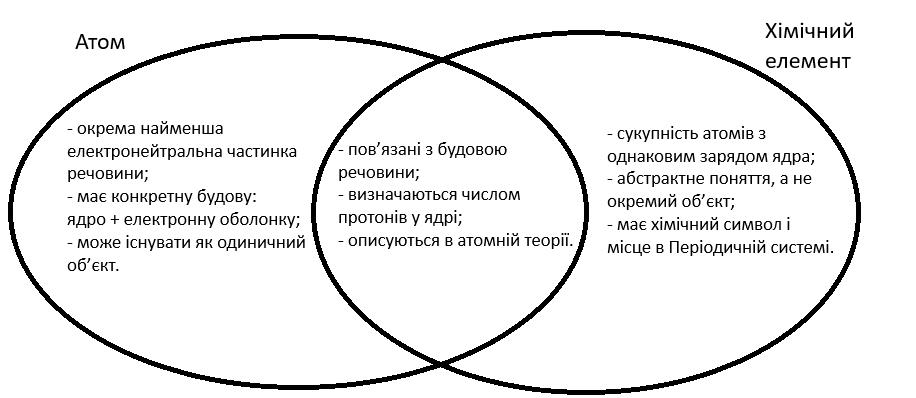
307. Визначте склад атомів таких нуклідів: 17O, 14C, 137Cs, 60Co, 130I, 65Zn, 19F, 56Fe, 39K, 90Sr, 206Pb, 40Ca, 294Ts.
17O: P = 8, E = 8, N = 17 – 8 = 9.
14C: P = 6, E = 6, N = 14 – 6 = 8.
137Cs: P = 55, E = 55, N = 137 – 55 = 82.
60Co: P = 27, E = 27, N = 60 – 27 = 33.
130I: P = 53, E = 53, N = 130 – 53 = 77.
65Zn: P = 30, E = 30, N = 65 – 30 = 35.
19F: P = 9, E = 9, N = 19 – 9 = 10.
56Fe: P = 26, E = 26, N = 56 – 26 = 30.
39K: P = 19, E = 19, N = 39 – 19 = 20.
90Sr: P = 38, E = 38, N = 90 – 38 = 52.
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
206Pb: P = 82, E = 82, N = 206 – 82 = 124.
40Ca: P = 20, E = 20, N = 40 – 20 = 20.
294Ts: P = 117, E = 117, N = 294 – 177 = 177.
308. Чим відрізняються за складом ядра атомів нуклідів:
а)
У
Літію 6Li і 7Li;
Літію Z = 3, тобто в обох ядрах по 3 протони.
P = 3, N = 6 – 3 = 3
P = 3, N = 7 – 3 = 4
Відрізняються кількістю нейтронів (3 і 4).
б) Урану 235U і 239U?
У Урану Z = 92, тобто в обох ядрах по 92 протони.
P = 92, N = 235 – 92 = 143
P = 92, N = 235 – 92 = 147
Відрізняються кількістю нейтронів (143 і 147).
309. Запишіть символи нуклідів:
а) Натрію, який містить таке саме число нейтронів, що
24Mg; Z = 12 ⇒ N = 24 – 12 = 12
Для Na: Z = 11, треба N = 12 ⇒ A = 11 + 12 = 23
б) Оксигену,
13С. Z = 6 ⇒ N = 13 – 6 = 7
Для O: Z = 8, треба N = 7 ⇒ A = 8 + 7 = 15
310. Із наведеного списку виберіть:
а) ізотопи;
Карбон: ¹²₆C і ¹⁴₆C
Нітроген: ¹⁴₇N і ¹⁵₇N
Оксиген: ¹⁵₈O і ¹⁶₈O
б) нукліди з однаковим нейтронним числом;
Однакове нейтронне число (8):
¹⁶₈O → 8 нейтронів
¹⁴₆C → 8 нейтронів
¹⁵₇N → 8
нейтронів
Однакове нейтронне число (7):
¹⁴₇N → 7 нейтронів
¹⁵₈O → 7
нукліди з однаковим нуклонним
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
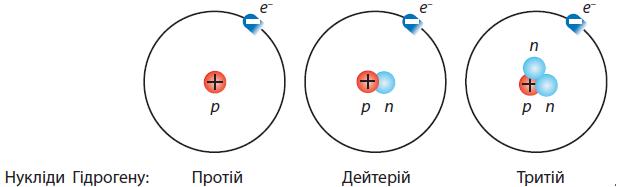
через це різна і маса. Отже,
вони отримали такі назви?
• Протій — від “перший/найпростіший”: у ядрі лише одна частинка (протон).
• Дейтерій — від “другий/подвійний”: у ядрі дві частинки (протон + нейтрон), тобто маса приблизно вдвічі більша за протій.
• Тритій
•
•
•
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Ar(Li) ≈ 6,94 — між 6 і 7 ⇒ у
Ar(P) ≈ 30,97 ≈ 31
Ar(Cu) ≈ 63,546 — між 63 і 65 ⇒
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
інші гіпотези щодо будови атома.
схарактеризуйте, чим вони відрізняються.
1. «Кексова» модель Вільяма Томсона (1902):
• Атом — це суцільна позитивно заряджена речовина.
• Електрони рівномірно розподілені всередині, як родзинки в кексі.
• Ядра немає.
2. «Кексова» модель Джозефа Джона Томсона (1904):
• Також немає ядра.
• Електрони розміщені впорядковано — в одній площині, утворюють концентричні кільця.
• Позитивний заряд заповнює
3. Модель атома Хантаро Наґаоки (1904):
• Вперше з’являється позитивно заряджене
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
ядра немає.
• Модель Резерфорда: позитивний
• Пояснює результати
•
Сторінка
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Сторінка
• 1-й рівень: 2 електрони
• 2-й рівень: 8 електронів
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
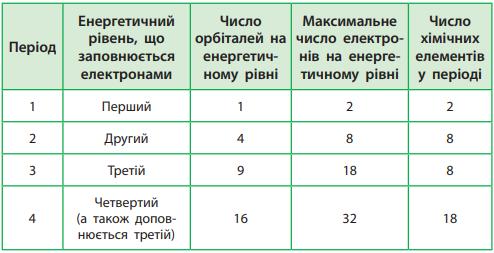
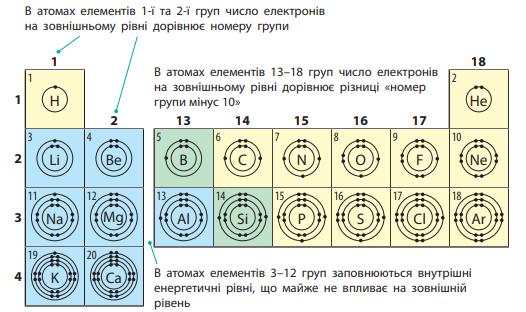
C → 2 рівні
Si → 3 рівні
Ge → 4 рівні
б) Берилію, Магнію, Кальцію;
Be → 2 рівні
Mg → 3 рівні
Ca → 4 рівні в) Флуору, Хлору, Йоду?
F → 2 рівні
Cl → 3 рівні
I → 5 рівнів
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
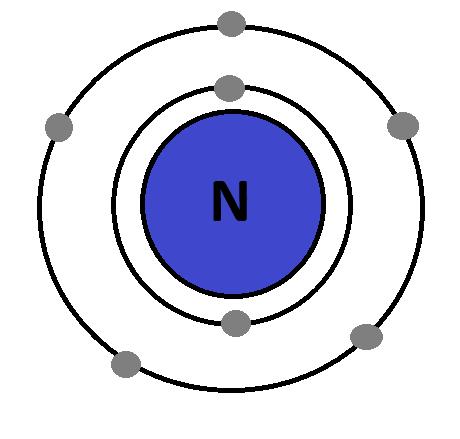
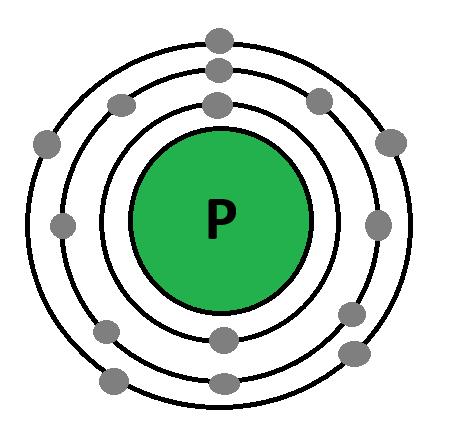
•
•
•
•
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
(Se)
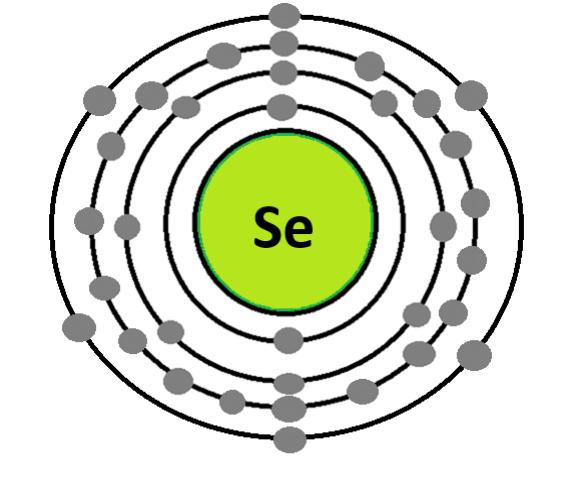
• Атоми з 1–3 електронами на
• Атоми
•
•
Сторінка 249
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Сторінка 254
Робота з інформацією
328. Запишіть
а) лужних;
Оксид: M2О
Гідроксид: MOH
б) лужноземельних.
Оксид: MO
Гідроксид: M(OH)2
Використовуючи
M2O + H2O → 2MOH
MO + H2O → M(OH)2
329.
2Li + I2 → 2LiI
Ca + I2 → CaI2
2Al + 3I2 → 2AlI3 г)
H2+I2→2HI
330.
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Be, Ca, Sr, Ba
F, Cl, Br, I
He, Ne, Xe Al, S, Fe, H
333.
334.
«галогени», «халькогени» та «пніктогени»?
Галогени
• гало — «сіль», генеа — «народження»
• Значення: «ті, що утворюють солі».
• Чому так назвали: ці елементи легко реагують із металами, утворюючи солі (NaCl, KBr).
Халькогени
• халько — «мідь», генеа — «народження»
• Значення: «ті, що утворюють мідні руди».
• Чому так назвали: Оксиген, Сульфур та інші елементи
складу руд і мінералів металів.
Пніктогени
• пнікто — «задушливий», генеа — «народження»
•
•
256
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Сторінка 262 Робота з інформацією 337. Чим зумовлені металічні та неметалічні властивості хімічних елементів?
• числом електронів на зовнішньому енергетичному рівні;
• силою притягання цих
до ядра. Метали легко віддають електрони, неметали — приймають.
338. Чому атоми приймають або віддають електрони в хімічних реакціях?
енергетичного рівня (як у інертних
• протонів — 13
• електронів — 13
йон Al3+?
• протонів — 13
• електронів — 10,
•
•
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
а) Оксигену; б) Хлору; в) Силіцію?
До завершення зовнішнього рівня (до 8 електронів):
а) Оксиген (O) має 6 → бракує 2 електрони.
б) Хлор (Cl) має 7 → бракує 1 електрона.
в) Силіцій (Si) має 4 → бракує 4 електрони.
345. Йон певного хімічного елемента E2+ має таку саму електронну
Неону. Визначте цей елемент. Йон E2+ має таку саму будову, як Ne (10 електронів).
Отже, нейтральний атом E мав 12 електронів (бо віддав 2) → Z = 12.
Елемент: Магній (Mg).
346. За періодичною таблицею
віддавати або приєднувати в хімічних
Фосфор P (група 15) має
Сторінка 263
Mg: 12 e⁻ (2, 8, 2).
• йон Mg²⁺: 10 e⁻ (2, 8).
Сторінка
Сторінка 271
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
• Аргон (Ar, 39,95) стоїть
• Кобальт (Co, 58,93) стоїть
(K, 39,10)
(Ni, 58,69)
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
в Стибію, а неметалічні — сильніші в Арсену.
• у групі
Б: n + 2 = 11 →
(Na) В: n + 4 = 13 →
(Al)
Відповідь: Б — Натрій (Na).
є А?
Інертні гази мають Z = 2, 10, 18, 36, 54, 86,…
Тобто n + 4n має
A: Z = 82 → Свинець Pb
Б: Z = 84 → Полоній Po (металічний елемент)
В: Z = 86 → Радон Rn (інертний
Відповідь: A — Pb.
n + 4 = 86 ⇒ n = 82
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
означає, що:
• елемент не дуже легкий (як S),
• але й не дуже важкий (як Te).
Із трьох можливих елементів:
• S → водню було б більше,
• Te → водню було б менше,
• Se → значення близьке до 2,47%.
Відповідь: Se.
Сторінка 274
Сторінка
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
• Валентні (зовнішні) електрони визначають
• Спільні електронні пари
• Неспільні (вільні) пари залишаються
молекули.
• Запроваджено електронно

• Нітроген (N) — має 5 → бракує 3
• Хлор (Cl) — має 7 →
• Сульфур (S) — має 6 → бракує 2
• Карбон (C) — має 4 → бракує 4
• Флуор (F) — має 7 → бракує 1
• Оксиген (O) — має 6 →
2
•
•
•
•
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
між атомами Гелію.
Енергія зв’язку H–H ≈ –430 000 Дж/моль.
Енергія притягання He–He ≈ –76,1 Дж/моль.
430000
76,1 ≈ 5650
Відповідь: так.
■
атомами Гелію.
Для H–H: 0,74 Å.
Для He–He: 3 Å. 3 0,74 ≈ 4,05
Відповідь: ні, в 4 рази більша.
• Нітроген (N) — 5
•
(O) — 6
Сторінка 285
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Робота з інформацією 363. Латиною co означає «спільний»,
«ковалентний».
Спосіб утворення зв’язку між атомами,
електронні пари, що належать одночасно
парою. Його називають ordinary
365. Скільки
Хлор (Cl):
• електронних пар: 3
• неспарених електронів: 1 Формула Льюїса: б) Сульфур (S):

• електронних пар: 2
• неспарених електронів: 2 Формула Льюїса:

в) Фосфор (P):
• електронних пар: 1
• неспарених електронів: 3 Формула Льюїса:
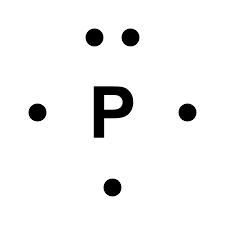
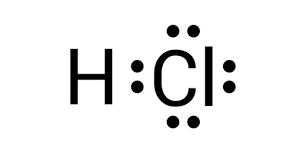
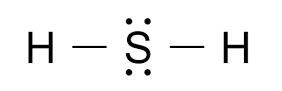
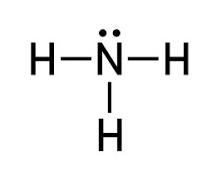
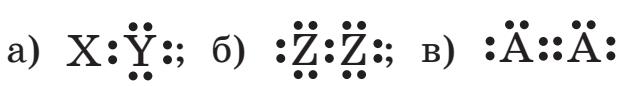
375. Випишіть
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
OF2, F2, ClF3, P4, NO2, NO, N2.
Неполярний: S₈, O₂, F₂, P₄, N₂.
Полярний: NH₃, OF₂, ClF₃, NO₂, NO.
376. Користуючись форзацем 1, обчисліть різницю між
елементів у парах: Li–Cl, Be–Cl, B–Cl, C–Cl, N
полярним і найменш полярним зв’язками.
ΔЕН = |ЕН(Cl) − ЕН(елемента)|
Li–Cl: ΔЕН = |3,16 − 0,98| = 2,18
Be–Cl: ΔЕН = |3,16 − 1,57| = 1,59
B–Cl: ΔЕН = |3,16 − 2,04| = 1,12
C–Cl: ΔЕН = |3,16 − 2,55| = 0,61
N–Cl: ΔЕН = |3,16 − 3,04| = 0,12
O–Cl: ΔЕН = |3,16 − 3,44| = 0,28
F–Cl: ΔЕН = |3,16 − 3,98| = 0,82
Найбільш полярний зв’язок: Li–Cl = 2,18
Найменш полярний зв’язок: N–Cl = 0,12
377. Визначивши різницю
молекули: H2, HCl, HF, ClF, Cl2, F2.
а) Н2: ∆EH = 2,2 – 2,2 = 0;
б) HCl: ∆EH = 3,16 – 2,2 = 0,96;
в) HF: ∆EH = 3,98 – 2,2 = 1,78;
г) ClF: ∆EH = 3,98 – 3,16 = 0,82;
д) Cl2: ∆EH = 3,16 – 3,16 = 0;
е) F2: ∆EH = 3,98 – 3,98 = 0.
Найполярнішою є молекула
H2O, сірководень H2S,
HI: |2,66 − 2,20| = 0,46
HCl: |3,16 − 2,20| = 0,96
HBr: |2,96 − 2,20| = 0,76
H2O (H–O): |3,44 − 2,20| = 1,24
H2S (H–S): |2,58 − 2,20| = 0,38
Cl2: |3,16 − 3,16| = 0
CH4 (C–H): |2,55 − 2,20| = 0,35
PH3 (P–H): |2,19 − 2,20| ≈ 0 Порівняння
величиною?
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Електронегативності (за Полінгом):
H = 2,20
Cl = 3,16
F = 3,98
Молекула HCl
Cl електронегативніший за H: 3,16 > 2,20
Спільна електронна пара зміщується до Cl →
на Cl частковий від’ємний заряд (δ−).
Молекула ClF
F
електронегативніший за Cl: 3,98 > 3,16
Спільна електронна пара зміщується до F →
на Cl частковий додатний заряд (δ+).
Де більший заряд за модулем
Порівняємо різницю електронегативностей:
HCl: 3,16 − 2,20 = 0,96
ClF: 3,98 − 3,16 = 0,82
Більша різниця
0,96 > 0,82, отже в HCl
Відповідь:
Відповідь обґрунтуйте. Знайдемо різницю
H–O: 3,44 − 2,20 = 1,24
H–S: 2,58 − 2,20 = 0,38
H–Se: 2,55 − 2,20 = 0,35
H–Te: 2,10 − 2,20 ≈ 0,10
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
• зарядом ядра;
• відстанню валентних електронів від ядра;
• екрануванням внутрішніми електронами.
Чому вона змінюється в періодах і групах?
У періодах (зліва направо) електронегативність зростає, тому що:
• збільшується заряд ядра;
• кількість енергетичних рівнів не змінюється;
• ядро сильніше притягує спільну електронну пару.
У групах (зверху вниз) електронегативність зменшується, тому що:
• збільшується радіус атома (з’являються нові енергетичні рівні);
• посилюється екранування валентних електронів внутрішніми;
• притягання електронів до ядра слабшає. Назвіть
• Найбільш електронегативний
Сторінка
Розуміння
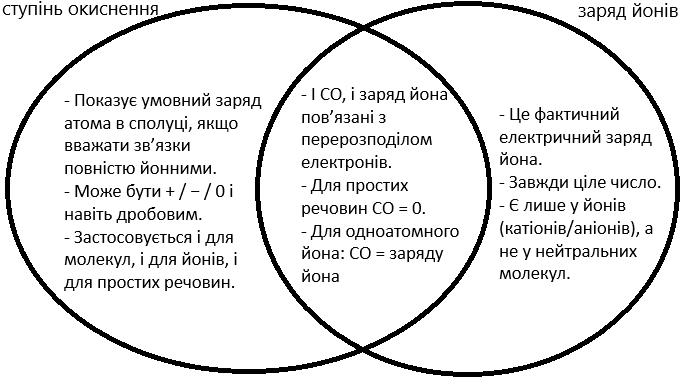
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
а) H2, H2O, HCl, NaOH, NaH;
• H₂: H = 0
• H₂O: H = +1, O = −2
• HCl: H = +1, Cl = −1
• NaOH: Na = +1, O = −2, H = +1
• NaH: Na = +1, H = −1
б) PH3, NO2, H2O2;
• PH₃: H = +1
Нехай P = x x + 3·(+1) = 0
x + 3 = 0
x = −3
Відповідь: P = −3, H = +1
• NO₂:
O = −2
Нехай N = x
x + 2·(−2) = 0
x − 4 = 0
x = +4
Відповідь: N = +4, O = −2
• H₂O₂: H = +1, O = −1
в) HCl, Cl2, CuCl2,KClO3;
• HCl: H = +1, Cl = −1
• Cl₂: Cl = 0
• CuCl₂:
Cl = −1
Нехай Cu = x
x + 2·(−1) = 0
x − 2 = 0
x = +2
Відповідь: Cu = +2, Cl = −1
• KClO₃: K = +1, O = −2
Нехай Cl = x
(+1) + x + 3·(−2) = 0
1 + x − 6 = 0
x − 5 = 0
x = +5
Відповідь: K = +1, Cl = +5, O = −2
г) N2, N2H4, N2O3, HNO3.
• N₂: N = 0
• N₂H₄: H = +1
Нехай N = x
2x + 4·(+1) = 0
2x + 4 = 0
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
2x = −4
x = −2
Відповідь: N = −2, H = +1
• N₂O₃: O = −2
Нехай N = x
2x + 3·(−2) = 0
2x − 6 = 0
2x = 6
x = +3
Відповідь: N = +3, O = −2
• HNO₃: H = +1, O = −2
Нехай N = x
(+1) + x + 3·(−2) = 0
1 + x − 6 = 0
x − 5 = 0
x = +5
Відповідь: H = +1, N = +5, O = −2
цього хімічного елемента.
Негативні СО Нітрогену:
• NH₃ (N −3)
• N₂H₄ (N −2)
Позитивні СО Нітрогену:
• NO (N +2)
• NO₂ (N +4)
• HNO₃ (N +5)
Сторінка 298
(якщо
Натрій, Кальцій, Карбон, Плюмбум, Алюміній.
• Хлор (Cl, 17 група) вищий: +7; нижчий: −1; проміжні: +1, +3, +5
• Фосфор (P, 15 група) вищий: +5; нижчий: −3; проміжні: +3
• Натрій (Na, 1 група) вищий і єдиний: +1; нижчий: 0 (у простій речовині)
• Кальцій (Ca, 2 група) вищий і єдиний: +2; нижчий: 0
• Карбон (C, 14 група) вищий: +4; нижчий: −4; проміжні: +2 (часто), інколи −2
• Плюмбум (Pb, 14 група, метал) вищий: +4; нижчий (типовий): +2; (0 у простій речовині)
• Алюміній (Al, 13 група) вищий і типовий: +3; нижчий: 0
387. Обчисліть ступені
сполуках: CH4, CH3Cl,CH2Cl2, C2H5Cl, C2H2Cl4, С2Cl6.
• CH₄: H = +1
Нехай C = x
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
x + 4·(+1) = 0
x + 4 = 0
x = −4
Відповідь: C = −4
• CH₃Cl:
H = +1, Cl = −1
x + 3·(+1) + (−1) = 0
x + 3 − 1 = 0
x + 2 = 0
x = −2
Відповідь: C = −2
• CH₂Cl₂: H = +1, Cl = −1
x + 2·(+1) + 2·(−1) = 0
x + 2 − 2 = 0
x = 0
Відповідь: C = 0
• C₂H₅Cl: H = +1, Cl = −1
2x + 5·(+1) + (−1) = 0
2x + 5 − 1 = 0
2x + 4 = 0
2x = −4
x = −2
Відповідь: C = −2
• C₂H₂Cl₄:
H = +1, Cl = −1
2x + 2·(+1) + 4·(−1) = 0
2x + 2 − 4 = 0
2x − 2 = 0
2x = 2
x = +1
Відповідь: C = +1
• C₂Cl₆: Cl = −1
2x + 6·(−1) = 0
2x − 6 = 0
2x = 6
x = +3
Відповідь: C = +3
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
•
•
• погано стискаються.
• мають
•
•
Сторінка 301
Поміркуйте
Визначте
• частинки розміщені щільно. Відмінне:
• рідина: частинки
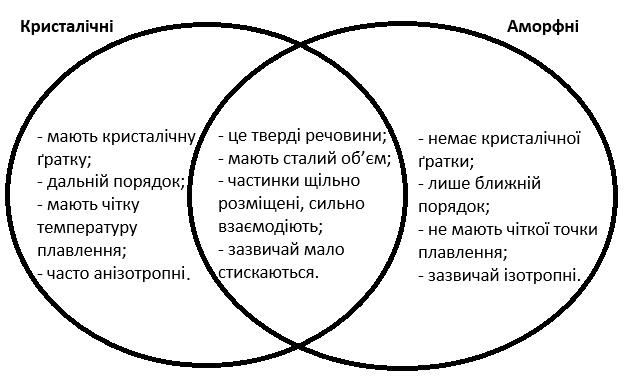
• відсутність чіткої
• відсутність кристалічної ґратки;
• ізотропність (властивості
•
•
•
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
393.
• вони не мають впорядкованої кристалічної будови;
• їхні частинки розміщені хаотично, без регулярної ґратки;
• через це вони не утворюють правильних геометричних форм.
Розуміння явищ природи (робота в групах)
394. Чому аморфні речовини не мають чіткої температури плавлення?
• зв’язки між частинками різної міцності;
• руйнуються поступово;
• речовина повільно розм’якшується в інтервалі температур. Чому кристалічні речовини не розм’якшуються перед плавленням?
Кристалічні речовини мають чітку, впорядковану ґратку,
• усі зв’язки приблизно однакові;
• при досягненні
• речовина переходить з твердого стану
395. Як ви розумієте твердження: «Кристалічним
форми»?
• форма кристалічної
• вони не деформуються
сіль, тверде мило? Аморфні речовини:
• Віск — аморфний
• Парафін — аморфний
• Поліетилен — аморфний (у
• Скло — аморфне
• Тверде мило — аморфне Не аморфні (кристалічні):
• Сухий лід (CO₂) — кристалічний
• Кухонна сіль (NaCl) — кристалічна
якими властивостями
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
Сторінка
Поміркуйте
Як ви вважаєте, чим
молекулярної та немолекулярної будови?
Молекулярні речовини:
• слабші міжмолекулярні сили;
• низькі температури плавлення й кипіння;
• часто гази або рідини.
Немолекулярні речовини:
• сильні зв’язки (йонні, атомні, металічні);
• високі температури плавлення;
• зазвичай тверді.
Сторінка 306
Поміркуйте
Чому з-поміж усіх речовин
• лише молекули
Сторінка
розкладаються;
• Кальцій карбонат (CaCO₃) → CaO + CO₂(вапняк, крейда)
• Кухонна сода (NaHCO₃) → Na₂CO₃ + CO₂ + H₂O
• Амоній хлорид (NH₄Cl) — при
розкладається на NH₃ і HCl б) плавляться;
• Лід (H₂O)
• Парафін
• Віск
• Цукор (спочатку плавиться,
• Кухонна сіль (NaCl) — за дуже
температури в) сублімують.
• Лід (H₂O)
• Парафін
• Віск
• Цукор (спочатку плавиться, потім
• Кухонна сіль (NaCl) — за
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
сульфур(VI) оксид
запахом, tпл. = 16,8 °C, tкип. = 45 °C
Молекулярна кристалічна ґратка
Сторінка 308
Розуміння явищ природи (робота в групах)
400. Якими взаємодіями утримуються: а) атоми в молекулі;
Ковалентними хімічними зв’язками б) молекули в молекулярному кристалі;
Міжмолекулярними взаємодіями в) атоми в атомному кристалі?
Ковалентними зв’язками по всьому
401. Поясніть, чому
Випишіть окремо
стані: F2, CO2, He, C (графіт), HBr, S8 (сірка), H2, SiO2, O3.
Молекулярні ґратки: F₂, CO₂, HBr, S₈, H₂, O₃ Атомні (ковалентні) ґратки: C (графіт), SiO₂ Атомна (інертний газ): He 403. Чи можна замінити:
405.
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
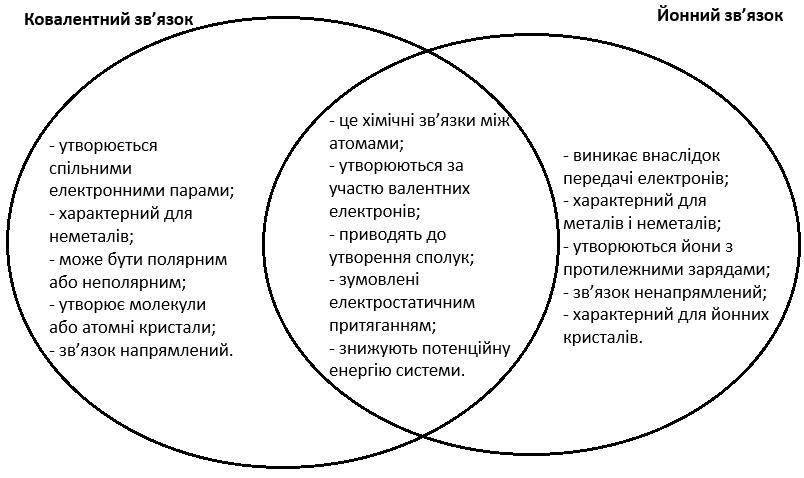
408. Із-поміж
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
HBr, Na2O, CaO, CO2, CO, NO2, K3N, NH3, N2, NF3, MgF2.
Na₂O, CaO, K₃N, MgF₂.
Всі інші мають – ковалентний.
409. Зобразіть схему утворення йонів на прикладі:
а) калій фториду KF;
Передача 1 електрону:
К → К + + e F + e → F
Утворення сполуки: K+ + F → KF
Реакція з простих речовин:2K + F2 → 2MKF
б) магній оксиду MgO;
Передача 2 електронів: Mg → Mg 2+ + 2e
О + 2e → О2−
Утворення сполуки: Mg 2+ + О → MgО
Реакція з простих речовин: 2Mg + О2 → 2MgО
в) алюміній броміду AlBr3.
Передача 3 електронів: Al → Al3+ + 3e 3Br + 3e → 3Br
Утворення сполуки: Al3+ + 3Br → AlBr3
Реакція з простих речовин: 2Al + 3Br2 → 2AlBr3
410. Проаналізуйте
(Б) за аналогією з
Модель А:
Mg віддає 2 електрони, два
Mg → Mg 2+ + 2e
2Сl + 2e- → 2Cl
Утворюється: Mg 2+ i 2Cl → MgСl2
Реакція: Mg + 2Cl2 → MgСl2
Модель Б:
(А).
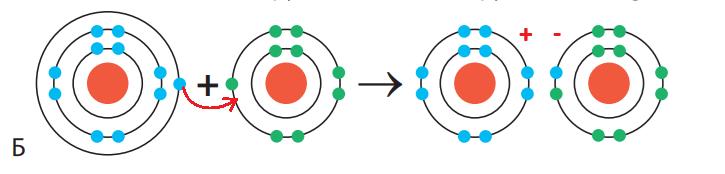
F + e - → F
Утворюється: Li+ i F → LiF
Реакція: 2Li + F2 → 2LiF
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
свій вибір.
Молекулярна будова: парафін, лимонна кислота, цукор, ацетон, спирт етиловий, йод.
(Низькі tплав і tкип, часто добре розчиняються в органічних розчинниках.)
Йонна будова: сіль кухонна, сода кальцинована.
(Високі tплав, добре розчинні у воді.)
Атомна будова:
графіт, скло кварцове.
(Дуже високі температури плавлення, нерозчинні.)
Сторінка 315
Визначаємо ризики
Під час дослідження
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
https://shkola.in.ua/2417-hdz-khimiia-8-klas-hryhorovych-2016.html
