AUTORES
COORDENADORES/AUTORES
Ricardo Jorge Dinis‑Oliveira
Professor catedrático de Toxicologia e Ciências Forenses, Agregação em Ciências Forenses, do Instituto Universitário de Ciências da Saúde da Cooperativa de Ensino Superior, Politécnico e Universitário e da Faculdade de Medicina da Universidade do Porto; Título de agregado em Ciências Forenses pela Fa culdade de Medicina da Universidade do Porto; Perito em Ciências Forenses, nomeadamente na área de Toxicologia Forense, e desenvolve a sua atividade científica e académica nas áreas da Toxicologia e Farmacologia das Substâncias Psicoativas, Pesticidas e Fármacos, nos seus aspetos pré ‑clínicos, clínicos e forenses; Diretor do Departamento de Ciências, coordenador das Licenciaturas em Ciências Foren ses e em Ciências Biomédicas e das Pós‑graduações em Perícias Forenses e Criminologia e em Análises Clínicas do Instituto Universitário de Ciências da Saúde da Cooperativa de Ensino Superior, Politécnico e Universitário; Coordenador da Pós‑graduação em Perícias Forenses da Faculdade de Medicina da Uni versidade do Porto; Diretor da 1H‑TOXRUN – Unidade de Investigação em Toxicologia & Uma Só Saúde; Investigador integrado e diretor do Laboratório de Toxicologia Translacional da Unidade de Ciências Biomoleculares Aplicadas (UCIBIO) e do Instituto para a Saúde e a Bioeconomia (i4HB); Licenciatura em Ciências Farmacêuticas e doutoramento em Toxicologia pela Faculdade de Farmácia da Universidade do Porto; Curso Superior de Medicina Legal (atual Curso de Especialização em Perícias Forenses) pela Faculdade de Medicina da Universidade do Porto; Integrou a World’s Top 2% Scientists List em 2021, 2022, 2023 e 2024 – ranking dos cientistas mais citados a nível mundial; Presidente e fundador da Associação Portuguesa de Ciências Forenses, Especialista Forense Nível 5.
Nuno Guerreiro Oliveira
Professor catedrático de Toxicologia Molecular Farmacêutica do Departamento de Ciências Farmacêu ticas e do Medicamento da Faculdade de Farmácia da Universidade de Lisboa; Título de agregado em Farmácia (Toxicologia) pela Universidade de Lisboa; Licenciatura em Ciências Farmacêuticas, mestrado em Controlo da Qualidade e Toxicologia dos Alimentos e doutoramento em Farmácia (Toxicologia) pela Faculdade de Farmácia da Universidade de Lisboa; Títulos de European Registered Toxicologist e de Espe cialista em Genética Humana pelo Colégio de Análises Clínicas e Genética Humana da Ordem dos Far macêuticos; Membro integrado e investigador principal do imed – Research Institute for Medicines da Universidade de Lisboa; Membro efetivo do Conselho Pedagógico e da Comissão de Creditação da Fa culdade de Farmácia da Universidade de Lisboa; Perito da Agência de Avaliação e Acreditação do Ensino Superior (A3ES); Foi coordenador da Secção de Toxicologia da Sociedade Portuguesa de Farmacologia.
Félix Carvalho
Professor catedrático de Toxicologia e responsável pelo Laboratório de Toxicologia da Faculdade de Farmácia da Universidade do Porto; Título de agregado em Ciências Químicas e Físico ‑Químicas pela Universidade do Porto; Licenciatura em Ciências Farmacêuticas e doutoramento em Toxicolo gia pela Faculdade de Farmácia da Universidade do Porto; Títulos de European Registered Toxicologist e de European Certified Pharmacologist; Membro numerário da Academia de Ciências Farmacêuticas de Portugal; Membro integrado e coordenador da linha temática em Saúde Humana e Segurança
Ambiental da Unidade de Ciências Biomoleculares Aplicadas (UCIBIO) e do Instituto para a Saúde e a Bioeconomia (i4HB); Membro da Comissão de Avaliação de Medicamentos do INFARMED; Presidente da Secção Regional Norte da Ordem dos Farmacêuticos; Foi presidente da Sociedade Portuguesa de Farmacologia (2019 2022) e da EUROTOX (2021 2023).
AUTORES
Alexandre Campos
Investigador auxiliar do Centro Interdisciplinar de Investigação Marinha e Ambiental (CIIMAR) da Uni versidade do Porto, na área de especialização de Toxicologia e Contaminação Ambiental; Doutoramento em Biologia pelo Instituto de Tecnologia Química e Biológica da Universidade NOVA de Lisboa; Tem dedicado especial atenção ao estudo das cianobactérias em águas continentais e da toxicologia dos metabolitos produzidos por estes organismos.
Ana Paula Leite
Coordenadora da Unidade de Nutrição do Instituto Português de Oncologia de Coimbra Francisco Gen til, EPE; Assessora superior de Nutrição; Especialista em Nutrição Clínica.
Ana R. Freitas
Professora auxiliar do Instituto Universitário de Ciências da Saúde da Cooperativa de Ensino Superior, Politécnico e Universitário; Investigadora integrada da Unidade de Ciências Biomoleculares Aplicadas (UCIBIO) e do Instituto para a Saúde e a Bioeconomia (i4HB).
Ana Rita Monteiro
Mestrado Integrado em Ciências Farmacêuticas pela Universidade Fernando Pessoa; Mestrado em Toxi cologia Analítica Clínica e Forense pela Faculdade de Farmácia da Universidade do Porto; Estudante de Doutoramento no Programa Doutoral em Ciência e Tecnologia Alimentar e Nutrição da Faculdade de Ciências da Universidade do Porto, Departamento de Química e Bioquímica/Laboratório Associado para a Química Verde – Rede de Química e Tecnologia (LAQV REQUIMTE).
Ana S. Serras
Mestrado em Ciências Farmacêuticas pelo Instituto de Ciências da Saúde Egas Moniz; Doutoranda da Faculdade de Farmácia da Universidade de Lisboa.
Ana Sofia Fernandes
Professora associada da Universidade Lusófona, onde é Diretora do Mestrado Integrado em Ciências Farmacêuticas; Investigadora do CBIOS – Centro de Investigação em Biociências e Tecnologias da Saúde da Universidade Lusófona; Licenciatura em Ciências Farmacêuticas e doutoramento em Farmácia, na es pecialidade de Toxicologia, pela Faculdade de Farmácia da Universidade de Lisboa; European Registered Toxicologist.
Andreia P. Oliveira
Investigadora do Laboratório Associado para a Química Verde (LAQV REQUIMTE); Licenciatura em Ciên cias Farmacêuticas pela Faculdade de Ciências da Saúde da Universidade Fernando Pessoa e doutora mento em Fitoquímica e Farmacognosia pela Faculdade de Farmácia da Universidade do Porto.
António Sebastião Rodrigues
Professor associado com agregação da NOVA Medical School|Faculdade de Ciências Médicas da Univer sidade NOVA de Lisboa.
Bernardo Brito Palma
Professor auxiliar da Universidade Lusófona; Investigador do CBIOS – Centro de Investigação em Bio ciências e Tecnologias da Saúde da Universidade Lusófona; Licenciatura em Bioquímica pela Faculdade de Ciências da Universidade de Lisboa e doutoramento na especialidade de Toxicologia Molecular pela Vrije Universiteit Amsterdam; Formador qualificado para empresas nas áreas da Toxicologia, Microbiolo gia e Segurança e Higiene no Trabalho; Tem experiência no setor agroquímico, como team leader de um Laboratório de Microbiologia, com certificação GLP, e qualificado como diretor de estudo.
Bruno Costa Gomes
Professor auxiliar da Escola de Psicologia e Ciências da Vida da Universidade Lusófona; Professor auxiliar convidado da NOVA Medical School|Faculdade de Ciências Médicas da Universidade NOVA de Lisboa; Investigador do Comprehensive Health Research Centre da NOVA Medical School|Faculdade de Ciências Médicas da Universidade NOVA de Lisboa.
Carla Miranda
Professora auxiliar do Instituto Universitário de Ciências da Saúde da Cooperativa de Ensino Superior, Politécnico e Universitário; Doutoramento em Ciências Veterinárias pelo Instituto de Ciências Biomédicas
Abel Salazar da Universidade do Porto; Investigadora integrada do Laboratório Associado para a Química Verde (LAQV REQUIMTE) da Universidade NOVA de Lisboa e colaboradora da 1H TOXRUN – Unidade de Investigação em Toxicologia & Uma Só Saúde da Unidade de Ciências Biomoleculares Aplicadas (UCIBIO).
Carla Novais
Professora auxiliar da Faculdade de Farmácia da Universidade do Porto; Investigadora da Unidade de Ciências Biomoleculares Aplicadas (UCIBIO) e do Instituto para a Saúde e a Bioeconomia (i4HB).
Carolina Bento
Nutricionista do The Royal Hospital Donnybrook (Dublin, Irlanda); Especialista em Nutrição Clínica pela Ordem dos Nutricionistas (Portugal).
Daniel José Barbosa
Professor auxiliar convidado do Instituto Universitário de Ciências da Saúde da Cooperativa de Ensino Superior, Politécnico e Universitário; Investigador do Laboratório de Toxicologia Translacional da Unida de de Ciências Biomoleculares Aplicadas (UCIBIO) e do Instituto para a Saúde e a Bioeconomia (i4HB).
David Miranda
Enólogo da Sogrape Vinhos, S.A.; Licenciatura em Viticultura e Enologia pela Universidade de Trás‑os ‑Montes e Alto Douro e mestrando em Tecnologia e Ciência Alimentar da Faculdade de Ciências da Universidade do Porto e da Universidade do Minho.
Diana Dias da Silva
Professora adjunta da Escola Superior de Saúde do Instituto Politécnico do Porto; Licenciatura em Ciên cias Farmacêuticas pela Faculdade de Farmácia da Universidade do Porto e doutoramento em Ciências
Forenses pela Faculdade de Medicina da Universidade do Porto; Cocoordenadora do Centro de Investi gação em Saúde e Ambiente (CISA@LAQV REQUIMTE); Investigadora sénior dos Grupos de Toxicologia e Ciências Forenses da Unidade de Ciências Biomoleculares Aplicadas (UCIBIO) e do Instituto para a Saúde e a Bioeconomia (i4HB).
Fernando Remião
Professor associado com agregação da Faculdade de Farmácia da Universidade do Porto, onde é diretor do Mestrado Integrado em Ciências Farmacêuticas, membro da Comissão Científica do Mestrado em To xicologia Analítica, Clínica e Forense e do Mestrado em Ciências Forenses; Investigador sénior do Grupo de Toxicologia da Unidade de Ciências Biomoleculares Aplicadas (UCIBIO) e do Instituto para a Saúde e a Bioeconomia (i4HB); Foi pró ‑reitor da Universidade do Porto entre 2014 e 2018 para a Inovação Peda gógica.
Helena Carmo
Professora auxiliar do Laboratório de Toxicologia do Departamento de Ciências Biológicas da Faculdade de Farmácia da Universidade do Porto; Diretora do Mestrado em Toxicologia Analítica, Clínica e Forense da Faculdade de Farmácia da Universidade do Porto; Licenciatura em Ciências Farmacêuticas e douto ramento em Toxicologia pela Faculdade de Farmácia da Universidade do Porto; Investigadora sénior do Grupo de Toxicologia da Unidade de Ciências Biomoleculares Aplicadas (UCIBIO) e do Instituto para a Saúde e a Bioeconomia (i4HB).
Inês Pádua
Nutricionista; Professora auxiliar do Instituto Universitário de Ciências da Saúde da Cooperativa de Ensi no Superior, Politécnico e Universitário; Investigadora integrada da 1H‑TOXRUN – Unidade de Investiga ção em Toxicologia & Uma Só Saúde.
Joana Barbosa
Professora auxiliar convidada do Instituto Universitário de Ciências da Saúde da Cooperativa de Ensino Superior, Politécnico e Universitário, lecionando nas áreas de Bioquímica, Imunologia, Genética e Ci togenética, Diagnósticos Moleculares, Técnicas Laboratoriais e Toxicologia Clínica e Forense em vários ciclos de estudos; Licenciatura e mestrado em Bioquímica pela Faculdade de Ciências e Instituto de Ciências Biomédicas Abel Salazar (ICBAS) da Universidade do Porto e doutoramento em Biomedicina pela Faculdade de Medicina da Universidade do Porto; Investigadora da 1H‑TOXRUN – Unidade de In vestigação em Toxicologia & Uma Só Saúde e do Laboratório de Toxicologia da Unidade de Ciências Biomoleculares Aplicadas (UCIBIO REQUIMTE); Copy editor da revista Scientific Letters
Joana Gante
Nutricionista do Hospital Pediátrico da Unidade Local de Saúde de Coimbra, EPE.
Joana P. Miranda
Professora associada com agregação do Departamento de Ciências Farmacêuticas e do Medicamento da Faculdade de Farmácia da Universidade de Lisboa; Licenciatura em Biologia Microbiana e Genética pela Faculdade de Ciências da Universidade de Lisboa e doutoramento em Bioquímica pelo Instituto de Tecnologia Química e Biológica da Universidade NOVA de Lisboa; Título de European Registered Toxicologist; Membro integrado do imed – Research Institute for Medicines da Universidade de Lisboa, onde coordena o laboratório Advanced Cell Models for Predictive Toxicology & Cell‑based Therapies.
Joana S. Rodrigues
Mestrado em Engenharia Biomédica pelo Instituto Superior Técnico da Universidade de Lisboa e dou toramento em Farmácia, na especialidade de Toxicologia, pela Faculdade de Farmácia da Universidade de Lisboa.
João Guilherme Costa
Professor auxiliar da Universidade Lusófona; Mestrado Integrado em Ciências Farmacêuticas e especia lização em Controlo da Qualidade e Toxicologia dos Alimentos pela Faculdade de Farmácia da Universi dade de Lisboa e doutoramento em Ciências da Saúde – Farmácia Experimental e Clínica pela Universi dade de Alcalá, Madrid; Investigador do CBIOS – Centro de Investigação em Biociências e Tecnologias da Saúde da Universidade Lusófona.
Jorge Barbosa
Investigador do Grupo Qualidade e Tecnologia Alimentar do Laboratório Associado para a Química Ver de (LAVQ REQUIMTE); Perito da European Food Safety Authority.
José Rueff†
Professor catedrático de Genética da NOVA Medical School|Faculdade de Ciências Médicas da Universi dade NOVA de Lisboa.
Juliana Faria
Professora auxiliar do Departamento de Ciências do Instituto Universitário de Ciências da Saúde da Cooperativa de Ensino Superior, Politécnico e Universitário; Licenciatura em Biologia e mestrado em Biologia pela Faculdade de Ciências da Universidade do Porto e doutoramento em Biomedicina pela Fa culdade de Medicina da Universidade do Porto; Investigadora do Laboratório de Toxicologia da Unidade de Ciências Biomoleculares Aplicadas (UCIBIO REQUIMTE) e da 1H‑TOXRUN – Unidade de Investigação em Toxicologia & Uma Só Saúde.
Maria Eduardo Figueira
Professora associada com agregação em Bromatologia Farmacêutica do Departamento de Ciências Far macêuticas e do Medicamento da Faculdade de Farmácia da Universidade de Lisboa; Investigadora do Laboratory of Systems Integration Pharmacology, Clinical and Regulatory Science do imed – Research Institute for Medicines da Universidade de Lisboa; Leader/PI no subgrupo Functional Foods and Food Supplements; Coordenadora do Mestrado em Qualidade Alimentar e Saúde da Faculdade de Farmácia da Universidade de Lisboa; Membro da Bolsa de Peritos do Grupo de Avaliação de Medicamentos Ve terinários da Direção‑Geral de Alimentação e Veterinária; Membro do Observatório Nacional de Riscos Emergentes da Autoridade de Segurança Alimentar e Económica.
Maria G. Campos
Professora associada com agregação da Faculdade de Farmácia da Universidade de Coimbra; Coorde nadora do Observatório de Interações Planta‑Medicamento da Faculdade de Farmácia da Universidade de Coimbra.
Maria Henriques Ribeiro
Professora associada do Departamento de Ciências Farmacêuticas e do Medicamento da Faculdade de Farmácia da Universidade de Lisboa; Licenciatura em Farmácia e doutoramento em Farmácia (Química
Farmacêutica e Terapêutica – Biotecnologia) pela Faculdade de Farmácia da Universidade de Lisboa; Membro integrado do imed – Research Institute for Medicines da Universidade de Lisboa; Group leader do Pharmaceutical Bioengineering, Biotechnology & Bioproducts do imed – Research Institute for Med icines da Universidade de Lisboa; Membro do Conselho Científico da Faculdade de Farmácia da Univer sidade de Lisboa; Coordenadora dos Segundos Ciclos da Faculdade de Farmácia da Universidade de Lisboa; Membro da Comissão Executiva do Departamento de Ciências Farmacêuticas e do Medicamento da Faculdade de Farmácia da Universidade de Lisboa; Membro da Comissão Cientifica do Doutoramen to em Ciências da Sustentabilidade da Universidade de Lisboa; Membro do Conselho Coordenador do Colégio Food, Farming and Forestry da Universidade de Lisboa; Integrou a World’s Top 2% Scientists List em 2022, 2023 e 2024 (ranking dos cientistas mais citados e mais influentes ao longo de toda a carreira a nível mundial).
Maria João Silva
Investigadora principal do Instituto Nacional de Saúde Doutor Ricardo Jorge, onde realizou provas pú blicas equivalentes ao grau de doutor em Genética Humana, na especialidade de Toxicologia; Especia lista em Genética Humana pela Ordem dos Farmacêuticos; European Registered Toxicologist; Licenciatura em Ciências Farmacêuticas pela Faculdade de Farmácia da Universidade de Lisboa; Investigadora res ponsável do Grupo de Investigação em Toxicologia Genética no Departamento de Genética Humana do Instituto Nacional de Saúde Doutor Ricardo Jorge; Membro integrado e ponto focal do Instituto Na cional de Saúde Doutor Ricardo Jorge no Comprehensive Health Research Centre da NOVA Medical School|Faculdade de Ciências Médicas da Universidade NOVA de Lisboa.
Maria Paula Duarte
Professora auxiliar do Departamento de Química da Faculdade de Ciências e Tecnologia da Universidade NOVA de Lisboa; Licenciatura em Química Aplicada, mestrado em Tecnologia Alimentar e doutoramen to em Ciências do Ambiente pela Faculdade de Ciências e Tecnologia da Universidade NOVA de Lisboa; Investigadora do Centro de Engenharia Mecânica e Sustentabilidade de Recursos (MEtRICs).
Marta Pingarilho
Professora auxiliar da Unidade de Saúde Pública Global do Instituto de Higiene e Medicina Tropical da Universidade NOVA de Lisboa; Lincenciatura em Química Tecnológica pela Faculdade de Ciências da Universidade de Lisboa, mestrado em Biotecnologia (Engenharia Bioquímica) pelo Instituto Superior Técnico da Universidade de Lisboa e doutoramento em Ciências da Vida (especialidade Genética) pela NOVA Medical School|Faculdade de Ciências Médicas da Universidade NOVA de Lisboa; Investigadora do Global Health and Tropical Medicine do Instituto de Higiene e Medicina Tropical da Universidade NOVA de LIsboa.
Matilde Castro
Professora catedrática jubilada da Faculdade de Farmácia da Universidade de Lisboa.
Nelson G. M. Gomes
Professor auxiliar convidado do Instituto Universitário de Ciências da Saúde da Cooperativa de Ensi no Superior, Politécnico e Universitário; Mestrado Integrado em Ciências Farmacêuticas pela Faculdade de Farmácia da Universidade de Coimbra e doutoramento em Ciências Biomédicas pelo Instituto de Ciências Biomédicas Abel Salazar (ICBAS) da Universidade do Porto; Investigador auxiliar do Laboratório
Associado para a Química Verde (LAQV REQUIMTE); Professor visitante da Universidade de Kasetsart (Tailândia); Vice ‑presidente da Assembleia‑Geral da Associação Portuguesa de Ciências Forenses; Mem bro do Observatório de Interações Planta‑Medicamento da Faculdade de Farmácia da Universidade de Coimbra; Associado da Sociedade Portuguesa de Fitoquímica e Fitoterapia.
Patrícia Antunes
Professora associada da Faculdade de Ciências da Nutrição e Alimentação da Universidade do Porto; Investigadora da Unidade de Ciências Biomoleculares Aplicadas (UCIBIO) e do Instituto para a Saúde e a Bioeconomia (i4HB).
Pedro Queiroz
Diretor Geral da Federação das Indústrias Portuguesas Agroalimentares; Professor convidado da Facul dade de Medicina da Universidade de Lisboa e da Faculdade de Farmácia da Universidade de Lisboa; Licenciatura em Engenharia Biotecnológica pela Universidade Lusófona e mestrado em Biotecnologia (Engenharia Bioquímica) pelo Instituto Superior Técnico.
Pedro Reis Costa
Investigador principal do Instituto Português do Mar e da Atmosfera; Doutoramento em Biologia e Eco logia pela Universidade de Lisboa; Tem centrado a sua investigação na compreensão da transferência de biotoxinas na cadeia trófica marinha e os seus impactos para o ambiente e a produção de bivalves e outros organismos da fileira da pesca.
Renata Silva
Investigadora auxiliar do Laboratório de Toxicologia da Faculdade de Farmácia da Universidade do Por to, do Grupo de Toxicologia da Unidade de Ciências Biomoleculares Aplicadas (UCIBIO) e do Instituto para a Saúde e a Bioeconomia (i4HB); Licenciatura em Ciências Farmacêuticas pela Faculdade de Far mácia da Universidade do Porto, mestrado em Toxicologia pela Universidade de Aveiro e doutoramento em Ciências Farmacêuticas – Especialidade em Toxicologia pela Faculdade de Farmácia da Universidade do Porto.
Rita Manguinhas
Licenciatura em Bioquímica pela Faculdade de Ciências e Tecnologia da Universidade NOVA de Lisboa e mestrado em Ciências Biofarmacêuticas pela Faculdade de Farmácia da Universidade de Lisboa, onde é doutoranda.
Sandra Leal
Professora associada do Instituto Universitário de Ciências da Saúde da Cooperativa de Ensino Superior, Politécnico e Universitário; Investigadora integrada da 1H‑TOXRUN – Unidade de Investigação em Toxi cologia & Uma Só Saúde.
Sérgio P. Camões
Professor auxiliar convidado do Departamento de Ciências Farmacêuticas e do Medicamento; Licencia tura em Biologia e mestrado em Biologia Evolutiva e do Desenvolvimento pela Faculdade de Ciências da Universidade de Lisboa e doutoramento em Farmácia, na especialidade de Toxicologia, pela Faculdade de Farmácia da Universidade de Lisboa; Membro integrado do imed – Research Institute for Medicines da Universidade de Lisboa.
Susana Bandarra
Técnica superior de diagnóstico do Laboratório de Patologia Molecular Synlab Lisboa; Assistente convi dada do Instituto Universitário Egas Moniz.
Susana Margarida Rodrigues
Técnica superior do Laboratório Nacional de Referência de Biotoxinas Marinhas do Instituto Português do Mar e da Atmosfera, desempenhando atividades no âmbito do controlo oficial de biotoxinas mari nhas na costa portuguesa e de investigação na área da toxicologia e segurança alimentar no que diz res peito às biotoxinas marinhas em recursos marinhos; Licenciatura em Engenharia Química pelo Instituto Superior Técnico e mestrado em Controlo de Qualidade e Toxicologia dos Alimentos pela Faculdade de Farmácia da Universidade de Lisboa.
Susana Nunes Silva
Professora auxiliar convidada da NOVA Medical School|Faculdade de Ciências Médicas da Universidade NOVA de Lisboa; Investigadora do Comprehensive Health Research Centre da NOVA Medical School|Fa culdade de Ciências Médicas da Universidade NOVA de Lisboa.
Vanessa Teixeira
Doutoranda em Biologia Molecular e Celular do Instituto de Ciências Biomédicas Abel Salazar (ICBAS) da Universidade do Porto e do i3S – Instituto de Investigação e Inovação em Saúde da Universidade do Porto.
Vera M. Costa
Investigadora da Faculdade de Farmácia da Universidade do Porto; Membro da Comissão Coordena dora e da Comissão Executiva da Unidade de Ciências Biomoleculares Aplicadas (UCIBIO); Professora convidada em várias instituições universitárias, lecionando nas áreas de Toxicologia e Farmacologia; Licenciatura em Ciências Farmacêuticas e doutoramento em Toxicologia pela Faculdade de Farmácia da Universidade do Porto; Membro externo do Conselho Jurisdicional da Secção Regional do Norte da Ordem dos Farmacêuticos.
Vítor Seabra
Professor associado do Instituto Universitário de Ciências da Saúde da Cooperativa de Ensino Superior, Politécnico e Universitário, onde é diretor do Departamento de Ciências Farmacêuticas e coordenador do Mestrado Integrado em Ciências Farmacêuticas e do Doutoramento em Toxicologia; Licenciatura em Ciências Farmacêuticas pela Faculdade de Farmácia da Universidade do Porto e doutoramento em To xicologia pela The School of Pharmacy da Universidade de Londres, Reino Unido, e pela Faculdade de Farmácia da Universidade do Porto; Investigador da unidade 1H TOXRUN – Unidade de Investigação em Toxicologia & Uma Só Saúde; Presidente do Conselho Jurisdicional da Secção Regional do Norte da Ordem dos Farmacêuticos.
PREFÁCIO
A Toxicologia, ciência que estuda os efeitos nocivos produzidos por agentes químicos, físicos e bio lógicos sobre os seres vivos e o ecossistema, tem vindo a expandir se progressivamente nas sociedades industrializadas. Esta expansão tem contribuído para o conhecimento dos mecanismos de toxicidade e das consequências decorrentes da exposição a agentes tóxicos presentes em diversos ambientes, como locais de trabalho, atmosfera, recursos hídricos e alimentos. É precisamente neste último tópico que este livro se centra.
A Toxicologia Alimentar é uma área da Toxicologia cujo início remonta ao final do século xix, aquan do do conhecimento crescente sobre os efeitos tóxicos resultantes do uso de aditivos alimentares sinté ticos. Atualmente, esta área especializada, multidisciplinar e aplicada da Toxicologia moderna dedica se à identificação, à caracterização e à avaliação de potenciais efeitos nocivos decorrentes da exposição a agentes tóxicos presentes nos alimentos, quer de forma natural quer aditivada. De facto, a complexa composição dos alimentos inclui uma variedade de substâncias naturais, algumas das quais exibem propriedades antinutritivas ou tóxicas, bem como xenobióticos, que resultam do processamento e da manipulação a que os alimentos são submetidos e do seu armazenamento.
O papel dos toxicologistas é, portanto, de inegável importância tanto na garantia do controlo e na promoção da segurança dos alimentos consumidos, como na mitigação dos riscos associados à exposi ção a substâncias prejudiciais. Os avanços metodológicos observados atualmente, ao nível instrumental e analítico, são fundamentais para a avaliação do risco e o estabelecimento de limites seguros de exposi ção a agentes tóxicos. Esta obra reveste se, na minha opinião, de um grande interesse para um leque di versificado de leitores. Destaca se pelo seu cuidado, tanto a nível pedagógico como científico, podendo, assim, tornar se numa referência nesta área para estudantes universitários pertencentes a ciclos de es tudos relacionados direta ou indiretamente com a saúde. Além disso, os profissionais de saúde de todas as áreas, investigadores especializados na área do alimento, reguladores, decisores políticos e jornalistas podem encontrar neste livro informação concisa e atualizada, a qual pode ajudar a adquirir ou comple tar conhecimentos, bem como a esclarecer dúvidas e mitos que, por vezes, surgem nesta exigente área da Toxicologia Alimentar. Esta temática assume particular importância para os farmacêuticos, uma vez que a “execução, interpretação e validação de análises toxicológicas, hidrológicas, e bromatológicas” integra, desde há muito, o conteúdo do ato farmacêutico nos Estatutos da Ordem dos Farmacêuticos. Além disso, ao longo da História, diversas tragédias registadas conduziram à necessidade da implemen tação de um exigente conjunto de estudos toxicológicos obrigatórios no desenvolvimento dos medica mentos, implicando um envolvimento direto do farmacêutico também nesta área da Toxicologia.
Este livro, coordenado e redigido por um grupo de autores altamente qualificados e de reconhecida competência, proporciona uma visão holística sobre as diversas dimensões da Toxicologia Alimentar. Ao longo de 24 capítulos, é feita uma introdução à Toxicologia Alimentar e são abordadas sucessivamen te as diversas classes de agentes tóxicos presentes nos alimentos, as diferentes reações de hipersensibili dade aos alimentos, bem como os desafios, as problemáticas e as oportunidades nesta área.
Nesta obra, encontra se em destaque a revisão relativa aos aspetos regulamentares das micotoxinas, incluindo as consideradas emergentes, além da caracterização fenotípica clínico patológica, enquanto procedimento fundamental na monitorização de doenças associadas a alimentos e na consequente im plementação de medidas de controlo das mesmas.
A abordagem “Uma Só Saúde” (One Health) reconhece que as interações entre indivíduos, animais e ambiente, incluindo a degradação dos ecossistemas e as alterações climáticas, condicionam de forma inequívoca a saúde, que deve ser entendida de forma global. Um objetivo específico desta abordagem é a promoção e a conservação da segurança alimentar, através da proteção dos alimentos perante ris cos biológicos (como é o caso de agentes infeciosos), físicos (como a presença de corpos estranhos) e químicos (pela presença de uma grande variedade de compostos, como metais pesados ou pesticidas).
Neste livro, saliento a segurança necessária na produção das embalagens que acondicionam os ali mentos, as problemáticas decorrentes da produção intensiva de animais destinados ao consumo huma no e a presença de resíduos de pesticidas em produtos que servem de alimento a animais na atividade agrícola.
Através de uma extensa e abrangente compilação de informação especializada, a presente obra representa um contributo inestimável para todos os que que pretendem aprofundar os seus conheci mentos, proporcionando uma visão global e integrada da Toxicologia Alimentar e do seu impacto na sociedade.
Helder Mota Filipe Bastonário da Ordem dos Farmacêuticos
Existem ainda as pectenotoxinas e as iessotoxinas, embora estas toxinas não tenham sido associadas a episódios de intoxicação humana.
De modo a prevenir intoxicações agudas devi do ao consumo de marisco contaminado, existem programas de monitorização de biotoxinas com base em legislação específica que rege a produ ção e a colocação no mercado de moluscos bival ves. Estão estabelecidos os limites para a presença dos vários grupos de toxinas na legislação euro peia (Tabela 5.1) e no Codex Alimentarius1, assim como as regras específicas para o controlo oficial das zonas de produção de moluscos bivalves. O programa de monitorização de toxinas mari nhas em bivalves da costa portuguesa teve início em 1986. Deste então, este programa sofreu vá rias alterações, de modo a incluir novas zonas de produção, espécies de bivalves e grupos de toxi nas a monitorizar.
TOXINAS MARINHAS REGULAMENTADAS
Toxinas
hidrofílicas
Toxinas amnésicas
As toxinas amnésicas foram detetadas pela primeira vez em 1987 no Canadá num episódio de intoxicações associado ao consumo de mexi lhão, do qual resultaram 107 pessoas afetadas e pelo menos quatro óbitos. Neste episódio, foi des coberto que o mexilhão estava contaminado com um composto natural, o ácido domoico, produzido por uma diatomácea marinha, a Pseudo -nitzschia multiseries. A sintomatologia observada no episó dio canadiano teve um quadro gastrointestinal e neurológico. Os sintomas gastrointestinais surgi ram 24 horas após o consumo do mexilhão e os sintomas neurológicos observaram‑se em alguns
Tabela 5.1. – Principais síndromes de intoxicação humana por toxinas marinhas e respetivos limites regulamentares estabelecidos na legislação europeia.
Síndrome de intoxicação humana
Microalga produtora
ASP Pseudo-nitzschia spp (diatomáceas)
PSP
DSP
AZP
Associada a iessotoxinas
Gymnodinium catenatum, Alexandrium spp (dinoflagelados)
Dinophysis spp, Prorocentrum spp (dinoflagelados)
Azadinium spinosum (dinoflagelados)
Lingulodinium polyedrum, Protoceratium reticulatum, Gonyaulax spinifera
Ácido domoi co e análo gos
Saxitoxina e análogos
Ácido oca daico e dino fisistoxinas
Azaspiráci dos e análo gos
Iessotoxina e análogos
Mecanismo de ação Sintomatologia Limite regulamentar*
Interação com os recetores do glutamato
Bloqueio da bomba do ca nal de sódio
Inibição das fosfatases pro teicas do tipo PP1 e PP2A
Lesões no citoesqueleto
Ativação das fosfodieste rases
Sintomas neurológicos e gastrointes tinais
Sintomas neu rológicos
Sintomas gas trointestinais
Sintomas gas trointestinais
Nunca repor tada
20 mg de ácido domoico/kg
800 µg de saxi toxina equivalen tes/kg
160 µg de ácido ocadaico equi valentes/kg
160 µg de azas pirácidos equi valentes/kg
3,75 mg de iessotoxinas equivalentes/kg
* Adaptado de Regulamento (CE) n.º 853/2004 do Parlamento Europeu e do Conselho, de 29 de abril de 2004, e de Regulamento (UE) n.º 786/2013 da Comissão, de 16 de agosto de 2013.
1 https://www.fao.org/fao‑who‑codexalimentarius.
é desacoplador da fosforilação oxidativa mitocon drial, através de um mecanismo provavelmente relacionado com a substituição competitiva (“mi metismo”) do fosfato inorgânico na formação de adenosina trifosfato (ATP).
Além destes efeitos, diversos outros meca nismos têm sido propostos para a toxicidade e a carcinogenicidade do arsénio. O arsénio e meta bolitos têm a capacidade de produzir produtos reativos e lesões oxidativas no ADN, de causar alterações do estado de metilação do ADN e instabilidade genómica, bem como de alterar os mecanismos de reparação do ADN e de aumentar a proliferação celular.
CÁDMIO
O cádmio (Cd) é um contaminante ambiental do grupo dos metais pesados. Os géneros alimen tícios são a principal fonte de exposição ao cádmio para a população não fumadora. A absorção via alimentar do cádmio é relativamente baixa (3 5%), mas a carga total de cádmio no organismo é cru cial para se determinar a toxicidade. O cádmio é retido no rim e no fígado, apresentando uma semi vida biológica longa, que varia entre 10 30 anos.
O cádmio é um metal de transição do grupo 12 da tabela periódica e, na sua forma elemen tar, é um sólido azulado à temperatura ambiente. O estado de oxidação da quase totalidade de compostos de cádmio é +2. A exposição ao cád mio que resulta em toxicidade ocorre geralmente por via ocupacional ou dietética. O cádmio e os compostos de cádmio são conhecidos por serem cancerígenos em humanos, com base em evidên cias suficientes de carcinogenicidade em estudos clínicos, incluindo estudos epidemiológicos.
O cádmio ocorre naturalmente no meio am biente, sendo mais concentrado na proximidade de algumas minas. A contaminação ocupacio nal foi observada no final da década de 1940 na Suécia, durante a produção de pilhas alcalinas. Mostrou se que muitos dos sintomas observa dos foram similares aos reportados no Japão na chamada “doença de Itai Itai”. No período após a
Primeira Guerra Mundial, nas margens do rio Jint su, na região de FunchuMachi no Japão, plantado res de arroz e pescadores foram vítimas dos des pejos industriais da mina de zinco e chumbo e da respetiva indústria de processamento de chumbo e zinco, localizadas a 50 km nas margens do rio.
A doença, causada pelo cádmio, ficou conhecida na ciência médica como “Itai Itai” (expressão de dor), sendo caracterizada por insuficiência renal e anemia, bem como por fortes dores ósseas, arti culares e musculares, resultantes da perda exces siva de cálcio (consultar a secção “Mecanismos e sinais de toxicidade”, mais à frente, neste capítu lo), numa população que, à partida, tinha níveis baixos de cálcio endógeno. Além disso, os ossos ficam tão frágeis que podem fraturar com muita facilidade.
Fontes de exposição dietética ao cádmio
A maior exposição a cádmio na população não fumadora geralmente ocorre através do con sumo de alimentos cultivados em áreas contami nadas com cádmio, como mencionado. Muitas plantas acumulam cádmio do solo, a partir de fontes naturais ou antropogénicas. Emissões in dustriais, alguns fertilizantes e o uso de água para irrigação contaminada com cádmio levam a uma bioacumulação lenta, embora constante, de cád mio em vegetais ao longo dos anos. Num estudo da EFSA em vários países da Europa, os grupos de alimentos que contribuíram para a grande parte da exposição dietética ao cádmio foram os cereais e os produtos derivados de cereais, os legumes, as nozes e as leguminosas, as raízes ricas em ami do ou batatas e também a carne e os produtos cárneos (EFSA CONTAM, 2009a).
O Joint FAO/WHO Expert Committee on Food Additives (JECFA) estabeleceu uma ingestão men sal tolerável provisória de 25 µg/kg de peso cor poral, enquanto o CONTAM da EFSA indicou uma ingestão semanal tolerável de 2,5 µg/kg de peso corporal para a garantir proteção de todos os con sumidores.
Altos níveis de cádmio foram encontrados em formulações de algas, produtos à base de cacau, crustáceos, miudezas comestíveis, cogumelos, se mentes oleaginosas, algas marinhas e moluscos aquáticos. Concentrações elevadas de cádmio podem também ser encontradas em vegetais de folhas verdes (alface e espinafre, entre outros), raí zes ricas em amido (por exemplo, batatas), cereais e grãos, nozes e leguminosas (nomeadamente, amendoim, soja e sementes de girassol). Grãos de cereais, como arroz e trigo, assim como o ta baco, podem apresentar níveis até 10 150 µg de cádmio/kg. Concentrações significativas de cád mio foram também já encontradas na carne e no peixe. Determinados crustáceos (ostras, etc.) e de terminados órgãos de animais (rim e fígado, entre outros) têm elevados valores de cádmio, pois acu mulam e concentram este metal. O marisco pode acumular níveis de 1 2 mg/kg de peso, enquanto o fígado e os rins de animais podem apresentar níveis >50 µg/kg.
Toxicocinética
Os dados toxicocinéticos mais conhecidos são os obtidos para o cádmio 2+. A biodisponibilida de do cádmio elementar é desconhecida. Sais de cádmio são mal absorvidos por via oral (5 20% da dose administrada). O transportador de me tais divalentes 1 (DMT1, do inglês divalent metal transporter 1) transporta o ferro e o cádmio no intestino. As mulheres em idade fértil têm níveis baixos de ferritina sérica, o que resulta numa taxa de absorção de cádmio por via oral 2 vezes supe rior. A absorção de cádmio pode ser aumentada por deficiências nutricionais de cálcio ou ferro e por dietas pobres em proteínas. A absorção de cádmio após inalação é geralmente maior do que a absorção por via oral, variando de 5 35%, em função do composto, da deposição e do tamanho de partícula.
Depois de ser absorvido, o cádmio liga se à albumina e a outras proteínas de alto peso molecular, como a α2 macroglobulina. No san gue, o cádmio é encontrado principalmente nos
eritrócitos. A metalotioneína também está presen te no plasma sanguíneo e serve como transporta dora do cádmio para os rins. As metalotioneínas provavelmente evoluíram como um mecanismo para regular os níveis de zinco e a sua distribuição dentro das células, embora o cádmio possa substi tuir o zinco nestes casos. O cádmio pode também ligar se a outros péptidos de baixo peso molecular ou aminoácidos ricos em grupos sulfidrilo, como a glutationa e a cisteína, respetivamente.
Cerca de 50 75% do cádmio retido é encon trado no fígado e nos rins (em maior quantidade no primeiro). O cádmio entra em órgãos alvo atra vés de três mecanismos: i) transportadores de zin co e cálcio; ii) absorção de complexos de cádmio com glutationa ou cisteína por transportadores de proteínas; e iii) endocitose de cádmio quando está em complexos proteicos. Depois de ser incor porado no fígado e no rim, o cádmio induz a sín tese de metalotioneína, com a qual se complexa.
A metalotioneína é um péptido endógeno de bai xo peso molecular rico em tiol que é produzido em ambos os órgãos e que se liga com elevada afinidade a metais. O complexo cádmio metalo tioneína é protetor e funciona como um agente quelante natural com uma forte afinidade para o metal. Ainda assim, a metalotioneína desem penha um papel crucial na concentração tubu lar proximal de cádmio. Em detalhe, no fígado, a metalotioneína liga se e sequestra cádmio, sendo este complexo excretado pela bílis e seguidamen te reabsorvido para a corrente sanguínea através da circulação entero hepática. Novamente no sangue, a pequena dimensão do complexo me talotioneína cádmio permite que este complexo seja filtrado através da membrana dos túbulos glo merulares. Em seguida, o complexo é reabsorvido por endocitose nas células tubulares proximais. O cádmio não ligado à metalotioneína não é reab sorvido na mesma proporção. No rim, as vesículas endocíticas fundem se com os lisossomas, onde a metalotioneína é degradada, libertando cádmio livre. A acumulação de cádmio no rim explica, em parte, a razão de este ser o principal órgão alvo
insaturados produzindo hidroperóxidos, sem sub tração de H (fotoxidação do tipo II). No entanto, os hidroperóxidos produzidos por fotoxidação do tipo II são estruturalmente diferentes dos res tantes produtos de auto ‑oxidação, uma vez que neste mecanismo não existe envolvimento de es pécies radicais, sendo, neste caso, a utilização de antioxidantes limitada.
Oxidação enzimática
A oxidação enzimática de lípidos é um pro cesso mediado pelas lipoxigenases e por algumas isoformas do citocromo P450. Os hidroperóxidos (LOOH) formados pelo processo de oxidação enzi mática são intermediários no processo de síntese de prostaglandinas (PG) e eicosanoides. No en tanto, estes mecanismos enzimáticos também catalisam a oxidação de lípidos nos alimentos, contribuindo para o seu aumento. A oxidação en zimática é uma reação regioespecífica e esteroes pecífica, pelo que a geração de isómeros é menor, se comparada com a oxidação não enzimática. Os ácidos gordos insaturados presentes nos alimentos podem ser oxidados enzimaticamen te por ação das lipoxigenases, dando origem a hidroperóxidos (LOOH), ou pelo citocromo P450, originando metabolitos epóxidos, hidroxilos e hidroperóxidos. Adicionalmente, os triglicéridos presentes podem ser hidrolisados pela enzima lipase e convertidos em glicerol e ácidos gordos livres, que poderão posteriormente sofrer catálise pela lipoxigenase e pelo citocromo P450 (Figura 11.1).
Oxidação do colesterol
O colesterol contém uma ligação dupla entre o carbono 5 (C5) e o carbono 6 (C6). Como acontece com os ácidos gordos, esta ligação dupla é susce tível ao ataque por radicais e pode sofrer reações de decomposição, produzindo álcoois, cetonas e epóxidos. A via de oxidação do colesterol começa com a formação de um hidroperóxido no carbo no 7 (C7). Este hidroperóxido pode decompor‑se num radical alcoxilo, que, por sua vez, pode sofrer rearranjos em 5,6 epóxidos, 7‑hidroxilcolesterol e 7‑cetocolesterol. Os produtos de oxidação do co lesterol encontram‑se principalmente em alimen tos de origem animal submetidos a processamen to térmico, como carnes cozidas, sebo, banha, manteiga e ovos.
PRODUTOS SECUNDÁRIOS
DA DEGRADAÇÃO LIPÍDICA
Como anteriormente descrito, a degradação oxidativa dos lípidos dos alimentos origina uma grande diversidade de produtos. O trato gastro intestinal está, assim, constantemente exposto a compostos originados pela oxidação lipídica dos alimentos. Os hidroperóxidos lipídicos são os principais produtos primários destas reações. Embora sejam muito tóxicos quando adminis trados por via intravenosa, a administração oral destas substâncias é consideravelmente menos tóxica, o que se deve à sua fraca absorção e à ocor rência de processos de destoxificação. Não sendo facilmente absorvidos, os efeitos deletérios dos Triglicéridos
Figura 11.1. – Mecanismos de oxidação enzimática de lípidos.
assim, um prolongamento da sua validade. É im portante salientar que tais características terão obrigatoriamente de estar adaptadas aos reque rimentos específicos de cada produto alimentar (por exemplo, embalagens para frutas ou vegetais têm necessidades de embalamento distintas das embalagens para alimentos processados).
Contenção dos alimentos
Uma outra função importante das embala gens consiste em terem a capacidade de conter o alimento a que se destinam, sendo que um ali mento líquido requer embalagens com caracte rísticas distintas das embalagens utilizadas para alimentos sólidos. Assim, diferentes alimentos possuem necessidades de embalagens específi cas, o que possibilita que sejam comercializados de forma segura e eficaz.
Comunicação
Como resultado da crescente competitivida de nos diferentes setores da sociedade, nomea damente na indústria alimentar, um mesmo tipo de produto pode ser comercializado por marcas distintas. Neste sentido, a embalagem desempe nha um papel central na capacidade de captar a atenção do consumidor para uma determinada marca, em detrimento de outras. Do ponto de vista do consumidor, algumas características das embalagens têm grande impacto no momento da escolha de um determinado alimento. A este nível, diversas estratégias de marketing têm sido adotadas, as quais passam por uma melhoria constante dos aspetos estéticos das embalagens, do ponto de vista da forma, do tamanho, da cor e da sua funcionalidade. Todos estes esforços per mitem uma diferenciação alimentar competitiva entre diferentes fornecedores, influenciando a de cisão de compra de um produto em detrimento de outro.
Além da função comercial, existe a vertente in formativa de uma embalagem alimentar, que tem como objetivo informar o consumidor acerca do produto que acondiciona, incluindo a informação
nutricional, a forma como o alimento deve ser utilizado, o prazo de validade e as regras de con servação e de armazenamento. É importante re ferir que as informações que devem constar das embalagens destinadas a acondicionar produtos alimentares se encontram perfeitamente regula mentadas [Regulamento (UE) n.º 1169/2011, do Parlamento Europeu e do Conselho, de 25 de ou tubro de 2011].
Conveniência
As constantes alterações nos estilos de vida da sociedade imprimem uma persistente adapta ção das suas necessidades. Assim, à semelhança do que acontece noutras vertentes comerciais, também a indústria alimentar tem vindo a adap tar os seus produtos para facilitar a utilização dos alimentos por parte dos consumidores. A este ní vel, regista se, por exemplo, o aparecimento de alimentos pré confecionados facilmente cozinha dos no micro ondas, permitindo reduzir o tempo e o esforço despendidos pelo consumidor na pre paração de uma refeição. No entanto, isto requer o desenvolvimento de embalagens adequadas para tais fins.
Adicionalmente, o tamanho da embalagem desempenha um papel importante no momento de escolha por parte dos consumidores. Assim, a embalagem deverá conter uma quantidade de alimento passível de ser consumido antes de se deteriorar, evitando, desta forma, a perda de re cursos por parte do consumidor. Aliada à comuni cação, a função de conveniência das embalagens para uso alimentar é das vertentes mais trabalha das no âmbito do marketing alimentar.
MATERIAIS UTILIZADOS
EM EMBALAGENS PARA PRODUTOS ALIMENTARES
A gama de materiais usados no processo de embalamento é vasta e adequa se ao tipo de produto alimentar. A escolha de um determinado material em detrimento de outro segue um con junto de requerimentos, incluindo a facilidade
de transporte, as características ideais para o acondicionamento, a proteção e a conservação de determinado alimento, passando também por questões relacionadas com a conveniência do consumidor.
Entre os materiais mais frequentemente uti lizados para acondicionamento alimentar, estão o vidro, o metal, o papel/cartão e o plástico.
Vidro
O vidro é considerado um dos materiais mais antigos, resistentes e duráveis utilizados no em balamento de bens alimentares. Feito a partir de areia de sílica, óxido de cálcio e óxido de sódio, o vidro torna se num material estável e inerte, que permite um contacto direto e seguro com os alimentos. Além disso, as embalagens de vidro são totalmente reutilizáveis e recicláveis. Apesar de todas estas vantagens, o vidro tem vindo a ser evitado, ou preterido por outros materiais, na pro dução de embalagens, devido à sua fragilidade, peso e custo.
Metal
Leve, maleável e resistente, o metal é am plamente utilizado na produção de embalagens alimentares. Adicionalmente, a sua elevada con dutibilidade térmica, resistência à oxidação e opa cidade tornam o metal num excelente material para a proteção de bens alimentares.
Existem diversos metais que podem ser usa dos no fabrico de embalagens, sendo o aço e o alumínio os mais frequentes. Mais precisamente, a folha de flandres, constituída por aço revestido de estanho, é a liga metálica mais comummente presente em embalagens metálicas. O risco de corrosão e de lesão física, bem como a impossibi lidade de visualização do alimento, representam importantes inconvenientes deste tipo de emba lagens.
Papel/Cartão
A criação do papel como hoje é conhecido terá tido origem na China, por volta do ano 105.
O papel é um material heterogéneo, tendo em conta a variedade de comprimentos, a distri buição anisotrópica e a origem das suas fibras. É formado por fibras de celulose, normalmente derivadas da madeira do pinheiro ou do eucalip to. Estruturalmente, a celulose é um polímero de cadeia linear composto por múltiplas moléculas de glicose unidas por ligações β 1,4 glicosídicas. Adicionalmente, entre os grupos hidroxilo livres das macromoléculas de glicose, são estabelecidas ligações de hidrogénio que conferem um carácter hidrófilo à celulose.
Na criação de embalagens, utilizam se dife rentes gramagens de papel e tratamentos, de modo a melhor adaptar a embalagem ao seu conteúdo. Com uma elevada versatilidade e capa cidade de processamento, o kraft é o tipo de pa pel mais utilizado no fabrico de embalagens para acondicionamento de alimentos, podendo ser combinado com outros materiais ou ser subme tido a tratamentos químicos que conferem maior resistência e impermeabilização. A baixa resistên cia à humidade e a fragilidade são desvantagens relevantes das embalagens de papel/cartão.
Plástico
Atualmente, o plástico representa o principal material utilizado em embalagens para alimentos. Além de ser um material versátil e barato, o plásti co tem uma excelente capacidade de isolamento térmico, é facilmente moldável e altamente resis tente, inclusive à corrosão. Os plásticos são gera dos a partir de um processo químico denominado polimerização, no qual cadeias moleculares mais pequenas (monómeros) se unem e dão origem a cadeias maiores (polímeros). De modo a melhorar as propriedades do plástico, vários aditivos po dem ser acrescentados à sua composição, como fibras de reforço, estabilizadores e antioxidantes.
A principal matéria prima para a obtenção de plástico é o petróleo, mais especificamente um dos seus constituintes denominado nafta, a par tir do qual se extrai o mais comum dos monóme ros constituintes do plástico, o eteno (também
Tabela 15.1. – Classificação dos pesticidas segundo a sua composição química.
Classe
Organoclorados
Organofosforados
Carbamatos
Piretroides
Estrutura química/Características Exemplos
• Compostos apolares, lipofílicos, que incluem átomos de car bono, hidrogénio e cloro
• Elevada toxicidade e persistência no ambiente
• Tendência para se acumularem no tecido adiposo dos animais e para sofrerem biomagnificação ao longo da cadeia alimen tar
• Compostos alifáticos, cíclicos e heterocíclicos que possuem um átomo central de fósforo na sua molécula
• Solubilidade em água e em solventes orgânicos, com menor persistência no ambiente do que os organoclorados
• Afetação do SNC
• Estrutura química baseada no alcaloide da planta Physostig ma venenosum
• Baixa persistência no ambiente
• Afetação do SNC
• Compostos análogos às piretrinas obtidos das plantas Chry santhemum cinerariaefolium e Chrysanthemum coccineum
• Menor persistência ambiental, quando comparados aos ou tros pesticidas
• Afetação do SNC
SNC – sistema nervoso central.
aos organoclorados, são considerados pesticidas biodegradáveis.
Com estrutura similar aos organofosforados, os pesticidas do grupo dos carbamatos são com postos orgânicos derivados do ácido carbâmico, diferindo, assim, na sua origem. A toxicidade dos carbamatos está intimamente dependente da sua estrutura molecular, sendo que os compostos apresentam, na sua generalidade, um curto tem po de semivida e baixa persistência ambiental, quando comparados aos organoclorados e aos organofosforados.
Os pesticidas da classe dos piretroides são compostos orgânicos sintéticos derivados do composto natural piretrina, obtido das plantas do género Chrysanthemum. Estes pesticidas apresen tam maior estabilidade e eficácia, uma vez que as piretrinas são facilmente degradadas por serem instáveis no ar e fotossensíveis. Os piretroides de monstram baixa solubilidade em água e reduzida probabilidade de bioacumulação.
DDT, lindano, aldri na, clordano
Malatião, para tião, clorpirifos, diazinão, glifosato
Carbaril, amino carbe, tiodicarbe, carbofurano
Cipermetrina, cialotrina, delta metrina
Via de exposição
Em função da via de entrada na espécie ‑alvo, os pesticidas podem ser divididos em sistémicos, de contacto, por envenenamento gástrico, fumi gantes e repelentes (Tabela 15.2). Os pesticidas sistémicos são pesticidas absorvidos por animais e plantas, atingindo facilmente zonas distantes do ponto de aplicação. Os pesticidas de contac‑ to necessitam de entrar em contacto físico com a praga para serem ativados, provocando a morte do organismo por envenenamento após a pene tração na epiderme. No caso dos pesticidas que atuam por envenenamento gástrico, as pes tes são controladas por envenenamento após a entrada dos pesticidas pelo sistema digestivo da espécie ‑alvo, depois de estes organismos se alimentarem das plantas tratadas. Os pesticidas fumigantes atuam na espécie ‑alvo através da formação de vapor, quando aplicados, entrando no organismo através do seu sistema respiratório. Por fim, os pesticidas repelentes, ao contrário
dos anteriores, não provocam a morte do orga nismo, mas atuam no sentido de repelir as pragas das áreas tratadas.
Espécie - alvo e mecanismo de ação
A classificação dos pesticidas em função da espécie ‑alvo é vulgarmente adotada pela adição do sufixo “cida” ao nome do alvo no qual atuam, refletindo, assim, a sua atividade (Tabela 15.3). Por exemplo, os inseticidas eliminam insetos, os bac tericidas atuam nas bactérias e os herbicidas exer cem a sua ação em ervas denominadas daninhas. As três classes de pesticidas mais conheci das e utilizadas na agricultura são os inseticidas, os fungicidas e os herbicidas (Tabela 15.4). Conhecer o mecanismo de ação dos pestici das torna‑se vantajoso, uma vez que, após uma
exposição ocupacional ou mesmo habitacional, é possível prever os possíveis efeitos tóxicos para a saúde humana, bem como os possíveis meca nismos de resistência por parte das pragas. Os inseticidas atuam principalmente em três grandes alvos do SNC, nomeadamente nos rece tores da acetilcolina, na acetilcolinesterase e nos canais de sódio dependentes da voltagem. Já os fungicidas atuam principalmente nos processos metabólicos e bioquímicos, como a inibição da biossíntese de esteróis e a inibição da oxidação do succinato na mitocôndria, produzindo, assim, efeitos tóxicos. Por último, os herbicidas interfe rem principalmente nas vias metabólicas e hor monais das plantas, na regulação da divisão celu lar e na síntese de aminoácidos.
Tabela 15.2. – Classificação dos pesticidas segundo a via de entrada na espécie ‑alvo.
Classe
Características
Sistémico São absorvidos, por exemplo, pelo sistema vascular da planta e direcionados às zonas não tratadas
De contacto
Por envenenamento gástrico
Fumigante
Repelente
Entram no organismo via epiderme, após o contacto físico com a espécie‑alvo
Atingem a espécie‑alvo após a ingestão das plantas tratadas
Eliminam a praga por produção de vapor, atingindo a espécie‑alvo após a entrada pela via respiratória
Repelem a espécie‑alvo em vez de a eliminar, prote gendo, assim, as zonas tratadas
Exemplos
Ácido 2,4‑diclorofenoxiacético, glifosato
Paraquato, diquato
Malatião
1,3‑dicloropropeno
Antranilato de metilo
Tabela 15.3. – Classificação dos pesticidas segundo a espécie ‑alvo.
Principais classes Espécie-alvo
Inseticida Insetos
Herbicida Ervas daninhas e outras plantas indesejadas
Fungicida Fungos
Bactericida Bactérias
Rodenticida Ratos e outros roedores
Avicida Aves
Nematodicida Parasitas nematoides
Exemplos
Aldicarbe, clorpirifos‑metilo
Isoxabena, glifosato
Miclobutanil, azoxistrobina
8‑hidroxiquinolona
Bromadiolona, varfarina
Avitrol
Oxamil, 1,3‑dicloropropeno
Metodologias avançadas in vitro para avaliação da toxicidade alimentar | 303
grandes expectativas, devido à sua potencial utilização para o desenvolvimento de medica mentos e para estudos toxicológicos. No entanto, os estudos que demonstram a utilização de iPSC, ou mesmo de outras células estaminais, em en saios de toxicidade para produtos alimentares são ainda muito escassos.
MODELOS CELULARES AVANÇADOS
Além do tipo de células usadas nos modelos de cultura in vitro, o microambiente onde estas se en contram reveste ‑se de elevada importância. Tradi cionalmente, in vitro, as células são cultivadas em monocamada ou em cultura bidimensional (2D), constituindo sistemas simples, reprodutíveis e re lativamente pouco dispendiosos. Estes sistemas estão amplamente descritos para estudos celula res numa fase inicial de avaliação e de desenvolvi mento, devido ao facto de permitirem a avaliação de um grande número de substâncias em simultâ neo (por exemplo, high-throughput). No entanto, a reduzida complexidade e a representação limita da da arquitetura celular observada in vivo resul tam num baixo poder preditivo destes modelos e,
Células estaminais humanas
subsequentemente, num potencial limitado para avaliação da toxicidade de xenobióticos, incluin do os veiculados pelo alimento. De facto, in vivo, as células possuem uma morfologia definida e es tão organizadas numa arquitetura tridimensional (3D). Assim, os modelos 3D apresentam‑se como uma alternativa para mimetizar a complexidade tecidular ao serem promovidas interações célula ‑célula e célula‑matriz extracelular, replicando os sinais mecânico ‑estruturais existentes in vivo
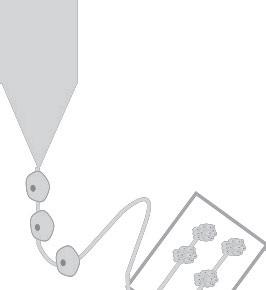
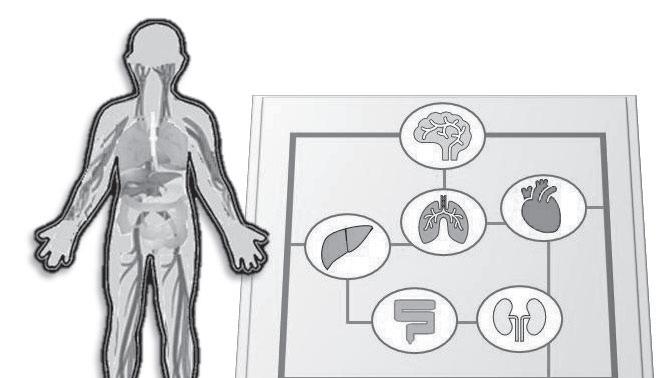
Os sistemas 3D englobam culturas de esferoi des, organoides, bioimpressão e plataformas de microfluídica (Figura 23.1). Estes sistemas variam na sua complexidade e monitorização e permi tem um controlo do fluxo de fluidos e nutrientes, gradientes de compostos e trocas gasosas, po dendo ainda ser adaptados para high-throughput e a uma maior escala de produção. No entanto, o aumento da complexidade também implica um aumento da variabilidade entre lotes, a baixa reprodutibilidade e o baixo throughput. A Tabela 23.1 sumaria os diversos sistemas avançados de cultura 3D no que respeita às suas características e respetivas vantagens e desvantagens.
Esferoides Organoides Bioimpressão 3D Organ-on-a-chip
Complexidade Relevância fisiológica
Figura 23.1. – Os modelos de cultura in vitro avançados permitem uma melhor recapitulação do microambiente encontrado in vivo, constituindo sistemas com maior valor preditivo e alternativas aos testes em animais. Os vários modelos podem ser organizados de acordo com o seu nível de complexidade, que é determinado, entre outros aspetos, pela organização celular em 3D, pela interação entre diferentes tipos de células de um mesmo tecido ou de órgãos diferentes, pela possibilidade de perfusão e pela possibilidade de controlar e de monitorizar parâmetros. Adicionalmente, a utilização de células estaminais humanas constitui um fator determinante para a representação da fisiologia humana, respondendo às limitações da utilização de células primárias ou de linhas celulares.
Sistema de cultura
Esferoides multicelulares
Organoides
Matrizes e hidrogéis
Características
• Com base na capacidade de autoagregação das células em esferoides
• Sistemas de cultura está ticos em superfícies não aderentes, hanging‑drop, estruturas micro/nanopa dronizadas, etc.
• Sistemas de cultura dinâ micos em spinner flasks, biorreatores, etc.
• Estruturas multicelulares auto‑organizadas, especí ficas de um órgão, que se desenvolvem a partir de células estaminais ou pro genitoras
• Estruturas/Matrizes 3D que, através da manipu lação de fatores como a porosidade, a permeabili dade e as características mecânicas, permitem mimetizar um microam biente específico
• Construção de tecidos vivos em 3D pela bioim pressão de células em ma teriais biocompatíveis ou componentes de suporte
Bioimpressão
• Modelos miniaturizados, na ordem dos micróme tros, de um órgão ou tecido humano em plata formas customizadas de microfluídica
Microfluídica (organ‑on‑a ‑chip)
Vantagens
• Simplicidade de manipulação
• Protocolos padronizados
• Arquitetura semelhante ao in vivo
• Interação célula‑célula e célula ‑matriz extracelular
• Permissão de escalabilidade
• Permissão da cocultura de vá rios tipos de células
• Adaptabilidade a HTS e HCS
• Complexidade e arquitetura semelhantes ao in vivo
• Interação célula‑célula e célula ‑matriz extracelular
• Possível inclusão de células específicas do paciente
• Adaptação específica do mate rial para as funções organotípi cas específicas
• Interação célula‑matriz extrace lular
• Permissão da cocultura de vá rios tipos de células
• Adaptabilidade a HTS e HCS
• Elevada precisão e resolução (100 µm)
• Criação customizada de estrutu ras que mimetizam a complexi dade de um tecido
• Permissão da criação de uma rede de vascularização
• Disponibilidade de várias bio tintas
• Perfusão e fluxo dinâmicos con trolados
• Simulação de processos fisioló gicos
• Permissão da criação de gra dientes químicos e vasculariza ção
• Número de células e volume de reagentes reduzidos
• Permissão da representação da interação entre vários tecidos
• Controlo preciso do microam biente
• Permissão da criação de mode los específicos para o âmbito do estudo
Desvantagens
• Microambiente simples
• Ausência de difusão eficiente de nutrien tes e produtos de excreção nos siste mas estáticos
• Pouco controlo sobre o tamanho e a distribuição dos esferoides
• Limitada maturidade das células
• Ausência de vascu latura
• Elevada variabili dade
• Arquitetura simples
• Variabilidade entre lotes (hidrogéis naturais)
• Necessidade de biofuncionalização (hidrogéis sintéticos)
• Custos elevados
• Baixa escalabilidade
• Necessidade de equipamento e pes soal especializado
• Desafio na adapta ção entre materiais e células
• Difícil adaptação a HTS
• Custos elevados
• Baixa escalabili dade
• Reduzida quantida de de amostra para teste
• Necessidade de equipamento e pes soal especializado
Tabela 23.1. – Modelos 3D avançados de cultura in vitro.