Рецензенти
Уредник
уредник
За издавача др Милорад
37.016:54(075.3)
МАРКОВИЋ, Миленија, 1963Хемија : уџбеник за 2. разред гимназије општег типа и природно-математичког смера и средње стручне школе у подручју рада: пољопривреда, производња и прерада хране за образовне профиле: зоотехничар и техничар хортикултуре; текстилство и кожарство, за образовне профиле: текстилни техничар, конфекцијски техничар, техничар моделар коже; здравство и социјална заштита за образовне профиле: санитарно-еколошки техничар, педијатријска сестра-техничар, гинеколошко-акушерска сестра, медицинска сестра-васпитач, зубни техничар; остало - личне услуге / Миленија Марковић, Славица Вељовић ; [илустрације аутори уџбеника, Софија Бунарџић]. - 1. изд. - Београд : Завод за уџбенике, 2021 (Београд : Портал). - 190 стр. : илустр. ; 27 cm
Тираж 2.000. - Напомене уз текст. - Решење тестова: стр. 185-188. - Библиографија: стр. 189.
ISBN 978-86-17-20590-2
1. Вељовић, Славица, 1970- [аутор] [илустратор] COBISS.SR-ID 42684937
оксиди и пероксиди, 4. Метали s, p и d блока Периодног система елемената, 5. Комплекси, 6. Неметали, металоиди и племенити гасови, 7. Индустријски процеси, 8. Неорганске загађујуће супстанце, 9. Прилози и 10. Литература. Ова поглавља одабрана
Земљина кора
Природне или вештачки добијене супстанце, органске или неорганске, изграђене су од 118 хемијских елемента. Од
тих елемената и више од 80 милиона до сада створених различитих хемијских једињења изграђени су природа и предмети које користимо.
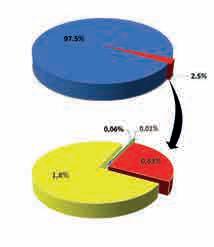
елементи нису равномерно распоређени, нити

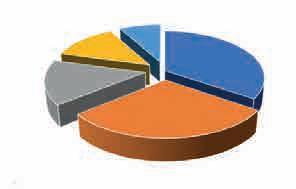
заступљеност елемената у Земљи је следећа: гвожђе 34,6%, кисеоник 29,5%, силицијум 15,2%, магнезијум 12,7% и 8% остали елементи (сл. 2).







0графит

1талк Mg3H2(SiO3)4

2гипс CaSO4∙ 2H2O

3калцит CaCO3

4флуорит CaF2

5апатит Ca5(PO4)3(F, Cl, OH)

6ортоклас K[Al(Si3O8)]

7кварц SiO2

8топаз Al2(SiO4)(F, OH)2


9корунд Al2O3 10

структура, јако чврста и
стена – налазиште:
структура, беле или сиве боје; налазишта: Јелен До (Пожега), Каона
гипс беле боје или без боје, мала тврдоћа; налазишта: околина Крагујевца, долина реке Груже.
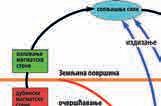
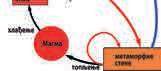
Метаморфне стене настају метаморфозом магматских и седиме-
стена при високом притиску и високој температури (сл. 3).
Метаморфоза се у овом случају односи на трансформацију стене
при високом притиску и температури, када се мењају њена физичка
и хемијска својства.
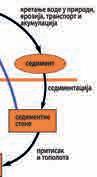
Најраспрострањеније метаморфне
стене су: гнајс, мермер и
(таб. 5). Седиментни
грађевински материјал, цементна, прехрамбена и фармацеутска индустрија
– карбонати (калцит, мермер, магнезит, азурит),
– сулфати (гипс),
– нитрати (чилска шалитра),
– борати (боракс) и
– силикати (кварц, циркон, смарагд, аквамарин).
Самородни елементи у изворном стању су злато, бакар, платина, дијамант, графит и сумпор.
Драгуљи
Драго камење (драгуљи) су веома ретки минерали природног порекла, јонског карактера, осим дијаманта. Високо је цењено због своје лепоте, сјаја, боје и постојаности. Гемологија се бави драгим камењем као интердисциплинарна област.
Драгуљи су део
корунд, Al2O3 рубин, црвен
корунд, Al2O3 сафир, плав Fe2+ Шри Ланка, Бурма, Тајланд, Камбоџа
берил, Be3Al2(Si6O18)смарагд, зелен
берил, Be3Al2(Si6O18)
аквамарин, светлоплав
берил, Be3Al2(Si6O18)хелиодор, жут
циркон, Zr(SiO4)
кварц,SiO2
кварц,SiO2
циркон, разне боје
аметист, љубичаст
опал, разне боје
алуминосиликати, Al2(SiO4)(F,OH)2 топаз, жут
комплексни
алуминијум-фосфати, CuAl6(PO4)4(OH)8 4H2O
тиркиз, светлоплав
Колумбија, Русија, Замбија
Fe2+ Бразил, Русија
Бразил, Русија
Шри Ланка, Аустралија, Камбоџа
Fe3+ Бразил, Русија
Fe3+
Fe3+
Cu2+
Чешка, Аустралија, Бразил, Мексико
Бразил, Русија, Бурма, Мексико
Иран, Кина, Египат
2. Редукција до метала Добијени концентрат припрема се за даљу
за редукцију до метала: MO + CO M + CO2 (M ‒ метал, MO ‒ оксидна руда). У добијању метала као редукционо средство највише се употребљава металуршки кокс (угљеник). Редукционо деловање кокса C појачава се дејством (угљеник(II)-оксида) CO насталог непотпуним сагоревањем
2C(s) + O2(g) 2CO(g)
пржи (загревање
2ZnS + 3O2 2ZnO + 2SO2(g) Карбонатна
ZnCO3 ZnO + CO2(g)
2ZnO + C 2Zn + CO2(g)

1)
2)
3)
језерима од 50 до 100 година (у зависности од дубине језера, од тога да ли је проточно итд.) и у рекама од 2 месеца до 6 месеци. У ужим рекама и потоцима вода се измени за 7–10 дана. Физичка
и врши хидратација јона.
Вода се одликује и одређеном
Важна својства воде, која утичу на
њен квалитет, јесу pH и количина
раствореног кисеоника. Чиста вода
је неутрална и има pH 7, с pH мањим
од 7 је кисела, а с pH већим од 7 је
базна. За живот у води неопходан
је кисеоник. Ако је концентрација
кисеоника у води ниска, водени
организми могу да угину. Удео ки-
сеоника у води смањује се с порастом
температуре воде.
Вода веома слабо апсорбује све-
тлост, због чега је прозирна. Све-
тлост при проласку кроз водену средину, са порастом дубине, мења
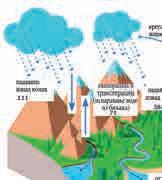

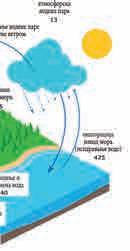
кисеоник, угљен-диоксид, оксиди азота и сумпора. Атмосферска вода садржи и прашину, чађ, микроорганизме, споре и сл. Вода при отицању с површине земљишта или при проласку кроз земљиште раствара супстанце (сл. 6). На тај начин вода хемијски
представити: мека вода – од 0 до 50 mg/l, средње тврда – од 50 до 150 mg/l, тврда – од 150 до 300 mg/l и веома тврда вода > 300 mg/l. Укупну тврдоћу воде чине стална и пролазна тврдоћа воде.
Хлориди, сулфати, нитрати, фосфати, силикати и хумати чине сталну или некарбонатну тврдоћу воде, а карбонати и бикарбонати чине
пролазну или карбонатну тврдоћу. Карбонатна тврдоћа воде се може смањити прокувавањем воде (дестилована вода сл. 7.а). Површинска
вода је мекша од подземне услед мањег контакта с минералима и
појаве падавина. Тврде воде нису погодне за употребу. Отежана је примена сапуна јер граде соли калцијума и магнезијума које су нерастворне. У парним котловима ствара се каменац, што узрокује губитак топлоте, а често и експлозију котла. Из истих разлога знатно се скраћује



Ваздух
Атмосфера
али се претежно састоји од око 78% азота, око 21% кисеоника и око 1% осталих
гасова (CO2, H2O, CH4, O3, H2,Ar, He, Ne, Kr...). Азот, кисеоник и аргон чине 99,96% укупне
запремине ваздуха. У састав ваздуха улазе и гасовите загађујуће супстанце: амонијак, водоник-сулфид, оксиди азота и сумпора. Хемијски састав ваздуха прилично је уједначен до 60 km изнад површине Земље. Људи активно користе атмосферу до висине од 100 km. Као граница атмосфере и свемира често се
ваздухопловна федерација прихватила као границу разграничења Земљине атмосфере
из ваздуха. Изузетно је важан у биосфери за синтезу протеина.
ве-
Кисеоник је гас без боје, мириса и укуса, не гори (потпомаже горење) и није отрован. Највећим делом је биолошког порекла. Потиче из процеса фотосинтезе. Највећи про-
извођачи кисеоника су сувоземне биљке, посебно шуме, затим алге које живе у води и
фитопланктони с водених површина. Апсорбује се у текуће и стајаће воде, па омогућава
опстанак живота у воденим екосистемима.
Озон настаје услед фотодисоцијације молекула кисеоника.
Угљен-диоксид,
из земљишта и под
сунчеве светлости и хлорофила, фотосинтезом, стварају угљене хидрате (глукозу C6H12O6(s)) и
6CO2(g) + 6H2O(l) C6H12O6(s) + 6O2(g) Физичка
ПИТАЊА И ЗАДАЦИ
1. Опишите како
2. Која је разлика у физичким својствима H2O и D2O?
3. Упоредите састав атмосфере
начин.
4. Представите хемијском једначином реакцију
5.
Тест 1.
1.
2.
3.
4.
5. халит
6. кварц (Тачан одговор написати на црти поред
6. Тврдоћа и постојаност минерала може се
(уписати назив скале).
7. Дата су по три примера стена
пишите врсту стене по пореклу.
1. гранит, дијабаз, базалт
2. шљунак, кречњак, гипс
3. гнајс, мермер, кварцит
8. Поред драгог камена напишите број
1. рубин
2. сафир
3. смарагд
4. топаз
5. аметист
6. тиркиз
стена
Понуђени одговори: 1. плав, 2. зелен, 3. жут, 4. црвен, 5. љубичаст и 6. светлоплав.
9. Допуните започету реченицу.
Челик је легура и .
Наведите примену
14. Израчунајте
15.
16. Прикажите
17.
19.
Fe2+
Mg2+
20.
(6, 7, 9, 12...).
Највећи број хемијских елемената су супстанце
која је у течном агрегатном стању, у чврстом су агрегатном
2Na + 2H2O 2NaOH + H2
2K + 2H2O 2KOH + H2 При овим
1.
2.
Cl2 + 2KBr 2KCl +Br2
Cl2 + 2KI 2KCl +I2
Br2 + 2KI 2KBr +I2
једињења калијум-бромида.
2Na + O2 Na2O2
Na2O2 + 2H2O 2NaOH + H2O2
Настали натријум-хидроксид боји
сид.
2Mg + O2 2MgO
MgO + H2O Mg(OH)2
Настали магнезијум-хидроксид такође
P4 + 5O2 P4O10
P4O10 + 6H2O 4H3PO4
S + O2 SO2
2SO2 + O2 2SO3
Настали сумпор(VI)-оксид с
SO3 + H2O H2SO4
Teст 2. Периодична
1.
2. Завршите реакције.
Cl2 + KBr
Cl2 + KI
Br2 + KI
3. Зашто
4.
5.
6.
7.
8.
9.
елемената 1. и од елемената 17. групе, па се најчешће изучава
ве-
енергију јонизације (1.312 кЈ/mol).
Електронегативност му је знатно мања од електронегативности елемената 17. групе (2,1), тако да тешко прима електрон.
Водоник је гас, без боје, мириса и укуса.
молекул. Атоми водоника су
H2(g)
За лабораторијскo
селином, HCl, или са сумпорном
Zn(s) + 2HCl(aq) ZnCl2(aq) + H2(g)
Реакција
(Mg, Fe, Al…) да
M + киселина со + H2
Лабораторијски се може добити реакцијом
Ca + 2H2O Ca(OH)2 + H2
За индустријске сврхе
1) провођењем водене
H2O + C CO + H2
2) електролизом
Распрострањеност
оксид
+ H2
CuO + H2 Cu + H2O Водоник
2H2(g)+ O2(g) 2H2O(g)
+ H2O
H2SO4.
број +1. Стабилност хидрида овог типа, опада у свим групама са порастом редног броја, јер ковалентна веза са
је експлозивна: H2 + F2 2HF флуороводоник
H2 + Cl2 2HCl хлороводоник H2 + Br2 2HBr
H2 + I2
NaH + H2O NaOH + H2
CaH2 + 2H2O Ca(OH)2 + 2H2.
Ови хидриди
Хидрид
Хидриди 16. и 17. групе, осим воде, су кисели хидриди. Вода је амфотеран хидрид. Хидриди
азота и фосфора су базни.
Кисело
NH3 + H2O NH4+ + OH –
HCl + H2O H3O+ + Cl–
H2S + H2O H3O+ + HS
MnO2 као катализатора).
2KClO3 2KCl + 3O2
хлората
2HgO 2Hg + O2
Загревањем калијум-нитрата
2KNO3 2KNO2 + O2
2KMnO4 K2MnO4 + MnO2 + O2
Једињења кисеоника
Кисеоник
Na2O.
Na2O + H2O 2NaOH
Na2O + H2SO4 Na2SO4 + H2O
Амфотерни
Al2O3
Al2O3 (s) + 6HCl(aq) 2AlCl3 + 3H2О(g)
Al2O3 (s) + 2NaOH(aq) + 3H2O 2Na[Al(OH)4] (aq)
Неутрални оксиди се не растварају у
сности од
‒1.
Најважнији је водоник-пероксид H2O2.
Водоник-пероксид је безбојна течност

Слика 3. – Водоник-пероксид Базни
BaO2 + H2SO4 BaSO4 + H2O2
баријум-пероксид,
Na2O2 + 2H2O 2NaOH + H2O2
натријум-пероксид.
кисеоник добија лабораторијски?
3. Шта су пероксиди?
4. Наведите
5.
7.
9.
с водом? (РЕШЕЊЕ: 2,24 dm3)
11.
дроксида? (РЕШЕЊЕ: 7,1 g)
12. Kолико dm3 водоника настаје у реакцији цинка са 100 cm3 раствора хлороводоничне киселине концентрације 0,1 mol/dm3
Својства киселина
Имају кисео укус.
Мењају боју плаве лакмус хартије у црвено. Реагују с неким металима уз издвајање водоника.
Неутралишу базе градећи
Киселине
HCl(aq) + NaOH(aq) NaCl(aq) + H2O(l)
Киселине
без кисеоника.
Бинарне
киселина, HCl(aq). Старо
обично као 36–38% раствор HCl. Има
HCl(g), у води, добија се хлороводонична киселина. HCl(g) HCl(aq)
остатка.
NH3 + H2O NH4+ + OH–
2КОH + H2SO4 K2SO4 + 2H2O, настајање
КОH + H2SO4 KHSO4 + H2O, настајање
калијум-хидрогенсулфат, Ca(OH)2 + HCl CaOHCl + H2O,
калцијум-хидроксихлорид.
NaOH HCl
OH HCl
Киселина Анјони
Натријумова соКалцијумова со HCl
хлороводонична Cl –хлоридни јон
NaCl
натријум-хлорид
CaCl2
калцијум-хлорид HBr
бромоводонична Br –бромидни јон
NaBr
натријум-бромид
CaBr2
калцијум-бромид HI
јодоводонична I –јодидни јон
NaI
натријум-јодид
CaI2
калцијум-јодид H2S
сумпорводонична S2–сулфидни јон
Na2S
натријум-сулфид
CaS
калцијум-сулфид HCN
цијановодонична CN –цијанидни јон
HNO3
азотна NO3 –
нитратни јон
NaCN
натријум-цијанид
NaNO3
натријум–нитрат
Ca(CN)2
калцијум-цијанид
Ca(NO3)2
калцијум-нитрат HNO2
азотаста NO2–
нитритни јон
NaNO2
натријум-нитрит
Ca(NO2)2
калцијум-нитрит H2SO4
сумпорна SO42–сулфатни јон
Na2SO4
натријум-сулфат
CaSO4
калцијум-сулфат H2SO3
сумпораста SO32–сулфитни јон
H3PO4
фосфорна PO43–фосфатни јон
H2CO3
угљена CO32–
карбонатни јон
HClO
хипохлоритна ClO –хипохлоритни јон
HClO2
хлораста ClO2 –
HClO3
хлорна
HClO4
перхлорна
HCOOH
мравља
CH3COOH
сирћетна
хлоритни јон
ClO3 –
хлоратни јон
ClO4 –
перхлоратни јон
HCOO –
формијатни јон
CH3COO –
ацетатни јон
Na2SO3
натријум-сулфит
Na3PO4
натријум-фосфат
Na2CO3
натријум-карбонат
NaClO
натријум-хипохлорит
NaClO2
натријум-хлорит
NaClO3
натријум-хлорат
NaClO4
натријум-перхлорат
HCOONa
CaSO3
калцијум-сулфит
Ca3(PO4)2
калцијум-фосфат
CaCO3
калцијум-карбонат
Ca(ClO)2
калцијум-хипохлорит
Ca(ClO2)2
калцијум-хлорит
Ca(ClO3)2
калцијум-хлорат
Ca(ClO4)2
калцијум-перхлорат
натријум-формијат (HCOO)2Ca
калцијум-формијат
CH3COONa
натријум-ацетат (CH3COO)2Ca
калцијум-ацетат
H2O
H2SO4 H+ + HSO4 – хидрогенсулфатни јон
H2O
HSO4– H+ + SO42– сулфатни јон
H2O
H2SO4 2H+ + SO42– укупна
H2O
NaOH Na+ + OH–
H2O
Ca(OH)2 Ca2+ + 2OH–
Соли При дисоцијацији
H2O
NaCl Na+ + Cl–
H2O
Na2SO4 2Na+ + SO42–
H2O
AlCl3 Al3+ + 3Cl–
H2O
Fe2(SO4)3 2Fe3+ + 3SO42–
Амонијум
као и остале соли.
NH4Cl NH4+ + Cl–
H2O H2O
(NH4)2CO3 2NH4++ CO32–
ПИТАЊА И ЗАДАЦИ
1. Напишите формуле једињења: а) натријум-карбонат, б) амонијум-хидрогенфосфат, в) калцијум-хидроксихлорид.
2. Дефинишите киселине и базе по Аренијусу.
3. Именујте једињења: а) NaCl CaCl2 NaCN Ca(CN)2 NH4Cl CaSO4 , б) HClO4 HNO2 H2SO4 H3PO4 CH3COOH HNO3 .
4. Прикажите једначинама дисоцијацију следећих једињења: а) CaCl2 б)NaCN, б) Ca(CN)2, в) CaSO4, г) (NH4)3PO4.
5. Напишите једначинама реакције
а) калијум-хидроксида и бромоводоничне
б) магнезијум-хидроксида и хлоратне киселине,
в) амонијум-хидроксида и угљене киселине.
6.
а) калијум-хидрогенсулфит, б) баријум-хидроксибромид
Јаки електролити
HCl H+ + Cl–
NaOH Na+ + OH–Koд
HF
Kd = [H+][ F–]/[
H3PO4 H+ + H2PO4–
Kd = [H+][H2PO4– ]/[ H3PO4] = 7,5 ∙ 10–3
H2PO4– H+ + HPO42–
Kd = [H+][ HPO42– ]/[ H2PO4–] = 6,2 ∙ 10–8
HPO42– H+ + PO43–
Kd = [H+][ PO43–]/[ HPO42-] = 3,6 ∙ 10–13
Koнстанте
На пример:
Кd = 1 ∙ 10–9
рКd
слабих електролита, α је степен дисоцијације
ПИТАЊА И ЗАДАЦИ
1. Напишите израз за константу дисоцијације сирћетне киселине.
2. Која једињења не дисосују у воденом раствору: јодоформ, метан, хлороводонична киселина, натријум-хидроксид, мравља киселина.
3. На основу pKb, одредите
a) pKb(HCOO–) = 10,2, б) pKb(NH3) = 4,8, в) pKb(CO32–) = 3,7.
4. Koja киселина је најјача? а) Ка(HNO3) = 4 ∙ 10–4 б) Ка(HF) = 6,6 ∙ 10–4 в) Ка(HClO) = 5 ∙ 10–5.
NaOH NaCl
CH3COO– + H2O CH3COOH + OH–
3. пример. – Раствори соли слабих
Бикарбонатни пуфер (неоргански пуфер)
Фосфатни пуфер (неоргански пуфер)
Амонијачни пуфер (неоргански пуфер)
HCO3–Амонијачни
CH3COO– + H3O+ CH3COOH + H2O
Aко се у
NH3 + H3O+ NH4+ + H2O
NH4+ + ОН– NH3 + H2O
испред цинка и према томе, магнезијум је јаче редукционо средство од цинка. Због тога
магнезијум може да истисне цинк из раствора
његове соли, на пример цинк-хлорида.
Супротна реакција није спонтана.
Мg + ZnCl2 MgCl2 + Zn
Zn + CuCl2 ZnCl2 + Cu
Fe + ZnCl2 није могућа реакција,
Cu + 2AgNO3 Cu(NO3)2 + 2Ag
Fe + CuSO4 FeSO4 + Cu
Ag + Cu(NO3)2 није могућа реакција,
Cu + FeSO4 није могућа реакција.
на киселине.
водоника:
M + HA со + H2
Mg + 2HCl MgCl2 + H2
Zn + H2SO4 ZnSO4 + H2
Ag + HCl није могућа реакција,
Fe + H2SO4 FeSO4 + H2
Cu + HCl није могућа реакција.
M + HA сo + гас + вода
Cu + 2H2SO4 сc CuSO4 + SO2 + 2H2O
3Cu + 8HNO3(аq) 3Cu(NO3)2 + 2NO + 4H2O
Cu + 4HNO3сc Cu(NO3)2 + 2NO2 + 2H2O
ПИТАЊА И ЗАДАЦИ
1. Koje од наведених соли подлежу хидролизи? а) Na2S, б) NaNO3, в) CaSO4, г) FeSO4, д) NaCl
2. Шта је хидролиза?
3. Како реагује водени раствор амонијум-нитрата услед хидролизе?
4. Утврдите који од наведених водених раствора реагује базно? а) NaHCO3, б) FeCl3, в) CaOHBr, г) HCOOK
5. Kojoj врсти соли по структури припадају соли из претходног задатка?
6. Kако ће реаговати водени раствор амонијум-сулфата? Одговор илуструјте хемијским једначинама реакција.
7. Завршите могуће једначине реакција.
а) цинк и хлороводонична киселина
б) алуминијум и бакар(II)-сулфат
в) калај и цинк-хлорид
г) алуминијум и гвожђе(II)-оксид
д) натријум и цинк(II)-хлорид
ђ) хлор и калијим-јодид
е) бром и натријум-хлорид
Тест 3.
1.
2.
3.
а) KHCO3 б) AlCl3 в) NaOH г) CH3COONa д) NaCN ђ) KNO2
14. Напишите једначине дисоцијације: а) калцијум-хлорида, б) натријум-сулфата, в) бакар(II)-нитрата.
15. Завршите реакције које су могуће. а) Zn + CuCl2 б) Fe + ZnCl2 в) Cu + AgNO3
2K(s) + 2H2O(l) 2KOH(aq) + H2(g)
исти начин ће реаговати Са и Na, међутим Mg, Al, Zn истискиваће
Mg(s) + 2HCl(aq) MgCl2(aq) + H2(g)
K K+ + e–
Ca Ca2+ + 2e–
Na Na+ + e–
Mg Mg2+ + 2e–
Al Al3+ + 3e–
Zn Zn2+ + 2e–
Fe Fe2+ + 2e–
Sn Sn2+ + 2e–
Pb Pb2+ + 2e–
H2 2H+ + 2e–
Cu Cu2+ + 2e–
Ag Ag+ + e–
Au Au3+ + 3e–
Zn(s)/ZnSO4(aq) || CuSO4(aq) | Cu(s)
кључа (моста). Данас
Корозија метала
Fe(s) Fe2+(aq) + 2e–
O2(g) + 2H2O(l) + 4e– 4OH
2Fe + O2 + 2H2O 2Fe(OH)2
Гвожђе(II)-хидроксид
4Fe(OH)2 + O2 + 2H2O 4Fe(OH)3
Fe(OH)2:
Fe(OH)3
K(–) 2Na+(l) 2Nao(s)
A(+) 2Cl–(l) Cl2o(g)
2NaCl(l) електролиза 2Na(s) + Cl2(g) У
2Ag+(aq) + Cu(s) 2Ag(s) + Cu2+(aq)
Међутим, хидрометалуршким
У
Rb, цезијум, Cs и францијум, Fr.
Физичка својства
У
само један електрон.
Елементарни су сиве боје, осим цезијума, који је
Алкани метали боје пламен карактеристичним бојама: Li –црвено, Na – жуто, K – љубичасто.
Добијање алкалних метала
Алкални метали откривени су релативно
Углавном се
(–) Катода: 2Na+ + 2e– 2Na
(+) Aнода: 2Cl– – 2e– Cl2
2NaCl 2Na + Cl2 Хемијска својства

лама под вакуумом. Истискују
4KO2 + 2CO2
2K2CO3 + 3O2 Калијум
Oксиди
4Li + O2 2Li2O
2Na(s) + O2(g) Na2O2(s) натријум-пероксид. А само у великом вишку метала настаје натријум-оксид:
4Na(s) + O2(g) 2Na2O(s) натријум-оксид.
Остали метали граде супероксиде: KO2, CsO2 i RbO2.
Хидроксиди
Оксиди алкалних метала су
киселинама граде соли.
Na2O(s) + H2О(l) 2NaOH(aq) натријум-хидроксид. Због
LiOH. Пошто растварањем
NaOH(s) Na+(aq) + OH–(aq)
Натријум-хидроксид
влагу – хигроскопна је.
Нагриза кожу, тако да се мора опрезно ру-
ковати овом супстанцом.
Лабораторијски се добија реакцијом метала
или оксида с водом а индустријски електро-
лизом раствора натријум-хлорида.
2NaCl(aq) + H2O(l) 2NaOH(aq) + Cl2(g) + H2(g)
Натријум-хидроксид се чува у добро затвореним посудама јер реагује с угљен-диоксидом и превлачи се слојем
2NaOH + CO2 Na2CO3 + H2O натријум-карбонат.











































хидрогенкарбонат (сода-бикарбона), NaHCO3.
Na2CO3+ H2O + CO2 2NaHCO3
У реакцији натријум-хидроксида са хлором наградиће се натријум-хипохлорит, натријум-хлорид и вода.
2NaOH + Cl2 NaOCl + NaCl + H2O
ФормулаНазив соли
Уобичајена имена
NaCl натријум-хлорид кухињска со
Na2CO3 натријум-карбонат сода
NaHCO3 натријум-хидрогенкарбонат сода бикарбона
NaNO3 натријум-нитрат
KNO3 калијум-нитрат
Na2CO3∙10H2O натријум-карбонатдекахидрат
чилска шалитра
шалитра
кристална сода
у засићен раствор
+ NH3(g) + H2O(l) + CO2(g)
ПИТАЊА
1. Шта су по хемијском саставу:
2. Напишите формуле и одредите оксидационе бројеве у једињењима: натријум-пероксид, калијум-хидрид, калцијум-хидроксид, натријум-сулфат.
3. Напишите реакције: а) калијума с водом, б) калијум-оксида с водом, в) калијум-хидрида с водом.
4. Представити једначинама хемијских реакција
Na NaH NaOH Na2SO4.
5. Колико
6. Одредите
7.
раствора натријум-хлорида.
Елементи 2. групе – земноалкални метали
Берилијум, Be, магнезијум, Mg, калцијум, Ca, стронцијум, Sr,
Добијање
Земноалкални метали углавном се добијају
MgCl2 Mg2+ + 2Cl–
(–) Катода: Mg2+ + 2e– Mg
(+) Aнода: 2Cl– – 2e– Cl2
MgCl2 Mg + Cl2
Хемијска својства
Земноалкални метали имају ниске
и граде стабилне М2+ јоне.
растопа соли.
Изузетак је берилијум, који гради ковалентна једињења због малог полупречника, већег коефицијента
Њихов оксидациони број је увек +2. Земноалкални метали су мање

Хидриди
Добијају се реакцијом метала и водоника на
Ca(s) + H2(g) CaH2(s), калцијум-хидрид.
Хидриди земноалкалних метала су
базу.
CaH2 (s) + 2H2О(l) Ca(OH)2(s) + 2H2(g)
Oксиди
Сви земноалкални метали граде
који гради пероксид BaO2:
2Ca(s) + O2(g) 2CaO(s) калцијум-оксид.
Калцијум-оксид (негашени креч)
вештачко ђубриво.
Хидроксиди земноалкалних метала
теран). У реакцији с водом
CaO(s)+ H2О(l) Ca(OH)2(aq), ΔН < 0 калцијум-хидроксид.
Све базе друге
Ca(OH)2(s) + CO2(g) CaCO3(s) + H2O
Калцијум-хлорид, CaCl2, је хигроскопна
(BaCl2) се
(CaCO3) се
CaCO3 + H2O + CO2 Ca(HCO3)2
температури:
1.
2. Напишите
3. Напишите формуле: калцијум-хидрида, баријум-сулфата
4. Напишите једначине хемијских реакција: а) Мg+HCl, б) Ca+H2O.
5. Колико се топлоте ослобађа при сагоревању 2 g калцијума?
ΔfH°(CaO) = –636 kJ/mol (РЕШЕЊЕ: 63,6 kJ)
Метали p блока
Бор, B, алуминијум, Al, галијум, Ga, индијум, In, и талијум, Tl, налазе се у 13. групи
реакција с водом.
2Alamalgam(s) + 6H2O 2Al(OH)3(s) + 3H2(g)
Алуминијум је амфотеран, посебан је
2Al(s) + 6HCl(aq) 2AlCl3 + 3H2(g)
2Al(s) + 2NaOH(aq) + 6H2O 2Na[Al(OH)4](aq) + 3H2(g)
Примена


алуминијума је амфотеран.
Al2O3 (s) + 6HCl(aq) 2AlCl3(aq) + 3H2O(l)
Al2O3 (s) + 2NaOH(aq) + 3H2O(l) 2Na[Al(OH)4](aq)
електролитичко добијање алуминијума. Због велике отпорности,
Алуминијум-хидроксид, Al(OH)3, такође je амфотеран.
са
температура
2Al(OH)3 Al2O3 + 3H2O
Соли
ПИТАЊА И ЗАДАЦИ
1. Шта значи појам алуминотермија?
2. Која је примена алуминијума?
3. Прикажите једначинама: Аl2O3 AlCl3 Al(OH)3.
4. Приказати једначину дисоцијације калијум-алуминијумове стипсе.
5. Зашто се алуминијум, који је нерастворљив у води, раствара у воденом раствору натријум-карбоната?
6. Израчунајте колико се топлоте
Калај, Sn

2PbS + 3O2 2PbO + 2SO2
2PbO + C 2Pb + CO2
Олово је

3Pb(s) + 8HNO3(aq) 3Pb(NO3)2(aq) + 2NO(g) + 4H2O, олово(II)-нитрат (раствара се у води).
Под дејством разблажене сумпорне
нерастворни олово(II)-сулфат, који га штити од даљег реаговања.
Базе не реагују са оловом.
Једињења олова
Оксиди олова: олово(II)-оксид, PbO, и олово(IV)-оксид, PbO2, јесу амфотерни оксиди. Реагују са и у киселинама и базама:
PbO(s) + 2HCl(aq) PbCl2(aq) + H2O
PbO (s) + NaOH(aq) + H2O Na[Pb(OH)3](aq), натријум-трихидроксоплумбат(II).
PbO се користи као глазура за керамичке производе.
Oлово(II,IV)-оксид, Pb3O4 (минијум), кристални је
1.
2.
3.
6.

2C + O2 2CO,
Fe2O3 + 3CO 2Fe + 3CO2.
цијум, манган,
Гвожђе се раствара у разблаженим неоксидујућим киселинама (концентрована сумпорна и азотна киселина га пасивизирају).
Fe + 2HCl FeCl2 + H2
FeO
Fe2O3
FeCl3
гвожђе(II)-оксид, феро-оксид
гвожђе(III)-оксид, фери-оксид
гвожђе(III)-хлорид
FeSO4 ∙ 7H2Oзелена галица
Табела 11. – Најважнија једињења гвожђа
ПИТАЊА И ЗАДАЦИ
1. Напишите електронску конфигурацију јона Fe3+.
2. Наведите биолошка једињења у чији састав улази гвожђе.
3. Напишите једначине реакција
Fe2O3 Fe2(SO4)3 Fe(OH)3
Cr
је хромит, FeO ∙ Cr2O3 Хром се добија
Cr2O3 + 2Al 2Cr + Al2O3
Хром је биогени елеменат.
Најважнија једињења хрома су с оксидационим бројевима хрома +3 и +6.
Хром(III)-оксид, Cr2O3, је амфотеран оксид, који се раствара у киселинама и базама, а не раствара се у води.
Cr2O3 + 6HCl 2CrCl3 + 3H2O
Cr2O3 + 2NaOH 2NaCrO2 + H2O, натријум-хромит.
Хром(VI)-оксид, CrO3, је кисео оксид. У реакцији с водом гради хромну киселину, H2CrO4 (1) и дихромну киселину, H2Cr2O7 (2).
(1) CrO3 + H2O H2CrO4
(2) 2CrO3 + H2O H2Cr2O7
Хромна киселина
Хромна киселина и њене соли (хромати) су
2CrO42- + 2H+ Cr2O72- + H2O
жут наранџаст У киселој средини преовлађује дихромат а у
у раствор наранџастог дихромата сипамо хидроксид, раствор поново постаје жут.
Од растворних соли хрома, технички је најважнији натријум-дихромат, Na2Cr2O7. Калијум-дихромат, К2Cr2O7, с
(NH4)2Cr2O7 Cr2O3 + N2 + 4H2O, (NH4)2Cr2O7, експлозиван, отрован, штетан
Maнган, Mn Један

Слика 8. – Раствор калијум-перманганата, КMnO4 Т°
Oглед
У епрувету сипати 2–3 ml раствора КMnO4, неколико капи раствора H2SO4, и полако додати раствор FeSO4. Тада КMnO4 изгуби боју и догађа се реакција.
2KMnO4 + 8H2SO4 + 10FeSO4 2MnSO4 + K2SO4 + 5Fe2(SO4)3 + 8H2O
Потребне хемикалије: водени раствор калијум-перманганата, водени раствор гвожђе(II)-сулфата и разблажена сумпорна киселина (1 : 10) У неутралној средини манган из калијум-перманганата се редукује до оксидационог стања +4.
МnO4– + 2H2O + 3e– MnО2+ 4OH–У базној средини се редукује до оксидационог стања +6:
МnO4– + e– MnО42–. Kалијум-перманганат се користи
2KMnO4 K2MnO4 + MnO2 + O2
2KMnO4 + 16HCl 2KCl + 2MnCl2 + 5Cl2 + 8H2O
базан оксид и нерастворан
у води
MnO + 2HCl MnCl2 + H2O
aмфотеран оксид MnO2 + 4HCl MnCl2 + Cl2 + 2H2O MnO2 + 2KOH K2MnO3 + H2O,
кисео оксид Mn2O7 + H2O 2HMnO4
HMnO4 перманганова киселина MnO манган(II)-оксид
KMnO4 калијум-перманганат
К2MnO4 калијум-манганат
Табела 12. – Оксиди мангана Табела 13. –
MnO2 манган(IV)-оксид
К2MnO3 калијум-манганит Mn2O7 манган(VII)-оксид
ПИТАЊА И ЗАДАЦИ
1. Зашто атом хрома има један електрон у
2. Зашто се метали хромирају?
3. Одредите оксидационе бројеве мангана у
а) H2MnO3, б)MnO, в)Na2MnO4, г)MnO4–.
4. Напишите електронску конфигурацију Mn2+ јона.
5. Из ког оксида настаје хромна, односно дихромна
дначине реакције.
6.
7.
8.
Бакар, Cu
Бакар
кције с кисеоником, угљен-диоксидом
технички метал.
Бакар спада у биогене елементе – има
у
(утиче на синтезу хемоглобина), јетри, мишићима, костима.
Најважније руде су халкопирит, CuFeS2, халкозин, Cu2S, и ковелин, CuS. Бакар се добија из рудa пирометалуршким поступком.
2Cu2S +3O2 2Cu2O + 2SO2, 2Cu2O +Cu2S 6Cu + SO2
и хидрометалуршки:
CuSO4 + Fe Cu + FeSO4
Cu + 2H2SO4сc. CuSO4 + SO2 + 2H2O
3Cu + 8HNO3(aq) 3Cu(NO3)2 + 2NO + 2H2O
Cu + 4HNO3сc Cu(NO3)2 + 2NO2 + 2H2O
Једињења бакра
Бакар (II)-оксид, CuO То је базни оксид који се не раствара у води, али с киселинама гради соли:
CuO + 2HCl CuCl2 + H2O, бакар(II)-хлорид.
Дејством јаких база на соли бакра, добија се бакар(II)-хидроксид.
CuCl2 + 2NaOH Cu(OH)2 + 2NaCl
Хидроксид бакра је базан, раствара се у киселинама, а не раствара се у базама, осим у
нијаку, с којим гради комплексно једињење: Cu(OH)2 + 4NH3 [Cu(NH3)4](OH)2 aq, тетрааминбакар(II)-хидроксид.
Његов раствор користи се за растварање целулозе.
Најважнија со бакра је бакар(II)-сулфат, CuSO4, супстанца
CuSO4
5H2O
Сребро, Ag Најважнија
4Ag + O2 + 2H2S 2Ag2S + 2H2O
2Ag + 2H2SO4сc Ag2SO4 + SO2 + 2H2O
3Ag + 4HNO3(aq) 3AgNO3 + NO + 2H2O
Ag + 2HNO3сc AgNO3 + NO2 + H2O
Једињења сребра
Технички су најважнији халогениди сребра. У води се раствара само сребро(I)-флуорид, АgF.
Сребро(I)-хлорид, AgCl, се лако раствара у амонијаку, у цијанидима и у тиосулфатима
градећи комплексно једињење:
AgCl + 2NH3 [Ag(NH3)2]Cl, диаминсребро(I)-хлорид,
AgCl + 2CN– [Ag(CN)2]– + Cl–, дицијанидоаргентат(I),
AgCl + 2S2O32– [Ag(S2O3)2]3– + Cl–, дитиосулфатоаргентат(I). Сребро(I)-бромид, AgBr, раствара се у цијанидима и тиосулфатима.
AgBr + 2CN– [Ag(CN)2]– + Br–
AgBr + S2O32– [Ag(S2O3)2]3– + Br–
Сребро(I)-јодид, AgI, раствара се само у цијанидима.
AgI + 2CN– [Ag(CN)2]– + I–
Moже се закључити да је сребро-хлорид најрастворљивији, затим сребро-бромид, а најмање растворљив од свих халогенида сребра је сребро-јодид. Ова комплексна једињења сребра користе
+ 4HNO3 3AgNO3 + NO + 2H2O
+ HCl
+ HNO3
Цинк, Zn Цинк
Добар је проводник струје и топлоте.
Главне руде су му сфалерит, ZnS, и смитсонит, ZnCO3
Цинк спада у биогене елементе. Цинк (из ZnSO4) je неопходан људском организму.
Добија се пирометалуршки пржењем руде сфалерита, ZnS, а затим редукцијом његовог
оксида помоћу кокса.
2ZnS + 3O2 2ZnO + 2SO2
ZnO + C Zn + CO
Цинк показује амфотерна својства, раствара
водоника.
Zn + 2HCl ZnCl2 + H2
Цинк реагује и у базама:
Zn + 2NaOH + 2H2O Na2[Zn(OH)4] + H2, натријум-тетрахидроксоцинкат(II).
Цинк
ZnO, је
зубног цемента.
ZnО + 2HCl ZnCl2 + H2О
ZnО + 2NaOH + H2O Na2[Zn(OH)4]
Пошто се цинк-оксид
на соли цинка.
ZnCl2 + 2NaOH Zn(OH)2 + 2NaCl
Цинк-хидроксид је амфотеран.
Раствара се у амонијаку:
Zn(OH)2 + 4NH3 [Zn(NH3)4](OH)2, тетрааминцинк(II)-хидроксид.
1.
2.
3.
4.
5.
6.
Zn + HCl
Zn + NaOH +H2O
Zn + CuSO4
Zn + NaCl
7. Хемијским једначинама прикажите амфотерност оксида цинка.
8.
CuCO3 CuO Cu(OH)2.
9. Колико грама цинка треба додати у 10 грама 2% раствора CuSO4? (РЕШЕЊЕ: 0,08 g)
10. Колико m3 гаса (н. у.) се добија растварањем 10 kg сребра у разблаженој азотној киселини? (РЕШЕЊЕ: 0,0007 m3)
Тест 4. Mетали s, p и d блока Периодног система
1. Шта су по хемијском саставу: кухињска со, жива сода, сода бикарбона?
2. Која од једињења имају само јонски тип везе? а) CaCl2 б) CaCO3 в) CaH2 г) CaO
3. Одредите запремину гаса која се добија у реакцији 5,7 g алуминијума са сумпорном киселином при нормалним условима.
4. Хемијским реакцијама прикажите амфотерност оксида олова.
5. Колико се грама чистог калаја раствара у 0,2 dm3 36% хлороводоничне киселине чија је густина 1,18 g/cm3? Kолико се dm3 гаса приликом тога издваја при нормалним условима?
6. Колика је запремина раствора
грани хемије, координационој хемији.
Због велике разноврсности и бројности комплексних једињења, тешко их је дефинисати. Комплекси постоје у кристалном облику и у раствору. Јони или молекули везани за централне јоне метала називају се лиганди (лат. ligare – везати). Кажемо да су координовани лиганди за централни јон метала (лат. coordinatio – придруживање)
Електронска конфигурација атома Електронска конфигурација јона
25Mn 1s22s22p63s23p64s23d5 Mn2+1s22s22p63s23p64s0 3d5 Mn – 2e – Mn2+
26Fe 1s22s22p63s23p64s23d6 Fe3+1s22s22p63s23p6 4s03d5
29Cu 1s22s22p63s23p64s13d10 Cu+ 1s22s22p63s23p6 4s03d10 Cu – e – Cu+
30Zn1s22s22p63s23p64s23d10 Zn2+ 1s22s22p63s23p6 4s03d10 Zn – 2e – Zn2+
Mn2+ 4s0 3d5
MnO32– (Mn4+) 4s0 3d3
MnO42– (Mn6+) 4s0 3d1
рене електроне у 3d поднивоу. Цинк не гради јоне с већим
1.
трални метални јон,
2. лигандима, који су анјони, даје се наставак -о (хидроксидо OH–, хлоридо Cl–, цијанидо CN–),
3. називи неутралних лиганада се не мењају, осим код изузетака (аква за H2O, амин за NH3, карбонил за CO, нитрозил за NO),
4. број појединих лиганада у комплексу означен је префиксом ди-, три-, тетра-, пента-, хекса-, a за сложеније лиганде, као што је етилен-диамин, употребљавају се префикси бис-, трис-, тетракис-,
5. оксидациони број централног јона означава се римским бројем (и ставља се после имена комплекса) и
6. ако је комплексни јон анјон, додаје му се наставак -ат, а ако је комплексни јон катјон, не добија наставак.
Често се употребљавају и неки уобичајени
за јон
FK (CN) e 4 6
+2+1 –1 , анјонски
][ FK (CN) e 3 6
+3+1 –1 , анјонски
тетрахлоридодиаминплатина (IV)
калијум-хексацијанидоферат(II)
калијум-хексацијанидоферат(III) ] [ C (NH ) o 2 34
+3 Cl –1 Cl –1 0 , (H O) 2 0 катјонски
][ C (NH ) u 234 +2 Cl –1 0 , катјонски
][ C (en) u 42 +2 SO –2 0 , катјонски
хлоридоакватетрааминкобалт(III)-хлорид
тетрааминбакар(II)-хлорид
бис(етилендиамин)бакар(II)- сулфат
Анјонски лиганд добија наставак -о, F – (флуоридо), Cl– (хлоридо), Br – (бромидо), I– (јодидо), O2–(оксо), OH– (хидроксидо), CN– (цијанидо), ONO– (нитрито), S2– (тио), SCN– (тиоцијанато), O22–(пероксо), SO42– (сулфато), S2O32– (тиосулфато), CO32– (карбонато), C2O42– (оксалато). Дати су примери назива за комплексне анјоне (таб. 5).
Формула
Назив
[Fe(CN)6]4- хексацијанидоферат(II)-јон
[Fe(CN)6]3-
[AlF6]3-
хексацијанидоферат(III)-јон
хексафлуоридоалуминат(III)-јон
[Cr(C2O4)3]3- триоксалатохромат(III)-јон
[Ag(S2O3)2]3- дитиосулфатоаргентат(I)-јон
Формула
[Co(NH3)6]3+
[CrCl2(H2O)4]+
[CoCO3(NH3)4]+
[Co(ОNO)(NH3)5]2+
[CoSO4(NH3)5]+
Назив
хексааминкобалт(III)-јон
дихлоридотетрааквахром(III)-јон
карбонатотетрааминокобалт(III)-јон
нитритопентааминкобалт(III)-јон
сулфатопентааминкобалт(III)-јон
Формула Назив и боја
K3[Co(NO2)6]калијум-хексанитрокобалтат(III) (жута)
[Ni(H2O)6]SO4 хексаакваникл(II)-сулфат (зелена)
[Cu(NH3)4]Cl2 тетрааминбакар(II)-хлорид (плава)
К4[Fe(CN)6] калијум-хексацијанидоферат(II) (светлозелена)
[Cu(H2O)6](OH)2 хексааквабакар(II)-хидроксид (плавичаста)
[Cu(H2O)6]Cl2
[Ni(H2O)6](OH)2
K3[Co(NO2)6]
4. Одредите оксидационе бројеве у комплексу ксенон-хексафлуоридоплатинат(V) Xe[PtF6]
5. Који је координациони број у комплексу бис(етилендиамин)бакар(II)-сулфату, молекулске формуле [Cu(en)2]SO4?
а) 2, б) 6, в) 4.
(анјонски тип) или без наелектрисања.
Дисоцијација
тетрааминбакар(II)-хлорида [Cu(NH3)4]Cl2 у води:
[Cu(NH3)4]Cl2 [Cu(NH3)4]2+ + 2Cl– .
Дисоцијација катјонског комплекса хлоридоакватетрааминкобалт(III)-хлорида
[Cо(NH3)4(H2O)Cl]Cl2 у води:
[Cо(NH3)4(H2O)Cl]Cl2 [Cо(NH3)4(H2O)Cl]2+ + 2Cl–
Дисоцијација анјонског комплекса калијум-хексацијанидоферата(III) K3[Fe(CN)6] у води:
K3[Fe(CN)6] 3K+ + [Fe(CN)6]3–.
K3[Co(NO2)6] 3K+ + [Co(NO2)6]3–
K3[Co(NO2)6] у води:
комплексу калијум-хексацијанидоферат(III) K3[Fe(CN)6] успостављене су следеће хемијске везе: – координативна ковалентна
(CN–) и
јони
Комплексне соли
Ag+ са цијанидним јонима CN–, градећи дицијанидоаргентат(I) јон [Ag(CN)2]–.
Ag+ + 2CN– [Ag(CN)2]–
Комплексни катјони
с молекулима, нпр. Cu2+ с молекулима NH3, градећи тетрааминбакар(II)јон [Cu(NH3)4]2+
Cu2+ + 4NH3 [Cu(NH3)4]2+
Наелектрисање комплексних
јона и његових лиганада. [Ag(CN)2]–, +1 + 2(–1) = –1, [Cu(NH3)4]2+, +2 + 4(0) = +2
ни физиолошка својства.

ПИТАЊА И ЗАДАЦИ
1. Напишите називе комплексних једињења:
а) [Ag(NH3)2]Br б) Na2[Zn(OH)4]
2. Представите дисоцијацију комплексних соли у води.
K3[Co(NO2)6]
[Ni(H2O)6]SO4
[Cu(NH3)4]Cl2
К4[Fe(CN)6]
3. Тетрааминбакар(II)-сулфат при дисоцијацији
а) Cu2+, NH4+, SO42–, б) [Cu(NH3)4]2+, SO42–,
в) Cu2+, 4NH3, SO42–
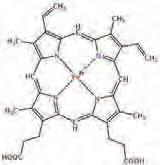
4) Који од наведених елемената улазe у састав хлорофила, хемоглобина и витамина B12?
а) Co, Mn и Fe, б) Cu, Fe и Co, в) Mg, Fe и Co, г) Mn, Cu и Fe
5) Која од наведених соли је комплексна?
а) KAl(SO4)2 . 12H2O, б) [Cu(NH3)4]SO4, в) CuSO4 . 5H2O
Тест 5.
Kомплекси
1. Завршите започету реченицу. Прелазни елементи углавном имају мале јоне великог наелектрисања, неспарене d електроне или непопуњене s, p и d орбитале
2. Прикажите електронску конфигурацију: а) атома гвожђа, 26Fe, б) феро-јона, Fе2+ в) фери-јона, Fе3+.
3.
4.
5. Елементи с малим бројем електрона у 3d поднивоу
6. Напишите називе за: а) неутрални комплекс [PtCl4(NH3)2] , б) анјонски комплекс K4 [Fe(CN)6] , в) катјонски комплекс [Cu(NH3)4]Cl2 .
7. Прикажите дисоцијацију у води следећих комплексних соли: а) неутрални комплекс [PtCl4(NH3)2] , б) анјонски комплекс K4 [Fe(CN)6] , в) катјонски комплекс [Cu(NH3)4]Cl2 .
8. Које комплексне соли су неелектролити? а) катјонска, б) анјонска, в) неутрална
9. У [Ag(NH3)2]Cl постоји: а) само поларна ковалентна веза, б) поларна ковалентна и координативна ковалентна веза, в) само јонска веза, г) јонска, поларнаковалентна и координативна ковалентна веза.
10. У ком од наведених једињења не постоји јонска веза? 1) NH4NO3, 2) [Ag(NH3)2]Cl, 3) [PtCl4(NH3)2]
11. Прикажите
НЕМЕТАЛИ, МЕТАЛОИДИ
Пре него што почнете изучавање ове области, треба да поновите поделу и номенклатуру (називе) неорганских једињења.
Подела
Неорганска једињења могу се груписати
зависе од електронегативности елемената који их изграђују
става и структуре.
Према номенклатури ковалентних једињења
атом мање електронегативности, и његов оксидациони број ако има више
оксидационих стања: H2S (водоник-сулфид), CO (угљеник (II)-оксид), CO2 (угљеник (IV)-оксид). У
увек се
анјона: LiH – литијум-хидрид, Na2O – натријум-оксид, Ca(OH)2 – калцијум-хидроксид, Fe2(SO4)3 – гвожђе(III)-сулфат.
Називи катјона се граде тако што се елементу
наставак: Na+ (натријумов јон), Mg2+ (магнезијумов јон), Cu+ (бакров(I)јон) и Cu2+ (бакров(II)јон). У старијој номенклатури се нижа валенца означавала наставком -о, а виша наставком -и: Cu+ (бакров(I)јон) или купро јон) и Cu2+ (бакров(II)јон или купри јон).
Називи моноатомних анјона добијају се додавањем наставка -ид латинском имену елемента: H- (јон хидрид), Cl– (јон хлорид), O2– (јон оксид), S2– (јон сулфид) и C4– (јон карбид). Мало вишеатомних анјона има наставак –ид: OH– (хидроксид), O22– (пероксид) и CN– (цијанид).
Јонима као што су HS– и HO2– испред назива се дода префикс хидроген (хидрогенсулфид, HS–, хидрогенпероксид, HO2–).
а оној са мање кисеоника наставак -итна киселина.
Назив полиатомских киселина: по централном атому HNO3 азотна киселина, по анјону нитратна киселина; по централном атому HNО2 азотаста киселина, по анјону нитритна
киселина; HClO хипохлорна киселина, по анјону хипохлоритна; HClO2 хлорна киселина, по анјону хлоритна киселина; HClO3 хлорна киселина, по анјону хлоратна киселина; HClO4 перхлорна киселина, по анјону перхлоратна киселина.
Нека неорганска једињења имају тривијалне називе који се односе на име проналазача, или
потичу од њихових својстава, или од начина добијања (нпр. Глауберова со, Na2SO4 .10H2O, масна сода, NaOH, сода, Na2CO3, кречњак, CaCO3, сона киселина, HCl).
Неметали
Представници

2.
3.
Флуор, F
Флуор је најреактивнији халогени елемент. Има способност да с племенитим гасом ксеноном, Xе, награди
групу једињења: XeF2, XeF4 и XeF6. У природи се налази у
облику минерала флуорита, CaF2 (сл. 2).
Експлозивно реагује флуор с водом градећи слабу флу-
оридну киселину HF.
2F2(g) + 2H2O(l) 4HF(g) + O2(g)
Флуор и паре HF су отровне.
Флуоридна киселина HF(aq) реагује са силицијум(IV)-оксидом SiO2(s) градећи силицијум-тетрафлуорид SiF4(g)
SiO2 (s)+ 4HF(aq) SiF4(g) + 2H2O(l)
Како је SiO2 састојак стакла,
пластичним боцама. Флуор се у
CaF2. Сматра се


1) у реакцији хлороводоничне
KMnO4:
2KMnO4(s) + 16HCl(aq) 5Cl2(g) + 2KCl(aq) + 2MnCl2(aq) + 8H2O(l), 2) у реакцији хлороводоничне
(s):
MnO2(s) + 4HCl(aq) Cl2(g) + MnCl2(aq) + 2H2O(l)

На графитној аноди (А) издвојиће се елементарни хлор према
једначини:
А (+) : 2Cl–(aq) – 2e– Cl2(g).
Хлоридни јон се оксидовао до елементарног хлора.
Настали хлор реагује с многим елементима, а знатно је мање
реактиван од флуора.
Средства на бази хлора
највећи
за дезинфекцију
воде, натријум-хипохлорит, NaClO, хлор(IV)-оксид, ClO2 и
други. Гасовити хлор с водом гради хипохлорасту киселину, која је оксидационо средство.
Cl2(g) + H2O(l) HClO(aq) + H+ (aq) + Cl–(aq)
Хипохлораста киселина, HClO, разлаже се на HCl и насцентни (атомски) кисеоник, који је врло реактиван и уништава бактерије.
HClO HCl + O
При реакцији водоника и хлора настаје HCl(g).
H2 (g) + Cl2(g) 2HCl(g), ΔrH < 0
Молекул HCl у гасовитом стању
4. Настали хлороводоник се добро раствара у

HCl (сона киселина)
Једна запремина воде раствара 500 запремина хлороводоника.
HCl(aq) је хлороводонична (сона) киселина, HCl (сл. 5). Хлороводонична
средство. С њом реагује већина метала, укључујући ту
Au(s) + 3HCl(aq) + HNO3(aq) AuCl3(aq) + NO(g) + 2H2O(l)
Хлориди су растворни у води, осим сребро(I)-хлорида, AgCl, жива(I)-хлорида, Hg2Cl2, бакар(I)-хлорида, Cu2Cl2, и олово(I)-хлорида, Pb2Cl2.
азотне киселине, настаће
3Hg(l) + 6HCl(aq) + 2HNO3(aq) 3HgCl2(aq) + 2NO(g) + 4H2O(l)
Ставити
Назив киселине и формула
Назив киселог оксида (анхидрида киселине) и формула
Формула калијумове соли Назив соли
хипохлораста киселина, HClO хлор(I)-оксид, Cl2O KClOкалијум-хипохлорит
хлораста киселина, HClO2 хлор(III)-оксид, Cl2O3, KClO2 калијум-хлорит
хлорна киселина, HClO3 хлор(V)-оксид, Cl2O5 KClO3 калијум-хлорат
перхлорна киселина, HClO4 хлор(VII)-оксид, Cl2O7 KClO4 калијум-перхлорат
Табела 3. – Једињења хлора (оксиди, кисеоничне киселине и соли)
атома у молекулу, смањује се густина електронског облака око
Ba(ClO4)2 (aq) + H2SO4(aq) BaSO4(s) + 2HClO4(aq)
HClO4(aq) H+(aq) + ClO4–(aq)


Cl2(aq) + NaOH(aq) NaClO(aq) + HCl (aq) Овако
оксидационог дејства, хипохлорити се користе као средство
(сл. 6). Хлорни креч, мешовита со хипохлорасте
Cl2 +
Бром, Br

јоне?
а) CHCl3, б) MgCl2, в) Cl2O7, г) NaOCl У ком од наведених случајева се јавља хемијска реакција?
а) KBr + I2
б) KCl + Br2
в) NaCl + F2
г) NaF + Cl2
3. При електролизи растопа NaCl на аноди се издваја:
а) Cl2, б) H2, в) O2, г) H2O2.
4. Попуните табелу.
Анхидрид киселине КиселинаФормула солиНазив соли HClO NaClO
Cl2O3 KClO2
HClO3 магнезијум- хлорат Cl2O7 Ca(ClO4)2 – алуминијум-хлорид
5. а) Колико се dm3 Cl2 ослободи ако се на 0,1 mol KMnO4 делује вишком разблажене HCl (нормални услови)? (РЕШЕЊЕ: 5,6 dm3) б) Завршите започету хемијску једначину: KMnO4 + HCl KCl + MnCl2 +
сумпора у неполарном угљен-дисулфиду, CS2. Кад се
сумпор сипа у хладну воду, гради се пластичан (аморфан) сумпор, који стајањем прелази у ромбичан.
Сумпор се налази у минералима у
сулфидних руда бакра (халкозин, Cu2S, и халкопирит, CuFeS2), сребра (аргентит, Ag2S), цинка (сфалерит, ZnS), олова (галенит, PbS).
Заступљен је и у облику сулфатних руда калцијума и магнезијума. Морска вода садржи сумпор у облику сулфатног јона, SO42–(aq).
Сумпор се углавном добија
2H2S(g) + O2(g) 2S(s) + 2H2O(g)


H2(g) + S(s) H2S(g)
2FeCl3 (aq) + H2S(g) 2FeCl2(aq) + S(s) + 2HCl(aq)
SO2(g) + H2O(l) H2SO3(aq)
Сумпораста киселина је двобазна и гради два типа соли, киселу (хидрогенсулфити, HSO3–) и нормалну со (сулфити, SO32–). На
пример натријум-сулфит је јонско једињење (сл. 13).
Сумпор(VI)-оксид, SO3, добија се оксидацијом сумпор(IV)-оксида, SO2, с ваздушним кисеоником у присуству катализатора Pt или V2O5, уз ослобађање топлоте.
2SO2(g) + O2(g) 2SO3(g) , ΔrH < O
Сумпор(VI)-оксид је на собној температури безбојна течност која кључа на 317,7 K, a нa 290 K прелази у чврсто стање. На влажном ваздуху јако се пуши образујући димну завесу од настале сулфатне киселине. Употребљава се
SO3(g) + H2O(l) H2SO4(aq)
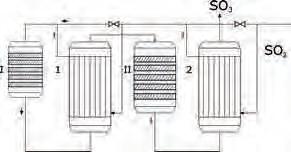
Сумпорна киселина добија се индустријски каталитичком оксидацијом (контактни поступак), SO2 у SO3 на површини чврстог катализатора, ванадијум(V)-оксида V2O5 (сл. 14).
Концентрована H2SO4 је безбојна пушљива течност јер отпушта SO3(g) док
не постигне константан састав (96%, густина 1.834 kg/m3). Јака је полипротична
киселина и с натријум-хидроксидом гра-
ди две врсте соли, киселу (натријум-хи-
дрогенсулфат, NaHSO4):
H2SO4 + NaOH NaHSO4 + H2O,
и нормалну (натријум-сулфат, Na2SO4):
H2SO4 + 2NaOH Na2SO4 + 2H2O
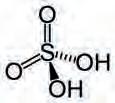
Пошто су за неутрализацију два мола јона H+ потребна два мола јона OH–, ова киселина је полипротична, вишебазна (сл. 15).
Разблажена H2SO4 реагује с металима чији је редокс-потенцијал негативнији од водоника, на пример са цинком, Zn (видети Напонски низ метала, поглавље 10).
Zn + H2SO4 ZnSO4(aq) + H2(g)
Концентрована H2SO4 може бити
металима чији је
са сребром, Ag. 2Ag + 2H2SO4 Ag2SO4(aq) + SO2 + 2H2O
сумпора,
смањује се с повишењем температуре воде.
Сулфатима расте растворљивост у води
температуру. Сулфат бакра, Cu(II)-сулфатпентахидрат (плава галица, CuSO4 . 5H2O) и сулфат гвожђа, Fe(II)-сулфат хептахидрат (зелена галица, FeSO4 . 7H2O) кристалишу с водом (сл. 16).
Познато је још неколико кисеоничних киселина сумпора у којима сумпор има оксидациони број +6: тиосумпорна киселина, H2S2O3 (нпр. со натријум-тиосулфат, Na2S2O3), пероксосумпорна, H2SO5 (нпр. со натријум-пероксосулфат, Na2S2O5), пиросумпорна, H2S2O7 (нпр. со натријум-пиросулфат, Na2S2O7 ), тетратионатна, H2S4O6 (нпр. со натријум-тетратионат, Na2S4O6 ) итд.




2.
калцијум-хидрогенсулфид H2S2O3 натријум-тиосулфат
3. Колико атома водоника настаје у реакцији 0,54 g Al са H2SO4 (нормални услови)?
(Решење: 3,66 . 1022 атома H)
4. У којој од наведених реакција је сумпораста киселина оксидационо средство?
а) H2SO3 + H2O2 H2SO4 + H2O
б) H2SO3 + I2 + H2O H2SO4 + 2HI
в) H2SO3 + 2H2S 3S + 3H2O
5. У реакцији HNO3 са H2SO3 настају H2SO4, NO и H2O. Колико ће се cm3 азот(II)-оксида
ослободити у реакцији 4,92 g H2SO3 (нормални услови)? (РЕШЕЊЕ: 896 cm3 NO)
арсен, As и антимон, Sb и метал бизмут, Bi. Предмет изучавања су неметали, азот и фосфор.
Азот, N Налажење, добијање и својства
Mолекул азота има двоатомну структуру, N2, у којој су атоми повезани троструком неполарном ковалентном везом. Енергија троструке везе је велика, чиме је условљена мала реактивност азота. На собној температури

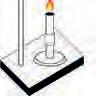
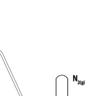
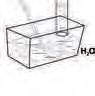
NH4Cl, и натријум-нитрита, NaNO2 (сл. 18).
NH4Cl(aq) + NaNO2(aq) N2 (g) + NaCl(aq) + 2H2O(l)
броја. Атоми азота могу, за разлику од осталих чланова групе, да граде двоструке и троструке везе (као у N2, N2O4, CN–). Услед присуства вишеструких
веза, оксиди азота су мономери, N2O3 и N2O5, а остали чланови групе формирају димерне молекуле оксида (на пример фосфор, P4O6 и P4O10).
Једињења азота Елементи 15. групе граде с водоником ковалентне хидриде,
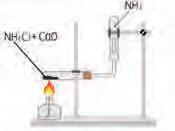
Слика 19. –
се лабораторијски добија загревањем амонијум-хлорида, NH4Cl, и калцијум-оксида, CaO (сл. 19).
2NH4Cl(s) + CaO(s) 2NH3(g) + CaCl2(s) + H2O

3H2(g) + N2(g) 2NH3(g)
слабу
амонијум-хидроксид, NH4OH.
NH3 + H2O NH4OH База дисосује на
NH4+, и хидроксидни јон, OH–NH4OH NH4+ + OH– Kb = 1,8 10–5 mol/l
су амонијум-сулфат, (NH4)2SO4, амонијум-нитрат, NH4NO3, и уреа, CO(NH2)2. Употребљавају се у
Формула оксида
N2Oазот(I)-оксид (азот-субоксид)
NOазот(II)-оксид (азот-моноксид)
N2O3
(нитрозо)
азот(III)-оксид (азот-триоксид) Кисео оксид, у реакцији с водом гради нитритну киселину, HNO2.
NO2 азот(IV)-оксид (азот-диоксид)
N2O5 азот(V)-оксид (азот-пентоксид)
Кисео оксид, у реакцији с водом гради нитритну киселину, HNO2, и нитрaтну киселину, HNO3.
Кисео оксид, у реакцији с водом гради нитрaтну киселину, HNO3.
Азот(III)-оксид, N2O3(s), с водом гради слабу нитритну
киселину, HNO2 (сл. 21).
N2О3(s) + H2O(l) 2HNO2(aq)
Азотаста (нитритна) киселина постоји само у
растворима, слабо дисосована на хидронијум, H3O+, и нитритни NO2– јон.
HNO2(aq) H3O+(aq) + NO2 –(aq) Ка = 4,5 · 10-4 mol/l
Азотаста киселина је једнобазна и њене соли нитрити
примењују се и као оксидациона
Азотна киселина, HNO3, настаје у природи у малим количинама при електричном пражњењу у атмосфери.
N2О5(s) + H2O(l) 2HNO3(aq)
Киселина
NO3– јон.
HNO3(aq) H3O+(aq) + NO3 –(aq)
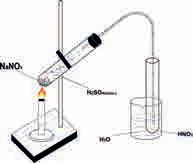
(азотну) киселину (сл. 22).
NaNO3(s) + H2SO4(cc) HNO3 (g) + NaHSO4(aq) H2O
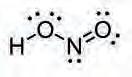
Слика 21. – Структура молекула HNO2
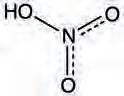
Слика 22. – Структура молекула HNO3
хлороводоничне киселине).
Деловањем
2KNO3(l) 2KNO2(l) + O2(g)
Нитрати
Примена
белог фосфора на температури вишој од 260°C. При претварању
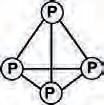
у облику минерала фосфорита.
Фосфор се добија из фосфорита, Ca3(PO4)2, редукцијом с угљеником C, у присуству кварцног песка SiO2(s), при температури од 1.300°C.
2Ca3(PO4)2(s) + 10C(s) + 6SiO2(s) P4(s) + 10CO(g) + 6CaSiO3(l)
Добијени фосфор користи се у индустрији вештачких ђубрива, за производњу шибица и у војној индустрији за производњу димних бомби.
Једињења
P4(s) + 3O2(g) P4O6(g)
P4O6(g) у реакцији с
P4O6 (g) + 6H2O(l) 4H2PHO3(aq)
се
4H2PHO3(aq) PH3 + 3H3PO4(aq)
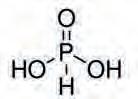
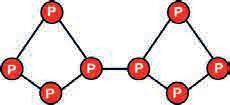
Слика 25. –
молекула H2PHO3
P4 (g) + 5O2(g) P4O10(s)
P4O10(g) + 6H2O(l) 4H3PO4(aq)
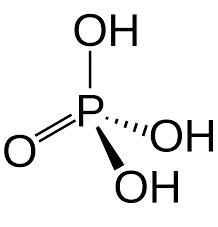
Слика 26.
H3PO4(aq) (сл. 26).
молекула H3PO4
H2PO4– и секундарни фосфат јон HPO42–) и нормалне или терцијарне фосфате (фосфат јон PO43–). Водени раствори дихидрогенфосфата, H2PO4–, делују слабо кисело, хидрогенфосфата, HPO42–, реагују слабо базно, а нормалних фосфата, PO43–,базно. Ортофосфорна киселина, H3PO4, је мономер за настанак полифосфатних киселина, које из ње настају загревањем, уз
пирофосфaтна киселина, H4P2O7:
2H3PO4 H4P2O7 + H2O,
HPO3 + H2O



1.
3. Колико ml H3PO4 (ω = 0,85, ρ = 1,7 g/cm3) треба одмерити за прављење 250 ml раствора количинске концентрације c = 0,4 mol/l? (РЕШЕЊЕ: 6,8 ml H3PO4)
4. Колико је cm3 O2 потребно за добијање 1,42 g фосфор(V)-оксида из фосфина (нормални услови)? (РЕШЕЊЕ: 896 cm3 O2)
5. Сребрни новчић m = 8,1 g растворен је у разблаженој HNO3, тако да је све сребро прешло у одговарајућу со која са NaCl гради 8,61 g AgCl(s). Колики је % Ag у новчићу? (РЕШЕЊЕ: 80,29% Ag) Елементи
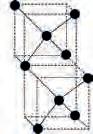
и у елементарном стању. Углавном се налази као угаљ, сирова нафта и

(сл. 30).
у 20 шесточланих и 12 петочланих прстенова, налик фудбалској лопти. Због овакве структуре добио је назив фудбален. Има кристалну структуру и проводник је. Примењује се у области соларне енергије, електронике, оптике,
2C(s) + O2(g) 2CO(g)
чистим кисеоником и трансфузија крви. Ватрогасци, док
користе специјалне маске пуњене сребро-перманганатом, AgMnO4, и калцијум-оксидом, CaO.
Угљен-моноксид је јако редукционо средство, везује кисеоник из оксидних руда, MO (М –метал) и примењује се у металургији за добијање метала M(s).
МО(s) + CO(g) M(s) + CО2(g)
Угљеник с кисеоником (потпуно сагоревање) гради угљеник(IV)-оксид (угљен-диоксид) CO2
C(s) + O2(g) CO2(g)
Оглед
1)
C2H5OH:
C6H12O6 2CO2(g) + 2C2H5OH(l), 2) термичким
CO2 (g) + CaO(s), ΔH > 0
CO2(g) + Ca(OH)2(aq) CaCO3(s) + H2O(l)
CO2, је гас без боје и мириса, слабо киселог укуса. Тежи
угљен-диоксид се
течности за различите неутрализационе процесе. Чврст
ма 1 запремина воде раствара 1,7 запремина CO2. С повишењем
растворљивост гаса се повећава, према Хенријевом закону (W. Henry). CO2 је
постоје истовремено две равнотеже.
CO2(g) + H2O(l) H2CO3(aq) H+(aq) + HCO3–(aq)
Равнотежа се успоставља тренутно.
H2CO3(aq) H+(aq) + HCO3–(aq) K1 = 4,3 . 10–7
Угљена киселина је слаба дипротична киселина која гради два типа соли: хидрогенкарбонате (хидроген-карбонат јон HCO3–) и карбонате (карбонат јон CO32-). Водени раствори хидроген-карбоната делују слабо базно.
HCO3– + H2O H2CO3 + OH–
У води су растворни хидроген-карбонати,
(изузев литијум-карбоната).
T
CaO(s) + 3C(s) CаC2(s) + CO(g)
C2H2.
CаC2(s) + 2H2O Cа(OH)2 + C2H2(g)
Примена
1. Које су сличности и разлике у структури и својствима дијаманта и графита?
2. Прикажите хемијском једначином доказну реакцију за угљен-диоксид.
3. Представите хемијским једначинама дисоцијацију угљене киселине у води.
4. Хемијска веза у калцијум-карбиду, CaC2, је: а) неполарна ковалентна
јонска
б) јонска веза, в) неполарна и поларна ковалентна веза.
5. Колико молекула CO2 може да апсорбује 3,1 kg Li2O (нормални услови)?
(РЕШЕЊЕ: 6,2 1025 молекула CO2)
Металоиди
Својства
Елементи p блока су неметали, металоиди и метали.
елементи бор,
су од метала. Углавном
нема слободних у природи. Ако их има, врло су ретки. Атоми металоида ипак лакше постижу
стабилну електронску конфигурацију примањем електрона,
Једињења бора
Оксид, хидрид, киселине и соли
Бор(III)-оксид, B2O3, добија се на температури од 100°C, дехидратацијом (одузимањем воде) из боратне (борне) киселине, H3BO3 (сл. 31).
2H3BO3 B2O3 + 3H2O
При загревању боратна киселина дехидратацијом прелази у метаборну киселину, HBO2, потом у бор(III)-оксид, B2O3(s). Овај оксид се јавља у облику љуспастих провидних
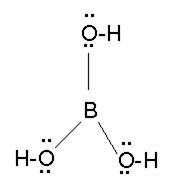
H3BO3 (aq)
H+(aq) + H2BO3–(aq) Ka = 6
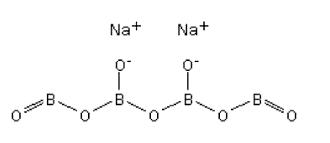
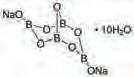
силицијум(IV)-оксид
Аморфни силицијум, настао од скелета ситних морских животињица (инфузорија), назива се инфузоријска земља. Због
На основу електронске конфигурације, атом силицијума (14Si 1s2 2s22p63s23p2), са 4 валентна електрона, може да гради 4 једноструке ковалентне везе ако је sp3 хибридизован. Молекул силицијум(IV)оксида има просторни облик тетраедра због sp3 хибридизације атома силицијума (сл. 33).
Редукција кварцa коксом
SiO2(s) + 2C (s) Si(s) + 2CO(g)
Редукција кварца магнезијумом
SiO2(s) + 2Mg (s) Si(s) + 2MgO(s) Т Т
у
транзисторској техници као полупроводник, у изради соларних батерија и исправљача струје.
Једињења силицијума
Силицијум, Si са хлором, Cl2 гради со, силицијум-тетрахлорид, SiCl4
Si(s) + 2Cl2(g) SiCl4 (s)
Силицијум-тетрахлорид на влажном ваздуху ствара маглу, па служи за замагљивање.
Силицијум с базама реагује градећи соли силикате, уз ослобађање водоника.
Si(s) + 2NaOH(aq) + H2O(l) 2Na2SiO3(aq) + 2H2(g)
Si(s) с киселинама не реагује.
Силицијум(IV)-оксид, SiO2(s) је чврста
собној температури
SiO2(s) + 4HF (g) SiF4(g) + 2H2O(l)
SiF4.
Силикагел, SiO2 nH2O, има способност да упија влагу, па се нашироко
Топљењем силицијум(IV)-оксида, SiO2(s) с натријум-хидроксидом, NaOH, настају водено стакло, натријум-силикат, Na2SiO3, и вода.
SiO2(s) + 2NaOH(aq) Na2SiO3(aq) + H2O(l)
Натријум-силикат, Na2SiO3, користи се у производњи детерџената, као додатак бетону да не пропушта воду, у грнчарији за израду глазуре, у производњи лепка за дрво итд.
Када се раствор натријум-силиката, Na2SiO3 закисели хлороводоничном киселином, HCl(aq), настају силикатна (силицијумова) киселина, H2SiO3 и натријум-хлорид, NaCl(aq).
Na2SiO3(aq) + 2HCl(aq) H2SiO3(aq) + 2NaCl(aq)
Оглед
су соли силицијумових
H2SiO3,
Примена
Племенити
Својства и налажење
Eлементе
нивоа ns2 np6. Само је код хелијума, He, формирана једна s орбитала (1s2). Електронске конфигурације су врло стабилне. Атоми
са халогеним елементима и с кисеоником. Објашњење за реактивност је да се атоми Kr и Xe преведу у ексцитовано (побуђено) стање и да формирају неспарене електроне
XeF6
Примена
1.
2. Зашто He и Ne не граде једињења?
3. Напишите формуле једињења племенитих
однос.
4.
5. Израчунајте:
ПСЕ): а) 14. групе ПСЕ , б) 15. групе ПСЕ , в) 16. групе ПСЕ , г) 17. групе
3.
4.
1) H2O < H2S < H2Se, 2) H2S < H2O < H2Se 3) H2Se < H2S < H2O
5. Завршите започете хемијске једначине.
а) SO2 + H2O
б) SO3 + H2O
в) P4O6 +H2O
г) P4O10 +H2O
д) CO2 +H2O
ђ) N2O3 + H2O
е) N2O5 + H2O
ж) H2 +Cl2
6.
кружите тачан одговор.
1) P2O3, CaO, PbO, FeO
2) N2O3, CO2, P2O5, SO2
3) CO, SO2, Al2O3, CuO
7. Анхидрид хлорне киселине је:
1) ClO, 2) Cl2O5, 3) Cl2O, 4) Cl2O3, 5) Cl2O7.
8. Један од наведених
1) N2O5, 2) SiO2, 3) Cl2O, 4) P4O10
9. У ком од наведених низова се налазе само
1) Cl, P, C, Na, B
2) Si, N, P, B, C 3) B, Si, S, Cl, P
10. У ком од наведених низова се налазе само
селина?
1) CO2, P2O3, SO3, SO2, 2) SO2, SO3, NO2, N2O3, 3) CO2, P2O3, CO, SO3
неутралне соли?
1) ZnO, 2) Al2O3, 3) H2O
12.
неутралне соли?
1) Al2O3, 2) B2O3, 3) Na2O, 4) Fe2O3
13.
14.
15. Колико
калцијум-хидроксида (нормални услови)?
16. Колико има молова амонијум-сулфата у једном
при реакцији с натријум-хидроксидом ослобађа 448 ml амонијака (нормални услови)?
17. Колико ће се грама калцијум-бикарбоната добити растварањем 3
у води која садржи угљен-диоксид?
18. Колико ће се l азота ослободити реакцијом 10,7 g амонијум-хлорида и одговарајуће количине натријум-нитрита?
19. Колико се мола гаса издваја при растварању
киселине, концентрације 0,02 mol/l?
20. У реакцији молекулског фосфора с
Металургија
2C + O2 2CO
3Fe2O3 + CO 2Fe3O4 + CO2
Fe3O4 + CO 3FeO + CO2
FeO + CO Fe + CO2,
SiO2 + CaO CaSiO3



разлику од претходног, обложен је изнутра базним материјалом. Користе се магнезит и доломит, који загревањем граде
4P + 5O2 P4O10 + топлота Згура која се добија овим процесом
се спроводи
(E. W. Siemens (1816–1892)) и P. Martin (1824–1915). Оксидацију

(са
NaAlO2 + 2H2O NaOH + Al(OH)3 Талог се одвоји цеђењем
Al(OH)3
2Al(OH)3 Аl2O3 + 3H2O Б) Електролиза




1.
2.
3.
4.
5.
материјали
неправилни кристали SiO2 називају се кремен, а аморфни облици су
воде).
Силицијум(IV)-оксид SiO2 је хемијски прилично инертан. При топљењу с алкалним хидроксидима, нпр. с NaOH, настају силикати, натријум-силикат, Na2SiO3.
SiO2 + 2NaOH Na2SiO3 + H2O
Најраспрострањенији
по неколико капи фенолфталеина. Своја запажања унесите у свеску.
Према хемијском саставу, стакло се дели на: алкално-кречно, алкално-оловно и алуминијум-бор-силикатно. У алкално-кречна стакла спадају натријумово и калијумово стакло.
Оловно стакло („кристал”) садржи PbO уместо CaO.
Алуминијум-бор-силикатно је јенско стакло (пирекс), које, осим основних састојака, садржи борну киселину, H3BO3, оксид алуминијума, Al2O3, оксид цинка, ZnO, и баријума, BaO.
Отпорно је на промену температуре (има мали коефицијенат ширења) и хемијске агенсе. Производња стакла обухвата припрему сировина, топљење, обликовање и хлађење.
Основне сировине за добијање
(SiO2), сода (Na2CO3 ∙10H2O), кречњак (CaCO3) и стаклени крш (од 20 до 30%). Стаклени крш (топитељ) се додаје
производа.
+ xSiO2 Na2O
xSiO2 + CO2





1. Дефинишите појам стакло.
2. Завршите започету реченицу.
стакласту структуру, (боратно стакло) и (силикатно стакло)
3. Опишите састав, структуру и примену
4. Завршите започету хемијску једначину реакције матирања стакла флуороводоничном киселином, HF: _ + 4HF SiF4 + _H2O.
5. Да ли се стаклени производи из твог окружења разликују
употреби?
маса. Пластични материјали мешају се
(песак
(стакло, гвожђе(III)-оксид,



каменинафајансопека



порозне (таб. 2).


синтетизованих полупроизвода унапред одређеног састава (оксиди метала, затим нитриди, силициди, карбиди, бориди). Класична керамика је термички отпорна, али је крта и не подноси велике температурне промене. Савремени керамички материјали су: оксидна керамика, неоксидна керамика, нуклеарна керамика, керамика за електронику, специјални керамички материјали, композитни керамички материјали и угљенични материјали.
Чиста оксидна керамика заснована је на следећим оксидима: Al2O3, BeO, MgO и ZnO. Примењује се за хемијске реакторе, кондензаторе, аутомобилске свећице.
Неоксидна керамика
карбиди и бориди).
Нуклеарна керамика се примењује у нуклеарној
изведена је суперпроводна оксидна
мика на бази итријума, баријума и бакра, која показује феномен суперпроводности на температурама течног азота и
области од 70 до 90 К.
Биоактивна керамика, служи за израду вештачких зглобова, кукова,

Слика 17. – Композитна керамика, тениски рекет
изводњом композита: керамика–метал, керамика––стакло, керамика–угљенична влакна. Композити керамика–метал називају се кермети, а композити керамика–стакло, витрокерамика. Данас је незамислива израда квалитетне спортске опреме: скија, штапова за голф, тениских рекета, без примене ових савремених керамичких материјала (сл. 17).
ПИТАЊА
1.
2. Које
3.
Калцијум-оксид,
CaO + H2O
Гашење
опека (цигала). Овај везивни материјал
кречену површину наносе боје, које улазе у слој
танак слој насталог калцијум-карбоната, CaCO3, те су слике дуговечне. Гипс се
цијум-сулфата дихидрата, CaSO4 ∙ 2H2O. Ако се
греје у пећима на температури од 130°С до 160°C,
добија се штукатурни (грађевински) гипс, калцијум-сулфат пола хидрат, CaSO4 ∙ 0,5H2O. На
температури од 800°С до 1200°C настаје естрих
гипс, калцијум-сулфат, CaSO4. Гипс очвршћава везујући воду. Штукатурни

пластичан материјал, већ то својство добија тек кад се фино самеље (цемент). Цемент је хигроскопан, те се складишти у сувим просторијама. Пакује се у вишеслојне вреће од натрон папира (смеђ папир, водоотпоран, чврст на истазање).
Портланд цемент је хидраулично везиво које се добија печењем природне
вештачке смесе кречњака и глине до температуре синтеровања. Основна сировина за добијање
цемента је
зидних површина, за украсна малтерисања.

тераца,
1.
2.
3.
4.
5.
резервоарима стајањем
ситнијих састојака седиментацијом (таложењем). Колоидне честице, које се тада не таложе, ефикасно се издвајају процесом коагулације (поступак неутрализације колоидне честице). Као флокулациона средства (групишу коагулисане честице), најчешће се употребљавају соли алуминијума (на пример алуминијум-сулфат, Al2(SO4)3). Јони алуминијума с водом при слабо базној реакцији граде желатинозни талог алуминијум-хидриксида.
Al3+(aq) + 3H2O (l) Al(OH)3 + 3H+(aq)
Пошто се за јон метала координацијом везују молекули воде, настаје хидратисани алуминијум-хидроксид, [Al(OH)3(H2O)3]. Већина честица суспендованих
2H2S (aq) + O2(aq)
+ H2O (l) HOCl (aq) + H+(aq)+ Cl–(aq)
Cl2(aq) + 2NH3(aq) NH2Cl (aq) + NH4+(aq) + Cl–(aq)
2Cl2(aq) + 3NH3(aq) NHCl2(aq) + 2NH4+(aq) + 2Cl–(aq)
водом. Карбонати и
чине
тврдоћу, а хлориди, сулфати, силикати, нитрати, фосфати и хумати чине сталну тврдоћу. Обе заједно чине укупну тврдоћу.
(C17H35COOK)
Ca2+(aq) + 2CH3 (CH2)16 COO–(aq) (CH3 (CH2)16 COO)2Ca (s)
Mg2+.
Ca2+(aq) + 2HCO3–(aq) CaCO3(s) + CO2(g) + H2O (l)
CaSO4.
Ca2+(aq) + SO42–(aq) CaSO4(s)
CaCO3.
CaCO3
Ca2+(aq) + CO32–(aq) CaCO3(s),
Mg(OH)2. Mg2+(aq) + 2CO32–(aq) + 2H2O(l) Mg(OH)2(s) + 2HCO3–(aq)
HCO3–
Ca2+(aq) + 2HCO3–(aq) + Ca2+(aq) + 2OH–(aq) 2CaCO3(s) + 2H2O(l)
водоснабдевања и економска одрживост.
Еколошки аспект подразумева обраду и одлагање отпадних токова од припреме воде.
Током процеса припреме воде, који се састоји углавном од низа одвојених поступака, све
материје које су уклоњене из воде (гасови, микроорганизми, суспендоване

4.
5.
воде неопходна и једињења неких елемената („макроелементи” N, P, K, Ca, Mg, Fe и S и „микроелементи”B, Si, Mn, Zn, Cu, Na и многи други), као и састојци хумуса, витамини, хормони и антибиотици. Природа је биљке снабдела са довољно светлости, воде, угљен-диоксида и већином потребних елемената из земљишта. Међутим, неке минерале
газдинствима пољопривредних
су: стајњак, компост, зеленишно ђубриво, слама и тресет.
су остаци или споредни производи у преради биљних и животињских делова (остаци индустрије шећера, безалкохолних
отпаци кланица, разна брашна). Та ђубрива садрже нешто
ђубрива имају позитиван утицај на физичка својства
у земљишту могу се подесити кондиционирањем. Уобичајени поступак кондиционирања
кречњаком.
Вештачка ђубрива се по хемијском
киселина и чист амонијак.
NH3 + HNO3(сс) NH4NO3 Амонијум-нитрат
(NH4)2SO4,
2NH3 + H2SO4 (NH4)2SO4 Пошто
2NH3 + CO2 + H2O (NH4)2CO3
(NH4)2CO3 + CaSO4 (NH4)2SO4 + CaCO3
настаје амонијум-карбамат, NH2COONH4
2NH3 + CO2 NH2COONH4
Амонијум-карбамат је со карбаминске киселине, NH2COOH.
другој фази уреа се добија дехидратацијом амонијум-карбамата, NH2COONH4.
NH2COONH4 CO(NH2)2 + H2O
CO(NH2)2 + 2H2O (NH4)2CO3
Амонијум
2NH3 + 3O2 2HNO2 + 2H2O
2HNO2 + O2
фосфорит
апатит, који представљају смешу калцијум-фосфата, Ca3(PO4)2, калцијум-флуорофосфата, Ca5(PO4)3F, калцијум-хлорофосфата, Ca5(PO4)3Cl, или калцијум-хидроксофосфата, Ca5(PO4)3OH. Такође, могу се користити руде гвожђа које садрже фосфор, затим гуано настао вишевековним
Ca3(PO4)2 + 4H3PO4 + 3H2O 3
неутрализацију
кречњака уситњеног поступком млевења. Процес
CaCO3 + H2O + CO2 Ca(HCO3)2
Ca(HCO3)2 Ca2+ + 2HCO3–
CaO + H2O Ca(OH)2
Ca(OH)2 + 2CO2 Ca(HCO3)2
Ca(HCO3)2 Ca2+ + 2HCO3–.
Кречна
Оглед


ПИТАЊА
1. Израчунајте
2. Завршите хемијску једначину: __+2H2SO4 + 5__ Ca(H2PO4)2 ∙ H2O + 2CaSO4 ∙ 2H2O.
3.
Елементи 16. групе, сл. 14). Као сировина користи се сумпор
сумпор(IV)-оксида.
S(s) + O2(g) SO2(g)
Овај гас добија се и
2MS(s) + 3O2(g) 2MO(s) + 2SO2(g)
+ V2O5(s) SO3(g) + 2VO2(s)
H2S2O7(aq) + H2O(l) 2H2SO4(aq)
Технички
96% олеум (96 делова SO3 и 4 дела H2SO4).
У
киселина, HCl По индустријском значају, хлороводонична
индустрији за добијање хлорида,
2NaCl(s) + H2SO4(сс) Na2SO4 (s) + 2HCl(l)
добија се трговачка хлороводонична киселина која се
са садржајем од 36% HCl.
Хлороводонична киселина је врло корозивна према већини
хлороводоника
3.
+ NO(g) + 2H2O(l)
4. Допуните започету једначину.
3Hg(l) + 6HCl(aq) + 2HNO3(aq) 3HgCl2(aq) + ___(g) + 4H2
амонијака који учествује у процесу. Амонијачни поступак заснива се на увођењу амонијака у засићен раствор натријум-хлорида под притиском, а затим на увођењу угљеник(IV)-оксида,
NaHCO3.
NaCl(s) + NH3(g) + CO2(g) + H2O(l) NH4Cl (aq) + NaHCO3(aq) Натријум-бикарбонат (NaHCO3) се најтеже раствара
ши, тако да се
загревањем лако добија натријум-карбонат (сода), Na2CO3(aq).
2NaHCO3(aq) Na2CO3(aq) + CO2(g) + H2O(l),
NH3(g) + CO2(g) + H2O(l) NH4HCO3(aq).
Из амонијум-хлорида (споредни производ) помоћу
амонијак, NH3:
2NH4Cl (aq) + Ca(OH)2(aq) 2NH3(g) + CaCl2(s) + 2H2O(l),
који се
-диоксида, добија
CaCO3(s) CaO(s) + CO2(g) Калцијум-оксид
CaO(s) + H2O(l) Ca(OH)2(aq) ΔrH < 0
CaCO3:
2NaCl(aq) + CaCO3(s) Na2CO3(aq) + CaCl2(s)
Ca(OH)2,
језера засновани су на различитој
раствора. Мању количину калијумових соли садрже споредни производи добијени у неким
индустријским процесима.
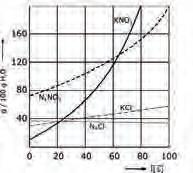
Шалитра се индустријски добија из засићеног раствора натријум-нитрата и калијумхлорида на температури од 20°C.
Na+(aq) + NO3–(aq) + K+(aq) + Cl–(aq) KNO3(s) + Na+(aq) + Cl–(aq)
На тој температури је најмања растворљивост
калијум-нитрата, и он се издваја при хлађењу раствора (дијаграм 1). Шалитра кристалише у облику
N2 + 3H2 2NH3 ΔH = –92,1 kJ (0°C, 101,3 kPa)
је реакција егзотермна (ослобађа се топлота у околину) принос амонијака ће
нижим температурама. Услови који се у
пракси примењују су: притисак од 10 MPa–100 MPa, температура од 450–600°С и катализатор, гвожђе
оксида алуминијума.
На проналажењу катализатора
је
амонијака врло много се радило, јер он снижава активациону енергију и снижава трошкове производње овог гаса. Постојаност и активност катализатора се знатно мењају
на T = 450°C и P = 10 MPa принос амонијака у
чистог Fe је око 5,5%, у присуству Fe активираног
стабилизованог са Al2O3 је око 9,35%, а Fe са Al2O3 и K2O принос је око 16,5%.
Реакциону брзину
1.
2.
3.
4.
5.
2.
11.
12
13.
14.
15.
16.
17. Напишите 4 формуле
18.
19.
20.
21.



ефекта „стаклене баште”. То је својеврстан начин
(M.J. Molina)
(F. S. Rowland) још 1974. године упозорили су
штетно деловање фреона на озонски омотач. Фреони су група халогених деривата алкана, од којих су најзначајнији фреон 11 (флуор-трихлорметан, CCl3F) и фреон 12 (дифлуор-дихлорметан, CCl2F2; сл. 2).
Фреони
расхладних витрина. Из спрејева се фреони директно распршују
Cl. + O3 ClO + O2
ClO + O. Cl. + O2 Тако мала количина




у зависности од степена и врсте загађења (сл. 4). Уколико је земљиште загађено тешким металима, потребно га је третирати: 1) постављањем огледа с више култура ради добијања плодног земљишта, 2) применом физичко-хемијских мера, 3) пошумљавањем, производњом садног материјала и сетвом траве и 4) микробиолошким третманом. Ако на такав начин није могуће поново вратити уништени пејзаж и плодност земљишта, чине се дугогодишњи
комбиновањем


и топлане, термоелектране и нуклеарне електране, индустријски и занатски објекти, саобраћајна средства и природне појаве (ерупције вулкна
убацују у атмосферу нове и веће количине штетних супстанци, које далеко превазилазе моћ атмосфере да их рециклира. Емисија загађујућих супстанци и њихов ниво у атмосфери су у директној зависности од температуре, ваздушних струјања, влажности, облачности, падавина и атмосферског притиска. Дакле, ниво
атмосфере. Нестабилно стање атмосфере се карактерише јаким вртложним кретањима ваздуха, која спречавају појаву веће загађености ваздуха. Стабилно стање атмосфере одликује се јаким








1.
2.


3.



спољашње и унутрашње температуре није већа од 5°C;
8. Ужину конзумирати свеже припремљену у ђачкој кухињи или код куће од сезонских намирница и с




ПИТАЊА
1.
2.
3.
4.
5.
7.
8.
9.
привреде са .
10. Који су основни загађивачи ваздуха
11. Колико има штетних материја у диму цигарете?
12. Опишите штетно дејство цигарета
никотина: , б) угљен-моноксида: , в) катрана:
13. Које се мере код нас примењују за сузбијање
14. Завршите започету реченицу. Декомпозицијом
17. Ко су загађивачи ваше животне
су : а, загађујуће супстанце су:
18. Како поступате с отпадом у школском простору?
У лабараторији:
У учионици: в) У школском дворишту: г) У ђачкој кухињи:____________________________________
19. Чему служе пиктограми?
20. Наведите 5 примера еколошког
K+ + e – K –2,92
Ca2+ + 2e – Ca –2,87
Na+ + e – Na –2,71
Mg2+ + 2e – Mg –2,37
Al3+ + 3e – Al –1,66
Zn2+ + 2e – Zn –0,76
Fe2+ + 2e – Fe –0,44
Sn2+ + 2e – Sn –0,14
Pb2+ + 2e – Pb –0,13
2H+ + 2e – H2 0
Cu2+ + 2e – Cu +0,34
Ag+ + e – Ag +0,80
Pt2+ + 2e – Pt +1,25
Au3+ + 3e – Au +1,50
ВАЖНО
Метал који се
може редуковати метал
раствора његове соли. На пример:
Мg + ZnCl2 MgCl2 + Zn, Zn + CuCl2 ZnCl2 + Cu, Fe + ZnCl2 није могућа.
Метал који се налази лево
реагује са киселинама уз издвајање водоника. На
Mg + 2HCl MgCl2 + H2(g), Zn + H2SO4 ZnSO4 + H2(g),
Ag + HCl није могућа. Метал
Cu + 2H2SO4(сс.) CuSO4 + SO2(g) + 2H2O, 3Cu + 8HNO3(aq) 3Cu(NO3)2 + 2NO(g) + 4H2O, Cu + 4HNO3(сс.) Cu(NO3)2 + 2NO2(g) + 2H2O.
Назив јединице Ознака
Величина
метар m дужина
килограм kg
секунда s време
келвин K температура
мол mol количина супстанце
ампер A јачина електричне струје
кандела Cd јачина светлости
Назив јединице
квадратни метар m2 површина
кубни метар m3
употребљених растварача посебно се скупљају у посуде
од стакла,
(сл.
паковању, обележавању и
Правилника).
Отровно (Т) Јако отровно (Т–)
Запаљиво (F) Самозапаљиво (F*)
Експлозивно (Е) Оксидативно Биохазард (B) Нагризајуће тј. корозивно (C)
Опасно по здравље
Штетно (Xn) Надражујуће (Xl)
Штетно за околину (N)
Слика 1. – Пиктограми
ТЕСТ 1.
1. 92
2. Кисеоник, силицијум и алуминијум
3. Кисеоник, гвожђе и силицијум
4. Минерали су састојци стена. Руда је минерал из кога се метали добијају на економичан начин.
Легуре су хомогене смеше метала са металима и
неметалима које имају корисне особине.
5. 1. графитна оловка 2. накит 3. пудер 4. паста за зубе 5. кухињска со 6. стакло
6. Mohs- ове скале тврдоће.
7. 1. магматске стене 2. седиментне стене.
3. метаморфне стене.
8. 1. 4 2. 1 3. 2 4. 3 5. 5 6. 6
9. Гвожђа и угљеника Примена : у домаћинству и индустрији.
10. Легуре злата. Бакром, сребром.
11. 1. Десалинизација морске воде, 2. Добијање воде из ледника.
12. Не.
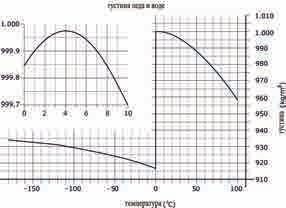
13. 1. Чврсто агрегатно стање
2. Молекули граде водоничну везу.
3. Кристална структура
1.Течно агрегатно стање
2. Молекули граде водоничну везу.
3. Највећа густина воде
14. 11,11% H И 88,89% O
15. Азот, кисеоник, вода, угљен-диоксид и аргон.
16. 6CO2 + 6H2O C6H12O6 + 6O2
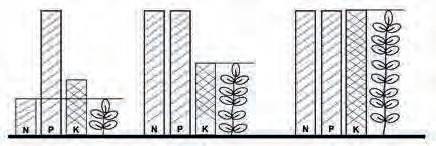
17. Биљка ће се развијати док јој дозвољава присуство најмање заступљеног минерала у земљишту.
18. C6H12O6 + 6O2 6CO2 + 6H2O + енергија
19. Fe2+ је у процесу оксидо-редукције , Mg2+ у процесу фотосинтезе.
20. 1. Редовна исхрана (три главна оброка и две ужине).
2. Разноврсна исхрана (воће, поврће, месо, млеко, црни хлеб...)
3. Умерена исхрана (мале количине соли, масти, слаткиша, газираних пића...).
ТЕСТ 2.
1. Правило је да је реактивнији елеменат који истискује елеменат из његових једињења. На пример, у реакцији хлора и калијум-бромида издваја се бром, то јест хлор истискује бром из калијум-бромида. Cl2 + 2KBr 2 KCl +Br2
2. Cl2 + 2KBr 2KCl +Br2
Cl2 + 2KI 2KCl +I2
Br2 + 2KI 2KBr +I2
3. Калијум има мању енергију јонизације од натријума, па ће лакше отпуштати валентни електрон и бурније реаговари с водом.
4. 2Na + 2H2O 2NaOH + H2
2K + 2H2O 2KOH + H2
5. Боја се мења јер у реакцији настаје раствор
фенолфталеин је ружичаст.
6. Својства елемената се правилно и периодично
7. Елементи који се налазе у истој групи имају исту општу
енергетског
само се разликују по нивоу на којем су ти валентни електрони. А пошто хемијска својства зависе од електронске конфигурације последњег енергетског нивоа, и елементи исте групе имаће слична хемијска својства. 8. Кисеоник постоји у облику две алотропске модификације, као кисеоник (О2) и као озон (О3). Сумпор је елеменат који има више од 30 алотропских модификација. Најзаступљенија алотропска модификација сумпора је S8, у којој су атоми сумпора везани у цикличну структуру. 9. Кристалне супстанце имају правилне и уређене структуре, строго одређен распоред честица, који се назива кристална решетка. Аморфне супстанце
ТЕСТ 3.
1. NH3 – амонијак, ковалентна веза; HF – флуороводоник, ковалентна веза; KH – калијум-хидрид, јонска веза
2. 27,8 kJ/mol
3. г)
4. Zn, Fe, Mg
5. CO2 + H2O → H2CO3; Na2O + H2O → 2NaOH
6. Al2O3(s) + 6HCl(aq) → 2AlCl3 + 3H2О(l)
Al2O3(s) + 2NaOH(aq) + 3H2O(l) → 2Na[Al(OH)4] (aq)
7. 2KMnO4 → K2MnO4 + MnO2 + O2.
8. Константе дисоцијације киселина и константе
дисоцијације база
9. Амонијак, вода, флуороводоник
10. а) NaOH + HCl → NaCl + H2; б) KOH + HNO3
11. Ca(OH)2 + HCl → CaOHCl + H2O
12. а, в, г, д
13. a, г, д, ђ
14. a) CaCl2 → Ca2+ + 2Cl–; б) Na2SO4 → 2Na+ + SO42–; в) Cu(NO3)2 → Cu2+ + 2NO3–
15. а) Zn + CuCl2 → ZnCl2 + Cu; б) Fe + ZnCl2 → није могућа реакција; в) Cu + 2AgNO3 → Cu(NO3)2 + 2 Ag
ТЕСТ 4.
1. NaCl; NaOH; NaHCO3
2. a); в); г)
3. 3,36 dm3
4. PbO(s) + 2HCl(aq) PbCl2(aq) + H2O; PbO(s) + NaOH(aq) + H2O Na[Pb(OH)3](aq)
5. 142,04 g; 26,8 dm3
6. 0,2 dm3
7. 223,9 kg Fe; 134,7 m3 CO2
8. 31,6 g
9. 434,6 g
10. тетрааминцинк(II)-хидроксид; Zn(OH)2 + 4NH3 [Zn(NH3)4](OH)2
11. у амонијаку, у цијанидима и у тиосулфатима; AgCl + 2NH3 [Ag(NH3)2]Cl; AgCl + 2CN– [Ag(CN)2]– + Cl–,; AgCl + 2S2O32– [Ag(S2O3)2]3– + Cl–
12. 25 g
13. 0,17 mol/dm3
14. 92,82%
15. 526,3 kJ
ТЕСТ 5.
1. Комплексна
2. а) 26Fe 1s2 2s2 2p6 3s2 3p6 4s2 3d6 б) Fe2+ 1s2 2s2 2p6 3s2 3p6 4s1 3d5 в) Fe3+ 1s2 2s2 2p6 3s2 3p6 3d5
3. d-d
4. K2Cr2O7
5. Јонске везе
6. а) тетрахлородиаминплатина (IV) б) калијум-хексацијанида (II) в) тетрааминбакар (II)-хлорид
7. а) не дисосује б) 4K+ + [Fe(CN)6 ]4–в) [Cu(NH3)4]2+ + 2Cl–
8. в)
9. г)
10. 3)
11. [Ag(CN)2]–
12. [Cu(NH3)4]2+
13. јона прелазног метала
14. Mg2+
15. Fe2+
16. Co3+
17. Фотосинтезе.
18. Анемија.
19. Hg, Pb, As , мокраћом.
20. линеарна, квадратно планарна и тетраедарска, октаедарски.
ТЕСТ 6.
1. а) ns2 np2 (-2, -4, +2, +4)
б) ns2 np3 (-3, +1,+3, +5)
в) ns2 np4 (-2, +2, +4, +6)
г) ns2 np5 (-1, +1,+3, +5, +7)
д) ns2 np6 (+2, +4, +6, +8)
2. 6C 1s2 2s2 2p2 4. група, 2. периода ; 7N 1s2 2s2
2p3 5. група, 2. периода; 16S 1s2 2s2 2p6 3s2 3p4 6. група, 3. периода; 17Cl 1s2 2s2 2p6 3s2 3p5 7. група, 3. периода.
3. Кисели оксиди: CO2, N2O3, NO2, N2O5, P4O6, P4O10, SO2, SO3,Cl2O, Cl2O3, Cl2O5, Cl2O7
Неутрални оксиди: CO, N2O и NO.
4. 1)
5. а) SO2 + H2O H2SO3
б) SO3 + H2O H2SO4
в) P4O6 + 6H2O 4H2PHO3
г) P4O10 + 6H2O 4H3PO4
д) CO2 + H2O H2CO3
ђ) N2O3 + H2O 2HNO2
е) N2O5 + H2O 2HNO3
ж) H2 + Cl2 2HCl
6. 2)
7. 2)
8. 2)
9. 3)
10. 1)
11. 1)
12. 3)
13. 2)
14. 69,4l CO2
15. 3.17g CaOCl2
16. 0,25 mol/l (NH4)2SO4
17. 4,86g Ca(HCO3)2
18. 4,48l N2
19. 1,25 ∙ 10-4 mola SiF4
20. 2P4 + 3NaOH + 9H2O 5PH3 + 3NaH2PO4, 2,48 ∙10-1g P4
ТЕСТ 7.
1. Легура с 2,5–5% угљеника, у којој су примесе и
других елемената у количини до 5% (фосфор, манган и силицијум)
2. легуре гвожђа које садрже највише до 1,7% угљеника
3. 3Fe2O3 + CO 2Fe3O4 + CO2; Fe3O4 + CO → 3FeO + CO2; FeO + CO Fe + CO2
4. Oксидацијом
5. Жарењем алуминијум-хидроксида
6. 2Al2O3 4Al + 3O2
катода: Al2O3 + 6e– 2Al + 2AlO33–анода: 2AlO33– + 3C 3CO + 6e– + Al2O3
7. Стакло, керамику и грађевинске везивне материјале.
8. Не.
9. SiO2 силицијум (IV)- оксид.
10. Na2O ∙ CaO ∙ 6SiO2
11. Отпорно је на промену температуре и хемијске
агенсе и користи се за израду лабараторијског poсуђа и ватросталног посуђа у домаћинству.
12. SiO2 + 4HF → SiF4 + 2H2O.
13. Глина.
14. Глина је хидратисани алуминијум – силикат опште формуле Al2O3 ∙ SiO2 ∙ XH2O.
15. Порозни: фајанс, мајолика, обична грнчарија (с глазуром) и опека, цреп, теракота (без глазуре). Непорозни: порцелан и каменина.
16. Оксиди метала, нитриди, силициди, карбиди, бориди итд.
17. Al2O3, BeO, MgO и ZnO.
18. У савременим технологијама: космичкој, компијутерској, нуклеарној технологији, затим у изради спортске опреме, аутомобилској и авио-индустрији.
19. Малтер је смеша везивног средства с водом и пуниоцима. Везивна средства која очвршћавају на ваздуху су: иловача, креч и гипс, а на ваздуху и под водом очвршћава цемент. Пуниоци су: песак,шљунак, туцаник и згура. Они дају порозност, олакшавају очвршћавање и спречавају превелико скупљање малтера. Примена у грађевинарству.
20. CaCO3 → CaO + CO2 (Т=1000 до 1200°C).
21. Ca(OH)2 + CO2 CaCO3 + H2O.
22. Састав бетона: цемент, песак, шљунак и вода. Врсте бетона: лаки (у бетон се уграђује уместо шљунка лакши материјал – шљака или опека), армирани (у бетон се уграђују гвоздене или челичне шипке) и преднапрегнути (у бетон се уграђују челичне или гвоздене жице упредене у каблове).
23. H2O + Cl2 HClO + H+(aq) + Cl–(aq)
24. Зависно од квалитета сирове воде технологија припреме воде за пиће обухвата углавном следеће фазе: филтрацију, седиментацију, флокулацију, коагулацију, аерацију и дезинфекцију.
25. Тресети су органске супстанце настале од изумрлих биљних врста под дејством микроорганизама у анаеробним
Механичке сулфатне пећи израђују се од материјала отпорног на високе температуре и дејство киселине (од челика и опеке).
ТЕСТ 8.
1. Енергетика, саобраћај, пољопривреда, рударство, депоније комуналног и индустријског отпада, отпадне воде из индустрије и домаћинства итд.
2. Повећана потрошња фосилних горива, уништавање шума, смањење биљног света у мору због депоновања отровног отпада и многи други процеси изазивају нагомилавање CO2 и других гасова у атмосфери, што доводи до појаве глобалног загревања земљине површине (ефекат „стаклене баште“).
3. Фреони су загађујуће супстанце, по хемијском саставу халогени деривати алкана (фреон 11, CCl3F и фреон 12, CCl2F2). Они са другим загађујућим супстанцама гасовитог агреганог стања угрожавају озонски заштитни слој изазивајући разлагање озона у кисеоник 2O3(g) 3O2(g).
4. Оксиде азота (N2O3, NO2, N2O5), оксиде сумпора (SO2 и SO3), оксид угљеника (CO2) и испарљиве органске киселине (мравља киселина, HCOOH и сирћетна киселина, CH3COOH).
5. Штетно делују на здравље људи, оштећују биљни и животињски свет, смањују квалитет земљишта, ваздуха и воде и утичу на убрзано пропадање материјала
6. Биоремедијација
10.
прашина.
11. Око 4000.
12.
13.
нас се примењују законске уредбе за
у радном простору. Нису мере довољне (у ресторанима пушачи и непушачи бораве у
просторији, само у другом делу објекта).
14. Метан, CH4 и угљеник (IV)-оксид, CO2, повећава ефекат стаклене баште.
15. 1) Да 2) Наша околина се може унапредити и у естетском и у хигијенском смислу. Можемо је унапредити поштујући важећу законску регулативу.
16. Увођење нових технологија у индустрију, селекција отпада и примена обновљивих извора енергије.
17. Загађивачи: индустријска постројења, саобраћај, топлане и приватна ложишта... Загађујуће супстанце: оксиди азота, никотин, угљен-диоксид, метан, фреони...
18. а) Према упутству за рад у хемијској лабараторији.
б) Раздваја се отпад према врсти и одлаже на предвиђено место.
в) Поштују се правила понашања у школи.
г) Поштују се правила понашања у ђачкој кухињи.
19. Пиктограми су сликовни знаци за обележавање
запаљиве, отровне, корозивне и експлозивне супстанце.
20. 1. Редовно се проветрава радни и санитарни простор.
2. Затварају се потпуно славине после употребе.
3. Отпад се одлаже на предвиђено место.
4. Гаси се светло по напуштању просторије.
5. Ужина се конзумира упакована у папирну амбалажу.
ЛИТЕРАТУРА
1. Филиповић, И., Липановић, С., Опћа и анорганска кемија, Школска књига, Загреб, 1995.
2. Арсенијевић, С., Општа и неорганска хемија, Партенон, Београд, 2001.
3. Рајић, С., Неорганска хемија, Завод за уџбенике, Београд, 2011.
4. Чековић, Ж., Хемијска читанка, Завод за уџбенике и наставна средства, Београд, 2001.
5. Ђурић, Д., Петровић, Љ., Загађење животне средине и здравље човека, Веларта, Београд, 1996.
6. Бојановић, Ј., Чорбић, М., Општа хемија, Медицинска књига, Медицинске комуникације, Београд, 1997.
7. Хорват, Р., Неорганска хемија, Завод за уџбенике, Београд, 1994.
8. Нешић, С., Јоветић, М., Хемијски практикум, Завод за уџбенике, Нови Сад, 1992.
9. Виторовић, Д., Хемијска технологија, Научна књига, Београд, 1982.
10. Исаковић, Г., Лукић, Љ., Исаковић, М., Панајотовић, Н., Општа и неорганска хемија, Завод за издавање уџбеника, Нови Сад, 1987.
11. Јелић, М., Агрохемија, Пољопривредни факултет, Косовска Митровица, 2012.
12. Јанчетовић, М., Комерцијално познавање робе, Завод за уџбенике, Београд, 2014.
13. Вујовић, З., Караџић, И., Вујић, В., Гопчевић, К., Вукићевић, Р., Ђурђевић, П., Николић, Г., Трутић, Н., Поповић, М., Збирка задатака, ЦИБИД, Београд, 2011.
14. Ђукановић, М., Еколошки изазов, Елит, Београд, 1991.
15. Трифуновић, С., Сабо, Т., Општа хемија, Институт за хемију, Београд, 2004.
16. Лакушић, Д., Шинжар-Секулић, Ј., Ракић, Т., Сабољевић, М., Основи екологије, Биолошки факултет, Београд, 2015.
17, Далмација, Б., Агбаба, Контрола квалитета воде за пиће, Природно-математички факултет, Департман за хемију, Нови Сад, 2006.
