
RADIVOJ NIKOLAJEVIÃ · mr MILENA ŠURJANOVIÃ


RADIVOJ NIKOLAJEVIÃ · mr MILENA ŠURJANOVIÃ
za opštu gimnaziju i prirodno-matematiåki smer gimnazije, za struåne škole u podruåjima rada: poqoprivreda, prerada i proizvodwa hrane, zdravstvo i socijalna zaštita i prirodno-matematiåko podruåje rada
978-86-17-21023-4
I POGLAVQE
Fiziåke veliåine i merne jedinice ......................................................... 7
Fiziåke veliåine 7
Merne jedinice ............................................................................................... 9
Zadaci 15
II POGLAVQE
Struktura atoma 17
Polupreånici atoma ..................................................................................... 17
Elektronski omotaå atoma 21
Kvantni brojevi i atomske orbitale ........................................................ 22
Izgraðivawe elektronskog omotaåa atoma i periodni sistem elemenata ...................................................................... 27
Energija jonizacije (Ei) 28
Afinitet prema elektronu (E a)
Zadaci ..............................................................................................................
III POGLAVQE
Hemijska veza ..................................................................................................
veza
Jonska veza .......................................................................................................
Vodoniåna veza 49
IV POGLAVQE
Hemijske reakcije 55
Kvantitativno znaåewe simbola i formula .......................................... 55
Relativna molekulska masa (M r).................................................................55
Koliåina supstance ...................................................................................... 56
Molarna masa (M) 57
Molarna zapremina (V m) 59
Izraåunavawa na osnovu hemijskih jednaåina ........................................ 59
Jonske reakcije i jonske jednaåine 61
Oksido-redukcione reakcije ...................................................................... 62
Klasifikacija hemijskih reakcija 68
REŠEWA
PERIODNI SISTEM ELEMENATA
Zbirka se sastoji iz sedam poglavqa i to: Fiziåke veliåine i merne jedinice, Struktura atoma, Hemijska veza, Hemijske reakcije, Rastvori, Kiseline i baze, Pregled hemijskih elemenata i wihovih vaþnijih jediwewa.
U prvih šest poglavqa obraðeno je gradivo opšte hemije koje se izuåava u ¡ razredu. Ova poglavqa strukturisana su tako da su u uvodnom delu svake nastavne celine najsaþetije obraðeni oni pojmovi i definicije åije je poznavawe neophodno za uspešno rešavawe odabranih zadataka.
Sedmo poglavqe obuhvata gradivo neorganske hemije koje se izuåava u ¡¡ razredu. U ovom poglavqu nema uvodnog teorijskog dela, veã uåenici treba da znawa iz opšte hemije, steåena u ¡ razredu, samostalno primewuju kod rešavawa konkretnih hemijskih problema. Sem toga, nabrajawe specifiånih podataka o hemijskim elementima i wihovim jediwewima predstavqalo bi ponavqawe uybeniåkog teksta. Gde god je bilo potrebno, u tekstu zadataka navedenih u sedmom poglavqu date su neophodne informacije koje uåenicima treba da olakšaju shvatawe problema i rešavawe zadataka. U ovom poglavqu ima dosta zadataka vezanih za industrijske procese proizvodwe vaþnijih elemenata i wihovih jediwewa.
Postupak rešavawa zadataka detaqno je objašwen na nizu primera. U Zbirci su korišãena dva naåina rešavawa raåunskih zadataka: pomoãu veliåinskih jednaåina i pomoãu proporcija. Takvim pristupom uåenicima je pruþena moguãnost da se u individualnom radu opredele za onu metodu koja im više odgovara. Kako su uåenici u nastavi fizike veã ovladali metodikom rešavawa raåunskih zadataka uz pomoã veliåinskih jednaåina, ovom postupku je u Zbirci posveãena veãa paþwa.
Posle teorijskog dela i rešenih primera slede zadaci za individualni rad uåenika. Zadaci su raznovrsni po sadrþini i formi, kao i po teþini, te se mogu koristiti u redovnoj nastavi za uveþbavawe, u kreativnoj primeni steåenih znawa, kao i u dodatnoj nastavi za proširivawe i produbqivawe preðenog gradiva. Kod korišãewa Zbirke u praksi nije neophodno da svi uåenici reše sve zadatke, veã nastavnici treba samostalno da odaberu zadatke odgovarajuãe teþine za uåenike razliåitog nivoa znawa i sposobnosti. Radi lakšeg korišãewa Zbirke u individualnom radu uåenika, zadaci su navedeni onim redosledom koji odgovara redosledu teorijskog gradiva obraðenog u uvodnom delu nastavnih celina prvih šest poglavqa.
Pored raåunskih, u Zbirci je dat i odreðen broj kvalitativnih zadataka, koji su åesto problemski postavqeni. Ovi zadaci su nameweni razvijawu hemijskog mišqewa, kao i produbqivawu i utvrðivawu teorijskog gradiva obraðenog na åasovima hemije.
Da bi uåenici dobili povratne informacije o uspešnosti rešavawa zadataka, na kraju Zbirke data su rešewa svih zadataka.
Veština rešavawa raåunskih zadataka stiåe se upornim i sistematskim veþbawem. Stoga preporuåujemo uåenicima da samostalno reše što veãi broj zadataka, jer tada ni uspeh neãe izostati.
Autori
Ova Zbirka zadataka iz hemije doþivela je do sada trinaest izdawa i dobro je primqena u nastavnoj praksi. Prema našim saznawima, koriste je i uåenici drugih obrazovnih profila, a ne samo onih kojima je namewena. Zbirka je uvršãena i u popis obavezne literature za pripremawe prijemnih ispita iz hemije na nekim fakultetima.
Na zahtev izdavaåa preradili smo i inovirali odreðene delove Zbirke, modernizovawem nekih zastarelih pojmova i unošewem novih odeqaka koji treba da doprinesu produbqivawu i proširivawu znawa uåenika iz opšte i neorganske hemije.
Znaåajnije izmene izvršene su u sledeãim odeqcima: Elektronski omotaå atoma (uneti su kvantni brojevi), Koliåina supstance (preciznije je definisana Avogadrova konstanta), Tipovi hemijskih reakcija (modernizovana je i proširena klasifikacija neorganskih reakcija, a obraðena je i jonsko-elektronska metoda sastavqawa jednaåina oksido-redukcionih reakcija, dok su postojeãi zadaci za veþbu zameweni aktuelnijim), Brzina hemijske reakcije (preciznije je definisan pojam brzine reakcije a uneto je i nekoliko kvantitativnih zadataka). U šestom poglavqu Zbirke obraðena su dva nova pojma (hidroliza i indikatori kiselosti i baznosti), dok su puferski sistemi modernizovani. Time je zaokruþena i upotpuwena slika koju uåenici treba da steknu o protolitiåkim reakcijama u vodenim rastvorima elektrolita.
U sedmom poglavqu Zbirke (Pregled vaþnijih hemijskih elemenata i wihovih jediwewa) odreðeni broj zadataka zamewen je kompleksnijim i kvantitativnim zadacima. Tipske zadatke (kojih u Zbirci ima najviše) uglavnom nismo mewali niti dodavali nove, pošto smatramo da sâmi nastavnici mogu po potrebi znatno poveãati wihov broj varirawem brojåanih vrednosti, promenom hemijskih reakcija i sl.
Verujemo da ãe ovako modernizovana Zbirka pruþiti uåenicima šire moguãnosti za uspešno ovladavawe nastavnim sadrþajima i osposobiti ih za samostalnu primenu steåenih znawa kod rešavawa konkretnih hemijskih problema. Nastavnicima hemije dat je širi izbor nastavnih sadrþaja i ostavqena moguãnost da po sopstvenom nahoðewu odaberu pojmove koje ãe obraditi u nastavnom procesu.
Na kraju, þelimo da izrazimo zahvalnost urednici ovog izdawa Zbirke, dr Svetlani Radosavqeviã, za korisne sugestije i uloþeni trud da Zbirka svojim izgledom i grafiåkim rešewima bude što lepša i atraktivnija.
Autori

Prirodne nauke izuåavaju prirodne pojave u koje spadaju fiziåka tela i zbivawa ili stawa. U hemiji se izuåavaju sledeãa fiziåka tela: atomi, molekuli, joni, hemijski elementi itd. Zbivawa su, npr., hemijske reakcije, kretawe, ravnoteþa i sl.
U ciqu opisivawa prirodnih pojava, nauka se sluþi merewem nekih wihovih svojstava. Merqiva svojstva prirodnih pojava su ona svojstva koja se mogu kvantitativno izraziti. Ta svojstva nazivaju se fiziåke veliåine. Tako su, na primer, masa, duþina i temperatura tela merqiva svojstva, tj. fiziåke veliåine.
Merewe je postupak kojim se odreðuje vrednost neke fiziåke veliåine pomoãu odgovarajuãih tehniåkih sredstava. Pri merewu se fiziåka veliåina uporeðuje sa istorodnom veliåinom koja je odabrana za jedinicu – tzv. mernom jedinicom. Tako, npr., pri merewu duþine stola odreðuje se odnos izmeðu duþine stola i duþine metra. Ako je duþina stola 2 m, znaåi da je odnos
duþina stola = 2. duþina jednog metra
Prema tome, merewem se dobija broj koji pokazuje koliko je puta posmatrana fiziåka veliåina veãa ili mawa od istorodne fiziåke veliåine koja je uzeta za jedinicu.
Nazivi i simboli fiziåkih veliåina. – Svaka fiziåka veliåina ima svoj naziv. Nazivi mnogih fiziåkih veliåina su internacionalni, tj. imaju istu osnovu u razliåitim jezicima. Na primer: masa, energija, temperatura, entalpija itd.
Radi lakšeg sporazumevawa, dogovoreno je da simboli fiziåkih veliåina budu jednaki u celom svetu. U tablici 1 navedeni su nazivi i simboli fiziåkih veliåina koje se koriste u hemiji.
Simbol mase je, na primer, m Taj simbol oznaåava masu uopšte. Ako þelimo da izrazimo masu uzorka natrijum-hlorida, moramo pored simbola m staviti u zagradu formulu natrijum-hlorida. Prema tome,
masa natrijum-hlorida oznaåava se sa m(NaCl), molarna masa natrijum-hidroksida oznaåava se sa M(NaOH), gustina sumporne kiseline oznaåava se sa ρ(H2SO4), koliåina molekula hlora oznaåava se sa n(Cl2) itd.
Merne jedinice (ili kraãe: jedinice) sluþe za izraþavawe vrednosti fiziåkih veliåina. Jedinice imaju posebne nazive. Tako je naziv za jedinicu mase kilogram, za jedinicu vremena sekunda itd. U tekstu se naziv jedinice piše poåetnim malim slovom.
Svaka jedinica ima svoj znak (simbol). Tako je znak kilograma kg, sekunde s, metra m, itd.
Vrednost fiziåke veliåine jednaka je umnošku brojåane vrednosti i merne jedinice. Na primer:
masa = 10 ⋅ gram.
Kako je simbol mase m, a grama g, moþemo napisati:
m = 10 g
U ovoj kwizi korišãene su jedinice Meðunarodnog sistema jedinica (SI) koji se prema Zakonu o mernim jedinicama i merilima, u našoj zemqi primewuje od 1. ¡ 1981.
Tablica 2. Osnovne SI-jedinice
Izvedene SI-jedinice. – Pomoãu sedam osnovnih SI-jedinica moþe se, po potrebi, izvesti više jedinica, koje se zovu izvedene SI-jedinice. Izvoðewe tih jedinica zasniva se na jednaåinama koje povezuju odgovarajuãe fiziåke veliåine. Navedimo jedan primer. Molarna masa (M) definiše se kao odnos mase åiste supstance (m) i koliåine supstance (n):
M = m n .
Kako je jedinica mase kilogram, a koliåine supstance mol, iz definicije molarne mase sledi jedinica molarne mase, kg/mol. Znaåi, kg/mol je izvedena SI-jedinica.
Neke izvedene SI -jedinice imaju posebne nazive i simbole (tablica 3).
Tablica 3. Neke izvedene SI-jedinice
Decimalne SI-jedinice. – Ukoliko je neka SI-jedinica suviše velika ili suviše mala za izraþavawe vrednosti fiziåke veliåine (npr. metar za izraþavawe polupreånika atoma), koriste se decimalne SI-jedinice. One se dobijaju mnoþewem SI-jedinica odgovarajuãim decimalnim brojevima.
Nazivi decimalnih SI-jedinica dobijaju se tako što se ispred naziva jedinice stavi odgovarajuãi prefiks (predmetak). Prefiks se piše zajedno sa nazivom jedinice. Na primer: kilometar, milimol, mikrosekunda itd.
Simboli decimalnih jedinica dobijaju se na taj naåin što se simbol odgovarajuãeg prefiksa stavi ispred simbola jedinice, tako da sa wim åini odgovarajuãi znak. Na primer: km, mmol, µs.
Treba napomenuti da je SI-jedinica mase – kilogram izuzetak od opšteg pravila za formirawe decimalnih jedinica, pošto ona veã sadrþi jedan prefiks (kilo). Stoga se decimalne jedinice mase izvode od jedinice gram, a ne kilogram (npr. miligram, a ne mikrokilogram).
Tablica 4. SI-prefiksi
Vrednost
Пример 1
Izraziti duþinu od 2,4 cm u nanometrima (nm).
U tablici 4 nalazimo da je 1 nm = 10–9 m. Kako je 1 m = 102 cm, 1 nm = 10–7 cm. Sledi da je 1 cm = 107 nm. Prema tome, 2,4 cm pretvoriãemo u nanometre mnoþewem sa 107:
2,4 cm = 2,4 ⋅ 107 nm
Odgovor: Duþini od 2,4 cm odgovara 2,4 ⋅ 107 nm.
Пример 2
Pretvoriti 0,086 kg u miligrame. 1 kg = 103 g = 106 mg
Prema tome, 0,086 kg pretvoriãemo u miligrame mnoþewem sa 106:
0,086 kg = 0,086 ⋅ 106 mg = 8,6 ⋅ 104 mg
Odgovor: Masi od 0,086 kg odgovara 8,6 ⋅ 104 mg
Пример 3
Pretvoriti 450 cm3 u dm3 . Kako je 1 cm3 = 10–3 dm3, 450 cm3 ãemo pretvoriti u dm3 mnoþewem sa 10–3:
450 cm3 = 450 ⋅ 10–3 dm3 = 0,45 dm3
Odgovor: Zapremini od 450 cm3 odgovara 0,45 dm3
Пример 4
Izraziti temperaturu kquåawa teånog azota (– 196 °C) u kelvinima. Izmeðu Celzijusove i termodinamiåke temperature postoji sledeãi odnos:
T(K) = t (°C) + 273 (1)
Prema tome,
T(K) = – 196 °C + 273 = 77 K
Odgovor: Celzijusovoj temperaturi od – 196 °C odgovara termodinamiåka temperatura od 77 K.
Izuzetno dozvoqene jedinice. – Prema našim zakonskim propisima dozvoqena je upotreba nekoliko jedinica izvan SI (tablica 5).
Tablica 5. Neke dozvoqene jedinice izvan SI
Fizi~ka veli~ina JedinicaSimbol
Definicija pomo}u SI-jedinice
zapremina litar l, L 1 L = 10–3 m3
masa unificirana atomska jedinica mase u 1 u = 1,6605 · 10–27 kg
pritisak bar bar 1 bar = 105 Pa
energijaelektronvolt eV 1 eV ≈ 1,602 · 10–19 J
Celzijusova temperatura stepen celzijusa °C °C = K
Našim zakonom zabrawena je upotreba mnogih jedinica koje su se ranije koristile u nauci i tehnici. Kako se u starijoj hemijskoj literaturi najåešãe sreãu ove jedinice, u tablici 6 navedene su neke od tih jedinica, kao i faktori za wihovo pretvarawe u SI-jedinice.
Tablica 6. Neke zabrawene jedinice
Fizi~ka veli~ina Jedinica Simbol Definicija pomo}u SI-jedinice
du`inaangstrem Å 1 Å = 10–10 m = = 10–8 cm = 100 pm
fizi~ka atmosfera
pritisak
tehni~ka atmosfera milimetar `ivinog stuba
energija, rad erg termohemijska kalorija
elektri~ni
at mm Hg
at = 98 066,5 Pa 1 mm Hg = 133,3 Pa
erg = 10–7 J
calth
Пример 5
Polupreånici atoma ranije su izraþavani u angstremima (Å). Tako, na primer, polupreånik atoma bakra iznosi 1,28 Å. Izraziti ovu vrednost u decimalnim SI-jedinicama – nanometrima i pikometrima.
U tablici 6 nalazimo da je 1 Å = 10–8 cm. Kako je 1 nm = 10–9 m = = 10–7 cm, 1 Å = 0,1 nm. Znaåi, angstreme ãemo pretvoriti u nanometre mnoþewem sa 0,1:
1,28 Å = 1,28 ⋅ 0,1 nm = 0,128 nm.
U istoj tablici nalazimo da je 1 Å = 100 pm. Prema tome, 1,28 Å = 1,28 ⋅ 100 pm = 128 pm
Odgovor: Polupreåniku atoma bakra od 1,28 Å odgovara 0,128 nm, odnosno 128 pm
Пример 6
Atmosferski pritisak oåitan na barometru iznosi 742 mm Hg. Izraziti ovu vrednost u kilopaskalima.
U tablici 6 nalazimo da je 1 mm Hg = 133,3 Pa, odnosno 0,133 kPa
Prema tome, 742 mm Hg = 742 ⋅ 0,133 kPa = 98,68 kPa.
Odgovor: Atmosferskom pritisku od 742 mm Hg odgovara 98,68 kPa.
Tablica 7. Brojåane vrednosti nekih vaþnijih fiziåkih konstanti.
Fizi~ka veli~ina SimbolVrednost brzina svetlosti u vakuumu
naelektrisawe protona
Plankova konstanta
Avogadrova konstanta
masa elektrona
masa protona
masa neutrona
Faradejeva konstanta
univerzalna gasna konstanta
NA 6,02 ⋅ 1023 mol–1
1. Koje fizi~ke veli~ine imaju slede}e merne jedinice: a) nanometar, b) kiloyul, v) gram po kubnom centimetru, g) mol, d) kelvin, |) kubni metar?
2. Pretvorite 4,5 · 10–6 m u nanometre.
3. Izrazite du`inu od 160 pm u metrima.
4. Izrazite sredwu brzinu molekula vode od 580 m/s u kilometrima na ~as.
5. Pretvorite 0,050 dm3 u kubne centimetre.
6. Pretvorite 6,2 m2 u: a) dm2 , b) cm2 , v) mm2
7. Pretvorite 250 mm3 u kubne metre.
8. Izrazite 5 g u: a) kilogramima, b) miligramima, v) mikrogramima.
9. Izrazite 5 mg u atomskim jedinicama mase (u).
10. Izrazite gustinu `ive od 13,6 g/cm3 u gramima po litru.
11. Gustina metana je 6,67 · 10–4 g/cm3. Izrazite ovu vrednost u kilogramima po kubnom metru.
12. Izrazite temperaturu topqewa natrijum-hlorida od 801 ºC u kelvinima.
13. Izrazite temperaturu kqu~awa vode (100 ºC) u kelvinima.
14. Izrazite temperaturu od 40 K u stepenima celzijusa.
15. Izrazite pritisak od 500 at u kilopaskalima.
16. Pretvorite 762 mm Hg u milibare.
17. Pretvorite 986 mbar u kilopaskale.
18. Pretvorite 70 kcal u kiloyule.


Atomi su izvanredno sitne, hemijski nedeqive åestice, od kojih su izgraðene sve supstance u prirodi. Sastoje se od jezgra (nukleusa) i elektronskog omotaåa.
Polupreånici atoma izraåunavaju se na osnovu podataka dobijenih merewem rastojawa izmeðu jezgara atoma u kristalima ili gasovitim molekulima. Izraåunati polupreånici atoma istog hemijskog elementa mogu se meðusobno dosta razlikovati, zavisno od toga koje su vrednosti uzete kao osnova za izraåunavawe.
Tablica 8. Polupreånici atoma alkalnih metala
Hemijski elemenat
Пример 7
Izraåunati koliko se atoma kalijuma moþe poreðati, jedan pored drugog, na duþini od 1 mm. U tablici 8 nalazimo da je polupreånik atoma kalijuma 220 pm. Prema tome, preånik tog atoma je 440 pm
Pretvorimo 440 pm u milimetre: 1 pm = 10–12 m = 10–9 mm, 440 pm = 440 ⋅ 10–9 mm = 4,4 ⋅ 10–7 mm.
Broj atoma kalijuma koji se mogu poreðati na duþini od 1 mm izraåunaãemo iz sledeãe proporcije: 1 : 4,4 ⋅ 10–7 mm = x : 1 mm, x = 1 1 mm 4,4 ⋅ 10–7 mm = 1 4,4 ⋅ 107 = 0,23 ⋅ 107 = 2,3 106
Odgovor: Na duþini od 1 mm moþe se poreðati 2,3 miliona atoma kalijuma.
Atomi su izvanredno sitne åestice åije se mase ne mogu neposredno izmeriti. Za odreðivawe mase atoma koriste se posredni, veoma sloþeni postupci.
Tablica 9. Proseåne mase atoma nekih hemijskih elemenata Hemijski
· 10–27
· 10–26
· 10–26
2,656 · 10–26
5,324 · 10–26
5,887 · 10–26 gvo`|e 9,274 · 10–26 `iva 3,331 · 10–25
Kilogram je isuviše velika i neprikladna jedinica za izraþavawe mase atoma. Stoga se ona iskazuje pomoãu unificirane atomske jedinice mase (u), koja je jednaka 1/12 mase atoma ugqenikovog izotopa C–12 (tj. izotopa 12 6 C ): u = 1 12 ⋅ ma ( 12 6 C) = 1,6605 ⋅ 10–27 kg. (2)
Odnos mase nekog atoma i unificirane atomske jedinice mase naziva se relativna atomska masa i obeleþava sa A r:
A r = ma u . (3)
Пример 8
Relativna atomska masa cinka Ar (Zn) = 65,37. Izraåunati masu atoma tog elementa i izraziti je u gramima.
Iz jednaåine (3) sledi:
ma = A r u
ma(Zn) = 65,37 x 1,6605 ⋅ 10–27 kg = 108,5 10–27 kg = 1,085 10–25 kg = 1,085 ⋅ 10–22 g.
Odgovor: Masa atoma cinka je 1,085 ⋅ 10–22 g.
Jezgro atoma je pozitivno naelektrisano i nalazi se u samom središtu atoma. U wemu je koncentrisana skoro sva masa atoma. U odnosu na veliåinu atoma jezgro je veoma sitno – wegov preånik je oko 10 000 puta mawi od preånika atoma i reda je veliåine 10–14 m (tj. 0,01 pm).
Jezgro atoma se sastoji od protona i neutrona.
Proton (oznaåava se simbolom p ) je pozitivno naelektrisana åestica koja nosi najmawu moguãu koliåinu pozitivnog elektriciteta, jednaku 1,6 ⋅ 10–19 kulona (vidi tablicu 7). Masa protona je pribliþno jednaka unificiranoj atomskoj jedinici mase (u)
Atomi svakog pojedinog elementa sadrþe u jezgru taåno odreðen broj protona, jednak atomskom broju tog elementa (Z):
Z = N(p).
(4)
Neutron (n) je elektriåno neutralna åestica åija je masa pribliþno jednaka masi protona.
Maseni broj elementa (A) jednak je zbiru broja protona i neutrona u jezgru:
A = N(p) + N(n)
(5)
Prema tome, broj neutrona u jezgru atoma dobiãemo kada od masenog broja elementa oduzmemo broj protona:
N(n) = A – N(p)
(6)
Maseni broj piše se pored hemijskog znaka elementa kao levi gorwi indeks, a atomski broj kao levi dowi indeks. Na primer: 31 15 P, 56 26 Fe, 65 29 Cu.
Broj neutrona u jezgrima atoma istog elementa nije uvek stalan. Tako se, npr. element kalcijum (Z = 20) sastoji od tri vrste atoma koji u jezgru sadrþe 20, 22 ili 23 neutrona. Znaåi da su maseni brojevi navedenih vrsta atoma kalcijuma razliåiti i iznose 40, 42 i 43. To se skraãeno moþe napisati ovako:
40 20 Ca, 42 20 Ca, 43 20 Ca
Atomi istog hemijskog elementa koji u jezgru sadrþe razliåit broj neutrona usled åega se razlikuju po svojoj masi, nazivaju se izotopi
Veãina hemijskih elemenata u prirodi javqa se u obliku dva ili više stabilnih izotopa. Izuzeci su, npr. fluor, natrijum i fosfor, koji se u prirodi sreãu samo u obliku jednog izotopa.
Пример 9
Odrediti broj protona i neutrona u jezgru izotopa stroncijuma 90 38 Sr.
N(p) = Z = 38
N(n) = A – N(p) = 90 – 38 = 52.
Odgovor: U jezgru izotopa stroncijuma 90 38 Sr nalazi se 38 protona i 52 neutrona.
Mase atoma navedene u tablici 9 predstavqaju proseåne (sredwe) vrednosti, izraåunate na osnovu koliåinskih udela izotopa datog elementa u prirodnoj smeši i wihovih masa. I relativne atomske mase, navedene u tablici periodnog sistema, takoðe predstavqaju proseåne vrednosti, koje se izraåunavaju na naåin objašwen u primeru 10.
Пример 10
Prirodni hlor sastoji se od 75,77 % izotopa 35Cl i 24,23 % izotopa 37Cl. Izraåunati relativnu atomsku masu hlora.
Koliåinski udeli oznaåavaju se simbolom x. Prema tome, moþemo napisati:
x(35Cl) = 75,77 % = 0,7577 x(37Cl) = 24,23 % = 0,2423 A r(Cl) = ?
Relativna atomska masa nekog elementa izraåunava se tako što se koliåinski udeli izotopa datog elementa pomnoþe wihovim relativnim atomskim masama (koje su pribliþno jednake masenim brojevima izotopa), a dobijeni proizvodi saberu.
Relativna atomska masa hlora, prema tome, biãe jednaka:
A r(Cl) = x(35Cl) ⋅ A r(35Cl) + x(37Cl) ⋅ A r(37Cl)
A r(Cl) = 0,7577 ⋅ 35 + 0,2423 ⋅ 37 ≈ 35,5.
Odgovor: Relativna atomska masa hlora pribliþno je jednaka 35,5.
Elektronski omotaå atoma sastoji se od odreðenog broja elektrona koji se velikom brzinom kreãu u prostoru oko atomskog jezgra.
Elektron (e) je negativno naelektrisana åestica åija je masa 1836 puta mawa od mase protona. Elektron nosi najmawu moguãu koliåinu negativnog elektriciteta, jednaku 1,6 ⋅ 10–19 kulona (vidi tablicu 7).
Atomi su elektriåno neutralne åestice, što znaåi da su izgraðeni od istog broja elektrona i protona:
N(e) = N(p). (7)
Zakoni kretawa elektrona u atomu bitno se razlikuju od zakona klasiåne mehanike, koji opisuju kretawe makrotela. Stawa elektrona u atomu izuåava i tumaåi kvantna ili talasna mehanika
Prema zakonima kvantne mehanike kretawe elektrona u atomu dosta je sloþeno i ne moþe se svesti na obrtawe oko jezgra po taåno odreðenim kruþnim putawama kao u planetarnom (Borovom) modelu atoma. U kvantnoj mehanici se kretawe elektrona razmatra kao oscilovawe (treperewe, talasawe) u prostoru oko atomskog jezgra, pri åemu se formira „oblak“ negativnog elektriciteta. U skladu s tim, umesto precizno utvrðenih putawa odreðenog polupreånika, izraåunava se verovatnoãa nalaþewa elektrona na odreðenoj udaqenosti od jezgra. Na slici 1 gustina elektronskog oblaka slikovito je predstavqena gustinom taåkica.
Energetski nivoi. – Elektroni u atomu su, zavisno od svoje energije, rasporeðeni na jednom ili više energetskih nivoa (slojeva). Ti nivoi se na energetskom dijagramu slikovito predstavqaju u vidu lestvica, razliåito udaqenih jedna od druge.
Slika 1. Gustina elektronskog oblaka u atomu vodonika
Energetski podnivoi. – Eksperimentalno je utvrðeno da se elektroni na istom energetskom nivou (sem prvog) malo razlikuju po svojoj energiji. Kaþemo da se energetski nivoi sa vrednostima n > 1 „cepaju“ na dva ili više podnivoa koji imaju veoma sliåne energije.
Spin elektrona je jedno posebno svojstvo elektrona u atomu koje se veoma uprošãeno moþe predstaviti kao obrtawe elektrona oko sopstvene ose. Moguãa su dva smera obrtawa elektrona: u smeru kazaqke na satu i u suprotnom smeru.
Energetski podnivoi sastoje se od odreðenog broja orbitala, koje se karakterišu kombinacijom kvantnih brojeva. Orbitalama se moþe pripisati sledeãi fiziåki smisao: orbitala je oblast prostora oko atomskog jezgra u kojoj je verovatnoãa nalaþewa elektrona najveãa.
Kvantni brojevi. – Ponašawe i svojstva elektrona u atomu karakterišu se sa åetiri kvantna broja: glavnim (n), sporednim (l), magnetnim (m) i spinskim (s)
Glavni kvantni broj (n) – karakteriše energiju elektrona u atomu i wihovu proseånu udaqenost od jezgra. Moþe imati sve celobrojne vrednosti od 1 do ∞, dok za atome u osnovnom stawu ima vrednosti 1–7:
n = 1, 2, 3, ... 7
Svakoj vrednosti n odgovara odreðeni nivo energije elektrona i odreðena proseåna udaqenost od jezgra. Što je vrednost glavnog kvantnog broja mawa, elektronski oblak je bliþe jezgru koje ga jaåe privlaåi, te je mawih dimenzija (ali veãe gustine) i åvršãe je vezan za jezgro. Ako je, npr., n = 1, elektron se nalazi na prvom (najniþem) energetskom nivou, tj. poseduje najniþu energiju i kreãe se najbliþe jezgru.
Maksimalno moguã broj elektrona na niþim energetskim nivoima (do n = 4) izraåunava se po formuli:
N = 2 n2, gde je n – glavni kvantni broj. (8)
Пример 11
Izraåunati maksimalno moguã broj elektrona na treãem energetskom nivou.
Treãi energetski nivo oznaåava se vrednošãu glavnog kvantnog broja n = 3. Zamenom ove vrednosti u izraz (8) dobijamo:
N = 2 ⋅ 32 = 18.
Odgovor: Na treãem energetskom nivou mogu se nalaziti najviše 18 elektrona.
Glavni kvantni broj takoðe odreðuje i broj energetskih podnivoa na datom nivou. Ako je, na primer, n = 4, na åetvrtom energetskom nivou nalaze se åetiri energetska podnivoa.
Sporedni kvantni broj (l) – karakteriše oblik atomskih orbitala. Moþe imati sve celobrojne vrednosti od nule do (n–1) : l = 0, 1, 2, ... (n–1).
Ako je n = 1, l ima samo jednu vrednost (0); ako je n = 2, l moþe imati dve vrednosti (0 ili 1) itd.
Ukupan broj orbitala na energetskim podnivoima jednak je (2 l + 1).
U sluåaju kada je vrednost sporednog kvantnog broja l = 0, orbitale imaju loptast oblik. Vrednosti l = 1 odgovaraju orbitale koje po svom obliku podseãaju na telo dobijeno obrtawem brojke 8 oko vertikalne ose. Veãim vrednostima l odgovaraju orbitale sloþenijeg oblika.
Vrednostima l = 0, 1, 2, 3, ... odgovaraju s, p, d, f... energetski podnivoi, odnosno orbitale koje se na wima nalaze. Ako je l = 0, dati energetski podnivo oznaåava se sa s, baš kao i orbitale koje se na wemu nalaze. Ako je l = 1, govorimo o p-podnivou sa p-orbitalama; ako je l = 2, radi se o d-podnivou i d-orbitalama itd. (slika 2).
Orbitale se oznaåavaju simbolima koji se dobijaju tako što se arapskom cifrom oznaåi vrednost glavnog kvantnog broja, a pored we se dopiše slovo s, p, d... zavisno od vrednosti sporednog kvantnog broja, odnosno energetskog podnivoa na kome se date orbitale nalaze. Tako se npr., orbitala koja se karakteriše sa n = 1, l = 0 obeleþava sa 1s; orbitale koje se karakterišu vrednostima n = 2, l = 0,1 oznaåavaju se sa 2s, odnosno 2p Magnetni kvantni broj (m) – karakteriše moguãe orijentacije orbitala u prostoru oko atomskog jezgra. Ovaj broj moþe imati sve celobrojne vrednosti od – l do + l, ukquåujuãi i nulu:
m = 0, ± 1, ± 2, ...
Svakoj vrednosti m odgovara jedna orbitala koja je na odreðeni naåin orijentisana u prostoru.
Ako je l = 0, magnetni kvantni broj ima samo jednu vrednost (0). Znaåi da se na svakom s-podnivou nalazi samo po jedna s-orbitala, što je i razumqivo s obzirom da s-orbitale imaju oblik lopte te se orijentišu u prostoru oko atomskog jezgra uvek na isti naåin (slika 3).
Orbitale se grafiåki prikazuju u pravouglom koordinatnom sistemu, s tim što se uzima da se atomsko jezgro nalazi u koordinatnom poåetku.
Ako je l = 1, magnetni kvantni broj ima tri razliåite vrednosti (1, 0, –1). Pošto svakoj vrednosti m odgovara jedna orbitala, znaåi da se na p-podnivoima mogu nalaziti po tri energetski ekvivalentne p-orbitale koje se razlikuju po orijentaciji u prostoru.
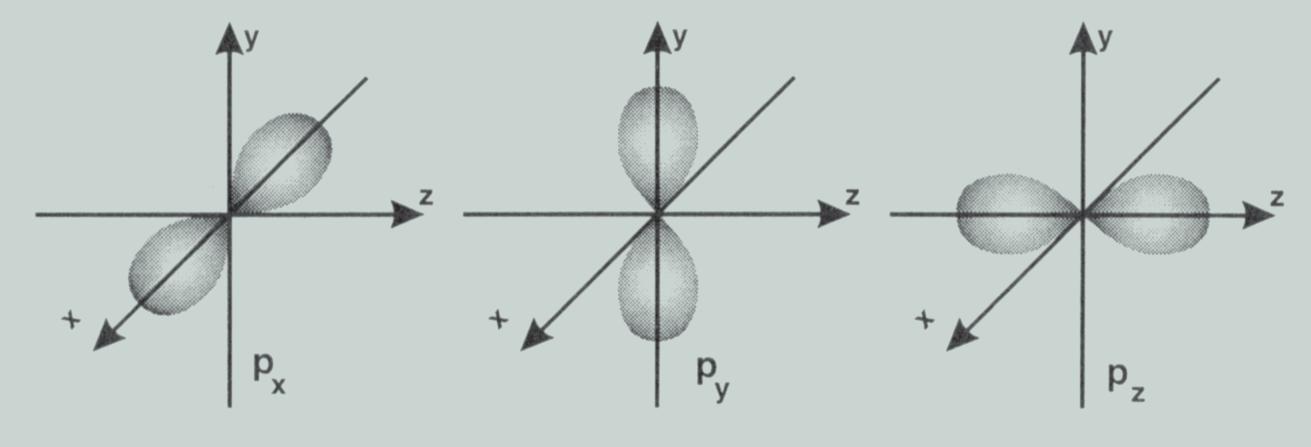
p-orbitale se prostiru uzduþ osa pravouglog koordinatnog sistema, tj. meðu sobom zaklapaju ugao od 90°, te se obeleþavaju sa px, py i pz (slika 4).
Ako je l = 2, magnetni kvantni broj ima pet vrednosti (2, 1, 0, –1, –2), što znaåi da se na d-podnivoima nalazi po pet energetski ekvivalentnih d-orbitala, koje su razliåito orijentisane u prostoru (slika 5).
Slika 2. Shematski prikaz prva tri energetska nivoa i odgovarajuãih podnivoa elektrona u atomu
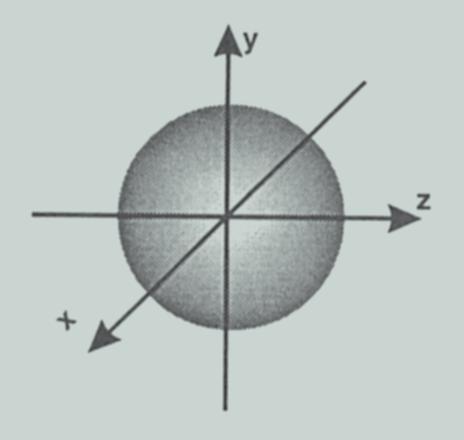
Slika 3. Oblik s-orbitale
4.
Slika 5. Облик d-орбиталa
s = +1/2 s = –1/2
Slika 6. Спин
Kombinacija glavnog, sporednog i magnetnog kvantnog broja karakteriše prostorni raspored elektrona oko atomskog jezgra. Kasnije je radi potpunijeg opisa uveden još jedan kvantni broj koji se zove spinski (s).
Spinski kvantni broj (s) – karakteriše spin elektrona, tj. wihovo obrtawe oko sopstvene ose. Kako su moguãa samo dva smera obrtawa, spinski kvantni broj ima dve vrednosti: + 1/2 i – 1/2
Paulijev princip zabrane glasi: U jednoj orbitali mogu se nalaziti najviše dva elektrona suprotnih (antiparalelnih) spinova.
Shematsko predstavqawe orbitala i elektrona. – Orbitala se shematski prikazuje kvadratiãem , elektron strelicom ↑, a orijentacija spina elektrona – smerom strelice. Prema tome, orbitala koja sadrþi dva elektrona antiparalelnih spinova shematski se prikazuje ovako: ↑↓
Da bi se naglasilo o kojoj orbitali je reå, ispod kvadratiãa se stavqa simbol orbitale.
Na primer: ↑↓ . 1s
Maksimalno moguã broj orbitala na energetskim podnivoima je sledeãi: s-podnivoi sadrþe po jednu s-orbitalu, p-podnivoi sadrþe po tri p-orbitale, d-podnivoi sadrþe po pet d-orbitala, itd. (slika 7).
Slika 7. Shematski prikaz rasporeda orbitala na energetskim podnivoima prva tri energetska nivoa
Redosled popuwavawa orbitala. – Danas je poznata graða elektronskih omotaåa atoma svih poznatih hemijskih elemenata. U skladu sa principom minimuma energije, elektroni u atomu najpre popuwavaju orbitale najniþe energije, pa tek onda one sa višom energijom. Prema tome, u atomima sa više elektrona orbitale se popuwavaju po redosledu koji odgovara porastu wihove energije i to:
1s→2s→2p→3s→3p→4s→3d→4p→5s→4d→5p→6s→4f итд.
Treba naglasiti da, zbog malih razlika u energiji orbitala na višim energetskim nivoima, kod atoma nekih elemenata dolazi do odstupawa od navedenog redosleda popuwavawa orbitala. Tako, npr., u atomu bakra (Z = 29) 4s-orbitala nije popuwena, veã sadrþi samo jedan elektron, dok je svih pet 3d-orbitala popuweno sa ukupno deset elektrona.
Hundovo pravilo. – Orbitale na istom energetskom podnivou prvo se popuwavaju sa po jednim elektronom, pa tek onda dolazi do „sparivawa“ elektrona u orbitalama.
Prikazati shematski graðu elektronskog omotaåa atoma azota. U tablici periodnog sistema nalazimo da je atomski broj azota Z = 7. Znaåi da atom azota sadrþi u jezgru 7 protona, a u omotaåu 7 elektrona.
Utvrdimo najpre raspored elektrona po energetskim nivoima u atomu azota. Primenom izraza (8) dobijamo da je maksimalan broj elektrona na prvom energetskom nivou:
N = 2 12 = 2 elektrona,
a na drugom energetskom nivou:
N = 2 22 = 8 elektrona.
Prema tome, prvi energetski nivo u atomu azota je popuwen sa maksimalnim brojem od 2 elektrona, dok se preostalih 5 elektrona nalazi na drugom energetskom nivou:
nivo
= 1)
Prema Paulijevom principu zabrane, u svaku orbitalu moþe se smestiti najviše dva elektrona antiparalelnih spinova. Znaåi da se 7 elektrona u atomu azota mogu rasporediti u orbitale na sledeãi naåin:
Meðutim, ovakav raspored elektrona u orbitalama nije u skladu sa Hundovim pravilom, stoga ãemo u svaku p-orbitalu smestiti po jedan elektron:
Dokazano je da ovakav raspored elektrona u orbitalama atoma azota odgovara stvarnosti.
Elektronske konfiguracije. – Graða elektronskih omotaåa atoma saþeto se prikazuje tako što se napišu jedan pored drugog simboli onih orbitala u atomu koje sadrþe elektrone, i to po redosledu wihovih rastuãih energija. Broj elektrona u orbitalama oznaåava se kao desni gorwi indeks. Dobijeni izraz naziva se elektronska konfiguracija atoma datog elementa.
Пример 13
Napisati elektronsku konfiguraciju atoma azota. Iz shematskog prikaza graðe elektronskog omotaåa atoma azota (primer 12) sledi da je elektronska konfiguracija ovog atoma 1s22s22p3. Navedeni izraz åita se: jedan es dva, dva es dva, dva pe tri.
Hemijski elementi su u periodnom sistemu poreðani po rastuãim atomskim brojevima. Periodni sistem sastoji se od 7 horizontalnih redova elemenata (perioda) i 8 vertikalnih kolona (grupa)
Periode. – Na poåetku svake periode nalaze se alkalni metali, åiji atomi u najvišem energetskom nivou sadrþe po jedan elektron u s-orbitali. Porastom atomskih brojeva elemenata, odnosno broja elektrona u najvišem energetskom nivou, smawuje se metalni, a raste nemetalni karakter elemenata. Pri kraju perioda nalaze se najizrazitiji nemetali (halogeni elementi). Prvih šest perioda završava se plemenitim (inertnim) gasom.
Svaka naredna perioda poåiwe elementom åiji atom ima jedan elektron na novom, višem energetskom nivou. Prema tome, atomi elemenata iste periode imaju isti broj energetskih nivoa, jednak broju periode. U skladu sa principom minimuma energije, kod atoma elemenata iste periode elektronima se popuwavaju sledeãi energetski podnivoi:
Периода 123 4 567 Енергетски поднивои 1s2s2p3s3p4s3d4p5s4d5p6s4f5d6p7s5f6d
Grupe. – Elementi koji se nalaze u istoj grupi periodnog sistema imaju u najvišem energetskom nivou jednak broj elektrona. Ti elektroni odreðuju valencu elemenata i nazivaju se valentni elektroni. U veãini sluåajeva broj valentnih elektrona odgovara broju grupe. Pošto hemijska svojstva elemenata uglavnom zavise od broja valentnih elektrona, elementi koji se nalaze u istoj grupi periodnog sistema imaju sliåna hemijska svojstva.
Пример 14
Atomi jednog hemijskog elementa imaju sledeãu elektronsku konfiguraciju: 1s22s22p63s23p64s2. Odrediti atomski broj elemenata i wegov poloþaj u periodnom sistemu.
Atomski broj elemenata odgovara broju protona u jezgru, odnosno broju elektrona u omotaåu. Kako dati element sadrþi u omotaåu 20 elektrona, atomski broj mu je 20.
Iz navedene elektronske konfiguracije sledi da atomi nepoznatog elementa popuwavaju elektronima åetvrti energetski nivo; znaåi da se element nalazi u åetvrtoj periodi.
Slika 9. Poloþaj s, p, d i f-elemenata u periodnom sistemu
Atomi datog elementa sadrþe u najvišem energetskom nivou dva elektrona u 4 s-orbitali. Prema tome, element se nalazi u drugoj grupi periodnog sistema.
Odgovor: Nepoznati element ima atomski broj 20, a nalazi se u åetvrtoj periodi i drugoj grupi periodnog sistema. Iz tablice periodnog sistema saznajemo da se radi o elementu kalcijumu.
Da bi se istakle razlike izmeðu elemenata iste grupe periodnog sistema, svaka od osam grupa podeqena je na dve podgrupe (ili ogranka) – A i B, u kojima se nalaze hemijski srodni elementi. Kod elemenata ¡A i ¡¡A grupe elektronima se popuwavaju s-orbitale u najvišem energetskom nivou, stoga se ti elementi nazivaju s-elementi.
Kod elemenata od ¡¡¡A do nulte grupe elektronima se popuwavaju p-orbitale u najvišem energetskom nivou, pa se ti elementi zovu p-elementi.
Za elemente u grupama od ¡¡¡B-¢¡¡¡ (ukquåujuãi i grupe ¡B i ¡¡B) karakteristiåno je popuwavawe (n-1) d-orbitala. To su orbitale koje se nalaze na jednom energetskom nivou niþe nego s i p-orbitale. Ti elementi nazivaju se d-elementi.
Lantanoidi i aktinoidi spadaju u f-elemente, pošto je za wih karakteristiåno popuwavawe 4f, odnosno 5f-orbitala.
Od periodiåno promenqivih svojstava hemijskih elemenata razmotriãemo energiju jonizacije i afinitet prema elektronu.
Energija jonizacije je ona energija koja je potrebna za udaqavawe elektrona iz najvišeg energetskog nivoa slobodnog atoma u gasovitom stawu. Proces jonizacije atoma nekog hemijskog elementa (X) moþe se prikazati na sledeãi naåin:
X(g) Ei X+(g) + e
Kod atoma sa više elektrona poznato je više energija jonizacije: prva (Ei,1) druga (Ei,2), treãa (Ei,3) itd. One odgovaraju udaqavawu prvog, drugog, treãeg, kao i narednih elektrona. Ukoliko nije posebno naglašeno, u daqem tekstu se pod pojmom „energije jonizacije“ podrazumevaju prve energije jonizacije.
Najmawe energije jonizacije imaju elementi na poåetku perioda –alkalni metali. Porastom atomskih brojeva elemenata, wihove energije jonizacije postepeno rastu (mada ne sasvim pravilno), do najveãe vrednosti koja odgovara plemenitom gasu.
Tablica 10. Energije jonizacije elemenata druge periode
Tablica 11. Energije jonizacije elemenata ¡A grupe
Energije jonizacije elemenata u grupama pravilno opadaju sa porastom wihovih atomskih brojeva.
Пример 15
Izraåunati molarnu energiju jonizacije (Ei, m) berilijuma. U tablici 10 nalazimo da je energija jonizacije berilijuma Ei = 1,49 aJ. Molarnu energiju jonizacije berilijuma dobiãemo mnoþewem Ei ovog elementa Avogadrovom konstantom:
Ei, m = Ei ⋅ NA = 1,49 aJ × 6,02 ⋅ 1023 mol–1 = 8,97 ⋅ 1023 aJ/mol.
Kako je 1 aJ = 10–18 J = 10–21 kJ,
Ei, m = 8,97 ⋅ 1023 × 10–21 kJ/mol = 8,97 ⋅ 102 kJ/mol = 897 kJ/mol
Odgovor: Molarna energija jonizacije berilijuma iznosi 897 kJ/mol
Energija koja se oslobaða pri vezivawu elektrona za neutralni atom u gasovitom stawu naziva se afinitet prema elektronu. Opisani proces moþe se prikazati sledeãom jednaåinom:
X(g) + e → X–(g) + Ea
Afinitet prema elektronu elemenata u periodama raste sa porastom wihovih atomskih brojeva
U grupama najveãi afinitet prema elektronu najåešãe ima element koji se nalazi na poåetku grupe. Sa porastom atomskih brojeva elemenata, wihov afinitet prema elektronu se smawuje.
Halogeni elementi imaju najveãi afinitet prema elektronu (tablica 12). Atomima tih elemenata nedostaje samo jedan elektron do stabilne elektronske konfiguracije najbliþeg plemenitog gasa, i zato oni lako vezuju elektrone.
Tablica 12. Afinitet prema elektronu elemenata ¢¡¡A grupe
Задаци
19. Atom bakra mo`e se predstaviti u obliku kuglice pre~nika 2,6 10–8 cm. Koliko je puta pre~nik modela tog atoma, jednak 5,2 cm, ve}i od pre~nika atoma bakra?
20. Borov polupre~nik atoma vodonika iznosi 53 pm, a polupre~nik loptice za stoni tenis 1,8 cm. Izra~unajte koliko puta je ve}i polupre~nik loptice za stoni tenis od Borovog polupre~nika atoma vodonika.
21. Po lupre~nik atoma aluminijuma je 0,143 nm. Izra~unajte koliko se atoma aluminijuma mo`e pore|ati, jedan pored drugog, na du`ini od 1,923 cm
22. Polupre~nik atoma gvo`|a je 1,26 10–8 cm. Izra~unajte zapreminu ovog atoma i izrazite je u kubnim centimetrima. Za izra~unavawe koristite formulu: V(lopte) = 4r3π/3
23. Izra~unajte mase atoma slede}ih mononuklidnih elemenata (tj. elemenata koji se javqaju u obliku jednog stabilnog izotopa): a) fluora, b) fosfora, v) joda.
Dobijeni rezultat izrazite u gramima.
24. Relativna atomska masa kadmijuma je 112,4. Kolika je masa jednog atoma kadmijuma izra`ena u gramima?
25. Izra~unajte prose~nu masu atoma olova. Dobijeni rezultat izrazite u miligramima.
26. Na osnovu podataka navedenih u tablici 9 izra~unajte prose~ne relativne atomske mase slede}ih elemenata: a) azota, b) kiseonika, v) `ive.
27. Na osnovu vrednosti relativnih atomskih masa navedenih u tablici periodnog sistema, izra~unajte mase atoma slede}ih elemenata: a) joda, b) srebra, v) silicijuma.
Dobijene vrednosti izrazite u kilogramima.
28. Napi{ite simbol jednog od izotopa kalaja koji u jezgru sadr`i 50 protona i 71 neutron.
29. Napi{ite simbole slede}ih izotopa: a) magnezijuma – 24, b) kalcijuma – 40, v) gvo`|a – 56.
30. Napi{ite simbole tri izotopa kiseonika (Z = 8), koji u jezgru sadr`e 8, 9 i 10 neutrona.
31. Kako se tuma~i ~iwenica da su atomi elektri~no neutralni i pored toga {to sadr`e naelektrisane ~estice?
32. Koliko se neutrona nalazi u jezgrima atoma slede}ih izotopa:
33. Odredite broj protona i neutrona u jezgrima atoma slede}ih izotopa:
34. Koriste}i tablicu periodnog sistema dopunite slede}u tablicu podacima koji nedostaju:
35. Litijum se u prirodi nalazi u obliku dva izotopa: 6Li i 7Li. Koli~inski udeo 6Li u prirodnoj sme{i je 6 %, a 7Li 94 %. Izra~unajte relativnu atomsku masu litijuma.
36. Elementarni bor se sastoji od izotopa 10V i 11V, ~iji je koli~inski udeo 18,83 % odnosno 81,17 %. Izra~unajte relativnu atomsku masu bora.
37. Bakar je sme{a dva izotopa – 63Cu i 65Cu. Koli~inski udeo atoma 63Cu u prirodnoj sme{i je 69,17 %, a 65Cu 30,83 %. Izra~unajte relativnu atomsku masu bakra.
38. Stawa atoma vodonika opisana su slede}im vrednostima glavnog kvantnog broja: n = 2, n = 4, n = 1, n = 3, n = 5. Kojoj vrednosti n odgovara: a) najmawa energija elektrona, b) najve}a energija elektrona?
39. Stawe atoma opisano je vredno{}u glavnog kvantnog broja n = 4. Odredite: a) mogu}e vrednosti sporednog kvantnog broja, b) broj energetskih podnivoa.
40. I zra~unajte maksimalan broj elektrona na slede}im energetskim nivoima:
a) drugom, b) tre}em, v) ~etvrtom.
41. Od koliko se energetskih podnivoa sastoji tre}i energetski nivo? Kojim se vrednostima sporednog kvantnog broja karakteri{u ti podnivoi?
42. Napi{ite simbole orbitala koje se karakteri{u slede}im vrednostima glavnog i sporednog kvantnog broja:
a) n = 2, l = 1, g) n = 4, l = 3,
b) n = 1, l = 0, d) n = 3, l = 1. v) n = 3, l = 2,
43. Po ~emu su sli~ne, a po ~emu se razlikuju 1s, 2s i 3s-orbitale?
44. Date su slede}e orbitale: 2p, 4s, 3d, 2s, 3s, 4p, 3p. Razvrstajte u grupe orbitale koje se nalaze na istom energetskom nivou.
45. Koliki je ukupan broj orbitala na ~etvrtom energetskom nivou?
46. Utvrdite na kom se energetskom nivou i podnivou nalaze slede}e orbitale:
a) 3d, b) 2s, v) 4f
47. Koja se orbitala pre popuwava elektronima:
a) 3p ili 4s, b) 4d ili 5s, v) 5d ili 4f?
48. Odredite vrednosti glavnog i sporednog kvantnog broja za slede}e orbitale:
a) 3d, b) 1s, v) 4f, g) 3p, d) 2s.
49. Odredite vrednosti glavnog, sporednog i magnetnog kvantnog broja za 3p-orbitale.
50. Odredite dozvoqene vrednosti magnetnog kvantnog broja za l = 3.
51. Dopunite slede}u tablicu podacima koji nedostaju:
n l Tipovi orbitala
Broj orbitala na energetskom podnivou
Ukupan broj orbitala na energetskom nivou
Ukupan broj elektrona na energetskom nivou 1 2 3
52. Prika`ite shematski (pomo}u kvadrati}a i strelica) raspored 5 elektrona u orbitalama na drugom energetskom nivou.
53. Prika`ite shematski raspored 6 elektrona u 3d-orbitalama.
54. Prika`ite shematski gra|u elektronskog omota~a atoma slede}ih elemenata: a) berilijuma, b) ugqenika, v) kiseonika.
55. Atom jednog hemijskog elementa ima slede}u gra|u elektronskog omota~a:
Napi{ite elektronsku konfiguraciju atoma tog elementa.
56. Napi{ite elektronske konfiguracije atoma slede}ih elemenata: a) bora, b) kalcijuma, v) broma.
57. Napi{ite elektronske konfiguracije atoma slede}ih elemenata i wihovih jona: a) kalijuma i jona K+, b) kiseonika i jona O2–, v) aluminijuma i jona Al3+
58. Odredite atomske brojeve elemenata ~iji atomi imaju slede}e elektronske konfiguracije:
a) 1s22s22p5, b) 1s22s22p63s1, v) 1s22s22p63s23p64s23d104p6
59. Napi{ite elektronske konfiguracije atoma fosfora i arsena, i odgovorite za{to se ovi elementi nalaze u istoj grupi periodnog sistema.
60. Napi{ite elektronsku konfiguraciju najvi{eg energetskog nivoa slede}ih atoma: a) kiseonika, b) ugqenika.
61. Koliko elektrona u najvi{em energetskom nivou sadr`e atomi fluora, hlora, broma, joda i astata? Kako su ti elektroni raspore|eni po energetskim podnivoima?
62. Razmotrite elektronsku konfiguraciju 1s22s22p53s1, i utvrdite koji iskaz nije ta~an:
a) Atomski broj elementa je 10. b) Navedena elektronska konfiguracija ne odgovara najstabilnijem stawu atoma.
v) Pri prelasku u stawe 1s22s22p6 atom vezuje energiju. g) 1s i 2s-orbitale su popuwene.
63. Utvrdite koji je od navedenih iskaza ta~an. Horizontalni redovi u periodnom sistemu sadr`e elemente:
a) koji imaju sli~na hemijska svojstva, b) koji pripadaju istoj periodi, v) ~iji atomi imaju istu elektronsku konfiguraciju najvi{eg energetskog nivoa.
64. Utvrdite koji elementi imaju slede}e elektronske konfiguracije najvi{eg energetskog podnivoa:
a) 2s1 , b) 3p4 ,
v) 3s2 , g) 3p6,
d) 1s2
65. Utvrdite u kojim se periodama nalaze elementi ~iji atomi imaju slede}e elektronske konfiguracije:
a) 1s22s22p3,
b) 1s22s22p63s23p1,
v) 1s22s22p63s23p3,
g) 1s22s22p63s23p64s23d104p4,
d) 1s22s2
66. Napi{ite elektronske konfiguracije atoma 9 4 Be, 24 12 Mg i 40 20 Ca i, na osnovu broja elektrona u najvi{em energetskom nivou, odredite u kojoj se grupi periodnog sistema ti elementi nalaze.
67. Utvrdite u kojim se grupama periodnog sistema nalaze elementi ~iji atomi imaju slede}e elektronske konfiguracije:
a) 1s1 ,
b) 1s22s22p2,
v) 1s22s22p6,
g) 1s22s22p63s23p4 ,
d) 1s22s22p4 ,
|) 1s22s22p63s23p64s23d104p5
68. Atomi jednog hemijskog elementa imaju slede}u elektronsku konfiguraciju: 1s22s22p63s23p3. Utvrdite:
a) atomski broj elementa,
b) periodu i grupu u kojoj se on nalazi, v) broj valentnih elektrona u atomu tog elementa, g) broj nesparenih elektrona u atomu tog elementa.
72. Утврдите
73.
75. На основу
76.


KOVALENTNA VEZA
Kovalentna veza se obiåno uspostavqa izmeðu atoma nemetala (istih ili razliåitih), koji se po svojim svojstvima (energiji jonizacije i afinitetu prema elektronu) ne razlikuju toliko da bi se vezali jonskom vezom.
Prvu savremenu teoriju kovalentne veze dao je G. W. Luis. Prema wegovoj oktetnoj teoriji valence, kovalentna veza nastaje kao rezultat teþwe atoma da postignu stabilnu elektronsku konfiguraciju najbliþeg plemenitog gasa. Do uspostavqawa takvih konfiguracija dolazi stvarawem zajedniåkih elektronskih parova. Svaki od vezanih atoma daje po jedan valentni elektron za obrazovawe zajedniåkog elektronskog para. Pri vezivawu atoma nastaju molekuli koji imaju niþu potencijalnu energiju od slobodnih atoma.
Пример 16
Prikazati pomoãu Luisovih simbola i formula nastajawe molekula HCl
Kod pisawa Luisovih struktura, valentni elektroni se prikazuju taåkicama oko simbola elemenata. Zajedniåki elektronski par koji povezuje atome predstavqa se parom taåkica izmeðu simbola. Dvostruka ili trostruka veza oznaåava se sa dva, odnosno tri para taåkica. U skladu sa navedenim pravilima za pisawe Luisovih struktura, nastajawe molekula HCl moþe se prikazati ovako:
H + Cl : → H : Cl : .. ..
Ako se u elektronskim formulama zajedniåki elektronski parovi prikaþu crticama, a izostave slobodni elektroni, dobijaju se strukturne formule.
Prema tome, strukturna formula hlorovodonika je H–Cl.
Kvantnomehaniåko tumaåewe kovalentne veze. – Postoje dve kvantnomehaniåke teorije (ili metode) kovalentne veze: teorija valentne veze i teorija molekulskih orbitala Teorija valentne veze – Prema ovoj teoriji, kovalentna veza izmeðu dva atoma nastaje prekrivawem onih orbitala iz najvišeg energetskog nivoa atoma koje sadrþe po jedan elektron suprotnih (antiparalelnih) spinova. Do uspostavqawa stabilne kovalentne veze izmeðu dva atoma dolazi pri odreðenom ravnoteþnom rastojawu izmeðu jezgara, kada je potencijalna energija sistema najmawa. Tako npr., ravnoteþno rastojawe izmeðu jezgara atoma vodonika u molekulu H2 iznosi 74 pm. Daqim pribliþavawem jezgara, energija sistema naglo raste usled pojaåanog odbijawa dva jezgra, kao i dva elektrona.
Pri prekrivawu atomskih orbitala uzduþ ose koja povezuje atomska jezgra, nastaje σ(sigma)-veza. Ova veza nastaje prekrivawem sledeãih atomskih orbitala: s i s, s i pz, pz i pz.
Prikazati shematski obrazovawe molekula HCl prekrivawem odgovarajuãih atomskih orbitala vodonika i hlora. Atom vodonika sadrþi jedan nespareni elektron u 1s-orbitali koja ima oblik lopte.
Elektronska konfiguracija atoma hlora u osnovnom stawu je 1s22s22p63s23p5. Prikaþimo pomoãu kvadratiãa i strelica graðu najvišeg energetskog nivoa atoma tog elementa:
Kao što vidimo, atom hlora ima jedan nespareni elektron u 3p-orbitali. Prema teoriji valentne veze, u formirawu kovalentne veze uåestvuju samo nespareni elektroni iz najvišeg energetskog nivoa atoma. Stoga pri shematskom prikazivawu obrazovawa molekula HCl neãemo crtati sve orbitale atoma hlora, veã samo polupopuwenu 3pz-orbitalu koja prekrivawem sa 1s-orbitalom atoma vodonika gradi kovalentnu vezu: 3s 3p
π (pi)-veza nastaje boånim prekrivawem polupopuwenih px ili py-orbitala. To je sekundarna veza koja nastaje tek posle povezivawa dva atoma primarnom, σ-vezom. S obzirom da je prekrivawe orbitala uzduþ ose koja povezuje atomska jezgra veãe od boånog prekrivawa orbitala, σ-veza je jaåa od π-veze.
Ako su dva atoma povezana dvostrukom ili trostrukom kovalentnom vezom, tada je samo jedna od tih veza σ-veza, dok su ostale π-veze.
Prikazati shematski obrazovawe molekula N2 prekrivawem odgovarajuãih orbitala dva atoma azota.
Iz elektronske konfiguracije atoma azota (1s22s22p3) se vidi da atom tog elementa sadrþi u najvišem energetskom nivou tri nesparena
elektrona u 2p-orbitalama. Kada se dva atoma azota dovoqno pribliþe jedan drugome, najpre se prekrivaju wihove 2pz-orbitale i grade σ-vezu. Zatim dolazi do boånog prekrivawa dve 2px i dve 2py-orbitale pri åemu nastaju dve dodatne π-veze koje se oznaåavaju sa π x i π y (na slici 11 prikazane su isprekidanim linijama).
Nepolarna i polarna kovalentna veza. – Ako su kovalentnom vezom povezana dva ista atoma, koji imaju isti afinitet prema elektronu, zajedniåki elektronski parovi ãe biti simetriåno raspodeqeni u prostoru izmeðu atomskih jezgara. Takva veza naziva se nepolarna kovalentna veza.
U sluåaju kada su kovalentnom vezom povezana dva razliåita atoma, zajedniåki elektronski parovi su pomereni ka atomu koji ima veãi afinitet prema elektronu. Usled toga dolazi do asimetriåne raspodele negativnog elektriciteta u prostoru, tj. stvara se elektriåni dipol. Takva veza naziva se polarna kovalentna veza, a molekul u kome se ona javqa – polarni ili dipolni molekul
Polarnost molekula eksperimentalno se odreðuje merewem wegovog dipolnog momenta (µ). Ova fiziåka veliåina definiše se na sledeãi
naåin:
µ = q l, (9)
gde je:
q – apsolutna vrednost naelektrisawa elektrona (1,6 10–19 C),
l – rastojawe izmeðu centara pozitivnog i negativnog naelektrisawa u dipolnom molekulu (tzv. duþina dipola).
SI – jedinica dipolnog momenta je kulonmetar (Cm).
Пример
Duþina dipola u molekulu HCl iznosi 0,215 . 10–8 cm. Izraåunati dipolni momenat ovog molekula.
q = 1,6 10–19 C
l = 0,215 10–8 cm = 0,215 10–10 m
µ = ?
Uvrštavawem odgovarajuãih brojåanih vrednosti u izraz (9) dobijamo:
µ = q l = 1,6 10–19 C × 0,215 10–10 m = 0,344 10–29 Cm = 3,44 10–30 Cm.
Odgovor: Dipolni momenat molekula HCl iznosi 3,44 10–30 kulonmetara.
Što je dipolni momenat molekula veãi, kovalentna veza u tom molekulu je polarnija i ima veãi udeo jonskog karaktera, kao i veãu energiju.
Tablica 13. Dipolni momenti molekula halogenovodonika
Mолекул
Диполни моменат, µ (Cm)
6,37 10–30
10–30
. 10–30
1,27 10–30
Višeatomni molekuli sa polarnim kovalentnim vezama mogu u celini biti nepolarni. Takav sluåaj javqa se kod molekula u kojima su elektronski oblaci veza simetriåno rasporeðeni u prostoru. Usled toga dipolni momenti veza se poništavaju unutar samog molekula, te je wegov dipolni momenat ravan nuli.
Dipolni momenat je vektorska veliåina, usmerena od pozitivnog kraja dipolnog molekula ka negativnom kraju. Zbirni dipolni momenat molekula jednak je vektorskom zbiru dipolnih momenata svake pojedine veze.
Molekuli tipa AB2, na primer, mogu biti linearni i savijeni (slika 12).
Ukoliko je molekul AB2 linearne graðe (slika 12a), dipolni momenti dveju veza A–B su suprotnog smera i meðusobno se poništavaju.
U sluåaju savijenog molekula (slika 12b), vektorski zbir dipolnih momenata dveju veza A–B je razliåit od nule, stoga takav molekul poseduje odreðeni dipolni momenat.
Postojawe ili odsustvo dipolnog momenta molekula moþe da posluþi kao jedan od pokazateqa wihove geometrijske strukture.
Elektronegativnost (χ)* je empirijska veliåina koja sluþi za procenu sposobnosti atoma da u molekulu privlaåi zajedniåke elektronske parove sa drugim atomima. Što je elektronegativnost nekog hemijskog elementa veãa, wegovi atomi jaåe privlaåe elektrone. Drugim reåima, u molekulima izgraðenim od razliåitih atoma, zajedniåki elektronski parovi ãe biti pomereni ka atomu najveãe elektronegativnosti.
Elektronegativnost elemenata brojåano se izraþava pomoãu koeficijenta wihove relativne elektronegativnosti. Najåešãe se koristi Polingova skala relativnih elektronegativnosti elemenata, prikazana u tablici 14.
Tablica 14. Polingova skala relativnih elektronegativnosti elemenata
Razlika u relativnoj elektronegativnosti vezanih atoma (∆χ) uzima se kao kriterijum za procenu karaktera veze: ukoliko je ta razlika veãa, kovalentna veza u molekulu imaãe izraþeniji jonski karakter i biãe jaåa.
Ako je razlika u relativnoj elektronegativnosti vezanih atoma veãa od 1,7, jediwewe ima preteþno jonski karakter. Ukoliko je ta razlika mawa od 1,7, jediwewe ima preteþno kovalentni karakter.
Na slici 13 grafiåki je prikazana zavisnost stepena jonskog karaktera veze (izraþene u procentima) od razlika relativnih elektronegativnosti vezanih atoma (∆χ).
Пример 20
Odrediti karakter veze u molekulu HCl. U tablici 14 nalazimo da je χ (H) = 2,1, χ (Cl) = 3,0. Razlika u relativnoj elektronegativnosti hlora i vodonika
∆χ = 3,0 – 2,1 = 0,9.
Na grafikonu prikazanom na slici 13 oåitamo da toj razlici odgovara oko 18 % jonskog karaktera veze.
Odgovor: Veza izmeðu vodonika i hlora u molekulu HCl je kovalentna veza sa 18 % jonskog karaktera, tj. spada u polarnu kovalentnu vezu.
Duþina kovalentne veze je rastojawe izmeðu jezgara atoma vezanih kovalentnom vezom. To rastojawe moþe se izraåunati sabirawem kovalentnih polupreånika vezanih atoma. Izraåunate duþine veza u molekulima nepolarnih elementarnih supstanci (npr. Cl2 i F2) slaþu se sa eksperimentalno dobijenim vrednostima. To je i razumqivo, pošto se kovalentni polupreånik atoma nemetala definiše kao polovina
rastojawa izmeðu centara vezanih atoma u molekulima elementarnih supstanci (tj. kao polovina duþine kovalentne veze).
Kod molekula izgraðenih od razliåitih atoma, eksperimentalno odreðene duþine veza su obiåno mawe od izraåunatih. To se tumaåi polarizacijom kovalentnih veza, te one u odreðenoj meri dobijaju jonski karakter (postaju kraãe i åvršãe).
Eksperimentalno odreðene duþine veza su utoliko mawe od izraåunatih ukoliko je razlika u elektronegativnosti vezanih atoma veãa.
Izraåunati duþine kovalentnih veza (lkov) u molekulima F2 i HF. Kovalentni polupreånik atoma fluora je rkov(F) = 64 pm, a atoma vodonika rkov(H) = 37 pm.
Uporediti izraåunate duþine veza sa eksperimentalno dobijenim vrednostima: 128 pm za vezu F–F, odnosno 92 pm za vezu H–F
lkov(F–F) = 2 rkov(F) = 2 64 pm = 128 pm
lkov(H–F) = rkov(H) + rkov(F) = 37 pm + 64 pm = 101 pm
Odgovor: Izraåunata duþina F–F veze slaþe se sa eksperimentalno dobijenom vrednošãu. Izraåunata duþina H–F veze je za 9 pm veãa od eksperimentalno dobijene vrednosti.
Energija veze – Energija veze je merilo jaåine kovalentne veze. To je energija potrebna za raskidawe odreðene vrste veze u molekulu koji se nalazi u gasovitom stawu. Obiåno se pod energijom veze podrazumeva molarna energija veze, koja se odnosi na 6,02 . 1023 veza. Dobija se mnoþewem energije jedne veze Avogadrovom konstantom. Izraþava se u kJ/mol. Energija veze u molekulu izgraðenom od dva razliåita atoma moþe se izraåunati sabirawem doprinosa energiji veze svakog od vezanih atoma .
Пример 22
Izraåunati energiju H–F veze, ako je energija H–H veze 436 kJ/mol, a F–F veze 153 kJ/mol. Uporediti izraåunatu energiju veze sa eksperimentalno dobijenom vrednošãu (565 kJ/mol).
Energija H–F veze izraåunava se tako što se uzima da energiji ove veze atom vodonika doprinosi sa polovinom energije H–H veze, a atom fluora sa polovinom energije F–F veze:
436 kJ/mol–1 + 153 kJ/mol–1 EH–F = = 294,5 kJ/mol. 2
Odgovor: Eksperimentalno odreðena energija H–F veze (565 kJ/mol) je za 270,5 kJ/mol veãa od izraåunate vrednosti. To se tumaåi polarizacijom ove veze, što doprinosi poveãawu wene jaåine.
lkov – duþina kovalentne veze rkov – kovalentni polupreånik atoma je lkov
Slika 14.
Pored polarizacije, na energiju kovalentne veze utiåu i drugi faktori, kao na primer, stepen prekrivawa atomskih orbitala (najveãi je pri obrazovawu σ-veze, stoga je ona i najåvršãa). Energija veze zavisi i od toga da li je veza jednostruka, dvostruka ili trostruka. Tako je, na primer, energija C–C veze 333,8 kJ/mol, energija C=C veze 615 kJ/mol, a C≡C veze 841 kJ/mol
Hibridizacija orbitala. – Eksperimentalno je utvrðeno da se u mnogim sluåajevima uglovi izmeðu veza razlikuju od uglova koje predviða teorija valentne veze. Za tumaåewe mehanizma obrazovawa kovalentnih molekula, kao i wihove geometrijske strukture, tj. usmerenosti valentnih veza u prostoru, koriste se predstave o mešawu ili hibridizaciji orbitala centralnog atoma. Smatra se, naime, da tokom obrazovawa hemijske veze dolazi do mešawa atomskih orbitala koje se ne razlikuju mnogo po svojoj energiji. Tako mešawem jedne s i jedne p-orbitale istog atoma nastaju dve energetski ekvivalentne sp-hibridne orbitale, koje meðu sobom zaklapaju ugao od 180° (slika 15).
Od p-orbitala duþe su sp-hibridne orbitale i boqe se prekrivaju sa drugim orbitalama, gradeãi jaåe veze.
Pored sp-hibridnih orbitala, poznate su i druge hibridne orbitale, nastale mešawem razliåitog broja s, p ili d-atomskih orbitala. Upoznajmo se pobliþe sa sp2 i sp3-hibridnim orbitalama.
Mešawem jedne s i dve p-orbitale iz istog energetskog nivoa atoma nastaju sp2-hibridne orbitale. Leþe u jednoj ravni, a meðu sobom zaklapaju ugao od 120° .
Mešawem jedne s i tri p-orbitale iz istog energetskog nivoa atoma nastaju sp3-hibridne orbitale. Po obliku su sliåne sp i sp2-hibridnim orbitalama. Usmerene su prema rogqevima pravilnog tetraedra, zaklapajuãi meðu sobom ugao od 109,5°
Treba naglasiti da hibridne orbitale nisu eksperimentalno otkrivene u slobodnim atomima. To je i razumqivo, s obzirom na to da je hibridizacija atomskih orbitala u suštini matematiåki proces, kojim se uspešno tumaåi geometrijska struktura molekula i karakteristike hemijske veze.
Пример 23
Eksperimentalno je utvrðeno da su u molekulu bor(¡¡¡)-fluorida, BF3, sve tri B–F veze energetski ekvivalentne, da leþe u istoj ravni, a meðu sobom zaklapaju ugao od 120°. Objasniti geometrijsku strukturu molekula BF3. Elektronska konfiguracija atoma bora u osnovnom stawu je 1s22s22p1. To znaåi da atom ovog elementa sadrþi samo jedan nespareni elektron u 2p-orbitali. Kako je bor u jediwewu BF3 trovalentan pošto vezuje tri atoma fluora, pretpostavqa se da u procesu formirawa hemijske veze dolazi do prelaska jednog elektrona iz popuwene 2s-orbitale atoma bora u praznu 2p-orbitalu: energija
Prekrivawem 2s i 2p-orbitala pobuðenog atoma bora sa polupopuwenim 2p-orbitalama tri atoma fluora mogle bi se formirati tri σ-veze. Meðutim, one bi se razlikovale po svojoj energiji, i ne bi zaklapale ugao od 120°.
Ekvivalentnost triju σ-veza u molekulu BF3, kao i utvrðeni ugao od 120°, tumaåe se mešawem jedne 2s i dve 2p-orbitale pobuðenog atoma bora. Pri tome nastaju tri energetski ekvivalentne sp2-hibridne orbitale (slika 16). Te orbitale prekrivawem sa polupopuwenim 2p-orbitalama tri atoma fluora grade planarni molekul BF3.
Teorija molekulskih orbitala (MO) moþe da predvidi i protumaåi strukturu i svojstva niza molekula i jona, izgraðenih od istih ili razliåitih atoma. Najveãi uspeh teorija MO je postigla u tumaåewu magnetnih svojstava molekula, energije veza i strukture nekih jona, åije se postojawe i svojstva ne mogu objasniti teorijom valentne veze.
Prema teoriji MO, pri obrazovawu molekula dolazi do linearne kombinacije atomskih orbitala (AO) reagujuãih atoma. To je u suštini matematiåki postupak, koji se sastoji u sabirawu i oduzimawu talasnih funkcija (tj. atomskih orbitala). Pri tome nastaju MO koje popuwavaju elektroni iz jednog i drugog atoma. Tako, npr., pri obrazovawu molekula H2 dolazi do kombinacije dve AO dva atoma vodonika (tj. 1s-orbitala) i nastaju dve MO. Te orbitale se po svojoj energiji razlikuju od AO od kojih su nastale: jedna ima niþu energiju i naziva se vezujuãa MO, a druga višu energiju i naziva se razvezujuãa MO (slika 18).
U opštem sluåaju, iz n atomskih orbitala nastaje n molekulskih orbitala, koje se pri obrazovawu molekula popuwavaju elektronima na isti naåin kao i AO slobodnih atoma: po redosledu rastuãih energija, uz primenu Paulijevog principa zabrane i Hundovog pravila.
Stabilna hemijska veza izmeðu atoma obrazuje se u sluåaju kada je broj elektrona u vezujuãim MO veãi od broja elektrona u razvezujuãim
Slika 18.
MO. Naime, elektroni u razvezujuãim MO nalaze se u nestabilnom stawu visoke energije, i ne doprinose obrazovawu veze.
Kako svaku hemijsku vezu åini jedan elektronski par (tj. dva elektrona), broj veza izmeðu atoma (tzv. red veze) dobija se tako što se višak vezujuãih elektrona podeli sa 2:
N (vez. elektroni) – N (razv. elektroni) red veze = (10) 2
Prema teoriji MO, red veze ne mora uvek biti ceo broj. Što je red veze veãi, veza je åvršãa, tj. ima veãu energiju.
Elektroni na niþim, popuwenim energetskim nivoima atoma ne daju nikakav doprinos vezi izmeðu atoma. Ti elektroni nazivaju se nevezujuãi elektroni. Obrazovawu veze doprinose samo MO nastale iz AO valentnih elektrona.
Пример 24
Eksperimentalno je utvrðeno da su molekuli B 2 (otkriveni u parama bora na visokoj temperaturi) paramagnetiåni, što znaåi da sadrþe nesparene elektrone. Objasniti ovu åiwenicu sa stanovišta teorije MO.
Elektronska konfiguracija atoma bora je 1s22s22p1. Prikaþimo shematski raspored 10 elektrona dva atoma bora u MO molekula B2:
Kao što vidimo, molekul B2 sadrþi dva nesparena elektrona u dve π2p-orbitale. To uslovqava paramagnetiåna svojstva molekula B2 U vezujuãim MO molekula B2 nalazi se 6 elektrona, a u razvezujuãim 4 elektrona. Prema tome, 6 – 4 red veze = =1. 2
Odgovor: Molekul B2 sadrþi dva nesparena elektrona u π 2p-molekulskim orbitalama, stoga je paramagnetiåan. Red veze izmeðu dva atoma bora u molekulu B2 je 1.
Jonska veza se obrazuje izmeðu suprotno naelektrisanih jona, koji nastaju prelaskom valentnih elektrona sa atoma metala na atome nemetala. Pozitivni joni metala i negativni joni nemetala uzajamno se privlaåe jakim elektrostatiåkim silama (Kulonovim silama) i grade jonski par. Oko vezanih jona u svim pravcima deluju elektrostatiåke privlaåne sile, stoga jonska veza nije usmerena u prostoru. Zahvaqujuãi tome, svaki od vezanih jona moþe da privuåe odreðen broj jona suprotnog znaka. To znaåi da jonski parovi imaju izraþenu sposobnost asocijacije. Jonska jediwewa u åvrstom stawu grade jonske kristalne rešetke, u kojima je svaki jon okruþen odreðenim brojem jona suprotnog znaka.
U tim rešetkama ne postoje izolovani jonski molekuli, veã åitav kristal predstavqa „yinovski“ molekul izgraðen od ogromnog broja jona. Oksidacioni brojevi elemenata u jonskim jediwewima jednaki su naelektrisawu jona.
Zbog jakog elektrostatiåkog privlaåewa izmeðu jona u kristalnoj rešetki, jonska jediwewa se pri obiånim uslovima nalaze u åvrstom kristalnom stawu, i imaju visoke temperature topqewa i kquåawa (tablica 15).
Pošto joni u kristalnoj rešetki ne mogu slobodno da se kreãu, jonska jediwewa u åvrstom stawu ne provode elektriånu struju. Meðutim, wihovi vodeni rastvori i rastopi dobro provode struju.
Tipiåna jonska jediwewa grade elementi ¡A i ¡¡A grupe periodnog sistema (izraziti metali) pri reakciji sa elementima ¢¡A i ¢¡¡A grupe (izrazitim nemetalima).
Što je razlika u relativnoj elektronegativnosti vezanih atoma veãa, jediwewe ima izraþeniji jonski karakter.
Prikazati pomoãu Luisovih simbola i formula nastajawe natrijum-hlorida, reakcijom izmeðu natrijuma i hlora. Odrediti takoðe oksidacione brojeve natrijuma i hlora u natrijum-hloridu.
Atom natrijuma sadrþi u najvišem energetskom nivou jedan elektron u 3s-orbitali, a atom hlora sedam elektrona u 3s i 3p-orbitalama. Kada se atomi ovih elemenata naðu zajedno, u uslovima pogodnim za reakciju, dolazi do prelaska valentnog 3s-elektrona sa atoma natrijuma na atom hlora. Nastali joni Na+ i Cl– meðusobno se privlaåe i grade jonski par Na+Cl–: .. .. Na + Cl : → [Na]+ + [: Cl :]–
Pri asocijaciji jonskih parova Na+Cl– nastaju kristali kuhiwske soli. Kako su oksidacioni brojevi elemenata u jonskim jediwewima jednaki naelektrisawu jona, oksidacioni broj natrijuma u natrijum-hloridu je + 1, a hlora – 1.
VODONIÅNA VEZA
Vodoniåna veza se uspostavqa izmeðu molekula u kojima je atom vodonika vezan sa atomom velike elektronegativnosti (fluorom, kiseonikom ili azotom). Obrazovawe vodoniånih veza izmeðu molekula uslovqava wihovu asocijaciju (polimerizaciju). Vodoniåna veza javqa se i u kristalnim rešetkama åvrstih supstanci (npr. u kristalnoj rešetki leda).
Vodoniåna veza je znatno slabija od jonske i kovalentne veze – wena energija kreãe se od 8 do 40 kJ/mol. Ona uslovqava anomalno visoke temperature topqewa i kquåawa nekih jediwewa (npr. HF, H2O i NH3), pošto je za raskidawe vodoniånih veza potrebno utrošiti dodatnu energiju.
Задаци
83. Prika`ite pomo}u Luisovih simbola i formula nastajawe slede}ih kovalentnih supstanci:
a) molekula azota, N2, b) amonijaka, NH3, v) vode, H2O.
84. Na osnovu elektronskih formula molekulskih vrsta iz prethodnog zadatka, napi{ite wihove strukturne formule.
85. Napi{ite Luisovu strukturu molekula CO2
86. Napi{ite elektronske i strukturne formule molekula slede}ih supstanci:
a) fluorovodonika, HF, b) etana, C2H6, v) hidrazina, N2H4
87. Utvrdite koji sistem ima ni`u energiju:
a) dva slobodna atoma hlora, 2 Cl ili molekul hlora, Cl2, b) dva slobodna atoma neona, 2 Ne ili molekul neona, Ne2 Obrazlo`ite svoj odgovor.
88. Zaokru`ite parove orbitala koje prekrivawem formiraju δ-vezu izme|u dva atoma:
a) s–pz,
b) pz–pz, v) py–py, g) s–s, d) px–px
89. Prika`ite shematski obrazovawe molekula Cl2 prekrivawem odgovaraju}ih orbitala dva atoma hlora.
90. Prika`ite shematski obrazovawe molekula selen-vodonika, H2Se, prekrivawem odgovaraju}ih orbitala. Uzmite u obzir da je ugao izme|u σ-veza u tom molekulu jednak 90°
91. Prika`ite shematski obrazovawe molekula Cl2O prekrivawem odgovaraju}ih orbitala atoma hlora i kiseonika.
92. Napi{ite elektronske konfiguracije atoma sumpora, joda i broma i odgovorite koje orbitale u atomima tih elemenata u~estvuju u formirawu slede}ih molekula:
a) S2, b) HI, v) Br2
93. Du`ina dipola molekula fluorovodonika iznosi 4 10–11 m
Izra~unajte dipolni momenat ovog molekula.
94. Dipolni momenti molekula HCN i NH3 iznose 0,96 10–30 cm i 0,46 10–30 cm.
Izra~unajte du`inu dipola ovih molekula i izrazite je u metrima. U kom je molekulu veza polarnija?
95. Dipolni momenat molekula SO2 iznosi 5,3 10–30 Cm, a molekula SO2 je ravan nuli. Prika`ite shematski geometrijsku strukturu molekula SO2 i CO2.
96. Kako biste objasnili ~iwenicu da je dipolni momenat molekula CCl4 ravan nuli, mada se u wemu nalaze ~etiri polarne kovalentne veze?
97. Koji od navedenih molekula ima najve}i dipolni momenat: a) H2O, b) H2S, v) H2Se?
98. Kako biste na osnovu elektronegativnosti vezanih atoma objasnili smawewe dipolnog momenta molekula halogenovodonika idu}i od HF prema HI?
99. Kako biste objasnili ~iwenicu da, sa porastom atomskih brojeva, elektronegativnost elemenata u periodama raste, a u grupama opada?
100. Napi{ite elektronsku formulu molekula IBr i odgovorite na slede}a pitawa:
a) da li je veza izme|u atoma joda i broma polarna, b) ako jeste, prema kom atomu je pomeren zajedni~ki elektronski par?
101. Pore|ajte molekule HI, HF, BrCl, HCl и HBr prema porastu wihove polarnosti.
102. Na osnovu razlike u relativnoj elektronegativnosti kalijuma i sumpora, odredite procenat jonskog karaktera veze u jediwewu K2S
103. Odredite tip veze u slede}im molekulima:
a) CS2, b) HBr, v) Cl2
104. Napi{ite elektronsku i strukturnu formulu molekula hloroforma, CHCl3, i utvrdite koje su veze u ovom molekulu najpolarnije.
105. Izra~unajte razliku u elektronegativnosti atoma koji obrazuju veze H–O i O–X (gde je X=Cl, Br, I) u jediwewima tipa HOX, i utvrdite koja od veza ima u ve}oj meri izra`en jonski karakter.
106. Na osnovu razlike u elektronegativnosti vezanih atoma, pore|ajte navedena jediwewa prema porastu energije veze u wihovim molekulima:
a) LiCl (g), b) LiI (g), v) LiF (g), g) LiBr (g)
107. Izra~unajte du`inu kovalentnih C–H veza u molekulu metana, CH4, na osnovu slede}ih podataka: rkov (C) = 77 pm, rkov (H) = 37 pm
108. Na osnovu razlike u relativnoj elektronegativnosti vezanih atoma, predvidite kako se mewa du`ina kovalentnih veza u molekulima HF, HCl, HBr и HI
109. Energija H–Cl veze iznosi 4,43 eV. Izra~unajte molarnu energiju te veze i izrazite je u kJ/mol
110. Molarna energija disocijacije molekula azota na atome iznosi 946 kJ/mol
Izra~unajte sredwu energiju veze u tom molekulu. Da li su sve tri veze u molekulu azota energetski ekvivalentne? Ako nisu, koja je od wih ja~a?
111. Za raskidawe ~etiri C–H veze u molekulu metana treba utro{iti 1 665 kJ/mol. Izra~unajte sredwu molarnu energiju C–H veze.
112. Za postepeno otkidawe atoma vodonika u molekulu amonijaka, NH3, treba utro{iti 439 kJ/mol, 376,5 kJ/mol i 347 kJ/mol. Izra~unajte sredwu energiju N–H veze i izrazite je u kJ/mol
113. Na osnovu razlike u relativnoj elektronegativnosti vezanih atoma, predvidite kako }e se mewati energija veze u slede}em nizu jediwewa: Hl, HBr, HCl, HF
114. Koliki }e biti ugao izme|u veza u molekulu PH3 ako su sve r-orbitale u atomu fosfora nehibridizovane?
115. Da li u procesu formirawa molekula MgBr2 dolazi do hibridizacije orbitala u atomu magnezijuma, ako su obe Mg–Br veze energetski ekvivalentne i me|u sobom zaklapaju ugao od 180º?
116. Objasnite geometrijsku strukturu molekula berilijum-hidrida, koja se shematski mo`e prikazati ovako:
H Be H
117. Pomo}u kojih orbitala se uspostavqaju ~etiri δ-veze u molekulu SiCl4 koji ima oblik tetraedra?
118. Eksperimentalno je utvr|eno da su u molekulu metana, CH4, sve ~etiri C–H veze energetski ekvivalentne i me|u sobom zaklapaju ugao od 109,5º. Objasnite geometrijsku strukturu molekula metana.
119. Odredite broj nesparenih elektrona i red veze u molekulu O2.
120. Predvidite uz pomo} teorije MO elektronsku strukturu, red veze i broj nesparenih elektrona u molekulu azot(úú)-oksida, NO.
121. Procenite sa stanovi{ta teorije MO koji se od navedenih molekula karakteri{e ve}om energijom veze – molekul B2 ili C2
122. Jo{ krajem pro{log veka bilo je utvr|eno postojawe dosta stabilnog molekulskog jona vodonika H2+. Teorija valentne veze ne mo`e da objasni postojawe ovog jona, po{to vezu ~ini samo jedan elektron. Kako biste objasnili sa stanovi{ta teorije MO stabilnost ovog jona?
123. Za{to ne mo`e postojati stabilan molekul He2?
124. Napi{ite elektronske konfiguracije atoma litijuma i fluora, i objasnite na koji na~in ti atomi mogu posti}i stabilnije stawe ni`e energije.
125. Za{to se jonska jediwewa pri obi~nim uslovima nalaze u obliku jonskih kristala a ne izolovanih molekula?
126. Atom cezijuma ima jedan elektron u najvi{em energetskom nivou, a atom selena {est. Napi{ite formulu cezijum-selenida. Koji tip veze se uspostavqa izme|u cezijuma i selena?
127. Prika`ite pomo}u Luisovih simbola i formula obrazovawe slede}ih jonskih jediwewa:
a) Na2S, b) AlF3, v) KI.
128. Odredite oksidacione brojeve elemenata u slede}im jonskim jediwewima:
a) AlCl3, b) Na2O, v) LiBr, g) CaF2, d) MgO.
129. Napi{ite formule jonskih jediwewa koja grade slede}i parovi elemenata:
a) Sr и Cl, b) Rb и S, v) Ca и N, g) Al и O
130. Koja su od navedenih svojstava karakteristi~na za jonska jediwewa: a) niska temperatura topqewa i kqu~awa, b) u kristalnom stawu dobro provode elektri~nu struju, v) u vodenim rastvorima sadr`e suprotno naelektrisane jone, g) u rastopqenom stawu dobro provode elektri~nu struju, d) u vodenim rastvorima sadr`e molekule?
131. Utvrdite koji od navedenih parova hemijskih elemenata ne grade jonska jediwewa:
a) O и H,
b) Ca и O,
v) Ba и I,
g) C и Cl,
d) Li и Cl
132. Utvrdite koji od navedenih iskaza nisu ta~ni:
a) Dvostruka veza se sastoji od dva elektronska para.
b) Za raskidawe hemijske veze tro{i se energija.
v) Izolovani atomi imaju mawu energiju od atoma vezanih u molekul.
g) Trostruku vezu ~ine tri elektrona.
d) Pri obrazovawu jona uspostavqaju se stabilne elektronske konfiguracije plemenitog gasa.
133. Izaberite iz slede}e grupe elemenata: F, H, Cl, Mg, K, odgovaraju}e parove elemenata i napi{ite formule nastalih jediwewa u kojima }e veza biti:
a) jonska, b) polarna kovalentna, v) nepolarna kovalentna.
Kod re{avawa zadatka koristite tablicu relativnih elektronegativnosti elemenata.
134. Izme|u kojih se od navedenih molekula mogu obrazovati vodoni~ne veze: a) HCOOH, б) HF, в) H2Te, г) NH3, д) PH3?
135. Kako biste objasnili ~iwenicu da sumpor-vodonik, H2S – jediwewe istog tipa kao i voda, kqu~a na – 60 ºC, dok voda kqu~a na + 100 ºC?
136. Utvrdite koji od navedenih iskaza nije ta~an. Supstance izme|u ~ijih se molekula obrazuju vodoni~ne veze: a) imaju ni`e temperature kqu~awa od o~ekivanih, b) me|usobno se dobro me{aju, v) imaju vi{e temperature topqewa od o~ekivanih.


Pod hemijskim reakcijama podrazumevaju se one promene supstanci pri kojima od polaznih supstanci (reaktanata) nastaju nove supstance koje se po sastavu i osobinama bitno razlikuju od polaznih.
Tokom hemijskih reakcija dolazi do raskidawa veza izmeðu atoma u supstancama koje stupaju u reakciju, a osloboðeni atomi se meðusobno povezuju u novim kombinacijama gradeãi proizvode reakcije.
Svaki hemijski znak prikazuje odreðeni element, kao i jedan atom tog elementa. Tako simbol H oznaåava element vodonik i jedan atom vodonika, a simbol O – element kiseonik i jedan atom kiseonika.
Hemijska formula prikazuje odreðeni element ili jediwewe, kao i jedan wegov molekul (odnosno formulsku jedinku*). Tako, npr., formula N2 predstavqa molekulski azot i jedan molekul azota; formula NH3 – amonijak i jedan molekul amonijaka, a formula Na2SO4 natrijum-sulfat i jednu formulsku jedinku tog jediwewa.
Po analogiji sa relativnom atomskom masom (izraz 3), relativna molekulska masa se definiše kao odnos mase molekula (odnosno formulske jedinke, mf) i atomske jedinice mase, u:
mf M r = . (11) u
Relativna molekulska masa izraåunava se tako što se saberu relativne atomske mase atoma koji åine dati molekul (odnosno formulsku jedinku).
* Pod formulskom jedinkom podrazumeva se skup atoma ili jona prikazanih hemijskom formulom. Tako formula HCl oznaåava formulsku jedinku, ali i molekul hlorovodonika, pošto se ovo jediwewe sastoji od molekula HCl. Meðutim, formula NaCl ne oznaåava molekul natrijum-hlorida veã samo formulsku jedinku, pošto se u jonskim kristalima te supstance ne nalaze slobodni molekuli NaCl Obiåno se sve formulske jedinke nazivaju molekulima, pa se i NaCl moþe smatrati molekulom u širem smislu.
Пример 26
Izraåunati relativnu molekulsku masu sumporne kiseline, H2SO4. U tablici periodnog sistema nalazimo da je:
A r(H) = 1,008; A r(S) = 32,06; A r(O) = 16,00.
M r(H2SO4) = 2 A r(H) + A r(S) + 4 A r(O) = 2 ⋅ 1,008 + 32,06 + 4 ⋅ 16,00 = 98,08.
Odgovor: Relativna molekulska masa sumporne kiseline je 98,08
Пример 27
Relativna molekulska masa amonijaka, Mr(NH3) = 17,03. Izraåunati masu jednog molekula amonijaka i izraziti je u gramima.
Iz jednaåine (11) sledi:
mf(NH3) = M r(NH3) u
U tablici 5 nalazimo da je 1 u = 1,6605 ⋅ 10–27 kg. Uvrštavawem brojåanih vrednosti u gorwi izraz dobijamo:
mf(NH3) = 17,03 1,6605 10–27 kg = 28,28 ⋅ 10–27 kg = 2,828 ⋅ 10–26 kg = = 2,828 ⋅ 10–26 ⋅ 103 g = 2,828 ⋅ 10–23 g.
Odgovor: Masa molekula amonijaka je 2,828 ⋅ 10–23 g
Od sedam osnovnih SI-jedinica (tablica 2), u hemiji najveãi znaåaj ima mol – jedinica za koliåinu supstance (n).
Mol je koliåina supstance koja sadrþi onoliko åestica (atoma, molekula, jona i sl.) koliko ima atoma u 12 g ugqenikovog izotopa C–12
U 12 g ugqenikovog izotopa C–12 nalazi se 6,02 ⋅ 1023 atoma. Znaåi da 1 mol bilo koje åiste supstance sadrþi 6,02 ⋅ 1023 åestica. Broj 6,02 ⋅ 1023 ima mernu jedinicu mol–1 i naziva se Avogadrova konstanta, NA (vidi tablicu 7):
6,02 1023
NA = 6,02 ⋅ 1023 mol–1, odnosno . mol
Ovaj ogromni broj (åita se šest stotina dve trilijarde) odabran je iz praktiånih razloga, pošto se moþe precizno eksperimentalno odrediti i veoma je pogodan za stehiometrijska izraåunavawa. Naime,
ako relativnu atomsku ili relativnu molekulsku masu neke supstance izrazimo u gramima i supstancu izmerimo na vagi, u dobijenom uzorku nalaziãe se upravo 6,02 ⋅ 1023 åestica (atoma, molekula ili jona).
Kod izraþavawa koliåine åestica u nekom uzorku, treba naznaåiti o kojim åesticama je reå. To se åini tako što se u zagradi pored simbola n navede znak åestica. Na primer:
n(Cl) oznaåava koliåinu atoma hlora,
n(Cl2) oznaåava koliåinu molekula hlora,
n(Cl–) oznaåava koliåinu jona hlora.
Brojnost åestica u nekom uzorku, N i koliåina supstance, n su proporcionalne veliåine; konstanta proporcionalnosti je Avogadrova konstanta, NA:
N = n NA (12)
Пример 28
Izraåunati broj molekula CO2 u 0,34 mol gasovitog ugqenik(¡¢)-oksida.
n(CO2) = 0,34 mol
N(CO2) = ?
N(CO2) = n(CO2) NA = 0,34 mol 6,02 1023 mol–1 = 2,05 1023.
Odgovor: U 0,34 mol ugqenik(¡¢)-oksida nalazi se 2,05 ⋅ 1023 molekula CO2
Molarna masa je fiziåka veliåina koja se definiše kao odnos mase åiste supstance, m i koliåine te supstance, n(B):
m M(B) = (13) n (B)
SI-jedinica molarne mase je kg/mol. U hemiji se åešãe koristi decimalna jedinica g/mol
Molarna masa neke supstance izraåunava se mnoþewem wene relativne atomske (odnosno relativne molekulske mase) mernom jedinicom g/mol:
M = A r ⋅ g/mol, odnosno (14)
M = M r ⋅ g/mol (15)
gde su: A r – relativna atomska masa, M r – relativna molekulska masa.
Izraz (14) odnosi se na atome, a izraz (15) na molekule i formulske jedinke.
Пример 29
Izraåunati molarnu masu sumporne kiseline, ako je relativna molekulska masa te supstance 98,08. Molarna masa sumporne kiseline biãe prema izrazu (15) jednaka:
M(H2SO4) = M r(H2SO4) g/mol = 98,08 g/mol.
Odgovor: Molarna masa sumporne kiseline je 98,08 g/mol. Prikaþimo na dva primera kako se koristi izraz (13) za preraåunavawe mase i koliåine supstance.
Пример 30
Izraåunati koliåinu molekula H2O u 100 g åiste vode, ako je M(H2O) = 18,0 g/mol.
m(H2O) = 100 g, M(H2O) = 18,0 g/mol, n(H2O) = ?
Iz izraza (13) sledi: n = m M . Uvrštavawem brojåanih vrednosti u ovaj izraz dobijamo:
100 g
n(H2O) = = 5,55 mol. 18,0 g/mol–1
Odgovor: U 100 g åiste vode nalazi se 5,55 mol H2O.
Пример 31
Za reakciju su potrebna 0,2 mol bakar(¡¡)-oksida, CuO. Koliko te supstance treba odmeriti na vagi, da bi se u dobijenom uzorku nalazilo 0,2 mol CuO?
M(CuO) = 79,53 g/mol, n(CuO) = 0,2 mol, m(CuO) = ?
Iz izraza M = m n sledi: m = n ⋅ M. Uvrštavawem brojåanih vrednosti u taj izraz dobijamo:
m(CuO) = 0,2 mol ⋅ 79,53 g/mol = 15,9 g.
Odgovor: Za reakciju u kojoj su potrebna 0,2 mol bakar(¡¡)-oksida treba odmeriti na vagi 15,9 g te supstance.
Molarna zapremina supstance B, Vm(B) definiše se kao odnos zapremine te supstance, V i wene koliåine, n(B): V Vm(B) = (16) n (B)
SI-jedinica molarne zapremine je m3/mol, ali se u hemiji obiåno koristi decimalna jedinica dm3/mol
Molarna zapremina zavisi od pritiska i temperature. Idealni gas pri normalnim uslovima (0 ºC i 101,3 kPa) ima molarnu zapreminu 22,4 dm3/mol.
Пример 32
Izraåunati koliåinu molekula H2 u 1 dm3 vodonika pri normalnim uslovima (n.u.). Uzeti da je molarna zapremina vodonika jednaka 22,4 dm3/mol.
Iz jednaåine (16) sledi: n = . Uvrštavawem zadanih vrednosti u ovaj izraz dobijamo:
1 dm3 n(H2) = = 0,045 mol = 45 mmol. 22,4 dm3/mol–1
Odgovor: U 1 dm3 vodonika pri n.u. nalazi se 45 milimolova molekula H2
Hemijske jednaåine prikazuju supstance koje stupaju u reakciju i supstance koje pri reakciji nastaju, kao i koliåinske i masene odnose meðu wima (primeri 33 i 34).
Пример 33
Izraåunati koliko molova þiva(¡¡)-oksida, HgO treba razloþiti za dobijawe 0,1 mol kiseonika.
Napišimo najpre jednaåinu reakcije termiåkog razlagawa þiva(¡¡)-oksida:
2 HgO → 2 Hg + O2. V Vm
Iz jednaåine se vidi da se dve formulske jedinke þiva(¡¡)-oksida razlaþu na dva atoma þive i jedan molekul kiseonika. Kako je broj åestica proporcionalan wihovim koliåinama (izraz 12), pri razlagawu 2 mol HgO nastaje 2 mol Hg i 1 mol O2:
2 HgO → 2 Hg + O2
2 mol 2 mol 1 mol
Iz datih koliåinskih odnosa reaktanata i proizvoda reakcije sledi da je za dobijawe 0,1 mol O2 potrebno 0,2 mol HgO
Odgovor: Za dobijawe 0,1 mol kiseonika treba razloþiti 0,2 mol þiva(¡¡)-oksida.
Пример 34
Izraåunati koliko je grama cinka potrebno za reakciju sa 6 g joda u cink-jodid, ZnI2.
Jednaåina reakcije sjediwavawa cinka i joda u cink-jodid glasi:
Zn + I2 → ZnI2.
Vidimo da se jedan atom Zn jedini sa jednim molekulom I2 i gradi jednu formulsku jedinku ZnI2. Pošto su brojnost i koliåina proporcionalne veliåine, znaåi da se jedan mol Zn jedini sa jednim молom I2 i gradi jedan mol ZnI2.
Mase jednog mola Zn i jednog mola I2 iznose:
m(Zn) = 65,38 g,
m(I2) = 253,8 g.
Dakle, 65,38 g Zn jedini se sa 253,8 g I2 u ZnI2. Masu cinka koja reaguje sa 6 g joda izraåunaãemo iz sledeãe proporcije:
65,38 g : 253,8 g = x : 6 g
65,38 g ⋅ 6 g x = = 1,54 g. 253,8 g
Odgovor: Za reakciju sa 6 g joda treba uzeti 1,54 g cinka.
Danas je poznat ogroman broj hemijskih reakcija koje se odigravaju svuda oko nas. Jedan od osnovnih zadataka hemiåara jeste izuåavawe wihovih spoqašwih obeleþja, brzine, uslova koje treba obezbediti da bi tekle þeqenom brzinom i sl. Takoðe ih treba razvrstati u grupe radi lakšeg izuåavawa.
Pre nego što preðemo na razmatrawe savremene klasifikacije hemijskih reakcija, upoznaãemo dva osnovna tipa – jonske i oksido-redukcione reakcije, koje u hemiji i srodnim naukama imaju najveãi znaåaj i predstavqaju osnovu na kojoj se zasniva opšta klasifikacija hemijskih reakcija o kojoj ãemo govoriti kasnije.
Jonske reakcije se odigravaju izmeðu jona u vodenim rastvorima elektrolita. Po svojoj brzini spadaju u trenutne reakcije.
Jonske reakcije obiåno teku u smeru nastajawa slabo rastvorqivih, slabo disosovanih ili lakoisparqivih proizvoda. Prikazuju se pomoãu jonskih jednaåina, koje se sastavqaju prema sledeãim pravilima:
1 Jaki elektroliti u vodenom rastvoru prikazuju se u obliku jona, a slabi u obliku molekula.
2. Slabo rastvorqivi i gasoviti proizvodi reakcije prikazuju se u obliku molekula.
3. Ukupan broj atoma s leve i desne strane jednaåine mora biti isti.
4 Algebarski zbir pozitivnih i negativnih naelektrisawa jona mora biti ravan nuli.
Пример 35
Napisati u jonskom obliku jednaåinu reakcije izmeðu rastvora srebro-nitrata i natrijum-hlorida.
Napišimo najpre jednaåinu navedene reakcije u molekulskom obliku:
AgNO3 + NaCl → AgCl + NaNO3.
AgNO3, NaCl i NaNO3 su jaki elektroliti, te ih prikazujemo u obliku jona (pravilo 1). AgCl je slabo rastvorqivo jediwewe koje prikazujemo u obliku molekula (pravilo 2):
Ag+ + NO3 – + Na+ +Cl– → AgCl + Na+ + NaNO3 –
Joni NO3–i Na+ pojavquju se s obe strane jednaåine, što znaåi da ne uåestvuju u reakciji, te ih moþemo eliminisati. Tako dobijamo:
Ag+ + Cl– → AgCl
Oksido-redukcione reakcije praãene su prelaskom elektrona s jednog atoma ili jona na drugi. Pri tome dolazi do promene oksidacionih brojeva elemenata.
Oksidacioni broj elementa u jediwewu predstavqa zamišqeno svojstvo atoma tog elementa koje pokazuje u kom se oksidacionom stawu on nalazi. Poznavawe oksidacionih brojeva olakšava sastavqawe jednaåina oksido-redukcionih reakcija.
Oksidacioni broj moþe imati pozitivnu, negativnu ili nultu vrednost. Oznaåava se u hemijskoj formuli iznad simbola elementa arapskim ciframa, sa odgovarajuãim predznakom. Na primer:
+1 –1 H Cl.
Oksidacioni brojevi elemenata u slobodnom stawu ravni su nuli, bez obzira da li ih prikazujemo u vidu atoma ili molekula. Na primer:
0 0 0 0 0 Cl2, Fe, O2, P4, Cu.
Oksidacioni brojevi elemenata u jonskim jediwewima jednaki su wihovoj elektrovalenci, tj. broju elektrona koje atomi otpuštaju ili vezuju pri obrazovawu jonske veze.
Oksidacioni brojevi elemenata u kovalentnim jediwewima definišu se kao zamišqeno naelektrisawe koje bi wihovi atomi imali kada bi elektroni u potpunosti prešli na atom veãe elektronegativnosti (tj. kovalentnom jediwewu se pripisuje jonska struktura).
Algebarski zbir oksidacionih brojeva elemenata u elektriåno neutralnom molekulu ravan je nuli, a u sloþenom jonu jednak je naelektrisawu jona. U skladu s ovim pravilom, moguãe je odrediti oksidacioni broj bilo kog atoma u molekulu ili jonu, na osnovu poznatih oksidacionih brojeva ostalih atoma.
Пример 36
a) Odrediti oksidacioni broj azota u hidroksilaminu, NH2OH. U molekulu hidroksilamina nalaze se tri atoma vodonika [3 ⋅ (+1) = = + 3], i jedan atom kiseonika (–2). Znaåi da oksidacioni broj azota u ovom jediwewu mora biti jednak – 1, kako bi molekul u celini bio elektriåno neutralan.
Odgovor: Oksidacioni broj azota u hidroksilaminu je –1.
b) Odrediti oksidacioni broj ugqenika u oksalnoj kiselini, C2H2O4. Napišimo najpre strukturnu formulu oksalne kiseline: Kod odreðivawa oksidacionog broja ugqenika u organskim jediwewima, oksidacioni broj svakog C-atoma odreðuje se posebno, s tim što se veze izmeðu C-atoma ne uzimaju u obzir.
Iz strukturne formule oksalne kiseline se vidi da su za svaki C-atom vezana po dva atoma kiseonika [2 ⋅ (–2) = – 4] i jedan atom vodonika (+1). Prema tome, oksidacioni broj oba C-atoma je +3
Odgovor: Oksidacioni broj oba atoma ugqenika u molekulu oksalne kiseline je +3.
Пример 37
Odrediti oksidacione brojeve elemenata u sledeãim elementarnim supstancama, jediwewima i sloþenim jonima.
a) Cl2, S8, P4,
b) NaCl, CaO, Al2O3,
v) CH4, CO2, HCl, 2– 2– g) SO4, CO3, MnO4–
Odgovor: a) Oksidacioni brojevi hlora, sumpora i fosfora u navedenim elementarnim supstancama ravni su nuli:
0 0 0
Cl2, S8, P4
b) Oksidacioni brojevi elemenata u jonskim jediwewima jednaki su wihovoj elektrovalenci:
NaCl, CaO, Al2O3.
v) Kod kovalentnih jediwewa, pozitivne oksidacione brojeve imaju elementi mawe elektronegativnosti. Negativne oksidacione brojeve imaju elementi veãe elektronegativnosti, prema kojima su pomereni zajedniåki elektronski parovi:
, CO3, HCl.
g) Kod sloþenih jona, algebarski zbir oksidacionih brojeva svih atoma koji åine dati jon jednak je naelektrisawu jona:
Sastavqawe jednaåina oksido-redukcionih reakcija – sastoji se u odreðivawu koeficijenata ispred formula reaktanata i proizvoda reakcije. Koeficijenti se mogu odrediti i metodom proba i pogrešaka, ali je to u veãini sluåajeva sporo i nepraktiåno, naroåito kada se radi o sloþenijim reakcijama, sa više reaktanata i proizvoda reakcije. Za sastavqawe jednaåina oksidoredukcionih reakcija koriste se dve metode: metoda oksidacionih brojeva i jonsko-elektronska metoda.
Metoda oksidacionih brojeva
Redosled operacija (koraka) kod odreðivawa koeficijenata ovom metodom razmotriãemo na jednom primeru.
Пример 38
Sastaviti jednaåinu katalitiåke oksidacije amonijaka, NH3, pri kojoj nastaju azot(II)-oksid, NO i vodena para.
1. Napisati shemu reakcije, tj. formule polaznih supstanci i proizvoda reakcije:
NH3 + O2 „ NO + H2O
2. Odrediti oksidacione brojeve elemenata i napisati ih iznad wihovih simbola u formulama reaktanata i proizvoda reakcije –3 +1 0 +2 –2 +1 –2
NH3 + O2 „ NO + H2O
3. Na osnovu promena oksidacionih brojeva elemenata utvrditi koji se element oksiduje, a koji redukuje. Ovde vaþi sledeãe pravilo: oksiduje se onaj element åiji se oksidacioni broj poveãava, a redukuje element åiji se oksidacioni broj smawuje. Vidimo da azot i kiseonik pri reakciji mewaju oksidacione brojeve: azot se oksiduje (oksidacioni broj mu se poveãava od –3 na +2), a kiseonik redukuje (oksidacioni broj mu se smawuje od 0 na –2).
4. Napisati sheme polureakcija oksidacije i redukcije, u koje treba uneti samo one elemente åiji se oksidacioni brojevi mewaju:
3 +2
(a) N – 5 e – „ N (oksidacija)
0 –2
(b) O2 + 4 e– „ 2 O (redukcija).
5. Izjednaåiti broj otpuštenih i primqenih elektrona mnoþewem polureakcija (a) i (b) odgovarajuãim brojevima:
–3 +2
(a) (N – 5 e – „ N) ⋅ 4
0 –2
(b) (O2 + 4 e – „ 2 O) ⋅ 5
Nakon mnoþewa dobijamo:
3 +2
(a) 4 N – 20 e– „ 4 N
0 –2
(b) 5 O2 + 20 e– „ 10 O.
Iz dobijenih reakcija sledi da na åetiri atoma N (odnosno åetiri molekula NH3) dolazi deset atoma (tj. pet molekula) O2. Ove koeficijente unosimo u shemu reakcije:
4 NH3 + 5 O2 „ NO + H2O.
6. Odrediti koeficijente i ispred formula ostalih supstanci:
4 NH3 + 5 O2 „ 4 NO + 6 H2O.
Da bi se proverila taånost dobijenog rešewa, treba utvrditi broj atoma svakog pojedinog elementa s leve i desne strane jednaåine. Ukoliko je on isti, jednaåina oksido-redukcione reakcije pravilno je napisana.
Ova metoda primewuje se za sastavqawe jednaåina oksido-redukcionih reakcija koje se odigravaju u vodenim rastvorima. Zasniva se na formirawu jonskih shema polureakcija oksidacije i redukcije, koje se nakon izjednaåewa broja otpuštenih i primqenih elektrona objediwuju u zbirnu jonsku jednaåinu.
Analogno metodi oksidacionih brojeva, i ova metoda se moþe rašålaniti na odreðeni broj koraka. Redosled koraka upoznaãemo na sledeãem primeru:
Пример 39
Sastaviti jednaåinu oksido-redukcione reakcije izmeðu rastvora kalijum-jodida, KI i kalijum-hlorata, KClO3 u kiseloj sredini. Proizvodi reakcije su: elementarni jod, I2, kalijum-hlorid, KCl, kalijum-sulfat, K2SO4 i voda.
1. Napisati shemu reakcije u molekulskom obliku:
KI + KClO3 + H2SO4 „ I2 + KCl + K2SO4 + H2O.
2. Napisati shemu reakcije u jonskom obliku, s tim što jake elektrolite u vodenom rastvoru treba prikazati u obliku jona, a slabe elektrolite, gasovite i åvrste supstance – u obliku molekula. Shema reakcije se piše u skraãenom obliku, eliminisawem jona koji neposredno ne uåestvuju u reakciji, tj. pojavquju se s obe strane izraza:
I– + ClO3– + H+ „ I2 + Cl– + H2O.
3. Uneti u jonsku shemu reakcije oksidacione brojeve elemenata. Oksidacioni brojevi elementarnih jona se ne oznaåavaju, pošto odgovaraju naelektrisawu jona:
+5 0
I– + ClO3 – + H+ „ I2 + Cl– + H2O.
4. Utvrditi koji se element oksiduje a koji redukuje. Vidimo da se jod oksiduje (oksidacioni broj mu se poveãava od –1 na 0), dok se hlor redukuje (oksidacioni broj mu se smawuje od +5 na –1).
5. Napisati sheme polureakcija oksidacije i redukcije, u koje se unose joni ili molekuli koji stvarno postoje u reakcionoj smeši (razlika od metode oksidacionih brojeva). U shemu se takoðe unosi broj otpuštenih i primqenih elektrona:
(a) 2 I– – 2 e– „ I2 (oksidacija)
(b) ClO3– + 6 H+ + 6 e– „ Cl– + 3 H2O (redukcija).
S obzirom da se reakcija odvija u kiseloj sredini, levoj strani polureakcije (b) dodajemo šest protona, koji sa tri atoma kiseonika iz jona ClO3– grade tri molekula vode. Pošto smo izjednaåili ukupan broj atoma s leve i desne strane polureakcije (b), to treba uåiniti i sa zbirnim naelektrisawem svih jona. Joni s leve strane imaju zbirno naelektrisawe +5, a s desne –1, stoga levoj strani treba dodati šest elektrona. Tada zbirno naelektrisawe s obe strane polureakcije (b) iznosi –1.
6. Izjednaåiti broj otpuštenih i primqenih elektrona. U tom ciqu polureakciju (a) treba pomnoþiti sa 3:
(a) (2 I–– 2 e – „ I2) ⋅ 3
Tako dobijamo:
(a) 6 I–– 6 e– „ 3 I2
(b) ClO3–+ 6 H+ + 6 e– „ Cl– + 3 H2O
7. Sabrati polureakcije (a) i (b):
6 I– + ClO3 – + 6 H+ „ 3 I2 + Cl– + 3 H2O.
Ispravnost dobijene jonske jednaåine proveravamo poreðewem broja atoma svakog pojedinog elementa, kao i zbirnog naelektrisawa s leve i desne strane jednaåine.
8. (eventualno). Ukoliko þelimo da dobijemo molekulski oblik jednaåine, svakom anjonu i katjonu s leve strane treba dodati odgovarajuãe katjone i anjone. Zatim te iste jone u istom broju unosimo i na desnu stranu jonske jednaåine, nakon åega jone objediwujemo u molekule. Takvim postupkom preciziramo koje supstance treba uzeti za izvoðewe konkretne oksido-redukcione reakcije:
6 I– + ClO3 – + 6 H+ „ 3 I2 + Cl– + 3 H2O 2– 2– 7 K+ 3 SO4 7 K+ 3 SO4
6 KI + KClO3 + 3 H2SO4 „ 3 I2 + KCl + 3 K2SO4 + 3 H2O.
Neorganske hemijske reakcije se mogu podeliti u dve velike grupe, zavisno od toga da li su praãene promenom oksidacionih brojeva elemenata ili ne. Svaka od ovih osnovnih grupa reakcija deli se na tri podgrupe: reakcije analize, sinteze i zamene (ili razmene). Navedena klasifikacija pregledno se moþe prikazati ovako:
Analiza je hemijska reakcija razlagawa sloþenih supstanci na dve ili više novih, prostijih supstanci. Zajedniåko obeleþje reakcija analize je da u wima uåestvuje jedan reaktant (koji je uvek neko jediwewe), a nastaju dva, tri ili više proizvoda reakcije (elemenata, jediwewa ili wihovih kombinacija). Na primer:
+5 –2 zagr. –1 0 2 KClO3 → 2 KCl + 3 O2 –3 +6
zagr. +3 0 (NH4)2 Cr2O7 → Cr2O3 + N2 + 4 H2O
zagr. CaCO3 → CaO + CO2
Prve dve reakcije su oksido-redukcije, dok kod treãe ne dolazi do promene oksidacionih brojeva elemenata. Sinteza je hemijska reakcija sjediwavawa dve ili više prostijih supstanci u novu, sloþeniju supstancu. Sinteza je po svom karakteru reakcija suprotna analizi. Zajedniåko obeleþje mnogih reakcija ovog tipa je da u wima uåestvuje dva ili više reaktanata (elemenata, jediwewa ili wihovih kombinacija), a najåešãe nastaje jedan reakcioni proizvod (hemijsko jediwewe). Na primer:
0 0 +2 –2 2 Mg + O2 → 2 MgO (oksido-redukcija)
CaO + H2O → Ca(OH)2.
Zamena (supstitucija) je hemijska reakcija zamene atoma ili grupa atoma u molekulima reaktanata drugim atomima ili atomskim grupama. Zajedniåko obeleþje reakcija zamene je da je broj reaktanata jednak broju proizvoda reakcije, i da u reakcijama dolazi do promene oksidacionih brojeva elemenata, tj. one spadaju u oksido-redukcije. Na primer:
+2 0 +2 0
CuSO4 + Fe „ FeSO4 + Cu
0 +1 +2 0
Zn + 2 HCl → ZnCl2 + H2
Reakcije zamene se obiåno odvijaju u vodenim rastvorima, i po svojoj suštini predstavqaju jonske reakcije. Tako dve prethodne reakcije moþemo prikazati u jonskom obliku ovako:
0 0 2+
Cu2+ + Fe „ Cu + Fe
0 0 Zn + 2 H+ → Zn2+ + H2
Razmena je hemijska reakcija razmene atoma ili grupa atoma izmeðu molekula reaktanata. Pri reakcijama razmene oksidacioni brojevi elemenata se ne mewaju, a broj reaktanata jednak je broju proizvoda reakcije. Tako, na primer, reakcija izmeðu rastopqenih soli – barijum-sulfata i natrijum-karbonata spada u ovu grupu:
BaSO4 + Na2CO3 „ BaCO3 + Na2SO4
Poznat je veliki broj reakcija izmeðu rastvora elektrolita koje se formalno mogu uvrstiti u razmenu, dok po svojoj suštini spadaju u jonske reakcije. Na primer:
HCl + NaOH → NaCl + H2O, odnosno
H+ + OH– „ H2O
AgNO3 + HCl → AgCl + NaNO3, odnosno
Ag+ + Cl– „ AgCl.
Pri spajawu suprotno naelektrisanih jona koji se nalaze u rastvorima reaktanata nastaju slabo disosovani molekuli (u prvom primeru to je H2O), odnosno supstance koje se izdvajaju iz rastvora u vidu taloga (AgCl u drugom primeru) ili gasa
Protolitiåke reakcije (str. 110) takoðe se formalno mogu uvrstiti u reakcije razmene, s obzirom da se sastoje u razmeni protona izmeðu kiseline i baze, pri åemu ne dolazi do promene oksidacionih brojeva elemenata. Na primer:
HCl + H2O → H3O+ + Cl–. kis. baza
Treba napomenuti da zbog ogromnog broja poznatih hemijskih reakcija i wihove raznovrsnosti nije stvorena univerzalna klasifikacija kojom bi bile obuhvaãene sve poznate neorganske reakcije. Tako npr. klasifikacijom koju smo upoznali nisu obuhvaãene sloþene oksido-redukcione reakcije kao što je ona razmotrena u primeru 39, a takoðe i neke druge vrste reakcija.
Grana hemije koja izuåava toplotne efekte hemijskih reakcija zove se termohemija. Hemijske reakcije se zavisno od toplotnih efekata dele na egzotermne i endotermne. Prve su praãene oslobaðawem, a druge vezivawem toplotne energije.
Entalpija (sadrþaj toplote). – Svaka supstanca, svaki reakcioni sistem sadrþi odreðenu koliåinu toplote, vezane u obliku hemijske energije. Toplotni sadrþaj supstanci naziva se entalpija, a oznaåava se sa H.
H = U + pV (17)
gde je:
U – unutrašwa energija sistema, koja obuhvata sve oblike energije datog sistema, p – pritisak, V – zapremina.
Apsolutna vrednost entalpije sistema pre i posle reakcije nije poznata. To nije ni potrebno, pošto se toplotni efekat hemijske reakcije izraþava promenom entalpije sistema, a ne wenim apsolutnim vrednostima. Promena entalpije sistema, ∆H jednaka je:
∆H = ∆U + p∆V (18)
gde je:
∆U – promena unutrašwe energije sistema, p∆V – rad širewa, tj. energija koja se troši za savlaðivawe spoqašweg pritiska.
Hemijske reakcije se najåešãe izvode u otvorenim sudovima, tj. pri stalnom pritisku. U tom sluåaju, promena entalpije sistema, ∆H jednaka je toplotnom efektu reakcije odreðenom pri stalnom pritisku, Qp :
∆H = Qp. (19)
Iz jednaåine (19) sledi da se promena entalpije sistema eksperimentalno moþe odrediti merewem koliåine toplote koja se pri reakciji oslobaða ili vezuje.
Entalpija je funkcija stawa sistema, koja karakteriše wegovu energiju na stalnom pritisku i temperaturi. U skladu sa zakonom o odrþawu energije, promena entalpije sistema ne zavisi od puta reakcije, veã samo od polaznog i krajweg stawa sistema.
* Симболом (s) иза хемијског знака
или формуле обележавају се супстан-
це које се налазе у чврстом стању.
Симболом (c) означавају се супстанце у кристалном стању, а симболом (g) супстанце у гасовитом стању.
Симболом (l) означавају се супстанце
у течном стању, а симболом (aq)
супстанце које се налазе у воденом раствору.
Reakciona toplota (entalpija reakcije), ∆ r H je toplota koja se oslobaða ili vezuje pri hemijskoj reakciji. Izraþava se u kiloyulima po molu nekih od formulskih jedinki koje figuriraju u jednaåini reakcije, tj. predstavqa molarnu reakcionu toplotu. Meðutim, reå „molarna” se obiåno izostavqa.
Toplotni efekti reakcija izmeðu gasovitih supstanci zavise od pritiska, stoga se izraþavaju pri standardnom pritisku od 101,3 kPa Reakcione toplote svedene na standardni pritisak oznaåavaju se sa ∆ r Hq . Kako reakcione toplote zavise i od temperature, pored oznake ∆ r Hq u zagradu treba staviti temperaturu na kojoj se reakcija odigrava. S obzirom da su sve vrednosti reakcionih toplota navedenih u ovoj kwizi preraåunate na temperaturu od 298 K (25 °C), neãemo uz svaku vrednost ∆ r Hq pisati 298 K. Radi pojednostavqewa izostaviãemo i simbol q. Kod egzotermnih reakcija promena entalpije sistema ima negativan predznak (∆ r H < 0). Na primer:
H2(g) + 1/2 O2(g) → H2O(g), ∆ r H = – 241,8 kJ/mol.
Kod endotermnih reakcija promena entalpije sistema ima pozitivan predznak (∆ r H > 0). Na primer:
1/2 N2(g) + O2(g) → NO2(g), ∆ r H = + 33,9 kJ/mol.
Jednaåine u kojima su prikazani toplotni efekti hemijskih reakcija nazivaju se termohemijske jednaåine. U tim jednaåinama mora se navesti i agregatno stawe supstanci*, pošto i od toga zavisi reakciona toplota.
Toplota (entalpija) stvarawa jediwewa, ∆fH je ona koliåina toplote koja se oslobaða ili vezuje pri nastanku jednog mola nekog jediwewa iz elemenata (koji se nalaze u svom najstabilnijem obliku). Izraþava se u kJ/mol.
Po dogovoru, toplote stvarawa alotropskih najstabilnijih modifikacija hemijskih elemenata ravne su nuli. Polazeãi od te åiwenice, moþe se, izborom pogodnih koeficijenata u termohemijskoj jednaåini sinteze nekog jediwewa iz elemenata, podesiti da koeficijent ispred formule proizvoda reakcije bude ravan 1. U tom sluåaju reakciona toplota jednaka je toploti stvarawa datog jediwewa iz elemenata. Na primer:
1/2 H2(g) + 1/2 Cl2(g) → HCl(g), ∆ r H = – 92,5 kJ/mol.
Na osnovu izloþenog sledi da je:
∆fH(HCl) = ∆ r H = – 92,5 kJ/mol.
U tablici 16 navedene su standardne entalpije stvarawa nekih vaþnijih hemijskih jediwewa.
Tablica 17. Standardne entalpije stvarawa nekih vaþnijih hemijskih jediwewa
једињење DfH (kJ/mol)
Al2O3 (s) – 1 670,0 H2O(g) – 241,8
CH4(g) – 74,8 H2O(l) –
C2H2(g) + 226,7 H2O2(l) – 187,5
C2H4(g) + 52,3 H2S(g) – 20,1
C2H6(g) – 84,7MgO(s) – 602,5
C2H5OH(l) – 277,6 NH3(g) – 46,0
CO(g) – 110,9 NH4Cl(s) – 315,6
CO2(g) – 393,5NO(g) + 90,5
CaO(s) – 636,0NO2(g) + 33,9
CuO(s) – 155,1 P2O5(s) – 1 492,0
Fe2O3(s) – 822,2SO2(g) – 297,1
HCl(g) – 92,5SO3(g) – 395,8
HI(g) + 25,9ZnO(s) – 348,2
Ako su poznate standardne entalpije stvarawa reaktanata i proizvoda reakcije, moþe se izraåunati standardna entalpija te reakcije, tako što se od zbira entalpija stvarawa proizvoda reakcije oduzme zbir entalpija stvarawa reaktanata:
∆ r H = Σp∆fH (proizv.) – Σr∆fH (reakt.) (20)
gde su:
p – stehiometrijski koeficijenti proizvoda reakcije u jednaåini reakcije, r – stehiometrijski koeficijenti reaktanata.
Пример 40
Izraåunati standardnu entalpiju reakcije
4 NH3(g) + 5 O2 (g) → 4 NO (g) + 6 H2O (g)
Dobijeni rezultat izraziti u kiloyulima po molu NH3. U tablici 17 nalazimo da je:
∆fH(NH3) = – 46,0 kJ/mol,
∆fH(NO) = + 90,5 kJ/mol,
fH(H2O(g)) = – 241,8 kJ/mol.
U skladu sa jednaåinom (20), moþemo napisati:
∆ r H = 4 ∆fH(NO) + 6 ∆fH(H2O) – 4 ∆fH(NH3) – 5 ∆fH(O2).
Kako je ∆fH(O2) = 0, standardna entalpija reakcije jednaka je:
∆ r H / kJ mol–1 = 4 90,5 + 6(–241,8) – 4(46,0) = – 904,8.
∆ r H = – 904,8 kJ/mol.
Standardna entalpija reakcije odnosi se na mol jedinki navedenih u jednaåini reakcije. U našem primeru to su hipotetiåne jedinke 4 NH3, 5 O2, 4 NO i 6 H2O. Prema tome, izraåunata vrednost ∆ r H odnosi se na jedan mol jedinki 4 NH3, 5 O2, 4 NO ili 6 H2O. Kao što vidimo, formulske jedinke mogu biti i skupovi molekula.
Kako se u zadatku traþi da se izraåunata vrednost ∆ r H izrazi po molu NH3, moramo vrednost – 904,8 kJ/mol podeliti sa 4, pošto se svaka hipotetiåna jedinka 4 NH3 sastoji od 4 jedinke NH3.
Odgovor: Standardna entalpija reakcije iznosi – 226,2 kJ/mol NH3
Izraåunati standardnu entalpiju stvarawa etana, C2H6, ako je standardna entalpija sagorevawa etana, ∆ r H = – 1 427,7 kJ/mol. Napišimo najpre termohemijsku jednaåinu reakcije sagorevawa etana:
C2H6(g) + 7/2 O2(g) → 2 CO2(g) + 3 H2O(g), ∆ r H = – 1427,7 kJ/mol.
U tablici 17 nalazimo:
∆fH(CO2) = – 393,5 kJ/mol,
∆fH(H2O(g)) = – 241,8 kJ/mol,
∆ r H = 2 ∆fH(CO2) + 3 ∆fH(H2O) – ∆fH(C2H6),
∆fH(C2H6) = 2 ∆fH(CO2) + 3 ∆fH(H2O) – ∆ r H
Ako u ovaj izraz uvrstimo brojåane vrednosti, dobiãemo:
∆fH(C2H6) / kJ mol–1 = 2(–393,5) + 3(–241,8) – (–1427,7)
∆fH(C2H6) = – 84,7 kJ/mol.
Odgovor: Standardna entalpija stvarawa etana iznosi – 84,7 kJ/mol.
Hesov zakon. – Toplotni efekat hemijske reakcije je stalan, bez obzira da li se ona odigrava u jednom ili više stupweva, pod uslovom da se polazi od istih reaktanata i da nastaju isti proizvodi reakcije. Iz Hesovog zakona sledi da je zbir reakcionih toplota svih stupweva neke reakcije jednak reakcionoj toploti direktne reakcije, tj. reakcije pri kojoj se od reaktanata neposredno dobijaju proizvodi reakcije. Primenom Hesovog zakona mogu se izraåunati i one reakcione toplote koje se teško odreðuju eksperimentalno.
Пример 42
Ugqenik(¡¢)-oksid, CO2, moþe nastati iz elemenata na dva naåina: neposredno:
C(s) + O2(g) → CO2(g), ∆ r H a = – 393,5 kJ/mol (a)
preko meðuproizvoda, ugqenik(¡¡)-oksida, CO:
C(s) + 1/2 O2(g) → CO(g), ∆ r Hб = ? (b)
CO(g) + 1/2 O2(g) → CO2(g), ∆ r H в = – 282,6 kJ/mol. (v)
Standardna reakciona toplota oksidacije C u CO (∆ r Hб ) ne moþe se odrediti eksperimentalnim putem, pošto se pri reakciji jedan deo nastalog CO uvek oksidiše u CO2. Stoga se ova reakciona toplota izraåunava na osnovu Hesovog zakona.
Da bi se boqe shvatila suština postupka, procesi opisani jednaåinama (a), (b) i (v) prikazani su grafiåki na slici 20
Na slici 20 se vidi da je reakciona toplota direktne reakcije (a) jednaka zbiru reakcionih toplota meðureakcija (b) i (v):
Odatle je:
r Hб = – 393,5 kJ/mol – (–282,6 kJ/mol) = – 110,9 kJ/mol.
Odgovor: Standardna reakciona toplota oksidacije ugqenika u ugqenik(¡¡)-oksid iznosi –110,9 kJ/mol.
Kod rešavawa zadataka ovog tipa termohemijske jednaåine se mogu mnoþiti ili deliti istim brojem i sabirati i oduzimati jedna od druge, po istim pravilima kao i algebarske jednaåine. Ciq je dobijawe termohemijske jednaåine procesa åiji je toplotni efekat nepoznat.
Brzina hemijske reakcije, v, definiše se kao promena koncentracije reaktanata ili proizvoda reakcije sa vremenom:
1 ∆c (B) v = ± · , (21) vb ∆t
gde je:
νb (åita se „ni-be”) – stehiometrijski koeficijent ispred formule komponente B u jednaåini reakcije (tj. one komponente pomoãu koje se izraþava brzina reakcije). Koeficijenti se moraju uzeti u obzir, kako se izraåunate brzine iste reakcije ne bi razlikovale zavisno od toga koja je supstanca u reakcionoj smeši uzeta za izraåunavawe brzine. Stehiometrijski koeficijenti ispred formula reaktanata uzimaju se sa negativnim predznakom, pošto napredovawem reakcije koncentracija reaktanata opada. I obratno – stehiometrijski koeficijenti ispred formula proizvoda reakcije imaãe pozitivni predznak, pošto napredovawem reakcije koncentracija proizvoda reakcije raste.
∆c(B) – veoma mala promena koncentracije komponente B u kratkom vremenskom intervalu ∆ t. Kako je promena neke fiziåke veliåine ∆ x jednaka razlici wene krajwe i poåetne vrednosti (x2 – x1), ∆ c = c2 – c1 (krajwa koncentracija komponente B minus wena poåetna koncentracija).
Iz jednaåine (21) sledi da je SI-jedinica brzine reakcije mol/dm3 s. Brzina hemijske reakcije moþe se izraziti promenom koncentracije bilo koje komponente u reakcionoj smeši. U praksi se obiåno bira ona komponenta åija se koncentracija najlakše moþe odrediti eksperimentalno (npr. merewem zapremine izdvojenog gasa, mase dobijenog taloga, pH-vrednosti rastvora, promenom intenziteta obojenosti rastvora pomoãu specijalnih aparata i sl.).
Izraåunati brzinu hemijske reakcije A2 + B2 → 2 AV, ako je 35 sekundi posle poåetka reakcije koncentracija reaktanata A2 iznosila 0,265 mol/dm3, a 38 sekundi posle poåetka reakcije 0,258 mol/dm3 .
c1(A2) = 0,265 mol/dm3 ; t1 = 35 s
c2(A2) = 0,258 mol/dm3 ; t2 = 38 s.
1 ∆c (B)
v = ± __ · _______ (B = A2; νB = –1).
vb ∆t
∆ c (A2) (c2 – c1) (c1 – c2)
v = – = – ______ = ∆ t (t2 – t1) (t2 – t1)
0,265 mol ⋅ dm–3 – 0,258 mol ⋅ dm–3
v = 38 s – 35 s
0,007 mol ⋅ dm–3
v = = 0,0023 mol/dm3 ⋅ s = 2,3 ⋅ 10–3 mol/dm3 ⋅ s. 3 s
Dobijeni broj pokazuje da se u jednoj sekundi koncentracija reaktanta A2 smawuje za 2,3 ⋅ 10–3 mol/dm3
Brzina hemijske reakcije zavisi od više faktora. Najvaþniji su: koncentracija reaktanata, temperatura, prisustvo katalizatora i veliåina dodirne površine reaktanata.
Uticaj koncentracije reaktanata na brzinu reakcije. – Prema teoriji sudara, brzina hemijske reakcije zavisi od broja sudara izmeðu åestica reaktanata u jedinici vremena. Porastom koncentracije reaktanata, raste broj åestica u jedinici zapremine, a time i broj sudara, te je reakcija brþa.
Kvantitativna zavisnost brzine reakcije od koncentracije reaktanata definisana je zakonom o dejstvu masa koji glasi: Brzina hemijske reakcije na stalnoj temperaturi upravo je proporcionalna proizvodu koncentracija reaktanata.
Пример 44
Prikazati zavisnost brzine reakcije
A + B → AB
od koncentracije reaktanata.
Navedena reakcija spada u jednostepene reakcije, koje teku u jednom stupwu. Prema zakonu o dejstvu masa, brzina reakcije u odreðenom trenutku wenog napredovawa proporcionalna je proizvodu koncentracija reaktanata:
v = k[A] [B],
gde je: k – konstanta brzine reakcije, koja zavisi od prirode reaktanata i temperature, [A] i [B] – koncentracije reaktanata A i B, izraþene u mol/dm3
Veoma su retke reakcije pri kojima se istovremeno sudaraju tri ili više åestica. One obiåno teku u nekoliko stupweva (meðureakcija), tj. spadaju u sloþene reakcije. Kod takvih reakcija zakon o dejstvu masa moþe se primeniti samo na pojedinaåne stupweve, a ne i na reakciju u celini.
U izraz za brzinu reakcije ulaze samo one komponente åija se koncentracija tokom reakcije moþe mewati, a to su gasovi i rastvorene supstance. Koncentracije åvrstih supstanci i åistih teånosti ne ulaze u izraz za brzinu reakcije.
Пример 45
Za koliko ãe se puta poveãati brzina jednostepene reakcije 2 NO(g) + O2(g) → 2 NO2 (g), ako se zapremina reakcionog suda smawi 3 puta? Pre smawewa zapremine, brzina reakcije jednaka je:
v1 = k [NO]2[O2].
Ako izvršimo zamenu: [NO] = a, [O2] = b, dobijamo:
v1 = k ⋅ a2 ⋅ b (a)
Zbog trostrukog smawewa zapremine, koncentracije reaktanata se poveãavaju 3 puta. Znaåi da je:
v2 = k(3a)2 ⋅ 3b = k ⋅ 9a2 ⋅ 3b = 27 k ⋅ a2 ⋅ b (b)
Ako jednaåinu (b) podelimo sa jednaåinom (a), dobiãemo odnos izmeðu krajwe i poåetne brzine reakcije:
v2 27 k a2 b = = 27.
v1 k a2 b
Odgovor: Pri trostrukom smawewu zapremine reakcionog suda brzina reakcije se poveãava 27 puta.
Hemijske reakcije koje teku u jednom smeru do kraja nazivaju se nepovratne reakcije. Najveãi broj hemijskih reakcija spada u povratne reakcije, koje pod istim uslovima istovremeno teku u oba smera.
Uzmimo kao primer povratnu reakciju prikazanu jednaåinom
v1
aA + bB „ cC + dD. v2
Reakcija u smeru → naziva se direktna reakcija, a u smeru ¬ povratna reakcija.
Na poåetku reakcije, kada su koncentracije reaktanata najveãe, brzina direktne reakcije (v1) je najveãa (zakon o dejstvu masa). Napredovawem reakcije smawuje se koncentracija reaktanata, a raste koncentracija proizvoda reakcije, te brzina v1 opada, a brzina v2 raste. U jednom trenutku izjednaåuju se brzine direktne i povratne reakcije (v1 = v2), i u sistemu se uspostavqa hemijska ravnoteþa. U stawu ravnoteþe koncentracije reaktanata i proizvoda reakcije se više ne mewaju.
Ako primenimo zakon o dejstvu masa na navedenu povratnu reakciju, dobijamo:
k1 [C]c [D]d ___ = K= (22) k2 [A]a [B]b
Odnos k1 / k2 naziva se konstanta ravnoteþe povratne reakcije, a oznaåava se sa K. Ova konstanta za svaku povratnu reakciju na odreðenoj temperaturi ima stalnu vrednost. Što je brojåana vrednost K veãa, u stawu ravnoteþe je veãa koncentracija proizvoda reakcije u odnosu na koncentraciju reaktanata, tj. ravnoteþa je pomerena udesno.
Koncentracije komponenata u izrazu (22) su ravnoteþne koncentracije, koje svaki od uåesnika reakcije postiþe nakon uspostavqawa hemijske ravnoteþe.
U izraz za konstantu ravnoteþe ulaze samo koncentracije gasovitih i rastvorenih supstanci.
Kod homogenih ravnoteþnih reakcija u gasovitim sistemima, ravnoteþne koncentracije mogu se zameniti parcijalnim pritiscima gasova. Naime, koncentracije i pritisci gasova na odreðenoj temperaturi su proporcionalne veliåine.
Пример 46
Izraåunati konstantu ravnoteþe sledeãe povratne reakcije:
CO(g) + Cl2(g) → COCl2(g), ako je uzorak gasne smeše na 200 ºC sadrþao 0,2 mol/dm3 ugqenik(¡¡)-oksida, 0,3 mol/dm3 hlora i 1,2 mol/dm3 fozgena. Napišimo izraz za konstantu ravnoteþe navedene reakcije:
[COCl2]
K = __________ [CO] [Cl2]
Ako u ovaj izraz uvrstimo zadane brojåane vrednosti, dobijamo:
1,2 mol dm–3
K = _______________________ = 20 dm3/mol. (0,2 mol dm–3) (0,3 mol dm–3)
Odgovor: Konstanta ravnoteþe reakcije iznosi 20 dm3/mol.
Пример 47
U zatvorenom sudu nalazi se 0,8 mol supstance A i 0,8 mol supstance B. Na odreðenoj temperaturi te supstance reaguju i grade proizvode reakcije C i D:
A(g) + B(g) „ C(g) + D(g)
Utvrðeno je da se nakon uspostavqawa hemijske ravnoteþe u sudu nalazilo 0,6 mol C. Izraåunati konstantu ravnoteþe ove reakcije. Napišimo najpre izraz za K: [C] [D]
K = ________ [A] [B]
Ravnoteþne koncentracije komponenata mogu se zameniti wihovim koliåinama, zapreminama ili masenim udelima. Takva zamena je moguãa u sluåaju kada se reakcija zbiva u homogenom sistemu, a ukupan broj molekula reaktanata u jednaåini reakcije je jednak ukupnom broju molekula proizvoda reakcije.
Moþemo, dakle, napisati sledeãi izraz za K:
n (C) · n (D)
K = ___________
n (A) · n (B)
Iz jednaåine reakcije se vidi da pri reakciji iz 1 mol A i 1 mol B nastaje 1 mol C i 1 mol D. Ako se nakon uspostavqawa ravnoteþe u sistemu nalazilo 0,6 mol C, znaåi da je pri reakciji nastalo i 0,6 mol D. Za stvarawe te koliåine proizvoda reakcije potrebno je po 0,6 mol A i B. Kako
su koliåine reaktanata na poåetku reakcije iznosile po 0,8 mol, nakon uspostavqawa ravnoteþe u sistemu je zaostalo:
0,8 mol – 0,6 mol = 0,2 mol A i isto toliko B.
n(A) = n(B) = 0,2 mol,
n(C) = n(D) = 0,6 mol.
Ako u izraz za K uvrstimo ove vrednosti, dobiãemo:
0,6 mol · 0,6 mol K = _______________ = 9 0,2 mol · 0,2 mol
Odgovor: Konstanta ravnoteþe reakcije iznosi 9
Na poloþaj hemijske ravnoteþe utiåu sledeãi faktori: koncentracija reaktanata, temperatura i pritisak.
Koncentracija reaktanata. – Ukoliko se sistemu u stawu ravnoteþe doda jedan od reaktanata, ubrzava se direktna reakcija i ravnoteþa se pomera udesno. Ako se ravnoteþnom sistemu doda jedan od proizvoda reakcije, ubrzava se povratna reakcija i ravnoteþa se pomera ulevo. Tako se ravnoteþni sistem opire promeni koncentracije komponenata. Na isti naåin moþe se objasniti i pomerawe ravnoteþe udesno pri odvoðewu nekog od proizvoda reakcije iz ravnoteþnog sistema.
Temperatura. – Ako je hemijska reakcija u jednom smeru endotermna, u suprotnom smeru je egzotermna. Na primer:
endotermna reakc.
1/2 N2(g) + 1/2 O2(g) NO(g), ∆ rH = + 90,5 kJ/mol. egzotermna reakc.
Zagrevawe ravnoteþnog sistema izaziva ubrzawe endotermne reakcije, a hlaðewe – egzotermne reakcije. Na taj naåin kompenzuje se dejstvo spoqašweg uticaja.
Pritisak. – Promena pritiska utiåe na poloþaj hemijske ravnoteþe samo kod gasovitih ravnoteþnih sistema. Poveãawe pritiska gasne smeše izaziva pomerawe ravnoteþe u smeru stvarawa maweg broja molekula, jer se tada smawuje pritisak i tako kompenzuje spoqašwi uticaj. Tako, npr., pri poveãawu pritiska gasovitog ravnoteþnog sistema 2 SO2(g) + O2(g) „ 2 SO3(g), ravnoteþa se pomera udesno, tj. u smeru nastanka maweg broja molekula. Pri smawewu pritiska gasne smeše dolazi do pomerawa ravnoteþe u smeru stvarawa veãeg broja molekula, åime se poveãava pritisak gasne smeše.
Iz izloþenog sledi da promena pritiska gasne smeše ne utiåe na poloþaj ravnoteþe jedino u sluåaju kada je ukupan broj molekula sa leve i desne strane jednaåine isti.
Le Šateqeov princip. – Svaki spoqašwi uticaj na sistem koji se nalazi u stawu ravnoteþe, izaziva pomerawe ravnoteþe u onom smeru u kome dolazi do smawewa tog uticaja.
137. Napi{ite izraze za:
a) dva molekula fluora, b) pet atoma gvo`|a, v) tri formulske jedinke natrijum-karbonata.
138. [ta ozna~avaju slede}i izrazi:
а) 7 CO2, б) 2 KCl, в) 3 Cl2?
139. Izra~unajte relativne molekulske mase slede}ih elementarnih supstanci:
a) kiseonika, O2, b) sumpora, S8, v) belog fosfora, P4
140. Izra~unajte relativne molekulske mase slede}ih jediwewa:
a) kalijum-hlorata, KClO3, b) kalcijum-hidroksida, Ca(OH)2, v) fosforne kiseline, H3PO4
141. Izra~unajte mase molekula slede}ih jediwewa:
a) hlorovodonika, b) metanola, v) vode.
Dobijeni rezultat izrazite u gramima.
142. Izra~unajte masu formulske jedinke kalijum-hidroksida. Dobijeni rezultat izrazite u miligramima.
143. Napi{ite znake za koli~inu:
a) molekula sumpor(VI)-oksida, b) formulskih jedinki bakar(II)-sulfata, v) atoma cinka, g) amonijum-jona, d) molekula broma.
144. Napi{ite znake za brojnost: a) atoma bakra, b) jona natrijuma, v) molekula hlorovodonika, g) formulskih jedinki natrijum-karbonata.
145. Izra~unajte koli~inu molekula NH3 u uzorku koji sadr`i 2,71 · 1021 molekula amonijaka. Dobijeni rezultat izrazite u milimolovima.
146. U zatvorenom sudu nalazi se 3,8 · 1024 molekula H2. Izra~unajte koli~inu molekula vodonika u tom sudu.
147. Izra~unajte broj atoma S u 9,35 mol sumpora.
148. Izra~unajte broj molekula u:
a) 0,2 kilomola C2H5OH, b) 3,9 mola NO2, v) 21,15 milimola H2S
149. Koliko se molekula SO2 nalazi u 1,56 mol gasovitog sumpor(IV)-oksida?
150. Izra~unajte koliko je godina potrebno da bi se prebrojali molekuli H2O u 1 g vode. Uzmite da je brzina brojawa jedan molekul u sekundi i da godina ima 365 dana.
151. Kolika je molarna masa:
a) molekula P4,
b) atoma Fe,
v) formulske jedinke NaOH?
152. Izra~unajte molarne mase slede}ih jediwewa:
a) KMnO4, б) HNO3, в) (NH4)2CO3.
153. Izra~unajte koli~inu atoma O u 35 g molekulskog kiseonika.
154. Izra~unajte koli~inu molekula S8 u 15 g ~istog sumpora. Dobijeni rezultat izrazite u milimolovima.
155. Izra~unajte koli~inu molekula CO2 u 11 g ugqenik(IV)-oksida.
156. Koliko se molova SO2 nalazi u 100 g gasovitog sumpor(IV)-oksida?
157. Izra~unajte koli~inu formulskih jedinki u:
a) 0,1 g NaCl, b) 30 mg Al2O3, v) 1 g CaO. Dobijene rezultate izrazite u milimolovima.
158. Koliko se molova H2SO4 nalazi u 1 dm3 96 % sumporne kiseline, gustine 1,84 g/cm3?
159. Koliko treba odmeriti ~istog gvo`|a za 1,2 mol?
160. Izra~unajte masu 0,75 mol kalijum-jodida.
161. Izra~unajte masu uzorka gasovitog amonijaka koji sadr`i 5,6 1020 molekula NH3. Dobijeni rezultat izrazite u miligramima.
162. Izra~unajte koliko se atoma Ag nalazi u 1 g metalnog srebra.
163. Koliko se molekula HCl nalazi u 15 g gasovitog hlorovodonika?
164. Da li ima vi{e atoma u 1 g srebra ili 1 g zlata?
165. Koju }e zapreminu zauzeti 3 g hlora pri normalnim uslovima?
166. Koliko se milimolova O2 nalazi u 1 dm3 vazduha pri n.u., ako je zapreminski udeo kiseonika u vazduhu 21 %?
167. Izra~unajte koli~inu molekula O2 u 17 cm3 kiseonika pri normalnim uslovima. Dobijeni rezultat izrazite u milimolovima.
168. Izra~unajte masu 50 cm3 gasovitog acetilena (etina), C2H2 na 20 ºC i pritisku od 101,3 kPa. Molarna zapremina gasova pri ovim uslovima je 24,37 dm3/mol
169. Uzorak gasa mase 0,329 g na 20 ºC i pritisku od 101,3 kPa ima zapreminu 500 cm3. Izra~unajte molarnu masu gasa, pod uslovom da je molarna zapremina gasa pri navedenim uslovima 24,37 dm3/mol
170. Izra~unajte molarnu masu gasa, ako je masa 600 cm3 tog gasa pri n.u. jednaka 1,714 g.
171. Izra~unajte koliko je molova metalnog aluminijuma potrebno za reakciju sa 0,5 mol l2 u AlI3
172. Koliko se molova AgCl mo`e dobiti dejstvom hlorovodoni~ne kiseline na rastvor koji sadr`i 34 g AgNO3?
173. Izra~unajte koliko se grama kiseonika dobija pri termi~kom razlagawu 10 g `iva(II)-oksida.
174. Hlorovodonik se industrijski obi~no dobija neposrednim sjediwavawem vodonika i hlora. Koliko je kilograma ovih gasova potrebno za dobijawe 1000 kg hlorovodonika?
175. Kalcijum-hidroksid (ga{eni kre~), Ca(OH)2 nastaje pri reakciji kalcijum-oksida sa vodom. Izra~unajte masu vode koja je potrebna za reakciju sa 50 kg kalcijum-oksida.
176. Izra~unajte koliko }e grama magnezijum-oksida nastati pri sagorevawu 12 g metalnog magnezijuma na vazduhu.
177. Rastvoru koji sadr`i 1 g KOH dodat je rastvor u kome se nalazi 1 g ~iste HNO3. Koja supstanca }e ostati u vi{ku? Kolika je wena masa?
178. Koliko je grama `iva(II)-oksida potrebno za dobijawe 1,5 g kiseonika?
179. U zatvorenom sudu izme{ano je 7,3 g gasovitog HCl sa 4,0 g gasovitog NH3. Izra~unajte koliko je grama NH4Cl nastalo pri reakciji. Tako|e odredite masu nesjediwenog gasa.
180. Koliko se kubnih decimetara etina, C2H2 pri n.u. mo`e dobiti reakcijom 0,8 kg kalcijum-karbida, CaC2 sa vodom?
181. Prika`ite u jonskom obliku jedna~ine slede}ih hemijskih reakcija koje se odvijaju u vodenim rastvorima:
a) H2SO4 + 2 KOH „ K2SO4 + 2 H2O,
b) CuSO4 + Na2S „ CuS + Na2SO4, v) NaHCO3 + HCl „ NaCl + CO2 + H2O
182. Napi{ite u jonskom obliku jedna~ine reakcija izme|u vodenih rastvora slede}ih jediwewa:
a) hlorovodoni~ne kiseline i natrijum-karbonata, b) azotne kiseline i barijum-hidroksida, v) aluminijum-hlorida i natrijum-hidroksida.
183. Napi{ite u jonskom obliku jedna~ine talo`nih reakcija izme|u vodenih rastvora slede}ih jediwewa:
a) srebro-nitrata i kalijum-jodida, b) cink-hlorida i kalijum-hidroksida, v) olovo(II)-nitrata i sumporne kiseline.
184. Napi{ite jedna~ine reakcija izme|u odgovaraju}ih jona, pri kojima nastaju slede}a slaborastvorqiva jediwewa:
a) BaSO4, b) PbS, v) Cu(OH)2
185. Odredite oksidacioni broj azota u slede}im jediwewima:
a) HNO3, b) NH4Cl, v) N2N4, g) NH3, d) HNO2
186. Odredite oksidacioni broj hlora u slede}im jediwewima:
a) HClO, b) HClO4, v) ClO2, g) Cl2O7, d) CCl4
187. Odredite oksidacioni broj ugqenika u slede}im jediwewima: a) CH4, b) C2H4, v) CO, g) CO2
188. Odredite oksidacione brojeve elemenata u slede}im jediwewima:
a) KMnO4, b) Ca(OCl)2, v) H2SO4, g) Na2HPO4, d) Na2B4O7, |) HgCl2
189. Odredite metodom oksidacionih brojeva koeficijente u slede}im shemama oksido-redukcionih reakcija:
a) KMnO4 + HCl „ KCl + MnCl2 + H2O + Cl2,
b) K2Cr2O7 + H2S + H2SO4 „ S + Cr2(SO4)3 + K2SO4 + H2O,
v) KI + KNO2 + H2SO4 „ I2 + NO + K2SO4 + H2O,
g) H2S + O2 „ SO2 + H2O,
d) I2 + KOH „ KIO3 + KI + H2O
190. Odredite jonsko-elektronskom metodom koeficijente u slede}im shemama oksido-redukcionih reakcija:
a) H2SO4 + Mg „ MgSO4 + H2S + H2O,
b) KIO4 + KI + HCl „ KCl + H2O + I2,
v) KMnO4 + NH3 „ KNO3 + MnO2 + KOH + H2O,
g) K2Cr2O7 + KBr + H2SO4 „ Cr2(SO4)3 + K2SO4 + Br2 + H2O,
d) HNO3 + Ag2S „ AgNO3 + NO2 + S + H2O
191. Odredite koeficijente u slede}im shemama oksido-redukcionih reakcija prikazanih u jonskom obliku:
a) Fe2+ + Cr2O7 2–+ H+ „ Fe3+ + Cr3+ + H2O,
b) Br – + BrO3 –+ H+ „ Br2 + H2O,
v) ClO4–+ Sn2+ + H+ „ Cl– + Sn4+ + H2O,
g) Cr2O7 2–+ Br– + H+ „ Cr3+ + Br2 + H2O
192. Izra~unajte koliko se litara hlora (n. u.) osloba|a ako se na 0,1 mol kalijum-permanganata deluje vi{kom hlorovodoni~ne kiseline.
193. Izra~unajte koliko se molova elementarnog joda oksiduje u jodnu kiselinu (HIO3) uz pomo} koncentrovane azotne kiseline, ako se pri tome osloba|a 9,96 l azot(IV)-oksida (n.u.). Kod re{avawa ovog zadatka najpre treba da sastavite jedna~inu oksido-redukcione reakcije, pa tek onda da pristupite stehiometrijskim izra~unavawima.
194. Izra~unajte standardnu entalpiju reakcije
SO2(g) + 1/2 O2(g) „ SO3(g)
195. Izra~unajte standardnu entalpiju reakcije
Fe2O3(s) + 2 Al(s) → Al2O3(s) + 2 Fe(s)
196. Reakcija termi~ke disocijacije amonijum-hlorida mo`e se prikazati slede}om hemijskom jedna~inom:
NH4Cl(s) → NH3(g) + HCl(g)
Izra~unajte standardnu entalpiju ove reakcije.
197. Izra~unajte standardnu entalpiju reakcije sagorevawa metana, koja se mo`e prikazati slede}om jedna~inom: CH4(g) + 2 O2(g) → CO2(g) + 2 H2O(l)
198. Izra~unajte standardnu entalpiju reakcije 3 CO(g) + Fe2O3(s) → 2 Fe(s) + 3 CO2(g).
199. Izra~unajte standardnu entalpiju slede}e hemijske reakcije: H2S(g) + 3/2 O2(g) → H2O(g) + SO2(g)
200. Izra~unajte standardnu entalpiju stvarawa HCl(g) na osnovu slede}e termohemijske jedna~ine: 1/2 H2(g) + 1/2 Cl2(g) → HCl(g), DrH = – 92,5 kJ/mol.
201. Izra~unajte standardnu entalpiju stvarawa etanola na osnovu slede}e termohemijske jedna~ine:
C2H5OH(l) + 3 O2(g) → 2 CO2(g) + 3 H2O(l) , DrH = – 1 366,8 kJ/mol
202. Izra~unajte standardnu entalpiju stvarawa PH3(g) polaze}i od slede}e termohemijske jedna~ine: 2 PH3(g) + 4 O2(g) → P2O5(s) + 3 H2O(l), DrH = – 2 360 kJ/mol
203. Pri reakciji 2,1 g gvo`|a sa sumporom osloba|a se 3,77 kJ toplote. Izra~unajte standardnu entalpiju stvarawa FeS
204. Izra~unajte standardnu entalpiju stvarawa CuO(s), ako se pri redukciji 20 g CuO pomo}u ugqenika vezuje 11,11 kJ toplote.
205. Koliko se toplote osloba|a pri sagorevawu 1 g vodonika u te~nu vodu?
206. Pri sagorevawu 6,538 g cinka u ~istom kiseoniku osloba|a se 34,82 kJ toplote. Izra~unajte standardnu reakcionu toplotu tog procesa.
207. Koliko se toplote osloba|a pri sagorevawu 1 g metalnog kalcijuma?
208. Izra~unajte koliko se toplote osloba|a pri sagorevawu 34 g te~nog etanola, C2H5OH. Uzmite u obzir da je nastala voda u te~nom stawu.
209. Vodonik-peroksid, H2O2, poznato sredstvo za beqewe kose razla`e se prema jedna~ini: H2O2(l) „ H2O(l) + 1/2 O2(g), DrH = – 98,2 kJ/mol Izra~unajte koliko se toplote osloba|a pri razlagawu 1 g H2O2.
210. Na osnovu termohemijskih jedna~ina: 1/2 N2(g) + 1/2 O2(g) → NO(g), DrH1 = + 90,5 kJ/mol, NO(g) + 1/2 O2(g) → NO2(g), DrH2 = – 56,6 kJ/mol, izra~unajte reakcionu toplotu oksidacije azota u azot(IV)-oksid prema jedna~ini: 1/2 N2(g) + O2(g) „ NO2(g), DrH3 = ? Tre}u termohemijsku jedna~inu dobi}ete sabirawem prve i druge jedna~ine.
211. Na osnovu termohemijskih jedna~ina:
As2O3(s) + O2(g) → As2O5(s) , DrH1 = – 271 kJ/mol
3 As2O3(s) + 2 O3(g) → 3 As2O5(s), DrH2 = – 1 096 kJ/mol
Izra~unajte standardnu entalpiju stvarawa ozona iz molekulskog kiseonika prema jedna~ini:
3 O2(g) → 2 O3(g), DrH3 = ?
Dobijeni rezultat izrazite u kJ po molu O3
Da bismo vam pomogli pri re{avawu zadatka, napomiwemo da se tre}a termohemijska jedna~ina dobija tako {to se prva jedna~ina pomno`i sa 3, a zatim od dobijenog izraza oduzme druga jedna~ina.
212. Izrazite brzinu reakcije C2H5Cl → C2H4 + HCl promenom koncentracije hlorovodonika sa vremenom.
213. Izrazite brzinu reakcije 2 NOCl → 2 NO + Cl2 promenom koncentracije azot(II)-oksida sa vremenom.
214. Izrazite brzinu reakcije 2 SO2 + O2 „ 2 SO3 promenom koncentracije SO2 sa vremenom.
215. Izra~unajte brzinu reakcije C + D → CD promenom koncentracije reakcionog proizvoda CD sa vremenom. U jednom trenutku wegova koncentracija iznosila je 0,506 mol/dm3, a 5 sekundi nakon toga 0,512 mol/dm3 .
216. Brzina reakcije A + 2 V → AV2 iznosi 1,6 10–2 mol/dm3 s. U nekom trenutku t1 koncentracija reaktanta A iznosila je 0,13 mol/dm3
Izra~unajte koncentraciju te komponente 5 sekundi posle toga.
217. Brzina reakcije A + V → AV iznosi 8 · 10–4 mol/dm3 · s. Izra~unajte za koje }e se vreme koncentracija komponente A smawiti od 0,04 na 0,032 mol/dm3
218. Napi{ite izraze za brzine slede}ih jednostepenih reakcija:
a) A(g) + 2 V(g) → C(g),
b) 2 A(l) + V(g) → C(s),
v) A(aq) + 2 V(aq) → C(aq), primenom zakona o dejstvu masa.
219. Napi{ite izraz za brzinu slede}e heterogene reakcije: C(s) + O2(g) → CO2(g), primenom zakona o dejstvu masa.
220. Brzina hemijske reakcije
2 NO(g) + O2(g) → 2 NO2(g) pri koncentraciji reaktanata [NO] = 0,3 mol/dm3 i [O2] = 0,15 mol/dm3 iznosi 1,2 · 10–3 mol/dm3 · s. Izra~unajte konstantu brzine ove reakcije.
221. Koliko se puta pove}ava brzina reakcije 2 A + V → A2V, ako se koncentracija komponente A pove}a 2 puta, a koncentracija komponente V smawi 2 puta?
222. U reakcionom sistemu CO(g) + Cl2(g) → COCl2(g) koncentracija CO pove}ana je sa 0,3 na 1,2 mol/dm3, a koncentracija hlora sa 0,2 na 0,6 mol/dm3. Koliko puta se pove}ala brzina reakcije?
223. Napi{ite izraze za konstante ravnote`e slede}ih homogenih reakcija:
a) 2 SO2(g) + O2(g) „ 2 SO3(g),
b) COCl2(g) „ CO(g) + Cl2(g), v) N2(g) + 3 H2(g) „ 2 NH3(g)
224. Napi{ite izraze za konstante ravnote`e slede}ih reakcija:
a) Zn(s) + 2 Ag+(aq) „ Zn2+(aq) + 2 Ag(s),
b) PbI2(s) „ Pb2+(aq) + 2 I–(aq),
v) CN–(aq) + H2O(l) „ HCN(aq) + OH–(aq).
225. Izra~unajte konstantu ravnote`e reakcije:
2 SO2(g) + O2(g) „ 2 SO3(g), ako je ravnote`na koncentracija SO2 0,04 mol/dm3, O2 0,06 mol/dm3, a SO3 0,02 mol/dm3
226. Izra~unajte konstantu ravnote`e reakcije
2 HI(g) „ H2(g) + I2(g), na 448 ºC, ako su na toj temperaturi parcijalni pritisci gasova u stawu ravnote`e jednaki: p(H)2 = 7,5 · 10–3 bar, p(I2) = 4,3 · 10–5 bar, p(HI) = 4 · 10–3 bar
227. Pri sintezi amonijaka iz elemenata pod odre|enim uslovima, u ravnote`i se nalazi 0,1 mol/dm3 N2, 0,2 mol/dm3 H2 i 0,8 mol/dm3 NH3. Izra~unajte konstantu ravnote`e ove reakcije, kao i polazne koncentracije N2 i H2
228. U sistemu A(g) + 2 V(g) „ C(g) ravnote`ne koncentracije iznose: [A] = 0,6 mol/dm3 , [V] = 1,2 mol/dm3 , [S] = 2,16 mol/dm3. Izra~unajte konstantu ravnote`e ove reakcije, kao i polazne koncentracije reaktanata.
229. U zatvorenom sudu odigrava se reakcija H2(g) + I2(g) „ 2 HI Na 450 ºC konstanta ravnote`e ove reakcije, K = 50. Kolika }e biti konstanta ravnote`e povratne reakcije (tj. reakcije razlagawa HI) na istoj temperaturi?
230. Izra~unajte konstantu ravnote`e reakcije Cl2(g) „ 2 Cl(g), ako je polazna koncentracija Cl2 bila 0,04 mol/dm3, a tokom reakcije se 5 % molekulskog hlora razlo`ilo na atome.
231. Polazne koncentracije CO i H2O u ravnote`nom sistemu
CO(g) + H2O(g) „ CO2(g) + H2(g) su iste i iznose 0,03 mol/dm3. Izra~unajte ravnote`ne koncentracije CO i H2O, ako su ravnote`ne koncentracije CO2 i H2 jednake 0,01 mol/dm3
232. U zatvorenom sudu zapremine 1 dm3 na odre|enoj temperaturi reaguje 2,94 mol I2 i 8,1 mol H2, grade}i 5,64 mol HI. Izra~unajte ravnote`ne koncentracije I2 i H2
233. Konstanta ravnote`e reakcije H2(g) + I2(g) „ 2 HI(g) na odre|enoj temperaturi iznosi 36. Izra~unajte koli~inu molekula HI u sudu nakon uspostavqawa ravnote`e, ako su koli~ine H2 i I2 u stawu ravnote`e iste i iznose 0,5 mol
234. Koliko }e grama HI(g) nastati pri reakciji 0,1 mol H2(g) sa 0,2 mol I2(g)? Pri reakciji temperatura i pritisak su takvi da se 20 % H2 pretvara u HI
235. U kojem se smeru pomera ravnote`a reakcije
3 Fe(s) + 4 H2O(g) „ Fe3O4(s) + 4 H2(g), ako se pove}a koncentracija vodonika?
236. Kako }e na polo`aj ravnote`e sistema Ag+(aq) + Cl–(aq) „ AgCl(s) uticati dodatak vi{ka AgCl(s)?
237. Kako }e uticati na polo`aj ravnote`e zagrevawe slede}eg ravnote`nog sistema:
N2(g) + 3 H2(g) „ 2 NH3(g), DrH = – 92 kJ/mol?
238. Da li }e se pri zagrevawu ravnote`nog sistema
2 HI(g) „ H2(g) + I2(g), DrH = – 25,9 kJ/mol pove}ati ili smawiti ravnote`na koncentracija HI?
239. U kom se smeru pomera ravnote`a reakcije
2 NO2(g) „ N2O4(g), DrH = – 57,3 kJ/mol pri: a) pove}awu pritiska, b) smawewu temperature?
240. Predvidite, na osnovu Le [ateqeovog principa, u koju }e se stranu pomeriti ravnote`a pri sabijawu slede}ih ravnote`nih sistema:
a) N2(g) + 3 H2(g) „ 2 NH3(g),
b) CO(g) + 2 H2(g) „ CH3OH(g),
v) H2(g) + I2(g) „ 2 HI(g)
241. Kako }e uticati smawewe pritiska na polo`aj ravnote`e slede}eg sistema:
2 H2(g) + O2(g) „ 2 H2O(g)?
242. Koliko }e se puta promeniti brzine v1 i v2 slede}e povratne reakcije:
v1
2 NO(g) + O2(g) „ 2 NO2(g), v2 ako se pritisak gasne sme{e pove}a 2 puta (pri konstantnoj temperaturi)?
243. Razmotrite povratnu reakciju
4 HCl(g) + O2(g) „ 2 H2O(g) + 2 Cl2(g), DrH = – 112,9 kJ/mol,
i odgovorite kako }e na ravnote`nu koncentraciju Cl2 uticati slede}e promene:
a) povi{ewe temperature reakcionog sistema, b) smawewe pritiska gasne sme{e, v) pove}awe koncentracije kiseonika.
244. Reakcija razlagawa PCl5 prikazana je slede}om termohemijskom jedna~inom:
PCl5(g) „ PCl3(g) + Cl2(g), DrH = + 92,6 kJ/mol
Kako treba promeniti: a) pritisak, b) temperaturu, v) koncentracije komponenata, da bi se ravnote`a pomerila u smeru razlagawa PCl5?
Disperzni sistemi se dobijaju tako što se usitwene åestice jedne supstance ravnomerno raspodele izmeðu åestica druge supstance. Supstanca koja se raspodequje zove se disperzna faza, a supstanca u kojoj se disperzna faza raspodequje – disperzno sredstvo
Prema veliåini åestica disperzne faze, disperzni sistemi se dele na:
1. grubo disperzne – åestice disperzne faze su veãe od 100 nm, i åesto se vide golim okom. Grubo disperzni sistemi su nestabilni – åestice disperzne faze se izdvajaju u vidu taloga ili isplivavaju na površinu (tj. teånost se raslojava).
2. koloidno disperzne – veliåina åestica disperzne faze kreãe se od 1 nm do 100 nm
3. molekulsko disperzne – veliåina åestica disperzne faze (molekula ili jona) mawa je od 1 nm Ovakvi sistemi su homogeni i stabilni i nazivaju se rastvori.
Svaki rastvor sastoji se od dve komponente: rastvaraåa i rastvorene supstance. Kao rastvaraå najviše se koristi voda, koja dobro rastvara mnoge åvrste, teåne i gasovite supstance. Rastvaraå je ona komponenta koje ima najviše, ili se nalazi u istom agregatnom stawu kao i rastvor. Rastvori mogu biti u åvrstom, teånom i gasovitom agregatnom stawu. Primer åvrstih rastvora je zlato za nakit, koje predstavqa rastvor bakra u zlatu. Primer teånih rastvora su vodeni rastvori razliåitih soli u vodi. Åist vazduh je primer gasovitog rastvora kiseonika, argona i nekih drugih gasova u azotu.
Rastvorqivost åvrstih supstanci u vodi veoma je razliåita, i zavisi od prirode supstance i temperature. Porastom temperature rastvorqivost åvrstih supstanci najåešãe raste.
Kao merilo rastvorqivosti åvrstih supstanci u vodi sluþi koncentracija wihovih zasiãenih rastvora.
Koncentracija zasiãenih rastvora jonskih supstanci obiåno se izraþava masom bezvodne soli koja moþe da se rastvori u 100 g vode na odreðenoj temperaturi.
Tablica 18. Rastvorqivost nekih soli u 100 g vode na razliåitoj temperaturi
Температура (°C) 0 102030 40506080 100
3 13,320,931,645,863,978,6108,3168,8246 NH4Cl 29,433,137,241,445,850,455,365,677,3
35,735,735,936 36,436,637 37,939,1
Poznavawe rastvorqivosti soli na razliåitim temperaturama omoguãava izraåunavawe mase soli koja ãe se iskristalisati pri hlaðewu rastvora.
Пример
Koliko ãe se grama amonijum-hlorida iskristalisati pri hlaðewu 250 g zasiãenog rastvora te soli od 60 °C na 10 °C?
U tablici 18 nalazimo da je rastvorqivost NH4Cl na 60 °C 55,3 g , a na 10 °C 33,1 g. Rastvarawem 55,3 g NH4Cl u 100 g vode na 60 °C dobija se 155,3 g zasiãenog rastvora.
Masu amonijum-hlorida koji se nalazi u 250 g zasiãenog rastvora na 60 °C izraåunaãemo iz sledeãe proporcije:
155,3 g : 55,3 g = 250 g : x,
55,3 g · 250 g x = ____________ = 89 g. 155,3 g
U 250 g zasiãenog rastvora na 60 °C nalazi se:
250 g – 89 g = 161 g vode.
Postupak rešavawa zadataka ovog tipa zasniva se na åiwenici da se pri hlaðewu rastvora masa vode ne mewa.
Masu NH4Cl koji se nalazi u 161 g vode na 10 °C izraåunaãemo iz sledeãe proporcije:
33,1 g : 100 g = x : 161 g,
33,1 g · 161 g x = ____________ = 53,3 g. 100 g
Razlika 89 g – 53,3 g = 35,7 g predstavqa masu NH4Cl koji se izdvaja u obliku kristala pri hlaðewu 250 g zasiãenog rastvora od 60 °C na 10 °C
Odgovor: Pri hlaðewu zasiãenog rastvora izdvaja se 35,7 g kristalnog amonijum-hlorida.
KVANTITATIVNI SASTAV RASTVORA
Kvantitativni sastav rastvora izraþava se pomoãu više fiziåkih veliåina. Mi ãemo upoznati tri takve veliåine, koje se u hemiji najviše koriste, a to su: maseni udeo, koliåinska koncentracija i molalnost.
Maseni udeo supstance B u rastvoru, w(B) definiše se kao odnos mase te supstance, m(B) i ukupne mase rastvora, m:
m(B) w(B) = ______ . (23) m
Maseni udeo je brojåana veliåina, åija je merna jedinica 1. Obiåno se izraþava u procentima.
Пример
Izraåunati maseni udeo natrijum-hlorida u rastvoru koji je dobijen rastvarawem 5 g NaCl u 200 g vode.
m(NaCl) = 5 g,
m(H2O) = 200 g, w(NaCl) = ?
Ukupna masa rastvora, m jednaka je zbiru mase soli i vode:
m = 5 g + 200 g = 205 g.
Uvrštavawem zadanih brojåanih vrednosti u jednaåinu (23) dobijamo: 5 g
w(NaCl) = _____ = 0,024 = 2,4 %. 205 g
Odgovor: Maseni udeo NaCl u rastvoru je 2,4 %.
Пример
Koliko je grama KOH potrebno za pripremawe 500 cm3 40 % rastvora, gustine ρ = 1,4 g/cm3?
Izraåunajmo najpre masu 500 cm3 40 % rastvora KOH:
m = ρ · V = 1,4 g/cm3 · 500 cm3 = 700 g.
Iz jednaåine (23) sledi:
m(KOH) = w(KOH) · m = 0,40 · 700 g = 280 g.
Odgovor: Za pripremawe 500 cm3 40 % rastvora KOH potrebno je 280 g KOH
Koliåinska koncentracija supstance B u rastvoru, c(B), definiše se kao odnos koliåine te supstance, n(B) i zapremine rastvora, V:
n(B)
c(B) = (24) V
SI-jedinica koliåinske koncentracije je mol/m3, ali se u hemiji najåešãe koristi decimalna SI-jedinica mol/dm3
Пример 51
Izraåunati koliko je grama bezvodnog natrijum-karbonata, Na2CO3 potrebno za pripremawe 500 cm3 rastvora koliåinske koncentracije 0,5 mol/dm3. Molarna masa natrijum-karbonata je 106 g/mol.
V = 500 cm3 = 0,5 dm3 ,
c(Na2CO3) = 0,5 mol/dm3 ,
M(Na2CO3) = 106 g/mol,
m(Na2CO3) = ?
Potrebnu koliåinu Na2CO3 izraåunaãemo prema izrazu (24) ovako:
n(Na2CO3) = c · V = 0,5 mol/dm3 · 0,5 dm3 = 0,25 mol.
Prema jednaåini 13 (vidi str. 57), masa 0,25 mol Na2CO3 jednaka je:
m(Na2CO3) = n · M = 0,25 mol · 106 g/mol = 26,5 g
Odgovor: Za pripremawe 500 cm3 rastvora Na2CO3, c = 0,5 mol/dm3 , treba odmeriti na vagi 26,5 g natrijum-karbonata.
Пример 52
Koliko je kubnih centimetara 96 % sumporne kiseline, gustine 1,84 g/cm3, potrebno za pripremawe 1 dm3 rastvora koliåinske koncentracije 0,1 mol/dm3? Molarna masa sumporne kiseline je 98 g/mol. Izraåunajmo najpre koliåinu åiste sumporne kiseline koja je potrebna za pripremawe rastvora zadane koncentracije:
n(H2SO4) = c(H2SO4) · V = 0,1 mol/dm3 · 1 dm3 = 0,1 mol.
Odredimo masu 0,1 mol H2SO4:
m(H2SO4) = n · M = 0,1 mol · 98 g/mol = 9,8 g.
Masu 96 % sumporne kiseline koja sadrþi 9,8 g åiste kiseline izraåunaãemo iz sledeãe proporcije:
100 g : 96 g = x : 9,8 g,
100 g · 9,8 g x = = 10,2 g. 96 g
Izraåunajmo zapreminu 10,2 g 96 % sumporne kiseline:
m 10,2 g
V(96 % H2SO4) = = = 5,5 cm3
ρ 1,84 g cm–3
Odgovor: Za pripremawe 1 dm3 rastvora H2SO4, c = 0,1 mol/dm3 , potrebno je 5,5 cm3 96 % sumporne kiseline.
Molalnost rastvorene supstance b(B) definiše se kao odnos koliåine te supstance, n(B) i mase rastvaraåa: n(B)
b(B) = (25)
m (rastvaraåa)
SI-jedinica molalnosti je mol/kg.
Izraåunati molalnost rastvora saharoze koji je dobijen rastvarawem 20 g te supstance u 500 g vode. Molarna masa saharoze je 342,3 g/mol.
Izraåunajmo najpre koliåinu molekula C12H22O11 u 20 g saharoze:
m 20 g
n(C12H22O11) = = = 0,058 mol.
M 342,3 g mol–1
Molalnost rastvora saharoze izraåunaãemo prema izrazu (25) na sledeãi naåin:
n(C12H22O11) 0,058 mol
b(C12H22O11) = = = 0,12 mol/kg.
m(H2O) 0,5 kg
Odgovor: Molalnost rastvora saharoze je 0,12 mol/kg.
Razblaþeni rastvori neelektrolita poseduju neka svojstva koja u najveãoj meri zavise od broja åestica rastvorene supstance. Ova svojstva rastvora, koja se nazivaju koligativna, su: osmotski pritisak, sniþewe temperature mrþwewa, povišewe temperature kquåawa itd.
Osmoza i osmotski pritisak. – Ako su dva rastvora razliåitih koncentracija razdvojena polupropustqivom membranom (koja propušta samo molekule rastvaraåa), tada ãe molekuli rastvaraåa difundovati kroz membranu i razblaþivati rastvor veãe koncentracije. Taj proces naziva se osmoza
Pretpostavimo da se rastvor neelektrolita nalazi u staklenom sudu åiji je gorwi kraj izvuåen u usku cev, a dno zatvoreno polupropustqivom membranom. Ako ovaj sud stavimo u åašu napuwenu åistim rastvaraåem, primetiãemo da nivo teånosti u cevi postepeno raste usled prodirawa rastvaraåa kroz polupropustqivu membranu u sud (slika 21).
Proces teåe sve dotle dok se hidrostatiåki pritisak teånosti u cevi ne izjednaåi sa pritiskom molekula rastvaraåa na polupropustqivu membranu. Taj ravnoteþni hidrostatiåki pritisak naziva se osmotski pritisak rastvora.
Osmotski pritisak rastvora jednak je pritisku koji bi vršili molekuli rastvorene supstance kada bi se nalazili u gasovitom stawu pri istoj temperaturi i u zapremini jednakoj zapremini rastvora. Prema tome, razblaþeni rastvori neelektrolita ponašaju se kao idealni gasovi.
Izraz za osmotski pritisak rastvora identiåan je sa jednaåinom stawa idealnih gasova:
π = c R T, (26) gde je:
π – osmotski pritisak rastvora, c – koliåinska koncentracija rastvorene supstance, R – univerzalna gasna konstanta, jednaka 8,31 J/K mol, T – termodinamiåka temperatura.
Пример 54
Izraåunati osmotski pritisak rastvora saharoze koliåinske koncentracije 0,1 mol/dm3 i temperature 10 °C (283 K).
c = 0,1 mol/dm3 = 100 mol/m3 , T = 283 K,
π = ?
π = c R T = 100 mol/m3 · 8,31 J/K mol · 283 K = 2,35 · 105 J/m3
Ako u ovaj izraz uvrstimo definiciju yula (kg m2 s–2) dobiãemo: kg m2 s–2
π = 2,35 · 105 = 2,35 · 105 kg m–1 s–2 m3
Kako je kg m–1 s–2 definicija paskala (vidi tablicu 3), osmotski pritisak rastvora je 2,35 · 105 Pa, odnosno 2,35 bar ili 235 kPa.
Odgovor: Osmotski pritisak rastvora saharoze je 235 kPa
Sniþewe temperature mrþwewa i povišewe temperature kquåawa. – Rastvori mrznu na niþoj temperaturi a kquåaju na višoj temperaturi od åistog rastvaraåa. Sniþewe temperature mrþwewa (odnosno povišewe temperature kquåawa) razblaþenih rastvora proporcionalno je wihovoj molalnosti:
∆T = K · b(B) (27)
gde je:
∆T – razlika izmeðu temperature mrþwewa (odnosno temperature kquåawa) rastvora i rastvaraåa, K – molalna konstanta sniþewa temperature mrþwewa (odnosno povišewa temperature kquåawa) rastvaraåa, b(B) – molalnost rastvorene supstance.
Molalna konstanta sniþewa temperature mrþwewa zove se krioskopska konstanta, Kk, a molalna konstanta povišewa temperature kquåawa – ebulioskopska konstanta, K e. U tablici 19 prikazane su vrednosti krioskopskih i ebulioskopskih konstanti nekih rastvaraåa.
Tablica 19. Krioskopske i ebulioskopske konstante nekih rastvaraåa
Na osnovu sniþewa temperature mrþwewa, odnosno povišewa temperature kquåawa razblaþenih rastvora neelektrolita, moþe se odrediti molarna masa rastvorene supstance. Kao osnova za izraåunavawe sluþi izraz (27) koji se transformiše u jednaåinu:
K · m(B)
M(B) = (28)
m(A) · ∆T
gde je:
M(B) – molarna masa rastvorene supstance, K – krioskopska (ili ebulioskopska) konstanta rastvaraåa,
m(B) – masa rastvorene supstance,
m(A) – masa rastvaraåa,
∆T – razlika izmeðu temperature mrþwewa (odnosno temperature kquåawa) rastvora i rastvaraåa.
Пример 55
U 325 g benzena rastvoreno je 40 g nepoznatog organskog jediwewa. Temperatura mrþwewa dobijenog rastvora je za 0,85 K niþa od temperature mrþwewa åistog benzena. Izraåunati molarnu masu organskog jediwewa.
m(benzen) = 325 g = 0,325 kg,
m(B) = 40 g,
∆T = 0,85 K,
Kk (benzen) = 5,12 K kg/mol,
M(B) = ?
5,12 K kg/mol–1 40 g
M(B) = ___________________ = 742 g/mol.
0,325 kg 0,85 K
Odgovor: Molarna masa nepoznatog organskog jediwewa je 742 g/mol.
Elektroliti su supstance åiji vodeni rastvori i rastopi provode elektriånu struju. U elektrolite spadaju kiseline, baze i soli.
Znatno je veãi broj supstanci åiji vodeni rastvori i rastopi ne provode struju. U ove supstance (tzv. neelektrolite) spada veãina organskih jediwewa. Na primer: etanol, saharoza i glicerol.
Prema teoriji elektrolitiåke disocijacije, elektroliti se pri rastvarawu u vodi disosuju (raspadaju) na pozitivno i negativno naelektrisane åestice – jone, koji provode struju kroz rastvor. Mehanizam obrazovawa jona u vodenim rastvorima elektrolita je razliåit, zavisno od prirode veza izmeðu åestica u ovim jediwewima.
Kristalne rešetke jonskih jediwewa sastoje se od pozitivno i negativno naelektrisanih jona. Disocijacija ovih jediwewa sastoji se u razgradwi wihovih kristalnih rešetki pod uticajem polarnih molekula vode, pri åemu se iz wih oslobaðaju odgovarajuãi joni.
Pri rastvarawu polarnih kovalentnih jediwewa u vodi, dolazi do hemijske reakcije izmeðu wihovih molekula i polarnih molekula vode, i nastaju joni. Ovaj proces naziva se jonizacija. Obrazovane jone u rastvoru okruþuju polarni molekuli vode, tj. oni se hidratizuju.
Stepen disocijacije, α, sluþi za izraþavawe jaåine elektrolita. Definiše se kao odnos izmeðu broja molekula disosovanih na jone, Ndis i ukupnog broja molekula koji su uneti u rastvor, Nuk
Ndis α = . (29) Nuk
Brojåana vrednost α kreãe se u intervalu od 0 do 1, odnosno od 0 do 100 %.
Jaki i slabi elektroliti. – Ako je stepen disocijacije elektrolita u rastvoru koncentracije 0,1 mol/dm3 veãi od 30 %, on spada u jake elektrolite. U jake elektrolite spada veãina soli dobro rastvorqivih u vodi. Od kiselina i baza, u jake elektrolite spadaju: H2SO4, HCl, HNO3, NaOH, KOH itd.
Kod slabih elektrolita koncentracije 0,1 mol/dm3 stepen disocijacije je mawi od 3 %. U slabe elektrolite spadaju: sirãetna kiselina, cijanovodoniåna kiselina, amonijak itd.
Jaki elektroliti su u vodenom rastvoru skoro u potpunosti disosovani na jone. Stoga proces disocijacije ovih jediwewa moþemo posmatrati kao nepovratni proces.
Disocijacija slabih elektrolita u vodenom rastvoru je povratni proces. U rastvorima ovih jediwewa uspostavqa se dinamiåka ravnoteþa izmeðu nedisosovanih molekula i nastalih jona. Prema tome, na proces disocijacije slabih elektrolita moþe se primeniti zakon o dejstvu masa bez ikakvih dopunskih uslova i popravki.
U opštem sluåaju, disocijacija slabog elektrolita AB u vodenom rastvoru moþe se prikazati sledeãom jednaåinom:
AB „ A+ + B–.
Konstanta ravnoteþe ove reakcije je:
[A+] [B–] K = . (30) [AB]
U izrazu (30) koncentracije [A+], [B–] i [AB] predstavqaju ravnoteþne koncentracije.
Konstanta ravnoteþe, K, navedenog procesa disocijacije slabog elektrolita naziva se konstanta disocijacije. Wena brojåana vrednost pokazuje jaåinu elektrolita – što je ona veãa, u stawu ravnoteþe je veãa koncentracija jona u odnosu na koncentraciju nedisosovanih molekula, i elektrolit je jaåi.
Konstanta disocijacije slabih elektrolita povezana je sa stepenom disocijacije sledeãim izrazom:
α2 c K = (31) 1 – α
gde je:
K – konstanta disocijacije, α – stepen disocijacije, c – koliåinska koncentracija elektrolita.
Kod jako slabih elektrolita α je veoma malo, te se moþe uzeti da je 1 – α ≈ 1. U tom sluåaju, izraz (31) se transformiše u jednaåinu:
K = α2 c (32)
Пример 56
Stepen disocijacije sirãetne kiseline u rastvoru koncentracije 0,1 mol/dm3 iznosi 0,0132. Izraåunati konstantu disocijacije ove kiseline. α2 c 0,01322 · 0,1 mol · dm–3 K = = ______________________ =1,77 · 10–5 mol/dm3 1 – α 1 – 0,0132
Odgovor: Konstanta disocijacije sirãetne kiseline je 1,77 10–5 mol/dm3
Пример 57
Konstanta disocijacije cijanovodoniåne kiseline iznosi 7,9 · 10–10 mol/dm3. Izraåunati stepen disocijacije ove kiseline u rastvoru koncentracije 10–3 mol/dm3 . Pošto je cijanovodoniåna kiselina u vodenom rastvoru veoma slabo disosovana, to se za pribliþno izraåunavawe moþe koristiti izraz (32). Iz ovog izraza sledi:
K 7,9 · 10–10 mol /dm–3 α = = = 8,9 · 10–4 . c 10–3 mol /dm–3
Odgovor: Stepen disocijacije cijanovodoniåne kiseline koncentracije 10–3 mol/dm3 je 8,9 · 10–4
245. U koju grupu disperznih sistema spada mutna re~na voda?
246. U koju grupu disperznih sistema spada bistra morska voda?
247. Homogenizovano mleko sadr`i veoma sitne kapqice mle~ne masti, ravnomerno raspore|ene po ~itavoj zapremini te~nosti. U koju grupu disperznih sistema spada mleko?
248. U 100 g vode na 20 °C rastvara se 204 g {e}era. Koja komponenta se smatra rastvara~em?
249. Koja se komponenta smatra rastvara~em u slede}im homogenim sme{ama: a) sme{i 1 g alkohola i 100 g vode, b) sme{i 1 g vode i 100 g alkohola?
250. Rastvorqivost kalijum-hlorata, KClO3, na 70 °C je 30,2 g, a na 30 °C 10,1 g. Koliko }e se grama ove soli iskristalisati iz 70 g zasi}enog rastvora ako se on ohladi od 70 °C na 30 °C?
251. Izra~unajte koliko }e se grama kalijum-nitrata iskristalisati pri hla|ewu 100 g zasi}enog rastvora te supstance od 80 °C na 20 °C
252. Izra~unajte koliko }e se grama `iva(II)-hlorida iskristalisati pri hla|ewu 500 g zasi}enog rastvora te supstance od 40 °C na 10 °C
253. Izra~unajte maseni udeo etanola u rastvoru koji je dobijen me{awem 30 g etanola sa 50 g vode.
254. Koliki je maseni udeo natrijum-karbonata u rastvoru ako je posle isparavawa 10 g tog rastvora u sudu zaostalo 0,06 g Na2CO3?
255. U 1 kg vode rastvoreno je 666 g kalijum-hidroksida. Izra~unajte maseni udeo KOH u rastvoru.
256. Izra~unajte koliko je grama natrijum-hidroksida i vode potrebno za pripremawe 250 g 10 % rastvora.
257. Koliko je grama bezvodnog bakar(II)-sulfata potrebno za pripremawe 500 g 9 % rastvora?
258. Rastvorqivost AgNO3 u vodi na 0 °C je 125,2 g. Izra~unajte maseni udeo AgNO3 u zasi}enom rastvoru na 0 °C
259. U koliko grama vode treba rastvoriti 100 g K2SO4 da bi se dobio 5 % rastvor?
260. Izra~unajte koliko grama FeSO4 · 7 H2O treba rastvoriti u vodi da bi se dobilo 400 g 4,2 % rastvora FeSO4.
261. Koliko je grama bezvodnog natrijum-sulfata potrebno za pripremawe 10 dm3 8 % rastvora, gustine 1,075 g/cm3?
262. Izra~unajte zapreminu 96 % sumporne kiseline (ρ = 1,84 g/cm3) i masu vode koja je potrebna za pripremawe 100 cm3 15 % rastvora H2SO4 (ρ = 1,1 g/cm3).
263. Koliko je kubnih centimetara 92 % sumporne kiseline, gustine 1,824 g/cm3 potrebno za pripremawe 5 dm3 20 % rastvora H2SO4 ~ija je gustina 1,14 g/cm3?
264. U 1 dm3 rastvora nalazi se 80 g natrijum-hidroksida. Izra~unajte koli~insku koncentraciju NaOH u rastvoru.
265. Posle uparavawa do suva 50 cm3 rastvora natrijum-hlorida u sudu je zaostalo 0,585 g te soli. Kolika je bila koli~inska koncentracija NaCl u rastvoru?
266. U 2 dm3 nalazi se 4,9 g sumporne kiseline. Izra~unajte koli~insku koncentraciju H2SO4 u rastvoru.
267. Izra~unajte koli~insku koncentraciju 95,7 % H2SO4 gustine 1,835 g/cm3
268. Izra~unajte koli~insku koncentraciju 20 % rastvora aluminijum-sulfata, Al2(SO4)3, gustine 1,23 g/cm3 .
269. Izra~unajte koliko je grama K2SO4 potrebno za pripremawe 200 cm3 rastvora koli~inske koncentracije 0,05 mol/dm3
270. Izra~unajte koliko se grama amonijum-hlorida, NH4Cl, nalazi u 0,6 dm3 rastvora koli~inske koncentracije 0,2 mol/dm3
271. Koliko se kubnih centimetara rastvora natrijum-hidrogenkarbonata, NaHCO3, koncentracije 1 mol/dm3 mo`e dobiti od 16,8 g NaHCO3?
272. Izra~unajte koliko je kubnih centimetara koncentrovane (36 %) hlorovodoni~ne kiseline, gustine 1,183 g/cm3, potrebno za pripremawe 100 cm3 rastvora koli~inske koncentracije 1 mol/dm3
273. Koliko je kubnih centimetara 40 % fosforne kiseline, H3PO4, (ρ = 1,25 g/cm3) potrebno za pripremawe 400 cm3 rastvora koli~inske koncentracije 0,25 mol/dm3?
274. Izra~unajte molalnost rastvora MgCl2 koji je dobijen rastvarawem 95 g te soli u 160 g vode.
275. Izra~unajte molalnost rastvora sumporne kiseline koji je dobijen rastvarawem 49 g ~iste H2SO4 u 1 kg vode.
276. Koliko je grama natrijum-karbonata i vode potrebno za pripremawe 100 g rastvora molalnosti 1 mol/kg?
277. Izra~unajte osmotski pritisak rastvora glukoze koli~inske koncentracije 0,5 mol/dm3 i temperature 25 °C. Dobijeni rezultat izrazite u megapaskalima.
278. Izra~unajte osmotski pritisak rastvora saharoze temperature 27 °C, ako se u 1 dm3 tog rastvora nalazi 91 g saharoze.
279. Izra~unajte temperaturu mr`wewa rastvora 54 g glukoze u 250 g vode.
M(C6H12O6) = 180 g/mol.
280. Izra~unajte temperaturu mr`wewa rastvora 2,60 g uree, CO(NH2)2, u 50 g vode. M(urea) = 60 g/mol.
281. Kolika je temperatura kqu~awa rastvora koji je dobijen rastvarawem 150 g saharoze u 260 g vode?
282. Temperatura kqu~awa etanola je 78,26 °C. Izra~unajte temperaturu kqu~awa rastvora koji sadr`i 0,25 g fenola u 4 g etanola.
M(fenol) = 94 g/mol
283. Pripremqena su dva rastvora: prvi, tako {to je u 1 kg vode rastvoreno 100 g glukoze i, drugi, tako {to je u 1 kg vode rastvoreno 100 g saharoze. Utvrdite koji }e rastvor imati vi{u temperaturu kqu~awa.
284. Rastvor 8 g nepoznate supstance u 100 g dietiletra kqu~a na 36,86 °C. Odredite molarnu masu rastvorene supstance, ako ~ist dietiletar kqu~a na 35,60 °C
285. Napi{ite jedna~ine reakcija disocijacije (jonizacije) slede}ih jediwewa u vodenom rastvoru: a) HCN, б) NaCl, в) NH3
286. Elektroliti A, V i S imaju konstante disocijacije KA, KV i KS, ~ije vrednosti stoje u slede}em odnosu: KS>KA>KV. Koji je od ovih elektrolita najja~i, a koji najslabiji?
287. Izra~unajte stepen disocijacije elektrolita, ako se od 1000 molekula unetih u rastvor 350 disosovalo na jone.
288. Date su vrednosti α za rastvore sir}etne kiseline razli~itih koncentracija:
s (mol/dm3) 0,1 0,080,03 0,01 α 1,34 10–2 1,5 10–2 2,45 10–2 4,15 10–2
Izra~unajte za svaku koncentraciju vrednost K.
289. Izra~unajte konstantu disocijacije fluorovodoni~ne kiseline, ako je u rastvoru koncentracije 0,1 mol/dm3 α= 0,074.
290. Izra~unajte stepen disocijacije hipohloritne kiseline, HClO u rastvoru koncentracije 0,2 mol/dm3. K = 5 · 10–8 mol/dm3
291. Izra~unajte stepen disocijacije azotaste kiseline, HNO2, u rastvoru koncentracije 0,05 mol/dm3. K = 4 · 10–4 mol/dm3


Prema ovoj teoriji kiseline su molekuli ili joni koji predaju vodonikov jon (proton) drugim molekulima ili jonima. Na primer:
H+
HCl + H2O „ H3O+ + Cl–, kis.
H+
H3O+ + OH– „ H2O + H2O, kis.
H+
HSO4– + H2O „ H3O+ + SO4 2–. kis.
Baze su molekuli ili joni koji primaju proton od drugih molekula ili jona. Na primer:
H+
NH3 + H2O „ NH4+ + OH–, baza
H+
CN– + H2O „ HCN + OH–. baza
Reakcije pri kojima dolazi do prelaska protona sa jednog molekula ili jona na drugi, nazivaju se protolitiåke reakcije. One se najåešãe odigravaju u vodenim rastvorima. Kiselo-bazne protolitiåke reakcije teku simultano. Pri svakoj reakciji izmeðu kiseline i baze nastaje novi par kiselina–baza. Na primer:
HCl + H2O „ H3O+ + Cl–kis. 1 baza 2 kis. 2 baza 1
Par kiselina–baza naziva se konjugovani (meðusobno povezani ili spregnuti par).
Tako kiselini 1 iz prethodnog primera (HCl) odgovara baza 1 (hloridni anjon Cl–), a bazi 2 (H2O ) odgovara kiselina 2 (hidronijum jon, H3O+ ). Što je kiselina (odnosno baza) jaåa, wena konjugovana baza (odnosno kiselina) je slabija i obratno. Tako je, npr., HCl jaka kiselina, stoga je wena konjugovana baza (Cl–) veoma slaba (slabija åak i od vode). Amonijak (NH3) je slaba baza, stoga je wegova konjugovana kiselina (amonijum jon, NH4+) jaåa kiselina od vode.
Voda moþe da se ponaša i kao baza i kao kiselina (tj. moþe da vezuje i otpušta proton), zavisno od toga sa kojom supstancom stupa u reakciju. Ona spada u amfoterne supstance
Jaåina kiselina i baza izraþava se wihovim konstantama disocijacije (vidi str. 103 i str. 111).
Prema protolitiåkoj teoriji, jonizacija jednobazne kiseline HA u vodenom rastvoru prikazuje se jednaåinom:
HA + H2O „ H3O+ + A–.
Ovaj naåin prikazivawa jonizacije kiselina je ispravniji od pojednostavqenog naåina pisawa:
HA „ H+ + A–,
pošto u vodenim rastvorima kiselina ne postoje slobodni joni H+ , veã hidratisani protoni, H3O+. Meðutim, drugi naåin pisawa je jednostavniji i åešãe se koristi, pa ãemo se i mi wime sluþiti. Takoðe ãemo sve ovakve reakcije nazivati reakcijama disocijacije, bez obzira na wihov mehanizam (vidi str. 103).
Konstanta ravnoteþe reakcije disocijacije kiseline HA jednaka je:
[H+] [A–] KA = (33) [HA]
i naziva se konstanta disocijacije kiseline, KA. Wena vrednost zavisi od prirode elektrolita i rastvaraåa i temperature, ali ne i od koncentracije rastvora. Što je brojåana vrednost KA veãa, kiselina je jaåa, i obratno.
Dvobazne i višebazne kiseline disosuju postepeno (tj. u nekoliko stupweva). Stoga je kod ovih kiselina poznato dve ili više konstanti disocijacije, od kojih je prva najveãa (tablica 20).
Tablica 20. Konstante disocijacije nekih slabih kiselina (na 25 °C)
Пример 58
Izraåunati ravnoteþne koncentracije H+ i CN– jona u rastvoru cijanovodoniåne kiseline koncentracije 0,5 mol/dm3 .
Prikaþimo najpre disocijaciju HCN u vodenom rastvoru:
HCN „ H+ + CN–
Izraz za konstantu disocijacije cijanovodoniåne kiseline glasi:
[H+] [CN–]
KA = __________ . [HCN]
Iz jednaåine disocijacije cijanovodoniåne kiseline se vidi da su ravnoteþne koncentracije H+ i CN– jona iste. Oznaåimo ove koncentracije sa x
Pošto se od 0,5 mol/dm3 HCN na jone disosovalo x mol/dm3, ravnoteþna koncentracija HCN jednaka je: 0,5 – x mol/dm3 .
Prema tome: x · x x2 KA = _____ = _____
HCN je veoma slaba kiselina, stoga se smawewe wene koncentracije usled disocijacije u prethodnom izrazu moþe zanemariti. Znaåi, uzeãemo da je 0,5 – x ≈ 0,5. Tako dobijamo:
x2
KA = Odavde je x = 0,5 · KA 0,5
U tablici 20 nalazimo da je konstanta disocijacije cijanovodoniåne kiseline 7,9 10–10 mol/dm3. Ako ovu vrednost uvrstimo u prethodnu jednaåinu, dobijamo:
x = 0,5 mol dm3 × 7,9 10–10 mol/dm–3 =
= 3,95 10–10 (mol dm–3)2 = 1,98 10–5 mol/dm3 .
Odgovor: Ravnoteþne koncentracije H+ i CN– jona u rastvoru HCN iznose 1,98 · 10–5 mol/dm3
Disocijacija baza u vodenom rastvoru moþe se prikazati sledeãom opštom jednaåinom:
B + H2O „ BH+ + OH–
Konstanta ravnoteþe ove reakcije
[BH+] [OH–]
KB = ____________ , (34) [B]
naziva se konstanta disocijacije baze, KB, i predstavqa merilo jaåine baze.
Konstanta disocijacije baze, K B i konstanta disocijacije wene konjugovane kiseline, KA, povezane su izrazom: KB · KA = K w. Odavde je:
K w KB = , (35) KA
gde je
K w – jonski proizvod vode (vidi str. 114).
Iz jednaåine (35) sledi da, ukoliko je baza jaåa (veãe KB), wena konjugovana kiselina je slabija (mawe KA), i obratno.
Пример 59
Konstanta disocijacije sirãetne kiseline je 1,8 · 10–5 mol/dm3 .
Izraåunati konstantu disocijacije wene konjugovane baze – acetatnih jona, CH3COO–.
K w 1· 10–14 mol2 dm–6
KB = = = 5,5 · 10–10 mol /dm3
KA 1,8· 10–5 mol dm–3
Odgovor: Konstanta disocijacije acetatnih jona je 5,5 · 10–10 mol/dm3 .
Amfoliti (amfoterni elektroliti) imaju svojstvo da se u vodenim rastvorima ponašaju i kao baze i kao kiseline, zavisno od reakcionih uslova. U amfolite spadaju slabo rastvorqivi hidroksidi aluminijuma, olova, hroma, cinka i nekih drugih metala. Ovi hidroksidi su u vodenom rastvoru hidratisani odreðenim brojem molekula vode. Tako je, npr., molekul aluminijum-hidroksida hidratisan sa tri molekula vode, te je wegova formula Al(H2O)3 (OH)3
Pri reakciji sa jakim kiselinama aluminijum-hidroksid se ponaša kao baza i prima protone:
3H+
Al(H2O)3(OH)3 + 3 H3O+ „ Al(H2O)6 3+ + 3 H2O. baza kis.
Pri reakciji sa jakim bazama aluminijum-hidroksid se ponaša kao kiselina i otpušta proton:
H+
Al(H2O)3(OH)3 + OH– „ [Al(H2O)2 (OH)4]– + H2O. kis. baza
Åista voda je veoma slab amfoterni elektrolit, koji u neznatnoj meri provodi elektriånu struju. Autoprotoliza vode moþe se prikazati sledeãom jednaåinom:
H2O + H2O „ H3O+ + OH–, odnosno H2O „ H+ + OH–
Izraz za konstantu disocijacije vode glasi:
[H+] [OH–] KB = __________ , (36) [H2O]
Na 25 °C konstanta disocijacije vode iznosi 1,8 · 10–16 mol/dm3 .
S obzirom da je u åistoj vodi neznatan broj molekula H2O disosovan na jone, moþe se uzeti da je ravnoteþna koncentracija nedisosovanih molekula vode, [H2O] , u izrazu (36) jednaka ukupnoj koncentraciji vode u 1 dm3 .
Izraåunajmo koliåinu molekula H2O u 1 dm3 (1000 g) vode:
m 1000 g n(H2O) = = = 55,5 mol. M 18 g mol–3
n(H2O) 55,5 mol
[H2O] = = = 55,5 mol/dm3 . V 1 dm3
Iz izraza (36) sledi:
[H+][OH–] = K[H2O] = 1,8 · 10–16 mol/dm3 x 55,5 mol/dm3 = = 1 · 10–14 mol2/dm6.
Dobijeni izraz naziva se jonski proizvod vode, K w. Na 25 °C on iznosi:
K w = [H+][OH–] = 1 · 10–14 mol2 / dm6 (37)
Promenom temperature mewa se i vrednost jonskog proizvoda vode. U åistoj vodi ravnoteþne koncentracije H+ i OH– jona su jednake, i na 25 °C iznose 10–7 mol/dm3 .
Ako u åistu vodu dodamo malo kiseline (tj. poveãamo koncentraciju H+ jona), smawiãe se koncentracija OH– jona, kako bi konstanta K w ostala ista.
Ako, pak, u åistu vodu dodamo malo rastvora baze (tj. poveãamo koncentraciju OH– jona), smawiãe se koncentracija H+ jona kako bi konstanta K w ostala ista. Prema tome,
u neutralnim rastvorima [H+] = [OH–] = 10–7 mol/dm3 ,
u kiselim rastvorima [H+] > 10–7 mol/dm3 ,
u baznim rastvorima [H+] < 10–7 mol/dm3
Пример 60
Izraåunati koncentraciju H+ jona u rastvoru u kome je koncentracija OH– jona 7,4 · 10–11 mol/dm3 .
Iz jednaåine (37) sledi:
Kw 1 · 10–14 mol2 dm–6
[H+] = = = 1,35 · 10–4 mol/dm3 [OH–] 7,4 · 10–11 mol dm–3
Odgovor: Koncentracija H+ jona u rastvoru iznosi 1,35 · 10–4 mol/dm3
VODONIÅNI EKSPONENT, rN
Vodoniåni eksponent sluþi za izraþavawe kiselosti i baznosti rastvora. Definiše se kao negativni dekadni logaritam koncentracije vodonikovih jona u rastvoru:
pH = – log [H+] / mol dm–3 (38)
Pošto se izraz (38) deli sa mol/dm3 , pH je brojåana (bezdimenziona) veliåina.
Analogno pH, moþe se definisati i pOH:
pOH = – log [OH–] / mol dm–3 (39)
Logaritmovawem izraza (37) i wegovim mnoþewem sa –1 dobijamo:
–log K w = –log[H+] + (–log[OH–]) = –log[H+] –log[OH–],
–log K w = pK w
Kako je – log[H+] = pH, – log[OH–] = pOH,
pK w = pH + pOH = 14 (40)
Iz ovog izraza se lako moþe izraåunati pOH na osnovu poznate vrednosti pH, i obratno.
Veza izmeðu koncentracije H+ i OH– jona u rastvoru; pH i pOH prikazana je u tablici 21.
Tablica 21. Veza izmeðu brojåanih vrednosti [H+], [OH–]; pH i pOH
Koncentracija OH– jona u rastvoru je 2,5 · 10–12 mol/dm3. Izraåunati pH rastvora
Odredimo najpre koncentraciju H+ jona u rastvoru: KW 1 · 10–14 mol2 dm–6 [H+] = = = 4 · 10–3 mol/dm3. [OH–] 2,5 · 10–12 mol dm–3 U skladu sa izrazom (38),
10–3) =
(0,6 – 3) = 3 – 0,6 = 2,4.
Odgovor: pH rastvora je 2,4.
Pri reakciji izmeðu vodenih rastvora kiselina i baza (neutralizaciji) nastaju soli i voda. Na primer: HCl + NaOH … NaCl + H2O, ili u jonskom obliku H+ + OH– … H2O. Kako je voda neutralna supstanca, moglo bi se oåekivati da i rastvori soli takoðe reaguju neutralno, tj. da im pH bude pribliþno jednak 7. Meðutim, poznate su mnoge soli åiji vodeni rastvori ne reaguju neutralno, veã kiselo ili bazno. Takvo ponašawe soli tumaåi se specifiånom protolitiåkom reakcijom koja se zove hidroliza Suštinu ove reakcije upoznaãemo na dva primera.
Пример 62
Objasniti baznu reakciju vodenog rastvora natrijum-karbonata, Na2CO3 (pH ≈ 10). Pri rastvarawu natrijum-karbonata u vodi dolazi do disocijacije:
H2O Na2CO3 … 2 Na+ + CO3 2–
Nastali karbonatni anjon, CO32–, kao konjugovana anjonska baza vrlo slabe kiseline (HCO3– jona), dosta je jaka baza, te moþe da otkine proton od molekula vode (koji se ponaša kao kiselina):
H+
CO32– + H2O „ HCO3– + OH–baza kis.
Kako se u rastvoru poveãava koncentracija OH– jona u odnosu na wihovu ravnoteþnu koncentraciju u åistoj vodi, rastvor Na2CO3 reaguje bazno.
U vodenom rastvoru Na2CO3 prisutni su i joni Na+, koji predstavqaju konjugovanu kiselinu veoma jake baze (NaOH). Stoga su oni izvanredno slaba kiselina, slabija åak i od vode, te s wom ne mogu da razmewuju protone.
Пример 63
Objasniti kiselu reakciju vodenog rastvora amonijum-hlorida, NH4Cl (pH ≈ 5,5) Pri rastvarawu amonijum-hlorida u vodi dolazi do disocijacije:
H2O
NH4Cl „ NH4+ + Cl–.
Amonijum jon, NH4+, kao konjugovana katjonska kiselina slabe baze (NH3) jaåa je kiselina od vode, te joj predaje proton:
H+
NH4+ + H2O „ NH3 + H3O+
Zahvaqujuãi ovoj reakciji, u rastvoru NH4Cl poveãava se koncentracija hidronijum jona, H3O+ u odnosu na wihovu ravnoteþnu koncentraciju u vodi, te rastvor reaguje kiselo. U vodenom rastvoru NH4Cl prisutni su i hloridni joni (Cl–), koji predstavqaju konjugovanu anjonsku bazu jake kiseline (HCl ). Stoga su oni slabija baza åak i od vode, te s wom ne mogu da razmewuju protone.
Iz navedenih primera se vidi da voda nije obiåan rastvaraå soli, veã stupa u hemijsku reakciju sa jednim od jona nastalih pri disocijaciji soli i, zahvaqujuãi svojoj amfoternosti, otpušta ili vezuje protone.
Hidroliza je protolitiåka reakcija izmeðu konjugovanih anjonskih baza odnosno katjonskih kiselina nastalih pri disocijaciji soli sa molekulima vode. Pri hidrolizi se u rastvorima soli poveãava koncentracija OH–odnosno H3O+ jona, te rastvori reaguju bazno ili kiselo.
Ako jednaåine reakcije hidrolize (npr. NH4+ + H2O „ NH3 + H3O+) åitamo s desna u levo, videãemo da one prikazuju neutralizaciju. Znaåi, hidroliza je protolitiåka reakcija suprotna neutralizaciji.
Hidrolizi podleþu soli izvedene iz jednog (ili oba) slaba elektrolita. Tako soli izvedene iz slabe baze i jake kiseline (npr. AlCl3, (NH4)2SO4 i NH4Cl) reaguju kiselo.
Soli izvedene iz jake baze i slabe kiseline (npr. NaNO2, K2CO3 i KCN) u vodenom rastvoru reaguju bazno
Soli izvedene iz slabe kiseline i slabe baze (npr. NH 4NO 2 i (NH4)2CO3) mogu reagovati bazno, kiselo ili neutralno, zavisno od konstanti disocijacije kiseline i baze.
Soli jake kiseline i jake baze (npr. NaCl, i NaNO3) ne podleþu hidrolizi.
Vodeni rastvori nekih soli (npr. AlCl3, CuSO4 i FeCl3), koje se åesto koriste u hemijskoj laboratoriji, reaguju usled hidrolize kiselo. Da bismo to objasnili protolitiåkom teorijom, moramo uzeti u obzir da su katjoni navedenih metala u vodenom rastvoru hidratisani, tj. okruþeni odreðenim brojem polarnih molekula vode. Tako je, npr. katjon Al3+ hidratisan sa šest molekula vode, te se prikazuje formulom [Al(H2O)6]3+ . Pri reakciji sa vodom ovaj katjon otpušta proton iz molekula vode u hidratnom omotaåu. Otpušteni proton vezuje se za molekul vode u rastvoru:
[Al(H2O)6]3+ + H2O „ [Al(H2O)5(OH)]2 + + H3O+ . kis. baza
Protolitiåka reakcija teåe i daqe, i to u onoliko stupweva koliko iznosi naelektrisawe hidratisanog katjona (u našem primeru u tri stupwa).
Puferski sistemi su rastvori åiji se pH veoma malo mewa pri dodatku male koliåine kiseline ili baze. To su obiåno smeše rastvora slabih kiselina i wihovih soli, odnosno slabih baza i wihovih soli. Te smeše imaju sposobnost da vezuju dodane H+ (odnosno OH–) jone, i tako odrþavaju pH rastvora pribliþno konstantnim.
Puferski sistemi imaju veliki praktiåni znaåaj u hemiji i hemijskoj industriji, pošto se mnoge reakcije odvijaju u þeqenom smeru samo u sluåaju kada je pH vrednost sredine stalna.
Odrþavawe konstantne vrednosti pH ima izuzetan znaåaj i u þivim organizmima. Tako se, na primer, pH krvi i krvnog seruma (7,3–7,4) reguliše proteinskim puferom – hemoglobinom, kao i nekim drugim puferskim sistemima. Ukoliko pH vrednost krvi opadne ispod 7,0 nastupa smrt, što znaåi da þivot åoveka zavisi samo od 0,3 jedinice pH.
Puferski sistemi mogu biti kiseli i bazni, zavisno od toga da li odrþavaju pH vrednost rastvora niþom ili višom od 7. Kiseli puferski sistemi sadrþe neku slabu kiselinu i wenu so, a bazni – slabu bazu i wenu so.
Najvaþniji puferski sistemi su: acetatni, karbonatni, fosfatni i amonijaåni puferi.
Пример 64
Objasniti mehanizam delovawa kiselog acetatnog pufera, koji predstavqa smešu slabe sirãetne kiseline i wene soli natrijum-acetata, CH3COONa.
Sirãetna kiselina u vodenom rastvoru disosuje prema jednaåini:
CH3COOH „ H+ + CH3COO–
Ako se sirãetnoj kiselini doda rastvor natrijum-acetata (soli koja je skoro u potpunosti disosovana na jone Na+ i CH3COO–), koncentracija acetatnih jona u rastvoru ãe se znatno poveãati. To izaziva pomerawe ravnoteþe gorwe reakcije ulevo, tj. suzbija se disocijacija sirãetne kiseline, te se kiselost rastvora smawuje, a pH raste.
Ako se acetatnom puferu doda rastvor kiseline, doãi ãe do reakcije izmeðu H+ jona i acetatnih jona, koji predstavqaju slabu anjonsku bazu:
CH3COO– + H+ „ CH3COOH, nastaju slabo disosovani molekuli sirãetne kiseline. Na taj naåin pufer se odupire promeni koncentracije H+ jona, sve dok u rastvoru postoje acetatni joni.
Ako se istom puferskom sistemu doda rastvor baze, sa OH– jonima reaguju molekuli sirãetne kiseline, tj. dolazi do reakcije neutralizacije:
CH3COOH + OH– „ CH3COO– + H2O.
Tako se puferski sistem odupire i promeni koncentracije OH– jona sve dotle dok u rastvoru postoje neizreagovani molekuli sirãetne kiseline.
Пример 65
Objasniti mehanizam delovawa baznog, amonijaånog pufera, koji predstavqa smešu vodenog rastvora amonijaka i amonijum-hlorida.
Mawi deo molekula amonijaka u vodenom rastvoru reaguje sa molekulima vode prema jednaåini:
NH3 + H2O „ NH4+ + OH–,
dok se amonijum-hlorid skoro u potpunosti disosuje na jone:
H2O
NH4Cl „ NH4+ + Cl–
Ako se ovom puferskom sistemu doda rastvor kiseline, doãi ãe do reakcije izmeðu molekula NH3 i H+ jona iz kiseline, pri kojoj nastaju joni NH4+ koji predstavqaju slabu katjonsku kiselinu:
NH3 + H+ „ NH4+ .
Na taj naåin puferski sistem se odupire promeni koncentracije H+ jona, sve dok u rastvoru postoje molekuli NH3
Ako se u puferski rastvor doda baza, sa OH– jonima reaguju joni N:
NH4+ + OH– „ NH3 · H2O
NH4OH
Tako se puferski sistem odupire promeni koncentracije OH– jona, sve dok u rastvoru postoje joni NH4+ .
Moþemo zakquåiti da pri dodatku kiseline puferskom sistemu, H+ jone vezuju anjonske ili molekulske baze, dok sa dodatim OH– jonima reaguju katjonske ili molekulske kiseline, usled åega se pH vrednost rastvora odrþava pribliþno konstantnom.
Granica do koje se puferski sistem odupire promeni pH naziva se kapacitet pufera. Smawewem koncentracije puferskog rastvora smawuje se wegova sposobnost regulisawa pH pri dodatku kiseline ili baze. Za rastvore kiselih pufera [H+] se izraåunava po formuli:
c(kis) [H+] = · KA (41) c(so)
gde je:
c(kis) – koliåinska koncentracija kiseline koju pufer sadrþi, c(so) – koliåinska koncentracija odgovarajuãe soli, KA – konstanta disocijacije kiseline.
Kod baznih puferskih smeša [OH–] se izraåunava po formuli
c(baza) [OH+] = · Kb (42) c(so)
gde je:
Kb – konstanta disocijacije baze koju pufer sadrþi. Iz jednaåina (41) i (42) pH i pOH se lako izraåunavaju primenom izraza (38) i (39).
Indikatori su slabe organske kiseline ili baze sloþene strukture koje u nedisosovanom, molekulskom obliku imaju jednu boju, a u disosovanom (jonskom) obliku drugu.
Ako indikator koji je po hemijskom sastavu slaba organska kiselina predstavimo pojednostavqenom formulom HIn, wegova disocijacija se moþe prikazati ovako:
HIn „ H+ + In–jedna boja druga boja
Ako nekoliko kapi indikatora ovog tipa dodamo u rastvor kiseline i tako poveãamo koncentraciju H+ jona, doãi ãe do suzbijawa disocijacije molekula HIn (ravnoteþa se pomera ulevo), te ãe boja rastvora poticati od nedisosovanih molekula HIn
Pri dodatku nekoliko kapi indikatora rastvoru baze, OH– joni iz
baze reagovaãe sa H+ jonima nastalim pri disocijaciji molekula HIn i nastaãe molekuli H2O. Zbog smawewa koncentracije H+ jona u rastvoru, ravnoteþa gorwe reakcije pomera se udesno, tj. u smeru disocijacije novih molekula HIn. To uslovqava poveãawe koncentracije jona In–, te ãe boja rastvora poticati od tih jona.
Ako indikator koji je po hemijskom sastavu slaba organska baza predstavimo pojednostavqenom formulom BOH, wegova disocijacija se moþe prikazati na sledeãi naåin:
BOH „ B+ + OH–jedna boja druga boja
Pri dodatku nekoliko kapi indikatora ovog tipa u rastovor kiseline, ravnoteþa ãe se pomeriti udesno, u smeru disocijacije novih molekula BOH, te ãe boja rastvora poticati od jona B+
Ako pak nekoliko kapi indikatora dodamo u rastvor baze, doãi ãe do suzbijawa disocijacije molekula BOH i ravnoteþa gorwe reakcije pomeriãe se ulevo, a boja rastvora poticaãe od nedisosovanih molekula BOH. Kao prirodni indikatori kiselosti i baznosti mogu se koristiti sokovi razliåitih biqaka, dobijenih npr. iz listova plavog kupusa, kruniånih listiãa crvene ruþe, qubiåice i zumbula, plodova višwe, korena cvekle, podzemnog stabla (lukovice) crnog luka itd. Poznati indikator lakmus dobija se iz nekih vrsta lišajeva koji rastu na obalama Sredozemnog mora.
Danas je poznat veliki broj sintetiåki dobijenih indikatora kiselosti i baznosti, na primer: metiloranþ, fenolftalein, metilcrveno, timolplavo itd. Oni se najviše koriste u analitiåkoj hemiji za odreðivawe završne taåke reakcije neutralizacije. Kako su indikatori organske kiseline, odnosno organske baze razliåite jaåine, mewaju boju u razliåitim intervalima pH. Tako, npr., metiloranþ mewa boju iz crvene u þutu u intervalu pH 3,1–4,4. To znaåi da ovaj indikator ispod pH 3,1 ima crvenu boju, a iznad pH 4,4 – þutu. Izmeðu ovih vrednosti pH boja metiloranþa je naranyasta. Ta boja naziva se prelazna boja indikatora. Lakmus mewa boju iz crvene u plavu u intervalu pH 4,5–8,3, fenolftalein iz bezbojne u qubiåastocrvenu u intervalu pH 8,3–10,0, metilcrveno iz crvene u þutu u intervalu pH 4,2–6,2 itd.
292. Napi{ite jedna~ine slede}ih protoliti~kih reakcija:
a) protolizu sumporne kiseline u vodenom rastvoru, b) protolizu mravqe kiseline u vodenom rastvoru, v) autoprotolizu vode.
293. Prika`ite jedna~inom protoliti~ku reakciju izme|u fluorovodoni~ne kiseline i acetatnih jona, CH3COO–. Koji je anjon ja~a baza – CH3COO– ili F–? (vidi tablicu 20)
294. Ozna~ite slovima k i b konjugovane parove kiselina i baza u slede}im reakcijama:
a) HBr + NH3 „ NH4 + + Br–,
b) HSO4– + H2O „ SO42– + H3O+ ,
v) NH3 + H2O „ NH4+ + OH–
295. Navedite konjugovane baze slede}ih kiselina:
a) HCN, b) NH4+, v) HCO3 –
296. Prika`ite hemijskim jedna~inama amfoternost vode pri reakciji sa:
a)HCl, b) NH3
297. Napi{ite izraze za konstante disocijacije slede}ih kiselina:
a) sir}etne, b) azotaste, v) hipohloritne.
298. Jednobazna kiselina HA u vodenom rastvoru disosuje prema jedna~ini: HA „ H+ + A–. U koju je stranu pomerena ravnote`a ove reakcije u slu~aju:
a) jake kiseline, b) slabe kiseline?
299. Na osnovu vrednosti konstanti disocijacije kiselina (tablica 20) utvrdite koja je od navedenih kiselina najja~a:
a) mravqa, b) azotasta, v) fluorovodoni~na.
300. Konstanta disocijacije H3O+ jona je 55 mol/dm3. Izra~unajte konstantu disocijacije konjugovane baze ove kiseline – vode. Задаци
301. Konstanta disocijacije amonijaka je 1,8 · 10–5 mol/dm3. Izra~unajte konstantu disocijacije wegove konjugovane kiseline – amonijum jona, NH4 +
302. Kako }e na polo`aj ravnote`e reakcije uticati dodatak rastvora baze?
HCOOH „ H+ + HCOO–
303. Razmotrite jedna~inu disocijacije sir}etne kiseline CH3COOH „ H+ + CH3COO–, i odgovorite, da li }e dodatak rastvora natrijum-acetata, CH3COONa usloviti pove}awe ili smawewe ravnote`ne koncentracije H+ jona.
304. Izra~unajte ravnote`ne koncentracije vodonikovih i acetatnih jona u rastvoru sir}etne kiseline koli~inske koncentracije 0,1 mol/dm3
305. Izra~unajte ravnote`ne koncentracije amonijumovih i hidroksidnih jona u vodenom rastvoru amonijaka, koli~inske koncentracije 0,01 mol/dm3. Konstanta disocijacije amonijaka je 1,8 · 10–5 mol/dm3 .
306. U vodenom rastvoru mravqe kiseline (s = 0,05 mol/dm3) koncentracija H+ jona je 3 · 10–3 mol/dm3. Izra~unajte konstantu disocijacije ove kiseline. Smawewe polazne koncentracije kiseline zbog disocijacije mo`ete zanemariti.
307. Izra~unajte konstantu disocijacije amonijaka, ako je u rastvoru koncentracije 0,1 mol/dm3 1,3 % molekula NH3 disosovano na jone.
308. Stepen disocijacije mravqe kiseline u rastvoru koncentracije 0,2 mol/dm3 iznosi 0,03. Izra~unajte konstantu disocijacije ove kiseline.
309. Izra~unajte koncentraciju H+ jona i pH rastvora u kome je koncentracija OH– jona 1 · 10–3 mol/dm3 .
310. Izra~unajte koncentraciju H+ jona i OH– jona u rastvoru HCl koncentracije 0,001 mol/dm3. Uzmite da je disocijacija molekula HCl u rastvoru potpuna.
311. U 6 dm3 rastvora nalazi se 180 g ~iste sir}etne kiseline.
Izra~unajte:
a) koli~insku koncentraciju rastvora, b) koncentraciju vodonikovih jona u rastvoru.
312. U 100 cm3 rastvora hlorovodoni~ne kiseline nalazi se 36,5 mg ~iste kiseline. Izra~unajte:
a) koncentraciju H+ jona u rastvoru, b) pH, v) pOH
Uzmite da je disocijacija molekula HCl u rastvoru potpuna.
313. Da li je u rastvoru koji ima pH 5 ve}a koncentracija H+ ili OH–jona?
314. Izra~unajte koncentraciju H+ jona u rastvoru u kome je koncentracija OH– jona 3,2 · 10–6 mol/dm3. Kako reaguje ovaj rastvor?
315. Izra~unajte koncentraciju OH– jona u rastvoru u kome je koncentracija H+ jona 1,4 · 10–12 mol/dm3. Kako reaguje ovaj rastvor?
316. Koliki je pH rastvora ~iji je pOH = 9,2?
317. Koliki je pOH rastvora ~iji je pH = 10,8?
318. Izra~unajte pH rastvora u kojima je koncentracija H+ jona jednaka:
a) 2 · 10–7 mol/dm3 ,
b) 8,1 · 10–3 mol/dm3 , v) 2,7 · 10–10 mol/dm3 .
319. Izra~unajte pH rastvora u kojima je koncentracija OH– jona jednaka:
a) 4,6 · 10–4 mol/dm3 ,
b) 5 · 10–6 mol/dm3 , v) 9,3 · 10–9 mol/dm3
320. Izra~unajte pOH i pH rastvora amonijaka koncentracije 0,1 mol/dm3 Smawewe koncentracije amonijaka zbog disocijacije mo`ete zanemariti. Konstanta disocijacije amonijaka je 1,8 · 10–5 mol/dm3
321. Izra~unajte pH rastvora HCl koncentracije 0,01 mol/dm3. Uzmite da je disocijacija HCl u rastvoru potpuna.
322. Izra~unajte pH rastvora NaOH koncentracije 0,1 g/dm3. Uzmite da je disocijacija NaOH u rastvoru potpuna.
323. Utvrdite koje od navedenih soli u vodenom rastvoru podle`u hidrolizi:
a) K2S, b) KNO3, v) MgSO4, g) FeSO4, d) KBr. Kako }e reagovati soli koje podle`u hidrolizi?
324. Utvrdite kakva }e biti boja lakmusa u vodenim rastvorima slede}ih soli:
a) FeCl3, b) KCN, v) KNO2, g) ZnBr2, d) HCOOK.
325. Utvrdite kako }e reagovati slede}e soli izvedene iz slabe kiseline i slabe baze:
a) (NH4)2CO3, b) CH3COONH4, v) NH4NO2 Kod re{avawa zadatka uzmite u obzir da je konstanta disocijacije amonijaka 1,8 · 10–5 mol/dm3, dok konstante disocijacije slabih
kiselina potra`ite u tablici 20.
326. Prika`ite hemijskim jedna~inama hidrolizu slede}ih soli u vodenom rastvoru:
a) NaHCO3, b) K2CO3, v) NaCN.
327. Prika`ite hemijskom jedna~inom prvi stupaw hidrolize bakar(II)-sulfata, CuSO4 u vodenom rastvoru. Kod re{avawa zadatka uzmite u obzir da je jon Cu2+ hidratisan sa ~etiri molekula vode.
328. Utvrdite koji od navedenih vodenih rastvora reaguju bazno usled
hidrolize:
a) KHCO3, b) AlCl3, v) NaOH, g) CH3COONa
329. Koje od navedenih sme{a rastvora imaju puferska svojstva: a) HCl + NaHCO3, b) H3PO4 + Na2HPO4, v) H2SO4 + NaHSO4, g) HNO3 + NH4NO3, d) NH3 + NH4NO3?
330. Bikarbonatni pufer se priprema tako {to se u vodeni rastvor NaHCO3 uvodi ugqenik(IV)-oksid, CO2. Koje ~estice u rastvoru ovog pufera reaguju:
a) sa H+ jonima iz dodate kiseline, b) sa OH– jonima iz dodate baze?
331. Izra~unajte pH rastvora acetatnog pufera koji sadr`i 0,5 mol/dm3 sir}etne kiseline i 0,5 mol/dm3 natrijum-acetata. Vrednost KA sir}etne kiseline potra`ite u tablici 20.
332. Izra~unajte pH rastvora pufera dobijenog me{awem rastvora amonijaka koncentracije 1 mol/dm3 i rastvora NH4Cl koncentracije 0,5 mol/dm3. Konstanta disocijacije amonijaka je 1,8 · 10–5 mol/dm3
333. Koliko grama ~vrstog amonijum-hlorida, NH4Cl treba rastvoriti u 250 cm3 rastvora amonijaka (s= 0,12 mol/dm3) da bi se dobio pufer ~iji je pH 9? Kb = 1,8 · 10–5 mol/dm3 .
334. Izra~unajte kolika je koncentracija sir}etne kiseline u acetatnom puferu potrebna da bi wegov pH bio 6. Koncentracija natrijum-acetata u puferu je 0,02 mol/dm3 , KA = 1,8 · 10–5 mol/dm3
335. Molekuli baznog indikatora (VOH) obojeni su crveno, dok su joni V+ bezbojni. Kakvu }e boju imati ovaj indikator u baznoj sredini?
336. Objasnite promenu boje indikatora HIn, ako ovaj indikator u molekulskom obliku ima crvenu, a u jonskom `utu boju.
337. Kakvu }e boju imati indikator fenolftaleina:
a) ispod pH 8,3,
b) iznad pH 10,0,
v) izme|u pH 8,3 – 10,0?


Vodonik
338. Zašto se vodonik svrstava i u ¡A i u ¢¡¡A grupu periodnog sistema?
339. Po åemu se jezgro atoma vodonika razlikuje od jezgara atoma drugih elemenata?
340. Prirodni vodonik predstavqa smešu izotopa 1 H ( A r = 1,00782) i 2D(A r = 2,0141). Izraåunajte koliåinski udeo deuterijuma u prirodnom vodoniku i izrazite ga u procentima. Uzmite da je relativna atomska masa prirodnog vodonika 1,00797.
341. Vodonik se laboratorijski obiåno dobija reakcijom izmeðu cinka i razblaþene sumporne kiseline. Koliko grama cinka treba da izreaguje sa kiselinom da bi se dobilo 5 dm3 vodonika (pri n.u.)?
342. Koliko je kubnih centimetara rastvora HCl (c = 4 mol/dm3) potrebno za reakciju sa 10 g cinka?
343. Izraåunajte da li se pri reakciji po 1 g litijuma, natrijuma i kalijuma sa vodom oslobaða ista zapremina vodonika.
344. Kako se proverava åistoãa vodonika u hemijskoj laboratoriji?
345. Kako se moþe dokazati razlika u reaktivnosti nascentnog i molekulskog vodonika?
346. Objasnite strukturu molekula H2 sa stanovišta teorije valentne veze i teorije molekulskih orbitala.
347. Koliko je grama vodonika potrebno za redukciju 3,5 g åistog bakar(¡¡)-oksida, CuO?
348. Za puwewe vazdušnih balona u poqskim uslovima ponekad se koristi vodonik, dobijen reakcijom kalcijum-hidrida, CaH2 sa vodom. Izraåunajte koliko je kilograma CaH2 potrebno za puwewe balona zapremine 500 m3 (pri n.u.).
349. U raketnim motorima kao izvor energije moþe se koristiti reakcija 1/2 H2(g) + 1/2 F2(g) ® HF(g). Izraåunajte koliko se toplote oslobaða pri reakciji 1 kg smeše vodonika i fluora u raketnom motoru. ∆fH(HF) = – 268,3 kJ/mol.
350. Odredite oksidacione brojeve vodonika u sledeãim jediwewima: a) NH3, b) LiH, v) HF, g) CaH2
351. Odredite oksidacione brojeve vodonika u sledeãim jonima: a) HF2 –, b) BH4–, v) NH4+ ,
352. U kom od hidrida elemenata druge periode veza izmeðu vodonika i odgovarajuãeg elementa ima najizraþeniji jonski karakter?
353. Izraåunajte koliåinu toplote koja se oslobaða pri reakciji 8 g natrijum-hidrida, NaH sa vodom. ∆fH(NaH) = – 56,4 kJ/mol; ∆fH(NaOH) = – 425,6 kJ/mol.
354. Koje se reakcije odigravaju pri sjediwavawu hidrida metala i nemetala sa vodom?
355. Eksperimentalno je utvrðeno da uglovi izmeðu N–H veza u molekulu amonijaka iznose 107º. Objasnite geometrijsku strukturu ovog molekula, polazeãi od pretpostavke da u procesu formirawa hemijske veze dolazi do hibridizacije orbitala atoma azota.
356. Oko 66 % mase tela odraslog åoveka åini voda. Izraåunajte koliko se vode nalazi u telu åoveka mase 70 kg.
357. U 150 g razblaþenog rastvora vodonik-peroksida, H2O2, dodano je malo katalizatora mangan(¡¢)-oksida, MnO2. Pri razlagawu H2O2 oslobodio se 1 dm3 kiseonika (na n.u.). Izraåunajte maseni udeo H2O2 u rastvoru.
Elementi ¡A grupe periodnog sistema
358. Koliko elektrona sadrþe atomi alkalnih metala u najvišem energetskom nivou?
359. Koji su najvaþniji minerali natrijuma?
360. Izraåunajte maseni udeo kalijuma u mineralu karnalitu, KCl MgCl2 6 H2O.
361. Maseni udeo soli u morskoj vodi je 3,5 %. Koliko grama soli zaostaje nakon isparavawa 10 kg morske vode?
362. Kako se u industriji dobijaju alkalni metali?
363. Napišite jednaåine oksido-redukcionih reakcija koje se odigravaju na katodi i anodi pri elektrolizi rastopqenog kalijum-hidroksida.
364. Izraåunajte koliko se kilograma metalnog natrijuma moþe dobiti elektrolizom 1 000 kg rastopqenog natrijum-hidroksida.
365. Kako se mewaju prve energije jonizacije alkalnih metala sa porastom wihovih atomskih brojeva? Kako se te promene tumaåe?
366. Kako se tumaåe åiwenice da je litijum dosta tvrd, i da ima znatno veãu temperaturu topqewa od ostalih alkalnih metala?
367. Izraåunajte koliko se atoma natrijuma izdvaja pri elektrolizi rastopqenog NaCl, ako se masa katode poveãala za 0,69 g
368. Kako se mewa hemijska aktivnost alkalnih metala iduãi od litijuma prema cezijumu. Kako se to tumaåi?
369. Koliki je oksidacioni broj alkalnih metala u wihovim jediwewima?
370. Prikaþite hemijskim jednaåinama reakcije natrijuma sa: a) kiseonikom, b) vodonikom, v) vodom, g) sumporom.
371. Kako se mewa jaåina baza u nizu LiOH–CsOH? Kako se to tumaåi?
372. Uz pomoã grafika prikazanog na slici 13, odredite procenat jonskog karaktera veze u sledeãim jediwewima alkalnih metala sa nemetalima:
a) Na2S, b) RbCl, v) Li2O
373. U åemu se åuvaju alkalni metali?
374. Izraåunajte broj Na+ i Cl– jona u 100 cm3 rastvora NaCl koncentracije 0,01 mol/dm3. Uzmite da je disocijacija NaCl u rastvoru potpuna.
375. Izraåunajte koliko je grama NaCl i vode potrebno za pripremawe 250 g fiziološkog rastvora, u kome je maseni udeo NaCl 0,95 %.
376. Kako se industrijski proizvodi natrijum-hidroksid?
377. Soda, Na2CO3, se industrijski proizvodi po Solvejevom postupku tako što se u zasiãen rastvor natrijum-hlorida uvodi amonijak, a zatim ugqenik(¡¢)-oksid. Napišite jednaåine reakcija dobijawa sode po Solvejevom postupku.
378. Izraåunajte utrošak sirovine za proizvodwu 1 t sode po Solvejevom postupku, i to: zapreminu rastvora NaCl koji u 1 dm3 sadrþi 300 g NaCl; zapreminu NH3 i CO2 (izraþenu u kubnim metrima pri n.u.). Uzmite da se samo 2/3 NaCl prevodi u Na2CO3, a CO2 koji nastaje pri þarewu NaHCO3 bez gubitaka se vraãa u proces.
379. Izraåunajte maseni udeo kristalne sode, Na2CO3 · 10 H2O u 10,85 % rastvoru Na2CO3.
380. Utvrdite koje od navedenih soli alkalnih metala podleþu hidrolizi u vodenom rastvoru: a) NaCl, b) CH3COOK, v) NaHCO3, g) KNO3.
381. Kalijum-nitrat, KNO3, dosta se koristi kao kalijumovo veštaåko ðubrivo. Izraåunajte maseni udeo kalijuma u ovom jediwewu.
382. Napišite elektronsku konfiguraciju najvišeg energetskog nivoa atoma zemnoalkalnih metala.
383. Zašto je treãa energija jonizacije zemnoalkalnih metala znatno veãa od prve i druge?
384. Koliki je oksidacioni broj zemnoalkalnih metala u wihovim jediwewima?
385. Kako se tumaåi åiwenica da su zemnoalkalni metali tvrði, veãe gustine i više temperature topqewa od alkalnih metala?
386. Uporedite reaktivnost zemnoalkalnih metala sa reaktivnošãu alkalnih metala.
387. Zašto se berilijum po svojim hemijskim svojstvima razlikuje od ostalih zemnoalkalnih metala?
388. Kakav karakter ima berilijum-hidroksid?
389. Izraåunajte koliko se kilograma magnezijuma i kalcijuma moþe dobiti elektrolizom 100 kg wihovih rastopqenih hlorida.
390. Zemnoalkalni metali (osim berilijuma) reaguju sa vodom i redukuju je do elementarnog vodonika. Koji je zemnoalkalni metal najjaåe redukciono sredstvo. Objasnite zašto.
391. Koje su soli zemnoalkalnih metala slabo rastvorqive u vodi?
392. Zemnoalkalni metali imaju izraþenu sposobnost sjediwavawa sa azotom, åak i na sobnoj temperaturi. Napišite formule jediwewa kalcijuma i magnezijuma sa azotom, i dajte im nazive.
393. Prikaþite hemijskim jednaåinama reakcije kalcijuma sa: a) kiseonikom, b) vodonikom v) azotom(III).
394. Moþe li magnezijum da gori u atmosferi ugqenik(¡¢)-oksida?
395. Izraåunajte koliko se magnezijum-oksida dobija þarewem 250 kg magnezita, MgCO3. Uzmite da je iskorišãewe procesa 85 %.
396. Magnezijum-sulfat (gorka so) kristališe sa 7 molekula kristalne vode. Izraåunajte koliko je grama ove soli potrebno za pripremawe 1 000 g 2 % rastvora MgSO4
397. Šta su po hemijskom sastavu sledeãi minerali kalcijuma: kreda, kreåwak, mermer i kalcit?
398. Napišite formule sledeãih jediwewa kalcijuma: a) normalnog kalcijum-fosfata, b) kalcijum-fluorida, v) kalcijum-karbonata.
399. Izraåunajte standardnu entalpiju reakcije razlagawa kreåwaka CaCO3(s)® CaO(s)+CO2(g), koja se primewuje za industrijsko dobijawe kalcijum-oksida.
∆fH(CaCO3) = – 1 207 kJ/mol Toplote stvarawa CaO i CO2 potraþite u tablici 17.
400. Kako biste pomerili ravnoteþu reakcije
CaCO3(s) „ CaO(s) + CO2(g) udesno, u smeru razlagawa CaCO3?
401. Pri rastvarawu u hlorovodoniånoj kiselini 5 g CaO koji sadrþi primese kalcijum-karbonata oslobaða se 140 cm3 CO2 (pri n.u.). Izraåunajte maseni udeo CaCO3 u kalcijum-oksidu.
402. Izraåunajte koliko se toplote oslobaða pri gašewu 1 kg kalcijum-oksida.
∆fH(Ca(OH)2) = – 986,6 kJ/mol.
Toplote stvarawa CaO(s) i H2O(l) potraþite u tablici 17.
403. Kalcijum-hlorid veoma je higroskopna supstanca koja se u hemijskim laboratorijama koristi za sušewe. Uzorak vlaþnog kalcijum-hlorida mase 0,15 g rastvoren je u vodi i hloridni joni istaloþeni pomoãu rastvora koji sadrþi 0,34 g AgNO3. Izraåunajte maseni udeo vode u uzorku CaCl2
404. Bistar rastvor kalcijum-hidroksida (kreåna voda) sluþi za dokazivawe CO2, jer se pri reakciji sa ovim gasom zamuti od izdvojenog CaCO3. Objasnite, zašto se pri duþem uvoðewu CO2 rastvor ponovo izbistri.
405. Izraåunajte koliko kubnih metara CO2 (pri n.u.) moþe da veþe 220 kg kalcijum-hidroksida.
406. Koje soli u prirodnoj vodi uslovqavaju wenu tvrdoãu?
407. Koje se hemijske reakcije odigravaju pri dodatku rastvora Na2CO3 tvrdoj vodi?
408. Šta su jonoizmewivaåi?
Elementi ¡¡¡A grupe periodnog sistema
409. Napišite elektronske konfiguracije atoma bora, aluminijuma i galijuma. Utvrdite koliko elektrona sadrþe atomi ovih elemenata u najvišem energetskom nivou
410. Kako se tumaåi åiwenica da su elementi ¡¡¡A grupe u svojim kovalentnim jediwewima obiåno trovalentni, mada imaju samo jedan nespareni elektron?
411. Koja su najvaþnija oksidaciona stawa elemenata ¡¡¡A grupe?
412. Kako se mewa karakter oksida elemenata ¡¡¡A grupe?
413. Po kojim svojstvima se bor razlikuje od ostalih elemenata ¡¡¡A grupe?
414. Da li postoje jediwewa bora u kojima je wegov oksidacioni broj negativan?
415. Pri zagrevawu do 700 ºC amorfni bor se pali i sagoreva u bor(¡¡¡)-oksid, B2O3. Izraåunajte koliko je kubnih decimetara vazduha (pri n.u.) potrebno za sagorevawe 1 mol bora. Uzmite da je zapreminski udeo kiseonika u vazduhu 21 %.
416. Mogu li da reaguju molekuli BF3 i NH3?
417. Kako se zove crveno, odnosno plavo obojeni mineral korund, Al2O3?
418. Šta je po hemijskom sastavu boksit?
419. U industrijskom procesu proizvodwe aluminijuma iz boksita kao meðuproizvod se dobija aluminijum-hidroksid, Al(OH)3, koji se þarewem prevodi u glinicu, Al2O3. Izraåunajte koliko je aluminijum-hidroksida potrebno za dobijawe 200 kg glinice.
420. Napišite jednaåine oksido-redukcionih reakcija koje se odigravaju na katodi i anodi pri elektrolizi rastopqene glinice.
421. Najvaþnija legura aluminijuma – duraluminijum sadrþi pored aluminijuma 4 % bakra i po 0,5 % mangana i magnezijuma. Izraåunajte koliko je kilograma Al, Cu, Mn i Mg potrebno za proizvodwu 1 t duraluminijuma.
422. Termitni postupak zavarivawa gvozdenih predmeta zasniva se na reakciji: Fe2O3(s) + 2 Al(s) ® Al2O3(s) + 2 Fe(s). Izraåunajte standardnu entalpiju ove reakcije.
423. Kao jako redukciono sredstvo aluminijum se koristi za dobijawe nekih metala iz wihovih oksida. Napišite jednaåinu reakcije hrom(¡¡¡)-oksida sa aluminijumom.
424. Kako se ponaša aluminijum pri reakciji sa kiselinama i bazama? Odgovor ilustrujte hemijskim jednaåinama.
425. Zašto se aluminijum, koji je praktiåno nerastvorqiv u vodi, rastvara u vodenim rastvorima NH4Cl i Na2CO3?
426. Pri zagrevawu na vazduhu fino usitweni aluminijum sagoreva bqeštavim plamenom uz izdvajawe velike koliåine toplote:
2 Al + 1,5 O2 ® Al2O3; ∆ r H = – 1670 kJ/mol.
Izraåunajte koliko se toplote oslobaða pri sagorevawu 81 kg aluminijuma.
427. Kako se dobija aluminijum-hidroksid?
428. Šta su aluminati?
Elementi ¡¢A grupe periodnog sistema
429. Napišite elektronsku konfiguraciju najvišeg energetskog nivoa atoma elemenata ¡¢A grupe. Koliko nesparenih elektrona sadrþe atomi ovih elemenata u najvišem energetskom nivou?
430. Kako se mewa karakter elemenata ¡¢A grupe sa porastom wihovih atomskih brojeva?
431. Koja su najvaþnija oksidaciona stawa elemenata ¡¢A grupe?
432. Koji su osnovni tipovi hibridizacije atomskih orbitala karakteristiåni za ugqenik?
433. Odredite oksidacioni broj ugqenika u sledeãim jediwewima: a) CH3OH, b) CaC2, v) H2CO3
434. Vodeni gas je gasovito gorivo koje se dobija prevoðewem vodene pare preko uþarenog ugqa. Izraåunajte koliko je grama ugqa potrebno za dobijawe 240 dm3 vodenog gasa (pri n.u.). Uzmite da se ugaq sastoji od åistog ugqenika.
435. Pri reakciji ugqenik(¡¡)-oksida, CO, sa hlorom nastaje fosgen, COCl2. Kako se mewa oksidacioni broj ugqenika i hlora pri ovoj oksido-redukcionoj reakciji?
436. Zašto se pri laboratorijskom dobijawu CO2 na mermer deluje razblaþenom hlorovodoniånom, a ne sumpornom kiselinom?
437. Iz 250 g mermera zagrevawem je dobijeno 53,4 dm3 CO2 (pri n.u.). Izraåunajte maseni udeo CaCO3 u mermeru.
438. U 1 dm3 vode na 20 ºC rastvara se 3,8 10–2 mol CO2. Izraåunajte koliko je to grama i kubnih centimetara (pri n.u.).
439. Napišite u jonskom obliku jednaåine sledeãih reakcija:
a) CaCO3 + 2 HCl ® CaCl2 + H2O + CO2,
b) 2 NaOH + CO2 ® Na2CO3 + H2O.
440. Sunåanih dana biqke vezuju oko 5 g CO2 po kvadratnom metru lisne površine. Izraåunajte koliko ãe grama ugqenika dnevno vezati suncokret åija je lisna površina 1,8 m2 .
441. Åovek dnevno izdahne do 1 300 g CO2. Izraåunajte koliku zapreminu zauzima ova masa CO2 (n.u.).
442. Vazduh sadrþi 0,03 zapreminska procenta CO2. Koliko ãe se grama BaCO3 istaloþiti ako se kroz rastvor Ba(OH)2 propusti 0,5 m3 vazduha (n.u.)?
443. Koliko kubnih decimetara CO2 (n.u.) treba propustiti kroz rastvor NaOH da bi se dobio 1 kg natrijum-karbonata?
444. Utvrdite kako reaguju sledeãe soli ugqene kiseline: a) Na2CO3, b) (NH4)2CO3, v) KHCO3
445. Kalcijum-karbid, CaC2 se industrijski dobija þarewem kalcijum-oksida i ugqa u elektriånim peãima. Izraåunajte masu CaO koja je potrebna za dobijawe 6,4 t CaC2. Koliko kubnih metara CO (n.u.) nastaje pri ovom procesu?
446. Izraåunajte koliko grama kalcijum-karbida treba sjediniti sa vodom da bi se dobilo 100 dm3 etina (acetilena) pri n.u.
447. Molekul ugqenik(IV)-oksida je linearan (sva tri vezana atoma leþe u istoj liniji). Prikaþite graðu ovog molekula i odgovorite, kojim bi se tipom hibridizacije orbitala atoma ugqenika ona mogla objasniti.
448. Koliko se silicijuma dobija pri redukciji aluminijumom 1 kg SiO2 koji sadrþi 16,6 % primesa?
449. Kako se tumaåi velika reaktivnost silicijuma prema rastvorima baza, dok jake kiseline, åak i one koje imaju izraþenu moã oksidacije, na silicijum praktiåno ne deluju?
450. Kako biste objasnili åiwenicu da SiO2 ima visoku temperaturu topqewa (1 700 ºC), dok åvrsti CO2 sublimuje veã na – 78,5 ºC?
451. Koliko je kilograma masne sode, koja sadrþi 95 % NaOH i peska, koji sadrþi 90 % SiO2 potrebno za dobijawe 1 t natrijum-silikata, Na2SiO3?
452. Izraåunajte koliko se grama vodenog stakla (natrijum-silikata, Na2SiO3) moþe dobiti pri rastvarawu 7 g silicijuma u rastvoru NaOH. 453. Koliko se kilograma stakla, sastava: 13 % Na2O, 11,7 % CaO i 75,3 % SiO2, moþe dobiti stapawem 376,5 kg SiO2 sa potrebnom koliåinom oksida natrijuma i kalcijuma?
454. Kakav karakter ima kalaj(¡¡)-hidroksid?
455. Kalaj(¡¢)-oksid, SnO2 se ponekad dobija sagorevawem metalnog kalaja u peãima specijalne konstrukcije. Izraåunajte koliko se kilograma SnO2 moþe dobiti iz 357 kg kalaja.
456. Kalaj (¡¢)-sulfid, SnS2 nastaje kao þuti talog pri uvoðewu gasovitog H2S u rastvore soli åetvorovalentnog kalaja. Izraåunajte koliko kubnih decimetara H2S (n.u.) treba uvesti u rastvor SnCl4 da bi se dobilo 3,66 g SnS2
457. Izraåunajte maseni udeo olova u sledeãim oksidima: a) Pb3O4, b) PbO2, v) PbO.
458. Objasnite, zašto se olovo ne rastvara u razblaþenoj hlorovodoniånoj i sumpornoj kiselini, mada se u naponskom nizu metala olovo nalazi ispred vodonika.
459. Na kojoj ãe temperaturi rastvorqivost olovo(¡¡)-nitrata i kalijum-nitrata biti pribliþno ista?
460. Izraåunajte koliko se grama olovo(¡¡)-nitrata, Pb(NO3)2 nalazi u 277 g zasiãenog rastvora na 50 ºC.
Elementi ¢A grupe periodnog sistema
461. Koliko nesparenih elektrona u najvišem energetskom nivou sadrþe atomi elemenata ¢A grupe?
462. Kako se mewa karakter elemenata ¢A grupe sa porastom wihovih atomskih brojeva? Obrazloþite svoj odgovor.
463. Koja su najvaþnija oksidaciona stawa elemenata ¢A grupe?
464. Prikaþite shematski obrazovawe molekula azota prekrivawem odgovarajuãih atomskih orbitala dva atoma azota. Kada uradite zadatak, objasnite veliku hemijski stabilnost molekulskog azota na sobnoj temperaturi.
465. Koji od elemenata ¢A grupe spada meðu najvaþnije biogene elemente?
466. Odredite oksidacioni broj azota u sledeãim jediwewima:
a) NO, b) NO2, v) N2O3
467. Izraåunajte maseni udeo azota u sledeãim oksidima: a) N2O5, b) N2O3.
468. Azot se industrijski dobija frakcionom destilacijom teånog vazduha. Izraåunajte koliko se kubnih metara azota teorijski moþe dobiti iz 200 m3 vazduha (pri n.u.). Uzmite da je zapreminski udeo azota u vazduhu 78 %.
469. U 1 dm3 vode na 20 ºC rastvara se 6,8 · 10–4 mola azota. Koliko je to miligrama, odnosno kubnih centimetara?
470. Koliko je grama natrijum-nitrita, NaNO2, potrebno sjediniti sa amonijum-hloridom da bi se dobio 1 dm3 azota (pri n.u.).
471. Izraåunajte masu azota koji se nalazi u 5 dm3 vazduha (n.u.). Uzmite da azot åini 75,5 % mase vazduha i da je masa 1 dm3 vazduha 1,29 g.
472. Izraåunajte: a) maseni udeo azota i vodonika u amonijaku, b) masu 1 dm3 amonijaka.
473. U 1 zapremini vode moþe da se rastvori 700 zapremina amonijaka. Izraåunajte koliko se molova NH3 moþe rastvoriti u 0,5 dm3 vode.
474. Prikaþite u jonskom obliku jednaåinu reakcije dobijawa amonijaka iz amonijumovih soli:
NH4Cl + NaOH ® NH3 + NaCl + H2O.
475. Objasnite, zašto se sinteza amonijaka iz vodonika i azota izvodi na visokom pritisku i visokoj temperaturi.
476. Izraåunajte koliko je kubnih metara azota i vodonika (n.u.) potrebno za sintezu 17 t amonijaka.
477. U balonu se nalazi 10 kg teånog amonijaka. Izraåunajte wegovu zapreminu pri n.u.
478. Maseni udeo NH3 u amonijaånoj vodi je 25 %. Izraåunajte u kojoj se masi amonijaåne vode nalazi 5 mol NH3
479. Izraåunajte pH rastvora amonijaka koncentracije 0,2 mol/dm3. Smawewe koncentracije amonijaka zbog disocijacije moþete zanemariti. Konstanta disocijacije amonijaka je 1,8 10–5 mol/dm3
480. Temperatura kquåawa amonijaka je – 33 ºC, a metana – 161 ºC. Zašto se wihove temperature kquåawa toliko razlikuju, i pored toga što su im relativne molekulske mase skoro iste?
481. Napišite elektronsku jednaåinu reakcije sjediwavawa gasovitog amonijaka i hlorovodonika.
482. Za prihrawivawe biqaka treba na svaki hektar zemqišta dodati po 10 kg azota u obliku rastvorqivih soli. Izraåunajte koliko je kilograma amonijum-nitrata, NH4NO3, potrebno za tu svrhu.
483. Prikaþite hemijskim jednaåinama postupak dobijawa azotne kiseline katalitiåkom oksidacijom amonijaka.
484. Izraåunajte koliko se kilograma åiste azotne kiseline teorijski moþe dobiti iz 1 000 m3 amonijaka (n.u.).
485. Izraåunajte koliko se kilograma åiste azotne kiseline moþe dobiti u apsorpcionom torwu pri reakciji 690 kg NO2 sa vodom u prisustvu kiseonika iz vazduha.
486. Izraåunajte koliko se tona 80 % azotne kiseline dobija iz 108 kg natrijum-nitrata i odgovarajuãe mase koncentrovane sumporne kiseline.
487. Koliko je kubnih centimetara 64 % azotne kiseline (ρ = 1,394 g/cm3) potrebno za pripremawe 5 dm3 rastvora koncentracije 1 mol/dm3?
488. Odredite koeficijente u jednaåini oksido-redukcione reakcije izmeðu azotne kiseline i bakra:
Cu + HNO3 ® Cu(NO3)2 + H2O + NO.
489. Sa kojim elementima fosfor gradi jediwewa u kojima je wegov oksidacioni broj pozitivan, a sa kojim jediwewa u kojima je wegov oksidacioni broj negativan?
490. Izraåunajte koliko se tona belog fosfora teorijski moþe dobiti u elektriånoj peãi iz 2,5 t åistog Ca3(PO4)2. Koliko je tona ugqa i peska potrebno utrošiti?
491. Kako biste najlakše razdvojili smešu belog i crvenog fosfora?
492. Izraåunajte koliko se toplote oslobaða pri prelasku 1 t belog fosfora u crveni, ako je standardna entalpija ove reakcije,
∆ r H = – 16,73 kJ/mol
493. Da li se pri sagorevawu belog i crvenog fosfora na vazduhu dobijaju ista, ili razliåita jediwewa?
494. Izraåunajte koliko ãe grama magnezijum-dihidrogenfosfata, Mg(H2PO4)2 nastati u reakciji magnezijum-hidroksida sa 250 cm3 rastvora fosforne kiseline, H3PO4, koncentracije c = 2 mol/dm3
495. Izraåunajte koliko je grama belog fosfora i kubnih decimetara kiseonika (n.u.) potrebno za dobijawe 568 g fosfor(¢)-oksida.
496. Koliki je oksidacioni broj fosfora u kiselinama HPO3 i H3PO4?
497. Fosforna kiselina se industrijski dobija delovawem sumporne kiseline na mineral fosforit:
Ca3(PO4)2 + 3 H2SO4 ® 3 CaSO4 + 2 H3PO4
Izraåunajte koliko se kilograma åiste fosforne kiseline teorijski moþe dobiti iz 31 t åistog fosforita.
498. Izraåunajte pH 1,96 % rastvora H3PO4 (ρ ≈ 1 g/cm3). Uzmite u obzir samo wenu prvu konstantu disocijacije (7,5 10–3 mol/dm3). Smawewe koncentracije H3PO4 zbog disocijacije moþete zanemariti.
499. U kostima se nalazi oko 58 % Ca3(PO4)2. Izraåunajte koliko kilograma fosfora ulazi u sastav 10 kg kostiju.
Elementi ¢¡A grupe periodnog sistema
500. Kako se mewaju prve energije jonizacije i elektronegativnost elemenata ¢¡A grupe sa porastom wihovih atomskih brojeva?
501. Kako se tumaåi porast temperature topqewa i kquåawa elemenata ¢¡A grupe iduãi od kiseonika prema polonijumu?
502. Kako se mewa elektriåna provodqivost elemenata ¢¡A grupe sa porastom atomskih brojeva? Na šta ukazuje ta pravilnost?
503. Koja su karakteristiåna oksidaciona stawa elemenata ¢¡A grupe?
504. Sa kojim elementima kiseonik i sumpor grade jonska jediwewa?
505. Kako se mewa jaåina kiselina u nizu H2O, H2S, H2Se, H2Te? Kako se to tumaåi?
506. Izraåunajte masu kiseonika u 1 m3 vazduha (n.u.), ako je zapreminski udeo kiseonika u vazduhu 21 %.
507. Izraåunajte koliko grama kalijum-permanganata treba razloþiti prema jednaåini
2 KMnO4 ® K2MnO4 + MnO2 + O2, za laboratorijsko dobijawe 500 cm3 kiseonika (n.u.).
508. Kiseonik se industrijski obiåno dobija iz teånog vazduha. Izraåunajte koliko je kubnih metara vazduha (n.u.) teorijski potrebno za dobijawe 8 t kiseonika.
509. Tehniåki kiseonik sadrþi 97 % O2. Izraåunajte zapreminu kiseonika (pri n.u.) koja se nalazi u 1 t tehniåkog kiseonika.
510. Kako se sa stanovišta teorije molekulskih orbitala tumaåi p aramagnetiånost molekula O2?
511. Odredite oksidacioni broj kiseonika u vodonik-peroksidu, H2O2
512. Filter hartija natopqena smešom rastvora kalijum-jodida i skroba u prisustvu ozona odmah poplavi. Kako se to objašwava?
513. Kako se dele oksidi prema kiselo-baznim svojstvima?
514. Izraåunajte maseni udeo kiseonika u sumpor(¡¢)-oksidu, SO2 i sumpor(¢¡)-oksidu, SO3
515. Odredite oksidacioni broj sumpora u sledeãim jediwewima:
a) kalcijum-sulfidu, b) kalcijum-sulfatu, v) kalcijum-sulfitu, g) kalcijum-hidrogensulfatu.
516. Odredite oksidacioni broj sumpora u sledeãim jediwewima:
a) SF6, b) SCl4, v) S2Br2.
517. Kako se laboratorijski dobija sumpor-vodonik? Napišite jednaåinu te reakcije.
518. Gvoþðe(¡¡)-sulfid obiåno sadrþi 97 % FeS. Izraåunajte koliko se kubnih decimetara H2S (n.u.) moþe dobiti reakcijom 1 kg FeS sa razblaþenom hlorovodoniånom kiselinom.
519. Napišite u jonskom obliku jednaåine reakcija sumpor-vodonika sa vodenim rastvorima:
a) olovo-acetata, b) bakar(¡¡)-sulfata.
520. Odredite koeficijente u sledeãoj jednaåini oksido-redukcione reakcije:
H2S + O2 ® H2O + SO2
521. Prikaþite hemijskim jednaåinama reakcije koje se odigravaju pri dobijawu sumporne kiseline kontaktnim postupkom, polazeãi od pirita, FeS2.
522. Izraåunajte koliko je kubnih metara vazduha (21 zapr. % O2, n.u.), teorijski potrebno za prþewe 1 t åistog pirita. Takoðe izraåunajte masu Fe2O3 i zapreminu SO2 (n.u.) koji nastaju pri ovoj reakciji.
523. Koliko se kilograma SO2 moþe dobiti prþewem 1 t pirita koji sadrþi 48 % sumpora, ako posle prþewa u nastalom Fe2O3 zaostaje 1 % sumpora?
524. Utvrdite koji od navedenih hidroksida pri reakciji sa 0,3 mola åiste sumporne kiseline gradi 0,1 mol neutralne soli:
a) NaOH,
b) Mg(OH)2, v) Fe(OH)3.
525. Zašto se pri proizvodwi sumporne kiseline SO3 apsorbuje u koncentrovanoj sumpornoj kiselini, a ne u vodi?
526. Kako ãe se tokom stajawa u otvorenom sudu mewati masa rastvora: a) jako razblaþene sumporne kiseline, b) koncentrovane sumporne kiseline?
527. Izraåunajte koliko je kubnih centimetara 98 % sumporne kiseline (ρ = 1,84 g/cm3) teorijski potrebno za rastvarawe 10 g bakra.
528. Izraåunajte koliko je kubnih centimetara sumporne kiseline (c = 2 mol/dm3) potrebno za reakciju sa 10 g MgO.
529. Napišite jednaåinu reakcije izmeðu bakra i koncentrovane sumporne kiseline pri zagrevawu.
530. Prikaþite u jonskom obliku reakciju izmeðu rastvora barijum-hlorida i sumporne kiseline.
531. Koliko se grama kristalne vode oslobaða pri þarewu 1 kg plavog kamena, CuSO4 5 H2O?
532. Utvrdite koji od navedenih oksida pri reakciji sa sumpornom kiselinom gradi so koja u vodenom rastvoru podleþe hidrolizi:
a) Na2O, b) BaO, v) BeO, g) K2O, d) CaO
Elementi ¢¡¡A grupe periodnog sistema
533. Koliko elektrona u najvišem energetskom nivou sadrþe atomi elemenata ¢¡¡A grupe?
534. Kako se tumaåe relativno niske temperature topqewa i kquåawa halogenih elemenata?
535. Kako se mewaju prve energije jonizacije i standardni elektrodni potencijal halogenih elemenata iduãi od fluora ka jodu?
536. Kako se mewa oksidaciona sposobnost halogenih elemenata sa porastom wihovih atomskih brojeva?
537. Hlor je jaåe oksidaciono sredstvo od joda, i istiskuje ga iz vodenih rastvora jodida. Predstavite ovaj iskaz hemijskom jednaåinom u jonskom obliku.
538. Zašto se halogeni elementi ne nalaze slobodni u prirodi?
539. Koje je najvaþnije oksidaciono stawe halogenih elemenata?
540. Zašto fluor, za razliku od ostalih halogenih elemenata, ne gradi jediwewa u kojima je wegov oksidacioni broj pozitivan?
541. Kakav karakter imaju jediwewa halogenih elemenata sa metalima iz ¡A i ¡¡A grupe periodnog sistema? Napišite opšte formule tih jediwewa (M = metal, H = halogeni element).
542. Da li se halogeni elementi u slobodnom stawu nalaze u obliku atoma ili molekula?
543. Kako se mewa jaåina halogenovodoniånih kiselina u nizu HF, HCl, HBr, HI? Obrazloþite svoj odgovor.
544. Odredite stepen jonskog karaktera veze u molekulima HF, HCl, HBr i HI .
545. Izraåunajte maseni udeo fluora u mineralu fluoritu, CaF2
546. Hlorna voda se dobija rastvarawem gasovitog hlora u vodi. Zašto se na identiåan naåin ne moþe dobiti fluorna voda?
547. Odredite koeficijente u sledeãim jednaåinama oksido-redukcionih reakcija koje se primewuju za laboratorijsko dobijawe hlora:
a) KClO3 + HCl ® Cl2 + KCl + H2O,
b) MnO2 + HCl ® MnCl2 + Cl2 + H2O.
548. Koliko je åiste kuhiwske soli teorijski potrebno za dobijawe 1 t hlora elektrolitiåkim putem?
549. Izraåunajte koliko je grama åiste hlorovodoniåne kiseline oksidovano mangan(IV)-oksidom, ako je dobijeni hlor istisnuo iz rastvora kalijum-jodida 12,7 g joda.
550. U balonu se nalazi 30 kg teånog hlora. Koju zapreminu ãe zauzeti ova masa hlora pri normalnim uslovima?
551. U 1 zapremini vode rastvara se pri n.u. 2,5 zapremine hlora. Koliko se grama hlora moþe rastvoriti u 1 dm3 vode?
552. Napišite jednaåine reakcija hlora sa: a) bakrom, b) gvoþðem, v) fosforom.
553. Odredite oksidacioni broj hlora u sledeãim jediwewima: a) ClO2, b) HCl, v) HClO, g) HClO4
554. Poreðajte prema porastu jonskog karaktera sledeãe veze: Cl–H, Cl–Cl, Cl–Br, Cl–S, Cl–P.
555. Koliko se kubnih decimetara hlorovodonika (n.u.) moþe dobiti reakcijom 1 mol H2 sa 1 mol Cl2?
556. U 100 g vode na 0 ºC rastvara se oko 82,3 g gasovitog hlorovodonika. Koliko molova vode dolazi na 1 mol hlorovodonika u tom rastvoru?
557. U jednoj zapremini vode sobne temperature rastvara se oko 442 zapremine hlorovodonika. Izraåunajte koliåinsku koncentraciju HCl u rastvoru. Uzmite da je molarna zapremina HCl na sobnoj temperaturi 24 dm3/mol.
558. U 2 000 cm3 rastvora HCl nalazi se 36,45 g åiste kiseline. Izraåunajte koncentraciju H+ i OH– jona u tom rastvoru. Uzmite da je disocijacija molekula HCl u rastvoru potpuna.
559. Za neutralizaciju 25,0 cm3 rastvora HCl nepoznate koncentracije utrošeno je 28,6 cm3 rastvora KOH koncentracije 0,1 mol/dm3. Izraåunajte koncentraciju rastvora HCl
560. Joni hlora u pijaãoj vodi mogu se dokazati pomoãu rastvora srebro-nitrata. Prikaþite u jonskom obliku ovu reakciju.
561. Izraåunajte koliko je grama åvrstog natrijum-hlorida potrebno uzeti za reakciju sa sumpornom kiselinom, da bi pri zagrevawu nastalo 3 l hlorovodonika (n.u.).
562. Hloratna kiselina, HClO3, se dobija delovawem sumporne kiseline na barijum-hlorat:
Ba(ClO3)2 + H2SO4 ® 2 HClO3 + BaSO4.
Izraåunajte koliko je grama barijum-hlorata potrebno za dobijawe 200 g 40 % hloratne kiseline.
563. Stepen disocijacije fluorovodoniåne kiseline u rastvoru koncentracije 0,1 mol/dm3 iznosi 0,08. Izraåunajte konstantu disocijacije ove kiseline.
564. Izraåunajte koliko se molekula Br2 nalazi u 1 mg broma.
565. U morskoj vodi se nalazi proseåno 4 10–3 % broma u obliku rastvorqivih soli. Koliko je tona morske vode potrebno za dobijawe 100 kg broma?
566. Na 0 ºC i atmosferskom pritisku u 1 zapremini vode rastvara se 600 zapremina bromovodonika. Izraåunajte maseni udeo HBr u dobijenom rastvoru.
567. Åoveku je dnevno potrebno 1 mg joda. Izraåunajte koliko miligrama KI treba uneti u organizam da bi se zadovoqila dnevna potreba za jodom.
568. Sadrþaj jodida u morskoj vodi iznosi 6,5 mg u 1 dm3 (preraåunato na KI). Koliko je kubnih metara morske vode potrebno za dobijawe 1 kg joda?
569. Koliko je grama hlora reagovalo sa rastvorom kalijum-jodida, ako je pri reakciji nastalo 25,4 g joda?
570. Koje od navedenih reakcija halogenih elemenata i wihovih jediwewa spadaju u oksido-redukcione reakcije:
a) KCl + AgNO3 ® AgCl + KNO3,
b) Cl2 + 2 KBr ® Br2 + 2 KCl,
v) NaCl + H2SO4 ® HCl + NaHSO4,
g) H2O2 + 2 KI ® 2 KOH + I2?
Prelazni elementi
571. U kom se delu periodnog sistema nalaze prelazni elementi?
572. Koliko elektrona u najvišem energetskom nivou sadrþe atomi prelaznih elemenata? Zašto se ovi elementi zovu d-elementi?
573. Koji prelazni elementi nemaju pravilan redosled popuwavawa s i d-orbitala elektronima?
574. U kojoj se periodi nalazi prvih deset prelaznih elemenata (Z = 21–30)?
575. U åemu su sliåne elektronske konfiguracije atoma bakra, srebra i zlata?
576. Napišite u skraãenom obliku elektronske konfiguracije atoma sledeãih prelaznih elemenata: a) hroma, b) mangana, v) gvoþða.
577. Prelazni elementi imaju razliåite oksidacione brojeve. Odredite oksidacione brojeve hroma i mangana u sledeãim jediwewima: a) Cr2O3, b) CrO3, v) MnO2, g) MnCl2, d) KMnO4.
578. Izraåunajte koliko se toplote oslobaða pri dobijawu 520 g hroma aluminotermijskim postupkom iz Cr2O3. Pri redukciji 1 mol Cr2O3 do metalnog hroma oslobaða se 456,1 kJ toplote.
579. Prikaþite u jonskom obliku taloþnu reakciju izmeðu rastvora olovo(¡¡)-nitrata i kalijum-hromata.
580. Odredite jonsko-elektronskom metodom koeficijente u sledeãoj shemi oksido-redukcione reakcije:
K2Cr2O7+ HCl ® KCl + CrCl3 + Cl2 + H2O.
581. Izraåunajte koliko je tona åistog ugqa (koji se oksiduje do CO2) potrebno za redukciju 8,7 t piroluzita, MnO2, do elementarnog mangana. Koliko se tona mangana dobija pri ovom procesu ako je piroluzit sadrþao 20 % primesa?
582. Koliko je grama mangan(¡¢)-oksida, MnO2, potrebno za dobijawe 112 dm3 hlora (n.u.) pri reakciji sa rastvorom hlorovodoniåne kiseline?
583. Izraåunajte maseni udeo gvoþða u sledeãim rudama:
a) hematitu, Fe2O3, b) magnetitu, Fe3O4, v) limonitu, 2 Fe2O3 3 H2O
584. Ruda gvoþða sadrþi 80 % Fe2O3. Izraåunajte maseni udeo gvoþða u ovoj rudi.
585. Prikaþite hemijskim jednaåinama procese koji se odigravaju u visokoj peãi pri dobijawu sirovog gvoþða iz hematita.
586. Izraåunajte koliko je kilograma koksa, koji sadrþi 98 % ugqenika, potrebno za dobijawe gvoþða iz 1 kg rude koja sadrþi 90 % Fe2O3, ako gubici u procesu iznose 20 %.
587. Izraåunajte koliko kilograma sirovog gvoþða i kubnih metara CO2 (n.u.) nastaje u visokoj peãi pri potpunoj redukciji 320 kg Fe2O3 pomoãu CO.
588. Izraåunajte koliko je tona åistog ugqenika potrebno za redukciju 696 t magnetita, Fe3O4, do elementarnog gvoþða, ako pri reakciji nastaje ugqenik(¡¡)-oksid, CO.
589. Pri sagorevawu uzorka åelika mase 5 g u struji kiseonika dobijen je 0,1 g CO2. Izraåunajte maseni udeo ugqenika u uzorku åelika.
590. Pri reakciji vodene pare sa uþarenim gvoþðem nastaje oksid gvoþða Fe3O4 i vodonik. Napišite jednaåinu ove reakcije i izraåunajte koliko je gvoþða potrebno za dobijawe 1 m3 vodonika (n.u.).
591. Koliko je kubnih centimetara rastvora HCl (c = 2 mol/dm3) potrebno za rastvarawe 0,56 g gvoþða?
592. Kolika je zapremina 26 % sumporne kiseline (ρ = 1,19 g/cm3) potrebna za rastvarawe 50 g gvoþða?
593. Pri reakciji gvoþða sa razblaþenom azotnom kiselinom dobija se gvoþðe(¡¡¡)-nitrat, azot(¡¡)-oksid i voda. Napišite jednaåinu ove reakcije.
594. Napišite jednaåine reakcija kojima bi se mogle ostvariti sledeãe hemijske promene:
(a) (b) (v) FeS2 Fe2O3 Fe2(SO4)3 Fe(OH)3.
595. Navedite nazive biološki vaþnih jediwewa u åiji sastav ulaze gvoþðe, kobalt i bakar.
596. Prikaþite hemijskim jednaåinama proces dobijawa bakra polazeãi od bakar(¡)-sulfida, Cu2S.
597. Izraåunajte koliko se grama srebro-nitrata moþe dobiti rastvarawem 100 g srebra u koncentrovanoj azotnoj kiselini.
598. Prikaþite u jonskom obliku reakciju izmeðu metalnog cinka i rastvora srebro-nitrata.
599. Cinkova bela (cink-oksid, ZnO) se industrijski dobija sagorevawem pare cinka na vazduhu. Izraåunajte koliko kilograma pare cinka treba sagoreti da bi se dobilo 810 kg cinkove bele.
600. Izraåunajte koliko je grama kristalnog cink-sulfata, ZnSO4 · 7 H2O potrebno za pripremawe 1 dm 3 rastvora ZnSO 4 koncentracije 0,1 mol/dm3.
601. Šta su amalgami?
602. Izraåunajte koliku zapreminu zauzima 200 kg teåne þive, ako je wena gustina 13,6 g/cm3
603. Koliko se kubnih centimetara pare þive (n.u.) moþe dobiti iz jedne kapqice þive mase 1 g?
604. Odredite koeficijente u sledeãoj shemi oksido-redukcione reakcije:
SnCl2 + HgCl2 ® SnCl4 + Hg2Cl2

POGLAVQE:
1. a) duþina, b) energija, v) gustina, g) koliåina supstance, d) termodinamiåka temperatura, ð) zapremina.
2. 4,5 ⋅ 103 nm.
3. 1,6 ⋅ 10–10 m.
4. 2 088 km/h.
5. 50 cm3 .
6. a) 6,2 ⋅ 102 dm2, b) 6,2 ⋅ 104 cm2, v) 6,2 ⋅ 106 mm2 .
7. 2,5 ⋅ 10–7 m3 .
8. a) 5 ⋅ 10–3 kg, b) 5 ⋅ 103 mg, v) 5 ⋅ 106 µg.
9. 3,01 ⋅ 1021 u.
10. 13,6 ⋅ 103 g/l.
11. 0,667 kg/m3 .
12. 1 074 K.
13. 373 K.
14. – 233 ºC
15. 49 033,3 kPa
16. 1 016 mbar.
17. 98,6 kPa
18. 292,9 kJ
¡¡ POGLAVQE: STRUKTURA ATOMA
19. 200 miliona puta.
20. 339 miliona puta.
21. 6,72 ⋅ 107 atoma.
22. 8,37 ⋅ 10–24 cm3
23. a) 3,15 ⋅ 10–23 g, b) 5,14 ⋅ 10–23 g, v) 2,11 ⋅ 10–22 g
24. 1,87 ⋅ 10–22 g
25. 3,44 ⋅ 10–19 mg
26. a) 14,00, b) 15,99, v) 200,6.
27. a) 2,107 ⋅ 10–25 kg, b) 1,792 ⋅ 10–25 kg, v) 4,664 ⋅ 10–26 kg.
28. 121 50 Sn.
29. a) 24 12 Mg,
30. a) 16 8 O,
b) 40 20 Ca, v) 56 26 Fe
b) 17 8 O, v) 18 8 O
31. Svaki atom sadrþi isti broj protona i elektrona, pa je stoga u celini elektriåno neutralan.
32. a) 33, b) 61, v) 125.
33. a) 4p 5n, b) 10p 10n, v) 16p 16n.
34.
35. 6,94.
36. 10,81.
37. 63,62.
38. a) n = 1, b) n = 5.
39. a) l = 0, 1, 2; b) 4
40. a) N = 8, b) N = 18, v) N = 32.
41. Sastoji se od tri energetska podnivoa (s, p, d), koji se karakterišu vrednostima l = 0, 1, 2.
42. a) 2p, b) 1s, v) 3d, g) 4f, d) 3p.
43. Sliåne su po obliku, a razlikuju se po veliåini.
44. a) 2s2p, b) 3s3p3d, v) 4s4p.
45. 16.
46. a) na treãem nivou i d-podnivou, b) na drugom nivou i s-podnivou, v) na åetvrtom nivou i f-podnivou.
47. a) 3p, b) 5s, v) 4f
48. a) n = 3, l = 2; b) n = 1, l = 0; v) n = 4, l = 3; g) n = 3, l = 1; d) n = 2, l = 0
49. n = 3, l = 1, m = 1,0 –1
50. m = 3, 2, 1, 0, –1, –2, –3.
51.
52. 53.
54. a) b) v)
55. 1s22s22p63s23p2 .
56. a) 1s22s22p1 , b)
57. K 1s22s22p63s23p64s1
K+ 1s22s22p63s23p6
O 1s22s22p4
O2– 1s22s22p6
Al 1s22s22p63s23p1
Al3+ 1s22s22p6
58. a) Z = 9, b) Z = 11, v) Z = 36.
59. P 1s22s22p63s23p3
As 1s22s22p63s23p64s23d104p3 Oba elementa nalaze se u petoj grupi, jer u najvišem energetskom nivou sadrþe po 5 elektrona.
60. a) 2s22p4 b) 2s22p2
61. Sadrþe po 7 elektrona, koji su na podnivoima rasporeðeni na sledeãi naåin: ns2np5
62. v.
63. b.
64. a) litijum, b) sumpor, v) magnezijum, g) argon, d) helijum.
65. a) u drugoj periodi, b) u treãoj periodi, v) u treãoj periodi, g) u åetvrtoj periodi, d) u drugoj periodi.
66. Be 1s22s2 – nalazi se u drugoj grupi, Mg 1s22s22p63s2 – nalazi se u drugoj grupi,
Ca 1s22s22p63s23p64s2 – nalazi se u drugoj grupi.
67. a) u ¡A grupi, b) u ¡¢B grupi, v) u nultoj grupi, g) u ¢¡B grupi, d) u ¢¡B grupi, ð) u ¢¡¡B grupi.
68. a) Z = 15, b) treãa perioda, peta grupa, v) 5, g) 3.
69. a) u treãoj periodi i sedmoj grupi, b) u åetvrtoj periodi i drugoj grupi, v) u petoj periodi i prvoj grupi.
70. 4 i 20, 7 i 15, 16 i 34.
71. Spada u p-elemente.
72. Spada u d-elemente.
73. Alkalni metali imaju najmawe, a plemeniti gasovi najveãe energije jonizacije.
74. a) B, jer se u periodi nalazi ispred N i F, b) K, jer se u grupi nalazi ispod Li i Na
75. a) 518 kJ/mol, b) 494 kJ/mol, v) 415 kJ/mol.
76. Gubitkom dva valentna elektrona atom Ca prelazi u jon Ca2+ koji ima stabilnu elektronsku konfiguraciju plemenitog gasa.
77. Kod åetvrte energije jonizacije, pošto nastali jon Al3+ ima stabilnu elektronsku konfiguraciju plemenitog gasa.
78. a) fluor, b) hlor, v) sumpor.
79. 3s23p3
80. 349 kJ/mol
81. a) S, O, Cl, Br, I, F; b) Mg, Ca, Na, Li, Al.
82. Najveãi afinitet prema elektronu ima element s atomskim brojem 17 (hlor), a najmawu energiju jonizacije element s atomskim brojem 11 (natrijum).
¡¡¡ POGLAVQE: HEMIJSKA
83. a) : N ⋅ + ⋅ N : → : N N : , H b) : N ⋅ + 3 H → : N : H , . H v) ⋅ O ⋅ + 2 H → H : O : H . .
84. H |
a) N≡N , b) N–H , v) H–O–H | H
85. .. .. :O: :C: :O:
86.
87. a) molekul Cl2, b) dva slobodna atoma Ne
88. a, b, g.
89. 91.
90.
92. a) 3p-orbitale, b) 5p-orbitale, v) 4p-orbitale.
93. 6,4 ⋅ 10–30 Cm.
94. a) 0,6 ⋅ 10–11 m, b) 0,29 ⋅ 10–11 m. Polarnija je veza u molekulu HCN. 95. S O C O O O
96. Atomi hlora su simetriåno rasporeðeni u prostoru oko atoma ugqenika (molekul CCl4 ima oblik tetraedra). Stoga se dipolni momenti C–Cl veza poništavaju unutar samog molekula.
97. Molekul H2O. H H H – N – N – H.
98. Iduãi od HF ka HI smawuje se razlika u relativnoj elektronegativnosti izmeðu atoma halogenog elementa i vodonika. Stoga su veze H–X (X=atom halogenog elementa) sve slabije polarne.
99. Sa porastom atomskih brojeva elemenata u periodama raste pozitivno naelektrisawe jezgra a opada veliåina atoma, te jezgro sve jaåe privlaåi elektrone. Elektronegativnost elemenata u grupama opada sa porastom atomskih brojeva, pošto rastu veliåine atoma a slabi privlaåno delovawe jezgra na spoqašwe elektrone.
100. : I : Br: a) jeste, b) zajedniåki elektronski par pomeren je ka atomu broma.
101. BrCl, HI, HBr, HCl, HF
102. Oko 50 % jonskog karaktera.
103. a) nepolarna kovalentna veza, b) polarna kovalentna veza, v) nepolarna kovalentna veza.
104.
Cl Cl
H : C : Cl H –C–Cl. Najpolarnije su veze C–Cl
Cl Cl
105. Veza H–O
106. LiI, LiBr, LiCl, LiF.
107. 114 pm
108. Duþina veze raste iduãi od HF ka HI
109. 427 kJ/mol
110. 315,3 kJ/mol. Nisu, jaåa je sigma-veza.
111. 416,2 kJ/mol
112. 387,5 kJ/mol
113. Energija veze ãe rasti od HI prema HF.
114. 90 º
115. Da, dolazi do sp-hibridizacije.
116. U procesu formirawa hemijske veze dolazi do prelaska jednog elektrona iz popuwene 2s-orbitale atoma berilijuma u praznu 2p-orbitalu. Polupopuwene 2s i 2p-orbitale se hibridizuju i daju dve sp-hibridne orbitale. Te orbitale prekrivawem sa 1s-orbitalama dva atoma vodonika formiraju dve ekvivalentne sigma-veze.
117. Pomoãu åetiri sp3-hibridne orbitale atoma silicijuma i 3p-orbitala åetiri atoma hlora.
118. U procesu formirawa hemijske veze dolazi do prelaska jednog elektrona iz popuwene 2s-orbitale atoma ugqenika u praznu 2p-orbitalu. Mešawem jedne 2s i tri 2p-orbitale nastaju åetiri sp3-hibridne orbitale. Prekrivawem sa 1s-orbitalama åetiri atoma vodonika one grade åetiri ekvivalentne sigma-veze.
119. Molekul O2 sadrþi dva nesparena elektrona u π * 2p-orbitalama. Red veze je 2.
120. Red veze je 2,5, a molekul sadrþi jedan nespareni elektron u π * 2p-orbitali.
121. Red veze u molekulu B2 je 1, a u molekulu C2 je 2. Stoga je veza u molekulu C2 åvršãa.
122. Jon N2+ sadrþi jedan nespareni elektron u vezujuãoj σ 1s-orbitali. Red veze mu je veãi od nule (0,5), stoga je on energetski stabilan.
123. Red veze ovog molekula ravan je nuli, te se on i ne obrazuje.
124. Li 1s22s1 , F 1s22s22p5. Prelaskom jednog 2s-elektrona iz atoma litijuma u polupopuwenu 2p-orbitalu atoma fluora, tj. obrazovawem jonskog para Li+F–
125. Jonski parovi imaju izraþenu sposobnost asocijacije, te se meðusobno povezuju i grade jonske kristale.
126. Cs2Se. Veza ima preteþno jonski karakter.
127. . ..
a) 2 Na ⋅ + ⋅ S : → [Na]+ [ : S : ]2– [Na]+ , .. .. .. ..
b) Al ⋅ + 3 F : → [: F :]– [Al]3+ [: F :]– , [: F :]–
v) K ⋅ + ⋅ I : → [K]+ [: I :]–
128.
+3 –1 +1 –2 +1 –1 +2 –1 +2 –2
a) Al Cl3, b) Na2 O, v) Li Br, g) Ca F2, d) Mg O
129.
a) SrCl2, b) Rb2S, v) Ca3N2, g) Al2O3. 130. v, g.
131. O i H, C i Cl.
132. v, g.
133. a) MgF2, MgCl2, KF, KCl, b) HF, HCl, v) F2, H2, Cl2. 134. a, b, g.
135. Kiseonik je elektronegativniji od sumpora, stoga se izmeðu molekula H2O u teånoj vodi obrazuju znatno åvršãe vodoniåne veze nego izmeðu molekula H2S
136. a.
137. a) 2 F2, b) 5 Fe, v) 3 Na2CO3.
138. a) sedam molekula CO2, b) dve formulske jedinke KCl, v) tri molekula Cl2
139. a) 32,0, b) 256,5, v) 123,9.
140. a) 122,5, b) 74,09, v) 98,0.
141. a) 6,05 ⋅ 10–23 g, b) 5,32 ⋅ 10–23 g, v) 2,99 ⋅ 10–23 g
142. 9,32 ⋅ 10–20 mg
143. a) n(SO3), b) n(CuSO4), v) n(Zn), g) n(NH4+), d) n(Br2).
144. a) N(Cu), b) N(Na+), v) N(HCl), g) N(Na2CO3).
145. 4,5 mmol
146. n(H2) = 6,3 mol
147. N(S) = 5,63 ⋅ 1024.
148. a) 1,204 ⋅ 1026, b) 2,35 ⋅ 1024, v) 1,27 ⋅ 1022.
149. N(SO2) = 9,39 ⋅ 1023
150. 1,07 ⋅ 1015 godina.
151. a) 123,9 g/mol, b) 55,85 g/mol, v) 40,0 g/mol.
152. a) M(KMnO4) = 158,0 g/mol, b) M(HNO3) = 63,01 g/mol, v) M((NH4)2CO3) = 96,09 g/mol.
153. n(O) = 2,19 mol.
154. n(S8) = 58 mmol
155. n(CO2) = 0,25 mol.
156. 1,56 mol
157. a) 1,71 mmol, b) 0,29 mmol, v) 17,86 mmol.
158. 18,02 mol.
159. m(Fe) = 67,02 g.
160. m(KI) = 124,5 g.
161. m(NH3) = 15,8 mg
162. N(Ag) = 5,6 ⋅ 1021
163. N(HCl) = 2,47 ⋅ 1023
164. U 1 g srebra.
165. V(Cl2) = 0,95 dm3
166. 9,4 mmol.
167. n(O2) = 0,76 mmol.
168. 53,4 mg
169. M = 16,04 g/mol.
170. M = 64,00 g/mol.
171. 0,33 mol.
172. n(AgCl) = 0,2 mol.
173. 0,74 g
174. 27,65 kg vodonika i 972,35 kg hlora.
175. 16,06 kg.
176. m(MgO) = 19,9 g.
177. 0,11 g KOH
178. 20,30 g.
179. 10,71 g NH4Cl; 0,6 g NH3 ostalo je nesjediweno.
180. 279,5 dm3
181. a) 2 H+ + 2 OH– → 2 H2O, b) Cu2+ + S2– → CuS, v) HCO3– + H+ → CO2 + H2O
182. a) 2 H+ + CO3 2– → CO2 + H2O, b) 2 H+ + 2 OH– → 2 H2O, v) Al3+ + 3 OH– → Al(OH)3.
183. a) Ag+ + I– → AgI, b) Zn2+ + 2 OH– → Zn(OH)2, v) Pb2+ + SO4 2– → PbSO4
184. a) Ba2+ + SO4 2– → BaSO4, b) Pb2+ + S2– → PbS, v) Cu2+ + 2 OH– → Cu(OH)2.
185. a) +5, b) –3, v) –2, g) –3, d) +3.
186. a) +1, b) +7, v) +4, g) +7, d) –1.
187. a) –4, b) –2, v) +2, g) +4.
188. a) +1 +7 –2, b) +2 –2 +1, v) +1 +6 –2, g) +1 +1 +5 –2, d) +1 +3 –2, ð) +2 –1.
РЕШЕЊА
189. a) 2162285 b) 1343112 v) 2221222 g) 23 22 d) 36 153
190. a) 54 414 b) 178844 v) 83 3852 g) 1671437 d) 41 2212
191. a) 6114627 b) 51633 v) 148144 g) 1614237
192. 5,6 l
193. I2 + 10 HNO3 „ 2 HIO3 + 10 HNO2 + 4 H2O; oksiduje se 0,04 mola joda.
194. ∆ r H = – 98,7 kJ/mol.
195. ∆ r H = – 847,8 kJ/mol
196. ∆ r H = + 177,1 kJ/mol.
197. ∆ r H = – 890,3 kJ/mol.
198. ∆ r H = – 25,6 kJ/mol.
199. ∆ r H = – 518,8 kJ/mol.
200. ∆fH(HCl) = – 92,5 kJ/mol.
201. ∆fH(C2H5OH) = – 277,6 kJ/mol.
202. ∆fH(PH3) = + 5,3 kJ/mol.
203. ∆fH(FeS) = – 100,3 kJ/mol.
204. ∆fH(CuO) = – 155,1 kJ/mol
205. 141,76 kJ.
206. ∆ r H = – 348,2 kJ/mol.
207. 15,87 kJ
208. 1011,1 kJ.
209. 2,89 kJ.
210. ∆ r H3 = + 33,9 kJ/mol.
211. ∆fH(O3) = + 141,5 kJ/mol.
c (HCL)
212. v = .
(NO)
213. v = ⋅ .
2
214. v = – ⋅ .
2 ∆c (SO2)
215. 1,2 ⋅ 10–3 mol/dm3 ⋅ s.
216. 0,05 mol/dm3 .
217. Za 10 sekundi.
218. a) v = k [A] [B]2 , b) v = k [B], v) v = k [A] [B]2
219. v = k [O2]
220. k = 8,88 ⋅ 10–2 dm6/mol2 ⋅ s.
221. Poveãava se 2 puta.
222. 12 puta.
223.
224.
225. K = 4,16 dm3/mol.
226. K = 0,02.
227. K = 800, [N2] = 0,5 mol/dm3 , [H2] = 1,4 mol/dm3
228. K = 2,5 dm6/mol2. Polazna koncentracija komponente A je 2,76 mol/dm3 , a komponente B je 5,52 mol/dm3 .
229. K = 1/50 = 0,02.
230. K = 4,2 ⋅ 10–4 mol/dm3 .
231. [CO] = [H2O] = 0,02 mol/dm3 .
232. [I2] = 0,12 mol/dm3 , [H2] = 5,28 mol/dm3 .
233. n(HI) = 3 mol.
234. 5,1 g.
235. Ulevo.
236. Neãe uticati na poloþaj hemijske ravnoteþe.
237. Ravnoteþa se pomera ulevo.
238. Poveãaãe se.
239. a) udesno, b) udesno.
240. a) u stranu proizvoda reakcije, b) u stranu proizvoda reakcije, v) neãe doãi do pomerawa ravnoteþe.
241. Ravnoteþa se pomera ulevo.
242. Brzina direktne reakcije ãe se poveãati 8 puta, a brzina povratne reakcije 4 puta.
243. a) koncentracija Cl2 ãe se smawiti, b) koncentracija Cl2 ãe se smawiti, v) koncentracija Cl2 ãe se poveãati.
244. a) pritisak treba smawiti, b) temperaturu treba poveãati, v) koncentracije PCl3 i Cl2 treba smawiti.
245. Spada u grubo disperzne sisteme (tzv. suspenzije), pošto su dispergovane åestice peska i muqa veãe od 100 nm
246. Spada u molekulsko disperzne sisteme – rastvore razliåitih soli u vodi.
247. Spada u grubo disperzne sisteme (tzv. emulzije).
248. Voda, pošto se nalazi u istom agregatnom stawu kao i rastvor.
249. a) voda, b) alkohol.
250. 10,8 g.
251. 51,05 g.
252. 24,5 g.
253. 37,5 %.
254. 0,6 %.
255. w(KOH) = 40 %.
256. 25 g NaOH i 225 g vode.
257. 45 g
258. 55,6 %.
259. U 1 900 g
260. 30,75 g
261. 860 g
262. 9,34 cm3 H2SO4 i 92,8 g vode.
263. 679,38 cm3
264. 2 mol/dm3 .
265. 0,2 mol/dm3 .
266. 0,025 mol/dm3 .
267. c = 17,9 mol/dm3
268. c = 0,72 mol/dm3
269. 1,74 g
270. 6,42 g.
271. 200 cm3 .
272. 8,5 cm3 .
273. 19,6 cm3
274. 6,24 mol/kg
275. 0,5 mol/kg
276. 9,58 g Na2CO3 i 90,42 g vode.
277. 1,24 MPa.
278. 6,5 ⋅ 105 Pa.
279. – 2,23 ºC.
280. – 1,61 ºC
281. 100,86 ºC
282. 79,07 ºC
283. Rastvor glukoze.
284. 133,9 g/mol.
285. a) HCN „ H+ + CN–, ili: HCN + H2O „ H3O+ + CN–, b) NaCl → Na+ + Cl–, v) NH3 + H2O „ NH4+ + OH–
286. Najjaåi je elektrolit C, a najslabiji elektrolit B
287. α = 0,35 = 35 %.
288. K = 1,8 ⋅ 10–5 mol/dm3 za sve koncentracije.
289. K = 5,9 ⋅ 10–4 mol/dm3 .
290. α = 5 ⋅ 10–4.
291. α = 0,089.
РЕШЕЊА
292. a) H2SO4 + H2O „ H3O+ + HSO4–, b) HCOOH + H2O „ H3O+ + HCOO–, v) H2O + H2O „ H3O+ + OH–
293. HF + CH3COO– „ CH3COOH + F– Jaåa baza je anjon CH3COO–
294. a) k b k b, b) k b b k, v) b k k b.
295. a) CN–, b) NH3, v) CO32–
296. a) HCl + H2O „ H3O+ + Cl–, b) NH3 + H2O „ NH4+ + OH–. [H+] [CH3COO–] [H+] [NO2 –] [H+] [ClO–]
297. a) K = , b) K = , v) K = [CH3COOH] [HNO2] [HClO]
298. a) udesno, b) ulevo.
299. Fluorovodoniåna kiselina.
300. 1,8 ⋅ 10–16 mol/dm3 .
301. 5,5 ⋅ 10–10 mol/dm3
302. Izazvaãe pomerawe ravnoteþe udesno.
303. Usloviãe smawewe koncentracije H+ jona.
304. [H+] = [CH3COO–] = 1,3 ⋅ 10–3 mol/dm3 .
305. [NH4+] = [OH–] = 4,2 ⋅ 10–4 mol/dm3
306. 1,8 ⋅ 10–4 mol/dm3 .
307. 1,7 ⋅ 10–5 mol/dm3 .
308. 1,8 ⋅ 10–4 mol/dm3
309. [H+] = 10–11 mol/dm3 , pH = 11.
310. [H+] = 10–3 mol/dm3 , [OH–] = 10–11 mol/dm3 .
311. a) c = 0,5 mol/dm3 , b) [H+] = 3 ⋅ 10–3 mol/dm3
312. a) [H+] = 10–2 mol/dm3, b) pH = 2, v) pOH = 12.
313. Veãa je koncentracija H+ jona.
314. [H+] = 3,12 ⋅ 10–9 mol/dm3. Rastvor reaguje bazno.
315. [OH–] = 7,14 ⋅ 10–3 mol/dm3. Rastvor reaguje bazno.
316. pH = 4,8.
317. pOH = 3,2.
318. a) 6,7, b) 2,09, v) 9,57.
319. a) 10,66, b) 8,7, v) 5,97.
320. pOH = 2,87, pH = 11,13.
321. 2.
322. 11,4.
323. a) bazno, v) kiselo, g) kiselo.
324. a) crvena, b) plava, v) plava, g) crvena, d) plava.
325. a) bazno, b) neutralno, v) slabo kiselo.
H2O
326. a) NaHCO3 → Na+ + HCO3 –, HCO3– + H2O „ H2CO3 + OH–,
H2O b) K2CO3 → 2 K+ + CO32–CO32– + H2O → HCO3– + OH–,
H2O v) NaCN → Na+ + CN–
CN– + H2O → HCN + OH–.
327. [Cu(H2O)4]2+ + H2O „ [Cu(H2O)3(OH)]+ + H3O+
328. a, g.
329. b, d.
330. a) joni HCO3–, b) molekuli H2CO3
331. 4,75.
332. 9,55.
333. 2,9 g
334. 1,1 ⋅ 10–3 mol/dm3
335. Imaãe crvenu boju.
336. Pri dodatku H+ jona disocijacija HIn „ H+ + In– se suzbija i rastvor dobija crvenu boju; pri dodatku OH– jona disocijacija HIn se favorizuje i rastvor ãe imati þutu boju.
337. a) bezbojan, b) qubiåastocrven, v) ruþiåast.
338. U ¡A grupu svrstava se zato što wegov atom sadrþi jedan elektron u s-orbitali (analogija sa alkalnim metalima). U ¢¡¡A grupu svrstava se zato što mu nedostaje jedan elektron do stabilne elektronske konfiguracije plemenitog gasa (analogija sa halogenim elementima).
339. Jezgro atoma vodonika je elementarna åestica – proton, H+, koja je mnogo mawa od ostalih katjona, što uslovqava niz wegovih specifiånih svojstava.
340. 0,015 %.
341. 14,6 g.
342. 76,5 cm3 .
343. Ne, najveãa zapremina vodonika oslobaða se pri reakciji 1 g litijuma sa vodom.
344. Epruveta napuwena vodonikom prinese se plamenu. Ako vodonik mirno sagoreva, znaåi da ne sadrþi primese kiseonika iz vazduha.
345. Pomoãu rastvora kalijum-permanganata.
346. Prema teoriji valentne veze, veza u molekulu H2 je jednostruka, sigma-veza, nastala prekrivawem polupopuwenih 1s-orbitala dva atoma vodonika. Prema teoriji MO, dva elektrona u molekulu H2 popuwavaju σ1s vezujuãu MO. Red veze je 1.
347. 0,09 g
348. 470 kg
349. Oslobaða se 13 415 kJ.
350. a) + 1, b) –1, v) +1, g) –1.
351. a) +1, b) –1, v) +1.
352. U molekulu HF
353. Oslobaða se 27,8 kJ
354. Reakcije jonskih hidrida metala, kao i hidrida nekih nemetala (npr. SiH4 i B2H6) sa vodom su oksido-redukcione reakcije. Praãene su oslobaðawem vodonika. Reakcije polarnih hidrida nemetala (npr. HCl i NH3) sa vodom su protolitiåke reakcije, pri kojima se hidridi ponašaju kao kiseline ili baze.
355. Mešawem jedne popuwene 2s i tri polupopuwene 2p-orbitale atoma azota nastaju åetiri sp3-hibridne orbitale: jedna popuwena i tri polupopuwene. Prekrivawem triju polupopuwenih sp3-hibridnih
orbitala atoma azota sa 1s-orbitalama tri atoma vodonika nastaje molekul NH3. Zbog pojaåanog odbijawa izmeðu popuwene sp3-orbitale i triju orbitala sa vezujuãim elektronskim parovima, ugao izmeðu veza je nešto mawi od 109,5 º
356. 46,2 kg
357. 2,02 %.
Elementi ¡A grupe periodnog sistema
358. Po jedan elektron u s-orbitali.
359. Kamena so, NaCl; åilska šalitra, NaNO3 i kriolit, Na3AlF6.
360. 14,07 %.
361. 350 g
362. Elektrolizom rastopa wihovih hlorida ili hidroksida.
363. na katodi: 2 K+ + 2 e → 2 K; na anodi: 2 OH– → H2O + 1/2 O2 + 2 e.
364. 575 kg
365. Porastom atomskih brojeva alkalnih metala, vrednosti prvih energija jonizacije opadaju. To se objašwava åiwenicom da je valentni elektron sve udaqeniji od jezgra koje ga sve slabije privlaåi.
366. Atom litijuma je veoma malih dimenzija, što uslovqava veliku jaåinu metalne veze.
367. 1,8 ⋅ 1022.
368. Raste od litijuma ka cezijumu. To se tumaåi smawewem vrednosti wihovih prvih energija jonizacije, te se valentni s-elektron sve lakše otkida.
369. +1.
370. a) 4 Na + O2 → 2 Na2O, b) 2 Na + H2 → 2 NaH, v) 2 Na + 2 H2O → 2 NaOH + H2, g) 16 Na + S8 → 8 Na2S
371. Jaåina baza raste od LiOH ka CsOH. To se tumaåi porastom polupreånika jona alkalnih metala iduãi od Li ka Cs, usled åega se smawuje privlaåewe izmeðu jona metala i OH– jona, te je disocijacija baze olakšana.
372. a) 47 %, b) 70 %, v) 79 %.
373. Zbog velike reaktivnosti, alkalni metali se åuvaju u inertnim ugqovodonicima (petroleumu ili parafinskom uqu).
РЕШЕЊА
374. 6,02 ⋅ 1020
375. 2,37 g soli i 247,63 g vode.
376. Elektrolizom zasiãenog rastvora natrijum-hlorida u ãeliji sa þivinom katodom.
377. NH3 + CO2 + H2O → NH4HCO3, NH4HCO3 + NaCl → NaHCO3 + NH4Cl, 2 NaHCO3 → Na2CO3 + CO2 + H2O
378. 5,5 m3 rastvora NaCl; 422,6 m3 NH3 i 211,3 m3 CO2
379. 29,27 %.
380. b, v.
381. 38,67 %.
grupe periodnog sistema
382. ns2, gde n ima vrednosti od 2 do 7.
383. Gubitkom dva valentna elektrona atomi zemnoalkalnih metala prelaze u jone M2+, koji imaju stabilnu elektronsku konfiguraciju plemenitog gasa.
384. +2.
385. Atomi zemnoalkalnih metala su mawih dimenzija od atoma alkalnih metala. Oni takoðe daju po dva valentna elektrona za obrazovawe metalne veze, pa je ona jaåa nego kod alkalnih metala.
386. Zemnoalkalni metali su slabije reaktivni. To se objašwava razliåitim elektronskim konfiguracijama wihovih atoma, kao i veãim energijama jonizacije.
387. Zbog svoje velike energije jonizacije i elektronegativnosti (1,5), berilijum sa veãinom elemenata gradi jediwewa koja imaju preteþno kovalentni karakter.
388. Ima amfoterni karakter.
389. 25,5 kg Mg i 36,1 kg Ca
390. Barijum, jer ima najnegativniju vrednost standardnog elektrodnog potencijala.
391. Karbonati, sulfati i fosfati.
392. Ca3N2, kalcijum-nitrid; Mg3N2, magnezijum-nitrid.
393. a) 2 Ca + O2 → 2 CaO, b) Ca + H2 → CaH2, v) 3 Ca + N2 → Ca3N2.
394. Moþe. Pri toj reakciji magnezijum redukuje CO2 do elementarnog ugqenika, koji se izdvaja u vidu åaði: 2 Mg + CO2 → 2 MgO + C.
395. 101,6 kg.
396. 40,9 g
397. Svi ovi minerali su po hemijskom sastavu kalcijum-karbonat, CaCO3
398. a) Ca3(PO4)2, b) CaF2, v) CaCO3.
399. + 177,5 kJ/mol.
400. Odvoðewem CO2 iz ravnoteþnog sistema.
401. 12,5 %.
402. 1 157,1 kJ.
403. 26,7 %
404. Slabo rastvorqivi CaCO3 rastvara se u višku CO2, gradeãi kalcijum-hidrogenkarbonat: CaCO3 + CO2 + H2O „ Ca(HCO3)2
405. 66,6 m3
406. Hidrogenkarbonati kalcijuma i magnezijuma uslovqavaju prolaznu tvrdoãu vode, a sulfati i hloridi kalcijuma i magnezijuma stalnu tvrdoãu vode.
407. Ca2+(aq) + CO32–(aq) → CaCO3(s), Mg2+(aq) + CO32–(aq) → MgCO3(s).
408. Jonoizmewivaåi su prirodne ili sintetiåke smole koje imaju sposobnost da zamewuju jone Ca2+ i Mg2+ iz tvrde vode jonima Na+
Elementi ¡¡¡A grupe periodnog sistema
409. 5B 1s22s22p1 , 13Al 1s22s22p63s23p1 , 31Ga 1s22s22p63s23p63d104s24p1 Po tri elektrona, i to dva elektrona u s-orbitali, i jedan nespareni elektron u p-orbitali.
410. U procesu obrazovawa hemijske veze dolazi do rasparivawa elektrona u s-orbitalama, i do sp2-hibridizacije s i p-atomskih orbitala.
411. Bor, aluminijum, galijum i indijum u veãini jediwewa imaju oksidacioni broj +3, a talijum +1.
412. Oksid bora ima kiseo, oksid aluminijuma amfoteran, a oksidi ostalih elemenata imaju preteþno bazni karakter, koji raste od galijuma ka talijumu
413. Bor ima znatno veãu energiju jonizacije i elektronegativnost od ostalih elemenata ¡¡¡A grupe, što ukazuje da teško otpušta elektrone. Wegova jediwewa imaju preteþno kovalentni karakter.
414. Da, sa nekim metalima. Ta jediwewa zovu se boridi.
415. 80 dm3
416. Mogu. Veza izmeðu ovih molekula je koordinativno-kovalentna veza.
417. Rubin i safir.
418. Smeša hidroksida aluminijuma AlO(OH) i Al(OH)3
419. 305,9 kg.
420. na katodi: 2 Al2O3 + 6 e → 2 Al + 2 AlO33–na anodi: 2 AlO33– + 3 C → 3 CO + Al2O3 + 6 e.
421. 950 kg Al, 40 kg Cu, 5 kg Mn i 5 kg Mg.
422. ∆ r H = – 847,8 kJ/mol.
423. Cr2O3 + 2 Al → 2 Cr + Al2O3.
424. Aluminijum je amfoterni element koji se rastvara i u kiselinama i u bazama. Na primer:
2 Al + 6 HCl → 2 AlCl3 + 3 H2, 2 Al + 6 NaOH + 6 H2O → 2 Na3 [Al(OH)6] + 3 H2O
425. Vodeni rastvori ovih soli usled hidrolize reaguju kiselo, odnosno bazno.
426. 2,5 ⋅ 106 kJ.
427. Delovawem baza na rastvore aluminijumovih soli: Al3+ + 3 OH– → Al(OH)3.
428. Aluminati su kompleksna jediwewa aluminijuma koja nastaju rastvarawem aluminijum-hidroksida u bazama.
429. ns2np2, gde n ima vrednost od 2 do 6. Sadrþe po dva nesparena elektrona u p-orbitalama.
430. Smawuje se nemetalni, a raste metalni karakter.
431. + 2 i + 4.
432. sp3 i sp2-hibridizacija.
433. a) –2, b) –1, v) + 4.
434. 64,3 g
435. Oksidacioni broj ugqenika raste od +2 na +4, a hlora se smawuje od 0 na –1.
436. Kalcijum-sulfat koji nastaje pri reakciji mermera sa sumpornom kiselinom praktiåno je nerastvorqiv u vodi.
437. 95,4 %.
438. 1,67 g, odnosno 851 cm3 .
439. a) CaCO3 + 2 H+ → Ca2+ + H2O + CO2, b) 2 OH– + CO2 → CO32– + H2O.
440. 2,45 g
441. 661,6 dm3 .
442. 1,32 g
443. 211,3 dm3
444. Sve tri soli reaguju bazno usled hidrolize.
445. 5,6 t CaO; 2 240 m3 CO
446. 286,16 g
447. O = C = O, sp-hibridizacijom.
448. 389,8 g
449. Pri oksidaciji silicijuma u rastvorima kiselina na wegovoj površini se obrazuje åvrsta prevlaka SiO2 koja spreåava daqu reakciju. U rastvorima baza proizvodi oksidacije silicijuma prelaze u rastvorqiva jediwewa.
450. SiO2 je prostorni polimer izgraðen od tetraedara SiO4 povezanih jakim kovalentnim vezama. Da bi se SiO2 rastopio, potrebno je raskinuti ove veze. CO2 u åvrstom stawu gradi molekulsku kristalnu rešetku u kojoj su molekuli CO2 povezani slabim meðumolekulskim privlaånim silama.
451. 689,7 kg masne sode i 546,8 kg peska.
452. 30,4 g.
453. 500 kg
454. Ima amfoterni karakter.
455. 453,2 kg.
456. 0,89 dm3
457. a) 90,6 %, b) 86,6 %, v) 92,8 %
458. Na površini se prevlaåi zaštitnim slojem slabo rastvorqivog olovo-hlorida, odnosno olovo-sulfata.
459. Na 50 ºC.
460. 124,6 g
461. Sadrþe po tri nesparena elektrona u p-orbitalama.
Elementi ¢A grupe periodnog sistema
462. Porastom atomskih brojeva elemenata u ¢A grupi smawuje se wihov nemetalni, a raste metalni karakter. To se tumaåi smawivawem energija jonizacije, kao i elektronegativnosti elemenata.
463. – 3, + 3, + 5.
464. Trostruka kovalentna veza izmeðu atoma azota u molekulu N2 je veoma åvrsta, stoga je molekulski azot hemijski veoma slabo reaktivan.
x
465. Azot, koji ulazi u sastav svih belanåevina.
466. a) + 2, b) + 4, v) +3.
467. a) 25,9 %, b) 36,8 %.
468. 156 m3
469. 19 mg, odnosno 15,2 cm3
470. 3 g
471. 4,87 g.
472. a) 82,25 % azota, 17,75 % vodonika, b) 0,76 g.
473. 15,6.
474. NH4+ + OH– „ NH3 + H2O
475. Reakcija dobijawa amonijaka iz vodonika i azota je povratna i egzotermna. Da bi se poveãao prinos amonijaka potrebno je poveãati pritisak i sniziti temperaturu. Meðutim, na niþim temperaturama amonijak se gotovo i ne stvara. Stoga se reakcija izvodi na 500 °C kako bi se ona ubrzala. U ciqu brþeg uspostavqawa ravnoteþe koriste se katalizatori.
476. 11 200 m3 azota i 33 600 m3 vodonika.
477. 13,15 m3
478. U 340,7 g
479. 11,27.
480. U teånom amonijaku obrazuju se vodoniåne veze izmeðu molekula NH3
481. H:N: + H:Cl: → [ H:N:H ]+ + Cl–
482. 28,6 kg
483. 4 NH3 + 5 O2 → 4 NO + 6 H2O, 2 NO + O2 → 2 NO2 , 4 NO2 + O2 + 2 H2O → 4 HNO3.
484. 2 812,5 kg.
485. 945 kg.
486. 0,1 t.
487. 353,2 cm3 .
488. 3 Cu + 8 HNO3 → 3 Cu(NO3)2 + 4 H2O + 2 NO
489. Sa elektronegativnijim elementima (kiseonikom, sumporom i hlorom) fosfor gradi jediwewa u kojima je wegov oksidacioni broj pozitivan. Negativan oksidacioni broj fosfor ima u jediwewima sa elementima mawe elektronegativnosti (metalima).
490. 0,5 t belog fosfora. Treba utrošiti 0,48 t ugqa i 1,45 t peska.
491. Rastvarawem belog fosfora u ugqenik(¡¢)-sulfidu.
492. 5,4 ⋅ 105 kJ
493. Dobijaju se ista jediwewa.
494. 54,5 g
495. 247,8 g fosfora i 224 dm3 kiseonika.
496. + 5.
497. 19 581 kg
498. 1,4.
499. 1,16 kg
Elementi ¢¡A grupe periodnog sistema
500. Prve energije jonizacije i elektronegativnost elemenata ¢¡A grupe opadaju sa porastom wihovih atomskih brojeva. U istom smeru smawuje se nemetalni, a raste metalni karakter elemenata.
501. Poveãawem sloþenosti strukture elemenata.
502. Raste od kiseonika prema polonijumu. To ukazuje na porast metalnog karaktera elemenata.
503. – 2. Sumpor, selen i telur grade i jediwewa u kojima je wihov oksidacioni broj + 2, + 4 i + 6.
504. Sa alkalnim i zemnoalkalnim metalima.
505. Raste od H2O prema H2Te, zbog smawewa jaåine veza izmeðu vodonika i odgovarajuãeg elementa ¢¡A grupe. Stoga je disocijacija kiselina u vodenom rastvoru olakšana.
РЕШЕЊА
506. 300 g.
507. 7,05 g
508. 26 666 m3
509. 679 m3
510. Molekul O2 ima dva nesparena elektrona u razvezujuãim π * 2 px i π * 2py-orbitalama.
511. – 1.
512. Ozon je veoma jako oksidaciono sredstvo, koje oksiduje kalijum-jodid do elementarnog joda:
2 KI + H2O + O3 → I2 + 2 KOH + O2.
513. Dele se na kisele, bazne, neutralne i amfoterne.
514. 49,95 % i 59,9 %.
515. a) –2, b) +6, v) +4, g) +6.
516. a) + 6, b) + 4, v) + 1.
517. Reakcijom izmeðu gvoþðe(¡¡)-sulfida i razblaþene hlorovodoniåne kiseline: FeS + 2 HCl → FeCl2 + H2S.
518. 247 dm3 .
519. a) Pb2+ + S2– → PbS, b) Cu2+ + S2– → CuS.
520. 2 H2S + 3 O2 → 2 H2O + 2 SO2
521. 4 FeS2 + 11 O2 → 8 SO2 + 2 Fe2O3, 2 SO2 + O2 „ 2 SO3, SO3 + H2SO4 → H2S2O7, H2S2O7 + H2O → 2 H2SO4
522. 2 445 m3 vazduha. 665 kg Fe2O3 i 373 m3 SO2
523. 940 kg
524. v.
525. Gasoviti SO3 reaguje s vodom veoma sporo, dok åvrsti SO3 reaguje uz eksploziju.
526. a) masa ãe se smawiti, b) masa ãe se poveãati.
527. 17,1 cm3
528. 124 cm3
529. Cu + 2 H2SO4 → CuSO4 + SO2 + 2 H2O.
530. Ba2+ + SO4 2– → BaSO4.
531. 360,7 g.
532. v
Elementi ¢¡¡A grupe periodnog sistema
533. Sadrþe po 7 elektrona u p-orbitalama.
534. Van der Valsove privlaåne sile izmeðu nepolarnih molekula halogenih elemenata veoma su slabe.
535. Opadaju
536. Smawuju se.
537. Cl2 + 2 I– → 2 Cl– + I2
538. Zbog velike hemijske aktivnosti, halogeni elementi se u prirodi nalaze samo u obliku jediwewa.
539. –1. Halogeni elementi (osim fluora) sa elementima veãe elektronegativnosti (npr. sa kiseonikom) grade i jediwewa u kojima je wihov oksidacioni broj +1, +3, +5 i +7.
540. Od svih elemenata, fluor ima najveãu elektronegativnost (4). Stoga sa drugim elementima gradi jediwewa u kojima je wegov oksidacioni broj uvek negativan.
541. Imaju preteþno jonski karakter. MX, MX2
542. Nalaze se u obliku dvoatomnih molekula u kojima su atomi povezani jednostrukim kovalentnim vezama.
543. Raste od HF ka HI. Naime, u istom smeru slabi energija veze izmeðu vodonika i halogenog elementa, pa je disocijacija kiselina u vodenom rastvoru olakšana.
544. 60 %, 20 %, 12 %, 3 %.
545. 48,7 %.
546. Fluor je najjaåe oksidaciono sredstvo koje energiåno razlaþe vodu prema jednaåini:
2 F2 + 2 H2O → 4 HF + O2
547. a) KClO3 + 6 HCl → 3 Cl2 + KCl + 3 H2O, b) MnO2 + 4 HCl → MnCl2 + Cl2 + 2 H2O
548. 1,65 t
549. 14,6 g
550. 9,47 m3 .
551. 7,9 g.
552. a) Cu + Cl2 → CuCl2, b) 2 Fe + 3 Cl2 → 2 FeCl3, v) P4 + 6 Cl2 → 4 PCl3,
553. a) + 4, b) – 1, v) + 1, g) +7.
554. Cl–Cl, Cl–Br, Cl–S, Cl–P, Cl–H.
555. 44,8 dm3
РЕШЕЊА
556. 2,46 mol
557. 18,4 mol/dm3 .
558. [H+] = 0,5 mol/dm3 , [OH–] = 2 ⋅ 10–14 mol/dm3 .
559. 0,114 mol/dm3 .
560. Ag+ + Cl– → AgCl
561. 7,82 g.
562. 144,1 g
563. 6,9 ⋅ 10–4 mol/dm3
564. 3,73 ⋅ 1018
565. 2 500 t.
566. 68,42 %.
567. 1,31 mg.
568. 200 m3
569. 7,1 g
570. b, g.
Prelazni elementi
571. Nalaze se u åetvrtoj, petoj i šestoj periodi.
572. Sadrþe po dva elektrona u s-orbitalama. Porastom atomskih brojeva, elektronima se popuwavaju d-orbitale pretposledweg energetskog nivoa.
573. Hrom i bakar, kod kojih se javqaju konfiguracije 3d54s1, odnosno 3d104s1, koje su stabilnije.
574. U åetvrtoj periodi.
575. Imaju po deset d-elektrona i po jedan s-elektron u posledwim energetskim nivoima.
576. a) [Ar] 3d54s1 , b) [Ar] 3d54s2 , v) [Ar] 3d64s2 .
577. a) +3, b) +6, v) +4, g) +2, d) +7.
578. 2 280,5 kJ
579. Pb2+ + CrO42– „ PbCrO4
580. 1 14 2 2 3 7.
581. 0,96 t. 4,4 t.
582. 434,6 g.
583. a) 69,9 %, b) 72,4 %, v) 59,8 %.
584. 55,9 %.
585. C + O2 → CO2, CO2 + C → 2 CO, Fe2O3 + 3 CO → 2 Fe + 3 CO2.
586. 0,24 kg.
587. 223,9 kg Fe i 134,7 m3 CO2.
588. 144,49 t.
589. 0,54 %.
590. 4 H2O + 3 Fe → Fe3O4 + 4 H2 1,87 kg gvoþða.
591. 10 cm3
592. 282,8 cm3
593. Fe + 4 HNO3 → Fe(NO3)3 + NO + 2 H2O
594. a) 4 FeS2 + 11 O2 → 2 Fe2O3 + 8 SO2, b) Fe2O3 + 3 H2SO4 → Fe2(SO4)3 + 3 H2O,
v) Fe2(SO4)3 + 6 NaOH → 2 Fe(OH)3 + 3 Na2SO4 .
595. Hemoglobin, vitamin B–12, ferment disawa.
596. 2 Cu2S + 3 O2 → 2 Cu2O + 2 SO2, Cu2S + 2 Cu2O → 6 Cu + SO2.
597. 157,5 g.
598. Zn + 2 Ag+ „ Zn2+ + 2 Ag.
599. 650,7 kg.
600. 28,7 g.
601. Legure þive sa metalima.
602. 14,7 dm3 .
603. 112 cm3
604. SnCl2 + 2 HgCl2 → SnCl4 + Hg2Cl2
Radivoj Nikolajeviã • mr Milena Šurjanoviã
ZBIRKA ZADATAKA IZ HEMIJE
za ¡ i ¡¡ razred sredwe škole za opštu gimnaziju i gimnaziju prirodno-matematiåkog smera i za struåne škole u podruåjima rada: poqoprivreda, prerada i proizvodwa hrane, zdravstvo i socijalna zaštita i prirodno-matematiåko podruåje rada Двадесет
Izdavaå
ZAVOD ZA UYBENIKE, BEOGRAD Obiliãev venac 5 www.zavod.co.rs
Likovni urednik
BIQANA SAVIÃ
Ilustracije DRAGOQUB JEROMELA
Lektor DRAGICA TUBIÃ-OSTROVSKA
Grafiåki urednik MIROSLAV RADIÃ
Korektori
MARIJANA VASIÃ STJEPANOVIÃ MIRJANA IVANKOVIÃ
Kompjuterska obrada ABRAKA-DABRA, Novi Sad
Obim: 22 štamparska tabaka Format: 20,5 × 26,5 cm
Tiraþ: 4 500 primeraka
CIP - Каталогизација у публикацији
Библиотеке Матице српске, Нови Сад
37.016:54(075.3)(076)
НИКОЛАЈЕВИЋ, Радивој, 1936-2010 Збирка задатака из хемије : за I и II разред средње школе : за општу гимназију и природно-математички смер гимназије, за стручне школе у подручјима рада: пољопривреда, прерада и производња хране, здравство и социјална заштита и природно-математичко подручје рада / Радивој Николајевић, Милена Шурјановић ; [илустрације Драгољуб Јеромела]. - 25. изд. - Београд : Завод за уџбенике, 2024 (Београд : Планета принт). - 173 стр. : илустр. ; 27 cm
Тираж 4.500.
ISBN 978-86-17-21023-4 1. Шурјановић, Милена, 1931-2024 [аутор]
COBISS.SR-ID 147990281

