



Milan Raspopovi}
Jovan [etraj~i}
Zoran Raspopovi}






Milan Raspopovi}
Jovan [etraj~i}
Zoran Raspopovi}
Milan O. Raspopoviœ
Jovan P. Šetrajæiœ
Zoran Raspopoviœ

za drugi razred gimnazije opšteg i društveno-jeziækog smera

Рецензенти
Dr Branislav Cvetkoviœ, viši nauæni saradnik Instituta za fiziku u Beogradu
Jovica Milisavqeviœ, profesor u Matematiækoj gimnaziji u Beogradu
Biqana Vlaæiœ, profesor u gimnaziji „Laza Kostiœ” u Novom Sadu
Уредник
Tatjana Bobiœ
Одговорниуредник
Dr Tatjana Kostiœ
Главни уредник
Стефан Пауновић
За издавача
Стефан Пауновић, в.д. директора
Ministar prosvete Republike Srbije odobrio je ovaj uxbenik rešewem broj 650-02-659/2019-03 od 14. 5. 2020. godine za upotrebu u drugom razredu gimnazije opšteg i društveno-jeziækog smera.
© ZAVOD ZA UXBENIKE, Beograd (2020)
ISBN 978-86-17-21038-8 (2020–2024)
Ovo delo se ne sme umnoþavati, fotokopirati i na bilo koji drugi naæin reprodukovati ni u celini ni u delovima, bez pismenog odobrewa izdavaæa.

Uxbenik je napisan u skladu sa aktuelnim Nastavnim planom i programom. U wemu su obraðene tematske celine: Molekulsko-kinetiæka teorija gasova, Termodinamika, Osnove dinamike fluida, Molekulske sile i fazni prelazi, Elektrostatika i Jednosmerna struja. Molekulsko-kinetiæka teorija gasova se zasniva na tvrdwi da se svako telo sastoji iz molekula (atoma) koji se neprekidno haotiæno kreœu. Polazeœi od te pretpostavke opisuju se i tumaæe gasovi, wihova svojstva i pojave, zakoni kojima se gasovi pokoravaju i moguœnosti wihove praktiæne primene.
Oblast fizike koja se formirala u procesu prouæavawa toplotnih pojava i promene unutrašwe energije (energije molekula, atoma), odnosno toplotne energije za vršewe mehaniækog rada (toplotne mašine), naziva se termodinamika.
U okviru tematske celine Osnovi dinamike fluida upoznaœemo osnovna svojstva teænosti i gasova sa makroskopskog (fenomenološkog) stanovišta, wihove zakonitosti i konkretne primene.
Promene agregatnih stawa ili fazni prelazi mogu da se razmatraju sa makroskopskog (termodinamiækog) gledišta, ne uzimajuœi u obzir strukturu supstancije i u sklopu molekulsko-kinetiæke teorije supstancije. Pristupi su razliæiti, ali se ne iskquæuju, naprotiv, oni se uzajamno dopuwavaju.
O agregatnim stawima supstancije, wihovim svojstvima i uzajamnim prelazima (sa makroskopskog stanovišta) govori se u poglavqu Molekulske sileifazni prelazi. Svojstva naelektrisanih tela (æestica), wihovo uzajamno delovawe u stawu relativnog mirovawa (elektriæna sila), koje se ostvaruje posredstvom elektriænog (elektrostatiækog) poqa kao i zakonitosti elektriænih pojava razmatraju se u poglavqu Elektrostatika.
Jednosmerna struja koja se ne mewa u toku vremena, wena osnovna svojstva i efekti kao i odgovarajuœi zakoni, predmet su izuæavawa tematske celine Jednosmerna struja. U uxbeniku se insistira na problemskim oblicima nastave s namerom da se uæenik ukquæi u taj proces kao aktivni uæesnik (sagovornik) i da pomoœu uxbenika moþe i sam da reprodukuje osnovne fiziæke ideje i sadrþaje.
Sadrþaji uxbenika nisu uvedeni kao gotov skup æiwenica i definicija, veœ se nastoji da se predstavi proces kojim se do tih saznawa došlo. To se postiþe nizom odabranih problemskih situacija koje se u uxbeniku postupno razrešavaju.
Posebno smo nastojali da se sadrþaji uxbenika nastavqaju na predznawe uæenika iz osnovne škole i prvog razreda gimnazije, kako bi se oæuvao kontinuitet u izuæavawu fizike.
U ciqu da se potpunije shvati razvojna linija fizike, ukratko su date biografije fiziæara koji su najviše doprineli utemeqewu pojedinih oblasti fizike koje se interpretiraju u ovom uxbeniku.
U uxbeniku se naroæito istiæe uloga fiziækog ogleda i modela u konstrukciji fiziæke teorije. Izbegnuto je pozitivistiæko shvatawe prema kojem se uloga eksperimenta svodi samo na verifikacije teorijskih rezultata, a istaknuta je uloga ogleda u razvoju osnovnih ideja i nauænih teorija.
Kvantitativna interpretacija sadrþaja uxbenika usklaðena je sa Nastavnim planom i programom matematike (koliko je to bilo moguœe zbog neusaglašenosti programa ove dve nastavne discipline).

Imali smo na umu, da fizika ima dubok uticaj na razvoj drugih nauka i razliæitih tehniækih oblasti kao i da saznawa u fizici bitno utiæu na usmeravawe uæenika u daqem školovawu i pripremu za wihov profesionalni poziv.
Na kraju svake tematske celine dati su kratki izvodi i pitawa za samokontrolu i proveru znawa. Kratak pregled celine omoguœuje uæeniku da se usmeri na suštinu nastavnog sadrþaja, da konkretizuje prethodno steæeno znawe i da ga preko odgovora na postavqena pitawa primeni u osvajawu novih saznawa i za rešavawe praktiænih zadataka.
1.
1.1.
1.2.
1.3. Gasni
2.1. Unutrašwa energija, toplota i prvi princip termodinamike ..........................................25 Unutrašwa energija ......................................................................................................................25
2.2. Gasni izoprocesi
..........................................................................28
Rad gasa pri izobarskom procesu ....................................................................................................28
Rad gasa pri izotermskom procesu ................................................................................................29
Toplotni kapacitet i specifiæne toplotne kapacitivnosti gasova
2.3. Povratni i nepovratni termodinamiæki procesi ................................................................33
2.4. Toplotne mašine ..........................................................................................................................37
Princip rada i energetski bilans toplotnog motora ..........................................................38 Koeficijent korisnog dejstva ......................................................................................................39
3. OSNOVI DINAMIKE FLUIDA ......................................................................................................44 Uvod ..........................................................................................................................................................44
3.1. Jednaæina kontinuiteta ................................................................................................................45
3.2. Bernulijeva jednaæina ....................................................................................................................46
Primene Bernulijeve jednaæine ......................................................................................................48



4.
4.1. Molekulska sila ..............................................................................................................................52 Toplotno širewe tela ..................................................................................................................53
Struktura ævrstih tela. Kristali ........................................................................................54
Elastiænost ævrstih tela. Hukov zakon ..................................................................................56 Pitawa ....................................................................................................................................................58
4.2. Svojstva realnih teænosti ............................................................................................................59
zakonviskoznosti ................................................................................................59
zakon viskoznosti ................................................................................................61
napon teænosti ......................................................................................................61
4.3. Fazni prelazi ..................................................................................................................................65

5.1. Uzajamno delovawe naelektrisanih tela ....................................................................................73
Elektriæna sila. Kulonov zakon ..................................................................................................74 Elektriæno poqe ............................................................................................................................76 Jaæina elektriænog poqa ..............................................................................................................76
Potencijalna energija elektriænog poqa i elektriæni potencijal ....................................77 Rad elektriænog poqa i elektriæni napon ................................................................................78 Zakon odrþawa koliæine naelektrisawa ........................................................................79
5.2. Elektriæno poqe u razliæitim sredinama ..............................................................................81
Elektriæni fluks ..........................................................................................................................81
Ekvipotencijalne površi ............................................................................................................82
Jaæina i potencijal elektriænog poqa ......................................................................................83
Elektriæna kapacitivnost ........................................................................................................84
Elektriæni kondenzator ..............................................................................................................85
Vezivawe elektriænih kondenzatora .......................................................................................... 85
Energija elektrostatiækog poqa ................................................................................................86
Rezime ......................................................................................................................................................87 Pitawa ....................................................................................................................................................89

6. JEDNOSMERNA STRUJA ......................................................................................................................90
Uvod ..........................................................................................................................................................90
6.1. Elektriæna struja ..........................................................................................................................90
Elektriæni napon i elektromotorna sila ..............................................................................91
Jaæina i gustina elektriæne struje ............................................................................................92
Omov zakon i elektriæna otpornost provodnika ....................................................................94
Xul–Lencov zakon ............................................................................................................................96
Omov zakon za strujno kolo ............................................................................................................97
Kirhofova pravila ........................................................................................................................98
Vezivawe elektriænih otpornika ..............................................................................................99
Termoelektriæne pojave ..............................................................................................................
Kontaktni elektriæni potencijal ................................................................................101
Termoelektriæne pojave ....................................................................................................101
6.2. Elektriæna provodqivost elektrolita ..................................................................................103
Elektrolitiæka disocijacija ....................................................................................................103
Faradejevi zakoni elektrolize ..................................................................................................104
Faradejev zakon ..........................................................................................................105
Faradejev zakon ........................................................................................................106
elementi ............................................................................................................107
6.3. Elektriæna struja u gasovima ....................................................................................................109
Jonizacija i rekombinacija, nesamostalno praþwewe ..........................................................109
Udarna jonizacija i samostalnopraþwewe ..............................................................................110
....................................................................................................................................................111
............................................................................................................................114
..........................................................................................................................................116




Uprouæavawu svojstava i ponašawa gasova koriste se dva osnovna teorijska metoda: molekulsko-kinetiæki(statistiæki) i makroskopsko-termodinamiæki(fenomenološki) pristup.
Molekulsko-kinetiæki metod prouæavawa gasova polazi od molekulske strukture supstancije. Razmatraju se kretawa i uzajamna delovawa molekula (atoma) da bi se izveli zakquæci o svojstvima i ponašawu gasova kao celine. Uzimawem sredwih vrednosti brzina i kinetiækih energija ogromnog broja molekula mogu da se izraæunaju vrednosti veliæina koje karakterišu stawa makroskopskih gasovitih tela kao što su pritisak, temperatura, unutrašwa energija i druge. U ovakvim proraæunima koristi se statistika zasnovana na teoriji verovatnoœe. Stoga se ovaj pristup naziva i statistiæki metod, a zakoni dobijeni wegovom primenom – statistiæki zakoni.
Termodinamiæki(makroskopski) metod zanemaruje unutrašwu strukturu tela (gasova) kao što se u mehanici zanemaruje struktura tela prilikom primene modela materijalne taæke, krutog tela ili idealnog fluida . Termodinamiæko prouæavawe gasovitih tela zasniva se na dva principa termodinamike (prvi i drugi princip termodinamike, o kojima œemo posebno govoriti). Termodinamika uspostavqa veze meðu veliæinama koje karakterišu makroskopska stawa gasovitih tela kao što su: pritisak, zapremina, koliæina toplote, temperatura, entropija i druge. Pomoœu ovih veliæina opisuju se stawa i procesi u gasovima sa makroskopskog stanovišta. Takav metod opisivawa pojava naziva se još i makroskopski ili fenomenološki metod



U osnovnoj školi smo saznali da se molekuli (atomi) gasova kreœu neprekidno i haotiæno. Neureðenost (haotiænost) se ogleda u tome što su brzine molekula (atoma) u gasovima veoma razliæite po intenzitetu, pravcu i smeru. Vrednosti wihovih brzina mogu da budu u rasponu od neke minimalne vrednosti (æak i nulte vrednosti) do nekih maksimalnih vrednosti, od nekoliko stotina metara u sekundi. Svi su pravci i smerovi kretawa molekula (atoma) ravnopravni. Nema „privilegovanih“ pravaca i smerova, naravno, ako je reæ o gasnim stawima bez spoqašwih uticaja.
Pratiti kretawe pojedinaænih molekula (atoma) je skoro nemoguœe. Stoga se, obiæno, uzima sredwa brzina molekula (atoma) gasova. Usled neureðenog kretawa, broj wihovih meðusobnih sudara tokom jedne sekunde je ogroman, tako da je putawa molekula (atoma) izlomqena linija.

Treba pokazati kako su molekuli rasporeðeni po brzinama u nekom vremenskom trenutku ili kolika je verovatnoœa da jedan molekul u odreðenom trenutku poseduje brzinu iz odreðenog intervala brzina.
Ako DN od ukupnog broja N molekula u gasu poseduju brzine u intervalu v i v+ Dv, onda se moþe obrazovati tzv. funkcija raspodele: gde je DN/N relativan broj molekula koji imaju brzine u intrevalu Dv oko brzine v. Ovu funkciju raspodele odredio je Maksvel, a oblik funkcije raspodele prikazan je grafiæki (slika 1.2).
Na ovoj slici prikazana je funkcija raspodele za dve temperature. Iz grafika sledi:
1. Maksimum krive raspodele odgovara najverovatnijoj brzini vn oko koje se grupiše najveœi broj molekula.
2. Kriva raspodele nije simetriæna u odnosu na vertikalu koja prolazi kroz maksimum, nego je površina sa desne strane veœa, što znaæi da je veœi broj molekula sa veœom brzinom od vn nego sa leve strane sa mawom brzinom od vn.
1.2. Maksvelova raspodela za dve temperature


3. Poveœawem temperature maksimum funkcije se smawuje i pomera ka veœim brzinama a kriva razvlaæi, odnosno postaje neureðenije stawe gasa, pošto je zastupqen veœi broj razliæitih brzina.
Na osnovu merewa intenziteta brzina molekula naðene su sledeœe zakonitosti:
a) brzine molekula srazmerne su kvadratnom korenu iz apsolutne temperature; b) na stalnoj temperaturi, brzine molekula su obrnuto srazmerne kvadratnom korenu iz mase molekula gasa.
Na osnovu funkcije raspodele moþe se odrediti najverovatnija brzina molekula:
gde su k – Bolcmanova konstanta k = 1,38×10–23 J/K (xul po kelvinu), T – apsolutna temperatura, a m – masa molekula gasa.

Molekule gasa zamišqamo kao elastiæne kuglice zanemarqive zapremine æiji su meðusobni sudari, kao i sudari sa zidovima suda u kojem se gas nalazi, apsolutno elastiæni (kinetiæka energija molekula pre i posle sudara se ne mewa). Pri tim sudarima molekuli razmewuju impulse, usled æega se wihove putawe mewaju (slika 1.3) i imaju oblik izlomqene linije.
Broj molekula u gasu (bez obzira na zapreminu suda) je ogroman, ali wihovo meðusobno rastojawe je mnogo veœe u poreðewu sa rastojawima izmeðu molekula u teænim i ævrstim telima. Zato se uzajamno delovawe izmeðu molekula u gasu moþe zanemariti (privlaæne molekulske sile veoma brzo opadaju sa rastojawem). Uzajamno delovawe meðu molekulima gasa praktiæno se svodi na meðusobne sudare, kao i sudare sa zidova suda u kojem je gas zatvoren.

Kada kaþemo da se molekuli kreœu haotiæno, to se odnosi na intenzitet, pravac i smer brzine kretawa molekula. Nema, dakle, „privilegovanih“ pravaca i smerova (slika 1.3).

Ta pretpostavka se temeqi na æiwenici da pritisak gasa ostaje konstantan ako su stalni zapremina i temperatura. Naime, pritisak na zidove suda mikroskopski tumaæimo udarima molekula gasa o zidove suda. Pritisak gasa zato bitno zavisi od brzine molekula.
Za objašwavawe svojstava supstancije u gasovitom stawu koristi se model idealnog gasa. Pojam idealnog gasa je idealizacija, sliæno kao i model materijalne taæke ili model krutog tela.
Osnovna karakteristika modela idealnog gasa je data na prethodnoj strani. Moþe se dodati da molekuli (idealne male elastiæne loptice) uzajamno deluju samo pri neposrednim sudarima i pri udaru o zidove suda u kome se nalaze.
Ustanovqeno je da se model idealnog gasa moþe primeniti na realne gasove koji su dovoqno razreðeni i ako su wihove temperature iznad temperature kondenzovawa.

Jedan od prvih i vaþnih uspeha molekulsko-kinetiæke teorije suptancije bilo je kvalitativno i kvantitativno objašwewe pritiska gasa na zidove suda. Kvalitativno objašwewe sastoji se u tome, da molekuli idealnog gasa sa zidovima suda uzajamno deluju po zakonima elastiænog sudara. Neka je gas zatvoren u sudu oblika kocke (slika 1.4). Masa jednog molekula je m. Zamislimo i pratimo molekul koji se kreœe u smeru x-ose (prema naznaæenoj stranici) brzinom vx (sredwa brzina), normalno na zid suda. Posle sudara sa zidom suda molekul se odbija, pri æemu zadrþava intenzitet brzine, ali sa suprotnim predznakom (slika 1.5). U jednom sudaru sa zidom suda intenzitet proseænog impulsa molekula promeni se:
z
Slika 1.4. Molekuli (atomi) gasa kreœu se ravnomerno usvim smerovima i pravcima (nema „privilegovanih“ pravaca)
U vreme sudara molekul deluje na ovaj zid suda silom pritiska proseænog intenziteta: . xx x Fpmv tt 2 ∆ ∆∆ == () () xxxx pmvmvmv 2 ∆ = = y x
a) b) Slika 1.5. Sudar molekula gasa sa zidovima suda


Ovo je intenzitet jedne komponente proseæne sile jednog molekula koji normalno udara o posmatrani zid površine S. Ako ukocki postoji N molekula, onda u procesu udara o jednu stranicu kocke (od ukupno 6) uæestvuje N/6 Ukupna proseæna sila molekula koji uæestvuju u udarima o posmatrani zid (jedan od moguœa tri pravca a svaki pravac ima dva smera) je onda:
(indeks x kod v x je namerno izostavqen, jer to moþe da bude bilo koji pravac). Pritisak te sile, na osnovu definicije, predstavqa: .
Postavqa se pitawe: koji œe molekuli uæestvovati u procesu udara o zid suda? Odnosno, koliko je vreme (Dt) trajawa promene impulsa molekula? Kreœuœi se brzinom v , za vreme Dt, molekul preðe put A = v Dt. Znaæi: samo molekuli koji su na rastojawu najviše A od zida suda mogu dospeti do zida. Drugim reæima, samo molekuli koji se nalaze u zapremini:
uæestvuju u formirawu pritiska. Iz ove relacije sledi: , a kada se to uvrsti u izraz za pritisak i uvede koncentracija molekula: dobija se:
Ova jednaæina naziva se osnovna jednaæina molekulsko-kinetiæke teorije gasova. Ona povezuje mikroskopske veliæine: masu molekula i sredwu brzinu molekula i makroskopsku veliæinu – pritisak gasa.

Sredwu vrednost kinetiæke energije translatornog kretawa molekula idealnog gasa moþemo izraziti preko sredwe vrednosti kvadrata brzine:

Kako je sredwa kvadratna brzina gasa: a ona se moþe odrediti iz Makvelove raspodele f(v), sa slike 1.2, i iznosi: kT v m 23 = vvv v N 222 212N ... , +++ = Emv 2 k 1 2. = pnmv 2 0 1 3. N n V 0, = StV v ∆ ¸ = VSSvt ∆ = = A FNmv pSSt 3 ∆ == FNmv t 3 ∆ =

Zamenom ovog izraza u izraz za sredwu kinetiæku energiju idealnog gasa, dobijamo:
Sredwa kinetiæka energija molekula idealnog gasa srazmerna je apsolutnoj temperaturi.

Poreðewem osnovne jednaæine molekulsko-kinetiæke teorije sa definicijom sredwe kinetiæke energije lako dolazimo do drugog oblika jednaæine molekulsko-kinetiæke teorije gasova:
Pritisak idealnog gasa srazmeran je koncentraciji gasa (broju molekula u jedinici zapremine) i sredwoj kinetiækoj energiji molekula gasa.
Pošto je , moþe da se napiše:
Proizvod pritiska i zapremine odreðene koliæine gasa (N =const) srazmeran je sredwoj kinetiækoj energiji molekula gasa.
U prethodnom poglavqu je pokazano i konstatovano da je sredwa kinetiæka energija srazmerna apsolutnoj temperaturi gasa Ako se ovo zameni u gorwi izraz, dobija se:
Proizvod pritiska i zapremine odreðene koliæine gasa (N =const) srazmeran je apsolutnoj temperaturi tog gasa.
Ovo predstavqa iskaz opšte jednaæine stawa idealnih gasova.
Znaæajan doprinos razvoju kinetiæke teorije gasova dao je Klauzijus (Clausius Rudolf Emmanuel, 1822–1888), koji je uveo statistiæke predstave (sredwe veliæine), mikroskopski pristup u prouæavawu gasova. Uveo je pojmove: idealan gas, entropija, duþina slobodnog puta molekula (rastojawe izmeðu dva uzastopna sudara molekula) i na tim osnovama prvi izraæunao pritisak gasa na zidove suda. Pored Klauzijusa, posebno treba istaœi Maksvelove radove (Maxwell James Clerk, 1831–1879) i Bolcmanove zasluge (Boltzmann Ludwig, 1844–1906) u oblasti kinetiæke teorije gasova (Maksvel–Bolcmanova raspodela molekula gasa po brzinama u poqu sila).


Sa pojmom temperatura sa makroskopskog (fenomenološkog) stanovišta upoznali smo se u osnovnoj školi. Tada smo saznali za razliæite vrste termometara kojima se meri temperatura. Iako konstrukcija termometara moþe da bude razliæita, svi su zasnovani na pojavama koje su uzrokovane promenom stepena zagrejanosti, tj. temperature tela. Najæešœe se koriste termometri sa þivom i alkoholom, koje smo detaqno prouæavali.
Sa stanovišta kinetiæke teorije supstancije, temperatura je tesno povezana sa unutrašwom energijom koja se kod gasova praktiæno svodi na kinetiæku energiju molekula (atoma). Potencijalna energija uzajamnog delovawa molekula gasa moþe se zanemariti, jer su meðumolekulska rastojawa znatno veœa u odnosu na rastojawa izmeðu molekula (atoma) kod ævrstih i teænih tela.
Veœ smo rekli da je temperatura ona fiziæka veliæina koja karakteriše sredwu kinetiæku energiju molekula gasa.
Temperatura je srazmerna sredwoj kinetiækoj energiji haotiænog kretawa molekula gasa
Tmv12 ~ 2 373,15K
gde je m – masa molekula gasa, a v – sredwa vrednost intenziteta brzine kretawa molekula gasa.
Na ovaj naæin se definiše apsolutna temperatura. Obiæno se oznaæava sa T i predstavqa jednu od sedam osnovnih fiziækih veliæina.
Temperatura je jednaka nuli ako je sredwa kinetiæka energija ravna nuli. To je najniþa moguœa vrednost temperature (teorijski izraæunata), zato što kinetiæka energija ne moþe da ima negativnu vrednost. Temperatura na kojoj prestaje kretawe molekula (kinetiæka energija i brzina jednaka nuli) naziva se apsolutna nula.
Sredinom 19. veka, teorijskim putem je ustanovqeno da je najniþa moguœa temperatura –273,15 °C (apsolutna nula). Æesto se ova vrednost zaokruþuje na –273 °C. Temperatura koja se meri od apsolutne nule naziva se apsolutna ili Kelvinova temperatura. Jedinica temperature u Meðunarodnom sistemu jedinica je kelvin (K).
˚C
˚C

Slika 1.6. Kelvinova i Celzijusova skala
Na slici 1.6. su prikazane dve temperaturske skale: Kelvinova(apsolutna) i Celzijusova(konvenciona). Vidimo da promena temperature za odreðen broj stepeni u Celzijusovoj skali odgovara promeni za isti broj podeoka u Kelvinovoj skali. Na primer, ako promena temperature nekog tela iznosi 1°C, moþe se takoðe reœi da je ta promena 1K. Temperatura po Kelvinovoj skali izraæunava se tako što se broju 273 doda temperatura t merena u Celzijusovoj skali. Znaæi:
T =(273,15+ ) K.
Na primer, sobna temperatura od 20 °C u Kelvinovoj skali iznosi 293 K. t °C
Primer 1. Koliko iznosi najverovatnija brzina molekula kiseonika (O2) na temperaturi T = 300 K? Molska masa kiseonika je 0,032 kg/mol.
Podaci: T = 300 K, M = 0,032 kg/mol; vn = ?
Rešewe. Na osnovu izraza:

uzimajuœi u obzir da je masa molekula jednaka odnosu molske mase i Avogadrovog broja kao i da je univerzalna gasna konstanta: dobija se:
Primer 2. Kolika je sredwa kinetiæka energija translatornog kretawa molekula vazduha u prostoriji 6 m × 5 m × 3 m na atmosferskom pritisku od 100 kPa?
Podaci: p = 100 kPa; Ek=?
Rešewe.
Primer 3. Kolika je sredwa kinetiæka energija jednog molekula jednoatomskog idealnog gasa æija je temperatura 300 K?
Podaci: T =300K; Ek=?
Rešewe. Sredwa kinetiæka energija je:

Za potpuno odreðivawe stawa idealnog gasa treba istovremeno poznavati veœi broj parametara: koliæinu gasa, pritisak, zapreminu i temperaturu. Meðutim, mnoge procese u gasovima, koji se odvijaju u prirodi i ostvaruju u tehnici, moþemo posmatrati pribliþno kao procese u kojima se mewaju samo dva parametra, pri æemu, ostali imaju konstantne vrednosti (tosu izoprocesi).
• Jedan mol bilo koje supstancije sadrþi Avogadrov broj æestica: NA =6,023 1023 mol–1 , r je gustina þive.
• Normalni atmosferski pritisak odgovara pritisku stuba þive visine
76 cm: pgha32 kgm 136009,810,76m101325Pa. ms r
1.
2.
3.


Posebnu ulogu u fizici i tehnici imaju tri vrste ovakvih procesa: izotermski, koji se odvijaju pri stalnoj temepraturi (Bojl–Mariotov zakon), izohorski, pri kojima se ne mewa zapremina (Šarlov zakon) i izobarski, pri konstantnom pritisku (Gej-Lisakov zakon)
Svi gasni zakoni su prvo eksperimentalno utvrðeni. Tek na osnovu kinetiæke teorije gasova oni dobijaju adekvatnu kvalitativnu i kvantitativnu interpretaciju.


Robert Boyle (1627–1691)

Edme Mariotte (1620–1684)
ROBERT BOJL, engleski fiziæar i hemiæar irskog porekla, Wutnov savremenik i jedan od osnivaæa Britanske akademije nauka (The Royal Society of London). Radio je u Oksfordu i eksperimentalno utvrdio zavisnost pritiska gasa od wegove zapremine pri konstantnoj temperaturi.
Bojl je pokazao da teænost moþe da prokquæa na niþoj temperaturi od taæke kquæawa ako je izloþena pritisku niþem od atmosferskog. Za svoje oglede konstruisao je barometar.
EDM MARIOT, francuski fiziæar i sveštenik, jedan od prvih ælanova Francuske akademije nauka, nezavisno od Bojla, ustanovio je istu zakonitost. Zbog toga je kasnije ta zakonitost nazvana Bojl–Mariotov zakon. Mariot je utvrdio inverznu vezu izmeðu zapremine i pritiska kod gasova. Otkrio je i slepu mrqu na oku.
U drugoj polovini 17. veka Bojl i Mariot, nezavisno jedan od drugog, prouæavali su ponašawe gasova pri izotermskim uslovima, odnosno uzajamnu zavisnost pritiska i zapremine pri stalnoj vrednosti temperature. Eksperimentalnim putem su ustanovili da za izotermske procese vaþi relacija:
pV = const, za T = const i N = const.
Ova relacija je kasnije nazvana Bojl–Mariotov zakon
Proizvod pritiska i zapremine odreðene koliæine gasa pri stalnoj temperaturi je konstantan.


Da bismo prikazali Bojl–Mariotov zakon, posmatraœemo odreðenu koliæinu gasa u zatvorenom cilindru sa pokretnim klipom (bez trewa) koji je spojen sa manometrom M (slika 1.7a). Manometrom se meri pritisak gasa u cilindru. Utoku eksperimenta temperatura gasa se ne mewa. Stalna temperatura gasa se postiþe sporim pomerawem klipa kako bi se vršila razmena unutrašwe energije sa okolinom i tako odrþala stalna temperatura. Temperatura se odrþava stalnom tako što se cilindar sa klipom postavi u širi sud sa vodom konstantne temperature.
Slika 1.7. Prikaz Bojl–Mariotovog zakona
Ako se zapremina smawi dva puta pritisak gasa œe se dva puta poveœati, a pri tri puta mawoj zapremini pritisak gasa se tri puta uveœa itd. Tako proizvod pritiska i zapremine odreðene koliæine gasa pri stalnoj temperaturi ostaje uvek konstantan, to jest: p1V1 = p2V2 = = pnVn = const
Ili, u opštem sluæaju:
pV = const, za T = const; N = const.
Grafik izotermskog procesa naziva se izoterma. Izoterma se predstavqa u pravouglom Dekartovom sistemu u kojem su vrednosti zapremine nanesene na apscisnoj, a pritisak na ordinatnoj osi (p-V dijagram). Na slici 1.7b su prikazane izoterme za razliæite temperature iste koliæine gasa. Na višim temperaturama brzina molekula se poveœava, a time i broj wihovih sudara o zid suda kao i impuls koji se predaje pri tim sudarima. To uslovqava poveœawe pritiska za iste vrednosti zapremine. Zato je izoterma na višoj temperaturi iznad izoterme na niþoj temperaturi.


Zavisnost pritiska od temperature prvi je eksperimentalno prouæavao francuski fiziæar Šarl.
Šarlov zakon se moþe demonstrirati pomoœu aparature prikazane na slici1.8a. Odreðena koliæina gasa (vazduha) nalazi se u staklenom sudu (balonu) koji je spojen sa metalnim manometrom. Temperatura gasa se mewa grejawem vode u kojoj se nalazi balon s gasom. Ona se oæitava na termometru. Pritisak gasa se meri manometrom. Rezultati merewa su prikazani u p-t dijagramu (slika 1.8b).
a) b)
V=const
p [Pa]
p2 p1 t1 t3 p0 p –273,150
t [°C] tt2
Na osnovu ogleda se zakquæuje: povišewem temperature poveœava se pritisak i ta zavisnost ima linearni karakter (prava linija).
Uoæava se da u p-t sistemu prava linija preseca t-osu u taæki t = –273,15 °C, a p-osu u taæki p0.
Na osnovu toga, jednaæina ove prave je:
gde je g = (1/273,15) K–1 = (1/273,15) °C–1 – termiæki koeficijent pritiska odreðuje kolika je relativna promena pritiska pri izmeni temperature za 1 °C (1 K).
Relacija
p=p(1+gt) ; V= const, N= 0const. p pptpt 0 00(1), V const, N const. 273,15K
predstavqa matematiæki izraz Šarlovog zakona koji je eksperimentalno utvrðen 1783. godine, znaæi, znatno ranije od zasnivawa kinetiæke teorije gasova (poæetak druge polovine 19. veka).
Prava koja prikazuje linearnu zavisnost pritiska od temperature pri nepromewenoj zapremini gasa naziva se izohora. Proces promene stawa odreðene koliæine gasa pri stalnoj zapremini je, zbog toga, izohorski termodinamiæki proces.


GEJ-LISAK, francuski fiziæar i hemiæar, ælan Pariske akademije nauka. Eksperimentalno je ispitivao zavisnost zapremine gasa od temperature pri stalnom pritisku i ustanovio vezu meðu tim veliæinama koja je nazvana Gej-Lisakov zakon. Dokazao je da koeficijent širewa ima istu vrednost za sve gasove i odredio je wegovu brojnu vrednost: g = (1/273,15 °C)
Gej-Lisak ima velike zasluge i u oblasti hemije. Izdvojio je kalcijum, hlor i jod i ispitivao je svojstva sumpornih, azotnih i cijanskih jediwewa.
Izradio je niz pribora: hidrometar, barometar, termometar, razne pumpe. Jedan je od pionira avijacije. Podigao se balonom preko 6000 m vršeœi razna istraþivawa u atmosferi.

Gay-Lussac (1778–1850)
Eksperimentalno prouæavawe zavisnosti zapremine gasa od temperature pri stalnom pritisku (p = const) sproveo je 1802. godine francuski fiziæar Gej-Lisak. Izmena zapremine odreðene koliæine gasa pri promeni temperature pri stalnom pritisku naziva se izobarski proces.Izobarski proces se moþe demonstrirati pomoœu pribora prikazanog na slici 1.9a, koji se naziva dilatometar. On se sastoji od šireg suda napuwenog vodom, u kome se nalazi sud napuwen gasom. Obiæno je to stakleni balon, kroz æiji otvor prolazi staklena cev savijena pod pravim uglom. Iza horizontalnog dela ove cevi nalazi se skala, æiji jedan podeqak najæešœe oznaæava zapreminu cevi od 1 cm3. Cev je zatvorena kapqicom þive koja se, zavisno od zapremine gasa, pomera u horizontalnom delu cevi i to praktiæno bez trewa.
Kada se u sud sa vodom B unese dovoqna koliæina leda, posle izvesnog vremena temperatura vode u wemu i gasa u staklenom balonu A biœe 0 °C. Tada poloþaj þivine kapqe oznaæava zapreminu V0. Postepenim zagrevawem temperatura gasa œe se uveœavati i kapqa þive pomerati udesno, što znaæi da se gas u sudu širi. Zanemarujuœi širewe staklenog balona, promena zapremine gasa V oæitava se na skali S. To se ponavqa za nekoliko vrednosti temperature, recimo u intervalu od 0 °C do 80 °C, što se oæitava na termometru T.


Na osnovu rezultata merewa, zakquæuje se: promena zapremine odreðene koliæine gasa pri stalnom pritisku (u našem ogledu atmosferski pritisak) upravo je srazmerna promeni temperature gasa i zapremini gasa V0 na 0 °C, tj:
Pošto je t0 = 0 °C, dobija se matematiæki oblik Gej-Lisakovog zakona, izraþen preko temperature Celzijusovim stepenima (°C):
Zapremina odreðene koliæine gasa pri stalnom pritisku upravo je srazmerna wegovoj apsolutnoj temperaturi.
Koeficijent srazmernosti g naziva se termiæki koeficijent širewa gasa i za sve gasove iznosi: g = (1/273,15 °C).
Prava koja pokazuje zavisnost zapremine gasa od temperature pri stalnom pritisku naziva se izobara. Na dijagramu (sl. 1.9b) se vidi da izobara polazi od apsolutne nule. Iz apsolutne nule ne polazi samo izobara za izabrani pritisak, veœ i za pritisak bilo koje vrednosti. Proces promene stawa odreðene koliæine gasa pri stalnom pritisku je izobarski termodinamiæki proces i opisuje se Gej-Lisakovim zakonom linearne promene zapremine sa temperaturom.
Treba naglasiti da Gej-Lisakov zakon vaþi, kao i ostali gasni zakoni, samo za idealne gasove, odnosno za realne gasove relativno male gustine i za temperature iznad taæke kondenzovawa.

Opšta jednaæina stawa idealnog gasa: pV=NkT, pokazala je da jedno stawe u kojem se nalazi odreðena koliæina gasa karakterišu: pritisak, zapremina i temperatura. Ove veliæine nisu nezavisne, a wihova povezanost matematiæki je izraþena ovom jednaæinom.
Postavqa se pitawe: kolika je ta odreðena koliæina gasa? Koliæina supstancije je osnovna fiziæka veliæina i woj odgovara osnovna jedinica meðunarodnog sistema (SI) mera – mol. A šta predstavqa jedan mol? U definiciji se kaþe da je to koliæina supstancije koja ima isti broj æestica (nekih jedinki) – onoliko koliko ima atoma u masi od 0,012 kg ugqenika 12C. Ova definicija se moþe i drugaæije protumaæiti. Jedan mol svake supstancije sadrþi isti broj æestica:

N 231A6,02310mol = ¸ VVt0(1). γ =+ ()VVVtt 000~.
i predstavqa univerzalni – Avogadrov broj. Taj broj pokazuje da mol bilo koje supstancije, nezavisno od uslova u kojima se ta supstancija nalazi (npr. agregatno stawe), ima isti broj elementarnih jedinki. Ovo je jedan od iskaza Avogadrovog zakona. Prevedeno na stawe gasa, Avogadrov zakon ima oblik: na istim temperaturama i pritisku,jednake zapremine razliæitih gasova sadrþe isti broj molekula.
Ako neki uzorak (gas u sudu i sl.) sadrþi N molekula, onda se moþe definisati koliæina supstancije (broj molova) u tom uzorku:

Pomoœu ovoga broja, opšta jednaæina stawa idealnog gasa glasi: gde je univerzalna gasna konstanta.
RkN A 8,31JmolK = =
Ova jednaæina je specifiæna relacija koja povezuje sve veliæine (n,p,V,T) koje karakterišu jedno stawe idealnog gasa.
Primer 4. Pritisak gasa u zatvorenom sudu je 1,8 105 Pa. Hlaðewem gasa za 40 K pritisak se smawi na 1,4×105 Pa. Izraæunati poæetnu i krajwu temperaturu gasa.
Podaci: p1 = 1,8×105 Pa, DT = 40 K, p2 = 1,4×105 Pa; T1 =? T2 =?
Rešewe. Na osnovu Šarlovog zakona, za bilo koja dva stawa gasa je:
Primer 5. Zapremina gasa na 300 K iznosi 0,25 m3. Kolika œe biti zapremina toga gasa pri nepromewenom pritisku na temperaturi 600 K?
Podaci: V1 = 0,25 m3 , T1 = 300 K, p = const, T2 = 600 K; V2 = ?
Rešewe. Na osnovu Gej-Lisakovog zakona
Primer 6. Odreðena koliæina idealnog gasa zauzima u poæetnom stawu zapreminu 12 ". Koliku zapreminu œe zauzimati ako se nekim termodinamiækim procesom pritisak udvostruæi, a temperatura smawi na treœinu poæetne?
Podaci: V1=12 ", p2=2p1 i T2=; V2=?
Rešewe. Oznaæimo poæetno stawe indeksom 1, a konaæno indeksom 2. Za oba stawa vaþi jednaæina stawa
4. 5. 6.


Zadana veza izmeðu stawa 1 i 2 je: p2 = 2p1; . Uvrstimo te odnose u drugu jednaæinu stawa i dobijamo:
Podelimo tu jednaæinu sa prvom, pa dobijamo:
Zapremina œe se smawiti na šestinu poæetne zapremine.

• Saglasno osnovanim stavovima molekulsko-kinetiæke teorije:
1) Sva tela se sastoje od æestica: atoma, molekula.
2) Atomi i molekuli supstancije izvode neprekidno haotiæno (neureðeno) kretawe, koje se naziva toplotno kretawe.
3) Meðu molekulima postoji uzajamno delovawe koje zavisi od rastojawa meðu wima i moþe da bude privlaænog i odbojnog karaktera. Molekulske sile imaju elektromagnetnu prirodu.
Posebno vaþnu ulogu u postavkama molekulsko-kinetiæke teorije ima Braunovo kretawe æestica. Braunovo kretawe je toplotno kretawe molekula u teænosti ili gasu. Makroskopska tela se sastoje od ogromnog broja molekula æija je masa relativno mala. Zato se masa molekula i wihov broj æesto izraþavaju u relativnim jedinicama (relativna molekulska ili atomska masa).
• Idealan gas je model realnog gasa koji se sastoji od molekula (atoma), æije se dimenzije i uzajamno delovawe (molekulske sile) mogu zanemariti. Sredwa kinetiæka energija molekula gasa je znatno veœa od sredwe potencijalne energije wihovog uzajamnog delovawa (molekulske sile). Na osnovu toga se moþe zakquæiti da se unutrašwa energija idealnog gasa svodi na sredwu kinetiæku energiju molekula (atoma).
• Prema kinetiækoj teoriji, pritisak gasa se tumaæi kao posledica udara molekula o zidove suda u kojem je zatvoren gas.
Pritisak gasa odreðuje sredwa kinetiæka energija translatornog kretawa svih molekula koji se sadrþe u jediniænoj zapremini gasa:


gde je broj molekula u jedinici zapremine, a –sredwa kinetiæka energija haotiænog kretawa molekula.
• Sredwu kinetiæku energiju molekula definiše apsolutna temperatura gasa (T):
gde je k = 1,38×10–23 J/K – Bolcmanova konstanta.
Temperatura je mera sredwe kinetiæke energije haotiænog (toplotnog) kretawa molekula idealnog gasa.
Jednaæina stawa idealnog gasa ima oblik:
gde je R – univerzalna gasna konstanta (R = NAk = 8,31 )
Proizvod pritiska i zapremine odreðene koliæine gasa (n – konstanta),srazmeran je apsolutnoj temperaturi.
Jednaæina stawa idealnog gasa u bilo kojem od navedenih oblika omoguœuje da se reše zadaci koji se odnose na procese u gasovima. Kao konkretne (posebne) sluæajeve jednaæina opisuje gasne zakone:
– pri T = const, pV = const, N = const – Bojl–Mariotov zakon;
– pri p = const, = const, N = const – Gej-Lisakov zakon;
– pri V = const, = const, N = const – Šarlov zakon;
– pri p = const, T = const,=const, N = const – Avogadrov zakon
1. Objasnite pojam pritiska gasa.
2. Koje karakteristike ima idealan gas?
3. U æemu je razlika izmeðu Celzijusove i apsolutne (termodinamiæke) temperaturne skale?
4. Šta povezuje osnovna jednaæina kinetiæke teorije idealnih gasova?
5. Od æega zavisi sredwa kinetiæka energija molekula?
6. Da li Bolcmanova konstanta zavisi od vrste molekula gasa?
7. Kakva veza postoji izmeðu Bolcmanove i univerzalne gasne konstante?
8. Koje veliæine povezuje jednaæina idealnog gasnog stawa?
9. Šta definiše izraz:
10. Koliko ima molekula u 1cm3 gasa pri normalnim uslovima (Lošmitov broj)?



Uloga toplotnih pojava u svakodnevnom þivotu i tehnici je opštepoznata. Meðutim, fiziæko znaæewe i sadrþaj tih pojava se ne iscrpquju na nivou wihove tehniæke primene i uticaja na þivi svet. Pokazuje se da zakoni kojima se objašwavaju toplotne pojave i procesi, sliæno zakonima mehanike, imaju fundamentalni karakter. Oni se primewuju na makroskopske sisteme, koji se sastoje od ogromnog broja molekula i atoma, u raznim naukama (hemija, biologija i dr.).
Za prouæavawe tela (sistema) sa velikim brojem æestica (molekula, atoma i dr.), kao što je istaknuto, koriste se dva pristupa: termodinamiæki (makroskopski, fenomenološki) i molekulsko-kinetiæki (mikroskopski).
Termodinamika opisuje toplotne pojave sa energetske taæke gledišta. Toplotne pojave se prouæavaju na osnovu neposredno merqivih makroskopskih veliæina, kao što su temperatura, pritisak, zapremina itd. To su parametri termodinamiækog sistema.
Molekulsko-kinetiæka teorija, za razliku od termodinamike, prouæava toplotne pojave sa stanovišta fiziækih procesa meðu molekulima. Dakle, u molekulsko-kinetiækoj teoriji makroskopska svojstva tela (termodinamiækog sistema) posmatraju se kao rezultat zajedniækog delovawa molekula.
Fenomenološka termodinamika i statistiæka fizika (molekulskokinetiæka teorija) prilikom opisivawa fiziækih pojava se uzajamno dopuwavaju. Zakoni termodinamike mogu da se primene na sve makroskopske sisteme, nezavisno od vrste æestica koje ulaze u sastav tih sistema i tipa wihovih uzajamnih delovawa (interakcije), meðusobnih rastojawa tih æestica itd. S druge strane, molekulsko-kinetiæka (mikroskopska) teorija omoguœuje da se dubqe shvati mehanizam toplotnih procesa i wihovih zakona.


Svako telo, nezavisno od agregatnog stawa u kojem se nalazi (ævrsto, teæno ili gasovito), sastoji se od velikog broja molekula (atoma). Atomi su izgraðeni od jezgara i omotaæa. U omotaæu se nalaze elektroni koji se kreœu oko jezgra po odreðenim putawama. Jezgro se sastoji od nukleona (protona i neutrona). Sve nabrojane æestice kreœu se i uzajamno deluju jedne na druge. Usled toga one imaju kako kinetiæku, tako i potencijalnu energiju uzajamnog delovawa.
Energija koja zavisi od strukture i stawa tela (sistema) i predstavqa ukupan zbir energije wegovih sastavnih æestica,naziva se unutrašwa energija.
Unutrašwa energija tela (sistema) obuhvata kinetiæku energiju toplotnog kretawa æestica koje ulaze u sastav sistema (molekula, atoma, jona, i dr.), potencijalnu energiju æestica uslovqenu meðumolekulskim silama, kinetiæku i potencijalnu energiju elektrona u atomima i, najzad, energiju nukleona u atomskim jezgrima.
Formula za izraæunavawe unutrašwe energije tela (sistema) u opštem sluæaju, koja bi obuhvatala sve prethodno nabrojane komponente, ima veoma sloþen oblik. Meðutim, u odreðenim sluæajevima moþe da ima veoma jednostavan oblik
kao, na primer, kod modela idealnog gasa.
Unutrašwu energiju idealnog gasa æini kinetiæka energija haotiænog translatornog kretawa wegovih molekula.
U prethodnoj glavi smo nauæili da se sredwa kinetiæka energija jednog molekula idealnog gasa iskazuje formulom
UNENkTnRTNnNRkN ===== kAA ,, 3 2 3 2 jerje i EmvkT 2 k 13 22, ==
gde je T – apsolutna temperatura. Ako idealan gas sadrþi N jednoatomnih molekula, wegova unutrašwa energija œe biti:
gde su NA = 6,023 1023 mol–1 – Avogadrov broj, k = 1,38 10–23 J/K – Bolcmanova konstanta i R = 8,31 – univerzalna gasna konstanta i n – broj molova.
J molK
Jedinica mere unutrašwe energije je xul, ista kao i za bilo koji drugi vid energije.


Svako telo (sistem), buduœi da sadrþi ogroman broj molekula, ima veliku unutrašwu energiju. Nas obiæno interesuje samo promena unutrašwe energije tela (sistema) pri prelasku iz jednog stawa u drugo. Promena unutrašwe energije idealnog gasa zavisi samo od razlike konaæne i poæetne temperature:
Vaþno je zapamtiti da promena unutrašwe energije ne zavisi od naæina, odnosno vrste procesa kroz koji je gas prešao iz poæetnog u konaæno stawe. Promena unutrašwe energije tela (sistema) moþe da se ostvari na dva osnovna naæina:vršewem rada,ili toplotnom razmenom sa okolnim telima. Postoje sluæajevi kada se unutrašwa energija sistema mewa na oba naæina istovremeno.
Navešœemo neke primere promene unutrašwe energije tela (sistema) na raæun rada, odnosno kinetiæke energije. Udari masivnog metalnog æekiœa o ekser dovode do povišewa wihove temperature, odnosno unutrašwe energije. Upumpavawe vazduha u unutrašwu gumu toæka automobila uzrokuje zagrevawe pumpe.
Osim vršewa rada, postoji još jedan naæin koji moþe uzrokovati promenu unutrašwe energije tela (sistema). Na primer, pri dodiru tela razliæitih temperatura toplije telo se hladi, a hladnije zagreva. Prvom se smawuje, a drugom poveœava unutrašwa energija. Sve se to dešava bez vršewa rada.

Kada su dva tela (sistema) sa razliæitim temperaturama u toplotnom kontaktu, izmeðu wih nastaje toplotna razmena. Toplotna razmena se odvija sve dok se temperature tih tela ne izjednaæe. Za odreðivawe promene unutrašwe energije tela pri razmeni toplote uvedena je veliæina – koliæina toplote.
Kvantitativna mera promene unutrašwe energije tela pri toplotnoj razmeni naziva se koliæina toplote.
Koliæina toplote koju neko telo prima ili otpušta zavisi od mase, wegovih toplotnih svojstava i promene temperature:
QT = cm D
Ovde je c – specifiæni toplotni kapacitet tela (o kojem œemo posebno govoriti), DT = T2 – T1 razlika konaæne i poæetne temperature, a m masa tela. Ako je poæetna temperatura T1 viša od konaæne temperature T2, tada je DT negativno, pa œe prema prethodnom izrazu i koliæina toplote Q biti negativna. To oznaæava da je telo izgubilo (otpustilo) odreðenu koliæinu toplote.


Rad se ostvaruje za vreme delovawa jednog tela na drugo nekom silom, pri æemu dolazi do promena stawa kretawa oba tela. U toku tog procesa energija se predaje od jednog tela drugom. Analogno radu, koliæina toplote je takoðe oblik predavawa energije (unutrašwe) jednog tela drugome.
Primer 1. Na vodopadu, æija je visinska razlika 300 m, merena je temperatura vode na vrhu i wegovom dnu. Kolika je temperaturna razlika, ako je specifiæni toplotni kapacitet vode 4186 Jkg–1 K–1 ?
Podaci: h = 300 m, c = 4186 Jkg–1 K–1; DT = ?
Rešewe. Padom vode smawuje se wena gravitaciona potencijalna energija. Na raæun toga poveœava se unutrašwa energija te vode, prema relaciji:

Prvi princip termodinamike je poseban sluæaj zakona odrþawa energije primewen na toplotne procese (slika 2.1a). Jedna od formulacija Prvog principa termodinamike glasi: Koliæina toplote,dovedena izolovanom sistemu,moþe jednim delom da poveœa wegovu unutrašwu energiju,a drugi deo moþe da se pretvori u rad tog sistema.
Ova definicija Prvog principa termodinamike ilustrovana je na slici 2.1. Usudu sa pokretnim klipom (trewe zanemareno) nalazi se idealan gas. Tom sistemu se spoqa dovodi toplota, pri æemu se poveœava wegova unutrašwa energija i vrši odgovarajuœi rad. Grafiæki prikaz tog rada dat je na slici 2.1b.
Analizom Prvog principa termodinamike mogu se objasniti razliæite termodinamiæke pojave, zavisno od toga o kakvom je konkretnom sluæaju reæ.


a) Q = 0 – sistemu se ne dovodi toplota, niti se od wega oduzima. Tada je A =–DU – rad se vrši na raæun unutrašwe energije sistema, koja se usled toga smawuje. Termodinamiæki procesi bez razmene toplote se nazivaju adijabatski procesi. Smawewe unutrašwe energije sistema nije neograniæeno. Rad bilo koje mašine samo na raæun unutrašwe energije sistema je ograniæen. Obavqawe rada bez „utroška“ energije bilo bi isto što i stvarawe energije ni iz æega, što je u direktnoj suprotnosti sa zakonom odrþawa i meðusobnog pretvarawa energije, opštim i fundamentalnim zakonom prirode.
Uzimajuœi to u obzir, Prvi princip termodinamike se moþe formulisati i na sledeœi naæin:
Nemoguœe je konstruisati perpetuum-mobile prve vrste,to jest mašinu koja bi neprestano vršila rad,bez utroška bilo kog oblika energije.
b) DU = 0 – unutrašwa energija sistema se ne mewa. Tada je: Q = A – dovedena koliæina toplote u potpunosti se troši za vršewe rada. Ovakvi su izotermski procesi.
v) A = 0 – sistem ne vrši nikakav rad. Onda je Q = DU – sva dovedena koliæina toplote troši se za poveœawe unutrašwe energije sistema. To se dešava kod izohorskih procesa.
Prvi zakon termodinamike ukazuje na moguœnost pretvarawa toplote u rad i obrnuto – rada u toplotu. Ali, ostaje pitawe da li se sva koliæina toplote moþe pretvoriti u rad. Odgovor na to pitawe dobija se na osnovu Drugog principa termodinamike (o kojem œemo posebno govoriti).

2.2.
Neka se idealan gas nalazi u cilindru sa klipom koji moþe da se pomera u oba smera bez trewa (slika 2.2).
Najpre œemo odrediti rad koji se vrši pri izobarskom širewu gasa, odnosno rad sile pritiska kojim gas deluje na pokretni klip. Intenzitet te sile je:
F = pS, gde je p – pritisak gasa, a S – površina klipa. Delovawem te sile klip se pomera za rastojawe Dh = h2 – h1. U takvim uslovima rad sile pritiska pri širewu idealnog gasa je:

gde je DV – promena zapremine gasa. , .

Pri širewu gasa se vrši pozitivan rad, jer se smer sile kojom gas deluje na klip poklapa sa smerom pomerawa klipa. U procesu širewa, gas predaje energiju spoqašwim telima (u našem sluæaju klipu, a preko wega moþe i drugim telima).
Prilikom sabijawa gasa: V2 < V1 i zato je rad negativan (slika 2.3). Znaæi, rad spoqašwe sile nad gasom razlikuje se od rada koji vrši sila kojom gas deluje na klip (za ista pomerawa klipa) samo po predznaku. Zato rad spoqašwe sile koja deluje na gas iznosi:

2.2. Rad sile pritiska priširewu gasa
Pri izotermskom procesu unutrašwa energija idealnog gasa se ne mewa (DU =0), jer temperatura gasa ostaje konstantna (DT = 0). Uzimajuœi to u obzir, na osnovu prvog principa termodinamike se dobija
Q = A
Ova relacija karakteriše izotermski proces sa energijskog stanovišta: koliæina toplote koja se dovodi gasu u potpunosti se pretvara u rad koji vrši sila pritiska pri širewu tog gasa.
Slika 2.4. Smer razmene toplote pri izotermskom širewu i sabijawu gasa
Na slici 2.4a prikazan je smer predaje toplote sistemu pri izotermskom širewu gasa i izvršeni rad pri tom procesu. Kod izotermskog sabijawa gasa smer je obrnut (slika 2.4b).
Iz posledwe relacije se vidi da se znak koliæine toplote poklapa sa predznakom rada. Pri širewu gasa (A > 0) sistem prima odreðenu koliæinu toplote (Q > 0). Prilikom sabijawa gasa (A < 0) i (Q < 0), sistem predaje (otpušta) koliæinu toplote dobijenu radom spoqnih sila, okolnim telima (spoqnoj sredini).
Pri vršewu rada gas uvek mewa zapreminu.
Ako je DV = V2 –V1 pozitivno– gas vrši rad (širewe), a da bi bilo DV < 0 (sabijawe), potrebno je uloþiti neki rad spoqa. Koliki se onda rad izvrši kod izohorskih procesa?
Pošto nema promene zapremine (V= const) – nema vršewa rada! Sva koliæina toplote (dovedena ili odvedena) mewa samo unutrašwu energiju gasa.


Primer 2. U cilindru sa pokretnim klipom nalazi se gas. Wegovo stawe moþe se mewati na sledeœi naæin:
1) pri stalnoj zapremini poveœava se pritisak; 2) pri stalnom pritisku poveœava se zapremina; 3) pri stalnoj temperaturi poveœava se zapremina; 4) pri stalnom pritisku gas se vraœa u poæetno stawe.

Grafiæki prikazati promenu stawa gasa u p-V koordinatnom sistemu. Kod koje od te æetiri promene stawa je gas primio toplotu, a kod kojih je predao okolini? Trewe klipa o zidove suda zanemariti.
Rešewe. Na slici su prikazane moguœe promene stawa gasa u datom cilindru. Gas prima toplotu na delovima dijagrama 1–2, 2–3 i 3–4, a na delu 4–1 predaje toplotu okolini.
p
1 23 4

TOPLOTNI KAPACITET GASOVA
Sa pojmom toplotni kapacitet smo se upoznali u osnovnoj školi, ali se to odnosilo na sluæaj kada zapremina tela (sistema) ostaje stalna u toku toplotne razmene. U takvim situacijama rad se ne vrši (A = 0). Za ævrsta i teæna tela to je opravdano, jer se wihove zapremine neznatno mewaju ako temperaturne promene nisu suviše velike. Meðutim, kod gasova treba razlikovati specifiæni toplotni kapacitet pri stalnoj zapremini od one pri stalnom pritisku. Ako se odreðena koliæina toplote dovodi gasu pri stalnoj zapremini, ona ide na poveœawe samo unutrašwe energije, dok se ona kod gasa pri stalnom pritisku „troši“ i na poveœawe unutrašwe energije, ali i na vršewe rada. Molski toplotni kapacitet gasa pri stalnoj zapremini (CV) brojno je jednaka koliæini toplote koju treba da primi ili otpusti jedan mol gasa da bi mu se promenila temperatura za jedan kelvin pri stalnoj zapremini. Izraþava se jedinicom xul po molu i kelvinu (J/molK).


Molski toplotni kapacitet gasa pri stalnom pritisku (Cp) definiše se na isti naæin, samo što se umesto zapremine – konstantnim odrþava pritisak. Ako se specifiæni toplotni kapacitetgasa pri stalnom pritisku i stalnoj zapremini odnosi na jediniænu masu (1 kg) supstancije, onda se obiæno koriste oznake cp i cV Odnos Cp/CV koji se obiæno oznaæava sa g, ima razliæite vrednosti za jednoatomne, dvoatomne, troatomne... molekule. Pošto je specifiæni toplotni kapacitetgasa pri stalnom pritisku uvek veœi od specifiænog toplotnog kapacitetagasa pri stalnoj zapremini, dati odnos je veœi od jedinice. Za jednoatomne gasove iznosi za dvoatomne gasove g =1,40, a za gasove æiji se molekuli sastoje od tri ili više atoma g = 1,33.
3
Primer 3. U sudu se nalazi 10 g kiseonika pod pritiskom 3×105 Pa i na temperaturi 10 °C. Posle zagrevawa pri stalnom pritisku gas zauzima zapreminu 10 ". Naœi:
a) promenu unutrašwe energije gasa; b) rad koji izvrši gas, i v) koliæinu toplote koju prima gas.
Podaci: m = 10 g, p = 3×105 Pa, t = 10 °C, V2 = 10 "; p =const, M =32g/mol, T =283K
a) DU = ? b) A = ? v) Q = ?
Rešewe. Iz jednaæine stawa idealnog gasa: a) b) A = p (V2 – V1) = 2,26 kJ; v) Q = A + DU = 7,92 kJ.


Procesi koji se odvijaju bez toplotne razmene izmeðu gasa u nekom sudu i okoline (spoqnih tela) nazivaju se adijabatski procesi. Da bi se proces odvijao adijabatski, gas treba da bude potpuno toplotno izolovan. Postoji i druga moguœnost: proces se moþe izvesti tako brzo da pri tome ne doðe do toplotne razmene sa okolinom.
U praksi nema idealne toplotne izolacije, niti procesi mogu tako brzo da se odvijaju da uopšte ne doðe do toplotne razmene izmeðu gasa u nekom sudu (termodinamiækog sistema) i okoline. Stoga svaki realan proces moþe da se dešava samo više ili mawe pribliþno adijabatski. Pribliþnost zavisi od stepena toplotne izolacije ili od brzine odigravawa procesa.
Adijabatski karakter nekog procesa matematiæki se izraþava uslovom da je Q =0. Tada, na osnovu prvog principa termodinamike (Q = DU + A), sledi da je
adijabata
Slika 2.5. Zavisnost pritiska od zapremine pri izotermskom i adijabatskom procesu
Pri adijabatskom procesu, znaæi, rad i promena unutrašwe energije imaju razliæite predznake. Stoga se pri adijabatskom širewu gas hladi, a pri sabijawu zagreva.
Na slici 2.5. predstavqena je zavisnost pritiska (p) od zapremine (V) za izotermski i adijabatski proces u idealnom gasu. Kao što se vidi, adijabata ima strmiji tok od izoterme. Znamo da se Bojl–Mariotov zakon, predstavqen izotermom na grafiku, matematiæki izraþava formulom pV = const (za T =const).
Pri adijabatskoj promeni, pritisak i zapremina gasa povezani su formulom
Pošto je g > 1, adijabata je strmija od izoterme.
Kako Poasonov broj zavisi od broja stepeni slobode kretawa molekula, lako je uoæiti da je on najveœi za jednoatomske gasove, te da je tada adijabata najstrmija. == + & & L L S 9 2 pV const,
gde je Poasonov broj. Ova formula naziva se Poasonova jednaæina.


Dobro nam je poznato da postoje prirodne pojave kod kojih se fiziæki (transportni, provodni i sliæni) procesi odvijaju spontano (sami od sebe) u jednom odreðenom smeru, a nikada se ne vrše spontano u suprotnom smeru. Na primer, telo koje slobodno pada ili se kreœe niz strmu ravan teþi da zauzme poloþaj u kome œe wegovo teþište biti najniþe, a potencijalna energija najmawa. Gas iz boce pod pritiskom svojim kretawem teþi da izjednaæi pritisak sa okolnim i isticaœe sve dok ne nastupi ravnoteþa tih pritisaka. Kod vodopada ili uopšte, teænost teæe od višeg ka niþem gravitacionom nivou i proticaœe sve dok se nivoi teænosti ne izjednaæe. Sliæno, toplota prelazi sa toplijeg na hladnije telo sve dok se temperature ne izjednaæe i nastupi toplotna ravnoteþa. To znaæi da je osnovna karakteristika prirodnih procesa da se oni vrše u smeru ravnoteþnog stawa.
Iz iskustva znamo da se telo neœe samo od sebe kretati uz strmu ravan, a teænost ne moþe da se podigne sama od sebe sa niþeg na viši nivo, niti se gas moþe spontano vratiti u bocu sa veœim pritiskom. Toplota ne moþe da preðe sa tela niþe temperature na telo sa višom temperaturom.
Meðutim, telo se moþe popeti uz strmu ravan, teænost se moþe „prebaciti” na viši nivo, gas se moþe „ubaciti“ u bocu, toplota moþe preœi sa hladnijeg na toplije telo, ali samo uz utrošak, odnosno vršewe spoqašweg rada.
Za vršewe mehaniækog rada postoje prirodni energijski izvori. To su energija mišiœa æoveka i þivotiwa, energija strujawa vazduha i vode (vetar i reka). Meðutim, za potrebe savremenog civilizovanog qudskog društva (za pogon automobila, aviona, brodova itd.) koriste se drugi izvori. Oni potencijalnu energiju molekula (npr. sagorevawem) pretvaraju u kinetiæku energiju toplotnog kretawa, tj. u unutrašwu energiju i toplotu. Postavqa se problem pretvarawa energije haotiænog (toplotnog) – u svakom sluæaju, neureðenog kretawa æestica, u mehaniæki rad –tj. u ureðeno kretawe tela.
Preko mehaniækog rada, toplota se daqe moþe pretvoriti u druge vidove energije (kinetiæku, potencijalnu, elektriænu, itd.), ali i ponovo u toplotu, odnosno u unutrašwu energiju. Iz ovog ugla gledawa, procesi u prirodi mogu da budu povratni. To znaæi da sistem (radna mašina) moþe da preðe iz jednog (poæetnog: a) u drugo (krajwe: b) stawe – slika 2.6. Pri tome, ako se prelazi odvijaju po istim putawama (procesima), to su takoðe povratni procesi.
Slika 2.6. Termodinamiæki ciklus
Meðutim, iskustvo uvek pokazuje da se samo deo energije neureðenog toplotnog kretawa æestica moþe pretvoriti u mehaniæki rad. To znaæi da se sistem u poæetno stawe ne moþe vratiti po istoj putawi (procesu), veœ po nekoj drugoj (npr. 2, slika 2.6). Pri tome se prvobitna ekspanzija (širewe) gasa – proces 1, kada on vrši rad na raæun toplote (i unutrašwe energije), mora zameniti spoqašwim radom i poveœawem unutrašwe energije sistema – proces 2. () () abba12'll i


Na taj naæin je dobijen kruþni proces: Ako se on ponavqa u toku vremena, postaje periodiæan. Takvi su termodinamiæki procesi npr. u automobilskim motorima.
Prema tome, u principu, svi procesi u prirodi mogu biti: povratni(reverzibilni) i nepovratni (ireverzibilni). Povratan proces je takav proces koji moþe da se vrši u dva suprotna smera bez ikakvih izmena kod okolnih tela.
Iz iskustva vrlo dobro znamo da u prirodi nema idealnih povratnih procesa. Postoje prirodne pojave kod kojih se povratni proces moþe ostvariti u velikoj meri, na primer, pretvarawe potencijalne u kinetiæku energiju i obrnuto kod elastiænog ili fiziækog klatna i sliæno, praktiæno mogu da se smatraju povratnim procesima. Iako povratni procesi ne mogu da se ostvare u potpunosti, nego su samo idealizovani, oni imaju veliki znaæaj u prouæavawu termodinamiækih pojava. Dakle, sve dinamiæke pojave u prirodi su nepovratne, jer telo izvedeno iz jednog stawa ne moþe spontano, ili bez spoqašweg uticaja, da se vrati u to prvobitno stawe.
Sa energetskog stanovišta, svi termodinamiæki procesi su nepovratni, jer ne postoji idealna mašina koja bi radila bez gubitaka energije (npr. na trewe ili na savladavawe otpora vazduha). Kod motora sa unutrašwim sagorevawem –kod automobila, ovi gubici se nadoknaðuju potrošwom goriva (benzina).

Jedna od bitnih karakteristika svake toplotne pojave, procesa, je koliæina toplote koja se razmeni izmeðu termodinamiækih sistema ili sistema i okoline. Iako se koliæina toplote moþe direktno odrediti iz prvog zakona termodinamike, pokazalo se da ta veliæina nije uvek najpogodnija u rešavawu nekih praktiænih problema kao što su, na primer, pretvarawe unutrašwe energije u druge oblike energije, najæešœe u mehaniæku energiju. Pretvarawe unutrašwe energije tela (sistema) u druge oblike energije vrši se sa mawim gubicima ukoliko je wegova temperatura viša u odnosu na temperaturu okoline. S druge strane, praktiæno nije moguœe transformisati unutrašwu energiju tela (sistema) u druge oblike energije ako se wegova temperatura neznatno razlikuje od temperature okoline, a posebno ako je reæ o relativno niskim temperaturama. Tada je unutrašwa energija „rasejana” meðu telima i praktiæno je nekorisna. Neiskorišœene ogromne koliæine unutrašwe energije sadrþane su, na primer, u morima i okeanima, æija se temperatura relativno malo razlikuje od temperature okolne sredine.
Ta æiwenica je navela fiziæare da uvedu novu veliæinu, kojom se izbegavaju navedeni nedostaci, a definisana je pomoœu koliæine toplote i temperature. To je promena entropije:


Koliæina toplote koja se predaje ili oduzima sistemu (telu) po jedinici temperature,naziva se entropija sistema (tela).
Jedinica entropije je xul po kelvinu (J/K).
Pojam entropija je u fiziku uveo 1865. godine nemaæki fiziæar Rudolf Klauzijus prilikom razmatrawa pojava i rešavawa problema u termodinamici.
Za razliku od koliæine toplote, koja je karakteristika toplotnih procesa, entropija je, kao i unutrašwa energija, funkcija stawa sistema. To znaæi da ona zavisi samo od stawa sistema, odnosno od parametara koji karakterišu to stawe. Zbog fundamentalne vaþnosti termodinamiækih procesa – prelazaka sistema iz jednog u drugo termodinamiæko stawe, praktiæno znaæewe imaju samo promene entropije.
Obiæno nije moguœe neposredno izmeriti entropiju sistema, kao što nismo u stawu da izmerimo ni wegovu unutrašwu energiju. Mogu se, u stvari, meriti samo promene entropije posredstvom merewa drugih termodinamiækih veliæina (koliæine toplote, temperature, pritiska i zapremine). Te promene zavise samo od poæetnog i konaænog stawa, a ne zavise od puta (procesa) kojim je sistem ostvario taj prelazak.
U klasiænoj termodinamici se razmatraju procesi koji se dešavaju u izolovanom sistemu. Pri tome, promena entropije se povezuje s povratnošœu ili nepovratnošœu tih procesa.
Kod povratnih (idealizovanih) procesa entropija ostaje nepromewena, odnosno
Spov = const ili DSpov = 0 .
Svi realni procesi vezani su za odreðene gubitke energije, koja prelazi u „rasejanu“ energiju (koliæinu toplote). Sledi da su svi takvi procesi u mawem ili veœem stepenu nepovratni i da se karakterišu poveœawem entropije:
DSnep > 0.
Sve realne procese u izolovanom sistemu karakteriše poveœawe entropije.


Svakodnevno iskustvo pokazuje da toplota spontano prelazi od tela više na telo niþe temperature. Meðutim, prvi princip termodinamike ne bi bio narušen ako bi, obrnuto, toplota prelazila i od tela niþe na telo više temperature, pod uslovom da ukupna energija izolovanog sistema ostaje neizmewena (konstantna). Praksa pokazuje da se takav proces spontano nikad ne dešava.
Prvi princip termodinamike daqe dopušta potpuno pretvarawe kako kinetiæke energije u unutrašwu (pri sudaru tela, trewu i sliæno), tako i unutrašwe energije u kinetiæku. To bi znaæilo da se telo koje se usled trewa zaustavilo (wegova kinetiæka energija u celini se pretvorila u unutrašwu energiju tela i okoline – podloge) moþe ponovo dovesti u kretawe, æak i da stekne istu onu brzinu koju je imalo pre zaustavqawa, iskquæivo na raæun osloboðene unutrašwe energije prilikom zaustavqawa tela. Ili, na primer, da telo koje je palo sa odreðene visine moþe da se vrati na prvobitnu visinu na raæun unutrašwe energije osloboðene prilikom udara u podlogu. Tako nešto se, meðutim, nikad ne dešava.
Slika 2.7. Spontani prelaz toplote
Prema tome, moþe se zakquæiti da se smer toplotnih procesa, wihova nepovratnost, ne moþe objasniti pomoœu prvog principa termodinamike. Smer toplotnih procesa odreðuje drugi princip termodinamike. On moþe biti formulisan na više naæina. Jedna od najjednostavnijih definicija drugog principa termodinamike, koja je rezultat uopštavawa velikog broja æiwenica, glasi:
Toplota spontano prelazi samo sa tela više temperature na telo niþe temperature;obrnuto,prelazak toplote sa hladnijeg tela na toplije ne moþe se vršiti sam od sebe (spontano).
Prvi princip termodinamike govori o moguœnostima pretvarawa odreðene koliæine toplote u rad i obrnuto. Pri tome nema ograniæewa koji se deo date koliæine toplote moþe pretvoriti u rad. Meðutim, ogledi pokazuju da nije moguœe pretvoriti u rad svu koliæinu toplote koju je termodinamiæki sistem primio. Uzimajuœi to u obzir, drugi princip termodinamike se definiše i na sledeœi naæin:
Ne postoji termodinamiæki proces u kojem bi jedini rezultat bio pretvarawe toplote u rad. Kada bi takvi procesi bili moguœi, tada bismo rad mogli proizvoditi crpeœi toplotu iz mora i okeana ili iz nekog drugog toplotnog rezervoara, i to u ogromnim razmerama. Sva tela u prirodi, a naroæito voda mora i okeana, atmosferski vazduh, Zemqina kora i dr. sadrþe ogromne koliæine unutrašwe energije, ali je moguœe samo deo te energije pretvoriti u koristan rad.

Na osnovu toga je nastala još jedna formulacija drugog principa termodinamike: Nemoguœe je konstruisati perpetuum mobile druge vrste.
Da bi toplotna mašina mogla da vrši rad, mora biti povezana sa grejaæem od koga se oduzima odreðena koliæina toplote i hladwakom, kome se predaje deo primqene koliæine toplote. Ovo je neophodno da bi se (ponovo) ostvarili poæetni uslovi i da bi mašina ponovo mogla da izvrši mehaniæki rad (kruþni proces).

Rad mašine koja bi, na primer, koristila unutrašwu energiju atmosfere, morske ili okeanske vode (grejaæa) ne bi bio u suprotnosti sa prvim zakonom termodinamike, jer bi ona koristila postojeœu unutrašwu energiju, transformišuœi je u druge oblike, a voda bi se postepeno hladila. Zato je takvoj mašini i dat naziv perpetuum mobile druge vrste. Meðutim, prema drugom principu termodinamike, konstrukcija takve mašine je nemoguœa jer bi za dobijawe rada na raæun te unutrašwe energije (grejaæa – morske ili okeanske vode) bila neophodna i druga sredina sa niþom temperaturom (hladwak sa niþom temperaturom kome se predaje deo primqene koliæine toplote). Za dobijawe takvih uslova potrebno je trošiti energiju.
U zatvorenom i toplotno izolovanom sistemu entropija moþe samo da raste, dostiþuœi maksimum u stawu termodinamiæke ravnoteþe sistema.
DS ³ 0 .
Znak nejednakosti odnosi se na neravnoteþna stawa, a znak jednakosti na stawe termodinamiæke ravnoteþe.
Drugi princip termodinamike ima ograniæenu primenu. Prvo wegovo ograniæewe ogleda se u tome što se on ne moþe primeniti na skup (sistem) malog broja æestica (molekula, atoma i dr.). Tako, na primer, u sudu od 10 molekula moguœa su znatna odstupawa od najverovatnijeg stawa (wihova razliæita koncentracija u sudu). Ako je reæ o sistemu sa ogromnim brojem molekula, onda je, bez spoqnih uticaja, najverovatnije stawe ravnomerne koncentracije, pritiska i temperature. Meðutim, kada je reæ o skupu od 10 molekula, iako je najverovatnije da se oni homogeno rasporede u raspoloþivom prostoru, moþe se desiti, i to dosta verovatno, da se svih 10 molekula naðu u jednoj æetvrtini ili još mawem delu zapremine suda. Dakle, drugi princip termodinamike ne vaþi u „malom“; on se moþe primeniti samo na sistem velikog broja æestica (molekula).
Druga ograniæewa ovog principa vezana su za moguœnost primene samo na termodinamiæke procese (toplotne pojave). Kod drugih oblika kretawa materije (mehaniæko, elektromagnetno, nuklearno) ovaj princip se ne moþe primeniti, a još mawe kod kretawa koja karakterišu þivi svet. Svi ovi realni procesi su i disipativni (postoji „rastur“ energije) i otvoreni (razmewuju, tj. mewaju broj i vrstu æestica). Prema tome, oni su i nepovratni!
Þivot savremenog æoveka se ne moþe zamisliti bez korišœewa toplotnih mašina. One sluþe za dobijawe elektriæne energije, pokretawe velikog broja transportnih objekata.

Veoma je znaæajna primena moœnih parnih turbina u elektranama za obrtawe rotora generatora. Parne turbine ugraðuju se i na nuklearnim elektranama, gde se za dobijawe visokotemperaturne pare koriste nuklearni procesi.
Savremeni transport koristi sve tipove toplotnih motora. U automobilima, traktorima, kombajnima koriste se motori sa unutrašwim sagorevawem. U avijaciji se široko primewuju gasne turbine. Reaktivni motori, koji takoðe rade na principu rada toplotnih mašina, koriste se u kosmiækim raketama.


U savremenoj tehnici mehaniæka energija se dobija uglavnom na raæun unutrašwe energije. Ureðaji u kojima se vrše takve transformacije energije nazivaju se toplotni motori.
Toplotni motori su ureðaji u kojima se na raæun unutrašwe energije dobija mehaniæka energija.
Svaka toplotna mašina, osim pretvarawa unutrašwe energije u rad, vrši još „nešto“, a to „nešto“ je predaja jednog dela primqene koliæine toplote okolnim telima. Za dobijawe rada je neophodno da stalno postoji temperaturna razlika izmeðu grejaæa od koga radno telo (gas ili para) prima odreðenu koliæinu toplote i hladwaka (to je obiæno atmosfera ili neka druga sredina) kome se predaje neiskorišœena koliæina toplote.
Svaka toplotna mašina se, znaæi, sastoji iz tri dela: radnog tela, grejaæa temperature T1 i hladwaka temperature T2 (slika 2.8). U svojstvu hladwaka najæešœe se koristi atmosfera, vodena sredina, a moþe i zemqa. Kao radno telo obiæno se koristi gas ili para zatvoreni u sudu sa pokretnim klipom.
Slika 2.8. Toplotni motor
U procesu širewa, radno telo (gas ili para) prima neku koliæinu toplote Q1 od grejaæa temperature T1, to jest od tela u kome se na raæun sagorevawa nafte, benzina ili nuklearnih reakcija odrþava konstantno visoka temperatura T1 Uprocesu sabijawa, radno telo (gas ili para) predaje neku koliæinu toplote Q2 hladwaku temperature T2, to jest telu ili sredini æija je temperatura uvek niþa od temperature grejaæa T1. Širewe gasa uzrokuje pomerawe klipa u cilindru motora. Pri širewu gasa wegov pritisak opada dok ne postane jednak spoqašwem pritisku. Tada se širewe gasa zaustavqa i gas u cilindru prestaje da vrši rad. Nakon toga je neophodno putem sabijawa vratiti gas u poæetno stawe. Sabijawe gasa moþe da se vrši samo pod dejstvom spoqašwe sile. Posle toga ponovo se odvijaju procesi širewa i sabijawa gasova. Znaæi, u toplotnom motoru se vrše periodiæni procesi (ciklusi) širewa i sabijawa gasa (pare).
Koliæina toplote koju prima radno telo toplotnog motora moþe da bude samo delom transformisano u mehaniæki rad. Na osnovu zakona odrþawa energije (prvog principa termodinamike), moþe se izvesti energetski bilans u jednom radnom ciklusu toplotnog motora, odnosno izraæunati koristan rad.


Posle završenog ciklusa, radno telo se dovodi u poæetno stawe, wegova unutrašwa energija nije se promenila (DU = U2 – U1 = 0). Uzimajuœi to u obzir, Prvi princip termodinamike se moþe napisati u obliku:
Q1 = Q2 + A + DQ ,
gde je DQ koliæina toplote koja je „izgubqena“ pri toplotnoj razmeni sa okolinom (trewe i sliæno). Odavde sledi da je koristan rad
A = Q1 – Q2 – DQ , odnosno A £ Q1 – Q2 ,
ako se zanemari DQ. Znak nejednakosti vaþi u sluæaju realnog, a jednakosti u sluæaju idealnog motora.
Prema naæinu dobijawa rada toplotni motori se dele na klipne (parne mašine i motori sa unutrašwim sagorevawem), rotacione (parna i gasna turbina) i reaktivne
Kod klipnih motora, pod uticajem sile pritiska gasa ili pare, u radnom cilindru se vrši povratno kretawe klipa, koje se preko odreðenog mehanizma pretvara u obrtno kretawe radilice motora. Kod motora sa unutrašwim sagorevawem, povišewe temperature nastaje pri sagorevawu goriva (nafte, benzina) unutar motora, a grejaæ æine sami usijani produkti goriva koji su istovremeno i radno telo. Ulogu hladwaka vrši atmosfera, u koju se izbacuju iskorišœeni gasovi.
Kod rotacionih motora, struja pare ili gasa usmerava se na lopatice radnog toæka, koji izvodi obrtno kretawe. Kod parnih turbina grejaæ je parni kotao, a hladwak atmosfera ili specijalni ureðaj za hlaðewe i kondenzovawe pare – kondenzator, a radno telo je sama para. U reaktivnim motorima, gasovi koji se stvaraju pri sagorevawu goriva u radnoj komori izbacuju se velikom brzinom, što izaziva kretawe objekta u koji je ugraðen motor, i to u suprotnom smeru.

Vratimo se termodinamiækom ciklusu kao celini (sl. 2.8) i razmotrimo wegov energetski bilans. Videli smo da u toku jednog dela ciklusa gas prima neku koliæinu toplote Q1 od grejaæa temperature T1, a u toku drugog dela gas predaje koliæinu toplote Q2 hladwaku æija je temperatura T2. Znaæi, u koristan se rad transformiše samo deo od koliæine toplote Q1. Taj deo iznosi Q1 – Q2 Zato je koeficijent korisnog dejstva ciklusa, koji se definiše kao odnos korisnog i uloþenog rada (energije):
Pretvarawe mehaniækog rada u toplotu poznato je od davnina. Isto tako, utvrðeno je da se, i obrnuto, toplota moþe pretvoriti u mehaniæki rad. Meðutim, tek u 19. veku Xul i Majer utvrdili su vezu izmeðu utrošenog rada i dobijene koliæine toplote. Došlo se do zakquæka da se mehaniæki rad moþe potpuno pretvoriti u toplotu dok je, pretvarawe toplote u mehaniæki rad moguœe samo delimiæno.


Kako se adijabatski procesi odvijaju bez razmene toplote, jasno je da se od mašine u prvom ciklusu odvodi toplota (Q1), a da se u treœem vrši ekspanzija i dovodi toplota (Q2).
U ovakvom teorijskom ciklusu vaþi odnos: Q2: Q1= T2: T1. Na osnovu toga, za koeficijent korisnog dejstva dobija se:
Ovo je teorijski najveœi koeficijent korisnog dejstva koji se moþe postiœi za temperature T1 i T2. Svaka realna toplotna mašina, koja pri radu koristi grejaæ temperature T1 i hladwak T2 ne moþe imati koeficijent korisnog dejstva veœe vrednosti od koeficijenta korisnog dejstva idealne toplotne mašine pri istim uslovima.
Gorwa formula daje teorijsku granicu za maksimalnu vrednost koeficijenta korisnog dejstva toplotnih motora. Ona pokazuje da je toplotni motor utoliko efikasniji ukoliko je viša temperatura grejaæa i niþa temperatura hladwaka. Samo pri temperaturi hladwaka jednakoj apsolutnoj nuli, moþe se postiœi h = 1. Naravno, u praksi je vrednost koeficijenta korisnog dejstva uvek mawa, jer je ciklus idealizovan (radno telo – idealan gas, zanemareno trewe, nema gubitaka putem toplotne razmene sa okolinom). Znaæi,
Koeficijent korisnog dejstva ili stepen iskorišœewa je neimenovan broj –bezdimenziona veliæina (J/J) i najæešœe se izraþava u procentima. Kod dobrih parnih mašina on, na primer, iznosi oko 0,2, tj. 20%, a kod savremenih motora sa unutrašwim sagorevawem i do 50%. Poreðewa radi, stepen iskorišœewa obiæne sijalice sa vlaknom iznosi oko 2%, a fluorescentne oko 15%.
Primer 5. Idealna toplotna mašina svake sekunde „troši“ koliæinu toplote 6×106 J, a hladwak prima koliæinu toplote od 3×106 J. Kolika je korisna snaga ove mašine?
Podaci: Q1 = 6 × 106 J, Q2 = 3 × 106 J; Pk = ?
Rešewe. Pošto je:
korisna snaga je:


• Za prouæavawe tela (sistema) sa ogromnim brojem æestica (molekula, atoma) koriste se dva pristupa: termodinamiæki (makroskopski) i molekulsko-kinetiæki (mikroskopski).
U prvom se prouæavaju makroskopska (fenomenološka) svojstva tela (sistema) kao celine, operišuœi odgovarajuœim veliæinama kao što su: pritisak, zapremina, gustina, temperatura, unutrašwa energija, koliæina toplote i druge ne ulazeœi pri tome u strukturu supstancije.
Molekulsko-kinetiæki (mikroskopski) pristup polazi od svojstava i ponašawa molekula (atoma, jona) koji saæiwavaju telo (sistem) i na osnovu toga se izvode zakquæci o svojstvima i ponašawu tela (sistema) kao celine.
Unutrašwa energija tela (sistema) moþe da se mewa vršewem mehaniækog rada i pri toplotnoj razmeni. Pri toplotnoj razmeni unutrašwa energija toplijeg tela spontano se predaje hladnijem telu (neposredni kontakt tela) bez vršewa rada.
Da bismo unutrašwu energiju mogli da koristimo za vršewe mehaniækog rada, potrebno je da se izmeðu toplijeg tela (grejaæa) i hladnijeg tela (hladwaka) nalazi radno telo (gas, para), koje se širi ili sabija bez dodira sa telima druge temperature.
Kada se gas izotermski širi pri stalnoj temperaturi grejaæa, on dobija od wega neku koliæinu toplote Q i vrši rad A:
DU = 0; A = Q
Unutrašwa energija samog gasa pri tome se ne mewa. Rad se vrši na raæun unutrašwe energije grejaæa. Pri adijabatskom širewu gasa izvršen rad A je jednak smawewu (promeni) unutrašwe energije gasa DU:
Q = 0; A = – DU
• Prvi princip termodinamike je zakon odrþawa i transformacije energije iz jednog u drugi oblik primewen na toplotne procese. Saglasno tome:
Q = DU + A


Koliæina toplote Q predata telu (sistemu) „troši“ se na izmenu wegove unutrašwe energije i na vršewe rada. Rad koji vrši termodinamiæki sistem protiv spoqašwih sila prilikom izobarskih procesa jednak je:
A = pDV,
gde je p – pritisak gasa, a DV – promena zapremine.
• Drugi princip termodinamike odreðuje smer toplotnih procesa. On negira moguœnost korišœewa ogromnih rezervoara unutrašwe energije kao što su, na primer, mora i okeani bez wihovog prevoda na niþi temperaturni nivo, to jest bez hladwaka.
• Koliæina toplote koja se predaje ili oduzima sistemu (telu) po jedinici temperature naziva se entropija sistema (tela).
SQ T . =
Entropija sistema, po svojim svojstvima, sliæna je unutrašwoj energiji. Praktiæno znaæewe imaju samo promene entropije koje se odnose na dato stawe sistema.
• U svim toplotnim mašinama moþe da se transformiše u mehaniæki rad samo deo koliæine toplote koji se od grejaæa Q1 usmerava prema hladwaku Q2. Vrednost koeficijenta korisnog dejstva toplotnih motora iznosi:
QQTT QT 1212 11 , =≤ h
gde su T1 i T2 – temperature grejaæa, odnosno hladwaka. Koeficijent korisnog dejstva iraþen preko temperature vaþi samo za idealan sluæaj.


1. Šta odreðuje unutrašwu energiju tela?
2. Na koje se naæine moþe promeniti unutrašwa energija termodinamiækog sistema (gasa u sudu)?
3. Zbog æega se pumpa pri pumpawu fudbalske lopte zagreje?
4. Koja je razlika izmeðu unutrašwe energije i koliæine toplote?
5. Da li je izvršeni rad pri promeni zapremine gasa odreðen samo poæetnim i krajwim stawima gasa?
6. Koliko specifiænih toplotnih kapacitivnosti postoji? Po æemu se one razlikuju?
7. Pri adijabatskom procesu, rad i promena unutrašwe energije imaju razliæite predznake. Šta to znaæi?
8. Na raæun æega se vrši rad pri pomerawu klipa usled širewa gasa u izotermskim i adijabatskim procesima?
9. Da li se adijabatski procesi mogu opisati i jednaæinom oblika: TVk-1=const., ako se iskoristi opšta jednaæina gasnog stawa?
10. Šta je povratan, a šta nepovratan proces? Navesti odgovarajuœe primere.
11. Kako se definiše entropija sistema?
12. Šta moþete da kaþete o smeru toplotnih pojava?
13. Da li se meðusobno iskquæuju perpetuum mobile prve i perpetuum mobile druge vrste?
14. Na koje sve naæine se moþe definisati drugi princip termodinamike?
15. Kojoj je veliæini sliæna entropija po svojim osnovnim svojstvima?
16. Kolika je entropija termodinamiækog sistema na apsolutnoj nuli?
17. Kada je entropija termodinamiækog sistema maksimalna?
18. Koja su osnovna svojstva gasova koja ih æine nezamenqivim u svojstvu radnog tela kod toplotnih motora?
19. Rad toplotnih motora zasniva se na zatvorenom termodinamiækom ciklusu. Objasniti zbog æega je izabran kruþni ciklus.
20. Koji uslov treba da bude zadovoqen da bi toplotni motor u toku jednog ciklusa izvršio pozitivan rad?
21. Definišite koeficijent korisnog dejstva kod toplotnih motora.
22. Na koje se osnovne naæine moþe poveœati koeficijent korisnog dejstva toplotnog motora?
23. U kakvoj je vezi princip rada toplotnih motora sa drugim principom termodinamike?


FIZIÆKI PARAMETRI IDEALNOG FLUIDA PRI KRETAWU
Pod„fluidom“ se podrazumeva zajedniæki naziv za teænosti i gasove. Ovaj objediwavajuœi naziv ukazuje na zajedniæka svojstva teænosti i gasova, naravno, ne iskquæujuœi i wihove razliæitosti. Teænosti i gasovi se prvenstveno razlikuju po stišqivosti, koja je kod gasova znatno veœa nego kod teænosti. Štaviše, teænosti se æesto aproksimativno tretiraju kao potpuno nestišqivi fluidi. Takva aproksimacija je prihvatqiva samo dok se teænosti uporeðuju sa gasovima. U poreðewu sa ævrstim telima (kristalima), stišqivost teænosti nije zanemarqiva. Zajedniæko za teænosti i gasove je to što wihovi molekuli imaju relativno veliku pokretqivost, znatno veœu od molekula ævrstih tela. Najjednostavniji model, koji moþe postuþiti kao korisna idealizacija u mnogim problemima dinamike fluida, jeste model idealnog fluida. U najuþem smislu reæi, to je neprekidna sredina koja poseduje sledeœa svojstva: ne postoji unutrašwe trewe meðu slojevima (viskoznost) i nestišqiva je (ne mewa svoju zapreminu pod dejstvom pritiska). Sliæno modelima (materijalna taæka ili apsolutno kruto telo), pojam neprekidne sredine takoðe je idealizacija kod koje se zanemaruje struktura supstancije (makroskopski model).
Pojam idealan fluid treba razlikovati od pojma idealan gas. Oni se suštinski razlikuju. Model idealnog gasa izraþava diskontinualnost, æestiænu strukturu gasa. Wime se gas predstavqa kao skup ogromnog broja molekula (atoma), koji se zamišqaju kao idealno elastiæne æestice koje uzajamno deluju samo u direktnim (neposrednim) meðusobnim sudarima i udarima o zidove suda.
Model idealnog gasa više odgovara za analizu i objašwewe pojava iz statike fluida i termodinamiækih procesa, a model idealnog fluida upotrebqiviji je za mehanizme i posledice mehaniækog kretawa teænosti. Model idealnog gasa obuhvata, na primer, razliæitosti koje se odnose na jedno, dvo i tro i višeatomske molekule gasa. Kod modela idealnog fluida takve razlike se ne uzimaju u obzir.
Kretawe idealnog fluida karakterišu æetiri osnovna makroskopska parametra: gustina,pritisak,temperatura i brzina deliœa fluida. U ovom sluæaju pod pojmom „deliœ“ podrazumeva se deo supstancije obuhvaœene elementarnom zapreminom, æije se dimenzije u odnosu na dimenziju prostora (suda), mogu zanemariti.
Pojam „deliœ“ moþe se poistovetiti sa pojmom æestice, ali æestice makroskopskog tipa. Tada se pojam æestica ne odnosi na mikroæesticu – atom, molekul itd., veœ na odreðenu koliæinu supstancije æija se zapremina moþe zanemariti u datim uslovima.
Razmotriœemo prvo najjednostavniji oblik kretawa fluida – stacionarno proticawe (strujawe). Kod stacionarnog proticawa nema nagomilavawa deliœa fluida, niti wihovog vrtloþnog kretawa. To znaæi da se stalno u toku vremena, kroz odreðenu taæku preseka cevi, deliœi idealnog fluida kreœu istom brzinom – po pravcu, smeru i intenzitetu.


Kada se u nekoj taæki prostora (unutar cevi kroz koju protiæe idealan fluid) brzine æestice ne mewaju u toku vremena, onda se fluid nalazi u stawu stacionarnog strujawa.
Pri tome, brzina kretawa æestice moþe biti razliæita od taæke do taæke duþ wene putawe.
Meðutim, u bilo kojoj taæki prostora brzine svih æestica koje proðu kroz tu taæku su jednake. Ako se, pak, ovi parametri mewaju u toku vremena u datoj taæki, onda je kretawe (strujawe) fluida nestacionarno.
Linije (putawe) duþ kojih se deliœi (æestice) fluida kreœu nazivaju se strujne linije. Pri stacionarnom kretawu (strujawu) fluida, strujne linije se poklapaju sa putawama æestica fluida i nigde se ne seku (sl. 3.1). Deo fluida ograniæen strujnim linijama naziva se strujna cev. Æestice fluida koje se u nekom trenutku nalaze u izvesnoj strujnoj cevi ne izlaze iz te cevi u toku kretawa.
Jedna od najopštijih zakonitosti, u okviru Wutnovske mehanike, jeste zakon oæuvawa (konzervacije) mase. Jednaæina kontinuiteta predstavqa konkretizaciju (ilustraciju) ovog opšteg zakona.

v 1
Neka je na preseku S1 duþ ose strujne cevi brzina idealnog fluida , a na osi preseka S 2 – brzina (sl. 3.2). Pošto je gustina u svakoj taæki ista (homogen raspored supstancije u prostoru), onda œe kroz oba preseka strujne cevi za isto vreme proticati ista koliæina fluida. Za vreme Dt kroz presek S1 stacionarno prostruji idealni fluid mase Dm1, a Dm2 – za to isto vreme, kroz S2. Znamo da je Dm1 = Dm2, a pošto je Dm = rSvDt (r – gustina fluida), dobija se: rS 1v1Dt = rS2v2Dt,odnosno

Ova formula predstavqa jednaæinu kontinuiteta (neprekidnosti) za stacionarno proticawe idealnog fluida. v 2
S1v1= S2v2
U opštem sluæaju, pošto su preseci proizvoqno izabrani:
S×v = const.


Veliæina S × v predstavqa zapreminu fluida koja u jedinici vremena prostruji kroz popreæni presek strujne cevi. Ona se obeleþava sa Q i naziva protok fluida. Znaæi,
Koristeœi ovaj izraz, jednaæina kontinuiteta ima jednostavniju formulu:
Q = const
Prilikom stacionarnog strujawa (proticawa),protok idealnog fluida je isti na svim presecima strujne cevi.
Protok se izraþava u kubnim metrima u sekundi
3 m (s) Q


BERNULI DANIJEL, švajcarski fiziæar i matematiæar, predstavnik ugledne porodice Bernuli. Prvi je matematiæki obradio kretawe teænosti. Osnovni wegov rad Hidrodinamika sadrþi fiziæke osnove mehanike teænosti. Zakon hidrodinamiækog pritiska, do kojeg je došao teorijski, poznat je kao Bernulijeva jednaæina. Ona predstavqa osnov cele hidromehanike. Dao je odreðene priloge molekulsko-kinetiækoj teoriji gasova. Uæestvovao je u formirawu teorije sudara elastiænih tela. Rešavao je i druge probleme mehanike kao što su obrtno kretawe, oscilovawe fiziækog klatna, oscilovawe struna i dr.
Rešavawe mnogih zadataka u dinamici fluida zasniva se na jednaæini koja izraþava zavisnost izmeðu osnovnih parametara: pritiska, brzine kretawa fluida, wegove gustine i poloþaja u poqu Zemqine teþe (visine u odnosu na neki nulti nivo). Ta zavisnost za idealne fluide u uslovima stacionarnog proticawa definisana je pomoœu Bernulijeve jednaæine. Ova jednaæina predstavqa konkretizaciju zakona odrþawa energije za idealne fluide u stacionarnom proticawu.


Posmatrajmo stacionarno proticawe idealnog fluida kroz strujnu cev razliæitog popreænog preseka (sl. 3.3).
Cev se nalazi u poqu Zemqine teþe i krajevi cevi su na razliæitim visinama. Usredsredimo paþwu na markiranu koliæinu fluida (mase Dm) koja se, s leve strane cevi, potiskuje pritiskom p1 i koja se istiskuje na desnom kraju cevi nasuprot pritisku p2. Brzine deliœa i popreæni preseci obeleþeni su na slici.
Fluid se kreœe s leva na desno i p1 > p2.
Rad sile pritiska u poloþaju 1 je
A1 = p1S1DA1, a u poloþaju 2: A2 = p2S2DA2. Kako su DV1 = S1DA1 i DV2 = S2DA2, onda su A1 = p1DV1 i A2 = p2DV2. Prema jednaæini kontinuiteta, pri stacionarnom strujawu nestišqive teænosti je
DV1 = DV2 = ... = DV
dobija se A1 = p1DV i A2 = p2DV
Slika 3.3. Analiza proticawa fluida kroz strujnu cev S2 v2 v1 p1
Zbog toga što je p1 > p2, proizlazi da je A1 > A2. Odavde sledi da je teænost posmatranog elementa zapremine pri pomerawu dobila izvesnu energiju, koja potiæe od razlike rada sila pritiska na mestima 1 i 2, tj.
A1 –A2 =(p1 –p2)DV.
Ova razlika jednaka je odgovarajuœoj promeni ukupne kinetiæke i gravitacione potencijalne energije:
pvghpvgh 22 111222 11 22,++ =+ + rrrr ppVmvmghmvmgh 22 122211 ()11 22 ¬ =+ +®
Preureðivawem ælanova i deobom ove jednaæine sa DV nalazi se
m V = ∆ ∆ r
gde je specifiæna gustina teænosti. Buduœi da su dati preseci cevi izabrani proizvoqno, onda gorwi zbir ælanova ostaje stalan za bilo koji presek strujne cevi, pa se konaæno dobija:
pghv12const. 2 ++ = rr
Sva tri ælana Bernulijeve jednaæine imaju dimenzije pritiska (proverite). Oni se nazivaju: p – statiæki (specifiæna potencijalna energija sile pritiska, odnosno potencijalna energija sile pritiska u jedinici zapremine); rgh – hidrostatiæki (specifiæna gravitaciona potencijalna energija, tj. gravitaciona potencijalna energija jedinicezapremineteænosti) i – v 12 2 ¸r


dinamiæki (specifiæna kinetiæka energija ili kinetiæka energija jedinice zapremine teænosti). Na osnovu toga, Bernulijeva jednaæina moþe se iskazati na sledeœi naæin:
Pri stacionarnom proticawu idealnog fluida kroz strujne cevi ukupni pritisak,jednak sumi statiækog,visinskog i dinamiækog pritiska,ostaje neizmewen (konstantan) u svakom popreænom preseku strujnih cevi.

Opisaœemo neke karakteristiæne sluæajeve primene Bernulijeve jednaæine: odreðivawe brzine isticawa fluida iz malog otvora (mlaznica) i Toriæelijeva teorema.

Neka teænost istiæe kroz boæni otvor na sudu (a mogao je da bude i na dnu suda). Ako je otvor mali, onda se brzina spuštawa nivoa teænosti u sudu moþe zanemariti u odnosu na brzinu isticawa teænosti kroz otvor. Uzmimo za nivo referencije, odnosno za nivo od kojeg merimo visinu h, horizontalu koja prolazi kroz boæni otvor. Na slobodnu površinu teænosti, kao i na teænost u otvoru, deluje atmosferski pritisak koji ima istu vrednost (visina h je relativno mala, pa je razlika atmosferskog pritiska praktiæno zanemarqiva). Za dati referentni nivo visina boænog otvora jednaka je nuli (slika 3.4).
=0 h1=h
Slika 3.4. Isticawe fluida iz rezervoara p1

Iz opšteg oblika Bernulijeve jednaæine
pri æemu su v1 ælanmoþe se zanemariti,
h2 = 0 i p1 = p2, dobija se Odavde je
vgh2. = ghv12 2. = rr 1 21 2 rv , pvghpvgh 22 111222 11 22,++ =+ + rrrr
Ova relacija predstavqa matematiæki izraz Toriæelijeve teoreme, koja glasi: Brzina isticawa teænosti kroz mali otvor suda jednaka je brzini koju bi telo imalo kada bi slobodno padalo sa visine koja odgovara visini nivoa teænosti u sudu.
Moþe se zakquæiti da brzina isticawa teænosti kroz otvor na sudu ne zavisi od gustine, odnosno mase teænosti.


Posmatramo isticawe fluida iz jako suþenog otvora (slika 3.5) pod dejstvom pritiska p (klip). Bernulijeva jednaæina, za ovaj sluæaj (h1 = h2), ima oblik:
pvpv 22 112 11 22, + =+ rr 61
a odatle:
()vvpp 22 112 1 2. = r
Kako su: p1 = p + pa i p2 = pa (gde je pa –atmosferski pritisak), to je p1 – p2 = p.
Kako je S1 >> S2, iz jednaæine kontinuiteta sledi v 1 << v , tj. v 2 – v 1 2 » v 2
Na osnovu toga se dobija:
vp 2 = r

2
Brzina isticawa fluida iz mlaznice zavisi samo od pritiska fluida u cevi ispred mlaznice.

Najjednostavniji oblik Pitoove cevi sluþi za odreðivawe brzine strujawa teænosti u nekom otvorenom kanalu. To je obiæna savijena staklena cev, æiji se otvor okreœe prema struji teænosti. Neka je nivo referencije horizontala koja prolazi kroz sredinu otvora cevi (sl. 3.6). U taæki (1) teænost je zaustavqena otvorom cevi, pa je v1 = 0.
U taæki 2 brzina v2 jednaka je brzini teænosti v Bernulijeva jednaæina se u ovom sluæaju zapisuje u formi:
ppv 2 12 1 2, =+ r
odnosno
ppv 2 12 1 2. = r
Slika 3.6. Pitoova cev
Razlika pritisaka je p1 – p2 = r×g×H, gde je H razlika nivoa teænosti u cevi i slobodne površine teænosti æija se brzina strujawa meri. Konaæno, odatle sledi:
vgH2. =
Merewem visine H moþe se odrediti brzina strujawa teænosti duþ pravca 1–2 ili u ma kom drugom mestu.


Primer: Iz horizontalno postavqenog medicinskog šprica istiskuje se fiziološki rastvor silom 10 N. Odrediti brzinu isticawa teænosti iz igle šprica. Gustina rastvora je 1030 kg/m3, a preænik klipa d = 1,5 cm, znatno je veœi od preænika otvora igle.
Podaci: F = 10 N, r = 1030 kg/m3; v2 = v; v = ?
Rešewe. Bernulijeva jednaæina primewena na preseke 1 i 2 (slika 3.5), ima oblik:
Na osnovu toga, uzimajuœi u obzir date podatke, dobija se:

• Pod pojmom „fluid“ se podrazumeva zajedniæki naziv za teænosti i gasove. Ovaj objediweni naziv ukazuje na zajedniæka svojstva teænosti i gasova, ne iskquæujuœi wihove razliæitosti.
• U dinamici teænosti i gasova se æesto koristi model idealnog fluida. Unajuþem smislu, idealan fluid je neprekidna sredina kod koje se zanemaruje unutrašwe trewe (viskoznost) i æija se stišqivost moþe zanemariti.
• Za opisivawe stacionarnog strujawa idealnog fluida koriste se dva osnovna pojma: strujne linije i strujna cev U opštem sluæaju, strujne linije se poklapaju sa putawama deliœa fluida i nigde se ne seku. Deo fluida ograniæen strujnim linijama naziva se strujna cev.
• Proizvod proizvoqnog popreænog preseka strujne cevi i brzine proticawa fluida kroz taj presek je protok fluida. On je stalan u sluæaju stacionarnog strujawa teænosti ili gasa kroz strujnu cev.
Q = Sv = const.
Ova formula predstavqa jednaæinu kontinuiteta za strujnu cev nestišqive teænostiiligasa. Iz ove formule jasno proistiæe da je brzina fluida mawa u veœem preseku, a veœa kroz presek mawe površine.

• Rešavawe mnogih problema (zadataka) u dinamici fluida zasniva se na zavisnosti izmeðu osnovnih parametara: pritiska, brzine kretawa fluida, wegove gustine i poloþaja u poqu Zemqine teþe (visine u odnosu na izabrani nulti nivo). Tu zavisnost za idealne fluide u uslovima stacionarnog proticawa definiše Bernulijeva jednaæina:
Na osnovu toga, Bernulijeva jednaæina se moþe iskazati na sledeœi naæin. Pri stacionarnom proticawu idealnog fluida kroz strujnu cev ukupan pritisak,jednak sumi statiækog hidrostatiækog i dinamiækog pritiska,ostaje neizmewen (konstantan) u svakom popreænom preseku strujne cevi.
1. Šta su idealni fluidi i koja su wihova osnovna svojstva?
2. Koja se zajedniæka svojstva teænosti i gasova istiæu u modelu idealnog fluida?
3. Da li postoji razlika izmeðu modela idealnog fluida i idealnog gasa?
4. Kakva je razlika izmeðu stacionarnog i nestacionarnog strujawa fluida?
5. Šta su strujne linije i strujna cev? U æemu se sastoji fiziæki smisao ove idealizacije?
6. Šta je protok fluida? Kojim jedinicama se izraþava?
7. Na osnovu kojih zakona odrþawa su izvedene Jednaæina kontinuiteta i Bernulijeva jednaæina?
8. Pod kojim uslovima vaþi Bernulijeva jednaæina?
9. Moþe li se Bernulijeva jednaæina primeniti na idealne gasove?
10. Šta je uloga mlaznice?
11. Kako radi vodeni šmrk?
12. Kojim ureðajem se meri brzina strujawa fluida? Da li wime moþe da se odredi i protok tog fluida?
13. Maseni protok predstavqa protok mase fluida kroz popreæni presek cevi u jedinici vremena: Da li vaþi relacija: M=rQ, gde je r – gustina, a Q – (zapreminski) protok fluida?


Osnovna svojstva tri agregatna stawa (faze) supstancije: ævrsto, teæno i gasovito stawe upoznali smo još u osnovnoj školi. Tada je ustanovqeno (što i obiæno iskustvo potvrðuje) da ævrsta tela, za razliku od teænosti i gasova, imaju stalan oblik i zapreminu. Meðutim, dovoqno jakim spoqašwim silama moþemo da mewamo wihov oblik i zapreminu, ali mnogo teþe nego teænostima i gasovima.
Agregatna stawa:ævrsto,teæno i gasovito,posledice su molekulskih sila i ponašawa velikog broja molekula* (atoma,jona),koji ulaze u sastav tela. Kod ævrstog agregatnog stawa molekulske sile su najveœeg intenziteta, kod teænih tela su slabijeg, a kod gasova su najmaweg intenziteta, osim u sluæajevima kada su gasovi pod vrlo velikim pritiskom.

Pri izuæavawu strukture supstancije ustanovqeno je da meðu molekulima (atomima) deluju molekulske sile. Trag krede ostaje na tabli, trag olovke po hartiji, dve kapqice teænosti pri dodiru slivaju se u jednu kap. Olovne ili æeliæne ploæe œe se „slepiti“ kada se dodirnu uglaæanim površinama, a staklo se dosta teško odvaja od vlaþne površi (podloge). Mnogi drugi primeri takoðe ubedqivo potvrðuju da meðu molekulima deluju privlaæne sile. Ali, mnoge druge æiwenice takoðe pokazuju da meðu molekulima postoje i odbojne sile. U telima molekulske sile, znaæi, imaju privlaæan i odbojan karakter. Ako to ne bi bilo tako, tela ne bi bila stabilna: ili bi se raspala (rasula) na sastavne æestice, ili bi se slila u kompaktnu celinu.

* Molekul je najmawa æestica date supstancije koja ima osnovna fiziæka svojstva date supstancije. Molekul se sastoji od istih (hemijski elementi) ili razliæitih atoma (jediwewa) meðusobno povezanih hemijskim vezama, koje nastaju u interakcijama spoqašwih valentnih elektrona atoma.

Molekulske sile mogu da budu privlaæne ili odbojne zavisno od meðusobnog rastojawa molekula (atoma): na veœim rastojawima od preænika molekula (atoma), reda veliæine 10–10 m, imaju privlaæan, a na mawim rastojawima odbojan karakter. Molekulske sile su kratkog dometa, stoga se one kod gasa pod malim pritiskom mogu zanemariti (meðusobna rastojawa molekula u gasovima su znatno veœa od preænika molekula).
Molekulska interakcija je elektromagnetne prirode. Molekuli (atomi) su sloþene æestice koje se sastoje od elektrona i atomskih jezgara. Elektroni iz omotaæa atoma jednog molekula privlaæno deluju na jezgra atoma drugog molekula, ali odbojno na elektrone iz omotaæa atoma tog drugog molekula. Jezgra atoma razliæitih molekula se takoðe odbijaju. Rezultat ovih komplikovanih interakcija je sloþeno elektromagnetno poqe. Tom poqu odgovara elektromagnetna sila (molekulska sila).
Uzajamno delovawe meðu molekulima (atomima) omoguœava da damo kvalitativno objašwewe pojave sile elastiænosti pri deformaciji tela. Npr. pri sabijawu ævrstog tela æestice se pribliþavaju, a pri istezawu se udaqavaju, što uslovqava pojavu sile elastiænosti koja nastoji da æestice vrati u ravnoteþne poloþaje. Isto tako, poznavawe molekulskih sila omoguœava rezumevawe pojave viskoznosti, površinskog napona i širewa tela pri zagrevawu.

Poznata nam je pojava da se tela šire kada se zagrevaju. Telefonske ili þice dalekovoda se izduþuju leti, a zimi se skrate i zategnu (slika 4.1). Kada ne moþemo da otvorimo poklopac tegle, postavimo je pod mlaz tople vode. Pošto se pri zagrevawu poklopac (metal) više širi od tegle (staklo), jasno je da œe se poklopac „odlepiti“ od staklene tegle. Ajfelova kula u Parizu leti je viša za oko 11 cm nego zimi.



Šta se, zapravo, dešava da se tela šire? Primajuœi odreðenu koliæinu toplote tela poveœavaju svoju unutrašwu energiju. Poveœava se intenzitet (haotiænog) toplotnog kretawa molekula (atoma) tog tela. Molekuli se meðusobno jaæe „guraju“. Zbog toga se poveœava prostor koji oni zauzimaju: telo se širi.
U procesu širewa telo srazmerno poveœava svoje dimenzije: Dl = l0 aDT, pa se poveœava i wegova zapremina: DV = V0 ×gDT, gde su: Dl = l – l0, DV = V – V0, l i V su duþina i zapremina zagrejanog tela na temperaturi t [°C], a l0 i V0 wegova duþina i zapremina na 0 °C i DT = t [°C]. Koeficijent širewa g3a zavisi od vrste materijala i ima male vrednosti, npr. za metale je
g= (2–5).10–5K–1 .
Linearno i zapreminsko širewe tela sa temperaturom moþe da se zapiše i u obliku:
l=l0 (1+ at),V = V0 (1 + gt).
Ævrsta tela zagrevawem ne mewaju svoj oblik, a teænosti zauzimaju oblik suda. Kako im se zapremina poveœava, jasno je da se wihova gustina smawuje.
m V = r
Za razliku od drugih teænosti, æista voda se ponaša drugaæije: zagrevawem vode od 0 °C do 4 °C wena zapremina se smawuje, a posle – zagrevawem iznad 4 °C, ona se poveœava. Zbog ove anomalije voda ima najveœu gustinu na + 4 °C. Kada se gasovi zagrevaju, ako je to pri izobarskom procesu, onda se oni ponašaju kao i teænosti i ævrsta tela: linearno im se poveœava zapremina (i smawuje gustina). Ali, gasovi mogu da se zagrevaju i u izohorskom termodinamiækom procesu. Tada ne mewaju zapreminu (veœ pritisak), pa im gustina ostaje ista.

Ævrsta tela, u odnosu na strukturu i osnovna svojstva, mogu da se podele u dve grupe. U prvu grupu spadaju kristalna, a u drugu amorfna tela.
U kristalima molekuli, atomi (joni) zauzimaju odreðene, ureðene poloþaje. Usled toga postoji pravilan (geometrijski) spoqašwi oblik kristala.
Ævrsta tela æije su æestice (joni,atomi,molekuli) pravilno periodiæno rasporeðene u prostoru tako da postoji trodimenzioni poredak u wihovoj strukturi,nazivaju se kristali.

Izmeðu molekula (atoma, jona) koji æine kristal deluju relativno jake molekulske privlaæne sile. Pošto je svaki molekul okruþen sa svih strana drugim molekulima, ove privlaæne sile su uravnoteþene i molekuli (wihovi centri) se nalaze u odreðenim poloþajima.

Kada se pravi model kristala, onda ti poloþaji – ravnoteþni poloþaji centara molekula predstavqaju taæke (male loptice) koje se nazivaju ævorovi. Meðumolekulske sile (veze izmeðu molekula) predstavqaju se duþima koje povezuju ævorove. Na taj naæin, u prostoru se dobija pravilna trodimenziona rešetka – model koji se naziva kristalna rešetka.
Na slici 4.2a prikazan je kristal kuhiwske soli (NaCl), a na slici 4.2b wen model – kristalna rešetka NaCl.
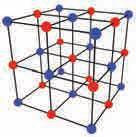
Osnovu kristalne rešetke predstavqa elementarna œelija oblika paralelopipeda, u æijim se rogqevima, ævorovima, nalaze molekuli (atomi ili joni). To je najmawi gradivni element kristala, a slagawem tih osnovnih strukturalnih jedinica duþ svake od tri dimenzije prostora dobija se kristalna rešetka.
Osnovno svojstvo svake kristalne strukture je periodiænost, koja æini ureðenost na daqinu, odnosno daqi poredak.
Grafit i dijamant su, na primer, dve kristalne forme ugqenika. Dijamant je izuzetno ævrsta supstancija. Bezbojan je kada je hemijski æist, veoma se teško lomi i slabo provodi elektriænu struju. Grafit je mek, crn i odliæan je provodnik elektriæne struje. Ove razlike izmeðu grafita i dijamanta potiæu samo od razliæitog rasporeda ugqenikovih atoma u grafitnoj (a) i dijamantskoj (b) kristalnoj rešetki (slika 4.3).





Kristalno ævrsto telo moþe biti monokristal ili polikristal. Monokristal ima pravilan oblik: ograniæen je ravnim i glatkim stranama (mnogougaonici), a ivice su pravolinijske (npr. drago kamewe na nakitu). Ævrsto telo kao celina se mnogo æešœe sastoji od ogromnog broja vrlo sitnih monokristala, koji su „srasli“ meðu sobom svojim razliæitim stranicama, pa su haotiæno rasporeðeni u telu. Takva tela se nazivaju polikristali (polikristalna tela).
Primena kristala je veoma velika u radiotehnici, optici i drugim oblastima tehnike i nauke. Na primer, kristali rubina su osnovni element u izradi rubinskog lasera. Odreðene vrste kristala kvarca koriste se za dobijawe ultrazvuænih oscilacija (talasa).
Po svojoj strukturi, amorfna ævrsta tela su bliska teænostima. Kao primer navedimo razne vrste smola, stakla i plastiæna tela. Ova ævrsta tela nemaju prostornu ureðenost. Wihova kristalna rešetka je „topqiva“.

Pod uticajem spoqašwih sila, ævrsta tela u mawoj ili veœoj meri mewaju zapreminu i oblik, deformišu se. Ako po prestanku delovawa spoqašwih sila (faktora) deformacija tela išæezava, vraœaju se u prvobitno stawe (poloþaj), onda su to elastiæna tela. Kada ostaju trajno deformisana, onda je reæ o plastiænim telima. Stepen elastiænosti i plastiænosti zavisi od prirode tela i intenziteta deformacione sile koja na wega deluje. Na primer, æelik i guma su elastiæni, a bakar i vosak uglavnom plastiæni.
Pri deformaciji tela, æestice (atomi, joni) u ævorovima kristalne rešetke meðusobno mewaju poloþaje (rastojawa). To uzajamno pomerawe æestica prati promena molekulskih privlaænih i odbojnih sila. Ono se makroskopski ogleda u postojawu neke unutrašwe sile, tzv. sile elastiænosti, koja deluje meðu æesticama ævrstog tela. Sile elastiænosti, koje se javqaju pri deformaciji tela, uvek su suprotne smeru pomerawa æestica tela.
Elastiæne deformacije tela mogu da budu veoma raznovrsne. Razlikujemo istezawe (ili sabijawe), savijawe, uvrtawe (torzija) i smicawe, ali se deformacije svode na dva osnovna oblika: istezawe i smicawe

Slika 4.4. Linearno istezawe i sabijawe tela
U praksi i tehnici najæešœe susreœemo linijska istezawa (izduþivawa) ili sabijawa. Na slici4.4. je prikazan takav oblik deformacije.

Linijsko istezawe (ili sabijawe) nastaje kada sile (sila) deluju samo duþ jednog pravca u telu (deformacije u drugim pravcima se zanemaruju). Pri linijskom istezawu mewaju se i zapremina i oblik tela: ono se izduþuje, isteþe najviše u pravcu delovawa sila. Promena duþine tela Dl u pravcu delovawa sila naziva se apsolutno istezawe (izduþewe). Od æega zavisi veliæina apsolutnog istezawa? Eksperimenti su pokazali da Dl zavisi, pre svega, od dimenzije tela, prirode (vrste) materijala i intenziteta sile koja vrši istezawe, (što je intenzitet sile veœi, i relativno istezawe je takoðe veœe), ali da zavisi i od površine popreænog preseka S normalnog na pravac delovawa sile (što je površina popreænog preseka veœa, apsolutno istezawe je mawe).
Hukov zakon istezawa, izraþava se formulom:
Uvoðewem pojmova normalni napon i relativno izduþewe, Hukov zakon moþe da se zapiše u obliku:
Ei je veliæina koja karakteriše elastiæna svojstva materijala (supstancije) i naziva se Jungov moduo istezawa. Ova veliæina iskazuje opirawe materijala elastiænoj linearnoj deformaciji (istezawu ili sabijawu). Tipiæne vrednosti ovog parametra za metale iznosi ~ 1011 N/m2
Drugi osnovni tip elastiæih deformacija je smicawe. Telo se ovde definiše po kristalnim slojevima, sliæno kao kad se karte u špilu svaka u odnosu na drugu malo smakne. Sila F koja vrši ovakvu deformaciju tangencijalna je na površ tela S i teþi da je smakne (slika 4.5). Dowa površ tela je ili priævršœena za pologu, ili na wu deluje deformaciona sila istog pravca i intenziteta, ali suprotnog smera. Hukov zakon smicawa ima oblik:
Slika 4.5. Smicawe tela
Relativno smicaweje srazmerno tangencijalnom naponu Jungov moduo smicawa Es je oko 1000 puta mawi od Jungovog modula istezawa Ei za istu supstanciju.
Ukoliko napon deformacije preðe neku (za tu supstanciju) kritiænu vrednost, telo œe se trajno deformisati, prvo plastiæno (neœe se vratiti u prvobitan poloþaj), a posle dolazi do kidawa ili drobqewa tela.
Materijali kod kojih ne postoji oblast elastiæne deformacije su plastiæni materijali, npr. vosak, glina, plastelin i druge.



1. Koja agregatna stawa supstancije postoje? Od æega zavise osobine tih agregatnih stawa?
2. Koja je priroda meðumolekulskih sila?
3. Kako se supstancija ponaša kada se zagreva? Koje je mikroskopsko objašwewe za ovaj efekat?
4. Kakav je koeficijent termiækog širewa vode u temperaturnom intervalu 0 °C – 4 °C, a kakav iznad 4 °C?
5. Ako se pri izotermskom procesu odreðenoj koliæini gasa dovodi toplota, šta se dešava sa wegovom zapreminom i gustinom?
6. Šta bi se desilo (leti/zimi) kada bi sastavi tramvajskih ili voznih šina bili zavareni?
7. Kakav je i šta uslovqava raspored molekula (atoma, jona) kod kristala?
8. Šta je kristalna rešetka i koje su joj osnovne karakteristike?
9. Šta je elementarna œelija kristala?
10. Kako nastaje polikristal? Šta je sitnozrnasta kuhiwska so?
11. Kakve su osnovne odlike amorfnih tela?
12. Koja je osnovna razlika izmeðu plastiænih i elastiænih deformacija tela?
13. Šta œe se desiti sa kristalnom rešetkom ako kristal pretrpi plastiænu deformaciju?
14. Po æemu se razlikuju normalni i tangencijalni napon?
15. Uporediti jedinice normalnog i tangencijalnog napona i Jungovih modula elastiænosti.
16. Širewe tanke ploæe zagrevawem opisuje se poveœawem wene površine: DS=S–S0= S0 bDT, gde je S – wena površina na temperaturi t [°C], a S0 – na 0 °C, pa je DT = t [°C] i b je termiæki koeficijent površinskog širewa. Da li se moþe zakquæiti da je veza sa koeficijentom linearnog širewa sledeœa: b 2a? ≈


Po nekim svojstvima, teænosti su sliæne gasovima, dok su po drugim sliæne ævrstim telima. Sliæno gasovima, teænosti takoðe istiskuju tela koja se u wima nalaze (potisak), a pritisak se prenosi podjednako na sve strane. Dok gasovi uvek ispuwavaju ceo raspoloþivi prostor i nemaju stalan sopstveni oblik niti stalnu zapreminu, teænosti, sliæno ævrstim telima, imaju stalnu sopstvenu zapreminu, ali nemaju stalan oblik.

Praœewe proticawa teænosti kroz cevi (na primer, pomoœu mastila ili drugih obojenih supstancija unesenih u teænost) pokazuje da se svi delovi teænosti ne kreœu istom brzinom. Najveœu brzinu imaju delovi teænosti duþ ose cevi, a najmawu delovi uz zidove cevi. Raspored brzina na preseku cevi, normalnom na pravac proticawa teænosti, prikazan je na slici 4.6. Teænost se kroz cev ne kreœe kao celina, veœ u slojevima koji klize jedan po drugome razliæitim brzinama. Pri proticawu teænosti kao da dolazi do wenog „raslojavawa“. Sliæno se dešava i pri kretawu, na primer, ravne daske, tankera ili splava po mirnom jezeru. Kada se telo pokrene, poæne i voda da se kreœe, ali ne kao celina, veœ po delovima (slojevima) koji imaju razliæite brzine. Poveœawem dubine od plovnog objekta brzina slojeva teænosti se smawuje (slika 4.7).
U teænostima se javqaju i sile koje se suprotstavqaju kretawu tela kroz teænosti.
Nabrojane æiwenice i pojave objašwavaju se kao posledica postojawa sile unutrašweg trewa u teænostima, viskoznost.
Sila viskoznosti usporava proticawe teænosti i kretawe tela kroz teænost.
Slika 4.6. Raspored brzina pojedinih slojeva teænosti na popreænom preseku cevi kruþnog oblika
Slika 4.7. Poveœawem dubine, brzina slojeva teænosti se smawuje

WUTNOVZAKONVISKOZNOSTI
Viskoznost – unutrašwi otpor teænosti se moþe definisati preko sile viskoznosti ukoliko je proticawe te teænosti laminarno. To znaæi da slojevi teænosti „klize“ jedan po drugome, ali tako da teænost iz jednog sloja ne prelazi u drugi.



Slika 4.8. Raspored brzina slojeva teænosti na normalnom popreænom preseku izmeðu pokretne i nepokretne ravne ploæe
Sila viskoznog trewa zavisi, pre svega, od vrste teænosti. Na primer, dok voda kod koje je ta sila relativno slaba, vrlo brzo istekne iz neke posude (recimo za nekoliko sekundi), ista koliæina uqa isticaœe iz iste posude veoma sporo (za nekoliko minuta).
Razmotriœemo teænost koja se nalazi izmeðu dve ravne paralelne i jednake ploæe (sl. 4.8).
Jedna od wih (A) kreœe se brzinom v ® , dok je druga (B) nepokretna. Vrlo tanak sloj teænosti, koji je u neposrednom dodiru sa ploæom (pokretnom, kao i nepokretnom), „prilepqen“ je za wenu površinu. Naime, teænosti dobro priawaju za ævrsta tela sa kojima su u dodiru (zidovi posude, zidovi cevi kroz koje protiæu, površina tela urowenih u teænost) pod uticajem molekulskih sila izmeðu razliæitih supstancija. Zbog toga nema klizawa izmeðu ævrstog tela i teænosti, pa se graniæni –dodirni sloj teænosti kreœe istom brzinom v kao i ploæa A. Sloj teænosti uz nepokretnu ploæu B takoðe je nepokretan. Ostali slojevi teænosti paralelni ploæama, kreœu se brzinama koje su srazmerne udaqenosti sloja od nepokretne ploæe.
Intenzitet viskozne sile (Fη) koja deluje na sloj teænosti uz pokretnu ploæu (a time posredno i za samu ploæu A) srazmeran je intenzitetu brzine v toga sloja (odnosno brzine ploæe), veliæini površine ploæe (S), a obrnuto je srazmeran rastojawu izmeðu ploæa (d):
d η η =
Ova formula predstavqa Wutnov zakon viskoznosti. Sila viskoznosti deluje u pravcu kretawa teænosti, a suprotnog je smera od brzine v ® . Na ovaj naæin sila viskoznosti prenosi se od jednog sloja na drugi, od nepokretne do pokretne ploæe. Stoga na svaki sloj deluju dve sile: (spoqašwa) i (unutrašwa) istog pravca i intenziteta, a suprotnih smerova. Rezultanta sila na svaki sloj je jednaka nuli, te se oni kreœu konstantnim brzinama. Slojevi teænosti deluju jedni na druge silom unutrašweg trewa (viskoznosti). Znaæi, ova sila karakteriše uzajamno delovawe unutar teænosti, a ne izmeðu ævrstog tela i teænosti.
Koeficijent viskoznosti je karakteristika svake teænosti i smawuje se poveœawem temperature. Jedinica za koeficijent viskoznosti je
Viskoznost je posledica meðumolekulskih sila privlaæewa. Pod dejstvom tih sila molekuli iz brþeg sloja „vuku“ molekule iz sporijeg sloja, odnosno, posredstvom tih sila predaju se odgovarajuœi impulsi molekulima sporijih slojeva koje im spoqašwa sila stalno nadoknaðuje. kgPas. sm =


STOKSOVZAKONVISKOZNOSTI

Sila viskoznosti teænosti utiæe na kretawe tela koja se u woj nalaze (podmornica, ronilac). Naime, teænost pruþa otpor takvom kretawu, a taj otpor potiæe od viskoznosti. Tanak sloj teænosti „prilepqen“ za tela kreœe se zajedno sa telom i istom brzinom kao telo. Usled toga se pokreœu i ostali slojevi teænosti. Pri malim brzinama, ovi slojevi se kreœu laminarno, i tada je intenzitet sile otpora Fv srazmeran brzini tela v: Fv = kv, što je eksperimentalno utvrðeno. Veliæina k zavisi od koeficijenta viskoznosti teænosti (h), zatim od dimenzija i oblika tela.
Za telo sfernog oblika k = 6phr, gde je r polupreænik sfere tela, stoga je intenzitet sile viskoznosti kojom teænost deluje na usporavawe kretawa tela: Fv = 6phrv.
Ova formula predstavqa Stoksov zakon viskoznosti. Sila otpora koju teænost pruþa kretawu sfernog tela usled viskoznosti srazmerna je polupreæniku tela i wegovoj brzini. Ova sila ima pravac brzine, ali je suprotnog smera.

U unutrašwosti teænosti molekuli su okruþeni sa svih strana susednim molekulima. Rezultanta privlaænih meðumolekulskih sila koje deluju na takav molekul (A) je stoga jednaka nuli. Meðutim, molekuli koji se nalaze u površinskom sloju teænosti izloþeni su molekulskim silama praktiæno samo sa jedne strane (slika 4.9).
Vazduh (gas)
R=0 B A
R¹0
Teænost
Molekuli (B) u površinskom sloju teænosti izloþeni su delovawu rezultante meðumolekulskih sila usmerene ka unutrašwosti teænosti. Zbog toga se energija molekula mewa kada se on iz unutrašwosti premesti na površinu. Naime, da bi se to pomerawe izvršilo, potrebno je raskinuti pribliþno polovinu veza izmeðu molekula i wegovih najbliþih suseda, a raskidawe svake veze zahteva utrošak odreðene energije. Pošto je molekul u površinskom sloju u proseku upola mawe vezan nego kada je u unutrašwosti, wegova energija je pribliþno dva puta veœa.
Slika 4.9. Molekulske sile upovršinskom sloju iunutrašwosti teænosti
Molekuli površinskog sloja stoga raspolaþu odgovarajuœom dodatnom potencijalnom energijom (površinska energija). Smawewem površine teænosti smawuje se površinska energija i obratno.


Da bi se poveœala površina teænosti, mora se, znaæi, izvršiti odreðeni rad. Koliki œe taj rad biti, zavisi pre svega od vrste teænosti, što se opisuje veliæinom koja se naziva koeficijent površinskog napona (g). Dakle:
A = g×DS ,
gde je DS poveœawe površine teænosti, a A rad koji se pri tome izvrši. Ovaj rad vrši sila površinskog napona F, koja deluje po duþini l izmeðu gorwe površi teænosti i suda u kojem se ona nalazi, tako da je:
F= gl.
Koeficijent površinskog napona izraþava se J/m2, ili wutnima po metru N/m i on je karakteristika date teænosti.
Poveœawu potencijalne energije molekula površinskog sloja pri uveœawu površi teænosti suprotstavqaju se molekulske sile teænosti. Zbog toga se gorwe površi teænosti ponašaju kao rastegnuta opna (membrana) koja teþi da smawi svoju površinu, pruþa otpor wenom poveœawu.
Pojava da se teænosti opiru poveœawu slobodne površi,odnosno teþe da je smawe,naziva se površinski napon.
Mehuri sapunice koji se izduvavaju iz cevæice ponašaju se sliæno naduvanim gumenim balonima: kada se cevæica odvoji od usta, mehur se smawuje. Metalni novæiœ ili igla paþqivo stavqeni na slobodnu vodenu površ neœe potonuti: površinski sloj vode se ugiba, ali ga teþina igle (novæiœa) ne moþe raskinuti. U tim pojavama dolaze do izraþaja sile površinskog napona, koje su posledica meðumolekulskih sila koje deluju na molekule u površinskom sloju teænosti.
Ako se teænost nalazi u sudu u poqu Zemqine teþe, popuniœe deo suda svojom zapreminom, a gorwa površ œe mu biti ravna (najmawe površine). Ako se, meðutim, paþqivo posmatra slobodna površ vode u æaši, primetiœe se da se ona „propiwe“ da pokvasi staklene zidove æaše. Za ovakvo ponašawe su odgovorne sile adhezije (izmeðu razliæitih molekula) i kohezije (izmeðu molekula iste vrste). U sluæaju voda – staklo, intenzivnije su athezione sile.
Ova pojava dolazi do izraþaja kod kapilara (slika 4.10). Kapilare su cevæice malog popreænog preseka (preænika ispod 1 mm). Ako se kapilara uroni u teænost koja kvasi wene zidove, teænost œe se u kapilari popeti iznad nivoa koji je u sudu gde je kapilara urowena. To je pojava koja odstupa od pravila spojenih sudova. Kapilarne pojave su æeste u prirodi. Ovim mehanizmom se vrši transport hranqivih sastojaka zajedno sa vodom od korena do najudaqenijih listova biqaka. Kapilarno se transportuju i krv i limfa kroz æoveæiji organizam.
Slika 4.10. Kvašewe zidova suda teænosti i kapilarnost


Primer 1. Staklena kuglica preænika 2 mm pada kroz teænost konstantnom brzinom v = 0,2 ms–1. Koliki je koeficijent viskoznosti te teænosti? Gustina stakla je 2400 kg/m3, a gustina teænosti 1000 kg/m3 .
Podaci: R = 2 mm, v = 0,2 m/s, rs = 2400 kg/m3 , rt = 1000 kg/m3; h = ?
Rešewe. Na kuglicu koja pada kroz teænost, osim sile viskoznosti intenziteta Fv = 6phrv, deluju i spoqašwe sile: Zemqina teþa Fg = r×V ×g i sila
potiska teænosti Fp = rtVg, gde je V zapremina kuglice. Pošto se kuglica kreœe stalnom brzinom, zbir tih sila je jednak nuli. Sila potiska i sila viskoznosti deluju u suprotnom smeru od smera Zemqine teþe, pa je:
Fg = Fp +Fv, odnosno
rsVg = rtVg + 6phrv.
Odavde sledi:
• Pod uticajem spoqašwe sile, mewaju se oblik i dimenzije ævrstih tela, tj. nastaje wihova deformacija. Ako deformacija nestaje (išæezava) nakon prestanka delovawa sile, onda je reæ o elastiænim telima, a ako je deformacija trajna (ostaje i posle prestanka delovawa sile) – o plastiænim telima.
Pri relativno mawim deformacijama za elastiæna tela vaþe Hukovi zakoni:
gde su E – moduli elastiænosti (Jungovi moduli koji zavise od vrste tela).
Modul elastiænosti Ei seodnosi na istezawe a Es na smicawe tela
• U procesu zagrevawa, ævrsta tela uveœavaju dimenzije, tj. ona se šire, a pri sniþewu temperature ona se skupqaju. Ova promena dimenzija je srazmerna promeni temperature.
• Po nekim svojstvima teænosti su sliæne gasovima, a po drugim ævrstim telima. Sliæno gasovima, teænosti takoðe istiskuju potopqena tela, a pritisak se podjednako prenosi u svim pravcima. Gasovi ispuwavaju ceo dostupni prostor, pa nemaju stalan oblik i zapreminu. Teænosti, sliæno ævrstim telima imaju stalnu zapreminu a oblik im je kao i oblik suda u kome se nalaze. Po stepenu stišqivosti, teænosti su znatno bliþe ævrstim telima nego gasovima.



• Površina teænosti se ponaša kao zategnuta membrana usled delovawa sile površinskog napona. Kapilarne pojave se ispoqavaju u odstupawu nivoa teænosti u kapilarnim cevima od zakona spojenih sudova.
• Unutrašwe trewe u teænostima naziva se viskoznost.
Intenzitet Wutnove sile viskoznosti se izraþava formulom:
FSv d . = hh
Intenzitet sile otpora kretawu sfernog tela kroz teænost izraþava se Stoksovim zakonom:
Fv = 6phrv


1. Po æemu su teænosti sliæne gasovima, a po æemu ævrstim telima?
2. Da li se pri proticawu teænosti kroz cevi svi weni delovi kreœu istom brzinom?
3. Šta je laminarno proticawe?
4. Da li sila viskoznosti deluje neposredno na telo koje se kreœe u teænosti?
5. Pri kojim uslovima vaþi Wutnov zakon viskoznosti?
6. Šta je površinski napon i kako se on ispoqava?
7. Zbog æega molekuli na površini teænosti raspolaþu dodatnom potencijalnom energijom?
8. Kakav je oblik slobodne površi teænosti koja kvasi zidove suda?
9. Zašto se kap vode „raširi“ po staklenoj površi?
10. Kako deluju sila površinskog napona i teþina stuba vode u staklenoj kapilari?

Obiæno iskustvo i ogledi pokazuju da sve supstancije promenom temperature mogu mewati agregatna stawa. Na primer, ævrsta tela se tope pri zagrevawu; daqim povišewem temperature ona isparavaju. Hlaðewe tela dovodi do obrnutih procesa – pretvarawe pare u teænost i teænosti u ævrstu supstanciju. Moguœi su sluæajevi kada se pri povišewu temperature ævrsta tela neposredno pretvaraju (prelaze) u gasovito stawe (paru). Takav oblik promene agregatnog stawa naziva se sublimacija
Posebno stawe istorodne supstancije, koje karakterišu odreðena fiziæka svojstva (raspored molekula, atoma, gustina i dr.) koja se odrþavaju u odreðenom domenu vrednosti pritiska, temperature i drugih veliæina, naziva se faza. Svaka supstancija ima tri osnovna agregatna stawa – tri osnovne faze: ævrsto, teæno i gasovito
Prelazak supstancije iz jednog agregatnog stawa u drugo,odnosno iz jedne u drugu fazu,naziva se fazni prelaz.

Prelazak supstancije iz jedne faze u drugu, pri zadatom pritisku, vrši se uglavnom uvek na strogo odreðenoj temperaturi. Na primer, pri atmosferskom pritisku led poæiwe da se topi na 0°C i pri daqem zagrevawu temperatura ostaje neizmewena, dok se sav led ne pretvori u vodu. U toku tog procesa led i voda postoje istovremeno, iako se nalaze u neposrednom kontaktu.
U odsustvu spoqašwih uticaja (dovoðewa toplote, na primer) na temperaturi faznog prelaza dve faze zajedno postoje (koegzistiraju) neograniæeno dugo. Ali, pri višim ili niþim temperaturama od temperature faznog prelaza (na datom pritisku), stabilno moþe postojati samo jedna od tih faza. Na primer, na temperaturama niþim od 0 °C, pri normalnom atmosferskom pritisku, moþe postojati samo led, a na višim od 0 °C samo voda.
Pod ævrstim stawem supstancije podrazumeva se samo kristalno stawe. Amorfno ævrsto telo se pri zagrevawu pretvara u teænost putem postepenog omekšavawa, bez skokovitog prelaza. Zato amorfno ævrsto stawe ne predstavqa posebnu fazu supstancije, veœ specifiænu meðufazu.

Prelazak kristalnog tela u teæno stawe zagrevawem naziva se topqewe. Obrnut prelazak supstancije – teænog stawa u ævrsto (kristalno), zove se oævršœavawe. Temperatura na kojoj se vrše ovi fazni prelazi zove se temperatura (taæka) topqewa, odno-sno temperatura (taæka) oævršœavawa ili kristalizacije.


Taæke topqewa i kristalizacije za datu supstanciju i pri odreðenim uslovima se poklapaju. Temperature (taæke) topqewa za neke supstancije, na pritisku od 105 Pa date su u tabeli 4.1.
SUPSTANCIJA
Þiva
Voda (led)
TEMPERATURA
TOPQEWA [°C]
SPECIFIÆNA KOLIÆINA
TOPLOTE TOPQEWA kJ kg ¯ ¡° ¡° ¢±
Tabela 4.1. Taæka topqewa i specifiæna koliæina toplote topqewa nekih supstancija
Koliæina toplote koju je potrebno da primi jedan kilogram supstancije na temperaturi topqewa,da bi iz ævrstog prešla u teæno stawe,naziva se specifiæna toplota topqewa.
Oævršœavawe ili kristalizacija je obrnut proces od topqewa tela. To je prelazak tela iz teænog u ævrsto stawe.
Pri zagrevawu tela, toplotno kretawe molekula (atoma) postaje sve intenzivnije. To uslovqava uveœawa rastojawa meðu æesticama koje obrazuju kristalnu rešetku, što uzrokuje weno rušewe, kidawe meðumolekularnih veza. Tada poæiwe proces topqewa, koji se pri datim uslovima odvija na strogo odreðenoj temperaturi, koja se ne mewa sve dok se proces ne završi, tj. dok sva data supstancija iz ævrstog ne preðe u teæno stawe.
U faznom prelazu kristal–teænost, kao i prilikom drugih faznih prelaza, dolazi do razmene unutrašwe energije izmeðu tela i spoqašwe sredine. U procesu topqewa, telu se dovodi odreðena koliæina toplote spoqa, a pri kristalizaciji ona se otpušta i predaje spoqašwim telima.
kriva topqewa i oævršœavawa
kriva isparavawa i kondenzacije
kriva sublimacije
Slika 4.11. Dijagrami faznih prelazaka
Temperatura topqewa zavisi od pritiska. Prelazak iz kristalnog u taæno stawe dešava se pri potpuno odreðenim uslovima, okarakterisanim taænim vrednostima pritiska i temperature. Skupu tih vrednosti odgovara kriva iznad trojne taæke (TT) na dijagramu (p, T), koja se naziva i linija topqewa ili kristalizacije (slika 4.11).
Taæka u kojoj se seku kriva isparavawa (kondenzacije), kriva topqewa (oævršœavawa) i kriva sublimacije na p – T dijagramu zove se trojna taæka.


Iznad slobodne (gorwe) površi svake teænosti, zavisno od wene prirode i temperature, obrazuje se para – teænost isparava.
Isparavawe je prelazak supstancije iz teænog u gasovito stawe (paru).
Što je temperatura viša, to je isparavawe teænosti intenzivnije. Meðutim, na istoj temperaturi teænosti razliæito isparavaju. Npr. etar ili benzin znatno brþe isparavaju nego voda i jestivo uqe. Etar ili benzin brþe isparavaju od vode (slika 4.12), zato što izmeðu wihovih molekula deluju sile maweg intenziteta nego izmeðu molekula vode.
Najintenzivniji prelaz u gasovito stawe teænost ima pri kquæawu. Tada molekuli iz cele zapremine teænosti napuštaju teænost. To se dešava na taæno odreðenoj temperaturi – taæki kquæawa (slika 4.13) i predstavqa fazni prelaz teænost – gas (sl. 4.11, izmeðu trojne TT i kritiæne taæke KT).
Koliæina toplote koju je potrebno dovesti jednom kilogramu teænosti da bi isparila pri konstantnoj temperaturi naziva se specifiæna (latentna) top-lota isparavawa.
Specifiæna toplota isparavawa i taæka kquæawa za neke supstancije date su u tabeli 4.2.
Slika 4.12. Etar brþe isparava od vode
Temperatura ( ˚ C) teænost para kquæawe teænost i para kraj isparavawa poæetak zagrevawa poæetak kquæawa vreme A BC D temperatura kquæawa
(ili Q)
Taæka (temperatura) kquæawa zavisi od pritiska. Voda moþe da kquæa i na 50 °C (pri sniþenom pritisku) i pri 120 °C (pri povišenom – iznad normalnog atmosferskog pritiska). Zato postoji kriva isparavawa, a ne samo jedna taæka.
Slika 4.13. Prelazak teænost–para (isparavawe)
Molekuli pare, kao i svakog gasa, vrše haotiæno (neureðeno) toplotno kretawe. Jedan deo od tih molekula se putem sluæajnih sudara vraœa u teænost iz koje je prethodno „ispario“. Molekuli koji su se vratili ponovo postaju molekuli teænosti. Istovremeno sa isparavawem, odvija se i obrnut proces –povratak molekula pare u teænost. Ta pojava se naziva kondenzacija pare, a prelazak molekula gasa direktno u ævrsto stawe – sublimacija.
Kondenzacija je prelazak supstancije iz gasnog stawa (pare) u teæno stawe.
Specifiæna toplota kondenzacije jednaka je specifiænoj toploti isparavawa. Naravno, odnosi se na istu temperaturu.

SUPSTANCIJA

TEMPERATURE KQUÆAWA [K]
2.
SPECIFIÆNA TOPLOTA ISPARAVAWA q MJ kg ¯ ¡° ¢±
Etar 307 0,35
Etil-alkohol 353 0,85
Þiva 630 0,27
Voda 373 2,26
Gvoþðe 3323 6,31
Tabela 4.2. Taæka kquæawa i specifiæna toplota isparavawa nekih supstancija
Koliæina toplote,potrebna za pretvarawe jedinice mase supstancije iz jednog u drugo agregatno stawe na temperaturi faznog prelaza (taæki topqewa ili taæki kquæawa) i normalnom pritisku,naziva se specifiæna (latentna) toplota faznog prelaza.
Izraz za koliæinu toplote konkretnog faznog prelaza nekog tela ima oblik
Qt = lm , tj. Qi=qm,
gde su m masa tela, a q i l – specifiæne toplote faznih prelaza. Na primer, specifiæna toplota faznog prelaza topqewa leda pri normalnom pritisku je l =3,35105 J/kg, a specifiæna toplota isparavawa vode, takoðe pri normalnom pritisku, iznosi q = 2,26 106 J/kg.
Primer 2. Led mase 1 kg i temperature –1 0 °C zagreva se toplotnim izvorom konstantne snage 330 W sve dok voda nastala iz leda potpuno ne ispari. Kolika je ukupna koliæina toplote potrebna za to pretvarawe leda u paru i koliko vremena traje proces? Nacrtati grafik koji pokazuje zavisnost temperature odvremena zagrevawa. Specifiæni toplotni kapacitet leda iznosi c 1 = 2,1 ×10 3 Jkg –1 K –1 , specifiæn i toplotni kapacitet vode c2 = 4,19×103 Jkg–1 K–1 , specifiæna toplota topqewa leda li = 3,35×105 J kg–1 i specifiæna toplota isparavawa vode qi = 2,26×106 Jkg–1 . Podaci: m =1 kg , t 1 = –1 0 °C , P =330 W , c 1 = 2,1 10 3 Jkg –1 K –1 , c2 = 4,19×103 Jkg–1 K–1 , qt = 3,35×105 Jkg–1 , li = 2,26×106 Jkg–1; Q = ?; t = ?
Rešewe.
Za topqewe leda na 0 °C potrebno je: Q2 = mqt = 335 kJ Q m . = λ
Za zagrevawe leda od t1 = –10 °C do t2 =0 °C potrebna je koliæina toplote
Q1 = mc1 (t2 – t1) = 21 kJ


Za zagrevawe dobijene vode (od 0 °C do t3 = 100 °C): Q3 = mc2 (t3 – t2) = 419 kJ
Konaæno, za isparavawe te vode Q4 = mli = 2260 kJ. Ukupna koliæina toplote je: Q = Q1 + Q2 + Q3 + Q4 = 3,035 MJ.
Potrebno vreme za odvijawe transformacije leda sa –10 °C u paru iznosi
odnosno, 2 sata, 33 min i 17 s. Od toga : t1 =1 min i 3,64 s, t2 =16 min i 55,15 s, t3 =21 min i 9,70 s i t4 =1h, 54 min i 8,49 s. Na osnovu datih i izraæunatih podataka moþe se nacrtati grafik zavisnosti temperature od vremena zagrevawa.
vreme)


• Agregatno stawe supstancije uslovqavaju molekulske sile. Kod ævrstog stawa molekulske sile su najveœeg intenziteta, kod teænog stawa maweg intenziteta, a kod gasova najmaweg intenziteta. Agregatna stawa, wihova svojstva i odgovarajuœe pojave posledice su molekulskih sila i ponašawa ogromnog broja molekula (atoma, jona) koji ulaze u sastav tela u tim stawima.
• Prelazak kristalnog tela u teæno stawe zagrevawem naziva se topqewe. Obrnut prelazak supstancije iz teænog u ævrsto (kristalno) stawe sniþewem temperature je oævršœavawe (kristalizacija). Temperatura na kojoj se vrše ovi prelazi zove se temperatura (taæka) topqewa , odnosno temperatura (taæka) oævršœavawa ili kristalizacije.
Koliæina toplote koju treba da primi jedan kilogram supstancije na temperaturi topqewa, da bi iz ævrstog prešla u teæno stawe, naziva se specifiæna (latentna) koliæina toplote topqewa. Specifiæna koliæina toplote topqewa jednaka je specifiænoj koliæini toplote oævršœavawa (kristalizacije), samo što u prvom sluæaju telo prima, a u drugom oslobaða odreðenu koliæinu toplote.
• Iznad površine svake teænosti, zavisno od wene prirode i temperature, obrazuje se para.
Isparavawe je prelazak supstancije iz teænog u gasovito stawe (paru).
Koliæina toplote koju je potrebno dovesti jednom kilogramu teænosti da bi isparila pri konstantnoj temperaturi,naziva se specifiæna (latentna) koliæina toplote isparavawa. Kondenzacija je prelazak supstancije iz gasnog stawa (pare) u teæno stawe.
Specifiæna koliæina toplote kondenzacije jednaka je specifiænoj koliæini toplote isparavawa (naravno, pri istoj temperaturi).
• Kada se teænost zagreje do odreðene temperature, pri datom pritisku,nastaje proces naglog isparavawa, i to ne samo po površini teænosti, veœ i u æitavoj wenoj zapremini. Ova pojava naziva se kquæawe teænosti. Poveœawem spoqašweg pritiska povišava se temperatura kquæawa i obratno.


1. Koje osnovne veliæine (parametri) karakterišu fazno stawe svake supstancije?
2. Koliko agregatnih stawa ima supstancija i koje su wihove osnovne karakteristike?
3. Svakoj supstanciji odgovara samo jedno teæno i samo jedno gasovito stawe. Da li to vaþi i za ævrsto stawe?
4. Ako se telu dovodi neka koliæina toplote, da li œe se uvek povišavati wegova temperatura?
5. Koji uslovi treba da budu ispuweni da bi se ostvario proces kquæawa teænosti? Kako taæka kquæawa teænosti zavisi od spoqašweg pritiska?


Osnove elektrostatike upoznali smo još u osnovnoj školi. Veœ tada smo se za opisivawe i objašwavawe elektriænih pojava pozivali na atomsku strukturu supstancije. Znamo da se atom sastoji od jezgra i omotaæa (slika 5.1). Atomsko jezgro ima sloþenu strukturu. Ono sadrþi dve vrste æestica pribliþno istih masa – pozitivno naelektrisane protone i neutralne neutrone Omotaæ atoma æine negativno naelektrisani elektroni, koji se kreœu oko jezgra sliæno kao planete oko Sunca. Zato se ovaj model (sa kojim smo se upoznali u osnovnoj školi) naziva planetarni model atoma. Koliæine naelektrisawa elektrona i protona su jednake, ali suprotnog predznaka. Obeleþavaju se sa e; elektron ima naelektrisawe –e, a proton +e. To su elementarna naelektrisawa (najmawa nedeqiva koliæina naelektrisawa).


Narušavawe ravnoteþe izmeðu broja elektrona i broja protona u nekom telu uslovqava wegova elektriæna svojstva.
Ako telo sadrþi veœi broj elektrona u odnosu na wihov broj u telu kada je ono elektriæno neutralno, onda je to telo negativno naelektrisano. Kod pozitivno naelektrisanih tela postoji nedostatak („mawak“) elektrona u odnosu na wihov broj u elektriæno neutralnom stawu.
U ævrstim telima, što je naroæito izraþeno kod metala, postoje takozvani slobodni elektroni (slika 5.2). To su elektroni koji su se nalazili na periferiji omotaæa (najudaqeniji od jezgra). Wihova uzajamna veza s jezgrom veoma je slaba i oni se lako oslobaðaju. To se dešava onda kada se formira kristalna rešetka (npr. pri oævršœavawu). Pošto periferni elektroni uæestvuju u organizaciji kristalnih veza, najæešœe ih ima više nego što je potrebno za formirawe veza. Taj „višak “ elektrona æini slobodne elektrone koji mogu da se kreœu kroz kristal. Ovi elektroni uglavnom i uslovqavaju elektriæna svojstva tela.

Naelektrisanost tela se moþe jednostavno konstatovati pomoœu elektroskopa. Na slici5.3a) prikazan je elektroskop sa listiœima (ureðaj koji smo upoznali u osnovnoj školi). Ako se kuglica elektroskopa dodirne nekim naelektrisanim telom, naelektrisawe preko šipke dolazi i na listiœe (ili kazaqku). Oni se tada razmaknu usled uzajamnog odbijawa wihovog istoimenog naelektrisawa. Ako elektroskop ima skalu pomoœu koje se meri veliæina zakretawa, on moþe da meri koliæinu naelektrisawa tela. Elektroskop sa skalom zove se elektrometar (slika 5.3b).
S makroskopskog (fenomenološkog) stanovišta, koliæina naelektrisawa moþe da se uporedi (u smislu analogije) s koliæinom fluida. Na osnovu toga se moþe dati odgovarajuœa formulacija:
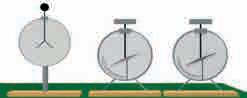
Koliæina naelektrisawa je kvantitativna mera za naelektrisawe tela. Sa gledišta atomske strukture supstancije, odnosno elektriciteta, definicija ove fiziæke veliæine glasi:
Koliæina naelektrisawa predstavqa celobrojni umnoþak elementarne koliæine naelektrisawa: q = ne, gde je q koliæina naelektrisawa (pozitivne ili negativne vrednosti), e – elementarna koliæina naelektrisawa, a n je ceo broj. Ako je reæ o negativnom naelektrisawu, onda se broj n odnosi na „višak“ elektrona u odnosu na wihov broj u elektriæno neutralnom stawu tela. Kod pozitivne koliæine naelektrisawa, broj n odnosi se na „mawak“ elektrona u odnosu na wihov broj u telu kada se ono nalazi u neutralnom stawu.
Jedinica koliæine naelektrisawa (elektriciteta) je kulon. Obeleþava se sa C i iznosi
C=6,22·1018 e ,
tj. koliæina naelektrisawa od jednog kulona sadrþi 6,22·1018 elementarnih naelektrisawa jedne iste vrste.
Prema tome, apsolutna vrednost koliæine naelektrisawa jednog elektrona ili protona, izraþena u kulonima, iznosi
e =1,602·10–19C.


Da bismo potpunije prouæili elektriæna svojstva tela (æestica) i elektriænih pojava, neophodno je naœi odgovarajuœe kvantitativne zakonitosti u kojima se povezuju odreðene fiziæke veliæine.

Coulomb Charles (1736–1806)
KULON ŠARL, francuski fiziæar i vojni inþewer. Prouæavao je elektricitet, magnetizam i neke delove klasiæne mehanike.
Na osnovu eksperimenta, preciznim merewem pomoœu svoje torzione vage, ustanovio je osnovni zakon elektrostatike (1775), nazvan Kulonov zakon. Prouæavao je uzajamno delovawe magneta, odnosno magnetnih polova i utvrdio da se, analogno (formalno) zakonu koji definiše uzajamno delovawe taækastih naelektrisanih tela, sve isto moþe primeniti i na uzajamno delovawe taækastih magnetnih polova.
Po znaæaju, Kulonov zakon u elektrostatici moþe da se uporedi sa Wutnovim zakonom gravitacije.
U Kulonovu æast, jedinica koliæine naelektrisawa je dobila naziv kulon (C).
Uzajamno delovawe naelektrisanih tela definiše se preko zakona elektriænog delovawa izmeðu æestica, æije su dimenzije zanemarqive u odnosu na meðusobna rastojawa (taækasta tela), pod uslovom da se te æestice nalaze u stawu relativnog mirovawa.
Intenzitet sile izmeðu dva naelektrisana taækasta tela u vakuumu srazmeran je proizvodu wihovih koliæina naelektrisawa,a obrnuto srazmeran kvadratu meðusobnog rastojawa:

gde je e0 – dielektriæna propustqivost (permitivnost) vakuuma, æija je brojna vrednost e0=8,85·10–12C2/Nm2, a r – rastojawe izmeðu naelektrisanih æestica. Koliæine naelektrisawa tela su oznaæene sa q1 i q2.

Sila je privlaæna ako su naelektrisawa tela (æestica) raznoimena (jedno pozitivno, a drugo negativno, slika 5.4a) i odbojna ako su naelektrisawa istoimena (oba pozitivna ili oba negativna, slika 5.4b). To je principijelna razlika izmeðu elektriænih i gravitacionih sila, koje su uvek privlaænog karaktera.
Za razliku od gravitacionih sila, elektriæne sile jako zavise i od svojstva sredine u kojoj se nalaze naelektrisana tela. Ako se nalaze u nekoj supstancionoj sredini, onda je intenzitet sile wihovog uzajamnog delovawa uvek mawi od intenziteta sile kojom data tela uzajamno deluju u vazduhu (vakuumu). Odnos intenziteta ovih sila naziva se relativna dielektriæna propustqivost (relativna permitivnost) i karakteristika je vrste supstancije (sredine, tabela 5.1). Dakle, tako da zakon uzajamnog delovawa taækastih naelektrisawa kada se nalaze u nekoj supstancionoj sredini ima sledeœi oblik:
5.4. Kulonov zakon
Elektriæna sila izmeðu naelektrisanih tela (æestica), na primer izmeðu protona i elektrona, mnogo je veœeg intenziteta od intenziteta gravitacione sile izmeðu tih æestica (oko 1039 puta, slika 5.5). Fqq r 12 er0 2 1 4; εεε
U tabeli 5.1. su date vrednosti za relativnu dielektriænu propustqivost nekih supstancija pri dnevnim temperaturama.
Supstancija er Supstancija er Supstancija er
Vazduh 1,0006 Parafin 2,1 Ebonit 2,5
Sumpor 4 Liskun 6–7 Petrolej 2,0
Vosak 7,8 Porcelan 5,7–6,3 Voda 80,4
Vodonik 1,0002 Staklo 4–7 Etanol 24,3
Helijum 1,00007 Kuhiwska so 5,6 Metanol 33,6
Tabela 5.1. Relativna permitivnost supstancija
Slika 5.5. Meðudelovawe protona i elektrona Fe Fe r + q1 q2


Elektriæno poqe karakteriše sila kojom naelektrisano telo koje „proizvodi“ poqe deluje na druga naelektrisana tela.
Elektriæno poqe se geometrijski prikazuje (predstavqa) linijama sile. Linije sile odreðuju pravac i smer kretawa pozitivno naelektrisane æestice u elektriænom poqu. Gustina linija sila odgovara koliæini, a wihov smer vrsti naelektrisawa tela „izvora“ poqa (slika 5.6).
+q –2 q +
Slika 5.6. Linije sile elektriænog poqa pozitivnog i negativnog tela
Elektriæno poqe, na sliæan naæin kao i gravitaciono, karakterišu fiziæke veliæine: jaæina elektriænog poqa,potencijal elektriænog poqa i odgovarajuœa energija.

Za opisivawe dejstva elektriænog poqa uvedena je fiziæka veliæina – jaæina elektriænog poqa.Fiziæka veliæina koja je brojno jednaka koliæniku elektriæne sile koja u datoj taæki deluje na taækasto naelektrisawe i koliæine naelektrisawa tog taækastog naelektrisawa,naziva se jaæina elektriænog poqa.
Prema tome, ako je ® Fe sila kojom elektriæno poqe deluje na taækasto naelektrisawe q, onda je jaæina elektriænog poqa na mestu gde se nalazi to naelektrisawe:
Jaæina elektriænog poqa je vektorska veliæina. Wen intenzitet u nekoj taæki prostora brojno je jednak intenzitetu elektriæne sile koja u toj taæki deluje na jedinicu pozitivnog naelektrisawa, a pravac i smer se poklapaju sa pravcem i smerom elektriæne sile ® Fe. F E q e =


Jaæina elektriænog poqa objektivno karakteriše elektriæno poqe u datoj taæki prostora. Ta karakteristika poqa postoji nezavisno od toga da li u toj taæki poqa postoji ili ne postoji neko naelektrisano telo.
Jaæina elektriænog poqa ima isti smer i pravac kao i elektriæna sila, koja bi u datoj taæki delovala na pozitivno naelektrisawe.
Smer linija elektriænih sila poklapa se sa smerom jaæine elektriænog poqa. Na rastojawu r od taækastog naelektrisawa q intenzitet jaæine elektriænog poqa biœe:
i izraþava se u
Ako je q – pozitivno naelektrisawe, smer vektora jaæine wegovog poqa je „od naelektrisawa“, a ako je q – negativno, onda je „ka naelektrisawu“ (slika 5.7).
Nije teško primetiti da je intenzitet jaæine elektriænog poqa isti u svim taækama koje su jednako udaqene od naelektrisawa – izvora tog poqa. Prema tome, u svim taækama koje se nalaze na sferi (u æijem se centru nalazi naelektrisano telo), intenzitet jaæine elektriænog poqa je isti, ali pravac i smer nisu isti (slika 5.7).

ELEKTRIÆNOG POQA I
ELEKTRIÆNI POTENCIJAL
Posmatrajmo dva taækasta naelektrisawa: q0 (nepomiæno) i q koje moþe da se pomera bez trewa (slika 5.8). Telo q0 „stvara“ elektriæno poqe koje privlaæi ili odbija q. Znaæi, posredstvom tog elektriænog poqa od q0 moþe da se pomera naelektrisawe q, tj. ono ima sposobnost da izvrši rad. Ovde, dakle, postoji elektriæna potencijalna energija, ili – Kulonova interakcija poseduje potencijalnu energiju. Sve dok ne doðe do pomerawa tela q, ovde imamo samo potencijalnu elektriænu energiju.
Slika 5.7. Jaæina elektriænog poqa taækastog naelektrisawa r q0 q
Slika 5.8. Elektriæno poqe moþe da vrši rad
Od æega moþe da zavisi ova energija? Naravno, od onoga od æega zavisi i samo delovawe (elektriæna sila) izmeðu ovih tela: od koliæina naelektrisawa i wihovog meðusobnog rastojawa.
Elektriæna potencijalna energija zavisi od sredine u kojoj se naelektrisana tela nalaze,srazmerna je koliæinama naelektrisawa tih tela,a linearno opada poveœawem rastojawa izmeðu wih:
r 0 p 1 4πε


Jednostavnom analizom ovog izraza se vidi da elektriæna potencijalna energija teþi nuli kada se rastojawe meðu naelektrisanim telima neograniæeno poveœava (r®¥). Potencijalna energija je pozitivna ako su naelektrisana tela istog znaka (odbojne sile), a negativna ako su naelektrisawa suprotnog znaka (privlaæne sile).
Daqom analizom izraza za elektriænu potencijalnu energiju moþemo uoæiti da je veliæina:
karakteristika elektriænog poqa u posmatranoj taæki date sredine. Ova fiziæka veliæina se naziva elektriæni potencijal. To je druga (pored jaæine) vaþna karakteristika elektriænog poqa i skalarna je veliæina (nema pravac ni smer, veœ samo brojnu vrednost). Elektriæni potencijal moþe biti pozitivan, ako je q0 – pozitivno naelektrisawe i negativan, ako je q0 – negativno.
Na osnovu posledwe dve formule sledi:
Elektriæni potencijal brojno predstavqa potencijalnu energiju elektriænog poqa koje deluje na jedinicu koliæine pozitivnog naelektrisawa tela koje se nalazi u tom poqu.

Ukoliko doðe do pomerawa naelektrisawa q pod dejstvom sile elektriænog poqa iz poloþaja 1 u 2 (slika 5.9), onda je pri tome izvršen rad elektriænog poqa. U ovom sluæaju mewa se elektriæna potencijalna energija, pa je: AEEE Aqq rr AqVV pp2p1 0 21 21 , 11 4, . ∆ V=J C E EqVV q p p. = º = Vq r 10 4, πε =
Jedinica elektriænog potencijala je volt: i nazvana je tako u æast istaknutog italijanskog nauænika – fiziæara Alesandra Volte (1745–1827).

Slika 5.9. Rad u elektriænom poqu q0 r1 r2 q 12

Fiziæka veliæina: U = U21 = V2 – V1
predstavqa razliku potencijala elektriænog poqa izmeðu dve taæke tog poqa i naziva se elektriæni napon
Iz zadwe dve relacije oæigledno sledi:
AqUA
Elektriæni napon izmeðu dve taæke elektriænog poqa brojno je jednak radu tog poqa na premeštawu jediniæne koliæine pozitivnog naelektrisawa izmeðu tih taæaka.
Jedinica razlike elektriænih potencijala (napona), kao i elektriænog potencijala, je volt (V)

Najmawa koliæina naelektrisawa je elementarno naelektrisawe (e =1,6·10–19C) i wega poseduje elektron (negativno) i proton (pozitivno).
Pošto ove æestice uæestvuju u izgradwi atoma, jasno je da je naelektrisawe „ugraðeno“ u samu supstanciju i nerazdvojivo je od we. Zbog toga ne postoje nenaelektrisana tela, ako posmatramo telo kao celinu sastavqenu od atoma. Mogu biti samo elektroneutralna tela u kojima su poništena uzajamna delovawa pozitivnih i negativnih naelektrisanih elementarnih æestica (protona i elektrona). Naelektrisanost je osnovno svojstvo supstancije, kao npr. masa, pa se kao takvo – ne moþenikada i nikako uništiti
Tela (æestice) mogu biti pozitivna ako imaju višak pozitivnih ili mawak negativnih naelektrisawa. Ona mogu biti negativna (ako imaju višak negativnih ili mawak pozitivnih elementarnih naelektrisawa). Ali, tela mogu biti i elektroneutralna kada sadrþe jednak broj pozitivnih i negativnih elementarnih naelektrisawa.
U kontaktu dva tela, ukoliko su ona razliæito naelektrisana (u stvari, ukoliko su im razliæiti elektriæni potencijali), u taæki kontakta dolazi do prelaska naelektrisanih æestica s jednog na drugo telo. Elementarne naelektrisane æestice mogu samo da se preraspodequju meðu telima ili u okviru tela. Pri svim procesima, dakle, nosioci naelektrisawa (joni, elektroni) se ne stvaraju i ne uništavaju; oni se samo prerasporeðuju u okviru samog tela ili meðu telima. Ukupan broj nosilaca pozitivnog i negativnog naelektrisawa, pre i posle tih procesa, ostaje nepromewen (stalan).
Pri svim procesima u izolovanom sistemu tela (æestica) koji se ostvaruju posredstvom elektriænih sila (interakcija) ukupna koliæina naelektrisawa ostaje konstantna.
Ovo je jedna od formulacija zakona odrþawa koliæine naelektrisawa. To je jedan od osnovnih zakona fizike (kao i drugi zakoni odrþawa: energije, impulsa, mase i dr.), potvrðen mnogobrojnim æiwenicama. Na osnovu tog fundamentalnog zakona objašwava se veliki broj elektriænih pojava i procesa.


Primer 1. Dva pozitivno naelektrisana tela nalaze se na meðusobnom rastojawu od 205 mm. U koju taæku A, na pravoj liniji koja spaja ta dva naelektrisana tela, treba postaviti treœe, negativno naelektrisano telo da bi se ono nalazilo u ravnoteþi sa prethodna dva naelektrisana tela? Koliæina naelektrisawa prvog tela je 1,67 nC, drugog 3,34 nC i treœeg –0,67 nC. Mase naelektrisanih tela, tj. gravitacionu interakciju zanemariti u odnosu na elektriænu.
Podaci: r = 205 mm, q1 = 1,67 nC, q2 = 3,34 nC, q3 = – 0,67 nC; x = ?, er = 1
Rešewe. Na telo naelektrisawa q3 deluju sile F ® 1 i F ® 2 koje potiæu od tela sa koliæinama naelektrisawa q1 i q2. Uslov ravnoteþe u skalarnom obliku u odnosu na poloþaj naelektrisawa q3 je: F1 –F2=0, odnosno F1 =F2.
Pošto je dobija se:
Napomena: Iz izraza za rešewe se moþe primetiti da x ne zavisi od koliæine naelektrisawa q3. Da li zavisi od wegovog predznaka?
Primer 2. Dva taækasta tela æije su koliæine naelektrisawa 6,7 nC i –13,2 nC nalaze se u vazduhu (er » 1) na meðusobnom rastojawu r. Odrediti intenzitet jaæine elektriænog poqa u taæki koja je udaqena 3 cm od tela sa pozitivnim naelektrisawem i 4 cm od negativno naelektrisanog tela.
Podaci: q1 = 6,7 nC, q2 = –13,2 nC, r1= 3 cm, r2= 4 cm; E = ?
Rešewe. Jaæina elektriænog poqa u taæki A je: E ® = E ® 1 + E ® 2 , gde je E ® 1 jaæina poqa koja potiæe od tela sa koliæinom naelektrisawa q1, E ® 2 jaæina poqa u taæki A uzrokovana telom sa koliæinom naelektrisawa q2. Znamo da su:
Ugao izmeðu vektora E ® 1 i E ® 2 je prav ugao, pa se moþe napisati:


1. Navedite suštinske razlike izmeðu gravitacione i elektriæne sile.
2. Da li elektriæna sila zavisi od sredine meðu naelektrisanim telima?
3.Strogo uzevši, u kojim sluæajevima vaþi Kulonov zakon?
4. Da li u istom prostoru mogu postojati istovremeno i gravitaciono i elektriæno poqe? Da li pri tome dolazi do wihovog meðusobnog „ometawa“?
5. Kojim se fiziækim veliæinama opisuje elektriæno poqe?
6. Koju karakteristiku poqa odreðuje vrednost sile koja u datoj taæki poqa deluje na jediniæno pozitivno naelektrisawe?
7. Da li rad elektriæne sile zavisi od oblika putawe po kojoj se pomera naelektrisano telo?
8. Koliki je rad Zemqine teþe ili elektriæne sile na premeštawu (naelektrisanog) tela po zatvorenoj putawi?
9. Ako se dva tela meðusobno privlaæe, na primer gravitacionim ili elektriænim delovawima, kakav se rad vrši (pozitivan ili negativan) pri udaqavawu tih tela?

ELEKTRIÆNI FLUKS
Linije sile poqa taækastog naelektrisawa ili ravnomerno naelektrisane sfere (lopte), kada u wenoj blizini nema drugih naelektrisanih tela, radijalno su rasporeðene. U poqu pozitivnog taækastog naelektrisawa (sfere) linije su usmerene od taækastog tela (od centra sfere), a u poqu negativnog taækastog naelektrisawa (sfernog tela) suprotno (sl. 5.6). Ovako definisan smer linija sile odreðen je smerom delovawa elektriæne sile na pozitivno naelektrisano telo uneto u dato poqe. Na osnovu toga se moþe reœi da: linije sile poæiwu („izviru“) na pozitivnim, a završavaju se („uviru“) na negativnim naelektrisanim telima (æesticama).


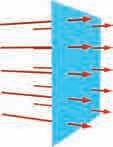
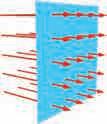
Da bi se pravila razlika meðu poqima, obiæno se uzima da je broj linija sile na jedinici površine normalne na pravac linija sile jednak brojnoj vrednosti jaæine elektriænog poqa. Znaæi, gde je gustina linija sila veœa,jaæina elektriænog poqa je veœeg intenziteta i obrnuto (slika 5.10).
Istakli smo da se jaæina poqa moþe prikazati gustinom linija sile, tj. brojem linija sile po jedinici površine koja je normalna na te linije, ili fiziækom veliæinom koja se naziva fluks elektriænog poqa. Fluks elektriænog poqa brojno je jednak broju linija sile koje prolaze kroz posmatranu (normalno postavqenu) površ.
Elektriæni fluks se moþe odrediti pomoœu osnovne karakteristike poqa, a to je wegova jaæina E i površine S normalne na pravac poqa (slika 5.11): F = ES .
Potencijal elektriænog poqa mewa se udaqavawem od naelektrisanog tela od kojeg potiæe dato poqe, prema formuli:

gde je r – rastojawe od tela koliæine naelektrisawa q do taæke u kojoj se izraæunava potencijal. Odavde proizilazi da sve taæke koje se nalaze u istorodnoj sredini na jednakom rastojawu od naelektrisanog tela imaju iste potencijale. Oæigledno, to su taæke na sferama sa centrom u kojem se nalazi naelektrisano telo.
Sve taæke koje imaju jednake vrednosti potencijala formiraju jednu ekvipotencijalnu površ.
Na slici 5.12. prikazane su ekvipotencijalne površi isprekidanim linijama (koncentriæni krugovi, tj. sfere) taækastog pozitivno naelektrisanog tela. Punim usmerenim linijama oznaæene su linije sile poqa koje potiæe od ovog naelektrisawa. Pravac linija sile u svakoj taæki poqa je normalan na ekvipotencijalne površi.


Znamo da je rad pri pomerawu naelektrisawa izmeðu dve taæke u elektriænom poqu jednak proizvodu koliæine naelektrisawa tela i razlike potencijala:
A = q (V2 – V1).
Rad elektriæne sile pri pomerawu naelektrisanog tela izmeðu dve taæke na ekvipotencijalnoj površi jednak je nuli, jer je V1 = V2.
Posmatrawem linija sile moþe se suditi o promenama jaæine poqa: mestima s veœom gustinom linija sile odgovara veœi intenzitet jaæine poqa i obrnuto. Na osnovu rasporeda ekvipotencijalnih površi moþe se govoriti o drugoj osnovnoj veliæini – potencijalu, koja karakteriše elektriæno poqe. Dakle, svako elektriæno (elektrostatiæko) poqe moþe se predstaviti linijama sile poqa i ekvipotencijalnim površima, a na osnovu wihove slike mogu se vršiti odreðene analize elektriænog poqa.

ELEKTRIÆNOG POQA
Rad elektriænih sila izraþava se na dva naæina: preko jaæine poqa i razlike potencijala meðu taækama poqa. Uzimajuœi to u obzir, izmeðu jaæine poqa i wegovog potencijala postoji odgovarajuœa veza (slika 5.13). Posmatraœemo dve ekvipotencijalne površi koje se nalaze na malom meðusobnom rastojawu. Neka je V1 potencijal površi M1N1 i V2 potencijal površi M2N2. U nekoj taæki prve ekvipotencijalne površi povucimo normalu D® n usmerenu ka drugoj ekvipotencijalnoj površi. Taæke preseka normale sa ekvipotencijalnim površima su B i B’ ; a rastojawe izmeðu wih je D® n Jaæina poqa ® E normalna je na ekvipotencijalnu površ i usmerena je duþ normale ® n .
V=const
Slika 5.12. Ekvipotencijalne površi taækastog naelektrisawa
Slika 5.13. Smer jaæine elektriænog poqa je ka smawivawu potencijala
Ako su taæke B i B’ vrlo bliske, moþe se pretpostaviti da je izmeðu wih intenzitet jaæine poqa E konstantan. Rad koji se vrši pri pomerawu naelektrisawa iz taæke B u B’ moþe se predstaviti u obliku:
EF q . =
A = F Dn = qE Dn, jer je, S druge strane, taj isti rad moþe biti izraþen preko razlike potencijala u taækama B i B’ : A = q (V2 – V1).
Uporeðivawem ovih formula za rad, nalazi se EDn = V2 – V1. Odavde sledi:
n ∆ ∆ =
Ovde je DV = V2 – V1 promena potencijala pri pomerawu za rastojawe Dn duþ normale na ekvipotencijalnoj površi, tj. duþ linija sile.



Ogledi pokazuju da razliæiti provodnici, naelektrisani jednakim koliæinama naelektrisawa, imaju razliæite elektriæne potencijale.
Fiziæka veliæina kojom se karakteriše svojstvo provodnika da pri istom potencijalu mogu da sadrþe razliæite koliæine naelektrisawa naziva se elektriæna kapacitivnost.
Elektriæna kapacitivnost provodnika zavisi i od rasporeda tela koja ga okruþuju i od sredine u kojoj se nalazi. Radi jednostavnosti, posmatraœemo usamqeni provodnik koji se nalazi u vakuumu, ili vazduhu (slika 5.14). Kada se posmatrana kugla naelektriše odreðenom koliæinom naelektrisawa, wen potencijal ima odgovarajuœu vrednost. Ako se koliæina naelektrisawa tog provodnika uveœa dva puta, i wegov potencijal œe porasti dva puta. Uopšte, koliko puta se poveœa koliæina naelektrisawa provodnika, toliko puta se poveœa i potencijal usamqenog provodnika. To znaæi da je koliæina naelektrisawa q takvog provodnika direktno srazmerna potencijalu provodnika: q = CV.

Slika 5.14. Otklon igle elektrometra je srazmeran koliæini naelektrisawa
Koeficijent srazmere C je fiziæka veliæina koja karakteriše elektriæna svojstva tela – provodnika i naziva se elektriæna kapacitivnost. Iz prethodnog izraza sledi da je:
V . =
Elektriæna kapacitivnost tela brojno je jednaka odnosu koliæine naelektrisawa tela i wegovog potencijala.
Meðutim, elektriæna kapacitivnost provodnika ne zavisi ni od koliæine naelektrisawa, a ni od elektriænog potencijala. Poveœawem (smawewem) koliæine naelektrisawa poveœava se (smawuje se) i potencijal provodnika, tako da wihov odnos ostaje uvek nepromewen. Kapacitivnost provodnika (tela) zavisi samo od wegovih geometrijskih dimenzija i od elektriænih svojstava sredine u kojoj se provodnik (telo) nalazi.
Jedinica elektriæne kapacitivnosti je farad (F):
F. V =
Kapacitivnost od 1 farada je veoma velika. Takvu kapacitivnost bi imala kugla polupreænika 9×109 m, što je za oko 1400 puta veœe od polupreænika Zemqe. U praksi se koriste mawe jedinice: mikrofarad (1mF = 10–6 F), nanofarad (1nF = 10–9 F) i pikofarad (1pF = 10–12 F). Kapacitivnost sfernog provodnika æija bi zapremina odgovarala zapremini Zemqe, iznosila bi oko 700 µF.


Ploæast elektriæni kondenzator æine dve paralelne metalne ploæe postavqene jedna naspram druge na rastojawu koje je malo u odnosu na duþinu ploæe. Izmeðu ploæa kondenzatora nalazi se dielektrik: vazduh, vakuum, staklo i dr. (slika 5.15).
Elektriæna kapacitivnost ploæastog (ravnog) kondenzatora zavisi od površine jedne od ploæa kondenzatora S i rastojawa meðu ploæama kondenzatora d:
d ;0r
gde je e – dielektriæna propustqivost vakuuma (e0 = 8,85.10–12 ); a er – relativna dielektriæna propustqivost date sredine.
Znaæi, ovaj sistem – ploæast kondenzator ima odreðenu elektriænu kapacitivnost, bez obzira da li su wegove ploæe naelektrisane ili nisu. Ako se, pak, jedna ploæa ovog kondenzatora naelektriše, npr. sa +q (druga œe imati istu koliæinu naelektrisawa samo suprotnog znaka, dakle: –q). Izmeðu ploæa œe se pojaviti razlika potencijala, tj. elektriæni napon U. Ove dve veliæine su povezane: q = C ×U
Slika 5.15. Ploæast (ravan) kondenzator C
Slika 5.16. Šematska oznaka elektriænog kondenzatora
Kondenzatori imaju razliæite oblike, a šematski se predstavqaju istim simbolom, kao na slici 5.16.

Elektriæni kondenzatori se mogu vezivati u tzv. kondenzatorske baterije radi postizawa wihovog efikasnijeg rada kao elementa elektriænih kola. Ako se poveþu paralelno, kao na slici 5.17, onda ova baterija ima veœu ukupnu koliæinu naelektrisawa. Naime,
Elektriæna kapacitivnost paralelno vezanih kondenzatora jednaka je zbiru pojedinaænih kapacitivnosti.
Slika 5.17. Paralelna veza elektriænih kondenzatora

Ako se kondenzatori poveþu redno (serijski) kao na slici 5.18. onda ova baterija ima veœi ukupni elektriæni napon:

Slika 5.18. Serijska veza elektriænih kondenzatora
. q
Reciproæna vrednost elektriæne kapacitivnosti serijske veze kondenzatora jednaka je zbiru reciproænih vrednosti pojedinaænih kapacitivnosti.

Naelektrisawe provodnika i odgovarajuœi potencijal vezani su relacijom q = CV,
gde je C – kapacitivnost provodnika. Grafiæki prikaz ove veze ima oblik prave koja poæiwe iz koordinatnog poæetka i æiji je koeficijent pravca definisan kapacitetom provodnika (slika 5.19).
Slika 5.19. Grafiæki prikaz povezanosti koliæine naelektrisawa i potencijala
Površina ograniæena datim vrednostima koliæine naelektrisawa i potencijala (šrafirani deo).
Formula za rad moþe se napisati kao:
Dobijeni izraz za gustinu energije vaþi ne samo za homogeno poqe ravnog kondenzatora, veœ i za bilo koje drugo elektrostatiæko poqe. Štaviše, dati izraz za gustinu energije moþe da se primeni i za promenqiva elektriæna poqa. Merna jedinica gustine energije elektriænog poqa i rada dobija se iz odgovarajuœih formula. w W V == 1 2 . 2 ε E EU d = AWqVCV q C e == == 1 2 1 22 2 2
Deobom jedne i druge strane posledwe relacije sa zapreminom (prostora izmeðu ploæa) V = Sd i dobija se formula kojom se izraþava gustina energije elektriænog poqa, odnosno energija po jedinici zapremine:


Primer 3. Kondenzator kapacitivnosti 6 mF na æijim oblogama je napon 127 V i kondenzator kapacitivnosti 4 mF, na æijim oblogama je napon 220 V povezuju se paralelno. Odrediti ekvivalentnu kapacitivnost dobijenog sistema kondenzatora i vrednost elektriænog napona na wegovim krajevima.
Podaci: C 1 = 6 mF, U1 = 127 V, C2 = 4 mF, U2 = 220V; Ce = ? U = ? Rešewe. Ekvivalentna kapacitivnost dva paralelno vezana kondenzatora je: Ce = C1 + C2 = 10 mF
Napon na krajevima tih kondenzatora iznosi:
gde je
Na osnovu toga imamo:
U CC 1122 22 164V. + == +
• Uzajamno delovawe naelektrisanih tela (æestica) ostvaruje se posredstvom elektriænog (elektrostatiækog) poqa. Zakon uzajamnog delovawa naelektrisanih tela (æestica) æije su dimenzije zanemarqive u odnosu na wihova meðusobna rastojawa, ili izmeðu naelektrisanih tela sfernog oblika pod uslovom da se naelektrisana tela (æestice) nalaze u stawu relativnog mirovawa, eksperimentalno je ustanovio Kulon (1785): Intenzitet sile izmeðu dva naelektrisana taækasta tela,ili izmeðu dva naelektrisana tela u obliku sfere srazmeran je proizvodu wihovih koliæina naelektrisawa,a obrnuto proporcionalan kvadratu meðusobnog rastojawa: gde je e0 – dielektriæna propustqivost vakuuma (e0 = 8,85× 10–12 ), a er je relativna permitivnost sredine. 2 2 C Nm Fqq r 12 er0 2 1 4;, εεε πε ==



• Elektriæno poqe kojim se ostvaruje uzajamno delovawe naelektrisanih tela (æestica) karakterišu (odreðuju) veliæine: jaæina elektriænog poqa,potencijal (napon) elektriænog poqa i energija elektriænog poqa.
Fiziæka veliæina odreðena koliænikom elektriæne sile koja u datoj taæki deluje na taækasto telo date koliæine naelektrisawa i te koliæine naelektrisawa,naziva se jaæina elektriænog poqa:
Jaæina elektriænog poqa je vektorska veliæina. Wen intenzitet u datoj taæki prostora brojno je jednak intenzitetu elektriæne sile koja u toj taæki deluje na jedinicu pozitivne koliæine naelektrisawa, a pravac i smer se poklapaju sa pravcem i smerom elektriæne sile ( ® Fe ).
Potencijal elektriænog poqa u vakuumu (vazduhu) u datoj taæki brojno je jednak odnosu potencijalne energije i jediniænog pozitivnog naelektrisawa u toj taæki,odnosno odnosu koliæine naelektrisawa tela koje „proizvodi“ elektriæno poqe i rastojawa do taæke u kojoj se posmatra potencijal poqa
gde je r – rastojawe od tela koliæine naelektrisawa q do taæke u kojoj se posmatra potencijal elektriænog poqa.
Poseban fiziæki smisao ima razlika elektriænog potencijala (napon). Posredstvom ove veliæine izraþava se rad sile elektriænog poqa pri premeštawu naelektrisanog tela
Razlika potencijala (napon) izmeðu dve taæke u elektriænom poqu brojno je jednaka radu sile elektriænog poqa pri pomerawu tela jediniæne pozitivne koliæine naelektrisawa izmeðu tih taæaka. Jedinica elektriænog potencijala i napona je volt (V).


• Elektriæno poqe se geometrijski prikazuje linijama sile. Linije sile odreðuju pravac i smer kretawa pozitivno naelektrisane æestice u elektriænom poqu. Gustina linija sila definiše jaæinu poqa, a wihov smer vrstu naelektrisawa tela koje „proizvodi“ poqe. Tangenta na liniju sile u bilo kojoj taæki ima pravac elektriænog poqa.
• Fluks elektriænog poqa je jednak broju linija sile koje prolaze kroz posmatranu (normalno postavqenu) površ:
Φ = ES
• Kapacitivnost provodnika brojno je jednaka odnosu wegove koliæine naelektrisawa i wegovog potencijala:

Elektriæna kapacitivnost provodnika ne zavisi od koliæine naelektrisawa provodnika. Koliko se poveœa (smawi) koliæina naelektrisawa, toliko se poveœa (smawi) potencijal provodnika, tako da se wihov odnos ne mewa. Kapacitivnost provodnika (tela) odreðuje se samo wegovim geometrijskim razmerama i oblikom, te elektriænim svojstvima sredine u kojoj se provodnik nalazi.
Elektriæna kapacitivnost ploæastog (ravnog) kondenzatora zavisi od površine jedne od ploæa kondenzatora i rastojawa meðu ploæama kondenzatora:
Kapacitivnost kondenzatora „pokazuje“ srazmeru izmeðu koliæine naelektrisawa na ravnoj ploæi i razlike potencijala izmeðu ploæa tog kondenzatora:
q = CU
• Energija elektriænog poqa ploæastog kondenzatora je:
a odatle i wena gustina:
Merne jedinice fiziækih veliæina izvode se na osnovu wihovih formula.
1. Šta su linije sila elektriænog poqa i æemu one sluþe?
2. Koje se informacije u kvalitativnom smislu mogu dobiti o elektriænom poqu na osnovu wegove slike (rasporeda i smera) linija sile?
3. Šta moþemo da kaþemo o pravcu i smeru linija sile elektriænog poqa?
4. Gde se nalazi „izvor“, a gde „uvir“ linija sile elektriænog poqa?
5. Mogu li se meðusobno presecati linije sile poqa?
6. Koje dve osnovne veliæine karakterišu elektriæno poqe?
7. Šta su ekvipotencijalne površi elektriænog poqa?
8. Mogu li linije sile i ekvipotencijalne površi zaklapati neki drugi ugao osim ugla od 90 °?
9. Æemu je jednaka energija i gustina energije elektriænog poqa ravnog kondenzatora u vazduhu?
10. Koju jedinicu ima gustina elektriæne energije?



Þivot
savremenog æoveka ne bi mogao da se zamisli bez korišœewa elektriæne struje. Elektriæna energija je omoguœila jeftiniju proizvodwu, brþi i udobniji saobraœaj, kosmiæke letove i skoro trenutno prenošewe informacija (slike i zvuka) na ogromna rastojawa. Da bismo odgovorili na pitawe šta je elektriæna struja, koristiœemo znawe o elektriænom poqu i strukturi supstancije. Podsetiœemo se definicije koju smo nauæili još u osnovnoj školi: elektriæna struja je usmereno kretawe naelektrisanih æestica (elektrona, jona).
U ovom poglavqu œemo detaqnije razmotriti prirodu elektriæne struje u raznim sredinama i pod razliæitim uslovima, razne efekte i primenu elektriæne struje.

Kada se atomi „povezuju“ u kristalnu rešetku, oni obrazuju svoje veze pomoœu elektrona iz svojih omotaæa. Tom prilikom, pogotovo kod metala, ostaje jedan ili više elektrona koji nisu u vezi – oni mogu da se kreœu kroz kristal. Zato su to slobodni elektroni.
Nosioci elektriæne struje u metalnim provodnicima su slobodni elektroni. Na slici 6.1. su prikazani slobodni elektroni i pozitivni joni kristalne rešetke. Ovaj prikaz nije dimenziono ispravan, ali moþe da posluþi za razumevawe nastanka elektriæne struje.
Slobodne elektrone u metalu moþemo da posmatramo kao æestice gasa koje se haotiæno kreœu kroz prostor izmeðu pozitivnih jona u kristalnoj rešetki metala. Zato se æesto za slobodne elektrone u metalima koristi i naziv elektronski gas

Elektroprovodqivost metala uslovqena je kretawem slobodnih elektrona,a u teænostima kretawem i pozitivnih i negativnih jona.

Osim ævrstih i teænih supstancija, gasovi takoðe mogu da budu provodnici, ali samo pod uslovom da su veoma razreðeni (mali pritisak) i da postoji relativno visok napon izmeðu elektroda (metalnih ploæa) postavqenih u gasnim cevima. Nosioci struje u gasovima su elektroni i joni.
Supstancije koje imaju malu koncentraciju slobodnih naelektrisanih æestica (elektrona, jona i dr.) spadaju u slabe provodnike ili izolatore. Izolatori su staklo, suva zemqa, suvo drvo, razne vrste guma, ugaq itd.
Pored provodnika i izolatora, postoje i poluprovodnici. Opšte svojstvo poluprovodnika je naglo poveœawe wihove elektroprovodqivosti pod uticajem izmene nekih spoqašwih faktora (uslova): temperature, osvetqenosti, pritiska, elektriænog poqa i dr. Od svih poluprovodnika najviše se koriste germanijum (Ge) i silicijum (Si). Posebno je vaþna wihova primena za izradu tranzistora, koji su osnovni elementi televizora, raæunara, robota i dr. Slobodni elektroni u metalima ponašaju se sliæno molekulima gasa: meðusobno se sudaraju, sudaraju se sa jonima kristalne rešetke. Usled toga se kreœu neureðeno (haotiæno), slika 6.2, mewajuœi neprestano intenzitet brzine i pravac kretawa. Uslov za pojavu struje je da postoji protok naelektrisanih æestica, što pretpostavqa usmereno kretawe naelektrisanih æestica. To se moþe postiœi delovawem sile elektriænog poqa na te æestice duþ provodnika (slika 6.3). Smer kretawa tih naelektrisanih æestica zavisi od vrste wihovog naelektrisawa. Delovawem sile elektriænog poqa, svaka slobodna naelektrisana æestica u provodniku stiæe komponentu brzine u pravcu te sile (duþ provodnika na slici 6.3). Na taj naæin kretawe æestica postaje ureðeno i u provodniku postoji elektriæna struja.
Slika 6.2. Slobodni elektroni u metalnom provodniku haotiæno se kreœu
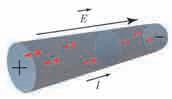
Slika 6.3. Metalan provodnik kroz koji protiæe struja
Da bi kroz provodnik proticala elektriæna struja,potrebno je da u provodniku postoji elektriæno poqe.

U tehnici i praksi elektriæno poqe u provodnicima se uspostavqa i moþe duþe vreme da se odrþava pomoœu izvora elektriæne struje, ili izvora elektromotorne sile. To su, na primer, elektriæna baterija, akumulator, generator i drugi. U izvorima elektriæne struje odvijaju se procesi koji dovode do razdvajawa pozitivno naelektrisanih od negativno naelektrisanih æestica.


Razdvojene naelektrisane æestice dospevaju na odreðene delove izvora koji se nazivaju polovi izvora struje, obrazujuœi izmeðu wih razliku elektriænih potencijala. Ova razlika potencijala (elektriæni napon) je karakteristika svakog izvora elektriæne struje i naziva se elektromotorna sila izvora struje
Razdvajawe (a ne stvarawe) naelektrisanih æestica unutar izvora elektriæne struje se vrši na raæun pretvarawa mehaniæke, hemijske ili unutrašwe energije u elektriænu energiju. Kretawe, pomerawe naelektrisanih æestica (elektrona i jona) u izvoru struje podrazumeva odgovarajuœi rad.
Elektromotorna sila omoguœuje prelazak jediniænog pozitivnog naelektrisawa sa jednog na drugi pol unutar izvora. Obiæno se obeleþava sa e.
Jedinica za elektromotornu silu je volt (V), isto kao i za razliku elektriænih potencijala (napon).
Iz definicije elektromotorne sile jasno proizlazi da ovde nije reæ o sili, vektorskoj veliæini, nego o skalarnoj veliæini – koliæniku rada i koliæine naelektrisawa (skalarne veliæine).
Treba voditi raæuna o tome da elektromotorna sila nije potpuno isto što i napon. Kada polovi izvora nisu spojeni, tada wihov napon (razlika potencijala) ima istu vrednost kao i elektromotorna sila tog izvora. Æim se polovi izvora spoje spoqašwim provodnikom i potekne elektriæna struja kroz kolo, napon na polovima izvora se smawi, dok elektromotorna sila ostaje nepromewena, tako da ove dve veliæine nemaju više jednake vrednosti.
Elektromotorna sila je osnovna kvantitativna karakteristika svakog izvora elektriæne struje. Druga osnovna karakteristika je unutrašwa elektriæna otpornost tog izvora. Ako su poznate ove dve karakteristike, izvor struje kao glavni element elektriænog kola u potpunosti je odreðen.

Elektrina struja se kvantitativno opisuje fiziækom veliæinom koja se naziva jaæina elektriæne struje. Ako kroz popreæni presek provodnika prolazi koliæina naelektrisawa Dq za vreme Dt, onda je jaæina struje I u provodniku (slika 6.4):


Jaæina struje brojno je jednaka koliæini naelektrisawa koje proðe kroz popreæni presek provodnika u jedinici vremena.
Kada elektriæna struja ima stalno istu vrednost, onda je reæ o stalnoj (nepromenqivoj) struji. Pri stalnoj struji kroz svaki popreæni presek provodnika proðu jednake koliæine naelektrisawa za iste intervale vremena.

Kada kroz provodnik protiæu razliæite koliæine naelektrisawa u toku jednakih intervala vremena, onda je to promenqiva struja. Jedinica jaæine elektriæne struje je amper i obeleþava se sa A. To je jedna od osnovnih jedinica SI sistema. Pošto je jedinica za koliæinu naelektrisawa kulon (C), sledi A=C/s, tj. C=A × s.
Jaæina elektriæne struje u baterijskoj sijalici je oko 0,1 A, u kuœnim aparatima od 0,5 A do 20 A, dok u elektriænim motorima tramvaja, vozova ili dizalica moþe dostiœi vrednost od nekoliko destina, pa i stotina ampera. Jaæine struje muwe i groma su veoma velike, nekoliko stotina hiqada ili æak miliona ampera. Veœina qudi poæiwe da „oseœa“ elektriænu struju kada wena jaæina u telu dostigne vrednost od oko 0,001 A, dok struja jaæine 0,01 A veœ moþe biti opasna za þivot.
Jaæina elektriæne struje je skalarna veliæina, ali se ovoj struji pripisuje smer zbog efekata koje ona proizvodi. Smer struje ne mora da se poklapa sa smerom ureðenog kretawa naelektrisanih æestica (nosilaca te struje). U metalnim provodnicima kreœu se elektroni, u elektrolitima pozitivni i negativni joni. Elektroni se kreœu u smeru suprotnom od smera elektriænog poqa, dok se pozitivni joni kreœu u smeru poqa. Meðutim, jaæina elektriæne struje ne zavisi od predznaka naelektrisawa wenih nosilaca; to se odnosi na efekte elektriæne struje. Ista koliæina naelektrisawa po apsolutnoj vrednosti moþe se prenositi kretawem bilo pozitivnih æestica u jednom, bilo negativnih u suprotnom smeru. Stoga je dogovorom utvrðeno da se pod smerom stalne struje podrazumeva smer u kome bi se pri datim uslovima u provodniku kretale pozitivno naelektrisane æestice. To je smer elektriænog poqa u provodniku – od višeg ka niþem potencijalu. Ovo je takozvani tehniæki smer elektriæne struje. Tehniæki smer elektriæne struje u provodniku (slika 6.5) je od wegovog kraja prikquæenog za pozitivan pol izvora ka kraju vezanom za negativan pol izvora.
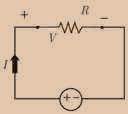
Elektriæna struja æiji se smer ne mewa tokom vremena naziva se jednosmerna struja.Takva je na primer struja koja se dobija iz baterije xepne lampe. Ako je jaæina jednosmerne struje konstantna u toku vremena, onda je to stalna jednosmerna struja.
Znaæajna je još jedna kvantitativna karakteristika elektriæne struje, koja se naziva gustina elektriæne struje. Ako je S površina popreænog preseka provodnika kroz koji protiæe struja jaæine I, onda je gustina te struje j definisana relacijom
Gustina elektriæne struje brojno je jednaka koliæniku jaæine te struje i površine popreænog preseka provodnika kroz koji ona protiæe.
Ako površina popreænog preseka provodnika nije ista duþ celog provodnika, onda œe strujna gustina imati razliæite vrednosti na raznim mestima provodnika. Meðutim, jaæina struje ostaje ista u bilo kom popreænom preseku. Na mestima gde je provodnik tawi, strujna gustina je veœa i obrnuto.
Jedinica strujne gustine na osnovu wene definicije je A/m2 . Konstatovano je da je jaæina elektriæne struje skalarna veliæina. Za razliku od toga, gustina te struje je vektorska veliæina. Gustina elektriæne struje prati tehniæki smer, tj. prati tok pozitivnih nosilaca naelektrisawa.



OM GEORG SIMON, nemaæki fiziæar, uveo je pojam elektriæne otpornosti kao vaþne karakteristike elektriænog kola. Eksperimentalno je ustanovio osnovni zakon elektriænog kola (1826), koji povezuje jaæinu struje, napon i otpor kola, nazvan Omov zakon elektriænog kola. Naredne godine je dao teorijsko obrazloþewe ovog zakona. U znak zahvalnosti, po Omu je nazvana jedinica elektriæne otpornosti – om (W).
Merewem jaæine elektriæne struje u odreðenom potrošaæu za razliæite vrednosti elektriænog napona (slika 6.6) nalazi se da je:
Ovde su U1, U2, U3, ... razliæite vrednosti elektriænih napona izmeðu krajeva provodnika, a I1, I2, I3, ... odgovarajuœe vrednosti jaæina elektriænih struja. Veliæina oznaæena sa R naziva se elektriæna otpornost provodnika.
Uopštavajuœi ovaj odnos elektriænog napona i jaæine elektriæne struje u provodniku, dobija se Omov zakon za jedan deo elektriænog kola:*
Slika 6.6. Prikaz Omovog zakona za deo elektriænog kola
Jaæina elektriæne struje u provodniku srazmerna je elektriænom naponu na wegovim krajevima,a obrnuto srazmerna elektriænoj otpornosti tog provodnika. Iz prethodne formule moþe da se napiše:
Elektriæna otpornost provodnika moþe da se odredi kao koliænik elektriænog napona na wegovim krajevima i jaæine elektriæne struje u tom provodniku. Jedinica elektriæne otpornosti je om: W = V/A. Elektriæna otpornost je fiziæka veliæina koja karakteriše svaki konkretni provodnik. Veoma je vaþno shvatiti da provodnik poseduje elektriænu otpornost i onda kada kroz wega ne protiæe elektriæna struja.

* Deo strujnog kola podrazumeva vezu izmeðu jaæine elektriæne struje koja protiæe kroz neki strujni element (npr. otpornik) i elektriæni napon na wegovim krajevima.

Eksperimentalno je utvrðeno da elektriæna otpornost pravolinijskog provodnika nepromenqivog preseka zavisi od vrste materijala od kojeg je naæiwen taj provodnik, od wegove duþine (A) i površine popreænog preseka (S):
, = ρ A R S . = ρA
Sa r je oznaæena specifiæna elektriæna otpornost koja zavisi od materijala (vrste supstancija) od kojih je naæiwen provodnik. Iz gorweg izraza sledi:
ali ova veliæina ne zavisi od dimenzija provodnika (videti tabelu 6.1).
Jedinica specifiæne elektriæne otpornosti je om metar (Wm).
Vrsta materijala
srebro
Specifiæna elektriæna otpornost r [W m]
1,6×10–8
bakar 1,7 10–8 aluminijum
2,8×10–8 volfram
5,5×10–8 gvoþðe 1,0×10–7
nikl
4,2 10–7 konstantan
5,0×10–7
cekas 11×10–7
Tabela 6.1. Specifiæne elektriæne otpornosti nekih metala i legura
Omov zakon povezuje jaæinu elektriæne struje i elektriæni napon na krajevima nekog provodnika (potrošaæa) preko karakteristike (elektriæne otpornosti) tog provodnika. Ova zavisnost se moþe prikazati i grafiæki.
Grafik zavisnosti jaæine elektriæne struje u metalnim provodnicima od veliæine elektriænog napona, je prava linija (slika 6.7).
Koeficijent pravca prave odreðuje vrednost elektriæne otpornosti provodnika. Ukoliko je veœi koeficijent pravca prave, to je veœa elektriæna otpornost provodnika i obratno.
Izvešœemo jedan drugi oblik Omovog zakona. Polazimo od veœ napisanog: UU IS R 1 == ρ A
6.7.


Ovu jednaæinu podelimo sa S i uoæimo da je – gustina elektriæne struje, a – intenzitet jaæine elektriænog poqa duþ provodnika. Na taj naæin dobijamo:
gde se veliæina – naziva specifiæna elektriæna provodnost i ima jedinicu Ω-1m-1 .
Još ispravnije napisana posledwa formula je:
® j= s ® E
(jer su gustina struje i jaæina poqa – vektorske veliæine) i predstavqa drugi oblik Omovog zakona.


XUL XEJMS PRESKOT, bogati vlasnik pivare u Manæesteru, fiziæar–amater, strasni i uporni eksperimentator. Skoro 40 godina je vršio eksperimente da bi otkrio prirodu toplote. Ustanovio je mehaniæki ekvivalent toplote i nezavisno od Majera – zakon odrþawa i uzajamnog pretvarawa energije (1843).
Xul je utvrdio zakon koji odreðuje koliæinu toplote koja se izdvaja u provodniku sa strujom (1841). Otprilike u isto vreme i nezavisno od wega taj zakon je otkrio i Lenc Stoga je taj zakon nazvan Xul–Lencov zakon. Jedinica za energiju, odnosno rad, nazvana je xul (J).

HAJNRIH FRIDRIH EMIL LENC, baltiæki nemaæki fiziæar, radio na Univerzitetu u Sankt Peterburgu. Prouæavao je i klimatske uslove i fiziæki sastav morske vode, a najpoznatiji je po Lencovom zakonu ili pravilu elektromagnetne indukcije (1833). Nezavisno od Xula, Lenc je 1842. godine otkrio zakonitost pretvarawa elektriæne u toplotnu energiju.
Svi provodnici – ævrsti, teæni i gasoviti – zagrevaju se kada kroz wih prolazi elektriæna struja, što znaæi da se pri tome poveœava wihova unutrašwa energija. Od æega zavisi koliæina toplote koja nastaje u provodniku kroz koji se propušta elektriæna struja?
Iz definicije elektriænog napona, , gde je A rad koji se izvrši pri premeštawu koliæine naelektrisawa q sa jednog na drugi wegov kraj provodnika, dobija se


Ovaj rad odgovara promeni unutrašwe energije, odnosno koliæini toplote koja se oslobodi u provodniku u toku proticawa struje. Kombinujuœi prethodnu
relaciju sa izrazom za jaæinu elektriæne struje , nalazi se formula za osloboðenu koliæinu toplote u provodniku, A = Q = UIt, odnosno, uzimawem u obzir Omovog zakona (U=RI): Q = RI2t
Prethodni izraz predstavqa matematiæku formulaciju Xul–Lencovog zakona: Koliæina toplote koja se oslobodi u provodniku srazmerna je kvadratu jaæine elektriæne struje koja kroz wega protiæe,elektriænoj otpornosti tog provodnika i vremenu proticawa ove struje.
Xul–Lencov zakon je, u stvari, zakon odrþawa energije koji se odnosi na konkretan sluæaj: pretvarawe elektriæne energije u unutrašwu energiju u provodnicima.

Upoznali smo Omov zakon za deo elektriænog strujnog kola. Zavisnost jaæine elektriæne struje od elektromotorne sile izvora i otpornosti svih provodnika (otpornika, potrošaæa), u sloþenom elektriænom kolu, odreðuje se na osnovu Omovog zakona za celo elektriæno kolo
Posmatraœemo najjednostavnije zatvoreno elektriæno kolo koje se sastoji od izvora elektriæne struje elektromotorne sile Ÿ i unutrašwe otpornosti r i spoqašweg provodnika (potrošaæa) otpornosti R (slika 6.8). Ovi elementi su spojeni u zatvoreno kolo pomoœu „idealnih“ provodnika (bez elektriæne otpornosti).
Jaæina elektriæne struje I ista je u svim delovima takvog, jednostavnog (nerazgranatog) elektriænog kola. Kao što znamo, u skladu sa zakonom odrþawa naelektrisawa, ne moþe doœi do nagomilavawa (razreðivawa) naelektrisanih æestica (nosilaca struje) u provodnicima elektriænog kola. Smer ove struje je isti u celom elektriænom kolu. U spoqašwem delu kola (provodniku, potrošaæu), od višeg ka niþem potencijalu, odnosno od kraja vezanog za pozitivan pol izvora ka kraju vezanom za negativan pol izvora. Kroz elektriæni izvor (unutrašwi deo kola) smer elektriæne struje je od niþeg potencijala (negativan pol izvora) ka višem potencijalu (pozitivan pol izvora).
Slika 6.8. Prosto elektriæno kolo jednosmerne struje
Na osnovu zakona odrþawa energije, primewenog na celo zatvoreno elektriæno kolo, elektriæno kolo utroši onoliko energije koliko se dobije u elektriænom izvoru. Elektriæna energija dobijena u elektriænom izvoru (na raæun transformacije mehaniæke, hemijske energije i drugih oblika energija u elektriænu energiju) pretvara se pri proticawu struje kroz elektriæno kolo u unutrašwu energiju izvora elektriæne struje i unutrašwu energiju otpornika (potrošaæa) vezanih u tom kolu: ŸIt = I2Rt + I2rt

Deobom ove jednaæine sa proizvodom It i rešavawem po I, dobija se formula Omovog zakona za zatvoreno elektriæno kolo:

Jaæina elektriæne struje u zatvorenom strujnom kolu srazmerna je elektromotornoj sili izvora,a obrnuto je proporcionalna zbiru elektriænih otpornosti svih provodnika (potrošaæa) u kolu.
U nerazgranatom elektriænom kolu moþe da bude veœi broj otpornika i izvora. Tada je jaæina struje u kolu srazmerna algebarskom zbiru svih elektromotornih sila u kolu, a obrnuto srazmerna zbiru svih otpornosti u kolu.


Kirchoff Gustav Robert (1824–1887)
KIRHOF GUSTAV ROBERT, nemaæki fiziæar, prouæavao je elektricitet, oblast mehanike i optike. Otkrio je zakonitosti u proticawu elektriæne struje u razgranatim elektriænim kolima (Kirhofova pravila). Uveo je pojam elektriænog potencijala. Doprineo je razradi metoda spektralne analize i otkrio element cezijum (1860). Uveo je pojam apsolutno crnog tela i otkrio osnovni zakon zraæewa apsolutno crnog tela (1860).
Do sada su razmatrana jednostavna (prosta) strujna kola, bez „granawa“, ali se najæešœe koriste sloþena (razgranata) elektriæna kola. Takva elektriæna kola imaju ævorove (taæke), u kojima se elektriæna struja razdvaja ili spaja kao što su to taæke
A i B na slici 6.9. U taæki A se elektriæna struja I grana na tri struje (I1, I2 i I3) koje prolaze kroz otpornike R1, R2, R3, pa onda one utiæu u ævor (taæku) B. U sloþenim elektriænim kolima, koja se sastoje od dve ili veœeg broja nerazgranatih kontura, jaæine elektriænih struja praktiæno je nemoguœe odrediti neposredno primenom Omovog zakona, veœ u kombinaciji sa ostalim fiziækim zakonima, tj. Kirhofovim pravilima.
Prvo Kirhofovo pravilo je posledica zakona odrþawa koliæine naelektrisawa, prema kojem ni u jednoj taæki elektriænog kola stalne elektriæne struje ne moþe da doðe do nagomilavawa naelektrisawa.

Algebarski zbir jaæina elektriænih struja u svakom ævoru elektriænog strujnog kola jednak je nuli:
SI = 0. IRr = +

Drugo Kirhofovo pravilo odnosi se na strujnu konturu, odnosno na svako nerazgranato ali zatvoreno strujno kolo od kojih se sastoji sloþeno, razgranato elektriæno strujno kolo.
U svakoj strujnoj konturi (razgranatog kola) algebarski zbir svih elektromotornih sila u toj konturi jednak je algebarskom zbiru elektriænih napona na svim otpornicima (potrošaæima) u istoj konturi.
SŸ = SRI
Drugo Kirhofovo pravilo je poseban oblik zakona odrþawa energije, primewen na strujno kolo. Na primer, ako pozitivna koliæina naelektrisawa q = I×t prolazi kroz celu zatvorenu konturu, prolazeœi kroz izvor elektriæne struje ona „dobija“ energiju qŸ, a prolazeœi kroz otpornik R u datoj konturi „gubi“ energiju qIR. Ukupna promena wegove energije prolaskom kroz celu konturu je jednaka nuli, pa je: qŸ = qIR Þ Ÿ = IR.

VEZIVAWE ELEKTRIÆNIH OTPORNIKA
Primena Omovog zakona i Kirhofovih pravila omoguœava da se reši problem vezivawa otpornika, odnosno odreðivawe ekvivalentne otpornosti kod serijske i paralelne veze otpornika.
U sluæaju serijske veze elektriænih otpornika (slika 6.10) elektriæna struja kroz oba otpornika protiæe istom jaæinom, pa sledi:
UUURIRI
URIRRR =+=+ =⋅⇒=+ 1212 12 ; SS
Slika 6.10. Serijska (redna) veza elektriænih otpornika
Ukupna (ekvivalentna) elektriæna otpornost serijski vezanih otpornika jednaka je zbiru pojedinaænih otpornosti.

Ukoliko su otpornici vezani paralelno (slika 6.11), elektriæna struja se grana, tako da se dobija:

Slika 6.11. Paralelna veza elektriænih otpornika
Reciproæna vrednost ekvivalentne otpornosti paralelno vezanih elektriænih otpornika jednaka je zbiru reciproænih vrednosti pojedinaænih otpornosti.
Primer 1. Kolika je unutrašwa elektriæna otpornost i elektromotorna sila izvora struje ako, pri spoqašwoj elektriænoj otpornosti od 2 Ω u kolu elektriæna struja ima jaæinu 0,8 A, a pri spoqašwoj otpornosti 3 Ω od 0,6 A?
Podaci: R1 = 2 Ω, I1 = 0,8 A, R2 = 3 Ω; I2 = 0,6 A; r = ? Ÿ = ?
Rešewa. Pošto u oba sluæaja elektromotorna sila izvora ima istu vrednost, sledi: I1R1 + I1r = I2R2 + I2r;
Odavde je:
Na osnovu Omovog zakona: Ÿ = I1(R1 + r) = 2, 4 V
Primer 2. Naœi vrednosti jaæine elektriænih struja u svakoj od tri grane elektriænog kola prikazanog na slici. Date su vrednosti: Ÿ = 25 V, R1 = 15 Ω, R2 = 10 Ω, R3 = 4 Ω. Unutrašwa otpornost izvora se zanemaruje.
Podaci: Ÿ = 25 V, R1 = 15 Ω, R2 = 10 Ω, R3 = 4 Ω; I1 = ? I2 = ? I3 = ?
Rešewa. Strelicama su oznaæeni pretpostavqeni smerovi elektriænih struja. Primenom Kirhofovih pravila, dobijaju se jednaæine:
Odavde sledi:



KONTAKTNIELEKTRIÆNIPOTENCIJAL
Krajem XVIII veka Volta je otkrio da se prilikom dodira dvaju razliæitih metala izmeðu wih javqa elektriæni potencijal koji je nazvan kontaktni potencijal. On je razliæit za razliæite parove metala i iznosi od nekoliko desetih delova volta do jednog volta. Mnogo zavisi i od æistoœe metala, a naroæito od æistoœe wihovih dodirnih površi.
Ustanovqeno je i to da kontaktni elektriæni potencijal dvaju metala A i B (slika 6.12) zavisi samo od temperature wihovog spoja i hemijskog sastava metala:
AB
Slika 6.12. kontaktni elektriæni potencijal dvaju metala A i B
UAB = DV = VA – VB = aT, gde je a – koeficijent koji zavisi od vrste metala (hemijskog sastava) i T – temperature spoja metala.
Sa stanovišta klasiæne elektronske teorije pojava kontaktnog elektriænog napona mogla bi se objasniti samo time što je broj slobodnih elektrona u razliæitim metalima razliæit. Oznaæimo broj elektrona u jedinici zapremine u metalu A sa nA, a u metalu B sa nB. Ako se pretpostavi da je nA < nB kroz dodirnu površ tih dvaju metala mawi broj elektrona œe difundovati u metal B nego iz metala B u metal A. Kao rezultat takvog stawa izmeðu metala A i B javqa se razlika potencijala. Usled toga nastaje elektriæno poqe æije je delovawe na elektrone takvo da se suprotstavqa procesu wihove daqe difuzije. Rezultat toga je da posle odreðenog vremena prestaje prelazak elektrona iz jednog metala u drugi.

Prethodno smo pokazali da se prilikom kontakta dvaju razliæitih metalnih provodnika stvara razlika elektriænih potencijala. Postavqa se pitawe da li se u sistemu od dva razliæita metalna provodnika A i B, koji su spojeni kao što pokazuje slika 6.13, moþe pojaviti elektriæna struja na raæun tog kontaktnog napona. Odgovor je negativan ako je ista temperatura oba spoja provodnika. Kada kontakti (spojevi) dva razliæita metalna provodnika imaju razliæite temperature, pojavquje se termoelektromotornasila, a time i elektriæna struja. Tu pojavu je prvi otkrio Zebek 1821. godine. Stoga se ova termoelektriæna pojava æesto naziva Zebekov efekat.


Ustanovqeno je da je termoelektromotorna sila kod metala srazmerna razlici temperature spojeva:
Ÿ = a(T2 – T1) = aDT Koeficijent srazmernosti a zavisi od prirode metalnih provodnika (hemijskog sastava i koncentracije slobodnih elektrona).
Slika 6.13. Spojevi dva metalna provodnika na razliæitim temperaturama
Zavisnost termoelektromotorne sile od razlike temperatura spojeva pribliþno je linearna ako te razlike nisu relativno velike. Meðutim, za veœe razlike temperatura ipak dolazi do odreðenih odstupawa, što se donekle moþe objasniti pojavom da se broj slobodnih elektrona u jedinici zapremine poveœava na visokim temperaturama. (Objasnite zašto se to dešava.)
Red veliæine termoelektromotorne sile iznosi nekoliko stohiqaditih delova volta za razliku temperature spojeva od jednog kelvina. Ako zamenimo jedan od metalnih provodnika poluprovodnikom, termoelektromotorna sila œe se znatno poveœati, pošto se koncentracija slobodnih elektrona u metalima i poluprovodnicima razlikuje za oko 105 puta. Veœa vrednost elektromotorne sile kod termopara metal–poluprovodnik u odnosu na termopar metal–metal pod istim uslovima potvrðuje se i eksperimentalno. Vrednost termoelektromotorne sile kod termoparova metal–poluprovodnik moþe imati vrednost reda veliæine 10–3 V za razliku temperatura spojeva od 1°C (1 K).
Termoelektriæne pojave mogu da se upotrebe za merewe visokih temperatura, kao i za indikaciju niskih temperatura. Za merewe vrlo visokih temperatura koriste se termoparovi ili termoelementi. Jedan kontakt stavqa se u sredinu æija je temperatura konstantna, na primer u sud sa ledom koji se topi, a drugi kontakt u sredinu æiju temperaturu treba izmeriti.
Termoelektromotorna sila koja se javqa u kolu meri se pomoœu milivoltmetra. Ako je temperatura jednog spoja poznata, na jednostavan naæin se nalazi temperatura drugog spoja. Za termoparove sastavqene od odreðenih metala, voltmetar moþe biti neposredno graduisan u stepenima (°C ili K).
Osim toga, termoparovi se mogu koristiti i kao izvori elektriæne struje. Odreðenim kombinacijama provodnika i poluprovodnika i vezivawem termoparova redno u termobateriju, moþe se dobiti termoelektromotorna sila i do nekoliko desetina volti. Wima se mogu napajati radio-prijemnici, razni ureðaji u nuklearnim reaktorima gde postoje velike razlike temperatura itd.


Kada elektriæna struja prolazi kroz metalne provodnike, u wima se ne dešavaju hemijske promene. Ovo se objašwava time što su nosioci struje u metalima – elektroni. Meðutim, postoje i takve vrste provodnika (rastvori soli, kiselina i baza) u kojima elektriænu struju prate hemijski procesi. Takvi provodnici se nazivaju elektroliti.

Hemijski æiste teænosti kao što su destilovana voda, alkohol, aceton, etar i mnoge druge praktiæno ne provode elektriænu struju. Ali, kada se u wima rastvore soli, kiseline ili baze, ove teænosti postaju elektriæni provodnici. Nosioci elektriæne struje u elektrolitima su pozitivni i negativni joni.
Kada se elektriæna struja propusti, na primer, kroz vodeni rastvor sone kiseline (HCl), dolazi do izdvajawa hlora na anodi i vodonika na katodi, ako su elektrode od platine (slika 6.14). U datom sluæaju nosioci struje su negativni joni hlora i pozitivni joni vodonika.
Nameœe se pitawe, kako se obrazuju slobodni joni u rastvorima soli, kiselina i baza? Dok nisu rastvorene, ove supstancije su dobri izolatori, kao što je to i sam rastvaraæ (voda, na primer). Utvrðeno je da joni nastaju prilikom rastvarawa nekih supstancija usled uzajamnog delovawa wihovih molekula sa molekulima rastvaraæa (najæešœe vode).
Slika 6.14. Elektrolit je provodnik elektriæne struje
Proces obrazovawa slobodnih jona pri rastvarawu soli,kiselina ili baza naziva se elektrolitiæka disocijacija (poznato iz hemije).
Molekuli soli, kiselina i baza sastoje se od pozitivnih i negativnih jona, koje u molekulu vezuju elektriæne sile. Molekuli rastvaraæa imaju asimetriæan raspored negativno naelektrisanih æestica (elektrona) i pozitivnih jezgara. Na jednoj strani molekula koncentracija elektrona je veœa a na suprotnoj strani mawa, tako da oni æine elektriæni dipol. Prilikom rastvarawa, molekuli rastvaraæa „opkoqavaju“ svaki molekul rastvorene supstancije, orijentišuœi se oko wegovih povezanih jona. Na slici 6.15. je prikazan (polarni) molekul sone kiseline rastvorene u vodi. Molekuli vode koji na ovaj naæin opkoqavaju molekul HCl deluju na wega veoma jakim elektriænim silama jer su meðumolekulska rastojawa u teænostima mala (reda veliæine 10–10m). Zato je voda dobar rastvaraæ. 6.2.



Usled toga molekul HCl postaje razvuæen i veza izmeðu wegovih jona (H+ i Cl–) toliko oslabi da se pri sudaru sa drugim molekulima, u toku toplotnog kretawa, lako raskida. Znaæi, joni H+ i Cl–, vezani u molekule HCl, koji su postojali i pre rastvarawa i disocijacije, oslobaðaju se u rastvoru usled oslabqene meðusobne veze i toplotnog kretawa. (Disocijacija znaæi razjediwavawe, raspad molekula.) Molekul date supstancije, bez obzira na vrstu rastvaraæa (voda, alkohol, i dr.), disosuje uvek na isti naæin: HCl se uvek raspada na H+ i Cl–, NaCl na Na+ i Cl–, H2SO4 na 2H+ i SO4 2 – itd.
Uporedo sa disocijacijom, dešava se suprotan proces. U toku haotiænog toplotnog kretawa dolazi i do susreta (sudara) jona suprotnih naelektrisawa i wihovog sjediwavawa u neutralan molekul. Ovaj proces se naziva rekombinacija jona. U poæetnoj fazi rastvarawa preovlaðuje disocijacija, ali se ubrzo uspostavqa dinamiæka ravnoteþa kada je broj rekombinacija izjednaæen s brojem disocijacija u jedinici vremena. Broj parova (pozitivan i negativan jon æine jedan par) slobodnih jona u rastvoru tada je konstantan, ako se ne mewaju temperatura i koncentracija rastvora. Elektrolitiæki procesi prikazuju se šematski na sledeœi naæin:
¶¶¶¶¶¶l + k¶¶¶¶¶¶
disocijacija rekombinacija katjonianjoni
¶¶¶¶¶¶l + k¶¶¶¶¶¶
¶¶¶¶¶¶l + k¶¶¶¶¶¶
¶¶¶¶¶¶l + k¶¶¶¶¶¶
¶¶¶¶¶¶l + k¶¶¶¶¶¶



FARADEJ MAJKL , poznati engleski fiziæar. Eksperimentima u oblasti elektromagnetizma postavio temeqe elektrotehnike.
Erstedov ogled (1820), kojim je otkriveno delovawe provodnika sa strujom na magnetnu iglu, inspirisao je Faradeja na daqa prouæavawa uzajamne veze elektriænih i magnetnih pojava. Faradej je prvi ostvario obrtawe magneta oko provodnika sa strujom i provodnika sa strujom oko magneta i time napravio model elektromotora (1821). Faradej je iste godine postavio sebi ciq: „pretvoriti magnetizam u elektricitet“.

Pojavu elektromagnetne indukcije Faradej je otkrio 1831. godine. Ustanovio je osnovni zakon elektromagnetne indukcije.
Faradej je otkrio osnovne zakone hemijske elektrolize (1833–1835). Postulirao je postojawe jona. Uveo je pojmove: elektrolit, elektroda, katoda i anoda Zato se Faradej smatra osnivaæem elektrohemije.
Faradej je prvi uveo pojam fiziæko poqe i slikovito ga prikazao linijama sile. Po Ajnštajnovim reæima, ideja poqa bila je najoriginalnija ideja i jedno od najveœih otkriœa u fizici od Wutnovih vremena. Kod Wutna se prostor posmatra kao „pasivan“ magacin (spremište) materije. Meðutim, kod Faradeja prostor uæestvuje u pojavama, prostor je, u stvari, spremište pojava, a ne samo tela i æestica. Za opisivawe elektriænog i magnetnog poqa Faradej je uveo predstavu o linijama sile. Na taj naæin Faradej je zaæetnik uæewa o elektromagnetnom poqu, koje kasnije i postaje predmet Maksvelovih prouæavawa.
U znak poštovawa Faradeja, uvedena je jedinica elektriæne kapacitivnosti farad (F).
Kada se u elektrolitu uspostavi elektriæno poqe, kretawe jona postaje ureðeno (usmereno) prema elektrodama. Pod dejstvom ovog poqa pozitivni joni (katjoni) kreœu se ka negativnoj elektrodi K (katodi), a negativni joni (anjoni) – ka pozitivnoj elektrodi A (anodi), slika 6.16. Usmereno kretawe jona u elektrolitima uslovqava pojavu elektriæne struje. Prolazak elektriæne struje kroz elektrolit prati pojava elektrolize
Elektroliza je izdvajawe supstancije na elektrodama u elektrolitu pri prolasku,odnosno pomoœu elektriæne struje.
Pri proticawu elektriæne struje kroz elektrolite, zajedno sa naelektrisawem prenosi se i supstancija, pošto su nosioci struje u tim provodnicima joni. Masa supstancije koja se izdvaja na elektrodama pri prolasku elektriæne struje kroz elektrolite odreðuje se Faradejevim zakonima elektrolize.
Slika 6.16. Tok elektriæne struje u elektrolitu

Masa supstancije koja se izdvaja na jednoj elektrodi,srazmerna je ukupnoj koliæini naelektrisawa koje proðe kroz elektrolit: m=kq=kIt, jer je I=q/t – jaæina stalne struje koja protiæe kroz elektrolit u toku vremena t. Koeficijent proporcionalnosti k naziva se elektrohemijski ekvivalent supstancije. To je karakteristiæna veliæina za svaki hemijski element (tabela 6.2).
Fiziæki smisao prvog Faradejevog zakona sadrþan je u mehanizmu jonske provodqivosti i pojave elektrolize. Što veœa koliæina naelektrisawa proðe kroz elektrolit, to je veœi broj jona dospeo do elektroda. Pozitivni joni, pri kontaktu s katodom, dopuwavaju mawak elektrona i izdvajaju se na katodi u


obliku neutralnih atoma. Negativni joni u kontaktu sa anodom otpuštaju višak elektrona i u neutralnom stawu se oslobaðaju na anodi. Svaki jon nataloþen na elektrodi prenosi odreðenu koliæinu naelektrisawa. Dakle, ukupna koliæina naelektrisawa prenešena svim jonima, jednaka je zbiru koliæine naelektrisawa svih jona pojedinaæno, što je neposredno vezano i za masu supstancije koja se izdvoji na elektrodama elektrolita
Supstancija Elektrohemijski ekvivalent (k), 10–6 kg/C.
Srebro 1,118
Vodonik 0,01045
Bakar 0,3294
Cink 0,0388
Tabela 6.2. Elektrohemijski ekvivalent nekih supstancija

Slika 6.17. Ilustracija drugog Faradejevog zakona elektrolize
Kroz niz elektrolita sa razliæitim elektrodama propušta se elektriæna struja iste jaæine (slika 6.17). Dakle, pri tome, kroz elektrolite u toku istog vremenskog intervala proðu jednake koliæine naelektrisawa. Merewem je utvrðeno da se na elektrodama izdvajaju razliæite mase supstancije.
Na osnovu merewa izvršenih sa razliæitim rastvorima, Faradej je došao do formulacije drugog zakona elektrolize. Elektrohemijski ekvivalent srazmeran je odnosu atomske mase elementa (A) i wegove valentnosti (z): kA Fz 1 . =


Odnosatomskemaseihemijskevalentnosti nazivase hemijskiekvivalent, pase drugi Faradejev zakon elektrolize moþe definisati i na drugaæiji naæin.
Elektrohemijski ekvivalenti supstancija srazmerni su wihovim hemijskim ekvivalentima.
Veliæina F je univerzalna konstanta, koja se naziva Faradejev broj, æija vrednost iznosi 9,65×104 C/mol
Kombinacijom prvog i drugog zakona dobija se:
a odakle je

Kada je uspostavqeno elektriæno poqe (prikquæewem elektroda na elektriæni napon) dolazi do proticawa elektriæne struje kroz elektrolit. Da li je moguœ obrnuti proces od elektrolize? Da li se moþe dobiti razlika potencijala na elektrodama ako su one potopqene u elektrolit?
To je moguœe ukoliko su elektrode od razliæitih metala. Kontaktni potencijal se tada uspostavqa izmeðu elektroda posredstvom elektrolita. Ukoliko se elektrode poveþu preko nekog potrošaæa (otpornika, sijalice, itd.), kroz wega œe proticati elektriæna struja. Slika 6.18 simboliæki predstavqa prvi takav sistem.
H2O+H2SO4
Ovakvi sistemi – galvanski elementi, na osnovu elektrolitiæke disocijacije i hemijskih reakcija, proizvode jone koji se kreœu ka razliæitim elektrodama. Elektrode se polarišu razliæitim elektriænim potencijalima. Izmeðu elektroda se pojavquje EMS i galvanski element sluþi kao izvor jednosmerne struje.
Slika 6.18. Voltin galvanski element
Najpoznatiji je Leklanšeov element – mi ga nazivamo baterijom. Wegova EMS iznosi 1,5 V, a ima jednu ugqenu šipku (anoda) unutar cilindra od cinka (katoda). Elektrolit je u ævrstom stawu.


4. 3.
Primer 3. Proces elektrolize ostvaruje se elektriænom strujom jaæine 5A utoku jednog sata. Kolika je temperatura izdvojenog vodonika u atomskom obliku, ako je pri pritisku 104Pa wegova zapremina 0,5 ", elektrohemijski ekvivalent vodonika 1,0 10–8 kg/C, a koeficijent korisnog dejstva ureðaja je 70%?
Podaci: t = 1 h = 3600 s; I = 5 A, p = 104 Pa, V = 0,5 " = 0,5×10–4 m3 , k =1,0×10–8 kg/C, h = 0,7; T = ?
Rešewe. Prema Faradejevom zakonu, masa izdvojenog vodonika, s obzirom na vrednosti koeficijenta korisnog dejstva ureðaja, iznosi
m = h kIt.
Iz jednaæine gasnog stawa, imamo:
gde je R – univerzalna gasna konstanta (R = 8,31 J/molK), M – molska masa vodonika, pa je onda
Primer 4. Kako se odnose mase hemijskih elemenata istih valentnosti, koje se izdvoje na elektrodama za isti vremenski interval i pri neizmewenoj vrednosti jaæine elektriæne struje?
Rešewe. Na osnovu Faradejevog zakona elektrolize, nalazi se da je: m1 =k1 It i m2 =k2 It, odnosno:
Nataloþene mase elemenata se pri elektrolizi takoðe odnose kao elektrohemijski ekvivalenti, odnosno wihovi maseni brojevi.

1. Šta su elektroliti?
2. Kako nastaju nosioci struje u elektrolitima?
3. Na osnovu æega se zakquæuje da su pozitivni i negativni joni vezani jedni za druge, dok se nalaze u molekulima pre rastvarawa?
4. Šta je elektrohemijski ekvivalent i od æega on zavisi?
5. Kako se na osnovu Faradejevih zakona moþe odrediti naelektrisawe jednog jona u elektrolitu?

U normalnim uslovima (kada su pod atmosferskim ili veœim pritiskom), gasovi su dobri izolatori jer nemaju slobodne elektrone ili jone. Meðutim, ako se deo molekula (atoma) jonizuje, gasovi mogu postati provodnici elektriæne struje.

Ako se od molekula (atoma) gasa pod nekim spoqašwim uticajem odvoji jedan ili više elektrona, onda nastaje proces koji se zove jonizacija. Tada dolazi do odvajawa (pojave) jona i slobodnih elektrona koji su nosioci elektriæne struje.
Elektriæna provodqivost u gasovima se ostvaruje jonima i slobodnim elektronima.
Jonizacija gasa se moþe izvršiti na više naæina: zagrevawem (disocijacijom molekula gasa na plamenu), izlagawem gasova rendgenskim i ultravioletnim zracima ili radioaktivnim æesticama uopšteno nazvanim jonizatori . Elektriæna provodqivost gasova je utoliko veœa ukoliko je intenzivniji proces jonizacije, to jest ukoliko postoji veœi broj pozitivnih jona i slobodnih elektrona.
Kada ne postoji elektriæno poqe koje bi usmeravalo kretawe slobodnih elektrona i jona u gasu, onda se oni kreœu haotiæno i interaguju jedni s drugima, i tako obrazuju neutralne molekule (atome). Proces sjediwavawa suprotno naelektrisanih jona (u gasovima najæešœe pozitivno naelektrisanih jona i slobodnih elektrona) naziva se rekombinacija.
Kada se elektriæna struja kroz gasove ostvaruje delovawem nekog spoqašweg uticaja (jonizatora), onda se takvo elektriæno praþwewe naziva nesamostalno praþwewe. Prestankom delovawa spoqašwih uticaja (plamena, radioaktivnog izvora, izvora rendgenskog zraæewa itd.), nesamostalno praþwewe se prekida. Za ispitivawe zavisnosti jaæine elektriæne struje od elektriænog napona meðu elektrodama, pri nesamostalnom praþwewu u gasu moþe se koristiti ureðaj æija je šema predstavqena na slici 6.19a. U staklenoj cevi postavqene su dve elektrode (metalne ploæice), katoda K, spojena s negativnim polom izvora jednosmerne struje, i anoda A, spojena s pozitivnim polom izvora. Cev se puni nekim æistim gasom do odreðenog pritiska, obiæno znatno maweg od atmosferskog. Elektriæni napon meðu elektrodama A i K reguliše se pomoœu potenciometra P i meri se voltmetrom V. Za merewe jaæine elektriæne struje koristi se osetqivi galvanometar G. Gas se jonizuje, na primer, rendgenskim zracima.


Na slici 6.19b prikazana je zavisnost jaæine elektriæne struje od elektriænog napona (tzv. strujna ili I–U karakteristika) kada se intenzivnost jonizacije, rastojawe izmeðu elektroda, vrsta gasa i pritisak ne mewaju.

Joni koji nastaju u gasovima neposredno pod uticajem spoqašweg jonizatora (na primer rendgenskog ili nekog drugog zraæewa) nazivaju se primarni joni. Oni na svom slobodnom putu (rastojawe izmeðu dva uzastopna sudara æestica) dobijaju izvesnu energiju od elektriænog poqa, koju pri interakciji (sudaru) predaju molekulima (atomima) gasa. Poveœawem napona meðu elektrodama, ova energija jona raste. Pri odreðenim vrednostima tog napona energija primarnih jona dostiþe vrednost koja je jednaka ili veœa od energije jonizacije molekula (atoma) gasa. Tada su inicijalni (primarni joni) u moguœnosti da jonizuju neutralne molekule (atome) kada sa wima stupe u interakciju. Tako nastaju tzv. sekundarni joni, koji se takoðe ubrzavaju elektriænim poqem i sa svoje strane mogu da jonizuju sledeœe molekule (atome) gasa. Usled toga broj naelektrisanih æestica naglo raste, pojavquje se jonska lavina. Nastaje tzv. proces udarne jonizacije (slika 6.20).
Normalno, u procesu udarne jonizacije naglo raste i jaæina elektriæne struje u kolu. Nagli porast ove struje pri udarnoj jonizaciji objašwava se time što sekundarni joni (elektroni i pozitivni joni) postaju dodatni nosioci elektriæne struje.

Pri dovoqno velikim vrednostima elektriænog napona, broj sekundarnih jona moþe biti toliko veliki da se broj primarnih jona moþe praktiæno zanemariti, a time i uticaj spoqašweg jonizatora na proticawe struje u gasovima.
Tada nesamostalno gasno praþwewe prelazi u samostalno praþwewe Kada elektriæna struja u gasovima moþe sama od sebe da se odrþava,praþwewe je samostalno.


Prelazak gasa u samostalno praþwewe zove se proboj gasa (Up, slika 6.17b), a vrednost elektriænog napona pri kome se to dešava – probojni napon
Napon pri kojem dolazi do proboja gasa je relativno visok i zavisi od pritiska, vrste gasa i od rastojawa meðu elektrodama. Za vazduh pod normalnim uslovima za proboj (pojavu elektriæne varnice) potrebno je elektriæno poqe od oko 30000 V/cm.
Ukoliko se u gasu uspostavi izuzetno velika koncentracija jona – visokojonizovano stawe, ono moþe da preðe u plazmu. Plazma predstavqa tzv. æetvrto agregatno stawe supstancije koje karakteriše kolektivno svojstvo: u tom stawu æestice (molekuli, zapravo sve su joni) „gube“ individualnost i ponašaju se svi udruþeno („socijalizovano“).
• Elektriæna struja je ureðeno (usmereno) kretawe naelektrisanih æestica (elektrona,jona i dr.).
Elektriæna provodqivost metala je uslovqena kretawem slobodnih elektrona, u teænim telima kretawem pozitivnih i negativnih jona, a u gasovima – kretawem elektrona i jona.
Usled uzajamnog delovawa nosilaca elektriæne struje oni gube kinetiæku energiju. Zato je za odrþavawe struje neophodan izvor struje. Svaki izvor elektriæne struje karakteriše elektromotorna sila i unutrašwa otpornost izvora. Elektromotorna sila odgovara razlici potencijala na polovima otvorenog izvora elektriæne struje.
• Kvantitativna karakteristika elektriæne struje je wena jaæina:
Jaæina struje brojno je jednaka koliæini naelektrisawa koja proðe kroz normalan popreæni presek provodnika za jediniæno vreme.
Odreðena je odnosom napona na krajevima provodnika i wegovog elektriænog otpora.
Jedinica jaæine struje je amper (A). Pošto je jedinica koliæine naelektrisawa kulon (C), sledi da je amper jednak kulon u sekundi (A=C/s).


• Omov zakon za deo elektriænog strujnog kola:

Jaæina elektriæne struje u delu elektriænog kola odreðena je odnosom napona na krajevima tog dela kola i wegove elektriæne otpornosti.
Elektriæna otpornost metalnog provodnika zavisi od prirode materijala od kojeg je izraðen, duþine i površine popreænog preseka:
gde je r – specifiæna elektriæna otpornost. Jedinica elektriæne otpornosti je om (Ω).
Drugi oblik Omovog zakona daje vezu izmeðu gustine elektriæne struje (®j ) koju izaziva elektriæno poqe i jaæine tog poqa ® E :
®j = s ® E,
gde je specifiæna elektriæna provodqivost materijala.
Omov zakon za celo elektriæno kolo odreðuje zavisnost izmeðu jaæine elektriæne struje,elektromotorne sile izvora i ukupne elektriæne otpornosti kola:
• Koliæina toplote koja se izdvaja u provodniku sa elektriænom strujom, saglasno Xul–Lencovom zakonu, jednaka je:
QIRtUItUt
Osloboðena koliæina toplote u provodniku (otporniku,potrošaæu) srezmerna je kvadratu jaæine elektriæne struje,otpornosti (potrošaæa) i vremenu proticawa ove struje. Jedinica za koliæinu toplote, odnosno energije je xul (J).
• Za rešavawe zadataka kod sloþenog (razgranatog) elektriænog strujnog kola, pored Omovog zakona, koriste se i Kirhofovapravila:


Prvo Kirhofovo pravilo odnosi se na ævorove u koje struje utiæu, odnosno iz kojih istiæu u pojedinim granama elektriænog kola.
1. Algebarski zbir jaæina elektriænih struja u ævoru strujnog kola jednak je nuli:
S I = 0.
Drugo Kirhofovo pravilo primewuje se na pojedine zatvorene konture sloþenog (razgranatog) elektriænog kola.
2. U svakoj strujnoj konturi razgranatog elektriænog kola algebarski zbir elektromotornih sila jednak je algebarskom zbiru elektriænih napona na svim otpornicima (potrošaæima) u toj strujnoj konturi:
S Ÿ = S IR .

• Proces spontanog obrazovawa slobodnih jona u rastvorima soli, kiselina i baza naziva se elektrolitiæka disocijacija.
Elektroliza je izdvajawe supstancije na elektrodama u elektrolitu pri prolasku elektriæne struje.
Faradejevi zakoni glase:
Prvi Faradejev zakon.Masa supstancije koja se izdvaja na jednoj elektrodi srazmerna je ukupnoj koliæini naelektrisawa koje proðe kroz elektrolit:
m=kq=kIt.
Elektrohemijski ekvivalent (k) je karakteristika elektrolita.
Drugi Faradejev zakon.Elektrohemijski ekvivalent srazmeran je odnosu atomske mase i wegove valentnosti:
Odnos atomske mase i hemijske valentnosti (A/z) naziva se hemijski ekvivalent. Faradejeva broj (F) brojno je jednaka koliæini naelektrisawa kojom se iz elektrolita izdvoji koliæina supstancije od jednog mola.
1. Na koje naæine se moþe prouzrokovati jonizacija gasova?
2. U æemu je razlika izmeðu disocijacije elektrolita i jonizacije gasova?
3. Zbog æega se broj jona u gasu koji je izloþen delovawu konstantnog jonizatora poveœava samo do odreðene vrednosti, a zatim postaje stalan?
4. Po æemu se razlikuje samostalno elektriæno provoðewe (praþwewe) gasa od nesamostalnog?


Avogadrov broj 15, 20
Avogadrov zakon 20
agregatno stawe 52, 64, 65
ævrsto 82–58, 64 teæno 52, 64, 65 gasovito 52, 64 amorfno telo 54, 56, 65 anjon 100
Bernulijeva jednaæina 46–51
Bolcmanova konstanta 10 brzina molekula (atoma) 9, 10, 12, 15 najverovatnija 9, 10, 15 sredwi kvadrat brzine 12
viskoznost 59, 60 koeficijent viskoznosti 60
Galvanski element 107
Deformacija tela 56–63 elastiæna 56, 57 istezawe 57 plastiæna 57 sabijawe 56 smicawe 57
dielektriæna propustqivost 72, 73 relativna 73 disocijacija 103
elektrolitiæka 103
Ekvipotencijalna površ 80, 81 elektriæna kapacitivnost 82, 86 jedinica (farad) 82 elektriæna provodqivost 89 elektriæna sila 72–74
elektriæna struja 88–98, 110 gustina struje 90, 91, 112 jaæina struje 90–98, 108 elektriæni napon (potencijal) 77 elektromotorna sila 89, 90 izvor struje 90 95–98
elektriæna struja u gasovima 109 varniæko praþwewe 109 nesamostalno praþwewe 111 samostalno praþwewe 111
elektriæno kolo 92–98
elektriæno poqe 74, 87 gustina energije 84, 86, 91 energija 84–87 jaæina 74–81, 86 linije sile 74–81 napon (potencijal) 75–81
elektroliza 104–107
elektrolit 103–107
elektron 70, 71, 88, 89
elektronski gas 88, 89
elektrohemijski ekvivalent 105 entropija, termodinamiæka 34–37, 41
Zakoni, gasni 15, 16
Bojl–Mariotov 16, 17, 23
Gej-Lisakov 19, 20, 23
Šarlov 18, 23
Zakon odrþawa koliæine naelektrisawa 77
Idealni gas 10–23
gasna (univerzalna) konstanta 15, 21, 22 jednaæina stawa 13, 20–22 model 10, 11 pritisak 11–13, 22 sredwa kinetiæka energija 12–15, 22 izolator, elektriæni 89 isparavawe teænosti 66, 67
Jednaæina kontinuiteta 45, 46, 50 joni 88, 89, 99–101 jonizator 109 jonizacija 109–111 Jungov moduo (modul) 57, 63
Kapilarne pojave 62 katjon 105 Kirhofova pravila 96–98, 112 koeficijent korisnog dejstva 39, 40, 43 koeficijent termiækog širewa54 koliæina naelektrisawa 71–78 jedinica (kulon) 71–78 elementarna 71 koliæina toplote 26–32, 41 kondenzator, elektriæni 83–87 energija 84 kondenzacija 66, 67 kontaktni potencijal 99 kruþni, termodinamiæki proces 33 Kulonov zakon 72, 73
Laminarno proticawe teænosti 59
Mašine (toplotne), motori 37, 38 Maksvelova raspodela molekula po brzinama 9 mlaznica 49 mol 20 molekulska sila 52, 53 monokristal 56
Nepovratni (termodinamiæki) proces 33, 34 neutron 70 normalni napon (kod deformacije) 56, 57
Wutnov zakon viskoznosti 59, 60, 63 Omov zakon (strujnog) kola 92, 93–98 otpornik, elektriæni 96–98 otpornost (otpor) provodnika 92, 93 jedinica (om) 92 specifiæni 93 oævršœavawe (kristalizacija) 65, 66, 68
Perpetuum mobile druge vrste 36 perpetuum mobile prve vrste 28
Pitoova cev 49 plazma 111 plastiæno telo 57 Poasonov broj 32
Poasonova formula (jednaæina) 32 povratni, termiæki proces 33 površinski napon teænosti 61, 63 polikristal 56 poluprovodnik 89 principi termodinamike drugi 36, 41 prvi 27, 41 provodnik, elektriæni 89 proton 70, 73, 77 procesi, u gasovima 15 adijabatski 32, 41 izobarski 20 izotermiski 16, 17, 41 izohorski 18, 28
Rad, sile 29, 76, 77, 79, 81, 86 elektriæne 76, 77, 81, 86 Zemqine teþe 79 pritiska gasa 29 rekombinacija 102
Sila 56, 57, 61–63 viskoznosti 59, 60, 63 elastiænosti 56, 57 molekulska 52, 61, 63 površinskog napona 61 specifiæna koliæina toplote isparavawa 66–69 kondenzovawa (isparavawa) 67–69 topqewa (oævršœavawa) 65, 67–69 faznog prelaza 65–69 Stoksov zakon viskoznosti 60, 63 sublimacija 66
Tangencijalni napon 57 taæka kquæawa 67–69 taæka oævršœavawa (kristalizacije) 65
taæka topqewa 65, 66 temperatura, apsolutna 14–27, 30–42 apsolutna nula 14 Kelvinova (apsolutna) skala 14 Celzijusova (konvencionalna) skala 14 termodinamika 24–42 termodinamiæki (kruþni) ciklus 33 termodinamiæko stawe ravnoteþe 37 termoelektriæne pojave 99 termoelektromotorna sila 106 termoelement 102 toplotna kapacitivnost 30, 31 toplotni motor 37–39 toplotno širewe tela 53, 54 Toriæelijeva teorema 48 trojna taæka 66
Unutrašwa energija 25–32, 41, 42, 95, 96
Fazni prelazi 64–70 Faradejevi zakoni elektrolize 104–106 drugi zakon 105, 106 prvi zakon 105 fluid, idealni 44–51 brzina 47–51 gustina 47–51 deliœ (æestica) 47, 48 pritisak 47–51 protok 46, 50 stacionarno strujawe 44–48 strujna linija 45–51 strujna cev 45–51
Hemijski ekvivalent 106 Hukov zakon 56, 57, 63
Ævrsto telo 54–57, 65 amorfno 54
elementarna œelija kristalne rešetke 55 kristalna rešetka (model) 54–56
Xul–Lencov zakon 94, 95
1.Milan O. Raspopoviœ, Jovan P. Šetrajæiœ, Zoran M. Raspopoviœ, Fizika za 2. razred gimnazije opšteg i društveno-jeziækog smera, Zavod za uxbenike, Beograd 2020.
2. David Halliday,Robert Resnick,Jearl Walker, Fundamentals ofPhysics,John Wiley & Sons,New York,1993.
3.James S. Walker, Physics,Prentice Hall,New Jersey,2001.
4.Randal Henly, Physics Today,CJ Fallon,Dublin,2000.
5.Nataša Æalukoviœ, Bojana Nikiœ, Milan Raspopoviœ, Zbirka zadataka iz fizike II deo, Klub NT, Beograd, 1993.
6.Mladi fiziæar, æasopis za uæenike osnovne škole, Društvo fiziæara Srbije, Beograd
7.Branko Radivojeviœ, Bogdan Pušara, Dragan Kaprin, Priruænik iz fizike za II razred gimnazije, Zavod za uxbenike i nastavna sredstva, Beograd, 1993.
8.D. Rakoviœ, Fiziæke osnove i karakteristike elektrotehniækih materijala FTN, Beograd 1995.
9.G. Dimiœ i M. Mitrinoviœ, Metrologija u fizici – kurs D, Graðevinska kwiga, Beograd 1990.
Коректура Зав од з