ХЕМИЈА

Dragi u~enici,
повезаности науке са свакодневним животом, али и пробудити свест о потреби очувања наше животне средине. Указаће вам, такође,
која у оквиру њих изучавате: биологијом, географијом, физиком и сл.
Онима међу вама чија научна радозналост превазилази програ-
Autori



























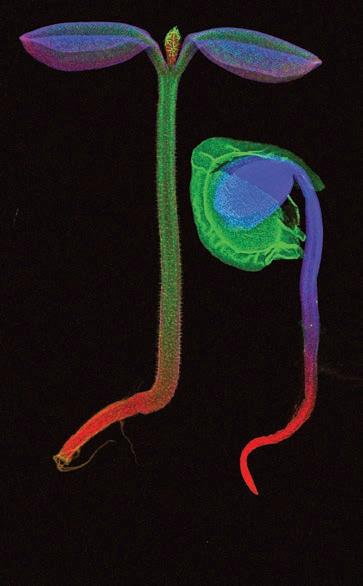
Zanimqivost iz biologije
Podsetnik















































Када се каже „злато”, одмах се помишља на нешто ексклузивно, вредно и луксузно. Није ни чудо јер је, у ствари, злато елемент који се налази у природи у елементарном стању. Његова хемијска стабилност, односно хемијска инертност на ваздуху, омогућила је трговину
који сија као Сунце.
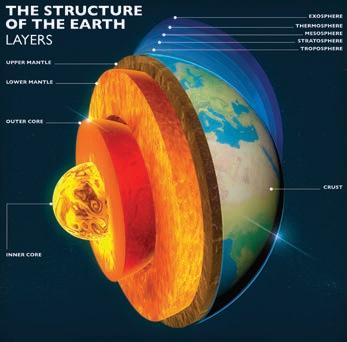
Шта су метали?
Метали заузимају
























































Zanimqivost iz biologije





открио је 1807. године енглески хемичар Хемфри Дејви (Sir Humphry Davy), први електролизом каустичне соде NaOH, други електролизом калијум-хидроксида KOH. Хемфри Дејви (17781829) је био енглески хемичар и физичар, члан Британског краљевског
Заслужан је
открића. Осим што је успео да електролизом раздвоји хемијске


овакав начин складиштења разјаснићемо једним једноставним огледом.
ДЕМОНСТРАЦИОНИ ОГЛЕД
Током извођења огледа обавезно носите заштитне рукавице и наочаре. Уколико немате прописну заштиту, извођење огледа препустите наставнику. За овај оглед потребни су вам елементарни натријум и/или калијум, пинцета, ножић, сахатно стакло или
стаклена плочица, лакмус хартија, стаклена чаша од најмање једног литра, коју ћете напунити водом.
Натријум се чува у петролеуму. Како је јако мекан, користећи
пинцету и ножић исеците врло мало парче и пажљиво убаците у стаклену чашу с водом. Тестирајте водени раствор лакмус хартијом. Своја запажања забележите
















Podsetnik





с магнезијумом и калцијумом су и берилијум, стронцијум,


као и пластична цевчица за сок.
Магнезијум и калцијум прво покушајте да
магнезијумову




кречњакнегашени
Ca(OH)2 +CO2 CaCO3 малтер
фекцију, заштиту


Podsetnik

металима, с тим што стабилну електронску
су алкал-
ПИТАЊА
1.
2.
3.
4.
5.


Гвожђе и бакар познати су од давнина; први елемент се на латинском каже ferrum, што значи гвожђе. Назив другог елемента потиче од латинског назива за Кипар cuprum, јер су стари Римљани
бакар издвајали из земље с острва Кипар. Алуминијум је 1827. године изоловао немачки научник Фридрих Велер. Овај елемент је
добио назив од латинске речи alumen, што значи стипса. (Стипса је
назив за једињење алуминијума.)
Фридрих Велер (18001882) је немачки хемичар који је, осим за
откриће алуминијума, заслужан и за откриће берилијума. Први је
успео да синтетише органску супстанцу (уреу-карбамид) од неорганских, што се у то време сматрало немогућим. Слика – 1.28. Фридрих
Гвоздено доба је период протоисторије (1200550. пре н. е.), назван по једном од најпознатијих метала. Бакарно доба (35002000. пре н. е.), које се назива и енеолит, иако старије од гвозденог, име је добило по овом црвенкастом сјајном металу. Разлог што су ова доба добила имена баш по њима је изузетна употребна вредност ових метала, који су коришћени за израду оружја, оруђа, накита. (Да ли знате које доба је између гвозденог и бакарног?)
За разлику од изразитих метала, који су релативно сличних карактеристика, прелазни и остали метали су често специфичних
ковност, савитљивост. Иако се у природи налазе у
минерала и руда, неке мале количине гвожђа
тарном облику. Док су гвожђе
боје, бакар је црвенкаст.
духу, кородирају.
Шта је корозија?
Корозија је физичко-хемијска реакција оксидације метала која се одвија под утицајем кисеоника, водене паре, угљен-диоксида. Погледајмо то на примеру гвожђа, бакра и алуминијума:



речи







4 Fe+3 O2 2 Fe2O3
гвожђе(III)-оксид, 2Cu+O2 2 CuO


бакар(II)-оксид, 4 Al+3 O2 2 Al2O3
алуминијум-оксид.



























Podsetnik

















ОЛОВО И ЦИНК
Марграф (17091782) је био немачки хемичар који је увео неколико нових
хемију.
био једини који је изоловао цинк, њему се приписују заслуге јер је детаљно описао поступак изоловања овог елемента.
дуктилност (на латинском ductiles значи мек, означава својство
формира заштитни слој



Мањак цинка узрокује успоравање раста и правилног развоја, осетљивост на инфекције. Ензими са цинковим атомом у реактивном центру су распрострањени у биохемији (као што је алкохол-дехидрогеназа, коју ћемо разматрати касније). Техничке примене цинка су у електричним батеријама, малим неструктурним одливима и легурама као што је месинг.
су супстанце које мењају структуру или функције нервног система.



Позната су три оксида: PbO, PbO2 и Pb3O4 (који се назива и миниjум и комбинација је оксида 2PbO + PbO2). Оловo(II)-оксид, који се такође назива и олово-моноксид, јавља се у два полиморфна облика: црвени α-облик, и жути β-облик.
PbO сe углавном примењује за добијање индустријског стакла на бази олова и индустријске керамике, укључујући ту и рачунарске компоненте. У неким аспектима цинк је хемијски сличан магнезијуму: оба елемента су увек двовалентни.
2 Zn + O2 2 ZnO
Иако се природно појављује као минерал цинкит, већина цинковог оксида производи се синтетички. Бели прах цинк-оксида нерастворљив је у води и користи се као адитив у многим материјалима и производима, укључујући ту и гуме, пластику, керамику, стакло, цемент, мазива, боје, масти, лепковe, пигментe, храну, батерије, средства за гашење пожара, траке
Podsetnik


2.



тврдоћом и еластичношћу. Уколико додамо волфрам, хром, молибден, ванадијум, манган, никл, кобалт или неки други метал, појединачно или у комбинацијама, добијају се легирани челици, који се користе за специјалне сврхе. Тврдоћа, дуктилност, затезна чврстоћа и др. могу се даље контролисати комбинованим или појединачним методама као што су термичка обрада (жарење, каљење) и механичка прерада (ваљање, извлачење). Овако добијени челици имају широку примену.
Од легура алуминијума, можемо издвојити дуралуминијум и силумин. Прављењем обе легуре повећавамо тврдоћу алуминијума. Дуралуминијум добијамо мешањем алуминијума с манганом, бакром и магнезијумом. Добра механичка својства, проводљивост топлоте и отпорност на корозију узрок су што се од дуралуминијума праве клипови, блокови и пумпе мотора, делови за спортска
возила и летелице. Силумин, легура алуминијума са силицијумом (од 5 до 13%),
осим што има већу тврдоћу у односу на алуминијум, одликује се и великом отпорношћу на корозију и малом









Podsetnik


ПИТАЊА
1.
2.
3.
4.
Челик








1.
2.
3.




7.

KOH ________________ PbO ___________________
Fe(OH)3______________ PbO2
8.
Гвожђе(II)-хидроксид______________________
Гвожђе(III)-оксид_________________________
Натријум-оксид___________________________


Калцијум-оксид___________________________
Алуминијум-хидроксид_____________________
Цинк-хидроксид___________________________
Бакар(II)-оксид____________________________
9. Напиши једначине реакција:
а) синтезе магнезијум-оксида,
б) загревање алуминијум-хидроксида, в) калијума с водом, г) литијум-оксида с водом. 10. Колико




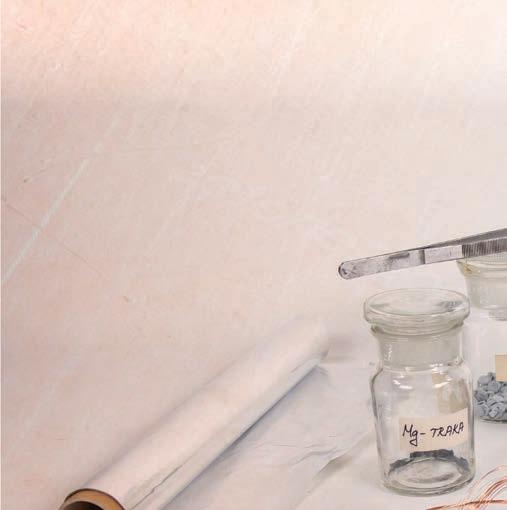



Пронађите предмете у вашем окружењу који су израђени од метала или легура метала. Детаљно испитајте њихова физичка и хемијска својства, нацртајте табелу у свеску и унесите своја запажања. Уколико испитивани метал реагује с разблаженом хлороводоничном киселином, запишите своја запажања у облику једначина хемијских реакција. Детаљна упутства за извођење вежби можете наћи у збирци са лабораторијским вежбама.


















ни металним везама и немају електронски облак. Што се проводљивости топлоте и електричне струје тиче, углавном спадају у изолаторе, а врло ретко у проводнике или полупроводнике (нешто више речи о томе биће касније).
Даље ћемо разматрати осам неметала: угљеник (C), азот (N), флуор (F), фосфор (P), сумпор (S), хлор (Cl), бром (Br) и јод (I). Водоник (H) и кисеоник (О) су нам већ добро познати, али ће и они играти веома важну улогу у реакцијама које следе.
Где можемо наћи неметале?
саставу ваздуха.
Неметали улазе у састав живих организама, јер су њихова једињења саставни

Podsetnik


2.
3. По којим својствима су неметали слични,

ХАЛОГЕНИ ЕЛЕМЕНТИ
Иако се о постојању флуора знало још 1813. године, када му је
научник Хенри Дејви и дао име по аналогији са хлором, велики
проблем је било изоловање овог елемента јер се чинило да ниједан суд није довољно отпоран према његовом хемијском дејству.
Тај проблем је решен тек 1886. године Моисановом методом.
Хлор је 1774. године изоловао Шеле, а назив му је дао Дејви по
грчкој речи хлор, што значи жутозелен.
Бром је 1826. године изоловао Балард. У преводу с грчког ње-
гов назив значи непријатног мириса.
Фердинанд Фредерик Хенри Моисан (1852–1907) био је француски хемичар, добитник Нобелове награде за хемију 1906. године
за рад на изоловању флуора.
Карл Вилхелм Шеле (1742–1786) био је шведски хемичар и фармацеут који је открио много хемијских елемената. Претпоставља се да је он тај који је 1771. године открио кисеоник пре Пристлија и Лавоазјеа. Први је окарактерисао винску, лимунску, бензоеву и јабучну киселину. Сматра се да је његова рана смрт
дугогодишњег излагања отровним супстанцама које је синтетисао. Халогени елементи се у ПСЕ налазе у 17. групи, одмах до племенитих гасова. Ова
флуор (F), хлор (Cl),
полураспада од 7,5 часова и њега у овом поглављу даље нећемо обрађивати.)
У елементарном стању ови елементи се јављају у виду двоатом-
молекула који су повезани једноструком ковалентном неполарном везом. У овим молекулима сви електрони су спарени.
У складу с порастом атомског броја халогених елемената, расту њихове атомске и молекулске запремине







Za one koji `ele da znaju vi{e
Халогени елементи реагују с водоником.
Сви халогени елементи реагују с водоником и формирају одговарајуће флуоро, хлоро, бромо и јодоводоничне киселине. Ова реакција може се збирно написати у следећем облику: H2 + X2 2 HX
Халогено-водоници, који су у овој реакцији приказани са HХ, за разлику од халогених елемената, растварају се у води, дисосују и понашају као киселине бојећи лакмус хартију у црвено: HX H+ + X -
ДЕМОНСТРАЦИОНИ ОГЛЕД
Током извођења огледа обавезно носите заштитне рукавице
немате
огледа препустите наставнику. За овај оглед су вам потребни дестилована вода, раствор хлороводоничне киселине, лакмус хартија, две чаше, стаклени штапић, сијалица, батерија и жица. У једну чашу сипајте дестиловану воду, а у другу хлороводоничну киселину. Тестирајте оба раствора








Podsetnik

Za one koji `ele da znaju vi{e
Vхлор(V)-оксидHClO3





Сумпор је познат од давнина.
Име сумпора изведено је из латинске речи sulphur . Сумпор је
десети најчешћи елемент у свемиру, а пети најчешћи на Земљи. Један је од главних хемијских елемената потребних за биохемијско функционисање свих живих организама. Улази у бројна органо-сумпорна једињења, као што су амино-киселине (цистеин, цистин и метионин) и два витамина (биотин и тиамин). Везе које гради сумпор дају механичку чврстоћу и нерастворљивост протеину кератина, који се налази у спољашњем делу коже, коси и перју. Где можемо наћи сумпор?
Иако сумпор у Земљиној кори није особито заступљен (масени удео је свега 0,035%), ипак се може
и као слободан елемент у природи. У укупном саставу Земље учествује са чак 2,9%, и зато се најчешће може наћи у вулканима. Осим вулканског порекла, постоје знатна налазишта
једињења која улазе у састав сумпорних
вода, као и биљног и животињског света.
Елементарни сумпор може да буде
и седиментног порекла. У нормалним условима атоми сумпора





сумпор(IV)-оксид. S + O2 SO2
Сумпор(IV)-оксид или сумпор-диоксид
нуспродукт рада аутомобилских
Уколико се раствори
SO2 + H2O H2SO3

гради једињења с водоником.
Водоник-сулфид H2S је отрован гас и аналоган је молекулу воде. Mоже да буде смртоносан у малим количинама. Мирише на покварена јаја. Може се наћи у вулканским гасовима, а у лабораторији га можемо добити уколико загрејемо елементарни сумпор под струјом водоника.
H2 +
S H2S
Растварањем водоник-сулфида у води настаје сумпороводонична киселина. Налази се у неким минералним водама. Многе бање су познате по сумпорним водама у којима се налази водоник-сулфид који настаје и током труљења органског
Podsetnik






АЗОТ
Азот je 1772. године открио eнглески научник Данијел Рaдepфopд. Haзив je изведен из грчких peчи нитрон гeнoз (νιτρον γενοζ), што значи градитељ шалитре. Лaвоазје је кacниje извео назив од грчких речи a зoe (α ζωον), што значи – нeживот. Где можемо наћи азот? Главни је састојак ваздуха, чини 78% његове запремине и, за разлику од кисеоника, слабо је реактиван. Уобичајени је елемент у свемиру, а у Млечном путу и Сунчевом систему отприлике седми по заступљености. Јавља се у свим организмима, пре свега у амино-киселинама (а самим тим и у протеинима), у нуклеинским киселинама (ДНК и РНК) и другим органским молекулима. Нека од занимљивих једињења азота су кевлар, који се користи у тканини велике чврстоће (панцирима) и цијаноакрилати, који се користе у суперлепку. Азот је саставни део сваке главне фармаколошке класе лекова, укључујући
a то је слаба растворљивост у води. Ово својство можемо
N2 + 3H2 2 NH3
Амонијак
Амонијак је једињење азота са три атома водоника, гас без
боје, оштрог, непријатног мириса. Одлично се раствара у води.
Да ли је амонијум-хидроксид кисео или базан?
Уколико гас амонијака уведемо у воду и овако добијени раствор тестирамо лакмус хартијом, видећемо да ће црвена хартија променити боју, док се плава неће променити. Растварањем амонијака добија се амонијум-хидроксид: NH3 + Н2О NH4ОН
Стрелице нам и овог пута
смера, односно да је реакција повратна или реверзибилна и да се амонијум-хидроксид
рава
Формула оксидаВаленцаНазив оксидаТривијални назив оксида
N2O Iазот(I)-оксидазот-субоксид NO IIазот(II)-оксидазот-моноксид
N2O3
IIIазот(III)-оксидазот-триоксид
NO2 IVазот(IV)-оксидазот-диоксид
N2O5 Vазот(V)-оксидазот-пентоксид
Не добијају



Азот-пентоксид
(нитратна)
N2O5 + H2O 2 HNO3
HNO3 H+ + NO3-
Азотна киселина реагује са свим металима, осим са златом, платином, иридијумом и родијумом. Злато се раствара у смеши концентроване азотне и хлороводоничне
Podsetnik

ПИТАЊА И ЗАДАЦИ
1. Зашто је азот слабо реактиван?
2. Опиши физичка својства азота.
3. Опиши физичка својства амонијака.
4. Наведи примену азота и његових једињења у свакодневном животу.
5. Напиши формуле: а) азот (III)-оксида, б) амонијака, в) азот-субоксида, г) азотне киселине.
6. Напиши једначине реакције добијања: а) амонијака, б) азотне киселине.


ФОСФОР
Фосфор
Где можемо наћи фосфор?
велике реактивности, фосфор се не налази слободан у природи. Убраја се у биогене елементе јер улази у састав ДНК, РНК,
АТП и фосфолипида. Самим тим, есенцијалан је за све ћелије.
Алотропски облици фосфора су бели, црвени и црни фосфор.
Бели фосфор (Р4) састоји се из четири атома који су неполарним
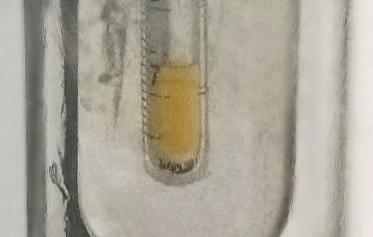
ковалентним везама везани у облик тетраедра. Јако је запаљив и отрован. Сија зеленкасто-жуто у мраку (у присуству кисеоника). Ова карактеристична физичка појава назива се фосфоресценција, односно хемилуминисценција. Мирис који се ослобађа при његовом сагоревању је налик мирису белог лука. Црвени фосфор добија се загревањем белог фосфора на 250°C, чиме се добија ланчани распоред
Црни фосфор има ромбичну


онај који је петовалентан. Бели фосфор је веома рективан,



Podsetnik

чијим растварањем у води настаје фосфорна киселина.
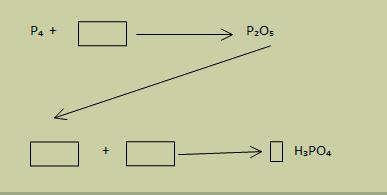
Угљеник је име добио по угљу (латински: carbo).
Где можемо наћи угљеник?
Угљеник је четврти најзаступљенији елемент у свемиру по маси након водоника, хелијума и кисеоника. У Земљиној кори је тек на 15. месту, што му не смета да гради разна једињења. Необична способност да формира полимере на температурама уобичајеним
елемент свих познатих живих бића. У елементарном стању




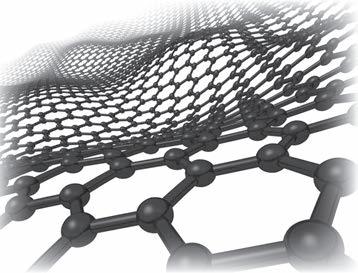
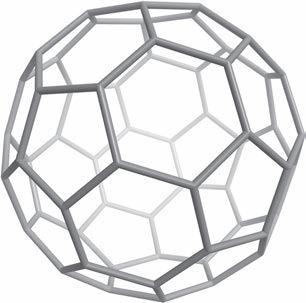








заштитним маскама.
Како сагорева угљеник?
Сагоревањем угљеника у присуству недовољне количине ваздуха добија се угљеник(II)-оксид или угљен-моноксид. 2C + O2 2 CO
Угљеник(II)-оксид је веома отрован гас


боје, укуса и мириса.
Удисање угљеник(II)-оксида у већим количинама доводи до смрти. Иако је у природи врло редак, у градској средини се налази у знатним количинама и производ је непотпуног сагоревања горива у моторима. Угљеник(II)-оксид не реагује с водом, односно није анхидрид киселине. Његовим даљим сагоревањем добија се угљеник(IV)-оксид или угљен-диоксид: 2CO + О2 2СО2
Исти молекул може настати и потпуним сагоревањем угљеника C + O2 CO2
Угљеник(IV)-оксид је безбојни гас, тежи од ваздуха. Састоји се од
атома угљеника који је са две
двоструке ковалентне везе пове-
зан за два атома кисеоника, тј.
атом угљеникa везан je за сваки
атом кисеоника двоструком везом. Јавља се природно у Земљиној атмосфери као гас и његова



Podsetnik
У епрувету ставите кашичицу уситњеног мермера и сипајте 10 cm3 раствора хлороводоничне киселине и







Видели смо да неметали имају различита физичка својства, упознали смо се с њиховим агрегатним стањима, бојама, мирисима. Нису тако добри у провођењу електричне струје и топлоте, с неким изузецима. Основно заједничко хемијско својство неметала је да граде киселине.
Како настају киселине?
У реакцији оксидације неметала настају њихови кисели оксиди – анхидриди киселина. У реакцији анхидрида с водом добијају се кисеоничне киселине . Међутим, поред киселина које у својим молекулима садрже кисеоник, постоје







2.
Cl
I
C
Br


S P
H2SO4 P2O5
H2CO3 SO2
H3PO4 N2O3




4.*
5.
у тим оксидима.
6. Напиши формуле и називе оксида азота.
7. Напиши формуле: а) амонијака, б) угљеник(II)-оксида, в) сумпорасте киселине,
г) хлор(VII)-оксида, д) водоник-сулфида, ђ) сумпор(VI)-оксида.
8. Допуни и изједначи једначине хемијских реакција.
а) H2 + Br2 ____________
б) _______ + O2 CO
в) SO2 + H2O _________
г) H2 + N2 ____________
9. Колико је грама сумпор(IV)-оксида потребно да се у реакцији
11.
ЛАБОРАТОРИЈСКА ВЕЖБА II
Испитивање физичких својстава неметала
Током извођења огледа обавезно носите
рукавице и наочаре. Уколико немате прописну заштиту, извођење огледа препустите наставнику. За овај оглед
различити елементарни неметали који су вам доступни у складу с могућностима, батерија, сијалица, жице, магнет, упаљач, чаша.
Детаљно испитајте физичка својства неметала и запажања унесите у табелу. Обавезно запишите своја запажања. Детаљна упутства за извођење вежбе можете наћи у збирци са лабораторијским вежбама.


















III. СОЛИ













Како састављамо формуле соли? Формуле соли састављамо врло једноставно. Како со мора бити без наелектрисања, то значи да морамо имати исту количину позитивног наелектрисања, које потиче од катјона и исту количину негативног наелектрисања, које потиче од анјона. Погледаjмо то на примеру писања формуле соли која настаје мешањем калцијум-хидроксида
CaCl2
калцијум-хлорид
Погледајмо пример именовања соли која се добија када помешамо хлороводоничну киселину и гвожђе(III)-оксид.
FeCl3
гвожђе(III)-хлорид У овом случају се након назива катjона у загради пише и валенца (сетите се да гвожђе може имати валенцу II и III); ово правило
важи уколико метал има више валентних стања. Амонијум јон, као катјон може да с хлороводоничном или сумпорном киселином
NH4OH + HCl NH4Cl + H2O
NH4 Cl
амонијум-хлорид, 2 NH4OH + H2SO4 (NH4)2SO4 + 2 H2O (NH4)2 SO4
амонијум-сулфат.
Приметимо да је амонијум катjон наелектрисан једном позитивно. Пошто је сулфатни анjон (киселински остатак сумпорне
NaHCO3
MgOHCl
магнезијум-хидроксихлорид, Al(OH)2 Cl
алуминијум-дихидроксихлорид.

Podsetnik
Соли су једињења која се састоје од катјона и анјона међусобно повезаних јонском везом. Формуле соли састављају се
на основу валенци. Називи соли формирају се тако што се прво
пише назив катјона, а затим назив киселинског остатка одвојеног цртицом од назива катјона.

ПИТАЊА И ЗАДАЦИ
1. Шта су соли?
2. Како дајемо називе солима?
3. Зашто се у називу неких соли у
код неких се не пише?
4. Напиши формуле.
а) калијум-хлорид
б) натријум-нитрат
в) алуминијум-сулфит
г) бакар(II)-сулфат
5. Напиши називе соли.
а) ZnSO₄
б) AlPO₄
в) Mg(NO₃)₂
г) Na₂SO₃
загради пише валенца, а

крв има одређену концентрацију соли и уколико је неко изгубио доста течности, не можемо му дати дестиловану воду. То мора да буде
раствор који ће омогућити нормално физиолошко стање – физио-
лошки раствор, који је, у ствари, 0,9%-ни раствор NaCl-а. Али уколико претерамо с концентрацијом, можемо изазвати и супротан
ефакат и со искористити за процес усољавања, односно конзервирања хране. Тиме спречавамо микроорганизме, као што су бактерије и гљивице, да нормално функционишу.
Да ли постоји неки безбеднији начин да се
Размислите... Соли се састоје од
огледа препустите наставнику. За овај оглед потребни
натријум-хидроксида исте концентрације, црвене
лакмус хартије, стаклени штапић, епрувете.

NaOH + HCl
хидроксидног анјона
NaCl
метал + неметал со Fe + S FeS 1 : 1
гвожђе(II)-сулфид (феро-сулфид);
метал + киселина со + водоник
Ca + 2 HCl CaCl2 + H2
1 : 2
калцијум-хлорид, Zn + H2SO4 ZnSO4 + H2
1 : 1 цинк-сулфат;
К2O + 2 HCl 2 КCl + H2O
1 : 2 калијум-хлорид, CaO + H2SO4 CaSO4 + H2O
1 : 1 калцијум-сулфат;
оксид неметала + база со + вода
SO3 + 2 КOH К2SO4 + H2O
1 : 2 калијум-сулфат,
CO2 + 2 NaOH Na2CO3 + H2O
1 : 2 натријум-карбонат; – и наравно, реакцијом потпуне неутрализације, односно реакцијом између хидроксида и киселина у стехиометријском односу настају со и вода:
киселина + база со + вода
2 H3PO4 + 3 Ca(OH)2 Ca3(PO4)2 + 6 H2O
2 : 3 калцијум-фосфат,
2 NaOH + H2SO4 Na2SO4 + 2 H2O
2 : 1 натријум-сулфат.
Међутим, уколико променимо стехиометријски однос реактаната, догодиће се реакција непотпуне неутрализације
Шта се догађа у реакцији непотпуне неутрализације?
Видели смо да увођењем угљеник(IV)-оксида у дестиловану воду можемо добити угљену киселину која је у реакцији с натријум-хидроксидом у стехиометријском односу 1 : 2, при чему се добијају со натријум-карбоната и вода:
CO2 + H2O H2CO3
H2CO3 + 2 NaOH
Na2CO3 + 2 H2O
1 : 2 со натријум-карбоната, или збирно: CO2 + 2 NaOH Na2CO3 + H2O
1 : 2
смањимо количину
и променимо стехиометријски однос у 1 : 1, догодиће

Podsetnik
Соли се могу добити на више начина, од којих издвајамо следеће реакције:
у директној реакцији метала и неметала,
у реакцији метала (не свих) и киселина,
у реакцији оксида метала (анхидрида базе) и киселина,
у реакцији оксида неметала (анхидрида киселина) и база,
у реакцији потпуне неутрализације хидроксида и киселина.

ПИТАЊА И ЗАДАЦИ
1. Шта је реакција неутрализације?
2. Допуни једначине хемијских реакција тако да буду тачне: а) ___________ + HNO₃ NaNO₃ + H₂O, б) ___________+ 2HCl 2NaCl + H₂O,
в) Ca(OH)₂ + H₂SO₃ ________ + H₂O.
3. Напиши реакцију добијања следећих соли реакцијом неутрализације из одговарајуће киселине и базе.
а) гвожђе(III)-сулфат, б) калцијум-хлорид, в) калијум-нитрит.
Како изгледају соли?
Физичка
турама топљења (кухињска со прелази у течни облик на 800°С).
Чврсте соли имају тенденцију да буду прозирне и могу да буду различитих боја. Могу имати свих пет основних укуса: слани, слатки, кисели, горки и умами. Умами је реч јапанског порекла (јап. うま味)
„пријатан укус” и један је од пет основних укуса, заједно са слатким, киселим, горким и сланим. Уколико су неиспарљиве, немају мирис, међутим често могу имати врло јак и специфичан мирис, на основу ког их можемо разликовати.
Соли су изразити изолатори и не проводе струју. Међутим, уколико их растворимо у води, њихов
растварања електролита називамо

наочаре. Уколико немате прописну
огледа препустите наставнику. За овај оглед потребни су вам разблажени раствор натријум-хидроксида и разблажени раствор гвожђе(III)-хлорида, 1%-ни раствор сребро-нитрата, 1%-ни раствор натријум-хлорида, кесица соде бикарбоне, разблажена хлороводонична киселина, стаклени штапић, епрувете, сахатно стакло.
У епрувету сипајте 3 cm3 разблаженог раствора гвожђе(III)-хлорида, FeCl 3 , а затим у капима додајте 3 cm 3 раствора натријум-хидроксида, NaOH. Протреситe епрувету и оставите је у сталку. У другу епрувету сипаjтe 3 cm 3 1%-ног раствора сребро-нитрата, АgNO 3 , и додаjтe једнаку запремину

FeCl3 + 3 NaOH Fe(OH)3 + 3NaCl
AgNO3 + NaCl AgCl + NaNO3

NaHCO3

Zanimqiva geografija
На часу географије можете разматрати



ПИТАЊА И ЗАДАЦИ
1. Опиши физичка својства кухињске соли
и калцијум-карбоната.
2. Наведи примену кречњака и гипса у свакодневном животу.
3. Напиши једначине следећих хемијских реакција: а) гвожђе(II)-сулфат са цинком, б) алуминијум-сулфат с натријум-хидроксидом, в) сребро-нитрат с калцијум-хлоридом.


Podsetnik




1.
с другим солима.
д) Соли се могу добити у реакцији метала с киселином.
2. Разврстај формуле датих једињења: NaNO2, CaO, KOH, MgCl2, CaCO3, Na2O, HCl, MgSO4, Li2O, Fe(OH)2, H3PO4 на:
а) киселине:_______________________________,
б) оксиде: ________________________________,
в) хидроксиде: _____________________________, г) соли: __________________________________.
3. Поред формуле једињења у левој колони напиши број којим је
десној колони.
NaOH____
1. Калцијум-оксид
CaO______ 2. Сумпорна киселина
NaNO3____
NaHCO3____
NaCl ______
3. Натријум-хлорид
4. Натријум-нитрат
5. Натријум-хидрогенкарбонат
H2SO4_______ 6. Натријум-хидроксид
4. Напиши називе следећих једињења:
а) Na2SO3, б) Mg(OH)2, в) FeO,
г) HNO2, д) K3PO4, ђ) Fe(OH)3
5. Напиши по једну формулу оксида гвожђа,
Формула оксида бакра: ____________
Формула оксида гвожђа: ___________
Формула оксида алуминијума: ___________
6. Напиши једначину реакције

ОПШТА

СВОЈСТВА






се ради о маленој амеби од само једне ћелије, невидљивој људском оку или киту, највећем сисару, тешком
до 80 тона, састављеном од више од милијарду милијарди ћелија, они имају заједничко име – организам. Према томе, молекуле који чине организме и саму основу живота који познајемо на планети Земљи називамо органска једињења. Област хемије која се бави органским молекулима, њиховом структуром и хемијским својствима називамо органска хемија.
Како настају

соли



Podsetnik
4. Структурно представи








V. УГЉОВОДОНИЦИ














де можемо наћи угљоводонике и каква су им физичка својства?
Када сипамо гориво, бензин или дизел у резервоар аутомоби-
ла с унутрашњим сагоревањем, срећемо се с угљоводоницима. Када желимо нешто да угрејемо на шпорету на „гас”, срећемо се с угљоводоницима. Када се шетамо тротоаром направљеним од битумена, поново се срећемо с угљоводоницима. Мириси цвећа, парфеми и феромони инсеката су јако често угљоводоници, као и наранџаста боја шаргарепе.

ослобађају знатну количину енергије. На собној температури могу постојати као гасови, течности и чврсте супстанце.

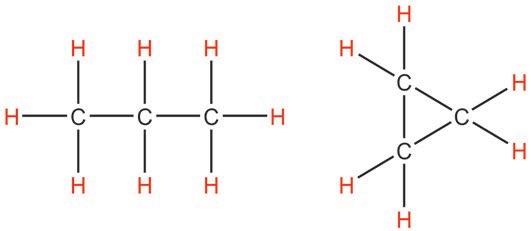
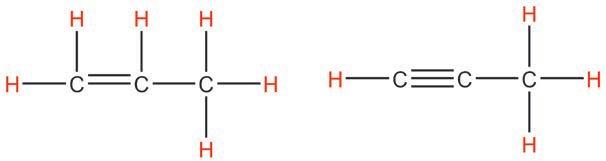
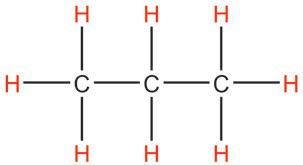
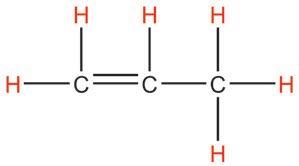
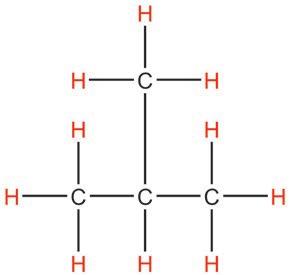
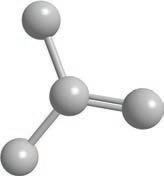
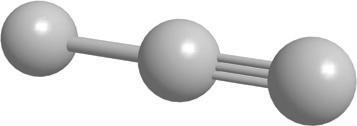
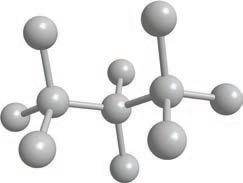
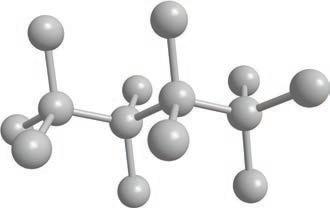
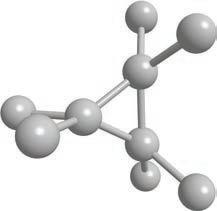
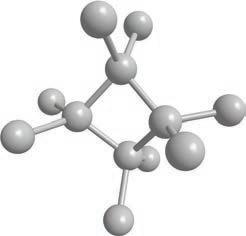
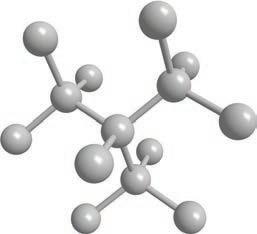
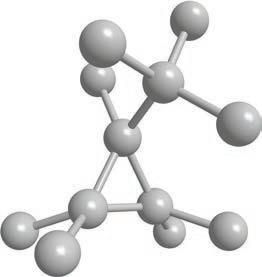
CH3 CH CH3
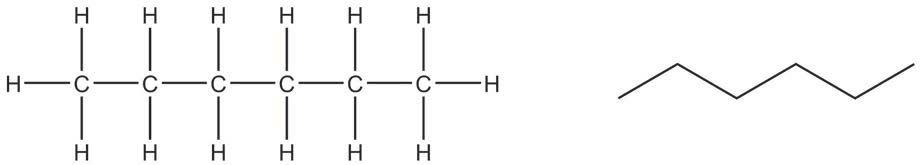
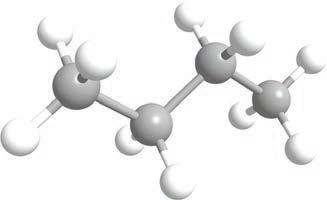
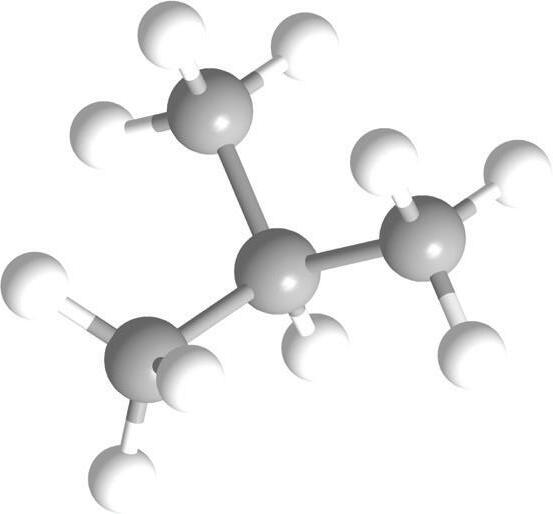
Структурнаискелетнаформула
визуелизујете као тродимензионалне. Ради лакшег сналажења, све угљоводонике

















органских молекула. IUPAC (International Union for Pure and Applied Chemistry), – Интернационална унија
то
језик говоре
потичу.
хемији посвећена је плава књига, а он-лајн верзију
Podsetnik

ПИТАЊА И ЗАДАЦИ
1. Шта су угљоводоници?
2. Опиши општа физичка
3. Структурном, рационалном структурном
4.






C4H10 CH3-CH2-CH2-CH3
C5H12
C6H14
C7H16
C8H18
C9H20
C10H22
CH3-CH2-CH2-CH2-CH3
CH3-CH2-CH2-CH2-CH2-CH3
CH3-CH2-CH2-CH2-CH2-CH2-CH3
CH3-CH2-CH2-CH2-CH2-CH2-CH2-CH3
CH3-CH2-CH2-CH2-CH2-CH2-CH2-CH2-CH3
CH3-CH2-CH2-CH2-CH2-CH2-CH2-CH2-CH2-CH3
Прва три члана хомологног низа алкана немају
се
Интересантно
елиминишемо један атом водоника настају групе које називамо алкил-групама и врло су важне за именовање алкана који



сваког ставља број за позицију супституента. Уколико
Podsetnik

се
низа. Алкани се именују по систематским правилима.
5. Напиши називе следећих алкана: а) , б) . Засићени угљоводоници или алкани су угљоводоници повезани само једноструким везама. Њихова имена се завршавају суфиксом -ан. Угљоводоници с истим бројем атома у молекулу, али с различитим структурним рационалним формулама јесу изомери, а та
ПИТАЊА И ЗАДАЦИ
1. Шта су алкани?
2. Наведи првих десет чланова хомологног низа алкана.
3. Која је општа формула алкана?
4. Напиши рационалне структурне формуле следећих алкана: а) 2,3-диметилхексан, б) n-хептан, в) 3-метилпентан, г) 2,2,3,4-тетраметилоктан, д) 2-етилхептан.



ВЕЖБА V
Састављање модела молекула угљоводоника,
именовање угљоводоника




Podsetnik
Незасићени угљоводоници су угљоводоници који могу бити повезани двоструким (алкени) и/или троструким везама (алкини). Њихова имена завршавају се суфиксом -ен, односно -ин. У незасићеним


ПИТАЊА И ЗАДАЦИ
1. Шта су алкени?
2. Шта су алкини?
3. Која је општа формула: а) алкена, б) алкина?
4. Који је: а) пети члан хомологног низа алкина, б) седми члан хомологног низа алкена?
5. Објасни појам изомерија положаја на примеру хексена.
6. Напиши рационалне структурне формуле следећих угљоводоника: а) 2-бутен, б) 2-метил-1-хексен, в) 3,3-диметил-1-пентин, г) 3-етил-1-хексен.
7. Напиши називе следећих угљоводоника:


Већ смо рекли да се угљоводоници користе као гориво и да се на тај начин ослобађа енергија која се може користити и претварати у разне друге облике, као што су механичка, топлотна и електрична енергија. Неки од енергената који имају широку примену су земни и рафинеријски гас, бензин, дизел-гориво, мазут.
Која се хемијска промена одиграва сагоревањем угљоводоника?
Хајде да сагоревање видимо на једном огледу.
ДЕМОНСТРАЦИОНИ ОГЛЕД
Током извођења огледа обавезно носите заштитне рукавице и наочаре. Уколико немате прописну заштиту, извођење огледа препустите наставнику.
За овај оглед потребни су вам палидрвце (шибица), порцуланска шољица, сахатно стакло, штипаљка, хексан или медицински бензин, нафта и други угљоводоници које можете наћи, као, на пример, петрол-етар.
У порцуланску шољицу ставите малу количину (неколико капи је сасвим довољно) неког од испитиваних угљоводоника и запалите упаљеним палидрвцем. Врху пламена штипаљком принесите сахатно стакло. Своја запажања забележите.
Сви угљоводоници сагоревају у кисеонику, при чему настају угљеник(IV)-оксид и вода и ослобађа се знатна количина енергије. Ево примера ове реакције с алканима,
CH4 + 2 O2 CO2 + 2 H2O + 802 kЈ
2 C3H6 + 9 O2 6 CO2+ 6 H2O + 4.116

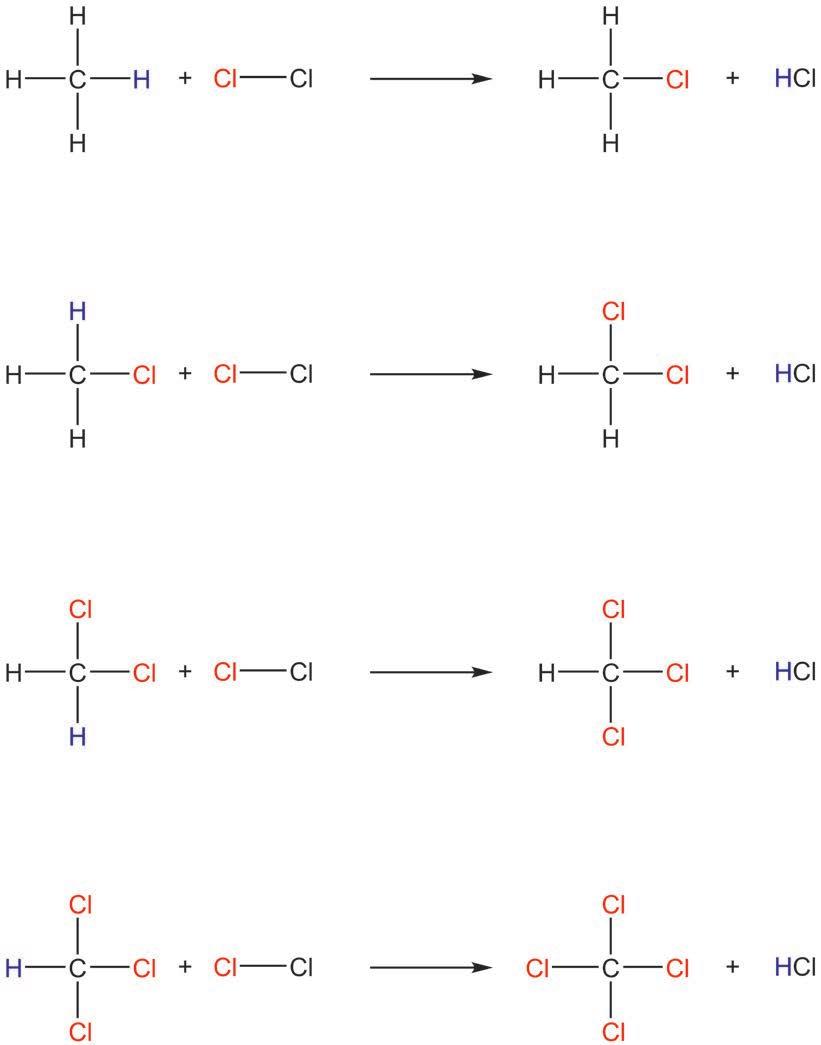
CH4 + Cl2 CH3Cl + HCl
хлорметан (метил-хлорид)
CH3Cl + Cl2 CH2Cl2 + HCl
дихлорметан (метилен-хлорид)
CH2Cl2 + Cl2 CHCl3 + HCl
трихлорметан (хлороформ)
CHCl3 + Cl2 CCl4 + HCl
тетрахлорметан (угљен-тетрахлорид)
У реакцијама супституције












овом случају се водоник замењује хлором, при чему
рајући хлорметани и хлороводоник.
фреона, боја, инсектицида. Међутим, они понекад могу

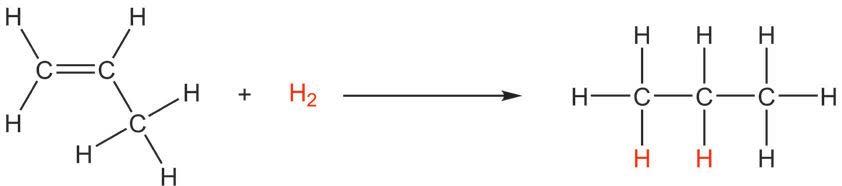
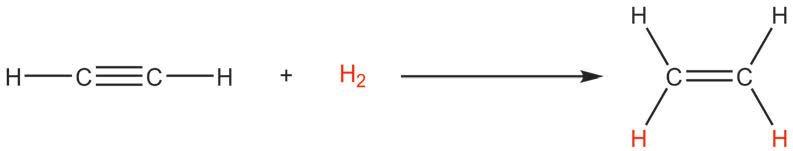
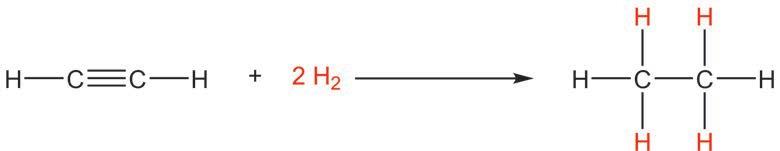
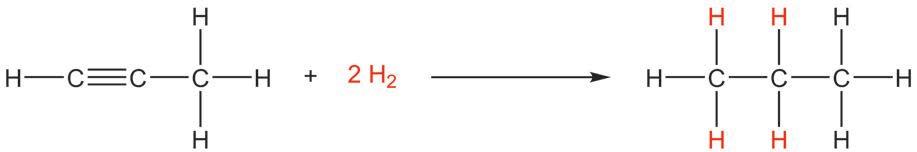

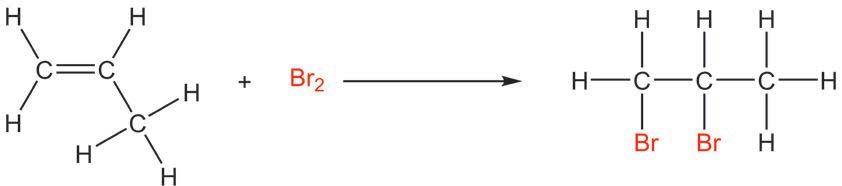

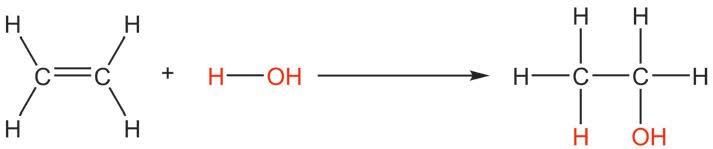
катализатор катализатор
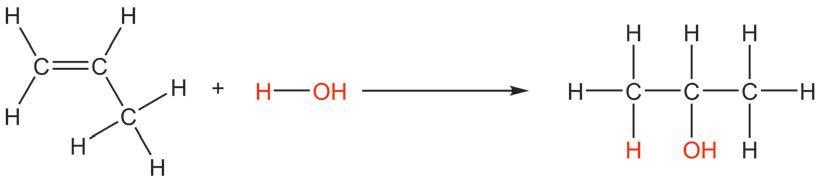
катализатор



што су флашице, кесе, цеви итд. Направите табелу у свесци и у њу унесите њихове физичке и хемијске карактеристике. Упоредите
шите разлике и сличности у хемијским формулама. Полиамиди (ПА) или најлони – влакна,
(ПВЦ) – водоводне цеви и олуци, електрична изолација


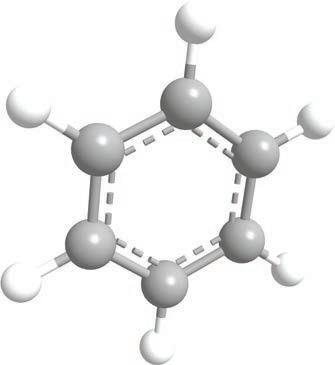
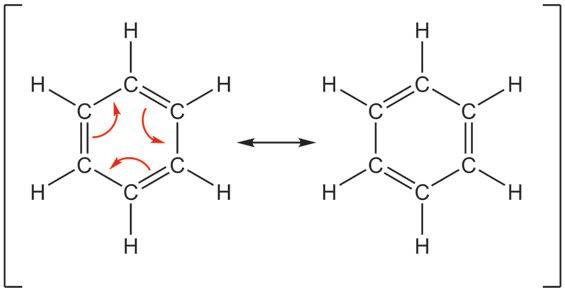
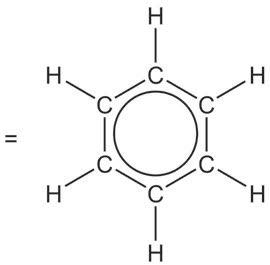
Како реагује бензен?
Иако им je по незасићености сличан,
пустите наставнику. За
циклохексен,
манганата, разблажена сумпорна
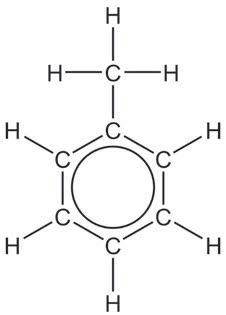
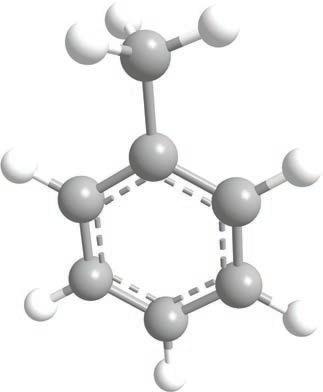
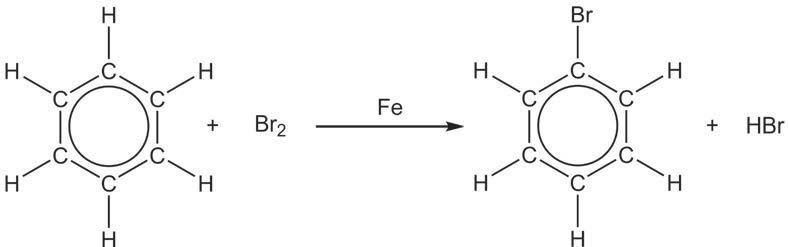
Za one koji `ele da znaju vi{e
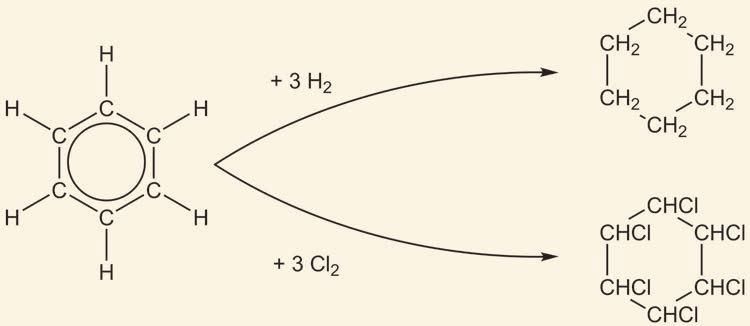
без присуства ваздуха) при чему настаје катран – течна, сложена фракција из које се даље арени фракционишу. На собној температури бензен је безбојна течност карактеристичног ароматичног мириса, по ком је ова група једињења и добила име. Растварају се у неполарним

Podsetnik

ПИТАЊА И ЗАДАЦИ
1. Шта су полимери?
2. Наведи неке од примена полимера у свакодневном животу.
3. Шта су ароматични угљоводоници?
4. Опиши физичка својства бензена.
5. Напиши структурну формулу: а) бензена, б) толуена.
6. По којим хемијским својствима су ароматични угљоводоници слични алканима?
животињских организама који су изумрли веома давно, пре неколико милиона година и услед разних поремећаја и померања Земљине коре доспели су у дубину Земље. Њиховим распадањем под посебним условима (високом притиску, температури и у одсуству кисеоника), настала су ова фосилна горива.
Нафта je густа, уљаста течност, тамне боје и непријатног мириса. По хемијском саставу, то је сложена смеша засићених ацикличних, цикличних и ароматичних угљоводоника и других једињења која, осим угљеника и водоника, могу садржати
кисеоник, азот, сумпор и атоме других елемената. Иако




Podsetnik





ПИТАЊА И ЗАДАЦИ
1. Опиши физичка својства нафте и земног гаса.
2. Шта је нафта по хемијском саставу?
3. Шта је земни гас по хемијском саставу?
4.Опиши
5. Наведи












сим угљеника и водоника, још један елемент је изузетно важан када разговарамо о органским молекулима. То је кисеоник.
Као што смо видели код угљоводоника, увођење новог атома у органско једињење доводи до нових физичких и хемијских својстава тих једињења. Те нове атоме или групе атома називамо функционалне групе. Увођењем кисеоника, добијамо једну нову функционалну групу. Кисеоник може градити како једноструке везе с угљеником или водоником, тако и двоструке везе с угљеником. Органска једињења с кисеоником о којима ће бити речи су: – алкохоли, – карбоксилне киселине, – естри.
Покушајте да се сетите када сте раније говорили о некима од њих.


Где можемо наћи алкохоле?
етанол и угљеник(IV)-оксид: C6H12O6 2 CH3CH2OH + 2 CO2. глукоза етанол Да
сматрати дериватима воде. Како је
супстанца, тако ће и алкохоли захваљујући својој хидроксилној групи бити поларни. Због тога се неки алкохоли лако растварају у води и поларним растварачима и имају

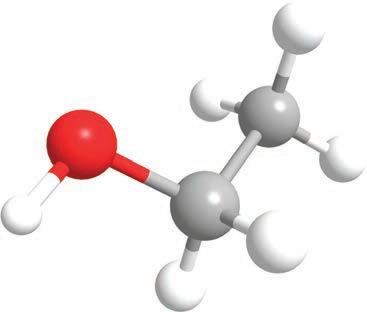
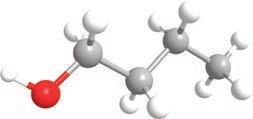

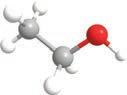
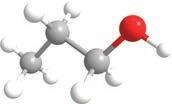
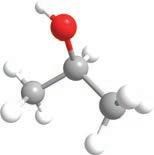
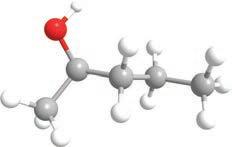
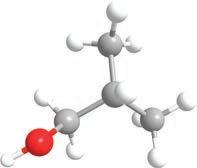
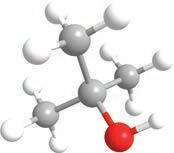
је COOH
група. Ако постоје монохидроксилни, претпостављате да постоје и полихидроксилни алкохоли . Пошто се за сваки угљеников атом може везати по једна хидроксилна група, њих може бити онолико колико има и угљеникових атома. Они се именују тако што се након имена главног низа и пре наставка -ол ставља инфикс -ди-, -три- или -тетра-, у зависности од тога колико има хидроксилних група: две, три или четири итд. Ево неких примера најпознатијих полихидроксилних алкохола с њиховим систематским, као и несистематским (тривијалним) називима.
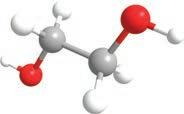
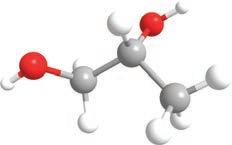
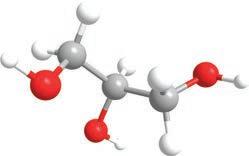
етан-1,2-диол пропан-1,2-диол пропан-1,2,3-триол
етилен-гликол пропилен-гликол глицерол У зависности од тога где се налази хидроксилна група у молекулу, можемо разликовати три групе алкохола: – примарни алкохоли, код којих
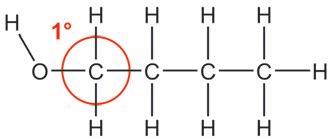
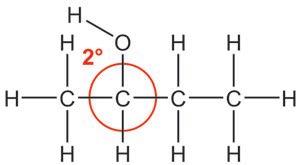
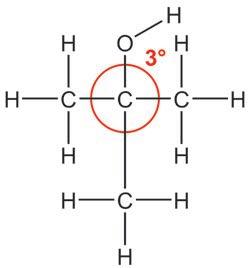

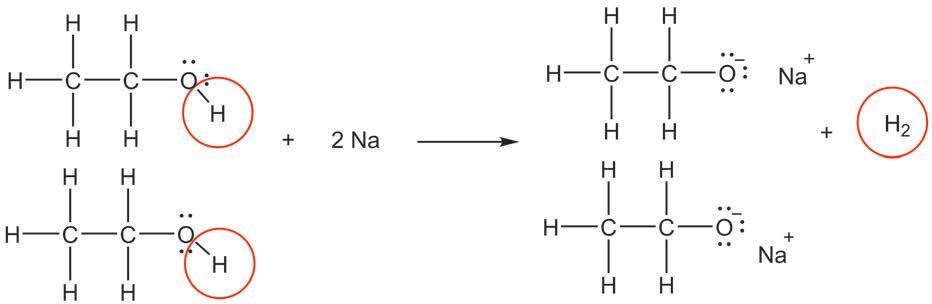
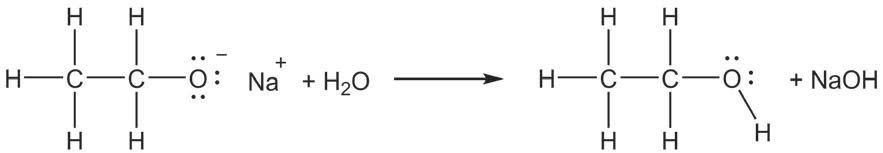
Ипак је јако важно да раствор у ком се реакција одвија буде кисео, односно да садржи H+ јоне. Овом реакцијом се, на пример, могу добити халогено-алкани на врло једноставан начин. Приметите да у овој реакцији учествује цела хидроксилна група.
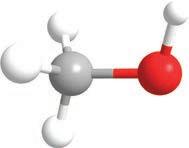
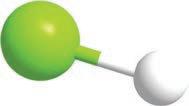
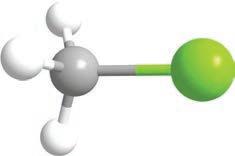

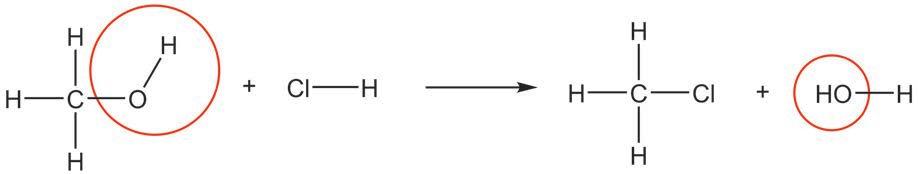
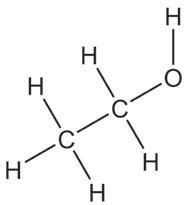
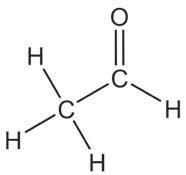
ензимска
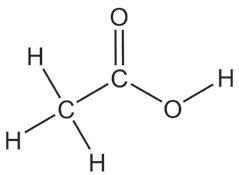
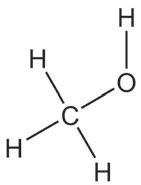
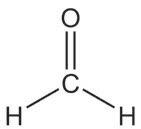
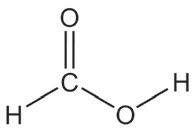
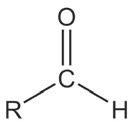
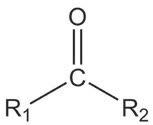
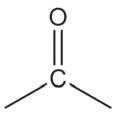
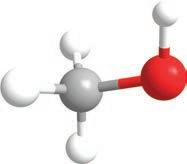
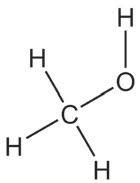
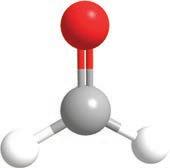
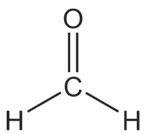
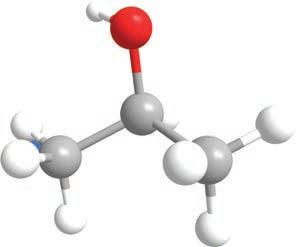
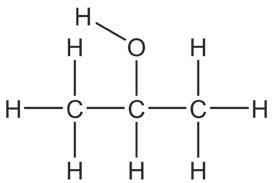
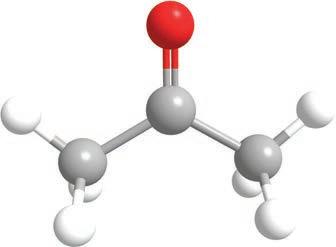
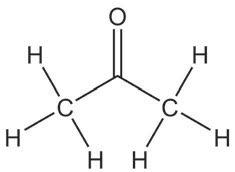
2-пропанол пропанон изопропил-алкохол ацетон
Где се најчешће примењују алкохоли, алдехиди и кетони?
Метанол, иако отрован, нашао је своју примену као сировина за производњу метанске киселине и пластичних маса, као растварач боја и лакова и као гориво.
Етанол се примењује у производњи козметичких средстава, полазна
етанол се користи у медицини као дезинфекционо средство.
Етилен-гликол, када се помеша с водом, добија се смеша позната под називом антифриз; ова течност се зими сипа у хладњаке моторних возила јер снижава тачку мржњења воде.
Пропан-1,2,3-триол (глицерол) примењује се у производњи
козметичких препарата, лекова, прехрамбеној индустрији и производњи експлозива.
Формалдехид, иако отрован, има широку примену у индустрији пластичних маса и коже, као дезинфекционо
Podsetnik


ПИТАЊА И ЗАДАЦИ
1. Шта су алкохоли? Која је њихова функционална група?
2. Опиши поступак добијања етанола из глукозе.
3. Напиши структурну формулу и назив једног примарног, секундарног и једног терцијарног монохидроксилног алкохола.
4. Напиши формуле следећих алкохола: а) 1-хексанол, б) 2-метил-2-пропанол, в) 2-пентанол.
5. Напиши називе следећих алкохола: а) б)
6. Напиши једначине хемијских реакција: а) сагоревања пропанола, б) етанола с калијумом.
7. Којој класи органских једињења припадају: а) пропанал, б) бутанон?
8. Шта су карбонилна


је да при нумерисању карбоксилна група има предност над двоструком везом.

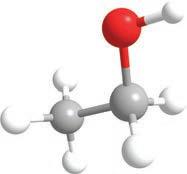
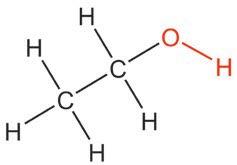
-групе, можемо разликовати
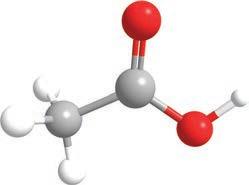
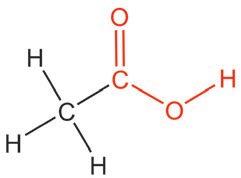

(Л. acetum)
CH3CH2COОHпропанскапропионскапропионати
CH3(CH2)2COОHбутанска бутернабутирати
CH3(CH2)3COОHпентанскавалеријанскавалеринатикорен
CH3(CH2)4COОHхексанскакапронскакапроати
CH3(CH2)14COОHхексадеканскапалмитинскапалмитати
CH3(CH2)16COОHоктадеканскастеаринскастеарати
HOОC-COОHетан-дикиселинаоксалнаоксалати
CH2(COOH)2 пропан-дикиселина
(л. Caper)
(л. oxalis)
као сирћетно врење и као споредан
производ при сувој дестилацији дрвета.
Чиста сирћетна киселина (100%-на) назива се и глацијална (ледена) сирћетна киселина јер је на око 17°C у чврстом кристалном облику, који је сличан леду. Такође се користи и као
зачин у концентрацијама 3–9%.
Која је разлика између карбоксилних (органских) и неорганских киселина?
До сада сте се вероватно навикли на то да је хемијска
Лакмус хартијом тестирајте сваку од
рите проводљивост.
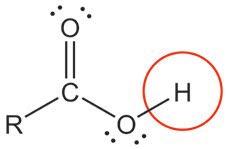
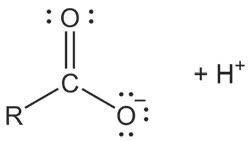
палмитинска и стeapинскa киселина, које су засићене
монокарбоксилне киселине, док је oлeинскa кисeлинa незасићена и садржи једну двоструку везу. На собној температури палмитинска и стеаринска киселина су у чврстом агрегатном стању и беле су
Podsetnik
2.




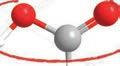




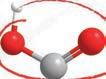




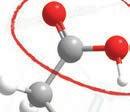
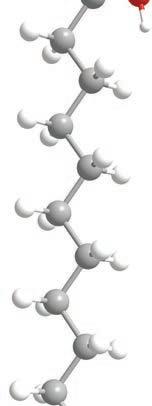
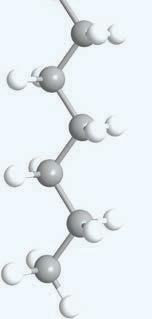


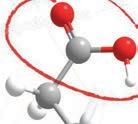

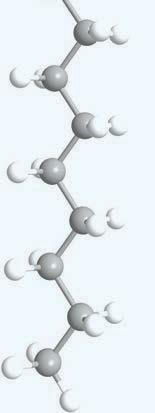

смеше.
Где можемо наћи естре?
Естри су распрострањени у природи и много се користе у индустрији.
Естри глицерола и масних киселина су у ствари масти и уља. Арому многим врстама воћа, укључујући јабуке, крушке, банане, ананас и јагоде, дају естри. Годишње се индустријски производи неколико милијарди килограма разних
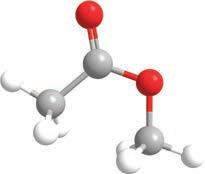
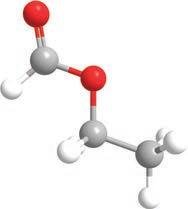
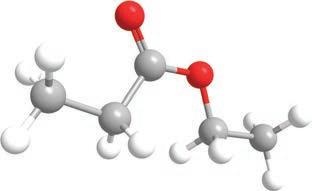












Podsetnik


ПИТАЊА И ЗАДАЦИ
1. Како настају естри?
2. Наведи примену естара у свакодневном животу.
3. Напиши рационалне структурне формуле следећих естара: а) метил-пропаноат, б) пропил-бутаноат,
в) метил-бутаноат.
4. Напиши једначине реакције
а) етанска киселина и етанол,
б) метанска киселина
в) етанска киселина
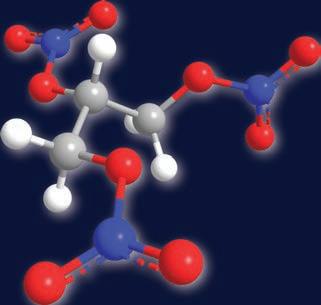
добијених естара:




ЈЕДИЊЕЊА









д чега је изграђен један организам?
Да бисмо правилно одговорили на ово питање, морамо се
подсетити неких ствари које смо до сада научили из биологије. Узмемо ли за пример нас и ако се погледамо у огледалу, видећемо да наше тело има различите делове. Можемо видети косу, кожу, очи, уши, нокте, зубе. Сигурно до сада знате, иако не можете да их видите, да унутар тела такође имамо кости, срце, јетру, мозак. Све те делове тела називамо органи. Уколико наставимо да анализирамо органе, знамо да се они састоје од појединачних ћелија, које су различите за различите органе. На пример, знамо да се мозак углавном
Zanimqiva biologija
органска једињења
сврстати у свега неколико група,
уља, шећери, протеини, витамини, нуклеинске киселине), потребно је уложити енергију. И обрнуто, разградњом великих једињења на мања једињења, добија се енергија. Ова два процеса позната су као анаболизам и катаболизам и ове реакције се стално одвијају заједно. Тај круг називамо






МАСТИ И УЉА
Шта су масти и уља?
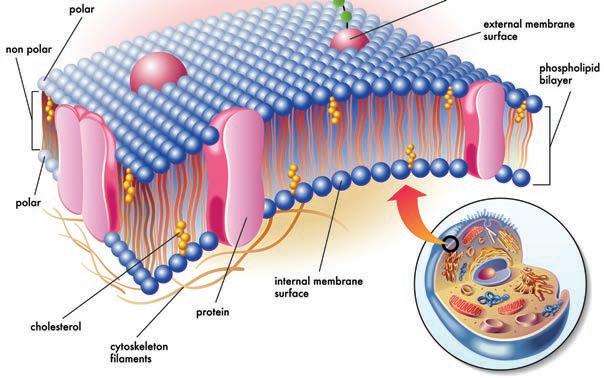
По хемијској структури и масти и уља су у ствари естри. Као што смо већ видели, естри су једињења која се састоје од алкохола и карбоксилних киселина повезаних естарском везом. Међутим, масти и уља не чине било који алкохоли, већ је то нама познати, 1,2,3-пропантриол-глицерол. Естарске везе, међутим, граде карбоксилне киселине, које имају дугачке угљоводоничне низове, које још називамо и више масне киселине. Глицерол може градити три естарске везе са три




мрежица, силиконска шпатула и термометар.
једној чаши пажљиво растворите 31g NaOH у 68 ml дестиловане воде. У другу сипајте



Podsetnik


ПИТАЊА
1. Шта су триацилглицероли?
2.
3.
4.
5.
6.
7.



Кључне речи
угљени хидрати
фотосинтеза
моносахариди
глукоза
фруктоза
алдохексоза, кетохексоза, дисахариди, сахароза
лактоза
инвертни шећер
олигосахариди
полисахариди скроб
целулоза
Cn(H20)n + n O2
угљени хидрати Можемо слободно
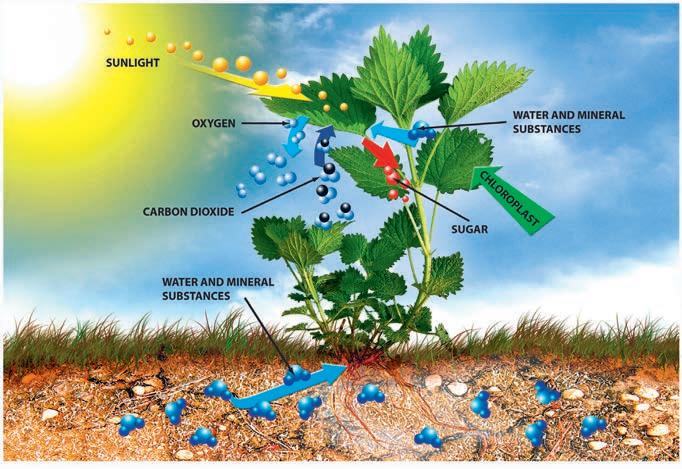
Шта су угљени хидрати?
Угљени хидрати су органски молекули који у свом хемијском саставу имају угљеник, водоник и кисеоник. Међутим, анализом њихове молекулске формуле може се доћи до
је однос ових атома такав да
сваки атом угљеника C долази један молекул воде H 2O. Такође су познати и као сахариди или једноставно шећери.
Молекулска формула глукозеC6H12O6 Однос C:H:O
6:12:6 1:2:1 Општа формула шећераCn(H20)n Важно је напоменути да, иако је ова формула општа за све угљене хидрате, и друга органска једињења могу имати сличну моле-
кулску и општу формулу. Пример је етанска или сирћетна киселина, која има тачно такав однос, али није угљени хидрат (CH 3COOH = C2(H2O)2).
Каква је хемијска структура молекула угљених хидрата?
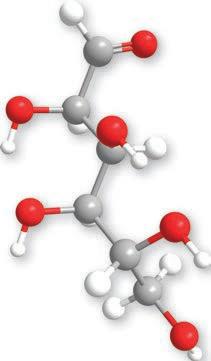
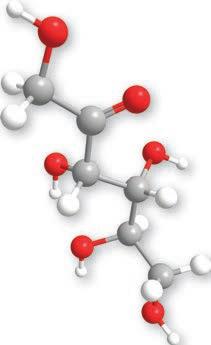
Основна јединица грађе свих угљених
угљене хидрате. У зависности од броја угљеникових атома у молекулу, моносахариди ce деле на триозе, тетрозе, пентозе и хексозе, коje имajу три, четири, пет и шест угљеникових
нији. Према овој
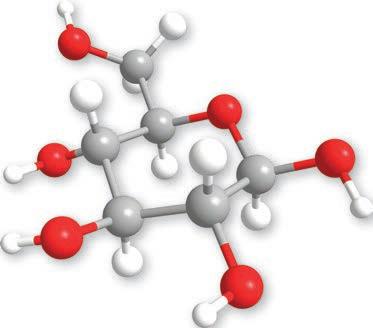
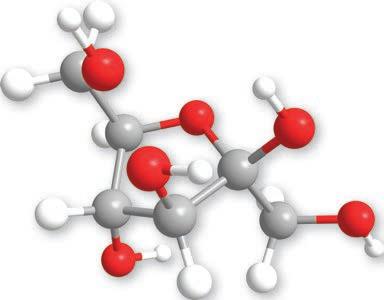

ДЕМОНСТРАЦИОНИ
Током извођења огледа обавезно носите заштитне рукавице и наочаре. Уколико немате прописну заштиту, извођење огледа препустите наставнику. За овај оглед потребни су вам сталак с епруветама, шпиритусна лампица, раствор глукозе, Толенсов реагенс.
Сипајте 1cm 3 растворa глукозе и додајте 3 cm 3 Толенсовог реагенса. Промућкајте и благо загревајте епрувету на шпиритусној лампи до појаве елементарног сребра. Запишите своја запажања.
Уколико се сетите алкохолног врења,




































Олигосахариди садрже између две и десет јединица моносахарида.
Подгрупа олигосахарида су дисахариди, који се састоје од само два моносахарида. Два примера за која сте сигурно чули су сахароза и лактоза.
Сахароза, позната и као бели или стони шећер, јесте дисахарид, који се састоји од међусобно повезаних моносахаридних цикличних јединица глукозе и фруктозе. Она се индустријски добија из шећерне репе или шећерне трске.
Лактоза или млечни шећер се налази у млеку и састоји се од
глукозе и галактозе. Она беби обезбеђује довољну количину енергије за нормалан раст и развој.
Како од дисахарида можемо добити моносахариде?
Уколико направимо раствор сахарозе и затим га закиселимо неком киселином као што је хлороводонична, раскинуће се везе и у раствору ћемо имати глукозу и фруктозу. Смеша глукозе и фруктозе назива се инвертни шећер, а овако добијени раствор је раствор инвертног шећера. Ако се
C12H22O11+ H2O
C6H12O6+ C6H12O6
сахароза и вода глукоза и фруктоза инвертни
разлика између сахарозе и инвертног шећера. Једно од њих





ДЕМОНСТРАЦИОНИ ОГЛЕД
Током извођења огледа обавезно носите заштитне рукавице и наочаре. Уколико немате прописну заштиту, извођење огледа препустите наставнику. За овај оглед потребни су вам нож, кртола кромпира и Луголов раствор.
Пресеците кртолу кромпира и каните неколико капи Луголовог раствора на место пресека. Своја запажања забележите.
МОНОСАХАРИДИДИСАХАРИДИПОЛИСАХАРИДИ АГРЕГАТНО
чврсточврсточврсто
СТАЊЕ
СТРУКТУРА кристална структура
кристална структура
аморфна или кристална структура
БОЈАбелабелабела
РАСТВОРЉИВОСТ
У ВОДИ
растворљивирастворљивинерастворљиви
Физичка својства угљених хидрата



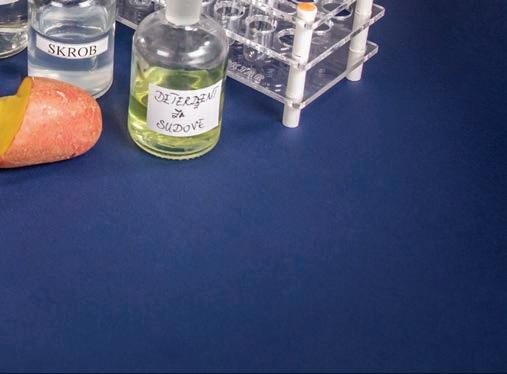
Podsetnik
Угљени хидрати или шећери су органска једињења састављена од атома угљеника, кисеоника и водоника с општом формулом C n(H 2O) n. Обично су полихидроксилни алдехиди или кетони с различитим бројем угљеникових атома, па се и према томе именују (наставак -оза). Могу се налазити у развијеном и цикличном облику. Према степену сложености, могу да буду моносахариди, дисахариди, олигосахариди и
полисахариди. Угљени хидрати имају превасходно енергетску улогу у свим организмима, док код биљака имају и градивну улогу.

ПИТАЊА И ЗАДАЦИ
1. Шта су угљени хидрати?
2. Како можемо поделити угљене хидрате?
3. Шта су: а) моносахариди, б) дисахариди, в) полисахариди?
4. Наведи сличности и разлике у физичким својствима моносахарида, дисахарида и полисахарида.
5. Каква је улога угљених хидрата у живим бићима?
6. Напиши структурне формуле: а) фруктозе, б) глукозе.
7. На који начин можемо доказати присуство скроба у кромпиру?
8. Шта је инвертни шећер?
9. Наведи примену угљених хидрата у свакодневном животу.
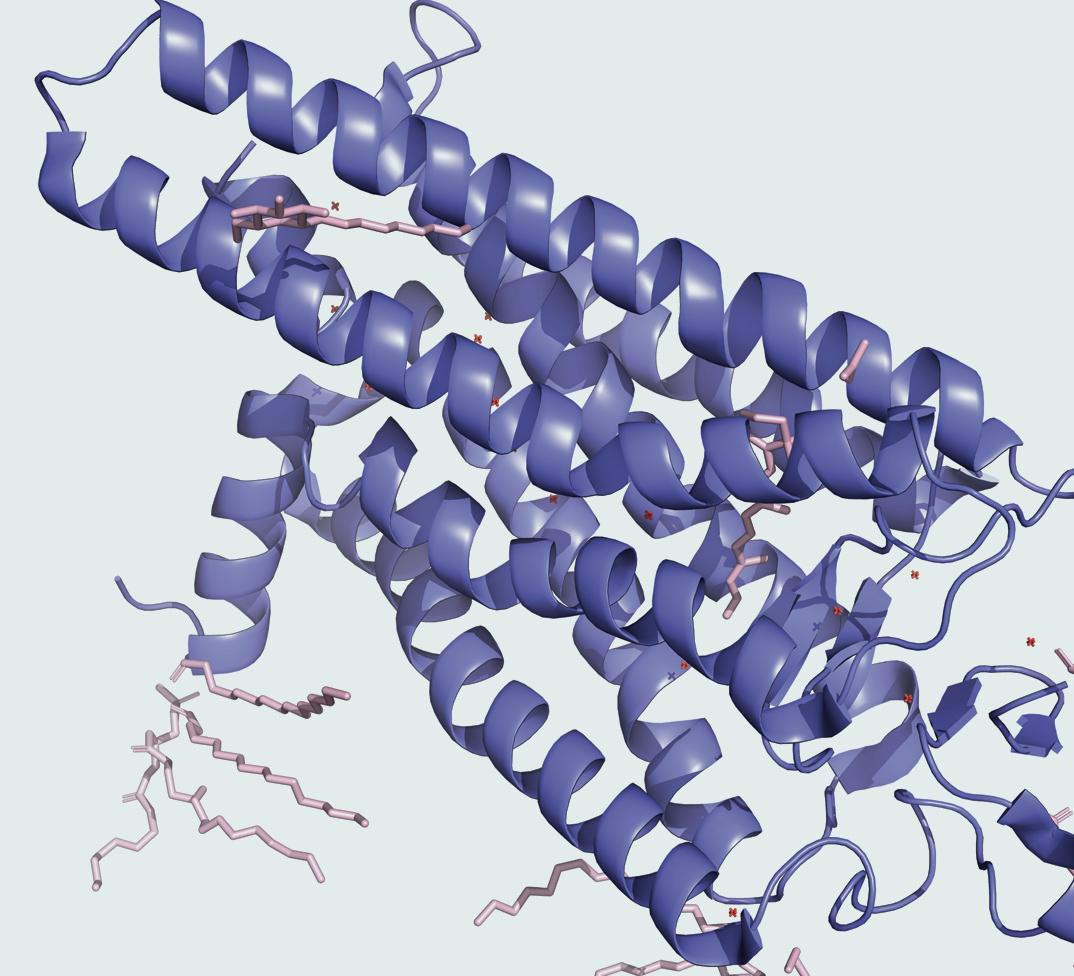
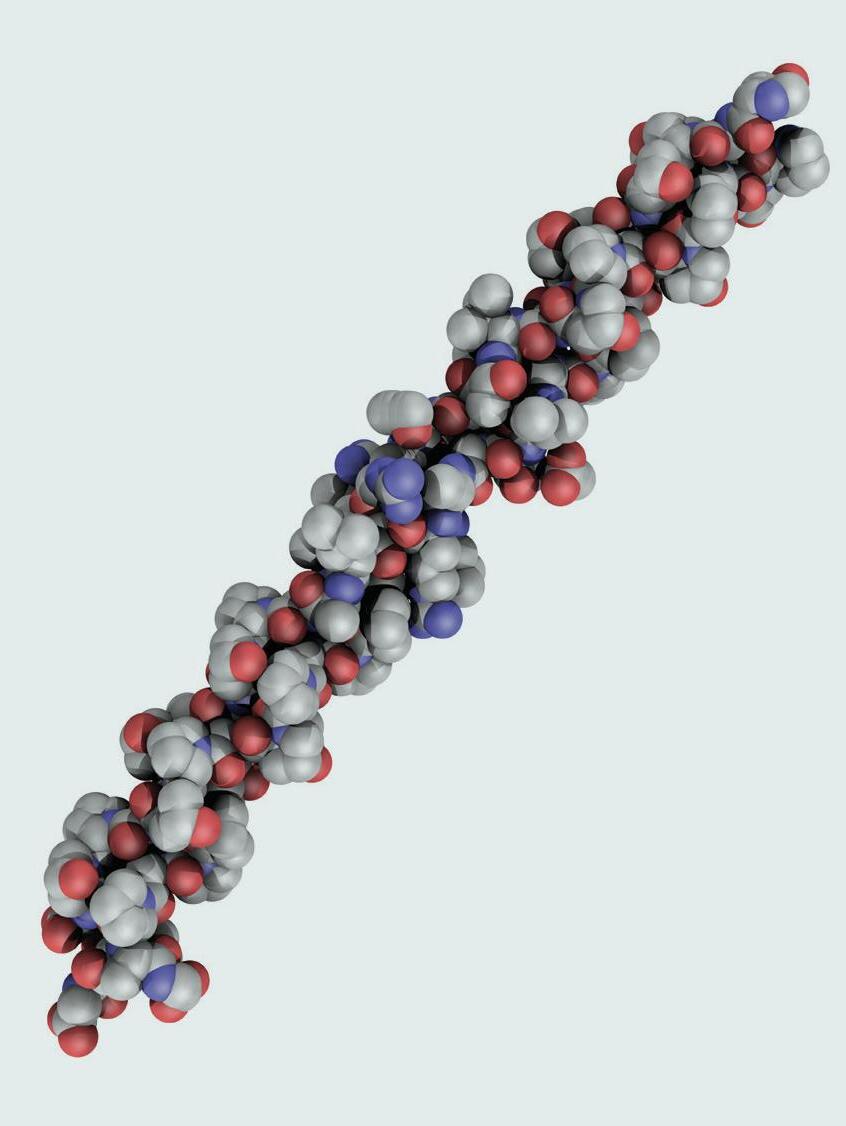
ПРОТЕИНИ
Име им потиче од грчке речи πρώτειος (протеиос), која значи
први или најважнији. И заиста је тако, они су основ функције и
грађе свих живих организама. Такође их називамо беланчевине
јер су јако често беле боје.
Шта су по хемијском саставу протеини?
Готово сви протеини су јако велики молекули и често за њих
кажемо да су макромолекули. Међутим, њиховим дугогодишњим
проучавањем хемичари су увидели да се протеини састоје од малих
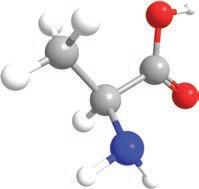
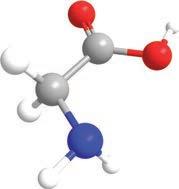
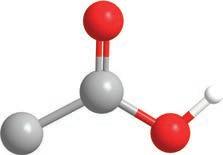
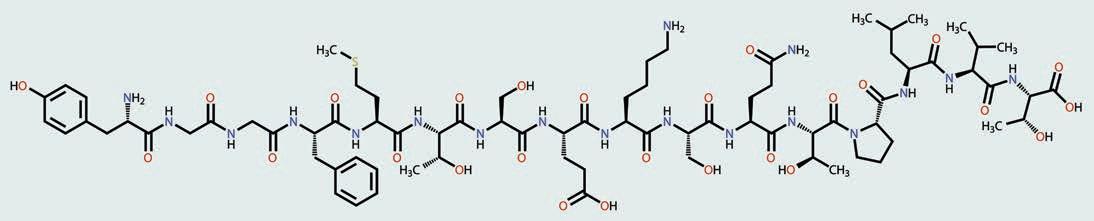
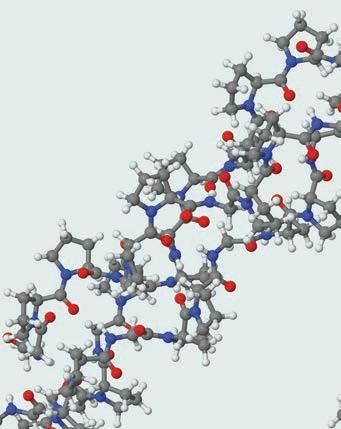
градивних јединица – амино-киселина . Свака амино-киселина
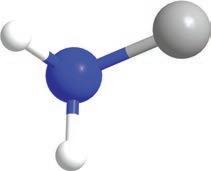
састоји се од два дела, две функционалне групе. Први је амински
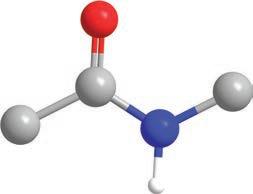
део и може се посматрати као амонијак код ког је азот, уместо с три водоника, везан за угљеник и два водоникова атома. Друга функционална група је карбоксилна група, која је једном везом повезана с истим угљениковим атомом са којим је повезан амонијак, односно амино-група. Ове две групе су одговорне за хемијска својства молекула амино-киселина. Угљеников атом, за који су везане амино-група, карбоксилна група
остатак, називамо





















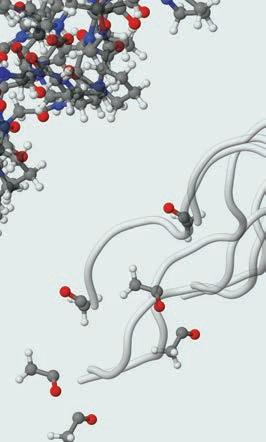




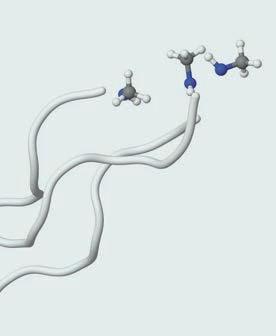



ДЕМОНСТРАЦИОНИ ОГЛЕД
За овај оглед вам није потребна заштитна опрема. Све што вам треба су млеко, газирани сок који садржи ортофосфорну киселину, беланце, шпиритусна лампа, епрувета и чаше.
У чаши помешајте млеко и сок. Сипајте беланце у епрувету и загревајте га на шпиритусној лампи. Запишите своја запажања.
Шта се догодило?
Структура протеина може се нарушити како хемијски, дејством соли, киселина, база или органских растварача, тако и физички, замрзавањем и грејањем. Уколико млеко, које је, као што знамо, смеша и садржи протеине, сипамо у газирани сок, који је кисео, нарушиће се структура протеина. Исто тако, ако загрејемо беланце, такође можемо нарушити структуру протеина којима оно обилује. Овај процес назива се денатурација протеина и њом они губе своје биолошке функције.





Podsetnik
Протеини су макромолекули изграђени од мањих градивних јединица –амино-киселина. Повезане пептидним везама, амино-киселине граде ланце који чине пептиде. У


ПИТАЊА И ЗАДАЦИ
1. Шта су амино-киселине?
2. Која је разлика између протеинских и есенцијалних амино-киселина?
3. Како настаје пептидна веза?
4. Шта су протеини?
5. Која су два најчешћа облика протеина?
6. Каква је улога протеина у живим бићима?
7. Шта је денатурација протеина?




ВИТАМИНИ
A, B, C, D, Е, К
Не, ово нису случајно одабрана слова. Ово су витамини , од
латинске речи vita, што значи живот и, слично као и протеини, основни су грађевински блокови који омогућавају нормално функционисање организма. Витамини су разнолика и понекада врло
комплексна органска једињења, која су нам потребна у малим
количинама за правилан метаболизам. Због тога их понекада
називамо и микронутријентима.
Која је улога витамина у биолошким системима?
Они су градитељи, браниоци и радници на одржавању и из-
градњи мишића и костију. Они су помоћници у
и разградњи других молекула. Они „хватају” енергију
њено коришћење. Они зацељују ране. Начин на који је откривена њихова важност
ница у исхрани узрокује појаву специфичних обољења. Стари морнари у својим дуготрајним


























је идеја уношења
суплементима добра, кључ за правилно функционисање је балансирана
минерали и вода. ВИТАМИН

А 2 mg
D0,005 mg
шаргарепа, спанаћ, бундева, бресква,
диња, млеко, путер, јаја
рибље уље и
месо, печурке, масни сир
E10 mg уље пшеничних клица, сунцокрет, бадем, лешник
K60 – 80 μg
зелено поврће, жуманце
АВИТАМИНОЗАХИПЕРВИТАМИНОЗА
кокошје (ноћно) слепило
рахитис
дегенеративне промене на
јетри, дијареја
појављивање масница на
телу, умањена коагулација, дијареја
висок крвни притисак, поремећај рада бубрега
крварење и споро зарастање рана
осип, свраб и црвенило коже
C30 – 70 mg
B11,4 mg
B21,7 mg
свеже воће
и поврће
– паприка, шипак, киви, лимун, броколи
јаја, махунарке, животињска јетра, житарице, квасац
јаја, млеко, риба,
животињска јетра
B320 mg
B510 mg
B62 mg
B730 μg
јаја, риба, јетра, лешници, печурке
јаја, јетра, месо, махунарке, печурке, квасац
јаја, јетра, риба, житарице, печурке, млеко, семенке, квасац
животињска јетра, жуманце, квасац, махунарке, лешник
скорбут – болест чији су симптоми
запаљење
десни, испадање зуба, поткожна
крварења
берибери –болест чији су симптоми
грчење мишића, слабљење рада срца, поремећај крвотока
упала слузокоже, промене на кожи
пелагра –
болест која се
манифестује
дијареја, мучнина
дрхтање тела, нервоза, алергије
свраб, осетљивост
променама на кожи, слабошћу, губитком апетита црвенило коже
стомачне тегобе, повраћање, несаница
мучнина, дијареја
анемија, нервни поремећаји, проблеми с кожом
нестабилан ход, ноћна узнемиреност
промене на кожи и коси није познато
B90,4 mg
B120,005 mg
Podsetnik
тамнозелено
лиснато
поврће,
квасац,
жуманце, јетра, шаргарепа,
кајсија, бундева
јетра, месо, млеко, јаја, сир, риба
анемијанеуролошки проблеми
нервни поремећаји, анемија, стомачне тегобе
проблеми с кожом

ПИТАЊА И ЗАДАЦИ
1. Шта су витамини?
2. Како се деле витамини према растворљивости?
3. Шта је авитаминоза, а шта хипервитаминоза?
4. Која је улога витамина?
5. Коју болест изазива недостатак витамина С? Који су симптоми ове болести?






Денатурација протеина За овај оглед потребне су








VIII. ЗАШТИТА
ЖИВОТНЕ СРЕДИНЕ И
ЗЕЛЕНА
















та чини животну средину?
Животна средина je насељени део Земље или неких делова Земље. То је простор где људи, животиње и биљке могу да настану, расту, развијају се и живе. Животна средина обухвата и интеракцију свих живих врста, климу, временске прилике и природне ресурсе који утичу на њихов опстанак и њихову активност.
Како људи утичу на животну средину? У првим корацима цивилизације











ЗАГАЂИВАЧИ, ЗАГАЂУЈУЋЕ СУПСТАНЦЕ
ПОСЛЕДИЦЕ ЗАГАЂИВАЊА
Шта су загађујуће супстанце?
Загађење представља нарушавање услова који омогућавају нормално функционисање живих организама. Према томе, загађујућа супстанца је свака супстанца која, када се унесе у животну средину, има нежељене ефекте или негативно утиче на њу. Многе од тих загађујућих супстанци исте су као и оне које налазимо у природи, али су у већим концентрацијама. Циркулисање природних хемијских једињења измењено је човековим деловањем испуштањем превеликих количина једињења која се не могу асимиловати, премештати или трансформисати истом брзином као раније у делове животне средине. То резултује утицајем на животну средину и здравље високим концентрацијама природних једињења и елемената у одређеном окружењу,
Бројне природне елементе




Угаљ и нафта често садрже сумпорна једињења и њиховим сагоревањем такође настаје сумпор(IV)-оксид. Лако се оксидује у сумпор(VI)-оксид (SO 3) на ваздуху, који се раствара у кишници и пошто је анхидрид киселина, воду чини јако киселом. Овакву кишу баш зато називамо кисела киша. Она је врло штетна не само за живи свет већ и за грађевинске
прераде хране као што су масти, инсектициди и хербициди, нафту и њене деривате, индустријске органске раствараче,
за личну хигијену, козметичким производима, као и разне лекове.
Неорганске загађујуће супстанце воде
од
су неки и киселине, амонијак, вештачка ђубрива, тешки метали.
Велики проблем представља макроскопски
који је, у ствари, смеће. Папир, пластика или


тла су олово, цинк, никал, кадмијум,
хром,
Они
потицати из више извора, као што су рударске, пољопривредне активности, електронски отпад (е-отпад) и медицински отпад.
Полициклични ароматични угљоводоници Полициклични

Podsetnik
















же рециклиране материјале. Када идете у куповину, потражите производе који се лако могу рециклирати
садрже рециклиране материјале.
Како можемо препознати који производи садрже рециклиране материјале?
ДЕМОНСТРАЦИОНИ ОГЛЕД За овај оглед није
1 – PET (polyethylene terephthalate)
2 – HDPE (high density polyethylene)
3 – PVC (polyvinylchloride)
4 – LDPE (low density polyethylene)
пластика је
које постоји најмања вероватноћа испуштања штетних супстанци.
Пластика коју би требало избегавати када се ради
паковању производа за личну употребу.
20
намењене за транспорт –таласасти картон)
21 разне врсте папира (новине, часописи, каталози – раван картон)
22канцеларијски папир, књиге

90пластика/алуминијум
91пластика/бели лим
92пластика/разноврсни метали
6 – PS (polystyrene)Пластика за једнократну
употребу јер може
испустити стирен, једињење које, по неким истраживањима, може утицати на појаву рака.
7 – PC (или без ознаке)
Бројчана
Најлошија врста пластике за прехрамбене производе јер може испустити хемикалију BPA (bisphenol A).
40FE
челик97стакло/бели лим
Podsetnik
Рециклажа је процес претварања отпадних материја у употребљиве материјале и предмете. Обухвата три корака: прикупљање и обраду рециклажног материјала, производњу употребом рециклираних материјала и куповину и коришћење производа од рециклираних материјала.


170170
41ALU
алуминијум98стакло/разноврсни метали



Зелена хемија
Шта је зелена хемија?
Зелена хемија

1. Превенција Боље је спречити него лечити.
2. Атомска економичност
3. Мање
4.
7. Коришћење
8. Смањење
9. Катализа
10. Пројектована
11.
I n-хексан
II 2-метилпентан
III 3-метилпентан
IV 2,3-диметилбутан
V 2,2-диметилбутан
1-пентин
Podsetnik

смањују или елиминишу коришћење и генерисање загађивача. Заснива се на дванаест принципа, и то: превенције, атомске економичности, мање опасне хемијске синтезе, пројектовања сигурнијих хемикалија, сигурнијих растварача и помоћних супстанци, енергетски ефикасних процеса, коришћења обновљивих сировина, смањења дериватизације, катализе, пројектоване деградације, аналитике у реалном времену ради спречавања загађења и суштински сигурнијих хемијских процеса којима се спречавају хаварије.
A
Алдехиди – органска једињења која у свом мо-
лекулу садрже карбонилну функционалну групу – угљеников атом везан за један атом водоника и једну алкил-групу једноструком везом, а за један
атом кисеоника двоструком везом. Могу настати
оксидацијом примарних алкохола. Општа формула алдехида је RCHO.
Алкани – засићени угљоводоници отвореног низа. Атоми угљеника и водоника, од којих се ал-
кени састоје повезани су искључиво једноструким везама. Први члан хомологног низа алкана је
метан. Алкани се могу наћи у три основна агрегатна стања, нерастворљиви су у води и састојци су природног гаса и нафте. Карактеристична ре-
акција алкана је реакција супституције. Општа формула алкана је CnH2n + 2
Алкени – незасићени угљоводоници
Анхидрид
с водом даје хидроксид.
Анхидрид киселине – оксид неметала
Ароматични угљоводоници – незасићени циклични угљоводоници. Први члан хомологног низа ароматичних угљоводоника је бензен C6H6 Ови угљоводоници се могу добити из катрана каменог угља и нафте. Нерастворљиви су у води и изузетно су токсични и канцерогени. Ароматичне угљоводонике
Дестилација
две или више течних супстанци с различитим температурама кључања такође се могу раздвојити, а тај процес се назива фракциона дестилација. Е
Електролитичка дисоцијација – разлагање
једињења с јонском и поларном ковалентном везом на јоне, у растворима поларних молекула
која садрже остатак молекула киселине и остатак молекула алкохола. Мирис воћа
уља
алкохола јесте RCOOR.
Етанол – монохидроксилни алкохол, чија је хе-
стања, растворљив у води и има неуротоксична и психоактивна дејства. Може се добити
алкохолним врењем шећера. Има изузетну употребну вредност у индустрији и, између осталог, користи се као растварач, средство за дезинфекцију, за конзервирање, и као полазна сировина у синтези комплексних органских једињења итд.
једињења
која садрже карбонилну групу. За разлику од алдехида,
Инвертни шећер – смеша
својства.
с
оксидације, при чему настају њихови оксиди. Базни оксиди неких метала реагују с водом
дајући хидроксиде. У реакцији с киселинама метали или њихови јони граде соли.
Метан – први члан хомологног низа алкана, чија је хемијска формула CH4. То је гас без боје и мириса, лакши од ваздуха. У смеши с ваздухом је
лако запаљив. Може настати разлагањем органског материјала под дејством микроорганизама и може се наћи у рудницима угља, као састојак
вулканских гасова. Може се употребљавати као гориво, као сировина у индустрији итд.
Моносахариди – угљени хидрати најпростије структуре. Могу бити полихидроксилни алдехи-
ди – алдозе, или полихидроксилни кетони – кетозе, а према броју угљеникових атома, разликујемо триозе, тетрозе, пентозе, хексозе. Примери су глукоза (грожђани шећер) и фруктоза (воћни шећер). Моносахариди имају сладак укус, растварају су у води, у биолошким системима имају градивну улогу и важан су извор енергије. Добијају се у процесу фотосинтезе.
којом се одвија. Добијена једињења називају се оксиди.
Олигосахариди – угљени хидрати који се састоје од више моносахаридних јединица (од две до десет). Олигосахарид
Нафта – сложена смеша засићених ацикличних, цикличних и ароматичних угљоводоника и других једињења,
или умрежени молекули добијени повезивањем мањих градивних јединица реакцијом полимеризације. Веома су велика група једињења која се налазе у свим биолошким системима. Синтетички добијени пластични полимери употребљавају се за производњу пластичних фолија, играчака, вештачких влакана, а пошто су сјајни изолатори, користе
хидрати који имају више од десет моносахаридних јединица
атом неког молекула замењује другим атомом или се група атома неког
молекула замењује другом групом атома. Атом
Општа формула угљених хидрата је Cn(H2O)n
Угљоводоници – органска једињења која садрже само угљеник и
може
нарушити животна средина.
Реакција сапонификације – хемијска реакција
разлагања естара на алкохол и со карбоксилне
киселине (сапун) јаким базама.
Реакција полимеризације – реакција ланчане
адиције малих молекула,



















De Depoposi s tpho h tos

Wi


Dr D Anton o y vaan der Ent
BAASc S , MS M c, c PhD

Seninior or Resesea e rc r h Fellow
The Univerrsity y of f Qu Q ee e nsland, Australia (с
. 13 1 )







CIP - Каталогизација у публикацији - Народна библиотека Србије, Београд
37.016:54(075.2)
ВАТИЋ, Саша, 1988Хемија : уџбеник за осми разред основне школе / Саша Ватић, Биљана Алавуковић ; [фотографије Страхиња Лукић]. - 2. изд. - Београд : Завод за уџбенике, 2021 (Београд : Бирограф). - 177 стр. : илустр. ; 27 cm
Тираж 3.500. - Речник основних хемијских појмова: стр. 174-177.
ISBN 978-86-17-20664-0
1. Алавуковић, Биљана, 1981- [аутор] COBISS.SR-ID 54750729