

COMPOSTAJE DINÁMICA DEL
Uso efectivo de microorganismos
Daniela Rosero-Murillo, Paúl Arias-Muñoz, Santiago Cabrera-García, Oscar Rosales-Enríquez & Gabriel Chimbo-Yépez.
DEL
COMPOSTAJE DINÁMICA
Uso efectivo de microorganismos

DEL
COMPOSTAJE DINÁMICA
Uso efectivo de microorganismos



Edita
Editorial Universidad Técnica del Norte
Avenida 17 de Julio, 5 21
Ibarra - Ecuador
Telf. 593 (6) 299 7800 editorial@utn.edu.ec
Pares revisores académicos externos
MSc Klever Mauricio Quimbiulco Sánchez
Universidad Yachay Tech kquimbiulco@yachaytech.edu.ec
MSc Diego Marcelo Caicedo Rosero Universidad Politécnica Estatal del Carchi - UPEC diego.caicedo@upec.edu.ec
Corrección de estilo
PhD. Carlos Andrés Bolaños Carriel
Evaluador Revisor de Estilo
Fotografía
Diseño y diagramación
Lic. Carla Perugachi carlaperugachi@gmail.com
© de los textos y fotografías sus respectivos autores, 2025
© de esta edición
Editorial Universidad Técnica del Norte
Prohibida la reproducción total o parcial de esta obra sin la previa autorización escrita por parte de la editorial.
Edición digital
DOI: 10.53358/libficaya/UJLF5647
ISBN: 978-9942-572-39-4
Autores
Daniela Rosero-Murillo mdroserom1@utn.edu.ec https://orcid.org/0009-0002-0061-6801
Paúl Arias-Muñoz dparias@utn.edu.ec ttps://orcid.org/0000-0002-1263-2748
Santiago Cabrera-García jscabrera@utn.edu.ec https://orcid.org/0000-0001-6114-2043
Oscar Rosales-Enríquez oarosales@utn.edu.ec https://orcid.org/0000-0001-7131-6203
Gabriel Chimbo-Yépez gachimbo@utn.edu.ec https://orcid.org/0000-0001-8595-6703
4.3.2.
5.Normativa
5.1.Bioinsumos
5.3.Tolerancia
5.4.Manejo
5.4.1.Principales
5.4.2.Medidas
Figuras
Principales géneros de microorganismos beneficiosos en el proceso de compostaje.
Funciones de las bacterias en el proceso de compostaje. Fuente: Brey, (2023).
Mecanismos beneficiosos de las microalgas para el mejoramiento del compostaje61
Figura 23 ...............................................................................................................
Proceso de bioprospección para la obtención de microorganismos benéficos para el proceso de compostaje. 69 Figura 24 ...............................................................................................................
Mapa global de áreas clave para la bioprospección, destacando hábitats ricos en biodiversidad con potencial para descubrimientos científicos e industriales. .......
Figura 25 ...............................................................................................................
Proceso de Tinción de Gram para la identificación de bacterias.
Figura 26 74
Proceso de Tinción Diferencial para la identificación de actinomicetos y hongos. 74
Figura 27 75
Proceso de la Reacción en Cadena de la Polimerasa (PCR). .............................. 75
Figura 28 ............................................................................................................... 76
Proceso de electroforesis en gel en gradiente desnaturalizante para la identificación de microorganismos.
Figura 30 77
Proceso de Secuenciación de Next Generation. Fuente: Park & Kim, (2016). ..... 77
Figura 31 ............................................................................................................. 121
Distribución de tierras dedicadas a la agricultura orgánica por continente 121
Indice Tablas
Rango de pH para el crecimiento óptimo de los microorganismos en el
Tabla 12 .............................................................................................................
Tipos de tinción para la identificación de los microorganismos..........................
13 ............................................................................................................
Técnicas moleculares para la identificación de los microorganismos. ...............
Tabla 14 ............................................................................................................
Genes de uso frecuente para evaluar procesos microbianos específicos usando PCR. ......................................................................................................
Tabla 15 .............................................................................................................
Efectos positivos en cultivos al hacer uso de inóculos microbianos en el proceso de compostaje. ...................................................................................................
16 .............................................................................................................
Enzimas secretadas por el actinomiceto Streptomyces griseorubens. ..............
17 .............................................................................................................
Enzimas que secreta el hongo Phanerochaete chrysosporium.
que secreta la bacteria Paracoccus denitrificans. .............................
que secreta la bacteria Ureibacillus thermosphaericus.
Límites establecidos de metales pesados por diferentes normativas en un . insumo orgánico. ..............................................................................................
24 ..........................................................................................................
Límites establecidos de patógenos por diferentes normativas en un fertilizante orgánico. .........................................................................................
25 ...........................................................................................................
Almacenamiento de los microorganismos a corto y largo plazo. .....................
Prólogo
El documento presenta una investigación exhaustiva sobre el uso adecuado de los microorganismos en el proceso de compostaje. Este está redactado desde la perspectiva de las ciencias agrícolas con énfasis en la biotecnología agrícola y microbiología. El objetivo principal de este trabajo es sintetizar la información más relevante para la correcta inoculación de microorganismos en el compost a través de una revisión de trabajos experimentales de alto impacto y de bibliografía especializada a nivel mundial.
En esta obra se explorarán aspectos claves del uso de los microorganismos como lo son: fases del proceso de compostaje, materiales utilizados, métodos de compostaje, microbiología del compostaje, microorganismos benéficos en el compostaje, bioprospección de microorganismos, inoculación de microorganismos en la composta, inocuidad en el compostaje, y normativa y regulación del uso de abonos orgánicos.
El libro se plantea como una herramienta para productores, proveedores de insumos, investigadores, funcionarios públicos, funcionarios de organizaciones no gubernamentales, estudiantes de ciencias agrícolas y ciencias biológicas. Ya que con su información permitirá tomar decisiones adecuadas sobre el uso de microorganismos para mejorar el proceso de descomposición y mineralización de la materia orgánica.
Finalmente, los autores buscan que se contextualice a la obra como un análisis detallado de elaboración del compostaje desde un contexto científico y técnico. Además, se persuade a la modificación de paradigmas en el uso del compost como una enmienda que aporta nutrientes, a un biofertilizante que cataliza los ciclos biogeoquímicos y potencia los servicios ecosistémicos en los suelos en los que es aplicada.
Introducción
El acelerado crecimiento poblacional y las actividades económicas asociadas a este fenómeno han dado lugar a importantes problemas sociales, económicos y ambientales (contaminación del suelo, aire y agua) (Gligo et al., 2021). Uno de los efectos más significativos de esta explosión demográfica sin precedentes es el aumento en la demanda de alimentos, lo que conlleva a la intensificación de la producción agropecuaria (Manea et al., 2024; Nadarajah & Abdul Rahman, 2023). Para mantener altos niveles de productividad se ha hecho imperioso la aplicación de insumos tanto orgánicos como de tipo sintético.
Ecuador no está exento de estos desafíos ambientales y de salud pública, según datos del INEC (2021) aproximadamente el 56.8% de la superficie ocupada con cultivos permanentes (cacao, maíz, papa, banano, flores) aplican insumos de síntesis química, mientras que en apenas el 3% del área cultivada se utiliza únicamente productos de origen orgánico. De estos últimos, los que destacan y se aplican con mayor frecuencia en las unidades productivas son los bioestimulantes, bioles, extractos de plantas, y biofertilizantes. En este último grupo la enmienda de mayor relevancia y difusión es el compost.
El uso del compostaje ha ganado relevancia como una metodología para solventar los crecientes desafíos de la gestión de residuos orgánicos, la fertilidad del suelo y la agricultura sostenible (Moreano & Mancheno, 2020). Este método se fundamenta en la biodegradación en condiciones controladas de la materia orgánica, lo que resultaría en una enmienda del suelo con carbono orgánico estable (humus) y libre de patógenos (Termorshuizen et al. 2004). La obtención de un compost de calidad requiere tres componentes clave: materia orgánica, una población microbiana inicial y condiciones óptimas (oxígeno, humedad, temperatura, pH y la relación C: N) (Wurff et al. 2016).
El compost, como una enmienda bien elaborada, posee diversas funciones y ofrece servicios que pueden modificar de manera positiva al suelo donde es aplicado generando un sistema resiliente (Termorshuizen et al. 2004). En este contexto, este biofertilizante puede ser considerado como un acondicionador de la matriz edáfica que puede mejorar las propiedades físicas, químicas y biológicas del suelo (Goldan et al. 2023). La modificación positiva de la matriz edáfica en sus propiedades conlleva un incremento en su fertilidad y capacidad de dotar a la planta de un ambiente adecuada para su desarrollo como se detalla en la Figura 1 (FAO, 2023).
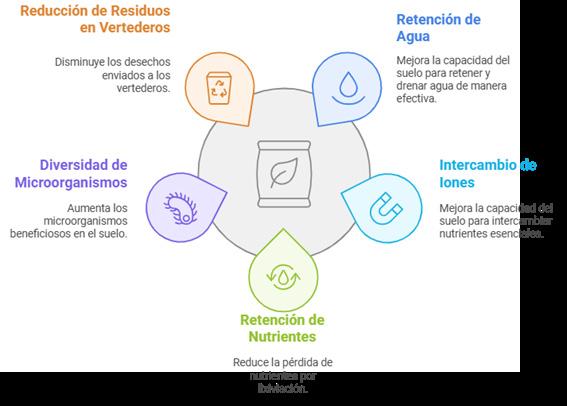
Figura 1 Beneficios de la aplicación del compost en las propiedades del suelo y sus funciones ecológicas.
En el aspecto físico, la matriz del suelo puede ser descrita como una estructura compuesta de partículas minerales y orgánicas y espacios vacíos ocupados por agua o aire. La aplicación del compost influencia de manera positiva a las propiedades del suelo como la estructura, densidad y textura, donde son modificadas mediante la estabilización de los agregados del suelo (Kranz et al. 2020). Consecuentemente, procesos como el drenaje, la conductividad hidráulica, contenido de agua y la capacidad de almacenamiento de agua son parámetros que son optimizados en consecuencia de la aplicación de este biofertilizante (Kranz et al. 2020).
En el caso de las propiedades químicas del suelo, el compost se considera una fuente de nutrientes, un elemento de captura de carbono, y también un buffer de pH y de la conductividad eléctrica del suelo. El valor nutricional del compost se basa fundamentalmente en tres grupos: los componentes minerales, macronutrientes primarios (N, P y K), secundarios (Ca, Mg y S) y micronutrientes (Cl, Fe, B, Mn, Zn, Cu, Ni). En general, las concentraciones esperadas de los macronutrientes son aproximadamente 1.5% de N, 0.2% de P y 1.0% de K (Sánchez et al. 2017).
Al tratarse de una fermentación aeróbica, la aplicación de compost en el suelo permite estabilizar el nitrógeno, minimizando las emisiones de gases de efecto invernadero (Joo et al. 2015; Azim et al. 2018). De la misma forma, su aplicación regula la acidificación del suelo y la eutrofización del agua (Bonilla et al., 2012; Sun et al., 2022). Estos efectos en las características químicas del suelo provienen principalmente del aumento de materia orgánica (MO) (Garcia et al., 2014; Graziani et al., 2020; Xie et al., 2023).
Estos contenidos nutricionales son insuficientes para satisfacer las necesidades de los cultivos extensivos (Sánchez et al. 2017). Por lo tanto, las capacidades modificadoras del
suelo que posee este bioinsumo no provienen únicamente de su contenido mineral, sino de otra de sus propiedades. En este aspecto, el compost tiene características biológicas que lo hacen un producto que genera beneficios adicionales al momento de su aplicación al suelo (Pang et al. 2017). Los microrganismos beneficiosos presentes en el biofertilizante son aquellos que otorgan las características mejoradoras del suelo (Trello 2022).
En este sentido, hay varios tipos de microorganismos en las pilas de compost (Nemet et al., 2021). Estos son denominados Microrganismos Efectivos (EM, por sus siglas en inglés). Un EM consiste en un consorcio de microorganismos benéficos, de ocurrencia natural entre los que se enumeran las bacterias, bacterias ácido lácticas, levaduras, actinomicetos y ciertos organismos fotosintéticos (Van Fan et al. 2017; Sumiyati et al. 2022). Los EM desempeñan varias funciones en el compost desde la descomposición, reciclaje de nutrientes, regulación de temperatura, supresión de patógenos y formación de humus (Li et al., 2019; Rastogi et al., 2020; Yánez Yánez et al., 2016).
Queda claro que los microorganismos desempeñan un rol vital en las funciones de un compost de calidad (He et al., 2023; Liu et al., 2023). Sin duda, aprovechar los microorganismos para mejorar el compost representa un enfoque prometedor y sostenible para abordar los desafíos que enfrenta el sector agrícola del país (Yarzábal & Chica, 2021). Más aun en el contexto nacional, la potencialidad de recursos microbianos ofrece una oportunidad para enriquecer enmiendas compostadas (Díaz et al. 2021).
Para aprovechar todo el potencial de los microorganismos en el compostaje, se deben considerar varios aspectos críticos, como la selección de cepas de microbios adecuadas, las condiciones óptimas y el desarrollo de métodos rentables y eficientes (Chroni et al., 2009; Gaspar et al., 2022). Por ello, el objetivo del presente trabajo es brindar información acerca del uso de microrganismos para el mejoramiento del compostaje, donde se realiza una exploración integral, profundizando con aspectos científicos sobre compostaje enriquecido con microorganismos, sus aplicaciones en diferentes entornos agrícolas, los microorganismos específicos involucrados y los beneficios ambientales que se pueden obtener a través de esta práctica sustentable.
BIBLIOGRAFÍA
Azim, K., Soudi, B., Boukhari, S., Perissol, C., Roussos, S., & Thami Alami, I. (2018). Composting parameters and compost quality: a literature review. Organic Agriculture, 8(2), 141–158. https://doi.org/10.1007/s13165017-0180-z
Bonilla, N., Gutiérrez-Barranquero, J. A., De Vicente, A., & Cazorla, F. M. (2012). Enhancing soil quality and plant health through suppressive organic amendments. Diversity, 4(4), 475–491. https://doi.org/10.3390/ d4040475
Chroni, C., Kyriacou, A., Georgaki, I., Manios, T., Kotsou, M., & Lasaridi, K. (2009). Microbial characterization during composting of biowaste. Waste Management, 29(5), 1520–1525. https://doi.org/10.1016/j.wasman.2008.12.012
Díaz, M., Jarrín-V, P., Simarro, R., Castillejo, P., Tenea, G. N., & Molina, C. A. (2021). The Ecuadorian Microbiome Project: a plea to strengthen microbial genomic research. Neotropical Biodiversity, 7(1), 223–237. https://doi.org/10.1080/23766808.2021.193 8900
Food and agriculture organization. (2013). Manual de compostaje del agricultor. In Oficina Regional de la FAO para América Latina y el Caribe. http://www.fao.org/3/a-i3388s. pdf
Garcia, D., Lima, L., Ruiz, L., & Calderon, P. (2014). Métodos y parámetros para determinar la madurez en el compost a nivel de fincas. Cub@: Medio Ambiente Y Desarrollo, 14(26). https://cmad.ama.cu/index.php/ cmad/article/view/194
Gaspar, S. S., Assis, L. L. R., Carvalho, C. A., Buttrós, V. H., Ferreira, G. M. dos R., Schwan, R. F., Pasqual, M., Rodrigues, F. A., Rigobelo, E. C., Castro, R. P., & Dória, J. (2022). Dynamics of microbiota and physicochemical characterization of food waste in a new type of composter. Frontiers in Sustainable Food Systems, 6. https://doi.org/10.3389/ fsufs.2022.960196
Gligo, N., Alonso, G., Barkin, D., Brailovsky, A., Brzovic, F., Carrizosa, J., Durán, H., Fernández, P., Gallopín, G., Pengue, W., Sejenovich, H., Sunkel, O., & Villamil, J. (2021). La tragedia ambiental de América
Latina y el Caribe. In La tragedia ambiental de América Latina y el Caribe. https://doi. org/10.18356/9789210047425
Goldan, E., Nedeff, V., Barsan, N., Culea, M., Panainte-Lehadus, M., Mosnegutu, E., Tomozei, C., Chitimus, D., & Irimia, O. (2023). Assessment of Manure Compost Used as Soil Amendment A Review. Processes, 11(4), 1–16. https://doi.org/10.3390/pr11041167
Graziani, P., Manfredi, I., Ferrari, M., Quintana, J., Alarcon, V., & Silva, A. (2020). Manual de aprovechamiento de residuos orgánicos municipales. Ministerio de Ambiente y Agua, 1–79. www.ambiente.gob.ec
He, X., Cong, R., Gao, W., Duan, X., Gao, Y., Li, H., Li, Z., Diao, H., & Luo, J. (2023). Optimization of composting methods for efficient use of cassava waste, using microbial degradation. Environmental Science and Pollution Research, 30(17), 51288–51302. https://doi.org/10.1007/s11356-02325818-8
INEC. (2021). Módulo de Información Ambiental y Tecnificación Agropecuaria. https://www. ecuadorencifras.gob.ec/
Joo, S. H., Monaco, F. Dello, Antmann, E., & Chorath, P. (2015). Sustainable approaches for minimizing biosolids production and maximizing reuse options in sludge management: A review. Journal of Environmental Management, 158, 133–145. https://doi. org/10.1016/j.jenvman.2015.05.014
Kranz, C. N., McLaughlin, R. A., Johnson, A., Miller, G., & Heitman, J. L. (2020). The effects of compost incorporation on soil physical properties in urban soils – A concise review. In Journal of Environmental Management (Vol. 261, p. 110209). Elsevier Ltd. https:// doi.org/10.1016/j.jenvman.2020.110209
Li, C., Li, H., Yao, T., Su, M., Ran, F., Han, B., Li, J., Lan, X., Zhang, Y., Yang, X., & Gun, S. (2019). Microbial inoculation influences bacterial community succession and physicochemicalharacteristics during pig manure composting with corn straw. Bioresource Technology, 289(March), 121653. https:// doi.org/10.1016/j.biortech.2019.121653
Liu, X., Zubair, M., Kong, L., Shi, Y., Zhou, H., Tong, L., Zhu, R., Lv, Y., & Li, Z. (2023). Shifts in bacterial diversity characteristics during the primary and secondary fermentation
stages of bio-compost inoculated with effective microorganisms agent. Bioresource Technology, 382(April), 129163. https://doi. org/10.1016/j.biortech.2023.129163
Manea, E. E., Bumbac, C., Dinu, L. R., Bumbac, M., & Nicolescu, C. M. (2024). Composting as a Sustainable Solution for Organic Solid Waste Management: Current Practices and Potential Improvements. Sustainability (Switzerland), 16(15), 1–25. https://doi. org/10.3390/su16156329
Moreano, J., & Mancheno, C. (2020). Analysis of the productivity and competitiveness of the agricultural sector in Ecuador. Dominio de Las Ciencias, 6(5), 412–428. https://doi.org/ http://dx.doi.org/10.23857/dc.v6i5.1610
Nemet, F., Perić, K., & Lončarić, Z. (2021). Microbiological activities in the composting process: A review. Columella: Journal of Agricultural and Environmental Sciences, 8(2), 41–53. https://doi.org/10.18380/szie. colum.2021.8.2.41
Pang, G., Cai, F., Li, R., Zhao, Z., Li, R., Gu, X., Shen, Q., & Chen, W. (2017). Trichoderma-enriched organic fertilizer can mitigate microbiome degeneration of monocropped soil to maintain better plant growth. Plant and Soil, 416(1–2), 181–192. https://doi. org/10.1007/s11104-017-3178-0
Rastogi, M., Nandal, M., & Khosla, B. (2020). Microbes as vital additives for solid waste composting. Heliyon, 6(2), e03343. https:// doi.org/10.1016/j.heliyon.2020.e03343
Sánchez, Ó. J., Ospina, D. A., & Montoya, S. (2017). Compost supplementation with nutrients and microorganisms in composting process. Waste Management, 69(26), 136–153. https://doi.org/10.1016/j.wasman.2017.08.012
Sumiyati, S., Priyambada, I. B., Zahra, S. A. F., Pradhana, D. R., Haritsa, R. T., Rahman, T., Haq, M. F. Q., & Harjanti, A. W. P. (2022). Addition of Local Microorganisms (MOL) Organic Waste as Compost Bioactivator. IOP Conference Series: Earth and Environmental Science, 1098(1). https://doi. org/10.1088/1755-1315/1098/1/012057
Sun, S., Abdellah, Y. A. Y., Miao, L., Wu, B., Ma, T., Wang, Y., Zang, H., Zhao, X., & Li, C. (2022). Impact of microbial inoculants combined with humic acid on the fate of estro-
gens during pig manure composting under low-temperature conditions. Journal of Hazardous Materials, 424(PD), 127713. https:// doi.org/10.1016/j.jhazmat.2021.127713
Termorshuizen, A. J., Moolenaar, S. W., Veeken, A. H. M., & Blok, W. J. (2004). The value of compost. Reviews in Environmental Science and Biotechnology, 3(4), 343–347. https://doi.org/10.1007/s11157-004-23332
Trello, B. (2022). The Composting Biotechnology: A Microbial Aerobic Solid Substrate Fermentation. Compag Technologies International
Van Fan, Y., Lee, C. T., Ho, C. S., Klemeš, J. J., Wahab, R. A., Chua, L. S., & Sarmidi, M. R. (2017). Evaluation of microbial inoculation technology for composting. Chemical Engineering Transactions, 56(January), 433–438. https://doi.org/10.3303/CET1756073
Wurff, A. W. G., Funchs, J. G., Raviv, M., & Termorshuizen, A. J. (2016). Handbook for Composting and Compost Use in Organic Horticulture (Issue January). https://doi. org/http://dx.doi.org/10.18174/375218
Xie, S., Tran, H. T., Pu, M., & Zhang, T. (2023). Transformation characteristics of organic matter and phosphorus in composting processes of agricultural organic waste: Research trends. Materials Science for Energy Technologies, 6, 331–342. https://doi. org/10.1016/j.mset.2023.02.006
Yánez Yánez, W., Villacís-Aldaz, L. A., León-Gordón, O. A., Velástegui-Espín, G. P., López-Villacís, I. C., & Cruz-Tobar, S. E. (2016). Efectos de un compost enriquecido con microorganismos eficientes sobre la germinación de semillas recalcitrantes de Artocarpus altilis (Parkinson) Fosberg y Theobroma cacao L. . Journal of the Selva Andina Biosphere, 4(2), 100–108. https:// doi.org/10.36610/j.jsab.2016.040200100
Yarzábal, L. A., & Chica, E. J. (2021). Microbial-Based Technologies for Improving Smallholder Agriculture in the Ecuadorian Andes: Current Situation, Challenges, and Prospects. Frontiers in Sustainable Food Systems, 5(March), 1–8. https://doi. org/10.3389/fsufs.2021.61744

CAPÍTULO 1
1. El compostaje
El compostaje es un proceso biológico, técnico y controlado que transforma los residuos orgánicos en un material homogéneo, estable y con propiedades óptimas para el suelo y desarrollo vegetal (Azim et al. 2018). Este proceso puede ser resumido como una ecuación en la cual el sustrato y el oxígeno ingresan a un sistema y como resultados generan compost, dióxido de carbono (CO2), agua (H2O), amoniaco (NH3), y biomasa (Ecuación 1).
Sustrato +O 2
Compost + CO2 +H 2 O+ NH3 +B iomasa
Ecuación 1. Resumen del proceso de compostaje
A pesar de que esta descripción puede ser muy simplista, para términos prácticos se puede representar como se observa en la Figura 2. En esta se muestra que los microorganismos (bacterias, hongos, actinomicetos) presentes en el sustrato utilizan el nitrógeno (N) y el carbono (C) disponibles en este para sintetizar su propia biomasa. Además, se produce calor, gases como NH3 y CO2, vapor de agua, y la formación de materia orgánica estable denominada compost, (Nemet et al., 2021; Rastogi et al., 2020).
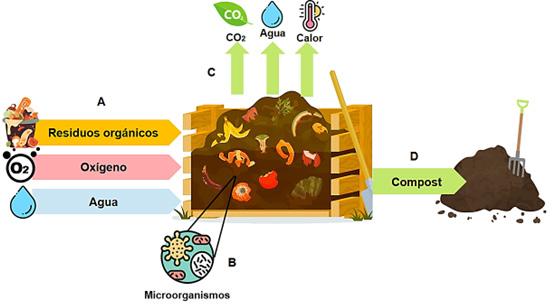
Figura 2
Esquema del proceso de compostaje aeróbico. Se utiliza: residuos orgánicos, presencia de oxígeno y agua (A), estos son necesarios para que los microorganismos descompongan el sustrato orgánico (B). Se liberan CO₂, H₂O y calor (C) y se genera compost que es beneficioso para el suelo (D).
Un compost bien elaborado puede ser considerado un abono orgánico que promueve diferentes beneficios en el suelo y en el desarrollo de las plantas. Sin embargo, para que este cumpla con estas funciones debe presentar una calidad agronómica adecuada (Bárcena et al. 2012; Domínguez Núñez 2015). Factores como la presencia de impurezas en la materia prima, composición, estabilidad de la materia orgánica (MO), y la posible presencia de contaminantes pueden alterar la calidad del compostaje (FAO, 2013; Garcia & Herran, 2014). Por ello, resulta imprescindible un análisis detallado del proceso de producción del compost y de los componentes que lo constituyen. A continuación, se detallan las etapas del proceso y las condiciones en las cuales se desarrolla.
1.1. Elaboración del compostaje
Para un buen compostaje se debe colocar capas de materiales de abono en la pila o contenedor, así como alternar entre materiales verdes (ricos en nitrógeno), como leguminosas que producen bacterias nitrificantes y materiales marrones (ricos en carbono) (Bhattacharya 2023).
En la mayoría de los casos, se usa 60% de aserrín, 30% de abono verde de y 10% de estiércol (Figura 3). Esto ayuda a mantener una proporción equilibrada de carbono y nitrógeno (25:1), que es esencial para la actividad microbiana (Azim et al., 2018; FAO, 2013; Ministerio de Agricultura y Ganadería, 2021). Es de suma importancia voltear o mezclar periódicamente el compost para airearlo y distribuir la humedad y los microorganismos de manera uniforme. El volteo se realiza según la temperatura del compost. Por lo general, se realiza después del segundo día del proceso de compostaje, cuando se haya alcanzada la temperatura límite de 75 °C (Nakasaki & Hirai, 2017).
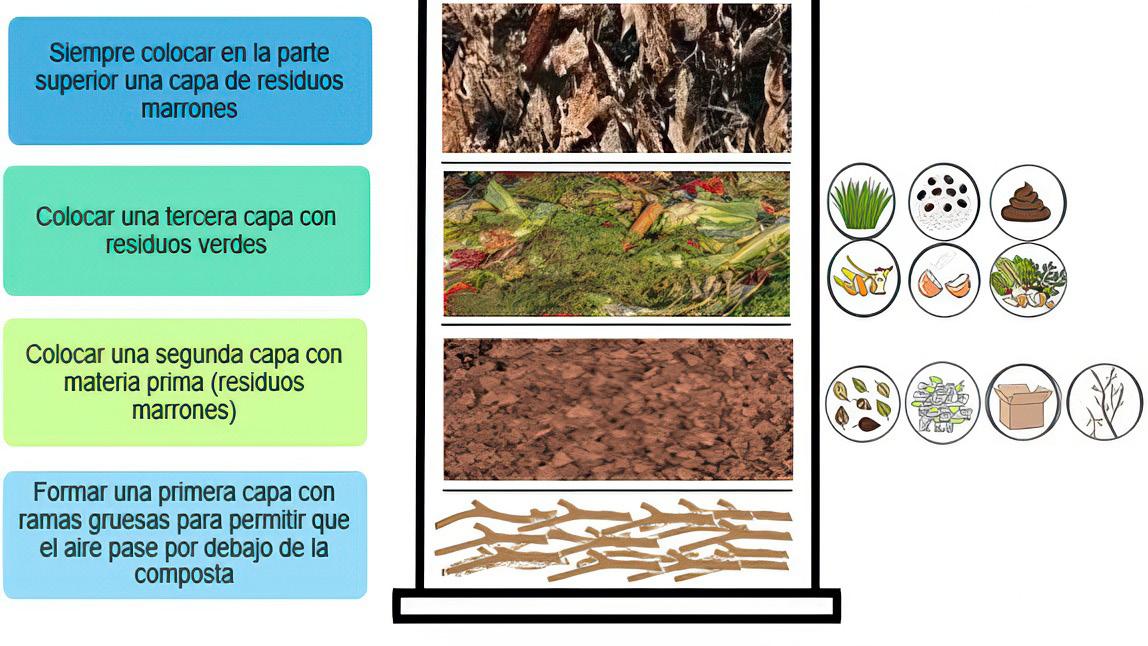
Este proceso se divide en dos etapas: Descomposición y Maduración. La primera comprende tres fases (mesófila, termófila y de enfriamiento), durante las cuales, inicia con la oxidación de los compuestos orgánicos fácilmente degradables, seguido de la estabilización o descomposición de las moléculas orgánicas complejas (Nemet et al., 2021; Xie et al., 2023). Por otra parte, la segunda se caracteriza por la reorganización de la mat eria orgánica en moléculas estables y la conversión de una parte de la materia orgánica restante en sustancias húmicas (Sánchez et al. 2017; Azim et al. 2018; Hernández-Lara et al. 2022). En la Figura 4 se observa que en cada etapa y fase existe la participación de diversos grupos microbiológicos que son los responsables de conseguir un compostaje de calidad.
Figura 3
Proceso de la elaboración del compost.
1.2. Etapas del compostaje
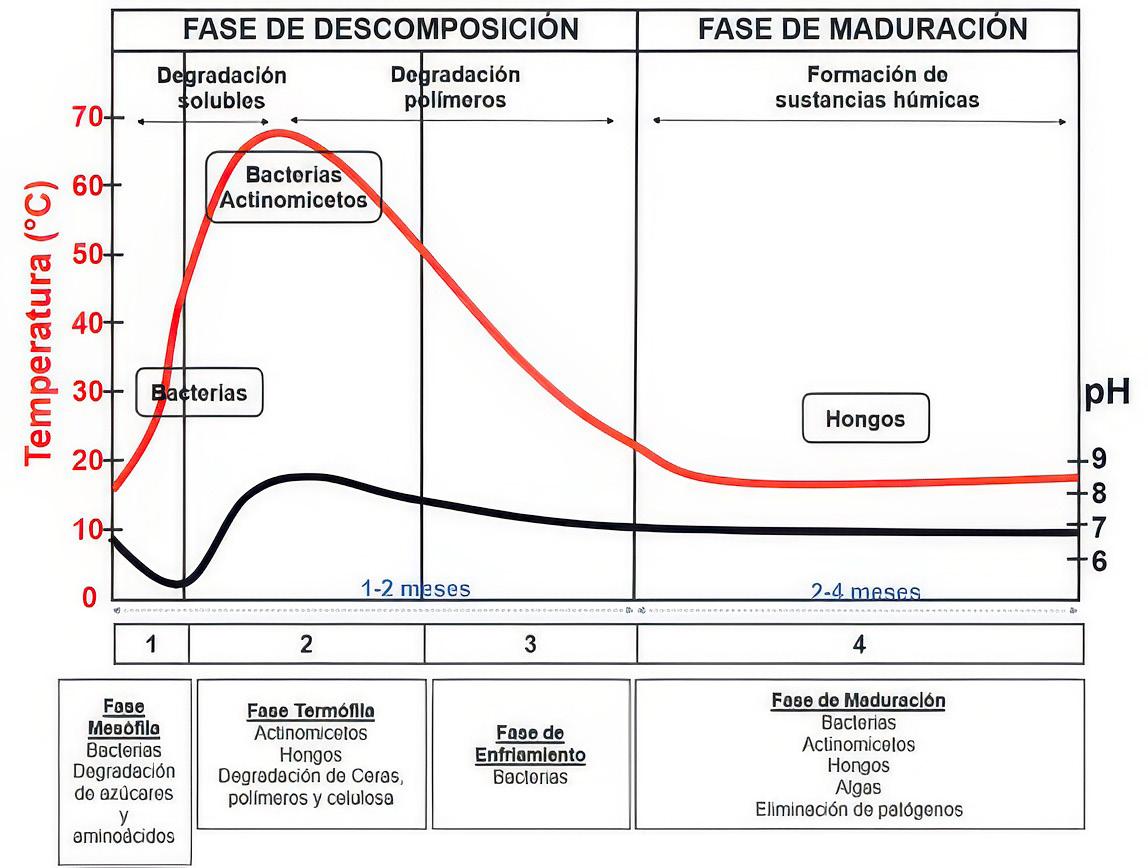
Figura 4
Sucesión microbiana, Fuente: Moreno & Moral, 2008.
1.2.1. Etapa de descomposición
Esta etapa se caracteriza por ser un proceso biológico, donde los microorganismos metabolizan el material orgánico en sus componentes minerales y se transforma parcialmente en humus (Meena et al., 2021; Toleikiene et al., 2020; Wichuk & McCartney, 2010). Se compone de tres fases: una fase mesófila, con alta proliferación de la microbiota, una fase termófila en la que se produce una elevada tasa de biodegradación y la inhibición de organismos no termotolerantes y la fase de enfriamiento (Villar et al. 2016; Nikoloudakis et al. 2018).

Fase mesófila
El proceso de descomposición inicia con el crecimiento de microorganismos mesófilos como bacterias, hongos y actinomicetos que degradan azúcares solubles y almidones, formando ácidos orgánicos que disminuyen el pH (Villar et al. 2016; Bhattacharya 2023). Además, aumenta la temperatura hasta los 45°C por acción de la actividad metabólica microbiana (FAO, 2013; Liu et al., 2023). Se ha establecido que el rango de temperatura ideal es de 20 a 45°C y el pH debe ser inferior a 5.

Fase termófila
En esta fase se produce la descomposición de proteínas, grasas, celulosa y hemicelulosa mediante la acción de poblaciones mixtas de bacterias termófilas, actinomicetos y hongos que son tolerantes a altas temperaturas (Chen et al., 2011). Esta actividad microbiana da lugar al aumento de temperatura (45-65°C) y a la transformación de N en NH3 por lo que el pH aumenta (Azim et al., 2018; Nemet et al., 2021). Asimismo, en esta etapa el O2 se debe reponer mediante aireación pasiva, forzada o volteando la pila de compost (Chen et al., 2011).
Por otra parte, en la fase termófila se lleva a cabo una desinfección del material compostado, puesto que las temperaturas superiores a 50°C destruyen microorganismos patógenos y desactivan los virus comunes en los desechos orgánicos y semillas de malezas (Rivero, 2014; Soobhany et al., 2017). Sin embargo, si la temperatura excede los 70°C, los termófilos tienden a morir por el calor excesivo, incluso, temperaturas mayores a 90°C puede ocasionar que la pila de compost se incendie (Chen et al., 2011). Es importante recalcar que la temperatura ideal va desde los 45 hasta los 65°C y el pH debe estar entre 7.5 y 8.5.

Fase de enfriamiento
A medida que se agotan las fuentes de carbono y nitrógeno, se restablecen los microorganismos mesófilos, la temperatura disminuye por debajo de los 45°C y el pH se mantiene ligeramente alcalino (Xie et al., 2023). Durante esta etapa, se produce una degradación lenta y prolongada de la lignina y otros componentes resistentes (celulosa y la hemicelulosa) por acción de actinomicetos y hongos (Fig. 4) con capacidad de formar esporas (Rivero 2014; López-González et al. 2015; Hernández-Lara et al. 2022). En esta fase la temperatura debe ser inferior a 45°C y el pH debe ser cercano a la neutralidad (pH 7).
Finalmente, como consecuencia del desarrollo de estas fases se producen condiciones aeróbicas que junto a reacciones exotérmicas producen la desintegración de la mayor parte de los componentes orgánicos que se desencadena por acción de las enzimas producidas por los microorganismos (Nikoloudakis et al., 2018; Xie et al., 2023). Por ejemplo, la celulasa da lugar a la descomposición de la celulosa, la amilasa para los almidones y la proteasa para las proteínas (FAO, 2013; Lin et al., 2022; Nemet et al., 2021). El resultado de esta etapa ayuda a la liberación de nutrientes y al funcionamiento de la red alimentaria (Bhattacharya 2023).
1.2.2.
Etapa de maduración
En esta etapa la composta atraviesa un proceso biológico y químico crucial para convertirse en un producto estable, inocuo e inodoro (Xu et al., 2019; Zeng et al., 2009). Durante esta fase, la temperatura desciende (20-30ºC) y, por ende, se agota la materia orgánica fácilmente degradable y la materia orgánica más resistente, como la lignocelulosa, sufre una degradación lenta (Figura 4) (Xu et al., 2019). Además, se produce la polimerización y condensación de compuestos carbonados para la formación de sustancias húmicas (Garcia & Herran, 2014; Meena et al., 2021).
Las sustancias húmicas (HS) son un conjunto de polímeros de materiales orgánicos con diversos pesos moleculares y con la característica de ser altamente recalcitrantes (Kelleher & Simpson 2006). Las HS son altamente reactivas debido a que en su estructura tienen una infinidad de grupos funcionales (Liang et al. 2011). Estos han sido formados por las acciones de microorganismos y enzimas.
Entre las características que poseen estas sustancias se encuentran: aumentar la porosidad del suelo, mejorar la biodisponibilidad de nutrientes, la capacidad de retención de agua y suprimir varios fitopatógenos (Ao et al., 2024; Guo et al., 2019; Omoniyi et al., 2021).
Se distinguen varias clases de HS, no obstante, los más representativos son los ácidos
húmicos (AH) que son sustancias solubles en álcalis y precipitan en ácidos, tienen alto peso molecular con más carbono aromático; los ácidos fúlvicos (AF) solubles en álcalis y también en ácidos, de bajo peso molecular que contienen más carbonos alifáticos y grupos carboxílicos y, finalmente las sustancias hidrofílicas (Hy) que son sustancias solubles en agua (Gungor & Let, 2010; Li et al., 2017; Ming et al., 2023; van Zomeren & Comans, 2007).
La etapa de maduración es clave para mejorar la calidad de los productos del compost y superar las deficiencias del compostaje tradicional (Liu et al., 2023; Xie et al., 2023). El resultado son productos ricos en metabolitos microbianos y nutrientes vegetales, que pueden promover el crecimiento y desarrollo de las plantas, y además inhibir enfermedades. Por lo tanto, esta etapa permite obtener un compost de alta calidad que no presenta problemas de fitotoxicidad para ningún cultivo (Liu et al., 2023; Wang et al., 2014).
1.3. Factores que influyen
en el proceso de compostaje
Al ser un proceso biológico, los microorganismos juegan un papel crucial en el proceso de compostaje, por lo tanto, se deben tener en cuenta los factores que afectan el crecimiento y la reproducción de estos microorganismos (Meena et al. 2021). Generalmente se clasifican como parámetros internos y externos; entre los primeros se incluyen la relación carbono:nitrógeno (C:N), el contenido de humedad, el pH, el tamaño de las partículas del material y la temperatura (Azim et al. 2018; Bhattacharya 2023). Por otra parte, en los segundos se identifican la temperatura, la ventilación, el suministro de oxígeno, y dotación de energía (Tabla 1).
Tabla 1
Factores que influyen el compostaje y valores óptimos.
Fuente: Nemet et al., 2021;Ozores-Hampton et al., 2022; Xie et al., 2023
1.3.1. Parámetros internos

Relación C:N
La relación C:N es un parámetro que expresa las unidades de carbono (C) por unidades de nitrógeno (N) que contiene un sustrato (Guo et al. 2012). El carbono sirve como fuente de energía, mientras que el nitrógeno es esencial para la síntesis de proteínas, moléculas elementales y ácidos nucleicos (Rivero 2014). Su importancia radica sobre el impacto en la actividad microbiana y la calidad del producto final. Durante la fermentación aeróbica,
Los microorganismos consumen de 15 a 30 veces más carbono que nitrógeno (Tripetchkul et al. 2012; Khater 2015). Por tal motivo, la relación de C y N en el compost suele oscilar entre 25:1 y 35:1, según los materiales de origen y el tiempo de compostaje (Tripetchkul et al. 2012; Azim et al. 2014; Ozores-Hampton et al. 2022).
Una relación C:N superior a la recomendada (30:1) (Tabla 1) ralentiza el compostaje (Guo et al. 2012), especialmente para materiales con carbono recalcitrante y puede provocar una deficiencia de nutrientes en la comunidad microbiana debido a la acumulación excesiva de sustratos (Chroni et al., 2009; Voběrková et al., 2017; Zhang et al., 2014). Por otra parte, pueden provocar una pérdida lenta de carbono y la necesidad de correcciones para facilitar el compostaje (Azim et al. 2014). Es posible que sean necesarios ajustes, como la adición de sustancias ricas en nitrógeno para promover el compostaje (Trello 2022).
Por el contrario, proporciones bajas de C:N pueden dar lugar a un mayor contenido de nitrógeno por carbono degradable, lo que potencialmente conduce a la pérdida de nitrógeno en forma de amoníaco a través de la volatilización o nitratos por lixiviación (Rastogi et al. 2020). La relación inicial de C:N sirve como un indicador crucial para la calidad del compost, y sus desviaciones conducen a una posible fitotoxicidad o bloqueo biológico del nitrógeno (Tripetchkul et al. 2012). Además, este proceso puede provocar la liberación de compuestos indeseables, como olores y sales, que son desfavorables para el desarrollo de las plantas (Azim et al. 2018).

pH
El pH es una medida de la acidez o alcalinidad de una sustancia, que se expresa como la concentración de iones hidrógeno [H+]. En la escala de pH los valores menores a 7 son considerados ácidos y valores superiores a 7 son alcalinos o bases (Oshins & Miche, 2022). Este parámetro tiene influencia directa en el compostaje debido a su acción en la degradación de residuos y la actividad microbiana (Meena et al., 2021; Rivero, 2014; Wang et al., 2019). El rango de pH recomendado para el compostaje generalmente se encuentra entre 6.5 y 8.0. Sin embargo, existen rangos óptimos para el desarrollo de diferentes microorganismos. Para las bacterias está entre 6.0 y 7.5; mientras que los hongos está entre 5.5 y 8.0 (Tabla 2) (Azim et al., 2018; Nemet et al., 2021; Xie et al., 2023).
Tabla 2
Rango de pH para el crecimiento óptimo de los microorganismos en el compostaje
Esta variación de pH se debe a la actividad de descomposición en las diferentes fases del proceso de compostaje. En la fase mesófila, el pH es ácido porque se producen ácidos a partir de los residuos; en la fase termófila el pH es alcalino por la formación de amoniaco y en la fase de maduración, el pH se considera neutro, indicando la formación de humus (Sánchez et al. 2017; Hernández-Lara et al. 2022).
No obstante, si el pH presenta una valor más bajo de 7.0, el proceso de compostaje no
se considerada adecuado (Graziani et al., 2020; Nemet et al., 2021). Una disminución del pH durante el compostaje puede estar relacionada con la volatilización del NH3 y la nitrificación microbiana, lo que resulta en una mayor producción de CO2 (Figura 5) (He et al., 2023; Parihar & Choudhary, 2022). Por otro lado, un pH superior a 9.0, provoca la alcalinización de la masa de compost, lo que dificulta la supervivencia de microorganismos (Adams, 2008; Nemet et al., 2021).
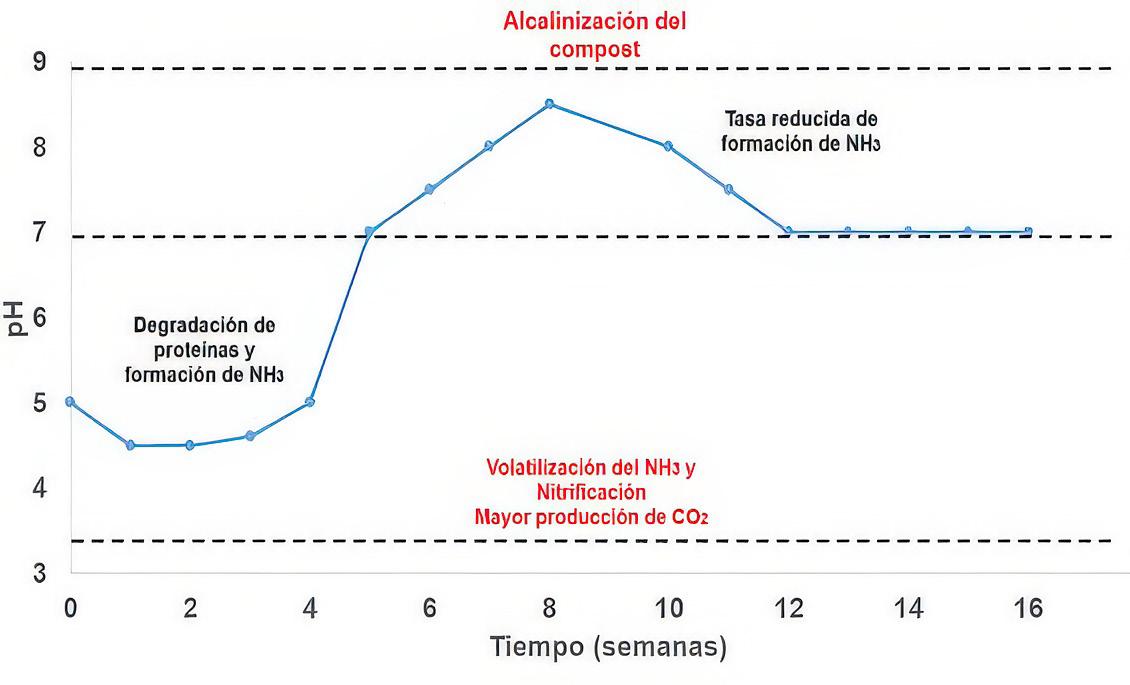
Figura 5
Variación del pH durante el proceso de compostaje.

Humedad
La variación en el contenido de humedad durante el compostaje está influenciada por factores como la temperatura, la ventilación, y la actividad microbiana (Khater 2015; Garrett 2021). Mantener niveles óptimos de humedad es crucial, ya que tanto los valores bajos como los altos pueden alterar la actividad microbiana, la tasa de absorción de oxígeno, la temperatura y los niveles de porosidad (Rivero 2014). El rango de humedad se encuentra alrededor del 50% al 60% (v/p), adaptado a la composición de la materia prima, con un espacio poroso ocupado por aire entre 30 y 36% (Makan et al. 2013).
Existe una relación inversa entre el contenido de humedad y la temperatura, ya que la temperatura aumenta a medida que disminuye el contenido de humedad. Las temperaturas elevadas dan como resultado una mayor evaporación, lo que lleva a disminuir el contenido de humedad (<40%), provocando que las actividades de la vida microbiana sean limitadas y a una tasa reducida de descomposición de la MO (Figura 6) (Lin et al., 2022; Wichuk & McCartney, 2010). En consecuencia, es necesario volver a humedecer las pilas de tratamiento para mantener condiciones de humedad adecuadas y garantizar el funcionamiento adecuado de la microbiota residual (Goldan et al. 2023).
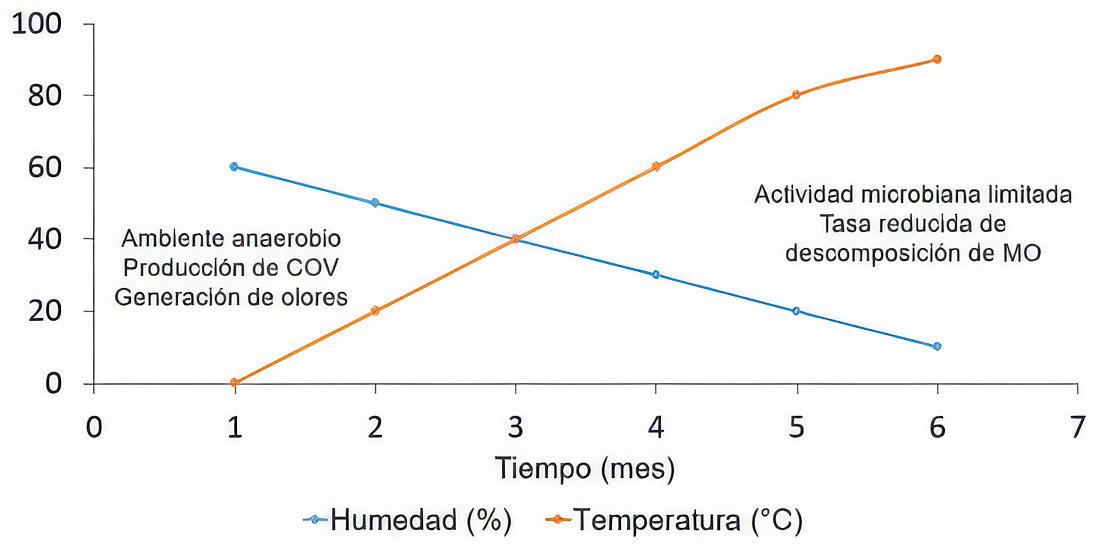
Figura 6 Relación entre el contenido de humedad y la temperatura en el compostaje.
Al contrario, un contenido de humedad elevado (>70%) causa que la pila de compostaje sea relativamente densa, afectando la circulación del aire volviendo el ambiente anaerobio. Como resultado ocurre una producción de Compuestos Orgánicos Volátiles (COV) y la generación de olores, lo que podría detener el procedimiento de compostaje (Figura 6) (Ozores et al., 2022; Wichuk & McCartney, 2010).

Tamaño de la partícula
El tamaño de las partículas en una masa de compost desempeña un papel crucial para garantizar niveles adecuados de porosidad, facilitar una aireación adecuada y regular el intercambio gaseoso (Vigneswaran et al. 2016). Triturar y picar los residuos en trozos más pequeños contribuye a lograr un tamaño de partícula adecuado, proporcionando más superficie para la actividad microbiana durante el compostaje y entrega como resultado una degradación más rápida (Rivero 2014). El rango ideal del tamaño de las partículas se encuentra entre 1-5 cm, lo que proporciona condiciones físicas y químicas adecuadas para la bioactividad durante el proceso de compostaje (Michel et al. 2022; Xie et al. 2023).
La elección del tamaño de partícula es una consideración crítica para equilibrar los beneficios de una mayor actividad microbiana y una degradación más rápida frente al riesgo de compactación y condiciones anaeróbicas (Michel et al. 2022). Partículas de tamaños excesivamente pequeños pueden provocar una compactación inicial de la materia prima (Figura 7) (Guo et al., 2019; Mendoza & Espinoza, 2017; Oshins & Miche, 2022). Mientras que las partículas de gran tamaño disminuyen el área de contacto para los microorganismos. Esto, sumado a la formación de bolsas de aire que aíslan térmicamente la matriz, disminuye la temperatura y ralentiza el proceso de descomposición (Garrett 2021).
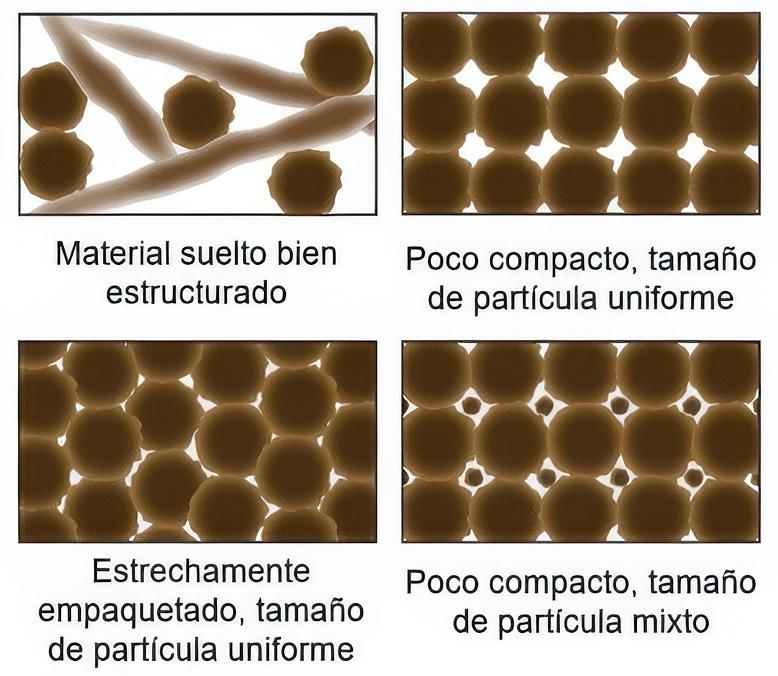
Figura 7. Efecto del tamaño y la forma de las partículas en la porosidad. Fuente: Michel et al., 2022.

Carbono orgánico total (TOC)
El Carbono Orgánico Total (TOC) es un parámetro que indica la cantidad de carbono presente en los residuos orgánicos obtenidos desde el compostaje. Generalmente el TOC constituye el 90% del carbono total, este varía dependiendo de la materia prima utilizada, donde los residuos agrícolas contienen entre 20-30%, los residuos domésticos entre 2550% y los biosólidos entre 30-40% (Naeem et al. 2022; Ming et al. 2023). Se ha determinado que el valor más bajo de TOC (16.6%) corresponde al estiércol de ganado y el valor más alto (23.9%) se obtuvo desde el compost de residuos agrícolas como los residuos de plantas de caña de azúcar (Yousif Abdellah et al. 2022; Aydın Temel 2023; Ming et al. 2023).
Sin embargo, el contenido de TOC disminuye durante el compostaje a causa de la degradación de los sustratos por acción de los microorganismos, lo que lleva a su mineralización como CO2. Cuando el proceso de compostaje tiene una mala aireación, se libera metano (CH4) en la fase termófila, representando menos del 2% del TOC inicial (Sánchez et al. 2017; Indoria et al. 2018; Hernández-Lara et al. 2022). En el caso de una oxidación incompleta del Carbono, causa la emisión de ácidos grasos volátiles, esto ocurre en la fase mesófila y representan menos del 10% del TOC y contribuyen a disminuir el pH (Khater 2015; Indoria et al. 2018; Ming et al. 2023).
1.3.2. Parámetros externos

Aireación
Es el proceso de suministro y circulación controlada de oxígeno, con el objetivo de mantener condiciones aeróbicas óptimas. Es un aspecto crítico del compostaje que regula procesos biológicos, temperatura, humedad y la eliminación del exceso de CO2 (Mendoza & Espinoza, 2017). Para un compostaje deseable es necesario mantener una concentración de oxígeno entre 15 y 20%, así se mantiene la dinámica microbiana y el control de temperatura (Malinowski 2021). Una aireación suficiente, particularmente en las primeras etapas, reduce el tiempo del proceso, promueve la transformación completa del carbono en dióxido de carbono, y minimiza las emisiones de metano (Huzairi et al. 2012; Williams et al. 2019; Garrett 2021).
La aireación excesiva puede provocar un compostaje deficiente, porque afecta la temperatura y baja el nivel de humedad. Esto último debido al proceso de evaporación, el cual reduce las tasas de descomposición de los residuos (Sánchez et al. 2017; Meena et al. 2021). Una tasa de aireación más alta durante el compostaje de residuos puede moderar la relación C:N, reducir la generación de NH3 y minimizar la liberación de olores, sin embargo, puede afectar negativamente la madurez del compost (Makan et al. 2013; Meena et al. 2021; Ozores-Hampton et al. 2022).
Al contrario, bajas tasas de aireación dan como resultado una degradación orgánica más lenta, una producción reducida de NH3 y una disminución significativa de la temperatura, la humedad y la pérdida de calor, lo que afecta a las poblaciones microbianas (Anusha et al. 2021; Lin et al. 2022). Para evitar tanto la aireación excesiva como las bajas tasas, el desarrollo de técnicas adicionales para garantizar una adecuada aireación es crucial. Por ejemplo, la mezcla diaria con volteo mecánico o el uso de aireación forzada y aireación pasiva (Figura 8), han mostrado resultados positivos en la mejora de la calidad del compost para diversos materiales de desecho (Makan et al. 2013).

Figura 8
Sistemas de aireación en el proceso de compostaje. La aireación pasiva utiliza tubos perforados para permitir el flujo natural de aire a través del compost (A). La aireación forzada emplea ventiladores para inyectar o extraer aire, acelerando la descomposición (B). El volteo mecánico usa maquinaria para mezclar el compost, mejorando la oxigenación y uniformidad (C).

Temperatura
La temperatura es un factor crucial que influye en el crecimiento y la actividad metabólica de las comunidades microbianas dentro de las masas de compost (Chen et al. 2011a). Además, es un indicador de la tasa de degradación de la materia prima, monitoreando en si todo el proceso de fermentación (Tripetchkul et al. 2012; Azim et al. 2018). La temperatura varía según la fase de compostaje, tomando en cada una un rango óptimo (Figura 9). La fase mesófila, donde inicia la descomposición, alcanza temperaturas de hasta 45°C. En la fase termófila, puede llegar hasta los 65°C. y en la fase de enfriamiento, descender gradualmente hasta los 45°C. Finalmente, en la fase de maduración, el compost se estabiliza a temperatura ambiente, entre 20 y 30°C, completando así su transformación.
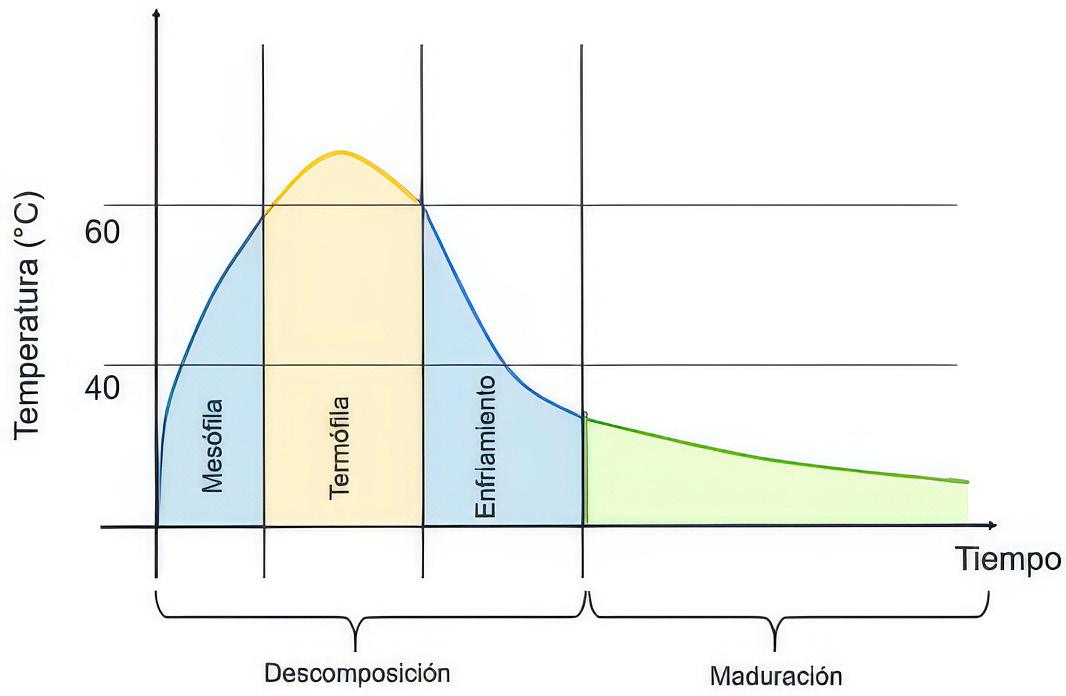
Figura 9
Cambio de temperatura en el proceso de compostaje. Fuente: Nikoloudakis et al., (2018)
Una temperatura alta durante la fase termófila (45-65°C) se asocia con una mayor degradación microbiana de polisacáridos, proteínas y grasas (Guo et al., 2019). Además, cuanto antes se produzca esta fase, antes se degradarán y estabilizarán las materias orgánicas (Rivero, 2014; Sun et al., 2022). Es por ello, necesario garantizar que el compost maduro no contenga patógenos vegetales ni humanos. Es así que, la fase termófila es el factor determinante para la destrucción del patógeno y la eficiencia está relacionada con el tiempo de exposición (Tabla 3) (Adegoke et al. 2016).
Tabla 3
Temperatura y tiempos necesaria para la eliminación de patógenos.
Fuente: Adegoke et al., 2016; Jones y Martin, 2003.Microbiología del compostaje
La población microbiana, tanto nativa como introducida, desempeña un papel fundamental en la regulación y el funcionamiento del ecosistema edáfico durante el compostaje (Bolan et al. 2022; Aguilar-Paredes et al. 2023; Bhattacharya 2023). Sus actividades contribuyen la degradación controlada de la materia orgánica, la disponibilidad de nutrientes, regulación del ciclo biogeoquímico de elementos esenciales, control de patógenos, degradación de contaminantes, e incluso la mitigación de las emisiones de gases de efecto invernadero (GEI). Para ello, el desarrollo adecuado de la microbiota de la composta dependen de la biodisponibilidad de nutrientes minerales (N, P, K, Mg, S, Ca, Zn, Cu, Co, Fe) (Sumiyati et al. 2022; Agrawal et al. 2023).
Los microorganismos pueden variar entre hongos, actinomicetos, bacterias y en menor proporción, levaduras y protozoos, siendo esta población la que cambia continuamente durante el proceso (Rivero, 2014; Sun et al., 2022). Dentro de los géneros de microorganismos predominantes se encuentran: Trichoderma, Bacillus, Nitrosomonas, Nitrobacter, Azotobacter, Azospirilum, Bacteromycetes, Pseudomonas y Aspergillus, quienes favorecen un proceso activo de degradación acelerada de los materiales orgánicos y contribuyen a la producción de un compost de alta calidad (García et al., 2023; Nemet et al., 2021) (Tabla 6). El diverso conjunto de microorganismos involucrados puede influir positiva o negativa en el proceso de compostaje.
La producción enzimática específica de los microorganismos individuales desempeña un papel importante en la descomposición de la MO (Tabla 4). Las cualidades de producción de enzimas permiten a los microorganismos degradar compuestos orgánicos complejos
y luego absorber los compuestos más simples en sus células (Villar et al. 2016; Azim et al. 2018). Además, las enzimas presentes en cada grupo catalizan reacciones en las que se oxidan azúcares, almidones, proteínas y otros compuestos orgánicos (HernándezLara et al. 2022; Lin et al. 2022). Entre los principales grupos de microrganismos con esta propiedad se encuentran Trichoderma, Bacillus, Nitrosomonas, Nitrobacter, Azotobacter, Azospirilum, Bacteromycetes, Pseudomonas y Aspergillus (Bhattacharya 2023; García et al. 2023; Xie et al. 2023).
De este modo, cada comunidad microbiana genera diversas enzimas termoestables (proteasas, celulasas, hemicelulasas y modificadoras de lignina), considerándose factores clave que promueven y aceleran los procesos bioquímicos implicados en la descomposición progresiva de la materia orgánica (Cotta et al. 2023; Finore et al. 2023). Además, la actividad enzimática se puede utilizar para evaluar el nivel de actividad microbiana en una muestra de compost.
Tabla 4
Enzimas producidas por los microorganismos presentes en el compostaje.
1.3.3. Microorganismos benéficos
El conjunto de microorganismos involucrados en el compostaje pueden considerarse benéficos cuando son capaces de transformar la materia orgánica en presencia de oxígeno, degradar compuestos contaminantes y presentar actividad antagónica contra patógenos
Fuente: (Li et al. 2018; Rios et al. 2018; Raza et al. 2021; Finore et al. 2023)
(Chroni et al. 2009; Bhattacharya 2023). Entre los microorganismos benéficos durante el proceso de compostaje destacan las bacterias, hongos y actinomicetos (Figura 10).

Figura 10
Principales géneros de microorganismos beneficiosos en el proceso de compostaje. Fuente: Bhattacharya, 2023.
Las bacterias son los microorganismos más abundantes en el proceso de compostaje, se caracterizan por tener una gran versatilidad metabólica y participan en las diferentes fases dependiendo de sus requerimientos de temperatura (psicrófilas, mesófilas y termófilas) (Hernández-Lara vet al. 2022). En la fase mesófila, se han identificado especies de los géneros Bacillus, Pseudomonas, Arthrobacter y Alicaligenes donde se encargan de la descomposición de azúcares y proteínas simples (Jurado et al., 2014). A medida que la temperatura aumenta durante el proceso, colonizan las termófilas como Bacillus subtilis, Geobacillus stearothermophilus y Bacillus licheniformis que proliferan y degradan materiales más resistentes, como la celulosa, lignina y grasas (He et al., 2023; Lu et al., 2021; Xu et al., 2022). Su actividad en la fase de descomposición, permite la eliminación de patógenos (Wichuk & McCartney, 2010).
Los hongos tienen la capacidad de utilizar diferentes sustratos de carbono como fuentes de alimento y sobrevivir en condiciones de baja concentración de nitrógeno. Tienen alta producción de enzimas extracelulares que permiten la degradación de sustratos recalcitrantes (Hernández-Lara et al. 2022). La mayoría de los hongos son mesófilos con una temperatura óptima de trabajo que varía entre 25 y 30°C y aunque pueden crecer en amplios rangos de pH, prefieren un medio más ácido (Aguilar-Paredes et al. 2023). Los hongos del filo Ascomycota son los más dominantes, seguidos por los Basidiomycota, y el subfilo Mucoromycotina (Huzairi et al., 2012; Mori et al., 2016). Los géneros predominantes son: Aspergillus, Penicillium, Fusarium, Trichoderma y Chaetomonium (Garcia y Herran, 2014).
Los actinomicetos se caracterizan por su estructura con hifas ramificadas, los cuales secretan enzimas como amilasas, lipasas y celulasas, que facilitan la degradación de la lignina. Además, son fijadores de nitrógeno, capaces de romper los enlaces de los átomos de nitrógeno orgánico y producir antibióticos naturales que pueden suprimir patógenos en el compost (Javed et al., 2021; Wang et al., 2022). Entre los más destacados se encuentran Streptomyces, Micromonospora, Thermoactinomyces, Norcardia, Microbispora, Micromonospora, Actinomyces, Actinoplanes y Streptosporangium (Aguilar-Paredes et al., 2023; Cuesta et al., 2012; Nemet et al., 2021). Estos microorganismos, en conjunto, mejoran el proceso de compostaje al promover la transformación de la materia orgánica,
degradar los contaminantes y ejercer efectos antagónicos contra los patógenos dañinos.
1.3.4.
Microorganismos perjudiciales
En el proceso de compostaje, los microorganismos patógenos pueden estar presentes en los residuos orgánicos iniciales o propagados mediante el ineficiente proceso. Esto representa un riesgo para la salud humana, animal y vegetal si no son eliminados adecuadamente. Entre los patógenos perjudiciales se encuentran bacterias, hongos, virus y parásitos que afectan negativamente causando enfermedades. La supervivencia de patógenos en el compostaje se debe a temperaturas desiguales, mezcla inadecuada, contaminación cruzada, lixiviados y adición de material fresco (Rivero 2014; Soobhany et al. 2017; De Corato 2020). Estos factores impiden la eliminación efectiva de patógenos, resaltando la importancia de un manejo adecuado del compostaje.

Patógenos de humanos y animales
Algunos patógenos como Salmonella, Escherichia coli, Listeria monocytogenes (Figura 11) y Clostridium difficile pueden persistir durante el compostaje y, si están presentes en cantidades suficientes, representan un riesgo para los seres humanos y los animales (Sunar et al. 2014; De Corato 2020). Esto es especialmente preocupante en el caso del compost derivado de materiales como estiércol, desechos de alimentos o biosólidos (Storino et al., 2016). Uno de los patógenos más peligrosos es Escherichia coli, porque puede persistir en el compost y representar un riesgo para la salud humana.
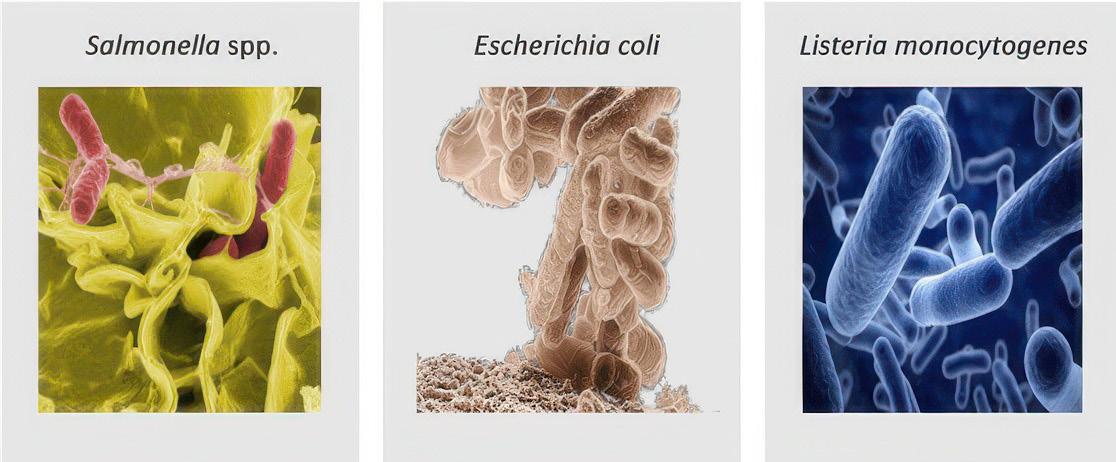
Figura 11
Microorganismos patógenos presentes en el compostaje. Fuente: Gestema, 2021.
Bacterias como E. coli, presente en estiércol bovino, sobrevive a temperaturas superiores a 50°C por fallas en la rotación del compost y periodos cortos de compostaje (Soobhany 2018). Algunas cepas mutantes de Salmonella spp. pueden encontrarse en estiércol y restos de alimentos, estas soportan temperaturas entre 42 y 54 °C y su proliferación depende de la humedad, nutrientes o microbiota viable (Aguilar-Paredes et al., 2023; Nakasaki & Hirai, 2017). La Unión Europea (UE), en su reglamento exige la ausencia de Salmonella spp. en 25 gramos de abono, menos de 103 unidades formadoras de colonias de E. coli por gramo de material (NMPg-1) y la ausencia de virus entéricos, debido al riesgo de enfermedades en humanos (Regulation EU 2019).

Patógenos vegetales
Los fitopatógenos constituyen un riesgo importante para la sanidad de los cultivos, porque ocasionan enfermedades como, marchitamiento pre y post-emergente, marchitamiento vascular y pudriciones de raíz, cuello y corona (Wang et al., 2022). Estas patologías se atribuyen a la acción de hongos (Rhizoctonia solani, Sclerotium spp., Fusarium sp. y Verticillium sp.), oomicetos (Pythium sp. y Phytophthora spp.) y bacterias (Ralstonia solanacearum, Pectobacterium carotovorum) que pueden persistir en los residuos vegetales mal compostados (Suárez-Estrella et al. 2013; Lutz et al. 2020). Los oomicetos Pythium spp. y Phytophthora spp. provocan enfermedades de pudrición radicular y vascular (Figura 12). Pythium spp. afecta principalmente a plántulas en su fase temprana, mientras que Phytophthora spp. es conocido por causar la devastadora “tizón tardío” en cultivos como papa y tomate (Neher et al. 2021).
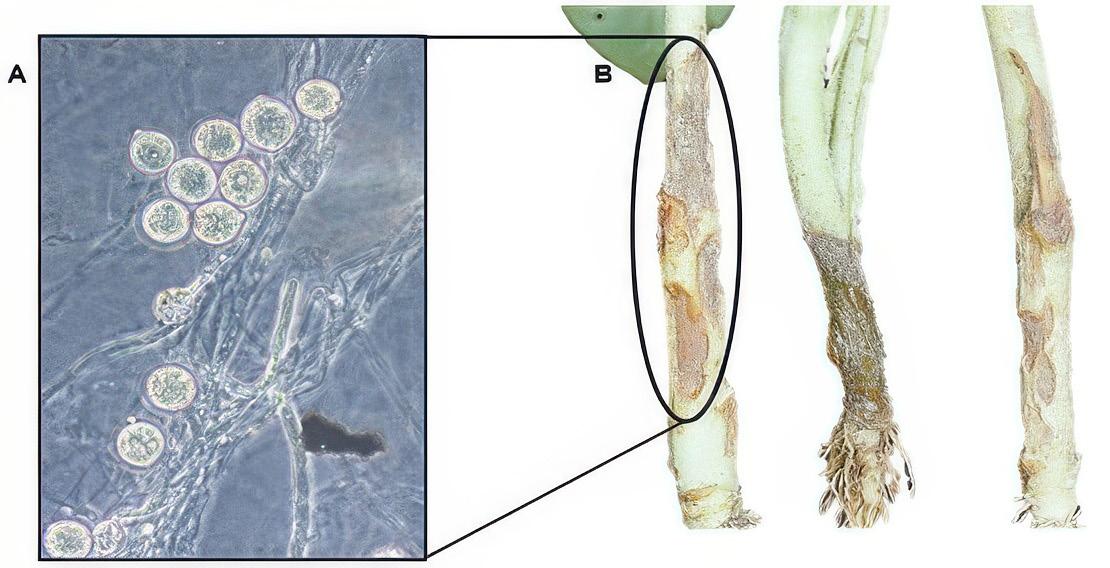
Figura 12
Pythium, patógeno del suelo generalista. Vista microscópica de Pythium spp (A). Afecta a todo tipo de plantas y provoca marchitamiento fúngico, podredumbres y crecimiento reducido (B). Fuente: Biobest, 2020; Clemson University –USDA, 2018.
Los fitopatógenos pueden afectar la salud de los cultivos al causar enfermedades que varían desde marchitamientos hasta pudriciones. El hongo Rhizoctonia solani es un patógeno del suelo que causa el “damping-off”, es decir, ataca varios cultivos en las fases iniciales (Lamichhane et al. 2017). Microrganismos como el Fusarium spp., y el Fusarium oxysporum, causan la “marchitez por fusarium”, y el Verticillium spp. es responsable del marchitamiento vascular en gramíneas y cereales (Al-Askar et al. 2015; De Corato et al. 2016). Bacterias como Ralstonia solanacearum, Pectobacterium carotovorum, y Pseudomonas syringae son responsables de enfermedades vasculares y pudriciones en diversos cultivos (Neher et al. 2021).

Toxinas provenientes de microorganismos
El compost puede tener trazas de moléculas tóxicas para las plantas y alergénicas para los seres humanos, estas son producto de metabolitos secundarios generados por los patógenos y otros microorganismos que habitan las pilas de compostaje (Domingo & Nadal 2009). Las bacterias son capaces de generar endotoxinas, mientras que los hongos producen micotoxinas, siendo las más relevantes las aflatoxinas (Domingo & Nadal 2009). Para reducir y mitigar las toxinas se deben seguir prácticas adecuadas de compostaje. Esto incluye mantener el equilibrio adecuado de carbono y nitrógeno, garantizar niveles adecuados de aireación y humedad y alcanzar temperaturas que puedan matar eficazmente los patógenos (De Corato 2020; Ozores-Hampton et al. 2022).
1.3.5. Eliminación de patógenos
Si bien la mayoría de los patógenos se inactivan con el calor generado durante el compostaje, es probable que algunos microorganismos sobrevivan o vuelvan a crecer (Adegoke et al., 2016; Lutz et al., 2020; Wang et al., 2019). Por ello, la actividad de los microorganismos benéficos puede inactivar patógenos al producir compuestos antimicrobianos. Los ácidos volátiles son eficaces contra bacterias y virus al atacar su envoltura y su genoma (AbdelRahman et al. 2016; Storino et al. 2016; Hernández-Lara et al. 2022). Compuestos como el amoníaco (NH3) afectan a la mayoría de los patógenos, incluidos los huevos de Ascaris, y los virus ssRNA (Lepesteur 2022). Entre los agentes de biocontrol se encuentran varios tipos de microorganismos benéficos (Tabla 5).
Tabla 5
Microorganismos benéficos que suprimen los patógenos en el proceso de compostaje.
1.4. Compostaje y tipos de residuos
El compost es un producto versátil derivado de una amplia gama de materias primas que suelen ser de origen vegetal o animal (Villar et al. 2016). La mayor parte está ocupada por sustratos vegetales, y los componentes animales y microbianos están ocupados por
fracciones más pequeñas en la mezcla de compost (Díaz et al. 2021). El tipo de compostaje está definido por los tipos de residuos, incluyendo materiales vegetales de campos agrícolas, desechos animales (estiércol), desechos sólidos municipales, desechos de jardín (recortes de jardines y parques), desechos de alimentos domésticos y comerciales, y biosólidos provenientes del procesamiento de aguas residuales industriales (Chatterjee et al. 2013; Xiao et al. 2017).
1.4.1. Residuos agrícolas
Son desechos orgánicos procedentes de una cosecha o por una labor agrícola. Están integrados por varios componentes como tallos, fibras, cutículas, cáscaras, bagazos, rastrojos, restos de podas y frutas (Figura 13). Suelen contener altos niveles de lignocelulosa, incluida la lignina, la celulosa y la hemicelulosa. Dado que estos componentes son bastante recalcitrantes, su degradación suele ser el principal factor que limita la eficiencia del compostaje (Ao et al., 2024; Wang et al., 2019).
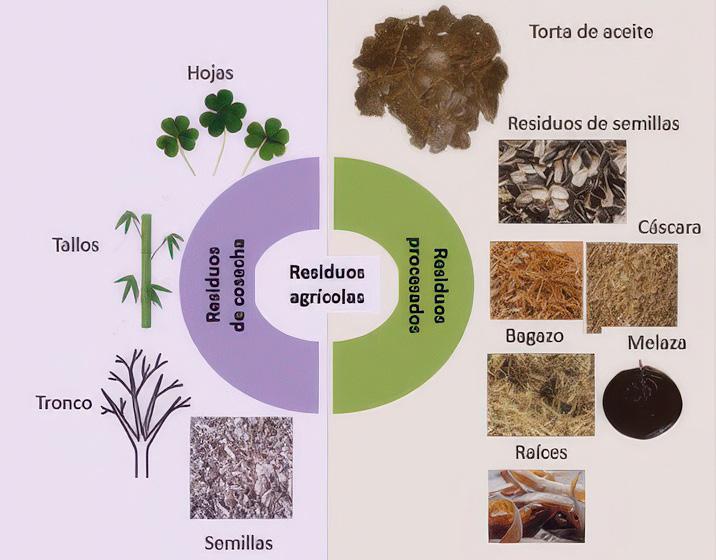
Figura 13
Diferentes tipos de residuos agrícolas utilizados para compostar. Fuente: Rai et al., 2021.
Los residuos podrían ser clasificados en dos categorías. La primera se define como desechos agrícolas verdes, estos son caracterizados por contener cantidades apreciables de N, P, micronutrientes y tiene relaciones C:N bajas (Tabla 6) (Wichuk & McCartney, 2010). La segunda categoría son los residuos marrones entre ellas materias primas como el heno y las hojas secas de las plantas. Estos tienen altas relaciones C:N (Agrawal et al., 2023; Rai et al., 2021; Rivero, 2014). Generalmente, el compost elaborado a partir de residuos agrícolas suele contener N: 26.8 g/kg, P: 0.36 g/kg, y K: 0.42 g/kg con un 90% de materia orgánica, aunque esto varía según el tipo de residuo vegetal (Tabla 6) (Garrett 2021; Xie et al. 2023).
Tabla 6
Contenido nutricional de residuos agrícolas
Fuente: Howeler, 2017; Indoria et al., 2018.
Los residuos agrícolas verdes permiten aumentar la porosidad del suelo y a la vez suministran energía para la actividad microbiana (Garrett, 2021; Xie et al., 2023). Son considerados materias primas limpias con una adecuada descomposición y con poco riesgo de olor. Sin embargo, es importante que los residuos agrícolas se conviertan en abono a temperaturas termófilas. La mayoría de los subproductos agrícolas contienen patógenos vegetales, semillas de malezas y, en algunos casos, residuos de pesticidas (De Corato et al., 2016; Rynk & Schwarz, 2022).
1.4.2. Residuos sólidos domésticos
Son todos aquellos desechos sólidos generados por las actividades domésticas como la cocina y la jardinería, representan alrededor del 30% de todos los residuos orgánicos (Machhar et al. 2022). Entre los residuos ricos en nitrógeno (verdes) se encuentras los restos de frutas y verduras, recortes de césped, bolsas de té, cáscaras de huevo (trituradas) y residuos ricos en carbono (marrones) tales como hojas secas, papel triturado, astillas y cartón triturado (Tabla 7) (Storino et al. 2016; Indoria et al. 2018). El componente alimentario de este tipo de residuo presenta, de forma general, un contenido de humedad de 60 a 80%, donde el compost a partir del mismo, contiene 88% de materia orgánica, 9.6 g/ kg de N total, 0.11 g/kg de P y 0.76 g/kg de K y se descompone rápidamente (Parihar & Choudhary, 2022; Rynk & Schwarz, 2022).
Tabla 7
Contenido nutricional de residuos domésticos.
Fuente: Indoria et al., 2018
1.4.3. Residuos sólidos municipales (RSU)
Son desechos sólidos generados en las actividades de los comercios, industrias, instituciones y eventos (Rastogi et al. 2020). El compostaje de este tipo de residuos contribuye a la protección de la degradación ambiental, el ahorro de área de vertedero y el costo de la incineración. El uso de compost de RSU es limitado ya que generalmente es pobre en nutrientes esenciales para las plantas y los cultivos no responden a su adición exclusiva (Tabla 8) (Sultana et al. 2021). Los residuos provenientes de la actividad industrial tienen concentraciones de metales pesados en los compost. Debido a que, generalmente son producidos a partir de desechos mixtos y flujos de desechos industriales (Barrena et al. 2014; Villar et al. 2016).
Dentro de este tipo de residuos se encuentran los lodos de depuradora (biosólidos) que son la acumulación de biomasa microbiana y otros sólidos orgánicos generados en las plantas de tratamiento de aguas residuales y contienen una gran proporción de MO y son ricos en nitrógeno (2-7%) (Tabla 8), y presentan un contenido de humedad de 70% a 85% (Li et al., 2017; Rynk & Schwarz, 2022). El compostaje de biosólidos requiere de dos a cuatro volúmenes de enmienda seca por volumen de biosólidos para utilizarse potencialmente como modificadores del suelo y fertilizantes (Garbowski et al. 2023). Los RSU pueden presentar efectos tóxicos en los organismos y una potencial de acumulación en la cadena alimentaria (Barrena et al. 2014; Villar et al. 2016). La biodisponibilidad de los metales pesados puede cambiar con el tipo y madurez del compost (Barrena et al., 2014; El Fels et al., 2014).
Tabla 8
Contenido nutricional de residuos sólidos municipales.
Fuente: Indoria et al., 2018; Markos et al., 2021; Sultana et al., 2021
1.5. Sistemas de compostaje
Hay varias alternativas disponibles, como compostaje en pilas estáticas aireadas, compostaje en hileras y compostaje en contenedores. Para seleccionar la mejor opción se debe optar por aquella que mejor se adapte a las características del espacio, los recursos, los tipos de sustratos y las necesidades particulares (Tabla 9) (Ozores-Hampton et al. 2022).
Tabla 9
Uso de sistemas de compostaje de distintos tipos de residuos orgánicos.
Residuo orgánico
Estiércol de ganado/cerdo
Sólidos digeridos de planta de biogás
Residuos de plantas de tomate
Residuos agrícolas
Lodos de depuradora secos
Residuos de cocina y jardín
Residuos de alimentos y verduras
Fuente: Lim et al., 2016.
1.5.1. Compostaje en contenedores
Sistema de compostaje
Pila/Contenedor
Contenedor cilíndrico
Pila
Pila estática
Hilera
Contenedor
Hilera
Son recipientes cerrados que se caracterizan por retener el calor y optimizar las condiciones de compostaje. Dentro del contenedor se pueden tratar grandes cantidades de residuos de todo tipo como desechos de comida, recortes de jardín, estiércol animal y sólidos municipales, ocupando un espacio reducido (Figura 14) (FAO, 2013; Garcia & Herran, 2014). Este tipo de sistema permite tener un control sobre parámetros como, la temperatura dentro de un rango óptimo entre 50-65°C, la circulación de aire entre 15-20% y la humedad entre 50-60%, favoreciendo la descomposición, la reducción de olores y el riesgo de plagas (FAO, 2013; Garcia y Herran, 2014; Singh et al., 2016).
Se puede utilizar contenedores de plástico, de madera y reactores aeróbicos. Los contenedores de plástico tienen una altura aproximada de 1 m y 60 cm de diámetro, con capacidad de 250 L, utilizados para el bricolaje y jardinería. Los contenedores de madera presentan una altura de 1.5-2m. Los reactores aeróbicos están disponibles en diferentes tamaños, desde 60 a 80L para uso doméstico hasta de más de 1000L para uso industrial (De Corato et al., 2016; Markos et al., 2021; Moller y Surco, 2022).
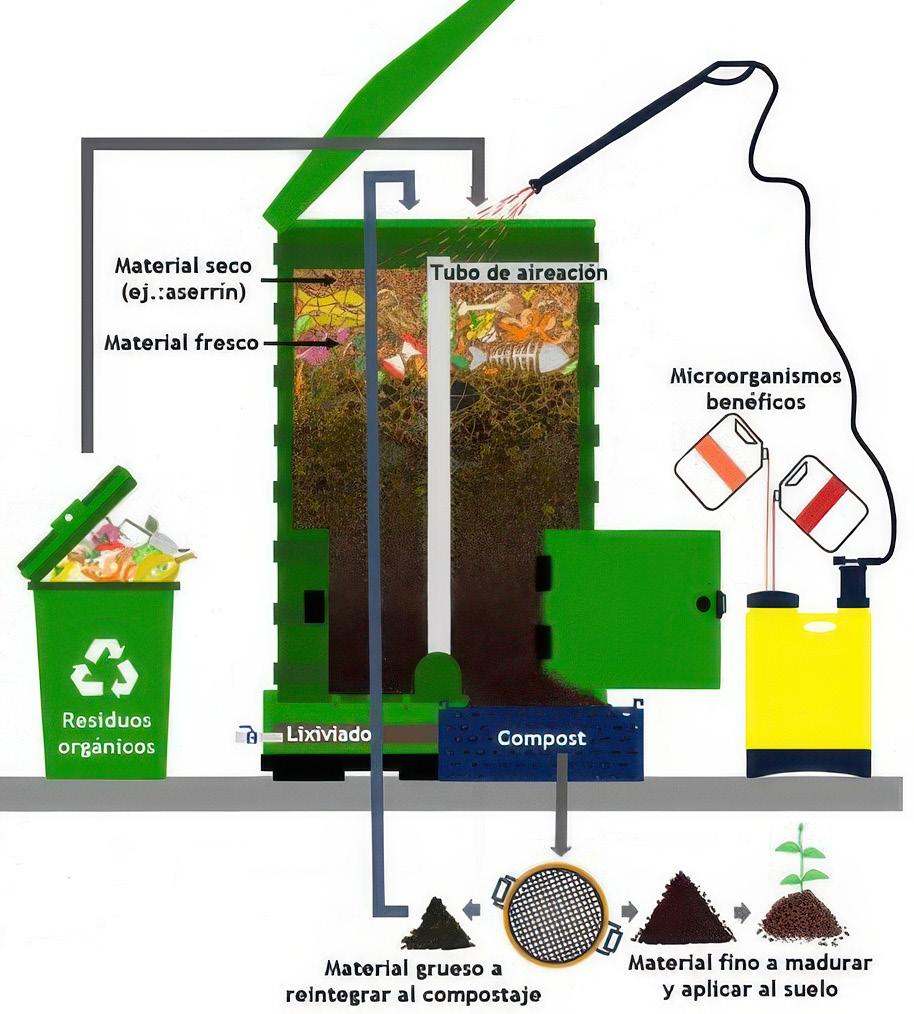
Figura 14
Sistema de compostaje basado en un contenedor. El material grueso corresponde a partículas de 5 cm y el material fino corresponde a partículas de 1cm. Fuente: Biohbac, (2020).
1.5.2. Pilas
Son montones de material orgánico que se colocan en el suelo sin un recipiente estructural específico (Figura 15). Este sistema permite el compostaje de grandes volúmenes de residuos y es común en aplicaciones agrícolas e industriales. Por lo general, tienen una altura de 2-5m y aproximadamente 3m de ancho (FAO, 2013; Michel et al., 2022).
Para este sistema se emplea astillas de madera con el propósito de regular la porosidad del compost; posteriormente, se separa este material de carga mediante un proceso de tamizado del compost. Para lograr un rendimiento óptimo, es necesario mantener una temperatura de al menos 55°C y garantizar un suministro de oxígeno para el proceso biológico a través de un sistema de ventilación pasiva o forzada. De esta forma, se elimina la necesidad del volteo manual o mecánico (Garrett 2021). Este método ayuda a reducir los sólidos volátiles, eliminar patógenos y controlar eficazmente los olores (Ozores-Hampton et al. 2022).
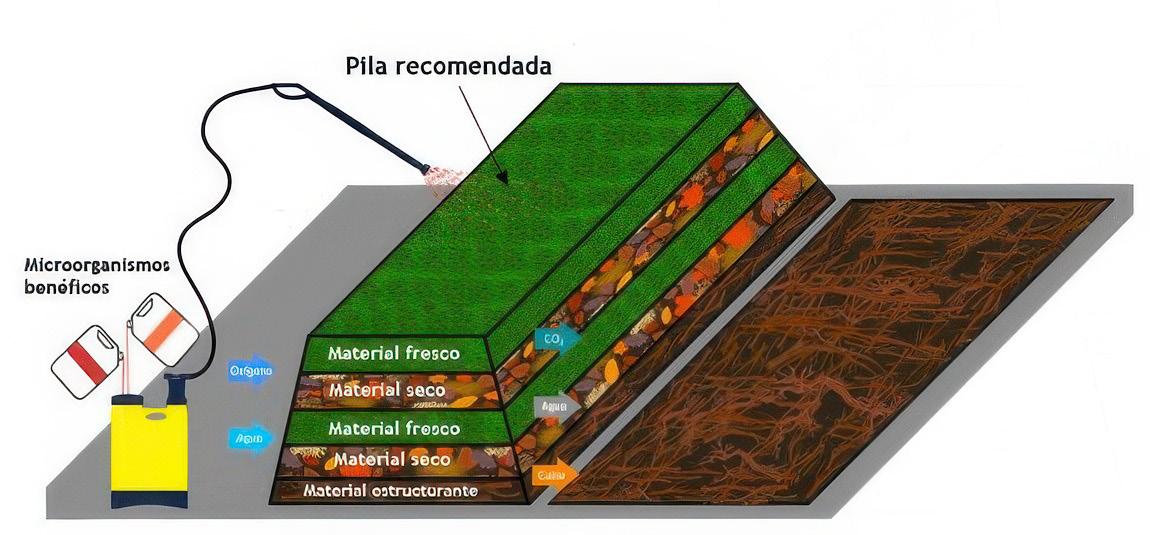
1.5.3. Compostaje en tambor rotativo
El tambor rotativo es un recipiente cilíndrico horizontal que permite una lenta mezcla de los componentes a compostar mediante una rotación (Michel et al. 2022). Las materias primas se agregan en un extremo y el compost se retira en el extremo opuesto. La aireación forzada es común, pero no siempre se utiliza para tambores pequeños (Figura 16) (Michel et al. 2022). Se utilizan para procesar residuos sólidos urbanos (RSU), estiércol, restos animales, poda y residuos orgánicos separados en origen (Kalamdhad y Kazmi, 2009). Los tambores suelen tener entre 200 y 500L de capacidad para uso doméstico o pequeño comercial, mientras que los sistemas industriales pueden alcanzar volúmenes mucho mayores (Bhatia et al., 2013; Sudharsan Varma y Kalamdhad, 2015). Los tambores industriales pueden alcanzar diámetros de 3-4m y longitudes de hasta 40m, con una capacidad de 45 toneladas diarias y un tiempo de residencia de 3-5 días (Michel et al. 2022).
Figura 15
Sistema de compostaje basado en una pila. Fuente: Biohbac, (2020).
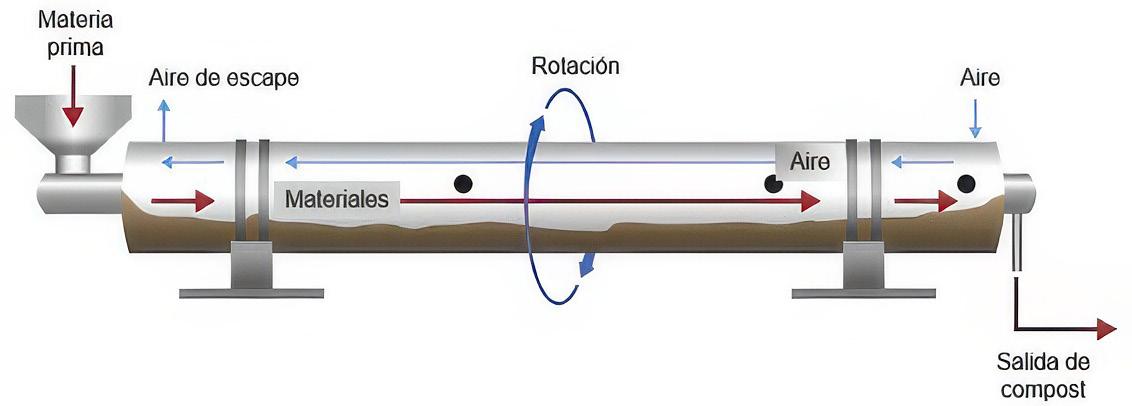
El tambor rotativo proporciona altas temperaturas, agitación y contención, lo que acelera la descomposición y facilita la reducción rápida de patógenos (Coronado-Reyes et al. 2022). Aunque el compost requiere etapas adicionales para alcanzar la estabilidad, el material descargado tras 3 días presenta un grado avanzado de descomposición, siendo menos húmedo y más fácil de tamizar. Gracias a ello, los tambores rotatorios son eficaces en la conversión rápida de residuos que puede seguir madurando en hileras o sistemas de aireación forzada (FAO, 2013; Joo et al., 2015).
Figura 16
Sistema de compostaje basado en un tambor rotativo. Fuente: Michel et al., 2022
BIBLIOGRAFÍA
Abdel-Rahman, M. A., Nour El-Din, M., Refaat, B. M., Abdel-Shakour, E. H., Ewais, E. E. D., & Alrefaey, H. M. A. (2016). Biotechnological Application of Thermotolerant CelluloseDecomposing Bacteria in Composting of Rice Straw. Annals of Agricultural Sciences, 61(1), 135–143. https://doi.org/10.1016/j. aoas.2015.11.006
Adams, J. D. W. (2008). Discussion of “Effect of inoculation in composting processes: Modifications in lignocellulosic fraction” Waste Management 27 (2007) 10991107. Waste Management, 28(11), 2428–2429. https://doi.org/10.1016/j. wasman.2007.09.008
Adegoke, A. A., Awolusi, O. O., & Stenström, T. A. (2016). Organic Fertilizers: Public Health Intricacies. In Organic Fertilizers - From Basic Concepts to Applied Outcomes. https://doi.org/10.5772/64195
Agrawal, S., Jena, L., Talukdar, N., Saikanth, D., Agrawal, S., Mangaraj, A., Boruah, A., Bahadur, R., & Ashraf, S. (2023). Impact of crop residue management on crop productivity and soil health: A review. International Journal of Statistics and Applied Mathematics, 8(6), 599–605.
Aguilar-Paredes, A., Valdés, G., Araneda, N., Valdebenito, E., Hansen, F., & Nuti, M. (2023). Microbial Community in the Composting Process and Its Positive Impact on the Soil Biota in Sustainable Agriculture. Agronomy, 13(2). https://doi. org/10.3390/agronomy13020542
Al-Askar, A. A., Rashad, Y. M., Hafez, E. E., Abdulkhair, W. M., Baka, Z. A., & Ghoneem, K. M. (2015). Characterization of alkaline protease produced by Streptomyces griseorubens E44G and its possibility for controlling Rhizoctonia root rot disease of corn. Biotechnology and Biotechnological Equipment, 29(3), 457–462. https://doi.org /10.1080/13102818.2015.1015446
Anusha, G., Maruthi Venkatesh, K., Aravind, M., & Ramakrishnan, S. (2021). Microbial Composting. IOP Conference Series: Materials Science and Engineering, 1145(1), 012019. https://doi.org/10.1088/1757899x/1145/1/012019
Ao, G., Wang, Z., Shi, Y., Ling, H., Sun, S., & Ping, W. (2024). Effects of exogenously added
humic acid on the fate of aminoglycoside antibiotics and humification process during aerobic compost. Chemical Engineering Journal, 498(June). https:// doi.org/10.1016/j.cej.2024.155704
Aydın Temel, F. (2023). Evaluation of the influence of rice husk amendment on compost quality in the composting of sewage sludge. Bioresource Technology, 373(January), 128748. https://doi. org/10.1016/j.biortech.2023.128748
Azim, K., Ouyahia, K., Amellouk, A., Perissol, C., Thami-Alami, I., & Soudi, B. (2014). Dynamic composting optimization through C/N ratio variation as a startup parameter. 4th ISOFAR Scientific Conference. ‘Building Organic Bridges’, at the Organic World Congress, 3, 787–790. http:// orgprints.org/23554/
Azim, K., Soudi, B., Boukhari, S., Perissol, C., Roussos, S., & Thami Alami, I. (2018). Composting parameters and compost quality: a literature review. Organic Agriculture, 8(2), 141–158. https://doi. org/10.1007/s13165-017-0180-z
Bárcena, A., Berdegué, J., & Otero, M. (2012). Perspectivas de la agricultura y del desarrollo rural en las Américas. In Una mirada hacia América Latina y el Caribe. https://repositorio.cepal.org/ bitstream/handle/11362/47208/1/CEPALFAO21-22_es.pdf
Barrena, R., Font, X., Gabarrell, X., & Sánchez, A. (2014). Home composting versus industrial composting: Influence of composting system on compost quality with focus on compost stability. Waste Management, 34(7), 1109–1116. https:// doi.org/10.1016/j.wasman.2014.02.008
Bhatia, A., Madan, S., Sahoo, J., Ali, M., Pathania, R., & Kazmi, A. A. (2013). Diversity of bacterial isolates during full scale rotary drum composting. Waste Management, 33(7), 1595–1601. https:// doi.org/10.1016/j.wasman.2013.03.019
Bhattacharya, S. (2023). Organic Matter Decomposition: A View on The Fate of Lignocellulosic Materials. Transactions on Networks and Communications, 11(3), 22–31. https://doi.org/10.14738/ dafs.113.14605
Bolan, N., Srivastava, P., & Kirkham, M. B. (2022).
Microbial responses to immobilization of potentially toxic elements in soils. Appraisal of Metal(Loids) in the Ecosystem, 315–330. https://doi.org/10.1016/B978-0-32385621-8.00009-1
Bonilla, N., Gutiérrez-Barranquero, J. A., De Vicente, A., & Cazorla, F. M. (2012). Enhancing soil quality and plant health through suppressive organic amendments. Diversity, 4(4), 475–491. https://doi. org/10.3390/d4040475
Chatterjee, N., Flury, M., Hinman, C., & Cogger, C. G. (2013). Chemical and Physical Characteristics of Compost Leachates. 54.
Chen, L., De Haro Marti, M., Moore, A., & Falen, C. (2011). The composting process. Dairy Manure Compost Production and Use in Idaho, 1, 1–5.
Chen, L., Marti, M. D. H., Moore, A., & Falen, C. (2011). Dairy Compost Production and Use in Idaho: On-Farm Composting Management. The Composting Process, 1–5. www.extension.uidaho.edu/ nutrient%0AIssued
Chroni, C., Kyriacou, A., Georgaki, I., Manios, T., Kotsou, M., & Lasaridi, K. (2009). Microbial characterization during composting of biowaste. Waste Management, 29(5), 1520–1525. https://doi.org/10.1016/j. wasman.2008.12.012
Coronado-Reyes, J. A., Salazar-Torres, J. A., Juárez-Campos, B., & GonzálezHernández, J. C. (2022). Chlorella vulgaris, a microalgae important to be used in Biotechnology: a review. Food Science and Technology (Brazil), 42, 1–11. https:// doi.org/10.1590/fst.37320
Cotta, S. P. M., Marins, M. S., Marriel, I. E., Lana, U. G. P., Gomes, E. A., Figueiredo, J. E. F., & Oliveira-Paiva, C. A. (2023). Thermo-resistant enzyme-producing microorganisms isolated from composting. Brazilian Journal of Biology, 83, 1–12. https://doi.org/10.1590/1519-6984.244205
Cuesta, G., García-de-la-Fuente, R., Abad, M., & Fornes, F. (2012). Isolation and identification of actinomycetes from a compost-amended soil with potential as biocontrol agents. Journal of Environmental Management, 95(SUPPL.), S280–S284. https://doi. org/10.1016/j.jenvman.2010.11.023
De Corato, U. (2020). Disease-suppressive compost enhances natural soil suppressiveness against soil-borne plant pathogens: A critical review. Rhizosphere, 13(November 2019), 100192. https://doi. org/10.1016/j.rhisph.2020.100192
De Corato, U., Viola, E., Arcieri, G., Valerio, V., & Zimbardi, F. (2016). Use of composted agro-energy co-products and agricultural residues against soil-borne pathogens in horticultural soil-less systems. Scientia Horticulturae, 210, 166–179. https://doi. org/10.1016/j.scienta.2016.07.027
Díaz, M., Jarrín-V, P., Simarro, R., Castillejo, P., Tenea, G. N., & Molina, C. A. (2021). The Ecuadorian Microbiome Project: a plea to strengthen microbial genomic research. Neotropical Biodiversity, 7(1), 223–237. https://doi.org/10.1080/23766808.2021.19 38900
Domingo, J. L., & Nadal, M. (2009). Domestic waste composting facilities: A review of human health risks. In Environment International (Vol. 35, Issue 2, pp. 382–389). Elsevier Ltd. https://doi.org/10.1016/j. envint.2008.07.004
Domínguez Núñez, T. (2015). Adición de enmiendas a suelos contaminados España-Encalado, estercolado (Spanish).
Du, N., Shi, L., Yuan, Y., Sun, J., Shu, S., & Guo, S. (2017). Isolation of a potential biocontrol agent Paenibacillus polymyxa NSY50 from vinegar waste compost and its induction of host defense responses against Fusarium wilt of cucumber. Microbiological Research, 202(6), 1–10. https://doi.org/10.1016/j. micres.2017.04.013
El Fels, L., Lemee, L., Ambles, A., & Hafidi, M. (2014). Identification and biotransformation of lignin compounds during co-composting of sewage sludge-palm tree waste using pyrolysis-GC/MS. International Biodeterioration and Biodegradation, 92, 26–35. https://doi.org/10.1016/j. ibiod.2014.04.001
Finore, I., Feola, A., Russo, L., Cattaneo, A., Di Donato, P., Nicolaus, B., Poli, A., & Romano, I. (2023). Thermophilic bacteria and their thermozymes in composting processes: a review. Chemical and Biological Technologies in Agriculture, 10(1), 1–22. https://doi.org/10.1186/ s40538-023-00381-z
Food and agriculture organization. (2013). Manual de compostaje del agricultor. In Oficina Regional de la FAO para América Latina y el Caribe. http://www.fao.org/3/ai3388s.pdf
Garbowski, T., Bar-Michalczyk, D., Charazińska, S., Grabowska-Polanowska, B., Kowalczyk, A., & Lochyński, P. (2023). An overview of natural soil amendments in agriculture. Soil and Tillage Research, 225(April 2021). https://doi.org/10.1016/j. still.2022.105462
Garcia, C., & Herran, J. (2014). Manual para la producción de abonos orgánicos y biorracionales. In Fundación produce Sinaloa, A.C. (Vol. 1, Issue 1). https:// medium.com/@arifwicaksanaa/ pengertian-use-case-a7e576e1b6bf
García, R., Gallardo, J., González, L., Islas, M., & Quiñones, N. (2023). Producción y uso de compostas. In Producción y uso de biunsumos para la Nutrición vegetal y conservación de la fertilidad del suelo (pp. 367–439).
Garrett, H. (2021). Handbook for Composting and Compost Use in Organic Horticulture. In A. J. ( Van der Wurff, A.W.G., Fuchs, J.G., Raviv, M., Termorshuizen (Ed.), Dear Dirt Doctor. https://doi.org/10.7560/728479003
Goldan, E., Nedeff, V., Barsan, N., Culea, M., Panainte-Lehadus, M., Mosnegutu, E., Tomozei, C., Chitimus, D., & Irimia, O. (2023). Assessment of Manure Compost Used as Soil Amendment—A Review. Processes, 11(4), 1–16. https://doi. org/10.3390/pr11041167
Graziani, P., Manfredi, I., Ferrari, M., Quintana, J., Alarcon, V., & Silva, A. (2020). Manual de aprovechamiento de residuos orgánicos municipales. Ministerio de Ambiente y Agua, 1–79. www.ambiente.gob.ec
Gungor, E. B. O., & let, M. (2010). Zinc release by humic and fulvic acid as influenced by pH, complexation and DOC sorption. Geoderma, 159(1–2), 131–138. https://doi. org/10.1016/j.geoderma.2010.07.004
Guo, R., Li, G., Jiang, T., Schuchardt, F., Chen, T., Zhao, Y., & Shen, Y. (2012). Effect of aeration rate, C/N ratio and moisture content on the stability and maturity of compost. Bioresource Technology,
112, 171–178. https://doi.org/10.1016/j. biortech.2012.02.099
Guo, X. xia, Liu, H. tao, & Wu, S. biao. (2019). Humic substances developed during organic waste composting: Formation mechanisms, structural properties, and agronomic functions. Science of the Total Environment, 662, 501–510. https://doi. org/10.1016/j.scitotenv.2019.01.137
He, X., Cong, R., Gao, W., Duan, X., Gao, Y., Li, H., Li, Z., Diao, H., & Luo, J. (2023). Optimization of composting methods for efficient use of cassava waste, using microbial degradation. Environmental Science and Pollution Research, 30(17), 51288–51302. https://doi.org/10.1007/ s11356-023-25818-8
Hernández-Lara, A., Ros, M., Cuartero, J., Bustamante, M. Á., Moral, R., AndreuRodríguez, F. J., Fernández, J. A., EgeaGilabert, C., & Pascual, J. A. (2022). Bacterial and fungal community dynamics during different stages of agro-industrial waste composting and its relationship with compost suppressiveness. Science of the Total Environment, 805. https://doi. org/10.1016/j.scitotenv.2021.150330
Howeler, R. (2017). Nutrient sources and their application in cassava cultivation. In Achieving sustainable cultivation of cassava (Issue September, pp. 331–354). https://doi.org/10.19103/as.2016.0014.35
Huzairi, M., Zainudin, M., Zulkarnain, A., Azmi, A. S., Muniandy, S., Sakai, K., Shirai, Y., & Hassan, M. A. (2012). Enhancement of Agro-Industrial Waste Composting Process via the Microbial Inoculation : A Brief Review. Agronomy, 12, 198.
Indoria, A. K., Sharma, K. L., Sammi Reddy, K., Srinivasarao, C., Srinivas, K., Balloli, S. S., Osman, M., Pratibha, G., & Raju, N. S. (2018). Alternative sources of soil organic amendments for sustaining soil health and crop productivity in India - impacts, potential availability, constraints and future strategies. Current Science, 115(11), 2052–2062. https://doi.org/10.18520/cs/ v115/i11/2052-2062
Javed, Z., Tripathi, G. D., Mishra, M., & Dashora, K. (2021). Actinomycetes – The microbial machinery for the organic - cycling, plant growth, and sustainable soil health. Biocatalysis and Agricultural Biotechnology,
31(November 2020). https://doi.org/https:// doi.org/10.1016/j.bcab.2020.101893
Joo, S. H., Monaco, F. Dello, Antmann, E., & Chorath, P. (2015). Sustainable approaches for minimizing biosolids production and maximizing reuse options in sludge management: A review. Journal of Environmental Management, 158, 133–145. https://doi.org/10.1016/j. jenvman.2015.05.014
Jurado, M., López, M. J., Suárez-Estrella, F., Vargas-García, M. C., López-González, J. A., & Moreno, J. (2014). Exploiting composting biodiversity: Study of the persistent and biotechnologically relevant microorganisms from lignocellulose-based composting. Bioresource Technology, 162, 283–293. https://doi.org/10.1016/j. biortech.2014.03.145
Kalamdhad, A. S., & Kazmi, A. A. (2009). Rotary drum composting of different organic waste mixtures. Waste Management and Research, 27(2), 129–137. https://doi. org/10.1177/0734242X08091865
Kelleher, B. P., & Simpson, A. J. (2006). Humic Substances in Soils: Are They Really Chemically Distinct? Environmental Science & Technology, 40(15), 4605–4611. https://doi.org/doi:10.1021/es0608085
Khater, E. S. G. (2015). Some Physical and Chemical Properties of Compost. International Journal of Waste Resources, 05(01), 1–5. https://doi.org/10.4172/22525211.1000172
Lamichhane, J. R., Dürr, C., Schwanck, A. A., Robin, M. H., Sarthou, J. P., Cellier, V., Messéan, A., & Aubertot, J. N. (2017). Integrated management of dampingoff diseases. A review. Agronomy for Sustainable Development, 37(2). https:// doi.org/10.1007/s13593-017-0417-y
Lepesteur, M. (2022). Human and livestock pathogens and their control during composting. Critical Reviews in Environmental Science and Technology, 52(10), 1639–1683. https://doi.org/10.1080 /10643389.2020.1862550
Li, S., Li, D., Li, J., Li, G., & Zhang, B. (2017). Evaluation of humic substances during cocomposting of sewage sludge and corn stalk under different aeration rates. Bioresource Technology, 245(July), 1299–1302. https:// doi.org/10.1016/j.biortech.2017.08.177
Li, Y., Gu, J., Zhang, S. Q., Shi, L. X., Sun, W., Qian, X., Duan, M. L., Yin, Y. N., & Wang, X. J. (2018). Effects of adding compound microbial inoculum on microbial community diversity and enzymatic activity during cocomposting. Environmental Engineering Science, 35(4), 270–278. https://doi. org/10.1089/ees.2016.0423
Liang, L., Luo, L., & Zhang, S. (2011). Adsorption and desorption of humic and fulvic acids on SiO2particles at nano- and micro-scales. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 384(1–3), 126–130. https://doi.org/10.1016/j. colsurfa.2011.03.045
Lim, S. L., Lee, L. H., & Wu, T. Y. (2016). Sustainability of using composting and vermicomposting technologies for organic solid waste biotransformation: Recent overview, greenhouse gases emissions and economic analysis. Journal of Cleaner Production, 111, 262–278. https://doi. org/10.1016/j.jclepro.2015.08.083
Lin, C., Cheruiyot, N. K., Bui, X. T., & Ngo, H. H. (2022). Composting and its application in bioremediation of organic contaminants. Bioengineered, 13(1), 1073–1089. https:// doi.org/10.1080/21655979.2021.2017624
Liu, X., Zubair, M., Kong, L., Shi, Y., Zhou, H., Tong, L., Zhu, R., Lv, Y., & Li, Z. (2023). Shifts in bacterial diversity characteristics during the primary and secondary fermentation stages of bio-compost inoculated with effective microorganisms agent. Bioresource Technology, 382(April), 129163. https://doi. org/10.1016/j.biortech.2023.129163
López-González, J. A., Vargas-García, M. del C., López, M. J., Suárez-Estrella, F., Jurado, M. del M., & Moreno, J. (2015). Biodiversity and succession of mycobiota associated to agricultural lignocellulosic waste-based composting. Bioresource Technology, 187, 305–313. https://doi.org/10.1016/j. biortech.2015.03.124
Lu, J., Wang, J., Gao, Q., Li, D., Chen, Z., Wei, Z., Zhang, Y., & Wang, F. (2021). Effect of Microbial Inoculation on Carbon Preservation during Goat Manure Aerobic Composting. Molecules, 26, 1–16.
Lutz, S., Thuerig, B., Oberhaensli, T., Mayerhofer, J., Fuchs, J. G., Widmer, F., Freimoser, F. M., & Ahrens, C. H. (2020). Harnessing the Microbiomes of Suppressive Composts for
Plant Protection: From Metagenomes to Beneficial Microorganisms and Reliable Diagnostics. Frontiers in Microbiology, 11(July). https://doi.org/10.3389/ fmicb.2020.01810
Machhar, K., Shukla, P., & Shukla Assistant Professor, P. J. (2022). A Review on Organic Waste Management Through Composting. Journal Of Xi’an Shiyou University, 18(6), 1–11. http://xisdxjxsu.asia
Makan, A., Assobhei, O., & Mountadar, M. (2013). Effect of initial moisture content on the invessel composting under air pressure of organic fraction of municipal solid waste in Morocco. Journal of Environmental Health Science and Engineering, 10(1), 1–9.
Malinowski, M. (2021). Impact of Air-Flow Rate and Biochar Addition on the Oxygen Concentration in Waste and Emitted Gases During Biostabilization of Undersized Fraction from Municipal Solid Waste. Journal of Ecological Engineering, 22(6), 136–144. https://doi.org/10.12911/22998993/137362
Markos, A., Aschalew, A., & ... (2021). Analysis of physical composition and nutrient content of decomposed municipal solid waste in fonko town of Analemo district, Southern Ethiopia. Indian Journal of …, December. https:// www.indianjournals.com/ijor.aspx?target=ijor:ije1&volume=48&issue=4&article=024
Meena, A. L., Karwal, M., & Dutta, D. (2021). Composting: Phases and Factors Responsible for Efficient and Improved Composting Network Project on Organic Farming View project. Agriculture and Food:E-Newsletter, 3(01), 1–7. https://doi. org/10.13140/RG.2.2.13546.95689
Mendoza, R., & Espinoza, A. (2017). Guía Técnica para muestreo de suelos. Universidad Nacional Agraria, 1–56. https://repositorio. una.edu.ni/3613/1/P33M539.pdf
Michel, F., O’Neill, T., & Rynk, R. (2022). Contained and in-vessel composting methods and methods summary. In The Composting Handbook (pp. 267–301). https://doi. org/10.1016/B978-0-323-85602-7.00013-3
Ming, L., Dou, S., Wang, H., & Zhu, Y. (2023). Study of the Humification Process and Humic Acid-like Structure Characteristics of Kitchen Waste with the Addition of Biochar. Agronomy, 13(2). https://doi.org/10.3390/ agronomy13020465
Ministerio de Agricultura y Ganadería. (2021). Ministerio de Agricultura y Ganadería. Tungurahua: Implantación de Microorganismos En Los Cultivos Genera Una Producción Limpia. https:// www.agricultura.gob.ec/tungurahuaimplantacion-de-microorganismos-en-loscultivos-genera-una-produccion-limpia/
Moller, J., & Surco, R. (2022). Contenedor ecológico para la generación de compost en la Institución Educativa Emancipación Americana - Tinta, Cusco. In Universidad Continental. https://repositorio.continental. edu.pe/handle/20.500.12394/12139
Moreno, J. & Moral, R. (2008). Compostaje. (pp. 75-163). Madrid: Mundi-Prensa.
Mori, A. S., Isbell, F., Fujii, S., Makoto, K., Matsuoka, S., & Osono, T. (2016). Low multifunctional redundancy of soil fungal diversity at multiple scales. Ecology Letters, 19(3), 249–259. https://doi.org/10.1111/ ele.12560
Naeem, U., Qazi, M. A., Haq, I. U., & Afzaal, M. (2022). Aspergillus niger as the rapid press mud composting agent. Journal of Animal and Plant Sciences, 32(2), 515–525. https:// doi.org/10.36899/JAPS.2022.2.0449
Nakasaki, K., & Hirai, H. (2017). Temperature control strategy to enhance the activity of yeast inoculated into compost raw material for accelerated composting. Waste Management, 65, 29–36. https://doi. org/10.1016/j.wasman.2017.04.019
Neher, D. A., Hoitink, H. A., Biala, J., Rynk, R., & Black, G. (2021). Compost use for plant disease suppression. In The Composting Handbook: a how-to and why manual for farm, municipal, institutional and commercial composters. Elsevier Inc. https://doi.org/10.1016/B978-0-323-856027.00015-7
Nemet, F., Perić, K., & Lončarić, Z. (2021). Microbiological activities in the composting process: A review. Columella: Journal of Agricultural and Environmental Sciences, 8(2), 41–53. https://doi.org/10.18380/szie. colum.2021.8.2.41
Nikoloudakis, Y., Panagiotakis, S., Manios, T., Markakis, E., & Pallis, E. (2018). Composting as a service: A real-world IoT implementation. Future Internet, 10(11), 1–15. https://doi.org/10.3390/fi10110107
Omoniyi, O., Arthur, G., Omowumi, O., Coopoosamy, R., & Naidoo, K. (2021). Biostimulants: potential benefits of enhancing nutrition efficiency in agronomic and horticultural crops. In Biostimulants for crops from seed germination to plant development (pp. 427–443). https://doi.org/ https://doi.org/10.1016/B978-0-12-8230480.00006-X
Oshins, C., & Miche, F. (2022). The composting process. In The Composting Handbook (pp. 51–96). https://doi.org/10.1016/B978-0323-85602-7.00013-3
Ozores-Hampton, M., Biala, J., Evanylo, G., Faucette, B., Cooperband, L., Roe, N., Creque, J. A., & Sullivan, D. (2022). Compost use. In The Composting Handbook (Academic P, pp. 777–846). Elsevier. https://doi.org/10.1016/B978-0-323-856027.00013-3
Parihar, P., & Choudhary, R. (2022). Influence of Organic Waste on Nutrient Composition of Compost and the Impact of Sawdust on Composting Process. Current World Environment, 17(3). https://doi. org/10.12944/cwe.17.3.9
Rai, Shalini & Solanki, Manoj & Anal, Ajit & Sagar, Alka & Solanki, Anjali & Kashyap, Brijendra & Pandey, A. (2021). Waste to Energy: Prospects and Applications. Emerging Frontiers of Microbes as Agro-Waste Recycler. https://doi.org/10.1007/978-98133-4347-4_1.
Rastogi, M., Nandal, M., & Khosla, B. (2020). Microbes as vital additives for solid waste composting. Heliyon, 6(2), e03343. https:// doi.org/10.1016/j.heliyon.2020.e03343
Raza, A., Bashir, S., Pothula, R., Abdelgaffar, H., Tabassum, R., Anwar, M. I., Awais, M. M., Akhtar, M., & Jurat-Fuentes, J. L. (2021). Expression and functional characterization in yeast of an endoglucanase from Bacillus sonorensis BD92 and its impact as feed additive in commercial broilers. International Journal of Biological Macromolecules, 176, 364–375. https://doi.org/10.1016/j. ijbiomac.2021.02.022
Regulation EU. (2019). Regulation of the european parliament and of the council laying down rules on the making available on the market of EU fertilising products and amending Regulations (EC) No 1069/2009 and (EC) No 1107/2009 and repealing Regulation
(EC) No 2003/2003. Official Journal of the European Union, 2019(2003), 114.
Rios, N. S., Pinheiro, B. B., Pinheiro, M. P., Bezerra, R. M., dos Santos, J. C. S., & Barros Gonçalves, L. R. (2018). Biotechnological potential of lipases from Pseudomonas: Sources, properties and applications. Process Biochemistry, 75(September), 99–120. https://doi.org/10.1016/j. procbio.2018.09.003
Rivero, A. (2014). Caracterización fisicoquímica de compost obtenido a partir de residuos orgánicos alimenticios y de Poda de la facultad de ciencias y tecnología de la Universidad Estadual Paulista “Júlio de Mesquita Filho” [Tesis de grado]. Universidad Nacional de Cuyo Facultad de Ciencias Agrarias, Brasil.
Ros, M., Raut, I., Santisima-Trinidad, A. B., & Pascual, J. A. (2017). Relationship of microbial communities and suppressiveness of Trichoderma fortified composts for pepper seedlings infected by Phytophthora nicotianae. PLoS ONE, 12(3), 1–16. https:// doi.org/10.1371/journal.pone.0174069
Rynk, R., & Schwarz, M. (2022). Compost feedstocks. In The Composting Handbook (pp. 103–151). https://doi.org/10.1016/ B978-0-323-85602-7.00013-3
Sánchez, Ó. J., Ospina, D. A., & Montoya, S. (2017). Compost supplementation with nutrients and microorganisms in composting process. Waste Management, 69(26), 136–153. https://doi.org/10.1016/j. wasman.2017.08.012
Singh, J. S., Kumar, A., Rai, A. N., & Singh, D. P. (2016). Cyanobacteria: A precious bioresource in agriculture, ecosystem, and environmental sustainability. Frontiers in Microbiology, 7(APR), 1–19. https://doi. org/10.3389/fmicb.2016.00529
Soobhany, N. (2018). Preliminary evaluation of pathogenic bacteria loading on organic Municipal Solid Waste compost and vermicompost. Journal of Environmental Management, 206, 763–767. https://doi. org/10.1016/j.jenvman.2017.11.029
Soobhany, N., Mohee, R., & Garg, V. K. (2017). Inactivation of bacterial pathogenic load in compost against vermicompost of organic solid waste aiming to achieve sanitation goals: A review. Waste Management, 64, 51–62. https://doi.org/10.1016/j.
wasman.2017.03.003
Storino, F., Arizmendiarrieta, J. S., Irigoyen, I., Muro, J., & Aparicio-Tejo, P. M. (2016). Meat waste as feedstock for home composting: Effects on the process and quality of compost. Waste Management, 56, 53–62. https://doi. org/10.1016/j.wasman.2016.07.004
Suárez-Estrella, F., Arcos-Nievas, M. A., López, M. J., Vargas-García, M. C., & Moreno, J. (2013). Biological control of plant pathogens by microorganisms isolated from agroindustrial composts. Biological Control, 67(3), 509–515. https://doi.org/10.1016/j. biocontrol.2013.10.008
Sudharsan Varma, V., & Kalamdhad, A. S. (2015). Evolution of chemical and biological characterization during thermophilic composting of vegetable waste using rotary drum composter. International Journal of Environmental Science and Technology, 12(6), 2015–2024. https://doi.org/10.1007/ s13762-014-0582-3
Sultana, M., Jahiruddin, M., Rafiqul Islam, M., Mazibur Rahman, M., Abedin, M. A., & Solaiman, Z. M. (2021). Article nutrient enriched municipal solid waste compost increases yield, nutrient content and balance in rice. Sustainability (Switzerland), 13(3), 1–12. https://doi.org/10.3390/su13031047
Sumiyati, S., Priyambada, I. B., Zahra, S. A. F., Pradhana, D. R., Haritsa, R. T., Rahman, T., Haq, M. F. Q., & Harjanti, A. W. P. (2022). Addition of Local Microorganisms (MOL) Organic Waste as Compost Bioactivator. IOP Conference Series: Earth and Environmental Science, 1098(1). https:// doi.org/10.1088/1755-1315/1098/1/012057
Sun, S., Abdellah, Y. A. Y., Miao, L., Wu, B., Ma, T., Wang, Y., Zang, H., Zhao, X., & Li, C. (2022). Impact of microbial inoculants combined with humic acid on the fate of estrogens during pig manure composting under low-temperature conditions. Journal of Hazardous Materials, 424(PD), 127713. https://doi.org/10.1016/j. jhazmat.2021.127713
Sunar, N. M., Stentiford, E. I., Stewart, D. I., & Fletcher, L. A. (2014). The Process and Pathogen Behavior in Composting: A Review. 78–87. http://arxiv.org/abs/1404.5210
Syed-Ab-Rahman, S. F., Carvalhais, L. C., Chua, E., Xiao, Y., Wass, T. J., & Schenk, P. M. (2018). Identification of soil bacterial isolates suppressing different phytophthora spp.
And promoting plant growth. Frontiers in Plant Science, 871(October), 1–18. https:// doi.org/10.3389/fpls.2018.01502
Toleikiene, M., Arlauskiene, A., Fliessbach, A., Iqbal, R., Sarunaite, L., & Kadziuliene, Z. (2020). The decomposition of standardised organic materials in loam and clay loam arable soils during a non-vegetation period. Soil and Water Research, 15(3), 181–190. https://doi.org/10.17221/31/2019-SWR
Trello, B. (2022). The Composting Biotechnology: A Microbial Aerobic Solid Substrate Fermentation. Compag Technologies International.
Tripetchkul, S., Pundee, K., Koonsrisuk, S., & Akeprathumchai, S. (2012). Co-composting of coir pith and cow manure: initial C/N ratio vs physico-chemical changes. International Journal of Recycling of Organic Waste in Agriculture, 1(1), 1–8. https://doi. org/10.1186/2251-7715-1-15
Tsolakidou, M. D., Stringlis, I. A., FanegaSleziak, N., Papageorgiou, S., Tsalakou, A., & Pantelides, I. S. (2019). Rhizosphereenriched microbes as a pool to design synthetic communities for reproducible beneficial outputs. FEMS Microbiology Ecology, 95(10), 1–14. https://doi. org/10.1093/femsec/fiz138
van Zomeren, A., & Comans, R. (2007). Measurement of Humic and Fulvic Acid Concentrations and Dissolution Properties by a Rapid Batch Procedure. 41(19), 6755–6761.
Vigneswaran, S., Kandasamy, J., & Johir, M. A. H. (2016). Sustainable Operation of Composting in Solid Waste Management. Procedia Environmental Sciences, 35, 408–415. https://doi.org/10.1016/j. proenv.2016.07.022
Villar, I., Alves, D., Garrido, J., & Mato, S. (2016). Evolution of microbial dynamics during the maturation phase of the composting of different types of waste. Waste Management, 54, 83–92. https://doi. org/10.1016/j.wasman.2016.05.011
Voběrková, S., Vaverková, M. D., Burešová, A., Adamcová, D., Vršanská, M., Kynický, J., Brtnický, M., & Adam, V. (2017). Effect of inoculation with white-rot fungi and fungal consortium on the composting efficiency of municipal solid waste. Waste Management, 61, 157–164. https://doi.org/10.1016/j.
wasman.2016.12.039
Wang, C., Tu, Q., Dong, D., Strong, P. J., Wang, H., Sun, B., & Wu, W. (2014). Spectroscopic evidence for biochar amendment promoting humic acid synthesis and intensifying humification during composting. Journal of Hazardous Materials, 280, 409–416. https:// doi.org/10.1016/j.jhazmat.2014.08.030
Wang, P., Han, S., & Lin, Y. (2022). Role of microbes and microbial dynamics during composting. In Current Developments in Biotechnology and Bioengineering: Advances in Composting and Vermicomposting Technology (First Edit). Elsevier Ltd. https://doi.org/10.1016/B9780-323-91874-9.00011-5
Wang, Q., Awasthi, M. K., Zhang, Z., & Wong, J. W. C. (2019). Sustainable composting and its environmental implications. In Sustainable Resource Recovery and Zero Waste Approaches. Elsevier B.V. https:// doi.org/10.1016/B978-0-444-642004.00009-8
Wichuk, K. M., & McCartney, D. (2010). Compost stability and maturity evaluation - a literature review. Canadian Journal of Civil Engineering, 37(11), 1505–1523. https:// doi.org/10.1139/L10-101
Williams, S. R., Zhu-Barker, X., Lew, S., Croze, B. J., Fallan, K. R., & Horwath, W. R. (2019). Impact of Composting Food Waste with Green Waste on Greenhouse Gas Emissions from Compost Windrows. Compost Science and Utilization, 27(1), 35–45. https://doi.org/10.1080/106565 7X.2018.1550023
Xiao, R., Awasthi, M. K., Li, R., Park, J., Pensky, S. M., Wang, Q., Wang, J. J., & Zhang, Z. (2017). Recent developments in biochar utilization as an additive in organic solid waste composting: A review. Bioresource Technology, 246, 203–213. https://doi. org/10.1016/j.biortech.2017.07.090
Xie, S., Tran, H. T., Pu, M., & Zhang, T. (2023). Transformation characteristics of organic matter and phosphorus in composting processes of agricultural organic waste: Research trends. Materials Science for Energy Technologies, 6, 331–342. https:// doi.org/10.1016/j.mset.2023.02.006
Xu, J., Jiang, Z., Li, M., & Li, Q. (2019). A compost-
derived thermophilic microbial consortium enhances the humification process and alters the microbial diversity during composting. Journal of Environmental Management, 243(May), 240–249. https:// doi.org/10.1016/j.jenvman.2019.05.008
Xu, M., Yang, M., Sun, H., Meng, J., Li, Y., Gao, M., Wang, Q., & Wu, C. (2022). Role of multistage inoculation on the co-composting of food waste and biogas residue. Bioresource Technology, 361(July), 127681. https://doi. org/10.1016/j.biortech.2022.127681
Yousif Abdellah, Y. A., Shi, Z. J., Luo, Y. Sen, Hou, W. T., Yang, X., & Wang, R. L. (2022). Effects of different additives and aerobic composting factors on heavy metal bioavailability reduction and compost parameters: A meta-analysis. Environmental Pollution, 307(February), 119549. https://doi.org/10.1016/j. envpol.2022.119549
Zeng, G. M., Huang, H. L., Huang, D. L., Yuan, X. Z., Jiang, R. Q., Yu, M., Yu, H. Y., Zhang, J. C., Wang, R. Y., & Liu, X. L. (2009). Effect of inoculating white-rot fungus during different phases on the compost maturity of agricultural wastes. Process Biochemistry, 44(4), 396–400. https://doi.org/10.1016/j. procbio.2008.11.012
Zhang, J., Zeng, G., Chen, Y., Liang, J., Zhang, C., Huang, B., Sun, W., Chen, M., Yu, M., Huang, H., & Zhu, Y. (2014). Phanerochaete chrysosporium inoculation shapes the indigenous fungal communities during agricultural waste composting. Biodegradation, 25(5), 669–680. https://doi. org/10.1007/s10532-014-9690-5

2. Uso de microorganismos benéficos en el compostaje
La inoculación de microorganismos es una práctica sustentable y ampliamente utilizada en el compostaje. Esta tiene como objetivo mejorar la eficiencia del proceso y la calidad del producto final, tanto en términos de estabilidad como de contenido nutritivo (Li et al., 2019; Van Fan et al., 2017). La introducción de poblaciones microbianas ya sea individualmente o en consorcios, representa un enfoque prometedor. Estos inóculos son seleccionados por sus capacidades enzimáticas que les permite actuar en la descomposición de la materia orgánica (MO), la optimización de la humificación, la supresión de patógenos y de mejorar la salud del suelo (Huang et al., 2015; Manea et al., 2024; Sun et al., 2022; Xu et al., 2019).
El uso de microorganismos depende de la meta que se desea alcanzar en el compostaje. Si la meta es mejorar la biodegradación de compuestos recalcitrantes y acortar el tiempo del compostaje, se emplean especies de hongos como, Trichoderma spp., Trichoderma viride o Aspergillus niger, conocidos por su capacidad de descomponer celulosa y lignina (De Corato et al., 2016; Voběrková et al., 2017; Zin & Badaluddin, 2020). Si la meta es optimizar la retención de nitrógeno y favorecer la formación de compuestos estables, se introducen bacterias nitrificantes y fijadoras de nitrógeno, como Azotobacter o Rhizobium (Maeda et al., 2011; Sun et al., 2020).
En cambio, si la meta es el control biológico de patógenos, se introducen microorganismos antagonistas como Bacillus y Pseudomonas, ya que promueven la supresión de enfermedades (Bhattacharya, 2023; Jurado et al., 2015; Malinowski, 2021; Wang et al., 2020). En los siguientes ítems se detallan características de microrganismos benéficos como: bacterias, hongos, actinomicetos y microalgas, sus principales beneficios e incluso sus limitaciones.
2.1. Bacterias
La inoculación de bacterias presenta múltiples beneficios en el proceso de compostaje (Figura 17). Las ventajas van desde la rápida descomposición de compuestos orgánicos simples y complejos en las primeras etapas del compostaje, particularmente en la fase mesófila y termófila hasta la supresión de patógenos (Robledo-Mahón et al. 2020).
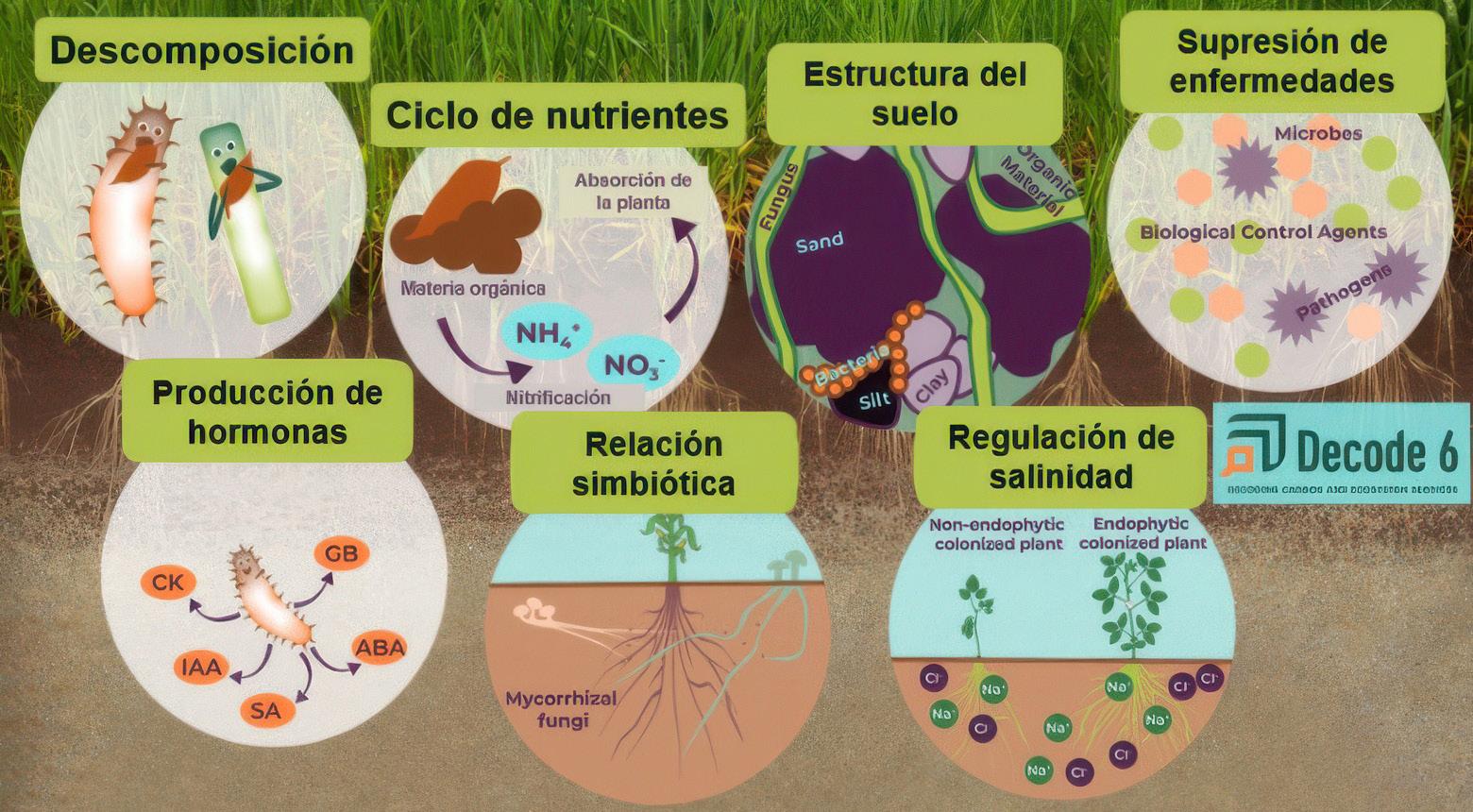
Funciones de las bacterias en el proceso de compostaje. Fuente: Brey, (2023).
Figura 17
Una de las funciones principales de las bacterias es la intervención en el ciclo del C, S y N, ya que retienen los nutrientes mientras descomponen la materia orgánica compleja en sustancias más simples (Lowenfels & Lewis, 2021). La acción de sus enzimas puede transformar materiales como carbohidratos, proteínas y grasas en moléculas más pequeñas que otros microorganismos (Sun et al., 2022). Las bacterias tienen mayor tolerancia térmica, por lo que dominan en el proceso de compostaje, especialmente en la fase termófila (Hernández-Lara et al. 2022). Los filos bacterianos dominantes durante este proceso son: Firmicutes, Actinobacteria, Proteobacteria, Bacteroidetes, y Cloroflexi (Aguilar-Paredes et al. 2023). Cada uno de ellos cumple una función en la mineralización y descomposición de materia orgánica que sucede a lo largo del compostaje (Tabla 10).
Tabla 10
Filos bacterianos dominantes en el proceso de compostaje.
Entre los siete filos dominantes existe uno que se le puede considerar como uno de los principales, el filo Firmicutes. Este filo es un conjunto de bacterias Gram positivas, formadoras de esporas, anaerobios obligados y con forma de coco o de bastón, cuyas funciones principales son, la producción de análogos directos de las hormonas vegetales, la degradación de compuestos complejos como la cafeína, los alcaloides, los fenoles, y el control del desarrollo de patógenos vegetales (Figura 18) (Hashmi et al., 2020; Jurado et al., 2014; Li et al., 2018)
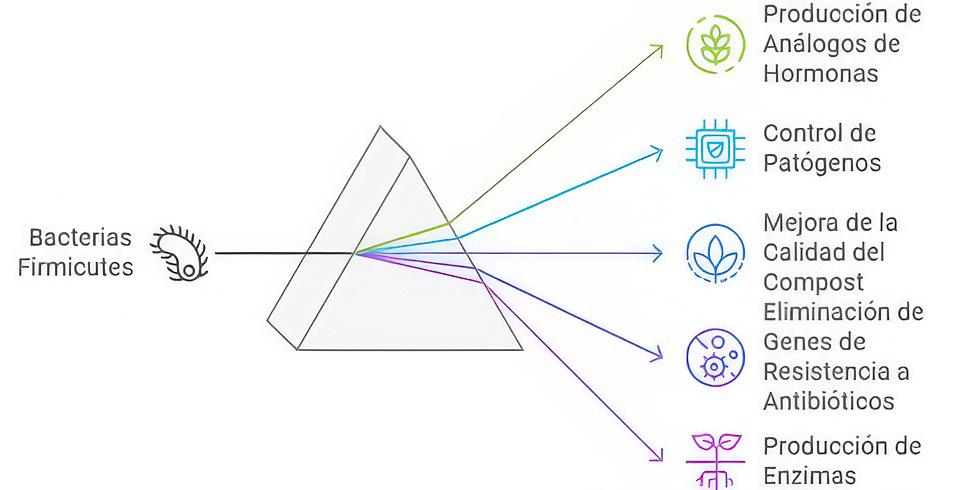
Figura 18
Roles multifacéticos del género Firmicutes en el compostaje.
En el grupo Firmicutes se destacan los géneros Bacillus, por su capacidad de producir enzimas termoestables como proteasas, celulasas y enzimas modificadoras de lignina, las cuales son indispensables durante la degradación de la MO (Manea et al. 2024). Además, estimulan la acumulación de NH4+‐N, NO3 ‐N y nitrógeno total (TN), eliminan patógenos y genes de resistencia a antibióticos (ARG) como fluoroquinolonas, nucleósidos y nitroimidazol (Maeda et al. 2011; Cao et al. 2024). Es así como, la adición de Bacillus megatherium puede promover el proceso de oxidación de NH3 y reducir su emisión. En cambio, Bacillus subtilis (Figura 19), reduce la mineralización durante las etapas de enfriamiento y maduración del compostaje enriqueciendo así los contenidos de carbono orgánico total (TOC) y sustancias húmicas (Duan et al. 2020; Hernández-Lara et al. 2022)0.5%, 1%, and 2% w/w compost.
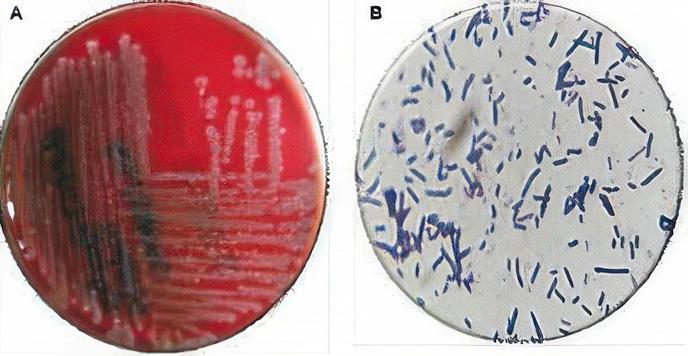
Figura 19
Cultivo de Bacillus subtilis. Colonia de bacterias cultivadas en agar sangre (A). Tinción Gram (+) evidenciando las bacterias en forma de bacilo (B). Fuente: Duan et al., (2020).
Algunas bacterias tienen la capacidad de inmovilizar metales pesados, evitando que se filtren al medio ambiente. Este proceso implica la unión de metales pesados a las superficies de las células bacterianas o la formación de complejos insolubles (Robledo-Mahón et al. 2020). Especies bacterianas como Pseudomonas y Enterobacter, son conocidas por su capacidad de unión a metales (Kapahi & Sachdeva, 2019). Las superficies de las células bacterianas a menudo contienen grupos funcionales (carboxilo, amino, fosfato) que pueden unirse con iones de metales pesados (Chatterjee et al. 2013).
2.2. Hongos
Los hongos son organismos eucariotas que carecen de clorofila y tejido vascular, presentan estructuras especializadas para la formación de esporas, algunos forman relaciones simbióticas con plantas y animales (Naranjo-Ortiz & Gabaldón, 2019). Los hongos, sin duda, pueden desempeñar un rol crucial en el proceso de compostaje, contribuyendo a la descomposición de la materia orgánica, la disponibilidad de nutrientes y el control biológico de patógenos (Lu et al. 2022). Algunas redes simbióticas pueden crecer en condiciones ambientales muy severas y también pueden mejorar la estabilidad de las redes bacterianas (Wichuk & McCartney, 2010). A continuación, se describen algunos tipos de hongos relevantes en este proceso, destacando sus funciones específicas.
Los hongos inoculados desempeñan un papel clave, al poseer la capacidad de producir una gran cantidad de enzimas extracelulares. Especies como, Penicillium vinaceum y Eupenicillium hirayama presentan fuertes actividades enzimáticas en la producción de celulasa, lacasa, lipasa, proteasa, amilasa y quitinasa (Ameen & Al-Homaidan, 2021). También los hongos producen compuestos aromáticos ricos en grupos carbonilo, y carboxilo. Toda esta maquinaria metabólica les permite descomponer diferentes compuestos poliméricos como la celulosa, carboximetilcelulosa, hemicelulosa, xilano y arabinoxilano (HernándezLara et al., 2022; López-González et al., 2015; Robledo-Mahón et al., 2020).
Algunos hongos tienen la capacidad de inmovilizar los metales pesados como Cadmio (Cd), Plomo (Pb) y Cromo (Cr). Por ejemplo, Pleurotus sp. y Klebsiella oxytoca han demostrado que pueden disminuir la biodisponibilidad de estos metales presentes en las pilas de compostaje (Aguilar-Paredes et al., 2023; Hernández-Lara et al., 2022; Kapahi & Sachdeva, 2019). De esta manera reducen la absorción por la planta y potencial tóxico de estos elementos y sus consecuencias para el desarrollo vegetal como para la salud humana.
La especie Phanerochaete chrysosporium, por su parte, promueve la degradación continua de la lignina, al aumentar la abundancia relativa de Talaromyces y Coprinopsis, mejora el reciclaje de nitrógeno orgánico a inorgánico y la humificación es más intensa y temprana (Huang et al., 2015; Tyagi et al., 2014; Voběrková et al., 2017). Las pruebas de fitotoxicidad (índices de germinación, IG) realizadas a esta especie, demostraron que su introducción es segura para su aplicación al suelo (Jurado et al., 2015). En cambio, otras especies de hongos micorrízicos (HMA) como Glomus fasciculatum y el no patógeno Pythium oligandrum permiten a las plantas acceder a los nutrientes del compost, mejorando la entrega de nutrientes y aumentando el rendimiento de los cultivos (80–89% N y P) (Hernández-Lara et al., 2022; Zhang et al., 2014).
La presencia de hongos inoculantes como, Trametes versicolor y Fomes fomentarius, conduce a una mayor tasa de degradación y un mejor grado de madurez, aumentando la
producción de enzimas, especialmente deshidrogenasa y proteasa (Voběrková et al. 2017; Machado et al. 2020). La actividad de la proteasa, que está estrechamente relacionada con el ciclo del nitrógeno y cataliza la hidrólisis de las proteínas, permite aumentar la degradación de sustratos al comienzo del proceso. Esto probablemente se deba a la adecuada disponibilidad de oligopéptidos y polipéptidos en la mezcla inicial (Voběrková et al. 2017).
Un hongo catalogado como importante es Trichoderma harzianum (Figura 20). Se categoriza como hongo descomponedor por tener naturaleza saprófita, por lo que su función es aportar MO especialmente en el proceso de provisión de compost (Islam et al. 2014; Thaha et al. 2020). Se ha demostrado que la inoculación de este hongo permite acelerar el proceso de compostaje debido a su capacidad para producir enzimas que pueden degradar celulosa, hemicelulosa y lignina (Organo et al., 2022). El producto obtenido, gracias a la capacidad descomponedora de este hongo, proporciona una gran fuente de nutrientes como N (0.91%), P (2.13%) y K (6.68%) y mejora la acidez del suelo y la conductividad eléctrica (50.40 μS/cm) (Organo et al., 2022; Siddiquee et al., 2017).
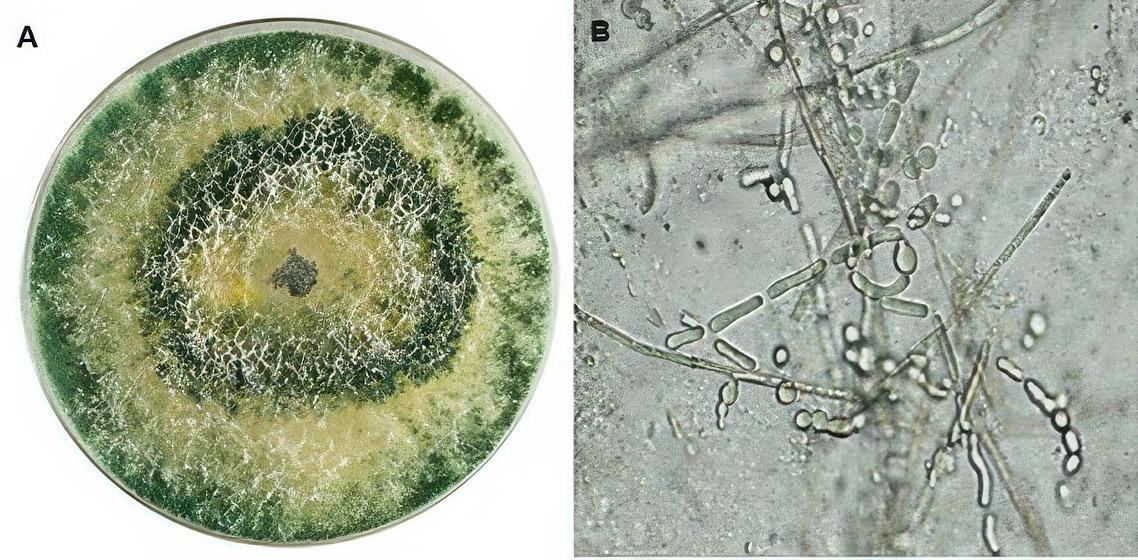
Figura 20
Cultivo de Trichoderma harzianum. Cultivo de hongo en una placa de Petri con crecimiento esporulado y zonas de diferente densidad micelial (A). Micrografía muestra la estructura filamentosa del hongo, incluyendo hifas septadas y esporas en desarrollo (B). Fuente: Acosta-Suárez et al., (2013); Silva et al., (2023)
Otras especies como, P. vinaceum y E. hirayama mejoran el contenido de MO en el compost en rangos de 33 a 36%. También aumentan el contenido y biodisponibilidad de N en un promedio de 5% (Aguilar-Paredes et al., 2023; Ameen & Al-Homaidan, 2021). Consecuentemente, estos hongos modifican la capacidad fertilizante de una pila de compost haciéndola más apta para su aplicación en cultivos.
2.3. Actinomicetos
Los actinomicetos son organismos procariotas que crecen en condiciones de pH de 6 a 8, alta temperatura o estrés hídrico. Morfológicamente, se parecen a los hongos debido a sus células alargadas que se ramifican en filamentos o hifas (Pepper & Gentry, 2015). Sin embargo, son bacterias filamentosas que intervienen en la descomposición de los materiales resistentes en el compost, como fenoles, taninos, celulosa y lignina. Se destacan los géneros de Micromonospora, Streptomyces y Actinomyces capaces de producir hormonas y enzimas especializadas en la protección de la salud de las plantas, en particular contra plagas de insectos y patógenos (Aguilar-Paredes et al. 2023). Presentan múltiples beneficios como, la fijación de nitrógeno, incremento de la
biodisponibilidad de minerales (P, K y Zn), la quelación de Hierro (Fe) y la secreción de hormonas de crecimiento vegetal (auxina) (Gopalakrishnan et al. 2020). Una de las principales ventajas del uso de estos inoculantes radica en su capacidad para secretar enzimas extracelulares que podrían hidrolizar la lignocelulosa y solubilizar sus monómeros básicos para un mayor metabolismo (Cuesta et al. 2012; Gaspar et al. 2022). Además, degradan materiales difíciles de descomponer, como la celulosa y la quitina, y también son activos a niveles altos de pH (Gaspar et al., 2022; Jurado et al., 2014; Robledo-Mahón et al., 2020). Entre las enzimas principales se incluye: manganeso peroxidasa, lignina peroxidasa y lacasas, que pueden degradar la lignina y una amplia variedad de compuestos aromáticos (Cuesta et al. 2012).
Dentro de este grupo, se destacan los actinomicetos termoestables, por ejemplo, Streptomyces sp. y Actinobacteria bacterium. Se caracterizan porque aceleran la degradación de celulosa y aumentan el contenido de sustancias húmicas, lo cual permite el secuestro de carbono y la reducción de gases de efecto invernadero (Zhao et al. 2017). Otros géneros como, Streptomyces (Figura 21), o el Microbacterium, y el Thermobifida, poseen la capacidad de solubilizar el fosfato. El fósforo (P) es un elemento esencial para el desarrollo de las plantas. En la naturaleza, las formas inorgánicas y orgánicas de P disponibles en el suelo no son asimiladas por las plantas. Para hacerlas accesibles, estos microorganismos pueden solubilizar fosfatos inorgánicos produciendo ácidos de bajo peso molecular (Meenakshi et al., 2024; Robledo-Mahón et al., 2020; Silva et al., 2022).
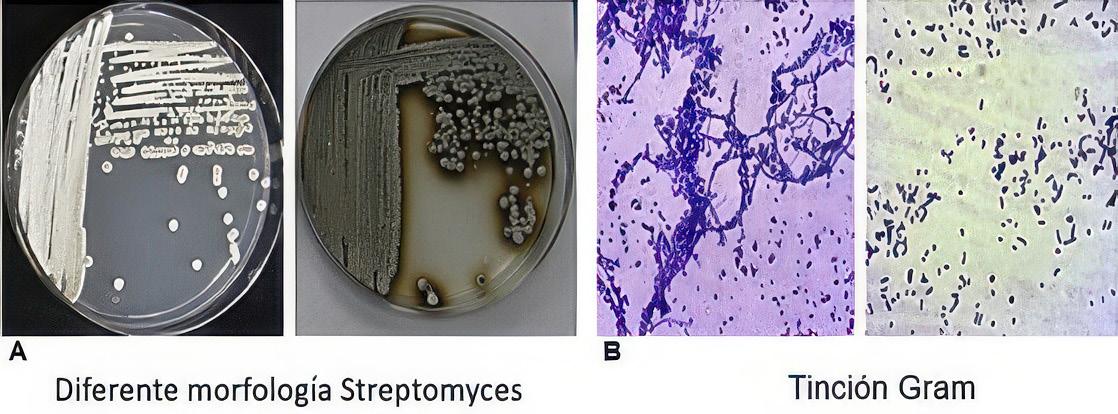
Figura 21
Streptomyces. Morfología de Streptomyces cultivado en agar almidón caseína (A). Tinción de Gram donde se evidencia que corresponde a una Gram positiva y ácido-alcohol negativa (B). Fuente: Gopalakrishnan et al., 2020.
2.4. Microalgas
Las microalgas son un grupo de microorganismos fotosintéticos unicelulares que viven en ambientes terrestres y acuáticos, incluyendo agua dulce y salada. Las microalgas pueden ser tanto procariotas como eucariotas, y pueden crecer rápidamente en hábitats con condiciones fotoautotróficas. Se clasifican como Chlorophyceae (algas verdes), Cyanophyceae (algas verdeazuladas), Chrysophyceae (algas doradas), Rhodophyceae (algas rojas), Phaeophyceae (algas pardas) y Bacillariophyceae (diatomeas) (Prasanna et al. 2015; Alvarez et al. 2021; Moreno Osorio et al. 2021). Dentro de las algas verdes destacan, Chlorella sp., Chlorococcum sp., Pseudokirchneriella subcapitata, Scenedesmus sp., Coelastrum sp. y Nannochloropsis gaditana y las especies principales de las algas azules son Spirulina platensis, Microcystis aeruginosa y Synechocystis salina (Alvarez et al., 2021; Kong et al., 2024).
Entre las funciones biológicas que estos microorganismos pueden cumplir, se enumeran la fijación biológica del N, roles en el ciclo del P, síntesis de fitohormonas, la formación
de asociaciones simbióticas con raíces, biocontrol y la estabilización del suelo (Figura 22) (Alvarez et al. 2021). Además, tienen un gran potencial para mejorar el contenido de C orgánico del suelo mediante la asimilación del CO2 y N2, proporcionando un mejor ambiente edáfico a las plantas y a la microbiota normal asociada (Prasanna et al. 2013; Díaz-Pérez et al. 2023).
Asimismo, actúan como remediadores de metales pesados mediante el mecanismo de adsorción, donde no solo genera radicales libres para eliminar estos contaminantes, sino que también promueve la síntesis de antioxidantes como glutatión reductasa, superóxido dismutasa (SOD), peroxidasa, ascorbato peroxidasa y catalasa (Coronado-Reyes et al. 2022; Díaz-Pérez et al. 2023). Esto es gracias a los componentes de la pared celular que poseen estos organismos, constituida de proteínas orgánicas, polisacáridos, lípidos, péptidos y exopolisacáridos, con varios grupos funcionales para unir metales pesados (Song et al. 2022).
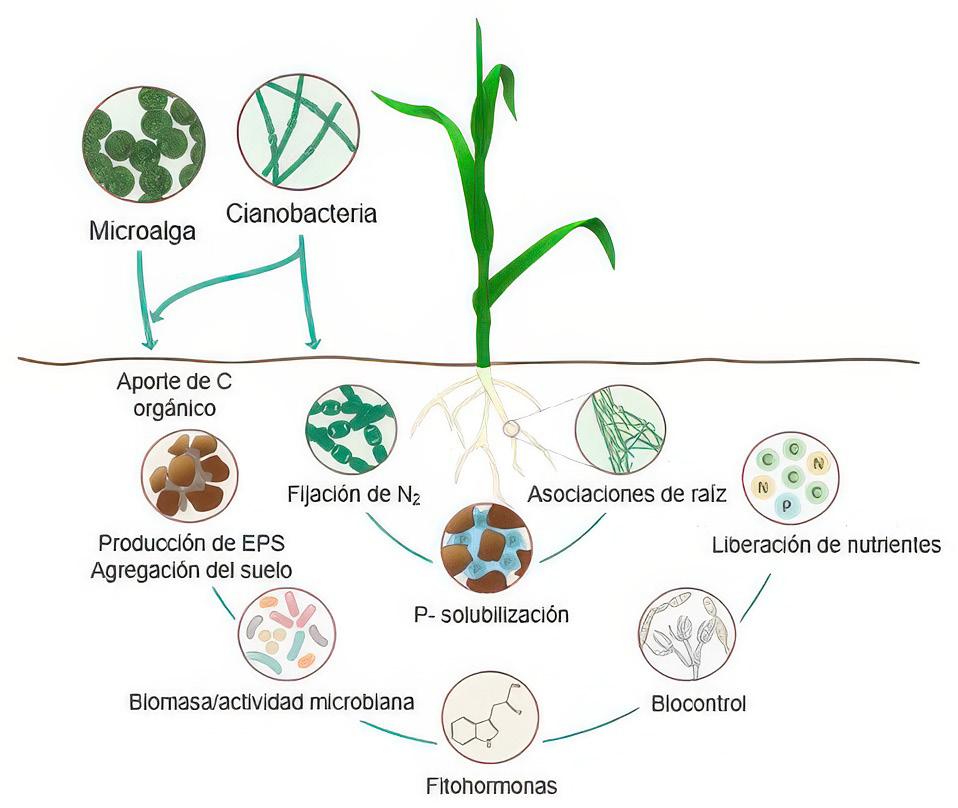
Figura 22
Mecanismos beneficiosos de las microalgas para el mejoramiento del compostaje. Fuente: Alvarez et al., (2021).
Por otro lado, las cianobacterias, un grupo diverso de microalgas, se consideran biofertilizantes debido a su capacidad para fijar nitrógeno y solubilizar fósforo inmovilizado. Las cianobacterias prosperan en la rizósfera, formando asociaciones simbióticas con plantas, favoreciendo condiciones con poca luz, alta disponibilidad de P, pH neutro a ligeramente alcalino y temperaturas de 30 a 35°C (Singh et al. 2016).
Dentro del grupo de las cianobacterias se destaca Anabaena sp., una cianobacteria filamentosa que forma estructuras multicelulares y tiene la capacidad de fijar N2 gracias a la presencia de heterocistos especializados (Prasanna et al., 2015; Wang & Husain, 2015). Además, ha demostrado tener una correlación positiva con la actividad fungicida, lo que sugiere que puede ser útil en la protección biológica de las plantas contra patógenos, por ejemplo, contra el marchitamiento por Fusarium, un hongo fitopatógeno común que afecta a plantas de tomate (Wang & Husain, 2015). La integración del cultivo de microalgas con compost se considera una técnica potencial, ofreciendo un enfoque sostenible para mejorar la fertilidad del suelo y el crecimiento de las plantas (Prasanna et al. 2013).
BIBLIOGRAFÍA
Acosta-Suárez, M., Pichardo, T., Roque, B., Cruz-Martín, M., Mena, E., Leiva-Mora, M., Castro, R., Alvarado-Capó, Y., & Autora, *. (2013). Antagonismo in vitro de Trichoderma harzianum Rifai contra Mycosphaerella fijiensis Morelet. Artículo Original Biotecnología Vegetal, 13(4), 397.
Aguilar-Paredes, A., Valdés, G., Araneda, N., Valdebenito, E., Hansen, F., & Nuti, M. (2023). Microbial Community in the Composting Process and Its Positive Impact on the Soil Biota in Sustainable Agriculture. Agronomy, 13(2). https:// doi.org/10.3390/agronomy13020542
Alvarez, A. L., Weyers, S. L., Goemann, H. M., Peyton, B. M., & Gardner, R. D. (2021). Microalgae, soil and plants: A critical review of microalgae as renewable resources for agriculture. Algal Research, 54(December 2020), 102200. https://doi.org/10.1016/j. algal.2021.102200
Ameen, F., & Al-Homaidan, A. A. (2021). Compost inoculated with fungi from a mangrove habitat improved the growth and disease defense of vegetable plants. Sustainability (Switzerland), 13(1), 1–13. https://doi.org/10.3390/ su13010124
Bhattacharya, S. (2023). Organic Matter Decomposition: A View on The Fate of Lignocellulosic Materials. Transactions on Networks and Communications, 11(3), 22–31. https://doi.org/10.14738/ dafs.113.14605
Cao, R., Huang, Y., Li, R., Li, K., Ren, Z., & Wu, J. (2024). Regulation of nitrogen transformation and microbial community by inoculation during livestock manure composting. Environmental Microbiology Reports, 16(2), 1–14. https://doi.org/10.1111/17582229.13256
Chatterjee, N., Flury, M., Hinman, C., & Cogger, C. G. (2013). Chemical and Physical Characteristics of Compost Leachates. 54. http://www.wsdot.wa.gov/research/
reports/fullreports/819.1.pdf
Coronado-Reyes, J. A., Salazar-Torres, J. A., Juárez-Campos, B., & GonzálezHernández, J. C. (2022). Chlorella vulgaris, a microalgae important to be used in Biotechnology: a review. Food Science and Technology (Brazil), 42, 1–11. https://doi.org/10.1590/fst.37320
Cuesta, G., García-de-la-Fuente, R., Abad, M., & Fornes, F. (2012). Isolation and identification of actinomycetes from a compost-amended soil with potential as biocontrol agents. Journal of Environmental Management, 95(SUPPL.), S280–S284. https://doi. org/10.1016/j.jenvman.2010.11.023
De Corato, U., Viola, E., Arcieri, G., Valerio, V., & Zimbardi, F. (2016). Use of composted agro-energy co-products and agricultural residues against soilborne pathogens in horticultural soilless systems. Scientia Horticulturae, 210, 166–179. https://doi.org/10.1016/j. scienta.2016.07.027
Díaz-Pérez, F. J., Díaz, R., Valdés, G., Valdebenito-Rolack, E., & Hansen, F. (2023). Effects of microalgae and compost on the yield of cauliflower grown in low nutrient soil. Chilean Journal of Agricultural Research, 83(2), 181–194. https://doi.org/10.4067/ S0718-58392023000200181
Du, N., Shi, L., Yuan, Y., Sun, J., Shu, S., & Guo, S. (2017). Isolation of a potential biocontrol agent Paenibacillus polymyxa NSY50 from vinegar waste compost and its induction of host defense responses against Fusarium wilt of cucumber. Microbiological Research, 202(6), 1–10. https://doi. org/10.1016/j.micres.2017.04.013
Duan, M., Zhang, Y., Zhou, B., Qin, Z., Wu, J., Wang, Q., & Yin, Y. (2020). Effects of Bacillus subtilis on carbon components and microbial functional metabolism during cow manure–straw composting. Bioresource Technology, 303(January). https://doi.org/10.1016/j. biortech.2020.122868
Gaspar, S. S., Assis, L. L. R., Carvalho, C. A., Buttrós, V. H., Ferreira, G. M. dos R., Schwan, R. F., Pasqual, M., Rodrigues, F. A., Rigobelo, E. C., Castro, R. P., & Dória, J. (2022). Dynamics of microbiota and physicochemical characterization of food waste in a new type of composter. Frontiers in Sustainable Food Systems, 6. https:// doi.org/10.3389/fsufs.2022.960196
Gopalakrishnan, S., Srinivas, V., & Prasanna, S. L. (2020). Streptomyces. In Beneficial Microbes in Agro-Ecology: Bacteria and Fungi. Elsevier Inc. https:// doi.org/10.1016/B978-0-12-8234143.00005-8
Hashmi, I., Bindschedler, S., & Junier, P. (2020). Firmicutes. In Beneficial Microbes in Agro-Ecology (pp. 363–396). https://doi.org/10.1016/b978-012-823414-3.00018-6
Hernández-Lara, A., Ros, M., Cuartero, J., Bustamante, M. Á., Moral, R., Andreu-Rodríguez, F. J., Fernández, J. A., Egea-Gilabert, C., & Pascual, J. A. (2022). Bacterial and fungal community dynamics during different stages of agro-industrial waste composting and its relationship with compost suppressiveness. Science of the Total Environment, 805. https://doi. org/10.1016/j.scitotenv.2021.150330
Huang, H. li, Zeng, G. ming, Luo, L., Zhang, J. chao, Yu, M., & Qin, P. feng. (2015). Effect of inoculation during different phases of agricultural waste composting on spectroscopic characteristics of humic acid. Journal of Central South University, 22(11), 4177–4183. https:// doi.org/10.1007/s11771-015-2965-0
Islam, M. A., Mostafa, M. G., & Rahman, M. R. (2014). Conversion of solid organic waste into compost using Trichoderma spp. And its application on some selected vegetables. International Journal of Environment and Waste Management, 14(3), 211–221. https:// doi.org/10.1504/IJEWM.2014.064570
Jurado, M., López, M. J., Suárez-Estrella, F., Vargas-García, M. C., López-González, J. A., & Moreno, J. (2014). Exploiting composting biodiversity: Study of the persistent and biotechnologically relevant microorganisms from lignocellulose-based composting. Bioresource Technology, 162, 283–293. https://doi.org/10.1016/j. biortech.2014.03.145
Jurado, M. M., Suárez-Estrella, F., López, M. J., Vargas-García, M. C., López-González, J. A., & Moreno, J. (2015). Enhanced turnover of organic matter fractions by microbial stimulation during lignocellulosic waste composting. Bioresource Technology, 186, 15–24. https://doi.org/10.1016/j. biortech.2015.03.059
Kapahi, M., & Sachdeva, S. (2019). Bioremediation Options for Heavy Metal Pollution. J Health Pollution, 9(24).
Kong, W., Kong, J., Feng, S., Yang, T. T., Xu, L., Shen, B., Bi, Y., & Lyu, H. (2024). Cultivation of microalgae–bacteria consortium by waste gas–waste water to achieve CO2 fixation, wastewater purification and bioproducts production. Biotechnology for Biofuels and Bioproducts, 17(1), 1–21. https://doi. org/10.1186/s13068-023-02409-w
Li, C., Li, H., Yao, T., Su, M., Ran, F., Han, B., Li, J., Lan, X., Zhang, Y., Yang, X., & Gun, S. (2019). Microbial inoculation influences bacterial community succession and physicochemicalharacteristics during pig manure composting with corn straw. Bioresource Technology, 289(March), 121653. https://doi.org/10.1016/j. biortech.2019.121653
Li, Y., Gu, J., Zhang, S. Q., Shi, L. X., Sun, W., Qian, X., Duan, M. L., Yin, Y. N., & Wang, X. J. (2018). Effects of adding compound microbial inoculum on microbial community diversity and enzymatic activity during co-composting. Environmental Engineering Science, 35(4), 270–278.
https://doi.org/10.1089/ees.2016.0423
López-González, J. A., Vargas-García, M. del C., López, M. J., SuárezEstrella, F., Jurado, M. del M., & Moreno, J. (2015). Biodiversity and succession of mycobiota associated to agricultural lignocellulosic waste-based composting. Bioresource Technology, 187, 305–313. https://doi.org/10.1016/j. biortech.2015.03.124
Lowenfels, J., & Lewis, W. (2021). Cultivar con microbios: La guía del cultivador orgánico de la red de nutrientes del suelo. In Вестник Росздравнадзора (Vol. 4, Issue 1).
Lu, X., Yang, Y., Hong, C., Zhu, W., Yao, Y., Zhu, F., Hong, L., & Wang, W. (2022). Optimization of vegetable waste composting and the exploration of microbial mechanisms related to fungal communities during composting. Journal of Environmental Management, 319(July), 115694. https://doi. org/10.1016/j.jenvman.2022.115694
Machado, A. S., Valadares, F., Silva, T. F., Milagres, A. M. F., Segato, F., & Ferraz, A. (2020). The Secretome of Phanerochaete chrysosporium and Trametes versicolor Grown in Microcrystalline Cellulose and Use of the Enzymes for Hydrolysis of Lignocellulosic Materials. Frontiers in Bioengineering and Biotechnology, 8(July), 1–15. https://doi.org/10.3389/ fbioe.2020.00826
Maeda, K., Hanajima, D., Toyoda, S., Yoshida, N., Morioka, R., & Osada, T. (2011). Microbiology of nitrogen cycle in animal manure compost. Microbial Biotechnology, 4(6), 700–709. https://doi.org/10.1111/j.17517915.2010.00236.x
Malik, M. M. R., Akhtar, M. J., Ahmad, I., & Khalid, M. (2014). Synergistic use of Rhizobium, compost and nitrogen to improve growth and yield of mungbean (Vigna radiata). Pakistan Journal of Agricultural Sciences, 51(2), 393–398.
Malinowski, M. (2021). Impact of Air-Flow Rate and Biochar Addition on the Oxygen Concentration in Waste and Emitted Gases During Biostabilization of Undersized Fraction from Municipal Solid Waste. Journal of Ecological Engineering, 22(6), 136–144. https:// doi.org/10.12911/22998993/137362
Manea, E. E., Bumbac, C., Dinu, L. R., Bumbac, M., & Nicolescu, C. M. (2024). Composting as a Sustainable Solution for Organic Solid Waste Management: Current Practices and Potential Improvements. Sustainability (Switzerland), 16(15), 1–25. https://doi. org/10.3390/su16156329
Meenakshi, S., Hiremath, J., Meenakshi, M. H., & Shivaveerakumar, S. (2024). Actinomycetes: Isolation, Cultivation and its Active Biomolecules. In Journal of Pure and Applied Microbiology (Vol. 18, Issue 1, pp. 118–143). https://doi. org/10.22207/JPAM.18.1.48
Moreno Osorio, J. H., Pollio, A., Frunzo, L., Lens, P. N. L., & Esposito, G. (2021). A Review of Microalgal Biofilm Technologies: Definition, Applications, Settings and Analysis. Frontiers in Chemical Engineering, 3(October), 1–23. https://doi.org/10.3389/ fceng.2021.737710
Naranjo-Ortiz, M. A., & Gabaldón, T. (2019). Fungal evolution: diversity, taxonomy and phylogeny of the Fungi. Biological Reviews, 94(6), 2101–2137. https:// doi.org/10.1111/brv.12550
Organo, N. D., Granada, S. M. J. M., Pineda, H. G. S., Sandro, J. M., Nguyen, V. H., & Gummert, M. (2022). Assessing the potential of a Trichoderma-based compost activator to hasten the decomposition of incorporated rice straw. Scientific Reports, 12(1), 1–12. https://doi.org/10.1038/s41598-02103828-1
Pepper, I., & Gentry, T. (2015). Chapter 4Earth Environments. In Environmental Microbiology (pp. 59–88). https://doi.
org/https://doi.org/10.1016/B978-0-12394626-3.00004-1
Prasanna, R., Babu, S., Bidyarani, N., Kumar, A., Triveni, S., Monga, D., Mukherjee, A. K., Kranthi, S., Gokte-Narkhedkar, N., Adak, A., Yadav, K., Nain, L., & Saxena, A. K. (2015). Prospecting cyanobacteria-fortified composts as plant growth promoting and biocontrol agents in cotton. Experimental Agriculture, 51(1), 42–65. https://doi. org/10.1017/S0014479714000143
Prasanna, R., Sood, A., Ratha, S. K., & K. Singh, P. (2013). Cyanobacteria as a “green” option for sustainable agriculture. Cyanobacteria: An Economic Perspective, 145–166. https:// doi.org/10.1002/9781118402238.ch9
Robledo-Mahón, Gómez-Silván, C., Andersen, G. L., Calvo, C., & Aranda, E. (2020). Assessment of bacterial and fungal communities in a full-scale thermophilic sewage sludge composting pile under a semi-permeable cover. Bioresource Technology, 298(October 2019), 122550. https://doi. org/10.1016/j.biortech.2019.122550
Siddiquee, S., Shafawati, S. N., & Naher, L. (2017). Effective composting of empty fruit bunches using potential Trichoderma strains. Biotechnology Reports, 13, 1–7. https://doi. org/10.1016/j.btre.2016.11.001
Silva, G. da C., Kitano, I. T., Ribeiro, I. A. de F., & Lacava, P. T. (2022). The Potential Use of Actinomycetes as Microbial Inoculants and Biopesticides in Agriculture. Frontiers in Soil Science, 2(February), 1–20. https://doi. org/10.3389/fsoil.2022.833181
Silva, P. H. V., Souza, A. G. V., de Araujo, L. D., Frezarin, E. T., de Souza, G. V. L., da Silveira, C. M., & Rigobelo, E. C. (2023). Trichoderma harzianum and Bacillus subtilis in Association with Rock Powder for the Initial Development of Maize Plants. Agronomy, 13(3), 1–15. https:// doi.org/10.3390/agronomy13030872
Singh, J. S., Kumar, A., Rai, A. N., & Singh, D. P. (2016). Cyanobacteria: A precious bio-resource in agriculture, ecosystem, and environmental sustainability. Frontiers in Microbiology, 7(APR), 1–19. https://doi.org/10.3389/ fmicb.2016.00529
Song, X., Bo, Y., Feng, Y., Tan, Y., Zhou, C., Yan, X., Ruan, R., Xu, Q., & Cheng, P. (2022). Potential applications for multifunctional microalgae in soil improvement. Frontiers in Environmental Science, 10(October), 1–10. https://doi.org/10.3389/ fenvs.2022.1035332
Stegenta-Dąbrowska, S., Sobieraj, K., Rosik, J., Sidełko, R., Valentin, M., & Białowiec, A. (2022). The Development of Anammox and Chloroflexi Bacteria during the Composting of Sewage Sludge. Sustainability (Switzerland), 14(16). https://doi.org/10.3390/ su141610248
Suárez-Estrella, F., Arcos-Nievas, M. A., López, M. J., Vargas-García, M. C., & Moreno, J. (2013). Biological control of plant pathogens by microorganisms isolated from agro-industrial composts. Biological Control, 67(3), 509–515. https://doi.org/10.1016/j. biocontrol.2013.10.008
Sun, B., Gu, L., Bao, L., Zhang, S., Wei, Y., Bai, Z., Zhuang, G., & Zhuang, X. (2020). Application of biofertilizer containing Bacillus subtilis reduced the nitrogen loss in agricultural soil. Soil Biology and Biochemistry, 148(June), 107911. https://doi.org/10.1016/j. soilbio.2020.107911
Sun, S., Abdellah, Y. A. Y., Miao, L., Wu, B., Ma, T., Wang, Y., Zang, H., Zhao, X., & Li, C. (2022). Impact of microbial inoculants combined with humic acid on the fate of estrogens during pig manure composting under low-temperature conditions. Journal of Hazardous Materials, 424(PD), 127713. https://doi. org/10.1016/j.jhazmat.2021.127713
Thaha, A. R., Umrah, U., Asrul, A., Rahim, A., Fajra, F., & Nurzakia, N. (2020). The role of local isolates of Trichoderma sp. as a decomposer in the substrate of cacao pod rind (Theobroma cacao L.). AIMS Agriculture and Food, 5(4), 825–834. https://doi.org/10.3934/ agrfood.2020.4.825
Tyagi, S., Kumar, V., Singh, J., Teotia, P., Bisht, S., & Sharma, S. (2014). Bioremediation of pulp and paper mill effluent by dominant aboriginal microbes and their consortium. International Journal of Environmental Research, 8(3), 561–568.
Van Fan, Y., Lee, C. T., Ho, C. S., Klemeš, J. J., Wahab, R. A., Chua, L. S., & Sarmidi, M. R. (2017). Evaluation of microbial inoculation technology for composting. Chemical Engineering Transactions, 56(January), 433–438. https://doi.org/10.3303/CET1756073
Voběrková, S., Vaverková, M. D., Burešová, A., Adamcová, D., Vršanská, M., Kynický, J., Brtnický, M., & Adam, V. (2017). Effect of inoculation with whiterot fungi and fungal consortium on the composting efficiency of municipal solid waste. Waste Management, 61, 157–164. https://doi.org/10.1016/j. wasman.2016.12.039
Wan, L., Wang, X., Cong, C., Li, J., Xu, Y., Li, X., Hou, F., Wu, Y., & Wang, L. (2020). Effect of inoculating microorganisms in chicken manure composting with maize straw. Bioresource Technology, 301(November 2019), 122730. https://doi.org/10.1016/j. biortech.2019.122730
Wang, Y., & Husain, T. (2015). Use of bluegreen algae: to improve the chemial quality of municpal solid waste compost. The Harris Centre Memorial University. http://research.library.mun. ca/id/eprint/11582
Wichuk, K. M., & McCartney, D. (2010). Compost stability and maturity evaluation - a literature review.
Canadian Journal of Civil Engineering, 37(11), 1505–1523. https://doi. org/10.1139/L10-101
Xu, J., Jiang, Z., Li, M., & Li, Q. (2019). A compost-derived thermophilic microbial consortium enhances the humification process and alters the microbial diversity during composting. Journal of Environmental Management, 243(May), 240–249. https://doi. org/10.1016/j.jenvman.2019.05.008
Xu, M., Yang, M., Sun, H., Meng, J., Li, Y., Gao, M., Wang, Q., & Wu, C. (2022). Role of multistage inoculation on the cocomposting of food waste and biogas residue. Bioresource Technology, 361(July), 127681. https://doi. org/10.1016/j.biortech.2022.127681
Zhang, J., Zeng, G., Chen, Y., Liang, J., Zhang, C., Huang, B., Sun, W., Chen, M., Yu, M., Huang, H., & Zhu, Y. (2014). Phanerochaete chrysosporium inoculation shapes the indigenous fungal communities during agricultural waste composting. Biodegradation, 25(5), 669–680. https://doi.org/10.1007/ s10532-014-9690-5
Zhao, Y., Zhao, Y., Zhang, Z., Wei, Y., Wang, H., Lu, Q., Li, Y., & Wei, Z. (2017). Effect of thermo-tolerant actinomycetes inoculation on cellulose degradation and the formation of humic substances during composting. Waste Management, 68, 64–73. https://doi. org/10.1016/j.wasman.2017.06.022
Zin, N. A., & Badaluddin, N. A. (2020). Biological functions of Trichoderma spp. for agriculture applications. Annals of Agricultural Sciences, 65(2), 168–178. https://doi.org/10.1016/j. aoas.2020.09.003

3. Obtención de microorganismos potenciales para el compostaje
La obtención de microorganismos es un paso fundamental para su inoculación en el compostaje. En este capítulo se detallan diversas metodologías que permiten llevar a cabo la inoculación de microorganismos efectivos para mejorar la calidad del compostaje.
3.1. Bioprospección
La bioprospección microbiana es la búsqueda de microorganismos en diferentes ambientes naturales, incluidos aquellos sometidos a condiciones extremas (Nabil et al. 2022). Su función principal radica en encontrar especies o genotipos de microrganismos potencialmente capaces de cumplir con diversas funciones ecológicas. Lo que se pretende con la bioprospección es encontrar organismos que presenten nuevas rutas metabólicas, producción de enzimas con capacidad de degradar compuestos, y productos catalizados. Al utilizar estos inóculos, se enriquece el compost y se convierte en un producto óptimo para la agricultura sostenible (Becker & Wittmann, 2020; Nambisan, 2017).
Este proceso de bioprospección manejado técnicamente incluye diversos pasos que van desde la identificación de zonas geográficas, toma de las muestras, identificación, aislamiento, métodos de cultivo, la evaluación de la actividad y su implementación en el ámbito agrícola o industrial (Figura 23) (Mgbechidinma et al. 2024). El paso final sería llegar a inocularlos en un sistema de compostaje que pueda, en cierta medida contribuir a la agricultura sostenible.
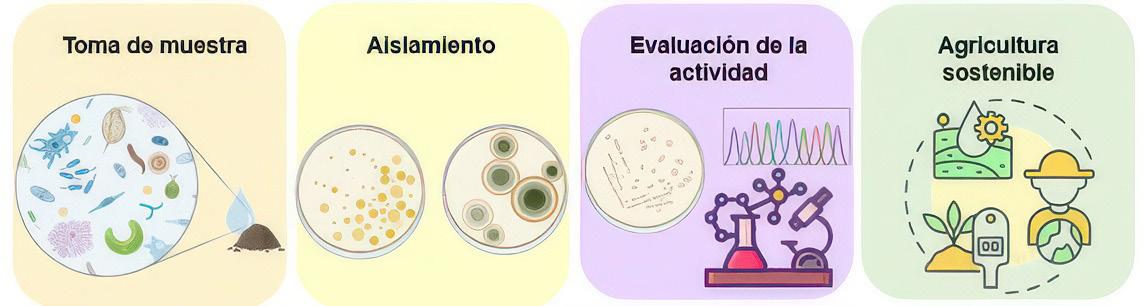
Figura 23
Proceso de bioprospección para la obtención de microorganismos benéficos para el proceso de compostaje.
-Antonie van Leewenhoek (1680)
3.1.1.
Identificación de la zona geográfica de estudio
Es el primer paso en la bioprospección, debido a que la diversidad y las propiedades únicas de cada ecosistema influyen directamente en el tipo y la funcionalidad de los microorganismos que se pueden encontrar. Los beneficios derivados de la bioprospección se han originado a partir de una diversidad tan extensa de organismos y ecosistemas a nivel global como, bosques nativos o no perturbados, fincas agrícolas, remanentes boscosos o inclusive zonas urbanas, estiércol, y cuerpos de agua (Figura 24) (Al-Dhabi et al., 2019; Gowen & Fong, 2011; Nambisan, 2017). Comprenden una gama inesperada de productos, incluyendo compuestos bioactivos, genes de interés, rutas metabólicas, estructuras moleculares, materiales innovadores y patrones conductuales adaptativos (AlDhabi et al. 2019; Nabil et al. 2022).
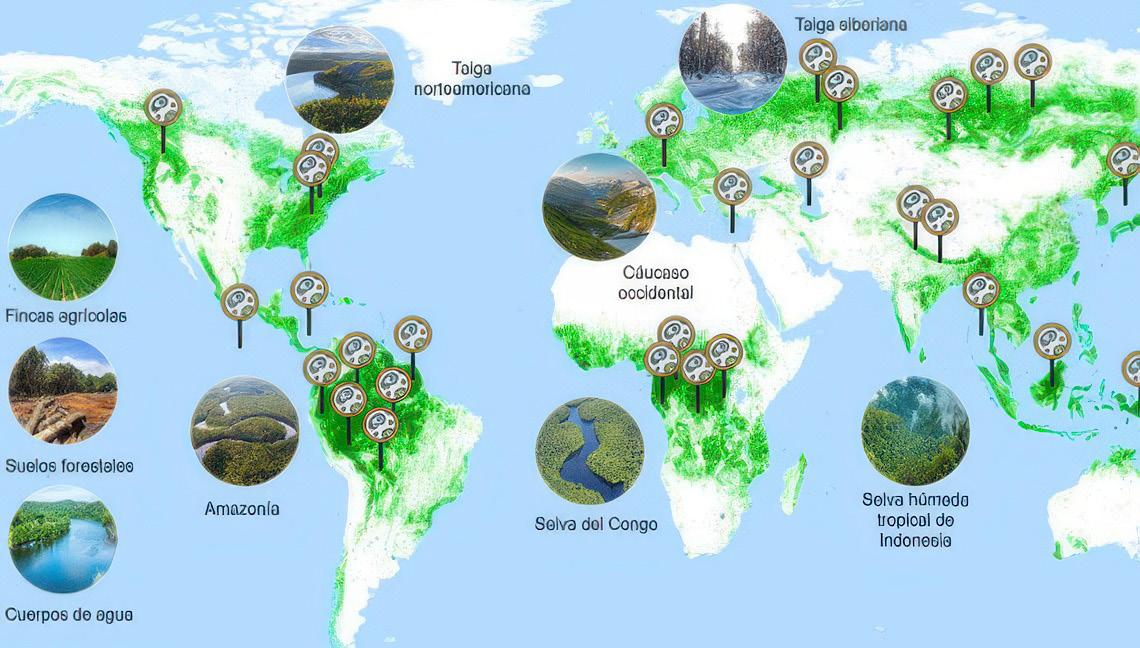
Figura 24
Mapa global de áreas clave para la bioprospección, destacando hábitats ricos en biodiversidad con potencial para descubrimientos científicos e industriales.
Una de las principales zonas de identificación de microorganismos son los bosques no perturbados, puesto que albergan una biodiversidad microbiana rica y poco explorada, debido a su aislamiento y al bajo impacto humano. Estos microorganismos suelen presentar adaptaciones únicas y pueden producir compuestos bioactivos de alto valor, tales como antibióticos, anti fúngicos, y antioxidantes (Gowen & Fong, 2011; Nambisan, 2017). Los ecosistemas acuáticos como ríos y lagos también son hábitats de microorganismos con adaptaciones a condiciones de humedad y, en muchos casos, a niveles extremos de pH, salinidad o temperatura. Los compuestos bioactivos de estos organismos incluyen enzimas termoestables, halotolerantes y con un elevado potencial de aplicación en industrias como la alimentaria, farmacéutica y biotecnológica (Davidson & Niepa, 2022; Nambisan, 2017; Nawy, 2017).
3.2. Métodos de cultivo de microorganismos
Para el cultivo de microorganismos se utilizan técnicas dependientes de cultivo como la técnica de enriquecimiento. Esta técnica se define como un cultivo in vitro donde se trata
de replicar las condiciones ambientales y los recursos de un nicho ecológico en el que habita el microorganismo/s de interés para favorecer su crecimiento selectivo (Davidson & Niepa, 2022; Franco-Duarte et al., 2019). Para evitar sesgos en esta técnica, se recomienda realizar diluciones de la muestra a analizar previo al enriquecimiento. Esto permite eliminar los microorganismos indeseados que presentan un crecimiento rápido, permitiendo el desarrollo de otros más lentos (Madigan et al. 2015).
Por otro lado, se destaca la técnica de aislamiento que se define como un cultivo axénico o denominado cultivo puro, el cual se basa en el crecimiento de una sola clase de microorganismos. Esta técnica se puede llevar a cabo mediante la siembra en placa por estrías, la dilución en agar y la dilución en líquido (Madigan et al. 2015; Hanišáková et al. 2022).
De este modo, se destacan los medios de cultivo óptimos para cada tipo de microorganismo. Estos son geles o líquidos diseñados para el entorno natural donde comúnmente se desarrollan los actinomicetos, bacterias y hongos. Los caldos nutritivos y las placas de agar son los medios de crecimiento más habituales para los microorganismos. Sin embargo, algunos requieren medios especiales para su crecimiento (Tabla 11).
Tabla 11
Medios de cultivo utilizados para el crecimiento de los diferentes microorganismos.
Fuente: Homthong et al., 2016; Ismail et al., 2021; Kheiralla et al., 2013; Meenakshi et al., 2024.
Dentro de los caldos nutritivos, se desataca el Agar Triptona Soja (TSA), un medio para el aislamiento y cultivo de microrganismos exigentes y poco exigentes. El medio presenta un pH de 7.3 ± 0.2 a 25°C, contiene digestos enzimáticos de caseína y soja, que aportan aminoácidos y otras sustancias nitrogenadas, y el cloruro de sodio (NaCl) que mantiene el equilibrio osmótico, lo que lo convierte en un medio nutritivo para una variedad de organismos como Bacillus subtilis, Aspergillus brasiliensis, y Pseudomona aeruginosa (Merck KGaA 2018; Valadão et al. 2023).
Por otra parte, se encuentra el Agar Nutriente, medio general para el crecimiento de bacterias, contiene extracto de levadura que proporciona compuesto de N, C y vitaminas. Tiene un pH de 5.5 ± 0.2 a 25°C (Saffari et al. 2017; Ismail et al. 2021).
Para el aislamiento y cultivo de hongos, actinomicetos y levaduras, se utiliza el agar Dextrosa Sabouraud (SDA), que presenta un pH de 5.6 ± 0.2 a 25°C (Scognamiglio et al. 2010; Mentese et al. 2017). Este medio aísla selectivamente hongos de muestras ambientales como el aire y el suelo, mantiene cultivos fúngicos puros y cultiva hongos para distinguir e identificar diferentes especies. En este medio, la peptona aporta compuestos nitrogenados y la dextrosa es la fuente de energía.
Un medio alternativo es el Agar Papa Dextrosa (PDA), medio de cultivo ampliamente utilizado en microbiología para el aislamiento, cultivo y mantenimiento de hongos filamentosos y levaduras (Scognamiglio et al. 2010; Mentese et al. 2017). Presenta un pH de 5.6 ± 0.2, ligeramente ácido, inhibiendo el crecimiento de bacterias. Permite el estudio de la morfología colonial, la producción de esporas y la investigación en biocontrol (Homthong et al., 2016; Mentese et al., 2017).
En el caso de los actinomicetos, se lleva a cabo en medios selectivos mediante técnicas de dilución seriada y siembra en diferentes tipos de medios tales como: Agar AlmidónCaseína, Agar Glucosa-Levadura, agar para aislamiento de actinomicetos y Agar Vitamina-Carbón suplementado con cantidades considerables de agentes antibacterianos y antifúngicos (Cuesta et al. 2012; Al-Dhabi et al. 2019; Gopalakrishnan et al. 2020). Aún más específico, para el aislamiento de actinomicetos del suelo de montaña, se hace uso del Agar vitamina-Ácido Húmico con pH variado, donde el ácido húmico sirve como fuente de carbono y nitrógeno para el crecimiento de microorganismos (Braz et al. 2009; Aksoy et al. 2012; Meenakshi et al. 2024).
3.3.
Métodos de identificación
Existen diversos métodos para la identificación de microorganismos, que van desde la microscopia hasta la secuenciación de ADN. La microscopía sirve para la caracterización de los microorganismos, mientras que, la secuenciación de ADN es utilizada para medir la biodiversidad y su potencial metabólico mediante técnicas moleculares.
3.3.1. Microscopía
Esta técnica permite la identificación de los microorganismos mediante la observación de sus características morfológicas y para organismos en estado viable pero no cultivable (VBNC) en una muestra natural. El resultado de la microscopia permite la visualización de la forma, la motilidad y su clasificación (Franco-Duarte et al. 2019). En general se utiliza los tipos de tinción (Tabla 12).
Tabla 12
Tipos de tinción para la identificación de los microorganismos.
Para bacterias se utiliza la prueba de Tinción de Gram que proporciona la identificación y clasificación de bacterias mediante su visualización (Figura 25). El resultado de este método diferencia a las Gram positivas que se tiñen de color púrpura y las Gram negativas de color rosa (Becerra et al., 2016; Smith & Hussey, 2016).
Además, la forma, la disposición y el tamaño del organismo pueden proporcionar más información para ayudar a identificar el organismo. Las formas comunes que se ven en la tinción de Gram incluyen cocos, que se parecen a esferas; bacilos, que se parecen a bastoncillos; o cocobacilos, que son una combinación de los dos. Los cocos pueden estar dispuestos en patrones, como racimos o cadenas (Madigan et al., 2015; Smith & Hussey, 2016; Villar et al., 2016).
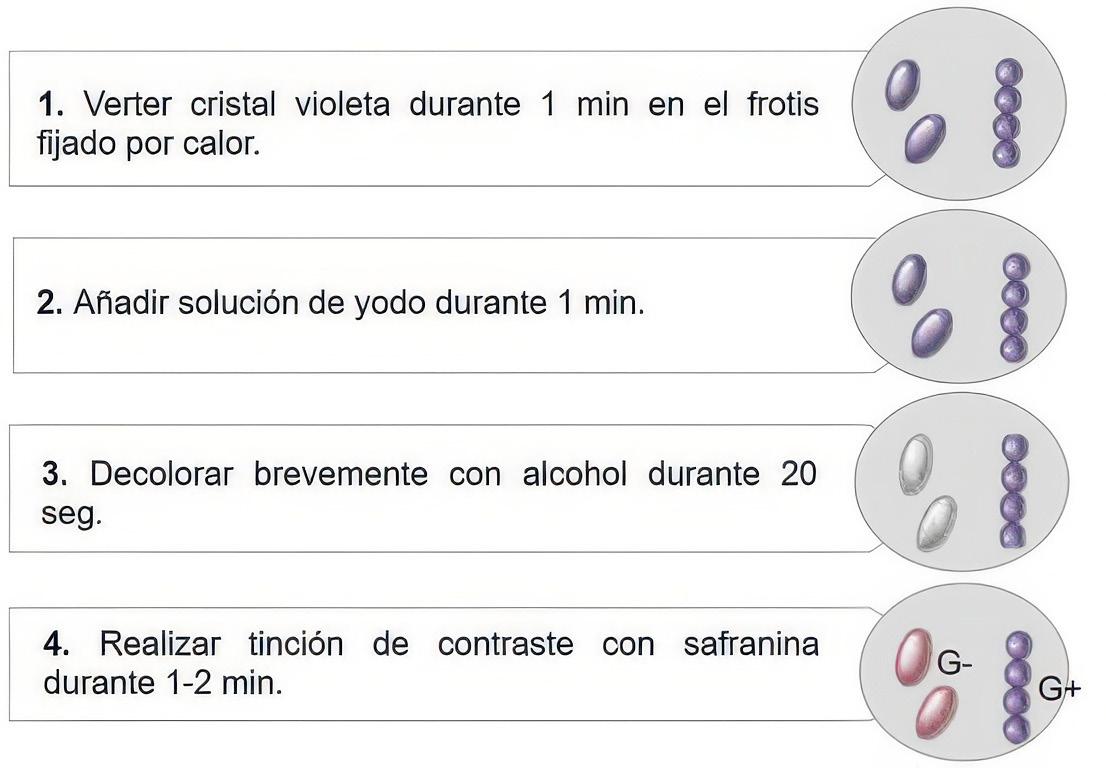
Figura 25
Proceso de Tinción de Gram para la identificación de bacterias.
Otro método es la tinción diferencial, que se usa para la identificación y clasificación de mico bacterias y actinomicetos, donde las bacterias ácido resistentes conservan el colorante primario (rosa o rojo) y los microorganismos restantes son decolorados por el
ácido y toman el color azul (Figura 26) (Cuesta et al. 2012; Madigan et al. 2015; Meenakshi et al. 2024).
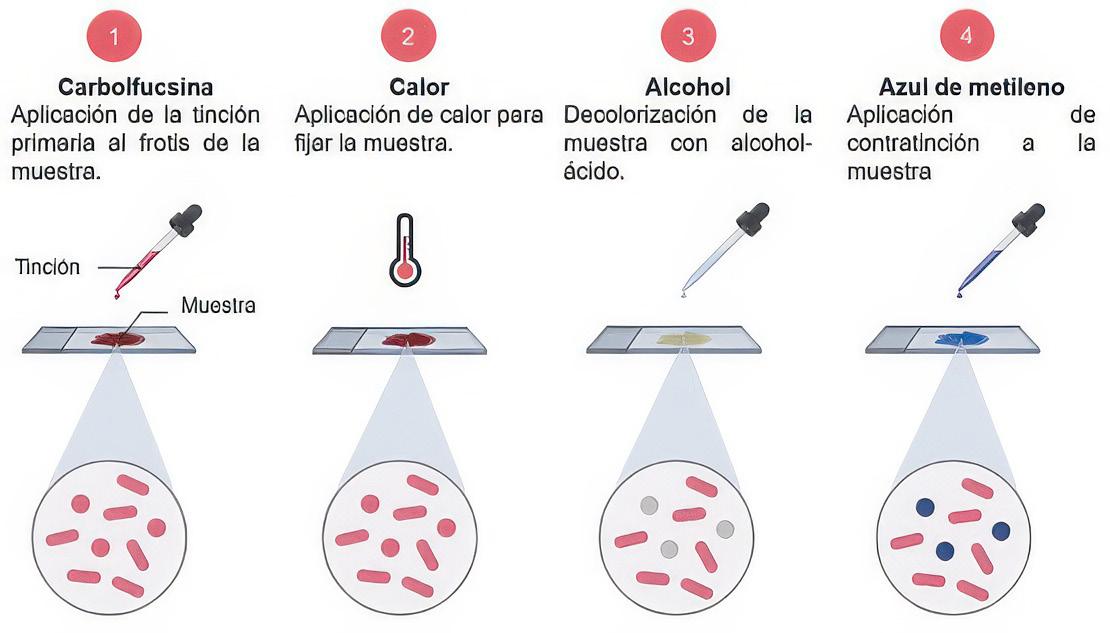
Figura 26
Proceso de Tinción Diferencial para la identificación de actinomicetos y hongos. Fuente: Madigan et al. 2015.
3.3.2. Técnicas moleculares
El uso de herramientas como la Reacción en Cadena de la Polimerasa (PCR) y secuenciación de ADN permite la identificación de microorganismos a nivel genético (Tabla 13) (Madigan et al. 2015).
Tabla 13
Técnicas moleculares para la identificación de los microorganismos.
Fuente: Rath et al., (2022)

Reacción en cadena de la polimerasa (PCR)
Es una técnica de amplificación de ácidos nucleicos que se utiliza para desnaturalizar y renaturalizar segmentos cortos de secuencias de ácido desoxirribonucleico (ADN) o ácido ribonucleico (ARN) utilizando la enzima ADN polimerasa I, y un aislado de Thermus aquaticus, conocido como ADN Taq (Madigan et al. 2015; Saffari et al. 2017; Franco-Duarte et al. 2019). El procedimiento se detalla en la Figura 27. Durante cada ciclo de amplificación la cantidad de ADN diana original se duplica, lo que provoca un aumento exponencial en el ADN. En la práctica se realizan normalmente de 20 a 30 ciclos, lo que produce un aumento en la secuencia diana de 106 a 109 veces (Madigan et al. 2015).
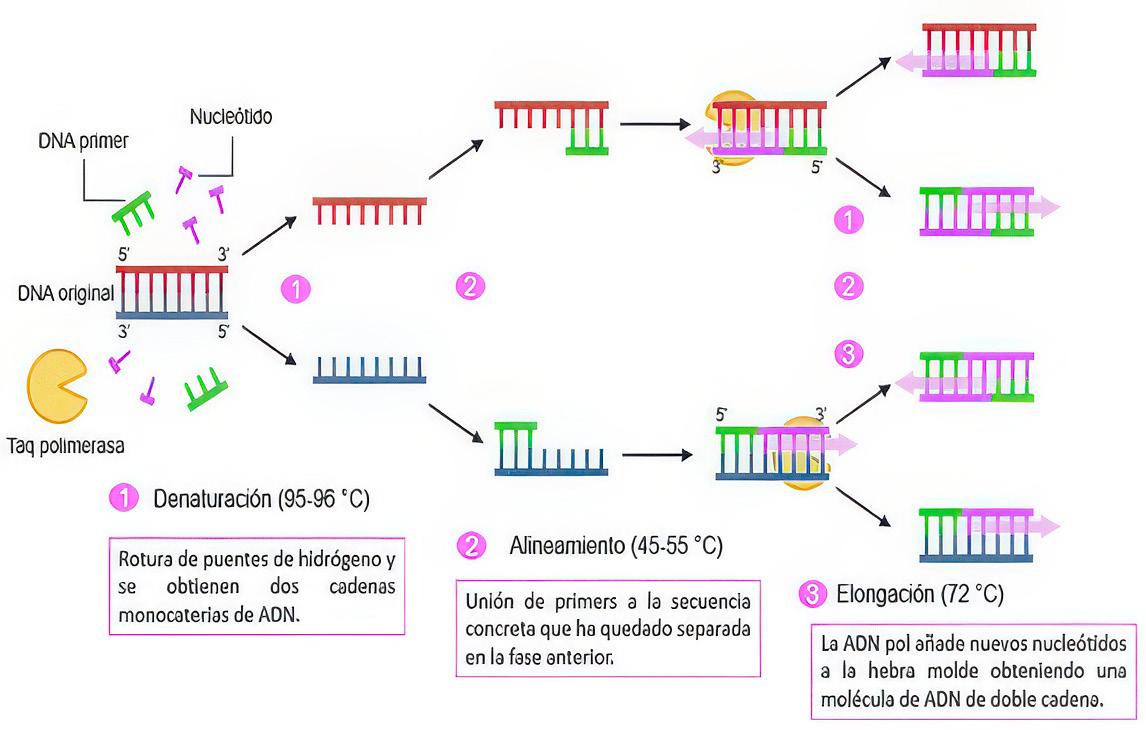
Figura 27
Proceso de la Reacción en Cadena de la Polimerasa (PCR).
La técnica PCR permite amplificar el gen de la subunidad menor ribosomal (SSU) rRNA que proporcionan información filogenética, facilitando la identificación de microorganismos difíciles de cultivar por los métodos convencionales (Madigan et al. 2015). Además, se puede hacer uso de genes que codifican enzimas con funciones metabólicas únicas para una especie o un grupo de especies (Tabla 14).
Tabla 14
Genes de uso frecuente para evaluar procesos microbianos específicos usando PCR.
Fuente: Madigan et al., (2015).

Electroforesis en gel en gradiente desnaturalizante (DGGE)
Es una técnica utilizada para separar fragmentos de ADN de igual tamaño, pero con diferentes secuencias de bases que emplea un gel que contiene un gradiente de sustancias desnaturalizantes, como urea y formamida, afectando la estabilidad del ADN (Aydin et al., 2015; Wang et al., 2011). A medida que los fragmentos de ADN migran a través del gel, aquellos con diferentes secuencias de bases se desnaturalizan a diferentes puntos del gradiente, lo que resulta en la separación de los fragmentos (Figura 28) (Aydin et al. 2015).
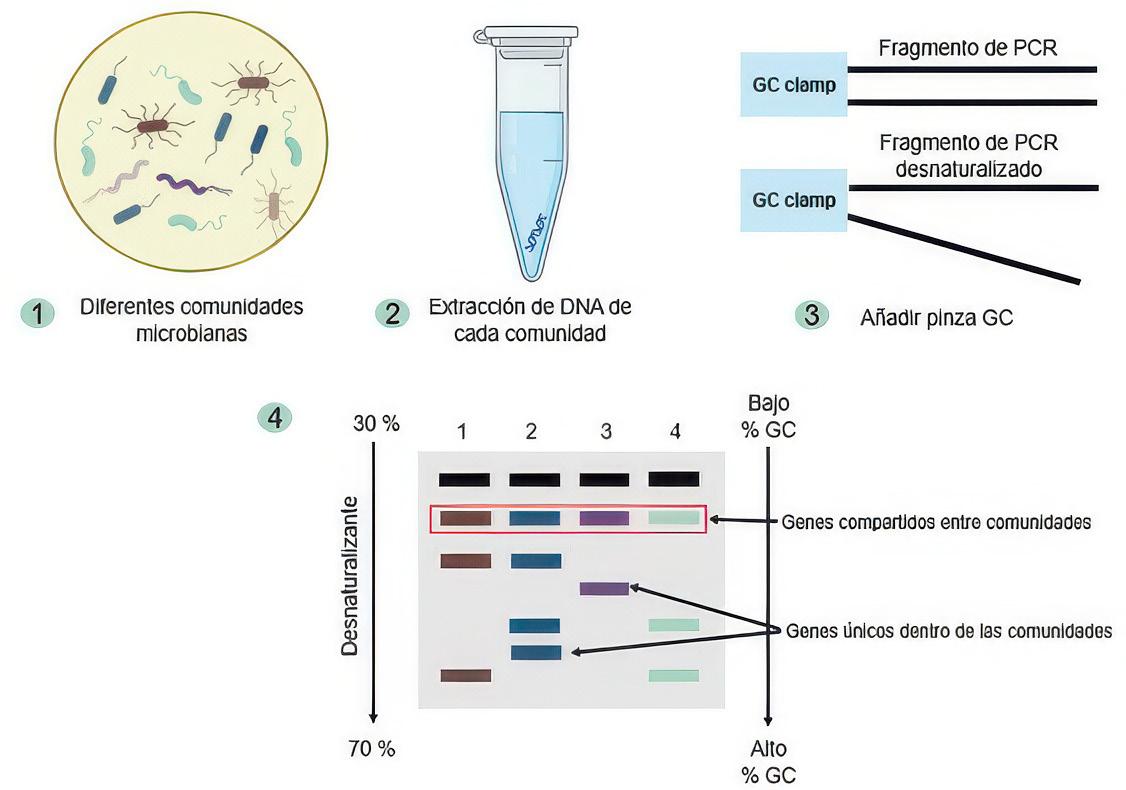
Figura 28
Proceso de electroforesis en gel en gradiente desnaturalizante para la identificación de microorganismos. Fuente: Aydin et al., (2015).

Secuenciación
Es una técnica general de laboratorio empleado para identificar con precisión la secuencia de nucleótidos, o bases, en una molécula de ADN. Esta secuencia de bases (A: adenina, T: timina, C: citosina y G: guanina) contiene la información biológica esencial para el desarrollo y funcionamiento celular (Adams, 2025), además, permite la comparación con regiones homólogas lo que permite inferir relaciones en estudios filogenéticos (Simpson 2010).
La secuenciación de Sanger es un método de primera generación donde la secuencia se determina mediante la producción de copias del ADN original de cadena sencilla con la intervención de la enzima ADN polimerasa, que añade trifosfatos de desoxirribonucleótidos (Figura 29). Además, utiliza didesoxinucleótidos marcados con fluorescencia que terminan la cadena de ADN durante la síntesis (Madigan et al., 2015; Park & Kim, 2016).
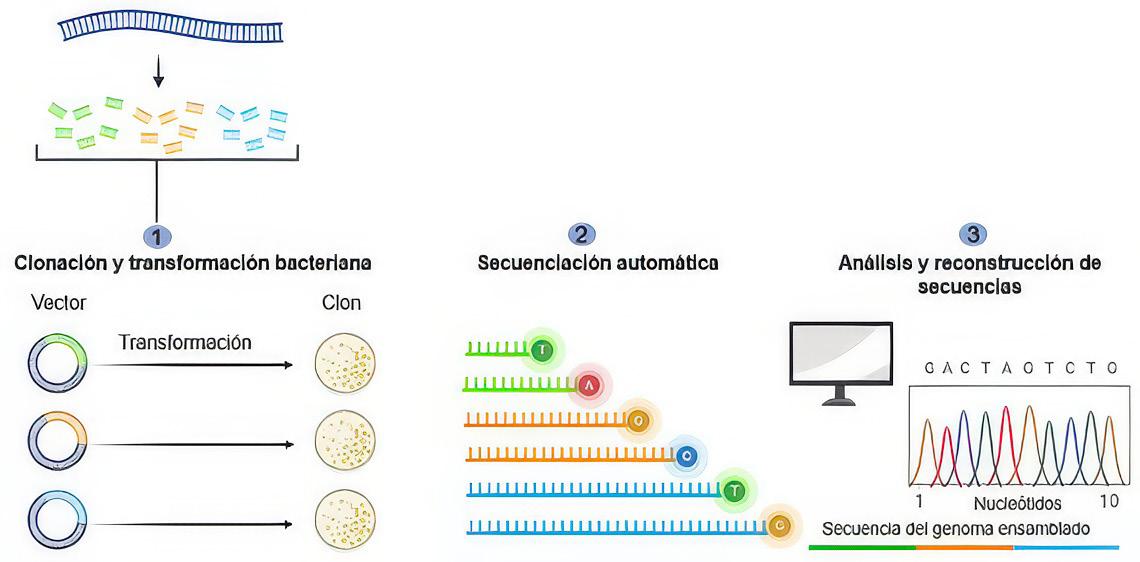
La Secuenciación de Next Generation (NGS) es una técnica molecular que se basa en la secuenciación de ácidos nucleicos y la detección de mutaciones. Se destaca debido a la capacidad de secuenciar miles de genes o el genoma completo en un periodo de tiempo corto. Además, no requiere un procedimiento de clonación bacteriana (Figura 30). Permite secuenciar comunidades microbianas completas mediante estudios metagenómicos (Park & Kim, 2016; Qin, 2019).
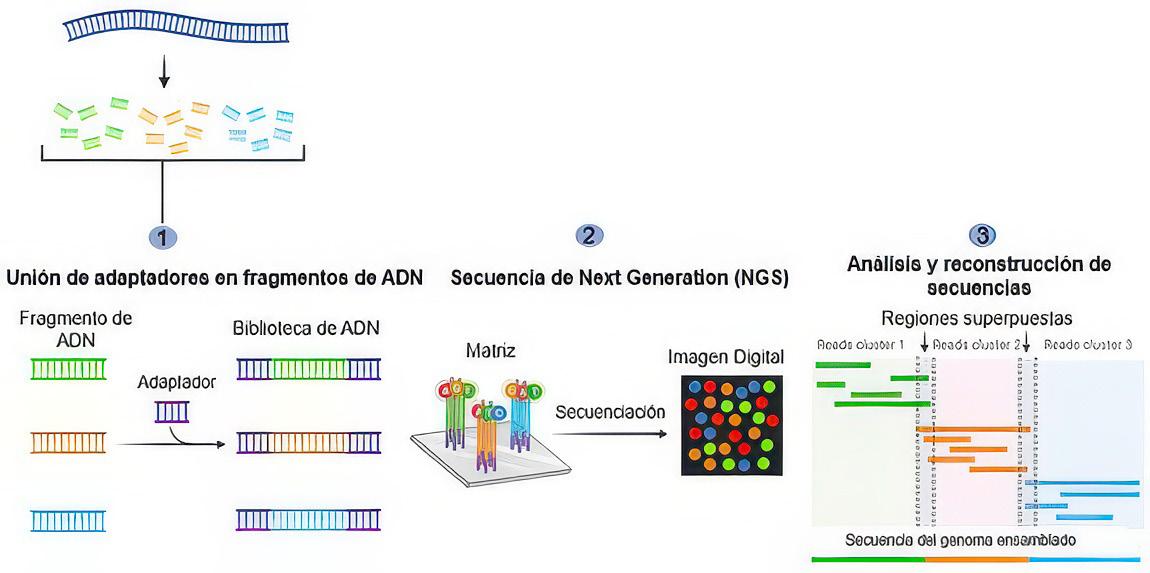
Figura 29
Proceso de la Secuenciación de Sanger. Fuente: Park & Kim, (2016).
Figura 30
Proceso de Secuenciación de Next Generation. Fuente: Park & Kim, (2016).
BIBLIOGRAFÍA
Adams, D. (2025). ADN sequencing. National Human Genome Research Institute. https://www.genome.gov/geneticsglossary/DNA-Sequencing
Aksoy, S. Ç., Uzel, A., & Hameş Kocabaş, E. E. (2012). Extracellular serine proteases produced by Thermoactinomyces strains from hot springs and soils of West Anatolia. Annals of Microbiology, 62(2), 483–492. https://doi. org/10.1007/s13213-011-0280-z
Al-Dhabi, N. A., Mohammed Ghilan, A. K., Esmail, G. A., Valan Arasu, M., Duraipandiyan, V., & Ponmurugan, K. (2019). Bioactivity assessment of the Saudi Arabian Marine Streptomyces sp. Al-Dhabi-90, metabolic profiling and its in vitro inhibitory property against multidrug resistant and extended-spectrum beta-lactamase clinical bacterial pathogens. Journal of Infection and Public Health, 12(4), 549–556. https://doi.org/10.1016/j. jiph.2019.01.065
Aydin, S., Shahi, A., Ozbayram, E. G., Ince, B., & Ince, O. (2015). Use of PCRDGGE based molecular methods to assessment of microbial diversity during anaerobic treatment of antibiotic combinations. Bioresource Technology, 192, 735–740. https://doi. org/10.1016/j.biortech.2015.05.086
Becerra, S. C., Roy, D. C., Sanchez, C. J., Christy, R. J., & Burmeister, D. M. (2016). An optimized staining technique for the detection of Gram positive and Gram negative bacteria within tissue. BMC Research Notes, 9(1), 1–10. https:// doi.org/10.1186/s13104-016-1902-0
Becker, J., & Wittmann, C. (2020). Microbial production of extremolytes highvalue active ingredients for nutrition, health care, and well-being. Current Opinion in Biotechnology, 65, 118–128. https://doi.org/10.1016/j. copbio.2020.02.010
Braz, S. C. de M., Motta, C. M. de S., Massa,
D. M. de L., Neves, R. P., & Magalhães, O. M. C. (2009). Viability, taxonomic confirmation and enzymatic detection of Acremonium species preserved under mineral oil in the URM Culture Collection. Revista Da Sociedade Brasileira de Medicina Tropical, 42(1), 63–66. https://doi.org/10.1590/s003786822009000100013
Cuesta, G., García-de-la-Fuente, R., Abad, M., & Fornes, F. (2012). Isolation and identification of actinomycetes from a compost-amended soil with potential as biocontrol agents. Journal of Environmental Management, 95(SUPPL.), S280–S284. https://doi. org/10.1016/j.jenvman.2010.11.023
Davidson, S. L., & Niepa, T. H. R. (2022). MicroTechnologies for Assessing Microbial Dynamics in Controlled Environments. Frontiers in Microbiology, 12(January), 1–14. https://doi.org/10.3389/ fmicb.2021.745835
Franco-Duarte, R., Černáková, L., Kadam, S., Kaushik, K. S., Salehi, B., Bevilacqua, A., Corbo, M. R., Antolak, H., DybkaStępień, K., Leszczewicz, M., Tintino, S. R., de Souza, V. C. A., Sharifi-Rad, J., Coutinho, H. D. M., Martins, N., & Rodrigues, C. F. (2019). Advances in chemical and biological methods to identify microorganisms from past to present. Microorganisms, 7(5). https://doi.org/10.3390/ microorganisms7050130
Gopalakrishnan, S., Srinivas, V., & Prasanna, S. L. (2020). Streptomyces. In Beneficial Microbes in Agro-Ecology: Bacteria and Fungi. Elsevier Inc. https://doi. org/10.1016/B978-0-12-8234143.00005-8
Gowen, C. M., & Fong, S. S. (2011). Applications of systems biology towards microbial fuel production. Trends in Microbiology, 19(10), 516–524. https://doi.org/10.1016/j. tim.2011.07.005
Hanišáková, N., Vítězová, M., & Rittmann,
S. K. M. R. (2022). The Historical Development of Cultivation Techniques for Methanogens and Other Strict Anaerobes and Their Application in Modern Microbiology. Microorganisms, 10(2). https://doi.org/10.3390/ microorganisms10020412
Homthong, M., Kubera, A., Srihuttagum, M., & Hongtrakul, V. (2016). Isolation and characterization of chitinase from soil fungi, Paecilomyces sp. Agriculture and Natural Resources, 50(4), 232–242. https://doi.org/10.1016/j. anres.2015.09.005
Ismail, A., Safi, A., Ahmed, A. H., & Mohammed, G. B. (2021). Studies on Seed-Borne Fungi Associated with the Seeds of Three Acacia species by Using Nutrient Agar Test. 3(2), 33–39.
Kheiralla, Z. H., El-Din, S. M. B., Malek, S. M. A., & Aziz, D. H. A. (2013). Optimization of cultural conditions for lignin peroxidase production by Phanerochaete chrysosporium and Pleurotus ostreatus. Academia Journal of Biotechnology, 1(6), 087–095. http:// dx.doi.org/10.15413/ajb.2013.0115
Madigan, M., Martinko, J., Bender, K., Buckley, D., & Stahl, D. (2015). Métodos de estudio en ecología microbiana. In Brock. Biología de los microorganismos (pp. 610–630). Pearson.
Meenakshi, S., Hiremath, J., Meenakshi, M. H., & Shivaveerakumar, S. (2024). Actinomycetes: Isolation, Cultivation and its Active Biomolecules. In Journal of Pure and Applied Microbiology (Vol. 18, Issue 1, pp. 118–143). https://doi. org/10.22207/JPAM.18.1.48
Mentese, S., Otkun, M. T., & Palaz, E. (2017). Comparison of dichloran rose bengal chloramphenicol and Sabouraud dextrose agar with cycloheximide and chloramphenicol for airborne mold sampling. Aerobiologia, 33(2), 211–219. https://doi.org/10.1007/s10453016-9462-2
Merck KGaA. (2018). 22091 Tryptic Soy Agar
(Tryptone Soya Agar, TSA, CASO Agar, Soybean Caseindigest Agar). Lett. Appl. Microbiol, 10, 1–2.
Mgbechidinma, C. L., Akan, O. D., Mgbechidimma, O. M. M., & Wakil, S. M. (2024). Bioprospecting for sustainable and eco-friendly bioproducts: A case study of multienzyme production by soil microbes. Journal of Environmental Chemical Engineering, 12(6), 114340. https://doi. org/10.1016/j.jece.2024.114340
Nabil, R., Chamundeeswari, M., & Tamilarasan, K. (2022). Recent trends in genomic approaches for microbial bioprospecting. In Bioprospecting of Microbial Diversity (pp. 13–26). https:// doi.org/https://doi.org/10.1016/B9780-323-90958-7.00022-4
Nambisan, P. (2017). Biodiversity and Sharing of Biological Resources. An Introduction to Ethical, Safety and Intellectual Property Rights Issues in Biotechnology, 189–209. https:// doi.org/10.1016/b978-0-12-8092316.00008-9
Nawy, T. (2017). Capturing microbial interactions. Nature Methods, 14(1), 35. https://doi.org/10.1038/nmeth.4117
Park, S. T., & Kim, J. (2016). Trends in nextgeneration sequencing and a new era for whole genome sequencing. International Neurourology Journal, 20, 76–83. https://doi.org/10.5213/ inj.1632742.371
Qin, D. (2019). Next-generation sequencing and its clinical application. Cancer Biology and Medicine, 16(1), 4–10. https://doi.org/10.20892/j.issn.20953941.2018.0055
Rath, P. P., Das, K., & Pattanaik, S. (2022). Microbial Activity during Composting and Plant Growth Impact: A Review. Journal of Pure and Applied Microbiology, 16(1), 63–73. https://doi. org/10.22207/JPAM.16.1.53
Saffari, H., Pourbabaee, A. A., Asgharzadeh,
A., & Besharati, H. (2017). Isolation and identification of effective cellulolytic bacteria in composting process from different sources. Archives of Agronomy and Soil Science, 63(3), 297–307. https://doi.org/10.1080/036 50340.2016.1198006
Scognamiglio, T., Zinchuk, R., Gumpeni, P., & Larone, D. H. (2010). Comparison of inhibitory mold agar to sabouraud dextrose agar as a primary medium for isolation of fungi. Journal of Clinical Microbiology, 48(5), 1924–1925. https://doi.org/10.1128/JCM.0181409
Simpson, M. G. (2010). Plant Molecular Systematics. Plant Systematics, 585–601. https://doi.org/10.1016/b978-012-374380-0.50014-2
Smith, A., & Hussey, M. (2016). Gram Stain Protocols. American Society for Microbiology, September 2020, 1–9. https://asm.org/protocols/gram-stainprotocols
Valadão, T. B., da Costa, L. V., Dos Reis, C. M. F., da Silva Braga, L. M. P., Do Nascimento, L. G., de Andrade, J. M., de Miranda, R. V. d. S. L., Mattoso, J. M. V., da Silva, I. B., & Brandão, M. L. L. (2023). Evaluation of the Nutritive Capacity of Soybean Tryptic Agar for Environmental Control in the Pharmaceutical Industry. Revista Cubana de Farmacia, 56(4), 1–18.
Villar, I., Alves, D., Garrido, J., & Mato, S. (2016). Evolution of microbial dynamics during the maturation phase of the composting of different types of waste. Waste Management, 54, 83–92. https://doi.org/10.1016/j. wasman.2016.05.011
Wang, W., Yan, L., Cui, Z., Gao, Y., Wang, Y., & Jing, R. (2011). Characterization of a microbial consortium capable of degrading lignocellulose. Bioresource Technology, 102(19), 9321–9324. https://doi.org/10.1016/j. biortech.2011.07.065

4. Inoculación de microorganismos benéficos en el compostaje
La inoculación de microrganismos en el compostaje puede activar la biodegradación de la materia orgánica, acelerar la mineralización, incrementar la actividad de las enzimas microbianas y mejorar la calidad del compost (Kannan & Kallapiran, 2023; Xu et al., 2019).
En la Tabla 15, se observa algunos de los microorganismos que normalmente son utilizados para mejorar el proceso de compostaje.
Tabla 15
Efectos positivos en cultivos al hacer uso de inóculos microbianos en el proceso de compostaje.
Fuente: Aguilar-Paredes et al., (2023).
Para evitar la competencia entre la inoculación y los microorganismos nativos, se debe agregar el inóculo microbiano en la primera etapa, segunda etapa o en múltiples etapas del proceso de compostaje (Liu et al., 2023; Xi et al., 2015). Además, se ha afirmado que la mejor manera de resolver el problema de la competencia con los microorganismos nativos de la pila de compostaje es agregar un consorcio microbiano (Li et al., 2018; Rastogi et al., 2020).
En las siguientes secciones, se abordan la inoculación de diferentes tipos de actinomicetos, hongos, bacterias y la producción de enzimas. Si bien se definen las condiciones óptimas para la inoculación, también se establecen los tipos de enzimas producidas por estos organismos, las cuales desempeñan un papel clave en la degradación de la MO. Además, se explorarán los usos potenciales en la mejora del compost, así como la fase del compostaje en la que su inoculación resulta más efectiva.
INOCULACIÓN DE ACTINOMICETOS
4.1. Inoculación de actinomicetos
4.1.1. Streptomyces griseoruben

Es una bacteria Gram positiva perteneciente a la familia Streptomycetaceae, conocida por su capacidad de producir esporas aéreas y de sintetizar diversos compuestos bioactivos, como antibióticos y enzimas hidrolíticas (Suárez-Estrella et al. 2013; De Corato et al. 2016). Su crecimiento se caracteriza por la producción de un micelio filamentoso y pigmentos que pueden ser de color gris o rosado (Kotrbová et al. 2022).

Clasificación taxonómica
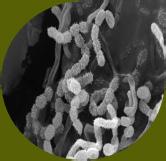
Reino Bacteria
Filo Actinomycetota
Clase Actinomycetes
Orden Kitasatosporales
Familia Streptomycetaceae
Género Streptomyces
Especie Streptomyces griseorubens
ID: 66897, NCBI.

Producción de enzimas
Los actinomicetos pertenecientes al género Streptomyces se caracterizan por la producción de antibióticos, compuestos bioactivos y enzimas extracelulares útiles para las industrias agrícolas, biotecnológicas y farmacéuticas (Beroigui & Errachidi, 2023). Entre ellos, se
encuentra Streptomyces griseorubens que se destaca por la fabricación de enzimas degradadoras de la pared celular tales como: celulosa, hemicelulasa, quitinasa y xilasa (Tabla 16) (Prasad et al. 2013; Rashad et al. 2017). Estas enzimas inhiben la acción de los microorganismos patógenos, intervienen en el ciclo de nutrientes, promueven el crecimiento de las plantas y están involucrados en la degradación primaria de la MO (Ayswaria et al. 2020; Al Hamad et al. 2021).
Tabla 16
Enzimas secretadas por el actinomiceto Streptomyces griseorubens.

Beneficios para el compostaje
La inoculación de S. griseorubens activa la producción de enzimas como CMCase, xilanasa y lignina peroxidasa, logrando mayores tasas de degradación de la MO, aumenta la temperatura de compostaje permitiendo una mejor desactivación de los patógenos presentes, obteniendo así, altos índices de maduración y elevado contenido de N, P y K en el producto final (Beroigui & Errachidi, 2023; Chi et al., 2020; Feng et al., 2021).
En cuanto a la influencia en la microbiota del suelo, se ha evidenciado que aumenta la abundancia relativa de Actinobacteria en la fase termófila y Firmicutes en fases de enfriamiento y maduración (Cuesta et al. 2012). A nivel de género, aumenta la abundancia de bacterias degradadoras de MO como Virgibacillus y hongos degradadores de lignocelulosa como Chaetomium y Melanocarpus; así mismo, disminuye la abundancia de hongos patógenos como Geosmithia y Acremonium (Chi et al. 2020; Feng et al. 2021).
Además, se destaca su potencial antifúngico contra Rhizoctonia solani (agente causal de la pudrición radicular en algunos cultivos) por la actividad proteolítica. También ha sido demostrado que estos microorganismos controlan Fusarium oxysporum f. sp. lycopersici, causante de la enfermedad del marchitamiento por Fusarium del tomate (Al-Askar et al. 2015).

Fase de inoculación en el compostaje
La inoculación de S. griseorubens se recomienda en la fase de termófila del proceso de compostaje, que es la etapa en la que se alcanzan temperaturas elevadas (generalmente entre 45-65°C). Durante esta fase, la actividad enzimática se ve que alcanza su máximo rendimiento, y la temperatura facilita la descomposición acelerada de compuestos complejos (Feng et al. 2021).

Condiciones de cultivo
Para el aislamiento de S. griseorubens de la rizósfera del suelo se utiliza la técnica estándar de placa de dilución seriada en Agar Almidón-Caseína (SCA) en un pH neutro de 7 a 30 °C en un agitador rotatorio (160 rpm) durante 5 días. Posteriormente, las colonias purificadas de actinomicetos se deben mantener en el medio del Proyecto Internacional Streptomyces (ISP-2) (Beroigui & Errachidi, 2023; Meenakshi et al., 2024).
EJEMPLO 1

INOCULACIÓN DE HONGOS
4.2. Inoculación de hongos
4.2.1. Acremonium alternarum
Es un hongo filamentoso que pertenece al filo Ascomycota y es conocido por su capacidad para colonizar residuos vegetales en descomposición. Este hongo produce conidios pequeños y esporas que se propagan fácilmente en el aire. Puede desempeñar un papel en la degradación de materia orgánica (Feng et al., 2021; Li et al., 2018).

Clasificación taxonómica
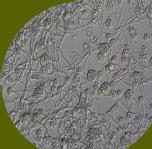
• Producción de enzimas
Reino Fungi
Filo Ascomycota
Clase Sordariomycetes
Orden Hypocreales
Familia Hypocreaceae
Género Acremonium
Especie
Acremonium alternatum
ID: 45275, NCBI.
A. alternatum se caracteriza por la producción de celulasas, pectinasas y quitinasas (Tabla 17), importantes para descomponer celulosa y otros polisacáridos complejos presentes en los restos vegetales (Fujii et al., 2009; Li et al., 2018).
Tabla 17
Enzimas secretadas por el hongo Acremonium alternatum

Beneficios en el compostaje
A. alternatum permite una rápida y eficiente descomposición de celulosa y pectina en las fases iniciales (mesófila y termófila) del compostaje, debido a la mejora en la actividad enzimática, tales como: celulasa (15-19.8%), ureasa (2.3-71.4%) y polifenol (0.3-28.4%) (Li et al., 2018; Zhang et al., 2014). Esto da como resultado una optimización en la reducción de la duración de la etapa de maduración y aumenta el contenido de nutrientes.
La presencia de A. alternatum promueve la diversidad de la comunidad bacteriana de los géneros Firmicutes, Bacillus, Acinetobacter, Pseudomonas y Phormidium, mejorando la calidad y la eficiencia del compostaje, por ende, aumenta la estabilidad de los productos húmicos (Li et al., 2018; Xu et al., 2022).
Además, actúa como un agente potencial de biocontrol contra diversas plagas y fitopatógenos, donde se incluye las larvas de la polilla dorso de diamante, el mildiú polvoroso y Plasmodiophora brassicae (Suárez-Estrella et al. 2013; Berková et al. 2024). Por otra parte, se ha determinado que el género Acremonium se destaca por promover la tolerancia a la sal, debido a que da lugar a la señalización del ácido abscísico, lo que lleva a niveles reducidos de ROS, mejorando la fotosíntesis (Berková et al. 2024).

Fase de inoculación en el compostaje
Para la obtención de un compost de calidad, A. alternatum se debe inocular en la fase inicial (mesófila) del proceso de compostaje ya que ayuda a iniciar la descomposición de compuestos complejos y permite una transición más rápida hacia las posteriores fases. La inoculación da lugar a una mejor mineralización durante la fase termófila, lo que a su vez puede incrementar la temperatura, favoreciendo a la eliminación de patógenos y degradación de la materia recalcitrante (Cho et al. 2009; Suárez-Estrella et al. 2013)

Condiciones de cultivo
El hongo A. alternatum se puede aislar a partir de suelos y residuos vegetales en descomposición. Su cultivo se realiza comúnmente en medios de agar Sabouraud o agar extracto de malta, incubándose a temperaturas de 20–25°C. Las condiciones óptimas para la producción enzimática de este hongo incluyen temperaturas de 25–30°C y un pH cercano a 6, en presencia de fuentes de celulosa (Patil et al. 2015).
Para evaluar la funcionalidad de las enzimas extracelulares, se debe cultivar los aislados en agar papa dextrosa (PDA) durante un periodo de 6 a 7 días a 25°C. Después de la incubación, se puede colocar tapones de micelio de 5 mm en medios sólidos específicos para medir la actividad enzimática de las amilasas, proteasas, celulasas y lipasas, que reflejan la capacidad del hongo para degradar diferentes compuestos orgánicos (Berková et al. 2024).
4.2.2. Aspergillus awamori
Es un hongo filamentoso de la familia Aspergillaceae, conocido por su capacidad para producir enzimas amilolíticas y proteolíticas, como la amilasa y la proteasa, que son útiles en la industria de alimentos y bebidas (Sharma et al. 2014; Mostafa et al. 2024). Este organismo también se utiliza en procesos de fermentación debido a su eficiencia en la producción de ácidos (Mostafa et al. 2024).

Clasificación taxonómica
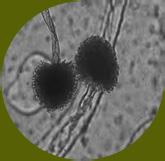

Producción de enzimas
ID: 105351, NCBI
A. awamori es conocido por su capacidad de secretar una amplia gama de enzimas hidrolíticas y oxidativas que desempeñan un papel esencial en la descomposición de los componentes lignocelulosos presentes en los residuos vegetales. Entre las enzimas más destacadas se encuentran la asparaginasa, hemicelulasa, celulasa, proteasa y xilanasa (Islam et al. 2014; Health Canada 2019).
En el caso de las hemicelulasas, existen diversas enzimas responsables de la degradación de la hemicelulosa. Por ejemplo, las xilanasas actúan despolimerizando el xilano, mientras que la β-mananasa (EC 3.2.1.78) y la β-manosidasa (EC 3.2.1.25) son responsables de la ruptura de la cadena principal del polímero de glucomanano (Teixeira et al. 2010; Mostafa et al. 2024). Las enzimas del sistema xilanolítico tienen la capacidad de eliminar el recubrimiento de hemicelulosa de las microfibrillas de celulosa y disminuir la barrera de lignina (Mostafa et al. 2024).

Beneficios en el compostaje
A. awamori brinda varios beneficios, como la mejora en el proceso de degradación de materia orgánica, aumenta la temperatura en el compost, y proporciona una mayor disponibilidad de nutrientes esenciales (N, P y K) para el crecimiento y desarrollo de las plantas (Jain et al. 2010; Mostafa et al. 2024).
Por otra parte, se ha demostrado que este hongo puede incrementar la actividad de enzimas como la fosfatasa, caracterizándose por la capacidad de solubilizar varias formas de fosfatos inorgánicos en un amplio rango de temperaturas, lo cual aumenta la disponibilidad de P en el suelo lo que conlleva a una mayor productividad de los cultivos (Biswas 2011; Jain et al. 2012). Asimismo, se maximiza la producción de la celulasa y la xilanasa, facilitando la fragmentación de la materia orgánica compleja en el compost, acelerando el proceso de humificación en un 4.82% (Sharma et al. 2014; Shinde et al. 2024).

Fase de inoculación en el compostaje
La inoculación se realiza durante la fase termófila del compostaje, donde las temperaturas elevadas activan su metabolismo y potencian su capacidad de descomponer polímeros complejos (Romero et al. 2009; Biswas 2011). Las altas temperaturas alcanzadas en la fase termófila, junto con la actividad enzimática de A. awamori, ayudan a reducir la carga
de patógenos presentes en el compost, mejorando así la calidad y seguridad del producto final (Sharma et al. 2014). Así mismo, permite que este hongo compita de manera eficiente contra otros microorganismos, estableciéndose como una fuente importante de enzimas degradativas en el proceso (Romero et al. 2009; Sharma et al. 2014). Estas características hacen de A. awamori un hongo altamente beneficioso para optimizar el compostaje y producir una enmienda orgánica de calidad para la agricultura sostenible.

Condiciones de cultivo
Puede aislarse de suelos ricos en materia orgánica o en descomposición. Para su cultivo, se emplea agar papa dextrosa (PDA) a temperaturas de 25–30°C. Además, su óptimo crecimiento se lleva a cabo a 30–35°C con un pH entre 5-6, lo cual beneficia para una alta producción de amilasas en presencia de almidón (Health Canada 2019; Mostafa et al. 2024).
4.2.3. Aspergillus niger
Es un hongo celulolítico mesófilo, especie común de hongos Aspergillus, ampliamente distribuida en el suelo, los alimentos y los productos vegetales (Heidarzadeh et al. 2019; Dong et al. 2024). Utilizado industrialmente para la producción de ácido cítrico, enzimas y otros metabolitos secundarios. Este organismo se caracteriza por sus conidios de color negro y es conocido por su capacidad de degradar materia orgánica compleja mediante la producción de enzimas hidrolíticas (Heidarzadeh et al. 2019; Dong et al. 2024).

Clasificación taxonómica


Producción de enzimas
ID: 5061, NCBI
A. niger es ampliamente utilizado en la biotecnología por su capacidad de secretar una gran variedad de enzimas hidrolíticas y lignocelulolíticas, esenciales para metabolizar las fracciones insolubles de los residuos orgánicos complejos para liberar nutrientes (Izmirlioglu & Demirci, 2016; Naeem et al., 2022). Se lleva a cabo mediante la síntesis de las celulasas, β-glucanasas, xilanasas, pectinasas e invertasas, así como α-amilasa y glucoamilasa (Tabla 18) (Hmida-Sayari et al. 2012; Ahmed et al. 2016).
Tabla 18
Enzimas secretadas por el hongo Aspergillus niger.

Beneficios en el compostaje
La inoculación de A. niger permite disminuir el período de compostaje con una duración de 30 días, donde se evidencia que la presencia del hongo conduce a una reducción significativa en Carbono Orgánico Total (TOC) en un 21.2%, la relación C:N en un 21.3%, el aumento del contenido de Nitrógeno Total en un 10.5%, P disponible en un 9.2%, K en 41% y el contenido de humus, dando como resultado un producto final de calidad (Ahamed & Vermette, 2008; Ajijolakewu et al., 2017).
La presencia de este hongo, aumenta la abundancia de genes CAZymes responsables de la degradación de la lignocelulosa y de genes relacionados con el glucometabolismo que contribuyen a la generación de calor, manteniendo la temperatura durante la etapa termófila, acelerando el compostaje (Irawan et al. 2023; Dong et al. 2024).
En relación a la actividad antifúngica, inhibe el crecimiento de micotoxinas (aflatoxinas), generando un compost seguro con un índice de germinación (IG) de 96.5%, lo que representa un enfoque más económico, efectivo y sostenible para el uso de residuos orgánicos (Naeem et al. 2022).
Por otra parte, A. niger es capaz de reducir o eliminar antibióticos presentes en el estiércol animal. Se ha demostrado que el compostaje inducido por este inoculante eliminó el 8393% de tilosina y el 50-65% de oxitetraciclina (Dela Cruz et al. 2022).

Fase de inoculación en el compostaje
La inoculación de A. niger se realiza idealmente en las fases mesófila y termófila del compostaje, debido a su habilidad para degradar azúcares y compuestos orgánicos complejos. Sin embargo, suele iniciarse alrededor del día 7 del proceso de compostaje, durante la fase mesófila, momento en que prospera y ayuda a acelerar la degradación inicial (Dela Cruz et al. 2022; Dong et al. 2024).

Condiciones de cultivo
Su cultivo se puede llevar a cabo en Agar Papa Dextrosa (PDA), Agar de Extracto de Malta (MEA), Agar de Autolisado de levadura de Czapek (CYA) o en Agar Sabouraud a temperaturas entre 25–30°C. Al ser aislado de varios entornos, se puede utilizar diferentes residuos agrícolas como única fuente de carbono, tales como: bagazo de caña de azúcar (Saccharum officinarum), pulpa de yuca (Manihot esculenta) y cáscara de plátano (Musa paradisiaca) (Heidarzadeh et al. 2019; Dong et al. 2024).
Para una máxima producción, la temperatura óptima de A. niger se encuentra entre 20-40°C, sin embargo, puede sobrevivir a 60°C, su pH es de 5–7, al ser una especie xerófila requiere una Aw mínima (agua disponible) de 0.77 y se desarrolla especialmente en presencia de carbohidratos simples (Bonner, 2018).
4.2.4. Phanerochaete chrysosporium
Es un hongo ligninolítico de la clase Agaricomycetes, conocido por su capacidad de degradar la lignina mediante enzimas como la lignina peroxidasa y la manganeso peroxidasa. Este hongo desempeña un papel importante en el tratamiento de desechos y la biorremediación de suelos contaminados (Zhang et al. 2014; Voběrková et al. 2017).

Clasificación taxonómica
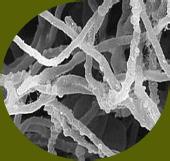

Producción de enzimas
ID: 2822231, NCBI.
P. chrysosporium es un hongo perteneciente a las especies conocidas como “Podredumbre blanca”. Se especializan en degradar los principales polímeros recalcitrantes como celulosa, hemicelulosa y lignina mediante reacciones extracelulares hidrolíticas y oxidorreductoras (Machado et al. 2020). Estas capacidades hacen que P. chrysosporium sea un organismo clave en procesos de descomposición y biorremediación.
Para la mineralización de la lignina, el hongo excreta múltiples peroxidasas de lignina (LiPs, EC 1.11.1.7) y manganeso (MnPs, EC 1.11.1.7) que se caracterizan por presentar la capacidad de generar radicales libres que despolimerizan los componentes lignocelulósicos, permitiendo así la descomposición de estos polímeros en compuestos más simples. Además de estas peroxidasas, produce otras enzimas tales como: lacasa (Lac), xilanasas, celulasas, glucosa-1-oxidasa y glucosa-2-oxidasa (Tabla 19) (Liu et al., 2020; Machado et al., 2020; Wang et al., 2023).
Tabla 19
Enzimas que secreta el hongo Phanerochaete chrysosporium.

Beneficios en el compostaje
Este hongo ha sido el más estudiado, no solo por las potenciales enzimas secretadas sino también por los beneficios que aporta a la agricultura sostenible. Entre los principales usos se destaca la degradación de una amplia variedad de compuestos recalcitrantes como la lignina presente en residuos agrícolas (Nemet et al., 2021; Zhang et al., 2014).
Se ha demostrado que su inoculación permite la degradación de un 58% de celulosa y un 73% de lignina, obteniendo un aumento del 82% en el contenido de sustancias húmicas, mejorando la humificación y la estabilidad del producto final del compostaje (Gao et al. 2023; Wang et al. 2023). En cuanto a la microbiota del suelo, la presencia de P. chrysosporium en la etapa de enfriamiento, resulta ser positiva al mejorar la estructura y la diversidad de
las comunidades fúngicas y la reproducción de las bacterias termófilas (Wang et al. 2023). Además, actúa como un componente clave en la rápida descomposición de materia prima utilizada en el proceso de compostaje. De modo que, un tiempo de 16 semanas son óptimas para obtener un compost estable y maduro apto para su uso como bioinsumo (Huang et al., 2017). Por otra parte, su inoculación contribuye significativamente a la inmovilización de metales pesados como Plomo (Pb) y Manganeso (Mn), cabe mencionar que el segundo en concentraciones altas puede ser tóxico para las plantas, afectando los procesos metabólicos relacionados con la fotosíntesis, la respiración y la síntesis de proteínas (Huang et al. 2017; Chen et al. 2019; Gao et al. 2023).

Fase de inoculación en el compostaje
La presencia de los hongos de podredumbre blanca ha mostrado beneficios significativos en la eficiencia y calidad del compost al ser inoculados en la fase de enfriamiento puesto que las condiciones térmicas se vuelven menos extremas, favoreciendo la actividad de P. chrysosporium (Gong et al. 2017). En esta fase permite una degradación más eficiente de la lignina y celulosa restantes, lo que conlleva a una reducción de los tiempos de maduración (Huang et al., 2015; Zeng et al., 2009). Los estudios muestran que esta práctica incrementa la retención de nutrientes, mejora la relación C:N y aumenta la disponibilidad de materia orgánica estabilizada, elevando el valor agrícola del compost final (Gao et al., 2023; Voběrková et al., 2017; Zhang et al., 2014).

Condiciones de cultivo
Para una mayor producción de enzimas, el cultivo de P. chrysosporium se lleva a cabo en Sabouraud a un pH de 5.0, a una temperatura de 30°C y se incuba durante un periodo de 4 días. Se utiliza la urea como única fuente de N y la fructosa como única fuente de C (Kheiralla et al. 2013).
4.2.5. Trichoderma harzianum
Es un hongo filamentoso de la familia Hypocreaceae, utilizado como agente de biocontrol debido a su capacidad de antagonizar hongos fitopatógenos. Este organismo produce diversas enzimas y metabolitos secundarios que inhiben el crecimiento de otros hongos, y también degrada la materia orgánica (Acosta-Suárez et al. 2013; Zhou et al. 2015).

Clasificación taxonómica
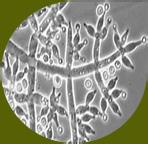
ID: 5544, NCBI.

Producción de enzimas
T. harzianum es ampliamente reconocido por su potencial como agente de control biológico, particularmente en el contexto agrícola. Este hongo saprofito, es capaz de sintetizar una variedad de enzimas hidrolíticas (Tabla 20) y metabolitos secundarios que favorecen el control de fitopatógenos (Acosta-Suárez et al. 2013). Entre las enzimas asociadas al control de patógenos se destacan las enzimas líticas como las quitinasas, las β-1,3 glucanasas y las proteasas (Delabona et al., 2016; Gajera y Vakharia, 2012). T. harzianum también produce enzimas capaces de hidrolizar y metabolizar la celulosa y hemicelulosa presente en la biomasa vegetal, como las enzimas activas en carbohidratos (CAZymes) (Benoliel et al. 2013; Maruyama et al. 2020)
Tabla 20
Enzimas que produce el hongo Trichoderma harzianum.

Beneficios en el compostaje
Se ha evidenciado que la aplicación de T. harzianum en compostaje mejora la eficiencia del proceso al acelerar la descomposición de la materia orgánica, debido a la producción de celulasas y quitinasas (Delabona et al. 2016). Esto reduce el tiempo necesario para alcanzar un compost maduro. Además, contribuye a la estabilización del pH del suelo y aumenta el contenido de macronutrientes como N (0.98-1.60%), P (0.19-1.10%) y K (0.55-6.70%) esenciales para el crecimiento de las plantas (Siddiquee et al. 2017). Entre otros beneficios que aporta se destaca la mitigación de las emisiones de gases de efecto invernadero (GEI) y la fijación biológica de N (Bernal-Vicente et al. 2012; Asghar et al. 2024).
En relación con el microbiota del suelo, la inoculación con T. harzianum impacta de manera positiva puesto que aumenta la abundancia relativa de bacterias beneficiosas
como Streptomyces spp. y de especies de hongos que poseen actividad quitinolítica y antagonizan a patógenos del suelo (Siddiquee et al. 2017). Este hongo tiene funciones como agente de biocontrol, inhibiendo el crecimiento de hongos patógenos al competir por el espacio y los nutrientes, así mismo, produce toxinas perjudiciales para hongos fitopatógenos del género Fusarium, Pythium, y Phytophthora, Sclerotinia y Rhizoctonia, minimizando el riesgo de enfermedades en el compost y, en última instancia, en los cultivos que recibirán este compost como enmienda (Zhou et al. 2015; Ros et al. 2017; Asghar et al. 2024). Estas interacciones microbianas contribuyen a la resiliencia del ecosistema del compost.
Por otra parte, se ha demostrado que la adición de T. harzianum al proceso de compostaje aumenta la actividad antioxidante en las plantas, específicamente mediante la regulación de enzimas del sistema de reciclaje de ascorbato como monodehidroascorbato reductasa (MDHAR), dehidroascorbato reductasa (DHAR) y peroxidasa (Bernal-Vicente et al. 2012; Blaya et al. 2013). Este efecto bioestimulante mejora la tolerancia de las plantas a condiciones de estrés, lo que da como resultado en una mejor eficiencia fotosintética, tasa de crecimiento e hidratación de las hojas. Se ha evidenciado que la regulación positiva de genes como P5CS y TAS14, involucrados en las respuestas de las plantas al estrés por baja temperatura, está ligado a la inoculación con T. harzianum (Donoso et al. 2008; Islam et al. 2014)

Fase de inoculación en el compostaje
Es recomendable realizar la inoculación de T. harzianum al inicio de la fase de maduración. Durante esta fase, el compost tiene una temperatura moderada (20-30°C) que favorece el crecimiento del hongo puesto que crece de manera óptima a 23°C, esto le permite establecerse y colonizar eficazmente la materia orgánica en descomposición (AcostaSuárez et al. 2013; Blaya et al. 2013). La inoculación en esta etapa ha demostrado reducir la incidencia de patógenos y la gravedad de enfermedades en las plantas que utilizan compost como enmienda (Bernal-Vicente et al. 2012)

v Condiciones de cultivo
T. harzianum se aísla de los suelos y MO en descomposición. Para su cultivo se recomienda el uso de un medio PDA incubado a una temperatura entre 25-30°C, con un pH de 5-6 durante 5 días sin condiciones de luz con el objetivo de obtener microorganismos en crecimiento activo (Benoliel et al. 2013; Islam et al. 2014). Para una mayor producción enzimática, este hongo requiere medios ricos en celulosa o hemicelulosa, que promueven una mayor actividad enzimática. Además, en el medio se suele colocar antibióticos como estreptomicina esterilizada para evitar la contaminación por la presencia de otros microorganismos (Blaya et al. 2013)
4.2.6. Trichoderma viride
Es un hongo saprófito que pertenece al género Trichoderma, reconocido por su alta capacidad de transformación de biomasa. Este microorganismo se utiliza en la agricultura como biofungicida, ya que produce enzimas hidrolíticas que descomponen las paredes celulares de hongos patógenos y facilita el control de enfermedades en plantas (Elgorban et al., 2016; Gajera & Vakharia, 2012).

Clasificación taxonómica
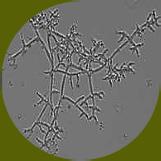

Producción de enzimas
ID: 5547, NCBI
T. viride es considerado un agente de control biológico (BCA) que puede producir diversas enzimas hidrolíticas, entre ellas exoglucanasas celulasas, quitinasas, poligalacturonasas y proteasas (Zahra et al. 2020). Estas enzimas son esenciales para la descomposición de componentes vegetales en la materia orgánica y contribuyen al ciclo de nutrientes en el suelo (Wahyuni & Nasution, 2019).
Este grupo de enzimas está representado principalmente por la β-1,4-endoglucanasa (EC 3.2.1.4), que cataliza la ruptura aleatoria de los enlaces glucosídicos internos en las regiones amorfas de la celulosa, lo cual se obtiene como resultado la generación de polisacáridos con grados de polimerización más bajos que la fibra de origen (Gupta et al. 2014; Kamaluddeen and Madika 2023). Dentro de este grupo las enzimas clave son la celobiohidrolasa (EC 3.2.1.91) que cataliza la escisión de moléculas de celobiosa (disacárido de glucosa con enlace β-1,4) a partir de los extremos reductores (CBH tipo I) o no reductores (CBH tipo II) de las fibras de celulosa y la glucanohidrolasa (EC 3.2.1.74) (Gupta et al. 2014; Sharma et al. 2014).
Cabe destacar que el mecanismo de antagonismo contra hongos patógenos se lleva a cabo mediante la eliminación de toxinas en forma de enzima β-1,3 glucanasa, quitinasa y celulasa que pueden inhibir su crecimiento e incluso matar estos patógenos (Wahyuni & Nasution, 2019).

Beneficios en el compostaje T. viride es eficiente en la degradación de residuos vegetales y, al igual que T. harzianum, actúa como agente biocontrolador. Tiene la capacidad de biotransformar sustratos altamente lignocelulósicos como el bagazo de caña de azúcar, el rastrojo de cosechas de gramíneas y los residuos de algunas especies de leguminosas (Elaine et al. 2020). De tal manera que aumenta el valor nutritivo del compost en los niveles de N (3.55%), P (3.46%) y K (1.58%) (Elaine et al. 2020).
Este hongo se destaca por su acción agresiva contra fitopátogenos, actuando mediante un conjunto de mecanismos sinérgicos que incluyen antibiosis a través de la producción de metabolitos secundarios, micoparasitismo a través de la secreción de enzimas
hidrolíticas, competencia por espacio y nutrientes, e inducción de resistencia sistémica en las plantas (Elhadi et al., 2023; Sultana et al., 2021; Wahyuni & Nasution, 2019). En el caso del micoparasitismo, este microorganismo puede suprimir parcialmente el crecimiento de Fusarium oxysporum f.sp cubense y los géneros Rhizoctonia y Botrytis (Elhadi et al. 2023).

Fase de inoculación en el compostaje
Es recomendable en la fase de enfriamiento para evitar dañar los inóculos con altas temperaturas, por ende, se aprovechan las temperaturas moderadas (30-40°C), que son adecuadas para el crecimiento y la actividad enzimática (Kausar et al., 2013; Wahyuni & Nasution, 2019). En esta etapa, la inoculación ayuda a completar la descomposición de la materia orgánica lignocelulósica resistente, como la celulosa y la hemicelulosa (Lu et al., 2021). Además, contribuye a la supresión de patógenos que puedan haberse introducido en el compost y mejora la calidad del producto final, al incrementar la disponibilidad de nutrientes esenciales para las plantas.

Condiciones de cultivo
T. viride se encuentra en suelos y en material en descomposición, es recomendable cultivar en medios como PDA o SDA. Las condiciones óptimas para la actividad enzimática son a una temperatura entre 20-30°C, pH de 5.5-6.5 y el uso de desechos agrícolas ricos en celulosa (40-50%), hemicelulosa (20-30%) y lignina (10-15%), que pueden contribuir a la producción a gran escala de celulasa (Elaine et al. 2020; Elhadi et al. 2023; Kamaluddeen and Madika 2023). Asimismo, el crecimiento de T. viride se ve estimulado por la presencia de compuestos nitrogenados tales como metionina, ácido glutámico y leucina, donde la primera ha demostrado ser altamente efectiva, mientras que la leucina y el ácido glutámico han evidenciado un efecto menos eficiente en el crecimiento del hongo (Kamaluddeen & Madika, 2023; Lu et al., 2021).

INOCULACIÓN DE BACTERIAS
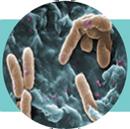
4.3. Inoculación de bacterias
4.3.1. Bacillus lincheniformis
Es una bacteria Gram positiva esporulante, que pertenece a la familia Bacillaceae. Este organismo es conocido por su capacidad para producir enzimas extracelulares, como proteasas y amilasas, y se utiliza en la industria alimentaria y farmacéutica. Su capacidad para sobrevivir en condiciones extremas lo hace útil en aplicaciones de biorremediación (Jurado et al., 2014; Lu et al., 2021).

Clasificación taxonómica
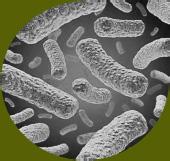

Producción de enzimas
ID: 1402, NCBI.
B. licheniformis produce enzimas de alto valor, tales como, amilasa, arginasa, amilosacarasa y proteasa. Las enzimas presentan características termoestables como es el caso de las amilasas (50–70°C), la β-glucosidasa, quitinasa, endogluconasa y xilasa (Cotta et al., 2023; De Marco et al., 2017).
Al ser un microorganismo saprófito, su secretoma está dirigido a la degradación de un alto número de compuestos que incluyen lípidos, polisacáridos, proteínas y otras sustancias. En este sentido, esta bacteria puede producir un número extremadamente alto de enzimas diferentes como: alantoinasa, celulasa, quitinasa, cicloglucosiltransferasa, dextranasa, endoarabinasa (ABNase), glucosidasa, glucanasa, galactosidasa, levanasa, lipasa, mananasa, pectato liasa, penicilinasa, pentosanasa o xilanasa, y varias proteasas, incluyendo una proteasa tipo clostripaína, serina proteasas, zinc proteasas, glutamil endopeptidasa, metaloproteasas y otras endo y exopeptidasas (Abdel-Rahman et al., 2016; Su et al., 2024; Xiao et al., 2024).

Beneficios
en el compostaje
En el compostaje, tiene una relevancia destacada al aumentar la degradación de celulosa en un 69.9%, acelerando la maduración del compost al contener mayor cantidad de HA en un 20% (Chang et al. 2023). Con respecto a la comunidad microbiana, la presencia de esta bacteria mejora las funciones metabólicas de los microorganismos nativos relacionados con el metabolismo de los carbohidratos, del almidón y la sacarosa al enriquecer los genes funcionales afines (Nallusamy et al. 2016; Chang et al. 2023). Además, estudios investigativos han informado que la inoculación permite enriquecer la presencia de Bacillus, Lactobacillus y Streptomyces durante la fase termófila, al mismo tiempo, que elimina la abundancia de Pseudomonas y Oceanobacillus, mejorando las interacciones microbianas positivas (Nallusamy et al. 2016; Su et al. 2024).
Otro aspecto positivo de su inoculación, es la capacidad de estimular el crecimiento de las plantas y mejorar la tolerancia de los cultivos a las enfermedades mediante la activación de la vía de señalización del ácido jasmónico/etileno (Samaniego-Gámez et al. 2017).
Por otro lado, se ha evidenciado que esta bacteria es fundamental en el mejoramiento del contenido de nutrientes y la reducción de contaminantes. Se ha demostrado que B. licheniformis influye en el crecimiento del arroz (Oryza sativa) en suelos contaminados con níquel (Ni), la biofortificación del trigo con selenio (Se) y la eliminación de mercurio (Hg) con la capacidad de eliminar más del 70% de Hg en condiciones óptimas (Brunetti et al. 2012; Du et al. 2017).

Condiciones de cultivo
Es una bacteria anaerobia facultativa no exigente que puede crecer en sustratos de carbono de bajo costo como sacarosa, maltosa y almidón. Además, puede prosperar a altas temperaturas (50-55°C). Para la producción de enzimas como amilasa y celulosa, la temperatura óptima es de 50°C a un pH de 7 (Nallusamy et al. 2016; Chang et al. 2023).
4.3.2. Bacillus sonorensis
Es una bacteria Gram positiva, termófila y esporulante, perteneciente a la familia Bacillaceae. Se aisló inicialmente en el desierto de Sonora y es conocida por su capacidad para producir enzimas termoestables, lo que la hace útil en procesos industriales que requieren altas temperaturas (Abdel-Rahman et al. 2016).

Clasificación taxonómica
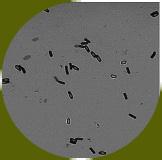

Producción de enzimas
ID: 119858, NCBI.
B. sonorensis se destaca por la producción de enzimas hidrolíticas significativas como quitinasas, quitosanasas, glucanasas, celulasas, lipasas y proteasas, las cuales son cruciales para la descomposición de compuestos complejos en el compostaje (Bhosale et al. 2016; Raza et al. 2021). Estas enzimas participan en la degradación de diversos sustratos, tales como proteínas, lípidos, celulosa y quitina, lo que mejora la eficiencia del compostaje y en la eliminación de patógenos mediante la lisis celular (Mehra et al. 2023).
Dentro de las quitinasas (EC 3.2.1.14) se encuentran las glicósido hidrolasas que degradan los enlaces β-1,4-glicosídicos en la quitina, el segundo polisacárido naturalmente disponible más abundante y el principal componente de la pared celular de los hongos, lo que sugiere su potencial para el control de enfermedades fúngicas en plantas (Abdel-Rahman et al. 2016; Raza et al. 2019; Miljaković et al. 2020). Por otra parte, se descompone la quitina y
sirve como fuente de energía. Además, las quitosanasas (EC 3.2.1.132) son importantes para el ciclo de carbono y nitrógeno (Miljaković et al. 2020).

Beneficios en el compostaje
La inoculación de B. sonorensis en el compostaje ha demostrado actividad antagónica contra una amplia gama de patógenos vegetales debido a su capacidad de producir endosporas duras y resistentes, entre ellos se encuentra Macrophomina phaseolina, un patógeno que causa la pudrición en las plantas (Ansari et al. 2023; Mehra et al. 2023). Este tipo de interacción es crucial para la supresión de enfermedades. Por otra parte, produce antibióticos y sideróforos, lo cual se es benéfico para mejorar la respuesta de la planta al ataque de patógenos al desencadenar la resistencia sistémica inducida (ISR) (Ansari et al. 2023).
A su vez, se destaca por llevar a cabo la desaminización de la acetil-CoA carboxilasa (ACC), la fijación de N, la solubilización del P, la producción de ácido inol-3-acético (IAA) y de amoníaco (Shafi et al. 2017). Por lo cual, reduce el tiempo de compostaje en un 40-43% correspondiente a 51-58 días en comparación con el tiempo general que se lleva a cabo en el proceso de compostaje que tiene un tiempo de 89-96 días y resulta en una mayor disminución en el Carbono Orgánico Total (TOC) y la relación C:N, así como un aumento en la calidad del compost mediante un aumento en el contenido total de N, P, y K (AbdelRahman et al. 2016; Shafi et al. 2017; Harindintwali et al. 2020).

Fase del compostaje
Las especies de Bacillus, especialmente B. sonorensis, son capaces de crecer a temperaturas elevadas, lo que las hace ideales para la inoculación en la fase termófila del compostaje (Abdel-Rahman et al. 2016; Shafi et al. 2017). La presencia de esta bacteria puede acelerar la descomposición y mejorar la calidad del compost, haciendo el proceso más eficiente.

Condiciones de cultivo
Para el aislamiento y cultivo de B. sonorensis, se utilizan medios como el agar carboximetilcelulosa (CMC), que favorece el crecimiento de bacterias celulolíticas (Harindintwali et al. 2020). Se cultivan a una temperatura de 50°C durante un tiempo de 3-7 días en un medio modificado de nitrato de almidón con sales inorgánicas, donde el almidón se reemplaza por sustratos de celulosa (Abdel-Rahman et al. 2016; Saffari et al. 2017). Estos medios optimizan la producción de enzimas celulolíticas que facilitan la degradación de los residuos orgánicos y mejoran la eficiencia del proceso de compostaje.
4.3.3. Bacillus subtilis
Es una bacteria del suelo aeróbica, Gram positiva, formadora de esporas y de crecimiento rápido que ha sido ampliamente utilizada para la producción de proteínas heterólogas (Duan et al. 2020; Dong et al. 2024). Este organismo es conocido por su producción de enzimas, antibióticos y otras sustancias bioactivas. Además, su resistencia a condiciones adversas permite su uso en la agricultura como promotor del crecimiento vegetal y en la biotecnología (He et al. 2023).

Clasificación
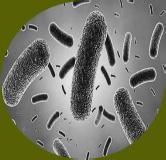

Producción de enzimas
ID: 1423, NCBI.
B. subtilis es conocida por su capacidad para secretar numerosas enzimas encargadas de degradar una variedad de polímeros complejos, lo que le permite sobrevivir en un entorno en continuo cambio al adaptarse a diversas fuentes de carbono disponibles en su medio ambiente. Entre las enzimas extracelulares se destacan, la α-amilasa (EC 3.2.1.1), levansacarasa, xilanasa (EC. 3.2.1.8), β-glucanasas y enzimas lipolíticas diferentes (Malik & Javed, 2021; Mehra et al., 2023; Su et al., 2020).
Esta bacteria se ha convertido en un organismo ideal para la producción de enzimas industriales debido a su rápido crecimiento en sustratos diversos, fuerte capacidad de secreción de proteínas, no patogenicidad y favorable procesamiento posterior, (Tyagi et al. 2014; Lu et al. 2021). Se estima que las enzimas producidas a partir de esta especie representan aproximadamente el 50% del mercado global de enzimas (Lu et al., 2021; Su et al., 2020).
Por otro lado, se destaca la eficiencia de la quitanasa producida por B. subtilis contra Rhizoctonia solani y Fusarium verticillioides que causa la pudrición del tallo y la mazorca del maíz (Sidorova et al. 2020; Rosazza et al. 2023).

Beneficios para el compostaje
B. subtilis puede mejorar significativamente la calidad del compost, promoviendo tanto la maduración como la retención de carbono, lo que contribuye a la mejora de la estructura del suelo y al crecimiento de los cultivos (Duan et al. 2020; He et al. 2023; Dong et al. 2024). De igual forma, disminuye la nitrificación y aumenta la desnitrificación. Por lo tanto, reduce la acumulación de NO3−-N en el suelo y reduce en gran medida la escorrentía de N y la pérdida por lixiviación (Sun et al., 2020).
Se ha identificado que la inoculación con un 0.5% de B. subtilis prolonga la fase termófila, reduce la mineralización en las fases de enfriamiento y maduración, aumenta los niveles de Carbono Orgánico Total (TOC) y disminuye eficazmente la abundancia de genes funcionales del metabolismo del carbono (Duan et al. 2020).
La acción enzimática de B. subtilis facilita la degradación de la lignina y otros compuestos
complejos mediante la secreción de lacasas, lipasas y peroxidasas (Rosazza et al. 2023). Así mismo, al resistir altas temperaturas y condiciones ácidas y alcalinas, es muy eficaz en la degradación de celulosa (Novikova & Titova, 2024). En este contexto, B. subtilis no solo mejora la eficiencia del compostaje, sino que también incrementa la calidad del producto final al aumentar la formación de humus.
Por otro lado, se ha evidenciado el aumento en la abundancia de los géneros Bacteroidetes y Chloroflexi, que desempeñan papeles importantes en la degradación de la materia orgánica del suelo (Duan et al., 2020; Niu & Li, 2022).

Fase de inoculación en el compostaje
La inoculación con B. subtilis se realiza generalmente en las etapas iniciales del compostaje, es decir, cuando la fase termófila está en su apogeo (Li et al., 2023; Wang et al., 2023). Esto permite que las enzimas producidas, como las celulasas y proteasas, comiencen a actuar rápidamente sobre los residuos orgánicos, acelerando su descomposición (Saffari et al. 2017). Además, la inoculación en etapas iniciales asegura que las condiciones óptimas de pH y temperatura sean aprovechadas para maximizar la actividad microbiana de la bacteria, lo que optimiza el tiempo de maduración del compost (Ribeiro et al. 2017).

Condiciones de cultivo
El crecimiento de B. subtilis es estrictamente aeróbico, por lo que requiere condiciones de cultivo oxigenadas. Se recomienda llevar a cabo su cultivo en Agar Nutriente, donde crece de manera óptima a temperaturas que oscilan entre 25-37°C, con un pH ideal entre 5-9, lo que hace a B. subtilis adaptable a una amplia gama de ambientes (iGEM 2014; Sidorova et al. 2020). Para el almacenamiento de sus cepas, se emplean métodos como la conservación en glicerol a -80°C para almacenamiento a largo plazo y la preservación en placas de agar o en cultivos líquidos bajo condiciones aeróbicas (Saffari et al. 2017).
4.3.4. Paracoccus denitrificans
Es una bacteria Gram negativa que pertenece a la familia Rhodobacteraceae, anaerobio facultativo capaz de metabolizar N, NO3, y NH3. Esta bacteria desempeña un papel importante en los ciclos del N en ambientes acuáticos y terrestres y es utilizada en el tratamiento de aguas residuales (Alonso-Vargas et al. 2023). Además, es uno de los microorganismos por excelencia, conocido por su notable versatilidad metabólica. Al ser facultativo, puede respirar con una amplia gama de aceptores finales de electrones (Alonso-Vargas et al. 2023).

Clasificación taxonómica
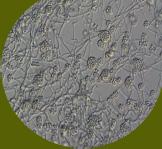
ID: 266, NCBI.

Producción de enzimas
P. denitrificans es una bacteria clave tanto para la respiración aeróbica como para participar en el proceso de desnitrificación, mediante el cual produce varias enzimas que catalizan la reducción progresiva de NO3 hasta gas nitrógeno (N₂), contribuyendo significativamente al ciclo de N, entre ellas se encuentran la nitrato reductasa (Nar), nitrito reductasa (Nir), óxido nítrico reductasa (Nor) y óxido nitroso reductasa (Nos) (Tabla 21) (Maeda et al. 2011; OlayaAbril et al. 2018; Alonso-Vargas et al. 2023).
Estas enzimas no solo son fundamentales en el ciclo biogeoquímico del N, sino que también tienen aplicaciones potenciales en la mitigación de emisiones de gases de efecto invernadero, como el óxido nitroso (N₂O), potente gas de efecto invernadero (Olaya-Abril et al. 2018; Pascual et al. 2020).
Tabla 21
Enzimas que secreta la bacteria Paracoccus denitrificans.

Beneficios en el compostaje
P. denitrificans desempeña un papel clave en la prevención de la acumulación de NO2, facilitando un proceso de compostaje más sostenible. Este microorganismo es capaz de desnitrificar hasta su último paso, convirtiendo el N2O en nitrógeno gaseoso (N2), lo que ayuda a mitigar la liberación de gases de efecto invernadero durante el proceso (Shi et al. 2020; Jiang et al. 2023). La reducción de N2O es particularmente relevante, ya que este gas tiene un potencial de calentamiento global mucho mayor que el dióxido de carbono (CO2) (Jiang et al. 2023).
La desnitrificación de P. denitrificans utiliza NO3 o NO2 como aceptores de electrones, con donadores de electrones como succinato, NADH, glucosa, acetato o metanol. Se ha demostrado que puede reducir la emisión de N2O en un 70% (Pascual et al. 2020).

Fase del compostaje
Debido a que P. denitrificans presenta una temperatura óptima de crecimiento entre 25-
35°C, se establece que la inoculación se debe llevar a cabo en la fase de maduración. Así mismo, se ha demostrado que la abundancia de microorganismos desnitrificantes es relativamente rara en la fase de calentamiento de compostaje y aumenta gradualmente de madurez (Shi et al. 2020; Alonso-Vargas et al. 2023).

Condiciones de cultivo
Para el cultivo de P. denitrificans, se utilizan medios de cultivo como Luria-Bertani (LB), que favorece su crecimiento aeróbico a 30°C, con agitación constante (150 rpm) hasta la fase de crecimiento logarítmico tardío. Una vez alcanzada esta fase, las células se recolectan por centrifugación (4500 rpm durante 5 min), se lavan dos veces con PBS (0.1 M, pH 7.4) y se resuspenden en PBS previo a su uso en aplicaciones específicas (Albertsson et al. 2019; Pascual et al. 2020).
4.3.5. Ureibacillus thermosphaericus
Es una bacteria aerobia termófila, Gram positiva, formadora de endosporas que pertenece a la familia Bacillaceae. Este microorganismo es capaz de prosperar en temperaturas elevadas (47°C) y se utiliza en la biodegradación de compuestos orgánicos y en el compostaje debido a su tolerancia al calor (Abbasalizadeh et al. 2012).

Clasificación taxonómica
ID: 51173, NCBI.

Producción de enzimas
U. thermosphaericus se caracteriza por su capacidad para secretar enzimas termoestables que tienen aplicaciones industriales significativas. Estas enzimas incluyen amilasas, catalasas, esterases, y deshidrogenasas (Tabla 22), las cuales son cruciales en diversos procesos bioquímicos, especialmente en el tratamiento de residuos y en la producción de compuestos específicos para la industria alimentaria, farmacéutica y ambiental (Samoylova et al., 2018).
Dentro de las enzimas termoestables, se destaca especialmente las esterasas (EC 3.1.1.3) debido a la tolerancia a temperaturas altas (50-70°C). Su función es catalizar la escisión de los enlaces éster en una molécula de triglicérido (Samoylova et al., 2018; Sorokina et al., 2020). Por otra parte, se considera una bacteria degradante de lignina al producir lacasa y lignina peroxidasa (Nakamura & Kurosawa, 2021; Wang et al., 2011).
Tabla 22
Enzimas que secreta la bacteria Ureibacillus thermosphaericus.

Beneficios para el compostaje
La inoculación con U. thermosphaericus ha demostrado ser eficiente en la mejora del proceso de compostaje. Este microorganismo es capaz de acelerar la descomposición de la MO, especialmente en la fase termófila, lo que resulta en la conversión rápida de residuos orgánicos en compost de alta calidad (Nakamura & Kurosawa, 2021). Durante el proceso, la bacteria desempeña un papel fundamental en la disminución de la lignina, un componente de difícil descomposición en la materia orgánica, puesto que reduce el contenido de lignina en un rango entre 17.23-24.34%, lo que mejora la calidad del compost (Nakasaki et al. 2009; Ohnishi et al. 2011).

Condiciones de cultivo
Para su cultivo se emplea el medio Agar Caldo de Soja Tripticasa, con respecto a las condiciones óptimas para la actividad catalítica se requiere un pH alcalino de 10.5 a una temperatura de 65°C. Esta cepa se cultiva a temperaturas elevadas, ideales para su actividad termofílica. En condiciones de cultivo, U. thermosphaericus exhibe un crecimiento rápido, favoreciendo la producción de enzimas termoestables que son útiles en diversas aplicaciones industriales (Akita et al. 2011; Sorokina et al. 2020).


Bibliografía
Abbasalizadeh S, Jouzani GS, Juibari MM, et al (2012) Draft genome sequence of Ureibacillus thermosphaericus strain thermo-BF, isolated from Ramsar hot springs in Iran. J Bacteriol 194:4431–4431. https://doi.org/10.1128/JB.00634-12
Abdel-Rahman MA, Nour El-Din M, Refaat BM, et al (2016) Biotechnological Application of Thermotolerant Cellulose-Decomposing Bacteria in Composting of Rice Straw. Ann Agric Sci 61:135–143. https://doi. org/10.1016/j.aoas.2015.11.006
Acosta-Suárez M, Pichardo T, Roque B, et al (2013) Antagonismo in vitro de Trichoderma harzianum Rifai contra Mycosphaerella fijiensis Morelet. Biotecnología Vegetal 13:397
Aguilar-Paredes A, Valdés G, Araneda N, et al (2023) Microbial Community in the Composting Process and Its Positive Impact on the Soil Biota in Sustainable Agriculture. Agronomy 13. https://doi. org/10.3390/agronomy13020542
Ahamed A, Vermette P (2008) Enhanced enzyme production from mixed cultures of Trichoderma reesei RUT-C30 and Aspergillus niger LMA grown as fed batch in a stirred tank bioreactor. Biochem Eng J 42:41–46. https://doi.org/10.1016/j. bej.2008.05.007
Ahmed I, Zia MA, Hussain MA, et al (2016) Bioprocessing of citrus waste peel for induced pectinase production by Aspergillus niger; its purification and characterization. J Radiat Res Appl Sci 9:148–154. https://doi.org/10.1016/j. jrras.2015.11.003
Ajijolakewu AK, Peng C, Nadiah W, Abdullah W (2017) Optimization of production conditions for xylanase production by newly isolated strain Aspergillus niger through solid state fermentation of oil palm empty fruit bunches. Biocatalysis and Agricultural Biotechnology 11:239–247. https://doi. org/10.1016/j.bcab.2017.07.009
Akita H, Fujino Y, Doi K, Ohshima T (2011) Highly stable meso-diaminopimelate dehydrogenase from an Ureibacillus thermosphaericus strain a1 isolated from a Japanese compost: Purification,
characterization and sequencing. AMB Express 1:1–8. https://doi. org/10.1186/2191-0855-1-43
Akram S, Ahmed A, He P, et al (2023) Uniting the Role of Endophytic Fungi against Plant Pathogens and Their Interaction. Journal of Fungi 9, 72. https://doi.org/10.3390/ jof9010072
Al-Askar AA, Rashad YM, Hafez EE, et al (2015) Characterization of alkaline protease produced by Streptomyces griseorubens E44G and its possibility for controlling Rhizoctonia root disease of corn. Biotechnology and Biotechnological Equipment 29:457–462. https://doi.org/10 .1080/13102818.2015.1015446
Al Hamad BM, Al Raish SM, Ramadan GA, et al (2021) Effectiveness of augmentative biological control of Streptomyces griseorubens uae2 depends on 1-aminocyclopropane-1-carboxylic acid deaminase activity against Neoscytalidium dimidiatum. J Fungi 7. https://doi. org/10.3390/jof7110885
Albertsson I, Sjöholm J, ter Beek J, et al (2019) Functional interactions between nitrite reductase and nitric oxide reductase from Paracoccus denitrificans. Sci Rep 9:1–12. https://doi.org/10.1038/s41598-01953553-z
Alonso-Vargas M, Portillo-Torres LA, MercadoFlores Y, et al (2023) The Respiratory Way without Microbial Growth of Paracoccus denitrificans. Microbiol Res (Pavia) 14:1834–1842. https://doi.org/10.3390/ microbiolres14040125
Anli M, Symanczik S, El Abbassi A, et al (2020) Use of arbuscular mycorrhizal fungus Rhizoglomus irregulare and compost to improve growth and physiological responses of Phoenix dactylifera ‘Boufgouss’ Plant Biosyst 3504:1–9. https://doi.org/10.1080/11263504.2020.1 779848
Ansari MM, Singh T, Majhi B, et al (2023) Biosurfactant producing plant growth–promoting bacteria: eco-friendly approaches for charcoal rot management. In: Macrophomina Phaseolina: Ecobiology, Pathology and Management. pp 313–321
Asghar W, Craven K, Kataoka R, et al (2024) The application of Trichoderma spp., an old
but new useful fungus, in sustainable soil health intensification: A comprehensive strategy for addressing challenges. Plant Stress 12:100455. https://doi. org/10.1016/j.stress.2024.100455
Awasthi MK, Duan Y, Awasthi SK, et al (2020) Effect of biochar and bacterial inoculum additions on cow dung composting. Bioresour Technol 297:122407. https:// doi.org/10.1016/j.biortech.2019.122407
Ayswaria R, Vasu V, Krishna R (2020) Diverse endophytic Streptomyces species with dynamic metabolites and their meritorious applications: a critical review. Crit. Rev. Microbiol. 46:750–758
Benoliel B, Gonçalves Torres FA, de Moraes LMP (2013) A novel promising Trichoderma harzianum strain for the production of a cellulolytic complex using sugarcane bagasse in natura. Springerplus 2:1–7. https://doi.org/10.1186/2193-1801-2-656
Berková V, Berka M, Štěpánková L, et al (2024) The fungus Acremonium alternatum enhances salt stress tolerance by regulating host redox homeostasis and phytohormone signaling. Physiol Plant 176:1–15. https:// doi.org/10.1111/ppl.14328
Bernal-Vicente A, Ros M, Pacual J (2012) Inoculation of Trichoderma harzianum during maturation of vineyard waste compost to control muskmelon Fusarium wilt. Bioresources 7:1948–1960
Beroigui O, Errachidi F (2023) Streptomyces at the Heart of Several Sectors to Support Practical and Sustainable Applications: A Review. Prog Microbes Mol Biol 6:1–46. https://doi.org/10.36877/pmmb.a0000345
Bhosale H, Shaheen U, Kadam T (2016) Characterization of a Hyperthermostable Alkaline Lipase from Bacillus sonorensis 4R. Enzyme Res 2016. https://doi. org/10.1155/2016/4170684
Biswas DR (2011) Nutrient recycling potential of rock phosphate and waste mica enriched compost on crop productivity and changes in soil fertility under potato-soybean cropping sequence in an Inceptisol of Indo-Gangetic Plains of India. Nutr Cycl Agroecosystems 89:15–30. https://doi. org/10.1007/s10705-010-9372-6
Blaya J, López-mondéjar R, Lloret E, et al (2013) Changes induced by Trichoderma
harzianum in suppressive compost controlling Fusarium wilt. Pestic Biochem Physiol 107:112–119. https://doi. org/10.1016/j.pestbp.2013.06.001
Bonner JT (2018) A Study of the Temperature and Humidity Requirements of Aspergillus Niger. Mycologia 40:728–738. https://doi. org/10.1080/00275514.1948.12017741
Boros K, Gal L, Gal CA, et al (2024) Immobilization of D-amino acid dehydrogenase from Ureibacillus thermosphaericus. Process Biochem 140:45–55. https://doi. org/10.1016/j.procbio.2024.02.014
Braz SC de M, Motta CM de S, Massa DM de L, et al (2009) Viability, taxonomic confirmation and enzymatic detection of Acremonium species preserved under mineral oil in the URM Culture Collection. Rev Soc Bras Med Trop 42:63–66. https://doi.org/10.1590/ s0037-86822009000100013
Brunetti G, Farrag K, Soler-Rovira P, et al (2012) The effect of compost and Bacillus licheniformis on the phytoextraction of Cr, Cu, Pb and Zn by three brassicaceae species from contaminated soils in the Apulia region, Southern Italy. Geoderma 170:322–330. https://doi.org/10.1016/j. geoderma.2011.11.029
Chang Y, Zhou K, Yang T, et al (2023) Bacillus licheniformis inoculation promoted humification process for kitchen waste composting: Organic components transformation and bacterial metabolic mechanism. Environ Res 237. https://doi. org/10.1016/j.envres.2023.117016
Chen Y, Chen Y, Li Y, et al (2019) Changes of heavy metal fractions during cocomposting of agricultural waste and river sediment with inoculation of Phanerochaete chrysosporium. J Hazard Mater 378. https://doi.org/10.1016/j. jhazmat.2019.120757
Chi CP, Chu S, Wang B, et al (2020) Dynamic bacterial assembly driven by Streptomyces griseorubens JSD-1 inoculants correspond to composting performance in swine manure and rice straw co-composting. Bioresour Technol 313:123692. https:// doi.org/10.1016/j.biortech.2020.123692
Cho KM, Kwon EJ, Kim SK, et al (2009) Fungal diversity in composting process of pig manure and mushroom cultural waste
based on partial sequence of large subunit rRNA. J Microbiol Biotechnol 19:743–748. https://doi.org/10.4014/jmb.0807.455
Copetta A, Bardi L, Bertolone E, Berta G (2011) Fruit production and quality of tomato plants (Solanum lycopersicum L.) are affected by green compost and arbuscular mycorrhizal fungi. Plant Biosyst 145:106–115. https://doi.org/10.1080/11263504.20 10.539781
Cotta SPM, Marins MS, Marriel IE, et al (2023) Thermo-resistant enzyme-producing microorganisms isolated from composting. Brazilian J Biol 83:1–12. https://doi. org/10.1590/1519-6984.244205
Cuesta G, García-de-la-Fuente R, Abad M, Fornes F (2012) Isolation and identification of actinomycetes from a compost-amended soil with potential as biocontrol agents. J Environ Manage 95: S280–S284. https:// doi.org/10.1016/j.jenvman.2010.11.023
da Silva Delabona P, Lima DJ, Robl D, et al (2016) Enhanced cellulase production by Trichoderma harzianum by cultivation on glycerol followed by induction on cellulosic substrates. J Ind Microbiol Biotechnol 43:617–626. https://doi.org/10.1007/ s10295-016-1744-8
De Corato U, Viola E, Arcieri G, et al (2016) Use of composted agro-energy co-products and agricultural residues against soilborne pathogens in horticultural soilless systems. Sci Hortic (Amsterdam) 210:166–179. https://doi.org/10.1016/j. scienta.2016.07.027
De Marco ÉG, Heck K, Martos ET, Van Der Sand ST (2017) Purification and characterization of a thermostable alkaline cellulase produced by Bacillus licheniformis 380 isolated from compost. An Acad Bras Cienc 89:2359–2370. https://doi. org/10.1590/0001-3765201720170408
Dela Cruz RSJP, Ballesteros FC, R J, et al (2022) Assessment of Aspergillus niger and Aspergillus flavus in Inoculant Induced Composting to Remove Antibiotics in Poultry Manure. Ecol Environ Conserv 28:677–684. https://doi.org/10.53550/ eec.2022.v28i02.015
Dong W, Zhou R, Li X, et al (2024) Effect of simplified inoculum agent on performance and microbiome during cow manure-
composting at industrial-scale. Bioresour Technol 393:130097. https://doi. org/10.1016/j.biortech.2023.130097
Donoso E, Lobos GA, Rojas N (2008) Effect of Trichoderma harzianum and compost in nursery Pinus radiata seedling. Bosque 29:52–57
Du N, Shi L, Yuan Y, et al (2017) Isolation of a potential biocontrol agent Paenibacillus polymyxa NSY50 from vinegar waste compost and its induction of host defense responses against Fusarium wilt of cucumber. Microbiol Res 202:1–10. https:// doi.org/10.1016/j.micres.2017.04.013
Duan M, Zhang Y, Zhou B, et al (2020) Effects of Bacillus subtilis on carbon components and microbial functional metabolism during cow manure–straw composting. Bioresour Technol 303. https://doi.org/10.1016/j. biortech.2020.122868
Elaine C, Cabrera V, Vázquez MA, et al (2020) Production of lignocellulases enzymes from Trichoderma viride M5-2 in wheat bran (Triticum aestivum) and purification of their laccases. Cuba J Agric Sci 54:55–66
Elgorban AM, Al-Rahmah AN, Sayed SR, et al (2016) Antimicrobial activity and green synthesis of silver nanoparticles using Trichoderma viride. Biotechnol Biotechnol Equip 30:299–304. https://doi.org/10.108 0/13102818.2015.1133255
Elhadi A, Hakim S, Alshammari W, et al (2023) Capability of Trichoderma viride to Produce Cellulolytic and Pectolytic Enzymes. Adv Life Sci – Int Q J Biol Sci 10:491–497
Feng J, Wang B, Zhang D, et al (2021) Streptomyces griseorubens JSD-1 promotes rice straw composting efficiency in industrial-scale fermenter: Evaluation of change in physicochemical properties and microbial community. Bioresour Technol 321:124465. https://doi.org/10.1016/j. biortech.2020.124465
Ferreira Filho JA, Horta MAC, Beloti LL, et al (2017) Carbohydrate-active enzymes in Trichoderma harzianum: A bioinformatic analysis bioprospecting for key enzymes for the biofuels industry. BMC Genomics 18:1–12. https://doi.org/10.1186/s12864017-4181-9
Fujii T, Fang X, Inoue H, et al (2009) Enzymatic hydrolyzing performance of Acremonium
cellulolyticus and Trichoderma reesei against three lignocellulosic materials. Biotechnol Biofuels 2:1–8. https://doi. org/10.1186/1754-6834-2-24
Gajera HP, Vakharia DN (2012) Production of lytic enzymes by Trichoderma isolates during in vitro antagonism with Aspergillus niger, the causal agent of collar rot of peanut. Brazilian J Microbiol 43:33–52. https://doi. org/10.1590/s1517-83822012000100005
Gao L, Huang D, Cheng M, et al (2023) Effect of Phanerochaete chrysosporium inoculation on manganese passivation and microbial community succession during electrical manganese residue composting. Bioresour Technol 370. https://doi.org/10.1016/j. biortech.2022.128497
Gong X, Li S, Sun X, et al (2017) Maturation of green waste compost as affected by inoculation with the white-rot fungi Trametes versicolor and Phanerochaete chrysosporium. Environ Technol (United Kingdom) 38:872–879. https://doi.org/10. 1080/09593330.2016.1214622
Guo W, Yang J, Huang T, et al (2021) Synergistic effects of multiple enzymes from industrial Aspergillus niger strain O1 on starch saccharification. Biotechnol Biofuels 14:1–12. https://doi.org/10.1186/s13068021-02074-x
Gupta VK, Donovan AO, Tuohy MG, Sharma GD (2014) Trichoderma in Bioenergy Research: An Overview. In: Biotechnology and Biology of Trichoderma. Elsevier, pp 325–336
Harindintwali JD, Zhou J, Yu X (2020) Lignocellulosic crop residue composting by cellulolytic nitrogen-fixing bacteria: A novel tool for environmental sustainability. Sci Total Environ 715:136912. https://doi. org/10.1016/j.scitotenv.2020.136912
He X, Cong R, Gao W, et al (2023) Optimization of composting methods for efficient use of cassava waste, using microbial degradation. Environ Sci Pollut Res 30:51288–51302. https://doi.org/10.1007/ s11356-023-25818-8
Health Canada (2019) Screening assessment for aspergillus awamori strain and aspergillus brasiliensis strain. Environment and Climate Change Canada. https://www.canada. ca/content/dam/eccc/documents/pdf/
pded/aspergillus/Screening-assessmentaspergillus-awamori-brasiliensis.pdf
Heidarzadeh MH, Amani H, Javadian B (2019) Improving municipal solid waste compost process by cycle time reduction through inoculation of Aspergillus niger. J Environ Heal Sci Eng 17:295–303. https://doi. org/10.1007/s40201-019-00348-z
Hmida-Sayari A, Taktek S, Elgharbi F, Bejar S (2012) Biochemical characterization, cloning and molecular modeling of a detergent and organic solvent-stable family 11 xylanase from the newly isolated Aspergillus niger US368 strain. Process Biochem 47:1839–1847. https://doi. org/10.1016/j.procbio.2012.06.010
Huang C, Zeng G, Huang D, et al (2017) Effect of Phanerochaete chrysosporium inoculation on bacterial community and metal stabilization in lead-contaminated agricultural waste composting. Bioresour Technol 243:294–303. https://doi. org/10.1016/j.biortech.2017.06.124
Huang H li, Zeng G ming, Luo L, et al (2015) Effect of inoculation during different phases of agricultural waste composting on spectroscopic characteristics of humic acid. J Cent South Univ 22:4177–4183. https://doi.org/10.1007/s11771-0152965-0
iGEM (2014) Growthco nditions,storage, media and antibiotics for Bacillus subtilis. iGEM LMU Munich. http://2014.igem.org/ Team:LMU-?‐Munich
Irawan B, Saputra A, Farisi S, et al (2023) The use of cellulolytic Aspergillus sp. inoculum to improve the quality of Pineapple compost. AIMS Microbiol 9:41–54. https://doi. org/10.3934/microbiol.2023003
Islam MA, Mostafa MG, Rahman MR (2014) Conversion of solid organic waste into compost using Trichoderma spp. And its application on some selected vegetables. Int J Environ Waste Manag 14:211–221. https://doi.org/10.1504/ IJEWM.2014.064570
Izmirlioglu G, Demirci A (2016) Strain selection and medium optimization for glucoamylase production from industrial potato waste by Aspergillus niger. J Sci Food Agric 96:2788–2795. https://doi.org/10.1002/ jsfa.7445
Jain R, Saxena J, Sharma V (2010) The evaluation of free and encapsulated Aspergillus awamori for phosphate solubilization in fermentation and soil-plant system. Appl Soil Ecol 46:90–94. https://doi. org/10.1016/j.apsoil.2010.06.008
Jain R, Saxena J, Sharma V (2012) Effect of phosphate-solubilizing fungi Aspergillus awamori S29 on mungbean (Vigna radiata cv. RMG 492) growth. Folia Microbiol (Praha) 57:533–541. https://doi. org/10.1007/s12223-012-0167-9
Ji Y, Wang N, Yang N, et al (2023) Multivariate insights into the effects of inoculating thermophilic aerobic bacteria on the biodegradation of food waste: Process properties, organic degradation and bacterial communities. Environ Technol Innov 29:102968. https://doi.org/10.1016/j. eti.2022.102968
Jiang M, Wu Y, He P, et al (2023) Assembled denitrifying consortia for efficient nitrate removal under low-COD/N conditions. Chem Eng J 460:141655. https://doi. org/10.1016/j.cej.2023.141655
Jurado M, López MJ, Suárez-Estrella F, et al (2014) Exploiting composting biodiversity: Study of the persistent and biotechnologically relevant microorganisms from lignocellulose-based composting. Bioresour Technol 162:283–293. https:// doi.org/10.1016/j.biortech.2014.03.145
Kamaluddeen SY, Madika A (2023) Production of Cellulase by Trichoderma viride via Submerged Fermentation using Corncob as Substrate. Niger J Pure Appl Sci 4512–4520. https://doi.org/10.48198/njpas/22. b12
Kannan R, Kallapiran K (2023) Bacterial Consortia as a Suitable Innovation for Management of Agriculture Solid Waste. In: Emerging Issues in Agricultural Sciences. pp 146–159
Kausar H, Razi M, Mohd H, et al (2013) Use of Lignocellulolytic Microbial Consortium and pH Amendment on Composting Efficacy of Rice Straw Use of Lignocellulolytic Microbial Consortium and pH Amendment on Composting Efficacy of Rice Straw. Compost Sci y Util 37–41. https://doi.org /10.1080/1065657X.2013.842131
Kheiralla ZH, El-Din SMB, Malek SMA, Aziz DHA
(2013) Optimization of cultural conditions for lignin peroxidase production by Phanerochaete chrysosporium and Pleurotus ostreatus. Acad J Biotechnol 1:087–095
Kotrbová L, Lara AC, Corretto E, et al (2022) Evaluation and comparison of antibiotic susceptibility profiles of Streptomyces spp. from clinical specimens revealed common and region-dependent resistance patterns. Sci Rep 12:1–12. https://doi. org/10.1038/s41598-022-13094-4
Li H, He Y, Yan Z, et al (2023) Insight into the microbial mechanisms for the improvement of spent mushroom substrate composting efficiency driven by phosphate-solubilizing Bacillus subtilis. J Environ Manage 336:117561. https://doi.org/10.1016/j. jenvman.2023.117561
Li Y, Gu J, Zhang SQ, et al (2018) Effects of adding compound microbial inoculum on microbial community diversity and enzymatic activity during co-composting. Environ Eng Sci 35:270–278. https://doi. org/10.1089/ees.2016.0423
Li Z, Yang Y, Xia Y, et al (2019) The succession Pattern of Bacterial Diversity in Compost Using Pig Manure Mixed with Wood Chips Analyzed by 16S rRNA Gene Analysis. bioRxiv. https://doi.org/10.1101/674069
Liu J, Yang J, Wang R, et al (2020) Comparative characterization of extracellular enzymes secreted by Phanerochaete chrysosporium during solid-state and submerged fermentation. Int J Biol Macromol 152:288–294. https://doi.org/10.1016/j. ijbiomac.2020.02.256
Liu X, Zubair M, Kong L, et al (2023) Shifts in bacterial diversity characteristics during the primary and secondary fermentation stages of bio-compost inoculated with effective microorganisms agent. Bioresour Technol 382:129163. https://doi. org/10.1016/j.biortech.2023.129163
Lu J, Wang J, Gao Q, et al (2021) Effect of Microbial Inoculation on Carbon Preservation during Goat Manure Aerobic Composting. Molecules 26:1–16
Machado AS, Valadares F, Silva TF, et al (2020) The Secretome of Phanerochaete chrysosporium and Trametes versicolor Grown in Microcrystalline Cellulose
and Use of the Enzymes for Hydrolysis of Lignocellulosic Materials. Front Bioeng Biotechnol 8:1–15. https://doi. org/10.3389/fbioe.2020.00826
Maeda K, Hanajima D, Toyoda S, et al (2011) Microbiology of nitrogen cycle in animal manure compost. Microb Biotechnol 4:700–709. https://doi.org/10.1111/ j.1751-7915.2010.00236.x
Malik WA, Javed S (2021) Biochemical Characterization of Cellulase from Bacillus subtilis Strain and its Effect on Digestibility and Structural Modifications of Lignocellulose Rich Biomass. Front Bioeng Biotechnol 9:1–15. https://doi. org/10.3389/fbioe.2021.800265
Manu MK, Kumar R, Garg A (2017) Performance assessment of improved composting system for food waste with varying aeration and use of microbial inoculum. Bioresour Technol 234:167–177. https:// doi.org/10.1016/j.biortech.2017.03.023
Maruyama CR, Bilesky-José N, de Lima R, Fraceto LF (2020) Encapsulation of Trichoderma harzianum Preserves Enzymatic Activity and Enhances the Potential for Biological Control. Front Bioeng Biotechnol 8:1–14. https://doi.org/10.3389/fbioe.2020.00225
Meenakshi S, Hiremath J, Meenakshi MH, Shivaveerakumar S (2024) Actinomycetes: Isolation, Cultivation and its Active Biomolecules. J. Pure Appl. Microbiol. 18:118–143
Mehra V, Pai A, Bhat BB, et al (2023) Prospective potential of enzymes from Novel Bacillus sonorensis: Insights into the Structural aspects, Industrial and Therapeutic significance. Res J Pharm Technol 16:4671–4676. https://doi. org/10.52711/0974-360X.2023.00759
Miljaković D, Marinković J, Balešević-Tubić S (2020) The significance of bacillus spp. In disease suppression and growth promotion of field and vegetable crops. Microorganisms 8:1–19
Mostafa FA, Wehaidy HR, Sharaf S, et al (2024) Aspergillus awamori MK788209 cellulase: production, statistical optimization, pea peels saccharification and textile applications. Microb Cell Fact 23:1–13. https://doi.org/10.1186/s12934-02302286-w
Naeem U, Qazi MA, Haq IU, Afzaal M (2022) Aspergillus niger as the rapid press mud composting agent. J Anim Plant Sci 32:515–525. https://doi.org/10.36899/ JAPS.2022.2.0449
Nakamura S, Kurosawa N (2021) Decomposition of Rice Chaff Using a Cocultivation System of Thermobifida fusca and Ureibacillus thermosphaericus. Actas 66 31. https:// doi.org/10.3390/proceedings2020066031
Nakasaki K, Tran LTH, Idemoto Y, et al (2009) Comparison of organic matter degradation and microbial community during thermophilic composting of two different types of anaerobic sludge. Bioresour Technol 100:676–682. https:// doi.org/10.1016/j.biortech.2008.07.046
Nallusamy S, Amira AZ, Saif AB, et al (2016) Isolation and characterization of cellulolytic Bacillus licheniformis from compost. African J Biotechnol 15:2434–2446. https://doi.org/10.5897/ajb2016.15641
Nemet F, Perić K, Lončarić Z (2021) Microbiological activities in the composting process: A review. Columella J Agric Environ Sci 8:41–53. https://doi.org/10.18380/szie. colum.2021.8.2.41
Niu J, Li X (2022) Effects of Microbial Inoculation with Different Indigenous Bacillus Species on Physicochemical Characteristics and Bacterial Succession during Short-Term Composting. Fermentation 8:. https://doi. org/10.3390/fermentation8040152
Novikova I, Titova J (2024) Multirecycled polyfunctional biologics based on Bacillus subtilis together with compost in potato organic farming. Res Sq 1–25
Ohnishi A, Nagano A, Fujimoto N, Suzuki M (2011) Phylogenetic and physiological characterization of mesophilic and thermophilic bacteria from a sewage sludge composting process in Sapporo, Japan. World J Microbiol Biotechnol 27:333–340. https://doi.org/10.1007/ s11274-010-0463-y
Olaya-Abril A, Hidalgo-Carrillo J, Luque-Almagro VM, et al (2018) Exploring the denitrification proteome of Paracoccus denitrificans PD1222. Front Microbiol 9:1–16. https:// doi.org/10.3389/fmicb.2018.01137
Pascual MB, Sanchez-Monedero MA, Cayuela ML, et al (2020) Biochar as electron donor
for reduction of N2O by Paracoccus denitrificans FEMS Microbiol Ecol 96:1–11. https://doi.org/10.1093/femsec/ fiaa133
Patil MG, Pagare J, Patil SN, Sidhu AK (2015) Extracellular Enzymatic Activities of Endophytic Fungi Isolated from Various Medicinal Plants. IntJCurrMicrobiolAppSci 4:1035–1042
Prasad P, Singh T, Bedi S (2013) Characterization of the cellulolytic enzyme produced by Streptomyces griseorubens (Accession No. AB184139) isolated from Indian soil. J King Saud Univ - Sci 25:245–250. https:// doi.org/10.1016/j.jksus.2013.03.003
Rashad YM, Al-Askar AA, Ghoneem KM, et al (2017) Chitinolytic Streptomyces griseorubens E44G enhances the biocontrol efficacy against Fusarium wilt disease of tomato. Phytoparasitica 45:227–237. https://doi.org/10.1007/ s12600-017-0580-3
Rastogi M, Nandal M, Khosla B (2020) Microbes as vital additives for solid waste composting. Heliyon 6: e03343. https:// doi.org/10.1016/j.heliyon.2020.e03343
Raza A, Bashir S, Pothula R, et al (2021) Expression and functional characterization in yeast of an endoglucanase from Bacillus sonorensis BD92 and its impact as feed additive in commercial broilers. Int J Biol Macromol 176:364–375. https://doi. org/10.1016/j.ijbiomac.2021.02.022
Raza A, Bashir S, Tabassum R (2019) Statistical based experimental optimization for co-production of endo-glucanase and xylanase from Bacillus sonorensis BD92 with their application in biomass saccharification. Folia Microbiol (Praha) 64:295–305. https://doi.org/10.1007/ s12223-018-0654-8
Ribeiro N de Q, Souza TP, Costa LMAS, et al (2017) Aditivos microbianos no processo de compostagem. Cience Agrotecnologia 41:159–168. https://doi. org/10.1590/1413-70542017412038216
Romero M, Romero L, Álvarez-Gallego C (2009) Comparision of Three Preatments for Organic Matter Solubilization from Ofmsw. Pulse 1–4
Ros M, Raut I, Santisima-Trinidad AB, Pascual JA (2017) Relationship of microbial
communities and suppressiveness of Trichoderma fortified composts for pepper seedlings infected by Phytophthora nicotianae PLoS One 12:1–16. https:// doi.org/10.1371/journal.pone.0174069
Rosazza T, Eigentler L, Earl C, et al (2023) Bacillus subtilis extracellular protease production incurs a context-dependent cost. Mol Microbiol 120:105–121. https:// doi.org/10.1111/mmi.15110
Saffari H, Pourbabaee AA, Asgharzadeh A, Besharati H (2017) Isolation and identification of effective cellulolytic bacteria in composting process from different sources. Arch Agron Soil Sci 63:297–307. https://doi.org/10.1080/0365 0340.2016.1198006
Samaniego-Gámez BY, Reyes-Ramírez A, Moreno-Valenzuela OA, Tun-Suárez JM (2017) Resistencia sistémica inducida contra virus fitopatógenos mediada por la inoculación con la rizobacteria Bacillus spp. Rev Protección Veg 32:2224–4697
Samoylova Y V., Sorokina KN, Piligaev A V., Parmon VN (2018) Preparation of stable cross-linked enzyme aggregates (CLEAs) of a Ureibacillus thermosphaericus esterase for application in malathion removal from wastewater. Catalysts 8 https://doi.org/10.3390/catal8040154
Samoylova Y V., Sorokina KN, Romanenko M V., Parmon VN (2018b) Cloning, expression and characterization of the esterase estUT1 from Ureibacillus thermosphaericus which belongs to a new lipase family XVIII. Extremophiles 22:271–285. https://doi. org/10.1007/s00792-018-0996-9
Shafi J, Tian H, Ji M (2017) Bacillus species as versatile weapons for plant pathogens: a review. Biotechnol Biotechnol Equip 31:446–459. https://doi.org/10.1080/1310 2818.2017.1286950
Sharma A, Sharma R, Arora A, et al (2014) Insights into rapid composting of paddy straw augmented with efficient microorganism consortium. Int J Recycl Org Waste Agric 3. https://doi.org/10.1007/s40093-0140054-2
Shi M, Zhao Y, Zhu L, et al (2020) Denitrification during composting: Biochemistry, implication and perspective. Int Biodeterior Biodegrad 153. https://doi.org/10.1016/j.
ibiod.2020.105043
Shinde T, Borate V, Chavan S, Pol V (2024) Composting of sugarcane trash by using a microbial consortium. Int J Res Agron 7:641–644. https://doi. org/10.33545/2618060x.2024.v7.i4i.615
Siddiquee S, Shafawati SN, Naher L (2017) Effective composting of empty fruit bunches using potential Trichoderma strains. Biotechnol Reports 13:1–7. https://doi.org/10.1016/j.btre.2016.11.001
Sidorova TM, Asaturova AM, Homyak AI, et al (2020) Optimization of laboratory cultivation conditions for the synthesis of antifungal metabolites by Bacillus subtilis strains. Saudi J Biol Sci 27:1879–1885. https://doi.org/10.1016/j.sjbs.2020.05.002
Slivinski CT, Machado AVL, Iulek J, et al (2011) Biochemical characterisation of a glucoamylase from Aspergillus niger produced by solid-state fermentation. Brazilian Arch Biol Technol 54:559–568. https://doi.org/10.1590/S151689132011000300018
Sorokina KN, Samoylova Y V., Parmon VN (2020) Thermostable Esterase estUT1 from Ureibacillus thermosphaericus: Effect of TrxA Tag on the Enzyme Properties. Catal Ind 12:148–154. https://doi.org/10.1134/ S2070050420020099
Su J, Zhou K, Chen W, et al (2024) Enhanced organic degradation and microbial community cooperation by inoculating Bacillus licheniformis in low temperature composting. J Environ Sci (China) 143:189–200. https://doi.org/10.1016/j. jes.2023.08.037
Su Y, Liu C, Fang H, Zhang D (2020) Bacillus subtilis: A universal cell factory for industry, agriculture, biomaterials and medicine. Microb Cell Fact 19:1–12. https://doi. org/10.1186/s12934-020-01436-8
Suárez-Estrella F, Arcos-Nievas MA, López MJ, et al (2013) Biological control of plant pathogens by microorganisms isolated from agro-industrial composts. Biol Control 67:509–515. https://doi.org/10.1016/j. biocontrol.2013.10.008
Sultana M, Jahiruddin M, Rafiqul Islam M, et al (2021) Article nutrient enriched municipal solid waste compost increases yield, nutrient content and balance in rice.
Sustain 13:1–12. https://doi.org/10.3390/ su13031047
Sun B, Gu L, Bao L, et al (2020) Application of biofertilizer containing Bacillus subtilis reduced the nitrogen loss in agricultural soil. Soil Biol Biochem 148:107911. https:// doi.org/10.1016/j.soilbio.2020.107911
Teixeira RSS, Siqueira FG, De Souza MV, et al (2010) Purification and characterization studies of a thermostable β-xylanase from Aspergillus awamori. J Ind Microbiol Biotechnol 37:1041–1051. https://doi. org/10.1007/s10295-010-0751-4
Tyagi S, Kumar V, Singh J, et al (2014) Bioremediation of pulp and paper mill effluent by dominant aboriginal microbes and their consortium. Int J Environ Res 8:561–568
Voběrková S, Vaverková MD, Burešová A, et al (2017) Effect of inoculation with whiterot fungi and fungal consortium on the composting efficiency of municipal solid waste. Waste Manag 61:157–164. https:// doi.org/10.1016/j.wasman.2016.12.039
Wahyuni S, Nasution D (2019) Utilization of Trichoderma viride as organic fertilizer to induce the resistance of banana seeds on Fusarium oxysporum f. sp cubense (FOC) Utilization of Trichoderma viride as organic fertilizer to induce the resistance of banana seeds on Fusarium oxys. Earth Environ Sci 260. https://doi.org/10.1088/17551315/260/1/012149
Wang L, Wang T, Xing Z, et al (2023a) Enhanced lignocellulose degradation and composts fertility of cattle manure and wheat straw composting by Bacillus inoculation. J Environ Chem Eng 11:109940. https://doi. org/10.1016/j.jece.2023.109940
Wang W, Yan L, Cui Z, et al (2011) Characterization of a microbial consortium capable of degrading lignocellulose. Bioresour Technol 102:9321–9324. https://doi. org/10.1016/j.biortech.2011.07.065
Wang Y, Wei Y, Zhou K, et al (2023b) Regulating pH and Phanerochaete chrysosporium inoculation improved the humification and succession of fungal community at the cooling stage of composting. Bioresour Technol 384:1–9. https://doi.org/10.1016/j. biortech.2023.129291
Xi B, He X, Dang Q, et al (2015) Effect of multi-
stage inoculation on the bacterial and fungal community structure during organic municipal solid wastes composting. Bioresour Technol 196:399–405. https:// doi.org/10.1016/j.biortech.2015.07.069
Xiao F, Zhang Y, Zhang L, et al (2024) Advancing Bacillus licheniformis as a Superior Expression Platform through Promoter Engineering. Microorganisms 12:1–14. https://doi.org/10.3390/ microorganisms12081693
Xu J, Jiang Z, Li M, Li Q (2019) A compostderived thermophilic microbial consortium enhances the humification process and alters the microbial diversity during composting. J Environ Manage 243:240–249. https://doi.org/10.1016/j. jenvman.2019.05.008
Xu Z, Li R, Wu S, et al (2022) Cattle manure compost humification process by inoculation ammonia-oxidizing bacteria. Bioresour Technol 344:126314. https:// doi.org/10.1016/j.biortech.2021.126314
Zahra T, Irfan M, Nadeem M, et al (2020) Cellulase Production by Trichoderma viride in Submerged Fermentation using Response Surface Methodology. Punjab Univ J Zool 35:223–228. https://doi.org/10.17582/ JOURNAL.PUJZ/2020.35.2.223.228
Zeng GM, Huang HL, Huang DL, et al (2009) Effect of inoculating white-rot fungus during different phases on the compost maturity of agricultural wastes. Process Biochem 44:396–400. https://doi. org/10.1016/j.procbio.2008.11.012
Zhang D, Luo Y, Chu S, et al (2016) Enhancement of Cellulase and Xylanase Production Using pH-Shift and Dissolved Oxygen Control Strategy with Streptomyces griseorubens JSD-1. Appl Biochem Biotechnol 178:338–352. https://doi. org/10.1007/s12010-015-1875-9
Zhang J, Zeng G, Chen Y, et al (2014) Phanerochaete chrysosporium inoculation shapes the indigenous fungal communities during agricultural waste composting. Biodegradation 25:669–680. https://doi. org/10.1007/s10532-014-9690-5
Zhao Y, Jiang T, Han B, et al (2015) Preparation of some metabolites of timosaponin BII by biotransformation in vitro. Process Biochem 50:2182–2187. https://doi.
org/10.1016/j.procbio.2015.09.022
Zhou C, Liu Z, Huang ZL, et al (2015) A new strategy for co-composting dairy manure with rice straw: Addition of different inocula at three stages of composting. Waste Manag 40:38–43. https://doi. org/10.1016/j.wasman.2015.03.016

5. Normativa y regulación de uso de abonos orgánicos
Se conoce que existen 75 países que han promulgado efectivamente regulaciones integrales que rigen la agricultura orgánica. De los cuales, 19 países han implementado normas orgánicas que aún no se aplican plenamente, y 14 países están actualmente en el proceso de redactar la legislación (Willer et al. 2024). Dentro de este tipo de normativa, se toma en cuenta los límites de tolerancia de patógenos y la concentración mínima de metales pesados en los abonos orgánicos para garantizar la seguridad alimentaria y la salud pública.
Esto denota que cada vez más gobiernos a nivel mundial están impulsando políticas agroecológicas y mostrando su compromiso mediante la implementación de iniciativas y programas con objetivos definidos (Figura 31). Ejemplos destacados son países como Tanzania, Vietnam, Camboya, Japón y Taiwán (Esteves et al. 2021; Willer et al. 2024).
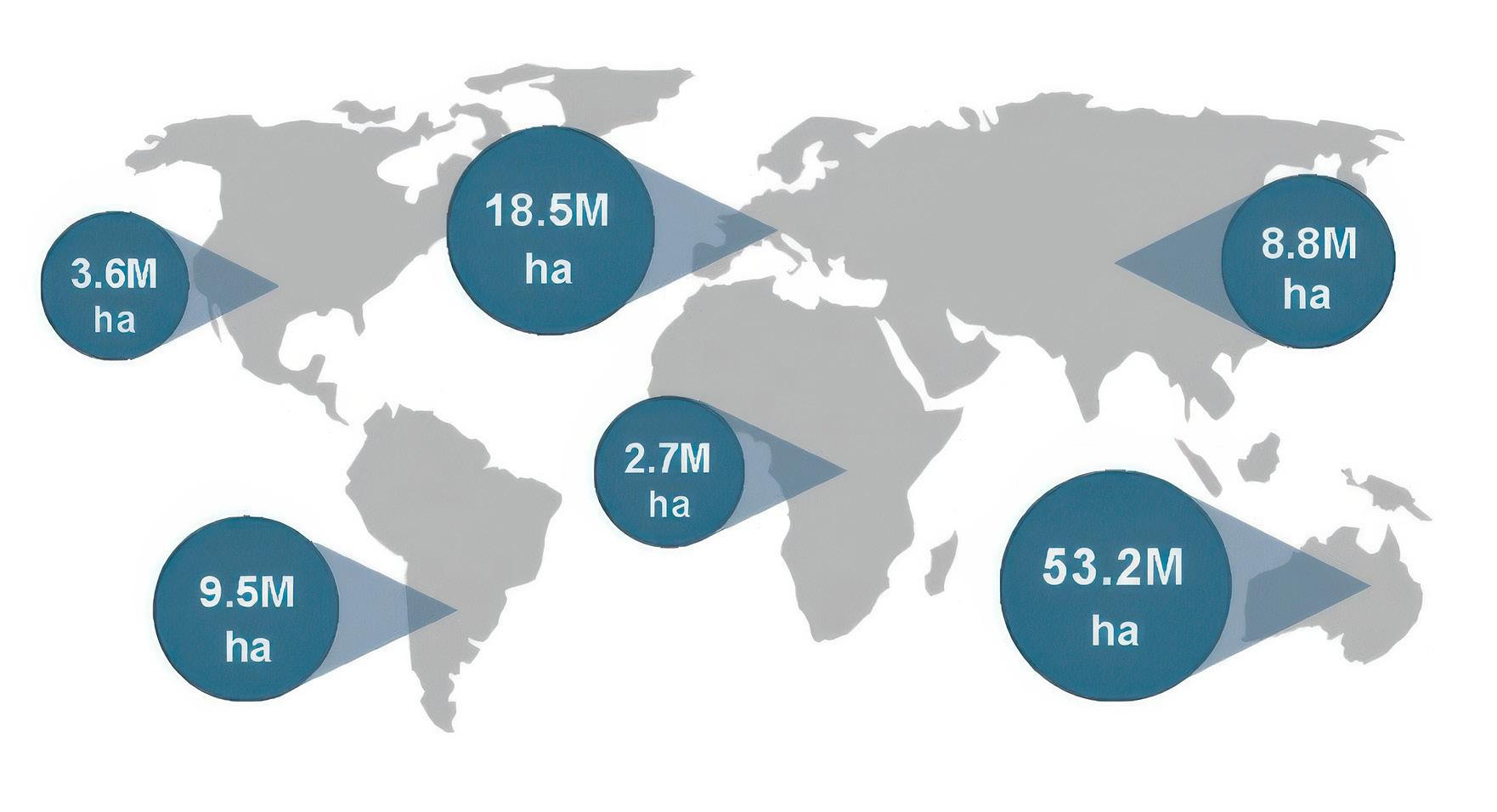
Figura 31
Distribución de tierras dedicadas a la agricultura orgánica por continente. Las áreas están indicadas en millones de hectáreas. Fuente: Willer et al., 2024.
En Ecuador, la agricultura sigue prácticas sostenibles, buscando proteger la biodiversidad y promover la economía local. La agroecología es una práctica que está cobrando relevancia, promovida tanto por organizaciones locales como por el Gobierno, que apoya la transición hacia métodos de cultivo más respetuosos con el medio ambiente (Ministerio del Ambiente 2013; Yánez Yánez et al. 2016; PNGIDS 2021). El uso de biofertilizantes, la rotación de cultivos y la reducción del uso de agroquímicos son algunos de los enfoques implementados para fomentar una agricultura más sostenible y adaptada a las condiciones ecológicas del país (Filgueira 2019; Security 2023). Siendo así, que Ecuador cuenta con la certificación Demeter en 76 granjas agrícolas, repartidas en una extensión de más de 314 hectáreas (Willer et al. 2024).
5.1. Bioinsumos en la agricultura sostenible
Los bioinsumos se clasifican en biofertilizantes y bioestimulantes, productos sustitutos para los insumos de síntesis química y una solución para una agricultura regenerativa. La diferencia radica principalmente en que los biofertilizantes cumplen la función de aportar nutrientes a las plantas, mientras que los bioestimulantes mejoran los procesos de absorción de los nutrientes (Regulation EU 2019).
5.1.1. Biofertilizante
Son formulaciones que contienen microorganismos vivos, como bacterias y hongos, cuya función se basa en colonizar las raíces de las plantas y mejorar la disponibilidad de nutrientes en el suelo. La presencia de estos organismos facilita la fijación de nitrógeno, la solubilización de fósforo y el reciclaje de otros nutrientes esenciales (Castro & Gómez, 2010).
Dentro de los biofertilizantes se encuentran los Microorganismos Promotores del Crecimiento Vegetal que presentan una amplia capacidad para inducir el crecimiento de las plantas, entre los géneros principales se destacan Pseudomonas, Azospirillum, Azotobacter, Anthrobacter Bacillus y Serratia (Ameen & Al-Homaidan, 2021; Rath et al., 2022; Zin & Badaluddin, 2020). Las funciones de estos microorganismos van desde la fijación de nitrógeno, solubilización de fosfato y la mineralización de compuestos orgánicos hasta la producción de fitohormonas (IAA, ácido abscísico (ABA), etileno (ET) y auxinas) (Sánchez et al. 2017; Rath et al. 2022).
El Instituto Colombiano de Agricultura (ICA) clasifica a los biofertilizantes en Bioabonos que son productos formulados a partir materiales orgánicos con la adición de microorganismos benéficos viables y los Inoculantes biológicos que son productos que contienen microorganismos viables capaces de actuar, directa o indirectamente (ICA 2020).
El Reglamento 2019/1009 de la Unión Europea, clasifica a los biofertilizantes como: Abono Orgánico (sólido y líquido) y Abono órgano-mineral (sólido y líquido). Además, se debe cumplir una concentración mínima de nutrientes primarios (N, P, K) en el caso de los abonos orgánicos sólidos, donde estos productos deben contener 2.5% de nitrógeno (N), 2% de pentóxido de fósforo (P2O5) y 2% de óxido de potasio (K2O) (Regulation EU 2019).
5.1.2. Bioestimulante
Son sustancias o microorganismos que, cuando se aplican a las plantas, promueven su crecimiento de manera indirecta, mejorando procesos fisiológicos como la absorción de nutrientes, la tolerancia al estrés abiótico y la calidad del cultivo (Cueva 2022). En Agrocalidad, los bioles son considerados dentro de esta categoría. El Reglamento de la Unión Europea estable que un bioestimulante vegetal es un producto que tiene como objetivo, estimular los procesos de nutrición de las plantas independientemente del contenido de nutrientes del producto (Regulation EU 2019).
5.2. Concentración Mínima de Metales Pesados
Las normativas que regulan los límites de metales pesados en insumos orgánicos son esenciales y aunque varían ligeramente entre Ecuador, Colombia, Estados Unidos y la Unión Europea, comparten un objetivo común de prevenir el deterioro de la salud del ecosistema al evitar la contaminación de los cultivos y, por ende, proteger la salud pública.
Los metales pesados son un grupo de elementos químicos que resultan indeseables debido a que no se pueden descomponer, sino que solo cambian su estado de oxidación (Chatterjee et al., 2013; Wang et al., 2019; Yang et al., 2017). Estos elementos tienen efectos perjudiciales en la salud humana y afectan la cadena alimentaria tanto en ambientes terrestres como acuáticos. Aunque están presentes de forma natural, cuando su concentración supera ciertos límites, pueden acumularse en tejidos vegetales o en órganos vitales (como el hígado, el cerebro y el tejido graso), provocando efectos generalmente crónicos a largo plazo (Yang et al., 2017).
La concentración de metales pesados varía en función de la composición de la materia prima utilizada para producir un biofertilizante. Los contenidos de metales pesados son altos en los composts originados a partir de estiércol animal o lodos de depuradora (Ingelmo et al., 2012; Mohee & Soobhany, 2014). Sin embargo, los metales pesados pueden reaccionar con la materia orgánica y su especiación puede cambiar.
En Ecuador, los límites de metales pesados en insumos orgánicos están regulados por la Agencia de Regulación y Control Fito y Zoosanitario (AGROCALIDAD). Esta entidad sigue normativas nacionales y se basa en estándares internacionales para establecer los límites permitidos de metales pesados como cadmio (Cd), plomo (Pb), mercurio (Hg), y arsénico (As) (Cueva 2022).
La normativa de Colombia establece que los abonos deben ser sometidos a análisis periódicos para asegurar que cumplan con estos límites, garantizando que su uso no resulte en la acumulación de metales pesados en el suelo. Los biofertilizantes que deseen garantizar porcentajes de carbono orgánico tanto en el registro como en la etiqueta, deberán reportar contenido de carbono orgánico oxidable total mínimo de 20%, valor de pH y concentración de metales pesados en mg/Kg (ppm): Arsénico (As) 41, Cadmio (Cd) 39, Cromo (Cr) 1200, Mercurio (Hg) 17, Níquel (Ni) 420 y Plomo (Pb) 300 (ICA 2020).
A continuación, en la Tabla 23 se compara los diferentes límites de concentración de metales pesados en insumos orgánicos.
Tabla 23
Límites establecidos de metales pesados por diferentes normativas en un insumo orgánico.
5.3. Tolerancia de microorganismos patógenos
Los microorganismos en el suelo incluyen patógenos que pueden ser perjudiciales para la salud humana y animal. En materiales como los estiércoles, pueden encontrarse bacterias patógenas, destacando Salmonella spp. y Escherichia coli, que son perjudiciales debido a su papel en las enfermedades transmitidas por alimentos (ETA) (De Corato et al. 2016; Soobhany 2018). Estos patógeno representan una de las principales amenazas en la transmisión de infecciones relacionadas con la ingesta de alimentos contaminados.
En Ecuador, el control de la calidad de los abonos orgánicos está regido por el Instituto Nacional de Investigaciones Agropecuarias (INIAP) y AGROCALIDAD donde los abonos orgánicos deben indicar la ausencia en 25 g o 25 ml de Salmonella sp., Listeria monocitogenes, Shigella spp., y Staphylococcus aureus como organismos patógenos (Cueva, 2022; Sánchez y Zambrano, 2019). Para ello, se debe realizar un análisis fitopatológico de hongos y bacterias para determinar la ausencia de fitopatógenos. El resultado de laboratorio deberá estar reportado al menos por género. Para Escherichia coli y coliformes totales se acepta límites de 1000 UFC (g-1 o ml-1) (Flores, 2022).
En Colombia, el ICA es el encargado de regular los abonos orgánicos, en este caso, la resolución No. 068370, capítulo V sobre del registro de productos bioinsumos para uso agrícola, artículo 18, párrafo 5 establece que los biofertilizantes que utilicen sustratos no estériles deben presentar los soportes de análisis de laboratorio donde se garanticen los límites máximos permitidos para patógenos donde no se pueda llegar a contaminar los suelos y cultivos (ICA 2020).
En Estados Unidos, la EPA y el USDA establecen las normativas para los abonos orgánicos. Además, el Programa Nacional Orgánico (NOP) establece requisitos para el compostaje, que deben incluir mantener la temperatura del compost a un mínimo de 55°C durante al menos 3 días consecutivos para pilas estáticas o 15 días, con al menos 5 volteos, para compostaje en pilas (EPA, 2003). Estas medidas aseguran que los abonos orgánicos sean seguros para su uso en la producción de alimentos (Departamento de agricultura de Estados Unidos 2015).
La Unión Europea regula los abonos orgánicos a través del Reglamento (UE) 2019/1009. Este reglamento establece criterios estrictos para la presencia de patógenos en los abonos orgánicos, además, toma en cuenta el límite de tolerancia de hongos fitopatógenos como Plamodiophora brasicae (Regulation EU 2019).
A continuación, en la Tabla 24 se compara los diferentes límites de concentración de patógenos en insumos orgánicos.
Tabla 24
Límites establecidos de patógenos por diferentes normativas en un fertilizante orgánico.
NMP: número más probable. UFC: Unidades formadores de colonias.
A pesar de las variaciones regionales, todas estas normativas comparten un mismo objetivo sobre minimizar los riesgos microbiológicos asociados con el uso de abonos orgánicos en la agricultura. En el caso del compostaje, el tratamiento térmico es fundamental para cumplir con estas normativas, garantizando que los abonos orgánicos sean seguros para su uso en la agricultura.
5.4. Manejo de productos microbianos
La bioseguridad en el compostaje es un aspecto crítico que garantiza que la manipulación de microorganismos, tanto aquellos presentes naturalmente como los introducidos, se realice de manera segura, protegiendo tanto a las personas como al medio ambiente. A continuación, se detallan las principales precauciones de seguridad:
5.4.1. Principales riesgos en la manipulación
Existen tres posibles escenarios de mayor riesgo (Figura 32), entre ellos está la inhalación de esporas y partículas de ciertos hongos, como Aspergillus que pueden ser liberadas al realizar el volteo manual del compost y puede provocar enfermedades respiratorias; otro factor es el contacto directo con la piel o mano-boca con los patógenos, en el caso de que el compostaje no alcanza las temperaturas adecuadas, patógenos como Salmonella y E. coli pueden sobrevivir y representar un riesgo al manipular el compost; y por último, puede existir la contaminación cruzada cuando los microorganismos patógenos presentes en el compost pueden entrar en contacto con el agua o los cultivos, representando un riesgo para la seguridad alimentaria (Brown, 2016; Burguet y Brito, 2013; Galdós et al., 2018).
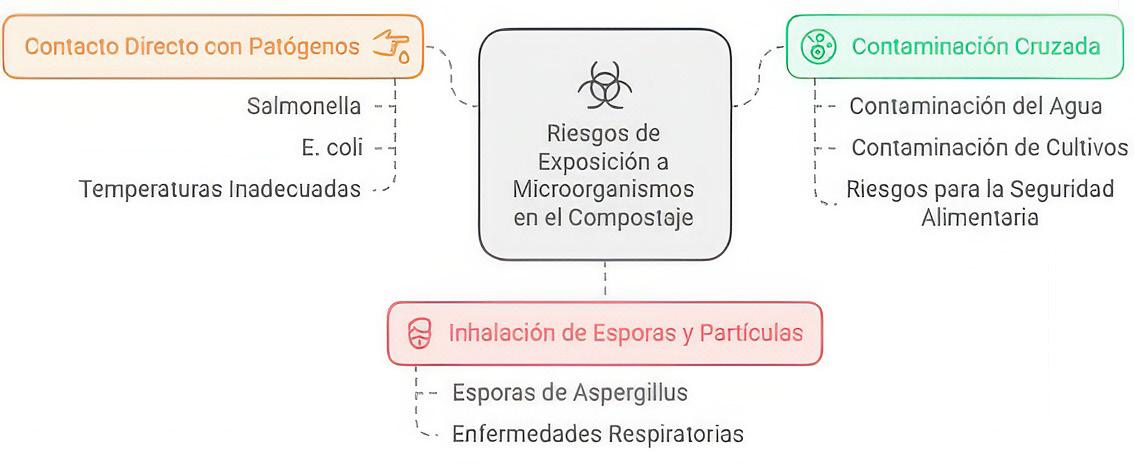
32
Principales riesgos en la manipulación de microorganismos durante el compostaje.
5.4.2. Medidas de bioseguridad para el Manejo de Inoculantes Microbianos
Para minimizar los riesgos asociados a la manipulación de microorganismos en el compostaje, es fundamental seguir varias medidas de bioseguridad. El uso de Equipo de Protección Personal (EPP) es de suma importancia, incluye el uso de guantes para evitar el contacto directo con los microorganismos al actuar como barreras de protección; portar
Figura
la mascarilla previene la inhalación de esporas fúngicas o partículas; uso de las gafas de seguridad brindan protección a los ojos ante posibles salpicaduras y las batas o monos desechables que evitan la contaminación de la ropa (Pastorino et al. 2017; Chiong et al. 2018).
Por otro lado, la higiene personal y el lavado de manos es primordial ante el manejo del compost o de los residuos que van a ser compostados. Así mismo, se debe llevar a cabo el lavado de manos antes y después de haber manipulado los productos microbianos y la desinfección de las superficies de trabajo (Brown 2016).
Es importante realizar análisis microbiológicos regulares para verificar que los niveles de patógenos se mantengan dentro de los límites aceptables según las normativas locales e internacionales. En la Unión Europea, por ejemplo, el Reglamento (UE) 2019/1009 establece límites estrictos para la presencia de microorganismos patógenos en compost y productos orgánicos (Chiong et al. 2018; Galdós et al. 2018). Cabe mencionar que, la manipulación de microorganismos para la inoculación en el proceso de compostaje debe ser realizada en un laboratorio equipado para llevar a cabo, la esterilización de todo el material utilizado mediante calor húmedo en autoclave a 121ºC durante 20 minutos (Brown 2016; Chiong et al. 2018).
5.4.3. Almacenamiento
Para un correcto almacenamiento se debe mantener los productos en lugares frescos, secos y bien ventilados. En el caso de los inoculantes comerciales, se debe seguir las indicaciones del fabricante en cuanto a temperatura y humedad. Para el almacenamiento de los microorganismos no comerciales, se debe almacenar en condiciones adecuadas (temperatura, humedad, luz) según las especificaciones de su origen y etiquetar claramente todos los recipientes con información detallada sobre el contenido, fecha de recolección y condiciones de almacenamiento (Burguet & Brito, 2013; Dong et al., 2022; Wan et al., 2020).
En relación con los microorganismos recolectados de diferentes ambientes, el almacenamiento difiere para bacterias, hongos y actinomicetos, donde es crucial mantener condiciones que preserven su viabilidad y funcionalidad a largo plazo (Tabla 25). Cabe mencionar que, en todos los casos, es importante evitar cambios bruscos de temperatura y proteger las muestras de la luz directa y de condiciones que puedan inducir oxidación o contaminación.
25
Almacenamiento de los microorganismos a corto y largo plazo.
Fuente: Hahn et al., 2019; Meenakshi et al., 2024; Scognamiglio et al., 2010
Tabla
Bibliografía
Ameen, F., & Al-Homaidan, A. A. (2021). Compost inoculated with fungi from a mangrove habitat improved the growth and disease defense of vegetable plants. Sustainability (Switzerland), 13(1), 1–13. https://doi.org/10.3390/ su13010124
Brown, N. J. (2016). Composting Safety and Health. Cornell Waste Management Institute, 1–35.
Burguet, N., & Brito, L. (2013). Medidas de bioseguridad adoptadas en el manejo con materiales biológicos en laboratorios liorad. Revista Cubana de Farmacia, 47(1), 57–66.
Castro, H., & Gómez, M. (2010). Fertilidad de suelos y fertilizantes. In H. Burbano & F. Silva (Eds.), Ciencia del Suelo. Principios básicos. Sociedad Colombiana de la Ciencia del Suelo (pp. 217–303).
Chatterjee, N., Flury, M., Hinman, C., & Cogger, C. G. (2013). Chemical and Physical Characteristics of Compost Leachates. 54. http://www.wsdot.wa.gov/research/ reports/fullreports/819.1.pdf
Chiong, M., Leisewitz, A., Márquez, F., Vironneau, L., Álvarez, M., Tischler, N., Piñones, O., & Moreno, R. (2018). Manual de Normas de Bioseguridad y Riesgos Asociados. Working in Biosafety Level 3 and 4 Laboratories: A Practical Introduction, 75–82. https:// doi.org/10.1002/9783527675357.ch8
Cueva, C. (2022). Manual Técnico Para El Registro Y Control De Fertilizantes , Enmiendas. https://www.agrocalidad. gob.ec/wp-content/uploads/2022/06/ Manual-fertilizantes-ver7.pdf
De Corato, U., Viola, E., Arcieri, G., Valerio, V., & Zimbardi, F. (2016). Use of composted agro-energy co-products and agricultural residues against soilborne pathogens in horticultural soilless systems. Scientia Horticulturae, 210, 166–179. https://doi.org/10.1016/j.
scienta.2016.07.027
Departamento de agricultura de Estados Unidos. (2015). Manual del Programa Nacional Orgánico: Directrices e instrucciones para agentes certificadores acreditados y operaciones certificadas.
Dong, L., Zhang, Z., Zhu, B., Li, S., He, Y., Lou, Y., Li, P., Zheng, H., Tian, Z., & Ma, X. (2022). Research on safety and compliance of imported microbial inoculants using high-throughput sequencing. Frontiers in Medicine, 9(September), 1–9. https://doi. org/10.3389/fmed.2022.963988
Esteves, R. C., do Amaral Vendramini, A. L., & Accioly, F. (2021). A qualitative metasynthesis study of the convergence between organic crop regulations in the United States, Brazil, and Europe. Trends in Food Science and Technology, 107(September 2019), 343–357. https:// doi.org/10.1016/j.tifs.2020.10.044
Filgueira, Á. M. C. U. M. J. J. (2019). Agricultura sostenible del Ecuador. In Centro de Investigación y Desarrollo del Ecuador (Vol. 11, Issue 1).
Galdós, M., Basulto, M., & Quesada, L. (2018). Gestión del conocimiento en Bioseguridad: su conveniencia para la disminución de riesgos en los laboratorios. EduMeCentro, 10(4), 2. http://www.revedumecentro.sld.cu
Hahn, M. W., Koll, U., & Schmidt, J. (2019). Isolation and Cultivation of Bacteria. https://doi.org/10.1007/978-3-03016775-2_10
Hugo Sánchez, V., & Zambrano Mendoza, J. L. (2019). Adopción e impacto de las tecnologías agropecuarias generadas en el Ecuador. La Granja, 30(2), 28–39. https://doi.org/10.17163/lgr. n30.2019.03
ICA. (2020). Resolución Bioinsumos N 068370. Instituto Colombiano Agropecuario - ICA, 068370(068370), 1–37. https://www.ica.gov.co/
getattachment/Areas/Agricola/ Servicios/Fertilizantes-y-Bio-insumosAgricolas/Resolucion-068370-del-27de-mayo-de-2020.pdf.aspx?lang=esCO
Ingelmo, F., Molina, M. J., Soriano, M. D., Gallardo, A., & Lapeña, L. (2012). Influence of organic matter transformations on the bioavailability of heavy metals in a sludge based compost. Journal of Environmental Management, 95(SUPPL.), S104–S109. https://doi. org/10.1016/j.jenvman.2011.04.015
Meenakshi, S., Hiremath, J., Meenakshi, M. H., & Shivaveerakumar, S. (2024). Actinomycetes: Isolation, Cultivation and its Active Biomolecules. In Journal of Pure and Applied Microbiology (Vol. 18, Issue 1, pp. 118–143). https://doi. org/10.22207/JPAM.18.1.48
Ministerio del Ambiente. (2013). Beneficios del manejo sostenible de la tierra. Ministerio Del Ambiente, 1–32. https:// bit.ly/3vCtklf
Mohee, R., & Soobhany, N. (2014). Comparison of heavy metals content in compost against vermicompost of organic solid waste: Past and present. Resources, Conservation and Recycling, 92, 206–213. https://doi.org/10.1016/j. resconrec.2014.07.004
Pastorino, B., de Lamballerie, X., & Charrel, R. (2017). Biosafety and Biosecurity in European Containment Level 3 Laboratories: Focus on French Recent Progress and Essential Requirements. Frontiers in Public Health, 5(May), 1–11. https://doi.org/10.3389/ fpubh.2017.00121
PNGIDS. (2021). Programa Nacional para la Gestión Integral de Desechos Sólidos (PNGIDS). Ministerio Del Ambiente Ecuador, 10, 98.
Rath, P. P., Das, K., & Pattanaik, S. (2022). Microbial Activity during Composting and Plant Growth Impact: A Review. Journal of Pure and Applied Microbiology,
16(1), 63–73. https://doi.org/10.22207/ JPAM.16.1.53
Regulation EU. (2019). Regulation of the european parliament and of the council laying down rules on the making available on the market of EU fertilising products and amending Regulations (EC) No 1069/2009 and (EC) No 1107/2009 and repealing Regulation (EC) No 2003/2003. Official Journal of the European Union, 2019(2003), 114. https:// eur-lex.europa.eu/legal-content/EN/ TXT/PDF/?uri=CELEX:32019R1009&from=EN
Sánchez, Ó. J., Ospina, D. A., & Montoya, S. (2017). Compost supplementation with nutrients and microorganisms in composting process. Waste Management, 69(26), 136–153. https:// doi.org/10.1016/j.wasman.2017.08.012
Scognamiglio, T., Zinchuk, R., Gumpeni, P., & Larone, D. H. (2010). Comparison of inhibitory mold agar to sabouraud dextrose agar as a primary medium for isolation of fungi. Journal of Clinical Microbiology, 48(5), 1924–1925. https:// doi.org/10.1128/JCM.01814-09
Security, F. (2023). Seguridad Alimentaria Sostenible en Ecuador y Producción Agrícola Food Security and Sustainable Agricultural Production in Ecuador. 2, 1–20.
Soobhany, N. (2018). Preliminary evaluation of pathogenic bacteria loading on organic Municipal Solid Waste compost and vermicompost. Journal of Environmental Management, 206, 763–767. https://doi. org/10.1016/j.jenvman.2017.11.029
Wan, L., Wang, X., Cong, C., Li, J., Xu, Y., Li, X., Hou, F., Wu, Y., & Wang, L. (2020). Effect of inoculating microorganisms in chicken manure composting with maize straw. Bioresource Technology, 301(December 2019), 122730. https:// doi.org/10.1016/j.biortech.2019.122730
Wang, Q., Awasthi, M. K., Zhang, Z., & Wong, J. W. C. (2019). Sustainable composting
and its environmental implications. In Sustainable Resource Recovery and Zero Waste Approaches. Elsevier B.V. https://doi.org/10.1016/B978-0-44464200-4.00009-8
Willer, H., Trávníček, J., & Bernhard, S. (2024). The World of Organic Agriculture Statistics and Emerging Trends 2024.
Yánez Yánez, W., Villacís-Aldaz, L. A., LeónGordón, O. A., Velástegui-Espín, G. P., López-Villacís, I. C., & Cruz-Tobar, S. E. (2016). Efectos de un compost enriquecido con microorganismos eficientes sobre la germinación de semillas recalcitrantes de Artocarpus altilis (Parkinson) Fosberg y Theobroma cacao L. . Journal of the Selva Andina Biosphere, 4(2), 100–108. https://doi. org/10.36610/j.jsab.2016.040200100
Yang, X., Li, Q., Tang, Z., Zhang, W., Yu, G., Shen, Q., & Zhao, F. J. (2017). Heavy metal concentrations and arsenic speciation in animal manure composts in China. Waste Management, 64, 333–339. https://doi.org/10.1016/j. wasman.2017.03.015
Zin, N. A., & Badaluddin, N. A. (2020). Biological functions of Trichoderma spp. for agriculture applications. Annals of Agricultural Sciences, 65(2), 168–178. https://doi.org/10.1016/j. aoas.2020.09.003


