aplicación de aceites esenciales
en alimentos
S. L. Recio-Cázares*, A. López-Malo y E. Palou
*Programa de Doctorado en Ciencia de Alimentos
Correo electrónico: scarlette.reciocs@udlap.mx • enrique.palou@udlap.mx
RESUMEN
En los últimos años, la creciente demanda de productos más parecidos a los naturales por parte de los consumidores ha promovido el uso de aceites esenciales (ae) en la industria alimentaria como aditivos, suplementos, insecticidas y sanitizantes. Se han estudiado distintos métodos de aplicación de ae en alimentos, sin embargo, un factor importante para su uso industrial es el efecto de estos en los atributos sensoriales, por lo que actualmente, muchas investigaciones están centradas en los métodos que permitan su incorporación en alimentos, buscando la aceptación del consumidor. Por lo tanto, el objetivo de este trabajo es la recopilación de literatura actual donde se mencionen los métodos de aplicación de ae, describiendo sus fundamentos, ventajas y desventajas, y especialmente su efecto en los atributos sensoriales. Además, se abordarán nuevos usos de los ae en industrias relacionadas con la cadena de producción de alimentos.
Palabras clave: aceites esenciales, métodos de aplicación, conservadores naturales, atributos sensoriales.
ABSTRACT
In recent years, a growing demand for more natural-like products by consumers has promoted the use of essential oils (eos) in the food industry as additives, food supplements, insecticides, and sanitizers. Different methods of applying eos in food have been studied; however, an important factor for their industrial use is the effect of eos on sensory attributes. So currently, research is mainly focused on methods that allow the incorporation of eos in foods, seeking consumer acceptance. Therefore, the objective of this work is to compile current literature reporting several methods of application of eos, describing their fundamentals, advantages and disadvantages, and especially their effect on sensory attributes. Moreover, new uses of eos in industries related to the food production chain are considered.
Keywords: essential oils, application methods, natural preservatives, sensory attributes.
INTRODUCCIÓN
La vida útil, las propiedades nutricionales, los atributos sensoriales y la calidad microbiana de los productos alimenticios son aspectos importantes para los consumidores. Debido a esto, las industrias alimentarias buscan hacer uso de sustancias o compuestos que aseguren la inocuidad de sus productos sin comprometer su calidad (Cueva et al., 2011).
Durante la elaboración de alimentos se utilizan distintos conservadores para asegurar la inocuidad y calidad de estos (Prakash y Kiran, 2016). No obstante, la mayoría de los conservadores utilizados son sintéticos y algunos han sido asociados con problemas a la salud a largo plazo, como fallas renales, hipertiroidismo, cirrosis hepática, cáncer, entre otros (Scotter y Castle, 2004; Faleiro, 2011; Manning, 2015; Silano y Silano, 2015; Singh y Ghandi, 2015; Szűcs et al., 2019). Como resultado, existe una demanda creciente de productos naturales que puedan servir como conservadores (Cueva et al., 2011).
Los aceites esenciales (ae) son metabolitos secundarios obtenidos de diferentes plantas, que han sido ampliamente utilizados como conservadores naturales debido a que son, en muchos casos, más seguros que los sintéticos tanto para los seres humanos como el medioambiente (Burt, 2004). Asimismo, se ha demostrado que tienen propiedades biológicas, entre las que destacan las antibacterianas, antiparasitarias, antifúngicas, antioxidantes, desinfectantes e insecticidas (SolórzanoSantos y Miranda-Novales, 2012).
Debido a sus propiedades, los ae han sido utilizados en la industria agroalimentaria. Se han aplicado directamente en los sistemas alimentarios, ya sea en forma de polvo o líquido, por medio de películas o recubrimientos comestibles, en fase vapor, como nanoemulsiones y liposomas (Gyawali e Ibrahim, 2014).
Sin embargo, su aplicación en la industria es limitada debido a su impacto en el sabor y olor, especialmente a concentraciones en las que muchos ae presentan un efecto antimicrobiano. Por lo que, la concentración más aceptable en términos tanto de seguridad como de calidad alimentaria estará en función de tipo
de ae, así como de sus compuestos activos, el tipo de alimento al que se incorpora, el método de aplicación y los métodos de producción de alimentos (Goñi et al., 2009).
Por todo lo anterior, el objetivo de este trabajo es la recopilación de literatura actual donde se mencionen diversos métodos de aplicación de los ae, describiendo sus fundamentos, alcances y limitaciones, especialmente su efecto en los atributos sensoriales. Además, se abordarán nuevos usos de los ae en industrias relacionadas con la cadena de producción de alimentos.
REVISIÓN BIBLIOGRÁFICA
1. Métodos de aplicación de aceites esenciales en alimentos y sus efectos en atributos sensoriales
1.1. Contacto directo
Este método de aplicación consiste en agregar el ae, ya sea en forma de polvo o líquido, directamente en los sistemas alimentarios. Sin embargo, su aplicación es limitada, debido al fuerte olor y sabor que los ae imparten a los productos alimenticios, especialmente a concentraciones en las que son considerados agentes antimicrobianos. Por lo que muy pocos ae cumplen con las características químicas (composición cualitativa y cuantitativa, concentración requerida), físicas (solubilidad, volatilidad) y sensoriales (fuertes sabores o aromas) requeridas para ser aplicados por contacto directo (Ribeiro-Santos et al., 2017).
Estudios in vitro e in vivo, han reportado que el efecto antimicrobiano de los ae se debe a la presencia de diferentes compuestos activos que actúan de manera sinérgica (Cava et al., 2007; Budka y Khan, 2010; Jahani et al., 2020). No obstante, Fisher y Phillips (2006) mencionaron que las concentraciones obtenidas en condiciones in vitro no siempre son eficaces cuando se aplican en un alimento, por lo que la concentración de ae necesaria para observar el mismo efecto podría aumentar y afectar los niveles sensoriales aceptables (Ribeiro-Santos et al., 2017).
1.1.1. Aplicación de aceites esenciales en contacto directo y su efecto en diversos atributos sensoriales La aplicación de ae por contacto directo se ha probado en diferentes alimentos, como productos cárnicos (hamburguesas de carne, carne molida, salchichas, pescado, entre otros) y frutas (piña, mango, guayaba y manzana). En general, los ae de canela (Cinnamomum verum), hierbabuena (Mentha spicata), toronjil (Melissa officinalis), ajedrea (Satureja montana) y enebro (Juniperus communis) han presentado buenos resultados contra bacterias patógenas como Pseudomonas aeruginosa, Salmonella Thypimurium y Escherichia coli (De Sousa Guedes et al., 2016; Ghabraie et al., 2016; Sharma et al. 2017; Abdeldaiem et al., 2017; Nikkhah y Hashemi, 2020). Por su parte, los ae de romero (Salvia rosmarinus) y canela reducen y previenen el crecimiento de bacterias Gram positivas como Staphylococcus aureus y Listeria monocytogenes (Ghabraie et al., 2016; Abdeldaiem et al., 2017), las cuales son más sensibles a la presencia de ae (Bhavaniramya et al., 2019).
El efecto sobre los atributos sensoriales de ae aplicados por contacto directo en sistemas alimentarios se muestra en la tabla I. Algunos autores reportan su aplicación en la conservación del pescado, Abdeldaiem et al. (2017) adicionaron 4 tipos de ae: hinojo (Foeniculum vulgare), cardamomo (Elettaria cardamomum), canela o romero en dedos de pescado y evaluaron su aceptabilidad (apariencia, olor y textura) durante el almacenamiento a -4 °C; observándose que, además de alargar la vida útil del producto a un total de 12 días durante el almacenamiento (la de la muestra de control sin ae fue de 4 días), también mejoraron sus características sensoriales. El ae de romero presentó los mejores resultados, ya que fue aceptado en los tres atributos mencionados. Por otro lado, Emir Çoban et al. (2014) evaluaron los ae de romero, tomillo (Thymus vulgaris), salvia (Salvia officinalis) y clavo (Syzygium aromaticum), en filetes de trucha ahumada almacenados a 4 °C. A diferencia de los resultados anteriores, los filetes de pescado con ae de romero tuvieron una aceptabilidad sensorial más baja en comparación con los otros ae utilizados (tomillo, salvia y clavo), lo cual podría
deberse a que los filetes de trucha se evaluaron ahumados y no crudos, como los dedos de pescado, afectando la afinidad de los ae con el producto alimenticio. Burt (2004) menciona que el efecto sensorial negativo puede ser minimizado mediante una correcta selección del ae según el tipo de alimento, por ejemplo, la canela tiene mejor afinidad con diversas frutas y sus productos (Pateiro et al., 2018; Perricone et al., 2015).
Un claro ejemplo de lo anterior se observó en burfi (un postre de la India) adicionado con ae de clavo y curri (Murraya koenigii) (Badola et al., 2018) y en jugos de guayaba, piña, mango y manzana cashew con ae de hierbabuena y toronjil (De Sousa Guedes et al., 2016). En ambos estudios se logró la inhibición de microorganismos; sin embargo, las propiedades sensoriales se vieron afectadas negativamente, ya que el sabor del ae disminuía la aceptabilidad sensorial (sabor, olor, resabio o aceptabilidad general).
Uno de los usos más comunes de los ae por contacto directo es en productos cárnicos. Se ha reportado que el ae de canela al 0.25 % y una combinación de canela china (Cinnamomum cassia) y corteza de canela al 0.05 % generan una buena aceptabilidad sensorial en carne lista para comer y salchichas de pollo, respectivamente (Ghabraie et al., 2016; Sharma et al., 2017). Al igual que la pimienta china en sashimi, donde los atributos sensoriales estudiados fueron aceptables (He et al., 2019).
Por otro lado, el ae de ajedrea, el cual es poco común, se aplicó en salchichas de cerdo (Šojić et al., 2019) y carne de res marinada con vino (Vasilijević et al., 2019). En ambos trabajos se hace notar que el sabor del ae afectó negativamente los atributos sensoriales (olor y sabor). Sin embargo, el método de extracción del ae puede modificar su composición. Šojić et al. (2019) reportaron que el ae de ajedrea extraído mediante hidrodestilación poseía un olor picante, debido a que la concentración de terpenos volátiles fue más alta, a diferencia del ae extraído mediante fluido supercrítico, esta tecnología disminuyó la cantidad de compuestos volátiles (terpenos) y puede mejorar la aceptabilidad sensorial al reducir los olores/sabores picantes.
Efecto de algunos aceites esenciales aplicados por contacto directo sobre los atributos sensoriales de diversos alimentos
Aceite Concentración Alimento
Salvia (Salvia officinalis), romero (Salvia rosmarinus), tomillo (Thymus vulgaris) y clavo (Syzygium aromaticum)
600 ppm
Hisopo (Hyssopus officinalis) y cilantro (Coriandrum sativum) 0.02 %
Hierbabuena (Mentha spicata) y toronjil (Melissa officinalis)
Combinación de canela china (Cinnamomun cassia) y corteza de canela (Cinnamomum verum)
Hinojo (Foeniculum vulgare), cardamomo (Elettaria cardamomum), canela y romero
Clavo, albahaca (Ocimum basilicum), tomillo y canela china
Clavo y curri (Murraya koenigii)
0.625 y 1.25 μL/mL, respectivamente
0.05 %
Trucha arcoíris ahumada
Atributo sensorial
Apariencia, sabor y olor
Carne de res molida Olor y sabor
Jugos de piña, mango, guayaba y nuez de la India
Carne lista para comer y carne molida magra
10 mL/kg
0.25, 0.125, 0.25 y 0.125 %
Dedos de pescado
Apariencia, olor, viscosidad, sabor, resabio y aceptabilidad general
Sabor y olor en ambos tipos de carne
Apariencia, olor y textura
Resultados principales
El ae de clavo tuvo mayor aceptación en todos los atributos.
ae de cilantro tuvo mayor aceptación en ambos atributos.
Ambos ae tuvieron efectos negativos en el sabor, el resabio y la aceptabilidad general. El ae de hierbabuena tuvo mayor aceptación en los otros atributos estudiados.
El ae tuvo mayor aceptación en ambas carnes, en ambos atributos.
El ae de romero tuvo mayor aceptación en todos los atributos hasta los 12 días de almacenamiento.
Salchichas de pollo
0.05, 0.15 y 0.25 % Burfi
Apariencia, sabor, jugosidad, textura y aceptabilidad general
Sabor, cuerpo, textura, color, apariencia y aceptabilidad general
El ae de canela china al 0.25 % tuvo mayor aceptación en todos los atributos.
El sabor y aceptabilidad general se vieron afectados conforme se aumentó la concentración del ae. El ae de clavo al 0.15 % tuvo la mayor aceptación.
Referencias
Emir Çoban et al., 2014
Michalczyk et al., 2012
De Sousa Guedes et al., 2016
Ghabraie et al., 2016
Abdeldaiem et al., 2017
Sharma et al., 2017
Badola et al., 2018
Ajedrea (Satureja montana)
0.075 y 0.150 μL/g
Salchichas de cerdo
Sabor, olor y aceptabilidad general
El ae obtenido por extracción con fluido supercrítico a una concentración de 0.075 μL/g tuvo mayor aceptación en todos los atributos.
et al., 2019
Tabla I.
Efecto de algunos aceites esenciales aplicados por contacto directo sobre los atributos sensoriales de diversos alimentos (continuación)
Aceite
Concentración Alimento
Enebro (Juniperus communis) y ajedrea
0.0625, 0.125, 0.25 y 0.5 %
Carne de res marinada con vino
Pimienta china (Zanthoxylum piperitum) 0.3 % Sashimi
Combinación de tomillo, romero y canela
ae = aceite esencial/aceites esenciales.
0.078, 0.625 y 0.156 g/L, respectivamente Jujube
Atributo sensorial
Sabor marinado y defectos de olor
Color, olor, textura y aceptabilidad general
Textura, sabor, aroma y aceptabilidad general
Resultados principales
El ae de enebro al 0.25 % tuvo mayor aceptación en ambos atributos. Como defectos de sabor y olor, se reporta un sabor picante, agudo y artificial con el ae de ajedrea.
Tuvo buena aceptabilidad en todos los atributos hasta los 15 días de almacenamiento.
La combinación de ae no generó efectos negativos en los atributos evaluados.
Referencias
Vasilijević et al., 2019
He et al., 2019
Nikkhah y Hashemi, 2020
1.2. Fase vapor
Este método de aplicación consiste en evaluar el vapor generado por los ae sobre distintos sistemas alimentarios. Se ha reportado que tiene un mayor efecto antimicrobiano en comparación con los ae en forma líquida aplicados por contacto directo, debido a que se requiere más volumen de ae líquido para lograr el mismo efecto biológico que en forma gaseosa (Reyes-Jurado et al., 2019).
La volatilidad de los ae depende de factores como el peso molecular de sus componentes, ya que entre más pequeña sea la molécula, su difusividad es más alta (Saifullah et al., 2019); adicionalmente, al elevar la temperatura del ambiente fomenta la migración de los compuestos volátiles (Ribeiro-Santos et al., 2017). Debido a que no existe un método estándar y a la variación en la composición (determinada tanto cualitativa como cuantitativamente) de los ae, la comparación de los resultados de la actividad antimicrobiana en fase vapor es difícil. Uno de los métodos más prometedores para este propósito parece ser la
prueba de volatilización de disco (Mejía-Garibay et al., 2015), el cual puede ser modificado para la conservación de alimentos generando «empaques activos», que permiten la volatilización y migración de los co ponentes activos del «disco en el empaque» al alimento (Ribeiro-Santos et al., 2017).
1.2.1. Aplicación de aceites esenciales en fase vapor y su efecto en diversos atributos sensoriales El efecto en distintos atributos sensoriales de una selección de ae aplicados en fase vapor en diferentes sistemas alimentarios se enlista en la tabla II. Se han utilizado ae contra diversos mohos patógenos (Aspergillus, Alternaria, Penicillium y Botrytis) en frutas como manzanas y uvas. En el caso específico de las uvas, se realizó un análisis sensorial a través de una prueba triangular para observar si el tiempo de exposición del ae afectaba los atributos sensoriales; los resultados indicaron que la exposición a ae de lavanda (Lavandula), romero (Salvia rosmarinus) y menta (Mentha piperita) podían ser percibidos
Tabla I.
incluso 24 horas después del tratamiento, debido a la gran cantidad de compuestos aromáticos que contienen (Servili et al., 2017). Por otro lado, Frankova et al. (2016) evaluaron la aceptabilidad sensorial de manzanas tratadas con ae de orégano (Origanum vulgare), canela (Cinnamomum verum) y clavo (Syzygium aromaticum) en fase vapor con una escala no estructurada; al aumentarse la concentración de los ae de orégano y canela presentaron aromas diferentes a la manzana. Aunque el ae de orégano mostró mejor actividad antifúngica (cmi: 2 µL de ae/laire), afectó negativamente los atributos sensoriales
cuando se usaba a esta concentración. Esto puede deberse a que se ha reportado que el ae de orégano proporciona un sabor herbáceo, a diferencia del sabor dulce que imparte el ae de canela (Pateiro et al., 2018; Perricone et al., 2015). Este último también ha sido evaluado y aceptado en vegetales como champiñones (Jiang et al., 2015). Por lo tanto, una solución para minimizar los cambios sensoriales es reducir el tiempo de exposición a los vapores de los aceites o prolongar el tiempo entre el tratamiento y el consumo del producto tratado (Servili et al., 2017).
Efecto de algunos aceites esenciales aplicados por fase vapor sobre los atributos sensoriales de diversos alimentos
Aceite Concentración Alimento Atributo sensorial Resultados principales Referencias
Canela (Cinnamomum verum), tomillo (Thymus vulgaris) y clavo (Syzygium aromaticum)
5 μL/L Champiñones Olor y apariencia
Orégano (Origanum vulgare), canela y clavo 4 y 16 mL/L Manzanas Sabor y olor
Lavanda (Lavandula), romero (Salvia rosmarinus) y menta (Mentha piperita)
Pimienta gorda (Pimenta dioica), romero y tomillo
5 mL Uvas Sabor
0.8-11.7 mL/ Laire
Semillas de alfalfa germinadas
Tomillo, comino, clavo y orégano 125-500 μL
ae = aceite esencial/aceites esenciales.
Rebanadas de pan
Grado de diferencia en general entre las semillas germinadas con y sin ae
Aceptabilidad general de olor y sabor
El ae de canela tuvo mayor aceptación en ambos atributos durante 20 días de almacenamiento.
El ae de canela tuvo mayor aceptación en ambos atributos hasta los 14 días de almacenamiento.
Los jueces percibieron la diferencia entre el control sin ae y con ae hasta las 24 horas. El ae más percibido fue el de lavanda.
Jiang et al., 2015
Frankova et al., 2016
Servili et al., 2017
Hubo una diferencia moderada en las semillas con ae de pimienta gorda y tomillo, y diferencia ligera con el ae de tomillo. Además, los germinados de las semillas tratadas con ae de pimienta gorda tuvieron mayor aceptación sensorial. LorenzoLeal et al., 2019
Hubo buena aceptabilidad con ae de tomillo y comino hasta los 4 días de almacenamiento.
Císarová et al. (2020)
Tabla II.
De igual forma, Mani López et al. (2018) y Císarová et al. (2020) evaluaron la exposición de diferentes ae en pan para la inhibición de mohos de los géneros Penicillium [ae de zacate limón (Cymbopogon citratus)] y Aspergillus [ae de tomillo (Thymus vulgaris), clavo, comino (Cuminum cyminum) y orégano], respectivamente. En ambos trabajos reportan que los atributos sensoriales de olor, sabor y aceptabilidad general fueron aceptables incluso después de 21 días de almacenamiento con el ae de zacate limón y 14 días con los ae de tomillo y comino. Por otra parte, Lorenzo-Leal, Palou y López-Malo (2019) evaluaron la actividad antimicrobiana en fase de vapor de ae de pimienta gorda (Pimenta dioica), tomillo y romero, contra Listeria monocytogenes y Salmonella Typhimurium en semillas de alfalfa. Además, realizaron un análisis sensorial a través de una prueba triangular con la que encontraron que la diferencia entre las muestras fue moderada entre ae de pimienta gorda y tomillo, y ligeramente para las semillas germinadas tratadas con ae de romero. Estos autores destacan que la mayoría de los panelistas prefirieron los brotes de las semillas tratadas con ae de pimienta gorda y de romero a las muestras de control que no contenían ae. Esto comprueba que algunos ae en fase vapor a una concentración adecuada pueden tener un impacto positivo en los atributos sensoriales de diversos productos alimenticios.
1.3. Nanoemulsiones
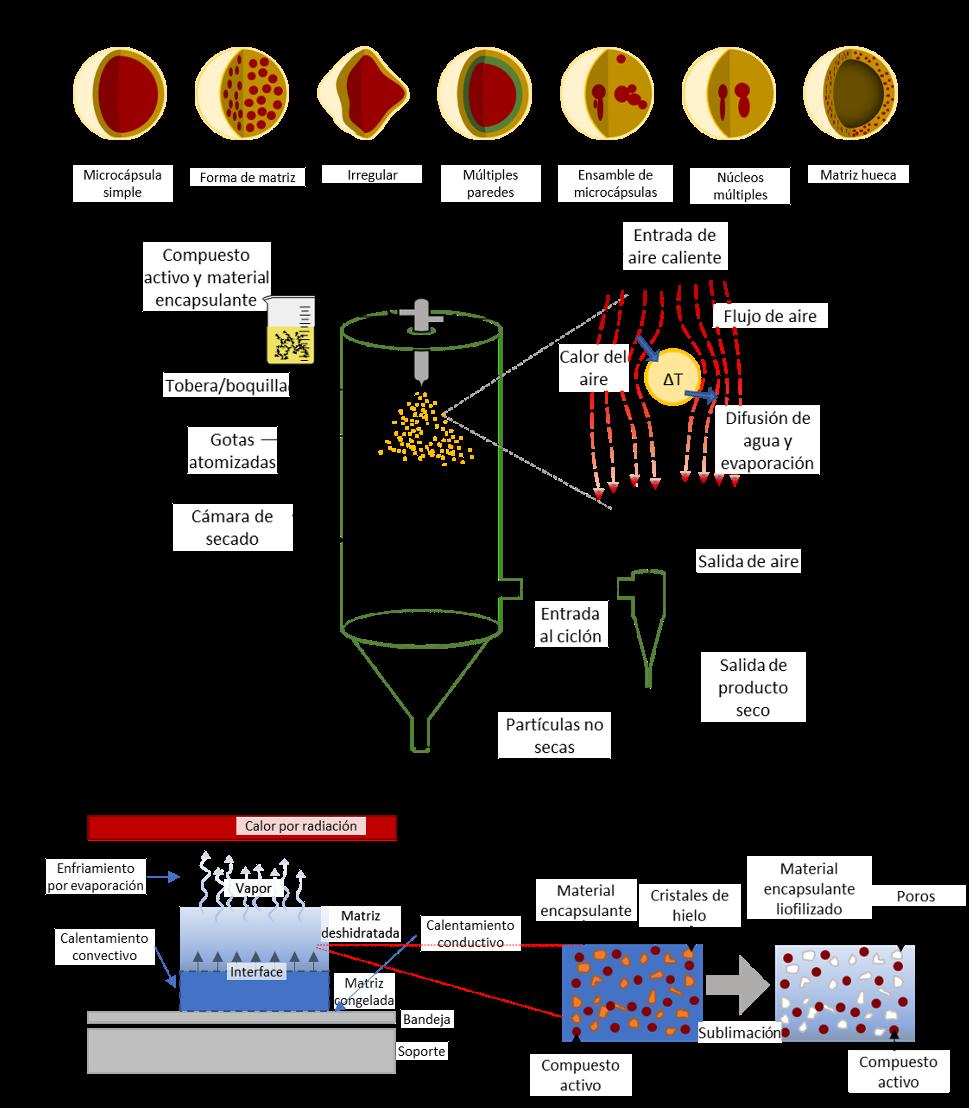
Otra alternativa para la aplicación de ae es la encapsulación; esta se define como una tecnología que permite atrapar componentes sensibles en una matriz homogénea o heterogénea, lo cual le brinda protección e incrementa su estabilidad a condiciones adversas, además, ayuda a controlar su liberación (García-Ceja y López-Malo, 2012). Existen diferentes métodos de encapsulación, entre ellos se encuentra la coacervación simple o compleja, el secado por aspersión, el recubrimiento por lecho fluidizado, y las emulsiones/nanoemulsiones (Velázquez-Contreras et al., 2014).
Las emulsiones han demostrado ser buenas portadoras para la entrega de sustancias lipídicas como lo son los ae. Las emulsiones se componen de dos fases, la oleosa (o) y la acuosa (w). La emulsión aceite en agua (o/w) consiste en pequeñas gotas de aceite como fase dispersa contenidas en el agua como fase continua; y en la emulsión de agua en aceite (w/o) las gotas de
la fase dispersa son de agua y la fase continua es aceite. En la industria de alimentos, las emulsiones más comunes son del tipo o/w, así como las micro- o nano-emulsiones.
La característica primordial de las nanoemulsiones es su tamaño de gota (entre 20 y 1000 nm) y se puede preparar utilizando diferentes métodos, como la homogenización a alta presión, la microfluidización, la homogenización mecánica a alta velocidad, ultrasonidos, emulsión espontánea y la inversión de fase, entre otros (Jin et al., 2016; Walker et al., 2015). Su importancia radica en que el tamaño de partícula nanométrica permite aumentar la biodisponibilidad, bioeficiencia y estabilidad (McClements, 2011).
1.3.1. Aplicación de aceites esenciales por nanoemulsiones en alimentos y su efecto en diversos atributos sensoriales
El uso e incorporación de las nanoemulsiones de ae en alimentos es una técnica que ha ganado relevancia, debido a que el incremento de la superficie de contacto mejora la actividad antimicrobiana, ya que los componentes activos están más disponibles (Otoni et al., 2014). Aunque las nanoemulsiones han tenido mayor aplicación en alimentos que otros métodos, el enfoque sensorial aún es escaso, puesto que pocos reportes han estudiado el efecto de las nanoemulsiones en las propiedades sensoriales de los alimentos.
La aplicación de nanoemulsiones en alimentos se ha probado principalmente en la conservación de pescados (tabla III). Ozogul et al. (2017) evaluaron el efecto antimicrobiano de nanoemulsiones con ae de romero (Salvia rosmarinus), laurel (Laurus nobilis), tomillo (Thymus vulgaris) y sábila (Aloe vera) sobre la calidad de trucha arcoíris. Los resultados del análisis microbiológico indicaron que los ae redujeron hasta 3 Log ufc/g el recuento de bacterias anaerobias mesofílicas, bacterias psicrótrofas (principales microorganismos responsables del deterioro de pescado fresco) y enterobacterias; además incrementó 3 días más la vida útil del pescado tratado con los ae, llegando a un total de 17 días (la de la muestra de control sin ae fue de 14 días). Del mismo modo, Alfonzo et al. (2017) evaluaron el efecto antimicrobiano del ae de limón (Citrus × limon) contra las mismas bacterias, teniendo como resultado la reducción de solo 2 Log ufc/g. En cuanto a la evaluación sensorial, ambos estudios
utilizaron una escala hedónica de 9 y 10 puntos, respectivamente, para la evaluación del sabor, olor y textura en los pescados. Los ae probados en ambos pescados tuvieron una buena aceptabilidad en todos los atributos, con excepción del ae de romero, el cual obtuvo la calificación más baja debido a que le daba un sabor amargo a la trucha.
Del mismo modo, se han evaluado nanoemulsiones con ae de orégano (Origanum vulgare), tomillo y anís estrellado (Illicium verum) en carpa china (Huang et al., 2018), así como orégano, tomillo y ajo en salmón y bacalao (Pedrós-Garrido et al.,
2020). En ambos estudios se determinó que el ae de orégano, además de presentar la mejor actividad antimicrobiana contra Pseudomonas (reducción de 1 Log ufc/g) y Listeria (cmi 0.02 %), también mostraba la mejor aceptabilidad sensorial en cuanto a olor, color y textura y podía alargar la vida útil en carpa china por 2 días, logrando un total de 4 días (la de la muestra de control sin ae fue de 2 días). Sin embargo, los ae probados en bacalao enmascaraban el sabor característico de este pescado, por lo que no todos los ae tienen un efecto positivo en las propiedades sensoriales de los pescados.
Efecto de algunos aceites esenciales aplicados por nanoemulsiones sobre los atributos sensoriales de diversos alimentos
Limón (Citrus × limon) 0.3 y 1 % Sardinas saladas
Romero (Salvia rosmarinus), laurel, tomillo (Thymus vulgaris) y sábila (Aloe vera) 4 % Trucha arcoíris
Orégano (Origanum vulgare), tomillo y anís estrellado 0.1 % Carpa china
Canela (Cinnamomum verum), romero y orégano 10 % Apio
Orégano y romero 40 y 80 μL/mL, respectivamente
Zacate limón (Cymbopogon citratus), ajo (Allium sativum), orégano y tomillo
Queso fresco
0.2, 0.4 y 0.8 % Salmón y bacalao
ae = aceite esencial/aceites esenciales.
Olor, textura y sabor
Sabor, olor, color y aceptabilidad general
Color, olor, textura y aceptabilidad general
Olor, color, textura, apariencia, sabor y aceptabilidad general
Olor, apariencia, sabor y textura
Generar los atributos sensoriales para cada uno
Hubo buena aceptación en todos los atributos con ambas concentraciones de ae.
Los ae de tomillo y laurel tuvieron mayor aceptación en todos los atributos.
El ae de orégano tuvo mayor aceptación en todos los atributos hasta los 10 días de almacenamiento.
El ae de canela tuvo mayor aceptación en todos los atributos.
Ambos ae tuvieron un efecto positivo en aroma y sabor hasta los 21 días de almacenamiento.
El ae de orégano al 0.2 % tuvo la mayor aceptación para el salmón. Mientras que todos los ae probados enmascararon el sabor propio del bacalao.
Alfonzo et al., 2017
Ozogul et al., 2017
Huang et al., 2018
Dávila et al., 2019
Diniz-Silva et al., 2019
PedrósGarrido et al., 2020
Tabla III.
Por su parte, Dávila-Rodríguez, López-Malo, Palou, RamírezCorona y Jiménez-Munguía (2019) evaluaron la actividad antimicrobiana contra E. coli y Listeria monocytogenes de los ae de canela (Cinnamomum verum), romero y orégano encapsulados por nanoemulsiones (o/w), comparando con los mismos aceites no encapsulados. Estos últimos fueron menos eficaces que las nanoemulsiones. Para inhibir la misma carga microbiana (5 Log ufc/g) se requirió 50 % menos ae cuando se aplicó en nanoemulsión. Al mismo tiempo, realizaron el análisis sensorial utilizando una escala hedónica de 9 puntos, evaluando los atributos de olor, color, textura, apariencia, sabor y aceptabilidad general, aplicando las nanoemulsiones de los ae en apio fresco. Como resultado encontraron que el apio con las nanoemulsiones del ae de canela fue el mejor aceptado, ya que enmascaraba el sabor típico del apio, el cual no suele ser tan aceptado por algunos consumidores. Al igual que Ozogul et al. (2017), encontraron que el ae de romero era el menos aceptado debido al aroma herbáceo y sabor amargo que imparte, por lo que este ae no es aceptado en varios tipos de alimentos.
1.4. Películas comestibles
El uso de materiales biodegradables puede ser un medio importante para la incorporación de ae. Debido a esto y con la finalidad de reducir el consumo de empaques plásticos, se han generado empaques biodegradables, así como películas y recubrimientos comestibles para el almacenamiento de alimentos frescos o procesados.
Una película comestible (pc) es una capa preformada de materiales comestibles, elaborada a base de biopolímeros como carbohidratos, proteínas y lípidos (Sánchez Aldana et al., 2014), que puede aplicarse sobre los alimentos para prolongar su vida útil. Estudios previos han demostrado que las películas elaboradas a partir de carbohidratos son ampliamente utilizadas debido a que presentan buenas propiedades mecánicas y actúan como barrera contra compuestos de baja polaridad; sin embargo, pueden presentar alta permeabilidad contra la humedad (Parra et al., 2004). Por otro lado, las películas comestibles elaboradas a base de proteína, como la gelatina, son excelentes barreras al oxígeno, dióxido de carbono y algunos compuestos aromáticos; no obstante, sus propiedades mecánicas no son tan eficientes (Jang et al., 2011).
Además de la matriz polimérica principal, es necesaria la incorporación de algunos aditivos como agentes plastificantes. Los cuales son sustancias no volátiles de bajo peso molecular que, al adicionarse a un material polimérico, modifican las propiedades físicas y mecánicas, por ejemplo, su flexibilidad, manejabilidad y habilidad de extensión (Osés et al., 2009).
1.4.1. Aplicación de aceites esenciales por películas en alimentos y su efecto en diversos atributos sensoriales La aplicación de empaques comestibles como coadyuvantes en la conservación (almacenamiento, calidad y seguridad) de alimentos, es una de las soluciones más eficaces para asegurar la inocuidad de estos (Gómez-Estaca et al., 2014).
Las películas comestibles pueden aplicarse como envoltura, método de embalaje, o separación entre capas (Ribeiro-Santos et al., 2017). No obstante, cuando la película recubre directamente al producto, al ser ingerida puede modificar las características sensoriales del producto. Por otro lado, la migración de los compuestos presentes en la película puede ocurrir, similar al fenómeno de transferencia de masa en la fase vapor, dando el mismo resultado en la alteración del aroma y sabor. A pesar de esto, muy pocos estudios han realizado el análisis sensorial para evaluar la aceptabilidad de los diferentes alimentos que han utilizado películas comestibles a base de ae como método de conservación.
En la tabla IV se presentan diversos estudios donde se han aplicado películas comestibles con ae y su efecto en las características sensoriales de diversos productos cárnicos y pescados. En general, los ae modificaron los atributos sensoriales estudiados. Se han evaluado pc de alginato de sodio con ae de orégano (Origanum vulgare) y romero (Salvia rosmarinus) en filetes de carne de res (Vital, Guerrero, Kempinski et al., 2018), y con ae de jengibre (Zingiber officinale) y orégano en filetes de tilapia (Vital, Guerrero, Ornaghi et al., 2018).
Los resultados indicaron que las pc con ae de orégano afectaban negativamente las propiedades sensoriales (olor, sabor y aceptabilidad general) en ambos productos y los evaluadores preferían los filetes de res y tilapia con ae de romero y jengibre, respectivamente. No obstante, se ha reportado que el ae de orégano aplicado en pc de quitosano en pargo rojo, mantiene buenos atributos sensoriales (olor y sabor) incluso después de 20 días de almacenamiento (Vatavali et al., 2013).
Un ae menos común es el de zataria (Zataria multiflora), cuyo componente principal es el timol (sabor a especias y madera), el cual fue incorporado a una pc de almidón y confirió buenas propiedades sensoriales a empanadas de carne molida (Amiri et al., 2019). Este mismo compuesto se encuentra presente en el ae de tomillo (Thymus vulgaris), el cual ha sido evaluado por Agrimonti
et al. (2019) en las afectaciones al color, olor y sabor de carne molida; Yemiş y Candoğan (2017), por su parte, analizaron la apariencia, color, olor, sabor y aceptabilidad general en carne de res; mientras que Soncu et al. (2018) estudiaron el olor, color, sabor y aceptabilidad general en salchichas. Todos estos autores destacan que el uso del ae de tomillo generó buenos atributos sensoriales.
Efecto de algunos aceites esenciales aplicados por películas comestibles (PC) sobre los atributos sensoriales de diversos alimentos
pc Aceite Concentración Alimento Atributo sensorial Resultados principales Referencias
Quitosano
Orégano (Origanum vulgare) 0.1 Pargo rojo Olor y sabor
Quitosano Anís (Pimpinella anisum) 1.5 y 2
Hamburguesas de pollo Olor y sabor
Hubo buena aceptabilidad para ambos atributos durante 20 días de almacenamiento.
Hubo buena aceptabilidad en todos los atributos durante 12 días de almacenamiento.
Soya
Tomillo (Thymus vulgaris) y orégano 1, 2 y 3
Carne de res
Goma farsi
Clavo (Syzygium aromaticum) y tomillo 1 y 2
Quitosano
Romero (Salvia rosmarinus) y tomillo
Alginato de sodio
Alginato de sodio
Trucha arcoíris
0.2-0.1 Sucuk
Orégano y romero 0.1
Jengibre (Zingiber officinale) y orégano 0.1
Filetes de carne de res
Filetes de tilapia
Apariencia, color, olor, sabor, textura y aceptabilidad general de la carne cocida
Textura, color, olor y aceptabilidad general
Olor, color, sabor y aceptabilidad general de las salchichas crudas y cocidas
Sabor, olor y aceptabilidad general
Olor, sabor, textura y aceptabilidad general
No hubo diferencia significativa en apariencia, color, olor y textura.El ae de tomillo al 1 % tuvo mayor aceptación en sabor y aceptabilidad general.
La combinación de los ae al 2 % mostró mejores resultados en todos los atributos hasta el día 12 de almacenamiento.
El ae de tomillo al 1 % tuvo mayor aceptación en todos los atributos en ambas salchichas.
La pc con ae de romero tuvo mayor aceptación en todos los atributos.
El olor fue el único atributo que mostró diferencias; el ae de jengibre tuvo mayor aceptación.
Vatavali et al., 2013
Mahdavi et al., 2017
Yemiş y Candoğan, 2017
Dehghani et al., 2018
Soncu et al., 2018
Vital, Guerrero, Kempinski et al., 2018
Vital, Guerrero, Ornaghi et al., 2018
Tabla IV.
Efecto de algunos aceites esenciales aplicados por películas comestibles (PC) sobre los atributos sensoriales de diversos alimentos (continuación)
pc Aceite Concentración Alimento
Celulosa
Orégano, tomillo y canela (Cinnamomum verum) 1
Almidón Zataria (Zataria multiflora) 6
ae = aceite esencial/aceites esenciales.
Carne de res picada
Empanadas de carne molida
Color, olor y sabor en la carne cocida
Sabor, color y olor de la carne cocida.
Los ae de orégano y tomillo tuvieron mayor aceptación en todos los atributos, en relación con el ae de canela, hasta los 15 días de almacenamiento.
Hubo buena aceptación en todos los atributos evaluados.
Agrimonti et al., 2019
Amiri et al., 2019
1.5. Liposomas
Los liposomas son otro método de encapsulación y se definen como vesículas con una estructura esférica, constituidas por una bicapa fosfolípida (o dos o más de esas bicapas, separadas por regiones líquidas) que encierran material acuoso o soluble en lípidos. Los liposomas, cuyo tamaño puede variar desde unos pocos nanómetros hasta 1 µm de diámetro, suelen emplearse como sistemas de suministro de una amplia variedad de compuestos bioactivos como los ae (Khorasani et al., 2018).
El proceso convencional de fabricación de liposomas se basa en el uso de solventes orgánicos para disolver las unidades de construcción de los liposomas, la eliminación del disolvente para formar la bicapa lipídica y la subsiguiente dispersión de alta energía de la bicapa en agua para formar los liposomas. Sin embargo, su baja capacidad de carga, el alto costo de los materiales y la necesidad de procedimientos de preparación complejos, limitan su aplicación en producciones a gran escala (Fathi et al., 2019).
1.5.1. Aplicación de aceites esenciales por liposomas en alimentos y su efecto en diversos atributos sensoriales Para superar la volatilidad e inestabilidad de los ae, se han estudiado las ventajas de los liposomas para encapsular los ae y
protegerlos contra entornos externos que podrían acelerar su volatilidad (Lin et al., 2018). Shidhaye et al. (2008) informaron que los liposomas podrían mejorar la estabilidad química y la biodisponibilidad de los antimicrobianos hidrofóbicos como los ae y sus compuestos bioactivos. Se ha estudiado el efecto antimicrobiano de los liposomas con distintos ae, tales como curri, eucalipto, canela, romero y nuez moscada (Valencia-Sullca et al., 2016; Cui et al., 2017; Tang y Ge, 2017 ; Maccioni et al., 2019; Zhu, Li, Cui y Lin, 2020 ); sin embargo, la aplicación y el estudio en alimentos aún es escaso.
En general, los pocos estudios de liposomas con ae aplicados en alimentos se han evaluado en distintos tipos de carne. Lin et al. (2019) evaluaron el efecto antimicrobiano del ae de crisantemo (Chrysanthemum) en diferentes concentraciones en liposomas (de triple capa) de quitosano y pectina, contra Campylobacter jejuni en pollo fresco. Se demostró que los liposomas presentan una alta actividad antimicrobiana contra C. jejuni en el pollo, logrando reducir 3.2 Log ufc/mL. Además, realizaron un análisis sensorial a través de una escala hedónica de 7 puntos, en donde evaluaron diferentes atributos como el color, olor, sabor y aceptación general del pollo. Los resultados indicaron que los liposomas de triple capa con el ae de crisantemo no solo podían minimizar el deterioro del pollo, sino también mantener su calidad sensorial.
Tabla IV.
Por otra parte, Wu et al. (2019) realizaron liposomas para encapsular ae de laurel (Laurus nobilis) (50 µL) y nanopartículas de plata, mezclados con quitosano con el fin de recubrir películas de polietileno para empacar carne de cerdo. Se demostró una buena actividad antimicrobiana contra Escherichia coli y Staphylococcus aureus, manteniendo la calidad de la carne de cerdo a 4 °C durante 15 d. De forma paralela, se realizó el análisis sensorial a través del método descriptivo; los parámetros del análisis sensorial de la carne incluyeron color, viscosidad, elasticidad y sabor, evaluados y calificados con una escala de 1 a 10. La evaluación sensorial mostró que los liposomas tienen un efecto positivo en la conservación de la calidad de la carne de cerdo (color, sabor, viscosidad y elasticidad) y podrían utilizarse para prolongar la vida útil de la carne de cerdo fresca almacenada a 4 °C.
2. Ventajas y desventajas de los métodos de aplicación de AE en alimentos
En la tabla V se enlistan las ventajas y desventajas de los métodos de aplicación de ae mencionados en esta revisión. Dentro de estas se destaca que el uso de nanoemulsiones o aplicados en fase vapor requieren una menor cantidad de ae para lograr los mismos efectos que los generados por contacto directo (Tongnuanchan y Benjakul, 2014), debido primordialmente a que se incrementa el área de exposición (Císarová et al., 2016; Artiga-Artigas et al., 2018). Sin embargo, un aspecto negativo es que no hay métodos estandarizados para la aplicación de ae en fase vapor y la inestabilidad de las nanoemulsiones puede generar separación de las fases y no lograr una correcta incorporación del ae en el alimento (Císarová et al., 2016; ArtigaArtigas et al., 2018).
En el caso de las películas comestibles, se requieren métodos de dispersión previos para su preparación; sin embargo, son efectivas y reemplazan el uso de materiales como el plástico (Umaraw et al., 2020), el cual es muy utilizado en el área alimentaria. Por otra parte, el uso de liposomas parece ser un método
prometedor; sin embargo, su aplicación en alimentos todavía es escasa. Esto representa una oportunidad de investigación para su posible empleo en la conservación de alimentos.
Debido a las diferencias inherentes en los métodos de aplicación, no puede realizarse una adecuada comparación entre ellos, ya que tanto las concentraciones de los ae como su liberación controlada o la migración de algunos de sus compuestos, pueden alterar las propiedades sensoriales de los alimentos tratados. Con base en los diferentes estudios, el método de aplicación influirá en las características sensoriales de los productos alimenticios, por lo que la selección del método dependerá del ae y de la matriz alimenticia. En general, se busca que el uso de ae en alimentos proporcione atributos sensoriales favorables. Es importante enfatizar que, de acuerdo con los compuestos activos de cada ae, estos brindarán características sensoriales diferentes en cada grupo alimenticio, por lo que es fundamental conocer qué compuestos son responsables del aroma y/o sabor.
3. Nuevas tendencias de aceites esenciales en la industria agroalimentaria
3.1. Sanitización de superficies
La inocuidad de los productos alimenticios es una preocupación fundamental tanto para los consumidores como para la industria alimentaria. La presencia de microorganismos patógenos puede reducirse al aumentar las medidas de higiene a lo largo de toda la cadena alimentaria, implementando prácticas seguras durante la preparación y almacenamiento de alimentos. Sin embargo, no siempre es suficiente; en ocasiones las superficies contaminadas por bacterias, como Salmonella y Escherichia coli, pueden comprometer la seguridad alimentaria (Chia et al., 2009; Duffy et al., 2009).
Para reducir la propagación de bacterias a través de superficies contaminadas, se utilizan rutinariamente productos químicos para sanitizar y desinfectar las superficies que están en contacto con alimentos (Phillips, 2016). Sin embargo,
Alimento Atributo sensorial
Contacto directo
Fase vapor
La aplicación es fácil y rápida. La actividad antimicrobiana contra distintos microorganismos patógenos es buena.
Nanoemulsiones
Se requiere menor cantidad de ae para lograr la inactivación microbiana. Pueden no afectar las propiedades sensoriales.
Presentan una mayor relación superficie activa/volumen debido a su tamaño de gota, lo que mejora el transporte de compuestos activos a través de membranas biológicas. Hay una reducción de la concentración de ae para la inactivación microbiana. Mejora la aceptación sensorial debido a la baja concentración de ae
Películas comestibles
Liposomas
Son biodegradables, previenen la pérdida de humedad, el desvanecimiento del color, la oxidación de lípidos y la formación de olores desagradables. Pueden mejorar la vida útil de algunos alimentos.
Tienen buena dispersabilidad en agua, buena biocompatibilidad, baja difusión, liberación lenta y actividad residual prolongada.
ae = aceite esencial/aceites esenciales.
Resultados principales
Se requiere de mayor cantidad de ae, lo que afecta las propiedades sensoriales de los alimentos. Proporcionan un olor y sabor fuerte a los alimentos. Tienen una alta hidrofobicidad y volatilidad.
Es necesario crear empaques o sistemas modelo para su aplicación. El componente activo de los aceites puede migrar por difusión a la superficie del alimento, afectando sus características sensoriales. La composición del alimento puede interactuar con los ae, reteniendo algunos compuestos.
Se requiere el uso de surfactantes y estabilizantes. Su estabilidad no ha sido probada en algunos sistemas alimenticios.
El costo de inversión para nuevos equipos de producción es alto. En muchos casos hacen falta materiales con las funcionalidades deseadas y hay una falta de regulaciones. Su aplicación se dificulta en algunos tipos de alimentos.
Su efectividad durante el almacenamiento es poca y no alarga la vida útil. Su aplicación en alimentos es escasa.
Referencias
Tongnuanchan y Benjakul, 2014
Císarová et al., 2016; RibeiroSantos et al., 2017
Artiga-Artigas et al., 2018
Umaraw et al., 2020
Chen et al., 2019
Ventajas y desventajas de diversos métodos de aplicación de aceites esenciales en alimentos
Tabla V.
la presencia de productos como cloro, peróxido y peroxiácido, pueden generar subproductos, por ejemplo, trihalometanos, ácidos haloacéticos y otros compuestos potencialmente cancerígenos; por otro lado, algunos sanitizantes pueden contribuir al desarrollo de resistencia en las bacterias (Coroneo et al., 2017; Halden, 2014; Xue et al., 2017).
Los ae han demostrado ser una alternativa al uso de agentes químicos sintéticos, puesto que son seguros para el consumo humano y amigables con el medioambiente (Sánchez y Aznar, 2015). Falcó, Verdeguer, Aznar, Sánchez y Randazzo (2018) evaluaron nueve ae para desarrollar una solución desinfectante natural para tratar superficies de contacto con alimentos. Entre los ae probados, el ae de tomillo andaluz (Thymbra capitata), que contiene hasta un 93.31 % de monoterpenos oxigenados (principalmente carvacrol), mostró la mayor actividad antimicrobiana. La solución desinfectante se evaluó en superficies de acero inoxidable, vidrio y polipropileno. Los resultados mostraron que concentraciones de 25 % del ae de T. capitata aplicadas durante 10 minutos reducen los niveles de Escherichia coli y Salmonella enterica en 3 y 1 Log ufc/g, respectivamente, en las tres superficies probadas.
Por otra parte, los ae se han probado solo en superficies de acero inoxidable como en los trabajos de Valeriano et al. 2012, donde evaluaron soluciones desinfectantes de ae de menta (Menta piperita) y zacate limón (Cymbopogon citratus) al 0.8 % contra la biopelícula de Salmonella entérica; los resultados demostraron que, después de 20 y 40 minutos de contacto, ambos ae inhibían por completo el crecimiento bacteriano. De igual manera, Pereira et al. (2019) encontraron una reducción de 5.8 Log ufc/g en la biopelícula producida por Pseudomonas aeruginosa al aplicar una solución desinfectante que contenía 0.4 % de ae de canela.
Estos estudios confirman que el uso de ae es una alternativa fácil para preparar soluciones desinfectantes que pueden reducir la colonización microbiana de las superficies de procesamiento de alimentos. Asimismo, los ae podrían proporcio-
nar métodos alternativos o complementarios para la desinfección eficiente de superficies industriales poco contaminadas. Sin embargo, es importante enfatizar que algunos parámetros, como el tiempo de contacto y la temperatura, requieren ajustes para la aplicación de agentes antimicrobianos a escala industrial. De acuerdo con De Oliveira, Brugnera, Nascimento, Batista y Piccoli (2012), no se produce un olor residual a concentraciones bajas de soluciones con ae; una ventaja más para su aplicación.
3.2. Insecticidas
Las plagas de insectos representan una pérdida económica considerable para la industria agroalimentaria. El uso excesivo de insecticidas sintéticos como organofosforados y piretroides para controlar las plagas ha provocado problemas graves como la resistencia de plagas y la contaminación de ambientes terrestres y acuáticos (Campos et al., 2018; Pourya et al., 2018). El desarrollo de estrategias ecológicas se ha considerado alrededor del mundo para reemplazar estos pesticidas convencionales.
En consecuencia, los bioinsecticidas basados en ae parecen ser un método adecuado para el control de plagas de insectos (Campolo et al., 2017; Mossa, 2016; Yeom et al., 2018).
Los ae y sus componentes activos son selectivos, biodegradables y disminuyen los efectos negativos sobre los animales y el medio ambiente de los insecticidas sintéticos (Bedini et al., 2018; Hashem et al., 2018; Karan et al., 2018).
Yeguerman et al. (2020) evaluaron los ae de menta (Menta piperita), palmarosa (Cymbopogon martinii), geranio (Geranium), lavanda (Lavandula) y romero (Salvia rosmarinus) contra la cucaracha alemana (Blatella germanica L). Los ae de menta y palmarosa fueron los más eficaces, con una concentración letal de LC 50 de 245.95 y 246 µg/cm2, respectivamente; y se incluyeron en una matriz de polietilenglicol para obtener nanopartículas poliméricas cargadas con ae. Las nanopartículas potenciaron los efectos letales y subletales de los ae
de menta y palmarosa contra B. germanica. Las nanopartículas se diseñaron debido a que algunos factores de los ae, como su baja solubilidad en agua, alta volatilidad y rápida oxidación de sus componentes, limitan su uso en aplicaciones a gran escala (Campos et al., 2018; Werdin González et al., 2017). Por lo que estos resultados sugieren que los nanoinsecticidas podrían utilizarse con éxito para controlar distintas plagas. De la misma manera, el ae de menta fue evaluado por Pang et al. (2020) contra el gorgojo de harina (Tribolium castaneum), el gorgojo de tabaco (Lasioderma serricorne) y Liposcelis bostrychophila, obteniendo concentraciones letales LC50 que fueron de 18.1, 68.4 y 0.6 mg/Laire, respectivamente.
En la misma línea, Matos et al. (2020) evaluaron los ae de anís estrella (Illicium verum) y clavo (Eugenia caryophyllus) contra el gorgojo (Callossobruchus maculatus) del caupí (Vigna unguiculata), que es una legumbre comestible en Asia y América (Lopes et al., 2018). Los valores de las concentraciones letales LC 50 y LC95 en la prueba de contacto se estimaron en 9.62 y 32.78, así como 1.27 y 11.95 µL/20 g, para los ae de anís estrella y clavo, respectivamente. En las pruebas de repelencia, ambos ae redujeron la cantidad de huevos e insectos. Cabe señalar que el gorgojo es un insecto de importancia en la industria agroalimentaria, ya que es muy común que aparezca en distintos cereales, por lo que esta aplicación podría extenderse a la conservación de otros productos como el sorgo, arroz, trigo y cebada, entre otros.
3.3. Efecto de los aceites esenciales sobre la microbiota de animales
El uso dietético de los antibióticos se ha aprovechado durante décadas en la producción animal; sin embargo, la creciente preocupación pública por los posibles riesgos para la salud y las repercusiones ambientales del uso excesivo de antibióticos como promotores del crecimiento en la producción animal ha dado lugar a la prohibición de su aplicación dietética en algunos países. Por lo cual, las industrias que intervienen en la cadena
de producción animal, incluidos los productores primarios, los procesadores, los distribuidores y los minoristas, buscan constantemente sustancias eficaces, seguras y rentables con propiedades similares (Simitzis, 2017).
Debido a esto, los ae tienen el potencial de convertirse en una nueva generación de productos para la nutrición y la salud animal, debido a sus efectos positivos en la digestión, la comunidad microbiana intestinal, el rendimiento del crecimiento y el bienestar (Bento et al., 2013; Bianchini et al., 2014; Giannenas et al., 2013).
Los efectos de los suplementos dietéticos de los ae en la microbiota intestinal, la morfología y la actividad enzimática y los parámetros de rendimiento del crecimiento han sido estudiados ampliamente, en especial en pollos de engorda (Alp et al., 2012; Abudabos y Alyemni, 2013; Khattak et al., 2014; Bozkurt et al., 2016). En general, los ae parecen suprimir los microorganismos dañinos, estimulan la microbiota benéfica como Lactobacillus, regulan la actividad de las enzimas y protegen las vellosidades intestinales, pero no propician el aumento de peso corporal. La disminución del número de bacterias patógenas en el intestino y el mantenimiento de un equilibrio bacteriano adecuado entre el número de bacterias benéficas y las bacterias dañinas en el intestino parecen mejorar la capacidad de las células epiteliales para regenerar las vellosidades y así mejorar la capacidad de absorción intestinal (Bozkurt et al., 2016).
Por otro lado, el efecto de los ae también se ha estudiado en la alimentación de peces. Giannenas et al. (2012) evaluaron un producto comercial encapsulado que contenía los principales componentes (carvacrol y timol) del ae de tomillo (Thymus vulgaris), en la dieta de la trucha arcoíris. El objetivo de su trabajo fue evaluar el efecto de los diferentes tratamientos dietéticos en las poblaciones de bacterias intestinales; se emplearon técnicas microbiológicas convencionales con medios de agar selectivo. Tanto el carvacrol como el timol modularon las comunidades microbianas intestinales al reducir las bacterias anaeróbicas totales, mientras que las cargas de lactobacilos fueron menores en el grupo tratado con timol en comparación con los
grupos tratados con carvacrol y el de control. De igual forma, Ran et al. (2016) evaluaron los efectos de un producto comercial de mezcla de timol y carvacrol en tilapia híbrida (Oreochromis niloticus); después de 6 semanas de alimentación observaron un cambio positivo en la microbiota intestinal de la tilapia.
CONCLUSIONES Y COMENTARIOS FINALES
Los compuestos químicos derivados de fuentes naturales, como los aceites esenciales aquí estudiados, han demostrado su eficacia como antimicrobianos. Sin embargo, es importante enfatizar que el método de aplicación de dichos aceites esenciales o sus componentes dependerá de factores como el alimento a tratar y el tipo de microorganismos a eliminar. Asimismo, el reto actual radica en su uso para incrementar la seguridad alimentaria sin afectar la calidad del producto, en especial sus atributos sensoriales. En este contexto, el análisis sensorial de alimentos tratados con aceites esenciales o sus componentes es escaso, y abre un campo de investigación para identificar las preferencias de los consumidores. Por otro lado, el uso de aceites esenciales en las diferentes etapas de la cadena de producción de alimentos es prometedor, lo que podría favorecer la disminución de su costo, a fin de que el empleo de conservadores naturales sea competitivo frente a otros procesos de conservación convencionales.
AGRADECIMIENTOS
S. L. Recio Cázares agradece a la Universidad de las Américas Puebla (udlap) y al Consejo Nacional de Humanidades, Ciencia y Tecnología (conahcyt) —hoy Secretaría de Ciencia, Humanidades, Tecnología e Innovación (secihti)—, por el financiamiento para sus estudios de doctorado.
REFERENCIAS
Abdeldaiem, M. H., Ali, H. G. y Ramadan, M. F. (2017). Impact of different essential oils on the characteristics of refrigerated carp (Cyprinus carpio) fish fingers. Journal of Food Measurement and Characterization, 11(3), 1412-1420.
Abudabos, A. M. y Alyemni, A. H. (2013). The effect of feeding a commercial essential oil product to broilers challenged with Clostridium perfringens. African Journal of Microbiology Research, 7(36), 4539-4545.
Agrimonti, C., White, J., Tonetti, S. y Marmiroli, N. (2019). Antimicrobial activity of cellulosic pads amended with emulsions of essential oils of oregano, thyme and cinnamon against microorganisms in minced beef meat. International Journal of Food Microbiology, 305, 108246.
Alfonzo, A., Martorana, A., Guarrasi, V., Barbera, M., Gaglio, R., Santulli, A., Settanni L., Galati A., Moschetti G. y Francesca, N. (2017). Effect of the lemon essential oils on the safety and sensory quality of salted sardines (Sardina pilchardus Walbaum 1792). Food Control, 73, 1265-1274.
Alp, M., Midilli, M., Kocabağli, N., Yilmaz, H., Turan, N., Gargılı, A. y Acar, N. (2012). The effects of dietary oregano essential oil on live performance, carcass yield, serum immunoglobulin G level, and oocyst count in broilers. Journal of Applied Poultry Research, 21(3), 630-636.
Amiri, E., Aminzare, M., Azar, H. H. y Mehrasbi, M. R. (2019). Combined antioxidant and sensory effects of corn starch films with nanoemulsion of Zataria multiflora essential oil fortified with cinnamaldehyde on fresh ground beef patties. Meat Science, 153, 66-74.
Artiga-Artigas, M., Guerra-Rosas, M., Morales-Castro, J., Salvia-Trujillo, L. y Martín-Belloso, O. (2018). Influence of essential oils and pectin on nanoemulsion formulation: a ternary phase experimental approach. Food Hydrocolloids, 81, 209-219.
Badola, R., Panjagari, N. R., Singh, R. R. B., Singh, A. K. y Prasad, W. G. (2018). Effect of clove bud and curry leaf essential oils on the anti-oxidative and anti-microbial activity of burfi, a milk-based confection. Journal of Food Science and Technology, 55(12), 4802-4810.
Bedini, S., Flamini, G., Ascrizzi, R., Venturi, F., Ferroni, G., Bader, A., Girardi, J. y Conti, B. (2018). Essential oils sensory quality and their bioactivity against the mosquito Aedes albopictus. Scientific Reports, 8(1), 17857.
Bento, M. H. L., Ouwehand, A. C., Tiihonen, K., Lahtinen, S., Nurminen, P., Saarinen, M. T., Schulze, H., Mygind, T. y Fischer, J. (2013). Essential oils and their
use in animal feeds for monogastric animals — Effects on feed quality, gut microbiota, growth performance and food safety: a review. Veterinarni Medicina, 58(9), 449-458.
Bhavaniramya, S., Vishnupriya, S., Al-Aboody, M. S., Vijayakumar, R. y Baskaran, D. (2019). Role of essential oils in food safety: Antimicrobial and antioxidant applications. Grain & Oil Science and Technology, 2(2), 49-55.
Bianchini, A., Stratton, J., Weier, S., Cano, C. y Garcia, L. M. (2014). Use of essential oils and plant extracts to control microbial contamination in pet food products. Journal of Food Processing and Technology, 5, 357.
Budka, D. y Khan, N. (2010). The effect of Ocimum basilicum, Thymus vulgaris, Origanum vulgare essential oils on Bacillus cereus in rice-based foods. European Journal of Biological Sciences, 2(1), 17-20.
Bozkurt, M., Ege, G., Aysul, N., Akşit, H., Tüzün, A. E., Küçükyılmaz, K., Borum, A. E., Uygun, M., Akşit, D., Aypak, S., Şimşek, E., Seyrek, K., Koçer, B., Bintaş, E., y Orojpour, A. (2016). Effect of anticoccidial monensin with oregano essential oil on broilers experimentally challenged with mixed Eimeria spp. Poultry Science, 95(8), 1858-1868.
Burt, S. (2004). Essential oils: their antibacterial properties and potential applications in foods—a review. International Journal of Food Microbiology, 94(3), 223-253.
Campolo, O., Cherif, A., Ricupero, M., Siscaro, G., Grissa-Lebdi, K., Russo, A., Cucci, L. M., Di Pietro, P., Satriano, C., Desneux, N., Biondi, A., Zappalà, L., y Palmeri, V. (2017). Citrus peel essential oil nanoformulations to control the tomato borer, chemical properties and biological activity. Scientific Reports, 7(1), 13036.
Campos, E. V. R., Proença, P. L. F., Oliveira, J. L., Bakshi, M., Abhilash, P. C. y Fraceto, L. F. (2018). Use of botanical insecticides for sustainable agriculture: future perspectives. Ecological Indicators, 105, 483-495.
Cava, R., Nowak, E., Taboada, A. y Marin-Iniesta, F. (2007). Antimicrobial activity of clove and cinnamon essential oils against Listeria monocytogenes in pasteurized milk. Journal of Food Protection, 70(12), 2757-2763.
Chen, W., Cheng, F., Swing, C. J., Xia, S. y Zhang, X. (2019). Modulation effect of core-wall ratio on the stability and antibacterial activity of cinnamaldehyde liposomes. Chemistry and Physics of Lipids, 223, 104790.
Chia, T. W. R., Goulter, R. M., McMeekin, T., Dykes, G. A. y Fegan, N. (2009). Attachment of different Salmonella serovars to materials commonly used in a poultry processing plant. Food Microbiology, 26(8), 853-859.
Císarová, M., Tančinová, D., Medo, J., y Kačániová, M. (2016). The in vitro effect
of selected essential oils on the growth and mycotoxin production of Aspergillus species. Journal of Environmental Science and Health, Part. B, Pesticides, Food Contaminants, and Agricultural Wastes, 51(10), 668-674.
Císarová, M., Hleba, L., Medo, J., Tančinová, D., Mašková, Z., Čuboň, J., Kováčik A., Foltinová D., Božik M. y Klouček, P. (2020). The in vitro and in situ effect of selected essential oils in vapour phase against bread spoilage toxicogenic aspergilli. Food Control, 110, 107007.
Coroneo, V., Carraro, V., Marras, B., Marrucci, A., Succa, S., Meloni, B., Pinna, A., Angioni, A., Sanna, A. y Schintu, M. (2017). Presence of Trihalomethanes in ready-to-eat vegetables disinfected with chlorine. Food Additives and Contaminants, 1-7.
Cueva, C., Moreno-Arribas, M. V., Bartolomé, B., Salazar, Ó., Vicente, M. F. y Bills, G. F. (2011). Antibiosis of vineyard ecosystem fungi against food-borne microorganisms. Research in Microbiology, 162(10), 1043-1051.
Cui, H., Li, W. y Lin, L. (2017). Antibacterial activity of liposome containing curry plant essential oil against Bacillus cereus in rice. Journal of Food Safety, 37(2), e12302.
Dávila-Rodríguez, M., López-Malo, A., Palou, E., Ramírez-Corona, N., y JiménezMunguía, M. T. (2019). Antimicrobial activity of nanoemulsions of cinnamon, rosemary, and oregano essential oils on fresh celery. LWT- Food Science and Technology, 112(7), 108247.
De Oliveira, M. M. M., Brugnera, D. F., do Nascimento, J. A., Batista, N. N. y Piccoli, R. H. (2012). Cinnamon essential oil and cinnamaldehyde in the control of bacterial biofilms formed on stainless steel surfaces. European Food Research and Technology, 234(5), 821-832.
De Sousa Guedes, J. P., Da Costa Medeiros, J. A., De Souza e Silva, R. S., De Sousa, J. M. B., da Conceição, M. L. y de Souza, E. L. (2016). The efficacy of Mentha arvensis L. and M. piperita L. essential oils in reducing pathogenic bacteria and maintaining quality characteristics in cashew, guava, mango, and pineapple juices. International Journal of Food Microbiology, 238, 183–192.
Dehghani, P., Hosseini, S. M. H., Golmakani, M.-T., Majdinasab, M. y Esteghlal, S. (2018). Shelf-life extension of refrigerated rainbow trout fillets using total Farsi gum-based coatings containing clove and thyme essential oils emulsions. Food Hydrocolloids, 77, 677-688.
Diniz-Silva, H. T., Batista de Sousa, J., da Silva Guedes, J., Ramos do Egypto Queiroga, R. de C., Madruga, M. S., Tavares, J. F. y Magnani, M. (2019). A synergistic mixture of Origanum vulgare L. and Rosmarinus officinalis L. essential oils to preser-
ve overall quality and control Escherichia coli O157:H7 in fresh cheese during storage. LWT- Food Science and Technology, 112, 107781.
Dos Passos Braga, S., Lundgren, G. A., Macedo, S. A., Tavares, J. F., Dos Santos Vieira, W. A., Câmara, M. P. S. y De Souza, E. L. (2019). Application of coatings formed by chitosan and Mentha essential oils to control anthracnose caused by Colletotrichum gloesporioides and C. brevisporum in papaya (Carica papaya L.) fruit. International Journal of Biological Macromolecules, 139, 631-639.
Duffy, L. L., O’Callaghan, D., McAuley, C. M., Fegan, N. y Craven, H. M. (2009). Virulence properties of Escherichia coli isolated from Australian dairy powder factory environments. International Dairy Journal, 19(3), 178-179.
Emir Çoban, Ö., Patir, B. y Yilmaz, Ö. (2014). Protective effect of essential oils on the shelf life of smoked and vacuum-packed rainbow trout (Oncorhynchus mykiss W.1792) fillets. Journal of Food Science and Technology, 51(10), 2741-2747.
Falcó, I., Verdeguer, M., Aznar, R., Sánchez, G. y Randazzo, W. (2018). Sanitizing food contact surfaces by the use of essential oils. Innovative Food Science & Emerging Technologies, 51, 220-228.
Faleiro, M. L. (2011). The mode of antibacterial action of essential oils. En A. Méndez Vilas (Ed.), Science Against Microbial Pathogens: Communicating Current Research and Technological Advances (pp. 1143-1156). Brown Walker Press.
Fathi, M., Vinceković, M., Jurić, S., Viskić, M., Režek Jambrak, A. y Donsì, F. (2019). Food-grade colloidal systems for the delivery of essential oils. Food Reviews International, 37(11), 1-45.
Fisher, K. y Phillips, C. A. (2006). The effect of lemon, orange and bergamot essential oils and their components on the survival of Campylobacter jejuni, Escherichia coli O157, Listeria monocytogenes, Bacillus cereus and Staphylococcus aureus in vitro and in food systems. Journal of Applied Microbiology, 101(6), 1232-1240.
Frankova, A., Smid, J., Bernardos, A., Finkousova, A., Marsik, P., Novotny, D., Legarová, V., Pulkrabek, J. y Kloucek, P. (2016). The antifungal activity of essential oils in combination with warm air flow against postharvest phytopathogenic fungi in apples. Food Control, 68(1-2), 62-68.
García-Ceja, A. y López-Malo, A. (2012). Biopolímeros utilizados en la encapsulación. Temas Selectos de Ingeniería de Alimentos, 6(1), 84-97.
Ghabraie, M., Dang Vu, K., Tata, L., Salmieri, S. y Lacroix, M. (2016). Antimicrobial effect of essential oils in combinations against five bacteria and their
effect on sensorial quality of ground meat. LWT - Food Science and Technology, 66, 332-339.
Giannenas, I., Triantafillou, E., Stavrakakis, S., Margaroni, M., Mavridis, S., Steiner, T. y Karagouni, E. (2012). Assessment of dietary supplementation with carvacrol or thymol containing feed additives on performance, intestinal microbiota and antioxidant status of rainbow trout (Oncorhynchus mykiss). Aquaculture, 350-353, 26–32.
Giannenas, I., Bonos, E., Christaki, E. y Florou-Paneri, P. (2013). Essential oils and their applications in animal nutrition. Medicinal and Aromatic Plants, 2(6), 1-12.
Gómez-Estaca, J., López-de-Dicastillo, C., Hernández-Muñoz, P., Catalá, R. y Gavara, R. (2014). Advances in antioxidant active food packaging. Trends in Food Science & Technology, 35(1), 42-51.
Goñi, P., López, P., Sánchez, C., Gómez-Lus, R., Becerril, R. y Nerín, C. (2009). Antimicrobial activity in the vapour phase of a combination of cinnamon and clove essential oils. Food Chemistry, 116(4), 982-989.
Gyawali, R. e Ibrahim, S. A. (2014). Natural products as antimicrobial agents. Food Control, 46, 412-429.
Halden, R. U. (2014). On the need and speed of regulating triclosan and triclocarban in the United States. Environmental Science and Technology, 48(7), 3603-3611.
Hashem, A. S., Awadalla, S. S., Zayed, G. M., Maggi, F. y Benelli, G. (2018). Pimpinella anisum essential oil nanoemulsions against Tribolium castaneum-insecticidal activity and mode of action. Environmental Science and Pollution Research, 25(19), 18802-18812.
He, Q., Li, Z., Yang, Z., Zhang, Y. y Liu, J. (2019). A superchilling storage–ice glazing (ss-ig) of Atlantic salmon (Salmo salar) sashimi fillets using coating protective layers of Zanthoxylum essential oils (eos). Aquaculture, 514, 734506.
Huang, Z., Liu, X., Jia, S., Zhang, L. y Luo, Y. (2018). The effect of essential oils on microbial composition and quality of grass carp (Ctenopharyngodon idellus) fillets during chilled storage. International Journal of Food Microbiology, 266, 52-59.
Jahani, M., Pira, M. y Aminifard, M. H. (2020). Antifungal effects of essential oils against Aspergillus niger in vitro and in vivo on pomegranate (Punica granatum) fruits. Scientia Horticulturae, 264, 109188.
Jang, S., Shin, Y. J. y Song, K. B. (2011). Effect of rapeseed protein-gelatin film containing grapefruit seed extract on ‘Maehyang’ strawberry quality. In-
ternational Journal of Food Science and Technology, 46(3), 620-625.
Jiang, T., Luo, Z. y Ying, T. (2015). Fumigation with essential oils improves sensory quality and enhanced antioxidant ability of shiitake mushroom (Lentinus edodes). Food Chemistry, 172, 692-698.
Jin, W., Xu, W., Liang, H., Li, Y., Liu, S. y Li, B. (2016). Nanoemulsions for food: Properties, production, characterization and applications. En A. M. Grumezescu (Ed.), Emulsions. Nanotechnology in the Agri-Food Industry Volume 3 (pp. 1-36). Academic Press.
Karan, T., Şimşek, S., Yildiz, I. y Erenler, R. (2018). Chemical composition and insecticidal activity of Origanum syriacum L. Essential oil against Sitophilus oryzae and Rhyzopertha dominica International Journal of Secondary Metabolite, 5, 87-93.
Khattak, F., Ronchi, A., Castelli, P. y Sparks, N. (2014). Effects of natural blend of essential oil on growth performance, blood biochemistry, caecal morphology, and carcass quality of broiler chickens. Poultry Science, 93(1), 132-137.
Khorasani, S., Danaei, M. y Mozafari, M. R. (2018). Nanoliposome technology for the food and nutraceutical industries. Trends in Food Science and Technology, 79, 106-115.
Lin, L., Gu, Y., Sun, Y. y Cui, H. (2019). Characterization of chrysanthemum essential oil triple-layer liposomes and its application against Campylobacter jejuni on chicken. LWT - Food Science and Technology, 107, 16-24.
Lin, L., Zhu, Y., Thangaraj, B., Abdel-Samie, M. A. y Cui, H. (2018). Improving the stability of thyme essential oil solid liposome by using β-cyclodextrin as a cryoprotectant. Carbohydrate Polymers, 188, 243-251.
Lopes, L. M., Sousa, A. H., Santos, V. B., Silva, G. N. y Abreu, A. O. (2018). Development rates of Callosobruchus maculatus (Coleoptera: chrysomelidae) in landrace cowpea varieties occurring in southwestern Amazonia. Journal of Stored Products Research, 76, 111-115.
Lorenzo-Leal, A. C., Palou, E. y López-Malo, A. (2019). Evaluation of the efficiency of allspice, thyme and rosemary essential oils on two foodborne pathogens in in-vitro and on alfalfa seeds, and their effect on sensory characteristics of the sprouts. International Journal of Food Microbiology, 295, 19-24.
Maccioni, A., Santo, A., Falconieri, D., Piras, A., Manconi, M., Maxia, A. y Bacchetta, G. (2019). Inhibitory effect of rosemary essential oil, loaded in liposomes, on seed germination of Acacia saligna, an invasive species in Mediterranean ecosystems. Botany, 97(5), 283-291.
Mahdavi, V., Hosseini, S. E. y Sharifan, A. (2017). Effect of edible chitosan film enri-
ched with anise (Pimpinella anisum L.) essential oil on shelf life and quality of the chicken burger. Food Science and Nutrition, 6(2), 269–279.
Mani López, E., Valle Vargas, G. P., Palou, E. y López-Malo, A. (2018). Penicillium expansum inhibition on bread by lemongrass essential oil in vapor phase.
Journal of Food Protection, 81(3), 467-471.
Manning, L. (2015). Categorizing food related illness: have we got it right? Critical Reviews in Food Science and Nutrition, 57(9), 1938-1949.
Matos, L. F., Barbosa, D. R., Lima, E. D., Dutra, K. D., Navarro, D. M., Alves, J. L. y Silva, G. N. (2020). Chemical composition and insecticidal effect of essential oils from Illicium verum and Eugenia caryophyllus on Callosobruchus maculatus in cowpea. Industrial Crops and Products, 145, 112088.
McClements, D. J. (2011). Edible nanoemulsions: Fabrication, properties, and functional performance. Soft Matter, 7(6), 2297-2316.
Mejía-Garibay, B., Palou, E. y López-Malo, A. (2015). Composition, diffusion, and antifungal activity of black mustard (Brassica nigra) essential oil when applied by direct addition or vapor phase contact. Journal of Food Protection, 78(4), 843-848.
Michalczyk, M., Macura, R., Tesarowicz, I. y Banaś, J. (2012). Effect of adding essential oils of coriander (Coriandrum sativum L.) and hyssop (Hyssopus officinalis L.) on the shelf life of ground beef. Meat Science, 90(3), 842-850.
Nikkhah, M. y Hashemi, M. (2020). Boosting antifungal effect of essential oils using combination approach as an efficient strategy to control postharvest spoilage and preserving the jujube fruit quality. Postharvest Biology and Technology, 164, 111159.
Mossa, A.-T. (2016). Green pesticides: essential oils as biopesticides in insect-pest management. Journal of Environmental Science and Technology, 9(5), 354-378.
Osés, J., Fernández-Pan, I., Mendoza García, E. M. y Maté, J. I. (2009). Stability of the mechanical properties of edible films based on whey protein isolate during storage at different relative humidity. Food Hydrocolloids, 23(1), 125-131.
Otoni, C. G., de Moura, M. R., Aouada, F. A., Camilloto, G. P., Cruz, R. S., Lorevice, M. V., Soares, N. de F. F. y Mattoso L. H. C. (2014). Antimicrobial and physical-mechanical properties of pectin/papaya puree/cinnamaldehyde nanoemulsion edible composite films. Food Hydrocolloids, 41(41), 188-194.
Ozogul, Y., Yuvka, İ., Ucar, Y., Durmus, M., Kösker, A. R., Öz, M. y Ozogul, F. (2017). Evaluation of effects of nanoemulsion based on herb essential oils (rosemary, laurel, thyme and sage) on sensory, chemical and microbiological quality of
rainbow trout (Oncorhynchus mykiss) fillets during ice storage. LWT - Food Science and Technology, 75, 677-684.
Pang, X., Feng, Y. X., Qi, X. J., Wang, Y., Almaz, B., Xi, C. y Du, S.S. (2020). Toxicity and repellent activity of essential oil from Mentha piperita Linn. leaves and its major monoterpenoids against three stored product insects. Environmental Science and Pollution Research, 27, 7618-7627.
Parra, D. F., Tadini, C. C., Ponce, P. y Lugao, A. B. (2004). Mechanical properties and water vapor transmission in some blends of cassava starch edible films. Carbohydrate Polymers, 58(4), 475-481.
Pateiro, M., Barba, F. J., Domínguez, R., Sant’Ana, A. S., Mousavi Khaneghah, A., Gavahian, M. y Lorenzo, J. M. (2018). Essential oils as natural additives to prevent oxidation reactions in meat and meat products: a review. Food Research International, 113, 156-166.
Pedrós-Garrido, S., Clemente, I., Calanche, J. B., Condón-Abanto, S., Beltrán, J. A., Lyng, J. G., Brunton, N., Bolton D. y Whyte, P. (2020). Antimicrobial activity of natural compounds against Listeria spp. and their effects on sensory attributes in salmon (Salmo salar) and cod (Gadus morhua). Food Control, 107, 106768.
Pereira, L. A. S., Oliveira, M. M. M. de, Martins, H. H. de A., Vale, L. A. do, Isidoro, S. R., Botrel, D. A. y Piccoli, R. H. (2019). Sanitizing cinnamaldehyde solutions against Pseudomonas aeruginosa biofilms formed on stainless steel surfaces. Brazilian Journal of Food Technology, 22(0), 1-8.
Perricone, M., Arace, E., Corbo, M. R., Sinigaglia, M. y Bevilacqua, A. (2015). Bioactivity of essential oils: a review on their interaction with food components. Frontiers in Microbiology, 6(76), 1-5.
Phillips, C. A. (2016). Bacterial biofilms in food processing environments: a review of recent developments in chemical and biological control. International Journal of Food Science and Technology, 51(8), 1731-1743.
Pourya, M., Sadeghi, A., Ghobari, H., Taning, C. N. T. y Smagghe, G. (2018). Bioactivity of Pistacia atlantica Desf. Subsp. Kurdica (Zohary) Rech. F. and Pistacia khinjuk Stocks essential oils against Callosobruchus maculatus (F, 1775) (Coloeptera: Bruchidae) under laboratory conditions. Journal of Stored Products Research, 77, 96–105.
Prakash, B., y Kiran, S. (2016). Essential oils: a traditionally realized natural resource for food preservation. Current Science, 110(10), 1890-1892.
Reyes-Jurado, F., Navarro-Cruz, A. R., Ochoa-Velasco, C. E., Palou, E., López-Malo, A. y Ávila-Sosa, R. (2019). Essential oils in vapor phase as alternative antimicro-
bials: a review. Critical Reviews in Food Science and Nutrition, 1-10.
Ribeiro-Santos, R., Andrade, M., de Melo, N. R. y Sanches-Silva, A. (2017). Use of essential oils in active food packaging: recent advances and future trends. Trends in Food Science & Technology, 61, 132-140.
Saifullah, M., Islam Shishir, M. R., Ferdowsi, R., Tanver Rahman, M. R. y Van Vuong, Q. (2019). Micro and nano encapsulation, retention and controlled release of flavor and aroma compounds: a critical review. Trends in Food Science & Technology, 86, 230-251.
Sánchez Aldana, D., Contreras-Esquivel, J. C., Nevárez-Moorillón, G. V. y Aguilar, C. N. (2014). Caracterización de películas comestibles a base de extractos pécticos y aceite esencial de limón mexicano. CyTA - Journal of Food, 13(1), 17-25.
Sánchez, G. y Aznar, R. (2015). Evaluation of natural compounds of plant origin for inactivation of enteric viruses. Food and Environmental Virology, 7(2), 183-187.
Scotter, M. J. y Castle, L. (2004). Chemical interactions between additives in foodstuffs: a review. Food Additives and Contaminants, 21(2), 93-124.
Servili, A., Feliziani, E. y Romanazzi, G. (2017). Exposure to volatiles of essential oils alone or under hypobaric treatment to control postharvest gray mold of table grapes. Postharvest Biology and Technology, 133, 36-40.
Sharma, H., Mendiratta, S. K., Agarwal, R. K., Kumar, S. y Soni, A. (2017). Evaluation of antioxidant and anti-microbial activity of various essential oils in fresh chicken sausages. Journal of Food Science and Technology, 54(2), 279-292.
Shidhaye, S. S., Vaidya, R., Sutar, S., Patwardhan, A. y Kadam, V. J. (2008). Solid lipid nanoparticles and nanostructured lipid carriers – Innovative generations of solid lipid carriers. Current Drug Delivery, 5(4), 324-331.
Silano, M. y Silano, V. (2015). Food and feed chemical contaminants in the European Union: regulatory, scientific, and technical issues concerning chemical contaminants occurrence, risk assessment, and risk management in the European Union. Critical Reviews in Food Science and Nutrition, 57(10), 2162-2217.
Simitzis, P. (2017). Review. Enrichment of animal diets with essential oils-a great perspective on improving animal performance and quality characteristics of the derived product. Medicines, 4(35), 1-21.
Singh, P. y Gandhi, N. (2015). Milk preservatives and adulterants: processing, regulatory and safety issues. Food Reviews International, 31(3), 236-261.
Šojić, B., Pavlić, B., Tomović, V., Ikonić, P., Zeković, Z., Kocić-Tanackov, S., Đurović S., Škaljac, S., Jokanović, M. e Ivić, M. (2019). Essential oil versus supercritical
fluid extracts of winter savory (Satureja montana L.) - Assessment of the oxidative, microbiological and sensory quality of fresh pork sausages. Food Chemistry, 287, 280-286.
Solórzano-Santos, F. y Miranda-Novales, M. G. (2012). Essential oils from aromatic herbs as antimicrobial agents. Current Opinion in Biotechnology, 23(2), 136-141.
Soncu, E. D., Arslan, B., Ertürk, D., Küçükkaya, S., Özdemir, N. y Soyer, A. (2018). Microbiological, physicochemical and sensory characteristics of Turkish fermented sausages (sucuk) coated with chitosan-essential oils. LWT, 97, 198-204.
Szűcs, V., Szabó, E., Guerrero, L., Tarcea, M. y Bánáti, D. (2019). Modelling of avoidance of food additives: a cross country study. International Journal of Food Sciences and Nutrition, 70, 1020-1032.
Tongnuanchan, P. y Benjakul, S. (2014). Essential oils: extraction, bioactivities, and their uses for food preservation. Journal of Food Science, 79, 1231-1249.
Umaraw, P., Munekata, P. E. S., Verma, A. K., Barba, F. J., Singh, V. P., Kumar, P. y Lorenzo, J. M. (2020). Edible films/coating with tailored properties for active packaging of meat, fish and derived products. Trends in Food Science & Technology, 98, 10-24.
Utami, R., Khasanah, L. U., Manuhara, G. J. y Ayuningrum, Z. K. (2019). Effects of cinnamon bark essential oil (Cinnamomum burmannii) on characteristics of edible film and quality of fresh beef. Pertanika Journal of Tropical Agricultural Science, 42(4), 1173-1184.
Valencia-Sullca, C., Jiménez, M., Jiménez, A., Atares, L., Vargas, M. y Chiralt, A. (2016). Influence of liposome encapsulated essential oils on properties of chitosan films. Polymer international, 65(8), 979-987.
Valeriano, C., de Oliveira, T. L. C., de Carvalho, S. M., Cardoso, M. das G., Alves, E. y Piccoli, R. H. (2012). The sanitizing action of essential oil-based solutions against Salmonella enterica serotype Enteritidis S64 biofilm formation on aisi 304 stainless steel. Food Control, 25(2), 673-677.
Vasilijević, B., Mitić-Ćulafić, D., Djekic, I., Marković, T., Knežević-Vukčević, J., Tomasevic, I. y Nikolić, B. (2019). Antibacterial effect of Juniperus communis and Satureja montana essential oils against Listeria monocytogenes in vitro and in wine marinated beef. Food Control, 100, 247-256.
Vatavali, K., Karakosta, L., Nathanailides, C., Georgantelis, D. y Kontominas, M. G. (2013). Combined effect of chitosan and oregano essential oil dip on the microbiological, chemical, and sensory attributes of red porgy (Pagrus pagrus) stored in ice. Food and Bioprocess Technology, 6(12), 3510-3521.
Velázquez-Contreras, C., Osorio-Revilla, G. y Gallardo-Velázquez, T. (2014). Encapsulation of orange oil in spout-fluid bed dryer with a draft tube on a bed of inert solids. Drying Technology, 32(14), 1718-1726.
Vital, A. C. P., Guerrero, A., Kempinski, E. M. B. C., Monteschio, J. O., Sary, C., Ramos, T. R. Campo, M. D. M. y do Prado, I. N. (2018). Consumer profile and acceptability of cooked beef steaks with edible and active coating containing oregano and rosemary essential oils. Meat Science, 143, 153-158.
Vital, A. C. P., Guerrero, A., Ornaghi, M. G., Kempinski, E. M. B. C., Sary, C., Monteschio, J. O., Matumoto-Pintro, P. T., Ribeiro, R. P. y do Prado, I. N. (2018). Quality and sensory acceptability of fish fillet (Oreochromis niloticus) with alginate-based coating containing essential oils. Journal of Food Science and Technology, 55(12), 4945-4955.
Walker, R. M., Decker, E. A. y McClements, D. J. (2015). Physical and oxidative stability of fish oil nanoemulsions produced by spontaneous emulsification: effect of surfactant concentration and particle size. Journal of Food Engineering, 164, 10-20.
Werdin González, J. O., Jesser, E. N., Yeguerman, C. A., Ferrero, A. A. y Fernández Band, B. (2017). Polymer nanoparticles containing essential oils: new options for mosquito control. Environmental Science and Pollution Research, 24(20), 17006-17015.
Wu, Z., Zhou, W., Pang, C., Deng, W., Xu, C. y Wang, X. (2019). Multifunctional chitosan-based coating with liposomes containing laurel essential oils and nanosilver for pork preservation. Food Chemistry, 295, 16-25.
Xue, R., Shi, H., Ma, Y., Yang, J., Hua, B., Inniss, E. C., Adams, C. D. y Eichholz, T. (2017). Evaluation of thirteen haloacetic acids and ten trihalomethanes formation by peracetic acid and chlorine drinking water disinfection. Chemosphere, 189, 349-356.
Yeguerman, C., Jesser, E., Massiris, M., Delrieux, C., Murray, A. P. y Werdin González, J. O. (2020). Insecticidal application of essential oils loaded polymeric nanoparticles to control German cockroach: design, characterization and lethal/ sublethal effects. Ecotoxicology and Environmental Safety, 189, 110047.
Yemiş, G. P. y Candoğan, K. (2017). Antibacterial activity of soy edible coatings incorporated with thyme and oregano essential oils on beef against pathogenic bacteria. Food Science and Biotechnology, 26(4), 1113-1121.
Yeom, H-J., Lee, H-Y., Lee, S-C., Lee, J-E., Seo, S-M. y Park, I-K. (2018). Insecticidal activity of Lamiaceae plant essential oils and their constituents against Blattella germanica L. Adult. Journal of Economic Entomology, 111, 653-661.
Uso de gomas naturales en la microencapsulación de pigmentos (antocianinas, betalaínas y carotenoides) mediante secado por atomización y liofilización
O., Jiménez- González* y J.A., Guerrero-Beltrán
*Programa de Doctorado en Ciencia de Alimentos
Correo electrónico: oscar.jimenezgz@udlap.mx • angel.guerrero@udlap.mx
RESUMEN
La microencapsulación es útil para la conservación y estabilidad de pigmentos. Los métodos más utilizados son el secado por atomización y la liofilización; ambos métodos requieren agentes encapsulantes. Las gomas de origen natural se han convertido en un ingrediente importante, ofreciendo múltiples beneficios estructurales para la microcápsula y protectores para el componente activo. La goma arábiga, goma de mezquite, goma xantana y goma guar, han sido probadas en la microencapsulación de antocianinas, betalaínas y carotenoides. El uso de estas gomas incrementa la estabilidad de los pigmentos, además, su empleo permite la obtención de colorantes en polvo de fácil incorporación a matrices alimenticias complejas. El objetivo de esta revisión es presentar el uso que tienen estas gomas en la encapsulación de pigmentos mediante el secado por atomización y liofilización; además de discutir los factores que afectan su estabilidad y analizar los trabajos que han llevado a cabo la incorporación en matrices alimenticias.
Palabras clave: microencapsulación, secado por atomización, liofilización, pigmentos, gomas naturales.
ABSTRACT
Microencapsulation is a useful technique for the preservation and stability of pigments. The most commonly used methods are spray drying and freeze drying; both methods require encapsulating agents. Natural gums are important ingredients, as they offer numerous structural benefits for the microcapsule and protection for the core compounds. Gum arabic, mesquite gum, xanthan gum and guar gum, have been tested to encapsulate anthocyanins, betalains and carotenoids. It has been observed that these gums increase pigments’ stability, in addition, their utilization allows the obtention of powder-state colorants that can be easily incorporated into food matrices. The aim of this review is to present the use of these gums in the encapsulation of pigments through spray drying and freeze drying; furthermore, to discuss factors that affect their stability, and to analyze the studies concerning the incorporation into food matrices.
Keywords: microencapsulation, spray drying, freeze drying, natural pigments, natural gums.
INTRODUCCIÓN
El color es uno de los aspectos sensoriales más importantes en la industria alimentaria, ya que puede modificar el comportamiento del consumidor, influenciando la selección, aceptabilidad, preferencia y deseo sobre un alimento (Clydesdale, 1993; Garber et al., 2016; Paakki et al., 2019; Piqueras-Fiszman y Spence, 2015; Wadhera y Capaldi-Phillips, 2014). El color agradable de un alimento puede ser un factor de calidad (Francis, 1995; Sukkwai et al., 2018). Asimismo, el color de los alimentos ayuda a la identificación de sabores u olores (Garber et al., 2016; Porcherot et al., 2013; Spence, 2015; Spence et al., 2010).
La adición de colorantes en alimentos permite dar uniformidad de color entre lotes de un mismo producto, aumentar la intensidad del color, obtener el color esperado de acuerdo con las expectativas del consumidor (por ejemplo, el color amarillo en helado de vainilla), restaurar el color que se ha perdido debido al procesamiento (por ejemplo, en la pasteurización de jugos), colorear alimentos que carecen de color (por ejemplo, refrescos, bebidas saborizadas, dulces, entre otros), o enmascarar características indeseables (Lehto et al., 2017; Martins et al., 2016; Scotter, 2011).
Los colorantes alimentarios se dividen en artificiales o sintéticos, idénticos a los naturales (análogos a los naturales, pero producidos sintéticamente) y naturales (Scotter, 2011). El término «colorante natural», puede referirse a extractos purificados o concentrados de frutas o vegetales ricos en pigmentos (Lehto et al., 2017; Scotter, 2011). Existe una gran variedad de pigmentos presentes en la naturaleza, los cuales pueden ser extraídos y usarse en la industria alimentaria. En general, las antocianinas, betalaínas y carotenoides, son los pigmentos más estudiados, con múltiples tonalidades como azules-rojos-morados (antocianinas), amarillos-rojos (betalaínas) y amarillos-naranjas-rojos (carotenoides) (Martins et al., 2016; Rodriguez-Amaya, 2016; Rodriguez-Amaya, 2019).
El uso y consumo de pigmentos ha ganado importancia debido a que presentan propiedades benéficas para la salud humana, como la reducción de síntomas o prevención de enfermedades crónico-degenerativas o cardiovasculares, así como la protección de las funciones cognitivas, además, pueden actuar como antiinflamatorios, analgésicos, entre otros (Chawla et al., 2016; He y Giusti, 2010; Rodriguez-Amaya, 2016; Rodriguez-Amaya, 2019). Esto va de la mano con las nuevas tendencias del consumo de alimentos. Actualmente, los consumidores demandan alimentos
más saludables, de origen vegetal, ricos en antioxidantes y con menos aditivos artificiales (Martins et al., 2016). No obstante, una de las principales desventajas del uso de estos pigmentos es la inestabilidad ante condiciones ambientales (pH, luz, oxígeno, temperatura, entre otros) y la dificultad al momento de su incorporación en alimentos (Ngamwonglumlert et al., 2017; Rodriguez-Amaya, 2019). El desarrollo de pigmentos microencapsulados ha sido una de las principales opciones para su conservación, ya que de esta forma se incrementa su estabilidad (Castro-Enríquez et al., 2019; Mahdavi et al., 2014) y, en algunos casos, su solubilidad (De Marco et al., 2013; Kshirsagar et al., 2010). Al mismo tiempo, sirve como método de transporte de compuestos bioactivos y permite controlar la liberación de los mismos (Niu et al., 2020; Ye et al., 2018).
Se han utilizado diferentes agentes de encapsulación para la formación de la microcápsula. En especial, el uso de biopolímeros como las gomas provenientes de exudados de árboles y bacterias, o extraídas de semillas (Ahmad et al., 2019; Hamdani et al., 2019), las cuales presentan propiedades que ayudan a la formación de la pared y actúan como emulgentes (Hamdani et al., 2019; Salarbashi y Tafaghodi, 2018), además de ser biocompatibles, biodegradables y seguras para su consumo (Gupta et al., 2018). Se ha reportado el uso de gomas para la microencapsulación de pigmentos, como la goma arábiga, goma de mezquite, goma xantana, goma guar, entre otras (Antigo et al., 2017; Ochoa-Velasco et al., 2017; Pavón-García et al., 2011; Ravichandran et al., 2014; Venil et al., 2016).
El objetivo de la presente revisión es proveer información acerca del uso de gomas naturales, en la encapsulación de pigmentos (antocianinas, betalaínas y carotenoides) mediante microencapsulación usando secado por atomización y liofilización, analizar el efecto de los factores de inestabilidad de pigmentos microencapsulados bajo diferentes condiciones de almacenamiento, así como la aplicación de los pigmentos en matrices alimenticias.
REVISIÓN BIBLIOGRÁFICA
1. Microencapsulación de pigmentos
La microencapsulación permite que diferentes compuestos, entre ellos pigmentos, sean recubiertos por una matriz polimérica (homogénea o heterogénea) (Zhang et al., 2020). Dentro de los
factores que influyen en la formación de la microcápsula, se encuentran el tamaño y las características de la microcápsula (figura 1a), el método de encapsulación (químico, físico o fisicoquímico), las condiciones del proceso, el método de homogeneización y la naturaleza física y química de la solución debido a los agentes de encapsulación (Aguiar et al., 2016; Gharsallaoui et al., 2007).
Existen diferentes métodos de encapsulación para la conservación de compuestos activos naturales; no obstante, la liofilización y el secado por atomización son las técnicas más usadas (Corrêa et al., 2019; Ephrem et al., 2018; Labuschagne, 2018).
1.1. Obtención de pigmentos en polvo
1.1.1. Secado por atomización
El secado por atomización es la tecnología más utilizada para la microencapsulación, debido a que es barata, reproducible, capaz de operar en continuo y ofrece altos rendimientos (Bakry et al., 2016: Çam et al., 2014; Labuschagne, 2018). El proceso de microencapsulación mediante secado por atomización se basa en la eliminación de agua usando aire caliente y la reducción de tamaño de la gota mediante atomización (figura 1b) (Bakry et al., 2016; Santos et al., 2018). La eficiencia de encapsulación dependerá de los parámetros de operación (temperatura de entrada y salida, presión, flujo del aire de atomización y velocidad de alimentación) y del agente encapsulante. Diferentes autores han descrito el proceso de secado por atomización (Bakry et al., 2016; Gharsallaoui et al., 2007; Santos et al., 2018), el cual se puede resumir en tres etapas principales:
i. Preparación de la mezcla de encapsulación. Esta puede llevarse a cabo por métodos físicos (agitación magnética, emulsión con un mezclador tipo ultraturrax, por ultrasonido o microfluidización) (Mahdi Jafari et al., 2006; Santana et al., 2016; Verma y Singh, 2015) o métodos químicos (coacervación simple o compleja; mayormente aplicada para pigmentos liposolubles, como los carotenoides) (Gomez-Estaca et al., 2016; Jain et al., 2016; Qv et al., 2011; Shaddel et al., 2018; Thakur et al., 2017).
ii. Atomización. Durante esta etapa, la mezcla de alimentación se divide en pequeñas gotas, aumentando el área de contacto y mejorando la transferencia de energía y masa, lo cual agiliza la evaporación de agua (Santos et al., 2018; Steiner
et al., 2018). La forma y tamaño de la gota dependerán del tipo de atomización y la naturaleza de la solución alimentada (Santos et al., 2018).
iii. Deshidratación de la gota. Al entrar en contacto con el aire caliente (las temperaturas comúnmente usadas oscilan entre 150 y 220 °C), la transferencia de energía y masa ocurren de manera simultánea (figura 1b) (Bakry et al., 2016; Gharsallaoui et al., 2007). El proceso de deshidratación es casi instantáneo. Durante este, ocurre un incremento de la temperatura, difusión y evaporación del agua desde el centro hasta el exterior de la cápsula, encogimiento de la cápsula, concentración del material activo, y formación de la costra o pared (Dolinsky, 2001; Santos et al., 2018).
1.1.2. Liofilización
La liofilización es el segundo método de microencapsulación más usado, pese a que los costos pueden aumentar entre 30 y 50 veces más que el método de secado por atomización. Es excesivamente tardado, ya que el secado por atomización se puede llevar a cabo en segundos y la liofilización puede tardar días. Sin embargo, la liofilización es ideal cuando el compuesto activo es altamente termolábil (Bakry et al., 2016; Labuschagne, 2018) o cuando se desea retener todos los compuestos volátiles y/o preservar el color (Clark, 2009)
Durante la liofilización, la deshidratación ocurre después de la congelación bajo condiciones de vacío, lo cual propicia la sublimación (Morais et al., 2016). El proceso básico se representa esquemáticamente en la figura 1c. Consta de tres etapas principales, la primera es el congelamiento, a temperaturas menores a 0 °C (entre -18 y -80 °C) durante algunas horas (Ravichandran et al., 2014; Rezende et al., 2018; Yu y Lv, 2019); esta etapa ayuda a controlar los cristales de hielo (orientación, tamaño y morfología) (Fang y Bhandari, 2012). Se recomiendan lotes pequeños cuando la matriz a deshidratar es líquida (solución acuosa o suspensión) (Fang y Bhandari, 2012).
Las siguientes dos etapas son las de deshidratación, en la primera ocurre la sublimación del agua y el transporte del vapor de agua a la cámara de condensación. Uno de los problemas durante esta etapa, se da cuando la vaporización del hielo deja poros abiertos, donde el oxígeno presente en el aire puede interactuar con el compuesto activo y propiciar su degradación (Fang y Bhandari, 2012; Kuck y Noreña, 2016; Ozkan et al., 2019) o la su-
Esquemas relacionados con la microencapsulación: a) tipos de microcápsula, b) proceso de deshidratación mediante secado por atomización, c) proceso de deshidratación mediante liofilización.
blimación incompleta debido a la formación de una barrera que impide el paso del vapor de agua (Kuck y Noreña, 2016). En la segunda etapa de deshidratación se aplica energía para remover el agua remanente (agua ligada / no congelable) (Clark, 2009; Fang y Bhandari, 2012). Una vez concluida esta etapa, el polvo se obtiene mediante un molido (manual o mecánico), lo que resulta en partículas irregulares y de tamaños diversos (Rezvankhah et al., 2020).
1.2. Importancia de la temperatura de transición vítrea (Tg) La temperatura de transición vítrea (Tg) es una propiedad
termofísica de los polímeros amorfos, la cual está relacionada con la identidad, peso molecular y concentración de los productos en la mezcla «compuesto activo-agente de encapsulación» (Bhandari y Howes, 1999; Santos et al., 2018). Se trata del paso de un material amorfo a su estado cristalino. El aumento de la temperatura por encima de la de transición vítrea (superior a 10-20 °C) genera cambios en las propiedades físicas, como el incremento en la capacidad calorífica (Cp) y cambios en las propiedades viscoelásticas (Bhandari y Howes, 1999). Estos cambios en el secado por atomización
Figura 1.
pueden propiciar que el producto se adhiera a las paredes de la cámara de secado o la aglomeración del producto (Santos et al., 2018). Por otro lado, si durante la liofilización la temperatura de deshidratación es mayor a la Tg (conocida como temperatura de colapso) puede disminuir la viscosidad del material debido al cambio de la estructura sólida-cristalina a una gomosa-amorfa (Morais et al., 2016); como resultado la estructura puede colapsar o deformarse y el producto final tener exceso de agua residual y problemas de rehidratación (Bhandari y Howes, 1999). Asimismo, a lo largo del almacenamiento, la Tg está relacionada con algunos mecanismos de deterioración de la microcápsula y del compuesto activo (Naik et al., 2017).
Los compuestos presentes en los extractos usados para la encapsulación, como ácidos orgánicos o la fructosa, glucosa (monómeros) y sacarosa (disacárido), son de bajo peso molecular y, por consiguiente, de baja Tg —en los tres últimos, de 5, 31 y 62 °C, respectivamente—, a diferencia de la maltodextrina (mdx) de 10 ed (pm = 1800 g/mol), cuya Tg es de 160 °C. Por otro lado, el valor de la Tg se basa en las fracciones molares de los componentes en la mezcla, por lo que cada uno influye en el valor final de la Tg (Bhandari et al., 1993). La adición de compuestos que incrementen la Tg, permite el secado a temperaturas más altas y ayuda a la formación de la pared que protege a los pigmentos (Zhang et al., 2020). Los polímeros más comunes son hidrolizados de almidón como la mdx, almidones modificados, proteínas o gomas (Villacrez et al., 2014). La selección del agente encapsulante dependerá de factores como la solubilidad, el peso molecular, la Tg, el punto de fusión, la cristalinidad, la difusividad, las propiedades para formar una película, y las propiedades emulgentes, además de la aplicación deseada del producto final (Bakry et al., 2016; Gharsallaoui et al., 2007).
2. Gomas usadas en la microencapsulación de pigmentos
Mahdavi et al. (2014) mencionan que en la microencapsulación los factores morfológicos del polvo, así como la baja humedad y actividad de agua, son tan importantes como la solubilidad y la higroscopicidad, ya que en ellos se basa la estabilidad de los compuestos. Además, la interacción de los grupos funcionales, la estructura y el grado de ramificaciones presentes en las gomas, influye en la estabilidad de los pigmentos (Zhang et al., 2020), dando como resultado que el uso de los diferentes agentes encapsulantes resulte en propiedades fisicoquímicas carac-
terísticas de cada uno de ellos. En la tabla I se muestran los trabajos realizados en los últimos años en la encapsulación de pigmentos con gomas. Asimismo, en la tabla II se resumen algunas de las características de las gomas mencionadas en esta revisión.
2.1. Goma arábiga o acacia
De las gomas mencionadas en este trabajo, la goma arábiga o goma acacia (ga) es la más utilizada para la encapsulación de pigmentos (tabla I). La goma arábiga (ga) es el exudado del árbol de Acacia senegal o Acacia seyal y es una molécula compleja (heteropolisacárido ramificado, tabla II), casi esférica (figura 2), constituida por un arabinogalactano o unidades de β-D galactopiranosil unidas por los carbonos 1 → 3 y 1→6 como cadena principal y ramificaciones β-D glucopiranosil ácido urónico unidas por los carbonos de 1→6. Estas cadenas pueden contener ácido glucurónico, galactopiranosa, arabinofuranosa y ramnosa (Nie et al., 2013; Zhao et al., 2015).
La ga presenta buena solubilidad en agua, puede formar una película que favorece la encapsulación de pigmentos, se usa como estabilizante, espesante (en solución acuosa presenta comportamiento newtoniano), gelificante, y emulgente (posiblemente por su fracción proteica de aproximadamente 2 %), puesto que permite la encapsulación de compuestos como los carotenoides (Gharsallaoui et al.,2007; Zhang et al., 2020).
Se ha utilizado ampliamente en la encapsulación de antocianinas, betalaínas y carotenoides (tabla I). Como se mencionó, los factores morfológicos son importantes en la estabilidad. Zhang et al. (2020) compararon el uso de mdx, ga y la mezcla de ambos en la encapsulación de jugo de arándano. Los resultados de este estudio demostraron que las partículas fueron más esféricas, sin grietas o rupturas sobre la superficie, pero presentaban rugosidades. Los autores hipotetizan que la rugosidad puede deberse a la rápida formación de la costra por la presencia de la ga y la deshidratación desigual de la partícula, promoviendo un encogimiento irregular y mayor contenido de humedad. Estos resultados concuerdan con los de Yu y Lv (2019), quienes mencionan que las moléculas cuya cadena estructural es más larga impiden el paso o salida del agua de la microcápsula. Por el contrario, otros agentes de encapsulación, como la mdx, a pesar de ser capaces de formar una película, lo hacen con mayor lentitud y, si bien permiten una deshidratación más uniforme, el compuesto activo se encuentra más expuesto a ser deteriorado debido a la temperatura (Zhang et al., 2020).
Tabla I.
Secado por atomización y liofilización como métodos de microencapsulación de pigmentos naturales
Fuentes Método de secado a Agente encapsulante
Jugo de arándanos (Vaccinium myrtillus)
Rosa japonesa (Rosa rugosa)
Pulpa de morera (Morus alba)
Pulpa de mora andina (Rubus glaucus Benth)
1:50, 1:60, 1:70, 1:80, 1:90, 1:100, 1:110 w/w
Antocianinas
Villacrez et al., 2014
Extracto de mora azul (Vaccinium corymbosum)
Tatar Turan et al., 2015 sd (atomizador ultrasónico, 60 kHz, 1-15 W)
Extracto de bagazo de uva fd ga (solución, 30 % sólidos totales)
Stoll et al., 2016 ga-mdx (1:1, solución, 30 % sólidos totales)
Frambuesas negras (Rubus occidentalis) fd
Extracto de piel de berenjena
(conservación)
(atomizador rotatorio)
Pulpa de palmito sd ga-almidón modificadowpc o spi
Uso de gomas naturales en la microencapsulación de pigmentos (antocianinas, betalaínas y carotenoides) mediante secado por atomización y liofilización
Secado por atomización y liofilización como métodos de microencapsulación de pigmentos naturales (continuación)
Maqui (Aristotelia chilensis) fd
Jugo de tamarillo (Solanum betaceum)
Chokeberry (Aronia melanocarpa) liofilizado
sd (atomizador rotatorio)
sd
ga-mdx 18 20ed
(3:37, solución, 40 % sólidos)
gg-mdx 18-20ed
(3:37, solución, 40 % sólidos)
Arroz negro (Oryza sativa L.)
(Hibiscus sabdariffa)
(Renalmia alpinia)
RomeroGonzález et al., 2020
Ramakrishnan, et al., 2018)
Pieczykolan y Kurek, 2019
Tabla I.
Secado por atomización y liofilización como métodos de microencapsulación de pigmentos naturales (continuación)
Fuentes Método de secado a Agente encapsulante b Concentración
Condiciones de encapsulación c Eficiencia % L* a* b* Referencia
JiménezAguilar et al., 2011
Cai et al.
Jugo de betabel (Beta vulgaris) sd
parcialmente hidrolizada
polidextrosa
parcialmente hidrolizada
gg parcialmente hidrolizadapolidextrosa
parcialmente hidrolizada
Betalaínas
Ravichandran et al., 2014
Tabla I.
Secado por atomización y liofilización como métodos de microencapsulación de pigmentos naturales (continuación)
Fuentes Método de secado a Agente encapsulante
20ed (1:19)
20ed (0.5:19.5)
gg-mdx 20ed (1:19)
gg-mdx 20ed (0.5:19.5)
et al., 2014
Chranioti et al., 2015 ga-almidón modificado (1:1, solución 15 %)
sd gx-mdx (solución, 0.5:99.5)
gx-mdx (solución, 0.5:99.5)
sd (atomizador de disco rotatorio)
Jugo de cereza brasileña (Eugenia uniflora L.) fd
Azafrán (Crocus sativus) fd
(sólidos totales) w/w
ga-mdx (1:1) 25 % (sólidos totales) w/w
Carotenoides
Antigo et al., 2017
Janiszewska, 2014
Rutz et
(solución, 15 %)
Chranioti et al., 2015 ga-almidón modificado (1:1, solución 15 %)
Luteína sd ga (solución, 11 %)
ga-almidón modificado (1:1, solución 11 %)
ÁlvarezHenao et al., 2018 ga-mdx (1:1, solución 11 %)
ga-mdxalmidón modificado (1:1:1, solución 11 %)
Tabla I.
Betabel
Secado por atomización y liofilización como métodos de microencapsulación de pigmentos naturales (continuación)
Fuentes Método de secado a Agente encapsulante b Concentración Condiciones de encapsulación c Eficiencia % L
Algas sd ga-mdx (4:6)
Astaxantinas de Haematococcus pluvialis
Referencia
Achiote (bixina) sd
Maracuyá (Passiflora edulis) sd
(1:1) 1:4 v/v
ga-gmez-mdx 10ed (17:17:66 %) 30 % sólidos totales
T in = 135 °C; T out = 80 °C
CarrilloNavas et al., 2011 ga-gmez-mdx 10ed (17:66:17 %) 30 % sólidos totales
Cantaxantina de Dietzia natronolimnaea sd ga (solución, 10 %) 1:4
Fucoxantina de alga (Eisenia bicyclis) fd
T in = 170 °C;
de pescado (1:1) 1.50
Hojjati et al., 2014
Quan et al., 2013
Rascón et al., 2011
Sea buckthorn (Hippophae rhamnoides L.)
a sd, secado por atomización (spray drying); fd, liofilización (freeze drying); b ga, goma arábiga; gmez, goma de mezquite; gg, goma guar; gx, goma xantana; gt, goma tara; mdx, maltodextrina; wpc, concentrado de proteína de suero de leche; spi, aislado de proteína de soya; cmc, carboximetilcelulosa; c T, temperatura de liofilización; T in, temperatura de entrada en el secado por atomización; T out, temperatura de salida en el secado por atomización; t, tiempo en horas; P, presión.
Tabla I.
No obstante, en algunos casos la combinación de más de un agente encapsulante es necesaria para obtener las propiedades de encapsulación esperadas del producto final. La mezcla ga-mdx, ha sido evaluada por diferentes autores, demostrando que la combinación tiene un efecto significativo en la retención de pigmentos, incrementando en un 13.5 % el contenido de antocianas de jugo de arándano microencapsulado mediante secado por atomización, frente a los resultados obtenidos al utilizar ga como único agente encapsulante (Zhang et al., 2020). Por el contrario, Stoll, Costa, Jablonski, Flôres y de Oliveira Rios (2016), así como Romero-González, Shun Ah-Hen, Lemus-Mondaca y Muñoz-Fariña (2020) no encontraron diferencias entre el uso de ga y ga-mdx en la encapsulación de antocianinas, usando liofilización, para el bagazo de uva y de frutos de maqui (Aristotelia chilensis [Mol.] Stuntz), respectivamente. En el caso de los carotenoides, Álvarez-Henao et al. (2018) encapsularon luteína mediante secado por atomización, encontrando que la ga presentó los valores más altos en la retención del pigmento; 53 % superior comparado con el que usó de ga-mdx, 55 % más que usando ga-almidón modificado y 26 % más que con una mezcla ternaria de ga-mdx-almidón modificado.
Otras mezclas que han sido utilizadas son ga-inulina, ga-mdxinulina (Romero-González et al., 2020), ga-gelatina (Shaddel et al., 2018) y ga-polidextrosa (Kuck y Noreña, 2016), para an-
tocianinas. Santana et al. (2016) usaron ga-almidón modificadowpc (concentrado de proteína de suero de leche) o spi (aislado de proteína de soya), para la encapsulación de antocianinas, usando un diseño de mezclas para la optimización de diferentes parámetros físicos y antioxidantes, obteniendo mejores resultados en la retención del pigmento al utilizar las mezclas ternarias. De igual forma, se ha utilizado ga-almidón modificado para betalaínas (Chranioti, et al., 2015); ga-almidón modificado para luteína (Álvarez- Henao et al., 2018), ga-inulina y ga-wpc para astaxantinas (Bustos-Garza et al., 2013), y ga-gelatina de pescado para fucoxantinas (Quan et al., 2013).
Se ha visto también que el método de encapsulación influye en la retención de los pigmentos. Antocianinas de rosa japonesa (Rosa rugosa) encapsuladas con ga-mdx (1 : 1), secadas por liofilización, presentaron 2.32 % más antocianinas en comparación con las secadas por atomización; lo cual se vio reflejado en el color de los polvos, incrementando los valores de a* (relacionados con la presencia de antocianinas) (Yu y Lv, 2019). En otro estudio similar, Tatar Turan, Cengiz y Kahyaoglu (2015) realizaron el secado de antocianinas de mora azul (ga-mdx, 1 : 4), obteniendo aproximadamente 18 % más antocianinas microencapsuladas con liofilización que con secado por atomización y un valor de ΔE menor (con respecto al extracto sin deshidratar) de todos los tratamientos evaluados.
Figura 2.
Estructura molecular de goma arábiga.
II.
Resumen de las propiedades de algunas gomas usadas en la encapsulación de pigmentos
Nombre Carga
Arábiga Aniónico Exudado de plantas
Mezquite Aniónico Exudado de plantas
Xantana No iónico Exudado de bacterias
Guar No iónico Semillas
Tetra-heteroglicano; emulgente, estabilizante, gelificante, formador de película y encapsulante
Sal neutra de un polisacárido ramificado ácido complejo; puede sustituir a la goma arábiga, emulgente, espesante, agente encapsulante para emulsiones, aromas, colores, agente espumante, capaz de formar película
Tri-heteroglicano; útil en la suspensión de partículas, emulgente, estabilizante, formador de película
Di-heteroglicano; espesante, estabilizante, útil en la suspensión de partículas
Adaptada de Ahmad et al., 2019; Hamdani et al., 2019; López-Franco et al., 2009; Taheri y Jafari, 2019.
β-D-ácido glucopiranurónico, α-L-rhamnopiranosa, β-Dgalactopiranosa, β-D-4Meácido glucopiranurónico, α-L-arabinosefuranosa, α-Dgalactopiranosa
Galactopiranosilo y manopiranosilo en (proporción 2:1) cadena principal enlazada con unidades de arabinosilo, ramnopiranosilo, glucuronosilo y metilglucuronosilo
β-D-glucosa, β-d-manosa, α-dmanosa ácido D-glucurónico
β-d-manopiranosa, α-Dgalactopiranosa
250,000820,000
2,120,864
300,0008,000,000
200,0008,000,000
2.2. Goma de mezquite
Al igual que la goma arábiga, la goma de mezquite (gmez) es un exudado que proviene del árbol de mezquite, originario de México (Vernon-Carter et al., 2000). Su uso en alimentos es bastante común, pues es altamente soluble en agua; incluso se le ha considerado un sustituto de la goma arábiga. Se considera de menor calidad debido a que, en solución acuosa, toma una coloración café (López-Franco et al., 2009; Mishra, 2015).
La gmez es la sal neutra de un polisacárido ácido complejo ramificado o un heteropolielectrolito aniónico ramificado (García-Márquez et al., 2015; López-Franco et al., 2009). La estructura molecular de la gmez (figura 3), consta de una cadena principal formada de residuos β-D-galactosa, unidos por los enlaces (1→3). Sus ramificaciones unidas por los enlaces 1→6 presentan L-arabinosa, L-ramnosa, β-D-glucuronato y 4-O-metil- β-D-glucoronato (azúcar simple u oligosacárido) (Bosquez-Molina et al., 2003). Contiene una pequeña porción de proteína (entre 0.7
y 6 %) unida de manera covalente a la cadena principal, la cual juega un papel importante durante la emulsión (García-Márquez et al., 2015; Vernon-Carter et al., 2000).
En la tabla II se presentan algunas propiedades de la gmez. Se ha utilizado en la encapsulación de sabores, como agente espumante, estabilizante y como agente ligante (Vernon-Carter et al., 2000). El incremento en el uso de esta goma representaría una oportunidad para las comunidades productoras de este aditivo (Rodríguez-Rodríguez et al., 2018).
Muy pocos trabajos han reportado el uso de la gmez para la encapsulación de pigmentos (tabla I). Uno de ellos es el realizado por Jiménez-Aguilar et al. (2011) para la encapsulación de antocianinas de mora azul (Vaccinium corymbosum) mediante secado por atomización. En este trabajo, la temperatura fue el factor principal que afectó la degradación de los pigmentos. Por otro lado, Ochoa-Velasco et al. (2017) utilizaron antocianinas de flor de Jamaica y probaron diferentes concentraciones de gmez (1, 2,
Tabla
Figura 3.
Estructura molecular de goma de mezquite.
3, 4, 5 %), las cuales fueron deshidratadas por atomización. Los resultados obtenidos muestran que incrementar la cantidad de gmez en la mezcla de alimentación no tiene efecto en la humedad del producto final, pero incrementa el rendimiento. No obstante, los autores argumentan que la adición excesiva de goma al extracto genera polvos con baja calidad nutrimental. Además, el incremento en la concentración de gmez afecta el color del producto, disminuyendo los valores del parámetro de color a*. No obstante, gracias al uso de la gmez, el contenido de antocianinas y el color pueden mantenerse, con ligeras variaciones, hasta por un año en condiciones de refrigeración (4 °C).
Al igual que la ga, el uso de la gmez resulta en partículas con rugosidades sobre la superficie de la esfera (Ochoa-Velasco et al., 2017), esto puede deberse a las similitudes entre ambas gomas (López-Franco et al., 2009; Vernon-Carter et al., 2000), ocasionando la formación de una costra y el secado desigual de la partícula (Zhang et al., 2020).
La gmez, en combinación con ga y mdx, ha sido utilizada para la encapsulación de jugo de maracuyá. Los resultados obtenidos por Carrillo-Navas et al. (2011) demostraron que la combinación de los tres agentes encapsulantes genera polvos altamente higroscópicos por el gran número de grupos hidrofílicos presentes en los tres agentes. De las dos formulaciones probadas (mayor concentración de gmez o mayor concentración de mdx), los polvos donde la gmez se encontraba en mayor proporción presentaron mejores características de rehidratación, retención de vitamina C y color (determinación visual) en el producto reconstituido.
La encapsulación de aceite de cardamomo (Beristain et al., 2001) y aceite de naranja (Beristain et al., 2002; Beristain y Vernon-Carter, 1994) ha demostrado que compuestos liposolubles como los carotenoides pueden ser estabilizados utilizando gmez y secado por atomización. Hasta el momento no se encontraron reportes del uso de la gmez en la encapsulación de betalaínas, o su uso en el secado por liofilización de cualquiera de los pigmentos.
2.3. Goma xantana
La goma xantana (gx) es un polisacárido soluble en agua obtenido de la fermentación por Xanthomonas campestris. Se utiliza glucosa o sacarosa como fuente de carbono; una alternativa para su obtención es el uso de residuos agroindustriales (Palaniraj y Jayaraman, 2011).
La estructura molecular de la gx (figura 4) consta de una cadena primaria compuesta de β-D-glucosa unida por los carbonos 1→4 y cadenas laterales con ácido glucurónico entre dos moléculas de manosa como residuo (Habibi y Khosravi-Darani, 2017). Algunas de sus características funcionales se encuentran en la tabla II. La gx es ampliamente usada en alimentos; como espesante (altamente viscosa a bajas concentraciones) presenta un comportamiento pseudoplástico en soluciones acuosas en un amplio intervalo de pH (2-12) y es estable a altas temperaturas (Kumar et al., 2018). Tiene la capacidad de estabilizar emulsiones evitando la floculación (Fu et al., 2019). Asimismo, la gx puede generar estructuras en forma de red mediante el entrecruzamiento intramolecular y contracción de sus mismas cadenas laterales (Kumar et al., 2018).
Debido a esas mismas características, se ha utilizado en la encapsulación de pigmentos (antocianinas, betalaínas y carotenoides) (tabla I). Sin embargo, este agente encapsulante debe usarse en concentraciones muy bajas (Antigo et al., 2017; Ravichandran et al., 2014; Rutz et al., 2013).
Para la encapsulación de antocianinas de mora azul mediante liofilización, Cai et al. (2019) probaron distintas concentraciones de carboximetilcelulosa y gx (30 : 1, 60 : 1, 90 : 1, 120 : 1, 150 : 1, w/w). Los resultados de ese trabajo demostraron que la eficiencia de encapsulación no depende de la relación entre los agentes encapsulantes, ya que todos se encontraron entre 96 y 97 %. Los autores destacan que la combinación de ambos agentes de encapsulación tiene un efecto sinérgico en la absorción de antocianinas y genera la formación de una película debido a las propiedades fisicoquímicas de ambas moléculas. Los autores también indican que las cargas negativas de la carboximetilcelulosa se repelen unas con otras, adsorbiendo agua y, dada la naturaleza hidrofílica de la gx, se une a la carboximetilcelulosa formando una red o película que protege a las antocianinas de la degradación durante el secado. Este efecto se confirmó mediante espectroscopía infrarroja por transformada de Fourier (ftir).
Por otro lado, Ravichandran et al. (2014) y Antigo et al. (2017) reportan investigaciones enfocadas en la encapsulación de betalaínas con gx-mdx en betabel, comparando el efecto del método de encapsulación (secado por atomización contra liofilización). Los resultados obtenidos por Ravichandran et al. (2014) sugieren que el método ideal para la encapsulación es la liofilización, ya que se retuvo 1.3 veces más betalaínas que con el secado por atomización. El color de los polvos obtenidos mediante secado por atomización resultó más claro (valores de L* más altos). Los valores de a* disminuyeron cerca de la mitad, en comparación con los obtenidos por liofilización; haciendo evidente el efecto de la temperatura como un factor determinante en la obtención de los pigmentos microencapsulados.
2.4. Goma guar
La goma guar (gg) proviene del endospermo de la semilla de Cyamopsis tetragonolobus. Es un galactomanano cuya ausencia de ácido urónico la distingue del resto de las gomas provenientes de semillas (Cano-Barrita y León-Martínez, 2016; George et al., 2019).
La estructura molecular (figura 5) consiste en una cadena principal constituida por unidades de α-D-galactosa unidas por los carbonos 1→4. La estructura tiene múltiples ramificaciones al azar de manosa/galactosa, las cuales se encuentran en proporción 2 : 1 (Hasan y Abdel-Raouf, 2018). De las gomas presentadas en este trabajo, la gg tiene el peso molecular más alto (tabla II).
La gg presenta propiedades similares a la gx, sin embargo, se caracteriza por su capacidad de absorber agua. Cuando la gg interactúa con el agua, la galactosa en las ramificaciones de la molécula unida a la cadena principal de manosa forma entrelazamientos intermoleculares, lo cual puede incrementar la viscosidad de la solución, incluso a bajas concentraciones (1 % w/v, solución acuosa, 10,000 cP) (Sharma et al., 2018).
La microencapsulación por el método de liofilización de pigmentos con gg es más conveniente que el secado por atomización. Para este último es necesario llevar a cabo la hidrólisis de la goma, debido a que las propiedades de rehidratación y de entrecruzamiento incrementan la viscosidad, lo que impide el paso a través de la tobera (Kuck y Noreña, 2016; Ravichandran et al., 2014). De acuerdo con Kuck y Noreña (2016), la encap-
sulación de antocianinas usando gg parcialmente hidrolizada y secado por atomización resultó en los valores más altos en la retención de antocianinas (combinada con polidextrosa o sola), con valores similares a los presentes al extracto sin deshidratar. Por el contrario, la liofilización fue capaz de retener parte de las antocianinas, pero los valores fueron menores a los obtenidos mediante secado por atomización, por lo que la gg
hidrolizada no protege a las antocianinas durante la liofilización. En lo que respecta a la retención del color, se registró el mismo comportamiento que en el contenido de antocianinas, siendo que el secado por atomización presentó los valores de a* más altos, alrededor de 41 % más retención del color rojo en comparación con la liofilización.
5.
Estructura molecular de la goma guar.
Figura
Figura 4.
Estructura molecular de la goma xantana.
3. Estabilidad de los pigmentos
Durante la preparación de alimentos, los ingredientes se someten a diferentes procesos. Estos pueden involucrar cambios en la temperatura; incrementándose debido a la pasteurización, escaldado, esterilización, o bien disminuyendo debido a las condiciones de almacenamiento en refrigeración o congelación, de igual forma pueden presentarse cambios químicos (pH, oxígeno) (Başlar et al., 2014; Ling et al., 2015).
3.1. Efecto de las condiciones de almacenamiento
Algunos autores hacen uso de herramientas estadísticas y probabilísticas para observar el comportamiento de los materiales de encapsulación y el compuesto activo bajo diferentes condiciones de almacenamiento (Yu y Lv, 2019). La cinética de reacción de la mayoría de los procesos estudiados en la degradación de pigmentos microencapsulados corresponde a un comportamiento de primer orden C t = C0e–kt, donde C0 es la concentración inicial; C t , la concentración al tiempo (t); y k es la constante de degradación, la cual se utiliza para el cálculo de la vida media (t½ = log(2)/k). En la tabla III se muestra un resumen de los datos cinéticos de degradación de antocianinas, betalaínas y carotenoides microencapsulados bajo diferentes condiciones de almacenamiento. En los siguientes apartados se explican a detalle los efectos de diversos factores durante el almacenamiento de los pigmentos microencapsulados y la degradación de algunas de sus propiedades.
3.1.1. Efecto de la temperatura
De forma general, los autores que han evaluado el efecto de la temperatura sobre la constante de degradación observaron que, al incrementar la temperatura durante el almacenamiento, también lo hace k, lo cual se refleja en la pérdida de pigmentos y una t½ más corta (Akhavan Mahdavi et al., 2016; Bustos-Garza
et al., 2013; Hojjati et al., 2014; Jiménez-Aguilar et al., 2011; Yu y Lv, 2019; Zhang et al., 2020). Por el contrario, temperaturas de refrigeración disminuyen el valor de k, ya que limitan la movilidad de las moléculas de agua que pueden estar presentes en el producto (pigmentos microencapsulados), además, temperaturas por debajo de la Tg, hacen menos probable que sucedan las reacciones. No obstante, la reducción de la temperatura por debajo de la Tg no es el único parámetro del cual depende la estabilidad de los pigmentos microencapsulados (Pitalua et al., 2010).
3.1.2. Influencia del agente encapsulante
Chranioti et al. (2015) observaron la influencia de diferentes agentes de encapsulación (ga y ga-almidón modificado) a condiciones fijas de almacenamiento (T = 40 °C, HR = 20 % y ausencia de luz) sobre la degradación de betalaínas y carotenoides. Ellos reportan que el uso exclusivo de mdx protege mejor a ambos pigmentos en comparación con ga y ga-almidón modificado. También indican que, al agregar ga a la mezcla, incrementaba la estabilidad en comparación con almidón modificado y quitosano. En otro estudio, Zhang et al. (2020) evaluaron ga y ga-mdx a las mismas condiciones de almacenamiento (T = 40 °C, HR = 40 %, sin luz); observaron que la adición de mdx incrementó el valor de k aproximadamente dos veces más que solo ga, lo cual disminuye el valor de t½ de almacenamiento, de 495 a 25 días. Lo anterior puede estar relacionado con la compatibilidad del compuesto activo con el agente encapsulante y la formación de moléculas más estables (Jimenez-Gonzalez et al., 2018; Moser et al., 2017).
3.1.3. Influencia de la humedad relativa
Rascón, Beristain, García y Salgado (2011) evaluaron el efecto de la humedad relativa (hr) en pigmentos de paprika microencapsulados con ga mediante secado por atomización,
mientras que Pitalua et al. (2010) hicieron lo propio en betalaínas de betabel y ga. Ambos estudios concluyen que las mejores condiciones de almacenamiento son por debajo del 52 % de humedad relativa (hr), ya que valores más altos provocan un colapso en la estructura de la cápsula y degradación de los compuestos encapsulados (Pitalua et al., 2010). Además, por encima del 70 % de hr se produce absorción de agua y cambios de estado físico (Rascón et al., 2011); si bien, los autores reportan que este cambio de estado generó a una especie de masa que actuó como una barrera protectora contra el oxígeno y mantuvo los pigmentos durante más tiempo, el cambio de estado dificulta su adición cuando se utiliza como colorante en alimentos.
3.1.4. Influencia por exposición a la luz
El efecto de la luz es otro de los parámetros que más se ha estudiado. Jiménez-Aguilar et al. (2011), Rutz et al. (2013), Hojjati et al. (2014) y De Marco et al. (2013) observaron antocianinas de mora azul (Vaccinium corymbosum) encapsuladas con gmez, carotenoides de jugo de cereza brasileña (Eugenia uniflora L.) encapsulados con gx, cantaxantinas de Dietzia natronolimnaea encapsuladas con ga, y bixina de achiote (Bixa orellana) encapsulada con ga-mdx, respectivamente. En todos los casos se concluyó que se degradaban a mayor velocidad (mayor valor de k, menor valor de t½) por la exposición de la luz durante el almacenamiento. En el caso de las antocianinas encapsuladas, Jiménez-Aguilar et al. (2011) reportaron una reducción de 717 a 70 días en los valores de vida media (t½) por la exposición de los microencapsulados a la luz (3000 lx / 25 °C). Mientras que De Marco et al. (2013) agregaron los pigmentos de bixina encapsulados a una solución acuosa, almacenada por 450 horas, al exponerlos a luz fluorescente (15 W / 25 °C), observaron una disminución de 231 a 44 días en el t½
3.1.5. Influencia de la morfología e interacción con el oxígeno
Como se mencionó previamente, la estructura de la microcápsula puede dictar la estabilidad de los pigmentos debido a las rugosidades, tamaño de partícula, grietas, entre otros. Al incrementar el área superficial, los compuestos activos pueden estar más expuestos a la interacción con el oxígeno (Zhang et al., 2020), dando como resultado una degradación de los pigmentos. Este fenómeno ha sido reportado por Haas et al. (2019), quienes encapsularon concentrado de zanahoria mediante secado por atomización y liofilización, obteniendo diferentes tamaños de partícula (área superficial). Los pigmentos encapsulados mediante secado por atomización con mayor área superficial fueron más estables después de 91 días de almacenamiento, con aproximadamente un 20 % más carotenoides al finalizar el experimento. Por otro lado, el polvo obtenido mediante liofilización en dos morfologías (polvo fino, y polvo más grande y amorfo), las partículas más grandes retuvieron cerca de un 10 % más carotenoides que el polvo fino.
Además, el método de encapsulación afecta a la retención, ya que las partículas más uniformes, como las obtenidas mediante secado por atomización, protegen mejor a los pigmentos que las obtenidas por liofilización (Haas et al., 2019); pues la molienda del producto puede ser manual, generando partículas grandes e irregulares. Asimismo, el contenido de humedad en la microcápsula, el espesor de la pared, la porosidad, higroscopicidad, entre otros, estarán en función del método de encapsulación y pueden ser factores importantes en la degradación de los pigmentos debido a la interacción con el oxígeno.
3.1.6. Efecto del pH
Debido a que la adición de los pigmentos se hace en matrices de diferente composición (lácteos, cárnicos, jugos, dul-
ces, entre otros), los valores de pH son diferentes. La evaluación de la estabilidad bajo diferentes valores de pH ha sido estudiada por Bustos-Garza et al. (2013), quienes observaron que la estabilidad depende del agente encapsulante en microencapsulados de astaxantina con ga, ga-inulina, ga-mdx y ga-wpc, adicionados a soluciones con valores de pH entre 3 y 7, almacenados durante 96 horas. Los microencapsulados de ga-wpc (1 : 1) y ga-inulina (1 : 3) fueron más estables
en soluciones con pH 6. Mientras que betalaínas de betabel encapsuladas con gx no mostraron dependencia al pH, pero sí al método de encapsulación. Los polvos obtenidos mediante secado por atomización y adicionados a una solución con pH 6 fueron menos estables que los obtenidos por liofilización, con una degradación al final del periodo de almacenamiento (7 días) del 44.9 % y 19.6 %, respectivamente (Antigo et al., 2017).
Cinéticas de degradación de los pigmentos microencapsulados
Fuente Goma a Método de secado b Condiciones de almacenamiento c k × 10³ (días -1) t½ (días)
T(°C) = 4; O2 = libre; Luz = no; RH % = 40 - -
Referencias
Jugo de arándanos (Vaccinium corymbosum) ga sd
ga-mdx (1:1) sd
ga-mdx (1:1) sd
Rosa japonesa (Rosa rugosa)
ga-mdx (1:1) fd
Jamaica (Hibiscus sabdariffa) ga-mdx (1:3) sd
Mora azul (Vaccinium myrtillus) gmez sd
Jugo de betabel ga (30 %) sd
T(°C) = 25; O2 = libre; Luz = no; RH % = 40 - -
T(°C) = 45; O2 = libre; Luz = no; RH % = 40 1.4 495
T(°C) = 4; O2 = libre; Luz = no; RH % = 40 - -
T(°C) = 25; O2 = libre; Luz = no; RH % = 40 - -
T(°C) = 45; O2 = libre; Luz = no; RH % = 40 2.77 25
T(°C) = 70 2088 0.33
T(°C) = 80 3283 0.21
T(°C) = 90
T(°C) = 70
= 80
T(°C) = 90 3974 0.17
T(°C) = 4; Luz = no
T(°C) = 25; Luz = no
T(°C) = 35; Luz = no
T(°C) = 42; Luz = no
T(°C) = 4; Luz = no 0.1295 259
Zhang et al., 2020
Yu y Lv, 2019
Mahdavi et al., 2016
et al., 2011 T(°C) = 25; Luz = sí
70 T(°C) = 25; Luz = no
T(°C) = 30; RH % = 11 - -
T(°C) = 30; RH % = 32.6 - -
T(°C) = 30; RH % = 52.1 - -
et al., 2010
Akhavan
Jiménez-Aguilar
Pitalua
Tabla III.
Cinéticas de degradación de los pigmentos microencapsulados (continuación)
Fuente Goma a
Betabel (Beta vulgaris)
Método de secado b Condiciones de almacenamiento c k × 10³ (días -1) t½ (días)
ga (15 %) fd
T(°C) = 40; Luz = no; RH % = 20
ga-almidón modificado (1:1) fd T(°C) = 40; Luz = no; RH % = 20
pH = 3; T(°C) = 30; O2 = no
pH = 4; T(°C) = 30; O2 = no
gx-mdx
(0.5:99.5) sd
5.8
Referencias
Chranioti et al., 2015
Jugo de cereza brasileña (Eugenia uniflora L.)
gx-mdx
(0.5:99.5) fd
Fuente Goma a
(1:1)
pH = 5; T(°C) = 30; O2 = no
pH = 6; T(°C) = 30; O2 = no
pH = 3; T(°C) = 30; O2 = no
= 4; T(°C) = 30; O2 = no
= 5; T(°C) = 30; O2 = no
= 6; T(°C) = 30; O2 = no
Método de secado b
Azafrán (Crocus sativus) ga fd
ga-almidón modificado (1:1)
Astaxantinas de Haematococcus pluvialis ga sd
ga-inulina (1:1)
ga-mdx (1:1)
5.8
Antigo et al., 2017
7.5
6.5
Condiciones de almacenamiento c - -
T(°C) = 40; Luz = no; RH % = 20
T(°C) = 40; Luz = no; RH % = 20
T(°C) = 30 - -
T(°C) = 40 - -
T(°C) = 50
ga-wpc (1:1) pH = 3; T(°C) = 25
ga-inulina
(0.25:0.75) pH = 4; T(°C) = 25
ga-mdx (0.25:0.75) pH = 5; T(°C) = 25
ga-wpc
(0.25:0.75)
Achiote (bixina) (Bixa orellana) ga-mdx (1:1) sd
Rutz et al., 2013
Referencias
Chranioti et al., 2015
Bustos-Garza et al., 2013
pH = 6; T(°C) = 25 -pH = 7; T(°C) = 25 - -
Luz = sí
De Marco et al., 2013 Luz = no
Tabla III.
Tabla III.
Cinéticas de degradación de los pigmentos microencapsulados (continuación)
Fuente Goma a Método de secado b
Cantaxantinas de Dietzia natronol imnaea ga sd
Condiciones de almacenamiento c
T(°C) = 4; Luz = sí - -
T(°C) = 25; Luz = sí - -
T(°C) = 45; Luz = sí - -
T(°C) = 4; Luz = no - -
T(°C) = 25; Luz = no - -
T(°C) = 45; Luz = no - -
Paprika (Capsicum annuum) ga (0.03 %) sd T(°C) = 35; RH % = 10.8
T(°C) =
Referencias
Hojjati et al., 2014
Rascón et al., 2011
a ga, goma arábiga; gmez, goma de mezquite; gx, goma xantana; gt, goma tara; mdx, maltodextrina; wpc, concentrado de proteína de suero de leche sp; b secado por atomización (spray drying); fd, liofilización (freeze drying); c T (°C), temperatura en grados centígrados; O2, oxígeno; RH %, humedad relativa.
4. Aplicación de pigmentos microencapsulados en matrices alimenticias
Es importante evaluar la estabilidad de los pigmentos en matrices alimenticias, ya que aún son pocos los estudios que han reportado los efectos de la incorporación de pigmentos en alimentos (tabla IV).
Xu, Cheng, Liu y Zhu (2019) incorporaron extractos de morera (Morus alba) como antioxidantes y colorantes en jamón y observaron que la adición de los microencapsulados inhibía la oxidación de lípidos y proteínas durante la preparación y el almacenamiento del producto.
Los pigmentos microencapsulados también se utilizan en golosinas. La incorporación de antocianinas de la piel de berenjena (Solanum melongena) para la elaboración de gomitas ha reportado mejoras en el color y buena aceptabilidad sensorial cuando se agrega del 1 al 1.5 % de polvo (Sarabandi et al., 2019).
Otros trabajos han evaluado los resultados de su uso con goma de mascar como matriz alimenticia, incorporando betalaínas de betabel (Beta vulgaris) (Chranioti et al., 2015), carotenoides de azafrán (Crocus sativus) (Chranioti et al., 2015) o de microalgas (Nannochloropsis oculata; Isochrysis galbana) (Palabiyik et al., 2018). En todos los casos, se observó que la incorporación de los pigmentos microencapsulados incrementó el color e hizo más agradables los productos. De igual forma, carotenoides de zanahoria (Daucus carota) han sido incorporados en caramelos macizos, donde las características físicas de la matriz alimenticia minimizaron el contacto con el ambiente, manteniendo los pigmentos adicionados (Shaaruddin et al., 2019).
La incorporación de pigmentos microencapsulados a productos que sufren cambios de temperatura, específicamente el proceso de cocción en la elaboración de pan, también ha sido evaluada. Tatar Turan et al. (2015) observaron la incorporación
Tabla IV. de antocianinas de mora azul con gg, mientras que Papillo et al. (2018) examinaron la de arroz negro con ga (Oryza sativa L., var. Artemide). Se ha notado que, si bien existe una reducción en las antocianinas debido al calor, la microencapsulación protege los pigmentos de la degradación térmica. Sin un cambio de color aparente, los resultados son favorables, ya que a altas temperaturas los compuestos polifenoles, como las antocianinas, generan O-quinonas con tonalidades cafés (Sant’Anna et al., 2013). Asimismo, se han evaluado los efectos del uso de carotenoides en pan y se observa que al adicionar licopeno encapsulado con almidón modificado, la encapsulación protegió a los pigmentos durante el horneado (Rocha et al., 2012). Por su parte, Ursache et al. (2018) incorporaron carotenoides encapsulados con ga en muffins (panecillos); los panelistas prefirieron aquellos que contenían carotenoides debido a que el color amarillo resultaba más agradable. Los autores mencionan que, además del color, la adición de los carotenoides tuvo un efecto antimicrobiano, ya que durante el almacenamiento de los panecillos no se observó el crecimiento de hongos ni levaduras.
Otros productos en los que se ha analizado los efectos de la adición de pigmentos microencapsulados son las bebidas sin alcohol adicionadas con bixina de achiote sabor mandarina (Tupuna et al., 2018) y con betalaínas de tuna roja (Opuntia stricta) (Obón et al., 2009); gelatinas con antocianinas de pulpa de jussara (Euterpe edulis Martius) (Bernardes et al., 2019); helado con antocianinas de mora azul (Tatar Turan et al., 2015); y yogur con betalaínas de pitaya (Stenocereus pruinosus) (Vargas-Campos et al., 2018) y tuna roja (Obón et al., 2009). En todos los casos se reportaron mejoras tanto en el color como en las propiedades antioxidantes debido a la presencia de los pigmentos. Vemos entonces que los pigmentos microencapsulados son una fuente importante de antioxidantes que puede incorporarse a la dieta a través del consumo de alimentos comunes.
CONCLUSIONES Y COMENTARIOS FINALES
Los métodos de encapsulación mediante secado por atomización y liofilización son eficaces en la protección de los pigmentos, incrementando su estabilidad y ayudando a obtener polvos de fácil incorporación a diferentes productos. Con base en los
Incorporación de pigmentos microencapsulados a matrices alimenticias
Fuente Adición a alimentos
Antocianinas
Pulpa de morera (Morus alba)
Referencias
Antioxidante y colorante en jamón de cerdo Xu et al., 2019
Extracto de mora azul (Vaccinium corymbosum) Helado y pan
Extracto de bagazo de uva
Tatar Turan et al., 2015
Películas activas biodegradables Stoll et al., 2016
Extracto de piel de berenjena (Solanum melongena) Gomitas Sarabandi et al., 2019
Arroz negro (Oryza sativa L.) Biscochos
Papillo et al., 2018
Jussara (Euterpe edulis Marius) Gelatinas Bernardes et al., 2019
Betalaínas
Betabel (Beta vulgaris) Goma de mascar
Chranioti et al., 2015
Pitaya (Stenocereus pruinosus) Yogur VargasCampos et al., 2018
Tuna roja (Opuntia stricta) Yogur y bebidas
Carotenoides
Azafrán (Crocus sativus) Goma de mascar
Zanahoria (Daucus carota) Caramelo macizo
Semillas de achiote (Biza orellana) Bebida isotónica sabor mandarina
Sea buckthorn (Hippophae rhamnoides L.)
Obón et al., 2009
Chranioti et al., 2015
Shaaruddin et al., 2019
Tupuna et al., 2018
Muffins (sustitución del 6 % del total de harina) Ursache et al., 2018
Microalgas (Nannochloropsis oculata; Isochrysis galbana) Goma de mascar
Licopeno comercial Pastel
Palabiyik et al., 2018
Rocha et al., 2012
estudios presentados en esta revisión, las gomas muestran una excelente protección de los pigmentos con ambos métodos de encapsulación. La goma arábiga, la goma de mezquite, la goma xantana y la goma guar pueden ser utilizadas para la encapsulación de pigmentos (antocianinas, betalaínas y carotenoides), pero es necesario seleccionar las condiciones óptimas de encapsulación, así como tener en cuenta la interacción entre el agente encapsulante y el compuesto activo, el método de encapsulación, y las condiciones de operación. En particular, debido a las propiedades físicas de las soluciones, vemos que la goma arábiga y la de mezquite son más adecuadas para el secado por atomizació, mientras que la goma xantana y la guar lo son para la liofilización.
Se debe agregar que, si bien la estabilidad de los pigmentos mejora después de la microencapsulación, factores como la temperatura, la exposición a la luz, el oxígeno, el tiempo, y los niveles de pH, son los más importantes durante el almacenamiento e incorporación. A pesar de ello, se observa que, sin importar el pigmento microencapsulado, el agente encapsulante o el método de encapsulación, la adición de los pigmentos mejora los productos tanto visual como nutricionalmente.
Finalmente, vale la pena notar que aún es necesario el estudio de la degradación sobre condiciones reales de incorporación, así como del consumo de estos productos después de la adición de los pigmentos microencapsulados con los diferentes agentes encapsulantes mencionados en la revisión. Ambos son campos de investigación importantes para futuros trabajos.
AGRADECIMIENTOS
El autor Jiménez-González, O. agradecen a la Universidad de las Américas Puebla (udlap) y al Consejo Nacional de Humanidades, Ciencia y Tecnología (conahcyt) —hoy Secretaría de Ciencia, Humanidades, Tecnología e Innovación (secihti)—, por el apoyo para la realización de sus estudios doctorales en Ciencia de Alimentos.
REFERENCIAS
Aguiar, J., Estevinho, B. N. y Santos, L. (2016). Microencapsulation of natural antioxidants for food application – The specific case of coffee antioxidants – A review. Trends in Food Science & Technology, 58, 21-39. doi: 10.1016/j. tifs.2016.10.012
Ahmad, S., Ahmad, M., Manzoor, K., Purwar, R. y Ikram, S. (2019). A review on latest innovations in natural gums based hydrogels: preparations & applications. International Journal of Biological Macromolecules, 136, 870-890. doi: 10.1016/j.ijbiomac.2019.06.113
Akhavan Mahdavi, S., Jafari, S. M., Assadpour, E., & Ghorbani, M. (2016). Storage stability of encapsulated barberry’s anthocyanin and its application in jelly formulation. Journal of Food Engineering, 181, 59-66. doi: 10.1016/j. jfoodeng.2016.03.003
Álvarez-Henao, M. V., Saavedra, N., Medina, S., Jiménez Cartagena, C., Alzate, L. M. y Londoño-Londoño, J. (2018). Microencapsulation of lutein by spray-drying: characterization and stability analyses to promote its use as a functional ingredient. Food Chemistry, 256, 181-187. doi: 10.1016/j.foodchem.2018.02.059
Antigo, J. L. D., Bergamasco, R. de C. y Madrona, G. S. (2017). Effect of pH on the stability of red beet extract (Beta vulgaris l.) microcapsules produced by spray drying or freeze drying. Food Science and Technology, 38(1), 72-77. doi: 10.1590/1678-457x.34316
Bakry, A. M., Abbas, S., Ali, B., Majeed, H., Abouelwafa, M. Y., Mousa, A. y Liang, L. (2016). Microencapsulation of oils: a comprehensive review of benefits, techniques, and applications. Comprehensive Reviews in Food Science and Food Safety, 15(1), 143-182. doi: 10.1111/1541-4337.12179
Başlar, M., Karasu, S., Kiliçli, M., Us, A. A. y Sağdiç, O. (2014). Degradation kinetics of bioactive compounds and antioxidant activity of pomegranate arils during the drying process. International Journal of Food Engineering, 10(4), 839848. doi: 10.1515/ijfe-2014-0080
Beristain, C. I., Azuara, E. y Vernon-Carter, E. J. (2002). Effect of water activity on the stability to oxidation of spray-dried encapsulated orange peel oil using mesquite gum (Prosopis Juliflora) as wall material. Journal of Food Science, 67(1), 206-211. doi: 10.1111/j.1365-2621.2002.tb11385.x
Beristain, C. I., García, H. S. y Vernon-Carter, E. J. (2001). Spray-dried encapsula-
Uso de gomas naturales en la microencapsulación de pigmentos (antocianinas, betalaínas y carotenoides) mediante secado por atomización y liofilización
tion of cardamom (Elettaria Cardamomum) essential oil with mesquite (Prosopis Juliflora) gum. LWT - Food Science and Technology, 34(6), 398401. doi: 10.1006/fstl.2001.0779
Beristain, C. I. y Vernon-Carter, E. J. (1994). Utilization of mesquite (Prosopis julijlora) gum as emulsion stabilizing agent for spray drying encapsulated orange peel oil. Drying Technology, 12(7), 1727-1733. doi: 10. 1080/07373939408962195
Bernardes, A. L., Moreira, J. A., Tostes, M. das G. V., Costa, N. M. B., Silva, P. I. y Costa, A. G. V. (2019). In vitro bioaccessibility of microencapsulated phenolic compounds of jussara (Euterpe edulis Martius) fruit and application in gelatine model-system. LWT, 102, 173-180. doi: 10.1016/j.lwt.2018.12.009
Bhandari, B. R. y Howes, T. (1999). Implication of glass transition for the drying and stability of dried foods. Journal of Food Engineering, 40(1-2), 71-79. doi: 10.1016/S0260-8774(99)00039-4
Bhandari, B. R., Senoussi, A., Dumoulin, E. D. y Lebert, A. (1993). Spray drying of concentrated fruit juices. Drying Technology, 11(5), 1081-1092. doi: 10.1080/07373939308916884
Bonilla-Ahumada, F. de J., Khandual, S. y Lugo-Cervantes, E. del C. (2018). Microencapsulation of algal biomass (Tetraselmis chuii) by spray-drying using different encapsulation materials for better preservation of beta-carotene and antioxidant compounds. Algal Research, 36, 229-238. doi: 10.1016/j.algal.2018.10.006
Bosquez-Molina, E., Guerrero-Legarreta, I. y Vernon-Carter, E. J. (2003). Moisture barrier properties and morphology of mesquite gum–candelilla wax based edible emulsion coatings. Food Research International, 36(9–10), 885–893. doi: 10.1016/S0963-9969(03)00097-8
Bustos-Garza, C., Yáñez-Fernández, J. y Barragán-Huerta, B. E. (2013). Thermal and pH stability of spray-dried encapsulated astaxanthin oleoresin from Haematococcus pluvialis using several encapsulation wall materials. Food Research International, 54(1), 641-649. doi: 10.1016/j.foodres.2013.07.061
Cai, X., Du, X., Cui, D., Wang, X., Yang, Z. y Zhu, G. (2019). Improvement of stability of blueberry anthocyanins by carboxymethyl starch/xanthan gum combinations microencapsulation. Food Hydrocolloids, 91, 238-245. doi: 10.1016/j. foodhyd.2019.01.034
Çam, M., İçyer, N. C. y Erdoğan, F. (2014). Pomegranate peel phenolics: microencapsulation, storage stability and potential ingredient for functional food
development. LWT - Food Science and Technology, 55(1), 117-123. doi: 10.1016/j.lwt.2013.09.011
Cano-Barrita, P. F. de J. y León-Martínez, F. M. (2016). Biopolymers with viscosity-enhancing properties for concrete. En F. Pacheco-Torgal, et al. (Eds.), Biopolymers and Biotech Admixtures for Eco-Efficient Construction Materials (pp. 221-252). doi: 10.1016/B978-0-08-100214-8.00011-7
Carrillo-Navas, H., González-Rodea, D. A., Cruz-Olivares, J., Barrera-Pichardo, J. F., Román-Guerrero, A. y Pérez-Alonso, C. (2011). Storage stability and physicochemical properties of passion fruit juice microcapsules by spray-drying. Revista Mexicana de Ingeniería Química, 10(3), 421–430.
Castro-Enríquez, D. D., Montaño-Leyva, B., Del Toro-Sánchez, C. L., Juaréz-Onofre, J. E., Carvajal-Millan, E., Burruel-Ibarra, S. E., Tapia-Hernández, J. A., BarrerasUrbina, C. G. y Rodríguez-Félix, F. (2019). Stabilization of betalains by encapsulation—a review. Journal of Food Science and Technology, 57(5), 1587-1600. doi: 10.1007/s13197-019-04120-x
Chawla, H., Parle, M., Sharma, K. y Yadav, M. (2016). Beetroot: a health promoting functional food. Inventi Rapid: Nutraceuticals, 1(1), 8-12.
Chranioti, C., Nikoloudaki, A. y Tzia, C. (2015). Saffron and beetroot extracts encapsulated in maltodextrin, gum Arabic, modified starch and chitosan: incorporation in a chewing gum system. Carbohydrate Polymers, 127, 252-263. doi: 10.1016/j.carbpol.2015.03.049
Clark, J. P. (2009). Freeze Drying. En J. P. Clark (Ed.), Case Studies in Food Engineering (pp. 67-73). doi: 10.1007/978-1-4419-0420-1_8
Clydesdale, F. M. (1993). Color as a factor in food choice. Critical Reviews in Food Science and Nutrition, 33(1), 83-101. doi: 10.1080/10408399309527614
Corrêa, R. C. G., Garcia, J. A. A., Correa, V. G., Vieira, T. F., Bracht, A. y Peralta, R. M. (2019). Pigments and vitamins from plants as functional ingredients: current trends and perspectives. Advances in Food and Nutrition Research, 90, 259303. doi: 10.1016/bs.afnr.2019.02.003
De Marco, R., Vieira, A. M. S., Ugri, M. C. A., Monteiro, A. y Bergamasco, R. de C. (2013). Microencapsulation of annatto seed extract: stability and application. Chemical Engineering Transactions, 32, 1777-1782. doi: 10.3303/CET1332297
Dolinsky, A. A. (2001). High-temperature spray drying. Drying Technology, 19(5), 785-806. doi: 10.1081/DRT-100103770
Ephrem, E., Najjar, A., Charcosset, C. y Greige-Gerges, H. (2018). Encapsulation of natural active compounds, enzymes, and probiotics for fruit juice fortification,
preservation, and processing: an overview. Journal of Functional Foods, 48, 6584. doi: 10.1016/j.jff.2018.06.021
Fang, Z. y Bhandari, B. (2012). Spray drying, freeze drying and related processes for food ingredient and nutraceutical encapsulation. En N. Garti y D. J. McClements (Eds.), Encapsulation Technologies and Delivery Systems for Food Ingredients and Nutraceuticals (pp. 73-109). doi: 10.1533/9780857095909.2.73
Francis, F. J. (1995). Quality as influenced by color. Food Quality and Preference, 6(3), 149-155. doi: 10.1016/0950-3293(94)00026-R
Fu, D., Deng, S., McClements, D. J., Zhou, L., Zou, L., Yi, J., Lui, C. y Liu, W. (2019). Encapsulation of β-carotene in wheat gluten nanoparticle-xanthan gum-stabilized Pickering emulsions: enhancement of carotenoid stability and bioaccessibility. Food Hydrocolloids, 89, 80-89. doi: 10.1016/j.foodhyd.2018.10.032
Garber, L. L., Hyatt, E. M. y Nafees, L. (2016). The effects of analogous food color on perceived flavor: a factorial investigation. Journal of Food Products Marketing, 22(4), 486-500. doi: 10.1080/10454446.2015.1072866
García-Márquez, E., Román-Guerrero, A., Cruz-Sosa, F., Lobato-Calleros, C., Álvarez-Ramírez, J., Vernon-Carter, E. J. y Espinosa-Andrews, H. (2015). Effect of layer (calcium phosphate–chitosan)-by-layer (mesquite gum) matrix on carotenoids-in-water-emulsion properties. Food Hydrocolloids, 43, 451-458. doi: 10.1016/j.foodhyd.2014.07.005
George, A., Shah, P. A. y Shrivastav, P. S. (2019). Guar gum: versatile natural polymer for drug delivery applications. European Polymer Journal, 112, 722-735. doi: 10.1016/j.eurpolymj.2018.10.042
Gharsallaoui, A., Roudaut, G., Chambin, O., Voilley, A. y Saurel, R. (2007). Applications of spray-drying in microencapsulation of food ingredients: an overview. Food Research International, 40(9), 1107-1121. doi: 10.1016/j.foodres.2007.07.004
Gomez-Estaca, J., Comunian, T. A., Montero, P., Ferro-Furtado, R. y Favaro-Trindade, C. S. (2016). Encapsulation of an astaxanthin-containing lipid extract from shrimp waste by complex coacervation using a novel gelatin–cashew gum complex. Food Hydrocolloids, 61, 155-162. Doi: 10.1016/j.foodhyd.2016.05.005
Gupta, V. K., Sood, S., Agarwal, S., Saini, A. K. y Pathania, D. (2018). Antioxidant activity and controlled drug delivery potential of tragacanth gum-cl- poly (lactic acid-co-itaconic acid) hyidrogel. International Journal of Biological Macromolecules, 107(B), 2534-2543. doi: 10.1016/j.ijbiomac.2017.10.138
Haas, K., Obernberger, J., Zehetner, E., Kiesslich, A., Volkert, M., y Jaeger, H. (2019). Impact of powder particle structure on the oxidation stability and color of encapsulated crystalline and emulsified carotenoids in carrot concentrate powders. Journal of Food Engineering, 263, 398-408. doi: 10.1016/j.jfoodeng.2019.07.025
Habibi, H. y Khosravi-Darani, K. (2017). Effective variables on production and structure of xanthan gum and its food applications: a review. Biocatalysis and Agricultural Biotechnology, 10, 130-140. doi: 10.1016/j.bcab.2017.02.013
Hamdani, A. M., Wani, I. A. y Bhat, N. A. (2019). Sources, structure, properties and heal-
th benefits of plant gums: a review. International Journal of Biological Macromolecules, 135, 46-61. doi: 10.1016/j.ijbiomac.2019.05.103
Hasan, A. M. A. y Abdel-Raouf, M. E. (2018). Applications of guar gum and its derivatives in petroleum industry: a review. Egyptian Journal of Petroleum, 27(4), 1043-1050. doi: 10.1016/j.ejpe.2018.03.005
He, J. y Giusti, M. M. (2010). Anthocyanins: natural colorants with health-promoting properties. Annual Review of Food Science and Technology, 1(1), 163-187. doi: 10.1146/annurev.food.080708.100754
Hojjati, M., Razavi, S. H., Rezaei, K. y Gilani, K. (2014). Stabilization of canthaxanthin produced by Dietzia natronolimnaea hs-1 with spray drying microencapsulation. Journal of Food Science and Technology, 51(9), 2134-2140. doi: 10.1007/s13197-012-0713-0
Jain, A., Thakur, D., Ghoshal, G., Katare, O. P. y Shivhare, U. S. (2016). Characterization of microcapsulated β-carotene formed by complex coacervation using casein and gum tragacanth. International Journal of Biological Macromolecules, 87, 101-113. doi: 10.1016/j.ijbiomac.2016.01.117
Janiszewska, E. (2014). Microencapsulated beetroot juice as a potential source of betalain. Powder Technology, 264, 190-196. doi: 10.1016/j.powtec.2014.05.032
Jiménez-Aguilar, D. M., Ortega-Regules, A. E., Lozada-Ramírez, J. D., Pérez-Pérez, M. C. I., Vernon-Carter, E. J. y Welti-Chanes, J. (2011). Color and chemical stability of spray-dried blueberry extract using mesquite gum as wall material. Journal of Food Composition and Analysis, 24(6), 889-894. doi: 10.1016/j. jfca.2011.04.012
Jimenez-Gonzalez, O., Ruiz-Espinosa, H., Luna-Guevara, J. J., Ochoa-Velasco, C. E., Luna Vital, D. y Luna-Guevara, M. L. (2018). A potential natural coloring agent with antioxidant properties: microencapsulates of Renealmia alpinia (Rottb.) Maas fruit pericarp. NFS Journal, 13, 1-9. doi: 10.1016/j.nfs.2018.08.001
Kuck, L. S. y Noreña, C. P. Z. (2016). Microencapsulation of grape (Vitis labrusca var. Bordo) skin phenolic extract using gum Arabic, polydextrose, and partially hydrolyzed guar gum as encapsulating agents. Food Chemistry, 194, 569-576. doi: 10.1016/j.foodchem.2015.08.066
Kumar, A., Rao, K. M. y Han, S. S. (2018). Application of xanthan gum as polysaccharide in tissue engineering: a review. Carbohydrate Polymers, 180, 128-144. doi: 10.1016/j.carbpol.2017.10.009
Kshirsagar, A. C., Yenge, V., Sarkar, A., Zamre, M. y Singhal, R. S. (2010). Evaluation of microencapsulated turmeric oleoresin for pre-extrusion coloring using response surface methodology. Journal of Food Processing and Preservation, 34(2), 302-315. doi: 10.1111/j.1745-4549.2009.00371.x
Labuschagne, P. (2018). Impact of wall material physicochemical characteristics on the stability of encapsulated phytochemicals: a review. Food Research International, 107, 227-247. doi: 10.1016/j.foodres.2018.02.026
Lehto, S., Buchweitz, M., Klimm, A., Straßburger, R., Bechtold, C. y Ulberth, F. (2017). Comparison of food colour regulations in the eu and the us: A review of cu-
rrent provisions. Food Additives & Contaminants: Part A, 34(3), 335-355. doi: 10.1080/19440049.2016.1274431
Ling, B., Tang, J., Kong, F., Mitcham, E. J. y Wang, S. (2015). Kinetics of food quality changes during thermal processing: a review. Food and Bioprocess Technology, 8(2), 343-358. doi: 10.1007/s11947-014-1398-3
López-Franco, Y., Higuera-Ciapara, I., Lizardi-Mendoza, J., Goycoolea, F. M. y Wang, W. (2009). Other exudates: Tragacanth, karaya, mesquite gum and larchwood arabinogalactan. En G. O. Phillips y P. A. Williams (Eds.) Handbook of Hydrocolloids (pp. 495-534). doi: 10.1533/9781845695873.495
Mahdavi, S. A., Jafari, S. M., Ghorbani, M. y Assadpoor, E. (2014). Spray-drying microencapsulation of anthocyanins by natural biopolymers: a review. Drying Technology, 32(5), 509-518. doi: 10.1080/07373937.2013.839562
Mahdi Jafari, S., He, Y. y Bhandari, B. (2006). Nano-emulsion production by sonication and microfluidization—a comparison. International Journal of Food Properties, 9(3), 475-485. doi: 10.1080/10942910600596464
Martins, N., Roriz, C. L., Morales, P., Barros, L. y Ferreira, I. C. F. R. (2016). Food colorants: challenges, opportunities and current desires of agro-industries to ensure consumer expectations and regulatory practices. Trends in Food Science & Technology, 52, 1-15. Doi: 10.1016/j.tifs.2016.03.009
Mishra, M. (Ed.). (2015). Handbook of Encapsulation and Controlled Release. crc Press. doi: 10.1201/b19038
Morais, A. R. do V., Alencar, É. do N., Xavier Júnior, F. H., De Oliveira, C. M., Marcelino, H. R., Barratt, G., Fessi, H, Do Egito, E. S. y Elaissari, A. (2016). Freeze-drying of emulsified systems: a review. International Journal of Pharmaceutics, 503(1-2), 102-114. doi: 10.1016/j.ijpharm.2016.02.047
Moser, P., Telis, V. R. N., De Andrade Neves, N., García-Romero, E., Gómez-Alonso, S. y Hermosín-Gutiérrez, I. (2017). Storage stability of phenolic compounds in powdered BRS Violeta grape juice microencapsulated with protein and maltodextrin blends Food Chemistry, 214, 308-318. doi: 10.1016/j.foodchem.2016.07.081
Naik, R., Arunsandeep, G., & Chandramohan, V. (2017). Numerical simulation for freeze drying of skimmed milk with moving sublimation front using tri-diagonal matrix algorithm. Journal of Applied Fluid Mechanics, 10(3), 813-818. doi: 10.18869/acadpub.jafm.73.240.27054
Ngamwonglumlert, L., Devahastin, S. y Chiewchan, N. (2017). Natural colorants: pigment stability and extraction yield enhancement via utilization of appropriate pretreatment and extraction methods. Critical Reviews in Food Science and Nutrition, 57(15), 3243-3259. doi: 10.1080/10408398.2015.1109498
Nie, S.-P., Wang, C., Cui, S. W., Wang, Q., Xie, M.-Y. y Phillips, G. O. (2013). A further amendment to the classical core structure of gum arabic (Acacia senegal). Food Hydrocolloids, 31(1), 42-48. doi: 10.1016/j.foodhyd.2012.09.014
Niu, B., Shao, P., Luo, Y. y Sun, P. (2020). Recent advances of electrosprayed particles as encapsulation systems of bioactives for food application. Food Hydroco-
lloids, 99, 105376. doi: 10.1016/j.foodhyd.2019.105376
Obón, J. M., Castellar, M. R., Alacid, M. y Fernández-López, J. A. (2009). Production of a red–purple food colorant from Opuntia stricta fruits by spray drying and its application in food model systems. Journal of Food Engineering, 90(4), 471479. doi: 10.1016/j.jfoodeng.2008.07.013
Ochoa-Velasco, C. E., Salazar-González, C., Cid-Ortega, S. y Guerrero-Beltrán, J. A. (2017). Antioxidant characteristics of extracts of Hibiscus sabdariffa calyces encapsulated with mesquite gum. Journal of Food Science and Technology, 54(7), 1747-1756. doi: 10.1007/s13197-017-2564-1
Ozkan, G., Franco, P., De Marco, I., Xiao, J. y Capanoglu, E. (2019). A review of microencapsulation methods for food antioxidants: Principles, advantages, drawbacks and applications. Food Chemistry, 272, 494-506. doi: 10.1016/j. foodchem.2018.07.205
Paakki, M., Sandell, M. y Hopia, A. (2019). Visual attractiveness depends on colorfulness and color contrasts in mixed salads. Food Quality and Preference, 76, 81-90. doi: 10.1016/j.foodqual.2019.04.004
Palabiyik, I., Durmaz, Y., Öner, B., Toker, O. S., Coksari, G., Konar, N. y Tamtürk, F. (2018). Using spray-dried microalgae as a natural coloring agent in chewing gum: Effects on color, sensory, and textural properties. Journal of Applied Phycology, 30(2), 1031-1039. doi: 10.1007/s10811-017-1324-y
Palaniraj, A. y Jayaraman, V. (2011). Production, recovery and applications of xanthan gum by Xanthomonas campestris. Journal of Food Engineering, 106(1), 1-12. doi: 10.1016/j.jfoodeng.2011.03.035
Papillo, V. A., Locatelli, M., Travaglia, F., Bordiga, M., Garino, C., Arlorio, M. y Coïsson, J. D. (2018). Spray-dried polyphenolic extract from Italian black rice (Oryza sativa L., var. Artemide) as new ingredient for bakery products. Food Chemistry, 269, 603-609. doi: 10.1016/j.foodchem.2018.07.059
Pavón-García, L. M. A., Pérez-Alonso, C., Orozco-Villafuerte, J., Pimentel-González, D. J., Rodríguez-Huezo, M. E. y Vernon-Carter, E. J. (2011). Storage stability of the natural colourant from Justicia spicigera microencapsulated in protective colloids blends by spray-drying: Colour storage stability. International Journal of Food Science & Technology, 46(7), 1428-1437. doi: 10.1111/j.13652621.2011.02634.x
Pieczykolan, E. y Kurek, M. A. (2019). Use of guar gum, gum arabic, pectin, betaglucan and inulin for microencapsulation of anthocyanins from chokeberry. International Journal of Biological Macromolecules, 129, 665-671. doi: 10.1016/j.ijbiomac.2019.02.073
Piqueras-Fiszman, B. y Spence, C. (2014). Colour, pleasantness, and consumption behaviour within a meal. Appetite, 75, 165-172. doi: 10.1016/j. appet.2014.01.004
Pitalua, E., Jimenez, M., Vernon-Carter, E. J. y Beristain, C. I. (2010). Antioxidative activity of microcapsules with beetroot juice using gum Arabic as wall material. Food and Bioproducts Processing, 88(2-3), 253-258. doi: 10.1016/j.fbp.2010.01.002
Porcherot, C., Delplanque, S., Gaudreau, N. y Cayeux, I. (2013). Seeing, smelling, feeling! Is there an influence of color on subjective affective responses to perfumed fabric softeners? Food Quality and Preference, 27(2), 161-169. doi: 10.1016/j.foodqual.2012.06.011
Quan, J., Kim, S.-M., Pan, C.-H. y Chung, D. (2013). Characterization of fucoxanthin-loaded microspheres composed of cetyl palmitate-based solid lipid core and fish gelatin–gum arabic coacervate shell. Food Research International, 50(1), 31-37. doi: 10.1016/j.foodres.2012.09.040
Qv, X.-Y., Zeng, Z.-P. y Jiang, J.-G. (2011). Preparation of lutein microencapsulation by complex coacervation method and its physicochemical properties and stability. Food Hydrocolloids, 25(6), 1596-1603. doi: 10.1016/j.foodhyd.2011.01.006
Ramakrishnan, Y., Adzahan, N. M., Yusof, Y. A. y Muhammad, K. (2018). Effect of wall materials on the spray drying efficiency, powder properties and stability of bioactive compounds in tamarillo juice microencapsulation. Powder Technology, 328, 406-414. doi: 10.1016/j.powtec.2017.12.018
Rascón, M. P., Beristain, C. I., García, H. S. y Salgado, M. A. (2011). Carotenoid retention and storage stability of spray-dried encapsulated paprika oleoresin using gum Arabic and Soy protein isolate as wall materials. LWT - Food Science and Technology, 44(2), 549-557. doi: 10.1016/j.lwt.2010.08.021
Ravichandran, K., Palaniraj, R., Saw, N. M. M. T., Gabr, A. M. M., Ahmed, A. R., Knorr, D. y Smetanska, I. (2014). Effects of different encapsulation agents and drying process on stability of betalains extract. Journal of Food Science and Technology, 51(9), 2216-2221. doi: 10.1007/s13197-012-0728-6
Rezende, Y. R. R. S., Nogueira, J. P. y Narain, N. (2018). Microencapsulation of extracts of bioactive compounds obtained from acerola (Malpighia emarginata dc) pulp and residue by spray and freeze drying: hhemical, morphological and chemometric characterization. Food Chemistry, 254, 281-291. doi: 10.1016/j. foodchem.2018.02.026
Rezvankhah, A., Emam-Djomeh, Z. y Askari, G. (2020). Encapsulation and delivery of bioactive compounds using spray and freeze-drying techniques: a review. Drying Technology, 38(1-2), 235–258. doi: 10.1080/07373937.2019.1653906
Rocha, G. A., Fávaro-Trindade, C. S. y Grosso, C. R. F. (2012). Microencapsulation of lycopene by spray drying: characterization, stability and application of microcapsules. Food and Bioproducts Processing, 90(1), 37-42. doi: 10.1016/j. fbp.2011.01.001
Rodriguez-Amaya, D. B. (2016). Natural food pigments and colorants. Current Opinion in Food Science, 7, 20-26. doi: 10.1016/j.cofs.2015.08.004
Rodriguez-Amaya, D. B. (2019). Update on natural food pigments – A mini-review on carotenoids, anthocyanins, and betalains. Food Research International, 124, 200-205. doi: 10.1016/j.foodres.2018.05.028
Rodríguez-Rodríguez, R., Espinosa-Andrews, H., Morales-Hernández, N., LobatoCalleros, C. y Vernon-Carter, E. J. (2018). Mesquite gum/chitosan insoluble
complexes: relationship between the water state and viscoelastic properties. Journal of Dispersion Science and Technology, 40(9), 1345-1352. doi: 10.1080/01932691.2018.1513848
Romero-González, J., Shun Ah-Hen, K., Lemus-Mondaca, R. y Muñoz-Fariña, O. (2020). Total phenolics, anthocyanin profile and antioxidant activity of maqui, Aristotelia chilensis (Mol.) Stuntz, berries extract in freeze-dried polysaccharides microcapsules. Food Chemistry, 313, 126115. doi: 10.1016/j.foodchem.2019.126115
Rutz, J. K., Zambiazi, R. C., Borges, C. D., Krumreich, F. D., Da Luz, S. R., Hartwig, N. y Da Rosa, C. G. (2013). Microencapsulation of purple Brazilian cherry juice in xanthan, tara gums and xanthan-tara hydrogel matrixes. Carbohydrate Polymers, 98(2), 1256-1265. doi: 10.1016/j.carbpol.2013.07.058
Salarbashi, D. y Tafaghodi, M. (2018). An update on physicochemical and functional properties of newly seed gums. International Journal of Biological Macromolecules, 119, 1240-1247. doi: 10.1016/j.ijbiomac.2018.06.161
Sant’Anna, V., Gurak, P. D., Ferreira Marczak, L. D. y Tessaro, I. C. (2013). Tracking bioactive compounds with colour changes in foods – A review. Dyes and Pigments, 98(3), 601-608. doi: 10.1016/j.dyepig.2013.04.011
Santana, A. A., Cano-Higuita, D. M., De Oliveira, R. A. y Telis, V. R. N. (2016). Influence of different combinations of wall materials on the microencapsulation of jussara pulp (Euterpe edulis) by spray drying. Food Chemistry, 212, 1-9. doi: 10.1016/j.foodchem.2016.05.148
Santos, D., Maurício, A. C., Sencadas, V., Santos, J. D., Fernandes, M. H. y Gomes, P. S. (2018). Spray drying: an overview. En R. Pignatello y T. Musumeci (Eds.), Biomaterials – Physics and Chemistry – New Edition. InTech. doi: 10.5772/intechopen.72247
Sarabandi, K., Jafari, S. M., Mahoonak, A. S. y Mohammadi, A. (2019). Application of gum Arabic and maltodextrin for encapsulation of eggplant peel extract as a natural antioxidant and color source. International Journal of Biological Macromolecules, 140, 59-68. doi: 10.1016/j.ijbiomac.2019.08.133
Scotter, M. J. (2011). Emerging and persistent issues with artificial food colours: natural colour additives as alternatives to synthetic colours in food and drink. Quality Assurance and Safety of Crops & Foods, 3(1), 28-39. doi: 10.1111/j.1757-837X.2010.00087.x
Shaaruddin, S., Mahmood, Z., Ismail, H., Mohd Ghazali, H., Hamzah, Mohd. Y. y Muhammad, K. (2019). Stability of β-carotene in carrot powder and sugar confection as affected by resistant maltodextrin and octenyl succinate anhydride (osa) starches. Journal of Food Science and Technology, 56(7), 3461-3470. doi: 10.1007/s13197-019-03832-4
Shaddel, R., Hesari, J., Azadmard-Damirchi, S., Hamishehkar, H., Fathi-Achachlouei, B. y Huang, Q. (2018). Use of gelatin and gum Arabic for encapsulation of black raspberry anthocyanins by complex coacervation. International
Journal of Biological Macromolecules, 107, 1800-1810. doi: 10.1016/j.ijbiomac.2017.10.044
Sharma, G., Sharma, S., Kumar, A., Al-Muhtaseb, A. H., Naushad, Mu., Ghfar, A. A., Mola, G. T. y Stadler, F. J. (2018). Guar gum and its composites as potential materials for diverse applications: a review. Carbohydrate Polymers, 199, 534545. doi: 10.1016/j.carbpol.2018.07.053
Spence, C. (2015). Visual contributions to taste and flavour perception. En M. J. Scotter, Colour Additives for Foods and Beverages (pp. 189-210). doi: 10.1016/B978-1-78242-011-8.00007-6
Spence, C., Levitan, C. A., Shankar, M. U. y Zampini, M. (2010). Does food color influence taste and flavor perception in humans? Chemosensory Perception, 3(1), 68-84. doi: 10.1007/s12078-010-9067-z
Steiner, B. M., McClements, D. J. y Davidov-Pardo, G. (2018). Encapsulation systems for lutein: A review. Trends in Food Science & Technology, 82, 71-81. doi: 10.1016/j.tifs.2018.10.003
Stoll, L., Costa, T. M. H., Jablonski, A., Flôres, S. H. y De Oliveira Rios, A. (2016). Microencapsulation of Anthocyanins with Different Wall Materials and Its Application in Active Biodegradable Films. Food and Bioprocess Technology, 9(1), 172-181. doi: 10.1007/s11947-015-1610-0
Sukkwai, S., Kijroongrojana, K., Chonpracha, P., Pujols, K. D., Alonso-Marenco, J. R., Ardoin, R. y Prinyawiwatkul, W. (2018). Effects of colorant concentration and ‘natural colour’ or ‘sodium content’ claim on saltiness perception, consumer liking and emotion, and purchase intent of dipping sauces. International Journal of Food Science & Technology, 53(5), 12461254. doi: 10.1111/ijfs.13704
Taheri, A. y Jafari, S. M. (2019). Gum-based nanocarriers for the protection and delivery of food bioactive compounds. Advances in Colloid and Interface Science, 269, 277-295. doi: 10.1016/j.cis.2019.04.009
Tatar Turan, F., Cengiz, A. y Kahyaoglu, T. (2015). Evaluation of ultrasonic nozzle with spray-drying as a novel method for the microencapsulation of blueberry’s bioactive compounds. Innovative Food Science & Emerging Technologies, 32, 136-145. doi: 10.1016/j.ifset.2015.09.011
Thakur, D., Jain, A., Ghoshal, G., Shivhare, U. S. y Katare, O. P. (2017). Microencapsulation of β-carotene based on casein/guar gum blend using zeta potential-yield stress phenomenon: an approach to enhance photo-stability and retention of functionality. AAPS PharmSciTech, 18(5), 1447-1459. doi: 10.1208/s12249-017-0806-1
Tupuna, D. S., Paese, K., Guterres, S. S., Jablonski, A., Flôres, S. H. y De Oliveira Rios, A. (2018). Encapsulation efficiency and thermal stability of norbixin microencapsulated by spray-drying using different combinations of wall materials. Industrial Crops and Products, 111, 846-855. doi: 10.1016/j.indcrop.2017.12.001
Ursache, F. M., Andronoiu, D. G., Ghinea, I. O., Barbu, V., Ioniţă, E., Cotârleţ, M.,
Dumitraşcu, L., Botez E., Râpeanu, G. y Stănciuc, N. (2018). Valorizations of carotenoids from sea buckthorn extract by microencapsulation and formulation of value-added food products. Journal of Food Engineering, 219, 16-24. doi: 10.1016/j.jfoodeng.2017.09.015
Vargas-Campos, L., Valle-Guadarrama, S., Martínez-Bustos, F., Salinas-Moreno, Y., Lobato-Calleros, C. y Calvo-López, A. D. (2018). Encapsulation and pigmenting potential of betalains of pitaya (Stenocereus pruinosus) fruit. Journal of Food Science and Technology, 55(7), 2436-2445. doi: 10.1007/s13197-018-3161-7
Venil, C. K., Khasim, A. R., Aruldass, C. A. y Ahmad, W. A. (2016). Microencapsulation of flexirubin-type pigment by spray drying: Characterization and antioxidant activity. International Biodeterioration & Biodegradation, 113, 350-356. doi: 10.1016/j.ibiod.2016.01.014
Verma, A. y Singh, S. V. (2015). Spray drying of fruit and vegetable juices – a review. Critical Reviews in Food Science and Nutrition, 55(5), 701-719. doi: 10.1080/10408398.2012.672939
Vernon-Carter, E. J., Beristain, C. I. y Pedroza-Islas, R. (2000). Mesquite gum (Prosopis gum). En G. Doxastakis y V. Kiosseoglou (Eds.), Developments in Food Science Vol. 41, (pp. 217-238). doi: 10.1016/S0167-4501(00)80011-4
Villacrez, J. L., Carriazo, J. G. y Osorio, C. (2014). Microencapsulation of Andes berry (Rubus glaucus Benth.) Aqueous extract by spray drying. Food and Bioprocess Technology, 7(5), 1445-1456. doi: 10.1007/s11947-013-1172-y
Wadhera, D. y Capaldi-Phillips, E. D. (2014). A review of visual cues associated with food on food acceptance and consumption. Eating Behaviors, 15(1), 132-143. doi: 10.1016/j.eatbeh.2013.11.003
Xu, L., Cheng, J.-R., Liu, X.-M. y Zhu, M.-J. (2019). Effect of microencapsulated process on stability of mulberry polyphenol and oxidation property of dried minced pork slices during heat processing and storage. LWT, 100, 62-68. doi: 10.1016/j. lwt.2018.10.025
Ye, Q., Georges, N. y Selomulya, C. (2018). Microencapsulation of active ingredients in functional foods: From research stage to commercial food products. Trends in Food Science & Technology, 78, 167-179. doi: 10.1016/j.tifs.2018.05.025
Yu, Y. y Lv, Y. (2019). Degradation kinetic of anthocyanins from rose (Rosa rugosa) as prepared by microencapsulation in freeze-drying and spraydrying. International Journal of Food Properties, 22(1), 2009-2021. doi: 10.1080/10942912.2019.1701011
Zhang, J., Zhang, C., Chen, X. y Quek, S. Y. (2020). Effect of spray drying on phenolic compounds of cranberry juice and their stability during storage. Journal of Food Engineering, 269, 109744. doi: 10.1016/j.jfoodeng.2019.109744
Zhao, C., Zhao, Q., Zhang, Y. y Zhou, M. (2015). The effect of gum Arabic on the dispersion of cement pastes. En F. Dong (Ed.), Proceedings of the 11th International Congress for Applied Mineralogy (ICAM) (pp. 483-494). Springer. doi: 10.1007/978-3-319-13948-7_47
Modificación de la transferencia de masa durante la deshidratación osmótica de frutas y hortalizas: factores de proceso y métodos no térmicos
J. E. González-Pérez* y A. López-Malo
*Programa de Doctorado en Ciencia de Alimentos
Correo electrónico: julio.gonzalezpz@udlap.mx • aurelio.lopezm@udlap.mx
RESUMEN
La osmodeshidratación de frutas y hortalizas es un proceso lento debido a la resistencia en la transferencia de masa (tm). Dicha resistencia se puede modificar variando la solución osmótica, las condiciones del proceso o implementando tratamientos no térmicos (tnt). Los tnt permiten modificar la permeabilidad de la pared celular, bien por el incremento de la superficie de contacto con la disminución de la presión de vacío (pulsos de vacío), por el aumento de la presión del sistema (altas presiones hidrostáticas), o bien por la formación de poros en la membrana celular (campo eléctrico pulsado) o microcanales (ultrasonido y osmo-sonicación). Las características de la tm ocasionadas por cambios de las condiciones experimentales se pueden describir con modelos matemáticos, como la segunda ley de Fick. El objetivo de esta revisión es analizar distintos factores que modifican la tm durante la osmodeshidratación, así como la aplicación de tnt para modificarla. Además, se analizará el estudio de modelos que describen estos procesos.
Palabras clave: deshidratación osmótica, permeabilidad de la membrana celular, métodos no térmicos, transferencia de masa.
ABSTRACT
Osmodehydration of fruits and vegetables is a slow process due to resistance in mass transfer (mt). This resistance can be modified by varying the osmotic solution, the process conditions or by implementing non-thermal treatments (ntt). ntt allow modifying the permeability of the cell wall by increasing the contact surface area with the decrease in atmospheric pressure (vacuum pulses), by increasing the system pressure (high hydrostatic pressures), or by the formation of pores in the cell membrane (pulsed electric field) or microchannels (ultrasound and osmo-sonication). Mathematical models, such as Fick’s second law, can be used to describe the characteristics of mt caused by changes in experimental conditions. The aim of this review is to analyze the different factors that modify mt during osmo-dehydration, as well as the application of ntt to modify it. Furthermore, it will analyze the study of models that describe these processes.
Keywords: osmotic dehydration, cell wall permeability, non-thermal treatments, mass transfer.
INTRODUCCIÓN
Las frutas y hortalizas contribuyen al adecuado balance de la dieta humana al ser una fuente crucial de compuestos nutraceúticos. Estos compuestos pueden ser vitaminas, minerales, fibra, colorantes naturales, o antioxidantes, los cuales pueden ser benéficos para el cuerpo humano (Ciurzyńska et al., 2016; Omolola et al., 2017; Ramya y Jain, 2017). No obstante, las frutas y hortalizas tienen un elevado contenido de humedad que propicia cambios bioquímicos y microbiológicos que disminuyen su vida de anaquel (Rahman, 2017; Chitrakar et al., 2019). La deshidratación permite obtener alimentos de humedad baja (menor a 20 %, p/p) o humedad intermedia (2050 %, p/p), que pueden almacenarse por largos periodos (Barbosa de Lima et al., 2016; Qiu et al., 2019). Los principales métodos de deshidratación involucran el uso de temperatura, lo cual puede generar pérdida de nutrientes termosensibles, además de modificaciones de características sensoriales (provocadas por reacciones químicas o enzimáticas), así como cambios morfométricos, entre otros parámetros de calidad (Sabarez, 2018; Qiu et al., 2019).
La deshidratación osmótica es un método que permite obtener alimentos de humedad intermedia. Además, ayuda a inhibir el oscurecimiento enzimático, mejorando la apariencia y el sabor de frutas y hortalizas gracias a la incorporación de solutos presentes en una solución hipertónica y a la eliminación simultánea de agua (Omolola et al., 2017; Ramya y Jain, 2017). Sin embargo, durante este proceso la transferencia de masa es lenta (Kuo et al., 2018) y puede haber pérdida de vitaminas, minerales o algunos ácidos orgánicos a través de lixiviación de sólidos (Yadav y Singh, 2014). Para acelerar los mecanismos de transferencia de masa, se han estudiado diferentes parámetros que podrían estar involucrados en la velocidad del proceso como: el agente osmótico (composición y concentración), la matriz alimenticia (modificaciones físicas o químicas) o las condiciones de proceso (tiempo, agitación o temperatura) (Monnerat et al., 2010; Pacheco-Angulo et al., 2016; Fernandes y Rodrigues, 2017; Cichowska et al., 2019;
González-Pérez et al., 2019; Nowacka, Laghi et al., 2019). En la industria alimentaria, el principal parámetro utilizado para reducir el tiempo de operación durante el proceso de deshidratación osmótica es la temperatura. El aumento de la temperatura durante la deshidratación osmótica de frutas y hortalizas incrementa la permeabilidad de su membrana celular y acelera la transferencia de masa (Assis et al., 2016; Akharume et al., 2019). Sin embargo, temperaturas elevadas pueden afectar negativamente y disminuir la calidad del producto (color, textura, sabor, entre otros) (Barbosa de Lima et al., 2016; Sabarez, 2018). Algunas de las alternativas son el uso de métodos no térmicos, como las altas presiones hidrostáticas, los pulsos de vacío, los pulsos eléctricos, el ultrasonido y la osmo-sonicación (Martín-Belloso y Morales-de la Peña, 2018; Nowacka et al., 2018; Dash et al., 2019; de Mello et al., 2019; Osae et al., 2019).
La osmodeshidratación de frutas y hortalizas asistida por métodos no térmicos no afecta la calidad del producto final y permite alterar la permeabilidad de su membrana celular. Esta alteración ayuda a reducir los tiempos de proceso gracias a que incrementa la tasa de transferencia de masa (Dermesonlouoglou et al., 2016; Onwude et al., 2017; Deng et al., 2019).
El objetivo de esta revisión es abordar estudios recientes sobre la modificación de la transferencia de masa durante la deshidratación osmótica de frutas y hortalizas, considerando algunos parámetros de proceso y métodos no térmicos analizados a través de modelos y cinéticas de proceso.
REVISIÓN BIBLIOGRÁFICA
1. Mecanismos de deshidratación osmótica
La deshidratación osmótica es un proceso de deshidratación parcial de alimentos mediante la transferencia de masa por contacto sólido-líquido; consiste en la inmersión de un material alimenticio en una solución hipertónica (Pacheco- Angulo et al., 2016; Muñiz-Becerá et al., 2017). En la figura 1 se presenta esquemáticamente el proceso de deshidratación osmó-
Modificación de la transferencia de masa durante la deshidratación osmótica de frutas y hortalizas: factores de proceso y métodos no térmicos
tica de frutas y hortalizas. Este proceso ocurre debido a que la concentración de solutos presentes en la solución osmótica (agente osmótico) es mayor a la de la matriz alimenticia. El agua de la matriz alimenticia (presente en el protoplasto de sus células) pasa a la solución hipertónica a través de la membrana celular (plasmalema). El plasmalema se comporta como una membrana semipermeable, ya que, además de la pérdida de agua, permite la ganancia de algunos solutos presentes en la solución osmótica (sales, azúcares, ácidos orgánicos, minerales, colorantes, entre otros). Después de atravesar el plasmalema, estos solutos ocupan el volumen entre la pared celular y el plasmalema (Ahmed et al., 2016; Ciurzyńska et al., 2016; Dash et al., 2019). Durante este proceso, los flujos simultáneos de solutos y agua se extienden desde la superficie del producto hasta el centro del material gracias a la diferencia de presión osmótica entre la matriz alimenticia y la solución osmótica. El
proceso finaliza cuando se alcanza un estado de equilibrio osmótico, es decir, cuando la diferencia entre las presiones osmóticas es casi nula (Ahmed et al., 2016).
2. Factores que afectan el proceso de deshidratación osmótica
La velocidad de transferencia de masa durante la deshidratación osmótica de frutas y hortalizas depende de muchos factores, entre ellos la naturaleza de la matriz alimenticia, la composición del agente osmótico (tablas I y II) y las condiciones de proceso, como temperatura, velocidad de agitación o tiempo de inmersión (tabla II) (Pacheco-Angulo et al., 2016; Liu y Peng, 2017; Shete et al., 2018). La selección de las condiciones óptimas de cada factor de proceso depende de las características deseadas en el producto osmodeshidratado (Ciurzyńska et al., 2016).
Transferencia de masa durante el proceso de deshidratación osmótica de frutas u hortalizas. Adaptada de Mavroudis et al. (2012).
Figura 1.
I.
Transferencia de masa durante la deshidratación osmótica de frutas y hortalizas con diferente porosidad
Matriz a Agente osmótico b
Fruta u hortaliza Porosidad
NaCl c Sacarosa d Jugo concentrado de chokeberry d
Provence
a Rebanadas cilíndricas (diámetro = 18 mm, espesor = 3.35 mm), a w = 0.9830 - 0.9940; b 45 °C, 3 g agente osmótico / g producto durante 90 min; c 0.05 g NaCl / g solución; aw, NaCl = 0.9851; d 40 °Brix; a w, sacarosa = 0.9808; aw, jugo = 0.9449; e GS: ganancia de solutos (g soluto / g producto fresco); f PA: pérdida de agua (g agua / g producto fresco). Adaptada de Lech et al. (2018).
Factores que afectan al proceso de deshidratación osmótica de frutas y hortalizas Tabla II.
Agente osmótico
0.02 - 0.2 g NaCl / g solución
NaCl
0.05 - 0.15 g NaCl / g solución
Condiciones de operación
Matriz
Observaciones Referencias Tipo Concentración
Soluciones con un solo componente
40 °C, 4 - 20 ml solución / g producto, 1,440 min y 190 rpm
40 - 60 °C y 150 min
Zanahoria
Ñame (Amorphophallus spp.)
La disminución de la relación de agente osmótico y matriz alimenticia condujo a una reducción de la pérdida de agua y de la ganancia de solutos (en el equilibrio).
La concentración de la solución y la temperatura del proceso modifican el transporte de masa.
Pacheco-Angulo et al. (2016)
Sangeeta y Hathan (2016)
Tabla
Factores que afectan al proceso de deshidratación osmótica de frutas y hortalizas (continuación)
Agente osmótico
Tipo Concentración
0.05 - 0.25 g NaCl / mL solución
NaCl
0.10 y 0.25 g NaCl / g solución
Condiciones de operación
30 - 70 °C, 1 ml solución / g producto, 150 min
40 - 80 °C, 15 g producto / g solución, 180 min, 120 rpm
30 - 50 °C, 20 g solución / g producto, 240 min, 120 rpm
30 - 50 °Brix
Sacarosa
35 - 65 °Brix
30 - 50 °C, 5 - 15 g solución / g producto, 30 - 180 min
40 °C, 2 g solución / g producto, 360 min, con agitación
40 - 70 °Brix
Jarabe de maíz (jm) 0.44 - 0.56 g jm / g solución
40 - 70 °C, 20 g solución / g producto, 1,800 rpm
Matriz
Calabaza (Cucurbita moschata)
Champiñón blanco (Agaricus bisporus)
Litchi (Litchi chinensis Sonn)
Amla, grosella espinosa india o amalak (Emblica officinalis L.)
Papaya var. Khaek dam (Carica papaya L.)
Uchuva (Physalis peruviana L.)
Observaciones Referencias
Los principales factores que modificaron el transporte de masa durante este proceso fueron la concentración y temperatura de la solución osmótica y el tiempo de inmersión.
La pérdida de agua y ganancia de sólidos influyen en la disminución del volumen del producto.
La concentración de la solución y la temperatura influyen en la velocidad de transferencia de masa.
Las relaciones de agente osmótico y matriz alimenticia de este experimento no tienen influencia significativa en los parámetros de transferencia de masa.
La reducción de actividad de agua se incrementó en función del aumento de sacarosa.
En temperaturas mayores a 55 °C se incrementa la reducción de carotenoides totales (aproximadamente 50 %).
Soluciones con más de un componente
34 - 46 °C, 10 g solución / g producto, 120 - 210 min
Soluciones de NaCl y sacarosa
A) 5 % NaCl y 50 % sacarosa / mL solución
B) 15 % NaCl y 50 % sacarosa / mL solución
A) 10 % NaCl
Soluciones de NaCl
(pm = 58.44 g / mol), KCl (pm = 74.55g / mol) y CaCl2 (pm = 110.93g / mol)
B) 7.5 % NaCl y 25 % KCl
C) 7.0 % NaCl, 2.5 % KCl y 0.5 % CaCl2
D) 5% NaCl, 4% KCl y 1 % CaCl2
5 - 50 °C, 20 g solución / g producto, 60 - 180 min
Papaya (Carica papaya L.)
Calabazas (Cucurbita spp.)
La ganancia de solutos (de la matriz osmodeshidratada) obtenidas en soluciones de jm son inferiores a las de soluciones de sacarosa debido a su alta viscosidad y contenido de polisacáridos.
La velocidad de transferencia de masa se ve influenciada en mayor medida por la concentración de NaCl.
Rahman et al (2015)
González-Pérez et al. (2019)
Bera y Roy (2015)
Tiroutchelvame et al. (2015)
Rongtong et al. (2018)
Luchese et al (2015)
El-Aouar et al. (2006)
Mokhtarian et al. (2014)
30 °C, 10 g solución / g producto y 120 min
Berenjena (Solanum melongena L.)
Los experimentos con 10 % NaCl (a w = 0.9450) alcanzaron una mayor pérdida de agua (7 - 16 %) respecto a las que tienen sustitutos de NaCl. Las muestras con CaCl2, presentaron una ganancia de solutos más alta (21 %) respecto a las que no tienen CaCl2.
De Jesus Junqueira et al. (2017)
Tabla II.
Factores que afectan al proceso de deshidratación osmótica de frutas y hortalizas (continuación)
Agente osmótico
Tipo Concentración
Soluciones de glicerol
(pm = 92.09 g / mol), sorbitol (pm = 182.17 g / mol) y lactato de calcio en soluciones de 30 - 70 % de sorbitol o glicerol
Soluciones de sacarosa (pm = 342.30 g / mol), inulina
(pm = 6,178.02 g / mol), sacarosa-inulina, sacarosa-jugo concentrado de chokeberry (jcc) (1 : 1) e inulina-jcc (4 : 1)
Soluciones de glicerol
(pm = 92.09 g / mol), eritritol (pm = 122.12 Da), glicósidos de esteviol (pm = 318.45 g / mol) y Citrox
A) 30, 50 y 70 % de glicerol o sorbitol
B) 30, 50 y 70 % de glicerol o sorbitol adicionado con 20 g lactato de calcio / L solución
50 °Brix
Condiciones de operación Matriz
30 °C, 20 g solución / g producto, 720 min y 1,000 rpm
30 y 50 °C, 2 g solución / g producto, 360 min, con agitación
Yacón (Smallanthus sonchifolius)
Fresa var. Honeoye
40 - 60 % glicerol, 12.5 % eritritol, 1.25 % glucósidos de esteviol y 0.2 % Citrox
Soluciones de sacarosa, miel y miel-sacarosa (1 : 1) A) 60 - 80 °Brix B) 74 °Brix
25 – 45 °C, 5 g solución / g producto, 240 min Durazno
Manzana (jcm) 40 °Brix
30 y 50 °C, 7 g solución / g producto, 210 min
Piña (Ananas comosus L.)
Jugos concentrados
40 °C, 2 g solución / g producto, 120 min
Cereza agria var. Turgieniewka (Prunus cerasus L.)
Observaciones Referencias
A) El sorbitol tuvo una menor permeabilidad en la matriz alimenticia debido a su peso molecular. El glicerol se usa para mejorar textura (plastificante); el sorbitol se usa como edulcorante.
B) El lactato de calcio ayudó a prevenir el colapso celular.
La sustitución parcial de sacarosa (con jcc o inulina) permite obtener productos con menor humedad, mayor valor nutricional (menos azúcar simple) y enriquecidos con compuestos bioactivos. Debido a su peso molecular, se obtiene una menor transferencia de masa con inulina.
El glicerol permitió reducir la aw; el eritrirol y los glicósidos de esteviol sirvieron como endulzante, y el Citrox como antimicrobiano. La velocidad de transferencia de masa se vio favorecida por el incremento de la temperatura y la concentración de glicerol.
Las soluciones de sacarosa y miel-sacarosa registraron una mayor pérdida de agua que los productos tratados con soluciones de miel. Las muestras osmodeshidratadas con la solución miel-sacarosa tuvieron una mejor aceptación sensorial.
El producto osmodeshidratado incrementó un 16 % el contenido de polifenoles y un 35 % la actividad antioxidante respecto al producto fresco.
Brochier et al. (2015)
Kowalska et al. (2017)
Dermesonlouoglou y Giannakourou (2019)
Sethi y Kaur (2019)
Nowicka et al. (2015)
jcc (Aronia melanocarpa) 40 °Brix
50 °C, 3 ml solución / g producto, 120 min
Remolacha var. Alto F1
La aplicación de jcc durante la etapa de deshidratación osmótica podría mejorar la funcionalidad y el color de los productos secos, al transferir compuestos bioactivos y organolépticos activos a la matriz alimenticia.
Lech et al. (2015)
Tabla II.
Modificación de la transferencia de masa durante la deshidratación osmótica de frutas y hortalizas: factores de proceso y métodos no térmicos
II.
Factores que afectan al proceso de deshidratación osmótica de frutas y hortalizas (continuación)
Agente osmótico
Tipo Concentración
Condiciones de operación
45 °C, 3 ml / g producto, 120 min
40 °Brix
45 °C, 2 ml solución / g de producto, 90 min
jcc (Aronia melanocarpa)
60 °Brix
65 °Brix
40 y 60 °C, 4 g solución / g producto, 120 min, 60 rpm
45 °C, 4 g solución / g producto, 1,440 min, 60 rpm
Matriz
Chokeberry negro (Aronia melanocarpa)
Arilos de granada var. Mollar de Elche (Punica granatum L.)
Manzana var. Braeburn
Manzana var. Gala
Observaciones
Los productos secos pretratados por osmodeshidratación mostraron un incremento de porosidad y una reducción de amargura en comparación con las muestras sin tratamiento.
El uso de jcc durante la deshidratación osmótica mejora la aceptación sensorial (parámetros de apariencia y homogeneidad del color) en comparación con las muestras sin tratamiento.
El color de las muestras osmodeshidratadas con jcc es más estable (p < 0.05) que muestras osmodeshidratadas con sacarosa (a las mismas condiciones) durante 12 meses de almacenamiento.
El uso de jcc durante la deshidratación osmótica de manzana mejora la aceptación sensorial (parámetros de color y sabor) en comparación con el producto osmodeshidratado con soluciones de sacarosa a las mismas condiciones.
Referencias
Calín-Sánchez et al. (2015)
Cano-Lamadrid et al. (2017)
Cichowska y Kowalska (2018)
Samborska et al. (2019)
Granada var. Wonderful (gw); gw-jcc (1 : 1, v / v); gw-jcm (1 : 1, v / v); jcm-jcc (1 : 1, v / v); jcm-jcc (3 : 1, v / v)
Grosella negra (jcgn); cereza ácida (jcca); frambuesa (jcf); membrillo (jcmb); flor de membrillo (jcfmb); jcm; jcc
40 °Brix
45 °C, 2 mL solución / g producto, 90 min
Arilos de granada var. Mollar de Elche (Punica granatum L.)
Las soluciones permitieron obtener arilos osmodeshidratados con el mismo contenido de humedad. El uso de gw y gw-jcc mejoró la ganancia de solutos, incrementando el contenido de antocianinas totales.
Cano-Lamadrid et al. (2017)
40 °Brix
40 °C, 2 ml / g de producto, 90 min
Cereza (Prunus cerasus L.)
Las soluciones de jcca y jccc enriquecieron 6.4 - 22.4 % de polifenoles; la de jcc aumentó hasta 1.5 la cantidad de procianidinas poliméricas y la de jcgn redujo el 10.14 % de antocianinas de la matriz alimenticia.
Nowicka et al. (2015)
Tabla
2.1. Factores relacionados con la matriz alimenticia
Durante la osmodeshidratación de frutas y hortalizas, la composición química y algunas propiedades físicas de la matriz alimenticia influyen en las cinéticas de transferencia de masa. En el caso de la composición química de la matriz alimenticia, algunos estudios indican que la variedad y el grado de madurez pueden afectar la velocidad del proceso debido al tipo y concentración de los compuestos presentes en el producto (Ahmed et al., 2016; Sulistyawati et al., 2018). Mavroudis, Dejmek y Sjöholm (2004) compararon la ganancia de agua y pérdida de solutos durante la osmodeshidratación (50 °Brix de sacarosa a 5-40 °C) de diferentes variedades de manzana —específicamente Kim, Mutsu y Jonagold. Los autores encontraron que la transferencia de masa durante el proceso no tuvo el mismo comportamiento para todas estas variedades de manzana. Las variedades Kim y Jonagold registraron una mayor pérdida de agua (0.20-0.45 g agua/g producto) en relación con la ganancia de solutos (0.10-0.12 g soluto/g producto). En el caso de la variedad Mutsu, el proceso redujo muy poco su humedad, pero logró una mayor ganancia de sólidos, lo que permitió tener un producto adecuado para confitería. Por su parte, Sulistyawati et al. (2018), osmodeshidrataron (60 °Brix de sacarosa a 60 °C) mangos de la variedad Keny con diferente grado de madurez (inmaduros, 13.2 °Brix y maduros, 15.7 °Brix). Encontraron que el mango inmaduro mostró una ganancia de sólidos 2-5 veces mayor que los maduros.
Las cinéticas de proceso también pueden verse afectadas por las propiedades físicas de la matriz alimenticia, como la piel, porosidad, tamaño, forma, entre otros (Chandra y Kumari, 2015; Deng et al., 2019). Se ha observado que la piel de frutas y hortalizas ejerce una resistencia a la transferencia de masa (Ketata et al., 2013; Alfaro et al., 2018). A pesar de que esta resistencia se puede reducir removiendo la piel o cortando el producto (Gómez-Ramírez et al., 2013), la calidad (textura, color característico, entre otros atributos) de algunos productos puede modificarse al remover la piel. Por ello, la matriz alimenticia se somete a tratamientos que permiten incrementar la permeabilidad de la piel (Allahdad et al., 2019). Alfaro et al. (2018), modificaron la permeabilidad de la piel de Vaccinium angustifolium Ait., sumergiéndolo en nitrógeno líquido (-196 °C, durante 10 segundos). Este tratamiento permitió que durante el proceso de deshidratación osmótica (60 °Brix de sacarosa a 40 °C por 8 horas) se alcanzara una reducción de humedad de un 20 % y un incremento de solutos del 23 %, con relación al mismo producto sin pretratamiento.
En la tabla I, se muestra cómo la porosidad de la matriz alimenticia afecta la transferencia de masa durante la deshidratación osmótica en diferentes agentes osmóticos. Lech, Michalska, Wojdyło, Nowicka, y Figiel (2018) encontraron que la porosidad de la matriz alimenticia podría tener un impacto en la deshidratación osmótica. Entre más pequeña es la porosidad, más espacio disponible tiene la matriz alimenticia para la transferencia de masa, lo que implica una mayor pérdida de agua y ganancia de solutos (como el rábano var. Omny y la zanahoria var. Nerac), en comparación con las que tienen una mayor porosidad (manzana var. Champion).
Asimismo, Ruiz-López, Huerta-Mora, Vivar-Vera, MartínezSánchez y Herman-Lara (2010) compararon las características de transferencia de masa durante la deshidratación osmótica (0.10 y 0.25 g NaCl/g solución, 4 g solución/g producto a 25 °C durante 3 horas) de prismas de chayote con diferentes dimensiones (1 × 1 × 2 y 1 × 1 × 4 cm). Los autores encontraron que las muestras con dimensiones más pequeñas alcanzaban rápidamente el estado de equilibrio. Finalmente, se concluyó que el tiempo de proceso fue proporcional a la longitud característica de la matriz alimenticia. González-Pérez et al. (2019) analizaron los cambios de la velocidad de transferencia de masa ocasionados por el encogimiento y deformación de la matriz alimenticia durante el proceso de osmodeshidratación (0.10 y 0.25 g NaCl/g solución, 15 g solución/g producto, 40, 60 y 80 °C) de píleos de champiñón blanco. Los autores hallaron que, si se considera que el volumen del producto permanece constante durante el proceso de osmodeshidratación, se genera una sobreestimación del 39113 % en los parámetros correspondientes a la pérdida de agua y del 24-66 % para los relacionados con la ganancia de solutos.
2.2. Agente osmótico
La naturaleza del agente osmótico (solución osmótica) es un factor importante en el desarrollo de frutas y hortalizas osmodeshidratadas (Akharume et al., 2019). El tipo de agente osmótico y su concentración influyen en la presión osmótica (tablas I y II). Esta presión es la única fuerza impulsora para la transferencia de masa durante la osmodeshidratación de alimentos, por lo que la rapidez del proceso dependerá, en mayor medida, de las características de este parámetro (Cheng et al., 2014).
2.2.1. Tipos de agente osmótico
Las características del agente osmótico que deben ser consideradas en el proceso de deshidratación osmótica son la actividad de agua, el peso molecular y la solubilidad o el estado iónico de las
especies químicas presentes en la solución (Lech et al., 2017). La actividad de agua (a w) es la propiedad fisicoquímica más importante del agente osmótico durante la deshidratación osmótica de frutas y hortalizas (Lech et al., 2017). Entre más grande es la diferencia de la a w del agente osmótico y la de la matriz alimenticia, mayor es la fuerza impulsora para la transferencia de masa. En la tabla I se presentan algunos ejemplos relacionados con la influencia de la a w en la transferencia de masa de diferentes frutas y hortalizas con a w = 0.9830 - 0.9940. El jugo concentrado de chokeberry (a w = 0.9449) permitió obtener mayores pérdidas de agua y ganancias de solutos, a diferencia de las alcanzadas con la solución de NaCl (a w = 0.9851). Esto se atribuye a que la diferencia entre la a w del jugo concentrado de chokeberry y la a w de la matriz alimenticia fresca es mayor que la de la de soluciones de NaCl. Por otro lado, un agente osmótico con menor peso molecular puede penetrar fácilmente en las células de las frutas y verduras, en comparación con el agente osmótico de mayor peso molecular (Brochier et al., 2015).
El tipo de solución osmótica utilizada depende principalmente de la compatibilidad con la matriz sometida al proceso osmótico. Generalmente, se emplea NaCl para vegetales, carnes rojas, pescado, camarón, entre otros. Mientras que para la osmodeshidratación de frutas y hortalizas se utilizan sacarosa, edulcorantes o concentrados de frutas u hortalizas (Lech et al., 2018). La influencia de varios agentes osmóticos se muestra en la tabla II.
2.2.2. Concentración de la solución osmótica
La concentración de la solución juega un papel importante en la velocidad de transferencia de masa. Algunos estudios indican que un aumento en la concentración de solutos da como resultado mayor pérdida de agua y ganancia de sólidos (Shete et al., 2018). Este comportamiento se ha visto principalmente en soluciones de NaCl y sacarosa (Bera y Roy, 2015; Sangeeta y Hathan, 2016; Rongtong et al., 2018; GonzálezPérez et al., 2019). Para las soluciones osmóticas con más de un componente, la velocidad de transferencia se modifica principalmente por la concentración del compuesto con menor peso molecular, como se indica en algunos estudios de la tabla II (Mokhtarian et al., 2014; De Jesus Junqueira et al., 2017; Dermesonlouoglou y Giannakourou, 2019).
2.3. Condiciones de proceso
La influencia de las condiciones de proceso de deshidratación osmótica ha sido estudiada en los últimos años (Lech et al., 2018). En la literatura encontramos diversos estudios sobre cómo las varia-
ciones en temperatura, la relación de agente osmótico y la matriz alimenticia, el tiempo de inmersión y la agitación del sistema osmótico afectan la transferencia de masa (tabla II).
2.3.1. Temperatura de la solución osmótica
Algunas investigaciones encontraron que el incremento de la temperatura de la solución osmótica favorece la ganancia de solutos, ya que, a medida que la temperatura se eleva, también lo hace la solubilidad de los solutos en el líquido (Salim et al., 2016); lo que modifica la viscosidad del medio osmótico (El-Aouar et al., 2006). Asimismo, el incremento térmico del sistema puede acelerar en mayor porcentaje la pérdida de agua (Sangeeta y Hathan, 2016; Dermesonlouoglou y Giannakourou, 2019). Sin embargo, el proceso no debe exceder los 60 °C, ya que estas temperaturas pueden dañar los tejidos vegetales, favoreciendo al colapso de la matriz alimenticia (Ramya y Jain, 2017), o incrementar la pérdida de compuestos como los carotenoides (Luchese et al., 2015).
2.3.2. Relación del agente osmótico y matriz alimenticia
La relación entre el peso (o volumen) del agente osmótico y el peso de la muestra es de gran importancia durante el tratamiento osmótico de frutas y hortalizas. Puede afectar a la cinética de transferencia de masa, ya que el agua que piede el alimento durante el proceso disminuye la concentración de la solución osmótica (Ahmed et al., 2016). Se recomienda una relación de producto y solución osmótica de al menos 1 : 15 cuando se trabaja con soluciones de NaCl, o de 1 : 2 o 1 : 3 para soluciones de sacarosa. Sin embargo, la elección de esta relación dependerá de la concentración que alcanzará la solución osmótica, considerando la dilución generada por el agua que el producto pierde durante el proceso (Tiroutchelvame et al., 2015; Pacheco-Angulo et al., 2016; Shete et al., 2018).
2.3.3. Tiempo de inmersión
El aumento del tiempo de inmersión provoca una mayor transferencia de masa. Al comienzo del proceso de deshidratación osmótica los fenómenos de transferencia de masa son rápidos, conforme la solución osmótica gana agua, la diferencia entre las presiones se reduce, lo que resulta en una velocidad de transferencia de masa más baja, hasta alcanzar un estado de equilibrio másico (Ahmed et al., 2016). De manera simultánea, el tejido del producto puede sufrir una contracción a lo largo del proceso de deshidratación, reduciendo el espacio para llevar a cabo la transferencia de masa (Ramya y Jain, 2017).
2.3.4. Agitación
El agua eliminada del producto osmodeshidratado puede diluir la solución osmótica a los alrededores del producto osmodeshidratado (Assis et al., 2016). El uso de agitación durante el proceso de deshidratación osmótica homogeneiza el contacto entre el producto y la solución osmótica, disminuyendo el tiempo de transferencia de masa. Por lo general, para soluciones con solutos de bajo peso molecular, como NaCl, se utilizan velocidades de agitación de 120-190 rpm; esta velocidad también se ha usado para soluciones de 30-50 °Brix de sacarosa (Bera y Roy, 2015; Tiroutchelvame et al., 2015). Cuando el agente osmótico es más viscoso (soluciones de sacarosa, sorbitol o glicerol con concentraciones mayores a 60 °Brix) las velocidades de agitación son de 1,000-1,800 rpm (Brochier et al., 2015; Luchese et al., 2015).
3. Métodos no térmicos aplicados en la osmodeshidratación para modificar la transferencia de masa Como se presentó en secciones anteriores, la única fuerza impulsora para la transferencia de masa durante la osmodeshidratación es la presión osmótica. Esta fuerza impulsora requiere mucho tiempo para alcanzar un estado de equilibrio osmótico, a menos que se incremente la permeabilidad de la membrana celular (Deng y Zhao, 2008; Cheng et al., 2014). La membrana celular de frutas y hortalizas ejerce una resistencia a la transferencia de masa. Si se consigue dañar la membrana celular con métodos no térmicos, se puede mejorar la eficiencia del proceso y la calidad de producto (Ahmed et al., 2016). Se han estudiado una serie de métodos no térmicos en combinación con la deshidratación osmótica para mejorar la eficiencia del proceso y la calidad del producto final. Estas técnicas incluyen tratamiento con altas presiones hidrostáticas, con pulsos de vacío, pulsos eléctricos, ultrasonido y osmo-sonicación (Ramya y Jain, 2017; Feng et al., 2019).
3.1. Altas presiones hidrostáticas
El tratamiento de alimentos con altas presiones hidrostáticas (hhp) implica la aplicación de presión hidrostática (501,000 mpa) sobre un producto (Witrowa-Rajchert et al., 2014). La
combinación de hhp con deshidratación osmótica (do-hhp) consiste en colocar la matriz alimenticia en bolsas de polietileno con 3-20 g de solución osmótica/g de producto y sellar al vacío (George et al., 2016; Luo et al., 2018). Posteriormente, esta bolsa se coloca en un sistema cerrado que contiene al medio de transmisión de la presión (agua destilada o 30 % de propilenglicol) (Verma et al., 2014; Dermesonlouoglou et al., 2019), este medio va a ejercer presión por compresión física mediante reducción mecánica de volumen (figura 2). Cuando frutas y hortalizas se tratan previamente con hhp, la membrana celular se permeabiliza, lo que facilita la difusión y proporciona mayores tasas de deshidratación (Deng et al., 2019).
En la tabla III se muestran ejemplos de la aplicación de hhp para asistir la deshidratación osmótica de frutas. Algunos investigadores usaron las hhp para incrementar la pérdida de agua a través de la ruptura de la pared celular (Verma et al., 2014; Sulistyawati et al., 2018). Sin embargo, la modificación de la pared celular no siempre influye en la transferencia de masa (Núñez-Mancilla et al., 2013, 2014; Dermesonlouoglou et al., 2019). Núñez-Mancilla et al. (2013), analizaron tratamientos de Fragaria vesca en soluciones a 40 °Brix de sacarosa con do-hhp, sin encontrar diferencias significativas en los parámetros de transferencia de masa en presiones hidrostáticas mayores a 400 mpa. Dermesonlouoglou et al. (2019) hallaron que las modificaciones a la pared celular de duraznos y albaricoques, debido al tratamiento de hhp (100 mpa) con deshidratación osmótica, afectaban principalmente a la dureza del producto final. Por otro lado, también se observa que la deshidratación osmótica asistida con hhp influye en la composición nutricional y las características de calidad del producto; se ha demostrado la inhibición de microorganismos, lo cual incrementa la vida útil en comparación con las muestras osmodeshidratadas convencionalmente (Dermesonlouoglou et al., 2016, 2017). No obstante, el incremento de hhp puede tener un impacto negativo en el color, pues en el tratamiento de fresa con hhp a 300-500 mpa se generó un mayor oscurecimiento del producto osmodeshidratado, en comparación con las tratadas a 200-300 mpa (Núñez-Mancilla et al., 2013).
Modificación de la transferencia de masa durante la deshidratación osmótica de frutas y hortalizas: factores de proceso y métodos no térmicos
Aplicaciones del proceso de deshidratación osmótica asistido por altas presiones
Matriz Variables de proceso
Durazno (Prunus persica L.) y albaricoque (Prunus armeniaca L.)
Fresa var. Camarosa (Fragaria Vesca)
600 mpa; velocidad de la rampa de 600 mpa / min; temperatura: 25 °C; tiempo de tratamiento: 5 min
100, 200, 300, 400 y 500 mpa; velocidad de rampa de 1,020 mpa / min; temperatura: 15 °C; tiempo de tratamiento: 10 min; tiempo de descompresión: 5 s
100, 200, 300, 400 y 500 mpa; velocidad de rampa de 1,020 mpa / min; temperatura: 15 °C; tiempo de tratamiento: 10 min; tiempo de descompresión: 5 s
Condiciones de deshidratación osmótica
50 % glicerol (p / p), 12.5 % eritritol (p / p), 3.5 % NaCl (p / p), 1.5 %
CaCl2 (p / p), 1.25 % glucósidos de esteviol (p / p) y 0.2 % Citrox (p / p); 5 g solución osmótica / g producto; 45 °C; 45 min
Conclusiones a Referencias
El uso de hhp incrementó la dureza de los duraznos y albaricoques osmodeshidratados.
Dermesonlouoglou et al. (2019)
Jitomate var. Heinz 3402
600 mpa; velocidad de la rampa de 600 mpa / min; temperatura: 25 °C; tiempo de tratamiento: 5 min
40 °Brix de sacarosa, 4 g solución osmótica / g producto
600 mpa; velocidad de la rampa de 600 mpa / min; temperatura: 25 °C; tiempo de tratamiento: 5 min
40 °Brix de sacarosa, 4 g solución osmótica / g producto
50 % glicerol (p / p), 12.5 % eritritol (p / p), 1 % glucósidos de esteviol (p / p), 0.2 % ácido ascórbico (p / p), 1.5 % CaCl2 (p / p), 1 % ácido cítrico (p / p), 0.20 % L-cisteína HCl (p / p) y 0.1 % Citrox (p / p); 5 g de solución osmótica / g producto; 15 - 45 °C, 240 min
50 % glicerol (p / p), 12.5 % eritritol (p / p), 3.5 % NaCl (p / p), 1.5 % CaCl2 (p / p) y 0.2 % Citrox (p / p); 5 g solución osmótica / g producto; 35 °C, 90 min
Los polisacáridos aumentaron con la presión. La alta presión provoca ondulación de la pared celular, lo que a su vez afecta las propiedades de textura debido a la pérdida de turgencia celular, firmeza e integridad de la pared celular.
El contenido fenólico total aumentó con el incremento en la presión. El contenido de vitamina C no mostró cambios con el aumento de la presión. Después de 400 mpa no se observaron incrementos en la transferencia de masa.
El tratamiento no modificó los parámetros de transferencia de masa. La vida útil se prolongó significativamente tanto para do-hhp como para do (hasta 10 y 4 meses a 5 ° C, respectivamente).
Núñez-Mancilla et al. (2014)
La vida útil de las muestras do y do-hhp se estimó en 77 y 181 días, respectivamente, a 5 °C.
Núñez-Mancilla et al. (2013)
Dermesonlouoglou et al. (2016)
Dermesonlouoglou et al. (2017)
Tabla III.
Aplicaciones del proceso de deshidratación osmótica asistido por altas presiones (continuación)
Matriz
Mango (Mangifera indica L.) maduro e inmaduro
Plátano (Musa cavendishii)
Variables de proceso
300 mpa; velocidad de la rampa de 402 mpa / min; temperatura: 50 °C; tiempo de tratamiento: 3 - 5 min; tiempo de descompresión: 10 s
200 mpa; velocidad de la rampa de 200 mpa / min; temperatura: 25 °C; tiempo de tratamiento: 5 min; tiempo de descompresión: 10 s
Condiciones de deshidratación osmótica
60 °Brix de sacarosa, 2 % lactato de calcio (p / p) o 0.0048 % pme b (ml / g), 4 g solución osmótica / g producto, 30 - 240 min
30 - 70 °Brix de sacarosa, 5 g solución osmótica / g producto, 30 - 70 °C, 480 min, 120 rpm
Conclusiones a Referencias
Resultó favorable usar mango inmaduro y aplicar do-hhp sin pme para obtener una ganancia de solutos alta y una pérdida de agua baja (mango confitado).
Se registró una mayor pérdida de agua (22 %) y ganancia de solutos (50.5 %) en comparación con las muestras sin tratar, esto se atribuyó a la ruptura de la pared celular por la presión aplicada.
Sulistyawati et al. (2018)
Verma et al. (2014)
a hhp: Altas presiones hidrostáticas; do: deshidratación osmótica; do-hhp: deshidratación osmótica asistida con altas presiones hidrostáticas; b pme: pectinmetilesterasa.
Representación esquemática de la reducción mecánica de volumen para generar altas presiones.
Tabla III.
Figura 2.
Modificación de
3.2. Pulsos de vacío
La deshidratación osmótica asistida con vacío (do-pv) consiste en la aplicación de presión de vacío a un sistema sólido-líquido, seguido de la restauración de la presión atmosférica. Durante la aplicación del vacío, el gas o líquido contenido en los poros del producto se elimina. Cuando se restablece la presión atmosférica, la solución externa penetra en el espacio poroso del alimento (Sulistyawati et al., 2018). Esto implica un aumento de la superficie de contacto sólido líquido y, por ende, un incremento de la transferencia de masa (Ahmed et al., 2016).
En la tabla IV se muestran algunas aplicaciones del proceso de do-pv. La mayoría de estos estudios se han aplicado a frutas y hortalizas sumergidas en soluciones osmóticas de sacarosa (30-70 °Brix); las presiones de vacío van de 0.0099 a 0.0253 mpa, y los tiempos de aplicación del vacío oscilan en-
de
y hortalizas: factores de proceso y métodos no térmicos
tre los 2 y los 20 minutos. Estos estudios demostraron que el incremento de la presión de vacío durante la do-pv ayuda a obtener productos con menor contenido de agua y menor ganancia de solutos (Şahin y Öztürk, 2018). Asimismo, la velocidad de transferencia de masa se ve afectada por la porosidad de la matriz alimenticia (Mújica-Paz et al., 2003). Además, la do-pv puede mejorar la composición nutricional o la calidad del producto osmodeshidratado, ya que algunos estudios han encontrado que permite impregnar probióticos en manzana mediante el incremento de solutos presentes en soluciones de sacarosa y emulsiones (W1/O/W2) formadas con Lactobacillus rhamnosus LC70/aceite de semillas de uva/proteína de suero de leche (Flores- Andrade et al., 2017). También puede mejorar el color, la textura y el sabor de alimentos secos (Ramya y Jain, 2017; An et al., 2019).
Aplicaciones del proceso de deshidratación osmótica asistido por pulsos de vacío
Variables de proceso
Matriz
Higos (Ficus carica L.)
Presión de vacío Tiempo
0.99 × 10-2 mpa (74 mmHg) 5 min
Manzana var. Ligol
1.31 × 10-2 mpa (98 mmHg), 15 min 15 min
Condiciones de deshidratación osmótica
40 - 60 °Brix de sacarosa, 40 °C, 10 g solución osmótica / g producto, 240 min
50 °Brix de sacarosa, 50 °C, 4 g solución osmótica / g producto, 165 min
2.53 × 10-2 mpa (190 mmHg) 15 min
0.008, 0.0067 y 0.080 mpa (60, 502.5 y 600 mmHg) 2 min
50 °Brix de sacarosa, 50 °C, 4 g solución osmótica / g producto, 180 min
30, 50 y 70 °Brix de sacarosa, 5 g solución osmótica / g producto, 25 °C, 180 min
Conclusiones a Referencias
El aumento de la concentración de sacarosa incrementó la pérdida de agua y la ganancia de solutos.
El uso de deshidratación osmótica asistida por pv acortó el periodo de secado, en tanto favoreció la eliminación de agua y resultó en una menor ganancia de solutos.
La deshidratación osmótica asistida por pv redujo el tiempo de secado, sin embargo, las muestras tratadas con este proceso se encogieron más (3 %) que las muestras sin tratamiento.
A mayor presión de vacío, se registró una menor ganancia de sólidos.
De Mello et al (2019)
Şahin y Öztürk (2016)
Şahin y Öztürk (2018)
Muszyński et al. (2016)
Tabla IV.
Aplicaciones del proceso de deshidratación osmótica asistido por pulsos de vacío (continuación)
Variables de proceso
Matriz
Manzana var. Granny Smith
Jengibre chino (Zingiber officinale Roscoe)
Manzana, mango, melón
Manzana (Malus pumila Mill)
Conclusiones a Referencias Presión de vacío Tiempo
0.0114 mpa (85.4 mmHg) 20 min
Condiciones de deshidratación osmótica
9 g de sacarosa / g de emulsión W1 /O / W2 (emulsión agua en aceite, W1 / O se formó con la 9.98 × 108 ufc de Lactobacillus rhamnosus LC705 / ml y 62 g aceite de semilla de uva; finalmente
30 g de la emulsión W1 / O se dispersó en 70 g de solución de 14 % de concentrado de proteína de suero de leche);
40 - 60 °Brix; 20 g solución osmótica / g producto; 320 min
0.013 mpa (97.5 mmHg) 15 min
0.01350.067 mpa (101.25 -505.5 mmHg) 10 min
0.02 mpa (150 mmHg) 5 y 10 min
0.50 g sacarosa y 0.10 g NaCl / g solución, 4 g solución / g producto, 30 °C, 30 min
40 - 60 °Brix de sacarosa, 10 g solución osmótica / g producto, 25 °C, 20 min
30 - 60 °Brix de sacarosa, 10 - 55 °C, 10 g solución osmótica / g producto, 240 min
Se promovió una mayor incorporación de probióticos cuando la ganancia de sólidos aumenta con el tiempo. Asimismo, la deshidratación osmótica asistida con pv produce una mayor impregnación de Lactobacillus rhamnosus respecto al proceso a presión atmosférica (7.52 × 107 - 1.75 × 108 ufc / g).
La deshidratación osmótica asistida con pulsos de vacío permite reducir más de un 80 % la actividad de polifenol oxidasa e incrementa (80 %) la actividad de peroxidasa.
La velocidad de transferencia de masa es favorecida en frutas con altos niveles de porosidad (manzana).
Las muestras sin presión de vacío tuvieron mayor ganancia de solutos.
An et al. (2019)
Mújica-Paz et al. (2003)
Wang et al. (2018)
a pv: pulsos de vacío; ufc: unidades formadoras de colonia.
3.3. Pulsos eléctricos
El tratamiento por campo eléctrico consiste en la aplicación de corriente eléctrica a través de un material alimenticio (figura 3) (Simpson et al., 2015). Este tratamiento puede causar cambios en la permeabilidad de la membrana celular —conformada por una bicapa de fosfolípidos— de frutas y hortalizas, debido a una electroporación o a electrocompresión (Kusnadi y Sastry, 2012). La electroporación se produce cuando el campo eléctrico externo induce cambios conformacionales y una reorganización de
la bicapa fosfolipídica generando poros (Traffano-Schiffo et al., 2016). Mientras que la electrocompresión se produce debido a la acumulación de cargas (electrolitos) en ambos lados de la membrana celular, las cuales se atraen entre sí hasta generar un poro (Traffano-Schiffo et al., 2017).
El incremento de la permeabilidad de la membrana celular de frutas y hortalizas generado por la aplicación de corriente eléctrica, puede ser causado mediante campos eléctricos pulsados (pef), campos eléctricos pulsados de intensidad mode-
Flores-Andrade et al. (2017)
Tabla IV.
Modificación de la transferencia de masa durante la deshidratación osmótica de frutas y hortalizas: factores de proceso y métodos no térmicos
Representación esquemática del sistema de tratamiento de alimentos sólidos con pulsos eléctricos. Adaptada de Parniakov et al. (2016).
rada (mef) y campos eléctricos pulsado de alta intensidad (help) (Yildiz et al., 2016). El método más estudiado es el de pef (Dermesonlouoglou et al., 2018), en la figura 3 se muestra un esquema representativo (Parniakov et al., 2016; Wu et al., 2020). El método consiste en la aplicación de pef a través de un material situado entre dos electrodos durante períodos de tiempo muy cortos (de microsegundos a milisegundos) (Traffano-Schiffo et al., 2017). Los electrodos pueden estar en contacto directo con el alimento sólido (a través de placas metálicas o de alambres) o con una solución electrolítica (NaCl) colocada en la cámara de tratamiento, esta solución permitirá una mayor superficie de contacto de la corriente eléctrica con el alimento sólido (Tylewicz et al., 2017).
Las modificaciones en la permeabilidad de la membrana celular ocasionadas por pef han sido de gran ayuda para
mejorar procesos de transferencia de masa durante la deshidratación osmótica de alimentos (Dellarosa et al., 2016). En la tabla V se muestran algunos estudios de la aplicación de pef en frutas y hortalizas; estos demuestran que el uso de pef como tratamiento previo a la deshidratación osmótica mejora la velocidad de transferencia de masa. Específicamente, se reportaron mejoras en la pérdida de agua (Traffano-Schiffo et al., 2016; Nowacka, Wiktor et al., 2019) y reducciones en el tiempo de deshidratación osmótica (Yu et al., 2017). En lo que respecta a ganancia de sólidos, algunos estudios encontraron que los pef pueden incrementarla (Amami et al., 2014; Yu et al., 2018) o reducirla (Traffano-Schiffo et al., 2017; Nowacka, Wiktor et al., 2019), dependiendo del tipo de agente osmótico (Tylewicz et al., 2017) o del número de pulsos (Nazari et al., 2019).
Figura 3.
V.
Aplicaciones del proceso de deshidratación osmótica asistido por campo eléctrico pulsado
Matriz Variables de proceso
Intensidad del campo:
5.5 kV / cm
Arándano (Vaccinium oxycoccus)
Blueberries (Vaccinium spp.)
Número de pulsos: 10
Intervalo entre pulsos: 2 segundos
Frecuencia: 0.5 Hz
Intensidad del campo:
3 kV / cm
200 pulsos / segundos
Duración del pulso: 1 μs
Duración: 5 min
Temperatura: 20 °C
Intensidad del campo:
0.1 - 0.4 kV / cm
Duración del pulso: 100 μs
Frecuencia: 100 Hz
Temperatura: 25 °C
Solución: NaCl
Intensidad del campo: 0.1, 0.25 y 0.4 kV / cm
Número de pulsos: 60
Intervalo entre pulsos:
Kiwi var. Hayward, Actinidia
100 μs
Frecuencia: 100 Hz
Tiempo de repetición: 10 ms
Temperatura: 25 °C
Intensidad del campo: 1, 1.5 y 2 kV / cm
Número de pulsos: 8, 16 y 24
Duración del pulso: 0.02, 0.026 y 0.05 s
Temperatura constante
Condiciones de deshidratación osmótica
0.61 y 0.30 °Brix de sacarosa, 0.001 g glicósidos de esteviol / g solución, 4 g solución osmótica / g producto, 40 °C, 4,320 min
0.70 g sacarosa y 0.00025 g de NaCl / g producto, 2 g solución osmótica / g producto, 40 °C, 200 rpm
40 °Brix de sacarosa o trehalosa, 4 g solución osmótica / g producto, 25 °C, 120 min
61.5 °Brix de sacarosa, 4 g solución / g producto, 25 °C, 0 - 120 min
50 °Brix de sacarosa, 20 g solución osmótica / g producto, 40 °C, 140 rpm
Conclusiones a Referencias
El uso de pef promovió la aceleración de la transferencia de masa durante la deshidratación osmótica y redujo el contenido de sacarosa en los productos finales.
El tratamiento con pef redujo el tiempo de deshidratación osmótica de 130 a 48 h e incrementó la pérdida de agua y ganancia de solutos.
Al aplicar una intensidad de campo eléctrico más baja (100 V / cm) se registró un aumento en la pérdida de agua tras una hora de deshidratación osmótica, para las fresas deshidratadas en solución de sacarosa (12 %) y trehalosa (6 %). El tratamiento de pef incrementó la ganancia de solutos para los experimentos con sacarosa, pero con trehalosa se redujeron.
El tratamiento con pef incrementó la pérdida de agua y redujo la ganancia de sacarosa durante la deshidratación osmótica.
La duración del pulso tuvo menor efecto en la pérdida de agua y ganancia de sólidos en comparación con la intensidad de campo y el número de pulsos. La aplicación de 8 - 16 pulsos durante el proceso dopef incrementó los parámetros de transferencia de masa hasta los 24 pulsos, a partir de entonces estos estos se reducen.
Nazari et al. (2019)
Nowacka, Wiktor et al. (2019)
Yu et al. (2018)
Fresa var. Alba
Tylewicz et al. (2017)
deliciosa
TraffanoSchiffo et al. (2017)
Manzana
Tabla
Aplicaciones del proceso de deshidratación osmótica asistido por campo eléctrico pulsado (continuación)
Matriz Variables de proceso
Manzana
Zanahoria
Plátano
Intensidad del campo:
0.90 kV / cm
Número de pulsos: 750
Intervalo entre pulsos:
100 μs
Intensidad del campo:
0.30 kV / cm
Número de pulsos: 500
Intervalo entre pulsos:
100 μs
Intensidad del campo:
0.60 kV / cm
Número de pulsos: 500
Intervalo entre pulsos:
100 μs
Temperatura: 60 y 80 °C
Condiciones de deshidratación osmótica
65 °Brix de sacarosa, 3 g solución osmótica / g producto, 25 °C, 1,500 rpm
a pef: campo eléctrico pulsado, do-pef: deshidratación osmótica asistida por campo eléctrico pulsado.
Conclusiones a Referencias
Durante la deshidratación osmótica, las muestras tratadas con pef mostraron una mayor pérdida de agua (4 - 35 %) y ganancia de solutos (15 - 60 %) que las muestras sin tratar.
et al (2014)
3.4. Ultrasonido y osmo-sonicación
El ultrasonido es un tipo de energía sonora emitida por ondas con frecuencias mayores a 20 kHz. Se clasifican en ondas de alta frecuencia (baja energía e intensidad, frecuencias mayores a 100 kHz) y baja frecuencia (alta energía e intensidad, frecuencias de 20-100 kHz) (Fernandes y Rodrigues, 2017). La cavitación —desarrollo e implosión de burbujas de gas—, que resulta de un ultrasonido con energía de baja frecuencia y alta intensidad, produce una variedad de efectos, entre ellos la regulación del contenido enzimático (activación o inactivación), y la mejora de la tasa de transferencia de masa y energía durante procesos de secado, congelación y deshidratación (Onwude et al., 2017).
Aplicar ultrasonido antes de la deshidratación osmótica de frutas y hortalizas tiene como objetivo generar cambios en la estructura del tejido celular para modificar la transferencia
de masa. El tratamiento consiste en sumergir el alimento sólido en agua destilada (deshidratación osmótica asistida con ultrasonido, do-us), o bien, en una solución osmótica de menor o igual concentración al proceso de deshidratación osmótica (osmo-sonicación) (Bozkir et al., 2019; Osae et al., 2019). Posteriormente, a través de este medio líquido se propagan ondas ultrasónicas (emitidas, ya sea por un transductor de sonda, o en baño) (figura 4). Durante este tratamiento se originan dos fenómenos: el «efecto esponja» (compresión y expansión del material) y la formación de cavitaciones (desarrollo e implosión de burbujas de gas en el medio líquido) (Nowacka et al., 2018). Las burbujas formadas debido a las cavitaciones implosionan (figura 4), generando una presión sobre la superficie de la matriz alimenticia, permitiendo así la remoción de partículas de agua fuertemente ligadas y la creación de microcanales que
Amami
Tabla V.
4.
Representación esquemática del sistema de tratamiento de osmo-sonicación de alimentos y colapso asimétrico de burbujas de vapor causadas por ultrasonido. Adaptada de Miano et al. (2017).
mejoran la transferencia de masa (Miano et al., 2017). Nowacka, Tylewicz, Laghi, Dalla Rosa y Witrowa-Rajchert (2014) demostraron que se requiere de al menos 10 minutos de tratamiento para la formación de microcanales.
En la tabla VI se muestran algunas aplicaciones de la deshidratación osmótica asistida por ultrasonido y osmo-sonicación de frutas y hortalizas. Se ha registrado que el incremento de la frecuencia ultrasónica y el tiempo de tratamiento reducen la actividad de agua, puesto que generan una mayor pérdida (Kek et al., 2013; Amami et al., 2017; Allahdad et al., 2019; Bozkir et al., 2019). Sin embargo, durante las primeras etapas del proceso se observan pérdidas de negativas de agua, es decir, el producto
absorbe agua (Dias da Silva et al., 2016; Allahdad et al., 2019). Asimismo, durante la do-us puede ocurrir ganancia de sólidos negativa debido a la lixiviación de sólidos (Dias da Silva et al., 2016). Por otro lado, el incremento de la frecuencia ultrasónica, la concentración de la solución osmótica (osmo-sonicación) y el tiempo de proceso resultaron en un aumento de sólidos (GarciaNoguera et al., 2014; Nowacka et al., 2014). Además de los beneficios que tiene el uso de ultrasonido al proceso de deshidratación osmóticas, estos tratamientos ayudan a aumentar los compuestos bioactivos, inactivar enzimas, así como mejorar el color y la textura del producto final (Kek et al., 2013; Garcia-Noguera et al., 2014; Osae et al., 2019).
Figura
Modificación de la transferencia de masa durante la deshidratación osmótica de frutas y hortalizas: factores de proceso y métodos no
Matriz
Arilos de granada
Caqui (Diospyros kaki L.)
Aplicaciones del proceso de deshidratación osmótica asistido por osmo-sonicación o ultrasonido
Tipo de tratamiento ultrasónico
Osmosonicación
Osmosonicación
Variables de proceso a
f = 25 y 40 kHz
P = 100 W
T = 30 °C
t = 10 - 80 min
f = 35 kHz
P = 480 W
T = 30 °C
t = 10, 20 y 30 min
Medio: 45 °Brix de sacarosa
Osmosonicación
Cranberry (Vaccinium oxycoccus)
Osmosonicción y ultrasonido
f = 35 y 130 kHz
t = 10 - 80 min
f = 21 kHz
P = 180 W
(I = 3.6 W / g)
t = 30 min
Medio: 4 g agua / g producto
f = 25 kHz
Osmosonicación
P = 60 W
T = 30 °C
t = 10 - 45 min
f = 40 kHz
I = 0.20 W / m2
Osmosonicación
Guayaba
Osmosonicación y ultrasonido
T = 20 - 40 °C
t = 10, 20 y 30 min
Sonicación indirecta:
f = 0 – 25 kHz
P = 1, 1.75 y 2.5 kW
t = 20 - 60 min
Sonicación indirecta:
f = 20 kHz
P = 400 W
A = 15, 25 y 35 %
t = 6 - 20 min
Condiciones de deshidratación osmótica
50 °Brix de sacarosa, 4 g solución osmótica / g producto, 30 °C, 70 rpm
70 °Brix de sacarosa, 4 g solución osmótica / g producto, 30 °C, 100 rpm
40 - 60 °Brix sacarosa y 0 - 0.08 g NaOH / g solución, 10 g de solución osmótica / g, 25 °C, 150 rpm
0.62 g sacarosa / g solución, 0.3 g sacarosa con 0.001 g glicósido de esteviol / g solución y 0.4 g trehalosa / g solución, 4 g solución osmótica / g producto, 40 °C, 4,320 min
25 y 50 °Brix de sacarosa, 4 g solución osmótica / g producto, 30 °C
32.5 y 65 °Brix de sacarosa, 20 - 40°C
Conclusiones
La pérdida de agua aumentó con el tiempo de sonicación. Las muestras a 25 kHz mostraron la mayor cantidad de solutos filtrados; la menor actividad del agua se alcanzó a 40 kHz.
El tratamiento incrementó la pérdida de agua y ganancia de solutos; además esto se ve influenciado por el tiempo de sonicación y la frecuencia ultrasónica.
El incremento de la frecuencia ultrasónica disminuyó la dureza y actividad de agua del producto.
Los parámetros de transferencia de masa durante la deshidratación osmótica fueron influenciados por la aplicación de ultrasonido y osmo-sonicación y por la actividad de agua de las soluciones osmóticas. Laosmo-sonicación permitió obtener mayor pérdida de agua.
El pretratamiento con ultrasonido y la deshidratación osmótica mejoraron el color en las muestras de fresa, especialmente después de una exposición ultrasónica prolongada y la aplicación de altas concentraciones de sacarosa con el pretratamiento.
La pérdida de agua aumentó con a la par del tiempo de sonicación; el corto tiempo de sonicación minimizó las pérdidas de color.
La energía y amplitud del ultrasonido y el tiempo de osmo-sonicación incrementaron la pérdida de agua y ganancia de sólidos.
Referencias
Allahdad et al. (2019)
et al. (2019)
et al. (2012)
et al. (2018)
Noguera et al. (2014)
Amami et al. (2017)
35 y 70 °Brix
La sonicación indirecta mostró mejor aceptación sensorial (color).
Kek et al (2013)
Bozkir
Shamaei
Nowacka
Fresa var. Camarosa
Garcia-
Tabla VI.
Matriz
Melón (Cucumis melo L.) var. cantalupensis Naud
Aplicaciones del proceso de deshidratación osmótica asistido por osmo-sonicación o ultrasonido (continuación)
Tipo de tratamiento ultrasónico
Osmosonicación y ultrasonido
Variables de proceso a
f = 25 kHz
I = 4870 W / m2
T = 30 °C
t = 10, 20 y 30 min
f = 33 kHz
P = 600 W
T = 30 °C
t = 30 min
Para ultrasonido
Rebanadas de jengibre (Zingiber officinale Roscoe)
Zanahoria negra (Daucus carota ssp. sativus)
Osmosonicacción y ultrasonido
Condiciones de deshidratación osmótica
50 °Brix sacarosa, 4 g solución osmótica / g producto, 30 °C
Osmosonicación
Medio: 10 g agua / g producto
Para osmosonicación
Medio: 10 g solución osmótica / g producto
f = 37 kHz
P = 550 W
T = 40 °C
t = 5, 10 y 15 min
Medio: 45 °Brix de sacarosa
20 °Brix de sacarosa, 10 g solución osmótica / g producto, 30 °C
Conclusiones
Al comienzo del proceso, la deshidratación osmótica asistida con ultrasonido presentó pérdidas de agua negativas (el producto absorbió agua) y la ganancia de sólidos incrementó a la par del tiempo de inmersión.
El tratamiento de osmo-sonicación ayuda a inactivar las enzimas polifenol oxidasa y peroxidasa.
Referencias
0.05, 0.1 y 0.15 g NaCl / g producto, 4 g solución osmótica / g producto, 40 °C, 125 rpm
La osmo-sonicación promovió la rotura de la estructura de los tejidos e incrementó la transferencia de masa.
a f: frecuencia ultrasónica; P: potencia; I: intensidad; T: temperatura; t: tiempo de tratamiento; A: amplitud de onda.
da Silva et al. (2016)
et al. (2019)
et al. (2019)
4. Modelos y cinéticas de transferencia de masa durante el proceso de deshidratación osmótica
Al comienzo del proceso de deshidratación osmótica, como la diferencia entre la concentración de solutos de la solución osmótica y de la matriz alimenticia es grande, la pérdida de agua es muy rápida. Conforme el contenido de agua de la matriz alimenticia se reduce, la diferencia de concentraciones (presión osmótica) se vuelve más pequeña, por lo que la velocidad de transferencia disminuye hasta alcanzar un estado de equilibrio (Salim et al., 2016). Como en la deshidratación osmótica ocurre un intercambio de agua y soluto, el proceso de deshidratación osmótica puede evaluarse mediante los parámetros de pérdida de agua, PA y ganancia de solutos, GS (Assis et al., 2018), los cuales se pueden calcular con las siguientes ecuaciones (Allahdad et al., 2019):
Dias
Osae
Sucheta
Tabla VI.
Ecuación 1.
Ecuación 2.
Modificación de la transferencia de masa durante la deshidratación osmótica de frutas y hortalizas: factores de proceso y métodos no térmicos
Donde PA es la pérdida de agua del producto (g agua/g producto fresco); GS, la ganancia de solutos (g soluto/g producto fresco); mw0, la masa de agua inicial (g); mwDO, la masa de agua del producto osmodeshidratado (g); mp0, la masa del producto fresco (g); m s, la masa del producto osmodeshidratado seco; y ms0 corresponde a la masa del producto fresco seco (g). Los modelos de transferencia de masa para la deshidratación osmótica desprecian el flujo de soluto proveniente de la matriz alimenticia, ya que es muy pequeño comparado con la PA y GS (Pacheco-Angulo et al., 2016). Los modelos que permiten predecir las cinéticas de PA y GS se clasifican en empíricos, semi-empíricos y fenomenológicos (Muñiz-Becerá et al., 2017). En la tabla VII se presentan algunos modelos usados para describir estas curvas de proceso. Los modelos empíricos y semi empíricos dependen de las condiciones experimentales, ya que únicamente son válidos para las condiciones en que se calcularon. Además, algunos permiten predecir los valores de equilibrio con pocos puntos experimentales de la cinética (Azuara et al., 1992; Alam et al., 2019), por lo que, generalmente, se utili-
VII.
zan para calcular el estado de equilibrio para resolver algunos modelos fenomenológicos. Estos modelos tienen en cuenta los mecanismos del proceso, usan geometrías clásicas y se basan en la segunda ley de Fick para representar el mecanismo de difusión (Assis et al., 2016).
En la tabla VIII vemos algunos ejemplos de la difusividad de transferencia de masa de frutas y hortalizas sometidas a deshidratación osmótica asistida por pulsos de vacío, altas presiones hidrostáticas, campos eléctricos pulsados y osmosonicación. Se muestra un incremento en la difusividad de transferencia de masa en los procesos de deshidratación osmótica asistida por estos métodos no térmicos. Asimismo, se observa un incremento en la difusividad de transferencia de masa debido a soluciones osmóticas con menor peso molecular (Dash et al., 2019), debido al incremento en la concentración del soluto presente en la solución osmótica (George et al., 2016; De Jesus Junqueira et al., 2018) o al aumentar la magnitud del tratamiento no térmico (hhp y pef) (Simpson et al., 2015; Dermesonlouoglou et al., 2016; Luo et al., 2018; Dash et al., 2019).
Modelos matemáticos usados para describir la transferencia de masa durante la deshidratación osmótica de frutas y hortalizas
Modelo
Descripción
Referencias Nombre Ecuación a
Modelos empíricos y semi-empíricos
Modelo de Azuara
Modelo de Peleg
Modelo de Page
Modelo de Weibull
s 1, s 2, constantes de velocidad relativa a la PA y GS
k 1,A , k 1,S , constantes de velocidad (s∙kg de sólidos secos / kg de agua);
k 2,A , k 2,S , constantes de capacidad (kg de sólidos secos / kg de agua);
Azuara et al. (1992)
PA0, GS0 , PA y GS al inicio del proceso Peleg (1988)
α A , α S , constantes asociadas a PA y GS
β A , β S , constantes de Page para PA y GS
Alam et al. (2019)
γ A , γ S , δ A , δ S , parámetros asociados al modelo de Weibull Pei et al. (2019)
Tabla
Nombre
Modelos matemáticos usados para describir la transferencia de masa durante la deshidratación osmótica de frutas y hortalizas (continuación)
Modelo
Ecuación a
Descripción
Modelos fenomenológicos obtenidos de la segunda ley de Fick
Solución analítica de Crank
Geometría: placa plana; l, longitud característica (m); D i , difusividad de transferencia de masa (m2 / s); i = A
o S; A = agua; S = solutos;
ψi = A = 1 - PA e / PA;
ψi = S = 1 - GS e ⁄ GS; n, número de nodos
Geometría: esférica; r, radio (m); t, tiempo (s); D i , difusividad de transferencia de masa (m2 / s); i = A
o S; A = agua; S = solutos;
ψi = A = 1 - PA e / PA;
ψi = S = 1 - GS e ⁄ GS; n, número de nodos
Referencias
MuñizBecerá et al. (2017)
a PA: pérdida de agua (g agua / g producto fresco); GS: ganancia de solutos (g solutos / g producto fresco); t: tiempo de inmersión (s); PA e (g agua / g producto fresco); GS e (g solutos / g producto fresco); PA; GS en el equilibrio.
Tabla VIII.
Matriz (geometría)
Rebanadas de Zingiber officinale
Roscoe (placa plana)
Difusividad de transferencia de masa de frutas y hortalizas sometidas a proceso de deshidratación osmótica asistido por pulsos de vacío, altas presiones, tratamiento eléctrico y osmo-sonicación
Condiciones de proceso
Tratamiento
Presión: 200 - 600 mpa
Tiempo de tratamiento: 0.25 - 15 min
Deshidratación osmótica
Altas presiones hidrostáticas (HHP)
Agente osmótico: glucosa, fructosa y sacarosa
Concentración de agente osmótico: 60 °Brix
Relación agente osmótico y matriz: 4 g
agente osmótico / g producto
Temperatura: 40 °C
Difusividad × 109 (m² / s)
Agua / soluto
0.322 / 0.199 glucosa
Referencias
Dash et al., (2019) 0.362 / 0.165 fructosa
0.396 / 0.396 sacarosa 2.2773.725 / 1.7302.608 glucosa, hhp 2.6184.027 / 1.4832.291 fructosa, hhp 2.8904.293 / 1.2834.293 sacarosa, hhp
Tabla VII.
Modificación de la transferencia de masa durante la deshidratación osmótica de frutas y hortalizas: factores de proceso y métodos no térmicos
VIII.
Matriz (geometría)
Difusividad de transferencia de masa de frutas y hortalizas sometidas a proceso de deshidratación osmótica asistido por pulsos de vacío, altas presiones, tratamiento eléctrico y osmo-sonicación (continuación)
Condiciones de proceso
Difusividad × 109 (m² / s)
Tratamiento Deshidratación osmótica Agua / soluto
/ 0.22 kk
Rebanadas de manzana (placa plana)
Presión: 400 mpa Tiempo de tratamiento: 10 min
Cilindros de ciruela china, Prunus mume Siebet Zucc (cilindro infinito)
Rodajas de berengena, Solanum melongena L. (placa plana)
Presión: 50, 100, 200 y 400 mpa Tiempo de tratamiento: 10 min
Agente osmótico: jugo de kokum (kk) y una mezcla de sacarosa y kokum (ss-kk) Concentración de agente osmótico: 10, 30 y 50 °Brix
Relación agente osmótico y matriz: 3 g agente osmótico / g producto Temperatura: 40 °C
Agente osmótico: sacarosa
Concentración de agente osmótico: 40 °Brix
Relación agente osmótico y matriz: 20 g agente osmótico / g producto
Temperatura: 22 °C Tiempo: 360 min
Pulsos de vacío (PV)
/
/ 0.23 kk, hhp
-
/
/ - -
0.376 / - hhp
Referencias
Rebanadas de manzana var. Granny Smith (placa plana)
Presión de vacío: 108.8 mmHg Tiempo: 10 min
Agente osmótico: 10 % NaCl; 7.5 % NaCl + 2.5 % KCl; 7 % NaCl + 2.5 % KCl + 0.5 % CaCl2 (1); y 5 % NaCl + 4.0 % KCl + 1. % CaCl2 (2)
Relación agente osmótico y matriz: 10 g agente osmótico / g producto Temperatura: 30 °C Tiempo: 10 - 360 min
0.459 / 0.257 NaCl : KCl
0.453 / 0.312 NaCl : KCl : CaCl2 (1)
0.411 / 0.305 NaCl : KCl : CaCl2 (2)
0.504 / 0.325 NaCl – PV
George et al. (2016)
Luo et al. (2018)
Presión de vacío: 0.0114 mpa (85.4 mmHg) Tiempo: 20 min
Agente osmótico: 9 g de sacarosa / g de emulsión W1 / O / W2 (la emulsión agua en aceite se formó con la 9.98 × 108 ufc de Lactobacillus rhamnosus LC705 / ml y 62 g aceite de semilla de uva; finalmente 30 g de la emulsión W1 / O se dispersó en 70 g de solución de 14 % de concentrado de proteína de suero de leche)
Concentración: 40 - 60 °Brix
Relación agente osmótico y matriz: 20 g agente osmótico / g producto Tiempo: 320 min
0.546 / 0.287 NaCl : KCl - PV
0.434 / 0.255 NaCl De Jesus Junqueira et al. (2017)
0.533 / 0.355 NaCl : KCl : CaCl2 (1) – PV
0.499 / 0.111
NaCl : KCl : CaCl2 (2) - PV
0.1630.241 / 0.570.744 sin tratar FloresAndrade et al. (2017) 0.2390.301 / 0.8531.548 pv
Tabla
Matriz (geometría)
Discos de manzana var. Jonagold (discos de espesor infinito)
Difusividad de transferencia de masa de frutas y hortalizas sometidas a proceso de deshidratación osmótica asistido por pulsos de vacío, altas presiones, tratamiento eléctrico y osmo-sonicación (continuación)
Condiciones de proceso
Tratamiento
Intensidad de campo
eléctrico: 800 V / cm
Número de pulsos: 10
Duración del pulso: 100 μs
Intervalo entre pulsos: 100 ms
Tiempo de relajación: 10 s
Energía específica de consumo: 12 kJ / kg
Temperatura constante
Intensidad de campo eléctrico: 70, 110 y 180 V / cm
Rebanadas de Kiwi var. Hayward (placa plana)
Rebanadas rectangulares de manzana var. Golden delicious (prisma rectangular)
Manzana var. Granny Smith
Número de pulsos: 250
Duración del pulso: 15 μs
Frecuencia: 300 Hz
Energía específica de consumo: 8, 16.6 y 42.3 kJ / kg
Temperatura: 20 °C
Tratamiento eléctrico
Intensidad de campo eléctrico: 20 - 32 V / cm
Tiempo: 10 - 30 s
Temperatura: 30 °C
Intensidad de campo
eléctrico: 9, 13 y 17 V / cm
Voltaje: 70 - 130 V
Temperatura: 40 °C
Deshidratación osmótica
Campo eléctrico pulsado (PEF)
Agente osmótico: 0.20 y 0.60 g glicerol / g jugo de manzana
Relación agente osmótico y matriz: 20 g agente osmótico / g producto
Temperatura: 20 °C
Tiempo: 180 min
Agente osmótico: 0.30 g glicerol, 0.10 g trehalosa, 0.20 maltodextrina, ácido ascórbico, 0.1 g CaCl2 y 0.002 g ácido cítrico / g solución
Relación agente osmótico y matriz: 5 g solución osmótica / g producto
0.50 -
Difusividad × 109 (m2 / s)
Agua / soluto
/
-
pef
Temperatura: 25 - 45 °C Tiempo: 240 min 0.3231.13 / 1.251.81 sin tratar
/
Agente osmótico: sacarosa
Concentración de agente osmótico: 50 °Brix
Temperatura: 40 °C
Relación agente osmótico y matriz: 15 g agente osmótico / g producto
Velocidad de agitación: 180 rpm
Agente osmótico: sacarosa con sorbato de potasio y CaCl2
Concentración de agente osmótico: 45 - 65 °Brix con 7 mg sorbato de potasio / L y 1.27 - 1.13 g CaCl2 / L
Temperatura: 40 °C
Relación agente osmótico y matriz: 11 g agente osmótico / g producto
Osmo-sonicación (OUS)
Agente osmótico: glucosa y sacarosa
Concentración de agente osmótico:
-
-
pef
0.0132 / 0.271 sin tratar
Referencias
et al. (2016)
Dermesonlouoglou et al. (2016)
Yildiz et al. (2016) 0.1240.262 / 0.1010.277 pef-moderado
0.1480.181 / - sin tratar
et al. (2015) 0.1630.514 / - pef
Mitades de ciruela var. Victoria (semi esfera)
Frecuencia: 25 kHz
Tiempo: 30 y 60 min
0.50 g (glucosa o sacarosa) / g solución
Relación agente osmótico y matriz: 4 g agente osmótico / g producto
Temperatura: 30 °C Tiempo: 180 min - / 17.3 glucosa y sacarosa
Rahaman et al. (2019) - / 17.119.2 glucosa, ous - / 18.518.6 sacarosa, ous
Parniakov
Simpson
Tabla VIII.
Modificación de
de masa durante
osmótica de frutas y hortalizas: factores de proceso y métodos no térmicos
Difusividad de transferencia de masa de frutas y hortalizas sometidas a proceso de deshidratación osmótica asistido por pulsos de vacío, altas presiones, tratamiento eléctrico y osmo-sonicación (continuación)
Matriz (geometría)
Cubos de pepino (placa plana)
Rebanadas de Agaricus bisporus (placa plana)
Tratamiento
Frecuencia: 30 y 70 %
Tiempo: 20 y 60 min
Condiciones de proceso
Deshidratación osmótica
Agente osmótico: maltodextrina con NaCl
Concentración de agente osmótico:
0.565 g maltodextrina, 0.05 o 0.045 g NaCl / g solución
Relación agente osmótico y matriz: 5 g solución osmótica / g producto
Temperatura: 25 °C
Agente osmótico: sacarosa, glucosa y NaCl
Frecuencia: 40 kHz
Energía: 200 W
Temperatura: 30 °C
Tiempo: 15 – 75 min
Concentración 0.40 - 0.60 g (sacarosa o glucosa) / g de solución 0.10 - 0.20 g NaCl / g de solución
Relación agente osmótico y matriz: 10 g agente osmótico / g producto
0.004 -
Difusividad × 109 (m2 / s)
Agua / soluto
-
/
ous
0.6410.776 / 0.4910.551 sacarosa, ous
-
/
1.111 glucosa, ous
1.948 / 0.6110.667 NaCl, ous
Referencias
Kiani et al. (2018)
Pei et al. (2019)
CONCLUSIONES Y COMENTARIOS FINALES
Se han publicado avances acerca de la modificación de la transferencia de masa durante la deshidratación osmótica de frutas y hortalizas, considerando diversos parámetros, métodos no térmicos, modelos y cinéticas de proceso. La mayoría de los estudios indican que la selección de los parámetros óptimos del proceso, como el tiempo, la temperatura, la concentración del agente osmótico o el tipo de tratamiento no térmico, pueden modificar la calidad del producto e incrementar la transferencia de masa. Asimismo, el uso de tratamientos no térmicos y diferentes condiciones de proceso pueden generar frutas u hortalizas con diferente concentración de solutos. Finalmente, el uso de modelos matemáticos, como la segunda ley de Fick, junto con el modelo de Azuara o Page, son de gran ayuda para comprender mejor y predecir los fenómenos de transferencia
de masa de tratamientos no térmicos o diferentes condiciones de proceso.
A pesar de que estas tecnologías son prometedoras para la obtención de productos osmodeshidratados con alta calidad nutricional, no hay estudios que reporten la aplicación de estos métodos no térmicos con agentes osmóticos más complejos (como concentrados de frutas y hortalizas). Asimismo, se requieren mayores estudios que permitan escalar estos procesos a nivel industrial.
AGRADECIMIENTOS
El autor González-Pérez, J. E. agradece a la Universidad de las Americas Puebla (udlap) y al Consejo Nacional de Humanidades, Ciencia y Tecnología (conahcyt) —hoy Secretaría de Ciencia, Humanidades, Tecnología e Innovación (secihti)—, por el apoyo recibido para el financiamiento de sus estudios de posgrado.
Tabla VIII.
REFERENCIAS
Ahmed, I., Qazi, I. M. y Jamal, S. (2016). Developments in osmotic dehydration technique for the preservation of fruits and vegetables. Innovative Food Science & Emerging Technologies, 34, 29-43. doi: 10.1016/j.ifset.2016.01.003
Akharume, F., Smith, A., Sivanandan, L. y Singh, K. (2019). Recent progress on osmo-convective dehydration of fruits. SDRP Journal of Food Science & Technology, 4(9), 956-969. doi: 10.25177/JFST.4.9.RA.613
Alam, M. S., Kaur, M. y Ramya, H. G. (2019). Mass transfer kinetics for osmotic dehydration of kinnow fruit in sugar solution. Proceedings of the National Academy of Sciences, India Section B: Biological Sciences, 89(1), 361-370. doi: 10.1007/s40011-017-0951-z
Alfaro, L., Siramard, S., Chouljenko, A. y Sathivel, S. (2018). Effects of liquid nitrogen pretreatment on the osmotic dehydration and quality of cryogenically frozen blueberries (Vaccinium angustifolium Ait.). Food Bioscience, 22, 165-169. doi: 10.1016/j.fbio.2018.02.006
Allahdad, Z., Nasiri, M., Varidi, M. y Varidi, M. J. (2019). Effect of sonication on osmotic dehydration and subsequent air-drying of pomegranate arils. Journal of Food Engineering, 244, 202-211. doi: 10.1016/j.jfoodeng.2018.09.017
Amami, E., Khezami, L., Jemai, A. B. y Vorobiev, E. (2014). Osmotic dehydration of some agro-food tissue pre-treated by pulsed electric field: impact of impeller’s Reynolds number on mass transfer and color. Journal of King Saud University - Engineering Sciences, 26 (1), 93-102. doi: 10.1016/j.jksues.2012.10.002
Amami, E., Khezami, W., Mezrigui, S., Badwaik, L. S., Bejar, A. K., Perez, C. T. y Kechaou, N. (2017). Effect of ultrasound-assisted osmotic dehydration pretreatment on the convective drying of strawberry. Ultrasonics Sonochemistry, 36, 286-300. doi: 10.1016/j.ultsonch.2016.12.007
An, K., Tang, D., Wu, J., Fu, M., Wen, J., Xiao, G. y Xu, Y. (2019). Comparison of pulsed vacuum and ultrasound osmotic dehydration on drying of Chinese ginger (Zingiber officinale Roscoe): Drying characteristics, antioxidant capacity, and volatile profiles. Food Science & Nutrition, 7(8), 2537-2545. doi: 10.1002/fsn3.1103
Assis, F. R., Morais, R. M. S. C. y Morais, A. M. M. B. (2016). Mass transfer in osmotic dehydration of food products: Comparison between mathematical models. Food Engineering Reviews, 8(2), 116-133. doi: 10.1007/s12393-015-9123-1
Assis, F. R., Morais, R. M. S. C. y Morais, A. M. M. B. (2018). Mathematical modelling of the osmotic dehydration of physalis. Brazilian Journal of Food Technology, 21. doi: 10.1590/1981-6723.10217
Azuara, E., Beritain, C. y García, H. (1992). Development of a mathematical model to predict kinetics of osmotic dehydration. Journal of Food Science and Technology, 29, 239-242.
Barbosa de Lima, A. G., Da Silva, J. V., Pereira, E. M. A., Dos Santos, I. B. y De Lima, W. M. P. B. (2016). Drying of bioproducts: Quality and energy aspects. En J. M. P. Q. Delgado y A. G. Barbosa de Lima (Eds.), Drying and Energy Technologies (pp. 1-18). Springer Cham. doi: 10.1007/978-3-319-19767-8_1
Bera, D. y Roy, L. (2015). Osmotic dehydration of litchi using sucrose solution: Effect of mass transfer. Journal of Food Processing & Technology, 6(7). doi: 10.4172/2157-7110.1000462
Bozkir, H., Rayman Ergün, A., Serdar, E., Metin, G. y Baysal, T. (2019). Influence of ultrasound and osmotic dehydration pretreatments on drying and quality properties of persimmon fruit. Ultrasonics Sonochemistry, 54, 135-141. doi: 10.1016/j.ultsonch.2019.02.006
Brochier, B., Marczak, L. D. F. y Noreña, C. P. Z. (2015). Osmotic dehydration of yacon using glycerol and sorbitol as solutes: water effective diffusivity evaluation. Food and Bioprocess Technology, 8(3), 623-636. doi: 10.1007/ s11947-014-1432-5
Calín-Sánchez, Á., Kharaghani, A., Lech, K., Figiel, A., Carbonell-Barrachina, Á. A. y Tsotsas, E. (2015). Drying Kinetics and Microstructural and SensoryProperties of Black Chokeberry (Aronia melanocarpa) as Affected by Drying Method. Food and Bioprocess Technology, 8(1), 63-74. doi: 10.1007/ s11947-014-1383-x
Cano-Lamadrid, M., Lech, K., Michalska, A., Wasilewska, M., Figiel, A., Wojdyło, A. y Carbonell-Barrachina, Á. A. (2017). Influence of osmotic dehydration pre-treatment and combined drying method on physico-chemical and sensory properties of pomegranate arils, cultivar Mollar de Elche. Food Chemistry, 232, 306-315. doi: 10.1016/j.foodchem.2017.04.033
Chandra, S. y Kumari, D. (2015). Recent development in osmotic dehydration of fruit and vegetables: a review. Critical Reviews in Food Science and Nutrition, 55(4), 552-561. doi: 10.1080/10408398.2012.664830
Cheng, X., Zhang, M., Adhikari, B. y Islam, M. N. (2014). Effect of power ultrasound
and pulsed vacuum treatments on the dehydration kinetics, distribution, and status of water in osmotically dehydrated strawberry: a combined nmr and dsc study. Food and Bioprocess Technology, 7(10), 2782-2792. doi: 10.1007/s11947-014-1355-1
Chitrakar, B., Zhang, M. y Adhikari, B. (2019). Dehydrated foods: are they microbiologically safe? Critical Reviews in Food Science and Nutrition, 59(17), 27342745. doi: 10.1080/10408398.2018.1466265
Cichowska, J., Figiel, A., Stasiak-Różańska, L. y Witrowa-Rajchert, D. (2019). Modeling of osmotic dehydration of apples in sugar alcohols and dihydroxyacetone (dha) solutions. Foods (Basel, Switzerland), 8(1), 20. doi: 10.3390/foods8010020
Cichowska, J. y Kowalska, H. (2018). Effect of osmotic pre-treatment and temperature storage conditions on water activity and colour of dried apple. International Journal of Food Engineering, 14(2). doi: 10.1515/ijfe-2017-0158
Ciurzyńska, A., Kowalska, H., Czajkowska, K. y Lenart, A. (2016). Osmotic dehydration in production of sustainable and healthy food. Trends in Food Science & Technology, 50, 186-192. doi: 10.1016/j.tifs.2016.01.017
Dash, K. K., Balasubramaniam, V. M. y Kamat, S. (2019). High pressure assisted osmotic dehydrated ginger slices. Journal of Food Engineering, 247, 19-29. doi: 10.1016/j.jfoodeng.2018.11.024
De Jesus Junqueira, J. R., Corrêa, J. L. G., De Mendonça, K. S., De Mello Júnior, R. E. y De Souza, A. U. (2018). Pulsed vacuum osmotic dehydration of beetroot, carrot and eggplant slices: Effect of vacuum pressure on the quality parameters. Food and Bioprocess Technology, 11(10), 1863-1875. doi: 10.1007/s11947-018-2147-9
De Jesus Junqueira, J. R., Corrêa, J. L. G., De Mendonça, K. S., Resende, N. S. y De Barros Vilas Boas, E. V. (2017). Influence of sodium replacement and vacuum pulse on the osmotic dehydration of eggplant slices. Innovative Food Science & Emerging Technologies, 41, 10-18. doi: 10.1016/j.ifset.2017.01.006
De Mello, R. E., Jr., Corrêa, J. L. G., Lopes, F. J., De Souza, A. U. y Da Silva, K. C. R. (2019). Kinetics of the pulsed vacuum osmotic dehydration of green fig (Ficus carica L.). Heat and Mass Transfer, 55(6), 1685-1691. doi: 10.1007/ s00231-018-02559-w
Deng, L.-Z., Mujumdar, A. S., Zhang, Q., Yang, X.-H., Wang, J., Zheng, Z.-A., Gao, Z.-J. y Xiao, H.-W. (2019). Chemical and physical pretreatments of fruits and vegetables: effects on drying characteristics and quality attributes – a comprehensive review. Critical Reviews in Food Science and Nutrition, 59(9), 1408-1432. doi: 10.1080/10408398.2017.1409192
Deng, Y. y Zhao, Y. (2008). Effects of pulsed-vacuum and ultrasound on the osmodehydration kinetics and microstructure of apples (Fuji). Journal of Food Engineering, 85(1), 84-93. doi: 10.1016/j.jfoodeng.2007.07.016
Dermesonlouoglou, E. K., Angelikaki, F., Giannakourou, M. C., Katsaros, G. J. y Taoukis, P. S. (2019). Minimally processed fresh-cut peach and apricot snacks of extended shelf-Life by combined osmotic and high pressure processing. Food and Bioprocess Technology, 12(3), 371-386. doi: 10.1007/s11947-018-2215-1
Dermesonlouoglou, E. K., Bimpilas, A., Andreou, V., Katsaros, G. J., Giannakourou, M. C. y Taoukis, P. S. (2017). Process optimization and kinetic modeling of quality of fresh-cut strawberry cubes pretreated by high pressure and osmosis. Journal of Food Processing and Preservation, 41(5), 1-14. doi: 10.1111/jfpp.13137
Dermesonlouoglou, E. K., Chalkia, A., Dimopoulos, G. y Taoukis, P. (2018). Combined effect of pulsed electric field and osmotic dehydration pre-treatments on mass transfer and quality of air dried goji berry. Innovative Food Science & Emerging Technologies, 49, 106-115. doi: 10.1016/j.ifset.2018.08.003
Dermesonlouoglou, E. K. y Giannakourou, M. C. (2019). Evaluation and modelling of osmotic pre-treatment of peach using alternative agents in a multiple-component solution. Journal of the Science of Food and Agriculture, 99(3), 12401249. doi: 10.1002/jsfa.9296
Dermesonlouoglou, E. K., Zachariou, I., Andreou, V. y Taoukis, P. S. (2016). Effect of pulsed electric fields on mass transfer and quality of osmotically dehydrated kiwifruit. Food and Bioproducts Processing, 100(B), 535-544. doi: 10.1016/j.fbp.2016.08.009
Dias da Silva, G., Barros, Z. M. P., De Medeiros, R. A. B., De Carvalho, C. B. O., Rupert Brandão, S. C. y Azoubel, P. M. (2016). Pretreatments for melon drying implementing ultrasound and vacuum. LWT, 74, 114-119. doi: 10.1016/j.lwt.2016.07.039
Dellarosa, N., Ragni, L., Laghi, L., Tylewicz, U., Rocculi, P. y Dalla Rosa, M. (2016). Time domain nuclear magnetic resonance to monitor mass transfer mechanisms in apple tissue promoted by osmotic dehydration combined with pulsed electric fields. Innovative Food Science & Emerging Technologies, 37(C), 345-351. doi: 10.1016/j.ifset.2016.01.009
El-Aouar, Â. A., Azoubel, P. M., Barbosa, J. L. y Xidieh Murr, F. E. (2006). Influence of the osmotic agent on the osmotic dehydration of papaya (Carica papaya L.). Journal of Food Engineering, 75(2), 267-274. doi: 10.1016/j. jfoodeng.2005.04.016
Feng, Y., Yu, X., Yagoub, A. E. A., Xu, B., Wu, B., Zhang, L. y Zhou, C. (2019). Vacuum pretreatment coupled to ultrasound assisted osmotic dehydration as a novel method for garlic slices dehydration. Ultrasonics Sonochemistry, 50, 363-372. doi: 10.1016/j.ultsonch.2018.09.038
Fernandes, F. A. N. y Rodrigues, S. (2017). Osmotic dehydration and blanching: Ultrasonic pre-treatments. En M. Villamiel et al. (Eds.), Ultrasound in Food Processing (pp. 311-328). Wiley-Blackwell. doi: 10.1002/9781118964156.ch11
Flores-Andrade, E., Pascual-Pineda, L. A., Alarcón-Elvira, F. G., Rascón-Díaz, M. P., Pimentel-González, D. J. y Beristain, C. I. (2017). Effect of vacuum on the impregnation of Lactobacillus rhamnosus microcapsules in apple slices using double emulsion. Journal of Food Engineering, 202, 18-24. doi: 10.1016/j. jfoodeng.2017.02.005
Garcia-Noguera, J., Oliveira, F. I. P., Weller, C. L., Rodrigues, S. y Fernandes, F. A. N. (2014). Effect of ultrasonic and osmotic dehydration pre-treatments on the colour of freeze dried strawberries. Journal of Food Science and Technology, 51(9), 2222-2227. doi: 10.1007/s13197-012-0724-x
George, J. M., Senthamizh Selvan, T. y Rastogi, N. K. (2016). High-pressure-assisted infusion of bioactive compounds in apple slices. Innovative Food Science & Emerging Technologies 33, 100-107. doi: 10.1016/j.ifset.2015.11.010
Gómez-Ramírez, C., Sosa-Morales, M. E., Palou, E. y López-Malo, A. (2013). Aspergillus niger time to growth in dried tomatoes. International Journal of Food Microbiology, 164(1), 23-25. doi: 10.1016/j.ijfoodmicro.2013.03.017
González-Pérez, J. E., López-Méndez, E. M., Luna-Guevara, J. J., Ruiz-Espinosa, H., Ochoa-Velasco, C. E. y Ruiz-López, I. I. (2019). Analysis of mass transfer and morphometric characteristics of white mushroom (Agaricus bisporus) pilei during osmotic dehydration. Journal of Food Engineering, 240, 120-132. doi: 10.1016/j.jfoodeng.2018.07.026
Kek, S. P., Chin, N. L. y Yusof, Y. A. (2013). Direct and indirect power ultrasound assisted pre-osmotic treatments in convective drying of guava slices. Food and Bioproducts Processing, 91(4), 495-506. doi: 10.1016/j.fbp.2013.05.003
Ketata, M., Desjardins, Y. y Ratti, C. (2013). Effect of liquid nitrogen pretreatments on osmotic dehydration of blueberries. Journal of Food Engineering, 116(1), 202-212. doi: 10.1016/j.jfoodeng.2012.10.035
Kiani, H., Karimi, F., Labbafi, M. y Fathi, M. (2018). A novel inverse numerical modeling method for the estimation of water and salt mass transfer coefficients during ultrasonic assisted-osmotic dehydration of cucumber cubes. Ultrasonics Sonochemistry, 44, 171-176. doi: 10.1016/j.ultsonch.2018.02.003
Kowalska, H., Marzec, A., Kowalska, J., Ciurzyńska, A., Samborska, K., Cichowska, J., Rybak, K. y Lenart, A. (2017). Osmotic dehydration of Honeoye strawberries in solutions enriched with natural bioactive molecules. LWT - Food Science and Technology, 85, 500-505. doi: 10.1016/j.lwt.2017.03.044
Kuo, C.-H., Lin, J., Huang, C.-Y., Hsieh, S.-L., Li, S., Kuo, J.-M. y Shieh, C.-J. (2018). Predicting sugar content of candied watermelon rind during osmotic dehydration. Food Science and Technology, 38, 228-235. doi: 10.1590/fst.18817
Kusnadi, C. y Sastry, S. K. (2012). Effect of moderate electric fields on salt diffusion into vegetable tissue. Journal of Food Engineering, 110(3), 329-336. doi: 10.1016/j.jfoodeng.2012.01.004
Lech, K., Figiel, A., Wojdyło, A., Korzeniowska, M., Serowik, M. y Szarycz, M. (2015). Drying kinetics and bioactivity of beetroot slices pretreated in concentrated chokeberry juice and dried with vacuum microwaves. Drying Technology, 33(13), 1644-1653. doi: 10.1080/07373937.2015.1075209
Lech, K., Michalska, A., Wojdyło, A., Nowicka, P. y Figiel, A. (2017). The influence of the osmotic dehydration process on physicochemical properties of osmotic solution. Molecules, 22(12), 2246. doi: 10.3390/molecules22122246
Lech, K., Michalska, A., Wojdyło, A., Nowicka, P. y Figiel, A. (2018). The influence of physical properties of selected plant materials on the process of osmotic dehydration. LWT, 91, 588-594. doi: 10.1016/j.lwt.2018.02.012
Liu, B. y Peng, B. (2017). Modelling and optimization of process parameters for strawberry osmotic dehydration using central composite rotatable design. Journal of Food Quality, 2017(1), 1-7. doi: 10.1155/2017/2593213
Luchese, C. L., Gurak, P. D. y Marczak, L. D. F. (2015). Osmotic dehydration of physalis (Physalis peruviana L.): evaluation of water loss and sucrose incorporation and the quantification of carotenoids. LWT - Food Science and Technology, 63(2), 1128-1136. doi: 10.1016/j.lwt.2015.04.060
Luo, W., Tappi, S., Wang, C., Yu, Y., Zhu, S. y Rocculi, P. (2018). Study of the effect of High Hydrostatic Pressure (HHP) on the osmotic dehydration mechanism and kinetics of wumei fruit (Prunus mume). Food and Bioprocess Technology, 11(11), 2044-2054. doi: 10.1007/s11947-018-2165-7
Martín-Belloso, O. y Morales-de la Peña, M. (2018). Fruit preservation by ohmic
Modificación de la transferencia de masa durante la deshidratación osmótica de frutas y hortalizas: factores de proceso y métodos no térmicos
heating and pulsed electric fields. En A. Rosenthal et al. (Eds.), Fruit Preservation (pp. 441-456). Springer. doi: 10.1007/978-1-4939-3311-2_16
Mavroudis, N. E., Dejmek, P. y Sjöholm, I. (2004). Osmotic-treatment-induced cell death and osmotic processing kinetics of apples with characterised raw material properties. Journal of Food Engineering, 63(1), 47-56. doi: 10.1016/ S0260-8774(03)00281-4
Mavroudis, N. E., Gidley, M. J. y Sjöholm, I. (2012). Osmotic processing: effects of osmotic medium composition on the kinetics and texture of apple tissue. Food Research International, 48(2), 839-847. doi: 10.1016/j.foodres.2012.06.034
Miano, A. C., Rojas, M. L. y Augusto, P. E. D. (2017). Other mass transfer unit operations enhanced by ultrasound. En D. Bermudez-Aguirre (Ed.), Ultrasound: Advances for Food Processing and Preservation (pp. 369-389). Academic Press. doi: 10.1016/B978-0-12-804581-7.00015-4
Mokhtarian, M., Heydari Majd, M., Koushki, F., Bakhshabadi, H., Daraei Garmakhany, A. y Rashidzadeh, S. (2014). Optimisation of pumpkin mass transfer kinetic during osmotic dehydration using artificial neural network and response surface methodology modelling. Quality Assurance and Safety of Crops & Foods, 6(2), 201-214. doi: 10.3920/QAS2012.0121
Monnerat, S. M., Pizzi, T. R. M., Mauro, M. A. y Menegalli, F. C. (2010). Osmotic dehydration of apples in sugar/salt solutions: concentration profiles and effective diffusion coefficients. Journal of Food Engineering, 100(4), 604-612. doi: 10.1016/j.jfoodeng.2010.05.008
Mújica-Paz, H., Valdez-Fragoso, A., López-Malo, A., Palou, E. y Welti-Chanes, J. (2003). Impregnation and osmotic dehydration of some fruits: effect of the vacuum pressure and syrup concentration. Journal of Food Engineering, 57(4), 305314. doi: 10.1016/S0260-8774(02)00344-8
Muñiz-Becerá, S., Méndez-Lagunas, L. L. y Rodríguez-Ramírez, J. (2017). Solute transfer in osmotic dehydration of vegetable foods: a review. Journal of Food Science, 82(10), 2251-2259. doi: 10.1111/1750-3841.13857
Muszyński, S., Kornarzyński, K. y Gładyszewska, B. (2016). Osmotic dehydration of apples under reduced pressure conditions. Agricultural Engineering, 20(3), 135-143. doi: 10.1515/agriceng-2016-0051
Nazari, A., Salehi, M. A. y Abbasi Souraki, B. (2019). Experimental investigation of effective factors of pulsed electric field in osmotic dehydration of apple. Heat and Mass Transfer, 55(7), 2049-2059. doi: 10.1007/s00231-019-02571-8
Nowacka, M., Laghi, L., Rybak, K., Dalla Rosa, M., Witrowa-Rajchert, D. y Tylewicz, U. (2019). Water state and sugars in cranberry fruits subjected to combined treat-
ments: Cutting, blanching and sonication. Food Chemistry, 299, 125122. doi: 10.1016/j.foodchem.2019.125122
Nowacka, M., Tylewicz, U., Laghi, L., Dalla Rosa, M. y Witrowa-Rajchert, D. (2014). Effect of ultrasound treatment on the water state in kiwifruit during osmotic dehydration. Food Chemistry, 144, 18-25. doi: 10.1016/j.foodchem.2013.05.129
Nowacka, M., Tylewicz, U., Tappi, S., Siroli, L., Lanciotti, R., Witrowa-Rajchert, D. y Romani, S. (2018). Ultrasound assisted osmotic dehydration of organic cranberries (Vaccinium oxycoccus): study on quality parameters evolution during storage. Food Control, 93, 40-47. doi: 10.1016/j.foodcont.2018.05.005
Nowacka, M., Wiktor, A., Anuszewska, A., Dadan, M., Rybak, K. y Witrowa-Rajchert, D. (2019). The application of unconventional technologies as pulsed electric field, ultrasound and microwave-vacuum drying in the production of dried cranberry snacks. Ultrasonics Sonochemistry, 56, 1-13. doi: 10.1016/j. ultsonch.2019.03.023
Nowicka, P., Wojdyło, A., Lech, K. y Figiel, A. (2015a). Chemical composition, antioxidant capacity, and sensory quality of dried sour cherry fruits pre-dehydrated in fruit concentrates. Food and Bioprocess Technology, 8(10), 2076-2095. doi: 10.1007/s11947-015-1561-5
Nowicka, P., Wojdyło, A., Lech, K. y Figiel, A. (2015b). Influence of osmodehydration pretreatment and combined drying method on the bioactive potential of sour cherry fruits. Food and Bioprocess Technology, 8(4), 824-836. doi: 10.1007/s11947-014-1447-y
Núñez-Mancilla, Y., Pérez-Won, M., Uribe, E., Vega-Gálvez, A. y Di Scala, K. (2013). Osmotic dehydration under high hydrostatic pressure: effects on antioxidant activity, total phenolics compounds, vitamin C and colour of strawberry (Fragaria vesca). LWT - Food Science and Technology, 52(2), 151-156. doi: 10.1016/j.lwt.2012.02.027
Núñez-Mancilla, Y., Vega-Gálvez, A., Pérez-Won, M., Zura, L., García-Segovia, P. y Di Scala, K. (2014). Effect of osmotic dehydration under high hydrostatic pressure on microstructure, functional properties and bioactive compounds of strawberry (Fragaria vesca). Food and Bioprocess Technology, 7(2), 516-524. doi: 10.1007/s11947-013-1052-5
Omolola, A. O., Jideani, A. I. O. y Kapila, P. F. (2017). Quality properties of fruits as affected by drying operation. Critical Reviews in Food Science and Nutrition, 57(1), 95-108. doi: 10.1080/10408398.2013.859563
Onwude, D. I., Hashim, N., Janius, R., Abdan, K., Chen, G. y Oladejo, A. O. (2017). Non-thermal hybrid drying of fruits and vegetables: a review of current
technologies. Innovative Food Science & Emerging Technologies, 43, 223238. doi: 10.1016/j.ifset.2017.08.010
Osae, R., Zhou, C., Xu, B., Tchabo, W., Tahir, H. E., Mustapha, A. T. y Ma, H. (2019). Effects of ultrasound, osmotic dehydration, and osmosonication pretreatments on bioactive compounds, chemical characterization, enzyme inactivation, color, and antioxidant activity of dried ginger slices. Journal of Food Biochemistry, 43(5), 1-14. doi: 10.1111/jfbc.12832
Pacheco-Angulo, H., Herman-Lara, E., García-Alvarado, M. A. y Ruiz-López, I. I. (2016). Mass transfer modeling in osmotic dehydration: equilibrium characteristics and process dynamics under variable solution concentration and convective boundary. Food and Bioproducts Processing, 97, 88-99. doi: 10.1016/j.fbp.2015.11.002
Parniakov, O., Bals, O., Lebovka, N. y Vorobiev, E. (2016). Effects of pulsed electric fields assisted osmotic dehydration on freezing-thawing and texture of apple tissue. Journal of Food Engineering, 183, 32-38. doi: 10.1016/j.jfoodeng.2016.03.013
Pei, F., Xiao, K., Chen, L., Yang, W., Zhao, L., Fang, Y., Ma, N., Mariga, A. M. y Hu, Q. (2019). Mass transfer characteristics during ultrasound-assisted osmotic dehydration of button mushroom (Agaricus bisporus). Journal of Food Science and Technology, 56(4), 2213-2223. doi: 10.1007/s13197-019-03707-8
Peleg, M. (1988). An empirical model for the description of moisture sorption curves. Journal of Food Science, 53(4), 1216-1217. doi: 10.1111/j.13652621.1988.tb13565.x
Qiu, L., Zhang, M., Tang, J., Adhikari, B. y Cao, P. (2019). Innovative technologies for producing and preserving intermediate moisture foods: a review. Food Research International, 116, 90-102. doi: 10.1016/j.foodres.2018.12.055
Rahaman, A., Zeng, X.-A., Kumari, A., Rafiq, M., Siddeeg, A., Manzoor, M. F., Baloch, Z. y Ahmed, Z. (2019). Influence of ultrasound-assisted osmotic dehydration on texture, bioactive compounds and metabolites analysis of plum. Ultrasonics Sonochemistry, 58, 104643. doi: 10.1016/j.ultsonch.2019.104643
Rahman, M. S. (2017). State diagram of foods and Its importance to food stability during storage and processing. En J. Ahmed (Ed.), Glass Transition and Phase Transitions in Food and Biological Materials (pp. 251-260). John Wiley & Sons. doi: 10.1002/9781118935682.ch11
Rahman, S. M. A., Hoque, M.E., Rahman, S. y Hasanuzzaman, M. (2015). Osmotic de-
hydration of pumpkin using response surface methodology -influences of operating conditions on water loss and solute gain. Journal of Bioprocessing & Biotechniques, 5(5). doi: 10.4172/2155-9821.1000226
Ramya, V. y Jain, N. K. (2017). A review on osmotic dehydration of fruits and vegetables: an integrated approach. Journal of Food Process Engineering, 40(3), 124-140. doi: 10.1111/jfpe.12440
Rongtong, B., Suwonsichon, T., Ritthiruangdej, P. y Kasemsumran, S. (2018). Determination of water activity, total soluble solids and moisture, sucrose, glucose and fructose contents in osmotically dehydrated papaya using near-infrared spectroscopy. Agriculture and Natural Resources, 52(6), 557564. doi: 10.1016/j.anres.2018.11.023
Ruiz-López, I. I., Huerta-Mora, I. R., Vivar-Vera, M. A., Martínez-Sánchez, C. E. y Herman-Lara, E. (2010). Effect of osmotic dehydration on air-drying characteristics of chayote. Drying Technology, 28(10), 1201-1212. doi: 10.1080/07373937.2010.482716
Sabarez, H. T. (2018). Thermal drying of foods. En A. Rosenthal et al. (Eds.), Fruit Preservation (pp. 181–210). Springer. doi: 10.1007/978-1-4939-3311-2_7
Şahin, U. y Öztürk, H. K. (2016). Effects of pulsed vacuum osmotic dehydration (pvod) on drying kinetics of figs (Ficus carica L). Innovative Food Science & Emerging Technologies, 36, 104-111. doi: 10.1016/j.ifset.2016.06.003
Şahin, U. y Öztürk, H. K. (2018). Comparison between Artificial Neural Network model and mathematical models for drying kinetics of osmotically dehydrated and fresh figs under open sun drying. Journal of Food Process Engineering, 41(5), e12804. doi: 10.1111/jfpe.12804
Salim, M. N. S., Garièpy, Y. y Raghavan, V. (2016). Effects of operating factors on osmotic dehydration of broccoli stalk slices. Cogent Food & Agriculture, 2(1). doi: 10.1080/23311932.2015.1134025
Samborska, K., Eliasson, L., Marzec, A., Kowalska, J., Piotrowski, D., Lenart, A. y Kowalska, H. (2019). The effect of adding berry fruit juice concentrates and by-product extract to sugar solution on osmotic dehydration and sensory properties of apples. Journal of Food Science and Technology, 56(4), 1927-1938. doi: 10.1007/s13197-019-03658-0
Sangeeta y Hathan, B. S. (2016). Studies on mass transfer and diffusion coefficients in elephant foot yam (Amorphophallus spp.) during osmotic dehydration in sodium chloride solution: Studies on mass transfer and diffusion coefficients
in elephant foot yam. Journal of Food Processing and Preservation, 40(3), 521-530. doi: 10.1111/jfpp.12631
Sethi, K. y Kaur, M. (2019). Effect of osmotic dehydration on physicochemical properties of pineapple using honey, sucrose and honey-sucrose solutions. International Journal of Engineering and Advanced Technology, 9(1), 6257-6262. doi: 10.35940/ijeat.A2026.109119
Shamaei, S., Emam-Djomeh, Z. y Moini, S. (2012). Ultrasound-assisted osmotic dehydration of cranberries: effect of finish drying methods and ultrasonic frequency on textural properties: ultrasound-osmotic dehydration of cranberry. Journal of Texture Studies, 43(2), 133-141. doi: 10.1111/j.17454603.2011.00323.x
Shete, Y. V., Chavan, S. M., Champawat, P. S. y Jain, S. K. (2018). Reviews on osmotic dehydration of fruits and vegetables. Journal of Pharmacognosy and Phytochemistry, 7(2), 1964-1969.
Simpson, R., Ramírez, C., Birchmeier, V., Almonacid, A., Moreno, J., Nuñez, H. y Jaques, A. (2015). Diffusion mechanisms during the osmotic dehydration of Granny Smith apples subjected to a moderate electric field. Journal of Food Engineering, 166, 204-211. doi: 10.1016/j.jfoodeng.2015.05.027
Sucheta, Chaturvedi, K. y Yadav, S. K. (2019). Ultrasonication assisted salt-spices impregnation in black carrots to attain anthocyanins stability, quality retention and antimicrobial efficacy on hot-air convective drying. Ultrasonics Sonochemistry, 58, 104661. doi: 10.1016/j.ultsonch.2019.104661
Sulistyawati, I., Dekker, M., Fogliano, V. y Verkerk, R. (2018). Osmotic dehydration of mango: effect of vacuum impregnation, high pressure, pectin methylesterase and ripeness on quality. LWT, 98, 179-186. doi: 10.1016/j.lwt.2018.08.032
Tiroutchelvame, D., Sivakumar, V. y Maran, P. (2015). Mass transfer kinetics during osmotic dehydration of amla (Emblica officinalis L.) cubes in sugar solution. Chemical Industry and Chemical Engineering Quarterly, 21(4), 547-559. doi: 10.2298/CICEQ140712011T
Traffano-Schiffo, M. V., Laghi, L., Castro-Giraldez, M., Tylewicz, U., Rocculi, P., Ragni, L., Dalla Rosa, M. y Fito, P. J. (2017). Osmotic dehydration of organic kiwifruit pre-treated by pulsed electric fields and monitored by nmr Food Chemistry, 236, 87-93. doi: 10.1016/j.foodchem.2017.02.046
Traffano-Schiffo, M.V., Tylewicz, U., Castro-Giraldez, M., Fito, P. J., Ragni, L. y Dalla Rosa, M. (2016). Effect of pulsed electric fields pre-treatment on mass trans-
port during the osmotic dehydration of organic kiwifruit. Innovative Food Science & Emerging Technologies, 38, 243-251. doi: 10.1016/j.ifset.2016.10.011
Tylewicz, U., Tappi, S., Mannozzi, C., Romani, S., Dellarosa, N., Laghi, L., Ragni, L., Rocculi, P. y Dalla Rosa, M. (2017). Effect of pulsed electric field (pef) pre-treatment coupled with osmotic dehydration on physico-chemical characteristics of organic strawberries. Journal of Food Engineering, 213, 2-9. doi: 10.1016/j. jfoodeng.2017.04.028
Verma, D., Kaushik, N. y Rao, P. S. (2014). Application of high hydrostatic pressure as a pretreatment for osmotic dehydration of banana slices (Musa cavendishii) finish-dried by dehumidified air drying. Food and Bioprocess Technology, 7(5), 1281-1297. doi: 10.1007/s11947-013-1124-6
Wang, J., Law, C.L., Nema, P. K., Zhao, J.H., Liu, Z.L., Deng, L.Z. y Xiao, H.W. (2018). Pulsed vacuum drying enhances drying kinetics and quality of lemon slices. Journal of Food Engineering, 224, 129-138. doi: 10.1016/j.jfoodeng.2018.01.002
Witrowa-Rajchert, D., Wiktor, A., Sledz, M. y Nowacka, M. (2014). Selected emerging technologies to enhance the drying process: a review. Drying Technology, 32(11), 1386-1396. doi: 10.1080/07373937.2014.903412
Wu, X., Wang, C. y Guo, Y. (2020). Effects of the high-pulsed electric field pretreatment on the mechanical properties of fruits and vegetables. Journal of Food Engineering, 274, 109837. doi: 10.1016/j.jfoodeng.2019.109837
Yadav, A. K. y Singh, S. V. (2014). Osmotic dehydration of fruits and vegetables: A review. Journal of Food Science and Technology, 51(9), 1654-1673. doi: 10.1007/ s13197-012-0659-2
Yildiz, H., Icier, F., Eroglu, S. y Dagci, G. (2016). Effects of electrical pretreatment conditions on osmotic dehydration of apple slices: experimental investigation and simulation. Innovative Food Science & Emerging Technologies, 35, 149159. doi: 10.1016/j.ifset.2016.05.001
Yu, Y., Jin, T. Z., Fan, X. y Wu, J. (2018). Biochemical degradation and physical migration of polyphenolic compounds in osmotic dehydrated blueberries with pulsed electric field and thermal pretreatments. Food Chemistry, 239, 1219-1225. doi: 10.1016/j.foodchem.2017.07.071
Yu, Y., Jin, T. Z., Fan, X. y Xu, Y. (2017). Osmotic dehydration of blueberries pretreated with pulsed electric fields: effects on dehydration kinetics, and microbiological and nutritional qualities. Drying Technology, 35(13), 1543-1551. doi: 10.1080/07373937.2016.1260583
Obtención de compuestos bioactivos y enzimas a
partir de la fermentación de algas
A. Pérez-Alva*, M. M. Ramírez-Rodrigues y D. K. Baigts-Allende
*Programa de Doctorado en Ciencia de Alimentos
Correo electrónico: alexa.perezaa@udlap.mx
RESUMEN
El objetivo de este artículo de revisión es proporcionar información actualizada sobre las diferentes aplicaciones de la fermentación de micro y macroalgas para obtener compuestos bioactivos y enzimas. Los estudios de fermentación de algas se han centrado en analizar la mejora del contenido fenólico, que está relacionado positivamente con la capacidad antioxidante. Además, se ha estudiado la producción de enzimas, carotenoides y polisacáridos, así como la mejora de la digestibilidad y biodisponibilidad de los péptidos. A pesar de que se ha investigado la producción de alimentos fermentados a base de algas y piensos para la acuicultura, este es un nicho que aún se encuentra en desarrollo, puesto que la mayoría de los estudios estudia el uso de algas para la obtención de biocombustibles y tratamiento de aguas residuales.
Palabras clave: fermentación, macroalgas, microalgas.
ABSTRACT
The objective of this review is to provide current information on the different applications of micro and macroalgae fermentation to obtain bioactive compounds and enzymes. The algal fermentation studies have focused on the improvement of the phenolic content, which is positively correlated to the antioxidant capacity. In addition, the production of carotenoids, enzymes and polysaccharides, as well as the improvement of the digestibility and bioavailability of peptides have also been studied. Notwithstanding the investigations regarding fermented algae-based foods and feed for aquaculture, this is a research segment that is still developing, since most studies focus on the use of algae for obtaining biofuels and wastewater treatment.
Keywords: fermentation, macroalgae, microalgae.
ABREVIATURAS
abts
Inhibición del 2, 2’-azinobis-3-etilbenzotiazolina-6-ácido sulfónico, por sus siglas en inglés
aptt Tiempo de tromboplastina parcial activado, por sus siglas en inglés
do Densidad óptica
dpph
frap
gae
orac
pge
Inhibición del 2,2-difenil-1-picrilhydrazil, por sus siglas en inglés
Capacidad antioxidante para reducir ion férrico, por sus siglas en inglés
Equivalentes de ácido gálico, por sus siglas en inglés
Capacidad de absorción de radicales de oxígeno, por sus siglas en inglés
Equivalentes de floroglucinol dihidrato, por sus siglas en inglés
te Equivalentes de trolox, por sus siglas en inglés
INTRODUCCIÓN
Las algas son un grupo heterogéneo de organismos que generalmente se describen como plantas acuáticas. Japón, China y Corea tienen una larga historia consumiéndolas (Takei et al., 2017). De hecho, las microalgas azul-verdes se han empleado como alimento por miles de años, mientras que la literatura más antigua en la que se menciona su uso como tributo y alimento es el Código Taiho Ritsuryo promulgado en 701 d. C. en Japón. Sin embargo, fue hasta principios de la década de 1950 que se implementó el cultivo de microalgas como fuente novedosa de proteína (Spolaore et al., 2006; Takuei et al., 2017).
Las algas, al ser organismos fotoautótrofos, producen metabolitos primarios y secundarios, que pueden presentar beneficios nutrimentales y actividad biológica por sus propiedades antioxidantes, antimicrobianas y antiinflamatorias, entre otras (Amorim
et al. 2012; Chye et al., 2018; Tanna y Mishra, 2018). Durante los últimos años, los metabolitos primarios, como péptidos y polisacáridos, así como los metabolitos secundarios, entre los que se encuentran polifenoles y pigmentos, han despertado el interés de la población, por lo que se han investigado diversos métodos para su obtención, como la hidrólisis ácida, la digestión enzimática y la extracción con solventes. A pesar de que los métodos estudiados son efectivos, al ser procedimientos complejos y tener costos elevados, pueden tener limitaciones. Debido a esto, se han buscado métodos de producción alternativos de menor costo, que sean amigables con el ambiente y en los que no se generen residuos tóxicos (Shobharani et al., 2013). La fermentación es una buena alternativa, ya que es capaz de generar compuestos de alta calidad y alta actividad, sin el riesgo de la toxicidad asociada a solventes orgánicos (Martins et al., 2011). La fermentación es una de las tecnologías de procesamiento de alimentos más antiguas e importantes, no solo aumenta la vida útil de los alimentos, sino que les confieren propiedades nutrimentales y sensoriales únicas (Navarrete-Bolaños, 2012; Erkmen y Bozoglu, 2016; Niccolai et al., 2019). La fermentación de algas inició entre 1970 y 1980, con el objetivo de producir biocombustibles y como fuente de energía. Fue hasta hace pocos años que se comenzó a investigar la posibilidad de utilizar algas como sustrato para la producción de compuestos bioactivos por medio de fermentaciones ácido lácticas o alcohólicas (Uchida y Miyoshi, 2013). El objetivo de este artículo de revisión es proporcionar información actualizada sobre las diferentes aplicaciones de la fermentación de micro y macroalgas para obtener compuestos bioactivos y enzimas.
REVISIÓN BIBLIOGRÁFICA
1. Generalidades de las algas
Las algas son un grupo de organismos muy comunes que habitan la Tierra. Se estima que el número conocido de especies varía entre 30,000 y 1 millón (Ścieszka y Klewicka, 2018). Son organismos fotosintéticos que se pueden desarrollar en hábitats diversos, pero predominantemente crecen en ecosistemas acuáticos, ya
sea en agua dulce o salada. Sin embargo, también pueden encontrarse en rocas, paredes, tierra e incluso en plantas y animales, en simbiosis (Kim, 2011; Amorim-Carrilho et al., 2014; Tebbani et al., 2014; Ścieszka y Klewicka, 2018). Adicionalmente, tienen la capacidad de adaptarse a condiciones extremas, como cambios en la salinidad, temperatura, nutrientes e incluso radiación uv-vis (Amorim-Carrilho et al., 2014). Con la finalidad de sobrevivir, durante el proceso de adaptación, producen una gran variedad de metabolitos primarios y secundarios que no pueden ser encontrados en otros organismos (Ścieszka y Klewicka, 2018). Algunos de estos compuestos son polisacáridos y polifenoles, los cuales han sido reconocidos por tener aplicaciones farmacológicas y terapéuticas (Shobharani et al., 2013).
Las algas tienen la capacidad de convertir la energía lumínica y fuentes de carbono —como el dióxido de carbono— en biomasa (Kim, 2011; Tebbani et al., 2014). Su morfología y tamaño son muy variables, por lo que se suelen dividir en dos grupos principales: macroalgas y microalgas (Kim, 2011). Las macroalgas son organismos multicelulares, que pueden medir hasta 70 m de longitud y tener un crecimiento de 50 cm diarios. Por otra parte, las microalgas pueden medir entre 3-10 µm (Tebbani et al., 2014; Ścieszka y Klewicka, 2018).
1.1. Macroalgas
Generalmente, las macroalgas se encuentran en litorales (Kim, 2011). De acuerdo con los tipos de pigmentos que producen, se dividen en tres subgrupos principales: algas pardas (Phaeophyceae), algas rojas (Rhodophyceae) y algas verdes (Chlorophyceae) —algunos autores agregan como cuarto grupo a los pastos marinos (Magnoliophyceae)—. En las algas pardas predomina el color café debido a la presencia de fucoxantina, mientras que en las rojas se encuentran pigmentos como la ficoeritrina y ficocianina, y las algas verdes contienen clorofilas del tipo a y b (Kim, 2011; Ścieszka y Klewicka, 2018). Las macroalgas se componen principalmente de carbohidratos (50-70 % b.s.) y contienen, además, vitaminas y minerales (Uchida y Miyoshi, 2013; Chye et al., 2018). Los carbohidratos presentes varían dependiendo del tipo de alga. En las algas pardas predominan los alginatos y fucanos, en las algas rojas se
pueden encontrar galactanos sulfatados, xilanos y almidón floridiano. Mientras que las algas verdes contienen almidón, xilanos, mananos, polisacáridos iónicos que contienen grupos sulfato, ácidos iónicos, ramnosa, xilosa, galactosa y arabinosa. También se ha reportado que todas las algas contienen celulosa (Hamed et al., 2015). Las algas pardas también contienen ácidos grasos, como el ácido 18:3 α-linolénico y el ácido 20:5 eicosapentaenoico (Abidov et al., 2010).
1.2. Microalgas
Las microalgas se consideran los primeros organismos productores de oxígeno y se estima que se han encontrado en los océanos desde hace tres billones de años. Son responsables de haber transformado la composición de la atmósfera, permitiendo así el desarrollo y evolución de plantas y animales (Tebbani et al., 2014). Las microalgas, también conocidas como fitoplancton, tienen una gran capacidad de adaptación y supervivencia que les ha permitido colonizar la mayoría de los ecosistemas. Se pueden encontrar en aguas termales, hielo, agua con elevadas concentraciones de sal o acidez, cuevas, en simbiosis, e incluso como parásitos (Kim, 2011; Tebbani et al., 2014). Las cianobacterias son también conocidas como algas azul-verde y se suelen clasificar con las algas, específicamente con las microalgas, debido a que poseen similitudes fisiológicas y fotosintéticas. Estas pueden crecer como células individuales o asociadas en cadenas o pequeñas colonias (De Freitas Coêlho et al., 2019; Nicoletti, 2016).
De manera tradicional, las microalgas se clasifican de acuerdo a sus características morfológicas y citológicas, tipo de metabolitos de reserva, pigmentos y componentes de su pared celular (Ścieszka y Klewicka, 2018). Dentro de este grupo se encuentran las diatomeas (Bacillariophyta), dinoflagelados (Dinophyta), flagelados verdes y marrones (Chlorophyta, Prasinophyta, Prymnesiophyta, Cryptophyta, Chrysophyta y Rhaphidiophyta), y las algas azul-verde (Cyanophyta) (Kim, 2011).
En general, las microalgas, tienen tres principales pigmentos: clorofilas, carotenoides y ficobiliproteínas. En cuanto a su morfología, pueden ser esféricas, en forma de media luna, de espiral, gota e incluso en forma de estrella (Tebbani et al., 2014). Estas
diferencias se pueden ver reflejadas en los metabolitos que producen y su utilización. Algunas especies producen compuestos como carotenoides y ácidos grasos, los cuales son importantes para la salud, mientras que otras especies se utilizan en el tratamiento de aguas residuales o en la agricultura como acondicionadores de suelos (Paul et al., 2013).
Entre las microalgas más conocidas se encuentran Chlorella y Arthrospira. Mientras que la primera es una microalga unicelular, la segunda es una cianobacteria filamentosa, multicelular. Ambas microalgas viven en agua dulce y poseen compuestos bioactivos. El nombre de Chlorella proviene del griego chloros y el latín ella, que significa verde y pequeño, respectivamente. Por otra parte, el nombre de Spirulina, que comúnmente se da a Arthrospira, se debe a su forma espiral. Sin embargo, también se han identificado microalgas pertenecientes a este género que presentan una forma lineal. Estas microalgas se denominan comúnmente como algas-cianobacterias de color azul-verdoso (Andrade et al., 2018). Debido a esta denominación, para fines de este trabajo se considerará a A. platensis como una microalga y se incluirá en el apartado de fermentación de microalgas.
2. Fermentación de macroalgas para la obtención de compuestos bioactivos
Para abordar los estudios sobre la fermentación de macroalgas, se han dividido de acuerdo a su clasificación en algas pardas, rojas y verdes. En la tabla I se puede observar un resumen de las especies de algas y microorganismos utilizados, así como las condiciones de fermentación y el resultado obtenido en varios estudios.
2.1. Fermentación de algas pardas
Las algas pardas son el grupo de algas más estudiado para llevar a cabo distintos tipos de fermentación. La mayoría de autores han realizado una fermentación ácido-láctica (Mun et al., 2017), utilizando Lactobacillus plantarum (Gupta et al., 2011; Nemoto et al., 2017; Takei et al., 2017), Lactobacillus brevis (Lee et al., 2010; Cha et al., 2011; Kang, et al., 2011; Kang et al., 2012; Lee et al., 2013) o mezclas de 2 o más lactobacilos (Uchida et al., 2007; Shobharani et al., 2013; Eda et al., 2016; Kuda et al.,
2016; Mun et al., 2017). Algunos autores las han utilizado para la obtención de ácido butírico (Oh et al., 2019) y carotenoides (Leyton et al., 2019). Mientras que otros han buscado mejorar su capacidad antiinflamatoria (Lin et al.,2016; Lee et al., 2011 y Mun et al. 2017).
Algunos autores han demostrado que es posible obtener polisacáridos con diferente bioactividad mediante el proceso de fermentación. Tal es el caso del trabajo realizado por DeZoysa et al. (2008), quienes obtuvieron polisacáridos sulfatados con capacidad anticoagulante mediante la fermentación de Sargassum fulvellum. Sin embargo, los polisacáridos obtenidos requirieron mayor concentración (180 mg/ml) que la heparina (60 mg/ml) para tener el mismo tiempo de coagulación en el tiempo de tromboplastina parcial activado (attp). Por otra parte, Lee et al (2011) reportaron la obtención de polisacáridos con capacidad antiinflamatoria mediante la fermentación de Ecklonia cava Además, observaron un aumento en el contenido de carbohidratos, proteína cruda y lípidos, pero una disminución en el contenido de polifenoles. En otro estudio con la misma alga, se obtuvieron polisacáridos con efecto radio protector, el cual disminuyó la apoptosis de esplenocitos expuestos a radiación ionizante (Lee et al., 2013).
Asimismo, es posible mejorar la capacidad antioxidante de las algas mediante la fermentación. Presentándose solo un resultado contradictorio por parte de Takei et al. (2017), quienes no fueron capaces de fermentar las algas Sargassum fusiforme y Eisenia bicyclis. Los autores mencionan que la elevada concentración de compuestos fenólicos presentes en las algas pardas pudo haber tenido un efecto antimicrobiano, afectando el proceso de fermentación. Dichos autores cuantificaron el contenido de polifenoles y capacidad antioxidante de las algas sin fermentar, obteniendo un contenido de polifenoles de 0.6 y 0.8 mmol pge/l, respectivamente. Ambas algas tuvieron un porcentaje de inhibición de dpph del 60-80 %, el cual fue similar a los resultados con el método de frap, siendo valores que mostraron una correlación positiva con el contenido de polifenoles. Sin embargo, los resultados con el método orac fueron muy bajos en ambas muestras (10-40 %).
Obtención de compuestos bioactivos y enzimas a partir de la fermentación de algas
Fermentación de macroalgas para la obtención de diversos compuestos
Tipo de algas Especie
Chorda filum
Origen del alga
Península Noto
Dictyopteris polypodioides Karachi, Pakistán
Isla Jeju, Corea del Sur
Ecklonia cava
Algas pardas
Ecklonia kurome
Ecklonia stronifera
Fucus vesiculosus
Laminaria digitata
Laminaria japonica
Laminaria saccharina
Microorganismo
Lactobacillus
plantarum AN6 y Lactococcus lactis subsp. lactis Noto-SU1
Bacillus licheniformis, Aspergillus flavus y Aspergillus terreus
Candida utilis, Lactobacillus brevis y Saccharomyces cerevisiae
No se menciona C. utilis
Península Noto
Península Noto
L. plantarum AN6 y L. lactis subsp. lactis Noto-SU1
L. plantarum AN6 y L. lactis subsp. lactis Noto-SU1
Praia Norte, Viana do Castelo, Portugal Aspergillus niger psh y Mucor sp.
Irlanda L. plantarum atcc 8014
Busan, Corea del Sur L. brevis BJ20
Costa Yantai, Shandong, China Yarrowia lipolytica
Quemoy, Taiwán Bacillus subtilis
Irlanda L. plantarum atcc 8014
Condiciones de fermentación
Resultado obtenido
30 °C por 2 d ↑ capacidad antioxidante
Fermentación de sustrato sólido y sumergida
30 °C por 4 d (hongos)
37 °C por 24 h (bacteria)
30 °C, agitación de 1,200 rpm por 24 h
30 °C, agitación de 120 rpm por 4 d
Enzimas pectinolíticas
Referencia
(Kuda et al., 2016)
(Pervez et al., 2017)
Polisacárido con capacidad anti inflamatoria (Lee et al., 2011)
↑ polifenoles ↑ capacidad antioxidante (Wijesinghe et al., 2012)
30 °C por 2 d ↑ capacidad antioxidante (Kuda et al., 2016)
30 °C por 2 d ↑ capacidad antioxidante (Kuda et al., 2016)
Fermentación de sustrato sólido
36 °C por 92 h Enzimas fucoidanasas
(RodríguezJasso et al., 2013)
37 °C por 14 h Es posible llevar a cabo su fermentación (Gupta et al., 2011)
37 °C por 5 d ↑ ácido γaminobutírico (gaba) (Lee et al., 2010)
30 °C por 72 h Oligosacáridos de alginato (Li et al., 2019)
37 °C, agitación de 150 rpm por 72 h ↑ capacidad anti inflamatoria (Lin et al., 2016)
37 °C por 14 h
Es posible llevar a cabo su fermentación (Gupta et al., 2011)
Tabla I.
Fermentación de macroalgas para la obtención de diversos compuestos (continuación)
Tipo de algas Especie
Origen del alga Microorganismo
Macrocystis pyrifera Puerto Montt, Chile Rhodotorula mucilaginosa
Sargassum fusiforme
Península de Miura
L. plantarum Miura-SU1 y L. lactis subsp. lactis Miura-SU2
Sargassum fulvellum Isla Jeju, Corea del Sur No se menciona
Sargassum horneri
Saccharina japonica
Península de Miura
L. plantarum Miura-SU1 y L. lactis subsp. lactis Miura-SU2
Seúl, Corea del Sur 13 cepas de Clostridium tyrobutyricum
Sargassum sp. Costa oeste de India
Algas pardas
Sargassum thunbergii
Pediococcus Acidilactici, Weissella paramesenteroides, Pediococcus Pentosaceus y Enterococcus faecium
Parajeju, provincia de Jeju, Corea del Sur Lactobacillus sp. SH-1
Sargassum wightii Karachi, Pakistán B. licheniformis, A. flavus y A. terreus
Península de Miura
Península Noto
Undaria pinnatifida
Bahía de Shizugawa, Miyagi, Japón
Tokio, Japón
L. plantarum Miura-SU1 y L. lactis subsp. lactis Miura-SU2
L. plantarum AN6 y L. lactis subsp. lactis Noto-SU1
L. plantarum Sanriku-SU7
L. brevis, L. plantarum, Lactobacillus casei y Lactobacillus rhamnosus
Condiciones de fermentación
Resultado obtenido Referencia
25 °C, agitación de 150 rpm por 3 d Carotenoides (Leyton et al., 2019)
30 °C por 2 d ↑ capacidad antioxidante (Eda et al., 2016)
25 °C por 10 semanas, agitación diaria 200 rpm por 5 min
Polisacáridos sulfatados con actividad anticoagulante
(De Zoysa et al., 2008)
30 °C por 2 d ↑ capacidad antioxidante (Eda et al., 2016)
50 °C por 48 h Ácido butírico (Oh et al., 2019)
Pre-tratamiento enzimático para remover celulosa, incubación a 37 °C por 12 d
↑ polifenoles, ↑ capacidad antioxidante, ↑ anticoagulante
(Shobharani et al., 2013)
30 °C por 2 d ↑ capacidad antiinflamatoria (Mun et al., 2017)
Fermentación de sustrato sólido y sumergida 30 °C por 4 d (hongos) 37 °C por 24 h (bacteria)
Enzimas pectinolíticas (Pervez et al., 2017)
30 °C por 2 d ↑ capacidad antioxidante (Eda et al., 2016)
30 °C por 2 d ↑ capacidad antioxidante (Kuda et al., 2016)
30 °C por 3 d ↑ capacidad antioxidante (Nemoto et al., 2017)
20 °C por 11 d
Es posible llevar a cabo su fermentación (Uchida et al., 2007)
Tabla I.
Tipo de algas
Algas rojas
Fermentación de macroalgas para la obtención de diversos compuestos (continuación)
Especie Origen del alga
Chondrus elatus
Chondrus ocellatus
Gelidiaser sp
Gloiopeltis furcata
Kappaphycus alvarezii
Pyropia sp.
Pyropia yezoensis
Compradas en Suzuki Nori Co., Choshi, Chiba, Japón
Compradas en Suzuki Nori Co., Choshi, Chiba, Japón
Compradas en Suzuki Nori Co., Choshi, Chiba, Japón
Compradas en Suzuki Nori Co., Choshi, Chiba, Japón
Compradas en Suzuki Nori Co., Choshi, Chiba, Japón
Compradas en Suzuki Nori Co., Choshi, Chiba, Japón
Okayama , Japón
Codium tomentosum Karachi, Pakistán
Microorganismo
Bacterias ácido lácticas aisladas de la península de Boso, Japón
Bacterias ácido lácticas aisladas de la península de Boso, Japón
Bacterias ácido lácticas aisladas de la península de Boso, Japón
Bacterias ácido lácticas aisladas de la península de Boso, Japón
Kappaphycus alvarezii
Bacterias ácido lácticas aisladas de la península de Boso, Japón
Tetragenococcus halophilus
B. licheniformis, A. flavus y A. terreus
Condiciones de fermentación
30 °C por 5 d
30 °C por 5 d
Resultado obtenido Referencia
↑ orac, ↑ polifenoles, frap y dpph se mantuvieron constantes (Takei et al., 2017)
↑ orac, ↑ polifenoles, frap y dpph se mantuvieron constantes
30 °C por 5 d ↑ orac, ↑ polifenoles, frap y dpph se mantuvieron constantes
30 °C por 5 d
Fermentación de sustrato sólido
30 °C por 2-6 d
30 °C por 5 d
23 °C por 2 años
Fermentación de sustrato
sólido y sumergida
30 °C por 4 d (hongos)
37 °C por 24 h (bacteria)
↑ orac, ↑ polifenoles, frap y dpph se mantuvieron constantes
↑ polifenoles de 46.93 % para la variedad amarilla, 319.33 % para la variedad verde y 166.29 % la morada.
↑ orac, ↑ polifenoles, frap y dpph se mantuvieron constantes
Salsa de algas fermentadas similar a salsa de soya o salsa de pescado
(Takei et al., 2017)
(Takei et al., 2017)
(Takei et al., 2017)
(Nor et al., 2019)
(Takei et al., 2017)
(Uchida et al., 2017)
Enzimas pectinolíticas (Pervez et al., 2017)
Enteromorpha prolifera Xiamen, China
Monostroma nitidum
Algas verdes
Compradas en Suzuki Nori Co., Choshi, Chiba, Japón
L. acidophilus y S. cerevisiae
Bacterias ácido lácticas aisladas de la península de Boso, Japón
Ulva lactuca Karachi, Pakistán B. licheniformis, A. flavus y A. terreus
Qingdao, China
Ulva prolifera
Qingdao, China
Ulva reticulata Forsskål Nha Trang, Khanh Hoa, Vietnam
Catenovulum sp.
Alteromonas sp. A321
30 °C por 5 d
30 °C por 5 d
Fermentación de sustrato sólido y sumergida
30 °C por 4 d (hongos)
37 °C por 24 h (bacteria)
28 °C por 24 h, 400 rpm, pH inicial 7, aeración 1.5 vvm
28 °C por 24 h, 400 rpm, aeración 1.5 vvm
↑ proteína en alga fermentada, ↑ tamaño de tilapias alimentadas con alga fermentada (Yang et al., 2016)
Polifenoles y capacidad antioxidante se mantuvieron constantes (Takei et al., 2017)
Enzimas pectinolíticas (Pervez et al., 2017)
Enzimas «ulvan» liasas (Qiao et al., 2020)
↑ proteína, ↑ polifenoles y ↑ manitol, ↑ tamaño, peso y grado de verde de la concha de abulones alimentados con el alga fermentada
(Chi et al., 2018)
Halomonas sp. BL6
37 °C por 60 h a 200 rpm
Obtención de piruvato (55.23 g/l) (Anh et al., 2020)
Tabla I.
Por otra parte, el grupo de trabajo de Shobharani et al. (2013) sí pudo llevar a cabo la fermentación. Utilizaron el alga Sargassum spp, y obtuvieron 30.09 ± 1.23 µg gae/mg de polifenoles. También el grupo de Eda et al. (2016) tuvieron éxito con la fermentación de algas utilizando Sargassum horneri, S. fusiforme y Undaria pinnatifida, reportaron un contenido final de polifenoles de entre 0.9 y 1.2 µmol pge/ml. Por otro lado, Kuda et al. (2016) reportaron un contenido de polifenoles <1 µmol pge/ml para Chorda filum, 3 µmol pge/ml para U. pinnatifida, y 8 µmol pge/ ml para Ecklonia stronifera, resultados mayores a los obtenidos por Eda et al. (2016). Mientras que Wijesinghe et al. (2012) analizaron el contenido de polifenoles antes y después de fermentar el alga Ecklonia cava, observaron que la fermentación tuvo un aumento significativo en el contenido de polifenoles. Asimismo, Nemoto et al. (2017) cuantificaron el contenido de polifenoles de distintas partes del alga U. pinnatifida antes de fermentarla, las esporofilas fueron la parte que presentó mayor contenido de polifenoles (21.71 ± 1.05 µmol pge/ml), valores incluso mayores a los obtenidos por Eda et al. (2016) y por Kuda et al. (2016).
Como ya se ha mencionado, la fermentación incrementa el contenido de polifenoles. Además, se ha observado una relación positiva en el contenido de polifenoles y la capacidad antioxidante, cuantificada como porcentaje de inhibición de dpph, tal como lo han reportado Shobharani et al. (2013), Eda et al. (2016) y Kuda et al. (2016). Mientras que Kuda et al. (2016) reportaron 30 y 85 % de inhibición de dpph para las algas U. pinnatifida y E. stronifera , respectivamente; Eda et al. (2016) reportaron 40 % de inhibición para todas las muestras analizadas (S. horneri, S. fusiforme y U. pinnatifida). Wijesinghe et al. (2012) también mencionan que la capacidad antioxidante, cuantificada como porcentaje de inhibición de dpph, aumentó de manera proporcional al contenido de polifenoles. Sin embargo, Nemoto et al (2017) obtuvieron resultados contradictorios, en tanto que no observaron cambios visibles en la capacidad antioxidante (cuantificada como porcentaje de inhibición de dpph). Otro resultado opuesto es el reportado por Takei et al. (2017), quienes cuantificaron la capacidad antioxidante mediante el método de orac. Ellos relacionaron este resultado a que la capacidad para secuestrar radicales de O2 puede estar más relacionada con el contenido de polisacáridos que con el de polifenoles (Takei et al., 2017).
Tal como reportan Shobharani et al. (2013), la fermentación no solo aumenta la capacidad antioxidante cuantificada como porcentaje de inhibición de dpph, sino que el efecto quelante de iones férricos también se ve incrementado. Este grupo de autores reportaron que el control presentó 58.6 % de efecto quelante, a diferencia de las muestras fermentadas, que presentaron un valor de 80-84 %. Otra manera de cuantificar la capacidad antioxidante es mediante el método de frap, utilizado tanto por Eda et al. (2016) como Kuda et al. (2016). El valor más bajo reportado fue 0.75 do a 700 nm para el alga U. pinnatifida (Kuda et al., 2016), mientras que Eda et al. (2016) reportaron una do a 700 nm par a U. pinnatifida, S. horneri y S. fusiforme de 1.0, 1.5 y 1.5, respectivamente, y el mayor valor obtenido fue 2.25 do para E. stronifera (Kuda et al., 2016). A pesar de que ambos grupos de trabajo utilizaron la misma alga parda (U. pinnatifida), esta no provino del mismo sitio de origen, por lo que es factible inferir que esta puede ser una causa de las variaciones en los resultados obtenidos. Otra diferencia en sus estudios fueron las cepas de microorganismos utilizadas para la fermentación, mientras que Kuda et al. (2016) emplearon L. plantarum AN6 y L. lactis subsp. lactis Noto-SU1, Kuda et al (2016), utilizaron L. plantarum Miura-SU1 y L. lactis subsp. lactis Miura-SU2.
Además de estos métodos de capacidad antioxidante, Shobharani et al. (2013) también reportaron el potencial reductor, expresado como µg/mg de ácido ascórbico. Este grupo mencionó que el potencial reductor fue 3.5 veces mayor en las muestras control (8.41 ± 0.29 µg/mg de ácido ascórbico) que en las muestras fermentadas (2.43 ± 0.04). Siendo una de las pocas pruebas en las que la capacidad antioxidante no mejoró con la fermentación. Esto se puede relacionar a que los métodos para capacidad antioxidante tienen distintos mecanismos de acción, y durante la fermentación hay compuestos que pueden ser hidrolizados, disminuyendo su capacidad antioxidante. Tanto Kuda et al. (2016) como Eda et al. (2016) cuantificaron la capacidad antioxidante como actividad secuestradora del radical anión superóxido (O2-) y obtuvieron valores similares, reportando entre 60 y 80 % de inhibición.
2.2. Fermentación de algas rojas
Algunas especies de algas rojas (tabla I) han sido utilizadas para obtener polifenoles con capacidad antioxidante (Takei et al., 2017; Nor et al., 2019) y antiglicante (Eda et al., 2016; Kuda
et al., 2016), así como polisacáridos con actividad anticoagulante (Nikapitiya et al., 2007; Pushpamali et al., 2008) y algunos alimentos, como bebidas fermentadas (Prachyakij et al., 2008), y salsas fermentadas estilo salsa de soya (Uchida et al., 2017) y yogurt (Nuñez y Picon, 2017).
Se ha encontrado que a través de la fermentación es posible mejorar la capacidad antioxidante de distintas algas rojas, tal es el caso de Nor et al. (2019), Eda et al. (2016) y Kuda et al. (2016). A diferencia de estos autores, Takei et al. (2017) reportaron que, a pesar de que la capacidad antioxidante mejoró, en la fermentación de las especies de algas rojas que estudiaron no se observaron mejoras en el contenido de polifenoles, corroborado mediante el método de orac
Para la fermentación de algas rojas se han utilizado diferentes microorganismos. Mientras que Nor et al. (2019) emplearon el hongo Aspergillus oryzae para llevar a cabo una fermentación de sustrato sólido, la mayoría de los autores han optado por una fermentación ácido láctica utilizando diferentes especies de bacterias. Tanto Takei et al. (2017), como Eda et al. (2016) y Kuda et al. (2016) utilizaron L. plantarum, los dos últimos, también utilizaron Lactococcus lactis. A pesar de estas diferencias, todos los estudios reportaron un aumento en el contenido de polifenoles y una mejora en la capacidad antioxidante. Esto demuestra que existe más de una especie de microorganismos capaces de llevar a cabo la fermentación de algas de manera exitosa.
A pesar de que Takei et al. (2017), Eda et al. (2016) y Kuda et al. (2016) realizaron el mismo tipo de fermentación, sus resultados muestran diferencias. Takei et al. (2017) reportaron que las algas Gelidiaser sp y Chondrus elatus tuvieron una baja concentración de polifenoles (< 0.20 y 0.20 mmol pge/l, respectivamente), mientras que las algas C. ocellatus, Pyropia sp y Gloiopeltis furcata tuvieron una concentración de polifenoles de 0.45, 0.70 y 0.80 mmol pge/l, respectivamente. Kuda et al. (2016) reportaron <1 µmol pge/ml para las algas Gelidium elegans y Campylaephora hypnaeoides, y 1.6 µmol pge/ml para el alga Porphyra sp. Para el alga G. elegans, Eda et al. (2016) reportaron <0.4 µmol pge/ml, y para el alga Pyropia sp., 3.5 µmol pge/ml. Las diferencias observadas en el contenido de polifenoles del alga G. elegans pueden deberse a la región donde el alga fue cosechada, Kuda et al. (2016) obtuvieron sus muestras en la región de la península de Noto y Eda et al. (2016) en la región de la península de Miura. Se puede observar —al igual que en las algas pardas— una relación en el contenido de polifenoles y la capacidad antioxi-
dante, reportada como porcentaje de inhibición de dpph. Eda et al. (2016) reportaron <20 % de inhibición de dpph para G. elegans y 60 % de inhibición de dpph, y Takei et al. (2017) reportaron un porcentaje de inhibición de dpph de las algas que estudiaron de entre 10 y 40 %, obteniendo mayores valores para las algas con mayor contenido de polifenoles (Pyropia sp y G. furcata). Sin embargo, en el estudio de Kuda et al. (2016) no se observa esta relación, sino un valor elevado de polifenoles (3.5 µmol pge/ml) en el alga Porphyra sp., pero el porcentaje de inhibición de dpph fue <20 %. En cuanto a los resultados de la prueba frap, Eda et al. (2016) reportaron el valor más elevado (2.5 do a 700 nm) para Pyropia sp., mientras que para G. elegans reportaron <0.5 do a 700 nm, valor similar al observado por Takei et al. (2017) (0.10-0.40 do a 700 nm). Adicionalmente, Takei et al. (2017) reportaron valores elevados de inhibición de O2- (50-90 %), cuantificados mediante orac, resultado que relacionan con el contenido de polisacáridos y no con el de polifenoles.
Referente a la actividad secuestradora del radical anión superóxido (O2-), Kuda et al. (2016) reportaron una inhibición del 50 % para las algas G. elegans, C. hypnaeoides y Porphyra sp, Eda et al. (2016) reportaron, para la misma prueba, <20 % de inhibición para G. elegans y 20 % de inhibición para Pyropia sp Se puede observar que los resultados reportados por Eda et al (2016) fueron considerablemente más bajos que los reportados por Kuda et al. (2016). Sin embargo, una similitud en los resultados de los tres grupos de autores es que los resultados de orac no se relacionan con el contenido de polifenoles, como se ha observado en la inhibición de dpph, sino que tienen una mayor relación al contenido de otros compuestos solubles en agua —como péptidos y productos obtenidos de reacciones de Maillard generadas durante el secado de las algas— (Takei et al., 2017). Finalmente, Eda et al. (2016) y Kuda et al. (2016) mencionaron que el proceso de fermentación mejora las propiedades antiglicantes de las algas rojas que estudiaron, propiedades que se encuentran relacionadas a la capacidad antioxidante y contenido de polifenoles.
El efecto de la fermentación en términos de contenido de polifenoles y capacidad antioxidante se ve afectado tanto por la especie como por la variedad de alga roja utilizada, tal como se observa en el estudio realizado por Nor et al. (2019). Este grupo de autores utilizó el hongo Aspergillus oryzae para fermentar tres variedades del alga roja Kappaphycus alvarezii, la
amarilla, verde y morada. Una de las diferencias que se observó es que la variedad amarilla alcanzó su máxima concentración (4.479 mg gae/g) en el sexto día, mientras que las variedades morada y verde alcanzaron su máxima concentración en el cuarto día (4.037 y 10.022 mg gae/g, respectivamente). También se puede resaltar que, a pesar de que antes de la fermentación todas las algas presentaron un contenido similar de polifenoles (1.5-2 mg gae / g), la fermentación favoreció especialmente el aumentó en el contenido de polifenoles en la variedad verde. Esta variedad tuvo un aumento del 319.33 %, mientras que las variedades amarilla y morada aumentaron un 46.93 % y 166.29 %, respectivamente. Estas diferencias podrían deberse a los pigmentos de cada variedad de alga y a cómo estos afectan el rendimiento de los microorganismos fermentadores.
A diferencia del contenido de polifenoles, la capacidad antioxidante reportada como porcentaje de inhibición de dpph mostró una tendencia similar para las tres variedades. La capacidad antioxidante aumentó gradualmente hasta el cuarto día, para después disminuir. Sin embargo, la variedad verde fue la que presentó mayor inhibición del radical dpph (72.47 %). Tanto en esta variedad como en la morada se observó una fuerte correlación entre el contenido de polifenoles y la capacidad antioxidante, R2 = 0.951 y R2 = 0.823 (p < 0.01), a diferencia de la variedad amarilla, que mostró una correlación menor (R2 = 0.441). Otros autores han demostrado que es posible obtener polisacáridos sulfatados con capacidad anticoagulante mediante la fermentación de las algas. Nikapitiya et al. (2007) utilizaron el alga roja Grateloupia filicina, mientras que Pushpamali et al. (2008) utilizaron las algas Lomentaria catenata, Gracilaria verrucosa, Gloiopeltis furcata y Gracilaria textorii. En ambos estudios, los autores realizaron una fermentación «natural» por 10 semanas. Para ello, mezclaron alga con sacarosa y agua, e incubaron la mezcla a 25 °C. Nikapitiya et al. (2007) encontraron que el tiempo de tromboplastina parcial (aptt) aumentaba de manera significativa (p < 0.05) con el tiempo de fermentación hasta la sexta semana y después disminuía. De acuerdo con Pushpamali et al. (2008), las algas obtuvieron su mayor tiempo de aptt en menor tiempo (cuarta semana) y no hubo disminución con el transcurso de las semanas, como lo reportaron Nikapitiya
et al. (2007). De igual manera, se pueden observar diferencias en el tiempo de coagulación, siendo menor para G. verrucosa con 38.6 segundos (Pushpamali et al., 2008), G. textorii con 49.1 (Pushpamali et al., 2008), G. furcata con 51.7 (Pushpamali et al., 2008), seguidas de G. filicina con 800 segundos (Nikapitiya et al., 2007). El alga que presentó el mayor tiempo de coagulación en la prueba de aptt fue L. catenata con >1000 segundos (Pushpamali et al., 2008). Todas las algas presentaron mayor tiempo de coagulación que los controles utilizados (36.8 segundos).
Los autores de ambos estudios mencionan que, con la fermentación, el contenido de galactanos sulfatados aumenta, teniendo como consecuencia un incremento en la actividad anticoagulante de las algas (Nikapitiya et al., 2007; Pushpamali et al., 2008).
2.3. Fermentación de algas verdes
Las algas verdes han ganado atención como fuente renovable para la obtención de diversos productos. A pesar del gran potencial de estas algas, su utilización se ha limitado mayormente a la producción de etanol (Anh et al., 2020). Sin embargo, algunos autores han estudiado la posibilidad de obtener diversos compuestos valiosos. Este es el caso de Anh et al. (2020), quienes analizaron la obtención de piruvato mediante la fermentación de varias algas (tabla I), entre ellas Ulva lactuca. Mientras que Chi et al. (2018) usaron el alga Ulva prolifera para examinar el efecto de su fermentación en el crecimiento de abulón. La fermentación de algas verdes (Enteromorpha prolifera) también ha sido utilizada para mejorar el crecimiento de tilapia, como estudiaron Yang et al. (2016).
Vemos que la fermentación de algas verdes no se ha enfocado en la obtención de compuestos bioactivos. Solo un grupo de investigación (Takei et al., 2017) ha estudiado el uso de algas verdes (Monostroma nitidum y Ulva sp. [tabla I]) para mejorar su capacidad antioxidante. El contenido de polifenoles de ambas algas fue <0.2 mmol PGE/l, el porcentaje de inhibición de dpph (20 %), y los resultados del frap (<0.2 do a 700 nm), valores que los autores consideraron muy bajos. Sin embargo, presentaron buen porcentaje de inhibición de O2- (orac), 60 y 90 % para M. nitidum y Ulva sp., respectivamente. Únicamente fue posible realizar la fermentación de M. nitidum
3. Fermentación de microalgas para la obtención de compuestos bioactivos
La mayoría de los estudios observan la fermentación de la microalga A. platensis, también conocida como Spirulina. Distintos autores se han enfocado en mejorar su perfil bioactivo mediante el aumento de la capacidad antioxidante (Choi et al., 2018; Wang et al., 2018; De Marco Castro et al., 2019; Niccolai et al., 2019), así como en disminuir el aroma y los off-flavors de la micro-
Especie Microorganismo
Arthrospira platensis
Pavlova lutheri
Lactobacillus plantarum,
Lactobacillus acidophilus y Bacillus subtilis
L. plantarum atcc 8014
L. plantarum
L. plantarum HY-08
Hansenula polymorpha
Candidia rugopelliculosa
Condiciones de fermentación
37 °C por 24 h
37 °C por 72 h
37 °C por 72 h
37 °C por 96 h
37 °C por 3, 6 y 12 d
33.57 °C, 236.38 rpm, pH 6.17 y 23.82 h
alga, los cuales dificultan su utilización (Bao et al., 2018). Otra microalga que ha sido estudiada es Pavlolva lutheri. Esta se ha empleado para obtener péptidos bioactivos, así como para estudiar su capacidad antioxidante en macrófagos de ratón y células humanas. En la tabla II se pueden observar las microalgas más estudiadas, así como los microorganismos utilizados para su fermentación, las condiciones del proceso de la fermentación y el resultado obtenido.
Resultado obtenido Referencia
↑ hidrolisis proteica (30 %), mejora del perfil de aroma y color (Bao et al., 2018)
↑ polifenoles, ↑ capacidad antioxidante (Niccolai et al., 2019)
↑ polifenoles, ↑ capacidad antioxidante, ↑ metionina libre (De Marco Castro et al., 2019)
↑ carotenoides, ↑ capacidad antioxidante y perfil neuroprotectivo (Choi et al., 2018)
↑ capacidad antioxidante modificación del perfil de aminoácidos (Qian et al., 2012)
Péptidos de cadena corta (Ryu et al., 2012)
Algunos autores, como Qian et al. (2012), Ryu et al. (2012) y Bao et al. (2018), han reportado cambios en el perfil de aminoácidos. A pesar de que Qian et al. (2012) y Ryu et al. (2012) utilizaron la misma microalga (P. lutheri) para sus estudios, no utilizaron los mismos microorganismos para llevar a cabo su fermentación; Hansenula polymorpha en el caso de Qian et al. (2012) y Candidia rugopelliculosa en el caso de Ryu et al. (2012). Esta diferencia puede ser una de las causas de que presenten resultados opuestos en el perfil de aminoácidos del alga fermentada. En ambos casos se reportaron aumentos en el ácido aspártico, arginina, fenilalanina, prolina, histidina y tirosina. Así como disminuciones en el contenido de lisina, isoleucina, treonina y ácido glutámico. Sin embargo, Qian et al. (2012) reportaron un aumento en alanina, valina, leucina y prolina; con una disminución en serina y glicina. Mientras que Ryu et al. (2012) reportaron un aumento en serina, glicina, metionina, cisteína y triptófano, y una disminución en alanina, valina y leucina. A pesar de estas diferencias, coincidieron en observar una mejora en la capacidad antioxidante del alga fermentada.
Otro estudio realizado por Bao et al. (2018) analizó el cambio en el perfil de aminoácidos en A. platensis, reportando que, al realizar una fermentación acido-láctica, se observó un aumento en el contenido de arginina y una disminución en alanina y ácido glutámico. Estos autores también mencionan que, al
Fermentación de microalgas para la obtención de diversos compuestos
Tabla II.
fermentar la microalga, el contenido de lípidos totales disminuyó; sin embargo, el contenido de ácidos grasos aumentó de 6 a 19 %. Adicionalmente, la microalga cambió de verde oscuro a un verde claro y el aroma mejoró.
Bao et al. (2018) utilizaron 2 cepas de L. plantarum, 2 cepas de L. acidophilus y una cepa de Bacillus subtilis, obteniendo los mejores resultados al combinar una cepa de L. plantarum. y B. subtilis para la fermentación de A. platensis. A diferencia de Bao et al. (2018), otros autores que han realizado fermentación ácido-láctica en A. platensis únicamente han utilizado L. plantarum (Choi et al., 2018; De Marco Castro et al., 2019; Niccolai et al., 2019). Todos ellos registraron resultados similares, con un aumento en el contenido de polifenoles (De Marco Castro et al., 2019; Niccolai et al., 2019) y de carotenoides (Choi et al., 2018), así como una mejora en la capacidad antioxidante.
Niccolai et al. (2019) reportaron que el contenido de polifenoles aumentó de 4.5 a 18.9 mg gae/g después de dos días de fermentación y, después de 72 horas, disminuyó a 10.9 mg gae/g. Por su parte, De Marco Castro et al. (2019) reportaron que el mayor contenido de polifenoles se dio a las 36 horas, con un 17.87 ± 0.77 mg gae/g, resultado similar al obtenido por Niccolai et al. (2019). Además, De Marco Castro et al. (2019) observaron el mayor contenido de ficocianina (187.0 ± 3.79 µg de ficocianina/mg) a las 36 horas; mientras que Choi et al. (2018) se enfocaron en el contenido de carotenoides y reportaron que este fue mayor cuando el alga fue fermentada (1.62 ± 0.22 mg/g).
En cuanto a la capacidad antioxidante, reportada como inhibición de dpph, Niccolai et al. (2019) reportaron que mejoró, de 20.5 ± 1.7 a 36.6 ± 1.2 % al finalizar las 72 horas. Además, identificaron dos compuestos (ácido láctico L-3-[4-hidroxifenil] y ácido láctico L-indol-3) producidos por L. plantarum, que presentaron propiedades antioxidantes, concluyendo que sea una de las posibles causas de la mejora en la capacidad an-
tioxidante de la microalga fermentada. Por su parte, De Marco Castro et al. (2019) obtuvieron la mayor inhibición de dpph (21.00 ± 0.8 %) a las 24 horas. Además, cuantificaron la capacidad antioxidante mediante frap y orac, registrando los valores más elevados de frap y orac a las 36 horas, 482.00 ± 6.02 µg te/g (b.s.) y 66.14 ± 1.09 µmol te/g (b.s.), respectivamente. Mientras que Choi et al. (2018) observaron un 49.01 % de inhibición de dpph, el cual es considerablemente mayor al reportado por los otros autores (De Marco Castro et al., 2019; Niccolai et al., 2019).
4. Fermentación de macroalgas para la obtención de enzimas
Se ha observado la obtención de enzimas mediante fermentación en algas pardas (Pervez et al., 2017), rojas (Nor et al., 2019) y verdes (Rodríguez-Jasso et al., 2013; Pervez et al., 2017; Qiao et al., 2020). Para ello, las algas funcionan como sustrato. Las enzimas obtenidas pueden tener diversos fines; las proteasas alcalinas son empleadas como detergente (Abidi et al., 2008), para la obtención de etanol para biocombustibles (Zhang et al., 2018) o para desarrollar fertilizantes agroquímicos (Wang et al., 2016).
Todos los grupos de autores concuerdan en la importancia de controlar las condiciones de fermentación, como el pH inicial, la temperatura y el tiempo. Adicionalmente, algunos han estudiado la agitación, concentración inicial de sustrato y pretratamiento del alga. Sin embargo, la mayoría reporta diferencias en cuanto a las condiciones óptimas para la producción de enzimas. Los valores reportados del pH inicial en los diferentes sistemas de fermentación se encuentran en un rango de 5-7 (Pervez et al., 2017; Zhang et al., 2018; Zhang et al., 2019; Qiao et al., 2020). Estas diferencias de pH pueden estar relacionadas con el microorganismo empleado para la fermentación, ya que las bacterias (Catenovolum sp lp y Bacillus licheniformis kibge-ib4) por lo general tienen un mejor desarrollo en ambientes neutros y alcalinos, a diferencia
de los hongos y levaduras (Meyerozyma guilliermondii) que prefieren un ambiente ligeramente ácido (tabla I). Otro factor importante es la temperatura de fermentación, la cual puede estar relacionada con el tipo de microorganismo empleado, así como la enzima objetivo de cada investigación. Pervez et al. (2017) determinaron que la temperatura óptima en su estudio fue 37 °C, mientras que Qiao et al. (2020) obtuvieron mejores resultados al iniciar la fermentación a 32 °C y después disminuirla a 28 °C.
Para la obtención de las enzimas celulasa, xilanasa y β-glucosidasa, así como diferentes compuestos bioactivos, Nor et al. (2019) estudiaron tres variedades del alga roja K. alvarezii. Todas mostraron una tendencia similar en la producción de enzimas, sin embargo, a diferencia del contenido de polifenoles y capacidad antioxidante, donde la variedad amarilla presentó los valores más bajos, esta variedad presentó el mayor contenido de celulasa (270 U/ml) y de xilanasa (75 U/ml). La variedad verde presentó el mayor contenido de polifenoles y porcentaje de inhibición de dpph, así como los valores más bajos de xilanasa y celulasa (50 y 150 U/ml, respectivamente). La β-glucosidasa fue la única enzima en la que no se observó esta tendencia, con 14 U/ml, a diferencia de la variedad amarilla, que presentó 11 U/ml, y la variedad morada, 8 U/ml. Estas diferencias se atribuyen a que la β-glucosidasa puede estar relacionada con la liberación de compuestos fenólicos.
La fermentación para la obtención de enzimas puede llevarse a cabo mediante sustrato sólido (ssf, por sus siglas en inglés), es decir en una matriz sólida con bajo contenido de agua libre, o sumergida (smf, por siglas en inglés) (tabla I). Si bien varios autores han obtenido resultados exitosos con la fermentación ssf, Pervez et al. (2017) compararon ambos (ssf y smf), y observaron un mayor contenido de pectinasa al utilizar fermentación sumergida (2500 U/mg) en comparación con la fermentación de sustrato sólido (1500 U/mg). Encontraron que el microorga-
nismo (Bacillus licheniformis kibge-ib4) se desarrollaba con mayor velocidad en un medio líquido en comparación de un medio sólido, lo que favorecía la producción de enzimas.
CONCLUSIONES Y COMENTARIOS FINALES
Las macro y microalgas son organismos mediante los cuales se pueden obtener diversos compuestos. La mayoría de los estudios han demostrado que la fermentación ácido-láctica puede ser muy útil, ya que puede ser utilizada para casi todas las algas, tanto micro como macroalgas. También vemos que es posible utilizar distintos hongos o levaduras. El microorganismo a utilizar dependerá del objetivo de la fermentación y las características del alga. Mientras que la mayoría de los autores se han enfocado en el contenido de polifenoles y su capacidad antioxidante, también se ha demostrado que es posible obtener polisacáridos, los cuales también pueden presentar actividad bioactiva. De igual manera, se han utilizado las algas como sustrato para la obtención de enzimas. Sin embargo, se puede observar que es un área en la que hay un gran potencial para mayores investigaciones, ya que la mayoría de los estudios hasta el momento se han enfocado en la utilización de las algas pardas y de la microalga A. platensis
AGRADECIMIENTOS
La autora A. Pérez-Alva agradece a la Universidad de las Américas Puebla (udlap) y al Consejo Nacional de Humanidades, Ciencia y Tecnología (conahcyt) —hoy Secretaría de Ciencia, Humanidades, Tecnología e Innovación (secihti)—, por el financiamiento para sus estudios de doctorado.
REFERENCIAS
Abidi, F., Limam, F. y Nejib, M. M. (2008). «Production of alkaline proteases by Botrytis cinerea using economic raw materials: Assay as biodetergent». Process Biochemistry, 43(11), 1202-1208. https://doi.org/10.1016/j.procbio. 2008.06.018
Abidov, M., Ramazanov, Z., Seifulla, R. y Grachev, S. (2010). «The effects of XanthigenTM in the weight management of obese premenopausal women with non-alcoholic fatty liver disease and normal liver fat». Diabetes, Obesity and Metabolism, 12(1), 72-81. https://doi.org/10.1111/j.14631326.2009.01132.x
Amorim, K., Lage-Yusty, M.-A. y López-Hernández, J. (2012). «Changes in bioactive compounds content and antioxidant activity of seaweed after cooking processing». CyTA - Journal of Food, 10(4), 321-324. https://doi. org/10.1080/19476337.2012.658871
Amorim-Carrilho, K., Lage-Yusty, M. A. y López-Hernández, J. (2014). «Variation of bioactive compounds in dried seaweed Himanthalia elongata subjected to different culinary processes». CyTA - Journal of Food, 12(4), 336-339. https:// doi.org/10.1080/19476337.2013.877082
Andrade, L., De Andrade, C. J., Dias, M., Nascimento, C. y Mendes, M. (2018). «Chlorella and Spirulina Microalgae as sources of functional foods, nutraceuticals, and food supplements; an overview». MOJ Food Processing & Technology, 6(1), 00144.
Anh, H. T. L., Kawata, Y., Tam, L. T., Thom, L. T., Ha, N. C., Hien, H. T. M., Thu, N. T. H., Huy, P. Q. y Hong, D. D. (2020). «Production of pyruvate from Ulva reticulata using the alkaliphilic, halophilic bacterium Halomonas sp. BL6». Journal of Applied Phycology, 32, 2283-2293. https://doi.org/ 10.1007/s10811-020-02035-1
Bao, J., Zhang, X., Zheng, J.-H., Ren, D.-F. y Lu, J. (2018). «Mixed fermentation of Spirulina platensis with Lactobacillus plantarum and Bacillus subtilis by random-centroid optimization». Food Chemistry, 264, 64-72. https://doi. org/10.1016/j.foodchem.2018.05.027
Cha, J.-Y., Lee, B.-J., Je, J.-Y., Kang, Y.-M., Kim, Y.-M. y Cho, Y.-S. (2011). «GABA-enriched fermented Laminaria japonica protects against alcoholic hepatotoxicity in sprague-dawley rats». Fisheries and aquatic sciences, 14(2), 79-88. https:// doi.org/10.5657/FAS.2011.0079
Chi, Y., Qiao, L., Zuo, S., Yan, H., Du, C., Hwang, H. y Wang, P. (2018). «Submer-
ged liquid fermentation of Ulva prolifera Müller tissue and applications for improving growth performance in juvenile abalone (Haliotis discus hannai Ino)». Journal of Applied Phycology, 30(4), 2639-2647. https://doi. org/10.1007/s10811-018-1413-6
Choi, W. Y., Kang, D. H., Heo, S.-J. y Lee, H. Y. (2018). «Enhancement of the neuroprotective effect of fermented Spirulina maxima associated with antioxidant activities by ultrasonic extraction». Applied Sciences, 8(12), 2469. https://doi. org/10.3390/app8122469
Chye, F. Y., Ooi, P. W., Ng, S. Y. y Sulaiman, M. R. (2018). «Fermentation-derived bioactive components from seaweeds: functional properties and potential applications». Journal of Aquatic Food Product Technology, 27(2), 144-164. https://doi.org/10.1080/10498850.2017.1412375
De Freitas Coêlho, D., Lacalendola Tundisi, L., Santos Cerqueira, K., Da Silva Rodrigues, J. R., Gava Mazzola, P., Basile Tambourgi, E. y Rodrigues de Souza, R. (2019). «Microalgae: cultivation aspects and bioactive compounds». Brazilian Archives of Biology and Technology, 62, e19180343. https://doi.org/10.1590/1678-4324-2019180343
De Marco Castro, E. de M., Shannon, E. y Abu-Ghannam, N. (2019). «Effect of fermentation on enhancing the nutraceutical properties of Arthrospira platensis (spirulina)». Fermentation-Basel, 5(1), 28. https://doi.org/ 10.3390/fermentation5010028
De Zoysa, M., Nikapitiya, C., Jeon, Y.-J., Jee, Y. y Lee, J. (2008). «Anticoagulant activity of sulfated polysaccharide isolated from fermented brown seaweed Sargassum fulvellum». Journal of Applied Phycology, 20(1), 67-74. https:// doi.org/10.1007/s10811-007-9182-7
Eda, M., Kuda, T., Kataoka, M., Takahashi, H. y Kimura, B. (2016). «Anti-glycation properties of the aqueous extract solutions of dried algae products harvested and made in the Miura Peninsula, Japan, and effect of lactic acid fermentation on the properties». Journal of Applied Phycology, 28(6), 3617-3624. https://doi. org/10.1007/s10811-016-0891-7
Erkmen, O. y Bozoglu, T. F. (2016). «Basic principles of food fermentation». En Erkmen, O. y Bozoglu, T. F., Food Microbiology: Principles into Practice (pp. 228-252). India Wiley. https://doi.org/10.1002/9781119237860.ch39
Gupta, S., Abu-Ghannam, N. y Scannell, A. G. M. (2011). «Growth and kinetics of Lactobacillus plantarum in the fermentation of edible Irish brown seaweeds». Food and Bioproducts Processing, 89(4), 346-355. https:// doi.org/10.1016/j.fbp.2010.10.001
Hamed, I., Özogul, F., Özogul, Y. y Regenstein, J. M. (2015). «Marine bioactive compounds and their health benefits: a review». Comprehensive Reviews in Food Science and Food Safety, 14(4), 446-465. https://doi.org/10.1111/ 1541-4337.12136
Kang, Y. M., Lee, B.-J., Kim, J. I., Nam, B.-H., Cha, J.-Y., Kim, Y.-M., Ahn, C.-B., Choi, J.-S., Choi, I. S. y Je, J.-Y. (2012). «Antioxidant effects of fermented sea tangle (Laminaria japonica) by Lactobacillus brevis BJ20 in individuals with high level of γ-gt: a randomized, double-blind, and placebo-controlled clinical study». Food and Chemical Toxicology, 50(3-4), 1166-1169. https://doi. org/10.1016/j.fct.2011.11.026
Kang, Y.-M., Qian, Z.-J., Lee, B.-J. y Kim, Y.-M. (2011). «Protective effect of GABA-enriched fermented sea tangle against ethanol-induced cytotoxicity in HepG2 Cells». Biotechnology and Bioprocess Engineering, 16(5), 966-970. https:// doi.org/10.1007/s12257-011-0154-z
Kim, S. K. (Ed.). (2011). Handbook of Marine Macroalgae: Biotechnology and Applied Phycology. India: John Wiley & Sons.
Kuda, T., Eda, M., Kataoka, M., Nemoto, M., Kawahara, M., Oshio, S., Takahashi, H., y Kimura, B. (2016). «Anti-glycation properties of the aqueous extract solutions of dried algae products and effect of lactic acid fermentation on the properties». Food Chemistry, 192, 1109-1115. https://doi.org/10.1016/j. foodchem.2015.07.073
Lee, B.-J., Kim, J.-S., Kang, Y. M., Lim, J.-H., Kim, Y.-M., Lee, M.-S., Jeong, M.-H., Ahn, C.-B. y Je, J.-Y. (2010). «Antioxidant activity and γ-aminobutyric acid (GABA) content in sea tangle fermented by Lactobacillus brevis BJ20 isolated from traditional fermented foods». Food Chemistry. 122(1), 271-276 https://doi. org/10.1016/j.foodchem.2010.02.071
Lee, W., Ahn, G., Lee, B.-J., Wijesinghe, W. a. J. P., Kim, D., Yang, H., Kim, Y. M., Park, S. J., Jee, Y. y Jeon, Y.-J. (2013). «Radio-protective effect of polysaccharides isolated from Lactobacillus brevis-fermented Ecklonia cava». International Journal of Biological Macromolecules, 52, 260-266. https://doi. org/10.1016/j.ijbiomac.2012.10.004
Lee, W.-W., Ahn, G., Wijesinghe, W. A. J. P., Yang, X., Ko, C.-I., Kang, M.-C., Lee, B.-J. y Jeon, Y.-J. (2011). «Enzyme-assisted extraction of Ecklonia cava fermented with Lactobacillus brevis and isolation of an anti-inflammatory polysaccharide». Algae, 26(4), 343-350. https://doi.org/10.4490/algae.2011.26.4.343
Leyton, A., Flores, L., Mäki-Arvela, P., Lienqueo, M. E. y Shene, C. (2019). «Macrocystis pyrifera source of nutrients for the production of carotenoids by a marine
yeast Rhodotorula mucilaginosa». Journal of Applied Microbiology, 127(4), 1069-1079. https://doi.org/10.1111/jam.14362
Li, S.-Y., Wang, Z.-P., Wang, L.-N., Peng, J.-X., Wang, Y.-N., Han, Y.-T. y Zhao, S.-F. (2019). «Combined enzymatic hydrolysis and selective fermentation for green production of alginate oligosaccharides from Laminaria japonica». Bioresource Technology, 281, 84-89. https://doi.org/10.1016/j.biortech.2019.02.056
Lin, H.-T. V., Lu, W.-J., Tsai, G.-J., Chou, C.-T., Hsiao, H.-I. y Hwang, P.-A. (2016). «Enhanced anti-inflammatory activity of brown seaweed Laminaria japonica by fermentation using Bacillus subtilis». Process Biochemistry, 51(12), 1945-1953. https://doi.org/10.1016/j.procbio.2016.08.024
Martins, S., Mussatto, S. I., Martínez-Avila, G., Montañez-Saenz, J., Aguilar, C. N. y Teixeira, J. A. (2011). «Bioactive phenolic compounds: production and extraction by solid-state fermentation. A review». Biotechnology Advances, 29(3), 365-373. https://doi.org/10.1016/j.biotechadv.2011.01.008
Mun, O.-J., Kwon, M. S., Karadeniz, F., Kim, M., Lee, S.-H., Kim, Y.-Y., Seo, Y., Jang, M.S., Nam, K.-H. y Kong, C.-S. (2017). «Fermentation of Sargassum thunbergii by kimchi-derived Lactobacillus sp. sh-1 attenuates lps-stimulated inflammatory response via downregulation of jnk». Journal of Food Biochemistry, 41(2), e12306. https://doi.org/10.1111/jfbc.12306
Navarrete-Bolaños, J. L. (2012). «Improving traditional fermented beverages: how to evolve from spontaneous to directed fermentation». Engineering in Life Sciences, 12(4), 410-418. https://doi.org/10.1002/elsc.201100128
Nemoto, M., Kuda, T., Eda, M., Yamakawa, H., Takahashi, H. y Kimura, B. (2017). «Protective Effects of Mekabu aqueous solution fermented by Lactobacillus plantarum sanriku-su7 on human enterocyte-like HT-29-luc cells and dssinduced murine ibd model». Probiotics and Antimicrobial Proteins, 9(1), 48-55. https://doi.org/10.1007/s12602-016-9226-x
Niccolai, A., Shannon, E., Abu-Ghannam, N., Biondi, N., Rodolfi, L. y Tredici, M. R. (2019). «Lactic acid fermentation of Arthrospira platensis (spirulina) biomass for probiotic-based products». Journal of Applied Phycology, 31(2), 10771083. https://doi.org/10.1007/s10811-018-1602-3
Nicoletti, M. (2016). «Microalgae nutraceuticals». Foods, 5(3), 54. https://doi. org/10.3390/foods5030054
Nikapitiya, C., Zoysa, M. D., Jeon, Y.-J., Lee, J. y Jee, Y. (2007). «Isolation of sulfated anticoagulant compound from fermented red seaweed Grateloupia filicina» Journal of the World Aquaculture Society, 38(3), 407-417. https:// doi.org/10.1111/j.1749-7345.2007.00112.x
Nor, N. M., Haiyee, Z. A., Razak, W. R. W. A. y Muhammad, S. K. S. (2019). «Enhancement and bioavailability of phenolic content in Kappaphycus alvarezii through solid substrate fermentation». Malaysian Journal of Fundamental and Applied Sciences, 15(6), 867-871. https://doi.org/10.11113/mjfas.v15n6.1455
Nuñez, M. y Picon, A. (2017). «Seaweeds in yogurt and quark supplementation: influence of five dehydrated edible seaweeds on sensory characteristics». International Journal of Food Science & Technology, 52(2), 431-438. https://doi.org/10.1111/ijfs.13298
Oh, H. J., Kim, K.-Y., Lee, K. M., Lee, S.-M., Gong, G., Oh, M.-K. y Um, Y. (2019). «Enhanced butyric acid production using mixed biomass of brown algae and rice straw by Clostridium tyrobutyricum atcc25755». Bioresource Technology, 273, 446-453. https://doi.org/10.1016/j.biortech.2018.11.037
Paul, S. N. A., Tseng, C. K. y Borowitzka, M. M. (2013). «Seaweed and microalgae». En J. S. Lucas y P. C. Southgate, Aquaculture: Farming Aquatic Animals and Plants (pp. 268-293). John Wiley & Sons, Ltd. https://doi. org/10.1002/9781118687932.ch13
Pervez, S., Shahid, F., Aman, A. y Qader, S. A. U. (2017). «Algal biomass: a sustainable, economical and renewable approach for microbial production of pectinolytic enzymes using submerged and solid state fermentation techniques». Biocatalysis and Biotransformation, 35(6), 442-449. https:// doi.org/10.1080/10242422.2017.1364731
Prachyakij, P., Charernjiratrakul, W. y Kantachote, D. (2008). «Improvement in the quality of a fermented seaweed beverage using an antiyeast starter of Lactobacillus plantarum dw3 and partial sterilization». World Journal of Microbiology and Biotechnology, 24(9), 1713-1720. https:// doi.org/10.1007/s11274-008-9662-1
Pushpamali, W. A., Nikapitiya, C., Zoysa, M. D., Whang, I., Kim, S. J. y Lee, J. (2008). «Isolation and purification of an anticoagulant from fermented red seaweed Lomentaria catenata». Carbohydrate Polymers, 73(2), 274-279. https://doi. org/10.1016/j.carbpol.2007.11.029
Qian, Z.-J., Jung, W.-K., Kang, K.-H., Ryu, B., Kim, S.-K., Je, J.-Y., Heo, S.-J., Oh, C., Kang, D.-H., Park, W. S. y Choi, I.-W. (2012). «In vitro antioxidant activities of the fermented marine microalga Pavlova lutheri (haptophyta) with the yeast Hansenula polymorpha». Journal of Phycology, 48(2), 475-482. https:// doi.org/10.1111/j.1529-8817.2012.01117.x
Qiao, L., Yang, X., Xie, R., Du, C., Chi, Y., Zhang, J. y Wang, P. (2020). «Efficient production of ulvan lyase from Ulva prolifera by Catenovulum sp. lp based on stage-controlled fermentation strategy». Algal Research, 46, 101812. https:// doi.org/10.1016/j.algal.2020.101812
Rodríguez-Jasso, R. M., Mussatto, S. I., Sepúlveda, L., Agrasar, A. T., Pastrana, L., Aguilar, C. N. y Teixeira, J. A. (2013). «Fungal fucoidanase production by solid-state fermentation in a rotating drum bioreactor using algal biomass as substrate». Food and Bioproducts Processing, 91(4), 587-594. https://doi. org/10.1016/j.fbp.2013.02.004
Ryu, B., Kang, K.-H., Ngo, D.-H., Qian, Z.-J. y Kim, S.-K. (2012). «Statistical optimization of microalgae Pavlova lutheri cultivation conditions and its fermentation conditions by yeast, Candida rugopelliculosa». Bioresource Technology, 107, 307-313. https://doi.org/10.1016/j.biortech.2011.12.014
Ścieszka, S. y Klewicka, E. (2018). «Algae in food: a general review». Critical Reviews in Food Science and Nutrition, 59(21), 1-10. https://doi.org/10 1080/10408398.2018.1496319
Shobharani, P., Halami, P. M. y Sachindra, N. M. (2013). «Potential of marine lactic acid bacteria to ferment Sargassum sp. For enhanced anticoagulant and antioxidant properties». Journal of Applied Microbiology, 114(1), 96107. https://doi.org/10.1111/jam.12023
Spolaore, P., Joannis-Cassan, C., Duran, E. y Isambert, A. (2006). «Commercial applications of microalgae». Journal of Bioscience and Bioengineering, 101(2), 8796. https://doi.org/10.1263/jbb.101.87
Takei, M., Kuda, T., Eda, M., Shikano, A., Takahashi, H. y Kimura, B. (2017). «Antioxidant and fermentation properties of aqueous solutions of dried algal products from the Boso Peninsula, Japan». Food Bioscience, 19, 85-91. https:// doi.org/10.1016/j.fbio.2017.06.006
Tanna, B. y Mishra, A. (2018). «Metabolites unravel nutraceutical potential of edible seaweeds: an emerging source of functional food». Comprehensive Reviews in Food Science and Food Safety, 17(6), 1613-1624. https://doi. org/10.1111/1541-4337.12396
Tebbani, S., Lopes, F., Filali, R., Dumur, D. y Pareau, D. (2014). «Microalgae». En S. Tebbani et al., CO2 Biofixation by Microalgae (pp. 1-22). John Wiley & Sons, Ltd. https://doi.org/10.1002/9781118984475.ch1
Uchida, M., Kurushima, H., Ishihara, K., Murata, Y., Touhata, K., Ishida, N., Niwa, K. y
Araki, T. (2017). «Characterization of fermented seaweed sauce prepared from nori (Pyropia yezoensis)». Journal of Bioscience and Bioengineering, 123(3), 327-332. https://doi.org/10.1016/j.jbiosc.2016.10.003
Uchida, M. y Miyoshi, T. (2013). Algal fermentation—The seed for a new fermentation industry of foods and related products. Japan Agricultural Research Quarterly: JARQ, 47(1), 53-63. https://doi.org/10.6090/jarq.47.53
Uchida, M., Murata, M. y Ishikawa, F. (2007). «Lactic acid bacteria effective for regulating the growth of contaminant bacteria during the fermentation of Undaria pinnatifida (Phaeophyta)». Fisheries Science, 73(3), 694-704. https://doi.org/10.1111/j.1444-2906.2007.01383.x
Wang, M., Chen, L., Liu, Z., Zhang, Z., Qin, S. y Yan, P. (2016). «Isolation of a novel alginate lyase-producing Bacillus litoralis strain and its potential to ferment Sargassum horneri for biofertilizer». MicrobiologyOpen, 5(6), 1038-1049. https://doi.org/10.1002/mbo3.387
Wang, S., Yang, R., Li, H., Jiang, J., Zhang, L., Zhang, Q. y Li, P. (2018). «Evaluation and comparison of in vitro antioxidant activities of unsaponifiable fraction of 11 kinds of edible vegetable oils». Food Science & Nutrition, 6(8), 2355-2362. https://doi.org/10.1002/fsn3.823
Wijesinghe, W. A. J. P., Won-Woo, L., Young-Mog, K., Young-Tae, K., Se-Kwon, K., Byong-Tae, J., Jin-Soo, K., Min-Soo, H., Won-Kyo, J., Ahn, G., Lee, K.-W. y Jeon, Y.-J. (2012). «Value-added fermentation of Ecklonia cava processing by-product and its antioxidant effect». Journal of Applied Phycology, 24(2), 201-209. https://doi.org/10.1007/s10811-011-9668-1
Yang, H., Li, Z.-B., Chen, Q., Li, W.-J., Sun, Y.-Z. y Lu, J. (2016). «Effect of fermented Enteromopha prolifera on the growth performance, digestive enzyme activities and serum non-specific immunity of red tilapia (Oreochromis mossambicus × Oreochromis niloticus)». Aquaculture Research, 47(12), 4024-4031. https://doi.org/10.1111/are.12856
Zhang, W., Xia, X. y Zhang, Z. (2019). «Alginate lyase of a novel algae fermentation strain». Chemical and Biochemical Engineering Quarterly, 33, 125-131. https://doi.org/10.15255/CABEQ.2018.1291
Zhang, W.. Zhang, Z., Bao, L., Zang, X. y Cui, H. (2018). «Alcohol dehydrogenase of a novel algae fermentation strain Meyerozyma guilliermondii». Chemical and Biochemical Engineering Quarterly, 32(1), 117-123. https://doi. org/10.15255/CABEQ.2016.836
Métodos de sanitización de semillas para consumo directo
*Programa de Doctorado en Ciencia de Alimentos Correo electrónico: abril.garciasn@udlap.mx • mariat.jimenez@udlap.mx y de semillas para germinados
A.E. García-Santiesteban*, E. Palou y M.T. Jiménez-Munguía.
RESUMEN
Las semillas y germinados son productos naturales cuya popularidad ha cobrado importancia entre consumidores debido a sus múltiples beneficios, tanto nutricionales como para la salud. Debido a su origen y cultivo en el campo, son alimentos con baja calidad microbiológica y alta probabilidad de contener microorganismos patógenos. Por ello, para prevenir afecciones a la salud de los consumidores, se han emitido recomendaciones para evitar su contaminación y asegurar el uso de desinfectantes en los casos aplicables. Sin embargo, este esfuerzo ha sido insuficiente. De acuerdo con cifras oficiales, los brotes de enfermedades producidos por el consumo de este tipo de alimentos prevalecen.
El objetivo de este artículo es presentar la información disponible sobre los métodos de sanitización probados, así como su eficacia, en semillas y germinados, con la finalidad de analizar su efectividad, ventajas y desventajas, y mostrar soluciones alternativas a los problemas de inocuidad en este tipo de productos de interés a nivel mundial.
Palabras clave: semillas, germinados, sanitización, Salmonella spp., Escherichia coli, Listeria monocytogenes.
ABSTRACT
Seeds and seed sprouts are natural products whose popularity has grown among consumers due to their many nutritional and health benefits. Given their origin and cultivation in the field, these are products with low microbiological quality and high probability of containing pathogens. In order to prevent health risks to consumers, recommendations have been issued to avoid their contamination. However, this effort has been insufficient. According to official information, disease outbreaks caused by the consumption of these types of foods still prevail.
This article aims to present available information on proven sanitation methods and their effectiveness, for seeds and seed sprouts, in order to analyze their effectiveness, advantages and disadvantages, and to display alternative solutions to this worldwide problem.
Keywords: seeds, sprouts, food safety, sanitization, Salmonella spp., Escherichia coli, Listeria monocytogenes.
INTRODUCCIÓN
Tanto las semillas de consumo directo como los germinados de semillas son alimentos con valor nutricional comprobado. Contienen abundantes vitaminas y minerales, además de altos niveles de proteínas (Ding et al., 2013). Diversos estudios han confirmado sus importantes beneficios a la salud por sus propiedades anticolesterolémicas, antiartríticas y anticancerígenas (Kim et al, 2019; Kumar et al., 2006). Esto ha llevado a un incremento en la demanda y el consumo de semillas y sus germinados; sin embargo, a pesar de sus beneficios, las semillas son alimentos cuyo origen en el campo implica un alto riesgo de contaminación microbiológica con patógenos, por lo que han causado importantes brotes de enfermedades transmitidas por alimentos (eta) (Yang et al., 2013).
Para asegurar su inocuidad, el Departamento de Agricultura de Estados Unidos y la Administración de Alimentos y Medicamentos (usda y fda, respectivamente, por sus siglas en inglés) han emitido manuales de buenas prácticas agrícolas (bpa) para prevenir, en la medida de lo posible, la contaminación de estos alimentos con patógenos, como Salmonella spp., Listeria monocytogenes, Escherichia coli y Bacillus cereus (Kim et al., 2019; Yang et al., 2013). Para el caso específico de los germinados, la fda recomienda la desinfección de las semillas —principal fuente de contaminación— con una solución de hipoclorito de calcio que contenga 20,000 ppm de cloro libre. Sin embargo, este método de sanitización no suele ser utilizado para el grupo de semillas de consumo directo, como semillas de girasol, calabaza o sésamo, entre otras. Esto se debe a que la solución acuosa afecta el contenido de humedad de las semillas, reduciendo su periodo de almacenamiento y ocasionando cambios en detrimento de la calidad sensorial de las mismas. En lugar de ello, para este grupo de semillas se emplean comúnmente métodos térmicos, cuyo principal objetivo es disminuir el contenido de humedad de la semilla para alargar su vida útil y controlar la población microbiana (Himathongkham et al., 2001; Kumar et al., 2006; Yang et al., 2013).
A pesar de estas recomendaciones, de acuerdo con información proporcionada por los Centros para el Control y
Prevención de Enfermedades (cdc, por sus siglas en inglés), cada vez es mayor el número de brotes de eta por consumo de semillas. Se trata de un área de oportunidad importante en el aseguramiento de la inocuidad de estos alimentos, por lo que algunos investigadores se han interesado por el estudio y aplicación de nuevas tecnologías que aseguren una sanitización efectiva, mientras conserva las características nutricionales y sensoriales de las semillas (Himathongkham et al., 2001; Kim et al., 2019; Yang et al., 2013).
La presente revisión busca presentar la información disponible sobre los métodos de sanitización, así como su eficacia, en semillas y germinados, con la finalidad de analizar su efectividad, ventajas y desventajas, y mostrar soluciones alternativas a los problemas de inocuidad en este tipo de productos de interés a nivel mundial.
REVISIÓN BIBLIOGRÁFICA
1. Riesgos microbiológicos asociados con el consumo de semillas
Las principales fuentes de contaminación de las semillas se presentan durante la pre-cosecha y son todas aquellas a las que la semilla se encuentra expuesta durante su cultivo; como el agua de irrigación, heces de animales salvajes, excretas de aves, estiércol de ganado en abonos orgánicos y la propia calidad microbiológica del suelo de cultivo. Todo ello expone a la semilla a un amplio rango de contaminación por microorganismos patógenos (Martínez-Villaluenga et al., 2008; Tamber et al., 2016; Willis et al., 2009; Yang et al., 2013).
Durante la producción, los microorganismos patógenos se introducen en la microbiota de las semillas de diferentes maneras. La práctica frecuente del uso de estiércol como fertilizante representa una opción barata y fácil para mejorar la calidad del suelo. Sin embargo, el estiércol puede contener bacterias patógenas, como Campylobacter spp. y Salmonella spp., las cuales se introducen al suelo y después —por diversos factores— pueden migrar al producto (Yang et al., 2013). Cuando animales domés-
ticos y salvajes tienen acceso al cultivo, la probabilidad de contaminación por patógenos aumenta por la presencia de heces de estos animales. Bacterias patógenas, como Salmonella spp. y E. coli O157:H7, pueden sobrevivir en restos de heces y en el suelo de cultivo por periodos de varios días, incluso meses. Se ha demostrado que Salmonella spp. puede sobrevivir hasta 60 días en heces durante el invierno; mientras que E. coli O157:H7 sobrevive por periodos de hasta 97 días en estiércol y suelo, y hasta 109 días en agua de riego (O’Neill et al., 2011; Yang et al., 2013).
Por otro lado, las características propias de la planta cobran relevancia. Por ejemplo, las semillas de girasol suelen tener mejor calidad microbiológica debido a que la mata puede medir hasta 2 metros de altura. Esta distancia que guarda del suelo le da una ventaja en comparación con semillas cuya planta tiene menor altura y cuya semilla se encuentra más cercana al suelo, como la semilla de chía o de alfalfa (Tamber et al., 2016; Willis et al., 2009).
La etapa de cosecha es otro punto crítico, puesto que durante este proceso las semillas suelen ser extendidas sobre el suelo, quedando expuestas a diversos factores de contaminación, como heces de roedores, aves, animales salvajes, entre otros, aumentando el riesgo de contaminación. Asimismo, tanto el equipo utilizado durante la cosecha como el sitio de almacenamiento y los contenedores en los que las semillas se almacenan o transportan, juegan un papel importante como factor de contaminación. Si estos no han sido adecuadamente lavados o sanitizados, pueden contribuir a la contaminación cruzada de patógenos en las semillas, tanto por presencia de microorganismos provenientes de lotes anteriores como por presencia de heces de roedores y otros animales que suelen introducirse en los mismos en búsqueda de comida (Yang et al., 2013).
1.1. Riesgos microbiológicos presentes en la producción de semillas para consumo directo Debido a que el contenido de humedad de este tipo de semillas, como la de girasol, calabaza, sésamo, chía, lino, entre otras, suele alcanzar niveles superiores al 20 % después de su cosecha, es común someterlas a un proceso térmico de secado con el objetivo
de disminuir su contenido de humedad a menos de 10 %. Este proceso suele involucrar la extensión de las semillas sobre el suelo para secarlas al sol directo, o deshidratarlas en horno con aire forzado, incrementando el riesgo de contaminación y disminuyendo su calidad microbiológica (Tamber et al., 2016; Willis et al., 2009).
En otros casos, la reducción de humedad se realiza junto con el proceso de tostado, el cual involucra un tratamiento térmico que puede no ser efectivo para la eliminación de bacterias, ya que el calor utilizado no siempre se encuentra en un rango de temperatura suficiente para asegurar la inactivación de todas las bacterias patógenas. Esto se debe a que muchas de las propiedades nutricionales, y algunas propiedades sensoriales, de las semillas pueden verse afectadas al utilizar las temperaturas efectivas para la inactivación de microorganismos patógenos (Willis et al., 2009).
Aunque el riesgo microbiológico relacionado con el consumo de este tipo de semillas se encuentra ligado al origen de las mismas, existen pocos datos publicados sobre la calidad microbiológica de semillas secas comestibles. Un estudio realizado en 2009 en Gran Bretaña demostró que el consumo de semillas deshidratadas se asocia con un alto riesgo de salud pública debido a la alta probabilidad de contaminación con Salmonella spp. y E. coli a través de todas sus etapas, desde la producción hasta su consumo (Harvey et al., 2016; Willis et al., 2009).
En los últimos años, se han reportado diversos incidentes con Salmonella relacionados con semillas comestibles y sus productos. Uno de los más grandes —con implicaciones internacionales— se dio en el año 2001 y asociaba el consumo de semillas con Salmonella Typhimurium en Suecia, Noruega, Alemania y Australia (Harvey et al., 2016; Willis et al., 2009). Sin embargo, aunque ese brote encendió las alertas alimentarias a nivel mundial sobre el riesgo que representa este tipo de productos, la incidencia de este tipo de enfermedades por su consumo no ha disminuido. En la tabla I se incluyen los brotes más relevantes de eta relacionados con la ingesta de semillas durante la última década. Como se observa, es importante establecer controles en la producción, métodos de inactivación microbiana y explorar nuevas alternativas para mejorar la inocuidad de las semillas de consumo directo.
Brotes de enfermedades transmitidas por alimentos (eta) durante la última década generados por bacterias tras el consumo de semillas y sus germinados
Escherichia coli (stec O145) 1 3842
Salmonella serotipo I 4,[5],12:i: 140 33
Fenogreco Alemania y Francia cdc, 2020; ecdc, 2010
Mix (alfalfa, rábano, fenogreco y trébol)
Escherichia coli O26 (stec O126) 29 7
coli O12 (stec O121) 19 9
Semilla de girasol en ensaladas preparadas EE. UU., Canadá cdc, 2020
Tabla I.
1.2. Riesgos microbiológicos presentes en la producción de semillas para germinados El germinado de algunas semillas como la alfalfa, el trigo y la soya, entre otras, es de consumo común en diferentes países. Las principales fuentes de contaminación de los germinados se relacionan con los distintos factores a los cuales están expuestas las semillas durante su etapa de producción en el campo (Lorenzo-Leal et al., 2019; Yang et al., 2013).
Durante el proceso de producción de los germinados, las semillas se remojan en agua, posteriormente, se mantienen en condiciones de humedad y temperatura de incubación (20-40 °C) por periodos de 2 a 7 días. Estas condiciones son ideales, no solo para la germinación, sino también para la proliferación bacteriana (Weiss et al., 2007). La etapa de germinación es crítica en el desarrollo de contaminación bacteriana, ya que algunas bacterias presentes en la semilla pueden internalizarse en los tejidos durante su germinación (Thomas et al., 2003; Yang et al., 2013). Diversos estudios han demostrado que la carga microbiana en las semillas suele estar entre 103 y 106 ufc/g, cuenta que puede incrementar entre 102 y 103 ufc/g durante el primer día de germinación, alcanzando poblaciones de hasta 109 ufc/g durante todo el periodo de germinación (Martínez-Villaluenga et al., 2008; Weiss et al., 2007; Yang et al., 2013).
Para prevenir riesgos, la fda recomienda a los consumidores cocinar los germinados para inhibir o eliminar la presencia de bacterias (Weiss et al., 2007; Yang et al., 2013). Sin embargo, se sigue prefiriendo su consumo crudo debido a que se preservan los nutrientes y glucosinolatos que contienen, los cuales son potentes antioxidantes y pueden inducir la apoptosis o muerte celular de células cancerígenas (Bellostas et al., 2007; Yang et al., 2013).
El número de brotes de eta causados por germinados de semillas ha ido en aumento durante la última década, siendo la alfalfa la fuente más común —como se puede observar en la tabla I—. En general, las bacterias patógenas o agentes etiológicos comúnmente asociados con los brotes son Salmonella spp., Escherichia coli O157, y E. coli O104:H4. Sin embargo, también se reporta la presencia de otros patógenos en semillas para germinados, como Aeromonas hydrophila, Bacillus cereus, Listeria monocytogenes, Shigella y Staphylococcus aureus, aunque en menor cantidad (Rosenquist et al., 2005; Thomas et al., 2003; Yang et al., 2013).
Un estudio detallado sobre la flora bacteriana en germinados de alfalfa a la venta en California determinó que, dentro de
la flora nativa, se encuentran bacterias de los grupos Proteobacteriaceae, Enterobacteriaceae y Moraxellaceae. El mismo estudio demostró, además, que las condiciones de crecimiento y germinación de la alfalfa son ideales para el desarrollo de especies patogénicas como E. coli O157:H7 y Salmonella (Loui et al., 2008; Weiss et al., 2007).
2. Métodos térmicos de sanitización de semillas
La temperatura desempeña un papel vital en la afección de los mecanismos de supervivencia de los microorganismos patógenos, por lo que los tratamientos térmicos son efectivos para incrementar la seguridad microbiana de las semillas. En la última década, se han realizado diversos estudios sobre la eficacia de dos tipos de tratamiento térmicos para la inactivación de patógenos: calor seco y calor húmedo (Yang et al., 2013). El primer tipo es más propicio para las semillas de consumo directo, mientras que el segundo ha sido estudiado principalmente en semillas para germinado.
2.1. Tipos de tratamientos térmicos
Las principales variables de control en este tipo de tratamientos son la temperatura y el tiempo, las cuales dependen de factores como el tipo de semilla, su composición y el microorganismo patógeno que se busca inactivar (Yang et al., 2013). Estos tratamientos se pueden clasificar en tratamientos de calor seco y húmedo de acuerdo con el medio y fuente de calor. En la tabla II se comparan los métodos de todos aquellos ensayos donde se obtuvo una reducción mayor a 104 ufc/g del patógeno estudiado en semillas.
2.1.1. Calor seco
Se han observado variables en la eficacia desinfectante del tratamiento de semillas a temperaturas alrededor de 50 °C por periodos prolongados de tiempo —desde varias horas hasta días— (Ding et al., 2013). Una temperatura de 50 °C resultó adecuada para reducir la presencia de E. coli O157:H7 a niveles debajo de los detectables en semillas de rábano, brócoli y alfalfa. Sin embargo, los tiempos de tratamiento necesarios fueron prolongados, variando entre las 17 y 24 horas. Con estas mismas condiciones, no se lograron resultados significativos en la reducción de E. coli O157:H7 en semillas de fríjol mungo (Bari et al., 2010). Asimismo, otro estudio realizado por Hu et al. (2004), reportó una reducción de 105 ufc/g de E. coli y de 103 ufc/g de Salmonella en el mismo tipo de frijol, utilizando una temperatura de 55 °C. De manera similar, Feng et al.
Métodos y condiciones de sanitización que cumplen el criterio del Comité Consultivo Nacional sobre Criterios Microbiológicos para Alimentos (nacmcf) sobre una reducción logarítmica mínima de 104 cfu/g
Método de Sanitizacion Semilla Condiciones de tratamiento Patógenos
Métodos térmicos
Reducción logarítmica (cfu/g)
Referencia
Alfalfa y brócoli 50 °C/17 o 24 h Escherichia coli O157:H7 5 Bari, Sugiyama et al., 2009
Frijol mungo 55 °C/4 d
Calor seco
coli O157:H7 5 Hu et al., 2004
Frijol mungo 55 °C/4 d Salmonella Typhimurium 3 Hu et al., 2004
Alfalfa y brócoli 55 °C/6 d E. coli O157:H7 8 Feng et al., 2007
Alfalfa y brócoli 55 °C/6 d Salmonella Typhimurium 8
Calor húmedo Frijol mungo 85 °C, 40 s/30 s agua fría 2 h agua con 2,000 ppm de cloro
+ Choque térmico Frijol mungo
+ Agentes químicos Alfalfa
+ Irradiación
Ca(OCl)2
EO carvacrol acidificado
Ácido acético gaseoso
Ácido málico
Feng et al., 2007
E. coli O157:H7 y Salmonella spp >6
Bari et al., 2008 Métodos térmicos (calor húmedo) + otro
90 °C, 90 s/30 s agua fría
E. coli O157:H7 y Salmonella spp >6
Métodos térmicos (calor seco) + otro
50 °C/17 h y 1 % ácido oxálico, 0.03 % ácido fítico, 50 % etanol E. coli O157:H7 >5
Rábano y frijol mungo 50 °C/17 h y 1 kGy
Brócoli y alfalfa 50 °C/17 h y 0.25 kGy
coli O157:H7 >6
E. coli O157:H7 >6
Bari, Nei et al., 2010
Bari, Nei et al., 2009
Bari Nei et al., 2009
Bari Nei et al., 2009 Métodos químicos
Alfalfa 10 min Salmonella Stanley 5 Gandhi y Mathews, 2003
Alfalfa 15 min E.
Frijol mungo
O157:H7
Lang et al., 2000
Bang et al., 2011
Sharma et al., 2002
Aplicado en nanoemulsión Salmonella enterica 4 Landry et al., 2006
Rábano y alfalfa 8.7 % (v/v), 55 °C, 3 h E. coli O157:H7 y de Salmonella spp >5 Nei et al., 2011
10 % ácido málico, 1 % tds
coli O157:H7 4* Fransisca et al., 2011
Tabla II.
Métodos de sanitización de semillas para consumo directo y de semillas para germinados
Métodos y condiciones de sanitización que cumplen el criterio del Comité Consultivo Nacional sobre Criterios Microbiológicos para Alimentos (nacmcf) sobre una reducción logarítmica mínima de 104 cfu/g (continuación)
Método de Sanitizacion
plai
Semilla Condiciones de tratamiento Patógenos
Tecnologías emergentes
Reducción logarítmica (cfu/g)
Alfalfa 8 cm, 90 s E. coli O157:H7 >4
Chía 15 s, fluencia 19.35 J/cm2
Berro 300 mpa, 15 min, 4 °C
Referencia
Sharma y Demirci, 2003
Salmonella Typhimurium, E. coli mg1655 y Listeria innocua 6 Wuytack et al., 2003
Alfalfa 650 mpa, 15 min, 20 °C E. coli O157:H7 >5 Neetoo et al., 2008
Salmonella Typhimurium 4 ReyesJurado et al., 2019 aph
Alfalfa 550 mpa, 2 min, 40 °C
sc-co2 Alfalfa 4000 psi, 50 °C, 60 min
Radiaciones ionizantes
coli O157:H7 >5 Neetoo et al, 2009
Shigella flexneri y E. coli lmm1010 4 Wuytack et al., 2003
coli K12 >4 Jung et al. 2009
Germinados de alfalfa 3.3 kGy L. monocytogenes 6 Schoeller et al., 2002
Germinados de alfalfa 0.5 kGy Salmonella enterica >4 Rajkowski et al., 2003
Germinado de brócoli
kGy
Frijol mungo 1 kGy
Bari et al. 2005
monocytogenes 4.57 Bari et al. 2005
Abreviaciones utilizadas: hipoclorito de calcio (Ca(OCl)2), dióxido de cloro (ClO2), aceites esenciales (eo, por sus siglas en inglés), pulsos de luz de alta intensidad (plai), altas presiones hidrostáticas (aph), dióxido de carbono supercrítico (sc-co2).
*En estos estudios se comprobó que, a pesar de las altas reducciones logarítmicas en las poblaciones bacterianas, estas alcanzaron niveles superiores a los 106 cfu/g durante la etapa de germinación de las semillas.
(2007) lograron reducciones de 102 y 108 ufc/g, respectivamente, para Salmonella y E. coli O157:H7, pero utilizando semillas de alfalfa, y tiempos de hasta 6 días (Feng et al., 2007; Hu et al., 2004). Esto indica que es difícil estandarizar las variables de control, ya que la respuesta dependerá, en gran medida, de la composición y estructura de la semilla utilizada, así como del mecanismo de supervivencia aplicado por el patógeno objetivo.
Por otro lado, un tratamiento rápido a temperaturas superiores a los 90 °C durante 90 segundos, seguido de un choque térmico, a 0 °C por 30 segundos, mejoró la desinfección, logrando reducciones de 6.08 ufc/g y 5.3 ufc/g en las poblaciones iniciales de E. coli y Salmonella spp., respectivamente. Este método reportó incluso la inactivación total de dichos patógenos, mientras que los tratamientos a menores temperaturas y tiempos más
Tabla II.
prolongados, alcanzaron reducciones máximas de 4 ufc/g, sin lograr la total inactivación de los patógenos (Bari et al., 2008). Sin embargo, debido a la disminución en las tasas de germinación en temperaturas mayores a 75 °C, este método no es aplicable para su uso en semillas para germinados (Bari, Nei et al., 2009), pero podría utilizarse para semillas de consumo directo.
En el caso particular de semillas para consumo directo, su tostado implica una serie de reacciones de oscurecimiento que, aunque en muchos casos mejoran sus características sensoriales, también afectan la composición química de las semillas. En un estudio realizado en chía sobre el efecto del tostado a diferentes temperaturas (160-200 °C) por 5 a 15 minutos, se demostró que la capacidad de retención de agua de la semilla cambió rápidamente a los 180 °C, indicando que a dicha temperatura se producen cambios químicos en la estructura del mucílago. Estos cambios pueden impactar en las características sensoriales, nutricionales y tecnológicas buscadas en esta semilla para su aplicación en diversas áreas (Song et al., 2018).
En muchos casos, la combinación de diferentes tipos de tratamiento puede llevar no solo a mejores resultados en cuanto a la inactivación microbiológica, sino también respecto a la preservación de las características sensoriales y nutricionales propias del producto. Por ejemplo, la combinación de tratamientos prolongados (17 horas) de calor seco a 50 °C con tratamientos químicos (1 % ácido oxálico, 0.03 % ácido fítico, 50 % etanol) dio como resultado la reducción a niveles no detectables de E. coli O157:H7 inoculada en semillas de alfalfa (mayor a 105 ufc/g), rábano y brócoli, sin comprometer la calidad sensorial de sus germinados. Sin embargo, estas mismas condiciones no fueron suficientes para eliminar completamente el patógeno en semillas de alfalfa y rábano, en cuyos germinados se alcanzó una población de 107 ufc/g de E. coli O157:H7 posterior a su germinación. La aplicación de calor seco bajo estas condiciones, más una dosis de irradiación de 1.0 kGy, eliminó por completo la población de E. coli O157:H7 en semillas de rábano y frijol mungo, mientras que una radiación mínima de 0.25 kGy fue suficiente para eliminar el patógeno en las semillas de brócoli y alfalfa. La combinación de calor seco con radiación a dichas dosis, no afectó significativamente la tasa de germinación de las semillas de alfalfa, brócoli o rábano, pero sí disminuyó el tamaño de los brotes de frijol mungo (Bari, Nei, et al., 2009).
2.1.2. Calor húmedo
Los tratamientos con calor húmedo pueden emplear agua caliente o vapor de agua. La desinfección con agua caliente fue uno de los primeros tratamientos estudiados y aplicados para la sanitización de semillas para germinados. Sin embargo, este tipo de tratamientos muestra una pérdida de viabilidad de la semilla cuando se utilizan tiempos prolongados y temperaturas elevadas (Yang et al., 2013).
Algunos tratamientos con calor húmedo suelen implicar un choque térmico, mientras que otros añaden el uso de algún químico para reforzar el efecto inhibitorio. Un estudio en frijol mungo con un tratamiento con agua caliente a 85 °C por 40 segundos, seguido de la inmersión de la semilla en agua fría por 30 segundos y por 2 horas en agua con 2,000 ppm de cloro, logró una reducción hasta límites no detectables de E. coli O157:H7 y Salmonella spp. Se obtuvo el mismo resultado cuando este frijol fue tratado en agua a 90 °C durante 90 segundos, seguido por la inmersión del mismo en agua fría por 30 segundos. Ambos tratamientos lograron la desinfección de la semilla, sin una reducción significativa en el porcentaje de germinación del frijol mungo (Bari et al., 2010; Bari et al., 2008).
Los tratamientos con calor húmedo pueden ser aplicables, de igual manera, en el germinado, tal como han demostrado algunos estudios (Pao et al., 2008). Sin embargo, el alcance de esta revisión se limita a los métodos de desinfección de las semillas.
3. Métodos químicos
Se han observado un gran número de métodos químicos para la desinfección de semillas, utilizando diversos agentes químicos como cloro, agua electrolizada, ozono y otros compuestos ácidos (Yang et al., 2013). Los agentes químicos más utilizados para la desinfección de semillas suelen tener resultados altamente variables (Ding et al., 2013).
3.1. Cloro, dióxido de cloro e hipoclorito de sodio y de calcio
El cloro es el agente químico más ampliamente utilizado para sanitizar productos frescos. Para el caso específico de las semillas para germinados, la fda recomienda el uso de soluciones de 20,000 ppm de cloro activo, como hipoclorito de calcio (Ca [OCl] 2), durante 15 minutos. Además, recomienda monitorear la calidad microbiológica del agua de irrigación para mitigar los riesgos de eta con relación al consumo de germinados (Yang et al., 2013).
Las semillas de alfalfa inoculadas con Salmonella Stanley y tratadas con 20,000 ppm de Ca(OCl)2 durante 10 minutos a temperatura ambiente, tuvieron una reducción de más de 105 ufc/g de la población inoculada, hasta alcanzar niveles no detectables. Sin embargo, durante la etapa de germinación, la población de este microorganismo alcanzó rápidamente cuentas superiores a 107 ufc/g en germinados de 2 días (Gandhi y Matthews, 2003). Estos resultados se encuentran en concordancia con los reportados por Lang et al. (2000). En ese estudio, las semillas de alfalfa inoculadas con E. coli O157:H7 fueron tratadas por 15 minutos a temperatura ambiente, alcanzando una reducción hasta niveles no detectables; pero estos mismos niveles incrementaron hasta 108 ufc/g durante el germinado, por lo que concluyeron que el tratamiento no logró garantizar la muerte total de los patógenos presentes en la semilla.
Se ha observado también que la inmersión de semillas de trigo y de sus germinados en una solución con una concentración de hipoclorito de sodio con 400 ppm durante 30 minutos, seguida de un enjuague con agua corriente durante 3 minutos, logró una reducción de 1.03 ciclos logarítmicos de E. coli, sin impacto en la capacidad de germinación de las semillas (Tornuk et al., 2011).
En años recientes, se han investigado los efectos de la aplicación de cloro en forma de dióxido de cloro (ClO2), con resultados prometedores en la eliminación de patógenos en semillas para germinados. El ClO2 se diferencia del hipoclorito, no solo en su formulación química, sino también porque se encuentra en estado gaseoso a temperatura ambiente. Bang et al. (2011) utilizaron ClO2 en combinación con un tratamiento térmico, reportando una reducción de 5.9 ciclos logarítmicos de E. coli en semillas de rábano tratadas con 500 µg/ml de ClO2 por 5 minutos, secadas a 45 °C durante 24 horas y, por último, sometidas a un tratamiento térmico con calor seco a 70 °C por 48 horas.
Se ha demostrado que, cuando la carga microbiana inicial es alta, el cloro es inefectivo en la sanitización de alimentos. Semillas de alfalfa, inoculadas con cargas iniciales de 106 ufc/g de E. coli O157:H7, fueron sometidas a tratamientos de lavado con 10 mg/l de ClO2 entre 3 y 10 minutos a 21 °C. La máxima reducción microbiana obtenida bajo estas condiciones fue de 1.24 ciclos logarítmicos. También se observó que la población de E. coli incrementó rápidamente a niveles similares a los del control durante la etapa de germinación de semillas tratadas, por lo que estos resultados se consideran insuficientes para lograr la inocuidad de estas semillas con este método y bajo
estas condiciones (Singh et al., 2003). El tratamiento con una concentración de entre 200 y 20,000 ppm de hipoclorito de sodio (NaOCl), durante 20 minutos, logró una reducción máxima de 1.64 ciclos logarítmicos de E. coli O157:H7 en semillas de rábano. Sin embargo, el conteo incrementó rápidamente a niveles incluso mayores que los del control durante el germinado (Fransisca et al, 2011).
Estos resultados son desalentadores, pues reflejan que una reducción de patógenos en la semilla no garantiza la inocuidad del producto final. Esto se debe a la proliferación de los mismos microorganismos durante el germinado, etapa en la cual la disponibilidad de nutrientes y condiciones físicas del medio favorecen su desarrollo. La superficie propia de cada semilla puede facilitar que algunas células bacterianas se protejan en grietas, poros y escamas; lo cual ocasiona que las soluciones tengan limitaciones para alcanzar todos los sitios de desinfección. Es posible que ahí radique la falta de consistencia y efectividad en los resultados obtenidos de estos métodos, puesto que se observan mayores reducciones en semillas de superficie lisa. Sin embargo, la ventaja de este método radica en que este tipo de tratamientos no tiene ningún efecto en la tasa de germinación de las semillas (Ding et al., 2013).
Considerando estas limitaciones, se están realizando estudios explorando otros posibles tratamientos, como el uso de ozono, aceites esenciales en fase de vapor, agua electrolizada y otros agentes químicos, con el objetivo de mejorar las técnicas convencionales de descontaminación.
3.2 Ozono
El tratamiento con ozono ofrece diversas ventajas, en comparación con los tratamientos químicos convencionales, como su eficacia antimicrobiana a concentraciones relativamente bajas y con cortos periodos de exposición. Además de su descomposición espontánea en O2, la cual permite que al final del proceso no queden residuos químicos que puedan representar un riesgo adicional para la salud o el medio ambiente (Yang et al., 2013).
Un estudio realizado en germinados de alfalfa y de rábano inoculados con Shigella demostró que la inmersión de los germinados en agua con una concentración de ozono de 2 ppm durante 5 minutos logra reducciones <102 ufc/g. Sin embargo, utilizando la misma concentración de ozono en combinación con un 2 % de ácido málico, se maximiza la inhibición de Shigella, por lo que los autores del estudio lo sugieren como
una potencial opción comercial para el control de Shigella en germinados crudos (Singla et al., 2011). A pesar de ello, otro estudio realizado en alfalfa inoculada con E. coli O157:H7 y tratada con ozono en una concentración de 21 ppm no logró una reducción significativa en comparación con el control, a pesar del tiempo de tratamiento (2-64 minutos). Es probable que esto se deba a la rápida disminución de la concentración de ozono tras el contacto con la superficie del germinado. Sin embargo, otro estudio con recirculación de ozono a 60 °C por 3 horas tuvo éxito, al lograr una reducción de 4.8 ciclos logarítmicos de E. coli O157:H7 en semillas de alfalfa (Sharma et al., 2002).
3.3. Agua electrolizada
El agua electrolizada se genera por electrólisis de una solución de NaCl, se puede dividir en alcalina y ácida, dependiendo del pH de la solución, y puede tener diferentes propiedades, como el potencial de óxido-reducción y la concentración del ion Cl en ella (Liu y Yu, 2017). El agua electrolizada ácida (aew, por sus siglas en inglés) es la más investigada como una alternativa novedosa a otros métodos químicos de desinfección. Se caracteriza por un pH menor a 2.7, un alto potencial de óxidoreducción (>1000 mV), concentraciones de Cl de entre 40-90 ppm y un amplio espectro antibacteriano comparado con otros tratamientos antimicrobianos (Yang et al., 2013; Zhang, Lu, Li, Shang, Zhang y Cao, 2011). A pesar de sus ventajas, se ha demostrado que su efecto es limitado sobre E. coli O157:H7 en semillas de alfalfa, cuya reducción alcanzada fue de 2.72 ciclos logarítmicos en tratamientos con constante agitación por 2, 4, 8, 16, 32 y 64 minutos totales (Sharma y Demirci, 2003). Dichos niveles son comparables con el tratamiento clásico con 2000 ppm de hipoclorito de sodio, pero con la desventaja de que el agua electrolizada puede afectar la viabilidad de las semillas debido al pH fuertemente ácido (Fransisca et al., 2011; Len et al., 2002; Liu y Yu, 2017; Yang et al., 2013).
3.4. Aceites esenciales
Los aceites esenciales (eo, por sus siglas en inglés) son compuestos aromáticos derivados de diversas partes de plantas, como flores, brotes, semillas, hojas, ramas, hierbas, madera, frutas y raíces. Su actividad antimicrobiana contra patógenos presen-
tes en alimentos ha sido ampliamente estudiada (Burt, 2004; Lee et al., 2018). Se ha observado que los eo de pimienta, tomillo, romero y orégano han tenido comprobada efectividad contra diferentes cepas, como L. monocytogenes, Staphylococcus aureus, Staphylococcus epidermidis, Micrococcus luteus, Bacillus cereus, E. coli, Pseudomonas aeruginosa, Enterococcus feacalis, Vibrio alginolyticus, Salmonella Typhimurium, Rhizoctonia solani, Macrophomia phaseolina, Salmonella Senftenberg, Aspergillus ochraceus, A. parasiticus, y A. niger (Burt, 2004; Kotan, et al., 2013; Lorenzo-Leal et al., 2019).
Los eo de orégano, tomillo y corteza de canela aplicados en fase vapor demostraron tener una fuerte actividad antibacteriana contra Listeria monocytogenes en medio de cultivo (mic y mlc 78.1 µl/l). Estos mismos aceites aplicados en la superficie de germinados de rábano en concentraciones de 156 µl/l durante 24 horas a 30 °C y 43 % hre, lograron reducciones de L. monocytogenes de hasta 2.1 ciclos logarítmicos. Bajo las mismas condiciones y con una concentración de 625 µl/l se lograron reducciones entre 2.7 y 3 ciclos logarítmicos. Sin embargo, estos resultados no aseguran la inactivación total del patógeno, por lo que su aplicación bajo estas condiciones no asegura la inocuidad de los germinados (Lee et al., 2018). Un estudio realizado con eo de pimienta, tomillo y romero en fase de vapor aplicados en semillas de alfalfa inoculadas con Salmonella Typhimurium y Listeria monocytogenes concluyó que el aceite de tomillo es el más efectivo del grupo para inhibir el crecimiento de ambos patógenos. Con una dosis de 4.0 ml/l se inhibió significativamente el crecimiento de ambas bacterias en las semillas durante su germinación, sin tener ningún efecto negativo en la tasa de germinación o en las propiedades sensoriales de los germinados (Lorenzo-Leal et al., 2019). Estos resultados concuerdan con estudios que demuestran que la aplicación en fase de vapor ejerce actividad antimicrobiana en áreas mayores que en fase líquida. Asimismo, se ha observado que algunos eo son más efectivos contra bacterias y organismos deteriorativos cuando se aplican en fase gaseosa que en fase líquida (Lee et al., 2018; Seo et al., 2015).
Los eo también pueden ser aplicados por medio de nanoemulsiones. Landry et al. (2016) aplicaron carvacrol acidificado (50 mM ácido levulínico) por medio de nanoemulsiones en
semillas de brócoli y de frijol mungo con el objetivo de inactivar Salmonella enterica Enteriditis, previamente inoculada en las semillas. Los resultados mostraron una reducción de 104 ufc/g de Salmonella en frijol mungo y de 102 ufc/g en semilla de brócoli. En el primer caso, no se detectó presencia del patógeno en el germinado de las semillas tratadas por 30 minutos con la nanoemulsión (Landry et al., 2016).
Una de las principales ventajas que ofrecen estos compuestos en su aplicación es que muchos de los aceites estudiados han sido reconocidos como compuestos naturales y seguros, por lo que podrían ser una alternativa que reemplace los conservadores químicos (Lee et al., 2018). Sin embargo, la presencia de olores y sabores fuertes podría ser un obstáculo para su aplicación por sus efectos en las propiedades organolépticas (Lee et al., 2018; Seo et al., 2015; Tyagi et al., 2012).
3.5. Compuestos ácidos
Los compuestos ácidos tienen un alto efecto antimicrobiano atribuido principalmente a la forma disociada de este tipo de moléculas, las cuales se mueven a través de la membrana celular y liberan protones estando ya en el citoplasma, reduciendo así el pH celular, inactivando enzimas intracelulares, inhibiendo mecanismos de transporte de nutrientes y disminuyendo las reservas energéticas de la célula. Este es uno de los mecanismos por los cuales ciertas frutas con altos contenidos de ácidos orgánicos son más resistentes a la contaminación bacteriana (Yang et al., 2013).
El tratamiento de semillas de rábano y de alfalfa con 8.7 % (v/v) de ácido acético en estado gaseoso a 55 °C por un periodo de entre 2 y 3 horas demostró efectividad para reducir poblaciones mayores a 105 ufc/g de E. coli y Salmonella spp. en ambos tipos de semillas. Por otra parte, con 48 horas de tratamiento se obtuvo la inhibición total de E. coli, aun después de la etapa del enriquecimiento. Sin embargo, ninguna de las condiciones estudiadas tuvo éxito en eliminar por completo la población de Salmonella (Nei et al., 2011). A pesar de ello, este tratamiento es más eficiente que el recomendado con 20,000 ppm de hipoclorito de calcio, que como ya se describió previamente, puesto que obtiene reducciones menores a 102 ufc/g para ambas especies. No obstante, el punto débil de la desinfección con compuestos ácidos sigue siendo la etapa de germinación. Otros estu-
dios han comprobado que, a pesar del éxito obtenido, la cuenta microbiana se eleva considerablemente durante la germinación de la semilla (Singh et al., 2005). El uso de ácido peroxiacético (paa) tiene una efectividad similar a la del uso de 20,000 ppm de cloro, con una reducción de Salmonella spp. y E. coli O157:H7 apenas un poco mayor que 1 ciclo logarítmico en semillas de alfalfa tratadas con concentraciones de entre 1-3 % de paa por tiempos variables entre 10 a 20 minutos, sin que se observaran reducciones mayores con el incremento en el tiempo de tratamiento o en la concentración de paa (Rajkowski y Ashurst, 2009). La utilización de ácido láctico al 5 % durante 10 minutos a 42 °C redujo hasta límites no detectables la población de Salmonella spp., sin embargo, esta alcanzó niveles superiores a 107 ufc/g durante la germinación, indicando que la inactivación total de dicho patógeno no se alcanzó (Lang et al., 2000).
Por su parte, Chang et al. (2010) investigaron la eficiencia del ácido caprílico (ac) y monocaprílico (mc) a concentraciones entre 25 y 75 mM, a 4 °C y tiempos entre 30 y 90 minutos, para la desinfección de semillas de alfalfa previamente inoculadas con Salmonella spp. y E. coli O157:H7. Aunque los resultados demostraron que concentraciones mayores y tiempos más prolongados mejoraban la reducción bacteriana, tanto el ac como el mc tenían un efecto bacteriano limitado con una máxima reducción de 1.56 ciclos logarítmicos para E. coli O157:H7 y de 2.56 ciclos logarítmicos para Salmmonella spp (Chang et al., 2010). Con la aplicación de 10 % de ácido málico (am) con 1 % de tds (sulfato de dilauril tiamina), se obtuvo una reducción de E. coli O157:H7 de una población inicial de 104 ufc/g a niveles por debajo de los detectables. Sin embargo, esta misma población aumentó a 107-108 ufc/g tras la etapa de germinación de la semilla (Fransisca et al., 2011).
4. Tecnologías emergentes
Muchos estudios realizados recientemente emplean tratamientos físicos, como altas presiones, irradiación, tratamientos con dióxido de carbono supercrítico (sc-co2), pulsos de luz de alta intensidad, entre otras tecnologías, con el objetivo de reducir o eliminar los patógenos presentes en semillas para germinados y consumo directo. Métodos
4.1. Pulsos de luz de alta intensidad
Los pulsos de luz de alta intensidad (plai), utilizan pulsos de luz de amplio espectro ricos en luz ultravioleta de onda corta (uv-c) para la desinfección de superficies. Se ha probado que resultan más eficientes para la sanitización de alimentos que los tratamientos convencionales con luz uv-c debido a su mecanismo de acción, que actúa sobre la estructura de adn de las bacterias, impidiendo su replicación (Demirci y Keklik, 2012; Gómez-López et al., 2007). Los plai se producen utilizando tecnología que multiplica la potencia de emisión de luz por el almacenamiento de electricidad en un capacitor por periodos de tiempo relativamente largos para, posteriormente, liberarlos en millonésimas de segundo (Fernández Molina et al., 2001; Gómez-López et al., 2007; Rowan, 2019). Los plai fueron aprobados por la fda para la producción, procesamiento y manejo de alimentos, en 1999. La dosis acumulada permitida de uv es de hasta 12 J/cm2 con el espectro de emisión entre 200 y 1100 nm (Demirci y Keklik, 2012; Fernández Molina et al., 2001).
A pesar de que se trata de una tecnología que está siendo ampliamente investigada, no existen suficientes estudios sobre su aplicación en semillas para la inactivación de patógenos (Gómez-López et al., 2007). Uno de los primeros estudios, realizado por Sharma y Demirci (2003), demostró que un tratamiento por 90 segundos a una distancia de 8 centímetros de la fuente logra una reducción mayor a 104 ufc/g en semillas de alfalfa inoculadas con E. coli O157:H7. El modelo matemático desarrollado en este estudio permitió optimizar el proceso para lograr obtener una reducción de hasta 8 ciclos logarítmicos del patógeno estudiado; sin embargo, estas condiciones optimizadas no se comprobaron experimentalmente. Este estudio también demostró que el grosor de la muestra es un factor relevante, dado que una de las variables de estudio fue el grosor de la capa de semillas de alfalfa. Los resultados mostraron que este factor afecta significativamente, reduciendo la efectividad del tratamiento a mayor grosor de la capa distribuida de la muestra.
Kim et al. (2019) estudiaron la aplicación de plai en semillas de rábano y pak choi para la reducción de la cuenta bacteriana de estas semillas. Las condiciones del tratamiento incluyeron
una distancia fija de 20 centímetros de la fuente lumínica y tiempos entre 0-180 segundos (fluencia de 0 a 37.80 J/cm2). El tiempo, 180 segundos, brindó la mejor inhibición bacteriana, con una reducción de 1.41 ciclos log ufc/g de mesófilos aerobios en las semillas de rábano, y 1.78 ciclos log ufc/g en las semillas de pak choi. Ninguna de las condiciones mostró un efectosignificativo en la tasa de germinación de las semillas. Sin embargo, el mayor efecto inhibitorio de bacterias se dio en una fluencia mayor al límite máximo permitido por la fda (12 J/cm2) (Kim et al., 2019). Por su parte, Hwang et al. (2017) estudiaron la aplicación de esta tecnología para la descontaminación de semillas de sésamo, obteniendo una reducción máxima de 1.46 ciclos log ufc/g en semillas cuya carga inicial de mesófilos aerobios se encontraba entre 104-105 ufc/g, con 120 segundos de tratamiento.
Una de las complicaciones que presenta este método es el tipo de equipo disponible para su aplicación, puesto que resulta complicado asegurar la distribución uniforme de los pulsos de luz por todas las caras del alimento. El estudio realizado por Hwang et al. (2017) resulta valioso en este sentido también, puesto que propone un diseño de equipo de flujo continuo para la aplicación de los plai. Sin embargo, se requieren más estudios en equipos con este diseño para comprobar si existe una diferencia significativa en su efecto descontaminante para el caso específico de semillas (Hwang et al., 2017).
Reyes-Jurado et al. (2019) aplicaron la tecnología de plai en semillas de chía inoculadas con Salmonella Typhimurium, obteniendo una reducción de 104 ufc/g con un tratamiento de 15 segundos (19.35 J/cm2). La relevancia de este estudio se debe a que la chía es una semilla cuya desinfección por otros métodos es complicada, ya que una elevada humedad produce la absorción de agua por parte del mucílago contenido en la semilla, lo que lleva a una alteración en las características fisicoquímicas y sensoriales en la semilla. Este es un claro ejemplo de que los plai pueden ser una novedosa alternativa para la desinfección de semillas sin producir cambios en sus propiedades.
Una de las principales desventajas del uso de esta tecnología es el «efecto de sombra» que se da en algunas superficies
rugosas o porosas de los alimentos. Debido a esto, las bacterias encuentran refugio en la topografía característica del alimento, volviendo a este método menos efectivo. Por otro lado, tratamientos prolongados pueden producir un calentamiento en el producto, lo que podría afectar la composición y características de textura del producto (Gómez-López et al., 2007; Sharma y Demirci, 2003).
4.3. Altas presiones hidrostáticas
El uso de altas presiones hidrostáticas (aph) es un método no térmico novedoso, cuya eficacia para inactivar patógenos sin alterar sus propiedades sensoriales y nutricionales en diversos alimentos ha sido comprobada (Rendueles et al., 2011; Yang et al., 2013).
Los primeros estudios para la aplicación de esta tecnología en la descontaminación de semillas fueron realizados por Wuytack et al. (2003) y Ariefdjohan et al. (2006). Una de las principales conclusiones alcanzadas en sus investigaciones fue que la efectividad de los tratamientos con aph se encuentra también en función de la temperatura, presión, tiempo de exposición, pretratamiento y tipo de semilla.
De igual manera, la efectividad del tratamiento de las aph depende de la resistencia que tienen diferentes tipos de bacterias. Esto se ha observado en algunos estudios, como el realizado por Wuytack et al. (2003), donde se obtuvo una reducción de 106 cfu/g de S. Typhiurium, E. coli mg1655 y Listeria innocua con un tratamiento de 300 mpa por 15 minutos, a 4 °C, en semillas de berro. Por su parte, para Shigella flexneri y E. coli lmm1010—cepas resistentes a las presiones— se logró una reducción de 104 cfu/g. La menor reducción lograda con estas condiciones se obtuvo en Staphylococcus aureus con tan solo 102 ufc/g (Wuytack et al., 2003).
La aplicación de plai en semillas de alfalfa demostró que Listeria monocytogenes es más resistente que E. coli O157:H7 a las altas presiones (Ariefdjohan et al., 2006). Mientras que otros estudios comprobaron que un tratamiento en semillas de alfalfa de 650 mpa y 20 °C por 15 minutos, tiene el mismo efecto que uno con 550 mpa, a 40 °C por 2 minutos, para inactivar E. coli O157:H7 (Neetoo et al., 2008; Neetoo et al., 2009). Igual-
mente, en alfalfa se demostró que remojar previamente las semillas mejora la inactivación de E. coli O157:H7 y de Salmonella spp., pero disminuye la viabilidad para germinar en las semillas de alfalfa (Neetoo y Chen, 2010).
4.4. Dióxido de carbono supercrítico (sc-co2)
El efecto bactericida del dióxido de carbono supercrítico (sc-co2) se debe probablemente a la reducción del pH intracelular, provocando la inactivación de enzimas claves para el metabolismo de la célula, disrupción bacteriana y un incremento en la presión interna de la célula, modificaciones en la membrana celular, y la extracción de sustancias intracelulares (Spilimbergo y Bertucco, 2003).
Los estudios que han observado la aplicación de esta tecnología a semillas para germinados reportan mejores resultados con mayores presiones de sc-co2, temperatura o tiempo de tratamiento. Mazzoni et al. (2001) lograron reducciones del 92.8 % (>104 ufc /g) de E. coli K12 inoculada en semillas de alfalfa, utilizando SC-CO2 a 4000 psi y 50 °C por 60 minutos, sin afectar las características de germinación de las semillas. El mismo estudio confirmó que un tratamiento con dicha presión y temperatura, por solo 15 minutos, la inhibición fue mayor al 50 %, por lo que la duración es un factor importante a considerar. De igual manera, se obtiene una reducción de 3.51 ciclos logarítmicos de E. coli O157:H7 con un tratamiento a 15 mpa y 35 °C por 10 minutos, mientras que para lograr reducciones cercanas a 103 ufc/g en colonias de L. monocytogenes y S. Typhimurium fue necesario un tratamiento a 10 mpa a 45 °C por 5 minutos. Por su parte, se logró una reducción de más de 107 ufc/g de estos tres patógenos con un tratamiento a 20 mpa y 45 °C por 15 minutos; sin embargo, bajo estas condiciones la capacidad de germinación disminuyó (Jung et al., 2009).
Los estudios disponibles muestran que el tratamiento con sc-co 2 por sí solo no es capaz de alcanzar una reducción igual o mayor a 105 ufc/g de patógenos en las semillas utilizadas, por lo que no cumple los estándares recomendados por el Comité Consultivo Nacional sobre Criterios Microbiológicos para Alimentos (nacmcf, por sus siglas en inglés) (Yang et al., 2013).
4.5. Radiaciones ionizantes
Las radiaciones ionizantes son tecnologías no térmicas con efectividad comprobada para mejorar la inocuidad de los alimentos, extendiendo su vida de anaquel (Song et al., 2009). Estas incluyen a los rayos gamma producidos por fuentes de cobalto 60 o cesio 137, electrones generados por máquinas como el «e-beam» (haz de electrones) y los rayos X (Komolprasert, 2007). A pesar de diversas controversias, la fda ha aprobado su uso para el tratamiento de semillas con una dosis máxima de 8 kGy (Yang et al., 2013).
Rajkowski et al. (2003) reportaron la inactivación total de Salmonella en germinados de alfalfa procedentes de semillas tratadas con radiación gama y dosis iguales o mayores a 0.5 kGy. Pero esta tecnología ha sido investigada en su aplicación no solo a semillas, sino también al producto ya germinado. Schoeller et al. (2002) realizaron un estudio en germinado de alfalfa, donde obtuvieron reducciones superiores a 106 cfu/g de Listeria monocytogenes con dosis de 3.3 kGy de radiación beta. Los resultados mostraron que dichos tratamientos no generaron cambios en apariencia u olor del alimento. Por su parte, Bari et al. (2005) observaron reducciones de 4.88 y 4.57 ciclos logarítmicos en germinados de brócoli y frijol, respectivamente, tras un tratamiento con 1 kGy.
De igual manera, se ha estudiado la aplicación de esta tecnología en combinación con otras. Bari, Nei et al. (2009) utilizaron la radiación en combinación con un tratamiento térmico para suprimir el crecimiento de E. coli O157:H7 en frijol mungo (tabla II). Cabe mencionar que dicha reducción no fue alcanzada por el tratamiento térmico o por la irradiación por sí solas cuando se probaron por separado.
La principal ventaja de la aplicación de radiación en germinados, aparte de la efectividad en la inactivación de patógenos, es la extensión de la vida útil de estos alimentos debido a la disminución, en general, de microorganismos deteriorativos. Estudios de vida de anaquel en germinados de alfalfa y de brócoli han demostrado que esta extensión puede ser de hasta 10 días utilizando una dosis baja de 2 kGy. Sin embargo, es en su aplicación en la semilla donde se encuentra la principal des-
ventaja, ya que se ha observado que dosis altas de radiación tienen efectos adversos en el porcentaje de germinación, la tasa de rendimiento, así como en la morfología (largo y ancho) del germinado (Rajkowski et al., 2003).
Por otro lado, la aplicación de dosis bajas de radiación (menores a 3 kGy) no altera las características del germinado, ni tiene algún efecto significativo en su germinación. Sin embargo, estas dosis no garantizan la inocuidad del producto germinado. Estudios realizados sobre el efecto de dosis bajas (1 kGy) en semilla de frijol mungo inoculado con E. coli y Salmonella Typhimurium mostraron una reducción de 2.6 ciclos log ufc/g en la semilla, pero esta población alcanzó un recuento de hasta 108 ufc/g tras 48 horas de germinación de las semillas previamente tratadas (Saroj et al., 2007).
CONCLUSIONES Y COMENTARIOS FINALES
Las semillas y sus germinados son productos naturales con muchos beneficios nutricionales y asociados a la salud; sin embargo, su naturaleza los hace proclives a la contaminación con microorganismos patógenos. En atención al elevado riesgo que ello implica, se han emitido varias recomendaciones con el objetivo de mitigar las causas de posibles enfermedades transmitidas por alimentos. Estas recomendaciones se han orientado principalmente hacia la implementación de buenas prácticas de agricultura y manufactura durante su producción, en el caso de las semillas de consumo directo. Para las semillas para germinados, la fda recomienda su sanitización con una solución con 20,000 ppm de hipoclorito de calcio; no obstante, esta práctica tiene una alta variabilidad y limitada eficacia. Así lo respalda el hecho de que, a pesar de su existencia, cada año se reportan enfermedades transmitidas por alimentos, y producidas por patógenos como E. coli, Salmonella spp y Listeria monocytogenes en estos productos.
Dado que los métodos químicos presentan limitaciones debido, por un lado, a su inhabilidad para alcanzar las bacterias escondidas en superficies rugosas de las semillas y, por otro, a que por sus características no pueden ser aplicados en el grupo de semillas de consumo directo, ya que alteran sus propiedades sensoriales, se han buscado otro tipo de tecnologías. Entre las investigadas, los mejores resultados aplicando un solo tipo de tecnología se han obtenido con métodos físicos, especialmente los tratamientos con altas presiones, irradiación y tratamientos térmicos con calor seco a temperaturas cercanas a los 50 °C y prolongados periodos de tiempo. Sin embargo, también hay que considerar que dichos tratamientos no afecten la calidad nutricional de las semillas, ni su capacidad para germinar cuando se trate de semillas para germinados. Tal es el caso de la irradiación de semillas; si bien se ha comprobado su alta efectividad de inactivación microbiana, afecta el crecimiento del brote del germinado en dosis elevadas.
Los mejores resultados obtenidos, considerando la reducción e inactivación total de los patógenos en semillas, ha sido la combinación de dos o más tecnologías, como el tratamiento térmico con posterior irradiación o tratamientos con ozono seguido de irradiación a dosis muy bajas que no afecten la tasa de germinación de las semillas. Estos resultados apuntan a que una posible alternativa a las 20,000 ppm de cloro recomendadas por la fda se encuentre en el diseño y aplicación de alguna de estas combinaciones de tecnologías para lograr asegurar la inocuidad de estos productos.
AGRADECIMIENTOS
La autora del presente artículo agradece a la Universidad de las Américas Puebla (udlap) y al Consejo Nacional de Humanidades, Ciencia y Tecnología (conahcyt) —hoy Secretaría de Ciencia, Humanidades, Tecnología e Innovación (secihti)—, por el financiamiento otorgado para sus estudios en el Doctorado en Ciencia de Alimentos de la udlap
REFERENCIAS
Ariefdjohan, M. W., Nelson, P. E., Singh, R. K., Bhunia, A. K., Balasubramaniam, V. M., y Singh, N. (2006). Efficacy of high hydrostatic pressure treatment in reducing Escherichia coli O157 and Listeria monocytogenes in alfalfa seeds. Journal of Food Science, 69(5), M117-M120. https:// doi.org/10.1111/j.1365-2621.2004.tb10718.x
Bang, J., Kim, H., Kim, H., Beuchat, L. R. y Ryu, J.-H. (2011). Inactivation of Escherichia coli O157:H7 on radish seeds by sequential treatments with chlorine dioxide, drying, and dry heat without loss of seed viability. Applied and Environmental Microbiology, 77(18), 6680-6686. https://doi.org/10.1128/AEM.05715-11
Bari, M. L., Enomoto, K., Nei, D., y Kawamoto, S. (2010). Scale-Up seed decontamination process to inactivate Escherichia coli O157:H7 and Salmonella enteritidis on mung bean seeds. Foodborne Pathogens and Disease, 7(1), 51-56. https:// doi.org/10.1089/fpd.2009.0389
Bari, M. L., Inatsu, Y., Isobe, S., y Kawamoto, S. (2008). Hot Water treatments to inactivate Escherichia coli O157:H7 and Salmonella in mung bean seeds. Journal of Food Protection, 71(4), 830-834. https://doi.org/10.4315/0362-028X-71.4.830
Bari, M. L., Nakauma, M., Todoriki, S., Juneja, V. K., Isshiki, K., & Kawamoto, S. (2005). Effectiveness of irradiation treatments in inactivating Listeria monocytogenes on fresh vegetables at refrigeration temperature. Journal of Food Protection, 68(2), 318-323. https://doi.org/10.4315/0362-028x-68.2.318
Bari, M. L., Nei, D., Enomoto, K., Todoriki, S. y Kawamoto, S. (2009). Combination treatments for killing Escherichia coli O157:H7 on alfalfa, radish, broccoli, and mung bean seeds. Journal of Food Protection, 72(3), 631-636. https://doi.org/10.4315/0362-028X-72.3.631
Bari, M. L., Sugiyama, J., y Kawamoto, S. (2009). Repeated quick hot-and-chilling treatments for the inactivation of Escherichia coli O157:H7 in mung bean and radish seeds. Foodborne Pathogens and Disease, 6(1), 137-143. https://doi.org/10.1089/fpd.2008.0143
Bellostas, N., Kachlicki, P., Sørensen, J. C. y Sørensen, H. (2007). Glucosinolate profiling of seeds and sprouts of B. oleracea varieties used for food. Scientia Horticulturae, 114(4), 234-242. https://doi.org/10.1016/j.scienta.2007.06.015
Burt, S. (2004). Essential oils: Their antibacterial properties and potential applications in foods. International Journal of Food Microbiology, 94(3), 223-253. https://doi.org/10.1016/j.ijfoodmicro.2004.03.022
cdc (Centers for Disease Control and Prevention Foodborne Outbreak). Online Database. 2020. Disponible en: http://www.cdc.gov/foodborneoutbreaks/ Default.aspx. Consultado en febrero 2020
Chang, S., Redondo-Solano, M. y Thippareddi, H. (2010). Inactivation of Escherichia coli O157:H7 and Salmonella spp. On alfalfa seeds by caprylic acid and monocaprylin. International Journal of Food Microbiology, 144(1), 141-146. https://doi.org/10.1016/j.ijfoodmicro.2010.09.011
Demirci, A. y Keklik, N. M. (2012). Process design involving pulsed uv light. En J. Ahmed y M. S. Rahman (ed.), Handbook of food process desing (pp. 11661239). Wiley-Blackwell.
Ding, H., Fu, T.-J. y Smith, M. A. (2013). Microbial contamination in sprouts: How effective is seed disinfection treatment?: seed disinfection for sprouts. Journal of Food Science, 78(4), R495–R501. https://doi.org/10.1111/1750-3841.12064
ecdc (European Center for Disease Prevention and Control). Online Database. 2020. Disponible en: https://www.ecdc.europa.eu/en/publicationsdata?s=food+outbreaks. Consultado en febrero 2020.
Feng, G., Churey, J. J. y Worobo, R. W. (2007). Thermal inactivation of Salmonella and Escherichia coli O157:H7 on alfalfa seeds. Journal of Food Protection, 70(7), 1698-1703. https://doi.org/10.4315/0362-028X-70.7.1698
Fernández Molina, J. J., Barbosa-Cánovas, G. V. y Swanson, B. G. (2001). Tecnologías emergentes para la conservación de alimentos sin calor. Arbor, 168(661), 155170. https://doi.org/10.3989/arbor.2001.i661.827
Fransisca, L., Zhou, B., Park, H. y Feng, H. (2011). The effect of calcinated calcium and chlorine treatments on Escherichia coli O157:H7 87-23 population reduction in radish sprouts. Journal of Food Science, 76(6), M404-M412. https://doi. org/10.1111/j.1750-3841.2011.02270.x
Gandhi, M. y Matthews, K. R. (2003). Efficacy of chlorine and calcinated calcium treatment of alfalfa seeds and sprouts to eliminate Salmonella. International Journal of Food Microbiology, 87(3), 301-306. https://doi.org/10.1016/ S0168-1605(03)00108-9
Gómez-López, V. M., Ragaert, P., Debevere, J. y Devlieghere, F. (2007). Pulsed light for food decontamination: a review. Trends in Food Science & Technology, 18(9), 464-473. https://doi.org/10.1016/j.tifs.2007.03.010
Harvey, R. R., Zakhour, C. M. y Gould, L. H. (2016). Foodborne disease outbreaks associated with organic foods in the United States. Journal of Food Protection, 79(11), 1953-1958. https://doi.org/10.4315/0362-028X.JFP-16-204
Himathongkham, S., Nuanualsuwan, S., Riemann, H. y Cliver, D. O. (2001).Reduction of Escherichia coli O157:H7 and Salmonella Typhimurium in artificially contaminated alfalfa seeds and mung beans by fumigation with ammonia. Journal of Food Protection, 64(11), 1817-1819. https://doi. org/10.4315/0362-028X-64.11.1817
Hu, H., Churey, J. J. y Worobo, R. W. (2004). Heat treatments to enhance the safety of mung bean seeds. Journal of Food Protection, 67(6), 1257-1260. https://doi. org/10.4315/0362-028X-67.6.1257
Hwang, H.-J., Cheigh, C.-I. y Chung, M.-S. (2017). Construction of a pilot-scale continuous-flow intense pulsed light system and its efficacy in sterilizing sesame seeds. Innovative Food Science & Emerging Technologies, 39, 1-6. https:// doi.org/10.1016/j.ifset.2016.10.017
Jung, W. Y., Choi, Y. M. y Rhee, M. S. (2009). Potential use of supercritical carbon dioxide to decontaminate Escherichia coli O157:H7, Listeria monocytogenes, and Salmonella Typhimurium in alfalfa sprouted seeds. International Journal of Food Microbiology, 136(1), 66-70. https://doi.org/10.1016/j. ijfoodmicro.2009.08.014
Kim, S.-M., Hwang, H.-J., Cheigh, C.-I. y Chung, M.-S. (2019). Bactericidal effect of intense pulsed light on seeds without loss of viability. Food Science and Biotechnology, 28(1), 281-287. https://doi.org/10.1007/s10068-018-0456-4
Komolprasert, V. (2007). Packaging for foods treated by ionizing radiation. En J. H. Han (ed.) Packaging for nonthermal processing of food (pp. 87-116). Blackwell Publishing. https://doi.org/10.1002/9780470277720.ch6
Kotan, R., Dadasoğlu, F., Karagoz, K., Cakir, A., Ozer, H., Kordali, S., Cakmakci, R. y Dikbas, N. (2013). Antibacterial activity of the essential oil and extracts of Satureja hortensis against plant pathogenic bacteria and their potential use as seed disinfectants. Scientia Horticulturae, 153, 34-41. https://doi.org/10.1016/j.scienta.2013.01.027
Kumar, M., Hora, R., Kostrzynska, M., Waites, W. M. y Warriner, K. (2006). Inactivation of Escherichia coli O157:H7 and Salmonella on mung beans, alfalfa,
and other seed types destined for sprout production by using an oxychlorobased sanitizer. Journal of Food Protection, 69(7), 1571-1578. https://doi. org/10.4315/0362-028X-69.7.1571
Landry, K. S., Komaiko, J., Wong, D. E., Xu, T., McClements, D. J. y McLandsborough, L. (2016). Inactivation of Salmonella on sprouting seeds using a spontaneous carvacrol nanoemulsion acidified with organic acids. Journal of Food Protection, 79(7), 1115-1126. https://doi.org/10.4315/0362-028X.JFP-15-397
Lang, M. M., Ingham, B. H. y Ingham, S. C. (2000). Efficacy of novel organic acid and hypochlorite treatments for eliminating Escherichia coli O157:H7 from alfalfa seeds prior to sprouting. International Journal of Food Microbiology, 58(1-2), 73-82. https://doi.org/10.1016/S0168-1605(00)00297-X
Lee, G., Kim, Y., Kim, H., Beuchat, L. R. y Ryu, J.H. (2018). Antimicrobial activities of gaseous essential oils against Listeria monocytogenes on a laboratory medium and radish sprouts. International Journal of Food Microbiology, 265, 49-54. https://doi.org/10.1016/j.ijfoodmicro.2017.11.001
Len, S.V., Hung, Y.C., Chung, D., Anderson, J. L., Erickson, M. C. y Morita, K. (2002). Effects of storage conditions and ph on chlorine loss in electrolyzed oxidizing (eo) water. Journal of Agricultural and Food Chemistry, 50(1), 209-212. https://doi.org/10.1021/jf010822v
Liu, R. y Yu, Z.-L. (2017). Application of electrolyzed water on reducing the microbial populations on commercial mung bean sprouts. Journal of Food Science and Technology, 54(4), 995-1001. https://doi.org/10.1007/s13197-016-2445-z
Lorenzo-Leal, A. C., Palou, E. y López-Malo, A. (2019). Evaluation of the efficiency of allspice, thyme and rosemary essential oils on two foodborne pathogens in in-vitro and on alfalfa seeds, and their effect on sensory characteristics of the sprouts. International Journal of Food Microbiology, 295, 19-24. https://doi. org/10.1016/j.ijfoodmicro.2019.02.008
Loui, C., Grigoryan, G., Huang, H., Riley, L. W. y Lu, S. (2008). Bacterial communities associated with retail alfalfa sprouts. Journal of Food Protection, 71(1), 200204. https://doi.org/10.4315/0362-028X-71.1.200
Martínez-Villaluenga, C., Frías, J., Gulewicz, P., Gulewicz, K. y Vidal-Valverde, C. (2008). Food safety evaluation of broccoli and radish sprouts. Food and Chemical Toxicology, 46(5), 1635-1644. https://doi.org/10.1016/j.fct.2008.01.004
Mazzoni, A. M., Sharma, R. R., Demirci, A. y Ziegler, G. R. (2001). Supercritical carbon dioxide treatment to inactivate aerobic microorganisms on alfalfa seeds. Journal of Food Safety, 21(4), 215-223. https://doi.org/10.1111/j.17454565.2001.tb00320.x
Neetoo, H. y Chen, H. (2010). Pre-soaking of seeds enhances pressure inactivation of E. coli O157:H7 and Salmonella spp. on crimson clover, red clover, radish and broccoli seeds. International Journal of Food Microbiology, 137(2-3), 274-280. https://doi.org/10.1016/j.ijfoodmicro.2009.11.026
Neetoo, H., Pizzolato, T. y Chen, H. (2009). Elimination of Escherichia coli O157:H7 from alfalfa seeds through a combination of high hydrostatic pressure and mild heat. Applied and Environmental Microbiology, 75(7), 1901-1907. https://doi.org/10.1128/AEM.02531-08
Neetoo, H., Ye, M. y Chen, H. (2008). Potential application of high hydrostatic pressure to eliminate Escherichia coli O157:H7 on alfalfa sprouted seeds. International Journal of Food Microbiology, 128(2), 348-353. https://doi.org/10.1016/j.ijfoodmicro.2008.09.011
Nei, D., Latiful, B. M., Enomoto, K., Inatsu, Y. y Kawamoto, S. (2011). Disinfection of radish and alfalfa seeds inoculated with Escherichia coli O157:H7 and Salmonella by a gaseous acetic acid treatment. Foodborne Pathogens and Disease, 8(10), 1089-1094. https://doi.org/10.1089/fpd.2011.0901
O’Neill, C. J., Bolton, D. J. y Fanning, S. (2011). Comparative studies on the survival of verocytotoxigenic Escherichia coli and Salmonella in different farm environments. Agriculture, Food and Analytical Bacteriology, 1, 116-122.
Pao, S., Kalantari, A. y Khalid, M. F. (2008). Eliminating salmonella enterica in alfalfa and mung bean sprouts by organic acid and hot water immersions. Journal of Food Processing and Preservation, 32(2), 335-342. https://doi.org/10.1111/ j.1745-4549.2008.00182.x
Rajkowski, K. T. y Ashurst, K. (2009). Use of 1% peroxyacetic acid sanitizer in an air-mixing wash basin to remove bacterial pathogens from seeds. Foodborne Pathogens and Disease, 6(9), 1041-1046. https://doi.org/10.1089/ fpd.2009.0267
Rajkowski, K. T., Boyd, G. y Thayer, D. W. (2003). Irradiation d-values for Escherichia coli O157:H7 and Salmonella sp. on inoculated broccoli seeds and effects of
irradiation on broccoli sprout keeping quality and seed viability. Journal of Food Protection, 66(5), 760-766. https://doi.org/10.4315/0362-028X-66.5.760
Rendueles, E., Omer, M. K., Alvseike, O., Alonso-Calleja, C., Capita, R., y Prieto, M. (2011). Microbiological food safety assessment of high hydrostatic pressure processing: a review. LWT - Food Science and Technology, 44(5), 1251-1260. https://doi.org/10.1016/j.lwt.2010.11.001
Reyes-Jurado, F., Navarro-Cruz, A. R., Méndez-Aguilar, J., Ochoa-Velasco, C. E., Mani-López, E., Jiménez-Munguía, M. T., Palou, E., LóPez-Malo, A. y Ávila-Sosa, R. (2019). High-intensity light pulses to inactivate Salmonella Typhimurium on Mexican chia (Salvia hispanica L.) seeds. Journal of Food Protection, 82(8), 1272-1277. https://doi.org/10.4315/0362-028X.JFP-18-577
Rosenquist, H., Smidt, L., Andersen, S. R., Jensen, G. B. y Wilcks, A. (2005). Occurrence and significance of Bacillus cereus and Bacillus thuringiensis in ready-to-eat food. FEMS Microbiology Letters, 250(1), 129-136. https://doi.org/10.1016/j. femsle.2005.06.054
Rowan, N. J. (2019). Pulsed light as an emerging technology to cause disruption for food and adjacent industries – Quo vadis? Trends in Food Science & Technology, 88, 316-332. https://doi.org/10.1016/j.tifs.2019.03.027
Saroj, S. D., Hajare, S., Shashidhar, R., Dhokane, V., Sharma, A. y Bandekar, J. R. (2007). Radiation processing for elimination of Salmonella Typhimurium from inoculated seeds used for sprout making in india and effect of irradiation on germination of seeds. Journal of Food Protection, 70(8), 1961-1965. https://doi. org/10.4315/0362-028X-70.8.1961
Schoeller, N. P., Ingham, S. C. y Ingham, B. H. (2002). Assessment of the potential for listeria monocytogenes survival and growth during alfalfa sprout production and use of ionizing radiation as a potential intervention treatment. Journal of Food Protection, 65(8), 1259-1266. https://doi.org/10.4315/0362-028X-65.8.1259
Seo, H.-S., Beuchat, L. R., Kim, H. y Ryu, J.H. (2015). Development of an experimental apparatus and protocol for determining antimicrobial activities of gaseous plant essential oils. International Journal of Food Microbiology, 215, 95-100. https://doi.org/10.1016/j.ijfoodmicro.2015.08.021
Sharma, R.R., y Demirci, A. (2003). Inactivation of Escherichia coli O157:H7 on inoculated alfalfa seeds with pulsed ultraviolet light and response surface modeling. Journal of Food Science, 68(4), 1448-1453. https://doi.org/10.1111/j.1365-2621.2003.tb09665.x
Sharma, R. R., Demirci, A., Beuchat, L. R. y Fett, W. F. (2002). Inactivation of Escherichia coli O157:H7 on inoculated alfalfa seeds with ozonated water and heat treatment. Journal of Food Protection, 65(3), 447-451. https://doi. org/10.4315/0362-028X-65.3.447
Singh, B. R., Chandra, M., Agarwal, R. y Babu, N. (2005). Curing of salmonella enterica, serovar typhimurium-contaminated cowpea seeds and sprouts with vinegar and chlorination. Journal of Food Processing and Preservation, 29(3-4), 268277. https://doi.org/10.1111/j.1745-4549.2005.00027.x
Singh, N., Singh, R. K. y Bhunia, A. K. (2003). Sequential disinfection of Escherichia coli O157:H7 inoculated alfalfa seeds before and during sprouting using aqueous chlorine dioxide, ozonated water, and thyme essential oil. LWTFood Science and Technology, 36(2), 235-243. https://doi.org/10.1016/ S0023-6438(02)00224-4
Singla, R., Ganguli, A. y Ghosh, M. (2011). An effective combined treatment using malic acid and ozone inhibits Shigella spp. On sprouts. Food Control, 22(7), 1032-1039. https://doi.org/10.1016/j.foodcont.2010.12.012
Song, H. P., Kim, B., Jung, S., Choe, J. H., Yun, H., Kim, Y. J. y Jo, C. (2009). Effect of gamma and electron beam irradiation on the survival of pathogens inoculated into salted, seasoned, and fermented oyster. LWT - Food Science and Technology, 42(8), 1320-1324. https://doi.org/10.1016/j.lwt.2009.03.018
Song, K. Y., Joung, K. Y., Shin, S. Y. y Kim, Y. S. (2018). Effects of chia (salvia hispanica l.) Seed roasting conditions on quality of cookies. Italian Journal of Food Science, 31(1). https://doi.org/10.14674/IJFS-1198
Spilimbergo, S. y Bertucco, A. (2003). Non-thermal bacterial inactivation with dense CO2. Biotechnology and Bioengineering, 84(6), 627-638. https://doi. org/10.1002/bit.10783
Tamber, S., Swist, E. y Oudit, D. (2016). Physicochemical and bacteriological characteristics of organic sprouted chia and flax seed powders implicated
in a foodborne salmonellosis outbreak. Journal of Food Protection, 79(5), 703-709. https://doi.org/10.4315/0362-028X.JFP-15-529
Thomas, J. L., Palumbo, M. S., Farrar, J. A., Farver, T. B. y Cliver, D. O. (2003). Industry practices and compliance with U.S. Food and Drug Administration guidelines among California sprout firms. Journal of Food Protection, 66(7), 1253-1259. https://doi.org/10.4315/0362-028X-66.7.1253
Tornuk, F., Ozturk, I., Sagdic, O. y Yetim, H. (2011). Determination and improvement of microbial safety of wheat sprouts with chemical sanitizers. Foodborne Pathogens and Disease, 8(4), 503-508. https://doi.org/10.1089/fpd.2010.0709
Tyagi, A. K., Malik, A., Gottardi, D. y Guerzoni, M. E. (2012). Essential oil vapour and negative air ions: A novel tool for food preservation. Trends in Food Science & Technology, 26(2), 99-113. https://doi.org/10.1016/j.tifs.2012.02.004
Weiss, A., Hertel, C., Grothe, S., Ha, D. y Hammes, W. P. (2007). Characterization of the cultivable microbiota of sprouts and their potential for application as protective cultures. Systematic and Applied Microbiology, 30(6), 483-493. https:// doi.org/10.1016/j.syapm.2007.03.006
Willis, C., Little, C. L., Sagoo, S., de Pinna, E. y Threlfall, J. (2009). Assessment of the microbiological safety of edible dried seeds from retail premises in the United Kingdom with a focus on Salmonella spp. Food Microbiology, 26(8), 847-852. https://doi.org/10.1016/j.fm.2009.05.007
Wuytack, E. Y., Diels, A. M. J., Meersseman, K. y Michiels, C. W. (2003). Decontamination of seeds for seed sprout production by high hydrostatic pressure. Journal of Food Protection, 66(6), 918-923. https://doi.org/10.4315/0362-028X-66.6.918
Yang, Y., Meier, F., Ann Lo, J., Yuan, W., Lee Pei Sze, V., Chung, H.J. y Yuk, H.-G. (2013). Overview of recent events in the microbiological safety of sprouts and new intervention technologies: sprout safety and control. Comprehensive Reviews in Food Science and Food Safety, 12(3), 265-280. https://doi. org/10.1111/1541-4337.12010
Zhang, C., Lu, Z., Li, Y., Shang, Y., Zhang, G. y Cao, W. (2011). Reduction of Escherichia coli O157:H7 and Salmonella enteritidis on mung bean seeds and sprouts by slightly acidic electrolyzed water. Food Control, 22(5), 792-796. https://doi. org/10.1016/j.foodcont.2010.11.018