

Temas Selectos de Ingeniería de Alimentos














Volumen 7 / No. 1
Ene –Mayo 2013
DIRECTORIO
TEMAS SELECTOS DE INGENIERÍA DE ALIMENTOS
UNIVERSIDAD DE LAS AMÉRICAS PUEBLA
PUBLICACIÓN SEMESTRAL
VOLUMEN 7, NÚMERO 1 (ENERO - MAYO 2013)
EDITORA RESPONSABLE
María Eugenia Bárcenas Pozos
CONSEJO EDITORIAL
María Teresa Jiménez Munguía
Emma Mani López
María Elena Sosa Morales
Fidel Tomás Vergara Balderas
CERTIFICADO DE RESERVA DE DERECHOS:
04-2010-080615025900-102
CERTIFICADO DE LICITUD DE TÍTULO Y CONTENIDO: 15430
DOMICILIO:

Fundación Universidad de las Américas, Puebla
Ex hacienda Sta. Catarina Mártir S/N
San Andrés Cholula, Puebla. C.P. 72810, México
Teléfono: 222 229 2126
DISTRIBUIDO POR:
Departamento de Ingeniería Química, Alimentos y Ambiental
Fundación Universidad de las Américas, Puebla
IMPRESIÓN:
Talleres gráficos
Universidad de las Amércias Puebla
Ex hacienda Sta. Catarina Mártir S/N
San Andrés Cholula, Puebla. C.P. 72810, México

Temas Selectos de Ingeniería de Alimentos Vol. 7 / No. 1

Cuerpo editorial
Dra. María Eugenia Bárcenas Pozos
Dra. María Elena Sosa Morales
Dra. María Teresa Jiménez Munguía
Dra. Emma Mani López
M. C. Fidel Vergara Balderas

Contenido
Temas Selectos de Ingeniería de Alimentos Vol. 7 / No. 1

Volumen 7 / No. 1 Enero – Mayo 2013
Cuerpo editorial
Artículos de Revisión
Utilización de películas comestibles yciclodextrinas para la liberación controlada de aceites esenciales como agentes antimicrobianos en vegetales
R.H.Hernández-Figueroa,E.PalouyA.López-Malo
Prebióticos: su importancia en la salud humana y propiedades funcionales en tecnología de alimentos
D.Morales-Koelliker*yJ.F.Vélez-Ruíz
El ajo ysus aplicaciones en la conservación de alimentos
D.Bender-Bojalil*yM.E.Bárcenas-Pozos
Mecanismos de transferencia de calor que ocurren en tratamientos térmicos de alimentos
M.E.Pérez-ReyesyM.E.Sosa-Morales
Microencapsulación de compuestos activos con quitosano
I.A.Flores-Belmont*y M.T.Jiménez-Munguía
Vegetales como fuentes de nitritos: una alternativa para el curado de carnes
E.E.Montiel-Flores*,A.López-MaloyM.E.Bárcenas-Pozos
Efecto de la radiación UV-C en frutas y verduras
J.F.Haro-Maza*y J.A.Guerrero-Beltrán
Potencial antimicrobiano de mezclas que incluyen aceites esenciales o sus componentes en fase vapor
M.A.Olivares-Cruz*yA.López-Malo
Propiedades del alginato yaplicaciones en alimentos
G.C.Avendaño-Romero*,A.López-MaloyE.Palou
Artículo de Investigación
Extracción, composición ycaracterización de los aceites esenciales de hoja ysemilla de cilantro (Coriandrum sativum)
E.Leal-Torres*,A.López-MaloyM.E.Sosa-Morales

Editorial
Temas Selectos de Ingeniería de Alimentos Vol. 7 / No. 1

El desarrollo profesional en el área de la ciencia, tecnología en ingeniería de alimentos conlleva el estudio profundo deun sinnúmero de áreas relacionadas con alimentos. Desdelaconservación enfresco,hastalaobtencióndealimentosprocesadospordiferentestecnologías,esnecesarioque éstoscumplanconsucometidoenlaalimentaciónhumana;esdecir,quecontenganlosnutrientes necesarios para el organismo. Es así que, en la actualidad se está tratando de, por un lado, optimizar los procesos de obtención y conservación de alimentos para ofrecer al consumidor alimentos nutricionalmente valiosos en los que se conserven las propiedades funcionales, en muchosdeellos,conprebióticos,enmuchosotros,yademásqueseansabrososyatractivos ypor otro que sean, desde el punto de vista físico, quimio y microbiológicamente seguros y sensorialmente agradables. Lainvestigación actual está enfocada a eso, aobtener alimentos de la más alta calidad nutricional que tenga beneficios a la salud del consumidor. Así, se le ha dado la importancia a los prebióticos y a los alimentos funcionales con características antioxidantes que tengan un plus para el consumidor. El estudio del procesamiento de alimentos por tecnologías tradicionalesyemergentes,eldesarrollodenuevosproductosylaconservaciónenfrescoseestán esforzando para brindar al consumidor alimentos con un procesamiento mínimo para obtenerlos con características lo más parecidas a los frescos. Es así como en el Departamento de Ingeniería
Química, Alimentos y Ambiental (DIQAA) de la Universidad de las Américas Puebla se están haciendo estudios relacionados con alimentos funcionales y con prebióticos, entre otros. Los estudiantes de licenciatura, maestría y doctorado, así como posdoctores están involucrados en la investigación de alimentos o productos para alimentos funcionales y con prebióticos bajo la dirección del grupo de investigación del DIQAA. El esfuerzo y entusiasmo que ponen los estudiantes de licenciatura y posgrado, junto con sus profesores, para la producción de artículos en el área alimentaria es invaluable. Una muestra de ello se presenta en esta entrega de la revista TemasSelectosdeIngenieríadeAlimentos.
José Ángel Guerrero Beltrán
Profesor Departamento de Ingeniería Química, Alimentos y Ambiental Universidad de las Américas Puebla

Temas Selectos de Ingeniería de Alimentos 7 - 1 (2013): 1 -11

Utilización de películas comestibles y ciclodextrinas para la liberación controlada de aceites esenciales como agentes antimicrobianos en vegetales
R. H. Hernández - Figueroa*, E. Palou - García y A. López - Malo
Departamento de Ingeniería Química, Alimentos y Ambiental, Universidad de las Américas Puebla. Ex hacienda Sta. Catarina Mártir S/N, San Andrés Cholula, Puebla. C.P.72810, México.
Resumen
Las exigencias de los consumidores por la demanda de alimentos vegetales más naturales, han generado un esfuerzo por desarrollar tecnologías de conservación que dejen a un lado la utilización de agentes químicos como conservadores. Una alternativa a esto, es el uso de aceites esenciales de especias, los cuales han demostrado tener una capacidad antimicrobiana. Sin embargo, la incorporación directa de estos aceites genera problemas sensoriales en el alimento y la eficiencia de los mismos es baja, debido a la volatilización de sus compuestos activos. Una alternativa a este problema es la utilización de películas comestibles y ciclodextrinas para la liberación controlada de las sustancias activas. El propósito de esta revisión es presentar un panorama general de las investigaciones realizadas acerca del uso de películas comestibles y ciclodextrinas para la liberación controlada de aceites esenciales y su uso para la conservación de vegetales mínimamente procesados.
Palabras clave: vegetales mínimamente procesados, aceites esenciales, películas comestibles, ciclodextrinas.
Abstract
The consumers demands of eating more natural vegetable foods, have led an effort to develop conservation technologies that put aside the use of chemicals as preservatives. An alternative to this is the use of essential oils of spices, which have been shown to have antimicrobial activity. However, the direct incorporation of these oils causes sensory problems in food and the efficiency thereof is low due to volatilization of the active compounds. An alternative to this problem is the use of edible films and cyclodextrins for controlled release of active substances. The purpose of this review is to present an overview of research conducted on the use of edible films and cyclodextrins for controlled release of essential oils and their use for conservation of minimally processed vegetables.
Keywords: minimally processed vegetables, essential oils, edible films, cyclodextrins.
Introducción
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: ricardoh.hernandesf@udlap.mx
Hoy en día el consumo de alimentos vegetales mínimamente procesados ha aumentado de manera considerable, lo cual ha generado un esfuerzo importante en la investigación de nuevas tecnologías de conservación, así como en el desarrollo de nuevos productos. Por otro lado, la industria de estos productos ha experimentado un crecimiento acelerado convirtiéndose en una de las más exitosas en
los últimos años. Este crecimiento se atribuye a la tendencia a ingerir alimentos saludables por parte de los consumidores (Sanford et al., 2008). Sin embargo, los productos vegetales mínimamente procesados son sumamente susceptibles al crecimiento microbiano, limitandodeestamaneralaseguridadylavida de anaquel de estos alimentos. Procesos mínimos como el pelado, picado, cortes en cubos y triturado, generan daño celular y de esta manera favorecen la liberación del contenido líquido del vegetal, el cual, por su alto contenido en ácidos orgánicos y azúcares, representa una buena fuente de nutrientes para el crecimiento debacterias, levaduras ymohos (Ayala et al.,2008a).
En cuanto a la seguridad de los consumidores, en los dos últimos años se identificaron diversos brotes de bacterias patógenas asociadas al consumo de vegetales mínimamente procesados. Se identificaron casos de Salmonella en espinacas, mangos, melones, lechuga y brotes de alfalfa; casos de Escherichia coli O157:H7 en lechugas y espinacas y un brote asociado a Listeria monocytogenes enmelones(CDC,2013).
Los conservadores convencionales o sintéticos adicionados a los vegetales mínimamente procesados, pueden reducir de manera importante la tasa de decaimiento del producto; sin embargo, hoy en día existe un particular interés en el consumo de productos libres de aditivos sintéticos (Ayala-Zavala et al., 2009). Por esta razón, se ha generado un interés particular por la investigación de nuevas tecnologías de conservación, involucrando sustancias naturales que ayuden a extender la vida útil de estos productos y aseguren la inocuidad de los mismos. Una tecnología de preservación para los vegetales mínimamente procesados últimamente estudiada, es la aplicación directa de aceites esenciales provenientes de especias, los cuales han demostrado en numerosos estudios, su actividad antimicrobiana para una amplia
7-1 (2013): 1 - 11
variedad de microorganismos (Lanciotti et al., 2004). Sin embargo, las sustancias activas de los aceites esenciales se evaporan rápidamente, generando de esta manera una limitante para extender la vida de anaquel de los productos. A su vez, el impacto sensorial de la adición directa del aceite esencial en el sabor de los vegetales mínimamente procesados,tienerepercusionesimportantesen la aceptabilidad por parte del consumidor, debido al sabor no característico del vegetal pero característico del aceite esencial añadido (Ayala-Zavala et al., 2008a). Una alternativa para evitar este problema es la incorporación del aceite esencial en películas comestibles (Ávila et al., 2010)ylaencapsulacióndeestos aceite en β-ciclodextrinas (Ayala et al., 2008a), para controlar la liberación de los mismos. Por esta razón, el objetivo del presente artículo de revisión, es la recolección de información acerca de las nuevas tecnologíasbasadasenlaliberacióncontrolada de los aceites esenciales y su aplicación en productosvegetalesmínimamenteprocesados.
Revisión bibliográfica
1. Aceites esenciales ysu efecto antimicrobiano
Los agentes antimicrobianos naturales derivados de fuentes tales como los aceites esenciales de plantas, han sido reconocidos y utilizados como conservadores en alimentos durante siglos. Sin embargo, en los últimos añoslainvestigaciónacercadelaspropiedades antimicrobianas de estas substancias ha aumentado. Los recientes estudios realizados enfocados a cubrir en mayor medida las exigencias de los consumidores, han provocado que las especias y sus aceites esenciales sean utilizados por las industrias de alimentos como agentes naturales de conservación, enfocándose en extender la vida deanaqueldelosproductos,reduciroeliminar
bacterias patógenas e incrementar la calidad general de los alimentos procesados (Tajkarimi et al.,2010).
Un aceite esencial es un líquido concentrado, hidrófobo que contiene una mezcla de compuestos volátiles aromáticos, con características antimicrobianas, comúnmente derivados de tejidos vegetales (Ha et al., 2008). Los aceites esenciales presentan un aroma distintivo a la planta de origen y son comúnmente extraídos por destilación por arrastre con vapor; sin embargo, existen otros métodos de extracción tales como la maceración, prensado en frío o extracción con disolventes. Por otro lado, los compuestos de los aceites esenciales son principalmente cadenas cortas de hidrocarburos complementadas con oxígeno, nitrógeno y/o átomos de azufre, unidos en diversos puntos de la cadena (Braca et al., 2008). Tales mezclas de diferentes moléculas aromáticas con átomos altamente reactivos, otorgan a estas sustancias las diferentes propiedades funcionales que podrían ser consideradas para muchas aplicaciones en la ciencia y tecnología de los alimentos. A su vez, la configuración química de los componentes, la proporción en la cual se encuentran y la interacción entre ellos, afectan las propiedades bioactivas (Fisher y Phillips, 2008). Se ha demostrado en diversas investigaciones, que la actividad antimicrobiana de los aceites esenciales es mayor cuando se utilizan como tales, en comparación a la actividad que presentan sus constituyentes mayoritarios por separado (Marino et al., 1999, 2001; Chang et al., 2008). Esto sugiere que los componentes que se encuentran en menor proporción, no necesariamente tienen un papel importante en laactividadantimicrobianadelaceiteesencial.
En cuanto a su modo de acción, los componentes de los aceites esenciales afectan funciones metabólicas importantes en la célula microbiana, como la respiración o la
producción de toxinas o ácidos; sin embargo, pueden presentar diferente especificidad en función de los sitios activos de la célula microbiana, de acuerdo a la composición de la misma (López-Malo et al., 2005). Por otro lado, se ha demostrado en diversos estudios que los aceites esenciales pueden provocar deterioro importante en la pared celular de los microorganismos, daño en la membrana citoplasmática, daño a las proteínas esenciales de la membrana, filtración de los contenidos celulares, coagulación del citoplasma, agotamiento de las fuerzas motrices de los protones, deterioro en diversos sistemas enzimáticos y cambios en la funcionalidad del material genético de la célula. (López-Malo, 1995: Burt, 2004; Luqman et al., 2007; AyalaZavala et al.,2008a;Gutiérrez et al.,2008a).
La actividad antimicrobiana de diferentes aceites esenciales de especias y hierbas, ha sido evaluada y estudiada en un gran número de investigaciones (Tabla I), demostrando su capacidad para ser una alternativa eficaz a los antimicrobianos tradicionales en el control del crecimiento de diversos microorganismos. Sin embargo, la aplicación directa de la mayoría delos aceites esenciales sevelimitada, debido a que las concentraciones necesarias para lograr un efecto antimicrobiano son lo suficientemente altas para modificar el sabor delos alimentos adicionados con estos aceites, generando de esta manera alteraciones poco agradables y rechazos por parte del consumidor. Los niveles de concentración requeridos no pueden reducirse debido a que los factores como la migración de los compuestos volátiles del aceite esencial hacia el alimento, la reacción de los compuestos del aceite esencial con lípidos, proteínas, carbohidratos y otros aditivos, y la volatilización de los compuestos del aceite esencial debido a las temperaturas de almacenamiento,provocanunadisminuciónen la actividad antimicrobiana de lo aceites esenciales. Ponce et al. (2004) reportaron que el uso de aceites esenciales en productos
vegetales mínimamente procesados afecta de manera importante la aceptabilidad del producto, debido a la migración de olores y sabores provenientes del aceite esencial hacia el producto. De igual forma, Gutiérrez et al. (2009) estudiaron la capacidad antimicrobiana de los aceites esenciales de orégano y tomillo (0.5%,1% y2%),incorporadosdirectamentea lechuga yzanahorias, ysu efecto en la calidad sensorial de estos productos. Los resultados obtenidos por estos investigadores demostraron que estos aceites esenciales son eficaces paramejorarla vidadeanaquel delos vegetales estudiados; sin embargo, la lechuga tratada con aceites esenciales presentó una aceptabilidadmenor,queelproductosinaceite esencial.
Debido a estos problemas, se han generado nuevas tecnologías basadas en la liberación controlada de los aceites esenciales, con el fin degenerarunaalternativaalareducciónenlos atributos de sabor en el alimento debida a la adición de los mismos. Estas tecnologías involucran la utilización de películas comestibles adicionadas con antimicrobiano, y recientemente, la encapsulación de los aceites enciclodextrinas.
2 Liberación controlada deaceites esenciales
2.1 Utilización depelículas comestibles
Las películas comestibles se definen como matrices continuas que pueden ser formadas porproteínas,polisacáridosy/olípidos,conlas cuales se recubren los alimentos para mejorar su vida de anaquel. De igual forma, la utilización de agentes plastificantes y otros aditivos, es parte importante de la formación de las películas, ya que estos componentes modifican las propiedades físicas o funcionales de las mismas, y de esta manera ayudan a mejorar la calidad del recubrimiento en los alimentos. Los mecanismos para la formación de las películas comestibles incluyen la formación de diferentes tipos de
enlaces (covalentes, interacciones hidrofóbicas, fuerzas de Van der Waals y/o interacciones iónicas) entre las cadenas que conforman al polímero, formando una red semirrígidaqueatrapae inmovilizaal solvente (HanyGennadios,2005).
Por otro lado, las películas comestibles se han desarrollado como una nueva tecnología, que no pretende sustituir a los empaques sintéticos diseñados para alimentos, sino actuar como un accesorio que presenta la capacidad de mejorar la calidad de los mismos, ya que los protegen a del deterioro físico, químico y biológico, extendiendo su vida de anaquel y aumentando la eficiencia de los empaques, mediante la incorporación de diversas sustancias que enriquecen sus propiedades funcionales (Kester y Fenemma, 1986). De igual manera, las películas comestibles ayudan a retardar la deshidratación en la superficie del alimento, la absorción de humedad, la oxidación de los ingredientes, la pérdida de aroma, la absorción de aceite durante el freído, así como a controlar la maduración y el deterioro microbiano en el alimento (Han y Gennadios, 2005).
Otra característica de las películas comestibles, es la capacidad que presentan en cuanto a la liberación controlada de sustancias activas. Dependiendo de la aplicación, durante la liberación controlada se requieren diversas velocidades de migración de las sustancias activas al medio, que pueden incluir la liberación inmediata, gradual o lenta, una velocidad específica de liberación o la no migración. Las películas comestibles tienen la capacidad de controlar las velocidades de liberación de manera específica y con ello ayudanaalcanzarlaefectividadmáximadelas funciones de las sustancias activas incorporadas (Han, 2003). Algunas de las sustancias que requieren de una velocidad controlada para alcanzar su máxima eficacia son los antioxidantes, saborizantes, colorantes,
TablaI. Características antimicrobianas de los aceites esenciales.
Vegetal
Ajo (Allium sativum)
Efecto antimicrobiano contra
Constitutyente volatil mayor BacteriasHongosReferencia
Metil disulfuro, alil sulfuro, alil disulfuro, alil trisulfuro, trimetileno trisulfuro, alil tetrasulfuro
Bacillus cereus, Escherichia coli, Shigella spp., Vibrio parahaemolyticus, Yersina enterolitica, Salmonella enteritidis, Salmonella infantis, Salmonella typhimurium, Bacillus subtilis, Enterococcus faecalis, Streptococcus faecalis.
Alternaria alternata
Albahaca (Ocimum basilicum)
Canela (Cinnamomum zeylanicum)
Cilantro (Coriandrum sativum)
Clavo (Eugenia aromaticum)
Linalool, metil chalvicol,eugenol, metil eugenol, metil cinamato, 1,8 cineol, cariofileno
Cinamaldehído, eugenol, copaeno, β-cariofileno
2E-Decanal, 2E-dodecanal, linalool
Eugenol, acetato de eugenilo, cariofileno
Bacillus brevis, E. coli, E. faecalis, Klebsiella pneumoniae, Pseudomona aeruginosa, Staphylococcus aureus, Listeria monocytogenes, Lactobacillus plantarum.
E. coli, Escherichia coli O157:H7, P. aeruginosa, E. faecalis, S. aureus, K. pneumoniae, Salmonella sp., V. parahemolyticus.
E. coli, L. monocytogenes, L. plantarum, S. aureus.
B. brevis, B. subtilis, Clostridium botulinum, E. faecalis, E. coli, E. coli O157:H7, K. pneumoniae, P. aeruginosa, S. aureus, S. sp., S. enterica, L. monocytogenes
Aspergillus flavus, Aspergillus niger, Penicillium corylophilum
A. alternata, A. flavus, A. niger, P. corylophilum
Ross et al., 2001; AyalaZavala et al., 2008b
Oregano (Origanum vulgare )
Sabinil monoterpenos, terpinen4-ol, γ-terpineno, carvacrol, timol
B. cereus, B. subtilis, C. botulinum, E. faecalis, E. coli, E. coli O157:H7, S. aureus, L. monocytogenes, K. pneumoniae, P. aeruginosa, S. sp.
Candida sp., Aspergillus flavus, Aspergillus niger, Penicillium corylophilum, Rhizopus nigricans
A. niger, Rhizopus stolonifer
Hammer et al., 1999; Elgayyar et al., 2001; Guynot et al., 2003; Opalchenova y Obreshkova, 2003
Chang et al., 2001; Guynot et al., 2003; Rojas-Graü et al., 2006; López-Malo et al., 2007; Du et al., 2009; Yossa et al., 2012
Elgayyar et al., 2001
Hammer et al., 1999; Guynot et al., 2003; Burt, 2004; López, et al., 2007; Du et al., 2009; Xing et al., 2011
Oregano mexicano (Lippia berlandieri Shauer)
Laurel (Laurus nobilis )
Menta piperita (Mentha piperita )
Romero (Rosmarinus officinalis
Carvacrol, p -cymeno, Caryofileno
1,8-cineole, acetato de α-terpinil, linalool, metil eugenol
Mentol, mentone, metil acetato, mentofurano
Borneol, verbenona, camfor, a-pineno, 1,8-cineole
Tomillo (Thymus vulgaris )
Timol, ρ-cymene, γ-terpinene, linalol
B. cereus, E. coli, S. aureus
S. aureus, B. cereus, Micrococcus luteus, E. faecalis
B. brevis, E. coli, E. faecalis, K. pneumoniae, P. aeruginosa, S. aureus
B. cereus, E. coli, E. faecalis, P. aeruginosa, K. pneumoniae, L. monocytogenes, S.sp., S aureus
B. cereus, C. botulinum, E. faecalis, E. coli, S. aureus, L. monocytogenes, K. pneumoniae, S. sp, P. aeruginosa
Penicillium sp., Geotrichum sp., Aspergillus sp., A. flavus, A. niger, Bipolaris sp. A. flavus, A.s niger, P. corylophilum
A. flavus, A. niger, P. corylophilum
A. flavus, A. niger, P. corylophilum, Botrytis cinerea, R. stolonifer
Hammer et al., 1999; Elgayyar et al., 2001; Burt, 2004; Rojas-Graü et al., 2006; Gutierrez et al., 2008b; Dos Santo et al., 2012
Portillo et al., 2005; Avila et al., 2010; Ayala-Zavala et al., 2010; Gómez-Sánchez et al., 2011
Demo y de las Mercedes Oliva, 2009
Hammer et al., 1999; Guynot et al., 2003
Hammer et al., 1999; Elgayyar et al., 2001; Guynot et al., 2003; Burt, 2004
Bhaskara et al., 1997, Hammer et al., 1999; Elgayyar et al., 2001; Guynot et al., 2003; Lee et al., 2005
Adaptado de Ayala-Zavala et al., (2009)
pesticidas, repelentes de insectos y los agentes antimicrobianos(HanyGennadios,2005).
Debido a las capacidades que presentan las películas comestibles en relación al aumento de calidad del producto, y a la liberación controlada de agentes antimicrobianos, se han desarrollado diversas investigaciones con base en la incorporación de aceites esenciales de plantas y hierbas a películas comestibles, para la conservación de los alimentos o la disminución del deterioro microbiano. De igual manera, el aumento de la eficiencia de los aceites esenciales debido a su incorporación en las películas comestibles, en comparación a la utilización directa, hace de esta tecnología una alternativa importante para la aplicación de estos aceites como agentes antimicrobianos en la conservación de productosvegetalesmínimamenteprocesados.
En este sentido, varios investigadores han desarrollado estudios sobre la elaboración de películas comestibles a partir de puré de tomate, puré de manzana y almidón de papa, adicionadas con aceite esencial de diferentes especias (orégano, pimienta, ajo, citronela y canela). Estas películas han presentado un efecto inhibitorio en el crecimiento de Listeria monocytogenes, Salmonella enterica y Escherichia coli O157:H7,bacteriaspatógenas importantes en alimentos. De igual forma, demostraron que las concentraciones de aceites esenciales añadidas a las películas comestibles, que presentaban efecto antimicrobiano, son menores en comparación a las utilizadas en la incorporación directa en el alimento (Rojas-Graü et al., 2006; Du et al., 2009;Fabienne et al., 2011).
También se han generado estudios acerca de la actividad antimicrobiana que pueden presentar las películas comestibles a base de quitosano adicionadas con aceites esenciales. Sánchez et al. (2011), así como Ávila et al. (2010) demostraron que las películas de quitosano adicionadas con aceite esencial de
(2013): 1 - 11
árbol de té (Melaleuca alternifolia), yorégano mexicano, respectivamente, presentan una capacidad inhibitoria sobre el crecimiento de L. monocytogenes, así como una actividad antifúngicasobreelcrecimientode Aspergillus niger y Penicillium spp. De igual forma, se han realizado diversos estudios para investigar los efectos benéficos del recubrimiento de productos vegetales mínimamente procesados con películas de quitosano. Dos Santos et al. (2012) demostraron la capacidad que presentan las películas de quitosano, adicionadas con concentraciones menores a la mínima inhibitoria de aceite esencial de orégano (Origanum vulgare L.), en el control del crecimiento de A. niger y Rhizopus stolonifer en uva, así como la capacidad de las mismas para conservar la calidad general de las uvas y sus atributos sensoriales durante 12 díasdealmacenamiento.
De igual forma, las películas comestibles a base de alginato adicionadas con aceite esencial han demostrado tener un efecto antimicrobiano. Varios estudios han demostrado la capacidad de estas películas para inhibir el crecimiento de bacterias patógenas importantes en alimentos (Bacillus subtilis, L. monocytogenes, Staphylococcus epidermis, Pseudomona aeruginosa, Salmonella typhimurium, E. coli O157:H7), así como demohos ylevaduras importantes en eldeteriorodealimentos(Maizura et al., 2007; Rojas-Graü et al., 2007; Norajit y Hyung, 2011).
Así mismo, las películas comestibles a base de alginato adicionadas con aceites esenciales han demostrado tener una capacidad importante para mantener la calidad de los productos vegetales mínimamente procesados. Varias investigaciones demostraron que las películas de alginato adicionadas con aceites esenciales (citronela, orégano, palmarosa, limón) ayudan de manera importante a la conservación de manzanas, melones y fresas mínimamente procesados, mejorando la vida
de anaquel de estos productos, así como disminuyendo el deterioro microbiano en estos alimentos. De igual manera, estas investigaciones han demostrado que las películas de alginato adicionadas con aceites esenciales, presentan una capacidad inhibitoria sobre el crecimiento de bacterias patógenas importantes en los productos vegetales mínimamente procesados (Raybaudi et al., 2007; Rojas-Graü et al., 2007; Perdones et al., 2012).
2.2 Utilización deciclodextrinas
Las ciclodextrinas son oligosacáridos de glucosa cíclicos no reductores. Existen tres tipos de ciclodextrinas comunes: α-, β-, y γciclodextrinas, con 6, 7 u 8 residuos de Dglucopiranosil, respectivamente, unidos por enlacesglucosídicos α-(1-4)(DelValle,2003). Las ciclodextrinas presentan una conformación circular con fondo en forma de “tazón o cono truncado”, estabilizada por la formación de puentes de hidrógeno entre los grupos hidroxilos 2 y 3 alrededor del borde exterior. Debido a sus enlaces glucosídicos α(1-4), todos los grupos hidroxilos primarios (C-6) se encuentran orientados hacia uno de los bordes del cono truncado y los grupos hidroxilos secundarios (C-2 y C-3) se encuentran colocados en el otro borde. Por otro lado, la molécula presenta en su cavidad interior un ambiente hidrofóbico con una gran densidad de electrones en el medio. La existencia de una cavidad hidrófoba y la presencia de anillos hidrofílicos, le dan a las ciclodextrinas la propiedad de formar complejos con una amplia variedad de moléculas orgánicas en medio acuoso. Las βciclodextrinas las más utilizadas por las industrias farmacéuticas y de alimentos, que las α-, y γ-ciclodextrinas, ya que presentan un precio más bajo, mayoraccesibilidad, han sido aprobadasporlaFDA ytienenlacapacidadde generar complejos con moléculas aromáticas y/oheterocíclicas(DelValle,2003).
7-1 (2013): 1 - 11
Las ciclodextinas poseen una habilidad única para actuar como contenedores moleculares, ya que tienen la capacidad de atrapar moléculas huésped en su cavidad interna. Durante este proceso, la molécula huésped (menos polar) sustituye a las moléculas de agua que se encuentran en una situación energéticamente desfavorable en el interior de la cavidad de la ciclodextrina. Este proceso está regulado por interacciones no covalentes (fuerzas de Van der Waals, puentes de hidrógeno e interacciones electrostáticas) entre la molécula huésped y la molécula anfitrión (ciclodextrina) (Ayala-Zavala et al., 2008a).
La capacidad de las ciclodextrinas para formar complejos con moléculas huésped está en función de dos factores clave. El primer factor está relacionado al impedimento estérico, el cual es función directa del tamaño de la molécula huésped y el tamaño de la cavidad interna de la ciclodextrina; si la molécula huésped no se ajusta correctamente en la cavidad interna, la estabilidad del complejo disminuye de manera importante. El segundofactorcríticoseencuentrarelacionado a las interacciones termodinámicas entre los diferentes componentes del sistema (ciclodextrinas, huésped y solvente).
Rekharsky y Inoue (1998) investigaron las implicaciones termodinámicas del proceso de inclusión de moléculas huésped en las ciclodextrinas, concluyendo que los factores más importantes en la formación del complejo son (1) penetración de la molécula huésped en la parte hidrofóbica, (2) deshidratación de la molécula orgánica, (3) formación de puentes de hidrógeno, (4) liberación de moléculas de agua por parte de la cavidad interna de la ciclodextrina, y (5) cambios conformacionales o disminución de la tensión del complejo durantelaunióndemoléculas.
Porotrolado,las β-ciclodextrinaspresentan una mayor eficiencia para encapsular y
proteger moléculas aromáticas y/o heterocíclicas en comparación con las otras dos clases de ciclodextrinas. De igual forma, cuando la microencapsulación toma lugar, la molécula huésped puede sufrir cambios en sus propiedades físicas y químicas tales como menor degradación de la molécula por la exposición a la luz o al oxígeno, modificaciones en la reactividad química, incremento en la solubilidad en agua, fijación de compuestos volátiles e incremento en la liberación controlada de los mismos (AyalaZavala et al., 2008a).
Gracias a las características de las βciclodextrinas, la microencapsulación de aceites esenciales por medio de las mismas y el uso de estos microencapsulados en la conservación de alimentos, han despertado el interés de los investigadores por desarrollar y aplicar esta nueva tecnología. Como se mencionó anteriormente, la incorporación directa de los aceites esenciales en el alimento presenta desventajas importantes tales como la afectación de las características sensoriales del alimento y la evaporación o inactivación de las sustancias activas del aceite. La formación de complejos a partir de βciclodextrinas y aceites esenciales, representa una posible solución a estos problemas (Ayala-Zavala et al., 2010a).
En este sentido, se han desarrollado diversas investigaciones en relación a la microencapsulación de aceites esenciales por medio de β-ciclodextrinas y su efecto antimicrobiano. Varios investigadores observaron que los complejos β-ciclodextrinas y aceite esencial (β-CD-AE) presentaban una mayor estabilidad y versatilidad en la liberación controlada de las sustancias activas del aceite esencial y de esta manera contribuían a la eficiencia en la actividad antimicrobiana que presentan los aceites esenciales. De igual manera, observaron que cuando el complejo antimicrobiano (β-CDAE) se encuentra expuesto a humedades
7-1 (2013): 1 - 11
relativas altas la interacción del complejo se debilita y de esta manera el aceite esencial es liberado pasivamente al medio ambiente (Ayala-Zavala et al., 2008b; Toro et al., 2010; Ciobanu et al., 2013)
Por otro lado, existen investigaciones acerca de la capacidad que presentan los complejos β-CD-AE, para la conservación de vegetales mínimamente procesados. Estas investigaciones demostraron la efectividad de complejos elaborados a partir de compuestos volátiles derivados del aceite esencial de mostaza y aceite esencial de ajo para la conservación microbiana y la inhibición del crecimiento de bacterias patógenas en cebollas y tomates mínimamente procesados. De igual manera, las investigaciones demostraron que laeficienciaenlaliberacióndeloscompuestos volátiles de los aceite esenciales es mucho mayor cuando éstos se encuentran encapsulados en β-ciclodextrinas, mejorando de esta manera la calidad general de los vegetales mínimamente procesados. Por último, las diversas investigaciones señalan la posibilidaddelaencapsulaciónsatisfactoriade aceites esenciales y por medio de ciclodextrinas, y su viabilidad para ser utilizadas como un nuevo método de conservación de vegetales mínimamente procesados (Ayala-Zavala y González, 2010; Piercey et al., 2011).
Conclusiones y comentarios finales
Los aceites esenciales de especias representan una opción eficaz a los antimicrobianos tradicionales en la conservación de alimentos vegetales mínimamente procesados. Sin embargo, su uso se ve limitado, debido a que las concentraciones necesarias para lograr un efecto antimicrobiano significativo, son lo suficientemente altas para generar cambios indeseables en el sabor de los productos vegetales y por consiguiente generar un
R. H. Hernández - Figueroa et al. / Temas Selectos de Ingeniería de Alimentos 7-1 (2013): 1 - 11
rechazo del alimento por parte de los consumidores. Por esta razón, las películas comestibles, así como el uso de ciclodextrinas para la liberación controlada de aceites esenciales, representan unaalternativaeficaz y eficiente para la conservación de vegetales mínimamente procesados, sin afectar de manera importante los cambios indeseables en elsaborylaaceptación.
Agradecimientos
R.H.HernándezFigueroaagradecealConsejo Nacional de Ciencia y Tecnología (CONACyT) y a la Universidad de las Américas Puebla, por el financiamiento de sus estudios de posgrado y el apoyo para realizar estetrabajo.
Ayala-Zavala, J. F. y González A. 2010. Optimizing the use of garlic oil as antimicrobial agent on fresh-cut tomato through a controlled release system. Journal of Food Science. 75(7): M398-M405.
Bhaskara, M. V., Angers, P., Gosselin, A. y Arul, J 1999. Characterization and use of essential oli from Thymus vulgaris against Botrytis cinrea and Rhizopus stolonifer in strawberry fruits. Phytochemistry. 47(8): 1515-1520.
Braca A., Siciliano, T. D’Arrigo, M. y Germano, M. P. 2008. Chemical composition and antimicrobial activity of Momordica charantia seed essential oil En Ayala, J. F., González A., A., del Toro, L. 2009 Enhancing safety and aroma appealing of fresh-cut fruits and vegetables using the antimicrobial and aromatic power of essential oils. Journal of Food Science. 74(7): R84-R91.
Burt, S. 2004. Essential oils: their antibacterial properties and potential applications in foods - a review. International Journal of Food Microbiology. 94:223-253.
Chang, S. T., Chen, P. F. y Chang, S. C. 2001. Antibacterial activity of leaf essential oils and their constituents from Cinnamomum osmophloeum. Journal of Ethno-pharmacology. 77: 123-127.
Referencias
Ávila, R., Hernández, E., López, I., Palou, E., Jiménez, M. T., Nevárez, G. V. y López-Malo, A. 2010. Fungal inactivation by Mexicano regano (Lippia berlandieri Shauer) essential oil added to amaranth, chitosan, or starch edible films. Journal of Food Science. 75(3): M127-M133.
Ayala-Zavala, J. F., del Toro, L., Apvarez, E. y Gonzalez, G. A. 2008a. High relative humidity inpackage of fresh-cut fruits and vegetables: advantage or disadvantage considering micorbiological problems and antimicrobial delivering system?. Journal of Food Science. 73 (4): R41-R47.
Ayala-Zavala, J. F. Soto, H., González, A., Álvarez, E., Martín, O. y González, G. A. 2008b. Microencapsulation of cinnamon leat (Cinnamomum zeylanicum) and garlic (Allium sativum) oils in βcyclodextrin. Journal of Inclusion Phenomena and Macrocyclic Chemistry. 60:359-368.
Ayala-Zavala, J. F. Gonzáles, G. A. y del Toro, L. 2009. Enhancing safety and aroma appealing of fresh-cut fruits and vegetables using the antimicrobial and aromatic power of essential oils. Journal of Food Science. 74(7): R84-R91.
Chang, H., T., Cheng, Y., H., Wu, C., I., Chang, S., T., Chang, T., T. y Su, Y., C. 2008. Antifungal activity of essential oil and its constituents from Calocadrus macrolepis var. Formosana Florin leaf against plant pathogenic fungi. Bioresource Tecnology. 99: 62666270.
Ciobanu, A., Mallard, i., Landy, D., Brabie, G., Nistor, D. y Fourmentin, S. 2013. Retention of aroma compounds from Mentha piperita essential oil by cyclodextrin and crosslinked cyclodextrin polymers. Food Chemistry. 138: 291-297.
Demo M. S., de las Mercedes O. M. 2009. Antimicrobial activity of medicinal plants from South America. In: Botanical medicine in clinical practice. Oxfordshire, Reino Unido. p 152–63. En: Ayala-Zavala, J. F. Gonzáles, G. A. y del Toro, L. 2009. Enhancing safety and aroma appealing of fresh-cut fruits and vegetables using the antimicrobial and aromatic power of essential oils. Journal of Food Science. 74(7): R84-R91.
Del Valle, E. M. 2003. Cyclodextrins and their uses: a review. Process Biochemistry. 39: 1033-1046.
Del Toro, C. L., Ayala, J. F., Machi, L., Santacruz, H., Villegas, M. A., Alvarez, E. y González, G. A. 2010. Controlled release of antifungal volatiles of thyme essential oil from β-cyclodextrin capsule. Journal of
Inclusion Phenomena and Macrocyclic Chemistry. 67:431-441.
Dos Santos, N. S., Athayde, A. J., Vasconcelos, C. E., de Sales, C. V., de Melo, S., Sousa da Silva, R., Montenegro, T. C. y Leite, E. 2012. Efficacu of the application of coating composed of chitosan and Origanum vulgare L. essential oil to control Rhizopus stolonifer and Aspergillus niger in grapes (Vitis labrusca L.). Food Microbiology. 32: 234353.
Du, W. X., Olsen, C. W., Avena-Bustillos, R. J., McHugh, T. H., Levin, C. E., y Friedman, M. 2009. Antibacterial effects of allspice, garlic, and oregano essential oils in tomato films determined by overlay and vapor-phase methods. Journal of Food Science. 74(7): 390-397.
Elgayyar, M., Draughon, A., Golden, D. A. y Mount, J. R. 2001. Antimicrobial activity of essential oil from plants against selected pathogenic and saprophytic microorganisms. Journal of Food Protection. 64(7): 1019-1024.
Fabienne, E., Ehivet, E., Min, B., Park. M. K. y Oh, J. H. 2011. Characterization and antimicrobial activity of sweetpotato starch-based edible film containing origanum (Thymus capitatus) oil. Journal of Food Science. 76(1): 178-184.
Fisher, K. Y Phillips, C. 2008. Potential antimicrobial uses of essential oils in food: is citrus the answer?. Trends in Food Science and Technology. 19:156164.
Gómez-Sánchez, A., Palou, E. y López-Malo, A. 2011. Antifungal activity evaluation of Mexicano regano (Lippia berlandieri Schauer) essential oil on the growth of Aspergillus flavus by gaseous contact Journal of Food Protection. 74(12): 2192-2198.
Gutierrez, G. , Barry-Ryan, C., y Bourke, R. 2008a. The antimicrobial efficacy of plant essential oil combinations and interactions with food ingredients. International Journal of Food Microbiology. 124:91-97.
Gutierrez, J., Rodriguez., Barry-Ryan, C. y Bourke, P. 2008b. Efficacy of plant essential oils against foodborne pathogens and spoilage bacteria associated with ready-to-eat vegetables: antimicrobial and sensory screening. Journal of food Protection. 71(9): 1846-1854.
Gutierrez, G., Bourke, P., Lonchampa, J. y Barry-Ryan, C. 2009. Impact of plant essential oil on microbiological, organoleptic and quality markers of minimally processed vegetables. Innovative Food Science and Emerging Technology. 10 (2): 195-202.
Guynot, M. E. Ramos, A. J. Setó, L. Purroy, P., Sanchis, V. y Marín, S. 2003. Antifungal activity of volatile compounds generated by essential oils against fungi commonly causing deterioration of bakery products. Journal of Applied Microbiology. 94: 893-899.
Ha, HKP., Maridable, J., Gaspillo, P., Hasika, M., Lalaluan, R. y Kawasaki, j. 2008. Essential oil from lemongrass extracted by supercritical carbón dioxide and steam destillation.The Philippine Agricultural Scientist. 91:36-41.
Hammer , K. A., Carson, C. F. y Riley, T. V. 1999. Antimicrobial activity of essential oils and other plant extracts. Journal of Applied Microbiology. 86: 985-990.
Han, J. H. 2003. Antimicrobial food packaging. En: Novel Food Packaging Techniques. Reino Unido. Editor. R. Ahvenainen. Woodhead Publishing Ltd. pp 50-70
Han, J. H., y Gennadios, A. 2005. Edible films and coatings: a review. Innovation in Food Packaging 239- 262
Kester, J. M. y Fennema, O. R. 1986. Edible films and coatings: a review. Food Technology. 48(12): 47-59. En: Han, J. H., y Gennadios, A. 2005. Edible films and coatings: a review. Innovation in Food Packaging. 239- 262.
Lanciotti, A. A., Gianotti, A., Patrignani, F., Belleti, H., Guerzonu, M. E. y Gardini, F. 2004. Use of natural aroma compounds to improve shelf-life and safety of minimally processed fruits. Trends in Food Science and Technology. 15(3): 201-208.
Lee, S. J., Umano, K., Shibamoto, T. y Lee, K. G. 2005. Identification of volatile components in basil (Ocimun basilicum L.) and thyme leaves (Thymus vulgaris L.) and their antioxidant porperties. Food Chemistry. 91: 131-137.
López, P., Sánchez, C., Batlle, R. y Nerín, C. 2007 Vapor phase activities of cinnamon, thyme, and oregano essential oils and key constituents against foodborne microorganisms. Journal of Agricultural and Food Chemistry. 55(11):4348–56.
López-Malo, A. 1995. Efecto de diversos factores sobre la capacidad antimicótica de vainilla. Tesis de Maestría. Universidad de las Américas Puebla, México.
López-Malo, A. Palou, E. y Alzamora, S. 2005. Naturally occuring compounds – plant source, En: Antimicrobials in Food. Tercera edición. EE.UU. Editores. P. Michael Davidson, Johmn N. Sofos y A. L. Branen. Editorial Taylor y Francis Group.
López-Malo, A. Barreto, J. Palou, E. y San Martín, F. 2007. Aspergillus flavus growth response to cinnamon extracta and sodium benzoate mixtures. Food Control. 18: 1358-1362
Luqman, S., Dwivedi, G., Darokar, M., Kaira, A. y Khanuja, S. 2007. Potential of Rosemary oil to be used in drug-resistant infections. Alternative therapies. 13 (5): 54-59.
Maizura, M., Fazilah, A., Norzia, M. H. y Karim, A. A. 2007. Antibacterial activity and mechanical properties of partially hyfrolyzed sago starchalginate edible film containing lemongrass oil. Journal of Food Science. 72(6): C324-C330.
Marino, M. BErsani, C. y Comi, G. 1999. Antimicrobial activity if the essential oils of Thymus vulgaris L. measured using a bioimpedometric method. Journal of Food Protection. 62:1017-10123.
Marino, M. Bersano, C. y Comi, G. 2001.Impedance measurements to study the antimicrobial activity of essential oils from Lemiacea and Compositae. Journal of Food Microbiology. 67:187-195.
Norajit, K. y Hyung, G. 2011. Preparation and properties of antibacterial alginate films incorporating extruded White ginseng extract. Journal of Food Processing and Preservation. 35: 387-393.
Opalchenova, G. y Obreshkova, D. 2003. Comparative studies on the activity of basil- an essential oil from Ocimum basilicum L.- against multidrug resistant clinical isolates of the genera Staphylococcus, enterococcus and Pseudomonas by usinf diffetent tes methods. Journal of Microbiology Methods. 54: 105-110.
Perdones, A., Sánchez, L., Chiralt, A. y Vargas, M. 2012. Effect of chitosan-lemon essential oil coatings on storage-keeping quality of strawberry. Postharvest Biology and Technology. 70: 32-41.
Ponce, A. G., del Valle, C., y Roura, S. I. 2004. Shelf life of leafy vegetables treated with natural essential oils. Journal of food Science. 69 (2): M50-M56.
Piercey, M. J., Mazzanti, G., Budge, S. M., Delaquis, P. J., Paulson, A. T. y Truelstrup, L. 2012. Antimicrobial activity of cyclodextrin entrapped allyl isothicyanate in a model system and packaged fresh-cut onions. Food Microbiology. 30: 213-128.
Raybaudi, R. M., Mosqueda, J. y Martín, O. 2007. Edible alginate-based coating as carrier of antimictobials to improve shelf-life and safety of fresh-cut melon. International Journal of Food Microbiology. 121:313-327.
de Alimentos 7-1 (2013): 1 - 11
Rekharsky, M. V. y Inoue, Y. 1998. Complexation thermodynamics of cyclodextrins. Chemical Review. 98: 1875-1917. En: Ayala, J. F., del Toro, L., Apvarez, E. y Gonzalez, G. A. 2008. High relative humidity in-package of fresh-cut fruits and vegetables: advantage or disadvantage considering micorbiological problems and antimicrobial delivering system?. Journal of Food Science. 73 (4): R41-R47.
Rojas-Graü, M. A., Avena-Bustillos, R. J., Friedman, M., Henika, P. R., Martin-Belloso, O. y McHugh, T. 2006. Mechanical, barrier, and antimicrobial properties of Apple puree edible films containing plant essential oils. Journal of Agricultural and Food Chemistry. 54(24): 9262-9267.
Rojas-Graü, M. A., Raybaudi, R. M., Soliva, R. C., Avena-Bustillos, R. J., McHugh, T. H. y Martín, O. 2007. Apple puree-alginate edible coatings as carrier of antimicrobial agents to prolong shelf-life of freshcut apples. Postharvest Biology and Technology. 45:254-264.
Ross, Z. M. O’Gara, E. A., Hill, D. J., Sleightholme, H. V. y Maslin, D. J. 2001. Antimicrobial properties of garlic oil against human enteric bacteria: Evaluation of methodologies and comparisons with garlic oil sulfides and garlic powder. Applied and Eviromental Microbiology. 67(1): 475-480.
Sanchez, L., Cháfer, M., Hernández, M., Chiralt, A. y Gonzáles, C. 2011. Antimicrobial activity of polysaccharide films containing esential oils. Food Control. 22: 1302-1310.
Sanford K. A., Johnston, E. M., Porter, J. L., Lowe, J. y Oxby, D. M. 2008. Dietitians attitudes, perception, and usage patterns for fresh-cut fruit and vegetables. Canadian Jorunal of Dietetic Practice and Research. 69: 7-13.
Tajkarimi, M. M., Ibrahim, S. A. y Cliver, D. O. 2010. Antimicrobial herb and spice compounds in food. Food Control. 21: 1199-1218.
Xing, Y., Xu, Q., Li, X., Che, Z. y Yun, J. 2011. Antifungal activities of clove oil against Rhizopus nigricans, Aspergillus flavus and Penicillium citrinum in vitro and in wounded fruit test. Journal of Food Safety. 32: 84-93.
Yossa, N., Patel, J., Millner, P. y Martin, Y. 2012 Essential oils reduce Escherichia coli O157:H7 and Salmonella on spinach leaves. Journal of Food Protection. 75(3): 488-496.

Temas Selectos de Ingeniería de Alimentos 7 - 1 (2013): 12 - 24

Prebióticos: su importancia en la salud humana y propiedades funcionales en tecnología de alimentos
D. Morales - Koelliker* y J.F Vélez - Ruíz
Departamento de Ingeniería Química, Alimentos y Ambiental, Universidad de las Américas Puebla. Ex hacienda Sta. Catarina Mártir S/N, San Andrés Cholula, Puebla. C.P.72810, México.
Resumen
Los prebióticos son ingredientes alimentarios no digeribles que benefician al huésped mediante la estimulación selectiva del crecimiento y/o la actividad de un número limitado de bacterias en el colon. En el presente artículo, se revisan ingredientes que cumplen criterios para ser considerados prebióticos, sus beneficios para la salud, las propiedades funcionales y físicas conferidas a los productos adicionados y sus aplicaciones en la industria alimentaria. Al revisar su efecto en las propiedades físicas de los alimentos a los que se les añade, se detalla su utilidad como sustitutos de grasa y optimizadores de la textura. Se concluye que para obtener productos con bajo contenido de grasa con la reología y la consistencia similares a las de los productos enteros, son necesarias mayores concentraciones de prebióticos. Por último, la utilización de prebióticos como ingredientes alimentarios permite a los fabricantes satisfacer y superar las expectativas de los consumidores que viven preocupados por su salud.
Palabras clave: prebióticos, tracto gastrointestinal, propiedades físicas, nutrición.
Abstract
Prebiotics are non-digestible food ingredients which benefit the host by selectively stimulating the growth and/or activity of a limited number of bacteria in the colon. In this article, the ingredients that meet the criteria to be considered as prebiotics, their health benefits, physical and functional properties conferred to added products and their applications in the food industry are reviewed. Moreover, the effect of prebiotics on the physical properties of foodstuff to which these are added are analyzed, its effects as fat substitute and texture optimizer are described. It is concluded that a higher concentration of prebiotics are needed to obtain products with low fat content and with rheological properties and thickness similar to whole fat products. Finally, the use of prebiotics as food ingredients allows manufacturers to meet and go beyond the expectations of today's consumers who are health concerned.
Keywords: prebiotics, gastrointestinal tract, physical properties, nutrition.
Introducción
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
El concepto de prebióticos fue definido por primera vez por Gibson y Roberfroid (1995) como ‘ingredientes no digeribles que benefician al huésped estimulando selectivamente el crecimiento y/o la actividad de una o de un limitado número de bacterias residentes del colon (bifidobacterias y lactobacilos, principalmente)’. Posteriormente,
Dirección electrónica: diana.moraleskr@udlap.mx
la definición fue actualizada por los autores para describirlos como ‘ingredientes selectivamente fermentados que permiten cambios específicos en la composición de la microbiota gastrointestinal y que confieren beneficios en el bienestar y la salud del huésped’ (Gibson et al., 2004). Dada la naturaleza de la fermentación por lactobacilos o bifodobacterias, es poco probable que existan prebióticos de origen proteico o lipídico. Por ello, Cummings y Macfarlane (2002) propusieron una definición alterna delimitando a los prebióticos como un grupo de carbohidratos de cadena corta no digeribles por enzimas humanas ni animales y con un grado de polimerización que va de dos a sesenta. En ambas definiciones, existen criterios de selección que permiten la clasificación de un ingrediente como prebiótico tales como la resistencia al proceso digestivo esto es, la resistencia a la acidez gástrica, a la hidrólisis por enzimas y a la absorción intestinal (Gibson et al., 2004; Wang,2009).
Partiendo de la premisa de que los prebióticos tienen el poder de controlar la composición de la microbiota del colon y así, conferir beneficios al bienestar y salud del huésped, en la actualidad se ha incrementado su inclusión en unaampliagamadealimentos. Este aumento en su utilización también responde,debidoalaspropiedadesfuncionales y físicas inherentes a los prebióticos, a las exigencias del consumidor por obtener productos con un sabor agradable, de bajo valor calórico y que contengan poca cantidad de grasa. Tomando en cuenta todo lo anterior, el objetivo de este artículo de revisión es reconocer a los ingredientes que cumplen los criterios para ser considerados prebióticos así como revisar su potencial benéfico para la salud, sus propiedades funcionales y físicas y, por último, revisar sus aplicaciones en la industriaalimentaria.
Revisión bibliográfica
1. Composición química y clasificación de los prebióticos
Con la excepción de la inulina -una mezcla de fructooligosacáridos y polisacáridos- los prebióticos que hasta ahora se consideran para su uso en la industria alimentaria son mezclas de oligosacáridos no digeribles que constan de 3 a 10 monómeros de ciertos carbohidratos (Saad et al., 2013). Los oligosacáridos candidatos aprebióticos pueden clasificarsede acuerdo a sus componentes químicos y a su grado de polimerización, se incluyen entonces a fructooligosacáridos (FOS), galactooligosacáridos (GOS), oligosacáridos de soya, isomaltooligosacáridos, xylooligosacáridos, pirodextrinas y lactulosa (Mcfarlane et al., 2008) (Tabla I). Considerando que la inulina, FOS, GOS y trans-galactoologosacáridos (TOS) son los únicos candidatos que cumplen todos los criterios para clasificarse como prebióticos (Roberfroid, 2007), a continuación se presenta una breve descripción de la composición químicadeellos.
La inulina ha sido definida como un carbohidrato polidisperso que consiste de manera casi exclusiva de enlaces fructosilfructosa β-(1 ←2), por eso el término inulina se utiliza genéricamente para todas las moléculas lineales con esta conformación. Además de la inulina nativa, también se produce la inulina comercial, que puede estar compuesta principalmente por inulina de cadena corta (2 a 7 unidades) o de cadena larga (22 a 25 unidades). Su hidrólisis enzimática parcial se denomina oligofructosa, y junto al término FOS se consideran sinónimos de inulina y sus mezclas con un grado de polimerización menor a 10 (Roberfroid,2007;Tárrega et al., 2011;Meyer et al., 2011).
Tabla I. Clasificacióndecarbohidratoscomoingredientesprebióticos
NombreComposiciónPrebióticoGP
InulinaFructanos β-(1 ←2) Sí11-65
FructooligosacáridosFructanos β-(1 ←2) Sí2-10
GalactoligosacáridosOligogalactosa85%,glucosaylactosaSí2-5
LactulosaDisacáridosintético(gal-fruct) β (1→4)IP2-4
OligosacáridosdesoyaMezcladerafinosayestaquiosaND3-4
PirodextrinasOligosacáridosyglucosaNDVariable XylooligosacáridosXylosa β (1→4)IP2-4
IsomaltooligosacáridosGlucosa β (1→4),glucosaramificada β (1→6)IP2-8
Adaptado de Macfarlane et al . (2006) y Roberfroid (2007). GP, grado de polimerización; IP, Información preliminar, hace falta mayor investigación; ND, información no disponible.
La β-galactosidasa es la responsable de la obtención de varios productos de GOS, 24 al 55% corresponden a oligosacáridos. Los GOS son producto de la hidrólisis de lactosa, generando mezclas de diversos grados de polimerización y que contienen de 2 a 9 moléculas de galactosa unidas a una de glucosa terminal mediante un enlace β (1→4), aunquetambién se presentan enlaces β (1→2) y β (1→3). La variabilidad en sus enlaces glicosídicos podría ser una de las razones por las cuales los GOS son resistentes a la digestión (Macfarlane et al., 2008). Por su parte, los TOS son una mezcla de oligosacáridos resultante de la transglicosilación de la lactosa. En general, sontrisacáridosapentasacáricosconuniones β (1→6), β (1→3) y β (1→4) (Roberfroid, 2007).
2. Importancia delos prebióticos en la salud
El tracto gastrointestinal (TGI) representa un ecosistema complejo y la interacción de su flora bacteriana es un tópico de gran interés actual, aunque el conocimiento es limitado a pesar de los avances en investigación en años recientes. Un epitelio intestinal sano, en asociación a una flora intestinal óptima, proporciona una barrera vital contra la penetración de microorganismos patógenos,
antígenos y compuestos dañinos provenientes de la luz intestinal. Las funciones fisiológicas principales de la microflora intestinal son: barrera funcional y restauración de la misma, estimulación del sistema inmune, mantenimiento de la mucosa, producción de nutrimentos y estimulación de la motilidad intestinal(HonzapfelySchillinger,2002).
El TGIde un adulto humano promedio está colonizado por aproximadamente 1x1014 célulasmicrobianas(Eckburg et al.,2005)yes este enorme potencial metabólico lo que sugiere un extraordinario efecto regulatorio en las funciones corporales, especialmente en el colon donde se encuentran en mayor concentración, superior a 5x1011 bacterias por gramo. La diversidad de la flora intestinal está determinada, entre otros factores, por la dieta, aspectos genéticos, el segmento específico del TGIyelestadofisiológicodelhuésped.
Algunos grupos de bacterias residentes en el colon como las bifidobacterias, los lactobacilos y las eubacterias pueden ser estimuladas selectivamente por los carbohidratos indigeribles de la dieta o prebióticos. Es importante que los prebióticos alcancen la región del intestino llamada ‘ciego’ para ser fermentados y utilizados por bifidobacterias y lactobacilos o bien, inhiban
varias cepas bacterianas patogénicas para el hombre (Clostridium difficile, Escherichia coli, Campylobacter jejuni, Enterobacterium, Salmonella Enteritidis o S. Typhimurium, por mencionaralgunas)(Saad et al.,2013).
Tomandoencuentaquelaintoleranciaalos prebióticos se alcanza al ingerir altas dosis de los mismos, debido al potencial osmótico y/o una fermentación excesiva, en ocasiones se presentan algunos efectos indeseables como: mayor cantidad de flatulencias, inflamación y dolor abdominal e incluso diarrea (Honzapfel y Schillinger, 2002). Sin embargo, a dosis sugeridas, el beneficio fundamental de los prebióticos es indirecto pues, como se ha mencionado, alimentan selectivamente auno o más microorganismos que modifican la microfloraintestinal. Son estas modificaciones en la microflora intestinal –y no los prebióticos por sí mismos- las que producen efectos reconocidos como tratamiento de desórdenes intestinales, influencia favorable en la digestión y absorción de azúcar, prevención de cáncer y disminución de colesterol sérico, entre otros (Honzapfel y Schillinger,2002).
2.1 Efecto de los prebióticos en la salud intestinal
La mayoría de los beneficios conferidos al consumo de prebióticos se encuentran asociados a la optimización de la función y metabolismo del colon, tales como el incremento en el peso de la materia fecal, la reducción en el pH del intestino, el decremento en productos nitrogenados finales y la modulación del sistema inmune (Saad et al., 2013). Desde hace años se ha recomendado el consumo de prebióticos como parte del tratamiento de síndrome de intestino irritable. De igual forma, se sugiere que las modificaciones de la flora intestinal por la ingestión de prebióticos interactúan con la respuesta inmunológica del intestino y, por su asociación con el tejido linfoide, proveen
efectos protectores sistémicos (principalmente respiratorios y en piel) más allá de sólo proteger el sistema gastrointestinal (Wang, 2009). Aunque no existe información suficientesobrecómolosmicroorganismosdel hospedero reconocen a los prebióticos ingeridos en el proceso de la expresión modulatoria del sistema inmune, se supone que las respuestas inmunes innatas son activadas mediante su interacción con fracciones de los oligosacáridos (Saad et al., 2013).
Acerca del estudio de enfermedades del colon, la ingesta de inulina mostró efectos anti-inflamatorios para la colitis distal inducida en ratas, así como mejoras en las lesiones del intestino (Videla et al. 2001). Komiyama et al. (2011), por su parte, presentaron resultados de un estudio sobre el uso de prebióticos, entre ellos un alimento de cebadagerminada, ysu efecto enlamicroflora intestinal. Concluyeron que los prebióticos podrían ser un complemento útil en el tratamiento de colitis ulcerativa tan bueno comoeltratamientoconantibióticos.
2.2 Metabolismo delípidos
Entre los incontables intentos de reducir los triglicéridos séricos por medio de la modificación de hábitos alimentarios, se encuentra la ingestión terapéutica de prebióticos. Los efectos hipotrigliceridémicos de fructooligosacáridos, almidones resistentes e inulina han sido descritos recientemente por Delzenne et al. (2002) en animales, y posteriormente en humanos (Delzenne et al., 2005). Elhígadojuegaunpapelprimordial en la homeostasis de las lipoproteínas ricas en triacilglicéridos, ya que es el encargado de la síntesis y secreción de lipoproteínas de muy bajadensidad(VLDLporsussiglaseninglés). En modelos animales se ha comprobado que tras la ingesta de prebióticos existe una disminuciónenlacapacidaddelhígadoparala síntesis de lípidos (principalmente VLDL),
ocasionada por una reducción en la actividad en todas las enzimas lipogénicas (acetil-CoA sintetasa, enzima málica, ATP citratoliasa y glucosa-6-fosfato deshidrogenasa), hasta en 50% (Delzenne et al., 2002). La baja tasa lipogénicadel hígado, posterioral consumo de prebióticos, especialmente de oligofructosa, sugierequesuadministraciónpodríadisminuir la expresión genética de las enzimas lipogénicas (Delzenne y Kok, 2001). Los resultados en humanos son menos contundentes, en estudios clínicos realizados se propone a la inulina como el prebiótico con más efecto en comparación a la oligofructosa (Saad et al.,2013).
2.3 Efecto sobre absorción de carbohidratos y peso corporal
Losefectosdelaadministracióndeprebióticos en la síntesis de lípidos y la concentración de insulina y glucosa plasmática postprandial, en animales, ha sido descrita ampliamente desde los años noventa. Por ejemplo, la administración de almidones resistentes a la digestión demostró una disminución significativa en la concentración de triacilglicéridos en sangre, decremento de la actividad enzimática asociada a lípidos y disminución en lainsulinaséricadespués dela ingesta de alimentos (Takase et al., 1994). Respecto a la investigación en humanos, los efectos aún no están del todo elucidados. Sin embargo, se considera que la suplementación de prebióticos genera los siguientes efectos: 1) retardo en el vaciamiento gástrico al comparar los índices glucémicos después de diferentes dietas, 2) reducción de la hidrólisis del almidón en el duodeno y, 3) incremento en las concentraciones plasmáticas del péptido intestinal (péptido similar al glucagón 1 y péptido YY). Todos ellos podrían contribuir, en parte, a los cambios en la sensación de apetito y en las respuestas de la glucosa posteriora laingesta de alimentos (Cani et al., 2009). Laposiblerelaciónentreelincremento en la concentración de péptidos intestinales y
la pérdida de peso corporal ha sido poco estudiada en humanos, limitándose a evaluar los efectos en la saciedad. Por otro lado, se ha estudiado el efecto de los prebióticos como moduladores del metabolismo y del peso corporal tras la reducción de un proceso inflamatorio inducido por la dieta. Las dietas altas en grasa producen un estado llamado endotoxemia, el cual se promueve cuando disminuyen las proporciones de bifidobacterias a causa de un aumento de lipopolisacáridosenelintestinoyseacompaña de resistencia a la insulina y aumento de peso corporal. La suplementación con FOS ha demostrado disminuir la endotoxemia, restaurar el nivel óptimo de bifidobacterias y, consecuentemente, mejorar la tolerancia a la glucosa, incrementar la saciedad, reducir la producción de glucosa y disminuir el peso corporalenhumanos(Kootte et al.,2012).
2.4 Prevención decáncer
Existe un número importante de investigaciones en relación a prebióticos y cáncer, pero muchas de estas investigaciones se han hecho en animales, donde el papel de los prebióticos parece ser benéfico, mientras que los estudios en humanos se han centrado en la identificación temprana de biomarcadores y en su posible efecto contra el cáncer, al lograr reducir la inflamación mediante su unión con las sustancias carcinogénicas, coadyuvando a disminuir la síntesis de enzimas que metabolizan procarcinógenos en carcinógenos y favoreciendo la actividad antitumorígena (Macfarlane et al., 2008). Probablemente los datos más notables respecto al papel de los prebióticos en la prevencióndelcáncersonloscorrespondientes a cáncer de colon y recto, donde se ha observado que en células humanas los derivados de productos de la fermentación de prebióticos inhiben el crecimiento celular, la diferenciación y modulan las actividades de reducción de la reproducción y proliferación de células cancerígenas (Pool-Zobel, 2005;
Clark et al., 2012). En la Tabla II se presentan algunas investigaciones recientes con respecto a cáncer de colon y recto, relacionadas con el consumodeprebióticos.
7 – 1 (2013): 12 - 24
2.5 Absorción deminerales
Los carbohidratos no digeribles (prebióticos) han sido erróneamente identificados como secuestradores de minerales, es decir, que
Tabla II. Estudios sobre el efecto de prebióticos en cáncer de colon y recto
Sujetos estudio
PrebióticoTratamientoCaracterísticasResultadosReferencias
RatasGOS5% o 20%
RatonesFOS, inulina100 g/kg
Cáncer inducido químicamente. A los 28 días cambio de grupo.
Menor aumento en células cancerígenas en el cambio del grupo 5% al 20%
Wijnands et al. (2001)
Cáncer y patógeno intestinal (Candida albicans, Listeria monocytogenes o Salmonella Typhimurium) inoculados.
Menor aumento en células cancerígenas y 50% menos con C. albicans que los controles. Murieron menos que controles de L.monocytogenes o S. Typhimurium
Buddington et al. (2002)
Humanos
Synergy 1®
L.rhamnosus
GG, B.lactis
Bb12®
HumanosFOS, inulina
12 g de prebiótico. Probiótico sin conteo 12 semanas, estudio doble ciego controlado. Sujetos con cáncer de colon Cambios signficativos en microflora y decremento de proliferación de células cancerígenas
Rafter et al . (2007)
15 g/día, 2 semanas
Humanos Inulina con OF 12 g/día, 6 meses
Adultos sin antecedentes de enfermedad gastrointestinal
Adultos mayores de 40 años con historial de resección por CC
Sin efectos en la proliferación de células
Sin efectos en la proliferación o muerte de células
Adaptado de Macfarlane et al. (2008). GOS, galactooligosacáridos; FOS, fructooligosacáridos; OF, oligofructosa; CC, cáncer colorrectal.
Langlands et al . (2004)
Limburg et al . (2011)
impiden su absorción. Sin embargo, esto sólo ocurre en el intestino delgado, ya que al alcanzar el colon, la alta concentración de ácidos carboxílicos de cadena corta, producto de la fermentación de prebióticos, favorece la absorción de minerales. En el colon, los minerales son liberados de la matriz de carbohidratos y se facilita su absorción, en especial de Ca2+ y Mg2+ mediante difusión pasiva, acción beneficiada por el medio ácido en el que sucede (Roberfroid, 2000). Abrams et al. (2005)observaron queelconsumodiario de una combinación de prebióticos de cadena larga y corta de inulina incrementa significativamente la absorción de calcio y mejora la mineralización ósea en el crecimiento durante la pubertad. Sugiere además, que los efectos de la ingesta de prebióticos en la absorción de calcio podrían estar modulados por factores genéticos, entre ellos los polimorfismos específicos del receptorgenéticodevitaminaD.
3. Propiedades funcionales de los prebióticos en tecnología dealimentos
Desde hace algunas décadas, la industria de alimentos ha incrementado el uso de carbohidratos prebióticos para modificar la viscosidad, la capacidad emulgente, la formación de gel, el punto de congelación yel color de los alimentos. Debido a su alta capacidad para retener la humedad, los oligosacáridos también pueden emplearse en alimentos procesados para disminuir la temperatura de congelación, controlar el oscurecimiento no enzimático y evitar un secado excesivo del producto al que se le añaden (Mussatto y Mancilha, 2007; Saad et al., 2013). Por otro lado, los prebióticos podrían disminuir la densidad energética de los productos al poseer un valor calórico bajo, entre 1.5 a 2.0 kcal/g (Roberfroid, 2007), lo que equivale al 40-50% de la energía que aportan los carbohidratos digeribles como la sacarosa. De acuerdo a Roberfroid y Slavin (2000), el poder edulcorante de los prebióticos
es inversamente proporcional a la longitud de sucadenaestructural.
En términos generales, los prebióticos oligosacáridos poseen un nivel bajo de dulzura, característica útil en la producción de alimentos cuando se requiere de un agente espesante poco dulce (Mussatto y Mancilha, 2007). En comparación con los mono- y disacáridos, el alto peso molecular de los oligosacáridos incrementa la viscosidad de los sistemas en los que son incorporados, haciéndolos útiles para alimentos que requieren mejorar su textura y palatabilidad (Macfarlane et al.,2008). Laestabilidaddelos oligosacáridos es variable y depende de la presencia de azúcares reductores, la forma del anillo, la configuración anomérica y los tipos de enlace. Los enlaces β de su estructura aseguran la estabilidad, aun así, los medios ácidos(pH <4),lastemperaturaselevadas yun tiempo prolongado de almacenamiento a temperaturaambienteprovocahidrólisis delos oligosacáridos con la pérdida nutrimental y de las propiedades fisicoquímicas correspondiente(MussattoyMancilha,2007).
3.1 Inulina
La inulina de cadena corta es soluble y relativamentedulceporloquepuedeserusada como sustituto de sacarosa. En contraste, la inulina de cadena larga es menos soluble y concede mayor efecto sobre la viscosidad, por lo que suele ser utilizada para dar estructura a productos bajos en grasa (Tárregas et al., 2011). Cuando la inulina es añadida en bajas concentraciones, las propiedades reológicas del producto no se modifican y la calidad sensorialnosufregrandescambiosdebidoasu poca dulzura y su limitado efecto en la viscosidad. El añadir 5% de inulina de cadena largaalechefermentadabajaengrasanotiene un efecto específico en la pseudo-plasticidad del producto, pero incrementa significativamente la velocidad de flujo y la viscosidad aparente. Se considera que esta
velocidad de corte es percibida en el paladar comocorteenlaboca(Meyer et al., 2011). La habilidad de la inulina para influir en las propiedadesdeflujodelosproductosalosque se les añade, parece responder a tres factores: a) la capacidad de la inulina para retener agua, b) en presencia de agua, la formación de microcristales que interactúan unos con otros, formando pequeños agregados que pueden ocluirunagrancantidad deaguaycrearungel particulado yc)unmayorcontenidodesólidos totales (González-Tomás yCostell, 2006). Las características del gel dependerán de factores tales como laconcentración deinulina ydelas condiciones del proceso que afectan a la nucleación,lacristalizaciónyladisposiciónde los cristales de inulina (Arcia et al., 2011; Tárregas et al., 2011). Villegas y Costell (2007) mostraron que se puede alcanzar la viscosidad de una bebida de vainilla a base de leche entera, si a una bebida de leche descremada se le añade de 4 a 10% de inulina de cadena corta o 4-6% de inulina de cadena larga.Estosdatosdemuestranquelainulinade cadena larga incrementa eficazmente la viscosidad en sistemas de esta naturaleza. Asociado al poder de la inulina de producir una sustancia cremosa, existe información de que las interacciones de inulina con hidrocoloides pueden resultar en sistemas con viscosidad sinérgica en combinación con una velocidaddeflujodelaquepuedencarecerlos sistemas hidrocoloidales de agua pura. Respecto al efecto en la textura, Meyer et al. (2011) evaluaron el efecto de la adición de inulinadecadena media alarga(1.3 o 5%)en el coeficiente de fricción y en el perfil sensorial de leche descremada, reportando efectos significativos en el primero (principalmente en el uso de inulina de cadena larga) yefectos mínimos en las sensaciones de la boca (sólo los atributos relacionados con la fricción oral fueron menores conforme disminuyólalongituddelacadenadeinulina).
Tales propiedades respaldan la aplicación de la inulina para aumentar la viscosidad, dando cuerpo yoptimizando la textura de las bebidas
bajas en calorías, así como paraincrementar la capacidaddedifusión alosproductoslíquidos, semisólidos y sólidos, bajos o sin grasa, como yogures, aderezos para ensaladas, cremas, entre otros (Leite-Toneli et al., 2007). Como ejemplos de productos semisólidos se toman a yogures y natillas, en los que se ha comprobado que la adición de inulina incrementa la viscosidad aparente y tiene efectos en los atributos de textura, haciendo los productos más espesos, pegajosos, cremosos yairados y, reduciendolasinéresise histéresis (los efectos son significativamente mayores a medida que aumenta la longitud de cadena de la inulina) (Kip et al., 2006; González-Tomás et al., 2009; Lobato et al., 2009). Además, en la investigación de González-Tomás et al. (2009)sedemostróque los postres lácteos con leche descremada y 7.5% de inulina de cadena larga, presentaron propiedades de flujo y consistencia similares a los postres de leche entera, a no ser por una ligera aspereza reportada en el producto final. Este último efecto podría ser debido a la presenciadepequeñoscristalesoagregadosde cristales de inulina de cadena larga en el producto, concordante a lo confirmado por Torres et al. (2010) en su estudio de las propiedades reológicas y de distribución de tamaño de partícula durante el almacenamiento en postres lácteos que contienen inulina de cadena larga. Dichos autores manifestaron que las muestras control sin inulina resultaron ser estables durante el almacenamiento y que las propiedades reológicas de postres que contienen inulina presentaron cambios con el tiempo conduciendo a un sistema más tixotrópico, consistente, pseudo-plástico y elástico. Los cambios en las muestras que contenían inulina se produjeron gradualmente durante 6 días, presentaban asentamiento en el día siete, poseían partículas menores a 10 µm y de un intervalo de tamaño similar a los glóbulos de grasa. Por su parte, Hennelly et al. (2006) compararon un gel de inulina incorporado por batido y una solución de inulina calentada,
ambas incorporadas a una imitación de queso conelfinderemplazarel63%delagrasa.Los autores observaron que a niveles equivalentes de humedad, los quesos con inulina presentaron una dureza significativamente mayor que las muestras control, independientemente de cómo fue incorporada la inulina; sin embargo no hubo diferencia en el nivel de dureza cuando se agregaron diferentescantidadesdeinulina(5o13.5%).
3.2. Otros preobióticos
Sobre el efecto de la adición de prebióticos en la estimulación de la viabilidad de las bifidobacterias en leches fermentadas durante eltiempodealmacenamientodelosproductos, se ha observado que los FOS son los prebióticos más eficaces y que la concentración en que se adicionan incrementa su efecto estimulador. Además, el recuento de células es significativamente influenciado por el grado de polimerización de los FOS (Mohammadi y Mortazavian, 2011). La utilización de FOS por las bifidobacterias resulta mejor cuando el grado de polimerización está por debajo de 6 unidades deacuerdo con Kaplan yHutkins (2000) ypor debajo de 10 de acuerdo con Roberfroid y Slavin(2000).
Por su parte, dado que los GOS comercialmente disponibles son mezclas, sus propiedades fisicoquímicas dependerán, en cierta medida, de la composición de las mismas. Entre sus propiedades fisicoquímicas se encuentran las siguientes: solubilidad en agua aproximadamente del 80%, apariencia traslúcida y sin color, viscosidad similar a la del jarabe de maíz de alta fructosa, estabilidad a 160 °C durante 10 minutos a pH 7, a 100 °C durante 10 minutos a pH 2 y a 37 °C a pH 2 durante varios meses; poseen una dulzura típica de 0.3 a 0.6 veces la de sacarosa, disminuyen el punto de congelación de los alimentos a los que se les añaden y previenen el secado excesivo al tener una capacidad alta
de retención de humedad (Macfarlane et al., 2008). El aumento en el tamaño molecular ocasiona decremento en su dulzura, solubilidad, osmolalidad, capacidad de formar cristales y reactividad (para las reacciones de Maillard),adiferenciadelaviscosidad,lacual sufre un incremento (Playne y Crittenden, 2009). De manera similar a otros oligosacáridos no digeribles, los GOS otorgan unsaboragradableypuedenmejorarlatextura y palatabilidad de los alimentos que se encuentran adicionados con ellos, además de proporcionar propiedades de volumen similares a la sacarosa. Por último, los GOS son resistentes a la degradación salival, haciéndolos inaccesibles para la microbiota oral y útiles como sustitutos de azúcar de bajo riesgocariogénico(Torres et al.,2010).
5. Aplicaciones en la tecnología dealimentos
Como ya se mencionó, los prebióticos presentan una doble utilidad para la industria alimentaria. Desde un punto de vista mejoran la composición nutrimental haciéndola más balanceada, además de conferirle propiedades bifidogénicas al producto; y por el aspecto tecnológico, incrementan su calidad organoléptica mejorando tanto el sabor como la palatabilidad (Honzapfel y Schillinger, 2002;Wang,2009).
A partir de hace dos décadas, una cantidad significativa de oligosacáridos ha sido introducida para su uso como ingredientes funcionales en la industria de alimentos. La elección del oligosacárido más apropiado para una aplicación en la industria de alimentos en específico varía de acuerdo al tipo de propiedades fisicoquímicas y fisiológicas deseadas en la mezcla preparada (Crittenden y Playne, 1996). Su utilización se ha enfocado principalmente en bebidas (café, chocolate, té, refrescos, bebidas alcohólicas y bebidas saludables), productos lácteos (leche fermentada, polvos instantáneos, leche enriquecida y helado) y productos simbióticos
(una mezcla de prebióticos ymicroorganismos potencialmente benéficos para el consumidor). Sin embargo, los oligosacáridos están incluidos en una extensa gama de productos como: postres (pudines, gelatinas y helados); productos de confitería como dulces, galletas, bísquets, cereales para desayunar, chocolates; pan y productos de bollería; mermeladas y jaleas; y en productos cárnicos como pasta de pescadoytofu(MussattoyMancilha,2007).
Losusostecnológicosdelainulinasebasan en sus propiedades como sustituto de azúcar, sustituto de grasa y regulador de la textura. Como sustituto de grasa en productos lácteos, contribuyeamejorarlasensaciónenlaboca, y la adición de inulina de cadena larga, incrementa la cremosidad del producto por ejemplo, de helado de yogur, queso bajo en grasa y mousse de chocolate (Meyer et al., 2011). Considerando el incremento en obesidad a nivel mundial, la inulina tiene gran demanda en la industria de alimentos al
– 1 (2013): 12 - 24
desarrollar una textura deseable en los productos bajos en grasa, tal como se ha mencionadopreviamente.
La inclusión de los GOS, como ingredientes prebióticos en los alimentos para bebés, ha atraído un interés comercial considerable dado que el establecimiento de una flora intestinal en lactantes se ha atribuido a la presencia de oligosacáridos que contienen galactosa. Varias compañías están implicadas en su producción a partir de lactosa, entre ellas: Yakult Honsha, Nissin Sugar Manufacturing Company y Snow Brand Milk Products (Crittenden y Playne, 1996). Otro ejemplo en la utilización de GOS es el pan, durante la fermentación con levaduras y la cocción, estos no se degradan y se obtiene un pan de excelente sabor y textura (Mussatto y Mancilha, 2007). Un resumen de las aplicaciones de los prebióticos en la industria alimentaria se presenta en la Tabla III.
Tabla III. Aplicaciones comunes de prebióticos en la tecnología de alimentos
ProductoAplicaciones
BebidasSustituto de azúcar, modificación en textura, sensación en la boca, estabilización de espumas
Productos lácteos y postresSustituto de azúcar, miméticos de grasa, modificación en textura y sensación en la boca, fibra, efecto prebiótico
Productos de panificaciónSustituto de azúcar y/o de grasa, modificación en textura, retención de humedad, efecto prebiótico
Productos cárnicosMiméticos de grasa, modificación en textura, estabilidad, fibra
Productos dietéticosSustituto de azúcar y/o de grasa, fibra, efecto prebiótico
Sopas y salsasSustituto de azúcar y efecto prebiótico
Alimentos para bebéModificación en textura y sensación en la boca, fibra, estabilidad y efecto prebiótico
Adaptado de Wang (2009).
Conclusión
Debido a la evidencia reconocida de la capacidad de los prebióticos para generar cambios en la composición de la flora intestinal del huésped, a través de su administración o su consumo, y proporcionar beneficios para la salud así como constituir un buen medio de prevención y remedio contra una gama de infecciones y trastornos intestinales, su consumo ha despertado el interésmundial.Elefectodelosprebióticosen la modulación del metabolismo de los triglicéridos, la modulación de la insulinemia, la mejora de la biodisponibilidad de calcio de la dieta y la modulación negativa de la carcinogénesis de colon son las áreas más prometedorasparafuturasinvestigaciones.
Además, en este artículo se revisan las propiedades funcionales de los prebióticos en la tecnología de alimentos. De hecho, su aplicación en la industria de alimentos está en crecimiento en el mercado global y son bien reconocidos como ingredientes alimentarios que brindan un valor agregado al producto al queseles añadeal mantener ymejorarnuestra salud sin sacrificar la calidad sensorial del producto.
Agradecimientos
La autora, Morales-Koelliker D., agradece al Consejo Nacional de Ciencia y Tecnología (CONACYT) y a la Universidad de las Américas Puebla (UDLAP) por el financiamientodelosestudiosdeposgrado.
Referencias
Abrams, S.A., Griffin, I.J., Hawthorne, K.M., Liang, L., Gunn, S.K., Darlington, G., Ellis, K.J. 2005. A combination of prebiotic short- and long-chain inulin-type fructans enhances calcium absorption and bone mineralization in young adolescents. American Journal of Clinical Nutrition.82: 471-476.
7 – 1 (2013): 12 - 24
Arcia, P.L., Navarro, S., Costell, E., Tárrega, A. 2011. Effect of inulin seeding on rheology and microstructure of prebiotic dairy desserts. Food Biophysics. 6:440–449.
Buddington, K.K., Donahoo, J.B., Buddington, R.K. 2002. Dietary oligofructose and inulin protect mice from enteric and systemic pathogens and tumour inducers. Journal of Nutrition. 132: 472–477.
Cani, P.D., Lecourt, E., Dewulf, E.M., Sohet, F.M., Pachikian, B.D., Naslain, D., De Backer, F., Neyrinck, A.M., Delzenne, N.M. 2009. Gut microbiota fermentation of prebiotics increases satietogenic and incretin gut peptide production with consequences for appetite sensation and glucose response after a meal. American Journal of Clinical Nutrition. 90:1236-1243.
Clark, M.C., Robien, K., Slavin, J.L. 2012. Effect of prebiotics on biomarkers of colorectal cancer in humans: a systematic review. Nutrition Reviews. 70(8): 436-443.
Crittenden, R.G., Playne, M.J. 1996. Production, properties and applications of food-grade oligosaccharides. Trends in Food Science and Technology. 7:353-361.
Cummings, J.H., Macfarlane, G.T. 2002. Gastrointestinal effects of prebiotics. British Journal of Nutrition. 87(2): S145–S151.
Delzenne, N.M., Kok, N. 2001. Effects of fructan-type prebiotics on lipid metabolism of inulin and oligofructose modulate lipid metabolism. American Journal of Clinical Nutrition. 73:456-458.
Delzenne, N.M., Daubioul, C., Neyrinck, A., Lasa, M., Taper, H.S. 2002. Inulin and oligofructose modulate lipid metabolism in animals, review of biological events and future prospects. British Journal of Nutrition. 87(1): 255-259.
Delzenne, N.M., Cani, P.D., Daubioul, C., Neyrinck, A. 2005. Impact of inulin and oligofructose on gastrointestinal peptides. British Journal of Nutrition. 93(1): S157-S166.
Eckburg, P.B., Bik, E.M., Bernstein, C.N. 2005. Diversity of the human intestinal microbial flora. Science. 308: 1635–1638.
Gibson, G.R., Roberfroid, M.B. 1995. Dietary modulation of the human colonie microbiota: Introducing the concept of prebiotics. Journal of Nutrition. 125: 1401-1412.
Gibson, G.R., Probert, H.M., Van Loo, J., Rasrall, R.A., Roberfroid, M.B. 2004. Dietary modulation of the human colonie microbiota: Updating the concept of prebiotics. Nutrition Research Reviews. 17: 259-275.
González- Tomás, L., Costell, E. 2006. Sensory evaluation of vanilla dairy desserts by free choice profile. Journal of Sensory Studies. 21: 20-33.
González-Tomás, L., Barrayi, S., Costell, E. 2009. Inulin-enriched dairy desserts: Physicochemical and sensory aspects. Journal of Dairy Science. 92(9): 4188-4199.
Hennelly, P.J., Dunne, P.G., Sullivan, M.O., Riordan, E.D.O. 2006. Textural, rheological and microstructural properties of imitation cheese containing inulin. Journal of Food Engineering. 75: 388–395.
Honzapfel, W.H., Schillinger, U. 2002. Introduction to pre- and probiotics. Food Research International. 35: 109–116.
Kaplan, H., Hutkins, R.W. 2000. Fermentation of fructooligosaccharides by lactic acid bacteria and bifidobacteria. Applied and Environmental Microbiology. 66: 2682–2684.
Kip, P., Meyer, D., Jellema, R.H. 2006. Inulins improve sensoric and textural properties of low-fat yoghurts. International Dairy Journal. 16: 1098–1103
Kootte, R.S., Vrieze, A., Holleman, F., Dallinga-Thiel, G.M., Zoetendal, E.G., de Vos, W.M., Groen, A.K., Hoekstra, B.L. Stroes, E.S., Nieuwdorp, M. 2012. The therapeutic potential of manipulating gut microbiota in obesity and type 2 diabetes mellitus. Diabetes, Obesity and Metabolism. 14:112-120.
Komiyama, Y., Mitsuyama, K., Masuda, J., Yamasaki, H., Takedatsu, H., Andoh, A., Tsuruta, O., Fukuda, M., Kanauchi, O 2011. Prebiotic treatment in experimental colitis reduces the risk of colitic cancer. Journal of Gastroenterology & Hepatology 26(8): 1298-1308.
Langlands, S.J., Hopkins, M.J., Coleman, N. 2004. Prebiotic carbohydrates modify the mucosa associated microflora of the human large bowel. Gut. 53: 1610-1616.
Leite-Toneli, J.T.C., Mürr, F.E.X., Martinelli, P., Dal Fabbro, I.M., Park, K.J. 2007. Optimization of a physical concentration process for inulin. Journal of Food Engineering. 80: 832-838.
Limburg, P.J., Mahoney, M.R., Ziegler, K.L.A. 2011. Randomized phase II trial of sulindac, atorvastatin,
7 – 1 (2013): 12 - 24
and prebiotic dietary fiber for colorectal cancer chemoprevention. Cancer Prevention Research. 4: 259–269.
Lobato, L.P., Grossmann, M.V.E., Benassi, M.T. 2009 Inulin addition in starch-based dairy desserts: Instrumental texture and sensory aspects. Food Science and Technology International. 15: 317-323.
Macfarlane, S., Macfarlane, G.T., Cummings, J.H. 2006. Review article: Prebiotics in the gastrointestinal tract. Alimentary, Pharmacology and Therapeutics. 24: 701–714.
Macfarlane, G.,T., Steed, H., Macfarlane, S. 2008. Bacterial metabolism and health-related effects of galacto-oligosaccharides and other prebiotics. Journal of Applied Microbiology. 104: 305-344.
Meyer, D., Bayarri, S., Tárrega, A., Costell, E. 2011. Inulin as texture modifier in dairy products. Food Hydrocolloids. 25: 1881-1890.
Mohammadi, R., Mortazavian, A.M. 2011. Review Article: Technological Aspects of Prebiotics in Probiotic Fermented Milks. Food Reviews International. 27: 192–212.
Mussatto, S.I., Mancilha, I.M. 2007. Non-digestible oligosaccharides: A review. Carbohydrate Polymers. 68: 587-597.
Palframan, R., Gibson, G.R., Rastall, R.A. 2003. Development of a quantitative tool for the comparison of the prebiotic effect of dietary oligosaccharides. Letters in Applied Microbiology. 37: 281-284.
Playne, M.J., Crittenden, R.G. 2009. Galactooligosaccharides and other products derived from lactose. En: McSweeney PLH, Fox PF, editores. Lactose, water, salts and minor constituents. 3ra edición. NewYork: Springer. p 121–201.
Pool-Zobel, B.L. 2005. Inulin-type fructans and reduction in colon cancer risk: review of experimental and human data. British Journal of Nutrition. 93(1): S73-S90.
Rafter, J., Bennett, M., Caderni, G., Clune, Y., Hughes, R., Karlsson, P.C., Klinder, A., O’ Riordan, M. 2007. Dietary synbiotics reduce cancer risk factors in polypectomized and colon cancer patients. American Journal of Clinical Nutrition. 85: 488–496.
Roberfroid, M.B. 2000. Prebiotics and probiotics: are they functional foods? American Journal of Clinical Nutrition. 71: 1682S-1687S.
Roberfroid, M. B., Slavin, J. 2000. Nondigestible oligosaccharides. Critical Reviews in Food Science and Nutrition. 40: 461-48
Roberfroid, M.B. 2007. Prebiotics: The concept revisited. Journal of Nutrition. 137: 830S-837S.
Saad, N., Delattre, C., Urdaci, M., Schmitter, JM., Bressollier, P. 2013. An overview on the last advances in probiotic and prebiotic field. Food Science and Technology. 50: 1-16.
Takase, S., Goda, T., Watanabe M. 199). Monostearylglycerol-starch complex: its digestibility and effects on glycemic and lipogenic responses. Journal of Nutritional Science. 40:23-36.
Tárrega, A., Torres, J.D., Costell, E. 2011. Influence of the chain-length distribution of inulin on the rheology and microstructure of prebiotic dairy desserts. Journal of Food Engineering. 104:356-363.
Torres, D.P.M., Gonçalves, M.P.F., Teixeira, J.A., Rodrigues, L.R. 2010. Galacto-oligosaccharides: Production, properties, applications, and significance as prebiotics. Comprehensive Reviews in Food Science and Food Safety. 9: 438-454.
Torres, J. D., Tárrega, A., Costell, E. 2010. Storage stability of starch-based dairy desserts containing long-chain inulin: rheology and particle size distribution. International Dairy Journal. 20: 46-52.
Videla, S., Vilaseca, J., Antolin, M., García-Lafuente, A., Guarner, F., Crespo, E. 2001. Dietary inulin improves distal colitis induced by detran sodium sulfate in the rat. American Journal of Gastroenterology. 96: 1486-1493.
Villegas, B., Costell, E. 2007. Flow behaviour of inulin–milk beverages. Influence of inulin average chain length and of milk fat content. International Dairy Journal. 17: 776–781.
Wang, Y. 2009. Prebiotics: Present and future in food science and technology. Food Research International. 42: 8-12.
Wijnands, M.V.W., Schoterman, H.C., Bruijntjes, J.P., Hollanders, V.M.H., Woutersen, R. A. 2001. Effect of dietary galacto-oligosaccharides on azoxymethane-induced aberrant crypt foci and colorectal cancer in Fischer 344 rats. Carcinogenesis. 22: 127–132.

Temas Selectos de Ingeniería de Alimentos 7 - 1 (2013): 25 - 36

El ajo y sus aplicaciones en la conservación de alimentos
D. Bender - Bojalil* y M. E. Bárcenas - Pozos
Departamento de Ingeniería Química, Alimentos y Ambiental, Universidad de las Américas Puebla. Ex hacienda Sta. Catarina Mártir S/N, San Andrés Cholula, Puebla. C.P.72810, México.
Resumen
El ajo (Allium sativum) es un bulbo perteneciente a la familia Liliaceae, que contiene una gran cantidad de compuestos azufrados, entre ellos la alicina, varias enzimas, aminoácidos libres y algunos minerales que contribuyen a su actividad antioxidante y antimicrobiana. La alicina es el principal compuesto activo en el ajo; sin embargo, es un componente muy volátil e inestable, cuya vida media es muy corta y puede descomponerse rápidamente en otros compuestos azufrados, que aún mantienen su actividad biológica. Dada la amplia funcionalidad del ajo, este vegetal ha ganado interés entre los investigadores como fuente de compuestos antimicrobianos y antioxidantes naturales para incrementar la vida de anaquel de distintos alimentos. Los resultados de diversos estudios, han demostrado la efectividad del ajo en la conservación de alimentos.
Palabras clave: ajo, Allium sativum, alicina, actividad antimicrobiana, actividad antioxidante.
Abstract
Garlic (Allium sativum) is a bulb member of the Liliaceae family which contains numerous organosulphur compounds, such as allicin, enzymes, aminoacids and a few minerals which contribute to its antioxidant and antimicrobial potential. Allicin is the main biologically active compound found in garlic, nevertheless, it is very unstable and decomposes rapidly into other organosulphur compounds, which still have remaining activity. Due to the wide functionality of garlic, it has gained interest by many investigators who have used it as a natural source of antimicrobial and antioxidant compounds to increase the shelf life of food. The results of several studies have demonstrated the efectiveness of garlic when used in food preservation.
Keywords: garlic, Allium sativum, allicin, antimicrobial activity, antioxidant activity.
Introducción
En los últimos años, los consumidores han mostradopreocupaciónporreducirelconsumo dealimentosconteniendoaditivos“sintéticos”, buscando cada vez más ingerir alimentos naturales o cercanos a lo “natural”. Esto ha
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Direccion electrónica: denisse.benderbl@udlap.mx
estimulado a los científicos a llevar a cabo estudios sobre la efectividad de productos naturales como aditivos, específicamente como antimicrobianos y antioxidantes. Entre los productos que han sido evaluados se encuentra el ajo, el cual ha despertado gran interés, debido a que desde tiempos antiguos ha sido utilizado con fines curativos con éxito. Se piensa que si el ajo es capaz de combatir a los microorganismos causantes de
enfermedades, es probable que también afecte a los responsables del deterioro de los alimentos. Se ha demostrado que el ajo contiene compuestos bioactivos con propiedades antimicrobianas y antioxidantes, que le permiten ser considerado como un alimento funcional. Es debido a lo anterior, que en este artículo se pretende presentar una descripción del ajo, así como abordar la capacidad antioxidante y antimicrobiana, la estabilidad y los usos de sus componentes activos en la conservación de los alimentos conelfindemostrarsudiversafuncionalidad.
Chile y Perú, concentran el 90% de la superficie cultivada a nivel mundial (Greco, 2011).
1.1. Características botánicas
Elgénero Allium contienemásde300especies de plantas; entre ellas se encuentra el Allium sativum, que es un bulbo perteneciente a la familia Liliaceae y subfamilia Allioideae. Sus características olorosas le permiten su denominación con el uso del término Allium quesignifica“oloroso”enlatín(Greco,2011).
Revisión bibliográfica
1. Aspectos generales del ajo
Diversas especies del género Allium, al que pertenece el ajo, han sido cultivadas durante miles de años por sus propiedades terapéuticas, higiénicas, su significado religioso, su sabor y aroma. Esta hortaliza es un condimento natural por excelencia y forma partedeloshábitosalimentarios yterapéuticos demuchasculturas(Greco,2011).
Su origen se ubica en Asia Central, en donde se utilizaba desde la más remota antigüedad. En China se estima que en el año 2000A.C.yaseconocíaelajoyformabaparte de la dieta diaria como condimento y componentemedicinalimportante.Tambiénse sabe que en Egipto alimentaban con ajos a los esclavos que construían las pirámides, porque se pensaba que les aportaba energía (López, 2007).
En la actualidad se cultivan diversas variedades de ajo en numerosos países del mundo. Los principales países productores son en su mayoría países asiáticos como China, India, Corea y Tailandia. Éstos, junto a otros 12 países, entre los cuales se encuentran España, Estados Unidos, Brasil, Argentina,
El ajo se caracteriza por tener un sistema radicular, al tener una raíz bulbosa compuesta de 6 a 12 bulbillos, reunidos en su base por medio de una película delgada para formar la “cabeza del ajo”. Cada bulbillo se encuentra envuelto por una hoja protectora blanca o rojiza, membranosa muy delgada. De la parte superior del bulbo nacen las partes fibrosas, que se introducen en la tierra para alimentar y anclar a la planta. Los tallos de la planta son fuertes y crecen desde 40 a más de 55 centímetros de largo, terminando por las flores. Las flores se encuentran contenidas en una espata membranosa que se abre longitudinalmente en el momento de la floración(Greco,2011).
1.2. Composición
El ajo fresco posee distintos componentes entre los que se destacan el agua y los carbohidratos, como la fructosa, compuestos azufrados, fibra y aminoácidos libres. Tiene altos niveles de vitaminas A y C y bajos niveles de vitaminas del complejo B. Asimismo, posee un alto contenido de compuestos fenólicos, polifenoles y fitoesteroles (Rahman, 2003). En la Tabla I se presentalacomposicióndelajofresco.
En general, el ajo presenta un mayor contenidodeproteínaqueotrosvegetales,pero asuveztieneuncontenidodegrasamenor.En
Tabla I. Composición en 100 g de ajo fresco
Composición
UnidadesCantidad
Aguag58.58
Energíakcal149
Proteínag6.36
Lípidos totalesg0.5
Carbohidratos (por diferencia)g33.06
Fibra total dietéticag2.1
Azúcares totalesg1
Lípidos
Ácidos grasos saturadosg0.089
Ácidos grasos monoinsaturadosg0.011
Ácidos grasos poliinsaturadosg0.249
Colesterolmg0
Vitaminas
Vitamina Cmg31.2
Tiaminamg0.2
Riboflavinamg0.11
Niacinamg0.7
Vitamina B6 mg1.235
Folatoµg3
Vitamina AUI9
Vitamina Emg0.08
Vitamina Kµg1.7
Minerales
Calciomg181
Hierromg1.7
Magnesiomg25
Fósforomg153
Potasiomg401
Sodiomg17
Zincmg1.16
Adaptado de USDA (2013)
cuanto a los minerales, el ajo tiene niveles importantes de potasio, fósforo, magnesio, sodio, calcio y hierro. También presenta un contenido moderado de selenio y germanio, pero su concentración depende de los minerales presentes en el suelo donde crece el
bulbo. Algunos compuestos en ajo intacto como lectinas (proteínas más abundantes en el ajo), prostaglandinas, fructanos, pectina, adenosina, algunas vitaminas y ácidos grasos, glicolípidos y fosfolípidos han sido ampliamente estudiados por su efecto
biológico. De interés actual se ha demostrado la importancia de algunas saponinas y sapogeninas, como β-clorogenina, ya que ha mostrado actividad antimicrobiana y antiinflamatoria, entre otras. Otros componentes, como alixina y selenio, se han investigado por sus propiedades antioxidantes (KrejciyPacurar,2010).
1.3. Propiedades ytoxicidad
El ajo tiene características muy variables, lo que lo hace ser un alimento funcional de muchos usos. Tiene una gran capacidad antioxidante, atribuida a sus compuestos azufrados, aminoácidos libres y selenio. También actúa como antimicrobiano, pues se hautilizadocomoconservadordealimentos,al inhibir el crecimiento de microorganismos debido a la presencia de sus componentes activos. Además, desde épocas remotas ha sido utilizado como saborizante para la preparación de muchos tipos de alimentos (Bhandari, 2012). Asimismo, estimula la destoxificación de las células y se ha utilizado como quimiopreventivo o coadyuvante para tratarelcáncer(Elkins,1995).
El ajo también se ha utilizado como descongestionante, ayudandoaliberareltracto respiratorio de mucosa. Adicionalmente, tiene características anti- ateroscleróticas, ya que disminuye la cantidad de depósitos grasos en los vasos sanguíneos. Funciona como antibiótico, al estimular el sistema inmunológico y ha demostrado tener propiedades anticoagulantes y antiparasitarias (Elkins,1995).
Sus características antiinflamatorias han permitido que se utilice en pacientes que padecen artritis, al reducir la inflamación de las articulaciones. Por otro lado, el ajo actúa como coadyuvante en la purificación de la sangre, al estimular el sistema linfático a eliminar los materiales residuales del cuerpo. También se ha visto que controla la tolerancia
a la glucosa y su consumo resulta benéfico para personas que padecen de hipo e hiperglicemia. Por último, el ajo tiene funciones anti hipertensivas y en Japón se reconoce como el tratamiento oficial para la altapresiónarterial(Bhandari,2012).
A pesar de que este vegetal se ha utilizado demaneraseguraenáreasculinarias, asícomo para fines médicos, se sabe que un consumo excesivo de ajo puede causar reacciones adversas. Es por ello que se recomienda una ingestión diaria máxima de dos dientes de ajo para adultos (Bhandari, 2012). En relación a esto, se ha demostrado que el componente activo mayoritario del ajo, la alicina, causa irritación cuando se consume excesivamente. De igual manera, otros compuestos azufrados liposolubles presentes en el ajo también han resultado ser tóxicos en grandes concentraciones(Rahman,2007).
Es por ello que se han realizado investigaciones con el fin de determinar el nivel de toxicidad y los efectos adversos que pudiera causar el ajo al abusar de su consumo. Amagase et al. (2001) realizaron estudios para determinar la seguridad de diferentes preparaciones de ajo y descubrieron que el consumo de este vegetal produce olor en el aliento y piel, y ocasionalmente reacciones alérgicas. Otros efectos adversos asociados con el ajo son desórdenes de estómago, diarrea, disminución de proteínas séricas y calcio, anemia, asma y dermatitis. También se considera que las personas que sufren trastornos de coagulación de la sangre deben usarel ajocon precaución,debidoaquepuede favorecer la aparición de hemorragias (López, 2007).
2. Potencial del ajo como agente antimicrobiano
Históricamente se cree que Louis Pasteur fue el primero que describió el efecto antibacteriano en jugo de ajo en 1858, para
tratar infecciones (Kumar yJain, 2010). El ajo contiene por lo menos 33 compuestos azufrados, varias enzimas, 17 aminoácidos y algunos minerales que contribuyen a su actividad antimicrobiana. De todas las especies de Allium, el ajo es el que contiene la mayor concentración de compuestos azufrados, lo que le da una actividad antimicrobiana muy potente. Los principales compuestos azufrados son la aliína, alicina, ajoeno, trisulfuro de dialilo, salilcisteína, vinilditiínas, disulfuro de alilpropilo, S-alilmercapto cisteína, entre otros. Entre las enzimas importantes en la actividad antimicrobiana se encuentran la alinasa, peroxidasa y mirosinasa. Los aminoácidos y sus glucósidos, en especial la arginina, también influyen de manera importante en la actividad antimicrobiana, al igual que el selenio, germanio, telurio y trazas de otros minerales(Bhandari,2012).
El compuesto biológico más activo en el
ajo es la alicina, que se genera por reacciones enzimáticas cuando el ajo se tritura o se corta. Este compuesto se forma cuando la aliína, aminoácido azufrado inodoro que se encuentra en el citoplasma de las células del ajo fresco intacto, entra en contacto con la alinasa, enzima presente en la vacuola, como consecuencia de la ruptura celular causada por la trituración o el corte (Fig. 1) (Bhandari, 2012). La reacción anterior ocurre extremadamente rápido, en ella más del 80% de aliína se metaboliza en los primeros 2 minutos(KyungyLee,2001).
La alicina es un componente muy volátil e inestable, tiene una vida media muy corta, incluso a temperatura ambiente. En unas cuantas horas, ésta puede descomponerse en muchos tipos de tiosulfinatos (Fig. 2) a través de diferentes vías metabólicas (Harris et al., 2001). Por medio de otras degradaciones no enzimáticas, los tiosulfinatos se transforman en otros compuestos azufrados tales como
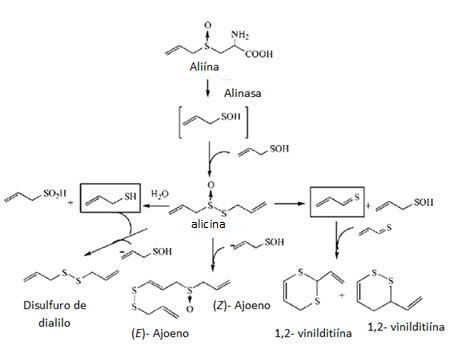
Fig. 1. Reacción enzimática de aliína. Adaptado de Kyung y Lee (2001).
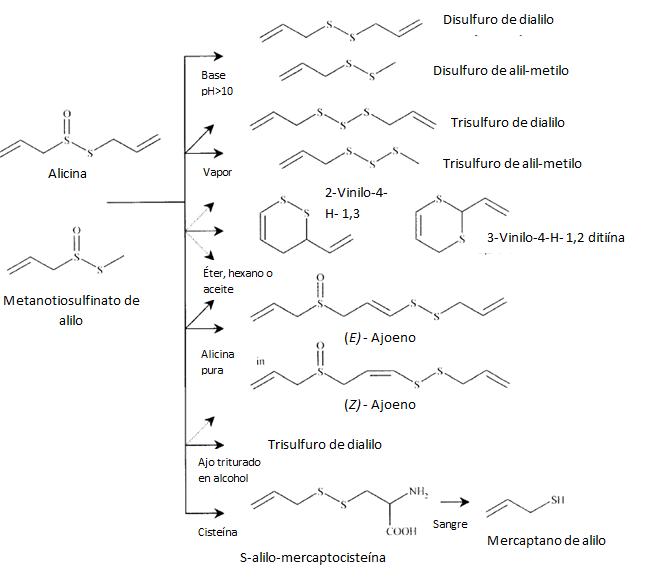
2. Descomposición de alicina en los principales tiosulfinatos. Adaptado de Harris et al. (2001).
mono, di, tri y tetrasulfuros, tioles, tiofenos y anhídridosulfuroso(Harris et al., 2001).
Fujisawa et al. (2008) estudiaron la estabilidad de la alicina en diferentes soluciones acuosas y etanólicas, así como en aceite vegetal. Comprobaron que la alicina es más estable en etanol que en agua, ya que mantiene su actividad 11 y 6 días en cada medio, respectivamente. En cuanto al aceite vegetal, la alicina mostró ser completamente inestable en este medio, conservándose solamente0.8horas.
Paraasegurarlaestabilidad delaalicina, en muchos procesos de deshidratación de ajo se han agregado β-ciclodextrinas y carbamidas, que forman complejos con la alicina para protegerla y prolongar su actividad hasta por 60días(Ilic et al., 2011).
Se considera que la alicina tiene actividad antimicrobiana porque modifica la biosíntesis de los lípidos y síntesis del RNA de los microorganismos y disminuye el perfil de lípidos de los mismos. Este compuesto activo reacciona rápidamente con grupos tiol libres, por ello se cree que el principal mecanismo antimicrobiano se produce a través de la
Fig.
interacción de alicina con enzimas que contienen grupos tiol, como proteasas y alcoholdehidrogenasas(Rahman,2007).
La alicina inhibe a más de 300 bacterias, tanto Gram-positivas como Gram-negativas, tales como Bacillus subtilis, Bacillus megaterium, Bacillus sphaericus, Bacillus polymyxya, Staphylococcus aureus, Escherichia coli (Kumar y Jain, 2010), Salmonella Typhy, Salmonella Paratyphy (Abraham, 2010) y Helicobacter pylori (O’Garaet al., 2000),entreotras.
En cuanto a hongos, se ha probado que los extractos de ajo disminuyen su absorción de oxígeno, reducen su crecimiento, inhiben la síntesisdelípidos,proteínasyácidosnucleicos y dañan sus membranas. El componente principal del ajo que inhibe el crecimiento de hongos es la alicina, aunque también se ha demostrado que otros compuestos activos
(trisulfuro de dialilo y ajoeno) tienen propiedades antifúngicas al inhibir la biosíntesis de fosfatidilcolina, provocando de esta manera la muerte celular (Harris et al., 2001). Entrelas cepas queson inhibidas porel ajo, se encuentra el Aspergillus luchuensis, Aspergillus flavus, Penicillium oxalicum, Rhizopus stolonifer, Mucor spp. y Scopulariopsis sp. (KumaryJain,2010).
Por otro lado, este vegetal también ha demostrado tener propiedades antiprotozoarias y antivirales. Se ha comprobado en varios estudios que la alicina, el ajoeno y varios compuestos organosulfurados son antiprotozoarios eficaces, ya que tienen efecto contra Trypansomes, Entamoeba histolytica, Giardia lamblia (Lun et al., 1994), Opalina ranarum, Opalina dimidicita, Balantidium enterozoon, Leishmania, Leptomas y Crithidia (Reuter et al., 1996). En cuanto a los efectos antivirales se han estudiado poco, aunque se ha demostrado que la alicina, el ajoeno y el trisulfuro de dialilo muestran actividad contra la influenza A y B, el citomegalovirus, rinovirus, el VIH, el virus del herpes simple tipo 1 y 2, la neumonía viral y el rotavirus (Harriset al., 2001).
3. Potencial como agenteantioxidante
El ajo tiene una capacidad antioxidante muy potente, debido a que muchos de sus componentes activos son eficaces para inhibir la formación de radicales libres. Además refuerzan el mecanismo de captación de radicales endógenos, aumentan las enzimas antioxidantes celulares como la superóxido dismutasa, catalasa y glutatión peroxidasa y protegen a las lipoproteínas de baja densidad delaoxidacióncausadaporlosradicaleslibres (López,2007).
Esta propiedad antioxidante sólo la adquiere el ajo cuando está manipulado, permitiendo que bajo esas condiciones se
forme la alicina y otros compuestos importantes. De manera contraria, el ajo intacto contiene una actividad oxidante, lo que noesdeseable(Bhandari,2012).
Entre los componentes antioxidantes de importancia en el ajo se encuentran los compuestos azufrados, selenio y aminoácidos libres, en especial la cisteína, glutamina, isoleucina y metionina. El componente que tiene la mayor capacidad antioxidante es la alicina, aunque su efecto es dependiente de la dosis y del tiempo (López, 2007). Ésta actúa como antioxidante al reaccionar con las enzimas que tienen grupos tiol libres, atrapando radicales libres, en especial radicales hidroxilo y de esta manera inhibiendo la producción de superóxido en el cuerpohumano(Rahman,2007).
Debido a la inestabilidad de la alicina, se han obtenido algunos extractos de ajo envejecido, que además de mantener su potencial antioxidante por más tiempo,
modifican compuestos inestables, como la alicina e incrementan el número de componentes estables hidrofílicos y altamente biodisponibles como el S-allil-mercapto cisteína y la S-allil cisteína. Estos extractos también contienen fitoquímicos, selenio y flavonoides, en especial la alixina, que mejoran su capacidad antioxidante (Rahman, 2007).
4. Aplicaciones del ajo como agente antimicrobiano y/o antioxidanteen alimentos
Debido a que los componentes activos del ajo tienen un espectro antimicrobiano amplio, se ha evaluado su uso en la conservación de diversos productos alimenticios. En cuanto a su capacidad antioxidante, se ha considerado esta propiedad para aumentar la vida de anaquel de algunos alimentos, buscando retardar principalmente la oxidación de lípidos en productos cárnicos. Es por ello, que continuamente se han realizado estudios para determinar la efectividad del ajo como agente antimicrobiano o antioxidante, con el fin de diversificar su uso en una mayor cantidad de alimentos.
En este sentido, Ayala-Zavala y GonzálezAguilar(2010)encapsularon aceiteesencial de ajo con β-ciclodextrinas para incrementar la estabilidad de los compuestos activos y lo aplicaron a tomates cortados frescos, extendiendo su vida útil hasta cinco semanas. Por otro lado, Gomes et al. (2011) probaron la efectividad de extractos de ajo encapsulados con β-ciclodextrinas como coadyuvantes en el proceso de irradiación, con el fin de disminuir la dosis para la inactivación de Salmonella spp. y Listeria spp., así como para reducir el impacto del tratamiento en la calidad sensorial de espinacas frescas. Se obtuvo un efecto sinérgico y una reducción del 50% de la dosis de irradiación. Por su parte, Luna (2012) demostró que la adición de ajo fresco a la formulación de pan parcialmente horneado almacenadoenrefrigeraciónpermiteprolongar
la vida útil del producto 14 días más de lo que selograconelpansinajo.
En otras investigaciones, Sallam et al. (2004) observaron el efecto de ajo fresco, ajo en polvo y aceite esencial de ajo en el crecimiento microbiano y la oxidación de lípidos en salchicha de pollo cruda. De la misma manera, Dewi et al. (2010) estudiaron el efecto de ajo fresco y en polvo en salchicha de pato. En ambas investigaciones, tanto la oxidación como el crecimiento de microorganismos se redujeron significativamente, permitiendo extender la vida útil de los productos sin importar el tipo de ajo utilizado. Similarmente, Kim et al. (2009) comprobaron el efecto antimicrobiano y antioxidante de diferentes formulaciones de ajo y butilhidroxianisol (BHA) en salchicha tipo emulsión, demostrando que la adición de BHA no incrementaba significativamente la efectividad antioxidante y antimicrobiana del ajo, pero la adición de este último, mejoraba significativamentesuconservación.
En cuanto a otros estudios relacionados con productos cárnicos, Park y Chin (2010) evaluaron la capacidad antioxidante y antimicrobiana de extractos de ajo utilizando distintos solventes y adicionándolos a medallones de carne de cerdo molida, con el fin de determinar si éstos podrían sustituir a los aditivos sintéticos. Los resultados mostraron que todos los extractos retardaban la oxidación de lípidos significativamente e inhibían el crecimiento de Listeria monocytogenes y Escherichia coli O157:H7. De igual forma, se investigó el potencial antioxidante y antimicrobiano de algunos compuestos azufrados presentes en el ajo contra la decoloración, oxidación de lípidos y crecimiento microbiano de carne de res. Se obtuvo un retraso significativo en la oxidación de oximioglobina y de los lípidos y una inhibición de cinco cepas inoculadas intencionalmente (Salmonella Typhimurium,
Otros estudios han probado la efectividad de extractos de ajo en la conservación de canales de aves frescas almacenadas en refrigeración, obteniendo una reducción significativa de la contaminación microbiana, al inhibir el crecimiento de microorganismos mesófilos y al reducir el crecimiento de coliformes totales y fecales (De MouraOliverira et al.,2005).
Asimismo, Pacheco-Guerrero et al. (2011) estudiaron el efecto de ajo en solución acuosa sobre la calidad microbiológica y oxidación lipídica en rebanadas de bagre dorado (Brachyplatystoma rousseauxii)almacenadasa 4 ºC, mostrando un retraso significativo en la oxidación de lípidos, así como en la proliferación de bacterias psicrotróficas, bacterias productoras de sulfuro de hidrógeno, bacterias ácido lácticas y del género Enterobacteriaceae,poralmenos15días.
En otras investigaciones, Schwartza et al. (2011) evaluaron el efecto de ajo en la calidadyestabilidaddeunapastadeaceitunas, obteniendo parámetros microbiológicos adecuados, así como una menor oxidación de lípidosenlapasta.
Del mismo modo, se probó la adición de diferentes concentraciones de ajo a yogurt asentado y batido para determinar el efecto de éste en parámetros físicos, químicos, microbiológicos y sensoriales durante su almacenamiento. Los resultados reflejaron una ausencia de mohos y levaduras en el yogurt. Además,laadicióndeajonoprovocó cambios significativos en la acidez, contenido de grasa, proteínas ni acetaldehído y mejoró su conservación hasta por 18 días (Gündoğdu et al.,2009).
Escherichia coli O157:H7, Listeria monocytogenes, Staphyllococcus aureus y Campylobacter jejuni) (Yin y Cheng, 2003). Por otra parte, Gheisari y Ranjbar (2012) investigaron la capacidad antioxidante y antimicrobiana de diferentes presentaciones de ajo (fresco, en polvo y aceite esencial) adicionadasacarnedecamello,almacenadaen refrigeración. Los resultados mostraron un retardo en la oxidación de lípidos y crecimiento microbiano, siendo los ingredientes más efectivos el ajo fresco o en polvo para la conservación de este producto. Asimismo,Park et al. (2008)adicionaronajo y cebolla en polvo a lomo y panza de cerdo con el fin de evaluar sus propiedades fisicoquímicas, antioxidantes y antimicrobianas, obteniendo un incremento en las tonalidades rojizas y amarillas del producto. La adición de estos componentes redujo el índice de peróxido, el contenido de productos oxidativos volátiles y la cuenta microbiana. Los investigadores concluyeron que la capacidad antioxidante que presenta el ajo es comparable a la que posee el ascorbato desodio.Kim et al. (2010)marinaroncarnede cerdo con jugo de ajo o cebolla para determinarsu efecto en laoxidación delípidos y calidad durante el almacenamiento en refrigeración.Seobtuvounadisminucióndela luminosidad ytonalidades amarillas respecto a la carne sin adición de jugos, así como un aumento en las sustancias reactivas al ácido tiobarbitúrico.Sensorialmente,losjugosdeajo y cebolla le proporcionaron a la carne una mayorsuavidadymejoresatributosdesabor.
Navas et al. (2006) evaluaron las propiedades antioxidantes y la estabilidad de aceite de maíz refinado ante el calor, adicionado con ajo. Los investigadores observaron que el ajo retardaba la oxidación delípidos,sinembargo,éstenomostróreducir la velocidad de oxidación a temperaturas de freído. Por otra parte, Gambacorta et al. (2007) adicionaron ajo a aceite de oliva extra virgen, demostrando que su adición incrementa la estabilidad del aceite significativamente.
También se ha utilizado el aceite esencial de ajo como antimicrobiano adicionado a películas comestibles. Pranoto et al. (2005) lo adicionaron a películas de quitosano, Du et al. (2009) a películas a base de puré de tomate, mientras que Seydim y Sarikus (2006) lo agregaron apelículas de aislado deproteínade suero de leche. Estos investigadores probaron su efectividad antimicrobiana contra Escherichia coli O157:H7, Staphylococcus aureus, Salmonella spp. y Listeria monocytogenes, obteniendo una inhibición satisfactoriadeestospatógenos.
Por todo lo anterior es posible afirmar que el ajo puede utilizarse efectivamente para inhibir o retardar el crecimiento microbiano, así como las reacciones de oxidación de lípidos.
AméricasPuebla(UDLAP),porelapoyo en el financiamientodesusestudiosdeposgrado.
Referencias
Abraham, J. 2010. Evaluation of antimicrobial activity of herbal extracts against Salmonella. Journal of Pharmacy Research. 3(8):1981-1983.
Amagase, H., Petesch, B.L., Matsuura, H., Kasuga, S. e Itakura, Y. 2001. Intake of garlic and its components. Journal of Nutrition. 131:955S-962S.
Ayala-Zavala, J. F. y González-Aguilar, G. A. 2010. Optimizing the use of garlic oil as antimicrobial agent on fresh-cut tomato through a controlled release system. Journal of Food Science. 75(7):M398- M405.
Bhandari, P. R. 2012. Garlic (Allium sativum L.): A review of potential therapeutic applications. International Journal of Green Pharmacy. 2:118.
Conclusiones y comentarios finales
A partir de la revisión anterior sobre el ajo y sus componentes activos, se puede entender más ampliamente la funcionalidad que tiene el mismo en la salud y dentro del área alimenticia. Debido a las capacidades antioxidantes yantimicrobianas intrínsecas del ajo, se han realizado cada vez más estudios que demuestran la efectividad del ajo en la conservación de alimentos, lo que ha permitidodiversificarsu uso. Lo anteriorseha hecho con el fin de crear más alternativas que permitan darle al consumidor un beneficio adicional, asegurando que los componentes activos del ajo no se pierdan durante su manipulaciónoextracción.
De Moura-Oliverira, K., Santos-Mendonça, R., De Miranda Gomide, L. y Vanetti, M. 2005. Aqueous garlic extract and microbiological quality of refrigerated poultry meat. Journal of Food Processing and Preservation. 29(2):98-108.
Dewi, M., Huda, N. e Ismail, N. 2010. Use of fresh garlic and garlic powder in duck sausages during refrigerated storage. Asian Journal of Food and Agro-Industry. 3(5):526-534.
Du, W. X., Olsen, C. W., Avena-Bustillos, R. J., Mchung, T. H., Levin, C. E., Mandrell, R. R., y Friedman, M. 2009. Antibacterial effects of allspice, garlic, and oregano essential oils in tomato films determined by overlay and vapor-phase methods. Journal of Food Science. 74(7):M390M397.
Elkins, R. 1995. Garlic: Nature’s amazing nutritional and medicinal wonder food. Woodland Publishing, Inc. Utah, EE. UU. 32 p.
Fujisawa, H. Watanabe, K., Suma, K., Origuchi, K., Kumagai, H., Seki, T. y Ariga, T. 2008. Biological and chemical stability of garlic-derived allicin. Journal of Food Chemisitry. 56:4229-4235.
Agradecimientos
La autora D. Bender-Bojalil agradece al Consejo Nacional de Tecnología y Ciencia (CONACYT) y a la Universidad de las
Gambacorta, G., Faccia, M. Pati, S. Lamacchia, C., Baiano, A. y La Notte, E. 2007. Changes in the chemical and sensorial profile of extra virgin olive
oils flavored with herbs and spices during storage. Journal of Food Lipids. 14:202–215.
Gheisari, H. R. y Ranjbar, V. R. 2012. Antioxidative and antimicrobial effects of garlic in ground camel meat. Turkish Journal of Veterinary and Animal Sciences. 36(1):13-20.
Gomes, C., Moreira, R. G., y Castell-Pérez, E. 2011. Microencapsulated antimicrobial compounds as a means to enhance electron beam irradiation treatment for inactivation of pathogens on fresh spinach leaves. Journal of Food Science. 76(6):E479-E488.
Greco, M .F. 2011. Estudio de procesos de deshidratación industrial de ajo con la finalidad de preservar alicina como principio bioactivo. Tesis de Licenciatura. Universidad Nacional de Cuyo. Argentina. 60 p.
Gündoğdu, E., Çakmakçi, S. y Dağdemir, E. 2009. The effect of garlic (Allium sativum L.) on some quality properties and shelf-life of set and stirred yoghurt. Turkish Journal of Veterinary and Animal Sciences. 33(1):27-35.
Harris, J. C., Cottrell, S. L., Plummer, S. y Lloyd D. 2001. Antimicrobial properties of Allium sativum (garlic). Applied Microbiology and Biotechnology 57:282–286.
Ilic, D. P., Nikolic, V. D. Nikolic, L. B., Stankovic, M. Z. Sanojevic, L. P. y Cakic, M. D. 2011. Allicin and related compounds: biosynthesis, synthesis and pharmacological activity. Physics, Chemistriy and Technology. 9(1):9-20.
Kim, Y. J., Jin, S. K., Park, W. Y., Kim, B. W., Joo, S. T. y Yang, H. S. 2010. The effect of garlic or onion marinade on the lipid oxidation and meat quality of pork during cold storage. Journal of Food Quality. 33:171-185.
Kim, Y. J., Nahm, B. A. y Choi, I. H. 2009. An evaluation of the antioxidant and antimicrobial effectiveness of different forms of garlic and BHA in emulsion-type sausages during refrigerated storage. Journal of Muscle Foods. 21:813–825.
Krejci, G. y Pacurar, M. 2010. Garlic Consumption and Health. Nova Science Publishers. Nueva York, EE. UU. 60 p.
Kumar, R. y Jain, P. 2010. Antimicrobial activity of Allium sativum ethanolic extract against food associated bacteria and fungi. Drug Invention Today: 2(4):229-232.
Kyung, K. H. y Lee, Y. C. 2001. Antimicrobial activities of sulfur compounds derived from salk(en)yl-l-cysteine sulfoxides in allium and brassica. Food Reviews International. 17(2):183–198.
López, M. T. 2007. El ajo, propiedades farmacológicas e indicaciones terapéuticas. Fitoterapia. 26(1):7881.
Lun, Z. R., Burri, C., Menzinger, M. y Kaminsky, R. 1994. Antiparasitic activity of diallyl trisulfide (Dasuansu) on human and animal pathogenic protozoa (Trypanosoma sp., Entamoeba histolyica and Giardia lamblia) in vitro Annales de la Societe Belgue de Medecine Tropicale. 74:51–59.
Luna, M. 2012. Evaluación de ajo como agente antimicrobiano para la conservación de pan parcialmente horneado y almacenado en refrigeración. Tesis de Maestría. Universidad de las Américas Puebla. México. 39 p.
Navas, P. B., Carrasquero-Durán, A. y Flores, I. 2006. Effect of black tea, garlic and onion on corn oil stability and fatty acid composition under accelerated oxidation. International Journal of Food Science and Technology. 41:243–247.
O’Gara E. A., Hill D. J. y Maslin D. J. 2000. Activities of garlic oil, garlic powder, and their diallyl constituents against Helicobacter pylori. Applied Environmental Microbiology.66:2269–2273.
Pachecho-Guerrero, J. V., Tomé, E., Guerra, M. y Raybaudi, R. 2011. Efecto antioxidante y antimicrobiano de sales de ácidos orgánicos y extractos naturales en filete de bagre (Brachyplatystoma rousseauxii) refrigerados. Revista Venezolana de Ciencia y Tecnología de Alimentos. 2(1):16-40.
Park, S. Y., y Chin, K. B. 2010. Evaluation of preheating and extraction solvents in antioxidant and antimicrobial activities of garlic, and their application in fresh pork patties. International Journal of Food Science and Technology. 45(2):365-373.
Park, S. Y., Yoo, S. S., Shim, J. H. y Chin, K. B. 2008. Physicochemical properties, and antioxidant and antimicrobial effects of garlic and onion powder in fresh pork belly and loin during refrigerated storage. Journal of Food Science. 73(8):C577-C584.
Pranoto, Y, Rakshit, S. K. y Salokhe, V. M. 2005. Enhancing antimicrobial activity of chitosan films by incorporating garlic oil, potassium sorbate and nisin. Food Science and Technology. 38(8):859-865.
Rahman, K. 2003. Garlic and aging: new insights into an old remedy. Ageing Research Reviews. 2(1):5793.
Rahman, M. S. 2007. Allicin and other functional active components in garlic: Health benefits and bioavailability. International Journal of Food Properties. 10:245–268.
Reuter, H. D., Koch, H. P. y Lawson, L. D. 1996. Therapeutic effects and applications of garlic and its preparations. Williams and Wilkins, EE. UU. 213 p.
Sallam, K. I., Ishioroshi, M y Samejima, K. 2004. Antioxidant and antimicrobial effects of garlic in chicken sausage. Food Science and Technology 37(8):849-855.
Seydim, A. C. y Sarikus, G. 2006. Antimicrobial activity of whey protein based edible films
incorporated with oregano, rosemary and garlic essential oils. Food Research International. 39(5):639-644.
Schwartza, M. M., Quitralb, V. V., Daccaretta, C. C. y Callejas, R. R. 2011. Efecto de la adición de ajo en la estabilidad y calidad sensorial de una pasta de aceituna. Grasas y Aceites. 62(3):337-343.
USDA. 2013. Nutrient data for raw garlic. Disponible: http://ndb.nal.usda.gov/ndb/foods/show/2953?fg=Ve getables+and+Vegetable+Products&man=&lfacet= &format=&count=&max=25&offset=150&sort=&ql ookup=. Accesado: 27/01/2013.
Yin, M. C. y Cheng, W. S. 2003. Antioxidant and antimicrobial effects of four garlic-derived organosulfur compounds in ground beef. Meat Science. 63(1):23-28.

Temas Selectos de Ingeniería de Alimentos 7 - 1 (2013): 37 - 47

Mecanismos de transferencia de calor que ocurren en tratamientos térmicos de alimentos
M.E. Pérez - Reyes* y M. E. Sosa - Morales
Departamento de Ingeniería Química, Alimentos y Ambiental, Universidad de las Américas Puebla. Ex hacienda Sta. Catarina Mártir S/N, San Andrés Cholula, Puebla. C.P.72810, México.
Resumen
Con frecuencia, durante el procesamiento, los alimentos se someten a diferentes tratamientos térmicos, con la finalidad de extender su vida de anaquel. En esta revisión se presentan los principales mecanismos de transferencia de calor involucrados en los diferentes tratamientos térmicos en alimentos, aplicados tradicionalmente en la industria, así como en las nuevas tecnologías que se están investigando. El objetivo de la revisión es dar a conocer los mecanismos de transferencia de calor que ocurren en cada uno de estos tratamientos, los principios que los rigen y algunas limitaciones.
Palabras claves: tratamiento térmico, mecanismos de transferencia de calor, microondas, radiofrecuencia, esterilización, cocción, freído, horneado.
Abstract
Often during processing foods are subjected to different heat treatments in order to extend their shelf life. In this review we present the main heat transfer mechanisms involved in the different heat treatments in food, traditionally applied in the industry, as well as new technologies that are being investigated. The aim of the review is to present the heat transfer mechanisms occurring in each of these treatments, the principles that govern and some limitations.
Keywords: thermal treatment, heat transfer mechanisms, microwave, radiofrequency, sterilization, cooking, frying, baking.
Introducción
El proceso mediante el cual se transmite energía de un medio o material a otro de menor temperatura se conoce con el nombre de transferencia de calor. La transferencia de calor ocurre en los tratamientos térmicos a los que se someten los alimentos, con los objetivos de aumentar su estabilidad, cocinarlosocalentarlosparasuconsumo.
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: marco.perezrs@udlap.mx
Existen tres diferentes mecanismos de transferenciadecalor:conducción,convección y radiación. Estos mecanismos de transferencia se pueden observar en los tratamientos térmicos de alimentos. Los tratamientos térmicos tradicionales generalmente involucran mecanismos de conducción y convección, mientras que han surgido nuevas tecnologías que utilizan la
radiación principalmente como mecanismo de transferenciadecalor.
La conducción ocurre cuando existe un gradiente de temperatura en un cuerpo, ya que se presenta una transferencia de energía de la región de alta temperatura a la de baja temperatura,porejemplocuandosecolocauna pieza de carne sobre una plancha caliente para cocinar. La convección es la transferencia de calor entre partes relativamente frías y calientes de un fluido por mezclado, por ejemplo,cuandosehierve agua.Porotrolado, la radiación es el mecanismo que implica la transferencia de energía radiante de una fuente a un receptor. Cuando esto sucede parte de la energía es absorbida por el receptor, lo que genera un aumento de temperatura en el mismo, como cuando se expone un material al sol o cuando un alimento se calienta en horno demicroondas.
El objetivo de esta revisión es analizar los mecanismos involucrados en la transferencia de calor durante algunos tratamientos térmicos tradicionales yaquéllos que ocurren cuando se
usan nuevas tecnologías. Los tratamientos discutidos son los que se aplican a alimentos quedeben calentarse, lapartedeingenieríadel fríonoseráabordadaenestetrabajo.
Revisión bibliográfica
1. Mecanismos detransferencia decalor involucrados en tratamientos térmicos tradicionales
La transferencia de calor está relacionada con el intercambio de calor entre cuerpos calientes y fríos los cuales son llamados fuente y receptor. Existen tres maneras diferentes en que el calor pasa de la fuente al receptor. Muchas delas aplicaciones en los tratamientos térmicos convencionales son combinaciones de ellas, conducción, convección y radiación (Kern, 1999). En la Fig. 1 se muestran los esquemas que ejemplifican la transferencia de calorbajolosdiferentesmecanismos.
A continuación se presentan algunos tratamientos térmicos tradicionales que involucranestosmecanismos.
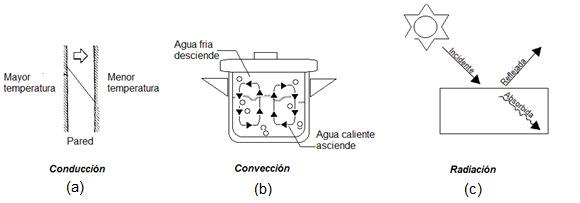
Fig. 1. Esquemas de transferencia de calor: a) conducción, b) convección y c) radiación. (Adaptada de Kern, 1999).
1.1 Pasteurización
La pasteurización ha sido el tratamiento térmico más extensamente usado para la conservación de alimentos en el siglo XX (Moraga et al., 2011). Es ampliamente utilizado en alimentos líquidos que son un buen sustrato para el desarrollo microbiano, como la leche, sin embargo puede ocasionar cambios nutricionales ó sensoriales, los cuales dependerán de la temperatura y el tiempo del tratamiento (Lang et al.,2010).
Existen varios métodos para pasteurización de alimentos líquidos. En el caso particular de la leche, se pueden mencionar tres, el primero es conocido como método de baja temperatura y largo tiempo, LTLT (por sus siglas en inglés), que consiste en aplicar temperaturas de 63-66oC durante 30 min. El segundo usa temperaturas de 71 a 75ºC durante 15s y es conocido como el método de altas temperaturas en un corto tiempo, HTST (por sus siglas en inglés). En ambos casos el producto requiere refrigeración posterior al tratamiento para lograr una vida de anaquel de alrededorunpardesemanas.El tercermétodo consiste en aplicar temperaturas de 135 a 140oCdurante2-10s,porsuscaracterísticases nombradocomoultrapasteurización,UHT(por sus siglas en inglés). Aunque en su nombre aparece la palabra pasteurización en realidad es un proceso más severo. Los alimentos ultrapasteurizados (UHT) se envasan asépticamente, no requieren refrigeración para su almacenamiento y su vida de anaquel es de 3a4meses(Badui,1993).
Los equipos con los que se efectúa generalmente la pasteurización de alimentos son los llamados intercambiadores de calor, aunque también se puede pasteurizar alimentos dentro de su envase y no usar intercambiadores. El intercambiadordeplacas, PHE (por sus siglas en inglés), es utilizado para el método HTST, consiste en un paquete
de placas de acero inoxidable sujetas en un marco. Las placas están corrugadas en un patrón diseñado para aumentar la turbulencia del flujo del medio y del producto (Riverol y Napolitano, 2005). Es muy utilizado en las industrias de alimentos, debido a su tamaño compacto y facilidad para el desmontaje y limpieza(GutyPinto,2003).
Usualmente la transferencia de calor en los líquidos es por convección, especialmente cuando éstos tienen una viscosidad baja. La convecciónnatural,inducidaporlosefectosde empuje térmico en un campo de fuerza gravitacional, se observa en el tratamiento de pasteurización LTLT. No obstante, la transferencia de calor por conducción se produce al mismo tiempo, sin embargo es intrascendente en comparación con la transferencia de calor por convección, para esteproceso(Erdogdu et al.,2010).
Durante la pasteurización por HTST, el alimentocirculaenun tuboosedeslizaenuna placa que se encuentra a una temperatura elevada. Estaplacaotuboseráelmedio quele transfiere calor al alimento y por lo tanto energía térmica (fase de calentamiento). Así, éste se calienta mediante un mecanismo de transferencia de calor por convección (Duarte yCristianini,2011).
La tasa de transferencia de calor está determinada por la ley del enfriamiento de Newton (Ec.1), que representa el efecto global delaconvección.
q=hAT −T (Ec.1)
donde q es la tasa de transferencia de calor, T −T es el gradiente de temperatura, Tp es la temperatura del medio que transfiere calor yT∞ latemperatura del alimento líquido, A es el área de transferencia de calor y h es el coeficiente de transferencia de calor, el cual depende de las propiedades del fluido
(densidad,viscosidad,expansióntérmica)ylas propiedades del proceso, como presión, velocidad y características del flujo (Duarte y Cristianini,2011).
1.2 Esterilización comercial
En los últimos años, los alimentos enlatados han sido considerados como el medio más efectivo de conservación, incluso con los avances recientes en otras técnicas (Duarte et al., 2009). La esterilización comercial es el proceso que ha llevado a generar este tipo de productos estables sin refrigeración, con una vida de anaquel incluso de varios años. Duranteelproceso,losalimentossonelevados a una temperatura específica, la cual es mantenida por un tiempo predeterminado y luego enfriados, en un recipiente herméticamente sellado. Estos efectos térmicos aseguran la inactivación enzimática y microbiana, generando un producto estable. Sin embargo éstos mismos causan la pérdida de propiedades sensoriales y nutricionales (DuarteyCristiniani,2011).
Los mecanismos de transferencia de calor durante el tratamiento térmico de un alimento enlatado son de conducción para los sólidos, convección para alimentos líquidos, convección y conducción para alimentos líquidos quecontienen partículas yconvección seguida de conducción para alimentos líquidos que contienen almidón o exhiben alta viscosidad (Erdogdu et al., 2010). La transferencia de calor en la esterilización de alimentos sólidos es descrita por la ecuación deFourier(Ec. 2), con condiciones defrontera descritas por su relación con el coeficiente de transferencia de calor h en la superficie del envase(Ec.3)(Santana et al., 2011).
k∗∇T=ρ∗ ∗ (Ec.2)
donde k es la conductividad térmica, es la densidad, Cp es el calor específico, n es el número de moles, T es la temperatura y t es el tiempodecalentamiento.
En alimentos como atún enlatado, jarabes espesos, purés y concentrados, se debe suponer que la transferencia de calor es por conducción para este tipo de tratamiento (Erdogdu et al.,2010).La cantidaddeflujode calorporconvección dQ,esdadapor(Ec.4)
− (Ec.4)
donde el término –dt/dx se llama gradiente de temperatura, tiene un signo negativo debido a que la temperatura mayor durante este proceso se encuentra en la cara exterior del alimento enlatado y menor en el interior de este. Por lo tanto la cantidad instantánea de transferencia de calor es proporcional al área A y a la diferencia de temperatura dt que impulsa el calor a través del espesor del alimento dx (Kern,1999).
1.3 Cocción por medio acuoso yasado
La cocción de los alimentos conduce a la mejora de las cualidades microbiológicas y organolépticas, destruye las toxinas y los factores antinutricionales, y aumenta la digestibilidad y la biodisponibilidad de los nutrientes(Gouado et al.,2011).
La transferencia de calor en la cocción por medio acuoso es por convección. A pesar de usar temperaturas relativamente bajas, es un método bastante rápido debido a la densidad del agua y la temperatura de condensación (McGee et al., 1999). Sin embargo si se encuentran partículas solidas en el medio acuoso latransferenciadecaloren estas es por conducción.
=h∗(T −T ) (Ec.3)
La transferencia de calor en la cocción por asado ocurre por conducción. Se observa
cuandounalimentoescolocadoenlaparrillaa una temperatura aproximada de 160°C, el calor es transmitido de la superficie de la parrilla al alimento. En ese momento inicia el proceso de cocción, cuando el calor empieza a penetrar el alimento. Posteriormente, la temperatura del alimento excederá los 100°C, el aguaseevapora ydependiendo del alimento ocurren reacciones que provocan diferentes tipos de oscurecimiento (Zorrilla y Singh, 2000).
Una vez que el calor ha sido transferido del medio de cocción a la superficie del alimento, éste debe seguir penetrando a través del alimento hasta llegar al centro. La medida de una cocción eficiente depende del grado de penetración del calor al centro del alimento (McGee et al.,1999).
Sin embargo, una cocción excesiva ocasionalapérdidadealgunosmicronutrientes importantes(Gouado et al.,2011).
1.4. Freído
El freído es un tratamiento térmico tradicional para la preparación de alimentos en todo el mundo, debido a la comodidad y rapidez en la preparación de alimentos semielaborados para cocinar en casa (Debnath et al., 2012), esto se debe a la velocidad del proceso, como también, a los sabores, aromas y texturas que se producen en el alimento (Sunisa et al., 2011). De igual forma, ha influido en la popularidaddelproceso,lagrandisponibilidad de freidoras eléctricas compactas y cerradas (Debnath et al.,2012).
La calidad de los productos obtenidos dependedelascondicionesenqueserealiceel freído, el tipo de aceite y alimento durante el proceso(Alvis et al.,2009).Elaceite juegaun rol doble en la elaboración de productos fritos ya que sirve como un medio para la transferencia de calor y también contribuye a
la textura y el sabor del alimento (Debnath et al.,2012).
Al ser sumergido el alimento en aceite caliente, su temperatura aumenta rápidamente, el agua que contiene se evapora, por lo que la superficie de éste empieza a deshidratarse, se forma una corteza, la evaporación empieza a trasladarse al interior del producto. La temperatura de la superficie del alimento alcanzaladelaceite ylainternaaumentahasta llegar a los 100°C. La velocidad de transferencia de calor al alimento depende de la diferencia de temperaturas entre éste y el aceite, así como también del coeficiente de transferencia de calor por convección. Por lo tanto, la transferencia de calor en este tratamiento es por convección en la superficie del alimento y por conducción en el interior delmismo(Alvis et al,2009).
La velocidad de transferencia de calor por convección depende de la oportunidad de formación de corrientes en el líquido y de la velocidad del flujo en dichas corrientes. El rango de operación de alta temperatura para que el alimento experimente las debidas transformaciones químicas yfísicas es de 140180°C(Ziaiifar et al., 2008).
El freído es una operación unitaria interesante que se ha estudiado ampliamente, desde el punto de vista de transferencia de masa (pérdida de humedad y ganancia de aceite), así como de transferencia de energía, ya que estos factores afectan la velocidad de transferencia de calor. En la Tabla I se muestran algunos coeficientes convectivos de transferencia de calor para el freído de diversosalimentos.
1.5. Horneado
El horneado es un proceso de transferencia de calor y de masa simultáneo. Durante la cocción, el calor se transfiere principalmente
Tabla I. Coeficientesconvectivosdetransferenciadecalor(h )reportados paraalgunosprocesosdefreído.
AlimentoTemperaturade freído(°C)
Mediodefreído h (W/m2°C) Referencia
Ñame 140-180 Aceitedesoya148-204Alvis et al .(2009)
Papas120Aceitedegirasol250Yamsaengsung et al (2008)
Carnedecerdo90-110Aceitedegirasoló mantecadecerdo 174-226Sosa-Morales et al (2006)
Placasdepollo130-150Aceitedegirasol207-331Vélez-Ruiz et al. (2002)
Panfrito175Aceitedegirasol300
por: (a) convección del medio de calentamiento, (b) por la radiación de las paredes del horno y (c) por conducción como resultado del calentamiento por contacto con la superficie caliente en la parte inferior (Dermirkol et al., 2006). Este tratamiento se caracteriza por la baja humedad y las altas temperaturas(DumasyMital,2002).
Generalmente el horneado por convección forzada es preferido, al usar hornos con circulación de aire inducida. El calor es transferido al alimento por el aire circundante (Dumas y Mital, 2002), con flujo paralelo al alimento (Banooni et al., 2008). La radiación de calor en el horno implica un método sin contacto por medio de un calentamiento electromagnético, por ejemplo, radiación infrarroja(DumasyMital,2002).
A pesar de usar altas temperaturas, el horneado es un método lento, ya que la trasferencia de calor por convección del aire o radiación por las paredes del horno, es poco eficiente (McGee et al., 1999). Algunos coeficientes convectivos del proceso de horneadosereportanenlaTablaII.
McGee et al. (1999)
2. Mecanismos detransferencia decalor involucrados en tratamientos térmicos que emplean nuevas tecnologías
2.1 Microondas
Además del uso de hornos de microondas a nivel doméstico, en los últimos años las microondas se han utilizado como una alternativa a diferentes tratamientos térmicos, como el escaldado, la pasteurización y el secado. Esto es debido a las ventajas que presenta en cuanto a la generación de energía frente a otros tratamientos (Sosa-Morales et al.,2009).
El calentamiento por microondas es una técnica relativamente nueva, para el tratamiento térmico selectivo, corto e intenso. La velocidad del calentamiento por microondas ha sido probada numerosas veces y en muchos casos ha resultado superior a los tratamientos tradicionales. Algunas desventajas de esta tecnología son calentamiento no uniforme, disminución o no presencia de dorado y una incompleta destrucción microbiana (Choi et al., 2011).
Tabla II.Coeficientesconvectivosdetransferenciadecalor(h)reportadosparaalgunosprocesosdehorneado.
Alimento
Masa“Mlenci”
Temperaturadeaireenel horno(°C) h (W/m2°C)
Referencia
70°C9.745 Seruga et al .(2007)
Galletas190-210°C30-38.1Dermirkol et al .(2006)
Pizza191-218°C780-801DumasyMittal.(2002)
Galletas190-210°C30-38.1Dermirkol et al .(2006)
Este calentamiento se origina por la interacción del campo electromagnético con la materia por medio de mecanismos dieléctrico (Kowalsi et al., 2012) y depende tanto de las características del alimento, como de su composición química, su estado físico, su geometría (Swain et al., 2004). En los hornos domésticos, las microondas son generadas por un dispositivo conocido como magnetrón, que transforma la frecuencia de la línea (60 Hz) a microondas (2450 MHz). Las ondas son conducidas a través de una guía o canal hasta la cavidad del horno, donde penetran el alimento yrebotan en las paredes, volviendo a penetrar en el alimento. Un esquema del funcionamiento del horno de microondas se muestraenlaFig.2.
El calentamiento por microondas es favorecido por la presencia de moléculas de aguaenelalimento(Kowalsi et al.,2012).Los alimentos que contienen moléculas polares como el agua se calientan rápidamente cuando se expone a la radiación de microondas, debido alafricción molecular, generadaporla rotación dipolar de moléculas en la presencia de un campo eléctrico alternativo (Kowalsi et al.,2012).
La temperatura final que alcanza el alimento se debe a la absorción de energía eléctrica desde el campo de microondas y a la
transferencia de calor por conducción y convección(Swain et al., 2004).
2.2 Radiofrecuencia
El calentamiento por radiofrecuencia, o calentamiento dieléctrico capacitivo, es reconocido como una tecnología de electrocalentamiento rápido el cual emplea un rango de frecuencias de 1 a 300 MHz (Farag et al., 2011). Es una tecnología prometedora para la aplicación en alimentos, ya que permite el calentamiento rápido yrelativamenteuniforme deéstos(Anese et al.,2008).
El calentamiento es generado cuando un generador de radiofrecuencia produce un campoeléctricoalternoentredoselectrodosen un sistema de radiofrecuencia. El alimento sujeto al tratamiento se coloca entre los electrodos, donde la corriente alterna provoca que las moléculas polares en el alimento oscilen continuamente al tratar de alinearse con el campo eléctrico, un esquema de este movimiento se muestra en la Fig.3 (Ahmed et al, 2007). Por ejemplo en 27.12 MHz, la alternancia del campo eléctrico es de 27, 120,000 ciclos por segundo. La fricción resultante del movimiento de rotación de las moléculas y el desplazamiento de carga espacial, provocan el aumento de la temperatura(Orsat et al.,2004).
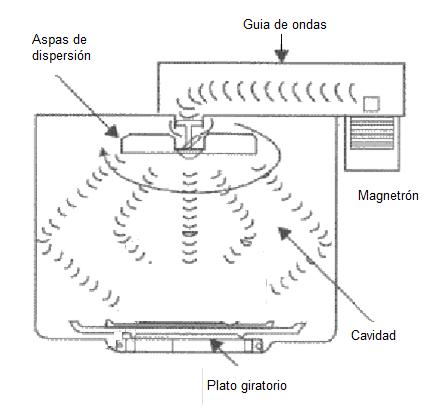
Fig. 2. Representación gráfica de la generación y distribución de microondas en un horno doméstico (Adaptada de Bastian et al., 2001).
Las propiedades dieléctricas afectan la distribución de energía electromagnética durante el calentamiento. Estas son la constante dieléctrica dependiente de la temperatura, la cual se describe como la capacidad del alimento paraalmacenarenergía ante la presencia de un campo eléctrico aplicado y el factor de pérdida dieléctrica el cualsedefinecomolacapacidaddedisipación de energía. Estas propiedades dieléctricas pueden variar ampliamente en los alimentos (Basaran-Akgul et al.,2008).
En cuanto a alimentos, se están investigando tratamientos con radiofrecuencia con el objetivo de erradicar plagas en frutas y leguminosas, así como pasteurizar productos secos como las almendras. La Tabla III
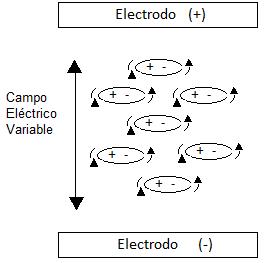
Fig. 3. Esquema de la rotación dipolar de moléculas durante el tratamiento con radiofrecuencia (Adaptado de Singh y Heldman, 2009).
muestra algunos reportes de las aplicaciones deradiofrecuenciaconestosfines.
Conclusiones y comentarios finales
Los mecanismos de transferencia de calor: conducción, convección y radiación aparecen en los tratamientos térmicos para alimentos de manera individual o combinada. El grado de efectividad de éstos dependerá de las condiciones de proceso y del alimento. Las nuevas tecnologías buscan combinar estos mecanismos para lograr una mayor eficiencia y rapidez en la transferencia de calor en los alimentos y de esta manera conservar en mayorgradosuspropiedades.
Tabla III.Aplicaciónde radiofrecuencia con diferentes fines enalimentos.
AlimentoAplicaciónReferencia
Garbanzo,chícharo ylentejas
Mangos
Desinfestacióncontra mosca India Wang et al. (2010)
Desinfestacióncontra moscas de la fruta
Sosa- Morales et al. (2009)
ArrozErradicaciónde plagasMirsoheini,S.M.H. et al. (2009)
Arroz
Desinfestacióncontra gusano de la fruta
Laguna-Solar et al. (2007)
HuevoPasteurización Dumas yMittal. (2006)
Manzanas Desinfestacióncontra gusano de la manzana Wang et al. (2006a)
NuezDesinfestación contra polillas Wang et al. (2006b)
NaranjasDesinfestacióncontra moscas de la fruta
Agradecimientos
LosautoresagradecenalCONACYT(Consejo Nacional de Ciencia y Tecnología) y a la UDLAP (Universidad de las Américas Puebla) por las becas otorgadas a M.E. Pérez Reyes para realizar sus estudios de Maestría en Ciencias, así como al CONACYT por el proyecto168990. Referencias
Ahmed, J., Ramaswamy, H.S. y Alli, I. 2007. Protein denaturation, rheology, and gelation characteristics of radio-frequency heated egg white dispersions. International Journal of Food Properties.10:145161.
Alvis, A., Córtes, L.E., y Páez, M. 2009. Transferencia de calor y materia durante la fritura de trozos de ñame (Dioscorea alata). Información Tecnológica 20(1): 99-109.
Anese, M., Sovrano, S. y Bortolomeazzi, R. 2008. Effect of radiofrequency heating on acrylamide
Birla et al. (2005)
formation in bakery products. European Food Research and Technology. 226: 1197-1203.
Badui, S. 1993. Química de los alimentos. Cuarta edición. Pearson Educación. México. 603-604p.
Banooni, S., Hosseinalipour, S.M., Mujumdar y A.S., Taheran, E. 2008. Impingement heat transfer effects on baking of flat bread. Drying Technology. 26: 910919.
Basaran-Akgul, N., Basaran, P., y Rasco, B.A. 2008. Effect of temperature (−5 to 130 °C) and fiber direction on the dielectric properties of beef semitendinosus at radio frequency and microwave frequencies. Journal of Food Science. 73(6): 243249.
Bastian, P., Either, W., Huber, F., Jaufmann, N., Manderla, J., Spielvogel, O., Springer, G., Stricker, F.D. y Tkotz, K. 2001. Electrotecnia. Primera edición. Ediciones Akal. España. 423p.
Birla, S.L, Wang, S., Tang, J., Fellman, J.K., Mattinson, D.S. y Lurie, S. 2005. Quality of oranges as influenced by potential radio frequency heat treatments against Mediterranean fruit flies. Postharvest Biology and Technology. 38: 66–79.
Choi, W., Nguyen, L.T., Hyun. S. y Jun, S. 2011. A microwave and ohmic combination heater for
uniform heating of liquid–article food mixtures. Journal of Food Science. 7(9): E576-E585.
Debnath, S., Rastogi, N.K., Gopala, A.G. y Lokesh, B.R. 2012. Effect of frying cycles on physical, chemical and heat transfer quality of rice bran oil during deep-fat frying of poori: An Indian traditional fried food. Food and Bioproducts Processing. 90: 249-256.
Dermirkol, E., Erdogdu, F. y Koray, T. 2006. A numerical approach with variable temperature boundary conditions to determine the effective heat transfer coefficient values during baking cookies. Journal of Food Process Engineering. 29: 478-497
Duarte, P.E., y Cristianini, M. 2011. Determining the convective heat transfer coefficient (h) in thermal process of foods. International Journal of Food Engineering. 7(4): 1-22.
Duarte, P.E., Ferramola , T., Lima, A.A., y Cristianini, M. 2009. Evaluation of methodologies for mathematical modeling of packaged conductive foods heat process. International Journal of Food Engineering. 5(4): 1-15.
Dumas, C., y Mittal, G.S. 2002. Heat and mass transfer properties of pizza during baking. International Journal of Food Properties. 5(1): 161-177.
Erdogdu , F., Uyar, R., y Koray, T. 2010. Experimental comparison of natural convection and conduction heat transfer. Journal of Food Process Engineering 33: 85-100.
Farag, K.W., Lyng, J.G., Morgan, D.J. y Cronin, D.A 2011. A comparison of conventional and radio frequency thawing of beef meats: effects on product temperature distribution. Food and Bioprocess Technology. 4: 1128-1136.
Gouado, I., Demasse, M.A., Etame, L.G., Meyimbo, O., Ruphine, S. Ejoh, A. y Fokue, E. 2011. Impact of three cooking methods (steaming, roasting on charcoal and frying) on the β-carotene and vitamin C contents of plantain and sweet potato. American Journal of Food Technology. 6(11): 994-1001.
Gut, J.A.W. y Pinto, J.M. 2003. Selecting optimal configurations for multisection plate heat exchangers in pasteurization processes. Industrial & Engineering Chemistry Research. 42(24): 61126124.
Kern, D.Q. 1999. Procesos de transferencia de calor Trigésima primera edición. CECSA. México. 1416p.
Kowalsi, S., Lukasiewickz, M., Bednarz, S. y Panus, M. 2012. Diastase number changes during thermal and microwave processing of honey. Czech Journal of Food Science. 30(1): 21-26.
Lagunas-Solar, M. C., Pan, Z., Zeng, N. X., Truong, T. D., Khir, R. yAmaratunga K. S. P. 2007. Application of radiofrequency power for non‐chemical disinfestation of rough rice with full retention of quality attributes. Applied Engineering in Agriculture. 23(5): 647‐654.
Lang, X.Y., Wang, J.Q., Bu D.P., Shen, J.S., Zheng, N. y Sun, P. 2010. Effects of heating temperatures and addition of reconstituted milk on the heat indicators in milk. Journal of Food Science. 75(8): 653-658.
McGee, H., McInerney, I y Harrus, A. 1999. The virtual cook: Modeling heat transfer in kitchen. Physics Today. 30(5): 30-36.
Mirhoseini, S.M.H., Heydari, M., Shoulaie, A. y Seidavi, A.R. 2009. Investigation on the possibility of foodstuff pest control using radiofrequency based on dielectric heating (case study: rice and wheat flour pests). Journal of Biological Sciences. 9(3): 283-287.
Moraga, N., Torres, A., Guarda, A. y Galotto, M.J. 2011. Non-Newtonian canned liquid food, unsteady fluid mechanics and heat transfer prediction for pasteurization and sterilization. Journal of Food Process Engineering. 34: 2000-2025.
Orsat, V., Bai, L. y Raghavan, G.S.V. 2004. Radiofrequency heating of ham to enhance shelf-life in vacuum packaging. Journal of Food Process Engineering. 27: 267-283.
Riverol, C., y Napolitano, V. 2005. Estimation of fouling in a plate heat exchanger through the application of neural networks. Journal of Chemical Technology and Biotechnology. 80: 594-600.
Santana, F., Duarte, P.E. y Cristianini, M. 2011. Determination of the convective heat transfer coefficient (h) in the sterilization of retortable pouches. International Journal of Food Engineering. 7(1): 3-14.
Seruga, B., Budzaki, S. y Ugarcic, Z. 2007. Individual heat transfer modes during baking of “mlinci” dough. Agriculturae Conspectus Scientificus 72(3): 257-263.
Singh, R.P. y Heldman, D.R. 2009. Introduction to food engineering. Cuarta edición. Academic Press. China. 373p.
Sosa-Morales, M.E., Tiwari G., Wang, S., Tang, J., Garcia, H.S. y Lopez-Malo, A. 2009. Dielectric heating as a potential post-harvest treatment of desinfesting mangoes, Part I: Relation between dielectric properties and ripening. Biosystems Engineering. 103: 297-303.
Sosa-Morales, M.E., Orzuna-Espíritu, R. y Vélez-Ruiz, J.F. 2006. Mass, thermal and quality aspects of deep-fat frying of pork meat. Journal of Food Engineering. 77: 731-738.
Sunisa, W., Worapong, U., Sunisa, S., Saowaluck, J. y Saowakon, W. 2011. Quality changes of chicken frying oil as affected of frying conditions. International Food Research Journal. 18: 615-620.
Swain, M.V.L., Rusell, S.L., Clarke, R.N. y Swain, M.J. 2004. The development of food simulants for microwave oven testing. International Journal of Food Science and Technology. 39: 623-630.
Velez-Ruiz, J.F., Vergara-Balderas, F.T. y SosaMorales, M.E. 2002. Effect of temperature on the physical properties of chicken strips during deep-fat frying. International journal of food properties. 5(1): 127-144.
Wang, S., Birla, S.L., Tang, J. y J.D. Hansen. 2006a. Postharvest treatment to control codling moth in fresh apples using water assisted radio frequency
heating. Postharvest Biology and Technology. 40: 89–96.
Wang, S., Tang, J., Sun, T., Mitcham, E.J., Koral, T. y Birla, S.L. 2006b. Considerations in design of commercial radio frequency treatments for postharvest pest control in in-shell walnuts. Journal of Food Engineering. 77: 304–312.
Wang, S., Tiwari, G., Jiao, S., Johnson, J.A. y J. Tang. 2010. Developing postharvest disinfestation treatments for legumes using radio frequency energy. Biosystems Engineering. 5: 341-349.
Yamsaengsung, R., Rungsee, C. y Prasertsit, K. 2008. Simulation of the heat and mass transfer processes during the vacuum frying of potato chips. Songklanakarin Journal of Science and Technology. 30(1): 109-115.
Ziaiifar, A.M., Achir, N., Courtois, F., Trezzani, I y Trystram, G. 2008. Review of mechanisms, conditions, and factors involved in the oil uptake phenomenon during the deep-fat frying process. International Journal of Food Science and Technology. 43: 1410-1423.
Zorrilla, S., y Singh, P. 2000. Heat transfer in meat patties during double-sided cooking. Food Science and Technology Research. 6(2): 130-135.

Temas Selectos de Ingeniería de Alimentos 7 - 1 (2013): 48 - 56

Microencapsulación de compuestos activos con quitosano
I. A. Flores - Belmont* y M. T. Jiménez - Munguía
Departamento de Ingeniería Química, Alimentos y Ambiental, Universidad de las Américas Puebla.
Ex hacienda Sta. Catarina Mártir S/N, San Andrés Cholula, Puebla. C.P.72810, México.
Resumen
La microencapsulación de diversos compuestos bioactivos empleando las técnicas de emulsión y extrusión, incrementa la biodisponibilidad de éstos. Además, el secado por atomización se ha reportado como una técnica muy viable, debido a que se obtienen partículas de diámetros pequeños y su aplicación es amplia. La elaboración de microcápsulas depende en gran medida del tipo de agente encapsulante utilizado. El quitosano es un biopolímero que, debido a su peso molecular y a su grado de desacetilación, resulta ser un buen material encapsulante. En la presente revisión se dan a conocer los principios de diversas técnicas de microencapsulación, en las cuales se ha utilizado al quitosano, resaltando las propiedades de éste como buen agente encapsulante.
Palabras claves: quitosano, microencapsulación, secado por atomización, extrusión, emulsión, compuestos bioactivos.
Abstract
The microencapsulation of several bioactive compounds, using the emulsification and extrusion techniques, increases the bioavailability of these. Besides, spray drying has been reported as a very efficient technology for microencapsulation due to the particles obtained of small particle diameters and its wide application. The preparation of microcapsules depends largely on the nature of the encapsulating agent used. Chitosan is a biopolymer that, due to its molecular weight and its degree of deacetylation, demonstrates to be a good encapsulating material. In this review, the principles of some microencapsulation techniques are presented, highlighting the use of chitosan as a good encapsulating agent.
Keywords: chitosan, microencapsulation, spray-drying, extrusion, emulsion, bioactive compounds.
Introducción
Laestructuradelos alimentos yel contenido denutrientessonfactoresdeterminantespara lapromocióndelaactividadbiológicadelos compuestos bioactivos, los cuales benefician
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: isela.floresbt@udlap.mx
a la salud (Onwulata, 2012). La microencapsulaciónesunprocedimientoque incrementa o mantiene la viabilidad de diversos compuestos bioactivos. Actualmente, esta técnica se emplea para conservar una amplia variedad de probióticos, vitaminas, antioxidantes, sabores,entreotros.
Existen diversas técnicas para la microencapsulación de compuestos con actividad biológica, de las cuales, el secado por atomización, emulsificación y extrusión hanreportadoresultadosfavorables.
En la industria de alimentos se emplean diversos materiales que funcionan como recubrimiento, mejor conocidos como materiales encapsulantes. Estos materiales pueden ser de origen natural o sintético. Algunosbiopolímerosbiodegradablesquese han sugerido en diversas investigaciones son colágeno, gelatina, albúmina, quitosano yalginato,entreotros.
Específicamente, el quitosano ha demostrado ser un excelente material encapsulante gracias a las propiedades que presenta,entre lasquedestacanlaliberación selectiva de compuestos activos en el intestino, además de otorgar a las micropartículas mayor estabilidad, una forma más definida y un tamaño homogéneo.
En consecuencia, el propósito de esta revisión es proporcionar información acerca de las diversas técnicas de microencapsulación de compuestos activos conquitosanocomomaterialencapsulante.
Revisión bibliográfica
1. Microencapsulación de compuestos bioactivos
La microencapsulación es una técnica mediante la cual pequeñas gotas líquidas, partículas gaseosas o sólidas, se recubren con una pared polimérica porosa conteniendo una sustancia activa. El término microencapsulación en la industria de alimentos se refiere a la encapsulación de sustancias de bajo peso molecular o de
pequeñas cantidades de determinados compuestos(Parra,2011).Lupo et al.(2012) se refieren a esta técnica como la obtención de una barrera que aletarga reacciones químicas, entre el compuesto activo y el medio ambiente, fomentando el aumento de la vida útil, promoviendo la liberación gradual y facilitando su manipulación al modificar el estado físico del compuesto activo.
En la industria, esta técnica ha obtenido un importante valor debido a la protección que adquieren las sustancias encapsuladas, resguardándolas de factores ambientales (calor y humedad) y salvaguardando su integridad cuando son empleadas en la elaboración de alimentos funcionales (Parra, 2011).
La selección de la técnica de microencapsulación adecuada se rige por las propiedades físicas y químicas del núcleo y el recubrimiento (material encapsulante) asó como por la aplicación que se le dará a las microcápsulas obtenidas. La Tabla Imuestra diferentes métodos usados para la preparación de sistemas alimentarios microencapsulados. Los materiales de recubrimiento normalmente son materiales capaces de formar películas y se pueden seleccionar de una amplia variedad de polímeros naturales o sintéticos, dependiendo el compuesto a encapsular (DesaiyPark,2005a).
2. Quitosano como agenteencapsulante
Los materiales encapsulantes deben ser sustancias capaces de formar estructuras alrededor de los compuestos bioactivos (núcleo), llamadas paredes, que protejan al núcleo contra el deterioro y liberación bajo condicionesdeseadas(Parra,2011).
Estudios recientes aluden la importancia del quitosano como material encapsulante.
Tabla I. Materiales empleados para la microencapsulación de compuestos activos.
Categoría
Carbohidratos
Celulosa
Gomas
Lípidos
Proteína
Material encapsulante Técnica empleada
Almidón, maltodextrina, quitosano, sólidos de jarabe de maíz, dextrina, almidón modificado, ciclodextrinas
Carboximetilcelulosa, metilcelulosa, etilcelulosa metilcelulosa, etil celulosa,
Goma acacia, agar, alginato de sodio, carragenina
Cera, parafina, cera de abejas, aceites, grasas
Gluten, caseína, gelatina, albumina, péptidos
Adaptada de Desai y Park (2005a)
Según Lopretti et al. (2007), tanto el peso molecular como el grado de desacetilación (representando la porción de unidades desacetiladas) son características que hacen del quitosano un excelente material encapsulante, las cuales son determinadas por las condiciones de reacción mediante el procesodepreparacióndeéste.
En particular, el peso molecular del quitosano (50-2000 KDa) influye notablemente sobre el tamaño, potencial zeta, morfología y comportamiento de liberación controlada de compuestos bioactivos delas microcápsulas, así como en la eficiencia de encapsulación, cuando este compuesto es usado como material encapsulante(DesaiyPark,2006).
Como resultado de sus características, el quitosano muestra un alto potencial para la conservación efectiva de diversos compuestos bioactivos, además de una
Secado por atomización, extrusión, coacervación, inclusión
Coacervación, secado por atomización
Secado por atomización, emulsificación (formación de esferas)
Emulsificación, formación de películas, liposomas
Emulsificación, secado por atomización
liberación selectiva de estos compuestos (Ivanovska et al.,2012).
La adición de sales (p. e. alginato de sodio) en una mezcla con quitosano, incrementa la solubilidad de los microgránulos, además de modificar las propiedades de las partículas. Específicamente, la incorporación de acetato incrementa el contenido de humedad y disminuye la densidad en los gránulos de quitosano-acetato respecto a los elaborados con unamezcladequitosanoyascorbato.El empleo de agentes entrecruzadores (p. e. tripolifosfato ) a la solución del biopolímero con sales, hace posible la modificación de la estructura de las micropartículas (Adamiee y Modrzejewska,2005).
El planteamiento de las consideraciones antes descritas ha impulsado a la industria a investigar sobre materiales encapsulantes coadyuvantes a la microencapsulación, que
muestren una gran biocompatibilidad y garanticen la viabilidad de diversas sustancias activas, pudiendo así enriquecer la gama de productos funcionales accesibles alosconsumidores.
En 1859, Rouget descubrió el quitosano, observando que al tratar a la quitina con una solución caliente de hidróxido de potasio se obtenía un compuesto soluble en ácidos orgánicos, al cual nombró “quitina modificada”. Este compuesto se tornaba de color violeta en soluciones diluidas de yoduro y ácido, mientras la quitina era verde. Hacia el año 1894, Hoppe-Seyler le otorgó el nombre de quitosano (Lárez, 2003).
La quitina es un polímero que se encuentra distribuido abundantemente en la naturaleza. Presenta una tasa de reposición alta en la biósfera (duplicando el porcentaje de reposición de la celulosa), lo que le otorga la clasificación de recurso renovable (Hernández et al., 2009). La principal fuente de obtención de la quitina son los exoesqueletos de crustáceos (por ejemplo, camarones, cangrejos, langostas, entre otros).
El proceso de desacetilación completa de la quitina produce un compuesto soluble en medio ácido, mejor conocido como quitano. Cuando la desacetilación del material de partida es incompleta, se forma una mezcla de cadenas, la cual contiene diversas proporciones de unidades β(1-4)-2acetamido-2-desoxi-D-glucosa y β(1-4)-2amino-2-desoxi-D-glucosa. La relación existente entre éstas estriba en las condiciones de reacción, generando así compuestos con propiedades desiguales, como es el caso del quitosano (Lárez, 2003). Este compuesto es un polímero catiónico lineal, biodegradable, con un alto peso
molecular (Mármol et al., 2011). Según Lárez (2006) y Paz et al. (2012), el quitosano se puede encontrar de forma natural en las paredes celulares de plantas y hongos; a nivel industrial la obtención de este compuesto a base de la desacetilación química o enzimática de la quitina, ha propiciadosuproducciónagranescala.
Lárez (2003) en su investigación afirma que la presencia de grupos aminas en la cadena polimérica del quitosano, le otorga a éste diversas propiedades que lo vuelven un material versátil, debido a la posibilidad de realizar numerosas modificaciones, entre las cuales se pueden citar el anclaje de enzimas, reacciones de injerto y obtención de películas,pormencionaralgunas.
3. Técnicas deencapsulación con quitosano
Parra (2011) reporta diversas técnicas de microencapsulación, las cuales se dividen en dos: químicas y mecánicas. Esta tipificación se esquematiza en la Fig. 1, en donde se puede apreciar las subdivisiones de las clasificacionesmencionadasanteriormente.
Para fines particulares de este artículo, se han revisado diversas técnicas en las que se emplea quitosano como material encapsulante, sin embargo, las técnicas que han reportado resultados favorables y de las cuales hay mayor cantidad de aplicaciones sonelsecadoporatomizaciónylaextrusión.
3.1 Secado por atomización
El secado por atomización es el método de microencapsulación comúnmente empleado en la industria de alimentos. En esta técnica, una suspensión líquida o pasta de baja viscosidad, quecontiene los componentes de la matriz de las micropartículas y diversos compuestosactivos,seconvierteenpolvode
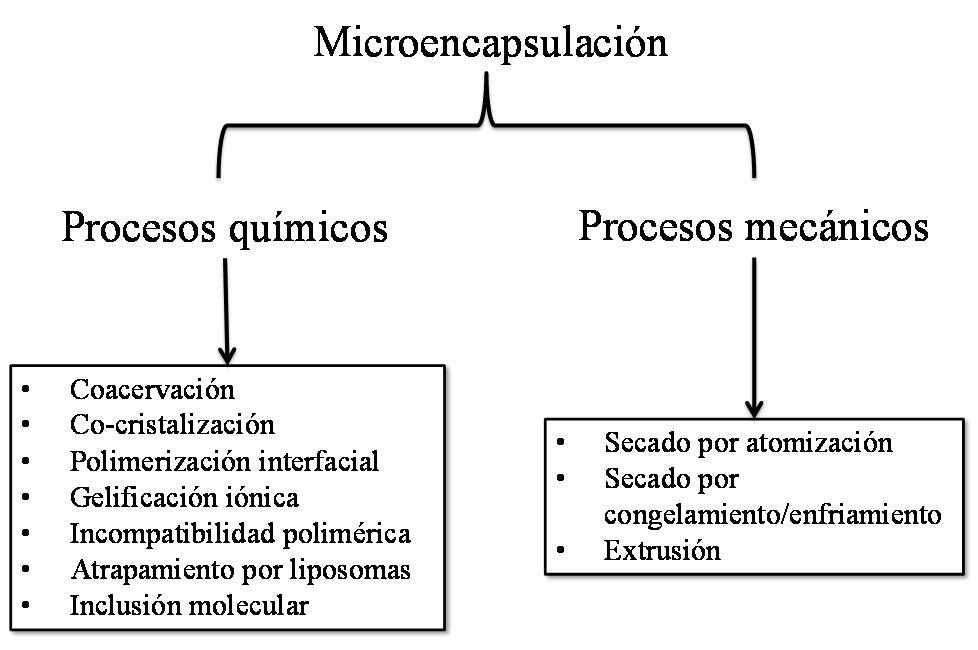
flujo libre. Este procedimiento implica la dispersión del material del núcleo en una solución de polímero, la cual puede ser una emulsión o dispersión. Posteriormente, la mezclaesatomizadaenlacámaradesecado, procedimiento que conduce a la evaporación del solvente y, por lo tanto, a la formación de microcápsulas sólidas. Entre las ventajas deestatécnicaseencuentralaposibilidad de operar el procedimiento sobre una base continua. Las propiedades físicas del producto resultante, como el tamaño, forma de partículas y contenido de humedad, se puedencontrolaratravésdelaconfiguración del equipo empleado y la manipulación de las variables del proceso (flujo de entrada y temperatura del secado) (Rodrigues et al., 2012).
En algunas investigaciones (Desai et al., 2006, Desai y Park, 2005b) el quitosano se hautilizadocomomaterialencapsulantepara proteger ácido ascórbico. Se concluye que el peso molecular del quitosano tiene una influencia notable tanto en la eficiencia de encapsulación como en el tamaño, potencial zeta,morfologíadelasuperficiey velocidad de liberación en el intestino de las microesferas de ácido ascórbico. En general, el tamaño de partículas de vitamina C encapsuladas con quitosano osciló entre 4.1 y 4.7 mm; sin embargo, el tamaño de
partícula se redujo ligeramente con agentes entrecruzadores como el tripolifosfato (TPP), formaldehído (FA) y glutaraldehído (GA), a una concentración de 2% p/p (Desai y Park, 2005b). La morfología de la superficie de las microcápsulas tiende a ser esférica y con una superficie lisa, sin embargo, el uso de un agente entrecruzador, específicamente FA o GA, permite obtener superficies más deprimidas (Desai y Park, 2005b). La eficiencia de la encapsulación y la tasa de liberación de este compuesto activo disminuyeron con el aumento en el peso molecular del biopolímero. Además, el ácido ascórbico no presentó problemas de dispersiónenlasuspensióndelquitosano.
En otra investigación, en donde también encapsularon ácido ascórbico (Liu et al., 2011), se demostró que tanto la temperatura de secado como el tiempo de almacenamiento delasolución dequitosano, además dela adición delactosa, son factores que determinan la forma y las características de la superficie de las microcápsulas de quitosano. La lactosa fue añadida a la solución de quitosano, con la finalidad de controlar la viscosidad y de este modo determinar la influencia que el contenido de sólidos en la solución del biopolímero tiene sobre la morfología de las partículas. Al final se concluyó que la incorporación de
Fig.1. Esquema de las diferentes técnicas de microencapsulación.
lactosa en conjunto con quitosano, sí modificalamorfologíadelasmicrocápsulas; a medida que la concentración de lactosa se incrementa se obtienen partículas con mayor grado de esfericidad y con una superficie máslisa.
Por otro lado, la microencapsulación de probióticos mediante secado por atomización es muy utilizada en la industria de alimentos; sin embargo, la aplicación del quitosano como agente encapsulante en este caso se encuentra en investigación, con la finalidad de establecer parámetros que garanticen la aplicación de este biopolímero como material de recubrimiento para la encapsulación de probióticos. En general, estos microorganismos han reportado tasas altas de supervivencia, mediante la optimizacióndelascondicionesdelatécnica y la incorporación de agentes de protección en la formulación antes del secado. Por ejemplo, Yang et al. (2010) reportaron que la incorporación de leche descremada, oligofructosa y polidextrosa en formulaciones probióticas, permitió una supervivencia mayor al 60% de Lactobacillus rhamnosus y del 100% de Bifidobacterium lactis, cuando fueron encapsuladosconquitosano.
Unadelas principales desventajas de esta técnica es la pérdida de la viabilidad de los probióticos, resultante de la deshidratación simultánea y la inactivación térmica de las células probióticas. Ivanovska et al. (2012) propusieron añadir prebióticos durante el proceso de microencapsulación para disminuirlas pérdidas de laviabilidad delos microorganismos encapsulados una vez que éstosseliberen.Alcompararlaviabilidadde L. casei encapsulado con quitosano y quitosano-alginato-fructooligosacáridos, se observó que la mezcla del biopolímero más la sustancia prebiótica, incrementó la supervivencia del probiótico un total de cuatro ciclos logarítmicos, incrementando
así la viabilidad del microorganismo. Con el mismo objetivo, Kanmani et al. (2011) utilizaron una mezcla de quitosano-alginato desodiomástrehalosaal5%einulinaal1% para microencapsular Streptococcus phocae. Para determinar la supervivencia y la actividad metabólica o fermentativa de los probióticos, las cápsulas fueron almacenadas a -20, 4 y 35 °C durante seis meses. Al término del experimento se pudo constatar que la adición de sustancias prebióticas garantiza la supervivencia de probióticos encapsuladosmedianteestatécnica.
3.2 Extrusión
La microencapsulación por extrusión es una técnica de múltiples etapas. Mediante esta técnica se obtienen partículas esféricas de tamaño uniforme. El procedimiento inicia con una etapa de granulación, en donde se mezclan un agente bioactivo, estabilizadores y otros ingredientes con un aglutinante líquido(normalmenteagua),paraformaruna masa húmeda o pasta. Posteriormente se procede a la extrusión, con tornillo o arietes, de la masa húmeda a través de un troquel que permite formar hebras cilíndricas de longitud y diámetro uniformes (Rokka y Rantamäki, 2010). Los filamentos formados se vuelven esferas al cortarlos en longitudes iguales antes del redondeo en pellets de forma esférica sobre una placa de marumerizado. Para concluir el procedimiento se procede a recoger las esferas húmedas, para secarlas en un lecho fluidizado o bien en un secador de bandeja (Bajaj et al., 2010). La presión y la temperatura empleadas en este procedimiento son normalmente menos de 100 psi y alrededor de 115 °C. La funcionalidad de esta técnica se basa en la capacidad del material encapsulante de solidificarse al contacto con los líquidos, formando así una matriz que atrapa fácilmente al contenido del núcleo (Rodrigues et al., 2012). En la industria de
alimentos, este método es usualmente empleado paralaencapsulación desabores y probióticos.
En diferentes estudios se investigó la viabilidad de diversos probióticos encapsulados con quitosano mediante la técnica de extrusión. Corbo et al. (2011) establecieron el rendimiento de encapsulación de partículas de quitosano y alginato. Para este estudio se determinó la viabilidad de Lactobacillus delbrueckii subsp. delbrueckii y L. plantarum, los cuales se mantuvieron viables durante un periodo de 32.5 y 51.8 días, respectivamente. En general, el rendimiento de las partículas obtenidas fue del 50%. Por su parte, Ivanovska et al. (2012) reportaron que las células bacterianas de L. acidophilus y L. casei, sobrevivieron mejor en condiciones de pH bajo; además, L. gasseri y Bifidobacterium bifidum sobrevivieron en condiciones gastrointestinales simuladas, quedandoasídemostradasuviabilidady,por lo tanto, la adecuada aplicación de la técnica paralaconservacióndeestosprobióticos.
Azarnia et al. (2008) encapsularon L. rhamnosus con quitosano y alginato (2% p/v) de sodio, y observaron que a medida que la concentración del quitosano incrementaba (0-0.3% p/v), la eficiencia del encapsulado y la viabilidad del probiótico encapsulado fueron superiores. También evaluaron la eficiencia de las partículas después de la incorporación de CaCl2 como agente entrecruzador y encontraron que conforme las concentraciones de quitosano (1% p/v) y CaCl2 (1M) aumentaban, se obtuvieron superficies de partícula lisas, tamaños pequeños (<1µm) y formas más homogéneas. Por otro lado, Charoenthai et al. (2007) emplearon la técnica de extrusión/esferonización, para la obtención de gránulos de quitosano con celulosa microcristalina y alginato de sodio. Las partículas elaboradas con quitosano de bajo
peso molecular (190 kDa) mostraron una formamásdefinida.Medianteestatécnicase logró utilizar al biopolímero en una concentración del 60% (p/p) con la ayuda del alginato de sodio, lo que resultó en una excelente capacidad de liberación del fármaco encapsulado. Debido a que esto último no ha sido probado en alimentos, se considera que sería interesante investigar mássobreestatécnica.
3.3 Emulsificación
La técnica de microencapsulación por emulsificación está definida como el procedimientodedispersióndeunlíquidoen otro en el cual es inmiscible, en donde la fase dispersa consta de la matriz que incluye el compuesto bioactivo a encapsular. Esta metodología requiere la adición de un tensoactivo para mejorar la formación y estabilidad de la emulsión, además de facilitar la distribución de tamaño de partículas. Puede realizarse utilizando el mismo mecanismo que la gelificación, tanto interna como externa. En general, el proceso de gelificación se inicia a partir de una solución de sal de alginato y una fuente de calcio externa o interna desde donde el ión calcio puede difundirse formando así una cadenapolimérica, reordenando la estructura de los compuestos, y dando como resultado la formación de materiales sólidos capaces deencapsularsustanciasactivas(Lupo et al., 2011).
Por su parte, la gelificación externa en emulsión se forma a partir de la dispersión de una mezcla de una solución quitosanocomponente,enunafasecontinuanoacuosa, despuésdelaadicióndeunafuentedecalcio capaz de fundirse en la fase dispersa, incidiendo así en la gelificación y dando lugar a la encapsulación. La gelificación interna se cimenta en la liberación del ión calcio desde un complejo insoluble adicionando un agente secuestrante,
contenido en una solución de quitosanocomponente, el cual es dispersado en una fase continua no acuosa formando una emulsión agua en aceite (w/o). La liberación delcalciosepresenta mediantelaadiciónde un ácido orgánico soluble en la fase continua, disminuyendo el pH del medio, solubilizando la sal y dando pie a la gelificación(Lupo et al.,2011).
En alimentos, este procedimiento se ha empleado para la encapsulación de B. bifidum y L. acidophilus, incrementando la viabilidad de éstos al mantener vivas el número total de bacterias probióticas encapsuladas con quitosano y alginato. Se demostró que las colonias de L. rhamnosus encapsuladas en una matriz de quitosano y alginato, mantuvieron su viabilidad durante más de 48 h a pH 2, mientras que los microorganismos no encapsulados no sobrevivieron a estas mismas condiciones. Los microorganismos encapsulados mediante esta técnica fueron empleados para laelaboracióndequesosporParra(2011).
En otro estudio se determinó que L. casei encapsulado con quitosano mediante esta técnica, disminuyó su viabilidad celular en 0.5 ciclos logarítmicos, mientras que L. acidophilus y L. rhamnosus mostraron una eficacia de atrapamiento (UFC/g encápsuladasenun sistema,enrelación alas UFC/g inoculadas) del 99.8%. En contraparte, la encapsulación de L. rhamnosus mediante una emulsión doble empleando quitosano y sólidos de suero de leche como emulgentes, disminuyó la viabilidad del probiótico 1.5 ciclos logarítmicos(Ivanovska et al.,2012).
sustancias con actividad biológica. El quitosano es un biopolímero que, recientemente, se ha empleado como material encapsulante y que ha demostrado tener biocompatibilidad con distintos compuestos bioactivos (vitaminas y probióticos). La adición de diversos compuestos al quitosano como agentes entrecruzadores, modifica sustancialmente las características delas partículas formadas. En general, tanto el secado por atomización, como la extrusión y la emulsificación, resultan ser técnicas viables para la obtención de microcápsulas de compuestos bioactivos recubiertas con quitosano, debido a que promueven la formación de microcápsulas con diámetros de partícula pequeñosyformashomogéneas.
Agradecimientos
La autora Isela A. Flores Belmont reconoce al Consejo Nacional de Ciencia y Tecnología (CONACyT) y a la Universidad de las Américas Puebla (UDLAP), por el financiamientootorgadoparasusestudiosde posgrado.
Referencias
Ademiec, J. y Modrzejewska, Z. 2005. Some structural properties of spray-dried chitosan microgranules. Drying Technology. 23:16011611.
Azarnia, S., Lee, B. H., Robert, N. y Champagne, C. P. 2008. Microencapsulation of reconminant aminopeptidase (PepN) from Lactobacillus rhamnosus S93 in chitosan coated alginate beads. Journal of Microencapsulation. 25(1):46-58.
Conclusión y comentarios finales
La microencapsulación es una técnica que promueve la subsistencia de diversas
Bajaj, P. R., Survase, S. A., Bule, M. V. y Singhal, R. S. 2010. Studies on viability of Lactobacillus fermentum by microencapsulation using extrusion spheronization. Food Biotechnology. 24:150-164.
Corbo, M. R., Bevilacqua, A. y Sinigaglia, M. 2011. Shelf life of alginate beads containing lactobacilli
and bifidobacteria: characterization of microspheres containing Lactobacillus delbrueckii subsp. bulgaricus International Journal of Food Science & Technology. 46: 2212-2217.
Charoenthai, N., Kleinebudde, P. y Puttipipatkhachorn, S. 2007. Use of chitosanalginate as alternative pelletization aid to microcrystalline cellulose in extrusion/spheronization. Journal of Pharmaceutical Sciences. 96(9):2469-2484.
Desai, K. G., Liu, C. y Park, H. J. 2006. Characteristics of vitamin C encapsulated tripolyphosphate-chitosan microspheres as affected by chitosan molecular weight. Journal of Microencapsulation. 23(1):79-90.
Desai, K. G. y Park, H. J. 2005a. Recent developments in microencapsulation of food ingredients. Drying Technology. 23:1361-1394.
Desai, K. G. y Park, H. J. 2005b. Encapsulation of vitamin C in tripolyphosphate cross-linked chitosan microspheres by spray drying. Journal of Microencapsulation. 22(2):179-192.
Desai, K. G. y Park, H. J. 2006. Effect of manufacturing parameters on the characteristics of vitamin C encapsulated tripolyphosphate-chitosan microspheres prepared by spray-drying. Journal of Microencapsulation. 23(1):91-103.
Hernández, H., Águila, E., Flores, O., Viveros, E. L. y Ramos, M. E. 2009. Obtención y caracterización de quitosano a partir de exoesqueletos de camarón. Superficies y Vacío. 22(3):57-60.
Ivanovska, T. P., Petruševska-Tozi1, L., Kostoska, M. D., Geškovski, N. y Grozdanov, A. 2012. Microencapsulation of lactobacillus casein in chitosan-Ca-alginate microparticles using spraydrying method. Macedonian Journal of Chemistry and Chemical Engineering. 31:115-123.
Kanmani, P., Kumar, R. S., Yuvaraj, N., Paari, K. A., Pattukumar, V. y Arul, V. 2011. Cryopreservation and microencapsulation of probiotic in alginatechitosan capsules improves survival in simulated gastrointestinal conditions. Biotechnology and Bioprocess Engineering. 16:1106-1114.
Lárez, C. 2003. Algunos usos del quitosano en sistemas acuosos. Revista Iberoamericana de Polímeros. 4(2):91-109.
Lárez, C. 2006. Quitina y quitosano: materiales del pasado para el presente y el futuro. Avances en Química. 1(2):15-21.
Liu, W., Duo-Wu, W., Selomulya, C. y Dong-Chen, X. 2011. Uniform chitosan microparticles prepared by a novel spray-drying technique. International Journal of Chemical Engineering 2(1):1-7.
Lopretti, M., Barreiro, F., Fernandes, I., Damboriarena, A., Ottati, C. y Olivera, A. 2007. Microencapsulación de compuesto de actividad biológica. Publicación Anual del Laboratorio Tecnológico del Uruguay. 2:19-23.
Lupo, B., González, C. y Maestro, A. 2012. Microencapsulación con alginato en alimentos. Técnicas y aplicaciones. Revista Venezolana de Ciencia y Tecnología de Alimentos. 3(1):130-151.
Mármol, Z., Páez, G., Rincón, M., Araujo, K., Aiello, C., Chandler, C. y Gutiérrez, E. 2011. Quitina y quitosano polímeros amigables. Una revisión de sus aplicaciones. Revista Tecnocientifica URU 1:53-58.
Onwulata, C. I. 2012. Microencapsulation and functional bioactive foods. Journal of Food Processing and Preservation. 2012:1-23
Parra, R. A. 2011. Revisión: microencapsulación de alimentos. Revista Facultad Nacional de Agronomía. 63(2):5669-5684.
Paz, N., Fernández, M., López, O. D., Nogueira, A., García, C. M., Pérez, D., Tobella, J. L., Montes, Y. y Díaz, D. 2012. Optimización del proceso de obtención de quitosano derivada de la quitina de langosta. Revista Iberoamericana de Polímeros 13(3):103-116.
Rodrigues, F., Sarmento, B., Andrade, J. y Oliveira, B. 2012. Review: can microencapsulation be a means to increase survival of probiotics in cheese? International Journal of Probiotics and Prebiotics. 7(2):65-80.
Rokka, S. y Rantamäki, P. 2010. Protecting probiotic bacteria by microencapsulation: challenges for industrial applications. European Food Research and Technology. 231:1-12.
Sris.s, J., Seethadevi, A., Prabha, K. S., Muthuprasanna, P. y Pavitra, P. 2012. Microencapsulation: a review. International Journal of Pharma and Bio Sciences. 3(1):509531.
Yang, D., Chi, M., Sanguansri, L., Weerakkody, R., Burgar, I. y Agustin, M. A. 2010.Microencapsulated Lactobacillus rhamnosus GG powders: relationship of powder physical properties to probiotic survival during storage. Journal of Food Science. 75(9):588-595.

Temas Selectos de Ingeniería de Alimentos 7 - 1 (2013): 57 - 67

Vegetales como fuentes de nitritos: una alternativa para el curado de carnes
E. E. Montiel - Flores*, A. López - Malo y M. E. Bárcenas - Pozos
Departamento de Ingeniería Química, Alimentos y Ambiental, Universidad de las Américas Puebla. Ex hacienda Sta. Catarina Mártir S/N, San Andrés Cholula, Puebla. C.P.72810, México.
Resumen
La generación de las características particulares de los productos curados (color, aroma y sabor), se basa en la incorporación de nitritos y nitratos, siendo el nitrito el verdadero agente de curado. Esta sustancia, además de modificar las características sensoriales, imparte seguridad microbiana al producto terminado. En la actualidad los consumidores tienen mayor interés en comprar alimentos más saludables, con ingredientes orgánicos o naturales, es por ello que surge la necesidad de investigar fuentes naturales de nitritos y nitratos. Es bien sabido que los vegetales como el apio son fuente de nitrato, por lo que tienen potencial como alternativa para el curado. El empleo de estas fuentes naturales requiere el uso de cultivos inciadores capaces de promover la reducción de nitrato a nitrito. El objetivo de este artículo es proporcionar información sobre alternativas naturales de curado para la elaboración de embutidos y otros productos cárnicos curados.
Palabras clave: nitrito, nitrato, vegetales con nitrito, curado, cultivo iniciador.
Abstract
The development of particular attributes in cured products (color, aroma and flavor), is based on the addition of nitrite and nitrate, being the nitrites is the true curing agent. This substance also modifies the sensory characteristics, and imparts microbial safety to the product. Today, consumers are more interested in healthier foods, organic or natural ingredients. Thus, research on natural sources of nitrites and nitrates is necessary. It is well known that plants, such as celery, are source of nitrate which could be considered as potential alternatives for curing. The addition of these natural sources requires the use of starter cultures, capable to promote the reduction of nitrate to nitrite. The aim of this article is to provide information on natural alternatives for curing in the preparation of sausages and cured meat products.
Keywords: nitrite, nitrate, vegetables with nitrites, curing, starter culture.
Introducción
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: ermesto.montielfs@udlap.mx
El diseño y desarrollo de nuevos productos alimenticios de hoy en día toma en cuenta las consideraciones de los consumidores. En la actualidad las personas tienen más conciencia de lo que consumen día a día, por lo que les preocupa la cantidad de sustancias químicas que ingieren de los alimentos, motivándolos así a consumir productos alimenticios elaboradosconsustanciasnaturalesodeforma
natural. Esto ha provocado un auge en la demanda de productos etiquetados como naturales u orgánicos. La industria cárnica, en especial aquella que elabora embutidos, tiene queadaptarseaestanuevacorriente, yaqueen las etiquetas se mencionan gran cantidad de ingredientes, muchos de los cuales son de origensintético.Elingredienteprincipaldelos productoscárnicoscuradoseselnitrito,elcual desarrolla las características propias de estos productos. Sin embargo, este ingrediente en la mayoríadeloscasos es deorigensintético. De aquíqueelretoseagenerarproductoscárnicos curados sin adicionar nitritos sintéticos, con las mismas características sensoriales y de seguridad microbiológica que los productos elaborados con la formulación convencional. Con estefin, en años recientes sehapropuesto el uso de algunos vegetales, ya sea en polvo o en jugo, para el curado decarnes, porserricos en nitratos. A partir de las consideraciones previamente planteadas, el objetivo de este artículo es proporcionar información acerca del uso devegetales como fuentes denitritos y nitratosparaelcuradodecarnes.
como color, sabor y olor (Sebranek y Bacus, 2007b).
Deacuerdo con la NormaOficial Mexicana 213 (NOM-213-SSA1-2002), los productos curados son aquéllos “a los que se agreguen por vía húmeda o seca, sal o azúcares, nitratos o nitritos, independientemente de que sean sometidos a algún tratamiento térmico, a maduraciónosemanejencrudos”.
Por su parte, la Norma Oficial Mexicana 145 (NOM-145-SSA1-1995) clasifica a los productoscárnicoscuradoscomo:
“Madurados” a aquéllos elaborados con cortes definidos de las especies animales consideradas aptas para consumo humano, sometidos a curación, parcialmente deshidratados, ahumados o no, madurados por cierto tiempo por medio de cultivos microbianos o de la adición de azúcares de manera que se asegure su calidad sanitaria. Los productos correspondientes a este grupo son: salami, jamón serrano, jamón tipo Westfalia, salchichón, lomo embuchado, entre otros.
Revisión bibliográfica
1. Productos cárnicos curados
Los productos cárnicos son ampliamente consumidos en el mundo. Existe una gran variedad de productos cárnicos, los cuales pueden ser crudos o cocidos y éstos a su vez pueden ser curados o no. El término curado, que es ampliamente usado, está relacionado con la adición de sales de nitrito o nitrato, clorurodesodio yotrosingredientesalacarne procesada que se utilizan para transformar químicamente las propiedades físicas, químicasyavecesmicrobiológicasdelacarne (Sebranek yBacus, 2007a). Sin embargo, es la adición de nitrito la que da lugar a las características distintivas de la carne curada
“Troceados” a aquéllos cuya carne curada, fue troceada o picada hasta lograr trozos no menores de 2 mm, pudiendo ser crudos, madurados por medio de cultivos microbianos o de la adición de azúcares cocidos o no y ahumados o no. Los productos correspondientes a este grupo son: chorizo, longaniza, queso de puerco, salami cocido, chistorra,entreotros.
Existen muchos métodos de curado para producir los productos cárnicos. El más antiguo es el curado en seco, en el cual la sal de curación es aplicada sobre la superficie de la carne. El curado con salmuera consiste en sumergir la carne en la salmuera. En ambos casos la sal de cura penetra lentamente en la carne. Otro método de curado consiste en inyectar la salmuera, este método tiene la
ventaja de reducir el tiempo de producción, ya que la sal de cura es inyectada homogéneamente en el interior de la carne (Yamanaka et al.,2005).
1.1 Reacciones químicas del curado
El color de la carne depende del estado químico de la mioglobina, proteína que contieneelgrupohemo.Elcolorrojocerezaes atribuido a la oximioglobina, sin embargo, la oximioglobina no es estable durante el almacenamiento y el calentamiento. La decoloración indeseable en la superficie de la carneduranteelalmacenamientoesdebidaala acumulación del pigmento obscuro metamioglobina. La oxidación de la mioglobina está relacionada con la oxidación delacarne(Arihara et al,. 1993).
Las reacciones químicas del curado involucran procesos complejos que dependen del pH, la concentración de mioglobina, el potencial redox, la distribución del agente de curado, la temperatura y la humedad relativa (Gotterup et al., 2007). Los dos ingredientes principales para desarrollar las reacciones químicasdelcuradosonnitratosynitritos.
El nitrato de potasio fue reconocido como el primer agente del curado y se ha utilizado para curar la carne durante cientos de años. A finales del siglo XIX se descubrió que el nitrato es convertido anitrito porbacterias con capacidad reductora y que el nitrito es el verdadero agente de curado (Sebranek y Bacus,2007b).
La química del nitrito en la carne curada es una mezcla compleja de reacciones químicas que involucran diferentes reactantes. El nitrito es un compuesto altamente reactivo que puede funcionar como agente oxidante, reductor y nitrosilante, y que puede ser convertido en ácido nítrico, óxido nítrico y nitrato (Sebranek yBacus,2007b).
El efecto más importante del nitrito en el procesodecurado eseldesarrollodecolor. En este proceso el nitrito es transformado en óxido nítrico, lo cual es facilitado por agentes reductores como el ascorbato. El óxido nítrico reacciona con el grupo ferroso de la mioglobina y la metamioglobina de la carne fresca, para formar pigmentos (nitrosilhemocromo) (Fig. 1). Sin embargo, muchas otras reacciones están involucradas en la formación de pigmentos en la carne; por ejemplo, cuando el nitrito es adicionado a la carne picada, ésta se torna café rápidamente debido a la metamioglobina formada, porque el nitrito actúa como un fuerte oxidante hemo. Además, el nitrito también puede reaccionar con los grupos sulfhidrilo delas proteínas para producir óxido nítrico (Sebranek y Bacus, 2007b).
1.2 Otras funciones delos nitritos en los productos curados
Los nitritos funcionan como agentes antimicrobianos en las carnes curadas. Inhiben fuertementealas bacterias anaeróbicas, lamás importante Clostridium botulinum, y contribuyen al control de otros microorganismos como Listeria monocytogenes (Sebranek yBacus, 2007b). Se necesita menos nitrito para proveer el desarrollo del color que para el control bacteriano (Sindelar et al., 2007a). El mecanismo inhibitorio del nitrito para C. botulinum dependedelpH,laconcentraciónde NaCl, el contenido de hierro, entre otros. Probablemente el óxido nítrico es el compuesto que tiene la función antimicrobiana. En jamones y salchichas almacenados a 10 °C no se presentan toxinas de C. botulinum, durante un periodo de 10 semanas(Tompkin,2005;Wanless,2010).
Así mismo, los nitritos funcionan como antioxidantes en los productos curados, debido a que evitan la oxidación de las grasas, las cuales dan lugaralaformación decompuestos
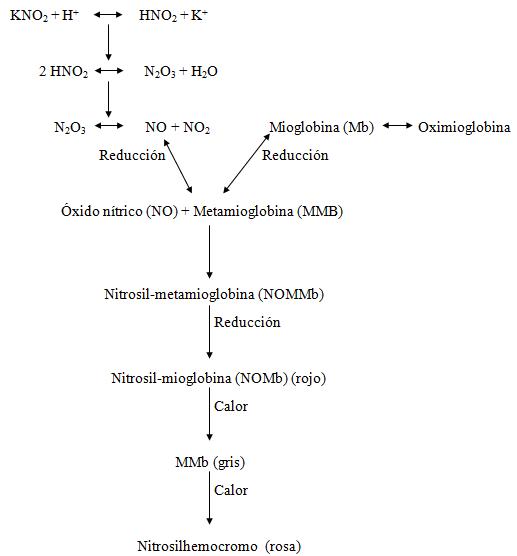
Fig.1. Reacciones involucradas en el desarrollo de color rosa característico de la carne curada (adaptado de Ranken, 2003 yHonikel, 2008).
de bajo peso molecular que producen sabores y olores desagradables. Existen mecanismos propuestos que incluyen la reacción con el grupohemodelasproteínas ylosmetales, yla formación de compuestos nitrosos y nitrosilados, que cumplen con esa función antioxidante(SebranekyBacus,2007b).
Adicionalmente, los nitritos son los responsables de la formación de los compuestos volátiles que imparten sabor a la carne curada, aunque este aspecto es el que menos se tiene comprendido (Sebranek y Bacus,2007b).
Por otro lado, los nitritos son reconocidos como compuestos tóxicos, ya que pueden formar compuestos cancerígenos en el alimento o al ingerirlo. No obstante, el uso
controlado de nitritos en las carnes procesadas norepresentaunriesgoparaelconsumidor.En estudios realizados por Cassens (1997) y Archer (2002), se ha demostrado que menos del 5% de los nitritos consumidos proviene de losproductoscárnicos;elrestoprovienedelos vegetalesylasaliva.
1.3 Concentraciones de nitratos y nitritos permitidas en productos curados
Para productos triturados, el nivel máximo permitido de nitrito de sodio o nitrito de potasio es de 156 ppm con base en el peso de la carne fresca. El máximo nivel de nitrato para estos productos es de 1718 ppm. Por otro lado, para los productos que se desarrollan por inmersión, masajeado y bombeado, los niveles máximos permitidos de sales de nitrito de
sodio o potasio son 200 ppm y 700 ppm, respectivamente, con base en el peso de la carne fresca. En productos curados secos sólo se pueden usar 625 y 2187 ppm de nitrito y nitrato, respectivamente, según lo establecido por el Departamento de Agricultura de los Estados Unidos (USDA) (Sebranek y Bacus, 2007b). En México, la Norma Oficial Mexicana 213 establece que el nivel máximo de nitritos y nitratos permitido es de 156ppm para productos cocidos, curados crudos y curadosmadurados(NOM-213-SSA1-2002).
Es importante recordar que la regulación también establece un mínimo de 120 ppm de nitrito para todos los productos curados con la leyenda “consérvese en refrigeración”, a menos que su seguridad sea controlada por otros procesos de conservación como tratamientotérmico,controldepHohumedad.
2. Alternativas naturales para el curado de productos cárnicos
Existe gran interés entre los consumidores por lo natural, orgánico y saludable en los alimentos, impulsando la demanda de los productos no adicionados con nitritos sintéticos (Sindelar et al., 2007a). Así mismo, laleydeproduccióndealimentosorgánicosen
Estados Unidos establece una lista de sustancias permitidas y prohibidas que pueden ser usadas como ingredientes en los alimentos etiquetados como orgánicos; en esta lista se prohíbe específicamente la adición de nitritos onitratos(Sebranek et al., 2012).
El problema es que el nitrito adicionado directamente o en forma indirecta derivado de nitrato,esunasustanciaúnica,distintivadelos productos cárnicos curados, para la cual no hay un reemplazo. Por lo tanto, se necesitan cambios significativos en la formulación y proceso de los productos cárnicos curados, para elaborar productos naturales u orgánicos yasíofreceralosconsumidoresproductoscon
las mismas características que los convencionales(SebranekyBacus,2007b).
Una alternativa es usar vegetales como fuentes de nitritos debido a que hay vegetales con un contenido significativo de nitrato, que cuando son adicionados en un nivel suficiente junto con un reductor de nitrato o un cultivo iniciador que reduzca el NO3 - a NO2 -, pueden proveer una cantidad adecuada de nitritos para completarlasreaccionesdelprocesodecurado natural(Sindelar et al., 2007a).
2.1. Ingredientes usados como alternativas
Durante muchos años, los polvos de vegetales han sido utilizados en la carne como agentes saborizantes, mientras que los cultivos iniciadores que reducen nitratos han sido utilizados desde la década de 1950. Sin embargo, la idea de combinar estos dos ingredientes para crear un proceso natural de curado surgió hasta la década de 1990 (Sebranek et al., 2012).
Los vegetales, como ya se mencionó, son una buena fuente de nitrato; algunos como apio, lechuga y betabel tienen concentraciones de entre 1500 y 2800 ppm de nitrato. Los jugos y polvos de vegetales están disponibles en el mercado y pueden ser usados como ingredientes en productos naturales u orgánicos, ya que ofrecen gran potencial para introducir de manera simple nitratos en las carnes procesadas y tienen la ventaja de suministrar dichos compuestos en forma concentrada(Sebranek et al., 2012).
La adición de un concentrado natural de polvo de apio (que contiene 3% de nitrato, lo cual significará 30,000 ppm) a la carne a una concentración típica de 0.3%, resulta en 90 ppm de nitrito en la mayoría de los productos cárnicos curados. Cuando seagregaun vegetal en polvo al 0.2%, significa que hay en el producto 69 ppm de nitrato, mientras que en
una concentración de 0.4% habrá 138 ppm. Como ya se mencionó, el nivel máximo permitido es de 156 ppm de nitrito, sin embargo, aun cuando haya el 100% de conversión,esdifícildeterminarlacantidadde nitrato que se convierte a nitrito, ya que la reacción es muy rápida (Sebranek et al., 2012).
Al analizar algunos jugos de vegetales disponibles en el mercado, se encontró que los jugos de zanahoria, apio, betabel y espinaca contenían 171 ppm, 2114 ppm, 2273 ppm y 3227 ppm de nitrato, respectivamente. Después de 10 días de almacenamiento a temperaturaambiente, los niveles denitrato en estos jugos bajaron entre 14 y 22%. El nitrito no fuedetectado inicialmente, pero después de 10 días de almacenamiento a temperatura ambiente se detectaron concentraciones de entre 128 y 189 ppm. Probablemente este contenido de nitrito fue generado por las bacterias reductoras de nitrato presentes en estosjugos(SebranekyBacus,2007b).
El jugo de apio, líquido o en polvo, es altamente compatible con las carnes curadas, ya que aporta muy pocos pigmentos (opuesto al betabel, zanahoria, acelga y espinaca) y tienen un perfil de sabor suave, similar al del apio crudo, porlo queno compitecon el sabor del producto terminado (Sebranek y Bacus, 2007b). Además, el polvo de apio (Apium graveolens var. Dulce) contiene una alta concentración de nitrato (Sebranek et al., 2012).
Sindelar et al. (2007b) concluyen que al emplearapioenpolvoenunaconcentraciónde 0.2% en jamón, se obtienen características similares a las que presentan los productos cárnicos curados convencionalmente. Otro vegetal de interés que recientemente se ha evaluado en este sentido es la acelga en polvo, la cual se ha usado en una concentración de entre0.15y0.3%(Gaudy,2012).
Las características típicas de los productos curados convencionalmente (color, sabor y estabilidad del sabor) se desarrollan con al menos 50 ppm de nitrito formado del nitrato durante el proceso de curado con fuentes naturales de nitrato. Sin embargo, se sabe que cuando el nitrito es completamente consumido habrá cambios en el sabor y el color, por lo que es esencial asegurar que haya nitrito residual para mantener las propiedades típicas del curado. Tal parece que una concentración de entre 5 y 15 ppm de nitrito residual es un indicador razonable para mantener la estabilidad del producto (Sebranek y Bacus, 2007a).
Un aspecto fundamental para considerar a los vegetales como una alternativa al curado convencional, es la adición de cultivos iniciadores, ya que éstos propiamente son los responsables de reducir el nitrato proveniente de los vegetales a nitrito. Los cultivos iniciadores han sido empleados paragarantizar la seguridad, contribuir al color y sabor y extender la vida útil del producto. Estos cultivos generalmente son bacterias ácido lácticas como Lactobacillus curvatus, Lactobacillus sakei, Staphylococcus carnosus y/o Staphylococcus xylosus. (Morot-Bizot et al., 2006).
En este sentido, se ha demostrado que bacterias como Lactobacillus fermentum, Lactobacillus plantarum y Leuconostoc mesenteroides, tienen la capacidad de convertir la metamioglobina en nitrosilmioglobina, el pigmento característico delosproductoscurados(Li et al.,2013).
De igual forma, los cultivos coagulasa negativa cocci tales como Kocuria varians (formalmente Micrococcus), S. xylosus, S. carnosus, entre otros, reducen el nitrato a nitrito a temperaturas entre 15 y 20 °C; pero son mucho más efectivos a temperaturas mayores a los 30 °C (Sebranek y Bacus,
2007b). Específicamente, S. xylosus genera nitrosilmioglobina en untiempo de incubación de 8 horas a 30 °C (Li et al., 2013). Otras especies que producen los mismos efectos son Staphylococcus simulans, Staphylococcus saprophyticus, Staphylococcus epidermidis, Staphylococcus haemolyticus, Staphylococcus marneri y Staphylococcus equorum (Rossi et al., 2001).
De manera similar, S. xylosus y S. carnosus presentan, además de su actividad reductora, propiedades proteolíticas ylipolíticas (Aksu et al., 2008), las cuales contribuyen al desarrollo de aroma, ya que modulan el nivel y la naturaleza de los compuestos volátiles derivados de la oxidación de lípidos y el catabolismo de aminoácidos. Ambas especies producen compuestos de sabor, como metil ácidos, metil aldehídos y metil alcoholes, a partir del catabolismo de aminoácidos de cadenaramificada (Morot-Bizot et al.,2006).
Por su parte, L. sakei tiene la capacidad de inhibir el crecimiento de bacterias deteriorativas de los productos cárnicos, contribuye a la reducción de nitrito residual y mejora las características sensoriales (Wang et al., 2013).
Por otro lado, se ha observado que un cultivo iniciador se puede incluir para controlar la microflora de este tipo de productos. Kawahara et al. (2006) probaron el uso de L. sakei en jamón de lomo. Esta bacteria aumentó la vida de anaquel hasta 28 días, la cual fue mayor que la de los productos libres de nitrito en condiciones anaerobias; además, este microorganismo tiene la ventaja dedesarrollarcolorrojoenelproducto.
Finalmente,cabemencionarqueesdesuma importancia monitorear la población de los cultivos iniciadores durante el proceso de producción de embutidos, ya que si son inhibidos por diversos factores como pH,
concentración desal, actividad deaguau otros microorganismos predominantes, la calidad final del producto no será la esperada (DiMaría et al., 2002). Así mismo, en un estudio llevado a cabo por Sindelar et al. (2007a), se encontró que el tiempo de incubación es un factor más crítico que la concentración de vegetalesenpolvo.
2.2. Consideraciones especiales
2.2.1
Seguridad
Debido aquelacantidad deapio en polvo está delimitada por el sabor que aporta a la carne, las mejoras en esta alternativa se centran en reducir el sabor para poder aumentar la concentración denitrito, paraquesedesarrolle mejor el curado y así incrementar la estabilidad en el control microbiano (Sebranek et al., 2012). También es importante señalar que la adición de estos nuevos ingredientes aporta microorganismos, que pueden ser deteriorativos y/o patógenos, a los productos curados, por lo que es necesario aplicar tratamientos para eliminar los microorganismos y por ende asegurar el mismo nivel de calidad que los productos curados convencionalmente. Algunos procesos que se han propuesto incluyen la pasteurización a 131 °C durante 10 segundos, calentamientoporaltafrecuenciapormediode microondas, radio frecuencia y aplicación de altas presiones (alrededor de 600 MPa) (Sebranek et al., 2012). En el caso de productos esterilizados, en los que el tratamiento térmico es suficiente para asegurar la estabilidad microbiana de los productos cárnicos curados, no es necesario emplear otro tratamiento(MandreanyTita,2011).
Por otro lado, de acuerdo con Ahn et al. (2002) la irradiación gamma, al menos 20 kilograys, puede ser aplicada a los productos cárnicos curados para reducir los compuestos carcinogénicos y el nitrito residual.
2.2.2 Proceso
En el curado con ingredientes naturales, una buenadistribución dela fuentedenitrato ydel cultivo iniciador es esencial para que el proceso sea uniforme (Sebranek y Bacus, 2007b). Sin embargo, no es recomendable mezclar el cultivo iniciador con algún otro factor que afecte su viabilidad, por ejemplo especias o sal, y por ende su capacidad de reducirelnitrato(SebranekyBacus,2007b).
Por otro lado, para productos en los que se inyecta la salmuera con el cultivo iniciador es crítica la forma de inyección, debido a que los cultivos iniciadores no migrarán mucho desde los puntos de inyección (Sebranek y Bacus, 2007b).
Es importante señalar que en la elaboración de estos productos es fundamental que los cultivos iniciadores dispongan de tiempo suficiente para reducir los nitratos a nitritos. Con este propósito se lleva a cabo una incubación previa de los cultivos iniciadores. Sin embargo, la adición de este paso al proceso incrementa el tiempo de elaboración para algunos productos, particularmente el de aquellos de diámetro pequeño, los cuales requieren tiempos cortos de calentamiento. Para reducir este tiempo se incuba el jugo de apio con el cultivo iniciador antes de adicionarlo al producto cárnico (Sebranek et al., 2012). El tratamiento con jugo de apio y cultivo iniciador es efectivo en jamones, pero en este caso la cantidad de apio en polvo es más crítica. Por otro lado, parece que en productos de mayor diámetro el incremento lento de la temperatura del proceso térmico típico provee suficiente tiempo para que el cultivo reduzca el nitrato. Sin embargo, el delicado perfil de sabor de algunos productos como por ejemplo jamones, hace que éstos sean más susceptibles a la contribución de sabor por los vegetales empleados. Por su parte, los embutidos fermentados no requieren ajustes en su proceso de elaboración, debido a
que la etapa de fermentación permite la conversión de nitrato a nitrito (Sebranek y Bacus,2007b).
2.2.3
Aditivos
Debido aquelaconcentración denitrito delos productos curados utilizando fuentes naturales de esta sal es menor que la de los curados convencionalmente, se ha propuesto la adición de ácido ascórbico. El ácido ascórbico es conocido como un acelerador del proceso de curado y facilita la conversión de nitrito a óxido nítrico para el desarrollo de color. También sirve como agente reductor para ayudar a mantener el color del curado durante elperiododealmacenamiento(Sebranek et al., 2012).Comofuentenaturaldeácidoascórbico puede usarse cereza en polvo (Sebranek y Bacus,2007b).
Otros ingredientes que pueden ser considerados en el desarrollo de productos curados en forma natural son el vinagre y el jugo de limón, debido a que los ácidos tienen el potencial de acelerar las reacciones del nitrito, ya que un descenso en el pH de apenas 0.2 unidades es suficiente para duplicar la velocidad de formación de nitrito. Sin embargo,generalmentevaloresdepHmenores a 5.5 no son deseables, debido a que los cambios en el pH afectan la carga de las proteínas que componen el músculo. Estos cambios alteran la separación entre las fibras de la carne, yel cambio en la estructura afecta la forma en la que la luz es reflejada y absorbida, lo cual afecta la apariencia visual (BolesyPegg,2008).
En los productos elaborados con carne picada, el efecto de la adición de ingredientes queafecten elpH esinsignificante,debidoala capacidad de la carne para amortiguar los cambios de pH. Por otro lado, la adición de agentesacidulantes yreductoresdalugarauna menor concentración de nitrito residual en la carne curada. Así mismo, el pH de las
salmueras es crítico para alcanzar un curado natural óptimo y una textura adecuada en el producto, debido a que los fosfatos y otros amortiguadores usados en el curado convencional, no pueden ser incluidos en productos etiquetados como orgánicos o naturales(SebranekyBacus,2007a).
En cuanto aantioxidantes naturales, pueden usarse especias como romero y otras; para proveer protección al sabor y retardar la oxidación de lípidos en las carnes procesadas (SebranekyBacus,2007b).
Los derivados de productos cítricos también pueden ser utilizados como ingredientes en la formulación de productos cárnicos curados naturalmente. Viuda-Martos et al. (2009) proponen el uso de la fibra dietética de naranja, extraída del albedo, para la reducción del porcentaje de nitrito residual enproductoscárnicos.
Por otro lado, la pasta de tomate con 12% de sólidos solubles adicionada en una concentración de 12% en la elaboración de salchichas, tiene un efecto positivo en el color rojo y consecuentemente en la aceptabilidad por los consumidores, sin ningún efecto negativo en el proceso y en las características de calidad del producto en el almacenamiento (Deda et al.,2007).
2.2.4 Etiquetado
Los productos curados que son elaborados sin laadicióndirectadenitrato ynitrito,deben ser claramente etiquetados como “no curados”, debido a que son significativamente diferentes a los productos curados tradicionales (Sebranek y Bacus, 2007b). Con el fin de proporcionar la mejor información a los consumidores, un término más apropiado para estos productos sería “curado naturalmente”, porque el producto realmente es curado con fuentes naturales de nitrato y nitrito; así se
eliminará la leyenda “sin nitrito o nitrato añadido”(SebranekyBacus,2007a).
El Departamento de Agricultura de los Estados Unidos (USDA) establece como mínimo 120 ppm de nitrito para asegurar que el producto se clasifique en la categoría “consérvese en refrigeración”, a menos que se asegure la calidad por otros procesos de conservación como tratamiento térmico, modificación de pH o control de humedad. A concentraciones menores que ésta habrá crecimiento microbiano, especialmente de C. botulinum, ya que esta bacteria sobrevive, crece y produce toxinas (Sindelar et al., 2007a). Conclusiones y comentarios finales
Algunos vegetales, como el apio, junto con cultivos iniciadores (bacterias ácido lácticas como S. xylosus y S. carnosus), son una alternativa importante como fuente natural de nitritos para la elaboración de productos cárnicos curados. Debido a esto, es importante continuar investigando sobre este tema, específicamente sobre el uso de estas fuentes de nitrito en las formulaciones de productos cárnicos curados distintos a los estudiados hasta el momento (jamón y salchicha, principalmente), con el fin de generar productos libres deaditivos sintéticos, con una “etiqueta limpia”, que sean mejor aceptados porlosconsumidores.
Agradecimientos
El autor Ernesto Montiel agradece al Consejo Nacional de Ciencia y Tecnología (CONACYT) y a la Universidad de las Américas Puebla (UDLAP), por el financiamiento otorgado para sus estudios de posgrado.
Referencias
Ahn, H. J., Kim, J. H., Jo, C., Lee, C. H. y Byun, M. W. 2002. Reduction of carcinogenic N-nitrosamines and residual nitrite in model systems sausage by irradiation. Jounal of Food Science. 67(4):13701373.
Aksu, M. I., Kaya, M. y Oz, F. 2008. Effect of Lactobacillus sakei and Staphylococcus xylosus on the inhibition of Escherichia coli O157:H7 in pastrana, a dry-cured meat product. Journal of Food Safety. 28:47-58.
Archer, D. L. 2002. Evidence that ingested nitrate and nitrite are beneficial to heatlh. Journal of Food Protection. 65:872-875.
Arihara, K., Kushida, H., Kondo, Y., Itoh, M., Luchansky, J. B. y Cassesns, R. G. 1993. Conversion of metmyoglobin to bright red myoglobin derivates by Chromobacterium violaceum, Kurthia sp., and Lactobacillus fermentum JCM1173. Journal of Food Science. 58(1):36-42.
Boles, J. A. y Pegg, R. 2008. Meat color. University of Saskatchewan. http://www.safespectrum.com/pdfs/meatcolor.pdf accesada 01/02/2013.
Cassens, R. G. 1997. Composition and safety of cured meats in the USA. Food Chemistry. 59:561-566.
Deda, M. S., Bloukas, J. G. y Fista, G. A. 2007. Effect of tomato paste and nitrite level on processing and quality characteristics of frankfurters. Meat Science. 76:501-508.
Di-María, S., Basso, A. L., Santoro, E., Grazia, L. y Coppola, R. 2002. Monitoring of Staphylococcus xylosus DSM 20266 added as starter during fermentation and ripening of soppressata molisana, a typical italian sausage. Journal of Applied Microbiology. 92:158-164.
Gaudy, A. 2012. Comunicación personal. Naturex Inc. South Hackensack, NJ. EEUU. Citado en: Sebranek, J. G., Jackson-Davis, A. L., Myers, K. L. y Lavieri, N. A. 2012. Beyond celery and starter culture: advances in natural/organic curing processes in the United States. Meat Science. 92:267-273.
Gotterup, J., Olsen, K., Knochel, S., Tjener, K., Stahnke, L. H. y Moller, J. K. S. 2007. Colour formation in fermented sausages by meat-associated sthaphylococci with different nitrite- and nitratereductase activities. Meat Science. 78:492-501.
Honikel, K. O. 2008. The use and control of nitrite for the processing of meat products. Meat Science. 78:68-76.
Kawahara, Y., Nakamura, M., Sakagami, I. y Suzuki, Y. 2006. Bright red color formation of cooked pork loin cured with lactic acid bacteria starter culture without adding nitrite during low-temperature storage. Food Science Technology Research. 12(2):101-107.
Li, P., Kong, B., Chen, Q., Zheng, D. y Liu, N. 2013. Formation and identification of nitrosylmyoglobin by Staphylococcus xylosus in raw meat batters: A potential solution for nitrite substitution in meat products. Meat Science. 93:67-72.
Mandrean, N. L. y Tita, O. 2011. Celery, a natural alternative to chemical nitrite added to meat products. Bulletin UASVM Agriculture. 68(2):1-4.
Morot-Bizot, S. C., Leroy, S. y Talon, R. 2006. Monitoring of staphylococcal starters in two French processing plants manufacturing dry fermented sausages. Journal of Applied Microbiology. 102:238-244.
NORMA OFICIAL MEXICANA NOM-213-SSA12002. Productos y servicios. Productos cárnicos procesados. Especificaciones sanitarias. Métodos de prueba. México. D.F.
NORMA OFICIAL MEXICANA NOM-145-SSA11995. Productos cárnicos troceados y curados. Productos cárnicos curados y madurados. Disposiciones y especificaciones sanitarias. México. D.F.
Ranken, M. D. 2003. Manual de industrias de la carne. Primera edición. AMV Ediciones. Madrid, España. 76 p.
Rossi, F., Tofalo, R., Torriani, S. y Suzzi, G. 2001. Identification by 16S-23S rDNA intergenic región amplification, genotypic and phenotypic clustering of Staphylococcus xylosus strains from dry sausages. Journal of Applied Microbiology. 90:365-371.
Sebranek, J. B. y Bacus, J. N. 2007a. Natural and organic cured meat products: regulatory, manufacturing, marketing, quality and safety issues American Meat Science Association White Paper Series. 1:1-15.
Sebranek, J. B. y Bacus, J. N. 2007b. Cured meat products without direct addition of nitrate or nitrite: what are the issues? Meat Science. 77:136-147.
Sebranek, J. G., Jackson-Davis, A. L., Myers, K. L. y Lavieri, N. A. 2012. Beyond celery and starter
culture: advances in natural/organic curing processes in the United States. Meat Science. 92:267-273.
Sindelar, J. J., Cordray, J. C., Sebranek, J. G., Love, J. A. y Ahn, D.U. 2007a. Effects of vegetables juice powder concentration and storage time on some chemical and sensory quality attributes of uncured, emulsified cooked sausages. Journal of Food Science. 72(5):324-332.
Sindelar, J. J., Cordray, J. C., Sebranek, J. G., Love, J. A. y Ahn, D.U. 2007b. Effects of varying levels of vegetable juice powder and incubation time on color, residual nitrate and nitrite, pigment, pH, and trained sensory attributes of ready-to-eat uncured ham. Journal of Food Science. 72(6):388-395.
Tompkin, R. B. 2005. Nitrite. En: P. M. Davison, J. N. Sofos y A. L. Branen (Eds.) Antimicrobials in Food. Tercera edición. FL: CRC Press. Boca Raton.
Viuda-Martos, M., Férnandez-López, E., Sayas-Barrera, E., Sendra, E., Navarro, C., y Pérez-Álvarez, J.A. 2009. Citrus co-products as technological strategy to reduce residual nitrite content in meat products. Journal of Food Science. 74(8):93-99.
Wang, X. H., Ren, H. Y., Liu, D. Y., Zhu, W. Y. y Wang, W. 2013. Effects of inoculating Lactobacillus sakei starter cultures on the microbiological quality and nitrite depletion of Chinese fermented sausages. Food Control. 32:591-596.
Wanless, B. 2010. The effect of natural nitrite and antimicrobials against Clostridium botulinum in frankfurter and ham products. Tesis de maestría. Universidad de Wisconsin-Madison.
Yamanaka, H., Akimoto, M., Sameshima, T., Arihara, K. y Itoh, M. 2005. Effect of bacterial strains on the development of the ripening flavor of cured pork lions. Animal Science Jounal. 76: 499-506.

Temas Selectos de Ingeniería de Alimentos 7 - 1 (2013): 68 - 77
Efecto de la radiación UV-C en frutas y verduras
J. F. Haro - Maza* y J. A. Guerrero - Beltrán

Departamento de Ingeniería Química, Alimentos y Ambiental, Universidad de las Américas Puebla. Ex hacienda Sta. Catarina Mártir S/N, San Andrés Cholula, Puebla. C.P.72810, México.
Resumen
Actualmente, los consumidores han tomado conciencia acerca del decremento que los tratamientos térmicos pueden ejercer sobre los atributos sensoriales y nutricionales de los alimentos. Se han buscado alternativas a estos inconvenientes y una de las tecnologías, por su versatilidad y resultados, es el procesamiento de alimentos con radiación ultravioleta C de onda corta (UV-C). Esta revisión da a conocer los resultados de investigaciones actuales sobre frutas y verduras, tratadas con radiación UV-C, bajo dos enfoques: el antimicrobiano y los efectos sobre los atributos nutricionales, químicos y sensoriales de los alimentos. Contiene información acerca de los cambios post-tratamiento que los frutos y vegetales, tratados con UV-C, experimentan durante el almacenamiento debido a las dosis de radiación empleadas. De manera general se puede concluir que el tratamiento UV-C ideal debería: reducir la carga microbiana, incrementar algunas propiedades nutricionales y no generar atributos sensoriales negativos.
Palabras clave: dosis, reducción microbiana, radiación UV-C, frutas, verduras.
Abstract
Nowadays, consumers have become aware about the decrease that heat treatments may have on sensory and nutritional attributes of foods. They have been looking for alternatives to these drawbacks and one of the technologies, for its versatility and results, is the shortwave ultraviolet-C (UV-C) radiation. This review inform the results of current research on fruits and vegetables, treated with UV-C radiation, under two points of view: the antimicrobial and the effects on the nutritional, chemical and sensory attributes of foods. It contains information about post-treatment changes that fruits and vegetables, treated with UV-C radiation, may have during storage due to the radiation doses. In general, it can be concluded that the UVC treatment should ideally be: to reduce microbial load, to increase some nutritional properties and do not create negative sensory attributes.
Keywords: dosses, microbiological reduction, UV-C radiation, fruits, vegetables.
Introducción
Durante las últimas décadas se ha observado un incremento en el interés de los consumidores por adquirir alimentos que ofrezcan beneficios a la salud. Los beneficios
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Direccion electrónica: jose.haroma@udlap.mx
ocasionados por el consumo variado de frutas y verduras frescas son ampliamente conocidos por la comunidad científica y el público en general (Barros y Rocha, 2012); sin embargo, el ritmo de vida actual ha orillado a algunos sectores de la población a consumir productos vegetales listos para comer, los cuales debido, a sus características de consumo inmediato, han tenido que ser procesados térmicamente
para garantizar su seguridad microbiana. Si bien estos productos son microbiológicamente seguros, sus atributos, tanto nutricionales comosensoriales,sehanvistodisminuidospor eltipodetratamiento.
Debido a ello, se han propuesto nuevas tecnologías de proceso cuyo objetivo es crear alimentos microbiológicamente seguros que no impacten de manera negativa los atributos sensoriales y nutricionales de los productos. Una de las más importantes es el procesamiento con radiación ultravioleta C de ondacorta(UV-C).Actualmenteelusodeesta tecnología está bien establecido para casos como, el tratamiento de agua, la desinfección del aire y la desinfección de superficies; sin embargo, su aplicación en alimentos listos paraconsumo, incluidos los frutos yvegetales, está aún en investigación y su difusión es aún insuficiente. No obstante, el tratamiento con radiaciónUV-Ctieneun ampliopotencialpara ser usado de manera comercial en frutos rebanados (Ribeiro et al., 2012) debido al grado de efectividad que esta tecnología posee para inhibir ciertos tipos de microorganismos, incluyendo a los virus (Guerrero-Beltrán y Barbosa-Cánovas,2004).
Debido a las demandas de alimentación actuales de la población, la cadena de suministros(supermercados)debeenfrentarun doble reto; por un lado, se necesita almacenar alimentos frescos y por el otro, deben ser de consumo inmediato. Lo anterior implica una pérdida substancial cuando se manejan productos como lechuga y espinacas, que son fácilmente lastimados o contaminados durante el proceso y transporte; en este caso, la tecnología de radiación UV-C ofrece una solución a dichas pérdidas, evitando que proliferen microrganismos en las lesiones de lasverduras(Ortoneda et al.,2008).
Sin embargo a pesar de los beneficios de esta tecnología, el público en general aún está
un tanto inseguro respecto a su uso, debido a que, al ser un tipo de radiación, esta podría acarrear riesgos para la salud, por lo que la Administración de Alimentos y Fármacos (FDA por sus siglas en inglés) de Estados Unidos, así como el Departamento de Agricultura (USDA) del mismo país, después de varias investigaciones concluyeron que el uso de esta radiación es completamente seguro. En el año 2000 la FDA aprobó esta tecnología como una alternativa a la pasteurizacióndejugosfrescos(U.S.Foodand DrugAdministration,2000).
Se debe a los puntos anteriores que el uso de esta tecnología se está incrementando; sin embargo, la difusión existente respecto al uso de la misma es aún insuficiente. La presente investigación tiene como objetivo difundir algunos de los resultados obtenidos en el tratamiento de frutas y verduras, ya sea listas paraconsumo, o bien parasu almacenamiento, post-cosecha.
Revisión bibliográfica
1. Efecto dela radiación UV-C
1.1. Generalidades
La radiación ultravioleta, en su forma natural, proviene del sol. El espectro de dicha radiación, que penetra en la atmósfera terrestre, se ha dividido en tres regiones dependiendo de su longitud de onda. Dichas regiones ejercen diferentes características sobrelosorganismos(Mahdavian et al.,2008). En la Tabla I se presenta una clasificación de la longitud de onda de la radiación ultravioleta.
Es debido a las propiedades germicidas de la radiación UV-C, que se han creado fuentes
Tabla I. Clasificación de la longitud de onda de la radiación UVa ClasificaciónLongitud de ondaEfectos en organismos
Larga320-400nm
Media280-320nm
Cambios en la piel humana (bronceado)
Quemaduras serias (cáncer)
Corta200-280nmEfecto germicida aAdaptado de Guerrero-Beltrán y Barbosa-Cánovas (2004).
de radiación artificiales (lámparas) con fines prácticos, generalmente con propósitos de desinfección. Estas fuentes de radiación son fabricadas utilizando lámparas de mercurio de baja presión, que producen radiación con una longitud de onda de 254nm (efecto germicida) (Guerrero-BeltrányBarbosa-Cánovas,2004).
A pesar de la elaboración de fuentes de radiación estándar, cuando éstas se emplean para la desinfección de alimentos, existen muchas variables que pueden afectar la eficiencia del tratamiento. El tiempo de exposición, la intensidad de la fuente de radiación, la rugosidad de la superficie a tratar y el tipo de tratamiento (por lotes o continuo) sonalgunasdeellas.
Como el tratamiento con radiación UV-C tiene tantas variables es difícil establecer parámetros respecto a la intensidad del tratamiento, ya que cada alimento necesitauna dosis específica de radiación. Debido a ello, para un mismo alimento se pueden tener rangos de dosis muy diversos. En general yde manera no oficial, la mayoría de los investigadores consideran una dosis de radiación como baja cuando ésta es menor o igual a 1 kJ/m2 y es considerada como alta cuandoladosisesmayoroiguala15kJ/m2 .
Aun tomando en cuenta estas variables, la tecnología de radiación UV-C puede ser un tratamiento válido en lo que respecta a los
protocolos de análisis de riesgos y control de puntos críticos (Hazard Analysis and Critical Control Points, HACCP, por sus siglas en inglés), debido a su efectividad para reducir el número de microorganismos en la superficie dealimentosobienenlasuperficiedeproceso delosmismos(Yaun et al.,2004).
1.2. Efecto antimicrobiano de la radiación UV-C en frutas
La radiación UV-C afecta el ADN de los microorganismos, causando mutaciones mediante la separación de la doble hélice, evitando de esta manera su reproducción (Gardner y Shama, 2000). Es así como esta tecnología no térmica puede ser aplicada para inactivar diversos tipos de microorganismos incluyendo virus. La generación de radiación ultravioleta monocromática (254nm) es considerada como un medio físico de desinfección cuya aplicación en alimentos está aúnsiendoinvestigada.
1.2.1 Radiación UV-C como único tratamiento
Existen diversas investigaciones respecto al tratamiento con radiación UV-C con propósitos germicidas. Algunas estudios son muy similares entre sí: este es el caso de Stevens et al. (2005) y Manzoco et al. (2011), ellos trataron de incrementar la resistencia a la deterioración microbiana en manzanas. Stevens et al. (2005) además incluyeron
duraznos y tangerinas. Las dosis utilizadas en lasinvestigacionesfueronde1.2a24kJ/m2,la mayor diferencia radicó en que Stevens et al. (2005) trabajaron con rebanadas de fruta inoculadas con Colletotrichum gloeosporioides, Monilinia fructicola y Penicillium digitatum, mientras que Manzoco et al. (2011) trabajaron con cuentas viables totales (bacterias, mohos ylevaduras). Las dos investigaciones concluyeron que se logró aumentar la resistencia al deterioro microbiano, mediante la reducción de 1 a 2 cicloslogarítmicos.
En otra investigación realizada por Schenk y Guerrero (2008), se buscó identificar el efecto que una dosis máxima de 87 kJ/m2 podría tener sobre rebanadas de pera (Pyrus communis L.) fresca, además de analizar la reducción en las cuentas de Listeria innocua, Listeria monocytogenes, Escherichia coli y Zygosaccharomyces bailii, con las cuales fue inoculada la fruta. La dosis máxima probada generó una mayor reducción en las rebanadas depera(3.4cicloslogarítmicos).Sinembargo, al aumentar el tiempo de exposición y por ende la dosis de radiación, encontraron una menor reducción, ya que los microorganismos desarrollaron resistencia. De manera similar, Jian et al. (2010) analizaron el efecto que una radiación UV-C, de 1 a 10 kJ/m2, podría ejercer sobre la germinación de las esporas de Monilinia fruticola, obteniendo como resultado una inhibición completa de la germinación en pera Yali (Pyrus bretschneideri Rehd)
Adicionalmente, se ha demostrado que dosis menores a 7 kJ/m2 tienen un efecto antimicótico en frutas, como lo demostraron Stevens et al. (1998) en duraznos inoculados con Monilinia fruticola yPerkins-Veazie et al. (2008) en moras azules inoculadas con Colletotrichum acutatum. En general se reporta que una mayor dosis de radiación disminuirálacargamicrobianaenelproducto.
En la Tabla II se muestran algunas frutas tratadasconradiaciónUV-C.
1.2.2. Radiación UV-C en combinación con otros métodos
La combinación de la radiación UV-C con otros tratamientos ha demostrado tener un efecto sinérgico en la conservación de muchos alimentos. Una combinación que ha demostrado buenos resultados es el tratamiento de frutas con una solución desinfectante (ácidos orgánicos o sales de las mismas) seguida de la aplicación de radiación UV-C. En este sentido, se ha reportado que cubos de sandía pre-tratados con una solución de lactato de sodio (1%) y ácido ascórbico (0.5%) seguida de una dosis de 4.1 kJ/m2 de radiación UV-C fueron efectivas para inhibir la flora nativa (mesófilos aerobios, mohos y levaduras) de la fruta (Fonseca y Rushing, 2006). Asimismo, un pretratamiento con solución de ácido málico (1.5%) seguido de radiación UV-C (0.96 - 8.64 kJ/m2) en rebanadas de papaya Maradol, fueron suficientes para inhibir Rhodotorula glutinis (Calderón-Gabaldón et al.,2012).
Por otra parte, se ha probado que la combinación de radiación UV-C con atmósferas modificadas son un buen método para conservar alimentos como lo muestra el estudio de López-Rubira et al. (2005) quienes probaron dichos tratamientos combinados en semillas degranada, obteniendo unareducción importante en las cuentas de Enterobacteriaceae (López-Rubira, et al., 2005).
Por otro lado Kim yHung (2012) evaluaron el efecto de la combinación de un tratamiento con radiación UV-C, ozono y agua electrolizada oxigenada con el objetivo de inhibir E. coli O157:H7 en mora azul. Se encontró que esta combinación con una radiación de 7 kJ/m2 era capaz de inhibir de 1.96a4cicloslogarítmicos.
Tabla II. Frutas tratadas con radiación UV-C FrutaDosisMicroorganismosAutores
Manzanas, duraznos y tangerinas
1.3 y 7.5 kJ/m2
Colletotrichum gloeosporioides, Monilinia fruticola y Penicillium digitatum
Stevens et al (2005)
Pera 87 kJ/m2
Manzana 1.2, 6.0, 12.0 y 24 kJ/m2
Listeria innocua, Listeria mnocytogenes, Escherichia coli y Zygosaccharomyce s bailii
Cuentas viables totales (Bacterias, mohos y levaduras)
Durazno < 7.0 kJ/m2 Monilinia fruticola
Mora azul < 7.0 kJ/m2
Sandía 4.1 kJ/m2
Papaya Maradol
Colletotrichum acutatum
Schenk y Guerrero (2008)
Manzoco et al. (2011)
Stevens et al. (1998)
Perkins-Veazie et al. (2008)
Población nativa microbiana de sandía Fonseca y Rushing (2006)
0.96-8.64 kJ/m2 Rhodotorula glutinis
1.3. Efecto antimicrobiano de la radiación UV-C en verduras
Es bien sabido que en cualquier industria que maneje alimentos, las condiciones higiénicas del proceso son parte fundamental de la cadena de producción, además se debe reducir la cuenta microbiana en los vegetales procesados, para así, minimizar las pérdidas (Steffen et al., 2010). En este sentido la radiación UV-C brinda una respuesta satisfactoria como medio de conservación, ofreciendo productos microbiológicamente seguros y con atributos sensoriales muy parecidos al alimento fresco. Los efectos de la radiación se pueden observar de manera inmediata después del tratamiento, o bien pueden aparecer algunos efectos durante el periododealmacenamiento.
CalderónGabaldón et al. (2012)
En cuanto a estudios relacionados con los efectos inmediatos, Liu et al. (1993) estudiaron el efecto de esta tecnología en tomates (Lycopersicon esculentum) inoculados con Alternaria alternata, Botrytis cinerea y Rhizopus stolonifer, encontrando que al utilizardosisde1.3a4kJ/m2 sepodíaninhibir casi en su totalidad las infecciones ocasionadas por estos hongos. Similarmente, Yaun et al. (2004) determinaron los efectos germicidas de la radiación UV-C en tomates Roma y chiles jalapeños inoculados con Salmonella spp. Se utilizaron dosis de 0.5 y 4 J/cm2, obteniendo una reducción microbiológica de 2.6 a 3.8 ciclos logarítmicos. En el mismo contexto, se han tratado champiñones por medio de radiación UV-C como lo muestra la investigación de Guan et al. (2012), quienes inocularon este vegetal con E. coli O157:H7 ylo sometieron a
radiaciones de 0.45 a 3.15 kJ/m2, obteniendo una reducción inmediata de hasta 0.89 ciclos logarítmicos. Respecto a los efectos producidos durante el almacenamiento, Liu et al. (2011) estudiaron los resultados de la radiación UV-C en tomates frescos. Un día después del tratamiento se encontró que utilizando una dosis de 4 kJ/m2 se podía inhibir la microflora nativa de los vegetales mediante un incremento en las defensas del alimento generado por la radiación. Dicho efecto involucró el metabolismo de lípidos y fotosíntesis en algunos casos. De la misma manera, Escalona et al. (2010) aplicaron dosis de 0, 2.4, 7.2, 12 y 24 kJ/m2 en hojas de espinacas tiernas. Los resultados mostraron la efectividad del tratamiento al reducir las poblaciones microbianas de Listeria monocytogenes, Salmonella enterica y Pseudomonas marginalis durante los primeros 8 días de almacenamiento. Sin embargo, pasados los 8 días, estas hojas exhibieron una cuenta microbiana mayor que aquellas que no fueron tratadas. Por su parte, Erkan et al. (2001) trataron rebanadas de calabacita con una dosis de 9.86 kJ/m2 y aunque esta no disminuyó de manera considerable la carga microbiana, el mayor efecto se observó medianteladisminucióndelareproducción de los mircoorganismos durante el almacenamiento.
Tomando en cuenta el efecto inmediato y durante el almacenamiento, Allende y Artés (2003) expusieron lechuga ‘Lollo Rosso’ (Lactuca sativa) a dosis de 0.4 a 8.14 kJ/m2 , logrando reducir inmediatamente después del tratamiento el contenido de bacterias psicrótrofas, coliformes y levaduras. En contraste, se indicó que la radiación UV-C incrementó de manera significativa la tasa de respiración del alimento durante el almacenamiento, provocando así cambios indeseables en el producto, debido a un aumento en la cantidad de bacterias ácidolácticas dentro de los empaques. Siguiendo la línea de investigación anterior, Allende et al.
(2006) sometieron hojas de lechuga “Red oak leaf” a tratamiento con radiación UV-C. Los géneros de bacterias seleccionados fueron los asociados con infecciones en el vegetal (Enterobacter, Erwinia, Escherichia, Leuconostoc, Pantoea, Pseudomonas, Rahnela, Salmonella, Serratia y Yersinia). La mayoría de los organismos se inhibieron inmediatamente con una dosis de 30 J/m2 Mientras que para la completa erradicación de Erwinia carotovora, Leuconostoc carnosum, Salmonella Typhimorium y Yersinia aldovae se necesitó una dosis de 85 J/m2. En cuanto al almacenamiento, se encontró que aplicando una dosis de 7.11 kJ/m2, el efecto germicida continuó aún en días posteriores al tratamiento, aumentando la vida de anaquel delproducto.
En la Tabla III se muestran algunas verdurastratadasconradiaciónUV-C.
1.4. Otros efectos de radiación UV-C en vegetales
1.4.1. Vitaminas, actividad antioxidante y otros compuestos químicos
La radiación UV-C además de poseer un efecto germicida, también puede alterar algunas de las propiedades nutricionales del producto, como lo es el contenido de vitamina C, la actividad y los compuestos antioxidantes y el contenido de terpenos de algunos alimentos.
Yong-Gui y He (2012) evaluaron los efectos de la radiación UV-C en la calidad de rebanadas de piña frescas. Las rebanadas se trataron a4.5kJ/m2 contiemposdeexposición de60y90segundos.Observaronquetodoslos tratamientos redujeron de manera importante el contenido de vitamina C en el producto. Similarmente, Allende et al. (2007) encontraron que la radiación UV-C podía disminuir el contenido de vitamina C en fresas. Por otro lado, se evaluó la degradación
VerduraDosisMicroorganismoAutor
Lechuga 30 y 85 J/m2
Espinacas 2.4, 7.2, 12 y 24 kJ/m2
Enterobacter, Erwinia, Escherichia, Leuconostoc, Pantoea, Pseudomonas, Rahnela, Salmonella, Serratia y Yersinia
Listeria monocytogenes, Salmonella entérica y Pseudomonas Marginalis
Tomates 0.5 y 4 J/cm2 Salmonella spp
Jalapeños 0.5 y 4 J/cm2 Salmonella spp.
de ácido ascórbico en un sistema modelo de jugo de manzana tratado con tecnologíaUVC.Enel estudioseconcluyequelaradiación UV-C acelera la degradación de ácido ascórbico y que el almacenamiento en oscuridad disminuye la degradación de esta vitamina aún después deser tratada con UVC(Rohan et al., 2011).
En cuanto a la actividad antioxidante, se ha observado que la exposición de vegetales a radiación UV-C puede incrementar la concentración de ésta. Lemoine et al. (2010) analizaron el efecto que la radiación UV-C, con una dosis de 8 kJ/m2, podría ejercer sobre los compuestos fenólicos y capacidad antioxidantedebrotesdebrócoli.Seobservó que tanto los compuestos fenólicos, como la capacidad antioxidante se incrementaron con el tratamiento. Erkan et al. (2008) encontraron que la radiación UV-C, por si sola, puede incrementar la capacidad antioxidante en fresas, utilizando dosis de 0.43,2.15y4.30kJ/m2,medianteelaumento del contenido de compuestos fenólicos y antocianinas de la fruta. También se ha logrado incrementar el contenido de compuesto fenólicos totales yflavonoides en mango, mediante el tratamiento con radiación UV-C (González-Aguilar, et al., 2007). Los autores concluyen, que después de tratar mangos frescos con radiación, la
Allende et al. (2006)
Escalona et al. (2010)
Yaun et al . (2004)
Yaun et al (2004)
actividad antioxidante incrementa considerablemente respecto a las frutas no tratadas.
En el mismo contexto, otros compuestos antioxidantes que se han podido incrementar mediante el tratamiento con UV-C son los flavonoides. Según Wang et al. (2009) las dosis de radiación adecuadas para incrementar el contenido de flavonoides en mora azul van de 2.15 a 6.45 kJ/m2. En adiciónaloanterior,sehademostradoquela radiación de UV-C en dosis de 2.8 kJ/m2 ejercen efectos positivos en el contenido de licopeno de sandía fresca (Artéz-Hernández et al.,2010).
Una de las razones por las cuales es conocida la producción de terpenos en alimentos es porque origina fitoalexinas, las cuales protegen a las plantas contra ataques de herbívoros, infecciones u organismos polinizadores. Se sabe que la radiación UVC favorece la generación de terpenos en alimentos. Beaulieu (2007) trató de identificar el efecto que ejerce la radiación UV-C en la producción de terpenos yésteres en rebanadas de melón. Encontró que la exposición a la radiación UV-C aumenta la concentración de terpenos en el tejido de las rebanadas. Otros investigadores quienes enfocaron la radiación UV-C hacia la
Tabla III. Verduras tratadas con radiación UV-C
generación de compuestos de autodefensa natural de los frutos fueron Guerrero et al. (2010), quienes trataron uvas para vinatería con el propósito de incrementar el contenido de estilbenos. En el estudio se encontró que el tratamiento con radiación UV-C incrementaba el contenido de estos compuestos 3.2 veces más que en las uvas sin tratamiento. De igual manera BenYehoshua (2003) logró incrementar el contenido de fitoalexinas en mandarina, medianteeltratamientoconradiaciónUV-C.
1.4.2. Atributos sensoriales
Uno de los atributos más importantes en los alimentos son sus características sensoriales, ya que estas dotan a los productos de un conjunto de factores organolépticos particulares que permiten identificarlos y en la medida en que estos sean afectados o no, se podrá decidir si la calidad del producto es aceptable.
En este sentido, se determinó el efecto de la radiación UV-C en los atributos sensoriales de brócoli fresco, al aplicar una dosis de 8 kJ/m2. Los resultados mostraron un cambio positivo en la textura, obteniendo una mayor integridad del tejido. Concluyeron también que esta tecnología puede reducir la senescencia y puede ayudar amantenerunamayorcalidadsensorialenel producto (Lemoine et al., 2010). Igualmente, se logró retardar el reblandecimiento en rebanadas depiña y fresaal inhibir laacción enzimática de las pectinasas, cuando se aplicaron dosis de 4.5 kJ/m2 (Pombo et al., 2011;Yong-GuiyHe,2012).
En otros casos, la radiación ultravioleta parece no tener un efecto inmediato sobre el tejido de los vegetales, como sucedió en el estudio de Erkan et al. (2001) donde el tratamiento en calabacita no mostró daño alguno después de ser tratada con una dosis de 9.86 kJ/m2. Sin embargo, después de una semana en refrigeración, está exhibió una coloración marrón-rojiza ocasionada por el tratamientoconradiaciónUV-C.
Basaran (2009) estudió el efecto que generó la radiación UV-C sobre los atributos sensoriales de avellanas. Realizando una comparación pareada entre las avellanas tratadas y las avellanas sin tratamiento, se determinó que no hubo diferencias significativas en el color, textura, olor y sabor. Se concluyó que la radiación no genera atributos sensoriales indeseables en estetipodeproductos.
Conclusiones y comentarios finales
En esta investigación documental se presentan algunos de los resultados obtenidos en frutas y verduras tratadas con radiación UV-C, ya sea listas para consumo, obienparasualmacenamientopost-cosecha. Puede concluirse, entre otras cosas, que el uso que se le dé a la radiación UV-C dependerá del objetivo particular de la aplicación, ya que, a juzgar por las investigaciones analizadas, esta tecnología genera cambios en cuatro aspectos importantes: carga microbiológica, características nutricionales, compuestos químicos y atributos sensoriales del producto. La magnitud del cambio o de que éste no se presente está en función de la dosis ydelascaracterísticasdel alimento, ya que cada alimento necesita una dosis de radiación específica dependiendo de su composición y de los objetivos del tratamiento. Se puede deducir que un tratamiento ideal con radiación UV-C debería tener las siguientes propiedades: reducción de carga microbiológica, no tener efectos negativos en los atributos sensoriales del alimento, aumentar las características nutrimentales propias del producto y por consecuencia incrementar su vida de anaquel.
Agradecimientos
El autor J. F. Haro-Maza agradece al Consejo Nacional de Ciencia y Tecnología (CONACYT) y a la Universidad de Las
Américas Puebla el financiamiento otorgado pararealizarsusestudiosdeposgrado.
Referencias
Allende, A., Marín, A., Buendía, B., TomásBarberán, F. y Gil-Muñóz., M. I. 2007. Impact of combined postharvest treatments (UV-C light, gaseous O3, superatmospheric O2 and high CO2) on health promoting compounds and shelf-life of strawberries. Postharvest Biology and Technology 46(3): 201–211.
Allende, A., McEvoy, J., Luo, Y., Artéz, F. Y. y Wang C. Y. 2006. Effectiveness of two-sided UVC treatments in inhibiting natural microflora and extending the shelf-life of minimally processed “Red Oak Leaf” lettuce. Food Microbiology. 23(3):241-249.
Allende, A, y Artéz, F., 2003. UV-C radiation as a novel technique for keeping quality of fresh processed ‘Lollo Rosso’ lettuce. Food Research International. 36(7): 739-746.
Artéz-Hernández, F., Robles, P. A., Gómez, A., Tomás-Callejas. y Artéz, F. 2010. Low UV-C illumination for keeping overall quality of freshcut watermelon. Postharvest Biology and Technology. 55:114-120
Barros, M. y Rocha, A. 2012. Food handler's perception of fresh cut products. Journal of Agricultural Science and Technology B. 2(4B): 482-486.
Basaran, P. 2009. Reduction of Aspergillus parasiticus on hazelnut surface by UV-C treatment. International Journal of Food Science and Technology, 44(9), 1857-1863.
Beaulieu, C. 2007. Effect of UV irradiation on cut cantaloupe: terpenoids and esters. Journal of Food Science. 72(4): 272-281.
Ben-Yehoshua, S. 2003. Effects of postharvest heat and UV application on decay, chilling injury and resistance against pathogens of citrus and other fruit and vegetables. Acta Horticulturae. 599:159167.
Calderón-Gabaldón, M., Raybaudi-Massilia, R., Mosqueda-Melgar, J., yTapia, M. 2012. Efecto de la luz UV-C y ácido málico sobre poblaciones de Rhodotorula glutinis y vida útil de rebanadas de papaya Maradol. Bioagro. 24(2):103-114.
Erkan, M., Wang, S., y Krizek. D, T., 2001. UV-C irradiation reduces microbial populations and
deterioration in Cucurbita pepo fruit tissue. Environmental andExperimental Botany. 45:1-9.
Erkan, M., Wang, S. Y. y Wang., C. Y. 2008. Effect of UV treatment on antioxidant capacity, antioxidant enzyme activity and decay in strawberry fruit. Postharvest Biology and. Technology. 48(2):163–171.
Escalona, V. H., Aguayo, E., Martínez- Hernández G. B. y Artés, F. 2010. UV-C doses to reduce pathogen and spoilage bacterial growth in vitro and in baby spinach. Postharvest Biology and Technol. 56:223–231.
Fonseca, M. J. y Rushing, J. W. 2006. Effect of ultraviolet-C light on quality and microbial population of fresh-cut watermelon. Postharvest Biology andTechnology. 40(3):256–261.
Gardner D. W. M. y Shama G. 2000. Modeling UVinduced inactivation of microorganisms on surfaces. Journal of Food Protection. 63(1): 6370.
González-Aguilar, G., Villegas-Ochoa, M., MartinezTellez, M., Gardea, A. y Ayala-Zavala, J. 2007. Improving antioxidant capacity of fresh-cut mangoes treated with UV-C. Journal of Food Science. 72(3):S197-S202.
Guan, W., Fan X. y Yan, R. 2012. Effects of UV-C treatment on inactivation of Escherichia coli O157:H7, microbial loads, and quality of button mushrooms. Postharvest Biology and Technology. 64:119 – 125.
Guerrero-Beltrán, J. A. y Barbosa-Cánovas, G.V. 2004. Advantages and limitations on processing foods by UV-C light. Food Science and Technology International. 10(3): 137-147.
Guerrero, R. F., Puertas, B., Jiménez, M. J., Cacho, J. y Cantos-Villar. E. 2010. Monitoring the process to obtain red wine enriched in resveratrol and piceatannol without quality loss. Food and Chemistry. 122:195-202.
Jian, L., Qian, Z., Yang, C., Jiaqi, Y., Jiankang, C., Yumei, Z. y Weibo, J. 2010. Use of UV-C Treatment to inhibit the microbial growth and maintain the quality of Yali pear. Journal of Food Science. 75(7): M503-M507.
Kim, C., y Hung, Y. 2012. Inactivation of E. coli O157:H7 on Blueberries by Electrolyzed Water, Ultraviolet Light, and Ozone. Journal Of Food Science, 77(4): M206-M211.
Lemoine, L., Civello, M., Chaves, R. y Martínez., A 2010. Influence of a combined hot air and UV-C treatment on quality parameters of fresh-cut broccoli florets at 0⁰C. International Journal of FoodScience andTechnology 45:1212–1218.
Liu C., Cai, L., Han X., y Ying. T. 2011. Temporary effect of postharvest UV-C irradiation on gene expression profile in tomato fruit. Gene. 486:5664.
Liu, J., Steven, C., Khan, V. A., Lu, J. Y., Wilson, C. L., Adeveve, O., Kabwe, M. K., Pusey, P. L., Chalutz, E. Sultana, T. y Droby, S., 1993 Application of ultraviolet-C light on storage rots and ripening of tomatoes. Journal of food protection 56(10):868-873.
López-Rubira, V., Conesa, A., Allende, A. y Artés, F. 2005. Shelf life and overall quality of minimally processed pomegranate arils modified atmosphere packaged and treated with UV-C. Postharvest biology and technology 37(2):174-185.
Mahdavian, K., Ghorbanli, M. y Kalantari, M. 2008. The effects of ultraviolet radiation on the contents of chlorophyll, flavonoid, anthocyanin and proline in Capsicum annuum L. Turkish Journal of Botany 32:25-33.
Manzoco, L., Da-Pieve, S., Bertolini, A., Bartolomeoli, I., Maifreni, M., Vianello, A. y Nicoli, M. C. 2011. Surface decontamination of fresh-cut apple by UV-C light exposure: Effects on structure, color and sensory properties. Postharvest Biology and Technology. 61(23):165– 171.
Ortoneda, M., O’keeffe, S., Cullen, J., Shamma, A. y Phipps, D. 2008. Experimental investigations of microwave plasma UV lamp for food applications. Journal of Microwave Power and Electromagnetic Energy. 42(4):14-23.
Perkins-Veazie, P., Collins, J. K. y Howard, L. 2008. Blueberry fruit response to postharvest application of ultraviolet radiation. Postharvest Biology and Technology. 47(2):280–285.
Pombo, H. G., Rosli, G. A., Martínez y Civello. P. M. 2011. UV-C treatment affects the expression and activity of defense genes in strawberry fruit (Fragaria ananassa.). Postharvest Biology and Technology. 59:94–102.
Ribeiro, C., Canada, J. y Alvarenga, B. 2012. Prospects of UV radiation for application in
postharvest technology. Journal of Food Agriculture. 24 (6): 586-597.
Rohan-V, T., Ramaswamy, C. A. y LaBorde, L. F. 2011. Ascorbic acid degradation in a model apple juice System and in apple juice during ultraviolet processing and storage. Journal of Food Science 75(2): 62-71.
Schenk, M. y Guerrero, S. 2008. Response of some microorganisms to ultraviolet treatment on freshcut pear. Food Bioprocess Technology. (1): 384–392.
Steffen, H., Zumstein, P. y Rip, G. R. 2010. Fruit and vegetables disinfection at SAMRO, Ltd. using hygienic packaging by means of ozone and UV radiation. Science andEngineering. 32: 144–149.
Stevens, C., Khan, V. A., Lu, J. Y., Wilson, C. L., Puseyc, P. L., Kabwea, M. K. Igwegbea, E. C. K., Chalutz, E. y Droby S. 1998. The germicidal and hormetic effects of UV-C light on reducing brown rot disease and yeast microflora of peaches. Crop Protection. 17(1): 75–84.
Stevens, C., Khan V. A., Wilson, C. L., Lu, J. Y., Chalutz, E., E. y Droby, S. 2005. The effect of fruit orientation of postharvest commodities following low dose ultraviolet light-C treatment on host induced resistance to decay. Crop Protection. 24(8):756–759.
U.S. Food and Drug Administration. 2000. Irradiation in the Production, Processing and Handling of Food, 21 CFR Part 179. Federal Registration. 65:71056–71058.
Wang, C. Y., Chen, C. T. y Wang, S. Y. 2009. Changes of flavonoid content and antioxidant capacityin blueberries after illumination with UVC. Foodand Chemistry. 117:426-432.
Yaun, B. R., Sumner, S. S., Eifert, J. D. yMarcy, J. E. 2004. Inhibition of pathogens on fresh produce by ultraviolet energy. Journal of Food Microbiology 90(1):1-8.
Yong-Gui, P. yHe Z. 2012. Effect of UV-C Radiation on the Quality of Fresh-cut Pineapples. Procedia Engineering. 37:113–119.

Temas Selectos de Ingeniería de Alimentos 7 - 1 (2013): 78 - 86

Potencial antimicrobiano de mezclas que incluyen aceites esenciales o sus componentes en fase vapor
M. A. Olivares - Cruz* y A. López - Malo
Departamento de Ingeniería Química, Alimentos y Ambiental, Universidad de las Américas Puebla. Ex hacienda Sta. Catarina Mártir S/N, San Andrés Cholula, Puebla. C.P.72810, México.
Resumen
El estudio de los aceites esenciales en fase vapor surge debido a la demanda de los consumidores sobre disminuir el uso de aditivos sintéticos en los alimentos y por lo tanto, la industria de alimentos está tratando de cambiarlos por aditivos naturales y sin modificar su perfil sensorial. Se ha reportado que los aceites esenciales en fase vapor tienen potencial como agentes antimicrobianos, al igual que las mezclas de los componentes principales presentes en los aceites esenciales, pero sus estudios son escasos. El objetivo de este trabajo es revisar investigaciones recientes acerca del potencial del empleo como agentes antimicrobianos de mezclas que incluyen aceites esenciales y sus componentes principales en fase vapor, para dar un panorama del posible desarrollo de sinergias, antagonismos, o aditividad al utilizar mezclas relevantes para la industria alimentaria.
Palabras clave: aceites esenciales, fase vapor, antimicrobianos naturales, mezclas.
Abstract
The study of essential oils in vapor phase has gained importance because of the consumer’s demand to reduce the use of synthetic additives in food. Thus, the food industry is trying to replace them by natural additives without modifying the food product sensory attributes. It has been reported that essential oils in vapor phase have the potential to act as antimicrobial agents, as well as the main components present in the essential oils; however, their study is scarce. The aim of this work is to review current research about of the potential use as antimicrobial agents of combinations that include essential oils and their major components in vapor phase, to present an overview of possible synergy, antagonism or additivity when using combinations relevant for the food industry.
Keywords: essential oil, vapor phase, natural antimicrobial, combinations.
Introducción
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: miguel.olivarescz@udlap.mx
Uno de los principales objetivos de la industria de alimentos es la seguridad o inocuidad alimentaria. Por ello, esta industria se encuentra en una constante búsqueda de nuevos y mejores agentes antimicrobianos, que cumplan con las demandas de los consumidores, los cuales exigen el uso de aditivos naturales que sustituyan a los aditivos sintéticos, con altos estándares de calidad adaptándose a la tendencia “verde” que se experimentaenlaactualidad.
Debido a estas demandas, los aceites esenciales se han estudiado como agentes antimicrobianos por su amplio espectro de inhibición microbiana y su origen natural. El enfoqueprincipaldeestosestudiosradicaenla aplicación directa de estos aceites y, en menor escala, el empleo en fase vapor. Actualmente, existe poca información sobre el efecto antimicrobiano de emplear mezclas de aceites esenciales en fasevapor o sobresu interacción con otros componentes presentes en los alimentos.
En el estudio de las mezclas de aceites esenciales y en la combinación con otros aditivos en alimentos, es de gran importancia determinar si la mezcla o combinación resulta en situaciones sinérgicas, antagónicas o de aditividad, ya que estas situaciones ocurren entre los componentes que forman los aceites esenciales (Rocha, 2012). Es por ello que el objetivo de este trabajo es revisar investigaciones actuales acerca de los efectos antimicrobianos de mezclas de aceites esenciales, componentes principales en fase vapor, y mezclas de aceites esenciales con aditivos en alimentos que dan como resultado sinergia,antagonismooaditividad.
eninglés GenerallyRecognized as Safe),como lo ha establecido la FDA (Food and Drug Administration) de los Estados Unidos y aunque otros lugares no se guíen por esta regulación, la lista de sustancias GRAS es aceptada en muchos países. Algunos ejemplos de antimicrobianos agregados a alimentos son los siguientes: acetaldehído, ácido acético, ácido ascórbico, acido benzoico, ácido cítrico, quitosano, CO2, diacetil, EDTA, H2O2, nitritos, ácido sórbico, sulfitos, entre muchos otros(RayyBhunia,2008).
1.1. Antimicrobianos naturales
Revisión bibliográfica
1. Agentes antimicrobianos
Un aditivo es aquella sustancia que se agrega intencionalmente al alimento durante las etapas de producción, envasado y conservación. Los aditivos pueden ser de origen natural o sintético (Badui, 2006). Dentro de los aditivos se encuentran los agentes antimicrobianos, que se definen como las sustancias que pueden inactivar microorganismosocontrolarsucrecimientoen los alimentos (Prescott et al., 2002). Los antimicrobianos que son agregados a los alimentos tienen que ser GRAS (por sus siglas
Los métodos convencionales de conservación para prolongar la vida de anaquel de alimentos, como lo son el calor, el empleo de atmósferas modificadas, empaques al vacío o refrigeración, no eliminan el total de microorganismos inicialmente presentes en el alimento, o no garantizan (dependiendo de la intensidad del método o factor de conservación aplicado) la extensión de la fase lag para cumplir con la vida útil del producto. Por ello, los procesos se combinan con la aplicación de agentes antimicrobianos (la mayoría de ellos sintetizados químicamente) para el control de microorganismos. En algunos casos y si los antimicrobianos químicos exceden la normativa vigente, pueden tener un potencial toxicológico (Sagar et al., 2012). Debido a ello, la industria de alimentos busca nuevas fuentes de agentes antimicrobianos, que cumplan además con el requisitodesernaturales.
En años recientes se ha observado la tendencia para usar agentes antimicrobianos naturales, para tener una oferta de alimentos frescos, naturales, mínimamente procesados y garantizarqueéstos sean inocuos (Sagar et al., 2012). Además, existen otras razones importantes para buscar alternativas. Una razón es que la sociedad experimenta una tendencia “verde” de consumo, con una demanda de menos aditivos sintéticos
añadidos a los alimentos, pero mayor seguridadycalidad(Nedorostova et al.,2009).
La acción antimicrobiana puede ser lograda mediante algunos compuestos químicos naturalmente presentes en los alimentos, y en cantidades suficientes, como la lisozima presente en el huevo y algunos ácidos orgánicos en frutas. En algunos casos se pueden formar durante el procesamiento, como el ácido láctico durante la fermentación de la leche para la producción del yogur (Ray y Bhunia, 2008). Existe una amplia variedad de alimentos que contiene antimicrobianos naturales o biocomponentes que pueden actuar como antimicrobianos, que abarcan desde la sal común, pasando por alimentos como la zanahoria, rábanos picantes, ajo, cebolla, entre muchos otros. De la misma forma, se encuentran especias y hierbas con acción contrabacterias ymohos como:tomillo,clavo, orégano, romero, o canela, entre otras (Marcen, 2000). Los aceites esenciales de plantas y frutas también tienen una acción antimicrobiana, los cuales también pueden ser agregados como antimicrobianos naturales a losalimentos.
2. Aceites esenciales ysu aplicación
Los aceites esenciales son componentes de plantas; están compuestos de una mezcla de terpenos, terpenoides, aldehídos y alcoholes, de los cuales un porcentaje alto es volátil (Laird y Phillips, 2011); estos compuestos son los responsables de su actividad antimicrobiana. Los estudios sobre aceites esenciales cobran más auge, ya que un porcentaje considerable de ellos, fueron nombrados como sustancias GRAS en el año 2005porlaFDA(Espina et al.,2011).
2.1. Fuentes deaceites esenciales
Existen diversos tipos de aceites esenciales que han sido reportados con efectos antimicrobianos.
Los aceites esenciales pueden variar en algunas de sus propiedades físicas (por ejemplo densidad, viscosidad), rendimiento, y sobre todo, en la composición de compuestos volátiles con actividad antimicrobiana. El tipo de material vegetal del cual se extraiga el aceite esencial afectará las características del mismo, pero también la diversidad de lugares, formas y condiciones de cultivo de la hierba, fruta o especia afectará la composición del aceite esencial y por lo tanto su actividad antimicrobiana (López-Malo et al., 2005). Algunos ejemplos de fuentes de aceites esencialesson:
1) Frutos cítricos. Espina et al. (2011) extrajeron aceites de naranja (Citrus sinensis), limón (Citrus lemon) y mandarina (Citrus reticulata), los cuales mostraron actividad antimicrobiana contra microorganismos patógenos (Enterococcus faecium, Staphylococcus aureus, Pseudomonas aeruginosa y Salmonella enterica).
2) Hierbas. Se ha reportado el efecto antimicrobiano de sus aceites esenciales en sobre al menos una bacteria, como: Allium sativum (ajo), Armoracia rusticana (rábano), Caryopteris clandonensis (espirea azul), Hyssopus officinalis (hisopo), Mentha villosa (menta), Nepeta faassenii (hierba gatera), Origanum majorana (mejorana), Origanum vulgare (orégano), Satureja montana (ajedrea), Thymus pulegioides (tomillo sanjuanero), y Thymus vulgaris (tomillo) (Nedorostova et al.,2009).
3) Especias. Algunas especias han sido utilizadas para el control microbiano, como la canela (Cinnamomum zeylaicum Blume) y el orégano Mexicano (Lippia berlandieri Schauer). El aceite esencial de canela ha demostrado en pruebas in vivo que controla el desarrollo de hongos endógenos del trigo (Triticum spp.), además de que puede inhibir la producción de aflatoxinas (Camarillo, 2006). El orégano es la especia más
comúnmente estudiada con actividad antimicrobiana(Portillo-Ruiz et al.,2012).
Con lo anterior, podemos notar que existe una amplia variedad de fuentes de aceites esenciales, estos aceites deben ser estudiados para saber su capacidad antimicrobiana e investigar las posibles interacciones que pueden presentarse al combinarlos o al mezclarlos con otros aditivos que se añaden a losalimentos.
2.2. Métodos deobtención
Los aceites esenciales son obtenidos por diferentes métodos como prensado, extracción con solventes y maceración. Existen otros métodos como el de extracción por medio de dióxido de carbono líquido en condiciones supercríticas, los cuales dan un mayor rendimiento y mejores atributos, pero el costo es mayor. El método más usado es destilación por arrastre con vapor y recientemente se ha implementado extracción asistida por microondas. Otro método de obtención de los aceites esenciales es por medio de solventes, este método puede influir en la acción antimicrobiana, ya que los aceites esenciales extraídos con hexano han demostrado mayor eficacia antimicrobiana que los destilados por arrastre con vapor (Burt, 2004). Sin embargo, existe un costo extra asociado a la separación del solvente por lo que es una técnica poco utilizada para la obtención de aceites esenciales.
2.3. Aceites esenciales en adición directa y en fasevapor
Los aceites esenciales son aplicados principalmente de dos maneras: uno en fase directa (líquida) y otra en fase vapor. Cabe mencionar que la aplicación se ha probado en sistemas modelos que tratan de simular las condiciones en alimentos, y pocas investigaciones reportan la aplicación de los aceitesesencialesenalimentosreales.
Para la aplicación en fase directa, el aceite esencial se coloca en el sistema modelo, generalmente a base de agar (el cual puede variar de acuerdo al estudio). Se ajusta a las concentraciones que se desean evaluar, y en cada una de las concentraciones se inocula la cepaquesequiereestudiar.
Unejemplodeaplicaciónenfasedirectaes el reportado en el estudio realizado por Portillo-Ruiz et al. (2012), para la evaluación de la actividad antimicrobiana del orégano mexicano (Lippia berlandieri Schauer). Este trabajo fue realizado en un medio de laboratorio (agar), al cual después de la esterilizaciónseleagregoelaceiteesencialdel orégano mexicano diluido en alcohol, en diferentes concentraciones 50, 100, 150 y 200 mg/kg. Posteriormente, los medios fueron inoculados con cepas de algunos mohos (Aspergillus, Penicillium, y Rhizopus spp) en el centro de las cajas. Se incubaron a temperatura ambiente, teniendo un monitoreo cada48hpor40días.Lasconcentracionesque lograron la inhibición fueron 150 mg/kg para Rhizopus spp,150mg/kgpara Aspergillus spp. y200mg/kgpara Penicillium spp.
Por otra parte, la aplicación en fase vapor, se lleva a cabo generando una atmósfera al colocar el aceite esencial en un sistema herméticamente cerrado (Fig. 1) en donde se colocan cajas Petri inoculadas con las cepas microbianas a evaluar y en el fondo el aceite esencial en diferentes concentraciones permitiendo su volatilización (mL/L de aire, mmol/L de aire o µL/L de aire) sin tener contacto directo con los cultivos (VelázquezNuñez et al., 2013).
Esta técnica se describe en el estudio hecho por Tunc et al. (2006), donde se utilizó un sistema (frasco) herméticamente cerrado que contiene cajas Petri de 8.5 cm de diámetro descubiertasenelcentrodelsistema.Lascajas contenían 10 mL del medio de ensayo (agar) inoculadas en el centro con 104 esporas del
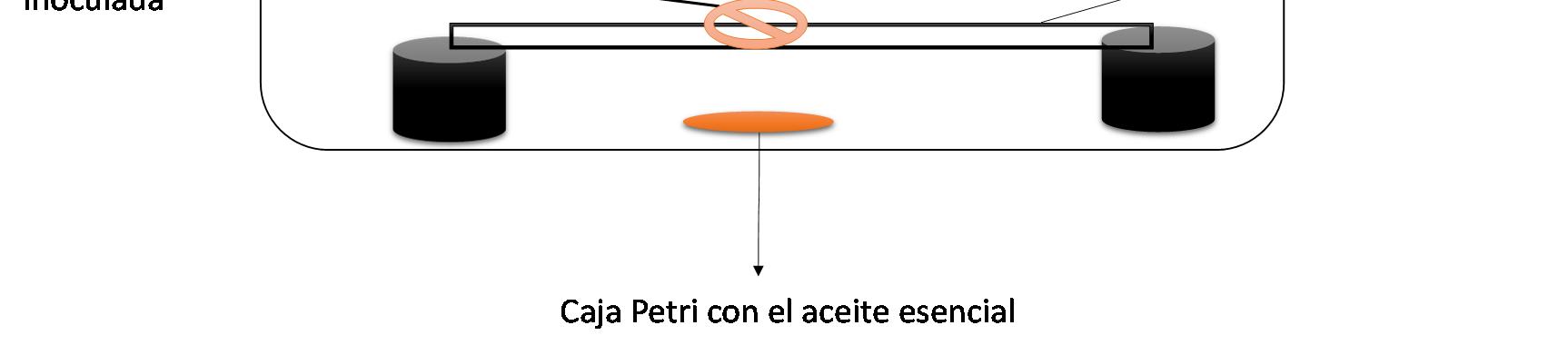
Fig.1. Diagrama esquemático de un sistema herméticamente cerrado para la aplicación de aceites esenciales en fase vapor.
microorganismo a evaluar (Penicillium notatum), los compuestos carvacrol, cinamaldehído y alil-isotiocianato (AITC), constituyentes mayoritarios de los aceites esenciales de orégano, tomillo y de plantas de la familia Cruciferae, respectivamente, se introdujeron en un papel filtro sin tener contacto directo con el inóculo. La respuesta de crecimiento del moho fue evaluada diariamente, encontrando que la concentración mínima inhibitoria (CMI) fue de 32.5 μmol/L deaireparaelcarvacrol, de3.9 μmol/Ldeaire para el cinamaldehído y de 3.8 μmol/L de AITC.
3. Mezclas que incluyen aceites esenciales o sus componentes en fase vapor.
3.1. Interacciones delas mezclas
Los conceptos de sinergia, antagonismo y aditividad están muy ligados a los posibles efectosantimicrobianosdelempleodemezclas deagentesantimicrobianos.
Goñi et al. (2009) mencionan que la sinergia se presenta cuando el efecto de las sustancias combinadas es mayor que la suma
de los efectos individuales; el antagonismo se observa cuando el efecto de la mezcla es menor que cuando se aplican individualmente yunefecto aditivoseobservacuandoelefecto combinado es igual a la suma de los efectos individuales.
Por lo cual, al combinar los aceites esenciales entre ellos mismos o con otros aditivos, se pueden encontrar varias formas de interacción, las cuales tienen importancia en la industriadealimentos.
3.2 Aplicaciones demezclas
Los aceites esenciales son muy volátiles, por lo cual son ideales para ser evaluados en fase vapor. Varias investigaciones sugieren que algunos compuestos presentes en los aceites esenciales, como lo son los terpenos, tienen una mayor actividad antifúngica en fase vapor (Vilela et al.,2009). Laactividadinherentedel aceite esencial se relaciona con su composiciónquímicaylainteracciónentresus componentes. Algunos estudios mencionan que los aceites esenciales en su conjunto tienenunaactividadantimicrobianamayorque las mezclas de sus componentes mayoritarios,
demostrando que los componentes que conforman al aceite esencial son los responsables de la actividad antimicrobiana y por lo tanto pueden presentar efectos sinérgicos(Rocha,2012).
La información reportada en la literatura sobre las posibles mezclas que se pueden dar entre aceites esenciales es muy diversa, pero también existen reportes en donde la combinación se evalúa entre aceites esenciales y compuestos químicos, o con películas comestibles,entreotrosposiblesaditivos.
Estudios llevados a cabo por Goñi et al (2009) mencionan que las mezclas de vapores generados por la combinación de aceites esenciales de canela y clavo tienen acción antimicrobiana sobre bacterias (Escherichia coli, Yersinia enterocolitica, Pseudomonas aeruoginosa y Salmonella choleraesuis). Las Concentraciones mínimas inhibitorias (CMI) para las mezclas de aceites de canela y clavo (1:1) obtenidas se muestran en la Tabla I. Estos autores encontraron un efecto antagonista entre el aceite esencial de canela y clavo para E. coli pero encontraron efectos aditivos para las demás bacterias, Y.
enterocolitica, S. choleraesuis, B. cereus, L. monocytogenes, E. faecalis y S. aureus; mientras que usando las concentraciones de la máxima inhibición (Tabla 1), encontraron tres situaciones de sinergia contra B. cereus, L. monocytogenes y Y. enterocolitica y efectos aditivos para las demás bacterias, E. coli, S. choleraesuis, E. faecalis, y S. aureus.
López et al. (2007) evaluaron diferentes aceites esenciales y mezclas con sus componentes químicos más relevantes, para probar posibles interacciones entre los componentes. El aceite esencial de canela fue combinado con cinamaldehído y el aceite esencial de tomillo con timol. Los resultados de los efectos de sinergia, antagonismo y aditividad sobre los microorganismos evaluadossemuestranenlaTablaII.
Por otro lado, también existen reportes sobre las combinaciones de aceites esenciales o sus componentes mayoritarios con otros aditivos como el dióxido de azufre y los vapores de etanol, que han sido usados para prolongar la vida de anaquel de productos de panadería; sin embargo, el uso de estos aditivos conlleva efectos adversos (daños a los
Tabla I. Concentraciones mínimas inhibitorias y de máxima inhibiciónpara varios microorganismos.
Concentraciones mínimas inhibitorias (mg/L)
Concentración de la máxima inhibición (mg/L)
E coli 9090
Y. enterocolitica 1890
S. choleraesuis 135180
B. cereus 36135
S. aureus 54135
L. monocytogenes 90180
E. faecalis 90135
Adaptado de Goñi et al . (2009). Las concentraciones son de aceite esencial de clavo y canela (1:1)
Tabla II. Sinergia, antagonismo y aditividad de mezclas de aceites esenciales y compuestos fénolicos contra diversos microoganismos. CompuestosSinergiaAntagonismoAditividad canela + cinamaldehido A. flavusS. choleraesuisL. monocytogenes, C. albicans
tomillo+ timol L. monocytogenes, S. choleraesuis, A. flavus
Adaptado de Coutinho et al . (2011)
alimentos, sabores desagradables y alergias). Ejemplo de ello es el trabajo de Tunc et al (2006) donde utilizaron mezclas de diversas concentraciones de dióxido de azufre y etanol con componentes de aceites esenciales en fase vaporcontra Penicillium notatum,encontrando seis situaciones sinérgicas: etanol/carvacrol, dióxidodeazufre/carvacrol,dióxidodeazufre/ (ITC, dióxido de azufre/ cinamaldehido, AITC/cinamaldehido, y cinamaldehido/ carvacrol. La mezcla etanol (0.86 mmol/L) y carvacrol (10 µmol/L) supone una acción sinérgica contra P. notatum, con potencial para ser usada en alimentos; el etanol (3.4 mmol/L) se combinó con cinamaldehido (3.1 µmol/L) y solo se observó un aumento en el tiempo para observar el crecimiento del moho (fungistático), la mezcla SO2 (0.16 mmol/L) y carvacrol (1.6 µmol/L) tuvo una acción sinérgica.
Estas acciones sinérgicas tienen un impacto importante al reducir las concentraciones de los aditivos químicos y mejorar los atributos sensoriales del alimento usando antimicrobianosnaturales.
Por otra parte, la adición de antimicrobianos naturales a empaques de alimentos ha tomado una gran importancia a nivel mundial. Kurek et al. (2013) probaron diferentes composiciones de películas comestibles a base de quitosano, con
C. albicans
diferentes concentraciones de carvacrol (su uso como antimicrobiano es reconocido, reportando también actividad en fase vapor) evaluando a los microorganismos: Bacillus subtilis, Escherichia coli, Listeria innocua y Salmonella enteritis, (los inóculos no tuvieron contacto directo con la película de quitosano). Se obtuvieron resultados favorables para las películasformuladasconquitosanoycarvacrol en las siguientes concentraciones: 4.62 x 10-8 g/mL y 6.41 x 10-8 g/mL de carvacrol, mostrando un fuerte efecto antimicrobiano contra casi todos los microorganismos probados,peronocontra S. enteritidis.
De manera similar, se probó la eficacia de la fase vapor del aceite esencial de canela combinada con películas plásticas de polietileno y polietilentereftalato, las cuales tampoco tuvieron contacto directo con el inóculo. La película activa, empezó a tener actividad cuando se añadieron 2% y 4% de aceite esencial de canela (0.071 g/m2 y 0.142 g/m2), estas concentraciones produjeron inhibición total de Aspegillus flavus (Manso et al.,2013).
Conclusiones
Las combinaciones entre los aceites esenciales, sus componentes y aditivos en
alimentos, son muy importantes y de gran utilidad, ya que ayudan a reducir la cantidad de aditivos sintéticos necesarios para eliminar o inhibir microorganismos patógenos o causantes del deterior de alimentos, y así cumplir con las expectativas del consumidor que demanda alimentos mínimamente procesados, libres de aditivos sintéticos y que continúelatendencia“verde”queexperimenta la sociedad. Estas combinaciones de aceites esenciales en fase vapor reportadas hasta el momento han mostrado actividad antimicrobiana, la efectividad de estas combinaciones se dan mayoritariamente por los componentes que constituyen a los aceites (timol,cinamaldehído,carvacrol,etc.)
Aunque existe casos reportados de sinergia, aditividad y antagonismo, son necesarios más estudios en donde la aplicación se evalúe en alimentos ynosoloensistemasmodelo,porlo cual la línea de investigación se encuentra abierta para encontrar más interacciones entre diferentes tipos de aceites esenciales y combinaciones con aditivos. Además, las mezclas que han sido reportadas como sinérgicas en sistemas modelo deben aplicarse en alimentos para posteriormente evaluar los efectos sobre la calidad sensorial y con ello la aceptacióndelconsumidor.
Burt, S. 2004. Essential oils: their antibacterial properties and potential applications in foods—a review. International Journal of Food Microbiology 94:223–253.
Camarillo, E. 2006. Actividad antifúngica de aceites esenciales de canela (Cinnamomum zeylanicum Blume) y Orégano (Origanum vulgare L.) y su efecto sobre la producción de aflatoxinas en nuez pecanera. Revista Mexicana de Fitopatología. 1(24):8-12.
Coutinho, H.D.M., Rodrigues, F.F.G., Nascimento, E.M.M., Costa, J.G.M., Falcão-Silva y SiqueiraJunior, J.P. 2011. Synergism of gentamicin and norfloxacin with the volatile compounds of Lippia microphyla Cham (Verbenaceae). Journal essential oil Research 23:24-28.
Espina, L., Somolinos, M., Lorán, S., Conchello, P., García, D. y Pagán, R. 2011. Chemical composition of commercial citrus fruit essential oils and evaluation of their antimicrobial activity acting alone or in combined processes. Food Control. 22:896– 902.
Goñi, P., López, P., Sánchez, C., Gómez-Lus, R., Becerril, R. y Nerín, C. 2009. Antimicrobial activity in the vapor phase of a combination of cinnamon and clove essential oils. Food Chemistry. 116:982–989.
Kurek, M., Moundanga, S., Favier, C., Gali, K. y Debeaufort, F. 2013. Antimicrobial efficiency of carvacrol vapour related to mass partition coefficient when incorporated in chitosan based films aimed for active packaging. Food Control. 32:168-175.
Laird, K., y Phillips, C. 2011. Vapor phase: a potential future use for essential oils as antimicrobials?. Letters in Applied Microbiology. 54:169–174.
Agradecimientos
El autor M. A. Olivares-Cruz agradece al Consejo Nacional de Ciencia y Tecnología (CONACYT) y a la Universidad de las Américas Puebla (UDLAP) por el apoyo y financiamientodesusestudiosdeposgrado.
López, P., Sánchez, C., Batlle, R. y Nerin, C. 2007 Vapor-phase activities of cinnamon, thyme, and oregano essential oils and key constituents against foodborne microorganisms. Jounal of Agriculture and Food Chemistry. 55:4348-4356.
López-Malo, A. Alzamora, S.M. y Palou, E. 2005. Naturally Occurring Compounds – Plant Sources. En: P.M. Davidson, J.N. Sofos y A.L. Branen (Eds.). Antimicrobials in Foods. Tercera edición. CRC Press, NewYork. pp. 429 - 451.
Referencias
Badui S. D. 2006. Química de alimentos. Cuarta edición. Pearson educación. México. 716p.
Manso, S., Cacho-Nerin, F., Becerril, R., y Nerín, C. 2013. Combined analytical and microbiological tools to study the effect on Aspergillus flavus of cinnamon essential oil contained in food packaging. Food Control. 30:370-378.
Marcen, J.J. 2000. Antimicrobianos naturales. Medicina Naturista. 2:104-108.
Nedorostova, L., Kloucek, P., Kokoska, L., Stolcova, M. y Pulkrabek, J. 2009. Antimicrobial properties of selected essential oils in vapour phase against foodborne bacteria. Food Control. 20:157–160.
Portillo-Ruiz, M., Sánchez, R., Ramos, S., Muñoz, J. y Moorillón, G. 2012. Antifungal effect of mexican oregano (Lippia berlandieri Schauer) essential oil on a wheat flour-based medium. Journal of Food Science. 77(8):441-445.
Prescott, L. Harley, J. y Klein, D. 2002. Microbiology. Quinta edición. Mc Graw Hill, EE.UU. 1135 p.
Ray, B. y Bhunia, A. 2008. Fundamental Food Microbiology. Cuarta edición. CRC Press, E.E.U.U. 492 p.
Rocha, P. 2012. Synergistic antibacterial activity of the essential oil of Aguribay (Schinus molle L.). Molecules. 17:12023-12036.
Sagar, K., Akshatha, R. y Prasad, S. 2012. Antimicrobial efficacy of some natural
cosmeceuticals, neutraceuticals and medicinal plant extract and ultrastuctural alterations in foodborne pathogens. International Journal of Pharmacy and Pharmaceutical Sciences. 4, suppl. 1:113-120.
Tunc, S., Chollet, E., Chalier, P., Preziosi-Belloy, L. y Gontard, B. N. 2006. Combined effect of volatile antimicrobial agents on the growth of Penicillium notatum International Journal of Food Microbiology. 113: 263–270.
Velázquez-Nuñez, M.J., Avila-Sosa, R., Palou, E. y Lopez-Malo, A. 2013. Antifungal activity of orange (Citrus sinensis var. Valencia) peel essential oil applied by direct addition or vapor contact. Food Control. 31:1-4
Vilela, G. R., de Almeida, G. S., D'arce, A.B.R., Moraes, M.H.D., Brito, J.O., da Silva, M.F.G. F., Silva S.C., Piedade, S.M. de S., Calori-Domingues, M.A. y da Gloria, E.M. 2009. Activity of essential oil and its major compound, 1,8-cineole, from Eucalyptus globulus Labill., against the storage fungi Aspergillus flavus Link and Aspergillus parasiticus Speare. Journal of Stored Products Research. 45:108–111.

Temas Selectos de Ingeniería de Alimentos 7 - 1 (2013): 87 - 96
Propiedades del alginato y aplicaciones en alimentos
G. C. Avendaño - Romero*, A. López - Malo y E. Palou

Departamento de Ingeniería Química, Alimentos y Ambiental, Universidad de las Américas Puebla. Ex hacienda Sta. Catarina Mártir S/N, San Andrés Cholula, Puebla. C.P.72810, México.
Resumen
La industria de alimentos busca ingredientes que al ser adicionados a un alimento, prolonguen su vida útil y reduzcan la tasa de cambios que el producto alimenticio podría experimentar durante su almacenamiento, transporte y manipulación. Entre de estos aditivos, los alginatos, han adquirido gran importancia en los últimos años. Éstos tienen la capacidad de actuar como agentes estabilizantes, gelificantes, espesantes y formadores de películas. Además, son fáciles de obtener a partir de algas marinas que se encuentran en todos los mares del mundo y tienen relativamente bajo costo. Debido las propiedades mencionadas, los alginatos son utilizados en postres, productos de panadería, helados, conservas, aderezos de ensaladas, embutidos, bebidas y geles de repostería, entre otros muchos productos alimenticios. Recientemente se han utilizados en la formación de películas comestibles aplicadas a frutas mínimamente procesadas, con el fin de mantener los atributos de frescura. Por lo anteriormente mencionado, el objetivo de esta revisión es aportar información acerca de su proceso de obtención, como sus propiedades y aplicaciones en alimentos.
Palabras clave: alginato, gelificación, espesantes, formadores de películas, aplicaciones.
Abstract
The food industry seeks for food ingredients to extend the shelf-life and reduce changes during storage, transportation and handling. In recent years, production of alginates has gained importance. Alginates have the ability to act as stabilizer, gelling agents, thickeners and film formers. They are easily obtained from seaweed found in all oceans of the world, and have low cost. Thus, alginates are added in desserts, baked goods, ice cream, salad dressings, sausages, drinks and are employed as ingredients and confectionery gels among other foodstuffs. Also, alginates have been used in edible film formation applied to cover fruit minimally processed, in order to maintain their freshness. The purpose of this review is to provide information about the production process of alginates, their properties and applications in foods.
Keywords: alginate, gelation, thickeners, film formers, food applications.
Introducción
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Durante los últimos años se ha observado un interés sobrelas propiedades del alginato en la industria alimentaria. Tales aspectos han sido compilados en la literatura por Imeson (2010), resaltando el efecto prebiótico de los alginatos de bajo peso molecular, los beneficios de su ingesta como fibra para la reducción de los niveles de azúcar y colesterol en sangre, así
Dirección electrónica: gabrielac.avendanoro@udlap.mx
como la capacidad para prolongar la vida útil de los productos (Parra-Huertas, 2010). Estas ventajas del alginato y las recientes tendencias tecnológicas se han fusionado y se proponen ahora alternativas del empleo de los alginatos para reducir los efectos que alteran frutas y vegetales mínimamente procesados, al ser recubiertos con películas formadas con alginato, y para reducir el uso indiscriminado de empaques para alimentos, ya que generalmente no son biodegradables, lo que provocaaltos niveles decontaminación anivel mundial(SrinivasayTharanathan,2007).
El ácido algínico es un compuesto químico que se encuentra en la pared celular de las algas marinas pardas (feofíceas). Los alginatos son sales del ácido algínico que pueden ser formadas con Na, K, Mg, Ca, entre otros, formando sales con diferentes grados de solubilidad en agua, lo cual confiere diversos grados de viscosidad (Yabur et al., 2007). Los primeros estudios relacionados con la extracción dealginatos apartirdealgas pardas fueron realizados por el químico británico E. C. Stanford en el año de 1883. Stanford, a través de procedimientos de digestión de las algas pardas con carbonato sódico, observó que se formaba una sustancia gelatinosa a la cual denominó “algina”, por ser una sustancia derivadadealgas(MedinayLedo,2010).
El ácido algínico en su forma salina es un polímero biodegradable y biocompatible, que forma geles con facilidad en presencia de iones calcio. Este polímero, por su gran versatilidad, ha sido utilizado como estabilizador, aglutinante, espesante, gelificante y formador de películas delgadas sobre superficies. La siguiente revisión tiene por objetivo aportar información acerca de las propiedadesyaplicacionesdelosalginatos,así comodesuprocesodeobtención.
Revisión bibliográfica
1. Aspectos generales del alginato
Los alginatos son los polisacáridos más abundantes presentes en las algas marinas. Comprenden hasta 40% de su peso seco. Son los componentes estructurales de la pared celular de las algas, cuya función principal es dar rigidez, elasticidad, flexibilidad y capacidad de enlazar agua (Hernández et al., 2005). Los alginatos son extraídos principalmente de tres especies de algas marrones. Éstas incluyen Laminaria hyperborea, Ascophyllum nodosum y Macrocystis pyrifera. En su estado natural, los alginatos se presentan como una mezcla de sales de los cationes que comúnmente se localizan en el agua de mar, principalmente Ca2+, Mg2+ yNa+. Las proporciones en las que estos iones están unidos al alginato dependen desucomposición,así comodelaselectividad de enlace de los cationes alcalinotérreos por el alginato (Yabur et al., 2007)
Los alginatos son una familia de polisacáridos lineales, conteniendo cantidades variables de ácido β-D-manurónico (M: 1,4enlace ácido β-D-manopiranosilurónico 4C1) y de ácido α-L-gulurónico (G: 1,4-enlace ácido α-L-gulopiranosilurónico 1C4). Su composición (dada por la relación característica manurónico/gulurónico M/G) y secuenciasvaríandependiendodela fuentede la cual proviene el polisacárido. Este polímero debe su carácter polianiónico a los grupos carboxiloqueaparecenalolargodelacadena. La composición y extensión de las secuencias y el peso molecular determinan las propiedades físicas de los alginatos (Lupo et al., 2012).Éstosseagrupanenosedistribuyen en secciones constituyendo homopolímeros
tipo bloques G (-GGG-), bloques M (-MMM-) o heteropolímeros en los que los bloques M y G se alternan (-MGMG-). Tanto la distribución de los monómeros en la cadena polimérica como la carga y volumen de los grupos carboxílicos, confieren al gel formado características de flexibilidad o rigidez dependiendo del contenido de gulurónico. Si enlaestructurapoliméricahaymayorcantidad de bloques G, generalmente el gel es duro y frágil, mientras que con la presencia de mayor proporción de bloques M, el gel formado se presenta suave y elástico. Los bloques de secuenciasMM,MG, se encuentran unidos por enlaces glucosídicos β (1-4); y los bloquesGG,GM, unidos por enlaces glucosídicos α (1-4)(Lupo et al.,2012).
Las sales del ácido algínico están formadas por tres bloques, M, G y MG. Cuando dos cadenas de bloque G se alinean, se forman sitios de coordinación. Debido a la forma de bucles de estas cadenas, existen cavidades entre ellas que tienen el tamaño adecuado para acomodar al ion calcio y además están revestidas con grupos carboxílicos y otros átomos de oxígeno electronegativos. Después de la adición de iones de calcio, el alginato sufre cambios conformacionales, dando lugar al conocido modelo de gelificación del alginato conocido como “caja de huevo” (Fig 1). Esto se basa en la dimerización de la cadena y, finalmente, en la mayor agregación
de los dímeros. Se encontró que la fuerza de los geles de alginato depende del número de enlaces cruzados formados, del tipo de reticulación iónica, y de la longitud y la rigidez de los bloques entre los enlaces (Mancini et al., 1999). Lo anterior es importante, ya que los alginatos que presentan grandes regiones de bloques G forman un gel de fuerza alta y exhiben una alta porosidad. Los que presentan grandes bloques M forman un gel de fuerza media, pero con una alta resistencia a la sinéresis y exhiben poros más pequeños que los hacen más suaves (Hernández et al., 2005).
Laviscosidaddelassolucionesdealginatos depende de la longitud de las moléculas, cuanto mayor sea la longitud de las cadenas, más alta será la viscosidad. Al disolverse en agua, las moléculas se hidratan y aumenta su viscosidad. En una solución ácida el alginato formará un gel, ya que a pH bajo los grupos carboxílicos de los ácidos urónicos aceptan protones, lo que hace que se favorezca la formación de enlaces de los bloques G. La hidratación del ácido algínico a pH bajo conduce a la formación de un gel de alta viscosidad. En un medio ácido, la viscosidad se va incrementando por la disminución de la solubilidad del ácido algínico libre, precipitando en forma de gel a un pH en el intervalo de 3 a 4 (Lupo et al., 2012).
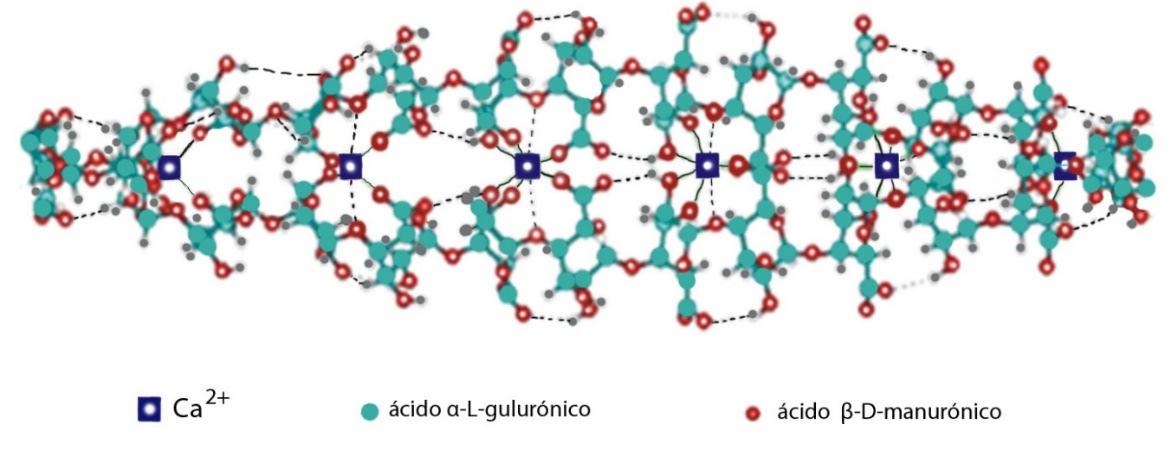
Fig.1. Modelo “caja de huevo” que describe la estructura del alginato. (Adaptada de Reddy y Reddy2010).
2. Obtención dealginato
La obtención del alginato se basa en un conjunto de reacciones de intercambio iónico para la extracción del ácido algínico del alga en forma de alginato de sodio. El proceso se ha ido modificando y optimizando con el tiempo, permitiendo la producción de alginato conmayorcalidad.
Existen dos procesos básicos para la obtención de alginato de sodio. En el primero, los principales intermediarios son alginato de calcio y ácido algínico. En el segundo, no se forma alginato de calcio, sólo ácido algínico. En ambos procesos, durante la etapa de conversión del ácido algínico a alginato de sodio se usa agua o alcohol como solvente, obteniendo resultados muy diferentes. En el proceso para alginato de calcio normalmente el solvente es agua y en el proceso para ácido algínico se emplea más el alcohol, debido al alto contenido de agua en el ácido algínico (Arvizu et al., 2002). El ácido algínico y el alcohol pueden ser mezclados en un recipiente con agitación, añadiendo la cantidad calculada del agente alcalino deseado, o bien, añadiéndolo simultáneamente con el alcohol. En algunas patentes se describen estos procesos, pero no se proporcionan detalles de la concentración o el volumen del solvente empleado. El método describe que el ácido algínico se lava con agua hasta obtener un pH de 4 y se mezcla con carbonato de sodio hasta obtener un pH de 7. Se incorpora el álcali dependiendo de su naturaleza: a) se añade carbonato de sodio, potasio o magnesio como polvo seco y molido; b) los hidróxidos de potasio o sodio se añaden como soluciones acuosasconcentradasosolucionesalcohólicas; c) el amoniaco se añade en la forma de amoniaco-agua, 28–29%, o como un gasen un recipientedepresión(Arvizu et al., 2002).
La obtención de alginato de sodio se inicia conlamoliendadelmaterial;enseguidaelalga molidaysecaeshidratadaconunasoluciónde
formaldehído.Posteriormenteserealizalapreextracción con ácido clorhídrico, para convertirlas sales dealginato aácido algínico. La extracción alcalina se puede realizar también con carbonato de sodio a alta temperatura para convertir el ácido algínico a su forma soluble, prosiguiendo con la precipitación con cloruro de calcio, para obtener alginato de calcio. Por último, se realiza el prensado, secado y reducción del producto obtenido a un tamaño apropiado, para su empaquetamiento. A partir de este proceso general, se realizan cambios químicos y físicos para obtener productos específicos para los diferentes usos en la industria alimentaria(Arvizu et al., 2002).
3. Propiedades dealginato
Existen diferentes estudios que indican la seguridad del uso de los alginatos en los alimentos. Los alginatos de sodio, potasio, calcio y amonio, ácido algínico y el alginato de propilenglicol, son aditivos alimenticios reconocidos como inocuos y seguros, según la Food and Drug Administration de los Estados Unidos (FDA por sus siglas en inglés) (FAO, 2001). De la misma manera, están enlistados en el Codex Alimentarius que provee la Food and Agriculture Organization (FAO por sus siglas en inglés) y la World Heald Organization (WHO por sus siglas en inglés) de las Naciones Unidas, donde se establece que los límites de ingesta diaria de ácido algínico y de sus sales derivadas para los humanos, es de 50 mg/kg de peso corporal, y del alginato de propilenglicol de 25 mg/kg de pesocorporal(FAO/WHO,2001).
La aplicación de los alginatos se basa en cuatro propiedades principales. La primera concierne a su habilidad como espesantes al ser disueltos en agua, generando un aumento en la viscosidad de la solución en la que se disuelven. La segunda a su capacidad de retener agua. La tercera se debe a su habilidad de formar un gel a partir de una serie de
reacciones químicas deintercambio iónico que dan lugar a la formación de enlaces entre las cadenas adyacentes del polímero del alginato; particularmente se realiza un intercambio de iones sodio por cationes divalentes o trivalentes. La cuarta se basa en la propiedad deformarpelículas(Funami et al., 2009).
La capacidad del alginato como estabilizante se mide en función de su grado de polimerización (GP), el cual es una medida del peso molecular promedio de las cadenas que lo constituyen y se relaciona directamente con la viscosidad de sus soluciones. La pérdidadeviscosidad en el almacenamiento es una medida del grado de despolimerización delalginato (McHugh1987).
Los alginatos con alto GP son menos estables que los que tienen un bajo GP. Los alginatos de sodio de baja viscosidad (50 mPa.s) se han almacenado a 10-20°C con ningún cambio observable en tres años. Alginatos de sodio de viscosidad media (400 mPa·s)muestranunapérdidade10%a25°C y de 45% a 33°C después de un año, y los alginatos de mayor viscosidad son menos estables. Alginatos de propilenglicol muestran una pérdida del 40% de la viscosidad después de un año a 25ºC y también se hacen menos solubles. El alginato de amonio es generalmente menos estable que cualquiera de los anteriores. El ácido algínico es el menos estable de los productos y cualquier material de cadena larga se degrada en cadenas más cortasenpocosmeses atemperaturaambiente. Sin embargo, el material de cadena corta es estable y el ácido algínico con un GP de aproximadamente 40 unidades de ácido urónico por cadena, muestrará muy pocos cambios durante un año a 20°C. Así mismo, para que estos alginatos sean más estables necesitan un intervalo de pH entre 5 y 9 (McDowell, 1977); pequeñas cantidades de calcio aumentan en gran medida la estabilidad de las soluciones de alginato de sodio. Las soluciones de alginato de propilenglicol son
estables a temperatura ambiente a pH de 3-4; por debajo de pH 2 y por encima de pH 6 pierden viscosidad rápidamente, incluso a temperatura ambiente (McNeely y Pettitt, 1973). Una condición que se debe tomar en cuentaparalosalginatoscomercialesesquese deben almacenar en un lugar fresco, a 25°C o inferior, ya que las temperaturas elevadas pueden causar despolimerización significativa que afecta a las propiedades comercialmente útiles, tales como la viscosidad y resistencia delgel(McHugh,1987).
Una característica interesante de los alginatos es su capacidad de retención de agua o adsorbente, la cual es de tal magnitud que incluso en algunas aplicaciones en otras industrias diferentes a la de alimentos los denominan como superabsorbentes. Es decir, pueden formar retículos poliméricos tridimensionales que poseen grupos hidrófilos capaces de absorber grandes volúmenes de agua o fluidos biológicos, desde diez hasta miles de veces su propio peso, y son capaces de retenerlos bajo presión. Pueden mencionarse como desventaja que los geles que se forman al absorber el agua pueden bloquearse y,porlotanto,perder lacapacidad de absorción y disminuir su velocidad de absorción de agua. Estos problemas pueden minimizarse por medio del aumento del número de grupos carboxílicos por unidad de ácido urónico, a través de reacciones de esterificación de los grupos hidroxilos (Hernández et al., 2005).
En cuanto a la capacidad gelificante de los alginatos, la cual se usa ampliamente, se sabe que la formación del gel se inicia a partir de unasolucióndesaldealginato yunafuentede calcio externa o interna, desde donde el ion calcio se difunde hasta alcanzar la cadena polimérica. Como consecuencia de esta unión seproduceun reordenamiento estructural en el espacio, resultando en un material sólido con las características de un gel. El grado de gelificación depende de la hidratación del
alginato, la concentración del ion calcio y la proporción deácido guluroníco (Funami et al., 2009).
Los mecanismos de gelificación iónica se llevan a cabo fundamentalmente por dos procesos: la gelificación externa y la gelificación interna. El proceso de gelificación externa ocurre con la difusión del ion calcio hacia la solución de alginato de pH neutro. La formación del gel se inicia en la interfaz y avanza hacia el interior a medida que la superficie se encuentra saturada de iones calcio, de manera que el ion sodio proveniente de la sal de alginato es desplazado por el catión divalente solubilizado en agua. Éste interacciona con los bloques G de diferentes moléculas poliméricas, enlazándolas entre sí. Aunque la fuente de calcio más usada ha sido el CaCl2, debido a su mayor porcentaje de calcio disponible, existen otras sales empleadas con menor frecuencia tales como el acetatomonohidratadodecalcio yellactatode calcio(Helgerud et al., 2010).
El proceso de gelificación interna consiste enlaliberacióncontroladadelióncalciodesde una fuente interna de sal de calcio insoluble o parcialmentesolubledispersaenlasoluciónde alginato de sodio. La liberación del ion calcio puede ocurrir si se tiene una sal de calcio insolubleapH neutro pero solubleapH ácido, por lo que es necesario adicionar un ácido orgánico que al difundirse hasta la sal permita la acidificación del medio consiguiendo solubilizar los iones calcio. En este caso, las sales de calcio más empleadas son el carbonato decalcio yelfosfatotricálcico, yen casos específicos el fosfato dicálcico y el citrato tricálcico. Para la acidificación del medio se emplean ácidos orgánicos como el acético, adípico y la glucono delta-lactona. Si la sal de calcio es parcialmente soluble, el proceso de gelificación interna consiste en la adición a la mezcla alginato-sal de calcio, de un agente secuestrante como fosfato, sulfato o citrato de sodio (Lupo et al., 2012). Al
adicionar un secuestrante éste se enlaza con el calcio libre retardando así el proceso de gelificación. El sulfato de sodio ha sido comúnmente el más empleado debido a su bajo costo y conveniente solubilidad (Helgerud et al., 2010).
La principal diferencia entre los mecanismos de gelificación externa e interna eslacinéticadelproceso.Siloquesepretende eselcontroldelatransiciónsolución-gel,enel proceso de gelificación externa los factores a manipular son la concentración de calcio y la composición del polímero. Mientras que para el proceso de gelificación interna se deben considerar la solubilidad y concentración de la sal de calcio y la concentración del agente secuestrante y del ácido orgánico empleados (Draget et al., 2002).
Las películas de alginato pueden ser de dos tipos con diferentes propiedades: películas solubles en aguautilizando alginato desodio y películas solubles en aceite utilizando alginato de calcio. Las películas solubles en agua se pueden formar por evaporación de una solución de alginato o por extrusión de una solución de alginato en un no-disolvente que semezclaconagua,tal comoacetonao etanol. Estas películas son impermeables a la grasa y ceras, pero permiten que el vapordeaguapase atravésdeellas;sonquebradizascuando están secas, pero pueden ser plastificadas con glicerol, sorbitol o urea. Cuando se necesita una película con alto contenido en sólidos, se debe utilizar un alginato de muy baja viscosidad y cuando se necesita una película con mayor resistencia se requiere el uso de alginatos de viscosidad más alta con un mayor grado depolimerización. Paraformarpelículas más suaves y flexibles se utiliza alginato y trietanolamina (McHugh, 1987). De la misma manera, la formación de películas insolubles en agua se puede lograr mediante el tratamiento de una película soluble en agua con un catión di-o trivalente y ácido. También se pueden elaborar por extrusión de una
solución de un alginato soluble en un baño de una sal de calcio. Estas películas de alginato insolubles no son repelentes al agua y se hinchan con la exposición prolongada al agua (McHugh1987).
4. Aplicaciones en alimentos
El alginato tiene varios usos en de la industria alimentaria gracias a las propiedades antes mencionadas. Los alginatos como agentes estabilizadores se utilizan en la fabricación de helados, ya que reducen la formación de cristales de hielo durante la congelación, dando como resultado un producto suave con velocidad de fusión lenta. Esto es especialmente importante cuando el helado se ablanda entre el supermercado yel congelador doméstico; sin alginato o estabilización análoga, se desarrollan cristales de hielo grandes, que producen una sensación indeseableenlaboca.
La capacidad espesante de los alginatos es útil en salsas, jarabes, coberturas para helados, y rellenos de pasteles. Los alginatos son usados como emulgentes en mezclas aguaaceite en la elaboración de mayonesa y aderezosparaensaladas,yaquelasemulsiones formadassonmenospropensasasepararse.
Lasmezclasdesalesdecalcio yalginatode sodio ayudan a la formación del gel; se utilizan en diferentes proporciones deacuerdo alasnecesidadesdefuerzadegeldeseadas.Al utilizar un gel retardador se reduce la interacción alginato-calcio; esto sirve para retrasar la formación de gel durante varios minutos, yes útil cuando es necesario añadir y mezclar otros ingredientes antes de que el gel comience a fijarse. Estos geles retardadores se utilizan para la producción de jaleas o postres instantáneos(FAO,2001).
Los geles de alginato se utilizan en productos alimenticios reestructurados o reformados. Por ejemplo, reestructurados de
carnes como nuggets depollo, asados, pasteles de carne, reestructurados de filetes de pescado apartir depescado picado yun gel dealginato de calcio, aros de cebolla elaborados a partir decebollasecaenpolvo,pimientosrellenosde aceitunas elaborados a partir de pasta de pimiento o rellenos de pastas con sabor, como ajo, hierbas, pimienta, limón y queso (FAO, 2001). El agente aglutinante puede ser un polvo de alginato de sodio, más la adición de carbonato de calcio, ácido láctico o lactato de calcio. Cuando se mezclan alginatos con carne cruda se pueden formar geles de alginato de calcio para promover que las piezas de carne seunan.
Las películas y recubrimientos a base de alginato se han usado para ayudar a conservar diferentesproductosmínimamenteprocesados. Un ejemplo son los productos a base de pescado, los cuales contienen aceites con tendencia rápida a la oxidación, incluso cuando son congelados. Si el pescado se congela con un recubrimiento de alginato de calcio, estará protegido del aire y por lo tanto delarancidezporoxidación.
Se han desarrollado alginatos modificados químicamente tales como el alginato de propilenglicol empleado en la fabricación de cervezas y aderezos para ensaladas por su alta solubilidad a bajos niveles de pH. En productos de alta acidez, el alginato de sodio no es útil, pero se puede utilizar el alginato de propilenglicol(PGA),yaqueesmásestableen condiciones ácidas. El PGA se utiliza en la estabilización de proteínas de la leche en condiciones ácidas, como se ha reportado en algunos yogures. En algunas bebidas de fruta que contienen pulpa de fruta añadida que se desea mantener en suspensión, se puede evitar la sedimentación de la pulpa al adicionar alginatos.Enlalechesaborchocolate,elcacao puede ser mantenido en suspensión por una mezcla de alginato/fosfato. En la nata batida, pequeñas cantidades de alginato pueden espesar y estabilizar este producto. Los
bebedores de cerveza prefieren algo de espuma en la parte superior de un vaso recién vertido, y una espuma pobre conduce a un juicio subjetivo que califica a la cerveza como de mala calidad. La adición de una concentración muy baja de alginato de propilenglicol proporcionará una espuma estable con mayor duración (FAO, 2001). También se han desarrollado otros derivados de la sal cuaternaria de amonio del ácido algínico y los obtenidos de reacciones con acrilato caracterizados por la obtención de geles fuertes y altamente deformables (Draget 2000).
En diferencia de la mayoría de los polisacáridos, el alginato forma geles prácticamente independientes de la temperatura, aspecto que lo ha hecho atractivo en la elaboración de cremas, quesos, salsas, y aderezos. Sin embargo, la exposición prolongada a tratamientos térmicos y variaciones extremas de pH, degradan al
polímero(Draget et al., 2002).
Estas ventajas del alginato y las recientes tendencias tecnológicas se han fusionado en la técnica de microencapsulación, resultando en un producto final que permite proteger a los compuestos encapsulados de factores adversos como el calor y la humedad, mejorando así su estabilidad y biodisponibilidad. Se han descrito diferentes aplicaciones de la microencapsulación empleando como principio activo: vitaminas, minerales, ácidos grasos, microorganismos probióticos, proteínas, aminoácidos, polifenoles, fibras y enzimas (Nieves et al., 2010). La microencapsulación ha permitido inmovilizar bacterias probióticas en una matriz de alginato con la finalidad de proteger y mejorar la biodisponibilidad de los microorganismos, tanto en los productos alimentarios como en el tracto intestinal (Krasaekoop et al., 2004). En la Tabla I se muestran algunos ejemplos de bacterias probióticas encapsuladas en alginato.
Tabla I. Aplicacionesdealginatoparamicroencapsulacióndeprobióticosagregadosaalimentos.
Bacterias
Lactobacillus acidophilus
Bifidobacterium lactis
Lactobacillus acidophilus
Bifidobacterium bifidum
MatrizAplicaciónenalimentos
AlginatoLeche,quesofeta
AlginatoQuesokasaryblanco
Lactobacillus plantarum AlginatoYogur
Lactobacillus acidophilus
Bifidobacterium lactis
Lactobacillus casei
Bifidobacterium lactis
Lactobacillus acidophilus
Bifidobacterium
Lactobacillus acidophilus
Alginato/pectina/quitosanoLechefermentada
AlginatoHelados
AlginatoPostrescongelados
Lactobacillus acidophilus Alginato/almidónYogur
Adaptada de Lupo et al., 2012.
Otras investigaciones reportan la encapsulación de bacterias ácido lácticas (probióticos y cultivos iniciadores) en perlas de alginato, lo que facilita la propagación de cepas que son sensibles al oxígeno (Champagne, 2006), y de extractos naturales con alto contenido en polifenoles provenientes de plantas medicinales, hierbas, flores y semillas (Nieves et al., 2010). Por ejemplo, un aceiteesencial muyutilizado en laindustriade bebidas refrescantes es el limoneno, el cual es muy sensible a altas temperaturas y al ser encapsulado en un sistema alginato-alcohol polivinílico mantiene tanto su sabor como su olor intactos (Nieves et al., 2010). La versatilidaddelencapsuladoinclusohallegado a ser aplicada en la alta cocina con el término “esferificación”, técnica culinaria cuyo propósito es modificar las propiedades texturalesdelos alimentos,paraasídesarrollar nuevas sensaciones en el comensal (Corell et al., 2007).
Conclusiones y comentarios finales
El alginato, al ser un material polimérico biocompatible, no tóxico y degradable, resulta adecuado para muchas aplicaciones en la industriadealimentos.
Diversas investigaciones demuestran que al ser un material natural disponible con múltiples ventajas y de fácil obtención, su aplicación para elaborar diferentes productos alimenticios es amplia y variada. La ventaja principal es que puede mantener sus propiedades funcionales durante el procesamiento y almacenamiento sin alterar el producto. Por esto, se encuentra como ingrediente en una amplia variedad de productos y sigue siendo evaluado en el desarrollodenuevosalimentos.
Agradecimientos
La autora G.C. Avendaño-Romero agradece al Consejo Nacional de Ciencia y Tecnología (CONACYT) y a la Universidad de las AméricasPuebla(UDLAP),porelapoyo en el financiamientodesusestudiosdeposgrado.
Referencias
Arvizu, H. D. L., Hernández C., Rodríguez-Montesinos E. 2002. Parámetros que afectan la conversión del ácido algínico en alginato de sodio. Ciencias Marinas. 28(1): 27–36
Corell, P., García-Segovia, P., Sapiña, F., Farré, I., Castells, P. y Martínez-Monzó, J. 2007. Efecto del ión calcio sobre las propiedades texturales de esferas de alginato aplicadas a cocina. Alimentaria. 388:7983.
Champagne, C. P. 2006. Starter cultures biotechnology: the production of concentrated lactic cultures in alginate beads and their applications in the nutraceutical and food industries. Chemistry Industry Chemical Engineerig. 12:11–17.
Draget, K.I., Smidsrød, O. y Skj˚ak-Bræk, G. 2002 Alginates from algae. En: Steinb¨uchel, A., De Daets, S., Vandame, E.J. y Springer, J. Appl Phycol 2007. 19:43–53 (eds) Biopolymers. vol 6: Polysacharides II. Wiley-VCH, Weinheim, Alemania, pp 215–240
Draget, K., I. 2000. Alginates. In Handbook of Hydrocolloids. Cambridge, Inglaterra: Woodhead Publishing Limited - Boca Raton, FL, EE.UU. CRC Press LLC. pp. 379-395.
FAO, 2001. Food and Agriculture Organization. Mercado de consumo de alginatos. www.fao.org/docrep/field/003/AB483S/AB483S04. htm. Adquirida el 01/02/2012
FAO/WHO. 2001. Food and Agriculture Organization of the United Nations-World Health Organization. Health and nutritional properties of alginate in food. http://www.fao.org/docrep/006/y4765e/y4765e08.ht m. Adquirida el 21/02/2013.
Funami, T., Fang, Y., Noda, S., Ishihara, S., Nakauma, M., Draget K., Nishinari, K. y Phillips, G. 2009. Rheological properties of sodium alginate in an aqueous system during gelation in relation to supermolecular structures and Ca2+ binding. Food Hydrocolloids. 23(7):1746-1756.
Hernández E. M., López G. Y. R. y García P. A. 2005
Evaluación de derivados carboximetilados del alginato de sodio como superabsorbente. Revista Cubana de Química. Vol. XVII. 3: 239-240.
Helgerud, T., Olav, G., Therese, F., Peder, O. A. y Larsen, C. K. 2010. Alginates. En: Food stabilizers. Thickeners and gelling agents. Reino unido: Wiley Blackwell, p. 50-72
Imeson, A. 2010. Alginates. Food stabilizers, thickeners and gelling agents. Reino Unido: Wiley Blackwell. 356 ps. 1th ed.
Krasaekoopt, W., Bhandari, B. y Deeth, H. 2004. The influence of coating materials on some properties of alginate beads and survivability of microencapsulated probiotic bacteria. International Dairy Journal. 14(8):737-743.
Lupo P. B., González A.C. y Maestro G. A. 2012. Microencapsulación con alginato en alimentos. Técnicas y aplicaciones. Revista Venezolana de Ciencia y Tecnología de Alimentos. 3 (1): 130-151.
Mancini, M., Moresi, M. y Rancini, R. 1999. Mechanical properties of alginate gels: empirical characterisation. Journal of Food Engineering. 39(4):369-378.
McDowell, R. H. 1977. Properties of alginates. London, Alginate Industries Ltd., 67 p.
McHugh D. J. 1987. "Production, Properties and Uses of Alginates". Department of Chemistry, University College. University of New South Wales. Australian Defence Force Academy. Campbell, ACT 2600, Australia.
McNeely, W.H. y Pettitt, D.J. 1973. Algin. En Industrial gums, edited by R.L. Whistler. Nueva York, Academic Press, pp.49-31. 2nd ed.
Medina, L. H. y Ledo P. R. M. 2010. Alginatos. Propiedades y Uso en la Reducción de Reflujo Gastroesofágico. Informe Médico. 12 (l0): 519-523
Nieves, N., Rodríguez K., Cid M., Lezcano, Y., Rodríguez, R. y Daquinta M., 2010. Encapsulación de ápices de eucalipto (Eucaliptus urograndis) en perlas de alginato. Influencia del AIBY el MH-5. Centro Agrícola, 37(4): 15-19.
Parra-Huertas, R. A., 2010. Revisión: microencapsulación de alimentos. Revista Facultad Nacional de Agronomía, Medellín. 63(2):5669-5684.
Reddy-K, R. y Reddy-P., S. 2010. Effect of different copolymers on sodium alginate microcapsules containing isoniazid. International Journal of PharmTech Research. 2(4):2198-2203.
Srinivasa, P. C. y Tharanathan, R. N. 2007. Chitin/Chitosan-Safe, ecofriendly packaging materials with multiple potential uses. Food Reviews International. 23: 53-72.
Yabur., Bashan Y. y Hernández-Carmona G. 2007 Alginate fromthe macroalgae Sargassum Sinicola as a Novel Source for Microbial Immobilization Material in Wastewater Treatment and Plant Growth Promotion. Fournal of Applied Phycology, 19(1):4353.

Temas Selectos de Ingeniería de Alimentos 7 - 1 (2013): 97 - 103

Extracción, composición y caracterización de los aceites esenciales de hoja y semilla de cilantro (Coriandrum sativum)
E. Leal – Torres*, A. López-Malo - Vigil, y M. E. Sosa - Morales
Departamento de Ingeniería Química, Alimentos y Ambiental, Universidad de las Américas Puebla. Ex hacienda Sta. Catarina Mártir S/N, San Andrés Cholula, Puebla. C.P.72810, México.
Resumen
El aceite esencial de cilantro se ha reportado como una fuente importante de antioxidantes y antimicrobianos naturales. En esta investigación se realizó la extracción de aceites esenciales de diferentes partes de la planta de cilantro (Coriandrum sativum), tales como semilla fresca, semilla almacenada y hoja seca de cilantro. Los aceites esenciales fueron obtenidos mediante extracción por arrastre de vapor, con rendimientos entre 0.01 y 0.25%. Se determinó la composición química de los diferentes aceites por medio de cromatografía de gases, observando que el principal componente del aceite reportado (linalol) sólo se encontró en el aceite de hoja en una proporción de 16.3%. Para la caracterización, se determinó la densidad de cada aceite (870-885 kg/m3) así como su índice de refracción (1.462 a 1.472). En conclusión, se observó que la frescura de las semillas, así como la parte de la planta afectan el rendimiento del aceite esencial, así como su composición y algunas características físicas.
Palabras clave: cilantro, Coriandrum sativum, aceite esencial, composición química, densidad, índice de refracción.
Abstract
Coriander essential oil has been reported as an important source of natural antioxidants and antimicrobials. In this study essential oil from different parts of the coriander plant (Coriandrum sativum), such as fresh seed, stored seed and coriander dry leaves was extracted. Essential oils were obtained by steam distillation, with yields between 0.01 and 0.25%. The chemical composition of the different oils was determined by gas chromatography, realizing that the main reported essential oil component (linalol), was found only in the oil from coriander leaves (16.3%). Within essential oil characterization, the density was determined for each oil (870-885 kg/m3) as well as the refractive index (1.462-1.472). In conclusion, the degree of ripeness in coriander seeds, and the part of the plant affected essential oil yield, as well as the composition and characteristics of the oils extracted.
Keywords: coriander, Coriandrum sativum, essential oil, chemical composition, density, refractive index.
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: eunice.lealts@udlap.mx
Introducción
El cilantro (Coriandrum sativum) es una planta herbácea anual, proveniente de la familia de las Apiaceae (Mahendra y Bisht, 2011), originaria de Europa y de otros países de la región mediterránea, es cultivada en Marruecos, Francia, Rumania, España, Italia, Rusia, India y México, entre otros países. De esta planta se utiliza la semilla (coriandro) y las hojas (cilantro) (Parry, 1969; Tainter y Grenis, 1993). Las frutas (comúnmente llamadas semillas) son usadas para dar sabor a alimentos, bebidas, en perfumería y en la industria del tabaco. Diversos estudios han encontrado que las hojas y las semillas del cilantro contienen antioxidantes, así como han demostrado que tienen un efecto antimicrobiano (Kanimozhi y Bai, 2012). También se le han encontrado diversas capacidades farmacológicas; en la medicina tradicional se ha usado para aliviar algunos problemas gastrointestinales, reumatismo y dolores articulares (Zeković et al., 2011). El contenido de aceite esencial de las frutas maduras y secas de cilantro varía entre 0.03 y 2.6% (Momin et al., 2012), mientras que en la hoja, Parthasarathy y Zachariah (2008) han reportadouncontenidodeaceiteesencialentre 0.04 y 0.12%; otra característica importante es que estos aceites presentan un color amarillo pálido, así como un olor característico a cilantro. Para la obtención de estos aceites esenciales se pueden utilizar diferentes métodos de extracción, tales como extracción supercrítica o subcrítica (Eikani et al., 2007) y la destilación por arrastre de vapor, siendo la última la más usada en la industria; la ventaja delaextracción porarrastredevapores queel solvente usado es agua, que no afecta al aceite obtenido, sin riesgo en caso de que éste se encuentre en contacto con alimentos o productos medicinales, al contrario de otro tipo de solventes, los cuales no son de grado alimenticio, como es el caso del método de extracción Soxhlet, que utiliza hexano para
separar los aceites (Eikani et al., 2007). Otra de las ventajas de la extracción por arrastre de vaporesquenosetienenquerealizarprocesos posteriores de purificación. El análisis de los componentes del aceite se puede realizar mediante cromatografía de gases (Zeković et al., 2011). Seha reportado quelacomposición de los aceites esenciales se puede ver afectada por diversos factores, como la estructura genética, los factores climáticos ylas prácticas agrícolas(Telci et al.,2006).
Debido a lo antes mencionado y a la exigencia de los consumidores por productos con menor cantidad de aditivos sintéticos, el objetivo de este estudio es evaluar el rendimiento de aceite de cilantro -por el métododeextracciónporarrastredevapor-así como la caracterización de los aceites esenciales de hoja seca, semilla fresca y semilla almacenada de cilantro (Coriandrum sativum), al igual que la composición de cada uno de éstos, con el fin de considerar sus posibles aplicaciones dentro de la industria alimenticia.
Materiales y métodos
1. Materia prima
Las semillas y las hojas secas de cilantro se adquirieron de la empresa Condimentos Naturales Tres Villas S.A de C.V, ubicada en elestadodePuebla.
Se utilizaron dos tipos de semillas, Semilla 1 (semilla almacenada por más de 6 meses) y Semilla 2 (semilla fresca, recién obtenida) al igual que hoja de cilantro seca y ligeramente quebrada. Se adquirieron lotes de aproximadamente 6 kg, tanto de semilla 1 y 2 comodehojasdecilantroydeunsegundolote de 5 kg solo de semilla 1 de cilantro. Las semillas fueron ligeramente troceadas
utilizando mortero y pistilo, para abrir la estructurayfavorecerlaextracción.
2. Extracción con destilación por arrastre de vapor
Para obtener los aceites esenciales, las diferentesmateriasprimasfueronsometidasde manera individual a una extracción por arrastre de vapor, por medio de un equipo que consta de los siguientes accesorios: parrilla, dosfrascosdevidrioPyrexde2L,frascode½ L para la recepción del destilado, cabeza del destilador, condensador adaptado al refrigerante, auto-separador con válvula, abrazaderas, mangueras de agua y telas de asbesto para aislamiento. Para realizar la extracción se agregaron 1.5 L de agua destiladaen el matraz de2 Lquevaen labase del sistemaarmado, así como 600 g desemilla (1 ó 2) troceada o en su caso 200 g de hojas secas. La extraccióndecadaunodelos aceites sellevóacaboduranteaproximadamente6hy la temperatura del condensador se mantuvo entre0y4°C.
3. Determinación de composición química por cromatografía degases
Los aceites recuperados tanto delas semillas 1 y 2, así como de la hoja, fueron sometidos al análisis por cromatografía de gases acoplado a espectrometría de masas para determinar la composición de cada uno de los aceites esenciales. Se realizó el análisis mediante el equipo Varian Star 2400cX equipado con la columna Supelcowax 28046-U (30 m de largo x0.25mmdiámetrointernox0.25 µmespesor de la película). El gas acarreador fue helio con un flujo de 3.8 mL/min y la temperatura del inyector fue de 200 °C. La columna se manejó a75 °C ysemantuvo la temperaturadurante4 minutos.Posteriormenteseincrementóarazón de 8 °C/min hasta alcanzar 200 °C y se mantuvo a esta temperatura durante 6 min. El espectrómetro de masas usado fue un equipo
Varian Saturn 2000, con la trampa a una temperatura de 170 °C. Se inyectaron 3 μL de cada muestra y se dejó correr la cromatografía por 41 min para obtener el espectrograma de cadaaceiteesencial, adaptado deJardim et al. (2008)
4. Caracterización delos aceites
Se determinó la densidad y el índice de refracción (NMX-F-075-SCFI-2006) de cada uno de los aceites esenciales. Para la densidad se utilizó la ecuación 1, así como un matraz aforado de 5 mL, las determinaciones se realizaronportriplicado.
= (Ec.1)
Para el caso del índice de refracción se utilizó el refractómetro manual ATAGO a 25 °C. Inicialmente, el refractómetro se calibró con agua destilada y se colocó una gota de muestra sobre el prisma, esta determinación serealizóportriplicado.
Resultados y Discusión
1. Rendimiento delos aceites extraídos
En la hoja de cilantro el rendimiento fue bajo, se obtuvo aproximadamente 0.01%. Posteriormente, se extrajo aceite de las semillas 2 en donde se encontró que el rendimiento fue mayor a 0.25%, mientras que para la semilla 1 se obtuvo un rendimiento bajo 0.03%. Burdock y Carabin (2009) reportaron cantidades de aceite esencial entre 0.30 y 1.10% para la semilla de cilantro, mientras que para la hoja se ha reportado un contenido de 0.10% (Bhuiyan et al., 2009). El rendimiento de aceite en este trabajo no coincide con lo reportado; esto puede deberse a la variedad de cilantro analizada, el lugar de cosecha, así como el tiempo de
almacenamiento de las muestras antes de ser extraídoelaceiteesencialparasuanálisis.
2. Composición de los aceites esenciales de cilantro
Seobtuvieron los espectrogramas del aceitede hoja (Fig. 1), aceites de semilla almacenada y fresca (Figs. 2 y 3), en donde se puede observar la presencia de d-linalol solo para la muestra de hoja de cilantro en una proporción del 16.33% según el análisis e interpretación de los espectrogramas (Tabla I), α-pineno en la semilla 2 con un 8.97%, β-pineno tanto en lasemilla1comoenlasemilla2conun2.06y 10.23%, respectivamente; geraniol en la semilla2conun26.34%,borneolenlasemilla 2 con un 7.47% y decil-aldehídos con diferentes pesos moleculares y por lo tanto diferentes tiempos de retención para el aceite esencial de la hoja, representando proporcionesde13.45,10.14y15.91%,(Tabla I). En los espectros se muestran algunas diferencias de composición en especial al compararelaceiteesencialdelahojaconelde las semillas, mientras que al comparar los espectros de la semilla 1 y la semilla 2 se observan compuestos similares (Tabla I) los cuales aparecen casi al mismo tiempo de retención. En las figuras 2 y 3, se muestra el tiempo de retención de cada uno de los compuestos, el cual está relacionado con el peso molecular y se encuentra en el rango de
1.5 a 20 min para los compuestos identificados.
Según lo reportado por Msaada et al. (2007), la cantidad y tipo de componentes dependerá de la maduración del fruto (semilla); durante su investigación con aceite esencial de semilla de cilantro identificaron 41 componentes durante todas las etapas de madurez, los resultados demostraron que los componentes variaban según el grado de madurez tanto de forma cuantitativa como cualitativa. El componente mayoritario fue linalol con diferentes porcentajes 36%, 40.68%, 45.27%, 72.35%, según el grado de madurez, desde la fase inicial hasta la completa maduración del fruto, respectivamente. Según la composición reportada por Burdock y Carabin (2009), el constituyente predominante del aceite esencial de semilla de cilantro es linalol (Kiralan et al., 2009; Eikani et al., 2007), pero también se observa que algunas variedades (Microcarpum vulgare) presentan un contenido de linalol inferior a lo reportado por los autores antes mencionados (37.65%) (Bhuiyan et al., 2009) lo cual depende también de la zona en la cual se cultivó el cilantro. Para la hoja madura de cilantro se han reportado (Burt, 2007) valores de26%delinalol.
Como se aprecia en la Tabla I, la presencia de d-linalol es mucho menor en la muestra de aceite esencial de la hoja, mientras que en el.
Tabla I. Comparaciónde compuestos identificados segúnelaceite esencialanalizado. Semilla 1Semilla Hoja2
decilaldehído*13.45% β-pineno2.06% α-pineno8.97% d-linalol16.33%canfeno5.34% β-pineno10.23% decilaldehído*10.14%careno30.03%borneol7.47% decilaldehído*41.33%d-limoneno2.23%alcanfor21.88% 1-hexadeceno15.91%benzaldehído51.45%decanol*12.31% timol2.56%alcanfor5.98%geraniol26.34% alcanfor0.27%linalipropana1.01%decanol*12.79% tujone1.91%
* Compuestos con tiempos de retención y cantidades en la columna diferentes
Leal - Torres et al. / Temas Selectos de Ingeniería de Alimentos 7 – 1 (2013): 97 - 103

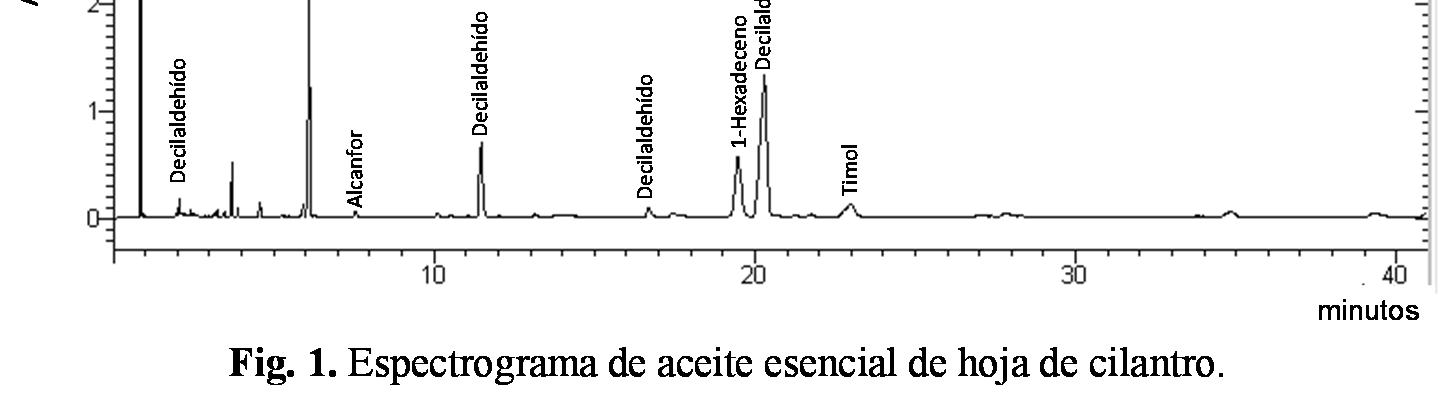

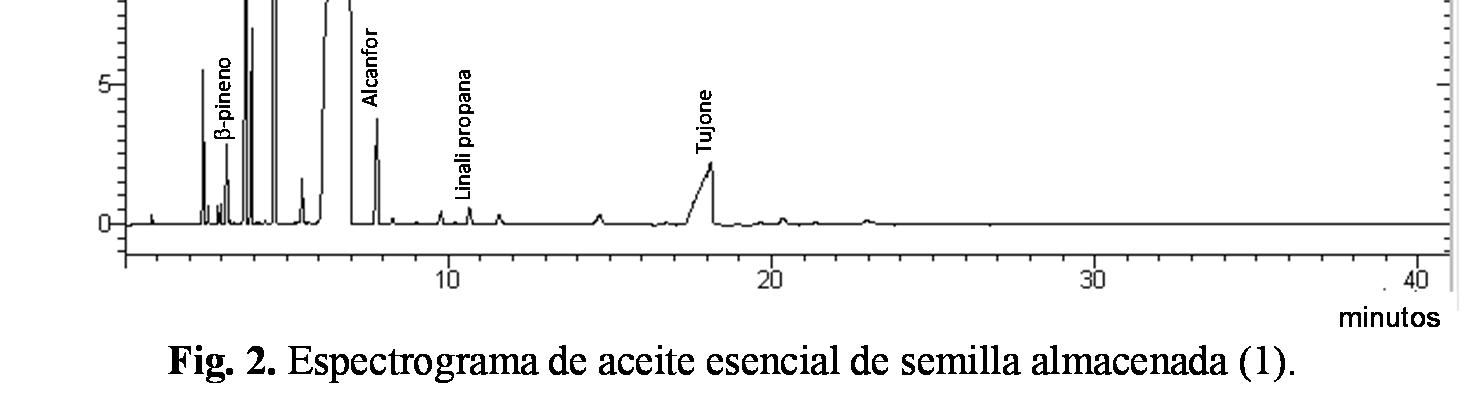


E.
caso de las semillas fue imperceptible por el cromatógrafo, esto en comparación a lo reportado por otros autores, puede deberse como se ha mencionado en diversas investigaciones a la variedad del cilantro y al lugar en donde se cultivó, estas condiciones pueden afectar considerablemente las características de los aceites esenciales obtenidos.
3. Densidad
La densidad a 25 °C de los aceites de hoja y semilla (1 y 2) de cilantro se muestran en la Tabla II. Como se puede observar, los aceites son menos densos que el agua. Esta diferencia dedensidades yladiferenciadepolaridades es lo que permitió la separación del aceite esencial del agua después de la hidrodestilación. Respecto a los valores, éstos se encuentran dentro del rango reportado en la literatura de 870 a 885 kg/m3 por el Food Chemical Codex (1996) y lo obtenido por Burdock yCarabin (2009), 863 y875 kg/m3, a diferencia de lo valores experimentales reportados por Anwar et al. (2011) de 831 kg/m3, para semillas de cilantro cultivadas en Pakistán.
Densidad (kg/m3)
Hoja*
Semilla 1*
Semilla 2
887
875
869 + 0.001
* No se realizaron triplicados, debido al bajo rendimiento
4. Índicederefracción
El índice de refracción obtenido para los aceites esenciales (Tabla III) se encuentra dentro del rango establecido por el Food Chemical Codex, (1996), que es entre 1.462 y 1.472 a una temperatura de 20 °C. Se obtuvieron promedios que se encuentran entre 1.459 y 1.464 según el tipo de muestra (Tabla III), lo cual es comparable con lo reportado
porBhuiyan et al.(2009),endondelosvalores de índice de refracción para la hoja y semilla de cilantro se ubicaron entre 1.428 y 1.459 a 32 °C; aun cuando las temperaturas varían los resultados obtenidos no difieren considerablemente.
Tabla III. Índice de refracciónde los aceites obtenidos.
Indice de Refracción
Hoja 1.4649+0.0006
Semilla 1 1.4594+0.0001
Semilla 2 1.4622+0.0005
Conclusión y comentarios finales
La siguiente conclusión parte de la investigación realizada sobre la extracción, composición química y caracterización de los aceites esenciales decilantro (semillas 1 y2, y hoja), en donde se pudo evaluar el rendimiento de aceite esencial de cilantro el cualfue bajo,tanto enlassemillascomoen la hoja seca, aunque se observa un mayor contenido en la semilla 2, la variación en el contenido de aceite esencial puede deberse a que la semilla fresca tiene el aceite esencial más disponible mientras que en la hoja y en la semilla 2 puede encontrarse en menor proporción; otras características importantes mencionadas por diversos autores es que el rendimiento varia principalmente debido a la variedad de la semilla u hoja utilizada, así como a su grado de madurez, los métodos de cultivo yel origen dela muestra. Con respecto a la composición de los aceites esenciales obtenidos se observó que fue afectada por el tipo de semilla y hoja utilizada, y se identificaron compuestos importantes tales como linalol, timol, alcanfor, α-pinenos, borneol y d-limoneno entre otros; los cuales son de importancia para la industria alimenticia, farmacéutica y médica. La densidad y el índice de refracción no varían
Tabla II. Densidad de los aceites obtenidos.
considerablemente según la variedad o grado demadurezdelasmuestras.
Agradecimientos
E. Leal Torres agradece al Consejo Nacional de Ciencia y Tecnología (CONACYT) y a la Universidad delas Américas Puebla(UDLAP) por el apoyo para la realización de sus estudiosdelicenciaturayposgrado..
Referencias
Anwar, F., Sulman, M., Hussain, A. I., Saari, N., Iqbal, S. y Rashid, U. 2011. Physicochemical composition of hydro-distilled essential oil from coriander (Coriandrum sativum L.) seeds cultivated in Pakistan. Journal of Medical Plants Research. 5 (15):3527-3544.
Bhuiyan, N. I., Begum, J. y Sultana, M. 2009. Chemical composition of leaf and seed essential oil of Coriandrum sativum L. from Bangladesh. Journal of the Bangladesh Pharmacological Society. 4:150153.
Burdok, G. y Carabin, I. 2009. Safety assessment of coriander (Coriandrum sativum L.) essential oil as a food ingredient. Food and Chemical Toxicology. 47: 22-34.
Burt, S. A. 2007. Antibacterial activity of essential oils: potential applications in food. International Journal of Food Microbiology.94: 223-253.
Eikani, M., Golmohammad F. y Rowshanzamir, S. 2007. Subcritical water extraction of essential oils from coriander seeds (Coriandrum sativum L.). Journal of Food Engeniering.80 (2): 735-740.
FCC. 1996. Food Chemical Codex. 4ta Edición. Washington, DC. National Academic Press. pp. 482483.
Jardim, C. M., Jham, G. N., Dhingra, O. D. yFreire, M. M. 2008. Composition and antifungal activity of the essential oil of the Brazilian Chenopodium ambrosioides L. Journal Chemical Ecology. 34: 1213-1218.
Kanimozhi, D. y Bai, V. R. 2012. Analysis of bioactive components of ethanolic extract of Coriandrum sativum L. International Journal of Research in Pharmacy and Science. 2 (3):97-110.
Kiralan, M., Calikoglu, E., Ipek, A., Bayrak, A. y Gurbuz, B. 2009. Fatty acid and volatile oil composition of different coriander (Coriandrum sativum) registered varieties cultivated in Turkey. Chemistry of Natural Compounds. 45(1):100-102.
Mahendra, P. y Bisht, S. 2011. Coriandrum sativum: A daily use spice with great medicinal effect. Pharmacognosy Journal.3 (21): 84-88
Momin, A., Acharya, S. y Gajjar, A. 2012. Coriandrum sativum- Review of advances in phytopharmacology. International Journal of Pharmaceutical Sciences and Research. 3(5): 12331239.
Msaada, K., Hosni, K., Taarit, M. B., Ouchikh, O. y Marzouk, B. 2007. Variations in essential oil composition during maturation of coriander (Coriandrum sativum L.) fruits. Journal of Food Biochemistry. 33: 603–612.
Norma Mexicana. NMX-F-075-SCFI-2006. Alimentos –Aceites y Grasas Vegetales o AnimalesDeterminación de la Densidad Relativa- Método de Prueba. http://200.77.231.100/work/normas/nmx/2006/nmxf-075-scfi-2006.pdf. accesada 10/10/2009
Parry, W. J. 1969. Spices, Volume I. The Story of Spices. Chemical Publishing Company, Inc. Nueva York. EE.UU. pp.108-111
Parthasarathy, V. A. y Zachariah, T. J. 2008. Coriander. En: V. Parthasarathy, B. Chempakam y T. J. Zachariah(Eds). Chemistry of Spices. CABI editorial. EE.UU. pp. 190-210.
Tainter, R. D. y Grenis, T. A. 1993. Especias y Aromatizantes Alimentarios. Editorial Acribia, S.A. España. Pp. 76-79
Telci, I., Toncer, O. y Sahbaz, N. 2006. Yield essential oil content and composition of Coriandrum sativum varieties (var. vulgare Alef and var. microcarpum DC.) grown in two different locations. Journal Essential Oil Reserch. 18: 189-193.
Zeković, Z., Adamovic, D., Ćetkovic, G., Radojkovic, M. y Vidović, S. 2011. Essential oil and extract of coriander (Coriandrum sativum L.). Acta Periódica Tecnológica. 42: 281-288.

Contenido
Volumen 7 / No. 1 Enero – Mayo 2013
Cuerpo editorial
Artículos de Revisión

Utilización de películas comestibles yciclodextrinas para la liberación controlada de aceites esenciales como agentes antimicrobianos en vegetales
R.H.Hernández-Figueroa,E.PalouyA.López-Malo
Prebióticos: su importancia en la salud humana y propiedades funcionales en tecnología de alimentos
D.Morales-Koelliker*yJ.F.Vélez-Ruíz
El ajo ysus aplicaciones en la conservación de alimentos
D.Bender-Bojalil*yM.E.Bárcenas-Pozos
Mecanismos de transferencia de calor que ocurren en tratamientos térmicos de alimentos
M.E.Pérez-ReyesyM.E.Sosa-Morales
Microencapsulación de compuestos activos con quitosano
I.A.Flores-Belmont*y M.T.Jiménez-Munguía
Vegetales como fuentes de nitritos: una alternativa para el curado de carnes
E.E.Montiel-Flores*,A.López-MaloyM.E.Bárcenas-Pozos
Efecto de la radiación UV-C en frutas y verduras
J.F.Haro-Maza*y J.A.Guerrero-Beltrán
Potencial antimicrobiano de mezclas que incluyen aceites esenciales o sus componentes en fase vapor
M.A.Olivares-Cruz*yA.López-Malo
Propiedades del alginato yaplicaciones en alimentos
G.C.Avendaño-Romero*,A.López-MaloyE.Palou
Artículo de Investigación
Extracción, composición ycaracterización de los aceites esenciales de hoja ysemilla de cilantro (Coriandrum sativum)
E.Leal-Torres*,A.López-MaloyM.E.Sosa-Morales

Departamento de Ingeniería Química, Alimentos y Ambiental Derechos Reservados 2012
