

Temas Selectos de Ingeniería de Alimentos















Volumen 6 / No. 2
DIRECTORIO
TEMAS SELECTOS DE INGENIERÍA DE ALIMENTOS
UNIVERSIDAD DE LAS AMÉRICAS PUEBLA
PUBLICACIÓN SEMESTRAL
VOLUMEN 6, NÚMERO 2 (AGO - DIC 2012)
EDITORA RESPONSABLE
María Eugenia Bárcenas Pozos
CONSEJO EDITORIAL
Aída Irma Gómez Sánchez
María Teresa Jiménez Munguía
Emma Mani López
María Elena Sosa Morales
Fidel Tomás Vergara Balderas
CERTIFICADO DE RESERVA DE DERECHOS:
04-2010-080615025900-102
CERTIFICADO DE LICITUD DE TÍTULO Y CONTENIDO: 15430
DOMICILIO:

Fundación Universidad de las Américas, Puebla
Ex hacienda Sta. Catarina Mártir S/N
San Andrés Cholula, Puebla.
C.P. 72810, México
Teléfono: 222 229 2126
DISTRIBUIDO POR:
Departamento de Ingeniería Química, Alimentos y Ambiental
Fundación Universidad de las Américas, Puebla
IMPRESIÓN:
Talleres gráficos
Universidad de las Amércias Puebla
Ex hacienda Sta. Catarina Mártir S/N
San Andrés Cholula, Puebla. C.P. 72810, México

Temas Selectos de Ingeniería de Alimentos Vol. 6 / No. 2

Cuerpo
editorial
Dra. María Eugenia Bárcenas Pozos
Dra. María Elena Sosa Morales
Dra. María Teresa Jiménez Munguía
Dra. Emma Mani López
Dra. Aída Gómez Sánchez
M. C. Fidel Vergara Balderas

Contenido
Temas Selectos de Ingeniería de Alimentos Vol. 6 / No. 2

Volumen 6 / No. 2 Ago – Dic 2012
Cuerpo editorial ………………………………………………………………………………….. i Editorial ………………………………………………………………………………………….. iii
Artículos de Revisión
Factores principales que intervienen en la estabilidad de una emulsión doble
C. E. Kosegarten-Conde* y M. T. Jiménez-Munguía ……………………..………………………..….. 1
Modelación del calentamiento dieléctrico (microondas y radiofrecuencia) en sistemas alimenticios modelo
N. Soto-Reyes*, R. Rojas-Laguna, M. E. Sosa-Morales ……………………………………………..… 19
Películas comestibles de proteína: características, propiedades y aplicaciones
C. Montalvo*, A. López-Malo y E. Palou ………………..………………………………………….….. 32 Propiedades funcionales de la jamaica (Hibiscus sabdariffa L.)
S. Cid-Ortega y J. A. Guerrero-Beltrán …………………………………………………………………
Bacteriocinas: antimicrobianos naturales y su aplicación en los alimentos
S. C. Beristain-Bauza, E. Palou y A. López-Malo ………………………………………………………
Radiación ultravioleta en jugos de frutas: fundamentos y aplicaciones
A. S. López-Díaz*, E. Palou y A. López-Malo ………….……………………………………………….
47
64
79 Cambios en frutas tropicales frescas, cortadas y empacadas en atmósfera modificada durante su almacenamiento en refrigeración
M. Rangel-Marrón* y A. López-Malo
Películas comestibles formuladas con polisacáridos: propiedades y aplicaciones
M. F. Domínguez-Courtney* y M. T. Jiménez-Munguía
Mecanismos de inestabilidad y métodos de estabilización de emulsiones múltiples
H. A. Peredo-Luna* y M. T. Jiménez-Munguía
Quesos frescos: propiedades, métodos de determinación y factores que afectan su calidad
C. Ramírez-López* y J. F. Vélez-Ruíz
Equipos para tratamientos de alimentos con radiación UVC
O.T. Antonio-Gutiérrez*, E. Palou y A. López-Malo
Métodos de control de crecimiento microbiano en el pan
A. A. Salgado-Nava* y M. T. Jiménez-Munguía
Polímeros utilizados para la elaboración de películas biodegradables
M. Rubio-Anaya* y J. A. Guerrero-Beltrán
Artículo de Investigación
Efecto del tiempo de uso y el tipo de aceite de freído en las propiedades de nuggets de pescado
E. F. Molina-Hernández* y M. E. Sosa-Morales

Editorial
Temas Selectos de Ingeniería de Alimentos Vol. 6 / No. 2

La escritura científica es una de las actividades más importantes para un investigador ya que no sólo es un medio de divulgación del conocimiento sino que también es un material que concreta, enparteoensutotalidad,unproyectopreviamentedefinido.
En el Departamento de Ingeniería Química, Alimentos y Ambiental (DIQAA), como parte de los compromisos en la formación de estudiantes de posgrado, se propuso la publicación de la Revista de Temas Selectos de Ingeniería de Alimentos con artículos creados por los estudiantes de posgrado, bajo la supervisión de su(s) director(es) de tesis ycon la delicada revisión por parte del Comité Editorial. Con el paso del tiempo, se ha constatado con los estudiantes, el desarrollo delashabilidadesdeescrituraconestaactividad,lacual implicaungranesfuerzoparael análisis de información, clasificación, comprensión, resumen y síntesis, para finalmente dar origen a un artículoderevisiónodeinvestigación.
En este número de la revista participaron tanto alumnos de Maestría como de Doctorado en Ciencia de Alimentos, conformando un contenido de gran diversidad de temas de investigación, los cuales comprenden las siguientes áreas: química de alimentos, microbiología de alimentos, propiedades físicas de alimentos y procesamiento mínimo o con tecnologías emergentes de alimentos.Lostemasabordadosmuestranlasdiferenteslíneasdeinvestigaciónqueseencuentran desarrollandoelgrupodeinvestigadoresdelDIQAA.
Como miembro del Comité Editorial me es muy grato presentarles este ejemplar, muestra de un trabajo conjunto de estudiantes ycolegas, con gran compromiso para su continuo desarrollo y divulgación,elcualesperoseadesuinterésyaquecontienetemasdevanguardiaenelárea.
María Teresa Jiménez Munguía Profesora Departamento de Ingeniería Química, Alimentos y Ambiental Universidad de las Américas Puebla

Temas Selectos de Ingeniería de Alimentos 6 - 2 (2012): 1 - 18

Factores principales que intervienen en la estabilidad de una emulsión doble
C.E. Kosegarten-Conde* y M.T. Jiménez-Munguía
Departamento de Ingeniería Química, Alimentos y Ambiental, Universidad de las Américas Puebla.
Ex hacienda Sta. Catarina Mártir S/N, San Andrés Cholula, Puebla. C.P.72810, México.
Resumen
Una emulsión doble es una emulsión simple dentro de otra emulsión. Su uso con fines comerciales para la industria alimentaria se encuentra limitado debido a que son sistemas termodinámicamente inestables, lo cual hace difícil mantener en el tiempo las características buscadas, así como controlar de manera exacta, la liberación del principio activo que se encuentra encapsulado en la emulsión interna. Muchas son la investigaciones realizadas que han aportado conocimiento para lograr entender la influencia que tiene el pH, el uso de electrolitos, la combinación de distintos emulgentes tanto monoméricos y poliméricos, como del tipo complejos proteína-polisacárido, la viscosidad, el tamaño de gota interna y externa, el balance hidrófilo lipófilo (BHL), la temperatura y las condiciones de preparación de la emulsión, entre otros, en la estabilidad de las emulsiones dobles. En este artículo se revisarán los factores mencionados.
Palabras clave: emulsión doble, emulgente, biopolímeros alimenticios, potencial zeta, encapsulación.
Abstract
A double emulsion is a simple emulsion within another emulsion. Its commercial use for the food industry is limited because they are thermodynamically unstable systems, which make difficult to maintain them, over time. Other challenge is to control the release of the active ingredient encapsulated in the inner emulsion. Many studies have contributed for achieving the comprehension of the influence of pH, the use of electrolytes, the combination of several monomeric and polymeric emulsifiers, such as the proteinpolysaccharide complex, viscosity, internal and external droplet size, the hydrophilic lipophilic balance (HLB), the temperature and the emulsification conditions, among others, in the double emulsions stability. In this review these factors are highlighted.
Keywords: double emulsions, emulsifier, food biopolymers, zeta potential, encapsulation.
Introducción
*Programa de Doctorado en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
La estabilidad ydisponibilidad de un principio activo es de gran interés en muchas áreas del conocimiento, incluyendo la ciencia de alimentos. De ahí que el lograr protegerlo del medio ambiente en que se encuentre, prolongarsuvidaútil ycontrolarsuliberación, son algunos de los retos que se enfrentan para cumplir con lo antes expuesto. Un intento para lograrlo es con la formación de emulsiones dobles, en donde las gotas de la fase dispersa contienen, dentro de ellas, pequeñas gotas
Dirección electrónica: carlos.kosegartence @udlap.mx
inmiscibles y también dispersas, conteniendo el principio activo, disuelto o encapsulado. Los sistemas así formados presentan dos interfases termodinámicamente inestables, cuya integridad depende del tipo de compuestos que forman la fase dispersa, la fase continua y las interfases, así como las proporciones en que se encuentran éstas y los emulgentes utilizados. La técnica y condiciones de elaboración de la emulsión doble jueganademás,unpapelimportante.
El lograr que una emulsión perdure con las características deseadas a través de un determinado tiempo, no es algo sencillo, depende entre otros factores de los emulgentes seleccionados; algunos han mostrado crear interfases más estables, pero con una inadecuada liberación del principio activo de interés o viceversa. En algunas investigaciones, se ha observado un efecto sinérgico en lautilizacióndemacromoléculas naturales en combinación con emulgentes monoméricos tradicionales. Otro factor a considerar,esel control delapresiónosmótica en la fase acuosa, la cual coadyuva de manera significativa en la estabilidad de las emulsiones dobles; es decir, a mantener sus características originales, como viscosidad, tamaño de gota y porcentaje del compuesto deseable encapsulado,al evitarquesepresente coalescencia o ruptura por hinchazón o encogimiento, las cuales son las principales causas por las que se pierde o rompe una emulsióndoble.
Existen dos razones principales para la aplicación de las emulsiones dobles en el área de alimentos, la primera es la de encapsular algún ingrediente sensible tal como un nutriente o compuesto de sabor y después liberarlo de manera controlada durante la digestión o masticación. La segunda es para obtener productos reducidos en grasa, más saludables.
Esta revisión pretende describir las variables más importantes a controlar, para tratar de obtener emulsiones dobles estables, para las posibles aplicaciones en el área de alimentos. Revisión bibliográfica
1. Generalidades
Las emulsiones múltiples o dobles están constituidas por una fase dispersa inmiscible en la fase continua, donde la fase dispersa contiene a su vez gotas que son inmiscibles en ésta. Este tipo de emulsiones, se encuentra dividido en dos grupos importantes; las llamadas emulsiones aceite en agua en aceite (O/W/O, por sus siglas en inglés), y las llamadas, emulsiones agua en aceite en agua (W/O/W, por sus siglas en inglés), en las cuales se enfoca el presente trabajo, y más investigaciónexiste.
El descubrimiento de las emulsiones dobles se atribuye a Seifriz en 1925 y una de las primerasaplicacionesdelasemulsionesdobles se reporta en 1965, por Herbert, encontrando enlaactualidad,aplicacionesimportantesenel área farmacéutica, cosmética, médica, y en el tratamiento de aguas residuales (Weiss y Mushiolik, 2007).
En la Fig. 1 se ilustra una representación de un conjunto de gotas internas acuosas (W1), dispersas en aceite (O), resultantes de una primera emulsión (W1/O) llamada agua en aceite,debidoaqueelporcentajeenpesodela fase acuosa es menor al de la fase de aceite; y éste a su vez (W1/O), disperso en una segunda fase acuosa (W2), formando una emulsión doble W1/O/W2. La gota de aceite presenta dos interfases, una con las gotas acuosas internas y otra con la fase acuosa externa. En
Fig.1. Representación esquemática de una gota en una emulsión W1/O/W2. Adaptado de Garti N. y Aserin A. (1996).
estas interfases están presentes, además, los emulgentes necesarios para la estabilización del sistema, localizados exactamente en la línea de contacto entre la fase acuosa y la fase de aceite (Garti y Aserin, 1996). En las emulsiones W1/O/W2, el compuesto encapsulado, para ejercer su acción, tiene que cruzar de la fase acuosa interna (W1) a la fase acuosa externa (W2) a través de la delgada película de aceite(O), llamada también, sistema de membrana líquida (Kumar et al., 2012;Li et al.,2011).
Un emulgente es una molécula anfifílica o anfipática que tiene una “cabeza” hidrófila, la cual tiene una alta afinidad por el agua, yuna “cola” lipófila, la cual tiene afinidad por el aceite. Los emulgentes se clasifican como lipófilos e hidrófilos, según su mayor afinidad por compuestos no polares o polares respectivamente, conservandoen ambos casos, su capacidad de disolverse en ambos tipos de compuestos(KralovaySjöblom,2009).
Las emulsiones dobles, se preparan básicamente en dos formas: homogeneizando en uno o dos pasos. Existe una gran cantidad de reportes para la preparación de emulsiones tipoW/O/W enunpaso;estoincluyeagitación mecánica fuerte de la fase acuosa que contiene
un emulgente hidrófilo, y una fase de aceite conteniendo grandes cantidades de emulgente lipófilo, para formar una emulsión W/O, pero parte de ésta, tiende a invertirse para dar una emulsión doble W/O/W (Garti y Aserin, 1996).
En la mayoría de los estudios recientes, las emulsiones dobles (W/O/W) se preparan en dos pasos: la primera emulsión (W/O) se prepara con emulgente lipófilo (10-30% p/p), bajo condiciones de agitación severa y la segunda (W/O/W), con el emulgente hidrófilo (0.5-5% p/p) con agitación no severa, para evitar romper las gotas formadas. Este proceso se realiza utilizando generalmente agitadores mecánicos convencionales, homogeneizadores a altas presiones, por ultrasonido u homogeneizadores de membrana (Kumar et al.,2012;McClements et al.,2009).
El reto para el científico en alimentos es desarrollar productos que utilicen no los emulgentes tradicionales de la industria farmacéutica y cosmética, sino aquellos de grado alimenticio estabilizados con biopolímeros naturales y no con emulgentes sintéticos, los cuales tienen restricciones de consumo. De esa manera, la atención se ha enfocado hacia la búsqueda de proteínas y
Fase externa acuosa (W2)
Gota (múltiple) de aceite (O)
Gotas acuosas internas (W1)
Películas de emulgente
polisacáridos que ofrezcan buenas características como emulgentes. Para el caso de alimentos bajos en grasa, se espera reemplazar cierta cantidad de aceite en la emulsión, por agua en el interior de las gotas deaceitesinquesealteresignificativamentela viscosidad total. En casos en los que la fase internano esfácilmenteliberada enla boca,se pueden diseñar emulsiones W/O/W para influenciar percepciones de sabor (ácidos, sales, compuestos amargos, etc.) modificando el grado en que la fase acuosa interactúa con las superficies orales. El problema, es que no es fácil elaborar emulsiones dobles alimentarias, debido a su inestabilidad. En otras aplicaciones, dicho problema se resolvería agregandolacantidaddeemulgente necesario, como los ésteres de sorbitán y copolímerossintéticos,peroparalosproductos alimenticios, existe restricción en ese tema (Garti y Lutz, 2004; Kralova y Sjöblom, 2009).
2. Problemas de inestabilidad
El rompimiento de una emulsión doble puede seguirunaseriede caminosdependiendodesu composición y microestructura. Una
representación esquemática se muestra en la Fig. 2, donde los principales mecanismos de rompimiento son: a) coalescencia de la gota exterior, b) coalescencia de la gota interior, c) coalescencia de la gota exterior e interior y d) hinchamiento o encogimiento de la gota interna, provocando en ambos casos la pérdida delmaterialencapsulado(Kumar et al.,2012).
La fase de aceite en una emulsión W/O/W es referida comúnmente como una especie de membrana líquida, que separa a la dos fases acuosas (interna y externa). Dependiendo del gradiente de presión osmótica entre ambas fases acuosas, existe una fuerza impulsora del aguadepasardeunladoalotroatravésdeesa película de aceite. Cuando la fase interna tiene una presión osmótica menor a la externa, se crea una contracción de las gotas internas, en el caso contrario, se produce una hinchazón de las mismas, con la subsecuente ruptura de la membrana de aceite y la pérdida del ingrediente encapsulado. De ahí que la incorporación de electrolitos en la dosis necesaria para controlar el balance osmótico del sistema,es muyútil paraevitar algunosde estos problemas (Dickinson, 2011).
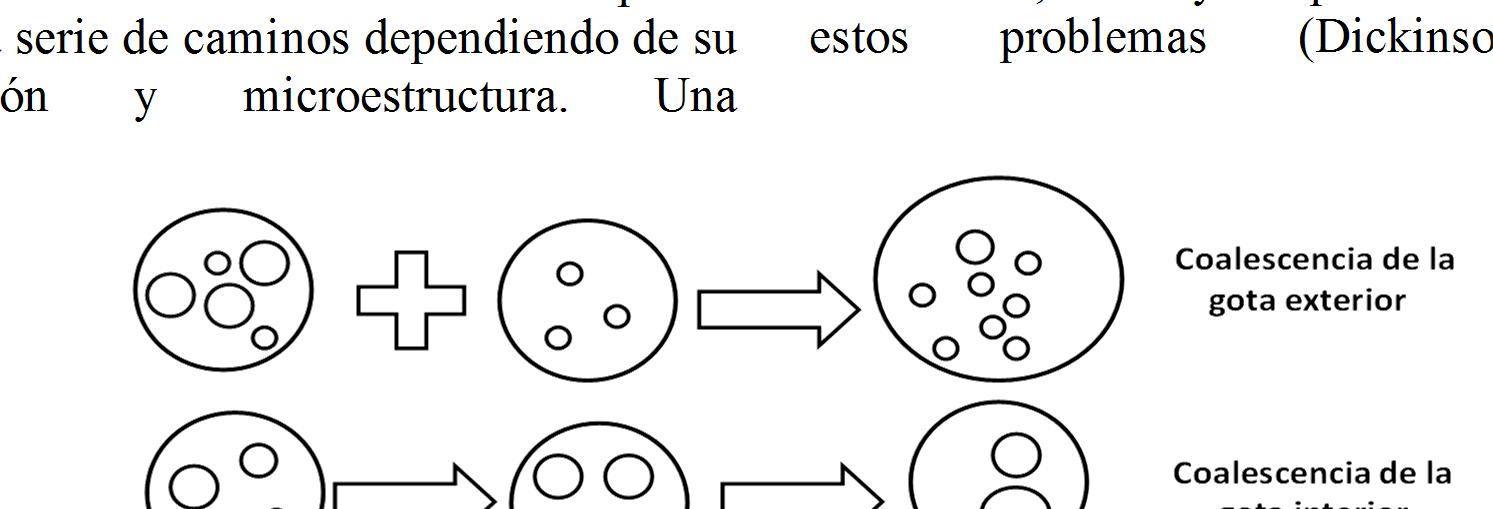
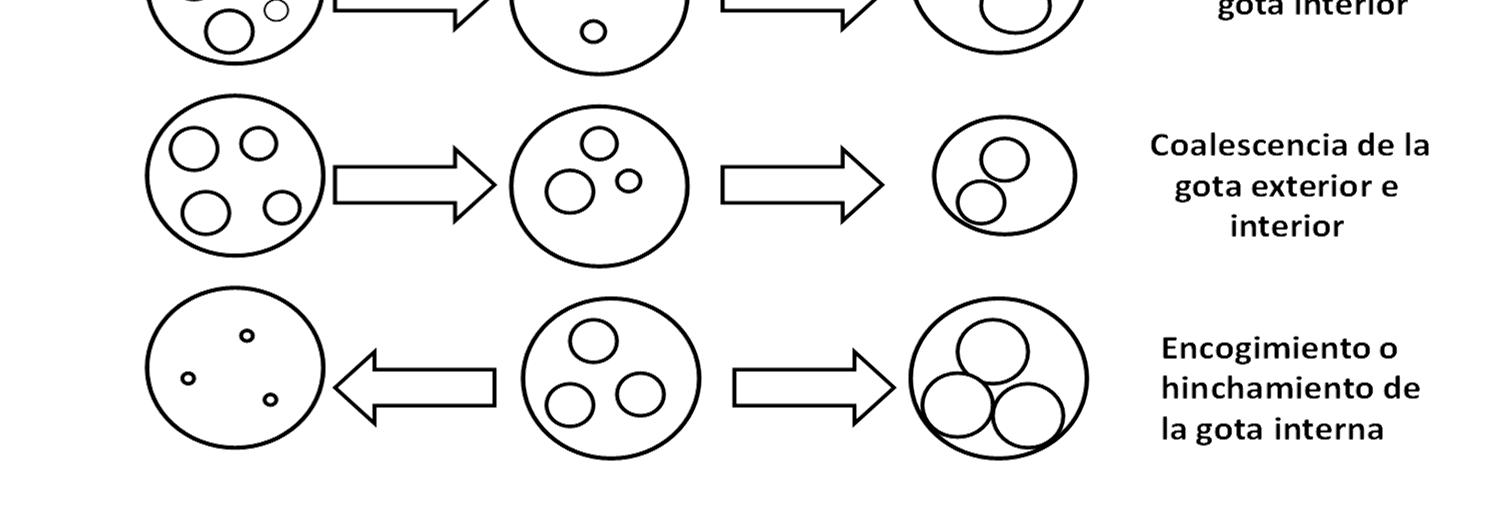
Fig.2. Representación esquemática de los principales mecanismos de rompimiento de una emulsión doble. Adaptado de Dickinson (2011).
Una manera de medir la estabilidad de una emulsión doble es el rendimiento, y se refiere al porcentaje de la fase acuosa de la primera emulsión (W1), que permanece en la fase interna al realizar la segunda emulsión. Durante la preparación de la segunda emulsión, se rompen algunas de las gotas formadas en la primera. Se dice que una emulsión tiene un buen rendimiento inmediatamente después de ser formada, si ésteesdel 95%, ysi esdel 70-80%despuésde algunas semanas de almacenamiento inactivo. En algunos casos se requiere que se libere rápidamente el principio activo, esto se logra diluyendo la emulsión en una solución hipoosmótica, aplicando una agitación moderada o sometiendo a la fase de aceite a un ciclo de congelado y descongelado (Dickinson, 2011; McClements et al.,2009).
3. Factores que afectan la estabilidad de una emulsión doble
3.1. Generalidades
Varios factores afectan la estabilidad de una emulsión W/O/W, los dos principales son: primero, la migración del emulgente lipófilo presente en la emulsión primaria, a la fase acuosa externa y segundo, la adecuada selección de la concentración del emulgente hidrófilo secundario. Una inadecuada elección de concentración del emulgente puede originar una inversión de fases de la emulsión múltiple W/O/W, a una emulsión sencilla O/W. Otro factor que interfiere en la estabilidad de estas emulsiones W/O/W, es la migración de agua entre la fase acuosa interna y la fase acuosa externa, que se ve afectada por las magnitudes de los gradientes de presión osmótica entre ambas fases, las que a su vez se ven influenciadasporlanaturalezayconcentración de los emulgentes de la fase oleosa, yde todos los ingredientes que se encapsulan en la fase acuosainterna,odeaquéllosqueseseparande la fase acuosa externa (Jager-Lezer et al., 1997).
Los compuestos ionizados no son los únicosmaterialesquepuedensertransportados a través de la membrana de aceite en una emulsión W/O/W. Se ha demostrado que moléculas de electrolitos y sustancias no electrolíticas solubles en agua, pueden fácilmente migrar a través de la membrana de aceite sin afectar la estabilidad de la emulsión doble (Kita et al., 1977). Se han sugerido dos posibles mecanismos para la permeación de agua y materiales solubles en agua a través de la fase de aceite; el primero “vía transporte micelarinverso” yel segundo,por“difusión a través de las delgadas láminas formadas por el emulgente”,dondelapelículadeaceiteesmuy delgada (Dickinson, 2011). El transporte micelar se presenta, cuando se excede la cantidad de emulgente lipófilo y se forman micelas, constituidas por el emulgente monomérico, la sección lipófila de la película de aceite y el principio activo hidrófilo localizado en la gota interna, el cual es arrastrado. La difusión, es el mecanismo más común y obedece a los principios de la ley de Fick(Kumar et al., 2012).
3.2. Tipo y concentración del emulgente
Sin duda, el tipo de emulgente o emulgentes seleccionados para la elaboración de una emulsión doble, es uno de los factores más importantes para la estabilidad de estas emulsiones. De ellos dependerá, entre otras cosas, qué tan resistente queda esa película estabilizadora que dará las características deseadas a la emulsión y que separa la fase acuosa interna de la externa. El tipo de morfología resultante depende asimismo, del método de preparación de la emulsión (DickinsonyMcClements,1996).
Las emulsiones W/O/W requieren al menos dos emulgentes, uno lipófilo y uno hidrófilo, que ayuden a formar y estabilizar la emulsión. Los emulgentes pueden ser clasificados de diferentes maneras; se clasifican por su número de regiones hidrófilas en
monofuncionales y multifuncionales. Los emulgentes monofuncionales poseen sólo una región hidrófila; los multifuncionales, en contraste, tienen varios grupos hidrófilos y también,enlamayoríadeloscasos,másdeun grupo lipófilo. Por su carga eléctrica se clasifican en aniónicos, anfotéricos, catiónicos y no iónicos. Pueden ser clasificados en poliméricos y monoméricos; tales clasificaciones no son excluyentes. Por ejemplo, el Grindsted o PGPR (poliglicerol polirricinoleato) puede ser clasificado como polimérico a pesar de ser multifuncional. Los emulgentes utilizados en la industria
alimentaria son principalmente no iónicos (monoacilgliceroles, ésteres de ácidos grasos de sacarosa), aniónicos (sales de ácidos grasos, estearoil-2-lactato de sodio), o anfotéricos (lecitina). En la Fig.3 se presenta una clasificación de emulgentes utilizados en la industria alimentaria. En el mercado existe un gran número de emulgentes pero no todos funcionan adecuadamente en cualquier alimento; de acuerdo con su composición y estado de dispersión, cada sistema requiere de un emulgente específico. Por esta razón, la selección del emulgente adecuado debe ser muy cuidadosa (Kralova y Sjöblom, 2009)
Iónicos
Naturales
No iónicos
Sales biliares
Fosfolípidos
Proteínas
Gomas
Colesterol
Saponinas
Gomas
Emulgentes
Iónicos
Sintéticos
No iónicos
Sales de ácidos grasos
Estearoil–2–lactato de sodio
Ésteres del glicerol
Ésteres del poliglicerol
Ésteres del propilenglicol
Ésteres de la sacarosa
Ésteres de ácidos grasos con sorbitán
Ésteres polioxietilénicos de sorbitán
Fig. 3. Clasificación de emulgentes usados en alimentos. (Adaptada de Badui-Dergal etal. (1999).
En la práctica, el método de las dos etapas de homogeneización es el que se ha empleado para lograr emulsiones de tamaño de gota reproducibles, e involucra el formar una fina emulsión agua en aceite (W/O) usando una alta proporción de emulgente lipófilo, yluego, dispersando la emulsión primaria en agua, utilizando un nivel bajo de un emulgente hidrófilo. Hasta hace pocos años, la mayoría de los estudios relacionados a emulsiones dobles reportaban el uso de emulgentes de bajo peso molecular (Spans, Tweens y Brijs), lo cual permitió establecer una serie de recomendaciones empíricas para la preparación de emulsiones dobles (McClements et al., 2009). El emulgente lipófilo, puede desestabilizar la emulsión doble si migra de la interfase agua-aceite interna a la interfase aceite-agua externa. Además, el emulgente hidrófilo presente durante la segunda etapa de la homogeneización, puede desestabilizar a la emulsión primaria original. Por ello se ha buscado optimizar la mezcla de emulgentes lipófilos e hidrófilos que mejores características otorguen a la emulsión doble (Sela et al., 1995). Otro efecto detrimental, ocurrecuandoseusaunaconcentraciónaltade emulgente hidrófilo (emulgente para la segunda emulsión) en la fase acuosa externa, ya que las gotas externas de la emulsión W/O/W se vuelven tan pequeñas, que durante el proceso de la segunda etapa de homogeneización, las gotas acuosas internas son alteradas o rotas. Por esta razón, se emplean por lo general muy bajas concentraciones de emulgente hidrófilo en la formulación de emulsiones W/O/W (DickinsonyMcClements,1996).
El uso de emulsiones dobles formuladas con emulgentes de bajo peso molecular no ha resultado exitoso en la práctica, ya que estos sistemas por lo general no pueden ser usados en procesos donde ocurren perturbaciones hidrodinámicas, que causan rompimiento de la emulsión interna y de la emulsión doble. Se
ha propuesto la incorporación de un espesante o un polímero gelificante en la fase acuosa internadelaemulsiónprimaria. Laideaesque la presencia de este polisacárido conduzca a una estructura viscoelástica tipo gel en todas las gotas acuosas internas y en la interfase entre la fase acuosa interna y la fase de aceite. La formación de una membrana gelatinosa en lainterfaseagua-aceiteactúacomounabarrera física, para evitar la coalescencia de las gotas internas (Dickinson y McClements, 1996; Kralova y Sjöblom, 2009; McClements et al., 2009).
Las investigaciones en el área de alimentos de este tipo de emulsiones dobles se han encaminado a mejorar su estabilidad usando mezclas binarias de emulgentes de bajo peso molecular en la formulación de la emulsión W1/O, y sustituyendo el emulgente hidrófilo presente en la fase acuosa externa, por materiales biopoliméricos. Considerando que varios factores fisicoquímicos afectan la estabilidad de la emulsión W1/O/W2, es necesario el uso de biopolímeros o mezclas de éstos que actúen como emulgentes, presentando no sólo una actividad superficial relativamente alta como las proteínas, sino también propiedades de solvatación de la fase acuosa, como los polisacáridos. Lo anterior, implica el uso de complejos proteínapolisacárido (Baeza et al., 2002; Tolstoguzov, 2003). La naturaleza y fuerza de las interacciones entre estas moléculas contribuyen a la estabilidad, características estructurales y funcionales del sistema disperso. En la Tabla I, se presentan las características comunes y diferencias entre proteínas y polisacáridos, como biopolímeros funcionales en sistemas alimenticios. Dependiendo de la química del biopolímero y delascondicionesdela solución(temperatura, pH, fuerza iónica, entre otras), estas interacciones pueden ser repulsivas o atractivas, débiles o fuertes, específicas o no específicas (Kruif y Tuinier, 2001).
Tabla I. Características comunes y diferencias entre proteínas y polisacáridos como biopolímeros funcionales en sistemas alimenticios.
Similitudes
Polímeros naturales
Ampliamente distribuidos en alimentos
Usados en farmacéuticos, cosméticos y productos personales
Polímeros amigables al medio ambiente
Estructura complicada
Comportamiento de agregación compleja
Agentes gelantes/estabilizantes
Diferencias
Proteínas
Estructuras muy diversas
Reactivas
Monodispersas
Muchos tipos de segmentos
Cadena lineal
Cadena flexible
Polisacáridos
Estructuras similares
No reactivas
Polidispersos
Pocos tipos de segmentos
Cadena lineal o ramificada
Cadena rígida
Peso molecular medio Alto peso molecular
Volumen molecular pequeño Alto volumen molecular
Amfifílicas
Hidrófilos
Superficialmente activas Sin actividad superficial
Polielectrolitos
Emulgente/espumante
No iónicos o cargados
Espesante/retención de agua
Sensible a la temperatura Insensible a temperatura
Fuerte interacción con surfactantes Baja interacción con surfactantes
Adaptado de Dickinson (2003).
3.2.1. Balance hidrófilo lipófilo (BHL)
El BHL es un método semiempírico que es ampliamente usado para la clasificación de emulgentesnoiónicos.ElvalordelBHLdeun emulgente es un indicador de su grado de solubilidad en la fase acuosa o en la fase oleosa, y puede ser usado dependiendo del tipo de emulsión que será formada. Cada emulgente tiene asignado un valor de BHL de acuerdo con su estructura química. En la escala utilizada los valores para este término
van de 0.5 a 19.5, el punto medio del balance es el 10, de ahí hacia abajo son cada vez más lipófilos y del 10 hacia el 19.5 van creciendo en hidrofilidad. Estos valores se calculan tomando en cuenta el porcentaje hidrófilo (peso molecular) de la molécula del emulgente y dividido entre cinco (únicamente por facilidad de manejo). Fue William C. Griffin (1971) quien acuñó el término y la metodología para el cálculo de su valor (Kralova y Sjöblom, 2009). Cuando se escucha un valor de BHL para un emulgente
iónico,essólounnúmerocomparativo ynoun cálculo matemático. Podemos decir que para emulsiones agua en aceite (W/O), escogeríamos un emulgente con un valor de BHL entre 4 y 6 y para aceite en agua (O/W), de entre 8 y 16; por lo tanto, para una emulsióndoble,seutilizaríaporlomenos,uno lipófilo y otro hidrófilo (Kralova y Sjöblom, 2009).
Algunos emulgentes utilizados en la industria alimentaria y su BHL son presentados en la Tabla II. Las mezclas de los distintos emulgentes ofrecen una alternativa cuando no se tiene uno con el valor deseado paraunsistemaenparticular.
Para la selección de un emulgente es necesario considerar primero si es aniónico o catiónico, no-iónico o anfotérico; segundo,
determinar la solubilidad buscada con base en el compuesto a disolver (hidrófilo o lipófilo); tercero, cómo afectará dicha solubilidad al comportamiento deseado, en el caso de emulsiones dobles es conveniente encontrar una mezcla apropiada de éstos, para ambas interfases.
La mayoría de los estudios entre los años 1970 y 1985 se enfocaban a la búsqueda de una mezcla apropiada de dichos emulgentes, que proporcionara las mejores características en la emulsión. En gran parte de los casos, la cantidad de emulgente interno es mayor que la del externo. Matsumoto et al. (1985) han establecidounarelación aproximadade10a1 entre el emulgente lipófilo e hidrófilo respectivamente, para la elaboración de emulsiones dobles (Jiménez-Alvarado et al., 2009).
EmulgenteBHL
Acido oleico
Monoglicéridos acetilados (ACETEM)
Dioleato de glicerol
Triestearato de sorbitán (Span 65)
Monoestearato de propilenglicol
Monoestearato de glicerol
Poliglicerol Polirricinoleato (Grindsted PGPR)
Monoestearato de sorbitán (Span 60)
Monoestearato de diglicerilo
Monopalmitato de sorbitán
Monoestearato de triglicerol 7
Ésteres del ácido acetil tartárico (Panodán DATEM) 8
Monolaurato de sorbitán 8.6
Dioleato de hexaglicerol 9
Trioleato de sorbitán y polioxietileno (Tween 85) 10.5
Triestearato de Sorbitán y polioxietileno (Tween 65) 10.9
Dioleato de decaglicerol 12
Monoglicérido etoxilado 13
Monooleato de decaglicerol 14
Monolaurato de sorbitán y polioxietileno (Tween 20) 14.9
Monooleato de sorbitán y polioxietileno (Tween 80) 15
Monopalmitato de sorbitán y polioxietileno (Tween 40)15.6
Oleato de sodio 18
Oleato de potasio 20
Estearoil-2-lactato de sodio 20
Información compilada de: McClements (2005), Badui-Dergal (1999).
Tabla II. Emulgentes empleados en la industria alimentaria y su BHL.
El valor del BHL para una mezcla de emulgentes corresponde al valor ponderado de sus BHL individuales y la proporción en peso utilizada. En un estudio como el de Schmidts et al. (2010), se realizaron una serie de mezclas de emulgentes y con éstos analizaron la estabilidad de las emulsiones dobles formadas, respecto al grado de cremosidad, viscosidad, tamaño de gota, conductividad y potencial Z. Así, encontraron la mezcla de emulgentes que mostró la mejor estabilidad paralaemulsióndobleencuestión.
3.2.2. Emulgentes poliméricos naturales
La estabilidad de las emulsiones dobles puede mejorarse formando una película polimérica en las interfases aceite-agua. Omotosho et al. (1990), han sugerido el uso de macromoléculas y emulgentes no iónicos para formar esos complejos estabilizadores. Al evaluarvariospolímeros conestepropósito,se encontró que la velocidad de liberación del material encapsulado, contenido dentro de la emulsión doble, depende del complejo formado, y esta razón de liberación sigue un patrón dependiendo la naturaleza de la fase de aceite según el siguiente orden: miristato de isopropilo > octadecano > hexadecano >dodecano >octano. Es decir, al aumentar el tamaño de cadena, se aumenta la razón de liberación, lo cual también es un reflejo del aumento del tamaño de gota en la emulsión. Los emulgentes con un BHL alto, usados como segundo agente emulgente, incrementan las razones de liberación principalmente por incrementar la razón de difusión a través de la membrana líquida no acuosa (Garti y Aserin, 1996;Dickinson,1993).
Después del trabajo original de Herbert, se han realizado muchos estudios acerca de la incorporación de proteínas como potenciales agentes activos en emulsiones W/O/W, para aplicaciones farmacéuticas. Se han encontrado que cantidades más bien bajas de esas proteínas como albúmina de suero de bovino,
en combinación con emulgentes lipófílos como el Span 80 o 60, mejoran la estabilidad de las emulsiones, posiblemente por formar barreras viscoelásticas más estables, que evitan la coalescencia y pérdida de moléculas pequeñasdelafaseinterna(Dickinson,2011).
Frank y Oza (1989), utilizaron celulosa microcristalina coloidal y varios emulgentes monoméricos para estabilizar emulsiones dobles, vía un mecanismo de estabilización mecánico. Se obtuvieron emulsiones dobles estables, por un mes. Se logró además, disminuir la razón de liberación por gelación de la fase de aceite. Garti et al. (1994), utilizaron albumina de suero de bovino (ASB) como emulgente polimérico, añadido a ambas fases acuosas, externa e interna, en ausencia y presencia de emulgentes convencionales monoméricos (Span 80 y Tween 80). Evaluaron el mecanismo de liberación de un electrolito (Na+1), de la fase acuosa interna hacia la externa, ya que se creía, que el mecanismo de liberación está asociado con el transporte micelar, el cual es controlado por difusión. Se realizaron intentos para obtener emulsiones dobles estables con gotas relativamente pequeñas, y un mínimo de capacidad de micelización. Los resultados revelaron, que la ASB al 0.2% en peso en la fase acuosa interna, disminuyó la velocidad de liberación. Además, las emulsiones permanecieron estables sin ningún cambio en tamaño de gota por 25 horas. De acuerdo a otros estudios, se sugiere que los emulgentes poliméricos forman un complejo con los emulgentes lipófilos monoméricos, siendo este complejo una película gruesa y de fuerte gelificación, la cual imparte resistencia a la ruptura de las gotas internas. La película mejora la estabilidad mecánica yestérica de la emulsión doble, y disminuye la razón de coalescencia. Además, parece ser que deprime la formación de micelas inversas en la fase de aceite, disminuyendo así el transporte de electrolitos vía este mecanismo. Sin embargo, los emulgentes monoméricos que cubren la
interfase externa, no previenen la coalescencia de las gotas externas en las emulsiones dobles. De hecho, después de una semana de almacenamiento, se detecta un incremento en la distribución del tamaño de gota así como una fuerte floculación. De tal manera que al agregar ASB, también a la fase acuosa externa, además de los emulgentes monoméricos,sedisminuyóeltamañodegota, lo cual contribuyó a mejorar la estabilidad de laemulsióndoble(GartiyLutz,2004).
El evitar la agitación vigorosa en la segunda homogeneización, previene la ruptura de las gotas y una posible inversión a una emulsión simple, con la consecuente pérdida de el principio a encapsular; por otro lado, la agitación demasiado lenta, no producirá gotas lo suficientemente pequeñas, locual disminuyelaestabilidaddelaemulsión doble y facilita la coalescencia. Con el uso de emulgentes poliméricos se busca encontrar un punto intermedio, optimizando la velocidad de agitación.
3.3. Biopolímeros en las gotas internas de emulsiones dobles
Dickinson (2011) señala tres beneficios técnicosdelusodebiopolímeroscomoagentes estabilizantesenemulsionesdobles:
1. Encomparaciónconlosemulgentesdebajo peso molecular, la migración de los biopolímeros por difusión u otro mecanismo hacialasfasesacuosasesmenor.
2. Los biopolímeros pueden formar estructuras de red estabilizadoras con las fases acuosasdispersasycontinuas.
3. Los biopolímeros de superficie activa, pueden usarse como estabilizadores efectivos delainterfaseexternaaceite-agua,enlasgotas externasdeemulsionesW/O/W.
Se han investigado varios biopolímeros alimenticios, como gelatina, caseína, proteína de suero, proteína de habas, goma acacia y goma de xantana. La gelatina (1% p/p), ha mostrado mejorar el rendimiento del material encapsulado en las gotas internas acuosas, así como un incremento en la estabilidad de las emulsiones. En emulsiones del tipo W/O/W, elaboradas con PGPR (poliglicerol polirricinoleato) como emulgente lipófilo, se encontró que el agregar 0.5% p/p de caseinato de sodio en la fase acuosa interna, ayudó a reducir del 8% al 2% en peso la cantidad de PGPR necesaria, sin afectar el rendimiento o estabilidad. Ese efecto sinérgico del caseinato, se atribuye no sólo a la formación de una barrera viscoelástica en la película, sino también, a su actuación como agente quelante de cationes como el magnesio, lo cual contribuye a evitar la pérdida de éstos y otros iones(Garti yLutz,2004;Mun et al.,2010).
Se ha utilizado almidón gelificado dentro de las gotas internas, logrando reducir la velocidad de liberación de un principio hidrófilo dentro de la gota. Pero, la presencia del almidón complica la formación de la emulsión doble; además, la alta viscosidad de la fase acuosa, incrementa la cantidad de emulgente necesario. Se crean asimismo, complejos no deseados, entre el almidón y los emulgentes no iónicos como el Span 80 y el Tween80(Dickinson,2011).
3.4. Biopolímeros en las gotas externas de emulsiones dobles
Las proteínas son muy buenos agentes estabilizadores de la segunda emulsión, tal como lo son para emulsiones simples. Una ventaja adicional, es que éstas son insolubles en aceite, por lo cual no tienden a migrar a la interfaseinterna aceite-agua,ointerferir conla estabilidad de la fase acuosa interna. En las emulsiones O/W, es común el agregar polisacáridos en baja concentración como agentes gelificantes y espesantes, para
alcanzar las propiedades reológicas deseadas. Estemismoprincipio, puedeaplicarseparalas emulsiones dobles (McClements et al., 2009; Weiss y Mushiolik, 2007; Garti y Reichman, 1993).
Para la estabilización de las gotas externas en las emulsiones dobles, se han estudiado diferentes proteínas incluyendo caseinato de sodio, gelatina, albumina de suero de bovino, y aislado de proteína de suero de leche; así como algunos hidrocoloides como goma arábiga y almidones modificados. Se han realizados pruebas con polisacáridos solubles como pectina, carragenina, alginato, xantano, gelano, semilla de algarroba, carboximetilcelulosa ypartículas coloidales de celulosa microcristalina. La presencia de un hidrocoloide como la maltodextrina o goma arábiga en la fase acuosa externa de una emulsión W/O/W, es esencial si dicha emulsión será convertida en microcápsulas por secado por aspersión. Utilizando caseinato de sodio como el segundo emulgente y altas presiones, se ha observado la producción de emulsiones finas W/O/W (gotas externas de micras) y un rendimiento relativamente alto, respecto a emulsiones preparadas sin altas presiones. En este caso, al aumentar la cantidad de caseinato, se disminuye el rendimientoyeltamañodegota,detalmanera que es necesario buscar un punto medio entre estos dos factores. Otro aspecto que afecta el rendimiento, es la intensidad de agitación o presión durante la segunda etapa de elaboración de la emulsión, al aumentar la presiónovelocidaddeagitación, disminuyeel rendimiento, debido posiblemente a ruptura o coalescencia de las gotas. Se ha encontrado, que el componente glicoproteico de la goma arábiga, confiere propiedades emulgentes únicas en las emulsiones, pero es necesario agregarla en concentraciones de alrededor del 10% (p/p). Esta glicoproteína provee una estabilidad coloidal contra la floculación, en un rangomayordepH(Dickinson,2011).
3.5. Complejos conjugados proteínapolisacárido
En estos complejos de biopolímeros, las moléculas de proteína ypolisacárido deben ser unidas permanentemente (vía enlace covalentes) o reversiblemente (vía interacciones electrostáticas) (Dickinson y McClements,1996).
Uno de los métodos más utilizados para la formación de híbridos proteína-polisacárido con enlaces covalentes es mediante el secado controlado. Esta conjugación tipo Maillard inducida por el tratamiento de calor seco, conduce a una mejora en la solubilidad de las proteínas y en la estabilidad de la emulsión, bajo condiciones desfavorables de la solución acuosa, como pH bajos y alta fuerza iónica. Esta mejora en la funcionalidad, se debe a un incremento en la hidrofilidad del conjugado y en su capacidad de estabilización estérica, comparadaconlaproteínasola.Unejemplode estos conjugados es el de caseína-dextrano, utilizado para estabilizar la gota externa en emulsiones W/O/W (Dickinson, 2003). Dickinson y McClements (1996) utilizaron un conjugado de este tipo en sustitución del caseinato de sodio, mostrando gotas más pequeñas a pH neutro, mejorando la estabilidad de la emulsión y evitando la coalescencia, bajo condiciones ácidas, además de una mejor encapsulación del principio activo (vitamina B12), dentro de las gotas internas.
Garti y Lutz (2004) han descrito la estabilización de emulsiones dobles con sistemas APS (aislado de proteína de suero de leche)-goma de xantana y APSgalactomananos (goma de algarroba, goma guarygomadefenogreco).
Jiménez-Alvarado et al. (2009) por su parte, investigaron sistemas con concentrado de proteína de suero -goma arábiga, pectina o goma de mesquite. En esos estudios, la
sensibilidad al pH de los complejos descritos, en la superficie de las gotas de las emulsiones W/O/W, era indicado por una combinación de mediciones reológicas y del potencial Z. En los trabajos indicados las propiedades de las emulsiones como son tamaño de gota y el encapsulado de principios activos, eran sustancialmente mejorados. Dependiendo del pH y el grado de esterificación, la pectina puede interactuar con proteínas de leche para formarunagamadeestructurasestabilizadoras en emulsiones y geles. De tal manera, la interacción de las pectinas con caseínas y proteínas de suero, tiene buen potencial en el desarrollo de nuevos productos alimenticios, que contienen gotas de emulsiones dobles. Por ejemplo, en el diseño de emulsiones dobles parapelículascomestibles.
3.6. Temperatura
Elefectodelatemperaturaparalaformacióny estabilidad de las emulsiones es importante. Deésta,dependeeltipodeinteracciones entre las moléculas presentes. Muchos de los conceptos y experimentos mencionados se manejan a temperaturas cercanas a 20-25°C, pero algunos procesos industriales manejan temperaturas alejadas de esos valores, lo cual es necesario considerar. La temperatura tiene acción directa en la solubilidad de todos los compuestos presentes (aceites, proteínas, polisacáridos, emulgentes) ysus interacciones, así como en la viscosidad de la emulsión (entre otros factores). La temperatura a la cual una emulsión cambia su fase dispersa a continua (W/O a O/W o viceversa), se denomina temperatura de inversión de fase (TIF) y se debe conocer en nuestro sistema a preparar, para evitar llegar a ese punto. Por otro lado, las emulsiones con componentes alimenticios, requerirán en muchas ocasiones, de algún tratamiento térmico que coadyuve a la estabilidad antimicrobiana. Otros procesos podrían incluir congelado-descongelado. Se espera que las emulsiones logradas, resistan
ciertas condiciones de temperatura esperadas (McClements et al.,2009).
Shinoda y Arai (1964) y Shinoda y Saito (1969), presentaron estudios muy interesantes que en la actualidad seguimos confirmando, con pocas excepciones, con la siguientes conclusiones: a) entre más soluble es el emulgente no iónico respecto a la fase oleosa y viceversa, más baja es la temperatura de inversión de fase (TIF); b) al aumentar la TIF, aumenta el punto de enturbiamiento (punto en el cual la emulsión pasa de transparente a turbia); c) entre más larga es la cadena hidrófiladel emulgente, másalta eslaTIF yel punto de enturbiamiento; d) los tamaños de gota en la emulsión cambian sustancialmente conlavariaciónenlatemperatura yelBHLde los emulgentes; e) el diámetro de las gotas es muy pequeño, pero menos estable contra la coalescencia cercano a la TIF; f) se pueden obteneremulsionesO/Westables,silasTIFde los sistemas obtenidos, son 20-65°C más grandes, que las temperaturas de almacenamiento; g) la estabilidad de las emulsiones se mejora, si éstas son enfriadas rápidamente,despuésdehabersidoformadasa temperaturas cercanas y por debajo de la TIF. Los estudios de Hsu y Nacu (2002) en aceite desoya,confirman lomencionado,respectoal tamaño de gota en la emulsión y la temperatura.
Es importante que la temperatura se mantenga por arriba de la temperatura de cristalización de los lípidos presentes, para evitar solidificación de grasas durante la homogeneización(McClements et al.,2009)
3.7. Potencial Z, tamaño de gota, pH y concentración de iones en la emulsión doble
A menor tamaño de gota, mayor es la estabilidad de la emulsión doble. El pH juega un papel importante a considerar en una emulsión, debido sobre todo, a las diferentes interacciones electrostáticas que se tienen al
variarlo y la manera en que afecta a la estructura de los biopolímeros presentes, misma que modificará las interacciones entre ellos y la estabilidad de la emulsión (McClements et al., 2009). La forma más común de medir estas interacciones es por medio del potencial Z. A continuación se dará una explicación breve de este concepto y su relación con el pH y la estabilidad de las emulsiones.
Las emulsiones se comportan como cualquier coloide y sus partículas (fase dispersa) en suspensión (en la fase continua) están cargadas en mayor o menor medida, lo cual las hace repelerse unas con otras y evitar acoplamientos o aglomeraciones que se darán más fácilmente entre menos carga exista. Esta carga puede variar de fuerte a débil; entre mayor sea, mayor será la repulsión y más estable será la emulsión. Si no existe repulsión, las partículas tienden a unirse unas con otras, lo cual provoca una separación de lasfases.
El potencial Z, es una medida del potencial eléctrico en la superficie interfacial de las partículas suspendidas. Sus unidades son los milivoltios (mV). En la Fig. 4 puede observarse su variación con respecto al pH. Valores de -30 a 30 mV indican inestabilidad en el sistema, valores por debajo de -30 y arriba de 30 mV, indican aumento en la
estabilidad, siendo ésta, cada vez mayor conformeaumenta(deformaabsoluta)elvalor delpotencialZ.
La medición se realiza en una celda electroforética, con dos electrodos conectados a una fuente de poder, esto crea un campo eléctrico. Los coloides migran, y dependiendo de su movimiento y dirección se tiene el valor delpotencialZ(Zeta-Meter,Inc,2012).
El valor del potencial Z se ve marcadamente afectado por el pH de la emulsión, por el efecto de éste en la carga de las partículas. Así, las variaciones en el pH resultarán en variaciones en el potencial Z y por tanto, en la estabilidad de la emulsión. En una dispersión proteica, por ejemplo, un potencial Z de cero a cierto pH, coincide con elpuntoisoeléctrico, yprovocaráprecipitación de estas macromoléculas (Maldonado et al., 2011).
La existencia de iones en la fase acuosa de laemulsión,tienetambiénunefectodirectoen el valor del potencial Z y por ende, en la estabilidad de la emulsión. El tamaño de gota, independientemente de que el tipo y concentración de emulgentes, temperatura y características de la homogeneización, tienen efecto sobre su tamaño, se ve asimismo, influenciado por los valores del pH y concentraciónelectrolítica.

Fig. 4. Representación gráfica de la variación del potencial Z en función del pH. Adaptado de Zeta-Meter, Inc. (2012).
Maldonado et al. (2011), en su estudio sobre la influencia del pH en la estabilidad de emulsiones elaboradas con proteínas de salvado de arroz, encontraron un tamaño de partícula significativamente menor a pH 8 que a pH 6 (37 y 63 micras respectivamente), siendolasolubilidadtambiénmayorapH8,lo cual contribuyó a crear una emulsión más estableaesevalor.
Weiss y Muschiolik (2007), realizaron un estudio para determinar el efecto de la composición de la fase oleosa, la tensión interfacial en las dos interfases y la viscosidad de la fase de aceite en el tamaño de partícula de la gota interna W1 y de la gota de aceite W1/O, concluyendo los siguiente: a) la tensión interfacial en la interfase W1/O aumenta, si se incrementa el porcentaje de ácidosgrasos de cadena media(C8,C10) enla fase de aceite, esto incrementa el tamaño de gota W1 y disminuye el tamaño de la gota de aceite (O); caso contrario para ácidos grasos de cadena larga (C16-C20); b) el tamaño de la gota W1/O, aumenta al aumentar la viscosidad del aceite y disminuye el tamaño de gota W1; c) la viscosidad del aceite no debe exceder cierto valor crítico, pues provocará que la fase dispersa W1/O no se rompa (segunda emulsión) en gotas lo suficientemente pequeñas para ser estable. Los autores mencionados, desarrollaron una ecuación para predecir el tamaño de gota W1 y W1/O, dependiendo de la concentración de ácidos grasos de cierto tamaño, de la tensión interfacial y de la viscosidad del aceite, con buenacorrelación.
Por otra parte, Onsaard et al. (2005), en su trabajo sobre propiedades y estabilidad de emulsiones estabilizadas con proteínas de leche de coco, analizaron, entre otras cosas, la influenciadelpH,concentracióndeNaClenla fase acuosa y el efecto de la temperatura del tratamiento térmico, sobre la estabilidad de la emulsión, encontrando que el potencial Z va de +60 mV a -70 mV cuando se pasa de pH 3
a 8, mostrando gran estabilidad a pH 7; el tamaño de partícula se incrementa al variar el pH, mostrando un máximo en los valores del punto isoeléctrico (floculación) y disminuyendo conforme éste sigue aumentando. Al aumentar la concentración de NaCl se encontró un aumento en el tamaño de partícula, efecto que fue compensado con el hecho de que aumentó a la vez, la solubilidad delasproteínas, ysugierenqueestosucede ya quelaproteínadebeestarsoluble, paramigrar a la interfase y ubicarse en ella. Hsu y Nacu (2002), en su investigación sobre el comportamiento de emulsiones de agua en aceite de soya estabilizadas por emulgentes no iónicos, confirmaron que el potencial Z es fuertemente dependiente del pH y que existe gran influencia también de éste y la concentración de los iones Na+1 y K+1, siendo grandes concentraciones de éstos, capaces de separar la fase oleosa de la emulsión; que los cationes divalentes Ca 2+ y Mg2+ a altas concentraciones, pueden llevar a la emulsión a una zona de carga cero, lo cual no sucede con cationestrivalentescomoAl3+ yFe3+ .
3.8. Viscosidad
La fracción de volumen de la emulsión primaria, en el sistema de emulsión doble, cambia debido a la difusión del agua. El cambio en esta fracción de volumen de la emulsión primaria, afecta las propiedades reológicas de la emulsión doble. Como en las emulsiones simples, la manera en que las emulsiones dobles fluyen, es una de sus características más importantes. Por eso, el entendimiento del comportamiento reológico de las emulsiones dobles es importante en la formulación, manejo, mezclado, procesado, transporte y almacenamiento de dichos sistemas. Aún más, los estudios reológicos pueden proveer información útil de la estabilidad y microestructura interna de las emulsionesdobles (JiaoyBurgess,2003).
En un estudio realizado por los autores antes citados, se analizó el comportamiento reológico de una emulsión doble, ante cambios en concentración para los emulgentes hidrófilo (Tween 80) y lipófilo (Span 83), encontrando que a medida que se aumenta la concentración del emulgente hidrófilo, disminuye la estabilidad de la emulsión, ya que la viscosidad de la película interfacial disminuye, al aumentar la solubilidad de la misma y hace que se rompan más fácilmente las gotas de aceite. Al aumentar el emulgente lipófilo, se incrementa el valor del módulo G´ y con ello la estabilidad de la emulsión. El NaCl tiene un efecto ambiguo en la estabilidad de las emulsiones dobles; por un lado, mejora algunos factores que ayudan a crear una película más firme, y por otro lado, puede alterar el balance osmótico de la fase interna, provocando coalescencia de las gotas internas.
La estabilidad de una emulsión W/O/W se incrementa con la disminución de la polaridad y el incremento de la viscosidad de la fase oleosa (Weiss y Muschiolik, 2007). La viscosidad de la fase de aceite tiene gran efecto en el tamaño de gotas en la emulsión y de ahí en la estabilidad de la misma. La composición del aceite en cuanto al largo de cadena de los ácidos grasos que lo contienen es importante. Al aumentar la proporción de ácidos grasos de cadena media (C8, C10) disminuye la viscosidad, caso contrario para ácidosgrasosdecadenamáslarga(C16-C20).
Conclusiones y comentarios finales
Las emulsiones dobles W/O/W ofrecen expectativas en aplicaciones para la industria alimentaria, siendo muchas de ellas, excelentes posibles soluciones para mejorar los productos existentes o desarrollar nuevos, debido a los componentes encapsulados que estos sistemas pudieran contener. Sin
embargo, casi no existen productos comercialesqueseencuentrenenelmercado y que utilicen la aplicación de dichas emulsiones. La razón principal es la inestabilidad de estas emulsiones y la liberación no controlada del componente encapsulado. Muchos de los estudios realizados respecto a los principales factores que hay que considerar para mejorar la estabilidaddeunaemulsióndoblevaríandeun sistema a otro, es decir, lo que para un caso funciona, puede no ser lo más apropiado para otro. Las tendencias de comportamiento al variar el pH, agregar un electrolito, combinar emulgentes, entre otros, siguen principios generales pero que a detalle, presentan variaciones que hacen que la investigación sobre las emulsiones en general, sea un tema apasionante. El estudio sistemático de nuevos emulgentes y su combinación con macromoléculas alimenticias, así como de las condiciones de homogeneización, nos llevará a lograr elaborar emulsiones cada vez más estables, con las características deseadas de viscosidadytamañodegota.
Agradecimientos
Los autores agradecen al Consejo Nacional de Ciencia y Tecnología (CONACYT) y a la Universidad de las Américas Puebla (UDLAP) porelapoyoparalarealizacióndeestetrabajo.
Referencias
Aoki, T., Decker, E. y McClements, D.J. 2005. Influence of environmental stresses on stability of O/W emulsions containing droplets stabilized by multilayered membranes produced by a layer-bylayer electrostatic deposition technique. Food Hydrocolloids. 19: 209-220.
Badui-Dergal, S., Bourges-Rodríguez, H. y AnzalduaMorales, A. 1999. Química de los alimentos. Cuarta edición. Ed. Alhambra Mexicana, México. 648 pp.
Baeza, R.I., Carp, D.J., Perez, O.E. y Pilosof, A.M.R. 2002. K-Carrageenan-protein interactions: effect of proteins on polysaccharide gelling and textural properties. Food Science and Technology. 35: 741747.
Dickinson, E. 2003. Hydrocolloids at interfaces and the influence on the properties of dispersed systems Food Hydrocolloids. 17: 25-39.
Dickinson, E. 2011. Double emulsions stabilized by food biopolymers. Food Biophysics. 6: 1-11.
Dickinson, E. y McClements, D.J. 1996. Advances in Food Colloids. Blackie Academic & Professional. London.
Dickinson, E. 1993. Protein-polysaccharide interactions in food colloids. En E. Dickinson, P. Walstra (Eds.), Food Colloids and Polymers: Stability and Mechanical Properties. 77-93.
Frank, S.G. y Oza, K. P. 1989. Multiple emulsions stabilized by colloidal microcrystalline cellulose. Journal of Dispersion Science and Technology. 10:163-185. Citado en: Garti, N. y Aserin, A. 1996. Double emulsions stabilized by macromolecular surfactants. Advances in Colloid and Interface Science. 65: 37-69.
Garti, N. y Reichman, D. 1993. Hydrocolloids as food emulsifiers and stabilizers. Food Structure. 12: 411426.
Garti, N., Aserin, A. y Cohen, Y. 1994. Mechanistic considerations on the release of electrolytes from multiple emulsions stabilized by BSA and nonionic surfactants Journal of Controlled Release 29: 41-51. Citado en: Garti, N. y Aserin, A. 1996. Double emulsions stabilized by macromolecular Surfactants. Advances in Colloid and Interface Science. 65: 37-69.
Garti, N. y Aserin, A. 1996. Double emulsions stabilized by macromolecular surfactants. Advances in Colloid and Interface Science. 65: 37-69.
Garti, N. y Lutz, R. 2004. Recent progress in double emulsions. Emulsions: Structure Stability and Interactions. 4: 587-605.
Hsu, J-P. y Nacu, A. 2002. Behavior of soybean oil-in water emulsion stabilized by nonionic surfactant Journal of Colloid and Interface Science. 259: 374381.
6 – 2 (2012): 1-18
Jager-Lezer, N., Terisse, I., Bruneau, F., Tokgoz S., Ferreira, L., Clausse, D., Seiller, M. y Grossiord, J.L. 1997. Influence of lipophilic surfactant on the release kinetics of water-soluble molecules entrapped in a W/O/W multiple emulsion. Journal of Controlled Release. 45: 1-3.
Jiménez-Alvarado, R., Beristain, C.I., Medina-Torres, L., Román-Guerrero, A. y Vernon-Carter, E.J. 2009. Ferrous bisglycinate content and release in W1/O/W2 multiple emulsions stabilized by proteinpolysaccharide complexes. Food Hydrocolloids. 23: 2425-2433.
Jiao, J. y Burgess, D. J. 2003. Rheology and Stability of water-in oil in-water multiple emulsions containing Span 83 and Tween 80. AAPS Pharm Scientists. 5: 1-12.
Kita, Y., Matsumoto, S. y Yonezawa, D. 1977. Viscometric method for estimating the stability of W/O/W type multiple-phase emulsions. Journal of Colloid Interface Sci. 62:87-94. Citado en: Dickinson, E. 2011. Double emulsions stabilized by food biopolymers. Food Biophysics. 6: 1-11.
Kralova, I. y Sjöblom, J. 2009. Surfactants used in food industry: A Review. Journal of Dispersion Science and Technology. 30: 1363-1383.
Kruif de, C.G. y Tuinier, R. 2001. Polysaccharide protein interactions. Food Hydrocolloids. 15: 555563.
Kumar, R., Kumar, M.S. y Mahadevan, N. 2012. Multiple emulsions: A Review. International Journal of Recent Advances in Pharmaceutical Research. 2(1): 9-19.
Li, B., Jiang, Y., Liu, F., Chai, Z., Li Y. y Leng, X. 2011. Study of the encapsulation efficiency and controlled release property of whey protein isolatepolysaccharide complexes in W1/O/W2 double emulsions. International Journal of Food Engineering. 7: 1-16
Maldonado, L., Latorre, K., Rocha, P., Medrano, A., Abirached, C. y Panizzolo, L.A. 2011. Influencia del pH en la estabilidad de emulsiones elaboradas con proteínas de salvado de arroz. Revista del Laboratorio Tecnológico de Uruguay. 6: 28-31.
Matsumoto, S., Koh, Y. y Michiura, J. 1985. Preparation of W/O/W emulsions in an edible form on the basis of phase inversion technique J. Dispersion Science and Technology. 6:507-521. Citado en: Jiménez-Alvarado, R., Beristain, C.I., Medina-Torres, L., Román-Guerrero, A. y VernonCarter, E.J. 2009. Ferrous bisglycinate content and
release in W1/O/W2 multiple emulsions stabilized by protein-polysaccharide complexes. Food Hydrocolloids. 23: 2425-2433.
McClements, D.J. 2005. Food Emulsions. Principles Practice and Techniques. 2nded. CRC Press. Elsevier. Florida. USA.
McClements, D.J., Decker, E.A., Park, Y. y Weiss, J. 2009. Structural design principles for delivery of bioactive components in nutraceuticals and functional foods. Critical Reviews in Food Science and Nutrition. 49:577–606.
Mun, S., Choi, Y., Rho, S.J., Kang, C.G., Park, C.H. y Kim, Y.R. 2010. Preparation and characterization of water/oil/water emulsions stabilized by polyglycerol polyricinoleate and whey protein isolate. Journal of Food Science. 75(2): 116-125.
Omotosho, J.A., Florence, A.T. y Whateley, T.L. 1990. Absorption and lymphatic uptake of 5-fluorouracil in the rat following oral administration of w/o/w multiple emulsions. International Journal of Pharm. 61:51-56. Citado en: Garti, N. y Aserin, A. 1996. Double emulsions stabilized by macromolecular surfactants. Advances in Colloid and Interface Science. 65: 37-69.
Onsaard, E., Vitatayanont, M., Srigam, S. y McClements, D. 2005. Properties and stability of oil in water emulsions stabilized by coconut skim milk proteins. Journal of Agricultural and Food Chemistry. 53: 5747-5753.
Schmidts, T., Dobler, D., Guldan, A.-C., Paulus, N. y Runkel, F. 2010. Multiple W/O/W emulsions using the required HLB for emulsifier evaluation. Colloids
6 – 2 (2012): 1-18
and Surfaces A: Physicochem. Eng. Aspects. 372: 48-54.
Seifriz, W. 1925. Studies in emulsions III. Double reversal of oil emulsions occasioned by the same electrolyte. J. Phys. Chem.-US, 29: 738–749. Citado en Weiss, J. y Mushiolik, G. 2007. Factors affecting the droplet size of water-in-oil emulsions (W/O) and the oil globule size in water-in-oil-in-water emulsions (W/O/W). Journal of Dispersion Science and Technology. 28: 703–716.
Sela, Y., Magdassi, S. y Garti, N. 1995. Release of markers from inner water phase of W/O/W emulsions stabilized by silicone based polymeric surfactants. Journal of Controlled Release. 33: 1-12.
Shinoda, K. y Saito, H. 1969. The stability of O/W type emulsions as functions of temperature and the HLB of emulsifiers: The emulsification by PIT-method Journal of Colloid and Interface Science. 30: 258263.
Shinoda, K. y Arai, H. 1964. The Correlation between phase inversion temperature in emulsion and cloud point in solution of nonionic emulsifier. The Journal of Physical Chemistry. 68: 3485-3490.
Tolstoguzov, V. 2003. Some thermodynamic considerations in Food formulation. Food Hydrocolloids. 17: 1-23.
Weiss, J. y Mushiolik, G. 2007. Factors affecting the droplet size of water-in-oil emulsions (W/O) and the oil globule size in water-in-oil-in-water emulsions (W/O/W). Journal of Dispersion Science and Technology. 28: 703–716.
Zeta-Meter, Inc. 2012. Curso sobre potencial zeta. Disponible en: http://www.zeta-meter.com Consultado el: 27 de septiembre de 2012.

Temas Selectos de Ingeniería de Alimentos 6 - 2 (2012): 19 - 31

Modelación del calentamiento dieléctrico (microondas y radiofrecuencia) en sistemas alimenticios modelo
N. Soto-Reyes*1, R. Rojas-Laguna2 y M.E Sosa-Morales1
1 Departamento de Ingeniería Química, Alimentos y Ambiental, Universidad de las Américas Puebla. Ex hacienda Sta. Catarina Mártir S/N, San Andrés Cholula, Puebla. C.P.72810, México.
2 División de Ingenierías Campus Irapuato-Salamanca. Universidad de Guanajuato. Carretera Salamanca-Valle de Santiago km 3.5+1.8. Comunidad de Palo Blanco, Salamanca, Guanajuato. C.P. 36885. México.
Resumen
El calentamiento dieléctrico, que incluye al generado por microondas y por ondas de radiofrecuencia, es ampliamente usado en diferentes áreas, entre ellas, la ciencia y tecnología de alimentos. Aunque presenta numerosas ventajas sobre otras formas de calentamiento, también tiene una desventaja importante: la falta de uniformidad en las temperaturas generadas en el material. Recientemente, la modelación del calentamiento dieléctrico ha sido propuesta como una herramienta para solucionar la falta de uniformidad del calentamiento. Este artículo de revisión presenta conceptos fundamentales para comprender los términos asociados al calentamiento dieléctrico. Además, se recopila información de los trabajos en los que se han estudiado las propiedades dieléctricas, físicas y térmicas de los materiales que se utilizan para elaborar los sistemas alimenticios modelo, en los cuales se ha aplicado la modelación del calentamiento dieléctrico. Al final de este artículo, los autores presentan su opinión sobre la información recopilada y de futuros trabajos en los que se estudie la modelación del calentamiento dieléctrico.
Palabras clave: calentamiento dieléctrico, microondas, radiofrecuencia, modelación.
Abstract
Dielectric heating, which involves microwave and radio frequency heating, is widely used in different areas, including food science and technology. Although, it has many advantages over other forms of heating, also has an important disadvantage: the lack of uniformity in temperatures generated in the material. Recently, modeling of dielectric heating has been proposed as a tool to solve the lack of uniformity of heating. This review presents fundamental concepts to understand the terms associated with dielectric heating. In addition, there is a compilation of information from works that had studied the dielectric, physical and thermal properties of materials that are used to prepare model food systems, in which the modeling of dielectric heating have been applied. At the end of this article, the authors present their opinion on the information gathered and about the future investigations concerning dielectric heating modeling.
Keywords: dielectric heating, microwaves, radiofrequency, modeling.
*Programa de Doctorado en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: nohemi.sotors@udlap.mx
Introducción
La preocupación por conservar el medio ambiente se ha incrementado en los últimos años, por lo que se están buscando procesos y tecnologías que sean amigables con éste, es decir, tecnologías que no generen humo, compuestos tóxicos ó radiactivos o aquéllos que dañen la capa de ozono. Una de estas tecnologías es el calentamiento dieléctrico, el cual puede reemplazar al calentamiento tradicional. Dentro del calentamiento dieléctrico se encuentra el calentamiento con microondas (MO) y el calentamiento con ondas de radiofrecuencia (RF). En ambos, la energía eléctrica es convertida a radiación electromagnética del tipo no ionizante y el calor es generado por una interacción directa entre la energía electromagnética y el alimento.
Las MO y ondas de RF se han utilizado en varios procesos alimenticios como cocción, horneado, descongelación, secado, pasteurización y recientemente como tratamiento de desinfestación postcosecha, entre otros. En comparación con el calentamientotradicional,el calentamientopor MOuondasde RF esmásrápido eimpacta en menor grado al medio ambiente. Además, al tener tiempos de procesamiento más cortos, el calentamiento por MO u ondas de RF causa menosdañoalaspropiedadesfisicoquímicas y nutricionales del alimento tratado térmicamente.
Para diseñar sistemas de calentamiento dieléctricos, es necesario tomar en consideración los factores que afectan la velocidad del calentamiento en el producto. Los factores principales son las propiedades dieléctricas del material, ya que determinan la distribución de la energía electromagnética durante el calentamiento dieléctrico. Se sabe que estas propiedades dependen de la composición, forma, tamaño, temperatura,
estado físico del agua y densidad del alimento, así como del tiempo de almacenamiento, por lo que estos aspectos deben conocerse para el diseñodesistemas efectivos.
Sin embargo, el calentamiento dieléctrico también presenta desventajas. La principal es que el calentamiento no es uniforme, ya que existen puntos de sobrecalentamiento en el alimento, así como zonascon puntos fríos. Por ello, ha surgido el interés de modelar el calentamiento dieléctrico para hallar soluciones a este problema. La modelación del calentamiento por MO y ondas de RF es una herramientaefectivapara estudiarlainfluencia de varios parámetros que afectan la uniformidaddel calentamiento.Éstasebasaen predecir patrones de temperatura y de distribución de la energía electromagnética en el material tratado térmicamente, utilizando programas computacionales basados en la solución de ecuaciones matemáticas. Es por esto que, el objetivo de esta revisión bibliográfica es compilar información científica sobre la modelación del calentamiento dieléctrico (MO y RF) en sistemas alimenticios modelo, describiendo la composición, propiedades físicas, térmicas y dieléctricas de éstos, así como las bases de la modelación y las soluciones propuestas para mejorarlauniformidaddelcalentamiento.
Revisión bibliográfica
1. Generalidades del calentamiento dieléctrico
El calentamiento eléctrico puede dividirse en calentamiento eléctrico directo e indirecto. En el primero, la energía eléctrica se aplica directamente al alimento (calentamiento óhmico); mientras que en el calentamiento eléctrico indirecto o calentamiento dieléctrico (calentamiento por microondas o radiofrecuencia)laenergíaeléctricaprimeroes
convertida a radiación electromagnética, la cualsubsecuentemente generacalordentrodel producto (Marra et al., 2009; Vandivambal y Jayas, 2010). Las microondas (MO) y las ondas de radiofrecuencia (RF) generan calor en materiales dieléctricos induciendo una vibración molecular como resultado de la rotación dipolar y/o por polarización iónica (RamaswamyyTang,2008).
1.1. Diferencias entre el calentamiento por microondas y por ondas de radiofrecuencia
LaprimeradiferenciaentrelasMOylasondas de RF es la región del espectro electromagnético en la que se encuentran. Las ondas de RF se ubican en el rango de frecuencia que abarca de 0.003 a 300 MHz, mientras que las microondas están en el rango de 300 a 300,000 MHz (Ramaswamy y Tang, 2008). Con respecto a las ondas de RF, sólo ciertas frecuencias (13.56±0.00678, 27.12±0.16272 y 40.68±0.02034 MHz) son permitidas para aplicaciones industriales, científicas y médicas (Marra et al., 2009). Las frecuencias permitidas para MO son 915 MHz y 2450 MHz (Venkatesh y Raghavan, 2004).
Las longitudes de onda de MO y RF también difieren, la longitud de onda de la RF es más larga (ej. 11 m a 27.7 MHz en el aire) que la de MO (ej. 0.12 m a 2450 MHz) (Marra et al., 2009),porloquelaenergíadelasondasdeRF penetra más que la de las MO (Chow Ting Chan et al.,2004).
Otra diferencia entre MO y RF es la configuración del calentamiento (ver Fig. 1). En el calentamiento por MO, tubos especiales oscilatorios conocidos como magnetrones emiten microondas, las cuales son transferidas por una guía de ondas al interior de una cámara metálica o cavidad, donde se coloca el material a ser calentado. Para mejorar la uniformidad del campo electromagnético que rodea al alimento, se utilizan bandejas giratorias o agitadores. Por otro lado, en el calentamiento por RF, la energía es generada porunaválvulatriodo yesaplicadaatravésde dos electrodos, los cuales están situados paralelamente (uno de los electrodos está conectado a tierra). El material a ser calentado se coloca entre los dos electrodos, pero sin estar en contacto directo con éstos (Marra et al.,2009).
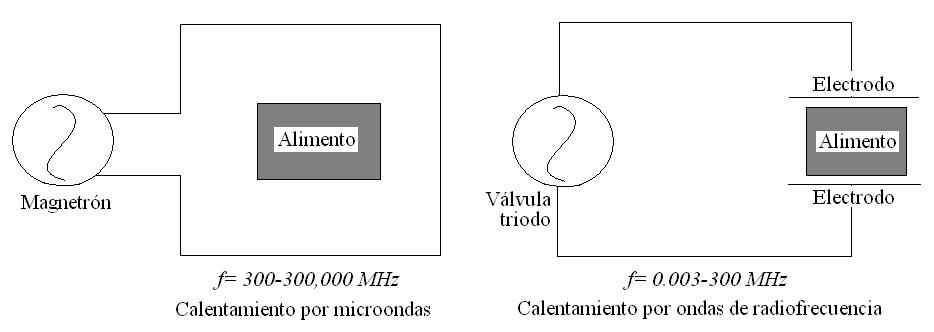
Fig. 1. Arreglo esquemático del calentamiento dieléctrico. Adaptado de Marra et al. (2009).
Cuando un alimento es sometido a un campo eléctrico alternante, pueden ocurrir dos fenómenos: lapolarizacióniónicaolarotación dipolar. En la primera, el movimiento de los iones positivos hacia la región negativa del campoeléctricoyviceversa,eselqueocasiona el calentamiento. El cambio continuo de polaridad en el campo eléctrico conduce a la oscilación de los iones hacia adelante y hacia atrás, dentro del alimento, lo que produce fricción entre ellos y por consiguiente, genera calor dentro del producto (Marra et al., 2009). En la rotación dipolar, las moléculas dipolares como el agua, también tratarán de alinearse adecuadamente con el cambio de polaridad de un campo eléctrico. El movimiento de estos dipolos también causa fricción entre las moléculas, lo cual lleva a la generación de calor (Marra et al., 2009; Hossan et al., 2010). Al comparar los mecanismos del calentamiento por MO y por RF, se reconoce que la polarización iónica es la que tiende a dominar en el mecanismo de calentamiento por RF, mientras que en el calentamiento por MO, también se presenta la rotación dipolar (Marra et al.,2009).
1.2. Ventajas y desventajas del calentamiento dieléctrico en alimentos
El calentamiento dieléctrico está ganando aceptación en el área del procesamiento de alimentos.Hasidoutilizadoenvariosprocesos alimenticios como: pasteurización, esterilización, secado, extracción rápida, cocción, horneado, descongelación, secado y en la mejora de la cinética de algunas reacciones (Ramasawamy y Tang, 2008; Campañone et al., 2012; Salazar-González et al.,2012).
Las ventajas que presenta el calentamiento dieléctrico (MO y RF) sobre el calentamiento convencional (convección y conducción) son: 1) menor impacto sobre el medio ambiente, debido a que no genera productos tóxicos; 2) ahorro de energía al compararlo con el método
convencional; 3) uso de energía limpia, si la energía eléctrica inicialmente es obtenida de fuentes renovables, como plantas eólicas; 4) facilidad en la operación de los equipos como limpieza, encendido yapagadoinstantáneos; y 5) menor tiempo de proceso, por lo que se conserva el contenido de nutrientes y las características sensoriales (Ramsawamy y Tang, 2008; Campañone et al., 2012; SalazarGonzález et al.,2012).
Como ya se mencionó anteriormente, la desventaja principal del calentamiento dieléctrico es la falta de uniformidad en la distribución de la temperatura, dando lugar a puntos fríos y calientes (Vandivambal yJayas, 2010, Campañone et al., 2012; SalazarGonzález et al., 2012). El problema mayor de este fenómeno es que puede sobrevivir algún microorganismo que dañe la salud del consumidor. Otra desventaja es que la transferencia de calor se ve afectada por factores como la geometría, el tamaño y las propiedades dieléctricas del alimento (Vandivambal y Jayas, 2010; SalazarGonzález et al.,2012).
2. Propiedades dieléctricas
Las propiedades dieléctricas de los alimentos son los parámetros principales que determinan la distribución de la energía electromagnética durante el calentamiento dieléctrico; dependen de la composición, forma, tamaño y densidad del alimento, además del tiempo de almacenamiento, temperatura y frecuencia (Wang et al., 2005; Marra et al., 2009). Estas propiedades junto con las propiedades físicas, térmicas y las características del campo electromagnético, determinan la absorción de la energía de MO yondas de RF,por loque es fundamental conocerlas para entender y modelarlarespuestadeunmaterialsometidoa un campo electromagnético con diferentes frecuencias y temperaturas (Salazar-González et al.,2012).
Las propiedades dieléctricas de los materiales son la permitividad, la constante dieléctrica y el factor de pérdida. A continuación se definirá cada uno de estos términos y otros parámetros dieléctricos importantes.
La permitividad es el término que se utiliza para describir a las propiedades dieléctricas que afectan la reflexión de ondas electromagnéticaseninterfacesylaatenuación de la energía de la onda dentro del material (Wang et al.,2005;Sosa-Morales et al., 2010). La permitividad compleja relativa (ε*), relacionada al espacio libre o vacío, se representaporlaEc.1:
donde los subíndices d y σ indican la contribución debida a la rotación dipolar ya la conducción iónica, respectivamente; σ es la conductividad iónica del material en S/m, f es la frecuencia en Hz, ε0 es la permitividad en el vacío (8.854×10-12 F/m) y ω es la frecuencia angularenrad/s.
La conductividad eléctrica o conductividad iónica (σ) es la habilidad que tiene un material para conducir electricidad(Marra et al.,2009). En un sistema dieléctrico alimenticio está relacionada con la polarización iónica y contribuye al valor del ε ´´. La σ puede ser calculadaporlaEc.3:
=2 ´´ (Ec.3)
donde ε ´ es la constante dieléctrica y ε ´´ el factor de pérdida y representan la parte real e imaginaria, respectivamente, de la permitividad,siendo j=√−1
La constante dieléctrica (ε ´) es la característica que determina la capacidad del material para absorber, transmitir y reflejar energía de una porción del campo eléctrico; es constante para cada material a una frecuencia dada, bajo condiciones constantes. El factor de pérdida (ε ´´) mide la cantidad de energía que se pierde del campo eléctrico, está relacionado con la forma en que la energía del campo es absorbida y convertida a calor en un material cuando pasa a través de éste (Swain et al., 2004; Wang et al., 2005; Marra et al., 2009; Sosa-Morales et al., 2010). Un material con bajo ε´´absorberá poca energía ypor lo tanto, se calentará poco debido a su transparencia a la energía electromagnética (Marra et al., 2009). Los mecanismos que contribuyen al ε´´ son la conducción iónica y la rotación dipolar (Wang et al.,2005):
´´= ´´ + ´´ = ´´ + (Ec.2)
Otro parámetro importante es la profundidad de penetración (dp), y se refiere a ladistanciapordebajodelasuperficiealaque la potencia de las MO y las ondas de RF disminuye e-1 de su valor, es decir, 36.8% de su valor transmitido. La profundidad de penetración puede ser calculada por la Ec. 4 (Sosa-Morales et al., 2010); ésta es inversamente proporcional a la frecuencia, por lo que hay mayor profundidad de penetración a frecuencias bajas en comparación con frecuenciasaltas.
=( √ ′)/(2 ′′) (Ec.4)
donde λ0 es la longitud de onda de la microonda en condiciones de vacío (para 2.45 GHz, λ0 es 12.2 cm). Otra expresión matemáticaparacalcular dp es:
= 2 2 1+( ⁄) −1 (Ec.5)
donde c es la velocidad de la luz en condiciones de vacío (3x108 m/s), f es la
frecuencia (Hz) y dp se expresa en metros (Sosa-Morales et al.,2010).
Los materiales dieléctricos alimenticios conviertenla energíade lasMO ylasondasde RF en calor. El aumento de temperatura en un material debido al calentamiento dieléctrico puede ser calculado aplicando la Ec. 6 (Wang et al., 2005; Sosa-Morales et al., 2010), considerando que es mínima la conducción de calor en el material y la pérdida de calor al medioquelorodea.
=55.33×10 ´´ (Ec.6)
donde Cp eselcalorespecíficodelmaterialen J/kg°C, ρ es la densidad del material en kg/ m3 , E es la intensidad del campo eléctrico en V/m, f es la frecuencia en Hz, dT es el incremento de temperatura en °C y dt es la duración del tratamiento en s. En la Ec. 6 se nota que el aumento de la temperatura es proporcional al factor de pérdida del material, a la intensidad del campo eléctrico, a la frecuencia y al tiempo del tratamiento (SosaMorales et al.,2010).
3. Sistemas alimenticios modelo usados para el análisis del calentamiento dieléctrico
3.1. Criterios de selección
Existe la necesidad de desarrollar modelos que simulen a los alimentos, los cuales deben presentar respuestas de transporte térmico yde masa similares a las del alimento real. Los posibles simuladores de alimentos o sistemas alimenticiosmodelopuedenserclasificadosen diferentes grupos químicos: polisacáridos, polímeros hidrofílicos, proteínas, suspensiones orgánicas y geles de alcohol (Swain et al., 2004).
De acuerdo a Swain et al. (2004), los criteriosparautilizarunmaterialcomosistema modeloson:
a. Resistencia al calentamiento: el material del sistema modelo debe resistir el calentamiento en el intervalo de temperatura del tratamientotérmicoalqueserásometido.
b. Estabilidad: debe permanecer estable al menos dos días a temperatura de refrigeración (5±2°C).
c. Seguridad:debeserseguroparaelpersonal, es decir, no debe contener químicos tóxicos, inflamablesopeligrosos.
d. Costo: no debe ser costoso, ser reutilizable o lo suficientemente barato para ser desechado.
e. Manufactura: su preparación debe ser sencilla y rápida, utilizando equipos que estén disponiblesencualquierlaboratorio.
f. Disponibilidad: los componentes del sistema modelo deben estar disponibles en cualquierpaís.
g. Propiedades térmicas: debe presentar el mismo comportamiento térmico que el alimento que representa. El calor específico y la conductividad térmica del sistema modelo debensersimilaresalosdelalimento.
h. Propiedades dieléctricas: su comportamiento dieléctrico debe ser similar al del alimento respecto a la constante dieléctrica yalfactordepérdidadieléctrico.
i. Propiedades de transferencia de masa: deben ser similares a las del alimento y poder medirse por la pérdida de peso después del calentamiento.
3.2. Propiedades dieléctricas, térmicas y físicas de sistemas alimenticios modelo
Como se mencionó previamente, es de suma importancia conocer las propiedades dieléctricas del material que será sometido al calentamiento dieléctrico. Los valores de las constantes dieléctricas y los factores de pérdida de diferentes materiales (gel de agar, carboximetilcelulosa, gel de gelano, gel de proteínadesuero)que se utilizanparaelaborar sistemas alimenticios modelo se presentan en las Tablas I y II. Se observa que la constante dieléctrica (ε ´) del gel de gelano a diferentes
Tabla I. Propiedades dieléctricas de sistemas modelo alimenticios.
Sistema modeloTemperaturaConstante dieléctricaFactor de pérdidaReferencia (°C) ε' (adimensional) ε'' (adimensional)
Gel de agar (2%)-73.611.5Barringer et al ., 1995
Gel de agar (2%)+ almidón (30%)-569Campañone et al ., 2012
Gel de agar (2%)+NaCl (3%)-7535Campañone et al ., 2012
Gel de agar (1%)+ azúcar (20.3%)+ sal (0.75%)*4058.620.3Sakai et al ., 2005
Carboximetilcelulosa (1%)a
Agua del grifo a
2085.488.6Wang et al ., 2008 3083103.1
4080.8119.7
5078.5136.4
6076.1155.6
2077.520.2Wang et al ., 2008 3073.523.4
4068.627.2
5064.631.1
6061.435.9 --0.48 T+84.740.33 T+11.1Birla et al ., 2008
Gel gelano (1%)+ NaCl (0.17%)-- 0.21 T+ 86.764.36 T+129.4Birla et al ., 2008
* Propiedades dieléctricas determinadas a 2450 MHz.
a Propiedades dielectricas determinadas a 27.12 MHz.
T = temperatura en °C
Tabla II. Propiedades dieléctricas de materiales para sistemas modelo alimenticios a frecuencias específicas. Sistema modeloTemperaturaReferencia (°C)
Constante dieléctrica (ε')* Frecuencia (MHz)
Factor de pérdida (ε'')* Frecuencia (MHz)
2740100915180027401009151800
Gel gelano (1%) + NaCl (0.17%)2082.5081.9079.2077.8077.60220.50149.2059.807.909.80Wang et al ., 2003a 3080.5079.5076.7075.4075.30256.80173.8069.408.208.80 4078.1077.0073.9072.6072.60301.50203.8081.308.908.30 5076.0074.5071.3070.0070.10346.60234.1093.409.808.10 6074.1072.2068.8067.4067.50393.60265.70105.8010.808.20
líquida de proteína de suero de lecheb
Gel de proteína de suero de lechea 2099.2388.27-59.0357.17835.97569.17-34.8023.30Wang et al ., 2003b 30101.9789.77-57.7755.87981.77668.13-39.1724.73 40104.9791.23-57.0054.671155.57785.47-44.1026.67 50107.7392.43-56.0353.431337.03907.60-49.5028.93 60110.5093.57-54.5351.831534.101040.33-54.6331.20 70113.3094.60-53.4350.601739.771178.67-60.9334.17 80117.2396.17-52.5749.431956.171323.93-67.5037.43 90121.3398.13-52.1048.332172.271473.57-73.9740.67 100126.07100.37-51.6347.302392.701622.67-80.5744.03 110130.40102.30-50.9746.372626.601781.23-87.8047.00 121.1137.97108.90-50.3344.972854.871935.13-95.2751.77 2088.1082.20-61.6558.90885.80596.85-33.5523.10Wang et al ., 2003b 3089.3082.25-60.4057.801061.45715.15-38.2524.65 4090.5582.40-59.0056.451255.60845.25-43.6026.75 5091.6582.45-57.4054.851469.90988.75-49.5529.35 6093.2082.70-55.7053.201683.351131.95-55.5532.00 7096.3083.95-54.2051.701879.151263.20-61.3034.75 80109.8094.05-52.9550.152088.951405.55-68.8638.40 90118.05100.00-52.0549.002294.601549.05-75.9041.90 100123.60103.50-51.6048.302567.551733.10-84.2546.10 110127.85105.55-50.7047.202800.251890.30-91.3049.70 121.1132.70107.80-49.7046.153084.252082.05-99.7553.90
* Adimensional a 20% de concentrado de proteína de suero de leche (Alacen 882), 2% glucosa, 0.59% NaCl y agua destilada b Mezcla de suero de leche en polvo, glucosa, NaCl y agua destilada
Mezcla
frecuencias (27 a 1800 MHz) disminuye al aumentar la temperatura. En cambio, el factor de pérdida (ε ´´) aumenta al incrementar la temperatura en el rango de frecuencia de 27 a 915 MHz, observándose que a 1800 MHz disminuyealaumentarlatemperatura.
Con respecto a las propiedades dieléctricas del gel de proteína de suero, en la Tabla II se observa que la ε ´ depende de la temperatura y frecuencia utilizada. A frecuencias bajas (27 y 40 MHz) la ε ´ aumenta al incrementar la temperatura, sin embargo, a frecuencias altas (915y1800MHz)disminuyealincrementarla temperatura. El ε ´´ incrementa al aumentar la temperatura sin importar la frecuencia a la que sedetermineestapropiedaddieléctrica.
De acuerdo a Wang et al. (2005), a frecuenciasbajasel ε ´´ aumentaal incrementar latemperaturadebidoalaconductanciaiónica, mientras que a frecuencias altas disminuye al incrementar la temperatura, debido a la dispersión del agua libre. Sin embargo, en los
datos presentados en las Tablas I y II se observa que este comportamiento cambia dependiendo del material analizado. Es de suma importancia resaltar que a frecuencias altas la ε ´ y el ε ´´ presentan valores pequeños en comparación a los obtenidos a frecuencias bajas. Esto se debe a la longitud de onda, ya que las longitudes de onda de frecuencias altas son menores, por lo que habría una menor penetración en el alimento, en comparación con las longitudes de onda de frecuencias bajas.
En la Fig. 2 se presentan las propiedades dieléctricas del gel de agar con diferentes concentraciones de sacarosa y del gel de agar con diferentes concentraciones de NaCl, determinadas por Sakai et al. (2005). Dichos investigadores encontraron que al aumentar la concentración de NaCl disminuye ligeramente la ε ´, y el ε ´´ incrementa significativamente. Por otro lado, la adición de sacarosa modifica principalmente a la ε ´. Los investigadores concluyen que la sacarosa, al no ser un

Fig. 2. Propiedades dieléctricas de gel de agar (1%) con sacarosa (A) y con NaCl (B). Adaptado de Sakai etal. (2005).
electrolito,nocambiasignificativamenteal ε ´´ , además, debido a que agregaron grandes cantidades de sacarosa (10%, 20%, 30% y 40%), disminuyeron el contenido de humedad y por lo tanto la ε ´ disminuye. Sin embargo, cuando añadieron azúcar y sal al gel de agar, ε ´ y ε´´ no pudieron ser cambiados independientemente, por lo que desarrollaron ecuaciones y un método para determinar la concentración de sal y azúcar necesaria para obtener propiedades dieléctricas específicas en el gel de agar (1%). Con este método, Sakai et al. (2005) lograron obtener propiedades dieléctricas similares a las de una salsa. En
En la Tabla III se muestran las propiedades físicas ytérmicas de gel de agar, gel de gelano y agua. Se observa que hay escasa información sobre estas propiedades en sistemas modelo alimenticios, por lo que sería de suma importancia realizar más estudios para determinar propiedades físicas y térmicas en éstos yotros materiales que se utilizan para emular a los alimentos en estudios de modelacióndelcalentamientodieléctrico.
4. Modelación del calentamiento dieléctrico en sistemas alimenticios modelo
La modelación es una herramienta útil para entender el efecto o la dependencia de diferentes factores durante un proceso en particular (Salazar-González et al., 2012). Los estudios de distribución de temperatura que se han realizado, utilizan diversos materiales alimenticios como alimentos listos para consumirse, diferentes tipos de carne, granos, sistemas modelo (Vandivambal y Jayas, 2010) y frutas (Birla et al., 2004; Sosa-Morales et al., 2009; Villa-Rojas et al., 2011); sin embargo, esta revisión se centrará en los estudios de modelación del calentamiento dieléctrico en sistemas modelo. En general, para modelar el calentamiento dieléctrico se utilizan ecuaciones matemáticas como la ley
particular, este trabajo muestra cómo la composición del material modifica a las propiedadesdieléctricas.
En general, los datos encontrados sobre propiedades dieléctricas de sistemas modelo en los últimos nueve años en revistas especializadas en la ingeniería y ciencia de alimentos son pocos, sobre todo del gel de agar, por lo que sería importante realizar más investigaciones para obtener las propiedades dieléctricas de este material, principalmente porque es económico y fácil de adquirir.
de Lambert, las ecuaciones de Maxwell, ecuaciones de onda y balance de energía (ver Anexo). Es de suma importancia resaltar que para resolver estas ecuaciones es necesario conocer datos del campo electromagnético, propiedades dieléctricas, térmicas y físicas de la muestra. Con las ecuaciones se elaboran matrices y se utilizan programas computacionales para resolverlas (MATLAB, Comsol Multiphysics, entre otros). De esta manera, los modelos matemáticos permiten evaluar los efectos que tienen las características particulares de los alimentos (composición, estructura, tamaño) sobre los perfilesdetemperaturaquesedesarrollanenel interior del material que es calentado (Campañone et al.,2012).
Aunque la simulación no puede reemplazar al trabajo experimental, si puede proveer de información valiosa para el diseño de sistemas de calentamiento con MO y ondas de RF (Chow Ting Chang et al., 2004; Marra et al., 2009; Ramaswamy y Tang, 2008). Su mayor desafío es validar los resultados con datos experimentales. Incluso, el Departamento de Agricultura de los Estados Unidos (USDA, 2000) ha identificado al estudio de los efectos de la formulación de los alimentos sobre los patrones de calentamiento durante la exposición a microondas como un área de investigación.
95) se elaboraron rebanadas de gel de agar (2%) con dos espesores (0.9 cm y 3 cm), las cuales fueron calentadas en un horno de MO durante 7 min. Estos investigadores midieron la temperatura de las muestras en diferentes puntosparadeterminarel perfildetemperatura experimental; éste fue comparado con las predicciones de potencia y de perfiles de temperatura obtenidos por las ecuaciones de Maxwell, la Ley de Lambert y una combinación de éstas, encontrando que las ecuaciones de Maxwell dieron predicciones más precisas. Además, constataron que el cambio de espesor en las rebanadas de gel de agar afecta el perfil de temperatura, para rebanadas angostas un cambio pequeño en su espesor causa una gran diferencia en la temperatura final, mientras que un cambio de espesor en rebanadas gruesas afecta en menor gradoalperfildetemperatura.
Yang y Gunasekaran (2004) elaboraron cilindros de gel de agar (2%) con diferentes dimensiones (radio: 3.5 y 4 cm; altura: 7cm), los cuales fueron sometidos a calentamiento utilizando energía de MO continua e intermitente. En este trabajo se predijo la distribución de temperatura dentro de la muestra utilizando la ley de Lambert y las ecuaciones de Maxwell, y al igual que Barringer et al. (1995), se demostró que las ecuaciones de Maxwell fueron más exactas estadísticamente. Los resultados experimentales ylos predichos en los cilindros de gel de agar sometidos a calentamiento intermitente mostraron una mayor uniformidad; sin embargo, el tiempo de proceso fue mayor en comparación al calentamiento continuo. Previamente, Yang y Gunasekaran (2001) determinaron los perfiles de temperatura en sistemas modelo cilíndricos de gel de agar (2%), los cuales fueron tratados térmicamente por MO en ciclos intermitentes; y encontraron mayor uniformidad en el
calentamiento intermitente con periodos de apagadomáslargos.
Campañone et al. (2012) desarrollaron un modelodesimulaciónparaelcalentamientoen hornos de MO y su uso para optimizar las estrategias de calentamiento. Para ello utilizaron diferentes programas de cómputo (Comsol Multiphysics 3.2 de elementos finitos, UMFPACK para resolver sistemas lineales y MATLAB 6.5), con los cuales resolvieron matrices de ecuaciones diferenciales basadas en las ecuaciones de Maxwell, que describieron la interacción entre la radiación electromagnética y el alimento. Además, resolvieron ecuaciones de balance de energía y de masa, con las cuales formaron ecuaciones diferenciales parciales no lineales. Estosautoresutilizaronlosdatosreportadosen laliteraturadesistemasmodelopararealizarla modelación, encontrando que en los productos pequeños, la potencia absorbida presenta un comportamientoondulatorio,elcualsepredice con más exactitud con las ecuaciones de Maxwell, mientras que para productos grandes (espesor mayor a 4 cm) el comportamiento es predicho con más exactitud por la ley de Lambert.
4.1. Calentamiento con radiofrecuencia
La simulación del calentamiento con RF utilizando herramientas de cómputo puede realizarseendoscategorías.Laprimerasimula la transferencia de calor dentro del producto que se encuentra entre los electrodos y se enfoca principalmente en la descripción de fenómenos de transporte dentro del alimento. La segunda categoría simula al calentamiento por RF en términos de sus campos magnéticos y eléctricos (Marra et al., 2009). En la simulación del calentamiento con RF se usan principalmente las ecuaciones de Maxwell en su forma diferencial, las cuales incluyen a las ecuaciones de las leyes de Faraday, Ampere y Gauss para campos eléctricos y la
correspondiente a la leyde Gauss para campos magnéticos (Marra et al., 2009). En conjunto con las anteriores también se han utilizado las ecuaciones de Navier-Stokes (Birla et al., 2008) y la de onda (Chow Ting Chang et al., 2004). Entre los programas de cómputo que se han utilizados para modelar el calentamiento por ondas de RF, de sistemas modelo, se encuentran: HFSS®, FEMLAB®, ANSYS® y CST Microwave Studio (Chow Ting Chang et al.,2004;Birla et al.,2008).
La medición de la temperatura, en los trabajos que han modelado el calentamiento con ondas de RF, se ha realizado con fibras ópticas, termopares y con cámara térmica infrarroja (Chow Ting Chang et al., 2004; Wang et al., 2008; Birla et al., 2008). Con las temperaturas obtenidas experimentalmente se realizan patrones de calentamiento; éstos pueden ser comparados con los perfiles de temperatura simulados (Chow Ting Chang et al.,2004),osirvenparaevaluarlauniformidad del calentamiento en el objeto analizado (Wang et al.,2008;Birla et al.,2008).
Chow Ting Chang et al. (2004) realizaron la modelación de un sistema de calentamiento con RF a nivel industrial, calentando soluciones de carboximetilcelulosa (CMC) al 1%, colocadas en contenedores de plástico en diferentes posiciones dentro del equipo; aunque este modelo de simulación no predijo exactamente las temperaturas, sí predijo los patrones de calentamiento en las soluciones de CMC.
Birla et al. (2008) modelaron el calentamiento con RF de frutas modelo (esféricas) sumergidas en agua, elaboradas con gel de gelano (1%). Encontraron que las frutas modelo sumergidas tuvieron un patrón de calentamiento más uniforme al compararlas con frutas modelo rodeadas de aire sometidas a calentamiento con RF; sin embargo, se presentaronpuntosmáscalientesenposiciones horizontales. Por lo que este estudio sugiere
que el movimiento yla rotación de los objetos esféricos podría ser una solución para mejorar launiformidaddelcalentamientoporRF.
Wang et al. (2008) evaluaron la uniformidad del calentamiento por RF en agua y en soluciones de carboximetilcelulosa (CMC) al 1%, las cuales fueron colocadas en dos tipos de charolas, una con contenedores pequeños y una lisa. Estos investigadores encontraronqueel áreamáscalientefuelaque estaba más cerca del centro del electrodo. Además, el gradiente de temperatura para las soluciones de CMC fue mayor que para el agua, por lo que estos autores concluyen que los materiales con un ε ´´ bajo se calientan más uniformemente que los materiales con un ε ´´ alto.
La geometría de los sistemas modelo alimenticios también ha sido abordada. Marra et al. (2007); Birla et al. (2008) y Romano y Marra (2008) han reportado que durante el calentamiento con RF hay una gran influencia de la geometría: los cubos mostraron calentamiento más uniforme, mientras que los cilindros deben ser colocados en posición vertical respecto a los electrodos para mejorar la uniformidad. Chow Ting Chang et al (2004) mencionan que la geometría, el tamaño y la posición de las muestras afectan los patrones de calentamiento, obteniéndose una mejor uniformidad al colocarlas verticalmente enelcentrodeloselectrodos.
Ladistribucióndetemperaturasescompleja yse requierenmásestudiosqueidentifiquenel efecto de la geometría, el tamaño y la composición sobre la misma, al someter un productoaMOuondasdeRF.
Conclusiones y comentarios finales
Es de suma importancia conocer las propiedades dieléctricas, físicas y térmicas de
los diferentes sistemas modelo para que la modelación del calentamiento dieléctrico sea más precisa. Entre los materiales que se han utilizado para la modelación del calentamiento dieléctrico están agar, gelano, carboximetilcelulosa y proteína de suero; sin embargo hay poca información sobre sus propiedadesdieléctricas,térmicasyfísicas.
La modelación matemática ayuda a entender el calentamiento con MO y ondas de RF en alimentos y es necesario continuar desarrollándola. Además, la modelación del calentamiento dieléctrico en sistemas modelo alimenticios ha propuesto diferentes soluciones para mejorar la uniformidad de la temperatura dentro del material tratado con MO u ondas de RF. Con los avances tecnológicos de los últimos años, además de la computadora, también se pueden incluir en los estudios de modelación instrumentos como la cámara infrarroja para obtener los perfiles de temperaturaporelanálisisdeimágenes.
Respectoa la modelacióndel calentamiento por MO, ésta se ha centrado en describir perfiles de temperatura y la falta de uniformidad de este tipo de calentamiento. Involucra la absorción de la energía de MO y la distribución de la temperatura dentro del producto. Depende de los ciclos de operación, y de la geometría, tamaño y propiedades del material. Además, la modelación del calentamientoporMOhasidomásinvestigada ensistemasmodelosólidosqueen líquidos.
Se sugiere que en futuras investigaciones sobre la modelación del calentamiento dieléctrico en sistemas modelo no sólo se evalúen los perfiles de temperatura, sino también se analice la presencia de factores como microorganismos patógenos o deteriorativos, insectos, nutrientes, entre otros, con el fin de saber cuál es el efecto del calentamientodieléctricoenellos.
Agradecimientos
LosautoresagradecenalCONACYT(Consejo Nacional de Ciencia y Tecnología) y a la UDLAP (Universidad de las Américas Puebla) por las becas otorgadas a N. Soto Reyes para realizarsusestudiosdeDoctoradoenCiencias, así como al CONACYT por el proyecto 168990.
Referencias
Barringer, S.A., Davis, E.A., Gordon, J., Ayappa, K.G. y Davis, H.T. 1995. Microwave-heating temperature profiles for thin slabs compared to Maxwell y Lambert law predictions. Journal of Food Science. 60 (5): 1137-1142.
Birla, S.L., Wang, S., Tang, J. y Hallman, G. 2004. Improving heat uniformity of fresh fruit in radio frequency treatments for pest control. Postharvest Biology and Technology. 33: 205-217.
Birla, S.L. Wang, S. y Tang, J. 2008. Computer simulation of radio frequency heating of model fruit immersed in water. Journal of Food Engineering. 84: 270-280.
Campañone, L.A., Paola, C.A. y Mascheroni, R.H. 2012. Modeling and simulation of microwave heating of foods under different process schedules. Food and Bioprocess Technology. 5: 738-749.
Chow Ting Chang, T.V., Tang, J. y Younce, F. 2004. 3-Dimensional numerical modeling of an industrial radio frequency heating system using finite elements. Journal of Microwave Power & Electromagnetic energy. 39(2): 87-105.
Hossan, M.R., Byun, D.Y. y Dutta, P. 2010. Analysis of microwave heating for cylindrical shaped objects. International Journal of Heat and Mass Transfer. 53: 5129-5138.
Marra, F., Lyng, J., Romano, V. y McKenna, B. 2007. Radiofrequency heating of foodstuff: Solution and validation of a mathematical model. Journal of Food Engineering. 79(3): 998–1006.
Marra, F., Zhang, L. y Lyng, J. 2009. Radio frequency treatment of foods: Review of recent advances. Journal of Food Engineering. 91: 497-508.
Romano, V. y Marra, F. 2008. A numerical analysis of radio frequency heating of regular shaped foodstuff. Journal of Food Engineering. 84: 449–457.
Ramaswamy, H. y Tang, J. 2008. Microwave and radio frequency heating. Food Science and Technology International. 14 (5): 423-427.
Sakai, N., Mao, W., Koshima, Y. y Watanabe, M. 2005
A method for developing model food system in
microwave heating studies. Journal of Food Engineering. 66: 525-531.
Salazar-González, C., San Martín-González, M.F., López-Malo, A. y Sosa-Morales, M.E. 2012. Recent studies related to microwave processing of fluid foods. Food and Bioprocess Tehcnology. 5: 31-46.
Sosa-Morales, M.E., Tiwari, G., Wang, S., Tang, J., García, H.S. y López-Malo, A. 2009. Dielectric heating as potential post-harvest treatment of disinfesting mangoes, part II: development of RFbased protocols and quality evaluation of treated fruits. Biosystems Engineering. 103: 287-296.
Sosa-Morales, M.E., Valerio-Junco, L., López-Malo, A. y García, H.S. 2010. Review: Dielectric properties of foods: reported data in the 21st century and their potential applications. Food Science and Technology. 43: 1169-1179.
Swain, M.V.L., Russell, S.L., Clarke, R.N. y Swain, M.J. 2004. The development of food simulants for microwave oven testing. International Journal of Food Science and Technology. 39: 623-630.
USDA. United States Food and Drug Administration. 2000. Kinetics of microbial inactivation for alternative food processing technologies. Microwave and radio frequency processing. Disponible en: http://vm.cfsan.fda.gov/~comm/ift-micr.html. Consultado el 07 de Noviembre de 2011.
Vandivambal, R. y Jayas, D.S. 2010. Non-uniform temperature distribution during microwave heating of food materials- A review. Food and Bioprocess Technology. 3: 161-171.
Venkatesh, M.S. y Raghavan, G.S.V. 2004. An overview of microwave processing and dielectric properties of agri-food materials. Biosystems Engineering. 88 (1): 1-18.
Villa-Rojas, R., López-Malo, A. y Sosa-Morales, M.E. 2011. Hot water bath treatments assisted by
microwave energy to delay postharvest ripening and decay in strawberries (Fragaria x ananassa). Journal of the Science of Food and Agriculture. 91: 2265-2270.
Wang, S., Tang, J. y Cavalieri R.P. 2001. Modelling fruit heating rates for hot air and hot water treatments. Postharvest Biology and Technology. 22: 257-270.
Wang, S., Tang, J., Cavalieri, R.P. y Davis, D.C. 2003a. Differential heating of insects in dried nuts and fruit associated with radio frequency and microwave treatments. Transaction of the ASAE. 46(4): 11751182.
Wang, Y., Wig, T.D., Tang, J. y Hallberg, L.M. 2003 b. Dielectric properties of foods relevant to RF and microwave pasteurization and sterilization. Journal of Food Engineering. 57: 257-268.
Wang, S., Monzon, M., Gazit, Y., Tang, J., Mitcham, E.J. y Amstrong, J.W. 2005. Temperature-dependent dielectric properties of selected subtropical and tropical fruits and associated insects pests. Transaction of the ASAE. 48(5): 1-9.
Wang, S., Luechapattanaporn, K. y Tang, J. 2008. Experimental methods for evaluating heating uniformity in radio frequency systems. Biosystems Engineering. 100: 58-65.
Yang, H.W. y Gunasekaran, S. 2001. Temperature profiles in cylindrical model food during pulsed microwave heating. Journal of Food Science. 66 (7): 998-1004.
Yang, H.W. y Gunasekaran, S. 2004. Comparison of temperature distribution in model food cylinders based on Maxwell’s equations and Lambert’s law during pulsed microwave heating. Journal of Food Engineering. 64: 445-453.

Temas Selectos de Ingeniería de Alimentos 6 - 2 (2012): 32 - 46

Películas comestibles de proteína: características, propiedades y aplicaciones
C. Montalvo*, A. López-Malo y E. Palou.
Departamento de Ingeniería Química, Alimentos y Ambiental, Universidad de las Américas Puebla. Ex hacienda Sta. Catarina Mártir S/N, San Andrés Cholula, Puebla. C.P.72810. México.
Resumen
Las películas comestibles se utilizan para alargar la vida útil de los alimentos actuando como barrera selectiva contra los gases y la humedad. Las películas elaboradas con proteína presentan buenas propiedades mecánicas y de barrera, debido a que las proteínas tienen una estructura única que les confieren un amplio espectro de propiedades, que están influenciadas por su estructura heterogénea, sensibilidad térmica y características hidrofílicas. Las interacciones poliméricas que se presentan en la proteína generan películas con una red proteica rígida, menos flexibles y menos permeables a los gases y vapores que otras películas. Estas propiedades pueden ser mejoradas aplicando métodos químicos, físicos o adicionando materiales hidrofóbicos u otros polímeros. En esta revisión se hace una descripción de las proteínas que se utilizan como materia prima para la elaboración de películas comestibles, de las propiedades que presentan y de cómo pueden ser mejoradas estas propiedades para ser aplicadas en alimentos.
Palabras clave: películas comestibles, proteínas, biopolímeros.
Abstract
Edible films can extend the shelf life of foods acting as selective barrier against gases and moisture. Protein edible films have good mechanical and barriers properties, because proteins have a unique structure which confers a wider range of properties, which are highly dependent on structural heterogeneity, thermal sensitivity, and hydrophilic characteristics. The polymer interactions result in films with strong network, but less flexible and less permeable to gases and vapors. These properties could be improved applying chemical or physical methods, or combining proteins with hydrophobic material or some polymers. This review shows a description of proteins that could be used like raw matter to make edible films, their properties and how it could be enhanced to be applied on foods.
Keywords: edible films, proteins, biopolymers.
Introducción
Las películas comestibles se definen como una capa delgada de polímero que puede ser consumida y empleada en la superficie de un alimento, que puede aplicarse como capas continuas entre los diferentes componentes o utilizarse como cubierta durante su elaboración (Kowalczyc y Baraniak, 2011).
*Programa de Doctorado en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: claudia.montalvopi@udlap.mx
Las películas comestibles se pueden formar a partir de biopolímeros que tengan la propiedad de formar películas como los polisacáridos, proteínas y lípidos, los cuales deberán ser
previamente dispersos y disueltos en un disolvente, generalmente agua, para posteriormente ser vertidas y secadas a la temperatura deseada para obtener el material de empaque. Actualmente se están desarrollandonuevastecnologíasenmateriales de empaque como una respuesta a las tendencias de comercialización global que permitan una mayor distribución de alimentos. Debidoa ello,se ha incrementado el interés en las películas comestibles para que cumplan con algunos requerimientos que apoyen en el control delascausasdedeteriorodel alimento, sin olvidar que estas necesidades dependerán de la naturaleza del alimento en el que se vayan a aplicar. Algunos requerimientos deseables en las películas son el control en la permeabilidad al vapor de agua y solutos, permeabilidad selectiva a gases y compuestos volátiles y control en la pérdida o intercambio desaborenlosalimentos,entreotros.
Aunque las películas comestibles elaboradas con biopolímeros presentan en general buenas propiedades de barrera al oxígeno, se considera que las películas de proteína son las más efectivas en este sentido. Esto debido a la estructura compleja que se forma como resultado de la interacción de los monómeros que pueden estar presentes en la matriz, los cuales, dependiendo de su naturaleza (hidrofóbica o hidrofílica), tendrán un efecto en las propiedades de la película comestible. Otros factores que pueden influir en las propiedades que presentan este tipo de películas son el valor de pH de la solución de proteína, el uso de plastificantes, las condiciones de formación y las sustancias incorporadas a la solución formadora de la película. Varios tipos de proteínas han sido utilizadas para la formación de películas comestibles, entre ellas se encuentran gelatina, caseína, proteína de suero, gluten de trigo y proteínas de soya, por mencionar algunas, todas ellas con propiedades funcionales particulares principalmente por el origen diversodelamatrizproteicautilizada.
El enfoque de este trabajo es conocer las diferentes fuentes de proteína que pueden ser utilizadas como materia prima en la elaboración de películas comestibles, hacer unarevisiónacercadelosmétodosquepueden utilizarse para su fabricación y de las propiedades funcionales que presentan, así como de algunas variantes que se utilizan durante su proceso de elaboración (plastificantes, aditivos, condiciones térmicas, etc.) con el fin de mejorar dichas propiedades. Además se incluye una sección acerca de las aplicaciones de este tipo de películas al ser utilizadas como recubrimientos en alimentos dediferentenaturaleza.
Revisión bibliográfica
1. Películas de proteína
La película comestible es una matriz preformada, delgada que se aplica directamente al alimento, que puede ser utilizada en forma de recubrimiento o que formará parte de la composición del alimento. Los polímeros naturales como las proteínas, ofrecen una gran oportunidad para ser utilizados como materia prima en la elaboración de películas comestibles debido a su biodegradabilidad y a que pueden suplementarelvalornutritivodelosalimentos. Por otro lado, le confieren al polímero un amplio rango de propiedades debido al potencial que tienen para formar enlaces intermoleculares(Bourtoom,2009).
Las proteínas pueden adquirir diversas conformaciones: estructura primaria, dependiendo de la secuencia de aminoácidos presentes; estructura secundaria, basada en atracciones electrostáticas, fuerzas de van der Waals, puentes de hidrógeno y enlaces disulfuro a lo largo de la cadena polimérica; estructura terciaria, que se refiere a cómo se pliega la estructura secundaria sobre sí misma y que utiliza los mismos tipos de enlaces y fuerzas de atracción antes mencionadas
(Damodaran, 1997). Con base en este tipo de estructura, se forman proteínas de tipo fibroso, que están asociadas estrechamente unas con otras en estructuras paralelas, y de tipo globular, enrolladas sobre sí mismas en estructurasesféricas(Badui,2006).Finalmente también se pueden formar estructuras cuaternarias donde una unidad proteica interacciona con otra para formar una estructura única que puede tener funcionalidad biológica, característica que es utilizada por las células para formar órganos y tejidos (Damodaran, 1997). Gracias a las diferentes conformaciones que pueden presentar las proteínas, es que se pueden formar películas con alto grado de cohesividad, que son estabilizadas cuando se forman nuevos enlaces ointeracciones.
Dentro de las proteínas fibrosas, el colágeno ha recibido una gran atención en la producción de películas comestibles (Villada et al.,2007);sinembargo,proteínasglobulares como el gluten de trigo, la zeína de maíz, la proteína de soya y la proteína de suero de leche, también están siendo investigadas para laformacióndepelículas(Rakotonirainy et al., 2001; Tanada-Palmu y Grosso, 2003; Bourtoom, 2008a). Adicionalmente se puede clasificar a las proteínas que se han utilizado para la elaboración de películas, en proteínas deorigenvegetal ydeorigenanimal.
1.1 Películas de proteínas de origen vegetal
Las frutas y vegetales generalmente tienen un bajo contenido de proteína, siendo los polisacáridoselcomponentemayoritariodelas mismas y que han sido utilizados como materia prima para la elaboración de películas y cubiertas comestibles. Por otro lado, los cereales y las leguminosas tienen un mayor contenido de proteínas en su composición (815% y 17-45%, respectivamente), siendo aisladas y estudiadas para la formación de películas comestibles (Olvera-Novoa y Olivera-Castillo,2000).
Las películas obtenidas de zeína (proteína mayoritaria del maíz) y de gluten de trigo, se obtienen por el secado de dispersiones alcohólicas utilizadas para solubilizar a la proteína, ya que debido a la gran cantidad de aminoácidos no polares que poseen (46% y 39%, respectivamente) son prácticamente insolubles en agua. Este tipo de proteínas forman películas con propiedades similares: brillantes, impermeables a la grasa, con bajos niveles de permeabilidad al O2 y CO2, y baja permeabilidad al vapor de agua en comparación con otras películas de proteína (Ghanbarzadeh et al., 2007). En el caso de leguminosas, investigadores como Rhim et al. (1999, 2000, 2002) y Cho et al. (2007) han estudiado el potencial de la proteína de soya para la formación de películas comestibles. Generalmente se utilizan aislados de proteína de soya, con más del 90% de proteína, obtenidos por extracciones ácidas y alcalinas, que posteriormente se solubilizan en soluciones acuosas alcalinas para formar las películas cuando se elimina el disolvente por secado (Rhim et al., 2000). Las películas de proteína de soya requieren de la adición de plastificantesparadarles textura yflexibilidad, siendo el glicerol y el sorbitol los más usados (Rhim et al., 2002; Kim et al., 2003). Sin embargo otras leguminosas que también se están usando para la obtención de películas comestibles son el frijol verde, haba, chícharo y garbanzo, aunque la información acerca de ellas todavía es limitada (Bourtoom, 2008b; Saremnezhad et al., 2011; Adebiyi y Aluko, 2011;KowalczykyBaraniak,2011).
1.2 Películas de proteínas de origen animal
Las proteínas derivadas de la leche, como las del suero y caseína, se han estudiado ampliamentedebidoasualtovalornutricional. La caseína se utiliza para obtener películas a partir de soluciones acuosas debido a su habilidad para formar enlaces intermoleculares (hidrógeno,electrostáticosehidrofóbicos),que incrementan la cohesión del polímero (Atarés
et al., 2010). Sin embargo, se prefiere utilizar caseinatos de sodio o potasio, debido a que se mejora su solubilidad en agua y se obtienen películasconmejorespropiedadesfuncionales: no presentan olor ni sabor, tienen buena flexibilidad y son transparentes, características que también se pueden encontrar en las películas obtenidas a partir de proteínas del suero(YooyKrochta,2011).Lasproteínasdel suero de leche están formadas por diferentes proteínas individuales globulares y termolábiles, constituidas principalmente por β-lactoglubulina, las películas comestibles a las que dan origen se caracterizan por presentar buenas propiedades de barrera al oxígeno, a los lípidos y a los aromas (Regalado et al.,2006).
Otra proteína de origen animal es el colágeno, se clasifica como fibrosa y está presente en piel y tejido conectivo, tiene puentes intra e intermoleculares debido a la formación de enlaces covalentes (ester, amida y enlaces peptídicos) que se forman en la matriz polimérica, aunque los enlaces disulfuro también juegan un rol importante en la estructura; sin embargo, estos no son muy numerosos debido al bajo contenido de cisteína presente en este tipo de proteína (Xiong, 1997). Las películas obtenidas a partir de este material se han usado para embutidos, ya que presentan una buena barrera a los gases y buenas propiedades mecánicas (Lacroix y Cooksey, 2005). Con la hidrólisis parcial del colágeno, llevada a cabo en condiciones alcalinas y temperaturas de 60 °C, se obtiene la gelatina, que también puede ser utilizada para obtener películas comestibles (Hoque et al., 2011). Este tipo de películas se caracterizan por ser claras, flexibles e impermeables al oxígeno; sin embargo, son muy hidrofílicas por lo tanto, no presentan buena permeabilidad al vapor de agua (Bourtoom,2008a).
Las proteínas miofribrilares (formadas por actina y miosina) se encuentran en el músculo
de mamíferos y peces, siendo estos últimos la principal fuente de proteína para la obtención de películas. Las películas que se obtienen generalmente presentan elevada permeabilidad al vaporde agua ynomuybuenaspropiedades mecánicas, por lo cual se deben someter a un proceso de desnaturalización proteica previo a la formación de la película comestible (Limpan et al., 2010).
2. Formación de películas de proteína
La formación de una red macromolecular de proteína requiere de tres pasos: 1) ruptura de enlaces intermoleculares de baja energía que estabilicen a los polímeros en el estado nativo, 2) arreglo y orientación de las cadenas poliméricas, y 3) formación de una red tridimensional que se estabilice por la formación de nuevos enlaces (Cuq et al., 1998).
La probabilidad de formar enlaces intermoleculares depende de la forma de la proteína y de las condiciones utilizadas durante el proceso de elaboración (Tian et al., 2011). Generalmente, las proteínas globulares deben ser desnaturalizadas por calentamiento, empleo de medios acuosos ácidos o básicos, o por solventes, con la intención de formar estructuras más extendidas que son requeridas para la formación de películas. Una vez extendida, las cadenas de proteínas pueden asociarse por uniones de hidrógeno, iónicas, hidrofóbicas y enlaces covalentes. La interacción entre cadenas produce una película cohesiva que es afectada por el grado de extensión de la cadena (estructura de la proteína), así como por la naturaleza y secuencia de los residuos de aminoácidos. La distribución uniforme de grupos polares, hidrofóbicos, y/o grupos tioles a lo largo del polímero incrementa la probabilidad de las interacciones(Krochta,1997).
Hay dos tecnologías que se utilizan comúnmente para preparar películas: el
proceso húmedo y el proceso seco (Fig.1). Para la formación de películas de proteína puede utilizarse cualquiera de los dos procesos, a nivel de investigación se utiliza más el método húmedo por su efectividad y bajo costo, aunque el método seco es más rápidoypuederequerirmenosenergía.
El proceso húmedo se basa en la dispersión osolubilizacióndelasproteínasenunsolvente y su posterior eliminación para dar lugar a la formación de la película (Guerrero et al., 2010). Algunas proteínas presentan poca solubilidad en agua debido al bajo contenido de aminoácidos polares ionizables que contienen, como en el caso de la zeína y kafirina(proteínadelsorgo);sinembargo,esto favorece la formación de películas en un ampliorangodepH(4.4-9.4)(Romero-Bastida et al., 2004; Ghanbarzadeh et al., 2007). En contraste, las películas de soya tienen una elevada cantidad de aminoácidos polares (25%), lo que limita la formación de la
Proceso Húmedo
Estructura
Condiciones de dispersión
Solución formadora de película
Condiciones de extensión
Película o cubierta
– 2 (2012): 32 - 46
película a valores de pH ligeramente ácidos; las condiciones recomendables, para promover reaccionesdeintercambiodepuentesdisulfuro quefavorezcanlaformacióndelapelícula,son valores de pH entre 7 y 10 y temperaturas mayores a 70 °C (Cuq et al., 1998; Rhim et al., 2000). La selección del solvente es uno de los factores más importantes, sobre todo para la formación de películas comestibles, donde agua, alcohol, ácido acético (en algunos casos) y sus mezclas son los solventes apropiados para este fin (Taylor et al., 2005). También puede ser necesaria la adición de agentes dispersantes (mercaptoetanol o sulfito de sodio, entre otros) para solubilizar la proteína yelajustedepHmediantelaadicióndeácidos (láctico, clorhídrico o acético) o bases (amonio, hidróxido de sodio o potasio) (Rhim et al., 2000; Rhim et al., 2002; Taylor et al., 2005; Byaruhanga et al., 2007). Todos los componentes deben ser disueltos para producir la solución formadora de película que podrá ser aplicada a superficies planas ya sea por
Proceso Seco
Proteínas
Estructura
Temperatura de fusión y de transición vitrea
Polvo o pellets
Condiciones de moldeado
Película o bioempaque
Propiedades funcionales de películas o bioempaques
Fig. 1. Representación esquemática de los dos procesos tecnológicos utilizados para obtener películas comestibles de proteína (Adaptada de Cuq etal., 1998).
vertido, rociado o paso por rodillos, y posteriormente ser sometida a condiciones controladas de temperatura y/o de humedad relativa para eliminar el solvente y formar la película comestible (Han y Gennadios, 2005; Ghanbarzadeh et al., 2007). Las condiciones de secado que se utilizan (temperatura del ambiente, luz UV, energía infrarroja o de microondas) pueden tener efecto en las propiedades físicas de la película formada, incluyendo morfología, apariencia y propiedades mecánicas y de barrera (Jangchud y Chinnan, 1999a; Rhim et al., 2000; Byaruhanga et al.,2007;Denavi et al.,2009).
El proceso seco se basa en las propiedades termoplásticasdelaproteínaencondicionesde humedad bajas, donde generalmente se realiza un prensado térmico o moldeado por compresión del polímero. Se deben alcanzar temperaturas por arriba del punto de fusión y de la transición vítrea de la proteína, para ello se puede utilizar una prensa hidráulica con placas previamente calentadas a temperaturas que pueden ir de 100 a 150 °C, como en el caso de las películas elaboradas con proteína de soya o gelatina (Guerrero et al., 2010; Krishna et al., 2012). Cuando se alcanza el punto de fusión en un polímero, su fracción cristalina se transforma en un líquido con estructura desordenada; mientras que en la transición vítrea se caracteriza por cambios en su fracción amorfa, pasando de un estado vítreo estable a un estado desordenado y gomoso donde el material se transforma en blando y flexible (Cuq et al., 1998). Estos cambios en las propiedades termoplásticas permiten que la matriz polimérica forme una película cohesiva (Byaruhanga et al., 2007). La cohesión del material es una propiedad muy importante, ya que puede tener efecto en las propiedades mecánicas del material final, y se define como la fuerza atractiva entre las moléculas de la misma sustancia (Han y Gennadios, 2005). Finalmente, las películas comestibles de proteína obtenidas se pueden
moldear por extrusión o compresión (Guerrero et al.,2010;Krishna et al.,2012).
3. Propiedades de las películas de proteína
Las conformaciones secundaria, terciaria y cuaternaria de las proteínas pueden ser modificadas por varios agentes físicos (temperatura, tratamientos mecánicos y presión) o químicos (adición de lípidos, ácidos o álcalis) (Tian et al., 2012). Estos agentes se utilizan generalmente en la formación de películas de proteína para optimizar la interacción entre aminoácidos y favorecer la formacióndepolímerosconmayorestabilidad.
3.1. Propiedades de barrera
La aplicación de las películas comestibles se debe en gran medida a las propiedades de barrera a gases y/o vapores que presenten, ya que éstas pueden influir en diferentes procesos que pueden ocurrir en los alimentos (oxidación, cambios de textura por pérdida o ganancia de humedad, pérdida de aromas, entreotros), yporlotantoincidirensucalidad final.
En las películas comestibles, durante el transporte de gas y/o vapor pueden ocurrir dos mecanismos: difusión capilar y difusión activa.Elprimeroocurreenmaterialesqueson porosos o que presentan imperfecciones, y la difusión activa incluye la solubilización del gas en la película, difusión a través del material y finalmente su difusión hacia el otro ladodelapelícula(Cayot et al.,2008).
El carácter polar de las proteínas determina las propiedades de barrera de las películas comestibles. En general la mayoría de los grupos hidrofílicos libres favorecen la sorción y transferencia de vapor de agua a través de la película, en comparación con la transferencia de gases (de naturaleza hidrofóbica), para los cuales será más difícil este mecanismo (Cuq et
al., 1998). Adicionalmente, la permeabilidad de los gases aumenta en relación a la fracción amorfa que se presenta en la estructura proteica, ya que se refiere a cadenas poliméricas con grupos laterales voluminosos mal empacados que favorecen la movilidad de lasmoléculas(McHughyKrochta,1994).Este tipo de permeabilidad también se ve afectada por las condiciones de humedad relativa en el ambiente, los valores elevados de humedad incrementan la permeabilidad de la película (Fabra et al., 2012). Por lo tanto es muy importante mantener una baja humedad relativa en el sistema para maximizar la efectividad de la película como barrera para gases.
En este sentido Bamdad et al. (2006) observaron que, la permeabilidad de películas de proteína de lenteja es mayor (0.30 ng / m s Pa) que la permeabilidad que presentan las películas de zeína (0.116 ng / m s Pa), presumiblemente por la diferencia en la cantidad de aminoácidos hidrofóbicos presentes, ya que para el caso de lenteja estos representan el 13.6% del peso total de la proteína, mientras que en la zeína corresponden al 35 %. Por otro lado, Limpan et al. (2010) reportaron que, en películas de proteína miofibrilares de pescado y alcohol polivinílico, la permeabilidad al vapor de agua aumenta al presentarse un mayor contenido de grupos hidroxilo libres (por incremento en la cantidad del alcohol polivinílico de hasta un 40 %), lo que favorece las características hidrofílicas del polímero, pero limita sus propiedades de barrera. En el caso de permeabilidad a los gases, se observó que en películas de caseinato, sometidas a diferentes humedades relativas (33%, 53% y 90%), se presentó una mayor permeabilidad a valores altosdehumedadrelativa.Estodebidoaquela interacción de las moléculas de agua con los grupos polares del polímero reduce las interacciones intramoleculares entre las proteínas que, aunado a la ruptura de puentes de hidrógeno, aumenta el espacio
intermolecular yfavorecelamovilidaddeO2 y CO2 ((Fabra et al.,2012).
3.2. Propiedades mecánicas
Las propiedades mecánicas permiten predecir la durabilidad de la película comestible y en un momento dado la integridaddel alimento. La interacción entre la proteína y pequeñas moléculas, como agua, plastificantes, lípidos y otros agentes dispersantes, tienen efecto en las propiedades mecánicas de la película comestible (Regalado et al., 2006).
La fuerza de tensión y porcentaje de elongación son dos de las mediciones más comunes utilizadas para evaluar las propiedades mecánicas de películas comestibles. La fuerza de tensión se refiere al máximo estrés desarrollado en una película al someterse a una prueba de tensión, mientras el valor de elongación representa la habilidad de estirarse (Guarda y Galotto, 2001). La magnitud de estas dos propiedades está estrechamente asociada con la cantidad de plastificante presente en la película. Generalmente un incremento en la cantidad de plastificante da como resultado películas con menor fuerza de tensión y una mayor elongación, efecto observado en películas de proteína de chícharo (Choi y Han, 2001), gelatina de pescado (Andreuccetti et al., 2009; Krishna et al.,2012)ydeproteínadeharinade triticale (híbrido de trigo y centeno) (Aguirre et al., 2011), donde las cantidades de glicerol varíande10a75gporcada100gdeaisladoo concentrado de proteína. Por otro lado, proteínas de alto peso molecular, por su estructura fibrosa, como colágeno y glutelina, generalmente favorecen la formación de películas con buenas propiedades mecánicas; mientras que las proteínas globulares (proteína de cacahuate, suero de leche o surimi), requieren ser desnaturalizadas previo a la formación de la película, con el fin de favorecer la formación de nuevos enlaces que
den mayor estabilidad al polímero y mejorando con ello sus propiedades mecánicas (Bourtoom et al.,1994; Jangchud y Chinnan, 1999a; Pérez-Gago et al., 1999; Iwata et al., 2000;Guo et al.,2012).
3.3 Propiedades de solubilidad
Es una propiedad importante que se relaciona con el uso que podrá tener la película comestible; por ejemplo si se desea que proporcione resistencia a la humedad e integridad al alimento se preferirá que la películacomestibleseainsoluble,mientrasque una película soluble se requiere sobre todo si contiene algún ingrediente específico (PérezGago et al.,1999).
Las proteínas insolubles en agua como zeína y kafirina producirán películas que son insolubles en agua; esto debido a la presencia de glutamina, aminoácido polar sin carga, que promuevelapresenciadeenlacesdehidrógeno en la película formada (Byaruhanga et al., 2007). Las proteínas solubles en agua producirán películas de solubilidad variable, dependiendo de la proteína y de sus condiciones de formación; como en el caso de las proteínas de suero de leche (lactoalbúmina y lactoglobulina), que producen películas comestibles 100% solubles en agua, y para modificar su estructura es necesario aplicar temperaturas de 70 a 100 °C para formar nuevos enlaces que la hagan insoluble (PérezGago et al., 1999; Vachon et al., 2000). De forma similar en películas a partir de proteína de frijol, el incremento de la temperatura favorecelaformaciónde puentesdehidrógeno e interacciones hidrofóbicas disminuyendo la solubilidaddelaproteína(Tang et al.,2009).
4. Modificaciones de las propiedades de películas de proteína
Existen muchas estrategias para mejorar las propiedades de barrera, mecánicas y de solubilidad de las películas comestibles de
proteína, las cuales se basan en la modificación de la estructura de la proteína o la interacción entre sus componentes; así mismo, se han elaborado películas compuestas por la introducción en la formulación de polisacáridosocompuestoshidrofóbicos.
Durante la elaboración de la solución formadora de película se adicionan agentes plastificantes (glicerol, sorbitol, polietilenglicol o propilenglicol) que disminuyen las fuerzas intermoleculares cuando interactúan con los grupos amino y ácido de la proteína, lo que trae como consecuencia un incrementando en la movilidad de la película (Guerrero et al., 2010). Estos cambios en la organización molecular modifican la funcionalidad de las películas incrementando su flexibilidad y disminuyendo su resistencia mecánica y rigidez (Jangchud y Chinnan, 1999b). Otras propiedades que se ven claramente afectadas enlaspelículasporlaadicióndeplastificantes, son las de barrera y solubilidad. En películas comestibles de proteínas de soya (Guerrero et al., 2010), haba (Saremnezhad et al., 2011) y chícharo (Choi y Han, 2001), la elongación y solubilidad se incrementaron y la fuerza de tensión disminuyó cuando la cantidad de glicerol se incrementó hasta 60 g por cada 100 g del aislado proteico. La permeabilidad al vapor de agua en películas de hidrolizado de suero de leche (Sothornvit y Krochta, 2000) y proteína de chícharo (Choi y Han, 2001; Kowalczyk y Baraniak, 2011), aumenta proporcionalmente con la concentración de glicerol adicionado debido al carácter fuertemente hidrofílico de esta molécula. Para evitar este efecto se puede sustituir por otro plastificante como sorbitol, molécula menos hidrofílica, que en películas comestibles de proteína de soya mejoró las propiedades de permeabilidad al vapor de agua (Kim et al., 2003). En películas de proteínas de chícharo (Choi y Han, 2001; Kowalczyk y Baraniak, 2011) y calabaza (Popović et al., 2012), la adición de glicerol no afecta
significativamentelasolubilidaddelapelícula, debido probablemente a la fuerte unión que ocurreentreelplastificanteylamatriz.
Otros agentes químicos que se pueden adicionar son surfactantes, como la lecitina que al adicionarse a películas de gelatina, se observó un incremento en la fuerza de tensión y disminución en la elongación y permeabilidad al vapor de agua (Andreuccetti et al.,2011).
Otra forma en que la estructura de la matriz poliméricapuedesermodificadaescambiando las condiciones de preparación de las soluciones formadoras de película. Se ha observado que dos factores pueden tener un efecto positivo en la formación del polímero: temperaturas elevadas, mayores a 70 °C, para lograr la desnaturalización del polímero, y valores de pH alcalinos para favorecer la ionización de los grupos funcionales, que faciliten la orientación de los grupos para formar el entrecruzamiento de la estructura polimérica. En películas de proteína de cacahuate (Jangchud y Chinnan, 1999a; Liu et al., 2004), de frijol verde (Bourtoom, 2008b), de haba (Saremnezhad et al., 2011) y de chícharo (Kowalczyk y Baraniak, 2011), cuando se aplicaron las condiciones antes mencionadas, se observó una disminución en la permeabilidad al vapor de agua y al oxígeno, así como un incremento en la fuerza de tensión. Esto contrasta con lo observado en películas de suero de leche donde únicamente se mejoró la fuerza de tensión por efecto de la temperatura, no así la permeabilidad al vapor deagua(Pérez-Gago et al., 1999).
También es posible lograr un entrecruzamiento entre los componentes de la película utilizando agentes físicos como la radiación gamma, este tipo de tratamiento se aplicó en películas de proteína soya con proteína de suero y de caseinato de calcio con proteína de suero de leche, logrando una disminución en la permeabilidad al vapor de
agua y una mejora en las propiedades mecánicas (Vachon et al., 2000; Sabato et al., 2001). También la humedad relativa puede modificarlaestructurapolimérica;enpelículas de caseinato, el incremento en la humedad relativa (del 33 al 75%), favoreció la movilidad de la estructura molecular (al aumentar el espacio intermolecular y reducir las interacciones proteicas intermoleculares), que tuvo como consecuencia un aumento en la permeabilidad del O2 y CO2 (Fabra et al., 2012).
Finalmente, la formación de películas compuestas es otra opción para modificar la estructura de la proteína y mejorar sus propiedades, para este fin se han utilizado lípidos. A películas de proteína de soya se les adicionóaceitedeoliva(enunaproporcióndel 5 al 15% con respecto a los g de proteína), obteniéndose una película comestible con menor fuerza de ruptura y mayor elongación (Guerrero et al., 2011). No siempre se logra una mejora en las propiedades mecánicas; por ejemplo Zahedi et al. (2010) adicionaron ácidos grasos a películas de proteína de pistache obteniendo una matriz heterogénea débil donde la fuerza de tensión decreció; de igual forma Pires et al. (2011) elaboraron una películacompuestadeproteínademerluzacon aceitedetomillo,peronoobservaronunefecto positivo en las propiedades mecánicas porque la concentración de aceite era muy baja (0.25 mlporcadagdeproteína)encomparacióncon el glicerol adicionado (59% con respecto al peso de proteína), así que el plastificante evitó la óptima interacción entre el lípido y el polímero.
Las propiedades de permeabilidad también pueden ser modificadas, como en el caso de películasde caseinatodonde,con la adiciónde aceites esenciales de canela y jengibre, se logró una disminución en la permeabilidad al vapor de agua (Atarés et al., 2010). Otros compuestos no polares que se han adicionado a este tipo proteínas son ácido oleico, cera de
abeja y sus mezclas, observándose una disminución en la permeabilidad al vapor de agua en las películas obtenidas; en las películas con cera de abeja también se logró una disminución en la permeabilidad al O2 y CO2; sin embargo, en las películas elaboradas solamente con ácido oleico la permeabilidad a estosgasesaumentó(Fabra et al., 2012).
5. Aplicaciones de películas comestibles de proteína
Las películas comestibles ayudan a mejorar la calidad y extender la vida útil de productos alimenticios. Para aplicar exitosamente esta tecnología de empacado se debe entender el problemaquepresentael alimento yestablecer claramente la función que la película ejercerá sobre él. Por lo tanto, es necesario tomar en cuenta algunas consideraciones como: la forma en que las propiedades de la solución formadora de la película pueden afectar el producto, cómo puede cambiar la película con el tiempo, la interacción que se establecerá entreel polímero yel alimento; así comohasta quépuntolapelículasepuedeverafectadapor las condiciones de almacenamiento (Bourtoom,2008a).
Las propiedades de barrera de las películas comestibles son muy importantes, ya sea para controlar el intercambio gaseoso de alimentos frescos u oxidables o para disminuir el intercambio de humedad con la atmósfera externa (Cuq et al., 1998). El oxígeno es responsable de muchos de los procesos de degradación que ocurren en los alimentos como oxidación lipídica, crecimiento de microorganismos, oscurecimiento enzimático y pérdida de vitaminas; por lo tanto, los procesos oxidativos ocasionan la degradación de proteínas, lípidos y pigmentos disminuyendo la vida de anaquel del producto (Bonilla et al., 2012). Por otro lado, la pérdida de humedad, trae consigo la pérdida de peso
del alimento y en alimentos frescos se manifiesta en una pérdida de turgencia y aparición de senescencia (Castro et al., 2010). Los productos mínimamente procesados como frutas y hortalizas se deterioran más rápidamente debido al daño mecánico que sufren durante las operaciones de cortado y pelado, además de que se aceleran procesos metabólicos que ocasionan pérdida de textura, pardeamiento enzimático, entre otras alteraciones; ocasionando características indeseables en los productos (Avena-Bustillos et al., 1994; Shon yChoi, 2011). Las películas comestibles también han sido utilizadas como acarreadores de sustancias activas (antioxidantes, antimicrobianos, entre otros), que son liberados lentamente en el alimento y retrasan el proceso de oxidación o contaminación microbiana (Baysal et al., 2010; Amal et al.,2010).Algunosejemplosde las aplicaciones de películas comestibles de proteínassepresentanenlaTablaI.
Conclusiones y comentarios finales
Las diversas fuentes a partir de las cuales se pueden obtener las proteínas (vegetales o animales) definen el tipo y ordenamiento de aminoácidos presentes en el polímero, lo que influye de manera decisiva en las propiedades de barrera, solubilidad y mecánicas de la película comestible. Sin embargo, muchas veces no todas las propiedades que presentan las películas comestibles son ventajosas para una aplicación específica, y en este sentido la composición compleja de la estructura proteica, puede usarse a favor, ya que puede ser modificada obteniendo un polímero con propiedades funcionales diferentes al de su origen. El estudio de las diferentes variables que afectan la estructura del polímero, ofrece una gran ventaja en ciencia y tecnología, ya que permite entender cómo mejorar las
C. Montalvo et al. / Temas Selectos en
TablaI. Aplicaciones de películas comestibles de proteína.
ProteínaAditivos AplicaciónFunción
Origen Vegetal
Gluten de trigo (7.5%)
Tomates, quesoBarrera a la permeabilidad al O2 y evita obscurecimiento
Gluten de trigo (9 %)Timol (1 %)FresaBarrera a la permeabilidad al agua y antimicrobiano
Soya (5 %)Vit. E (0.5 %) , BHA
(Butilhidroxilanisol) al 0.5 %
Soya (10 %)
MantecaBarrera a la permeabilidad al agua y gases, propiedades mecánicas y antioxidante
6 – 2 (2012): 32 - 46
Condicionesde almacenamiento Referencia
14 días / 10 °CTanada-Palmu, 2000
15 días / 25 °CAmal et. al. , 2010
5 semanas / 36 °CZhang et al ., 2010
Fresa liofilizada Velocidad de rehidratación 10 min / 25 °C Huang et al. , 2011
Soya (5 %)Manzana, papas, zanahoria, Barrera a la permeabilidad al agua y evita 5 días / 25 °CShon y Choi, 2011
Zeína (16%)Ácido oleico (16%)Brócoli Barrera al vapor de agua y gases
Zeína (16%)Ácido ascórbico (2.5%) y sorbato de potasio (0.25 %)
Origen Animal
Chabacanos deshidratados
6 días / 4 °CRakotonirainy et al ., 2001
Barrera a la permeabilidad al vapor de agua, antimicrobiana y 10 meses/ 5 y 25 °C Baysal et al ., 2010
Caseína (2 %)ZanahoriaBarrera al vapor de agua y gases 2 meses/ 10 °CAvena-Bustillos et al ., 1994
Caseinato de calcio (5 %)
Gelatina (4 %)Aceite de maíz (2.5%) y aceite de oliva (5%)
Gelatina (4 %)Aceite de orégano (0.25 %)
Suero de leche (5 %)
Suero de leche (5%)Ácido ascórbico (1%), ácido cítrico (1%) y ácido oxálico (0.05%)
Suero de leche deslactosado (5 %)
Suero de leche (5 %) Palmitato de ascorbilo (0.5 %) y tocoferol (0.5%)
Papa, manzanaBarrera a la permeabilidad al O2 y evita obscurecimiento
SalchichaBarrera a la permeabilidad al agua y gases, propiedades mecánicas y antioxidantes
UchuvaBarrera a la permeabilidad al vapor de agua
Papa, manzanaBarrera a la permeabilidad al O2 y evita obscurecimiento
130 min / 20 °CTien et al ., 2001
6 días / 25 °CLiu et al., 2007
35 días / 25 °CCastro et al ., 2010
130 min / 20 °CTien et al ., 2001
ManzanaEvita obscurecimiento15 días / 3 °CLee et al ., 2003
TomateBarrera a los gases y al vapor de agua 10 días / 4 °CGalietta et al. , 2005
Cacahuate Barrera al O2 y antioxidante 16 semanas/ 25 °CHan et al ., 2008
Suero de leche (5 %) Timol (1 %)FresaBarrera a la permeabilidad al agua y antimicrobiano 15 días / 25 °CAmal et. al ., 2010
Suero de leche (5 %) Aceite de arroz (0.2, 0.4 y 0.6 %)
KiwiPropiedades mecánicas y antioxidantes 4 semanas / 4 °CHassani et al. , 2012
propiedades que presentan las películas comestibles para ser aplicadas a un grupo de alimentos en particular (frutas, hortalizas, frutos secos, cárnicos o lácteos) y alargar su vidadeanaquel.
Aunque existen diversos estudios en esta área,lagrancantidaddeproteínaspresentesen lanaturaleza,queaúnnohansidoinvestigadas en su totalidad, así como el gran número de metodologías disponibles que pueden ser
utilizadas para modificar la estructura de las proteínas, proporciona un campo vasto en esta áreadeinvestigación.
Agradecimientos
A la Universidad de las Américas Puebla y al Consejo Nacional de Ciencia y Tecnología (CONACyT, México) por el financiamiento recibidopararealizarestetrabajo.
Referencias
Adebiyi, A. P. y Aluko, R. E. 2011. Functional properties of protein fractions obtained from commercial yellow field pea (Pisum sativum L.) seed protein isolate. Food Chemistry. 128(4):902908.
Aguirre, A., Borneo, R. y León, A. E. 2011. Properties of triticale flour protein based films. Food Science and Technology. 44(9):1853-1858.
Amal, S. H., Atress, El-Mogy, M. M., Aboul-Anaen, H. E. y Alsanius, B. W. 2010. Improving strawberry fruit storability by edible coating as a carrier of thymol or calcium chloride. Journal of Horticultural Science and Ornamental Plants. 2(3):88-97.
Andreuccetti, C., Carvalho, R. A. y Grosso, C. R. F. 2009. Effect of hydrophobic plasticizers on functional properties of gelatin-based films. Food Research International. 42(8):1113-1121.
Andreuccetti, C., Carvalho, R. A., Galicia-García, T., Martínez-Bustos, F. y Grosso, C. R. 2011. Effect of surfactants on the functional properties of gelatinbased edible films. Journal of Food Engineering. 103:129-136.
Atarés, L., Bonilla, J. y Chiralt, A. 2010. Characterization of sodium caseinate-based edible films incorporated with cinnamon or ginger essential oils. Journal of Food Engineering.100:678-687.
Avena-Bustillos, R. J., Cisneros-Zevallos, L. A., Krochta, J. M. y Saltveit, M. E. 1994. Application of casein-lipid edible film emulsions to reduce white blush on minimally processed carrots. Postharvest Biology and Technology. 4:319-329.
Badui, S. 2006. Química de los Alimentos. Cuarta edición. Editorial Pearson, México. 245p.
Bamdad, F., Goli, A. H., y Kadivar, M. 2006. Preparation and characterization of proteinous film from lentil (Lens culinaris). Food Research International. 39(1): 106–111.
Baysal, T., Bilek, S. E. y Apaydın, E. 2010. The effect of corn zein edible film coating on intermediate moisture apricot (Prunus armenica L.) quality. Gida Teknolojisi Derneği. 35(4):245–249.
Bonilla, J., Atarés, L., Vargas, M. y Chiralt, A. 2012. Edible films and coatings to prevent the detrimental effect of oxygen on food quality: Possibilities and limitations. Journal of Food Engineering. 110:208213.
Bourtoom, T., Chinnan, M. S., Jantawat, P. y Sanguandeeku, R. 1994. Effect of select parameters on the properties of edible film from water-soluble fish proteins in surimi wash-water. Food Science and Technology. 39(4):406–419.
Bourtoom, T. 2008a. Edible films and coatings: characteristics and properties. International Food Research Journal. 15(3):237–248.
Bourtoom, T. 2008b. Factors affecting the properties of edible film prepared from mung bean proteins. International Food Research Journal. 15(2):167–180.
Bourtoom, T. 2009. Edible protein films: properties enhancement. International Food Research Journal 16(1):1-9.
Byaruhanga, Y. B., Erasmus, C., Emmambux, M. N. y Taylor, J. R. N. 2007. Effect of heating cast kafirin films on their functional properties. Journal of the Science of Food Agriculture. 175:167–175.
Castro, R. A., Helena, G. y González, B. 2010. Recubrimiento comestible en la conservación de uchuva (Physalis peruviana L. var. Colombia). Revista de la Asociación Colombiana de Ciencia y Tecnología de Alimentos. 91(19):16–34.
Cayot, N., Dury-Brun, C., Karbowiak, T., Savary, G. y Voilley, A. 2008. Measurement of transport phenomena of volatile compounds: A review. Food Research International. 41(4):349–362.
Cho, S. Y., Park, J.-W., Batt, H. P. y Thomas, R. L. 2007. Edible films made from membrane processed soy protein concentrates. Food Science and Technology. 40(3):418–423.
Choi, W. y Han, J. 2001. Physical and mechanical properties of pea-protein based edible films. Journal of Food Science. 66(2):319–322.
Cuq, B., Gontard, N. y Guilbert, S. 1998. Proteins as agricultural polymers for packaging production. Cereal Chemistry. 75(1):1–9.
Damodaran, S. 1997. Food proteins: an overview. En: S. Damodaran y A. Paraf (Eds). Food proteins and their applications. New York, USA. pp. 1-24.
Denavi, G., Tapia-Blácido, D. R., Añón, M. C., Sobral, P. J. A., Mauri, A. N. y Menegalli, F. C. 2009. Effects of drying conditions on some physical properties of soy protein films. Journal of Food Engineering. 90(3):341-349.
Fabra, M. J., Talens, T., Gavara, R. y Chiralt, A. 2012. Barrier properties of sodium caseinate films as affected by lipid composition and moisture content. Journal of Food Engineering. 109:372-379.
Galietta, G., Harte, F., Molinari, D., Capdevielle, R. y Diano, W. 2005. Aumento de la vida útil poscosecha de tomate usando una película de proteína de suero de leche. Revista Iberoamericana de Tecnología Postcosecha. 6(2):117–123.
Ghanbarzadeh, B., Musavi, M., Oromiehie, A. R., Rezayi, K., Razmi Rad, E. y Milani, J. 2007. Effect of plasticizing sugars on water vapor permeability, surface energy and microstructure properties of zein films. Food Science and Technology. 40(7):11911197.
Guarda, G. y Galotto, M. G. 2001. Propiedades físicas de materiales plásticos. En: J. D. Alvarado y J. M Aguilera (Eds). Métodos para medir propiedades físicas en industrias de alimentos. Acribia, Zaragoza, España. pp. 285-308.
Guerrero, P., Retegi, A., Gabilondo, N. y De la Caba, K. 2010. Mechanical and thermal properties of soy protein films processed by casting and compression. Journal of Food Engineering. 100:145-151.
Guerrero, P., Hanani, N. Z., Kerry, J. P. y De la Caba, K. 2011. Characterization of soy protein-based films prepared with acids and oils by compression. Journal of Food Engineering. 107: 41-49.
Guo, X., Lu, Y., Cui, H., Jia, X., Bai, H. y Ma, Y. 2012. Factors affecting the physical properties of edible composite film prepared from zein and wheat gluten. Molecules. 17(4):3794–3804.
Han, J. H. y Gennadios, A. 2005. Edible films and coating: a review. En: J. H. Han (Eds). Innovations in food packaging. Elsevier Academic Press, London, UK. pp. 239-276.
Han, J. H., Hwang, H.-M., Min, S. y Krochta, J. M. 2008. Coating of peanuts with edible whey protein film containing alpha-tocopherol and ascorbyl palmitate. Journal of Food Science. 73(8):349–355.
Hassani, F., Garousi, F. y Javanmard, M. 2012. Edible coating based on whey protein concentrate-rice bran oil to maintain the physical and chemical properties of the kiwifruit (Actinidia deliciosa ). Trakia Journal of Sciences. 10(1):26–34.
Hoque, M. S., Benjakul, S. y Prodpran, T. 2011. Effects of partial hydrolysis and plasticizer content on the properties of film from cuttlefish (Sepia pharaonis) skin gelatin. Food Hydrocolloids. 25(1):82–90.
Huang, L., Zhang, M., Yan, W., Mujumdar, A. S. y Sun, D. 2011. Rehydration characteristics of freezedried strawberry pieces as affected by whey protein edible coatings. International Journal of Food Science &Technology. 46(4):671–677.
Iwata, K. I., Ishizaki, S. H., Handa, A. K. y Tanaka, M. U. 2000. Preparation and characterization of edible films from fish water-soluble proteins. Fisheries Science. 66(2):372–378.
Jangchud, A. y Chinnan, M. S. 1999a. Peanut protein film as affected by drying temperature and pH of film forming solution. Journal of Food Science 64(1):153–157.
Jangchud, A. y Chinnan, M. S. 1999b. Properties of peanut protein f ilm: sorption isotherm and plasticizer effect. Food Science and Technology. 32(2):89–94.
Kim, K. M., M arx, D. B., Weller, C. L y Hanna, M. A. 2003. Influence of sorghum wax, glycerin, and sorbitol on physical properties of soy protein isolate films. Journal of the American Oil Chemists’ Society. 80(1):71–76.
Kowalczyk, D. y Baraniak, B. 2011. Effects of plasticizers, pH and heating of film-forming solution on the properties of pea protein isolate films. Journal of Food Engineering. 105:295-305.
Krishna, M., Nindo, C. I. y Min, S. C. 2012. Development of fish gelatin edible films using extrusion and compression molding. Journal of Food Engineering. 108:337-344.
Krochta, M. J. 1997. Edible protein films and coatings. En S. Damodaran y A. Paraf (Eds). Food proteins and their applications. Primera edición. New York, USA. pp. 529-550.
Lacroix, M. y Cooksey, K. 2005. Edible films and coatings from animal-origin proteins. En J. H. Han (Eds). Innovations in food packaging. Elsevier Academic Press, London, UK. pp. 301-317.
Lee, J. Y., Park, H. J., Lee, C. Y. y Choi, W. Y. 2003. Extending shelf-life of minimally processed apples with edible coatings and antibrowning agents. Food Science and Technology. 36(3):323–329.
Limpan, N., Prodpran, T., Benjakul, S. y Prasarpran, S. 2010. Properties of biodegradable blend films based on fish myofibrillar protein and polyvinyl alcohol as influenced by blen composition and pH level. Journal of Food Engineering. 105:85-92.
Liu, C.-C., Tellez-Garay, A. M. y Castell-Perez, M. E. 2004. Physical and mechanical properties of peanut protein films. Food Science and Technology. 37(7):731–738.
Liu, L., Kerry, J. F. y Kerry, J. P. 2007. Application and assessment of extruded edible casings manufactured from pectin and gelatin/sodium alginate blends for use with breakfast pork sausage. Meat Science 75(2):196–202.
McHugh, T. H. y Krochta, M. J. 1994. Permeability properties of edible films. En J. M. Krochta, E. A Baldwin y M. N. Carriedo (Eds). Edible coatings and films to improve food quality. Primera edición. Pennsylvania, USA. pp. 139-189.
Olvera-Novoa, M. y Olivera-Castillo, L. 2000. Potencialidad del uso de las leguminosas como fuente proteica en alimentos para peces. Avances en Nutrición Acuícola IV. Memorias del IV Simposium Internacional de Nutrición Acuícola. La Paz, B.C.S., México. 15-18 Noviembre. En: Civera-Cerecedo, R., Pérez-Estrada, C.J., Rieque-Marie, K. y Cruz Suárez, L. E. (Eds.).
Pérez-Gago, M. B., Nadaud, P. y Krochta, J. M. 1999 Water vapor permeability, solubility, and tensile properties of heat-denatured versus native whey protein films. Journal of Food Science. 64(6):1034–1037.
Pires., C., Ramos, C., Teixeira., G., Batista, I., Mendes, R., Nunes, L. y Marques, A. 2011. Characterization of biodegradable films prepared with hake proteins and thyme oil. Journal of Food Engineering. 105:422-428.
Popović, S., Peričin, D., Vaštag, Z., Lazić, V. y Popović, L. 2012. Pumpkin oil cake protein isolate films as potential gas barrier coating. Journal of Food Engineering. 110:374-379.
Rakotonirainy, A. M., Wang, Q. y Padua, G. W. 2001. Evaluation of zein films as modified atmosphere packaging for fresh broccoli. Food Chemistry and Toxicology. 66(8):1108–1111.
Regalado, C., Pérez-Pérez, C., Lara-Cortés, E. y GarcíaAlmendarez, B. 2006. Whey protein based edible food packaging films and coatings. En R. G. Guevara-González e I. Torres-Pacheco (Eds). Advances in Agricultural and Food Biotechnology. Research Signpost, Kerala, India. pp. 237-261.
Rhim, J. W., Wu, Y., Weller, C. L. y Schnepf, M. 1999. Physical characteristics of a composite film of soy protein isolate and propyleneglycol alginate. Journal of Food Science. 64(1):149–152.
Rhim, J. W., Gennadios, A., Handa, A., Weller, C. L. y Hanna, M. A. 2000. Solubility, tensile, and color properties of modified soy protein isolate films. Journal of Agricultural and Food Chemistry. 48(10):4937–4941.
Rhim, J. W., Gennadios, A., Weller, C. L. y Hanna, M. A. 2002. Sodium dodecyl sulfate treatment improves properties of cast films from soy protein isolate. Industrial Crops and Products. 15(3): 199–205.
Romero-Bastida, C. A., Martin-Polo, M. O., Velazquez, G. y Torres, J. A. 2004. Effect of plasticizer, pH and hydration on the mechanical and barrier properties of zein and ethylcellulose films. Ciencia y Tecnología Alimentaria. 4(4):251–256.
Sabato, S. F., Ouattara, B., Yu, H., Aprano, G. D., Tien, C. L. y Mateescu, M. A. 2001. Mechanical and barrier properties of cross-linked soy and whey protein based films. Journal of Agricultural and Food Chemistry. 49:1397-1403.
Saremnezhad, S., Azizi, M. H., Barzegar, M., Abbasi, S. y Ahmadi, E. 2011. Properties of a new edible film made of faba bean protein isolate. Journal Agriculture Science and Technology. 13:181–192.
Shon, J. y Choi, Y. 2011. Effect of edible coatings containing soy protein isolate (SPI) on the browning and moisture content of cut fruit and vegetables. Journal Appl. Biol. Chem. 54(3): 190–196.
Sothornvit, R. y Krochta, J. M. 2000. Water vapor permeability and solubility of films from hydrolyzed whey protein. Journal of food Science. 65(4):700–703.
Tanada-Palmu, P. S. y Grosso, C. R. F. 2003. Development and characterization of edible films based on gluten from semi-hard and soft Brazilian wheat flours (development of films based on gluten from wheat flours). Ciência e Tecnologia de Alimentos. 23(2):264–269.
Tang, C.-H., Xiao, M.-L., Chen, Z., Yang, X.-Q. y Yin, S.-W. 2009. Properties of cast films of vicilin-rich protein isolates from Phaseolus legumes: influence of heat curing. Food Science and Technology. 42(10):1659–1666.
Taylor, J., Taylor, J. R. N., Dutton, M. F. y Kock, S. 2005. Identification of kafirin film casting solvents. Food Chemistry. 90(3):401–408.
Tian, H., Xu G., Yang, B. y Guo, G. 2011. Microstructure and mechanical properties of soy
protein/agar blend films: effect of composition and processing methods. Journal of Food Engineering. 107: 21-26.
Tian H., Wu, W., Guo, G., Gaolun, B., Jia, Q. y Xiang, A. 2012. Microstructure and mechanical properties of glycerol plasticized soy protein plastics containing castor oil. Journal of Food Engineering. 109:496-500.
Tien, L. C., Vahchon, C., Mateescu, M. A. y Lacroix, M. 2001. Milk protein coatings prevent oxidative browning of apples and potatoes. Food Chemistry and Toxicology. 66(4): 512–516.
Vachon, C., Yu, H. L., Yefsah, R., Alain, R., St-Gelais, D. y Lacroix, M. 2000. Mechanical and structural properties of milk protein edible films cross-linked by heating and gamma-irradiation. Journal of Agricultural and Food Chemistry. 48(8): 3202–3209.
Villada, H. S., Acosta, H. A. y Velasco, R. J. 2007. Biopolímeros naturales usados en empaques biodegradables. Temas Agrarios. 12(2):5–13.
Xiong, Y. L. 1997. Structure-function relationships of muscle proteins. En S. Damodaran y A. Paraf (Eds). Food proteins and their application. New York, USA. pp. 341-392.
Yoo, S. y Krochta, M. J. 2011. Whey proteinpolysaccharide blended edible film formation and barrier, tensile, thermal and transparency properties. Journal Science of Food Agriculture. 91:2628-2636.
Zahedi, Y., Ghanbarzadeh, B. y Sedaghat, N. 2010. Physical properties of edible emulsified films based on pistachio globulin protein and fatty acids. Journal of Food Engineering. 100(1):102-108.

Temas Selectos de Ingeniería de Alimentos 6 - 2 (2012): 47 - 63

Propiedades funcionales de la jamaica (Hibiscus sabdariffa L.)
S. Cid-Ortega1,2* y J. A. Guerrero-Beltrán1
1Departamento de Ingeniería Química, Alimentos y Ambiental, Universidad de las Américas Puebla. Ex hacienda Sta. Catarina Mártir S/N, San Andrés Cholula, Puebla. C.P.72810. México.
2Programa Educativo de Ingeniería en Procesos Alimentarios. Universidad Tecnológica de Izúcar de Matamoros. Prol. Reforma N° 168 Barrio Santiago Mihuacán, Izúcar de Matamoros 74420 Puebla, México
Resumen
Continuamente se encuentran nuevas evidencias científicas que apoyan el papel de los fitoquímicos para prevenir y tratar enfermedades crónicas y degenerativas, tales como el cáncer, las enfermedades cardiovasculares y los desórdenes y alteraciones de los lípidos. A este respecto, diversos estudios han demostrado las propiedades benéficas que tienen la flor de jamaica y sus extractos. Lo anterior hace que la elaboración de productos a base de éstos, represente una gran alternativa para la industria de alimentos y bebidas, principalmente en el sector de los denominados “alimentos funcionales” y que han tenido un aumento muy importante en el mercado nacional e internacional. En este sentido, se realizó una revisión en la cual se abordan los aspectos más importantes relacionados con las propiedades funcionales de los cálices y extractos de jamaica.
Palabras clave: fitoquímicos, extractos de jamaica, alimentos funcionales.
Abstract
Continually are disclosed new scientific evidences supporting the role of phytochemicals in the preventing and treating chronic and degenerative diseases such as cancer, cardiovascular diseases, and disorders and alterations of the lipids. In this respect, several studies have shown the beneficial properties that have the hibiscus flower and its extracts. The development products based on these represents a great alternative to the food and beverage industry, mainly in the sector referred to as “functional foods”, which have a significant increase in the national and international market. This review was conducted in presenting the most important aspects related to the functional properties of the calyces and extracts of hibiscus flower.
Keywords: phytochemicals, hibiscus flower extracts, functional foods..
Introducción
*Programa de Doctorado en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: sandro.cidoa@udlap.mx
Actualmente, la ciencia de la nutrición ha pasado de los conceptos clásicos de cómo evitar las deficiencias de nutrientes y la suficiencia nutricional básica, al concepto de nutrición “positiva” u “óptima”. Las investigaciones han pasado a centrarse más en la identificación de componentes biológicamente activos en los alimentos, que ofrezcan la posibilidad de mejorar las condiciones físicas y mentales, así como de reducir el riesgo a contraer enfermedades
(EUFIC, 2006). Los alimentos que tienen uno o más de estos componentes biológicamente activos se conocen como alimentos funcionales (Hasler, 2002; Falk, 2004). Por lo anterior, la industria de alimentos se ha enfocado en el diseño de nuevos productos, que contengan fitoquímicos (compuestos propios o intencionalmente adicionados) que coadyuven a una mejor calidad de vida para los consumidores. Los alimentos funcionales pueden ser similares en apariencia a los alimentos convencionales y ser consumidos como parte de una dieta habitual. En este sentido, es importante mencionar la diferencia entre lo que es un alimento funcional y un nutracéutico; los nutracéuticos son productos elaborados a partir de alimentos, los cuales se vendenen formade cápsulas,pastillas,polvos, o soluciones que generalmente no están asociadas con el alimento y que han demostrado ventajas fisiológicas y/o proveen protección contra enfermedades crónicas (Shahidi,2004).
Por otra parte, la jamaica y los extractos de ésta, se han propuesto como ingredientes para el desarrollo de alimentos funcionales. La parte que más se aprovecha de la planta de jamaica es el cáliz o flor, en México es consumida tradicionalmente como extracto acuoso para preparar bebidas refrescantes, así como mermeladas, jaleas, licores, harinas para galletas, etc. En los últimos años ha tenido un uso potencial en el área farmacológica debido a los beneficios que produce como medicina alternativa, atribuyéndole propiedades diuréticas, antifebriles, en la disminución del colesterol y la hipertensión. Derivado de lo anterior, se han realizado investigaciones con extractos de jamaica, demostrando que sus componentes como vitaminas (E y C), ácidos polifenólicos, flavonoides y antocianinas, poseenactividadantioxidante,contribuyendoa las acciones anticancerígenas y cardioprotectivas. Bajo este contexto, el objetivo principal de esta revisión es dar a conocer los aspectos más importantes
relacionados con las propiedades funcionales deloscálicesyextractosdejamaica.
Revisión bibliográfica
1. Aspectos generales de la flor de jamaica
1.1. Cultivo
Desde el punto de vista morfológico, la jamaica es una planta arbustiva semileñosa anual o bianual que pertenece a la familia Malvaceae y alcanza entre uno y tres metros de altura. Sus tallos son abundantes, muy ramificados y de corteza roja, con hojas alternas de bordes irregularmente aserrados (Ortiz-Marquéz, 2008). En la Tabla I se presenta la clasificación taxonómica de la jamaica, se piensa que es nativa de Asia (India hasta Malasia) o África tropical y actualmente se conocen más de 500 especies de Hibiscus en el mundo. Estas plantas son frecuentes en las regiones tropicales y subtropicales, y poseen cálices de color verde o rojo (Cisse et al.,2009).
La jamaica es muy popular en algunos países del Medio-Oriente sobre todo en Egipto. En Sudán, la jamaica representa un cultivo principal de exportación sobre todo en la parte occidental donde éste ocupa el segundo lugar después del mijo perla
Tabla I. Clasificacióntaxonómica de la jamaica (Hibiscus sabdariffa L.)
ReinoPlantae
Sub-reinoTracheobionta
DivisiónAnthophyta
ClaseMagnoliopsida
OrdenMalvales
FamiliaMalvaceae
Género Hibiscus
Especie sabdariffa L.
Adaptado de Ortiz-Marquéz (2008) y Meza-Chavarría (2012)
(Pennisetum glaucum) (Mahadevan yKamboj, 2009). En América, la planta es cultivada ampliamenteenlaszonastropicalesdel Caribe yCentroamérica,comouncultivodoméstico.
A nivel internacional se distinguen seis variedades (diferenciadas por el color, forma, apariencia, peso, fruto y tamaño de la planta) destacándose: sudán, china o morada, roja (larga y corta, americana), negra gigante (nigeriana), morada gigante (tailandesa) y la no ácida (Vietnam) (Meza-Chavarría, 2012).
La mayoría de las variedades son utilizadas como plantas ornamentales a excepción del tipo sabdariffa de la cual se han identificado dos subtipos, una de ellas es Hibiscus sabdariffa variedad Altissima y la otra, Hibiscus sabdariffa variedad Sabdariffa L, la cual es una planta alta, vigorosa, poco ramificada y muy fibrosa, por lo que es cultivada principalmente para la obtención de fibras, aunque también provee cálices comestibles. En México, las principales variedades que se cultivan son: criolla (variedad roja larga, con la mayor superficie cultivada), china, jerzy y sudán (DomínguezDomínguez et al.,2007).
1.2. Producción en México
La flor de jamaica en México se agrupa en el sector de especias y plantas medicinales,
siendo un cultivo no tradicional que se desarrolla en regiones donde predomina un clima cálido-seco. La producción a nivel mundial de este cultivo la encabeza China con 27.76% de la producción, seguido por la India (17.91%), Sudán (9.1%), Uganda (8.40%), Indonesia (6.23%), Malasia (5.53%) y en séptimo lugar México con el 5.14% (SAGARPA-CONACyT,2010).
En México, la producción nacional en los últimos 5 años ha sido en promedio de 5300 ±287 toneladas. Conforme a datos de la Fundación Produce de Guerrero A. C. (2012), la principal producción de jamaica se concentra en los estados de Guerrero con 77.52%, Oaxaca con 12.61%, Michoacán con 3.60%, Nayarit con 2.68%, Puebla con 1.89% yel 1.7%restanteseproduceenlosestadosde Campeche, Colima, Jalisco y Veracruz. En el estado de Puebla, la jamaica se cultiva en la mixteca, principalmente en los municipios de Chiautla de Tapia, Ixcamilpa de Guerrero, Cohetzala, Huehuetlán el Chico, Chietla, Acatlán de Osorio y Tehuitzingo; siendo la superficiesembradaenlosúltimosdosañosde 359 hectáreas (Tabla II). En la mixteca, solamente diez municipios tienen potencial productivo, siendo Chiautla de Tapia el principal productor, teniendo un importante aumento en la producción de flor de jamaica (de 19.5 a 92 toneladas) en los últimos 5 años (TablaII).
NacionalPueblaChiautla de Tapia
Año
Superfice sembrada (Ha) Produción (ton)
Superfice sembrada (Ha) Produción (ton)
Superfice sembrada (Ha) Produción (ton)
201118620.705673.31359.00182.00184.0092.00 201019020.505469.27359.00179.32184.0092.00 200918684.504926.48390.00257.00180.0072.00 200818906.505152.96302.0061.90188.0037.60 200718830.005281.40110.0032.8078.0019.50
1Ciclo: año agrícola otoño-invierno + primavera-verano, modalidad: riego+temporal. Datos obtenidos del SIAP (2012)
Tabla II. Producción1 de jamaica a nivel nacional,estado de Puebla y municipio de Chiautla de Tapia.
1.3. Composición química
De acuerdo al color de los cálices de jamaica se pueden distinguir tres tipos: verde, rojo y rojo obscuro. Los cálices de color rojo y rojo obscuro son utilizados para la obtención de extractos con los cuales se prepara una bebida refrescante, mientras que los cálices verdes son usados para preparar sopas con vegetales (Babalola et al., 2001). La composición en los cálices de jamaica varía, principalmente, de acuerdo a la variedad, color y diferencias genéticas. En la Tabla III se presenta la composición química de los cálices de jamaica, se puede apreciar un contenido importante de proteína, fibra cruda y ácido ascórbico. Con respecto al contenido de aminoácidos(Tabla IV), loscálicesdejamaica aportan la mayoría de los aminoácidos esenciales,aexcepcióndeltriptófano.
Respecto al contenido de compuestos bioactivos (principalmente fenoles y antocianinas), éste varía de acuerdo a la variedad de la flor de jamaica, así como al método de extracción utilizado. En un estudio
Elemento
realizado por Peng-Kong et al. (2002), reportan una concentración de antocianinas totales de 2520±50 mg/100 g de flor de jamaica (expresada como delfinidina-3glucósido). Así mismo, mencionan que, de acuerdo al análisis por cromatografía de líquidos de alta resolución (HPLC), las principales antocianinas presentes en la flor de jamaica son la delfinidina-3-sambubiosido (71.4%) y la cianidina-3-sambubiosido (26.6%). Galicia-Flores et al. (2008), reportaron un contenido de antocianinas totales entre 364.98-606.67 mg/100 g de muestra seca y molida (el extracto fue obtenido utilizando metanol acidificado al 1 % con ácido trifluoracético). En este mismo trabajo, la concentración de antocianinas fue menor (entre 172.58-296.99 mg/100 g de muestra seca de cálices enteros) al utilizar agua destilada. En otro estudio realizado por Abou-Arab et al. (2011), la concentración de antocianinas totales fue de 622.91±2.0 mg/100 g de muestra seca (como cianidina-3glucósido)yuncontenidodefenolestotalesde 3742±200 mg/100 g (como ácido gálico).
Tipos de cálices
Frescos1 Rojos2 Rojo-obscuros2 Rojos3 Blancos3
Humedad (%)9.2086.5085.3011.009.30
Proteina cruda (%)1.1517.40*8.60*7.887.53
Extracto etéreo (%)2.612.10*2.90*0.160.12
Fibra cruda (%)12.008.50*9.80*13.2012.00
Cenizas (%)6.906.50*6.80*10.609.50
Carbohidratos (%)68.1565.50*71.90*57.1661.55
Ácido ascórbico (mg/100 g)6.7063.5054.8011.0015.50
Caroteno (mg/100 g)0.03----
Tiamina (mg/100 g)0.12----
Riboflavina (mg/100 g)0.28----
Niacina (mg/100 g)3.77----
Adaptado de 1Morton (1987), 2Babalola et al . (2001) y 3Suliman et al . (2011)
*En base seca
Tabla III. Composición química de la jamaica (Hibiscus sabdariffa L.).
Tabla IV. Contenidodeaminoácidos(mg/gdemateriaseca)enlaflordejamaica. AminoácidosMorton(1987) Glew et al .(1997) Ácidoaspártico16.3010.50
Ácidoglutámico7.208.85
Prolina5.605.82
Leucina5.004.21
Lisina 3.902.77
Glicina3.802.47
Valina 3.803.33
Alanina3.703.46
Arginina 3.604.48
Serina3.502.65
Isoleucina 3.002.70
Treonina 3.002.36
Tirosina2.201.44
Histidina 1.501.19
CistinaoCisteína1.300.87
Metionina1.000.65
Fenilalanina1.002.32
Así mismo la jamaica es una fuente importante de calcio, magnesio y oligoelementos (Tabla V). Estos últimos compuestos no los puede producir el ser humano, por lo que se deben obtener de fuentes externas, ya que son necesarios para vivir y preservar la salud pues, intervienen en las funciones respiratorias, digestivas, neurovegetativas y musculares, como reguladores. Los oligoelementos que en la actualidad se consideran esenciales para el hombre son: cromo (Cr), cobre (Cu), cobalto (Co), flúor (F), yodo (I), hierro (Fe), manganeso (Mn), molibdeno (Mo), selenio (Se), vanadio (V), cinc (Zn), níquel (Ni), silicio (Si), arsénico (As) y estaño (Sn) (Alarcón-Corredor,2009).
2. Productos derivados de la flor y extractos de jamaica
EnMéxico,laindustriadelajamaicahatenido un avance muy importante, en el año 2005 se inició el diseño de una planta procesadora (Integradora Agroindustrial de Chiautla de Tapia S. A. de C. V.) para el desarrollo de nuevos productos derivados de la flor de jamaica (variedad criolla): licor, mermelada, jarabe,jalea,ate, extracto ybebida refrescante. Lo anterior benefició a 158 agricultores de cinco municipios de la mixteca poblana (Martínez-Martínez et al., 2006, Cid et al., 2007).
2.1. Aplicaciones de la flor de jamaica en alimentos
Los cálices de jamaica se han utilizado en la obtención de mermeladas, jaleas y ates. En un
ElementoGlew et al . (1997) Babalola et al (2001)
Ortiz-Márquez (2008) Cid-Ortega et al (2010)
Calcio (mg/100 g)1130.001584.00122.061230.00
Fósforo (mg/100 g)163.00---
Magnesio (mg/100 g)309.00316.004403.87500.00
Potasio (mg/100 g)-2060.00-2030.00
Sodio (mg/100 g)3.835.50-10.17
Hierro (mg/100 g)6.1437.80224.718.82
Manganeso10.00--8.77
Zinc (mg/100 g)2.717.50118.571.45
estudio realizado por Ashaye y Adeleke (2009), evaluaron las características fisicoquímicas y la aceptabilidad de mermelada de jamaica utilizando dos variedades de flor de jamaica (roja y roja obscura), empleando flor fresca yseca de cada una. La mermelada elaborada a partir de flor roja obscura fresca tuvo mayor aceptación en los atributos de calidad. Por lo anterior, los autores concluyen que es mejor elaborar la mermelada a partir de flor fresca y almacenarla a bajas temperaturas, ya que además este producto y bajo estas condiciones mantuvo un contenido de ácido ascórbico significativamente mayor que las elaboradas con flor seca y/o almacenadas a temperatura ambiente.
Henry y Badrie (2007) evaluaron el efecto delaadicióndenéctardejamaicaen yogur.El néctar lo prepararon a partir de un puré de cálices, jarabe de alta fructosa, sacarosa cristalina y goma xantana (0.6%) a 2 concentraciones, 60 y 67 °Bx. El néctar lo agregaron al yogur en 2 concentraciones (para cada néctar, 60 y 67 °Bx), 27% y 33% (v/v), además adicionaron saborizante artificial de jamaica en 2 concentraciones (0.2% y 0.6% v/v);finalmente,mezclaronparaobteneryogur batido. Los autores reportan que todos los yogures elaborados con el néctar de jamaica fueron mayormente aceptados que el yogur sin
néctar, resultando el mejor el que fue adicionado con 33% de néctar con 60 °Bx y saborizante artificial al 0.6%. Cabe mencionar que los autores mencionan que tuvieron que emplear sabor artificial de jamaica debido a queelsabordelnéctarnosepercibía.
La flor de jamaica se ha usado en la elaboración de productos de panificación y repostería debido a su contenido de fibra, calcio y hierro. Almana (2001) evaluó el efectodelpolvodeflordejamaicaenpastelde chocolate para enriquecerlo con calcio, hierro y fibra cruda. El autor adicionó diferentes concentracionesdelpolvo(0,1,3,5ó7%)con respecto a la harina de trigo utilizada en la formulación y observó que altas concentraciones del polvo disminuían el volumen y la firmeza del pastel, sin embargo, pudo contrarrestar este efecto modificando el pH de la masa con bicarbonato de sodio hasta un valor ~7. De esta manera logró incorporar 5% de flor de jamaica en polvo al pastel de chocolate, con lo que aumentó 5 veces más el contenido de fibra, 4 veces más el de calcio y 2 veces más el de hierro con respecto al pastel sinpolvo.
En Turquía, se ha evaluado el uso de los cálices de jamaica como antioxidante natural en “kavurma” (producto cárnico tradicional hecho a base de carne, grasa de res y sal). Se
Tabla V. Composición (mg/100 g de materia seca) en macro y micro minerales de la jamaica (Hibiscus sabdariffa L.).
probó y comparó el poder antioxidante de los cálices de jamaica, hojas de romero y BHT (butil-hidroxi-tolueno).Lajamaica yelromero se adicionaron en una concentración de 1 g (cálices secos u hojas secas) por kilogramo de carne y 3300 mg/kg para el BHT. Los autores reportanquelaadicióndeantioxidantesreduce la oxidación de grasas durante su cocimiento, por lo que la carne adicionada con romero presentó los valores más bajos de TBARS (sustancias reactivas al ácido tiobarbitúrico) (0.23±0.02 mg/kg), mientras que la adicionada con jamaica yBHT, fueron iguales (0.47±0.03 y 0.41±0.01 mg/kg respectivamente). Por otra parte, los atributos sensoriales (sabor, color y facilidad de corte) mejoran al adicionar la jamaica y romero, lo cual se puede deber a la presencia de ácidos orgánicos (Bozkurt y Belibağli,2009).
2.2. Aplicaciones de los extractos de jamaica en alimentos
En general una de las aplicaciones más comunes de la flor de jamaica es en la elaboración de bebidas refrescantes a partir de su extracto acuoso, a este respecto se han reportado trabajos en los cuales han evaluado diferentes variedades de jamaica (roja, roja obscura y amarilla), procesos de elaboración, aporte nutricional y las sustancias bioactivas (principalmenteantocianinas).
Con el objetivo de determinar la óptima relación de cálices de jamaica-agua caliente en el proceso de extracción para elaborar una bebida endulzada de jamaica, Bolade et al. (2009) evaluaron tres proporciones (p/v) de cálices-agua caliente: 1:52, 1:57 y 1:62; con tiempos de extracción de 20, 25 y 30 min. y una temperatura constante de 100±2 °C. Las mejores condiciones para la preparación de la bebida fueron una relación de 1:62 (p/v) y 30 minutos, la cual además se endulzó con azúcar al 13%. Bajo estas condiciones, el aporte de ácido ascórbico fue de 15.5 mg/100 mL. CidOrtega et al., 2010 diseñaron una bebida a
partir del extracto de jamaica (criolla roja) y evaluaron diferentes edulcorantes no calóricos y los compararon con el azúcar de caña. El extracto de jamaica se obtuvo con agua destilada en una proporción de 1:7 (p/v), a 60 °C durante 20 min. La extracción fue muy eficiente al obtener el 95±3% de los minerales K, Ca, Mg, Fe, Co, Mn y Zn, yel 64±2% para Na y Cu (ver Tabla V). El edulcorante no calórico mejor aceptado fue el Canderel® (aspartame+acesulfame-K) y el aporte de antocianinas totales fue de aproximadamente 5 mg por botella de agua de jamaica (500 mL), cubriendo el 22% de la ingesta diaria recomendada (23 mg/día) (Biruete-Guzmán et al., 2009). Nnam y Onyeke (2003), compararon bebidas hechas a partir de dos variedades de jamaica (roja y amarilla), encontrando que ambas tuvieron un contenido apreciable de Fe (roja: 833.00 mg/100 g y amarilla: 800.67 mg/100 g), β-caroteno (roja: 285.29RE/100g yamarilla: 281.28RE/100g) y ácido ascórbico (roja: 53 mg/100 g y amarilla: 56.83 mg/100 g); concluyendo que sonunafuenteimportantedeéstos.
Por otra parte, se han realizado estudios para determinar el efecto de la adición de extractodejamaicaenlaelaboracióndeyogur, evaluando sus propiedades fisicoquímicas y sensoriales. Iwalokun y Shittu (2007) determinaron el efecto del extracto acuoso de Hibiscus sabdariffa (20 mL/L de yogur) sobre el pH, acidez titulable, sinéresis, cenizas y contenido de humedad en yogur con bajo contenido de grasa elaborado a partir de leche reconstituidaaladicionarloantesodespuésdel proceso de fermentación. Los autores observaronquelaadicióndel extracto antesde la fermentación reduce el tiempo de este proceso (aprox. 42 min.), sugiriendo una reacción entre el extracto y los sustratos y productos de la fermentación. La abundancia de ácidos orgánicos en el extracto, pudieran provocar una sinergia con los cultivos iniciadores y de esta manera acelerar la reducción del pH y por consiguiente la
coagulación. La sinéresis de este yogur fue significativamente menor que la del yogur sin extracto o el adicionado después de la fermentación. En la evaluación sensorial, el yogur con extracto de jamaica presentó una menor aceptación que un yogur de fresa, debido tal vez a una acidez excesiva que causa unsabordesagradable,porloquerecomiendan el uso de aditivos como sacarosa, estabilizantes,mantequillay/olactosa.
Resultados similares encontraron Rasdhari et al. (2008), al utilizar el extracto acuoso de jamaica en un yogur probiótico (conteniendo L. casei) elaborado con leche pasteurizada. Ellos manejaron dos concentraciones del extracto en el yogur (1 y 2% en volumen). De manera general, la adición del extracto mejoró las propiedades antioxidantes y disminuyó la sinéresis.Adiferenciadel estudiode Iwalokun y Shittu (2007) la aceptabilidad mostró puntuaciones altas en los diferentes atributos, porloquelosautoresconcluyenquelaadición del extracto de jamaica tuvo un efecto benéfico en la calidad del yogur. Las diferencias entre estos trabajos probablemente sedebanaltipodelecheutilizada.
Daramola y Asunni (2006) evaluaron el efecto de la adición de extracto acuoso de jamaica como antioxidante y fortificante de hierro en pizzas, se utilizaron dos concentraciones (3 y 12.5 %). El extracto de jamaica mejoró algunas características sensoriales del producto, específicamente el sabor y la textura, no así, la apariencia (aspecto rugoso). La aceptación general fue igual para todas las pizzas. El efecto antioxidante se cuantificó mediante el monitoreo del índice de peróxido. Las pizzas con el extracto tuvieron menor índice de peróxidos, por lo que ayuda a prevenir la oxidación. Así mismo, las concentraciones de hierro fueron mayores en las pizzas enriquecidas con el extracto aportando 1.05 y 1.97 mg/g. Por lo anterior los autores sugieren elusodelextractoenbotanasfritas.
Recientemente, los polvos encapsulados de los extractos de jamaica representan una opción muyinteresante como colorante para la industria de alimentos y bebidas, principalmente por su aporte de compuestos bioactivos (antocianinas y fenoles). Duangmal et al. (2004), evaluaron la estabilidad del color de un extracto de jamaica liofilizado y encapsulado con maltodextrina (3%), en una bebida refrescante. Se probaron y compararon 3 colorantes: 0.1% de polvo liofilizado de jamaica,0.05%deSANREDRC® y0.05%de carmín artificial; en una bebida que además contenía 10% de azúcar y 0.5% de ácido cítrico, por 12 semanas. La bebida con polvo liofilizado de jamaica fue rechazada por los panelistas(enfuncióndel color)despuésde56 días (debido a la degradación de las antocianinas), mientras que las dos restantes fueron aceptadas hasta los 84 días. Sin embargo, la aceptación general fue superior para la bebida de jamaica. En otro estudio (Selim et al., 2008) similar, se utilizó el extracto de jamaica liofilizado y encapsulado conmaltodextrina(10%),comocoloranteenla elaboración de mermelada de fresa. El polvo se adicionó a diferentes concentraciones (0, 0.5, 1.0, 1.5 y 2.0 g/kg de mermelada) y se realizó un análisis sensorial para evaluar su aceptación. La mejor formulación fue la mermelada adicionada con el 1.0%. En cuanto a la estabilidad del color, éste se mantuvo estable a los 6 meses de almacenamiento. Las mermeladas adicionadas con el polvo de jamaica tuvieron una mayor aceptación que el control (mermelada sin polvo de jamaica), incluso después de 9 meses. De acuerdo a estas investigaciones, el uso de polvos liofilizados de extractos de jamaica puede tener un uso significativo como colorante en losalimentosybebidas.
3. Beneficios a la salud de los extractos de jamaica
Las investigaciones realizadas a la flor de jamaica, con el objetivo de evaluar sus
beneficios a la salud, se centran principalmente en sus extractos, los cuales se utilizan para enriquecer o fortificar diversos alimentos, como se mencionó en la sección anterior. Hasta el momento no se han publicado trabajos en los que se demuestren los efectos positivos de productos elaborados particularmente con la flor de jamaica y sus extractos, a excepción de las bebidas refrescantes. Por lo anterior, en esta sección se presentarán los principales beneficios que tienen los extractos de jamaica para tratar o prevenir padecimientos habituales en el ser humano. Estudios recientes con los extractos acuosos y etanólicos de jamaica demuestran que éstos podrían actuar como antioxidantes y contribuir a las acciones anticancerígenas, además de que ayudan a reducir enfermedades cardiovasculares y crónicas como la diabetes mellitus, las dislipidemias, y la hipertensión. Los principales compuestos antioxidantes en los extractos son los flavonoides y antocianinas, desde el punto de vista toxicológico, estos no presentan actividad tóxicanimutagénica.
3.1. Propiedades antioxidantes
Actualmente los seres humanos estamos expuestos a un gran número de agentes oxidantes, producto de la contaminación ambiental, situaciones de estrés, inhalación de humo del cigarro y compuestos químicos que se añaden a los alimentos (que mejoran sus propiedades sensoriales o su conservación). Porotrolado,comoproductodelasreacciones químicas el cuerpo produce radicales libres, por lo que si bien ordinariamente son neutralizados por los antioxidantes biológicos, pueden causar la oxidación de las membranas para después dañar el ADN, desencadenando una serie de reacciones no deseables que puedenconduciraldesarrollodeenfermedades como cáncer, problemas cardiovasculares, entre otros (Biruete-Guzmán et al., 2009). Los compuestos fenólicos, como el ácido protocatéquico, queseencuentra en el extracto
de las flores de jamaica, tienen fuertes propiedades antioxidantes. El ácido protocatéquico disminuye la peroxidación de lípidos, que es un mecanismo potencial del daño celular. Este ácido es un agente eficaz para inhibir la acción carcinogénica de la dietilnitroso-aminaenelhígado,dela1-óxido4-nitroquinoleína en la cavidad oral, del azoxymetano en el colon, de la N-metil-Nnitrosoureaenel tejidoglandulardel estómago y de la N-butil-N-(4-hidroxibutil) nitrosamina enlavesícula(Carvajal et al.,2006).
Diversos estudios han evaluado las propiedades antioxidantes de los extractos de jamaica.Usoh et al.(2005)evaluaronel efecto antioxidante de los extractos etanólicos de flores secas de Hibiscus sabdariffa L. en algunos biomarcadores de estrés oxidativo en ratas de raza Wistar. La administración oral del extracto (200 y 300 mg/kg de peso corporal) reduce significativamente la formación de malondialdehído (principal compuesto utilizado como indicador de la peroxidacióndelípidos)enelhígado,inducida porelarsenitodesodio,loquesugiereelpapel protector del extracto en contra del daño celular inducido. Así mismo, el tratamiento con los extractos mostró un aumento significativo en el hígado y una disminución en la sangre, de las enzimas dismutasa superóxido ycatalasa,loqueindicasueficacia antioxidanteysuefectoprotector.
En otro estudio (Hsieh et al., 2006) investigaron el daño oxidativo inducido por el ejercicio exhaustivo y el efecto protector de la adición del ácido protocatéquico de jamaica sobre los niveles de malondialdehído, superóxido dismutasa, glutatión peroxidasa y glutatión reductasa, en el músculo esquelético de ratas. La cantidad de ácido protocatéquico suministrado fue de 1 mg/kg de masa corporal por día, durante 7 días. Los resultados de este estudio mostraron que el ejercicio exhaustivo podría resultar en un estrés oxidativo y que la administración del ácido protocatéquico fue
favorable ya que mejoró la capacidad antioxidante e inhibió el estrés oxidativo. Mohamed y Subramanian, (2007), estudiaron los efectos del extracto etanólico de jamaica contra la hiperamonemia y como antioxidante enlostejidoscerebrales deratasconexcesode hiperamonemia, inducidas por cloruro de amonio. La administración oral del extracto de jamaica (250 mg/kg de peso corporal) normalizó de manera significativa los niveles de amoníaco, urea, ácido úrico, creatinina y nitrógenonoproteicoen lasangre.Así mismo, disminuyó significativamente los niveles de peroxidación de lípidos en el cerebro, cuantificados como TBARS (sustancias reactivas al ácido tiobarbitúrico) e hidroperóxidos. Esta investigación demuestra unasignificativaactividadanti-hiperamonemia y antioxidante del extracto etanólico de jamaica.
Sáyago-Ayerdi et al. (2007) demostraron la presencia de fibra dietética (0.66 g de fibra soluble/L) y compuestos bioactivos antioxidantes (66 mg/100 mL de compuestos fenólicos) en una bebida obtenida por decocción de los cálices de jamaica. Una porción de 250 mL de esta bebida aporta aproximadamente 166 mg de dicha fibra, lo que representa alrededor del 2% de la ingesta recomendada en México. Además, esta fibra dietética soluble contiene polifenoles asociados que confieren actividad antioxidante, posiblemente induciendo un efecto saludable en el colon, donde puede contrarrestar los efectos metabólicos de la microflora y que contribuye a un estado saludable.
Se ha investigado (Won-Kyoung et al., 2008)laacción anti-proliferativadelascélulas primarias de humanos cultivadas con leiomioma(neoplasiabenignadelmúsculoliso que es muy rara y puede ocurrir en cualquier órgano, pero las formas más comunes se producen en el útero, el intestino delgado y el esófago) debido a la ingesta del ácido
protocatéquico de jamaica. Las células de leiomioma uterino tratadas con una concentración de 5 mmol/L de ácido protocatéquico, redujo en un 70% el crecimiento de dichas células, en un tiempo de prueba de 72 h. Los resultados obtenidos en este trabajo indican que el ácido protocatéquico induce la apoptosis (proceso por el que la célula muere ante estímulos extra o intracelulares) en las células de leiomioma uterino in vitro, lo que indica su potencial en el tratamiento de este padecimiento en humanos.
Los efectos del extracto de jamaica sobre los padecimientos de cáncer también han sido estudiados. Akim et al. (2011) evaluaron la capacidad antioxidante de un jugo comercial dejamaicaentresperíodosdealmacenamiento y su efecto antiproliferativo sobre células de cáncer de mama (MCF-7 y MDA-MB-231), ovario (Caov-3) y cuello uterino (HeLa). En general, el jugo comercial de jamaica almacenadoendiferentesperíodos (unaño,un mes, y una semana), exhibieron una alta actividad antioxidante y ésta no fue significativamente diferente entre las muestras almacenadas. Así mismo, mostró actividad anti-proliferativa de células Caov-3, HeLa, MDA-MB-231 y MCF-7. En conclusión, los autores demostraron que el jugo comercial de jamaica posee propiedades antioxidantes y actividad antiproliferativa de células cancerígenas que podrían atribuirse a su contenidodeflavonoidesysaponinas.
Así mismo, se han estudiado las propiedades hemo-protectoras y citotóxicas (Ologundudu et al., 2009; 2010) del extracto de Hibiscus sabdariffa utilizando el modelo inducido de estrés oxidativo por 2,4dinitrofenilhidrazina en conejos. Los resultados hallados indican que las antocianinas, presentes en el extracto de los cálices secos de Hibiscus sabdariffa, protegen a la sangre contra los efectos de la oxidación inducida por 2,4-dinitrofenilhidrazina y
efectos hemolíticos, así como, la protección contra los efectos debidos a la peroxidación de lípidosycitotóxicos.
Josiah et al. (2010) investigaron el papel protector del extracto acuoso de Hibiscus sabdariffa en tejidos (cerebro, riñón, estómago, bazo, corazón e hígado) dañados de ratas, inducido por bromato de potasio. Las dosis utilizadas del extracto fueron de 250 y 500 mg/kg del peso corporal. No hubo diferencia significativa en la proporción del peso de los órganos en todos los tejidos investigados en ambas dosis, en comparación con el control. El nivel de malondialdehído en los grupos de ensayo se redujo significativamente de una manera dependiente deladosisutilizadadelextractodejamaica.
3.2.
Efecto como hipolipemiante
Se entiende por hipolipemiante a cualquier sustanciafarmacológicamenteactivaquetenga la propiedad de disminuir los niveles de lípidos en sangre. Ubani et al. (2010) demostraron una disminución significativa en el colesterol total y los niveles de LDL (lipoproteínasdebajadensidad),aladministrar extracto de Hibiscus sabdariffa L., en concentraciones de 0.5, 1.0, 1.5 y 2.0 mg/kg, en ratas inducidas con fenobarbitona. Resultados similares obtuvieron Gosain et al. (2010), al investigar el efecto hipolipidémico del extracto etanólico de Hibiscus sabdariffa L. en ratas hiperlipidémicas (niveles elevados delípidosenlasangre). El extractode jamaica fue evaluado en tres dosis: 100, 200 y 300 mg/kg,porvíaoral.Comofármacoestándarse utilizó atorvastatina (10 mg/kg, por vía oral).
Las concentraciones de 200 y 300 mg/kg de extracto de jamaica mostraron una reducción significativa en el nivel de colesterol sérico en un 18.5% y 22%, respectivamente, el nivel de triglicéridos en suero en un 15.6% y 20.6%, respectivamente; nivel sérico de LDL en un 24% y 30%, respectivamente, y el nivel de VLDL (lipoproteínas de muy baja densidad)
en suero en un 15.5% y 20.5%, respectivamente. Sin embargo, ningún cambio significativo en el nivel de HDL (liproteínas de alta densidad) fue observado. Estos resultados indican que el extracto etanólico de jamaica exhibe un efecto hipolipidémico y la mejorconcentraciónfuelade300mg/kg(pero menos eficaz que el fármaco estándar atorvastatina). No obstante, se requiere de más investigaciones con diferentes condiciones experimentales para justificar el efecto hipolipemiante de los extractos de Hibiscus sabdariffa.
Por otra parte, Chia-Wen et al. (2010) demostraronqueel extractodejamaicainhibió el crecimiento de las células musculares lisas de la aorta mediante apoptosis, siendo dependiente de la dosis administrada del extracto de jamaica (0.5 a 6 mg/mL), por lo que puede ser un componente natural útil para prevenir cambios patológicos de la aterosclerosis.
Hernández-Martínez et al. (2003), no encontraron diferencias en el efecto de disminuir el colesterol y las LDL, y aumentar las HDL, al consumir encapsulados (500 mg) del extracto de jamaica en polvo (dosis de 3 g/díadurantedosmeses)oelconsumodeagua de jamaica (10 g de flor en 1 litro de agua diarios) en pacientes con diversos grados de dislipidemia. Ellos comprobaron una disminución del colesterol total, con agua de jamaica del 23.6% y con encapsulados del 22.9%, LDL 30.2% y 31.5% y triglicéridos 21.2%y17.9%,alconsumiraguadejamaicao encapsulados respectivamente; mientras que, el nivel de HDL se elevó en un porcentaje similar, 17.5% y 21.0%, al consumir agua de jamaica o encapsulados respectivamente. Por otra parte, Carvajal-Zarrabal et al. (2005, 2009)demostraronqueelextractoetanólicode Hibiscus sabdariffa L. al 5% ayuda a reducir en un 35% los niveles de lípidos en suero de ratas. Así mismo, investigaron la acción del extracto etanólico de Hibiscus sabdariffa en la
absorción y excreción de grasas, y el peso corporal en ratas. La ganancia de peso fue menor en los grupos administrados con 10 y 15% del extracto de jamaica, revelando que estas concentraciones pudieran ser potenciales agentes contra la obesidad. Lo anterior, pareciera indicar que esas concentraciones de extracto de jamaica podrían inhibir la amilasa pancreática, y en consecuencia impedir el fraccionamiento de polisacáridos y su absorción.
Tzu-Li et al. (2007) evaluaron el efecto del extracto de Hibiscus sabdariffa en la reduccióndecolesterolenhumanos,utilizando una preparación oral de cápsulas de extracto de jamaica liofilizado. En este estudio, 42 voluntarios(entre18 y75añosconunnivelde colesterol de 175 a 327 mg/dL) fueron observados durante un período de 4 semanas. Los sujetos fueron asignados aleatoriamente a 3 grupos: grupo I (1 cápsula de extracto de jamaica liofilizada en cada comida por día, 3 en total), grupo II (6 cápsulas, 2 en cada comida), y grupo III (9 cápsulas, 3 en cada comida). Cada cápsula de liofilizado de jamaica contenía20.1±3.0mgde antocianinas, 14.0±2.8 mg de polifenoles y 10.0±2.5 mg de flavonoides. De manera general, el consumo de cápsulas con extracto de jamaica condujo a una disminución significativa en el nivel de colesterol sérico en los sujetos de los grupos I y II después de 4 semanas. El nivel de colesterol en suero para el 71% de los voluntarios del grupo II, se redujo significativamente en promedio 12%. Se concluye que una dosis de 2 cápsulas de extracto de jamaica (en cada comida) durante 1 mes puede reducir significativamente el nivel de colesterol sérico. La observación de niveles bajos de colesterol en suero en estos sujetos sugiere que el extracto de jamaica puede ser eficaz en pacientes hipercolesterolémicos.
3.3. Efectos positivos en afecciones cardiovasculares e hipertensivas
Uno de los principales factores de riesgo que predomina en el mundo es la hipertensión arterial, afectando a 900 millones de pacientes aproximadamente (420 millones en países desarrollados). Cuando esta enfermedad no se trata, puede producir engrosamiento de los vasos sanguíneos que propician enfermedades cardiovasculares (insuficiencia cardiaca e infarto agudo del miocardio), insuficiencia renal y accidentes cerebrovasculares (trombosis e ictus), las cuales son motivo de incapacidad permanente o muerte prematura (Blanquer et al., 2009). Entre los principales factores responsables de la hipertensión se encuentran la retención de agua y sodio, así como niveles elevados de dicarbopeptidasa, la cual se conoce como enzima convertidora de la angiotensina (por sus siglas en inglés, ACE: Angiotensin Converting Enzyme), es una enzima proteolítica que convierte la angiotensina I en angiotensina II, esta última causa hipertensión, ya que es un poderoso vasoconstrictor que funciona en el cuerpo controlando la presión arterial. Diversas investigaciones han evidenciado el efecto hipotensor de los extractos de jamaica, los cuales inhiben la enzima convertidora de la angiotensina II. Se ha reportado que los extractos acuosos de jamaica disminuyen la actividad de la ACE en un 30% (Blanquer et al., 2009). En un estudio se suministró diariamente a pacientes de 30 a 80 años, una infusión a partir de cálices de jamaica (10 g de flor en 500 mL de agua caliente, con un contenidode 9.6mgdeantocianinas) antesdel desayuno, durante 4 semanas. Los resultados mostraron una disminución en la hipertensión (presión arterial sistólica de 139.05 a 123.73 mm Hg ypresión arterial diastólica de 90.81 a 79.52 mm Hg) (Herrera-Arellano et al., 2004). Además, se evidenció un aumento en la
eliminación de sodio urinario, así como una reducción de la actividad en la ACE. Lo anterior demuestra el efecto del extracto de jamaica como diurético ycomo inhibidor de la ACE(Herrera-Arellano et al.,2007).
En otros estudios, se comprobó que el consumo diario (una porción en la mañana y otra por la tarde) de té de jamaica (2 g de flor en 250 mL de agua caliente y un tiempo de extracciónde20a 30minutos),durante1mes, en pacientes diabéticos, disminuyó su presión arterial (de 134.4±11.8/81.6±6.1 a 112.7±5.79/80.5±8.9 mm Hg) (MozaffariKhosravi et al., 2009). Resultados similares obtuvieron McKay et al. (2010), quienes demostraron que el consumo diario (2160 mL) de té de jamaica (1.25 g de flor en 240 mL de agua, sometido a ebullición por 6 minutos), durante 6 semanas, en personas adultas con hipertensión, disminuyó su presión arterial (de 129.4±4.8/78.9±7.7 a 122.3±10.3/75.8±8.6 mm Hg). Es importante mencionar que la aportación de compuestos bioactivos en una porción de 240 mL de esta bebida de jamaica fue de 21.85 mg de fenoles totales y 7.04 mg deantocianinastotales.
3.4. Propiedades diuréticas, antipiréticas y contra los efectos de la diabetes
Los alimentos con propiedades diuréticas tienenlacapacidaddefavorecerlaeliminación de líquidos y toxinas del organismo, ésta es una de las propiedades de los extractos acuosos de jamaica. Márquez-Vizcaino et al (2007), llevaron a cabo un estudio en el cual utilizaron extracto de jamaica en diferentes formas: extracto total acuoso liofilizado (en concentraciones de 20, 200 y 400 mg/kg de peso corporal), fracción en etanol liofilizado (en concentraciones de 20 y 200 mg/kg de peso corporal) y extracto total acuoso sin liofilizar (20 mg/kg de peso corporal); los cuales se administraron en ratas albinas macho. Los tratamientos que presentaron mayor actividad diurética fueron los
administrados con 20 mg/kg de extracto etanólico liofilizado yextracto total acuoso sin liofilizar, teniendo estos tratamientos un comportamiento similar al control positivo de hidroclorotiazida en la eliminación del volumen de orina. Por otra parte, la eliminación de sodio y potasio en la orina, fue mayor para las concentraciones de 20 y 200 mg/kg de extracto total acuoso liofilizado. De acuerdo a lo anterior, el extracto etanólico liofilizado en concentraciones de 20 mg/kg presentó el mejor efecto diurético, incluso superior a la hidroclorotiazida en las condicionesensayadas.
Otra de las propiedades que se han demostrado en los extractos de jamaica es el efecto antipirético. Se denomina antipirético a todasustanciaofármaco quehacedisminuirla fiebre. Reanmongkol e Itharat (2007) evaluaron la actividad antipirética del extracto acuoso (800 mg/kg) y etanólico (400 y 800 mg/kg) de la jamaica, en dicho estudio ambos extractos disminuyeron la fiebre inducida por levaduras en ratones albinos suizos y ratas Wistar. El extracto etanólico mostró un mayor efecto en la disminución de fiebre (1.2 y 1.1 °C) en comparación con el extracto acuoso (1 °C). Esto indica que posiblemente los extractos etanólicos contengan más componentes activos que promuevan una acción antipirética, que los extractos acuosos, así mismo, el efecto antipirético de los extractos de jamaica podría estar asociado a la inhibición de sustancias inductoras de fiebre, como las citocinas. Resultados similares obtuvo Velázquez-Hernández (2010), quien utilizó tres extractos de jamaica: extracto acuoso (100 g de cálices en 1 litro de agua, calentado a 100 °C por 30 min.), extracto concentrado en pigmentos (cálices extraídos con acetona y etanol, y posterior eliminación por destilación y evaporación) y extracto proteico (obtenido del residuo del extracto concentrado en pigmentos; concentración proteica de 100 µg/mL). Los tres extractos presentaron actividad antipirética, siendo el
mejor el extracto concentrado en pigmentos y ésteescomparablecon el paracetamol (control positivo).
Por otro lado, la diabetes es una enfermedad muy común en el mundo entero. Sus causas varían, pero generalmente están relacionadasala cuestióngenética ytambién a la obesidad. La característica de la diabetes es lafaltadesecrecióndeinsulinaenel páncreas.
Se ha demostrado que los extractos de jamaica presentan efectos hipoglucémicos (Wen-Chin et al., 2009); los cuales actúan sobre la glucosamina-nitrosourea que es un compuesto tóxico para las células beta, que son las responsables de producir la insulina. Resultados similares encontraron Sini et al. (2011), quienes realizaron un estudio en el cual se administró una dosis oral de extracto dejamaicade0.5mg/mLcomobebidadurante 5 semanas, a ratas albinas macho. Los resultados demostraron una reducción significativa en glucosa sanguínea y el peso corporal. El extracto de jamaica mostró actividad hipoglucémica, así como una disminución significativa en el nivel de colesterol sérico total y triglicéridos. El posible mecanismo por el cual el extracto de jamaica provoca su acción hipoglucemiante puede ser debido a un efecto potencial del aumento de la insulina en plasma o bien, mediantelasecreciónpancreáticadeinsulinaa partir de células beta de los islotes pancreáticos (células que se encargan de producir hormonas como la insulina y el glucagón,confunciónnetamenteendocrina).
Conclusiones y comentarios finales
Es evidente que la flor de jamaica, así como sus extractos, poseen propiedades funcionales que tienen la capacidad de proveer beneficios a la salud del ser humano, lo anterior debido principalmenteasugran aportedecompuestos bioactivos (principalmente fenoles y
antocianinas). Las investigaciones recientes nos permiten proyectar a la flor de jamaica y sus extractos, como una nueva alternativa para la industria de alimentos y bebidas, en el diseño de nuevos productos que coadyuven a la prevención y/o tratamiento de enfermedades crónico degenerativas. Sin embargo, el reto para la industria alimentaria es desarrollar y comercializar de manera efectiva alimentos funcionales a partir de la flor de jamaica y sus extractos, y para los científicos, el desafío consiste en aportar las pruebas científicas para comprender el impacto de estos alimentos funcionalesenlasalud.
Agradecimientos
S. Cid-Ortega agradece al PROMEP (Programa de Mejoramiento del Profesorado) y a la UTIM (Universidad Tecnológica de Izúcar de Matamoros) por la beca otorgada para la realización de sus estudios de doctorado.
Referencias
Abou-Arab, A. A., Abu-Salem, F. M. y Abou-Arab, E. A. 2011. Physico-chemical properties of natural pigments (anthocyanin) extracted from roselle calyces (Hibiscus subdariffa). Journal of American Science. 7(7):445-456.
Akim, A., Chooi, L. L., Rahmat, A. y Amiruddin, Z. Z. 2011. Antioxidant and anti-proliferative activities of roselle juice on Caov-3, MCF-7, MDA-MB-231 and HeLa cancer cell lines. African Journal of Pharmacy and Pharmacology. 5(7):957-965.
Alarcón-Corredor, O. M. 2009. Los elementos traza. Revista Médica de la Extensión Portuguesa. 4(3):107-124.
Almana, H. A. 2001. Karkade (Hibiscus sabdariffa) as a mineral and fiber supplement in chocolate cakes. Arab Universities Journal of Agricultural Sciences 9(1):283-295.
Ashaye, O. A. y Adeleke, T. O. 2009. Quality attributes of stored roselle jam. International Food Research Journal. 16(3):363-371.
Babalola, S. O., Babalola, A. O. y Aworh, O. C. 2001. Compositional attributes of the calyces of roselle (Hibiscus sabdariffa L.). Journal of Food Technology in Africa. 6(4):133-134.
Biruete-Guzmán, A., Juárez-Hernández, E., SieiroOrtega, E., Romero-Viruegas, R. y Silencio-Barrita, J. L. 2009. Los nutacéuticos. Lo que es conveniente saber. Revista Mexicana de Pediatría. 76(3):136145.
Blanquer, A., Herrera, A., Zamilpa, A., Olivar, T. y Martínez, M. 2009. Interés de la flor de hibisco en problemas cardiovasculares. Revista de Fitoterapia. 9(1):25-33.
Bolade, M. K., Oluwalana, I. B. y Ojo, O. 2009. Commercial practice of roselle (Hibiscus sabdariffa L.) beverage production: optimization of hot water extraction and sweetness level. World Journal of Agricultural Sciences. 5(1):126-131.
Bozkurt, H. y Belibağli, K. B. 2009. Use of rosemary and Hibiscus sabdariffa in production of kavurma, a cooked meat product. Journal of the Science of Food and Agriculture. 89:1168–1173.
Carvajal, O., Waliszewski, S. y Infanzón, R. M. 2006. Los usos y maravillas de la jamaica. La Ciencia y el Hombre. 19(2):37-40.
Carvajal-Zarrabal, O., Waliszewski, S. M., BarradasDermitz, D. M., Orta-Flores, Z., Hayward-Jones, P. M., Nolasco-Hipólito, C., Angulo-Guerrero, O., Sánchez-Ricaño, R., Infanzón, R. M. y Trujillo, P. R. L. 2005. The consumption of Hibiscus sabdariffa dried calyx ethanolic extract reduced lipid profile in rats. Plant Foods for Human Nutrition. 60 (4): 153159.
Carvajal-Zarrabal, O., Hayward-Jones, P. M., OrtaFlores, Z., Nolasco-Hipólito, C., Barradas-Dermitz, D. M., Aguilar-Uscanga, M. G., y PedrozaHernández, M. F. 2009. Effect of Hibiscus sabdariffa L. dried calyx ethanol extract on fat absorption-excretion, and body weight implication in rats. Journal of Biomedicine and Biotechnology, 2009: 1-5.
Chia-Wen, L., Hui-Pei, H., Kuei-Chuan, C., ChengHsun, W. y Chau-Jong W. 2010. Hibiscus sabdariffa extract induced apoptosis of proliferating smooth muscle cell. Journal of Food Biochemistry 34(3):549-563.
Cid, O. S., Navarro, F. A. E., Rodríguez, V. F. J., Caso, V. L. R. y Monroy, R. J. A. 2007. Industrialización
de jamaica (Hibiscus sabdariffa) en la mixteca poblana. Memorias del VII Coloquio Nacional de Investigación en Ingeniería Química. Orizaba, Veracruz, México. 14-15 Noviembre 2007. p. 25-29.
Cid-Ortega, S., Navarro-Frómeta, A. E., Rostagno, M A., López-Méndez, E. M. y Monterrosas-Fuentes, A. 2010. Sugar-free hibiscus water production: process design and economic evaluation. Memorias del XXXI Encuentro Nacional de la AMIDIQ. Huatulco, Oaxaca, México. 4-7 Mayo 2010. ISBN: 978-970764-976-7. p. 4947 – 4952.
Cisse, M., Dornier, M., Sakho, M., Ndiaye, A., Reynes, M. y Sock, O. 2009. Le bissap (Hibiscus sabdariffa L.): composition et principales utilisations. Fruits 64(3):179-193.
Daramola, B. y Asunni, O. A. 2006. Nutrient composition and storage studies on roselle extract enriched deep-fat-fried snack food. African Journal of Biotechnology. 5(19):1803-1807.
Domínguez-Domínguez, S., Domínguez-López, A., González-Huerta, A. y Navarro-Galindo, S. 2007. Cinética de imbibición e isotermas de adsorción de humedad de la semilla de jamaica (Hibiscus sabdariffa L.). Revista Mexicana de Ingeniería Química. 6(3):309-316.
Duangmal, K., Saicheua, B. y Sueeprasan, S. 2004. Roselle anthocyanins as a natural food colorant and improvement of its colour stability. Proceedings of the AIC 2004 Color and Paints, Interim Meeting of the International Color Association. Porto Alegre, Brazil. 2-5 Noviembre 2004. p. 155-158.
EUFIC, 2006. Functional foods. The European Food Information Council. http://www.eufic.org/article/en/expid/basicsfunctional-foods/, accesada 12/09/2012.
Falk, M. 2004. The impact of regulation on informing consumers about the health promoting properties of functional foods in the U.S.A. Journal of Food Science. 69(5):143-145.
Fundación Produce de Guerrero A. C. 2012. Jamaica. Agenda de innovación. Publicaciones gratuitas. http://fundacionproducegro.org.mx/publicaciones/gr atuitas/page/3/, accesada 11/10/2012.
Galicia-Flores, L. A., Salinas-Moreno, Y., EspinozaGarcía, B. M. y Sánchez-Feria, C. 2008. Caracterización fisicoquímica y actividad antioxidante de extractos de jamaica (Hibiscus sabdariffa L.) nacional e importada. Revista Chapingo Serie Horticultura. 14(2):121-129.
Glew R. H., Vanderjagt, D. J., Lockett, C., Grivetti, L. E., Smith, G. C., Pastuszyn, A. y Millson, M. 1997.
Amino acid, fatty acid, and mineral composition of 24 indigenous plants of Burkina Faso. Journal of Food Composition and Analysis. 10(3):205-217.
Gosain, S., Ircchiaya, R. y Sharma, P. 2010. Hypolipidemic effect of ethanolic extract from the leaves of Hibiscus sabdariffa L. in hyperlipidemic rats. Acta Poloniae Pharmaceutica-Drug Research 67(2):179-184.
Hasler, C. M. 2002. Functional foods: benefits, concerns and challenges (A position paper from the American Council on Science and Health). The Journal of Nutrition. 132(12):3772-3781.
Henry, N. y Badrie, N. 2007. Utilization of sorrel/roselle (Hibiscus sabdariffa L.) nectar in stirred yoghurts: physicochemical and sensory quality. Journal of Food Technology. 5(1):55-61.
Hernández-Martínez, A., Lobo-Moreno, J. A. y Noveron-Miranda, S. 2003. Efecto hipolipemiante de Hibiscus sabdariffa en pacientes con dislipidemia. Tesis de especialidad en acupuntura y fitoterapia, Universidad Autónoma MetropolitanaUnidad Iztapalapa. México. 40 p.
Herrera-Arellano, A., Flores-Romero, S., Chávez-Soto, M. A. y Tortoriello, J. 2004. Effectiveness and tolerability of a standardized extract from Hibiscus sabdariffa in patients with mild to moderate hypertension: a controlled and randomized clinical trial. Phytomedicine. 11(5):375-382.
Herrera-Arellano, A., Miranda-Sánchez, J. y AvilaCastro, P. 2007. Clinical effects produced by a standardized herbal medicinal product of Hibiscus sabdariffa on patients with hypertension. A randomized, double-blind, lisinopril-controlled clinical trial. Planta Medica. 73(1): 6-12.
Hsieh, C. C. C., Lee, M. Y., Chen, C. C., Hsu, J. J., Lu, H. K. y Wang, C. J. 2006. Hibiscus protocatechuic acid supplementation reduces oxidative stress induced by exhaustive exercise in rat muscle. Journal of Exercise Science and Fitness. 4(1):59-64.
Iwalokun, B. A. y Shittu, M. O. 2007. Effect of Hibiscus sabdariffa (calyce) extract on biochemical and organoleptic properties of yogurt. Pakistan Journal of Nutrition, 6 (2): 172-182.
Josiah, S., Omotuyi, O., Oluyemi, K., Ezea, I., Uhunmwangho, E., Nwangwu, S., Oyesola, O. y Njoya, H. 2010. Protective role of aqueous extract of Hibiscus sabdariffa (calyx) against potassium bromate induced tissue damage in wistar rats. African Journal of Biotechnology. 9(21):3218-3222.
Mahadevan, S. N. y Kamboj, P. 2009. Hibiscus sabdariffa Linn-An overview. Natural Product Radiance. 8(1):77-83.
Márquez-Vizcaino, R. L., de La Rosa-Torres, C., Agusto-Rivero, C. y Medina-Montes. M. 2007. Actividad diurética del extracto total acuoso de los cálices de Hibiscus sabdariffa L. administrado en ratas albinas variedad Wistar. Scientia et Technica. 13(33):377-381.
Martínez-Martínez. C. T., Cid-Ortega. S. y CamposReyes, L. 2006. Diseño de una planta agroindustrial de jamaica. Consejo de Ciencia y Tecnología del Estado de Puebla y Fundación Produce Puebla, A. C. Memorias: Cuarto Encuentro de Innovación Tecnológica para el fortalecimiento de las cadenas Agroalimentarias en el estado de Puebla. Puebla, México. 11 julio 2006. ISBN: 968-839-534-X. p. 72-76.
Mckay, D. L., Oliver-Chen, C. Y., Saltzman, E. y Blumberg, J. B. 2010. Hibiscus sabdariffa L. tea (tisane) lowers blood pressure in prehypertensive and mildly hypertensive adults. The Journal of Nutrition. 140(2):298-303.
Meza-Chavarría, P. 2012. Guía: flor de jamaica (Hibiscus sabdariffa L) e (Hibiscus cruentus Bertol). Asociación para el Desarrollo Eco-Sostenible (ADEES). Chinandega, Nicaragua. 25 p.
Mohamed, M. E, y Subramanian, P. 2007. Hibiscus sabdariffa affects ammonium chloride-induced hyperammonemic rats. Evidence-based Complementary and Alternative Medicine. 4(3):321325.
Morton, J. F. 1987. Roselle. http://www.hort.purdue.edu/newcrop/morton/roselle. html, accesada 18/09/2012.
Mozaffari-Khosravi, H., Jalali-Khanabadi, B. A., Afkhami-Ardekani, M., Fatehi, F. y Noori-Shadkam, M. 2009. The effects of sour tea (Hibiscus sabdariffa) on hypertension in patients with type II diabetes. Journal of Human Hypertension. 23(1):4854.
Nnam, N. M. y Onyeke, N. G. 2003. Chemical composition of two varieties of sorrel (Hibiscus sabdariffa L.), calyces and the drinks made from them. Plant Foods for Human Nutrition. 58(3):1-7.
Ologundudu, A., Ologundudu, A. O., Ololade, I. A. y Obi, F. O. 2009. Effect of Hibiscus sabdariffa anthocyanins on 2, 4-dinitrophenylhydrazineinduced hematotoxicity in rabbits. African Journal of Biochemistry Research. 3(4):140-144.
Ologundudu, A., Ologundudu, A. O., Oluba, O. M., Omotuyi, I. O. y Obi, F. O. 2010. Effect of Hibiscus sabdariffa anthocyanins on 2, 4dinitrophenylhydrazine-induced tissue damage in rabbits. Journal of Toxicology and Environmental Health Sciences. 2(1):1-6.
Ortiz-MArquéz, S. 2008. Composición en macronutrientes, minerales y metales pesados en cálices de jamaica cultivada en el estado Monagas. Tecnología y pensamiento, 3 (1 – 2): 61-75.
Peng-Kong, W., Yusof, S., Ghazali, H. M., y Che-Man, Y. B. 2002. Physico-chemical characteristics of roselle (Hibiscus sabdariffa L.). Nutrition and Food Science. 32(2):68-73.
Rasdhari, M., Parekh, T., Dave, N., Patel V. y Subhash, R. 2008. Evaluation of various physico-chemical properties of Hibiscus sabdariffa and L. casei incorporated probiotic yoghurt. Pakistan Journal of Biological Sciences. 11(17):2101-21 08.
Reanmongkol, W. e Itharat, A. 2007. Antipyretic activity of the extracts of Hibiscus sabdariffa L. calyces in experimental animals. Songklanakarin Journal of Science and Technology. 29(1):29-38.
Sagarpa-Conacyt, 2010. Fondo Sectorial de Investigación en materia agrícola, pecuaria, acuacultura, agrobiotecnología y recursos fitogenéticos. Anexo B. Demandas del sector 20107, demanda única: jamaica - “Generación de variedades de jamaica (Hibiscus sabdariffa L.) con alta concentración de compuestos bioactivos, de alto rendimiento y tolerantes a enfermedades para una producción sustentable en México”. http://www.encuentra.gob.mx/resultsAPF.html?q=C onvocatoria%2020107&client=conacyt&ts=all&geo=0, accesada 15/09/2012.
Sáyago-Ayerdi, S. G., Arranz, S., Serrano, J. y Goñi, I. 2007. Dietary fiber content and associated antioxidant compounds in Roselle flower (Hibiscus sabdariffa L) beverage. Journal of Agricultural and Food Chemistry. 55(19):7886-7890.
Selim, K. A., Khalil, K. E., Abdel-Bary, M. S. y AbdelAzeim, N. A. 2008. Extraction, encapsulation and utilization of red pigments from roselle (Hibiscus sabdariffa L.) as natural food colourants. Special Volume Conference. Alexandria Journal of Food Science and Technology. Alexandria University. 4-6 Marzo 2008. p. 7-20.
Shahidi, F. 2004. Functional foods: their role in health promotion and disease prevention. Journal of Food Science. 69(5):146-149.
SIAP (Servicio de Información Agroalimentaria y Pesquera). 2012. Cierre de la producción agrícola por cultivo. http://www.siap.gob.mx/index.php?option=com_wra pper&view=wrapper&Itemid=350, accesada 15/10/2012.
Sini, J. M., Umar, I. A. e Inuwa, H. M. 2011. The beneficial effect of extract of Hibiscus sabdariffa calyces in alloxan-diabetic rats: hypoglycaemic and hypolipidaemic activities. Journal of Medicinal Plants Research. 5(11):2182-2186.
Suliman, A. M. A., Ali, O. A., Idriss-Sharaf, E. A. A. y Abdualrahman, M. A. Y. 2011. A comparative study on red and white karkade (Híbíscus sabdariffa L.) calyces, extracts and their products. Pakistan Journal of Nutrition. 10(7):680-683.
Tzu-Li, L., Hui-Hsuan, L., Chang-Che, C., MingCheng, L., Ming-Chih, C. y Chau-Jong, W. 2007. Hibiscus sabdariffa extract reduces serum cholesterol in men and women. Nutrition Research 27(3):140-145.
Ubani, C. S., Joshua, P. E. y Oraeki, A. N. 2010. Influence of aqueous extract of Hibiscus sabdariffa calyces on lipid profile of phenobarbitone induces wistar albino rats. Journal of Pharmacy Research 3(2):319-324.
Usoh, I., Akpan, E., Etim, E. y Farombi, E. 2005. Antioxidant action of dried Hibiscus sabdariffa L. on sodium arsenite – induced oxidative stress in rats. Pakistan Journal of Nutrition. 4(3):135-141.
Velázquez-Hernández, M. E. 2010. Actividad antipirética de extractos crudos y proteicos de flor de jamaica (Hibiscus sabdariffa L.). Tesis de licenciatura, Universidad Michoacana de San Nicolás de Hidalgo. Morelia, Michoacán, México. 99 p.
Wen-Chin, L., Chau-Jong, W., Yu-Hsin, C., Jen-Dong, H., Su-Ya, C., Hong-Chen, C. y Huei-Jane, L. 2009. Polyphenol extracts from Hibiscus sabdariffa Linnaeus attenuate nephropathy in experimental type 1 diabetes. Journal of Agricultural and Food Chemistry. 57(6):2206-2210.
Won-Kyoung, S., Chi-Heum, C., Sabarish, R., DaeKyu, S., So-Jin, S., Sang-Hoon, K. y Soon-Do, C. 2008. Induction of apoptosis by hibiscus protocatechuic acid, in human uterine leiomyoma cells. Korean Journal of Gynecologic Oncology 19(1):48-56.

Temas Selectos de Ingeniería de Alimentos 6 - 2 (2012): 64 - 78

Bacteriocinas: antimicrobianos naturales y su aplicación en los alimentos
S.C. Beristain-Bauza*, E. Palou y A. López-Malo
Departamento de Ingeniería Química, Alimentos y Ambiental, Universidad de las Américas Puebla. Ex hacienda Sta. Catarina Mártir S/N, San Andrés Cholula, Puebla. C.P.72810. México.
Resumen
Las bacteriocinas son péptidos sintetizados por algunas bacterias ácido lácticas y presentan un amplio potencial como conservadores para inhibir el crecimiento de otros microorganismos. Actualmente, las bacteriocinas son utilizadas en una amplia categoría de alimentos incluyendo cárnicos, lácteos, productos enlatados, productos del mar, vegetales, jugos de frutas, y bebidas como cerveza y vino. Sus características de compatibilidad en dichos productos así como su modo de acción hacen atractivo su uso en los alimentos. En esta revisión se presentará un panorama general del concepto de bacteriocinas, su clasificación, actividad antimicrobiana, modo de acción y principalmente la importancia de su aplicación en la industria alimentaria. Actualmente, los investigadores continúan realizando estudios para ampliar la variedad de bacteriocinas y promover su aplicación como un sustituto de los conservadores sintéticos en alimentos.
Palabras clave: bacterias ácido lácticas, bacteriocinas, antimicrobianos, modo de acción.
Abstract
Bacteriocins are peptides synthesized by some lactic acid bacteria and it has been reported that they have potential as preservatives to inhibit the growth of selected microorganisms. Generally, they are employed in different foods including meat, dairy products, canned foods, seafoods, vegetables, juices, and beverages such as beer and wine. Their characteristics of compatibility in these products and their mode of action make them attractive to be used in foods. The objective of this review is to present an overview about bacteriocins, their classification, antimicrobial activity, mode of action, and the importance of their application in the food industry. Nowadays, the researchers continue their studies in order to find new bacteriocins and to promote their use as a substitute for synthetic preservatives in foods.
Keywords: lactic acid bacteria, bacteriocins, antimicrobial, mode of action.
Introducción
*Programa de Doctorado en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: silviac.beristainb@udlap.mx
Actualmente existe una tendencia importante por parte de los consumidores en demandar alimentos naturales o que sean mínimamente procesados ysinconservadoressintéticos. Los consumidores consideran que muchos alimentos procesados presentan una calidad nutricional pobre y que los aditivos sintéticos son peligrosos para la salud. Como resultado de estas demandas, se tiene un gran interés en desarrollar alimentos con agentes antimicrobianosnaturales,loscualesdebenser inocuos, que cumplan con los parámetros de calidad y seguridad de las normativas
aplicables para agentes antimicrobianos y que además presenten alto espectro de efectividad contramicroorganismos.
La industria alimentaria ha desarrollado la aplicación de bacteriocinas, producto del metabolismo secundario de algunas bacterias ácido lácticas (BAL) en la conservación de los alimentos. Las bacteriocinas se definen como péptidos de origen proteínico, que a bajas concentraciones presentan inhibición microbiológica efectiva (Beshkova y Frengova,2012).AlgunasBALproductorasde bacteriocinas han sido aisladas de alimentos como la carne y los productos lácteos, además pueden ser utilizadas como iniciadores en procesos de fermentación de otros alimentos. Porlotanto,lasBAL y/o bacteriocinaspueden ser utilizadas como conservadores biológicos puros, que en un momento dado podrían reemplazaralosconservadoressintéticos.
La mayoría de las bacteriocinas son efectivas contra microorganismos patógenos importantes involucrados en enfermedades transmitidas por alimentos, tales como: Listeria monocytogenes, Staphylococcus aureus, Escherichia coli y Salmonella spp. (Wu et al., 2004; Jeevaratnam et al., 2005). Sin embargo, sólo la nisina ha sido aprobada legalmente para su uso en alimentos por la Administración de alimentos y cosméticos, FDA por sus siglas en inglés, en la categoría Generalmente reconocidas como seguras, GRASporsussiglaseninglés.
Debido a esta razón, las bacteriocinas se han convertido en un campo importante de investigación yestudio en los últimos 25 años, por lo que el objetivo de esta revisión es dar a conocer un panorama general sobre el concepto de bacteriocinas, su clasificación, actividad antimicrobiana, modo de acción y principalmente la importancia de la aplicación de estos compuestos como agentes antimicrobianos naturales en la preservación delosalimentos.
Revisión bibliográfica
1. Características generales
Las bacteriocinas son péptidos antimicrobianos heterogéneos, con diferentes niveles y espectros de actividad, mecanismos de acción, peso molecular y propiedades fisicoquímicas (Stoyanova et al., 2012). Éstas pueden ser sintetizadas por bacterias Grampositivas y Gram-negativas (Jeevaratnam et al., 2005); sin embargo, las producidas por las BAL han sido de gran interés por la industria alimentaria debido a las siguientes razones: se encuentran fácilmente en BAL comerciales (lactococos, lactobacilos, pediococos), son consideradas seguras para su consumo, no son tóxicas para las células eucariotas y presentan un espectro de inhibición más amplio en comparación con los espectros de las bacteriocinas sintetizadas por bacterias Gramnegativas(Nes et al., 2007).
De acuerdo con Chen y Hoover (2003) las bacteriocinas, metabolitos secundarios de las BAL, se definen como productos de la síntesis ribosómica, conformados por péptidos entre 20 y 60 aminoácidos (lactococinas A, B, M y G,lactacinaB yhelveticinaJ,entreotras).Son secretados extracelularmente y presentan una alta actividad bactericida o bacteriostática sobre cepas o especies relacionadas y sobre microorganismos patógenos y deteriorativos dealimentos(Cotter et al., 2005).
Las bacteriocinas están conformadas por puentes disulfuro, tioéter o grupos tiol libres y cuentan con puntos isoeléctricos en un intervalodepH8.6a10.4(Cotter et al., 2005).
La producción de las bacteriocinas ocurre de forma natural durante la fase logarítmica del desarrollo bacteriano o al final de la misma, guardando una relación directa con la biomasa producida. Entre sus características principales destacan el ser estables al calor y a pH ácidos, ambas propiedades están
estrechamente relacionadas: es decir, un incrementodepHreducelaestabilidadalcalor (Chen y Hoover, 2003). Sin embargo, aunque las bacteriocinas presentan estabilidad a pH ácido o neutro, son fácilmente destruidas a pH mayor de 10 (Jack et al., 1995). La alta termorresistencia en las bacteriocinas con peso molecular menor a 5 kDa, les permite mantener su actividad después de tratamientos térmicos equivalentes a la pasteurización de la leche, pero son parcialmente destruidas por arriba de los 100ºC. Dicha estabilidad puede deberse a la formación de estructuras globulares pequeñas y a la presencia de regioneshidrofóbicas, así comoalaformación deenlacescruzadosestables(Alquicira,2006).
Debido a su naturaleza proteica, las bacteriocinas son inactivadas por proteasas, incluyendo las de origen pancreático y gástrico, debido a ello durante su paso por el tracto gastrointestinal son inactivadas, sin ser absorbidas como compuestos activos (Quintero, 2006), resultando así presuntivamenteinocuasparaelconsumidor.
Las bacteriocinas presentan un amplio espectro antimicrobiano, siendoactivas abajas concentraciones (menores a 10 ppm) frente a bacterias Gram-positivas patógenas o deteriorativas de alimentos. Se ha demostrado que dicha actividad también se extiende a bacterias Gram-negativas sub-letalmente dañadas por los tratamientos térmicos o por la presencia de agentes quelantes. Estudios comparativosdemuestranquepresentanmayor inhibición contra las bacterias Gram-positivas. Las bacteriocinas presentan inhibición potencial contra patógenos como Clostridium botulinum, Enterococcus faecalis, Listeria monocytogenes, Staphylococcus aureus, Salmonella, Escherichia coli y algunas especies de Bacillus (Wu et al., 2004; Jeevaratnam et al.,2005).
2. Clasificación de las bacteriocinas
Anteriormente las bacteriocinas producto de las BAL fueron clasificadas en cuatro clases principales, de acuerdo a su estructura, propiedades fisicoquímicas y propiedades moleculares (Chen y Hoover, 2003). Sin embargo, en la actualidad se ha reducido esa clasificación a tres grupos (Savadogo et al., 2006; De Vuyst y Leroy, 2007; Beshkova y Frengova, 2012), ya que la cuarta clasificación nohasidototalmentejustificada.
2.1 Clase I. Lantibióticos
Los lantibióticos son péptidos pequeños conformados por 19-38 aminoácidos (Savadogo et al., 2006; Montalbán-López et al., 2011), policíclicos, con un peso molecular menor a 5 kDa, con poca estabilidad al calor y son modificados postraduccionalmente (cambio químico ocurrido en las proteínas después de su síntesis proteica) por la deshidratación de la serina y la treonina formando aminoácidos como dehidroalanina (Dha) y dehidrobutirina (Dhb), estos residuos, pueden unirse a través de un grupo tioetér a cadenas laterales de cisteína dando lugar a los aminoácidos inusuales como lantionina (Lan) y α-metil-lantionina (MeLan) (Riley y Wertz, 2002) mostrados en la Fig. 1. Los lantibióticos son los únicos que se producen en el ribosoma como un prepéptido, que experimenta una modificación postraduccional extensa para formar un péptido activo (McAuliffe et al., 2001).
Los lantibióticos son subdivididos en dos grupos, de acuerdo a sus características estructurales y a su modo de acción contra microorganismos(Guder et al., 2000):
Clase Ia. Son péptidos elongados en forma de tornillos con moléculas anfipáticas, presentan


Fig. 1 Modificaciones postraduccionales de la lantionina y α-metillantionina de los lantibióticos (Adaptado de Suárez, 1997).
un peso molecular menor a 4 kDa, flexibles, con carga neta positiva, cuya actividad antimicrobiana se debe a la destrucción de la célula por la despolarización de la membrana citoplasmática (Chen y Hoover, 2003; Stoyanova et al., 2012). La bacteriocina más representativa de este grupo es la nisina (Cintas et al., 2001).
Clase Ib. Son péptidos globulares e hidrófobos, con un peso molecular entre 1.8 y 2.1 kDa. Presentan una carga neta negativa o sin carga. Su actividad antimicrobiana está relacionada principalmente con la inhibición enzimática (Riley y Wertz, 2002). Bacteriocinas como duramicina A, B, C y la cinamisina son representativas de este grupo (Naidu et al., 2006).
2.2 Clase II. No lantibióticos
Los no lántibioticos están conformados por bacteriocinas constituidas por 30 a 60 aminoácidos (Montalbán-López et al., 2011), con un peso molecular menor a 10 kDa, no contienen aminoácidos modificados y son estables al calor y al pH (Beshkova y Frengova, 2012). Este grupo de bacteriocinas es considerado como el mayor subgrupo de bacteriocinasprovenientesdelasBAL,nosólo por su gran número, sino también por su actividad antimicrobiana y aplicaciones potenciales.
Los no-lantibióticos son subdivididos en tresgrupos:
Clase IIa. Este grupo se caracteriza por contar con una secuencia amino terminal - TirosinaGlicina - Asparagina - Glicina - Valina - XaaCisteína (-Try-Gly-Asn-Gly-Val-Xaa-Cys-; donde Xaa indica cualquier residuo de aminoácido) y contiene uno o dos puentes disulfuro (Chen y Hoover, 2003). Este grupo es reconocido principalmente por su alta actividad antimicrobiana contra Listeria (Zouhir et al., 2010). Sólo tres bacteriocinas de este grupo han sido caracterizadas: pediocina PA-1, enterocina A y divercina V41 (ChenyHoover,2003).
Clase IIb. Este grupo está conformado por bacteriocinas con dos péptidos y la actividad antimicrobiana requiere de la presencia de ambos péptidos en proporciones similares (Oppegård et al., 2007), son formadores de poros en la membrana celular. La sakacina es la bacteriocina más representativa de este grupo(Cintas et al., 2001).
Clase IIc. Poseen una estructura cíclica como resultado de la unión covalente de sus extremos carboxilo y amino terminal, son termoestables y no modificados después de la traducción (Šušković et al., 2010). Éstos carecen de la secuencia amino terminal Tirosina - Glicina - Asparagina - GlicinaValina-Xaa-Cisteína-quecontienenlaclase IIa y IIb. La enterocina AS-48 producida por Enterococcus feacalis es la bacteriocina más representativa de este grupo (Dimov et al., 2005).
2.3 Clase III. Termolábiles
Este grupo es denominado “bacteriolisinas”, incluye péptidos con un peso molecular mayor a30kDa ysonlábilesal calor(Abriouel et al., 2011). Su mecanismo de acción se realiza a través de la catálisis e hidrólisis de la pared celular de las células sensibles; las bacteriolisinas más representativas son la helveticina J producida por Lactobacillus
helveticus y la enterocina producida por Enterococcus faecium (Naidu et al., 2006).
3. Actividad antimicrobiana y modo de acción de las bacteriocinas
De acuerdo con Cintas et al. (2001) se ha determinado que las bacteriocinas demuestran alta actividad bactericida que se relaciona principalmente con el contenido de cistina; y de acuerdo a ello, se establecen las tres espectrosdeacción:
a) Bacteriocinas con espectro inhibitorio estrecho, cuyos productos inhiben microorganismosdelamismaespecie.
b) Bacteriocinas con espectro inhibitorio intermedio, cuyos productos inhiben otros géneros de BAL, bacterias Gram-positivas y patógenospresentesenalimentos.
c) Bacteriocinas con amplio espectro de inhibición que actúan contra un gran número debacteriasGram-positivas.
La mayoría de las investigaciones han demostrado que la actividad bactericida de las bacteriocinas, se dirige principalmente contra bacterias Gram-positivas (Jack et al., 1995). Sin embargo, existen numerosas bacteriocinas que presentan un amplio rango de acción, inhibiendo especies Gram-negativas (MotaMeira et al., 2000; Chung y Yousef, 2005; Gautam y Sharma, 2009), hongos patógenos (Ennahar et al., 2000) y virus (Jenssen et al., 2006).
Cotter et al. (2005) determinaron que las bacteriocinas de bacterias Gram-positivas presentan diferentes modos de acción de acuerdoasuclasificación(Fig.2).
El modo de acción de los lántibioticos se atribuye a la desestabilización (debido a la formación de poros) de las funciones de la membrana citoplasmática. La estructura de estos péptidos, α-hélice o β-laminar, pueden formar dos caras, una hidrofílica y otra
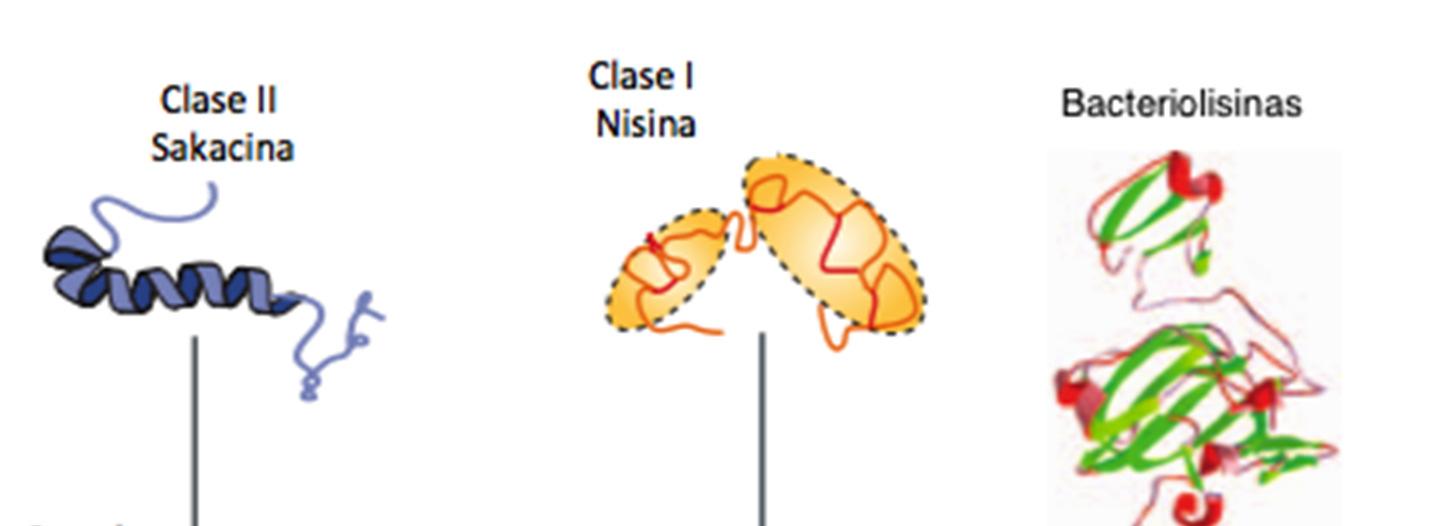
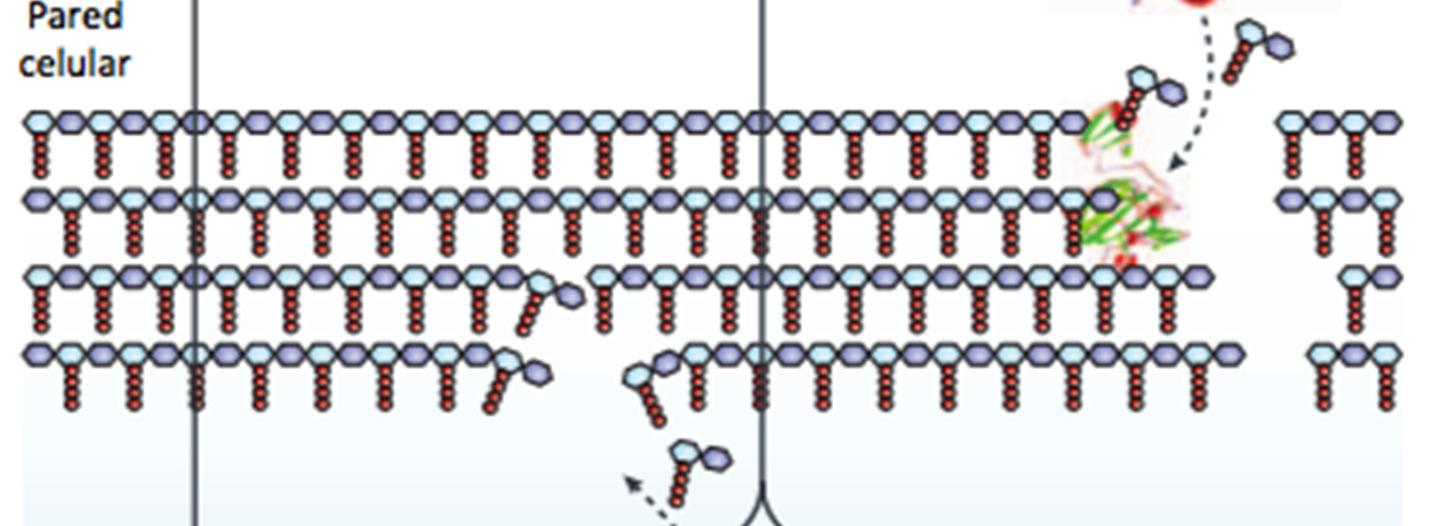
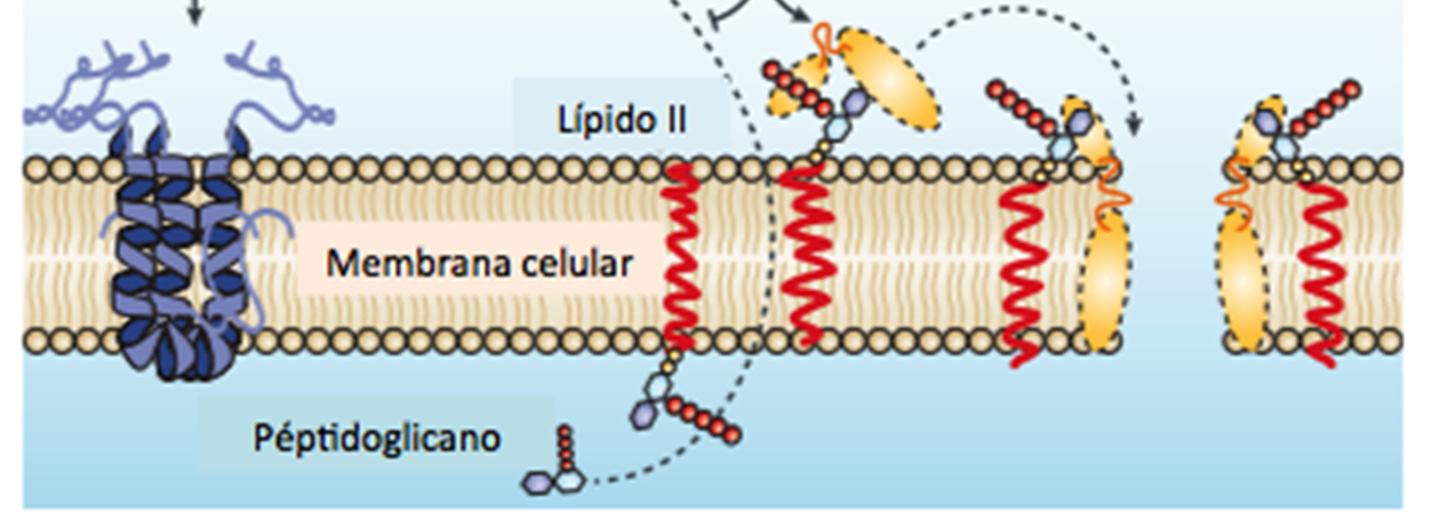
Fig. 2 Modo de acción de los lantibióticos (Clase I), no-lantibióticos (Clase II) y bacteriolisinas (Clase III) (Adaptado de Cotter etal., 2005).
hidrofóbica creando oligómeros que pueden atravesar la membrana formando poros (Chen yHoover,2003).Elladoapolardelamolécula se situará próxima a los lípidos de la membrana y el lado polar al centro del poro. Comoconsecuencia,seobservaunapérdidade iones K+, ATP y, en algunos casos aminoácidosymoléculaspequeñas.Lapérdida de estas sustancias origina a su vez una pérdida del potencial de la membrana, consumo de las reservas energéticas celulares, descenso de la síntesis de ADN, ARN y proteínas, originando la muerte celular (McAuliffe et al., 2001). Algunos miembros de la clase I, como la nisina, han demostrado
un modo de acción dual. La nisina, se une a la pared celular mediante atracciones electrostáticas, lo cual se facilita debido a la carga positiva de este péptido y las cargas negativas de los componentes de la pared celular. Posteriormente, la nisina se une al lípido II, el transportador principal de las subunidades de peptidoglicano desde el citoplasma a la pared celular, y por lo tanto previene la síntesis correcta de la pared celular, provocando la formación de un poro transmembranal permitiendo la salida de aminoácidos y ATP, lo que conduce a la muerte celular (Cotter et al., 2005; Hassan et al., 2012).
Los no-lantibióticos contienen dos péptidos en su estructura principal, los cuales pueden presentar actividades duales distribuidas a través de sus dos péptidos (Ennahar et al., 2000). En general, los péptidos de esta clase tienen una estructura anfifílica helicoidal, lo que les permite orientarse e insertarse en la membrana de la célula, provocando la muerte celular. El modo de acción principal se debe a las interacciones con la membrana celular, se inicia con el reconocimiento entre la bacteriocina y el receptor de la membrana celular, seguido de una serie de interacciones electrostáticas, quelepermiteinsertarsedentro de la membrana interfiriendo con su estructura y conduciendo a una despolarización y muerte (Hu et al., 2006). El mecanismo de la pediocina PA-1 es el más estudiado. En este caso, el extremo N-terminal de la molécula adopta una conformación β que es estabilizada por un puente disulfuro entre Cisteína-9 y Cisteína-14, para promover la unión de los aminoácidos catiónicos (Lisina-11 e Histidina12) a los fosfolípidos aniónicos, en la membrana a través de interacciones electrostáticas. Posteriormente el extremo Cterminal sufre una transformación donde el puente disulfuro entre Cisteína-24 y Cisteína44 ayuda a la formación de una estructura α–helicoidal que favorece el contacto con los lípidos de la membrana celular. La pediocina PA-1 se introduce en la membrana, causando la formación de poros y la disipación de protones lo que causa un colapso en el gradiente de la membrana, incrementando el voltaje celular y haciendo susceptible a la célula de perder iones intracelulares y ATP, absorbiendo radiación UV y evitando el transporte de aminoácidos; para finalmente provocarlamuertecelular(Naidu et al., 2006).
El mecanismo de acción de las bacteriocinas de la clase III “bacteriolisinas” es menos complejo con respecto a los lantibióticos y los no-lantibióticos, ya que actúan directamente sobre la pared celular de las bacterias Gram-positivas lo que conduce a
la muerte y lisis de la célula (Cotter et al., 2005).
Los investigadores se han centrado en realizar estudios para determinar el efecto inhibitorio que presentan las bacteriocinas sobre las bacterias Gram-negativas y han encontrado que su inhibición es menor. Esta resistencia posiblemente se debe a que éstas cuentan con la presencia de una membrana externa, conformada por lipopolisacáridos que actúa como una barrera de permeabilidad efectiva (Chung y Yousef, 2005). Debido a ello, los investigadores han propuesto la combinación de métodos, donde las bacteriocinas podrían ejercer un efecto sinérgico con tratamientos como altas presiones hidrostáticas (HHP) y pulsos eléctricos (Ananou et al., 2010; Saldaña et al., 2011). También han adicionado sustancias quelantes que hacen permeables la pared y membrana celular a las bacteriocinas permitiendo así la inactivación de las bacterias Gram-negativas(Rodgers,2001).
4. Bacteriocinas de uso potencial en alimentos
Las bacteriocinas son una opción atractiva como conservadores naturales para el desarrollo de alimentos mínimamente procesados. Actualmente, se ha demostrado que presentan alto potencial en la biopreservación de carne, productos lácteos, alimentos enlatados, pescado, bebidas alcohólicas, ensaladas, huevo, productos de panificación, vegetales fermentados, entre otros, ya sea solos o en combinación con otros métodos.
De acuerdo con lo propuesto por Cleveland et al. (2001), las bacteriocinas pueden ser utilizadas en los alimentos de las siguientes maneras:
a) Como cultivos iniciadores en alimentos fermentados.
b) Adicionadas directamente al producto, purificadasosemipurificadas.
c) Como un ingrediente en la elaboración de alimentos(aditivos).
Sin embargo, las bacteriocinas deben cumplir con importantes criterios de regulación para su aplicación en los alimentos (Gautam y Sharma, 2009) describiéndose a continuación:
a) La cepa productora debe estar dentro de la clasificaciónGRAS,esdecir,noestarasociada conproveeralgúnriesgoalasalud.
b) Deben ser reconocidas y aceptadas para su usoenalimentosporunaautoridadreguladora.
c) Deben cumplir con un espectro de inhibición que puede incluir microorganismos patógenos o tener actividad contra uno en particular.
d) Su adición en los productos debe de presentar efectos benéficos, tales como mejorarlaseguridad,calidady/osabor.
e) Alta actividad antimicrobiana a bajas concentraciones.
Entre las aplicaciones más importantes de las bacteriocinas en alimentos, se encuentran lassiguientes:
a) En los productos enlatados como en granos de elote, chícharos, papas, hongos y zanahoria se aplican para controlar el crecimiento de termófilos esporulados. Estos alimentos de baja acidez (pH mayor a 4.5), son susceptibles al crecimiento de esporas resistentes a los tratamientos térmicos como Bacillus stearothermophilus y Clostridium thermosaccharolyticum. La adición de la nisina además de inhibir dichos microorganismos, prolonga el almacenamiento de estos productos a temperatura ambiente (Delves-Broughton,2005).
b) El uso de las bacteriocinas en los productos del mar es muy complejo, debido a la constitución del producto (matriz baja en
azúcares), por lo tanto, la bacteriocina que se adicione, no debe ocasionar un deterioro en el producto, por la baja acidificación que ésta puede proveer. Sin embargo, en estos alimentos retoma importancia ya que las investigaciones actuales han demostrado la inhibición de L. monocytogenes en langosta y C. botulinum en alimentos marinos empacados con atmósferas modificadas (Pilet y Leroi, 2011).
c) En los productos cárnicos se utilizan para inhibir C. botulinum, L. monocytogenes, S. aureus, S. Typhimurium y E. coli (Naidu et al., 2006).Tambiénse busca reducir el usode los nitritos y sus derivados que pueden formar nitrosaminascarcinogénicas.
d) En el vino y cerveza, el objetivo principal es inhibir levaduras, el crecimiento de lactobacilos y pediococos como microorganismos deteriorativos. Las bacteriocinassonadicionadasenlosvinospara prevenir el crecimiento de las BAL y asegurar la ausencia de la fermentación maloláctica, evitando la disminución del pH del producto que causa defectos como la mucosidad y el exceso de acetato, que promueven un efecto negativo en la calidad del vino. En la cerveza, inhiben el crecimiento de lactobacilos y pediococos que conducen a una cerveza con exceso de acidez y sabores extraños, debido a laproduccióndediacetilo(Naidu et al., 2006).
e) El uso de las bacteriocinas en productos lácteos es más común. En los quesos, las bacteriocinas controlan el crecimiento de las BAL ya que un exceso de ellas proveerá de sabores extraños a los productos, por otro lado su aplicación promueve la aceleración de su maduración (Beshkova y Frengova, 2012). En los postres lácteos, se utilizan para extender su vida útil, ya que éstos no pueden ser completamente esterilizados sin dañar sus características sensoriales. En la leche, previene la esporulación de bacterias termofílicas resistentes al calor que pueden
sobrevivir a la pasteurización (Ekbal et al., 2012). Principalmente, la actividad antimicrobiana de las bacteriocinas en estos productos es inhibir microorganismos como Clostridium y Listeria (Cleveland et al., 2001).
Como lo demuestran los reportes de investigación, las bacteriocinas son potencialmente útiles para garantizar la inocuidad de los alimentos así como mejorar sus características sensoriales y fisicoquímicas. En la Tabla I, se muestra un resumen de algunas bacteriocinas provenientes de las BAL y sus principales aplicaciones en losalimentos.
6 - 2 (2012): 64 - 78
5. Bacteriocinas comerciales utilizadas en la industria alimentaria
5. 1 Nisina, regulación y su aplicación en los alimentos
La nisina es la bacteriocina comercial más importante y la primera aprobada para su uso en la industria alimentaria. La nisina es producida por Lactococcus lactis, es un péptido pequeño policíclico con un peso molecular de 3.4 kDa, se encuentra conformada por 34 aminoácidos, con residuos deshidratados (dehidrolanina y dehidrobutirina) y cinco anillos de lantionina
Tabla I. Bacteriocinas de uso potencialaplicadas en los alimentos.
BALBacteriocinaMicoorganismo suceptibleAlimentoReferencia
Enterococcus durans 41D Duracina GL Listeria monocytogenes SCOTT A
Queso artesanalDu et al., 2011
Lactobacilus curvatus Curvaticina FS47 L. monocytogenes Carne molidaNaidu et al., 2006
Lactobacillus sake Sakacina P
Enterococcus faecalis A-48-32
Enterocina AS-48 L. monocytogenes
Filetes de salmón
Jugo de lechugaSettanniy Corsetti, 2008 Bacillus cereus Purés y sopas de vegetales Grande et al., 2007
Alimento infantil a base de arroz Grande et al., 2006
Lactobacillus sake Sakacina L. monocytogenes CarneGarriga et al., 2002
Sakacina P L. monocytogenes
Pollo refrigeradoKatla et al., 2002
Enterococcus faecalis
Enterocina A y Enterocina B Listeria innocua CTC1014 SalchichasAymerich et al. , 2000
Lactococcus lactis Lacticina 3147
Staphylococcus aureus ATCC6538
Listeria innocua DPC1770
Leche y suero de lecheMorgan et al., 2000
Enterococcus faecalis Enterocina 226 NWC L. monocytogenes Queso mozarellaVillani et al., 1993
En 1969, la nisina fue reconocida por la Organización de las Naciones Unidas para la Alimentación y la Agricultura/Organización mundialdelasalud,FAO/WHO,porsussiglas en inglés, como un preservativo en los alimentos, pero fue hasta el año 1988 cuando la FDA aprobó su uso como un aditivo, estableciéndolo en el Código Federal de Regulaciones (CFR) título 21, apartado 184 de la sección 184.1538 “Preparación de nisina”. Su uso se permite en productos enlatados y quesos fermentados para la inhibición del crecimiento de C. botulinum y en procesos de pasteurización para inhibir L. monocytogenes, estableciendo un límite máximo de 250 ppm en el producto terminado, límite establecido por los métodos estándares del instituto británico(FDA,2012).
Debido a ello, la nisina ha sido uno de los conservadores más utilizados en la industria alimentaria, además sus características la convierten en un aditivo adaptable a la naturaleza de los alimentos; es aplicable en bebidas como vinos y cerveza, inhibiendo la fermentación de la levadura y evitando el deterioro del producto; en algunos jugos de
6 - 2 (2012): 64 - 78
frutas, es utilizada para inhibir el crecimiento de Bacillus; en lácteos, su principal aportación es la inhibición de L. monocytogenes por su alta estabilidad térmica y en productos enlatados la inhibición de C. botulinum; siendo éstas sus principales aplicaciones. La Tabla II muestra algunas de las aplicaciones más relevantes de la nisina en la industria alimentaria.
5.2 Pediocina, regulación y su aplicación en los alimentos
La pediocina es otra bacteriocina que tiene un amplio campo de aplicación en la industria alimentaria principalmente por el control que ejerce en la inhibición de patógenos como L. monocytogenes (Jack et al., 1995). La pediocina que pertenece a la clase II, nolantibióticos de la clasificación de las bacteriocinas, es sintetizada vía ribosomal por bacterias lácticas del género Pediococcus el cual está conformado por las siguientes especies: P. acidilactici, P. pentosaceus, P. damnosus, P. parvulus, P. inopinatus, P. halophilus, P. dextrinicus y P. urinaeequi (Naidu et al., 2006).
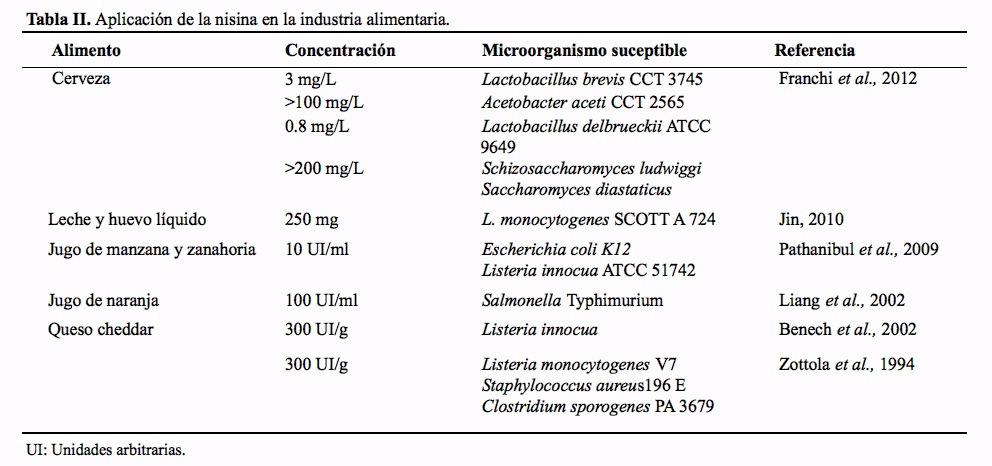
La pediocina es un péptido con un peso molecular de 4.6 kDa, se encuentra conformada por 44 aminoácidos que no se modifican postraduccionalmente. Es un péptido con carga neta positiva, anfifílico con altas regiones hidrofóbicas con la presencia de dos enlaces disufuro. Presenta un punto isoeléctrico entre 8.6 y 10. Es estable en soluciones acuosas diluidas, principalmente a pH 4 y pH 6, siendo inactivada a pH 7 (Ennahar et al., 2000). Tiene una amplia estabilidad térmica y durante periodos largos, se ha demostrado que presenta actividad inhibitoria después de un tratamiento a 80ºC durante 60 minutos (Rodríguez et al., 2002); sin embargo, en tratamientos con mayor temperatura, 120ºC, durante 15 min es parcialmente inactivada, es decir, se desnaturaliza debido a la interacción con el medio y la oxidación de las moléculas de metionina a sulfóxido de metionina (Quintero, 2006).
La pediocina junto con la nisina han sido las bacteriocinas con mayor aplicación en la industriaalimentaria; sin embargo, aunquehan demostrado alta efectividad antimicrobiana, la pediocina es comercializada y se encuentra incluida en varias patentes europeas y norteamericanas (Chen y Hoover, 2003), la FDA aún no le otorga el estatus GRAS lo que limitasuusoenlosalimentos.
La pediocina presenta un gran potencial para ser utilizada como un excelente agente antimicrobiano en los alimentos, principalmente en los cárnicos (Cleveland et al., 2001). Se han realizado varios estudios donde la pediocina es aplicada en salchichas, jugos de carne, lácteos (Cintas et al., 2001) y vegetales, principalmente para el control de bacterias deteriorativas y patógenas (Naidu et al., 2006).
La Tabla III, muestra las aplicaciones más relevantes de la pediocina en la industria alimentaria.
Conclusiones y comentarios finales
El empleo de bacteriocinas como antimicrobianos naturales es de gran interés en la industria alimentaria, principalmente por su amplio espectro antimicrobiano. Como se ha presentado, las bacteriocinas son aplicadas en una amplia variedad de productos lo que diversifica su uso, con alto potencial para sustituir a los conservadores sintéticos por naturales, abriendo paso a nuevas tecnologías enlabiopreservaciónalimentaria.
Es importante que los investigadores, intensifiquen la búsqueda de nuevas
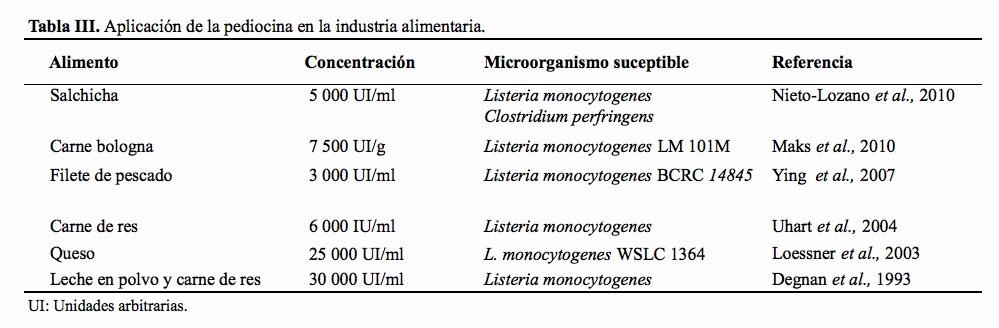
S.C. Beristain-Bauza et al. / Temas
bacteriocinas así como su análisis en los alimentos, logrando que en un futuro sean aprobadasparasuusoindustrial.
Agradecimientos
Beristain-Bauza, S.C. agradece al Consejo Nacional de Ciencia y Tecnología (CONACyT) por el financiamiento de sus estudios de doctorado y a la Fundación Universidad de las Américas Puebla (UDLAP) porlabecadeposgrado.
Referencias
Abriouel, H., Franz, C.M.A.P., Omar, N.B. y Gálvez, A. 2011. Diversity and applications of Bacillus bacteriocins. FEMS Microbiology Reviews. 35(1):201-232.
Alquicira, L. 2006. Determinación del mecanismo de resistencia a la acción inhibitoria de la bacteriocina producida por Pediococcus parvulus MXVK 133. Tesis de Maestría, Universidad Autónoma Metropolitana. México. 100 p.
Ananou, S., Garriga, M., Jofré, A., Aymerich, T., Gálvez, A., Maqueda, M., Martínez-Bueno, M. y Valdivia, E. 2010. Combined effect of enterocin AS-48 and high hydrostatic pressure to control food-borne pathogens inoculated in low acid fermented sausages. Meat Science 84(4):594-600.
Aymerich, T., Garriga, M., Ylla, J., Vallier, J., Monfort, J.M. y Hugas, M. 2000. Application of enterocins as biopreservatives against Listeria innocua in meat products. Journal of FoodProtection. 63:721-726.
Badr, S., Karem, H.A., Hussein, H. y El-Hadedy, D. 2005. Characterization of nisin produced by Lactococcus lactis International Journal of AgricultureandBiology. 7(3):499-503.
de Ingeniería de Alimentos 6 - 2 (2012): 64 - 78
Benech, R.O., Kheadr, E.E., Laridi, E., Lacroix, D. y Fliss, I. 2002. Inhibition of Listeria innocua in cheddar cheese by addition of nisin Z in liposomes or by in situ production in mixed culture. Applied and Environmental Microbiology. 68(8):3683-3690.
Beshkova, D., Frengova, G. 2012. Bacteriocins from lactic acid bacteria: microorganisms of potential biotechnological importance for the dairy industry. Engineering in Life Sciences. 12(4):1-14.
Cheigh, C-I. y Pyun, Y-R. 2005. Nisin biosynthesis and its properties. Biomedical and LifeSciences. 27(21):1641-1648.
Chen, H. y Hoover, D.G. 2003. Bacteriocins and their food applications. ComprehensiveReviews inFoodScienceandFoodSafety. 2:82-100.
Chung, H-J. y Yousef, A.E. 2005. Lactobacillus curvatus produces a bacteriocin-like agent active against gram-negative pathogenic bacteria. Food Science and Technology. 25(614):59-79.
Cintas, L.M., Casaus, M.P., Herranz, C., Nes, I.F. y Hernández, P.E. 2001. Review: bacteriocins of lactic acid bacteria. Food Science TechnologyInternational.7(4):281- 305.
Cleveland, J., Monteville, T.J., Nes, I.F. y Chikindas, M.L. 2001. Bacteriocins: safe, natural antimicrobials for food preservation. International Journal of Food Microbiology 71(1):1-20.
Cotter, P.D., Hill, C. y Roos, R.P. 2005. Bacteriocins: developing innate immunity for food. Nature Reviews Microbiology. 3(10):777788.
Degnan, A.J., Buyong, N. y Luchansky, J.B. 1993. Antilisterial activity of pediocin AcH in model food systems in the presence of an emulsifier or encapsulated within liposomes. International JournalofFoodMicrobiology. 18(2):127-138.
Delves-Broughton, J. 2005. Nisin as a food preservative. FoodAustralia. 57(12):525:527.
De Vuyst, L. y Leroy, F. 2007. Bacteriocins from lactic acid bacteria: Production, purification, and food applications. Journal of Molecular
MicrobiologyandBiotechnology.13:194-199.
Dimov, S.G., Ivanova, P.M., Harizanova, N.T. y Ivanova, I.V. 2005. Bioactive peptides used by bacteria in the concurrence for the ecological niche: general classification and mode of action (overview). Biotechnology and BiotechnologicalEquipement.(2):3-22.
Du, L., Somkuti, J., Renye, J. y Huo, G. 2011. Properties of durancin GI, a new antilisterial bacteriocin produced by Enterococcus durans 41D. JournalofFoodSafety. 32: 74-83.
Ekbal, M., Ibrahim, A. y Elbarbary, H.A. 2012. Effect of bacteriocin extracted from Lactobacillus acidophilus on the shelf-life of pasteurized milk. JournalofAmericanScience. 8(2): 620-626.
Ennahar, E., Sashihara, T., Sonomoto, K. y Ishizaki, A. 2000. Class IIa bacteriocins: biosynthesis, structure and activity. FEMS MicrobiologyReviews. 24(1):85-106.
FDA. 2012. Code of Federal Regulations (anual edition). Title 21-Food and Drugs. http://www.gpo.gov/fdsys/browse/collectionCfr .action;jsessionid=PJygQQ3hC6bGHVcCxp1D t2dh9ZbVn9JW3LlJ5qhnLXr7YpDhTw1R!394132962!533076816?selectedYearFrom=201 2&page.go=Go, accesada 12/09/2012.
Franchi, M., Tribst, A. y Cristianini, M. 2012. The effect of antimicrobials and bacteriocins on beer spoilage microorganisms. International FoodResearchJournal. 19(2):783-786.
Garriga, M., Aymerich, M.T., Costa, S., Monfort, J.M. y Hugas, M. 2002. Bactericidal synergism through bacteriocins and high pressure in a meat model system during storage. Food Microbiology. 19(5):509-518.
Gautam, N. y Sharma, N. 2009. Bacteriocin: safest approach to preserve food products. Indian JournalMicrobiology. 49(3):204-211.
Grande, M., Lucas, R., Abriouel, H., Valdivia, E., Nabil, B., Maqueda, M., Martínez-Bueno, M., Martínez-Cañamero, M. y Gálvez, A. 2006. Inhibition of toxicogenic Bacillus cereus in rice-based foods by enterocin AS-48. International Journal of Food Microbiology 106:185-194.
6 - 2 (2012): 64 - 78
Grande, M., Abriouel, H., López, R., Valdivia, E., Nabil, B., Martínez-Cañamero, M. Y Gálvez, A. 2007. Efficacy of enterocin AS-48 against Bacilli in ready-to-eat vegetable soups and purees. Journal of Food Protection. 70:23392345.
Guder, A., Wiedemann, I. y Sahl, H.G. 2000. Posttranslationally modifier bacteriocins-the lantibiotics. Biopolymers. 55(1):62-73.
Hassan, M., Kjos, M., Diep, D.B. y Lotfipour, F. 2012. Natural antimicrobial peptides from bacteria: characteristics and potential applications to fight against antibiotic resistance. Journal of Applied Microbiology. 1:1-14.
Hu, H., Moake, M. y Worobo, R. 2006. Genetic characterization of antimicrobial peptides. En: Shetty, K., Paliyath, G., Pometto, A. y Levin, R.E. (Eds). Food Biotechnology. Segunda edición, CRC Press, Boca Raton, Florida. pp.1349-1478.
Jack, R.W., Tagg, J.R. y Ray, B. 1995. Bacteriocins of gram-positive bacteria. MicrobiologicalReviews. 59(2):171-200.
Jeevaratnam, K., Jamuna, M. y Bawa, A.S. 2005. Biological preservation of foods- bacteriocins of lactic acid bacteria. Indian Journal of Biotechnology. 4:446-454.
Jenssen, H., Hamill, P. y Hancock, R.E.W. 2006. Peptide antimicrobial agents. Clinical MicrobiologyReviews. 19(3):491-511.
Jin, T. 2010. Inactivation of Listeria monocytogenes in skim milk and egg white by antimicrobial bottle coating with polylactic acid and nisin. Journal of Food Science. 75(2): M83-M88.
Katla, T., Moretro, T., Sveen, I., Aasen, I., Axelsson, L., Rorvik, L. y Naterstad, K. 2002. Inhibition of Listeria monocytogenes in chiken cold cuts by addition of sakacina P and sakacin P- producing Lactobacillus sakei Journal AppliedMicrobiology. 93(2):191-196.
Liang, Z., Mittal, G.S. y Griffiths, M.W. 2002. Inactivation of Salmonella Typhimurium in orange juice containing antimicrobial agents by pulsed electric field. Journal of Food
Protection. 65(7):1081-1087.
Liu, W. y Hansen, N. 1990. Some chemical and physical properties of nisin, a small-protein antibiotic produced by Lactococcus lactis. Applied and Environmental Microbiology. 56(8): 2551-2558.
Loessner, M., Guenther, S., Steffan, S. y Scherer, S. 2003. A pediocin-producing Lactobacillus plantarum strain inhibits Listeria monocytogenes in a multispecies cheese surface microbial ripening consortium. Applied and EnviromentalMicrobiology. 69(3):1854-1857.
Maks, N., Zhu, L., Juneja, V. y Ravishankar, S. 2010. Sodium lactate, sodium diacetate and pediocin: effects and interactions on the thermal inactivation of Listeria monocytogenes on bologna. FoodMicrobiology. 27:64-69.
McAuliffe, O., Ross, R.P. y Hill, C. 2001. Lantibiotics: structure, biosynthesis and mode of action. FEMS Microbiology Reviews. 25(3):285-308.
Montalbán-López, M., Sánchez-Hidalgo, M., Valdivia, E., Martínez-Bueno, M. y Maqueda, M. 2011. Are bacteriocins underexploited? novel applications for old antimicrobials. Current Pharmaceutical Biotechnology. 12(8):1205-1220.
Morgan, S.M., Roos, R.P., Beresford, T. y Hill, C. 2000. Combination of hydrostatic pressure and lacticin 3147 causes increased killing of Staphylococcus and Listeria. Journal of AppliedMicrobiology. 88:414-420.
Mota-Meira, M., LaPointe, G., Lacroix, C. y Lavoie, M.C. 2000. MICs of mutacin BNy266, nisina A, vancomycin, and ozacillin against bacterial pathogens. Antomicrobial AgentsandChemotherapy. 44(1): 24-29.
Naidu, A.S., Unal, R. y Tulpinski, J. 2006. Bacteriocins: antimicrobial activity and applications. En: Shetty, K., Paliyath, G., Pometto, A. y Levin, R.E. (Eds). Food Biotechnology. Segunda edición, CRC Press, Boca Raton, Florida. pp. 1391-1437.
Nes, I.F., Yoon, S-S. y Diep, D.B. 2007. Ribosomally synthesized antimicrobial peptides
6 - 2 (2012): 64 - 78
(bacteriocins) in lactic acid bacteria: a review. FoodScienceBiotechnology. 16(5):657-690.
Nieto-Lozano, J., Reguera-Useros, J., PeláezMartínez, M., Sacristán-Pérez-Minayo, G., Gutierrez-Fernández, A. y Hardisson de la Torre, A. 2010. The effect of the pediocin PA-1 produced by Pediococcus acidilactici against Listeria monocytogenes and Clostridium perfringens in Spanish dry-fermentes sausages and frankfurters. FoodControl. 21(5):679-685.
Oppergård, C., Rogne, P., Emanuelsen, L., Kristiansen, P.E., Fimland, G. y Nissen-Meyer, J. 2007. The two-peptide class II bacteriocins: structure, production, and mode of action. Journal of Molecular Microbiology and Biotechnology. 13(4):210-219.
Pathanibul, P., Taylor, T., Davidson, P. y Harte, F. 2009. Inactivation of Escherichia coli and Listeria innocua on apple and carrot juices using high pressure homogenization and nisin International Journal of Food Microbiology. 129: 316-320.
Pilet, M-F. y Leroi, F. 2011. Applications of protective cultures, bacteriocins and bacteriophages in fresh seafood and seafood products. In Protective Cultures, Antimicrobial Metabolites and Bacteriophages for Food and BeverageBiopreservation. 1:1-21.
Quintero, B.S. 2006. Incorporación de la pediocina producida por Pediococcus parvulus MXVK133 en películas y recubrimientos comestibles Tesis Doctoral, Universidad AutónomaMetropolitana. México. 111 p.
Riley, M.A. y Wertz, J.E. 2002. Bacteriocins: evolution, ecology and application. Annual Review of Microbiology. 56:117-137.
Rodgers, S. 2001. Preserving non-fermented refrigerated foods with microbial cultures-a review. Trends in Food Science and Technology. 12(8):276-284.
Rodríguez, J.M., Martínez, M.I. y Kok, J. 2002. Pediocin PA-1, a wide-spectrum bacteriocin from lactic acid bacteria. Critical Reviews in FoodScienceandNutrition. 42(2): 91-121.
Saldaña, G., Minor-Pérez, H., Raso, J. y Álvarez, I
2011. Combined effect of temperature, pH, and presence of nisin on inactivation of Staphylococcus aureus and Listeria monocytogenes by pulsed electric fields. Foodborne Pathogens and Disease. 8(7):797802.
Savadogo, A., Ouattara, A.T., Bassole, H.N. y Traore S.A. 2006. Bacteriocins and lactic acid bacteria - a minireview. African Journal of Biotechnology.5(9):678-683.
Settanni, L. y Corsetti, A. 2008. Application of bacteriocins in vegetable food biopreservation. International Journal of Food Microbiology. 121: 123-138.
Stoyanova, L.G., Ustyugova, E.A. y Netrusov, A.I. 2012. Antibacterial metabolites of lactic acid bacteria: their diversity and properties. Applied BiochemistryandMicrobiology. 48(3):229-243.
Suárez, G.A. 1997. Producción de anticuerpos frente a la nisina A: estrategias de inmunización y desarrollo de inmunoensayos. Tesis de Doctorado, Universidad Complutense de Madrid. España. 272 p.
Šušković, J., Kos, B., Beganović, J., Leboš, A., Habjanič, K. y Matošić, S. 2010. Antimicrobial activity - the most important property of probiotic and starter lactic acid bacteria. Food TechnologyandBiotechnology.48(3):296-307.
6 - 2 (2012): 64 - 78
Uhart, M., Ravishankar, S. y Marks, N.D. 2004. Control of Listeria monocytogenes with combined antimicrobials on beef franks stored at 4 degrees. Journal of Food Protection. 67(10):2296-2301.
Villani, F., Salzano,G., Sorrentino, E., Pepe, O., Marino, P. y Coppola, S. 1993. Enterocin 226NWC, a bacteriocin produced by Enterococcus faecalis 226, active against Listeriamonocytogenes. TheJournalofApplied Bacteriology. 74:380–387.
Wu, C.W., Yin, L.J. y Jiang, S.T. 2004. Purification and characterization of bacteriocins from Pediococcus pentosaceus ACCEL. Journal of Agricultural and Food Chemistry. 52:1146-1151.
Ying, L-Y., Wu, C-W. y Jiang S-T. 2007. Biopreservative effect of pediocin ACCEL on refrigerates seafood. Japanese Society of FischeriesScience. 73:907-912.
Zottola, E.A., Yezzi, T.L., Ajao, D.B. y Roberts R.F. 1994. Utilization of cheddar cheese containing nisin as an antimicrobial agent in other foods. International Journal of Food Microbiology. (1-2):227-238.
Zouhir, A., Hammami, R., Fliss, I. y Hamida, J.B. 2010. A new structure-based classification of gram-positive bacteriocins. Protein Journal 29(6):432-439.

Temas Selectos de Ingeniería de Alimentos 6 - 2 (2012): 79 - 93

Radiación ultravioleta en jugos de frutas: fundamentos y aplicaciones
A. S. López-Díaz*, E. Palou y A. López-Malo
Departamento de Ingeniería Química, Alimentos y Ambiental, Universidad de las Américas Puebla. Ex hacienda Sta. Catarina Mártir S/N, San Andrés Cholula, Puebla. C.P.72810. México.
Resumen
La radiación ultravioleta de onda corta (UVC) ha sido utilizada exitosamente para inactivar microorganismos que contaminan el agua y superficies de diversos materiales. Esta tecnología aplicada a alimentos promueve la inactivación microbiana, obteniendo productos con menor cambio en sus propiedades sensoriales y valor nutritivo. Actualmente, se ha incrementado el interés de la aplicación de radiación UVC para reducir la carga microbiana en jugos de frutas; sin embargo, se requiere de más investigación acerca de su efecto sobre la pérdida de nutrientes y capacidad antioxidante, tomando en cuenta que cada jugo necesita una dosis de tratamiento distinto según sus características. El objetivo de este artículo es proveer información acerca de los principios básicos de la radiación UVC, su aplicación en alimentos líquidos y la cinética de inactivación microbiana, haciendo énfasis en el tratamiento de jugos de frutas. Además, se revisarán las aplicaciones y eficacia de la radiación UVC en las investigaciones realizadas.
Palabras clave: radiación ultravioleta de onda corta, jugos de frutas, inactivación microbiana.
Abstract
The short-wave ultraviolet light has been used successfully to inactivate microorganisms contaminating water and surfaces of various materials. This technology applied to food promotes microbial inactivation, obtaining safer products with less change in their sensory properties and nutritional value. Currently, the interest in the application of short-wave ultraviolet light to reduce the food microbial load in fruit juices has increased; however, more research is needed about the effect on the loss of nutrients and antioxidant capacity, considering that each juice needs a different treatment dose according to its characteristics. The aim of this article is to provide information about the basic principles of short-wave ultraviolet light, its application in liquid foods, and food-borne microbial inactivation kinetics, emphasizing the treatment of fruit juices. In addition, the efficacy of the short-wave ultraviolet light and its applications will be reviewed.
Keywords: short-wave ultraviolet light, fruit juices, microbial inactivation.
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: andrea.lopezdz@udlap.mx
Introducción
Los distintos métodos de conservación de alimentospretendenincrementarlavidaútilde los productos durante su almacenamiento, aplicando técnicas que logren inhibir alteraciones microbianas, pero manteniendo su calidad. Para esto, muchos productos son tratados térmicamente, lo cual muchas veces modifica las características, tanto sensoriales (textura, sabor y color), como nutricionales (pérdidas de vitaminas, principalmente) del alimento. Debido a estos efectos adversos de los tratamientos a altas temperaturas, se encuentran en desarrollo procesos no térmicos de conservación, también denominados tecnologías emergentes. Son poco agresivos y tienen la ventaja de ofrecer productos semejantes a los frescos, manteniendo la calidad nutrimental y sensorial, y cumplir así conlasdemandasactualesdelmercado.
Uno de los métodos físicos de inactivación microbiana es la irradiación de alimentos líquidos con radiaciones ultravioleta de onda corta (UVC). Estas radiaciones se ubican en la región de energía del espectro electromagnético comprendida entre los 200 y 300 nm, el cual es el rango germicida. Los microorganismos son destruidos por la penetración de las radiaciones, las cuales son absorbidas por el ADN de éstos, causando una modificación en sus componentes, alterando su reproducción genética y quedando inhabilitadosparareplicarse(González,2001).
La aplicación de radiación UVC para destruir microorganismos no es nueva; ha sido reportada como un método efectivo para inactivar bacterias que contaminan agua y superficies de diversos materiales (Sizer y Balasubramaniam, 1999). Sin embargo, recientemente se ha reportado la aplicación de radiación UVC en el tratamiento de jugos y néctares de frutas, que a diferencia del agua, contienen diferentes componentes que se
oponenalapenetracióndelaradiación(Ochoa et al.,2011).
En el año 2000, el Departamento de Agricultura de los EE.UU. (USDA, por sus siglas en inglés) y la Administración de Alimentos y Medicamentos (FDA, por sus siglas en inglés), llegaron a la conclusión de que el uso de la radiación ultravioleta es seguro En ese mismo año, la FDA aprobó la radiación UVC como tratamiento alternativo a la pasteurización de jugos de frutas (FDA, 2000). El criterio de procesamiento definido por la FDA para el tratamiento de jugos de frutas es una reducción de cinco ciclos logarítmicos en el número del microorganismo en cuestión. Además, la definición de "pasteurización" para los alimentos ha sido revisada recientemente y ahora incluye a cualquier proceso, tratamiento o combinación de los mismos, que se aplica a los alimentos para reducir los microorganismos indeseables enunproducto(Koutchma,2008).
La radiación ultravioleta, como nuevo método de conservación, requiere de estudios profundos sobre los efectos benéficos, así comosobrelasdesventajasque pudieracausar enlosalimentos.Elobjetivodeesteartículoes proveer información acerca de los principios básicos de la radiación ultravioleta y la cinética de inactivación microbiana, haciendo énfasis en el tratamiento de jugos de frutas. Además, se revisarán las investigaciones realizadas en los últimos años sobre la aplicación de la radiación UVC para la conservacióndejugosdefrutas.
Revisión bibliográfica
1. Deterioro de los jugos de frutas
En general, los alimentos son perecederos, por lo que necesitan ciertas condiciones de tratamiento, manipulación y conservación. Si
los alimentos no son tratados adecuadamente, se producen cambios en la textura, color, olor y sabor (Domínguez y Parzanese, 2011). El deterioro de los alimentos es debido a tres alteraciones: químicas, físicas y biológicas (Argaiz et al., 2004). En el caso particular de los jugos de frutas, el oxígeno tiene un efecto negativo sobre algunas vitaminas, colores y sabores; además contribuye al crecimiento de microorganismos aerobios. Por otra parte, la luz destruye algunas vitaminas (riboflavina, vitaminas A yC) y afecta el color (Koutchma, 2008). A pesar de lo anterior, la proliferación de los microorganismos en los jugos es generalmente la causa principal de la descomposicióndeéstos.
Los microorganismos que se pueden encontrar en los jugos son: bacterias lácticas, mohos ylevaduras (Ancasi et al., 2006). Estos microorganismos, como consecuencia de su actividad metabólica, alteran los jugos, reduciendo su vida útil (Jay et al., 2006). Los mohosquecausandeterioroenestosproductos toleran una alta presión osmótica, un bajo pH y suelen crecer a temperaturas de refrigeración. Las levaduras no sólo pueden causar alteraciones sensoriales sino también producir gran cantidad de CO2 durante la fermentación de los monosacáridos (como en el caso de Zygosaccharomyces bailii) y en jugos enlatados el envase suele estallar o deformarse(Battey et al.,2002).
Algunas levaduras alteran el ambiente cambiando el pH o degradando los agentes antimicrobianos provenientes de ácidos orgánicos. Otras, como Saccharomyces cerevisiae y Z bailii, pueden crecer incluso a pH 2.8 y además en jugos concentrados (hasta niveles de 50° Brix), debido a que tienen un sistema enzimático que produce solutos compatibles (Ancasi et al., 2006). Las especies de levaduras presentes con mayor frecuencia en jugos y bebidas sin alcohol contaminados son: Brettanomyces bruxellensis, Candida tropicalis, Candida
stellata, Debaryomyces hansenii, Hanseniaspora uvarum, Issatchenkia orientalis, Pichia anomala, S. cerevisiae, Torulaspora delbrueckii, Z. bailii y Z. rouxii (Kurtzman y Fell, 1998; Arias et al., 2002). Otras especies contaminantes son Citeromyces matritensis, Metschnikowia pulcherrima, Pichia jadinii, Pichia subpelliculosa y Rhodotorula glutinis (DéakyBeuchat,1998).
Encuantoalaalteraciónenzimática,unode los principales defectos en la calidad de los jugos es la pérdida de turbidez a lo largo de su almacenamiento(“cloudloss”).Estefenómeno es causado por una enzima de origen vegetal, la pectin metil esterasa (PME), la cual tiene la función de degradar pectinas. Como consecuencia, el jugo pierde su turbidez característica, dando lugar a un líquido claro con un precipitado en el fondo. Además los jugos frescos, especialmente el de manzana, sufren con la exposición al aire, un oscurecimiento de origen enzimático (pardeamiento enzimático) que disminuye la calidad del producto (Marshall et al., 1985). Para el caso de los jugos de piña, guayaba y mango,laPME causa problemasdegelación y formacióndegrumos(Domínguez,2004).
2. Conservación de jugos de frutas
Laconservacióndelosalimentosincluyetodas las acciones realizadas para mantener el alimento con las propiedades deseadas por el mayor tiempo posible y garantizar la ausencia de microorganismos patógenos (Rahman, 1999; Alzamora y López-Malo, 2002). Los distintos métodos de conservación de alimentospretendenincrementarlavidaútilde los productos durante su almacenamiento, idealmente, aplicando técnicas que logren la inhibición o inactivación del crecimiento microbiano,peromanteniendolacalidad.
Existen regulaciones que especifican que se requieren procedimientos para inhibir microorganismos patógenos en los jugos, los cuales exigen una reducción de 5 ciclos logarítmicos del número de microorganismos (FDA, 2000). El tratamiento más utilizado es la pasteurización térmica, la cual puede provocarcambiossustancialesenelsabor. Por otro lado, la demanda de productos frescos y mínimamente procesados sin conservadores, promueve el uso de nuevas tecnologías (tratamientos no térmicos), las cuales son una alternativa a los tratamientos tradicionales de conservación.
2.1. Tratamientos térmicos
La mayoría de las tecnologías empleadas para la conservación de alimentos incluye: procedimientos que evitan que los microorganismos lleguen a los alimentos, procedimientos que inactivan a los microorganismos o procedimientos que previenen o reducen la velocidad de crecimiento de los mismos. Las tecnologías tradicionales de conservación comprenden procedimientos que actúan en cualquiera de estas tres formas (Gould, 1995). La eficacia de estos métodos depende de manera importante del cuidado en la higiene durante la producción, siendo su objetivo disminuir la cargamicrobianayevitarsudesarrollo.
Existen varias técnicas de conservación de jugos que inactivan microorganismos patógenos y alterantes, pero los más utilizados son los tratamientos térmicos. Uno de los métodos más comunes es la pasteurización, la cual consiste en un calentamiento a temperaturas menores que la de ebullición. El objetivo es destruir a los microorganismos patógenos y además inactivar las enzimas pectolíticas que hidrolizan la pectina y causan la precipitación de los sólidos en suspensión. Existen diferentes tratamientos térmicos, que varían en la temperatura y el tiempo de proceso. Las condiciones de pasteurización
son escogidas para cada bebida en base a sus propiedades específicas. En el caso de los jugos, la pasteurización se realiza a 95°C por 30segundos(Madrid,1994).
El procesamiento térmico de jugos a altas temperaturas si bien elimina la posibilidad de daño microbiológico y reduce la actividad enzimática, afecta la calidad del producto (Acevedo et al., 2004), modificando las características tanto sensoriales (textura, sabor y color), como nutricionales (principalmente pérdida de vitaminas) (Domínguez y Parzanese,2011).
2.2. Tratamientos no térmicos
Debido a los efectos adversos de los tratamientos a altas temperaturas para el tratamiento de alimentos líquidos, se encuentran en desarrollo procesos no térmicos de conservación, también denominados tecnologías emergentes (Domínguez y Parzanese, 2011). Éstas son poco agresivas y tienen la ventaja de ofrecer productos semejantes a los frescos, garantizando la inocuidad. Los métodos no térmicos de conservación de alimentos se han desarrollado para eliminar (o por lo menos minimizar) la degradación de la calidad de los alimentos que resultan del procesado térmico; y están bajo una intensa investigación para evaluar su potencial como procesos alternativos o complementarios a los métodos tradicionales deconservacióndealimentos(Pelayo,2009).
Durante el procesado no térmico, la temperatura del alimento se mantiene por debajo de la temperatura que normalmente se utilizaenelprocesadotérmico.Porlotanto,se espera que durante el procesado no térmico las vitaminas y los compuestos responsables del aroma y sabor no experimenten cambios o que éstos sean mínimos. Actualmente se están estudiando métodos físicos para la conservación de alimentos, como la aplicación de altas presiones hidrostáticas, pulsos
eléctricos, pulsos magnéticos, ultrasonido e irradiación con radiación ultravioleta de onda corta (UVC) (Barbosa-Cánovas et al., 1998; López-Malo yPalou,2004;Herrero yRomero, 2006).
Las altas presiones hidrostáticas se aplican sobre los alimentos de manera uniforme durante un tiempo variable, que puede oscilar desde unos minutos hasta incluso algunas horas, y tiene como efecto, la destrucción de microorganismos. En países como Japón, Estados Unidos y Alemania, pueden encontrarse en el mercado jugos y concentrados de frutas presurizados (Herrero y Romero,2006).
En la técnica de pulsos eléctricos, el efecto sobre los microorganismos se basa en la alteración o destrucción de la pared celular, cuando se aplica una intensidad de campo eléctrico que da lugar a una diferencia de potencial entre ambos lados de la membrana. Cuandoestadiferenciadepotencial alcanzaun valorcríticodeterminado,quevaríaenfunción del tipo de microorganismo, origina una formación de poros irreversibles en la membrana celular (electroporación) y en consecuencia, la pérdida de su integridad, incremento de la permeabilidad y finalmente destrucción de la célula afectada (BarbosaCánovas et al., 1998). Los jugos de frutas son un alimento idóneo para este método de conservación, y además es una de las mejores alternativas a los métodos convencionales de pasteurización, lo que hizo que se denominara pasteurizaciónfría.
Con pulsos magnéticos, el efecto conservador se debe fundamentalmente, a dos fenómenos: la ruptura de la molécula del ADN, de ciertas proteínas y de enlaces covalentes en moléculas con dipolos magnéticos. Los alimentos idóneos para someterse a este proceso de conservación son: jugos de frutas tropicales en soluciones azucaradas(HerreroyRomero,2006).
El ultrasonido también se utiliza generalmente para prolongar la vida útil de alimentos líquidos, tales como jugos de frutas. El efecto conservador del ultrasonido está asociado a los fenómenos complejos de cavitación gaseosa, que explican la generación y evolución de microburbujas en un medio líquido.
Por último, se encuentra la radiación UVC, la cual ha sido aprobada por la FDA como una novedosa tecnología para el tratamiento de jugos de frutas, la cual se explicará a continuaciónconmásdetalle(FDA,2000).
3. Radiación UVC
3.1. Generalidades
La radiación ultravioleta (UV), producida por el sol, es un agente esterilizador natural. Está ubicada en una región de energía del espectro electromagnético que se encuentra situada entre la luz visible y los rayos X, con una longitud de onda entre 10 y 400 nm. Se puede subdividir en: UV de vacío (10-200 nm), UV deondacortaUVC(200-280nm),UVdeonda media UVB (280-315 nm) yUV de onda larga UVA (315-400 nm) (González, 2001; Guerrero-Beltrán y Barbosa-Cánovas, 2004).
La máxima eficiencia para la desinfección se sitúa en el intervalo de la UVC, específicamente en 254 nm. En la Fig. 1 se muestra la región ultravioleta en el espectro electromagnético.
3.2. Mecanismo de acción de la radiación UVC
A excepción de las bacterias fotosintéticas, la mayoría de los microorganismos son susceptibles al daño por la radiación UV (Mendonca, 2002). El efecto destructivo de la radiación UV sobre los microorganismos está en función de la longitud de onda. Como se mencionó anteriormente, la radiación UV de longitud de onda a 254 nm, se absorbe en un
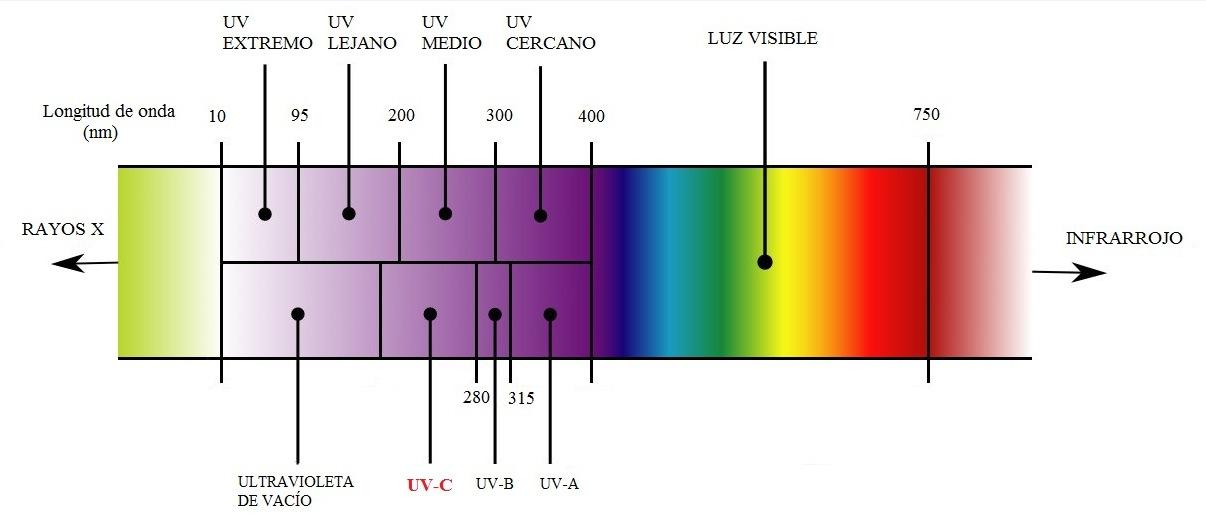
nivel que es suficiente para la desinfección; esto se debe a que ocasiona cambios físicos en los electrones y el rompimiento de enlaces en el ácido desoxirribonucleico (ADN), inactivando así los procesos de crecimiento y reproducción microbiana (Bolton y Cotton, 2001). La alta capacidad del ADN de absorber la radiación UVC se debe a las bases nitrogenadas, tanto las purinas como las pirimidinas, siendo estas últimas las más sensibles, especialmente la timina (Shama, 1999). La timina es la única base que tras la exposición a la radiación UVC sufre una reacción fotoquímica formando fuertes enlaces covalentes entre ellas (dímeros de timina) que alteran gravemente el material genético. Por lo tanto, cuando estos microorganismos se exponen a la radiación UV de 254 nm, ésta atraviesalaparedcelular,llegahastaelnúcleo, y si encuentra una región del ADN con dos timinas adyacentes, una de las bases absorbe un fotón y se forma un dímero de alta energía (AdamsyMoss,1995).Estosdímerosimpiden la replicación correcta del ADN, de forma que este método de desinfección se basa en la formación de suficientes parejas de dímeros para impedir la reproducción celular (Shama,
1999; Sastry et al., 2000; Bolton y Cotton, 2001). En la Fig. 2 se muestra una la molécula de ADN normal y la modificada por la radiación UVC. Estudios recientes han demostrado que la inactivación celular podría producirse debido a que la alteración del material genético pone en marcha señales que inducen la apóptosis celular (Álvarez, 2008).
De esta manera, la radiación UVC es un métodoeficienteparadesinfectarlíquidostales comoaguayjugos.
La resistencia de los microorganismos a los tratamientos de UVC está determinada principalmente por su capacidad para reparar el daño ocasionado sobre el ADN. Es entonces, cuando ocurre la fotorreactivación. El ADN puede ser reparado por factores proteínicos (Yajima et al., 1995) cuando las células dañadas se exponen a longitudes de onda superiores a 330 nm (Liltved y Landfald, 2000). Sepuedeestimularlaseparacióndelos dímeros del ácido nucleico mediante la activación de la enzima fotoliasa que monomeriza los dímeros (separación de timinas y otras pirimidinas) formados después del procesoderadiación(Stevens et al.,1998).
Fig. 1. Espectro electromagnético (Adaptada de Domínguez y Parzanese, 2011).

Fig. 2. Modificaciones en el ADN debido al tratamiento con radiación UVC (Adaptada de Álvarez, 2008).
Cabe mencionar que un ambiente oscuro puede evitar la fotorreactivación de productos tratados con radiación UVC. Las células que ya han experimentado una fotorreactivación, pueden ser más resistentes a la radiación UVC cuando se aplica un segundo tratamiento (Sastry et al.,2000).
3.3. Dosis UVC y cinética de inactivación microbiana
Para una desinfección eficaz es importante conocer la dosis de radiación ultravioleta necesaria para reducir la carga microbiana (González, 2001). La dosis de radiación UVC se obtiene del producto entre la intensidad yel tiempo de reacción. Esta relación se muestra en la Ec. 1. La intensidad (I) es la cantidad de energía de radiación UVC por unidad de área, medida en watts por metro cuadrado. El tiempo de reacción o de contacto (t) es el tiempo que el fluido es expuesto a la radiación UVC en el foto reactor (medido en segundos). La dosis de radiación UVC (D) es expresada en J/m² (1 Joule = 1 Watt x segundo) (Domínguez y Parzanese, 2011); aunque tambiénsueleexpresarseenmJ/cm2 .
=( )( ) (Ec.1)
La resistencia microbiana a la radiación UVC está dada de la siguiente manera: bacterias Gram-negativas < Gram-positivas < levaduras < esporas bacterianas < mohos < virus(Shama,1999;Sastry et al.,2000;Bolton y Cotton, 2001). Para asegurar una inactivación apropiada de microorganismos en jugos, la dosis de radiación debe ser mayor a 400 J/m2 en todo el producto (López-Malo y Palou, 2004; Sastry et al., 2000; Bintsis et al., 2000). La Tabla I muestra las dosis de radiaciónUVC requeridasparalainactivación de diversos microorganismos en alimentos líquidos.
La resistencia de los microorganismos se estudia sometiendo una población microbiana a la acción de la radiación UVC a una intensidad constante y se determina cómo va disminuyendo la cantidad de microorganismos de la población a lo largo del tiempo. Dicha evolución se representa en una gráfica de supervivencia, donde el eje de las ordenadas representa el logaritmo decimal de la concentración de los microorganismos supervivientes al tratamiento y el eje de las abscisas el tiempo de tratamiento. Generalmente en los estudios de resistencia microbiana a los distintos agentes letales se
Tabla I. Dosis de radiación UVCrequeridas para la inactivación de diversos microorganismos en alimentos líquidos.
MicroorganismoDosis UV, mJ/cm2 Reducción logarítmica
Sidra de manzana Escherichia coli O157:H79-613.8
Sidra de manzana Cryptosporidium parvum oocyst 14.325
Sidra de manzana Escherichia coli K1214.53-4
Sidra de manzana Saccharomyces cerevisiae 5.1351.34
Listeria innocua 4.29
Escherichia coli 5.1
Jugo de naranjaBacterias mesófilas aerobias12.3-1202
Levaduras, Mohos3
Saccharomyces cerevisiae 5.1352.71
Bacterias mesófilas aerobias, Levaduras, Mohos2.94
Néctar de mango
Saccharomyces cerevisiae 5.1352.71
Bacterias mesófilas aerobias, Levaduras, Mohos2.94
Sidra de manzana Escherichia coli K120.75<1
Jugo de guayabaLevaduras21.51.2
Jugo de piñaMohos21.51
Adaptado de Koutchma (2009).
obtienen 4 tipos de gráficas de supervivencia: gráficas de supervivencia lineales, gráficas de supervivencia con hombro, gráficas de supervivencia con cola y gráficas de supervivencia sigmoideas (ver Fig. 3) (Alzamora y López-Malo, 2002). En la mayoría de los tratamientos con radiación UVC, no existe una relación lineal entre el logaritmo de la fracción de supervivientes y la dosis, sino que las curvas de supervivencia obtenidas son generalmente sigmoideas. En ellas,seobservaprimero unamesetainicial (lo que se denomina “hombro”), que corresponde a la fase de acumulación de lesiones en el ADN hasta alcanzar un determinado umbral quesuperalacapacidaddereparacióncelulare induce su inactivación. A partir de este punto, los microorganismos supervivientes empiezan a disminuir. Al final de la curva, aparece una cola que puede deberse a la presencia de microorganismos resistentes, agregados celularesqueprotegena lascélulasdel interior
o sólidos en suspensión que protegen a los microorganismos de la irradiación (sombras) o ladipersan (Sastry et al., 2000).
El uso de la cinética de inactivación de primer orden para el modelado de gráficas de supervivencia fue propuesto por Chick en el año 1908. La relación entre la dosis y la destrucción de un microorganismo por tratamiento con radiación UVC puede expresarse comomuestra laEc.2 de acuerdo a la ley de Chick (Wright y Cairns, 1998; Shama,1999):
= (Ec.2)
en donde N0 se refiere al número inicial de microorganismos, N es el número de microorganismos después del tratamiento, k es la constante de velocidad de inactivación y D esladosis(mJ/cm2).
de tratamientoTiempo de tratamiento
de tratamiento
de tratamiento
Fig 3. Curvas de supervivencia microbiana, (a) lineal, (b) con hombro, (c) con cola y (d) sigmoidea.
Como en las gráficas de supervivencia se expresa la fracción de supervivientes en escala logarítmica, la ecuación anterior se puede transformarenlasiguiente:
(Ec.3)
Según la relación anterior, si se duplica la dosis aplicada, la destrucción de microorganismos aumentará en un factor de 10. Por lo tanto, al duplicar la dosis requerida para la destrucción del 90%, se reducirá el 99% de los microorganismos, si se triplica la dosis, la reducción producida será 99.9%, y asísucesivamente.
3.4. Ventajas y desventajas de la radiación UVC
La aplicación de las tecnologías emergentes a los procesos de conservación de alimentos deberán permitir obtener productos de
LaradiaciónUVC esunmétodofísicoenel cual la energía es el medio germicida, por lo que tiene la ventaja de no producir residuos químicos ni subproductos. Además es un proceso seco y frío que requiere poco mantenimiento y es de bajo costo (GuerreroBeltrán y Barbosa-Cánovas, 2004). También ha demostrado ser efectivo para la desinfeccióndediversassuperficies yeseficaz para la inactivación de muchos microorganismos. En la desinfección de alimentos líquidos con radiación UVC, no se producen alteraciones sensoriales y el producto conserva su valor nutrimental. Entre sus desventajas se encuentra el hecho de que (a) (b)
excelente calidad, a un precio razonable y, por encima de todo, seguros. En general, se busca que los nuevos métodos de tratamiento y conservación sean menos agresivos con el alimento, con menores consumos energéticos y más eficaces contra enzimas, microorganismosdeteriorativosypatógenos.
Tiempo
Tiempo
Tiempo
los microorganismos pueden ser protegidos por sólidos suspendidos, principalmente en los jugos de frutas, por lo que hay poca penetración de la radiación en líquidos no transparentes (Domínguez y Parzanese, 2011). También,como yasemencionóanteriormente, los microorganismos pueden reparar los efectos destructivos de la radiación UVC medianteunmecanismodefotorreactivación.
4. Uso de la radiación ultravioleta para el tratamiento de jugos de frutas
Los jugos frescos de frutas son bebidas populares en el mercado, debido a que son saludables y nutritivos. Es por esto que en los jugos y bebidas de frutas se espera que las técnicas de procesamiento empleadas conserven sus propiedades físicas, químicas y nutricionales. Recientemente, se ha incrementado el interés por la aplicación de la radiación UVC en jugos de frutas, por ser un proceso no térmico capaz de preservar las características del producto fresco y alargar su vida útil. Diversos estudios han demostrado un efecto insignificante de la radiación UVC en el color de los jugos de frutas, además de un resultado satisfactorio en sus atributos sensoriales y en la composición de nutrientes. Por lo anterior, los tratamientos con radiación UVC aplicados a jugos de frutas son una alternativa interesante para su conservación, dado que se genera una importante reducción en la carga microbiana de los mismos, sin ocasionar cambios sensoriales importantes. Actualmente, se están comercializando en Estados Unidos jugos de frutas tratados con radiación UVC. El éxito de esta técnica ha llevado a expandir su aplicación a otras bebidas como el té, de gran popularidad en el sur de Estados Unidos de América (Álvarez, 2008).
Existen algunos estudios publicados sobre los efectos de la radiación UVC en el sabor, color y contenido de nutrientes de los jugos, los cuales incluyen jugo y sidra de manzana,
jugo de naranja, néctar de mango, jugo de pitaya, jugos de uva blanca y roja, jugo de piña,jugodearándanoyjugodetoronja.
Un estudio reciente sobre el efecto del tratamiento con radiación UVC en jugo de manzana inoculado con Escherichia coli y Listeria inocua fue llevado a cabo para conocer la inactivación microbiana y las características fisicoquímicas del jugo tratado (Caminiti et al., 2012). De acuerdo con los resultados, el tratamiento no afectó el pH, °Bx y el contenido de fenoles totales, pero disminuyó la capacidad antioxidante; también se observó un ligero cambio de color al incrementar la dosis de radiación. Además la evaluación sensorial de las muestras tratadas con dosis bajas tuvieron una buena aceptabilidad. Sin embargo, los tratamientos aplicados solamente lograron la reducción de un ciclo logartítmico de los microorganismos inoculados en el jugo. Otro estudio realizado con jugo de manzana inoculado con E. coli, logró una reducción de 3.81 ciclos logarítmicos al variar las velocidades de flujo en un rango de 0.999 a 6.48 L/min, aunque la reducción microbiana no fue suficiente para alcanzar la recomendada para alimentos líquidos(FDA,2000;Wright et al.,2000). Al realizar comparaciones entre el tratamiento térmico tradicional y la radiación UVC para tratar jugo y sidra de manzana, se ha encontrado que no existen diferencias significativas en cuanto al sabor y preferencia entre los productos procesados. Sin embargo, en el caso de las sidras tratadas con radiación UVC, estas características no se mantienen después de una semana de almacenamiento (Tandon et al., 2003). En el jugo de manzana tratadoconradiaciónUVCsedemostróqueno existe cambio de color, pero el cambio de color fue notorio en la muestra sometida al tratamiento térmico. Comparado con el jugo fresco,elniveldecompuestosfenólicostotales disminuyó significativamente en el jugo tratado con radiación UVC, aunque la disminución fue menor que en el jugo
procesado térmicamente. La capacidad antioxidante no se vio afectada por ningún tratamiento. Estos resultados indican que la radiación UVC es un tratamiento adecuado para el procesamiento del jugo de manzana (Noci et al.,2008).
Algunos estudios han demostrado que el tratamiento UVC en jugo de naranja aumenta su vida de anaquel sin cambios en el color y sabor. Un tratamiento realizado en jugo recién exprimido aplicando una dosis de radiación UVC de 73.8 mJ/cm2, demostró que el color y el pH del jugo no tuvieron un cambio significativo y que la vida de anaquel fue de 5 días. Sin embargo, al incrementar la dosis de radiación a 100 mJ/cm2 se presentó una degradacióndelavitaminaC (17%),locual es similar al porcentaje reportado en los tratamientos térmicos. Además, la PME, que es la principal causante de la pérdida de turbidez en los jugos, no fue degradada, a diferencia del tratamiento térmico, en el cual es degradada hasta en un 70% (Tran y Farid, 2004). En otro estudio realizado en jugo de naranja, se demostró que la vida de anaquel aumentó de 2 a 7 días, pero la degradación de vitamina C fue del 18% y además, el tratamientoUVCnofueefectivoparainactivar enzimas. Por lo cual, se concluye que el tratamiento con radiación UVC en jugo de naranja no puede sustituir completamente al tratamiento térmico, debido a que éste es más eficiente para controlar la actividad enzimática (Torkamani yNiakousari,2011).
El efecto de penetración de la radiación UVC se ve afectada por diversos factores como el tipo de líquido, materia suspendida y principalmente por los sólidos solubles del jugo (Shama, 1999). En un estudio realizado con jugo de pitaya, que contenía 6.75% de sólidos solubles totales, se observó que no hubo un efecto significativo sobre el pH y los sólidos solubles totales. Sin embargo, el contenido de betalaínas y compuestos fenólicos disminuyó ligeramente, como
consecuencia, la actividad antioxidante disminuyó en el jugo. Se observó una reducción de 2 y 1.2 ciclos logarítmicos para bacterias mesófilas aerobias y mohos y levaduras, respectivamente, lo cual no es suficiente para garantizar la pasteurización. Esto puede deberse principalmente a los sólidos solubles presentes en el jugo que impiden la penetración de la radiación (Ochoa et al.,2011).
Un estudio con néctar de mango fue realizadopara evaluarel efectodel tratamiento UVC en la inactivación de S. cerevisiae y la actividad enzimática (Guerrero-Beltrán y Barbosa-Cánovas, 2006). De acuerdo con este estudio, se observó una reducción de 2.94 ciclos logarítmicos de S. cerevisiae. Además se presentó una reducción del 19% en la actividadenzimáticaalutilizardosisentre75y 450 kJ/m2, manteniéndose el néctar sin crecimiento microbiano durante 20 días de almacenamiento y manteniendo su color durante26días.
Para reducir la carga microbiana que contenían los jugos de mango y piña, Mukhopadhayay et al. (2011) sometieron los jugosauntratamientocon radiaciónUVC.En ambos jugos se observó que los coliformes totales, Vibrio y Salmonella disminuyeron en más del 50% después de 60 minutos de exposición a la radiación, pero los mohos y levaduras no se vieron afectados significativamente, observándose una disminución menor al 30%. En comparación con la pasteurización, los jugos tratados con radiaciónUVCnomostraroncambiosensabor y color. Los resultados mostraron que la radiación UVC puede ser aplicada satisfactoriamente para reducir la carga microbianaenjugosdefrutas.
El efecto del tiempo de almacenamiento sobre la calidad de jugo de piña tratado con UVC y térmicamente ha sido estudiado por Chia et al. (2012). Los resultados demostraron
que el jugo tratado con radiación UVC preservó mejor sus atributos de calidad que el jugo pasteurizado. Además el jugo tratado con radiación UVC aumentó su vida de anaquel 6 semanas más que el jugo fresco no tratado. En otro estudio realizado en jugo de piña se comparó el efecto del tratamiento térmico y el tratamiento con radiación UVC sobre el contenido de antioxidantes y capacidad antioxidante. El jugo tratado con radiación UVC mostró una mejor estabilidad respecto al contenido de ácido ascórbico, mientras que el jugo tratado térmicamente mostró mejor estabilidad a los flavonoides y carotenoides (Goh, et al.,2012).
La dosis de radiación UVC es un factor importante en la inactivación microbiana. Una investigación realizada con jugos de uva blanca y roja demostró que el tratamiento con dos recirculaciones y una dosis de 25.2 J/mL elimina completamente los microorganismos. Mientras que con dosis de 12.6 J/mL y con unasolarecirculaciónse obtuvounareducción de 3.51 (86.5%) y 3.59 (64.3%) ciclos logarítmicos en el recuento de bacterias mosófilas aerobias en jugos de uva blanca y roja. Para el caso de levaduras y mohos las reducciones fueron 2.71 (84.2%) en jugo de uva blanca y2.89 (55.2%) en jugo de uva roja (Uysal y Kirka, 2012). Fredericks et al (2011) observaron una inactivación similar en jugos de uva blanca y roja inoculados con S. cerevisiae, e indicaron que la eficacia del tratamientoconradiaciónUVCesafectadapor el color de los jugos. Estos autores reportaron 5.38 y 3.14 reducciones logarítmicas de S. cerevisiae inoculada en jugos de uva blanca y roja después de someterlos a una dosis de radiaciónde1.377J/mL.
Lorenzini et al.,2010probaronunadosisde 1000 J/L para tratar jugo blanco de uva. Los jugos tratados contenían altos niveles de levaduras (Saccharomyces bayanus). Después del tratamiento se obtuvo una reducción de 7 ciclos logarítmicos de la población microbiana
inicial. Por lo cual, el tratamiento con radiación UVC demostró ser eficaz en la disminución de S. bayanus. En el caso de las bacterias mesófilas aerobias, se obtuvo una reducción de 3 ciclos logarítmicos después del tratamiento. Se evaluaron también las características químicas del jugo antes y después del tratamiento, y no se observaron cambiosenestosparámetros(pH,color,acidez total y azúcares reductores) después del tratamientoconradiaciónUVC.
Jugos pasteurizados de uva, arándano y toronja inoculados con S. cerevisiae fueron procesadosconradiaciónUVCa6velocidades de flujo (0.073-1.02 L/min) y 6 dosis UVC (75-450 kJ/m2). La máxima reducción logarítmica (UFC/mL) que se alcanzó fue 0.53,2.51y2.42enlosjugosdeuva,arándano y toronja, respectivamente, después de 30 minutos de tratamiento a la máxima velocidad de flujo. La diferencia de color en los tres jugos de frutas probados incrementó conforme incrementó el tiempo de tratamiento UVC (Guerrero-Beltrán et al.,2009).
Conclusiones y comentarios finales
El tratamiento de jugoscon radiación UVC es una alternativa viable a los tratamientos térmicos convencionales. Esta tecnología permite aumentar la vida útil de estos productos conservando su calidad sensorial. Sin embargo, el principal inconveniente de esta técnica es la baja capacidad de penetración de la radiación UVC en los jugos, loquelimitasueficacia. Además,laradiación UVC puede afectar negativamente porque causa la degradación de antioxidantes. Se requieredemásinvestigaciónacercadelefecto de la radiación UVC sobre la pérdida de nutrientes y capacidad antioxidante, tomando en cuenta que cada jugo necesita una dosis de tratamiento distinto que se debe optimizar según las características del mismo. El estudio
de la cinética de inactivación microbiana permitirá optimizar el proceso para reducir al mínimo las pérdidas de nutrientes y asegurar una mayor reducción de microorganismos, esto para conseguir la mayor eficacia de inactivación y cumplir con las recomendacionesdelaFDA.
Agradecimientos
A la Universidad de las Américas Puebla y al Consejo Nacional de Ciencia y Tecnología (CONACyT, México) por el financiamiento paralarealizacióndeestetrabajo.
Food 9.Montpellier, Francia. 7- 11 marzo 2004. CDRom, ICEF9, France.
Arias, C. R, Burns, J. K., Friedrich, L. M., Goodrich, R. M., Parish, M. E. 2002. Yeasts species associated with orange juice: evaluation of different identification methods. Applied and Environmental Microbiology. 68(4): 1955-61.
Barbosa-Cánovas, G. V., Pothakamury, U. R., Palou, E. y Swanson, B. G. 1998. High intensity pulsed electric fields: Processing equipment and design. En: E. Palou (Ed). Nonthermal preservation of foods. Marcel Dekker, Inc., Nueva York. pp. 53-112.
Battey A. S., Duffy, S., Schaffner, D. W. 2002. Modeling yeast spoilage in cold-filled ready-todrink beverages with Saccharomyces cerevisiae, Zygosaccharomyces bailii and Candida lipolytica. Applied and Environmental Microbiology. 68(4): 1901-1906.
Referencias
Acevedo, B., Montiel, M. y Avanza, J. 2004. Estudio cinético de la degradación de la actividad antioxidante hidrosoluble de jugos cítricos por tratamiento térmico. FACENA. 20:91-95.
Adams, M. R. y Moss, M. O. 1995. Food Microbiology Tercera edición. The Royal Society of Chemistry, Cambridge. 577 p.
Álvarez, I. 2008. Pasteurización de zumos con luz ultravioleta. CTA Magazine. En: http://www.catedu.es/ctamagazine/index.php?option =com_content&view=article&id=699&catid=94:artl os-del-mes-archivo&Itemid=41, accesada 06/09/2012.
Alzamora, S. M y López-Malo, A. 2002. Microbial behavior modeling as a tool in the design and control of minimally processed foods. En: WeltiChanes, J., Barbosa-Cánovas, G. V. y Aguilera, J. M. (Eds.). Engineering and Food for the 21st Century. Nueva York. pp. 631-650.
Ancasi, E. G., Carrillo, M. R. y Benítez, A. 2006. Mohos y levaduras en agua envasada y bebidas sin alcohol. Revista Argentina de Microbiología. 38: 9396.
Argaiz, A., López-Malo, A., Jiménez, T., Ramírez, M., Milacatl, V. 2004. Thermal treatments optimization of mango nectar and puree products.Proceedings of the International Conference of Engineering and
Bintsis, T., Litopoulou-Tzanetaki, E. y Robinson, R 2000. Existing and potential applications of ultraviolet light in the food industry. Journal of the Science of Food and Agriculture. 80:637-645.
Bolton, J. R. y Cotton, C. 2001. Ultraviolet Applications Handbook. Segunda edición. American Water Works Association, EE.UU. 168 p.
Caminiti, I. M., Palgan, I., Muñoz, A., Noci, F., Whyte, P., Morgan, D. J., Cronin, D. y Lyng, J. G. 2012. The effect of ultraviolet light on microbial inactivation and quality attributes of apple juice. Food Bioprocess Technology, 5:680-686.
Chia, S. L., Rosnah, S., Noranizan, M. A. y Wan Ramli, W. D. 2012. The effect of storage on the quality attributes of ultraviolet-irradiated and thermally pasteurized pineapple juices. International Food Research Journal. 19(3): 1001-1010.
Déak, T. y Beuchat, L. R. 1998. Handbook of Food Spoilage Yeasts. Segunda edición. CRC Press, Boca Raton. 325 p.
Domínguez, C. 2004. Formulación y pasteurización de una bebida con mezclas de jugos no clarificados de piña-guayaba-mango. Tesis de maestría. Universidad de las Américas Puebla. México. 106 p.
Domínguez, L. y Parzanese, M. 2011. Luz ultravioleta en la conservación de alimentos. Revista Alimentos Argentinos. 52:71-76.
FDA (Food and Drug Administration). 2000. 21 CFR Part 179. Irradiation in the production, processing
and handling of food. Registro federal, 65, 71056–71058.
Fredericks, I. N., Du Toit, M. y Krügel, M. 2011. Efficacy of ultraviolet radiation as an alternative technology to inactivate microorganisms in grape juices and wines. Food Microbiology. 28(3): 510–517.
Goh, S. G., Noranizan, M., Leong, C. M., Sew, C. C. y Sobhi, B. 2012. Effect of thermal and ultraviolet treatments on the stability of antioxidant compounds in single strength pineapple. International Food research Journal. 19(3): 1131-1136.
González, C. 2001. Luz ultravioleta en la conservación de alimentos. Ambiental Socoter. En http://www.ambientalsocoter.cl/008_Luz%20Ultravi oletaDesinfAguayAire.pdf, accesada 27/08/2012.
Gould, G. W. 1995. New Methods of Food Preservation. Primera edición. Aspen Publishers, Gran Bretaña. 324 p.
Guerrero-Beltran, J. A. y Barbosa-Canovas, G. V. 2006. Inactivation of Saccharomyces cerevisiae and polyphenoloxidase in mango nectar treated with UV light. Journal of Food Protection. 69(2): 362–368.
Guerrero-Beltrán, J. A. y Barbosa-Cánovas, G.V. 2004. Advantages and Limitations on Processing Foods by UV Light. Food Science Technology International 10(3): 137-147.
Guerrero-Beltrán, J. A., Velti-Chanes, J., y BarbosaCánovas, G. V. 2009. Ultraviolet-C light processing of grape, cranberry and grapefruit juices to inactivate Saccharomyces cerevisiae. Journal of Food Process Engineering. 32(6): 916–932.
Herrero, A. y Romero, M. 2006. Innovaciones en el procesado de alimentos: Tecnologías no térmicas. Revista de Medicina de la Universidad Navarra. 50(4): 71-74.
Jay, J. M, Loessner, M. J, y Golden, D. A. 2006. Modern Food Microbiology. Séptima edición. Springer Science, EE.UU. 790 p.
Koutchma, T. 2008. UV light for processing foods. IUVA News. 10(4):24-29.
Koutchma, T. 2009. Advances in ultraviolet light technology for non-thermal processing of liquid foods. Food Bioprocess Technology. 2:138-155.
Kurtzman, C. P. y Fell, J. W. (Eds.). 1998. The yeasts, a taxonomic study. Cuarta edición. Elsevier Science, Nueva York. 1076 p.
Liltved, H. y Landfald, B. 2000. Effects of high intensity light on ultraviolet-irradiated and nonirradiated fish pathogenic bacteria. Water Research 34(2):481-486.
López-Malo, A. y Palou, E. 2004. Ultraviolet light and food preservation. En: Cano, M. P. y Tapia, M. S. (Eds). Emerging Technologies for the Food Industry. Marcel Dekker, Nueva York. pp. 405-421.
Lorenzini, M., Fracchetti, F., Bolla, E., Stefanelli, E., Rossi, F. y Torriani, S. 2010. Ultraviolet light (UVC) irradiation as an alternative technology for the control of microorganisms in grape juice and wine. Conferencia. 33° Congreso Mundial de la Viña y el Vino. Teatro Estatal Rustaveli, Tbilisi, Georgia. 2025 junio.
Madrid, A. 1994. Nuevo manual de industrias alimentarias. A. Madrid Vicente, Madrid. 595 p.
Marshall, M. R., Marcy, J. E. y Braddock, R. J. 1985. Effect of total solids level on heat inactivation of pectinesterasa in orange juice. Journal of Food Science. 50:220-222.
Mendonca, A. F. 2002. Inactivation by irradiation. En: V. K. Juneja y J. N. Sofos (Eds). Control of Foodborne Microorganisms. Marcel Dekker, New York. pp. 75-103.
Mukhopadhayay, M., Majumdar, M. y Pallabi, B. 2011. Microbial contamination of street vended fruit juices in Kolkata City. Internet Journal of Food Safety 13:1-5.
Noci, F., Riener, J., Walkling-Ribeiro, M., Cronin, D. A., Morgan, D. J. y Lyng, J. G. 2008. Ultraviolet irradiation and pulsed electric fields (PEF) in a hurdle strategy for the preservation of fresh apple juice. Journal of Food Engineering. 85: 141–146.
Ochoa, C. E., Luna, J. J. y Guerrero-Beltrán, J. A. 2011. Jugo de pitaya (Stenocereus griseus) tratado con luz ultravioleta. Conferencia. 8° Congreso Iberoamericano de Ingeniería de Alimentos. Centro de Convenciones del Colegio Médico de Perú, Lima, Perú. 23-26 octubre.
Pelayo, M. 2009. Alternativas a los tratamientos térmicos para garantizar la seguridad de los alimentos. Ingeniería de alimentos. 2(4): 16-17.
Rahman, M. S. (Ed). 1999. Handbook of Food Preservation. Segunda edición. Marcel Dekker, Inc., Nueva York. 809 p.
Sastry, S. K., Datta, A. K. y Worobo, R. W. 2000. Ultraviolet light. Journal of Food Science.
Supplement: Kinetics of microbial inactivation for alternative food processing technologies. 65(58): 90-92.
Shama, G. 1999. Ultraviolet light. En: Robinson, R. K., Batt, C. y Patel, P. (Eds). Encyclopedia of Food Microbiology. Academic Press, Londres. pp. 22082214.
Sizer, C. E. y Balasubramaniam, V. M. 1999. New intervention processes for minimally processed juices. Food Technology. 53:64–67.
Stevens, C., Kahn, V. A., Lu, Y. J., Wilson, C. L., Pusey, P. L., Kabwe, M. K., Igwegbe, E. C., Chalutz, E. y Droby, S. 1998. The germicidal and hermetic effects of UV-C light on reducing brown rot disease and yeast microflora of peaches. Crop Protection. 17(1):75-84.
Tandon, K., Worobo, R., Churley, J. y Padilla-Zakour, O. 2003. Storage quality of pasteurized and UVtreated apple cider. Journal of Food Processing Preservation. 27: 21–35.
Torkamani, A. E. y Niakousari, M. 2011. Impact of UVC light on orange juice quality and shelf life. International Food Research Journal. 18(4): 12651268.
Tran, M. T. y Farid, M. 2004. Ultraviolet treatment of orange juice. Innovative Food Science Emerging Technology. 5 (4): 495–502.
Uysal, C. y Kirka, A. 2012. Effects of UV-C light proccessing on some quality characteristics of grape juices. Food Bioprocess Technology, doi: 10.1007/s11947-012-0808-7.
Wright, H. B. y Cairns, W. L. 1998. Desinfección del agua por medio de luz ultravioleta. Simposio OPS: Calidad del Agua: Desinfección efectiva. Lima, Perú. 26-29 Octubre.
Wright, J. R., Sumner, S. S., Hackney, C. R., Pierson, M. D. y Zoecklein, B. W. 2000. Efficacy of ultraviolet light for reducing Escherichia coli O157:H7 in unpasteurized apple cider. Journal of Food Protection. 63(5): 563–567.
Yajima, H., Takao, M., Yasuhira, S., Zhao, J. H., Ishii, C., Inoue, H. y Yasui, A. 1995. A eukaryotic gene encoding an endonuclease that specifically repairs DNA damage by ultraviolet light. The EMBO Journal. 14(10): 2393–2399.

Cambios
Temas Selectos de Ingeniería de Alimentos 6 - 2 (2012): 94 - 109

en frutas tropicales frescas, cortadas y empacadas en atmósfera modificada durante su almacenamiento en refrigeración
M. Rangel-Marrón* y A. López-Malo
Departamento de Ingeniería Química, Alimentos y Ambiental, Universidad de las Américas Puebla. Ex hacienda Sta. Catarina Mártir S/N, San Andrés Cholula, Puebla. C.P.72810. México.
Resumen
Las frutas tropicales frescas cortadas forman parte de los alimentos mínimamente procesados, siendo susceptibles a disminuir su calidad y valor nutricional durante su preparación y almacenamiento. El empacado en atmósfera modificada (EAM) en refrigeración, ofrece la posibilidad de extender la vida de anaquel de este tipo de productos, dado que se puede generar una atmósfera diferente a la normal al disminuir la concentración de oxígeno y aumentar la concentración de dióxido de carbono, afectando la velocidad de respiración del fruto. La adecuada temperatura y composición gaseosa provistas, ayudan a mantener la apariencia, textura, compuestos bioactivos, calidad sensorial y estabilidad microbiológica de las frutas tropicales. El objetivo de la presente revisión es dar a conocer los principales químicos, microbiológicos y sensoriales de las frutas tropicales frescas cortadas y empacadas en atmósfera modificada durante su almacenamiento en refrigeración.
Palabras clave: frutas tropicales frescas cortadas, atmósfera modificada, empacado, refrigeración.
Abstract
Tropical fresh-cut fruits are part of so-called minimally processed foods, being susceptible to decrease its quality and nutritional value during their preparation and storage. The modified atmosphere packaging (MAP) in refrigeration temperatures, offers the possibility of extending the shelf life of these products, providing a different atmosphere throughout the reduction concentration of oxygen and the increased concentration of carbon dioxide, and affecting the respiration rate of the fruit. Temperature and gas composition, help to preserve the appearance, texture, bioactive compounds, sensory quality and microbiological stability of tropical fresh-cut fruits. The aim of this review is to present the main chemical, microbiological and sensory changes of tropical fresh-cut fruits packaged in modified atmosphere during their storage in refrigeration.
Keywords: tropical fresh-cut fruits, modified atmosphere, packaging, refrigeration.
*Programa de Doctorado en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: marcela.rangelmn @udlap.mx
Introducción
La demanda del mercado de frutas y hortalizas mínimamente procesadas es un área de oportunidad que ha venido en desarrollo por la necesidad de obtener productos con una alta calidad en todos los aspectos. Por lo tanto, ha atraído el interés de muchas facetas de la industria alimentaria, incluyendo áreas tan diversas como fabricantes, almacenistas de productos, restaurantes, establecimientos de alimentos para llevar y en especial, a los consumidores quienes demandan productos frescos con aceptables atributos de calidad, (apariencia, textura y sabor) listos para ser consumidos,defácilmanejoyalmacenamiento.
Los frutos tropicales son parte del mercado de los frutos frescos cortados mínimamente procesados. Estos productos son manipulados mediante diversas operaciones unitarias (selección, lavado, pelado, deshuesado y corte), higienizados y almacenados a temperaturasderefrigeración,locualmantiene sus atributos y cualidades de producto fresco por un tiempo relativamente corto. Las frutas tropicales después de haber sido cosechadas y aún después de haber sido mínimamente procesadas, continúan lentamente su proceso metabólico de respiración, transpiración y maduración, ocasionando cambios en color, sabor y calidad nutricional, siendo favorecidas en algunos casos las condiciones para la proliferacióndemicroorganismos.
Una opción para incrementar la vida útil de los productos mínimamente procesados es el empaque en atmósferas modificadas. Este métododeconservaciónconsisteencambiarla composición gaseosa dentro del empaque, la cual puede ser modificada de manera pasiva (a través de la respiración de los tejidos vegetales) o activa (generando la composición gaseosa antes de cerrar el empaque). Diferentes investigaciones (Lucera et al., 2011; Sandhya, 2010) han demostrado que dependiendo del tipo de atmósfera que se
genere, el oxígeno remanente se consumirá y el dióxido de carbono producido cubrirá el material vegetal hasta alcanzar el equilibrio con una atmósfera modificada; dicho equilibrio va a depender tanto de los cambios de temperatura como de la permeabilidad del material de empaque a los gases. La atmósfera generada será efectiva para mantener la apariencia visual y para reducir el crecimiento microbiano de muchas frutas y hortalizas frescascortadas.
El objetivo de la presente revisión es dar a conocer los principales cambios químicos, microbiológicos y sensoriales de las frutas tropicales frescas cortadas y empacadas en atmósfera modificada durante su almacenamientoenrefrigeración.
Revisión bibliográfica
1. Aspectos generales de la atmósfera modificada
Farber et al. (1993) definieron que un alimento almacenado en atmósfera modificada es un alimento perecedero almacenado en un ambiente de composición diferente a la del aire (78.08% N2, 20.96% O2,0.03% CO2 ytrazas de gases inertes). El envasado en atmósfera modificada (EAM) es un proceso dinámico que puede generarse de manera activa o pasiva, alterando la composición gaseosa dentro del empaque (película plástica), ya sea por la sustitucióndeungas,odeunamezcladegases; la selección del gas o mezcla de gases a emplear dependerá del tipo de producto a empacar y almacenar. La atmósfera gaseosa cambia continuamente durante todo el período de almacenamiento por la influencia de diferentes factores, como son la respiración del productoenvasado,loscambiosbioquímicosen el producto, la difusión de los gases a través de la película plástica en función de su espesor y área superficial expuesta, la masa del producto
envasado, y la temperatura de almacenamiento (Martín-Belloso yOms-Oliu, 2005;Caleb et al., 2012).
La atmósfera modificada pasiva consiste en la utilización de películas plásticas de diferente permeabilidad a los gases para crear de forma pasiva una atmósfera modificada favorable por efecto de la permeabilidad del envase, la respiración y actividad bioquímica del producto, entre otros factores (Day, 2000). Sin embargo, cuando la atmósfera modificada de equilibrio no se consigue antes de que se activen las reacciones que llevan al deterioro del producto, tales como el obscurecimiento enzimático o la pérdida de textura, se puede modificar de manera activa la atmósfera de envasado (Martín-Belloso y Oms-Oliu, 2005). En este caso, la atmósfera de equilibrio se consigue mediante la substitución mecánica del aire que rodea al producto por una mezcla adecuada de gases, de tal manera que la atmósfera en el envase se puede variar en función de las necesidades y respuesta del producto (Parry, 1993; Day, 2000). Otras formas de lograr la modificación activa de la atmósfera consisten en la incorporación de ciertos aditivos en el envase para modificar su atmósfera interior. Entre ellos se encuentran los
absorbedores de oxígeno y/o etileno, los absorbedores o emisores de CO2, y los generadores de vapores de etanol, entre otros (Kader,2002;Caleb et al., 2012).
Para modificar la atmósfera interior del envase es fundamental conocer las características de permeabilidad de la película plástica y del producto a los gases. Se sabe que la permeabilidad a los gases de un material de empaque depende de la naturaleza del gas, la estructura yespesordel material,latemperatura y la humedad relativa (Martín-Belloso y OmsOliu, 2005). La Fig. 1 representa el sistema general de envasado del producto y el intercambio de gases a través de la película poliméricautilizada.
Entre los materiales poliméricos utilizados para el EAM se encuentran: polietileno de alta y baja densidad (por sus siglas en inglés HDPE - LDPE), polietileno de baja densidad lineal (porsussiglaseninglés LLDPE), polipropileno (PP), cloruro de polivinilo (PVC), poliéster, tereftalato de polietileno (PET), cloruro de polivinilideno (PVDC), poliamida (Nylon) y acetato de celulosa entre otros (Mangaraj et al., 2009;Rodríguez-Félix et al.,2005).

Fig. 1. Sistema de envasado en atmósfera modificada. Adaptado de Rodríguez-Félix etal. (2005).
Cada uno de estos polímeros forman películas que tienen distintas características, tales como, permeabilidad a los gases y al vapor de agua (permeabilidad de barrera), resistencia mecánica, claridad o transparencia, durabilidad (propiedades físicas), facilidad de sellado y empañamiento (resultado de la respiración del producto)(Mangaraj et al.,2009). Uno de los gases utilizado comercialmente es el oxígeno, el cual desencadena reacciones de óxidoreducción degradativas. Con niveles bajos de oxígeno, las condiciones de envasado hipobáricas (productos envasados a presión y temperatura bajas, y HR alta) o superatmosféricas (elevadas concentraciones de oxígeno > 21%), reducen la respiración del producto y evitan el desarrollo de microorganismos aerobios. Así mismo, el oxígeno (O2) es un inhibidor de los microorganismos anaerobios ydel metabolismo fermentativo de los vegetales (Kader, 2002; Martín-BellosoyOmsOliu,2005).
El dióxido de carbono (CO2) es otro gas ampliamente utilizado por sus propiedades bacteriostáticas y fungistáticas; éste se disuelve rápidamente en agua (1.57 g/kg a 100 kPa y 20ºC) lo cual retarda el crecimiento de hongos ybacterias aerobias. El CO2 actúaretardandola fase lag del crecimiento microbiano, aunque éste efecto depende de la temperatura y su concentración (Al-Alti y Hotchkiss, 2002; Rodríguez-Félix et al., 2005; Caleb et al., 2012). Sin embargo, varios investigadores coinciden en que la acumulación excesiva de CO2 genera daño en la membrana celular y en la fisiología del producto, ocasionando pérdida de firmeza y un severo obscurecimiento enzimático (Kader, 1986; Yahia, 2006; Sandhya,2010).
El nitrógeno (N2) se utiliza fundamentalmente para desplazar el oxígeno. Además de retrasar la oxidación y prevenir el enranciamiento,seutilizaparaalmacenarfrutos secos. Tiene la característica de inhibir el crecimiento de microorganismos aerobios, más
no previene la proliferación de bacterias anaerobias; una de las funciones principales de este gas inerte consiste en actuar como relleno para evitar el colapso del envase y es importante mencionar que es necesario tener una concentración suficiente de nitrógeno en la mezcla de gases con el objetivo de balancear el volumen de CO2 que se disuelve en el alimento dentrodelempaque.
El monóxido de carbono (CO) y el empleo de gases nobles como helio (He), argón (Ar), xenón (Xe) y neón (Ne) tienen aplicaciones en el EAM; el CO se caracteriza por ser incoloro, inodoro, altamente tóxico y inflamable, además de ser poco soluble en agua. En EE.UU su empleo ha sido autorizado para prevenir el obscurecimiento en lechuga; sin embargo, su aplicacióncomercialestarestringida.
Dentro de los gases nobles, el argón que es más soluble en agua y en aceite que el nitrógeno, compite con el oxígeno por tener propiedades y tamaño similares, lo desplaza y previene la oxidación en productos con alto contenido de grasa. Así mismo, previene el crecimiento de microorganismos aerobios; de manera particular, los gases nobles han tenido aplicaciones en el empacado de botanas a base de papa (Lee et al., 2008; Sandhya, 2010). Qadir y Hashinaga (2001) reportan que el uso de Ar y óxido nitroso (N2O) favorece la actividad de los agentes antimicrobianos; por lo tanto, su uso tiene un efecto directo sobre la extensióndelavidaútildelasfrutas.Rocculi et al. (2004) encontraron efectos benéficos en la calidad de rebanadas de manzana “Golden Delicious” almacenada a 10ºC durante 10 días cuando utilizaron las siguientes AM: 90% N2O, 5% O2, 5% CO2 ó 65% N2O, 25% Ar, 5% O2, 5% CO2. En la Tabla I se muestran las concentraciones gaseosas recomendadas como atmósfera modificada para frutas tropicales frescascortadas.
En la Tabla I se observan diversas composiciones gaseosas utilizadas para el
Tabla I. Composiciones gasesoas recomendadas como atmósfera modicada para frutas tropicales frescas cortadas.
Producto
Envase
Atmósfera
TemperaturaReferencia
CocoBolsas PE-Nylon alta barrera7 - 160 - 4-4Sinigaglia et al. , 2003
Guayaba KumagaiLDPE35-10Jacomino et al., 2001
Guayaba RojaCharolas PET7.518-5Pereira et al., 2004
KiwiCharolas PP cubiertas con película PPP 55904Rocculi et al., 2005
PE laminado y PET (extruidos)173-5Del Nobile et al., 2007
Polietileno laminado155-1.5Pesis et al. , 2002
Mandarina PalazelliCharolas PP cubiertas con poliolefina11.7 - 183 - 8.3-4Del Caro et al., 2004
Mango Carabao Charola de PE03.5 y 10-5 y 13Poubol e Izumi, 2005
Mango Keitt Cryovac PD-941410-5Martínez-Ferrer et al., 2002
Mango Kent Frascos de vidrio210-5Rattanapanone et al., 2001
MangoTommy Atkins Frascos de vidrio410-5Rattanapanone et al., 2001 Película polimérica5-1025-8Brecht et al. , 2003
Naranja Shamouti Charolas PP cubiertas con poliolefina15.7-19.31.6-6-1-4Del Caro et al., 2004
PapayaPE y PET36-6Chauhan et al., 2006b
PiñaPET614-4Chonhenchob et al., 2007
Piña rojaCryovac B-900410-5Martínez-Ferrer et al., 2002
PlátanoPE laminado y PET (extruidos)171-4Del Nobile et al., 2007
Tangelo MinneolaCharolas PP cubiertas con poliolefina15.4 - 201 - 64Del Caro et al., 2004
envasado yalmacenamiento de frutas tropicales frescascortadas.Eltipodeenvaseutilizadoyla temperatura de almacenamiento son variables que tienen un efecto sobre el metabolismo del fruto y la velocidad de respiración. Estas variables influyen en el tiempo necesario para alcanzar el equilibro de la composición gaseosa delproductoylaatmósferaquelorodea,yaque lasdiferentesfrutascortadasono,poseencierta resistencia a la difusión de los gases a través de sus tejidos por efecto de la temperatura (Rodríguez-Félix et al., 2005).
2. Efecto de la atmósfera modificada sobre la velocidad de respiración de las frutas frescas cortadas
El término respiración se utiliza en las frutas y hortalizas frescas e involucra cambios en la composición gaseosa, como producto del metabolismodel material vegetal seliberaCO2, energía y calor, con o sin consumo de oxígeno. Esto implica la oxidación enzimática de las moléculas orgánicas como los carbohidratos
(azúcar y almidón), ácidos grasos y proteínas. Además, la respiración provee las necesidades básicas del tejido y células del fruto para mantener sus actividades fisiológicas y metabólicas (Zhuang et al., 2011). En general, la vida útil de un producto EAM es inversamente proporcional a la velocidad de la respiración; la velocidad de respiración es un excelente indicador de la actividad metabólica del fruto, siendo un proceso bioquímico complejo que es afectado por numerosos factores tales como el tamaño del corte del producto, la severidad de los procesos utilizados en su preparación, variedad del fruto, madurez y tipo de tejido; además, la velocidad de respiración permite establecer la vida de anaquel del fruto, e indica el final de su vida útil cuando el producto ha alcanzado una madurez completa (Day, 2000; Bai et al., 2001).
Existen dos tipos de respiración en el EAM de frutos frescos cortados, y ambos van a depender de si utilizan O2 en su proceso
fisiológico, es decir, respiración aerobia (presencia de oxígeno) o respiración anaerobia (ausencia de oxígeno < 1-3% O2). Las ecuaciones 1 y 2 muestran los productos generadosenlosdostiposdereacciones:
DondeEzesenzimasyEesenergía.
La respiración aerobia (Ec. 1) utiliza la materia orgánica presente en los tejidos vegetales, originado cambios o pérdida de fitonutrientes; si aumenta la concentración de O2, aumenta la velocidad de respiración, y existirá pérdida de nutrientes, en cambio si disminuye el O2 (1-5%), se reduce la tasa de respiración y consecuentemente, aumenta la vidadeanaquel del producto. Porotrolado,la respiración anaerobia (Ec. 2) genera productos de fermentación (etanol, acetaldehído y lactato) (Rodríguez-Félix et al., 2005; Zhuang et al., 2011).
La respiración difiere considerablemente dependiendo del tipo de producto y las condiciones de temperatura, humedad relativa (HR) y atmósfera a la que es expuesto. El objetivo del EAM es disminuir la respiración del producto y reducir los efectos del etileno (C2H4) (Rodríguez-Félix et al., 2005). El etilenodesempeñaunpapel central enel inicio de la maduración y es fisiológicamente activo en concentraciones traza (0.1 ppm), su producción decae a medida que la concentracióndeO2 seencuentraalrededordel 2.5%; al disminuir la presencia de O2 se reduce la velocidad de respiración del producto fresco, con lo cual se logra retardar su maduración y al mismo tiempo se inhibe la producción y acción del etileno (Sandhya, 2010; Lucera et al., 2011). Así mismo, los procesos metabólicos son sensibles a la temperatura y humedad relativa (HR); generalmente, las reacciones biológicas se
incrementan de dos a tres veces por cada 10ºC deaumento en latemperatura. Otrofactor que interviene en la velocidad de respiración del fruto, es la difusión de los gases a través de la película de empaque, la difusión, depende de la temperatura y la concentración de éstos, al aumentar la temperatura se incrementa la difusión de CO2 respecto a la del O2. Por el contrario, una alta HR favorece la condensación del vapor de agua dentro del empaque, afectando la permeabilidad de la película plástica a los gases (Zagory y Kader, 1988;Sandhya,2010).
La velocidad de respiración indica el consumo de O2 o la producción de CO2, se expresa como mLO2/kg·h ó mLCO2/kg·h a una temperatura específica, y la relación de CO2 producido con respecto al O2 consumido se conoce como coeficiente respiratorio (CR) y puede variar de 0.7 a 1.3, dependiendo del sustrato metabólico utilizado (Zagory y Kader, 1988; Kader, 2002). Además el EAM contribuye a reducir la incidencia de los desórdenes fisiológicos, alteraciones microbiológicas y deterioros bioquímicos, que solos o en conjunto originan cambios en el color, textura, y calidad sensorial del producto (VaroquauxyWiley,1994).
Chonhenchob et al. (2007) empacaron frutas tropicales frescas-cortadas tales como mango, piña, melón y mezcla de frutas en tres diferentes empaques rígidos, que por sus siglas en inglés son PET (politereftalato de etilenglicol), OPS (poliestireno orientado) y OPLA (polilactidaorientada)), yreportaron que las frutas tienen en promedio una velocidad de respiración de 64.47, 29.56, 26.92, y 38 mL de CO2/kg·h a 10ºC, para mango, piña, melón y la mezcla de frutas respectivamente cuando utilizaron empaques de PET. Paralelamente, determinaron el tiempo de equilibrio de la atmósfera y la composición gaseosa en los empaques de PET a 10ºC, reportaron un tiempo de equilibrio de 6-13 días, alcanzando una composición gaseosa de 7% O2 y 18% CO2
para mango, 6% O2 y14% CO2 para piña, 14% O2 y 8% CO2 para melón, y 8% O2 y 18% CO2 paralamezcladefrutas.
Por otro lado, Agar et al. (1999) estudiaron la influencia de bajas concentraciones de oxígeno en el metabolismo respiratorio y atributos de calidad de rodajas de kiwi frescas cortadas. Encontraron un aumento en el contenido de acetaldehído y etanol durante 12 días de almacenamiento cuando fueron empacadasen0.5kPadeO2 comocomposición gaseosa a 2ºC, las rodajas de kiwi alcanzaron una vida útil de 9-12 días, si además, recibían tratamientos previos con CaCl2 al 1% o lactato decalcioal2%.
En el estudio realizado por Pereira et al. (2004) para guayaba deshidratada osmóticamente (DO) y guayaba fresca EAM a 5ºC alcanzaron una velocidad de respiración de 79±8y53±11mLCO2/kg/h,respectivamente obteniéndose un incremento en la producción de CO2 causado por el daño mecánico previo (corte de la fruta) a la deshidratación osmótica Por una razón similar, los productos dañados o cortados presentan una mayor actividad respiratoria que los productos enteros. De acuerdo a los estudios realizados por Rodríguez et al. (2006) determinaron que el impacto del EAM en papaya fresca y papaya deshidratada osmóticamente (DO) a 50ºBx a 23ºC; así como también señalan que la fruta fresca por debajo de 5ºC incrementa significativamente (p<0.05) su velocidad de respiración a diferencia de la papaya DO. Las muestras de papaya DO causaron una modificación interna de la composición gaseosa obteniendo 1% O2 y 13.62% de CO2, mientras que para las muestras de papaya fresca alcanzaron 12.91% de O2 y 5.35% de CO2. Pereira et al. (2004) y Rodríguez et al. (2006) concluyen que el incremento del CO2 se atribuyen al daño mecánicoprevioaladeshidrataciónosmótica.
En la investigación realizada por Bender et al. (2000) para mango de las variedades Haden
y Tommy Atkins, se observó que la atmósfera reducida de O2 (2-3 kPa) a 15ºC y 12ºC, aumenta la tasa de producción de etanol para ambas variedades de mango, lo cual se atribuye a la regulación positiva de alcohol por la isoenzima deshidrogenasa, observando que las variedades de mango tienen una baja demanda de energía, lo que limita el flujo de carbono a travésdelavíaglucolítica.
Otros investigadores han utilizado como EAM la aplicación de concentraciones de O2 superatmosférico (elevadas concentraciones de oxígeno ≥ 70 kPa de O2). Sugieren que la atmósfera puede estimular, no tiene efecto o disminuye la velocidad de respiración y producción de etileno dependiendo de factores talescomolamadurez ynaturalezadelfruto,de la concentración de O2, CO2 y C2H4 presentes en la atmósfera, y del tiempo y la temperatura de almacenamiento. La concentración de los gases pueden prevenir reacciones fermentativas e inhibir el crecimiento microbiano de bacterias psicrófilas. Oms- Oliu et al. (2008) empacaron melón fresco cortado y lo almacenaron a atmósferasde2.5kPadeO2 y7kPadeCO2,21 kPa de O2 y 70 kPa de O2 (siendo estas últimas dos concentraciones superatmósfericas de oxígeno) y CO2 reducido a 4ºC y observaron que la generación de CO2 de la fruta alcanzó una vida útil de 14 días empacada a 70 kPa de O2 yunaatmósferareducidaenCO2.
3. Cambios en frutas tropicales frescas, cortadas y empacadas en atmósfera modificada y almacenadas en refrigeración
3.1. Cambios en color y textura
Las características de color y textura de las frutas tienen un rol muy importante en la evaluacióndecalidad yaceptabilidadporparte del consumidor. El color deriva de los pigmentos naturales de las frutas,a muchos de los cuales cambian a través de la maduración de la planta y fuera de ella. Pereira et al. (2004) concluyen que el color siempre ha sido
uno de los principales criterios de evaluación de la calidad de un fruto. De acuerdo a Chauhan et al. (2006a), la superficie de los frutos mínimamente procesados es susceptible al obscurecimiento por la pérdida acelerada de los pigmentos afectando la aceptabilidad del producto en términos de color. Los pigmentos primarios que confieren calidad al color del vegetal son las clorofilas (verdes) y los carotenoides (amarillos, naranjas y rojos). Dentro de los pigmentos solubles en agua se encuentran las antocianinas (rojas y azules), flavonoides (amarillos) y betalainas (rojas) (Barret et al. 2010). Por otro lado, Lin y Schyvens, (1995) reportaron que la textura es uno de los atributos más importantes de calidad ya que la pérdida de turgencia del tejido del fruto afecta la aceptabilidad del mismo. La firmeza está asociada al contenido de agua, así como a la actividad de distintas enzimas (transformación de protopectina a pectinas solubles en agua), los cuales inducen cambios en los componentes de la pared celular que ocurren durante la senescencia, generando descenso de la cristalinidad de la celulosa, disminución del contenido de ácido galacturónico, reducción enel volumen celular y adelgazamiento de la pared celular; estos aspectos son afectados en el fruto cortado manifestándosecomoablandamientodel tejido vegetal (King y Bolin, 1989; Varoquaux y Wiley,1994).
Pereira et al. (2004) estudiaron los cambios de color en guayabas DO y EAM así como en guayabas empacadas con aire atmosférico; la preservación del color lo atribuyeron a la baja concentración de oxígeno, que evita la degradacióndeloscarotenoides,loscualesson los responsables del color característico de la guayaba.
En la investigación realizada por Bender et al. (2000),reportanquealevaluarlatolerancia a niveles reducidos de oxígeno (2,3,4,y 5 kPa de O2 más N2) ó 25 kPa CO2 más aire como atmósfera controlada y el control (aire) de dos
variedades de mango Haden yTommyAtkins; observaron que a niveles de oxígeno menores de5kPapresentanpocoefectoenlatexturadel mango verde para ambas variedades del fruto, a diferencia del empacado con aire. Por otro lado las mismas condiciones ó 25 kPa de CO2 lograron reducir los cambios de color durante 12díasa15ºC.
Chauhan et al. (2006a) evaluaron los cambios de color y textura en rebanadas de mango utilizando una composición gaseosa compuestade4%deO2,6%deCO2 y90%N2 como AM activa, observándose obscurecimiento en la superficie del fruto, así como disminución del color amarillo, siendo significativos los cambios de color durante el almacenamiento a 8ºC (p<0.05). Con respecto alatextura,ellosobservarondisminucióndela turgencia del fruto y este comportamiento lo asocianaunalentarespiracióndelproducto.
En otra investigación reportada por Jiang y Fu (1999) para la prevención del obscurecimiento de lichi EAM, se encontró quelacomposicióngaseosade3a5%deO2 y 97-95% CO2 almacenado a 1ºC y 90% de HR controla el obscurecimiento y se mantiene la calidad del fruto por más de 30 días. Los estudios realizados por Duan et al. (2004) sugieren que litchi variedad Huaizhi almacenado en oxígeno puro (100% O2 y 0% CO2) por 6 días a 28ºC mantiene el color del epicarpio (capa que rodea al fruto) sin presentar obscurecimiento, los autores concluyen que el haber utilizado O2 puro inhibe la actividad enzimática de PPO yde las antocianinas, siendo las responsables del obscurecimientodelfruto.
Aharoni y Houck (1982); Kader y BenYehoshua (2000) reportan el uso de 40-80 kPa de O2 (niveles de oxígeno superatmosférico) como una aplicación para mejorar el color del endocarpio y jugo de naranja por 4 semanas a 15ºC, las naranjas expuestas a las condiciones anteriores lograron extender su vida de
anaquel por 2 semanas adicionales, observando que el color se intensifica en el jugocuandosemantuvoa80kPadeO2.
Rocculi et al. (2005), estudiaron el efecto de almacenar kiwi a 4 ºC utilizando una mezcladegases (90% N2O,5%O2 y5%CO2) como atmósfera modificada mostrando que el N2O ayuda a mantener el color inicial del fruto.
Chauhan et al. (2006b) reportan una disminucióndelapérdidadetexturaenpapaya empacada en bolsas de polietileno (PE) y PET utilizando 3%O2, 6%CO2 y 91% N2 como atmósfera modificada durante el almacenamientoa6ºC.
La investigación realizadapor Ranasinghe et al. (2005) con plátano variedad Embul tratado con aceite esencial de orégano y EAM, recomiendan la combinación de los tratamientos como una alternativa para conservar el fruto por más de 21 días en refrigeración ypor 14 días a 28ºC sin afectar el colorylatextura.
3.2. Cambios en la composición
Los contenidos de sólidos solubles yde ácidos de los frutos frescos cortados pueden incrementar o disminuir en el tejido vegetal desdeelmomentodel corte,almacenamiento y hasta su consumo, ya que involucran reacciones enzimáticas que son favorecidas poreldañofísico,generandocambiosensabor y por lo tanto en la aceptabilidad por parte de losconsumidores(BeaulieuyBaldwin,2001)
Según Kader (1986) en las frutas frescas empacadas en atmósfera modificada se reduce la pérdida de acidez, cuando la concentración de CO2 es menor del 5%. De acuerdo a Martínez-Ferrer et al. (2002) en su investigación realizada para mango y piña EAM compararon distintos tratamientos (control, altos niveles de CO2, vacío y la
composición gaseosa de 10% CO2, 4% O2 y 86% N2) a 5 ºC, reportan que la acidez disminuye y el contenido de sólidos solubles aumenta al disminuir los almidones presentes durante el almacenamiento, concluyen que el tratamiento de 10% CO2, 4% O2 y86% N2 fue el que presentó el menor cambio de acidez y sólidossolubles.
Bender et al. (2000) en su investigación realizada para la tolerancia a la reducción de oxigeno (2, 3, 4, kPa de O2 ó 25kPa de CO2) en mango (Haden y Tommy Atkins) almacenados a 15ºC, encontraron que los niveles de azúcar no fueron afectados significativamente en comparación al empacado con aire, cuando ambas variedades fueron sometidas a bajas y altas concentraciones de O2 y CO2, respectivamente. En contraste, la acidez titulable se afectó significativamente (p<0.05) para ambas variedades en los tratamientos de bajoO2 yaltoCO2
Rocculi et al. (2005) observaron que los sólidos solubles totales de rebanadas de kiwi se mantienen al aplicar EAM activo con óxido nitroso (90% N2O, 5% O2 y 5%CO2) por 12 días a 4ºC en comparación con EAM pasivo y activo.
En la investigación realizada por Del Caro et al. (2004) para cítricos tangelo Minneola (híbrido entre mandarina y pomelo), mandarina Palazelli y naranja Shamouti, concluyen que el EAM pasivo mantiene el contenidodesólidossolublesyacideztitulable hasta12díasa4ºC.
3.3. Cambios en los compuestos bioactivos
Además de una gran cantidad de vitaminas, minerales, fibra, proteína y carbohidratos, las frutas contienen un grupo compuesto por fitonutrientes (sustancias orgánicas activas) que son los responsables de proveer el color, olor, sabor y aroma. Estos compuestos
bioactivos incluyen compuestos fenólicos, flavonoides, isoflavonoides, tioles, carotenoides, ácido ascórbico, tocoferoles, indoles, iso-tiocianatos y glucosinolatos (Yang, 2011). Los fitonutrientes tienen mecanismos complementarios de la actividad antioxidante,eliminandoradicaleslibres,iones metálicos, inhibición o reducción de diferentes enzimas (lipoxigenasas, xantina-oxidasa, ciclo-oxigenasas) e inducción a la actividad enzimática (oxidación o reducción) (Sadik et al.,2003).
Los compuestos fenólicos incluyen una serie de metabolitos que son biosintetizados a partir de los carbohidratos en las frutas, como el ácido fenólico, flavonoides y taninos, así como sus correspondientes flavonas, catequinas, antocianinas, e isoflavonoides, entre muchos otros (Hollman y Arts, 2000; Yang, 2011). Los carotenoides son los pigmentos naturales solubles en grasa provenientes de las plantas y algas susceptibles a la oxidación, se localizan en los cromoplastos y son responsables del color amarillo, naranja y rojo de muchas frutas y vegetales; se clasifican en carotenos sin oxígeno (α y β- caroteno y licopeno) y con oxígeno (xantofilas) Por ser antioxidantes naturales llegan a prolongar la vida de anaquel de los productos frescos cortados. Además, proveen provitamina A (retinol) al ser humano (DiMascio et al.,1989;OngyTee,1992).
El EAM se caracteriza por disminuir el contenido de clorofila y la biosíntesis de carotenoides presentes en las frutas y verduras (Kader, 1986). Pretel et al. (1998) observaron la influencia de la atmósfera modificada en la preservación de carotenoides en naranja procesada cuando en la composición gaseosa, se han reducido los niveles de oxígeno, generandounaumento delniveldedióxidode carbonodurante11díasdealmacenamiento.
Kader y Ben-Yehoshua (2000) encontraron que a altas concentraciones de oxígeno hay un
efecto benéfico en la retención de ácido ascórbico. De acuerdo al estudio realizado por Agar et al. (1999) al evaluar la influencia de varias condiciones de envasado sobre el contenido de ácido ascórbico en rodajas de kiwi, encontraron que disminuyó, después de 12 días de almacenamiento, alrededor de 7, 12 y 18% cuando se envasó en atmósferas de 0.5, 2y4kPadeO2,respectivamente.
Investigaciones en mango fresco cortado (González-Aguilar et al., 2000; MartínezFerrer et al., 2002) demostraron que el almacenamiento en refrigeración (7-10ºC) en AM, tratado con estabilizadores de color (ácido ascórbico), pueden extender la vida de anaquel hasta por 10 días sin presentar cambios aparentes en su calidad, pero con pérdidas del 10 y 5% en carotenos y vitamina Crespectivamente.
Gil et al. (2006) estudiaron los cambios en la calidad y retención de nutrientes en piña, reportaron que, cuando el fruto alcanzó 6 días de almacenamiento a 5ºC, presentó pérdida de carotenos (carotenos totales y -caroteno) y vitamina C hasta del 25 y 10% respectivamente. De acuerdo a los resultados obtenidos por los autores, sugieren que el EAM podría tener beneficios en la calidad del fruto y así evitar la pérdida de nutrientes principales.
3.4. Calidad sensorial
Calidad en los alimentos se define como la composición de las características individuales que diferencian un producto y se determina por su grado de aceptabilidad. La forma más directa de medir la calidad de un producto alimenticio es mediante la evaluación que el ser humano realiza con sus sentidos de los atributos sensoriales del producto a través de la evaluación sensorial. En las frutas y hortalizas existen 4 atributos que permite distinguir su calidad: 1) color y apariencia, 2) flavor (sabor y aroma), 3) textura y 4) valor
nutricional (Barret et al., 2010). En especial, las frutas frescas cortadas deben tener una apariencia atractiva, sabor y aroma aceptables, textura apropiada y mantener su valor nutricional.
Según Crisosto et al. (2003) el color y aparienciadel fruto atraenal consumidorhacia el producto porque indica calidad en sabor y frescura, por lo tanto en las frutas frescas son atributos que tienen influencia en la toma de decisión sobre la compra y consumo de un fruto. De la misma manera, el sabor y aroma están relacionados con la madurez de los frutos frescos cortados. De acuerdo a Barret et al. (2010), un defecto en la textura origina un rechazo total. Desafortunadamente, el valor nutricional de las frutas no tiene forma de ser distinguido de manera individual, es decir, cuál de ellas tiene mayor contenido de vitamina C, fibra, o fitonutrientes. Los efectos del EAM sobre la calidad de los frutas frescas cortadas han sido estudiados por numerosos autores, y a continuación se hará referencia de algunosdesusestudios.
Martínez-Ferrer et al. (2002) evaluaron la diferencia de mango y piña EAM con 10% CO2, 4% O2 y 86% N2 con respecto a los frutos frescos utilizando una escala de 10 puntos; los panelistas evaluaron textura, apariencia y color entre los tratamientos por cada fruta, y encontraron diferencias significativas (p<0.05) para el mango con respecto al control a diferencia de la comparación entre piña EAM y sin AM. Marrero y Kader (2006) estudiaron el efecto de la temperatura de almacenamiento y las concentraciones de 8 kPa de O2 y 10 kPa CO2 al empacar y almacenar piña, los investigadores reportan que la composición gaseosa utilizada, permite conservar las piezas del fruto por más de 2 semanas a 5 ºC sin presentarcambiosindeseablesenlacalidaddel producto.
Chauhan et al. (2006b) investigaron el
efecto sinérgico de la atmósfera modificada (3% O2, 6%CO2, 91% N2 o aire) y el procesamientomínimoconpre-tratamientosde agentes reafirmantes (CaCl2), antimicrobianos (sorbato de potasio y benzoato de sodio) y antioxidantes (ácido ascórbico), sobre la calidad de papaya cortada. Demostraron que no hubo pérdida de la calidad sensorial de la frutacuandoéstarecibiólospre-tratamientos y fue expuesta a la mezcla de gases compuesta por (3%O2, 6%CO2, 91% N2) como atmósfera modificadaa6ºC.
3.5. Estabilidad microbiológica
Las frutas y hortalizas mínimamente procesadas han sido catalogadas como posible vehículo de algunos microorganismos patógenos, así como el desarrollo de bacterias Gram-negativas, ácido lácticas y levaduras. Al mismo tiempo, estos alimentos son almacenados a temperaturas de refrigeración, por lo que son susceptibles a contaminación con microorganismos psicrotrofos como Pseudomonas fluorescens o Listeria monocytogenes si no existe un buen control de la temperatura (Nguyen-the y Carlin, 1994).
Las frutas, a diferencia de las hortalizas, contienen mayores cantidades de azúcar y un pH más ácido (4.6 o inferior). Este pH junto con los ácidos orgánicos provenientes de la naturaleza del fruto, hacen que normalmente seinhibaelcrecimientodelasbacteriasqueno sean las ácido lácticas. Por consiguiente, los hongos son los microorganismos predominantesenlasfrutas(Brackett,1987).
El control de crecimiento de los mohos en el EAM, está sujeto a la concentración de CO2 dentro del empaque; los mohos se caracterizan por ser microorganismos aerobios y pueden llegar a inhibirse a una alta concentración de CO2 (>10%) y a una baja concentración de oxígeno (< 3%) (Littlefield et al., 1966; Nguyen-theyCarlin,1994).
En el EAM a muy bajas concentraciones
de O2 pueden desarrollarse algunos microorganismos patógenos. Farber (1991) y Szabo et al. (2000) señalan como patógenos potenciales Yersinia enterocolítica, Aeromonas, A. caviae y L. monocytogenes. Microorganismos patógenos como L. monocytogenes, E. coli y C. botulinum llegana desarrollarse en atmósferas reducidas de O2 (Al-Alti y Hotchkiss, 2002). Cuando la concentración de oxígeno es suficientemente baja, la atmósfera modificada será afín a los anaerobios facultativos u obligados. El empleo de bajas temperaturas durante el almacenamiento incrementa los efectos inhibitorios del EAM al aumentar la solubilidad del CO2 en la fase líquida que rodea al alimento. Por lo tanto, la temperatura a la que se mantienen las frutas frescas cortadas y EAM es el factor más importante porque afecta el crecimiento microbiano (Sandhya,2010)
Pereira et al. (2004) ensuestudiorealizado para guayaba con y sin DO y empacada en AM y aire a 5ºC, reportaron que no hubo presencia de Salmonella ni de bacterias coliformes. Las guayabas empacadas en aire fresco presentaron crecimiento de 4.4 x 104 UFC/g para mohos ylevaduras. Las guayabas EAM (7.5% O2 y 18% CO2) mostraron estabilidadmicrobiana.
En la investigación realizada por MartínezFerrer et al. (2002) en mango y piña mínimamente procesadas y empacadas en atmósfera modificada (10% CO2, 4% O2 y 86% N2), reporta una mínima contaminación microbiana (104-105 UFC/g) al ser expuestas a altas concentraciones de CO2 (10%) para ambasfrutas.
En la investigación realizada por MonteroCalderón et al. (2008) para piña fresca cortada y almacenada a 5ºC durante 20 días, utilizaron dos tipos de atmósfera: activa (oxígeno al 11.4 y 40%) y pasiva (aire y recubrimiento comestible), encontraron que no hubo
diferencia significativa (p>0.05) entre las diferentes condiciones de empacado. Sin embargo si presentaron diferencias significativas (p<0.05) durante el tiempo de almacenamiento, donde obtuvieron recuentos iniciales de 103-104 UFC/g para mohos y levaduras en el día cero, alcanzando una población máxima de 107 UFC/g, comportamiento similar presentaron las bacterias mesófilas y psicrófilas (107 UFC/g) despuésde18díasdealmacenamientoa5ºC.
Rodríguez et al. (2006),estudiaronelefecto de empacar papaya deshidratada osmóticamente (DO) a 50ºBx durante 15 días a 5ºC, utilizando soluciones de sacarosa que contenían lactato de calcio (0.05M) y ácido láctico (0.02M) en tres tipos de empaques (PVC, LDPE y PET), empleando la composición gaseosa del aire como AM. Observaron, que las muestras de papaya (DO) y empacadas en contendores de PET, alcanzaron el 1% O2 y 13.62% CO2 como atmósfera modificada en el interior del empaque,lo cuál generó unamayor resistencia a la contaminación por mohos y levaduras en comparación con los otros empaques, alcanzando una detección menor de 102 UFC/g.
Bico et al. (2009) investigaron el efecto combinado de sumergir plátano variedad Cavendish en un solución compuesta de cloruro de calcio (1% w/v), ácido ascórbico (0.75% w/v) y cisteína (0.75% w/v), como segundo tratamiento, utilizaron la solución anterior yal mismotiempoemplearonel EAM (3% de O2 y 10% CO2) y como un tercer tratamiento, la combinación de las dos anteriores másel empleo de carregenina (0.5% w/v) como recubrimiento comestible. Los análisis microbiológicos mostraron en el día cero la presencia de microorganismos mesófilos aerobios en todas las muestras de plátano las cuales alcanzaron un mínimo de 101 UFC/g, en el segundo día fue significativo (p<0.05) el crecimiento de mesófilos aerobios
en el control con respecto a los tres tratamientosllegandoaalcanzarunapoblación máxima de 3 x 102 UFC/g al 5 día de almacenamiento a 5ºC; comportamiento similar obtuvieron para el recuento de coliformes totales, mohos y levaduras, donde observaron que en el segundo día de almacenamiento en refrigeración, los tratamientos propuestos presentaron los menores recuentos, logrando alcanzar una población inferior a 1.5 x 102 UFC/g correspondientealostratamientosdosytres.
Conclusiones y comentarios finales
En la presente revisión se dieron a conocer los principales cambios químicos, microbiológicos y sensoriales de las frutas tropicales frescas cortadas y empacadas en atmósfera modificada durante su almacenamiento en refrigeración. De acuerdo a las investigaciones revisadas, se observó que el empacado en atmósfera modificada es una tecnología que permite extender la vida de anaquel de las frutas frescas cortadas, porque conserva los principales componentes bioactivos (ácido ascórbico, carotenoides entre otros), además de mantener las características físicas, aceptabilidad sensorial y estabilidad microbiológica de las frutas tropicales frescas cortadas. Principalmente, el EAM se caracteriza por ser inocua al ser humano, debido a que las condiciones atmosféricas se restablecen al abrir el empaque. Al mismo tiempo, el dióxido de carbono tiene un efecto inhibitorio sobre la respuesta de los microorganismos. Por lo anterior, el EAM es una alternativa idónea que permite extender la calidad de las frutas tropicales frescas cortadas, y conjuntamente puede combinarse con recubrimientos comestibles, que combinados contribuirán a una mayor estabilidaddelalimento.
Es importante mencionar que una
inadecuadaatmósferamodificadapuedecausar desordenes fisiológicos y procesos fermentativos, logrando incrementar el riesgo de una contaminación microbiana por un mal manejo de la temperatura y humedad relativa del medio que rodea al fruto empacado. Por lo tanto, es relevante conocer la velocidad de respiración del fruto, así como realizar una adecuada selección del tipo de empaque y atmósfera a emplear con la finalidad de mantener los atributos físicos y nutricionales delproducto.
Agradecimientos
Marcela Rangel Marrón agradece al Programa de mejoramiento al profesorado (PROMEP) porlabecadoctoralotorgada.
Referencias
Agar, I. T., Massantini, R., Hess-Pierce, B. y Kader, A. A. 1999. Postharvest CO2 and ethylene production and quality maintenance of fresh-cut kiwifruit slices. Journal of Food Science. 64 (3):433-440.
Aharoni, Y. y Houck, L.G. 1982. Change in rind, flesh, and juice color of blood oranges stored in air supplemented with ethylene or in oxygen-enriched atmospheres. Journal of Food Science 47 (6):2091–2092.
Al-Alti, T. y Hotchkiss, H. 2002. Application of packaging and modified atmosphere to fresh-cut fruits and vegetables. En: O. Lamikanra (Ed.). Fresh cut fruits and vegetables: Science, Technology and Market. CRC Press: Boca Raton, FL, EE.UU. pp. 305-338.
Bai, J., Satner, R., Watada, A. y Lee, Y. 2001. Modified atmosphere maintains quality of fresh-cut cantaloupe (Cucumis melo L.). Journal of Food Science. 66 (8):1207 – 1211.
Barret, D. M., Beaulieu, J. C. y Shewfelt, R. 2010. Color, flavor, texure, and nutritional quality of freshcut fruits and vegetables: desiralbe levels, instrumental and sensory measurement, and the
effects of processing. Critical Reviews in Food Science and Nutrition. 50 (5):369-389.
Beaulieu J. C. y Baldwin E.A. 2001 Flavor and aroma of fresh-cut fruits and vegetables. En: O. Lamikanra (Ed.). Fresh cut fruits and vegetables: Science, Technology and Market. CRC Press: Boca Raton, FL, EE.UU. pp. 391-426.
Bender, R. J., Brecht, J. K., Sargent, S. A. y Huber, D. J. 2000. Mango tolererance to reduced oxygen levels in controlled atmosphere storage. Journal of the American Society for Horticultural Science. 125 (6):707-713.
Bico, S. L. S., Raposo, M. F. J., Morais, R. M. S. C. y Morais, A. M. M. B. 2009. Combined effects of chemical dip and/or carrageenan coating and/or controlled atmosphere on quality of fresh-cut banana. Food Control. 20 (5): 508-514.
Brackett, R. E. 1987. Microbiological consequences of minimally processed fruits and vegetables. Journal of Food Quality.10 (3):195-206.
Brecht, J. K., Chau, K. V., Fonseca, S. C., Oliveira, F. A. R., Silva, F. M., Nunes, M. C. M. y Bender, R.J. 2003. Maintaining optimal atmosphere conditions for fruits and vegetables throughout the postharvest handling chain. Postharvest Biology and Technology. 27 (1): 87-101.
Caleb, O. J., Opara, U. L. y Witthuhun, C. R. 2012. Modified atmosphere packaging of pomegranate fruit and arils: A Review. Food Bioprocess Technology. 5 (1):15-30.
Chauhan, O., Raju, P., Dasgupta, D., Shylaja, R., Rao, S. y Bawa, A. 2006a. Modified/controlled atmosphere storage of minimally processed mango slices (var. Arka anmol). American Journal of Food Technology. 1 (2):105-116.
Chauhan, O., Raju, P., Shylaja, R., Dasgupta, D. y Bawa, A. 2006b. Synergistic effects of modified atmosphere and minimal processing on the keeping quality of pre-cut papaya (Carica papaya L.). Journal of Horticultural Science and Biotechnology. 81 (5):903-909.
Chonhenchob, V., Chantarasomboon, Y. y Singh, S.P. 2007. Quality changes of treated fresh-cut tropical fruits in rigid modified atmosphere packaging containers. Packaging Technology and Science. 20 (1):27-37.
Crisosto, C., Crisosto, G. y Metheney, P. 2003. Consumer acceptance of "Brooks" and "Bing" cherries in mainly dependent on fruit SSC and visual
skin color. Postharvest Biology and Technology. 28 (1):159-167.
Day, B. 2000. Modified atmosphere packaging of fresh fruit and vegetables. An overview. Acta Horticulturae. 553:585-590.
Del Caro, A., Piga, A., Vacca, A. y Agabbio, M. 2004. Changes of flavonoids, vitamin C and antioxidant capacity in minimally processed citrus segments and juices during storage. Food Chemistry. 84 (1):99105.
Del Nobile, M., Licciardello, F., Scrocco, C., Muratore, G. y Zappa, M. 2007. Desing of plastic packages for minimally proceeed fruits. Journal of Food Engineering. 79 (1):217-224.
Di Mascio, P., Kaiser, S. y Sies, H. 1989. Lycopene as the most efficient biological carotenoid singlet oxygen quencher. Archives of Biochemistry and Biophysics. 274 (2):532-538.
Duan, X .W., Jiang, Y. M., Su, X. G. y Zhang, Z. Q. 2004. Effects of a pure oxygen atmosphere on enzymatic browning of harvested litchi fruit. Journal of Horticultural Science and Biotechnology. 79 (6): 859-862.
Farber, J. M. 1991. Microbial aspects of modifiedatmosphere packaging technology: A Review. Journal of Food Protection. 54 (1):58-70.
Farber, J., Warburton, D., Laffey, P., Purvis, U. y Gour, L. 1993. Modified-atmosphere packaged pasta. A microbiology quality assessment. Italian Journal of Food Science. 2:157-167.
Gil, M., Aguayo, E. y Kader, A. 2006. Quality changes and nutrient retention in fresh-cut versus whole fruits during storage. Journal of Agricultural and Food Chemistry. 54 (12):4284-4296.
González-Aguilar, G. A., Wang, C. Y. y Buta, J.G. 2000. Maintaining quality of fres-cut mangoes using antibrowning agents and modified atmosphere packaging. Journal of Agricultural and Food Chemistry. 48 (3):4204-4208.
Hollman, P. y Arts, I. 2000. Flavonols, flavones and flavanols-nature, occurrence and dietary burden. Journal of the Science of Food and Agriculture. 80 (7):1081-1093.
Jiang, Y.M. y Fu, J. R. 1999. Biochemical and physiological changes involved in browing of litchi fruit caused by water loss. Journal of Horticultural Science and Biotechnology. 74 (1):43-46.
Jacomino, A., Kluge, R., Sarantopoulos, C. y Sigrist, J. 2001. Evaluation of plastic packages for guava refrigerated preservation. Packaging Technology and Science. 14 (1):11-19
Kader, A. A. 1986. Biochemical and physiological basis for effects of controlled and modified atmospheres on fruits and vegetables. Food Technology. 40 (5):99-104.
Kader, A. A. y Ben-Yehoshua, S. B. 2000. Effects of superatmospheric oxygen levels on postharvest physiology and quality of fresh fruits and vegetables. Postharvest Biology and Technology. 20 (1):1-13
Kader, A. 2002. Modified atmospheres during transport and storage. En: A. A. Kader (Ed.). Postharvest technology of horticultural crops. 3era. Edición. University of California Publication. EE.UU. pp. 135-144.
King, A. y Bolin, H. 1989. Physiological and microbiological storage stability of minimally processed fruits and vegetables. Food Technology 43 (2):132-135,139
Lee, D. S., Yam, K. y Pergiovanni, L. 2008. Vacum/Modified atmosphere packaging. En: D. S. Lee, K. Yam y L. Piergiovanni (Eds.). Food packaging science and technology. CRC Press, Boca Raton, FL, EE.UU. pp. 397-424.
Lin, Z. y Schyvens, E. 1995. Influence of blanching treatments on the texture and color of some processed vegetales and fruits. Journal of Food Process Preservation. 19 (6):451-465.
Littlefield, N. A., Wankier, B. N., Salunkhe, D. y McGill, J. 1966. Fungistatic effects of controlled atmospheres. Applied microbiology. 14 (4):579-581.
Lucera, A., Costa, C., Mastromatteo, M., Conte, A. y Del Nobile, M. 2011. Fresh-cut broccoli florets shelf-life as affected by packaging film mass transport properties. Journal of Food Engineering. 102 (2):122-129.
Mangaraj, S., Goswami, T. y Mahajan, P. 2009. Applications of plastic films for modified atmosphere packaging of fruits and vegetables: A Review. Food Engineering Reviews. 1 (2):133-158.
Martín-Belloso, O. y Oms-Oliu, G. 2005. Efecto de la atmósfera modificada en las características físicoquímicas y nutricionales de la fruta fresca cortada Proyecto XI.22 Desarrollo de tecnologías para la conservación de vegetales frescos cortados. Simposium "Nuevas tecnologías de conservación y
envasado de frutas y hortalizas. Vegetales frescos cortados". La Habana,Cuba. pp 47-58. Marzo 2005.
Marrero, A. y Kader, A.A. 2006. Optimal temperature and modified atmosphere for keeping quality of fresh-cut pineapples. Postharvest Biology and Technology. 39 (2):163–168.
Martínez-Ferrer, M., Harper, C., Pérez-Muñoz, F. y Chaparro, M. 2002. Modified atmosphere packaging of minimally processed mango and pineapple fruits. Journal of Food Science. 67 (9):3365-3371.
Montero-Calderon, M., Rojas-Graü, M. A. y MartínBelloso, O. 2008. Effect of packaging conditions on quality and shelf-life of fresh-cut pineapple (Ananas comosus). Postharvest Biology and Technology. 50 (2-3):182-189.
Nguyen-the, C. y Carlin, F. 1994. The microbiology of minimally processed fresh fruits and vegetables. Critical Reviews in Food Science and Nutrition. 34 (4):371-401
Oms-Oliu, G., Soliva-Fortuny, R. y Martín-Belloso, O. 2008. Modeling changes of headspace gas concentrations to describe the respiration of freshcut melon under low or superatmospheric oxygen atmospheres. Journal of Food Engineering. 85 (3):401-409.
Ong, A. y Tee, E. 1992. Natural sources of carotenoids from plants and oils. Methods in Enzymology. 213:142-167
Parry, R. 1993. Envasado de los alimentos en atmósfera modificada. A. Madrid Vicente. Madrid, España. 331 p.
Pereira, L., Rodrigues, A., Sarantópoulos, C., Junqueira, V., Cunha, R. y Hubinger, M. 2004. Influence of modified atmosphere packaging and osmotic dehydratation on the quality maintenance of minimally processed guavas. Journal of Food Science. 69 (4):172-177.
Pesis, E., Dvir, O., Feygenberg, O., Arie, R. B., Ackerman, M. y Lichter, A. 2002. Production of acetaldehyde and etanol during maturation and modified atmosphere storage of litchi fruit. Postharvest Biology and Technology. 26 (2):157165.
Poubol, J., e Izumi, H. 2005. Shelf life and microbial quality of fresh-cut mango cubes stored in high CO2 atmospheres. Journal of Food Science. 70 (1):69-74.
Pretel, M., Fernández, P., Romojaro, F. y Martínez, A. 1998. The effect of modified atmosphere packaging
on ready-to-eat oranges. LWT - Food Science and Technology. 31 (4):322-328.
Qadir, A. y Hashinaga, F. 2001. Inhibition of postharvest decay of fruits by nitrous oxide. Postharvest Biology and Technology. 22 (3):279–283.
Ranasinghe, L., Jayawardena, B. y Abeywickrama, K. 2005. An integrated strategy to control post-harvest decay of embul banana by combining essential oils with modified atmosphere packaging. International Journal of Food Science & Technology. 40 (1):97103.
Rattanapanone, N., Lee, Y., Wu, T. y Watada, A. 2001. Quality and microbial changes of fresh-cut mango cubes held in controlled atmosphere. Horticultural Science. 36 (6):1091-1095.
Rocculi, P., Romani, S. y Dalla Rosa, M. 2004. Evaluation of physico-chemical parameters of minimally processed apples packed in nonconventional modified atmosphere. Food Research International. 37 (4):329-335.
Rocculi, P., Romani, S. y Rosa, M. 2005. Effect of MAP with argon and nitrous oxide on quality maintenance of minimally processed kiwifruit. Postharvest Biology and Technology. 35 (3):319328.
Rodríguez-Félix, A., Rivera-Domínguez, M. y González-Aguilar, G. 2005. Uso de atmósferas modificadas y controladas. En: G. A. GonzálezAguilar, A. A. Gardea, F. Cuamea-Navarro (Eds.). Nuevas tecnologías de Conservación de productos vegetales frescos cortados. CIAD, A.C. México. pp. 447-474.
Rodríguez, A. C. C., Pereira, L. M., Sarantópoulos, C. I. G. L., Bolini, H. M. A., Cunha, R. L., Junqueira, V C. A. y Hubinger, M. D. 2006. Impact of modified atmosphere packaging on the osmodehydrated papaya stability. Journal of Food Processing and Preservation. 30:563-581.
Sadik, C., Sies, H. y Schewe, T. 2003. Inhibition of 15lipoxygenase by flavonoids: structure-activity relations and mode of action. Biochemical Pharmacology. 65 (5):773-781.
Sandhya. 2010. Modified atmosphere packaging or fresh produce: Current status and future needs. LWT - Food Science and Technology. 43 (3):381-392.
Sinigaglia, M., Corbo, M., D'Amato, D., Campaniello, D. y Altieri, C. 2003. Shelf-life modelling of readyto-eat coconut. International Journal of Food Science and Technology. 38 (5):547-552.
Szabo, E., Scurrah, K. y Burrows, J. 2000. Survey for pyschrotrophic bacterial pathogens in minimally processed lettuce. Letters of Applied Microbiology. 30:456-460.
Varoquaux, P. y Wiley, R. 1994. Biological and biochemical changes in minimally processed refrigerated fruits and vegetables. En: R.C. Wiley (Ed.). Minimally Processed Refrigerated Fruits and Vegetables. Chapman-Hall, New York, EE.UU. pp. 226-268.
Yahia, E.M. 2006. Modified and controlled atmospheres for tropical fruits. Stewart Postharvest Review. 5 (6):1-10
Yang, J. 2011. Phytochemical changes of fresh-cut fruits and vegetables in controlled and modified atmosphere packaging. En: A. L. Brody, H. Zhuan y J. H. Han (Eds.). Modified atmosphere packaging for fresh-cut fruits and vegetables. Primera Edición. Wiley-Blackwell, EE.UU. pp. 101-140.
Zagory, D. y Kader A. 1988. Modified atmosphere packaging of fresh produce. Food Technology. 42 (9):70-77.
Zhuang, H., Barth, M. y Fan, X. 2011. Respiration and browning discoloration of fresh-cut produce in modified atmosphere packaging. En: A. L. Brody, H. Zhuang y J. H. Han (Eds.). Modifief atmosphere packaging for fresh-cut fruits and vegetables. Primera Edición. Wiley-Blackwell, EE.UU. pp 3156.

Temas Selectos de Ingeniería de Alimentos 6 - 2 (2012): 110 - 121

Películas comestibles formuladas con polisacáridos: propiedades y aplicaciones
M. F. Domínguez-Courtney * y M. T. Jiménez-Munguía
Departamento de Ingeniería Química, Alimentos y Ambiental, Universidad de las Américas Puebla. Ex hacienda Sta. Catarina Mártir S/N, San Andrés Cholula, Puebla. C.P.72810. México.
Resumen
Debido a la creciente preocupación de sustituir empaques plásticos por empaques biodegradables y a la búsqueda de tecnologías para prolongar la vida de anaquel de los alimentos, existen diversos estudios de películas comestibles. Las películas obtenidas con polisacáridos son una opción atractiva porque estos compuestos son abundantes en la naturaleza y renovables, además provienen de diversas fuentes. Sin embargo, las películas formuladas con polisacáridos presentan valores altos de permeabilidad al vapor de agua y limitaciones en cuanto a sus propiedades mecánicas. Para mejorar las propiedades mecánicas de estas películas, se ha estudiado la adición de plastificantes. Mientras que para disminuir las altas permeabilidades al vapor de agua se ha estudiado la adición de surfactantes o compuestos hidrofóbicos. Entre los polisacáridos estudiados el almidón produce las películas con mejores características mecánicas. Mientras que las películas formuladas con gomas presentan las menores permeabilidades al vapor de agua El objetivo de la presente revisión es exponer un panorama general de películas comestibles formuladas con polisacáridos adicionados de manera individual o en mezclas.
Palabras clave: películas comestibles, polisacáridos, propiedades mecánicas, permeabilidad al vapor de agua.
Abstract
Due to the increasing concern of plastic substitution in packaging with biodegradable materials and the quest of new technologies to increase shelf life of food products, there are several studies regarding edible films. Films produced using polysaccharides are a viable option because these materials are renewable, can be obtained from various sources and are abundant in nature. However, films produced with polysaccharides have high water vapor permeability and limited mechanical properties. The addition of plasticizer for improving mechanical properties has been studied, as well as addition of surfactants or hydrophobic materials in order to lower water vapor permeability. Among the studied polysaccharides films produced with starch showed the best mechanical properties. While gum formulated films had the lowest water vapor permeability values. The aim of this article is to give a general outline of edible films produced with polysaccharides formulated individually or in combination.
Keywords: edible films, polysaccharides, mechanical properties, water vapor permeability.
*Programa de Doctorado en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: mariaf.dominguezcy@udlap.mx
Introducción
Las películas en el área de alimentos funcionan como barreras selectivas para la transferencia de gases, humedad y nutrientes; son utilizadas porque ayudan a disminuir el deterioro de productos alimenticios causado por factores ambientales. De igual manera, se busca que eviten o disminuyan la oxidación y pérdida de compuestos volátiles responsables de sabores y propiedades específicas de los alimentos. La mayoría de las películas son elaboradas con materiales plásticos. Debido a la preocupación de sustituir empaques plásticos por empaques biodegradables, existen diversos estudios de películas comestibles, que además de las características otorgadas pueden ser ingeridas con el alimento.
Por otra parte, se busca que la materia prima provenga de una fuente renovable, abundante y económica, para que el uso industrial sea factible. Por tal motivo, se han realizado diversos estudios utilizando polisacáridos como materiales para la formulación de películas comestibles.
La formulación de cada película comestible depende directamente de la aplicación que se requiere; la cual determina las propiedades mecánicas y de barrera deseables. Diversos materiales han sido investigados para la formación de películas de forma individual o en sistemas con más de un compuesto. En muchas ocasiones, es necesario añadir un plastificante para que la película no sea quebradiza y se pueda manejar fácilmente.
Los polisacáridos se obtienen de fuentes naturales, principalmente de origen vegetal. Los más utilizados para la formación de películas comestibles incluyen celulosa y sus derivados, almidón de diversas fuentes, gomas, carrageninas y alginato.
En la presente revisión se expondrá un panorama general de películas comestibles formuladas con polisacáridos, se resumirán sus propiedades mecánicas y de barrera; y sus aplicaciones en alimentos.
Revisión bibliográfica
1. Materiales para la formación de películas
El deterioro de alimentos durante el almacenamiento puede ser retardado al mejorar los empaques. Se requiere que dicho empaque proteja al producto del medio ambiente, principalmente de los gases y de la humedad; además, es deseable que éste funcione como barrera contra microorganismos que puedan contaminar el alimento. De igual manera, existe una creciente preocupación por reducir la contaminación generada por el uso y la producción de envases alimenticios hechos con plástico. Como posible solución, se estudian materiales biodegradables. Debido a esto, se han buscado diversas alternativas; entre ellas y una de las más estudiadas es el desarrollo de películas comestibles (Rawdkuen etal., 2010).
Las películas comestibles deben funcionar como barrera selectiva a la transferencia de humedad y gases, además de evitar la oxidación de lípidos y la pérdida de compuestos volátiles responsables de aromas y sabores de ciertos alimentos (Espino-Díaz et al., 2010). Deben estar formuladas con compuestos de grado alimenticio y además cumplir con costos relativamente bajos de producción (Vargas et al., 2008). Los materiales probados para la formación de películas incluyen proteínas, polisacáridos y lípidos. Entre las proteínas principales se encuentran la gelatina, el colágeno y algunas proteínas de origen vegetal como las de soya y maíz. Los polisacáridos más estudiados incluyen celulosa y sus derivados, carrageninas, gomas, pectina, almidón y alginatos; mientras que los lípidos más utilizados son las ceras, triglicéridos y algunos ácidos grasos (Nanda y Nayak, 2009).
Los lípidos forman películas que tienen buenas propiedades de barrera contra el paso del agua, pero sus aplicaciones se ven limitadas porque las películas obtenidas son quebradizas (Liu et al., 2006). En cambio, las películas formuladas con polisacáridos o proteínas se caracterizan por ser buenas barreras al oxígeno; sin embargo, por ser fabricadas con compuestos hidrofílicos, son
permeables al agua (Vargas et al., 2008; Nanda y Nayak, 2009).
1.1. Polisacáridos
Los polisacáridos son utilizados en la industria de alimentos como gelificantes, espesantes estabilizantes, y formadores de películas comestibles, entre otras aplicaciones. Se obtienen principalmente de vegetales, algas y microorganismos. Entre los polisacáridos obtenidos de vegetales están la celulosa y el almidón; los polisacáridos obtenidos de algas que más se utilizan son los alginatos, las carrageninas y el agar; mientras que los polisacáridos obtenidos de microorganismos incluyen la goma xantana, el dextrano y la goma gellan, entre otros (Khan et al., 2007).
Al usar polisacáridos como compuestos para la formación de películas comestibles, se obtienen películas transparentes que presentan propiedades mecánicas moderadas. Sin embargo, las aplicaciones se limitan debido a que las películas son solubles en agua y permeables al vapor de agua. Para mejorar dichas condiciones es posible adicionar compuestos hidrofóbicos como ceras o aceites, y también se pueden realizar tratamientos para el entrecruzamiento de las moléculas (Vargas etal., 2008; Campos etal., 2011).
Debido a su naturaleza hidrofóbica, la adición de surfactantes mejora la resistencia al vapor de agua de las películas formuladas con polisacáridos; sin embargo, las aplicaciones se ven limitadas, debido a que se incrementa la opacidad de las películas resultantes. Por ejemplo, la opacidad de películas formuladas con metilcelulosa, glucomanan y pectina en proporción 1/4/1, presentaron un aumento en opacidad del 3% al adicionar éster de sacarosa como surfactante (Chambi y Grosso, 2011). Por un efecto sinérgico, la adición de una proteína a la formulación puede mejorar las propiedades mecánicas y de barrera de películas comestibles de polisacáridos (Chen et al., 2010; Espinoza-Herrera etal., 2011).
1.2. Plastificantes
Para la formación de películas comestibles muchas veces es necesario agregar un plastificante para mejorar las propiedades mecánicas de las mismas. Los plastificantes usados incluyen glicerol, polietilenglicol, sorbitol y algunos azúcares, entre otros. Debido a que el plastificante reduce los enlaces intermoleculares entre las cadenas de polímeros, los plastificantes modifican las propiedades mecánicas y producen películas más flexibles (Campos etal., 2011).
En un estudio realizado por Jongjareonrak etal (2006) se midieron las propiedades de películas comestibles formuladas con distintas concentraciones de glicerol, polietilenglicol, etilenglicol y sorbitol. En general, las películas formuladas con glicerol presentaron mayor flexibilidad y elongación, mientras que las formuladas con etilenglicol presentaron mayor fuerza tensil. En todos los casos, al aumentar la concentración del plastificante aumentó el porcentaje de elongación y se redujo la fuerza tensil. Por ejemplo, al aumentar la concentración de glicerol de 25 a 75% la fuerza tensil disminuyó de 46.87 a 11.72 MPa, mientras que el porcentaje de elongación aumentó de 10.87 a 98.14%.
Bozdemir y Tutas (2003) compararon los valores de permeabilidad al vapor de agua de películas de goma de algarrobo, utilizando distintos plastificantes en diferentes concentraciones. Para todos los sistemas, al aumentar la concentración de plastificante aumentó la permeabilidad al vapor de agua. Por ejemplo, las películas con 0.4% de glicerol mostraron valores de 4 × 10-11 g m-1 s-1 Pa-1 de permeabilidad al vapor de agua, mientras que con las que contenían 1.6% de glicerol se obtuvieron valores de 6 × 10-11 g m-1 s-1 Pa-1. Para la misma concentración de plastificante de 1.6%, las películas con glicerol presentaron valores de permeabilidad al vapor de agua del doble que las formuladas con la misma cantidad de polietilenglicol.
Javanmard etal. (2011) estudiaron la mezcla de glicerol y polietilenglicol (PEG) a distintas concentraciones en películas de almidón al 4%. La concentración de glicerol fue variada de 0 a 3%, mientras que los niveles de PEG utilizados fueron 0, 0.2, 0.3 y 0.4%. Las formulaciones de almidón que sólo contenían PEG no se pudieron despegar de los moldes, por lo que no formaron películas. Las películas con 2% glicerol y 0.2% PEG presentaron valores de 82.17% de elongación, mientras que con la misma concentración de glicerol y 0.4% de PEG la elongación aumentó a 96.92%. Los investigadores concluyeron que al aumentar el contenido de PEG de la mezcla de plastificantes, se incrementó la elongación, sin embargo, no hubo ningún efecto en las propiedades de barrera.
Aunque los valores de permeabilidad al vapor de agua de las películas adicionadas con glicerol son mayores que las formuladas con otros plastificantes, el glicerol es el plastificante más utilizado debido a que es muy estable y compatible con las cadenas de biopolímeros (Campos et al., 2011). Generalmente, el contenido de glicerol para la formación de películas se encuentra entre el 10 y el 30% (p/p biopolímero seco) (Osés et al., 2009; Tongdeesoontorn et al., 2011). Dentro de dichos límites, al aumentar el contenido de glicerol disminuye la fuerza tensil y aumenta el porcentaje de elongación. Por ejemplo, en un estudio realizado por Qiu-Ping y Wen-Shui, (2008), utilizando la misma composición de las películas al variar el porcentaje de glicerol de 10 a 24%, la fuerza tensil bajó de 39.23 a 28.83 MPa y el porcentaje de elongación aumentó de 8.9 a 110.7%.
Aún cuando la adición de plastificante ayuda a que las películas sean menos quebradizas y más flexibles, existen efectos adversos del uso de este tipo de agentes. En diversos estudios se ha comprobado que debido a su naturaleza, el glicerol es sumamente higroscópico y por tanto, las películas formadas presentan un aumento en el contenido de humedad, lo que a la vez provoca que tengan menores capacidades de protección (Karbowiak et al., 2006; Osés et al., 2009; Bergo etal., 2010).
2. Propiedades mecánicas y de barrera de las películas comestibles de polisacáridos
La fuerza tensil, la elongación y la fuerza de corte son propiedades mecánicas de las películas comestibles que pueden ser usadas para describir el comportamiento del material (Espinoza-Herrera et al., 2011). La fuerza tensil o dureza es la fuerza máxima por área que una película puede soportar antes de romperse; se obtiene dividiendo la fuerza máxima entre el área transversal de la película. La elongación es el porcentaje de cambio máximo en longitud de la película antes de romperse, a menor porcentaje de elongación menor flexibilidad. La fuerza de corte está definida como la fuerza requerida para cortar la película (Wang et al., 2007). En diversos estudios se ha observado que al aumentar el valor de la fuerza tensil, el porcentaje de elongación disminuye y viceversa (Peressini et al., 2004; Brindle y Krochta, 2008).
En un estudio realizado por Wang et al. (2007) a distintas concentraciones de proteínas y polisacáridos para la formación de películas comestibles, se determinó que en general las películas formuladas con polisacáridos tienen mayores valores de fuerza tensil en comparación con las películas formuladas con proteínas. Sin embargo, las películas con polisacáridos tienen menores valores de porcentaje de elongación. Por ejemplo, las películas de gelatina al 8% presentaron una fuerza tensil de 6.60 MPa y un porcentaje de elongación de 89.69%, mientras que con películas formuladas con carboximetilcelulosa al 2% se obtuvieron valores de 11.25 MPa de fuerza tensil y 10.53% de elongación.
Otra propiedad importante de las películas es su función como barreras contra la humedad, ya que se busca que las películas comestibles disminuyan la transferencia de humedad entre el producto y el medio. Dicha propiedad es medida con el valor de permeabilidad al vapor de agua. Se requiere que la permeabilidad al vapor de agua sea lo más baja posible (Qiu-Ping y Wen-Shui, 2008).
De igual manera, se requiere que las películas funcionen como barrera a gases, principalmente oxígeno y dióxido de carbono. Debido a las
M. F. Domínguez-Courtney et al. / Temas
reacciones de oxidación causadas por el oxígeno en varias aplicaciones de películas comestibles, se busca que las películas tengan bajas permeabilidades a éste gas (Fontes etal., 2011).
En la Tabla I se presenta un resumen sobre investigaciones recientes acerca de películas elaboradas con polisacáridos.
6 – 2 (2012): 110 - 121
2.1. Películas de carboximetilcelulosa
Debido a su bajo costo y a que son materiales biodegradables, los derivados de celulosa son utilizados en industrias de alimentos, farmacéuticas y en otras aplicaciones diversas (Espinoza-Herrera et al., 2011). Un derivado de celulosa es la carboximetilcelulosa (CMC),
Biopolímero
Concentraciónde biopolímero(p/v)
Concentraciónde glicerol (p/pbiopolímero)
Alginatode sodio0.02%0.6-2%
EstudioReferencia
Propiedades de barreraTapia et al .,2007
1-5%0-50% Efectos delplastificante enpropiedades Boateng et al .,2009
0.5-2%50%
Propiedades mecánicas a distintas concentraciones delpolímero
Wang et al .,2007
1.75%0.25% Propiedades mecánicasFazilahet al.,2011
Almidón1-5%0.30%
2%0,10,20,30%
1-3%50%
4%13,15,20,25,27%
2%0,15,30,45%
10%0
Carragenina0.03%0,15,30,45%
2-5%50%
Propiedades mecánicas de películasTongdeesoontorn et al .,2011
Propiedades de barreraOsés et al.,2009
Propiedades mecánicas a distintas concentraciones delpolímero
Wang et al .,2007
Efectos delplastificante enpropiedades mecánicas Pressini et al .,2004
Efectos delplastificante enpropiedades físicas Bergo et al .,2008
Propiedades mecánicasRachtanapun et al .,2012
Efectos delplastificante enpropiedadesKarbowiak et al .,2006
Propiedades mecánicas a distintas concentraciones delpolímero
Wang et al .,2007
3%30% Propiedades de barreraHambleton et al .,2008
5-10%25,50%
Carboximetilcelulosa1-5%0.30%
1-2%0,50%
Efectos delplastificante enpropiedades mecánicas Briones et al.,2004
Propiedades mecánicas de películasTongdeesoontorn et al .,2011
Efectos delplastificante enpropiedades mecánicas Boateng et al .,2009
3%0 Propiedades físicasEspinoza-Herrera et al .,2010
2-5%50%
2%0
Propiedades mecánicas a distintas concentraciones delpolímero Wang et al .,2007
Propiedades mecánicas de películas De Moura et al .,2011
Goma gellan0.50%0.6-2% Propiedades de barreraTapia et al .,2007
Goma guar1%50% Propiedades de barreraMehyar et al .,2011
Goma xantana0.01%0,50%
0.25-1%50%
Efectos delplastificante enpropiedadesBoateng et al .,2009
Propiedades mecánicas a distintas concentraciones delpolímero Wang et al .,2007
Tabla I. Estudios recientes sobre películas elaboradas conpolisacáridos.
obtenida mediante la adición de grupos carboximetilos a la molécula de celulosa; es un producto soluble en agua, no tóxico y que cada vez es más utilizado (Enebro etal., 2007).Las películas comestibles formadas con CMC son resistentes, transparentes y pueden ser flexibles con la adición de plastificantes como glicerol. Sin embargo, la disminución en la fuerza tensil debe ser considerada como una limitante para el contenido de glicerol. Se observó que en películas de CMC: glicerol 2:1 la fuerza tensil fue de 48 N, mientras que al aumentar la concentración de glicerol a una proporción 2:3 la fuerza tensil observada fue de 7.9 N. (Boateng etal., 2009).
Además de las propiedades mecánicas, las películas formuladas con CMC también tienen aplicaciones limitadas a causa de las altas permeabilidades al vapor de agua (EspinozaHerrera et al., 2011). Sin embargo, la permeabilidad al vapor de agua de dichas películas puede ser disminuida. En un estudio realizado por De Moura et al. (2011), las propiedades de las películas formadas con CMC al 2% mejoraron al adicionar quitosano. Al agregar nanopartículas de quitosano de 110 nm, bajaron los coeficientes de difusión, lo que causó que la permeabilidad al vapor de agua de las películas disminuyera de 1.12 a 0.65 g mm K-1 Pa-1 h-1 m-2 .
2.2. Películas de carragenina
Las carrageninas son polímeros obtenidos de varias algas marinas; son solubles en agua y tienen una cadena lineal de galactanos parcialmente sulfatados. Las carrageninas se clasifican en tres grupos, kappa (κ), iota (ι) y lambda (λ), dependiendo de la posición y el número de grupos sulfatados. Las carrageninas κ, ι y λ tienen grupos sulfatados de 20%, 33% y 41% (p/p), respectivamente. La carragenina ι tiene la capacidad de producir geles termorreversibles al ser enfriada por debajo de cierta temperatura. Por tal efecto, dicha carragenina es usada ampliamente para la formación de películas en el área de alimentos (Karbowiak etal., 2006).
La superficie que se obtiene al formar películas de carragenina es porosa, lo que puede provocar puntos débiles que disminuyen la fuerza tensil. En
un estudio realizado por Briones et al. (2004), se observó que las películas de carragenina al 5% sin plastificante presentaron menor elongación (106%) y mayor dureza (fuerza tensil 3.87 kg mm-2) en comparación con las películas adicionadas con glicerol al 5% que presentaron menor dureza (1.3 kg mm-2) y mayor flexibilidad (156.8%).
Las películas producidas con carragenina ι y glicerol muestran ventajas interesantes, tales como reducción de transferencia de oxígeno y buenas propiedades mecánicas. La adición de lípidos a la formulación de películas de dicho polisacárido disminuye la permeabilidad al vapor de agua de la película resultante. Las películas formadas con la combinación de carragenina y lípidos son una opción interesante para la encapsulación de sustancias activas, como por ejemplo agentes antimicrobianos (Hambleton et al., 2008; Campos etal., 2011).
2.3. Películas de almidón
Las fuentes de almidón son varias y tienen la gran ventaja de estar presentes de forma natural, lo que hace al polisacárido un excelente ingrediente a considerar en procesos industriales. El almidón es un carbohidrato que se compone de dos polímeros de unidades de glucosa: amilosa y amilopectina. La amilosa es un polímero lineal, mientras que la amilopectina es un polímero ramificado. La relación entre amilosa y amilopectina es un valor muy importante para la formación de películas comestibles y tiene influencia en las propiedades mecánicas y físicas de éstas (Tongdeesoontorn et al., 2011).
En general, un incremento en el contenido de amilosa dará como resultado películas con mayor dureza (Tharanathan, 2003). En un estudio realizado, se observó que al aumentar el contenido de amilosa de 14.2% a 18.4% la fuerza tensil tuvo un incremento de 7.4 a 9.6 MPa (Talja et al., 2008).
Independientemente del contenido de amilosa, las películas formuladas con almidón presentan propiedades mecánicas limitadas, ya que son quebradizas; aún así, son consideradas como las películas formuladas con polisacáridos que
presentan las mejores características de flexibilidad (Wang et al., 2007). Al igual que en otros casos, las propiedades mecánicas mejoran al adicionar plastificantes o al mezclar el almidón con otros biopolímeros (Tongdeesoontorn etal., 2011).
Un almidón en específico que se ha estudiado para la formación de películas es el de yuca. La película formulada únicamente con este material tiene la ventaja de ser resistente a los lípidos y al calor, pero al igual que otras fuentes de almidón, presenta la gran desventaja de formar películas quebradizas y muy solubles en agua caliente y en agua fría (Qiu-Ping y Wen-Shui, 2008; Bergo et al., 2010).
2.4. Películas de alginato de sodio
Debido a sus propiedades coloidales y a su capacidad de formación de geles al reaccionar con cationes de metales, el alginato de sodio es utilizado para la formación de películas comestibles (Tapia et al., 2007). La formación de películas con alginato se basa en la capacidad que tiene el compuesto para reaccionar con cationes divalentes y trivalentes como calcio, hierro y magnesio, entre otros (Vargas etal., 2008).
Las películas de alginato de sodio tienen menor resistencia al agua que las películas formadas con otros polisacáridos. En un estudio realizado por Fazilah et al. (2011), se demostró que las películas formuladas con alginato de sodio al 1.75% y 15% glicerol se disuelven en agua al 100% después de un minuto de contacto, mientras que las películas de almidón de fécula con las mismas condiciones se disuelven únicamente un 15%. La alta solubilidad del alginato de sodio puede ser explicada por la naturaleza hidrofílica del compuesto, que a su vez causa que las propiedades de barrera al vapor de agua de las películas obtenidas sean reducidas. Para disminuir este problema, se pueden agregar lípidos a la formulación (Tapia etal., 2007).
En cuanto a las propiedades mecánicas, las películas de alginato presentan menor flexibilidad que las formadas con otros polisacáridos como CMC y almidón. En un estudio de Wang et al (2007), las películas formadas con alginato al 1%
presentaron valores de elongación de 4.69%, mientras que las de CMC al 3% mostraron valores de 14.58% y las de almidón de papa al 2% tuvieron una elongación del 55.73%.
Para incrementar la fuerza tensil, se realizó un estudio con películas de alginato de sodio al 1.75% y 15% glicerol. Las películas fueron tratadas con cloruro de calcio mediante una inmersión en una solución al 2% durante un minuto, posteriormente se evaluó el efecto del tratamiento en las propiedades mecánicas. Las películas con cloruro de calcio mostraron un incremento significativo en la fuerza tensil de 40 a 60 MPa (Fazilah et al., 2011).
2.5.
Películas de gomas
La goma de algarrobo ha sido ampliamente estudiada para la formación de películas comestibles. En un estudio, se determinó que las películas obtenidas con dicha goma y plastificante presentaron valores de permeabilidad al vapor de agua bajos en comparación con otros polisacáridos. Para reducir aún más los valores de permeabilidad al vapor de agua, se agregaron estearoptenos y cera de abeja (Bozdmeir y Tutas, 2003).
La goma gellan también es un biopolímero utilizado para la formación de películas. En comparación con otros polisacáridos como el alginato de sodio, las películas obtenidas con la goma gellan presentan mejor protección contra el vapor de agua. En un estudio realizado por Tapia et al. (2007), al agregar aceite de girasol al 0.05% a películas formuladas con 0.5% goma gellan y 1% glicerol, la permeabilidad al vapor de agua disminuyó de 0.26 × 10-9 g m-1 s-1 Pa-1 a 0.20 × 1011 g m-1 s-1 Pa-1 .
Otra goma que ha sido probada en la elaboración de películas comestibles es la goma guar. En un estudio realizado por Mehyar et al. (2011), se demostró que las películas con goma guar adicionadas con sorbato de potasio conservaron mejor ciertos vegetales en comparación con películas de almidón formuladas con el mismo conservador. Por ejemplo, C. cucumerinum en pepinos después de 5 días de incubación tuvo una reducción de 1.5 log UFC/g
con la película formulada con 1% goma guar y 0.1% sorbato de potasio, mientras que la película de almidón al 4% y misma cantidad de conservador presentó una reducción de 0.4 log UFC/g.
También se han realizado estudios utilizando goma xantana para formar películas. Al igual que las películas formadas con CMC, las películas con goma xantana presentan la ventaja de ser transparentes. Sin embargo, al igual que al utilizar otros polisacáridos, se debe agregar glicerol a la formulación para mejorar las propiedades mecánicas de las películas comestibles obtenidas (Boateng etal., 2009).
2.6. Películas de mezclas de polisacáridos
Las películas producidas con un sólo tipo de material pueden presentar ciertos aspectos deseables, pero mostrar desventajas en otras áreas (Jia et al., 2009). Por tal motivo, en algunas ocasiones los materiales deben ser mezclados para obtener las características requeridas. Cada película, dependiendo de su formulación, tendrá propiedades diferentes (Liu etal., 2006).
Existen estudios con los compuestos almidóncarboximetilcelulosa usando distintas concentraciones de carboximetilcelulosa (de 0 a 40% peso/peso del almidón) y 30% glicerol como plastificante. Tongdeesoontorn et al. (2011) observaron que la fuerza tensil de películas de almidón aumentó de 5 N/mm2 a 30 N/mm2 al agregar carboximetilcelulosa en la misma cantidad. Mientras que la elongación bajó de 42 mm en las películas con almidón puro, a 18 mm en las películas con almidón y CMC. Por lo tanto, se concluyó que al aumentar la concentración de CMC se incrementó la fuerza tensil y se redujo la elongación; también se redujo la solubilidad en agua de las películas resultantes.
En una investigación de Peressini et al. (2004) se evaluaron películas de metilcelulosa y almidón a distintas concentraciones. Debido a la naturaleza hidrofílica de los compuestos, las películas preparadas no fueron buenas barreras al vapor de agua. No existió variación significativa del valor de permeabilidad al vapor de agua de todas las
formulaciones probadas (26.2 × 10-11 g m-1 s-1 Pa1). Sin embargo, las propiedades mecánicas en función de las distintas concentraciones estudiadas presentaron variaciones.
Otra combinación que ha sido estudiada es almidón al 3% con goma xantana y glicerol al 20%. La adición de goma xantana produjo un efecto positivo en las propiedades mecánicas; las películas con ambos compuestos presentaron mayor resistencia a la ruptura y más estabilidad que las películas formadas únicamente con almidón. A las mismas condiciones, las películas de almidón presentaron valores de 2.5 MPa de resistencia a la ruptura; mientras que al agregar 10% de goma xantana la resistencia aumentó a 5.5 MPa (Melo etal., 2011).
3. Aplicaciones en alimentos de películas comestibles preparadas con polisacáridos
Las películas comestibles presentan varias opciones de usos y aplicaciones en alimentos. Además de funcionar como barreras, las películas pueden ser usadas para ser acarreadoras de saborizantes, nutracéuticos, agentes antimicrobianos, antioxidantes e ingredientes funcionales como vitaminas y minerales (Vargas et al., 2008). En general, se busca que las películas comestibles ayuden a disminuir el oscurecimiento, la deshidratación y pérdida de agua, conserven sabores y retarden la putrefacción por microorganismos de diversos alimentos (RojasGraü etal., 2009).
Una aplicación ampliamente estudiada es utilizar películas comestibles adicionadas con agentes antimicrobianos para proteger a los alimentos del riesgo de crecimiento de microorganismos y por lo tanto, prolongar la vida de anaquel de los mismos (Campos et al., 2011). Tal es el caso de aplicaciones de películas comestibles en frutas y vegetales mínimamente procesados (Bourlieu et al., 2009). En frutas específicamente, se han estudiado las películas de alginato de sodio para retardar el deterioro de duraznos y fresas refrigeradas (Maftoonazad et al., 2008; Moayednia et al., 2009). También se ha estudiado la vida de anaquel de manzanas, pepinos y tomates refrigerados tratados con películas de
almidón adicionadas con sorbato de potasio (Mehyar etal., 2011). De igual forma, las películas de carboximetilcelulosa ayudan a prolongar la vida de anaquel de cerezas refrigeradas y de chiles verdes (Sabularse etal., 2009; Lim etal., 2011).
Para aumentar la vida de anaquel de alimentos, las películas comestibles se pueden combinar con el método de atmósfera modificada para la protección de frutas frescas cortadas; en otros casos, se les agrega algún ácido orgánico, aceite esencial o sulfitos (Rojas-Graü etal., 2009).
Otro método que se ha estudiado para aumentar la vida de anaquel de ciertos alimentos, es el de películas comestibles en conjunto con radiación. Hussain et al. (2010) demostraron que la vida de anaquel de peras refrigeradas aumentó 12 días, en comparación con el sistema control, al utilizar películas de 1% carboximetilcelulosa en conjunto con radiación gamma a 1.5 kGy.
Entre las aplicaciones estudiadas de películas de polisacáridos en el área de alimentos, está su uso en la deshidratación osmótica, con el fin de disminuir la absorción de sólidos e incrementar la pérdida de agua. Dehghannya et al. (2006) realizaron un estudio de deshidratación osmótica de manzanas rebanadas utilizando películas de CMC al 1%; estos investigadores observaron que en comparación con el sistema control la pérdida de agua de la fruta aumentó de 28.7 a 29.6%, mientras que la absorción de sal disminuyó de 4.75 a 3.22%.
La prevención de rancidez oxidativa de lípidos insaturados también ha sido estudiada como aplicación de películas formuladas con polisacáridos. En un estudio realizado usando películas de almidón de papa al 2% y 10% glicerol, se demostró que las películas comestibles actuaron como barrera contra el oxígeno y retardaron la rancidez en aceite de girasol con altos contenidos de ácidos grasos insaturados. El aceite cubierto con las películas presentó un valor de peróxido de 10 mEq O2 /kg de aceite después de 15 días con una prueba de rancidez, en comparación con el aceite sin tratar en el que el valor de peróxido fue de 25 mEq O2 /kg de aceite en las mismas condiciones. Los resultados obtenidos se pueden extender a
cualquier alimento o sustancia con un alto contenido de ácidos grasos poliinsaturados (Osés etal., 2009).
Otra aplicación de las películas comestibles es para mejorar el valor nutrimental de los alimentos. Las películas formadas con alginato, carragenina o algunos derivados de celulosa han sido utilizadas como barreras para que los alimentos fritos no absorban tanto aceite (Marrs et al., 2003; Fontes et al., 2011).
Las películas comestibles de polisacáridos también se utilizan en algunos procesos de dulces y pasteles. Para la producción de dulces, las películas son utilizadas para que los productos conserven su textura y sabor (Ergun et al., 2010). En un estudio se demostró que las películas de goma xantana al 1.2 y 2.4% fueron eficientes para reducir en un 3% la pérdida de humedad de un pastel sin azúcar después de seis días de almacenamiento (Panchev etal., 2005).
Conclusiones y comentarios finales
A partir de la revisión, se concluye que las películas comestibles formuladas con polisacáridos generalmente son quebradizas. Por lo que para mejorar sus propiedades mecánicas de películas se ha estudiado la adición de plastificantes. Las películas formuladas con glicerol son más flexibles en comparación con las obtenidas usando otros plastificantes. Entre los polisacáridos estudiados, el alginato de sodio produce las películas menos flexibles y con mayor dureza, mientras que las películas de almidón son más flexibles y con mayores porcentajes de elongación. Así mismo, para mejorar la fuerza tensil de películas de almidón se puede adicionar CMC o alguna goma.
Además las películas formuladas con polisacáridos presentan altos valores de permeabilidad al vapor de agua. La permeabilidad al vapor de agua de las películas formadas con gomas es generalmente menor que las películas obtenidas con otros polisacáridos y puede disminuir aún más con la adición de aceites vegetales.
M. F. Domínguez-Courtney et al. / Temas
Por las diversas aplicaciones que tienen las películas comestibles en el área de alimentos, la tendencia del mercado del uso de las mismas continúa aumentando; ya sea en forma individual o en conjunto con otros métodos. Las características de las películas comestibles formuladas con polisacáridos dependen directamente del tipo de producto y proceso. Por esta razón, las investigaciones continuarán hacia la búsqueda de nuevas tecnologías para mejorar las limitantes de las películas obtenidas con polisacáridos.
Agradecimientos
M. F Domínguez-Courtney agradece a la Universidad de las Américas Puebla y al Consejo Nacional de Ciencia y Tecnología (CONACYT, México) por las becas recibidas para la realización de los estudios de doctorado.
Referencias
Bergo, P. P., Sobral, P. A. y Prison, J. M. 2010. Effect of glycerol on physical properties of cassava starch films. Journal of Food Processing & Preservation (34):401-410.
Boateng, J. S., Stevens, H., N., Eccleston, G. M., Auffret, A., D., Humphrey, M. J. y Matthews K. H. 2009. Development and mechanical characterization of solvent-cast polymeric films as potential drug delivery systems to mucosal surfaces. Drug Development and Industrial Pharmacy. 35(8):986996
Bourlieu, C. C., Guillard, V. V., Valles-Pamies, B. B., Guilbert, S. S. y Gontard, N. N. 2009. Edible moisture barriers: how to assess of their potential and limits in food products shelf-life extension? Critical Reviews In Food Science & Nutrition 49(5):474-499.
Bozdemir, Ö. y Tutas, M. 2003. Plasticizer effect on water vapour permeability properties of locust bean gum-based edible films. Turkish Journal of Chemistry. 27(6):773-782.
Brindle, L. P. y Krochta, J. M. 2008. Physical properties of whey protein-hydroxypropylmethylcelullose blend edible films. Journal of Food Science. 73(9):446-454
6 – 2 (2012): 110 - 121
Briones, A. V., Ambal W. O., Estrella, R. R., Pangilinan, R., De Vera, C. J., Pacis, R. L., Rodriguez, N. y Villanueva M. 2004. Tensile and tear strength of carrageenan film from philippine eucheuma species. Marine Biotechnology. 6:148151
Campos, C. A., Gerschenson, L. N. y Flores S. K. 2011. Development of edible films and coatings with antimicrobial activity. Food Bioprocess Technol. 4:849-875
Chambi, H., y Grosso, C. 2011. Effect of surfactants on the functional properties of gelatin-polysaccharidebased films. European Food Research & Technology. 232(1):63-69.
Chen, C. P., Wang, B. W. y Weng, Y. M. 2010. Physiochemical and antimicrobial properties of edible aloe/gelatin composite films. International Journal of Food Science & Technology. 45(5):10501055.
Dehghannya, J. J., Emam-Djomeh, Z. Z., SotudehGharebagh, R. R. y Ngadi, M. M. 2006. Osmotic dehydration of apple slices with carboxy-methyl cellulose coating. Drying Technology. 24(1):45-50.
De Moura, M. R., Lorevice, M. V., Mattoso, L. C. y Zucolotto, V. 2011. Highly stable, edible cellulose films incorporating chitosan nanoparticles. Journal of Food Science. 76(2):25-29.
Enebro, J., Momcilovic, D., Siika-aho, M. y Karlsson, S. 2007. A new approach for studying correlations between the chemical structure and the rheological properties in carboxymethyl cellulose. Biomacromolecules. 8(10):3235-3257.
Ergun, R. R., Lietha, R. R. y Hartel, R. W. (2010). Moisture and shelf life in sugar confections. Critical Reviews In Food Science & Nutrition. 50(2):162192.
Espino-Díaz, M., Ornelas-Paz, J., Martínez-Téllez, M. A., Santillán, C., Barbosa-Cánovas, G. V., ZamudioFlores, P. B. y Olivas, G. I. 2010. Development and characterization of edible films based on mucilage of opuntia ficus-indica (L.). Journal of Food Science. 75(6):347-352.
Espinoza-Herrera, N., Pedroza-Islas, R., San MartínMartinez, E., Cruz-Orea, A., y Tomás, S. 2011. Thermal, mechanical and microstructures properties of cellulose derivatives films: a comparative study. Food Biophysics. 6(1):106-114.
Fazilah, A. A., Maizura, M. M., Abd Karim, A. A., Bhupinder, K. K. y Rajeev, B. B. 2011. Physical and
mechanical properties of sago starch-alginate films incorporated with calcium chloride. International Food Research Journal. 18(3):1027-1033.
Fontes, L. B., Ramos, K. K., Sivi, T. C. y Queiroz, F. C. 2011. Biodegradable edible films from renewable sources-potential for their application in fried foods. American Journal of Food Technology. 6(7):555567.
Hambleton, A., Debeaufort, F., Beney, L., Karbowiak, T. y Voilley, A. 2008. Protection of active aroma compound against moisture and oxygen by encapsulation in biopolymeric emulsion-based edible films. Biomacromolecules. 9(3):1058-1063.
Hussain, P. R., Meena, R. S., Dar, M. A. y Wani, A. M. 2010. Carboxymethyl cellulose coating and lowdose gamma irradiation improves storage quality and shelf life of pear (Pyrus Communis L., Cv. Bartlett/William). Journal of Food Science. 75(9):586-596.
Javanmard, M. M., Ahangari, R. R., y Tavakolipour, H. H. 2011. Effects of wheat starch edible films on rancidity and moisture uptake of pistachio kernels as a new package. Journal of Food Process Engineering, 34(4):1156-1171.
Jia, D., Yu, F. y Kai, Y. 2009. Water vapor barrier and mechanical properties of konjac glucomannanchitosan-soy protein isolate edible films. Food & Bioproducts Processing. 87(1):7-10.
Jongjareonrak, A., Benjakul, S., Visessanguan, W. y Tanaka, M. 2006. Effects of plasticizers on the properties of edible films from skin gelatin of bigeye snapper and brownstripe red snapper. European Food Research and Technology. 222(3-4):229-235.
Karbowiak, T., Hervet, H., Leger, L., Champion, D., Debeaufort, F. y Voilley, A. 2006. Effect of plasticizers (water and glycerol) on the diffusion of a small molecule in iota-carrageenan biopolymer films for edible coating application. Biomacromolecules 7(6):2011-2019.
Khan, T., Park, J. K. y Kwon, J. H. 2007. Functional biopolymers produced by biochemical technology considering applications in food engineering. Korean Journal of chemical Engineering. 24(5):816826.
Lim, R. R., Stathopoulos, C. E. y Golding, J. B. 2011. Effect of edible coatings on some quality characteristics of sweet cherries. International Food Research Journal. 18(4):1237-1241.
Liu, L., Kerry, J. F., & Kerry, J. P. 2006. Effect of food ingredients and selected lipids on the physical properties of extruded edible films/casings. International Journal of Food Science & Technology. 41(3):295-302.
Maftoonazad, N., Ramaswamy, H. S. y Marcotte, M. 2008. Shelf-life extension of peaches through sodium alginate and methyl cellulose edible coatings. International Journal of Food Science & Technology. 43(6):951-957.
Marrs, M., Titoria, P. y Madden, J. 2003. Ingredients That Gel. Prepared Foods. 172(6):67-76.
Mehyar, G. F., Al-Qadiri, H. M., Abu-Blan, H. A. y Swanson, B. G. 2011. Antifungal effectiveness of potassium sorbate incorporated in edible coatings against spoilage molds of apples, cucumbers, and tomatoes during refrigerated storage. Journal of Food Science. 76(3):210-217.
Melo, C., Grossmann, M., Yamashita, F., Youssef, E., Dall'Antonia, L. y Mali, S. 2011. Effect of manufacturing process and xanthan gum addition on the properties of cassava starch films. Journal of Polymers and The Environment 19(3):739-749.
Moayednia, N., Ehsani, M. R., Emamdjomeh, Z., Asadi, M. M., Mizani, M. y Mazaheri A.F. 2009. Effect of sodium alginate concentrations on viability of immobilized lactobacillus achidophilus in fruit alginate coating during refrigeration storage. Australian Journal of Basic and Applied Sciences. 3(4):3213-3226
Nanda, R. y Nayak, P. 2009. Edible biodegradable films for packaging applications. Popular Plastics & Packaging. 54(2):17-22.
Osés, J., Niza, S., Ziani, K., y Maté, J. I. 2009. Potato starch edible films to control oxidative rancidity of polyunsaturated lipids: effects of film composition, thickness and water activity. International Journal of Food Science &Technology. 44(7):1360-1366.
Panchev, I. N., Baeva, M. R. y Lambov, S. I. 2005. Influence of edible films upon the moisture loss and microstructure of dietetic sucrose-free sponge cakes during storage. Drying Technology. 23(4):925-940.
Peressini, D. D., Bravin, B. B. y Sensidoni, A. A. 2004. Tensile properties, water vapour permeabilities and solubilities of starch-methylcellulose-based edible films. Italian Journal of Food Science. 16(1):5-16.
Qiu-Ping, Z., y Wen-Shui, X. 2008. Physicochemical properties of edible and preservative films from chitosan/cassava starch/gelatin blend plasticized
with glycerol. Food Technology & Biotechnology. 46(3):262-269.
Rachtanapun, P., Pankan, D. y Srisawat, D. 2012. Edible films of blended cassava starch and rice flour with sorbital and their mechanical properties. Journal of Agricultural Science and Technology. (2):252-258.
Rawdkuen, S., Sai-Ut, S., y Benjakul, S. 2010. Properties of gelatin films from giant catfish skin and bovine bone: a comparative study. European Food Research &Technology. 231(6):907-916.
Rojas-Graü, M., Oms-Oliu, G., Soliva-Fortuny, R. y Martín-Belloso, O. 2009. The use of packaging techniques to maintain freshness in fresh-cut fruits and vegetables: a review. International Journal of Food Science &Technology. 44(5):875-889.
Sabularse, V. C., Montalbo, M. D., Hernandez, H. P., y Serrano, E. P. 2009. Preparation of nata de cocobased carboxymethylcellulose coating and its effect on the post-harvest life of bell pepper (Capsicum annuum l.) fruits. International Journal of Food Sciences &Nutrition. 60(7):206-218.
Talja, R. A., Peura, M., Serimaa, R. y Jouppila, K. 2008. Effect of amylose content on physical and
6 – 2 (2012): 110 - 121
mechanical properties of potato-starch-based edible films. Biomacromolecules. 9(2):658-663.
Tapia, M., Rojas-Graü, M., Rodriguez, F., Ramirez, J., Carmona, A. y Martin-Belloso, O. 2007. Alginateand gellan-based edible films for probiotic coatings on fresh-cut fruits. Journal of Food Science 72(4):190-196.
Tharanathan, R. N. 2003. Biodegradable films and composite coatings: past, present and future. Trends in Food Science &Technology. 14(3):71.
Tongdeesoontorn, W., Mauer, L. J., Wongruong, S., Sriburi, P. y Rachtanapun, P. 2011. Effect of carboxymethyl cellulose concentration on physical properties of biodegradable cassava starch-based films. Chemistry Central Journal. 5(6):1-8.
Vargas, M., Pastor, C., Chiralt, A., McClements, D. y Gonzalez-Martinez, C. 2008. Recent advances in edible coatings for fresh and minimally processed fruits. Critical Reviews In Food Science & Nutrition, 48(6):496-511.
Wang, L. Z., Li, L., Holmes, J., Kerry, J. F. y Kerry, J. P. 2007. Assessment of film-forming potential and properties of protein and polysaccharide-based biopolymer films. International Journal of Food Science &Technology. 42(9):1128-1138.

Temas Selectos de Ingeniería de Alimentos 6 - 2 (2012): 122 - 130

Mecanismos de inestabilidad y métodos de estabilización de emulsiones múltiples
H. A. Peredo-Luna* y M. T. Jiménez-Munguía
Departamento de Ingeniería Química, Alimentos y Ambiental, Universidad de las Américas Puebla. Ex hacienda Sta. Catarina Mártir S/N, San Andrés Cholula, Puebla. C.P.72810. México.
Resumen
La aplicación de las emulsiones múltiples es de gran interés en el área de alimentos. Éstas son sistemas termodinámicamente inestables, debido a que están conformadas por tres fases y por consecuencia dos interfaces de naturaleza diferente. Los mecanismos principales de inestabilización son la coalescencia de las gotas internas, la coalescencia de las gotas externas, la migración de líquido entre las fases interna y externa y la coalescencia de las gotas internas con la fase externa. En este trabajo se identifican las causas y consecuencias de la inestabilidad de las emulsiones múltiples. También se aborda la estabilización de las emulsiones múltiples: por los métodos de estabilización electrostática, estérica y mecánica, así como las estrategias de estabilización de la fase interna, selección de la fase intermedia y estabilización de la fase externa; además se exponen los biopolímeros alimentarios que funcionan como agentes emulgentes o estabilizantes.
Palabras clave: emulsiones múltiples, mecanismos de inestabilidad, coalescencia, estabilización, emulgentes.
Abstract
Multiple emulsions’ application is of great interest in food science. These systems are thermodynamically unstable due to the three phases which compose them and consequently two interfaces of different nature. The main mechanisms of instability are the inner droplet coalescence, the external droplet coalescence, fluid migration between internal and external phases and coalescence of the inner droplets with the external phase. In this review, the causes and consequences of the multiple emulsion instability are identified. It also addressed the stabilization of these systems: methods, electrostatic stabilization, steric and mechanical, and strategies, stabilization of internal phase, intermediate phase selection and stabilization of external phase; and the food biopolymers that serve as emulsifying agents and stabilizers.
Keywords: multiple emulsions, instability mechanisms, coalescence, stabilization, food emulsifiers.
*Programa de Doctorado en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: hilda.peredola@udlap.mx
Introducción
Las emulsiones múltiples pueden aplicarse dentro del área de los alimentos como una técnica de encapsulación para proteger compuestos sensibles, enmascarar sabores y olores o como una estrategia para la formulacióndeproductosreducidosengrasa.
Las emulsiones múltiples, o dobles, son sistemas coloidales en los que una emulsión simple se dispersa en una tercera fase para formar una nueva emulsión. Estos sistemas se componen de tres fases y, por esto, de dos tipos diferentes de interfaz, por lo que la inestabilidad termodinámica de estos sistemas es mayor, lo que causa que las fases tiendan a separarse con más facilidad, en comparación con las emulsiones simples. La pérdida de estabilidad provoca cambios en las característicasopropiedadesdelasemulsiones múltiples, lo que puede hacer que éstas dejen de cumplir con el propósito para el que fueron hechas. Por ejemplo, si el objetivo es proteger un compuesto sensible, la inestabilidad puede promover la migración del compuesto de la fase interna a la fase externa y en algunos casoscausarsudegradación.Laaplicaciónyel éxito industrial y comercial de las emulsiones múltiples dependen, por tanto, de su estabilidad.
Lainestabilidaddelasemulsionesmúltiples se da a través de diferentes mecanismos que ocurren simultáneamente, algunos análogos a los de las emulsiones simples, como la coalescencia. Estos mecanismos dependen de la composición y microestructura de las emulsiones múltiples y están relacionados fundamentalmente con fenómenos de transferencia de masa, gradientes en la presión osmótica y propiedades como la viscosidad y el pH. Por todo lo anterior, en esta revisión se describiránestosmecanismos,suscausas ysus efectos; junto con los métodos y estrategias principalesparacontrarrestarlos.
Revisión bibliográfica
Las emulsiones múltiples, o dobles, son sistemas coloidales en los que una emulsión simplesedispersaenotrafaseparaformaruna nueva emulsión. En general, se distinguen dos tipos de emulsiones múltiples: (a) agua en aceite, en agua (W/O/W por sus siglas en inglés) y (b) aceite en agua, en aceite (O/W/O por sus siglas en inglés). Explicado más detalladamente, una fase acuosa interna, W1, dispersa en una fase intermedia de aceite, O, forman lo que se conoce como emulsión primaria (W1/O); ésta es a su vez dispersada en una fase acuosa externa, W2, para formar así una emulsión múltiple W1/O/W2. Las emulsiones múltiples de tipo O1/W/O2 se forman de manera análoga. Estos sistemas se componen de tres fases y, por lo tanto, de dos tipos diferentes de interfaz; la de las gotas internas y la de las gotas externas, que al ser de naturaleza distinta requieren de un agente estabilizador o emulgente diferente. Debido a todo lo anterior, la inestabilidad termodinámica de estos sistemas es mayor, lo quecausaquelasfasestiendanasepararsecon más facilidad, en comparación con las emulsionessimples.
1. Mecanismos de inestabilidad de las emulsiones múltiples
En general se distinguen cuatro mecanismos predominantes de inestabilización: coalescencia de las gotas internas, coalescencia de las gotas externas, coalescencia de las gotas internas con la interfaz externa y migración de líquido entre las fases interna y externa. Estos se ilustran en la Fig. 1 y se describirán en las sub-secciones siguientes. Durante el desarrollo de los temas se tomará el caso de emulsiones múltiples del tipo W/O/W como ejemplo para ilustrar los mecanismos.
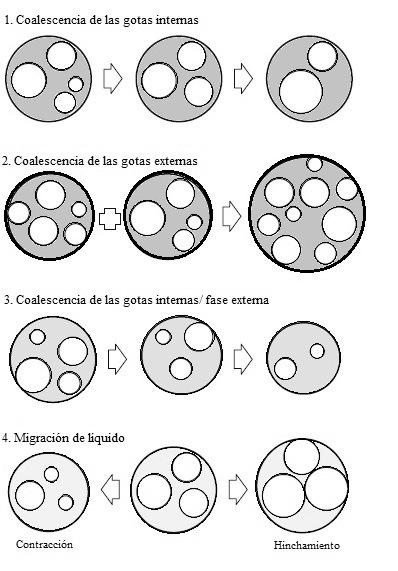
Fig. 1. Principales mecanismos de inestabilidad de las emulsiones múltiples (Adaptado de Dickinson, 2011).
1.1 Coalescencia de las gotas internas
La coalescencia ocurre cuando dos gotas adjuntas se unen en una sola entidad más grande debido a la ruptura de la membrana o película de la interfaz que las separa. Durante el desarrollo de este mecanismo no hay cambio en la interfaz de las gotas externas (Appelqvist et al.,2007;Dickinson,2011).
El adelgazamientodelapelículaprovocasu ruptura ydepende de la hidrodinámica relativa dentro de la película y de factores como: las propiedades reológicas de la fase en la que están dispersas las gotas, la concentración de la fase dispersa y la estabilización efectiva de las gotas y su capacidad de mantener la distancia entre las gotas. La ruptura interfacial depende de las propiedades mecánicas de la película y está influenciada por el cizallamiento, las condiciones de esfuerzo
cortante y la temperatura (Appelqvist et al., 2007). Esto produce un crecimiento desigual degotasinternas,quepodríaderivarhaciaotro mecanismodeinestabilidad,lacoalescenciade las gotas internas con la interfaz externa (Chávez-Páez et al., 2012). Un sistema W/O/W pierde estabilidad cuando se agregan cantidades considerables de agentes hidrófilos (Jiao y Burges, 2003; Schmidts et al., 2010). Las investigaciones sugieren que tales concentracionesaceleranlacoalescenciadelas gotasinternas(Pays et al.,2001).
1.2 Coalescencia de las gotas externas
Este mecanismo es análogo a lo que ocurre en las emulsiones simples, las gotas externas se unen en un proceso irreversible que crea unidades de mayor tamaño. El efecto de la gravedad sobre estas gotas más grandes puede llevar a la separación de las fases de la emulsión múltiple; produciendo “cremosidad”, lo que en inglés se denomina como “creaming”, que es la formación de una capa cremosaenlasuperficieosedimentación,enel caso contrario, en el que la capa separada se asienta (Appelqvist et al., 2007; Dickinson, 2011). Este fenómeno sucede cuando la repulsión entre las gotas es muy débil, la tensión interfacial y la viscosidad son bajas, y la película de la interfaz es poco elástica (Friberg y Yang, 1996; Bergenståhl y Claesson,1997).
1.3 Coalescencia de las gotas internas con la interfaz externa
Enestecasolasgotasinternascoalescenconla interfazdelasgotasexternas,loqueconducea la transferencia de materia de la fase interna hacia la fase continua externa. Esto puede ser causado por una inestabilidad en la interfaz debida a la migración de un exceso de surfactante hidrofílico hacia la fase interna, provocando la apertura y liberación repentina del contenido de la gota a la fase continua; también se puede observar este fenómeno
cuando hay una cantidad grande de gotas internas en contacto con la interfaz externa (Chávez-Páez et al,. 2012); y cuando la diferencia de tamaño entre las gotas internas y las gotas externas es muy grande, de aproximadamente 10 veces, a bajas concentraciones del emulgente hidrofílico en emulsiones W/O/W (Pays et al., 2001). Durante este proceso puede presentarse también la ruptura de la interfaz de las gotas externas (Garti y Lutz, 2004; Dickinson, 2011).
1.4 Migración de líquido entre la fase interna y la fase externa
Este mecanismo se da como resultado de la transferencia de masa desde o hacia las gotas internas. Para explicarlo, se considera que la fase intermedia de una emulsión múltiple es una especie de membrana líquida que separa las fases interna y externa. Entonces, la migración de líquido es consecuencia del intercambio difusivo entre las fases a través de la membrana líquida, en la que la dirección depende del gradiente en la presión osmótica (Dickinson, 2011). Por lo que la gota interna puede sufrir contracción cuando la fase interna tiene una presión osmótica menor a la de la fase externa y el líquido fluye a través de la membrana hacia la fase externa; o hinchamiento cuando ocurre lo contrario. Si el hinchamiento sucede más allá de un tamaño crítico se rompe la membrana líquida y hay coalescenciaconlafaseexterna.
El gradiente en la presión osmótica puede ser impulsado por la existencia de diferentes moléculas en cada una de las fases, interna y externa, o por la diferencia de concentraciones entreellas(Garti yLutz,2004).
2. Métodos de estabilización: mecanismos y estrategias
Las emulsiones múltiplesson estabilizadas por diferentes métodos y estrategias dependiendo delosobjetivosdesuaplicación.
2.1 Mecanismos
2.1.1 Estabilización electrostática
Este principio está relacionado con el efecto quelasfuerzaselectrostáticasrepulsivastienen en las gotas de la emulsión. En las emulsiones múltiples las gotas dispersas tienen un mayor tamaño,porloqueel efectodeestasfuerzases menospronunciado(GartiyLutz,2004).
Para que ocurra la coalescencia de las gotas en una emulsión; éstas deben de estar en contacto unas con otras, este fenómeno se conoce como floculación y para evitarlo, las gotas pueden mantenerse separadas por la repulsión entre sus superficies cargadas. Biopolímeros con actividad superficial como lasproteínas,lospolisacáridosysuscomplejos pueden proveer estabilidad electrostática, sus interacciones electrostáticas dependen de su concentración, el pH (punto isoeléctrico) y la fuerza iónica de la solución (Dickinson y Stainsby, 1988; Dikinson, 1989; Dickinson, 1998).
Cuando dos superficies o partículas cargadas idénticamente se aproximan en un medio fluido, generan una interacción repulsiva que, dependiendo de su magnitud, la distanciaentrelassuperficiesopartículas ylas fuerzas de atracción que puedan generarse, las mantendrá separadas. Estas interacciones representanunabarreradeenergíaqueayudaa reducir la coalescencia de las partículas (Myers,1996;BergenståhlyClaesson,1997).
Por ejemplo, las proteínas a valores de pH lejanos a su punto isoeléctrico están cargadas eléctricamente y, por lo tanto, hay una repulsión electrostática que previene que las partículas se aproximen estrechamente unas a otras (Dickonson y McClements, 1996). Este
fenómeno de estabilización suele ser débil; pero contribuye a la estabilización de emulsiones tomando en cuenta que sucede simultáneamente con la estabilización estérica y/o con otros métodos (Myers, 1996; Bergenståhl yClaesson,1997).
Un parámetro indicativo de la carga superficial y, por lo tanto, de las interacciones electrostáticas de las partículas, es el potencial zeta. De acuerdo a ciertas investigaciones (Aoki et al., 2005; Jiménez - Alvarado et al., 2009), valores altos del potencial zeta (>|40|) indica una alta estabilidad de las emulsiones debido a que las partículas se encuentran a mayordistanciaentreellas.
2.1.2 Estabilización estérica
La estabilización estérica, o el impedimento estérico, es un factor dominante cuando se trata con polímeros anfífilos que se usan como surfactantes macromoleculares, que se adsorben en la interfaz externa. Estos polímeros pueden mejorar la estabilidad de las emulsiones múltiples y retardar el transporte a través de las interfaces, ya que forman películasgruesas(GartiyLutz,2004).
Se distinguen diferentes mecanismos principales: (a) la estabilización por agotamiento por macromoléculas no adsorbentes que previenen la colisión entre gotasyproporcionanelasticidadalsistema;(b) la repulsión electrostática entre dos gotas que llevan la misma carga (por efecto de un volumen de exclusión) (Dickinson, 1998); y (c) la estabilización como resultado de las interacciones hidrofóbicas entre los polímeros adsorbidos(GartiyLutz,2004).
Los polímeros anfífilos son adsorbidos en la interfaz y forman películas gruesas semisólidas que promueven la estabilidad y retardan el transporte hacia la fase externa; esta estrategia es muy prometedora, ya que además requiere de cantidades menores de
surfactante yéstos pueden ser macromoléculas de origen natural. En general, los polímeros hidrofóbicos estabilizan las gotas internas, mientras que los hidrofílicos estabilizan a las interfacesexternas(Garti yLutz,2004).
Para aplicaciones en alimentos se recurre al uso de biopolímeros como proteínas y polisacáridos. Las investigaciones han llegado a buenos resultados mediante el uso de suero de albúmina de bovino, aislado de proteína de suero, caseínas, gelatina, maltodextrina, pectina y complejos con hidrocoliodes como goma xantana, goma guar, goma arábiga o goma de algarrobo (Garti y Lutz, 2004; Dickinson,2011).
La estabilización por agotamiento se basa en la adición de agentes que aumentan la viscosidad y agentes gelificantes en una de las fases para reducir la movilidad de los ingredientes atrapados. Estos agentes no se pueden considerar como emulgentes, pero si como estabilizantes y le proporcionan características de semi-sólido o tipo gel a las emulsiones. Las gomas pueden cumplir con esta función. Algunas de las propiedades que se ven afectadas son el tamaño de gota, la consistencia, la eficiencia o rendimiento de encapsulación, entre otros. La capa interfacial gruesa y la fase acuosa viscosa o gelificada podrían tener ventajas cuando se requiere la protección de compuestos sensibles adicionados. La presencia de hidrocoloides poliméricos en la fase interna acuosa, puede mejorar la estabilidad a la coalescencia y la estabilidadquímica(GartiyLutz,2004).
2.1.3 Estabilización mecánica
Lavidadeanaqueldelasemulsionesmúltiples puede mejorarse incorporando pequeñas partículas sólidas de surfactantes a las formulaciones. La idea es crear una barrera mecánica mediante la incorporación de partículas sólidas pequeñas adsorbidas en las interfaces(GartiyLutz,2004).
La mayor aplicación de este método de estabilización es en el campo farmacéutico. Estudios con celulosa microcristalina, arcilla hidrofóbicamente modificada y partículas de sílice, indican que la adición de partículas sólidas mejora la estabilidad de emulsiones múltiples debido a que la interfaz en la que se adsorben se vuelve rígida. Estudios con partículas de sílice indican que la concentración de partículas, y su carácter hidrofóbico o hidrofílico, afecta el tamaño de las gotas en emulsiones múltiples (Garti y Lutz,2004).
2.2 Estrategias
2.2.1 Estabilización de la interfaz interna
Las estrategias más usadas para la estabilización de la interfaz interna son: la reducción del tamaño de gota, la formación de microemulsiones o microesferas y el incremento de la viscosidad de la fase acuosa, principalmente(Garti yAserin,1996).
En investigaciones conducidas en años recientes,sehaestudiadolaformadecontrolar el tamaño de gota y las propiedades de emulsiones múltiples a través de la manipulación de la presión osmótica. Esto se logra por la diferencia en la concentración de electrolitos o solutos entre la gota interna y la faseexternaoalponerencontactolaemulsión con una solución. Este método, usado generalmente en microencapsulación, puede usarse para reducir el tamaño de gota o para lograr su efecto contrario (Pistel y Kissel, 2000; Tu y Lee, 2012), Así pues, la incorporación de electrolitos, azúcares y polisacáridos para controlar el balance osmótico es una estrategia esencial para mantener la estabilidad termodinámica de las emulsionesW/O/W(Dickinson,2011).
Dickinson (2011) hizo una revisión de los biopolímeros alimentarios que se han investigado en la estabilización de emulsiones
primarias de sistemas W/O/W, en la que incluye albúmina de suero bovino, gelatina, caseína, proteína de suero, proteína de haba, goma arábiga, goma xantana y celulosa microcristalina.Esteautordestacalaeficiencia del caseinato de sodio (0.5 % p/p) en combinación con éster poliglicerol de ácido poliricinoleico,comoemulgentelipofílico(2% p/p).
El uso del éster poliglicerol de ácido poliricinoleico está restringido para muchas aplicaciones en productos alimentarios. Una alternativa efectiva y legalmente aceptable es el uso de lecitina (Dickinson, 2011). En emulsiones W/O concentraciones de 2.5% de lecitina han demostrado proporcionar una buena estabilidad, la cual se relaciona con la alta viscosidad que desarrollan tales emulsiones (Muschiolik et al., 2006). El tamaño de gota en estas emulsiones puede ser reducido cuando la fase acuosa contiene aislado de proteína de suero (1.5%) y goma xantana (0.2%) (Knoth et al., 2005b). Matsumoto et al. (1978) encontraron que con lecitina (8 a 10%)-Span 80 en la fase oleosa y con éster de sacarosa-ácido graso (SE 160) en la fase acuosa (0.2 a 1.0%), emulsiones múltiplesW/O/Wtienenbuenaestabilidad.
Otra estrategia es convertir las gotas internas de una emulsión W/O/W, en una especie de partículas sólidas suaves. Para ello se adicionan biopolímeros que puedan formar geles con la aplicación de calor, como aislado de proteína de suero o gelatina, y se someten las emulsiones primarias W/O a tratamientos, relativamente cortos, con temperaturas de alrededor de 80 °C. También puede usarse almidón gelificado y en este caso se requiere provocar enfriamiento para completar la gelación(Dickinson,2011).
Las interfaces internas de emulsiones múltiples de tipo O/W/O mejoran su estabilidad al agregar conjugados o complejos proteína-polisacárido.
2.2.2 Selección de la fase intermedia
La fase intermedia no sólo debe seleccionarse apropiadamente, también puede modificarse incrementando su viscosidad, agregando portadoresdecargaoagentescomplejos(Garti yAserin,1996).
Eltipodefaseoleosausadoesdeterminante en la preparación de emulsiones W/O/W, ya que es responsable, en gran medida, de las características del sistema e influye en el patrón de liberación de los compuestos y la estabilidad. Mientras más alta sea la polaridad de un aceite, menor será su tensión interfacial lo que favorece más la transferencia de masa entre las fases interna y externa. Las fases oleosas usadas más frecuentemente son los hidrocarburos, los triglicéridos y los ésteres. Aunque los hidrocarburos mejoran la estabilidad de un sistema, no son adecuados para su aplicación en el área de alimentos. Sin embargo, algunos aceites vegetales y triglicéridos, proporcionan una buena estabilidad y las mezclas de éstos pueden mejorarla (Knoth et al., 2005a; Özer et al., 2006).
2.2.3 Estabilización de la interfaz externa
Las interfaces externas suelen estabilizarse mediante el uso de emulgentes poliméricos o agregando partículas coloidales sólidas para formar películas más fuertes y rígidas (Garti y Aserin,1996).
Las proteínas son agentes emulgentes y estabilizadores efectivos en interfaces de tipo O/W, ya que son insolubles en la fase oleosa, por lo que no tienden a migrar. También es comúnañadirpolisacáridosenconcentraciones bajas como agentes espesantes y gelificantes. Enlaestabilizacióndeemulsionesmúltiplesse han empleado diferentes tipos de emulgentes proteicos como caseinato de sodio, gelatina, albúmina de suero bovino, aislado de proteína de suero y algunos hidrocoloides como la
goma arábiga. Entre los diferentes tipos de polisacáridos que se han investigado están la pectina, la carragenina, el alginato, la goma xantana, la goma de algarrobo y la carboximetilcelulosa(Dickinson,2011).
Se ha encontrado que el caseinato de sodio reduce el tamaño de gota y que puede maximizar la eficiencia de encapsulación. La goma arábiga (Acacia de Senegal), por sus propiedades únicas de actividad superficial y emulgentes, permite alcanzar una buena estabilidad a largo plazo a concentraciones de alrededor del 10% (p/p) y proporciona estabilidad coloidal en un intervalo amplio de pH(Dickinson,2011).
Los conjugados o complejos proteínapolisacárido, formados con calor seco controlado, mejoran la solubilidad de la proteína y la estabilidad bajo condiciones de pH bajo y alta fuerza iónica. Esto es debido al incremento de su carácter hidrofílico y mayor capacidad de estabilización estérica. Conjugados de caseína–dextrano o caseína–maltodextrina producen gotas W/O/W más pequeñas a valores de pH neutros ymejoran la estabilidad contra la coalescencia en condiciones ácidas, junto con una mayor eficiencia de encapsulación. Las mezclas de proteína–polisacárido que han sido investigadas recientemente son las de aislado de proteína de suero con goma xantana, galactomananos (goma de algarrobo, goma guar y goma de fenogreco), carboximetilcelulosa o pectina modificada, y concentrado de proteína de suero con goma arábiga, pectina o goma de mezquite (Jiménez - Alvarado et al., 2009). Algunos de estos complejoshantenidoéxitoenlaencapsulación deelectrolitos(Dickinson,2011).
Conclusiones y comentarios finales
Los mecanismos de inestabilización de las emulsiones múltiples dependen, en gran medida, de la naturaleza de sus componentes, fase interna, fase intermedia, fase externa, agentes emulgentes y estabilizantes, así como de las propiedades de éstos. En cuanto a la aplicación de una u otra estrategia de estabilización es importante tomar en cuenta los objetivos y propósitos del uso de las emulsiones, ya que pueden existir algunas restricciones. Por ejemplo, en el área de alimentos no se deben utilizar compuestos que puedan ser tóxicos o no aptos para el consumo humano, como los aceites derivados de hidrocarburos. Por último, las investigaciones en el uso de biopolímeros, como proteínas y polisacáridos, han demostrado buenos resultados en su aplicación para contrarrestar lainestabilidaddeemulsionesmúltiples.
Agradecimientos
Las autoras agradecen al Consejo de Nacional de Ciencia y Tecnología (CONACyT) por financiamiento del proyecto (CB-2011-01, Núm. 168709) "Estudio del efecto de diferentes métodos de homogeneización en la estabilidad y liberación de aceites esenciales encapsulados mediante emulsiones múltiples". LaautoraPeredoLunaagradeceespecialmente a la Universidad de las Américas Puebla y al CONACyT por el apoyo proporcionado para susestudiosdeposgrado.
Referencias
Aoki, T., Decker, E. A. y McClements, D. J. 2005. Influence of environmental stresses on stability of
o/w emulsions containing droplets stabilized by multilayered membranes produced by a layer-bylayer electrostatic deposition technique. Food Hydrocolloids. 19: 209–220.
Appelqvist, I .A. M., Goldiing, M., Vreeker, R. y Zuidam. N .J. 2007. Emulsions as delivery sistems in foods. En: J. M. Lakis (Ed). Encapsulation and Controlled Release Technologies in Food Systems Blackwell Publishing. Iowa. E.E.U.U. pp. 41-81.
Bergenståhl, B. A. y Claesson, P. M. 1997. Surface forces in emulsions. En: S. E.Friberg y K Larsson (Eds). Food emulsions. Tercera edición. Marcel Dekker, Inc. Nueva York. pp. 57-109.
Chávez-Páez, M., Quezada, C. M., Ibarra-Bracamontes, L., González-Ochoa, H. O. y Arauz-Lara, J. L. 2012. Coalescence in double emulsions. Langmuir. 28:5934-5939.
Dickinson, E. 1989. Food colloids – an overview. Colloids and surfaces. 42: 191-204.
Dickinson, E. 1998. Stability and rheological implications of electrostatic milk proteinpolysaccharide interactions. Trends in Food Science and Technology. 9: 347-354.
Dickinson, E. 2011. Double emulsions stabilized by food biopolimers. Food Biophysics. 6: 1-11.
Dickinson, E. y Stainsby, G. 1988. Advances in Food Emulsions and Foams. Elsevier applied sience. Gran Bretaña. 397 p.
Dickonson, E. y McClements, D. J. 1996. Advances in Food Colloids. Blackie Academic and Profesional. Gran Bretaña. 333 p.
Friberg. S. E. y Yang, J. 1996. Emulsion stability. En: J. Sjöblom (Ed). Emulsions and emulsions stability Marcel Dekker, Inc. Nueva York. pp. 1-40.
Garti, N. y Aserin, A. 1996. Double emulsions stabilized by macromolecular surfactants. Advances in colloid and interfase science. 65: 37-69.
Garti, N. y Lutz R. 2004. Recent progress in double emulsions. En: Petsev, D.N. Emulsions: Structure stability and interactions. pp. 557-605.
Jiao, J. y Burgess, D. J. 2003. Rheology and stability on water-oil-water emulsions containing Span 83 and Tween 80. The AAPS Journal. 5(1): 62-73.
Jiménez - Alvarado, R., Beristain, C .I., Medina-Torres, L., Román-Gerrero, A. y Vernon-Carter, E. J. 2009. Ferreus bisgly cinate and release in w1/o/w2 multiple emulsions stabilized by proteinpolysaccharide complexes. Food Hidrocolloids. 23: 2425-2433.
Knoth, A., Scherze, I. y Muschiolik, G. 2005a. Effect of lipid type on water-in-oil-emulsions stabilized by phosphatidylcholine-depleted lecithin and polyglycerol polyricinoleate. European Journal of Lipid Science and Technologie. 107: 857–863.
Knoth, A., Scherze, I. y Muschiolik, G. 2005b. Stability of water-in-oil-emulsions containing phosphatidylcholine-depleted lecithin. Food Hydrocolloids. 19: 635–640.
Matsumoto, S., Ueda,Y., Kita, Y. y Yonezawa, D. 1978. Preparation of water-in-olive oil in-water multiple emulsions in an eatable form. Agricultural and Biological Chemistry. 42(4):739–43.
Muschiolik, G., Scherze, I., Preissler, P., Weiss, J., Knoth, A. y Fechner, A. Multiple emulsions –preparation and stability. 2006. IUFoST, doi: 10.1051/IUFoST:20060043
Myers, D.1996. Surfaces, interfaces and colloids: principles and applications. VCH Publishers. E.E.U.U. 433 p.
Özer, Ö., Aydin, B. y Yazan, Y. 2006. Effect of oil tipe on stability of W/O/W emulsions. Cosmetic and Toiletries magazine. 121(7): 57-64.
Pays,K. Giermanska, J., Pouligny., Bibette, J. y LealCalderon, F. 2001. Coalescence in surfactantstabilized double emulsions. Langmuir. 17(25): 7758-7769.
Pistel K. F. y Kissel T. 2000. Effects of salt addition on the microencapsulation of proteins using a w/o/w double emulsion technique. Journal of Microencapsulation. 17(4): 467-483.
Schmidts, T., Dobler, D., Guldan, G.-A., Paulus, N. y Runkel, F. 2010. Multiple w/o/w emulsions – using the required HBL for emulsifier evaluation. Colloids and Surfaces A: Physicochemical and Engineering Aspects. 372: 48-54.
Tu, F. y Lee, D. 2012. Controlling the stability and size of double-emulsion-templated poly(lactic-coglycolic) acid microcapsules. Langmuir. 28: 99446652.

Temas Selectos de Ingeniería de Alimentos 6 - 2 (2012): 131 - 148

Quesos frescos: propiedades, métodos de determinación y factores que afectan su calidad
C. Ramírez-López*, J.F. Vélez-Ruiz.
Departamento de Ingeniería Química, Alimentos y Ambiental, Universidad de las Américas Puebla. Ex hacienda Sta. Catarina Mártir S/N, San Andrés Cholula, Puebla. C.P.72810. México.
Resumen
El objetivo de la presente revisión se centra en describir uno de los productos lácteos de mayor consumo en México, el queso fresco; su proceso de elaboración, las principales propiedades que afectan su calidad como resultado de diversos factores ligados a su formulación, condiciones de proceso y almacenamiento, así como una revisión general de las metodologías existentes para la medición de las mismas. Esta revisión está dirigida principalmente a investigadores en tecnología de los alimentos, a los fabricantes de queso fresco y estudiantes en el campo de la ciencia de los alimentos y productos lácteos, que deseen conocer más de cerca los aspectos científico-técnicos en torno a las propiedades del queso fresco.
Palabras clave: queso fresco, propiedades, calidad
Abstract
The aim of this review focuses on describing one of the most consumed dairy products in Mexico (“queso fresco”), its manufacturing process, its main properties that affect its quality as a result of different factors related to its formulation, process and storage conditions, as well as, an overview of the existing methodologies for measuring them. This review is primarily targeted to researchers in food technology, cheese manufacturers and students in the field of food science and dairy products who want to learn more about the scientific and technical aspects of “queso fresco”.
Keywords: queso fresco, properties, quality.
Introducción
El queso es un alimento de amplio consumo a nivel mundial, cuyas características nutritivas, funcionales, texturales y sensoriales difieren entre cada tipo. Se estiman más de 2000 variedades de queso (Gunasekaran y Ak,
*Programa de Doctorado en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: carolina.ramirezlz@udlap.mx
2003), entre madurados, semi-madurados y frescos. No obstante en nuestro país predomina el consumo de quesos frescos, mismos que forman parte de una enorme variedad de platillos que constituyen nuestro legadogastronómico.
La práctica en torno a la elaboración del queso ha sufrido importantes cambios, transformándola de un arte empírico, a una tecnología industrial con fuertes bases
131
científicas. Se han identificado diversos factores como causantes de modificaciones en las propiedades del queso (microestructura, propiedades fisicoquímicas, texturales, reológicas y sensoriales), entre ellos la formulación, las condiciones de proceso y almacenamiento y las alteraciones provocadas por microorganismos. Razón por la cual, la comprensión de los aspectos científicotécnicos en torno a la elaboración del queso es de suma importancia para un adecuado control de las condiciones que pudieran afectar dichas propiedades en el queso y en consecuencia su calidadyaceptaciónporpartedelconsumidor.
El objetivo de la presente revisión es brindar al lector un panorama actual del conocimiento respecto a la ciencia y tecnología de quesos frescos, destacando sus propiedades principales, clasificación y métodos de elaboración. Así mismo, se incluye una descripción de los conceptos texturales y reológicos relacionados con este producto lácteo, las pruebas más comunes, su interpretación y correlación con otras técnicas como la evaluación sensorial, que contribuyan en su conjunto al desarrollo de productos de gran calidad y amplia aceptabilidad por parte delconsumidor.
especial yuna consistencia sólida o semisólida enelproductoobtenido(Vélez-Ruiz,2009).
De acuerdo al Codex Alimentarius de la FAO/OMS (2008), el queso es el producto sólido o semisólido, madurado o fresco, en el que el valor de la relación suero proteínas/caseína no supera al de la leche, y que es obtenido por coagulación (total o parcial) de la leche por medio de la acción del cuajo o de otros agentes coagulantes adecuados, con un escurrido parcial del lactosuero(Scott et al., 1998).
Desde el punto de vista fisicoquímico, el queso se define como un sistema tridimensional tipo gel, formado básicamente por la caseína integrada en un complejo caseinato fosfato cálcico, el cual por coagulación, engloba glóbulos de grasa, agua, lactosa, albúminas, globulinas, minerales, vitaminas y otras sustancias menores de la leche, las cuales permanecen adsorbidas en el sistema o se mantienen en la fase acuosa retenida(Walstra et al., 2006).
1.1. Proceso de elaboración
Revisión bibliográfica
1. Definición del queso
El queso es el producto obtenido por coagulación de la leche cruda o pasteurizada (entera, semidescremada y descremada), constituido esencialmente por caseína de la leche en forma de gel más o menos deshidratado (Eck, 2000). Mediante este proceso se logra preservar el valor nutritivo de la mayoría de los componentes de la leche, incluidas las grasas, proteínas y otros constituyentes menores, generando un sabor
El proceso de elaboración del queso es bastante simple, no obstante involucra fenómenos físicos y químicos muy complejos. Se trata esencialmente de un proceso de concentración, a partir de la coagulación de la proteína mayoritaria de la leche (caseína) por la acción enzimática (cuajo) u otro coagulante de tipo ácido (comúnmente ácido láctico) (JohnsonyLaw,2011).
En la Fig. 1 se muestra un esquema general para la elaboración de queso fresco. Para el caso de quesos suaves (panela, fresco, blanco y crema), la coagulación se desarrolla a temperatura de aproximadamente 38ºC, mientras que para el queso tipo Oaxaca la temperatura debe alcanzar los 42ºC, además algo distintivo es que se requiere una pre-
Leche
Pretratamiento
(Estandarización, Homogenización, Tratamiento térmico, Adición de cultivos iniciadores)
CaCl2
Cuajo, ácido o ácido/calor
Coagulación
Sinéresis
(Corte, Agitación, Cocción, Desuerado)
Queso suave (panela, blanco, fresco y crema)
Salado
Moldeado y Prensado
Empacado
Queso de pasta hilada (Oaxaca)
Fundido malaxado
Moldeado
Trenzado y empaquetado
Formación de correas y salado
Fig. 1. Diagrama general para la elaboración de queso fresco. Adaptado de Gunasekarany Ak, (2003).
acidificacióndelaleche,lacualselograporla adición de cultivos iniciadores (Caro et al., 1998).
El paso indispensable en la elaboración de los quesos, es la coagulación de la caseína, provocada mediante la acción combinada de enzimas proteolíticas (cuajos de distintos tipos) y calcio. El proceso de formación del coágulo incluye 2 etapas (Fig. 2). En la primera, se desarrolla un proceso enzimático modulado por la quimosina, la cual rompe los enlaces entre los aminoácidos fenilalanina y metionina(Fen-105yMet-106)presentesenla κ-caseína,liberándoseel glicomacropéptidoen lasolución.Enlasegundaetapa,losagregados de para-κ-caseína producen el coágulo (Udayarajan, 2007). Hasta la etapa de
coagulación, los procedimientos básicos en la elaboración de los diferentes tipos de quesos son muy similares; sin embargo, las etapas siguientes varía de acuerdo con el tipo de quesoaproducir.
Una vez que la leche se ha coagulado, se debe proceder al cortado del coágulo (cortes verticales y horizontales) en pequeños cubos, para favorecer la eliminación del suero (desuerado). Posteriormente se procede a su moldeado.
El moldeado tiene como finalidad dar forma al queso y ayudar a que los gránulos de la cuajada se aglomeren. Los moldes pueden ser cilíndricos, cuadrados o alargados. Generalmente, el moldeo y el prensado se
Micela de caseína
1ra Etapa
Proceso enzimático
Quimosina para-κ-caseína + Glicomacropéptido
realizan utilizando el mismo equipo, pues los moldes tienen dispositivos que ejercen presión sobre el queso. Comúnmente en el caso de quesos suaves como del tipo fresco, no es necesario aplicar presión, pues es suficiente con la que provoca el propio peso del queso (autoprensado).
El salado, además de proporcionar sabor al producto, evita la proliferación de microorganismos y contribuye a la formación de la corteza del queso. En el proceso, se utiliza sal cristalizada o salmueras de diferentes concentraciones, de acuerdo con el tipodequeso.
1.2.Clasificación y criterios de clasificación
El queso es producido en todo el mundo con una gran diversidad de sabores, aromas, texturas y formas, habiéndose recopilado en diversos catálogos y trabajos más de 2000 variedades y tipos (Fox et al., 2000). No obstante, la mayoría de los quesos que se elaboran en México son frescos o de corta duración, algunos con buena aptitud para el fundido(conpHentre5.1a5.3) yalgunoscon propiedades de desmoronamiento o fragmentación (García-Islas, 2006; JiménezGuzmán et al., 2009).
Existen diversos criterios de clasificación con base en las condiciones de proceso o las
2da Etapa No-enzimático
Ca+2 , ≥ 20ºC Coágulo
características fisicoquímicas del tipo de queso:
a) Por contenido de humedad, se clasifican en quesos duros (20-42%), semiduros (4455%) y blandos o suaves (aprox. 55%) (Scott et al., 1998).
b) De acuerdo al tipo de coagulación de la caseína, se clasifican en quesos de coagulación enzimática, quesos de coagulación ácida y quesos de coagulación ácida/térmica (Dalgleish, 1999; Fox et al., 2000;GunasekaranyAk,2003).
c) De acuerdo a su estado de maduración: frescos (6 días), semi-madurados (40 días) y madurados (>70 días) (McSweeney, 2004).
En la Fig. 3 se muestra una representación que engloba estos criterios de clasificación (Farkye,2004).
El queso fresco presenta distintos nombres según la región de producción y numerosas variantes en cuanto a las técnicas de elaboración. De acuerdo a la norma oficial mexicana (NOM-121-SSA1-1994) el queso fresco se caracteriza por un contenido de humedadelevado,unsaborsuave yunperiodo de vida de anaquel corto, por lo que debe ser refrigerado. Se consideran como quesos frescoslossiguientes:panela,fresco,ranchero, blanco, Oaxaca, asadero, adobera, requesón, quesocrema,entreotros.
Fig. 2. Formación del coagulo de caseína. Adaptado de Udayarajan(2007).
Coagulación ácida
Queso suave sin madurar Cottage
Queso suave coagulación ácida
Atributos
Queso crema
Queso suave ligeramente madurado
Queso suave coagulación ácida/calor
Queso suave coagulación enzimática
Brie Ricotta, Requesón, Mascarpone
Se incrementa la firmeza
Disminuye la humedad
Queso Blanco, Panela
Oaxaca Mozzarella
Queso semi-duro coagulación enzimática Edam Gouda
Suizo Queso Duro coagulación enzimática
Parmesano
Americano Cheddar Jack Colby
Generalmente aumenta el tiempo de maduración
1.3. Descripción de algunos tipos de quesos frescos
Queso fresco mexicano. Se dice que es, por mucho, el queso hispano más popular en los EE.UU. y México. Es un queso obtenido por coagulación con cuajo, elaborado a partir de leche descremada o semidescremada. Tiene un ligero sabor lácteo, con notas entre dulce y salado. En su proceso de elaboración, la cuajada se suele moler finamente antes de la salazón, lo que hace que el queso sea desmenuzable.Estetipodequesocontieneuna humedad entre 46-57%, 18-29% de grasa, 1721% de proteína, sal de 1-3% y un pH>6.1 (HwangyGunasekaran,2001;Path,1991).
Queso blanco. Es un queso cremoso y blanco elaboradoconlechedescremada,deacuerdoal proceso es una mezcla entre queso Cotija y queso Mozarella, tradicionalmente se coagula la leche con limón pero en la actualidad, en forma comercial, se elabora con cultivos y cuajo, por lo que tiene un sabor ligeramente ácido.Suelesuavizarseconelcalor,peronose funde. La cuajada no se muele finamente, por
Coagulación enzimática
loqueelresultadoesunquesocontexturamás dura que la de queso fresco. Contiene 51-53% de humedad, 19-25% de grasa, 20-22% de proteína, y 1.8-3% de sal y tiene un pH≤ 5.6 (Farkye et al.,1995).
Por sus características, el queso blanco puede ser producido en un periodo de tiempo muy corto. Primero la leche se calienta a 85ºC yse añadeun ácidoorgánicohastaalcanzarun pH de 5,3 (esto ocasiona la precipitación de la proteína o formación de la cuajada). Después deldesuerado,lacuajadaessalada ymoldeada en aros presionando para eliminar el exceso de suero. Finalmente el queso se empaqueta para suventainmediata(Farkye et al., 1995).
Queso panela. Es un queso fresco de coagulación enzimática de pasta blanda y fresca que no incluye maduración, prensado por su propio peso, elaborado con leche entera pasteurizada suplementada con cloruro de calcio.Unavezquelalechesecoagula,éstase corta en cubos de aproximadamente 1 pulgada y se cocina hasta alcanzar la firmeza deseada bajo agitación suave. Después se drena la
Fig. 3. Criterios de clasificación del queso. Adaptado de Farkye(2004).
mitad del lactosuero para proceder con la adición de sal, la cual se puede añadir directamente o en solución. Después de mezclar durante unos pocos minutos, la cuajada húmeda se transfiere a los moldes en formadecanastaocestaparadrenardurantela noche. El queso se envasa para su venta inmediata. Contiene alrededor de 53-58% de humedad, 19-25% de grasas, 18-20% de proteínas,1.3-1.8%desal yunpHde5.6a6.4 (Guisa,1999;Path,1991).
Requesón. Es un queso blando untable, que tiene un sabor ligeramente salado y textura granulada, similar al queso Ricotta. Se fabrica a partir de suero de leche pasteurizada complementado con leche entera o crema. La mezcla de suero de leche/leche se calienta a 85°C; se añade vinagre para ocasionar la coagulación de las proteínas de la leche y se añade sal para condimentar. La cuajada húmeda se transfiere a recipientes para drenar durante la noche; el queso terminado contiene alrededor de 75% de humedad (Van Hekken y Farkye,2003).
Queso Oaxaca. Es quizás el tipo de queso fresco de “pasta hilada” de mayor consumo en México. Es un queso suave de coagulación enzimática que incluye, sin embargo, adición previa de microorganismos (30-35ºC), es generalmente elaborado a partir de leche entera cruda y es producido ampliamente a nivel casero e industrializado en diferentes regiones de nuestro país. Respecto a sus propiedades fisicoquímicas, contiene una humedad entre 40-46%, 23% de grasas y 24%
de proteína, así como un pH entre 5.0-5.5 (Guisa, 1999). Se caracteriza por tener una textura fibrosa única, excelentes propiedades de fundido, sabor ligero, cuya presentación final en madeja de hilo es también muy característica(DeOca-Flores et al., 2009).
ElprocesodeelaboracióndelquesoOaxaca es similar al del queso Mozzarella, con algunas consideraciones (Fig. 1). Después de lacuajada,lapastasecuecea40-42°C,sedeja reposar en el suero para alcanzar el pH deseado. A continuación, la pasta se sumerge en agua caliente y se amasa. El queso fundido se estira en una hebra larga y plana, la cual se enfría al colocarla en agua fría, posteriormente el queso se saca del tanque después de que se solidifica. El salado se realiza frotando sal de grano sobre cada lado de la hebra, para a continuación enrollar la cadena en forma de boladehilo(VanHekkenyFarkye,2003).
2. Características y propiedades de los quesos frescos y sus métodos de medición
2.1. Composición química y valor nutritivo
El queso comparte casi las mismas propiedades nutricionales con la leche; a excepción de la lactosa, los otros componentes se encuentran más concentrados (Tabla I). Además de brindar un excelente aporte de proteínas de alto valor biológico, el queso se destacaporserunafuenteimportantedecalcio y fósforo (Alais, 1985; Van Hekken y Farkye, 2003;García-Islas,2006).
Tabla I. Composiciónquímicayvalornutritivodelalechedevacaconrespectoalosquesosfrescostipicamenteconsumidosen México.
Leche entera de vacaª Quesos frescob Queso Panelac Queso Oaxacac Queso blancoc Queso Asaderoc Requesónc
Humedad(%)87.546-5753.2-58.349.3-52.4 51-5340-4674-75
Grasa(%)3.518-2918.8-12.120.6-24.219-2523-257.0-8.0
Proteína(%)3.517-2118.4-20.520.4-22.4 20-2224-2711.0-12.0
Ceniza(%)0.7-0.9-2.5-2.73.2-3.7 -1.4-1.8
Lactosa(%)4.7-3.4-4.20.1-0.3-Calcio(%)1.3-1.8-23.9--Fósforo(%)1.0-2.3-18.4---
Sal 1.0-3.01.3-1.81.4-2.31.8-3.01.4-1.8<1.0 pH6.76.15.6-6.45.0-5.35.65.0-5.5
Valornutrimental (kcal/100g) 62-66255±37255±37288±22 a Alais,1985 b VanHekkenyFarkye,2003 c García-Islas,2006
2.2. Microestructura
Existe una estrecha relación entre la microestructuradelquesoysureología,ambas propiedadesasuvez estándeterminadasporla composición química del queso. El análisis de microestructuraesútilcuandosedeseaevaluar el efecto de diferentes ingredientes en la formulación o el uso de alguna tecnología de procesadoyconservación(Buffa et al., 2004).
En el queso, el análisis de microestructura se ha utilizado principalmente para observar la distribución de los glóbulos de grasa ymicelas de proteína (Lobato-Calleros et al., 2007; Cunha et al., 2010), para evaluar la incorporación de gomas (Liu et al., 2008; Tan et al., 2007) o el efecto de procesos enzimáticos, proteólisis y lipólisis, durante la maduración (Karami et al., 2009) o por acción microbiana (Pereira et al., 2009), el efecto del procesamiento térmico de la leche (MoralesCelaya et al., 2012) y almacenamiento en condiciones de congelación (Kuo y Gunasekaran, 2003; Ribero et al., 2009), entre otrosaspectos.
Para la observación de la microestructura del queso se han empleado diversas técnicas, entre las más comunes tenemos a la microscopía electrónica de barrido (LobatoCalleros et al., 2007; Kuo y Gunasekaran, 2003), la microscopía electrónica de transmisión (Udayarajan, 2007; Kuo y Gunasekaran, 2009) y la microscopía confocal de barrido láser sobre todo cuando se busca evidenciar la presencia de otros componentes no lácteos en la fórmula, tales como el almidón(Trivedi et al., 2008ay2008b).
Recientemente se ha hecho uso de la micro-tomografía de rayos X, de la que se señalan como principales ventajas no sólo el proporcionar un porcentaje preciso de la cantidad de grasa presente en productos como el queso, sino que también nos ayuda a revelar sudistribuciónespacial(Laverse et al., 2011).
2.3.
Propiedades
texturales y reológicas
Sinlugaradudasparaelconsumidorlatextura juega un rol importante en términos de inferir la calidad de un alimento. Particularmente en el queso, la textura es uno de los atributos más
importantes que ayudan a determinar la identidaddelmismo(Bourne,2002).
Otroaspectoimportantedelalimentoquese asocia con la textura es su comportamiento reológico. De manera general se puede definir a la reología, como el estudio de la deformación y flujo de materias primas, productos intermedios y productos terminados (Muller, 1973; Bourne, 2002; Shoemaker et al., 1987).
La información textural y reológica es importante en el diseño de procesos de transformación en alimentos (mezclado, flujo demateriales,calentamiento,enfriamiento),en la determinación de la funcionalidad de los ingredientes para el desarrollo de productos, en el control de calidad de productos intermedios yfinales,en estudiosdetiempode vida útil y en evaluaciones de propiedades texturales correlacionadas con pruebas sensoriales, entre otros (Steffe, 1996; VélezRuiz y Barbosa-Cánovas, 1997; TabiloMunizaga y Barbosa-Cánovas, 2005; FoegedingyDrake,2007).
El queso posee propiedades viscoelásticas, siendo los estudios reológicos esenciales para expresar sus características físicas y propiedades mecánicas (Bohlin et al., 1984). Para tal efecto, se han desarrollado numerosos instrumentos y métodos para evaluar las propiedades reológicas de los alimentos, en particular en lo que concierne a la textura de quesos. Esta diversidad de instrumentos suele ser agrupada y reconocida en tres grupos; empírico, imitativo y fundamental (Segards y Kapsalis, 1987; Rosenthal, 1999; Bourne, 2002; Gunasekaran yAk, 2003; Kilcast, 2004; Vélez-Ruiz,2009).
Las mediciones empíricas son aquellas pruebas que tienden a relacionar una variable medida con una propiedad del material, sin una base científica rigurosa. El penetrómetro, el tensómetro, la prueba de punción, y las
pruebas con compresores de bola, son ejemplos típicos de mediciones empíricas
(Gunasekaran y Ak, 2003). Cabe señalar, que estas pruebas no se consideran de precisión y frecuentemente los resultados que se obtienen son difícilmente comparables a los obtenidos con equipos de pruebas fundamentales (Bourne,2002).
Por otro lado, las pruebas imitativas (también denominadas pruebas semifundamentales), incluyen sistemas de medición mecánica con poco control de variables experimentales (tales como, el tipo de sonda, el tamaño y forma de la muestra, entre otras). Como su nombre lo indica son pruebas que tratan de imitar mecánicamente la evaluación sensorial realizada por evaluadores humanos. De hecho se recomienda emplearlas junto con la evaluación sensorial, a fin de obtener modelos más exactos de los atributos de textura del alimento (Gunasekaran y Ak, 2003). Una de las pruebas imitativas más comunes es el Análisis de Perfil de Textura (TPA,porsussiglaseninglés).
Finalmente, las pruebas fundamentales miden las propiedades físicas de acuerdo al módulo de viscosidad o elasticidad. Las muestras utilizadas en estas determinaciones deben tener una geometría específica y ser deformadas de manera controlada, a fin de permitir definir lo más exactamente posible la respuesta reológica del alimento Dentro de esta clasificación se incluyen; la prueba de compresión uniaxial a velocidad constante, la prueba de relajación y Creep y las pruebas dinámicasoscilatorias(Bourne,2002).
Sin embargo, desde un punto de vista práctico en la caracterización reológica de queso, las técnicas de compresión uniaxial a velocidad constante, la relajación ante el esfuerzo y el denominado TPA, son las pruebas más ampliamente utilizadas (Ibáñez et
al., 1998; Pavia et al., 1999). Por lo que a continuaciónsedescribenconmásdetalle.
2.3.1. Compresión uniaxial a velocidad constante
El método consiste en comprimir una muestra de queso de geometría y dimensiones conocidas mediante un plato descendente a velocidad constante, hasta un nivel de deformación superior al punto de fractura (generalmente a una distancia >75% de su altura original). Los parámetros reológicos obtenidos a través de este método se esquematizan en la Fig. 4 y son: el módulo de deformabilidad (MD), estimado como la regresión lineal de la parte inicial de la curva, la tensión o o esfuerzo (σf), la deformación (εf) yla energía (Wf) a la fractura (Castañeda, 2002).
2.3.2. Relajación y creep
El comportamiento viscoelástico del queso se puede describir mediante las pruebas de relajación y creep. En esta prueba se le aplica una deformación inicial a la muestra de queso, lacualsemantieneconstante ysemonitoreael esfuerzo necesario para mantener constante esta deformación. Por otro lado, la relajación del esfuerzo se describe como la habilidad del material para aliviar la aplicación de un esfuerzo impuesto en una deformación constante. Los datos obtenidos en la prueba de creep y en la relajación se representan gráficamente y/o mecánicamente por medio de curvas (Fig. 5) ymodelos como el Maxwell y eldeKelvin(Steffe,1996).
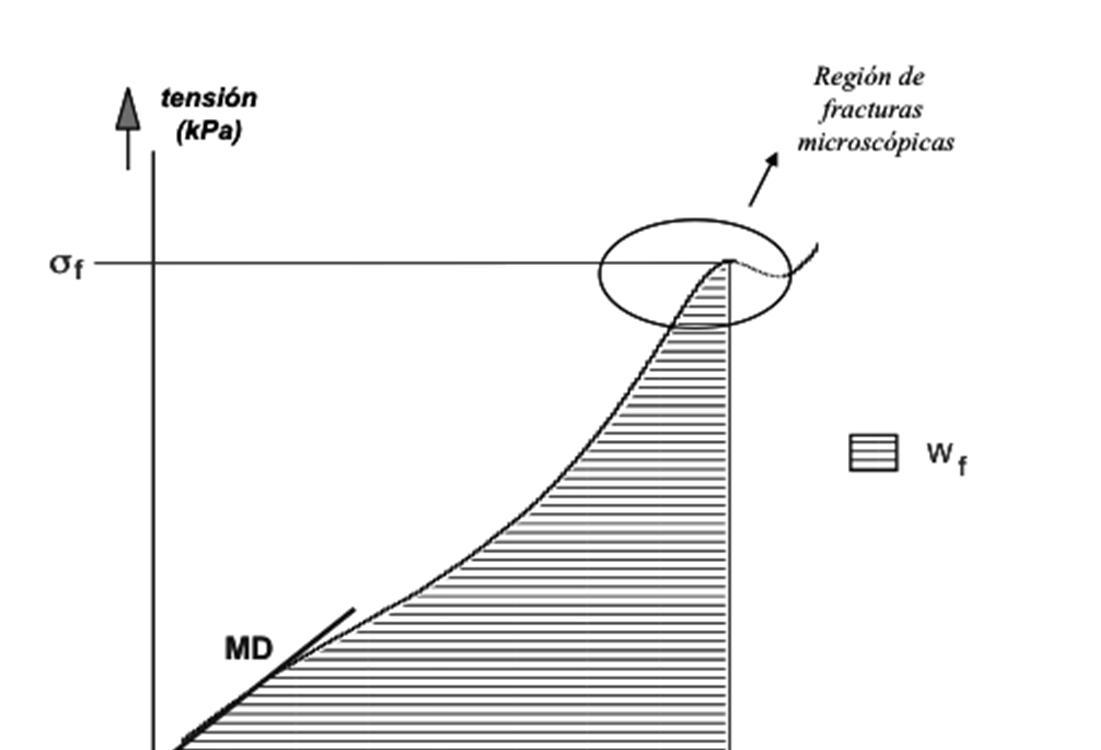

Esfuerzo
Deformación
Material elástico (no fluye)
Mat. VE
Material
Tiempo
2.3.3. Análisis de Perfil de Textura
El análisis de perfil de textura consiste en una prueba de doble compresión en las cuales se someten muestras del producto a una compresión del 80 a 90% de su altura inicial, la cual resulta casi siempre en la ruptura del alimento. Bourne (2002) cita los siguientes parámetros texturales obtenidos con el TPA: fractura, dureza, cohesión, adhesividad, elasticidad, gomosidad y masticabilidad, en la Fig. 6 se muestran un esquema típico de una pruebadeTPA,ylosparámetrosobtenidos.
En la Tabla II, se muestran los rangos de valores de la caracterización funcional (fundibilidad) y textural (dureza, masticabilidad y rigidez) para algunos quesos frescosmexicanos.
Así mismo, en la Tabla III se describen las condiciones para algunas de las pruebas texturales aplicadas a diferentes tipos de queso fresco.
Deformación
Esfuerzo
Material elástico ideal
Sólido viscoelástico
Líquido viscoelástico
Material viscoso ideal
Tiempo
Tabla II. Caracterizacióntexturalyfuncionalde algunos quesos frescos tradicionales mexicanos.
Tipo de queso
Dureza (mJ) Masticabilidad (kPa) Rigidez (N s) Fundibilidad (N) Oaxaca55-56130-23014-332.1-2.4
Panela42-4547-6428-521.0-1.3
Queso
Fresco 17-3319-2119-281.0-1.4
Queso
Blanco 43-5452-7436-561.0-1.3
Adaptado de Van Hekken y Farkye, 2003
3. Factores que afectan las propiedades del queso fresco
Independientemente del origen de la leche, las propiedades físicas del queso se rigen por la interacción entre las moléculas de caseína (Tunick, 2000). Algunos de los factores que influyen en estas interacciones varían en función del tipo de queso, el grado de maduración (Lucey et al., 2003), su composición química (en particular, el contenido de caseína y la distribución de la humedad yla grasa), el contenido de sal, pH y acidez (Guo et al., 2012; Scholz, 1995), así como determinadas condiciones
Fig 5. Curvas de creep y relajación del esfuerzo. Modificado de Steffe(1996).
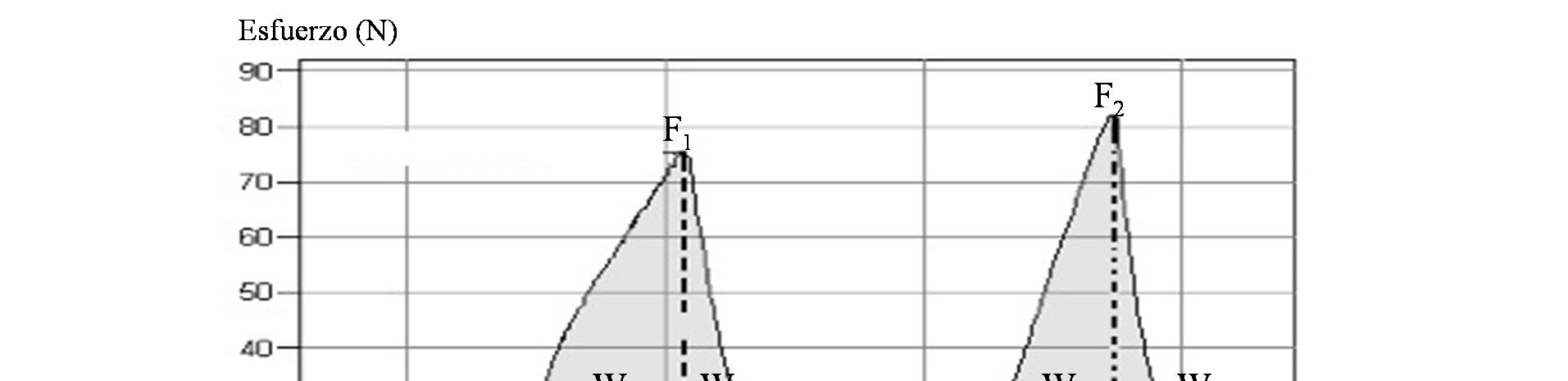
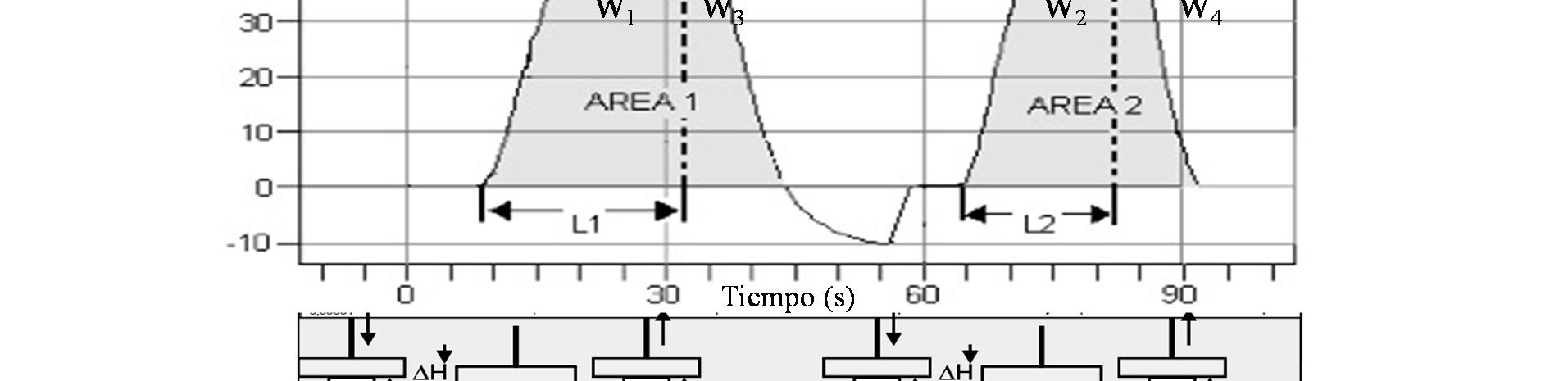

medioambientales como la temperatura (JohnsonyLaw,2011).
3.1. Cambios bioquímicos y propiedades fisicoquímicas
En términos generales, se habla de que existen dos fenómenos opuestos que controlan la firmeza del queso. El primero consiste en la acción de las diferentes enzimas proteolíticas sobre la matriz proteica, principalmente sobre la αs1-caseína, que da como resultado una disminución de la firmeza y en consecuencia, modificaciones en algunas propiedades como el color, la elasticidad y textura del queso (Lawrence et al., 1987; Lucey et al., 2003). El segundo es el efecto de pérdida de humedad, que al provocar una disminución de la hidratación de las proteínas conduce a una mayor interacción de las mismas provocando
el aumento de la firmeza de la matriz proteica (Adda et al. 1982;Walstra,1990).
Otro de los cambios bioquímicos que ocurren en el queso es la lipólisis. En la estructura del queso, la grasa se encuentra distribuida como material de relleno en la matriz proteica, por lo tanto si se incrementa su contenido en la formulación, el queso presentará menor firmeza y mayor elasticidad, mientras que cuando su contenido se reduzca (ya sea por acción lipolítica o intencional para fines de obtener un producto con bajo contenido en grasa) se obtendrán quesos más duros y rígidos (Theophilou y Wilbey, 2007; Brighenti et al., 2008).
Se reconoce también que el pH es uno de los parámetros que afecta sobretodo las propiedades texturales del queso, debido a su
Tabla III. Condiciones para la determinación de propiedades texturales en algunos tipos de queso fresco.
Prueba textural Tipo de queso
Compresión uniaxial
Queso fresco (sin iniciadores lácticos)
Geometría de la muestra
Cilindros de 25 mm de diámetro por 20 mm de altura
Compresión uniaxial Queso fresco elaborado con leche de cabra cruda, pasteurizada y tratada por altas presiones. Cubos de 10 mm de cada lado.
TPAQueso suave de leche de cabra Bloques cilíndricos de aprox. 14.5 mm de diámetro y altura.
TPAQueso fresco de México Cilindros de 15 mm de diámetro y 15 mm de altura.
Equipo utilizadoCondiciones de la pruebaParametros calculadosReferencia
TA-TX2 Texture Analyzera
Temperatura: 4ºC
% de compresión: 80% con respecto a la altura original.
Fuerza de fractura (σf)
Fuerza de deformación (εf)
Zamora, 2009
Plato de 50 mm de diámetro.
Velocidad: 0.8 mm/s
No. de mediciones por muestra: 6
TA-TX2 Texture Analyzera
Temperatura: 20ºC
80% de compresión con respecto a su altura original.
Velocidad: 80 mm/min = 1.3 mm/seg.
No. de mediciones por muestra: 6
NOTA: Las mediciones se realizaron bajo condiciones lubricadas.
Máquina universal de ensayos (modelo SM-25-155, Material Testing Products Systems Corp., Eden Prairie, MN).
Máquina universal de ensayos Sintech 1/G (MSS Systems, Eden Prairie, MN).
Relajación del esfuerzo Queso untable Cubos de 2 cm.Texture Analyzer
TA.XT2bempleando el software
Texture Expert versión 1.22.
CreepQueso untable
Cubos de 2 cm. Texture Analyzer
TA.XT2bempleando el software
Texture Expert versión 1.22.
PenetraciónQueso cremaBloques rectangulares de (12 × 6.8 × 3 cm).
Fuerza de fractura (σf)
Fuerza de deformación (εf)
Buffa et al., 2001
Doble compresión a 75% de su altura original
Velocidad: 100 mm/min
No. de mediciones por muestra: 4
Doble compresión a 75% de su altura original.
Velocidad: 100 mm/ min = 1.6 mm/s
No. de mediciones por muestra: 4
Se utilizó un plato de 3.6 cm de diámetro, se aplicó una fuerza de 0.5 N con 1 mm/s de velocidad, con una deformación del 50%.
Se utilizó un plato de 3.6 cm de diámetro, se aplico una fuerza de 0.2N con una velocidad de 1mm/s, midiendo distancia contra tiempo.
TA.XT2 Texture Analyzerb Se utilizó una sonda cónica con de acero inoxidable con ángulo de 45º (AT-15) la cual se introdujo 15 mm en las muestras a una velocidad de 1 mm /s.
efecto sobre la red de proteínas. Un pH cercano al punto isoeléctrico provoca fuertes fuerzas iónicas e hidrófobas, que resultan en una red de caseína compacta típica de los quesos duros, mientras que en el caso de un pH más alto las caseínas presentan una carga negativa, lo que genera repulsión entre los agregados proteicos, generándose un queso con mayor humedad, más elástico y menos compacto (Watkinson et al., 2001; Lu et al., 2008).
En los quesos frescos, la elevada humedad y el bajo pH, son condiciones que afectan notoriamente la textura y sabor durante la conservación, de forma que una excesiva proteólisispodríaocasionardefectoscomouna textura excesivamente blanda y un sabor amargo (Fox y McSweeney, 1996). Un
A partir de las gráfica de fuerza contra tiempo se calcularon: la dureza, cohesividad y fracturabilidad. Así como la masticabilidad (producto de Van Hekken et al., 2005
Dureza y cohesividad
Tunick y Van Hekken, 2010
Tiempo de relajación Carvajal-Cuéllar, 2004
Deformación como función del tiempo Carvajal-Cuéllar, 2004
DurezaBrighenti et al., 2008
ejemplo donde se hace más evidente este defecto es en el queso Oaxaca, que con el tiempo se ablanda, pierde elasticidad y definición visual del hilado, semejante al que se observa en el queso Mozzarella (Imm et al., 2003;ZisuyShah,2005).
La sal además de tener un papel en el sabor y conservación del queso, en altas concentraciones disminuye la actividad enzimática proteolítica, aumentando la salida de agua presente en la red proteica de la cuajada (sinéresis) ocasionando con ello, menor humedad y por lo tanto mayor dureza en el queso (Pinho et al., 2004; Guo et al., 2012).
La acidez, en el queso es otro factor que no sólo tiene incidencia sobre el sabor, sino
también directamente en los cambios que experimenta la red de proteína (cuajada) del queso, teniendo ésta una correlación directa en los fenómenos de sinéresis (es decir; a mayor acidez, mayor sinéresis) y textura final (Pinho et al., 2004). Además de la acidez, la sinéresis está afectada también por circunstancias propias del proceso de elaboración y por la presencia de calcio libre, el cual provoca la unión de la caseína en la red protéica de la cuajada(Walstra,1990).
3.2. Condiciones de proceso
No obstante que la composición original del queso es determinante en las características texturales del mismo, otros aspectos como la tecnología aplicada, la adición de cultivos iniciadores y las condiciones de maduración tendrían mayor impacto, determinando con ello la identidad y aceptabilidad del queso (Fox et al., 2000;Walstra et al., 2006;Johnson yLaw,2011).
3.2.1. Tratamiento térmico/Pasteurización
Aunque no existe un mecanismo claro, se ha observado que la pasteurización de la leche produce una desnaturalización ligera de las proteínas séricas (αS1 y β-caseínas), así como modificaciones leves en la capacidad de coagulación de la leche (Grappin y Beuvier, 1997). Provoca también la disminución significativa de péptidos de cadena corta y aminoácidos libres – compuestos precursores de aromas y sabores en el queso (Tunick y Van Hekken, 2010) y origina quesos con alto contenido de humedad con respecto a los elaborados con leche cruda (Ortigosa et al., 2001).
Para evitar los efectos del tratamiento térmico en las proteínas de la leche, se ha investigado la aplicación de altas presiones en queso y su potencial uso en la industria láctea (Buffa et al., 2001; Trujillo et al., 2002; Juan et al., 2007; Evert-Arriagada et al., 2012). Las
altas presiones inactivan el crecimiento de los microorganismos presentes en la leche y el queso,asímismoalteranlasvelocidadesdelas reaccionesenzimáticas (Ávila et al., 2007).
3.3. Alteraciones causadas por microorganismos
Como ya se mencionó, las propiedades físicas del queso pueden verse afectadas como consecuencia de procesos bioquímicos, tales como la proteólisis y la lipólisis. Las enzimas involucradas en estos procesos pueden estar presentes en el cuajo, la leche o bien, ser producidas por microorganismos (Sousa et al., 2001).
Algunos microorganismos utilizados como cultivos iniciadores, además de metabolizar la lactosa, pueden producir y liberar otros compuestos en el queso. JiménezGuzmán et al., (2009), evaluaron la presencia de un exopolisacárido producido por una cepa de Streptococcus thermophilus en la composición y propiedades de queso Panela, concluyendo que la presencia de dicho compuesto incrementó la retención de humedadygrasadentrodelamatrizdelqueso.
El principal mecanismo a través del cual un cultivo iniciador puede afectar las propiedades texturales, reológicas y funcionales del queso, tiene que ver con su capacidad de producción de ácido, que como ya se mencionó afecta la red proteica y a su capacidad para retener agua Un aumento en el contenido de humedad provocará una textura más blanda, menor firmeza, y en el caso del quesodepastahilada, unamayor capacidadde fusión(fundibilidad)(ZisuyShah,2005).
3.4.Otros factores
El uso de cuajo artesanal da como resultado quesos de mayor dureza (bajo prueba de compresión y penetración), adhesividad y elasticidad con respecto al cuajo comercial
(Álvarez, 2003). Esto se puede deber a la mayor capacidad proteolítica del coagulante artesanal frente al comercial, derivando en una mayorcremosidaddeestetipodequesos.
Algunosestudiosdemuestranqueelcambio de dieta del animal lactante modifica la composición de la leche y en consecuencia, puede ocasionar un cambio de leve a moderado en las propiedades reológicas y texturales de queso (Jaramillo et al., 2010; Álvarez,2003)
Finalmente, la oxidación de las grasas de los quesos es otro fenómeno presente en el queso en mayor o menor extensión. En quesos frescos la exposición a la luz es la causa principal de oxidación, aparición de aromas atípicos (desagradables) y cambios en el color (Mortensen et al., 2004).
en el caso del análisis de microestructura o los recientes estudios sobre análisis de textura mediante espectroscopía de infrarrojo cercano acoplada a sonda de fibra óptica, cuya aplicación resulta novedosa. Sin embargo, habría que reflexionar sobre el costo-beneficio dedichastécnicas.
Respecto a las diferentes pruebas que se empleanparaevaluarlosparámetrostexturales y reológicos, una de las ventajas de los métodos reológicos fundamentales, es la posibilidad de poder evaluar la influencia de modificaciones mínimas a la formulación, mientras que dichas diferencias, cuando son muy pequeñas, no pueden ser detectadas con métodosempíricosoimitativos.
Conclusiones y comentarios finales
Alolargodeestarevisiónsevelaimportancia de factores tales como la composición química y condiciones de proceso que afectan en menor o mayor medida las propiedades y características que por definición correspondenalosquesosfrescos.
La mayoría de las técnicas mencionadas para el análisis de las propiedades de los quesos frescos, han sido estandarizadas y ampliamente aceptadas por la comunidad científica. No obstante, dados los avances tecnológicos en los equipos empleados para la medición de las mismas, éstas se han perfeccionado e inclusive han surgido otras técnicas como la micro-tomografía de rayos X
Finalmente se destaca que el conocimiento de las características y propiedades del queso comoresultadodesuformulación,elaboración y proceso, así como el dominio de las técnicas ymétodos para su caracterización, son de gran relevancia no sólo para garantizar su calidad y aceptabilidad; sino también como una herramienta de identidad útil para diferenciar losdiversostiposdequesosfrescos.
Agradecimientos
La autora Carolina Ramírez López, agradece a la Universidad de las Américas Puebla y al Consejo Nacional de Ciencia y Tecnología (CONACyT, México) por el financiamiento recibidoparalarealizacióndeestetrabajo.Así mismo al Instituto Politécnico Nacional por el apoyo brindado a través de la licencia laboral otorgada a su servidora para la realización de estudios de doctorado.
Referencias
Adda, J., Gripon, J.C. y Vassal, L. 1982. The chemistry of flavour and texture generation in cheese. Food Chemistry. 9(1):115-129.
Alais, C. 1985. Ciencia de la leche: Principios de técnica lechera. Cuarta edición. Editorial Reverté S.A. Barcelona, España. 873 pp.
Álvarez, S. 2003. Influencia de la alimentación del ganado caprino en la caracterización físico-química y organoléptica del queso Majorero (D.O.). Tesis Doctoral, Universidad de La Laguna, España.
AOAC. 2005. Official Methods of Analysis. 18th ed. AOAC International, Gaithersburg, MD, EE.UU.
Ávila, M., Calzada, J., Nuñez, M. y Garde S. 2007. Effect of a bacteriocin-producing Lactococcus lactis strain and high-pressure treatment on the esterase activity and free fatty acids in Hispánico cheese. International Dairy Journal. 17: 1415-1423.
Bohlin, L., Hegg, P.O. y Ljusberg-Wahren H. 1984. Viscoelastic properties of coagulating milk. Journal Dairy Science. 67, 729-734.
Bourne, M.C. 2002. Food Texture and Viscosity: Concept and Measurement. 2da Edición. Academic Press. San Diego California, EE.UU. 427 pp.
Brighenti, M., Govindasamy-Lucey, S., Lim K., Nelson, K., y Lucey, J.A. 2008. Characterization of rheological, textural and sensory properties of samples of commercial US cream cheese with different fat contents. Journal of Dairy Science. 91: 4501-4517.
Buffa, M.N., Guamis, B., Saldo J., y Trujillo, A.J. 2004. Changes in organic acids during ripening of cheese made from raw, pasteurized or high-pressure treated goat´s milk. Lebensmittel-Wissenschaft and Technologie. Food Science and Technology. 37(2):247-253.
Buffa, M.N., Trujillo, A.J., Pavia, M. y Guamis, B. 2001. Changes in textural, microstructural, and color characteristics during ripening of cheeses made from raw, pasteurized or high-pressure-treated goat´s milk. International Dairy Journal. 11: 927-934.
Carvajal-Cuéllar, D.M. 2004. Estudio del comportamiento fisicoquímico y reológico de un queso untable. Tesis de Maestría. Universidad de las Américas Puebla. México.
Caro, I., Franco M.J., Mateo J. y Alonso, C. 1998. Influencia en la acidificación del queso tipo Oaxaca de la adición de distintas cantidades de fermentos mesófilos y termófilos a distintos tiempos de inoculación. XI Congreso Nacional de Microbiología de la SEM. Libro de ponencias, comunicaciones y posters. Pamplona, España.
Castañeda, R. 2002. La reología en la tipificación y la caracterización de quesos. En: Tecnología Láctea Latinoamericana. 20(26): 48-53.
Cunha, C.R., Dias, A.I. y Viotto, W.H. 2010. Microstructure, texture, colour and sensory evaluation of a spreadable processed cheese analogue made with vegetable fat. Food Research International. 43 (3): 723-729.
Dalgleish, D.G. 1999. The Enzymatic Coagulation of Milk. En: P.F. Fox (Ed). Cheese: Chemistry, Physics and Microbiology. Volumen 1. Aspen Publishers, Maryland, EE.UU. pp. 69-100.
De Oca-Flores, E. M., Castelán-Ortega, O. A., EstradaFlores, J. G. y Espinoza-Ortega, A. 2009. Oaxaca cheese: manufacture process and physicochemical characteristics. International Journal of Dairy Technology. 62(4):535-540.
Eck, A. 2000. What is a cheese?. En: A. Eck y J.C. Gilis (Eds). Cheesemaking: From Science to Quality Assurance. Lavoisier Publising. pp. 661-662.
Evert-Arriagada, K., Hernández-Herrero, M.M., Juan, B., Guamis, B. y Trujillo, A.J. 2012. Effect of high pressure on fresh cheese shelf-life. Journal of Food Engineering.110 (2): 248–253.
FAO/OMS. 2008. Leche y productos lácteos. 2da edición. Norma general del Codex para el queso. Codex Stan 283-1978. Revisión 1999, Enmienda 2006.
Farkye, N.Y. 2004. Cheese technology. International Journal of Dairy Technology. 57(2-3):91- 98.
Farkye, N.Y., Prasad, B.B., Rossi, R., y Noyes, O.R 1995. Sensory and textural properties of Queso Blanco-type cheese influenced by acid type. Journal of Dairy Science. 78:1649.
Foegeding, E.A. y Drake, M.A. 2007. Invited Review: Sensory and mechanical properties of cheese texture. Journal of Dairy Science. 90:1611-1624.
Fox, P.F., Guinne, T.P., Timothy, M.C. y McSweeney P.L.H. 2000. Fundamentals of Cheese Science Aspen Publishers, Maryland, EE.UU. pp. 392- 422.
Fox, F.P. y McSweeney P.L.H. 1996. Proteolysis in cheese during ripening. Food Reviews International. 12, 457-509.
García-Islas, B. 2006. Caracterización fisicoquímica de diversos tipos de quesos elaborados en el Valle de Tulancingo Hgo con el fin de proponer normas de calidad. Tesis de licenciatura. Universidad
Autónoma del Estado de Hidalgo. Tulancingo, Hgo. México. 98 pp.
Grappin, R. y Beuvier, E. 1997. Possible implications of milk pasteurization on the manufacture and sensory quality of ripened cheese. International Dairy Journal. 7: 751-761.
Guisa, F.L. 1999. Types of Mexican cheeses. Exploring cheeses of Mexico and Latin America. Artisan course. Universidad de Wisconsin, Madison. EE.UU.
Guo, L., Van Hekken, D.L., Tomasula, P.M., Tunick, M.H. y Huo, G. 2012. Effect of salt on microbiology and proteolysis of Queso Fresco cheese during storage. Milchwissenschaft. 67:74–77.
Gunasekaran, S. y Ak, M.M. 2003. Cheese Rheology and Texture. CRC Press. Nueva York, EE.UU. 437 pp.
Hwang, C.H. y Gunasekaran, S. 2001. Measuring crumbliness of some commercial Queso Fresco-type Latin American cheeses. Milchwissenschaft. 56: 446-450.
Ibáñez, F. C., Loygorri, S., Ordoñez, A. y Torre I.P. 1998. Evaluación instrumental y sensorial de la textura en quesos de oveja con denominación de origen. Alimentaria. 292:49-53.
Imm, J.Y., Oh, E.J., Han, K.S., Park, Y.W. y Kim S.H. 2003. Functionality and physco-chemical characteristics of bovine and caprine Mozzarella cheeses during refrigerated storage. Journal of Dairy Science. 86:2790-2798.
Jaramillo, D.P., Buffa, M., Rodríguez, I., Pérez-Baena, I., Guamis, B. y Trujillo, A.J. 2010. Effect of the inclusion of artichoke silage in the ration of lactating ewes on the properties of milk and cheese characteristics during ripening. Journal of Dairy Science. 93(4):1412-1419.
Jiménez-Guzmán, J., Flores-Nájera, A., Cruz-Guerrero, A.E. y García-Garibay, M. 2009. Use of an exopolysaccharide-producing strain of Streptococcus thermophilus in the manufacture of Mexican Panela cheese. Lebensmittel-Wissenschaft and Technologie-Food Science and Technology. 42:1508-1512.
Johnson, M. y Law, B.A. 2011. The fundamentals of cheese technology. En: Law B.A. y Tamime A.Y. (Eds). Technology of cheesemaking. Segunda edición. Wiley Blackwell, Reino Unido.
Juan, B., Trujillo, A.J., Guamis, V., Buffa M., y Ferragut, V. 2007. Rheologycal textural and sensory characteristics of high-pressure treated semi-hard ewe´s milk cheese. International Dairy Journal.17: 248-254.
Karami, M., Ehsani M.R., Mousavi S.M., Rezaei K., Safari M. 2009. Microstructural properties of fat during the accelerated ripening of ultrafiltered-Feta cheese. Food Chemistry. 113 (2): 424-434.
Kilcast, D. 2004. Texture in Foods. Vol. 2 Solid Food. CRC Press. Nueva York, EE.UU. pp. 205-236.
Kuo, M.I. y Gunasekaran, S. 2003. Effect of frozen storage on physical properties of pasta filata and non-pasta filata Mozzarella cheeses. Journal of Dairy Science, 86:1108–1117.
Kuo, M.I. y Gunasekaran, S. 2009. Effect of freezing and frozen storage on microstructure of Mozzarella and pizza cheeses. Lebensmittel-Wissenschaft and Technologie- Food Science and Technology. 42(1): 9-16.
Laverse, J., Mastromatteo, M., Frisullo, P., Del Nobile, M.A. 2011. X-ray microtomography to study the microstructure of cream cheese-type products. Journal of Dairy Science. 94 (1): 43-50.
Lawrence, R.C., Creamer, L.K. y Gilles, J. 1987. Syposium: cheese ripening technology. Texture development during cheese ripening. Journal of Dairy Science.70 (8): 1748-1760.
Liu, H., Xu, M.X. y Guo, S.D. 2008. Comparison of full-fat and low-fat cheese analogues with or without pectin gel through microstructure, texture, rheology, thermal and sensory analysis. International Journal of Food Science and Technology. 43(9): 1581-1592.
Lobato-Calleros, C., Reyes-Hernández, J., Beristain, C.I., Hornelas-Uribe, Y., Sánchez-García, J.E. y Vernon-Carter, E.J. 2007. Microstructure and texture of white fresh cheese made with canola oil and whey protein concentrate in partial or total replacement of milk fat. Food Research International. 40:529–537
Lu, N., Shirashoji, N. y Lucey, J.A. 2008. Effects of pH on the textural properties and meltability of pasteurized process cheese made with diffenrent types of emulsifying salts. JFS: Food Engineering and Physical Properties.73(8):E363-E369.
Lucey, J.A., Johnson, M.E. y Horne, D.S. 2003. Perspectives on the basis of the rheology and texture properties of cheese. Journal Dairy Science.86: 2725-2743.
McSweeney, P.L.H. 2004. Biochemistry of cheese ripening. International Journal of Dairy Technology. 57(2-3):127-144.
Morales-Celaya, M.F., Lobato-Calleros, C., AlvarezRamirez, J., Vernon-Carte, E.J. 2012. Effect of milk pasteurization and acidification method on the chemical composition and microstructure of a Mexican pasta filata cheese. LebensmittelWissenschaft and Technologie-Food Science and Technology. 45(2): 132-141.
Mortensen, G., Bertelsen, G., Mortensen, B.K. y Stapelfeldt, H. 2004. Ligth-induced changes in packaged cheeses –a review. International Dairy Journal. 14:85-102.
Muller, H.G. 1973. An introduction to Food Rheology William Heineman Ltd., Heineman, Londres. p. 14.
NOM-121-SSA1-1994. Norma oficial. Bienes y servicios. Quesos: frescos, madurados y procesados. Especificaciones sanitarias para lácteos y sus derivados.
Path, J. 1991. Hispanic cheeses: A promising new market for the specialty cheesemaker. UW Dairy Pipeline. 3(4):1-4.
Pavia, M., Trujillo, A.J., Guamis, B. y Ferragut, V 1999. Evolución de la composición y textura de un queso de oveja en la maduración. Alimentaria. 306: 43-47.
Pereira, C.I., Gomes, A.M.P., y Malcata, F.J. 2009. Microstructure of cheese: Processing, technological and microbiological considerations. Trends in Food Science and Technology. 20(5): 213-219.
Pinho, O., Mendes, E., Alves, M.M., Ferreira, IMPLVO. 2004. Chemical, physical, and sensorial characteristics of “Terrincho” ewe cheese: Changes during ripenind and intravarietal comparison. Journal of Dairy Science. 87(2):249-257.
Ortigosa, M., Torre, P. y Izco, J.M. 2001. Effect of pasteurization of ewe´s milk and use of a native starter culture on the volatile components and sensory characteristics of roncal cheese. Journal of Dairy Science. 8 (6):1320-1330.
Ribero, G.G., Rubiolo, A.C. y Zorrilla, S.E. 2009. Microstructure of Mozzarella as affected by the inmersion freezing in NaCl solutions and by the frozen storage. Journal of Food Engineering. 91: 516-520.
Rosenthal, A.J. 1999. Relation between instrumental and sensory measures of food texture. En: A.J.
Rosenthal (Ed). Food texture, measurement and perception. Aspen Publishers Inc. Nueva York, EE.UU.
Scholz, W. 1995. Elaboración de quesos de oveja y de cabra. Editorial Acribia. Zaragoza, España. 145 p.
Scott, R., Robinson, R.K. y Wilbey, R.A. 1998. Cheese varieties. En: Scott, R., Robinson, R.K. y Wilbey, R.A. (Eds). Cheesemaking Practice, Tercera edición. Kluwer Academic/Plenum Publishers, Nueva York, EE.UU. 449 pp.
Segards, R.A. y Kapsalis, J.G. 1987. Texture, rheology, psychophysics. En: J.G. Kapsalis (Ed). Objective methods in food quality assessment. CRC Press. Nueva York, EE.UU. pp. 155-184.
Shoemaker, C.F., Lewis, J.I. y Tamura, M.S. 1987. Instrumentation for rheological measurements of food. Food Technology. 41: 80-84.
Sousa, M.J., Ard, Y. y McSweeney, P.L.H. 2001. Advances in the study of proteolysis during cheese ripening. International Dairy Journal. 11, 327-345.
Steffe, J. 1996. Rheological Methods in Food Process Engineering. Segunda edición. Freeman Press, Michigan, EE.UU. pp. 1-10, 295-317, 258-262.
Tabilo-Munizaga, G. y Barbosa-Cánovas, G. 2005. Rheology for food industry. Journal of Food Engineering. 67:147-156.
Tan, Y.L., Ye, A.A., Singh, H. H. y Hemar, Y.Y. 2007. Effects of biopolymer addition on the dynamic rheology and microstructure of renneted skim milk systems. Journal of Texture Studies. 38(3): 404-422.
Theophilou, P., y Wilbey, R.A. 2007. Effects of fat on the properties of halloumi cheese. International Journal of Dairy Technology. 60(1):1-4.
Trivedi, D., Bennett, R.J., Hemar, Y., Reid, D.W., Lee, S., y Illingworth, D. 2008a. Effect of different starches on rheological and microstructural properties of (I) model processed cheese. International Journal of Food Science and Technology. 43(12):2191-2196.
Trivedi, D., Bennett, R.J., Hemar, Y., Reid, D.W., Siew, K.L. y Illingworth, D. 2008b. Effect of different starches on rheological and microstructural properties of (II) commercial processed cheese. International Journal of Food Science and Technology. 43(12): 2197-2203.
Trujillo, A. J., Capellas, M., Saldo, J., Gervilla, R., y Guamis, B. 2002. Applications of high-hydrostatic pressure on milk and dairy products: a review.
Innovative Food Science and Emerging Technologies. 3: 295–307.
Tunick M.H. 2000. Rheology of dairy foods that gel, stretch, and fracture. En: Symposium: Dairy products rheology. Journal of Dairy Science. 83:1892-1898.
Tunick, M.H. y Van Hekken, D.L. 2010. Rheology and texture of commercial queso fresco cheeses made from raw and pasteurized milk. Journal of Food Quality. 33:204-215.
Udayarajan, C. 2007. Relating physicochemical characteristics of cheese to its functional performance. Tesis doctoral. (PhD of Philosophy Food Science). Universidad de Wisconsin-Madison, EE.UU. 29 pp.
Van Hekken, D.L. y Farkye, N. 2003. Hispanic Cheeses: The quest for queso. Food Technology. 57:32-38.
Van Hekken, D.L., Tunick, M.H. y Park, Y.W. 2005. Effect of frozen storage on the proteolytic and rheological properties of soft caprine milk cheese. Journal of Dairy Science. 88:1966–1972.
Vélez-Ruiz, J.F. y Barbosa-Cánovas, C.G. 1997. Rheological properties of selected dairy products. Critical Reviews in Food Science and Nutrition. 37:311-359.
Vélez-Ruiz, J.F. 2009. Rheology and Texture of Cheese. En: Sosa-Morales, M.E. y Vélez-Ruiz, J.F. (Eds). Food Processing and Engineering Topics. Ed. Nova Science Publishers. Nueva York. EE.UU. pp 87-122.
Walstra, P. 1990. On the stability of casein micelles. Journal of Dairy Science. 73:1965-1979.
Walstra P., Wouters J.T.M. y Geurts T.J. 2006. Dairy Science and Technology. CRC Press. Nueva York, EE.UU. 140-155 pp.
Watkinson P., Coker C., Crawford R., Dodds C., Johnston K., McKenna A. y White N. 2001. Effect of cheese pH and ripening time on model cheese textural properties and proteolysis. International Dairy Journal. 11: 455–464.
Zamora A. 2009. Ultra high pressure homogenisation of milk: Effects on cheese making. PhD Tesis. Facultad de Veterinaria. Universidad Autónoma de Barcelona, España.
Zisu B., y Shah N.P. 2005. Textural and functional changes in low-fat Mozzarella cheeses in relation to proteolysis and microstructure as influenced by the use of fat replacers, pre-acidification and EPS starter. International Dairy Journal. 15, 957-972.

Temas Selectos de Ingeniería de Alimentos 6 - 2 (2012): 149 - 159

Equipos para tratamientos de alimentos con radiación UVC
O. T. Antonio-Gutiérrez*, E. Palou y A. López-Malo
Departamento de Ingeniería Química, Alimentos y Ambiental, Universidad de las Américas Puebla. Ex hacienda Sta. Catarina Mártir S/N, San Andrés Cholula, Puebla. C.P.72810. México.
Resumen
Actualmente, hay un gran interés por nuevas tecnologías más eficaces, baratas y menos destructivas de la calidad de los alimentos que los procesamientos térmicos tradicionales. La tecnología de radiación ultravioleta de onda corta (UVC) es muy prometedora como una alternativa a los métodos tradicionales. Esta revisión da a conocer algunos equipos UVC disponibles en el mercado y describe sus características más importantes, presenta equipos para tratar algunos alimentos sólidos y líquidos, y describe algunos avances tecnológicos de la fuente de radiación. Las lámparas de mercurio de baja y mediana presión son las más comunes; sin embargo, han surgido algunas alternativas como las lámparas UV de microondas, las cuales son más eficientes. Los equipos UVC disponibles en el mercado tienen pocas aplicaciones en alimentos; sin embargo, han tenido éxito a nivel de investigación, lo que genera entusiasmo y alienta a más investigación de esta tecnología para ampliar sus aplicaciones en la industria alimentaria.
Palabras clave: radiación ultravioleta, equipos UVC, fuente de radiación, alimentos.
Abstract
Nowadays, new technologies that are more efficient, cheaper and less disruptive to quality of foods than traditional thermal processing are of interest. Ultraviolet light technology (UVC) holds considerable promise as an alternative to traditional methods. This review discloses some commercially available UVC equipment and describes its most important features. Equipment to treat some solid and liquid foods are presented. Furthermore, the description and some technological advances of the UV radiation source are discussed. The low and medium pressure mercury lamps are the most common, but alternatives have emerged like microwave UV lamps which are more efficient. The UVC equipment available in the market has few applications in foods, however, it has been successful, which causes enthusiasm, and encourage to do more research for this technology in order to expand their applications in the food industry.
Keywords: Ultraviolet light, UVC equipment, radiation source, foods.
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: oscar.antoniogz@udlap.mx
Introducción
La tendencia actual de los consumidores es hacia productos alimenticios mínimamente procesados, los cuales mantengan al máximo sus características sensoriales y nutrimentales, con una vida de anaquel conveniente y aceptable, y microbiológicamente seguros. Debido a esto, los procesos no térmicos, yque utilizan como fundamento métodos físicos de destrucción microbiana y/o enzimática, aplicados a la conservación de alimentos sin los efectos colaterales de los tratamientos con calor, se encuentran en intensa investigación (López-Malo y Palou, 2004). Un procedimiento de este tipo es la irradiación de alimentos con radiación ultravioleta de onda corta (UVC), la cual ha sido aplicada en la industria de alimentos con fines de desinfección de empaques y superficies de trabajo, así como para la desinfección de agua y aire. Recientemente, la UVC ha sido utilizada para la desinfección de superficies de alimentos para obtener productos de mayor calidad (Bintsis et al., 2000). Además, se ha incrementado el interés por el uso de la UVC para el tratamiento de jugos de frutas y otros productoslíquidos(Farid et al.,2001).
Se sabe que los microorganismos tienen su máxima absorción de radiación ultravioleta a 260nm.Basadoenesto, seconstruyóenSuiza a principios de 1910, el primer prototipo de lámpara de radiación ultravioleta, que resultó eficaz para la destrucción de microorganismos tales como bacterias, levaduras y mohos en la desinfección de agua. A partir de 1940, se perfeccionó la fabricación de lámparas y en 1955seobtuvieronlasprimerasconstruidasen cuarzo, con longitudes de onda de 254 nm, las cuales resultaron ser más efectivas (González, 2001).
La UVC no produce residuos químicos, requiere de poco mantenimiento y es de bajo costo (Guerrero-Beltrán y Barbosa-Cánovas, 2004). Debido a esto, dicha tecnología ha
comenzado a comercializarse exitosamente para la desinfección de algunos alimentos líquidos y sólidos, por lo que resulta importante conocer las características y aplicaciones de algunos de los equipos UVC. Es por ello que el objetivo principal de este artículo es dar a conocer algunos equipos disponibles en el mercado y describir sus características principales. Además, un punto importante a tratar en este artículo es la descripción y algunos avances tecnológicos de una de las partes fundamentales de los equipos UVC,lafuentederadiación.
1. Radiación ultravioleta
La energía radiante puede considerarse como campos magnéticos y eléctricos que oscilan perpendicularmente a la dirección de desplazamiento. La luz visible es un ejemplo de este tipo de energía. Las energías radiantes se desplazan a la velocidad de la luz, pero difieren en frecuencia y longitud de onda. El espectro electromagnético abarca un amplio intervalo de energías (frecuencias) y, por lo tanto, de longitudes de onda. Entre de las diferentes regiones del espectro electromagnético, la radiación ultravioleta y las microondas son algunos ejemplos de interés en la industria de los alimentos (Mendonca,2002).
Las radiaciones ultravioleta (UV) se encuentran entre las bandas de rayos X y luz visible, con longitudes de onda que van desde 180 hasta 400 nm (Díaz y Serrano, 2005). Adicionalmente, las radiaciones ultravioleta se subdividenentresregiones: UVdeondalarga, UVdeondamediayUVdeondacorta(UVC). Esta última abarca longitudes de onda de 200 hasta 280 nm, intervalo considerado como germicida contra microorganismos tales como bacterias y levaduras (Bolton, 2001). Sin
Revisión bibliográfica
embargo, la longitud de onda de 254 nm es la más utilizada para esterilizar agua, aire y algunos alimentos, ya que se absorbe en un nivel que es suficiente para ocasionar cambios físicos en los electrones y rompimiento de enlaces en el ácido desoxirribonucleico (ADN), inactivando así los procesos de crecimiento y reproducción microbianos (Bolton, 2001). La alta absorción de UVC (254 nm) por el ADN se asocia con la capacidad de las bases pirimidina y purina para absorber radiación en esta longitud de onda (Shama, 1999). La UVC causa daños en el ADN de las células expuestas al promover la formación de enlaces entre timinas en cadenasadyacentesdelADN;estosdímerosde timinainhibenlareplicacióncorrectadelADN durante la reproducción de la célula (Adams y Moss,1995).
Existen ventajas y desventajas en cuanto al uso de la UVC para la desinfección de alimentos. Algunas ventajas son que esta tecnologíanoproduceresiduosquímicosyque requiere poco mantenimiento. Sus desventajas se relacionan con la baja penetración en diferentes alimentos; por ejemplo, la UVC sólo penetra a una profundidad muy pequeña en la superficie de líquidos que no sean agua (Shama,1999).
2. Fuentes de radiación UV
Las fuentesderadiación UVmáscomunesson las lámparas de arco de mercurio de baja y mediana presión, las cuales son capaces de generar radiación UV con una longitud de onda de 254 nm. Estas lámparas han sido utilizadasexitosamenteparaladesinfecciónde agua; sin embargo, la respuesta microbiana en alimentos a este tipo de lámparas continúa en investigación. Se han desarrollado además, otro tipo de fuentes de radiación UV como las lámparas UV de microondas y lámparas de pulsosUV.Estasnuevasalternativaspresentan diversas ventajas, por ejemplo, son independientes del efecto de la temperatura y
pueden ser aplicadas para el tratamiento de alimentos. A pesar de que ya son empleadas para la desinfección de agua, su uso en alimentos no ha sido del todo evaluado (Koutchma,2009).
2.1. Lámparas de mercurio
Una lámpara común de arco de mercurio se muestraenlaFig.1.Lalámparaconsistedeun tubo herméticamente cerrado de sílica vitreosa o cuarzo (ambos transmisores de radiación UV) con electrodos en ambos extremos (Phillips, 1983). El tubo es llenado con mercurio y un gas inerte, usualmente argón. Unelectrodoselocalizaencadaorilladeltubo conectado al exterior a través de un sello. Los electrodos están compuestos usualmente de tungsteno con una mezcla de metales alcalinotérreos, para facilitar la formación del arco dentro de la lámpara. La radiación UV es emitida desde la lámpara cuando el vapor de mercurio excitado por una descarga, retorna a un nivel de menor energía. El argón presente ayuda para el arranque de la lámpara, además extiende la vida de los electrodos y reduce las pérdidas térmicas. Este tipo de lámparas pueden ser operadas a baja y mediana presión (Masschelein,2002).
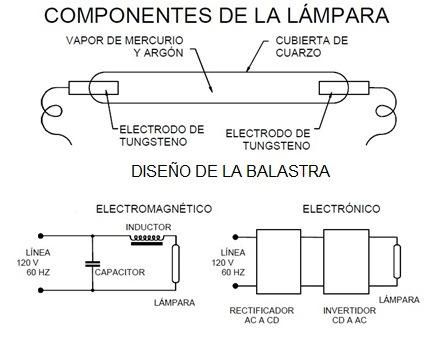
Fig. 1. Lámpara de arco de mercurio y diseños del balastro. Adaptada de Wright y Cairns (1998).
Debido a las características de resistencia eléctrica negativa de las descargas de gases, la operación estable de una lámpara de arco de mercurio requiere de una balastra adecuada. Las balastras son un componente que sirve para limitar el flujo de corriente y estabilizar el funcionamiento de las lámparas. Son diseñadas para operar las lámparas y proveer el voltaje requerido apropiado para el arranque yoperación.Si lalámparaes operada usando un suministro de corriente alterna, la balastra consiste usualmente de componentes inductivos y capacitivos. Las balastras se clasifican en electromagnéticas y electrónicas. La balastra electromagnética consiste básicamente deun núcleodeláminas de acero, rodeado por dos bobinas de cobre o aluminio. Estearreglotransformalapotenciaeléctricaen una forma apropiada para arrancar yregular la corriente de la lámpara. El capacitor es otro componente importante, el cual optimiza el factor potencia, de tal formaquepuede utilizar laenergíademaneramás eficiente. Labalastra electrónica está basada en una tecnología completamente diferente a la de la balastra electromagnética. Enciende y regula las lámparas en altas frecuencias, generalmente mayores a 20 kHz, usando componentes electrónicos en vez del tradicional trasformador(Martínez,2005).
2.1.1. Lámparas de mercurio de baja presión
Este tipo de lámparas, para la generación de radiación UV, son operadas a 102-103 Pascales. Esta presión corresponde a la del vapor del mercurio líquido a una temperatura de pared óptima de 40°C, y genera en la lámpara un arco eléctrico de energía de cerca de0.2a0.3W/cm(Phillips,1983).El espectro de emisión de la lámpara de mercurio de baja presión se limita a un número bien definido de líneas espectrales, y la fuente es denominada monocromática. Aproximadamente, el 85% de la radiación emitida es UV resonante con una longitud de onda de 253.7 nm, la cual es la más eficiente para la destrucción de
microorganismos. La Agencia de Medicamentos y Alimentos de los Estado Unidos de América (FDA, por sus siglas en inglés) ha aprobado el uso de lámparas de mercurio de baja presión para el procesamiento de jugos y éstas han sido exitosamentecomercializadas(FDA,2000).
2.1.2. Lámparas de mercurio de mediana presión
Estaslámparassonoperadasaproximadamente a 104-106 Pascales (Masschelein, 2002). Las temperaturas que alcanzan son elevadas, de entre 600 y 800°C. Es por ello que es absolutamente necesario usar envolturas de cuarzo ventiladas. Además, es importante evitar el contacto directo de la superficie de la lámpara con el fluido a tratar. Debido a la alta temperatura del plasma dentro de este tipo de lámparas, el mercurio vaporizado existe en varios estados de excitación. La emisión resultanteespolicromáticayelespectroabarca longitudes de onda que van de los 250 a los 600nm.Estaslámparasnosonmuyútilespara tratamientos germicidas; sin embargo, su fuerte radiación UV resulta en una penetración profunda. Con algunas modificaciones, las lámparas de mediana presión pueden ser empleadas para el procesamiento de algunos alimentos, especialmente en procesos de oxidación y fotodegradación (Koutchma, 2009).
2.2. Otras lámparas
Se han desarrollado diversas alternativas para la generación de radiación UV, esto debido principalmente a que la eficiencia de las lámparas de mercurio de baja o mediana presión se ve afectada por la temperatura. Algunas de estas tecnologías son las lámparas UVdemicroondas ylas lámparasde pulsosde UV; sin embargo, el uso de estas lámparas en alimentos continua en investigación (Koutchma,2009).
2.2.1. Lámparas UV de microondas
Esta clase de lámpara elimina la necesidad de usar electrodos, lo cual tiene ciertas ventajas. En vez de emplear electrodos, estas lámparas utilizanlaenergíadelasmicroondasgeneradas por un magnetrón. La radiación es generada dentro de una funda de cuarzo que es llenada con un gas inerte, generalmente argón, y con mercurio. La radiación se produce cuando los átomos de mercurio que son excitados regresan de un nivel excitado a uno de menor energía.Estaslámparaspuedenserprendidas y apagadas sin producirse deterioro en ellas y además su vida útil es tres veces mayor que la de las lámparas que utilizan electrodos (Little, 2007). Actualmente, el uso de esta tecnología para la desinfección de alimentos se encuentra en investigación. Ortoneda et al. (2008) estudiaron el efecto de la radiación UV generada por las microondas sobre diferentes microorganismos. Para ello, emplearon un magnetrón que operaba a 2.45 GHz generando una máxima intensidad de radiación UV a 254 nm de 10 W/m2. Los microorganismos expuestos a la radiación UV fueron E. coli, S. aureus y B. cereus, los cuales se hicieron crecer hasta obtener una población de 105-107 UFC/mL y se colocaron a 10 cm de distancia de la lámpara, obteniéndose en todos los tratamientos cinco reducciones logarítmicas. De acuerdo con sus resultados, esta tecnología promete ser una alternativa comercial sobre todoparaeltratamientodealimentossólidos.
2.2.2. Lámparas de pulsos UV
Este tipo de lámparas generan radiación electromagnética con longitudes de onda de entre 100 y1100 nm (Green et al., 2003). Esta radiación es producida almacenando energía eléctrica en un capacitor y liberándola en forma de pulsos de intensa emisión de radiación por pocos microsegundos. La FDA hadeterminadoalgunascondicionesdelusode esta tecnología para la desinfección de superficies de algunos alimentos. Esta
organización indica que los alimentos deben recibir esta radiación por no más de 2 milisegundosylaslámparasdebengeneraruna radiación con longitudes de onda de entre 200 y1000nm(FDA,2012).
3.
Equipos UV
Para alimentos líquidos se utilizan por lo general equipos UV de sistema cerrado. En este tipo de sistemas dos cilindros coaxiales delimitanlazonapordondecirculaellíquidoa tratar. Es posible comparar este tipo de sistemas con un intercambiador de calor de doble tubo, el líquido fluye por la parte anular y la lámpara se localiza en el centro recubierta por una funda de cuarzo. El líquido que fluye por el sistema se puede recircular o tratar continuamente en la parte anular y se puede conectar más de un sistema para lograr el efecto germicida deseado. El uso de bombas concontroldevelocidaddeflujoesimportante para aplicar la dosis requerida (GuerreroBeltrán yBarbosa-Cánovas, 2004). Contar con un sistema de refrigeración, sobre todo en sistemas con lámparas de mercurio de baja presión, es vital, debido a que la temperatura del líquido puede tener un impacto sobre la energía UV de salida de la lámpara. Esto dependerá del diseño de la funda de cuarzo, entreotrosfactores(WrihgtyCairns,1998).
La aplicación principal de este tipo de equipos en alimentos es en jugos de frutas y hortalizas. Sin embargo, en estos alimentos la radiación UVC penetra a muy poca profundidad por debajo de la superficie del líquido. Además, la mayoría de estos alimentos tienen densidades y viscosidades más altas que la del agua, lo cual afecta en el diseño y las dimensiones de los equipos (Koutchma et al., 2007). Para lograr una penetración efectiva de la radiación UV en alimentos líquidos se deben tener en cuenta diversos factores como el perfil de flujo, la composición del producto, entre otros (Guerrero-BeltrányBarbosa-Cánovas,2004).
La radiación UV también es utilizada en la industria de alimentos para desinfectar superficies. Generalmente se utiliza para desinfectar las superficies de equipos que tienen contacto directo con el alimento. Adicionalmente, la radiación UVC se emplea para la desinfección de empaques como cajas, latas y botes (Guillard et al., 2010). Para la desinfección de la superficie de alimentos como frutas, verduras ycarnes, esta tecnología tiene pocas aplicaciones, debido fundamentalmente a que la radiación UVC no puedepenetrarconsiderablementelasuperficie del alimento y además, la mayoría de los estudios de la radiación UVC son en medio acuoso o en aire. Sin embargo, la FDA ha determinado algunas condiciones del uso de la radiación UVC para la desinfección de la superficiesdealgunosalimentos(FDA,2012).
3.1. Equipos UVC para alimentos sólidos
Un ejemplo de un equipo comercial de radiación UVC para la desinfección de superficies de alimentos es diseñado y producido por Reyco Systems Inc. (Meridian, Idaho).Elequipoesempleadoporlacompañía Washington Potato Co. para la elaboración de productosde papa seca ycongelada,los cuales son remanufacturados para la obtención final de sopas, botanas, entre otros. La materia prima llega a la planta generalmente mostrando crecimiento inicial de bacterias coliformes en la superficie, lo cual es indeseable para la compañía. El diseño del equipo permite procesar cerca de 14,000 libras de producto por hora, cumpliendo con las necesidadesdelosclientes.Dentrodel tambor, que es la parte principal del equipo, se encuentran instaladas 32 lámparas UVC de mercurio de baja presión que operan a 60-70 W, las cuales son fabricadas por Steril Aire Inc. (Burbank, Calif.) y emiten la radiación UVC germicida necesaria, eliminando, de acuerdo con el fabricante, 99.9% de la contaminación microbiana presente en la superficie de algunos alimentos. Para asegurar
la completa desinfección, la radiación UVC rodea completamente a las papas gracias a que eltamboresgiratorio(Reyco,2012).
Otro ejemplo de equipo UVC disponible en el mercado es el desarrollado por C&S EquipmentCo.(Chapman,2003).Puedeserde tamborrotatoriooconunabandatrasportadora quemuevealalimentoatravésdelequipopara asegurar la exposición correcta a la radiación UVC. El equipo puede tratar diversos productos frescos como frutas, carne y productos congelados. Esta compañía emplea lámparas UVC desarrolladas por Steril Aire Inc. (Burbank, Calif.), generalmente del modelo UVC Emitters™ que operan a 70-85 W, las cuales pueden ser instaladas en diferentes configuraciones, lo que facilita su manejo.
3.2. Equipos UVC para alimentos líquidos
La FDA considera el uso de radiación ultravioleta para el procesamiento de jugos, un método seguro para la reducción de patógenos y otros microorganismos, siempre y cuando se use un flujo turbulento através de los tubos de los equipos con un valor mínimo de Reynolds de 2,200 (FDA, 2012). Un flujo turbulento es necesario en el procesamiento de jugos con radiación UVC, para lograr que todo el producto reciba la misma dosis (GuerreroBeltrányBarbosa-Cánovas,2004).
Los flujos laminares en los equipos UVC son de igual manera importantes. Gran parte de las investigaciones se han iniciado con un flujolaminar yademásenalgunosequiposuna película muy delgada del líquido a tratar es necesaria para lograr una desinfección adecuada. Por ejemplo, el tratamiento de leche con radiación UVC se enfrenta con diversos problemas, principalmente los sólidos suspendidos y la grasa que afectan en la profundidad de penetración de la radiación UVC (Gang et al., 2011). Para resolver este problema se han utilizado conductos
especiales para producir películas muy delgadas o capilares, las cuales han demostrado ser efectivas para la inactivación de microorganismos en leche (Matak et al., 2005).
Debido a la gran diversidad de microorganismos, los niveles de dosis requeridos para la desinfección pueden variar de acuerdo al efecto final deseado para cada tipodealimento.Elefectodepenetracióndela radiación UVC depende de diferentes factores como el tipo de líquido,la materia suspendida, entre otros (Guerrero-Beltrán y BarbosaCánovas,2005).
3.2.1. Equipos UVC de flujo laminar
Estos equipos están diseñados para generar una película muy delgada del líquido que circula a través del equipo UVC, lo cual contribuye a eliminar los problemas debidos a la falta de penetración de la radiación. Estas películas se caracterizan por ser un flujo laminar con un perfil de velocidad parabólico (KoutchmayParisi,2004).
Un novedoso sistema UVC ha sido diseñado con un tubo de cuarzo de diámetro muypequeño con geometría helicoidal, el cual rodea a una lámpara UVC localizada en el centro del sistema. El diámetro pequeño del tubo de cuarzo ayuda a formar un vórtice secundario conocido como “vórtice de Dean”, el cual aumenta la mezcla radial del líquido laminar (Hille et al., 1985). En la Fig. 2 se observalaparteprincipal delequipo,lacuales el tubo de cuarzo de forma helicoidal. Éste rodea a una lámpara de mercurio de baja presión capaz de emitir radiación de 254 nm. Ellíquidoatrataresbombeadoconunabomba peristáltica y pasa a través del equipo con un flujo laminar. Gang et al. (2011) utilizaron este equipo para tratar leche y demostraron que el vórtice de Dean que se forma durante el tratamiento tiene un efecto positivo en la inactivación de algunos microorganismos, logrando una inactivación de seis reducciones logarítmicas, utilizando una dosis UVC de 21.3mJ/cm2 conunflujode28.8L/h.
Un equipo UVC para tratar jugo de manzana actualmente disponible en el
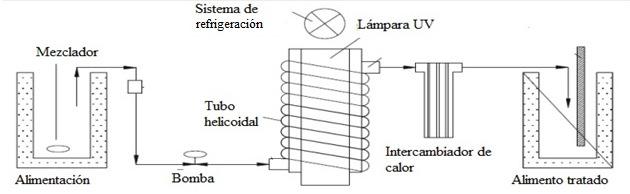
2. Diagrama de flujo del equipo UV con funda de cuarzo helicoidal. Adaptada de Gang etal. (2011).
Fig.
mercado es diseñado y construido por CiderSure (Rochester, NY). Extensas investigaciones llevadas a cabo por Worobo (2000),llevaronalacreacióndeldiseñoquese muestra en la Fig. 3. Las lámparas que se emplean son de mercurio de baja presión que operan a 125 W y se encuentran montadas en el centro del equipo con ayuda de fundas de cuarzo. Actualmente existen tres modelos, 2500, 3500 y 6500; los cuales contienen 8, 10 y 16 lámparas, respectivamente. El jugo es bombeadoatravésdelequipoycirculaentrela superficie interna del equipo y las fundas de cuarzo. El flujo másico es controlado por una computadora que permite operar el equipo de manera automática y además tiene la capacidad de detectar cualquier falla operacional como fallas de lámparas o bombas. El equipo es construido en acero inoxidable y puede procesar de 25 a 600 galones por hora, dependiendo del modelo. Una ventaja de estos equipos es su fácil instalación y montaje, lo que permite conectar unidades en serie. De acuerdo con el fabricante, los equipos construidos por la compañía cumplen con los requerimientos de la FDA y son efectivos contra diferentes microorganismos, incluido E. coli (CiderSure, 2012).
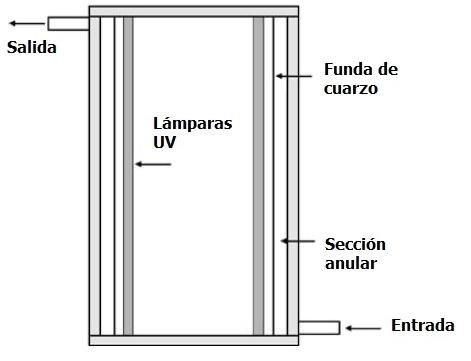
Forney et al. (2004) realizaron estudios en unequipoUVC llamado Taylor-Couette.En la Fig. 4 se observa la configuración de este equipo, donde el líquido a tratar es bombeado a través de una sección anular entre dos tubos concéntricos. En el centro del equipo se encuentra un cilindro, que rota a velocidades bajas para propiciar una mezcla uniforme del líquido dentro del equipo. Debido a los pocos milímetros de espesor de la sección anular, se genera un flujo laminar. La superficie exterior esunafundadecuarzoydoslámparasUVCse encuentran colocadas en esta superficie para proporcionar suficiente exposición de radiaciónUVCallíquidoquecirculadentrode la sección anular. Las investigaciones con este equipo han demostrado que logra de tres a cinco reducciones logarítmicas al tratar jugos de manzana y uva inoculados con E. coli utilizandounadosisUVCde9mJ/cm2 .
3.2.2. Equipos UVC de flujo turbulento
Los equipos UVC de flujo turbulento generalmente tienen la misma configuración quelosdeflujolaminar, esdecir,son cilindros concéntricos con lalámpara UVC en el centro. En la mayoría de los casos, los equipos se
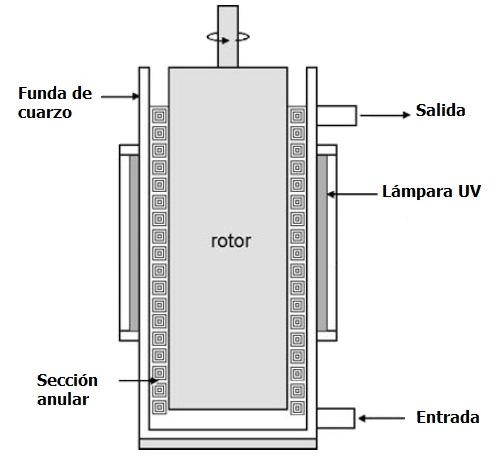
Fig. 3. Equipo UVC desarrollado por Cidersure. Adaptada de Cidersure (2012).
Fig. 4. Equipo UVC Taylor-Couette. Adaptada de Forney et al. (2004).
conectan en serie para incrementar la turbulencia, lo que proporciona una mayor homogeneidad del flujo; sin embargo, conforme la turbulencia se incrementa, las velocidades de flujo también aumentan, lo que reduceeltiempoderesidenciadellíquidoenel equipo. Para lograr una desinfección adecuada de alimentos líquidos en los equipos de flujo turbulento, se recomienda usar lámparas largas, conectar equipos en serie y/o modificar el equipo (Guerrero-Beltrán y BarbosaCánovas,2004).
Una modificación del equipo TaylorCouette de flujo laminar permite obtener flujo turbulento para el tratamiento de alimentos líquidos. La modificación principal se da en el cilindro central o rotor, el cual se puede diseñar con movimiento sinusoidal. El equipo modificado ha sido estudiado por Ye (2007) para la inactivación de E. coli en distintos jugos,obteniendobuenosresultados.
Por otro lado, Salcor, Inc. (Fallbrook, CA) ha diseñado un equipo de flujo turbulento que contiene una tubería de teflón transparente en espiral rodeada de lámparas UVC para el tratamientodejugos.EnlaFig.5semuestrael equipo, el cual está construido con acero inoxidable. Dentro del equipo se encuentran instaladas doce lámparas montadas paralelamente a la tubería de teflón. Cada par de lámparas tiene un reflector parabólico para incrementar la intensidad de la radiación. De acuerdo con el fabricante, este equipo puede monitorear la cantidad de luz UVC y presión de flujo durante el procesamiento para asegurar que el tratamiento del jugo sea satisfactorio (Guerrero-Beltrán y BarbosaCánovas,2004).
como consecuencia el desarrollo y comercialización de equipos UVC para el procesamiento de algunos alimentos líquidos y sólidos. Diversas empresas han diseñado equiposUVCparaeltratamientodealimentos, y al conocer sus características principales es posible diseñar nuevos equipos, mejorando los originales. Como una alternativa a los tratamientos térmicos tradicionales, la radiación UVC tiene un gran potencial para producir alimentos para las demandas actuales de los consumidores. Nuevas tecnologías de fuentes de radiación han aparecido, las cuales deben ser tomadas en cuenta para el diseño de nuevos equipos ysu estudio en la desinfección de alimentos. Los equipos UVC disponibles en el mercado tienen pocas aplicaciones en alimentos; sin embargo, para ampliar las aplicaciones en la industria alimentaria se requiere de mayor investigación que proporcione la información necesaria para el diseñodenuevosequipos.
Conclusiones y comentarios finales
Los avances recientes en la desinfección de alimentosconradiaciónultravioletahantenido
Agradecimientos
A la Universidad de las Américas Puebla y al Consejo Nacional de Ciencia y Tecnología (CONACyT, México) por el financiamiento paralarealizacióndeestetrabajo.
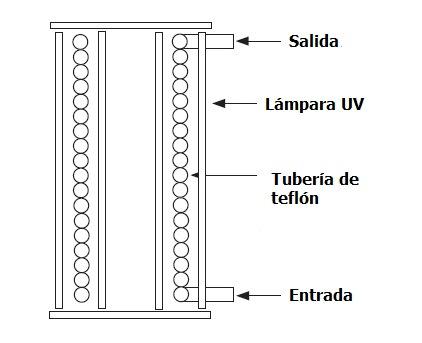
Fig. 5. Equipo UVC con tubería de teflón. Adaptada de Koutchma (2009).
Referencias
Adams, M.R. y Moss, M.O. 1995. Food Microbiology. Tercera edición. The Royal Society of Chemistry. Cambridge, UK. 447 p.
Bintsis, T., Litopoulou-Tzanetaki, E. y Robinson, R 2000. Existing and potential applications of ultraviolet light in the food industry. Journal of the Science of Food and Agriculture. 80:637-645.
Bolton, J.R. 2001. Ultraviolet Applications Handbook. Segunda edición. Bolton Photosciences, Inc. Canadá.
Chapman, S. 2003. New machines use tumbling process to decontaminate food. Food Chemical News. En http://www.agra-net.com/portal2/fcn/ accesada 11/09/2012.
CiderSure technology. 2012. Food Processing Equipment. Rochester, NY. En http://www.cidersure.com/index.html accesada 11/09/2012.
Díaz, D.M. y Serrano, O.L. 2005. Desinfección de Agua con Luz Ultravioleta. Germex S.A. de C.V. En http://www.germ-ex.com.mx/luz1.html, accesada 06/09/2012.
Farid, M., Chen, X., y Dost, Z. 2001. Ultraviolet sterilization of orange juice. Proceedings of the Eighth International Congress on Engineering and Food. J. Welti-Chanes, G.V. Barbosa-Cánovas, J.M. Aguilera, Eds. Technomic, Lancaster, Pennsylvania. pp. 1567-1572.
FDA Food and Drug Administration. 2012. CFR Title 21. Chapter 1. Part 179. Vol. 3.Irradiation in the production, processing and handling of food. En http://www.accessdata.fda.gov/scripts/cdrh/cfdocs/ accesada 10/09/2012.
FDA Food and Drug Administration. 2000. 21 CFR Part 179. Irradiation in the production, processing and handling of food. Registro federal, 65, 71056–71058.
Forney, L. J., Pierson, J.A y Ye, Z. 2004. Juice irradiation with Taylor-Couette flow: UV inactivation of Escherichia coli. Journal of Food Protection. 67: 2410–2415.
Gang, L., Chaolin, L. y Peng L. 2011. UV inactivation of milk-related microorganisms with a novel electrodeless lamp apparatus. Journal European Food Research and Technology. 233:79–87
González, C. 2001. Luz ultravioleta en la conservación de alimentos. Ambiental Socoter. En http://www.ambientalsocoter.cl/LuzUltravioletaDesi nfAguayAire.pdf, accesada 09/09/2012.
Green, S., Baskaran, N. y Swanson B.G. 2003. Highintensity light. En: P. Zeuthan y L.B. Sorenson (Eds). Food preservation techniques. Primera edición. CRC Press. Boca Raton, FL. pp. 284-301.
Guerrero-Beltrán, J.A. y Barbosa-Cánovas, G.V. 2004 Advantages and limitations on processing foods by UV light. Food Science Technology International 10(3): 137-147.
Guerrero-Beltrán, J.A. y Barbosa-Cánovas, V. 2005. Reduction of Saccharomyces cerevisiae, Escherichia coli and Listeria innocua in apple juice by ultraviolet light. Journal of Food Process Engineering. 28: 437–452.
Guillard, V., Mauricio-Iglesias, M. y Gontard, N. 2010. Effect of novel food processing. Food Science and Nutrition. 50:969–988
Hille, P., Vehrenkamp, R. y Schulz-Dubois, E. 1985. The development and structure of primary and secondary flow in a curved square duct. Journal of Fluid Mechanics. 151: 219-241.
Koutchma, T. 2009. Advances in ultraviolet light technology for non-thermal processing of liquid foods. Food and Bioprocess Technology: An International Journal. 2:138–155.
Koutchma, T., y Parisi, B. 2004. Biodosimetry of E. coli UV inactivation in model juices with regard to dose and RTD distribution in annular UV reactor. Journal of Food Science 69: 14–22.
Koutchma, T., Parisi, B. y Patazca, E. 2007. Validation of UV coiled tube reactor for fresh juices. Journal of Environmental Engineering and Science. 6(3): 319328
Little, R. 2007. An analysis of microwave generated UV devices, their track record and their potential. Poster No. 123. UV and Ozone World Congress. Los Angeles, Calif. 27-29 Agosto.
López-Malo, A. y Palou, E. 2004. Ultraviolet light and food preservation. En: M.P. Cano y M.S Tapia (Eds). Emerging Technologies for the Food Industry. Marcel Dekker, Inc., New York. pp 405421.
Martínez, D.A. 2005. Balastro electrónico mono-etapa. Tesis de licenciatura, Universidad de las Américas Puebla. México. 100 p.
Masschelein, W. J. 2002. UltravioletLlight in Water and Wastewater Sanitation. Segunda edición. Lewis Publishers. Boca Raton, FL. 192 p.
Matak, K.E., Churey, J.J., Worobo, R.W., Sumner, S.S. y Pierson, M.D. 2005. Efficacy of UV light for the reduction of Listeria monocytogenes in goat’s milk. Journal of Food Protection. 68: 2212–2216.
Mendonca, A.F. 2002. Inactivation by irradiation. En: V.K. Juneja y J.N. Sofos (Eds). Control of Foodborne Microorganisms. Marcel Dekker Inc., New York. pp. 75-103.
Ortoneda, M., Sinead, K., Cullen, D.J. y Phipps, A.D. 2008. Experimental investigations of microwave plasma UV lamp for food applications. Journal of Microwave Power and Electromagnetic Energy. 42(4): 13-23.
Phillips, R. 1983. Sources and Applications of Ultraviolet Radiation. Primera edición. Academic Press Inc. New York. 434 p.
Reyco Systems Inc. 2012. UVC light applied within the Tumbling Drum. Food Processing Equipment. En http://www.reycosystems.com/solutions/uv-drum/ accesada 11/12/2012.
Shama, G. 1999. Ultraviolet light. En: R.K. Robinson, C. Batt y P. Patel (Eds). Encyclopedia of Food Microbiology-3. Academic Press, London. pp. 22082214.
Worobo, R. W. 2000. Efficacy of the CiderSure 3500 ultraviolet light unit in apple cider. Ithaca, NY. Cornell University, Department of Food Science and Technology.
Wright, H.B. y Cairns, W.L. 1998. Desinfección de agua por medio de luz ultravioleta. Simposio OPS: Calidad del Agua: Desinfección Efectiva. Lima, Perú. 26-29 Octubre.
Ye, Z. 2007. UV disinfection between concentric cylinders. Tesis de doctorado, Instituto de Tecnología de Georgia, Atlanta. 152 p.

Temas Selectos de Ingeniería de Alimentos 6 - 2 (2012): 160 - 172

Métodos de control de crecimiento microbiano en el pan
A.A.
Salgado-Nava* y M.T. Jimenez-Munguía
Departamento de Ingeniería Química, Alimentos y Ambiental, Universidad de las Américas Puebla. Ex hacienda Sta. Catarina Mártir S/N, San Andrés Cholula, Puebla. C.P.72810. México.
Resumen
El pan como producto industrial, debe conservar su inocuidad por periodos de tiempo considerables, ya que debido a sus características físico-químicas es un alimento susceptible al deterioro por hongos y bacterias afectando así la salud del consumidor además de provocar pérdidas económicas a nivel industrial, por lo que debe tratarse bajo ciertos métodos de control de crecimiento microbiano. Se han llevado a cabo diversas investigaciones enfocadas a la inhibición del crecimiento microbiano en el pan, utilizando técnicas y tecnologías distintas a la adición de aditivos convencionales, en respuesta a la creciente demanda por parte del consumidor de los llamados “alimentos mínimamente procesados” (AMP) o con la menor cantidad de aditivos añadidos. El objetivo del presente artículo es hacer una recopilación de información acerca de los principales métodos de control de crecimiento microbiano propuestos actualmente, entre los que destacan atmósferas modificadas (usadas conjuntamente con absorbedores de oxígeno), la aplicación de ondas del espectro electromagnético y los antimicrobianos naturales tales como los aceites esenciales y las bacterias acido-lácticas (BAL). Se ha comprobado que tales métodos son más efectivos cuando son usados conjuntamente.
Palabras clave: deterioro, microorganismos, pan, control de crecimiento microbiano.
Abstract
The bread as an industrial product must retain its safety for considerable periods of time; due to their physicochemical characteristics it is susceptible of food spoilage by fungi and bacteria and it may affect the health of consumers as well as causing economic losses to the industry level. if not treated with a control method microbial growth, Several researches have been focused to the inhibition of microbial growth in the bread, using different technologies and techniques of conventional additives, in response to the increasing consumer demand for so-called "minimally processed foods" (AMP) or with the least amount of additives. The aim of this article is to gather information on the main control hurdle technologies proposed microbial growth, among which modified atmospheres (used in conjunction with oxygen scavengers), the application of the electromagnetic spectrum waves and natural antimicrobial such as essential oils and lactic acid bacteria. It has been found that such methods are most effective in combination.
Keywords: spoiled, microorganisms, bread, controlling microbial growth.
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: aida.salgadona@udlap.mx
Introducción
Elpanessindudaunalimentoqueformaparte de la dieta de las personas alrededor del mundo sin importar su condición social; ya que en su forma más básica se elabora con harina, agua, sal, azúcar y levadura. Desde el punto de vista tecnológico, es un alimento muy complejo, ya que la velocidad con la que se presentan cambios físico-químicos en su estructura es muy rápida. El principal problema del pan es la pérdida de humedad de la miga (endurecimiento), ablandamiento de la corteza y cambio en su sabor, dichos fenómenos son conocidos como “envejecimiento”, causado fundamentalmente por la retrogradación del almidón (Badui, 2006). Además, debido a sus características físico-químicas el pan es susceptible de ser deteriorado por hongos (mohos y levaduras) y bacterias. Si bien, el horneado es una etapa en donde se eliminan tanto mohos como levaduras, una vez que el producto ha salido del horno, su manipulación debe de ser bajo condiciones estériles, ya que la contaminación por mohos se produce a través del aire (Stanley et al., 2007). Se ha observado que los microrganismos que comúnmente causan deterioroenel pansonlosgéneros: Penicillum sppy Aspergillus spp (Moore et al., 2008); por otro lado, las bacterias tienen la capacidad de sobrevivir al horneado (Pepe et al., 2003; Ribotta y Tadini, 2009) incrementando el riesgo de causar daños en la salud del consumidor.
Desde hace ya varios años, se han llevado a cabo diversas investigaciones para poder asegurar la inocuidad del pan utilizando diversas tecnologías diferentes a la adición de conservadores convencionales, debido a la creciente demanda por la producción y consumodelosAMP.Se haprobadoel uso de antimicrobianos naturales como los aceites esenciales de especias y plantas (López et al., 2000; Nielsen y Rios, 2000; Suhr y Nielsen, 2003; Portillo et al., 2008; Sahan, 2011), así
como también la bioconservación a partir de los metabolitos producidos por microorganismos como son las BAL (Adams, 1999; Lavermicocca et al., 2000; Magunson et al., 2003; Sjögren et al., 2003; Hassan y Bullerman, 2008). Otras tecnologías emergentes son las atmósferas modificadas (Vermeiren et al., 1999; Fernández, 2000). y las ondas del espectro electromagnético (Datta y Davidson, 2000; Guan et al., 2003; Lakins et al.,2008;SperberyDoyle,2009).
Adicionalmente, estas tecnologías se aplican en combinación con factores de inhibición para producir un efecto sinérgico (tecnología de obstáculos o barreras) yobtener mejores resultados en la inhibición de microorganismos contaminantes. Es por ello que el objetivo del presente artículo es hacer una recopilación de información acerca de los principales métodos de control de crecimiento microbiano en el pan que han propuesto diversosinvestigadoresenlasúltimasdécadas.
Revisión bibliográfica
1. Generalidades del pan
El pan es un alimento que se consume desde tiempos muy remotos, actualmente, forma partedeladietatradicionaldemuchoshogares en casi todo el mundo, cada región le ha conferido características muy particulares. En Medio Oriente se elabora el pan pita (pan plano); en los países al este de Europa se acostumbra el pan de centeno con un sabor ligeramente ácido; en otras partes del mundo, el pan ácimo (pan sin levar) es el más común; la baguette de origen francés, con su muy particular corteza crujiente es mundialmente conocidayconsumida,entreotros.
La NMX-F-516-1992, define al pan como un producto alimenticio cocido por horneo de la masa previamente fermentada, elaborada a
partir de harina de trigo, agua, sal, azúcar y levadura principalmente. Generalmente en la elaboracióndepanseemplealaharinadetrigo debido a las propiedades de sus componentes, destacando así de otros cereales como el centeno, maíz, cebada yarroz. En panificación seutilizanlasharinasdenominadas“duras”,ya que poseen un alto contenido de proteínas y juegan un papel importante en la formación de la masa panaria; estas proteínas a su vez están constituidas principalmente por gluteninas y gliadinas, quienes junto con el agua, los lípidos, y mediante un proceso de amasado, forman el llamado gluten, responsable de las propiedades de cohesividad y viscoelasticidad de la masa; de esta forma, el carácter del pan depende principalmente de la formación de la red tridimencional, la cual permite retener el gas producido por la fermentación de las levaduras, confiriéndole de esta forma la texturaalpan.
El agua es un componente muy importante en la formulación del pan y su principal función radica en la hidratación de las proteínas y la formación del gluten. A su vez, la presencia de agua en la mezcla ayuda a hidratar los gránulos de almidón presentes en la harina, produciendo la gelatinización de estos gránulos durante el horneado (Badui, 2006).
La levadura que se utiliza en panadería es Saccharomyces cerevisiae, la cual produce dióxido de carbono (CO2) y algunos subproductos. La principal ventaja de la adición de levaduras a una formulación panaria radica enlacontribucióndeunsabor y aromaúnicos(Cauvain,2001).
La sal y la sacarosa también son indispensables en una formulación de pan, ya que además de conferirle sabor a la masa presentan otras propiedades funcionales, ya que la sal incrementa la fuerza del gluten, permite controlar la velocidad de fermentación debido a que retarda las reacciones generadas
por la levadura, sin embargo, un exceso de sal puede provocar que el gluten pierda la capacidad de ser elástico y/o que la fermentación se detenga por completo. Se recomienda utilizar este ingrediente en un porcentaje de 1.75 a 2.25% (Giannou et al., 2003).Lasacarosaseañadeconlafinalidadde que sea el sustrato de las levaduras durante la fermentaciónyayudaaldesarrollodelcoloren la corteza; adicionalmente, los azúcares actúan como agentes antiapelmazantes y como agentes antienvejecimiento, ya que contribuyen a la inhibición de la cristalización delalmidón(Giannou et al., 2003).
2. Deterioro microbiano del pan
En general, el pan es un producto que se deteriorarápidamente yaquepresentacambios en el sabor, pérdida de humedad de la miga y endurecimiento. Adicionalmente, los microorganismos pueden crecer en el pan, representando otro factor de deterioro decisivo en la vida útil de este alimento (Stanley et al., 2007; Ribotta y Tadini, 2009). Las principales alteraciones microbiológicas son causadas por mohos y bacterias, teniendo una menor persistencia las provocadas por levaduras. A continuación se describen las particularidades de las alteraciones provocadas por microorganismos.
2.1 Deterioro por mohos
Debido a sus características, el pan es susceptible a la germinación de mohos. Una vez queel panhasalido del horno, el riesgo se incrementa si no es manipulado bajo condiciones estrictamente asépticas, ya que el aire es el medio por el cual las esporas de mohos llegan a él (Stanley et al., 2007). Su crecimiento depende de la temperatura, la concentración de oxígeno (son aerobios estrictos) en el empaque y la contaminación del pan previa al empacado (Guynot et al., 2003; Nobile et al., 2003). Es por ello que se debe de poner especial atención mientras es
enfriado, rebanado, envasado y almacenado. El proceso de deterioro se acelera si el pan es guardado dentro de un recipiente cerrado y todavía no está completamente frío (después de salir del horno), debido al vapor que se genera aumentando la humedad del ambiente enelqueseencuentra(Stanley et al., 2007).
El deterioro que causan los mohos se conoce como “enmohecimiento”, y se manifiesta con la aparición de manchas contrastantes en la superficie del pan. Los mohos que suelen encontrarse en el pan son por lo general varias especies de los géneros Aspergillus, Penicillum, Rhizopus (Sahan, 2011) Cladosporium, Fusarium (Tarar et al., 2010), Mucor y Eurotium; de ellos, los géneros más comunes presentes en el enmohecimiento son Penicillium y Aspergillus (Moore et al., 2008).
El crecimiento de Penicillium es predominante, debido a su abundante produccióndeesporasyasuelevadapresencia en el ambiente; la temperatura adecuada para su proliferación es a temperaturas bajas de 7 a 10 ºC, mientras que la de Aspergillus y Eurotium es a temperaturas de 22 a 24 ºC, de esta forma, la prevalencia de Penicillium se reduce, aumentando así la persistencia de los otros dos géneros mencionados (Gorcmen y Sahin,1997).
Dentro del género Penicillum se han encontrado las especies P. commune, P. crustosum, P. brevicompactum, P. chrysogenum (Nielsen y Rios, 2000; Moore et al., 2008), siendo P. roqueforti la especie más importante dentro de este género, caracterizada por producir esporas de coloración verdosa (Jay, 2000); además, es más resistente que otras especies en condiciones adversas, ya que es capaz de crecer en un pH de 4 en presencia de propionatodecalcio(Ryan et al., 2008).
Las especies de Aspergillus que se han encontrado son: A. flavus, A. versicolor y A. sydowii (Nielsen y Rios, 2000). La especie más importante causante de deterioro dentro del género es A. niger la cual, produce esporas de diferentes colores que van desde verde hasta negro, en algunos casos produce un pigmento amarillo que se difunde en la superficiedelpan(Jay,2000).
2.2 Deterioro por bacterias y levaduras
Las bacterias son microorganismos que se han encontrado en la materia prima del pan (harina, azúcar y levaduras). Pattison et al. (2004) señalan que el crecimiento de bacterias en el pan es favorecido por climas cálidos (2530°C)yhúmedos40a60%.
A diferencia de los mohos y levaduras, el principal problema con las bacterias es que tienen la capacidad de sobrevivir al horneado, ya que al centro de la miga no se alcanzan los 100 °C y las esporas llegan a germinar durante el almacenamiento si encuentran las condiciones adecuadas (Pepe et al., 2003; RibottayTadini,2009).
El deterioro que causan las bacterias en el pan se conoce como “hilado”. El hilado, comienza con el desarrollo de un desagradable olor dulce afrutado, seguido por una degradaciónenzimáticadelamiga(debidoala producción de amilasas yproteasas), la cual se convierte en suave y pegajosa con cambios en elcolordelamisma(Pepe et al., 2003).
Las bacterias causantes del hilado son del género Bacillus spp. como B. subtilis (principalmente), B. licheniformis, B. cereus, B. firmus, B. pumilus, B. clausii (Pepe et al., 2003) y B. amyloliquefaciens (Valerio et al., 2012).
Por su parte, las levaduras implicadas en el
deterioro del pan son de dos tipos: las filamentosas y las fermentativas. Las primeras son las más comunes, presentan un crecimiento visible en la superficie del pan (manchas que pueden ser blancas, cremas o rosas),porloquetambiénsonconocidascomo “mohos tizosos” (su alteración es muy parecida a la producida por mohos, por lo que suelen causar confusión) yafectan a productos de alta actividad de agua. Las segundas ocasionan un deterioro fermentativo manifestado por una producción irregular de alcohol y/o de gases y afectan a productos con una baja actividad de agua, como el pudding denavidad(RibotayTadini,2009).
Las levaduras que causan deterioro en pan son: Saccharornycopsis fibuligera, Candida guilliermondii, Hansenula anomala, Debaromyces hansenii, Candida parapsilosis, Serratia marcescens, Endomyces fibuliger Zygosaccharomyces rouxii, y Pichia burtonii (Stanley et al., 2007).
De ellas, se ha divulgado más ampliamente el deterioro que causan las especies S. marcescens, E. fibuliger Z. rouxii, y P. burtonii como se menciona a continuación. En panificación, la especie S. marcescens causa el deterioro conocido como “pan rojo” debido a que este microorganismo tiene pigmentos rojos brillantes. E. fibuliger ocasiona que el pan tenga una apariencia de yeso en la superficie, debido a la generación de manchas blancas producidas por el microorganismo (Jay, 2000). Existen reportes de que P. burtonii es más resistente a conservadores que otros microorganismos deteriorativos (Stanley et al., 2007).
Enrepostería,la especie Z. rouxii al seruna levadura osmotolerante, causa deterioro en productos con alto contenido de azúcar (RibotayTadini,2009).
3. Métodos para la prevención del crecimiento microbiano en pan
El método tradicional de prevención del crecimiento de microorganismos en el pan ha sido la adición de antimicrobianos sintéticos en la formulación; sin embargo, desde hace algunas décadas se han estado implementando diversas técnicas y tecnologías diferentes ésta, debido a problemas de resistencia microbiana. Aunado a lo anterior, la creciente tendencia a la producción y consumo de los AMP ha llevado a combinar ciertos factores de conservación para lograr una sinergia entre ellos yasíobtenermayorestabilidad ycalidad sensorial en el producto durante el almacenamiento. A esta técnica se le conoce como“tecnologíadeobstáculosodebarreras”. Los obstáculos comúnmente usados en la preservación de alimentos son la temperatura (alta o baja), la actividad de agua (aw), la acidez (pH), el potencial redox (Eh), los conservadores sintéticos, los microorganismos competitivos asi como sus metabolitos; métodos no térmicos como los pulsos electricos,ondasdel aspectoelectromagnético; además de las atmósferas modificadas o controladas, altas presiones, entre otros. (Leistner,2000)
A continuación se hace una revisión de los métodos utilizados para la prevención del crecimientomicrobianoenpan.
3.1 Uso de antimicrobianos
Las características que debe presentar un buen antimicrobiano son: poseer un amplio espectro de acción, no ser tóxico, ser efectivo a bajas concentraciones,noafectarlacalidadsensorial de los productos (olor y sabor), poseer una buena solubilidad, conservar su estabilidad en las condiciones de proceso y durante el almacenamiento, no intervenir en los procesos
fermentativos y ser de bajo costo (Ribotta y Tadini,2009).
3.1.1 Convencionales
Entre los conservadores sintéticos más usados en el pan se encuentran: el ácido sórbico ysus sales (sorbatos), el ácido propiónico y sus sales(propionatos)ylosparabenos.
Los propionatos son los más adecuados en panificación debido a que su actividad sobre las levaduras es mínima, permitiendo así una buena fermentación de la masa; específicamente, ellos inhiben el crecimiento de bacterias y mohos. De los propionatos, destacan dos tipos: el propionato de sodio y el propionato de calcio; ambos tienen la misma actividad, sin embargo, cuando en la formulación también hay carbonatos o bicarbonatos, se recomienda la utilización del propionato de sodio, porque el propionato de calcio interfiere con la producción de dióxido de carbono. La concentración permitida es de 0.3% dentro de la formulación (Badui, 2006; Stanley et al., 2007).
Respecto al ácido sórbico, éste no sólo inhibe la actividad de los mohos, sino que también la de las levaduras, por lo tanto, no debe añadirse a la masa. Su adición se realiza una vez que el pan ha sido horneado por aspersión sobre la superficie del producto. Otro inconveniente es que no resulta efectivo para inhibir el desarrollo de mohos en productos porosos o con superficies irregulares, la cantidad permitida en una formulación de pan es del 1 a 6% en solución acuosa (asperjado en la superficie inmediatamente después del horneado). Se debe de considerar que la actividad antimicrobiana del ácido sórbico aumenta a medida que disminuye el pH (Ribotta y Tadini,2009).
Los parabenos son ésteres alquílicos del ácido p-hidroxilbenzoico, sus formas más comunes
son metil y propilparabenos. Son menos utilizados en la industria de la panificación debido a que son más efectivos contra mohos y levaduras que contra bacterias. Se usan en concentraciones de 0.01 a 0.1 g/100g (Chung et al., 2001).
3.1.2 Naturales
3.1.2.1
Aceites esenciales
Las propiedades antimicrobianas de hierbas y especias han sido reconocidas y usadas desde la antigüedad (Conner, 1993); recientemente ha vuelto a surgir interés en la preservación “natural” de alimentos a partir de la tendencia haciaelconsumoyproduccióndelosAMP.
Diversas investigaciones han reportado el efecto antifúngico de fuentes naturales como son especias, hierbas, plantas o microorganismos. Entre las especias con sustancias activas destacan el tomillo, laurel, orégano, canela, clavo y ajo, debido a su amplio espectro contra microorganismos patógenos ydeteriorativos (López et al., 2000; NielsenyRios,2000;Sahan,2011).
Las sustancias activas de los aceites esenciales son de diversos tipos, compuestos como el timol, eugenol, aldehídos, cetonas, alcoholes y otros hidrocarburos presentan alta actividad antimicrobiana debido a sus grupos fenólicos (Dorman y Deans, 2000; Özcan y Boyraz, 2000). En la Tabla I se enlistan los principales compuestos activos identificados por Cromatografía de gases acoplada a espectrometría de masas (GC-MS) encontrados en el aceite esencial de algunas plantas yespecias (Suhr yNielsen, 2003). Una de las sustancias que se ha demostrado que posee gran actividad antifúngica es el alil isotiocianato presente en el aceite esencial de mostaza (contiene de un 90 a 95% de la sustancia activa), ya que evita cualquier proliferación de mohos (Nielsen y Rios, 2000; Suhr y Nielsen, 2003; Sikes et al., 2005).
Tabla I. Principales compuestos activos de aceites esenciales de plantas y especies obtenidos por GC-Ms.
Aceite esencialPrincipales componentes
Contenido (%)
Laurel α-Pineno 8 a 42
D-Limoneno 2
Linalol 2 a 33
Carvicol 23 a 78
Eugenol 31 a 88
CanelaCinamaldehído 1 a 88
Eugenol 71 a 92
Benzil-benzoato 5 a 53
ClavoCariofileno 4 a 65
Eugenol 52 a 84
Hierba limónD-Limoneno 3 a 14
Gerianol 4 a 20
Geranial (citral a) 31 a 93
Neral (citral b) 45 a 99
MostazaAlil isotiocinato 99 a 100
Naranja β-Mirceno 2 a24
D-Limoneno 68 a 95
Linalol 0 a 33
Salvia α-Pireno 11 a 85
D-Limoneno 10 a 30
Eucaliptol 24 a 93
Alcanfor 22 a 53
TomilloTimol 52 a 89
Carvacol 3 a 54
Romero α-Pireno 17
Adaptado de Suhr y Nielsen (2003).
Eucaliptol 18 a 59
La selección del antimicrobiano natural así como la dosis del mismo dependerán de la naturaleza del alimento con el que interactuará, por lo que se tienen que considerar sus características sensoriales (sabor yolor),composición,pH yaw (López et al., 2000).
Existen diversos métodos para la aplicación de los compuestos activos de los aceites esenciales; ellos se pueden adicionar directamente al alimento o crear una microatmósfera conteniendo el aceite esencial en fase gas (Nielsen y Rios, 2000; Portillo et al., 2008).
Sehareportadoqueelefectoantifúngicode los aceites esenciales depende del método de aplicación, los compuestos fenólicos como el timol y el eugenol (de tomillo, canela y clavo) muestran mejores resultados si son adicionados directamente a los alimentos, mientras que el citral y el alil isotiocianato (hierba de limón y mostaza, respectivamente) son mas efectivos cuando son aplicados como extractosvolátiles (SuhryNielsen,2003).
La efectividad antifúngica de los aceites esenciales ha sido probada en pan. En un estudio llevado a cabo por Sikes et al. (2005) se comprobó la efectividad del aceite esencial de mostaza en el control del crecimiento microbiano en pan; la aplicación del aceite esencial fue en fase gas y la dosis recomendadaporlosautoresesde200ppm.
Algunos investigadores han optado por combinar ciertos factores de conservación; así, Nielsen y Rios (2000) utilizaron la tecnología de los envases activos en combinación con los extractos volátiles de aceites esenciales de diversasespeciastalescomocanela,ajo,clavo, vainilla, orégano y mostaza sobre pan recién horneado. Probaron dosis en un rango de 1.8 a 3.5 µg/mldecadaunadelassustanciasactivas en P. commune, P. roqueforti, A. flavus y E. fibuliger, en donde el aceite esencial de mostaza fue el mejor inhibidor de crecimiento microbiano, requiriendo concentraciones menores respecto de las demás especias. Portillo et al. (2008) probaron el efecto sinérgico del aceite esencial de orégano mexicano (Lippia berlandieri) en combinación con la disminución de la actividad de agua del pan para inhibir el crecimiento de tres mohos: Rhizopus, Penicillium y Aspergillus; de esta forma, ellos lograron obtener mejores resultados, ya que extendieron su vida útil considerablemente. Las concentraciones recomendadas fueron 100,150y200ppm.
3.1.2.2 Biopreservación
En años recientes, se ha presentado un creciente interés en la biopreservación de alimentos. Diversas investigaciones señalan que algunos de los metabolitos que producen ciertos microorganismos presentan actividad antimicrobiana, como ocurre con la nisina, pediocina y otras bacteriocinas como la pimaricina, subtilina y natamicina (Saranraj y Gueetha, 2011); de ellos destacan las BAL ya que han sido la forma más común de conservación, a partir de ellas se han transformado gran cantidad de alimentos graciasalafermentación.
Las BAL son de particular interés, ya que son capaces de producir diferentes tipos de moléculas bioactivas, tales como ácidos orgánicos, ácidos grasos, peróxido de hidrógeno, diacetil, reuterina, dióxido de carbono y bacteriocinas capaces de inhibir la microbiota indeseable, al mismo tiempo le confieren al alimento características de “flavor”muysingulares.Las incluyengéneros como Lactococcus, Streptococcus, Lactobacillus, Pediococcus, Leuconostoc, Enterococcus Canobacterium, Aerococcus, Oenococcus, Tetragenococcus, Vagococcus y Weisella (Adams, 1999). Se han llevado a cabo investigaciones que confirman la actividad antimicrobiana de dichas bacterias (Adams, 1999; Lavermicocca et al., 2000; Magunson et al., 2003; Sjögren et al., 2003; HassanyBullerman,2008).
En panificiación, es una práctica común adicionar BAL a la masa madre para asi asegurar su estabilidad desde el comienzo hasta el final del proceso. Algunas bacterias como Lactobacillus sakei KTU05-6 resiste tratamientos térmicos hasta de 100 ºC durante un periodo de 60 minutos (Digaitiene et al., 2012); además, se ha observado que ellos presentan un efecto sinérgico con el
propionato de calcio (PC) en la inhibición del crecimientomicrobianoindeseable.Ryan et al. (2008) determinaron el efecto antifúngico de Lactobacillus plantarum en la masa madre del pan y lograron inhibir el crecimiento de A. niger, Fusarium culmorum y P. expansum; sin embargo, el crecimiento de P. roqueforti no se vió afectado. Por lo tanto, hicieron una combinación de bacterias ácido lácticas y PC; asi consiguieron un efecto sinérgico sobre P. roqueforti, ya que el PC, por sí solo (en concentraciones de 3000 ppm) no detuvo el crecimiento del moho mencionado. En otro estudio, Gerez et al. (2009) analizaron 95 especies de bacterias, encontrado que cuatro de ellas presentaban actividad antimicrobiana: L. plantarum CRL 778, Lactobacillus reuteri CRL 1100 y dos subespecies de Lactobacillus brevis (CRL 772 y CRL 796). Los compuestos activos de estas bacterias son ácidos orgánicos como el láctico, acético, propiónico y el fenilacético. Dichos investigadoresestudiaronsuaplicaciónenpan, adicionando las bacterias en la masa madre. Los resultados revelaron su efectividad como inhibidoresdecrecimientomicrobiano,aunque obtuvieron mejores resultados si las combinaban con PC, pudiendo reducir la dosis del conservador sintético utilizada habitualmente en panificación hasta en un 50%.
3.2.
Atmósferas modificadas
El envasado con atmósfera modificada consiste en introducir el alimento en una película de alta barrera en la que ha sido modificado el ambiente gaseoso para disminuir la velocidad de respiración del alimento, el crecimiento microbiano y retardar el deterioro así enzimático,conel propósitode alargar la vida útil del producto. Generalmente, los gases que se utilizan son dióxido de carbono (CO2) y nitrógeno (N2) disminuyendo el porcentaje de oxígeno (O2) (Galic et al., 2009).
El dióxido de carbono es el gas más importante en el envasado bajo atmósferas modificadas, ya que presenta propiedades bacteriostáticas y fungistáticas. Se ha reportadoqueaconcentracionesbajas(5-10%) del gas se puede evitar el crecimiento de mohos y bacterias. Existen factores que contribuyen a la eficacia del dióxido de carbono, uno de ellos es la eliminación completa del oxígeno de la atmósfera (Galic et al., 2009).
Ya que el oxígeno residual en envases con atmósferasmodificadasrepresentadel1al2%, y debido a que estas concentraciones permiten elcrecimientodemohos,seharecurridoaluso de una tecnología complementaria: los materiales absorbedores de oxígeno. Dichos materiales se clasifican en metálicos y no metálicos. Dentro de los metálicos, el material más utilizado son las sales ferrosas (debido a su bajo costo) las cuales reaccionan con el oxígeno para formar óxido de hierro bajo determinadas condiciones de humedad; de esta forma, se tiene un agente reductor metálico hidratado que secuestra el oxígeno dentro del envase del producto, convirtiéndolo irreversiblemente en un óxido estable. Dentro de los no metálicos se incluyen a los que usan agentes reductores orgánicos tales como el ácido ascórbico, sus sales y el catecol (Ahvenainen,2003).
El absorbedor de oxígeno se introduce al empaque y reduce el oxígeno a niveles menores al 0.01%, manteniendo el nivel por periodosprolongados(Vermeiren et al., 1999). Además, ellos no producen ningún efecto sobre la calidad sensorial del pan durante el almacenamiento (Fernández, 2000). Vermeiren et al. (1999) reportaron la efectividad de la aplicación de estas dos tecnologías en la conservación de pan, ya que lograron retardar el crecimiento microbiano delproductomásde60días.
3.3. Ondas del espectro electromagnético
Se han investigado diversos métodos para destruir la contaminación una vez que el pan ha sido horneado, dichos métodos son: radiación ultravioleta, radiación infrarroja, calentamiento por microondas y radio frecuencias. Se ha estudiado la región ultravioleta del espectro (longitudes de onda menores a 450 nm), encontrándose que son más efectivos los niveles de longitud de onda de 260 nm. Las radiaciones ultravioleta (UV) sondebajapenetración,siendoadecuadaspara tratamientos en productos de panificación, sin embargo,enrepostería,sonineficaces(Ribotta y Tadini, 2009). Mediante las ondas del espectro electomagnético se alcanzan temperaturas de hasta 70 ºC en el pan, lo cual es suficiente para destruir a la mayoría de las bacterias y mohos contaminates. La radiación UV puede penetrar empaques transparentes para destruir los mohos contaminantes sin la generación de calor, que provocan la condensación de vapor de agua en en el empaque, siendo esto una ventaja sobre otros métodos. El tratamiento es efectivo en productos suaves, con superficies regulares y consecuentemente el efecto se ve reducido en productos con características contrarias, ya que la radiación UV no puede penetrar adecuadamente(SperberyDoyle,2009).
La literatura señala que la destrucción de microorganismos mediante la aplicación de microondas es posible debido a que se daña la membrana celular de los mismos (Datta y Davidson,2000).
Diversas investigaciones se han llevado a cabo para determinar si el calor electromagnético puede ser usado para esterilizar o pasteurizar alimentos (Guan et al., 2003). Lakins et al. (2008) utilizaron microondas para inhibir el crecimiento microbiano en pan blanco, el tratamiento fue breve (10 s a 2.45 GHz y 12.2 cm de longitud de onda) y se aplicó al producto previamente
empacado. Ellos encontraron que el tratamiento con microondas mantiene el pan empacado 60 días con un mínimo crecimiento de mohos. Respecto a la calidad del pan, reportaron pérdida de humedad, la cual, no fue percibidasensorialmente.
Se han reportado tratamientos llevados a cabo con radio frecuencias (RF) en pan horneado, han logrado reducir 4 ciclos logarítmicos de esporas inoculadas de Penicillium ssp. y Aspergillus ssp. durante 10 días de almacenamiento; sin embargo, el uso del método provoca cambios en la calidad, debidoaqueenlasuperficiedelpantratadose produce una condensación de vapor de agua como resultado de la diferencia de temperaturasentreel pan yel airecircundante, ya que éste no se calienta durante el tratamiento (Liu et al., 2011). Por lo tanto, los autores combinaron el tratamiento de RF (6 kW, 27.12 MHz) con la aplicación de aire caliente convencional (58 ºC durante 1.8 min) para lograr uniformidad en el calentamiento. Ellos lograron extender la vida útil del pan por 28 días después del tratamiento, almacenandoloaunatemperaturade23ºC.
Conclusiones y comentarios finales
Actualmente, es posible obtener pan de alta calidad y seguro desde el punto de vista microbiano por largos periodos. En las últimas décadas se ha probado la eficacia de diversos métodos de control de crecimiento microbiano distintos a los conservadores convencionales. Dentro de estos métodos destacan los antimicrobianos naturales, atmósferas modificadas y absorbedores de oxígeno, así como la aplicación de ondas del espectro electromagnético y el uso de bacterias ácidolácticas. Se ha comprobado que en algunos casos, tales métodos son más efectivos utilizadosconjuntamente.
Agradecimientos
El presente artículo de revisión no podría ser posible sin el apoyo del Consejo Nacional de Ciencia y Tecnología (CONACyT) así como delaUniversidaddelasAméricasPuebla.
Además, se agradece a la Dr. María Eugenia Bárcenas Pozos, Dr. Emma Mani López,alaDr.Aída IrmaGómez Sánchez ya la Dra. María Teresa Jimenez Munguía, por su valioso apoyo en el desarrollo y revisión del presenteartículo.
agents from plants: antibacterial activity of plant volatile oils. Journal of Applied Microbiology 88:308–316.
Fernández, A, M. 2000. Review: active food packaging. Food Science and Technology International. 6:97–108.
Fujikawa, H., Ushioda, H. y Kudo, Y. 1992. Kinetics of Escherichia coli destruction by elec- tromagnetic pasteurization. Applied and Environmental Microbiology 58(3):920-924.
Galic, K., Curic, D. y Gabric, D. 2009. Shelf life of packaged bakery good. Critical Reviews in Food Science and Nutrition. 49:405-426.
Gerez, C. L., Torino, M. I., Rollán, G. y Font de Valdez, G. 2009. Prevention of bread mould spoilage by using lactic acid bacteria with antifungal properties. Food Control. 20:144-148.
Referencias
Adams, M. R. 1999. Safety of industrial lactic acid bacteria. Journal of Biotechnology. 68:171-178.
Ahvenainen, R. 2003. Novel food packaging techniques Primera edición. CRC Press LLC. EE.UU. 521 p.
Badui, D. 2006. Química de los alimentos. Cuarta edición. Pearson educación. México. 716 p.
Cauvain, S. P. 2001. Cereals processing technology. Ed. G. Owens. Primera edición. Woodhead Publising Limited. England. 238 p.
Chung, D., Papadakis, S. y Yam, K. 2001. Release of propyl paraben from a polymer coating into water and food simulating solvents for antimicrobial packaging application. Journal of Food Processing and Preservation. 25:71-87.
Conner, D. E. 1993. Naturally occurring compounds in antimicrobials in Food. Davidson, P.M. and Branen, A.L. Primera edición. New York: Marcel Dekker. 468 p.
Datta, A. K. y Davidson, P. M. 2000. Microwave and radio frequency processing. Journal of Food Science 65:32-41.
Digaitiene, A., Hansen, A. S., Juodeikiene, G., Eidukonyte, D. y Josephsen, J. 2012. Lactic acid bacteria isolated from rye sourdoughs produce bacteriocin-like inhibitory substances active against Bacillus subtilis and fungi. Journal of Applied Microbiology. 112(4):732-742.
Dorman, H. J. D. y Deans, S. G. 2000. Antimicrobial
Giannou, V., Kessoglou, V. y Tzia, C. 2003. Quality and safety characteristics of bread made from frozen dough. Food Science and Technology. 14:99-108.
Gorcmen, D. y Shanin, D. 1997. Investigations of mould in microflora of bread and similar bakery products. Advance Food Science. 19:100-103.
Guan, D., Gray, P., Kang, D. H., Tang, J., Shafer, B., Ito, K., Younce, F. y Yang, T. C. S. 2003. Microbiological validation of electromagnetic pasteurization-circulated water combination heating technology by inoculated pack studies. Journal of Food Science. 68(4):1428–32.
Guynot, M. E., Sanchis, V., Ramos, A. J. y Marín, S 2003. Mold-free shelf-life extension of bakery products by active packaging. Journal of Food Science. 68(8):2547-2552.
Hassan, Y. I. y Bullerman, L. B. 2008. Antifungal activity of Lactobacillus paracasei ssp. tolerans isolated from a sourdough bread culture. International Journal of Food Microbiology, 121:112–115.
Jay, J. M. 2000. Microbiología moderna de los alimentos. Cuarta edición. Editorial Acribia, S.A. Zaragoza. España. 790 p.
Lakins, D. G., Echeverry, A., Alvarado, C. Z., Brooks, J. C., Brashears, M. T. y Brashears, M. M. 2008. Quality of and mold growth on white enriched bread for military rations following directional microwave treatment. Journal of Food Science. 73(3):99-103.
Lavermicocca, P., Valerio, F., Evidente, A., Lazzaroni, S., Corsetti, A. y Gobetti, M. 2000. Purification and
characterization of novel antifungal compounds from the sourdough Lactobacillus plantarun strain 21B. Applied Enviromental Microbiology. 66:40844090.
Leistner, L. 2000. Basic aspects of food preservation by hurdle technology. Review. International Journal of Food Microbiology 55:181–186.
Liu, Y., Tang, J., Mao, Z., Mah. J. H., Jiao, S. y Wang, S. 2011. Quality and mold control of enriched white bread by combined radio frequency and hot air treatment. Journal of Food Engineering. 104:492–498.
López, M. A., Alzamora S. M. y Guerrero, S. 2000. Natural Antimicrobials from Plants. En Minimally Processed Fruits and Vegetables .Fundamentals and Applications. Eds. SM Alzamora, MS Tapia y A López-Malo. Gaithersburg, Maryland, An Aspen Publication. 235 p.
Magunson, J., Ström, K., Roos, S., Sjögren, J. y Schnürer, J. 2003. Broad and complex antifungal activity among environmental isolates of lactic acid bacteria. FEMS Microbiology Letters. 219: 129–135.
Moore, M. M., Dal Bello, F. y Arendt, E. K. 2008. Sourdough fermented by Lactobacillus plantarum FST 1.7 improves the quality and shelf life of gluten-free bread. European Food Research Technology. 226:1309-1316.
Nielsen, P. V. y Rios, R. 2000. Inhibition of fungal growth on bread by volatile components from spices and herbs and the possible application in active packaging with special emphasis on mustard essencial oil. International Journal of Food Microbiology. 60:219-229.
Nobile, M. A., Martoriello, T., Cavella, S., Giudici, P. y Masi, P. 2003. Shelf life extension of durum wheat bread. Journal of Food Science. 15(3):383-393.
Norma Mexicana NMX-f-516-1992. Alimentos. Productos de panificación. Clasificaciones y definiciones. Normas Mexicanas. Dirección General de Normas. México.
Özcan, M. y Boyraz, N. 2000. Antifungal properties of some herb decoctions. European Food Research and Technology. 212:86-88.
Pattison, T., Lindsay, D. y Von Holy, A. 2004. Natural antimicrobials as potential replacements for calcium propionate in bread. South African Journal of Science. 100:342-348.
Pepe, O., Blaiotta, G., Moschetti, G., Greco, T. y Villani, F. 2003. Rope-producing strains of Bacillus spp. from wheat bread and strategy for their control by lactic acid bacteria. Applied and Enviromental Microbiology. 69(4):2321-2329.
Portillo, R. M. C., Viramontes, R. S, Gastélum, F. M. G., Muñoz, C. L., Torres M. J. y Nevárez M. G. 2008. Efecto antifúngico de aceite esencial de orégano mexicano (Lippia berlandieri Shauer) sobre hongos contaminantes en productos de panadería. Tercera Reunión Nacional sobre orégano. Saltillo, Coahula, México, 24 de Agosto.
Ribotta, P. D. y Tadini, C. C. 2009. Alternativas tecnológicas para la elaboración y la conservación de productos panificados. Primera edición. Universidad Nacional de Córdoba. Argentina. 327 p.
Ryan, L. A. M., Dal Bello, F. y Arendt, E. K. 2008. The use of sourdough fermented by antifungal LAB to reduce the amount of calcium propionate in bread. International Journal of Food Microbiology 125:274-178.
Sahan, Y. 2011. Effect of Prunus laurocerasus L. (Cherry Laurel) leaf extracts on growth of bread spoilage fungi. Bulgarian Journal of Agriculture Science. 17(1)83-92.
Saranraj, P. y Gueetha, M. 2011. Microbial spoilage of bakery products and its control by preservatives. Review. International Journal of Pharmaceutical and Biological Archives. 3(1):38-48
Sikes, A., Yang, T., Richardson, M. y Ehioba, R. 2005. Antifungal activity of volatile oil of mustard (VOM). U.S. Army Research, Developtment and Engineering Command Natick Soldier Center. Massachusetts 01760-5018.
Sjögren, J., Magnusson, J., Broberg, A., Schnürer, J. y Kenne, L. 2003. Antifungal 3- hydroxy fatty acids from Lactobacillus plantarum MiLAB 14. Applied and Environmental Microbiology, 69:7554–7557.
Sperber, W. H. y Doyle, M. P. 2009. Compendium of the Microbiological Spoilage of Foods and Beverages. Primera edición. Spinger Science+Business Media. EE.UU. 367 p.
Stanley, P., Cauvain S. P. y Young, L. S. 2007. Technology of bread making. Second edition. Springer Science+Business Media. New York. E.E.U.U. 389 p.
Suhr, K. I. y Nielsen, P. V. 2003. Antigungal activity of essential oils evaluated by two different application techniques against rye bread spoilage fungi. Journal
of Applied Microbiology. 4:665-674.
Tarar, O. M., Rehman, S., Mueen-Ud-Din, G. y Murtaza, M. A. 2010. Studies on the shelf life of bread using acidulants and their salts. Turkish Journal of Biology. 34,133-138.
Valerio, F., De Bellis, P., Di Biase, M., Lonigro, S. L., Giussani, B., Visconti, A., Lavermicocca, P. y Sisto, A. 2012. Diversiy of spore-forming bacteria and identification of Bacillus amyloliquefaciens as a
species frequently associated with the ropy spoilage of bread. International Journal of Food Microbiology 156(3):278-285.
Vermeiren, L., Devlieghere, F., Van Beest, M., De Kruijf, N. y Debevere, J. 1999. Developments in the active packaging of foods. Trends of Food Science and Technology 10:77-86.

Temas Selectos de Ingeniería de Alimentos 6 - 2 (2012): 173 - 181

Polímeros utilizados para la elaboración de películas biodegradables
M. Rubio-Anaya* y J. A. Guerrero-Beltrán
Departamento de Ingeniería Química, Alimentos y Ambiental, Universidad de las Américas Puebla. Ex hacienda Sta. Catarina Mártir S/N, San Andrés Cholula, Puebla. C.P.72810. México.
Resumen
El empaque de un alimento tiene como función principal preservar y proteger al producto que contiene, para así poder extender su vida útil. El uso excesivo de empaques elaborados a partir de materiales sintéticos ha generado graves problemas ambientales, debido a su total falta de biodegradabilidad. El creciente interés en los alimentos procesados de alta calidad y menor impacto ambiental ha llevado a la industria de alimentos a buscar diversas alternativas para satisfacer las demandas del consumidor. Hoy en día, se está generando una nueva tecnología en el envasado de alimentos, que tiene como principal objetivo sustituir los materiales convencionales en materia prima obtenida a partir de fuentes renovables que sean completamente biodegradables. El objetivo de identificar los diferentes polímeros utilizados para producir empaques biodegradables.
Palabras clave: películas, biodegradable, polímeros.
Abstract
Food packaging has as main function to preserve and protect the product to extend its self-life. The excessive use of packaging prepared from synthetic materials has led to serious environmental concerns, to their total lack of biodegradability. Increasing interest in high-quality food products and reduced environmental impact has led the food industry to find alternatives to meet these demands. Nowadays, a new technology in food packaging is being generated, which seeks to replace conventional plastic packaging materials prepared from renewable sources that are completely biodegradable. The aim of this review is to identify the different polymers used to produce biodegradable packaging.
Keywords: films, biodegradable, polymers.
Introducción
El empaque de un alimento es fundamental para la conservación del mismo. Sin embargo, una vez que el alimento es consumido, el empaque se desecha y pasa a formar parte de
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: marysol.rubioaa@udlap.mx
las grandes cantidades de basura que se acumulan día a día en el planeta. Adicionalmente, la mayor parte de los materiales usados en la fabricación de empaques para alimentos son plásticos, los cuales provienen de una fuente no renovable y no son biodegradables. Por dar un ejemplo, puede mencionarse que a finales de la década pasadaenelmundoseconsumíanalrededorde
100 millones de toneladas de poliestireno, material que se utiliza para la producción de empaques y utensilios desechables (platos, vasos, entre otros) para alimentos, de las cuales el 75% se convierte en basura luego de su uso y el 95% no es reciclable (S.M.A., 2008).
Debido a lo anterior, ha surgido una creciente preocupación entre los especialistas en la conservación de alimentos, por disponer de materiales de empaque que además de proteger a los productos que contienen, permitan reducir los problemas causados por la generación y acumulación de basura. Es así comoenlasúltimasdécadasseharealizadoun número importante de estudios relacionados con el desarrollo de materiales de empaque, específicamente películas, que puedan ser ingeridos junto con el alimento que protegen (películas comestibles) o que puedan descomponerse en corto tiempo como resultado de la acción de microorganismos y/o enzimas (películas biodegradables). Las investigaciones sobre estos últimos incluyen tanto polímeros de origen natural (hidratos de carbono, proteínas, lípidos) como de origen sintético (ácido poliláctico, polihidroxi alconato). El propósito de este artículo es presentar una revisión sobre dichos polímeros, así como sobre sus propiedades como materiales para la formación de películas para empacaralimentos.
Sin la existencia de los empaques sería casi imposible que la mayoría de los productos fabricados por las industrias procesadoras de alimentos fueran distribuidos y comercializados, debido a que éstos estarían expuestos a un gran número de factores que causarían su deterioro. Los efectos logrados al aplicar tratamientos a los alimentos frescos con el fin de preservarlos, estarían seriamente comprometidos si los productos obtenidos no fueron empacados. De aquí que la función principal de los empaques sea proteger a los productos. La protección que los empaques deben proporcionar a los alimentos depende principalmente de la naturaleza de éstos últimos.Lamayoríadelosalimentosnecesitan proteccióncontralacontaminaciónmicrobiana posterior al tratamiento de conservación, el daño causado por insectos y roedores, y el daño mecánico provocado por golpes, caídas y vibraciones. Muchos requieren protección contra la ganancia y/o pérdida de agua, y algunos otros deben ser protegidos del contacto con el oxígeno, la luz y las radiaciones ultravioleta, debido a que contienen compuestos susceptibles a estos factores. Otra función básica de un empaque es contener al alimento en porciones definidas y apropiadas para su venta. Además, el empaque sirve como medio para proporcionar al consumidor información sobre el producto (cantidad, ingredientes, valor nutricional, instrucciones para el almacenamiento y el consumo,entreotras)yparapromoverlo.
Revisión bibliográfica
1. Aspectos generales de los empaques
Se define empaque como aquel material que cubre todas las funciones que corresponden a envolver, contener y proteger los productos para su transporte, venta y consumo (Coles et al., 2003).
Debidoaquelosempaquestienenmúltiples funciones ya que son usados para envasar una gran diversidad de alimentos, sus características y propiedades son muy variadas. Los materiales usados para fabricarlos son tan distintos como papel, cartón, plásticos, vidrio, hojalata, aluminio y combinaciones de los mismos. En cuanto a su forma, se encuentran como cajas, latas, bolsas, frascos, películas, entre otros. Estas últimas se
definen como matrices continuas, delgadas, que se estructuran alrededor del alimento que protegen (García et. al., 2002). La mayoría de las películas usadas comercialmente están fabricadas con distintos tipos de plásticos, los cuales además de ser obtenidos a partir de hidrocarburos, presentan la desventaja de no ser biodegradables. Por esto y con el fin de reducirlosvolúmenesde basurageneradospor los empaques de alimentos, recientemente se han llevado a cabo estudios encaminados a producir películas usando materiales biodegradables.
2. Películas biodegradables
Un empaque biodegradable está definido por la ASTM como aquel que es capaz de descomponerse en bióxido de carbono, metano, agua, compuestos inorgánicos o biomasa, siendo el mecanismo dominante de descomposición la acción enzimática de los microorganismos y que los productos resultantes puedan ser obtenidos y medidos en un periodo determinado de tiempo (ASTM, 2005).
Existen dos tipos de biodegradación, la aerobia y la anaerobia. La biodegradación aerobia ocurre en presencia de oxígeno; los productos resultantes de este proceso de degradación son biomasas, dióxido de carbono, agua y compuestos inorgánicos. La biodegradación anaerobia no necesita oxígeno y los productos resultantes son biomasas, metano,metabolitosintermedios ycompuestos inorgánicos. El grado de biodegradación del empaque va a depender de las condiciones ambientales tales como temperatura, humedad, presión parcial del oxígeno, composición de la flora microbiana y pH del suelo (Kyrikou y Briassoulis,2007).
Los materiales utilizados para la elaboración de empaques biodegradables pueden ser polímeros de origen natural (proteínas, almidón, lípidos, quitosano, entre
otros) o de origen sintético (polihidroxialcanoatos y ácido poliláctico ) (Tharanathan,2003).
2.1 Polímeros de origen natural
Entrelospolímerosdeorigennaturalqueestán siendo utilizados para la elaboración de películas biodegradables se encuentran proteínas como colágeno, queratina, gelatina, gluten de maíz, gluten de trigo, proteínas de leche, proteínas de soya, entre otras; polisacáridos como almidón, derivados de celulosa, quitosano, alginato, carragenatos, pectinas, entre otras; y lípidos como ceras, ácidos grasos y moniglicéridos (Tang et al., 2012).
2.1.1 Hidratos de carbono
Almidón. Este polisacárido ha sido considerado durante muchos años como un polímero con alto potencial para formar películas biodegradables, debido a que es un material de alta disponibilidad, bajo costo, renovable y biodegradable (Stagner et al., 2012). Se usa en la fabricación de empaques en distintos niveles, ya que puede combinarse conplásticosenpequeñascantidadesconelfin de incrementar el grado de biodegradación de éstos o emplearse para fabricar empaques con muy altos contenidos de almidón. Los llamados “almidones plastificados” presentan propiedades mecánicas similares a las de los plásticos convencionales y son generalmente resistentes a las grasas y los alcoholes; sin embargo, son degradados cuando se exponen al agua caliente. Las propiedades de estos materialespuedenservariadas,modificando el contenido de almidón y otros materiales. Son completamente biodegradables y composteables y pueden reemplazar a los plásticos tradicionales en los empaques para alimentos. Usualmente su componente básico es el almidón de maíz (40 – 60%) y el resto son aditivos que mejoran la funcionalidad y otros materiales biodegradables. Cuando los
almidones plastificados son colocados en ambientes biológicamente activos, como compostas y sistemas de tratamiento de aguas de deshecho, presentan características de degradación similares a las hojas, cortezas y papel. Entre los procesos usados para la formación del almidón plastificado están la extrusión, el termoformado, el soplado y el moldeadoporinyección(Flieger et al., 2003).
Otro tipo de bioplásticos a base de almidón son los llamados “almidones termoplásticos”, los cuales contienen una alta concentración de este polisacárido (aproximadamente 90%). Éstos son estables en aceites y grasas; sin embargo, dependiendo del tipo pueden cambiar de estables a inestables en agua caliente o fría. También dependiendo del tipo, pueden ser degradados completamente en 5 días en sistemas acuosos y en 45 días en compostascontroladas (Flieger et al., 2003).
Además de los anteriores, existe un bioplástico con un contenido de almidón del 100% conocido como “espuma de almidón”. Es un material antiestático, aislante y amortiguador, completamente biodegradable y composteable, que puede sustituir a la espuma de poliestireno como material de empaque biodegradable o puede ser comprimido en láminas para productos de paredes delgadas, tales como charolas, platos desechables, entre otros. Las pruebas de composta confirman su degradación en pocas semanas sin acumulaciónderesiduos(Tiefenbacher,1993).
Celulosa. Este polisacárido es el biopolímero más abundante en la naturaleza. Es el constituyenteprincipal delasparedescelulares de las plantas y más de la mitad del carbono orgánico del planeta se encuentra en la celulosa. En comparación con el almidón, la celulosa es relativamente resistente a la biodegradación. Lednická et al. (2000) evaluaron más de 70 cepas bacterianas, organizadasentresgrupos, Cellulomonas spp., Cellvibrio spp. y Pseudomonas spp., para la
degradación de fibras de celulosa. Estas bacterias degradaron fibras de algodón y lino rápidamente, causando pérdidas de peso de entre el 40% y el 86% en 13 días. La degradación anaerobia de celulosa es mucho más lenta que la aerobia. Clarkson y Xiao (2000) publicaron los resultados de la bioconversión anaerobia de papel de prensa y papel de oficina, la cual fue casi completa a los 20 días, pero se completó después de aproximadamente165días.
Una categoría muy importante pero poco explotada de materiales a base de celulosa, es la que condujo a algunos de los primeros productos poliméricos industriales tales como el celuloide y el celofán. Esta categoría todavía ofrece nuevas posibilidades para materialespoliméricos(Simon et al., 1998)
Por otro lado cuando se incrusta celulosa natural conteniendo fibras en matrices poliméricas biodegradables, se obtiene una nueva generación de materiales fibrosos reforzados conocidos como “biocompuestos” (Herrmann et al., 1998). Mientras los polímeros tradicionales consisten de componentesmuyestables,loscualessonmuy difíciles de descomponer, los biocompuestos están totalmente hechos con materiales provenientes de fuentes biológicamente renovables. Esto ofrece posibilidades adicionales de eliminación conveniente después del final del tiempo de vida, es decir, biodegradación, composteo o combustión neutral a dióxido de carbono (Riedel yNickel, 2001).
Otra material derivado de la celulosa es el acetato de celulosa, el cual es un material termoplástico amorfo, translúcido, que pertenece a la familia de los ésteres de celulosa. Es obtenido introduciendo grupos acetilo en la celulosa (como algodón o fibras de madera) para producir un material plástico duro. Es especialmente adecuado para películas inflamables y otras aplicaciones de
recubrimiento que requieren alto punto de fusión, dureza, claridad y buena resistencia a las radiaciones ultravioleta, los químicos, los aceites y las grasas (Edgar et al., 2001). Con respecto a la biodegradación de los acetatos de celulosa, Buchanan et al. (1993) llevaron a cabo un estudio acerca de la biodegradación aeróbica de estos materiales en el que se demostró que las fibras y películas de acetato decelulosasonpotencialmentebiodegradables y que la velocidad de biodegradación puede ser controlada por el grado de acetilación. Las películas de monoacetato de celulosa requirieron de 10 a 12 días para una degradación extensiva; el 80% de las películas de diacetato de celulosa evaluadas se degradaron en 4 – 5 días; en cambio las películas preparadas con triacetato de celulosa permanecieron sin cambios después de 28 días. Por otro lado, Gartiser et al. (1998) compararon varios métodos para la determinación de la biodegradabilidad anaeróbica de acetatos de celulosas y demostraron que pueden ser degradados a metano.
Quitosano. Este material se obtiene mediante un proceso de desacetilación química o enzimática de la quitina, la cual es un polisacárido compuesto de N-acetil-Dglucosamina, que después de la celulosa, es el polisacárido más abundante en la naturaleza. Su producción industrial se basa principalmente en el tratamiento de los caparazones de crustáceos como camarones, langostas y cangrejos, los cuales se obtienen como desecho de las plantas procesadoras de estas especies (Avérous y Pollet, 2012). Se ha demostrado que bajo condiciones aeróbicas en ambientes acuosos, la quitina se degrada a CO2 en unos cuantos días (el 30% se degrada despuésdeundía)(Boyer,1994).
El quitosano es un material con alto potencial para la elaboración de películas y materiales de empaque, ya que además de ser biodegradable, no es tóxico y tiene
propiedades antimicrobianas que le permiten inhibir una amplia variedad de bacterias (Aider, 2010). Las películas elaboradas con este material son transparentes, cuentan con buenas propiedades mecánicas y presentan baja permeabilidad al O2 y CO2. Su principal inconveniente es que son altamente permeables al vapor de agua; sin embargo, esta dificultad puede minimizarse incorporando algunos aditivos (Avérous y Pollet,2012).
Alginatos. Estos polisacáridos se obtienen de diferentes especies de algas y forman geles cuando se les adiciona calcio. Estos geles se usan para elaborar películas y recubrimientos para alimentos, los cuales tienen buenas propiedades de barrera frente al oxígeno y los lípidos(Tang et al., 2012).
2.1.2 Proteínas
En su estado nativo, las proteínas pueden presentar dos tipos de arreglos estructurales: la fibrilar y el globular. Las proteínas fibrilares se caracterizan por ser insolubles en agua y son los constituyentes estructurales de los tejidos animales; están unidas a través de enlaces de hidrógeno, formando fibras. Por su parte, las proteínas globulares son solubles en agua y forman arreglos esféricos complejos; entre ellas se encuentran el gluten de trigo, la proteínadesoya,laproteínadel suerodeleche ylacaseína (Flieger et al., 2003).
Esta última proteína presenta características físicas interesantes para la elaboración de películas y recubrimientos comestibles, tales como solubilidad en agua y capacidad para actuar como emulgentes. El caseinato de sodio es altamente soluble, se dispersa rápidamente en mezclas acuosas, se homogeniza en presencia de grasa o aceite y forma fácilmente películas a partir de soluciones acuosas debido a su naturaleza espiral aleatoria ysu capacidad para formar enlaces de hidrógeno. Las películas de caseinato presentan alta
resistencia a la desnaturalización química y a la coagulación, lo que significa que se mantienen estables en un amplio intervalo de valores de pH, temperatura yconcentración de sal. Además, son menos permeables al oxígeno que las películas elaboradas a partir de polisacáridos. Sin embargo, debido a su carácter hidrófilo presentan una resistencia limitada a la transmisión de agua (Khwaldia, 2010).
Otro sistema proteico utilizado para formar películas es el gluten de trigo, el cual es una alternativa interesante debido a que presenta buenas propiedades de barrera a los gases y una naturaleza relativamente hidrófoba en comparación con otros polímeros naturales (Pallos et al., 2006).
La proteína de soya es otra de las proteínas globulares utilizadas para la formación de películas. En ella pueden distinguirse cuatro fracciones (2S, 7S, 11S y 15S) de acuerdo a las velocidades de sedimentación relativa (Gennadios et al., 1994). Las fracciones principales son la 7S (conglicinina) y la 11S (glicinina); ambas sonproteínasestrechamente plegadas. El grado de enlaces cruzados disulfuro de la conglicinina es limitado debido a que sólo hay dos o tres grupos cisteína por molécula; en cambio la glicinina contiene veinte enlaces disulfuro intramoleculares. Tanto el medio alcalino como el calentamiento, causan la disociación y el subsecuente desdoblamiento de la glicinina debido a la ruptura de los enlaces disulfuro (Kinsella yPhillips, 1979). Existen dos formas para elaborar películas biodegradables basadas en proteína de soya: a partir de leche de soya caliente o de soluciones de aislado de proteína desoya(GennadiosyWeller,1992).
2.1.3
Lípidos
Otro grupo de materiales que se utilizan para la elaboración de películas biodegradables son los lípidos. Los compuestos de naturaleza
lipídica usados como recubrimientos son: monoglicéridos acetilados, ceras naturales y surfactantes. Las sustancias lipídicas más efectivas son las ceras de parafina y la cera producida por las abejas. La principal función de las cubiertas lipídicas es obstruir el transporte de humedad, debido a su baja polaridad. Por el contrario, la hidrofobicidad característica de los lípidos da lugar a la formación de películas gruesas y frágiles. Consecuentemente las películas elaboradas a base de lípidos deben combinarse con proteínas o derivados de celulosa (Debeauford et. al., 1993). Generalmente, la permeabilidad al vapor de agua disminuye cuando la concentración de los materiales hidrofóbicos incrementa. Laspelículasabasedelípidosson a menudo soportadas sobre una matriz polimérica, usualmente un polisacárido que le proporciona fuerza mecánica (Bourtoom, 2008).
Ceras. Son los compuestos comestibles más eficientes para ser usados como barrera a la humedad. Además, sirven como barrera para losgasesymejoranlaaparienciasuperficialde varios alimentos. Si se aplican como una capa gruesa, como en los quesos, deben ser removidas antes de su consumo; cuando se aplican como capas delgadas, como en las frutas y vegetales crudos, son consideradas comestibles. Entre las ceras utilizadas en alimentosestán:ladeabeja,ladecarnauba(un exudado de las hojas de palma, Copoernica cerifera)yladecandelilla (Bourtoom,2008).
Acetoglicérido. La acetilación del glicerol monoesterato mediante su reacción con anhídrido acético, produce 1-estearodiacetina. Este monoglicérido acetilado presenta la característica particular de solidificarse del estado fundido a un sólido ceroso flexible (Feurge et. al., 1953). Muchos lípidos en el estado sólido pueden estirarse 102% de su longitud original antes de fracturarse. Sin embargo, el glicerol monoesterato acetilado, puede estirarse hasta el 800% de su longitud
original. La principal desventaja de estas películas es que su permeabilidad al vapor de agua es mucho menor que la de las películas de polisacáridos. A pesar de esto, han sido usadas en cubiertas de pollo y carne para retardar la perdida de humedad durante el almacenamiento(KesteryFennema,1986).
2.2 Polímeros de origen sintético
Los polímeros de origen sintético biodegradables, son resultado de la fermentación de polímeros primarios (celulosa, almidón, proteína, pectina, entre otros), utilizados como sustratos por diferentes microorganismos, obteniendo diferentes productos finales tales como el ácido poliláctico (PLA), polihidroxialcanoatos (PHA),entreotros(Robertson,2010).
Ácido poliláctico (PLA). Es un polímero biodegradable derivado de ácido láctico; es un material altamente versátil que se caracteriza por ser termoplástico, biodegradable y composteable; se produce a partir de recursos renovables y presenta propiedades mecánicas, térmicas y de barrera comparables a las de polímeros sintéticos de amplio uso como el poliestireno y el polietilen tereftalato. Se obtiene de cualquier material con alto contenidodealmidónoazúcares(porejemplo: maíz, caña de azúcar, papa, entre otros), el cual sirve de sustrato a bacterias productoras de ácido láctico. La conversión del ácido láctico a su dímero deshidratado (láctido), se lleva a cabo por el proceso de polimerización siempre y cuando se utilice el adecuado catalizador,dandocomoresultadounapelícula resistente que se usa para la elaboración de empaques para alimentos (Petnamsin et al., 2000). Este tipo de polímero posee características similares a las que tienen el PET (Tereftalato de Polietileno), es un material permanente e inodoro, claro y
brillante, resistente a la humedad y a las grasas. La fuerza extensible y la elasticidad que presenta es también comparable al polietileno, pero este es más hidrofílico, presenta una densidad más baja y estable a la luzultravioleta(Tharanathan,2003).
Polihidroxi alconato (PHA). Polímero de origen microbiano producido por Pseudomonas aeruginosa. Sintetizados en los cuerpos de las bacterias alimentadas con glucosa. Son polímeros extremadamente versátiles, completamente biodegradables, cristalinos, pueden ser manipuladas para proporcionar una amplia gama de propiedades mecánicas y de barrera, en algunos casos, que coinciden con el rendimiento de termoplásticos de ingeniería. Pueden ser degradados con una hidrólisis simple, sin requerir enzimas que la catalicen (Flieger et al., 2003; Tohyama et al., 2002). La producción industrial de PHA, se realiza extrayendo el polímeroapartirdelasbacterias mediante la optimización de las condiciones de la fermentación microbiana de glucosa. En la década de 1980, Imperial Chemical Industries desarrollo poli (3-hidroxibutiratoco-3-hidroxivalerato) obtenido por fermentación que fue nombrado "Biopol". Actualmente se encuentra disponible en el mercado bajo el nombre de "Biopol" y distribuido en los EE.UU. por Monsanto y Metabolix(Rudnik,2008).
Otro polímero producido por la fermentación microbiana es el polihidroxibutirano (PHB), este presenta propiedades similares a las del polipropileno y se pueden elaborar botellas por la técnica de moldeado por soplado. La mayor desventaja que presenta este polímero es su alto costo a comparación de los plásticos convencionales. Cuanta con baja densidad y puede alcanzar la biodegradación completa (Lee et al., 2008).
Conclusiones y comentarios finales
Los avances en el desarrollo de películas biodegradables como materiales de empaque paraalimentos,permiten suponerqueacortoo mediano plazo será posible disponer de películas que puedan degradarse en poco tiempo por la acción de agentes biológicos y que además cumplan adecuadamente las funciones de protección propias de un empaque. El incremento en los proyectos de investigación orientados a optimizar la calidad de estas películas y los procesos para su elaboración,serádeterminanteparael logro de estameta.
Buchanan C. Gardner R. y Komarek R. 1993. Aerobic biodegradation of cellulose acetato. Journal of Applied Polymer Science. 47: 1709 – 1719.
Clarkson W. y Xiao W. 2000. Bench-scale anaerobic bioconversion of newsprint and office paper. Water Science Technology. 41: 93 – 100.
Coles R, McDowell D. y Kirwan M. 2003. Food packaging technology. Blackwell Publishing. EE.UU. pp 346.
Debeaufort F, Martin-Polo M. y Voilley A. 1993. Polarity homogeneity and structure affect water vapor permeability of model edible films. Journal of Food Science. 58: 426-434.
Edgar K. Buchanan C, Debenham J, Rundquist P, Sieler B, Shelton M. y Tindall D. 2001. Advance in cellulose ester performance and application. Progress in Polymer Science. 26: 1605 – 1688.
Agradecimientos
El presente artículo de revisión no podría ser posible sin el apoyo del Consejo Nacional de Ciencia y Tecnología (CONACyT), por la otorgación del financiamiento a través del proyectodebecasparaestudiosdeposgrado.
Feurge R, Vicknair E. y Lovegren N. 1953. Modification of vegetable oils. XIII. Some additional; properties of acetostearin products. Journal of the American Oil Chemistry Society 30: 283 – 291.
Flieger M, Kantorovpa M, Rezanka T. y Votruba J. 2003. Biodegradable plastics from renewable sources. Folia Microbiologica. 48(1): 27 – 44.
García M, Ferrero C, Bértola N, Martino M. y Zaritzky N. 2002. Edible coatings from cellulose derivatives to reduce oil uptake in fries products. Innovative Food Science and Emerging Technologies. 3: 391 –397.
Referencias
Aider, M. (2010). Chitosan application for active biobased fi lms production and potential in the food industry. Food Science and Technology.43, 837 –842.
ASTM D5511 – 12. 2005. Standard Test Method for determining anaerobic biodegradation of plastic materials under high-solids anaerobic-digestion conditions. EE.UU.
Averous L. y Pollet E. 2012. Polymer degradation and Stability. Biopol-2011 special issue. EE.UU. pp 1851.
Bourtoom T. 2008. Edible films and coating: characteristics and properties. International Food Research Journal. 15(3): 1 – 12.
Boyer J. 1994. Aerobic and anaerobic degradation and mineralization of C14-chitin by water column and sediment inocula of York-river-estuary. Applied Environment Microbiology. 60: 174 – 179.
Gartiser S. Wallrabenstein M. y Stiene G. 1998. Assessment of several test methods for the determination of the anaerobic biodegradability of polymers. Journal of Environment Polymer Degradation. 6: 159 – 173.
Gennadios A. y Weller C. 1992. Tensile strength increase of wheat gluten films. International Winter Meeting American Society of Agricultural Engineers. (92):15 – 18.
Gennadios A, McHugh H, Weller L. y Krochta J. 1994. Edible coating and films based on protein. En Krochta J, Balwin E. y Niperos-Carriedo, M. (Eds.). Edible Coatings and Films to Improve Food Quality Technomic Publishing. EE.UU. pp. 201-277
Herrmann A, Nickel J. y Riedel U. 1998. Construction material based upon biologically renewable resources. Polymer Degradation and Stability. 59: 251 – 261.
Kester J. y Fennema O. 1986. Edible films and coatings: A review. Food Technology 40(12): 47-59.
Khwaldia K. 2010. Water vapor barried and mechanical properties of paper-sodium caseinate and papersodium caseinate-paraffin wax films. Journal of Food Biochemistry. 34: 998 – 1013.
Kinsella J. y Phillips L. 1979. Film properties of modified proteins. In Kinsella J. y Soucie W. Food Protein. The American Oil Chemists’s Society:7899.
Kyrikou I. y Briassoulis D. 2007. Biodegradation of agricultural plastic films: a critical review. Journal of Polymer Environment. 15: 125 – 50.
Lee D, Yam K. y Piergiovanni L. 2008. Food packaging science and technology. CRC Press. EE.UU. 629.
Lednická D, Mergaert J, Cnockaert M. y Swings J. 2000. Isolation and identification of cellulotytic bacteria involved in the degradation of natural cellulosic fibres. Systematic and Applied Microbiology. 23: 292 – 299.
Pallos F, Robertson G, Pavlath A. y Orts W. 2006. Thermoformed wheat gluten biopolimers. Journal of Agriculture of Food Chemistry. 54: 349 – 352.
Petnamsin C, Termvejsayanon N. y Sriroth K. 2000. Effect of particle size on physical properties and biodegradability of cassava starch/ polymer blend. Journal of Natural Sciences 34:254-261.
Riedel U. y Nickel J. 2001. Structural materials from renewable resource. Materialwissenschaft und Werkstofftechnik. 32: 493 – 498.
Robertson G. 2010. Food Packaging and Shelf Life. CRC Press. EE.UU. 388.
Rudnik E. 2008. Compostable polymer materials Elsevier. EE.UU.
Simon J, Muller H, Koch R. y Muller V. 1998. Thermoplastic and biodegradable polymers of cellulose. Polymers Degradation Stability. 59: 107 –115.
Stagner J, Dias V. y Narayan R. 2012. Application and performance of maleated thermoplastics starch-poly (butylene adipate-co-terephthalate) blends for films. Journal of Applied Polymer Science. 126(1): 135 –142.
S.M.A. 2008. “Norma Ambiental Estatal NAESEMADES-007/2008, Criterios y especificaciones técnicas bajo las cuales se deberá realizar la separación, clasificación y valorización de los residuos en el Estado de Jalisco”. Secretaría de Medio Ambiente. México.
Tang X, Kumar P, Alavi S. y Sandeep K. 2012. Recent advances in biopolymers and biopolymer-based nanocomposite for food packaging materials. Food Science and Nutrition. 52(2): 426 – 441.
Tharanathan R. 2003. Biodegradable films and composite coatings: past, present and future. Food Science and Technology. 14:71-78
Tiefenbacher K. 1993. Starch-based foamed material: use and degradation properties. Journal of Macromolecular Science-Pure and Applied Chemistry. 30: 727 – 731.
Tohyama A, Patarinska T, Qiang Z. y Shimizuki K. 2002. Modeling of the mixed culture and periodic control for PHB production. Biochemistry Engineering Journal. 9: 1 – 17.

Temas Selectos de Ingeniería de Alimentos 6 - 2 (2012): 182 - 190

Efecto del tiempo de uso y el tipo de aceite de freído en las propiedades de nuggets de pescado
E. F. Molina-Hernández* y M. E. Sosa-Morales.
Departamento de Ingeniería Química, Alimentos y Ambiental, Universidad de las Américas Puebla. Ex hacienda Sta. Catarina Mártir S/N, San Andrés Cholula, Puebla. C.P.72810. México.
Resumen
Durante el proceso de freído discontinuo de alimentos, el aceite se calienta repetidas veces a elevadas temperaturas, lo que ocasiona degradación del aceite que puede afectar las propiedades del alimento frito. El objetivo del presente estudio fue evaluar algunas propiedades de nuggets de pescado freídos en dos mezclas de aceites, frescas y después de 12 días de uso repetido para determinar el posible efecto del tipo de aceite y del tiempo en que el aceite se ha usado. La textura y el contenido de grasa de los nuggets no fueron afectados por el tipo de aceite ni por el tiempo de uso (p>0.05). Los nuggets fritos en la mezcla 1 tuvieron valores de peróxidos y de ácidos grasos libres mayores que los nuggets fritos en la mezcla 2 (p<0.05). Como resultado del análisis sensorial, no se detectó diferencia entre nuggets debida al tipo de mezcla usada para el freído (p>0.05). El aceite se encontraba principalmente localizado en la parte externa de los nuggets. Aunque no hubo diferencia en la mayoría de los parámetros analizados, es recomendable usar la mezcla 2 para el freído repetido de nuggets de pescado, debido a menores índices de rancidez.
Palabras clave: freído, nuggets de pescado, textura, análisis sensorial, índice de peróxidos, microestructura.
Abstract
During discontinuous frying process of foods, the oil is repeatedly heated to high temperatures. This repeated heating results in oil degradation, which may affect the properties of the fried food. The aim of this study was to evaluate selected properties of fish fried nuggets in two oil blends, fresh and after 12 days of repeated use, to determine the possible effect of oil type and the time during the oil has been used. Texture and fat content of nuggets were not affected by the oil type or by the time of use (p>0.05). Fish nuggets fried in oil blend 1 had higher values of peroxide index and free fatty acids than those nuggets fried in oil blend 2 (p<0.05). As a result of sensory analysis, no difference was detected between fish nuggets due to the oil blend used for frying (p>0.05). The oil was mainly located in outer part of fish nuggets. In spite, there was no difference in most of the evaluated parameters, it is recommended to employ the blend 2 for repeated frying of fish nuggets, due to lower rancidity index.
Keywords: fried, fish nuggets, texture, sensory analysis, peroxide index, microstructure.
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 1231471, fax: +52 222 229 2727
Dirección electrónica: erika.molinahz@udlap.mx
Introducción
Actualmente, el consumo de grasas degradadas químicamente está causando una gran preocupación en la población, debido a los efectos negativos que pueden ocasionar en la salud humana. Varias enfermedades han sido vinculadas con la ingesta de productos de degradación de aceites a elevadas temperaturas, como la arteriosclerosis y las enfermedades articulares inflamatorias, entre otras(Grootweld et al.,2001).
El uso repetido de los aceites puede afectar sutiempodevidao bien, alosalimentosfritos en ellos, desarrollando así rancidez oxidativa, polimerización y reacciones de degradación térmica junto con cambios en sus propiedades físicas, químicas, nutricionales y sensoriales, tanto en el aceite como en el alimento. La intensidad de estas reacciones dependen del tratamiento, de la duración, del medio de freído ydel tipo de alimento utilizado (Manral et al.,2008).
El freído por inmersión es uno de los procesos de producción de alimentos más empleados, en donde el alimento se sumerge en aceite caliente a temperaturas entre 150 y 200C con el propósito de ser cocido (Manral et al., 2008; Farinu y Baik, 2005). Es un proceso rápido, conveniente y eficiente en cuanto al método de cocción y al incremento de la palatabilidad, debido a la presencia de grasa. Los productos fritos poseen una corteza crujiente, color dorado, así como sabores y oloresagradables(FarhooshyMoosavi,2009).
Cuando se fríen alimentos con alto contenido de grasa como en el caso del pescado, estas grasas migran al medio de freído,portanto,agregan otrostiposdeaceites y el problema de degradación puede ser mayor, ya que cualquier aceite de pescado con una gran cantidad de ácidos grasos insaturados dará como resultado una rápida oxidación del aceite(Rossell,1998).
Existen pocos estudios en los que se han evaluado el efecto del uso repetido de aceites
de freído en los alimentos producidos. Andrikopoulos et al. (2002) frieron papas (8 lotes de 10 g) en diferentes aceites: aceite de oliva virgen, grasa vegetal y aceite de girasol, a las cuales se evaluó el contenido de peróxidos, viscosidad, valor de p-anisidina y suefectoenelcontenidodegrasaenlaspapas. El efecto del freído en la composición y propiedades nutricionales del pescado fue estudiado por Ansorena et al. (2010) quienes determinaron que la intensidad de los cambios sedebióa lanaturalezadelagrasao aceite ya la manipulación del alimento. En el caso de nuggets de pollo ypara papas a la francesa, se han hecho estudios con dos tipos de aceites de freído, uno con oleína de palma y otro con oleína de palma/canola 50:50 sin encontrar efectos en los contenidos de grasa y de humedad del alimento, pero sí en la textura debido al tipo de aceite usado (EnríquezFernández et al., 2011). Recientemente, Romano et al. (2012) extrajeron la grasa de papas a la francesa freídas en superoleína y en aceite de oliva, y analizaron algunos índices químicos para evaluar el nivel de oxidación y relacionarlo al desempeño de los aceites estudiados. Sin embargo, no hay reportes de estudios sobre el efecto del uso repetido del aceiteennuggetsdepescado.
La ingesta del pescado es altamente recomendada por su composición, en la que resalta el buen nivel de proteína y sus ácidos grasos, principalmente del tipo omega 3 (Ansorena et al., 2010). Los nuggets de pescado fritos son una buena opción en la dieta, siempre y cuando se asegure un buen procesodeproducción.
Por lo tanto, el objetivo de esta investigación fue evaluar diversas propiedades físicas, químicas, fisicoquímicas y sensoriales de nuggets de pescado freídos en dos mezclas de aceites, frescas ydespués de 12 días de uso repetido, para determinar el posible efecto del tipo de aceite y del tiempo de uso en dichas propiedades.
Materiales y métodos
1. Materiales
El estudio se llevó a cabo con dos mezclas de aceites: mezcla 1 (oleína de palma y aceite de canola) y mezcla 2 (oleína de palma y aceite de canola con alto contenido de ácido oleico), las cuales fueron suministradas por la empresa AarhusKarlshamn (AAK, Morelia, Mich.). Ambas mezclas contenían 200 ppm de TBHQ (ter-butilhidroquinona) como antioxidante. Los nuggets de pescado congelados (Fisher Boy, Portsmouth, New Hampshire, EE.UU.) fueron comprados en un establecimiento comercialenlaciudaddePuebla,México.
2. Procedimiento de freído
El proceso de freído por inmersión se llevó a cabo empleando una freidora eléctrica doméstica (modelo ODF550, Oster, Florida, EE.UU). La freidora fue llenada con 2.9 L de la mezcla de aceites fresca. Un lote consistió en freír 80 g de nuggets de pescado a 180˚C durante 2.5 min, el lote se escurrió durante 1 min. El estudio consistió en freír 30 lotes diariamente durante 12 días. Antes de iniciar un nuevo ciclo de freído por día, la freidora fue rellenada con la mezcla de aceite fresca para así completar el mismo volumen inicial (2.9L).Estametodologíafueseleccionadacon elfindereplicarlascondicionesconlasquese fríe habitualmente en establecimientos de comidarápida.
3. Métodos de análisis en nuggets de pescado
Los análisis se aplicaron en los nuggets de pescado fritos en ambas mezclas de aceites (1 y2)frescasydespuésde12díasdefreído.
3.1 Determinación del contenido de grasa
El contenido de grasa fue determinado por duplicado mediante el método 991.36 de la AOAC (1995), por extracción con equipo
Soxhlet durante 6 h y empleando éter de petróleocomosolvente.
3.2. Determinación de peróxidos
El índice de peróxidos fue determinado por duplicado,segúnlaNormaMexicana NMX-F154-1987. Se pesó 1 g de nugget adicionando 1 g de KI, 30 mL de una solución de ácido acético glacial-cloroformo 3:2 v/v, dejando en baño de agua caliente durante 1 min. Después se adicionaron 0.5 mL de una solución de KI al 5% y 30 mL de agua caliente dejando reposar durante 1 min y se agregaron 2.5 mL de una solución de almidón al 2%. Por último, se tituló con una solución de tiosulfato de sodio 0.01 N. El resultado se expresó como meq/kg.
3.3. Determinación de ácidos grasos libres
El contenido de ácidos grasos libres fue determinado de acuerdo a la técnica 940.28 de la AOAC (2000). Se pesaron 5g de nuggets y seadicionaron50mLdealcoholisopropílicoy fenolftaleína como indicador. Posteriormente se llevó a cabo una titulación con NaOH al 0.1N hasta observar un vire de color rosa característico. La determinación fue realizada porduplicado.
3.4. Observación de la microestructura
La microestructura en nuggets de pescado fue observada mediante un microscopio electrónico de barrido (JSM-5600LV, JEOL Ltd., Akishima, Japón), con un voltaje acelerado de 20 kV (Martínez-Ávila et al., 2010). En el microscopio se observó tanto la parteinternacomolacortezadelosnuggetsde pescado fritos en cada una de las mezclas de aceites. Para las observaciones de la parte externa, se obtuvo un corte delgado de la corteza de las muestras con un bisturí. Para las observaciones de la parte interna, se realizó un corte longitudinal a un ángulo de 45° y posteriormente, se cortó una lámina delgada
del centrodeunadelasmitades.Estasláminas y los cortes pequeños de la corteza fueron cubiertos con oro-paladio empleando un recubridor (Denton Vacuum Desk V, Moorestown, Nueva Jersey, Estados Unidos), aunespesorde200Å.
3.5. Medición de la textura
La textura de las muestras se determinó mediante un texturómetro TA.XT2 (Stable MicroSystems, Reino Unido) en modo manual. De acuerdo a lo establecido por Martínez-Ávila et al. (2010), se midió la fuerza máxima en la corteza de un nugget completo (1.64 ± 0.11 cm de espesor), utilizando una aguja de 1/8´´ a una velocidad de 1mm/s hasta penetrar 5 mm del espesor del producto. La textura se midió en 10 diferentes piezasdenuggets.
4. Análisis sensorial
El análisis sensorial se determinó mediante una prueba triangular con 18 jueces no entrenados (De la Fuente-Salcido et al., 2001). Cada juez probó 3 nuggets de pescado fritos, dos nuggets fueron freídos en la mezcla 1 fresca yun tercero que fue freído en la mezcla 2 fresca. A los jueces se les proporcionó agua para enjuagarse la boca entre muestra y muestra, y los datos de aciertos obtenidos fueron contados ycomparados con el de tablas a un nivel de confianza del 95% (Larmond, 1982).
5. Análisis estadístico
Los resultados fueron analizados mediante análisis de varianza (ANOVA), empleando el software Minitab Release versión 14 (Minitab
Inc., Pennsylvania, EE.UU.) con un nivel de confianzadel95%.
Resultados y discusión
1. Contenido de grasa y microestructura de nuggets de pescado
En la Tabla I se muestra el contenido de grasa en los nuggets de pescado fritos en ambas mezclas de aceites, sin diferencia significativa (p>0.05)entrelosdatos degrasadebidaaltipo de aceite, ni por el tiempo de uso. Los valores estuvieron en el rango de 20.68+2.81% a 29.44+1.89%. Estos valores son similares a lo reportado por Ansorena et al. (2010), quienes cuantificaron un contenido de grasa de 26.17+0.29% para salmón crudo, 28.74+0.98% para salmón frito en aceite de oliva extra virgen y 24.14+0.36% para salmón fritoenaceitedegirasol.
Tabla I. Contenido de grasa en nuggets de pescado fritos en dos mezclas de aceites.
Contenido de grasa (%)
Día Mezcla 1 Mezcla 2
0 29.44+1.89a 20.68+2.81a
12 23.99+0.37a 22.30+0.34a
Medias con la misma letra indican que no hay diferencia estadísticamente significativa entre ellas (p>0.05)
En nuestro estudio se comprobó que el aceite se encontraba principalmente localizado en la parte externa de los nuggets fritos, independientemente del tiempo de freído o del tipo de grasa usada (Fig. 1 y 2). Esta
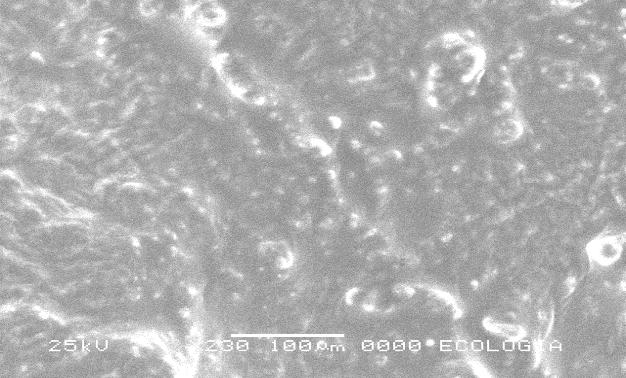
(a)
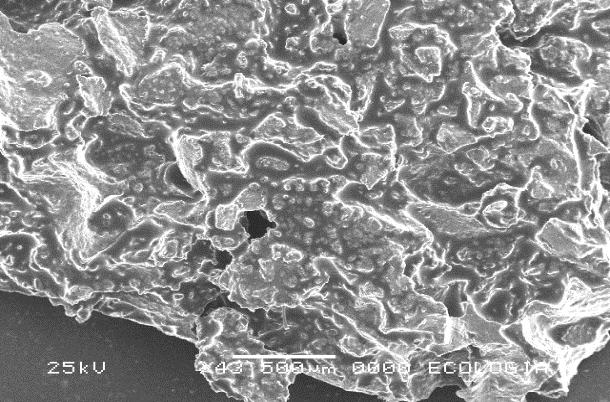
(c)

(b)

(d)
Fig. 1. Parte interna (a) y externa (b) al día 0 y parte interna (c) y externa (d) al día 12 de freído de nuggets de pescado en la mezcla 1 Las flechas indican mayor presencia de grasa en la corteza.
conclusión fue basada en que en las microfotografías, las regiones con grasa se distinguen como zonas lisas y brillantesmientras que la estructura de zonas magras luce con rugosidades y con superficie menos lisa. Esta observación fue reportada por Pedreschi et al. (2008), quienes verificaron mayorpresenciadegrasaenlacostraqueenel centro de las papas fritas usando microscopía electrónicadebarrido.
2. Textura
La textura juega un rol muy importante en las propiedades sensoriales del consumidor, ya que debido a esta propiedad, los consumidores aceptan o no algún producto frito. La Tabla II
presenta los resultados obtenidos de textura en los nuggets de pescado fritos a los 0 y 12 días de freído en ambas mezclas de aceites, donde no hubo diferencia (p>0.5) en la textura de los nuggets de pescado frito por el tiempo de uso, ni su efecto por el tipo de mezcla sobre la textura de los nuggets fritos. Esto se debe a la alta desviación estándar obtenida en algunas
Tabla II. Textura de nuggets de pescado fritos en dos mezclas de aceites.
DíaMezcla 1Mezcla 2 0 1.98+0.06a 1.40+0.20a 122.24+0.65a 1.44+0.15a
Dias con la misma letra indican que no hay diferencia estadisticamente significativa entre ellas (p>0.05)

(e)

(g)
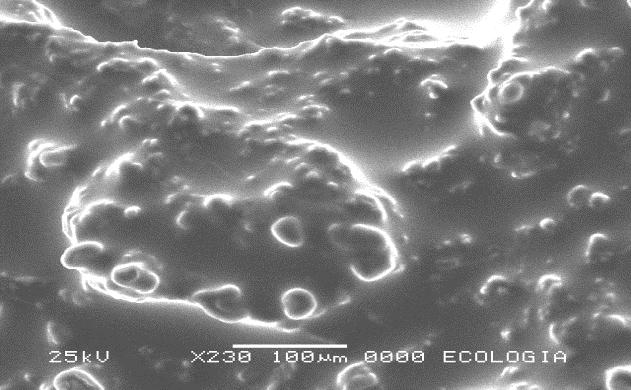
(f)

(h)
Fig. 2 Parte interna (e) y externa (f) al día 0 y parte interna (g) y externa (h) al día 12 de freído de nuggets de pescado en la mezcla 2. Las flechas indican mayor presencia de grasa en la corteza.
muestras, a pesar de que hubo 10 réplicas para la determinación. La dureza de los nuggets de pescado tuvo valores entre 0.65 y 1.98 N, menores a los reportados para nuggets de pollo, con valores entre 2 y 4.3 N, reportados porEnríquez-Fernándezetal.(2011).
3. Contenido de peróxidos y ácidos grasos libres
El índice de peróxidos es una medida de la cantidad de peróxidos formados en grasas y aceites a través de la oxidación durante el procesodefreído(Ghazali et al.,2009;Choe y Min, 2007; Pantzaris, 1998) y es el indicador de rancidez oxidativa primaria más aceptado. El índice de peróxidos de los nuggets de
pescado fritos en las mezclas frescas se muestra en la Tabla III con valores de 5.48+0.70 meq/kg para la mezcla 1 y 8.33+2.09 meq/kg para la mezcla 2. Cuando los nuggets fueron freídos en las mezclas usadas por 12 días, el valor fue de 21.25+2.15 meq/kg para la mezcla 1, significativamente diferente al inicial (p<0.05) y rebasando el límite permitido por la Norma Mexicana NMX-F-154-1987 que permite como valor máximo de peróxidos 20 meq/kg . Por otro lado, los nuggets freídos en la mezcla 2 después de 12 días de uso, tuvieron un índice de peróxidos con un valor de 4.91+0.09 meq/kg. Los peróxidos son compuestos inestables particularmente cuando son
Tabla III. Contenido de peróxidos y AGL en nuggets de pescado fritos.
DíaPeróxidos (meq/kg)AGL (%)
Mezcla 1
05.48+0.70 0.23+0.0a
12 21.25+2.15a 0.34+0.0a
Mezcla 2
08.33+2.09 0.42+0.04a
12 4.91+0.09 0.28+0.00a
Medias con la misma letra indican que no hay diferencia estadisticamente significativa entre ellas (p>0.05)
sometidos a altas temperaturas (Sunisa et al., 2011). Según lo mencionado por Badui (1999) el aumento de los peróxidos hasta que se alcanza un máximo es seguido por una descomposición en otros compuestos tales como aldehídos, cetonas y cetoácidos, la generación de estos compuestos son causantes de que los valores de peróxido disminuyan y estosotroscompuestossonprovenientesdelas degradaciones de oxidación en el freído de aceites y estos producen olores y sabores característicos de la rancidez que suelen ser desagradables.
En cuanto a los ácidos grasos libres, éstos son producidos durante una alteración hidrólitica de los aceites, la cual es fomentada principalmente por la presencia de humedad que migra del alimento (Andrikopoulos et al., 2002). La Tabla III presenta el porcentaje de ácidos grasos libres en los nuggets freídos en la mezcla 1 fresca el cual fue de 0.23+0.0%, mientras que los freídos en la mezcla fresca 2 fue de 0.42+0.04%, por lo que sí hubo efecto del tipo de mezcla de freído en los ácidos grasos libres (p<0.05). Cuando los nuggets se frieron en las mezclas usadas por 12 días, el porcentaje de los nuggets fritos en la mezcla 1 aumentó a 0.34±0.0% siendo significativamentemayorqueeldelosnuggets fritos en la mezcla fresca; los nuggets de pescado fritos en la mezcla 2 después de 12 díasdeusotuvieronunvalormenor alosdela mezcla fresca (0.28+0.0%). En este caso
(porcentaje de ácidos grasos libres), sí hubo efecto del tiempo de uso en el índice de rancidez hidrolítica de los nuggets fritos en ambas mezclas de aceites estudiadas. Sin embargo, todos los valores no excedieron el límite máximo permitido por la Norma Mexicana (2%) y por otras legislaciones internacionales(2-3%)(PaulyMittal,1996).
4. Análisis sensorial
Según la evaluación de 18 jueces no entrenados, sólo 3 acertaron en reconocer la diferencia entre los nuggets fritos con la mezcla 1 de la mezcla 2. Como el mínimo de aciertos para establecer diferencia entre muestras es 6 (Larmond, 1982), se concluye que no hubo diferencia estadísticamente significativa entre los nuggets freídos en cada una de las dos mezclas de aceites frescas (p>0.05); esto es, hubo similar percepción de los nuggets de pescado fritos tanto en la mezcla1comoenlamezcla2.
Conclusión
No hubo efecto del tipo de mezcla ni del tiempodeusodel aceite paraelfreídorepetido por 12 días sobre el contenido de grasa, distribución de aceite (observado con microestructura) y la textura de nuggets de pescado. Sin embargo, el contenido de ácidos grasoslibresydeperóxidossífueafectadopor el tipo de mezcla y el tiempo de uso. El valor de peróxidos de los nuggets freídos en la mezcla 1 excedió el límite máximo permitido por la Norma Mexicana cuando se usa esta mezcla por 12 días, por lo que se recomienda que la mezcla 2 (oleína de palma doblemente fraccionada y canola alto en ácido oleico) sea usadaparaelfreídoinclusodemanerarepetida hasta por 12 ciclos para nuggets de pescado. No hubo diferencia sensorial percibida debido al tipo de aceite en el alimento, por lo que las dos mezclas de aceite pueden ser utilizadas
para el freído de nuggets de pescado cuando estánfrescas.
Agradecimientos
Los autores agradecen el apoyo financiero del CONACyT (Consejo Nacional de Ciencia y Tecnología, México) y de la Universidad de las Américas Puebla por las becas otorgadas a Erika Florencia Molina-Hernández; así como al Sr. Tiburcio Laez del Laboratorio de Microscopía Electrónica (Instituto de Ecología, A.C., Jalapa, Veracruz, México) y a Aarhuskharlshamn,México.
Enríquez-Fernández, B.E., Álvarez de la Cadena y Yáñez, L. y Sosa-Morales, M.E. 2011. Comparison of the stability of palm olein and a palm olein/canola oil blend during deep-fat frying of chicken nuggets and French fries. International Journal of Food Science and Technology.46: 1231-1237.
Farhoosh, R. y Moosavi, S. M. R. 2009. Evaluating the performance of peroxide and conjugated diene values in monitoring quality of used frying oils. Journal of Agricultural Science and Technology. 11: 173-179.
Farinu, A. y Baik, O. D. 2005. Deep fat frying of foods transport phenomena. Food Review International 21: 389-410.
Ghazali, H. M., Tan, A., Abdulkarim, S. M. y Dzulkifly, M. H. 2009. Oxidative stability of virgin coconut oil compared with RBD palm olein in deep-fat frying of fish crackers. Journal of Food Agriculture Environment. 7(3-4):23-27.
Referencias
Andrikopoulos, N. K., Kalogeropoulos, N., Falirea, A. y Barbagianni, M. N. 2002. Performance of virgin olive oil and vegetable shortening during domestic deep-frying and pan-frying of potatoes. International Journal of Food Science and Technology. 37:177-190.
Ansorena, D., Guembe, A., Mendizábal, T. y Astiasarán, I. 2010. Effect of fish and oil nature on frying process and nutritional product quality. Journal of Food Science. 75(2):62-67.
AOAC. 1995. Official methods of analysis. Association of Official Analytical Chemists. EE.UU.
AOAC. 2000. Official methods of analysis.. Association of Official Analytical Chemists. EE.UU.
Badui, D. S. 1999. Química de los alimentos. Pearson Education. México. 268 p.
Choe E, y Min DB. 2007. Chemistry of deep-fat frying oils. Journal of Food Science. 72(5):77-86.
De la Fuente-Salcido, N. M., Meza, V. J. A. y Enríquez, M. 2001. Mejoramiento de color y textura de papa frita (chips) por pre-acondicionamiento térmico y cloruro de calcio. IX Congreso Nacional de Biotecnología y Bioingeniería, XIII Congreso Nacional de Ingeniería Bioquímica y II Congreso Internacional de Ingeniería Bioquímica, Veracruz, Ver. 10-14 de Septiembre.
Grootweld, M., Silwood, C. J. L., Addis, P., Claxson, A., Serra, B. B., y Viana, M. 2001. Health effects of oxidized heated oils. Foodservice Research International. 13(1):41-55. Citado en: Surai, P. y Fisinin, V. I. 2010. Health effects of food lipids: consequences of inadequate food processing, storage and cooking. En: “Modern dietary fat intakes in disease promotion”. Eds. DeMeester, F., Zibadi, S. y Watson, R. R. Human Press. EE.UU.
Larmond E. 1982. Laboratory methods for sensory evaluation of supply and services. Publication 1637 Department of Agriculture of Canada. Ottawa, Canadá.
Manral, M., Pandey, M. C., Jayathilakan, K., Radhakrishna, K., y Bawa, A.S. 2008. Effect of fish (Catla catla) frying on the quality characteristics of sunflower oil. Food Chemistry. 106: 634-639.
Martínez-Ávila, M., Vélez-Ruiz, J. F. y Sosa-Morales, M. E. 2010. Combination of hot drying and deep-fat frying to reduce the oil content in chicken nuggets International Journal of Food Science and Technology. 45:2101-2107.
Norma Mexicana NMX-F-154-1987. Alimentos. Aceites y grasas vegetales o animales. Determinación del índice de peróxido. Normas Mexicanas. Dirección general de normas. Disponible: http://www.colpos.mx/bancodenormas/nmexicanas/ NMX-F-154-1987.PDF. Consultado el 28 de Noviembre de 2011.
Pantzaris, T. P. 1998. Comparison of monoinsaturated and poliunsaturated oils in continuous frying. Grasas y Aceites. 49(3-4): 319-325.
Paul, S., y Mittal, G.S. 1996. Dynamics of Fat/Oil Degradation during Frying Based on Optical Properties. Journal of Food Engineering 30:389403.
Pedreschi, F., Cocio, C., Moyano, P. y Troncoso, E. 2008. Oil distribution in potato slices during frying. Journal of Food Engineering. 87:200-212.
6 – 2 (2012): 182 - 190
Romano, R., Giordano, A., Vitiello, S., Le Grottaglie, L., y Spagna Musso, S. 2012. Comparison of the frying performance of olive oil and palm superolein Jounal of Food Science. 77(5): C519-C531.
Rossell, J. B. 1998. Industrial frying process. Grasas y Aceites. 49 (3-4):282-295.
Sunisa, W., Worapong, U., Sunisa, S., Saowaluck, J. y Saowakon, W. 2011. Quality changes of chicken frying oil as affected or frying conditions. Food Research Journal. 18:615-620.

Contenido
Volumen 6 / No. 2 Ago – Dic 2012

Cuerpo editorial ………………………………………………………………………………….. i Editorial ………………………………………………………………………………………….. iii
Artículos de Revisión
Factores principales que intervienen en la estabilidad de una emulsión doble
C. E. Kosegarten-Conde* y M. T. Jiménez-Munguía ……………………..………………………..…..
Modelación del calentamiento dieléctrico (microondas y radiofrecuencia) en sistemas alimenticios modelo
N. Soto-Reyes*, R. Rojas-Laguna, M. E. Sosa-Morales ……………………………………………..…
Películas comestibles de proteína: características, propiedades y aplicaciones
C. Montalvo*, A. López-Malo y E. Palou ………………..………………………………………….…..
1
19
32 Propiedades funcionales de la jamaica (Hibiscus sabdariffa L.)
S. Cid-Ortega y J. A. Guerrero-Beltrán ………………………………………………………………… 47 Bacteriocinas: antimicrobianos naturales y su aplicación en los alimentos
S. C. Beristain-Bauza, E. Palou y A. López-Malo ……………………………………………………… 64 Radiación ultravioleta en jugos de frutas: fundamentos y aplicaciones
A. S. López-Díaz*, E. Palou y A. López-Malo ………….……………………………………………….
79 Cambios en frutas tropicales frescas, cortadas y empacadas en atmósfera modificada durante su almacenamiento en refrigeración
M. Rangel-Marrón* y A. López-Malo …………………….…………………………………………….
Películas comestibles formuladas con polisacáridos: propiedades y aplicaciones
M. F. Domínguez-Courtney* y M. T. Jiménez-Munguía
Mecanismos de inestabilidad y métodos de estabilización de emulsiones múltiples
H. A. Peredo-Luna* y M. T. Jiménez-Munguía
Quesos frescos: propiedades, métodos de determinación y factores que afectan su calidad
C. Ramírez-López* y J. F. Vélez-Ruíz
Equipos para tratamientos de alimentos con radiación UVC
O.T. Antonio-Gutiérrez*, E. Palou y A. López-Malo
Métodos de control de crecimiento microbiano en el pan
A. A. Salgado-Nava* y M. T. Jiménez-Munguía
Polímeros utilizados para la elaboración de películas biodegradables
M. Rubio-Anaya* y J. A. Guerrero-Beltrán
Artículo de Investigación
Efecto del tiempo de uso y el tipo de aceite de freído en las propiedades de nuggets de pescado
E. F. Molina-Hernández* y M. E. Sosa-Morales

Departamento de Ingeniería Química, Alimentos y Ambiental Derechos Reservados 2012
