

Temas Selectos de Ingeniería de Alimentos














Volumen 6 / No. 1
Ene –Mayo 2012
DIRECTORIO
TEMAS SELECTOS DE INGENIERÍA DE ALIMENTOS
UNIVERSIDAD DE LAS AMÉRICAS PUEBLA
PUBLICACIÓN SEMESTRAL
VOLUMEN 6, NÚMERO 1 (ENERO - MAYO 2012)
EDITORA RESPONSABLE
María Eugenia Bárcenas Pozos
CONSEJO EDITORIAL
Aída Irma Gómez Sánchez
María Teresa Jiménez Munguía
Emma Mani López
María Elena Sosa Morales
Fidel Tomás Vergara Balderas
CERTIFICADO DE RESERVA DE DERECHOS:
04-2010-080615025900-102
CERTIFICADO DE LICITUD DE TÍTULO Y CONTENIDO: 15430
DOMICILIO:

Fundación Universidad de las Américas Puebla
Exhacienda Santa Catarina Mártir S/N
San Andrés Cholula, Pue.
C.P. 72810 México
Teléfono: 222 229 2126
DISTRIBUIDO POR:
Departamento de Ingeniería Química, Alimentos y Ambiental
Fundación Universidad de las Américas Puebla
IMPRESIÓN:
Gutiérrez Mora Carina
18 Sur 6130 Local A. Col. Jardines San Manuel
Puebla, Pue. C.P. 72570

Temas Selectos de Ingeniería de Alimentos Vol. 6 / No. 1

Cuerpo editorial
Dra. María Eugenia Bárcenas Pozos
Dra. María Teresa Jiménez Munguía
Dra. Emma Mani López
Dra. Aída Gómez Sánchez
M. C. Fidel Vergara Balderas

Contenido
Temas Selectos de Ingeniería de Alimentos Vol. 6 / No. 1

Volumen 6 / No. 1 Enero – Mayo 2012
Cuerpo editorial …………………………………………………………………………………..
Artículos de Revisión
Queso Oaxaca: panorama del proceso de elaboración, características fisicoquímicas y estudios recientes de un queso típico mexicano
S. Ramírez-Nolla* y J. F. Vélez-Ruíz ……………………………………………………….. 1
Proceso de elaboración y propiedades fisicoquímicas de las leches condensada azucarada y evaporada
M. Marcelín-Rodríguez* y J. F. Vélez-Ruíz …………………………………………….… 13
Vapores de aceites esenciales: alternativa de antimicrobianos naturales
F. Reyes-Jurado*, E. Palou y A. López-Malo …………………………………………….. 29 El jitomate (Solanum lycopersicum): aporte nutrimental, enfermedades postcosecha y tecnologías para su almacenamiento en fresco
C. M. Notario-Medellín* y M. E. Sosa-Morales …………………………………………… 40
Propiedades del aceite esencial de albahaca (Ocimum basilicum L.) y sus aplicaciones en alimentos
G. A. Cardoso-Ugarte* y M. E. Sosa-Morales
Emulsiones simples y múltiples de compuestos bioactivos
B. Contreras-Reyes* y M. T. Jiménez-Munguía
Combinación de ultrasonido de baja frecuencia con factores convencionales y/o emergentes como método de inactivación de microrganismos en alimentos
54
66
A. Franco-Vega*, E. Palou y A. López-Malo ………………………………………. 73
Biopolímeros utilizados en la encapsulación
A. García-Ceja* y A. López-Malo
Cambios en las propiedades de frutas y verduras durante la deshidratación con aire caliente y su susceptibilidad al deterioro microbiano
E. M. Ceballos-Ortíz* y M. T. Jiménez-Munguía

Editorial
Temas Selectos de Ingeniería de Alimentos Vol. 6 / No. 1

El investigador actual debe estar informado y consciente del conocimiento que se genera día con día, pues sin esto su quehacer no tiene sentido. Por ello es necesario que desde su formación inicial como estudiante de posgrado desarrolle habilidades en la búsqueda de artículos y lecturas actualizadas, síntesis y comprensión de su área de investigación.
La revista “Temas Selectos en Ingeniería de Alimentos” tiene como objetivo ayudar en el desarrollo de las habilidades antes mencionadas, donde estudiantes del programa de Maestría y Doctorado en Ciencia de Alimentos realizan un ejercicio de escritura, que se concreta como un artículo de revisión. Los estudiantes inician su labor desde plantear un tema de interés que se integre con su trabajo de investigación, hacer una búsqueda bibliográfica, leer, seleccionar, estructurar y redactar una revisión. La sencilla descripción del trabajo parece minimizar el esfuerzo que estudiantes y asesores realizan; sin embargo, es una tarea que integra una de las habilidades más importantes del investigador que es conocer el estado del conocimiento en su área. En este número se presentan diversos tópicos de revisión. Cada artículo plasma lo más actual en su tema, sin dejar de lado su principio.
Como miembro del comité editorial espero que la revista siga llevando a cabo su cometido esencial que es ser una herramienta en el desarrollo de las habilidades de comunicación escrita de futuros investigadores. Aún existen retos por lograr, como mejorar su difusión y alcanzar un mayor reconocimiento, entre otros, pero esto será el resultado de trabajo continuo a largo plazo. Mientras tanto deseo que los lectores de este número encuentren en él información útil y de enriquecimiento.
Sinceramente, Emma Mani López
Miembro del Comité Editorial Departamento de Ingeniería Química, Alimentos y Ambiental Universidad de las Américas Puebla

Temas Selectos de Ingeniería de Alimentos 6 - 1 (2012): 1 - 12

Queso Oaxaca: panorama del proceso de elaboración, características fisicoquimicas y estudios recientes de un queso típico mexicano
S. Ramírez-Nolla* y J. F. Vélez-Ruiz
Departamento de Ingeniería Química, Alimentos y Ambiental, Fundación Universidad de las Américas Puebla. Exhacienda Sta. Catarina Mártir S/N, Cholula, Puebla. C.P.72810. México.
Resumen
La presente revisión incluye información sobre la definición, producción, proceso de elaboración y características fisicoquímicas y texturales del queso Oaxaca, producto de gran demanda en México con propiedades de formación de hebras y capacidad de fusión. Se analizan cada una de las etapas de fabricación del queso Oaxaca y su importancia dentro del proceso, poniendo especial interés en los procesos de coagulación y malaxado donde la cuajada adquiere características propias de este queso de pasta hilada. Se incluyen datos de las propiedades de este producto lácteo y su comercialización, mismos que son escasos. Se hace una recopilación de diversas investigaciones enfocadas al mejoramiento en el proceso de elaboración, concluyendo que aun cuando el queso Oaxaca es un producto apreciado a nivel nacional, la información sobre sus características y comercialización es muy escasa y los estudios recientes de optimización del proceso de elaboración no trascienden más allá del ámbito de la investigación.
Palabras clave: queso Oaxaca, queso de pasta hilada, características fisicoquímicas, elaboración.
Abstract
This review includes information on definition, production, manufacturing process, physicochemical and textural characteristics of Oaxaca cheese, a high-demand product in Mexico with properties of strands forming and melting capacity. It analyzes each of the manufacturing steps of Oaxaca cheese and its importance in the process, paying special attention on coagulation and malaxating processes, where curd acquires unique features of this filata cheese. It includes data on the properties of this dairy product and its marketing. It also includes a compilation of various studies aimed at improving the process, concluding that although the Oaxaca cheese is a nationally appreciated product, information on their characteristics and marketing is very scarce and recent studies of optimization process not transcend beyond the scope of investigation.
Keywords: Oaxaca cheese, filata cheese, physicochemical characteristics, manufacturing.
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: suyapa.ramirezna@udlap.mx
Introducción
El queso Oaxaca es un queso típico mexicano, que tiene una gran demanda a nivel nacional debido a su extenso uso en platillos regionales, ya que entre sus características principales cuenta con dos propiedades muy apreciadas por el consumidor, el hebrado y el fundido, lo que lo convierte en el segundo queso más consumido en la Republica Mexicana.
Su elaboración requiere de destreza y conocimiento en el control de ciertos puntos críticos, como la acidez adecuada en la leche y la cuajada, la determinación del punto de hebra y el amasado, que impactan de manera directa en las características fisicoquímicas, tecnológicas y sensoriales de este tan apetecido producto lácteo (Cervantes et al., 2006).
Dada la excesiva demanda y creciente mercado del queso Oaxaca, tanto los científicos, como el sector industrial se han dado a la tarea de reducir tiempos y costos en el proceso, así como controlar y mejorar las propiedades fisicoquímicas y sensoriales de este producto, dando como resultado una serie de investigaciones que tienen como finalidad la optimización y mejora continua de este típico queso mexicano.
El objetivo de este artículo es hacer una revisión detallada de la naturaleza del queso Oaxaca, su comercialización y sus características, haciendo énfasis en las propiedades fisicoquímicas que hacen de éste un queso tan particular; así mismo, se hace una revisión de investigaciones enfocadas en el mejoramiento del proceso de elaboración del queso Oaxaca.
Revisión bibliográfica
1. Queso
La leche y sus derivados, denominados productos lácteos, juegan un papel fundamental en la alimentación humana. Las hembras de algunos mamíferos producen leche después del nacimiento de sus crías, misma que (de algunas especies) el hombre procesa con el fin de producir leche de consumo limpia y/o transformarla en productos de larga duración como lo es el queso.
El queso es uno de los mejores alimentos de los que dispone el hombre, ya que contiene un alto valor nutritivo que se deriva de su contenido rico en grasa y proteínas, además de ser fuente de calcio y fósforo (Bernardo, 1997). Por otro lado, a nivel mundial tiene un consumo de aproximadamente 16 millones de toneladas al año (FAO, 2006). Es por esto que diferentes sectores económicos se han preocupado por el estudio de este producto lácteo de extensa variedad.
De acuerdo a la NOM-243-SSA1, un queso es un “producto elaborado de la cuajada de leche estandarizada y pasteurizada de vaca o de otras especies animales, con o sin adición de crema, obtenida de la coagulación de la caseína con cuajo, gérmenes lácticos, enzimas apropiadas, ácidos orgánicos comestibles y con o sin tratamiento ulterior, por calentamiento, drenada, prensada o no, con o sin adición de fermentos de maduración, mohos especiales, sales fundentes e ingredientes comestibles opcionales”.
El queso está compuesto básicamente por agua, grasa, proteínas (exclusivamente
caseína/paracaseína), minerales asociados con las proteínas (principalmente fosfatos y citratos de calcio) y sales que están directamente asociadas con las características fisicoquímicas de la leche. Ésta es el principal suministro en el proceso de elaboración de queso, constituyendo el 99% de la materia prima entrante total, de la cual únicamente entre el 9% y el 18% de su peso se retiene como queso y el resto sale en forma de suero. En la Tabla I se describen las características fisicoquímicas generales de la leche utilizada como materia prima para la elaboración de quesos.
Sólidos totales11-12%
Proteína2.9-3.4%
Grasa2.9-3.5%
Punto crioscópico -0.56°C
Índice de refracción37-39
de Silva (2006)
La clasificación de los quesos de acuerdo a su composición y características físicoquímicas es una tarea difícil y muchos son los criterios de selección que se han seguido (composición proximal, características de maduración, especie de procedencia de la leche, origen geográfico, aroma, sabor, etc.), obteniéndose de esta manera un gran número de clasificaciones diferentes (Scott, 1991).
Partiendo de la adición de ciertos ingredientes como fermentos, mohos especiales, sales fundentes e ingredientes comestibles opcionales, así como del tiempo de maduración, se da lugar a las diferentes variedades de quesos que de acuerdo a su proceso de elaboración se clasifican como frescos, madurados o procesados de la siguiente manera (NOM-243-SSA1-2010):
Quesos frescos, aquellos que además de cumplir con la descripción general de queso se caracterizan por su alto contenido de humedad (mayor al 45%) y por no tener corteza o tener corteza muy fina, pudiendo o no adicionarles aditivos e ingredientes opcionales. El queso Oaxaca se encuentra dentro de esta denominación.
Quesos madurados, aquellos que además de cumplir con la descripción general de queso, se caracterizan por ser de pasta dura, semidura o blanda y pueden tener o no corteza; sometidos a un proceso de maduración mediante adición de microorganismos, bajo condiciones controladas de humedad, temperatura y tiempo, para provocar en ellos cambios bioquímicos y físicos característicos del producto del que se trate, lo que permite prolongar su vida de anaquel, los cuales pueden o no requerir condiciones de refrigeración.
Quesos procesados, aquellos que además de cumplir con la descripción general de queso se caracterizan por ser elaborados con mezclas de quesos, fusión y emulsión con sales fundentes, aditivos para alimentos permitidos e ingredientes opcionales, sometidos a proceso térmico de 70°C durante 30 segundos o a cualquier otra combinación equivalente o mayor de tiempo y temperatura, lo que permite prolongar su vida de anaquel.
En la Tabla II, se ejemplifican las variedades de queso de acuerdo a su definición por la NOM-121-SSA1-1994.
Otra clasificación interesante y más completa, ya que considera varios aspectos, es la realizada por Eck (1990). En dicha clasificación se incluyen características sobre la dureza del queso, el contenido de humedad sobre materia desengrasada, el contenido graso y otras características relacionadas a su maduración (Tabla III).
Tabla I. Características fisicoquímicas de la leche.
Adaptado
TABLA II. Clasificación de quesos de acuerdo a la NOM-121-SSA1-1994
Clasificación Tipo de queso
FRESCOS
FrescalesPanela, Canasto, Sierra, Ranchero, Fresco, Blanco, Enchilado y Adobado
Pasta hilada Oaxaca, Asadero, Mozzarella, y Morral
AcidificadosCottage, Crema, Doble crema, Petit Suisse y Nuefchatel
MADURADOS
PrensadosCheddar, Chester, Chihuahua, Manchego, Brick, Edam, Gouda, Gruyere, Emmental, Provolone, Port Salut, Tilsiter, Bola y Jack
Prensados de pasta duraAñejo, Parmesano, Cotija y Reggianito.
Con mohosAzul, Cabrales, Camembert, Roquefort, Danablu, Limburgo y Brie
PROCESADOS
Fundidos y para untar Amarillo
Adaptado de la NOM 121-SSA1-1994
Tabla III. Clasificación de los quesos según su composición y características de la maduración.
DurezaH/MDContenido en g ras a MG/ESMaduración
Pasta extradura<51Queso muy graso>60Totalmente madurado Pasta dura49-55Queso graso45-60Madurado en superficie Pasta semidura53-63Queso semigraso25-45Madurado en masa Pasta semiblanda61-68Queso magro 10-25Con hongos en superficie o masa Pasta blanda>68Queso descremado<10Queso fresco
H/MD: Porcentaje del contenido en agua del queso por cada 100g de queso desengrasado.
MG/ES: Porcentaje de la materia grasa sobre el extracto seco.
Adaptado de Eck (1990)
2. Quesos de pasta hilada
2.1. Definición y generalidades
Entre los quesos frescos o de pasta blanda, se encuentra una subdivisión de quesos que tiene gran auge por poseer cualidades de hebrado y fundido únicas, a esta variedad de queso se le denomina “quesos de pasta hilada”.
De acuerdo al COVENIN 3822-2003, un queso de pasta hilada es “el producto elaborado a base de leche pasteurizada, entera, parcialmente descremadada o la mezcla pasteurizada de leche fresca entera con sólidos
totales de leche o derivados lácteos, adicionada o no de fermentos lácticos, cuajo u otros coagulantes, que después del proceso de coagulación, obtención de la cuajada y escurrido parcial del suero, es sometida a un proceso de amasado o malaxado y estirado mecánico en caliente, dando origen a una masa hilante homogénea”.
El queso Oaxaca y el Mozzarella pertenecen al grupo de los quesos de pasta hilada (filata, en italiano) debido a que durante su elaboración la cuajada, previamente acidificada, se somete a un amasado con agua caliente que permite plastificarla y estirarla; de
tal forma que pueda formar bandas, a su vez constituidas por estructuras un tanto alineadas que se pueden separar como “hilos” (Villegas de Gante, 2004).
A nivel internacional, el Mozzarella es el queso de pasta hilada más conocido; aunque en Europa también gozan de fama el Provolone y el Caciocavallo. En México, si bien se conoce el Mozzarella tipo americano (diferente al italiano original en varios aspectos, y cuya demanda parece incrementarse sensiblemente), el queso más conocido de esta familia es, sin duda, el Oaxaca. No obstante, en el país existen otros quesos de pasta hilada, como el Asadero, el Guaje (elaborado en la Huasteca Potosina) y el queso Trenzado de Veracruz (Villegas de Gante, 1993). En la Tabla IV se hace mención de algunas variedades de queso de pasta hilada y su país de origen.
Tabla IV. Quesos de pasta hilada.
VariedadesPaís de Origen
Doble crema, Huilense, Momposino y PeraColombia
Caciocavallo y Mozzarella Italia
Asadero, Guaje, Oaxaca yTrenzadoMéxico
TelitaVenezuela
Adaptado de Lodoño (2009)
El Oaxaca guarda grandes semejanzas con el Mozzarella italiano, por su forma y proceso general, sobre todo cuando ambos se fabrican artesanalmente. Esto a pesar de que el queso italiano desde antaño se elabora con leche de búfala de agua, y el mexicano con leche de vaca (curiosamente, la leche de cabra no es adecuada para elaborarlo, ya que la pasta no “hila” porque la proteína no tiene capacidad suficiente de estiramiento, y se rompe) (Villegas de Gante, 2004).
2.2. Fundamento de la elaboración
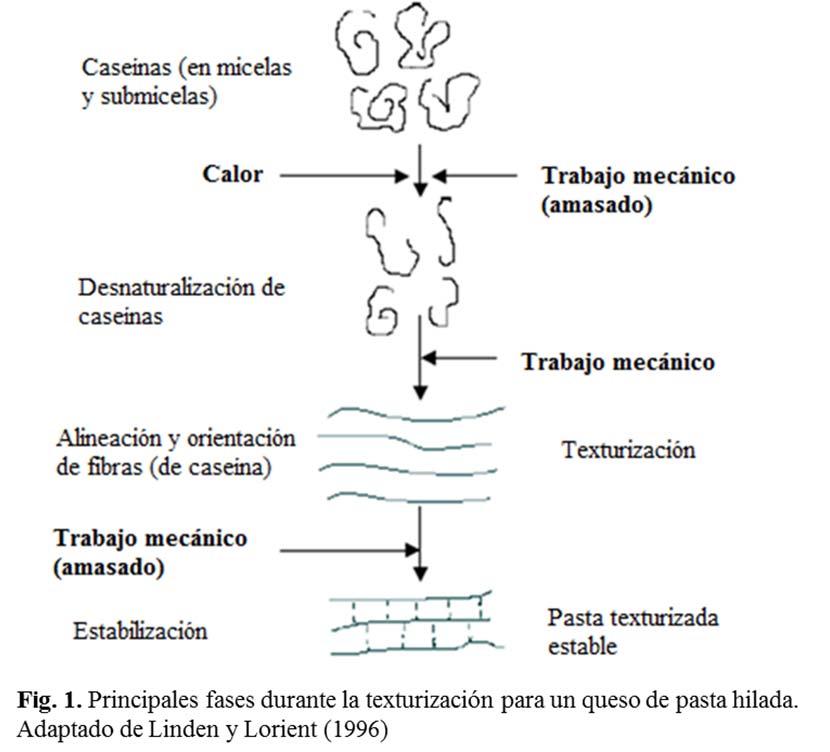
La textura hilada es la característica principal de estos quesos y puede explicarse, por el rearreglo estructural que las moléculas de
caseína (α, β y κ, que forman parte de las micelas descalcificadas) sufren al someter la pasta a calentamiento y trabajo mecánico. El hilado, desarrollado durante el amasado y el ascenso de temperatura, por el aporte de agua caliente, provoca la desnaturalización de parte de las moléculas de caseína, alterando su conformación β-placa y α-hélice (Linden y Lorient, 1996).
La continuación de la acción mecánica, y el estiramiento al que se somete la pasta en una dirección espacial, orientan y “alinean” a las proteínas, cual si fueran agregados de “hilos”. Entre moléculas contiguas de proteínas alineadas se establecen enlaces químicos de distinta naturaleza (v.g. por puentes de hidrógeno), que las mantendrán unidas (Linden y Lorient, 1996).
Asimismo, la grasa butírica, ya en la pasta amasada e hilada, se distribuye en “columnas” largas, siguiendo la orientación de los arreglos de las fibras caseínicas, según lo describen para el queso Mozzarella Mehmet y Sundaram (1997). La grasa estaría flotando, también, en “microcisternas” de suero y funcionará como un lubricante en la alineación de las fibras de caseína durante el trabajo mecánico del amasado e hilado.
En la Fig. 1 se representan los principales fenómenos relacionados en el hilado de la pasta quesera.
3. Queso Oaxaca
3.1. Definición y composición
El queso Oaxaca es un típico producto mexicano, nombrado así en honor al estado de Oaxaca que se encuentra al sur de México, de donde se cree es originario; sin embargo, es manufacturado y comercializado en la mayoría de los estados de la República (Raya et al 2005). Es un queso de pasta hilada elaborado
con leche de vaca, cuya presentación es en bolas que se forman a partir del enredo de filamentos de queso. Este queso se identifica sólo en México, donde se conoce también con el nombre de Quesillo y queso de hebra (Silva, 2006).
El queso Oaxaca se define como un queso de cuajada suave y plástica, desmenuzable, de cuerpo firme, color blanco cremoso y sabor suave, ligeramente ácido. La característica principal es su consistencia elástica, ya que la cuajada se puede moldear hasta darle una forma redonda y trenzada. Está clasificado como un queso fresco de pasta cocida, acidificado (NOM-121-SSA1, 1994).
El queso Oaxaca tiene características fisicoquímicas muy específicas; sin embargo su composición proximal no está claramente
definida. En la Tabla V se hace referencia a la composición proximal esperada en queso Oaxaca, la cual es el resultado del estudio y análisis comparativo de 10 marcas de este tipo de queso.
Tabla V. Composición proximal de queso Oaxaca.
ComponentePorcentaje
Humedad50.82
Adaptado de García (2006)
3.2. Proceso de elaboración
El proceso de elaboración del queso Oaxaca requiere de destreza y conocimiento, puesto que presenta ciertos puntos críticos cuyo
control es indispensable; por ejemplo, la acidez adecuada de la leche, la acidificación de la cuajada, la determinación del “punto de hebra” y el amasado de la pasta (Villegas de Gante, 1993). En la Fig. 2 se representa el diagrama de flujo de la elaboración de un queso Oaxaca tradicional.
A continuación se detallan los pasos para la elaboración de este queso fresco de pasta hilada (PROFECO, 2004).
1. Obtención y transporte: La leche debe ser de vaca, sin adición de antibióticos ni agua, en
6 – 1 (2012): 1 - 12
ausencia de microorganismos patógenos, con un pH de 6.6 a 6.7 y una composición proximal de alrededor de 3.2% de proteína y 3.5% de grasa butírica. El transporte se debe llevar a cabo en botes cerrados o pipas de acero inoxidable previamente higienizadas y a una temperatura de 4°C.
2. Filtración. Eliminación de materia contaminante adquirida en el transporte de la leche (insectos o polvo). Se lleva a cabo haciendo pasar la leche por una manta de cielo.

Fig. 2. Diagrama de flujo de la elaboración de queso Oaxaca, adaptado de Huerta, 2005.
3. Estandarización. Ajuste del nivel de grasa butírica, de tal manera que se obtenga una leche de alta calidad tecnológica (que se transforme bien). Se puede llevar a cabo de distintas maneras dependiendo de la composición de la leche. En caso de tener un bajo contenido de grasa se puede adicionar crema o se puede mezclar con leche rica en grasa. En caso de tener una leche alta en grasa, se puede mezclar con leche descremada o se puede emplear una descremadora con mecanismo para estandarizar el nivel de grasa, manual o automáticamente (Silva, 2006).
4. Pasteurización. Proceso térmico que tiene como objetivo reducir los agentes patógenos que puedan contener (bacterias, protozoos, mohos y levaduras, etc.). Puede ser lenta a (65°C durante 30 minutos) o rápida (75°C durante 15 segundos); posterior enfriamiento hasta temperatura de 38-40 °C (Hayes, 1993).
5. Acidificación. Proceso de desnaturalización que provoca la desmineralización de la leche donde las caseínas se desdoblan y comienzan a precipitarse. Se lleva a cabo por medio de la adición de bacterias lácticas o ácidos orgánicos hasta alcanzar un pH de 5.6 (Lindent y Lorient, 1996).
6. Coagulación. Retención de caseínas y glóbulos grasos de la leche en forma de matriz proteica, ligada principalmente por iones calcio, propiciada por la adición de la enzima quimosina o alguna sustancia que iguale sus propiedades coagulantes (pepsina, cuajos vegetales o microbianos). Se adicionan 0.2g de cloruro de calcio y 0.1ml de cuajo por cada litro de leche a elaborar y se deja reposar entre 20 y 30 minutos (Van der Berg, 1993).
7. Corte y agitación. Facilitación mecánica de la salida del suero de la cuajada (sinéresis). Se corta la cuajada en cubos de 2 ó 3 cm y se agita suavemente (como queso fresco) (Silva, 2006).
8. Desuerado. Eliminación total del suero de la cuajada. Se lleva a cabo filtrando la cuajada a través de un colador (Silva, 2006).
9. Malaxado. Trabajo mecánico con calor que permite la alineación y orientación de las proteínas así como la distribución de la grasa butírica. La cuajada se sumerge en agua a temperaturas mayores a 80 °C cubriendo todo el queso y se amasa. Se repite 3 ó 4 veces hasta que se tenga una pasta elástica, compacta sin poros ni protuberancias.
10. Formación de tiras. Moldeado de la masa que permite la alineación final de las proteínas hasta la formación de hilos (Lindent y Lorient, 1996). La pasta se toma de un extremo y se va estirando procurando formar una tira de forma redonda o de listón, de tamaño uniforme (2.5cm de diámetro o ancho) (Silva, 2006).
11. Enfriado. Suspensión total del proceso de moldeado que permite estabilizar a las tiras para que no sufran deformaciones. Conforme se va formando la tira se coloca en una cuba con agua a 4° C (Silva, 2006).
12. Salado. Adición de sal como potenciador de sabor. Se agregan de 20 a 30 gramos de sal por cada kilogramo de queso; se hace de manera directa espolvoreando la tira (Silva, 2006).
13. Enrollado. Moldeado final del queso para darle la forma de bola de estambre tradicional Consiste en enredar la tira de queso, dándole una forma determinada para producir una bola de queso (Silva, 2006).
14. Empacado. Método de conservación que consiste en evitar el contacto del queso con agentes exteriores contaminantes. Las bolas de queso se colocan dentro de bolsas de plástico.
15. Almacenado en refrigeración. Prolongación de la vida de anaquel del queso retardando la actividad enzimática y la
proliferación de microorganismos deteriorativos.
3.3. Propiedades fisicoquímicas y texturales
Las características fisicoquímicas y viscoelásticas de este queso, son las que lo hacen un tan apetecido producto lácteo. A continuación se llevará a cabo la descripción de estas propiedades y dado que no existe ninguna norma que puntualice sobre los estándares que un queso Oaxaca debe cumplir, se hará mención de datos obtenidos de la caracterización de típico queso Oaxaca en ciertos trabajos de investigación.
a) Fisicoquímicas
Características como el color, el pH y actividad de agua son las que permiten tanto al consumidor de manera empírica, como a la industria láctea de manera profesional, identificar las diferencias entre quesos y llevar a cabo un control de calidad de sus productos. En la Tabla VI se hace el listado de las propiedades fisicoquímicas del queso Oaxaca y sus valores de acuerdo a un estudio realizado a 10 diferentes marcas (Huerta, 2005).
Tabla VI. Parámetros fisicoquímicos de queso Oaxaca.
Característica
pH
Color tríestimulo
Actividad de agua
Adaptado de García (2006)
4.7 - 5.12
L= 83.9 - 88.1
a= 0.28 - 1.68
b= 17.8 - 21.6
0.969 - 0.978
medidas reológicas para medir parámetros de textura.
Aparatos como el texturómetro pueden describir a partir de una prueba única, realizada sobre la muestra, un conjunto de parámetros de textura o “perfil de textura” (dureza, elasticidad, cohesión y adhesividad, además de calcular otros dos, gomosidad y masticabilidad) que pueden ser fácilmente relacionados con las características sensoriales (Huerta, 2005).
El perfil de textura en el queso Oaxaca ha sido muy estudiado recientemente, sin embargo, no hay información consistente comparable. En la Tabla VII se describe el perfil de textura del queso Oaxaca de acuerdo a un estudio que se llevó a cabo en quesos de 10 diferentes marcas.
Tabla VII. Parámetros texturales de queso Oaxaca.
Característica
Fuerza (g)
Elasticidad
Adhesividad (g.s)
Cohesividad
Adaptado de García (2006)
1006 - 2028
0.678 - 0.777 -16
0.558 - 0.681
b) Texturales
La calidad organoléptica de un queso puede evaluarse de forma objetiva por métodos instrumentales directos o indirectos. Los métodos directos emplean, por ejemplo,
3.4.
Producción
El queso Oaxaca goza de gran popularidad nacional debido a su excelente aptitud para fundir, por lo que se consume, frecuentemente, acompañando platillos tradicionales de la cocina mexicana, específicamente los típicos “antojitos”.
Es uno de los quesos que gozan del mayor prestigio por su consumo en México, tanto entre las clases populares como entre las de mayor ingreso. Se elabora en casi todos los estados de la república. Se vende lo mismo en mercados ambulantes, sin empaque, que en
supermercados o tiendas de autoservicio, con mejor presentación y conservación (Cervantes et al., 2006).
De acuerdo a la SAGARPA (2011), el queso Oaxaca es el segundo queso más producido a nivel nacional después del panela y antes del manchego; a partir del año 2008 se registra un aumento anual en su producción del 5.4% con respecto al año anterior, alcanzando así en el año 2011 las 18,775 toneladas de producción anual.
Existen diferentes marcas que producen este queso, sin embargo, la venta mayoritaria aun cuando no ha sido monitoreada, es claro que se encuentra en las marcas de los pequeños productores y la venta a granel (Cervantes et al., 2006).
3.5. Investigaciones recientes del proceso de elaboración
Dado que el queso Oaxaca es un producto de alto consumo a nivel nacional, la mejora del proceso de elaboración se ha convertido en una prioridad.
El principal problema en la elaboración de queso Oaxaca radica en el paso de acidificación de la leche, ya que corresponde a la parte más larga y crítica del proceso, y de ella depende el que se obtengan o no las características fisicoquímicas y sensoriales deseadas en el producto (hebrado y fundido). Es por esto que se ha llevado a cabo una serie de investigaciones como las presentadas a continuación, que tienen como objetivo optimizar los tiempos de acidificación.
Villegas de Gante et al. (2005) obtuvieron evidencia de que la técnica por acidificación directa de la leche pasteurizada que consiste en agregar un ácido orgánico comestible directamente a la leche hasta alcanzar un pH de 5.2, produce mejores características texturales en el queso Oaxaca, al compararlo
con un queso que ha sido acidificado por medio de bacterias lácticas hasta alcanzar un pH de 5.2, es decir acidificado convencionalmente, lo que es un excelente indicativo para la reducción de tiempos en la elaboración de queso Oaxaca.
Aguilar-Uscanga et al. (2006) en una investigación donde se propuso agregar suero fermentado para acelerar la acidificación de la leche para elaborar queso Oaxaca, determinaron que el queso que recibió 30% de suero directo para sustituir el proceso de acidificación convencional, mostró mayor reducción de tiempo de manufactura (hasta 38.8%) respecto al testigo que fue elaborado con acidificación convencional. Además no hubo ningún tipo efecto inmediato en la composición química, el rendimiento y los atributos sensoriales (color, sabor, textura), lo que podría considerarse como un punto a favor. Sin embargo, la adición de suero aceleró la proteólisis y lipólisis modificando la textura y sabor de los quesos después de únicamente nueve días de almacenamiento en refrigeración, lo que es un mal indicador, ya que el tiempo mínimo de vida de este queso debe oscilar entre los 15 y 20 días de almacenamiento.
Otro de los grandes retos del queso Oaxaca radica en la etapa del malaxado, ya que se requiere de mucha destreza y experiencia para alcanzar el amasado que provea al queso de las características fisicoquímicas y texturales propias del mismo sin disminuir los rendimientos. Es por eso que dentro de esta categoría se han llevado a cabo algunos estudios como los siguientes:
López- Mejía (2001) determinó que el malaxado a una temperatura de entre 70°C y 75°C produce una buena formación de hebra con permanencia en el producto de hasta 15 días de almacenamiento. También determinó que a menor temperatura existe la necesidad de un mayor tiempo de malaxado, sin embargo
el malaxado a temperaturas entre 80°C y 85°C aun cuando es posible, termina por cocer la pasta y disminuir la permanencia de la hebra en el producto final. Finalmente, como dato importante reporta que para obtener un queso Oaxaca con buena calidad de hebra, en el malaxado se debe procurar que la temperatura interna de la pasta se encuentre entre 57°C y 60°C.
Por otro lado, Salinas-Ruíz (2000) determinó que el uso de un aparato de malaxado (malaxadora) reduce los tiempos de elaboración del queso Oaxaca, en relación con el proceso de malaxado artesanal que consta del amasado a mano. También determinó que el uso de una malaxadora permite a la pasta un procesado más gradual con menor choque térmico, dando como resultado un producto más homogéneo y con una humedad uniformemente distribuida a lo largo de la hebra. Finalmente, como dato práctico reporta una mejor conservación de hebra al utilizar una malaxadora aditada con un tornillo helicoidal en lugar de aspas y a una temperatura de malaxado de 75°C.
Cabe destacar que tanto las investigaciones para la mejora de la acidificación como del malaxado, tienen como prioridad la reducción de tiempos y costos de producción, con la premisa de mantener intactas las características fisicoquímicas, bromatológicas y texturales del tradicional queso Oaxaca.
parámetros fijos en cuanto a las características fisicoquímicas, bromatológicas y texturales que debe cumplir, por lo que está en riesgo su autenticidad.
Por otro lado, ya que sólo existe un sondeo del mercado de las grandes marcas comerciales dejando a un lado a los pequeños productores de queso Oaxaca, las cifras de producción a nivel nacional no reflejan el consumo y producción real de este producto.
Finalmente, si bien se han realizado una serie de investigaciones relacionadas con la mejora en la elaboración de queso Oaxaca, la realidad es que no trascienden más allá del ámbito de la investigación, lo que es lamentable, tomando en cuenta la importancia a nivel nacional de este producto.
Agradecimientos
La autora S. Ramírez-Nolla agradece al Consejo Nacional de Ciencia y Tecnología (CONACYT) y a la Universidad de las Américas Puebla (UDLAP), por el apoyo en el financiamiento de sus estudios de posgrado.
Conclusiones
Después de hacer una revisión detallada de la información sobre la naturaleza del queso Oaxaca, sus propiedades fisicoquímicas y texturales, procesamiento, comercialización y las investigaciones actuales sobre su elaboración, se puede concluir que aun cuando el queso Oaxaca es un producto único, mexicano y de alta demanda, no existen
Referencias
Aguilar-Uscanga, B., Montero-Lagunes, M., De la Cruz, J., Solís-Pacheco, A. y García, H. 2006. Uso de suero fermentado para reducir el tiempo de acidificación del queso Oaxaca. Revista Agrociencia. 40:569-575.
Bernardo, A. 1997. Fundamentos de la Elaboración de Quesos. En: González, A. Otero, R. Rodríguez y J.J. Sanz (Eds). Productos Cárnicos y Lácteos. Primera edición. Gráficas Celarayn, León España. pp. 333341.
Cervantes, F., Villegas de Gante, A., Cesín, A. y Espinoza, A. 2006. Los quesos mexicanos genuinos: un saber hacer que se debe rescatar y preservar. III
Congreso Internacional Red SIAL. Baeza, Jaen. España. 18-21 octubre.
COVENIN 3822-2003. Norma Venezolana. Queso de pasta hilada. Fondonorma. Caracas, Venezuela.
Eck, A. 1990. El queso. Ediciones Omega. Barcelona. España.
FAO. 2006. Perspectivas Alimentarias. http://www.fao.org/docrep/009/html. Consultada el 16 de febrero del 2012.
Galván-Martínez, B., Colin-Cruz, M.A. y EspinozaOrtega, A. 2011. Efecto de la temperatura de procesamiento sobre la vida de anaquel del queso Oaxaca. XII Congreso Nacional de Ciencias y Tecnología de los alimentos. Zacatecas, Zac. Mexico. 26-27 mayo.
Garcés-Espinoza, B., Colin-Cruz, M.A. y DublanGarcía, O. 2011.Queso Oaxaca: crecimiento de bacterias lácticas y proteólisis durante el almacenamiento por efecto de la temperatura de procesamiento. XII Congreso Nacional de Ciencias y Tecnología de los alimentos. Zacatecas, Zac. Mexico. 26-27 mayo.
García, B. 2006. Caracterización físico-química de diversos tipos de quesos elaborados en el valle de Tulancingo, Hgo., con el fin de proponer normas de calidad. Tesis de Licenciatura. Universidad Autónoma del Estado de Hidalgo. México. 111 p.
Hayes, P. 1993.Microbiología e higiene de los alimentos, Ed. Acribia S.A. Zaragoza, España, 1993.
Huerta, R. 2005. Determinación del punto de hebra y modificación de la textura después del fundido de quesos Oaxaca. Tesis Maestría. Universidad de las Américas, Puebla. México. 106 p.
Linden, G. y Lorient, D. 1996. Bioquímica agroindustrial. Ed. Acribia S.A. Zaragoza, España.
Lodoño, M. 2009. Caracterización del queso Momposino y comparación con otros elaborados con adición o no de cultivos iniciadores. Tesis de Maestría. Universidad Nacional de Colombia Colombia. 106 p.
López-Mejía, J. 2001. Efecto de la temperatura del agua de amasado en la formación y conformación de la hebra de queso tipo Oaxaca. Tesis de Licenciatura. Universidad Autónoma de Chapingo. México. 85 p.
Mehmet, A. y Sundaram, G. 1997. Anisotropy in tensile properties of mozzarella cheese. Journal of Food Science. 62:1031-1033.
– 1 (2012): 1 - 12
NOM-121-SSA1-1994. Norma Oficial Mexicana, bienes y servicios. Quesos: frescos, madurados y procesados. Especificaciones sanitarias.
NOM-243-SSA1-2010. Norma Oficial Mexicana. Productos y servicios. Leche, fórmula láctea, producto lácteo combinado y derivados lácteos. Disposiciones y especificaciones sanitarias. Métodos de prueba.
PROFECO. 2004. Tecnologías domésticas. http://bibliotecadigital.conevyt.org.mx/colecciones/c onsumidor.htm Consultada el 14 de febrero de 2012.
Raya, J. Soto, G. M. Orozco, M. L. Flores J. M. y González, M. L. 2005. Evaluación de rendimientos y costos de fabricación en: Queso Asadero, Oaxaca y Yogurt a nivel Industrial.http://www.respyn.uanl.mx/especiales/20 05/ee-13-2005/documentos/ CNA59.pdf. Consultada el 15 de febrero del 2012.
SAGARPA. 2011. Boletín de la leche, enero-marzo 2011.
Salinas-Ruíz, J. 2000. Efecto de la temperatura y el uso de aditamentos en el amasado, formación y conformación de hebra en queso Oaxaca. Tesis de Licenciatura. Universidad Autónoma de Chapingo México. 76 p.
Scott, R. 1991. Fabricación de queso. Acribia. Zaragoza. España.
Silva, G. 2006, Manual de elaboración de quesos CEDELE. Hidalgo, México.
Van der Berg, M. 1993. The transformation of casein in milk into paracasein structure of cheese and its relation to non casein milk components. Cheese yield and factors affecting its control. Proceeding of the international Dairy Federation Seminar. Cork, Ireland, IDF. Brucelas, Bélgica.
Villegas de Gante, A. 1993. Los quesos mexicanos. Ed. CIESTAAM. México.
Villegas de Gante, A. 2004. Dos famosos quesos de Pasta hilada. Ed. CIESTAAM. México.
Villegas de Gante, A. Antonio, G. Hernández, A. 2005. Evolución de la calidad textural de queso Oaxaca elaborado con tres técnicas distintas. Alfa Editores Técnicos. 1:29-36.

Temas Selectos de Ingeniería de Alimentos 6 - 1 (2012): 13 - 28

Proceso de elaboración y propiedades fisicoquímicas de las leches condensada azucarada y evaporada
M. Marcelín-Rodríguez* y J. F. Vélez-Ruíz
Departamento de Ingeniería Química, Alimentos y Ambiental, Fundación Universidad de las Américas Puebla. Exhacienda Sta. Catarina Mártir S/N, Cholula, Puebla. C.P.72810. México.
Resumen
La leche condensada azucarada y la leche evaporada son productos de gran consumo debido a sus peculiares características. Estos productos son obtenidos mediante la reducción del contenido de agua por medio del proceso de evaporación. Ambos productos tienen una vida de anaquel amplia, debido a la adición de sacarosa en la leche condensada azucarada y al proceso de ultra pasteurización y envasado estéril en la leche evaporada. Las propiedades fisicoquímicas son muy importantes, ya que de ellas va a depender la calidad y la conservación de las características de los productos. Se caracterizan por la consistencia que presentan, tienen un comportamiento no newtoniano, de tipo pseudoplástico y tixotrópico, principalmente en la leche condensada azucarada por la presencia de cristales de sacarosa. El objetivo de este artículo es recopilar información sobre el proceso de elaboración de las leches condensada azucarada y leche evaporada, así como de sus características fisicoquímicas y reológicas.
Palabras clave: leche condensada azucarada, leche evaporada, evaporación, leche.
Abstract
Sweetened condensed milk and evaporated milk are staple goods due to their unique characteristics. These products are obtained by reducing the water content through the evaporation process. Both products have a long shelf life due to the addition of sucrose in sweetened concentrated milk and ultra high temperature and sterile packaging in evaporated milk. Physicochemical properties are very important, since this influence the quality and preservation of the products. These products are distinguished by their particular consistency, showing a non-newtonian behavior, and specifically the sweetened condensed milk presents a pseudoplastic and thixotropic behavior, mainly, in the sweetened condensed milk due to the presence of sucrose crystals. The aim of this work is to gather information concerning the preparation of sweetened condensed milk and evaporated milk, and their physicochemical and rheological characteristics.
Keywords: sweetened condensed milk, evaporated milk, evaporation, milk.
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: mercedes.marcelinrz@udlap.mx
Introducción
La leche es uno de los productos base para la alimentación por su gran valor nutricional, ya que aporta muchos de los nutrientes esenciales para la dieta, es por eso que se considera uno de los productos más completos y nutritivos.
La industria láctea es una de las industrias alimentarias más importantes en México. La leche más consumida es la de origen bovino, en el año 2010, la producción fue de 10,711,625 millones de litros y tuvo un crecimiento de 1.54% con respecto al año 2009 (SAGARPA, 2011). En el mercado existe una gran variedad de productos lácteos, algunos son para consumo inmediato, mientras que otros son productos que se elaboran para alargar su vida útil. Un ejemplo de estos últimos son las leches concentradas, las cuales tienen características peculiares y son la base para la elaboración de otros productos lácteos como la leche condensada azucarada, leche evaporada y leche en polvo y productos de panadería y repostería.
La leche condensada azucarada y la leche evaporada son obtenidas mediante la reducción del contenido de agua por medio del proceso de evaporación y, en el caso de la leche condensada azucarada, la adición de sacarosa. En México en 1997, existían alrededor de 18 empresas que elaboran leche condensada, evaporada y en polvo (Valle y Álvarez, 1997), y en 2010 ya se exportaban 25,842 toneladas de leche condensada azucarada y 1,223 toneladas de leche evaporada (SAGARPA, 2011).
Si bien los procesos de elaboración de la leche condensada azucarada y de la leche evaporada son similares, algunas características son diferentes, tales como acidez, actividad de agua, pH, viscosidad y humedad, entre otros. Del adecuado proceso y estandarización de estas características dependerá que el producto final esté libre de
alteraciones y defectos, así como la estabilidad que tendrá durante el almacenamiento.
A pesar de que las leches condensada azucarada y evaporada son productos muy comercializados y cuyo comportamiento durante el almacenamiento ha sido estudiado por diversos autores (Ibarz et al., 1987; VélezRuiz y Barbosa-Cánovas, 1997; Bienvenue et al., 2003; Trinh, 2006; González et al., 2008) hay poca información sobre las características físicas de estos productos y ésta se encuentra dispersa. Es por esta razón que el objetivo de este artículo es recopilar la información sobre el proceso de elaboración de las leches condensada azucarada y evaporada, así como de sus características fisicoquímicas y reológicas.
Revisión bibliográfica
1. Generalidades de la leche
La leche es uno de los alimentos más antiguos consumidos por el hombre, tiene un valor nutricional muy alto, ya que posee una gran cantidad de energía, proteínas de fácil asimilación, grasa, calcio, fósforo y varias vitaminas necesarias para muchas etapas en la vida del ser humano (Maza y Legorreta, 2011). De acuerdo a la Norma Oficial Mexicana 155 (2003) la leche se define como “el producto obtenido de la secreción de las glándulas mamarias de las vacas, sin calostro, el cual debe ser sometido a tratamientos térmicos u otros procesos que garanticen la inocuidad del producto; además puede someterse a otras operaciones tales como clarificación, homogeneización, estandarización u otras, siempre y cuando no contaminen al producto y cumplan con las especificaciones de su denominación”.
En México los estados con mayor producción de leche bovina en el 2010 fueron:
Jalisco (1,961 millones de litros), Coahuila (1,243 millones de litros) y Durango (10000 millones de litros), mientras que Puebla tuvo una producción de 399 millones de litros (SAGARPA, 2011).
La leche es producida por todas las especies de mamíferos para alimentar a sus crías; sin embargo, la leche de cada especie tiene diferentes propiedades. En la Tabla I se presentan ejemplos de la composición de la leche de diferentes mamíferos (Alais, 2003; Chandan, 2006b). La leche se compone de agua, carbohidratos, lípidos, sustancias nitrogenadas, sales minerales, vitaminas, ácidos orgánicos, enzimas, gases y flora microbiana. El componente más abundante es el agua, la cual es el medio en el que todos los otros componentes de la leche (sólidos totales) son disueltos o están suspendidos; las sales y los azúcares se encuentran en solución; las proteínas, en su mayor parte, en estado coloidal y la materia grasa en forma de emulsión (Chamorro y Losada, 2002; Boland, 2003). El porcentaje de agua en la leche está entre 85.4% y 87.7%, este valor varía conforme se altera la cantidad de los demás componentes de la leche (Revilla, 1982; Chandan, 2006a).
– 1 (2012): 13 - 28
Las proteínas son el componente más valioso de la leche. La leche de vaca se le conoce como fuente excelente de proteína. Los lípidos se encuentran en forma de glóbulos microscópicos en una emulsión aceite en agua. Las propiedades funcionales de la grasa de la leche se atribuyen a su composición de ácidos grasos, además, proporciona a los lácteos, sus características únicas como apariencia, textura, sabor y saciabilidad. Generalmente la grasa de la leche está formada por 62% de grasa saturada, 29% de ácidos grasos monoinsaturados y 4% de ácidos grasos polinsaturados (Miller et al., 2000; Chandan, 2006a).
Los carbohidratos de la leche están compuestos mayoritariamente por lactosa, la cual aporta hasta el 25% de la energía total del producto lácteo, pero también contiene otros azúcares en menores porcentajes (glucosa y galactosa) y otros carbohidratos como glucolípidos, glucoproteínas y oligosacáridos (Bonet et al.¸ 2003; Miller et al., 2000). En cuanto a los minerales, la leche aporta elementos minerales indispensables para el organismo humano y es la fuente más importante de calcio; el nivel de calcio de la leche está en un rango de 0.7 a 1.0 mmol/g (Boland, 2003; Maza y Legorreta, 2011).
Tabla I. Composición de la leche de algunos mamíferos.
MamíferoSólidos totales (%) Grasa (%)Proteínas totales (%) Caseína (%) Proteína de suero (%) Lactosa (%) Cenizas (%)
Vaca12.23.43.42.80.64.70.7
Búfalo16.36.74.53.60.94.50.8
Cabra13.24.52.92.50.44.10.8
Oveja19.37.35.54.60.94.81
Camello13.64.53.62.70.950.7
Yegua11.21.92.51.31.26.20.5
Burra8.50.61.40.70.76.10.4
Yak17.36.55.8__4.60.9
Adaptada de Chandan (2006b).
La Norma Oficial Mexicana 155 (2003) agrupa a las leches procesadas en diferentes clasificaciones, ya sea por el tipo de grasa, procesos primarios, procesos secundarios o por el sabor (Tabla II). La leche fresca y las leches procesadas tienen un gran valor nutricional, pero su vida de anaquel es limitada, por esta razón son procesadas para que tengan una mejor estabilidad. Una de las operaciones más usadas es la reducción de la cantidad de agua, la cual reduce la actividad de agua, por medio de la concentración por evaporación y secado (Oliveira et al., 2009).
2. Proceso de evaporación
La evaporación es una operación unitaria de las más antiguas y ampliamente usadas en la industria alimentaria para la conservación de jugos, productos lácteos, sopas, jarabes, entre otros; se ha usado para prolongar la vida de anaquel del producto, reducir el volumen o peso de un producto líquido y así facilitar el transporte, inducir la consistencia y cambio de sabor, incrementar la estabilidad de éstos productos o bien como un paso previo al proceso de secado (Vélez-Ruiz, 2009; Varnam y Sutherland, 2001).
En 1822, el inventor Francés, Nicolás Appert dio los primeros pasos para conservar la leche sin afectar sus cualidades y su frescura, evaporando el agua por ebullición en
Tabla II. Clasificación de leches procesadas.
baño maría, y en 1829 trabajó al vacío, por lo que se le conoce como el inventor de la leche concentrada. En 1835 el inglés William Newton comprobó que se podía conservar la leche si se le añadía azúcar y por el efecto de vacío se podía calentar a una temperatura menos elevada. En 1855, Gail Borden fundó la primera fábrica de leche condensada azucarada y un año después, recibió la patente en Estados Unidos e Inglaterra por preservar la leche en un estado semifluido después de evaporarlo al vacío, y empacarlo en latas herméticamente selladas (Tur Marí, 2005; Farkye y UrRehman, 2011).
La evaporación es un proceso que se basa en el calentamiento de un líquido hasta su punto de ebullición para remover el agua como vapor. Los evaporadores utilizados en la industria láctea siempre operan al vacío, esto porque la leche es sensible al calor y una evaporación a 100°C da lugar a la desnaturalización de las proteínas de la leche, lo que haría al producto no apto para consumo humano, así que para disminuir el daño ocasionado por éste, se puede realizar la evaporación al vacío y lograr así la disminución o reducción del punto de ebullición (Goff, 2007; Tamime et al., 2007; Westergaard, 2004). Obviamente, el punto de ebullición de la leche se incrementa cuando contiene mayor cantidad de sólidos.
Tipo de grasaProceso primarioProceso secundario
Grasa ButíricaRehidratadaPasteurizada
EnteraReconstituidaUltrapasteurizada SemidescremadaDeslactosadaMicrofiltrada Ultra Parcialmente descremadaEvaporada Descremada
Condensada Azucarada
Grasa vegetalDeshidratada o en polvo
Con grasa vegetalConcentrada
Adaptada de Norma Oficial Mexicana 155 (2003)
Aunque la temperatura de ebullición del alimento está dada por la concentración de la leche y la presión hidrostática de la columna del líquido la mayoría de los evaporadores operan con temperaturas en un rango de 45 a 70 °C bajo presiones reducidas (Vélez-Ruíz, 2009; Varnam y Sutherland, 2001).
Existen diferentes tipos de evaporadores, los evaporadores de un sólo efecto, los cuales se utilizan para pequeñas cantidades; evaporadores de superficie raspada, que son muy útiles para fluidos de alta viscosidad porque ayudan a minimizar la deposición de sólidos en la superficie y los evaporadores de múltiple efecto, los cuales son muy usados en la concentración de la leche, jugos de frutas y purés (Vélez-Ruiz, 2009). Los evaporadores de película descendente, han sido ampliamente utilizados en la industria láctea (Varnam y Sutherland, 2001).
Los componentes principales de un evaporador son la cámara de condensación y la cámara de evaporación. En la primera, el vapor de agua se transforma en líquido cediendo su calor latente de condensación al alimento que se encuentra en la zona de evaporación. El agua se evapora rápidamente y sale del evaporador, separando así el vapor del líquido concentrado (Gèosta y López, 2003; Ibarz, 2005; Vélez-Ruiz, 2009).
La caldera se utiliza para generar el vapor que será necesario para suministrar de energía al evaporador y así alcanzar el punto de ebullición del alimento. Como el vapor utilizado es en grandes cantidades, se puede minimizar esta cantidad utilizando evaporadores de múltiple efectos. Esto significa que existen más de dos unidades, mismas que operan a presiones menores en cada efecto y logran un punto de ebullición más bajo en cada efecto. El vapor que se produce en el primer efecto servirá como medio de calentamiento para el efecto siguiente y así sucesivamente (Gèosta y
López, 2003). Existen varios aspectos del alimento que se deben tomar en cuenta para establecer las condiciones del proceso y seleccionar el equipo de evaporación que se va a utilizar (Vélez-Ruíz, 2009).
Durante el proceso de evaporación, la leche sufre cambios en sus propiedades, entre ellos, el pH y la acidez. El pH disminuye aproximadamente 0.3 unidades cuando se remueve la mitad del agua y 0.5 unidades cuando se remueve la tercera parte del agua del producto (Walstra et al., 2006). Otras propiedades modificadas de manera importante durante el proceso de evaporación, son el punto de ebullición, las propiedades reológicas, las propiedades térmicas y la densidad.
La leche concentrada por evaporación es la base para elaborar otros productos lácteos, dos de ellos son líquidos: la leche condensada azucarada y la leche evaporada. El otro es un producto sólido particulado de gran estabilidad, es la leche en polvo o deshidratada.
2.1. Leche condensada azucarada
La Norma Oficial Mexicana 155 (2003) define a la leche condensada azucarada como el producto que ha sido obtenido mediante la evaporación del agua de la leche a través de presión reducida, a la que se le ha agregado sacarosa y/o dextrosa u otro edulcorante natural, hasta alcanzar una determinada concentración de grasa butírica y sólidos totales. La leche utilizada puede ser entera, semidescremada o descremada, que se somete a un tratamiento térmico (pasteurización) y se conserva mediante adición de sacarosa (Zavala, 2005). Según la composición del producto, se le puede denominar: leche condensada, leche condensada desnatada (descremada), leche condensada parcialmente desnatada (descremada) o leche condensada de elevado contenido de grasa (SECOFI, 1999).
La leche condensada azucarada tiene un alto contenido energético y se ha usado en la elaboración de postres, bebidas, comidas dulces o adicionándola de manera directa sobre frutas ya que proporciona un mejor sabor y resalta la dulzura de estos productos alimenticios. La alta concentración de sacarosa en este producto aumenta la presión osmótica hasta tal punto, que la mayoría de los microorganismos son inactivados (Gèosta y López, 2003). La cantidad de sacarosa para garantizar la conservación del producto final está regulada y depende del peso seco lácteo de la leche condensada: el porcentaje de sacarosa mínimo es de 62.5 y el máximo es de 64.5% (SECOFI, 1999).
2.1.1. Proceso de elaboración
El primer paso para la elaboración de la leche condensada azucarada es realizar un tratamiento previo a la leche que se va a utilizar; éste consiste en normalizar la cantidad de grasa, de sólidos no grasos y aplicar un tratamiento térmico. Generalmente, el tratamiento térmico se realiza en un tiempo de 1 a 3 minutos a una temperatura de 100-120°C para así inactivar a algunos microorganismos (Gèosta y López, 2003; Carić et al., 2009). Una vez aplicado el tratamiento térmico se procede al bombeo de la leche hacia el evaporador para concentrarla. En el evaporador a vacío se debe cuidar que la temperatura esté entre 65 y 70 °C, no a temperaturas menores porque ocasionaría el desarrollo de esporas y bacterias resistentes al calor.
En el proceso de evaporación es donde se agrega sacarosa, el jarabe entra y se mezcla con la leche a mitad del proceso de condensación, si se añade antes de este proceso puede hacer que la viscosidad aumente y el proceso de evaporación sea dificultoso. El producto evaporado se pasa a un homogenizador para lograr obtener un tamaño de grasa uniforme. Posteriormente se
enfría a una temperatura aproximada de 14°C, este es uno de los puntos más importantes del proceso, ya que se presenta la cristalización de la lactosa (Gèosta y López, 2003; Hall y Hedrick, 1971).
Posteriormente, se vuelven a realizar análisis en el producto final para comprobar que el contenido de grasa, de sólidos no grasos y proteínas, además que sus propiedades físicas como viscosidad y color sean las adecuadas, según las Normas Oficiales de cada país. El último paso es el envasado y almacenamiento (Hall y Hedrick, 1971; Gèosta y López, 2003).
2.1.2. Defectos en la leche condensada azucarada
Si la leche condensada azucarada no se elabora o maneja de manera adecuada, puede presentar diversos defectos, como pueden ser una viscosidad excesiva, decoloración, cambios químicos y microbiológicos, arenosidad, sedimentación del azúcar y crecimiento de mohos (Hall y Hedrick, 1971; Farkye y UrRehman, 2011).
La lactosa se cristaliza en la leche condensada, por la pequeña cantidad de agua que resta después de la evaporación. Si el proceso de cristalización se lleva a cabo de manera lenta puede producir cristales gruesos (con tamaño mayor a 0.03 mm) y duros, producto que se identifica como “arenoso” y provoca un rechazo del cliente; para que esto no ocurra se deben estandarizar las condiciones adecuadas para que la formación de cristales (con un tamaño menor a 0.01 mm) se genere en una forma rápida. Muchas veces se agrega leche en polvo o lactosa finamente cristalizada, como núcleos para forzar a que el proceso de cristalización se lleve a cabo de manera adecuada (Alais, 2003; Zavala, 2005).
La leche condensada azucarada por su baja actividad de agua (0.83) y su alta cantidad de
azúcar es un producto en el cual los microorganismos casi no crecen. Sin embargo, ciertas bacterias y levaduras, como Torulopsis lactis-condensi, que producen gas pueden provocar un hinchamiento en las latas. Se han aislado algunos tipos de hongos como Aspergillus, Catenularia, Penicillium, Cladosporium y Actinomyces, y algunos tipos de bacterias como Micrococcus, Streptococcus, Staphylococcus, Bacillus y Mycobacterium. Estos microorganismos pueden provocar cambios de color, olor y sabor en el producto final, problemas que se pueden controlar por medio de una pasteurización efectiva, regulando las concentraciones de azúcar y medidas sanitarias adecuadas (Hall y Hedrick, 1971; Farkye y UrRehman, 2011).
El defecto físico más importante que se presenta es el cambio de viscosidad, ya que se da el fenómeno conocido como espesamiento por almacenamiento prolongado (“age thickening”) o viscosidad estructural. Este defecto puede deberse a variaciones en la composición de la leche o en el pretratamiento térmico, la cantidad de azúcar que se le agrega o la cantidad de sales estabilizadoras. Se presenta durante el almacenamiento y como consecuencia, el pH sufre una disminución, sin embargo puede ser interrumpido por agitación (Farkye y Ur-Rehman, 2011; Bienvenue et al., 2003). Este fenómeno ha sido mencionado en leches concentradas (Vélez-Ruíz y BarbosaCánovas, 1997; Vélez-Ruíz y BarbosaCánovas, 2000; Trinh, 2006; Bienvenue et al., 2003).
Otro defecto es el cambio de color, por el efecto del calor que recibe la leche en la evaporación, el color dorado se va incrementando conforme se incrementa el pH, en especial arriba de 7.0. Este problema se puede evitar al evaporar a una temperatura adecuada (Hall y Hedrick, 1971).
2.2. Leche evaporada
La leche evaporada, o leche doblemente concentrada, es un producto esterilizado, de color claro y de apariencia cremosa. Este tipo de leche es utilizado en muchos lugares donde no tienen acceso a la leche fresca o refrigerada, como sustituto de la leche materna (con la adición de vitamina D). El contenido es diluido en agua antes del consumo para asemejarse a la leche normal. Sin embargo, en la actualidad, se usan más los productos alternativos, como la leche entera en polvo o la leche recombinada. Se han desarrollado nuevas alternativas de uso de leches concentradas, así mismo, su proceso de empacado ha sido modificado. Es por esto que el consumo de las leches concentradas ha disminuido notablemente. Actualmente es utilizada para cocinar o como crema para café. Es elaborado con leche entera, leche desnatada o una combinación de leche desnatada con leche en polvo, grasa de leche anhidra y agua como principales ingredientes (Oliveira et al., 2009; Walstra et al., 2006).
Este producto lácteo contiene la misma cantidad de sólidos que la leche pero en un menor volumen de agua (Vélez-Ruiz y Barbosa-Cánovas, 1997). Se caracteriza porque comparado con otros productos lácteos tiene un largo periodo de anaquel a temperatura ambiente (hasta un año), lo cual facilita el manejo y la distribución de esta leche. La preservación de la leche evaporada se debe a que pasa por una esterilización o por ultra pasteurización (UAT) y es empacada en un recipiente estéril (Fan, 2007).
2.2.1. Proceso de fabricación
El primer paso del proceso es la estandarización del contenido graso y de sólidos. Posteriormente se realiza un precalentamiento, el cual sirve para mejorar la
estabilidad térmica, inactivar enzimas y microoganismos. Generalmente se realizan periodos largos de tratamiento térmico (20 min.) a temperaturas menores de 100°C, aunque la temperatura de calentamiento y el tiempo son parámetros definidos por la estabilidad térmica de la leche (Gèosta y López, 2003; Walstra et al.¸ 2006).
Después de realizado el tratamiento térmico se procede a la concentración en un evaporador a vacío. Para estandarizar la concentración, a la cual se quiere llegar, es necesario conocer la densidad de la leche, ya que si se concentra demasiado puede causar un bajo rendimiento y una pobre estabilidad térmica. Después de la concentración, el proceso para esterilizar varía, ya sea esterilización en lata o esterilización por medio de ultrapasteurización (Walstra et al. ¸ 2006).
Para el proceso de esterilización en lata, una vez evaporada la leche se procede a la homogenización (65°C a 22 y 5 MPa), la cual sirve para prevenir la formación de nata y la coalescencia, sin embargo, esta homogenización no debe ser brusca, por la baja estabilidad de este producto. Una vez homogenizada se enfría a 10°C para proceder a la estabilización, en la que se realizan pruebas para asegurarse que la leche no coagule durante la esterilización y para saber si es necesario que se le agregue algún estabilizante (fosfato disódico o trisódico) (Walstra et al.¸ 2006; Farkye y Ur-Rehman, 2011).
Por último, se precede al empacado en latas, la placa de estaño de éstas se recubre con un polímero para evitar que el hierro y el estaño se disuelvan en el producto. La esterilización se realiza una vez que el producto está en las latas, ésta puede ser aplicada por lotes, en un autoclave, a temperaturas entre los 115°C y 121°C por 15 o 20 minutos, seguido de un enfriamiento de 15
minutos a 25°C-30°C (Gèosta y López, 2003; Walstra et al.¸ 2006; Farkye y Ur-Rehman, 2011).
Para la esterilización por ultra pasteurización, primero se estabiliza con fosfato disódico o trisódico, posteriormente se esteriliza por 15 segundos a 140°C, usando calentamiento directo o indirecto, y se enfría a 60°C. Casi siempre se presenta coagulación por el calor, por lo que la homogenización sirve para reducir el tamaño de los agregados de proteínas formadas; ésta se lleva a cabo a 45 MPa, después se enfría la leche evaporada a 10°C. El empacado del producto es en latas asépticas, para evitar contaminación del producto (Farkye y Ur-Rehman, 2011). Una de las ventajas que tiene con este tipo de esterilización es que inactiva las esporas bacterianas más efectivamente que la esterilización en lata (Walstra et al., 2006).
Durante la evaporación de este producto se presentan una serie de cambios, como son la disminución de la aw, el incremento de la higroscopicidad, cambios en el equilibrio de las sales en la leche, generalmente se realizan con un aumento en la actividad de iones Ca2+ provocando que el fosfato de calcio no se disuelva, y también hay cambios conformacionales en las proteínas junto con un incremento en la asociación y compactación de éstas (Farkye y Ur-Rehman, 2011).
2.2.2. Defectos en la leche evaporada
Al igual que la leche condensada azucarada, si no se maneja adecuadamente o con parámetros mal definidos durante el proceso de elaboración, se pueden presentar defectos en el producto final. Los más importantes son cambio de sabor, coagulación, gelación o engrosamiento, separación de grasa, falta de esterilización, endurecimiento y separación de los minerales (Hall y Hedrick, 1971; VélezRuíz y Barbosa-Cánovas, 1997; Fan, 2007).
Durante el proceso de esterilización, los componentes termosensibles de la leche evaporada se ven sometidos a varios cambios que pueden ocasionar una pérdida de color y cambiar el producto a un color marrón; así mismo, se puede presentar un cambio de sabor, generando sabor a cocido. El color marrón es el resultado de la reacción de Maillard, lo cual ocurre entre los aminoácidos y la lactosa, azúcar reductor presente en la leche. Las altas temperaturas en la esterilización catalizan la reacción entre los aminoácidos y la lactosa para producir melanoidinas, que son los pigmentos de color marrón que se encuentran presentes en el producto final (Fan, 2007; Hall y Hedrick, 1971).
Comparado con otros productos alimentarios, la leche es muy estable al calor y puede soportar condiciones altas de procesamiento térmico, pero en ciertas condiciones puede ser inestable a los tratamientos térmicos debido a que se puede presentar una coagulación por el calor y más aún en productos concentrados, como la leche evaporada y la leche condensada azucarada (Sievanen et al., 2008). La caseína no coagula con el calor, a menos que se someta por un largo periodo a altas temperaturas, sin embargo, en la leche evaporada puede coagular por la temperatura a la cual se esteriliza (Brown, 2008).
La esterilización se debe llevar a cabo para que el producto tenga una mayor duración a temperatura ambiente, sin embargo, hay bacterias termodúricas y termófilas formadoras de esporas (son las causas más comunes de deterioro de las leches evaporadas) que pudieran crecer a temperaturas de 45°C. Se puede presentar un deterioro en el producto final si no se enfría a una temperatura adecuada o se almacena a alta temperatura, esto ocasiona que microorganismos como Bacillus stearothermophilus se puedan desarrollar
(Farkye y Ur-Rehman, 2011; Ledenbach y Marshall, 2009).
3. Propiedades fisicoquímicas de la leche evaporada y la leche condensada azucarada
3.1. Propiedades fisicoquímicas
Las propiedades de los productos lácteos son variadas y abundantes, y deben ser controladas y determinadas para conocer su calidad. Algunas propiedades físicas de la leche y productos lácteos como la densidad, viscosidad y tensión superficial dependen de sus constituyentes, mientras que otros como el índice de refracción y el punto crioscópico, dependen de las sustancias en solución. El pH y la conductividad, dependen únicamente de los iones o de los electrones, como también es el caso del potencial de óxido-reducción (Maza y Legorreta, 2011).
La densidad de la leche no tiene un valor constante, puede estar determinada por dos factores opuestos y variables. El primero es la concentración de los elementos disueltos y en suspensión (sólidos no grasos), la variación se da de manera proporcional. El segundo es la proporción de materia grasa, la densidad total de la leche varía inversamente al contenido graso, la densidad a 20°C es de 1029 kg/m3 (Alais, 2003).
La actividad de agua de la leche concentrada se puede medir porque es igual a la humedad relativa del aire en equilibrio con la leche concentrada. Se puede determinar estableciendo la humedad relativa a la que el producto no absorbe o libera agua. La actividad de agua de la leche evaporada es de 0.987 mientras que la de la leche condensada azucarada es de 0.830. La actividad de agua no depende del contenido de grasa (Walstra et al., 2006).
El pH tiene una influencia significativa en las propiedades reológicas por la pérdida de
repulsión electrostática cerca de los puntos isoeléctricos de la caseína y la sueroproteína (Trinh, 2006). Cuando el contenido de sólidos en la leche es de 45%, el pH disminuye y la fuerza iónica aumenta conforme se va eliminando el contenido de agua (Bienvenue et al., 2003).
La acidez es un parámetro importante para que la leche resista fuertes tratamientos térmicos, por eso la acidez de la leche debe ser baja, porque un cambio pequeño en la acidez (0.05%) tiene un efecto significativo en la estabilidad térmica y en la tendencia al espesamiento por almacenamiento prolongado (Gèosta y López, 2003; Trinh, 2006).
Las propiedades o características de la leche también varían conforme al porcentaje de humedad. Entre mayor sea el porcentaje de humedad los valores como grasa y proteínas disminuyen. Al reducir el porcentaje de agua que hay en los productos lácteos, por medio de la evaporación, los sólidos totales se concentren, obteniendo así la misma cantidad de sólidos totales pero en un menor contenido de agua. La composición química detallada de la leche entera, las leches condensadas azucaradas y las leches evaporadas se presenta en la Tabla III.
3.2. Propiedades reológicas
Existen varias razones por las cuales es necesario conocer la reología de la leche y de
los productos derivados, por ejemplo, contribuye al conocimiento de su estructura, sirven para efectuar el control de los procesos, para diseñar el equipo y los parámetros de proceso que se van a utilizar y ayuda al mejoramiento y caracterización de los atributos organolépticos del producto final (Zavala, 2005).
Las propiedades reológicas de muchos alimentos líquidos concentrados tienen cambios durante el almacenamiento causados por la temperatura y la concentración, tal es el caso del jugo de naranja, purés de frutas, jugos de frutas clarificados y extracto de café (TelisRomero et al., 2001). Los cambios reológicos durante el almacenamiento de la leche condensada azucarada o la leche evaporada han sido estudiados por algunos autores como Enríquez-Fernández et al. (2011), Fan (2007), González et al. (2008) y Vélez-Ruiz y Barbosa-Cánovas (1998).
Las propiedades reológicas de un alimento líquido, como lo son la leche evaporada y la leche condensada azucarada, son atributos de calidad que pueden afectar la preferencia del consumidor, ya que hay una estrecha relación entre las propiedades reológicas y sensoriales de un alimento (Telcioglu y Kayacier, 2007). Chandan (2006a) menciona que la viscosidad de los productos lácteos crea la impresión de “riqueza” para el consumidor y que, desde el punto de vista organoléptico, la viscosidad contribuye a la sensación de satisfacción en la boca y la liberación de sabor.
Tabla III. Composición química de la leche, leche evaporada y leche concentrada azucarada (g/100g).
ProductoHumedadGrasaProteínasCarbohidratosCenizas/minerales
Leche entera873.73.34.80.7
Leche desnatada90<0.13.44.90.75
Leche evaporada entera*72.7-74.77.5-8.06.5-7.19-10 1.3-1.6
Leche evaporada desnatada79.50.37.6111.6
Leche condensada azucarada2798551.8
Leche condensada azucarada desnatada 280.310592.3
*De acuerdo a un estandar Estadounidense. Adaptada de Tamime et al. ( 2007) .
A concentraciones elevadas de sólidos totales, por encima del 40%, pequeños cambios en la concentración crean un incremento muy grande en la viscosidad de las leches concentradas, pasando así de tener un comportamiento newtoniano a uno no newtoniano conforme los sólidos totales se incrementan (Vélez-Ruiz y Barbosa-Canovas, 1998). Esto ocasiona cambios significativos, como una reducción en la velocidad de flujo, disminución de turbulencia, entre otros factores (Bienvenue et al., 2003).
Existen diferentes modelos matemáticos para expresar el comportamiento reológico de fluidos no newtonianos, los más utilizados en la industria de alimentos son los siguientes (Vélez-Ruiz, 2012; Quintáns, 2008; VélezRuiz y Barbosa-Cánovas, 1997):
Modelo de Bingham ɳ (Ec. 4)
Donde: ɳ es la viscosidad (mPa*s); es el esfuerzo de cizalla (Pa); τo es el esfuerzo inicial (Pa); γ es la velocidad de cizalla (1/s); K es el coeficiente de consistencia (Pa*sn); n es el índice de flujo (adimensional) y ɳ viscosidad aparente. En la Tabla IV se presentan valores de K y n de distintos tipos de leches concentradas.
Modelo Newton ɳ (Ec. 1) (Ec. 1)
Modelo de Ley de Potencia (Ec. 2)
Modelo de Herschel-Bulkley: (Ec. 3)
La viscosidad aparente de las leches concentradas depende mucho de la cantidad de los sólidos totales, la temperatura, el tratamiento térmico previo y la composición de la leche fresca. La viscosidad aparente disminuye con el incremento de la velocidad de cizalla y sigue un comportamiento de la Ley de Potencia (Bienvenue et al., 2003; Trinh, 2006). En la Tabla V se pueden apreciar la densidad, viscosidad aparente y pH de algunos tipos de leche.
evaporada (a 25°C). ProductoTiempo de almacenamiento (semanas)
Coeficiente de consistencia (Pa*s n ) Índice de flujo (adimensional) Referencias
Leche concentrada (22.3% m/m)a 10.0041 20.0050.97 4 0.0050.96
Leche concentrada (42.4% m/m)a 10.0690.89
Vélez-Ruíz y BarbosaCánovas (1998)
Vélez-Ruíz y BarbosaCánovas (1998)
Leche condensada azucarada La Lechera® 0111.6250.821 González et al. (2008) 2120.4750.805 4132.480.777
Leche evaporadab 12 4.711.06 Fan (2007) 244.361 364.611 a: presentaron esfuerzo de cedencia; b: temperatura a 20°C.
Tabla IV. Propiedades reológicas de la leche concentrada, leche condensada azucarada y leche
Tabla V. Algunas propiedades fisicoquímicas de diferentes tipos de leche.
PropiedadLeche fresca Leche desnatada Leche evaporada Leche condensada azucarada
pH6.76.76.26.6
Viscosidad aparente ( mPa*s)
1.91.651715- 60
Densidad (kg*m-3) 1029103510701070
Adaptada de Walstra et al. ( 2006); Farkye y Ur-Rehman (2011).
La leche condensada azucarada es considerada un fluido no newtoniano de comportamiento pseudoplástico, es decir, la viscosidad aparente decrece cuando aumenta la velocidad de deformación. Este tipo de fluidos se caracterizan porque son menos viscosos cuando se someten a altas velocidades de deformación que cuando se someten a cizallamiento más lento. También presenta un comportamiento tixotrópico, es decir, que hay una disminución reversible de la viscosidad aparente con el tiempo, a una velocidad de cizallamiento constante (Ibarz et al., 1987; Vélez-Ruiz y Barbosa-Cánovas, 1997; Bienvenue et al., 2003; González et al., 2008).
Vélez-Ruíz y Barbosa-Cánovas (1998) estudiaron el comportamiento reológico de leche concentrada como función de la concentración, temperatura y tiempo de almacenamiento, y concluyen que estos tres factores tienen una fuerte influencia en el comportamiento reológico. La leche tiene un comportamiento newtoniano cuando contiene hasta un 22.3% de sólidos, pero cuando contiene una mayor cantidad de sólidos se comporta como un fluido no newtoniano. El cambio en el índice de flujo y el coeficiente de consistencia, muestran una relación exponencial con respecto a la concentración (Vélez-Ruíz y Barbosa-Cánovas, 2000).
Fan (2007) evaluó la viscosidad aparente de la leche evaporada (después de 3 semanas de almacenamiento) en función de la temperatura (a 20°C, 30°C y 40°C) y la velocidad de cizalla (a 122.3 s-1, 183.4 s-1 y 244.6 s-1), observó que la viscosidad aparente disminuye conforme aumenta la temperatura, a 20°C es de 6.2 mPa*s y tiene un decremento de aproximadamente 2 y 3 unidades a 30°C y 40°C. Así mismo, la viscosidad aparente se incrementa conforme se incrementa la velocidad de cizallamiento, a 20°C, 30°C y 40°C, incrementó un 0.5 mPa*s, 1.0 mPa*s y 1.5 mPa*s respectivamente.
Otra propiedad que se ve afectada es la textura, ya que está relacionada con los cambios estructurales que se presentan durante el almacenamiento de la leche condensada azucarada, haciendo que la fuerza de compresión y la adhesividad aumenten (González et al., 2008).
4. Investigaciones recientes
Se han llevado a cabo algunas investigaciones de la leche condensada azucarada y la leche evaporada, algunas de ellas son las que se citan a continuación.
Sievanen et al. (2008) analizaron la influencia de la adición de cloruro de calcio
(1-10 mmol/L) en la estabilidad térmica de la leche fresca y la leche concentrada. Como resultado, obtuvieron que la adición de cloruro de calcio en la leche fresca tiene un pronunciado efecto negativo frente al calor inducido por coagulación; en la leche concentrada el cloruro de calcio reduce considerablemente la estabilidad térmica. Mencionan que para una fortificación de la leche con calcio, particularmente con las tratadas con ultrapasteurización o esterilización, el calcio necesita estar adherido en una forma soluble, compleja o encapsulado, la cual no incrementa la concentración del calcio iónico o suero.
Mittal y Bajwa (2011) y González et al. (2008) analizaron la sustitución de la sacarosa y grasa, por un edulcorante no calórico con el fin de lograr un alimento bajo en calorías, y el efecto que tiene, principalmente, en la viscosidad y textura. González et al. (2008) intentaron obtener un producto similar a la leche condensada azucarada, mientras que Mittal y Bajwa (2011) analizaron la calidad de bebidas lácteas. La conclusión a la que llegaron, en ambas investigaciones, es que si se puede reducir el nivel calórico de los productos lácteos al sustituir el azúcar por un edulcorante no calórico, sin embargo al eliminar el azúcar se afecta la viscosidad y la sensación de saciedad, por eso es necesario adicionar un modificador de textura, así que adicionaron inulina o gomas, respectivamente. Estos últimos evaluaron las propiedades de flujo de los sistemas realizados, observando que los sistemas presentaron propiedades de fluido no Newtoniano, siguiendo el modelo de Ley de Potencia; el parámetro K aumenta con el tiempo de almacenamiento, mientras que el índice de flujo (n) disminuye, los dos parámetros fueron afectados por el tipo de leche, el tipo de edulcorante y por la presencia de gomas.
Šostakienė y Blazgienė (2010) y Fan (2007) analizaron los cambios que sufre la leche condensada azucarada y la leche evaporada
durante el almacenamiento. Fan (2007) elaboró leche concentrada por medio de la técnica de filtración de membrana y además caracterizó su composición química, color, viscosidad aparente, comportamiento de flujo y almacenamiento, comparándola con la leche evaporada comercial; mientras que Šostakienė y Blazgienė (2010) analizaron el cambio en la actividad de agua de ambos productos. Las conclusiones a la que llegan en las dos investigaciones son diferentes, Šostakienė y Blazgienė (2010) observaron que no hay cambios significativos en ambos productos, por lo que la posibilidad de crecimiento microbiano es baja, solamente después de 18 meses de almacenamiento se ve un ligero cambio en la leche condensada azucarada. Fan (2007) observó que la leche evaporada tiene un color más blanco que la leche evaporada comercial, una viscosidad aparente de 9.5 mPa*s a 30°C y su comportamiento fue de naturaleza pseudoplástica (n<1), así mismo, durante el almacenamiento el color mostró cambios significativos, perdió blancura y la viscosidad aparente tuvo un incremento, pero su comportamiento continuó siendo ligeramente pseudoplástico.
Conclusiones
En este artículo de revisión se recopiló información sobre la elaboración de la leche condensada azucarada y la leche evaporada y las características fisicoquímicas y reológicas presentes en estos productos. La leche condensada azucarada y la leche evaporada tienen muchos años en el mercado siendo productos muy consumidos que se han estudiado desde hace tiempo, sin embargo, no hay mucha información reciente para las propiedades físicas, por lo cual es necesario desarrollar nuevos estudios de las propiedades físicas que cambian en el proceso de estas leches concentradas.
Las propiedades fisicoquímicas y reológicas son muy importantes para obtener un producto final con las características apropiadas. Se deben tomar en cuenta desde el principio como parámetros críticos de su elaboración y con base a esto, monitorearlas. Así mismo, las propiedades reológicas son sumamente importantes en este tipo de productos, ya que la viscosidad es lo que los caracteriza. Las propiedades fisicoquímicas y reológicas sirven como parámetros de calidad y de ellas depende la aceptación o rechazo del cliente.
Carić, M, Akkerman, J. C., Milanović, S., Kentish, S. E. y Tamime, A. Y. 2009. Technology of Evaporators, Membrane Processing and Dryers. En: A.Y. Tamime (Ed). Dairy Powders and Concentrated Products. Wiley-Blackwell. West Sussex, Inglaterra. p 99-148
Chamorro, M. C. y Losada, M. M. 2002. El Análisis Sensorial de los Quesos. Mundi-Prensa. Madrid, España. 235 p.
Chandan, R. C. 2006a. Milk Composition, physical and processing characteristics. En: R. Chandan, White, C. H., Kilara, A. y Hui, Y. H (Eds). Manufacturing Yogurt and Fermented Milks. p. 17. Blackwell Publishing. Oxford, Inglaterra. p. 17-40.
Agradecimientos
La autora Marcelín-Rodríguez agradece al Consejo Nacional de Ciencia y Tecnología (CONACYT) y a la Universidad de las Américas Puebla (UDLAP) por el apoyo para sus estudios de posgrado.
Chandan, R. C. 2006b. History and consumption trends. En: R. Chandan, White, C. H., Kilara, A. y Hui, Y. H (Eds). Manufacturing Yogurt and Fermented Milks. Blackwell Publishing. Oxford, Inglaterra. p. 3-16.
Enríquez-Fernández, Camarillo-Rojas, C. y Vélez-Ruiz. Physical properties of concentrated milk and its influence on powder milk characteristics and spray dryer design parameters. Journal of Food Process Engineering (2011) DOI 10.1111/j.17454530.2011.00656.x
Referencias
Alais, C. 2003. Ciencia de la Leche: Principios de Técnica Lechera. Cuarta Edición. Ed. Reverté, S. A. Barcelona, España. 873 p.
Bienvenue, A., Jiménez-Flores, R. y Singh, H. 2003. Rheological properties of concentrated skim milk: Importance of soluble minerals in the changes in viscosity during storage. Journal of Dairy Science 86 (12): 3813-21.
Boland, M. 2003. Influence on raw milk quality. En: G. Smith (Ed). Dairy Processing. CRC Press. Boca Raton. Estados Unidos. p. 42-67.
Bonet, B., Juárez, M., Moreno, B., Ortega, R. M. y Suárez, L. 2003. El Libro Blanco de los Lácteos. España. En: www.lacteosinsustituibles.es/p/archivos/pdf/LibroBl anco.pdf. accesada 10/02/12.
Brown, A. 2008. Understanding Food: Principles and Preparation. Cuarta edición. Wadsworth, Cengage Learning. Belmont, Estados Unidos. p. 210-231.
Fan, E. 2007. Development and characterization of a novel concentrated milk product using membrane filtration technology. Honor Tesis, Research Honors Program. College of Agriculture and Life Sciences Physical Sciences of Cornell University (Estados Unidos). p. 39
Farkye, N. y Ur-Rehman. 2011. Concentrated fluid milk ingredients. En: White, C. H., Kilara, A. y Hui, Y. H (Eds). Dairy Ingredients for Food Processing Wiley-Blackwell. Boca Raton, Estados Unidos. p. 604.
Food Safety Standards Authority of India. 2011. Ministry of Health and family welfare. Nueva Delhi. En: www.dfda.goa.gov.in/uploads/Food%20safety%20a nd%20standards%20(Food%20product%20standard s%20and%20Food%20Additives)%20regulation,%2 02011.pdf. accesada 10/02/2012.
Gèosta, M. y López, A. 2003. Manual de Industrias Lácteas. Mundi-Prensa Libros. Madrid, España. p. 436.
González, A., Sosa, M. y Vélez. 2008. Efecto de la sustitución de sacarosa por otros edulcorantes en las propiedades de leche condensada-azucarada. Conferencia Internacional sobre Ciencia y
Tecnología de los Alimentos (CICTA-11). Habana, Cuba. Octubre 13-17/2008.
Goff, D. 2007. Dairy Product Processing Equipment. En: Myer Kutz (Ed.). Handbook of Farm, Dairy, and Food Machinery. William Andrew Publishing. Norwich, Nueva York, Estados Unidos. p.167-189.
Hall, C. y Hedrick, T. I. 1971. Drying of Milk and Milk Products. Segunda edición. The AVI Publising Company, Inc. Connecticut, Estados Unidos. p. 338.
Ibarz, A. 2005. Operaciones Unitarias en la Ingeniería de Alimentos. Mundi-Prensa Libros. Madrid, España. p. 864.
Ibarz, A., García, J. L. y Llorens, J. 1987. Análisis tixotrópico de leches concentradas. Alimentaria Octubre, p. 35-38.
Ledenbach, L. y Marshall. R. 2009. Microbiological spoilage of dairy products. En: W. Sperber y M. Doyle (Eds). Microbiological Spoilage of Dairy Products. Springer Science+Business Media. Nueva York, Estados Unidos. p. 41-67.
Maza, M. y Legorreta, P. 2011. Generalidades de la leche y los productos lácteos. En: Libro Blanco de la Leche y los productos Lácteos. Editorial Cámara Nacional de Industriales de la Leche (CANILEC), México, D.F. p. 26-43
Miller, G. D., Jarvis, J. K. y McBean, L. D. 2000. Handbook of Dairy Foods and Nutrition. Tercera edición. CRC Press LLC. Boca Raton, Estados Unidos. p. 407.
Mittal, S. y Bajwa, U. Effect of fat and sugar substitution on the quality characteristics of low calorie milk drinks. Journal of Food Science Technology (2011). DOI 10.1007/s13197-0100216-9
Norma Oficial Mexicana 155. NOM-155-SCFI-2003. 2003. “Leche, formula lácteas y producto lácteo combinado - Denominaciones, especificaciones fisicoquímicas, información comercial y métodos de prueba”.
Oliveira, M. N., Penna A. L. B. y García Nevarez, H. 2009. Production of evaporated milk, sweetened condensed milk and “Dulce de Leche”. En: A. Y. Tamime (Ed). Dairy Powders and Concentrated Products. Wiley- Blackwell. West Sussex, Inglaterra. p. 149-179.
Quintáns, L. 2008. Reología de productos alimentarios. Tesis de Doctorado. Universidad de Santiago de Compostela (España). p. 224.
Revilla, A. 1982. Tecnología de la Leche. Procesamiento, Manufactura y Análisis. Segunda edición. Ed. Instituto Interamericano de Cooperación para la Agricultura. San José, Costa Rica
SAGARPA. 2011. Boletín de la Leche: Enero-Marzo de 2011. México. En: www.campomexicano.gob.mx/portal_siap/Inte gracion/EstadisticaDerivada/ComercioExterior/ Estudios/BoletinLeche/Leche_marzo_2011.pdf accesada 16/02/2012.
SECOFI. Secretaria de Comercio y Fomento Industrial. 1999. Guías empresariales. Cajeta y otros dulces de leche. Ed. Aconcagua. México, D.F.
Sievanen, K., Huppertz, T., Kelly, A. y Fox, P. 2008. Influence of added calcium chloride on the heat stability of unconcentrated and concentrated bovine milk. International Journal of Dairy Technology 61 (2): 151-155.
Šostakienė, I. y Blazgienė, J. 2010. Water activity influence on the safe aging period of condensed milk. Annals of Food Science and Technology 11(1): 21-24.
Tamime, A. Y., Robinson, R. K. y Michel, M. 2007. Microstructure of concentrated and dried milk products. En: A. Y. Tamime (Ed.). Structure of Dairy Products. Blackwell Publishing. Oxford, Inglaterra. p. 104-133.
Telcioglu, A., y Kayacier, A. 2007. The effect of sweeteners and milk type on the rheological properties of reduced calorie salep drink. African Journal of Biotechnology 6(4): 465-469.
Telis-Romero, J., Ferreira, A., Gabas, A. y Nicoletti, V. 2001. Rheological properties and fluid dynamics of coffee extract. Journal of Food Process Engineering 24(4): 215-230.
Trinh, B. 2006. Rheological characterization of agethickening in milk concentrates. Tesis de Doctorado. Massey University, Nueva Zelanda. p. 494.
Tur Marí, J. A. 2005. La leche y los productos lácteos en la historia de la alimentación. En: J. Aranceta y U. Serra (Eds) LECHE, Lácteos y Salud. Editorial Médica Panamericana. Madrid, España. p. 1-8.
Valle, M. y Álvarez, A. 1997. La producción de leche en México en la encrucijada de la crisis y los acuerdos del TLCAN. En http://bibliotecavirtual.clacso.org.ar/ar/libros/lasa97/ delvrivalvarez.pdf. accesada 16/02/2012.
Varnam, A. H. y Sutherland, J. 2001. Milk and Milk Products: Technology, Chemistry, and Microbiology. Aspen Publishers, Inc. Nueva York, Estados Unidos. p. 451.
Vélez-Ruíz, J. 2009. Evaporation of liquid foods. En: M. E. Sosa-Morales y J. F. Vélez-Ruíz (Eds). Food Processing and Engineering Topics. Nova Science Publishers, Inc. Nueva York, Estados Unidos. p. 179.
Vélez-Ruíz, J. 2012. Apuntes de Propiedades Físicas de los Alimentos. Inéditos. Universidad de las Américas Puebla, México.
Vélez-Ruíz, J. y Barbosa-Cánovas, G. 1997. Rheological properties of selected dairy products. Critical Reviews in Food Science and Nutrition 37 (4): 311-359.
Vélez-Ruiz, J. y Barbosa-Cánovas, G. 1998. Rheological properties of concentrated milk as a function of concentration, temperature and storage time. Journal of Food Engineering, 35 (2): 177-190
6 – 1 (2012): 13 - 28
Vélez-Ruiz, J. y Barbosa-Cánovas, G. 2000. Flow and structure characteristics of concentrated milk. Journal of Texture Studies 31: 315-333.
Walstra, P., Wouters, J. y Geurts, T. 2006. Dairy Science and Technology. Segunda edición. Taylor & Francis Group. Boca Raton, Estados Unidos. p. 782.
Westergaard, V. 2004. Tecnología de la Leche en Polvo: Evaporación y Secado por Atomización. Niro A/S. Copenhague, Dinamarca. p. 318.
Zavala, M. J. 2005. Aspectos nutricionales y tecnológicos de la leche. Dirección General de Promoción Agraria Ministerio de Agricultura y Dirección de Crianzas. En: http://vaca.agro.uncor.edu/~pleche/material/Material %20II/A%20archivos%20internet/Biologia%20y%2 0fisiologia%20de%20la%20lactacion/agroin_doc2.p df. accesada 12/02/2012.

Temas Selectos de Ingeniería de Alimentos 6 - 1 (2012): 29 - 39

Vapores de aceites esenciales: alternativa de antimicrobianos naturales
F. Reyes-Jurado*, E. Palou y A. López-Malo
Departamento de Ingeniería Química, Alimentos y Ambiental, Fundación Universidad de las Américas Puebla. Exhacienda Sta. Catarina Mártir S/N, Cholula, Puebla. C.P.72810. México.
Resumen
La actividad antimicrobiana de aceites esenciales extraídos de plantas y especias adicionados en forma directa a sistemas modelo ha sido estudiada y evaluada constantemente durante los últimos años. Sin embargo, la actividad antimicrobiana de diversos aceites esenciales en fase vapor y su efectividad contra mohos, levaduras y bacterias empezó a investigarse recientemente, siendo aún escasos los aceites esenciales y los microorganismos evaluados. El objetivo de este trabajo es revisar investigaciones que muestren el efecto antimicrobiano que tienen los aceites esenciales en fase líquida y en fase vapor. Se incluyen las propiedades antimicrobianas que poseen los aceites esenciales, así como el uso potencial que tienen en alimentos. Si bien son escasas las investigaciones que se han realizado acerca de aceites esenciales en fase vapor, ellas han tenido resultados alentadores, por lo que la posible aplicación real de los aceites esenciales en alimentos parece rentable y aún sigue en estudio.
Palabras clave: actividad antimicrobiana, aceites esenciales, fase vapor.
Abstract
The antimicrobial activity of essential oils of plants and spices directly added to model systems has been studied and evaluated in recent years. However, the study of the antimicrobial activity of some essential oils in vapor phase and their effectiveness against molds, yeasts and bacteria has been studied recently, being evaluated just a few essential oils and microorganisms. The aim of this work is to review recent research works about the effectiveness of essential oils in liquid and vapor phase, refered to their antimicrobial properties as well as their potential use in food. In spite of there are scarce research works about the antimicrobial activity of essential oils at vapor phase, the results are encouraging and they suggest their possible use in food although it is still under study.
Keywords: the antimicrobial activity, essential oils, vapor phase.
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: fatima.reyesjo@udlap.mx
Introducción
A nivel mundial se puede apreciar, en los últimos años, una tendencia a consumir alimentos naturales, seguros y de buena calidad; aunado a esto, numerosas investigaciones indican el efecto antimicrobiano que tienen los aceites esenciales extraídos de plantas y especias (Inouye et al., 2001; 2006; Dao et al., 2008; Goñi et al., 2009). Así, el control microbiano mediante el uso de aceites esenciales se ha convertido en una de las áreas de investigación más importantes con la finalidad de sustituir conservadores sintéticos por naturales.
Una de las limitaciones en el uso de aceites esenciales como antimicrobianos en alimentos, es que al utilizarlos de manera directa (fase líquida), son menos eficaces en alimentos que de forma in vitro, por lo que se tienen que utilizar concentraciones mayores para obtener el mismo efecto, con el inconveniente de que se modifican los atributos sensoriales del alimento y se altera la calidad del mismo (Phillips et al., 2011); por ello es necesario experimentar otras alternativas de aplicación, como el uso de aceites esenciales en fase vapor.
Estudios recientes han demostrado que los vapores generados por aceites esenciales poseen efectos antimicrobianos (López et al., 2005; 2007; Gómez-Sánchez et al., 2011; Kloucek et al., 2011) por lo que algunos investigadores (Aslan et al., 2004; Tzortzakis, 2007; Ávila-Sosa et al. 2012) proponen utilizarlos como una alternativa de su aplicación como agentes antimicrobianos, ya que afectarían en menor grado las características sensoriales, asegurando así mismo la inocuidad del producto.
Por lo anterior, el objetivo de este trabajo es revisar las investigaciones que muestran los avances recientes sobre el mecanismo de acción de los aceites esenciales en fase líquida
y en fase vapor contra microorganismos patógenos o deteriorativos en alimentos, de tal manera que el uso de vapores de aceites esenciales sea una nueva alternativa de aplicación de antimicrobianos naturales, supliendo tanto los métodos tradicionales de adición directa como el empleo de los antimicrobianos sintéticos tradicionales.
Revisión bibliográfica
1. Aceites esenciales extraídos de plantas y especias
En diferentes países existe una gran variedad de plantas y especias, las cuales tienen diferentes usos conforme a la cultura y costumbres de cada región. Muchas de estas plantas y especias se han relacionado con propiedades antimicrobianas (RaybaudiMassilia et al., 2006; López-Malo et al., 2005). De acuerdo a Tajkarimi et al. (2010), se han encontrado alrededor de 1340 plantas a las que se les han atribuido propiedades antimicrobianas y en las cuales se han identificado alrededor de 30,000 componentes activos.
Los principales componentes de una planta y/o especia incluyen a los glucósidos, saponinas, taninos, alcaloides, ácidos orgánicos y componentes volátiles, entre otros; de los cuales muchos actúan como protección de las plantas y especias contra infecciones microbiológicas del medio ambiente (Tajkarimi et al., 2010).
Para la obtención de los aceites esenciales de plantas y/o especias, se utilizan diferentes métodos, dos de los principales son la destilación por medio de arrastre de vapor y la extracción con solventes orgánicos (Sivropoulou et al., 1996; Kalemba y Kunicka, 2003; Raybaudi-Massilia et al., 2006). En ambos casos, debe tenerse especial
cuidado en su manejo y almacenamiento, dado que los aceites esenciales son líquidos viscosos, altamente volátiles y sensibles a altas temperaturas (Kalemba y Kunicka, 2003; Raybaudi-Massilia et al., 2006).
La composición de los aceites esenciales varía de acuerdo a las diferentes partes de la planta de las cuales se extrae (Burt, 2004), y puesto que sus compuestos volátiles son los que presentan el efecto antimicrobiano, la determinación de su composición es importante; para ello, diversos investigadores emplean la cromatografía de gases acoplado a espectrometría de masas (CG-MS) (Caccioni et al., 1998; Lee et al., 2005; Tyagi y Malik, 2011; Gómez-Sánchez et al., 2011).
Asimismo, se ha demostrado que los principales componentes volátiles de estos aceites derivan de un grupo de terpenoides, sesquiterpenos y posiblemente diterpenos, los cuales a su vez contienen diferentes grupos de hidrocarburos, ácidos, alcoholes, aldehídos, ésteres, éteres y cetonas. Por lo tanto, de acuerdo al grupo químico funcional de cada aceite esencial, se derivan sus componentes principales. En la Tabla I se pueden apreciar algunos de los diferentes componentes dependiendo del grupo químico funcional al que pertenecen. Se ha reportado que los componentes mayoritarios pueden alcanzar hasta un 85% de la composición total del aceite esencial, mientras que los demás pueden estar presentes solo como trazas, lo cual puede observarse en la Tabla ІІ (Solórzano-Santos y Miranda-Novales 2011; Kalemba y Kunicka, 2003; Raybaudi-Massilia et al., 2006; Fisher y Phillips, 2008 y Tajkarimi et al., 2010).
2. Propiedades antimicrobianas y mecanismos de acción de aceites esenciales
Dado que el efecto antimicrobiano de cada aceite esencial es diferente su actividad
Tabla Ι. Algunos componentes volátiles de acuerdo al grupo funcional mayoritario del aceite esencial.
Grupo Químico FuncionalComponentes
Fenoles
Aldehídos
Alcoholes
Alcoholes sesquiterpenos
Cetonas
Ésteres
Éteres y Oxidos
Hidrocarburos
Adaptada de Inouye et al . (2006).
Carvacrol
Eugenol
Timol
Citral
Citronela
Benzaldehído
Perilaldehído
Cinamaldehído
Terpenos
Borneol
Mentol
Geraniol
Linalol
Feniletanol
Farnecol
Cedrol
Alcanfor
Carvona α-tujona
Acetato de linalilo
Salicilato de metilo
Etil acetato
Anetol
Metil timol
Anetol
Cineol
Careno
β-cariofileno
α-pineno
Limoneno
Tabla ΙΙ. Principales componentes volátiles de aceites esenciales de especias y plantas encontradas comúnmente.
Nombre común Nombre científicoComponente mayoritarioComposición aproximada (%)
Cilantro
Coriandrum sativum (seeds)
Canela Cinnamomum zeylandicum
Orégano
Origanum vulgare
Romero
Rosmarinus officinalis
Linalol70%
E-2-decanal-
Trans-cinamaldehido65%
Carvacroltraza 80%
Timoltraza 64%
У -Terpineno2-52%
p -cimenotraza 52%
α-pineno2-25%
Acetato de bornilo0-17%
Alcanfor2-14%
1,8 cineol3-89%
Alcanfor6-15%
α-pineno4-5%
β -pineno2-10%
1,8-cineol6-14%
α-tujona20-42%
Eugenol75-85%
Clavo
Syzygium aromaticum
Tomillo
Thymus vulgaris
Adaptada de Burt (2004).
antimicrobiana pueden ser evaluada como la concentración mínima inhibitoria (CMI), la cual se define como la concentración mínima requerida del aceite esencial que tenga la capacidad de frenar el crecimiento del microorganismo (propiedades bacteriostáticas o fungistáticas) (Smith-Palmer, et al., 1998) o la concentración mínima letal que asegure la reducción de un 99.9% de la población del microorganismo (propiedades bactericida y fungicida) (Burt, 2004). Además, la actividad de los aceites esenciales contra mohos también puede ser evaluada por el control de la
Acetato de eugenilo8-15%
Timol10-64%
Carvacrol2-11%
У -Terpineno2-31%
p -cimeno 10-56%
inhibición de la esporulación y la producción de toxinas (Kalemba y Kunicka, 2003).
En este sentido, se puede resumir que la actividad antimicrobiana de los aceites esenciales depende principalmente de tres características; su carácter hidrófilo o hidrófobo, sus componentes químicos y el tipo de microorganismo al que debe atacar (Kalemba y Kunicka 2003; López-Malo et al., 2005; Fisher y Phillips, 2008; SolórzanoSantos y Miranda-Novales, 2011).
Salvia officinalis L.
Salvia
El modo de acción de los aceites esenciales en cuestión a su carácter (hidrófilo o hidrófobo) se debe a que tienen la capacidad de alterar y penetrar en la estructura lipídica de la pared celular perturbando estructuras celulares lo que lleva a la desnaturalización de las proteínas y a la destrucción de la membrana celular, haciéndolas más permeables, lo que conduce a rupturas o fugas citoplásmicas, lisis celular y eventualmente la muerte del microorganismo. Respecto a sus componentes, ellos también pueden actuar como agentes que interfieren con la translocación de protones y la fosforilación del ATP (Smith-Palmer et al., 1998; Kalemba y Kunicka 2003; Holley y Patel, 2005; Fisher y Phillips, 2008; Solórzano-Santos y MirandaNovales 2011).
Delaquis et al. (2002) y Holley y Patel (2005) mencionan que los componentes fenólicos son los principales responsables de las propiedades antimicrobianas de los aceites esenciales. En el mismo sentido, en una investigación realizada por Fisher y Phillips (2008), ellos reportan que el carvacrol aumenta la fluidez de la membrana y causa fuga de protones e iones de potasio, lo que resulta en un colapso del potencial de membrana y la inhibición de la síntesis del ATP. Por otra parte, la citronela interfiere con los procesos de fotosíntesis, lo que sugeriría que los aceites esenciales no sólo pueden estar actuando en la pared celular, sino que además pueden tener un efecto mayor sobre los sistemas metabólicos. Del mismo modo, Fisher y Phillips (2008) refieren que el mentol tiene un efecto “antiplasmid” (secuencia extracromosómica de ADN que no pude ser compartida entre los patógenos) lo que hace interrumpir la eficiencia de la célula.
Por otro lado, en las bacterias Gramnegativas se ha observado mayor susceptibilidad a los aceites esenciales a diferencia de las Gram-positivas y aunque aún no se sabe exactamente la razón por la cual se
da este hecho, Smith-Palmer et al. (1998), Kalemba y Kunicka (2003) y Fisher y Phillips (2008) reportan que la susceptibilidad de las bacterias Gram-negativas puede estar relacionada con la membrana externa que poseen este tipo de bacterias, ya que la hidrofobicidad de la membrana la hace impermeable. Sin embargo, Fisher y Phillips (2008) mencionan que solo hay un retardo del efecto por lo que sugieren que para alcanzar el mismo efecto letal en ambos tipos de bacterias, se requeriría de un mayor periodo de tiempo de exposición a los aceites esenciales en los sistemas modelo. No obstante, esta sensibilidad de los diferentes tipos de bacterias solo se ha observado al utilizar aceites esenciales en forma in vitro, pero no en alimentos.
3. Efecto antimicrobiano de vapores de aceites esenciales
Aunque los aceites esenciales obtenidos de distintas plantas y especias tienen efectos antimicrobianos y muchos de ellos son considerados como GRAS (Ávila-Sosa et al., 2012 y López-Malo et al., 2005), su aplicación como aditivos en alimentos está limitada principalmente por las alteraciones que causan en sus características sensoriales (RaybaudiMassilia et al., 2006; López-Malo et al., 2005). En el mismo sentido, y con el fin de reducir éstos efectos, Suhr y Nielsen (2003) y Goñi et al. (2009) proponen una serie de soluciones a este problema, dentro de las que destacan la utilización de bajas concentraciones de aceites esenciales, mezclas sinérgicas de aceites o la utilización de los aceites esenciales en fase vapor.
3.1. Generación de vapores
La generación de vapores de aceites esenciales se basa en la creación de una atmósfera a una cierta temperatura, o un microambiente dado por los propios aceites (López et al., 2005). Hasta el momento, no se ha encontrado una
metodología estándar para evaluar la inhibición microbiana por medio del contacto con vapores de aceites esenciales; sin embargo existen algunos métodos reportados, dentro de los cuales destacan:
1) Uso de cajas invertidas, lo cual consiste en colocar los agares inoculados con el microorganismo de prueba de forma separada (aproximadamente 5 mm) de los aceites esenciales (previamente disueltos en acetato de etilo, o en algún otro solvente) sobre un papel filtro y manteniendo la temperatura controlada. Su principio se basa en la rápida volatilización de los vapores los cuales entran en contacto con el microorganismo. Por lo que esta técnica es mayormente utilizada para bacterias, las cuales tienen mayor velocidad de crecimiento en comparación con los mohos (Inouye et al., 2001; Edris y Farrag, 2003; Suhr y Nielsen, 2003; Inouye et al., 2006; Kloucek et al., 2011).
2) Creación de una atmósfera a partir de aceites esenciales, lo cual consiste en utilizar cámaras de plástico (aproximadamente de 11.7 litros) con tapa transparente y selladas herméticamente: en su interior y en el centro se coloca cierta concentración del aceite esencial y sobre una rejilla se colocan los agares inoculados; las cámaras se mantienen a una temperatura controlada en condiciones estándar para mohos a 25 °C por 72 horas (Suhr y Nielsen, 2003; Gómez-Sánchez et al., 2011) y 37 °C por 18-24 horas para bacterias (Kloucek, et al., 2011). De tal manera que los vapores generados por los aceites esenciales entran en contacto con los microorganismos, y consecuentemente su evaporación en el interior del microambiente puede generar zonas de inhibición. Este método se usa principalmente para mohos, ya que su velocidad de crecimiento es lenta.
Para la cuantificación de componentes en la fase vapor se utiliza la microextracción en fase sólida (SPME por sus siglas en inglés), en la
cual una gota (aprox. 1-3 μL) de un disolvente orgánico se suspende en la punta de una microjeringa (como medio de extracción) y se expone a la atmósfera creada por el aceite esencial durante un tiempo y temperatura conocidos (López et al., 2007).
En cualquier técnica utilizada posteriormente al periodo de incubación, la concentración mínima inhibitoria (CMI) se expresa como la mínima concentración de vapor (microlitros de aceite esencial por litro de aire) que inhibe el crecimiento visible ya sea de mohos, levaduras o bacterias (López et al., 2005, 2007; Tullio et al., 2007).
3.2 Actividad antimicrobiana en fase vapor
Algunas investigaciones han reportado que el uso de los vapores generados por aceites esenciales tiene mayor efecto antimicrobiano, en comparación con el contacto directo (forma líquida) (Tullio et al., 2007; Inouye et al., 2001, 2006; Fisher y Phillips, 2008). Esto ha tenido especial impacto contra mohos, ya que debido a su crecimiento superficial, ellos son más susceptibles a los vapores de los aceites esenciales (Edris y Farrag, 2003).
Los vapores generados por los aceites esenciales atacan al ciclo de vida de algunos mohos en la etapa de germinación, en la de crecimiento de la hifa y en la etapa de esporulación; la inactivación del conidio presente en el aire por los vapores de aceites esenciales es el proceso clave en la inhibición, dado que el conidio (suspendido en el aire) es estable al calor, a la luz y a los compuestos químicos químicos, siendo muy difícil de eliminar (Dao et al., 2008). Este efecto, afirman Suhr y Nielsen (2003), se ha observado sólo por contacto con vapores de aceites y no de forma directa, ya que los vapores pueden unirse a la hifa reproductiva a diferencia del contacto con una solución.
Estudios recientes señalan que la actividad antimicrobiana de los aceites esenciales en fase vapor es eficiente en concentraciones altas y en tiempos cortos (Dao et al., 2008). Aslan et al. (2004) evaluaron la actividad de tres aceites esenciales (tomillo, albahaca, y ajedrea) contra Bemisia tabaco (mosca blanca) y Tetranychus urticae (ácaro) ambos infestadores de plantas; los resultados mostraron que los tres aceites esenciales fueron tóxicos contra estos organismos, demostrando que al aumentar la dosis del aceite esencial aumentaba el efecto antimicrobiano.
En la misma línea, en un estudio realizado por López et al. (2005), se comparó la efectividad en fase vapor y en fase líquida (contacto directo) de aceites esenciales de canela, clavo, albahaca, romero, eneldo y jengibre contra 4 bacterias Gram-positivas (Staphylococcus aureus, Bacillus cereus, Enterococcus faecalis y Listeria monocytogenes), cuatro bacterias Gramnegativas (Escherichia coli, Yersinia enterocolitica, Salmonella choleraesuis y Pseudomonas aeruginosa) y tres hongos (una levadura, Candida albicans, y dos mohos, Penicillium islandicum y Aspergillus flavus); los resultados obtenidos demostraron que los aceites esenciales tuvieron mayor efectividad contra mohos que contra bacterias. Además, los aceites esenciales de canela y clavo mostraron la mayor actividad en ambos métodos, y los aceites esenciales de romero y albahaca no mostraron actividad antimicrobiana en fase vapor, pero sí en contacto directo.
Lo anterior sugiere que la actividad de los aceites esenciales depende del microorganismo que se desea atacar. Lo anterior se refuerza con un estudio realizado por Kloucek et al. (2011), en el cual ellos evaluaron el efecto antimicrobiano en fase vapor de sesenta y nueve aceites esenciales, demostrando que treinta y nueve de ellos
tuvieron actividad antimicrobiana en fase vapor; del mismo modo, señalan que los mohos son más susceptibles a dicho efecto a diferencia de las bacterias.
Del mismo modo, Inouye et al. (2001) compararon la eficacia en fase vapor de aceites esenciales (tomillo, té limón, pimienta, cilantro, canela, eucalipto, limón y lavanda) contra diferentes bacterias. En dicho estudio se demostró que los aceites esenciales de canela, té limón y tomillo tuvieron la mayor actividad antimicrobiana dado que sus componentes mayoritarios eran fenoles y aldehídos; sin embargo aceites esenciales provenientes de pimienta, lavanda y cilantro mostraron actividad moderada, y los aceites de limón y eucalipto mostraron una baja actividad antimicrobiana.
Asimismo, Inouye et al. (2006) realizaron una investigación con diferentes aceites esenciales en la cual evaluaron su efecto antifúngico; en este estudio se demostró que los fenoles eran los componentes mayoritarios que exhibían actividad antifúngica en fase vapor. Además, se obtuvo que la actividad antifúngica se fue reduciendo de acuerdo al siguiente orden de componentes principales: alcoholes >cetonas > éteres > óxidos. Los aceites que contenían alcoholes como su principal componente, (cilantro, geranio, lindera, palmarosa, menta, palo de rosa y tomillo), eran relativamente más potentes, dado que tuvieron la menor dosis mínima fungicida (DMF) de 6.25 μg/mL de aire. Sin embargo, los aceites esenciales que contenían cetonas como componente principal mostraron potencia moderada, ya que tuvieron mayor DMF (25 μg/mL de aire). Del mismo modo, los aceites que contenían ésteres, éteres y óxidos, mostraron la menor potencia, por lo que tuvieron la mayor DMF (50 μg/mL de aire).
Tullio et al. (2007) en otro estudio evaluaron la actividad antifúngica de siete
aceites esenciales (tomillo, salvia, hinojo, limón, pino, lavanda y clavo), e identificaron que el aceite esencial que tuvo mayor efectividad fue el tomillo, seguido por el de clavo y el de hinojo, y posteriormente por el de pino; por otra pate los aceites esenciales provenientes del limón y lavanda tuvieron muy poca actividad antifúngica. Por lo tanto, se demostró que cinco de los siete aceites esenciales evaluados tuvieron una CMI menor al ser aplicados en fase vapor respecto a la CMI en fase líquida, entre estos, el aceite esencial de tomillo exhibió la mayor actividad, seguido de los aceites esenciales de bálsamo, limón, clavo, lavanda y salvia; mientras tanto, la actividad de los aceites esenciales de hinojo y pino fue la más débil cuando se evaluaron de esta forma.
En la misma línea, López et al. (2007) realizaron una investigación con tres tipos de aceites esenciales (canela, tomillo y orégano); en este estudio se demostró la actividad antibacteriana y antifúngica que tuvieron los tres aceites. El aceite esencial de canela tuvo un mayor efecto antifúngico que antibacteriano, pues obtuvo una CMI muy baja contra un moho (Asperigllus flavus, 13.1 μL/L), a diferencia de una bacteria Grampositiva (Enterococcus faecalis, 52.4 μL/L). Por otra parte, en el aceite de orégano la CMI contra una bacteria Gram-negativa (Yersinia enterolitica, 4.4 μL/L) fue menor a la requerida para un moho (Penicillium islandicum, 17.5 μL/L). En el caso del aceite esencial de tomillo a diferencia de los dos aceites antes mencionados, las concentraciones mínimas requeridas para inhibir el crecimiento microbiano fueron notablemente mayores, ya que la CMI del aceite esencial del tomillo contra una levadura (Candida albicans) fue de 26.2 μL/L, y el de una bacteria Gram-positiva (Bacillus cereus) fue de 131 μL/L, notándose una gran diferencia respecto a los aceites de orégano y canela. Esto puede atribuirse a los componentes mayoritarios de cada aceite esencial, ya que como se mencionó
anteriormente los aceites esenciales que son ricos en compuestos fenólicos son lo que poseen mayor potencia antimicrobiana.
3.3 Aplicaciones reales o potenciales
Puesto que los efectos antimicrobianos de vapores generados por aceites esenciales contra diferentes microorganismos siguen en estudio, son escasos los reportes que indiquen su posible aplicación en alimentos. Sin embargo, dentro de estas investigaciones se ha mostrado un efecto positivo al utilizar los aceites esenciales en fase vapor principalmente en empaques activos (Nielsen y Rios, 2000; Skandamis y Nychas, 2002; Serrano et al., 2005). Asimismo Ávila-Sosa et al., (2012) sugieren que los vapores de aceites esenciales, se incorporen en películas comestibles de quitosano.
Tzortzakis (2007) evalúo la calidad de dos vegetales (fresa y jitomate), los cuales fueron expuestos a vapores de aceites esenciales de eucalipto y canela. En esta investigación, se demostró que los dos vegetales, además de tener una protección contra microorganismos, conservaron su calidad al estar expuestos a diferentes concentraciones de los aceites esenciales en fase vapor. El mismo autor menciona que hay un uso potencial al incluir los aceites esenciales (fase vapor) en empaques o envases activos.
En el mismo sentido, Phillips, et al. (2011) comprobaron el poder antifúngico de una mezcla de aceites esenciales en fase vapor de dos cítricos (bergamota y naranja), al exponerlos en tomates y granos; este estudio demostró que la mezcla de aceites esenciales en fase vapor, funcionó como antifúngico y no afectó las propiedades organolépticas de los alimentos. Asimismo, los autores sugieren el almacenamiento de granos en presencia de aceites esenciales en fase vapor, a fin de preservarlos.
A partir de lo anterior, el realizar estudios donde se evalúen las características organolépticas de un alimento expuesto a vapores de aceites esenciales, en comparación con aquellos en los que fueron añadidos directamente (en forma líquida), sería un excelente recurso para identificar la rentabilidad de los vapores de aceites esenciales como antimicrobianos naturales.
En este sentido, Jobling (2000) demostró que setas (champiñones) empacadas en bolsas de plástico con atmósfera modificada a base de dióxido de carbono, oxígeno y vapores de aceite esencial de eucalipto, tenían mejor apariencia (color), a diferencia de los que no habían sido expuestos a los vapores. Por otra parte, el crecimiento bacteriano se redujo significativamente.
Por su parte Nielsen y Rios (2000) emplearon empaques activos con base en la utilización de bolsas que contenían nitrógeno, dióxido de carbono y diferentes aceites esenciales en fase vapor (orégano, canela, clavo, vainilla, ajo y mostaza), para almacenar pan de centeno y un pan (media noche). En el estudio se observó que los aceites esenciales fueron capaces de controlar eficientemente el crecimiento de mohos, siendo el aceite de mostaza el que mostró mayor efecto antifúngico.
En la misma línea, Skandamis y Nychas (2002) evaluaron la calidad de carne fresca almacenada en empaques activos a base de atmósferas modificadas generadas por CO2, N2, O2 y en presencia de aceite esencial de orégano. En esta investigación, demostraron que la presencia del aceite esencial de orégano contribuía al nivel organoléptico y microbiológico, ya que la apariencia visual y sabor de la carne no se alteró. Sin embargo, se encontró que el aceite esencial de orégano en
fase vapor, empleado en empaques con atmosferas modificadas, inhibió en menor proporción el crecimiento de las bacterias, en comparación al utilizado de manera directa (líquida).
En otro estudio, Wang (2003) identificó el efecto que tenían algunos compuestos volátiles de aceites esenciales (entre ellos el aceite esencial del árbol de té) en empaques activos sobre la preservación de la calidad de frambuesa utilizando atmósferas modificadas. El autor demostró que los empaques activos almacenados a 10°C mantenían la calidad y retrasaban el deterioro de las frambuesas.
Por otra parte, Serrano et al. (2005) desarrolló empaques activos que contenían eugenol, mentol, timol y eucaliptol, para el almacenamiento de cerezas. En el estudio, se demostró que se redujo notablemente el crecimiento de levaduras y mohos igualmente, la calidad de las cerezas mejoró, manteniéndose el color y la firmeza de la fruta y disminuyendo la pérdida de peso.
De este modo, puede enfatizarse que los empaques activos con atmósferas modificadas han demostrado tener un efecto sinérgico con aceites esenciales, ya que muestran resultados favorables en el control microbiano de los alimentos (Jobling, 2000; Skandamis y Nychas, 2002; Wang, 2003; Serrano et al, 2005).
A partir de lo anterior, el realizar estudios donde se evalúen las características organolépticas de un alimento expuesto a vapores de aceites esenciales, en comparación con aquellos en los que fueron añadidos directamente (en forma líquida), sería un excelente recurso para identificar la rentabilidad de los vapores de aceites esenciales como antimicrobianos naturales.
Conclusiones
Se puede afirmar que los vapores generados por algunos aceites esenciales de plantas y de especias cumplen con la actividad necesaria para ser considerados como antimicrobianos naturales. Sin embargo, aún no se cuenta con información suficiente para poder darles aplicaciones reales en alimentos, por lo que se abre una puerta de oportunidad para seguir investigando su modo de acción y la forma en que pudieran aplicarse a nivel industrial, evaluando si modificarían o no las características organolépticas del alimento.
Agradecimientos
La autora Reyes Jurado agradece el apoyo financiero del Consejo Nacional de Ciencia y Tecnología (CONACYT) y de la Universidad de las Américas Puebla (UDLAP) por el apoyo para sus estudios de maestría en Ciencia de Alimentos.
antimicrobial action on Penicillium digitatum and Penicillium italicum International Journal of Food Microbiology. 43 (1-2): 73-79.
Dao, T., Bensoussan, M., Gervais, P. y Dantigny, P. 2008. Inactivation of conidia of Penicillium chrysogenum, P. digitatum and P. italicum by ethanol solutions and vapours. International Journal of Food Microbiology. 122 (1-2): 68-73.
Delaquis, P., Stanich, K., Girard, B. y Mazza, G. 2002. Antimicrobial activity of individual and mixed fractions of dill, cilantro, coriander and eucalyptus essential oils. International Journal of Food Microbiology. 74 (1-2): 101-109.
Edris, A. y Farrag, E. 2003. Antifungal activity of peppermint and sweet basil essential oils and their major aroma constituents on some plant pathogenic fungi from the vapor phase. Molecular Nutrition Food Research. 47(2):112-121.
Fisher, K. y Phillips C. 2008. Potential antimicrobial uses of essential oils in food: is citrus the answer?. Food Science and Technology. 19 (3): 156-164.
Gómez-Sánchez, A., Palou, E. y López-Malo, A. 2011. Antifungal Activity Evaluation of Mexican Oregano (Lippia berlandieri Schauer) Essential Oil on the Growth of Aspergillus flavus by Gaseous Contact. Journal of Food Protection. 74 (12): 2192-2198.
Referencias
Aslan, I., Özbek, H., Çalma¸sur, Ö. y Sah In, F. 2004. Toxicity of essential oil vapours to two greenhouse pests, Tetranychus urticae Koch and Bemisia tabaci Genn. Industrial Crops and Products. 19 (2): 167173.
Ávila-Sosa, R., Palou, E., Jiménez, M.T., NevárezMoorillón, G.V., Navarro, A. R. y López-Malo, A. 2012. Antifungal activity by vapor contact of essential oils added to amaranth, chitosan, or starch edible films. International Journal of Food Microbiology. 153 (1-2): 66-72.
Burt, S. 2004. Essential oils: their antibacterial properties and potential applications in foods a review. International Journal of Food Microbiology 94 (3): 223-253.
Caccioni, D., Guizzardi, M., Biondi, D., Renda, A. y Ruberto, G. 1998. Relationship between volatile components of citrus fruit essential oils and
Goñi, P., López P., Sánchez, C., Gómez-Lus, R., Becerril, R. y Nerín C. 2009. Antimicrobial activity in the vapour phase of a combination of cinnamon and clove essential oils. Food Chemistry. 116 (14): 982-989.
Holley, R. y Patel, D. 2005. Improvement in shelf-life and safety of perishable foods by plant essential oils and smoke antimicrobials. Food Microbiology. 22 (4): 273-292.
Inouye, S., Takisawa, T. y Yamaguchi, H. 2001.Antibacterial activity of essential oils and their major constituents against respiratory tract pathogens by gaseous contact. Journal of Antimicrobial Chemotherapy. 47 (5): 565-573.
Inouye, S., Uchida, K. y Abe, S. 2006. Vapor activity of 72 essential oils against a Trichophyton mentagrophytes Journal of Infection and Chemotherapy. 12 (4):210-216.
Joblin, J. 2000. Essential oils: A new idea for postharvest disease control. Good Fruit and Vegetables magazine. 11 (3): 50.
Kalemba, D. y Kunicka, A. 2003. Antibacterial and antifungal properties of essential oils. Current Medicinal Chemistry. 10 (10): 813-829.
Kloucek, P., Smid, J., Frankova, A., Kokoska, L., Valterova, I. y Pavela, R. 2011. Fast screening method for assessment of antimicrobial activity of essential oils in vapor phase. Food Research International. 0 (0): 1-5.
Lee, H. C., Cheng, S. S. y Chang, S.T. 2005. Antifungal property of the essential oils and their constituents from Cinnamomum osmophloeum leaf against tree pathogenic fungi. Journal of the Science of Food and Agriculture. 85 (12): 2047-2053.
López, P., Sánchez, C., Batle, R. y Nerín, C. 2005. Solid- and vapor-phase antimicrobial activities of six essential oils: susceptibility of selected foodborne bacterial and fungal strains. Journal of Agricultural and Food Chemistry. 53(17): 6939-6946.
López, P., Sánchez, C., Batle, R. y Nerín, C. 2007. Vapor-Phase activities of cinnamon, thyme, and orégano essential oils and key constituents against foodborne microorganisms. Journal of Agricultural and Food Chemistry. 55(11): 4348-4356.
López-Malo, A., Palou, E., León-Cruz, R. y Alzamora, S. 2005. Mixtures of natural and synthetic antifungal agents. Advances in Food Mycology. 571 (4): 261286.
Nielsen, P. y Rios, R. 2000. Inhibition of fungal growth on bread by volatile components from spices and herbs, and the posible application in active packaging with special emphasis on mustard essential oil. International Journal of Food Microbiology. 60 (2-3): 219-229.
Phillips, C.A., Laird, K. y Allen, S.C. 2011. The use of Citri-V™®- An antimicrobial citrus essential oil vapour for the control of Penicillium chrysogenum, Aspergillus niger and Alternaria alternate in vitro and on food. Food Research International. 0 (0):1-5.
Raybaudi-Massilia, R., Soliva R. y Belloso, O. 2006. Uso de agentes antimicrobianos para la conservación de frutas frescas y frescas cortadas. Simpósio IberoAmericano de Vegetales Frescos Cortados, San Pedro, SP Brazil
Serrano, M., Martínez-Romero, D., Castillo, S., Guillén, F. y Valero, D. 2005. The use of natural antifungal compounds improves the beneficial effect of MAP
in sweet cherry storage. Innovative Food Science and Emerging Technologies. 6 (1): 115-123.
Sivropoulou, A., Papanikolaou, E., Nikolaou, C., Kokkini, S., Lanaras, T. y Arsenakis M. 1996. Antimicrobial and cytotoxic activities of Origanum essential Oils. Journal of Agricultural and Food Chemistry. 44 (5): 1202-1205.
Skandamis, P. y Nychas, G-J. 2002. Preservation of fresh meat with active and modified atmosphere packaging conditions. Journal Food Microbiology. 79 (1-2): 35-45.
Smith-Palmer A., Stewart J. y Fyfe L. 1998. Antimicrobial properties of plant essential oils and essences against five important food-borne pathogens. Letters in Aplied Microbiology. 26 (2): 118-122.
Solórzano-Santos, F. y Miranda-Novales, MG. 2011. Essential oils from aromatic herbs as antimicrobial agents. Current Opinion in Biotechnology. 23 (0):16.
Suhr, K. y Nielsen, P. 2003. Antifungal activity of essential oils evaluated by two different application techniques against rye bread spoilage fungi. Journal of Applied Microbiology. 94 (4): 665-674.
Tajkarimi, M., Ibrahim, S. y Cliver D. 2010. Antimicrobial herb and spice compounds in food. Food Control. 21 (19): 1199-1218.
Tullio, V., Nostro, A., Mandras, N., Dugo, P., Banche, G.,Cannatelli, M. A., Cuffini, A. M., Alonzo, V. y Carlone, N. A. 2007. Antifungal activity of essential oils against filamentous fungi determined by broth microdilution and vapour contact methods. Journal of Applied Microbiology. 102 (6): 1544-1550.
Tyagi, A.K. y Malik, A. 2011. Antimicrobial potential and chemical composition of Eucalyptus globulus oil in liquid and vapour phase against food spoilage microorganisms. Food Chemistry. 126 (1): 228-235.
Tzortzakis N. 2007. Maintaining postharvest quality of fresh produce with volatile compounds. Innovative Food Science and Emerging Technologies. 8 (1): 111-116.
Wang, C. 2003. Maintaining postharvest quality of raspberries with natural volatile compounds. International Journal of Food Science and Technology. 38 (8): 869-875.

Temas Selectos de Ingeniería de Alimentos 6 - 1 (2012): 40 - 53

El jitomate (Solanum lycopersicum): aporte nutrimental, enfermedades postcosecha y tecnologías para su almacenamiento en fresco
C. M. Notario-Medellín* y M. E. Sosa-Morales
Departamento de Ingeniería Química, Alimentos y Ambiental, Fundación Universidad de las Américas Puebla. Exhacienda Sta. Catarina Mártir S/N, Cholula, Puebla. C.P.72810. México.
Resumen
Este trabajo trata sobre las variedades de jitomate (Solanum lycopersicum) producidas en México, sus propiedades nutrimentales, sus enfermedades postcosecha y las tecnologías empleadas para su almacenamiento en fresco. El jitomate es un alimento de importancia mundial cuyo consumo contribuye en la prevención de enfermedades cardiovasculares y varios tipos de cáncer, lo cual está asociado especialmente al licopeno. Las principales variedades cultivadas en México son bola, cherry y saladette, las cuales pueden ser atacadas por hongos y bacterias (particularmente por Botrytis cinerea). Por otra parte, existen varias técnicas para prolongar la vida útil de jitomate, tales como tratamientos térmicos, tratamientos con ozono, envasado en atmósferas modificadas, almacenamiento con atmósferas controladas y películas comestibles, y se puede concluir que para mantener la calidad del producto durante el almacenamiento en fresco, es necesario utilizar la combinación de algunos de estos métodos.
Palabras clave: jitomate (Solanum lycopersicum), propiedades nutrimentales, enfermedades postcosecha, tecnologías de almacenamiento.
Abstract
This work discusses the tomato varieties (Solanum lycopersicum) produced in Mexico, their nutritional properties, their postharvest diseases and the technologies used for their storage. Tomato is an important food around the world, its consumption contributes to cardiovascular diseases prevention, and to avoid several types of cancer, which is associated especially with its high lycopene content. The main varieties cultivated in Mexico are bola, cherry and saladette, which can be attacked by fungi and bacteria (mainly Botrytis cinerea). Moreover, to extend the shelf life of tomato, several techniques have been reported, such as cooling, heat treatments, ozone treatments, modified atmosphere packaging, storage in controlled atmospheres and edible films. In resume, it is necessary to use a combination of some of these methods in order to maintain product quality during storage.
Keywords: tomato (Solanum lycopersicum L.), nutritional properties, postharvest diseases, storage techniques.
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: carmen.notariomn@udlap.mx
Introducción
El jitomate (Solanum lycopersicum L.) es un producto agrícola con una alta importancia económica a nivel mundial y tiene una gran popularidad por ser cultivado en todo el mundo (FAOSTAT, 2011).
El consumo de esta hortaliza es una parte importante de la dieta humana, ya que es un alimento muy versátil, con formas de consumo variadas. Altas ingestas de este producto están estrechamente relacionadas con un impacto benéfico en la salud, ya que es capaz de reducir el riesgo de padecer enfermedades cardiovasculares y diferentes tipos de cáncer, atribuido principalmente a su alto contenido de antioxidantes (licopeno, ácido ascórbico y compuestos fenólicos) (Bugianesi et al., 2004; Borguini y Ferraz, 2009).
Por otra parte, el jitomate es altamente susceptible a ser atacado por microorganismos (bacterias y hongos), los cuales causan el deterioro de este alimento y disminuyen su calidad. Existen diferentes técnicas para su almacenamiento en fresco, las cuales aumentan su vida útil y mantienen sus características sensoriales en un nivel aceptable para los consumidores (Siripatrawan y Assatarakul, 2009; Rodoni et al., 2010; Das et al., 2006; Ramos-García et al., 2010).
El objetivo de este trabajo es investigar en la literatura las variedades de jitomate producidas en México, las propiedades antioxidantes del jitomate y las enfermedades que lo atacan, así como las tecnologías empleadas para su almacenamiento en fresco que eviten el ataque microbiano y que mantengan su calidad preservando sus propiedades físicas y nutrimentales.
Revisión bibliográfica
1. Generalidades
La palabra jitomate deriva de los vocablos náhuatl xictl (ombligo) y tomatl (tomate) que significa tomate de ombligo. Es originario de la región Sur Central de Perú, y por su amplia habilidad de adaptación puede cultivarse tanto en ambientes secos como húmedos. Debido a evidencias históricas, culturales, lingüísticas y etnobotánicas, se cree que fue domesticado en México alrededor del año 1523, distribuyéndose a Europa después de la conquista española (Moreno, 2010). En la Tabla I se muestra la clasificación taxonómica del jitomate.
Tabla I. Clasificación taxonómica del jitomate.
Reino Plantae
Subreino Trachobiota (plantas vasculares)
Sbdivisión Spermatophyta (plantas con semilla)
División Magnoliophyta (plantas con flores)
Clase Magnoliopsida (Dicotiledoneas)
Subclase Asteride
Orden Solanales
Familia Solanáceas
Género Solanum
Especia lycopersicum L.
USDA (2012).
El jitomate (Solanum lycopersicum L.), es uno de los productos básicos de mayor valor y producción a nivel mundial, ocupando en el año 2010, el décimo lugar con un valor de 53,270,325 USD y 145,751,507 ton producidas (FAOSTAT, 2011). En el mismo año, México se ubicó en décimo lugar con un aporte de 2,997,640 ton (1,107,819 USD), siendo China el principal productor con un volumen de 41,879,684 ton (15,477,223 USD), seguido de Estados Unidos de América con 12,902,000 ton (4,768,114 USD) (FAOSTAT, 2011). En la Tabla II se muestran
Tabla II. Principales países productores de jitomate en el periodo 2005 – 2010 (Toneladas).
China
Unidos de América
India
Egipto 7,600,000 8,576,070 8,639,020 10,985,400
Turquía
Italia
Adaptado de FAOSTAT (2011).
los 10 principales países productores de jitomate en el periodo de 2005 a 2010.
Por otra parte, México se ubicó en segundo lugar como país exportador de jitomate en el año 2009 (1,136,300 toneladas con un valor de 1,066 pesos/tonelada), superado únicamente por Países Bajos (976,435 toneladas con un valor de 1,607 pesos/tonelada) (FAOSTAT, 2011).
Dentro de la producción mexicana de esta hortaliza, Sinaloa es el estado con un mayor aporte (668,303 ton) seguido de Baja California (180,135 ton) y Michoacán de Ocampo (140,185 ton). Para este mismo año, el estado de Puebla se encontró en décimo sexto lugar con una producción de 29,954 toneladas (INEGI, 2011).
Las principales variedades de jitomate producidas en México son: bola, saladette, cherry y Río grande, siendo la variedad saladette la que en el año 2010 se ubicó en primer lugar de acuerdo a su producción (1,060,084 ton) y valor de producción (5,313,640 miles de pesos) (SIAP, 2011). En
la Tabla III se muestra la producción obtenida en el año 2010 para las diferentes variedades de jitomate.
El jitomate bola es una de las variedades más populares, se caracteriza por su forma redonda y tiene un peso promedio entre 70 y 100 g, un diámetro de 4.7 a 6.7 cm y posee de 4 a 6 lóculos (Costa y Heuvelink, 2005). El jitomate saladette se caracteriza por tener 3 lóculos, una forma larga elongada y un color rojo brillante. El jitomate cherry es la variedad más pequeña, es de color rojo y tiene un sabor
TablaIII. Volumendeproduccióndelasprincipales variedades de jitomate producidas en México en el año 2010.
Tipo/Variedad Producción (ton) Valor producción (miles de pesos)
Bola191,606 1,058,233
Bola invernadero38,520 251,048
Bola malla sombra90,655 564,548
Cherry33,330 244,047
Cherry orgánico13,087 146,814
Río grande3,541 17,107
Saladette1,060,084 5,313,640
Saladette invernadero3,360 26,880
Saladette malla sombra32,153 168,777
Adaptado de SIAP (2011).
muy dulce, con un peso entre 10 y 20 g y diámetro de 1.6 a 2.5 cm. (Costa y Heuvelink, 2005).
2. Propiedades del jitomate
2.1. Nutrimentales
En general, el jitomate es un alimento que se caracteriza por tener un alto contenido de humedad, la cual se encuentra entre 90 y 97%, es bajo en grasas, proteínas y azúcares (0.71.1%, 02.-0.7%, 1.2-2.5%, respectivamente), y es una fuente importante de -caroteno, licopeno y vitamina C, sin embargo, su aporte nutrimental depende de la variedad (FAO, 2010). En la Tabla IV se muestra la composición proximal de algunas variedades de jitomate (FAO, 2010).
2.2. Antioxidantes
Estudios recientes han demostrado que la ingesta de frutas y hortalizas reduce el riesgo de padecimiento de cáncer (Riboli y Norat, 2003; Liu, 2004; Greenwald et al., 2001), lo cual ha sido estrechamente relacionado con los compuestos antioxidantes que estos alimentos poseen, principalmente carotenoides (Liu, 2004; Perera y Yen, 2007). De acuerdo a varios estudios (Ilhay et al., 2011; Aherne et al., 2009; Muratore et al., 2005; Zanfini et al.,
2007) el jitomate es una fuente importante de carotenoides, principalmente licopeno y caroteno, los cuales pueden inhibir la reactividad de especies oxidantes responsables de muchas enfermedades (Ilhay et al., 2011). Por esta razón muchos trabajos se han centrado en la determinación de los carotenoides presentes en el jitomate, algunos de los cuales se describen a continuación y son resumidos en la Tabla V.
En un trabajo realizado por Strazzullo et al. (2007) determinaron la actividad antioxidante y contenido de carotenoides (licopeno y caroteno) tanto en la fracción hidrofílica como lipídica en jitomates procedentes de nueve cultivos diferentes, encontrando que la actividad antioxidante del jitomate es una respuesta de la interacción de los diferentes componentes antioxidantes presentes, entre ellos licopeno y -caroteno. En la fracción acuosa, se encontraron valores de Capacidad Antioxidante Equivalente a Trolox (TEAC por sus siglas en inglés) de 14.2 a 27.4 M, y en la fracción lipofílica estos valores variaron de 0.065 a 0.48 M, dependiendo del cultivo. En todos los casos, el caroteno mayoritario (en la fracción lipofílica) fue el -caroteno, que se encontró en concentraciones desde 0.005% hasta 0.06%, dependiendo del cultivo.
Daniela
Larga Vida
Lido62.314.994.7
Raf65.815.793.9
Rambo41.69.995.8
Adaptado de FAO (2010).
Tabla IV. Composición proximal de algunas variedades de jitomate.
Tabla V. Contenido de los carotenoides más representativos en algunas variedades de jitomate.
VariedadCarotenoide (mg/100g)ConsideracionesReferencia
Licopeno -carotenoFitoenoLuteína
Cherry1.81 - 2.30 0.462 - 0.4890.031 - 0.183Zona geográficaAherne et al., 2009
21.5 - 36.96.6CocidoBugianesi et al., 2004
3.430.99FrescoMuratore et al., 2005
2.46 - 13.270.49 - 0.710.13 - 1.990.015 - 0.021Estación, zona geográfica y madurez en cosecha Zanfini et al., 2007
Plum2.59 -7.9590.36 - 0.440.016 - 0.109Zona geográficaAherne et al., 2009
3.98 - 4.770.68 - 0.89Varios genotiposMuratore et al., 2005
Bola1.47 - 3.170.23 - 0.350.029 - 0.099Zona geográficaAherne et al., 2009
0.9170.035NingunaCandelas et.al., 2006
Salad1.94 - 2.350.21 -0.420.09 - 0.120.014 - 0.016Zona geográfica, estación de cosecha Zanfini et al., 2007
Cluster2.23 - 8.470.37 - 0.620.11 -0.440.014 - 0.020Estación, zona geográfica y madurez en cosecha Zanfini et al., 2007
Aherne et al. (2009), analizaron el impacto de la localización geográfica sobre el contenido y la bioaccesibilidad de carotenoides en diferentes variedades de jitomate (plum, cherry y bola). Sus resultados muestran que de los tres tipos de carotenoides determinados (-caroteno, licopeno y luteína), el compuesto antioxidante mayoritario en todos los casos fue el licopeno, con contenidos que van desde 1,471–3,169 μg/100 g para jitomate bola, hasta 2,589.0–7,959.9 g/100 g para variedad plum; la luteína se encontró en menor proporción en las tres variedades de jitomate, siendo la variedad plum la que tuvo la concentración más baja (16.5–109.8g/100 g) y la variedad cherry la más alta (31.8–183.4g/100 g).
Por otra parte, Zanfini et al. (2007), determinaron el contenido de diferentes carotenoides (luteína, licopeno, -caroteno y fitoeno), en tres variedades de jitomate (Salad, cluster y cherry) de tres regiones de Italia (Lazio, Toscana y Siclicia). Sus resultados concuerdan con lo reportado por Aherne et al. (2009), ya que en todas las variedades de jitomate analizadas, el licopeno se encontró en mayor proporción (2.35±0.53 a 13.27±2.82
mg/100 g) con respecto al contenido de caroteno, fitoeno y luteína, siendo esta última la que se encontró en cantidades más bajas (0.016±0.012 a 0.021±0.012 mg/100 g). Con respecto a la variedad, el jitomate cherry obtuvo las cantidades más elevadas de los cuatro componentes determinados, y el jitomate sald las más bajas; por otra parte, se analizó la influencia del grado de madurez y la estación de cosecha sobre el contenido de carotenoides, obteniendo los valores más altos en frutos cosechados en el verano y completamente maduros (rojos).
De acuerdo a lo anterior y a otras investigaciones realizadas (Aherne et al., 2009; Muratore et al., 2005; Zanfini et al., 2007; Bugianesi et al., 2004; Candelas et al., 2006), el licopeno es el carotenoide mayoritario en el jitomate; ello se puede observar en la Tabla V, la cual muestra el contenido de licopeno, -caroteno, fitoeno y luteína de las variedades de jitomate cherry, plum, bola, salad y cluster; puede observarse que el contenido de carotenoides depende de diferentes factores, tales como: variedad del jitomate, zona geográfica del cultivo, estado de madurez del jitomate y estado fresco o cocido del jitomate, siendo este último
(cocido) en el cual se observan los contenidos más altos de licopeno y -caroteno (21.5 mg/100 g y 6.6 mg/100 g, respectivamente).
Según lo citado por Singh y Goyal (2008), el consumo de licopeno tiene efectos positivos sobre la salud, ya que se ha comprobado que reduce ataques cardiacos y accidentes cerebro vasculares, además de reducir el riesgo a padecer diferentes tipos de cáncer (rectal, próstata, mama, pulmón y páncreas).
Además de los carotenoides presentes en el jitomate, esta hortaliza también es fuente importante de vitamina C, tocoferoles y fenoles, los cuales son compuestos antioxidantes cuya ingesta está relacionada con beneficios a la salud (Strazzullo et al., 2007; Ilhay et al., 2011; Jacob et al., 2010). En un trabajo realizado por Ilhay et al. (2011) se determinó el contenido de licopeno, caroteno, luteína, fenoles, flavonoides, ácido ascórbico, ácido dehidroascórbico, así como la actividad antioxidante de seis cultivos de jitomate de alto contenido de licopeno y un cultivo ordinario (Donald). Los resultados para el jitomate Donald fueron los siguientes: contenidos de licopeno y -caroteno de 96.9 y 5.8 mg/kg, respectivamente; compuestos fenólicos totales y flavonoides de 190 mg GAE/kg (mg de ácido gálico equivalente por kg de muestra) y 140 mg RE/kg (mg de rutina equivalente por kg de muestra), respectivamente; contenido total de vitamina C igual a 227.9 mg/kg; actividad antioxidante hidrofílica de 405.8 M Trolox/100 g y actividad antioxidante lipofílica de 133.5 M Trolox/100 g.
3. Enfermedades postcosecha comunes en jitomate
Los jitomates después de ser cosechados tienen una vida limitada, ya que no captan agua ni los nutrientes necesarios para continuar con sus funciones vitales. La senescencia ocurre de manera natural en el
producto, y ocasiona el ablandamiento de los tejidos y la pérdida de sustancias antimicrobianas naturales del alimento y lo hace más susceptible al ataque microbiano (Mahovic et al., 2006, Bartz y Brecht, 2005).
Aunque los microorganismos patógenos pueden encontrarse en lugares calientes y húmedos, el daño por frío (ocasionado por temperaturas inferiores a 15 °C) así como las grietas o heridas de la superficie del producto causada por daño mecánico en la manipulación y/o el almacenamiento, predisponen al alimento a las enfermedades postcosecha, ya que muchos organismos patógenos son oportunistas y lo invaden cuando éste está dañado (Bayer, 2010).
Los microorganismos principales causantes de la descomposición del jitomate durante su almacenamiento son las bacterias y los hongos, por lo que es posible dividir a las enfermedades postcosecha en bacterianas y fúngicas (Bartz y Brecht, 2005).
3.1. Enfermedades bacterianas en jitomate
Las enfermedades bacterianas frecuentes en el fruto de jitomate son: pudrición blanda, pudrición ácida y cáncer bacteriano; estas enfermedades se caracterizan por formar superficies viscosas y pegajosas sobre los jitomates (Mahovic et al., 2006; Cerkauskas, 2005; Bartz y Brecht, 2002).
3.1.1. Pudrición blanda
Esta enfermedad es producida por cuatro bacterias: Erwinia carotovora, Pseudomonas, Xanthomonas y Bacillus spp., las cuales se dispersan en soluciones acuosas y penetran el fruto a través de heridas o grietas. La enfermedad se favorece con una humedad relativa alta (90-95%) y temperaturas de 30 a 35°C. Los jitomates infectados presentan una masa viscosa sobre la piel, la cual posteriormente se seca y la piel se rompe,
dando lugar a una masa arrugada con olor a podrido (Fig. 3) (Mahovic et al., 2006; Cerkauskas, 2005; Bartz y Brecht, 2002).
3.1.2. Pudrición ácida
Las bacterias ácido lácticas gram positivas Lactobacillus spp. y Leuconostoc spp., ocasionan la pudrición ácida en jitomate, caracterizada por generar lesiones ligeramente blandas. Estas bacterias pueden propagarse a través de equipo contaminado y líquidos de frutos descompuestos (Mahovic et al., 2006; Bartz y Brecht, 2002).
3.1.3. Cáncer bacteriano
Es una enfermedad causada por Clavibacter michiganensis subsp. michiganensis (Cmm) cuyos brotes se producen anualmente en todo el mundo. Ocasiona pérdida del área fotosintética, marchitez, muerte prematura y pudrición de los frutos. Los primeros síntomas se presentan en las hojas (marchitez, rizado y bronceado), generalmente de un solo lado de la planta, provocando lesiones necróticas (6 mm) o puntos circulares (3 mm) y manchas similares en tallos y peciolos. En el centro se producen pequeñas manchas de color claro con el centro café y rugoso, las cuales se conocen como “ojos de pájaro” y pueden llegar a cubrir todo el fruto (Productores de Hortalizas, 2006; Álvarez y Delgadillo, 2004).
3.2. Enfermedades fúngicas en jitomate
Existen muchas especies fúngicas que causan descomposición en el jitomate, las cuales pueden reproducirse en calor y condiciones de humedad y producen esporas que pueden resistir a la sequedad. Las esporas se dispersan a través del agua, viento, animales y equipos. Dentro de estas enfermedades se encuentran la pudrición ácida fúngica, pudrición por Rhizopus, pudrición de semillas, pudrición por Fusarium, y moho gris, siendo esta última una
de las más importantes (Mahovic et al., 2006; Kader, 2011; Álvarez y Delgadillo, 2004).
3.2.1. Pudrición ácida fúngica
Es ocasionada por Geotrichum candidum que se caracteriza por formar un micelio de color blanco sobre el fruto; los frutos infectados presentan lesiones acuosas, decoloradas y opacas. La infección inicia por lo general en el pedúnculo, y posteriormente se extiende al resto del fruto, ocasionando su pudrición y rápida descomposición. Los frutos podridos poseen suficiente inóculo que puede ser transportado por insectos y contagiar a otros frutos. La temperatura óptima para el desarrollo de esta enfermedad es 30 °C, sin embargo, la enfermedad puede presentarse en alimentos refrigerados, principalmente en los que han sufrido daño por frío; la infección puede ocurrir en un rango de temperaturas de 5 °C a 38 °C (Kader, 2011).
3.2.2. Pudrición por Rhizopus.
Rhizopus stolonifer es el hongo que causa esta enfermedad, la cual se caracteriza por lesiones acuosas que segregan un líquido claro y se cubren de estructuras fúngicas algodonosas; además, se puede observar una esporulación que forma una corona oscura alrededor de la estructura algodonosa. El patógeno Rhizopus stolonifer necesita la presencia de grietas en el fruto para poder penetrarlo, y durante el almacenamiento puede contagiar a los frutos adyacentes; su temperatura óptima de crecimiento es de 25 °C, aunque también puede desarrollarse en condiciones de refrigeración (Bayer, 2010; TNAU, 2008; Mahovic et al. 2006).
3.2.3. Pudrición de semillas
Esta enfermedad, ocasionada por Phytophtora spp, generalmente se desarrolla en frutos que tienen contacto con el suelo, principalmente en condiciones húmedas y cálidas, y es propagada
por agua. La pudrición de semillas se manifiesta por pequeñas decoloraciones seguidas de una pudrición circular en forma de llagas que se oscurecen en el centro, y el micelio blanco se extiende a los lados (Mahovic et al., 2006; Álvarez y Delgadillo, 2004).
3.2.4. Pudrición del moho negro
Esta enfermedad es producida por los microorganismos Alternaria arborescens y Stemphyllium botryosum o S. consortiale; ellos atacan principalmente a los frutos completamente maduros que están expuestos a la humedad de una manera directa, ya sea por lluvia o por riego. La enfermedad inicia con lesiones pequeñas e irregulares y de tono marrón sobre el fruto; avanzada la enfermedad, las lesiones se vuelven negras y hundidas; y en condiciones cálidas y húmedas, puede formarse una capa negra y aterciopelada debido a la esporulación. Generalmente, estas lesiones aparecen sobre la cicatriz del pedúnculo o sobre grietas. Esta enfermedad no se extiende entre frutos contiguos (Ontario CropIPM, 2009; Mahovic et al., 2006).
3.2.5. Marchitamiento por Fusarium
El hongo Fusarium oxysporum f. sp. lycopersici generalmente ataca el jitomate antes de la cosecha, iniciando en la parte inferior del tallo y distribuyéndose al resto de la planta causando su muerte. Sin embargo, ocasionalmente puede encontrarse en el fruto, en el que se produce una decoloración del tejido vascular y se generan lesiones, las cuales se cubren de un micelio blanco con tonos rosados, naranjas o hasta violetas (TNAU, 2008; Gleason y Edmunds, 2006; Mahovic et al., 2006).
3.2.6.
Antracnosis
Esta enfermedad es producida por varias especies del género Colletotricum. Generalmente se presenta en frutos maduros y se caracteriza por lesiones que inicialmente son redondas, blandas y pequeñas con centro marrón, las cuales posteriormente se expanden, se hunden y se oscurecen, formando anillos concéntricos con pequeños puntos negros en el centro. En condiciones húmedas, las esporas forman áreas que van de tonos crema hasta rosa salmón; varias lesiones pueden unirse causando el deterioro de un área grande que puede ser aprovechada por otros microorganismos para causar la pudrición total del fruto (Kennelly, 2009; Delahaut y Stevenson, 2004; Gleason y Edmunds, 2006).
3.2.7. Moho gris
El microorganismo causal del moho gris es Botrytis cinerea. Esta enfermedad puede presentarse en cualquier etapa del desarrollo de la planta, principalmente en condiciones húmedas frías y se considera la enfermedad más importante en invernadero, ya que los daños pueden ser totales. Las condiciones óptimas de desarrollo de Botrytis cinerea son temperatura de 18 a 23 °C y humedad relativa superior a 85%. El moho es un patógeno oportunista, ya que aprovecha las lesiones presentes en el fruto para poder penetrarlo y atacarlo; durante la cosecha éste puede estar presente en forma latente y ocasionar lesiones muy pequeñas que no son detectables (pequeños anillos blancos conocidos como marcas fantasmas), sin embargo, la infección continua desarrollándose en etapas posteriores produciendo grandes pérdidas. Los frutos contaminados presentan manchas circulares con bordes blancos, seguido de necrosis caférojiza que posteriormente se cubre de un polvo grisáceo (Álvarez y Delgadillo, 2004; Mahovic et al., 2006).
4. Tecnologías para almacenamiento de jitomate fresco
Existen diversas técnicas para prolongar la vida útil de frutas y hortalizas durante su almacenamiento. Dentro de las tecnologías empleadas se puede encontrar el almacenamiento a bajas temperaturas, uso de atmósferas controladas y modificadas, tratamientos térmicos y películas comestibles, entre otros, algunos de los cuales son descritos a continuación (Quezada et al., 2003; Suslow y Cantwell, 2006; Akbudak et al., 2007; SosaMorales et al., 2011).
4.1. Refrigeración
La refrigeración es una técnica en la cual la temperatura del alimento es reducida por debajo de la del ambiente; el calor sensible es retirado del alimento para reducir su temperatura (de acuerdo a su comportamiento frente al frío), actuando sobre los procesos fisiológicos del producto (respiración, maduración, germinación) y de los microorganismos, lo que resulta en la prolongación de la vida útil del alimento (Brennan y Grandison, 2012; Bermúdez, 2000).
El almacenamiento a bajas temperaturas es ampliamente usado para reducir la velocidad de maduración y el daño causado por hongos en frutas y hortalizas, sin embargo, debido a la sensibilidad de los alimentos a temperaturas bajas, pueden ocasionarse daños por frío en los productos refrigerados (Siripatrawan y Assatarakul, 2009). En el caso de los jitomates, el daño por frío puede presentarse cuando son almacenados a temperaturas inferiores a 10 °C por periodos mayores a 2 semanas, y a 5 °C por periodos mayores a 6-8 días; éste se caracteriza por falta de madurez (color y sabor), color irregular, picaduras en la superficie, formación de áreas blandas y oscurecimiento de las semillas; de esta forma existe mayor susceptibilidad de que el
producto sea atacado por microorganismos (Suslow y Cantwell, 2006; El Assi, 2004). Para reducir el daño por frío causado en la refrigeración puede aplicarse en combinación con otras técnicas de conservación tales como tratamientos térmicos, atmósferas controladas y modificadas, entre otras (Siripatrawan y Assatarakul, 2009; El Assi, 2004).
4.2. Tratamientos térmicos postcosecha
El tratamiento térmico postcosecha de frutas y hortalizas es un tratamiento físico no contaminante que retarda el proceso de madurez y controla la actividad de los microorganismos presentes en el alimento, por lo que resulta ser efectivo para controlar el ataque microbiano (principalmente fúngico) en productos vegetales, además de inhibir algunas enzimas que causan su deterioro (Akbudak et al., 2007; Sosa-Morales et al., 2011).
Dentro de los tratamientos térmicos postcosecha, se encuentra la inmersión en agua caliente (baños de agua con temperatura superior a 40 °C), exposición a aire caliente (corriente de aire a 45 °C o más) o tratamientos con vapor (similar a la exposición a corriente de aire, pero utilizando aire saturado) (Sosa-Morales et al., 2011).
Akbudak et al. (2007) analizaron el efecto de la inmersión en agua caliente (54 °C por 5 minutos) previo al empacado en atmósferas modificadas sobre los parámetros de calidad (pérdida de peso, sólidos solubles totales, firmeza, acidez titulable y contenidos de ácido ascórbico, licopeno y -caroteno) del jitomate cherry durante su almacenamiento refrigerado (5-7 °C y 90±5% de humedad relativa) y encontraron que el tratamiento con agua caliente en combinación con un bajo contenido de O2 reducían la pérdida de calidad del producto durante su almacenamiento.
Por otra parte, Soto-Zamora et al. (2004), aplicaron un tratamiento con aire caliente (34 ó 38 °C por 34 horas) en jitomate “rhapsody”, y analizaron su efecto sobre la calidad durante el almacenamiento a 4 °C ó 20 °C por más de 4 semanas. Los jitomates sometidos a tratamiento con aire caliente a 38 °C y humedad relativa del 95% por 24 horas, y almacenados a 4 °C por 22 días mostraron daño por frío y bajas cantidades de licopeno. De igual manera, el calentamiento a 34°C tampoco previno el daño por frío en los jitomates almacenados a 4 °C durante 22 días, sin embargo, el daño fue menor que en los tratados a 38 °C, además de obtener un mayor contenido de licopeno. En ambos casos (jitomates tratados a 38 °C y a 34°C) el daño por frío fue mayor que en el control (sin tratamiento) al almacenarlos a 4 °C durante todo el periodo de almacenamiento (22 días).
4.3. Películas y recubrimientos comestibles
Una alternativa para la conservación de frutas y hortalizas es el uso de películas y recubrimientos comestibles, que son envolturas delgadas protectoras (a base de carbohidratos, lípidos y proteínas) que recubren la superficie del alimento y crean una berrera a los gases, reduciendo la cantidad de O2, aumentando los niveles de CO2 y resultando en la conservación de la calidad del alimento (Ramos-García et al., 2010).
Los recubrimientos comestibles (RC), son matrices continuas formadas alrededor del alimento, comúnmente por inmersión en la solución del recubrimiento, mientras que las películas comestibles (PC) son matrices preformadas que posteriormente se usan para cubrir el alimento. Ambas (RC y PC) disminuyen el deterioro del producto y además le proporcionar brillo, mejoran la textura de la corteza y disminuyen la pérdida de peso por deshidratación (Ramos-García et al., 2010; Quintero et al., 2010; Amaya et al., 2010). Los RC y PC además de servir como barrera,
funcionan como vehículo para la incorporación de aditivos (antioxidantes, colorantes y antimicrobianos) que le brindan características de funcionalidad al producto (Ramos-García et al., 2010).
En un trabajo realizado por Dávila-Aviña et al. (2011), se evaluó el efecto de películas a base de caranauba (Stafresh 2505™) y aceite mineral (Stafresh 151™) sobre la calidad de jitomate bola (cv. Grandela); las películas se aplicaron en el jitomate fresco y en dos estados de madurez (rayados y rojos), y la calidad del jitomate se evaluó a los 0, 5, 10, 15, 21 y 28 días de almacenamiento a una temperatura de 10 °C; para analizar la velocidad de respiración se mantuvieron a 20 °C por 16 días. Ellos obtuvieron que la película a base de caranauba redujo la actividad enzimática del jitomate, y en el caso de la película de aceite mineral éste redujo la velocidad de respiración, los cambios de color, la pérdida de peso y la actividad enzimática en ambos grados de madurez (rayados y rojos), sin afectar su firmeza, acidez y pH, por lo que concluyeron que la película a base de aceite mineral puede conservar la calidad y extender la vida útil del jitomate.
4.4. Tratamientos con ozono
El ozono posee un poder desinfectante que puede incrementar la vida útil de frutas y hortalizas; éste es atribuido a su potencial altamente oxidante que destruye los componentes vitales de las células de los microorganismos (ácidos grasos insaturados, aminoácidos, péptidos y proteínas), además de deteriorar los ácidos nucleicos (Han et al, 2002; Das et al., 2006; Bhat, 2012).
Rodoni et al. (2010) evaluaron el efecto del tratamiento con ozono sobre la calidad de jitomate. Los jitomates fueron expuestos a ozono gaseoso a una concentración de 10 L/L durante 10 minutos, y se observó una
disminución en el deterioro, en el reblandecimiento y en la pérdida de peso del jitomate, sin presentar cambios en el color, en el contenido de azúcares, en la acidez y en la actividad antioxidante.
4.5. Atmósferas controladas y modificadas
Tanto el envasado en atmósferas modificadas (EAM) como el almacenamiento en atmósferas controladas (AC) son usados para incrementar la vida útil de productos vegetales y reducir la presencia de microorganismos patógenos relacionados con el consumo de frutas y hortalizas frescas o mínimamente procesadas (Das et al., 2006).
El envasado en atmósferas modificadas consiste en la modificación de los niveles de O2 y CO2 de la atmósfera con el propósito de reducir la respiración y la producción de etileno, retardar la maduración y el reblandecimiento, y disminuir los cambios asociados con la madurez de frutas y hortalizas, alargando así su vida útil (Das et al. 2006).
La modificación de la atmósfera puede crearse de dos maneras: pasiva (intercambio entre la respiración del fruto con el medio, utilizando un material adecuado) o activa (inyección de mezcla específica de gases), para lograr los niveles de O2 (3-8%) y CO2 (25%) adecuados para reducir la respiración del producto (Das et al. 2006). Este método es comúnmente empleado para mantener la calidad de frutas y hortalizas; sin embargo, por sí solo no tiene la capacidad suficiente para extender su vida útil, y resulta conveniente combinarlo con otras técnicas (Corbo et al., 2004; Akbduak y Akbudak, 2007).
Por otra parte, según Baugher y Singha (2003), el almacenamiento en AC consiste en alterar la concentración de gases atmosféricos dentro de una cámara de refrigeración en la
cual se almacenan frutas y hortalizas con el objetivo de extender su vida útil.
El jitomate es un fruto climatérico, que aún después de ser cosechado, continúa con el proceso de respiración e incrementando la producción de etileno, lo cual impacta en los atributos de calidad (color y reblandecimiento del tejido) (Akbudak et al., 2007). Tanto EAM como AC han sido aplicadas en jitomate, principalmente en la variedad cherry, con el objetivo de incrementar la vida útil durante su almacenamiento (Akbudak et al., 2007; Das et al., 2006; Gómez y Camelo. 2002; Siripatrawan y AssatarakuL, 2009).
Gómez y Camelo (2002), determinaron el efecto del almacenamiento en atmósferas controladas de jitomate Diva, sobre el color y firmeza del mismo; ellos emplearon 3 niveles de baja concentración de O2 (1, 3 y 5%) y un testigo (21 %, completando hasta el 100% con N2). Encontraron que, conforme la concentración de O2 disminuyó, los cambios en color y firmeza se redujeron, alcanzando los niveles más aceptables por el consumidor a los 7, 12, 14 y 21 días de almacenamiento con 21%, 5%, 3% y 1% de O2, respectivamente.
Conclusiones
De acuerdo a la investigación realizada, se señala que en México las variedades más representativas de jitomate son la variedad cherry, bola y saladette. Este producto agrícola es rico en antioxidantes como: vitamina C, licopeno y carotenoides, los cuales pueden ayudar a la prevención de cáncer. El jitomate puede ser atacado principalmente por hongos y bacterias que producen diferentes enfermedades en el fruto, sin embargo, la enfermedad de mayor importancia, sobre todo cuando son producidos en invernadero, es el moho gris (manchas circulares cubiertas con polvo grisáceo) causado por Botrytis cinerea.
Diversos autores han reportado el uso de tecnologías de conservación tales como refrigeración, tratamientos térmicos, atmósferas controladas y modificadas, tratamientos con ozono y películas comestibles para alargar la vida útil del jitomate; sin embargo cabe mencionar que ningún método por sí solo logra mantener las características físicas (color y textura) y antioxidantes del producto, por lo que es necesario combinar estas técnicas para obtener una mejor calidad.
Agradecimientos
La autora C.M. Notario-Medellín, agradece al Consejo Nacional de Ciencia y Tecnología (CONACYT) y a la Universidad de las Américas Puebla (UDLAP), por el apoyo y financiamiento de sus estudios de posgrado.
Nacional de Horticultura. Invernaderos: Diseño, Manejo y Producción. Torreón, Coah, México. 1315 Octubre 2004.
Amaya, P., Peña, L., Mosquera, A., Villada, H. y Villada, D. 2010. Efecto del uso de recubrimientos sobre la calidad del tomate (Lycopersicon esculentum Mill). Dyna. 77(162):67-73.
Bartz, J. y Brecht, J. 2005. Postharvest Physiology and Pathology of Vegetables. Segunda edición. Taylor & Francis e-Library. EE. UU. 816 p
Baugher, T. A. y Singha, S. 2003. Concise encyclopedia of temperate tree fruit. Food Products Press, EE.UU. 313 p.
Bayer CropScience. 2010. Enfermedades de conservación del tomate. En http://oberon.bayercropscience.es/Conservaciontoma te.pdf. , accesada 18/02/2012.
Bermúdez, V. 2000. TecnologÍa Energética SPUPV / Universidad Politécnica de Valencia. Universidad Politécnica de Valencia, España. 303 p.
Libro docente
Bhat, R. 2012. Progress in Food Preservation. WILEYBLACKWELL. U.K. 238 p.
Referencias
Aherne, A. S. A., Jiwan, M. A., Daly, T. y O’Brien, N. M. 2009. Geographical Location has Greater Impact on Carotenoid Content and Bioaccesibility from Tomatoes than Variety. Plant Foods for Human Nutrition. 64:250-256.
Akbudak, B. y Akbudak, N. 2007. Effects of hot water treatment and modified atmosphere packaging on the quality and cold storage life of cherry tomatoes. Journal of Food Science and Technology. 44: 216–219.
Akbudak, B., Akbudak, N., Seniz, V. y Eris, A. 2007. Sequential treatments of hot water and modified atmosphere packing in cherry tomatoes. Journal of Food Quality.30:896-910.
Álvarez, R. y Delgadillo, F. 2004. Enfermedades del tomate y chile Bell. Memorias del IV Simposio
Cerkauskas, R. 2005. Tomato Diseases. Soft Rot. AVRDC. The World Vegetable Center. Fact Sheet. En http://www.avrdc.org/pdf/tomato/soft_rot.pdf, accesada 10/04/2012
Corbo, M. R., Altieri, C., Amato, D., Campaniello, D., Del Nobile, M. A. y Sinigaglia, M. 2004. Effect of temperature on shelf life and microbial population of
Borguini, R. y Ferraz, E. 2009. Tomatoes and tomato products as dietary sources of antioxidants. Food Reviews International. 25:313–325.
Brennan, J. G. y Grandison, A. S. 2012. Food Processing Handbook. Segunda edición. WILEYVCH, Singapur. 131 p
Bugianesi, R., Salucci, M., Leonardi, C., Ferracane, R., Catasa, G., Azzini, E. y Maiani, G. 2004. Effect of domestic cooking on human bioavilability of naringenin, chlorogenic acid, lycopene and carotene in cherry tomatoes. European Journal of Nutrition 43:360-366.
Candelas, M., Alanís, M. G. J. y Del Rí, F. 2006. Cuantificación de licopeno y otros carotenoides en tomate y polvo de tomate. Revista Mexicana de Agronegocios. 10(19):1-11
lightly processed cactus pear fruit. Postharvest Biology and Technology. 31: 93–104.
Costa, J. M. y Heuvelink, E. 2005. Introduction: the tomato crop and industry. En: E. Heuvelink (Ed). Crop production science in horticulture 13. Tomatoes. CABI Publishing. London, UK. pp. 1-19.
Das, E., Güaraka, G. C. y Bayindirli. 2006. Effect of controlled atmosphere storage, modified atmosphere packing and gaseous ozone treatment on eh survival of Salmonella Enteritidis on cherry tomatoes. Food Microbiology. 23:430-438.
Dávila-Aviña, J. E. J., Villa-Rodriguez, J., CruzValenzuela, R., Rodriguez-Armenta, M., EspinoDíaz, M., Ayala-Zavala, J. F., Olivas-Orozco, G. I., Heredia, B. y González-Aguilar, G. 2011. Effect of Edible Coatings, Storage Time and Maturity Stage on Overall Quality of Tomato Fruits. American Journal of Agricultural and Biological Sciences. 6 (1): 162-171.
Delahaut, K. y Stevenson, W. 2004. Tomato disorders: Post-harvest fruit diseases. University of Wisconsin System. En http://learningstore.uwex.edu/assets/pdfs/A3799.PD F, accesada 4/04/2012.
El Assi, N. M. 2004. Alleviating chilling injury and maintain quality of tomato fruit by hot water treatment. Journal of Agricultural Science.16 (1) 17.
FAO. 2010. INFOODS Food Composition Database for Biodiversity, version 1.0. En http://www.fao.org/infoods/tables_int_en.stm Accesada 9/02/2012
FAOSTAT. 2011. Organización de las naciones unidas para la alimentación y la agricultura. Food and Agricultural commodities production. En http://faostat.fao.org/site/339/default.aspx., accesada 9/02/2012.
Gleason, M. y Edmunds, B. 2006. Tomato Diseases and disorders. Iowa State University. Univerity Extension. En http://www.extension.iastate.edu/publications/pm12 66.pdf, accesada 2/04/2012.
Gómez, P. A., y Camelo, A. F. L. 2002. Calidad postcosecha de tomates almacenados en atmósferas controladas. Horticultura Brasileira. 20(1):38-43.
Greenwald, P., Cliffordb, C. K. y Milnerb, J. A. 2001. Dieta y prevención del cáncer. European Journal of Cancer. 1:365-382.
Han, Y., Floros, J. D., Linton, R. H., Nielsen, S. S. y Nelson, P. E. 2002. Response surface modeling for the inactivation of E.coli O157:H7 on green peppers (Capsicum annuum) by ozone gas treatment. Journal of Food Science. 67(3):1188–1193.
Ilhay, R., Hdider, Ch., Lenucci, M. S., Tlili, I. y Dalessandro, G. 2011. Phytochemical composition and antioxidant activity of high-lycopene tomato
(Solanum licopersicum L.) cultivars grown in southern Italy. Scientia Horiculturae. 127:255-261.
INEGI. 2011. INSTITUTO NACIONAL DE ESTADÍSTICA Y GEOGRAFÍA. Volumen de producción de tomate rojo (jitomate). En http://www2.inegi.org.mx/sistemas/mapatematicome xicocifras3d/default.aspx?e=0&m=0&src=0&sec=M &ind=1009000032&enn=Estados%20Unidos%20M exicanos&ani=2009, accesada 9/02/2012.
Jacob, K., García-Alonso, F. J., Ros, G. y Periago, M.J. Stability of carotenoids, phenolic compounds, ascorbic acid and antioxidant capacity of tomatoes during thermal processing. Archivos Latinoamericanos de Nutrición. 60(2):192-198
Kader, A. A. 2011. Postharvest Technology of Horticultural Crops. University of California. Agricultural and Natural Resources. En http://books.google.com.mx/books?hl=es&lr=&id= O1zhx2OWftQC&oi=fnd&pg=PR7&dq=postharves t+technology+of+horticultural+crops+pdf&ots=4fv0 41wlBO&sig=Qlb1dIAzA5VddD5wny5Y_l6VkRg# v=onepage&q&f=true, accesada 10/04/2012.
Kennelly, M. 2009. Tomato Leaf and Fruit Diseases and Disorders. Kansas State University. Plant Pathology. L721. En http://www.ksre.ksu.edu/library/plant2/l721.pdf, accesada 4/04/2012
Liu, R. H. 2004. Potential synergy of phytochemicals in cancer prevention: mechanism of action. The Journal of Nutrition. 134:3479S-3485S.
Mahovic, M. J., Sargent, S. A., Bartz, J. A. y Lon, E. 2006. Identificación y control postcosecha de las enfermedades del tomate en la florida. Institute of Food and Agricultural Sciences (IFAS). http://edis.ifas.ufl.edu/pdffiles/HS/HS33400.pdf, accesada 19/02/2012.
Moreno, Y. 2010. Diversidad morfológica y agronómica de poblaciones nativas de jitomate del centro, sur y sureste de México. Tesis de Maestría. Colegio de Postgraduados 129 p.
Muratore, G., Licciardello, F. y Maccarone, E. 2005. Evaluation of the chemical quality of new type of small-sized tomato cultivar, the plum tomato (Lycoersicon lycopersicum). Italian Journal of Food Science. 1(17):75-81.
Ontario CropIPM, 2009. Ministry of Agriculture Food and Rural Affairs. Black Mold (Alternaria Fruit Rot). En: http://www.omafra.gov.on.ca/IPM/english/tomatoes/ diseases-and-disorders/black-mold.html#advanced, accesada 2/04/2012.
Perera, C. O. y Yen, G. M. 2007. Functional properties of carotenoids in human health. International Journal of Food Properties. 10:201-230.
Productores de Hortalizas. 2006. Plagas y enfermedades del tomate. Guía de identificación y manejo. www.hortalizas.com, accesada 9/02/2012.
Quezada, J., Díaz, M., Gutiérrez, M., y Debeaufort, F. 2003. Application of edible coatings to improve shelf-life of Mexican guava. Acta Horticultura 599:589-594. Citado en Ramos-García, M.L., Bautista-Baños, S., Barrera-Necha, L.L., BosquezMolina, E., Alia-Tejacal, I. y Estrada-Carrillo, M. 2010. Compuestos antimicrobianos adicionados en recubrimientos comestibles para uso en productos hortofrutícolas. Revista Mexicana de Fitopatología 28: 44- 57.
Quintero, C., Falguera, V. y Aldemar, H. 2010. Películas y recubrimientos comestibles: importancia y tendencias recientes en la cadena hortofrutícola. Tumbaga. 5:93-118.
Ramos-García, M. L., Bautista-Baños, S., BarreraNecha, L. L., Bosquez-Molina, E., Alia-Tejacal, I. y Estrada-Carrillo, M. 2010. Compuestos antimicrobianos adicionados en recubrimientos comestibles para uso en productos hortofrutícolas. Revista Mexicana de Fitopatología 28:44- 57.
Riboli, E. y Norat, T. 2003. Epidemiologic evidence of the protective effect of fruit and vegetable on cáncer risk. Americal Jurnal of Clinical Nutrition 78(suppl):559S-69S.
Rodoni, L., Casadel, N., Concellón, A. Chaves, A. R. y Vicente, A. R. 2010. Effect of short-term ozone treatments on tomato (Solanum lycopersicum L.) fruit quality and cell call degradation. Journal of Agricultural and Food Chemistry. 58:594-599.
SIAP. 2011. Servicio de Información Agroalimentaria y Pesquera. Anuario Agropecuario http://www.siap.gob.mx/index.php?option=com_con tent&view=article&id=261&Itemid=429, accesada 9/02/2012.
Singh, P. y Goyal, G.K. 2008. Dietary lycopene: its properties and anticarcinogenic effects.
Comprehensive reviews in food science and food safety. 7:255-270.
Siripatrawan, U. y Assatarakul, K. 2009. Methyl jasmonate coupled with modified atmosphere packing to extend shelf life tomato (Lycopersicon esculntum Mill,) during cold storage. Institute of Food Science and Technology. 44:1065-1071.
Sosa-Morales, M. E., López-Malo, A. y García, H. S. 2011. Postharvest Heat Treatments in Fruits. Advances in Post-Harvest Treatments and Fruit Quality and Safety. Nova Science Piblishers, Inc. New York. pp 31-39.
Soto-Zamora, G., Yahia, E. M., Brecht, J. K. y Gardea, A. 2004. Efects of postharvest hot air treatment on the quality “rhapsody” tomato fruit. Journal of Food Quality. 28:492-504.
Strazzullo, G., De Giulio, A., Tommonario, G., La Pastina, C., Poli, A., Nicolaus, B. y De Prisco, R. 2007. Antioxidant activity and lycopene and bcarotene contents in different cultivars of tomato (Lycopersicon esculentum). International Journal of Food Properties. 10:321-329.
Suslow, T. V. y Cantwell, M. 2006. Tomato. Technology Research and information Center. Department of Plant Sciences. University of California. Davis, CA.
TNAU. 2008. TamilNadu Agricultural University. Coimbatore. Post harvest diseases: tomato. En http://agritech.tnau.ac.in/crop_protection/crop_prot_ crop%20diseases_postharvest_tomato.html, accesada 2/04/2012.
USDA. 2012. United States Department of Agriculture. Natural Resources Conservation Service. Clasificaction. En http://plants.usda.gov/java/profile?symbol=SOLY2, accesada 9/02/2012.
Zanfini, A., Dreassi, E., La rosa, C., Addario, C. y Corti, P. 2007. Quantitative variations of the main carotenoids in Italian tomatoes in relation to geographic location, harvest time, varieties and ripening stage. Italian Journal of Food Science. 19(2):181-190.

Temas Selectos de Ingeniería de Alimentos 6 - 1 (2012): 54 - 65

Propiedades del aceite esencial de albahaca (Ocimum basilicum L.) y sus aplicaciones en alimentos
G. A. Cardoso-Ugarte* y M. E. Sosa-Morales
Departamento de Ingeniería Química, Alimentos y Ambiental, Fundación Universidad de las Américas Puebla. Exhacienda Sta. Catarina Mártir S/N, Puebla. C.P.72810. México.
Resumen
Debido a sus múltiples propiedades, el aceite esencial de albahaca ha sido ampliamente utilizado a nivel mundial a lo largo de la historia. Sus usos más comunes se han dirigido a la industria farmacéutica, perfumería, medicina tradicional y como saborizante y aromatizante en el ámbito culinario. Sin embargo, enfocado a la industria alimenticia, los compuestos presentes en el aceite esencial han demostrado poseer propiedades de inhibición en el crecimiento fúngico y bacteriano, capacidad insecticida y reducción de la oxidación lipídica. Tales características lo convierten en un potencial aditivo alimenticio, que de ser implementado puede brindar beneficios funcionales, aumentando la vida de anaquel del producto y reduciendo las reacciones indeseables ocasionadas por el deterioro de lípidos. En este trabajo se presenta una recopilación bibliográfica de los diversos potenciales del aceite esencial de albahaca aplicados a la industria alimenticia.
Palabras clave: albahaca, aceite esencial, antioxidante, antifúngico, antibacteriano, insecticida.
Abstract
Due to its multiple properties, basil essential oil has been widely used all over the world along human history. Its most common uses have been conducted to pharmaceutics, perfumery, alternative medicine and as a flavoring ingredient in the culinary area. However, focused on the food industry, the composition of its essential oil has shown inactivation of both fungi and bacteria, insecticidal activity, and the reduction of lipid oxidation. These features make the basil essential oil a potential food additive that if it is added, it may confer functional benefits by increasing the product shelf life and reducing the undesirable reactions due to lipid oxidation. A review of basil essential oil potential uses applied to the food industry is presented in this paper.
Keywords: basil, essential oil, antioxidant activity, antifungal, antibacterial, insecticidal activity.
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: gabriel.cardosoue@udlap.mx
Introducción
La albahaca (Ocimum basilicum L.) perteneciente a la familia Lamiaceae, es una hierba aromática que se produce en todo el mundo, se cree que su origen se dio en la India e Irán, y después fue introducida en Europa durante el siglo XII, tradicionalmente, la albahaca ha sido ampliamente utilizada en alimentos como un agente saborizante, así como en perfumería e industrias farmacéuticas (Ijaz et al., 2008). De igual manera, en la medicina tradicional sus hojas y flores han sido empleadas como remedio de algunas enfermedades digestivas (Politeo et al., 2007; Ebrahim, 2006) y respiratorias (Simon et al., 1999). Por otra parte, es fuente de compuestos aromáticos y aceites esenciales con constituyentes biológicos que poseen propiedades insecticidas, nematicidas, fungistáticas y antimicrobianas (Politeo et al., 2007). Asimismo, sus compuestos fenólicos y flavonoides han mostrado ser potentes antioxidantes (Ijaz et al., 2008), capturadores de radicales libres y quelantes de metales (Jayasinghe et al., 2003).
Debido a la necesidad actual de crear alimentos seguros y funcionales de origen natural, el aceite esencial de albahaca tiene un amplio potencial de utilización como aditivo en alimentos, aportando funcionalidades y beneficios al producto final. Por lo anterior, el objetivo de la presente revisión es mostrar las aplicaciones del aceite esencial de albahaca en cuanto a sus propiedades antioxidantes, bactericidas, fungicidas e insecticidas dentro del área de alimentos, reportadas en investigaciones científicas.
Revisión bibliográfica
1. Aspectos generales de la albahaca
El género Ocimum comprende más de 150 especies y es considerado uno de los géneros más grandes de la familia Lamiaceae, la albahaca (Ocimum basilicum L.), miembro de esta familia, es una hierba anual que crece en muchas regiones alrededor del mundo, cuyo origen se cree que fue en la India, introduciéndose en Europa hacia el siglo XII (Wogiatzi et al., 2011). Existe un gran número de variedades de albahaca que varían en color de hoja (verde o morada) y en aroma; es una hierba de 20 a 60 cm de largo y sus flores son de colores blanco y morado (Ebrahim, 2006). Telci et al. (2006) reportan una clasificación basada en su producción geográfica, en la cual mencionan los tipos Europeo (Italia, Francia, Bulgaria, Egipto y Sudáfrica), Tropical (India, Pakistán y Guatemala), Reunion (Tailandia, Madagascar y Vietnam) y Norteamericano.
La planta ha sido utilizada en alimentos y productos de higiene bucal; asimismo, se han reportado sus actividades antivirales y antimicrobianas (Ebrahim, 2006). Sus hojas han sido utilizadas en el área farmacéutica como diurético debido a sus propiedades estimulantes y en perfumería (Chalchat y Musa, 2008). Es muy utilizada en medicina tradicional para efectos terapéuticos con diferentes funciones particularmente digestivas (Politeo et al., 2007), como carminativo (Ebrahim, 2006) y en la eliminación de lombrices estomacales e intestinales (Lee et al., 2005). Se ha reportado que las hojas contienen propiedades tónicas, antisépticas e insecticidas; asimismo, es sabido que sus hojas y flores pueden ser utilizadas para el tratamiento de tos y dolor (Gülcin et al. 2007), así como para tratar la dispepsia, constipación, mal funcionamiento de riñones (Lee et al., 2005) y como agente galactogogo y antiespasmódico (Ebrahim, 2006).
Como hierba culinaria tiene una larga historia, gracias a que aporta un sabor distinto a los alimentos (Politeo et al., 2007; Lee et al., 2005). Es una de las especias más utilizadas como sazonador ya sea en estado fresco o seco, y es ampliamente utilizada en la cocina Mediterránea en productos de tomate, vegetales, ensaladas, pizzas, carnes, sopas y mariscos (Chang et al., 2008). Se utiliza también en productos de confitería y de horneado y como condimento en productos tales como: embutidos, aderezos para ensaladas, bebidas no alcohólicas, helados, pasta de tomate, salsas, encurtidos y vinagres (Labra, 2004)
2. Aceite esencial de albahaca
El género Ocimum spp., contiene una amplia variedad de aceites esenciales ricos en compuestos fenólicos y una amplia gama de productos naturales entre los que se encuentran polifenoles tales como flavonoides y antocianinas. La composición química del aceite esencial de albahaca ha sido ampliamente estudiada, mostrando una gran variedad de compuestos y diferentes quimiotipos (Rattanachaikunsopon y Phumkhachorn, 2010). El aceite esencial de albahaca ha demostrado tener constituyentes biológicamente activos que actúan como insecticidas, nematicidas, fungistáticos y antimicrobianos; asimismo, es utilizado como saborizante en alimentos, como ingrediente activo en productos dentales y orales, en fragancias y en medicinas. (Simon et al. 1999). En la industria farmacéutica ha sido utilizado debido a su actividad antimicrobiana y a sus propiedades antioxidantes (Javanmardi et al., 2002).
2.1. Composición química
Las propiedades y usos que se le han dado al aceite esencial de albahaca pueden ser atribuidos a sus componentes mayoritarios tales como metilchavicol, eugenol, linalol,
alcanfor y metilcinamato. En 1999, Simon et al. describieron los componentes mayoritarios de 6 tipos de aceites esenciales comercializados, cada uno derivado de diferentes cultivos y quimiotipos. El aceite esencial de albahaca tipo Europeo es considerado como el de más alta calidad y el cual produce el más fino olor, contiene linalol y metilchavicol como componentes principales, y en porcentajes más bajos, 1,8cineol, alfa-pineno, ß-pineno, mirceno, ocimeno, terpinoleno, alcanfor, terpineno-4-ol, alfa-terpineol, eugenol y sesquiterpenos; el aceite esencial de la variedad Egipcia es similar al de la variedad Europea en cuanto a su composición, con la excepción de que la concentración de linalol es considerablemente más baja, mientras que la de metilchavicol es más alta; en contraste, el aceite esencial de la variedad Reunion contiene un bajo porcentaje de linalol y es un aceite más áspero y picoso, debido a su alta concentración de metilchavicol y un menor contenido de 1,8.cineol, borneol, alcanfor y eugenol; finalmente, los aceites esenciales de las variedades Bulgaria y Java son ricos en metilcinamato y eugenol respectivamente.
El aceite esencial de albahaca tiene una gran variedad de compuestos químicos, los cuales afectan su quimiotipo, color de las hojas y flores, aroma y origen (Da-Silva et al., 2003). Ijaz et al. (2008) llevaron a cabo un estudio en el cual demostraron que así como la composición química del aceite esencial de albahaca varía según las hojas, flores y su origen, el periodo de siembra y cosecha de la planta también influye de manera significativa en la composición del aceite esencial. Sin embargo, de manera general, sus principales componentes son monoterpenos y fenilpropanoides (Labra et al., 2004), monoterpenos oxigenados (Telci et al., 2006; Bozin et al., 2006), hidrocarburos monoterpenos, hidrocarburos monoterpenos aromáticos y oxigenados, hidrocarburos
sesquiterpenos, sesquiterpenos oxigenados y compuestos alifáticos (Bozin et al., 2006).
En la Tabla I se muestran los compuestos químicos encontrados en investigaciones recientes, en las cuales se evaluaron cuatro tipos de albahaca originarias de diferentes países. Al analizar la Tabla, se encontró que sólo el cariofileno está presente en todas las especies. Por otro lado, se encontró que los compuestos presentes en la mayoría de las especies son: 1,8-cineol, 1-octen-3-ol, 6-metil5-heptan-2-uno, alcanfor, fenchona, linalol, metilchavicol ó estragol, neral, óxido de cariofileno, α-bergamoteno, α-bisaboleno y αhumuleno; en total, fueron identificados 55 compuestos, y en todos los casos los aceites esenciales fueron extraídos mediante hidrodestilación.
2.2. Propiedades físicas
A pesar de que el estudio de la composición química y las diversas propiedades que posee el aceite esencial de albahaca han sido ampliamente reportados, pocas son las investigaciones que describen las propiedades físicas de su aceite esencial.
Ijaz et al. (2008) llevaron a cabo un estudio de aceites esenciales de albahaca cultivada en diferentes épocas del año, y describieron algunas propiedades físicas de cada uno de ellos, las cuales son mostradas en la Tabla II. El índice de refracción (25°C) se encontró entre 1.4995±0.002 y 1.5045±0.003, la densidad (25°C) fue reportada en el rango de 0.95±0.02 y 0.97±0.02 g/mL, mientras que el rendimiento fue de 0.5 a 0.8%. De manera general, el índice de refracción y la densidad no variaron en cuanto a la época del año, sin embargo, en el rendimiento se pudo observar una notable diferencia entre lo obtenido en invierno y en verano.
Por otra parte, Mohammad-Taghi y Karamatollah (2008) reportaron la densidad e
índice de refracción del aceite esencial de albahaca extraído por hidrodestilación y extracción asistida por microondas; la densidad reportada fue de 0.918 y 0.924 g/mL respectivamente, mientras que el índice de refracción fue de 1.5030 en ambos casos, concluyendo que las propiedades físicas del aceite esencial de albahaca no se ven modificadas por el método de extracción, al menos para los dos métodos empleados en dicho estudio.
3. Aplicaciones en alimentos
3.1. Capacidad antioxidante
Los antioxidantes han sido ampliamente utilizados como aditivos en alimentos para disminuir su oxidación. Asimismo, cumplen un rol importante en la prevención de enfermedades y envejecimiento, ya que están estrechamente relacionados con la peroxidación de lípidos (Noguchi y Niki , 1999).
La función tradicional de los antioxidantes ha sido un punto importante cuyo interés ha ido aumentando dentro de los procesos de elaboración y transformación de los alimentos. Como su nombre lo indica, actúan como inhibidores o reductores del desarrollo de rancidez oxidativa en alimentos con alto contenido en grasas, particularmente en carnes, lácteos y alimentos freídos. Los antioxidantes sintéticos más utilizados en alimentos, butilhidroxitolueno (BHT) y butilhidroxianisol (BHA), son altamente efectivos en su rol como antioxidantes, sin embargo, su uso ha ido disminuyendo debido a su inestabilidad así como a su posible acción carcinógena (Politeo et al., 2007). Por tal situación, existe un creciente interés en el estudio de aditivos naturales con potencial antioxidante (Tomaino et al., 2005).
Debido a su mecanismo de acción, el aceite esencial de albahaca es clasificado como
Tabla I. Comparación de la composición química del aceite esencial de albahaca de diferentes variedades.
Ebrahim (2006)
et al., (2006)
et al., (2010)
et al., (2007)
Compuesto químico
1,10-di-epi-cubenol
α-bergamoteno 0.85.27.962.2 α-bisaboleno 1.11.12.04
α-cadinol 7.1
α-copaeno 0.3
α-farnesano 1.52
α-guaieno 0.7
α-humuleno 1.10.50.60.2
α-pineno 0.2
α-terpineol 1.371.01
β-cubeneno 0.60.5
β-elemeno 1.90.3
β-eudesmol 0.2
β-farneseno 0.2
β-pineno 0.10.1
β-selineno 0.8
γ-cadineno 1.80.2
ρ-cimeno 0.1
Z- β- ocimeno 0.6
Bozin
Carovic
Politeo
Irán
Tabla II. Rendimiento y propiedades físicas del aceite esencial de albahaca de diferentes épocas del año.
Aceites esenciales
PrimaveraVeranoOtoñoInvierno
0.7±0.10.5±0.00.6±0.00.8±0.1
Porcentaje de rendimiento
Índice de refracción (25°C) 1.5017±0.0031.5045±0.0031.4995±0.0021.5015±0.004
Densidad (g/ml), 25°C 0.97±0.010.95±0.020.97±0.020.96±0.01
Adaptado de Ijaz et al. (2008).
antioxidante primario, debido a que actúa removiendo o inactivando los radicales libres producidos durante la reacción de oxidación a través de la donación de átomos de hidrógeno, interrumpiendo así la reacción en cadena. Se han llevado a cabo diversos métodos para determinar la actividad antioxidante de extractos y aceites esenciales in vitro. Entre los métodos más utilizados se encuentran la evaluación de la capacidad de extinción del radical libre 2.2-difenil-1-picril-hidrazil (DPPH٠) (Cichosky et al., 2011), así como la inhibición de peroxidación de lípidos (Bozin et al., 2006).
La determinación de la capacidad antioxidante de algún compuesto depende en gran manera del método de evaluación, ya que si ésta es determinada por un sólo método, los resultados pueden ser inadecuados y poco repetibles (Stupans et al., 2002). Jayasinghe et al. (2003), identificaron los principales componentes del aceite esencial de albahaca con actividad antioxidante por medio de tres métodos distintos: capacidad de extinción del radical libre DDPH٠, oxidación de la fosfatidilcolina de soya y determinación del hidroperóxido de fosfatodilcolina. Ijaz et al. (2008) llevaron a cabo tres pruebas distintas para determinar la capacidad antioxidante del aceite esencial de albahaca utilizando los métodos de captura del radical DDPH٠ , porcentaje de inhibición del ácido linoleico y blanqueabilidad de β-caroteno en el ácido
linoleico. Las tres pruebas comprobaron la capacidad antioxidante del aceite esencial de albahaca. Por otra parte, el método de conversión de aldehído/ácido carboxílico fue utilizado por Lee et al. (2005) para medir la capacidad antioxidante de los compuestos aromáticos de los aceites esenciales de albahaca y tomillo, comparándolos con el poder antioxidante de BHT y α-tocoferol; en ambos casos, los aceites esenciales mostraron una mayor actividad antioxidante.
Cichosky et al. (2011) llevaron a cabo un estudio en el cual probaron la eficacia del aceite esencial de albahaca como antioxidante de lípidos y proteínas tanto in vitro como en salami. Con los resultados de la capacidad antioxidante in vitro se determinó que la concentración mínima inhibitoria (CMI) del aceite esencial es de 12 mg/mL; asimismo la capacidad antioxidante del aceite esencial fue comparada con un control (eritorbato de sodio), mostrando éste una mayor capacidad antioxidante incluso al agregarse en menor concentración (0.75 mg/g) que el control (2.5 mg/g). Por otra parte, la capacidad antioxidante de proteínas fue descartada, debido a que no se mostró inhibición durante un periodo de almacenamiento de 28 días. Una menor concentración del aceite esencial de albahaca (0.39 mg/mL) con respecto a la del antioxidante sintético BHT (5.37 mg/ml) también mostró un mayor efecto antioxidante de lípidos en un estudio realizado por Bozin et
al. (2006), indicando que los compuestos responsables de la neutralización del radical DPPH٠fueron los monoterpenos fenólicos oxigenados (carvacrol, timol y metilchavicol) así como la mezcla de hidrocarbonos mono y sesquiterpenos.
Por otra parte, se ha reportado que uno de los componentes presentes en el aceite esencial de albahaca con alta capacidad antioxidante es el eugenol, por lo cual Politeo et al. (2007) compararon la capacidad antioxidante del eugenol con respecto al antioxidante sintético BHT, al aceite esencial de albahaca y a las agliconas volátiles del aceite esencial de albahaca. Al analizar los resultados de la capacidad de neutralización del radical DPPH٠ se descartó una mayor actividad antioxidante de las agliconas volátiles del aceite esencial de albahaca debido a que su actividad fue significativamente menor a la de los otros tratamientos. Por otro lado, se confirmó que el eugenol posee una actividad antioxidante ligeramente mayor a la del BHT y del aceite esencial de albahaca, a pesar de que en este último la concentración de eugenol fue relativamente baja (5.9%). Dichos resultados llevaron a la conclusión de que la capacidad antioxidante del aceite esencial de albahaca es debida a que el eugenol y sus demás componentes actúan sinérgicamente como antioxidantes, aunque algunos de ellos no reporten dicha actividad.
3.2. Capacidad antibacterial
La necesidad de preservar alimentos y el hecho de que la creación de nuevos productos alimenticios exige una mayor vida de anaquel y un alto grado de protección en contra de microorganismos patógenos han derivado en el interés de desarrollar nuevos métodos de preservación tales como el uso de aceites esenciales, ya que al ser aditivos antibacteriales los convierte en una opción natural de inhibición de bacterias (CarovicStanko et al., 2010).
El poder antimicrobiano de la albahaca se atribuye a la actividad biológica de algunos de sus componentes tales como linalol, 1,8cineol, eugenol, estragol y alcanfor (Rattanachaikunsopon y Phumkhachorn, 2010). Si se toma en cuenta que la albahaca contiene un gran número de compuestos químicos, es difícil afirmar que su actividad antimicrobiana está dada por un sólo mecanismo (Burt, 2004).
Se han propuesto diferentes mecanismos antimicrobianos de los aceites esenciales tales como degradación de la pared celular (Helander et al., 1998), daño a la membrana citoplásmica, daño a las proteínas de la membrana, coagulación del citoplasma y agotamiento de la fuerza motriz de los protones, asimismo, se ha demostrado que a pesar de que no todos los componentes químicos de los aceites esenciales de albahaca tienen propiedades antimicrobianas, dichos compuestos sirven como soporte o para aumentar el poder antimicrobiano de los demás (Rattanachaikunsopon y Phumkhachorn, 2010); tal es el caso del ρcimeno, el cual incrementó la actividad antimicrobiana del timol en el crecimiento de Bacilus cereus, tanto in vitro como en un alimento (Delgado et al., 2004).
Rattanachaikunsopon y Phumkhachorn (2010) probaron el poder antibacterial de aceites esenciales de diferentes hierbas, entre ellas albahaca, sobre diferentes cepas de Salmonella enteritidis; los resultados mostraron que el aceite esencial de albahaca fue el que tuvo la mayor actividad antibacterial en todas las cepas. Posteriormente, se probó el aceite esencial en una concentración de 50 ppm agregado a un embutido de origen tailandés llamado “nham” inoculado con S. enteritidis, después de 3 días de almacenamiento el número de bacterias disminuyó 3 ciclos logarítmicos; asimismo, en concentraciones de 100 y 150 ppm no se detectó crecimiento de la bacteria después de 3
días de almacenamiento y no se observó diferencia significativa (p<0.05) en cuanto a apariencia, aroma, sabor, textura y gusto general con respecto al alimento sin aceite esencial.
El poder antibacterial del aceite esencial de albahaca ha sido probado en bacterias Grampositivas (Micrococcus flavus, Sarcina lutea, Staphylococcus aureus, S. epidermis y Bacillus subtilis) y bacterias Gram-negativas (Escherichia coli, Pseudomonas aureaginosa, Salmonella typhi, S. enteritidis y Shigella sonei). De manera general, ambos tipos de bacterias son sensibles al aceite esencial de albahaca, sin embargo, las bacterias Grampositivas han mostrado una mayor sensibilidad (Bozin et al., 2006). Ijaz et al., (2008), compararon el poder antimicrobiano del aceite esencial de albahaca en ocho cepas distintas, encontrando que Staphylococcus aureus y Bacilus subtilis fueron las más sensibles. De igual forma, la inhibición de E. coli O157:H7 ha sido reportada para la variedad de albahaca “genovesa” en una concentración mínima inhibitoria de 400 ppm (Carovic-Stanko et al., 2010).
3.3. Capacidad antifúngica
La producción de aceites esenciales de plantas y especias ha sido atribuida en gran parte al mecanismo de defensa de las plantas contra microorganismos patógenos y pestes (Oxenham, 2003), y en efecto, los aceites esenciales han demostrado poseer propiedades antimicrobianas y antifúngicas.
El poder antifúngico del aceite esencial de albahaca ha sido probado sobre diferentes microorganismos en distintos alimentos por diversos investigadores, por ejemplo Oxenham et al. (2005), probaron el poder antifúngico del aceite esencial de albahaca contra Uromices fabae en habas verdes y Botritis fabae en chocolate, así como la reducción fúngica in vitro, determinando que a una concentración
de 1000 ppm se redujo en 78% el crecimiento fúngico (in vitro). Al analizar por separado los componentes mayoritarios encontrados en el aceite esencial de albahaca (metilchavicol, linalol, eugenol y eucaliptol), se encontró que éstos redujeron significativamente (p<0.05) el crecimiento fúngico, observando el mayor efecto fungicida a una concentración de 200 ppm de eugenol, en la cual se eliminó por completo el crecimiento de los mohos. Asimismo, al analizar el efecto de una combinación de los compuestos mayoritarios sobre los mohos, los resultados obtenidos fueron los mismos que con el aceite esencial. Para el control de las dos especies de hongos, se determinó que el tratamiento realizado 3 horas después de la inoculación del hongo en una concentración de 1000 ppm, fue el más efectivo, reduciendo la infección en un 96%.
Por otra parte, Bozin et al. (2006) probaron la capacidad antifúngica de los aceites esenciales de albahaca, orégano y tomillo en Candida albicans y 5 especies de dermatomicetos. Los resultados fueron favorables en cuanto a la capacidad fungicida y fungistática del aceite esencial, sin embargo dicha capacidad fue menor con respecto a la de los aceites esenciales de orégano y tomillo, lo que se atribuye al bajo contenido de carvacrol (0.33%) en el aceite esencial de albahaca empleado, así como la ausencia de timol. Cabe señalar que en las variedades de albahaca descritas químicamente en la presente revisión, sólo en una de ellas se reporta la presencia de carvacrol, y en ninguna la de timol.
El poder fungicida del aceite esencial de una variedad de albahaca africana sobre Aspergillus repens, Curvularia lunata y Fusarium moniliforme fue analizado por Amadi et al. (2010). Los resultados mostraron el poder fungicida del aceite esencial, sin embargo, su efectividad varió dependiendo del extractante utilizado (etanol, acetona y agua). La reducción e inhibición del crecimiento de los tres mohos fue mostrada por los tres
extractos obtenidos, siendo A. repens el más sensible; asimismo, una mayor efectividad se mostró con el aceite esencial extraído con acetona, mientras que la menor efectividad se mostró utilizando agua como extractante.
En otros estudios, el crecimiento del micelio y la inhibición de la espora de siete mohos por medio de la adición de aceite esencial de albahaca, fue evaluada por Piyo et al. (2009) en un estudio in vitro. En la inhibición del crecimiento de micelio, el aceite esencial mostró diferentes resultados a concentraciones diferentes: en 0.6% v/v, Fusarium moniliforme y Pyricularia arisea, fueron inhibidos al 100%, mientras que F. proliferatum fue inhibido en 49.6%; a una concentración de 2.0% v/v, Bipolaris oryzae, Alternaria brassicicola y Aspergillus flavus fueron inhibidos en un 97.4%, 94.6% y 59.2% respectivamente; sin embargo, no fue capaz de inhibir el crecimiento de Rhizoctonia solani. Por otra parte, los resultados de la inhibición de la germinación de la espora indicaron que a una concentración de 0.8% v/v, el aceite esencial retardó el crecimiento de F. moniliforme en un 91.31% y A. brassicicola en un 99.74%, y a una concentración de 2.0% v/v, F. proliferatum, P. arisea, B. orizae, R. solani y A. flavus fueron completamente inhibidos.
Otro estudio acerca del poder antifúngico del aceite esencial de albahaca fue el realizado por Saggiorato et al. (2012) el cual fue probado in vitro y en la superficie de un embutido tipo italiano. En la prueba in vitro, una concentración de 10 mg/mL de aceite esencial inhibió el crecimiento de Penicillium sp., mientras que para Aspergillus sp., la concentración mínima inhibitoria fue de 25 mg/mL. Asimismo, se realizaron mezclas de ambos hongos en concentraciones de 10, 25, 50 y 100 mg/mL las cuales fueron inoculadas en el embutido para evaluar la capacidad fungicida del aceite esencial; la inhibición de dichas mezclas a siete días de almacenamiento fue proporcional a la concentración del aceite
esencial, siendo la concentración de 10 mg/mL la que mostró una inhibición total. La capacidad antifúngica del aceite esencial fue atribuida a los compuestos 1,8-cineol, alcanfor, β-pineno y acetato de bornilo. Cabe mencionar que al llevar a cabo una prueba sensorial, no se detectó diferencia significativa (p<0.05) en el sabor del producto con todas las concentraciones probadas.
3.4. Capacidad insecticida
Debido a la restricción del uso de fumigantes comunes y la resistencia que han desarrollado ciertos insectos contra éstos, ha crecido la necesidad de crear nuevas alternativas para controlar las pestes de insectos. Entre dichas alternativas, los polvos de hierbas secas, extractos de plantas y sus aceites esenciales han mostrado efectos fumigantes ante dichas plagas (Pascual-Villalobos et al., 2003).
Para comprobar el poder insecticida de los aceites esenciales de albahaca, se ha probado el efecto de los vapores de aceites esenciales sobre el número de huevecillos y su toxicidad directa en insectos. Pascual-Villalobos et al. (2003) compararon el número de huevecillos de Causus maculatus en habas y frijoles en presencia de vapores de aceite esencial de albahaca y observaron que 7 de 18 aceites esenciales de distintas variedades de albahaca redujeron la cantidad de huevos con respecto al control en un porcentaje de 90%. Entre los componentes principales de los aceites esenciales que mostraron dicha capacidad insecticida se encontraron metilchavicol, geranial, geraniol y linalol. En relación a lo anterior, el linalol ha sido reconocido como un repelente efectivo contra insectos (RegnaultRoger y Hamraoui, 1995); Leal y Uchida (1998) identificaron que el geraniol contenido en limoncillo actúa como repelente de mosquitos y Pascual-Villalobos et al. (2003) observaron que la toxicidad de aceites esenciales de albahaca en Causus maculatus,
ha sido atribuida principalmente a la presencia de eugenol y metilchavicol.
Se han experimentado otros métodos para comprobar el poder insecticida del aceite esencial de albahaca, por lo que Keita et al. (2001) probaron la toxicidad del aceite esencial de albahaca al adicionarlo directamente como fumigante en Callosobruchus maculatus y sus huevos; asimismo, ellos evaluaron la actividad insecticida de un polvo (caolín) aromatizado con aceite esencial de albahaca sobre los insectos, concluyendo que el poder insecticida del aceite esencial de albahaca fue positivo en cada una de las pruebas.
Diversos compuestos químicos contenidos en el aceite esencial de albahaca han sido reportados como los responsables de su capacidad insecticida. Chang et al. (2009) probaron la capacidad insecticida de los compuestos trans-anetol, estragol, linalol y metil eugenol así como del aceite esencial en tres moscas tefrítidas de la fruta (Ceratitis capitata, Bactrocera dorsalis y B. cucurbitae).
A excepción del linalol, los tratamientos mostraron mortalidad de las moscas en una concentración de 2.5%; por otra parte, se demostró que el estragol y trans-anetol fueron los tratamientos más potentes y el metil eugenol fue altamente tóxico para C. capitata.
alimenticio que actúa como antioxidante, fungicida y bactericida, así como un efectivo insecticida de especies que atacan cultivos de alimentos.
La mayoría de las determinaciones de las propiedades antioxidantes, antimicrobianas e insecticidas del aceite esencial de albahaca, han sido llevadas a cabo mediante metodologías distintas de experimentación in vitro, sin embargo, su aplicación directa en alimentos aún es poco frecuente. La capacidad insecticida, se ha probado al agregarse directamente a la plaga, ya sea rociado o mediante polvos aromatizados. La acción del aceite esencial de albahaca como antifúngico ha sido probada con adición directa y mediante sus vapores, mientras que la determinación de la capacidad antioxidante del aceite esencial de albahaca sigue en estudio.
Finalmente, se concluye que el aceite esencial de albahaca es un potente antioxidante, fungicida, bactericida e insecticida, sin embargo aún existe escasez de experimentación y aplicación de este aditivo de manera directa en alimentos con la finalidad de obtener beneficios de sus propiedades funcionales.
Conclusiones
Las propiedades antioxidantes, antimicrobianas e insecticidas del aceite esencial de albahaca que fueron mencionadas en la presente revisión, están estrechamente relacionadas con la composición química de la planta, la cual se ve afectada entre otros factores por su origen , así como por su variedad y época de crecimiento. De manera general, se pudo confirmar que el aceite esencial de albahaca es un efectivo aditivo
Agradecimientos
El autor Cardoso-Ugarte agradece al Consejo Nacional de Ciencia y Tecnología (CONACYT) y a la Universidad de las Américas Puebla (UDLAP) por el apoyo para sus estudios de posgrado.
Referencias
Amadi, J., Salami, S. y Eze, C. 2010. Antifungal properties and phytochemical screening of extracts of
African Basil (Ocimum gratissimumL.).Agriculture and Biology Journal of North America.1 (2): 163-166.
Bozin, B., Mimica-Dukic, N., Simin, N. y Anackov, G. 2006. Characterization of the volatile composition of essential oils of some Lamiaceae spices and the antimicrobial and antioxidant activities of the entire oils. Journal of Agricultural and Food Chemistry. 54 (5): 1822-1828.
Burt, S. 2004. Essential oils: their antibacterial properties and potential applications in foods- a review. International Journal of Food Microbiology. 94 (31): 223-253.
Carovic-Stanko, K., Orlic, S., Politeo, O., Strikic, F., Kolak, I., Milos, M. y Satovic, Z. 2010. Composition and antibacterial activities of essential oils of seven Ocimum taxa. Food Chemistry. 119 (1): 196-201.
Chalchat, J. y Musa, M. 2008. Comparative essential oil composition of flowers, leaves and stems of basil (Ocimum basilicum L.) used as herb. Food Chemistry. 110 (2): 501-503.
Chang, C., Cho, Il. y Li, Qing. 2009. Insecticidal activity of basil oil, trans-anethole, estragole, and linalool to adult fruit flies of Ceratitis capitata, Bactrocera dorsalis, and Bactrocera cucurbitae. Journal of Economic Entomology. 102 (1): 203-209.
Chang, X., Alderson, P. y Wright, C. 2008. Solar irradiance level alters the growth of basil Ocimum basilicum L.) and its content of volatile oils. Environmental and Experimental Botany. 63 (1-3): 216223.
Cichosky, A., Cansian, R., De Oliveira, D., Gaio, I. y Saggirato, A. 2011. Lipid and protein oxidation in the internal part of italian type salami containing basil essential oil (Ocimum basilicum L.). Ciencia y Tecnología de Alimentos. 31 (2): 436-442.
Da-Silva, F., Santos, R., Diniz, E., Barbosa, L., Casali, V. y De-Lima, R. 2003. Content and composition of basil essential oil at two different hours in the day and two seasons. Revista Brasileira de Plantas Medicinais. 6 (1): 33-38.
Delgado, B., Palop, A., Fernández, P., Periago, P. 2004. Combined effect of thymol and cymene to control thegrowth of Bacillus cereus vegetative cells. European Food Research and Technology. 218: 188-193.
Ebrahim, S. 2006. Analysis of the essential oils of two cultivated basil (Ocimum basilicum L.). From Iran. DARU Journal of Pharmaceutical Sciences. 14 (3): 128130.
Gülcin, I., Elmastas, M. y Aboul-Enein, H. 2007. Determination of antioxidant and radical scavenging activity of basil (Ocimum basilicum L. family Lamiaceae) assayed by different methodologies. Phytotherapy Research. 21 (4): 354-361.
Helander, I., Alakomi, H., Latva-Kala, K., MattilaSandholm, T., Pol, I., Smid, E., Gorris, L. y Wright, A. 1998. Characterization of the action of selected essential oil components on gram-negative bacteria. Journal of Agricultural and Food Chemistry. 46 (9): 3590-3595.
Ijaz, A., Anwar, F., Hussain, S y Przybylski, R. 2008. Chemical composition, antioxidant and antimicrobial activities of basil (Ocimum basilicum) essential oils depends on seasonal variations. Food Science. 108: 986995
Javanmardi, J., Khalighi, A., Kashi, A., Bais, H. y Vivanco, M. 2002. Chemical characterization of basil (Ocimum basilicum L.) found in local accessions and used in traditional medicines in Iran. Journal of Agricultural and Food Chemistry. 50 (21): 5878-5883.
Jayasinghe, C., Gotoh, N., Aoki, T. y Wada, S. 2003. Phenolics composition and antioxidant activity of sweet basil (Ocimum basilicum L.). Journal of Agriculture and Food Chemistry. 51 (15): 4442-4449.
Keita, S., Vincent, C., Schmit, J., Arnason, J. y Belanger, A. 2001. Efficacy of essential oil of Ocimum basilicum L. and O. gratissimum L. applied as an insecticidal fumigantand powder to control Callosobruchus maculatus (Fab.)[Coleoptera: Bruchidae]. Journal of Stored Products Research. 37 (4): 339-349.
Labra, M., Miele, M., Ledda, B., Grassi, F., Mazzei, M. y Sala, F. 2004. Morphological characterization, essential oil composition and DNA genotyping of Ocimum basilicum L. cultivars. Plant Science. 167 (4): 725-731.
Leal, W. y Uchida, K. 1998. Application of GC-EAD to the determination of mosquito repellents derived from a plant, Cymbopogoncitratus. Journal of Asia Pacific Entomology. 1 (2): 217–221.
Lee, S., Umano, K., Shibamoto, T. y Lee, K. 2005. Identification of volatile components in basil (Ocimum basilicum L.) and thyme leaves (Thymus vulgaris L.) and their antioxidant properties. Food Chemistry. 91 (1):131-137.
Mohammad-Taghi, G. y Karamatollah, R. 2008. Comparison of microwave-assisted hydrodistillation with the traditional hydrodistillation method in the extraction of essential oils from Thymus vulgaris L. Food Chemistry. 109 (49): 925-930.
Noguchi, N. y Niki, E. 1999. Chemistry of active oxygen species and Antioxidants. Antioxidant Status, Diet, Nutrition, and Health. 3-20.
Oxenham, S., Svoboda, K. y Walters, D. 2005.Antifungal Activity of the Essential Oil of Basil (Ocimum basilicum L.). Journal of Phytopathology. 153 (3): 174180.
Oxenham SK. 2003. Classification of an Ocimum basilicum germplasm collection and examination of the antifungal effects of the essential oil of basil. Tesis de doctorado. Universidad de Glasgow. Reino Unido.
Pascual-Villalobos, M. y Ballesta-Acosta, M. 2003. Chemical variation in an Ocimum basilicum germplasm collection and activity of the essential oils on Callosobruchus maculatus. Biochemical Systematics and Ecology. 31 (7): 673-679.
Piyo, A., Udomsilp, J., Khang-Khun, P. y Thobunluepop, P. 2009. Antifungal activity of essential oils from basil (Ocimum basilicum L.) and sweet fennel (Ocimum gratissimum Linn.): Alternative strategies to control pathogenic fungi in organic rice. Asian Journal of Food and Agro-Industry. Special Issue, S2-S9.
Politeo, O., Jukic, M. y Milos, M. 2007. Chemical composition and antioxidant capacity of free volatile aglycones from basil (Ocimum basilicum L.) compared with its essential oil. Food Chemistry. 101 (1): 379-385.
Rattanachaikunsopon, P. y Phumkhachorn, P. 2010. Antimicrobial activity of basil (Ocimum basilicum L.) oil against Salmonella enteritidis in vitro and in food. Bioscience, Biotechnology and Biochemistry. 74 (6): 1200-1204.
Regnault-Roger, C., Hamraoui, A., 1995. Fumigant toxic activity and reproductive inhibition induced by
monoterpenes on Acanthoscelides obtectus (Coleoptera), a bruchid of kidney bean (Phaseolus vulgaris L.). Journal of Stored Products Research. 31 (4): 291–299.
Saggiorato, A., Gaio, I., Treichel, H., De Oliveira, D., Cichosky, A. y Cansian, R. 2012. Antifungal activity of basil essential oil (Ocimum basilicum L.): evaluation in vitro and on an Italian-type sausage surface. Food and Bioprocess Technology. 5 (1): 378-384.
Simon, J., Morales, M., Phippen, W., Fontes, R, y Hao, Z. 1999. Basil: A source of aroma compounds and a popular culinary and ornamental herb, Perspectives on new crops and new uses. 16 (45): 499-505.
Stupans, I., Kirlich, A., Tuck, K., Hayball, P. 2002. Comparison of radical scavenging effect, inhibition of microsomal oxygen free radical generation, and serum lipoprotein oxidation of several natural antioxidants. Journal of Agricultural and Food Chemistry. 50 (8): 2464-2469.
Telci, I., Bayram, E., Yilmaz, G. y Avci, B. 2006. Variability in essential oil composition of Turkish basils (Ocimum basilicum L.). Biochemical Systematics and Ecology. 34 (6): 489-497.
Tomaino, A., Cimino, F., Zimbalatti, V., Venuti, V., Sulfaro, V., De Pasquale, A. y Saija, A. 2005. Influence of heating on antioxidant activity and the chemical composition of some spice essential oils. Food Chemistry. 89 (4): 549–554.
Wogiatzi, E., Papachatzis, A., Kalorizou, H., Chouliara, A. y Chouliaras. 2011. Evaluation of essential oil yield and chemical components of selected basil cultivars. Biotechnology and Biotechonology equipment. 25 (3): 2525-2527.

Temas Selectos de Ingeniería de Alimentos 6 - 1 (2012): 66 - 72

Emulsiones simples y múltiples de compuestos bioactivos
B. Contreras-Reyes* y M.T. Jiménez-Munguía
Departamento de Ingeniería Química, Alimentos y Ambiental, Fundación Universidad de las Américas Puebla. Exhacienda Sta. Catarina Mártir S/N, Cholula, Puebla. C.P.72810. México.
Resumen
Las tendencias actuales en la industria de alimentos están encaminadas a desarrollar productos con valor agregado, por lo que se buscan tecnologías que permitan la elaboración de dichos alimentos. Las emulsiones han mostrado ser un buen vehículo para el desarrollo de estos productos por lo que su estudio se enfoca en el desarrollo de nuevas aplicaciones, así como en su estabilidad bajo distintas condiciones de producción y almacenamiento. Por ello, el objetivo de este trabajo es mostrar un panorama general respecto a las emulsiones simples y múltiples, exponiendo sus características generales, métodos de formación y aplicaciones presentando las ventajas y limitaciones actuales de éstas en los alimentos.
Palabras clave: emulsiones, emulsiones múltiples, componentes bioactivos, aplicaciones.
Abstract
Current trends in the food industry are aimed to develop value-added foods, thus the industry is looking for technologies which permit the production of such foods. Emulsions have shown a good vehicle for the development of these foods therefore, studies are focused on the improvement of new applications, such as optimizing the stability of emulsions under different conditions of production and storage. Hence, the aim of this paper is to show an overview about simple and multiple emulsions, explaining their general characteristics, training methods and applications, discussing the current advantages and limitations of these in the food area.
Keywords: emulsions, multiple emulsions, bioactive compounds, applications.
Introducción
Los alimentos además de aportar nutrimentos, tales como proteínas, vitaminas y minerales, entre otros, contienen una serie de componentes que no tienen una función nutricional definida, o no son considerados esenciales para el metabolismo, pero sin duda tienen un impacto significativo a largo
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: berenice.contrerasrs@udlap.mx
plazo en la salud, estos componentes son definidos como bioactivos. En la actualidad, éstos son ampliamente estudiados en distintos campos y se ha encontrado que las emulsiones constituyen un medio eficiente para su adición a los alimentos, para la conservación de sus propiedades (Mun et al., 2010), así como para conferir atributos sensoriales a los alimentos.
Aun cuando se ha comprobado que existe una gran oportunidad de desarrollo de
productos mediante el uso de emulsiones, una emulsión en principio es un sistema inestable (Pallandre et al., 2007; Rao et al., 2009). Es por ello que esta revisión pretende ofrecer un panorama general del conocimiento actual respecto a las emulsiones simples y múltiples, resumiendo sus características generales, presentando los métodos más comunes de formación, mencionando algunas de sus aplicaciones y finalmente presentando las ventajas y limitaciones actuales que existen en el área de los alimentos respecto a las emulsiones.
Revisión bibliográfica
1. Tipos de emulsiones
Una emulsión es un sistema que consiste en al menos dos fluidos inmiscibles, donde uno de los fluidos está disperso en pequeñas gotas (fase dispersa) en el otro fluido que constituye la fase continua. El tamaño de las gotas de la fase dispersa se encuentra típicamente en un intervalo de entre 0.1 a 100 micrómetros. La fase continua en la industria alimentaria generalmente es agua o aceite (McClements, 2007).
Las emulsiones son sistemas termodinámicamente inestables, que tienden a separarse en las fases que las forman, a través del tiempo, por diversos mecanismos. Debido a esto, es esencial el uso de emulgentes que brinden una estabilidad cinética por periodos razonables de tiempo (Rao, 1999; Choi et al., 2007; DeHoog, 2011). Un emulgente, es una sustancia anfifílica que facilita la formación de la emulsión disminuyendo la tensión interfacial entre la fase apolar (oleosa) y la polar (acuosa), además aporta estabilidad física durante un tiempo, que puede ser más o menos largo, dependiendo de la composición, características de procesado y
condiciones externas durante la vida de la emulsión (Muñoz et al., 2007).
Las emulsiones pueden clasificarse de acuerdo a sus diferentes características, según su distribución espacial o por su número de fases. En este caso se clasifican como simples o múltiples (McClements, 2007).
1.1. Emulsiones simples
En una emulsión simple o primaria existe una sola fase continua y una sola fase dispersa, y está constituida por las gotas de la fase dispersa distribuidas en la fase continua (Fig. 1). Dependiendo de la naturaleza de las fases dispersa y continua, las emulsiones se clasifican como O/W o W/O. Una emulsión O/W se denomina del tipo aceite en agua; en este caso la fase dispersa consiste en pequeñas gotas de un líquido de naturaleza oleosa, por tanto hidrófoba, y una fase continua, dominada por un medio normalmente acuoso. Algunos ejemplos de emulsiones O/W son: leche, mayonesa, nata y algunas salsas, entre otros alimentos (Muñoz et al., 2007).
En una emulsión agua en aceite (W/O), la fase dispersa es de naturaleza acuosa y la continua oleosa. Algunos ejemplos son la mantequilla y la margarina (Choi et al., 2007; Muñoz et al., 2007).
1.2 Emulsiones múltiples
Es posible crear emulsiones en las que hay más de una fase continua o una fase dispersa (Fig. 2), dando como resultado distintos tipos de emulsiones, tales como: aceite en agua en aceite (O/W/O), agua en aceite en agua (W/O/W), aceite en agua en agua (O/W/W), como ejemplos de las más comunes (McClements, 2007).
B. Contreras - Reyes et al. / Temas Selectos de
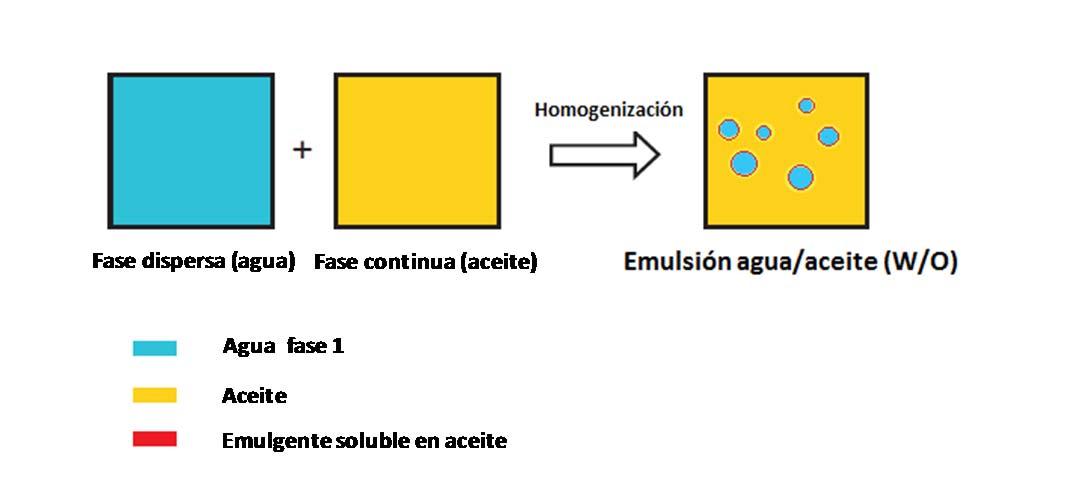
Fig. 1. Componentes básicos para la formación de una emulsión simple agua /aceite (W/O). Adaptada de De Hoog (2011).
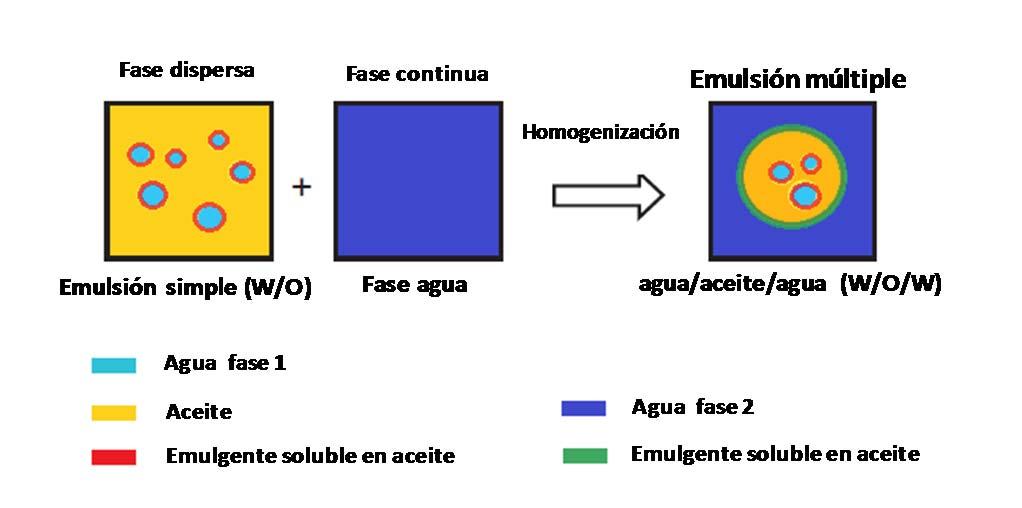
Fig. 2. Componentes básicos para la formación de una emulsión múltiple agua/ aceite/agua (W/O/W). (Adaptada de DeHoog, 2011).
Las emulsiones múltiples presentan una naturaleza diferente en sus fases oleosas y acuosas, por lo que son esperables diferencias significativas de densidad, las cuales conducen tarde o temprano a una separación de fases, que en la práctica supone el rompimiento de la emulsión y por tanto el fin de su vida útil. Es por ello que una de las propiedades más importantes de una emulsión es su estabilidad.
Es un hecho que las emulsiones múltiples son más complejas en su estructura que las emulsiones simples. Los mecanismos de desestabilización no sólo afectan a las gotas de la emulsión interna, sino también a las de la emulsión externa; esto significa que las emulsiones múltiples son más inestables (Choi et al., 2007).
Las emulsiones múltiples están diseñadas para optimizar la estabilidad bajo diversas condiciones de producción y almacenamiento en los alimentos, incluyendo tratamientos térmicos, mecánicos, de cambios de pH, de enfriamiento, congelación y fuerzas iónicas. Además, las emulsiones múltiples constituyen un grupo específico de emulsiones con beneficios denominados como funcionales (McClements, 2007; DeHoog, 2011).
2. Formación de emulsiones
Para la formación de una emulsión se debe efectuar un proceso de conversión de la fase dispersa a gotas de tamaño pequeño y su distribución homogénea en la fase continua (Remington, 2003).
En la industria alimentaria esto se puede lograr utilizando un mezclador que produzca un corte, altas presiones, un molino coloidal, un microfluidizador o un homogeneizador ultrasónico, entre otros (McClements, 2007).
a) Mezcladores mecánicos. Un sistema de homogenización por rotación mecánica se utiliza para producir emulsiones utilizando líquidos con viscosidad que va de media a alta (McClements, 2005; Mahdi, 2009); los líquidos se alimentan de manera gruesa o en forma de fases separadas y pasan a través de los discos giratorios y estáticos, formando la emulsión (Mahdi, 2009). El grado de mezclado y corte asociados dependen de factores relacionados con el equipo.
b) Molinos coloidales. Estos forman la emulsión al pasar los líquidos entre el rotor y el estator, son sometidos a una acción de corte que produce una dispersión fina y de tamaño uniforme, donde el tamaño de las gotas disminuye a medida que aumenta el tiempo de homogenización y la intensidad de ésta (Remington, 2003).
c) Homogeneizadores de alta presión o de rotación mecánica. Estos son utilizados para lograr una mayor reducción en el tamaño de
las gotas, así como para obtener un mayor grado de uniformidad y una buena estabilidad (Mahdi, 2009). En los sistemas de homogenización con altas presiones la mezcla de la emulsión se hace pasar a través de una válvula de mezclado fino bajo alta presión. La ventaja que presenta este método es que no incorpora aire a la emulsión, permitiendo una mayor estabilidad. Sin embargo, se generan emulsiones de consistencia y apariencia cremosa (Remington, 2003; DeHoog, 2011).
d) Dispositivos ultrasónicos. La emulsión se genera mediante vibraciones ultrasónicas, ya que se producen ondas de alta frecuencia que fluyen a través del líquido. Se han desarrollado diversos trabajos de investigación y hasta el momento los estudios indican que estos dispositivos producen emulsiones estables con líquidos de baja viscosidad. Sin embargo, este no es un método práctico para la producción de emulsiones a gran escala (Remington, 2003).
La preparación de emulsiones requiere de una cantidad de energía para formar la interfase entre las dos fases (continua y dispersa) y una cantidad de trabajo adicional para mezclar el sistema y contrarrestar la resistencia al flujo. Es por ello que a menudo se suministra calor al sistema para fundir y/o reducir la viscosidad de la fase oleosa. En consecuencia, la preparación de emulsiones en gran escala suele requerir el gasto de una cantidad considerable de energía para el calentamiento, la cual puede ser suministrada en los mezcladores (Remington, 2003).
3. Aplicación de emulsiones en alimentos
Las emulsiones múltiples son capaces de contener varios tipos de ingredientes tanto en las fases acuosas como oleosas y liberarlos en periodos controlados durante su consumo y digestión. Mediante el proceso de emulsificación, materiales solubles en agua pueden ser atrapados en la fase acuosa, mientras que materiales solubles en lípidos
pueden ser atrapados en la fase oleosa. Es importante controlar la difusión o migración de los materiales entre las fases internas y externas, así como estabilizar las gotas dentro de la emulsión (Dickinson, 2003). De esta manera, se considera que la inclusión de algún ingrediente activo, funcional o componente esencial, depende de su compatibilidad con el medio donde se incorpore, fundamentalmente: la fase oleosa (O), la fase acuosa (W) o la interfase (Muñoz et al., 2007).
La aplicación actual de las emulsiones está encaminada a desarrollar productos alimenticios que además de poseer propiedades del tipo funcional con beneficios a la salud, ofrezcan al consumidor buenos atributos sensoriales (DeHoog, 2011).
La fase oleosa de las emulsiones constituye uno de los puntos de progreso en lo que respecta a formulaciones innovadoras en el campo de las emulsiones alimentarias, es así como existe un creciente uso de aceites con propiedades funcionales, como por ejemplo: aceites vegetales enriquecidos en ácidos grasos polinsaturados y aceites esenciales. Otros compuestos liposolubles presentes en la emulsión que se concentran en la fase oleosa son los antioxidantes, fitoesteroles, vitaminas (Muñoz et al., 2007; Charoen et al., 2011).
3.1. Lípidos
Existen lípidos bioactivos que proveen de beneficios específicos a los humanos, tales como los ácidos grasos ω-3 y fitoesteroles. En muchos casos, es una ventaja el desarrollar lípidos bioactivos en un medio acuoso, debido a que se incrementa su palatabilidad, atractivo y bioactividad (McClements et al., 2007).
Estos lípidos varían en sus propiedades moleculares (pesos, estructura, grupos funcionales, polaridad y carga) lo que los hace diferentes en cuanto a sus propiedades fisicoquímicas y fisiológicas (solubilidad, estado físico, reología, propiedades ópticas, estabilidad química, superficie de actividad y
bioactividad) (Charoen et al., 2011; Muñoz et al., 2007). Por lo que cada sistema es desarrollado para ser compatible con un lípido en específico.
Los ácidos grasos como el ω-3, por ejemplo, tienen un fuerte impacto en la salud, ya que cumplen con numerosas funciones fisiológicas, razón por la que el manejo y estabilidad de este ácido graso han sido estudiados para su adición. Los alimentos con estos ácidos son susceptibles a la oxidación, por lo que las emulsiones constituyen una buena forma de conservarlos, por ejemplo, cubriendo el ácido graso con antioxidantes que lo hagan biodisponible en la dieta (McClements et al., 2007; DeHoog, 2011).
Los fitoesteroles son un grupo que se encuentra naturalmente en diversos alimentos en bajas concentraciones. Sin embargo, la producción de alimentos fortificados con fitoesteroles se ha hecho popular desde que se confirmó su habilidad para disminuir la concentración de lipoproteínas de baja densidad. No obstante, la incorporación de fitoesteroles en los alimentos se dificulta debido a su alto punto de fusión así como a su tendencia a formar cristales insolubles, por lo que los fitoesteroles son agregados generalmente a alimentos de alto contenido graso, donde su solubilidad y dispersión son relativamente sencillas. Se considera a los sistemas de emulsiones como una excelente opción para introducir los fitoesteroles en alimentos con base acuosa, además de que se aumenta la estabilidad oxidativa de éstos (McClements et al., 2007).
3.2. Minerales
Una cantidad limitada de minerales puede ser añadida a los alimentos mediante el uso de técnicas de elaboración regulares debido a que los minerales inducen a la floculación de las matrices proteicas. Sin embargo, se ha observado que mediante el uso de emulsiones múltiples, los minerales pueden ser protegidos
de la interacción con la matriz a la cual se incorporen, mientras se mantiene la proteína en la fase acuosa externa. Así, los productos permanecen estables, puesto que la interacción de los minerales con la proteína se limita. De esta manera, se han desarrollado productos que incluyen minerales en emulsiones tales como bebidas fortificadas, productos dietarios especiales para infantes y ancianos (Hemar et al., 2010).
En general las concentraciones de minerales en el producto pueden ser aumentadas, con valores nutricionales beneficiosos (DeHoog, 2011).
3.3. Compuestos que afectan atributos sensoriales en alimentos
Otras aplicaciones de las emulsiones en los alimentos están encaminadas a mejorar el producto sensorialmente, como en el caso del enmascaramiento del sabor, que es un beneficio potencial de las emulsiones para la incorporación de ingredientes que pudiesen no ser agradables al gusto, o del incremento de la sensación de jugosidad en un producto, para que se desarrollan emulsiones que logran la encapsulación de elevadas cantidades de agua (DeHoog, 2011).
También se puede buscar mantener las características del producto inicial, como en la reducción de grasa en los productos hasta en un 40%, ya que algunas de las gotas de aceite se sustituyen por agua, generando productos en los que no se percibe sensorialmente y se mantiene su estabilidad y agrado (McClements et al., 2007).
4. Ventajas y limitaciones
Diversos estudios realizados muestran que la formación de emulsiones múltiples es una tecnología que ofrece una buena solución al mercado cambiante de los alimentos, el cual requiere de mejoras continuas para cubrir necesidades de los consumidores tales como una reducción de la cantidad de grasa pero
manteniendo un sabor agradable, fortificación y adición de ingredientes saludables, manteniendo el valor nutricional sin comprometer en gran medida los atributos del sabor o textura, entre otros (DeHoog, 2011; Mun et al., 2010; Hemar et al., 2010).
La principal limitación de las emulsiones es que deben cumplir numerosas funciones a la vez, primero deben ser capaces de cubrir y mantener al componente activo, es decir, que se pueda incorporar a los alimentos sin afectar la apariencia, sabor, textura, o la vida de anaquel del producto. Además, el sistema debe proteger al componente activo de la degradación química durante la preparación, el almacenamiento, transporte y utilización para que éste permanezca en su estado activo. También se debe controlar la liberación de este agente en cierto periodo de tiempo en un sitio en particular y responder a estímulos ambientales específicos tales como pH, temperatura, o fuerza iónica para su liberación. Finalmente, debe prepararse con ingredientes de grado alimenticio (McClements et al., 2007; Djordjevic et al., 2008; Charoen et al., 2011).
Además, dependiendo del tipo de emulsión, fundamentalmente de su composición, el término estabilidad no sólo incluye los aspectos físicos que controlan principalmente la separación de fases, sino también químicos para controlar la oxidación e hidrólisis en la emulsión, así como cambios microbiológicos (Djordjevic et al., 2008; DeHoog, 2011).
No obstante, el diseño de una emulsión tiene que ser específico para cada aplicación, debido a que existen aspectos como las interacciones específicas aunadas a la complejidad de los productos alimenticios, las condiciones de transformación de la totalidad del producto, y los requisitos para el retraso o provocación de la liberación de los constituyentes (DeHoog, 2011).
Contreras - Reyes et al. / Temas Selectos de
Conclusiones
Existe una amplia variedad de sistemas de emulsiones, cada uno con sus propias ventajas y desventajas. En este artículo de revisión se ha mostrado una visión general de los sistemas de emulsiones, presentando los métodos más comunes de formación y mostrando las tendencias para sus aplicaciones. Sin embargo, es claro que el diseño de una emulsión tiene que ser específico para cada aplicación en particular, debido a las diversas formas en las que una emulsión puede utilizarse, así como a las limitaciones que existen al tratarse de un sistema de naturaleza inestable.
Agradecimientos
B. Contreras-Reyes agradece a la Universidad de las Américas Puebla y al Consejo Nacional de Ciencia y Tecnología (CONACyT, México) por el financiamiento recibido para sus estudios de posgrado.
Referencias
Charoen, R., Jangchud, A., Jangchud, K., Harnsilawat, T., Naivikul, O., y McClements, D. J. 2011. influence of biopolymer emulsifier type on formation and stability of rice bran oil-in-water emulsions: whey protein, gum arabic, and modified starch. Journal of Food Science. 76(1):165-172.
Choi, M. J., Briançon, S., Bazile, D., Royere, A. Min, S. G., y Fessi, H. 2007. Effect of cryoprotectant and freeze-drying process. Drying Technology 25(5):809-819.
DeHoog, E. 2011. Emulsions for new functionalities. Prepared Foods. 180(6):99-105.
Dickinson, E. 2003. Hydrocolloids at interfaces and the influence on the properties of dispersed systems
Food Hydrocolloids. 17(1):25–39.
Djordjevic, D., Cercaci, L., Alamed, J., McClements, D. J., y Decker, E. A. 2008. Chemical and physical
de Alimentos 6 – 1 (2012): 66 - 72
stability of protein and gum arabic-stabilized oil-inwater emulsions containing limonene. Journal of Food Science. 73(3):167-172.
Hemar, Y., Cheng, L., Oliver, C., Sanguansri, L., y Augustin, M. 2010. Encapsulation of resveratrol using water-in-oil-in-water double emulsions. Food Biophysics. 5(2):120 127.
Mahdi, J. S. 2009. Encapsulation of nano-emulsions by spray drying. Lambert Academic Publishing. Iran. 19-23 p.
McClements, D.J. 2005. Food emulsions: principles, practice, and techniques. CRC Press. Boca Raton. 295-339 p.
McClements, D. 2007. Critical Review of Techniques and Methodologies for Characterization of Emulsion Stability. Critical Reviews In Food Science & Nutrition, 47(7): 611-649.
McClements, D.J., Decker, E. A. y Weiss J. J. 2007. Emulsion-based systems for lipophilic bioactive components. Journal of Food Science. 72(8):109124.
Mun S., Choi Y., Rho S. J., Kang C. G., Park C. H. y Kim Y. R. 2010. Preparation and characterization of water/oil/water emulsions stabilized by polyglycerol polyricinoleate and whey protein isolate. Journal of Food Science. 75(2):116-125.
Muñoz J, Alfaro M, Zapata I. 2007. Avances en la formulación de emulsiones. Grasas y Aceites. 58(1):64-73.
Pallandre, S., Decker, E. A. y McClements, D. J. 2007. Improvement of stability of oil-in-water emulsions containing caseinate-coated droplets by addition of sodium alginate. Journal of Food Science. 72 (9):518-524.
Rao, J. J., Chen, Z. M y Chen B. C. 2009. Modulation and stabilization of silk fibroin-coated oil-in-water emulsions. Food Technology and Biotechnology 47(4):413-420.
Rao, M.A. 1999. Rheology of fluids and semisolid foods: principles and applications. Springer. New York. 48-50 p.
Remington, R. 2003. The science and practice of pharmacy. Ed. Médica Panamericana. Philadelphia. 859-867 p.

Temas Selectos de Ingeniería de Alimentos 6 - 1 (2012): 73 - 83

Combinación de ultrasonido de baja frecuencia con factores convencionales y/o emergentes como método de inactivación de microorganismos en alimentos
A. Franco-Vega*, E. Palou y A. López-Malo
Departamento de Ingeniería Química, Alimentos y Ambiental, Fundación Universidad de las Américas Puebla. Exhacienda Sta. Catarina Mártir S/N, Cholula, Puebla. C.P.72810. México.
Resumen
El proceso de sonicación de alimentos por medio de ultrasonido de baja frecuencia por si sólo ha resultado ser poco viable para la destrucción de microorganismos, debido a esto en la actualidad se ha propuesto el uso de tecnologías convencionales y emergentes en combinación con el ultrasonido para aumentar su efecto conservador. Dentro de las combinaciones que han sido estudiadas se encuentran aquémnllas en las cuales se utiliza la composición misma del alimento (pH y aw), compuestos químicos y las que se complementan con la variación de diferentes parámetros del proceso (temperatura, presión o su combinación). El uso del ultrasonido en combinación con estos factores, su mecanismo y efecto sobre los microorganismos son discutidos en este trabajo.
Palabras clave: ultrasonido de baja frecuencia, tratamientos combinados, inactivación de microorganismos.
Abstract
The use of low frequency ultrasound in the food industry had shown to be unfeasible for the destruction of bacterial cells due to the necessary large processing time to accomplish this task. Hence, nowadays the combination of ultrasound with conventional and emerging technologies has been proposed for enhancing their preservative effect. Within these combinations are those using the composition of the food (pH and aW), chemical compounds, and those used with variations of process parameters (temperature, pressure and/or their combination). The use of ultrasound combined with other factors, their mechanisms, and their effects on the microorganisms are discussed in this review.
Keywords: low frequency ultrasound, combined treatments, microbial inactivation.
Introducción
Hoy en día se están evaluando en la industria de alimentos nuevas tecnologías de conservación dentro de las cuales se encuentran tratamientos como altas presiones
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: avelina.francova@udlap.mx
hidrostáticas, pulsos eléctricos, campos magnéticos e irradiación con luz ultravioleta de onda corta entre otros. Si bien la capacidad de estos tratamientos para conservar alimentos no es precisamente novedosa, su desarrollo para ser usados como una opción de procesamiento ha recibido atención recientemente (Ross et al., 2003). El auge del estudio de estos tratamientos es en respuesta a
la necesidad de los procesadores y tecnólogos de alimentos de ofrecer al consumidor productos mínimamente procesados, que se apeguen a las nuevas tendencias de consumo y que a la vez se encuentren libres de riesgos microbiológicos (Demidrövel y Baysal, 2009). En un estudio realizado por la Food and Drug Administration (FDA, 2009) acerca de estas nuevas tecnologías de conservación de alimentos, se considera al ultrasonido de baja frecuencia como una de ellas.
El uso de ultrasonido se ha estudiado desde hace varios años para la inactivación de microorganismos y se ha demostrado que tiene la habilidad de dañar su pared celular, con lo cual logra inactivarlos (Feng y Weiss, 2010). Sin embargo, el ultrasonido por sí solo no es muy eficiente en la destrucción de los microorganismos presentes en los alimentos, debido a que maneja tiempos de procesamiento relativamente largos al ser aplicado a temperaturas sub-letales (Piyasena et al., 2003). En la literatura se han reportado inactivaciones de sólo un ciclo logarítmico en más de 60 minutos de procesamiento (Gabriel, 2012), presentándose además, daños en la calidad sensorial de los productos sometidos a estos tratamientos tan largos. Los daños observados se han atribuido a la desnaturalización de proteínas y generación de radicales libres que tienen la capacidad de afectar el sabor y olor del producto tratado.
Debido a esto, estudios recientes (Piyasena et al., 2003.; Ross et al., 2003.; Condón et al., 2005.; Lee et al., 2009) han propuesto el uso del ultrasonido en combinación con otras técnicas de conservación tradicionales y emergentes, para así someter a las células microbianas a un ataque desde varias direcciones (Demidröven y Baysal, 2009). Con lo anterior se busca lograr un mayor efecto en la inactivación por medio de una interacción sinérgica entre métodos tradicionales y emergentes (Leistner, 2000).
Dentro de las combinaciones que han sido probadas se encuentran aquellas en las cuales se aprovecha la composición del mismo alimento, como son el pH y la actividad de agua, la interacción con compuestos químicos (agentes antimicrobianos, ácidos orgánicos, algunas sales), y el uso de variables del proceso, como la temperatura y presión. Con estas combinaciones se han obtenido buenos resultados, no sólo en la inactivación de los microorganismos presentes si no también en una reducción de la cantidad de energía necesaria para el proceso y en la intensidad del tratamiento aplicado al alimento. El objetivo de este trabajo es hacer una revisión del efecto del ultrasonido de baja frecuencia al ser combinado con diferentes factores sobre la inactivación de microorganismos.
Revisión bibliográfica
1. Ultrasonido de baja frecuencia
El ultrasonido tiene un gran número de aplicaciones en diversas áreas de la industria alimentaria, como son los procesos de cristalización, emulsión y congelación (Gogate y Kabadi, 2009); sin embargo, uno de los más relevantes es su poder de actuar como un proceso de conservación siendo una alternativa en la inactivación de los microorganismos responsables del deterioro de los alimentos.
El ultrasonido está definido como el proceso en el cual se generan ondas de presión con frecuencias por arriba del umbral de la audición humana (>16 kHz) (Butz y Tauscher, 2002; Arroyo et al., 2011). El efecto antimicrobiano del ultrasonido está dado por las condiciones de alta temperatura y presión (1.1x104-1.07x105 KPa y 500 a 1500 °K) (Gogate y Kabadi, 2009) creadas durante el proceso y atribuidas a la generación, crecimiento y colapso de burbujas o cavidades
dentro del líquido. Este fenómeno es conocido como cavitación (Earnshaw, 1998).
Los cambios intensos de presión y temperatura causados durante la cavitación causan un rompimiento inducido de las paredes celulares y daño en el ADN de los microorganismos siendo atribuidos al desarrollo de radicales libres (OH-, HO2, y O3) (Furuta et al., 2004). Estos y otros daños que se pueden presentar, son los responsables de la inactivación microbiana (Ross et al., 2003).
Parámetros como la frecuencia, amplitud de onda, temperatura y viscosidad del medio a tratar influyen el grado de cavitación; sin embargo, la frecuencia de ultrasonido usado es uno de los factores más importantes en la efectividad del mismo (Patist y Bates, 2008). Para el procesamiento de alimentos es usado el ultrasonido de baja frecuencia que comprende de 20 a 100 kHz, también conocido como ultrasonido de alta potencia (Piyasena et al., 2003). Se ha demostrado que a estos valores es donde se genera el mayor tamaño de burbuja, lo cual logra que la energía creada en la cavitación sea mayor (Salleh-Mack y Roberts, 2007).
A pesar de que la cavitación da lugar a una fuerte mezcla de las suspensiones en las que es aplicado el ultrasonido, muchas veces los microorganismos tienden a concentrarse en planos nodales donde los cambios de presión y temperatura generados no son capaces de llegar, causando así que la inactivación se vea debilitada y que a la vez el tiempo necesario para que ésta sea relevante sea demasiado largo (Furuta et al., 2004). Debido a esta debilidad de su acción letal se ha considerado poco apto para la conservación de alimentos. Sin embargo, recientes estudios (López- Malo et al., 2005; Mañas y Pagan, 2005.; GómezDíaz et al., 2011) han demostrado que la combinación del ultrasonido con otras técnicas de inactivación incrementan sustancialmente la letalidad del tratamiento.
2. Combinación con factores propios de la composición del alimento
En el estudio de la capacidad de inactivación del ultrasonido se ha encontrado que la composición del alimento afecta tanto de manera negativa como positiva a este efecto. Dos de estos factores intrínsecos que se han determinado que pueden causar un efecto importante en el proceso de inactivación son el pH y la actividad de agua del medio, por lo cual se han estudiado sistemas tomándolos como una combinación de barreras (SallehMack y Roberts, 2007;vg Arroyo et al., 2011).
2.1. pH
Al igual que en otros procesos novedosos de inactivación microbiana el efecto de un descenso de pH ha demostrado reducir la resistencia de los microorganismos al proceso de sonicación (Salleh-Mack y Roberts, 2007). Algunos investigadores han examinado el efecto del pH al cual se realiza la sonicación de productos inoculados con Escherichia coli (Utsunomya y Kosaka, 1979; Salleh-Mack y Roberts, 2007), encontrando que, en efecto, la inactivación de este microorganismo aumenta a medida que el pH del medio disminuye. Resultados similares han sido reportados por Wong et al., (2008) para Salmonella spp tratada en dos medios con pH diferente, jugo de naranja a pH 3.2 y una solución de sacarosa a pH 6.6 por medio de sonicación. Estos investigadores encontraron que la reducción más significativa se presentó en la población inoculada en el jugo de naranja, debido entre otros factores al bajo pH de este producto.
Sin embargo, se ha demostrado que la efectividad de la combinación de pH y tratamiento por ultrasonido en la inactivación depende en cierta parte de la especie de microorganismo. (Ross et al, 2003). Kinsloe et al (1954) compararon como se afectaba la resistencia de Pseudomona aeruginosa y
Saccharomyces cerevisiae al ser tratadas con ultrasonido a dos pH diferentes (7 y 4) encontrando que no existía cambio significativo en la sensibilidad de estos microorganismos entre ambos tratamientos.
Uno de los factores importantes a tomar en cuenta al momento de decidir usar un proceso de ultrasonido en el cual se busca ayudar con una baja de pH es la concentración de ácido que será usada.(Salleh-Mack y Roberts, 2007). Sagong et al. (2011) demostraron que en la inactivación de E. coli en lechugas tratadas con ultrasonido y ácido málico, al utilizar una concentración de 1% del ácido se obtuvieron reducciones de 1.15 ciclos logarítmicos, mientras que al aumentar la concentración al doble (2%) la inactivación sólo aumentó 0.10%. Sin embargo, se ha demostrado que al combinar concentraciones iguales de ácido cítrico o málico con ultrasonido para la inactivación de E. coli, la diferencia de ácido no ha representado una diferencia significativa en el nivel de inactivación del proceso (SallehMack y Roberts, 2007)
2.2. Actividad de agua (aw)
La actividad de agua es uno de los factores que tienen mayor influencia en la resistencia de los microorganismos ante diferentes factores de estrés, incluyendo dentro de éstos al ultrasonido (Patterson, 2005).
En el caso de estudios realizados variando la actividad de agua por la adición de solutos, se ha encontrado que al tratar a Listeria monocytogenes en un medio con altas concentraciones de sacarosa, los valores de tiempo de reducción decimal del tratamiento por ultrasonido aumentaron (Piyasena et al., 2000)
Arroyo et al. (2011) demostraron que la resistencia al proceso aumentaba a medida que la actividad de agua del medio disminuía de valores de 0.99 a 0.94; observando que
después de un minuto de tratamiento se redujo en más de 2.5 ciclos logarítmicos a la población de Cronobacter sakazakii en un medio sin sacarosa (aw=0.99); mientras en un medio con 44.4% (p/v) (aw=0.94) se redujo en menos de 0.5 ciclos logarítmicos. Basados en estos resultados, concluyeron que este aumento en la resistencia puede deberse a que el descenso de la actividad de agua modifica la viscosidad del fluido. De igual manera, Condón et al. (2005), observaron que la resistencia de L. monocytogenes aumentó en un medio sonicado al variar su actividad de agua de 0.99 a 0.93.
Estudios como estos han demostrado que a diferencia de lo que sucede con el pH, los microorganismos sonicados presentan aumentos de resistencia de los cuando éstos se encuentran en soluciones con actividades de agua reducidas (Condón et al., 2005).
3. Combinación del ultrasonido con compuestos químicos
El uso de antimicrobianos es una técnica de conservación usada desde hace mucho tiempo en la industria de alimentos dando buenos resultados; sin embargo, aparte de la limitación que presentan por la regulación a la que están sujetos, su uso en los productos comerciales también está restringido por sus altos costos y por la inhibición de su efecto antimicrobiano en substratos complejos (Corbo et al., 2009).
La adición de estos antimicrobianos combinados con técnicas no térmicas de procesamiento han demostrado presentar un buen obstáculo para los microorganismos (Ross et al., 2003). Arce-García et al. (2002) lograron reducir la intensidad y duración del tratamiento de ultrasonido requerido en la inhibición de Zygosaccharomyces rouxii a un 67% y 33% del valor original por medio de la adición de sorbato de potasio, benzoato de sodio o eugenol en el medio. De igual manera
también se ha probado la efectividad de la combinación de antimicrobianos naturales con sonicación. Ferrante et al. (2007) investigaron la respuesta de Listeria monocytogenes en jugo de naranja tratado a temperatura moderada con ultrasonido de alta intensidad y la adición de diferentes concentraciones de vainillina y citral encontrando que la presencia de estos dos antimicrobianos aumentaron el efecto bactericida del proceso.
Por su parte, los ácidos orgánicos, han demostrado que además de tener la característica de ser generalmente reconocidos como seguros (GRAS por sus siglas en ingles), tienen la habilidad de inactivar a los microorganismos causantes del deterioro de alimentos (Sagong et al., 2011). Algunos ejemplos de los ácidos organicos añadidos a alimentos son el ácido cítrico, málico, láctico y acético. Dentro de sus ventajas como conservadores se encuentra su rápida acción y amplio espectro de acción. Además estos productos son efectivos a un amplio rango de temperaturas y no son afectados por la dureza del agua; sin embargo, su alto costo y corrosividad son algunos de sus defectos (Marriot y Gravani, 1991). Por estas razones es que en la actualidad se busca disminuir, dentro de la industria, la dosis de ácidos orgánicos utilizados en los procesos de desinfección, dando así pauta a la combinación de este proceso con nuevas tecnologías como el ultrasonido.
Existen reportes que indican que la combinación del ultrasonido con ácidos orgánicos, como el málico y el cítrico, tiene un efecto significativo sobre la reducción en la población de microorganismos (Salleh-Mack y Roberts, 2007; Singh et al. 2002). Esto se atribuye a que la combinación actúa de la misma manera que con los sanitizantes acuosos, penetrando en pliegues de hojas de frutas y vegetales, en donde los ácidos orgánicos no pueden acceder fácilmente por sí solos, y de esta manera incrementando la
velocidad de reacción entre el ácido y los componentes celulares (Ross et al., 2003).
Sagong et al. (2011) sometieron lechugas inoculadas con E. coli, L. monocytogenes y S. typhimurium con un tratamiento combinado de ácido málico, láctico o cítrico con ultrasonido. Los resultados demostraron que al combinar los tratamientos se mejora de manera general la efectividad de los ácidos orgánicos al inhibir a los patógenos presentes en las lechugas. Por otro lado, se ha reportado que en productos vegetales mínimamente procesados donde se compara la efectividad del tratamiento combinado contra el tratamiento de ultrasonido por sí solo, el tratamiento combinado además de ser capaz de inactivar a los microorganismos no causa cambios significativos en la apariencia del producto. Este es un factor de vital importancia, ya que el tratamiento por ultrasonido que es efectivo para la inactivación generalmente afecta la calidad sensorial del producto (Singh et al. 2002).
Es por esto que hoy en día el uso de ultrasonido combinado con ácidos orgánicos se puede considerar como una buena opción para la industria de alimentos orgánicos, ya que da la opción de que se aumente la seguridad microbiológica de sus productos y a la vez ésta pueda reducir la cantidad de ácido que usa dentro de sus procesos de conservación.
Los desinfectantes acuosos son otro método de conservación que ha sido probado en combinación con el ultrasonido. Una de las ventajas con las que cuenta combinar estos dos tratamientos radica en que puede dar pie a la reducción en la concentración de químicos necesarios para la sanitización y desinfección de alimentos. Además, en algunos métodos químicos de sanitización en los cuales los microorganismos han desarrollado resistencia al compuesto, el uso alternativo del ultrasonido se ha presentado como una opción
debido a la simplicidad del proceso y a la ausencia de producción de compuestos tóxicos (Furuta et al., 2004).
El lavado de productos frescos con sanitizantes acuosos como el cloro, el peróxido de hidrógeno y el fosfato trisódico ha sido ampliamente usado para reducir su carga microbiana (Sagong et al., 2011); sin embargo, se ha demostrado que usando concentraciones de 50 a 200 ppm (la cual es ampliamente usada para desinfectar productos) no es capaz de reducir poblaciones iniciales de microorganismos mayores a 102 Ufc/mL (Sapers, 2001).
Cuando el ultrasonido es usado en combinación con tratamientos químicos (Cl2, H2O2, O3), el intenso gradiente de presión promueve la penetración de los químicos a través de la membrana celular, y la cavitación facilita la desaglomeración de los grupos de microorganismos en la solución desinfectante; incrementando así su eficacia (Gogate y Kabadi, 2009). Phull et al. (1997) investigaron la aplicación de ultrasonido en combinación con cloro como una técnica de desinfección para E. coli y reportaron que la sonicación tuvo la ventaja de ampliar el efecto normal de la cloración y que la combinación tuvo mejores resultados sobre la reducción del microorganismo que la sonicación por sí sola.
Por otra parte, para la reducción de microorganismos aglomerados, lograda por la cavitación, Blume y Neis (2005) reportan la eficacia en tratamiento en aguas residuales en combinación con cloro, observando una notoria reducción en el tamaño de los mismos.
4. Combinación de ultrasonido con temperatura y presión
4.1. Termosonicación
Si bien es cierto que dentro del proceso de cavitación se genera en el fluido un aumento de temperatura, ésta no dura mucho tiempo ni es capaz de llegar a todas las células (Mañas y Pagan, 2005). La termosonicación es el método en el cual los alimentos son sometidos a una combinación de ultrasonido con altas temperaturas (Demidrövel y Baysal, 2009). El uso de esta combinación se ha dado debido a que se reducen las temperaturas y tiempos de proceso en tratamientos como la pausterización y esterilización; logrando los mismos valores de letalidad que con los procesos tradicionales.
Si bien, por debajo de los 50°C no existe un efecto significativo en la inactivación de la mayoría de los microorganismos, una vez que esta temperatura es rebasada, es notorio y considerable dicho efecto (Piyasena et al., 2003). Se ha dicho que el uso de temperatura combinado con ultrasonido puede llegar a afectar su capacidad de conservación de la sonicación; sin embargo, estos estudios se refieren a casos en los que se usa más de 80°C. Esta comprobado que a estas temperaturas la presión de vapor puede llegar a amortiguar el efecto de la cavitación disminuyendo la intensidad del colapso.
A medida que se usan temperaturas de proceso más altas durante el ultrasonido, las burbujas causantes de la cavitación se forman más rápidamente, esto junto con un incremento en la presión de vapor y una disminución en la tensión superficial (SallehMack y Roberts, 2007). Las células
bacterianas se vuelven más sensibles a los tratamientos térmicos si éstas han sido sometidas previamente a un tratamiento de ultrasonido. Un aumento en el número de células muertas ha sido observado en productos en los cuales se han combinado el ultrasonido con un tratamiento térmico, comparado con el mismo alimento sólo expuesto a ultrasonido. Algunos investigadores han reportado una reducción en la resistencia al tratamiento térmico de esporas bacterianas cuando son sonicadas en agua (Hua y Thompson, 2000) a una temperatura en el rango de los 70-95°C, e iguales reducciones se han observado en especies de Bacillus como B. cereus y B. stearothermophilus tratados con altas temperaturas a 20 kHz (Demidröven y Baysal, 2009).
En bacterias Gram negativas se ha encontrado una diferencia de más de un ciclo logarítmico de reducción al aumentar la temperatura de proceso sólo en 10°C (SallehMack y Roberts, 2007). Muñoz et al. (2011) reportaron la efectividad del proceso sobre E. coli presente en jugo de naranja en el cual se lograron de 1 a 2 ciclos logarítmicos de reducción. Sin embargo, los autores describieron que se manejaron dos temperaturas de termosonicación (40 y 50°C) y que a pesar de lo esperado, la mayor inactivación no se logró a la temperatura más alta sino a los 40°C con una reducción de 1.6 ciclos logarítmicos.
4.2. Manosonicación
La manosonicación es el proceso en el cual se usan ondas de ultrasonido de alta frecuencia bajo presión en combinación con temperaturas no letales (Arroyo et al., 2011). Cuando se incrementa la presión hidrostática del medio que se encuentra alrededor de las burbujas de cavitación, da como resultado un descenso en la presión de vapor dentro de la burbuja, y por lo tanto un incremento en la intensidad de la explosión de la burbuja. Los microorganismos
son capaces de resistir en muchos casos altas presiones, pero son incapaces de seguir resistiendo los rápidos cambios de presión producidos durante el procesamiento con ultrasonido (Salleh-Mack y Roberts, 2007).
Se han reportado mejoras en la inactivación al usar manosonicación en microorganismos como Y. enterocolitica, esporas de B. subtilis, L. monocytogenes, Salmonella spp. y Aeromonas hydrophila (Lee et al., 2009). En la inactivación de Listeria monocytogenes al combinar la sonicación con un aumento de presión a 200 kPa, el tiempo necesario para reducir el 90% de la carga microbiana se reduce a 1.5 min, siendo que en un tratamiento de sonicación por sí sólo, son necesarios 4.3 min (Piyasena et al., 2003).
A pesar de que se ha reportado la efectividad de la manosonicación, existe un límite en la presión que puede ser usada dentro de este procesamiento. Tal límite ésta marcado debido a que se han observado procesos en los cuales, a pesar de aumentar la presión ya no existe un efecto letal. Se ha encontrado que para la inactivación de Yersinia enterocolitica por medio de manosonicación, la presión máxima es de 400 kPa (Raso et al., 1998), ya que después de esta presión ya no existe una diferencia significativa en la reducción de la población. Según Lee et al. (2009) es posible que esto suceda ya que cuando la presión ha alcanzado su punto límite, la amplitud de la presión ultrasónica ya no es capaz de superar la presión hidrostática y la fuerza cohesiva del líquido.
Su ventaja en la sanitización y/o inactivación de microorganismos se ve más en productos sensibles al calor, o en aquellos en que las condiciones extremas de proceso pueden perjudicar la calidad del alimento. Además, otra ventaja de la manosonicación es que su capacidad de inactivación de microorganismos de una misma especie no varía con las diferentes cepas de éste, a
diferencia de lo que pasa con los tratamientos térmicos que dependen en gran medida de las especies y cepas de microorganismos que se encuentran en el material. Arroyo et al. (2011) encontraron que al aplicar ultrasonido a una amplitud de onda de 117 µm y 200 kPa de tratamiento a cuatro diferentes cepas de C. sakazakii no existían diferencias de resistencia entre ellas ante la misma intensidad de tratamiento.
4.3. Manotermosonicación
Se ha demostrado que al trabajar a presión atmosférica el poder del ultrasonido disminuye de manera drástica cuando es aplicado a temperaturas por debajo de los 60°C (Raso et al., 1999). Sin embargo, se ha encontrado que cuando las temperaturas del proceso exceden el punto de ebullición en el alimento hay una pérdida en el efecto de cavitación junto con una alta tensión de vapor de agua a estas temperaturas. La aplicación de presión estática a un tratamiento de termosonicación, también conocido como manotermosonicación (MTS) ha sido investigada para mejorar la intensidad de la cavitación de las burbujas creadas durante el proceso de sonicación (Raso et al., 1998).
Al presurizar el líquido durante la termosonicación, la cavitación se mantiene aún a temperaturas de ebullición. Este tratamiento ha sido usado de manera efectiva contra distintos microorganismos. Comparada la inactivación lograda con un tratamiento térmico a la misma temperatura, con la inactivación por MTS en bacterias Gram positivas (Listeria monocytogenes y Streptococcus faecium) y Gram negativas (Salmonella), se ha observado que existe un aumento de 3.4-4 y de 5-6.3 ciclos logarítmicos de reducción, respectivamente (Lee et al.; 2009). Por otra parte, cinco ciclos logarítmicos de reducción fueron logrados para L. monocytogenes al aplicar ultrasonido en combinación con 62°C y 200 kPa por 2
minutos, y en S. entérica a 60°C y 175 kPa por 0.9 minutos (Álvarez et al., 2003).
5. Combinación de ultrasonido con tecnologías emergentes
Las tecnologías emergentes son una opción que se ha venido estudiando en la industria alimentaria en la búsqueda de nuevas opciones de procesamiento de alimentos (Muñoz et al., 2011). Estas han demostrado tener la capacidad de inactivar microorganismos, sin embargo, para lograrlo por si solas necesitan del uso de intensidades de tratamiento muy altas, causando de esta manera cambios en las propiedades de los alimentos y aumentando el requerimiento de energía y por lo tanto el costo del proceso. Por lo anterior su uso en la industria de manera individual se ha convertido en una práctica poco factible.
Algunos de los factores que se han encontrado que más afectan la efectividad de estas tecnologías es la resistencia de las esporas bacterianas y la composición del alimento, entre otros (Leistner y Gould, 2002). Debido a esto es que se ha propuesto la combinación de estas tecnologías emergentes para optimizar su efecto antimicrobiano, formando de esta manera una tecnología de obstáculos.
En el caso del ultrasonido se ha probado combinarlo con pulsos eléctricos y se han logrado inactivar a la población inicial de B. subtilis hasta 4 ciclos logarítmicos (Jin et al., 1998). Este efecto aditivo también ha sido demostrado en la inactivación de E. coli en jugo de naranja, logrando inactivaciones de hasta 3.93 ciclos logarítmicos al utilizar 5.1 J/cm2 y 2.8 minutos de ultrasonido a 24 kHz y 100 µm (Muñoz et al., 2011). Gómez-Díaz et al. (2011) estudiaron la inactivación de Zygosaccharomyces bailli al tratar jugo de manzana con luz ultravioleta de onda corta y ultrasonido de baja frecuencia, los autores reportan el descenso de 7 ciclos logarítmicos
de una población inicial 108 ufc/mL cuando el jugo inoculado con la levadura se sometió a 20 kHz con una amplitud de onda de 120 µm en combinación con una intensidad de luz ultravioleta de 1100 µW/cm2.
En otros casos se ha estudiado la combinación del ultrasonido con alguna tecnología emergente además de la adición de un desinfectante para observar su sinergismo. Un ejemplo de esto es el caso de la combinación de sonicación con irradiación e hipoclorito de sodio en la inactivación de Bacillus cereus (Ji-Hyoung Ha et al., 2012).En este estudio se utilizaron tratamientos de irradiación de 0.1, 0.2 y 0.3 kGy, de 600 a 1000 ppm de hipoclorito de sodio y de 5 a 20 minutos de ultrasonicación, encontrando que las combinaciones destruyeron de manera total a la población inicial (103 ufc/mL) de esporas de esta bacteria, a diferencia del tratamiento en el cual sólo se combinaba la radiación con el ultrasonido en el cual solo se pudo reducir la población inicial a la mitad.
Sin embargo, el éxito de la combinación no sólo depende de su capacidad de inactivación de las diferentes tecnologías por separado, sino también de su compatibilidad técnica para el proceso; ya que existen combinaciones que limitan la utilidad del proceso. En el caso de las combinaciones de ultrasonido con otras tecnologías emergentes aquí mencionadas es evidente que la mayor desventaja es que el procesamiento está limitado a alimentos líquidos.
de los microorganismos presentes en los alimentos.
Estas diferentes combinaciones ofrecen la posibilidad de desarrollar procesos de conservación con los cuales se generen productos microbiológicamente seguros y en los cuales a la vez se logre el aprovechamiento de la composición propia del alimento, y una reducción en la concentración de los componentes químicos usados, así como del tiempo e intensidad del ultrasonido, convirtiéndose de esta manera en procesos que se adaptan a las nuevas tendencias en el consumo de alimentos.
Si bien en los diferentes métodos citados dentro de este trabajo se han presentado buenos resultados en la inactivación de los microorganismos a las condiciones que se realizaron, es necesario seguir investigando a nuevas condiciones en diferentes alimentos para así aumentar la información que pueda validar estos procesos. Además es importante tomar en cuenta las condiciones críticas de cada uno de estos procesos ya que de ello dependerá la relevancia de su acción como tecnología de conservación para los alimentos.
Conclusiones
En general, la combinación del proceso de ultrasonido de baja frecuencia con otros factores de estrés convencionales y emergentes ha demostrado tener un efecto sobre la eficiencia de esta tecnología en la inactivación
Agradecimientos
La autora Franco-Vega agradece al Consejo Nacional de Ciencia y Tecnología (CONACYT) y a la Universidad de las Américas Puebla (UDLAP) por el apoyo para sus estudios de posgrado.
Referencias
Álvarez, I., Mañas, P., Sala, F.J., Condón, S., 2003. Inactivation of Salmonella enteric serovar enteritidis by ultrasonic waves under pressure at different water
A. Franco - Vega et al. / Temas Selectos de Ingeniería de Alimentos 6 – 1 (2012): 73 - 83
activities. Applied and Environmental Microbiology. 69:668–672.
Arce-Garcia, M.R., Jimenez-Munguia, M.T., Palou, E., Lopez-Malo, A., 2002. Ultrasound treatments and antimicrobial agents effects on Zygosaccharomyces rouxii IFT Annual Meeting Book of Abstracts. 2002, Session 91E-18.
Arroyo. C., Cebrián. G., Pagán. R. y Condón, S. 2011. Inactivation of Cronobacter sakazakii by ultrasonic waves under pressure in buffer and foods. International Journal of Food Microbiology 144:446-454.
Blume. T. y Neis. U. 2005. Improving chlorine disinfection of wastewater by ultrasound application, Water Science. Technology. 52:139.
Butz, P. y Tauscher, B., 2002. Emerging technologies: chemical aspects. Food Research International 35 (2/3), 279 – 284.
Condón, S., Raso, J., Pagán, R., 2005. Microbial inactivation by ultrasound. En: Barbosa- Cánovas, G.V., Tapia, M.S., Cano, M.P. (Eds.), Novel Food Processing Technologies. CRC Press, Boca Ratón, pp. 423–442.
Corbo. M., Bevilacqua. A., Campaniello. D., D´Amato. D., Speranza. B. y Sinigaglia. M. 2009. Prolonging microbial shelf life of foods through the use of natural compounds and non-thermal approaches- a review. International Journal of Food Science and Technology. 44:223-241.
Demidrövel. A. y Baysal. T. 2009. The use of ultrasound and combined technologies in food preservation. Food Reviews International. 25:1-11.
Earnshaw, R.G., 1998. Ultrasound: a new opportunity for food preservation. En: Povey, M.J.W., Mason, T.J. (Eds.), Ultrasound in Food Processing. Blackie Academic and Professional, Londres. pp. 183 – 192.
Feng. H. y Weiss. J. 2010. Power ultrasound in food processing. En: D. R. Heldman. (Ed.) Encyclopedia of agricultural, food and biological engineering. CRC Press. Nueva York USA. P. 500-504.
FDA. Food and Drug Administration. US. 2009. Kinetics of Microbial Inactivation for Alternative Food Processing Technologies. http://www.fda.gov/Food/ScienceResearch/Res earchAreas/SafePracticesforFoodProcesses/ucm 100158.htm. Accesada 14 de febrero de 2012.
Ferrante. S., Guerrero. S y Alzamora, S. 2007. Combined use of ultrasound and natural antimicrobials to inactivate Listeria monocytogenes in orange juice. Journal of Food Protection. 70(8):1850‐1856.
Furuta. M., Yamaguchi. M., Tsukamoto. T., Yim. B., Stavarache. C., Hasiba. K. y Maeda. Y. 2004. Inactivation of Escherichia coli by ultrasonic irradiation. Ultrasonics Sonochemistry. 11:57‐60.
Gabriel. A. 2012. Microbial inactivation in cloudy apple juice by multi-frequency Dynashock power ultrasound. Ultrasonic Sonochemistry. 19:346-351.
Gogate. P. y Kabadi. A. 2009. A review of applications of cavitation in biochemical engineering/biotechnology. Biochemical Engineering Journal. 44:60-72.
Gómez-Díaz. J., Santiesteban-López. A., Palou. E. y López-Malo. A. 2011. Zygosaccharomyces bailii inactivation by means of UV light and lowfrequency ultrasound treatments. Journal of Food Protection. 74(10):1751-1755.
Ji-Hyoung Ha, Hyun-Joo Kim, Sang-Do Ha. 2012. Effect of combined radiation and NaOCl/ultrasonication on reduction of Bacillus cereus spores in rice. Radiation Physics and Chemistry. DOI 10.1016/jradphyschem.2012.01.026.
Hua. I y Thompson, J. 2000. Inactivation of Escherichia coli by sonication at discrete ultrasonic frecuencies. Water Research. 34(15):3888-3893.
Kinsloe, H., Ackerman, E., Reid, J.J., 1954. Exposure of microorganisms to measured sound fields. Journal of Bacteriology. 68:373–380.
Jin, Z.T., Su, Y., Tuhela, L., Singh, B., Zhang, Q.H., 1998. Inactivation of Bacillus subtilis using high voltage pulsed electric fields and ultrasonication. IFT Annual Meeting Book of Abstracts, 1998, Session 59C-15.
A. Franco - Vega et al. / Temas Selectos de Ingeniería de Alimentos 6 – 1 (2012): 73 - 83
Lee. H., Zhou. B., Liang.W., Feng. H. y Martin, S. 2009. Inactivation of Escherichia coli cells with sonication, manosonication, thermosonication, and manothermosonication: Microbial responses and kinetics modeling. Journal of Food Engineering. 93:354-364.
Leistner, L., 2000. Basic aspects of food preservation by hurdle technology. International Journal of Food Microbiology 55:181 – 186.
Leistner, L., Gould, G.W., 2002. Hurdle Technologies Combination Treatments for Food Stability, Safety and Quality. Kluwer Academic/Plenum Publishers, New York.
López-Malo. A., Palou. E., Jiménez-Fernández. M., Alzamora. M. y Guerrero, S. 2005. Multifactorial fungal inactivation combining thermosonication and antimicrobials. Journal of Food Engineering. 67(12):87-93.
Mañas y Pagan, 2005. Microbial inactivation by new technologies of food preservation. Journal of Applied Microbiology. 98:1387–1399.
Marriott, N.G. y Gravani, R.B., 1991. Principles of food sanitation. Food Chemistry. 41(3):363-364.
Muñoz. A., Palgan, I., Noci. F., Morgan. D., Cronin. D. Whyte.P. y Lyng. J. 2011. Combinations of High intensity light pulses and thermosonication for the inactivation of Escherichia coli in orange juice. Food Microbiology. 28:1200-1204.
Patist. A. y Bates, D. 2008. Ultrasonics innovations in the food industry: From the laboratory to commercial production. Innovative Food Science and Emerging Technologies. 9:147-154.
Patterson, M.F., 2005. Microbiology of pressure-treated foods. Journal of Applied Microbiology 98:1400–1409.
Piyasena. P., Mohareb, E. y McKellar, R. 2003. Inactivation of microbes using ultrasound: a review. International Journal of Food Microbiology 87:207-2016.
Phull. S., A.P. Newman, J.P. Lorimer, B. Pollet, T.J. Mason. 1997. The development and evaluation of
ultrasound in the biocidal treatment of water, Ultrasonics. Sonochemistry. 4:157.
Raso, J., Pagan, R., Condon, S. y Sala, F. J. 1998. Influence of temperature and pressure on the lethality of ultrasound. Applied and Environmental Microbiology. 64(2):465-471.
Raso. J., Mañas. P., Pagan. R. y Sala. F. 1999. Influence of different factors on the output power transferred into medium by ultrasound. Ultrasonics Sonochemistry. 5:157–162.
Ross. A., Griffiths. M., Mittal. G. y Deeth. H. 2003. Combining nonthermal technologies to control foodborne microorganisms. International Journal of Food Microbiology. 89:125-138.
Sagong. H., Lee. S., Chang. P.,Heu. S., Ryu. S., Choi. Y. y Kang. D. 2011. Combined effect of ultrasound and organic acids to reduce Escherichia coli O157:H7, Salmonella Typhimurium y Listeria monocytogenes on organic fresh lettuce. International Journal of Food Microbiology 145:287-292.
Salleh-Mack. S. y Roberts. J. 2007. Ultrasound pasteurization: The effects of temperature, soluble solids, organic acids and pH on the inactivation of Escherichia coli ATTCC 25922. Ultrasonics Sonochemistry. 14:323-329.
Sapers, G.M., 2001. Efficacy of washing and sanitizing methods for disinfection of fresh fruit and vegetable products. Food Technology and Biotechnology 39:305–311.
Singh, N., Singh, R.K., Bhunia, A.K., Stroshine, R.L., 2002. Efficacy of chlorine dioxide, ozone and thyme essential oil on a sequential washing in killing Escherichia coli O157:H7 on lettuce and baby carrots. Lebensmittel-Wissenschaft und Technologie 35:720–729
Utsunomya. Y. y Kosaka. Y. 1979. Application of supersonic waves to foods. Journal of the Faculty of Applied Biological Science. 18:225-231.
Wong. E., Pérez. A. y Vaillant. F. 2008. Combined effect of osmotic pressure and sonication on the Salmonella Spp. In concentrated orange juice. Journal of Food Safety. 28(4):499-513.

Temas Selectos de Ingeniería de Alimentos 6 - 1 (2012): 84 - 97
Biopolímeros utilizados en la encapsulación
A. García-Ceja* y A. López-Malo.

Departamento de Ingeniería Química, Alimentos y Ambiental, Fundación Universidad de las Américas Puebla. Exhacienda Sta. Catarina Mártir S/N, Cholula, Puebla. C.P.72810. México.
Resumen
La encapsulación es definida como una tecnología de recubrimiento de materiales sólidos y líquidos. Las microcápsulas selladas pueden liberar los contenidos a velocidades controladas bajo condiciones específicas, y pueden proteger el producto encapsulado de la luz, oxígeno y pH. La encapsulación consiste en micropartículas conformadas por una membrana polimérica porosa conteniendo a una sustancia activa. Entre los materiales más utilizados para la encapsulamiento se encuentran goma arábiga, goma xantana, kcarragenina, quitosano, alginato, almidón, gelatina y otras proteínas. Las aplicaciones de la encapsulación van dirigidas a la industria química, alimenticia, y farmacéutica. Las sustancias que se encapsulan son: vitaminas, minerales, pigmentos, microorganismos, antioxidantes, aceites esenciales y enzimas, entre otros. El presente documento tiene por objetivo el papel protector que tiene los agentes encapsulantes para la formación de las matrices con los diversos componentes activos.
Palabras clave: encapsulación, biopolímeros, alginato, almidón, gelatina, goma arábiga, goma xantana, carragenina, proteínas, quitosano.
Abstract
Encapsulation is defined as a technology for covering solids and liquids. The sealed microcapsules can release their contents at controlled rates under specific conditions, and can protect the encapsulated product from light, oxygen and pH. Encapsulation is formed by a micro-porous polymeric membrane containing an active substance. The materials used for micro encapsulation can be arabic gum, xanthan gum, carrageenan, chitosan, alginate, starch, gelatin, and other proteins. Encapsulation applications are exploited in the chemical, food, and pharmaceutical industries. The substances that can be encapsulated are: vitamins, minerals, pigments, microorganisms, antioxidants, essential oils, enzymes, among others. This document aims to have the protective role encapsulating agents for the formation of arrays with different active components.
Keywords: encapsulation, biopolymers, alginate, starch, gelatin, gum arabic, gum xanthan, carrageenan, proteins, chitosan.
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: adelfo.garciaca@udlap.mx
Introducción
La mayoría de los micronutrientes incluyendo las vitaminas y minerales son altamente inestables en la naturaleza; éstos pueden degradarse durante el procesamiento y almacenamiento, así como por el efecto de diferentes condiciones ambientales como la humedad relativa, el pH y la temperatura (Han et al., 2008). La encapsulación es un proceso en el que películas delgadas de materiales poliméricos, se aplican a pequeñas partículas sólidas o gotas de líquido, que contienen materiales sensibles y bioactivos. Esta técnica se utiliza para atrapar componentes activos que se pueden liberar bajo condiciones controladas (Deladino et al., 2008). Los sistemas de encapsulación son de gran utilidad para proteger micronutrientes o microorganismos probióticos porque reducen la interacción que tienen con el exterior, dándoles estabilidad a pH ácidos y condiciones extremas de humedad (Han et al., 2008). Diversos compuestos han sido encapsulados en la industria alimentaria, tales como: aminoácidos, vitaminas, minerales, antioxidantes, enzimas, edulcorantes, colorantes y microorganismos probióticos (Deladino et al., 2008). La encapsulación de probióticos ha sido un tema de investigación que busca mejorar su viabilidad en los alimentos y productos que los contienen, además de mantener su viabilidad durante el paso por el tracto gastrointestinal (Krasaekoopt et al., 2004). Es posible producir cápsulas y recubrimientos mediante la combinación de diferentes tipos de biopolímeros con el fin de aprovechar las ventajas de composición química de cada componente. Algunos estudios como el realizado por Arzate-Vázquez et al. (2012) han demostrado que mezclas de alginato y quitosano son biocompatibles por las relaciones electrostáticas que ocurren al formar una doble encapsulación. Sin embargo, hay pocos documentos que sinteticen la información existente en esta área. Es por ello que resulta interesante realizar una
investigación documental sobre la encapsulación y el papel protector que tiene los agentes encapsulantes para la formación de las matrices con los diversos componentes activos. Revisión bibliográfica
1. Encapsulación
La encapsulación es una tecnología que permite atrapar componentes sensibles en una matriz homogénea o heterogénea para su protección (Lian et al., 2003; Deladino et al., 2008; da Acosta et al., 2011; Nazzaro et al., 2011). En este proceso se forman películas delgadas o membranas semipermeables, utilizando diversos materiales como los biopolímeros (Yua et al., 2010). El desarrollo exitoso de estos sistemas de encapsulación se basa, en el conocimiento sobre la estabilidad del componente que se desea proteger (microorganismos, aceites esenciales, enzimas y antioxidantes, etc.), las propiedades de los materiales para la encapsulación (matriz), el método para la formación de la cápsulas y el alimento al cual se desea incorporar (Nazzaro et al., 2011).
La encapsulación ofrece numerosos beneficios a los consumidores. Ya que añade un valor agregado al alimento, una mayor estabilidad entre los diferentes componentes, así como la protección del componente activo contra la humedad, la temperatura, el daño mecánico, la permeabilidad y la reactividad (al pH y/o a la presencia de sales) que pueden deteriorarlo (Wang et al., 2004; Kashappa et al., 2005). Por otra parte también la encapsulación ayuda a que los componentes activos resistan las condiciones de procesamiento y empacado. En algunos casos el alimento no sufre alteración en sus atributos sensoriales (sabor, aroma y apariencia) y nutricionales por la presencia de las
microcápsulas (Parra, 2010; Sohail et al., 2011). Otro de los beneficios de la encapsulación es que los componentes se liberan de forma controlada por difusión, disolución, disociación y/o fracturación (Krasaekoopt et al., 2004; Kashappa et al., 2005); la cual es importante cuando los agentes activos deben ser liberados en un tiempo apropiado y/o bajo ciertas condiciones (Yuliani et al., 2004).
Existen diversos métodos de encapsulación los cuales se dividen en dos grupos: procesos
- 97
químicos y mecánicos (Yañez et al., 2002). En los procesos químicos se encuentran los métodos de coacervación y gelificación iónica; mientras que en los procesos mecánicos están los métodos de secado por aspersión, liofilización, por congelamiento o enfriamiento, extrusión, emulsión y recubrimiento en lecho fluidizado (Li et al., 2009; Favaro-Trindade et al., 2010; Nazzaro et al., 2011). Los métodos y su aplicación con los diferentes biopolímeros se presentan en la Tabla I.
Tabla I. Métodos utilizados para la encapsulación, biopolímeros y componentes activos.
Técnicas de encapsulaciónBiopolímerosComponentes activos
Secado por aspersión
Maltodextrina, goma arábiga, diferentes aislados de proteínas, caseinato de sodio, polisacárido de soya soluble, βciclodextrina, goma de mezquite
Inclusión molecular β -ciclodextrina
Coacervación
Extrusión
Secado por enfriamiento/congelamiento
Recubrimiento en lecho fluidizado
Gelatina, polifosfato de sodio, goma arábiga
Maltodextrina, azúcar simple o almidón modificado
Aceites vegetales hidrogenados o aceites vegetales de bajo punto de fusión
Hidrocoloides, polímeros solubles en disolvente, cabohidratos simples
Adaptada de Kashappa et al. (2005)
Aceite de naranja, acetato de linalol, cardamomo, d-limoneno
Linalol, aceite de cáscara de naranja, d-limoneno, aceite de limón, sabor café natural y sintético
Aceite de romero, aceite de menta, teobromina
Sabores, vitamina C, colorantes
Aditivos alimentarios sólidos, sabores sólidos
Sólidos, por lo general productos farmacéuticos
Actualmente se utilizan una gran variedad de biopolímeros para formar encapsulaciones sencillas y múltiples, la selección se basa en sus características y propiedades, así como la compatibilidad que se puedan tener entre si cada uno de ellos, para realizar dicha interacción y formar más de una capa. Es necesario tener dos tipos de materiales, uno que provenga del grupo de biopolímeros cargados negativamente como la goma arábiga, goma gellan, pectina, alginato, carboximetil celulosa y el otro del grupo de biopolímeros con carga positiva como la gelatina (cuando se ajusta el pH por debajo del punto isoeléctrico la carga neta en la gelatina es positiva) o el quitosano (único material que tiene carga positiva) (Saravanan y Rao, 2010; Burgain et al., 2011).
La técnica más común para realizar encapsulación múltiple es la emulsión, encapsulando vitaminas. En el área de los fármacos se utiliza el método de coacervación, para los medicamentos. Esta misma técnica se utiliza también para encapsular aceites esenciales como el de romero, y algunos lípidos (omega 3), también sabores como el del café y la β-lactoglobulina (Yuliani et al., 2004; Xie et al., 2006; Given, 2009; Saravanan y Roa, 2010; Jones et al., 2010; Li et al., 2010). Otra técnica es la gelificación iónica, en la cual se encapsulan agentes activos como vitaminas, antioxidantes y hierro, y una gran gama de probióticos (Zhou et al., 1998: Lakkis, 2007; Han et al., 2008; Li et al., 2008; Arzate-Vázquez et al., 2012). En cualquiera de los casos se forma la primera capa con alguno de los biopolímeros para inmovilizar al agente activo y después se cubre a las microcápsulas con el segundo material. Este proceso de encapsulación múltiple protege aun más al compuesto activo.
2. Biopolímeros utilizados en la encapsulación
Los biopolímeros son utilizados en diferentes áreas como la biomedicina, alimentaria y farmacéutica para formar, proteger y transportar los compuestos activos que van dirigidos a diferentes funciones especificas (Chen et al., 2006; Niebla, 2009). Los biopolímeros se clasifican de acuerdo a su origen en naturales y sintéticos. Los de origen natural provienen de cuatro grandes fuentes: origen animal (colágeno/gelatina), origen marino (algas/quitosano), origen vegetal (lípidos, hidrocoloides, proteínas y polisacáridos) y origen microbiano (ácido poliláctico y polihidroxialcanoatos) (Tharanathan, 2003; Yuliani et al., 2004; Ghodke, 2009; Tiwari1 et al., 2010; da Acosta et al., 2011) La mayoría de estos biopolímeros en estado vítreo, son solubles en agua y tienen una alta estabilidad física y química (Yuliani et al., 2004). Los usos más frecuentes son el mejoramiento de las características reológicas y de textura en los alimentos a los que se incorporan, así como ser agentes de revestimiento de medicamentos y agentes de encapsulación para la protección de microorganismos (Ruiz et al., 2009; Tiwaril et al., 2010). Por otra parte se encuentran los biopolímeros sintéticos, que a pesar de su éxito como sistemas encapsulantes, no pueden ser utilizados para su aplicación en alimentos, a menos que sean reconocidos generalmente como seguros, por su siglas en ingles GRAS (da Acosta et al., 2011).
2.1.
Alginato
Es un polímero natural derivado de algas marinas (Prakash y Soe-Lin, 2004). Este polisacárido natural está constituido por unidades de ácidos D-manurónico y L-
gulurónico unidos linealmente por enlaces (14)-glucosídico (Mokarram et al., 2009; Katouzi et al., 2011; Burgain et al., 2011; Sohail et al., 2011). Los alginatos con alto contenido de ácidos gulurónico tienden a formar geles más rígidos y de mayor porosidad, al contrario de alginatos ricos en ácido manurónico. Este ajuste estructural es un resultado directo del Ca+2 que tiene una mayor afinidad por el ácido gulurónico (Penichea, 2004; Prakash y Soe-Lin, 2004; Kailasapathy et al., 2006; Anal y Singh, 2007; Sohail et al., 2011). Éste biopolímero es el más utilizado para la formación de matrices en la industria de alimentos, debido a su facilidad de uso, biocompatibilidad, seguridad y bajo costo (Sohail et al., 2011; Brusch y Záchia, 2011; Burgain et al., 2011). Rodrigues et al. (2011) utilizaron seis biopolímeros (alginato, quitosano, goma xantana, proteína aislada de leche, carragenina y acetato ftalato de celulosa) a dos concentraciones (2 y 4%) evaluando la viabilidad, inmovilización y compatibilidad de estos biopolímeros con Lactobacillus acidophilus Ki, L. acidophilus La-5, L. casei 01, Bifidobacterium animalis BB-12 y B. lactis durante un periodo de 3 h a 37 °C en agua estéril, mostrando que las matrices de alginato son las que poseen una alta biocompatibilidad, inmovilización y viabilidad de los 5 probióticos durante el tiempo de estudio. En otro estudio utilizaron diferentes mezclas de alginato-pectina, alginato-β-ciclodextrina y alginato-trehalosa para encapsular a la invertasa (enzima) por tres métodos de secado (aspersión, enfriamiento al vacío y liofilización) para establecer la enzima en el menor tiempo posible. Se mostró que el método de secado por enfriamiento a vacío es el más adecuado para las tres mezclas, ya que presentó un tiempo de liberación de la enzima de 2 h en una solución de acetato de sodio, a diferencia de los otros métodos que se libero a las 4 h, esto es debido a que el tamaño del poro formado fue mayor en este método (Santagapita et al., 2011). Otros investigadores estudiaron una inmovilización de Bacillus
licheniformis y Saccharomyces cerevisiae a diferentes proporciones de alginato (1.4, 2.0, 2.5, 3.0 y 3.2%) para evaluar su viabilidad, obtuvieron que 3.2 y 2.5% (p/v) fueron las proporciones que presentaron mayor efectividad en la inmovilización y teniendo una mayor población de B. licheniformis y S. cerevisiae (2.6x107 UFC/g y 1.0x108 UFC/g respectivamente) en las cápsulas. Parra (2010) encapsuló L. acidophilus en una mezcla de alginato-inulina-goma-xantana logrando mantener la viabilidad del probiótico en jugo de zanahoria durante 8 semanas de almacenamiento a 4 °C y además de mantener la viabilidad del microorganismos cuando se simula su paso por el tracto gastrointestinal.
2.2. Quitosano
Es un polisacárido natural de alto peso molecular, se encuentra en el exo-esqueleto de los crustáceos y las paredes celulares de algunos hongos (Krasaekoopt et al., 2005; Burgain et al., 2011; Arzate-Vázquez et al., 2012). Este biopolímero natural, obtenido por desacetilación de la quitina (Nacetilglucosamina), posee una alta biocompatibilidad con otros componentes, es biodegrabable, no tóxico, insoluble en agua pero soluble en soluciones ácidas, comportándose en este medio como un polielectrolito catiónico (fácil de adherirse a superficies cargadas negativamente) lo que lo hace tener la capacidad de actuar como floculante, humectante y quelante (Gebelein y Carraher, 1994; Krasaekoopt et al., 2004; Anal y Singh, 2007; Li et al., 2009; Harris et al., 2011; Arzate-Vázquez et al., 2012). El quitosano ha sido utilizado ampliamente en diferentes áreas, una de ellas es la encapsulación de probióticos, mezclándose con otros polisacáridos para la formación de cápsulas. Estudios han demostrado que al utilizar una mezcla de alginato-quitosano para encapsular Escherichia coli DH5, se obtiene una estabilidad mecánica y química de las cápsulas, durante la simulación de su paso por
el tracto gastrointestinal en un periodo de 250 min, ya que esta bacteria se usa para tratamientos terapéuticos de enfermedades del sistema digestivo (Lin et al., 2008). Por otro lado, Brusch y Záchia (2011) realizaron una serie de mezclas con diferentes biopolímeros destacando la mezcla de alginato-quitosano para encapsular Lactobacillus plantarum BL011; mostrando que ésta provee una mayor estabilidad en la viabilidad del probiótico adicionado a yogur durante el almacenamiento en refrigeración (38 días), además de mejorar la supervivencia durante el paso por el tracto gastrointestinal en comparación con otras mezclas (alginato-pectina y alginato-caseína).
Otros estudios demostraron que al utilizar quitosano como revestimiento en cápsulas (perlas) de alginato incrementaron significativamente el tiempo de supervivencia de Lactobacillus rhamnosus de 40 a 120 min y para L. acidophilus de 90 a 120 min en condiciones ácidas (Sohail et al., 2011).
2.3. Gelatina
Es una proteína extraída del colágeno de los animales. La mayoría de la gelatina en el mundo se deriva de la piel del cerdo, huesos y cueros de los bovinos (Anal y Singh, 2007; Boran et al., 2010; Pranoto et al., 2011). La gelatina tiene diferentes propiedades, es el único hidrocoloide que es una proteína y que se funde de forma reversible por debajo de la temperatura corporal (Anal y Singh, 2007; Boran et al., 2010). Es de los materiales más utilizados en la industria alimentaria, farmacéutica, médica, cosmética y de la fotografía. La gelatina es el material más usada para la formación de cápsulas para medicamentos (Anal y Singh, 2007; Wangtueai et al., 2010). Igualmente se ha evaluado su uso para encapsular vitamina A y la efectividad que tiene, mediante el secado por aspersión en mezclas de gelatina-goma de durazno y gelatina-goma de melocotón, mostrando que la mejor mezcla fue la de gelatina-goma de melocotón obteniendo una
retención de vitamina del 97.4% a diferencia de la mezcla gelatina-goma de durazno que tuvo un 94.7% (Xie et al., 2006). da Costa et al. (2011) evaluaron el efecto que tienen las matrices de gelatina-azúcar e inulina-harina de arroz para encapsular aceite esencial de orégano por el método de secado por aspersión y liofilización, observaron que la mezcla de gelatina-azúcar utilizando liofilización presentó una alta actividad antioxidante y antimicrobiana durante un periodo de 2 meses. Otro estudio utilizó a la gelatina como recubrimiento de microesferas de alginato para encapsular al probiótico Bifidobacterium adolescentis 15703T, con el objetivo de aumentar la supervivencia durante la simulación de su paso por el tracto gastrointestinal, demostrando que al recubrir las perlas de alginato con gelatina, favoreció la viabilidad y supervivencia del probiótico con una población de 7.6x1010 UFC/g a diferencia de las perlas de alginato sin recubrir, que tuvieron una población de 6.4x107 UFC/g (Annan et al., 2008).
2.4. Almidón
Es un polisacárido que consiste en un gran número de unidades de glucosa unidas por enlaces glucosídicos. El almidón se compone principalmente de amilosa y amilopectina (Anal y Singh, 2007; Niebla, 2009). El almidón resistente es el que no es digerido por las enzimas pancreáticas (amilasas) en el intestino delgado y puede llegar al colón donde se fermenta; esta especificidad proporciona una buena característica de protección al utilizarse como material encapsulante y una mejor liberación de los probióticos o componentes activos en el intestino grueso (Anal y Singh, 2007; Niebla, 2009). Además, por su funcionalidad como agente prebiótico, el almidón resistente puede ser utilizado por los probióticos que se encuentran en el intestino grueso, por lo que es ideal para la encapsulación (Burgain et al., 2011). Esta clase de almidones (nativos o
modificados) por su tipo y estructura, se utilizan para encapsular sabores (Niebla, 2009; Burgain et al., 2011). El almidón de maíz liofilizado se ha sido utilizado como material de revestimiento de cápsulas de alginato, ya que mejora la resistencia de las cápsulas durante la simulación a la exposición de las enzimas pancreáticas (Mortazavian et al., 2007).
2.5. Gomas
Las gomas son polisacáridos de alto peso molecular, son obtenidas de plantas o por microorganismos. Tiene características hidrofílicas o hidrofóbicas, usualmente, tienen propiedades coloidales, con capacidad de producir geles al combinarse con solventes apropiados, tienen la capacidad de dispersar en agua fría o caliente, producen soluciones o mezclas viscosas. Entre las gomas más utilizadas como material de encapsulación se encuentran la goma xantana, la goma arábiga y la k-carragenina (Pasquel, 2001).
2.5.1. Goma xantana
Es un hetero-polisacárido producido por la bacteria Xanthomonas campestris (Gebelein y Carraher, 1994). Es utilizada en numerosas aplicaciones en las industria alimentaria y química como un agente espesante, estabilizante y emulsionante (Ahmed et al., 2005; Parra, 2010; Seyed et al., 2011). Otra de sus aplicaciones es ser utilizado como agente de encapsulación para diferentes biocomponentes. McMaster et al. (2005) realizaron una microencapsulación de Bifidobacterium lactis con una mezcla de goma xantana-goma gellan, utilizando una técnica de ultrasonido; demostraron una alta supervivencia de B. lactis durante un periodo de 21 días, almacenadas a 4 y 22 °C con una población de 1.0x1010 UFC/g y 1.1x1011 UFC/g, respectivamente en un yogur. Por otro lado se han utilizado diferentes mezclas de gomas de origen microbiano (goma xantana,
gellan, pullulan y jamilan), para encapsular a L. plantarum CRL 1815 y L. rhamnosus ATCC 53103 y determinar la efectividad que tienen como agentes encapsulantes durante el paso por el tracto gastrointestinal; los resultados indicaron que la mezcla con xantana (1%) y gellan (0.75%) prolongan la viabilidad de L. plantarum CRL 1815 y L. rhamnosus ATCC 53103 por 6 h al exponerlas a sales biliares y pancreatina (JiménezPranteda et al., 2011). Otros investigadores estudiaron la resistencia de L. acidophilus LA14 y B. lactis BI07 en diferentes sistemas encapsulantes, utilizando alginato como base principal, goma xantana y acetato ftalato de celulosa en diferentes proporciones por los métodos de extrusión, liofilización y secado por aspersión, mostrando que al incorporar 0.5 ó 1.0% de xantana y 3% de acetato ftalato de celulosa en mezcla con alginato, aumentaron la supervivencia de los probióticos en condiciones ácidas en un 63, 71 y 91% respectivamente por cada método (Albertini et al., 2010).
2.5.2. Goma arábiga
Es el exudado natural de la Acacia de Senegal, es un heteropolisacárido de alto peso molecular, está formado por una cadena lineal de moléculas de D-galactosa unidas por enlaces β- 1,4 y β- 1,6 (Ahmed et al., 2005; Lopera et al., 2009; Parra, 2010). La goma arábiga por sus características estructurales presenta un carácter anfifílico, lo que le permite absorber en superficies lipofílicas y actuar como coloide protector; como un buen agente formador de cápsulas y películas (Cubero et al, 2002; Yuliani et al., 2004; Lopera et al., 2009). Rascon et al. (2011) utilizaron la goma arábiga para retener y estabilizar carotenoides de paprika, por el método de secado por aspersión, mostrando que un polvo con una aw de 0.274 posee la máxima estabilidad al prevenir la oxidación de los carotenoides. Por otro lado Pitalua et al. (2010) encapsularon jugo de betabel con goma
arábiga, por el método de secado por aspersión a diferentes aw (0.110, 0.326, 0.521, 0.748 y 0.898), para observar su actividad antioxidante, mostrando que los polvos con una aw de 0.110, 0.326 y 0.521 no presentaron diferencia significativa entre ellas, sin embargo entre aw 0.748 y 0.898 incrementa la actividad antioxidante y disminuye la concentración de las betalaínas, protegiendo al agente antioxidante por 8 semanas. En otro estudio se microencapsuló oleorresina de cardamomo utilizando mezclas binarias de goma arábiga (GA), maltodextrina (MD) y almidón modificado (AM), a diferentes proporciones (25:75 (GA:MD), 50:50 (GA:MD), 75:25 (GA:MD), 25:75 (GA:AM), 50:50 (GA:AM) y 75:25 (GA:AM)), por el método de secado por aspersión, para protegerla de la luz, la temperatura y el oxígeno; encontrado que las mezcla de 75:25 (GA:MD), 25:75 (GA:AM) y 25:75 (GA:MD), fueron las que presentaron una mejor estabilidad y protección del componente durante 6 semanas (Krishnan et al., 2005).
Chee-Teck (1998) utilizó la goma arábiga como material de revestimiento para encapsular aceite de naranja por el método de emulsión, demostrando que durante 90 días la emulsión fue estable en una solución de azúcar, por lo cual se puede utilizar como base para la preparación de bebidas no alcohólicas. Otros autores microencapsularon un derivado de la Zn-clorofila extraído de la hoja Pandan utilizado como colorante verde, con goma arábiga, maltodextrina y almidón modificado como agentes encapsulantes por el método de secado por aspersión, mostrando que el mejor encapsulante fue el almidón modificado ya que no presentó degradación del pigmento a diferencia de los demás agentes encapsulantes durante un periodo de almacenamiento de 16 semanas (Porrarud y Pranee, 2010). Por otro lado Li et al. (2011) formaron emulsiones múltiples con una mezcla de proteína de suero de leche y polisacáridos (goma arábiga y goma guar a diferentes proporciones 5:0.1, 5:0.2, 5:0.3, 5:0.4, 5:0.5), encapsulando vitaminas E
y B2 para determinar la protección de las cápsulas a diferentes proporciones. Demostraron que al aumentar la concentración de la mezcla 0.1 a 0.5 de la goma guar incrementa la protección de la encapsulación de 73 a 88% de retención de las vitaminas E y B2.
2.5.3.
Carragenina
Es un polisacárido natural de alto peso molecular, se encuentra presente en la estructura de ciertas variedades de algas rojas, posee un contenido de éster sulfato del 15% al 40% formado por unidades alternadas de Dgalactosa y 3,6-anhidro-galactosa, unidas por enlaces α-1,3 y β-1,4 (Gebelein y Carraher, 1994). La posición y el número de grupos de éster sulfato así como el contenido de 3,6anhidro-galactosa determinan las diferencias primarias entre los tipos de carragenina kappa, iota y lambda (Anal y Singh, 2007; Nickerson et al., 2010; Burgain et al., 2011).De acuerdo al tipo de carragenina actúa como gelificante, retenedor de humedad, espesante, agente de suspensión y estabilizante (Anal y Singh, 2007; Nickerson et al., 2010; Burgain et al., 2011). Jones et al. (2010) utilizaron a la kcarragenina y pectina de alto y bajo metoxilo para encapsular a la β-lactoglobulina y determinar el efecto que pueden tener el agente encapsulante y el agente activo. Asimismo evaluaron el grado de desnaturalización de la proteína mediante la aplicación de calor y de enzimas, demostrando que la k-carragenina en presencia del agente activo no presentó deterioro en ambas condiciones. Mientras que las cápsulas elaboradas con pectinas de alto y bajo metoxilo fueron degradadas por las enzimas evaluadas. Dinakar y Mistry (1994) reportaron que al encapsular Bifidobacterium bifidum ATCC 15696 con k-carragenina, las células permanecieron viables y no tuvieron efecto en el proceso de elaboración y de maduración del queso cheedar por un periodo de 24 semanas. Otros autores encapsularon Streptococcus
salivarius subsp. thermophilus y L. casei con una mezcla de k-carragenina-goma de algaborro, para determinar el comportamiento de la difusión de las perlas en una solución de lactosa y agua, así como la viabilidad después de la encapsulación, mostrando que las perlas presentaron una mayor difusión en agua que en una solución de lactosa, para los dos microorganismos y obteniendo una viabilidad de 5.0x109 UFC/g (S. salivarius) y 1.8x1011 UFC/g (L. casei) una vez encapsulados (Arnaud y Lacroix, 2004).
2.6. Pectina
Es un polisacárido de alto peso molecular que se encuentra en los tejidos vegetales, como los de las frutas. Está compuesto de polímeros de ácido D-galacturónico, es un complejo aniónico y se clasifican como pectinas de alto metoxilo (para formar el gel se necesita un pH bajo) y pectinas de bajo metoxilo (forman un gel en contacto con cationes divalentes tales como iones Ca2+) (Villada et al., 2002; Ramos-García et al., 2010). Los recubrimientos hechos a base de pectinas han sido los más utilizados para recubrir frutos y otros componentes activos, y esto se debe a las propiedades mecánicas de adherencia y flexibilidad en la superficie (Villada et al., 2002; Ramos-García et al., 2010; Brusch y Záchia, 2011; Pliszczak et al., 2011). Mendanha et al. (2009) microencapsularon un hidrolizado de caseína por el método de coacervación, utilizando como material encapsulante una mezcla de pectina-proteína aislada de soya, para enmascarar su sabor amargo así como protegerlo de la humedad, logrando atenuar el sabor y reducir su higroscopicidad al compararlo con el no encapsulado. Por otro lado Pozippe et al. (2011) encapsularon el extracto de propóleo por el método de coacervación, utilizando la mezcla de pectina-proteína aislada de soya, obteniendo un polvo con características antioxidantes y antimicrobianas contra Staphylococcus aureus en alimentos,
omitiendo así el uso de alcohol como agente solubilizante del propóleo. Otro estudio inmovilizó L. casei en perlas hechas a base de pectina de bajo metoxilo y alginato de sodio, a diferentes proporciones (2:1, 4:1 y 6:1), reportando la mayor supervivencia del probiótico a una proporción de 6:1 cuando fue adicionado a yogur y al simular su paso por el tracto gastrointestinal (Sandoval-Castilla, 2010). En la encapsulación de L. casei con una mezcla de pectina-caseína, con el método de coacervación, observaron una alta compatibilidad entre el probiótico y el material de revestimiento; sin embargo, no se logró proteger al probiótico cuando se colocó en un ambiente con pH similar al del estómago humano (Oliveira et al., 2007).
2.7. Proteínas
Existen diferentes tipos de proteínas que se utilizan como agentes encapsulantes como son las lácteas y las de origen vegetal (Burgain et al., 2011). Las proteínas lácteas son vehículos naturales debido a sus propiedades estructurales y físicoquímicas, y se utilizan en una gran diversidad de productos (Tharanathan, 2003). Las proteínas de suero de leche forman películas transparentes, insípidas y flexibles, con una buena resistencia a la transferencia de oxígeno, aromas y lípidos (Ryu et al., 2002; Villada et al., 2002; Tharanathan, 2003; Wang et al., 2004; Chen et al., 2006; Sánchez et al., 2007; Burgain et al., 2011). Por otro lado se encapsuló aceite omega-3 de pescado con proteína de leche, logrando así estabilizarlo y evitar su oxidación al incorporarlo en un alimento (Torres-Giner et al., 2010). Molina et al. (2009) encapsularon al hidrolizado de caseína, utilizando al aislado de proteína de soya como agente encapsulante, para enmascarar el sabor amargo del hidrolizado, lográndose dicho objetivo al evaluar sensorialmente las cápsulas con una prueba hedónica. Se encapsularon Bifidobacterium breve R070 y Bifidobacterium longum R023 con grasa de
leche y proteína de suero de leche utilizando el método de emulsión y/o secado por aspersión, mostrando que después de la segunda técnica la supervivencia fue de 1.7x109 UFC/g y 8.1x107 UFC/g para B. breve R070 y B. longum R023, respectivamente. Además se evaluó la viabilidad de estos microorganismos con y sin encapsulación en un yogur durante 28 días, observado que los encapsulados tuvieron una mayor viabilidad y supervivencia (Picot y Lacroix, 2004). Por otro lado el caseinato de sodio se utilizó como agente encapsulante para proteger aceites esenciales (canela y jengibre) del vapor de agua y la oxidación; sin embargo, no fue posible mejorar su estabilidad (Atarés et al., 2010).
Conclusiones
La encapsulación es una técnica que permite la preservación o protección de un gran número de compuestos activos; tales como aceites esenciales, microorganismos probióticos, enzimas, pigmentos vegetales, minerales, vitaminas y aditivos alimenticios. Los principales agentes utilizados para encapsular son alginato, quitosano, gelatina, goma xantana, goma arábiga y proteínas (animal y vegetal). La encapsulación se lleva a cabo a través de procesos físicos o mecánicos; las técnicas más usadas son el secado por aspersión, extrusión y gelificación iónica. Existen pocos estudios sobre la encapsulación múltiple; así como los materiales compatibles para dicha encapsulación. Es de suma importancia el conocimiento de las propiedades y características de los materiales para la formación de las cápsulas así como de sus aplicaciones en la industria alimenticia.
Agradecimientos
A. García-Ceja agradece al Consejo Nacional de Ciencia y Tecnología (CONACyT) y a la Universidad de las Américas Puebla (UDLAP), por el apoyo y financiamiento para sus estudios de posgrado.
Referencias
Ahmed, J., Ramaswamy, H. S. y Ngadi, M. O, 2005. Rheological characteristics of arabic gum in combination with guar and xanthan gum using response surface methodology: effect of temperature and concentration. International Journal of Food Properties. (8): 179–192.
Albertini, B., Vitali, B., Passerini, N. Cruciani, F., Di Sabatino, M., Rodriguez y L., Brigidi P., 2010. Development of microparticulate systems for intestinal delivery of Lactobacillus acidophilus and Bifidobacterium lactis. European Journal of Pharmaceutical Sciences. 40) 359–366.
Anal, A. y Singh, H., 2007. Recent advances in microencapsulation of probiotics for industrial applications and targeted delivery. Food Science & Technology. (18): 240-251.
Annan, N.T., Borza, A.D., y Truelstrup Hansen L., 2008. Encapsulation in alginate-coated gelatin microspheres improves survival of the probiotic Bifidobacterium adolescentis 15703T during exposure to simulated gastro-intestinal conditions. Food Research International. (41): 184–193.
Arnaud, J. P. y Lacroix, C., 2004. Diffusion of lactose in k-carrageenan/locust bean gum gel beads with or without entrapped growing lactic acid bacteria. Biotechnology and Bioengineering. 38 (9): 10411049.
Arzate-Vázquez I., Chanona-Pérez, J., CalderónDomínguez, G., Terres-Rojas, E., Garibay-Febles, V., Martínez-Rivas, A. y Gutiérrez-López., G., 2012. Microstructural characterization of chitosan and alginate films by microscopy techniques and texture image analysis. Carbohydrate Polymers (142): 185-189.
Atarés, L., Bonilla, J. y Chiralt, A., 2010. Characterization of sodium caseinate-based edible films incorporated with cinnamon or ginger essential oils. Journal of Food Engineering. (100): 678-687.
Boran, G. G., Lawless, H. T. y Jones J. M., 2010. Regenstein effects of extraction conditions on the sensory and instrumental characteristics of fish gelatin. Journal of Food Science. (75): 9-15.
Brusch, G. B. y Záchia, A. M. A., 2011. Effect of microencapsulation on survival of Lactobacillus plantarum in simulated gastrointestinal conditions, refrigeration and yogurt. Journal of Food Engineering. (103): 123-128.
Burgain, J., Gaiani, C., Linder, M. y Scher, J., 2011. Encapsulation of probiotic living cells: from laboratory scale to industrial applications. Journal of Food Engineering. (104): 467-483.
Chee-Teck, T., 1998. Beverage flavor emulsion - a form of emulsion liquid membrane microencapsulation. International Flavors & Fragrances. (1): 29-42.
Chen, L., Remondetto, G. E. y Subirade, M., 2006. Food protein-based materials as nutraceutical delivery systems. Trends in Food Science & Technology. (17): 272-283.
Cubero, N., Monferrer, A. y Villalta, J., 2002. Aditivos alimentarios. Editorial Mundi-Prensa. Madrid, España, 242 p.
da Costa, S. B., Duarte, C., Bourbon, A. I., Pinheiro, A. C., Serra, A.T., Martins M. M., Nunes, J. M. I., Vicente, A. A., Delgadillo, I., Duarte, C. y da Costa, M. L. B., 2011. Effect of the matrix system in the delivery and in vitro bioactivity of microencapsulated oregano essential oil. Journal of Food Engineering, doi:10.1016/j.jfoodeng.2011.05.043.
Deladino L., Anbinder, P. S., Navarro A. S. y Martino M. N., 2008. Encapsulation of natural antioxidants extracted from (Ilex paraguariensis). Carbohydrate Polymers. (71): 126-134.
Dinakar, P. y Mistry,V.V., 1994. Growth and viability of Bifidobacterium bifidum in cheddar cheese. Journal of Dairy Science. 77 (10): 2854-2864.
Favaro-Trindade C.S., Santana, A.S., MonterreyQuintero E.S., Trindade, M.A. y Netto, F.M., 2010. The use of spray drying technology to reduce bitter taste of casein hydrolysate. Food Hydrocolloids (24): 336-340.
Gebelein, C. G. y Carraher, C. E. Jr. 1994. Biotechonology and bioactive polymers. First edition. Plenum Press. Florida, EE.UU, 342 p.
Ghodke S. K., 2009. Effect of guar gum on dough stickiness and staling in chapatti– an Indian unleavened flat bread. International Journal of Food Engineering. 5 (3): 7-15.
Given, P. S. J., 2009. Encapsulation of flavors in emulsions for beverages. Current Opinion in Colloid & Interface Science. (14): 43-47.
Han, J., Guenier, A., Salmieri, S. y Lacroix, M., 2008. Alginate and chitosan functionalization for micronutrient encapsulation. Journal of Agricultural and Food Chemistry. (56): 2528-2535.
Harris, R., Lecumberri, E., Mateos-Aparicio, I., Mengíbar, M. y Heras, A., 2011. Chitosan nanoparticles and microspheres for the encapsulation of natural antioxidants extracted from Ilex paraguariensis Carbohydrate Polymers. (84): 803-806.
Jiménez-Pranteda, M. L., Poncelet, D., Náder-Macías, M. E, Arcos, A., Aguilera, M., Monteoliva-Sánchez, M. y Ramos-Cormenzana, A., 2011. Stability of lactobacilli encapsulated in various microbial polymers. Journal of Bioscience and Bioengineering doi:10.1016/j.jbiosc.2011.10.010.
Jones, O., Decker, E. A. y McClements, D. J., 2010. Thermal analysis of b-lactoglobulin complexes with pectins or carrageenan for production of stable biopolymer particles. Food Hydrocolloids. (24): 239-248.
Kailasapathy, K., Perera, C., y Phillips, M. 2006. Evaluation of alginate-starch polymers for preparation of enzyme microcapsules. International Journal of Food Engineering. 2 (2): 1-13.
Kashappa, G., Desai, H., Park y H. J., 2005. Recent developments in microencapsulation of food ingredients. Drying Technology. (23): 1361-1394.
Katouzi, S., Majd, A., Fallahian, F. y Bernard, F., 2011. Encapsulation of shoot tips in alginate beads containing salicylic acid for cold preservation and plant regeneration in sunflower (Helianthus annuus L.). Australian Journal Of Crop Science. 5 (11): 1469-1474.
Krasaekoopt, W., Bhandari , B. y Deeth, H. C., 2004. The influence of coating materials on some properties of alginate beads and survivability of microencapsulated probiotic bacteria. International Dairy Journal. (14): 737-743.
Krasaekoopt, W., Bhandari, B. y Deeth, H. C., 2005. Survival of probiotics encapsulated in chitosancoated alginate beads in yoghurt from UHT- and conventionally treated milk during storage. LWT (39): 177-183.
Krishnan, S., Bhosale, R. y Singhal, R. S., 2005. Microencapsulation of cardamom oleoresin: evaluation of blends of gum arabic, maltodextrin and a modified starch as wall materials. Carbohydrate Polymers. (61): 95-102.
Lakkis, J., 2007. Encapsulation and controlled release technologies in food systems. First edition. Blackwell Publishing. New York, EE.UU, 239 p.
Li, B. G., Zhang, Y. . Zhang, W. J. y Hua, Z., 2008. Supercritical CO2 spray drying of ethyl cellulose (EC) for preparing microparticles. Drying Technology. (26): 464-469.
Li, B., Jiang, Y., Liu, F., Chai, Z., Li, Y. y Leng, X., 2011. Study of the encapsulation efficiency and controlled release property of whey protein isolate— polysaccharide complexes in w1/o/w2 double emulsions. International Journal of Food Engineering. 7 (3): 14-20.
Li, X. Y., Jin, L. J., Uzonna, J. E., Li, S.Y., Liu, J. J., Li, H. Q., Lu, Y. N., Zhen, Y. H. y Xu Y. P., 2009. Chitosan–alginate microcapsules for oral delivery of egg yolk immunoglobulin (IgY): In vivo evaluation in a pig model of Enteric colibacillosis Veterinary Immunology and Immunopathology. 4 (129): 132136.
Li, Y., Hu, M., Xiao H., Dua, Y., Decker, E. A. y McClements, D. J., 2010. Controlling the functional performance of emulsion-based delivery systems using multi-component biopolymer coatings. European Journal of Pharmaceutics. (76): 152-162.
Lian, W.C., Hsiao, H. C. y Chou, C. C., 2003. Viability of microencapsulated Bifidobacteria in simulated gastric juice and bile solution. International Journal of Food Microbiology. 86 (3): 293-301.
Lin, J., Yu, W., Liu, X., Xie, H., Wang, W. y Ma, X., 2008. In vitro and in vivo characterization of alginate-chitosan-alginate artificial microcapsules for therapeutic oral delivery of live bacterial cells. Journal of Bio Science and Bioengineering. 105 (6): 660-665.
Lopera, C. M. S., Guzmán O. C., Cataño R. C. y Gallardo C. C., 2009. Desarrollo y caracterización de micropartículas de ácido fólico formadas por secado por aspersión, utilizando goma arábiga y maltodextrina como materiales de pared. Vitae. 16 (1): 55-65.
McMaster, L. D., Kokott1, S. A., y Slatter, P., 2005. Micro-encapsulation of Bifidobacterium lactis for incorporation into soft foods. World Journal of Microbiology & Biotechnology. (21): 723-728.
Mendanha, D. V., Molina, O. S. E., Favaro-Trindade, C.S., Mauri, A., Monterrey-Quintero, E. S. y Thomazini, M., 2009. Microencapsulation of casein hydrolysate by complex coacervation with spi/pectin. Food Research International. (42): 10991104.
Mokarram, R. R., Mortazavi, S. A., Najafi, M. B. H. y Shahidi, F., 2009. The influence of multi stage alginate coating on survivability of potential probiotic bacteria in simulated gastric and intestinal juice. Food Research International. (42): 10401045.
Molina, O. S. E., Mauri, A. Monterrey-Quintero, E.S., Trindade M. A. Santana A.S., Favaro-Trindade C. S., 2009. Production and properties of casein hydrolysate microencapsulated by spray drying with soybean protein isolate. Food Science and Technology. (42): 919-923.
Mortazavian, A., Hadi Razavi, Mohammad S., Ehsani, R. y Sohrabvandi, S. 2007.Principles and methods of microencapsulation of probiotic microorganisms. Iranian Journal of Biotechnology. 5 (1): 154-165.
Nazzaro, F., Orlando, P., Fratianni, F. y Coppola, R., 2011. Microencapsulation in food science and biotechnology. Current Opinion in Biotechnology. (23): 1-5.
Nickerson, M. T., Darvesh, R. y Paulson A. T., 2010. Formation of calcium-mediated junction zones at the onset of the sol-gel transition of commercial κcarrageenan solutions. Journal of Food Science. 75 (3): 156-163.
Niebla, B. L., 2009. Evaluación de encapsulamiento de compuestos de sabor en matrices de almidón. Tesis de maestría, Instituto Politécnico Nacional, México. 97 p.
Oliveira, A. C., Moretti, T. S., Boschini, C., Baliero, J. C. C., Freitas, L. A. P. Freitas, O. y FavaroTrindade, C. S., 2007. Microencapsulation of B. lactis (BI 01) and L. acidophilus (LAC 4) by complex coacervation followed by spouted-bed drying. Drying Technology. (25): 1687-1693.
Parra, H. R.A., 2010. Food Microencapsulation: Review. Revista Facultad Nacional de Agronomía. 63 (2): 5669-5684.
Pasquel, A., 2001. Gomas: una aproximación a la industria de alimentos Revista Amazónica de Investigación Alimentaria. 1 (1): 1-8.
Penichea, C., Howlandb, I., Carrilloc, O., Zaldı´varc, C. y Arguelles-Monald, W., 2004. Formation and stability of shark liver oil loaded chitosan/calcium
alginate capsules. Food Hydrocolloids. (18): 865871.
Picot, A. y Lacroix, C., 2004. Encapsulation of bifidobacteria in whey protein-based microcapsules and survival in simulated gastrointestinal conditions and in yoghurt. International Dairy Journal. (14): 505-515.
Pitalua E., Jimenez, M. 0., Vernon-Carter, E. J. y Beristain, C. A., 2010. Antioxidative activity of microcapsules with beetroot juice using gum arabic as wall material. Food and Bioproducts Processing 8 (8): 253-258.
Pliszczak, D., Bourgeois, S., Bordes, C., Valour, J. P., Mazoyer, M. A., Orecchioni, A.M., Nakache. E. y Lantéri, P., 2011. Improvement of an encapsulation process for the preparation of pro-prebiotics-loaded and bioadhesive microparticles by using experimental design. European Journal of Pharmaceutical Sciences. (44): 83-92.
Porrarud, S. y Pranee, A., 2010. Microencapsulation of Zn-chlorophyll pigment from pandan leaf by spray drying and its characteristic. International Food Research Journal. (17): 1031-1042.
Pozippe, N. M., Favaro-Trindade , C. S., Matias de Alencar, S., Thomazini, M., de Camargo, B. J. C. y Contreras Castillo. C. J., 2011. Microencapsulation of propolis extract by complex coacervation. Food Science and Technology. (44): 429-435.
Prakash, S. y Soe-Lin, H., 2004. Strategy for cell therapy: polymers for live cell encapsulation and delivery. Trends Biomater. Artif. Organs. 18 (1): 24-35.
Pranoto, Y., Marseno, D. W. y Rahmawati, H., 2011. Characteristics of gelatins extracted from fresh and sun-dried seawater fish skins in Indonesia. International Food Research Journal. 18 (4): 13351341.
Ramos-García, M. L., Bautista-Baños, S., BarreraNecha, L. L., Bosquez-Molina, E., Alia-Tejacal, I. y Estrada-Carrillo, M., 2010. Compuestos antimicrobianos adicionados en recubrimientos comestibles para uso en productos hortofrutícolas. Revista Mexicana de Fitopatología. 28 (1): 44-57.
Rascón, M. P., Beristain, C. I., García, H. S. y Salgado, M. A., 2011. Carotenoid retention and storage stability of spray-dried encapsulated paprika oleoresin using gum arabic and soy protein isolate as wall materials. Food Science and Technology. (44): 549-557.
Rodrigues, D., Rocha-Santos, T., Sousa, S., Gomes, A., Pintado, M. M., Malcata, F. X., Sousa, L. J. M.,
Silva, J. P., Paulo Costa, Amaral M. H. y Freitas, A. C., 2011. On the viability of five probiotic strains when immobilized on various polymers. International Journal of Dairy Technology. 64: (1) 156-159.
Ruiz, M. A., Martín V. M. J., Morales H. M. E., Gallardo, L. V., 2009. Técnicas de microencapsulación: una propuesta para microencapsular probióticos. Ars pharmaceutica. 50 (1): 43-50.
Ryu, S., Rhim, J., Roh, H. y Kim, S. 2002. Preparation and physical properties of zein-coated high-amylose corn starch film. Food Science and Technology. (35): 680-686.
Sánchez, A., Sibaja, M., Vega-Baudrit, J. y Madrigal S., 2007. Síntesis y caracterización de hidrogeles de quitosano obtenido a partir del camarón langostino (Pleuroncodes planipes) con potenciales aplicaciones biomédicas. Revista Iberoamericana de Polímeros. 8 (4): 1568-1572.
Sandoval-Castilla, O., Lobato-Calleros, C., GarcíaGalindo, H.S., Alvarez-Ramírez, J. y Vernon-Carter, E. J., 2010. Textural properties of alginate–pectin beads and survivability of entrapped Lb. casei in simulated gastrointestinal conditions and in yoghurt. Food Research International. (43): 111-117.
Santagapita, R. P., Mazzobre, M. F. y Buera M. P., 2011. Formulation and drying of alginate beads for controlled release and stabilization of invertase. Biomacromolecules. (12): 3147-3155.
Saravanan, M. y Rao, K. P., 2010. Pectin–gelatin and alginate-gelatin complex coacervation for controlled drug delivery: Influence of anionic polysaccharides and drugs being encapsulated on physicochemical properties of microcapsules. Carbohydrate Polymers. (80): 808-816.
Seyed M.A., Razavi, T. y Moghaddam, M., 2011. Influence of different substitution levels of Lallemantia royleana seed gum on textural characteristics of selected hydrocolloids. Electronic Journal of Environmental, Agricultural and Food Chemistry. 10 (8): 2676-2688.
Sohail, A., Turner, M. S., Coombes, A., Bostrom, T. y Bhandari, B., 2011. Survivability of probiotics encapsulated in alginate gel microbeads using a novel impinging aerosols method. International Journal of Food Microbiology. (145): 162-168.
Sossa-Urrego, D., Navarro-Acevedo, M. A., Matiz Villamil, A. M. Mercado-Reyes, B. QuevedoHidalgo1, A. y Pedroza-Rodríguez, M., 2008. Immobilization of bacillus licheniformis and
saccharomyces cerevisiae for ethanol production from potato starch. Universitas Scientiarum. 13(2): 149-161.
Tharanathan, R., 2003. Biodegradable films and composite coatings: past, present and future. Critical Review in Food Science and Technology. (14): 7178.
Tiwaril, B. K., Muthukumarappan, K., O’Donnell1, C.P. y Cullen, P. J., 2010. Rheological properties of sonicated guar, xanthan and pectin dispersions. International Journal of Food Properties. (13): 223233.
Torres-Giner, S., Martinez-Abad, A., Ocio, M. J. y Lagaron J. M., 2010. Stabilization of a nutraceutical omega-3 fatty acid by encapsulation in ultrathin electrosprayed zein prolamine. Journal of Food Science. 75 (6): 69-79.
Villada, H. S., Acosta, H. A. y Velasco, J. R., 2002. Biopolymers naturals used in biodegradable packaging. Revista Temas Agrarios. 12 (2): 5-13.
Wang, Y., Dave, R. N. y Pfeffer, R., 2004. Polymer coating/encapsulation of nanoparticles using a supercritical anti-solvent process. Journal of Supercritical Fluids. (28): 85-99.
Wangtueai, S., Noomhorm, A. y Regenstein. J. M., 2010. Effect of microbial transglutaminase on gel
- 97
properties and film characteristics of gelatin from lizardfish (Saurida spp.) scales. Journal of Food Science. 75 (9): 101-109.
Xie, Y. L., Zhou, H. M. y Qian H. F., 2006. Effect of addition of peach gum on physicochemical properties of gelatin-based microcapsule. Journal of Food Biochemistry. (30): 302-312.
Yañez, J., Salazar, J., Chaires, L., Jimenez, J., Marquez, M. y Ramos, E., 2002. Aplicaciones biotecnológicas de la microencapsulación. Revista Avance y Perspectiva. (21): 313-319.
Yua, W., Lina, J., Liub, X., Xiea, H., Zhaoa, W. y Maa, X., 2010. Quantitative characterization of membrane formation process of alginate-chitosan microcapsules by gpc. Journal of Membrane Science. (346): 296-301.
Yuliani, S., Bhandari, B., Rutgers, R. y D’Arcy, B., 2004. Application of microencapsulated flavor to extrusion product. Food Reviews International. 20 (2): 163-185.
Zhou, Y., Martins, E., Groboillot, A., Champagne, C. P. y Neufeld, R. J., 1998. Spectrophotometric quantification of lactic bacteria in alginate and control of cell release with chitosan coating. Journal of Applied Microbiology. (84): 42-348.

Temas Selectos de Ingeniería de Alimentos 6 - 1 (2012): 98 - 110

Cambios en las propiedades de frutas y verduras durante la deshidratación con aire caliente y su susceptibilidad al deterioro microbiano
E. M. Ceballos-Ortiz* y M. T. Jiménez-Munguía
Departamento de Ingeniería Química, Alimentos y Ambiental, Fundación Universidad de las Américas Puebla. Exhacienda Sta. Catarina Mártir S/N, Cholula, Puebla. C.P.72810. México.
Resumen
Las frutas y verduras son alimentos ampliamente consumidos en el mundo entero y su conservación es necesaria. Debido a esto, se emplean diversas técnicas para su conservación, siendo la deshidratación por aire cliente una de las más utilizadas, ya que es económicamente viable y puede reducir la actividad de agua a un nivel en el cual los microrganismos no se pueden desarrollar. Sin embargo, esta técnica tiene desventajas como la pérdida de nutrimentos en el alimento, así como cambios físicos. Por estas razones es importante una revisión bibliográfica donde se analicen los cambios que ocurren en las propiedades físicas y químicas durante el proceso de deshidratación con aire caliente, así como una breve descripción de técnicas complementarias de deshidratación que pueden ayudar a mejorar la estabilidad de estos alimentos, para que finalmente se puedan obtener productos de alta calidad y con bajo riesgo de degradación microbiana.
Palabras clave: frutas, verduras, deshidratación por aire caliente.
Abstract
Fruits and vegetables are widely consumed in the world and their preservation is required. Different techniques are employed for the preservation of fruits and vegetables and hot air-drying is one of the most commonly used due to its economic viability and the advantages in the water activity reduction to an appropriate level where microbial growth is suppressed, however, this technique has various disadvantages such as the loss of some nutrients and undesirable physical changes. For these reasons, in this review it is analyzed the chemical and physical changes that occur during hot air drying, as well as a brief description of complementary drying techniques that can help improve the product stability in aim to obtain high quality products with low risk of microbial degradation.
Keywords: fruit, vegetables, hot air drying.
Introducción
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Las frutas y verduras son una fuente importante e indispensable de vitaminas y minerales para el ser humano. Su cultivo a gran escala constituye un sector importante de la economía de muchos países. Su consumo cada día está en aumento, por lo que se requieren mejores procesos de conservación para lograr prolongar su vida de
Dirección electrónica: edgar.ceballosoz@udlap.mx
almacenamiento. Además, este tipo de alimentos escasea en ciertas épocas del año, por lo que cuando son abundantes en el mercado conviene darles un tratamiento o transformación que permita conservarlos por un periodo mayor, para que puedan ser consumidos en épocas de escasez.
El agua contenida en las frutas y verduras representa más del 80% de su peso, lo cual es un factor determinante para su pronta descomposición microbiana. Se estima que en los países en vías de desarrollo, alrededor del 30 a 40% de las frutas y verduras cultivadas, se llega a perder debido a la falta de un adecuado manejo, transporte y almacenamiento; estas pérdidas se traducen en una pérdida física, nutrimental y por lo tanto, económica.
Para preservar las frutas y verduras se han empleado varias tecnologías a escala industrial, entre las cuales está la deshidratación con aire caliente (Hernández et al., 2010). Esta técnica da lugar a productos deshidratados con una larga vida de anaquel; sin embargo, este proceso también impacta negativamente la calidad de los alimentos, debido a los prolongados periodos de deshidratación y a las altas temperaturas utilizadas. La calidad de un producto deshidratado convencional es normalmente menor a la del producto fresco del que proviene, con un impacto en el color, la textura y otras características (Askari et al., 2009a). Las frutas y verduras deshidratadas con aire caliente, normalmente llegan a niveles intermedios de humedad, donde los valores de actividad de agua oscilan entre 0.6 y 0.8; a estos niveles, las frutas y verduras normalmente mantienen sus propiedades sensoriales y por lo general muestran una buena resistencia al ataque microbiano (Cao et al., 2007).
La calidad y el costo de las frutas y verduras deshidratadas están influenciados
fuertemente por las condiciones de secado; la calidad se evalúa por la cantidad de degradaciones físicas y bioquímicas que ocurren en el alimento y depende de la temperatura, el tiempo de secado y la actividad de agua que se alcanza (Juárez, 2005).
El estudio de las técnicas y condiciones adecuadas de deshidratación de frutas y verduras, como el secado con aire caliente, es necesario para conocer y minimizar los cambios físicos y químicos ocurridos durante el proceso, así como mantener sus propiedades nutrimentales, sensoriales y de vida de anaquel, y por lo tanto, desarrollar nuevos productos deshidratados, de alta calidad, atractivos a los consumidores y con alto valor nutricional.
Revisión bibliográfica
1. Deshidratación de frutas y verduras
En la deshidratación de frutas y verduras, se aplica calor para evaporar el agua y removerla después de su separación de los tejidos del fruto. La energía debe suministrarse para evaporar el agua y removerla en forma de vapor de la superficie del alimento. El calor se puede aplicar al alimento por conducción, radiación ó convección. Aunque estos tres mecanismos de transferencia de calor se pueden utilizar durante la deshidratación, normalmente, dependiendo del producto, uno de éstos es el que domina. El método más común para transferir el calor a frutas y verduras, en el proceso de deshidratación, es la utilización de una corriente de aire caliente, donde la convección es el principal fenómeno de transferencia. Una vez que el calor es suministrado a la superficie del alimento en el proceso de deshidratación, éste es distribuido a través del alimento por conducción. Esta técnica se puede definir como una operación, en la cual hay una transferencia simultánea de
calor y de masa, en la que la actividad de agua de un material es reducida a través de la remoción de agua por evaporación en una corriente de gas insaturado libre (Costa y Ferreira, 2007).
Los dos aspectos importantes de transferencia de masa durante la deshidratación, son la transferencia del agua del interior del alimento hasta la superficie de éste y la remoción de ésta de la superficie al medio ambiente. Una curva de secado relaciona el contenido de humedad del alimento con el tiempo, donde normalmente hay diversas fases: la primera representa un “periodo de acoplamiento” en donde las condiciones de la superficie del alimento llegan a un equilibrio con el aire caliente; normalmente es un periodo muy corto aunque a veces puede ser significativo. Posteriormente, se encuentra un periodo de velocidad de deshidratación constante y un periodo de velocidad de deshidratación decreciente. Durante el periodo de velocidad de deshidratación constante, el agua está fácilmente disponible en la superficie del producto en proceso de deshidratación y por lo tanto, la velocidad de deshidratación es determinada por la temperatura, la humedad relativa y la velocidad del flujo de aire. Éste es un corto periodo al inicio del proceso de deshidratación en el que la pérdida de agua es rápida. Cuando el alimento pierde la mayoría del agua en su superficie, el agua restante debe difundirse del interior del alimento a su superficie para poder ser evaporada; esto da lugar al periodo de velocidad de deshidratación decreciente, en el que se dificulta la pérdida de agua; este periodo corresponde a las últimas etapas del proceso. En este periodo, el factor limitante no es el suministro de calor, sino la disponibilidad del agua en la superficie donde se lleva a cabo la evaporación. El punto de transición entre el periodo de velocidad de deshidratación constante y el periodo de deshidratación decreciente, se le denomina contenido de
humedad crítico. Por último, en la fase final del periodo a velocidad decreciente, el contenido de humedad correspondiente es llamado contenido de humedad en equilibrio (Diamante et al., 2010). Estos periodos son de gran importancia para lograr un proceso rápido, alimentos deshidratados de alta calidad y asegurar la rentabilidad del proceso. Los principales factores que afectan a la velocidad de deshidratación y el tiempo de secado son las propiedades físicas del aire de secado (temperatura, velocidad y humedad relativa), las características del equipo de secado y las propiedades del alimento (Woodroof y Luh, 1975).
1.1. Proceso de deshidratación en túneles con aire caliente
La deshidratación con aire caliente por medio de túneles es uno de los procesos comerciales más usados en la conservación de productos alimenticios, principalmente de productos agropecuarios (Askari et al., 2009a). El aire es usado para conducir el calor al alimento y para retirar el agua que el alimento libera. Los túneles para la deshidratación de frutas y verduras son de varios tipos pero se basan en las mismas operaciones básicas. Las frutas o verduras son puestas en bandejas o en transportadores y expuestas a una corriente de aire caliente. Los secadores de túnel están clasificados con base en los mecanismos de movimiento de los alimentos y la dirección de la corriente de aire, la cual puede ser paralela o en contracorriente al alimento. Si la corriente de aire es paralela al alimento, las condiciones iniciales para la deshidratación son óptimas, pero conforme el aire remueve la humedad del alimento, la eficacia del aire para deshidratar al alimento decrece. Si el flujo de aire a contracorriente es usado exclusivamente, las condiciones para deshidratar son óptimas en la etapa final del proceso. Normalmente, estas dos direcciones de corriente de aire son combinadas en secadores de dos etapas. La corriente de aire paralela es usada en la
primera etapa y la corriente de aire a contracorriente en la segunda etapa; esto da los mejores resultados en cuanto a eficiencia de secado y calidad final del alimento. Las temperaturas del aire que son usadas dependen del alimento y se encuentran normalmente entre 70 y 90°C en la primera etapa y entre 55 y 70°C en la segunda, lo cual da como resultado un tiempo de deshidratación de 8 a 16 horas (Karmas y Harris, 1988).
Se han realizado diversos estudios acerca de la deshidratación de frutas y verduras para determinar los parámetros adecuados del proceso de deshidratación con aire caliente y optimizar los resultados en cuanto a tiempo, contenido de humedad y conservación de las propiedades de los alimentos. Como ejemplos se encuentran estudios realizados con chile poblano (Mendoza-Medina et al., 2005), chile rojo (Arora et al., 2006), manzana (Meisamiasl et al., 2010), cebolla (García et al., 2010), cereza (Aghbashlo et al., 2008), uvas (Li et al., 2008), peras (González-Martínez et al., 2006), durazno (Kingsly et al., 2007), papas (Hassini y Belghith, 2004) y plátanos (Jannot et al., 2004), entre otros, donde se reducen los tiempos de secado variando las condiciones de temperatura y velocidad de aire de secado para conservar mejor la calidad del producto.
1.2. Combinación de la deshidratación con aire caliente y otros métodos
Aunque la deshidratación con aire caliente es un método económico y efectivo para la obtención de frutas y verduras deshidratadas, se siguen investigando métodos de deshidratación que permitan obtener productos de mejor calidad a menores costos (Aktas et al., 2007).
Recientemente, la deshidratación con microondas ha sido propuesta como un método alternativo a la deshidratación convencional con aire caliente. Sin embargo, debido a su alto costo, no ha podido competir
con la deshidratación con aire caliente, por lo que se ha sugerido utilizarla en las etapas finales de este último proceso. Las ventajas de esta incluyen la reducción de los periodos de deshidratación, el mejoramiento de la calidad del producto, y la flexibilidad de producir una amplia variedad de productos deshidratados (Askari et al., 2009b). Como ejemplo, la deshidratación por microondas redujo el tiempo de secado en más de un 98% comparado con el secado por aire caliente en la deshidratación de dátiles (Benamara y Chekroune, 2009).
De la misma forma, se ha propuesto el uso de pre-tratamientos osmóticos para reducir los tiempos de deshidratación y conservar mejor las propiedades de las frutas y verduras deshidratadas. Haciendo un correcto uso de pre-tratamientos osmóticos se puede reducir considerablemente el tiempo de secado conservando el color, mejorando la textura y protegiendo el contenido de vitaminas y compuestos con alto valor nutricional de las frutas y verduras. Como ejemplos destacan los pre-tratamientos osmóticos en calabaza (Kolawole y Olufemi, 2010), chabacano (Riva et al., 2005), chayote (Ruiz-López et al., 2010), jitomate (Hassan, 2008), papaya (Pandey et al., 2008), pera (GonzálezMartínez et al., 2006) y piña (Nicoleti et al., 2001), donde se reducen los tiempos de secado con aire caliente y se conservan mejor las propiedades de los alimentos. En estudios realizados con trozos de chile poblano, se muestra que se pueden deshidratar parcialmente mediante deshidratación osmótica, reduciendo su peso un 40%; una vez deshidratados con aire caliente, la pérdida total de peso puede llegar hasta 94% (MendozaMedina et al., 2005). Por el contrario, existen estudios en frutas en los que no se han observado mejorías en el producto usando pretratamientos osmóticos, por ejemplo en el color y la textura del caqui (Igual et al., 2011). En el caso de manzanas, se ha notado una pérdida sustancial de ácido ascórbico usando
pre-tratamientos osmóticos, además de no lograr reducción en el tiempo de secado; sin embargo, sí se reduce considerablemente la actividad de agua (aw) de la fruta y se obtiene una mayor aceptación sensorial (Moreira et al., 2009). Los resultados de un estudio realizado por Vega et al. (2005) muestran que cuanto más agresivo es el pre-tratamiento osmótico en pimiento rojo, en cuanto a tiempo y concentración, mayor es la pérdida de vitamina C, menor la capacidad de rehidratación y aumenta el oscurecimiento no enzimático.
También existen procesos ultrasónicos, los cuales están todavía en desarrollo y se necesitan más estudios para comprender completamente los efectos del ultrasonido en el tejido de las frutas y verduras, así como en sus características sensoriales. Los estudios que se han realizado muestran un gran potencial de la aplicación de los tratamientos ultrasónicos para la deshidratación de frutas. Estos tratamientos consisten en sumergir las frutas en un medio líquido el cual puede ser agua o una solución osmótica. Como ejemplos de esta aplicación existen tratamientos aplicados en plátano, manzana, melón, papaya, piña y zapote, los cuales presentan una pérdida significativa de azúcares utilizando agua destilada como medio líquido (Fernandes y Rodrigues, 2008a, 2008b). Así mismo, el efecto del pre-tratamiento ultrasónico muestra un incremento en la difusividad de agua de las frutas en la mayoría de los casos, lo que ayuda a reducir los tiempos de deshidratación en el secado con aire caliente, probablemente debido a la formación de micro túneles tanto en la membrana celular como en la estructura del tejido de las frutas durante el proceso. También se ha estudiado el efecto del pretratamiento con ondas ultrasónicas utilizando un medio osmótico como medio líquido, en el que se ha notado un incremento en la pérdida de agua y ganancia de azúcares durante el proceso del pre-tratamiento. En general, este tipo de pre-tratamiento es viable cuando se
logra incrementar la difusividad del agua en la fruta y, por lo tanto, se disminuye considerablemente el tiempo de secado por aire caliente. Como ejemplos se han obtenido resultados en pruebas con melón, las cuales muestran una reducción en el tiempo de deshidratación con aire caliente del 25% usando un pre-tratamiento con ultrasonido (Fernandes y Rodrigues, 2007); lo mismo ocurre con el zapote, donde el tiempo de deshidratación se ha visto reducido en un 23% (Fernandes y Rodrigues, 2008b).
2. Cambios en las propiedades de frutas y verduras debidos a la deshidratación con aire caliente
La deshidratación con aire caliente da lugar a varios cambios en la estructura y las propiedades químicas de las frutas y verduras, debido a los procesos térmicos y mecánicos a los que son sometidas. De igual forma, la actividad de agua cambia, lo que da como resultado un cambio en el comportamiento de las reacciones oxidativas, enzimáticas, no enzimáticas, de oscurecimiento y caramelización, entre otras. Así mismo, la deshidratación causa cambios en las propiedades físicas como colapso, apelmazamiento y cambios en la densidad y viscosidad del producto (Maltini et al., 2003). En general, el proceso de deshidratación ofrece una buena retención de nutrientes con excepción del ácido ascórbico y beta caroteno. Las pérdidas de proteínas y deterioros en su calidad son mínimas y de vitaminas hidrosolubles, sin contar el ácido ascórbico, por lo general son del 5% (Karmas y Harris, 1988).
2.1. Cambios en las propiedades físicas de frutas y verduras deshidratadas con aire caliente
Las propiedades físicas son las más afectadas en los procesos de deshidratación con aire caliente, debido a los prolongados periodos de
exposición de la muestra y al uso de altas temperaturas. El color es una de las propiedades más importantes en las frutas y verduras, ya que es el primer atributo de calidad evaluado por los consumidores, además de ser un parámetro utilizado para determinar la vida útil de las frutas y verduras deshidratadas (Iciek y Krysiak, 2009). La forma de evaluar los cambios de color causados por efectos de oscurecimiento en frutas y verduras deshidratadas es midiendo la disminución de la luminosidad (cambio en el parámetro L en la escala de Hunter), así como el cambio de la cromaticidad rojo – verde y azul – amarillo (parámetros a y b en la escala de Hunter). Las reacciones no enzimáticas asociadas con la pérdida de color en las frutas y verduras deshidratadas básicamente son las reacciones de Maillard, las reacciones de oxidación como la conversión de polifenoles en policarbonilos y la degradación oxidativa del ácido ascórbico; además, las reacciones de degradación de pigmentos como los carotenoides (oxidación por oxígeno), la clorofila (cambia de colores verdes a amarillos y rojos), antocianinas y betalaínas (cambian a compuestos oscuros) afectan el color durante la deshidratación (Cortés y Chiralt, 2008; Jangam et al., 2010).
En la deshidratación de jitomate con aire caliente hay cambios de color no deseados. El incremento en la temperatura y el tiempo de deshidratación provocan oscurecimiento del tejido; el color rojo del jitomate se torna en un color rojo-café durante la deshidratación y después se torna completamente café, esto es debido a una combinación de oscurecimiento no enzimático y degradación del licopeno; la degradación del color es menos severa cuando la temperatura de deshidratación es reducida de 90 a 55°C (Kerkhofs et al., 2005). En pruebas con dátiles se encontró que el cambio neto de color se incrementa con el aumento del tiempo de deshidratación con aire caliente (Benamara y Chekroune, 2009). Estos resultados concuerdan con lo obtenido con
varios métodos de deshidratación para la concentración de jugo de granada. El cambio de color observado puede ser debido a la alta concentración de azúcares en la fruta, tomando en cuenta la habilidad de estos compuestos para formar compuestos oscuros responsables de la alteración del color (Benamara y Chekroune, 2009).
En otro estudio realizado, los valores de luminosidad (L) están reportados en función del aumento de la velocidad de aire y de la temperatura de deshidratación para rebanadas de naranja. La velocidad de aire está mayormente correlacionada con el oscurecimiento de las muestras (valores de L más pequeños) para cualquier temperatura de secado (de 65 a 87°C). Esto puede deberse a los largos periodos de tratamiento de la muestra y al favorecimiento de la reacción de Maillard por las altas temperaturas, así como a la oxidación de los pigmentos de la naranja, probablemente causada por condiciones de oxígeno forzado (De Pilli et al., 2008).
En cuanto a la textura, existe un colapso en la estructura de las frutas y verduras deshidratadas debido a la remoción del agua y a un desbalance en la presión producida entre la parte interna y externa del material del alimento causando encogimiento, deformación, cambios en la porosidad y algunas veces, fractura. Durante el proceso de deshidratación, las frutas y verduras pierden agua y su volumen es reducido proporcionlamente al volumen correspondiente de agua perdida; sin embargo, no siempre es el caso debido a que el encogimiento causado por la pérdida de agua está altamente influenciado por las condiciones del proceso, principalmente en las etapas iniciales de deshidratación. En estudios realizados por Boubekri et al. (2010) con dátiles se encontró una alta correlación entre la textura y el contenido de agua, donde se incrementa la firmeza linealmente con la pérdida de agua. Existen estudios similares
que evalúan el cambio en las características físicas de cebolla (García et al., 2010), pera (Ling et al., 2005) y jitomate (Askari et al., 2009a), donde se obtuvieron resultados parecidos.
La reducción de agua en las frutas y verduras deshidratadas induce a una reducción en la movilidad de sólidos, lo que produce un aumento en la viscosidad del alimento (Katekawa y Silva, 2007), sin embargo estudios realizados por Boubekri et al. (2010) muestran que temperaturas de secado superiores a 60°C en frutas con cáscara cerosa, inducen a una disolución de una cantidad significante de azúcares, reduciendo la viscosidad e incrementando la movilidad del agua, lo que resulta en la reducción significante del tiempo de secado.
Por otro lado, se han obtenido valores experimentales para la densidad real, densidad aparente y porosidad respecto al contenido de humedad de champiñón, pimiento verde, calabacín, espinaca, apio, puerro, cebolla, jitomate, ajo, zanahoria, chícharo y maíz. La densidad real se incrementa conforme el contenido de agua decrece, lo cual es esperado debido a que conforme el agua es removida, la densidad real alcanza el valor de la densidad del vegetal deshidratado. La densidad aparente oscila entre los valores de la densidad del agua y la densidad del vegetal completamente seco; como resultado, el valor de la densidad aparente a un alto contenido de humedad se aproxima a la densidad del agua, mientras que a bajos contenidos de humedad tiende a acercarse a los valores de densidad del vegetal completamente seco. En cuanto a la porosidad, ésta se incrementa con la remoción del contenido de humedad, debido a que depende solamente de la variación de la densidad aparente y la densidad verdadera (Boukouvalas et al., 2010).
2.2. Degradación de compuestos químicos en frutas y verduras deshidratadas con aire caliente
Existen diversos estudios que evalúan la estabilidad de los compuestos químicos y nutricionales durante la deshidratación de frutas y verduras usando aire caliente, siendo el ácido ascórbico el compuesto más estudiado debido a su amplia distribución en este tipo de alimentos y su importancia nutricional.
El ácido ascórbico es susceptible a diferentes factores. En el proceso de deshidratación por aire caliente las pérdidas de ácido ascórbico se deben principalmente a las altas temperaturas utilizadas, además de la exposición al oxígeno contenido en el aire de secado. El tiempo es otro factor importante para la degradación del ácido ascórbico, ya que en las primeras horas no se observa una disminución considerable, por lo que el empleo de tiempos cortos y temperaturas bajas en el proceso de deshidratación con aire caliente, pueden ayudar a retener el ácido ascórbico (Gómez, 2009). Munyaca et al. (2010) mostraron que la enzima ácido ascórbico oxidasa juega un papel importante en la pérdida de ácido ascórbico en las fases iniciales de deshidratación. También se han reportado pérdidas de ácido ascórbico en muestras de rebanadas de naranja al aumentar la velocidad de aire y temperatura de deshidratación, siendo éstas hasta del 47% (De Pilli et al., 2008), así como pérdidas sustanciales de ácido ascórbico en la deshidratación de higos, debido al decremento del pH (Piga et al., 2004). Goula y Adamopoulos (2006) reportaron pérdidas de ácido ascórbico del 95%, durante la producción de mitades de jitomate deshidratado y pulpa de jitomate, empleando jitomate de diversas variedades, usando altas temperaturas (110°C). En un estudio realizado por Kerkhofs et al. (2005) utilizaron una temperatura de deshidratación de 42°C durante
48 horas encontrando una pérdida de ácido ascórbico hasta del 75%.
Las altas temperaturas utilizadas en la deshidratación de frutas y verduras pueden ocasionar una degradación de los compuestos fenólicos, mientras los carotenoides son prácticamente degradados por la alta exposición al oxígeno (Madrau et al., 2009).
Kerkhofs et al. (2005) evaluaron el cambio en la capacidad antioxidante en jitomates deshidratados y reportaron pérdidas del 8 al 33% a una temperatura de secado de 42°C debido a la degradación de los compuestos fenólicos, ácido ascórbico y carotenoides lipofílicos, responsables principalmente de la actividad antioxidante en las frutas y verduras. Por el contrario, Rózek et al. (2008) demostraron que la deshidratación de frutas y verduras con aire a 40°C, no tiene un efecto significativo en los compuestos fenólicos. En la deshidratación de chabacanos, la capacidad antioxidante incrementa con el proceso de deshidratación; en ciruelas ocurre algo similar a pesar de que las altas temperaturas utilizadas en el proceso de deshidratación reducen significativamente el contenido de polifenoles y ácido ascórbico (Madrau et al., 2009). Kerkhofs et al. (2005) proponen utilizar una temperatura de deshidratación de 80°C o mayor durante un periodo corto (15 minutos) para que se desnaturalicen las enzimas oxidativas de los compuestos fenólicos y para liberar los compuestos fenólicos enlazados al tejido del fruto, de forma que se beneficie la calidad nutricional del alimento. Los mismos autores mostraron un mayor contenido de licopeno extraíble en jitomates deshidratados comparado con jitomates frescos, donde se observó que una temperatura media de secado (42°C) permite la liberación del licopeno de los tejidos.
En cuanto a los cambios ocurridos en azúcares, se han realizado estudios en la deshidratación de dátiles a una temperatura de 60°C durante 6 horas, donde no se observó una
variación significativa de azúcares; sin embargo, sí una conversión de sacarosa en azúcares reductores (glucosa y fructosa), donde se observa que el contenido total de azúcares no se pierden por reacciones de oxidación (Boubekri et al., 2010). En litchi deshidratado se han observado pocos cambios en la cantidad de sólidos solubles totales, acidez titulable y pH; en cambio, la actividad de la enzima polifenol-oxidasa decrece y la cantidad de compuestos fenólicos totales permanece estable (Aquino et al., 2010).
Las proteínas sufren desnaturalización con el aumento de la temperatura de secado, pueden ser susceptibles a oxidación debido a la luz y sufrir degradación enzimática. Además, los lípidos pueden sufrir hidrólisis enzimática en las etapas iniciales de deshidratación y a valores bajos de actividad de agua, puede ocurrir una auto-oxidación de ácidos grasos insaturados causando rancidez. La vitamina A, tiamina, riboflavina y niacina muestran una mínima degradación. Sin embargo, el contenido de fibra, minerales y aporte calórico, permanecen constantes durante la deshidratación de frutas y verduras con aire caliente (Jangam et al., 2010).
3. Estabilidad microbiana de frutas y verduras deshidratadas con aire caliente
La calidad microbiológica de las frutas y verduras deshidratadas depende fundamentalmente de la contaminación inicial proveniente de las frutas y verduras frescas, del método de deshidratación, de las condiciones de operación durante el deshidratado y de los tratamientos especiales realizados en las frutas y verduras antes y después del secado. Normalmente, a pesar de la suma de estos factores, no es probable encontrar una considerable carga microbiana en las frutas y verduras deshidratadas. Aunque durante el proceso de deshidratación se puede producir una reducción notable del número de microorganismos viables de diversas especies
microbiológicas, existen algunas que son altamente resistentes al proceso de deshidratación y son capaces de sobrevivir, aportando una cantidad importante de microrganismos al producto final. En general, los microorganismos más resistentes son las esporas bacterianas y fúngicas, algunos micrococos y las micobacterias. Es importante tener en cuenta que el uso de la deshidratación como método para preservar las frutas y verduras, está basado en la prevención del desarrollo de microorganismos deteriorativos del producto y de microrganismos patógenos (Fuselli et al., 2004).
Los principales microorganismos que contribuyen a los daños de frutas y verduras y por lo tanto, indicadores del deterioro de las frutas y verduras deshidratadas en general, son una gran variedad de bacterias y hongos (mohos y levaduras). Entre los microrganismos patógenos que se pueden encontrar en frutas y verduras deshidratadas están Clostridium perfringens, Bacillus cereus y Salmonella spp. (Stannard et al., 1997). Cada microrganismo tiene una temperatura óptima para su crecimiento y necesita de una cantidad mínima de agua para su desarrollo. El crecimiento microbiano en frutas y verduras resulta en la pérdida de características sensoriales, nutricionales y daños físicos causando que el alimento pierda su calidad (Jangam et al., 2010).
En un estudio realizado por García et al. (2010), se analizó la influencia de la temperatura de secado en la supervivencia de microorganismos en cebolla con diferentes tipos de microrganismos (bacterias aerobias mesofílicas, bacterias aerobias mesofílicas esporuladas, coliformes y mohos y levaduras). Estos microrganismos mostraron comportamientos distintos durante la deshidratación del alimento y en su supervivencia, dependiendo de la temperatura de secado; las bacterias aerobias mesofílicas y los coliformes decrecieron significativamente
con el aumento de la temperatura de deshidratación, sin embargo, a una temperatura de deshidratación de 50°C mostraron un incremento, por lo que a esta temperatura no son inactivadas. Las bacterias aerobias mesofílicas esporuladas y los mohos y levaduras, aunque también mostraron un decremento con el aumento en la temperatura, éste no fue significativamente importante.
La actividad de agua en las frutas y verduras deshidratadas juega un papel muy importante, debido a que ésta es de gran importancia para la estabilidad y para el desarrollo de microrganismos. Existe un valor crítico de actividad de agua a partir del cual los microorganismos no se pueden desarrollar; este valor es de aproximadamente 0.6. La mayoría de las bacterias patógenas dejan de crecer a un valor de actividad de agua de 0.85, mientras la mayoría de mohos y levaduras son más tolerantes a valores más bajos dejando de crecer a valores de actividad de agua de 0.62. Los alimentos deshidratados con una actividad de agua menor a 0.6, son microbiológicamente estables; la vida útil de estos alimentos no está limitada por el deterioro microbiano, siempre y cuando permanezcan secos. Las frutas y verduras mínimamente deshidratadas, así como las de humedad intermedia, normalmente tienen una actividad de agua mayor a 0.6, por lo que es necesario que sean conservadas combinando factores como pH reducido y algún tipo de conservador, debido a que normalmente se almacenan a temperatura ambiente (Rahman, 2009). Como ejemplo de la importancia de la actividad de agua, se realizó un estudio en el que se reportó una actividad de agua de 0.61 a 0.63 en higos deshidratados, lo que está por debajo de los niveles óptimos de crecimiento de Aspergillus flavus y A. parasiticus. El crecimiento de estos mohos se pudo apreciar en el fruto fresco, mientras que en el producto deshidratado ya no hubo crecimiento (Piga et al., 2004).
Existen otros estudios donde se analiza el comportamiento de la actividad de agua con la deshidratación de frutas y verduras para predecir su estabilidad en cuanto al deterioro microbiológico. Entre ellos están los realizados en dátiles (Chukwu, 2010), chabacano, manzana (Maltini et al., 2003), nopal (Fernández et al., 2006), así como plantas de la especie Brassica parachinensis (Cao et al., 2007).
Conclusiones
La deshidratación es una de las técnicas más antiguas y más utilizadas en la conservación de frutas y verduras debido a su amplio consumo, a su producción restringida a ciertas temporadas del año y a su alto contenido de humedad. La deshidratación por aire caliente es la técnica más utilizada para conservar este tipo de alimentos, sin embargo presenta desventajas como la pérdida nutricional del producto y el deterioro físico del mismo. En consecuencia, se han propuesto diversas técnicas de deshidratación complementarias para conservar las frutas y verduras como pretratamientos con soluciones osmóticas, deshidratación asistida por microondas o el empleo de ondas ultrasónicas. Aunque estas técnicas complementarias están siendo estudiadas, la deshidratación por aire caliente es el método mayormente utilizado. La calidad de las frutas y verduras deshidratadas se puede medir por la conservación y estabilidad de sus propiedades químicas y físicas durante el proceso de secado. Para obtener frutas y verduras deshidratadas de alta calidad, es necesario minimizar los tiempos de exposición a altas temperaturas de secado, así como utilizar temperaturas y velocidades de aire bajas de forma que se eviten reacciones químicas de degradación de compuestos que a su vez repercuten en cambios físicos indeseables en los productos. Es muy importante tomar en cuenta que el uso de bajas
temperaturas y velocidades de aire puede ocasionar una activación o aceleración de reacciones indeseadas como reacciones enzimáticas o crecimiento microbiano, por lo que es de suma importancia el estudio de las condiciones adecuadas de deshidratación para llegar a un equilibrio donde se puedan obtener productos estables y de alta calidad, dependiendo de las propiedades que se necesiten mantener y la naturaleza del alimento. De la misma forma, se debe considerar la reducción de la actividad de agua en frutas y verduras deshidratadas a un nivel adecuado, para así evitar el deterioro posterior del producto causado por el crecimiento de microrganismos deteriorativos.
Agradecimientos
E. M. Ceballos-Ortiz agradece al Consejo Nacional de Ciencia y Tecnología (CONACYT) y a la Universidad de las Américas Puebla (UDLAP), por el apoyo y financiamiento de sus estudios de posgrado.
Referencias
Aghbashlo, M., Kianmehr, M. y Hassan-Beygi, S. 2008. Drying and rehydration characteristics of sour cherry (Prunus Cerasus L.). Journal of Food Processing and Preservation. 34: 351 – 365.
Aktas, T., Fuji, S., Kawano, Y. y Yamamoto, S. 2007. Effects of pretreatments of sliced vegetables with trehalose on drying characteristics and quality of dried products. Food and Bioproducts Processing. 85(C3): 178 – 183.
Aquino, E., Corona, R., Villegas, A., Reyes, I., Guemes, N., Hernández, y A. Mercado, E. 2010. Effect of storage temperature and time on quality in minimally processed litchi fruit (Litchi Chinensis Sonn). Journal of Food Quality. 33: 299 – 311.
Arora, S., Bharti, S. y Sehgal, V. 2006. Convective drying kinetics of red chillies. Drying Technology 24: 189 – 193.
Askari, G., Emam-Djomeh Z. y Tahmasbi, M. 2009a. Effect of various drying methods on texture and color of tomato halves. Journal of Texture Studies 40: 371 – 389.
Askari, G., Emam-Djomeh, Z. y Mousavi, S. 2009b. An investigation of the effects of drying methods and conditions on drying characteristics and quality attributes of agricultural products during hot air and hot air/microwave-assisted dehydration. Drying Technology. 27: 831 – 841.
Benamara, S. y Chekroune, M. 2009. Colour change during hot air and microwave complementary dehydration of naturally dried date (Phoenix dactylifera L.) fruits. 2009. World Journal of Dairy and Food Sciences. 4(1): 8 – 13.
Boubekri, A., Benmoussa, H., Courtois, F. y Bonazzi, C. 2010. Softening of overdried “Deglet nour” dates to obtain high-standard fruits: Impact of rehydration and drying processes on quality criteria. Drying Technology. 28: 222 – 231.
Boukouvalas, Ch., Bisharat, G. y Krokida, M. 2010. Structural properties of vegetables during air drying. International Journal of Food Properties. 13: 1393 – 1404.
Cao, H., Zhang, M., Mujumdar, A., Xiao, G. y Sun, J. 2007. Study on reduction of water activity and storage stability for dehydrated Brassica parachinensis with intermediate moisture. Drying Technology. 25: 669 – 674.
Chukwu, O. 2010. Moisture-sorption study of dried date fruits. AU Journal of Technology. 13(3): 175 – 180.
Cortés, M. y Chiralt, A. 2008. Cinética de los cambios de color en manzana deshidratada por aire fortificada con vitamina E. Revista de la Facultad de Química Farmacéutica. Universidad de Antioquia, Medellín, Colombia. 15(1): 8 – 16.
Costa, A. y Ferreira, S. 2007. Sistema de secado solar para frutos tropicales. Información Tecnológica. 18(5): 49 – 58.
De Pilli, T., Lovino, R., Maenza, S., Derossi, A. y Severini, C. 2008. Study on operating conditions of
orange drying processing: Comparison between conventional and combined treatment. Journal of Food Processing and Preservation. 32: 751 – 769.
Diamante, L., Durand, M., Savage, G. y Vanhanen, L. 2010. Effect of temperatura on the drying characteristics, colour and ascorbic acid content of green and gold kiwifruits. International Food Research Journal. 17: 441 – 451.
Fernandes, F. y Rodrigues, S. 2007. Use of ultrasound as pretreatment for dehydration of melons. Drying Technology. 25: 1791 – 1796.
Fernandes, F. y Rodrigues, S. 2008a. Application of ultrasound and ultrasound-assisted osmotic dehydration in drying of fruits. Drying Technology. 26: 1509 – 1516.
Fernandes, F. y Rodrigues, S. 2008b. Dehydration of sapota (achras sapota L.) using ultrasound as pretreatment. Drying Technology. 26: 1232 – 1237.
Fernández, J., Alvarez, C. y Velásquez, M. 2006. Isotermas de sorción de mucílago de nopal (Opuntia ficus-indica (L.) Mill.) deshidratado. Ciencia y Tecnología de Alimentos 16(3): 34 – 37.
Fuselli, S., Filsinger, B., Fritz, R. y Yeannes, M. 2004. Estudio microbiológico de ajo (Allium sativum L.) y cebolla (Allium cepa L.) deshidratados. Revista Argentina de Microbiología. 36: 139 – 144.
García, S., Brumovsky, L., Fretes, R. y Schmalko, M. 2010. Influence of drying temperature on the physical and microbiological parameters and the quality of dried green onion. Drying Technology. 28: 1435 – 1444.
Gómez, M. 2009. Deshidratado de tomate saladette en un secador de charolas giratorias. Tesis de Licenciatura. Universidad Tecnológica de la Mixteca. Oaxaca, México. 76 p.
González-Martínez, C., Cháfer, M., Xue, K. y Chiralt, A. 2006. Effect of the osmotic pre-treatment on the convective air drying kinetics of pear var. blanquilla. International Journal of Food Properties. 9: 541 –549.
Goula A. y Adamopoulos, K. 2006. Retention of ascorbic acid during drying of tomato halves and tomato pulp. Drying Technology. 24: 57 – 64.
Hassan, N. 2008. Drying kinetics of osmotically-treated tomatoes. Misr Journal of Agricultural. Engineering. 25(3): 957 – 979.
Hassini, L. y Belghith, A. 2004. Estimation of the moisture diffusion coefficient of potato during hotair drying. Proceedings of the 14th International Drying Symposium. Sao Paulo, Brazil. 22 – 25 Agosto 2004.
Hernández, J., Quinto, P., Flores, F., Acosta, R. y Aguilar, J. 2010. Cinética del secado de productos agrícolas. Memorias del XII Congreso Nacional de Ingeniería Electromecánica y de Sistemas. México Distrito Federal, México. Noviembre 2010.
Iciek, J. y Krysiak, W. 2009. Effect of air parameters on the quality of dried potato cubes. Drying Technology. 27: 1316 – 1324.
Igual, M., Castelló, M., Roda, E. y Ortolá, M. 2011. Development of hot-air dried cut persimmon. International Journal of Food Engineering. 7(5): Art. 9
Jangam, S. Law, C. y Mujumdar, A. 2010. Drying of Food, Vegetables and Fruits, Volume 1, ISBN: 978981-08-6759-1.
Jannot, Y., Talla, A., Nganhou, J. y Puiggali, J. 2004. Modeling of banana convective drying by the drying characteristic curve (DDC) method. Drying Technology. 22: 1949 – 1968.
Juárez, E. 2005. Uso de la energía solar en deshidratación de frutas y verduras. Memorias del Primer Congreso Regional de Enseñanza y Divulgación de la Ciencia y la Técnica. Puebla, Puebla, México. 23 – 25 Junio 2005.
Karmas, E. y Harris, R. 1988. Nutritional evaluation of food processing. Tercera edición. The AVI Publishing Company, Inc. Nueva York, Estados Unidos. 786.
Katekawa, M. y Silva, M. 2007. On the influence of glass transition on shrinkage in convective drying of fruits: a case study of banana drying. Drying Technology. 25: 1659 – 1666.
Kerkhofs, N., Lister, C. y Savage, G. 2005. Change in colour and antioxidant content of tomato cultivars following forced-air drying. Plant Foods for Human Nutrition. 60: 117 – 121.
Kingsly, R., Goyal, R., Manikantan, M. y Ilyas, S. 2007. Effects of pretreatments and drying air temperature on drying behavior of peach slice. International Journal of Food Science and Technology. 42: 65 –69.
Kolawole, F. y Olufemi, S. 2010. Effect of pretreatments on air-drying pattern and color of dried pumpkin (cucurbita maxima) slices. Journal of Food Processing Engineering. 33: 1129 – 1147.
Li, L., Wang, Z., Hu, X., Wu, J., Liao, X., Chen, F. y Zhao, G. 2008. Drying effects of two air-drying shelters in a pilot test on sultana grapes. Journal of Food Process Engineering. 33: 162 – 178.
Ling, H., Birch, J. y Lim, M. 2005. The glass transition approach to determination of drying protocols for colour stability in dehydrated pear slices. International Journal of Food Sciences and Technology. 40: 921 – 927.
Madrau, M., Piscopo, A., Sanguinetti, A., Del Caro, A., Poiana, M., Romeo, F. y Piga, A. 2009. Effect of drying temperature on polyphenolic content and antioxidant activity of apricots. European Food Research and Technology. 228: 441 – 448.
Maltini, E., Torreggiani, D., Venir, E. y Bertolo, G. 2003. Water activity and the preservation of plant foods. Food Chemistry. 82: 79 – 86.
Meisami-asl, E., Rafiee, S., Keyhani, A. y Tabatabaeefar, A. 2010. Determination of suitable thin layer drying curve model for apple slices (variety-Golab). Plant Omics Journal. 3(3): 103 –108.
Mendoza-Medina, J., Martínez-Soto, G., MercadoFlores, J., López-Orozco, M. y Alcántara-González, M. 2005. Cinética de los parámetros de calidad de chile poblano durante su deshidratación. Memorias del V Congreso Iberoamericano de Ingeniería de Alimentos (CIBIA V). Puerto Vallarta, Jalisco, México. 4 – 7 Septiembre 2005.
Moreira, P., Abbas, A., Valeriano, R., Kurozawa, L., Colato, G., Xidieh, E. y Jin, K. 2009. Effect of osmotic dehydration on the drying kinetics and quality of cashew apple. International Journal of Food Science and Technology. 44: 980 – 986.
Munyaca, A., Makule, E., Oey, I., Van Loey, A. y Hendrickx, M. 2010. Thermal stability of L-ascorbic
acid and ascorbic acid oxidase in broccoli (Brassica oleracea var. italica). Journal of Food Science 75(4): 336 – 340.
Nicoleti, J., Telis-Romero, J. y Telis V. 2001. Airdrying of fresh and osmotically pre-treated pineapple slices: fixed air temperature versus fixed slice temperature drying kinetis. Drying Technology. 19(9): 2175 – 2191.
Pandey D., Verma, R. y Chahar, V. 2008. Effect of pretreatments on air drying of papaya cubes. International Journal of Food Engineering. 4(5): Art 6.
Piga, A., Pinna, I., Ozer, K., Agabbio, M. y Aksoy, U. 2004. Hot air dehydration of figs (Ficus carica L.): drying kinetics and quality loss. International Journal of Food Science and Technology. 39: 793 –799.
Rahman, M. 2009. Food stability beyond wáter activity and glass transition: macro-micro region concept in the state diagram. International Journal of Food Properties. 12: 726 – 740.
Riva, M., Campologno, S., Avitabile, A., Maestrelli, A. y Torreggiani, D. 2005. Structure-property relationships in osmo-air-dehydrated apricot cubes. Food Research International. 38: 533 – 542.
Rózek, A., Achaerandio, I., Güell, C., López, F. y Ferrando, M. 2008. Efecto del secado convectivo en
– 1 (2012): 98 - 110
la estabilidad de compuestos fenólicos añadidos a alimentos sólidos mediante deshidratación osmótica. Memorias del II Congreso Iberoamericano sobre Seguridad Alimentaria y el V Congreso Español de Ingeniería en Alimentos. Barcelona, España. 5 – 7 de Noviembre 2008.
Ruiz-López, I., Huerta-Mora, I., Vivar-Vera, M., Martínez-Sánchez., C. y Herman-Lara, E. 2010. Effect of osmotic dehydration on air-drying characteristics of chayote. Drying Technology. 28: 1201 – 1212.
Stannard, C., Bell, C., Greenwood, M., Hooker, J., Kyriakides, A. y Mills, R. 1997. Development and use of microbiological criteria for foods. Food Science and Technology Today. 11(3): 1997.
Vega, A., Andrés, A. y Fito, M. 2005. Aplicación de un tratamiento osmótico previo al secado por aire caliente del pimiento. Memorias del V Congreso Iberoamericano de Ingeniería de Alimentos (CIBIA V). Puerto Vallarta, Jalisco, México. 4 – 7 Septiembre 2005.
Woodroof, J. y Luh, B. 1975. Commercial fruit processing. Westport, Connecticut. The AVI Publishing Company, Inc. California, Estados Unidos. 710.

Contenido
Volumen 6 / No. 1 Ene – Mayo 2012
Cuerpo editorial
Artículos de Revisión

Queso Oaxaca: panorama del proceso de elaboración, características fisicoquímicas y estudios recientes de un queso típico mexicano
S. Ramírez-Nolla* y J. F. Vélez-Ruíz
Proceso de elaboración y propiedades fisicoquímicas de las leches condensada azucarada y evaporada
M. Marcelín-Rodríguez* y J. F. Vélez-Ruíz …………………………………………….… 13
Vapores de aceites esenciales: alternativa de antimicrobianos naturales
F. Reyes-Jurado*, E. Palou y A. López-Malo …………………………………………….. 29
El jitomate (Solanum lycopersicum): aporte nutrimental, enfermedades postcosecha y tecnologías para su almacenamiento en fresco
C. M. Notario-Medellín* y M. E. Sosa-Morales
Propiedades del aceite esencial de albahaca (Ocimum basilicum L.) y sus aplicaciones en alimentos
G. A. Cardoso-Ugarte* y M. E. Sosa-Morales
Emulsiones simples y múltiples de compuestos bioactivos
B. Contreras-Reyes* y M. T. Jiménez-Munguía
Combinación de ultrasonido de baja frecuencia con factores convencionales y/o emergentes como método de inactivación de microrganismos en alimentos
A. Franco-Vega*, E. Palou y A. López-Malo
Biopolímeros utilizados en la encapsulación
A. García-Ceja* y A. López-Malo
Cambios en las propiedades de frutas y verduras durante la deshidratación con aire caliente y su susceptibilidad al deterioro microbiano
E. M. Ceballos-Ortíz* y M. T. Jiménez-Munguía

Departamento de Ingeniería Química, Alimentos y Ambiental Derechos Reservados 2011
