

Temas Selectos de Ingeniería de Alimentos














Volumen 5/ No. 2
DIRECTORIO
TEMAS SELECTOS DE INGENIERÍA DE ALIMENTOS
UNIVERSIDAD DE LAS AMÉRICAS PUEBLA
PUBLICACIÓN SEMESTRAL
VOLUMEN 5, NÚMERO 2 (AGOSTO-DICIEMBRE 2011)
EDITORA RESPONSABLE
María Eugenia Bárcenas Pozos
CONSEJO EDITORIAL
Aída Irma Gómez Sánchez
María Teresa Jiménez Munguía
Emma Mani López
María Elena Sosa Morales
Fidel Tomás Vergara Balderas
CERTIFICADO DE RESERVA DE DERECHOS:
04-2010-080615025900-102
CERTIFICADO DE LICITUD DE TÍTULO Y CONTENIDO: 15430
DOMICILIO:

Fundación Universidad de las Américas Puebla
Exhacienda Santa Catarina Mártir S/N
San Andrés Cholula, Pue.
C.P. 72810 México
Teléfono: 222 229 2126
DISTRIBUIDO POR:
Departamento de Ingeniería Química, Alimentos y Ambiental
Fundación Universidad de las Américas Puebla
IMPRESIÓN:
Gutiérrez Mora Carina
18 Sur 6130 Local A. Col. Jardines San Manuel
Puebla, Pue. C.P. 72570

Temas Selectos de Ingeniería de Alimentos Vol. 5 / No. 2

Cuerpo editorial
Dra. María Eugenia Bárcenas Pozos
Dra. María Teresa Jiménez Munguía
Dra. Emma Mani López
M. C. Fidel Vergara Balderas

Temas Selectos de Ingeniería de Alimentos Vol. 5 / No. 2

Cuerpo editorial
Dra. María Eugenia Bárcenas Pozos
Dra. María Teresa Jiménez Munguía
Dra. Emma Mani López
M. C. Fidel Vergara Balderas

Contenido
Temas Selectos de Ingeniería de Alimentos Vol. 5 / No. 2

Volumen 5 / No. 2 Ago – Dic 2011
Cuerpo editorial …………………………………………………………………………………..
Artículos de Revisión
Envases activos con agentes antimicrobianos y su aplicación en los alimentos
Y. Martínez-Tenorio* y A. López-Malo ………………………………………………… 1
Tecnologías involucradas en el procesamiento mínimo de frutas y hortalizas
E. P. Pérez-Pérez* y A. López-Malo ……………………………………………………... 13
Escherichia coli de tipo patógeno en alimentos y modelación de su inactivación al aplicar diversos factores de conservación
E. Romero*, A. López-Malo y E. Palou ………………………………………………….. 28
Envejecimiento del pan: causas y soluciones
M. Luna-Fernández* y M. E. Bárcenas-Pozos …………………………………………… 40
Producción de café (Coffea arabica L.): cultivo, beneficio, plagas y enfermedades
A. L. Temis-Pérez*, A. López-Malo y M. E. Sosa-Morales ……………………………… 54
Propiedades nutricionales y antioxidantes del maíz azul (Zea mays L.)
A. Castañeda-Sánchez …………………………………………………………..…………. 75
Artículos de Investigación
Efecto del tiempo de almacenamiento y tipo de procesamiento en los antioxidantes de nopal
M. C. Flores-Álvarez*, F. T. Vergara-Balderas y J. A. Guerrero-Beltrán …………… 84

Editorial
Temas Selectos de Ingeniería de Alimentos Vol. 5 / No. 2

Bienvenid@s al más reciente número de la revista Temas Selectos de Ingeniería de Alimentos en la que se publican artículos de revisión sobre los temas de tesis emprendidos por l@s estudiantes del Posgrado en Ciencia de Alimentos de la Universidad de las Américas Puebla. Dichos artículos muestran el trabajo conjunto de nuestr@s estudiantes, sus asesor@s y el cuerpo editorial de la revista.
Entre las metas de nuestros programas de maestría y doctorado en Ciencia de Alimentos, ambos consolidados dentro del Padrón Nacional de Posgrado, se encuentra el contribuir a que nuestr@s egresad@s desarrollen ciertas competencias, entre las cuales resaltan en relación con esta revista, las habilidades de sintetizar y comunicar conocimientos, de pensar crítica y reflexivamente; así como las relacionadas con la comunicación escrita. Los artículos que ustedes leerán en este número permiten a nuestr@s estudiantes demostrar su desarrollo en dichas competencias, además de facilitar a la comunidad universitaria el acceso a los avances más prometedores de la investigación relacionada con ciencia, tecnología e ingeniería de alimentos (así como sus aplicaciones actuales o potenciales en la industria) de una manera fácil de leer, pero escritos de forma seria y sometidos a una rigurosa revisión por pares (arbitraje científico).
Aprovecho este espacio para agradecer y felicitar al cuerpo editorial por su gran dedicación y entusiasmo en el arbitraje, la edición y publicación de esta revista que cada año se consolida más y poco a poco se va convirtiendo en un referente en nuestra comunidad. La calidad de los artículos que se publican en Temas Selectos de Ingeniería de Alimentos debe hacerles sentir orgullos@s de su trabajo.
Enrique Palou
Profesor Departamento de Ingeniería Química, Alimentos y Ambiental Universidad de las Américas Puebla

Temas Selectos de Ingeniería de Alimentos 5 - 2 (2011): 1 - 12

Envases activos con agentes antimicrobianos y su aplicación en los alimento
Y. Martínez- Tenorio* y A. López-Malo Vigil
Departamento de Ingeniería Química, Alimentos y Ambiental, Fundación Universidad de las Américas Puebla. Exhacienda Sta. Catarina Mártir S/N, Cholula, Puebla. C.P.72810. México.
Resumen
En la actualidad los envases tienen un rol muy importante en la conservación, protección y comercialización de los alimentos, es por ello que se han desarrollado nuevas tecnologías que puedan cubrir ciertas funciones que antes no se consideraban como parte del envase, un ejemplo de esto son los envases activos, los cuales son capaces de tener una serie de interacciones con el producto extendiendo la vida de anaquel, manteniendo su calidad y mejorando la seguridad y atributos sensoriales. Los envases con agentes antimicrobianos son un tipo de envase activo con una funcionalidad específica en cuanto a la inhibición o reducción del crecimiento microbiano. Se pueden clasificar dependiendo de su función y el tipo de antimicrobiano añadido. Este tipo de envases se puede aplicar para cualquier tipo de alimentos (cárnicos, lácteos, productos de panificación). El objetivo de este trabajo es realizar una investigación documental acerca de los envases activos con agentes antimicrobianos y sus aplicaciones en los alimentos.
Palabras clave: envase activo, envase antimicrobiano, agentes antimicrobianos.
Abstract
Nowadays, packaging has an important role in food cost, preservation and marketing; therefore new packaging technologies have been developed. Some of these new technologies are focused on properties that were not considered as a function of the package. These new technologies include active packaging, which is capable of interact with the product extending shelf life, maintaining food quality, improving safety and sensory attributes. The antimicrobial packagings are types of active packaging, with specific functionality; they work in the inhibition or reduction of microbial growth. These types of packaging can be classified based on the function and the type of the added antimicrobial. These types of packaging can be applied to any type of food (meat, dairy, baked goods, among many others). The objective of this paper was to make a documentary research about active packaging with antimicrobial agents and their applications in food.
Keywords: active packaging, antimicrobial packaging, antimicrobial agents.
Introducción
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Tradicionalmente las funciones básicas de los envases para alimentos incluyen protección, comunicación, contención y seguridad en el transporte. Además otras funciones han sido mejoradas para un sector en específico de consumidores que demandan productos mínimamente procesados y con menores cantidades de conservadores (Sun Lee et al., 2008).
Dirección electrónica: yanela.martinezto@udlap.mx
El uso correcto de materiales y métodos de envase minimiza las pérdidas y asegura que los alimentos estén en óptimas condiciones para el consumidor. En los últimos años la innovación en envases para alimentos se ha dirigido hacia el desarrollo de nuevas tecnologías que aporten un beneficio adicional, entre estas tecnologías emergentes se encuentran los llamados envases activos e inteligentes redefiniendo algunas de las funciones de los envases (Suppakul et al., 2003).
El concepto de envases activos empezó con el cambio en las funciones de protección al pasar de envases pasivos a activos. Anteriormente los materiales de los envases primarios eran considerados como pasivos, refiriéndose a que su función sólo se limitaba a la protección contra el oxígeno y humedad a través de una barrera inerte, recientemente diversos materiales han sido desarrollados para poder tener una series de interacciones con el producto (Sun Lee et al., 2008).
Un envase activo está definido como un sistema que interactúa positivamente con el producto extendiendo la vida de anaquel y manteniendo su calidad nutrimental y microbiológica, mejorando la seguridad y sus atributos sensoriales (Ozdemir y Floros, 2010).
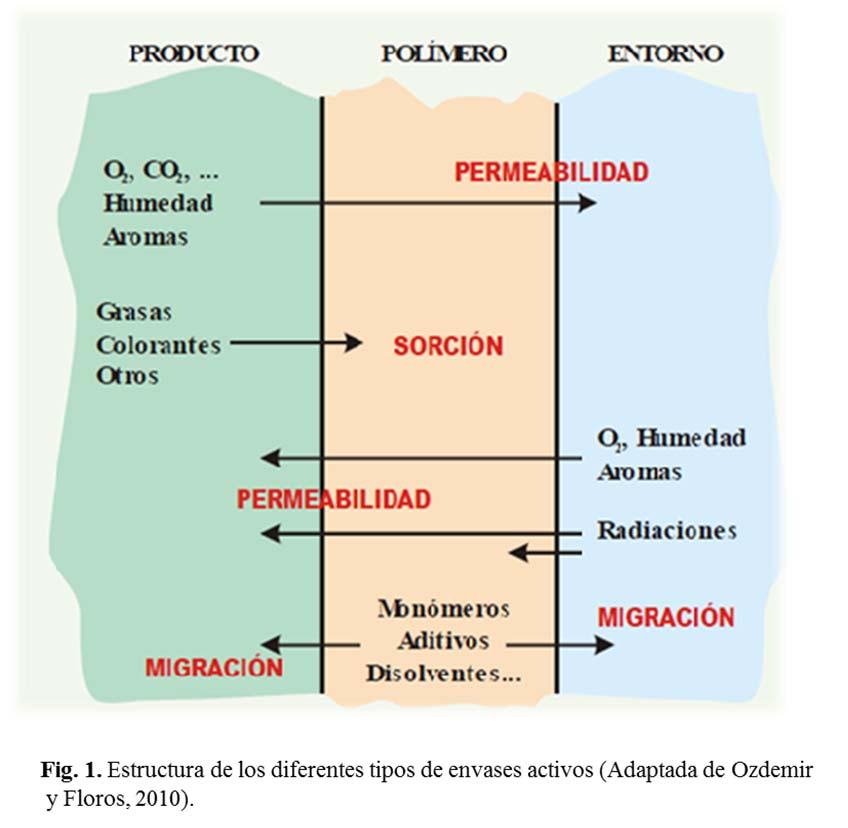
Las tecnologías de envases activos involucran algunas acciones físicas, químicas y biológicas para modificar las interacciones entre el envase, el producto y el espacio de cabeza entre el envase y el producto para alcanzar los resultados deseados. Según el tipo de interacción se dividen en tres principales categorías: sistemas de absorción, sistemas de emisión y otros tipos de sistemas (Sun Lee et al., 2008).
Dentro de los sistemas de emisión se encuentra clasificado un tipo de envase activo que incorpora agentes antimicrobianos en su estructura para evitar el crecimiento indeseable de microorganismos en la superficie del alimento, estos envases son conocidos como envases antimicrobianos (Vermeiren et al., 2002).
Los envases antimicrobianos se basan en el principio de liberar un componente activo a través
del material de envase hasta llegar al alimento, teniendo mayor efectividad que si se le incorporaran estos agentes al producto, debido al control durante la migración de los agentes hacia la superficie del alimento (Jokar et al., 2009).
La liberación controlada de los agentes antimicrobianos del envase a la superficie del alimento ha sido considerada como capaz de inhibir o reducir el crecimiento microbiano utilizando una cantidad mínima de agentes antimicrobianos en comparación con las cantidades necesarias si se incorporan al alimento. Por lo tanto, el control de la migración de los agentes antimicrobianos a través de los materiales del envase es la mejor manera de conferir la actividad antimicrobiana (Sun Lee et al., 2008).
Durante de la última década este tipo de envases ha tenido mucho auge y se han publicado diversos trabajos e investigaciones sobre este tema, es por ello que el objetivo de este trabajo es realizar una investigación documental para describir la funcionalidad de los diferentes tipos de envases activos con antimicrobianos y las posibles aplicaciones que tienen dentro del campo de los alimentos.
Revisión bibliográfica
1. Envases activos
Los envases activos es un sistema inteligente que involucra interacciones entre el envase o los componentes del envase con el alimento o la atmósfera interna de ellos y tienen la propiedad de cambiar sus condiciones con el fin de extender la vida de anaquel y mejorar la seguridad y propiedades sensoriales de los alimentos manteniendo así la calidad del producto envasado (Ozdemir y Floros, 2010).
El objetivo de los envases activos no es sólo incrementar la vida de anaquel del producto, también han tenido un resultado benéfico en la logística y distribución de los productos. Estos beneficios incluyen reducción del desperdicio de los materiales usados como materia prima,
reducción de costos en el producto, mejoras en el manejo, ahorro en el etiquetado, entre otros (Wilson, 2007).
1.1. Tipos y funcionalidad de envases activos
Según Sun Lee et al. (2008) los envases activos se pueden clasificar en tres categorías principales:
Sistemas de absorción: Esta tecnología usa películas o bolsas para remover los gases o substancias indeseadas de los envases, como oxígeno, dióxido de carbón, humedad, etileno y contaminantes, para poder alcanzar una atmosfera interna favorable.
Sistemas de emisión: Esta tecnología añade compuestos deseados, como etanol, dióxido de
carbono, antimicrobianos, antioxidantes, enzimas, sabores y nutraceúticos, para proteger y mejorar la calidad del producto.
Otros sistemas: Estos sistemas incluyen diferentes tareas como auto calentamiento o enfriamiento, indicadores de temperatura, receptor de microondas y películas selectivamente permeables.
La Fig. 1 muestra un diagrama sobre la estructura de los envases activos, en donde se ven las interacciones entre el producto, el envase y su entorno.
Basados en estas tres principales categorías, los envases activos se pueden clasificar en subcategorías. La Tabla I muestra los principales grupos según su tipo de función y sus aplicaciones.
TipoMaterialPrincipioEfecto y aplicación
Absorción de oxígeno
Hierro, ácido ascórbico, sulfitos, oxidasas, polidienos y nylon
Absorción de humedad
Sílica gel , poliacrilato, CaO, azúcar, sal inorgánica y propilenglicol.
Reacción de oxidación del hierro, ácido ascórbico, sulfitos o componentes poliméricos, además de una catálisis enzimática y catálisis
Prevención o reducción del crecimiento de microorganismos aeróbicos en productos de panificación y alimentos preparados Prevenir o reducir la deterioración
Absorción de dióxido de carbono Ca(OH)2, Na2CO3, sílica gel y zeolite
Absorción de etileno
Absorción de humedad, reacción de hidratación
Reacción química con CO2, adsorción física
KMnO4 con óxido de aluminio o sílica gel , SiO2, zeolite, carbón activado
Oxidación de etileno a ácido acético con alcohol, adsorción física
Retención del bajo contenido de humedad en alimentos con textura crujiente y mantener la calidad en productos secos; remover el exceso de agua en la superficie de alimentos cárnicos enteros o en trozos
Prevención del estallido del envase provocado por CO2 debido a la fermentación de ácido láctico
Retardo de los cambios en el alimento provocado por madurez y senescencia
Emisor de dióxido de carbono FeCO3, NaHCO3, Na2CO3, ácido ascórbico
Reacción de hidrólisis de FeCO3; reacción de NaHCO3 o Na2CO3 con ácidos orgánicos y oxidación del ácido ascórbico
Reducción e inhibición del crecimiento de bacterias Gramnegativas y hongos en productos de alimentos preparados: prevención del colapso del envase
Antimicrobianos
Antioxidantes
Antimicrobianos integrados o encapsulados en el material del envase o superficies intrínsecamente inhibitorias
Antioxidantes (BHA, BHT, tocoferol), integrados en el material del envase
Sabores incorporados en la matriz del envase
Liberación de los agentes antimicrobianos sobre la superficie de los alimentos. Liberación de vapor de etanol en el espacio de cabeza del envase
Inhibición del crecimiento microbiano
Otros
Enzimas inmóviles, tamiz molecular, sales ferrosas con ácidos orgánicos
aAdaptado de Sun Lee et al. (2008)
Liberación de antioxidantes o agotamiento de oxígeno
Retardo de los cambios en el alimento por oxidación y protección de los polímeros
Liberación de sabores indeseables Mejora en el sabor de los alimentos
Catalizan las reacciones de transformación para remover, naringina, lactosa o colesterol; adsorción u oxidación de los compuestos volátiles como sabores
Reducción de los sabores amargos en productos derivados de la uva, remoción de lactosa y colesterol en productos lácteos y reducción de los sabores indeseables en productos como pescado o aceites
Tabla I. Tipos de envases activos y sus funcionesa
Los envases activos han sido usados con muchos alimentos, por ejemplo, los sistemas de absorción de oxígeno se usan para envasar pasteles, pan, pasta, quesos y botanas; los sistemas emisores de etanol se usan en pizzas, pasteles y pescados; los sistemas antimicrobianos se usan en cereales, botanas, frutas, hortalizas, etc. (Coles et al., 2003).
1.2. Materiales usados en la elaboración de envases activos
Los materiales más utilizados en la elaboración de envases activos son los plásticos y los laminados, ya que tienen, o se pueden fabricar con diferentes propiedades y permiten la entrada y salida de los componentes, además de que su proceso de elaboración ayuda en la incorporación de aditivos como agentes antimicrobianos, antioxidantes, etc. (Marsh y Bugusu, 2007). Las películas plásticas pueden ser combinadas con otros plásticos por coextrusión, fundición, laminación o recubrimiento para poder conseguir las propiedades que se requieren para cada producto. También pueden ser recubiertas con otros tipos de materiales como celulosas, aluminio o papel, para que las propiedades en el manejo sean mejoradas, además se les pueden añadir aditivos como lacas, colores y otros aditivos que se incorporan dentro de la formulación de los envases dependiendo del objetivo en específico del envase (Coles et al., 2003).
La principal razón por la que los plásticos se usan en los envases de alimentos es la protección que ofrecen contra el deterioro y su facilidad para integrarse dentro del proceso e interactuar con los alimentos, son relativamente ligeros, no son susceptible a la fragmentación y se pueden obtener diferentes estructuras y diseños con costos accesibles (Coles et al., 2003). La Tabla II muestra los principales plásticos usados en la fabricación de envases para alimentos.
Las películas comestibles son consideradas también como envases activos. Para manufacturar este tipo de películas se usan diversos materiales como almidón, alginato, derivados de celulosa, quitosano, agar, ceras, gliceroles y ácidos grasos. La elección del material depende de la función
Tabla II. Plásticos usados en los alimentosa
Abreviaciaciones
Nombre
Polietileno (baja y alta densidad)
comunes (Por sus siglas en inglés)
PE (LDPE y HDPE)
PolipropilenoPP
Polietilen
tereftalato PET
Etileno vinil
acetato EVA
PoliamidasPA
PoliestirenoPS
Etilen vinil
alcohol EVOH
Acetato polivinil PVA
Cloruro de polivinilo
PVC
EstirenosS
aAdaptado de Coles et al. (2003)
deseada en el producto (Cha y Chinnan, 2004).
2. Envases activos con antimicrobianos
Los envases con antimicrobianos son un tipo de envase activo en el cual el producto, el envase y el ambiente interactúan entre sí para reducir o retardar el crecimiento microbiano con el fin de prolongar la vida de anaquel, manteniendo la calidad y seguridad del producto (Sun Lee et al., 2008).
Los envases antimicrobianos pueden ser efectivos para reducir las dificultades que trae consigo la adición de los agentes antimicrobianos directamente en el producto, incluyendo perdida de actividad por lixiviación y reacciones con otros compuestos como lípidos y proteínas, resultando una actividad antimicrobiana más extensa durante toda la cadena de distribución (Jokar et al., 2009).
Comparado con los objetivos convencionales de un envase de alimentos, los envases activos con antimicrobianos están específicamente diseñados para controlar el crecimiento de los microorganismos que afectan directamente a la
estabilidad del alimento, es por ello que las principales tareas que un envase antimicrobiano debe cumplir son: inocuidad de los alimentos, mantenimiento de la calidad y extensión de la vida de anaquel del producto (Ahvenainen, 2003).
Algunos métodos de conservación se basan en el concepto de envases antimicrobianos como son los embutidos, carnes ahumadas o saladas, la fermentación de algunos alimentos en barricas o salmueras; el principio básico de estos métodos de conservación es una tecnología de obstáculos, la función antimicrobiana de estos sistemas sólo se limita a proteger al alimento de los microorganismos; sin embargo, no contribuye a la protección del producto de daños físicos (Ahvenainen, 2003).
Cuando los agentes antimicrobianos se añaden dentro de la estructura del envase, además de la función de obstaculizar, también se alcanzan las siguientes tres propiedades: liberación, absorción e inmovilización. Los envases antimicrobianos que tiene la función de liberar, permiten la migración de los agentes antimicrobianos del envase hacia el alimento o hacia el espacio de cabeza de los envases e inhiben así el crecimiento microbiano. Los sistemas de absorción remueven los factores
– 2 (2011): 1 - 12
esenciales para el crecimiento de los microorganismos e inhiben éste. Los sistemas de inmovilización no liberan agentes antimicrobianos pero suprimen el crecimiento microbiano en la superficie de contacto con el alimento, estos sistemas pueden ser menos efectivos en alimentos sólidos que alimentos líquidos debido a que existe menor posibilidad de que todo el alimento esté en contacto con el envase (Ahvenainen, 2003).
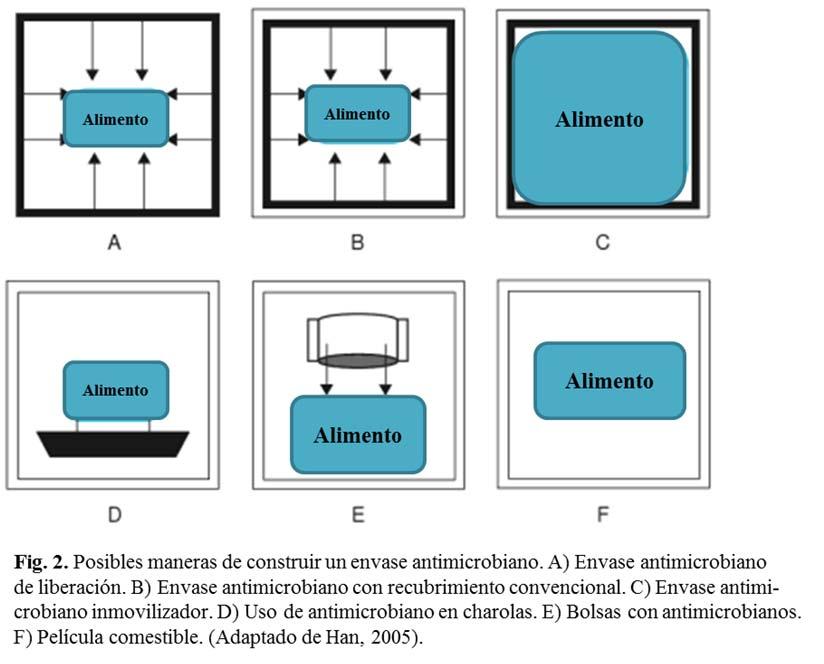
Los agentes antimicrobianos pueden ser incorporados de manera directa en los materiales de envase en forma de películas, recubrimientos, hojas, charolas y contenedores, o en los espacios disponibles en forma de insertos en las bolsas (Han, 2005). La Fig. 2 muestra las diferentes posibilidades de incorporar los agentes antimicrobianos en los envases. Las figuras 2A, 2B y 2E es la manera en que los antimicrobianos se liberan del empaque hacia el alimentos con unas pequeñas variaciones entre ellos (con o sin recubrimiento y directamente en una bolsa), las figuras 2C y2D son sistemas inmovilizadores en donde la superficie del alimento está en contacto con e antimicrobiano y finalmente la figura 2F son los agentes antimicrobianos en películas listas para consumirse.
2.1. Tipos de antimicrobianos usados en envases activos
Los agentes antimicrobianos tienen diferente actividad y afectan a diferentes microorganismos, es por ello que se tienen que caracterizar los mecanismos de acción de los agentes antimicrobianos y clasificarlos para cada tipo de microorganismo. Ejemplos de criterios para su clasificación: requerimientos de oxígeno (aerobios y anaerobios), composición celular (Gram positivos y Gram negativos), etapas de crecimiento (esporas y células vegetativas) y temperatura óptima de crecimiento (termófilos, psicrófilos, psicótrofos, mesófilos). Además de las características microbianas, el mecanismo de acción antimicrobiano de los agentes es muy importante para entender su eficacia así como sus limitaciones. Algunos agentes antimicrobianos inhiben el metabolismo esencial mientras que otros alteran la estructura de las paredes de las células (Ahvenainen, 2003).
Diferentes agentes antimicrobianos se pueden incorporar directamente en el material del envase, pueden ser colocados como recubrimientos o inmovilizados por diferentes polímeros. Los procesos térmicos como extrusión, fundición, inyección y moldeado han sido usados para la incorporación de los agentes antimicrobianos dentro de los envases, pero la estabilidad y compatibilidad de los polímeros con los antimicrobianos han limitado su uso a solo ciertas sustancias (Jokar et al., 2009).
La Tabla III enlista las substancias, que pueden ser unidas con diferentes polímeros para compartir las propiedades antimicrobianas. Estas substancias pueden ser usadas en películas antimicrobianas, contenedores o utensilios (Suppakul et al., 2003).
Existen numerosos estudios que han incorporado agentes antimicrobianos en la formación de envases. Weng y Hotchkiss (1992) desarrollaron la técnica para combinar polietileno (PE) con ácido metacrílico (PEMA), ácido benzoico y ácido sórbico en forma de contenedores. Dobias et al. (2000) investigaron las propiedades funcionales de anhídrido benzoico y parabenos incorporados en las películas de
polietileno de baja densidad (LDPE). La adición de parabenos en el polímero es más difícil que la adición del anhídrido benzoico, debido a su volatilidad. La incorporación de los antimicrobianos en la película cambió significativamente las características funcionales de los materiales de envase. Ouattara et al. (2000) incorporaron ácido acético y propiónico en películas de quitosano donde encontraron que la difusión de los agentes antimicrobianos no depende de los rangos de pH, sino de las temperaturas, entre más se acerca a los 4 °C los coeficientes de difusión se reducen. Cran et al. (2010) utilizaron componentes activos como linanol, carvacrol y timol con películas de LDPE para describir un modelo matemático de migración de los compuestos activos, para conocer la liberación que estos compuestos tienen a través de las resinas utilizadas en la formación del plástico.
2.2. Efectividad de los envases antimicrobianos contra diversos microorganismos.
Devlieghere et al. (2000) estudiaron la actividad antimicrobiana de las resinas de etileno vinil acetato (EVA) con LDPE adicionadas con sorbato de potasio. Debido a la limitada migración del sorbato de potasio a través de la película de EVA/LDPE, no existió inhibición en el crecimiento sobre Candida spp., Pichia spp., Trichosporon spp. y Penicillium spp.
Weng et al. (1997) adicionaron cloruro de benzoilo a películas de ionómero e investigaron su capacidad antimicrobiana contra Penicillium spp. y Aspergillus niger comparándolo con un tratamiento con ácido benzoico. Las películas tuvieron mayor efectividad antimicrobiana que el tratamiento con el ácido benzoico.
Ávila-Sosa et al. (2010) desarrolló películas comestibles de amaranto, almidón y quitosano adicionadas con aceite esencial de orégano para inhibir el crecimiento de Aspergillus niger y Penicillium spp., teniendo como resultado que una concentración de 0.5% (p/p) del aceite esencial de orégano incorporado a las películas logró inhibir estos microorganismos.
Tabla III. Agentes antimicrobianos usados en envases antimicrobianosa
Agente antimicrobianoEjemplo
Ácidos anhídridos
Anhídrido benzoico, anhídrido sórbico
AlcoholesEtanol
AminasHexametil entramina
Compuestos de amonio
Sales cuaternarias de amonio
AntibióticosNatamicina
Péptidos
Antimicrobianos
Antioxidantes fenólicos
Bacteriocinas
Cecropina, defensina, magainina
BHA, BHT y TBHQ
Bavaricina, brevicina, carnocina, lacticina, nisina, pediocina, subtilisina, sakacina
QuelantesCitrato, EDTA, polifosfato, conalbulmina, lactoferrina
Enzimas
Quitinasa, oxidasa etanol , β- glucanasa, glucosa oxidasa, lactoperoxidasa, lisozima
Ácidos grasosÁcido palmitoleico y ácido laurico
FungicidasImazalil, dióxido de azufre, benomil
Ácidos
Inorgánicos
Ácido fosfórico
MetalesCobre y plata
Fenoles naturales
Ácidos
Orgánicos
Sales de ácidos orgánicos
Catequinas, hidroquinonas, ρ -cresol
Ácido acético, ácido benzoico, ácido cítrico, ácido láctico, ácido málico, ácido propionico, ácido sórbico, ácido succínico y ácido tartárico.
Sorbato de potasio y benzoato de sodio
ParabenosEtil parabeno, metil parabeno, propil parabeno
Compuestos de plantas
Polisacáridos
Carvacrol, eugenol, linalol, timol, citrato, cineol, geraniol, terpinol, estragol
Quitosano
aAdaptado de Suppakul et al. (2003)
Chung et al. (2001) incorporaron parabenos en PE con un copolímero de acrilato reportando que la lenta liberación del propilparabeno inhibía el crecimiento de Saccharomyces cerevisiae.
Vermeiren et al. (2002) reportaron que una película de LDPE adicionada con 1% (p/p) de triclosan demuestra actividad antimicrobiana en contra de Staphylococcus aureus, Listeria monocytogenes, Escheriachia coli O157:H7, Salmonella enteritidis y Brocothrix thermosphacta. Las películas de triclosan tuvieron un fuerte efecto in vitro, en condiciones de vacío para casi todas las bacterias exceptuando L. monocytogenes.
Cutter et al. (2001) reportaron mayor eficiencia en la actividad antimicrobiana de la nisina incorporada en películas de PE; la nisina fue aplicada en PVC, LDPE y nylon y probada en pollos frescos logrando inactivar Salmonella Typhimurium que fue inoculada en ellos
3. Aplicaciones en alimentos
Los alimentos frescos pueden contener microorganismos tanto en su superficie como en el interior de ellos. Estos microorganismos, si no son inactivados o destruidos pueden generar descomposición de los alimentos. Los agentes antimicrobianos ayudan a prevenir este deterioro en los alimentos, por lo tanto los envases antimicrobianos tienen la misma función que cumplirían los antimicrobianos dentro de los alimentos (Cha y Chinnan, 2004). La Tabla IV muestra algunas aplicaciones de envases antimicrobianos en alimentos y sus microorganismos objetivos.
La Tabla V muestra las aplicaciones potenciales para envases antimicrobianos por grupo de productos.
3.1. Productos de panificación
Ghosh et al. (1973) desarrollaron bolsas fungistáticas con ácido sórbico y las usaron en pan. Las bolsas se hicieron de polietileno con un revestimiento a prueba de grasa añadiendo una solución acuosa de ácido sórbico al 2% de concentración. El uso de estas bolsas podía
conservar los alimentos que son susceptibles a deterioro por al menos de 10 días. Una vez que el pan se encontraba envuelto era necesario calentarlo a una temperatura entre 95-100 °C por un período de 30 a 60 min. Además se incorporó un antioxidante en la bolsa tratada y también se usó un absorbente de olor dentro de las bolsas de pan para minimizar los sabores/olores desagradables. El pan de caja fue evaluado sensorialmente los resultados de esta evaluación fueron aceptables después de un mes de almacenamiento.
Tabla IV. Aplicación de los envases antimicrobianos en alimentosa ProductoAgente antimicrobianoMicroorganismo objetivo
Carne, pescado y aves
Carne de resPediocina Listeria monocytogenes
Nisina Brochotrix thermosphacta
Triclosan
Carne molida
Extracto de semilla de uva
JamónLactacina y nisina
Brochotrix thermosphacta, Salmonella Typhimurium, Escherichia coli H 157:H7, Bacillus subtilis
Micrococcus flavus, E. coli, Staphylococcus aureus, B. subtilis
Lactococcus lactis, Listeria innocua, S. aureus
AvesNisina Salmonella Typhimurium
Embutidos Ácido acético, ácido propionico
Carne envasada al vacío
Lactobacillus sakei, Serratia liquefaciens
Nisina Lactobacillus helveticus, Brochotrix thermosphacta
Piel de polloNisina Salmonella Typhimurium
Vegetales
Fresas Sorbato de potasio, ácido cítrico
Tomate
Lechuga, producto de soya
Leche y productos lácteos
Mesofilos aeróbicos , psicótropos, coliformes, mohos y levaduras
Ácido cítrico, ácido acético, ácido sórbico, etanol Salmonella Montevideo
Extracto de semilla de uva E. coli, S. aureus
Leche descremada Nisina Lactobacillus curvatus
Queso Imazalil, lactacina y nisina
aAdaptado de Cha y Chinnan (2004)
Penicillium spp., Aspergillus toxicarius
Tabla V. Aplicaciones potenciales para envases antimicrobianos a
AntimicrobianoCárnicosLácteosPescadosPanificación
Ácidos orgánicos y sus sales
Carne de res, embutidos y pollo Quesos
Etanol
Bacteriocinas
Enzimas
Agentes quelantes
Carne de res, embutidos y pollo Quesos
Carne de res, embutidos y pollo Quesos
Carne de res, embutidos y pollo
Fungicidas
Sanitizantes
Quesos
Pescados y mariscos
Pescados y mariscos
Pescados y mariscos
Pan, galletas, pasteles
Futas /verduras/otros
Frutas, vegetales, mermeladas y gelatinas
5 – 2 (2011): 1 - 12
Bebidas Mínimamente procesados
Vino y jugo de frutas
Pasta, productos salados, fideos, arroz
NuecesPasta, sandwiches
Jamón, huevos, sandiwiches
Jamón
Frutas, gelatinas, jaleas
Jugo de frutas
Fruta pre cortada y salsas
Cítricos, arándanos, nueces
Carne de res, embutidos y pollo
Especias y aceites esenciales
Carne fresca y procesada , pollos, nuggets
Queso, queso rallado
Pescados y mariscos
Pescado, pescado seco y mariscos
Frutas y vegetales
Pasteles, galletas, pan
Nueces, arándanos, gelatina y mermelada
Ensalada pre cortada
Jugo de frutas
Pasta, arroz, embutidos, ensaladas, hamburguesas, sandwiches
Probióticos
Carne fresca y procesada, carne seca, embutidos y pollo
aAdaptado de Han (2005)
Queso rallado
Pescado seco
Pasteles, galletas, pan
Nueces, jales y gelatinas
Jugo de frutas y vino
Pasta, embutidos, arroz
Nielsen y Rios (2000) investigaron el efecto de los componentes volátiles de diversas especias y hierbas como canela, ajo, mostaza y orégano en películas comestibles sobre la inhibición de Penicillium comuna, P. roqueforti, Aspergillus flavus y Endomyces fibuliger en productos de panificación. El mayor efecto inhibitorio lo presentó el aceite esencial de mostaza, seguido de
canela y ajo, siendo el orégano la especie más débil contra estos hongos
3.2. Productos cárnicos
El uso de la nisina en los materiales de envase ha tenido mucho interés en los últimos años. Ming et al. (1997) aplicaron nisina y pediocina a películas
de celulosa para reducir L. monocytogenes en carnes y aves. Las películas recubiertas con pediocina inhibieron completamente el crecimiento de L. monocytogenes inoculada, durante 12 semanas de almacenamiento a 4 °C.
Siragusa et al. (1999) demostraron que la nisina incorporada en películas de PE puede evitar el crecimiento de las bacterias Lactobacillus helveticus y Brochothrix thermosphacta que causan el deterioro en la carne.
3.3. Productos lácteos
Devlieghere et al. (2000) probaron una película de EVA/LDPE con sorbato de potasio en cubos de queso no encontrando diferencias significativas sobre el crecimiento de mohos y levaduras en comparación con una película de referencia durante el almacenamiento del producto.
Scannell et al. (2000) desarrollaron materiales bioactivos de envasado de alimentos con nisina. El envase antimicrobiano redujo el recuento de bacterias ácido lácticas en rebanadas de queso almacenadas con atmósferas modificadas en refrigeración, por lo tanto, lograron prolongar la vida de anaquel del producto. Este envase logró reducir los niveles de Listeria innocua por debajo de 2 ciclos logarítmicos y 1.5 ciclos logarítmicos de S. aureus en el queso.
anaquel del producto y mantener su calidad e inocuidad.
Aún hace falta seguir investigando sobre estos tipos de envases, existe una área de oportunidad muy grande para realizar investigaciones con agentes antimicrobianos naturales y en productos como frutas y hortalizas en donde el campo de aplicación se ha limitado más para películas comestibles o envases activos como atmósferas modificadas, pero las investigaciones con películas no comestibles son aún escasas.
Agradecimientos
Y. Martínez- Tenorio agradece al Consejo Nacional de Ciencia y Tecnología (CONACyT) y a la Universidad de las Américas Puebla, por el financiamiento de sus estudios de posgrado y el apoyo para realizar este trabajo.
Referencias
Ahvenainen, R. 2003. Novel Food Packaging Techniques. CRC Press. Boca Raton, EE. UU. 590p.
Conclusiones
Esta investigación documental da una visión de los trabajos realizados en los últimos años sobre envases activos, enfocándose en los envases activos con antimicrobianos.
Los envases antimicrobianos no son exclusivos de un tipo de alimento o de un solo agente antimicrobiano, se observa que se pueden aplicar en diversos productos como cárnicos, lácteos, panificación, entre otros, la selección del agente antimicrobiano se debe hacer de acuerdo a las necesidades específicas para el tipo de alimento que se quiera envasar, para poder alargar la vida de
Ávila-Sosa, R. Hernández-Zamoran, E. LópezMendoza, I. Palou, E. Jiménez, M. NevárezMorillón, V. y López-Malo, A. 2010. Fungal Inactivation by Mexican Oregano (Lippia berlanderi Schauer) Essential Oil added to Amaranth, Chitosan, or Starch Edible Film. Journal of Food Science. 75(3):127-133.
Cha, D. S y Chinnan, M. S. 2004. Biopolymer-Based Antimicrobial Packaging.Critical Reviews in Food Science and Nutrition. 44(4):223-237.
Chung, D. H., Chikindas, M. L. y Yam, K. L. 2001. Inhibition of Saccharomyces cerevisiae by slow of propyl paraben from polymer coating. Journal of Food Protection. 64(9):1420-1424.
Coles, R., McDowell, D. y Kirwan M. J. 2003. Food Packaging Technology. CRC Press Boca Raton, EE. UU. 282 p.
Cran, M. J. Rupika, L. A .S. Sonneveld, K. Miltz, J. y Bigger, S. W. 2010. Release of Naturally Derived
Antimicrobial Agents from LDPE Films. Journal of Food Science. 75(2):126-133.
Cutter, C. N, Willet, J. L y Siragusa. G. R. 2001. Improved antimicrobial activity of nisi-incorporated polymer films by formulation change and addition of food grade chaletor. Food Microbiology. 33:325328.
Devlieghere, F., Vermeiren, L., Bockstal, A. y Debevere, J. 2000. Study on antimicrobial activity of a food packaging material containing potassium sorbate. Acta Alimentaria. 29:137-146.
Dobias, J., Chudackova, K., Voldrich, M. y Marek, M. 2000. Properties of polyethylene films with incorporated benzoic anhydride and/or ethyl and propyl esters of 4-hydroxybenzoic acid and their suitability for food packaging. Food Additives and Contaminants. 17(12):1047-1053.
Ghosh, K. G., Srivatsava, A. N., Nirmala, N. y Shama, T. R. 1973. Development and application of fungistatic wrappers in food preservation Part I: Wrappers obtained by impregnation method. Journal of Food Science Technology. 10:105-110.
Han, J. H. 2005.Innovations in food packaging .Elsevier Academic Press. London, UK. 517p.
Jokar, M., Rahman, R. A., Ibrahim, N. A., Abdulah, L. C. y Tan, C.P. 2009. Melt Production and Antimicrobial Efficiency of Low-Density Polyethylene (LDPE)- Silver Nanocomposite Film. Food Bioprocess Technol. 10(1):329-338.
Marsh, K. y Bugusu, B. 2007. Food Packaging – Roles, Materials and Environmental Issues. Journal of Food Science. 72(3):39-55.
Ming, X., Weber, G. H., Ayres, J. W. y Sandine, W. E. 1997. Bacteriocins applied to food packaging materials to inhibit Listeria monocytogenes on meats. Journal of food Science. 62(2):413-415
Nielsen, P. V. y Rios, R. 2000. Inhibition of fungal growth on bread by volatile components from spices and herbs, and the possible application in active packaging, with special emphasis on mustard
essential oil. International Food Microbiology. 60:219-229.
Ouattara, B., Simard, R. E., Piette, G., Begin, A. y Holley, R.A. 2000. Difussion of acetic and propionic acids from chitosan-based antimicrobial packaging films. Journal of Food Science. 65(5):768-773.
Ozdemir, M. y Floros, J. D. 2010. Active Food Packaging Technologies. Critical Reviews in Food Science and Nutrition. 44(3):185-193.
Scanell, A. G. M., Hill, C., R.oss, R. P., Marx, S., Hartmeier, W. y Arendt, K. E. 2000. Development of bioactive food packaging materials using immobilized bacteriocins lactacin and nisaplin. International Food Microbiology. 60:241-249.
Siragusa, G. R, Cutter, C. N. y Willet, J. L. 1999. Incorporation of bacteriocin in plastic retains activity and inhibits surface growth of bacteria on meat. Food Microbiology. 16:229-235.
Sun Lee, D., Yam, K. T. y Piergiovanni, L. 2008. Food Packaging Science and Technology. CRC Press. Boca Raton, EE. UU. 650 p.
Suppakul, P., Miltz, J., Sonneveld, K. y Bigger, S. W. 2003. Active packaging technologies with emphasis on antimicrobial packaging and its applications. Journal of Food Science. 68(2): 408-420.
Vermeiren, L., Devlieghere, F. y Debevere, J. 2002. Effectiveness of some recent antimicrobial packaging concepts. Food Additives and Contaminants. 19:163-171.
Weng, Y. M. y Hotchkiss. J. H. 1992. Inhibition of surface molds on cheese by polyethylene film containing antimycotic imazalil. Journal of Food Protection. 55(5):367-369.
Weng, Y. M:, Chen, M. J. y Chen, W. L. 1997. Benzoyl chloride modified ionomer films as antimicrobial food packaging materials. International Journal of Food Science Technology. 32:229-234
Wilson, C. 2007. Intelligent and Active packaging for Fruits and Vegetables. CRC Press Boca Raton, EE. UU. 336 p.

Temas Selectos de Ingeniería de Alimentos 5 - 2 (2011): 13 - 27

Tecnologías involucradas en el procesamiento mínimo de frutas y hortalizas
E. P. Pérez – Pérez* y A. López – Malo
Departamento de Ingeniería Química, Alimentos y Ambiental, Fundación Universidad de las Américas Puebla. Exhacienda Sta. Catarina Mártir S/N, Cholula, Puebla. C.P.72810. México.
Resumen
Uno de los segmentos de mayor crecimiento en la industria de alimentos es el de las frutas y hortalizas mínimamente procesadas. Esta nueva tendencia de mercado ha obligado a desarrollar nuevas tecnologías para conservar las características de frescura de estos productos, alargar su vida de anaquel y garantizar su inocuidad. Los tratamientos con aditivos, el envasado en atmósfera modificas, el uso de aceites esenciales como antioxidantes y antimicrobianos, y la aplicación de películas comestibles son algunas de las tecnologías más destacadas en los últimos años. Se ha observado una sinergia cuando se aplica más de una de estas tecnologías antes mencionadas. El objetivo del presente trabajo es revisar las últimas tecnologías desarrolladas para alargar la vida de anaquel de dichos productos.
Palabras clave: frutas y hortalizas mínimamente procesadas, envasado en atmósferas modificadas, aceites esenciales, películas comestibles.
Abstract
One of the major growth segments in the food retail industry is fresh and minimally processed fruits and vegetables. This new market trend has been forced to develop new technologies to preserve the characteristics of freshness of these products, extend the shelf-life and improve their microbiological safety. Additives, modified atmosphere packaging, the use of essential oils as antioxidants and antimicrobials, and the application of edible films are some of the leading technologies in recent years. Synergy has been observed when applying more than one of these technologies mentioned above. The aim of this paper is to review the latest technologies developed to extend the shelf-life of these products
Keywords: minimally processed fruits and vegetables, modified atmosphere packaging, essential oils, edible films.
Introducción
En la conservación de alimentos, mientras más severo sea el proceso que se utilice, por lo general la calidad sensorial de los alimentos disminuye. Por lo tanto, el consumidor
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: emmyp.perezpz@udlap.mx
prefiere alimentos mínimamente procesados, los cuales deben poseer características de frescura y deben ser microbiológicamente seguros y estables (Leistner, 2000). Los productos mínimamente procesados son uno de los principales segmentos de crecimiento en los establecimientos de ventas de alimentos al menudeo (Soliva-Fortuny y Martín-Belloso, 2003). Los consumidores y los
establecimientos de comida rápida exigen productos de conveniencia, ya sea por razones de costo, mano de obra e inclusive por higiene o seguridad. El procesamiento mínimo de frutas y hortalizas tiene dos propósitos: mantener los productos frescos y suministrarlos de forma conveniente sin perder su calidad nutricional; y además el producto debe tener una vida de anaquel suficiente para hacer posible su distribución a los consumidores previstos (Huxsoll y Bolin, 1989).
Los consumidores suelen juzgar la calidad de las frutas y hortalizas recién cortadas, con base en la apariencia y frescura en el momento de la compra. Sin embargo, las operaciones mínimas de procesamiento alteran la integridad de las frutas y hortalizas provocando efectos negativos en la calidad de las mismas, tales como el desarrollo de oscurecimiento, mal sabor y pérdida de textura. La presencia de microorganismos en la superficie del producto también puede comprometer la inocuidad de las frutas y hortalizas recién cortadas (Rojas-Graü et al., 2009a). Se han desarrollado tratamientos con desinfectantes, texturizantes, antioxidantes y antimicrobianos para aplicarse durante el procesamiento mínimo que ayuden a retardar las reacciones de deterioro y a disminuir el riesgo de crecimiento de microorganismos patógenos; pero en los últimos años ha prevalecido la exigencia por parte de los consumidores de reducir o eliminar, en los alimentos, los aditivos químicamente sintetizados. Por lo anterior, se han realizado diversas investigaciones para desarrollar tratamientos con aditivos naturales. Los aceites esenciales se destacan como una alternativa al uso de conservadores químicos en alimentos, cumpliendo con la demanda de los consumidores por productos naturales (Burt, 2004).
Una técnica que ha sido utilizada durante décadas para alargar la vida de anaquel de las
frutas y hortalizas mínimamente procesadas, es el envasado en atmósferas modificadas; en donde se logra disminuir la velocidad de respiración del vegetal y retrasar las reacciones deteriorativas. Pero bajo ciertas condiciones, el crecimiento de algunos microorganismos patógenos psicrófilos o psicrótrofos anaerobios o microaerofílicos puede presentarse o incluso estimularse. Las condiciones tradicionales de envasado en atmósferas modificadas, rara vez son suficientes para garantizar la seguridad y lograr productos de alta calidad. Las películas comestibles se pueden aplicar como complemento al envasado en atmósfera modificada, ya que reducen los efectos derivados del procesamiento mínimo, retardan el deterioro, mejoran su calidad y seguridad, ya que se les puede incorporar ingredientes funcionales, tales como aceites esenciales (Rojas-Graü et al., 2009b). En la preservación de alimentos se ha comprobado que se obtienen mejores resultados utilizando métodos combinados, en contraparte con las técnicas o tratamientos individuales.
El objetivo de este trabajo es revisar los fundamentos teóricos y aspectos a considerar en el procesamiento mínimo de frutas y hortalizas así como las últimas tecnologías desarrolladas para alargar la vida de anaquel de dichos productos.
Revisión bibliográfica
1. Generalidades del procesamiento mínimo
Las frutas y hortalizas mínimamente procesadas, también conocidas como “Freshcut” (en inglés) pueden ser definidas como cualquier fruta u hortaliza que ha sido físicamente modificada de su forma original, por procesos como pelado, lavado o cortado; para obtener un producto comestible que es subsecuentemente envasado y almacenado en
refrigeración (IFPA, 2005). De acuerdo con la Asociación Internacional de Productos Frescos Cortados, estos productos han estado disponibles en supermercados para su venta al consumidor desde 1930. Sin embargo, la industria de productos mínimamente procesados fue desarrollada en un principio para suministrar a hoteles, restaurantes y otras instituciones; ya que presentan una serie de ventajas, incluyendo una reducción de mano de obra durante la preparación de alimentos, de desperdicios y su posterior manejo, así como la preparación de platillos en poco tiempo, con formas específicas de frutas u hortalizas (Watada et al., 1996).
Las frutas y hortalizas mínimamente procesadas pueden ser fabricadas sobre la base de varios principios de procesamiento, tal y que se muestra en la Tabla I, dependiendo de la vida de anaquel que se desee. Si los productos están obligados a tener una vida de anaquel mayor a una semana, se requieren de métodos de procesamiento más avanzados y son necesarios tratamientos diseñados
13 - 27
utilizando el concepto de barreras (o tecnología de obstáculos), así como la correcta elección de materias primas que sean adecuadas para un procesamiento mínimo; la conservación se basa en una combinación de varios tratamientos (Ahvenainen, 1996).
Generalmente las frutas y hortalizas mínimamente procesadas se deterioran más rápido que sus contrapartes, la fruta u hortaliza intacta. En la elección de los tratamientos adecuados, es necesario entender los cambios fisiológicos y microbiológicos que pueden ocurrir durante y después de su manipulación, transformación y almacenamiento, que reducen la calidad del producto ó incluso ponen en riesgo la seguridad del mismo. En lo que respecta al deterioro de las frutas y hortalizas mínimamente procesados, se pueden hacer distinciones entre el deterioro fisiológico y el deterioro microbiológico, aunque se influyen mutuamente (Ragaert et al., 2011).
Tabla I. Requerimientos para la fabricación comercial de frutas y hortalizas peladas y/o pre-cortadasa
PrincipioDemandas del procesoCliente
Preparación hoy, consumo mañana
• Área de preparación estándar y herramientas higienizadas
• Un lavado ligero para pelar para su posterior corte, la papa es una excepción
• Los envases pueden ser recipientes retornables
Preparación hoy, el cliente utiliza el producto dentro de 3-4 días
• Desinfección
• Lavado de los productos pelados o cortados, al menos con agua
• Envases permeables, la papa es una excepción
Los productos son destinados también para la venta al menudeo
• Buena desinfección
• Lavado del producto pelado o cortado con agua clorada o acidificada
• Envases permables, la papa es una excepción
• Aditivos
aAdap tado de Ahvenainen (1996)
Vida de anaquel a 5° C (días)
Sector de la hotelería y catering, restaurantes, escuelas, industria
Ejemplos
1-2Mayoría de frutas y hortalizas
Sector de la hotelería y "catering", restaurantes, escuelas, industria
3-5
5-7 Tiendas al menudeo, además de los clientes antes mencionados
Zanahoria, col, lechuga, papa, remolacha, frutas ácidas y bayas
Zanahoria, col, lechuga, papa, remolacha, frutas ácidas y bayas
Desde el punto de vista fisiológico, las operaciones del procesamiento mínimo hieren al tejido vivo, con lo cual comienza una serie de reacciones metabólicas que resultan en cambios de textura, aceleración del proceso de maduración y senescencia, desarrollo de olores desagradables, cambios de color, y otros eventos indeseables que hacen al producto no apto para ser comercializado (Baldwin y Bai, 2011). La enzima causante del oscurecimiento en las frutas y hortalizas mínimamente procesadas es la polifenoloxidasa. El oscurecimiento enzimático requiere de la presencia de la enzima, oxígeno, cobre y el sustrato adecuado, así que, para evitar el oscurecimiento es necesario eliminar uno de estos componentes. Otra enzima importante es la lipo-oxidasa, la cual cataliza reacciones de peroxidación, provocando la formación de aldehídos y cetonas, causantes de malos olores (Ahvenainen, 1996).
La manipulación y el procesamiento acortan la vida de anaquel porque propician una mayor producción de etileno, que es una hormona gaseosa de la maduración de las plantas, que está relacionada con los cambios de color y textura de varias frutas y hortalizas; también aumenta la tasa de respiración, debido a que se utilizan azúcares y ácidos como sustratos (Breidt y Fleming, 1997). Con base en su patrón respiratorio y la síntesis de etileno durante la maduración, los frutos pueden ser clasificados como climatéricos y no climatéricos (Tabla II). Los frutos climatéricos, pueden ser madurados fuera de la planta. La tasa de respiración y la formación de etileno, incrementan de manera significativa a un pico climatérico, en el inicio de la maduración, después de lo cual, disminuye y es mínima en la madurez. Los frutos no climatéricos no son capaces de continuar su proceso de maduración, una vez que se separan de la planta. Además, estos frutos producen una cantidad muy pequeña de etileno endógeno y no responden al tratamiento con etileno exógeno. Los frutos no
climatéricos muestran un perfil relativamente bajo y una disminución gradual en su patrón de respiración y producción de etileno, en todo el proceso de maduración (Prasanna et al., 2007).
ManzanaCereza
AlbaricoquePepino
PlátanoUva
GuayabaLimón
KiwiLima
MangoLitchi
PapayaMandarina
GranadaMelón
PeraNaranja
ZapotePiña
TomateFresa
Desde el punto de vista de deterioro microbiológico, durante el pelado y corte, la superficie del producto está expuesta al aire y a la posible contaminación con bacterias, levaduras y mohos. Las principales fuentes de contaminación son los instrumentos que se utilizan para las operaciones unitarias del procesamiento. En particular, en el caso de las hortalizas mínimamente procesados, la mayoría de los cuales entran en la categoría de baja acidez (pH 5.8 a 6.0), la alta humedad y el gran número de superficies de corte pueden proporcionar las condiciones ideales para el crecimiento de microorganismos (Ahvenainen, 1996). La proliferación microbiológica se caracteriza por diferentes procesos, la producción de enzimas y de metabolitos, que dan como resultado defectos visuales y de textura, así como el desarrollo de malos olores. La composición de las frutas y hortalizas determinará el tipo de deterioro. En la Fig. 1 se presenta una visión general de los diferentes mecanismos de deterioro típicamente
Frutos climatéricos Frutos no climatéricos
Tabla II. Clasificación de los frutos con base en su maduracióna
a Adaptado de Prasanna et al. (2007)
asociados con hortalizas de hoja verde, frutas y hortalizas ricos en azúcar. Basado en una investigación científica y análisis microbiológicos del Laboratorio de Microbiología y Preservación de Alimentos (LFMFP en sus siglas en inglés, Universidad de Ghent, Bélgica), de diferentes tipos de hortalizas y frutas cortadas mínimamente procesadas, se proporcionan límites microbiológicos específicos para el deterioro causado por microorganismos (Tabla III), en donde se tomaron las siguientes
– 2 (2011): 13 - 27
consideraciones: el recuento total de aerobios psicrótrofos se realizó después de 5 días de incubación; el valor "Consúmase preferentemente antes de" marca el final de la vida de anaquel, por arriba de este límite se da lugar a un notable deterioro; y, cuando el número de bacterias ácido lácticas en la fecha "Consúmase preferentemente antes de" es mayor que 1x107 UFC/g el producto se rechaza sin considerar las desviaciones sensoriales (Ragaert et al., 2011).
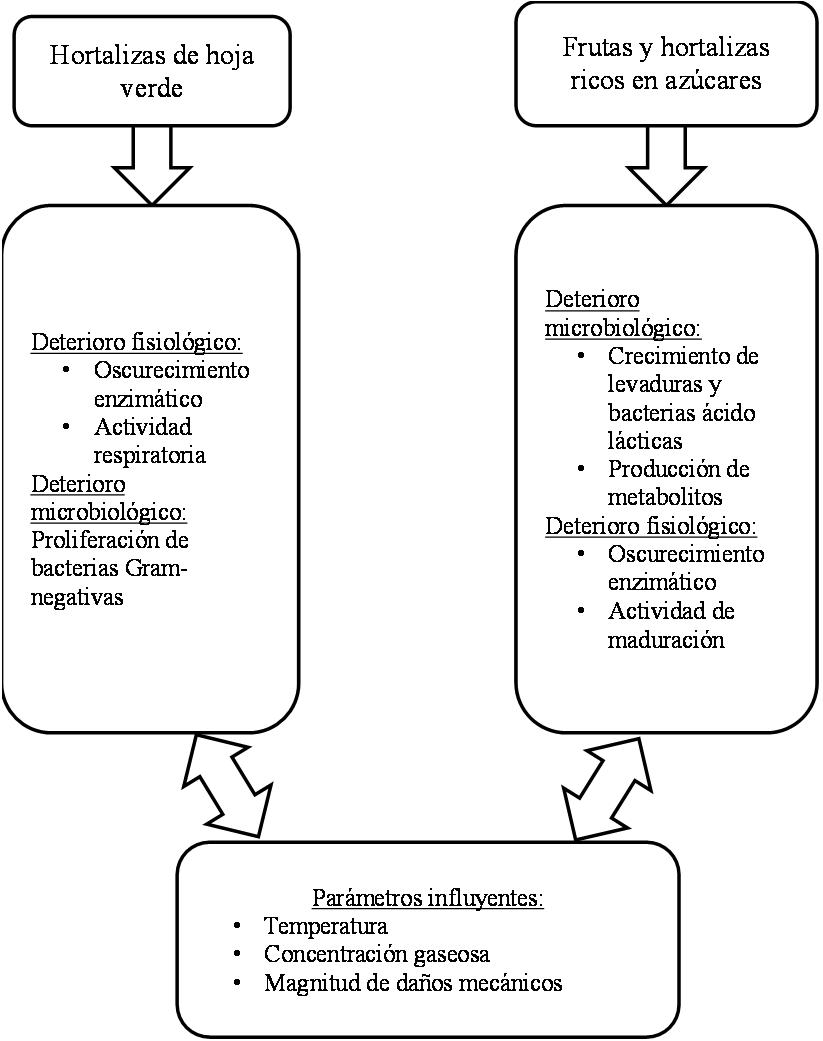
Figura 1. Mecanismos de deterioro de frutas y hortalizas (Adaptado de Ragaert et al., 2011).
Tabla III. Límites microbiológicos para el deterioro causado por microorganismos (UFC/g)a
Objetivo b Toleranciac Consumase preferentemente antes de d Parámetro
a Adaptado de Ragaert et al . (2011)
b El valor "Objetivo" es la población óptima para el día de producción, en las mejores condiciones de operación
c El valor "Tolerancia" es la población máxima para el día de producción
d El valor "Consúmase preferentemente antes de" marca el final de la vida de anaquel, arriba de este límite se da lugar a un notable deterioro
Por último, la eliminación de cáscara y los procesos de higienización alteran la ecología microbiana normal y permiten la posible contaminación con microorganismos patógenos (Breidt y Fleming, 1997). Los microorganismos patógenos pueden estar presentes en la materia prima o debido a una contaminación cruzada durante el procesamiento. Las fuentes de microorganismos típicas en la producción primaria son el agua, el suelo, o las aguas residuales que están contaminadas con materia fecal. Numerosos microorganismos patógenos han sido aislados de frutas y hortalizas mínimamente procesadas (Tabla IV), las cuales sirven como vehículos de enfermedades (Beuchat, 1996; Ragaert et al., 2011).
2. Tecnologías aplicadas para el procesamiento mínimo de frutas y hortalizas
Se han desarrollado varias tecnologías para retrasar los efectos negativos que el procesamiento mínimo provoca en las frutas y hortalizas. A continuación se explican las tecnologías más empleadas y en donde se han concentrado las investigaciones en los últimos años.
2.1. Uso de aditivos convencionales en el procesamiento mínimo de frutas y hortalizas
Muchos de los tratamientos y condiciones de almacenamiento aplicados a las frutas y hortalizas mínimamente procesadas, están diseñados para aminorar los efectos iniciales de las respuestas del tejido vegetal al corte. Diversos aditivos se aplican para reducir el deterioro en las frutas y hortalizas cortadas mínimamente procesadas, estos incluyen los sanitizantes o desinfectantes, antioxidantes y texturizadores, entre otros (Ayala-Zavala y González-Aguilar, 2011).
2.1.1. Desinfectantes
Los desinfectantes son productos químicos que son utilizados para reducir la población microbiana de las superficies del producto entero o cortado (Parish et al., 2003). Existe una gran variedad de desinfectantes, a continuación se presentan los más utilizados en la industria de frutas y hortalizas mínimamente procesadas: cloro, yodo y ácidos orgánicos.
El cloro ha sido, tal vez, uno de los desinfectantes más utilizados en la industria de alimentos, particularmente cloro líquido HortalizasFrutasHortalizasFrutasHortalizasFrutas
Tabla IV. Microorganismos patógenos de interés en frutas y hortalizas mínimamente procesadasa
Patógenos de interésPatógenos de posible interés
Listeria monocytogenesClostridium botulinum tipos B, E, F
Escherichia coli (O157:H7)
Shigella spp.
Salmonella spp.
Parásitos
Virus
a Adap tado de Rag aert et al (2011)
(soluciones de hipoclorito), para desinfectar los productos, las superficies de los equipos, así como para reducir la población microbiana en el agua utilizada en las operaciones de higienización, limpieza y empaque. Los compuestos de cloro son generalmente usados en niveles de 50-200 ppm, con un tiempo de contacto menor a 5 min, usualmente utilizados a valores de pH entre 6.0 y 7.5, para minimizar la corrosión de los equipos (Rico et al., 2007).
La máxima solubilidad de cloro se observa a 4°C, pero se recomienda mantener la temperatura del agua de proceso 10°C más alta con el fin de reducir la posibilidad de infiltración microbiológica, causada por una diferencia de presión, generada por la temperatura durante el proceso de higienización (Parish et al., 2003). Sin embargo, el cloro reacciona con la materia orgánica, por lo que algunos componentes de los tejidos del producto cortado pueden neutralizar el cloro antes de alcanzar a los microorganismos, y de esta forma reducir su efectividad (Ayala-Zavala y GonzálezAguilar, 2011).
Los yodóforos (combinaciones de yodo elemental y surfactantes no iónicos) tienen un amplio espectro de actividad antimicrobiana, es menos corrosivo que el cloro a temperaturas bajas, y son menos volátiles e irritantes para la piel que otros tipos de soluciones de yodo. Sin embargo, el yodo que contiene las soluciones desinfectantes puede ser corrosivo
Aeromonas hydrophila/caviae
Bacillus cereus
Yersenia enterocolitica
Campylobacter spp.
(vaporización por arriba de 50°C), su eficacia se reduce a bajas temperaturas, y puede manchar el equipo, la ropa y la piel. El uso de soluciones que contienen yodo como desinfectante por contacto directo al producto es limitado, debido a una reacción entre el yodo y el almidón del material vegetal, que se traduce en la aparición de un color moradoazulado. A pesar de estas limitaciones, las soluciones de yodo, tales como los yodóforos se utilizan como desinfectantes para superficies de contacto con los alimentos y equipos en la industria de procesamiento de alimentos (Parish et al., 2003).
Los ácidos orgánicos se utilizan comúnmente como acidulantes antimicrobianos para conservar a los alimentos, ya sea por adición directa o a través de la fermentación microbiológica. Dado que muchos microorganismos patógenos, no pueden crecer a valores de pH menores a 4.5, la acidificación puede actuar para prevenir la proliferación microbiana. Los ácidos orgánicos también pueden poseer capacidades bactericidas. La acción antimicrobiana de los ácidos orgánicos se debe a la reducción del pH del medio, la interrupción del transporte de membrana y su permeabilidad, la acumulación de aniones, entre otros. Muchos tipos de productos, especialmente las frutas, poseen naturalmente concentraciones significativas de ácidos orgánicos tales como acético, benzoico, cítrico, málico, sórbico, succínico y tartárico, que afectan negativamente a la viabilidad de
las bacterias contaminantes (Ayala-Zavala y González-Aguilar, 2011).
2.1.2. Antioxidantes
Para evitar el problema de oscurecimiento en frutas y hortalizas mínimamente procesadas se han aplicado diversos antioxidantes, principalmente por inmersión del producto, por atomización, o impregnación al vacío. Tradicionalmente los sulfitos habían sido utilizados para prevenir el oscurecimiento enzimático, pero su uso fue restringido ya que puede causar efectos secundarios en personas con asma. Los antioxidantes más utilizados en el tratamiento de frutas y hortalizas mínimamente procesados han sido ácido cítrico, ácido ascórbico, la cisteína, 4hexylresocinol, y N-acetilcisteína, entre otros; ya sea sólos o en combinación (Ahvenainen, 1996; Soliva-Fortuny y Martín-Belloso, 2003). Rojas-Graü et al. (2007a) observaron que un tratamiento de inmersión post-corte en una solución de N-acetilcisteína al 1% (p/v) evitaba el oscurecimiento en rebanadas de manzana y conservaban la apariencia inicial durante más de un mes, envasadas en atmósfera modificada y a temperatura de refrigeración.
2.1.3. Texturizadores
Los tratamientos con calcio se han utilizado para extender la vida de anaquel de frutas y hortalizas mínimamente procesadas, ya que ayuda a mantener la integridad de la pared celular vegetal mediante la interacción con la pectina para formar pectato de calcio. Por lo tanto, las frutas y hortalizas tratadas con calcio, generalmente se mantienen más firmes que sus contrapartes (fresco sin tratamiento), durante el almacenamiento (Rico et al., 2007). Las formas de calcio usados en la industria son lactato de calcio, cloruro de calcio, fosfato de calcio, propionato de calcio y gluconato de calcio, la elección de la fuente apropiada depende de la bioviabilidad, solubilidad, sabor
y su interacción con el alimento (Ayala-Zavala y González-Aguilar, 2011). El lactato de calcio se utiliza para tratar frutos delicados que tienen un índice de envejecimiento alto, como toronja, duraznos, melones cortados, manzanas, entre otros. Se utiliza en concentraciones de 0.5 a 2%, y se ha reportado como una buena alternativa al uso de cloruro de calcio, ya que evita el sabor amargo asociado con esta sal. El uso de tratamientos a base de calcio presenta una ventaja adicional, en algunos casos el producto final puede incrementar significativamente el contenido de calcio, lo que podría mejorar la apreciación de estos productos (Rico et al., 2007).
2.2. Envasado en atmósferas modificadas
El envasado en atmósfera modificada (EAM) es una técnica de conservación que es ampliamente usada en la industria de frutas y hortalizas mínimamente procesadas. El EAM implica alterar la composición gaseosa del ambiente que rodea al producto para producir una diferente a la del aire. Los bajos niveles de O2 y altos niveles de CO2 reducen la tasa de respiración con lo que se retrasa el proceso de senescencia, extendiendo así la vida de anaquel de los productos frescos. La atmósfera modificada se puede lograr de manera pasiva (el envase se sella bajo condiciones normales de aire) o activa (al envase se le suministra una mezcla de gases antes de sellar) (Rico et al., 2007); en ambos casos, seleccionando y utilizando adecuadamente los materiales de envase de acuerdo a su permeabilidad (Ahvenainen, 1996).
En el EAM pasivo, el intercambio de gases o vapor de agua se lleva a cabo dentro del envase, y esto es debido tanto a las respuestas fisiológicas (respiración, maduración, transpiración) del vegetal, como a la difusión de gases a través del envase. Después de un periodo de tiempo, la presión parcial del gas en el espacio de cabeza del envase llega a un estado de equilibrio, esto sucede cuando los
cambios difusivos a través de la película compensan exactamente la producción y consumo de gases y vapores. A lo anterior se le conoce como atmósfera modificada de equilibro, él cual debe ocurrir lo más pronto posible después de haber sido envasados los productos, y debe de estar cerca de la atmósfera óptima recomendada para preservar la calidad e inocuidad del producto (Guillaume et al., 2011).
Los principios para el intercambio de gases dentro del envase en el EAM activo, son los mismos que en el EAM pasivo, con la única variante de que la atmósfera inicial es diferente a la del aire (Guillaume et al., 2011). En general, el objetivo es tener una composición gaseosa de 2-5% de CO2, 2-5% de O2 y el resto de nitrógeno, dependiendo del producto (Ahvenainen, 1996). En el EAM activo se puede utilizar sistemas de barrido de gases y de emisión, integrados al envase o aplicados de forma separada (Guillaume et al., 2011).
En general, los productos frescos cortados son más tolerantes a altas concentraciones de CO2, que las frutas u hortalizas intactas (Rico et al., 2007). Sin embargo, uno de los principales problemas del EAM son los materiales disponibles en el mercado, ya que tienen algunas limitaciones debido a su estructura y características de permeabilidad. En algunos se puede promover la pérdida de agua, que se traduce en cambios de la textura, cambios de color y/o deshidratación superficial, o en contraparte, que puede incluso favorecer la condensación de agua y de esta forma beneficiar la proliferación microbiológica (Rojas-Graü et al., 2009b).
Bajas concentraciones de O2 inhiben el crecimiento de microorganismos aerobios, pero pueden estimular el crecimiento de microorganismo anaerobios psicrótrofos, incluyendo algunos de los patógenos transmitidos por alimentos (Rojas-Graü et al.,
2009b). Szabo et al. (2000) aislaron Yersinia enterocolitica, Aeromonas hydrophila, A. caviae y Listeria monocytogenes de lechuga cortada mínimamente procesada envasada en atmósfera modificada. El EAM tradicional rara vez es suficiente para garantizar la inocuidad y lograr productos de alta calidad.
La mayoría de los sistemas de EAM utilizados actualmente, por sí solos no previenen con eficacia los procesos de oscurecimiento y deterioro, que se activan cuando la integridad del tejido es dañado como consecuencia de las operaciones del procesamiento mínimo (Rojas-Graü et al., 2009b).
2.3.
Aceites esenciales
Los aceites esenciales, también llamados volátiles o etéreos aromáticos, son líquidos aceitosos obtenidos a partir de partes de la planta: flores, brotes, semillas, hojas, ramas, corteza, hierba, madera, frutas y raíces (Serrano et al., 2008). Los aceites esenciales han sido utilizados como aromatizantes de alimentos, pero como en los últimos años ha existido una presión por parte de los consumidores para reducir o eliminar los aditivos químicamente sintetizados en los alimentos, los aceites esenciales y sus componentes puros están ganando un creciente interés por sus propiedades antioxidantes y antimicrobianas (Rojas-Graü et al., 2009a).
Los aceites esenciales, en conjunto, muestran una actividad antioxidante. Su fraccionamiento ha indicado que el componente principal responsable del efecto antioxidante del orégano es el carvacrol (Milos et al., 2000), del tomillo el timol (Lee et al., 2005), el eugenol en el clavo de olor (Lee y Shibamoto, 2001), eucaliptol en el eucalipto (Amakura et al., 2002) y mentol en la menta (Shan et al., 2005). Tanto el eugenol, como el timol y el carvacrol son compuestos fenólicos
13 - 27
(Serrano et al., 2008) con actividad antioxidante y antimicrobiana.
Además, las propiedades antimicrobianas de los aceites esenciales han sido reconocidas empíricamente desde hace siglos, pero es en las últimas décadas que se realizaron investigaciones al respecto. La Tabla V muestra algunos de los aceites esenciales más comunes, así como el principal componente utilizado en la industria alimentaria con la descripción de los antioxidantes o propiedades antimicrobianas in vitro (Serrano et al., 2008).
La primordial actividad biológica y el posible uso de los aceites esenciales en la industria alimentaria se derivan de su capacidad antimicrobiana. Aunque el mecanismo exacto de acción de los aceites esenciales no sea completamente claro, algunos autores lo han atribuido a su hidrofobicidad, lo que les permite crear particiones y desbalancear el equilibrio de los iones celulares. Las principales desventajas del uso de estos compuestos naturales se
Tabla V. Aceites esenciales y sus componentesa
Nombre común Nombre científico
Fuente Componente mayoritario
relacionan con la persistencia de aromas fuertes que a veces afectan a las propiedades sensoriales de los alimentos (Serrano et al., 2008). Min y Krochta (2005) indicaron que la aplicación directa de agentes antimicrobianos en la superficie de los alimentos puede tener beneficios limitados, debido a que la actividad de las sustancias puede ser neutralizada o difundidas de la superficie hacia el interior del alimento, lo que podría limitar su efecto.
2.1.
Películas comestibles
Las películas comestibles han sido utilizadas para mantener la calidad y prolongar la vida de anaquel de algunos vegetales cortados mínimamente procesados, tales como cítricos, manzanas y pepinos. Las frutas y hortalizas son generalmente cubiertas por inmersión o aspersión con una amplia gama de materiales, en donde una membrana semipermeable se forma en la superficie para suprimir la respiración, controlar la pérdida de humedad y proporcionar otras funciones (Lin y Zhao, 2007).
AntioxidanteAntifúngicoAntibacterial
ClavoBroteEugenolLípido PenicilliumListeria monocytogenes
Syzygium aromaticum
Hoja AspergillusLactobacillus sakei
EucaliptoHojaEucaliptolÁcido tiobarbitúrico
Eucalyptus globulus
Menta Mentha canadensis
MaderaEucaliptoneDPPH
Hongos y levaduras Bacterias patógenas
HojaMentolABTS Botrytis Bacterias patógenas
OreganoHojaEugenolPeroxidasa BotrytisShigella sp. FlorCarvacrol Fusarium
Origanum vulgare
Timol Clavibacter
TomilloHojaCarvacrolAldehído/ Aspergillus Bacterias patógenas p-CimenoÁcido carboxílico
Thymus vulgaris
a Adaptado de Serrano et al. (2008)
Timol
Sin embargo, las películas y recubrimientos comestibles han sido reconocidos por usos más innovadores, ya que tienen un alto potencial para acarrear ingredientes activos como agentes anti-oscurecimiento, colorantes, saborizantes, nutrientes, especias y compuestos antimicrobianos que pueden extender la vida útil del producto y reducir el riesgo de crecimiento de patógenos en la superficie de los alimentos (Rojas-Graü et al., 2009a). Formuladas adecuadamente, su uso otorga beneficios potenciales (Figura 2) que incluyen (Lin y Zhao, 2007):
Protección contra la pérdida de humedad en la superficie de los productos. La pérdida de humedad durante el almacenamiento postcosecha de frutas y hortalizas conduce a la pérdida de peso y cambios en la textura, sabor y apariencia.
Barrera a los gases, suficiente para controlar el intercambio de gases entre el producto y la atmósfera circundante; lo cual disminuye la tasa de respiración y demora el deterioro. También podría retrasar la oxidación enzimática y proteger a los productos de oscurecimiento y ablandamiento durante el almacenamiento.
Restringe el intercambio de compuestos volátiles entre el producto fresco y su entorno, lo que evita la pérdida de compuestos volátiles aromáticos y componentes de color; así como la adquisición de olores extraños.
Protege contra daño físico causado por impactos mecánicos, presión, vibración, y otros factores mecánicos.
Transporta ingredientes funcionales.

Figura 2. Propiedades funcionales de una película comestible en las frutas y hortalizas mínimamente procesadas (Adaptado de Lin y Zhao, 2007).
Existe una amplia gama de compuestos que pueden ser utilizados en la formulación de películas comestibles y su elección depende principalmente del objetivo de su aplicación. Los principales componentes son polisacáridos, proteínas y lípidos. Otros componentes incluyen polioles que actúan como plastificantes (como glicerina) o compuestos ácido/base utilizados para regular el pH (como el ácido acético o láctico) (Vargas et al., 2008).
Los polisacáridos son los componentes más utilizados en películas comestibles para frutas, ya que están presentes en la mayoría de las formulaciones disponibles en el mercado. Muestran propiedades eficaces de barrera a los gases a pesar de que son hidrófilicos y una alta permeabilidad al vapor de agua en comparación con las películas de plástico comerciales. Los polisacáridos principales que se pueden incluir en las formulaciones de películas comestibles son el almidón y sus derivados, derivados de la celulosa, alginatos, carragenina, quitosano, pectina y gomas. Los polisacáridos varían en función de su peso molecular, grado de ramificación, la conformación y carga eléctrica. Las variaciones en estas características moleculares conducen a variaciones en su capacidad para formar revestimientos, así como en las variaciones de las propiedades físicoquímicas y el rendimiento de los recubrimientos formados. La mayoría de ellos son muy solubles en agua, por lo que no pueden ser utilizados para muestras que están sometidas a ambientes de alta humedad relativa. En algunos casos, se requieren tratamientos de entrecruzamiento con la presencia de iones monovalentes y bivalentes, para que se puedan formar las películas insolubles (Vargas et al., 2008).
Las proteínas que pueden ser utilizadas en la formulación de películas comestibles para frutas y hortalizas incluyen derivados de origen animal, como la caseína y proteína de
suero de leche, o bien se obtienen de plantas como el maíz, gluten de trigo, proteína de soya, proteína de cacahuate y las proteínas de semillas de algodón. Las proteínas presentan una amplia variedad de características moleculares en función de su origen biológico. Por ejemplo, las proteínas pueden variar en su peso molecular, conformación (globular, hélice), características eléctricas, flexibilidad y estabilidad térmica. Las diferencias en estas características moleculares, determinan la capacidad particular de formar la película e influyen en las características finales de la película formada (Rojas-Graü et al., 2009b).
Los lípidos usualmente utilizados en el desarrollo de películas comestibles son la cera de abeja, triglicéridos, monoglicéridos acetilados, ácidos grasos, alcoholes grasos y ésteres de ácidos grasos de sacarosa. Los recubrimientos comestibles con base en lípidos tienen una baja afinidad por el agua, por ende baja permeabilidad al vapor de agua. Esto último es muy importante, ya que un gran número de estudios han utilizado este tipo de recubrimientos sobre frutas y hortalizas frescas para controlar la deshidratación. En la formulación de la película, la polaridad de los componentes lípidos tiene que ser considerada, a medida que el número de carbonos de alcoholes grasos y ácidos grasos aumenta (de 14 a 18), también lo hace su eficacia para actuar como barrera contra la humedad y como consecuencia, la transferencia de humedad a través de la película (Morillon et al., 2002).
Rojas-Graü et al. (2007b) combinaron la eficacia de las películas comestibles de alginato con el efecto antimicrobiano de aceites esenciales (té limón y orégano) y vainilla, para prolongar la vida de anaquel de manzanas cortadas mínimamente procesadas, envasadas en atmósfera modificada pasiva. Observaron una reducción de cuatro ciclos logarítmicos en la población de Listeria innocua inoculada en las muestras, cuando se incorporaron a la película los aceites
esenciales de orégano y té limón. Películas comestibles elaboradas con suero de leche en polvo, proteína de soya y caseinato de calcio, aplicadas a manzana cortada, zanahoria, y papa redujeron los cambios de color y la pérdida de peso (Shon y Haque, 2007).
En general el tratamiento con películas comestibles alarga la vida de anaquel de las frutas y hortalizas mínimamente procesadas, algunos autores han reportado que la incorporación de agentes antimicrobianos a la película, puede impartir modificaciones sensoriales indeseables en los alimentos, especialmente los aceites esenciales (RojasGraü et al., 2009b).
2.4. Nanotecnología
Una nueva generación de películas comestibles se está desarrollando, con el objetivo de permitir la incorporación o la liberación controlada de compuestos activos utilizando la nanotecnología, como es la nanoencapsulación y sistemas multicapa (Bouwmeester et al., 2007). La micro y nanoencapsulación de compuestos activos con películas comestibles puede ayudar a controlar la liberación de estos bajo ciertas condiciones específicas, protegiéndolos así del calor, la humedad u otra condición extrema, mejorando de esta forma su estabilidad y viabilidad (Jiménez et al., 2004).
Por otra parte el uso de nanolaminados o sistemas multicapa ofrece perspectivas prometedoras, en donde las superficies de las frutas u hortalizas son recubiertas con películas interfaciales que constan de múltiples nanocapas. La preparación de estructuras multicapa consiste en la inmersión consecutiva del sustrato en dos o más soluciones que contienen especies de carga opuesta, además de agentes funcionales como antimicrobianos, antioxidantes, enzimas, o vitaminas, entre otros (Vargas et al., 2008).
Conclusiones
El concepto de utilizar múltiples tecnologías en la preservación de frutas y hortalizas mínimamente procesadas, para alargar la vida de anaquel, mejorar su calidad y asegurar su inocuidad es un ejemplo de la aplicación de métodos combinados. Se puede esperar que la combinación de aceites esenciales adicionados a películas comestibles, junto con el envasado en atmósferas modificadas presenten interacciones sinérgicas o antagónicas para la conservación de frutas y hortalizas. Por lo anterior, el conjunto de tecnologías o tratamientos propuestos para una fruta u hortaliza mínimamente procesada en específico, debe ser estudiado para comprender los mecanismos de acción que afectan al vegetal desde el punto de vista fisiológico, microbiológico, físicoquímico y sensorial, y de esta manera garantizar su inocuidad y el éxito en su comercialización.
A lo largo de esta revisión se observó que existen diversos trabajos sobre las aplicaciones de películas comestibles adicionadas con aceites esenciales como antimicrobianos en frutas; sin embargo, debido a la incompatibilidad en lo que respecta al aspecto sensorial, no se ha desarrollado una aplicación en la industria. Se recomienda realizar estudios sobre la aplicación de dichas películas en hortalizas, sobre todo en lo que respecta a hojas verdes, ya que pueden tener mejor compatibilidad desde el punto de vista sensorial al ser utilizadas en diversos platillos que usualmente son aderezados y que contienen entre sus ingredientes especies, que son fuentes de los aceites esenciales, como el clavo, ajo, orégano, entre otros.
El uso de la nanotecnología en películas comestibles para la liberación controlada de componentes activos es una tecnología relativamente nueva, en la cual se han observado pocas investigaciones con aplicaciones en frutas y hortalizas, que pueden
representar un campo de oportunidad; ya que además de las ventajas que el uso de las películas comestibles implica, estos productos pueden enriquecerse desde un punto de vista nutrimental.
Agradecimientos
Pérez-Pérez E. P. agradece al Consejo Nacional de Ciencia y Tecnología (CONACyT) y a la Universidad de las Américas Puebla, por el financiamiento de sus estudios de posgrado.
processed fruits and vegetables. Food Technology. 55:41-51.
Burt, S. 2004. Essential oils: their antibacterial properties and potential applications in foods: a review. International Journal of Food Microbiology. 94:223-253.
Guillaume, C., Guillard, V., y Gontard, N. 2011. Modified atmosphere packaging of fruits and vegetables modeling approach. En: O. MartínBelloso y R. Soliva-Fortuny (Eds). Advances in Fresh-Cut Fruits and Vegetables Processing. Boca Raton. pp. 255-284.
Huxsoll, C. C., y Boilin, H. R. 1989. Processing and distribution alternatives for minimally processed fruits and vegetables. Food Technology. 43:124-128.
Referencias
Ahvenainen, R. 1996. New approaches in improving the shelf life of minimally processed fruits and vegetables. Trends in Food Science & Technology 7:179-186.
Amakura, Y., Umino, Y., Tsuji, S., Ito, H., Hatano, T., y Yoshida, T. 2002. Constituents and their antioxidative effects in eucalyptus leaf extract used as a natural food additive. Food Chemistry. 77:4756.
Ayala-Zavala, J. F., y González-Aguilar, G. A. 2011. Use of additives to preserve the quality of fresh-cut fruits and vegetables. En: O. Martín-Belloso y R. Soliva-Fortuny (Eds). Advances in Fresh-Cut Fruits and Vegetables Processing. Boca Raton. pp. 231254.
Baldwin, E. A., y Bai, J. 2011. Physiology of fresh-cut fruits and vegetables. En: O. Martín-Belloso y R. Soliva-Fortuny (Eds). Advances in Fresh-Cut Fruits and Vegetables Processing. Boca Raton. pp. 87-113.
Beuchat, L. R. 1996. Pathogenic microorganisms associated with fresh produce. Journal of Food Protection. 59:204-216.
Bouwmeester, H., Dekkers, S., Noordam, M., Hagens, W., Bulder, A., y de Heer, C. 2007. Health impact of nanotechnologies in food production. RIKILT report 2007.014
Breidt, F., y Fleming, H. P. 1997. Using lactic acid bacteria to improve the safety of minimally
IFPA, International Fresh-cut Produce Association. 2005. The convenience, nutritional value and safety of fresh-cut produce. Disponible: http://www.gov. on.ca/GOPSP/en/graphics/053125.pdf. Accesada: 17/07/08. Citado en Rojas-Graü, A., Garner, E., y Martín-Belloso, O. (2011). The fresh-cut fruit and vegetables industry current situation and market trends. En: O. Martín-Belloso y R. Soliva-Fortuny (Eds). Advances in Fresh-Cut Fruits and Vegetables Processing. Boca Raton. pp. 1-11.
Jiménez, M., García, H. S., y Beristain, C. I. 2004. Spray-drying microencapsulation and oxidative stability of conjugated linoleic acid. European Food Research and Technology. 219: 588-592.
Lee, K. G., y Shibamoto, T. 2001. Antioxidant property of aroma extract isolated from clove buds (Syzygium aromaticum L.). Food Chemistry. 74: 443-448.
Lee, S. J., Umano, K., Shibamotto, T., y Lee, K. G. 2005. Identification of volatile components in basil (Ocimun basilicum L.) and thyme leaves (Thymus vulgaris L.) and their antioxidant properties. Food Chemistry. 91:131-137.
Leistner, L. 2000. Hurdle technology in the design of minimally processed foods. En: S. M., Alzamora, M. S., Tapia, y A., López-Malo (Eds.). Minimally Processed Fruits and Vegetables: Fundamental Aspects and Applications. Springer, Nueva Delhi, India, pp. 1-52.
Lin, D. y Zhao, Y. 2007. Innovations in the development and application of edible coatings for fresh and minimally processed fruits and vegetables. Comprehensive Reviews in Food Science and Food Safety. 6:60-75.
Milos, M., Mastelic, J., y Jerkovic, I. 2000. Chemical composition and antioxidant effect of glycosidically bound volatile compounds from oregano (Origanum vulgare L. ssp. hirtum). Food Chemistry. 71: 79-83.
Min, S., y Krochta, J. M. 2005. Inhibition of Penicillium commune by edible whey protein films incorporating lactoferrin, lactoferrin hydrolysate, and lactoperoxidase systems. Journal of Food Science. 70: M87-M94.
Morillon, V., Debeafort, F., Blond, G., Capelle, M., y Voilley, A. 2002. Factors affecting the moisture permeability of lipid-based edible films: A review. Crit. Rev. Food Sci. Nutr. 42:67–89.
Parish, M. E., Beuchat, L. R., Suslow, T. V., Harris, L. J., Garret, E. H., Farber, J. N., Busta, F. F. 2003. Methods to reduce/ eliminate pathogens from fresh and fresh-cut produce. Comprehensive Reviews in Food Science and Food Safety. 2(1):161-173.
Prasanna, V., Prabha, T. N., y Tharanathan, R. N. 2007. Fruit ripening phenomena. Critical Reviews in Food Science and Nutrition. 47:1-19.
Ragaert, P., Jacxsens, L., Vandekinderen, I., Baert, L., y Devlieghere, F. 2011. Microbiological and safety aspects of fresh-cut fruits and vegetables. En: O. Martín-Belloso y R. Soliva-Fortuny (Eds). Advances in Fresh-Cut Fruits and Vegetables Processing Boca Raton. pp. 53-86.
Rico, D. Martín-Diana, A. B. Barat, J. M. y Barry-Ryan, C. 2007. Extending and measuring the quality of fresh-cut fruit and vegetables: a review. Trends in Food Science & Technology. 18:373-386.
Rojas-Graü, M. A., Grasa-Guillem, R., y MartínBelloso, O. 2007a. Quality changes in fresh-cut fuji apple as affected by ripeness stage, antibrowning agents, and storage atmosphere. Journal of Food Science. 72(1):S36-S43.
Rojas-Graü, M. A. Raybaudi-Massilia, R. M. SolivaFortuny, R. C. Avena-Bustillos, R. J. McHughb, T. H. Martín-Belloso, O. 2007b. Apple puree-alginate edible coating as carrier of antimicrobial agents to
prolong shelf-life of fresh-cut apples. Postharvest Biology and Technology. 45:254-264.
Rojas-Graü, M. A., Soliva-Fortuny, R., y MartínBelloso, O. 2009a. Edible coatings to incorporate active ingredients to fresh cut fruits: a review. Trends in Food Science & Technology. 20: 438-447.
Rojas-Graü, M. A. Oms-Oliu, G. Soliva-Fortuny, R. y Martín-Belloso, O. 2009b. The use of packaging techniques to mantain freshness in fresh-cut fruits and vegetables: a review. International Journal of Food Science and Technology. 44:875-889.
Serrano, M,. Martínez-Romero, D., Guillén, F., Valverde, J. M., Zapata, P. J., Castillo, S., y Valero, D. 2008. The addition of essential oils to MAP as a tool to maintain the overall quality fruits. Trends in Food Science & Technology. 19: 464-471.
Shan, B. S., Cai, Y. Z., Sun, M., y Corke, H. 2005. Antioxidant capacity of 26 spice extracts and characterization of their phenolic constituents. Journal of Agricultural and Food Chemistry. 53: 7749-7759.
Shon, J., y Haque, Z. U. 2007. Efficacy of sour whey as a shelf-life enhancer: Use an antioxidative edible coating of cut vegetables and fruit. Journal of Food Quality. 30:581-593.
Soliva-Fortuny, R. C. y Martín-Belloso, O. 2003. New advances in extending the shelf-life of fresh-cut fruits: a review. Trends in Food Science & Technology. 14:341-353.
Szabo, E. A., Scurrah, K. J., y Burrows, J. M. 2000. Survey for psychrotrophic bacterial pathogens in minimally processed lettuce. Letters of Applied Microbiology. 30:456-460.
Vargas, M., Pastor, C., Chiralt, A., McClements, D. J., y González-Martínez, C. 2008. Recent advances in edible coatings for fresh and minimally processed fruits. Crit. Rev. Food Sci. Nutr. 48: 496-511.
Watada, A. E., Ko, N. P., y Minott, D. A. 1996. Factors affecting quality of fresh-cut horticultural products. Postharvest Biology and Technology. 9:115-125.

Temas Selectos de Ingeniería de Alimentos 5 - 2 (2011): 28 - 39

Escherichia coli de tipo patógeno en alimentos y modelación de su inactivación al aplicar diversos factores de conservación
E. Romero*, A. López-Malo y E. Palou
Departamento de Ingeniería Química, Alimentos y Ambiental, Fundación Universidad de las Américas Puebla. Exhacienda Sta. Catarina Mártir S/N, Cholula, Puebla. C.P.72810. México.
Resumen
Escherichia coli es un microorganismo de gran interés tanto en la industria de los alimentos como en la investigación debido, entre otras razones, a la capacidad de algunos de sus tipos para causar daño a la salud del ser humano. Es por ello que en el presente trabajo se hace una revisión sobre la información de mayor interés referente a E. coli de tipo patógeno, a su presencia en los alimentos, daños causados a la salud, así como a los factores que se emplean para su inactivación y estudios que se han llevado a cabo para predecir su respuesta al modelar su inactivación cuando se aplican de manera combinada diversos factores de conservación.
Palabras clave: Escherichia coli patógena, inactivación, modelación.
Abstract
Pathogenic E. coli is a microorganism of great interest for the food industry and for research projects as well, due to its capacity to cause harm to human health. For this reason this manuscript reviews important information regarding E. coli, its presence on foods, impact on human health, as well as preservation factors used for its inactivation and research that has been performed to predict its behavior by modeling its inactivation when several preservation factors are combined.
Keywords: pathogenic E. coli, inactivation, modeling.
Introducción
Existen alimentos para consumo humano que por su naturaleza o por el mal manejo durante su producción, son portadores de microorganismos causantes de daño a la salud del ser humano (microorganismos patógenos). En particular, Escherichia coli es una bacteria coliforme, de gran
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: ehira.romerocn@udlap.mx
interés para los productores de alimentos y el sector salud, ya que algunas de sus cepas poseen la capacidad de causar infecciones intestinales en el ser humano. Para eliminar E. coli en la industria de los alimentos se utilizan tratamientos como adición de antimicrobianos, altas temperaturas, cambios de pH y control de actividad de agua, entre otros. No obstante, no se conocen con exactitud los parámetros necesarios de estos tratamientos cuando actúan en combinación.
Por otro lado, para tomar decisiones relacionadas con la inactivación de
microorganismos en alimentos, se utiliza la microbiología predictiva, que consiste en el desarrollo y aplicación de expresiones matemáticas para describir la inactivación o los procesos bioquímicos de los microorganismos (Alzamora et al., 2001). De aquí que el objetivo de este artículo sea hacer una revisión sobre la información de mayor interés referente a esta bacteria en los alimentos, así como diversos estudios que se han llevado a cabo al modelar su inactivación cuando se aplican de forma combinada factores de conservación.
Revisión bibliográfica
2.1. Escherichia coli en alimentos
Escherichia coli es un bacilo de tamaño pequeño, alargado, casi siempre móvil, Gram negativo, no esporulado, anaerobio facultativo de la familia Enterobacteriaceae que se reproduce rápidamente en el intestino del ser humano; es capaz de fermentar tanto glucosa como fructosa (Pascual y Calderón y Pascual, 2000; Rodríguez-Ángeles, 2002).
2.1.1. Tipos patógenos de E. coli
Se han estudiado alrededor de 200 cepas que pueden causar enfermedades diarreicas así como del tracto urinario y que pueden poner en peligro la vida del paciente (Madigan et al., 2003). Por ello, con base en su mecanismo de patogenicidad y cuadro clínico, las cepas de E. coli causantes de diarrea se clasifican en seis grupos: enterotoxigénica (ECET), enterohemorrágica (ECEH), enteroinvasiva (ECEI), enteropatógena (ECEP), enteroagregativa (ECEA) y de adherencia difusa (ECAD) (Rodríguez-Ángeles, 2002).
2.1.1.1. E. coli enterotoxigénica
Su principal mecanismo de patogenicidad es la síntesis de toxina termolábil (TTL) y toxina termoestable (TTE), las cuales aumentan el nivel intracelular de cAMP (3'-5'-monofosfato de adenosina cíclico) y cGMP (monofosfato de guanosina cíclico) respectivamente, que se
encuentran en la membrana de las células intestinales, provocando la salida de agua y iones (Sears y Kapper, 1996). Las cepas ECETs son importantes en lactantes y la frecuencia de aislamiento de este grupo patógeno de E. coli en niños con diarrea es de 10 a 30%. En los niños en edad escolar y en adultos puede ser asintomática. La enfermedad tiene un periodo de incubación de 14 a 50 h y el cuadro clínico se caracteriza por diarrea aguda, generalmente sin sangre, sin moco, sin pus y en pocos casos se presentan fiebre y vómito. La diarrea producida por cepas ECETs puede ser leve, breve y autolimitada pero también puede ser grave (Nataro y Kapper, 1998). La contaminación fecal de agua y alimentos es la principal fuente de infección, siendo la dosis infectiva de 108 UFC (unidades formadoras de colonias) (Rodríguez-Ángeles, 2002).
2.1.1.2. E. coli
enterohemorrágica
Esta cepa es productora de una citotoxina con actividad en células Vero, por lo que se le llama verotoxina (VT), y a las cepas capaces de producirla se les denomina E. coli verotoxigénicas (ECVT) (Riley et al., 1983). Además de la toxina, las cepas ECEHs tienen otros mecanismos de patogenicidad como el fenómeno de adherencia y esfacelación (desprendimiento de tejido y formación de necrosidad) (A/E) así como el plásmido pO157 (el cual está constituido por fragmentos de ácidos nucleicos y que contiene el gen de la hemolisina) (Schmidt et al., 1995; Donnenberg et al., 1993; Huguet et al., 2002). En función de la presencia de sus factores de patogenicidad E. coli se clasifica en: a) cepas típicas cuando tienen el fago, el plásmido y presentan el fenómeno A/E y b) cepas atípicas, cuando no producen lesiones de A/E y pueden presentar o no el plásmido. Además, entre las cepas ECEHs se encuentran los serotipos E. coli O157:H7 y los no-O157:H7 que son alrededor de 200. El periodo de incubación de ECEH es de uno a ocho días; inicialmente produce diarrea sin sangre, con o sin vómito, dolor abdominal, fiebre, y después de uno a dos días puede encontrarse sangre en las heces y se intensifica el dolor abdominal. Después de cuatro a diez días las heces son abundantemente sanguinolentas (RodríguezÁngeles, 2002).
2.1.1.3. E. coli enteroinvasiva
Es una cepa descarboxilasa negativa, no móvil y lactosa negativa que ataca invadiendo el epitelio del colon. Para ello el primer paso es la adherencia de la bacteria a las vellosidades de la mucosa requiriendo de mucinasa y adhesinas, para después entrar por endocitosis a la célula y posterior multiplicación de la misma dentro de la célula afectada y diseminación a las demás células sanas. Además produce enterotoxinas que se relacionan con la producción de diarrea (Nataro y Kapper, 1998). Los síntomas característicos en personas infectadas por cepas ECEIs son diarrea acuosa, con sangre y moco, o únicamente diarrea. Las cepas ECEIs se asocian más con brotes que con casos aislados (Rodríguez-Ángeles, 2002; Eslava et al., 1994).
2.1.1.4. E. coli enteropatógena
Esta cepa actúa por adherencia entre la bacteria y la membrana de las células del epitelio intestinal, seguida de la destrucción de la microvellosidad, con polimerización de actina, que lleva a la alteración del citoesqueleto en donde se adhiere la bacteria ( Eslava et al., 1994; Nataro y Kapper, 1998). Las cepas ECEPs pueden ocasionar brotes o casos aislados de diarrea aguda, vómito y fiebre baja así como mala absorción y afecta principalmente a niños menores de dos años; sin embargo, se aísla en adultos enfermos o sanos con alguna predisposición como la diabetes. La forma de transmisión de la enfermedad es fecal-oral por manos contaminadas de manipuladores de alimentos (Rodríguez-Ángeles, 2002).
2.1.1.5. E. coli enteroagregativa
Son cepas cuya forma de actuar es mediante la adherencia agregativa caracterizada por autoaglutinación inespecífica de las bacterias entre sí. En el mecanismo de patogenicidad las cepas ECEAs incrementan la secreción de moco y éste atrapa a las bacterias autoaglutinadas en una fina película en el epitelio intestinal, lo cual se relaciona con producción de diarrea. Las cepas de ECEAs tienen como sitio blanco la mucosa del intestino grueso y delgado; su periodo de incubación es de menos de ocho horas y puede
durar hasta 18 o 20 días. La infección causada por estas cepas se manifiesta con diarrea líquida y alta secreción de moco con o sin sangre y sin o con poca fiebre (Nataro y Kapper, 1998; RodríguezÁngeles, 2002).
2.1.1.6. E. coli de adherencia difusa
Esta cepa no forma microcolonias cuando se adhiere a las células y más bien, este fenómeno de adherencia difusa se ha asociado con una proteína de membrana externa (Rodríguez-Ángeles, 2002). El grupo ECAD se puede aislar tanto de personas sanas como de personas con diarrea, siendo más importante en niños de 4 a 5 años. El principal síntoma que se presenta es diarrea acuosa sin sangre y sin leucocitos (Nataro y Kapper, 1998, Rodríguez-Ángeles, 2002).
2.1.2. Condiciones óptimas de crecimiento
E. coli es una bacteria que crece a una temperatura mínima de 7-8°C y máxima de 44-46°C; no obstante, su temperatura óptima está entre los 35°C y 40°C. Por otro lado, se reproduce de una mejor manera cuando se encuentra un pH entre 6 y 7, aunque tolera como mínimo 4.4 y como máximo 9. Sin embargo, particularmente. E. coli O157:H7 tolera condiciones de acidez más bajas que las demás cepas. Esto le permite permanecer incluso en el medio ácido del estómago sin verse afectada. En cuanto a la actividad de agua, E. coli se desarrolla óptimamente en medios con aw 0.995, pero también se manifiesta a aw 0.95 (Michanie, 2003).
2.1.3. Alimentos susceptibles
E. coli se origina de las canales de los animales sacrificados y debido a que la mayoría de sus cepas sobreviven por poco tiempo en el ambiente extraentérico, su presencia en los alimentos indica contaminación reciente (Pascual y Calderón y Pascual, 2010). Dado que crece en el intestino y se encuentra en la material fecal, se puede encontrar en bovinos, cabras, borregos y con menos frecuencia en cerdos y pollos; siendo su principal reservorio el intestino del ganado bovino. Por esto suele encontrarse en carne de res, sobre todo cuando no es bien cocida como en la carne molida
para hamburguesas o incluso se han encontrado brotes en roast beef (Madigan et al., 2003).
Por otro lado, existen alimentos que funcionan como vehículo de la bacteria; tal es el caso de las verduras frescas como la lechuga, rábanos, alfalfa, entre otras (Rodríguez-Ángeles, 2002; Madigan et al., 2003). Asimismo, se han reportado brotes asociado al consumo en productos industrializados como mayonesa y jugos de naranja y manzana no pasteurizados, aun cuando estos alimentos tengan un pH de 3.4, condición en la que puede sobrevivir varios días (Rodríguez-Ángeles, 2002).
Otros alimentos susceptibles al crecimiento de E. coli son algunos embutidos como el salami, rollos de carne curada, leche cruda sin pasteurizar, productos lácteos elaborados a partir de leche sin pasteurizar, aguas contaminadas, entre otros (ANMAT, 2008).
2.1.4. Enfermedades y epidemiología
Las diferentes cepas patógenas de E. coli son capaces de producir enfermedades tales como gastroenteritis leve o severa ocasionada por la diarrea no sanguinolenta, colitis hemorrágica ocasionada por la diarrea sanguinolenta, síndrome urémico hemolítico (SUH) que ocasiona una insuficiencia renal y en algunos casos anemia hemolítica (ANMAT, 2008).
E. coli se transmite mediante el consumo de alimentos insuficientemente cocidos o crudos, ingestión de agua contaminada, contacto persona a persona y contacto con materia fecal de animales (Michanie, 2003). Su distribución es mundial y es de particular importancia en los países con climas tropicales y en países subdesarrollados, en lugares de hacinamiento y con malas condiciones de higiene (Romero y Herrera, 2002).
Uno de los primeros brotes reportados fue el que afectó al menos a 47 personas en Oregon y Michigan, EE.UU., en 1982; en donde los pacientes presentaban dolor abdominal tipo cólico, diarrea acuosa y poca o ninguna fiebre. En este caso se asoció el brote al consumo de alimentos en una cadena de restaurantes de comida rápida y con el consumo de cualquiera de los tres sándwiches
que contenían tres ingredientes en común (hamburguesa de carne de vacuno, cebolla rehidratada, y encurtidos) en donde se descubrió Escherichia coli, O157:H7; sólo se conocía anteriormente de dicho serotipo un caso esporádico de colitis hemorrágica en 1975 (Riley et al., 1983).
Más tarde, en 1993, nuevamente surgieron más de 700 brotes de la misma cepa y serotipo en EE.UU., debido al consumo de hamburguesas en la cadena de comidas rápidas “Jack in the Box”. Se produjeron además de enfermos, cuatro muertos y millones de pérdidas para la empresa y el gobierno; sin embargo se observó que E. coli interactuaba con Shigella y que generaba una enterotoxina. La infección se asoció con el consumo en los 10 días anteriores a la aparición de los síntomas, de una hamburguesa regular en un restaurante de la cadena en Washington D.C. (EE.UU.), la cual había sido poco cocida (por debajo de 60°C); una vez identificado el problema se tuvieron que retirar del mercado 250.000 hamburguesas potencialmente contaminadas. A partir de este suceso se llevó a cabo la modificación de la legislación de los EE.UU. en cuanto a la temperatura de cocción de las hamburguesas y se desencadenó la aplicación del Sistema APPCC – Análisis de Peligros y Puntos Críticos de Control – en la industria de la carne de ese país y en los países que exportan alimentos a dicho destino (Bell et al., 1994; Michaine, 2003).
Otro brote importante fue el ocurrido en Japón, en la ciudad de Sakai, en 1996, en el que 7000 personas fueron infectadas al consumir rábano rojo contaminado con E. coli O157:H7 al parecer proveniente de las semillas del vegetal (Mermin y Griffin, 1999). En 2006, en EE.UU., 205 personas enfermaron de síndrome hemolítico urémico y tres fallecieron, nuevamente debido a E. coli O157:H7 encontrada en espinacas frescas envasadas, provenientes de California (INFOSAN, 2007).
En mayo de 2011 nuevamente surgió un brote en Alemania y se propagó por diversos países de Europa Central; en este caso la cepa responsable fue ECEH O104:H4 con producción de shigatoxina (vtx2a). En esta epidemia se reportaron al Instituto Robert Koch 4,321 casos, en los que 852 presentaron síndrome urémico hemolítico; en total murieron 50 pacientes, de los cuales 32
presentaban el síndrome. Además, 76 personas más fuera de la Unión Europea fueron contaminadas, de éstas 49 presentaron síndrome urémico hemolítico y una falleció. Se encontró que la causa fue el consumo de semillas germinadas de soya y frijol ocho días antes del brote, provenientes de una compañía del estado Niedersachsen de Alemania (Robert Koch Institute, 2011).
2.2. Inactivación de Escherichia coli
Como se ha comentado, existen cepas de E. coli que han causado daños a la salud del ser humano en las últimas décadas. Es por ello que en la industria de los alimentos se han concentrado esfuerzos para lograr la inactivación de la bacteria.
2.2.1 Tratamientos térmicos
Una temperatura elevada produce mal plegamiento o agregación de las proteínas de E. coli, y se ven afectados procesos celulares como la proteólisis, la síntesis de la pared celular, la división celular, el crecimiento y la replicación del ADN plásmido (Yura et al., 1993); además, se presentan daños en las proteínas citoplasmáticas (Chung et al., 2006).
La destrucción térmica de un patógeno depende en gran medida del tiempo de exposición a las altas temperaturas. Para determinar la eficiencia del tratamiento se utiliza el valor D que puede obtenerse con la siguiente ecuación (Richardson, 2004):
log N= log N0 –t/D (Ec. 1)
Donde N es el número de microorganismos sobrevivientes al tratamiento, N0 es el número inicial de microorganismos, t es el tiempo de calentamiento en minutos y D es el tiempo de reducción decimal en minutos; es decir, es el tiempo para reducir la población microbiana en una unidad logarítmica o para la destrucción del 90% de la población microbiana. Asimismo, se utiliza el valor de z que es el cambio del valor de D al modificar la temperatura; es decir, el número de grados que es necesario aumentar la temperatura para modificar el valor D en una unidad logarítimica y se obtiene de la siguiente ecuación:
log DT= log Dref – (T-Tref)/z (Ec. 2)
Donde DT es el valor en minutos a cualquier temperatura T, Dref es el valor correspondiente a la temperatura de referencia Tref (Richardson, 2004; Griffis y Osaili, 2009).
Se sabe que la inactivación de E. coli comienza alrededor de los 49.5°C o que a 55°C el valor de D es de 6.7 minutos y el de z de 3.6°C (Casp y Abril, 1998; Richardson, 2004; Chung et al., 2006).
2.2.2. Acidificación
El estrés ácido se describe como el efecto biológico de los iones H + (es decir, pH) y el efecto de los ácidos orgánicos que se encuentran en el medio ambiente como resultado de la fermentación o cuando se agregan como agentes conservadores en los alimentos. Los mecanismos de inactivación de E. coli por acidificación consisten en la acidificación intracelular, la cual daña o interrumpe procesos bioquímicos clave (Zhao et al., 1993; Garlant-Miller y Kaspar, 1994; Chung et al., 2006).
A bajos valores de pH (es decir, pH ≤ 3), el ingreso de protones es más rápida que la capacidad de las células para mantener la homeostasis. Los ácidos orgánicos penetran en la membrana celular y se disocian dentro de la célula, lo que produce que el protón liberado reduzca el pH intracelular. A menor pH en el exterior de la bacteria, mayor es el flujo de ácidos orgánicos hacia su interior. Asimismo, el ácido se acumula en la membrana y el constante flujo de protones con el tiempo hace que se agote la energía celular, causando la muerte. Se sabe que E. coli comienza a inhibirse a valores de pH menores a 4 (Bogh-Sorensen, 2003; Chung et al., 2006).
Otra variable de este factor de inactivación es el tipo de ácido y la concentración. Glass et al. (1992) determinaron que los ácidos orgánicos son mejores inhibidores, que por ejemplo el ácido hidroclórico. Asimismo, se ha estudiado que el ácido acético, para inactivar E. coli O157:H7, es mejor que el ácido láctico y éste último a su vez es mejor que el cítrico (Bogh-Sorensen, 2003).
Sin embargo, se ha encontrado que la mayoría de las cepas de E. coli pueden generar tolerancia al ácido en la fase estacionaria y esto no depende de la adaptación sino del medio y de las condiciones de crecimiento, debido a un sistema de oxidación y dos sistemas de resistencia a los ácidos, productos de la fermentación, en donde se involucra la participación de las enzimas glutamato descarboxilasa y arginina descarboxilasa (Lin et al., 1996; Buchanan y Doyle, 1997; Chung et al., 2006).
Es por ello que después de la ingestión de alimentos contaminados con E. coli, las bacterias adaptadass son capaces de sobrevivir al ácido gástrico y colonizar el intestino a través de la competencia con los microorganismos de la flora nativa (Chung et al., 2006).
Otra medida de defensa al ácido es la modificación en la composición de la membrana celular, ya que el contenido de ácidos grasos de la membrana citoplasmática cambia, aumentando los niveles de fosfolípidos. Algo importante de señalar es que se ha encontrado que cuando E. coli sobrevive al tratamiento con ácido, ocurre un efecto antagónico, haciendo una cepa más fuerte y resistente a tratamientos como el cambio de actividad de agua (Brown et al., 1997; Chang y Cronan, 1999; Bogh-Sorensen, 2003; Chung et al., 2006).
2.2.3. Disminución de la actividad de agua
En la industria de los alimentos y a nivel experimental se utiliza como un factor de inhibición microbiana la disminución de la actividad de agua, que se logra al aumentar la cantidad de compuestos osmóticamente activos (solutos) en el medio por la desecación del mismo, con lo cual se aumenta la presión osmótica. En condiciones normales, las células bacterianas mantienen su presión de turgencia, que es una presión osmótica interna superior a la del medio circundante. Como resultado, se ejerce presión hacia el exterior de la pared celular. La presión de turgencia es la fuerza mecánica de elongación normal de las células (Csonka, 1989; Chung et al., 2006).
Cuando la presión osmótica en el entorno es mayor, las células se encogen y ocurre eventualmente plasmólisis con lo que se puede decir que las condiciones de estrés osmótico son parecidas a las condiciones fisiológicas de hambre bacteriana. Además, una baja actividad de agua en las células de E. coli se asocia con la inhibición de la replicación del ADN, el crecimiento celular y la absorción de nutrientes. En E. coli esto sucede cuando la actividad de agua es menor a 0.96 (Csonka, 1989; Chung et al., 2006).
Sin embargo, también existen sistemas osmoreguladores que proporcionan una protección a las bacterias y equilibrio entre la presión intracelular y la presión ambiental, ya sea por el paso activo de solutos cargados o por el paso de solutos compatibles presentes en los alimentos. (Pichereau et al., 1999). En el caso de E. coli, acumula como solutos compatibles betaína y prolina; lo que provoca que aún en medios con actividad de agua baja, E. coli pueda sobrevivir (Gould, 1995; Pichereau et al., 1999; Chung et al., 2006).
2.2.4. Antimicrobianos
Son compuestos químicos que se encuentran en los alimentos, ya sea por su naturaleza o porque se les han añadido, que retardan el crecimiento de los microorganismos o, en su caso, los inactivan; haciendo que los alimentos cuenten con mayor calidad microbiológica (Davidson, 1996).
Los agentes antimicrobianos naturales más utilizandos contra E. coli son carvacrol y timol y entre los sintéticos se encuentra sorbato de potasio; estos tres se utilizan en concentraciones entre 100 y 3000 ppm (Santiesteban, 2002).
García (2005) demostró que para inhibir E. coli se necesitan concentraciones mínimas de carvacrol de 112.5 ppm, de timol de 100 ppm y de sorbato de potasio de 2000 ppm, siendo timol el antimicrobiano más eficaz para la bacteria en cuestión. Lo que sucede durante la inactivación con timol y carvacrol es que estos agentes antimicrobianos disminuyen el contenido de ATP intracelular de los microorganismos, al mismo tiempo que incrementan el ATP extracelular, lo que provoca el rompimiento de las membranas
plasmáticas. En el caso del sorbato de potasio, lo que sucede es que se alteran la morfología, integridad y función de la membrana celular, y se inhiben las funciones de transporte y actividad metabólica. Por otro lado, el sorbato disminuye la asimilación de carbono de algunos sustratos tales como glucosa, acetato, succinato, piruvato, lactato, oxalacetato, entre otros (Sofos, 1989).
2.2.5 Otros factores de inactivación
En la industria alimentaria así como en la investigación, se utilizan otros factores para la inactivación de E. coli. Kim et al. (2007), demostraron que el tratamiento con dióxido de carbono supercrítico (altas presiones) a 100 bares, 35 °C durante 50 min, redujo 8 ciclos logarítmicos la población de E. coli. Además, Aronsson et al. (2001) encontraron que tratar el medio donde se encuentra E. coli O157:H7 con un voltaje de 35kV/cm con 20 pulsos trajo como consecuencia una reducción de 6.2 ciclos logarítmicos.
Por otro lado, para evitar el deterioro de los alimentos tratados con altas temperaturas y la resistencia de los microorganismos a otros factores de conservación como disminución en el pH y actividad de agua, se comenzaron a utilizar los mismos pero de forma combinada. Sevilla y Gabriel (2010) llevaron a cabo un estudio en el que combinaron alta temperatura (hasta 62°C), cambios de pH (3-8) y reducción de la actividad de agua (0.93-0.99), encontrando que la temperatura es el factor más relevante en la inactivación de E. coli y que la combinación con mayor inactivación fue de pH 5.5, aw 0.96 y 62°C.
No obstante, esta combinación no siempre resulta en una situación aditiva (el efecto de uno se suma al del otro) sino que pueden llegar a ocurrir situaciones sinérgicas o antagónicas, por lo que se requiere de una menor o mayor intensidad de los factores (Buchanan y Whiting, 1996; Alzamora y López-Malo, 2002; Palou y López-Malo, 2009). Es por ello que tanto en la industria como en la investigación se emplean modelos matemáticos para predecir la inactivación de E. coli.
2.3 Microbiología predictiva
La microbiología predictiva es una herramienta útil para predecir el comportamiento de los microorganismos y consiste en el desarrollo y aplicación de expresiones matemáticas para describir el crecimiento, la supervivencia, la inactivación o los procesos bioquímicos de los mismos; por lo que es posible pronosticar su inactivación o inhibición en un medio determinado, teniendo resultados confiables para el control de la calidad de un alimento, la predicción de la inocuidad del mismo o la evaluación del riesgo, entre otras aplicaciones (Bozkurt y Erkmen, 1999; Alzamora et al., 2001).
Los modelos de inactivación térmica fueron los primeros ejemplos de microbiología predictiva utilizados en la industria de los alimentos. En éstos se calculaba la inactivación mediante un modelo lineal en el que se tomaba en cuenta la población de un tipo de microorganismo a una temperatura determinada en un lapso de tiempo; de este modelo resultaron los valores D y z (Duffy et al., 2004). En la mayoría de los estudios de inactivación térmica se utiliza para describir el comportamiento un modelo de reacción de primer orden. Hoyle (2000) concluyó que en un tratamiento de 70°C durante 2 minutos se conseguía una inactivación de seis ciclos logarítmicos de E. coli O157:H7; esto lo logró mediante la utilización de un modelo de primer orden con el que calculó el valor de D. El comportamiento de inactivación de E. coli mediante tratamiento térmico es lineal; sin embargo, cuando se utilizan factores combinados el comportamiento es no lineal (Lou y Nakai, 2001).
Hancock et al. (1994) utilizaron un modelo log lineal y otro log logístico y los combinaron. Lo que lograron fue un modelo con el cual concluyeron que la reducción del pH y la adición de NaCl, afectan considerablemente la resistencia térmica de E. coli. Señalaron que se lleva a cabo la inactivación a una mayor velocidad cuando las concentraciones de NaCl no son elevadas y el pH es alto.
Hosein (2010) generó un modelo matemático de primer orden utilizando la fórmula de Weibull, mediante el cual describió la inactivación de E. coli O157:H7 al combinar de 2 a 4% de NaCl, de 0 a 40mM de ácido acético y un pH de 3.2; lo que se encontró fue que un incremento en el ácido acético aumenta la inactivación de E. coli. Asimismo, generó un modelo lineal de segundo orden para determinar el tiempo necesario para reducir la carga de la bacteria en 5 ciclos logarítmicos; sin embargo, encontró que este modelo secundario sobreestimó el tiempo.
Blackburn et al. (1997) utilizaron un modelo log-logístico para describir la inactivación térmica de E. coli O157:H7 cuando se expone a varios valores de pH, ácidos orgánicos y NaCl. Sus resultados indican que un enfoque log-logístico da una mejor descripción de la cinética de muerte en comparación con la cinética de primer orden lineal. Asimismo, se encontró que los ácidos acético y láctico tienen un efecto letal mayor que el ácido clorhídrico; además, que el aumento de la concentración de NaCl tuvo un efecto protector (8.5% p/p).
McQuestin et al. (2009) realizaron un estudio con 44 sistemas en el que investigaron si en la inactivación de E. coli influyen el pH, la actividad de agua y la temperatura, así como el ácido láctico, todo ello sobre carne fermentada. Se utilizaron dos modelos mediante relaciones de Arrhenius con las siguientes ecuaciones:
La primera ecuación (Ec. 3) fue obtenida a través del ajuste de todos los sistemas, en los cuales la temperatura variaba de -20 a 62°C; mientras que en la segunda (Ec.4) se incluyeron únicamente los sistemas con una temperatura de entre 0 y 47°C, resultado de someter los datos de la primera ecuación a una regresión lineal. Lo que encontraron fue que el modelo representado por la Ecuación 4 es más parsimonioso ya que mostró una raíz media cuadrada del error de 1.01, mientras que la de la Ecuación 3 fue de 1.19; además se encontró que los factores causaron efecto de inactivación tanto cuando se utilizaron de modo separado, como cuando se utilizaron en combinación. Asimismo, bajos valores de pH y actividad de agua aumentan la inactivación; sin embargo, el aumento de la temperatura es el principal factor de inhibición, ya que la temperatura influye en la inactivación en un 61% mientras que el pH y la actividad de agua en un 8%.
Hosein (2010) comparó los modelos de Weibull, Gompertz, Cole y el Logístico para la inactivación de E. coli O157:H7 con dos soluciones de sal (NaCl y CsCl), encontrando que para la inactivación con NaCl, el modelo que menos se ajusta a los datos experimentales es el de Gomperz. Por el contrario, para CsCl es el de Cole. Posteriormente comparó estos dos y argumentó que en comparación con el modelo de Cole (loglogístico), el modelo de Gompertz es más adecuado para describir la inactivación de E. coli cuando se emplea como factor de inactivación la adición de alguna sal. El modelo más parsimonioso fue el de Weibull, seguido por el Logístico.
(Ec. 3) 2) ln(TI) =
(Ec. 4)
Donde TI es la tasa de inactivación (log10 UFC/mL/h) y T es la temperatura (°K)
Conclusiones
Es necesario que, en la industria de los alimentos así como en la investigación, se centre la atención sobre las cepas pertenecientes al grupo de E. coli enterohemorrágica para conseguir su inactivación, dado que son las cepas identificadas en la mayoría de los casos de brotes infecciosos por E. coli (en particular E. coli O157:H7) y cuya infección, causa consecuencias más graves sobre la salud del ser humano.
Para ello, se ha encontrado que el contenido de E. coli en los alimentos y en sistemas modelo disminuye cuando se utilizan diversos métodos como el uso de altas temperaturas, reducción de pH, actividad de agua y la adición de carvacrol; no obstante, no existe un trabajo en el que se combinen estos cuatro factores y se modelicen para generar una ecuación capaz de predecir su inactivación.
Asimismo, no existe información detallada sobre el daño específico, a nivel celular, que causan los factores combinados; sin embargo, esta información sería de gran utilidad, ya que con ella se enriquecerían los modelos de predicción, determinando con mayor exactitud los parámetros de los factores de inactivación y su efecto sobre E. coli.
http://www.femeba.org.ar/fundacion/quienessomos/ Novedades/ecolienterohemorragicaprev.pdf. Adquirido: 30/09/11.
Aronsson, K., Lindgren, M., Johansson, B. R. y Rönner, U. 2001. Inactivation of microorganisms using pulsed electric fields: the influence of process parameters on Escherichia coli, Listeria innocua, Leuconostoc mesenteroides and Saccharomyces cerevisiae Innovative Food Science and Emerging Technologies. 2:41-54.
Bell, B. P., Goldoft, M., Griffin, P. M., Davis, M. A., Gordon, D. C., Tarr, P. I., Bartleson, C. A., Lewis, J.H., Barrett, T. J. y Wells, J. G. 1994. A multistate outbreak of Escherichia coli O157:H7-associated bloody diarrhea and hemolytic uremic syndrome from hamburgers. The Washington experience. The Journal of the American Medical Association. 272(17):1349-53.
Agradecimientos
Ehira Romero Castelán agradece el apoyo y financiamiento recibido por el Consejo Nacional de Ciencia y Tecnología de México y la Universidad de las Américas Puebla, para sus estudios de maestría.
Blackburn, C. D. W., Curtis, L. M., Humpheson, L., Billon, C. y McClure. P. J. 1997. Development of thermal inactivation models for Salmonella enteritidis and Escherichia coli O157:H7 with temperature, pH and NaCl as controlling factors. International Journal of Food Microbiology. 38:3144.
Bogh-Sorensen, L. 2003. Food Preservation Techniques. Woodhead Publishing. Inglaterra. 581 p.
Referencias
Alzamora, S. M., Guerrero, S.N., Salvatori, D., LópezMalo, A. y Palou, E. 2001. Herramientas de Microbiología Predictiva. CYTED. Proyecto XI-15. CD-R. Argentina.
Alzamora, S. M. y López-Malo, A. 2002. Microbial behavior modeling as a tool in the design and control of minimally processed foods. En: WeltiChanes, G. Barbosa-Cánovas, J. M. y Aguilera , J. Engineering and Food for the 21st Century. CRC Press. Londres y EE.UU. 1,104 p.
ANMAT (Autoridad Reguladora de Referencia Regional para Medicamentos). 2008. Prevención de infecciones por Escherichia coli enterohemorrágica. Secretaría de Políticas, Regulación y Relaciones Sanitarias Disponible:
Bozkurt, H. y Erkmen, O. 1999. Modeling in protection and prediction of food quality. Journal of Food Technology, 4(1): 63-70.
Brown, C. A., Harmon, B. G., Zhao, T., y Doyle, M. P. 1997. Experimental Escherichia coli O157:H7 carriage in calves. Applied and Environmental Microbiology. 63: 27-32.
Buchanan, R. L. y Doyle, M. P. 1997. Foodborne Disease Significance of Escherichia coli O157:H7 and other Entrohemorrhagic E. coli. Food Technology. 51:69-75.
Buchanan, R. L. y Whiting, R.C. 1996. Risk assessment and predictive microbiology. Journal of Food Protection. 48:31-36.
Casp, A. y Abril, J. 1998 Procesos de Conservación de Alimentos. Ediciones Mundi-Prensa. Madrid, España. 488 p.
Chang, Y. Y. y Cronan J. E. 1999. Membrane cyclopropane fatty acid content is a major factor in acid resistance of Escherichia coli. Journal of Molecular Microbiology. 33:249-259.
Chung, H. J., Bang, W. y Drake M. A. 2006. Stress response of Escherichia coli Comprehensive Reviews in Food Science and Food Safety. 5:52-64.
Csonka, L. N. 1989. Physiological and genetic responses of bacteria to osmotic stress. Microbiology and Molecular Biology Reviews. 53: 121-147.
Davidson, P. M. 1996. Chemical pregservatives and natural antimicrobial compunds. En: Doyle, M. P., Beuchat, L. R. y Montiville, T. J. Food Microbiology Fundamentals and Frontiers. Segunda Edición. ASM Press Books. Washington DC, EE. UU. pp. 593-627.
Donnenberg, M. S. S., Tzipori, S., McKee, M. L., O´Brien, A. D., Alroy J. y Kaper, J. B. 1993. The role of the eae gene of enterohemorrhagic Escherichia coli in intimate attachment in vitro and in a porcine model. The Journal of Clinical Investigation. 92:1418-1424.
Duffy, G., Garvey, P. y McDowell, D. A. 2004. Verocytotoxigenic E. coli. John Wiley & Sons. Connecticut, EE.UU. 457 p.
Eslava, C., Mateo, J. y Cravioto, A. 1994. Cepas de Escherichia coli relacionadas con la diarrea. En Giono, S., Escobar, A. y Valdespino, J. L. Diagnóstico de laboratorio de infecciones gastrointestinales. Secretaria de Salud. México, 1994. 251 p.
García, R. M. 2005. Agentes bactericidas/bacteriostáticos a partir de sorbato de potasio, carvacrol y timol. Tesis de Maestría. Universidad de las Américas Puebla. México. 237 p.
Garlant-Miller, L. y Kaspar, C. W. 1994. Escherichia coli O157:H7 acid tolerance and survival in apple cider. Journal of Food Protection. 57:460-464.
Glass, K. A., Loeffelholz, J. M., Ford, J. P. y Doyle, M. P. 1992. Fate of Escherichia coli O157:H7 as affected by pH or sodium chloride and in fermented, dry sausage. Applied and Environmental Microbiology. 58:2413-2416.
Gould, G. W. 1995. Homeostatic mechanisms during food preservation by combined methods. En: Barbosa-Cánovas, G. W. y J. Welti-Chanes. Food Preservation by Moisture Control-Fundamentals and Applications. Technomic, Lancaster, Pensilvania EE.UU. pp. 397-410.
Griffis, C. L. y Osaili, T. M. 2009. Control of thermal meat processing. En Toldra, F. 2009. Safety of Meat and Processed Meat. Springer Science. Nueva York. EE.UU. pp. 229-253.
Hancock, D. D., Besser, T. E., Kinsel, M. L., Tarr, P. I., Rice, D. H. y Paros, M. G. 1994. The Prevalence of Escherichia coli O157:H7 in Dairy and Beef in Washington State. Epidemiology and Infection. 113:199-207.
Huguet, J., Huapaya, B. y Salazar, E. 2002. Determinación de factores de virulencia asociados a Escherichia coli enterohemorrágica en cepas peruanas aisladas entre 1999-2001. Revista Peruana de Medicina Experimental y Salud Pública. 19(2):63-67.
Hosein, A. M. 2010. Survival of Escherichia coli O157:H7 in Acidified Foods: A Predictive Modeling Approach. Tesis de Doctorado. Universidad de Carolina del Norte. EE.UU. 164 p.
Hoyle, B. 2000. Renewed concerns over E. coli O157:H7 in ground beef. American Society for Microbiology News. 66:331-332.
INFOSAN. 2007. Brote de Escherichia coli O157:H7 en espinacas. Organización Mundial de la Salud. Disponible: http://www.who.int/foodsafety/fs_management/No_ 01_spinach_Feb06_sp.pdf. Adquirido: 30/09/11.
/
Kim S. R., Rhee, M. S., Kim, B.C., y Kim, K, H. 2007. Modeling the inactivation of Escherichia coli O157:H7 and generic Escherichia coli by supercritical carbon dioxide. International Journal of Food Microbiology. 118(1):52-61.
Lin, J. M., Smith. K. C., Chapin, H. S., Baik, G., Bennet, N y Foster, J. W. 1996. Mechanisms of acid resistance in enterohemorrhagic Escherichia coli. Applied and Environmental Microbiology. 62:30943100.
Lou, W. y Nakai, S. 2001. Artificial neural networkbased predictive model for bacterial growth in a simulated medium of modified-atmosphere-packed cooked meat products. Journal of Agricultural Food Chemistry. 49:1799-1804.
Madigan, M. T., Martinko, J. M. y Parker, J. 2003. Brock: Biología de los microorganismos. Décima Edición. Pearson-Prentice-Hall, Madrid. 800 p.
McQuestin, O., Shadbolt, C. y Ross, T. 2009. Quantification of the Relative Effects of Temperature, pH, and Water Activity on Inactivation of Escherichia coli in Fermented Meat by Meta-Analysis. Applied and Environmental Microbiology. 75(22):6963-6972.
Mermin, J. H. y Griffin, P. M. 1999. Invited Commentary: Public Health in Crisis: Outbreaks of Escherichia coli O157:H7 Infections in Japan. American Journal of Epidemiology. 150(8):797-803
Michanie, S. 2003. Escherichia coli O157:H7, la bacteria que dispara el HACCP en la industria de la carne. Revista Ganado y Carne. 4(17):40-42.
Nataro J. P. y Kapper, J.B. 1998. Diarrheagenic Escherichia coli Clinical Microbiology Reviews 11:142-201.
Palou, E. y López-Malo, A. 2009. Relaciones matemáticas, viabilidad y expresión proteica de bacterias de interés en alimentos durante su inactivación al aplicar diversos factores de estrés microbiano: protocolo de investigación sometido a la convocatoria de Ciencia Básica 2009 de CONACYT.
Pascual, M. R y Calderón y Pascual, V. 2000. Microbiología Alimentaria. Segunda Edición. Ediciones Díaz de Santos. España. 441 p.
Pichereau, V., Bourot, S., Flahaut, S., Blanco, C., Auffray, Y. y Bernard, T. 1999. The osmoprotectant glycine betaine inhibits salt-induced cross-tolerance towards lethal treatment in Enterococcus faecalis. Microbiology. 145: 427-435
Richardson, P. S. 2004. Improving the Thermal Processing of Foods. Woodhead Publishing Limited. Cornwall, Inglaterra. 507 p.
Riley, L. W., Remis, R. S., Helgerson, S. D., McGee, H. B., Wells, J. G. y Davis, B. R. 1983. Hemorrhagic colitis associated with a rare Escherichia coli serotype. The New England Journal of Medicine. 308:681-685.
Robert Koch Institute. 2011. Presentation and Evaluation of Previous Epidemiological Findings regarding the EHEC/HUS O104:H4 Outbreak, May/June 2011. Robert Koch Institute. Disponible: http://www.rki.de/cln_160/nn_217400/EN/Home/E HEC__Report,templateId=raw,property=publication File.pdf/EHEC_Report.pdf. Adquirido: 20/09/11.
Rodríguez-Ángeles, G. 2002. Principales características y diagnóstico de los grupos patógenos de Escherichia coli Salud Pública de México 44(5):464-475.
Romero, R. y Herrera, I. F. 2002. Síndrome Diarreico Infeccioso. Editorial Médica Panamericana. Madrid, España. 682 p.
Santiesteban, L. N. A. 2002. Agentes Antibacterianos de Amplio Espectro a partir de Mezclas de Antimicrobianos Sintéticos y Naturales. Tesis de Maestría. Universidad de las Américas. México. 326 p.
Schmidt, H., Beutin, L. y Karch, H. 1995. Molecular analysis of the plasmid-encoded hemolysin of Escherichia coli O157: H7 strain EDL 933. Infection and lmmunity. 63:1055-1061
Sears, C. L. y Kapper J. B. 1996. Enteric bacterial toxins: Mechanisms of action and linkage to
E. Romero et al. / Temas Selectos de Ingeniería de Alimentos 5 – 2 (2011): 28 - 39
intestinal secretion. Microbiology Reviews. 60:167215.
Sevilla, K. P. y Gabriel, A. A. 2010. D values of Escherichia coli in Tilapia meat. Journal of Muscle Foods, 21: 167–176.
Sofos, J. N. 1989. Sorbate Food Preservatives. CRC Press, Inc. Boca Ratón, Florida, EE.UU. 237 p.
Yura, T., Nagai, H. y Mori, H. 1993. Regulation of heat shock response in bacteria. Annual Review of Microbiology. 47:321–50.
Zhao, T., Doyle, M. P. y Besser, R. E. 1993. Fate of enterohemorrhagic Escherichia coli O157:H7 in apple cider with and without preservatives. Applied and Environmental Microbiology. 59:2526–30.

Temas Selectos de Ingeniería de Alimentos 5 - 2 (2011): 40 - 53
Envejecimiento del pan: causas y soluciones
M. Luna-Fernández* y M. E. Bárcenas-Pozos

Departamento de Ingeniería Química, Alimentos y Ambiental, Fundación Universidad de las Américas Puebla. Exhacienda Sta. Catarina Mártir S/N, Cholula, Puebla. C.P.72810. México.
Resumen
El pan es un producto que se deteriora rápidamente debido a que envejece. Esto causa pérdidas económicas considerables tanto al fabricante como al distribuidor y al consumidor. El envejecimiento se manifiesta como dureza de la miga, textura correosa de la corteza, pérdida de agua y cambios en el sabor. Estas alteraciones son causadas por un conjunto de fenómenos complejos (retrogradación del almidón, migración del agua, alteraciones en los compuestos del aroma y del sabor, interacciones gluten-almidón), que ocurren simultáneamente y se relacionan entre sí, haciendo del envejecimiento un proceso complicado. Se han realizado un gran número de investigaciones con el fin de encontrar la forma de inhibir o retardar el envejecimiento, la mayoría de las cuales se han centrado en el uso de aditivos (enzimas, hidrocoloides, gluten, pentosanos, monoglicéridos, surfactantes, entre otros). También se han probado tecnologías de panificación alternativas como el uso de masas congeladas y el horneado en dos etapas. En este artículo se pretende hacer una revisión general de lo antes comentado.
Palabras clave: envejecimiento, pan, aditivos, alternativas en panificación
Abstract
Bread is a product that deteriorates quickly due to staling. This causes economic losses to both manufacturer and distributor and the consumer. Stailing is manifested as hardness of the crumb, chewy texture of the crust, water loss and changes in taste. These alterations are caused by a complex set of phenomena (retrogradation of starch, water migration, changes in the compounds of smell and taste, gluten-starch interactions) that occur simultaneously and interact with each other, making a complicated process of aging. There have been a large number of investigations to find ways to inhibit or retard stailing, most of which have focused on the use of additives (enzymes, hydrocolloids, gluten, pentosans, monoglycerides, surfactants, among others). I have also been tested bread-making technologies of alternatives such as using frozen dough and baked in two stages. This article is a general review of the above mentioned.
Keywords: stailing, bread, additives, bread-making alternatives.
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: mauro.lunafz@udlap.mx
Introducción
El pan de sal es un alimento que existe desde épocas muy antiguas y que en la actualidad sigue consumiéndose a diario en muchas partes del mundo. Sin embargo, es un producto que se deteriora en forma rápida, debido a que en él ocurren fenómenos que causan cambios de sabor, pérdida de aroma, pérdida de agua, endurecimiento de la miga y ablandamiento de la corteza. Todo esto provoca que el pan deje de ser aceptado por los consumidores tan sólo dos o tres días después de haber sido fabricado y que los excedentes de la producción sean desechados, con las consecuentes pérdidas económicas para los panaderos, distribuidores o consumidores.
El conjunto de cambios indeseables que sufre el pan después del horneado se conoce como “envejecimiento” y ha sido ampliamente estudiado desde hace varias décadas, con el propósito de comprenderlo y contrarrestarlo. Aunque las consecuencias del envejecimiento en la calidad del pan pueden detectarse con facilidad, sus causas son más complicadas, ya que involucran fenómenos fisicoquímicos complejos. Entre éstos, la retrogradación del almidón es reconocida como el principal responsable del endurecimiento del pan.
Un estudio llevado a cabo a principios de 1990 sobre la producción anual de pan en Estados Unidos, mostró que se producían aproximadamente 20 billones de libras de pan al año, de las cuales el 3% se desechaba debido al envejecimiento. Considerando que el precio del pan en el mercado era de dos dólares por libra, las pérdidas anuales debidas al deterioro del pan eran de 1.2 billones de dólares o más (Xie et al., 2004).
Este artículo tiene el propósito de presentar, en forma resumida, los fenómenos involucrados con el envejecimiento del pan,
de mayor importancia, así como algunas de las técnicas más utilizadas para retardar o contrarrestar este problema.
Revisión bibliográfica
1. Causas del envejecimiento del pan
Desde el momento en el que es retirado del horno, en el pan ocurren los fenómenos que dan lugar a los signos característicos de su envejecimiento. Entre éstos, los más importantes se describen a continuación.
1.1 Retrogradación del almidón
El compuesto más abundante en el pan es el almidón, ya que constituye alrededor del 55% del peso del pan recién horneado (Guinet y Godon, 1994). El almidón proviene de la harina de trigo que es el principal ingrediente de la formulación del pan.
En estado nativo, el almidón se encuentra en forma de gránulos ovoides agrupados en dos poblaciones: una de gránulos grandes de 25 a 35 µm de diámetro, y otra de gránulos pequeños de 2 a 10 µm. Cada gránulo está formado por capas concéntricas alternativamente cristalinas y amorfas. Estas capas se diferencian por la organización más o menos regular de las macromoléculas formadas por unidades de glucosa, constitutivas del almidón. En las zonas amorfas, las posiciones son irregulares; mientras que en las zonas cristalinas (que representan del 25 al 40% del gránulo) son muy regulares, a punto de formar agrupaciones de microcristales. Aunque, cada cadena macromolecular puede estar implicada en las zonas amorfas y cristalinas, fijando por tanto la estructura del almidón de forma rígida. Pruebas ópticas, térmicas y de rayos X han revelado una estructura granular
interna ordenada y parcialmente cristalina (Morris, 1990).
El almidón está formado por dos tipos de cadenas poliméricas de glucosa. Unas, que constituyen la amilosa, son largas cadenas flexibles, lineales, que asocian varios millares de moléculas de glucosa ligadas entre ellas para formar del 18 al 30% del almidón. Las otras, cadenas ramificadas, denominadas amilopectina, reúnen cerca de 100,000 unidades de glucosa, y constituyen del 70 al 80% del almidón. La amilopectina se presenta en forma arborescente y está constituida por una multitud de ramificaciones de 20 a 40 unidades de glucosa injertadas en una cadena más larga (Guinet y Godon, 1996). Las ramas agrupadas en paralelo de la amilopectina se encuentran plegadas como dobles hélices (Karaoglu, 2006).
Los gránulos de almidón son insolubles en agua. Pero cuando una suspensión acuosa de almidón es calentada a una temperatura superior a 55-60° C, los gránulos absorben agua, se hinchan, y pierden su estructura; además, la amilosa se solubiliza. Este fenómeno se conoce como gelatinización del almidón y da lugar a un sistema compuesto de gránulos hinchados y porosos (esqueletos de amilopectina), suspendidos en una solución caliente de amilosa (Morris, 1990).
Cuando la temperatura del almidón gelatinizado disminuye, se forma un gel progresivamente más rígido, que se retrae debido a que se elimina agua y a que las cadenas de amilosa y amilopectina se reorganizan bajo una forma cristalina mucho más generalizada que en el estado nativo del almidón. Esta reorganización se denomina retrogradación.
De acuerdo a los estudios de Miles et al. (1985), Ring et al. (1987), Clark (1990), y Gidley (1989), la retrogradación del almidón
ocurre como dos procesos cinéticamente distintos: la rápida gelación de la amilosa a través de la formación de segmentos de cadena de doble hélice que es seguida por la agregación hélice-hélice, y la recristalización lenta de las cadenas de amilopectina. Mientras la amilosa parece dominar las etapas iniciales de la retrogradación, los principales cambios en rigidez y cristalinidad de los geles de almidón son generalmente atribuidos a la amilopectina.
Katz (1928) propuso que la retrogradación de los polímeros del almidón era responsable del envejecimiento del pan, debido a que sus patrones de difracción de rayos X de pan fresco eran similares a aquellos del almidón recién gelatinizado, mientras que los patrones del pan envejecido eran parecidos a los del almidón retrogradado.
Desde entonces se han realizado un gran número de estudios que han llevado a concluir que los procesos que colectivamente constituyen la retrogradación del almidón, son los principales causantes del endurecimiento de la miga de pan.
1.2, Pérdida y redistribución de agua
Si la humedad relativa del aire que rodea al pan recién retirado del horno es inferior a la actividad de agua del mismo, habrá una salida de agua del pan hacia el entorno, de lo contrario el pan ganará agua. Por otro lado, la miga del pan recién horneado tiene una actividad de agua superior a la de la corteza; esta diferencia provoca que agua que se encuentra en el interior del pan se desplace a la superficie. Adicionalmente, la transferencia de humedad de un constituyente de la miga a otro es generalmente aceptada como un factor que contribuye al envejecimiento.
Las migraciones de agua que ocurren en el pan dan lugar a cambios en las características del producto. Los más notables son la resequedad de la miga y la pérdida de la naturaleza crujiente de la corteza. La redistribución y pérdida de agua en el pan y sus consecuencias han sido observadas y estudiadas desde hace algunas décadas por varios investigadores (Leung et al., 1983; Rogers et al., 1988; He y Hoseney, 1990).
Por ejemplo, se ha confirmado que existe una relación inversa entre el contenido de humedad y la velocidad de envejecimiento del pan. Sin embargo, se ha encontrado que la velocidad de retrogradación del almidón en el pan es directamente proporcional al contenido de humedad (Rogers et al., 1988; He y Hoseney, 1990).
Asimismo, Schiraldi y Fessas (2001) enfocaron su revisión hacia el contenido de agua, actividad de agua, migración de agua entre fases, y estructura alveolar de la miga de pan. Ellos sugirieron que la migración de agua de la miga a la corteza da lugar a una deshidratación local que hace las paredes de los alvéolos de la miga más rígidas y puede contribuir a un empaquetamiento cerrado de la estructura a través de la cual el agua se desplaza.
Por su parte, Baik y Chinachoti (2000) encontraron que el pan almacenado con su corteza llegó a ser significativamente más duro que el almacenado sin corteza y contuvo más amilopectina recristalizada, indicando que la redistribución de humedad de la miga hacia la corteza juega un papel significativo en el endurecimiento.
Además, usando resonancia magnética nuclear (NMR por sus siglas en inglés) se encontró que conforme el envejecimiento procede, el agua en el pan llega a ser menos móvil (Leung et al., 1983).
Por otro lado, se han realizado una gran cantidad de investigaciones para determinar si el envejecimiento involucra la deshidratación del gluten o del almidón. La mayoría de las evidencias sugieren una transferencia de agua del gluten hacia el almidón, conforme el almidón se cristaliza. En diferentes estudios Willhoft y sus colaboradores (Breaden y Willhoft, 1971; Willhoft, 1971; Kay y Willhoft, 1972) reportaron que el gluten se transforma durante el almacenamiento del pan, dando lugar a la liberación de agua, la cual es absorbida por el almidón que se está retrogradando. Leung (1981) y Leung et al. (1983) propusieron que conforme el almidón cambia a un estado cristalino, más moléculas de agua son inmovilizadas debido a su incorporación a las estructuras cristalinas. El uso de NMR y un mayor entendimiento del mecanismo de cristalización de los polímeros del almidón han permitido confirmar lo anterior.
1.3. Interacciones gluten-almidón
Estudios realizados por diferentes investigadores (Longton y Legrys, 1981; Biliaderis y Zawistowski, 1990; Sahlström y Brathen, 1997) han demostrado que la retrogradación del almidón no siempre se correlaciona con la dureza del pan. Esto ha llevado a investigar el papel de compuestos distintos a los polisacáridos, que se encuentran en el pan, en el envejecimiento de este producto.
Uno de los trabajos más conocidos en relación con este tema es el de Martín et al. (1991). Estos investigadores sugirieron que la dureza del pan es el resultado de la formación de enlaces de hidrógeno entre los gránulos de almidón gelatinizado y la red de gluten en el pan, enlazándose juntos la red de proteína continua y los gránulos remanentes discontinuos. Ellos propusieron que durante el horneado se forman enlaces
cruzados (enlaces de hidrógeno) entre el almidón y el gluten; luego, durante el almacenamiento, tanto el número de interacciones como su fuerza se incrementan. En el recalentamiento, la frescura del pan se recupera debido a que los enlaces de hidrógeno y las madejas formadas entre las moléculas de los polímeros del almidón y el gluten, son rotos.
Contrario a lo anterior, varios investigadores han concluido que la dureza de la miga no está significativamente correlacionada con el tipo de proteínas de la harina o con su concentración (Ponte et al., 1962; León et al., 1997; Gerrard et al., 2001). Every et al. (1998) sugirieron que, cualitativamente, las interacciones almidónalmidón y almidón-proteínas son de igual importancia para el envejecimiento del pan; pero cuantitativamente las interacciones almidón-almidón son más notables debido a que la harina de trigo convencional contiene 85% (bs) de almidón. Examinando pan libre de gluten, Morgan et al. (1997) sugirieron que la retrogradación del almidón por sí misma es suficiente para causar el endurecimiento del pan y que el gluten no es esencial para el proceso de endurecimiento.
1.4. Alteraciones en los compuestos responsables del sabor
El sabor del pan se deriva de los ingredientes y de las condiciones y métodos de procesamiento usados en su elaboración.
En cuanto a los ingredientes, la harina refinada tiende a mostrar un sabor bastante suave. Es la sal adicionada a la formulación del pan la principal modificadora del sabor, ya que además de impartir su sabor salado característico, funciona como potenciadora de otros sabores presentes en el pan. Por su parte, la levadura usada en la formulación también hace su propia y única contribución al sabor del pan.
Con respecto al procesamiento, durante la fermentación se generan nuevos productos de sabor en la masa, cuya intensidad y notas de sabor particulares cambian con el incremento en el tiempo de fermentación. Los cambios de sabor más comúnmente observados se asocian con el desarrollo de sabores ácidos provenientes de la actividad microbiana en la masa, los cuales son fácilmente detectados en el sabor de la miga. No toda esta actividad microbiana relacionada con el sabor viene de la levadura adicionada por el panadero; alguna proviene de levaduras y bacterias (especialmente bacterias ácido lácticas) salvajes, presentes en forma natural en la harina. Usualmente se requieren varias horas de fermentación antes de que hayan cambios significativos en el perfil de sabor de la miga de pan. En algunos procesos, el sabor del pan puede mejorarse usando un pre-fermento o “esponja”, el cual es posteriormente mezclado con el resto de los ingredientes para formar la masa para el proceso final (Cauvain, 2001).
El horneado es la etapa que más contribuye al sabor del pan. Durante el mismo, muchos de los compuestos de sabor presentes sufren cambios y otros se pierden; y, paralelamente, se forman nuevos compuestos. Estos cambios están asociados con las reacciones de Maillard, también responsables del obscurecimiento de la corteza, las cuales producen compuestos de sabor intenso. A esto se debe que la percepción del sabor del pan por los consumidores esté fuertemente influenciada por la relación corteza/miga (Cauvain, 2001).
El pan recién horneado tiene un sabor agradable y característico, el cual es debido a la presencia de compuestos volátiles formados durante la fermentación y el horneado. Dichos compuestos son alcoholes, aldehídos, diacetilos, cetonas y ésteres, entre otros. Conforme el tiempo transcurre, el
sabor del pan fresco es remplazado por el sabor típico del pan envejecido. Esto ocurre porque los volátiles se colocan en las hélices de amilosa, las cuales evitan que sean percibidos por el gusto, y porque se producen los compuestos de degradación responsables del sabor característico del pan viejo (Schiraldi y Fessas, 2001).
2. Métodos para contrarrestar el problema del envejecimiento del pan
La prolongación de la vida útil del pan continúa siendo un tema de investigación prioritario. Las estrategias empleadas para prolongar la frescura de este producto han incidido principalmente en la formulación de la masa, en la variación de los parámetros de proceso y en los métodos de producción. Algunas de estas estrategias se comentan a continuación.
2.1 Uso de aditivos
2.1.1
Hidrocoloides
Se han realizado un gran número de estudios cuyo propósito ha sido determinar el efecto de los hidrocoloides en el envejecimiento del pan (Davidou et al., 1996; Armero y Collar, 1998; Rosell et al., 2001; Guarda et al., 2004; Bárcenas et al,. 2004; Ribotta et al., 2004; Mandala, 2005; Asghar et al., 2006; Bárcenas y Rosell, 2006a; Lazaridou et al., 2007). Entre los hidrocoloides que se han estudiado están la pectina, la goma xantana, el alginato de sodio, la goma de algarrobo, la carboximetilcelulosa (CMC), la hidroxipropilmetilcelulosa (HPMC), la carragenina, la goma guar y la goma arábiga. Con varios de los hidrocoloides probados se han obtenido buenos resultados, ya que se ha conseguido reducir la velocidad de envejecimiento, así como fabricar pan de mayor volumen y textura más suave. Estos compuestos inducen cambios estructurales en los principales componentes de la masa
panadera (almidón, gluten, lípidos) durante la panificación, y posterior almacenamiento de los productos horneados. Específicamente, las interacciones entre los hidrocoloides y el almidón, modifican la estructura e influyen sobre los procesos de gelatinización y retrogradación (Collar y Armero, 1996; Rojas et al., 1999; Rosell et al., 2007) y el envejecimiento del pan (Armero y Collar 1998; Bárcenas et al., 2003).
Algunos hidrocoloides muestran efectos interesantes sobre la dureza de la miga. En particular, algunos derivados de la celulosa, (HPMC y CMC), disminuyen la textura inicial de ésta (Armero y Collar, 1998). Para panes blancos la HPMC y CMC se comportan como buenos agentes antiendurecimiento en procesos indirectos con masa agria; la eficacia de CMC es superior a tiempos cortos de almacenamiento y la de HPMC, a tiempos medios y largos (Collar y Armero, 1996). La HPMC ha mostrado ser un agente eficaz para prolongar la vida de conservación de panes sometidos a panificación interrumpida y bajas temperaturas, en cuyos sistemas el progresivo endurecimiento de la miga y la cristalización de las cadenas de amilopectina se desarrollan rápidamente (Bárcenas y Rosell, 2006a). La presencia de HPMC mejora los parámetros tecnológicos y disminuye la velocidad de envejecimiento, sin afectar los atributos sensoriales ni la microestructura de los sistemas panarios precocidos congelados o refrigerados (Bárcenas y Rosell, 2006a, 2007).
2.1.2 Enzimas
El retraso del envejecimiento del pan se puede efectuar, mediante el uso de enzimas amilolíticas y no amilolíticas como coadyuvantes tecnológicos. Además de las enzimas que hidrolizan el almidón (amilolíticas/dextrinizantes, sacarificantes y
desramificantes), la incorporación a las masas panarias de enzimas que degradan los polisacáridos diferentes del almidón, y/o de enzimas que modifican los lípidos y el gluten, ha demostrado ser eficaz para retardar el envejecimiento (Armero y Collar, 1997; Collar et al., 1998, 2000; Rosell y Collar, 2008) actuando sobre los polímeros mayoritarios de la harina.
Las amilasas han sido utilizadas ampliamente como inhibidores del envejecimiento del pan a través de la disminución de la velocidad de endurecimiento de la miga. Se han propuesto diferentes hipótesis para explicar el efecto anti-envejecimiento de estas enzimas. Algunos autores sostienen que las α–amilasas producen dextrinas de bajo peso molecular durante la cocción, y los productos de la hidrólisis interfieren en la retrogradación de la amilopectina y en las interacciones almidón–gluten, involucradas en el proceso de endurecimiento (Martinez–Anaya et al., 1998; Rojas et al., 2001). Durante el almacenamiento, la dureza de la miga aumenta, mientras que la elasticidad y la cohesividad disminuyen. En presencia de α–amilasa fúngica o α–amilasa bacteriana de termoestabilidad intermedia, los cambios son más lentos, lo que confirma su actividad antienvejecimiento (Armero y Collar, 1998; Blaszczak et al., 2004), particularmente evidente para la dureza, la cohesividad y la elasticidad (Collar y Bollaín, 2005). También se ha demostrado que las α–amilasas son eficaces agentes anti–endurecimiento en panes fabricados por panificación interrumpida (Bárcenas et al., 2003).
Por otro lado, la combinación de transglutaminasa y α–amilasa bacteriana de termostabilidad intermedia da lugar a una cinética de envejecimiento más lenta, particularmente para panes de harina blanca (Collar y Bollaín, 2005). Un estudio cinético
de la dureza a lo largo del almacenamiento muestra que la presencia de diferentes carbohidrasas reduce la velocidad de endurecimiento de la miga y disminuye la retrogradación del almidón, a la vez que proporciona a las xilanasas el mayor efecto (Haros et al., 2002). La adición de mezclas binarias de amilasa y lipasa mejora la conservación del pan mediante la formación de un complejo amilosa–lípido más termoestable y la inhibición de la retrogradación de la amilopectina por generación enzimática de dextrinas de bajo peso molecular (León et al., 2002).
2.1.3 Pentosanos
Se piensa que algunos polisacáridos no almidonosos, como los arabinoxilanos y arabinogalactanos, también tienen un efecto anti-envejecimiento. Estos compuestos son conocidos como pentosanos y son componentes nativos de las harinas de cereales. La adición de pequeñas cantidades de pentosanos a la formulación del pan puede producir un decremento significativo en la velocidad de endurecimiento del producto final. Se han propuesto varias teorías para explicar el efecto antienvejecimiento de los pentosanos; sin embargo, ha sido claramente demostrado que estos compuestos no afectan la retrogradación del almidón, aunque producen un retraso en el endurecimiento de la miga (Patil et al., 1976).
Una hipótesis es que los pentosanos pueden actuar como “pozos de agua” moleculares en la matriz de la miga, liberando agua en el curso del almacenamiento. Debido a su efecto plastificante, el agua liberada podría mantener la miga suave durante un lapso de tiempo más largo (Meuser y Suckow, 1986). Esta interpretación se basa en el hecho de que los pentosanos pueden retener grandes cantidades de agua (Michniewicz et al.,
1992). No obstante, en un estudio llevado a cabo por Courtin y Delcour (1998) se concluyó que los pentosanos nativos de la harina tienen una baja velocidad de absorción de agua.
De acuerdo con otras investigaciones, la estructura alveolar de la miga de pan producida con masas enriquecidas con pentosanos es más gruesa que la del pan control. Por tanto, la acción de los pentosanos podría estar enfocada a la formación de la masa y la estructura de la miga, lo cual podría afectar a la matriz que rodea a las celdas de gas formadas durante la fermentación y el inicio del horneado. El principal efecto de los pentosanos podría estar concentrado en el ambiente inmediato de la interfase gas/masa. La estructura alveolar de la miga tiene un papel importante en la textura del pan (Fessas y Schiraldi, 1998).
2.1.4
Gluten
En 1938, Steller y Bailey observaron una relación inversa (aunque no lineal) entre el contenido de proteínas y el envejecimiento del pan, durante el almacenamiento. Posteriormente, otros investigadores encontraron que el incremento en el nivel de proteínas producía un decremento en la dureza de la miga y en la velocidad de endurecimiento. Prentice et al. (1954) explicaron que el incremento en el contenido de proteínas podría disminuir cualquier asociación entre los gránulos de almidón, hinchados y embebidos en la red de gluten, retardando de este modo el endurecimiento de la miga. Ellos también sugirieron que el gluten puede servir como un reservorio de humedad para amortiguar cualquier cambio en la capacidad de hidratación del almidón. Por su parte, Erlander y Erlander (1969) sugirieron que las interacciones glutenalmidón pueden prevenir el envejecimiento del pan, posiblemente mediante la formación
de enlaces de hidrógeno entre los grupos amida de las gliadinas, gluteninas y tal vez albúminas, y los grupos hidroxilo del almidón. Además concluyeron que la relación almidón:proteínas en la masa es determinante en la velocidad de envejecimiento. Algo similar fue propuesto por Maleki et al. (1980), quienes postularon que el componente de la harina principalmente responsable de las diferencias en la velocidad de envejecimiento es el gluten.
2.1.5 Monoglicéridos y surfactantes
La adición de monoglicéridos y surfactantes (tales como el estearoil lactilato de sodio, SSL) a la formulación del pan, produce un efecto anti-envejecimiento significativo (Russell, 1983; Eliasson y Ljunger, 1988) y se han propuesto varios mecanismos para explicar su acción. Willhoft (1973) sugirió que el efecto anti-envejecimiento de los monoglicéridos puede deberse a una interacción con el gluten, lo cual ha sido confirmado por otros investigadores (De Stefanis et al., 1977; Quail, 1991). Por otro lado, se sabe que los surfactantes son atrapados por el gluten durante el amasado y liberados hacia el gel de almidón durante el horneado. Es probable que los surfactantes permanezcan principalmente en las regiones inter-granulares, donde pueden formar complejos con la amilosa lixiviada o con la amilopectina. Esto puede impedir la formación de puentes entre gránulos de almidón hinchados y, consecuentemente, evitar la retrogradación (Conde-Petit y Escher, 1994).
2.2 Uso de masas congeladas
Una de las estrategias usadas para disminuir las pérdidas debidas al envejecimiento del pan es la congelación de las masas, ya que este proceso permite ofrecer al consumidor un producto “recién elaborado”, de forma
permanente. En esta tecnología, la producción de las piezas de masa es centralizada en una industria panificadora, mientras que el horneado se efectúa en los puntos de venta. El amasado de los ingredientes se realiza de la misma manera que para la elaboración de productos frescos, luego se forman las piezas y posteriormente se congelan; la distribución se lleva a cabo en estado congelado. En los puntos de venta, a medida que el producto se consume, se hace la descongelación, la fermentación en piezas y el horneado (Ribotta et al., 2009). De esta forma, sólo se elabora el pan que se vende, eliminando o minimizando los excedentes, con lo que las pérdidas debidas al envejecimiento del pan se reducen de manera importante. La razón por la cual la fabricación de masas congeladas permite contrarrestar el envejecimiento, es que al no haberse llevado a cabo el horneado, el almidón de las masas no está gelatinizado y, por tanto, no retrograda durante el almacenamiento. Además, las bajas temperaturas inhiben las reacciones que pudieran ocurrir en las masas almacenadas.
La producción industrial de masas congeladas se realiza a través de procesos altamente mecanizados, lo que reduce los costos de producción y permite obtener productos con calidad constante. Sin embargo, desde el punto de vista económico, las masas congeladas presentan el inconveniente de requerir ser transportadas y mantenidas a -18 °C hasta el final del proceso. Adicionalmente, las masas congeladas son sistemas complejos más sensibles al cambio de los ingredientes y a las condiciones de proceso que las masas tradicionales. La congelación y el almacenamiento en estado congelado prolongado provocan pérdida en la calidad de los productos (Ribotta et al., 2009). El deterioro gradual de las masas durante el almacenamiento en congelación se atribuye a la pérdida en la capacidad de retener gases
de la masa. Este cambio se debe principalmente a una disminución de la fuerza de la masa y a la pérdida gradual de la actividad y la viabilidad de las levaduras (Inoue y Bushuk 1992; Stauffer, 1993; Casey y Foy, 1995; Ribotta et al., 2001). Las principales consecuencias de estos fenómenos son: mayores tiempos de fermentación, producción de panes con menor volumen y mayor deterioro de la textura final (Dubois y Blockcolsky, 1986).
2.3 Horneado en dos etapas
Esta tecnología es adecuada para contrarrestar el envejecimiento y obtener a cualquier hora del día un producto con una calidad similar a la del pan fresco. Consiste en llevar a cabo un proceso de panificación semejante al convencional a excepción del horneado, el cual se realiza en dos etapas. En la primera, se hornea durante un tiempo equivalente a aproximadamente un tercio del tiempo de horneado total del pan, obteniéndose pan parcialmente horneado (PPH). Este producto se conserva en refrigeración o congelación o envasado en atmósfera modificada o inerte, y se mantiene en dicho estado hasta su horneado final. En general se trata de un producto al que le faltan unos minutos para completar la cocción. La segunda etapa de horneado permite generar la corteza y liberar el aroma característico de los productos recién horneados (Rosell y Collar, 2009). La fabricación del pan por horneado en dos etapas, hace posible completar el horneado y tener pan fresco justamente en el momento de la venta o el consumo y en la cantidad requerida por los compradores o comensales. Así, la cantidad de pan sobrante es pequeña y las pérdidas por envejecimiento también. El horneado en dos etapas es una forma de contrarrestar el envejecimiento debido a que cuando el PPH es almacenado en congelación, la retrogradación del almidón y otras reacciones son inhibidas por la
reducción en la movilidad del sistema. Si el PPH es refrigerado o almacenado en atmósfera inerte o modificada, el almidón retrograda y la dureza del producto se incrementa; no obstante, al aplicar altas temperaturas durante la segunda etapa de horneado, la retrogradación se revierte y la textura blanda de la miga se recupera (Fik y Surowka, 2002; Bárcenas y Rosell, 2006b).
Entre las principales ventajas del horneado en dos etapas se encuentran: disponibilidad de pan caliente a cualquier hora del día y en diversos sitios, amplia gama de productos y ahorro de tiempo y mano de obra en los puntos finales de distribución. Cuando se efectúa un proceso de elaboración poco cuidadoso pueden surgir algunos inconvenientes; entre ellos pan con menos volumen, envejecimiento rápido y descascarillado.
Referencias
Armero, E. y Collar, C. 1997.Texture properties of formulated wheat doughs. Relationships with dough and bread technological quality. Food Science and Technology. 204.136-145.
Armero, E. y Collar. C. 1998. Crumb firming kinetics of wheat breads with antistaling additives. Journal of Cereal Chemistry. 28:165-174.
Asghar, H., Ishaq, Z., Zahir, M., Khalid, Z. y Arshad, M. 2006. Effect of water soluble pentosans on loaf volume of reconstituted gluten and starch doughs. Journal of Cereal Chemistry. 53: 44-1976.
Baik, M.Y. y Chinachoti, P. 2000. Moisture redistribution and phase transitions during bread staling. Journal of Cereal Chemistry. 77(4): 484488.
Bárcenas, M.E., Haros, M., Benedito, C. y Rosell, C.M. 2003. Effect of freezing and frozen storage on the staling of partly baked bread. Food Research International. 36:863-869.
Conclusiones
El envejecimiento del pan es un proceso que involucra varios fenómenos fisicoquímicos complejos, cuyas consecuencias (pérdida de la textura suave de la miga y crujiente de la corteza, resequedad del pan y pérdida del sabor característico) dan lugar a un producto desagradable para el consumidor. Además del deterioro en la calidad del pan, el envejecimiento causa pérdidas económicas importantes. Con el fin de contrarrestarlo se ha evaluado la adición de diferentes compuestos a la formulación del pan, encontrándose entre los más efectivos las amilasas y la HPMC. También se han probado procesos de panificación alternativos como el uso de masas congeladas y el horneado en dos etapas. Estos últimos son procesos de especial interés, si se considera la tendencia al consumo de alimentos con “etiqueta limpia”
Bárcenas, M.E., Benedito, C. y Rosell, C.M. 2004.Use of Hydrocolloids as Bread Improvers in Interrupted Baking Process with Frozen Storage. Food Hydrocolloids. 18 (5): 769-764.
Bárcenas, M.E., y Rosell, C.M. (2006a). Effect of frozen storage time on the bread crumb and aging of parbaked bread. Food Chemistry. 72: 92-99.
Bárcenas, M.E., y Rosell, C.M., (2006b). Effect of frozen storage time on the bread crumb and aging of parbaked bread. Food Chemistry. 95:438-445.
Bárcenas, M.E. y Rosell, C.M. 2007. Different approaches for increasing the shelf life of partially baked bread: Low temperatures and hydrocolloid addition. Food Chemistry. 100:1594-1601.
Biliaderis, C.G. y Zawistowski, J. 1990. Viscoelastic behavior of ageing starch gels: effects of concentration, temperature and starch hydrolysates on network properties. Cereal Chemistry. 67:240-246.
Blaszczak, W., Sadowska, J., Rosell, C.M. y Fornal, J. 2004. Structural changes in the wheat dough and bread with the addition of alpha amylases.
European Food Research and Technology. 219(4): 348-354.
Breaden, P.W. y Willhoft E.M.A. 1971. Bread staling. III. Measurement of the redistribution of moisture in bread by gravimetry. Journal of the Science of Food and Agriculture. 22: 647-649.
Casey, G. y Foy, J. 1995. Yeast performance in frozen doughs and strategies for improvement. Pages 1951 En: Frozen and Refrigerated Doughs and Batter. K. Kulp, K. Lorenz, and J. Brummer.Eds. American Association of Cereal Chemistry.St. Paul, MN.
Cauvain, S.P. 2001. Breadmaking cereals processing technology. Tercera edición. CRC press. EE. UU. 397 p.
Clark, R. B. 1990.Advances in Agronomy: physiology of cereals for mineral nutrient uptake, use, and efficiency. Primera edición. Academic Press. EE.UU. 300 p.
Collar, C. y Armero, E. 1996. Physicochemical mechanisms of bread staling during storage: formulated doughs as a technological issue for improvement of bread functionality and keeping quality. Recent Research Developments in Nutrition. 1: 115-143.
Collar, C., Armero, E. y Martinez, J.1998. Lipid binding of formula bread doughs. Food Research and Technology. 207:110-121.
Collar, C. y Bollaín, C. 2005. Impact of microbial transglutaminase on the staling behaviour of enzyme supplemented pan breads. European Food Research and Technology. 221 (3-4): 298-304.
Conde-Petit, B. y Escher, F.1994. Influence of starch lipid complexation on the ageing and baked goods and associated changes in textural properties. Journal of Texture Studies. 1(4): 272-477.
Courtin, C. M. y Delcour, J. A. 1998. Physicochemical and bread making properties of low molecular weight wheat derived arabinoxylans. Journal of Agriculture and Food Chemistry. 46: 4066-4073.
Davidou, S., Le, Meste., M, Debever. y Bekaert, D. 1996. A contribution to the study of staling of
white bread: effect of water and hydrocolloids. Food Hydrocolloids. 10:375-383.
De Stefanis, V., Ponte, J., Chung, F. y Ruzza, N. A. 1977.Binding of crumb softeners and dough strengtheners during breadmaking. Cereal Chemistry. 54:13-24.
Dubois, D. y Blockolsky, D. 1986. Frozen bread dough. Effect of dough mixing and thawing methods. American Institute of Baking Research Department Technology Bull. 1(8):1-7.
Eliasson, A.C. y Ljunger, G. 1988. Interaction between amylopectin and lipid additives during retrogradation in model system. Journal of Science of Food and Agriculture. 44: 353-361.
Erlander, S. y Erlander, L.1969. Explanation of ionic sequences in various phenomena. X. Proteincarbohydrate interactions and the mechanism of staling bread. Starch/Stärke. 21:305-315.
Every, D., Gerrard, J.A., Gilpin, M.J., Ross, M. y Newberry, M.P. 1998. Staling in starch bread: the effect of gluten additions on specific loaf volume and firming rate. Starch/Stärke. 50: 443-446.
Fessas, D. y Schiraldi, A.1998.Texture and staling of wheat bread crumb: effects of water extractable proteins and pentosans. Thermochimica Acta. 323: 17-23.
Fik, M. y Surowka, K. 2002. Effect of prebaking and frozen storage on the sensory quality and instrumental texture of bread. Journal of the Science of Food and Agriculture. 82: 1268-1275.
Gerrard, J.A., Abbot, R.C., Newberry, M.P., Gilpin, M.J., Ross, M. y Fayle, S.E. 2001. The effect of nongluten proteins on the staling of bread. Starch/Stärke. 53:278-280.
Gidley, M. J. 1989. Molecular mechanisms underlying amylose aggregation and gelation Macromolecules. 22:351-358.
Guarda, A., Rosell, C.M., Benedito, C. y Galotto, M.J. 2004. Different hydrocolloids as bread improvers and antistaling agents. Food Hydrocolloids. 18: 241-247.
Guinet, R. y Godon, B. J. 1994. La Panificación francesa: la ultracongelación .Primera edición Montagud.España.368 p.
Haros, M., Rosell, C. y Benedito, C. 2002. Effect of different carbohydrases on fresh bread texture and bread staling. European Food Research and Technology. 215:425-430.
He, H. y Hoseney, R.C. 1990. Changes in bread firmness and moisture during long term storage. Cereal Chemistry. 67(6): 603-605.
Inoue, Y., y Bushuk, W. 1992. Studies on frozen doughs. II. Flour quality requirements for bread production from frozen dough. Cereal Chemistry 69:423-428.
Karaoglu, M.M. 2006. Effect of Initial Baking and Storage Time on Pasting Properties and aging of Parbaked and Rebaked Rye Bread. International Journal of Food Properties. 9(3): 583-596.
Katz, J.R. 1928. Technology and engineering: gelatinization and retrogradation of starch in relation to the problem of bread staling. Primera edición.Walton RP. EE. UU. 669 p.
Kay, M. and Willhoft, E. M.A.1972.Bread staling. IV. Electrical properties of the crumb during staling. Journal of Science of Food and Agriculture. 23:321-331.
Lazaridou, A., Duta, D., Papageorgiou, M., Belc, N., y Biliaderis, C. G. 2007. Effects of hydrocolloids on dough rheology and bread quality parameters in gluten free formulations. Journal of Food Engineering. 79:1033-1047.
León, A., Duran, E., y Benedito De Barber, C. 1997. Firming of starch gels and amylopectin retrogradation as related to dextrin production by amylase. Food Chemistry. 12: 156-160.
León, A., Durán, E., Benedito de Barber C. 2002.Utilization of Enzyme Mixtures to Retard Bread Crumb Firming. Journal of Agricultural and Food Chemistry.50:1416-1419.
Leung, H.K. 1981. Structure and properties of water. Cereal Foods World. 26:350-352.
Leung, H.K., Magnuson, J.A. y Bruinsma, B.L. 1983. Water binding of wheat flour doughs and breads
as studied by deuteron relaxation. Journal of Food Science. 48:95-99.
Longton, J. y Legrys, G. A. 1981. Differential scanning calorimetry studies on the crystallinity of aging wheat starch gels. Starch-Stärke. 33:410414.
Maleki, M., Hoseney, R.C y Mattern, P.J. 1980. Effects of loaf volume, moisture content, and protein quality on the softness and staling rate of bread. Cereal Chemistry. 57:138-140.
Mandala, I. 2005. Physical properties of fresh and frozen stored, microwave reheated breads, containing hidrocolloids. Journal of Food Engineering. 66:291-300.
Martin, M., Zeleznak, K. y Hoseney, R. 1991. A mechanism of bread firming. I. Role of starch swelling. Cereal Chemistry. 68(1): 498-503.
Martinez-Anaya, M., Devesa, Andreu, P., Escriva, P. y Collar, C. 1998. Effects of the combination of starters and enzymes in regulating bread quality and shelf life. Food Science Technology Internatinal. 4: 425-435.
Meuser, F. y Suckow, P.1986. Physics and Chemistry of Baking. Non-starch polysaccharides. En J. M. V. Blanshard, P. J. Frazier, y T. Galliani Eds., Royal Society of Chemistry, London. p. 42.
Michniewicz, J., Biliaderis, C. y Bushuk, W. 1992. Effect of added pentosans on some properties of wheat bread. Food Chemistry. 43:251-257.
Miles, M. J., Morris, V.J., Orford, P.D. y Ring, S.G.1985. The roles of amylose and amylopectin in the gelation and retrogradation of starch. Carbohydrate Research. 135-271.
Morgan, K.R., Gerrard, J., Every, D., Ross, M. y Gilpin, M.1997. Staling in starch breads. The effect of antistaling alfa amylase. Starch/Stärke 49:54-59.
Morris,V. J.1990. Starch gelation y retrogradation. Trends in Food Science and Technology. 1: 2-6.
Patil, K., Finney, K., Shogren, M. y Tsen, C.1976. Water soluble pentosans of wheat flour. III. Effect of wáter soluble pentosans on loaf volume of
reconstituted gluten and starch doughs. Cereal Chemistry. 53(44):188-193.
Ponte, J., Titcomb, S., y Cotton, R. 1962. Flour as a factor in bread firming. Cereal Chemistry. 39:437444.
Prentice, N., Cuendet, L.S. y Geddes, W.F. 1954. Studies on bread staling. V. Effect of flour fractions and various starches on the firming of bread crumb. Cereal Chemistry. 31:188-206.
Quail, K.J., McMaster, G.J. y Wootton, M. 1991. The role of flour lipids in the baking of arabic bread. Journal Cereal Science. 14:131-134.
Ribotta, P., León, A., y Añon, M. C. 2001. Effect of freezing and frozen storage of doughs on bread quality. Journal Agriculture Food Chemistry. 49:913-918.
Ribotta, P., Pérez, G.T., León, A. y Añón, C. 2004. Effect of emulsifier and guar gum on micro structural, rheological and baking performance of frozen bread dough. Food Hydrocolloids. 18: 305313.
Ribotta, P., Alcantara, P. y Tadini, C. 2009. Masas congeladas .En:P.D., Ribota y C.C. Tadini (Eds.). Alternativas tecnológicas para la elaboración y la conservación de productos panificados. Universidad Nacional de Córdoba. Argentina. Pp.13-60.
Ring, G., Colonna, P., l’Anson, J., Kalichevski, M. T., Miles, M. J., Morris, V. J. y Orford, P. D. 1987. The gelation and crystallization of amylopectin. Carbohydrate Research. 162-277.
Rogers, D. E., Zeleznak, K. J., Lai, C. S. y Hoseney, R. C.1988. Effect of native lipids, shortening, and bread moisture on bread firming. Cereal Chemistry. 65:498-501.
Rojas, J.A., Rosell, C.M. y Benedito de Barber, C. 1999. Pasting properties of different wheat flour hydrocolloids systems. Food Hydrocolloids. 13:27-33.
Rojas, J. A., Rosell, C. M. y Benedito de Barber, C. 2001. Role of maltodextrins in the staling of starch gels. European Food Research and Technology. 212:364-368.
Rosell, C.M., Rojas, J.A. y Benedito de Barber, C. 2001. Influence of hydrocolloids on dough rheology and bread quality. Food Hydrocolloids. 15:75-81.
Rosell, C.M., Collar, C. y Haros, M. 2007. Assessment of Hydrocolloids Effects on the Thermo Mechanical Properties of Wheat Using the Mixolab. Food Hydrocolloids 21:452-462.
Rosell, C.M., y Collar, C. 2008. Effect of various enzymes on dough rheology and bread quality”. En: Recent Research Developments in Food Biotechnology. Enzymes as Additives or Processing Aids. Ed R. Porta, P. Di Pierro and L. Mariniello. Research Signpost, Kerala, India. pp 165-183.
Rosell, C.M. y Collar, C. 2009. Productos precocidos congelados y refrigerados. En: P.D., Ribotta y C.C. Tadini (Eds.). Alternativas tecnológicas para la elaboración y la conservación de productos panificados. Universidad Nacional de Córdoba. Argentina. pp. 61-86.
Russell, P. L. 1983. A kinetic study of bread staling by differential scanning calorimetry. The effect of painting loaves with ethanol. Starch-Stärke. 35: 277-281.
Sahlström, S. y Brathen, E. 1997. Effects of enzyme preparations for baking, mixing time and resting time on bread quality and bread staling. Food Chemistry. 58(1): 75-80.
Schiraldi, A. y Fessas, D. 2001. Bread Staling: mechanism of staling. Primera edición. CRC Press. EE.UU. 589 p.
Stauffer, E. 1993. Frozen bakery products. En “Frozen Food Technology”. Ed. A.C., Mallet. Blakie Academic and Professional. Londres, Reino Unido. p. 303.C.
Steller, W., Bailey, C. 1938. The relation of flour strength, soy flour and temperature of storage to the staling of bread. Cereal Chemistry. 15:39-401.
Willhoft, E.M.A. 1971. Bread staling. I. Experimental study. Journal of the Science of Food and Agriculture. 22(4): 176-180.
Willhoft, E. M. A. 1973. Mechanism and theory of staling of bread and baked goods and associated
changes in textural properties. Journal Texture Study. 4: 292-392.
Xie, F., Dowell, F.E. y Sun, X. S. 2004. Using visible and near-infrared reflectance spectroscopy and
differential scanning calorimetry to study starch, protein, and temperature effects on bread staling. Cereal Chemistry. 81(2):249-254.

Temas Selectos de Ingeniería de Alimentos 5 - 2 (2011): 54 - 74

Producción de café (Coffea arabica L.): cultivo, beneficio, plagas y enfermedades
A.L. Temis- Pérez *, A. López-Malo Vigil, M. E. Sosa- Morales
Departamento de Ingeniería Química, Alimentos y Ambiental, Fundación Universidad de las Américas Puebla. Exhacienda Sta. Catarina Mártir S/N, Cholula, Puebla. C.P.72810. México.
Resumen
El café es uno de los productos más populares alrededor del mundo. Esta preferencia le ha otorgado el segundo lugar en la lista de los productos de mayor importancia económica a nivel mundial. La calidad del café depende de muchos factores, comprendidos principalmente en tres aspectos: el cultivo, la industrialización y el almacenamiento. Los factores determinantes en el cultivo son las especies y variedades manejadas, así como las condiciones agronómicas y ambientales. Los criterios más utilizados para establecer la calidad del café son la variedad genética, el tipo de cosecha y el proceso de industrialización. El presente documento tiene por objetivo explorar lo concerniente al beneficiado del café, desde la descripción de la planta, tratamientos post y pre cosecha a los que se somete, hasta mencionar algunas enfermedades y plagas que lo afectan.
Palabras clave: café, Coffea arabica L., plagas, enfermedades, beneficio.
Abstract
Coffee is one of the most popular products around the world. This preference has been awarded second place in the list of products of major economic importance worldwide. The quality of coffee depends on many factors, mostly included on three areas: farming, industrialization and storage. The determining factors in the crop are the kind of species and varieties, as well as agronomic and environmental conditions. The criteria used to establish coffee quality is the genetic variety, crop type and the process of industrialization. The present document aims to explore coffee processing and its treatments, also diseases and pests that attack it during pre and post-harvest.
Keywords: coffee, Coffea arabica L., pests, diseases, processing.
Introducción
En la actualidad, el café tiene un valor económico y social de suma importancia; está presente en las costumbres de muchos pueblos, así como en la vida diaria de millones de hombres y mujeres. Actualmente, más de 80 países lo cultivan en sus diferentes tipos y poco más de 50 lo exportan.
*Programa de Maestría en Ciencia de Alimentos Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: anala.temispz@udlap.mx
El café es uno de los principales productos agrícolas; después del petróleo, es el producto comercial natural que mueve las mayores cifras de dinero en el mercado mundial, llegando a generar ingresos anuales superiores a los 15 mil millones de dólares para los países exportadores y dando ocupación directa e indirecta a poco más de 20 millones de personas. Estas razones son un gran motivo para su estudio (CEFP, 2011; Cinza-Borrelli, et al., 2002; Renard, 1993).
La calidad final del producto depende de manera directa de diferentes factores, como son los tratamientos a los que se somete después de su cosecha, además, es importante tomar en cuenta las enfermedades y plagas que lo afectan, tanto durante su cultivo como durante su procesamiento, almacenamiento y comercialización.
Por otro lado, los cambios climáticos, de temperatura y precipitación, aumentarán la prevalencia de plagas y enfermedades, ampliando el rango altitudinal en el que sobreviven diferentes plagas y enfermedades como “la broca de café” (Hypothenemus hampei) , que perfora el grano del café cereza cuando aún se encuentra en el árbol; la “roya del café” (Hemileia vastatrix), que afecta de forma principal las hojas del árbol; “minador de la hoja” (Leucoptera coffeella), que provoca fuertes defoliaciones; “ojo de gallo” (Mycena citricolor), que forma manchas en tallos, hojas y frutos; “mancha de fruto” (Cercóspora coffeicola Berke-Cooke); y algunos hongos de los géneros Aspergillus, Penicillium y Fusarium; Las plagas reconocidas como las más importantes son la broca y la roya del café, y de los mohos los del género Aspergillus (FAO, 2011a). El área afectada por estas plagas y enfermedades ha ido aumentando gradualmente en la última década y, actualmente, solo existen algunos pesticidas químicos efectivos de los cuales se sabe generan altos riesgos de salud para los agricultores que lo aplican y además deprimen
la capa de ozono. Esto representa un impacto económico en el mundo, y significará pérdidas por más de US$74.7 millones para el año 2050 para países del sur de América (Läderach et al., 2011).
En México, por ejemplo, las actuales zonas productoras con un alto nivel de aptitud (60% a 100%) disminuirán de 265,400 a 6,000 ha, lo que representa una pérdida de productividad de 259,400 ha, superior al 97%. Estas macroestadísticas significarán que los trabajadores al nivel de la finca y a lo largo de toda la cadena de suministros enfrentarán grandes dificultades (Läderach et al., 2011).
Es por ello que surge la necesidad de realizar una investigación documental para describir los tratamientos que recibe el café pre y post- cosecha, las enfermedades y plagas que lo afectan y que tienen importancia dentro del campo de los alimentos.
Revisión bibliográfica
1. Generalidades del café
El café se define como la semilla seca de la planta del café sin importar que haya sido tostada o molida (Badui, 1993). El cafeto, el árbol del que proviene el grano, es originario de África, su nombre se deriva de la ciudad de Kaffa, en Etiopía. Durante muchos años, la exportación de plantas de café fuera de las naciones musulmanas estuvo prohibida. La propagación a nivel mundial del género de la planta Coffea partió del trópico africano. Para 1510 su producción y consumo ya se habían extendido hasta El Cairo (Cinza-Borrelli et al., 2002; Renard, 1993).
A principios del siglo XVII, el café se introdujo en la India y a finales del mismo siglo, se llevó a la isla de Java, donde las condiciones climáticas y la fertilidad de las
tierras permitieron que el café se adaptara perfectamente en las Indias Orientales. A mediados del siglo XVIII, el consumo de café se extendió por Europa. En América, el café fue introducido durante el siglo XVIII, la planta se propagó por el Caribe y el continente. En 1727, el café fue introducido en Brasil y en 1731 a Jamaica y Santo Domingo, de donde su cultivo se extendió al resto de los actuales países productores de América. Con la revolución industrial y el crecimiento de la población mundial durante el siglo XX, el café prácticamente se convirtió en una bebida universal (Renard, 1993).
La introducción del cultivo en México ocurrió hace 200 años (Cano-Flores et al., 2004). A nivel mundial, México es el quinto productor de café, después de Brasil, Vietnam, Colombia e Indonesia. La especie Coffea arabica es la predominante, contribuyendo con el 97% de la producción. México es el primer productor mundial de café orgánico, y uno de los primeros en cafés "Gourmet”, aunque la modalidad de consumo está estrictamente relacionada con los hábitos y culturas de los países individuales (CinzaBorrelli et al., 2002; Renard, 1993). El café se
produce sobre una superficie de 761 mil hectáreas en 12 estados de la República Mexicana, situados en la parte centro-sur del país. La Fig. 1 muestra las zonas de producción de café a nivel internacional, la variedad de café que se siembra depende de la latitud a la que se encuentra la región (CEFP, 2011).
1.1 Botánica
La planta de café es una dicotiledónea, proviene de un arbusto perenne que pertenece a la familia de las Rubiaceae, puede alcanzar 10 m de altura de forma silvestre y en una plantación de café controlada alcanza 3 m de altura lo cual facilita el cosechado. Esta familia comprende alrededor de 500 géneros y más de 6 000 especies. La mayor parte son árboles y arbustos que crecen en el estrato más bajo de los bosques tropicales. Las ramas primarias se oponen, en sentido horizontal o caídos, y las hojas crecen en pares en tallos cortos.Son de alrededor de 15 cm de longitud, de color verde oscuro y brillante en apariencia (Doyle et al., 2001; Clarke y Macrae, 1985).
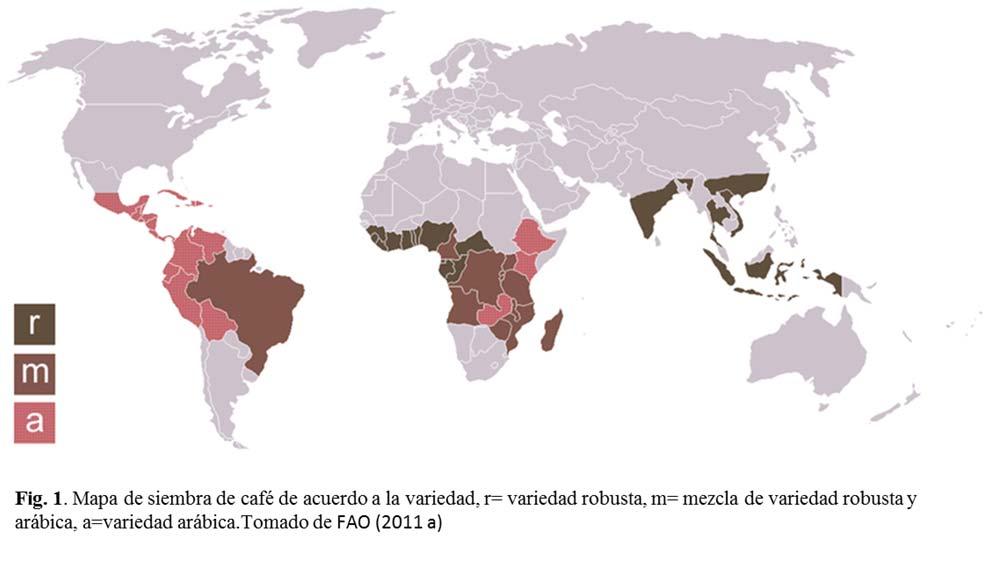
Las primeras flores (Fig. 2) son producidas entre los 3 y 4 años de edad, éstas son de color blanco cremoso y de aroma dulce, aparecen en racimos en las axilas de las hojas, la corola mide cerca de 20 mm de longitud, que en la parte más alta se divide en cinco pétalos (Clarke y Macrae, 1985). Después de que las flores se marchitan, los ovarios poco a poco se convierten en drupas ovaladas de hasta 18 mm de longitud y 10-15 mm de diámetro, éstos se convierten en lo que será más adelante el grano de café. Una flor forma un grano de café, que es la razón por lo que la planta florea en diferentes etapas durante el año.

1.1.1 Especies y variedades
Como se mencionó anteriormente los granos de café son las semillas de un arbusto de hoja perenne perteneciente a la familia Rubiaceae, y el género Coffea, que es sin duda, el miembro más importante de esta familia, desde el punto de vista económico, pues dos de sus especies son objeto de un abundante comercio. Las dos especies que son de importancia comercial son: Coffea arabica Linn y Coffea canephora Pierre ex Froehner. Éstas son conocidas en el comercio, respectivamente, como Arábica y Robusta. La especie de café Coffea arabiga representa aproximadamente el 80-90% de la producción mundial. Las dos variedades originales son generalmente reconocidas como C. arabica var. arabica (syn. var. ‘Typica’) y C. arabica
var. bourbon. La especie C. canephora representa cerca del 20% de la producción mundial. Las especies importantes de Coffea canephora, incluyen las distintas formas conocidas en el mercado como café robusta. El último nombre, “canephora”, se deriva de su nombre específico del C. robusta, pero hoy en día C. robusta es considerada como sinónimo de la variedad original de C. canephora. Existes tres variedades de robusta las cuales no tienen ningún valor en el mercado, que son: C. canephora var. Kouilouensis, C. canephora var. ’Nganda’ y C. canephora var ‘Niaouli’ (Cano-Flores et al., 2004; Doyle et al., 2001; Clarke y Macrae, 1985).
Otras dos especies conocidas son Coffea liberica Bull ex Hiern (conocida como libérica) y Coffea dewevrei De Wild y variedad Durand. Excelsa Chevalier (conocida como excelsa) se puede encontrar, pero su importancia comercial en la actualidad no es significativa, pues representan apenas el 1% de producción mundial (FAO, 2011a; Clarke y Macrae, 1985).
Existen diferencias importantes entre las dos principales especies comerciales y deben ser tomadas en cuenta. El café robusta se cultiva en altitudes relativamente bajas, tolera las altas temperaturas y lluvias muy intensas, exige un suelo más alto que contenga humus. Por lo general, es también mucho más resistente a las enfermedades que la arábica. Mientras que el grano de arábica es de color verde a verde pálido y de forma oval, el de robusta tiende a ser más redondo y puede ser marrón en lugar de verde. La especie arábica en general produce buenas infusiones con acidez, más sabor y aroma (FAO, 2011b; Clarke y Macrae, 1985).
1.1.2 Frutos del café
El fruto es a menudo llamado cereza, que según SAGARPA (PC-010, 2004) se define como el fruto fresco completo del árbol que
consta de una serie de capas que envuelven generalmente dos granos de café. Las capas externas se denominan como:
o Cáscara o pericarpio: envoltura externa del fruto de café.
o Pulpa o exocarpio: carne o tejido de la fruta que se encuentra por debajo de la cáscara.
o Mucílago o mesocarpio: sustancia viscosa y pegajosa que se encuentra adherida al endocarpio.
o Pergamino o endocarpio: tejido duro y compacto que recubre a la semilla o grano del café individualmente.
o Cutícula: membrana delgada de color blanquecino que se encuentra adherida a la semilla o grano del café. También conocida como película plateada. Episperma (sinónimo de espodermo).
o Grano de café: semilla(s) contenida en la fruta del café. Normalmente existen dos en cada fruta, pero puede haber sólo una o hasta tres.
Las partes que conforman el fruto de café se muestran en la Fig. 3.
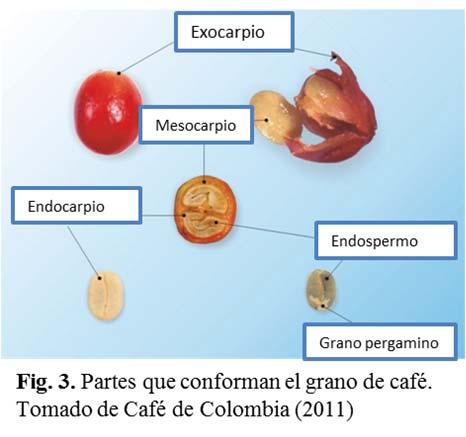
El tamaño del grano de café varía y éste se mide en zarandas, láminas con perforaciones redondas o bien pueden ser alargadas, las más
comunes se muestran en la Tabla I. Las medidas se expresan en 1/64 de pulgada (0.3968 mm).
Tabla I. Clasificación del grano de café por tamañoa
Número de zarandas
Terceras o grano pequeño14-15
Segundas o grano mediano16-17
Primeras o grano grande18
Grano superior19-20
aAdquirido de Aguilar-Ruiz (1999)
El fruto de café tiene como base el color llamado verde olivo o verde aceituna. Esta coloración va variando dependiendo de la cosecha, las condiciones del terreno y las condiciones atmosféricas. Desde que se da el brote en la planta, se corta y se madura el fruto, el cual pasa por diversas coloraciones que van de verde oscuro a morado, lo anterior se muestra en la Fig. 4.
El color del grano de café oro, es decir el café que ya fue procesado, varía de acuerdo con la región y altura donde se produce, sin embargo, puede alterarse radicalmente con el beneficiado. Por ello se debe tener mayor cuidado con la aplicación de temperaturas elevadas; esta aplicación de calor debe ser cuidadosamente controlada. Finalmente, el color también puede variar de acuerdo a las condiciones de almacenamiento (NiñoSandoval y Prieto-Ortiz, 2007; Badui, 1993).
1.2 Composición química del café en grano
El café verde sin procesar contiene agua, proteínas, cafeína, lípidos, diversos carbohidratos y ácidos (principalmente solubles y no volátiles), trigonelina y minerales. El café tostado contiene azúcares reductores, azúcares caramelizados,
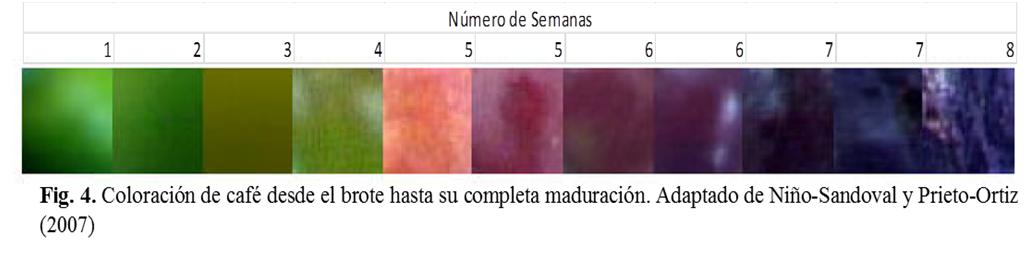
hemicelulosa, fibra, proteínas, ácidos no volátiles (caféico, clorogénico, cítrico, málico, oxálico, quínico y tartárico), cafeína, lípidos, trigonelina, y cenizas, en las cuales los principales elementos constituyentes son potasio, fósforo, y magnesio. Se ha sugerido que el contenido de ácido clorogénico puede ser un factor indicador de la calidad (CinzaBorrelli et al., 2002; Badui, 1993). La Tabla II muestra un resumen de los componentes químicos principales tanto en grano de café verde como tostado para la variedad arábica y robusta.
Entre los principales componentes químicos del grano de café están las melanoidinas que son definidas como macromoléculas de color café que contienen nitrógeno, y representan hasta un 25% de materia seca. Diferentes estudios sugieren que éstas son responsables de las fuertes propiedades antioxidantes, antibacterianos y quelantes mostradas por las bebidas de café (Cinza-Borrelli et al., 2002).
1.3 Beneficios a la salud
El café contiene más de 1000 compuestos distintos, incluyendo aminoácidos y otras sustancias nitrogenadas, polisacáridos, ácido clorogénico, entre muchos otros. Los ácidos clorogénicos son considerados como antioxidantes, es decir, tienen la capacidad de atrapar radicales libres, aunque la actividad antioxidante del café no sólo se debe atribuir a estos compuestos. También a la presencia de cafeína y de otros compuestos producidos durante el tostado, como las melanoidinas, que compensan la disminución de los ácidos clorogénicos que se producen durante este proceso. La cafeína inhibe la lipoperoxidación inducida por radicales hidroxilos (OH), peróxidos (ROO) y oxígeno, por lo tanto es un antioxidante tan potente como el glutatión y superior al ácido ascórbico (Higdon y Frei, 2006; Cinza-Borrelli et al., 2002).
La máxima actividad antioxidante se
ComponenteCafé verdeCafé TostadoCafé verdeCafé Tostado Minerales3.0-4.23.5-4.5
Ácido clorogénico5.5-8.01.2-2.3
Ácidos alifáticos1.5-2.01.0-1.5
Aminoácidos2.00
Proteínas11.0-13.013.0-15.0
Adaptado de Norrish (2001).
Tabla II. Resumen de datos de composición química (%b.s.) para café verde y tostado tanto para variedad arábica y robusta
Arábica
Robusta
detecta en el café medianamente tostado. En diversos países como Italia, Noruega, España, entre otros, el café aparece como el mayor contribuyente de la ingesta total diaria de antioxidantes, y esto lo convierte en una fuente dietética de antioxidantes de carácter único, con un perfil muy específico y con una alta capacidad antioxidante total (Cinza-Borrelli et al., 2002).
En diferentes estudios se ha relacionado al consumo de café con beneficios a la salud (Valenzuela, 2010). Higdon y Frei (2006) reportaron que se ha encontrado una correlación significativa que señala que en adultos sanos la ingesta diaria promedio de café promueve la actividad antioxidante y proporciona un beneficio en el lumen de colon. Por otro lado, la relación que existe entre el consumo de café y la diabetes tipo II se muestra favorable, pues se ha demostrado que la cafeína reduce en un 15% la sensibilidad a la insulina, esto se ve reflejado en los efectos secundarios que tiene el consumo de insulina, pues los pacientes tienden a ganar peso. En otros casos, la cafeína estimula la liberación de epinefrina lo que reduce notablemente la acción de la insulina. En cuanto a la enfermedad de Parkinson, que alrededor del 3% de la población mayor de 65 años la padece, se estima que esta cifra podría duplicarse en los siguientes 30-40 años. En los estudios realizados se sugiere un efecto protector ejercido por el consumo de café y aunque el mecanismo de protección aun no es conocido, en bibliografía se encuentra que al consumir 300 mg/día de café se logró reducir de 10.4 a 1.9 el número de sujetos enfermos de Parkinson, por cada 10,000 sujetos estudiados (Higdon y Frei, 2006 y Cinza-Borrelli et al., 2002).
Aunque hay discrepancias en cuanto a los efectos positivos y negativos del consumo de café a largo y a corto plazo; en el caso de los beneficios que puede causar el consumo del café en personas con diabetes, debido al gasto
energético inducido por el consumo de éste podría ser beneficioso a largo plazo en individuos con sobrepeso. En sujetos diabéticos, es posible que con el tiempo se desarrolle una tolerancia a la cafeína y desaparezcan los efectos agudos nocivos de ésta sobre la tolerancia a la glucosa (Higdon y Frei, 2006). En cuanto a efectos sobre el hígado se ha encontrado que hay una relación directa con el consumo de café, ya que se descubrió que con un consumo mayor a cuatro tazas diarias, un individuo puede desarrollar cirrosis hepática.
Según Valenzuela (2010), una taza en promedio aporta entre 90-200 mg de cafeína y el consumo de cafeína por encima de 600 mg/día, constituye un riesgo de hipertensión y por consiguiente para la salud cardiovascular. Se afirma que el consumo moderado de café parece aportar muchos más efectos benéficos que nocivos.
1.4 Importancia económica del café
Desde 1980 ha venido cobrando fuerza el comercio internacional alternativo de alimentos y bebidas que desafían las grandes empresas transnacionales. En 2005 se comercializaron más de 5.5 millones de toneladas de café en el mercado mundial.
La producción mundial de café se integra por tres tipos: los suaves, los arábigos y los robusta. Los primeros son procesados por medio del método de lavado (despulpado, lavado y secado inmediatamente después de haber sido recolectado). Los segundos generalmente son no lavados (el grano recolectado se seca y almacena con su pulpa o cáscara exterior, y se despulpa posteriormente antes de ser entregado al comprador) y su calidad es inferior a la de los suaves. Finalmente, los del tercer tipo son los menos cotizados en el mercado tanto por su calidad como por su precio (Cano-Flores et al., 2004; Cinza-Borrelli et al., 2002).
En la cosecha de 1999-2000 la producción a nivel nacional de café ascendió a 6 millones, 192 mil sacos de 60 kilos, de los cuales se exportaron 5 millones 137 mil sacos de 60 kilos a 52 países, es decir, el 83 % de la producción nacional de café se exporta y únicamente el 17 % restante se destina al mercado doméstico. En el ámbito nacional, Chiapas es el primer productor de café con una participación de 34.8 %, Veracruz con 25.2 %, Oaxaca y Puebla con un 28 %, por lo que cuatro estados aportan el 88 % del total nacional (CEFP, 2011). Le siguen Guerrero, Hidalgo, San Luis Potosí, Nayarit, Jalisco, Tabasco, Colima y Querétaro. Las llamadas regiones ecológicas del café están conformadas de la manera siguiente (CanoFlores et al., 2004):
o Vertiente del Golfo de México: comprende los Estados de San Luis Potosí, Querétaro, Hidalgo, Puebla, Veracruz y Tabasco.
o Vertiente del Océano Pacífico: constituida por las zonas de las entidades de Nayarit, Jalisco, Colima, Guerrero y Oaxaca.
o Región del Soconusco: comprende parte del estado de Chiapas, que geográficamente se ubica como perteneciente a la vertiente del Pacífico.
o Región Centro-Norte de Chiapas: constituida por la parte centro y norte de la entidad.
2. Procesamiento del café
2.1 Cosecha
El método de cosecha depende de una mezcla de exigencias del beneficiado, consideraciones económicas y disponibilidad de mano de obra. Por lo general se cosecha anualmente, cuando maduran las cerezas, es decir, cuando adquieren un color rojo brillante, tienen lustre y están firmes al tacto. El momento de la cosecha varía según la zona geográfica, pero en general la cosecha se realiza entre septiembre y marzo.
En general se pueden señalar cuatro sistemas: 1) cosecha selectiva en varias etapas (manual), en la que se recogen sólo las cerezas maduras; 2) cosecha selectiva en varias etapas en la que se arrancan los racimos cuando contienen principalmente cerezas maduras; 3) cosecha única en la que los trabajadores cosechan todo a su paso por el cafetal; 4) cosecha mecánica con maquinaria, a veces operada manualmente, que desprende el fruto del árbol mediante vibración. Además de estos métodos de cosecha, antes y después de la misma se llevan a cabo otras actividades, de algunas de las cuales también se obtiene fruta. A menudo se realiza una cosecha previa para recoger los frutos que han madurado prematuramente, también se lleva a cabo el deshierbe y la limpieza del cafetal para acelerar el extendido de las esterillas o la recogida de la fruta caída (FAO, 2011a; FAO, 2011b).
Después de la cosecha principal suelen recogerse los frutos no recolectados en la misma, parte de los cuales quedaron en los cafetos, aunque casi todos en el suelo. Normalmente esta práctica se realiza como una medida importante del manejo integrado de plagas, pero tradicionalmente este café ingresa en la cadena de alimentos para consumo humano.
La recolección selectiva de cerezas maduras evidentemente eleva al máximo la cantidad de café maduro que se cosecha, ya que los granos, que todavía no están maduros se dejan en el árbol para madurar, y las cerezas que se han pasado de madurez se evitan. De esta manera se lleva a cabo un control de calidad inicial sobre el producto. Desde el punto de vista de la calidad, es mejor evitar el uso de cerezas inmaduras, y también debe evitarse recoger cerezas del suelo ya que pueden estar muy contaminadas de esporas de hongos y presentar un elevado riesgo de presencia de OTA (ocratoxina A) (FAO, 2011 a).
Los factores económicos son cruciales para determinar el método de cosecha que se seleccione. La cosecha manual selectiva es la parte más costosa de la producción de café, suelen necesitarse entre 5 y 10 "pasadas" en una cosecha. La cosecha mecánica se ha perfeccionado desde la década de 1970 y ahora se utiliza mucho en países de América del Sur. Pero la cosecha mecánica es algo más que la simple introducción de una máquina, es necesario sembrar en setos dejando entre éstos espacios adecuados, lo que es más importante en entornos en los que se produce una considerable sincronización de la floración y las cerezas pueden tener una vida prolongada (Norris, 2001).
Recientemente se ha comprobado que se puede mantener las cerezas frescas temporalmente en agua limpia, después de haber sido cosechadas; pero este material se debe despulpar y lavar pronto. El producto de la cosecha debe corresponder al beneficiado previsto y evaluarse de acuerdo a esta correspondencia.
2.2 Procesamiento (beneficiado)
El beneficiado es el tratamiento del café cosechado hasta producir granos secos y estables, es decir, la transformación del fruto maduro de la planta de café conocido como “cereza”. El principal objetivo es separar los granos del café de la piel y la pulpa de la cereza, lo que representa la primera parte de la cadena agroindustrial. Asimismo, la utilización de ese café para la obtención de una serie de productos con un valor agregado más alto, representa una tendencia muy reciente en la que la diversificación de usos del café conforma la segunda parte de la cadena agroindustrial (Cinza-Borrelli et al., 2002; Fundación Produce, 2003).
Los frutos maduros de café pueden ser procesados por tres métodos distintos para obtener los granos verdes. El proceso más
sencillo y rústico es el procesamiento seco, que se utiliza para fermentar y secar café al sol sobre plataformas y/o cemento. Otro es el proceso húmedo, en el que la pulpa y/o mucílago es eliminado por medios mecánicos, y los granos se fermentan en depósitos con un gran volumen de agua. Y el proceso semi-seco que es una variación del proceso húmedo, en el que, de los frutos del café también se les quita la pulpa, pero el proceso de fermentación se realiza directamente en la plataforma (FAO, 2011a).
Los diferentes tipos de procesamiento producen bebidas con gustos y aromas que el cliente puede elegir de acuerdo a sus preferencias. La variedad arábica produce los cafés más apreciados por el bebedor de café más exigente, y se subdivide en el comercio en función de si el café ha sido procesado por el método húmedo o seco. Los cafés de mejor calidad, y por lo general los más caros, son los de la especie arábica preparados por el proceso húmedo y se les conoce como cafés suaves. Poseen un sabor fino, aromático y con cuerpo. Los granos de arábica preparados por el método seco están representados principalmente por Brasil, el mayor productor a nivel mundial (Marques- Vilela et al., 2010).
El beneficiado húmedo requiere cerezas de madurez uniforme. El producto principal del beneficiado húmedo es el café verde o pergamino. Las cerezas separadas pueden tener muchos defectos, algunos de los cuales, se asocian a un mayor riesgo de contaminación por OTA en comparación con los granos sanos producidos en el mismo lote (Clarke y Macrae, 1985).
En el beneficiado seco se seca toda la cereza con o sin medidas previas de selección o separación. Entre las variaciones está mantener el café cosechado en sacos, que no se remueven, antes de extenderlo para secar y abrir la cereza con medios mecánicos, como el
despulpado, pero donde el pergamino y la piel se secan como masa sin separar (FAO, 2011a).
El secado de la cereza, necesita de la aplicación de buenas prácticas y medidas de gestión tanto como en el método húmedo, que es más complicado. En el beneficiado seco hay que eliminar casi el doble de agua por kilogramo de café que en el beneficiado húmedo. Para observar mejor el proceso de beneficiado se muestra un diagrama de flujo en la Fig. 5.
Por otro lado, es importante tomar en
cuenta que hay estudios sobre el tema que demuestran que con frecuencia las cerezas recogidas se mantienen de tres a siete días en sacos o apiladas, sobre todo entre los pequeños productores. En estas condiciones se experimentan elevadas temperaturas y la fermentación se acelera, en forma diferente que la fermentación utilizada en el beneficiado húmedo. Por esto se recomienda que una vez cosechada, la cereza fresca se extienda enseguida para secarla. Además, la demora antes del beneficiado a menudo deteriora considerablemente la calidad del café.
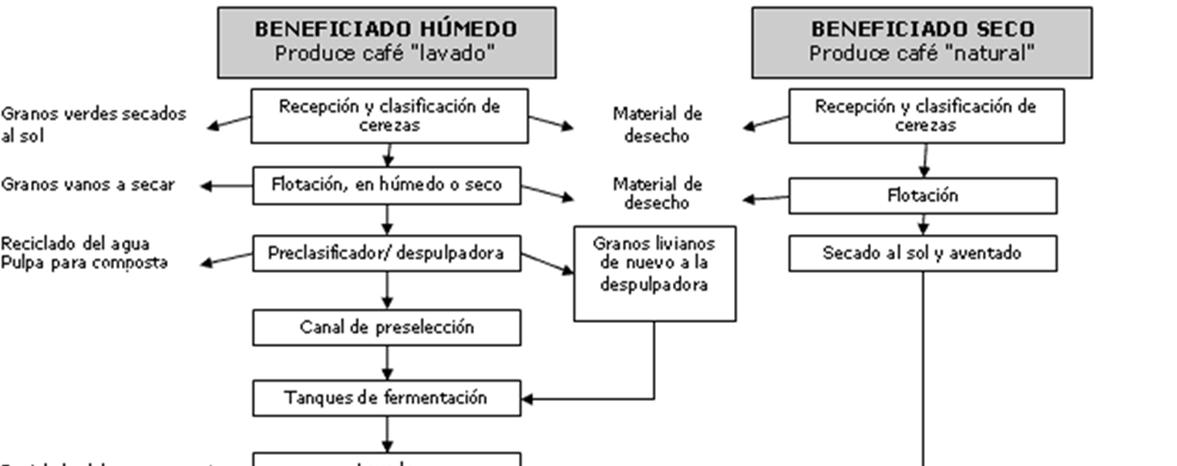
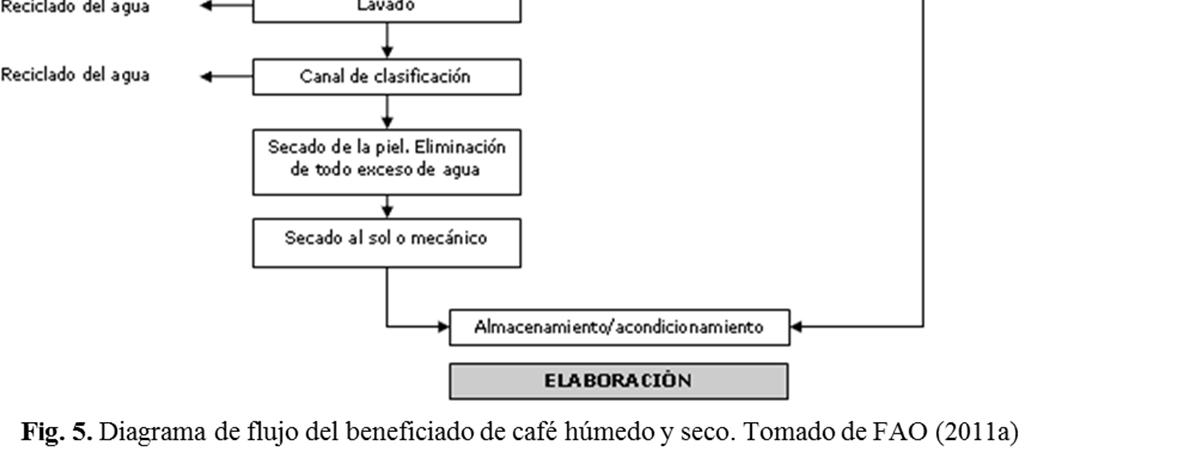
2.3 Almacenamiento del café
Es necesario tomar una serie de precauciones para mantener el café bien seco en buenas condiciones y sin deterioro ni pérdida de calidad durante el almacenamiento y el transporte. La humedad, el diseño y ubicación del almacén, la duración del almacenamiento y también evitar que el café se humedezca de nuevo durante el transporte, son factores importantes a considerar (ISO, 1986).
No deben almacenarse nunca las cerezas frescas antes de someterlas al procesamiento, y el lapso de tiempo entre la cosecha y el beneficiado debe reducirse al mínimo, a fin de que el peligro de contaminación por OTA sea menor. También es importante que todos los recipientes utilizados para transportar las cerezas frescas y el pergamino húmedo estén
limpios y no contengan cáscaras ni otras materias que pueden estar muy contaminadas por mohos.
Después del beneficiado, los granos verdes secos suelen almacenarse en sacos (lo mejor es que sean de yute para contener alimentos o de algún material equivalente), o en silos, antes de la elaboración final anterior a la exportación. Sólo deben utilizarse sacos y silos o recipientes metálicos secos y limpios. El café debe cubrirse durante el transporte y sólo se debe cargar y descargar cuando el tiempo es seco o manejarse en interiores. No se deben mezclar en el almacén los distintos tipos de café (café pergamino, cerezas secas o granos).
En la Fig. 6 se muestra un ejemplo de esquema de almacenamiento de café en sacos.
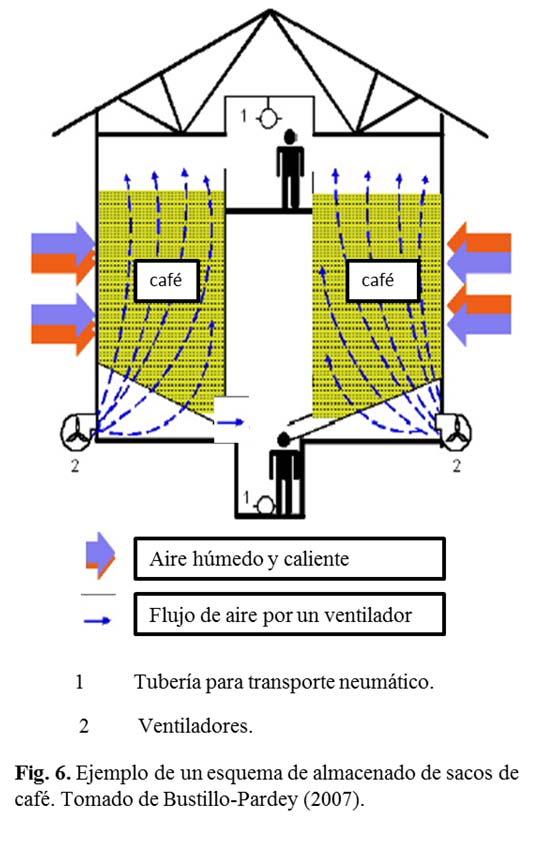
3. Enfermedades y plagas
3.1 Plagas en el café cereza
Las enfermedades y plagas de las plantas de café son variadas. Entre las plagas que atacan las raíces se encuentran las palomillas, escamas y nematodos. El tallo y las ramas son afectados por los cortadores y taladradores, mientras que las hojas son dañadas por los cortadores y chupadores, y algunos frutos por la broca (Bustillo-Pardey, 2001).
Entre las enfermedades, las más graves son: la roya (Hemileia vastatrix), cercospora, llaga negra, antracnosis, phoma, y otras como ojo de gallo y mal de hilachas que están ligadas a las condiciones ambientales. En definitiva, las plagas e insectos más importantes que atacan las plantas del café son la escama verde, la escama coma, la escama globosa, la escama algodonosa y la chinche harinosa. También el cortador o rosquillo, los bachacos, las palomillas, los nematodos y el minador, que es la larva de una mariposa pequeña, que ataca las hojas. Las plagas de las hojas son más habituales en épocas de sequía, en tanto que las de las raíces ocurren en épocas de lluvias. Las plantas jóvenes están más expuestas a las escamas, al igual que los cafés arábicos, que por otra parte, también son más propensos a palomillas y nematodos (Bustillo-Pardey, 2001; Morales-Ramos et al., 2000).
Una de las plagas de mayor importancia económica que afectan al café, que ya se mencionó anteriormente, es Hypothenemus hampei (Ferrari) (Coleoptera: Scolytidae) llamada broca del café; es la plaga más importante que afecta el café en el mundo. Es un insecto pequeño, responsable del mayor daño en los cultivos de café, y el que más preocupación ocasiona a los productores, pues daña el fruto del café al atacar la cereza y reproducirse internamente en el endospermo, causando la pérdida total del grano y en muchos casos, la caída prematura de los frutos.
Además, reduce la calidad del producto final (Bustillo-Pardey, 2007; Rodríguez-del-Bosque y Arredondo-Bernal, 2007).
3.2 Enfermedades en el café en grano
La biodiversidad microbiana presente en los frutos y los granos de café depende de la variedad de café, el método de procesamiento, el medio ambiente (factores de la región en la que se cultivan como humedad y temperatura) y el suelo (Batista et al., 2009). Se ha reportado la presencia de bacterias, levaduras y hongos filamentosos en la cereza y en los granos de café producido en Brasil, India, Hawái, Congo, Argentina, Colombia, Costa Rica, Etiopía y México (Avallone et al., 2001; Silva et al., 2004).
Según Alvindia y Acda (2010), la microbiota del grano de café es diversa y está compuesta por 26 especies de 14 géneros diferentes, entre los que se encuentran Acremonium, Aspergillus, Cladosporium, Cylindrocarpon, Crysosporim, Fusarium, Leptosphaerulina, Microascus, Microdiplodia, Mucor, Nigrospora, Penicillium, Pestalotiopsis y Rhizopus. Además mencionan que el género de hongo que predomina en su mayoría es Aspergillus, logrando aislar A. chevalier, A. flavus, A. fumigatus, A. japonicus, A. niger, A. ochraceus, A. restrictus y A. terreus; de éstos, dos Aspergillus negros fueron los encontrados con mayor frecuencia, ya que fueron aislados en un 55% del café analizado.
Algunos mohos presentes en el café producen micotoxinas durante el almacenamiento de los granos. La mayoría son de los géneros Aspergillus, Fusarium, Gilerella y Penicillium. Entre las micotoxinas que producen se encuentran las aflatoxinas y la ocratoxina A (OTA), ésta última siendo la de mayor importancia por los efectos negativos que provoca (Soliman, 2002; Perrone et al., 2007). Algunos de estos son los siguientes:
inhibición de la producción de energía, de la actividad de la ATPasa, de la síntesis de proteínas; modificación del citoesqueleto, de las funciones de los microfilamentos y microtúbulos celulares; acción sobre el sistema nervioso central induciendo temblores; y efecto cancerígeno, ya que provocan desarrollo de tumores en el hígado y en la corteza renal (Williams et al., 2004).
Se ha visto que durante la cosecha y almacenamiento existe un mayor riesgo de adquisición de enfermedades en el fruto. Se sabe que las semillas del café pueden contener OTA al momento de la cosecha, pero no es factible detectar estas semillas. Además en la recolección, como ya se mencionó anteriormente, el recoger las semillas del suelo también es un factor de riesgo para la presencia de esta micotoxina. Por otro lado, durante el almacenamiento, mantener el café en sacos puede producir, en forma desigual, elevados niveles de OTA y pérdida de calidad. Asimismo, secar en capas demasiado gruesas a velocidad lenta propicia la proliferación de mohos y la posible producción de micotoxinas. Se ha demostrado que en los botes de acondicionamiento se acelera poco el secado, de modo que el tiempo que el grano pasa en estos botes incrementa la posibilidad de descomposición (FAO, 2011 a).
Por otro lado Pardo et al. (2004) encontraron mayores niveles de OTA en granos de café verde provenientes de África, en comparación con aquéllos originarios de América y Asia; los autores concluyeron que el origen afecta el contenido de toxina que presenten en los granos de café verde.
La carga microbiana puede degradar los compuestos presentes en los granos e influir así en la calidad del producto final. Es por ello que tener conocimiento de las especies microbianas dominantes presentes en el café es relevante para su procesamiento (MarquesVilela et al., 2010).
La microbiota encontrada en el grano de café se encuentra clasificada según el tipo de microorganismo en la Tabla III
4. Tratamientos para el control de enfermedades y plagas
Para el tratamiento y control de enfermedades y plagas es importante considerar las Buenas Prácticas Agrícolas (BPA), pues éstas buscan que los alimentos y productos para el consumo humano, como el café en bebida, se fabriquen y elaboren en condiciones sanitarias adecuadas, con lo cual se protege la salud de la población mundial. El uso de prácticas higiénicas y buen manejo de los granos de café pueden minimizar la producción de hongos y micotoxinas en el café (Ferreira-Silva et al., 2008).
En otros países, se han decretado las Buenas Prácticas de Manufactura para la elaboración y expendio de alimentos. Esto promueve su implementación en las cadenas agrícolas del país. Cada sector elabora y adapta aquellas que le garanticen un sistema de aseguramiento de la calidad.
Es imprescindible que cada finca cumpla con requisitos higiénicos para los procesos del café, un programa de saneamiento que incluya procedimientos de limpieza y uso de desinfectantes, manejo de residuos sólidos y líquidos, y control de plagas (Bustillo-Pardey, 2007).
Las BPA deben planificar y seleccionar las prácticas de cultivo, los métodos fitosanitarios y el manejo de cosecha y post-cosecha, de tal forma que se mantenga el equilibrio en los agro- ecosistemas cafetaleros, se conserven los suelos, las fuentes de agua y se proteja a las personas. Dichas prácticas deben considerar que las semillas sean de buena calidad. Se recomiendan variedades con resistencia a la roya del cafeto, además se deben realizar: las
Tabla III. Microorganimos aislados en el beneficiado de café.
BacteriasLevadurasMohos filamentosos
Acicetobacter sppArula sp.Aspergillus sp.
Bacillus sp.Candida ernobiiAspergillus chevalieri
Bacillus cereusCandida fukuyamaensisAspergillus foetidius
Bacillus maceransCandida membranifaciensAspergillus niger
Bacillus megateriumCandida carpophilaAspergillus ochraceus
Bacillus subtillisHanseniaspora uvarumAspergillus tubigensis
Enterebacter agglomeransFloeckera sp.Aspergillus versicolor
Erwinia herbicolaKluyveromyces sp.Cladosporium sp.
Escherichia coliPichia anomalaCladosporium cladosporoides
Klebsiella pneumoniaePichia caribbicaCladosporium macrocarpum
Lactobacillus brevisRodotorula mucilaginosaCylindrocarpon sp.
Lactobacillus plantarumSaccharomyces bayanusEurotium chevalieri
Lactococcus lactisSaccharomyces sp.Fusariella sp.
Leuconostoc mesenteroidesTorulaspora delbrueckiiFusarium sp.
Serratia sp.Fusarium clamidosporum
Fusarium lateritium
Fusarium nivale
Fusarium solani
Fusarium sporotrichioides
Geotrichum sp.
Mucor hiermalis
Penicillium brevicompactum
Penicillium commune
Penicillium decumbens
Penicillium fellutanum
Penicillium implicatum
Penicillium roqueforti
Phoma sp.
Ulocladium sp.
remociones oportunas de hierbas, la fertilización en la frecuencia y dosis requerida, y los controles fitosanitarios basados en los principios de Manejo Integrado de Plagas y Enfermedades.
Las buenas prácticas en la recolección del café se deben cuidar durante la época de cosecha. Es por ello necesario verificar que los recolectores estén capacitados para la recolección selectiva de frutos maduros. El café cosechado debe ser empacado en sacos o recipientes limpios, libres de
contaminaciones, protegerse de daños físicos y de altas temperaturas, y entregarse pronto al beneficio, de tal forma que no se sobrefermente, humedezca o contamine. No se debe permitir que los granos verdes pasen al tanque de fermentación, ni al secado. Los frutos y granos recogidos del suelo deben tener un manejo separado que impida la proliferación de la broca, y la contaminación del café (Bustillo-Pardey, 2007).
En cuanto a las buenas prácticas en la recepción del café cereza, éste debe
Adaptado de Marques-Vilela et al.( 2010)
inspeccionarse y clasificarse antes del procesamiento. No se debe aceptar el café cereza, si se conoce que contiene contaminantes que no puedan reducirse a niveles aceptables por el procesamiento y la clasificación normal.
En los últimos años a nivel mundial, se ha propuesto el manejo integrado de plagas y enfermedades (IMPP, por sus siglas en inglés). Su uso ha sido limitado, ya que requiere información como topografía, tipo de suelo, prácticas agronómicas, biología de las plagas y opciones disponibles para suprimir su población, entre otros aspectos, que sólo son conocidos/manejados por expertos, lo que dificulta que los productores puedan aplicarlo. En Jamaica, por ejemplo, se ha propuesto un nuevo sistema correctivo (CPEST) más amigable para el productor, un sistema que localiza acciones correctivas en caso de que se presente un problema durante el cultivo y procesamiento del café (Mansingh et al., 2007).
4.1 Tratamientos durante el cultivo
Durante el cultivo del café se deben llevar a cabo diferentes prácticas para evitar enfermedades o plagas. Algunas de éstas son determinadas para cada tipo de enfermedad, pero entre las principales se encuentran las siguientes (Bustillo-Pardey, 2007):
o Usar insecticidas con adherentes.
o Realizar labores de raspa, repase y recolección de los granos que han quedado después de la cosecha, quemándolos de inmediato para disminuir los daños de la próxima cosecha.
o Usar plantas que procedan de viveros libres de plagas.
o Proporcionar a la planta una mayor luminosidad y ventilación, mediante podas y raleos de los árboles, deshierbe oportuno.
o Fertilizar en épocas y dosis adecuadas.
o Recoger y quemar las hojas enfermas.
o Controlar la sombra.
o Limpiar el cafetal y drenar los suelos, evitando la formación de charcos.
Mansingh et al. (2007) coinciden con que la fertilización previene el daño en hojas, y que el tratamiento químico contra insectos es sólo eficiente cuando la plaga ha infestado menos del 6% de las plantas.
Aunque el uso de insecticidas para el control de plagas es lo más común como medida de control, no es lo más recomendable. Esta práctica tiene el inconveniente de que cuando el insecto alcanza el interior de los frutos, ya no es útil; los insecticidas sólo deben usarse cuando los insectos están penetrando nuevos frutos. Además, el uso de insecticidas conlleva graves problemas de contaminación ambiental y residuos que dañan la vida animal y al hombre, pues elimina la fauna benéfica. Como consecuencia de ello, surge la introducción de enemigos biológicos como parasitoides y entomopatógenos (BustilloPardey, 2007).
Según Téllez-Jurado et al. (2009), los microorganismos tienen mecanismos de invasión únicos que les permiten atravesar de forma directa la cutícula o la pared del tracto digestivo de los insectos, lo que los hace excelentes agentes de control biológico, actuando como insecticidas de contacto. En algunas partes del mundo se han desarrollado programas de manejo integral con el fin de asegurar la biodiversidad y estabilidad ecológica de la zona cafetera, basados en procedimientos de control biológico de las plagas, de manera especial de Hypothenemus hampei (Ferrari) (Coleoptera: Scolytidae).
Al sur de América se introdujeron microorganismos, como Bauveria bassiana, Cephalonomia stephanoderis al principio de la década de los 90 y se desarrollaron procesos
de producción masiva y liberación en cafetales colombianos (Bustillo et al., 1999). A partir de esa época se han desarrollado estudios para su producción masiva y liberación en cafetales en otros países del mundo.
Otros microorganismos utilizados como control biológico son Bauveria tenella, Verticillium, Metarhizium, Fusarium, Paecilomyces tenuipes, Tolypocladium. Aunque se han encontrado más de 750 especies de hongos entomopatógenos y el aislamiento de nuevas cepas continua, los más utilizados son Metarhizum anisopliae (33.9 %), Bauveria bassiana (33.9 %), Isaria fumosorosea, (5.8 %) y Bauveria brongniartii (4.1 %). El desarrollo de la enfermedad en el insecto esta dividido en tres fases: 1) Adhesión y germinación de la espora en la cutícula del insecto, 2) penetración en el hemocele, 3) desarrollo del hongo, que generalmente resulta en la muerte del insecto (Vázquez et al., 2010; TéllezJurado, 2009; Bustillo et al., 1999).
Entre los microorganismos utilizados como control biológico se encuentran algunos parasitoides como: Cephalonomia stephanoderis Betrem, Prorops nasuta Waterston, Cephalonomia hyalinipennis, los dos primeros sin mucho impacto sobre la broca. Las tres especies viven como ectoparasitoides durante su estadio de larva y pupa, y generalmente depredan los huevos de H. hampei. Otro que podría ayudar a controlar la broca es Sclerodermus cadavericus Benoit (proveniente de África), sin embargo el manejo de esta avispa es complicado dada su agresividad, sus picaduras pueden causar severas dermatitis. Phymastichus coffea fue descubierto en Togo (África) en 1987. Ataca al adulto de la broca por lo cual es un buen candidato para el control. Se ha logrado cultivar en diferentes laboratorios de América, además se ha logrado establecer en varias decenas de
cafetales en Colombia, aun así se estudia su capacidad para establecerse a largo plazo. Estudios recientes de exploración en Uganda han permitido localizar poblaciones de Heterospilus coffeicola Schneideknecht como enemigo natural de la broca, pero desde entonces ha sido difícil reproducirlo tanto en el laboratorio como en el campo (BustilloPardey, 2005).
Otros organismos de control biológico son las hormigas (Hymenoptera: Formicidae). Por su parte, investigadores del Centro Nacional de Investigaciones de Café (Cenicafé, Colombia) han reportado que además de las hormigas otras familias de insectos están implicadas en la depredación de la broca: Anthocoridae (Hemiptera) y Cucujidae (Coleoptera). Las poblaciones de estos depredadores son mayores en plantaciones de café donde las fumigaciones son poco frecuentes. Algunos estudios sugieren que los cultivos intensivos de café disponen de condiciones menos favorables para los depredadores. La siguiente es una lista de géneros y especies que han sido observadas atacando a la broca. A) Formicidae: Solenopsis, Pheidole, Wasmannia, Paratrechina, Crematogaster, Brachymyrmex y Prenolepis. B) Anthocoridae: Calliodes y Scoloposcelis. C) Cucujidae: Cathartus quadricollis (Barrera, 2005).
Estos organismos han sido probados en cafetales en el control de la broca y luego reproducidos masivamente en forma comercial, logrando así manejar racionalmente un cultivo sano y seguir produciendo café para exportación (Bustillo-Pardey, 2005; MoralesRamos et al., 2000).
4.2. Tratamientos poscosecha
El café, por ser un producto tropical, tiene altas probabilidades de ser colonizado por diferentes especies de mohos del género Aspergillus (A. ochraceus y A. carbonarius),
capaces de sintetizar micotoxinas como la ocratoxina A (Mantle y Chow, 2000). La ocurrencia de ocratoxina A en café verde y tostado ha sido ampliamente reportada en la literatura (Otteneder y Majerus, 2001). Romani et al. (2000) mostraron que 106 de 162 muestras de café verde de varios países fueron positivas para la presencia de ocratoxina A, con concentraciones de hasta 48 ppb. La ocratoxina A puede presentarse en el grano de café expuesto a diversas condiciones ambientales (condiciones climáticas, tiempo anormalmente largo de almacenamiento, y transporte) y de procesamiento (vía húmeda o seca) (Smith et al., 1994; Yiani, 1996). Sería posible reducir la contaminación por ocratoxina A si se comprenden el escenario y las condiciones bajo las cuales los mohos crecen y este compuesto se produce durante la obtención y manejo del café verde (Bucheli et al., 1998). La ocratoxina A puede estar presente antes del almacenamiento de los granos. Los pasos críticos para la posible acumulación de esta micotoxina son la recolección y el manejo poscosecha de los granos de café y evitar el crecimiento y proliferación de los mohos productores.
Existen diferentes métodos propuestos para evitar el ataque de plagas o de microorganismos en frutos después de su cosecha. Como ya se ha mencionado, para el café sólo se aplica la fumigación, pero existen muchos otros tratamientos poscosecha aplicados y reportados para otros frutos que podrían explorarse en café, y que pudieran tener menor impacto ambiental. Éstos se mencionan a continuación.
Los tratamientos térmicos para el control de enfermedades y plagas en cultivos ofrecen numerosas ventajas como alternativa a la fumigación, entre ellas (Hansen y Johnson, 2007):
o Son tecnologías bien establecidas que han sido aprobadas por muchos países para el comercio internacional
o Pueden ser aplicadas para el control de numerosos insectos
o No dejan residuos dañinos o bioproductos químicos
o El calentamiento puede ser generado por diferentes fuentes
o Los costos son razonables
Los tratamientos térmicos incluyen tratamientos con agua caliente, vapor, aire caliente forzado, energía solar, y energía electromagnética, que comprende la aplicación de microondas u ondas de radiofrecuencia (Hansen y Johnson, 2007).
Por otro lado, se ha propuesto también la irradiación como tecnología para controlar plagas y enfermedades. La irradiación es el mecanismo de acción que rompe los enlaces químicos en el ADN y otras moléculas, lo que evita la madurez sexual. Otra posibilidad es el uso de atmósferas controladas que implica elevar el nivel de CO2 y reducir el nivel de O2 en combinación con calor o frío para reducir la duración del tratamiento letal y ayudar a mantener la calidad de los productos básicos (Follent y Neven, 2006). Sin embargo, debe tenerse un amplio conocimiento del manejo de la tecnología y de los residuos radioactivos, de otro modo representará un peligro a largo plazo para quienes los manejen.
De los tratamientos anteriormente mencionados, en cacahuates y almendras se han probado tratamientos de calentamiento cortos de entre 55 y 60°C durante 2 y 10 minutos durante 5, 15, 30 y 60 días de almacenamiento, para combatir la rancidez y promover la desinfestación de las oleaginosas (Buransompob et al., 2003). Sosa-Morales et al. (2009) aplicaron calentamiento con microondas (77.2 a 435.6 W) para inhibir el crecimiento de Colletotrichum gloesporioides en sistemas modelo, encontrando que las
microondas tienen potencial de ser aplicadas con fines antifúngicos. Por otro lado, Wang et al. (2006) dando tratamiento de radio frecuencia a cacahuates se logró el control de crecimiento de mohos, tanto en la cáscara como en el centro del fruto.
Otros tratamientos físicos, como la exposición a ozono, presión hiperbárica y vacío, no están actualmente en uso, pero pueden tener aplicación para el tratamiento de café en el futuro (Vázquez, 2010).
Referencias
Aguilar-Ruiz, R. 1999. Tomando café. Manual del catador. Litográfica Dorantes.México.116 pp.
Alvindia D. G., Acda, M. A. 2010. Mycoflora of coffee beans in the philippines. J. ISSAAS. 16(2)116-125.
Avallone, S., Guyot, B., Brillouet, J.M., Olguin, E., Guiraud, J.P. 2001. Microbiological and biochemistry study of coffee fermentation. Current Microbiology. 42, 252-256.
Badui, S. 1993.Química de los Alimentos. Pearson Education. México.736 pp.
Conclusiones
La comercialización del café en los últimos años ha tomado gran fuerza a nivel mundial, debido al impacto económico que representa. Por ello, es importante hacer más investigación en cuanto a tratamientos poscosecha, para eliminar enfermedades y plagas que afectan el fruto de la planta de café. También es necesario que se desarrollen mecanismos/tratamientos de acción en contra de éstas, pues hoy en día las demandas de este producto crecen. Además es importante asegurar no sólo la calidad del producto si no también su inocuidad, pues la seguridad del consumidor debe ser garantizada. El desarrollo de tratamientos poscosecha que eviten el uso de fungicidas químicos también debe ser considerado.
Barrera, J. F., 2005.Investigación sobre la broca del café en México: Logos, retos y perspectivas. Simposio sobre Situación Actual y Perspectivas de la Investigación y Manejo de la Broca del Café en Costa Rica, Cuba, Guatemala y México. J.F. Barrera (ed.). Sociedad Mexicana de Entomología y El Colegio de la Frontera Sur. Tapachula, Chiapas, México, p. 1-13.
Batista, L. R., Chalfoun S. M., Silva, C. F., Cirillo, M., Varga, E. A., Prado, G., Schwan, R. F., 2009. Ocratoxina A in coffee beans (Coffea arabica L.) processed by dry and wet methods. Food Control. (20):784-790.
Bucheli, P., Meyer, I., Pittet, A., Vuataz, G., Viani, R. Industrial storage of green Robusta coffee under tropical conditions and its impact on raw material quality and ochratoxin A content. Journal of Agricultural and Food Chemistry. 46, 4507–4511.
Buransompob, A., Tang, J., Mao, R., Swanson, G. 2003. Rancidity of walnuts and almonds affected by short time heat treatments for insect control. Journal of Food Processing Preservation. 27:445-464.
Agradecimientos
A. Temis-Pérez agradece al Consejo Nacional de Ciencia y Tecnología (CONACYT) y a la Universidad de las Américas Puebla, por el financiamiento de sus estudios de posgrado.
Bustillo, A., Bernal, M. G., Benavides, P., Chaves, B. 1999. Dynamics of Bauveria bassiana and Metarhizium anisopliae infecting Hypotenemus hampei (Coleoptera Scolytidae) populations emerging from fallen coffee berries. Florida Entomologist. (82):491-498.
Bustillo-Pardey, A. 2001 El manejo de cafetales y su relación con el control de la broca del café en Colombia. CENICAFE.
Bustillo-Pardey, A. E. 2005. El papel del control biológico en el manejo integrado de la broca del café, Hypothenemus hampei (Ferrari) (Coleoptera: Curculionidae: Scolytinae). Rev. Acad. Colomb.Cienc. 29 (110):55-68.
Bustillo-Pardey A.E. 2007. El manejo de cafetales y su relación con el control de la broca del café de Colombia. Nexo 1. Cenicafé. 40.
Cano- Flores, M., Delfín-Pozos, F. L., Díaz-Cerón, A. M., García-López, T., González-Hernández, R., Meneses-Aguirre, B., Oliva-Zárate, M., QuintanaRodríguez, J. T. Ramírez-Juárez, J., RamírezSánchez, J., Romero-Pedraza, E., y Sesma-Muñoz, B. 2004. Estudio de mercado sobre el consumo de café en la ciudad de Xalapa, Veracruz. Revista IIESCA. Univerdidad Verazruzana (2):108-127.
CEFP. 2011. Centro de Estudios de las Finanzas Públicas. Disponible en: www.cefp.gob.mx. Accesado: 03/11/2010.
Cinza-Borrelli, R., Visconti, A., Mennella, C., Anese, M., Fogliano, V. 2002. Chemical characterization and antioxidant propierties of coffe melanoidins. Journal of Agricultural and Food Chemistry 50:6527-6533.
Clarke, R. J., Macrae, R. 1985. Coffee. Volume 1: Chemistry. Eds. Clarke, R.J., Macrae, RELSEVIER. EUA. .306.
Doyle, M. P., Beuchat, L. R., Montville, T.J.2001. Food Microbiology: Fundamentals and Frontiers. ASM. Press. E.E.U.U. 768 p.
FAO a. Food and agriculture Organization of the United Nations 2011. Organización de las Naciones Unidas para la agricultura y la alimentación. Reducción de la ocratoxina A en café. Disponible en: http://www.coffee-ota.org. Accesada: Septiembre/2011.
FAO b. Food and agriculture Organization of the United Nations 2011. Organización de las Naciones Unidas para la agricultura y la alimentación. Directrices para prevenir la formación de moho en el café. Disponible en: ftp://ftp.fao.org/ag/agn/coffee/guidelines_final_es. pdf Accesada: Septiembre/2011.
Fundación Produce Chiapas A.C., Institito Tecnológico y de Estudios Superiores de
Monterrey. 2003. Programa Estrátegico de Necesidades de Investigación y Transferencia de Tecnología del Estado de Chiapas. Cadena Agroalimentaria del Café.
Ferreira-Silva, C., Batista, L. R., Freitas Schwan, R. 2008. Incidence and distribution of filamentous fungi during fermentation, dryieng and storage of coffee (Coffea arabica L.) beans. Brazilian Journal of Microbiology 39:521-526.
Follent, P. A., Neven, L. G. 2006. Current Trends in Quarantine Entomology. Annual Review of Entomoly. 51:359-385.
Hansen, J. D. Johnson, J. A. 2007. Introduction. in Heat Treatments for Postharvest Pest Control. J. Tang, E. Mitcham, S. Wang, y S. Lurie, Editores. CABI, Wallingford, Reino Unido.
Higdon, J. V., Frei, B. 2006. Coffee and Health: A review of recent human research. Critical Reviews in Food Science and Nutrition. 46:101-123.
ISO-8455-1986. International Organization of Standardization. Guía para el almacén y transporte del café verde en sacos. Agricultural Food Products.
Läderach, P., Haggar, J., Lau, C., Eitzinger, A.,Ovalle, O., Baca, M., Jarvis, A., Lundy, M. 2011.Café mesoamericano: Desarrollo de una estrategia de adaptación al cambio climático CIAT Políticas en Síntesis no. 2. Centro Internacional de Agricultura Tropical (CIAT), Cali, Colombia. 4 pp.
Mansingh, G., Heichgelt, H., Osei Bryson, K-M. 2007. CPEST: An expert system for the management of pests and diseases in the Jamaican coffee industry Expert Systems with Applications. 32:184-192.
Mantle, P. G.; Chow, A. M. 2000. Ochratoxin formation in Aspergillus ochraceus with particular reference to spoilage of coffee. International Journal of Food Microbiology, 56, 105–109.
Marques- Vilela, D., Vínicus-Pereira, G., Ferreira-Silva, C., Roberto-Batista, L., Freitas-Schwan R. 2010. Molecular ecology and polyphasic characterization of the microbiota associated with semi-dry processed coffee (Coffea arabica L.). Food Microbiology. (27):128-1135.
Morales-Ramos, J. A., Rojas, M. G., Sittertz-Bhatkar, H., Saldaña, G. 2000. Symbiotic relationship
between Hypothenemus hampei (coleóptera Scolytidae) and Fusarium solani (Moniliales: Tuberculariaceae). Arthropod Biology. 93 (3): 541-547.
Niño-Sandoval, Z. L., Prieto Ortiz, F. A. 2007. Caracterización de café cereza empleando técnicas de visión artificial. Revista Facultad Nacional Agrícola Medellín. 60(2):4105-4127.
Norris, C.P. 2001. Mechanization of the Harvesting of Coffee, Baker, P.S. (Editor). Coffee Futures: A Source Book of Some Critical Issues Confronting the Coffee Industry. Commodities Press: CABI. EE. UU. 480 p.
Otteneder, H.; Majerus, P. 2001. Ochratoxin A (OTA) in coffee: nationwide evaluation of data collected by German Food Control 1995–1999. Food Additives and Contaminants 18: 431–435.
Pardo, E.; Marín, S.; Ramos, A.J.; Sanchis, V. 2004. Occurrence of ochratoxigenic Fungi and Ochratoxin A in green coffee from different origins. Food Science and Technology International. 10: 45-50.
Perrone, G. Susca, A., Cozzi, G., Ehrlich, K., Varga, J., Frisvad, J. C., Mejier, M., Noomin, P., Mahakarnchnakul, W., Samson, R. A. 2007. Biodiversity of Aspergillus in some important agricultural products. Studies in Micology. 59:5366.
Renard, C. 1993. La comercialización internacional del café, Universidad Autónoma de Chapingo, Colección Cuadernos Universitarios, Serie Ciencias Sociales (11):11-12. México.
Rodríguez-del-Bosque, L. A., Arredondo-Bernal H. C (eds.). 2007 Teoría y Aplicación del Control Biológico. Sociedad Mexicana de Control Biológico. México. 303 p.
Romani, S., Sacchetti, G., Chaves Lopez, C., Pinnavaia, G. G., Dalla Rosa, M. 2000. Screening on the occurrence of ochratoxin A in green coffee beans of different origins and types. Journal of Agricultural and Food Chemistry. 48: 3616–3619.
SAGARPA y SE. 2004. PC-010-2004. Pliego de Condiciones para el uso de la marca oficial México calidad selecta en café verde. Certificación México Calidad Suprema para Café- verde.
Silva, C.F., Schwan, R.F., Dias, E.S., Wheals, A.E. 2004. Microbiota presente em frutos e grãos de café (Coffea arabica l.) despolpado e natural - uma revisão. Ciência e Tecnologia Alimentaria. 37:2228.
Smith, J. E., Solomons, G. L., Lewis, C. W., Anderson, J. G. 1994. Mycotoxins in Human Nutrition and Health; Technical Report; European Commission, Directorate XII: Studies on Science, Research and Development (SRD); EUR 16048 EN; SRD: Brussels, Belgium.
Soliman, K. M. 2002. Incidence, level, and behavior of aflatoxins during coffee bean roasting and decaffeination. Journal of Agricultural and Food Chemistry. 50:7477-7481.
Sosa-Morales, M.E., García, H.S., López-Malo, A. 2009. Colletotrichum gloesporioides growth-nogrowth interface after selected microwave treatments. Journal of Food Protection. 72(7):14271433.
Tellez-Jurado, A., Cruz-Ramírez, M. G., MercadoFlores, Y., Asaff-Torres, A., Arana-Cuenca, A.2009. Mecanismos de acción y respuesta en la relación de hongos entomopatógenos e insectos. Revista Mexicana de Micología.30:73-80.
Valenzuela, A. 2010. El café y sus efectos en la salud cardiovascular en la salud materna. Revista Chilena de Nutrición. 37(4):514-523.
Vázquez, M. 2010. Advances in Post-Harvest Treatments and Fruit Quality and Safety. Nova Science Publishers, Inc. Nueva York.
Vázquez, L. I., Elósegui, O., Leyva, L., Polanco, A., Becerra, M., Monzón, S., Rodríguez, A., Tamayo, E., Toledo, C., Navarro, A., García, M. 2010. Ocurrencia de Epizootias causadas por Beauveria bassiana (Bals.) Vuill. En poblaciones de la broca del café (Hypothenemus hampei Ferrari) en las zonas cafetaleras de cuba. Fitosanidad. 14(2):111116.
Yiani, R.1996. Fate of ochratoxin A (OTA) during processing of coffee. Food Additives and Contaminants. 13, 29–33.
Williams, J. H, Phillips, T. D, Jolly, P. E, Stiles, J, K, Jolly, C. M, Agarwal, D. 2004. Aflatoxinas humanas en países en desarrollo: revisión de toxicología,
L. Temis - Pérez et al. / Temas
exposición, consecuencias potenciales a la salud, e intervenciones. American Journal of Clinical Nutrition.80:1106-22
- 74
Wang, S., Monzon, M., Jonhnson, J.A., Mitcham, E. J., Tang, J., 2006. Industrial –scale radio frequency treatments for insect control in walnuts II: Insect mortality and product quality. Postharvest Biology and Technology. 45:247-253.

Temas Selectos de Ingeniería de Alimentos 5 - 2 (2011): 75 - 83

Propiedades nutricionales y antioxidantes del maíz azul (Zea mays L.)
A. Castañeda-Sánchez*
Departamento de Ingeniería Química, Alimentos y Ambiental, Fundación Universidad de las Américas Puebla. Exhacienda Sta. Catarina Mártir S/N, Cholula, Puebla. C.P.72810. México.
Resumen
El maíz (Zea mays L.) representa la base de la alimentación en México. Numerosos estudios han reportado que el maíz azul (Zea mays L.) es más nutritivo que otros variedades del grano; además de contener compuestos antioxidantes. Los alimentos con propiedades antioxidantes son muy importantes para el ser humano porque disminuyen el daño causado por los radicales libres. Por tanto en este artículo se realiza un análisis de las características nutricionales y antioxidantes del maíz azul (Zea mays L.).
Palabras clave: maíz azul, composición, antocianinas.
Abstract
Corn (Zea mays L.) is the basis of the diet in Mexico. Numerous studies have reported that the variety of blue corn (Zea mays L.) is more nutritious than the yellow and white corn, also contain antioxidant compounds. Antioxidant foods are very important for people because they decrease the damage caused by free radicals. In these paper performed an analysis of the blue corn (Zea mays L.).
Keywords: blue corn, composition, anthocyanins.
Introducción
El maíz representa el sector más importante de la producción agrícola en México. La variedad de maíz azul (Zea mays L.) posee gran cantidad de pigmentos antioxidantes y una calidad nutricional mayor que el maíz típico; blanco o amarillo Su nivel de fibra es uno de los más elevados comparado con el resto de cereales. Contiene altos niveles de
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: armando.castanedas@udlap.mx
carbohidratos de fácil digestión y es rico en magnesio, antioxidantes y vitaminas. Es un cereal que aporta grandes beneficios al consumidor. Además es la principal fuente de alimentación de la población. Por eso en este trabajo se pretende realizar un análisis de las propiedades nutricionales y antioxidantes del maíz azul (Zea mays L.).
Revisión bibliográfica
1. Maíz Azul
1.1 .Descripción
El maíz azul (Zea mays L.) pertenece al reino Plantae, a la clase angiosperma, a la subclase monocotiledónea, al orden de los cereales y a la familia de las gramíneas. En México las culturas prehispánicas llamaron centli a la mazorca y tlaolli al grano (Galarza, 2011).
La planta alcanza de uno a seis metros de alto dependiendo de la variedad. Las hojas forman una larga vaina enrollada al tallo y un limbo más ancho y alargado. Del tallo nacen dos o tres inflorescencias muy densas conocidas como mazorcas. El tallo de la planta está rematado en el extremo por una gran panoja de flores; cuando el polen ha sido aventado, se vuelven secas y parduscas (Galarza, 2011). En cada mazorca se ven las filas de granos cuyo número puede variar de ocho a treinta. A cada grupo le corresponde un largo hilo sedoso que sobresale por el extremo de la mazorca (Betrán et al., 2001).
La mayoría de los maíces son típicamente de grano harinoso. El endospermo es de textura suave. El color azul se encuentra en la capa de células llamada aleurona, donde una mayor concentración de pigmentos antociánicos hacen que los granos parezcan negros (Betrán et al., 2001).
1.2
Producción
La producción de maíz se relaciona con diversos factores ambientales como el agua, suelo, minerales, dióxido de carbono y oxígeno. Además el crecimiento de la planta depende del potencial genético de la semilla. Aunque la naturaleza parece ser la principal responsable del crecimiento de la planta, se
puede contribuir al buen desarrollo arando, fertilizando, regando y controlando malezas e insectos (Galarza, 2011).
El maíz se trabaja en dos ciclos productivos: primavera-verano y otoñoinvierno. En el ciclo otoño-invierno las regiones Noroeste y Norte son las que aportan los volúmenes más significativos de maíz en México, produciendo en forma conjunta el 77.8 % del total nacional. Los contribuyentes mayoritarios son Sinaloa, Durango, Zacatecas, Sonora, San Luis Potosí, Tamaulipas y Coahuila (Galarza, 2011).
En la producción del maíz en el ciclo primavera-verano, destacan las regiones del Altiplano Central, Pacífico Sur y Bajío. La producción de estas regiones asciende al 76 por ciento del total nacional del ciclo. Los principales productores son México, Guerrero, Michoacán y Jalisco (Galarza, 2011).
El rendimiento por hectárea varía de acuerdo con el sistema de producción. En el ciclo otoño-invierno el rendimiento promedio es de 3.6 toneladas por hectárea cosechada. En el ciclo primavera-verano el rendimiento promedio es de 2.08 toneladas por hectárea. Cabe mencionar que en el ciclo otoño-invierno la producción proviene de sistemas de riego, lo que se asocia a mejores niveles de tecnificación y a la práctica comercial del cultivo, redundando en mejores rendimientos en comparación a la producción de temporal que predomina en el ciclo primavera-verano (Galarza, 1998).
1.3 Consumo
El cultivo de maíz en México se caracteriza por la producción de una amplia gama de variedades, por lo que es posible generar una gran cantidad de productos finales. Los principales son tortillas, forrajes, aceites, biocombustibles, almidones, glucosa, fructosa, dextrosa y etanol. En México se hace mención
principalmente a tres variedades de maíz, el blanco, amarillo y azul. El maíz blanco se produce exclusivamente para el consumo humano por su alto contenido nutricional. El maíz amarillo se destina al procesamiento industrial y a la alimentación animal. El maíz azul se utiliza para la elaboración de atole, tortillas y tesguiño (De la Parra, 2008).
Para preparar alimentos, harina y otros productos, se machaca el maíz azul con un molino. Los granos enteros esencialmente se utilizan para elaborar diversos alimentos, mientras que la harina se mezcla con agua hirviendo para elaborar tortillas. El atole de maíz azul se hace con masa cocida, y en algunos casos con harina de grano seco (Méndez et al., 2005).
En México existe un déficit en la producción del maíz porque sólo se cosechan 21 millones de toneladas. Por esto es necesario importar alrededor de 6 millones de toneladas de maíz provenientes de Estados Unidos (Méndez et al., 2005).
2. Información nutricional
El maíz azul ofrece algunas características nutricionales muy interesantes destacando: una menor cantidad de almidón, un índice glucémico inferior menor al maíz normal (interesante para personas diabéticas), y una carga proteica superior en un 20 % al del maíz blanco (Méndez et al., 2005).
En México existe una gran diversidad de variedades de maíz azul. También existe variabilidad en tamaño, densidad y dureza del grano, así como en su composición química. Estas variables están definidas por el factor genético, prácticas de cultivo, condiciones climáticas y tipo de suelo, así como la interacción entre estos factores. En diferentes regiones del país se cultivan variedades criollas de maíz azul. Los más importantes son el tabloncillo y el chalqueño. La Tabla I
muestra la composición química de estas variedades (Agama, 2011).
Las diferentes partes del maíz también difieren en su composición. El pericarpio tiene un alto contenido en fibra, mientras que el endospermo es rico en almidón. El germen contiene la mayoría de las proteínas, grasas, azúcares y cenizas (Agama, 2011).
I. Composición química del maíz azul de las variedades tabloncillo y chalqueño.
ComponenteTabloncilloChalqueño
Humedad (%)8.58 ± 0.31 8.29 ± 0.17
Cenizas (%)1.63 ± 0.011.52 ± 0.03
Lípidos (%)5.36 ± 0.044.91 ± 0.02
Proteinas (%)9.04 ± 0.239.04 ± 0.12
Almidón (%)78.5 ± 0.9582.9 ± 0.86
*Agama (2011)
2. 1. Carbohidratos
El maíz azul es una fuente importante de carbohidratos. Los azúcares constituyen aproximadamente el 2 % del peso total del grano y cerca del 65 % de los azúcares del grano se encuentran en el germen. Contiene fructosa, glucosa, sacarosa, maltosa, rafinosa y algunos oligosacáridos (Boyer y Shannon, 2001).
Los carbohidratos complejos representan alrededor del 80 % del peso total del grano. Los polisacáridos más importantes en el maíz azul son los estructurales y los de reserva. Los del tipo estructural se encuentran en las paredes del grano y son la pectina, hemicelulosa, celulosa y lignina (Boyer y Shannon, 2001).
El polisacárido de reserva es el almidón y se encuentra en el endospermo. El almidón del maíz contiene en promedio un 75 % de amilopectina y un 25 % de amilosa. Sin embargo, esta proporción está determinada
Tabla
genéticamente y puede cambiar de semilla a semilla (Boyer y Shannon, 2001).
2. 2. Proteínas
Las proteínas son las macromoléculas más importantes desde el punto de vista nutricional. Representan aproximadamente el 10 % del grano. El maíz azul contiene albuminas, globulinas, glutelinas y prolaminas (Badui, 2006).
En la Tabla II se muestra el contenido de aminoácidos esenciales del maíz azul. Este cereal tiene un bajo contenido en triptófano. Aún con la ausencia de este componente, las albúminas contienen un adecuado balance de aminoácidos esenciales. La relación de eficiencia proteica (PER) es de 1.37 y la utilización proteica neta (NVP) es 72.78 % (Badui, 2006).
Tabla II. Composición de aminoácidos esenciales en el maíz azul (g/100g maíz).
AminoácidoContenido
Fenilalanina4.8
Histidina2.9
Isoleucina3.6
Leucina12.4
Lisina2.7
Metionina1.9
Treonina3.5
Triptófano0.5
Valina4.9
*Badui (2006)
2.3. Lípidos
Los lípidos representan el 5 % del maíz azul. Se encuentran en mayor proporción con el germen, conteniendo el 84 % de los lípidos del grano y el 16 % restante se encuentra en el endospermo. La mayoría de los lípidos son triglicéridos y se componen por los ácidos linoléico (50 %), oléico (35 %), palmítico (13
%), esteárico (4 %) y linolénico (3 %). Además los lípidos del maíz azul son muy estables, porque contienen altos niveles de antioxidantes naturales. Por lo tanto, el maíz azul es una excelente fuente de ácidos grasos y genera aceites de buena calidad (Boyer y Shannon, 2001).
2.4. Fibra
La fibra dietética está presente en el maíz azul como en todas las variedades de maíz. Se encuentra mayoritariamente en el pericarpio y en las paredes celulares del endospermo. Ciertos factores como la genética, clima y altura afectan el contenido de fibra. La Tabla III indica el contenido de fibra de maíz cosechado en diferentes condiciones (Dickerson, 2008).
Tabla III. Fibra de maíz cosechado a diferentes alturas (g/100g maíz).
Tipo de maízInsolubleSolubleTotal
De sierra10.94 ± 1.261.25 ± 0.4112.19 ± 1.30
De tierras bajas11.15 ± 1.081.64 ± 0.7312.8 ± 1.47
*Dickerson, (2008)
2.5. Vitaminas
El maíz azul posee vitaminas hidrosolubles y liposolubles. El grano contiene dos vitaminas liposolubles en concentraciones importantes: la vitamina A con 2.5 mg/kg y la vitamina E con 36 mg/kg. Además están presentes en menor proporción la vitamina B1, piridoxina, niacina y vitamina C en concentraciones muy bajas. En la aleurona, germen y endospermo están las proteínas hidrosolubles. Se han encontrado cantidades variables de tiamina y riboflavina. La concentración está determinada por el medio ambiente, las prácticas de cultivo y la genética (Dickerson, 2008).
2.6. Minerales
Los minerales se encuentran mayoritariamente en el germen del maíz azul. El fósforo es el más abundante y representa el 0.1 % del grano integral. El calcio es el mineral más importante del maíz azul, ya que es fundamental en el consumo humano. El contenido de calcio puede variar del 0.01 % al 0.1 % del peso seco del grano. Además posee cantidades considerables de potasio y magnesio. La Tabla IV muestra el contenido de minerales promedio del maíz azul (Dickerson, 2008).
Tabla IV. Contenido promedio de minerales del maíz azul (mg/100g).
MineralConcentración
Fósforo299.6 ± 57.8
Potasio324.8 ± 33.9
Calcio48.3 ± 12.3
Magnesio107.9 ± 9.4
Niquel59.2 ± 4.1
Hierro4.8 ± 1.9
Cobre 1.3 ± 0.2
Manganeso1.0 ± 0.2
Zinc4.6 ± 1.2
*Dickerson, (2008)
3. Propiedades antioxidantes
El consumo de maíz azul está asociado indirectamente con beneficios a la salud, debido a la presencia de compuestos antioxidantes, los cuales retrasan el daño causado por los radicales libres, con actividad anticancerígena, antineurodegerativa y antiinflamatoria (Kraft, 2008).
Estudios médicos han demostrado que pacientes con arteroesclerósis presentan contenidos bajos de antioxidantes al compararlos con individuos sanos (Durak et al., 2001). Ching et al. (2002) encontraron que al incrementar los niveles de antioxidantes en la sangre, los riesgos de presentar cáncer de
mama se ven disminuidos. Olsson et al. (2004) evaluaron el efecto de antocianinas, como la cianidina-3-glucósido, en la proliferación de células de cáncer de colon y de mama, encontrando actividad anticancerígena. Joseph et al. (2003) encontraron que el consumo de suplementos antioxidantes revierte los efectos degenerativos del envejecimiento. Una gran variedad de fitoquímicos son responsables de estos beneficios del maíz azul, entre ellos los compuestos fenólicos.
3.1. Compuestos fenólicos
El maíz azul es un cereal rico en compuestos fenólicos. Los fenoles son compuestos que poseen anillos aromáticos, con grupos sustituyentes hidroxilo, éster, glucósido, etc. Son metabolitos secundarios que contribuyen al aroma y al sabor de los alimentos. Son esenciales para el crecimiento y la reproducción del maíz, otorgan resistencia al estrés ocasionado por condiciones ambientales, así como a los daños por plagas (Su y Chien, 2007).
La familia de los fenólicos es muy grande, y existen muchas clasificaciones. Según su estructura química existen dos grandes grupos: no flavonoides y flavonoides. Los no flavonoides son ácidos fenólicos, así como derivados de moléculas un poco más complejas como los estilbenos y galotaninos (Seeram et al., 2008).
Los flavonoides están formados por dos grupos bencénicos unidos por un puente tricarbonato, por lo que su esqueleto básico es de 15 átomos de carbono. Además poseen varios grupos hidroxilo unidos a su estructura de anillo y se encuentran normalmente como glucósidos. Un subgrupo de los compuestos flavonoides que ha sido objeto de estudio son las antocianinas (Lila, 2004).
3.2.Antocianinas
El maíz azul es una fuente importante de antocianinas con potenciales aplicaciones antioxidantes. Las antocianinas se caracterizan por un esqueleto básico de 15 átomos de carbono de tipo 2-fenil benzopirona. Son sales de flavilio y glucósidos porque están unidos por un enlace glucosídico a una molécula de azúcar (Stintzing y Carle, 2004).
Las antocianinas tienen un sustituyente hidroxilo glicosilado, el cual les da estabilidad y solubilidad. Dependiendo de los otros sustituyentes se obtendrán diferentes colores. La variedad de antocianinas depende del número de grupos hidroxilo, azúcares, grupos alifáticos y ácidos aromáticos unidos a la estructura básica de las antocianinas. Los carbohidratos comúnmente unidos a las antocianidinas son glucosa, galactosa, xilosa, arabinosa y ramnosa (Chirinos et al., 2006).
Las diferencias en el perfil de antocianinas del maíz; ocasionan una diferencia enorme en el color y pigmentación de las diferentes variedades. Esta variación se define en colores que van desde el rojo, pasando por el morado hasta el casi negro (De la Parra, 2008).
La biosíntesis de antocianinas de la planta de maíz se lleva a cabo a partir de fenilalanina y piruvato. La función de las antocianinas en la planta está relacionada con su adaptación al ambiente. Las antocianinas del grano de maíz azul se concentran en el pericarpio y en menor proporción en la capa de aleurona. De acuerdo a esta localización se pueden determinar los diferentes usos del grano. Cuando se presenta una cantidad elevada de antocianinas en el pericarpio, las variedades tienen potencial para la extracción de pigmento (Del Valle et al., 2005).
El interés en los pigmentos antociánicos se ha intensificado recientemente debido a sus propiedades farmacológicas y terapéuticas.
Durante el paso del tracto digestivo al torrente sanguíneo de los mamíferos, las antocianinas permanecen intactas y ejercen efectos terapéuticos conocidos que incluyen la reducción de la enfermedad coronaria, efectos anticancerígenos, antitumorales, antiinflamatorios y antidiabéticos; además del mejoramiento de la agudeza visual y del comportamiento cognitivo. Los efectos terapéuticos de las antocianinas están relacionados con su actividad antioxidante. Estudios con fracciones de antocianinas han demostrado que éstas son efectivas para atrapar especies reactivas del oxígeno, además de inhibir la oxidación de lipoproteínas y la agregación de plaquetas (Timberlake, 2008).
Wang y Mazza (2002) han demostrado que vegetales ricos en antocianinas evidencian una alta actividad antioxidante contra el peróxido de hidrógeno y contra radicales peróxido, superóxido, hidroxilo y oxígeno singulete.
A las antocianinas también se les atribuye actividad antitumoral y anticancerígena. Hagiwara et al. (2002) demostraron que el suministro de antocianinas causa supresión de tumores. Kamei et al. (2008) reportaron la supresión de células cancerígenas HCT-15 provenientes del colon humano y de células cancerígenas gástricas AGS al suministrar fracciones de antocianinas.
Referente a la actividad antiinflamatoria, Wang y Mazza (2002) encontraron en extractos concentrados de antocianinas efecto inhibitorio de la producción de óxido nítrico en macrófagos activados. Por otra parte, Vuorela et al. (2005), encontraron efecto supresor de prostaglandina EG2, sinónimo de actividad antiinflamatoria en extractos antociánicos.
La mejora de la agudeza visual y del comportamiento cognitivo como resultado del consumo de antocianinas han sido reportados por Ohgami et al. (2005) quienes
suministraron extractos de frutas ricas en antocianinas a ratas con deficiencia ocular, lo cual resultó en un efecto antiinflamatorio y de aumento de la agudeza visual. Han demostrado que el comportamiento cognitivo y las funciones neuronales de ratas de laboratorio puede ser mejorado a través de suplementación nutricional con antocianinas.
Las antocianinas del maíz azul ya han sido caracterizadas. El perfil de antocianinas del grano de maíz azul presenta diez antocianinas diferentes, de los tipos aciladas y no aciladas. Las antocianinas más importantes son la cianidina-3-glucósido, pelargonidina-3glucósido y peonidina-3-glucósido. La Tabla V muestra las antocianinas mayoritarias del maíz azul. Los porcentajes promedio de estas antocianinas son 90 % de cianidina, 8 % de pelargonidina y alrededor de 2 % de peonidina (Styles y Ceska, 1972).
Zhao et al. (2008) identificaron siete antocianinas principales, que fueron la cianidina-3-glucosido, cianidina-3(malonilglucosido), peonidina-3-glucosido, peonidin-3-malonilglucósido, pelargonidina3-(6-malonilglucósido), cianida-3-glucosido2-malonilglucósido y peonidina-3(dimalonilglucósido).
Además Li et al. (2008) caracterizaron tres antocianinas más, que fueron la cianidina-3succinilglucósido, cianidina-3-(6(etilmalonil)glucósido) y cianidina-3rhamnosido. El mayor contenido de antocianinas lo encontraron en la cáscara del grano.
De la Parra et al. (2008) cuantificaron las antocianinas monoméricas totales del maíz azul, reportaron 266.2 mg equivalentes de ácido gálico/100 g de maíz azul y encontraron a la cianidina-3-glucósido en mayor proporción.
Martínez et al. (2009) reportaron un contenido de antocianinas en el rango de 409.5 a 933.8 mg /kg en grano sin germen. Además encontraron que el maíz híbrido presenta menor contenido que el maíz criollo.
También existen diferencias entre variedades del contenido de antocianinas. El maíz azul de la raza chalqueño posee en sus granos un mayor grado de antocianinas. El rango en el contenido de antocianinas es de 400 a 900 mg/kg en grano sin germen (De la Parra, 2008).
El principal destino de la producción de maíz azul en México es la elaboración de tortilla, atole y pinole. Sin embargo el proceso de nixtamalización es altamente agresivo para las antocianinas del grano. Por lo que las tortillas de maíz azul contienen solamente el 30 % de las antocianinas totales (De la Parra, 2008).
3.3. Ácidos fenólicos
Este grupo de compuestos se caracteriza por poseer en su estructura química el anillo aromático, el grupo hidroxilo y una función carboxílica (Scalbert y Willianson, 2000).
Se concentran en el pericarpio del grano en mayor medida. Pueden estar libres o esterificados a las cadenas de celulosa que conforman la estructura (Scalbert y Willianson, 2000).
Los ácidos fenólicos que tienen interés terapéutico y antioxidante son derivados del ácido benzoico o del ácido cinámico (cafeíco, ferúlico, p-cumárico). Los primeros son muy abundantes en la naturaleza tanto libres, como ácidos o aldehídos, (vainilla, anisaldehído), como combinados en formas heterosídicas, correspondiendo a esta grupo la unidad básica estructural (ácido gálico) de los taninos gálicos o hidrolizables. Los segundos también son
abundantes en la naturaleza, pero en este caso se encuentran casi siempre esterificados con azúcares, alcoholes alifáticos, ácido clorogénico, otros metabolitos secundarios o bien amidificados (Scalbert y Willianson, 2000).
Los ácidos fenólicos también reducen los daños oxidativos relacionados con la edad y combaten enfermedades como arteriosclerosis, diabetes, cáncer y cirrosis. Además los diferentes ácidos fenólicos presentan actividad sinergista entre sí (Scalbert y Willianson, 2000).
Se han detectado ocho ácidos fenólicos mayoritarios en el maíz azul. Ácido hidroxibenzoico, ácido vanílico, ácido cafeico, ácido sinápico, ácido p-cumárico, acido mcumárico, acido ferúlico y ácido o-cumárico. El ácido ferúlico es el ácido fenólico más importante en todos los tipos de maíz. Los ácidos o-cumárico y p-cumárico también se encuentran en concentraciones considerables. Las diferentes variedades de maíz tienen contenidos distintos de ácidos fenólicos (White, 2007).
Muchos ácidos fenólicos diferentes contribuyen al contenido de compuestos fenólicos. Los ácidos fenólicos decrecen en su actividad antioxidante en el siguiente orden: ácido cafeico, ácido hidroxibenzoico, ácido ferúlico, ácido vanílico, ácido sinápico y ácido cumárico. El ácido ferúlico es el ácido fenólico predominante ya que se puede encontrar aun después de la hidrólisis alcalina del grano (White, 2007).
Los fenoles libres se encuentran en las diferentes partes del grano. El contenido de fenoles libres promedio es de 3.46 a 5.91µmol/g en el pericarpio y de 1.24 a 3.76 µmol/g en el endospermo. Mientras que el contenido de fenoles totales promedio va de 8.98 a 14.56 µmol/g en pericarpio y de 2.93 a
4.98 µmol/g en endospermo (Scalbert y Willianson, 2000).
Conclusiones
El maíz azul es un excelente alimento desde el punto de vista nutricional. Contiene menos almidón que el maíz blanco y su índice glucémico es menor. Además, tiene más proteínas que otras variedades. El color se debe a las antocianinas, colorantes naturales con propiedades antioxidantes. De tal forma este cereal es un gran aliado en la dieta.
Referencias
Agama, E. 2011. Características físicas y químicas de dos razas de maíz azul. Revista Mexicana de Ciencias Agrícolas. 3:317-329.
Badui, S. 2006. Química de los alimentos. Cuarta Edición. Editorial Alhambra. México, D.F. 140-145.
Betrán, F., Bockholt, A. y Rooney, L. 2001. Blue corn in specialty corns. Food Hydrocolloids. 5:455-467.
Boyer, C. y Shannon, J. 2001. Carbohydrates of the kernel, corn: chemistry and technology. Journal of Cereal Science. 1:253-272.
Ching, S., Ingram, D., Hahnel, R. y Rossi, E. 2002. Serum levels of micronutrients, antioxidants and total antioxidant status predict risk of breast cancer in a case control study. Journal of Nutrition. 132:303-306.
De la Parra, C., Serna, S. y Hai, L. 2008. Effect of processing on the phytochemical profiles and antioxidant activity of corn for production of masa, tortillas and tortilla chips. Journal of Agricultural and Food Chemestry. 55:4177-4183.
Del Valle, G., Gonzalez, A. y Báez, R. 2005. Las antocianinas y su relación con el color. Revista de Fitotécnia. 28(4):359-368.
Dickerson, G. 2008. Nutritional analysis of New Mexico blue corn and dent corn kernels. Cooperative Extension of Agriculture. 20:7-8.
Durak, I., Kacmaz, M., Cimen, M., Buyukkock, U. y Ozturk, H. 2001. Blood oxidant/antioxidant status of arteroesclerotic patients, Journal of Cardiology. 77:293-297.
Galarza, J.M. 2011. Situación actual y perspectivas del maíz en México. SIAP. http://www.siap.gob.mx
Hagiwara, A., Yoshino, H. y Aoki, H. 2002. Food anthocyanins from purple sweet potato and red cabbage. Journal of Toxicology Science. 27:57-68.
Joseph, J., Arendas, G. y Gordon, M. 2003. Blueberry supplemenattion enhaces signaling and prevents behavioral déficits in an Azhaimer disease model. Neuroscience. 6:153-162.
Kamei, H., Hashimoto, Y. y Koide, T. 2008. Antitumor effect of metanol extracts from red and white wines. Cancer Biother Radiopharm. 13(6):447-452.
Kraft, T. 2008. Phytochemical composition and metabolic performance enhacing activity of dietary berries. Journal of Agriculture and Food Chemestry. 26:654-660.
Li, C., Kim, W., Won, R., Min, K., Park, Jin., Park, Y., Ahn, M. y Rhee, H. 2008. Corn husk as a potential source of anthocyanins. Journal of Agricultural and Food Chemistry. 56:11413-11416.
Lila, M. 2004. Anthocyanins and human health: an in vitro investigate approach. Journal of Biotechnology. 5:306-313.
Martinez, L., Ros, R. y Alfaro, G. 2009. Antioxidant activity, phenolic compounds and anthocyanins content of eighteen strains of mexican maize. Food Science and Technology. 42:1187-1192.
Méndez, G., Solorza, J. y Paredes, O. 2005. Composición química y colorimétrica de híbridos y variedades de maíz. Revista Agrociencia. 39:267274.
Ohgami, K., Illieva, L. y Yoshida, K. 2005. Antiinflammatory effects of aronia extradct on rat rndotoxin-induced uveítis. Journal of Biotechnology. 46:275-281.
Olsson, E., Gustavsson, K. y Duan, R. 2004. Inhibition of cáncer cell proliferation in vitro by extracts and correlations with antioxidant levels. Journal of Agricultural and Food Chemistry. 52:7264:7271.
Scalbert, A. y Willianson, G. 2000. Dietary intake and bioavailability of polyphenols. Journal of Nutrition. 1300:2073-2085.
Seeram, N. 2008. Comparison of antioxidant potency or commonly consumed polyphenol rich beverages in the United States. Journal of Agricultural and Food Chemistry. 56(4):1415-1422.
Stintizing, F. y Carle, R. 2004. Functional properties of anthocyanins in plants, food and human nutrition. Trends Food Science Technology. 15:19-38.
Styles, E. y Ceska, O. 1972. Flavonoid pigments in generic strains of maize. Journal of Phytochemistry. 11:3019-3021.
Su, M. y Chien, P. 2007. Antioxidant activity, anthocyanins and phenolics of blue corn (Zea mayz L.). Food Chemistry. 104:181-187.
Timberlake, F. 2009. Anthocyanins occurrence, extraction and chemistry. Food Chemistry. 120:6980.
Vuorela, S., Kreander, K. y Karonen, M. 2005. Preclinical evaluation of rapeseed, raspberry and pine bark phenolics for health related effects. Journal of Agricultural and Food Chemistry. 59:5922-5931.
Wang, J. y Mazza, G. 2002. Inhibitory effects of anthocyanins and other phenolic compounds on nitric oxide production. Journal of Agricultural and Food Chemistry. 50:850-857.
White, P. 2007. High amylose corn exhibits better antioxidant activity tha typical and waxy genotypes. Journal of Agricultural and Food Chemistry. 55:291298.
Zhao, X., Corrales, M., Zhang, C., Hu, X., Ma, Y. y Tauscher, B. 2008. Composition and termal stability of anthocyanins from Chinese purple corn (Zea mays L.). Journal of Agricultural and Food Chemistry. 56:10761-10766.

Temas Selectos de Ingeniería de Alimentos 5 - 2 (2011): 84 - 96

Efecto del tiempo de almacenamiento y tipo de procesamiento en los antioxidantes de nopal
M. C. Flores – Álvarez*, F. T. Vergara - Balderas y J. A. Guerrero - Beltrán
Departamento de Ingeniería Química, Alimentos y Ambiental, Fundación Universidad de las Américas Puebla. Exhacienda Sta. Catarina Mártir S/N, Cholula, Puebla. C.P.72810. México.
Resumen
El objetivo de este estudio fue determinar el efecto del tiempo de almacenamiento y del tipo de procesamiento sobre las características antioxidantes de nopales (Nopalea cochenillifera) frescos, secos y escaldados. Se realizaron análisis de compuestos fenólicos totales, capacidad antioxidante, clorofila y ácido ascórbico cada semana durante cuatro semanas para nopal fresco (NF) y nopal escaldado (NE) y cada dos semanas durante seis semanas para nopal seco (NS). Se observó una degradación del ácido ascórbico debido al tiempo de almacenamiento para NF y NE. Se observó una disminución de los valores de clorofila a y b para NF y NE después de dos semanas de almacenamiento, y posteriormente los valores mostraron una tendencia constante; en el caso del NS, la cantidad de clorofila a tendió a ser constante. Los compuestos fenólicos totales y la capacidad antioxidante aumentaron con el tiempo de almacenamiento para NF y NE.
Palabras clave: nopal, almacenamiento, capacidad antioxidante, compuestos fenólicos totales, clorofila, ácido ascórbico.
Abstract
The objective of this study was to determine the effect of storage time and type of processing on the antioxidant characteristics of fresh, dried and blanched cladodes (Nopalea cochenillifera). Analysis of total phenolic compounds, antioxidant capacity, chlorophyll and ascorbic acid were performed every week during four weeks for fresh cladodes (NF) and blanched cladodes (NE) and every two weeks during six weeks for dried cladodes (NS). A degradation of ascorbic acid, due to the storage time, for NF and NE was observed. A decrease of chlorophyll a and b for NF and NE, after two weeks of storage, were noted, afterward, the content was constant; for NS, the amount of chlorophyll a remained constant. Total phenolic compounds and antioxidant capacity of NF and NE samples increased with storage time.
Keywords: cladodes, storage time, antioxidant capacity, total phenolic compounds, chlorophyll, ascorbic acid.
Introducción
Los nopales son utilizados como verdura en
*Programa de Maestría en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: yanela.martinezto@udlap.mx
diversos platillos y están muy ligados con la historia de México (León-Portilla, 1983). La composición química de los mismos varía en función de su edad, de la variedad a la que
pertenezcan y de su tiempo de almacenamiento (Sáenz et al., 2006). Según lo establecido por Rodríguez-Félix y Cantwell (1988), la composición química de los nopales frescos es 91% agua, 1.5% de proteínas, 4.5% de carbohidratos totales (1.1% de los nopales es fibra), 0.2% de lípidos, 1.3% de cenizas (90% de las cuales es calcio); además contienen 11 mg de ácido ascórbico y 30 μg de carotenoides por 100 g de materia fresca.
Actualmente, la demanda del nopal está limitada a México y países con poblaciones de origen mexicano, donde los consumidores tienen el hábito de comerlo fresco o cocido. Sin embargo, existe una demanda creciente en los Estados Unidos de América y en algunos países europeos y asiáticos, donde los nopales son consumidos esporádicamente en pequeños volúmenes, como un alimento exótico (Sáenz, 1997). El nopal mínimamente procesado tiene una vida de anaquel de 2 a 3 días a temperatura ambiente y de 7 días a 5°C. La secreción de mucílago y el oscurecimiento son los principales problemas que limitan su vida de anaquel (Quevedo et al., 2005).
Si bien se han realizado investigaciones sobre el nopal (Jaramillo et al., 2003; PérezCacho et al., 2006; Aguilar-Sánchez et al., 2007; Gallegos-Infante et al., 2009), son pocos los estudios sobre el efecto que tiene el almacenamiento y el procesamiento en sus características, por ejemplo en sus propiedades antioxidantes (Nicoli et al., 1999; Reza et al., 2005). En los alimentos, el almacenamiento y el procesado pueden ocasionar efectos distintos, con frecuencia opuestos, sobre sus propiedades antioxidantes intrínsecas. Gran parte de los cambios se deben a las reacciones de oxidación que son producidas rápidamente por el calentamiento o de manera un poco retardada por el almacenamiento (Pokorný y Schmidt, 2001).
Los antioxidantes son compuestos que tienen la capacidad de retrasar o inhibir la
oxidación de lípidos, ácidos nucleicos o de otras moléculas, al inhibir la iniciación o propagación de las reacciones de oxidación en cadena (Shi, 2007). Los antioxidantes pueden clasificarse en sintéticos y naturales. Entre los sintéticos se encuentran el hidroxianisol butilado (BHA), la butilhidroquinona terciaria (TBHQ), el hidroxitolueno butilado (BHT), así como los ésteres de ácido gálico, por ejemplo el galato de propilo (PG). Los antioxidantes naturales son sustancias existentes en los tejidos de plantas y animales, también pueden ser sustancias formadas durante el cocinado o procesado de compuestos alimenticios vegetales o animales. Gran parte de ellos son compuestos fenólicos; dentro de esta subclasificación, los principales grupos son los flavonoides, los ácidos fenólicos y los tocoferoles; aunque también pueden citarse otros antioxidantes naturales, como el ácido ascórbico y la clorofila (White y Xing, 1997; Yanishlieva-Maslarova, 2001; Wildman, 2007).
Por el contrario, un prooxidante es una sustancia tóxica que puede causar daño oxidativo a lípidos, ácidos nucleicos y proteínas, resultando en diversos eventos patológicos o enfermedades. Entre las sustancias prooxidantes se pueden incluir a las especies reactivas de oxígeno (ERO) y a las especies reactivas de nitrógeno (ERN), que son productos de los procesos metabólicos aerobios normales (Cao y Prior, 2002).
La exposición a radicales libres provenientes de fuentes externas como humo de cigarro, contaminantes, químicos y toxinas ambientales puede aumentar la producción de ERO. Niveles altos de estas ERO o radicales libres, pueden crear estrés oxidativo, que conlleva al deterioro del metabolismo y al daño del ADN. Los distintos antioxidantes proveen protección contra radicales libres dañinos, además de que han sido asociados con una incidencia menor de varias enfermedades y menores tasas de mortalidad,
en adición a un gran número de otros beneficios a la salud (Shi, 2007).
Debido a lo anterior y por ser un alimento representativo de México, es importante que se realicen investigaciones sobre las propiedades antioxidantes del nopal frente al tiempo de almacenamiento y frente a los distintos tratamientos que se le pueden aplicar. Por ello, el objetivo de este estudio fue determinar el efecto del tiempo de almacenamiento y del tipo de procesamiento sobre las características antioxidantes de nopales frescos, secos y escaldados.
Materiales y métodos
1. Materia prima
Se utilizaron nopales criollos (Nopalea cochenillifera) sin espinas, con una madurez considerada óptima para ser consumidos; obtenidos en un mercado local de San Andrés Cholula, Puebla, los cuales fueron cultivados en San Gregorio Zacapechpan. Los nopales se adquirieron en los primeros días del mes de marzo del año 2010.
2. Prueba de polifenoloxidasa
Los nopales se escaldaron con agua a temperatura de ebullición durante distintos tiempos (0, 10, 15, 30, 60, 90 y 120 s). En cada una de las muestras tratadas, se determinó la actividad de la polifenoloxidasa (25 ó 30°C) espectrofotométricamente a 420 nm (espectrofotómetro Spectronic 20, Bausch and Lomb, Rochester, N.Y., EE.UU.), usando el método de Pizzocaro et al. (1993) con modificaciones (Flores-Álvarez, 2010). Para ello, se preparó un extracto enzimático mezclando 5 mL de nopal homogenizado con 5 mL de buffer McIlvaine (pH 6.6) a baja temperatura (4°C); extracto que se filtró a vacío usando papel Whatman No. 1. Se
preparó la mezcla de reacción (2 mL de buffer, 1 mL de catecol 0.175 M y 0.5 mL del extracto enzimático). La absorbancia de esta mezcla se registró durante 3 minutos cada 10 segundos y se graficó la absorbancia vs. el tiempo. La porción lineal de la gráfica fue empleada para determinar la actividad de la polifenoloxidasa. Los resultados se expresaron como unidades de actividad enzimática (U.A.E.). Una unidad de actividad enzimática se define como la cantidad de enzima que se requiere para producir un cambio de absorbancia de 0.001/min-mL a 420 nm (Ec. 1):
(Ec. 1)
donde:
U.A.E. son Unidades de Actividad Enzimática; m es la pendiente de la gráfica (Abs/s); V es el volumen del extracto enzimático (volumen total de la muestra homogenizada con buffer, 10 mL); v es el volumen del extracto enzimático utilizado para la reacción (0.5 mL); a es el volumen de la muestra usado para realizar el extracto enzimático (5 mL).
3. Preparación de la muestra
El nopal fresco utilizado para los tratamientos previos a su empacado, se lavó con agua y se cortó en tiras de aproximadamente 1 por 5 cm.
3.1. Nopal fresco empacado
El nopal fresco fue sanitizado por inmersión en una solución de cloro de 50 ppm durante 10 minutos. Se secó con papel absorbente, se empacó al vacío y se mantuvo en refrigeración (5°C) hasta el momento de su análisis.
3.2. Nopal escaldado
El nopal fresco se sometió a un proceso de escaldado con agua a temperatura de ebullición durante 30 s. Se secó con papel absorbente, se empacó al vacío y se almacenó en refrigeración (5°C) hasta el momento de su análisis.
3.3. Nopal seco
El nopal fresco se sometió a un proceso de escaldado con agua a temperatura de ebullición durante 30 s. Posteriormente, se secó en un deshidratador de alimentos (Excalibur #3900, Parallex, EE.UU.) con una temperatura de 37°C y velocidad del aire de 1.056 m/s. Se deshidrató hasta alcanzar peso constante, se pulverizó y se almacenó en frascos a una temperatura de 25°C, hasta su análisis.
4. Preparación de extractos
El agente extractante fue una mezcla de etanol al 96% y agua destilada (70:30 v/v) para el análisis de compuestos fenólicos totales, y agua destilada para la medición de la capacidad antioxidante; esta selección fue hecha de acuerdo a los resultados obtenidos por Flores-Álvarez (2010). La preparación de los extractos se llevó a cabo colocando 2.5 g de muestra, se aforó a 25 mL con el agente extractante y se mezcló perfectamente. Esta mezcla se transfirió a un vaso de precipitados forrado con papel aluminio y se mantuvo en agitación durante 2 h a temperatura ambiente; posteriormente, se filtró a vacío a través de papel Whatman No.1. El extracto obtenido se colocó en un tubo con rosca, forrado con papel aluminio y se mantuvo en refrigeración (5°C) hasta ser utilizado para las pruebas.
5. Compuestos fenólicos totales
El contenido de compuestos fenólicos totales fue determinado de acuerdo al método de Folin-Ciocalteau publicado por Gao et al. (2000). Cuando el reactivo de Folin-
Ciocalteau (Sigma-Aldrich, Química S.A. de C.V., México) interacciona con los compuestos fenólicos de la muestra analizada, genera óxidos de molibdeno y de wolframio, mismos que presentan una absorbancia máxima a 765 nm. Entre mayor sea la concentración de compuestos fenólicos, mayor es la absorbancia a dicha longitud de onda.
6. Ácido ascórbico
Para la evaluación del contenido de ácido ascórbico se utilizó el método 967.21 de la A.O.A.C. (2000), el cual consiste de una titulación directa con una solución estándar de indofenol.
7. Clorofila
La determinación de clorofilas a y b se realizó con base en el procedimiento descrito por Hansmann (1973). Este procedimiento consistió en preparar un extracto de la muestra utilizando acetona-agua (90:10 v/v), extracto al que se le midió la absorbancia a 665, 645 y 630 nm, realizando las diluciones necesarias para obtener una absorbancia alrededor de 0.8 a 665 nm. Como blanco se empleó acetonaagua (relación 90:10 v/v).
8. Capacidad antioxidante
Se evaluó utilizando la metodología de capacidad antioxidante equivalente a Trolox (TEAC) desarrollada por Re et al. (1999) y modificada por Kuskoski et al. (2004) y Flores-Álvarez (2010), basada en la inhibición de la absorbancia del radical ABTS por los antioxidantes de la muestra (Cao y Prior, 2002). El ABTS (2,2’azinobis-(3etilbenzotiazolin-6-ácido sulfónico)) fue adquirido de Sigma Chemical CO. (EE.UU.).
9. Análisis estadístico
Se tomaron dos bolsas de nopal fresco desinfectado y dos bolsas del escaldado,
semanalmente (durante 4 semanas) y los nopales de cada bolsa se analizaron por duplicado o triplicado según la prueba. Para el nopal en polvo, las pruebas se hicieron cada dos semanas (durante 6 semanas). A excepción de las determinaciones de ácido ascórbico y clorofila que se realizaron por duplicado, todas las otras pruebas se efectuaron por triplicado. Para el análisis estadístico se utilizó un análisis de varianza (ANOVA) con un nivel de confianza de 95% y la prueba de Tukey para la comparación de medias. Se empleó el software estadístico Minitab (v. 14, Minitab Inc., EE.UU.).
de escaldado óptimo para la inactivación de la enzima polifenoloxidasa en el nopal utilizado en este estudio.
Resultados y discusión
1. Determinación del tiempo de escaldado
Uno de los principales problemas que se presentan a lo largo del procesamiento y/o de la conservación de los nopales es el oscurecimiento enzimático, el cual se debe a la oxidación de compuestos fenólicos por la enzima polifenoloxidasa. Como la susceptibilidad al oscurecimiento está en función de la variedad de la muestra (AguilarSánchez et al., 2007), se determinó el tiempo
En la Fig. 1 se muestra el efecto del tiempo de escaldado sobre la actividad enzimática de la polifenoloxidasa en nopal. Como se puede observar, la actividad enzimática disminuyó hasta alcanzar valores muy cercanos a cero (2.64+1.96 U.A.E). Sin embargo, debido a que en esta investigación se buscó que el producto tuviera una apariencia lo más similar posible a la del producto fresco, y a que con tiempos de escaldado mayores a 30 s la apariencia general del nopal ya era la de un producto cocido, se decidió escoger el tiempo de escaldado de 30 s, con el que se obtuvo un valor de 48+0.00 U.A.E. Con este tiempo de escaldado se logró una reducción de 40 U.A.E., tomando como base las unidades obtenidas con el producto sin escaldar (88+13.86 U.A.E). Entre los resultados obtenidos con los diferentes tiempos de escaldado hubo diferencia estadísticamente significativa (p<0.05) con respecto al valor inicial, el cual se encontró dentro del intervalo publicado para gel de sábila (20.13 U.A.E. a 116.16 U.A.E.) (Cob et al., 2010).
Fig. 1. Efecto del tiempo de escaldado sobre la actividad de polifenoloxidasa de nopal (U. A. E. son unidades de actividad enzimática).
Tiempo (s)
2. Efecto del tiempo de almacenamiento sobre los compuestos antioxidantes del nopal
2.1. Compuestos fenólicos totales
El efecto del tiempo de almacenamiento sobre el contenido de compuestos fenólicos del nopal fresco, del nopal escaldado y del nopal en polvo se muestra en la Fig. 2. Según lo mencionado por Sáenz et al. (2006), la cantidad de compuestos fenólicos totales en los nopales varía dependiendo del estado de desarrollo de las pencas, así como de la variedad a la que pertenezcan.
Los resultados obtenidos para el nopal fresco desinfectado a los diferentes tiempos de almacenamiento fueron estadísticamente distintos (p<0.05) y su comportamiento, en general, fue incrementarse conforme el tiempo transcurrió. Los valores oscilaron entre 33.55+2.10 y 45.44+1.01 mg de equivalentes de ácido gálico por gramo de sólidos secos de nopal, lo cual equivale a 137.22+8.59 y 185.85+4.14 mg de equivalentes de ácido gálico por 100 g de nopal fresco. El rango de valores obtenidos fue similar al reportado por
Jaramillo et al. (2003) (158.9 mg de equivalentes de ácido gálico por 100 g de nopal fresco). Asimismo, los valores obtenidos fueron similares a los reportados para fresa (132.1+3.8), mayores a los de la piña (21.7+4.5) y maracuyá (20+2.6), y menores a los de mango (544.9+7.3) (Kuskoski et al., 2005).
Los valores obtenidos para el nopal escaldado se encontraron entre 34.44+1.48 y 42.59+5.42 mg de equivalentes de ácido gálico por gramo de sólidos secos de nopal, lo que equivale a 143.94+6.17 y 178.03+22.67 mg de equivalentes de ácido gálico por 100 g de nopal, en base húmeda. Estos datos fueron similares a los reportados por Kuskoski et al. (2005) para fresa, mencionados anteriormente. Según el análisis estadístico, el tiempo de almacenamiento tuvo un efecto significativo (p<0.05) sobre el contenido de compuestos fenólicos del nopal escaldado. Éste se mantuvo constante hasta la semana 2 y después aumentó en la semana 3, manteniéndose sin cambios hasta el final de la prueba.
Nopal fresco desinfectado
Nopal escaldado
Nopal en polvo
32 34 36 38 40 42 44 46 48 50 0246 Ácido gálico (mg/g s.s.)
Tiempo (semanas)
Fig. 2. Efecto del tiempo de almacenamiento, a 5°C(nopal fresco y escaldado) y a 25 °C (nopal en polvo),en el contenido de compuestos fenólicos totales (expresados como equivalentes de ácido gálico).
Los compuestos fenólicos en el nopal seco tuvieron una tendencia constante. Se mantuvieron entre 33.41+1.84 y 34.69+1.07 mg de equivalentes de ácido gálico por gramo de sólidos secos de nopal. No se observó diferencia estadísticamente significativa (p>0.05) respecto al tiempo de almacenamiento. Este comportamiento pudo deberse a que como fue un material con muy baja humedad, y por tanto menor actividad de agua que el nopal fresco o el escaldado, tuvo mayor estabilidad.
De acuerdo con el análisis estadístico, al principio del almacenamiento, no existió diferencia significativa (p>0.05) entre los valores obtenidos para las tres presentaciones de nopal, lo cual indica que el tratamiento térmico dado durante el escaldado y el secado no fue tan drástico como para afectar en gran medida el contenido de los compuestos fenólicos. Esto concuerda con lo publicado por Rózek et al. (2008), que mencionan que el secado convectivo parece no tener un efecto significativo en la degradación térmica de los polifenoles totales. Sin embargo, al final del almacenamiento de los nopales frescos y escaldados (semana 4), los valores obtenidos para el nopal seco fueron estadísticamente menores (p<0.05) que los valores de los
Ácido ascórbico (mg/g s.s.)
nopales escaldados y los nopales frescos.
2.2.
Ácido ascórbico
La Fig. 3 ilustra el efecto del tiempo de almacenamiento sobre el contenido de ácido ascórbico de los nopales. Para el nopal fresco desinfectado los valores oscilaron entre 2.36+0.83 y 0.61+0.09 mg de ácido ascórbico por gramo de sólidos secos de nopal, mismos que expresados en base húmeda serían 9.64+3.41 y 2.51+0.36, respectivamente.
De acuerdo con el análisis estadístico, los datos, que durante el almacenamiento mostraron una tendencia decreciente (nopal escaldado y nopal desinfectado), fueron significativamente distintos (p<0.05). El valor inicial (9.64+3.41 mg por 100 g de nopal fresco) se encontró dentro del intervalo publicado para nopal fresco, de 8 mg por 100 g de nopal (Instituto Nacional de Ecología y Comisión Nacional de las Zonas Áridas, 1994) a 12.7 mg por 100 g de nopal (Rodríguez-Félix y Cantwell, 1988). El hecho de que se haya manifestado una tendencia decreciente indica una degradación del ácido ascórbico a lo largo del almacenamiento debido a su oxidación (Ottaway et al., 2005).
Nopal fresco desinfectado
Nopal escaldado
Nopal en polvo
3. Efecto del tiempo de almacenamiento a 5 °C (nopal fresco y nopal escaldado) y a 25 °C (nopal en polvo) en el contenido de ácido ascórbico denopal.
Tiempo (semanas)
Fig.
Los valores para el nopal escaldado oscilaron entre 1.15+0.00 y 0.51+0.04 mg ácido ascórbico por gramo de sólidos secos. Los valores obtenidos para el nopal escaldado no fueron estadísticamente distintos que los del nopal fresco desinfectado, en ningún momento del almacenamiento (p>0.05).
El nopal seco presentó valores entre 0.45+0.06 y 0.62+0.08 mg de ácido ascórbico por gramo de sólidos secos, mostrando pocas variaciones a lo largo del almacenamiento; no se observó diferencia estadísticamente significativa entre los datos (p>0.05).
Tampoco hubo diferencia significativa (p>0.05) entre los valores de ácido ascórbico del nopal seco, los del fresco y los del escaldado, ni al principio del almacenamiento, ni en las semanas 2 y 4 del mismo.
2.3. Clorofila
En la Fig. 4 se muestra el contenido de clorofila a de nopal durante el almacenamiento. El nopal fresco presentó valores entre 1.34+0.02 y 1.13+0.05 mg clorofila a por gramo de sólidos secos, mismos
que corresponden a 5.47+0.10 y 4.61+0.22 mg de clorofila a por 100 g de nopal fresco, respectivamente. Estos valores fueron menores al reportado por Wang et al. (1998) (13.4+0.8 mg por 100 g de nopal fresco), lo que pudo deberse a diferencias en las variedades de las muestras analizadas o incluso al empleo de métodos distintos para la determinación de clorofila. Los valores de clorofila a del nopal fresco fueron estadísticamente diferentes entre sí (p<0.05) a lo largo del almacenamiento. Se observó una reducción en el contenido de clorofila a después de dos semanas de almacenamiento y, posteriormente, los valores mostraron una tendencia constante.
Los valores de clorofila a para el nopal escaldado oscilaron entre 1.36+0.06 y 1.06+0.02 mg por gramo de sólidos secos, los cuales equivalen a 5.68+0.23 y 4.42+0.09 mg de clorofila a por 100 g de nopal, en base húmeda. El dato inicial es similar al de la muestra fresca desinfectada (p>0.05) y menor al reportado por Wang et al. (1998). Los valores fueron estadísticamente distintos entre
a (mg/g s.s.)
Nopal fresco desinfectado
Nopal escaldado
Nopal en polvo
Clorofila
Tiempo (semanas)
Fig. 4. Evolución delcontenido declorofila a durante el almacenamiento a 5°C (nopal fresco y nopal escaldado) y a 25 °C (nopal en polvo).
sí (p<0.05) y presentaron un comportamiento similar a los del fresco desinfectado a partir de la segunda semana de almacenamiento. Por otro lado, los valores de clorofila a del nopal fresco desinfectado y los del escaldado no presentaron diferencia estadísticamente significativa entre ellos a lo largo del almacenamiento, a excepción de los de la semana 1 (p<0.05).
Los valores de clorofila a para el nopal en polvo tuvieron pocos cambios; no presentaron diferencia estadísticamente significativa (p>0.05) a lo largo del tiempo de almacenamiento, se mantuvieron entre 0.66+0.06 y 0.64+0.00 mg de clorofila a por gramo de sólidos secos. Como es posible observar, los datos del nopal en polvo fueron significativamente menores (p<0.05) que los del nopal fresco desinfectado y que los del nopal escaldado, lo cual pudo deberse a la degradación de la clorofila (transformación en feofitina) por la exposición del nopal al calor
durante el escaldado y el secado (Ozuna et al., 2007).
La Fig. 5 ilustra el comportamiento de la clorofila b durante el almacenamiento. Para el nopal fresco desinfectado el contenido de clorofila b se mantuvo entre 0.41+0.01 y 0.32+0.02 mg por gramo de sólidos secos, lo cual es equivalente a 1.69+0.06 y 1.29+0.08 mg por 100 gramos de nopal fresco, respectivamente. Sólo el valor de la semana cero (0.41+0.01 mg por gramo de sólidos secos) fue estadísticamente distinto a los de las otras semanas (p<0.05). Para el nopal escaldado, la clorofila b se mantuvo entre 0.36+0.01 y 0.25+0.03 mg por gramo de sólidos secos, lo que en base húmeda equivale a 1.51+0.05 y 1.04+0.14 mg por 100 gramos de nopal, respectivamente. Sólo el valor de la semana 3 fue estadísticamente distinto a los de las otras semanas (p<0.05). Los valores de clorofila b se encuentran por debajo del reportado por Wang et al. (1998) (3.5+0.2 mg
b (mg/g s.s.)
Nopal fresco desinfectado
Nopal escaldado
Nopal en polvo
0.05
5. Evolución del contenido de clorofila b durante el almacenamiento a 5°C (nopal fresco y nopal escaldado) y a 25 °C (nopal en polvo).
Clorofila
Tiempo (semanas)
Fig.
por 100 g de nopal fresco). En las semanas 0 y 3 hubo diferencia entre los valores de clorofila b de la muestra fresca y los de la muestra escaldada (p<0.05); en el resto de los tiempos de almacenamiento evaluados no se observaron diferencias estadísticamente significativas entre la muestra escaldada y la fresca desinfectada (p>0.05).
Para el nopal seco, este parámetro se mantuvo entre 0.19+0.003 y 0.06+0.004 mg clorofila b por gramo de sólidos secos. Sólo el valor de la semana 0 (0.19+0.003 mg por gramo de sólidos secos) fue estadísticamente distinto a los de las otras semanas (p<0.05). La clorofila b de la muestra en polvo fue significativamente menor (p<0.05) a la obtenida para el nopal fresco y para el escaldado, lo cual podría estar relacionado con el hecho de que recibió más tratamiento térmico y pudo haber ocurrido una transformación de clorofilas en feofitinas (Ozuna et al., 2007).
2.4 Capacidad antioxidante
El efecto del tiempo de almacenamiento sobre la capacidad antioxidante de nopal fresco desinfectado, nopal escaldado y nopal deshidratado puede apreciarse en la Fig. 6. Los valores de capacidad antioxidante para el nopal fresco desinfectado se encontraron entre 26.03+5.86 y 53.92+3.44 mg equivalentes a Trolox por gramo de sólidos secos de nopal; lo que equivale a 106.44+23.98 y 220.53+14.07 mg equivalentes a Trolox por 100 g de nopal fresco.
Se observó diferencia significativa (p<0.05) entre los valores obtenidos a lo largo del almacenamiento, mismos que, en general, mostraron una tendencia creciente. El intervalo de datos obtenidos incluyó a los reportados por Kuskoski et al. (2005) para mora (177.71 mg equivalentes a Trolox por 100 g de pulpa de mora), pero fue menor a los de fresa y mango (300.35 y 330.39 mg
equivalentes a Trolox por 100 g de pulpa, respectivamente) y mayor a los de maracuyá y piña (67.58 y 85.10 mg equivalentes a Trolox por 100 g de pulpa, respectivamente).
Los valores para el nopal escaldado (Fig. 6) se ubicaron en el intervalo de 19.72+2.40 y 33.18+3.40 mg equivalentes a Trolox por gramo de sólidos secos de nopal, lo cual equivale a 82.41+10.01 y 138.68+14.19 mg equivalentes a Trolox por 100 g de nopal, en base húmeda. La capacidad antioxidante del nopal escaldado mostró diferencias estadísticamente significativas (p<0.05) a lo largo del almacenamiento, y al final (semana 4) fue menor que la del nopal fresco desinfectado (p<0.05).
Por otro lado, se observa que este parámetro presentó un comportamiento similar al del contenido de los compuestos fenólicos totales, en el caso de las muestras frescas desinfectadas y de las escaldadas; por lo que podría existir una relación directa entre estas dos características del nopal. Sin embargo, según lo mencionado por Inchuen et al. (2010), las conexiones ambiguas entre el contenido de ciertos antioxidantes en particular y la actividad antioxidante son difíciles de explicar basándose únicamente en el análisis cuantitativo.
La capacidad antioxidante de la muestra en polvo (Fig. 6) se mantuvo sin grandes variaciones dentro del intervalo de 42.81+2.98 y 53.81+2.65 mg equivalentes a Trolox por gramo de sólidos secos de nopal; sin embargo, mostró diferencias estadísticamente significativas entre la semana 0 y la 4 (p<0.05). Es interesante notar que la muestra en polvo tuvo valores mayores de capacidad antioxidante que las otras dos presentaciones, por lo menos al principio del almacenamiento (p<0.05). Según lo mencionado por Nicoli et al. (1999), el aumento de la capacidad antioxidante en algunas muestras en polvo puede deberse a la formación de nuevos
Capacidad antioxidante (mg eq. Trolox / g de s.s.)
Nopal fresco desinfectado
Nopal escaldado
Nopal en polvo
Tiempo (semanas)
Fig. 6 . Efecto del tiempo de almacenamiento a 5°C (nopal fresco y nopal escaldado) y a 25 °C (nopal en polvo) sobre la capacidad antioxidante de nopal con diferentes tratamientos.
compuestos con actividad antioxidante o al hecho de que los polifenoles con un estado de oxidación intermedio pueden exhibir mayor eliminación de los radicales libres, que los no oxidados. Asimismo, Zheng y Wang (2001) y Kuskoski et al. (2005) sugieren que no sólo el nivel de antioxidantes, sino también la sinergia que ocurre entre ellos y los otros constituyentes de la muestra, pueden influir en las diferencias en la capacidad antioxidante de los extractos de plantas.
ascórbico de las muestras. Sí hubo efecto del tipo de tratamiento en el contenido de clorofilas a y b, ya que el nopal en polvo presentó valores menores de estos parámetros que los de las muestras frescas y las muestras escaldadas. También hubo efecto del tipo de tratamiento en la capacidad antioxidante, ya que, por lo general, el nopal en polvo tuvo mayor actividad antioxidante que el nopal fresco y el nopal escaldado.
Conclusión
Se observó que existe un efecto del tiempo de almacenamiento sobre las características antioxidantes de nopales frescos, secos y escaldados. Con el tiempo de almacenamiento aumentó el contenido de compuestos fenólicos totales y la capacidad antioxidante de las muestras escaldadas y de las muestras frescas. No hubo un efecto del tipo de tratamiento sobre el contenido inicial de los compuestos fenólicos totales, ni sobre el de ácido
Agradecimientos
Los autores agradecen el apoyo financiero del CONACYT (Consejo Nacional de Ciencia y Tecnología, México) por el apoyo al proyecto No. 206/62275-Z, “Extracción, caracterización y funcionalidad de compuestos de origen vegetal obtenidos de materiales mexicanos empleados como condimentos, obtención de agentes antimicrobianos, antioxidantes e ingredientes funcionales” y por la beca de la autora M. C. Flores-Álvarez; así como a la
M. C. Flores-Álvarez et al. / Temas
Universidad de las Américas Puebla por la beca de la misma autora.
Referencias
Aguilar-Sánchez, S. L., Martínez-Damián, D. M. T., Barrientos-Priego, P. A. F., Aguilar-Gallegos, G. N. y Gallegos-Vásquez, V. C. 2007. Potencial de oscurecimiento enzimático de variedades de nopalitos. Journal of the Professional Association for Cactus Development. 9: 165.
A.O.A.C. 2000. Official Methods of Analysis of A.O.A.C International. Decimo séptima edición. A.O.A.C. International, EE.UU.
Cao, G. y Prior, R. L. 2002. Measurement of total antioxidant capacity in nutritional and clinical studies. En: E. Cadenas y L. Packer (Eds.). Handbook of antioxidants. Segunda edición. CRC Press, EE.UU. pp. 47 - 55.
Cob, C. N. N., Tello, C. J., Escamilla, S. J., Vargas, V. L. y Tamayo, C. J. 2010. Actividad de la polifenoloxidasa en el gel de sábila (Aloe vera Mill). Revista Iberoamericana de Tecnología Postcosecha. 11 (2): 221 -227.
Flores-Álvarez, M. C. 2010. Efecto del tiempo de almacenamiento en las características fisicoquímicas, microbiológicas y antioxidantes de tres presentaciones de nopal: fresco, escaldado y seco. Tesis de Licenciatura, Universidad de las Américas Puebla. México. 154 p.
Gallegos-Infante, J. A., Rocha-Guzmán, N. E., GonzálezLaredo, R. F., Reynoso-Camacho, R., Medina-Torres, L. y Cervantes-Cardoso, V. 2009. Effect of air flow rate on the polyphenols content and antioxidant capacity of convective dried cactus pear cladodes (Opuntia ficus indica). International Journal of Food Sciences and Nutrition. 60 (S2): 80-87.
Gao, X., Ohlander M., Jeppsson N., Björk L., y Trajkovski V. 2000. Changes in Antioxidant Effects and Their Relationship to Phytonutrients in Fruits of Sea Buckthorn (Hippophae rhamnoides L.) during Maturation. Journal of Agricultural and Food Chemistry. 48 (5): 1485–1490.
Hansmann, E. 1973. Pigment analysis. En: J. R. Stein (Ed.). Handbook of phycological methods. Culture method and growth measurement. V.1. Cambridge University Press, Reino Unido. pp. 359 - 368.
5 – 2 (2011): 84 - 96
Inchuen, S., Narkrugsa, W. y Pornchaloempong, P. 2010. Effect of drying methods on chemical composition, color and antioxidant properties of thai red curry powder. Kasetsart Journal: Natural Science. 44 (1): 142-151.
Instituto Nacional de Ecología y Comisión Nacional de las Zonas Áridas. 1994. Nopal verdura. Opuntia spp. Cultivo alternativo para las zonas áridas y semiáridas de México. Conaza, México. 31 p.
Jaramillo, F. M. E., González, C. L., Cornejo, M. M., Dorantes, A. L., Gutiérrez, L. G. F. y Hernández, S. H. 2003. Effect of termal treatment on the antioxidant activity and content of carotenoides and phenolic compounds of cactus pear cladodes (Opuntia ficusindica). Food Science and Technology International 9 (4): 271-278.
Kuskoski, M., Asuero, A., García-Parrilla, M., Troncoso, A. y Fett, R. 2004. Actividad antioxidante de pigmentos antociánicos. Ciencia y Tecnología Alimentaria (México). 24 (4): 691-693.
Kuskoski, M., Asuero, A., Troncoso, A., Mancini-Filho, J. y Fett, R. 2005. Aplicación de diversos métodos químicos para determinar actividad antioxidante en pulpa de frutos. Ciência e Tecnologia de Alimentos 25 (4): 726-732.
León-Portilla, M. L. 1983. De Teotihuacán a los Aztecas: Antología de Fuentes e Interpretaciones Históricas. Volumen 11 de Lecturas Universitarias. Segunda edición. Universidad Nacional Autónoma de México, México. 611 p.
Nicoli, M. C., Anese, M. y Parpinel, M. 1999. Influence of processing on antioxidant properties of fruit and vegetables. Trends in Food Science and Technology 10: 94-100.
Ottaway, B. P., Ottaway, B. y Asociados Ltd. 2005. The stability of vitamins during food processing. En: C. J. K. Henry y C. Chapman (Eds.). The nutrition handbook for food processors. CRC-Woodhead Publishing Limited, EE.UU. pp. 247-264.
Ozuna, R. L. E., Goycoolea, F. M., Silveira, M. I. y Montoya, B. L. C. 2007. Uso del quitosano durante el escaldado del nopal (Opuntia ficus-indica) y efecto sobre su calidad. Revista Mexicana de Ingeniería Química. 6 (2): 193-201.
Pérez-Cacho, R. M. P., Galán-Soldevilla, H., Corrales, G. J. y Hernández, M. A. 2006. Sensory characterization of nopalitos (Opuntia spp.). Food Research International. 39: 285-293.
Pizzocaro, F., Torreggiani, D. y Gilardi, G. 1993. Inhibition of apple polyphenol oxidase (PPO) by ascorbic acid, citric acid and sodium chloride. Journal of Food Processing and Preservation. 17 (1): 21-30.
Pokorný, J. y Schmidt, S. 2001. Funcionalidad de los antioxidantes naturales durante el procesado de los alimentos. En: J. Pokorny, N. Yanishlieva y M. Gordon (Eds.). Antioxidantes de los Alimentos. Acribia, España. pp. 311-330.
Quevedo, P. K. L., Villegas, O. M. A., González, R. H. y Rodríguez, F. A. 2005. Calidad del nopal verdura mínimamente procesado. Efecto de temperatura e inhibidores del oscurecimiento. Revista Fitotecnia Mexicana. 28 (3): 261 – 270.
Re, R., Pellegrini, N., Proteggente, A., Pannala, A., Yang, M. y Rice-Evans, C. 1999. Antioxidant activity applying an improved ABTS radical cation decolorization assay. Free Radical Biology and Medicine. 26 (9-10): 1231-1237.
Reza, N. S., Flores, E. A. L., Alonso, N. M. y Ramírez, B. P. 2005. Evaluación de textura, color y aceptación del nopalito variedad Milpa Alta escaldado, a diferentes tiempos de inmersión en solución de NaCl y CaCl2, y empacado al vacío. Memorias del VII Congreso Nacional de Ciencia de los Alimentos y III Foro de Ciencia y Tecnología de Alimentos. Guanajuato, México. 1-3 Junio 2005.
Rodríguez-Félix, A. y Cantwell, M. 1988. Developmental changes in composition and quality of prickly pear cactus cladodes (nopalitos). Plant Foods for Human Nutrition. 38 (1): 83-93.
Rózek, A., Achaerandio, I., Güell, C., López, F. y Ferrando, M. 2008. Efecto del secado convectivo en la estabilidad de compuestos fenólicos añadidos a alimentos sólidos mediante deshidratación osmótica. Memorias del II Congreso Iberoamericano sobre Seguridad Alimentaria. V Congreso Español de
Ingeniería de Alimentos. Barcelona, España. 5-7 Noviembre 2008.
Sáenz, H. C. 1997. Cladodes: a source of dietary fiber. Journal of the Professional Association for Cactus Development. 2 : 117.
Sáenz, C., Berger, H., Corrales, G. J., Galletti, L., García, D. C. V., Higuera, I., Mondragón, C., RodríguezFélix, A., Sepúlveda, E. y Varnero, M. T. 2006. Utilización agroindustrial del nopal. Volumen 162 de Boletines Des Servicios Agricoles de la FAO. Volumen 162 de FAO agricultural services bulletin Food and Agriculture Organization, Italia. 165 p.
Shi, J. 2007. Functional food ingredients and nutraceuticals: processing technologies. CRC Press, EE.UU. 427 p.
Wang, N., Zhang, H. y Nobel, P. S. 1998. Carbon flow and carbohydrate metabolism during sink-to-source transition for developing cladodes of Opuntia ficusindica. Journal of Experimental Botany. 49 (328): 1835-1843.
White, P. J. y Xing, Y. 1997. Antioxidants from cereals and legumes. En: F. Shahidi (Ed.). Natural Antioxidants: Chemistry Health Effects and Applications. The American Oil Chemists Society, EE.UU. pp. 35 - 421.
Wildman, R. E. C. 2007. Handbook of Nutraceuticals and Functional Foods. Segunda edición. CRC Press, EE.UU. 541 p.
Yanishlieva-Maslarova, N. V. 2001. Inhibición de la oxidación. En: J. Pokorny, N. Yanishlieva y M. Gordon (Eds.). Antioxidantes de los Alimentos Acribia, España. pp. 23 - 68.
Zheng, W. y Wang, S. Y. 2001. Antioxidant activity and phenolic compounds in selected herbs. Journal of Agricultural and Food Chemistry. 49: 5165-5170.

Contenido
Temas Selectos de Ingeniería de Alimentos Vol. 5 / No. 2

Volumen 5 / No. 2 Ago – Dic 2011
Cuerpo editorial
Artículos de Revisión
Envases activos con agentes antimicrobianos y su aplicación en los alimentos
Y. Martínez-Tenorio* y A. López-Malo
Tecnologías involucradas en el procesamiento mínimo de frutas y hortalizas
E. P. Pérez-Pérez* y A. López-Malo
Escherichia coli de tipo patógeno en alimentos y modelación de su inactivación al aplicar diversos factores de conservación
E. Romero*, A. López-Malo y E. Palou
Envejecimiento del pan: causas y soluciones
M. Luna-Fernández* y M. E. Bárcenas-Pozos
Producción de café (Coffea arabica L.): cultivo, beneficio, plagas y enfermedades
A. L. Temis-Pérez*, A. López-Malo y M. E. Sosa-Morales
Propiedades nutricionales y antioxidantes del maíz azul (Zea mays L.)
A. Castañeda-Sánchez
Artículos de Investigación
Efecto del tiempo de almacenamiento y tipo de procesamiento en los antioxidantes de nopal
M. C. Flores-Álvarez*, F. T. Vergara-Balderas y J. A. Guerrero-Beltrán

Departamento de Ingeniería Química, Alimentos y Ambiental Derechos Reservados 2011
