

Temas Selectos de Ingeniería de Alimentos














Volumen 4 / No. 1 Ene -May2010
DIRECTORIO
TEMAS SELECTOS DE INGENIERÍA DE ALIMENTOS
UNIVERSIDAD DE LAS AMÉRICAS PUEBLA
PUBLICACIÓN SEMESTRAL
VOLUMEN 4, NÚMERO 1 (ENERO-MAYO 2010)
EDITORA RESPONSABLE
María Eugenia Bárcenas Pozos
CONSEJO EDITORIAL
María Teresa Jiménez Munguía
Emma Mani López
María Elena Sosa Morales
Fidel Tomás Vergara Balderas
Reserva de Derechos en Trámite
DOMICILIO:

Fundación Universidad de las Américas Puebla
Exhacienda Santa Catarina Mártir S/N
San Andrés Cholula, Pue.
C.P. 72810 México
Teléfono: 222 229 2126
DISTRIBUIDO POR:
Departamento de Ingeniería Química, Alimentos y Ambiental
Fundación Universidad de las Américas Puebla
IMPRESIÓN:
Gutiérrez Mora Carina
18 Sur 6130 Local A. Col. Jardines San Manuel
Puebla, Pue. C.P. 72570

Cuerpo editorial
Dra. María Eugenia Bárcenas Pozos
Dra. María Teresa Jiménez Munguía
M. C. Emma Mani López
M. C. Fidel Vergara Balderas


Contenido
Temas Selectos de Ingeniería de Alimentos Vol. 4 / No. 1

Volumen 4 / No. 1 Ene – Mayo 2010
Cuerpo editorial ………………………………………………………………………………….
Artículos de Revisión
Propiedades funcionales y aplicaciones industriales de los fructo-oligosacáridos
P. Hernández-Carranza* y M. T. Jiménez-Munguía …………………...……………………... 1
Pulsos eléctricos: fundamentos y aplicaciones en alimentos
T. G. Cerón-Carrillo*, E. Palou y A. López-Malo ………………………………...…..………… 9
Tecnologías de enmascaramiento de sabor amargo en alimentos
X. Villegas-Ruíz*, H. Ruíz-Espinosa y M. E. Bárcenas-Pozos ………………….……...……. 27
Algunas características de compuestos presentes en los frutos secos y su relación con la salud
J.J Luna-Guevara* y J. A. Guerrero-Beltrán …………………………………………………… 37
La tuna: una perspectiva de su producción, propiedades y métodos de conservación
C. E. Ochoa-Velasco* y J. A. Guerrero-Beltrán .……………………………………………..…...
Granada (Punica granatum L.): una fuente de antioxidantes de interés actual
O. A. López-Mejía*, A. López-Malo y E. Palou …………………………………………………… 64
Desinfección de agua mediante el uso de tecnologías emergentes basadas en procesos avanzados de oxidación
J. H. Castillo-Ledezma*, A. López-Malo Vigil, E. R. Bandala ……………………………………. 74
Piranoantocianinas: modificaciones estructurales de antocianinas
Ma. del Pilar Guzmán-Figueroa*, Ana E. Ortega-Regules, Cecilia Anaya-Berrios ……………

Editorial
Temas Selectos de Ingeniería de Alimentos Vol. 4 / No. 1

En el presente número de la revista Temas Selectos de Ingeniería de Alimentos se publican artículos de revisión sobre los temas de tesis abordados por los estudiantes del Doctorado en Ciencia de Alimentos de la Universidad de las Américas, Puebla. Los artículos de revisión contribuyen a dar una visión global de los fundamentos, avances y perspectivas de los tópicos más actuales en Ciencia de Alimentos para quienes se introducen en un nuevo tema, o para apoyar con referencias recientes y puntos de vista de los autores a quienes trabajan en un área específica. El reto de compilar, organizar y presentar la información publicada de forma coherente y compresible ha sido superado, y tenemos en este ejemplar, el fruto del trabajo bien llevado por los estudiantes, asesores y editores.
A partir de este número, la revista contará con registro ISSN (International Standard Serial Number ó Número Internacional Normalizado de Publicaciones Seriadas). El ISSN es un número único internacional que permite identificar una colección y evitar posibles errores de transcribir el título o la información contenida en la edición. Este registro seguramente impulsará la proyección de la revista como un foro de comunicación en los temas de ciencia, tecnología e ingeniería de alimentos, no sólo a nivel local, sino también con futuros impactos nacionales e internacionales.
Felicidades a los estudiantes, profesores y miembros del cuerpo editorial que participan en este número, quienes contribuyen con su trabajo al objetivo de la revista: iniciarse en la escritura de artículos científicos y aportar conocimientos valiosos para quienes formamos parte de la comunidad de Ingeniería de Alimentos.
Dra. María Elena Sosa Morales Profesora y Jefa de Laboratorios del Departamento de Ingeniería Química, Alimentos y Ambiental Universidad de las Américas, Puebla

Temas Selectos de Ingeniería de Alimentos 4 – 1 (2010): 1 – 8

Propiedades funcionales y aplicaciones industriales de los fructooligosacáridos
P. Hernández-Carranza* y M. T. Jiménez-Munguía
Departamento de Ingeniería Química, Alimentos y Ambiental. Universidad de las Américas, Puebla. Sta. Catarina Mártir, Cholula, Puebla. 72810. México
Resumen
El consumo de alimentos que proporcionen múltiples beneficios a la salud es una tendencia actual, debido a las enfermedades y/o padecimientos que se producen a causa de ciertas deficiencias nutricionales. En nuestros días los consumidores pueden seleccionar alimentos funcionales a partir de una amplia variedad de estos productos que contengan componentes como aminoácidos esenciales, antioxidantes, fibra dietética, probióticos y prebióticos. Los fructo-oligosacáridos son hidratos de carbono que poseen propiedades funcionales, aportan beneficios a la salud, sobre todo a nivel gastrointestinal, reducen la generación de enfermedades cardiovasculares, cancerígenas, entre otras. El objetivo de este trabajo es dar a conocer las propiedades funcionales de los fructo-oligosacáridos, así como sus aplicaciones a nivel industrial, lo cual podría permitir la generación de alimentos funcionales con beneficios adicionales para el consumidor.
Palabras claves: fructo-oligosacáridos, alimentos funcionales, prebiótico.
Abstract
Eating foods that provide multiple health benefits is a current trend, due to illness and / or conditions that occur because of nutritional deficiencies. These days consumers can select functional foods from a wide variety of these products containing components such as amino acids, antioxidants, fiber, probiotics and prebiotics. The fructo-oligosaccharides are carbohydrates that have functional properties, having benefits to health, especially in gastrointestinal functions, reducing the generation of cardiovascular disease and cancer. The aim of this paper is to show the functional properties of fructo-oligosaccharides and their application at industrial level, which could allow the generation of functional foods with added benefits for consumers.
Keywords: fructo-oligosaccharides, functional foods, prebiotic.
*Programa de Doctorado en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: paola.hernandezca@udlap.mx
Introducción
Los productos alimenticios son elaborados por el gusto, apariencia, costo y conveniencia para el consumidor. El diseño de productos alimenticios que confieren beneficios a la salud es una tendencia relativamente nueva, intentando generar productos que permitan la prevención de enfermedades, otorgando múltiples beneficios al consumidor. Es así como surgen los alimentos funcionales, los cuales aportan beneficios superiores a los de los alimentos tradicionales.
En la producción de algunos alimentos funcionales se emplean dos términos: probiótico y prebiótico.
El probiótico se refiere a microorganismos vivos que se adicionan a un alimento, los cuales permanecen activos en el intestino, ejerciendo importantes beneficios fisiológicos. En cambio, los prebióticos son ingredientes no digeribles que estimulan el crecimiento de los probióticos y generalmente son hidratos de carbono. En esta categoría de alimentos prebióticos se encuentran los fructooligosacáridos (FOS).
Los FOS representan una importante tendencia industrial por sus aplicaciones nutricionales y funcionales, siendo así que contribuyen a la mejora de enfermedades gastrointestinales, permiten la absorción de ciertos minerales, son utilizados en la industria alimenticia como edulcorantes, sustitutos de grasa, modificadores de textura, entre otros y tienen la peculiaridad de encontrarse en una gran variedad de alimentos, sobre todo en los de origen vegetal.
El objetivo de esta revisión es dar a conocer las propiedades funcionales de los FOS, así como su aplicación a nivel industrial, lo cual permitirá que puedan ser aprovechados de manera potencial, para el desarrollo de nuevos productos.
Revisión bibliográfica
1. ¿Qué son los fructo-oligosacáridos?
Los FOS son hidratos de carbono compuestos principalmente por fructosa y algunos escasos residuos de glucosa (Chacón, 2006). Son también conocidos como fructanos, oligofructanos, glucofructosanos, inulinos u oligosacáridos resistentes, cuya estructura se encuentra formada por uniones repetitivas de disacáridos tales como sacarosa, inulobiosa y levanobiosa. La unión de grupos fructosilos a la sacarosa en diferentes posiciones genera cetosas, las cuales son la base de todos los fructanos naturales (Madrigal y Sangronis, 2007).
Los FOS son fructosilpolímeros que consisten en cadenas lineales de D-fructosa (aunque se pueden observar diferentes grados de ramificación según la complejidad), presentan un enlace β 2-1 y usualmente tienen una molécula de D-glucosa terminal unida a una fructosa por un enlace α 2-1. La naturaleza de estos enlaces tiene importantes implicaciones bioquímicas que se asocian a una baja digestibilidad de los mismos cuando son consumidos por seres humanos (Perrin et al., 2001). La presencia del enlace β 2-1 hace que los FOS no sean digeribles como lo sería cualquier hidrato de carbono típico, lo que a su vez tiene como consecuencia que tengan un bajo valor calórico y una funcionalidad como fibra dietética (Niness, 1999). Debido a su estructura química, los FOS son solubles en agua (Chacón, 2006).
Los fructanos presentan algunas características químicas peculiares. Dependiendo de su origen (vegetal o microbiano) pueden ser lineales, cíclicos o ramificados, aunque en los FOS se presenta una estructura polimérica predominantemente lineal. Suelen definirse en términos del grado de polimerización promedio (GP prom) y grado de polimerización máxima (GP máx).
En los de origen vegetal, el GP máx no excede de 200 y puede ser tan alto como 100,000 en los de origen bacteriano. Sus pesos moleculares son muy variables según la fuente de obtención, pero en términos generales oscilan entre 1000 y 4500 Daltones (Madrigal y Sangronis, 2007).
Después del almidón, los FOS son los polisacáridos no estructurales más abundantes en la naturaleza; están presentes en muchas especies de plantas e inclusive en algunos mohos y bacterias (Franck, 2006).
1.1 Propiedades fisicoquímicas
Los FOS poseen un sabor entre neutro y ligeramente dulce. Así por ejemplo, los FOS de más bajo peso molecular pueden tener dulzuras equivalentes al 10% correspondiente a la sacarosa (Chacón, 2006). Presentan propiedades humectantes cuando se emplean como aditivos en la industria de alimentos. Las viscosidades de las disoluciones de FOS son generalmente más altas que las de las disoluciones de los demás hidratos de carbono a la misma concentración; estas disoluciones suelen ser de mayor estabilidad térmica.
Al ser consumidos, los FOS no son hidrolizados en el tracto digestivo dada la ausencia tanto de exoinulinasa como de exolevanasas, sufriendo posteriormente por ello una fermentación en el colon. Químicamente se hidrolizan por calentamiento en una disolución de ácido oxálico (Tita y Smeekens, 2003).
1.2 Fuentes de obtención
Los FOS son de origen vegetal y también microbiano, se encuentran en la dieta desde tiempos inmemoriales (A.A.C.C., 2001). Hasta 36 000 especies diferentes de plantas contienen entre sus hidratos de carbono de reserva a diversos tipos de fructanos; en algunas de estas plantas el contenido de
fructanos puede llegar a constituir hasta el 24% de la masa cruda (Tita y Smeekens, 2003).
Las principales familias de plantas que incluyen FOS en su composición son Liliaceae, Amaryllidaceae, Gramineae, Poaceae, Solanaceae y Compositae (Marquina y Santos, 2003). Es común encontrar FOS en alimentos tales como: trigo, ajo, cebolla, cebada, cacahuate, tomate, espárrago, puerro, plátano, entre otros. En estos alimentos los FOS aportan valores energéticos entre 1 y 1.5 kcal/g (Flickinger y Fahey, 2002).
No obstante, si de cantidades se trata, las principales fuentes de FOS son la achicoria (Cichorium intybus), alcachofa (Cynara scolymus), yacón (Smallanthus sonchifolius) y dalia (Dahlia pinnata) (Chacón, 2006).
2. Beneficios y desventajas de los FOS
Entre los FOS hay varios compuestos de interés, uno de los más importantes es la inulina, que es un hidrato de carbono no digerible que está presente en muchos vegetales, frutas y cereales. A nivel industrial, la inulina se obtiene de la raíz de la achicoria y se usa como ingrediente en los alimentos, ofreciendo ventajas tecnológicas importantes y beneficios a la salud. En la actualidad, la presencia de ciertas cantidades de inulina o sus derivados en la formulación de un producto alimenticio es condición suficiente para que dicho producto pueda ser considerado como alimento funcional. Tanto la inulina como los FOS se encuentran ampliamente presentes en la dieta de la mayoría de la población mundial, al punto que la ingesta suele ser de varios gramos diarios. Se ha estimado que la población de Estados Unidos consume un promedio de 1 a 4 g de FOS al día, mientras que los europeos ingieren entre 3 y 10 g diarios. Sin embargo se recomienda al menos una ingesta de 8 g de FOS en la dieta, de modo que sus funcionalidades nutricionales sean manifiestas en el organismo y no se presenten problemas de intolerancia (Sangeetha et al., 2005).
Los FOS producen efectos benéficos en la salud, debido a que son parte de la fibra dietética, la cual se define como “aquella parte de plantas o bien hidratos de carbono análogos que son resistentes a la digestión y a la absorción en el intestino delgado humano y que experimentan una fermentación parcial o total en el intestino grueso; incluyéndose en esta definición polisacáridos, oligosacáridos, lignina y sustancias vegetales asociadas” (A.A.C.C., 2001).
Además de ser un aporte en fibra dietética, los FOS pueden favorecer selectivamente el crecimiento de las bacterias lácticas y Bifidobacterium. Esta capacidad de estimular el crecimiento en el colon de bacterias específicas consideradas beneficiosas, y de estimular y hasta anular el crecimiento de bacterias patógenas, se conoce como efecto prebiótico (Roberfroid, 2001).
En Japón se han reconocido las propiedades beneficiosas para la salud de los oligosacáridos en general y desde principios de los años 90 se han desarrollado productos, especialmente bebidas, que se están comercializando por su contenido de oligosacáridos. Se venden en Europa productos simbióticos como el yogurt
SymBalnace® que contiene Lactobacillus reuteri, L. acidophilus, L. casei, bifidobacterias e inulina, producido por Tonilait® en Suiza y el producto holándes Fysiq® que contiene Lactobacillus acidophilus. Raftiline®, es un prebiótico registrado como marca comercial (Martí del Moral et al., 2003, Marquina y Santos, 2003), es por ello que los FOS se consideran desde el punto de vista funcional como prebióticos. Los prebióticos se definieron en 1995 como ingredientes alimentarios no digeribles que afectan de manera beneficiosa al hospedador, estimulando el crecimiento o la actividad de una o varias bacterias del colon y, por tanto, contribuyen a la salud. Los prebióticos más que proporcionar bacterias exógenas como los probióticos, se dirigen a favorecer a las bacterias ya presentes en el colon como los Lactobacillus y Bifidobacterium (Rao, 2001).
En la Tabla I se presentan ejemplos de agentes prebióticos que cumplen dos criterios:
1) Deben escapar de la digestión de las hidrolasas provenientes de las secreciones pancreáticas e intestinales y, por tanto, se dice que son resistentes.
2) Son fermentados (selectivamente o no) por las bacterias sacarolíticas de la microflora colónica (Delzenne y Williams, 2002).
Tabla I. Selección de prebióticos añadidos o presentes en la dieta (Adaptado de Delzenne y Williams, 2002) Clase de compuestoEfecto sobre flora colónicaEfecto sobre AGCC/pHDosis del tratamiento FructanosBifidobacteria y LactobacilliSí4-40g/día (Inulina, oligofructosa)
Galacto-oligosacáridosBifidobacteria y LactobacilliSí3-10g/día (oligosacáridos de leche humana, dextranos, oligodextranos)
Xilo-oligosacáridosBifidobacteria y BofodobacteriaSí3-10g/día (rafinosa, estaquiosa)
Otros oligosacáridosBifidobacteria lentose desconoce (arabinoxilanos)
AGCC: ácidos grasos de cadena corta.
La utilización de prebióticos por las bacterias colónicas conlleva, en numerosos casos, a la producción de ácidos grasos de cadena corta (AGCC). Estos agentes poseen un gran impacto sobre el ambiente del intestino grueso, el metabolismo de macronutrientes y la prevención de enfermedades. Los SCFA se absorben rápidamente y pueden utilizarse como fuente de energía entre comidas. Contribuyen al pH de las heces e influyen de manera importante en la función colónica, de forma que pueden incluso disminuir el riesgo de cáncer (Martí del Moral et al., 2003).
Curiosamente, numerosos trabajos también apuntan la posibilidad de que los prebióticos puedan ejercer acciones fisiológicas a nivel sistémico, relacionadas con efectos sobre el metabolismo lipídico y diversos factores de riesgo de enfermedades cardiovasculares (Delzenne y Williams, 2002).
Algunos prebióticos parecen tener un efecto sobre la absorción de los triacilglicéridos, con consecuencias sobre los niveles hepáticos o séricos, los cuales van en función del modelo experimental. En ratas o hámsters alimentados con dietas ricas en hidratos de carbono, se observó una disminución de los triacilglicéridos hepáticos o séricos cuando fructanos tipo inulina, almidón de arroz resistente a la fermentación, almidón de papa o de maíz rico en amilosa y FOS, se añadieron a la dieta durante varias semanas (Delzenne y Kok, 2001).
En ratas alimentadas con una dieta rica en lípidos con un 10% de fructanos, también se observó una menor trigliceridemia sin cambio a nivel hepático, lo que sugiere un efecto periférico. En general, parece ser que la acción de los prebióticos sobre el contenido lipídico sérico, hepático o corporal no es única, sino que los efectos dependen de los estados nutricionales y fisiopatológicos (Williams y Jackson, 2002).
Debido a su proceso fermentativo, los FOS pueden afectar el epitelio intestinal favoreciendo el desarrollo de la mucosa y aumentando la resistencia a las enfermedades intestinales por un mecanismo de barrera. Por esta misma razón, el consumo de FOS reduce la no aparición de lesiones intestinales ulcerativas, siendo el tratamiento de corto tiempo basado en la ingesta de FOS y bifidobacterias, una de las mejores terapias para la inflamación asociada a la colitis ulcerativa activa (Cherbut, 2002).
Se atribuye a los FOS la capacidad de evitar el estreñimiento al permitir una mejor formación del bolo fecal y favorecer la movilidad intestinal. El consumo diario de 3 a 10 g de fructanos genera un efecto anticonstipante en períodos tan cortos como una semana, lo cual es atribuible a un incremento en la producción de ácidos grasos de cadena corta y a un aumento en la peristalsis producido por la alta población de bifidobacterias (Tokunaga, 2004).
Lee et al. (2004) reportan que la ingesta de inulina es de mucha utilidad en la reducción de los factores de riesgo asociados a la hiperglicemia en mujeres.
El consumo de FOS ha demostrado mejorar la absorción de minerales tales como el calcio, magnesio, zinc, hierro y cobre. La absorción de minerales generalmente se da en forma mayoritaria en el intestino delgado, aunque el intestino grueso puede también representar un sitio de absorción, gracias a la ayuda de los ácidos grasos de cadena corta derivados de la fermentación (Tokunaga, 2004).
Sin embargo, no existe evidencia experimental alguna que indique que los FOS presentan algún grado de toxicidad, sin importar la cantidad ingerida como parte de la dieta; aunque en algunas personas se ha detectado que ingestas por encima de los 10 g diarios pueden llegar a producir un ligero
malestar. Usualmente, la tolerancia a los FOS no aumenta si se expone al individuo a ingestas continuas prolongadas. Ingestas inusualmente altas de fructanos puros pueden causar diarrea debido a una retención osmótica de fluidos tanto en el intestino grueso como en el intestino delgado. Motivos como el anterior hacen que aún no se considere del todo seguros a los fructanos para su inclusión en alimentos dirigidos a infantes, durante los primeros meses de vida. La máxima dosis de FOS que no causa diarrea en humanos es 0.3 y 0.4 g/kg de peso corporal en hombres y mujeres, respectivamente (Sangeetha et al., 2005).
En algunas personas, la rápida fermentación de los fructanos provoca una alta concentración de hidrógeno a nivel estomacal, lo que promueve la peristalsis del colon, que desemboca en sintomatologías similares a la intolerancia a la lactosa tales como las defecaciones irregulares, flatulencia e irritabilidad abdominal (Olesten y GudmondHoyer, 2000).
3. Aplicaciones en la industria
Las principales aplicaciones de los FOS son en la industria de alimentos; éstos son utilizados como sustitutos no carcinogénicos e hipocalóricos de azúcares, generando productos de confitería, chocolatería y bebidas de aceptación sensorial en general admisible en comparación con los productos edulcorados de forma convencional (Golob et al., 2004).
En alimentos de contenido de humedad muy elevado, especialmente en helados y otros derivados lácteos, así como en embutidos, los fructanos hidrolizados en concentraciones de 40-45% adoptan una textura y palatabilidad muy similar a la de la grasa, por lo cual se les puede emplear como sustitutos de ésta (Cherbut, 2002).
A diferencia de otras fibras, los FOS no dejan sabores residuales y pueden agregarse a la formulación de un producto convencional sin que esto involucre un incremento en la viscosidad de la matriz, por lo cual su uso permite aumentar el contenido de fibra sin que éste sea evidente.
En yogurt, experimentos efectuados por Guven et al. (2005) señalan que la suplementación de leche descremada con 1% de fructanos es capaz de generar un producto con atributos sensoriales parecidos a un yogurt fabricado con leche entera, aunque adiciones ligeramente mayores incrementaron la separación del suero.
Entre otras aplicaciones industriales de los FOS puede mencionarse: su uso como ingredientes de mayonesas ligeras, quesos bajos en calorías, productos de pastelería y panificación, y embutidos, contribuyendo a la reducción del contenido calórico y a la retención de agua de estos productos; su adición a las formulaciones de helado para evitar la formación de cristales de hielo; su empleo como emulgentes en la fabricación de margarinas; su utilización en los productos de panificación como sustitutos de azúcar; y en general su uso para modificar la textura o cremosidad de algunos alimentos son algunas de sus aplicaciones en esta área de investigación (Olesten y Gudmond-Hoyer, 2000).
A pesar de que la producción mundial de FOS está alcanzando alrededor de los 27 millones de kilogramos, éstos son prácticamente desconocidos en Estados Unidos. Lo anterior se debe primordialmente a las restricciones de la FDA, al temor de incursionar en terrenos desconocidos de muchas compañías y al poco o nulo etiquetado nutricional en idioma inglés para los productos importados. Esto explica el hecho de que los fructanos no se consuman masivamente, a
pesar de sus reconocidas cualidades funcionales (Cherbut, 2002).
Referencias
A.A.C.C. American Association Of Cereal Chemists. 2001. The definition of dietary fiber. Cereals Food World. 46(3):112-129.
Conclusiones
Los FOS son hidratos de carbono, que debido a su resistencia enzimática presentan un bajo contenido calórico y una funcionalidad como fibra dietética, la cual ejerce un efecto prebiótico para microorganismos probióticos, es debido a esta relación prebiótico-probiótico que se genera una funcionalidad para el organismo, el efecto de la combinación prebióticos-probióticos se ha definido como simbiótico, debido a que los prebióticos pueden estimular el crecimiento de cepas específicas y por tanto contribuir a la mejora de la microflora bacteriana intestinal con efectos benéficos a la salud, es por ello que se consideran a los FOS una alternativa como ingrediente para elaborar productos funcionales.
Además una ventaja de los FOS es que son muy fáciles de encontrar sobre todo en las fuentes vegetales, esto hace que puedan ser considerados una alternativa en la producción de alimentos.
Los beneficios que otorgan los FOS y que se mencionaron a lo largo de este trabajo permiten concluir que son compuestos con un gran potencial nutritivo y además que pueden ser aprovechados para la generación de nuevos productos.
Chacón, V. A. 2006. Perspectivas agroindustriales actuales de los oligofructosacáridos (FOS). Agronomía Mesoamericana. 17(2):265-286.
Cherbut, C. 2002. Inulin and oligofructose in the dietary fiber concept. British Journal of Nutrition. 87(2):S159-S162.
Delzenne, N. M. y Kok, N. 2001. Effects of fructans type prebiotics on lipid metabolism. Journal Clinical Nutrition. 73(2 Suppl):456S-458S.
Delzenne, N. M. y Williams, C. M. 2002. Prebiotics and lipid metabolism. Curr Opin Lipidol. 13:61-67.
Flickinger, E. A. y Fahey, G. C. 2002. Pet food applications of inulin, oligofructose and other oligosaccharides. British Journal of Nutrition. 87(2):297-300.
Franck, A. 2006. Inulin. En: Stephen A. (Editor). Marcel Dakker. Food Polysaccharides and their Applications. Segunda Edición. New York, EE.UU: pp 733-746.
Golob, T., Micovic, E., Bertoncelj, J., y Jaminik, M. 2004. Sensory acceptability of chocolate with inulin. Acta Agriculturae Slovenica. 83(2):221-231.
Guven, M., Yasar, K., Karaca, O. B. y Hayaloglu, A. A. 2005. The effect of inulin as a fat replacer on the quality of set-type low-fat yogurt manufacture. International Journal of Dairy Technology. 58(3): 180-184.
Lee, E. Y., Kim, Y. Y., Jang, K. H., Kang, S. y Choue, R. 2004. The effect of inulin supplementation on blood lipid levels, and fecal excretion of bile acid and neutral sterol in Korean postmenopausal women. Korean Journal of Nutrition. 37(5):352363.
Agradecimientos
Se agradece al Consejo Nacional de Ciencia y Tecnología (CONACYT) y a la Universidad de las Américas Puebla (UDLAP) por el apoyo para la realización de este trabajo.
Madrigal, L. y Sangronis, E. 2007. La inulina y derivados como ingredientes claves en alimentos funcionales. Archivos Latinoamericanos de Nutrición. 57(4)387-389.
Marquina, D. y Santos, A. 2003. Probióticos, prebióticos y salud. Revista Actualidad. 32:24-27.
Martí del Moral, A., Moreno-Aliaga, Ma. J. y Martínez, H. A. 2003. Efecto de los prebióticos sobre el
metabolismo lipídico. Nutrición Hospitalaria. (4):181-188.
Niness, K. 1999. Breakfast foods and the health benefits of inulin and oligofructose. Cereal Foods World. 44(2):79-81.
Olesten, M. y Gudmond-Hoyer, E. 2000. Efficacy, safety and tolerability of oligofructosaccharides in the treatment of irritable bowel syndrome. American Journal of Clinical Nutrition. 72:1570-1575.
Perrin, S., Warchol, M., Grill, J. P. y Schneider, F. 2001. Fermentations of fructooligosaccharides and their components by Bifidobacterium infants ATCC 15697 on batch culture in semi synthetic medium. Journal of Applied Microbiology. 90(6):859-865.
Rao, V. A. 2001. The prebiotic properties of oligofructose at low intake levels. Nutrition Research. 21:843-848.
Roberfroid, M. B. 2001. Prebiotics: preferential substrates for specific germs. American Journal of Clinical Nutrition. 65(5):405-408.
Sangeetha, P. T., Ramesh, M. N. y Prapulla, S. G. 2005. Recent trends in the microbial production, analysis and application of fructooligosaccharides. Trends in Food Science & Technology. 16:442-457.
Tita, R. y Smeekens, S. 2003. Fructans: beneficial for plants and humans. Current Opinion in Plant Biology. 6(3): 223-230.
Tokunaga, T. 2004. Novel physiological function of fructooligosaccharides. BioFactors. 21(1/4):89-94.
Williams, C. M. y Jackson K. G. 2002. Inulin and oligofructose: effects on lipid metabolism from human studies. British Journal of Nutrition. 87(2 Suppl):261-264.

Temas Selectos de Ingeniería de Alimentos 4 – 1 (2010): 9 – 26

Pulsos eléctricos: fundamentos y aplicaciones en alimentos
T. G. Cerón-Carrillo*, E. Palou y A. López-Malo
Departamento de Ingeniería Química, Alimentos y Ambiental. Universidad de las Américas, Puebla. Sta. Catarina Mártir, Cholula, Puebla. 72810. México
Resumen
Durante mucho tiempo se ha buscado la seguridad microbiana de los alimentos junto con una conservación de sus propiedades. Sin embargo, la mayoría de las veces, la seguridad es acompañada con la pérdida de sus características nutricionales, de textura y sabor; es por esto que se recurre a tecnologías no térmicas como los pulsos eléctricos. El objetivo de este trabajo es dar a conocer los fundamentos y aplicaciones de los pulsos eléctricos en la industria alimentaria. Según diversos estudios, esta tecnología permite la inactivación de muchas especies de microorganismos por medio de la formación de poros en la membrana celular. De igual forma, se emplea para la extracción de diversos compuestos como antioxidantes, antimicrobianos y colorantes, permitiendo mayores rendimientos de éstos. Además permite una mejor transferencia de masa para la deshidratación de especies vegetales debido a la permeabilización de las células. Las características antes mencionadas permitirán que en el futuro pueda ser implementada a gran escala.
Palabras clave: pulsos eléctricos, campos eléctricos, intensidad de campo, electroporación.
Abstract
Industries have been looking for microbial safety of foods, preserving its original nutritional properties. However, many times microbial safety means lost of nutritional, flavor and textural loses. For these reasons, non-thermal technologies such as electric pulses are important. The aim of this work is to describe the fundamentals and applications of pulse electric field in the food industry. According to several researchers, this technology allows the inactivation of many species of microorganisms due to pore formation or electroporation. Futhermore it could be applied for the extraction of antioxidants, antimicrobials, and colorants enhancing yields. Permeabilization of the cellular membrane enhances mass transfer in the dehydratation of vegetables. These characteristics will allow that in the future, pulsed electrics fields be implemented in greater scale.
Keywords: pulsed electric fields, high intensity, field intensity, electroporation.
Introducción
Desde hace décadas se han estudiado diversas
*Programa de Doctorado en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: teresa.ceronco@udlap.mx
tecnologías para la conservación de alimentos, buscando siempre un fin común: la seguridad alimentaria y la conservación de las propiedades organolépticas de los mismos. Una alternativa es el uso de electricidad, con la que se han realizado estudios que permitieron
incorporarla como una de estas tecnologías. Algunos estudios señalan que el uso de pulsos eléctricos podía higienizar alimentos líquidos como la leche sin afectar en gran medida su sabor y propiedades.
Actualmente, los pulsos eléctricos son considerados como una tecnología emergente, el tratamiento se realiza colocando alimentos líquidos, semisólidos o sólidos en una solución electrolítica y con baja conductividad térmica entre dos electrodos, mediante los cuales se hace pasar una corriente eléctrica con determinados tiempo (generalmente microsegundos s), intensidad y frecuencia. Los pulsos eléctricos pueden ser aplicados por lotes o de forma continua, variando en esta última, la configuración de las cámaras de tratamiento y por lo tanto, la manera en la que los pulsos eléctricos son aplicados.
Esta tecnología ha sido ampliamente utilizada en la inactivación de mohos, levaduras y bacterias en diversos tipos de alimentos donde se ha comprobado que al cambiar alguna de las variables de tratamiento, se ve afectada la efectividad de éste. De la misma manera se han usado para la inactivación de enzimas que afectan la calidad de diferentes alimentos así como auxiliar en el proceso de deshidratación. Otro más de sus usos es siendo un auxiliar en el proceso de extracción ya que la aplicación de electricidad conlleva a la formación de poros en las células vegetales y por lo tanto el líquido intracelular sale más fácilmente de la célula. Sin embargo, esta aplicación no ha sido ampliamente estudiada.
Debido a que los pulsos eléctricos son una tecnología emergente y ya que la información sobre sus fundamentos y sus aplicaciones se encuentra dispersa, en este trabajo se dará a conocer de qué manera funcionan los pulsos eléctricos, cuáles son sus características y los sistemas utilizados actualmente, así como diversas aplicaciones en el área de alimentos.
Revisión bibliográfica
1. ¿Qué son los pulsos eléctricos?
Desde los años 60’s se ha estado investigando la tecnología de los pulsos eléctricos para el procesamiento de alimentos. El investigador pionero que trabajó en el desarrollo de esta tecnología fue Doevenspeck, quien generó una patente que describe a los equipos y métodos para el procesamiento de salchichas (Doevenspeck, 1960). Años después Zimmerman et al. (1976) promovieron la electroporación reversible, dicho concepto fue un aporte fundamental en la biología celular y de desarrollos terapéuticos que le siguieron. Por esto, la electroporación como método para la manipulación genética ha sido aceptada y desarrollada. Después, en los 1980 Hülsheger et al. (1983) publicaron una serie de trabajos sobre inactivación microbiana con pulsos eléctricos, lo que conllevó a incrementar el interés en esta área.
Los pulsos eléctricos son un tratamiento no térmico para la conservación de alimentos en el cual se coloca un alimento fluido, semifluido o sólido en una solución electrolítica entre dos electrodos por periodos cortos de tiempo (menos de un segundo) y se aplica un determinado número de pulsos de alto voltaje que van de 20 a 80 kV/cm para la inactivación de microorganismos, de 2.5 a 90 kV/cm para la inactivación de enzimas y de 0.5 a 1 kV/cm (Ho et al., 1997; Van Loey y Hendrickx., 2002) para la extracción de compuestos intracelulares (Fincan y Dejmek, 2002; Lebovka et al., 2002). El beneficio de esta tecnología para los consumidores consiste en brindarles alimentos con características similares a los frescos y con una vida útil extendida (Rastogi et al., 1999).
El tratamiento térmico es altamente efectivo en productos alimenticios para lograr una mejor estabilización, inactivación de enzimas y destrucción de microorganismos
pero que muchas veces resulta en pérdidas de los nutrientes esenciales y cambios en sus propiedades organolépticas; por esto, el tratamiento de pulsos eléctricos ha incrementado su popularidad pues provee una alternativa a los cambios indeseables generados por la pasteurización (Knorr et al., 2001; Barroso-Espach et al., 2003). Los pulsos eléctricos son utilizados en alimentos fluidos que pueden tolerar altas intensidades de campo, que tengan poca conductividad eléctrica y que no formen burbujas (IFT, 2001).
En los trabajos realizados por investigadores se observa que hay dos tipos de sistemas de pulsos eléctricos, los cuales difieren en las posiciones de los electrodos así como en la forma de las cámaras de tratamiento.
2. Sistemas de pulsos eléctricos empleados para el procesamiento de alimentos
El sistema de tratamiento de pulsos eléctricos incluye una fuente de potencia, condensadores, cámara de tratamiento, sistema de medición de voltaje, computadora para el control de condiciones como el voltaje, temperatura y tiempo de proceso (Fig.1).
Se han propuesto dos tipos de sistemas para el tratamiento de alimentos: el sistema por lotes o estático y el sistema de flujo continuo. A continuación se presentarán las principales características de éstos.
2.1 Sistema de tratamiento por lotes
Estos sistemas consisten principalmente de un generador de pulsos de alto voltaje y una cámara de tratamiento. Esta cámara de tratamiento consiste de dos electrodos colocados de forma paralela y separados, por un espacio, el cual contendrá el volumen de
Depósito de alimento
Generador de pulsos
Bomba de control
Ordenador
Cámara de tratamiento
Enfriamiento
Sensor de temperatura
Fig. 1. Diagrama general de sistema de pulsos eléctricos (Adaptado de Barbosa-Canovas et al. , 1999).
alimento a tratar. Los electrodos se encuentran separados por materiales aislantes como teflón o plexiglás. La configuración de la cámara y los electrodos debe de ser tal que se evite la ruptura de la matriz alimenticia. Esto también se puede lograr colocando electrodos con bordes redondeados, eliminando impurezas del alimento, así como el aire, y desarrollando un campo eléctrico uniforme en toda la cámara de tratamiento (Zhang et al., 1995). Los parámetros de tratamiento utilizados para este tipo de sistemas se encuentran entre estos rangos: voltaje de 2.5-43 kV, fuerza de campo eléctrico de 0.6-100 kV/cm, distancia de electrodos de 3-77 mm, tiempo de pulso de 1 s a 10 s, frecuencia de pulso de 0.2-50 Hz, número de pulsos aplicados de 1 a 120 y volumen de la muestra de 0.5 mL a 1.6 L (Ho y Mittal, 2000). Este tipo de sistemas se puede apreciar en la Fig. 2.
La cámara de tratamiento es la parte más importante de estos sistemas. Básicamente es utilizada para mantener al alimento dentro del sistema al momento de aplicar los pulsos, pero también es importante tomar en cuenta, al aplicar una determinada fuerza de pulso, el concepto denominado como rompimiento dieléctrico del alimento. Este rompimiento ocurre cuando se excede la fuerza de campo eléctrico del alimento, ocasionando daños al electrodo e incrementando la presión, lo cual lleva a que la cámara de tratamiento explote y se formen burbujas de gas (Sepulveda y Barbosa-Cánovas, 2005).
Se han propuesto tres configuraciones diferentes para las cámaras de tratamiento de flujo continuo: platos paralelos, coaxial y colinear (Dunn, 2001).
2.2.1 Cámara coaxial
Las cámaras tienen electrodos cilíndricos por dentro y por fuera, con el alimento fluyendo entre éstos, con un flujo eléctrico uniforme. En una cámara de diseño simple, la intensidad del campo eléctrico no es uniforme (Zhang et al., 1995). Este tipo de cámara se puede apreciar en la Fig. 3.
2.2 Sistema de tratamiento de flujo continuo
Consiste de cinco componentes: una fuente de poder de alto voltaje, un capacitor almacenador de energía, una cámara de tratamiento, una bomba para conducir el alimento a través de la cámara de tratamiento y un enfriador. Además de voltaje, corriente, sistemas para medir la temperatura y una computadora para controlar las operaciones.
Llenado
Alimento
Electrodos
Fig. 2. Cámara de tratamiento de sistema de pulsos eléctricos por lotes o estático (Adaptado de la FDA, 2000). Alimento
Electrodo
Electrodo
Fig. 3. Configuración coaxial de cámara de tratamiento para sistema continuo (Adaptado de Barbosa-Cánovas y Altunakar, 2006).
Este tipo de cámaras ofrecen un tratamiento uniforme al producto debido a que la geometría radial asegura que la fuerza de campo disminuya hacia el electrodo exterior. Generalmente presentan baja resistencia de carga cuando se utilizan para tratar a la mayoría de los alimentos y el sistema de pulsos debe de proporcionar corrientes altas en los voltajes empleados (Barbosa-Cánovas y Altunakar, 2006).
2.2.2 Cámara colinear
Se introdujo por primera vez por Yin et al (1997). Posee dos electrodos huecos separados por un aislante dentro del cual se encuentra un tubo por el que fluye el producto (Fig.4). En ésta se puede manejar una mayor resistencia de carga permitiendo operar con corrientes bajas (Dunn, 2001), además permite un amplio rango de conductividades.
Su diseño es apropiado para procesar alimentos particulados además de poder adaptarse a un sistema de tuberías de tamaño industrial; también puede ocasionar una falta de uniformidad y así una falta de procesamiento de una parte del material (Barbosa-Cánovas yAltunakar, 2006).
2.2.3 Cámara de platos paralelos
Este tipo de cámara de tratamiento contiene diversas zonas de electrodos, los cuales se
aíslan unos de otros por medio de material aislante, y además se separan del alimento líquido por medio de una membrana y una solución electrolítica. El fluido que pasa a través de esta cámara horizontal recibe el tratamiento determinado sólo en algunas zonas. Este tipo de sistema tiene un ahorro de energía limitado ya que los electrodos son alimentados continuamente con alto voltaje (Dunn, 2001).
Sato et al., (2001) describen una cámara vertical la cual tiene dos electrodos concéntricos, con el electrodo, proveedor del alto voltaje, en el interior. El producto es tratado por flujo en el espacio de 5 mm entre los electrodos. Para eliminar el aire de la muestra, la cámara es llenada de abajo hacia arriba y con una sola pasada. Además se cuenta con un espacio de tratamiento de 400 mm a pesar de que los electrodos tenían un diámetro de 500 mm. En esta cámara se experimentó con cerveza sin gas que contenía Saccharomyces. cerevisiae a una concentración de 106 ufc/mL. Después del tratamiento con un flujo de 80 mL/min se obtuvo una reducción de 2 ciclos logarítmicos además de que no se encontró diferencia en la calidad del producto tratado respecto al testigo. La construcción de este sistema es fácil, seguro de operar y el flujo es fácil de monitorear. Sin embargo, la baja efectividad en la disminución de la carga microbiana se debe a la existencia de regiones de campo con baja intensidad.
Fig.4. Configuraciónco-lineardecámarade tratamientoparasistemacontinuo(Adaptadode Barbosa-CánovasyAltunakar,2006).
En otro trabajo propuesto por Qin et al., (1994) se experimentó con una cámara en la cual, la muestra fluía a través de una serie de cámaras de tratamiento en forma de U. El espacio entre electrodos era de 0.51 ó 0.95 cm dando lugar a un volumen de 8 ó 20 mL. Se implementó la circulación de agua a través de los electrodos para enfriarlos. El flujo y la fuerza del campo eléctrico son más difíciles de monitorear debido a los canales en forma de U. Se reportó una disminución de 4 ciclos
Alimento Electrodo
Electrodo
logarítmicos en leche descremada con una carga inicial de 8 x 108 ufc/mL de Escherichia coli; para este trabajo se emplearon ondas cuadradas, 50 kV/cm de fuerza de campo, con pulsos de 2 s, con un espacio entre electrodos de 0.51 cm y 6 pulsos, la temperatura de proceso fue mantenida por debajo de 30 °C.
Además del tipo de sistema a utilizar, para que el proceso tenga efecto sobre lo que se desea obtener, es necesario establecer las condiciones óptimas tanto del sistema como del alimento. Es importante que se conozca qué factor (es) son determinante(s) durante el proceso para el adecuado procesamiento del alimento.
3. Factores de importancia en los pulsos eléctricos
Algunos de los factores que afectan la efectividad del tratamiento se encuentran relacionados con las condiciones que se requieren para lograr ya sea la inactivación microbiana, la inhibición enzimática, la extracción, entre otras. Estos factores se pueden agrupar en 1) factores técnicos, que están relacionados con el equipo y los parámetros de procesamiento, 2) factores biológicos, que se relacionan con los microorganismos, y 3) factores del medio o también relacionados con el tipo y la condición del medio a tratar (Álvarez et al., 2006). Todos estos factores se describen a continuación.
3.1 Factores técnicos
3.1.1 Intensidad del campo eléctrico
La intensidad de campo eléctrico es uno de los factores que afectan de manera importante a la inactivación de microorganismos y cuando se estudia éste en combinación con el tiempo de tratamiento, se observa un rompimiento de la membrana, además de que se debe alcanzar
una intensidad crítica del campo eléctrico para que haya algún efecto (Hülsheger et al., 1981). En trabajos de investigación se observa una reducción que va de 0.3 a 3.2 ciclos logarítmicos cuando se aumenta la fuerza de campo 5 kV, para Staphyloccus aureus en diferentes medios, por lo tanto se establece que a mayor intensidad de campo existirá una mayor reducción microbiana (Raso et al., 1999; Evrendilek et al., 2004; Sobrino-López y Martín-Belloso, 2006).
Dentro de las características de este factor se presenta un concepto llamado fuerza crítica de campo eléctrico y cuando se sobrepasa este valor, se incrementa la sensibilidad de la membrana de los microorganismos al incrementar la fuerza de campo; es por esto que se ha utilizado este valor junto con la forma y el tamaño de los microorganismos para clasificarlos de acuerdo a la resistencia que poseen a los pulsos eléctricos (Hülsheger et al., 1981, 1983; Castro et al., 1993). Sin embargo, este valor es variable cuando cambia el tiempo de tratamiento (Álvarez et al., 2006).
3.1.2 Forma de los pulsos
Otro factor reconocido como importante para la efectividad de este tratamiento es la forma de los pulsos. La forma de la onda se conoce como la suma de las funciones positivas y negativas separadas por su duración. Las formas de ondas eléctricas más utilizadas son la forma cuadrada y la de caída exponencial (Fig. 5 y 6) (Jeyamkondan et al., 1999).
Los pulsos de caída exponencial consisten en un voltaje unidireccional que asciende rápidamente a un valor máximo y desciende lentamente al cero. Los pulsos de forma cuadrada son más letales y más eficientes, energéticamente, que los pulsos de caída exponencial. Los pulsos oscilatorios son los menos eficientes ya que evitan que la célula esté en contacto continuo con el pulso eléctrico de alta intensidad y por lo tanto evita
que tenga daños irreversibles (Jeyamkondan et al., 1999).
Además existen los pulsos monopolares y bipolares (Fig. 5 y 6). Los pulsos bipolares están formados por un pulso positivo y uno negativo, y son más letales que los pulsos monopolares, ya que el tratamiento ocasiona
que las moléculas cargadas se muevan en la membrana celular del microorganismo y un cambio en la polaridad del campo eléctrico ocasiona un cambio en las moléculas cargadas lo que causa estrés y ocasiona ruptura de la membrana (Qin et al., 1994; Ho et al., 1995; Barbosa- Canovas et al., 1999).
Voltaje (kV/cm)
(/s)
(/s)
Fig.5. Formasdepulsoseléctricosusados:a)formadedisminuciónexponencialmonopolarb) formadecaídaexponencialbipolar(AdaptadodeBarbosa-CánovasyAltunakar,2006).
Voltaje (kV/cm)
Tiempo (/s)
Tiempo (/s)
Fig.6. Formadepulsoseléctricosusados:a)pulsoscuadradosmonopolaryb)pulsoscuadradosbipolar (AdaptadodeBarbosa-CánovasyAltunakar,2006).
Tiempo
Tiempo
En el estudio realizado por Evrendilkek y Zhang (2005) se reportó que los pulsos bipolares disminuyen en 1.88 unidades logarítmicas a E. coli, en leche descremada, en comparación con los pulsos monopolares que sólo producen 1.27 unidades logarítmicas de reducción.
Qin et al.(1994) comprobaron que los pulsos de forma cuadrada poseen mayor eficacia al observar una mayor disminución de carga microbiana al someter a S. cerevisiae a tratamiento con pulsos de forma cuadrada con una fuerza de 12 kV/cm y con pulsos de forma exponencial con un pico máximo en 60 J/pulso.
3.1.3 Número y longitud de pulsos
La duración del pulso (ancho del pulso) es el tiempo entre las funciones de dos pasos (el borde líder y el borde de arrastre). Algunos autores establecen que hay una relación entre la duración del pulso y la temperatura final del tratamiento ya que a mayor duración del pulso, la temperatura se incrementa y por lo tanto hay una mayor inactivación de los microorganismos como sucedió con Listeria monocytogenes en un estudio realizado por Álvarez y Jin (2003).
Así mismo se observa que existe una relación directamente proporcional entre el número de pulsos y la reducción microbiana, ya que se observó mayor disminución de la carga microbiana cuando se sometió a Staphyloccus aureus, contenido en jugo de naranja, a un tratamiento de 50 pulsos a 35 kV/cm que con 150 pulsos y con las mismas condiciones de tratamiento (Sobrino-López y Martín-Belloso, 2006).
En otro estudio realizado por Jeyamkondan et al. (1999), afirman que la frecuencia de los pulsos aplicada al alimento juega un papel importante en la conservación de éstos, ya que
a mayor cantidad de pulsos se genera un incremento de temperatura en el alimento.
3.1.4 Temperatura y tiempo de tratamiento
Otro de los factores que es importante considerar en esta tecnología, es la temperatura. El principal motivo al aplicar pulsos eléctricos es su característica como un proceso no térmico para minimizar daños al alimento y pérdida de nutrientes. Sin embargo, al trabajar con los pulsos eléctricos junto con temperaturas letales y no letales, se observa que tiene un efecto sinérgico al inactivar microorganismos (Jayaram et al., 1991; Zhang et al., 1994; Pothakamury et al., 1996; Liang et al., 2002). Una mayor temperatura incrementa el movimiento de las moléculas del disolvente tanto en la corteza como en el núcleo de la célula y así las moléculas migran de un electrodo a otro (Stanley, 1991).
El tiempo de tratamiento se define como el tiempo efectivo durante el cual los microorganismos son sometidos al campo de fuerza. Se expresa como el producto del número de pulsos y la duración de estos y junto con la fuerza de campo, son los factores que determinan el efecto letal del tratamiento (Jayaram et al., 1991; Barsotti y Cheftel, 1999). En el trabajo de Hamilton y Sale (1967) se comprobó que con un aumento en cualquiera de estas dos variables, hay un incremento en la disminución de la población microbiana.
3.2 Factores del medio
3.2.1 Conductividad eléctrica
La conductividad eléctrica se define como la característica que posee cada alimento y es la facilidad con la que los electrones pueden pasar a través de él. Los alimentos líquidos poseen especies iónicas que tiene carga eléctrica y éstas permiten conducir la electricidad. Un incremento en la
conductividad eléctrica causa un incremento en la energía administrada y por lo tanto en la temperatura durante el proceso (Rhulman et al., 2001).
De acuerdo al trabajo realizado por Barbosa-Cánovas et al., (1999), los alimentos con conductividades eléctricas grandes, generan picos de campos eléctricos menores en la cámara de tratamiento, lo que se traduce en una disminución de la fuerza de campo verdadera y por lo tanto se presenta menos inactivación; por esto cuando se trata un alimento con mayor conductividad se debe aumentar el voltaje para que se mantenga la fuerza deseada.
Jayaram et al., (1992) experimentaron con Lactobacillus brevis y demostraron que a mayor conductividad del alimento, la resistencia de la cámara de tratamiento se redujo, lo cual reduce el ancho del pulso y disminuye el rango de inactivación. También un incremento en la diferencia de conductividad entre el medio y el citoplasma microbiano debilita la membrana debido al incremento en el flujo de sustancias iónicas a través de ésta.
3.2.2 pH
El pH del medio tratado es un factor del cual se han realizado muchos estudios; algunos autores han observado que la inactivación de microorganismos está directamente relacionada con el pH ácido del medio (Wouters et al., 1999; Álvarez et al.,2002) y otros han comprobado la falta de dependencia entre el pH y el poder de inactivación de los pulsos eléctricos (Heinz y Knorr, 2001; Smith et al., 2002). Sin embargo, se asume que, cuando se presenta inactivación a pH ácido, cambia la capacidad de la célula para mantener su gradiente de pH transmembrana debido a la formación de poros.
Se ha visto influencia sobre la inactivación cuando se usa un pH ácido y al variar el tipo de microorganismo. En el estudio realizado por García et al. (2005) se observa mayor sensibilidad con pH ácido en bacterias Grampositivas debido a la pérdida de continuidad de la membrana y la posterior desestabilidad del pH tanto intra como extra-celular que afecta al resto de sus componentes. Por otra parte, las bacterias Gram-negativas son más resistentes ya que la composición de éstas actúa como una barrera.
3.2.3 Actividad de agua
Se ha reportado que al disminuir la actividad de agua del alimento aumenta la resistencia de los microorganismos, ya que el agua sale de la célula y se observa una reducción en el volumen de ésta (Álvarez et al., 2002).
También se cree que debido a la reducción de la aw, se disminuye la permeabilidad y la fluidez de la membrana (Neidhardt et al., 1990).
También se ha observado que la reducción de microorganismos se ve afectada por el componente adicionado para disminuir la aw En un estudio se observó que, al adicionar glicerol para obtener una actividad de agua de 0.93, se produjo una mayor sensibilidad por parte de los microorganismos en comparación con la adición de sacarosa para obtener la misma aw. Se estableció que ésta sensibilidad es debido a la capacidad que tiene el glicerol, por su bajo peso molecular, para pasar a través de la membrana por difusión pasiva (Álvarez et al., 2006).
3.2.4
Composición del medio
Ya que se han estudiado diversos medios de tratamientos con muchas composiciones y variando algunos factores, no se ha podido llegar a conclusiones específicas para cada componente alimenticio.
De igual forma, factores como la composición del alimento afectan a estos tratamientos y debido a ello, Grahl y Markl (1996) proponen que la grasa actúa como factor protector de los microorganismos al aplicar pulsos eléctricos, esto es debido a que cuanto más contenido de grasa tiene el alimento (leche), menor conductividad presenta éste. De igual forma, Picart et al., (2002) experimentaron con L. monocytogenes inoculada en leche con distintos contenidos de grasa y crema, y tratadas con pulsos eléctricos, y encontrando que el contenido de grasa muestra un efecto protector para L. monocytogenes. Sin embargo, otros autores observaron que no hay relación entre la sensibilidad de los microorganismos y la adición de grasa y proteína. Esto puede ser debido a que el experimento se llevó a cabo en soluciones buffer y no en alimentos (Reina et al., 1998; Pol et al., 2001).
3.3Factores biológicos
3.3.1 Tipo de célula
La inactivación de microorganismos por pulsos eléctricos se ha estudiado ampliamente, y se ha demostrado que hay diferentes grados de inactivación para bacterias, mohos y levaduras, siendo las esporas bacterianas las más resistentes (Raso et al., 1998; Aronsson y Rönner, 2001; Wouters et al., 2001). Dicha resistencia se debe a que la envoltura de la espora previene la permeabilización causada por el tratamiento ya que para que se inactive la germinación de la espora, el protoplasma debe de salir de la envoltura (Hamilton y Sale, 1967; Álvarez et al., 2006).
La efectividad de este proceso también depende de las características de los microorganismos. Se ha comprobado que las células eucariotas son más sensibles que las procariotas, además, en la fase de crecimiento, los microorganismos son más sensibles que en cualquiera de sus otras fases (Zhang et al.,
1994; Pothakamury et al., 1995; Pothakamury et al., 1996).
3.3.2 Tamaño y forma de la célula
Los microorganismos poseen diferente grado de resistencia; el cual se encuentra directamente relacionado con el tamaño y la forma de la célula. Lado y Yousef (2002) establecen que no sólo existe diferencia en la resistencia entre los diversos microorganismos si no que además, existe una diferencia entre cepas bacterianas.
Con el trabajo realizado por Zimmerman et al., (1974) se comprobó que entre más pequeña sea la célula, más resistencia posee debido a que se presenta un menor valor de potencial de membrana inducido por un campo externo.
También es considerada la orientación espacial de los microorganismos dentro del campo eléctrico al estudiar la eficiencia de este tratamiento como función de la forma de la célula (Heinz et al., 2001).
4. Los alimentos y los pulsos eléctricos
4.1 Inactivación de microorganismos
Los primeros experimentos con pulsos eléctricos en alimentos se realizaron en leche, jugos de frutas y huevo líquido para obtener mayor seguridad y por lo tanto, extender su vida de anaquel (Raso et al., 1998; Jin y Zhang, 1999; Evrendilek et al., 2004; Fernández-Molina et al., 2006; Evrendilek et al., 2009).
Se considera que los pulsos eléctricos afectan a la membrana citoplasmática, lo que lleva a la formación de poros, filtración de componentes celulares y muerte. Este efecto puede ser reversible o irreversible dependiendo de la intensidad del tratamiento. Se debe de sobrepasar el valor límite de fuerza
de campo para inducir un potencial transmembrana crítico de -1 V. Se requiere una fuerza de campo de 30 kV/cm para la mayoría de las bacterias en un medio líquido; tratamientos con pulsos eléctricos con mayor fuerza de campo, resultan en una reducción del ancho de membrana, la formación de poros y por último, una gran pérdida de viabilidad celular (Heinz, et al., 2002). En experimentos realizados por Simpson et al. (1999) y Wouters et al. (2001) se miden efectos irreversibles, resultado de los tratamientos por pulsos eléctricos sobre el punto crítico; se observa que estos tratamientos afectan severamente la integridad de la célula. Este efecto fue demostrado a través de mediciones de viabilidad celular, integridad de la membrana y gradiente celular de pH.
Diversos autores reportan que los microorganismos que son sometidos a tratamientos por pulsos eléctricos no vuelven a regenerar su membrana celular y por lo tanto no pueden causar daños en el alimento y al consumidor (Simpson et al., 1999; Russell et al., 2000; Ulmer et al., 2002). Un ejemplo de estos microorganismos es la E. coli, la cual se sometió a un tratamiento de pulsos con una frecuencia de 2 Hz y tiempo de 2 s (García et al., 2002).
Puig et al. (2007) comprobaron que con un mayor tratamiento e intensidad de campo se observa una disminución de 2 a 4 ciclos logarítmicos para diferentes microorganismos, cuando se somete mosto inoculado a un tratamiento de pulsos eléctricos con una fuerza de 35 kV/cm, durante un tiempo de 5 s y 300 Hz de frecuencia.
En otro trabajo realizado por Zhang et al., (1994) comprobaron la reducción de 4 ciclos logarítmicos de S. cerevisiae inoculado en jugo de manzana en un sistema por lotes de pulsos eléctricos con un volumen de 25.7 mL, cuando se aplicaron 20 pulsos de onda
cuadrada de 260 J/pulso. De la misma manera Qin et al., (1995) reportaron una disminución de 6 ciclos logarítmicos de S. cerevisiae en jugo de manzana bajo las siguientes condiciones: campo de 45 kV/cm, ancho de pulso 2.5 s, frecuencia de pulso 1 Hz, y espacio entre electrodos de 0.6 cm. La temperatura se mantuvo a 30 °C.
Jeantet et al. (1999) lograron disminuir el crecimiento de Salmonella por 3.0 ciclos logarítmicos cuando se sometió a tratamiento con pulsos eléctricos con 35 kV/cm y con 8 pulsos de disminución exponencial durante 9 ms y con una frecuencia de 900 Hz en un sistema de flujo continuo.
Raso et al. (1998) comprobaron que existe una disminución de menos de 1 ciclo logarítmico cuando se aplicó un tratamiento de pulsos eléctricos que consistió de 2 pulsos con una fuerza de 30 kV/cm a jugo de tomate inoculado con conidiosporas de Byssochlamys fulva, y manteniendo la temperatura por debajo de 23 °C.
4.2 Extracción
Desde épocas antiguas se ha aplicado la extracción de especies vegetales para obtener de manera pura los compuestos responsables de sus propiedades curativas o nutritivas. Para mejorar el proceso de extracción se han utilizado tratamientos que permiten un mayor rendimiento de estos compuestos. Entre estos tratamientos se encuentran el flujo turbulento del disolvente, tratamiento ultrasónico, entre otros (Kondrat’eva et al., 1991). Sin embargo, en experimentos como el de Belaya et al., (2006) se demuestran que al utilizar a los pulsos eléctricos como parte del proceso de extracción de antioxidantes de la manzana, se obtiene una mayor cantidad de compuestos fenólicos, reduciendo el tiempo de proceso y la temperatura de éste.
La extracción sólido-líquido es una operación unitaria utilizada para obtener componentes alimenticios como azúcares, aceites, antioxidantes, etc. (Bazhal y Vorobiev, 2000). La cantidad de componentes extraídos con el disolvente depende de la cantidad de células dañadas, lo cual a su vez afecta el rendimiento de la extracción. Es por esto que se requieren de otras técnicas como pretratamientos para la desintegración de las células. Sin embargo, es muy importante que no se afecte la calidad del compuesto a extraer con altas temperaturas o con disolventes con los cuales reaccione de manera indeseable, es por esto que se han estudiado, aunque no de manera amplia, a los pulsos eléctricos como pre-tratamiento para extracción.
Por medio del trabajo de algunos autores, se conoce que se incrementa el rendimiento de la extracción de compuestos a partir de manzanas, zanahorias y cocos cuando son sometidos a pulsos eléctricos como tratamiento previo al proceso de extracción (Bazhal y Vorobiev, 2000; Bazhal et al., 2001; Knorr, 2003; Fincan et al., 2004).
En el estudio realizado por López et al. (2007) se comprobó que la extracción de betanina por medio de pulsos eléctricos (5 pulsos de 2 s con un campo de 7 kV/cm), produce un rendimiento del 90%, lo que significó un rendimiento cinco veces mayor que sin este pre-tratamiento.
La aplicación de los pulsos eléctricos también puede tener lugar en la manufactura de vinos. En estudios realizados por López et al., (2008) se observó una mejora en la extracción de compuestos fenólicos provenientes de las uvas. Por lo tanto, este tratamiento permite la realización de vinos con altos contenidos de compuestos fenólicos, los cuales tienen propiedades antioxidantes. La mejora en el rendimiento se debió a un incremento en la fuerza de campo eléctrico de 2 a 7 KV/cm.
Fincan y Dejmek (2003) estudiaron el efecto de los pulsos eléctricos sobre betabel para la extracción de pigmento rojo. Las condiciones bajo las cuales se extrajo el 90% del pigmento fueron con 270 pulsos rectangulares en 10 s a 1 kV/cm, con esto comprobaron que aumenta el rendimiento cuando se somete a un pre-tratamiento de pulsos eléctricos.
4.3 Otras aplicaciones
4.3.1 Deshidratación
Por mucho tiempo se ha buscado deshidratar frutas y hortalizas para extender su vida de anaquel y conservarla; esto, debido a que se previenen cambios bioquímicos y por lo tanto la contaminación del vegetal. La manera clásica de lograr la deshidratación de alimentos ha sido por calor; sin embargo el gasto energético de este proceso, puede ser importante (Bouzrara y Vorobiev, 2000). Por lo tanto, se busca reducir el tiempo de proceso implementando pre-tratamientos como el molido, blanqueado, aplicando altas presiones o pulsos eléctricos (Rastogi et al., 1999; Bouzrara y Vorobiev, 2000; Lebovka et al., 2007). Los pulsos eléctricos pueden ser utilizados como pre-tratamiento para la deshidratación ya que se mejora la transferencia de masa debido a un incremento en la permeabilidad de las células. El grado de electroporación y desintegración celular depende de diversos factores como tipo de alimento, intensidad del campo eléctrico, tipo de la onda, tiempo de tratamiento y número de pulsos (Rastogi, 2003).
Se han hecho varios estudios enfocados a la aplicación de esta tecnología para la deshidratación de especies vegetales, como es el caso de Gachovska et al., (2008) en el cual estudiaron la deshidratación de zanahorias y observaron que el tiempo de deshidratación (hasta alcanzar una cantidad aceptable de
humedad) disminuyó de manera significativa (p<0.05) cuando fueron pre-tratadas con pulsos eléctricos. Kehinde et al. (2003) reportaron una pérdida de agua del 14-60% para mitades de fresa pre-tratadas con pulsos eléctricos. También observaron que las fresas pre-tratadas mantienen sus propiedades de textura.
De la misma manera, Angersbach et al (1997) reportaron una mejora en la transferencia de masa y en la deshidratación cuando se trató papa. Ade-Omowaye et al. (2003), encontraron que existe pérdida de agua de hasta 50% del total encontrado en pimiento dulce debido a un tratamiento combinado de pulsos eléctricos y la adición de componentes osmóticos como sucrosa, en comparación con tratamientos tradicionales de deshidratación osmótica con un total de hasta 30% de pérdida de agua.
4.3.2 Inactivación de enzimas
Otro de los usos que se les puede dar a los pulsos eléctricos es la inactivación de enzimas responsables de daños en alimentos. Muchas de éstas, son sensibles a altas temperaturas sin embargo, muchas otras como las lipasas producidas por el género Pseudomonas, son resistentes. Es por esto que se recomienda el uso de tratamientos no térmicos para su inactivación (Calderón-Miranda et al., 1999; Bendicho et al., 1999).
En el trabajo realizado por Bendicho et al., (2002) se estudió el efecto de los pulsos eléctricos sobre la actividad de lipasa proveniente de Pseudomonas fluorescens en sistemas continuos y por lotes. En el sistema por lotes, comprobaron que la lipasa reduce su actividad en aproximadamente 60% con un tratamiento de 80 pulsos a 27.4 kV/cm. De la misma manera observaron en el sistema continuo, una reducción de la actividad de 13% con 80 pulsos a 37.3 kV/cm y con una frecuencia de 3.5 Hz. Algunos de los trabajos
realizados en leche fueron los realizados por Vega-Mercado et al., (1995) en los cuales estudiaron la inactivación de proteasa hasta en un 60%, y de hasta un 90% de plasmina y fosfatasa alcalina después del tratamiento con pulsos eléctricos de alta intensidad. Ho et al., (1997) observaron una disminución del 85% y 30% para lipasa y peroxidasa respectivamente. Sin embargo, en el mismo trabajo se observó un incremento en la actividad de la pepsina y lisozima.
Conclusiones
Los pulsos eléctricos pueden ser tratamientos no térmicos muy efectivos y como optimizadores de energía. Esta tecnología es muy versátil ya que puede aplicarse en procesos como extracción, deshidratación, inactivación de enzimas e inactivación de microorganismos.
En cuanto a la inactivación de microorganismos, se deben de realizar más estudios con más alimentos ya que muchos de éstos fueron conducidos en medios de cultivo, y en alimentos. Se deben de estandarizar las condiciones del proceso que se aplica, así como el equipo utilizado, ya que mientras algunos investigadores utilizan equipo comercial, otros utilizan equipo no comercial en el cual muchos factores no se encuentran estandarizados.
Tomando en consideración lo reportado en esta revisión, hay un gran campo de acción para la aplicación de los pulsos eléctricos y su combinación con otros tratamientos; así como su aplicación en gran cantidad de alimentos.
Se debería de considerar la aplicación de esta tecnología a nivel industrial, ya que permite mayor calidad en los productos a los cuales se les aplica este tratamiento así como que conserva sus propiedades nutricionales.
Agradecimientos
T.G. Cerón-Carrillo agradece al Consejo Nacional de Ciencia y Tecnología (CONACyT) y a la Universidad de las Américas Puebla por el apoyo económico otorgado para sus estudios de posgrado.
Referencias
Ade-Omowaye, B. I. O: Rastogi, N .K., Angerbasch, A., Knorr, D. 2003. Osmotic dehydration behavior of red paprika. Journal of Food Sciencie. 67(5): 17901796. Citado en: Puértolas, E., López, N., Saldaña, G., Álvarez, I., y Raso, J. 2010. Evaluation of phenolic extraction during fermentation of red grapes treated by a continuos pulsed electric fields process at pilot-plant scale. Journal of Food Engineering. 98:120-125.
Álvarez, I., Pagán, R., Raso, J., y Condón, S. 2002. Environmental factors affecting the inactivation of Listeria monocytogenes by pulsed electric fields. Letters of Applied Microbiology 35: 489-493.
Álvarez, V. B., y Ji, T. 2003. Emerging technologies and processing and preservation technologies for milk and dairy products. En: G.F. Gutierrez-López y G.V. Barbosa-Cánovas (Eds). Food science and food technology. CRC Press. Boca Raton, FL. pp:313327.
Álvarez, I., Condón, S., y Raso, J. 2006. Microbial inactivation by pulsed electric fields. En: J. Raso y V. Heinz (Eds). Pulsed electric Fields technology for the food industry. Springer Science and Business Media. Nueva York, NY, EUA. pp: 97-129.
Angerbasch, A., Heinz, V., Knorr, D. 1997. Elektrische Leitfahigkeit al Mab des ZellaufschluBgrades von zellularen materialien durchverarbeitungsprozesse.Lebensmittelverfahrenst echnik. 42: 195-200. Citado en: Gachovska, T.K., Adedeji, A.A., Ngadi, M., y Raghavan, G.V.S. 2008. Drying Characteristics of pulsed electric fieldtreated carrot. Drying Technology. 26: 1244- 1250.
Aronsson, K., y Ronner, U. 2001. Influence of pH, water activity and temperature on the inactivation of Escherichia coli and Saccharomyces cerevisiae by pulsed electric fields. International of Food Science of Technology. 2: 105-112.
Barbosa-Cánovas, G. V., Gongora-Nieto, M. M., Pothakamury, U. R., y Swanson, B. G. 1999. Preservation of foods with pulsed electric fields. Academic Press Ltd. London. EE UU. 654 p.
Barbosa-Cánovas, G. V. y Altunakar, B. 2006. Pulsed electric fields processing of foods: An overview. En: J. Raso y V. Heinz (Eds). Pulsed electric fields technology for the food industry. Nueva York, NY. EUA. pp:3-21.
Barroso-Espach, A., Barbosa-Canóvas, G. V., y MartínBelloso, O. 2003. Microbial and enzymatic changes in fruit juice induced by high-intensity pulsed electric field. Food Reviews International. 19(3):253-273.
Barsotti, L., Cheftel, J. C. 1999. Food processing by pulsed electric fields: 2. Biological aspects. Food Reviews International. 152(2):181-213.
Bazhal, M., y Vorobiev, E. 2000. Electrical treatment of apple cossetttes for intensifying juice pressing. Journal of Science of Food and Agriculture. 80: 1668-1674. Citado en: Lebovka, N., Praporscic, I., Ghnimi, S., y Vorobiev, E. 2005. Temperature enhanced electroporation under the pulsed electric field treatment of food tissue. Journal of Food Engineering. 60:177-184.
Bazhal, M. I.., Lebovka, N. I., y Vorobiev, E. 2001. Pulsed electric field treatment of Apple tissue during compression for juice extraction. Journal of Food Engineering 50: 129-139.
Bazhal, M. I., Lebovka, N., Vorobiev, E. 2003. Optimization of pulsed electric field strength for the electroplasmolysis of vegetable tissues. Biosystems Engineering. 86(3), 339-345.
Bendicho, S., Espachs, A., Stevens, D., Arantegui, J., y Martín, O. 1999. Effect of high intensity pulsed electric fields on vitamins of milk. European Conference of Emerging Food Science and Technology. Tampere, Finland. Pp: 108. Citado en: Bendicho, S., Estela, C., Giner, J., BarbosaCánovas, G.V., y Martin, O. 2002. Effects of high intensity pulsed electric field and thermal treatments on a lipase from Pseudomonas fluorescens. Journal of Dairy Science 85: 19-27.
Bendicho, S., Espachs, A., Arantegui, J y Martín, O. 2002. Effect of high intensity pulsed electric fields and heat treatments on vitamins of milk. Journal of Dairy Research 69: 113-123.
Belaya, N. I., Filippenko, T. A., Belyi, A. V., Gribova, N.Y. 2006. Electric field asssited extraction of
antioxidant from bearberry leaves. Pharmaceutical Chemistry Journal. 40(9): 504-506.
Bouzrara, H. y Vorobiev, E. 2000. Beet juice extraction by pressing and electric fields. International Sugar Journal. 102(1216): 195-200.
Calderón-Miranda, M. L., Barbosa-Cánovas, G. V., y Swanson, B. G. 1999. Inactivation of Listeria innocua in liquid whole egg by pulsed electric field and nisin. International Journal of Food Microbiology 51: 7-17.
Castro, A.J., Barbosa-Cánovas, G. V., y Swanson, B. G. 1993. Microbial inactivation of foods by pulsed electric fields. Journal of Food Process and Preservation. 17: 47-73.
Doevenspeck, H. 1960. Verfahren und vorrichtung zur gewinnung der einzelnen phasen nus dispersen systemen. Patente alemana1.237.541. Citado en: G. V. Barbosa-Cánovas y Q. H. Zhang (Eds). Pulsed electric fields in food processing. Technomic publication. Lancaster, Pennsylvania.pp: 1-5.
Dunn, J., 2001. Pulsed electric field processing: An overview. En: G. V. Barbosa-Cánovas y Q. H. Zhang (Eds). Pulsed electric fields in food processing, fundamental aspects and applications. Technomic Press. Lancaster, PA. Pp: 1-30.
Evrendilek, G., Zhang, Q. H., y Richter, E. 2004. Application of pulsed electric fields to skim milk innoculated with Staphylococcus aureus.Biosytems Engineering. 87: 137-144.
Evrendilek, J., Zhang, Q. H. 2005. Effects of pulse polarity and pulse delaying time on pulsed electric fields-induced pasteurization of Escherichia coli O157:H7. Journal of Food Engineering. 68: 271276.
Evrendilek G. A., Tok F. M, Soylu E. M., y Soylu S. 2009. Effect of pulsed electric field on germination tube elongation and spore germination of Botrytis cinerea inoculated into sour cherry juice apricot and peach nectar. Italian Journal of Food Science. 2(21):171-182.
Fernández-Molina, J. J., Bermudez-Aguirre, D., Altunakar B., Swanson, B.G., y Barbosa-Cánovas, G.V. 2006. Inactivation of Listeria innocua and Pseudomonas fluoresvcens by pulsed electric fields in skim milk. Energy requoirements. Journal of Food Enineering. 29: 561.
Fincan, M., y Dejmek, P. 2002. In situ visualization of the effect of a pulsed electric field on plant tissue. Journal of Food Engineering. 55: 223-230.
Fincan, M., y Dejmek, P. 2003. Effect of osmotic pretreatment and pulsed electric field on the viscoelastic properties of potatoe tissue. Journal of Food Engineering. 59: 169-175. Citado en: Lebovka, N., Praporscic, I., Ghnimi, S., y Vorobiev, E. 2005. Temperature enhanced electroporation under the pulsed electric field treatment of food tissue. Journal of Food Engineering. 60:177-184.
Fincan, M., DeVito, F., Dejmek, P.2004. Pulsed electric Field treatment for solid-liquid extraction of red beetroot pigment. Journal of of Food Engineering 64: 381-388.
Gachovska, T. K., Adedeji, A.A., Ngadi, M., y Raghavan, G.V.S. 2008. Drying Characteristics of pulsed electric field- treated carrot. Drying Technology. 26: 1244- 1250.
García, D., Gómez, S., Cóndon, J., Raso, J. y Pagán, R. 2002. Pulse electric field cause sublethal injury in Escherichia coli Letters in Appied Microbiology 36:140-144.
García, D., Gómez, N., Mañas, P., Condón, S., Raso, J., y Pagán, R. 2005. Ocurrence of sublethal injury after pulsed electric fields depending on the microorganisms, the treatment medium pH and the intensity of the treatment investigated. Journal of Applied Microbiology. 99:94-104.
Grahl, T., y Markl, H. 1996. Killing of microorganisms by pulsed electric field. Applied Microbiology and Biotechnology. 45: 148-57.
Hamilton, W. A. y Sale, A.J. H.1967. Effects of high electric field in microorganisms II. Mechanism of action of the lethal effect. Biochim Biophys Acta.789-800.
Heinz, V. y Knorr, D. 2001. Development of nonthermal methods for microbial control. En: S.S. Block (Ed). Desinfection, sterilization and preservation. Lippincott Williams & Wilkins. Philadelphia E.U. pp. 853-877.
Heinz, V., Álavarez, I., Angerbasch, A., y Knorr, D. 2001. Preservation of liquid foods by high intensity pulsed electric fields-basic concepts for process design. Trends of Food Science and Technology. 12:103-111.
Heinz, V., Álvarez, I., Angerbasch, A., y Knorr, D. 2002. Preservation of liquid foods by high intensity pulsed electric fields: basic concepts for process design. Trends of Food Science. 12:103-111.
Ho, S., Mittal, G. S., Cross, J. D. y Griffiths, M. W. 1995. Inactivation of Pseudomomas fluorescens by
high voltage electric pulses. Journal of Food Science. 60: 1337-1340.
Ho, S. Y., Mittal, G. S., y Cross, J. D., 1997. Effects of high field electric pulses on the activity of selected enzymes. Journal of Food Engineering. 31(1):6984.
Ho S y Mittal G. J. 2000. High voltage pulsed electrical field for liquid food pasteurization. Food Reviews International. 16(4):395-434.
Hülsheger, H., Pottel, J., y Niemann, E. G. 1981. Killing of bacteria with electric pulses of high field strength. Radiation and Environmental Biophysics. 20:53-65.
Hülsheger, H., Potel, J., y Niemann, E. G. 1983. Electric field effects on bacteria and yeast cells. Radiation and Environmental Biophysics. 22, 149162.
Institute of Food Technologists (IFT). 2001. Effect of preservation technologies and microbial inactivation in foods. En: Comprehensive Reviews in Food Science and Food Safety. Vol. 2. En: www.ift.org. Accesado 10/02/10.
Jayaram, S.H., Castle, G. S. P., y Margaritis, A. 1991. Effects of high electric field pulses on Lactobacillus brevis at elevated temperatures. IEEE Industry Applications Society. Meet. 5:674-681.
Jayaram, S., Castle, G. S. P., y Margaritis, A. 1992. Kinetics of sterilization of Lactobacillus brevis cells by the application of high voltage pulses. Biotechnology and Bioengineering. 40(11):14121420.
Jeantet, R., Baron, F., Nau, F., Roignant, M., y Brulé, G. 1999. High intensity pulsed electric fields applied to egg white: effect on Salmonella enteritidis inactivation and protein denaturation. Journal of Food Protection. 62: 1381-1386.
Jeyamkondan, S., Jayas, D. S. y Holley, R. A. 1999. Pulsed electric field processing of food. Journal of Food Protection. 62: 1088-1096.
Jin, Z. T., y Zhang, Q. H. 1999. Pulsed electric field inactivation of microorganisms and preservation of quality of cranberry juice. Journal of Food Processing and Preservation. 23:481.
Kehinde, A., Taiwo, M. Estiaghi, B, Ade-Omowaye, O, Knorr, D. 2003. Osmotic dehydration of strawberry halves: influence of osmotic agents and pretreatment methods on mass transfer and products
characteristics. International Journal of Food Science and Technology. 38: 693- 707.
Kondrat’eva, L. A., Ivanova, L. A., Zelikson, I. 1991. Technology of ready to use medicinal forms. Drug Technology. 2: 250-400.
Knorr, D. 2003. Impact of non-thermal processing on plant metabolites. Journal of Food Engineering. 56: 113-134. Citado en: López, N., Puértolas, E., Condón, S., Raso, J., y Álvarez, I. 2009. Enhancement of the extraction of betanine from red beetroot by pulsed electric fields. Journal of Food Engineering. 90:60-66.
Knorr, D., Angersbach, A., Eshtiaghi, M. N., Heinz, V., y Lee, D. U. 2001. Processing concepts based on high intensity electric pulses. Trends of Food Science and Technology. 12: 129-135.
Lado, B. H., y Yousef, A. E. 2002. Alternative food preservation technologies: Efficacy and mechanism. Microbes and Infection. 4: 433-440.
Lebovka., N. I., Shynkaryk, N. V.., Vorobiev, E. 2007. Pulsed electric field enhanced drying of potato tissue. Journal of Food Engineering. 78(2): 606613.
Lebovka, N. I., Bazhal, M. I., y Vorobiev, E. 2002. Estimation of characteristic damage time of food materials in pulsed electric fields. Journal of Food Engineering. 54:337-346.
Liang, Z., Mittal, G. S., y Griffiths, M. W. 2002. Inactivation of Salmonella typhimurium in orange juice containing antimicrobial agents by pulsed electric fields. Journal of Food Protection. 65: 1081-1087.
López N., Puértolas, E., Álvarez, I., y Raso, J. 2007. Effects of pulsed electric fields on the extraction of phenolics compounds during the fermentation of must of Tempranillo grapas. Innovative Food Science and Emerging Technologies. Doi: 10.1016/j.ifset.2007.11.001. Citado en: López, N., Puértolas, E., Condón, S., Raso, J., y Álvarez, I. 2009. Enhancement of the extraction of betanine from red beetroot by pulsed electric fields. Journal of Food Engineering. 90:60-66.
Lopez, N., Puertolas, E., Copndón, S., Alvarez, I., Raso, J. 2008. Application of pulsed electric fields for improving the maceration procfess during vinification of red wine: influence of grape variety. European Food Research and Technology. 227(4): 1099-1107.
Neidhardt, F. C., Ingraham, J. L., y Schaechter, M. 1990. The efects of temperature, pressure, and pH. En: Physiology of the bacterial cell. A Molecular Approach. Sinauer Associated. Sunderland, MA. pp: 226-246.
Picart, L., Dumay, E., y Cheftel, J. C. 2002. Inactivation of Listeria innocua in dairy fluids by pulsed electric fields: influence of electric parameters and food composition. Innovation of Food Science and Emerging Technology. 3: 357- 369.
Pothakamury, U. R., Monsalve-González, A., BarbosaCámovas, G. V., Swanson, B. G. 1995. Inactivation of Escherichia coli and Staphylococcus aureus in model foods by pulsed electric field technology. Food Research. International. 28: 167-171.
Pothakamury, U. R., Vega, H., Zhang, Q., BarbosaCánovas, G. V., y Swanson, B. G.1996. Effect of growth stage and processing temperature on the inactivation of Escherichia coli by pulsed electric fields. Journal of Food Protection. 59(11): 11671171.
Pol, I. E., Mastwijk, H. C., Slump, R. A., Popa, M. E., y Smid, E. J. 2001. Influence of food matrix on inactivation of Bacillus cereus by combination of nisin, pulsed electric treatment and carvacol. Journal of Food Protection. 64: 1012-1018.
Puig, A., Marselles, R., Olmos, P., Martín, O y Minguez, S. 2007. Inactivación de la población microbiana de los mostos mediante tratamiento por pulsos eléctricos de alta intensidad de campo. International Symposium: Microsafetywine. 21 y 22 de noviembre. Villafranca del Pénedes, España.
Qin, B., Chang, F., Barbosa-Cánovas, G. V., y Swanson, B.G. 1994. Non-thermal inactivation of Saccharomyces cerevisiae in Apple juice using pulsed electric fields. Journal of Food Science and. Technology. 28: 564.
Qin, B. L., Zhang, Q., Barbosa-Cánovas, G. V., Swanson, B., y Pedrow, P. D. 1995. Pulsed electric field treatment chamber design for liquid food pasteurization using finite element method. Transactions of the ASAE. 38(2): 557-565.
Raso J., Calderón-Miranda L., Góngora, M., BarbosaCánovas, G. V y Swanson, B. G. 1998. Inactivation of mold ascospores and conidiopspores suspended in fruit juices by pulsed electric fields. Lebens Wiss und Technol. 31: 668.
Raso, J., Góngora-Nieto, M. M., Calderón –Miranda, M.L., Barbosa-Cánovas, G. V. y Swanson, B. G. 1999. Resistant microorganisms to high intensity
pulsed electric field pasteurization of raw milk. En IFT Annual Meeting. Institute of Food Technologists. Atlanta Georgia. En http://ift.confex.com/ift/98annual/techprogram/acce pted/550.htm. Accesada 10/02/2010.
Rastogi, N. K. 2003. Application of high-intensity pulsed electrical fields in food processing. Food Reviews International. 19(3):229-251.
Rastogi, N. K., Eshtiaghi M.N., y Knorr D. 1999. Accelerated mass transfer during osmotic dehydration of high intensity electrical field pulsed pretreated carrots. Journal of Food Science. 64(6):1020-1023.
Reina, L. D., Jin, Z. T., Zhang, Q. H., y Yousef, A. E. 1998. Inactivation of Listeria monocytogenes in milk by pulsed electric field. J. Food Prot. 61: 12031206.
Ruhlman, K. T., Jin, Z. T., y Zhang, Q. H. 2001. Physical properties of liquid foods for pulsed electric field treatment. En: G. V. Barbosa-Cánovas y Q .H. Zhang (Eds). Pulsed electric fields in food processing. Technomic Publishing Company, Inc. Lancaster, EUA. pp: 45-56.
Russell, N. J., Colley, M., Simpson, R. K., Trivett, A. J. y Evans, R.I. 2000. Mechanism of action of pulsed high electric field on the membranes of foodpoisoning bacteria is an “all or nothing” effect. International Journal of Food Microbiology.55: 133-136.
Sato, M., Ishida, N., Sugiarto, A., Oshima, T., y Taniguchi, H. 2001. High efficiency sterilizer by high voltaje pulse using concentrated-field electrode system. IEEE Transactions of Industry Applications 37(6): 1646-1650. Citado en: Barbosa-Cánovas, G.V. y Altunakar, B. 2006. Pulsed electric fields processing of foods: An overview. En: J. Raso y V. Heinz (Eds). Pulsed electric fields technology for the food industry. Nueva York, NY. EUA. p:3-21.
Sepulveda, D., y Barbosa-Cánovas, G. V. 2005. Present status and the future of PEF technology. En: G.V. Barbosa-Cánovas, M.S. Tapia, y M.P. Cano (Eds). Novel Food Process Technologies. CRC Press, Boca Ratón, Fl. pp.1-45.
Simpson, R. K., Whittington, R., Earnshaw, R. G. y Russel, N. J. 1999. Pulsed high electric field causes “all or nothing” membrane damage in Listeria monocytogenes and Salmonella typhimurium, but membrane H-ATPase is not a primary target. International Journal of Food Microbiology. 48: 110.
Smith, K., Mittal, G. S., y Griffiths, M. W. 2002. Pasteurization of milk using pulsed electrical field and antimicrobials. Journal of Food Science. 67: 2304-2308.
Sobrino-López, A., y Martín-Belloso, O. 2006. Enhancing inactivation of Staphylococcus aureus in skim milk by combining high intensity pulsed electric fields and nisin. Journaol of Food Protection. 69: 345-353.
Stanley, D. W. 1991. Biological membrane deteoration and associated quality losses in food tissues. Critical Reviews of Food Science. 30: 487-553.
Ulmer, H. M., Herberhold, H., Fahsel, S., Ganzle, M. G., Winter, R. y Vogel, R. F. 2002. Effects of Pressure induced membrane phase transitions on inavctivation of HorA, and ATP-dependent multidrug resistance transporter, in Lactobaillus plantarum Applied and Environmental Microbiology .68: 1088-1095.
U.S. Food and Drug Administration. 2000. Kinetics of microbial inactivation for alternative food processing technologies. Center for Food Safety and Applied Nutrition. Disponible: http://alteredstates.net/barry/rife/pulsedelectricflds.htm. Adquirido: 17/01/10.
Van Loey, A. B. V., y Hendrickx, M. 2002. Effects of high electric pulses on enzymes. Trends of Food Science and Technology. 12:94-102.
Vega-Mercado, H., Powers, J. R., Barbosa-Cánovas. G. V., y Swanson, B. G. 1995. Plasmin inactivation with pulsed electric field. Journal of Food Science. 60: 1143-1146.
Wouters, P. C., Dutreux, N., Smelt, J. P., y Lelieveld, H. L. M. 1999. Effects of pulsed electric fields on inactivation kinetics of Listeria innocua. Applied Environmental Microbiology. 65(12): 5354-5371
Wouters P. C., Alvarez I y Rasos J. 2001. Critical factors determining unactivation kinetics by pulsed electric field food processing trends. Science and Technology. 12:112-121.
Yin, Y., Zhang, Q. H. y Sastry, S.K. 1997. High voltage pulsed electric field treatment chambers for the preservation of liquid food products. Ohio State University, US Patent 5,690,978.
Zhang, Q. H., Monsalve-Gonzalez, A., BarbosaCánovas G. V. y Swanson, B. G. 1994. Inactivation of E.coli and S cerevisiae by pulsed electric fields under controlled temperature conditions. Transactions of the ASAE. 2: 581.
Zhang, Q. H., Barbosa-Cánovas, G. V., y Swanson, B.G. 1995. Engineering aspects of pulsed electric fields pasteurization. Journal of Food Engineering 25(2):261-281.
Zimmerman, U., Pilwat, G., y Riemann, F. 1974. Dielectric Breakdown in cell membranes. Biophyical Journal. 14(11): 881-889
Zimmermann, U., Pilwat, G., Beckers, F., y Riemann, F. 1976. Effects of external electrical fields on cell membranes. Bioelectrochemistry and Bioenergetics 3: 58-83.

Temas Selectos de Ingeniería de Alimentos 4 – 1 (2010): 27 – 36

Tecnologías de enmascaramiento de sabor amargo en alimentos
X. Villegas-Ruíz*, H. Ruíz-Espinosa y M. E. Bárcenas-Pozos
Departamento de Ingeniería Química, Alimentos y Ambiental. Universidad de las Américas, Puebla. Sta. Catarina Mártir, Cholula, Puebla. 72810. México
Resumen
Una de las tendencias más importantes en la industria alimenticia de nuestros días está enfocada al desarrollo de productos alimenticios percibidos como saludables, ya sea por la inclusión de ingredientes específicos o de componentes nutraceúticos aislados de los mismos. Sin embargo, una limitante importante en la aceptación general de este tipo de productos radica en la percepción de sabores desagradables frecuentemente asociados con sustancias nutraceúticas, como ha sido reportado con diversas sustancias fenólicas, entre otras, responsables del sabor amargo. Por ello, se han desarrollado enmascaradores de sabor y como su nombre lo dice, disfrazan sabores percibidos como desagradables en los alimentos. El objetivo de este trabajo es proveer información acerca de los diversos compuestos que imparten el sabor amargo en alimentos, así como las tecnologías de enmascaramiento y su aplicación a alimentos considerados como funcionales que muchas veces presentan este sabor.
Palabras claves: sabor amargo, enmascaramiento, tecnologías de enmascaramiento.
Abstract
Nowadays, product development incorporating ingredients with specific isolated nutraceutical compounds is one of the most important trends in the food industry. However, unpleasant, bitter tastes associated with some nutraceutical compounds such as phenolics limit consumer acceptance and reduce their potential to deliver health benefits. Consequently some food additives have been developed to mask off-flavors, thus increasing consumer appeal. The aim of this review is to provide relevant information concerning known compounds with bitter flavors, the state-of-the-art technologies applied to overcome their perception and their use in certain food products.
Keywords: bitter taste, masking, masking technologies.
Introducción
*Programa de Doctorado en Ciencia de Alimentos
En los últimos años la producción de alimentos funcionales ha sido muy explotada por la ciencia de alimentos; este tipo de alimentos ha sido una fuente natural de beneficios relacionados principalmente con la salud. Lo anterior ha dado paso a que continuamente se exploten alimentos y se desarrollen ingredientes que sean capaces de proveer características que mejoren la calidad de
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: xadeni.villegasrz@udlap.mx
vida, para así tener como resultado un alimento funcional.
Entre estos ingredientes desarrollados están los llamados antioxidantes algunos de los cuales contienen en sus moléculas polifenoles, que a su vez como su nombre lo dice son responsables de la capacidad antioxidante. Esto ha llevado al continuo interés por la extracción de estos compuestos para que finalmente sean aplicados como ingredientes funcionales a diversos tipos de alimentos (bebidas, productos cárnicos, productos de panificación, lácteos, confitería y snacks).
Sin embargo, este tipo de compuestos funcionales son muchas veces los principales compuestos responsables de sabores desagradables, entre ellos el sabor amargo, la astringencia y pungencia de diversos alimentos. Este aspecto ha limitado la aplicación de estos ingredientes bajo el argumento de que la presencia de estos sabores limita la venta del producto al no ser atractivo a los consumidores. Por lo tanto, se han buscado y por ende, desarrollado técnicas que disminuyan principalmente el sabor amargo, tarea que no ha sido fácil y que ha resultado hasta cierto punto poco costeable, debido a que las tecnologías existentes siempre ofrecen algo más que el enmascaramiento de sabores amargos, sino también el de conferir características sensoriales favorables, todo con el fin de ofrecer algo más al producto, pero haciéndolo poco accesible económicamente. Por lo anterior, muchas de las industrias se han propuesto a desarrollar sus propias tecnologías enfocadas a la disminución del sabor amargo.
Las tecnologías de disminución de sabor amargo se conocen a nivel industrial con el nombre de enmascaradores de sabor y en términos generales están basadas en las diversas interacciones que establecen estos compuestos con otros ingredientes en términos químicos.
El propósito de este trabajo es dar a conocer las características generales del sabor amargo, los compuestos responsables de este sabor en alimentos, así como las alternativas que se ofrecen para la disminución de este sabor, es decir, las tecnologías de enmascaramiento y su aplicación.
Revisión bibliográfica
1. Sabor amargo
1.1 Química del sabor amargo
Particularmente, el sabor amargo no puede ser predicho solamente por la estructura de la molécula del compuesto. Depende básicamente del tamaño de la molécula, del grupo funcional presente, la posición del azúcar si es que está presente, la disminución de la hidrofobicidad y estereoquímica de la molécula (Inarejos-Garcia et al., 2009).
Químicamente las moléculas amargas presentan un determinado arreglo. Utilizando la nomenclatura propuesta por Shallenberger-AcreeKier, la cual es AH (un electrófilo), B’ (un nucleófilo) y X (un grupo hidrofóbico); se puede describir a un compuesto amargo como aquel que posee un grupo AH y X, en donde un amino o grupo hidrofóbico (AH) interactúa con el receptor llamado A’, el grupo hidrofóbico X se enlaza con el receptor X’ mientras que el receptor B’ debe quedar libre (Roy, 1992) (Fig. 1).
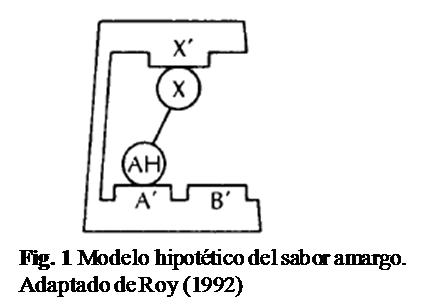
1.2 Receptores del sabor amargo
Las papilas gustativas son estructuras en forma de cebollas que contienen alrededor de 50 a 100 células gustativas. Los químicos provenientes de los alimentos o medicamentos ingeridos son disueltos por la saliva entrando por los poros gustativos. Aquí, interactúan tanto con la
superficie de las proteínas conocidas como receptores de gustos o con los poros de estas proteínas conocidos como canales iónicos. Este tipo de interacciones causan cambios eléctricos dentro de las células gustativas y como un detonador envían señales químicas que se transforman en una neurotransmisión hacia el cerebro. Particularmente, los gustos amargo y dulce interactúan con la superficie de las proteínas, mientras que los gustos ácido y salado están más ligados al tipo de canales iónicos. Las respuestas eléctricas que envían la señal al cerebro son el resultado de una variación en la concentración de la carga de los átomos o iones dentro de las células gustativas. En el caso particular del amargo, el estímulo actúa con un ligando con los receptores de las llamadas proteínas pareadas G (GPCRs) en la superficie de la célula gustativa. Estas proteínas pertenecen a una familia de receptores que median las respuestas provenientes de señales químicas funcionando como neurotransmisores (Temussi, 2009; Ley, 2008; Stier, 2004; Montmayeur y Matsunami, 2002; Walters, 1996).
El sabor amargo es una sensación común debida a la activación de receptores gustativos que responden a un estímulo químico. Estudios genéticos recientes mencionan que la habilidad de los humanos para detectar este sabor está determinada por un lugar del cromosoma 5 y posiblemente del cromosoma 7 (Montmayeur y Matsunami, 2002). Los receptores del sabor amargo son los llamados T2R ubicados en las células receptoras del gusto (TRC) tanto de la lengua como del paladar; éstos receptores son capaces de responder ante diversos compuestos amargos (Ley, 2008; Zhang et al., 2003; Montmayeur y Matsunami, 2002).
1.3 Alimentos y compuestos responsables del sabor amargo
En la naturaleza existen diversos alimentos que contienen determinados compuestos que les confieren el sabor amargo, lo cual los hace poco atractivos para el consumo en algunos casos, sin embargo, en otros, forma parte esencial de las características deseables en ese alimento y muchas otras a pesar de ser no grato, se compensa con los
aportes en términos de salud que dan estos compuestos de sabor desagradable.
Los compuestos responsables de sabor amargo tienen la particularidad general de poseer fenoles en su estructura molecular, sin embargo, podemos encontrar otros como los aminoácidos, péptidos, sulfimidas, flavonoides, isoflavonoides, glucosinolatos, ureas y tio ureas, ésteres, lactonas, terpenoides, poliacetilenos, isocoumarinas e isohomulonas (Fig. 2). A continuación se mencionarán algunos alimentos que por su naturaleza contienen sustancias específicas que le confieren el sabor amargo.
El aceite de oliva virgen presenta una nota amarga y ésta es dada por los compuestos derivados de oleuropeina y ligstrosida, provenientes de los frutos del olivo no maduros, cabe mencionar, que esta es una característica sensorial deseable en el producto terminado, debido a que principalmente potencializa las notas relacionadas con el mismo (Sinesio et al., 2005; Inarejos-Garcia et al., 2009).
La zanahoria es uno de los vegetales que posee compuestos a los cuales se les atribuye efectos anticancerígenos, pero la presencia de estos compuestos contribuyen al sabor amargo de las misma (Kreutzmann et al., 2007). También es rica en compuestos como ácidos fenólicos (principalmente en forma de ácidos clorogénicos como el ácido 5-caffeoilquinico, (5-CQA), ácidos ferúlicos, ácidos quinicos, ácidos cafeícos y ácidos p-coumaricosa, poliacetilenos (Falcarinol [(Z)heptadeca-1,9-dien-4,6-di-3-ol: FaOH], falcarindiol [(Z)-heptadeca-1,9-dien-4,6-di-3,8diol: FaDOH] y falcarindiol 3-acetato [(Z)-3acetoxi-heptadeca-1,9-dien-4,6-di-8-ol: FaDOAc]), isocoumarinas (6-Methoxymelin (3-metil-6metoxi-8-hidroxi-3,4-dihidro-isocoumarina; 6MM)) y 2,4,5-trimetoxi benzaldehído; todos ellos responsables del sabor amargo presente en los diversos genotipos de zanahoria (“Bolero”, “Mello Yello”, “Nairobi”, “Tornado”, “Purple Haze”, “Línea 1”, “Línea 2” y “Línea 3”) (Kreutzmann et al., 2007).
Dentro del grupo de los cítricos como la naranja, limón y toronja, la presencia de
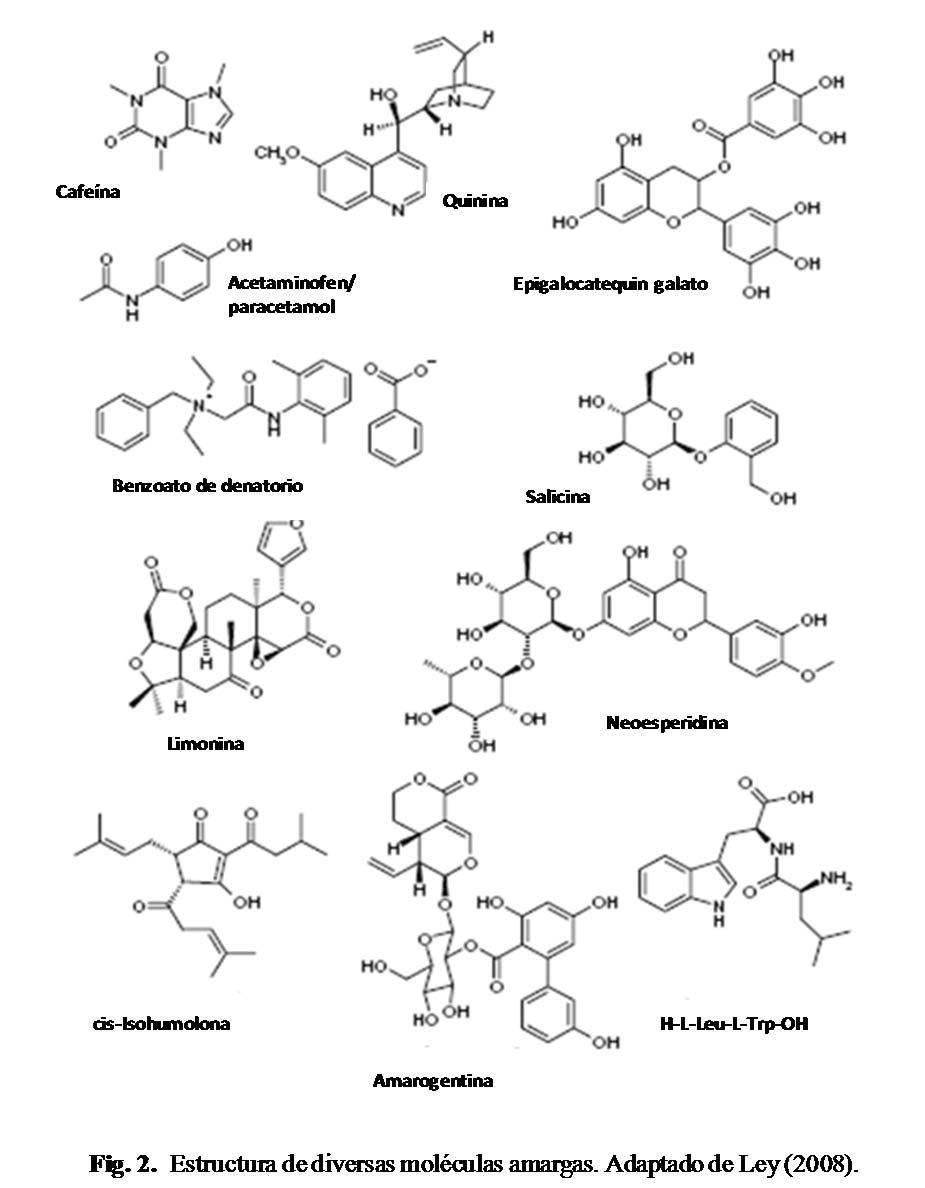
compuestos como la naringina y limonina proporcionan el sabor amargo característico de estas frutas que es indeseable para el consumo humano (Inarejos-Garcia et al., 2009; Szejtli y Szente, 2005).
En la coliflor se han identificado dos compuestos responsables del amargor los cuales
son: glucosinolato neoglucobrassicina y sinigrina (Dinehart et al., 2006).
Actualmente se ha reportado sabor amargo en diferentes plantas alimenticias como camote, frijoles, chícharos, col, pepinos, calabaza, lechuga, espinaca y coliflor, todas ellas tienen la
característica de contener toxinas amargas (Drewnoski y Gómez-Carneros, 2009).
Dentro de los productos alimenticios en donde el sabor amargo es una característica deseable, tenemos a la cerveza, el cual se forma a partir de la fermentación de malta, en donde se producen los llamados iso-α-ácidos ó isohumulonas, que muchas veces se utilizan como agentes para evitar reacciones de oxidación que dan lugar al desarrollo de sabores rancios en la cerveza (King y Duineveld, 1999); el chocolate, donde el sabor amargo está presente en los granos de cacao debido a la presencia de xantinas; la salsa de soya debido a la presencia de agliconas y en el café debido a la presencia de cafeína y ácidos clorogénicos (Szejtli y Szente, 2005; Roy, 1992). Otro tipo de productos que tiene sabor amargo, incluye el té verde, jugos y vinos de uva, esto se debe a la presencia de taninos que confieren este peculiar sabor. Precisamente dentro del grupo de bebidas alcohólicas se ha encontrado la presencia del compuesto llamado 6-n-propiltiouracil (PROP) responsable del amargor de éstas (Lanier et al., 2004; Dinehart et al. 2006). Otro ejemplo dentro de las bebidas es el agua tónica que contiene quinina que es considerada una sustancia amarga tolerable sólo en bajas concentraciones (Szejtli y Szente, 2005).
Es importante mencionar que los cambios de sabor amargo presentes en los alimentos dependen mucho de las condiciones de almacenamiento. Como regla general, este sabor disminuye en intensidad y duración conforme pasa el tiempo (Sinesio et al.,2005).
En términos generales los compuestos químicos que están dentro del grupo que exhiben un potencial antioxidante tales como polifenoles, antocianinas (en forma de flavonoides) y carotenoides, son responsables del sabor amargo (Ares et al., 2009).
Frank et al. (2004) mencionan una clasificación muy particular de las sustancias químicas que se utilizan como estímulos amargos en experimentos.
Ellos clasifican en estímulos amargos iónicos y no iónicos; para el primer grupo incluyen al benzoato de denatonio, la quinona hidroclorada –ambos cationes orgánicos hidrofóbicos- y el sulfato de magnesio, los cuales son amargos a muy bajas concentraciones. El segundo grupo incluyen a la cafeína y al octacetato de sacarosa (SOA).
Hasta el momento se ha estudiado la relación entre el sabor amargo y el dulce, debido a que muchas moléculas similares estructuralmente pueden ser dulces o amargas. La diferencia en que sean una u otra, radica solamente en la posición de un determinado grupo funcional (Walters, 1996) lo cual se puede observar en la Fig. 3.
2. Tecnologías de enmascaramiento
2.1 Principios generales
Existen diversas tecnologías de enmascaramiento, éstas están clasificadas con base en el tipo del método utilizado; se puede mencionar, por ejemplo, las tecnologías relacionadas con procesos, a las de adición de endulzantes artificiales, sabores e inclusive de otros compuestos amargos, ácidos y astringentes, así como también a las de la utilización de aditivos alimenticios. El objetivo general es prevenir la sensación del sabor amargo ya sea evitando el contacto de las moléculas amargas con los receptores gustativos o bien cubriendo este compuesto a través de la administración en conjunto con otras sustancias (Szejti y Szente, 2005).
Hay básicamente tres tipos de interacciones relacionadas con el sabor: interacciones fisicoquímicas, interacciones secundarias entre un componente del alimento y los receptores del gusto de otro componente y la supresión cognitiva central de una mezcla; con base al tipo de interacción presente, se puede aprovechar para reducir el sabor amargo de un determinado compuesto (Ares et al., 2009).
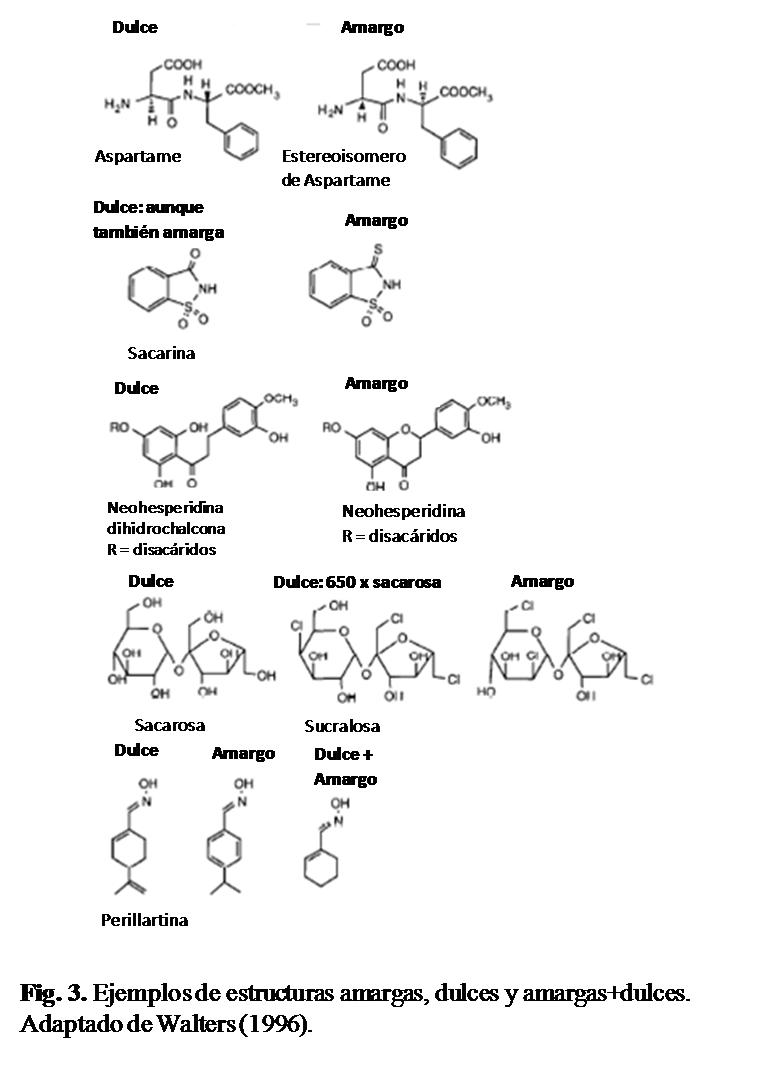
2.2 Métodos de enmascaramiento más utilizados y sus aplicaciones
Los mecanismos de los métodos para el enmascaramiento del sabor amargo pueden ser resumidos de la siguiente manera: en primera instancia, el enmascaramiento se puede hacer adicionando sabores, endulzantes o agentes efervescentes; y en segundo lugar, para evitar este sabor amargo es cubriendo o bien transformando el compuesto que imparte dicho sabor, lo cual muchas veces deriva en la presencia de sensaciones no agradables tal como la arenosidad.
En los años recientes, se han desarrollado métodos como la microencapsulación y la formación de microesferas, cuyo objetivo principal es el de crear barreras físicas que protejan al compuesto amargo al momento en que entra en contacto con las papilas gustativas y evitar que se libere el sabor (Xu et al., 2008). En este tipo de tecnología se recurre a la utilización de ciclodextrinas, las cuales pueden funcionar teóricamente de dos maneras: formando un complejo de inclusión que impide la interacción con las papilas gustativas, o bien, la interacción de la ciclodextrina directamente con las proteínas de
las papilas gustativas paralizándolas (Szejti y Szente, 2005). La ciclodextrina más utilizada es la conocida como polímero de βCD, formada por 7 unidades de gluporinosa. Dentro de las aplicaciones en alimentos de esta tecnología se tiene la eliminación del amargor en caseína hidrolizada de leche, disminución de la presencia de naringina y limonina en jugo de toronja y el enmascaramiento del amargor indeseable producido durante el tostado del café.
Una de las técnicas de procesamiento desarrolladas es la reportada y patentada por Nestec, conocida como “método de exsorción” que consiste en la extracción con fluidos supercríticos y absorción de carbón activado de las xantinas aplicado al cacao (Roy, 1992).
Por otro lado, la utilización de enzimas del grupo de α-transglucosidasas, en forma de ciclodextrina glucosiltransferasa, las cuales son muy aplicadas en el mejoramiento de las propiedades edulcorantes de la esteviosa y la glicirrina, que son de naturaleza amarga (Szejti y Szente, 2005; Roy, 1992), Otra enzima es la naringinasa, que es capaz de remover la naringina y limonina proveniente de los jugos de frutas. Finalmente la utilización de la llamada pancidasa NP-2, una proteasa utilizada para eliminar el amargor presente en el jugo de pimientos dulces (Roy, 1992).
Otro método muy utilizado para el enmascaramiento de sabor amargo, es el aplicado a tabletas de determinados medicamentos amargos, mediante la utilización de alginato sódico y gluconato cálcico, este proceso se da por la formación en la superficie del producto amargo de un gel insoluble en agua, lo cual permite que al momento de ser ingerido la saliva no penetre y libere el sabor desagradable presente en la tableta (Al-Omran et al., 2002).
El método más sencillo para reducir el amargor es simplemente con el incremento de dulzor (Walters, 1996) mediante la adición de edulcorantes tales como sacarosa, sucralosa y polidextrosa, aunque también la adición de leche contribuye a la reducción de este sabor amargo, dado por la interacción de los grupos fenólicos con
las proteínas de la leche, impidiendo que interactúen con las proteínas de la saliva, reduciendo el amargor. Se sabe que en el caso particular de la polidextrosa enmascara sabores indeseables a partir de la habilidad de establecer interacciones polares, puentes de hidrógeno e interacciones dipolo-dipolo con polifenoles, lo cual disminuye la interacción con las células receptoras de las proteínas de la saliva (Ares et al., 2009).
Barra et al. (1999) mencionan que un método común para evitar la sensación de sabor amargo es mediante el adormecimiento de las papilas gustativas con la ayuda de un agente analgésico o por un “enfriamiento” con mentol. Ellos realizaron pruebas de enmascaramiento de sabor amargo mediante el uso de sustancias sin sabor (etil celulosa e hidroxipropil metilcelulosa) mezcladas con medicamentos amargos (ácido niflúmico e ibuprofeno), encontraron que estas sustancias son capaces de reducir el amargor moliendo a un determinado tamaño de partícula, además de ser un proceso barato, en comparación con otros métodos como la microencapsulación.
La combinación de sales sódicas con L-arginina ha sido muy aplicada para la disminución de sabor amargo en diversos péptidos, sin embargo la utilización de esta técnica se ve limitada cuando se aplica en la elaboración de bebidas dulces o bien en alimentos salados que contienen notas dulces (Ley, 2008).
La adición de sabores es otro de los métodos de enmascaramiento más utilizados. Roy (1992) menciona la utilización de dos compuestos, uno llamado esclareolide, un saborizante diterpenoide natural aplicado principalmente en la reducción de amargor en los granos de café tostados y también en cítricos. El otro saborizante artificial es el maltol, utilizado para enmascarar el sabor amargo proveniente de las sales como el cloruro de potasio presente en determinados alimentos.
Paradójicamente, se utilizan compuestos amargos para enmascarar el mismo sabor amargo, claro ejemplo es la utilización de los taninos del fruto llamado caqui en la disminución de amargor en café y en la desaparición de olores desagradables (Roy, 1992).
2.3 Algunos productos existentes en el mercado
Actualmente existen diversos productos al alcance de empresas dedicadas al desarrollo de productos alimenticios para el enmascaramiento de sabor amargo, aunque también ofrecen las características tales como potenciador y mejorador de sensaciones en la boca. A continuación se mencionan los más comerciales:
2.3.1 Talin®
La empresa Talin (2010) desarrolló un producto con diversas funciones: enmascarador de sabor amargo, modificador y potenciador de sabor. Éste es el nombre comercial de la taumatina, la cual es una proteína estable a temperaturas utilizadas en procesos de ultra altas temperaturas (UHT), pasteurización, panificación y extrusión, en rangos de pH de 2 a 8, además es estable a la presencia de colorantes utilizados en la industria alimentos y bebidas. Es considerado un ingrediente natural, que posee propiedades únicas, una de ellas es el de potenciador de sabor, lo cual implica una ventaja en el mejoramiento del mismo. Otra propiedad es el enmascaramiento de sabor amargo, ya que es capaz de disfrazar el resabio amargo y es aplicado principalmente a alimentos funcionales y bebidas que presentan esta característica de sabor, además es proveedor de sensaciones en la boca. Una de las tendencias actuales es utilizar bajas cantidades de azúcares y grasas, aunque muchas de las características del producto final dependen de estos ingredientes, por lo anterior, se recurre a este tipo de aditivos que proveen sensaciones cremosas por un lado, y por el otro, puede reemplazar la adición de otros azúcares.
los sabores indeseables que los consumidores encuentran poco atractivos como el sabor amargo.
2.3.3 Gelita®
Desarrollada por Gelita Group (2010), es una proteína conocida con el nombre de colágeno hidrosilato, tiene la particularidad de ser utilizado como un edulcorante, y ha mostrado ser un ingrediente que ofrece beneficios para la salud como el mejoramiento de piel, cabello y uñas, promueve un balance nutricional y contribuye a la formación del tejido conectivo y formación de músculos. La gran ventaja es que produce sensaciones en la boca, sin sabor amargo y es compatible con cualquier ingrediente.
2.3.4 Eugradit® EPO
Creado por Degussa (2010), químicamente es un copolímero catiónico basado en dos compuestos: el metacrilato dimetillaminoetil y el éster metacrilico, es capaz de disolverse a pH menores a 5. Se utiliza mucho para microencapsulación de sabores amargos presentes en medicamentos. Se caracteriza por disolverse rápidamente en el estómago a un pH entre 1 y 3 sin que el medicamento pierda su biodisponibilidad y mantenerse intacto en la cavidad bucal a un pH de 5.8 a 7.4, proporcionando un buen enmascaramiento del sabor amargo (Xu et al., 2008).
2.3.5 Benzil amidas
2.3.2 Senserburst® Dairy booster
Creado por la compañía Belmay, Ltd (2010), éste es un potenciador que mejora el perfil de sabor con aplicaciones en productos lácteos, debido a que está especialmente diseñado para reemplazar los componentes presentes de manera natural en este tipo de productos; además este producto enmascara
Este tipo de compuestos han sido desarrollados por científicos de Symrise® -empresa internacional dedicada a la producción de sabores y fraganciaséstos son aplicables tanto a bebidas como a alimentos. Se ofrecen como una alternativa que sustituiría a los enmascaradores provenientes de flavonoides utilizados tanto en la industria de alimentos como en la farmacéutica; ya que este tipo de compuestos son mucho más caros debido a que su estereoquímica y subestructura no es común encontrarla en recursos naturales. Dentro de este grupo de ácidos benzoicos hidrolizados se tiene al ácido 2,4-dihidroxibenzoico y a la amida N-(4hidroxi-3-metoxibenzil), ya que son similares estructuralmente al homoeriodictiol, que es
químicamente una flavonona considerada como el enmascarador de sabor amargo principal utilizado en alimentos (Daniells, 2006).
Conclusiones
Las diversas tecnologías enfocadas al enmascaramiento de sabor amargo cada vez son más demandadas, principalmente por la exigencia de los consumidores ante sabores agradables. Hoy en día existen diversas tecnologías que involucran métodos y productos que ofrecen soluciones ante este tipo de problemas, sin embargo, el uso de estas tecnologías está restringido a empresas que puedan costearlas.
Belmay Ltd., 2010. Belmay. http://www.belmay.com/index.asp., accesada: 2/04/2010.
Daniells, S. 2006. Symrise explores cheaper alternatives in bitter-maskers. Food Navigator. http://www.foodnavigator.com, accesada: 13/02/ 2010.
Degussa. 2010. Degussa creating essentials. http://www.solimide.eu/en/pharmapolymers/eudragit /quality/spezifikationen_neu.Par.0001.TRow.0017.T Cell.0002.File.tmp/7.1.01_INFO7.1e_E100_EPO_E 12_5_200409.pdf, accesada: 2/04/2010.
Dinehart, M.E., Hayes, J.E., Bartoshuk, L.M., Lanier, S.L. y Duffy, V.B.2006. Bitter taste markers explain variability in vegetable sweetness, bitterness, and intake. Phisiology and Behavior, 87:304,313.
Drewnoski, A. y Gómez-Carneros, C. 2009. Sabor Amargo, Fitonutrientes y el Consumidor. Mundo Alimentario Julio/Agosto, 20-24.
Agradecimientos
Mi más sincero agradecimiento es para mi asesora, la Dra. María Eugenia Bárcenas Pozos, por su apoyo para la realización de este artículo; así como también a Roberto Terreros por la orientación dada. Además agradezco al Consejo Nacional de Ciencia y Tecnología por el apoyo económico otorgado y a la Universidad de las Américas Puebla por el apoyo para la realización de mis estudios de posgrado.
Referencias
Al-Omran, M.F., Al-Suwayeh, S.A., y El-Helw, A.M. 2002. Taste masking of diclofenac sodium using microencapsulation. Journal of Microencapsulation, 19 (1):45-52.
Ares, G., Barreiro, C., Deliza y R., Gámbaro, A. 2009. Alternatives to reduce the bitterness, astringency and characteristic flavour of antioxidant extracts. Food Research International. 42 (7):871-878.
Barra, J., Lescure, F. y Doelker, E. 1999. Taste masking as a consequence of the organisation of powder mixes. Pharmaceutica Acta Helvetiae, 74(1):37-42.
Frank, M.E., Bouverat, B.P., MacKinnon, B.I. y Hettinger, T.P. 2004. The distinctiveness of ionic and nonionic bitter stimuli. Physiology and Behavior, 80(4):421-431.
Gelita Group. 2010. Gelita improving quality of live. http://www.gelita.com/, accesada: 2/04/2010
Inarejos-Garcia, A.M., Androulaki, A., Desamparados, M.S., Fregapane, G., y Tsimidou, M.Z. 2009. Discussion on the objective evaluation of virgin olive oil bitterness. Food Research International. 42(2): 279-284.
King, B. M. y Duineveld, C. A. A. 1999. Changes in bitterness as beer ages naturally. Food Quality and Preference. 10(4-5):315-324.
Kreutzmann, S., Christensen, L.P. y Edelenbos, M. 2007. Investigation of bitterness in carrots (Daucus carota L.) based on quantitative chemical and sensory analyses. LWT - Food Science and Technology, 41(2):193-205.
Lanier, S.A., Hayes, J.E. y Duffy, V.B. 2004. Sweet and bitter tastes of alcoholic beverages mediate alcohol intake in of-age undergraduates. Physiology and Behavior, 83:821-831.
Ley, J.P. 2008. Masking bitter taste by molecules. Chemosensory Perception. 1:58-77.
Montmayeur, J-P. y Matsunami, H. 2002. Receptors for bitter and sweet taste. Sensory Systems, 12:366-371.
Roy, G. 1992. Bitterness: reduction and inhibition Trends in Food Science and Technology. 3: 85-91.
Sinesio, F., Moneta, E. y Esti, M. 2005. The dynamic sensory evaluation of bitterness and pungency in virgin olive oil. Food Quality and Preference 16(6):557-564.
Stier, R.E. 2004. Masking bitter taste of pharmaceutical actives. Drug Deliv Technol, 4(2):52, 54-57.
Szejtli, J. y Szente, L.2005. Elimination of bitter, disgusting tastes of drugs and foods by cyclodextrins. European Journal of Pharmaceutics and Biopharmaceutics, 61(3): 115-125.
Talin 2010. Talin a naturex product. http://www.pharmaceuticaltechnology.com/contractors/excipients/overseal/, accesada: 2/04/2010
Temussi, P.A. 2009. Sweet, bitter and umami receptors: a complex relationship. Cell Press, 34(56): 296-302.
Walters D.E. 1996 How are bitter and sweet tastes related?. Trends in Food Science and Technology, 7(12):399-403.
Xu, J., Bovet, L.L. y Zhao, K. 2008.Taste masking microspheres for orally disintegrating tablets. International Journal of Pharmaceutics, 359(1-2, 9): 63-69.
Zhang, Y., Hoon, M.A., Chandrashekar, J., Mueller, K. L., Cook, B., Wu, D., Zuker, C.S. y Ryba, N.J.P. 2003. Coding of Sweet, Bitter, and Umami Tastes: Different Receptor Cells Sharing Similar Signaling Pathways. Cell Press, 112: 293-301.

Temas Selectos de Ingeniería de Alimentos 4 – 1 (2010): 37 – 48

Algunas características de compuestos presentes en los frutos secos y su relación con la salud
J.J Luna-Guevara* y J. A. Guerrero-Beltrán
Departamento de Ingeniería Química, Alimentos y Ambiental. Universidad de las Américas, Puebla. Sta. Catarina Mártir, Cholula, Puebla. 72810. México
Resumen
El interés cada vez mayor por parte de la población en el cuidado de su salud ha puesto de manifiesto la necesidad de consumir alimentos con propiedades nutricionales que contribuyan a disminuir el riesgo de padecer enfermedades. Una alternativa fácil y de bajo costo es el consumo habitual de frutos secos, los cuales cuentan con un importante valor nutricional y una extensa variedad de compuestos bioactivos con características funcionales, entre las que destacan el elevado contenido de ácidos grasos tanto poliinsaturados como monoinsaturados, antioxidantes y minerales, entre otros. Éstos disminuyen la posibilidad de sufrir cardiopatías, obesidad, diabetes tipo II y algunos tipos de cáncer. El estudio de los beneficios del consumo de los frutos secos permitirá proveer información sobre la prevención de estas enfermedades que son la mayor causa de morbilidad y mortalidad del mundo occidental. En esta revisión se comentarán algunos trabajos científicos relacionados con los frutos secos, tanto los que se refieren a su producción y composición, como aquellas aportaciones en las que se expone la relación de su consumo y el cuidado de la salud.
Palabras clave: frutos secos, alimentos funcionales, salud.
Abstract
The growing interest of people in health issues has highlighted the need of consuming foods with properties that help them to reduce the risk of illnesses. An easy and low cost alternative to achieve this, is the regular intake of nuts which have an important nutritional value and a variety of bioactive compounds with functional properties, such as high content of polyunsaturated and monounsaturated fatty acids, antioxidants, minerals, and among other characteristics. These compounds may reduce the possibility of heart illness, obesity, type II diabetes and some types of cancer. Research regarding the benefits of nuts intake promote their consume and therefore, prevent these health problems which are the main cause of people morbidity and mortality in the western world. In this review we discuss some scientific advances related to nuts, and the relation of its consumption and the maintenance of health.
Keywords: nuts, functional foods, health.
*Programa de Doctorado en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: juan.lunaga@udlap.mx
Introducción
Los frutos secos han formado parte de la alimentación desde hace miles de años, siendo muy apreciados en una importante cantidad de platillos, preferentemente en dulces y postres.
Desde el punto de vista nutricional, a pesar del elevado contenido en lípidos, los frutos secos poseen una composición muy adecuada. Lo anterior radica en el contenido de ácidos grasos insaturados. De igual manera son fuentes importantes de proteínas, fibra, vitamina E, ácido fólico, minerales y compuestos con características funcionales.
Asimismo, estudios epidemiológicos demuestran que los frutos secos presentan beneficios sobre la salud, relacionando su consumo con una menor incidencia del riesgo de padecer enfermedades cardiovasculares, cáncer, diabetes tipo II y obesidad. Estas evidencias ponen de manifiesto que la ingesta de frutos secos es una forma accesible de prevenir estas enfermedades (Krauss et al., 2000).
Por otro lado, continuar con el estudio de este tipo de productos y su actividad funcional, permitirá incorporarlos a la dieta con los referidos beneficios que esto conlleva. En esta revisión se comentarán algunos reportes y avances relacionados con los frutos secos, tanto los que se refieren a su producción, composición y aquellas aportaciones que exponen la relación de su consumo con el resguardo de la salud.
de cáscara, a aquellos cuya parte comestible contiene menos de un 50% de agua. Se incluyen en esta definición a la almendra, avellana, nuez de Castilla, nuez de la India, nuez de Brasil, nuez pecanera, pistache y piñón. Asimismo se consideran dentro de este grupo, a las semillas de girasol y al cacahuete debido a la similitud en sus características nutricionales que tienen con los frutos secos, Tabla I.
2. Principales frutos secos que se producen en México
Debido a las características orográficas del país, en México, la producción de frutos secos se ha localizado en la porción centro y norte del mismo. Según el Sistema de Información Agroalimentaria y Pesquera (SIAP, 2008) la producción de nuez, cacahuate, piñón y pistaches representó un valor económico de producción por $3,541,200,800, lo que se traduce en una importante derrama económica para el país.
2.1
Nuez
El nogal es nativo de las cadenas montañosas que se extienden por el centro de Asia, es posible encontrar sus orígenes y gran diversidad genética en Nepal, Tíbet, China, India, la región del Cáucaso y el este de Turquía. La producción mundial de nuez con cáscara se encuentra principalmente en China (22%), Estados Unidos (20%), obtenida casi totalmente en California, Irán (12%) y Turquía (10%) (FAO, 2007). Producciones de menor entidad se obtienen en India, Francia, Italia, Grecia, Rumania, Chile y México.
Revisión bibliográfica
1. Definición
De acuerdo con la Norma Mexicana NMXFF-084-SCFI-2009 y el Código Alimentario Español (2010), se entiende por frutos secos o
En el país se producen básicamente dos tipos de nuez, la de “Castilla” (Juglans regia) y la denominada “cáscara de papel” o “nuez pecanera” (Carya illinoensis), la cual es originaria de la región del Mississippi en Estados Unidos y llegando hasta el sur de México; su producción mundial se encuentra
TablaI. Principalesfrutossecos.
Fruto secoEspecieGéneroFamilia
Almendra Prunus spp.PrunusRosaceae
Avellana Corylus avellana L.CorylusBetulaceae
Cacahuete Arachis hipogaeaArachisFabaceae
Nuez de Castilla Juglans regia L. Juglans Juglandaceae
Nuez Pecanera Carya illinoensisCaryaJuglandaceae
Pepitas de girasol Helianthus anuusHelianthusAsteroideae
Piñón Pinus pinea L.PinusPinaceae
Pistache Pistacea vera L.PistaceaAnacardiaceae
Nuez de la India Anacardium occidentaleAnacardiumAnacardiaceae
Nuez de Brasil Bertholletia excelsaBertholletiaLecythidaceae
Modificada de Merixtell etal. (2004)
dividida principalmente en Estados Unidos (67%) y México (30%) (Salas et al., 2005).
La producción de nuez total en 2008 fue de 79,769.55 toneladas, destacándose Chihuahua, Coahuila, Durango y Sonora, como los productores más importantes del país. La derrama económica generada por la explotación de la nuez ascendió a $2,960,631,600.
2.2
Cacahuate
De acuerdo con cifras proporcionadas por la Food and Agricultural Organization (FAO) (2007), entre los principales productores de cacahuate con cáscara se encuentra en primer lugar China, seguida de India, Nigeria y Estados Unidos. En México se cultiva mayoritariamente el cacahuate (Arachis hypogaea), aunque existen cuatro de las siete variedades botánicas reportadas a nivel
mundial. Éstas se cultivan principalmente (85%) en condiciones de temporal y en suelos pobres y marginales, en los estados del centro como: Morelos, Puebla y Oaxaca. En el norte, Sinaloa y Chihuahua son los principales productores. La producción en 2008 ascendió a 80,734.54 toneladas representando una utilidad de $552,806,800 (SIAP, 2008).
2.3 Piñón
La producción se realiza en masas forestales naturales o artificiales que proveen de madera, resina, procesos de reforestación y actualmente, el fruto es el producto de mayor explotación. La producción mundial se encuentra dividida primariamente en dos países España con 30% y Portugal con un 40%. Mundialmente se explotan diferentes especies del género Pinus productoras de piñones comestibles: P. cembroides, P. edulis, P. monophylla, P. quadrifolia y P. sabiniana
principalmente (Salas et al., 2005). El Pinus cembroides es la principal especie producida en México.
El estado de Nuevo León es el mayor productor de piñón siendo un producto agrícola valioso en las comunidades donde se encuentra, pero ha sido escaso e inadecuadamente aprovechado. Durante 2008, en México se produjeron 530 toneladas con un valor económico de $26,670,000 (SIAP, 2008).
2.4 Pistache
El centro del origen del árbol pistachero se encuentra en la región centro- oeste de Asia (Afganistán e Irán). Los principales productores son Irán (53%), Estados Unidos (20%), Siria (10%) y Turquía. Producciones menores se obtienen en China, Grecia, Italia, Afganistán, Túnez y Australia. En Irán, Estados Unidos y Turquía este producto ha tenido un substancial repunte en las últimas décadas (FAO, 2007). En México, el desierto Sonorense y Chihuahuense es donde se concentra la mayor producción de pistache (Pistacia vera). Sin embargo, nacionalmente este fruto no ha encontrado la difusión adecuada. La producción en 2008 sólo alcanzó las 20.5 toneladas y con un valor de producción de $1,093,000 (SIAP, 2008).
3. Algunas características composicionales de los frutos secos
Los frutos secos destacan por su elevado contenido energético, ya que en promedio, 100 g aportan entre 560 y 640 kcal. Este importante valor energético deriva de su escaso contenido en agua y, sobre todo, de su notable cantidad de grasas: entre un 48 y un 63%. No obstante, la importancia del contenido lipídico de estos alimentos no es únicamente cuantitativa, sino cualitativa, puesto que predominan los ácidos grasos insaturados. Todos los frutos secos tienen una
composición similar en proteínas (entre 13 y 27%) con un relativo valor biológico que, adecuadamente combinadas con cereales y legumbres, dan lugar a proteínas completas equivalentes a las de origen animal. Por otro lado, el aporte en hidratos de carbono en la mayoría de los frutos secos, su contenido está alrededor del 20%. Asimismo, constituyen una excelente fuente de algunas vitaminas especialmente E y del grupo B, además de proveer minerales y fibra (Solà, 2004).
Para la Sociedad Española de Dietética y Ciencias de la Alimentación (2009) es obvia la alta densidad energética de estos alimentos, por lo que la inclusión de los frutos secos en la dieta habitual debe hacerse en cantidades adecuadas y reemplazando el de otros productos calóricos, es decir, no debe añadirse como un suplemento más a la dieta diaria, sino como sustitución.
3.1 Proteínas
Los frutos secos contienen una notable proporción de proteínas, ésta oscila entre el 20% en almendras y el 14% en nueces, piñones y avellanas. En los cacahuetes el contenido proteico alcanza el 27%. Excepto en el caso de la lisina, que sería el aminoácido limitante para nueces y cacahuetes, y el de lisina, metionina y cistina en las almendras, el aporte de los otros aminoácidos esenciales es muy aceptable ya que cubre por encima del 75% del score. Para la FAO (1973) el score define la cantidad de aminoácido esencial/kg de proteína necesario para garantizar un correcto crecimiento en niños de edad escolar. Además de los aminoácidos esenciales, los frutos secos presentan interesantes cantidades de arginina, que desempeña un papel importante en los efectos cardiovasculares beneficiosos asignados a los frutos secos.
El elevado contenido en arginina, de los frutos secos, de 2 a 3 g por cien gramos de alimento de manera especial en las nueces,
constituye un factor positivo, dado el papel que juega este aminoácido en la formación de óxido nítrico, un potente vasodilatador de actividad similar a la nitroglicerina que induce la relajación del músculo liso por activación de la guanilato ciclasa, capaz de reducir la adhesión y la agregación plaquetaria en el endotelio vascular (Fraser et al.,1999; Brown y Hu, 2001). La relación lisina/arginina es inferior a 1, incluso menor que la de la soya, lo que se traduce como una proteína con efecto hipocolesterolemiante (Vázquez y Sánchez, 1994).
3.2 Lípidos
Desde el punto de vista del elevado contenido en lípidos, los frutos secos poseen una atractiva composición nutricional con un predominio en el aporte en ácidos grasos insaturados, donde los ácidos oleico y linoleico suministran más del 75% del aporte graso, aunque cada variedad tiene sus propias características (Chan, 2004).
Según la composición nutricional en ácidos grasos se pueden diferenciar dos grupos de frutos secos: los ricos en ácido linoleico (18:2) como los cacahuetes y las nueces y los ricos en ácido oleico como las avellanas, almendras, pistaches y nueces de macadamia. Las nueces son las únicas que contienen cantidades considerables de ácido alfa-linolénico (18:3n3) (Sleiman et al., 2002; Chan, 2004) en una proporción de hasta el 6.8% del contenido graso. Por ello, se puede considerar la fuente más importante de este ácido, después de la procedente del consumo de pescado (Albert et al., 2002). Sin embargo, este ácido graso se encuentra en menor cantidad en otros frutos secos, no alcanzando el 1% de los ácidos grasos. Por otro lado, en todos los frutos secos los niveles de ácidos grasos saturados no superan el 7% (Favier et al., 1995; Solà 2004) siendo el ácido esteárico el más abundante, el cual se ha definido con escaso efecto sobre el
colesterol total dada su fácil transformación en ácido oleico (Sánchez y Bastida, 2000).
3.3 Carbohidratos
Los hidratos de carbono presentes en los frutos secos son en su mayoría monosacáridos y disacáridos, el contenido de este macronutriente representa en promedio el 20%, a excepción de las castañas que son más ricas en hidratos de carbono que en grasa (son más harináceas que oleosas). El consumo de frutos secos contribuye a aumentar las ingestas diarias de fibra, que en los países industrializados se encuentra en niveles inferiores a las recomendadas.
Los frutos secos contienen cantidades apreciables de fibra dietética menores que las presentes en otros productos vegetales como legumbres y cereales integrales. La cantidad de fibra, es mayoritariamente insoluble y oscila entre 5 y 11 g por 100g del fruto seco, según las diversas variedades de fruto. Un consumo adecuado de fibra es importante para facilitar y regular el tránsito intestinal y el volumen de las heces; mantiene la sensación de saciedad (Salas et al., 2001) y evita el estreñimiento (Plessi et al., 1999).
No obstante, en los últimos años se han descrito nuevos efectos del consumo de fibra insoluble presente en los frutos secos, relacionando su consumo y un efecto preventivo en la aparición de enfermedades de tipo cardiovascular (Jenkins et al., 2000).
Además la fibra de tipo soluble produce una reducción del colesterol plasmático, mejora el control de la glicemia y es útil en la prevención y el tratamiento de la obesidad. Estos beneficios se deben a que la glucosa y los ácidos grasos son absorbidos más lentamente por la mucosa intestinal; reduciendo el ritmo y el grado de absorción del colesterol y favoreciendo el desarrollo de la flora bifidogénica con los efectos beneficiosos
para la salud que ello supone (Salas et al., 2006).
3.4
Antioxidantes
Para Araya y Lutz (2003) el interés en la relación entre alimentación y salud, va más allá de la acción preventiva de los nutrientes en los déficits nutricionales. Lo anterior se explica por las asociaciones que se han evidenciado entre el consumo de alimentos de origen vegetal, y sus efectos preventivos sobre algunas enfermedades (Hasler, 2002). Si bien no ejercen un rol nutricional, puesto que no se trata de sustancias indispensables para el organismo, su consumo supone una protección adicional contra la acción nociva de sustancias provenientes de la dieta y del entorno ambiental y que afectan la salud de la población. A este efecto de retardar y/o suprimir procesos dañinos, se le denomina en conjunto, quimioprevención a través de los alimentos que contienen carotenoides, polifenoles, vitaminas antioxidantes y otros fitoquímicos de efectos bioquímicos comprobados (Murakami et al., 1998). Los frutos secos son fuentes de antioxidantes, entre los cuales se encuentran los fitoquímicos, compuestos que en su gran mayoría son antioxidantes y que incluso pueden tener efectos sinérgicos con determinados nutrientes (Halverson et al., 2002). Algunos ejemplos de estos compuestos incluyen a las antocianinas, compuestos fenólicos, flavonoides, isoflavonas y minerales como el selenio que funge como cofactor con la vitamina E (USDA, 2006).
3.5 Vitamina E
Tradicionalmente los frutos secos han sido considerados como alimentos de gran valor nutricional por su capacidad de aporte de una extensa variedad de sustancias beneficiosas. Por ejemplo, son una buena fuente natural de vitamina E, en especial las almendras y las avellanas, que contienen unos 20 mg por 100 g
de producto, siendo las recomendaciones de esta vitamina de 10 mg/día. La importancia de la vitamina E radica en su acción antioxidante, responsable de la neutralización de radicales libres, disminución de la oxidación lipídica, y debido a ello, la protección de las membranas celulares. Hay evidencias de que la vitamina E es un agente que reduce el riesgo cardiovascular y un importante anticarcinógeno, por lo que ingestas deficientes en vitamina E se han asociado a un incremento en el riesgo de diferentes tipos de cáncer y por otro lado, con efectos positivos en la prevención de las alteraciones vasculares (Meritxell et al., 2004; Chen et al., 2005).
3.6 Ácido fólico
Otra vitamina que los frutos secos aportan en abundancia es el ácido fólico, con valores alrededor de 60-70 μg/100g, a excepción de los cacahuetes que contienen hasta 240 μg/100g. El consumo de 100 g de nueces proporciona aproximadamente el 16% por día de las cantidades recomendadas de ácido fólico. Éste desempeña un papel estratégico en el metabolismo de la homocisteína, al reducir sus niveles en el plasma y, en consecuencia, disminuir el riesgo arteriosclerótico (Thambyrajah y Tounend, 2000).
3.7
Minerales
El contenido en micronutrientes en los frutos secos también es relevante. Los principales minerales que contienen son magnesio, potasio, calcio, selenio, cobre y zinc (Cabrera et al., 2002), los cuales desempeñan acciones interesantes al participar a través de distintos mecanismos en el desarrollo y mantenimiento del esqueleto, del sistema nervioso y del sistema cardiovascular (Van-der-Schouw, 2000).
Los frutos secos (a excepción de castañas y piñones) son los alimentos más ricos en magnesio; en promedio aportan 260 mg/100g,
lo que supone más del 70% de las recomendaciones diarias de este mineral. Destacan sobre todo las almendras, anacardos y avellanas. El contenido en potasio también es muy elevado, alcanzando los 1042 mg/100g en los pistaches. Cacahuetes, almendras y piñones presentan niveles de potasio de 600800 mg/100g. Es destacable la riqueza en selenio, fundamentalmente en las nueces, dicho mineral presenta acción sinérgica antioxidante con la vitamina E, lo cual es muy positivo con respecto a las enfermedades cardiovasculares (Anderson, 2001). Por el contrario, su contenido en sodio es muy bajo, por lo que son aconsejables para el control de la hipertensión arterial, con la excepción de aquellos frutos secos a los que se ha añadido sal durante el procesado.
Son una buena fuente de calcio, especialmente las almendras, ya que aportan aproximadamente entre 200-270 mg de calcio por cada 100g de producto. Esto supone al menos una cuarta parte de las recomendaciones dietéticas de este mineral. Los frutos secos con menor contenido en calcio son los piñones (menos de 100mg/100 g). Su contenido en hierro tampoco es desdeñable, aunque es un hierro de difícil absorción. Sobresalen las avellanas y piñones con 6-9 mg/100g. El resto de los frutos secos presentan cantidades inferiores a 5 mg/100 g.
Por último, la presencia de zinc, confiere a estos alimentos propiedades de alto valor nutricional y funcional, al intervenir en procesos inmunológicos y de funcionamiento celular. Destacan por su contenido, los piñones y las almendras (USDA, 2006).
3.8 Fitoesteroles
Los frutos secos contienen un cierto número de esteroles, distintos del colesterol, algunos de ellos como el beta-sitosterol, presentes en una concentración relativamente alta. Otros esteroles que aparecen en menor cuantía son
estigmasterol, campesterol y avenasterol. Los esteroles vegetales, o fitoesteroles, desempeñan un papel importante en la fisiología corporal dado que contribuyen a reducir la absorción del colesterol. Dada la similitud química entre dichos esteroles y el colesterol, los fitoesteroles compiten con este último por su interacción con la acil-colesterol acil transferasa (ACAT), enzima responsable de regular el ritmo y la cuantía del colesterol a absorber. En presencia de esteroles vegetales, se favorece la eliminación del colesterol con las heces, lo que contribuye a incrementar el número de receptores para las lipoproteínas de baja densidad (LDL) del parénquima hepático, con lo que se acelera el catabolismo de éstas y se consigue un mejor control en los niveles del colesterol en el plasma (efecto hipercolesterolemiante) (Ikeda y Sugano, 1998). Por lo que se han reconocido los efectos de los fitoesteroles en la prevención de las enfermedades cardiovasculares y de ciertas enfermedades crónicas (Flight y Clifton, 2006).
3.9 Fitoestrógenos
Los fitoestrógenos se dividen en tres grupos desde el punto de vista químico, las isoflavonas, los cumestanos y los lignanos que muestran una actividad agonista estrogénica por interaccionar directamente con los receptores estrogénicos. Los fitoestrógenos más abundantes y más ampliamente estudiados son la genisteína y la daidzeína que pertenecen al grupo de las isoflavonas y tienen efectos positivos sobre el perfil lipoproteico al disminuir el colesterol total las LDL y los triglicéridos tanto en ratas como en humanos; estos efectos se han observado empleando altas concentraciones de dichas isoflavonas. Además, en función de la variedad de fruto seco empleado, la cantidad de genisteína y daidzeína es diferente, siendo el cacahuete el que presenta mayor cantidad de ambas. Su biodisponibilidad, absorción e interacciones potenciales con otros componentes de la dieta
resulta incierta hasta el momento (Meritxell et al., 2004).
4. Implicaciones de los componentes bioactivos de los frutos secos en el resguardo de la salud
Existen estudios científicos que demuestran que los frutos secos presentan beneficios sobre la salud, relacionando su consumo con una menor incidencia del riesgo de sufrir enfermedades cardiovasculares. También presentan efectos benéficos sobre varios tipos de cáncer, diabetes tipo II y obesidad (Fraser, 1999; González et al., 2001; Rui et al., 2002).
Estas evidencias ponen de manifiesto que la ingesta de frutos secos es una forma fácil de prevenir algunas enfermedades que son causa de morbi-mortalidad del mundo occidental (Krauss et al., 2000). En un reciente estudio controlado con nueces en pacientes hipercolesterolémicos de ambos sexos, se observó una reducción significativa del colesterol total y las LDL con la dieta enriquecida en nueces (alrededor de 50 g al día) en comparación con una dieta control, isoenergética y con la misma proporción de grasa total y de ácidos grasos monoinsaturados. Por tanto, el efecto hipocolesteromiante de las nueces parece ser aditivo al de la dieta mediterránea (Zambón, 2000).
En definitiva, los frutos secos constituyen uno de los alimentos más completos, ya que contienen una alta cantidad de nutrientes esenciales para el organismo con propiedades no sólo alimenticias sino funcionales y benéficas para la salud.
4.1 Cardiopatías
El estudio de los frutos secos, en particular su acción cardiosaludable y beneficio general sobre el sistema cardiovascular, ha sido objeto de numerosos estudios por especialistas de diversas disciplinas. Estos trabajos
multidisciplinarios revelan que el perfil nutricional único de estos alimentos hace que el consumo regular de frutos secos proteja sobre ciertos tipos de cáncer, ayude a controlar los niveles de colesterol y disminuya la mortalidad causada por enfermedades cardiovasculares, sin provocar exceso de peso u otros efectos colaterales en el consumidor. El primer estudio realizado en este ámbito fue efectuado en el seno de la comunidad religiosa de los Adventistas del Séptimo Día de California (Fraser et al.,1992). Los individuos que ingerían frutos secos 5 o más veces por semana tuvieron una reducción del 50% del riesgo de enfermedad coronaria en comparación con los que nunca los consumían.
Otros estudios epidemiológicos en sujetos con enfermedad coronaria isquémica y que han sufrido infarto de miocardio, han detectado bajos niveles de γ-tocoferol en sangre, pero no de α-tocoferol. Esto puede ser debido, entre otros factores, a que las células prefieren la captación de γ-tocoferol el cual es un antioxidante presente en las nueces y éste a su vez, favorece la captación de α-tocoferol, activando de este modo su efecto antioxidante (Gao et al., 2002).
Ensayos clínicos recientemente han demostrado beneficios consistentes del consumo de nuez y cacahuate en la disminución de padecer una enfermedad cardíaca coronaria. Un análisis combinado de 4 estudios epidemiológicos de EE. UU. mostró que los sujetos que contaban con un mayor consumo de frutos secos presentaban 35% menos el riesgo de padecer una cardiopatía coronaria (Albert et al., 2002). La reducción de la mortalidad por cardiopatía coronaria total se debió principalmente a una disminución de la muerte súbita cardíaca. Los estudios clínicos han evaluado los efectos de diferentes frutos secos y cacahuetes en la concentración de lípidos, lipoproteínas, y diversos factores de riesgo de cardiopatía coronaria, incluyendo la oxidación, la inflamación y la reactividad
vascular (Jiang et al., 2006). La evidencia de estos estudios muestra consistentemente un efecto benéfico sobre estos factores de riesgo. Por lo anterior, nueces y cacahuates son las fuentes de numerosos nutrientes cardioprotectores y si habitualmente son incorporados en la dieta, se espera que el riesgo de sufrir una cardiopatía coronaria disminuya considerablemente (Kris et al., 2008).
4.2
Diabetes
Recientemente, ha surgido interés por el valor potencial de las nueces en la dieta de las personas con diabetes. Los datos obtenidos en un grupo de enfermeras, que fueron sometidas a un estudio sobre su estado de salud, relacionan el consumo frecuente de frutos secos con un riesgo reducido de desarrollar diabetes y enfermedad cardiovascular (Hu et al., 2001). La aceptación actual de que los frutos secos ya no son perjudiciales y que ahora se pueden recomendar para las personas en riesgo de enfermedad cardiaca, ha llevado a una reevaluación de la posible función de los frutos secos en la dieta del diabético. Ensayos controlados aleatorios de pacientes con diabetes tipo II han confirmado los efectos beneficiosos de los frutos secos sobre los lípidos en sangre. Se concluye que no hay justificación para no considerar la inclusión de frutos secos en la dieta de las personas con diabetes en vista de su potencial para reducir el riesgo de una cardiopatía coronaria, aunque su capacidad para influir en el control glucémico sigue siendo incierto (Jenkins et al., 2008).
4.3 Cáncer
Si bien la mayoría de los estudios clínicos y epidemiológicos que se han realizado con frutos secos han sido dirigidos a evaluar el efecto de éstos sobre las enfermedades cardiovasculares, muy pocos han buscado encontrar una relación con el cáncer. Sin embargo, debido al importante aporte de
ácidos grasos poliinsaturados y de diferentes fitonutrientes, el consumo de frutos secos se ha relacionado con la disminución en la aparición de diferentes tipos de cáncer. No obstante, los datos experimentales sobre el papel de este grupo de alimentos en la carcinogénesis son limitados, algunos incluyen a las almendras en la ingesta diaria de ratas y su relación con la disminución en la aparición de tumores rectales. Los autores sugieren que el tipo de ácidos grasos que contienen las almendras o bien otros compuestos presentes en ellas, serían los responsables de la protección observada (Davis e Iwahashi, 2001). Otros estudios sobre pacientes humanos con cáncer de próstata han demostrado que los pacientes con esta patología ingerían menores cantidades de selenio, nutriente que se encuentra en grandes cantidades en diferentes frutos secos y especialmente en las nueces de Brasil (Brooks et al., 2001).
Por lo anterior es de suma importancia contar con más estudios experimentales y explorar los posibles efectos del consumo de frutos secos y los mecanismos bioquímicos relacionados con el estrés oxidativo, la cinética del ciclo celular y el riesgo de padecer cáncer (Paul et al., 2008).
4.4
Recomendaciones
Los frutos secos son fuentes ricas en múltiples nutrientes y su consumo se asocia con beneficios para la salud, incluida la reducción del riesgo de padecer una enfermedad cardiovascular. Esto ha llevado a recomendaciones para aumentar su consumo. Sin embargo, también son altos en grasa (aunque en gran parte no saturada). Las asociaciones entre estas propiedades, el balance energético positivo y el peso corporal, plantean preguntas sobre dichas recomendaciones. Esta cuestión se aborda a través de la asociación entre el consumo de frutos secos y el balance energético. Los
estudios epidemiológicos documentan una asociación inversa entre la frecuencia de consumo de frutos secos y el Indice de Masa Corporal (IMC). Los ensayos clínicos revelan que en poco o nada, se varía el peso con la inclusión de varios tipos de frutos secos en la dieta durante 6 meses (Sabaté, 1999). Por lo anterior, se sugiere que las nueces pueden ser incluidas en la dieta, con moderación, para mejorar la palatabilidad y calidad de los nutrientes sin representar una amenaza para el aumento de peso (King et al., 2008).
Finalmente, Lindsay (2008) plantea algunas áreas prioritarias de investigación sobre el consumo, composición y efectos en la salud de los frutos secos:
La composición, la biodisponibilidad de los nutrientes y otros componentes bioactivos.
Métodos para evaluar la ingesta de frutos secos, incluyendo marcadores biológicos y las cantidades de frutos secos que se consumen.
Viabilidad de la inclusión de los frutos secos y semillas como un grupo de alimentos por separado y de igual forma aumentar la ingesta de frutos secos.
Beneficios para la prevención de la insuficiencia cardíaca congestiva, incluidos los estudios clínicos en pacientes con esta condición, para evaluar los efectos de los frutos secos sobre los marcadores de riesgo de enfermedad cardíaca.
Efectos de los frutos secos en el control glucémico y la respuesta a la insulina, la glucemia postprandial, y la mejora en los factores de riesgo de enfermedad en pacientes con prediabetes y diabetes.
Reacciones alérgicas, incluyendo su prevalencia y consecuencias, las causas de la sensibilización, los biomarcadores de reacciones graves y la reactividad cruzada a los diferentes tipos de nueces.
Conclusiones
Los frutos secos y su moderado costo económico permite su consumo por parte de la población en general, traduciéndose en un bienestar social, debido a su producción y a la posibilidad de prevenir ciertas enfermedades como: la obesidad, cáncer, cardiopatías, diabetes tipo II y de aquellas relacionadas con la ingesta deficitaria de macronutrientes, fitonutrientes y oligoelementos. El consumo de frutos secos y su presencia en la ingesta constituyen una contribución preventiva eficaz ante enfermedades que por morbilidad y mortalidad, costos económicos, gastos asistenciales, decremento productivo y su descontrolada recurrencia en su conjunto, reducen de manera importante la calidad de vida. Dados los significativos aportes señalados, cobra pertinencia la continuidad de los estudios realizados sobre este tipo de alimentos abriendo la posibilidad de su incorporación en alimentos que no los contengan de manera habitual y por lo tanto conferirles la característica de alimentos funcionales, sin detrimento de su cualidad sensorial.
Agradecimientos
J.J. Luna-Guevara agradece al Consejo Nacional de Ciencia y Tecnología (CONACyT) y a la Universidad de las Américas, Puebla por el financiamiento de los estudios de doctorado.
Referencias
Albert, C., Gaziano J. M., Willett W., y Manson, J. 2002. Nut consumption and decreased risk of sudden cardiac death in the physicians health study. Archieves of Internal Medicine, 162 (12): 382-1387.
Anderson, J. B. 2001. Minerales. En: Mahan L.K. y Escote S. S. (Eds). Nutrición y Dietoterapia de Krause. McGraw-Hill Interamericana, México.pp. 120-126.
Araya, L. H. y Lutz, R. M. 2003. Alimentos Funcionales y Saludables. http://www.scielo.cl/scielo.php Accesada:25/01/2010.
Brooks, J., Metter, E., Chan D., Sokoll L. y Landis P.2001. Plasma selenium level before diagnosis and the risk of prostate cancer development. Journal of Urology. 166:2034-2038.
Brown, A. y Hu, F. 2001. Dietary modulation of endothelial function: implications for cardiovascular disease. American Journal of Clinical Nutrition. 73: 673-861.
Cabrera, C., Lloris, F., Giménez, R., Olalla, M., y López M. 2002. Mineral content in legumes and nuts: contribution to the spanish dietary intake. Science the Total Enviroment. 1:14.
Chan, W. 2004. Human nutrition. En: Jensen, W. K.; Davine, C. y Dikeman, M. (Eds.). Encyclopedia of Meat Science. Elsevier Science Ltd. London, UK. pp. 614-623.
Chen C., Milbury, P., Lapsley, K. y Blumberg J. 2005. Flavonoids fromalmond skins are bioavailable and act synergistically with vitamins C and E to enhance hamster and human LDL resistance to oxidation. Journal of Nutrition. 135:1366–73.
Código Alimentario Español. www.codexalimentarius.net . Accesada: 19/01/ 2010.
Davis, P. y Iwahashi C., 2001. Whole almonds and almond fractions reduce aberrant crypt foci in a rat model of colon carcinogenesis.CancerLetters. 165:27–33.
F.A.O. Food and Agricultural Organization. 2007. http://faostat.fao.org/site/339/default.aspx. Accesada: 20/02/2010
FAO/WHO.1973. Ad Hoc Expert Committee. Energy and protein requirements. WHO Tech Rep Ser 522/FAO Nutr Meet Rep Ser 52, WHO, Geneva/FAO, Rome.
Favier, J., Ripert, J., Toque C., y Feinberg, C.1995. Répertoire general des aliments. Table de composition. Paris: Technique and Documentation / Inra /Ciqual-Regal.
Flight, I. y Clifton P. 2006. Cereal grains and legumes in the prevention of coronary heart disease and
stroke: a review of the literature. European Journal of Clinical Investigation. 60:1145-1159.
Fraser, G., Jaceldo, K., Sabaté, J., Bennett, H. y Polehna P. 1999. Changes in body weight with a daily supplement of 340 calories from almonds for six months. FASEB Journal.13: A539
Fraser, G., Sabaté, J., Beeson, W. y Strahan T. 1992. A possible protective effect of nut consumption on risk of coronary heart disease: the Adventist Health Study. Archives of Internal Medicine. 152:14161424.
Fraser, G. 1999. Nut consumption, lipids and risk of a coronary event. Journal of Clinical Cardiology. 22(3):1-15.
Gao, R., William, L., Huang, T., Papas, M., A. y Qui M. 2002. The uptake of tocopherols by RAW 264.7 macrophages. Nutrition Journal. 1 (2): 1-9.
González, C., Agudo, A., Argilaga, S., Amiano, E., Ardanaz, A., Barricarte, N., Larrañaga, M., Chilarque M., Dorronsoro, C., Martínez C., Navarro J., Quirós M., Rodríguez M. y Tormo, M. 2001. Estudio prospectivo europeo sobre dieta, cáncer y salud (EPIC) y la investigación sobre dieta y cáncer en Europa. Anales del sistema sanitario de Navarra. 24 (1): 75-82.
Hasler,C. M. 2002. Functional foods: benefits, concerns and challenges- A position paper from the American Council on Science and health. Journal of Nutrition. 132: 3772-3781
Halverson, B.L., Holte K., Myhrstad C. W., Barikmo I., Hvattum E., Fagertun R. S., Wold A. B., Haffner K., Baugerod H., Andersen L. F., Moskaug J. O., Jacobs D.R y Blomhoff R. 2002. A systematic screening of total antioxidants in dietary plants. Journal of Nutrition.132: 461-471.
Hu, F., Manson, J., Stampfer, M., Colditz, G., Liu, S., Solomon, C. y Willett W. 2001. Diet, lifestyle, and the risk of type 2 diabetes mellitus in women. New England Journal of Medicine. 345:790-797.
Ikeda, I. y Sugano, M. 1998. Inhibition of colesterol absorption by plant sterols for mass intervention. Current Opinion in Lipidology. 9: 527-531
Jiang, R., Jacobs, D., Mayer, E., Szklo, M., Herrington D., Jenny, N., Kronmal R. y Barr, R.2006. Nut and seed consumption and inflammatory markers in the multi-ethnic study of atherosclerosis. American Journal of Epidemiology.163:222.
Jenkins, D., Hu, F., Tapsell, L., Josse A. y Kendall, C.2008. Possible benefit of nuts in type 2 diabetes. Journal of Nutrition.138:1752S–6S.
Jenkins, D., Kendall, C., Axelsen, M., Augustin, L. y Vuksan,V.2000.Viscous and nonviscous fibers, nonabsorbable and low glycaemic index carbohydrates, blood lipids and coronary heart disease. Current Opinion in Lipidology. 11:49-56.
King, J., Blumberg, J., Ingwersen, L., Jenab, M. y Tucker, K. 2008. Tree nuts and peanuts as components of a healthy diet. Journal of Nutrition.138:1736S–40S.
Krauss, R., Eckel, R., y Howard, B., 2000. AHA Dietary guidelines a statement for Healthcare professionals from the nutrition committee of the American Heart Association. Circulation.102: 22962311.
Kris, E., Hu, F., Ros, E. y Sabaté J. 2008. The role of tree nuts and peanuts in the prevention of coronary heart disease: multiple potential mechanisms. Journal of Nutrition.138:1746S–51S.
Lindsay, H. A. 2008. Priority Areas for Research on the Intake, Composition, and Health Effects of Tree Nuts and Peanuts.Journal of Nutrition. 138: S -1765.
Meritxell, N., Ruperto M., y Sánchez-Muniz F. 2004 Frutos secos y riesgo cardio y cerebrovascular. Una perspectiva española. ALAN.54(2):137-148.
Murakami, A., Koshimizu, K. y Ohigashi, H. 1998. Chemoprevention with food phytochemicals: screening, rodent studies, and action mechanisms. Journal of Medicinal Food. 1: 29-38.
Norma Mexicana NMX-FF-084-SCFI-2009 Productos Alimenticios no Industrializados para consumo Humano-Fruto Fresco-Nuez Pecanera Carya illinoensis (Wangenh) K. Koch Especificaciones y Métodos de Prueba.
Paul, A., Mazda, J., John, P., Vanden, H., Terence, F. y Steve, T. 2008. Tree nut and peanut consumption in relation to chronic and metabolic diseases including allergy.Journal of Nutrition.138: S -1762.
Plessi, M., Bertelli, D. y Monzani, A. 1999. Dietary fiber and some elements in nuts and wheat brans. Journal of Food Composition and Analysis.12: 9196.
Rui, J., Joan, M., Manson, E., Meir, J., Stampfer M., Simin, L., Walter, C., Willett, M., y Frank B. 2002. Nut and peanut butter consumption and risk of type II diabetes in women. The Journal of the American Medical Association. 288 (20): 2554-2560.
Sabaté, J. 1999. Nut consumption, vegetarian diets, ischemic heart disease risk, and all cause mortality: evidence from epidemiologic studies. The American Journal of Clinical Nutrition.70: 500-503.
Salas, S. J., Bullo, M., Perez, H., A., y Ros, E.2006. Dietary fibre, nuts and cardiovascular diseases. British Journal of Nutrition. 96 (2) 45S–51S
Salas, S. J., Megias, I., Arija, V., Cabré, P., Masana, L. y Solá A. 2001. Frutos secos. Sociedad Española Nutrición Comunitaria. editor. Guías alimentarias para la alimentación española, recomendaciones para una dieta saludable. IM&C, S.A. Madrid.España. pp:87-94.
Salas, S., Ros, R., E. y Sabaté, J. 2005. Frutos secos, salud y culturas mediterráneas. Glosa.España. pp 4649.
Sánchez, F. y Bastida, S. 2000. Biodisponibilidad de ácidos grasos. Revista de Nutrición Práctica 2000 4:48-64.
S.I.A.P. Sistema de información agroalimentaria y pesquera. www.siap.gob.mx. Accesada:19/01/2010.
Sleiman, R., Rodrigo, L. y Salas, S. 2002. Efecto de los frutos secos sobre la salud. Alimentos clave en la prevención de diferentes enfermedades. Alimentación, Nutrición y Salud. 9: 51-58.
Sociedad Española de Dietética y Ciencias de la Alimentación.2009. Frutos Secos.- Valor Nutricional.www.fiagro.org.sv/systemFiles/frutossec os.pdf. Accesada: 20/02/2009.
Solà, A. 2004. Efectos de los frutos secos sobre el colesterol y las enfermedades cardiovasculares. Ibérica: Actualidad Tecnológica.470:7-14.
Thambyrajah, J. y Townend, J. 2000. Homocysteine and atherothrombosis-mechanisms for injury. European Heart Journal. 21:967-974.
USDA National Nutrient Database for Standard.2006. www.nuthealth.org/nutrition/nutrient100g.html. Accesada: 20/02/2009.
Van-der-Schouw,Y. 2000. Phytoestrogens and cardiovascular disease risk. Nutrition, Metabolism Cardiovascular Disease.10:154.
Vázquez, J. y Sánchez, M.1994. Proteína de pescado y metabolismo del colesterol. Revista Española de Ciencia y Tecnología de Alimentos.34:589-608.
Zambón, D., Sabaté, J., Muñoz, S., Campero, B., Casals, E., Merlos, M., Laguna, J. y Ros, E. 2000. Substituting walnuts for monounsaturated fat improves the serum lipid profile of hypercholesterolemic men and women. A randomized crossover trial. Annals of Internal Medicine. 132: 538-546.

La
Temas Selectos de Ingeniería de Alimentos 4 – 1 (2010): 49 – 63

tuna: una perspectiva de su producción, propiedades y métodos de conservación
C. E. Ochoa-Velasco* y J. A. Guerrero-Beltrán
Departamento de Ingeniería Química, Alimentos y Ambiental. Universidad de las Américas, Puebla. Sta. Catarina Mártir, Cholula, Puebla. 72810. México
Resumen
La tendencia mundial actual se ha enfocado en el consumo de productos frescos, o muy similares a los frescos, en donde las frutas y hortalizas ocupan un lugar privilegiado. La tuna es una fruta que contiene componentes bioactivos y funcionales que han llamado la atención de los investigadores, debido a los diferentes efectos benéficos que estos tienen en la salud, siendo utilizada en tratamientos contra la gastritis, hiperglucemia, arteroesclerosis y diabetes. Sin embargo, para poder conservar estos componentes la tuna debe ser consumida en fresco, lo que representa un problema debido a que sus características fisicoquímicas y nutrimentales la hacen apta al ataque microbiano. Por lo tanto, es de vital importancia la investigación e implementación de tecnologías poscosecha que ayuden y coadyuven a las ya utilizadas en el aumento de la vida útil de la tuna. De aquí, que el objetivo de este artículo de revisión es dar a conocer las características fisicoquímicas, nutrimentales y funcionales de la tuna; así como, las tecnologías poscosecha que ayudarían a su almacenamiento y conservación.
Palabras clave: tuna, componentes bioactivos, poscosecha.
Abstract
Today, people around the world are trying to consume fresh food products or minimally processed food such as fruits and vegetables. Prickly pear possesses bioactive components which are excellent for human health; these components may be active against gastritis, hypoglycemia, arthrosclerosis and diabetes (just to mention some examples). However in order to keep these bioactive components intact in prickly pear, fruits have to be consumed in a fresh way. This could be a problem since prickly pear physicochemical and nutrimental properties make fruit perishable due to microbial spoilage. Therefore, it is important to improve the postharvest and preservation technology to increase the shelf life of prickly pear. The aim of this review is to present the physicochemical, nutritional and functional properties of prickly pear, as well as, the post-harvest technologies used for its storage and preservation.
Keywords: prickly pear, bioactive components, post-harvest.
*Programa de Doctorado en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: carlos.ochoavo@udlap.mx
Introducción
La tuna es una fruta perteneciente a la familia de las cactáceas y ha sido hasta ahora la más explotada y comercializada; junto con el nopal provee de alimentación a seres humanos y animales en algunas regiones de México. Sus demandas climáticas la hacen un cultivo muy apto para aquellas zonas donde no pueden desarrollarse otro tipo de plantas. México es el país con mayor producción y variedad de tuna a nivel mundial (SAGARPA, 2006).
Recientes estudios han demostrado que la tuna contiene altos niveles de agentes antioxidantes tales como ácido ascórbico, compuestos fenólicos y pigmentos betalainicos; así como altas concentraciones de compuestos como calcio, magnesio, prolina y taurina, que le proporcionan la característica de un alimento funcional (Galati et al., 2003). Sin embargo, la tuna al igual que otras frutas en México, requiere de una investigación básica integral que permita sentar las bases para mejorar las técnicas de producción, manejo y conservación.
Para la distribución y comercialización se necesita una fruta de buena presentación y calidad; lo cual no se logra de manera satisfactoria, debido a la corta temporada de producción, así como a que el tiempo de vida útil de la tuna en condiciones de almacenamiento normales es muy reducido. Por lo tanto, es una realidad la necesidad de buscar y probar tecnologías de procesamiento para la obtención de productos derivados, así como tecnologías poscosecha, empaque y embalaje tal como el almacenamiento bajo atmósferas modificadas y/o controladas que permitan un mejor aprovechamiento de la tuna.
El objetivo de esta revisión es dar a conocer datos sobre la producción mundial, nacional y estatal de la tuna, así como difundir información sobre la importancia nutricional y
funcional que tiene la tuna en la alimentación y las posibilidades de conservación y almacenamiento para prolongar su vida útil.
Revisión bibliográfica
1. Tuna
La tuna al igual que otras cactáceas tiene la peculiaridad de bajas necesidades de agua y por lo tanto, una alta eficiencia en el aprovechamiento de está, lo que les permite vivir en condiciones áridas y semiáridas (Gurrieri et al., 2000; Esquivel, 2004). Esta característica de eficiencia del agua se lo da su metabolismo ácido de las crasuláceas, donde los estomas se abren de noche y capturan el dióxido de carbono cuando la transpiración es baja (Mizrahi et al., 2002).
La tuna es una fruta carnosa (67 a 216 g de peso total) que varía en forma, tamaño y color dependiendo de la variedad, y tiene la característica de poseer una gran cantidad de semillas, un alto contenido de carbohidratos y una baja acidez, lo que le proporciona un sabor dulce y agradable (Piga, 2004; Cantwell, 1995). Existe una gran variabilidad en la constitución de la tuna que depende del tipo de cultivo, prácticas culturales, períodos de luz, clima y temporada de cosecha. Sin embargo, de manera general, está constituida por una cáscara gruesa y una pulpa jugosa. La cáscara, pulpa y semillas constituyen alrededor del 33 al 50%, 45 al 67% y del 2 al 10% del peso total del fruto, respectivamente. Durante el desarrollo de la tuna el contenido de pulpa se va incrementando, mientras que la cáscara se va haciendo más delgada restándole protección, pero ayudando al manejo poscosecha del fruto (Piga, 2004; Duru y Turker, 2005; Cantwell, 1995; Tesoriere et al., 2005b). Dependiendo de la variedad se pueden encontrar tunas de colores tales como blancas, verdes, amarillas, naranjas, rosadas, rojas y
púrpuras; así como tunas con y sin gloquideos, que consisten en espinas formadas por celulosa cristalina pura (Stintzing et al., 2001; Carrillo et al., 2002).
1.1 Producción de tuna
Se conocen aproximadamente 200 especies de tuna en el mundo. México se destaca como el mayor productor mundial; sin embargo, Chile, Argentina, Bolivia, Perú, Colombia, Marruecos, EUA, Sudáfrica, Italia, Grecia, Túnez, Egipto, Israel y Portugal entre otros, se han dedicado al cultivo de este fruto (Gurrieri et al., 2000; Esquivel, 2004; Inglese et al., 2002; Piga, 2004; Duru y Turker, 2005; Flores
y Corrales, 2003). Todos estos países basan su producción de tuna en una sola variedad, mientras que México tiene una riqueza varietal (Tabla I) que permite ofrecer al mercado una gran diversidad de tonalidades (blancas, amarillas, anaranjadas y rojas) y con un amplio periodo de cosecha que va desde mayo hasta noviembre, concentrándose la tuna de mayor calidad en los meses de julio y agosto.
La producción mundial de tuna en el año 2000 fue de 973,400 toneladas; aportando 7 países el 88% de la producción. México fue el principal productor aportando el 36% del total, seguido de Túnez con 12.8 % y Argentina 7.7%.
Tabla I. Principales variedades de tuna cultivadas en Méxicoa VariedadEstados de producciónEspecie VillanuevaPuebla--
AlfajayucanEstado de México, Hidalgo
Roja pirámidesEstado de México
BurronaZacatecas, Jalisco, San Luis Potosí
CristalinaZacatecas, Jalisco, San Luis Potosí, Aguascalientes
O. amiclaea T
O. amiclaea T
O. amiclaea T
O. amiclaea T
ReynaGuanajuato, Zacatecas O. amiclaea T
GaviaSan Luis Potosí O. amiclaea T
EsmeraldaGuanajuato, Querétaro O. amiclaea T
Rojo pelónZacatecas, Jalisco, San Luis Potosí, Guanajuato O. amiclaea T
Rubí reynaZacatecas, San Luis Potosí O. amiclaea T
TorreojaZacatecas, Jalisco, San Luis Potosí, Guanajuato O. amiclaea T
MoradaAguascalientes
O. amiclaea T
Amarilla montesaZacatecas, Jalisco O. amiclaea T
MiquihuanaTamaulipas, San Luis Potosí O. amiclaea T
Amarillo huesonaZacatecas, Jalisco O. amiclaea T
PicochuloZacatecas, Jalisco, Aguascalientes O. amiclaea T
CardónSan Luis Potosí, Zacatecas, Durango, Aguascalientes, Jalisco, Guanajuato, Querétaro.
aFlores y Gallegos, (1993)
O. streptacantha
La producción de tuna en México ha tenido un aumento gradual (Tabla II) en cuanto a rendimiento se refiere (ton/Ha). El Estado de México y Zacatecas se han convertido en los principales estados productores de tuna, seguidos de Hidalgo y Puebla. Los estados de Zacatecas y Guanajuato fueron los estados con mayor crecimiento durante el periodo de 20002006 con 45 mil ton y 6.6 mil toneladas, respectivamente (SAGARPA, 2006).
Para el año 2006, la producción nacional fue de 378,698 toneladas. En donde el Estado de México y Zacatecas representan el 72% de la producción nacional (64% de la superficie sembrada). Para el año 2008, los estados con mayor superficie sembrada fueron los estados de Zacatecas y el Estado de México con 19,428.81 Ha y 16,255.00 Ha, respectivamente. Sin embargo, el estado de Puebla ocupa el primer lugar nacional en rendimiento (toneladas/hectárea), seguida de Durango, Estado de México y Guanajuato con un rendimiento de 18.43, 14.00, 10.30 y 9.76, respectivamente (SAGARPA-SIAP, 2008).
Dentro de los principales destinos de la producción nacional de tuna se tiene a Estados Unidos, Bélgica, España, Alemania y Holanda, entre otros (SIAP, 2001). Sin embargo, México no es el principal país exportador, ya que Italia domina el mercado Europeo, debido a la calidad y al precio; este dispone de mejores instalaciones para el empaque y mejores redes de distribución que incluso llegan a exportar a países como Estado Unidos y Canadá, que deberían de estar cubiertos por México.
Tabla II. Producción de tuna en Méxicoa
(Ha)
Europa Oriental y los países árabes, representan oportunidades de mercados altamente factibles para exportación. Sin embargo, los principales problemas que limitan la competitividad de México en estas regiones del mundo, son el alto costo del transporte y que no se utilizan técnicas de conservación adecuadas (Flores et al., 1995).
1.2 Características de la tuna
En años recientes ha existido una tendencia global al consumo de frutas y hortalizas debido a las continuas evidencias de que sus componentes tienen un efecto protector contra el daño por oxidación en componentes celulares; así como en mantener la condición redox necesaria para controlar la función celular. Aparte del contenido de vitaminas y minerales, las frutas y hortalizas tienen otros componentes que han sido reconocidos como factores potenciales en beneficiar la salud humana (Tesoriere et al., 2008; Chae Lee et al., 2002; Butera et al., 2002).
La tuna ha sido reconocida en México por sus numerosas virtudes nutritivas, químicas, industriales, ecológicas, medicinales y simbólicas, entre otras. Pero últimamente ha llamado la atención debido a sus propiedades nutricionales y funcionales (Castellanos y Yahia, 2008).
Producción (Ton)
Rendimiento (Ton/Ha) Precio medio rural ($/ton)
200550,146.4143,167.91366,383.758.492,125.11 200650,762.9143,118.91378,697.948.781,830.03 200753,211.5643,999.56325,663.337.402,532.62 200854,294.6145,974.61393,506.498.562,657.92 aSIAP-SAGARPA, (2008)
1.2.1 Composición
de la tuna
La parte comestible de la tuna está compuesta principalmente por agua (84-90%) y carbohidratos (10-15%) (Piga, 2004; Cantwell, 1995). Los sólidos solubles de la tuna se encuentran en un rango de 10-17%, con glucosa y fructosa como los azúcares predominantes (Piga, 2004; Sawaya et al., 1983; Sáenz, 1996). Contiene un alto valor de pH (5.3-7.1) y una baja acidez (0.05-0.18%) expresada como ácido cítrico, lo que influencia fuertemente en las operaciones de procesado (Piga, 2004; Moßhammer et al., 2006). Dentro de los ácidos reportados en la tuna se encuentra el ácido cítrico (62 mg/100g), el ácido málico (23.3 mg/100g), el ácido quínico (19.1 mg/100g) y el ácido shikímico (2.8 mg/100g); mientras que los ácidos isocítrico, fumárico, glicolítico y succínico solo se encuentran en trazas (Stintzing et al., 2001).
1.2.2 Características nutricionales
El contendido nutrimental de la tuna (Tabla III) es similar al de otras frutas (Stintzing et al, 2001), con un aporte calórico de 47-67 kcal/100g. Sin embargo, el alto contenido de calcio, fosforo y magnesio, así como aminoácidos libres y fibra, hace a la tuna una fruta con características nutricionales especiales (Sáenz, 1996; Stintzing et al., 2001).
La tuna posee cantidades significativas de ácido ascórbico (18 - 23 mg/100g) (Piga, 2004; Stintzing et al., 2001). Esta cantidad de ácido ascórbico es mayor a la que se encuentra en frutas como la manzana, pera, uva y plátano, pero en vitaminas tales como vitamina A, tiamina, riboflavina y niacina sólo se encuentran cantidades trazas (Sawaya et al., 1983). Estudios recientes demuestran que la tuna es una buena fuente de calcio y magnesio con valores de 59 mg/100g y 98.4 mg/100g,
respectivamente, mientras que los niveles de sodio, potasio, hierro y fosforo se encuentra en los mismos niveles de las otras frutas (Askar y El-Samahy, 1981; Stintzing et al., 2001).
Adicionalmente, la tuna contiene altos niveles de prolina y taurina, lo cual es muy peculiar ya que este último aminoácido no es común en el reino vegetal (Tesoriere et al., 2005b). La pulpa de tuna puede ser utilizada como fortificante natural de alimentos, debido a los altos niveles de aminoácidos. Por ejemplo, en bebidas energéticas (El-Samahy et al., 2007).
1.2.3
Características funcionales
Actualmente los consumidores son más exigentes y educados acerca del valor nutrimental de los alimentos, lo que ha provocado un cambio en sus hábitos alimenticios; ellos demandan alimentos funcionales que sean ricos en componentes bioactivos, fibra dietética, colorantes naturales, vitaminas y minerales, bajos en grasas, libres de aditivos sintéticos y más prácticos (ElSamahy et al., 2007; Lund, 2002).
En los últimos años la comunidad científica ha mostrado mayor interés con respecto a los beneficios que proporciona la tuna a la salud. Diferentes investigaciones han demostrado la mejora de la función plaquetaría, la reducción de lípidos y triglicéridos en la sangre y el colesterol total y la reducción de las concentraciones de isoprotanos en la sangre lo cual indica un menor daño oxidativo. Sin embargo, son escasos los trabajos realizados y aún se desconocen los mecanismos de acción. La tuna ha sido muy utilizada en tratamientos contra la gastritis, hiperglucemia, arteroesclerosis y diabetes (Galati et al., 2003; Butera et al., 2002; Stintzing et al., 2005; Gurrieri et al., 2000; Tesoriere et al., 2005a).
Tabla III. Composición química de la pulpa de tuna a,b,c,d
NutrientesValores por cada 100 g de pulpa
NutrientesValores por cada 100 g de pulpa
Humedad (g)84-89Riboflavina (mg)0.060
Energía (kcal/kJ)47-67/196-280Niacina (mg)0.460
Proteína (g)0.73Vitamina B-6 (mg)0.060
Lípidos totales (g)0.51
Cenizas (g)1.64
β-Caroteno (mg)25
β-Cryptoxantina (mg)3
Carbohidratos (g)10-15.Vitamin A, (IU)43
Fibra total (g)3.6
Aminoácidos
Minerales Prolina (mg/L)1768.7
Calcio (mg)59Glutamina (mg/L)574.6
Hierro (mg)0.30Taurina (mg/L)572.1
Magnesio (mg)98.4Serina (mg/L)217.5
Fosforo (mg)24Alanina (mg/L)96.6
Potasio (mg)220Ácido glutámico (mg/L)83.0
Sodio (mg)5Metionina (mg/L)76.9
Zinc (mg)0.12Lisina (mg/L)53.3
Cobre (mg)0.080
Lípidos
Selenio (mcg)0.6Ácidos grasos (Saturados) (g)0.067
Vitaminas
Ácidos grasos (monoinsaturados) (g)0.075
Ácido ascórbico (mg)18-23Ácidos grasos (Poliinsaturados) (g)0.213
Tiamina (mg)0.014
aUSDA, (2009); bPiga, (2004); cStintzing et al ., (2001); dAskar y EL-Samahy, (1981)
Se presume que los beneficios del consumo de tuna se deben a que es una fuente importante de componentes funcionales y nutracéuticos, tales como el ácido ascórbico, compuestos fenólicos, flavonoides, αtocoferoles y betalainas en tunas rojas y amarillas (El-Samahy et al., 2006). Estudios en la tuna han demostrado que la actividad antioxidante de plantas bioactivas basan su acción de manera directa como secuestrante de radicales libres y de manera indirecta en la relación que tiene con la quelación de los elementos de transición (Chae Lee et al., 2002). No obstante, estas concentraciones de antioxidantes en general, parecen ser muy variables, ya que no solo existe una gran variabilidad de estos compuestos en las plantas, sino que además existen muchas variedades de tuna, así como una gran
diversidad de opiniones en los métodos adecuados para evaluar estos antioxidantes en los tejidos vegetales (El-Samahy et al., 2007; El- Samahy et al., 2006; Gurrieri et al., 2000).
En un estudio realizado por Butera et al. (2002) se evaluó la actividad antioxidante de tres variedades de tuna amarilla, roja y blanca. Encontraron que la tuna amarilla muestra la mayor cantidad de betalainas, siendo el pigmento principal la indicaxantina (89%). La betanina parece ser la de mayor concentración en tuna roja (66%) de los pigmentos betalainicos. Finalmente, la tuna blanca muestra la menor cantidad de betalainas y contiene exclusivamente indicaxantina. Algunos estudios demuestran que la indicaxantina es más biodisponible que la betanina (Kanner et al., 2001; Tesoriere et al.,
2008). Este mismo estudio demostró que el contenido de ácido ascórbico es muy similar y no se encontró diferencia significativa entre variedades, proporcionando aproximadamente del 30-40% de la capacidad antioxidante total. Butera et al. (2002) reportan que la capacidad antioxidante (ABTS) es mayor en la tuna amarilla que en la tuna roja y blanca. Sin embargo, en pruebas realizadas en glóbulos rojos expuestos a hidroperóxidos orgánicos utilizando α-tocoferol como referencia, muestran que la tuna blanca es más efectiva en la inhibición de la oxidación de lípidos, así como en el aumento de la resistencia a la oxidación.
Todo parece indicar que los pigmentos betalainicos contribuyen a la actividad antioxidante de las tunas. Aunque deben ser evaluados en función del efecto real de estos pigmentos para su uso en la dieta, su biodisponibilidad, bioactividad y su eventual digestión (Tesoriere et al., 2008).
2. Almacenamiento, conservación y productos de tuna
Los cambios socioculturales en los últimos años han creado la demanda de alimentos de consumo fácil y rápido; dirigiéndose a alimentos seguros, sanos, libres de aditivos y conservadores y en muchas ocasiones con un valor agregado. Estos alimentos tienen que ser frescos o con características muy similares a los frescos, lo cual ha provocado la demanda de frutas y hortalizas procesadas en fresco. Por lo tanto, ya no basta con prolongar la vida útil del fruto durante un período de tiempo más largo, sino que además llegue al consumidor final en condiciones sensoriales y de calidad óptimas (Zapata y Segura, 1996).
Una de las líneas de investigación que se ha centrado en el procesamiento de frutas y hortalizas es llamada procesamiento mínimo. Wiley (1997) describió el término de frutas y hortalizas mínimamente procesadas como
todas aquellas que mantienen tejidos vivos, así como, aquellas que han sufrido ligeras modificaciones en sus características de frescura, incluyendo como métodos de conservación la refrigeración así como la modificación y control de la atmósfera de envasado. Esta definición incluye al procesamiento mínimo dentro de las tecnologías poscosecha, que de manera general se refiere a la organización global del proceso de tratamiento, conjunto de métodos de conservación, empaquetado y transporte del producto desde su recolección hasta el consumo. Teniendo como objetivos primordiales conservar el producto durante un período más amplio, manteniendo al máximo su calidad y características sensoriales, nutritivas y sanitarias al tiempo que se reducen pérdidas y se minimiza el costo del proceso (Zapata y Segura, 1996).
2.1 Manejo poscosecha
Se estima que cerca del 25-80% de la producción hortofrutícola se pierde en poscosecha (Zapata y Segura, 1996) debido a un manejo y manipulación defectuosa. Al igual que otras frutas, la tuna presenta un elevado carácter perecedero, presentando manchas y podredumbres a escasos 9 días tras su recolección y a 20 días después de su cosecha se ha perdido del 70 al 80% de la producción (Cantwell, 1995; Corrales et al., 1997). Lo anterior es debido principalmente a los daños mecánicos, la deshidratación de la piel y el ataque de patógenos causantes de pudriciones entre los que se destacan Fusarium spp., Alternaria spp., Chlamydomyces spp., y Penicillium spp. (Cantwell, 1995). Adicionalmente se presenta el problema debido a la estacionalidad de la producción, afectándose con ello la rentabilidad de los sistemas de producción (Flores y Gallegos, 1993).
A continuación se presenta de manera resumida las etapas del manejo poscosecha de la tuna.
Recolección
La recolección de la tuna se realiza generalmente de dos maneras manuales. La primera es comúnmente llamada a torzón donde la tuna se gira y se trocea, mientras que la segunda forma es con cuchillo tratando de cortar una parte del nopal para evitar el daño a la tuna.
Transporte y recepción
Una vez cortados los frutos, estos son depositados en cajas de plástico o madera, para ser transportados hasta la empacadora en donde continuará el acondicionamiento de los frutos.
Desespinado
La tuna no se puede comercializar de forma normal sin antes haber pasado por el desespinado, en donde se eliminan los ahuates o gloquideos de las tunas. Actualmente el desespinado se hace de dos formas, la primera es de forma mecánica, en donde las tunas se hacen pasar por unas bandas transportadoras que contienen rodillos con cerdas de plástico, que eliminan el ahuate, la segunda forma es por medio de escobas en donde las personas limpian (barrido) las tunas, eliminando el ahuate.
Selección
La tuna se selecciona por calidad y tamaño. Posterior a la limpieza, las tunas caen a una banda transportadora la cual está provista de una serie de subdivisiones que se utilizan para separar los frutos seleccionados en base a su tamaño. Dependiendo de la zona geográfica son los tamaños que se manejan. De manera
general se manejan 5 tamaños: extra, primera, segunda, tercera y armada. La selección la deben realizar personas debidamente capacitadas para reconocer y separar frutos en buen estado de aquellos con daños mecánicos, podridos o malformados.
Empaque
La finalidad de empacar la tuna es proporcionar al producto las condiciones adecuadas para que durante el transporte al centro de comercialización no se dañe, facilitar su manipulación y darle una presentación atractiva que motive su compra y consumo (Barrios et al., 2003).
La tuna se empaca en cajas de madera para el mercado nacional y en cajas de cartón para el mercado de exportación. El envase de cartón presenta ciertas ventajas, ya que el peso de tuna por caja es menor, lo que provoca que no existan daños al producto, además sirve para imprimir el sello o marca comercial del producto.
Comercialización
La comercialización para el mercado nacional se da en las centrales de abasto de los principales centros de consumo, de ahí se distribuye a los mercados municipales haciendolas disponible para el consumidor final. El transporte se realiza en camiones o tráilers dependiendo del volumen demandado.
Todo el manejo poscosecha de la tuna se lleva a cabo sin una cadena de frío y modificaciones a la atmósfera que rodea al producto, por lo que el tiempo de vida útil es muy corto.
2.2 Almacenamiento en refrigeración
El almacenamiento a bajas temperaturas es el método de conservación más utilizado para productos en fresco. Ayuda a mantener una
adecuada calidad visual, reducir la respiración, frenar el ablandamiento y reducir el crecimiento microbiano (Artés et al., 2002; Brackett, 1987; Jacxsens et al., 2002). La temperatura de un producto debe disminuirse a un nivel justo por encima del punto de congelación del tejido o por encima de la temperatura umbral, ya que de lo contrario en productos sensibles a bajas temperaturas se produce el llamado daño por frío (Aguayo, 2003). Los efectos del daño por frío generalmente no son visibles a temperaturas de refrigeración, sino que se manifiestan a temperatura ambiente (Saltveit y Cabrera, 1987). Sin embargo, puede desarrollarse progresivamente durante la conservación a bajas temperaturas (Hong y Gross, 2001; Morris, 1982).
Existen pocos estudios reportados acerca del almacenamiento de tuna en refrigeración. En la mayoría de las investigaciones la variedad de tuna, así como la temperatura a la cual se almacena son los factores determinantes. Variaciones de 1 a 2 ºC afectan de manera significativa las características de la tuna. De manera general, los efectos de la refrigeración se ven reflejados en pérdida de peso durante el almacenamiento, llegando a perder el 10 % en peso en variedades como la Torreoja almacenada a 9ºC durante 1 mes, más 4 días de almacenamiento a temperatura ambiente (Corrales et al., 1997). Sin embargo, la variedad Burrona pierde tan solo 5% en peso después de 45 días de almacenamiento a 16-17ºC y una humedad relativa de 60% (Barrios et al., 2003). Piga et al. (1996), estudiaron el efecto del almacenamiento en refrigeración de tuna variedad Gialla, bajo condiciones de 6ºC a una humedad relativa de 95%, observando que después de 6 semanas de almacenamiento la tuna había perdido aproximadamente el 5% de su peso original. La pérdida de peso también tiene efecto de manera directa y proporcional sobre la turgencia, así como en el aumento en la
distancia de penetración de la cáscara (Corrales et al., 1997; Mercado et al., 2007).
El cambio de color es uno de los efectos importantes que tiene la refrigeración en el almacenamiento de la tuna. En la mayoría de las investigaciones se reportan cambios en la coloración pasando de los colores verdes, naranjas y rojos o púrpuras a un color amarillento, se cree que esto es debido a una disminución en la concentración de los pigmentos en cada variedad de tuna (Barrios et al., 2003; Corrales et al., 1997; Mercado et al., 2007). Otras características como el pH y los sólidos solubles tienden a disminuir, mientras que la acidez titulable tiende a aumentar con el tiempo de almacenamiento (Corrales et al., 1997; Piga et al., 1996; Mercado et al., 2007).
La temperatura de almacenamiento repercute de manera directa en tuna mínimamente procesada. En un estudio realizado por Ávila (2007) se almacenaron tunas por más de 10 días a una temperatura de 10ºC y se presentaron daños por microorganismos y pudriciones en aproximadamente 30-40% de las tunas, mientras que a 4ºC este mismo efecto se presentó sólo después de 25 días de almacenamiento.
De manera general se recomienda un almacenamiento de la tuna a una temperatura de 5-8ºC con 90-95% de humedad relativa y la adecuada ventilación para evitar los daños por frío y evitar la pérdida o deterioro de la tuna por aproximadamente 30 días (Kader, 2007).
2.3 Almacenamiento bajo atmósferas modificadas
Tras la cosecha de los productos hortofrutícolas los procesos de respiración siguen activos, dando como resultado que los carbohidratos, se conviertan en CO2, agua, energía y otros compuestos menores, usando el oxígeno necesario del aire circundante. El
agua formada en el proceso de respiración se torna parte del producto y el CO2 y el calor se difunden a la atmósfera. Cuando no existe suficiente oxígeno disponible, se forman otros subproductos como alcoholes, aldehídos y cetonas que imparten mal sabor a los alimentos, pudiendo dañar los tejidos celulares. Como consecuencia de estas reacciones, el producto vegetal se debilita y se vuelve susceptible al ataque de microorganismos. Por lo tanto, es de suma importancia que los productos hortofrutícolas sean envasados de manera adecuada para mantener la calidad durante su transporte, almacenamiento y comercialización (Zapata y Segura, 1996; Rodríguez et al., 2005).
La conservación de frutas y hortalizas bajo atmósferas modificadas consiste en empacar el producto en películas plásticas con una permeabilidad definida. Su fundamento se basa en el cambio de las condiciones gaseosas iniciales del entorno inmediato del producto como consecuencia de su metabolismo y la barrera que dé la película plástica. Existen muchas definiciones de atmósfera modificada, pero una de las más acertadas es la que define como aquella que se crea por alterar la composición gaseosa normal del aire (78% N2, 21% O2, 0,03% CO2 y trazas de gases nobles) para proporcionar una atmósfera óptima que permita prolongar la conservación, así como la calidad del producto (Zapata y Segura, 1996; Rodríguez et al., 2005).
Existen muy pocos trabajos presentados sobre el almacenamiento de tuna bajo atmósferas modificadas y/o controladas. Estos trabajos se pueden dividir en dos categorías, en los primeros la tuna es almacenada entera (con cáscara), mientras que la segunda categoría las tunas son tratadas mínimamente y empacadas bajo atmósferas modificadas.
El almacenamiento de tuna con cáscara bajo atmósferas modificadas y/o controladas se ha visto beneficiado en un aumento en la
vida útil, evitando el daño por frío y la pérdida de peso en tunas almacenadas bajo atmósfera modificada pasiva a 6ºC con 95% de humedad relativa, durante 3 semanas. Se ha reportado que la pérdida de peso fue de 3.7% y 1.5%, para tunas almacenadas sin empaque y con empaque (polietileno), respectivamente. Mientras que con las mismas condiciones de almacenamiento las pérdidas de peso fueron de alrededor del 7% para tunas sin empaque y 1.9% en tuna empacada con polietileno, durante un período de 6 semanas (Piga et al., 1996). Este mismo fenómeno fue observado en un estudio realizado por Morales (1995) observándose que la pérdida de peso es mayor en frutas almacenadas a temperatura ambiente (20ºC) en un 31%, mientras que a refrigeración (8ºC) es de 17.6% y en atmósferas controladas (10%CO2 y 5%O2) a 8ºC se da una pérdida de peso de 1-1.4%, debido a la reducción de la respiración y del calor producido. Piga et al. (1996) y Morales (1995) reportaron que los efectos del daño por frío (oscurecimiento de cáscara) se reducían en tunas almacenadas bajo atmósferas modificadas y controladas, respectivamente. Piga et al. (1996) reportaron que en tunas almacenadas sin empaque a 6ºC durante 3 semanas el daño por frío era de 35%; mientras que en tunas almacenadas en las mismas condiciones con empaque de polietileno el daño por frío era de 15%. Morales (1995) concluyó que las tunas no presentaban daño por frío después de 30 días de almacenamiento cuando las condiciones fueron de (10% de CO2 y 5% de O2).
El efecto del almacenamiento bajo atmósferas modificadas y/o controlados sobre el crecimiento de microorganismos todavía no está del todo claro ya que no se encontraron diferencias significativas sobre el crecimiento de mohos en tunas empacadas y almacenadas en atmósferas modificadas y/o controladas comparadas con tunas almacenadas sólo en refrigeración, por lo tanto se cree que el efecto inhibidor es únicamente por la temperatura de
almacenamiento (Piga et al., 1996; Morales, 1995).
La acidez titulable, pH, y sólidos solubles totales no se ven afectados por el empacado bajo atmósferas modificadas y/o controladas (Piga et al., 1996).
El almacenamiento bajo atmósferas modificadas en tuna (10%CO2+5%O2) evitan la degradación de la clorofila, manteniendo el color verde limón durante un período de almacenamiento de 30 días a 8ºC. Sin embargo, la textura no presenta diferencia significativa en tuna almacenada con y sin atmósferas modificadas (Morales, 1995).
2.4 Tuna mínimamente procesada
Ayala y Franco (1998) realizaron el almacenamiento de tunas mínimamente procesadas, las tunas fueron peladas y empacadas en dos diferentes tipos de películas plásticas (polipropileno y polietileno de baja densidad) y almacenadas a dos temperaturas de refrigeración (1.5 y 5.5ºC). Los resultados muestran que el polipropileno y la temperatura de 1.5ºC son las condiciones que mejor conservan las cualidades de la tuna, manteniendo el color verde por 10 días, una pérdida de peso de 0.6%, así como un incremento en la acidez y el contenido de azúcares reductores a los 20 días de almacenamiento; sin embargo, se reportó una desviación de la ruta respiratoria y el establecimiento de un metabolismo fermentativo. Ávila en 2007 reportó que tunas mínimamente procesadas empacadas y almacenadas a 10ºC durante 10 días tuvieron una pérdida de peso de 0.81% y 1.42% en tunas tratadas con preenfriamiento (aire forzado a 4ºC durante 2 horas) y sin preenfriamiento, respectivamente; mientras que las tunas partidas en mitades presentaron una pérdida de peso de 0.39%, y las tunas partidas en cuatro partes presentaron una pérdida de peso del 1.83%, esto debido al
mayor rompimiento de los tejidos celulares. Las tunas mínimamente procesadas (enteras y sin cáscara) y empacadas en bolsas de polipropileno tienen una vida útil prolongada por un período de almacenamiento de 20 días a 4ºC.
2.5 Productos procesados de tuna
Los pocos estudios realizados en tuna explican la carencia de productos procesados, más que aquellos productos naturistas.
La pulpa de tuna es la porción de la fruta más valiosa y como ya se mencionó anteriormente, tiene un pH elevado; por lo que se considera un producto de baja acidez, lo cual puede propiciar el crecimiento de microorganismos, especialmente de levaduras y bacterias mesofilas. La gran cantidad de semillas también es un obstáculo para su procesamiento y poder obtener un producto atractivo al consumidor (Moßhammer et al., 2006)
Diferentes investigadores han realizado estudios acerca de la estabilidad y viabilidad de productos procesados de tuna. A continuación se listan algunos productos obtenidos a partir de la tuna:
Jugo y concentrado de tuna, con una baja actividad de agua y 63-67 ºBrix que harían del concentrado un producto sumamente estable (Almendares et al., 1994)
Queso de tuna (Sáenz, 1995)
Mermeladas de tuna (Sawaya et al., 1983)
Productos enlatados (Joubert, 1993)
Frutas mínimamente procesadas y congelados (Moßhammer et al., 2006)
Bebidas refrescantes en polvo (Rodríguez et al., 2005)
Bebidas alcohólicas (Bustos, 1981).
Tuna deshidratada, útil en cereales, sopas, barras energéticas, etc. (Moßhammer et al., 2006)
Conclusiones
La investigación demuestra que ya no solo es una realidad, sino una necesidad el hecho de regresar al consumo de productos hortofrutícolas que proveen de una alimentación sana y segura, debido a la tendencia a enfermedades coronarias, oxidativas y de estrés. Productos del campo como la tuna no solo son capaces de alimentar, sino que además proveen de esos componentes bioactivos que ayudarían al tratamiento de las enfermedades crónico-degenerativas.
Dadas sus características, la tuna es un fruto que se prefiere consumir en fresco, por lo tanto, se deben de realizar mayores estudios para evaluar el efecto que tienen la temperatura, composición de gases y tipo de empaque sobre los componentes bioactivos, enzimas, microorganismos, parámetros fisicoquímicos y fisiológicos de la tuna durante el almacenamiento.
En México aún falta mucho por investigar y hacer en trabajo de campo, para proveer de información científica y tecnológica que pueda apoyar y por supuesto, ayudar en la aplicación de procesos y técnicas de conservación y tecnología poscosecha tales como las atmósferas modificadas y/o controladas. Así como las de procesamiento mínimo que actualmente están teniendo mucho auge por los múltiples beneficios que tienen en frutas y hortalizas como la tuna, ya que todo parece indicar que mantienen sus cualidades intactas.
Referencias
Aguayo, E. 2003. Innovaciones tecnológicas en la conservación de melón y tomate procesado en fresco. Tesis de doctorado. Universidad Politécnica de Cartagena, España.
Almendares, L., Sáenz, C. y Berger, H. 1994. Elaboración y concentración de jugo de tuna (Opuntia ficus indica (L) Mill), obtenido a partir de fruta fresca y con almacenaje refrigerado. X National congress of food science and technology. Pucón, Chile. Noviembre 11-13.
Artés, F., Gómez, P.A. y Artés, F. 2002. Alteraciones físicas, fisiológicas y microbianas de frutas y hortalizas procesadas en fresco. Alimentaria, 335, 69-74.
Askar, A. y El-Samahy, S. K. 1981. Chemical composition of prickly pear fruit. Deutsche Lebensmittel-Rundschau, 77(8): 279-281.
Ávila, J. 2007. Respuesta a diferentes condiciones de frigoconservación y películas plásticas de tuna (Opuntia amiclaea) mínimamente procesada. Tesis de licenciatura. Universidad Autónoma de Chapingo.
Ayala, G., y Franco, A. 1998. Efecto de películas plásticas en tuna (Opuntia Amiclaea) mínimamente procesada. Tesis de licenciatura. Universidad Autónoma de Chapingo.
Barrios, R. G., Hernández, A. B., Corrales, G. J. 2003. Avances sobre las respuestas de tuna (Opuntia spp.) variedad burrona, apacerada comercialmente. Datos no publicados.
Brackett, R.E. 1987. Microbiological consequences of minimally processed fruits and vegetables. Journal of Food Quality. 10:195-206.
Bustos, O.E 1981. Alcoholic beverage from Chilean Opuntia ficus-indica American Journal of Enology and Viticulture. 32: 228-229.
Agradecimientos
C.E. Ochoa Velasco agradece al Consejo Nacional de Ciencia y Tecnología (CONACyT) por el financiamiento de sus estudios de Doctorado.
Butera, D., Tesoriere, L., Di Gaudio, F., Bongiorno, A., Allegra, M., Pintaudi, A. M., Kohen, R. y Livrea, M. A. 2002. Antioxidant activities of Sicilian prickly pear (Opuntia ficus indica) fruit extracts and reducing properties of its betalains: betanin and indicaxanthin. Journal of Agricultural and Food Chemistry. 50:6895–6901
Cantwell, M. 1995. Postharvest management of fruits and vegetables stems. En Barbera, G., Inglese, P., Pimienta, E. (Eds). Agro-ecology cultivation and
uses of cactus pear. FAO. Plant Productión and Protection Paper No. 132. Rome, Italy. pp. 120-141.
Carrillo, A., Cruz, A., Cárabez, A., Guevara, F., Paredes, O. 2002. Hydrolytic Activity and Ultrastructural Changes in Fruit Skins from Two Prickly Pear (Opuntia spp.) Varieties during Storage. Journal of Agricultural and Food Chemistry. 50:1681-1685.
Castellanos, E. y Yahia, E. M. 2008. Identification and Quantification of Betalains from the fruits of 10 Mexican prickly pear cultivars by high-performance liquid chromatography and electrospray ionization mass spectrometry. Journal of Agricultural and Food Chemistry. 56:5758–5764.
Chae Lee, J., Ryul Kim, H., Kim, J. Suk Jang, Y. 2002. Antioxidant Property of an Ethanol Extract of the Stem of Opuntia ficus-indica var. Saboten. Journal of Agricultural and Food Chemistry. 50:6490-6496
Corrales, J., Andrade, J., Bernabe, E. 1997. Response of Six Cultivars of Tuna Fruits To Cold Storage. Journal of the Professional Association for Cactus Development. 2:160-168. http://www.jpacd.org, accesada 20/01/2010
Duru, B. y Turker, N. 2005. Changes in physical properties and chemical composition of cactus pear (Opuntia ficus-indica) during Maturation. Journal of the Professional Association for Cactus Development. 7:22-33. http://www.jpacd.org, accesada 21/01/2010
El-Samahy, S. K., El-Hady A. A., Habiba, A. y Moussa, T. E. 2006. Chemical and Rheological Characteristics of Orange-Yellow Cactus-Pear Pulp from Egypt. Journal of the Professional Association for Cactus Development. 8:39-51. http://www.jpacd.org, accesada 21/01/2010
El-Samahy, S.K., Abd El-Hady, E.A., Habiba, R.A., y Moussa, T.E. 2007. Cactus pear sheet and pasteurized and sterilized cactus pear juices. Journal of the Professional Association for Cactus Development. 9:136-148. http://www.jpacd.org, accesada 21/01/2010
Esquivel, P. 2004. Los frutos de las cactáceas y su potencial como materia prima. Agronomia Mesoaericana. 15(2):215-219.
Flores, C. A., de Luna, J. M., Ramírez, P. P. 1995. Mercado Mundial de la Tuna. Centro de Investigaciones Económicas, Sociales y Tecnológicas de la Agroindustria y de la Agricultura
Mundial (CIESTAAM). Universidad Autónoma de Chapingo. pp. 1-173.
Flores, C. A. y Corrales, J. J. 2003. Nopalitos y tunas, producción, comercialización, poscocecha e industrialización. Centro de Investigaciones Económicas, Sociales y Tecnológicas de la Agroindustria y de la Agricultura Mundial (CIESTAAM). Universidad Autónoma de Chapingo. pp. 1-7.
Flores, C. A. y Gallegos, C. 1993. Situación y perspectivas de la producción de tuna en la región Centro-Norte de México. Centro de Investigaciones Económicas, Sociales y Tecnológicas de la Agroindustria y de la Agricultura Mundial (CIESTAAM). Universidad Autónoma Chapingo, Chapingo, Edo. de México.
Galati, E. M., Mondello, M. R., Giuffrida, D., Dugo, G., Miceli, N., Pergolizzi, S., Taviano, M. F. 2003. Chemical characterization and biological effects of sicilian Opuntia ficus indica (L.) Mill. Fruit juice: antioxidant and antiulcerogenic activity. Journal of Agricultural and Food Chemistry. 51:4903-4908.
Gurrieri, S., Miceli, L., Lanza, C.M., Tomaselli, F., Bonomo, R.P., y E. Rizzarelli 2000. Chemical characterization of Sicilian prickly pear (Opuntia ficus indica) and perspectives for the storage of its juice. Journal of Agricultural and Food Chemistry. 48:5424-5431.
Hong, J.H. y Gross, K.C. 2001. Maintaining quality of fresh-cut tomato slices through modified atmosphere packaging and low temperatures storage. Journal of Food Science. 66:960-965.
Inglese, P., Basile, F., y M. Schirra 2002. Cactus pear fruit production. En: S. Park y Nobel, (Eds). Cacti: Biology and Uses. University of California Press. California, USA. 280p
Jacxsens, L., Devlieghere, F. y Debevere, J. 2002. Temperature dependence of shelf-life as affected by microbial proliferation and sensory quality of equilibrium modified atmosphere packaged fresh produce. Postharvest Biology and Technology., 26:59-73.
Joubert, E. 1993. Processing of the fruit of five prickly pear cultivars grown in South Africa. International Journal of Food Science and Technology 28: 377387.
Kader, A. A. 2007. Tuna. Recomendaciones para Mantener la Calidad Postcosecha. Postharvest technology. Research and information center.
http://postharvest.ucdavis.edu/Produce/ProduceFacts /Espanol/tuna.shtml, accesada: 01/02/2010
Kanner, J., Harel, S., Granit, R. 2001. Betalains. A new class of dietary antioxidants. Journal of Agricultural and Food Chemistry. 49:5178-5185
Lund, D. B. 2002. Food Engineering for the 21st Century. En: Welti, J., Barbosa, G., Aguilera, J. M. (Eds). Enginnering and food for the 21st century. Food preservation technology series. Crc press. Boca Raton, Florida. pp 3-12.
Mercado, J., López, M., Martínez, G., Sarahí, J., Arévalo, S. 2007. Estudio de las propiedades fisicoquímicas de las variedades de tuna rojo pelón (Opuntia ficus indica), morada, reina (Opuntia amyclaea) y Xoconostle (Opuntia matudae scheinvar) bajo almacenamiento refrigerado. IX Congreso de ciencia de los alimentos y V foro de ciencia y tecnología de alimentos. Guanajuato, Gto. Mayo 31.
Mizrahi, Y., Nerd, A., Sitrit, Y. 2002. New fruits for arid climates. En: J. Janick, A. Whipkey (eds.). Trends in new crops and new uses. ASHS Press, Alexandria, VA. pp. 378- 384.
Moßhammer, M. R., Stintzing, F. C., y Carle, R. 2006. Cactus Pear Fruits (Opuntia spp.): A Review of Processing Technologies and Current Uses. Journal of the Professional Association for Cactus Development. 8:1-25. http://www.jpacd.org accesada 20/01/2010
Morales, M. 1995. Efecto del ethrel en el desahuatado de tuna (Opuntia spp) y almacenamiento en atmósfera controlada. Tesis de licenciatura. Universidad Autónoma de Chapingo.
Morris, L.L. 1982. Chilling injury of horticultural crops: an overview. American Society for Horticultural Science. 17:161-162.
Piga, A., D’Aquino, S., Agabbio, M. y Schirra, M. 1996. Storage life and quality attributes of cactus pears cv “Gialla” as affected by packaging. Agricultura Mediterranea. 126:423-427.
Piga, A. 2004. Cactus pear: A fruit of nutraceutical and functional importance. Journal of the Professional Association for Cactus Development. 6:9-22. http://www.jpacd.org accesada 25/01/2010
Rodríguez, F., Rivera, A., González G. A. 2005. Uso de atmósferas modificadas y controladas. En: González, G. A., Gardea, A., Cuamea, F. (Eds). Nuevas Tecnologías de Conservación de Productos Vegetales Frescos Cortados. Ed. Logiprint Digital, México. pp. 447‐474.
Sáenz, C. 1995. "Food manufacture and by-products". Citado en Barbera, G., Inglese, P., Pimienta, E. (Eds). Agro-ecology cultivation and uses of cactus pear. FAO. Plant Productión and Protection Paper No. 132. Rome, Italy. pp. 137-143.
Sáenz, C. 1996. Foods products from cactus pear. Journal of the Professional Association for Cactus Development. 1:89-97. http://www.jpacd.org accesada 20/01/2010
SAGARPA, 2006. Retos y perspectivas para los pequeños productores mexicanos ante la apertura comercial. www.sagarpa.gob.mx accesada 16/02/2010
SAGARPA-SIAP, 2008. Anuario estadístico de la producción agrícola tuna.www.sagarpa.gob.mx, accesada 16/02/2010
Saltveit, M.E. y Cabrera, R.M. 1987. Tomato fruit temperature before chilling influences ripening after chilling. American Society for Horticultural Science 22(3):452-454
Sawaya, W.N., Khatchadourian, H.A., Safi, W.M., y. Al-Muhammad, H.M 1983. Chemical characterization of prickly pear pulp, Opuntia ficusindica, and the manufacturing of prickly pear jam. Journal of Food Technology. 18:183-193.
SIAP. 2001. Análisis agropecuario de la tuna. México. 10p.http://www.siea.sagarpa.gob.mx/InfOMer/analis is/tuna.html. accesada: 25/03/2010
Stintzing, F. C., Schieber, A., Carle, R. 2001. Phytochemical and nutritional significance of cactus pear. European Food Research and Technology 212:396–407.
Stintzing, F. C., Herbach, K. M., Mosshammer, M. R., Carle, R., Yi, W., Sellappan, S., Akoh, C. C., Bunch, R., Felker, P. 2005. Color, betalain pattern, and antioxidant properties of cactus pear (Opuntia spp.) clones. Journal of Agricultural and Food Chemistry 53:442- 451.
Tesoriere, L., Butera, D., Allegra, M., Fazzari M. y Livrea, M. A. 2005a. Distribution of betalain pigments in red blood cells after consumption of cactus pear fruits and increased resistance of the cells to ex vivo induced oxidative hemolysis in
humans. Journal of Agricultural and Food Chemistry. 53:1266-1270.
Tesoriere, L., Fazzari M., Allegra, M. y Livrea, M. A. 2005b. Biothiols, taurine, and lipid-soluble antioxidants in the edible pulp of sicilian cactus pear (Opuntia ficus-indica) fruits and changes of bioactive juice components upon industrial processing. Journal of Agricultural and Food Chemistry. 53:7851-7855.
Tesoriere, L., Fazzari, M., Angileri, F., Gentile, C. y Livrea, M. A. 2008. In Vitro Digestion of Betalainic Foods. Stability and Bioaccessibility of Betaxanthins and Betacyanins and Antioxidative Potential of Food Digesta. Journal of Agricultural and Food Chemistry. 56:10487–10492
USDA, 2009. Chemical composition of prickly pear pulp. National Nutrient Database for Standard Reference. http://www.ars.usda.gov/Research/docs.htm, accesada: 12/02/2010
Wiley, R.C. 1997. Introducción a las frutas y hortalizas refrigeradas mínimamente procesadas En: R.C. Wiley y J. Salguero (Eds). Frutas y hortalizas mínimamente procesadas y refrigeradas. Primera edición, Acribia. Zaragoza, España. pp 1-14.
Zapata, N.y Segura, P. 1996. Nuevas tecnologías de conservación de frutas y hortalizas: atmósferas modificadas. Cuadernos VALUE. Ediciones Mundiprensa.Madrid-Barcelona-México..

Temas Selectos de Ingeniería de Alimentos 4 - 1 (2010): 64 – 73

Granada (Punica granatum L): una fuente de antioxidantes de interés actual
O. A. López-Mejía*, A. López-Malo y E. Palou
Departamento de Ingeniería Química, Alimentos y Ambiental. Universidad de las Américas, Puebla. Sta. Catarina Mártir, Cholula, Puebla. 72810. México
Resumen
La granada (Punica granatum L.) es originaria de Irán y fue extendida a diversos países de Asia y la zona mediterránea. Este fruto fue introducido a América por misioneros españoles, y cultivado principalmente en México y Estados Unidos. En México, el cultivo se adaptó específicamente en el estado de Puebla. Sin embargo, por cuestiones de urbanización, hacía las décadas de 1970 y 1980, el cultivo fue desapareciendo. En Estados Unidos, el fruto ha sido cultivado en California y Arizona. La importancia actual de este fruto consiste, particularmente, en las propiedades que se han reportado en estudios recientes, los cuales revelan la presencia de componentes antioxidantes en el tallo, hojas, flores, cáscara, jugo y semillas. Estos componentes le confieren propiedades antiinflamatorias, antitumorales y anticancerígenas, entre otras, avaladas por investigaciones in vitro, así como in vivo. Debido a las propiedades de la granada y a su potencial como fuente de antioxidantes, se aplican estrategias para intensificar su cultivo en diversos países que incluyen las zonas de origen.
Palabras clave: granada, antioxidants.
Abstract
Pomegranate (Punica granatum L) is an Iran´s native fruit that was extended to several Asian and Mediterranean zone countries. It was brought to America by Spanish missioners and cultivated in Mexico and United States. In México, pomegranate was adapted to Puebla state. However, due to urbanization, during the 1970´s and 1980´s decades, most of the land utilized to cultivate this fruit in Puebla disappeared. In the United States, this fruit has been cultivated in California and Arizona. The current importance of pomegranate consists, specially, on its properties reported on recent studies. Such studies reveal antioxidant contents of stem, leaves, flowers, peel, juice, and seeds of pomegranate. These antioxidant compounds give to pomegranate anti-inflammatory, antitumor, and anticancer properties, among others; each one of these properties has been supported by in vitro and in vivo essays. Because of the mentioned pomegranate properties and its potential as an antioxidant source, several strategies to generate intensive cultivation zones are being developed in native lands and other countries.
Keywords: pomegranate, antioxidants.
*Programa de Doctorado en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: ofelia.lopezma@udlap.mx
Introducción
La granada (Punica granatum L.) es un fruto originario y producido en países de Medio Oriente que, hasta los 1980´s, fue ampliamente cultivado y consumido en el estado de Puebla. Al paso de los años, las áreas destinadas a su cultivo han ido desapareciendo, siendo substituidas por construcciones urbanas.
En la actualidad, este fruto ha cobrado importancia mundial por sus propiedades antioxidantes, mismas que le confieren propiedades farmacológicas anticancerígenas, antitumorales, antimicrobianas, antidiarreicas, hepatoprotectivas y para el control de enfermedades renales (Lansky y Newman, 2007; Syed et al., 2007; Bektas y Ozturk, 2007; Shahidi y Naczk, 2009; Celik et al., 2009). Otros autores refieren propiedades de reducción de riesgos cardiovasculares (Aviram y Dornfeld, 2001). Sus propiedades terapéuticas y farmacológicas se han investigado ampliamente (Borochov-Neori et al., 2009).
Además, por las tendencias actuales, la industria alimentaria requiere fuentes de antioxidantes naturales para aplicarse en el desarrollo de productos y aditivos. Por otro lado, la granada puede ser aprovechada como una de las fuentes de antioxidantes más importantes por los recientes hallazgos científicos, referentes a sus beneficios en la salud. El presente trabajo tiene el propósito de proporcionar información referente al fruto del granado, su origen, composición y sus propiedades antioxidantes recientemente investigadas.
Revisión bibliográfica
1. Generalidades
La granada, perteneciente a la familia Punicaceae, es un fruto nativo de Irán, su nombre Persa es "Anar" (Sheets et al., 2009; Mohseni, 2009). Actualmente, el fruto es cultivado de manera extensiva en el país de origen, las zonas áridas de sureste de Asia y la zona mediterránea de África. El fruto fue traído a América por misioneros españoles durante la conquista, y logró adaptarse en algunas zonas principalmente cálidas y áridas de Estados Unidos y México.
El árbol, denominado granado, generalmente se adapta a climas del tipo mediterráneo, generando un fruto sumamente jugoso. Es un arbusto de follaje abundante que posee tronco de ramas torcidas y levemente espinosas. Las hojas son color verde, alargadas, con superficie lisa y brillante, levemente onduladas. La flor es acampanada y está conformada por 5 a 8 pétalos color naranja brillante (Morton, 1987).
1.1 Características del fruto
La granada se caracteriza por ser un fruto de forma globosa de aproximadamente 6 a 12 centímetros de diámetro, con un cáliz en forma de corona (Fig. 1). Su corteza va del color amarillo rojizo a verde con zonas rojizas e inclusive al rojo escarlata; es delgada y correosa, cubre una gran cantidad de granos, ordenadamente distribuidos, jugosos y con un sabor que va del agridulce al dulce

dependiendo de la variedad. Los granos están separados por delgados tabiques membranosos de cualidad astringente. Cada grano tiene como centro una semilla blanquesina de estructura firme, cuya dureza varía (RAE, 2010).
1.2 La granada en el mundo
Los diferentes nombres con que se conoce al fruto en diversas partes del mundo son pomegranate en inglés, grenade en francés, granaatappe en holandés, granatapfel en alemán; melogranato, melograno granato, pomo granato, o pomo punico, en italiano. Gangsalan en Indonesia, tab tim en Tailandia, delima en Malasia. Los brasileños la conocen como roma, romeira o romazeira.
El término genérico, Punica, fue el nombre romano para Cartagena de donde llegaban las mejores granadas a Italia (Morton, 1987).
1.2.1
Cultivo
La granada en la actualidad está siendo cultivada extensivamente en todo el territorio de Irán, país de origen, excepto en la provincia de Hamedan, con 56,329 hectáreas de cultivo y 705,166 toneladas de producción anual (Mohseni, 2009).
Para poder llevar los cultivos a una producción intensiva, se están realizando interesantes estudios de selección basados en técnicas de caracterización de suelos y biología molecular, con el fin de mejorar e intensificar el cultivo, en países como Irán e Israel (Varasteh et al., 2009; Bar-Ya'akov et al., 2009).
En India, se siembran más de 100,000 hectáreas de granada, principalmente en el estado de Maharastra, que cultiva de manera extensiva el fruto, en varios distritos. El fruto, principalmente se comercializa en fresco (MPGRA, 2009). Las variedades más
sembradas en India poseen una gran cantidad de pulpa alrededor de la semilla y se denominan “sin semilla”. Entre las mejores variedades están las denominadas Bedana, de pulpa color rosa, dulce y semillas suaves, y la Kandhari, pulpa color rojo fuerte, ligeramente ácida y semilla dura (Morton, 1987).
En Oriente, las variedades cultivadas son Ahmar, Aswad, Halwa, principalmente en Iraq, y Mangulati en Arabia Saudita. Las variedades Wonderful y Red Loufani se producen en el sector judío de Israel, mientras que Malassi y Ras Baghl crecen adecuadamente en el sector árabe (Morton, 1987).
Entre los principales países productores, la diferencia se da en las estrategias de producción y comercialización. Por ejemplo, a pesar de que Turquía produce unas 80,000 toneladas por año y Túnez (norte de África) 50,000 toneladas en el mismo período en promedio, sus cultivos son fundamentalmente extensivos y poco especializados, con procesos de comercialización muy débiles. Estas deficiencias tan sólo permiten un 5% de producción exportada.
España es el país con la producción más importante en la Unión Europea. Se cultivan aproximadamente 2,325 hectáreas que producen alrededor de 27,389 toneladas, siendo la provincia de Alicante la principal productora con 2,047 hectáreas y 25,104 toneladas anuales. El cultivo se concentra en esta provincia con el 88% de la superficie nacional y el 92% de la producción. En la provincia de Murcia se cultiva prácticamente el resto de la producción de España. Aunque la producción media es de alrededor de 10.8 toneladas por hectárea, al tecnificar el cultivo se alcanzan las 25-30 toneladas por hectárea. El cultivo intensivo y especializado, así como una comercialización desarrollada, permiten exportar más del 90% de la producción. El cultivo de granada es muy conveniente en la actualidad, pues su precio se ha incrementado
debido a la difusión de información referente al fruto y sus propiedades (Melgarejo, 2008; Özgüven et al., 2009). El 90% de la producción del fruto en España se ha destinado a la producción de jugo para su exportación en Europa (CRFG, 1997).
En California, Estados Unidos, las variedades Spanish Ruby y Sweet Fruited fueron cultivadas en el siglo XIX, pero en el siglo XX fueron sustituidas por la variedad Wonderful (Morton, 1987).
En Sudamérica, dos países que en la actualidad están incursionando en la producción y comercialización de granada son Argentina y Chile (Mondragón y Juárez, 2008).
Hasta antes de 1990, en México la principal zona productora de granada se localizaba en Tehuacán, Puebla, donde aún permanecían viables cultivos de este fruto, según reporta Morton (1987). Desafortunadamente los cultivos de granada fueron desapareciendo ya que se sustituyeron por obras de urbanización. Las estadísticas del gobierno del estado de Puebla refieren que la producción ha disminuido drásticamente, con una superficie sembrada de cinco hectáreas y 30 toneladas anuales, produciéndose únicamente en 11 municipios del estado (Jiménez, 2007).
Actualmente, en México es incierta la cantidad de hectáreas cultivadas en el país. Sin embargo, existe interés por parte de investigadores del INIFAP (Instituto Nacional de Investigaciones Forestales, Agrícolas y Pecuarias), campo experimental del Bajío, de estudiar variedades adaptadas en México desde la llegada de los españoles (Mondragón, 2010). Este interés ha ido en crecimiento debido a los recientes hallazgos científicos referentes a las cualidades nutracéuticas, no sólo del fruto, sino de las hojas, flores y tallo. También los gobiernos municipales de Tehuacán, Puebla, se han preocupado por
recuperar el cultivo; sin embargo, sólo se ha realizado la siembra de árboles con fines ornamentales (Malfavón, 2010).
La granada se produce comercialmente sólo en los estados de Hidalgo y Guanajuato. La producción de los municipios de Apaseo el Alto y Apaseo el Grande, en Guanajuato, es comercializada principalmente en restaurantes de las ciudades de México, Guadalajara, Monterrey y Puebla, y en menor proporción, para su consumo en fresco.
1.2.2 Consumo y usos
En diversas partes del mundo, incluyendo los países de origen y de mayor producción, además de destinar la producción de granada a la comercialización para consumo en fresco y como jugo, se le dan usos en la herbolaria tradicional. Sus aplicaciones en medicina tradicional incluyen el uso de la corteza del árbol, hojas, flores y fruto; considerando de este último el jugo, las semillas y la cáscara.
Recientemente, ha cobrado importancia el procesamiento del fruto, teniendo como principal producto derivado el jugo envasado. Otros productos de importancia son mermeladas y confituras, así como helados, cremas y geles (Andreu-Sevilla et al., 2008).
En Turquía se consume principalmente como jugo, pero tiene otro tipo de aplicaciones importantes como la fabricación de ácido cítrico, conservas enlatadas y en la alimentación animal, entre otros (Özgüven et al., 2009).
Un uso que se da al jugo en diversas partes del mundo es la elaboración de la bebida denominada granadina, que recibe su nombre por el fruto que le da origen. La granadina es un refresco hecho con jugo de granada (RAE, 2010) y es consumido solo o mezclado con otras bebidas. Esta situación en la actualidad ha ido cambiando, debido a que esta bebida se
elabora y colorea a partir de materiales diferentes a la granada.
En la India, además de su aplicación en herbolaria tradicional, se le da uso como dentífrico y en la tinción de telas. Se aplica también en la fabricación de citrato de sodio y ácido cítrico, en la producción de bebidas refrescantes, carbonatadas y no carbonatadas, vino y jarabe (Tous y Ferguson, 1996; MPGRA, 2009).
En México, generalmente este fruto se consume en fresco y se usa en la elaboración de postres, así como en la decoración del platillo de identidad nacional denominado chiles en nogada. Otro de los usos más importantes es en la herbolaria tradicional; así, las hojas y el tallo se utilizan para tratamientos antidisentéricos, la pulpa y el pericarpio como antidisentéricos y antidiarreicos, la raíz como astringente y antihelmíntico. El pericarpio, hojas, tallo y raíz se consumen como infusión (Osuna et al., 2005); las infusiones de flores se utilizan en el tratamiento de inflamación bucal y de la garganta (Morton, 1987).
2. Composición
El Departamento de Agricultura de los Estados Unidos (USDA, 2009), reporta la composición de la variedad Wonderful, una de las que mejor se ha adaptado a suelos del continente americano. En la Tabla I esta tabla se presenta la composición proximal de la porción comestible, que consiste en los granos que contienen las semillas del fruto. También se presenta la composición específica de minerales, vitaminas y lípidos. Entre los aspectos más importantes de resaltar, está su contenido en azúcares y fibra, así como de minerales esenciales para el organismo humano como potasio y fósforo. Respecto a su composición en vitaminas, la granada es una fuente mediana, principalmente de folatos y vitamina K.
Uno de los aspectos que ha cobrado importancia en los últimos años es el contenido de sustancias antioxidantes tales como fenoles, polifenoles y antocianinas de la granada. En recientes investigaciones, a estos componentes se les han atribuído propiedades nutracéuticas y farmacológicas. En diversas variedades de granadas cultivadas en Irán, los compuestos fenólicos totales se encuentran entre 2.4 y 9.3 g/L de jugo, y las antocianinas entre 0.815 y 7.760 g/L (Mousavinejad et al., 2009).
Usando métodos analíticos se ha detectado la presencia de compuestos antioxidantes prácticamente en todas las partes del árbol de granado: corteza, raíz, hojas, flores y fruto (cáscara, jugo y semillas). Los componentes más importantes están en la corteza y las raíces, y son los flavonoides y taninos, los antioxidantes más abundantes (Vidal et al., 2003). Se encuentran presentes, entre otros, ácido ursólico, -tocoferol, ácido elágico, quercitina, elagitaninos, luteolina y apigenina (Lansky y Newman, 2007). Las hojas son una importante fuente de taninos; contienen glicósidos de apigenina, flavona con propiedades progesténicas y angiolíticas (Lansky y Newman, 2007). Las flores contienen compuestos que también se encuentran en la cáscara y las semillas, como es el caso de los ácidos gálico y ursólico (Huang et al., 2005). Las semillas conforman del 12 al 20% del peso total del fruto, 99% del aceite extraído de ellas son triacilgliceroles, el 80% es ácido octadecatrienoico, con alto contenido de ácido punícico. Los componentes menores incluyen esteroles, esteroides y cerebrósidos (Lansky y Newman, 2007). La matriz de las semillas incluye ligninas y ácidos hidroxicinámicos y derivados de lignina con alto poder antioxidante (Wang et al., 2004). El jugo posee principalmente antocianinas y flavonoides, mismos que le confieren su color brillante (Hernández et al., 1999).
Tabla I. Composición de la porción comestible de la granada variedad Wonderful.
NutrienteUnidadesValor por 100 g
Proximal
Aguag77.93
Energíakcal83.0
Proteínag1.67
Lípidos totales (grasa)g1.17
Cenizasg0.53
Carbohidratos (por diferencia)g18.7
Fibra dietaria totalg4.0
Azúcares totalesg13.67
Minerales
Calciomg10.0
Hierromg0.3
Magnesiomg12.0
Fósforomg36.0
Potasiomg236.0
Sodiomg3.0
Zincmg0.35
Cobremg0.158
Manganesomg0.119
Seleniomcg0.5
Vitaminas
Vitamina C, ácido ascórbico totalmg10.2
Tiaminamg0.067
Riboflavinamg0.053
Niacinamg0.293
Acido pantoténicomg0.377
Vitamina B-6mg0.075
Folato totalmcg38
Colina totalmg7.6
Vitamina E, alfa-tocoferolmg0.6
Vitamina Kmcg16.4
Lípidos
Ácidos grasos saturados g0.120
Ácidos grasos monoinsaturadosg0.093
Ácidos grasos poliisaturadosg0.079
Adaptada de la USDA (2009).
Dentro de diversos estudios referentes a la funcionalidad antioxidante de los compuestos de la granada, está el realizado por Iqbal et al. (2008), quienes obtuvieron extractos metanólicos de la cáscara. Estos extractos purificados fueron adicionados al aceite de girasol. Este aceite se sometió a una
comparación de funcionalidad antioxidante, contra un aceite adicionado con BHT (butilhidroxi-tolueno), antioxidante sintético de uso convencional en la conservación de grasas y aceites. Se compararon los valores de índice de peróxidos, actividad antioxidante de dienos conjugados y trienos conjugados. Los
resultados indicaron que el extracto de cáscara de granada es un potente antioxidante de aceite de girasol, comparable al BHT. Estos resultados comparativos contra BHT coinciden con lo reportado por Schubert et al. (1999).
Otro estudio (Singh et al., 2002) demostró la eficiencia de la capacidad antioxidante sobre radicales peróxido y en la oxidación de lipoproteínas humanas de baja densidad (LDL). Las pruebas se realizaron in vitro con extractos purificados, resultado de extracciones realizadas con metanol, con agua y con acetato de etilo, a partir de la cáscara y semillas.
Tezcan et al. (2009) estudiaron el contenido de compuestos antioxidantes y la actividad antioxidante en jugos comerciales de granada. Los resultados obtenidos indicaron una relación directa entre el contenido de compuestos fenólicos y la capacidad antioxidante en seis de las siete marcas comerciales estudiadas.
La presencia de compuestos fenólicos en el pericarpio, está relacionada con sus características antimicrobianas, aspecto que es revelado en el espectro in vivo, así como in vitro de extractos (Al-Zoreky, 2009). Su capacidad antimicrobiana se confirma una vez más en los estudios realizados por Haidari et al. (2009), quienes comprobaron que extractos con alto contenido de polifenoles, obtenidos del pericarpio de granada, inhiben la replicación del virus de la influenza humana A/Hong Kong (H3N2). Braga et al. (2005) confirmaron que el extracto metanólico de granada inhibió el crecimiento de Staphylococcus aureus y la subsecuente producción de su enterotoxina. Así también, se ha reportado la actividad antimicrobiana que presentaron extractos etanólicos y acuosos de cáscara de granada contra el serotipo hemorrágico y diarreico de Escherichia coli O157:H7 (Voravuthikunchai et al., 2004).
Otros hallazgos han mostrado que los antioxidantes fenólicos presentes en jugo de granada son agentes quimiopreventivos y anticancerígenos. Lo anterior fue probado en sistemas modelo in vitro, así como in vivo, en los que se determinó que estos componentes antioxidantes contribuyen a la reducción del estrés oxidativo y aterogénesis (Syed et al., 2007). Al respecto, Lansky y Newman (2007) también indican que los extractos funcionan para tratamientos y prevención de cáncer en experimentos ex vivo realizados en cultivos de tejido mamario de ratones. Los mismos autores reportan el efecto antiinflamatorio de extractos de granada en la garganta y la piel.
Los extractos acuosos, especialmente de la cáscara de granada, facilitan la reparación de la epidermis; lo mismo ocurre con los extractos de semillas (Aslam et al., 2006), lo que establece la posibilidad de uso cosmético.
Un hallazgo muy interesante también, es su propiedad terapéutica para la disfunción eréctil, encontrada en pruebas in vivo con ratones, debido a las propiedades antioxidantes de los compuestos fenólicos (Azadzoi et al., 2005).
Celik et al. (2009) reportan el papel hepatoprotector del jugo de granada y su relación con la capacidad antioxidante encontrada, utilizando modelos in vivo, en los que se administraron infusiones acuosas a ratas, a las que se les indujo carcinogénesis química con ácido tricloroacético. Los autores concluyeron que la administración constante de infusiones jugó un papel hepatoprotector sumamente importante.
Considerando evidencias como éstas, crece el interés por la granada, lo que ha llevado a la realización de investigaciones que establecen que el contenido de antioxidantes y la calidad sensorial de este fruto, incluyendo los componentes del árbol, pueden incrementarse llevando a cabo una elección de variedades
con máxima capacidad antioxidante y el cultivo controlado de las mismas (BorochovNeori et al., 2009).
3. Usos potenciales
Debido a la gran cantidad de trabajos de investigación referentes a las propiedades antioxidantes de la granada, se detectan diversos usos potenciales que atiendan las necesidades de la industria alimentaria, que en la actualidad busca nuevas fuentes naturales de antioxidantes para el desarrollo de alimentos nutracéuticos demandados por los consumidores. Otra aplicación potencial puede enfocarse a la industria de aceites y grasas, cuya tendencia es la aplicación de antioxidantes naturales. Las investigaciones de propiedades regeneradoras de la dermis y epidermis, apoyarían estudios más profundos para promover el uso y aplicación de extractos en la formulación de productos cosméticos. Los estudios de las propiedades antioxidantes de diversas partes del árbol de granada y su fruto, indican que tales características están íntimamente relacionadas con sus propiedades farmacológicas, por lo que los extractos de antioxidantes podrían tener una aplicación terapéutica y profiláctica para promover la salud y contrarrestar los efectos de enfermedades tan complicadas como el cáncer.
Conclusiones
Las propiedades antioxidantes que posee la granada llevan a proponer desde el consumo en fresco, hasta la obtención de extractos, industrial y farmacológicamente aplicables.
En México, donde en los últimos años se ha incrementado la proporción de población con enfermedades como el cáncer, bien valdría la pena recuperar cultivos de variedades de granada adaptadas a los climas del país y, particularmente, del estado de Puebla, con el
fin de promover su consumo en fresco, así como realizar investigaciones que apoyen la aplicación de extractos en el tratamiento de enfermedades y como ingrediente en la industria alimentaria.
Agradecimientos
Los autores agradecen el apoyo del Consejo Nacional de Ciencia y Tecnología (CONACyT) de México por el financiamiento del proyecto: Extracción, caracterización y funcionalidad de compuestos de origen vegetal obtenidos de materiales mexicanos empleados como condimentos. Obtención de agentes antimicrobianos, antioxidantes e ingredientes funcionales. O. A. López-Mejía agradece al CONACyT y a la Universidad de las Américas Puebla por las becas otorgadas para la realización de sus estudios doctorales. También se agradece a la Secretaría de Desarrollo Rural (SDR) Delegación Tehuacán, al Campo experimental Bajío del Instituto Nacional de Investigaciones Forestales, Agrícolas y Pecuarias (INIFAP) Bajío y a la Coordinación de Recursos Naturales del H. Ayuntamiento de Tehuacán, por la información proporcionada.
Referencias
Al-Zoreky, N.S. 2009. Antimicrobial activity of pomegranate (Punica granatum L.) fruit peels. International Journal of Food Microbiology 134:244–248.
Andreu-Sevilla, A., Signes-Pastor, A. J. y CarbonellBarrachina, A. A. 2008. La granada y su zumo. Producción, composición y propiedades beneficiosas para la salud. Alimentación 234:36-39
Aslam, M. N., Lansky, E. P. y Varani, J. 2006. Pomegranate as a cosmeceutical source: Pomegranate fractions promote proliferation and procollagen synthesis and inhibit matrix
metalloproteinase-1 production in human skin cells. Journal of Ethnopharmacology. 103:311–318.
Aviram, M. y Dornfeld, L. 2001. Pomegranate juice consumption inhibits serum angiotensin converting enzyme activity and reduces systolic blood pressure. Atherosclerosis. 158:195–198.
Azadzoi, K.M., Schulman, R.N., Aviram, M. y Siroky, M.B. 2005. Oxidative stress in arteriogenic erectile dysfunction: prophylactic role of antioxidants. Journal of Urology. 174:386–393.
Bar-Ya'akov, I., Trainin, T., Hefetz, H., Hatib, K. y Holland, D. 2009. Improving pomegranate cultivars in Israel. En Özgüven, A.I., Fideghelli, C. y Yalcin Mendi, Y. (Eds.) I International Symposium on Pomegranate and Minor Mediterranean Fruits. International Society for Horticultural Science, ISHS Acta Horticulturae. Adana, Turkia.
Bektas, N. y Ozturk, N. 2007. Antioxidant activity of Punica granatum (Pomegranate) flowers. Abstracts / Toxicology Letters. 172S S1–S240.
Borochov-Neori, H., Judeinstein, S., Tripler, E., Harari, M., Greenberg, A., Shomer, I. y Holland, D. 2009. Seasonal and cultivar variations in antioxidant and sensory quality of pomegranate (Punica granatum L.) fruit. Journal Food Composition and Analysis 22:189–195.
Braga, L.C., Shupp, J.W., Cummings, C., Jett, M., Takahashi, J.A., Carmo, L.S., Chartone-Souza , E. y Nascimento A.M.A. 2005. Pomegranate extract inhibits Staphylococcus aureus growth and subsequent enterotoxin production. Journal of Ethnopharmacology. 96:335–339.
Celik, I., Temur, A. y Isik, I. 2009. Hepatoprotective role and antioxidant capacity of pomegranate (Punica granatum) flowers infusion against trichloroacetic acid-exposed in rats. Food and Chemical Toxicology. 47:145–149.
CRFG. 1997. Pomegranate. California Rare Fruit Growers Inc. http://www.crfg.org/pubs/ff/pomegranate.html, accesada 10/11/2009.
Haidari, M., Ali, M., Casscells, S. W. y Madjid, M. 2009. Pomegranate (Punica granatum) purified polyphenol extract inhibits influenza virus and has a synergistic effect with oseltamivir. Phytomedicin. 16:1127–1136.
Hernández, F., Melgarejo, P., Tomas-Barberan, F.A. y Artes, F. 1999. Evolution of juice anthocyanins during ripening of new selected pomegranate (Punica granatum) clones. European Food Research and Technology. 210:39–42.
Huang, T.H., HYang, Q., Harada, M., Li, G.Q., Yamahara, J., Roufogalis, B.D. y Li, Y. 2005. Pomegranate flower extract diminishes cardiac fibrosis in zucker diabetic fatty rats: modulation of cardiac endothelin-1 and nuclear factor-kappaB pathways. Journal of Cardiovascular Pharmacology. 46:856–862.
Iqbal, S., Haleem, S., Akhtar, M., Zia-ul-Haq, M. y Akbar, J. 2008. Efficiency of pomegranate peel extracts in stabilization of sunflower oil under accelerated conditions. Journal of Food Research International. 41:194-200.
Jiménez, M. 2007. Cadenas productivas agropecuarias y acuícolas del Estado de Puebla. Gobierno del Estado de Puebla. 1ª Edición. Puebla México.
Lansky, E. P. y Newman, R. A. 2007. Punica granatum (pomegranate) and its potential for prevention and treatment of inflammation and cancer. Journal of Ethnopharmacology. 109:177–206.
MPGRA. 2009. Pomegranate Facts. Maharashtra Pomegranate Growers Research Association http://www.pomegranateindia.org, accesada 22/02/2010.
Malfavón, C. R. 2010. Comunicación Personal. Coordinación de Recursos Naturales. Dirección de Medio Ambiente y Ecología. H. Ayuntamiento de Tehuacán. Tehuacán, Puebla, México.
Melgarejo, P. 2008. Fruticultura alternativa para zonas áridas y semiáridas. Nuevas técnicas para el ahorro de agua y energía. EXPOZARAGOZA 2008 Tribuna del agua. Zaragoza, España. Junio 14 a Septiembre 14.
Mohseni, A. 2009. The situation of pomegranate orchards in Iran. En Özgüven, A.I., Fideghelli, C. y Yalcin Mendi, Y. (Eds.) I International Symposium on Pomegranate and Minor Mediterranean Fruits. International Society for Horticultural Science, ISHS Acta Horticulturae. Adana, Turkia.
Mondragón, J. C. 2010. Comunicación personal. Instituto Nacional de Investigaciones Forestales y Agrícolas y Pecuarias (INIFAP). Programa de Nopal y Frutales. Campo Experimental Norte de Guanajuato. Guanajuato, México.
Mondragón, J. C. y Juárez C. S. 2008. Granada Roja. Guía para su producción en Guanajuato. INIFAP, Campo Experimental del Bajío. Celaya, Guanajuato, México.
Morton, J. 1987. Pomegranate. Morton, J. F. (Ed.) En: Fruits of warm climates. Miami, FL. pp. 352-355. http://www.hort.purdue.edu/newcrop/morton/pomeg ranate.html, accesada 20/02/10.
Mousavinejad, G., Emam-Djomeh, Z., Rezaei, K., Hossein, M. y Khodaparast, H. 2009. Identification and quantification of phenolic compounds and their effects on antioxidant activity in pomegranate juices of eight Iranian cultivars. Food Chemistry. 115:1274–1278.
Osuna, T. L., Tapia, P. M.E y Aguilar, C.A. 2005. Plantas medicinales de la medicina tradicional mexicana para tratar afecciones gastrointestinales. Estudio etnobotánico, fitoquímico y farmacológico. Publicacions I Edicions de la Universitat de Barcelona. p113-115.
Özgüven, A.I., Yılmaz, M. y Yılmaz, C. 2009. The situation of pomegranate and minor mediterranean fruits in turkey. En Özgüven, A.I., Fideghelli, C., Yalcin Mendi, Y. (Eds.) I International Symposium on Pomegranate and Minor Mediterranean Fruits. International Society for Horticultural Science, ISHS Acta Horticulturae. Adana, Turkia.
RAE. 2010. Real academia española http://www.rae.es, accesada 12/02/2010.
Schubert, S. Y. Lansky, E. P. y Neeman, I. 1999. Antioxidant and eicosanoid enzyme inhibition properties of pomegranate seed oil and fermented juice flavonoids. Journal of Ethnopharmacology. 66:11-17.
Shahidi, F. y Naczk, M. 2009. Phenolics in Food and Nutraceuticals. CRC Press, Boca Ratón, Florida. EUA.
Sheets, M. D., Du Bois, M. L. y Williamson, J. G. 2009. La Granada en Florida. Departamento de Ciencias Hortícolas, University of Florida (HS1044). IFAS Extensión. http://edis.ifas.ufl.edu/hs294, accesada 10/01/10.
Singh, R., Chidambara, K. y Jayaprakasha, G. 2002. Studies on the antioxidant activity of pomegranate (Punica granatum) peel and seed extracts using in vitro models. Journal of Agricultural and Food Chemistry. 50: 81-86.
Syed, D. N., Afaq, F. y Mukhtar, H. 2007. Pomegranate derived products for cancer chemoprevention. Seminars in Cancer Biology. 17:377–385.
Tezcan, F., Gültekin-Özgüven, M. Diken, T., Özcelik, B. y Erim, B. 2009. Antioxidant activity and total phenolic organic acid and sugar content in comercial pomegranate juices. Journal of Food Chemistry 115:873-877.
Tous, J. y Ferguson, L. 1996. Mediterranean fruits. En: Janick J. (Ed.) Progress in new crops. ASHS Press, Arlington, VA. 416-430. http://www.hort.purdue.edu/newcrop/proceedings19 96/v3-416.html, accesada 20/02/10.
USDA. 2009. National Nutrient Database for Standard. United States Department of Agriculture. http://www.nal.usda.gov/fnic/foodcomp/search/, accesada 10/02/2010.
Varasteh, F., Arzani, K., Zamani, Z. y Mohseni, A. 2009.Evaluation of the most important fruit characteristics of some commercial pomegranate (Punica granatum L.) cultivars grown in iran. En: Özgüven, A.I., Fideghelli, C. y Yalcin Mendi, Y. (Eds.) I International Symposium on Pomegranate and Minor Mediterranean Fruits. International Society for Horticultural Science, ISHS Acta Horticulturae. Adana, Turkia.
Vidal, A., Fallarero, A., Pena, B.R., Medina, M.E., Gra, B., Rivera, F., Gutierrez, Y. y Vuorela, P.M. 2003. Studies on the toxicity of Punica granatum L. (Punicaceae) whole fruit extracts. Journal of Ethnopharmacology. 89:295–300.
Voravuthikunchai, S., Lortheeranuwat, A., Jeeju, W., Sririrak, T., Phongpaichit, S. y Supawita, T. 2004 Effective medicinal plants against enterohaemorrhagic Escherichia coli O157:H7. Journal of Ethnopharmacology. 94:49–54.
Wang, R.F., Xie, W.D., Zhang, Z., Xing, D.M., Ding, Y., Wang, W., Ma, C. y Du, L.J., 2004. Bioactive compounds from the seeds of Punica granatum (Pomegranate). Journal of Natural Products 67:2096–2098.

Temas Selectos de Ingeniería de Alimentos 4 – 1 (2010): 74 – 83

Desinfección de agua mediante el uso de tecnologías emergentes basadas en procesos avanzados de oxidación
J. H. Castillo-Ledezma*, A. López-Malo Vigil, E. R. Bandala
Departamento de Ingeniería Química, Alimentos y Ambiental. Universidad de las Américas, Puebla. Sta. Catarina Mártir, Cholula, Puebla. 72810. México
Resumen
La disponibilidad de agua segura para consumo humano es esencial para la conservación de la salud, y es bien conocido que su contaminación disminuye la calidad de vida del público usuario. A pesar de la eficacia de las tecnologías convencionales utilizadas para la desinfección de agua, estos poseen también serias desventajas tales como altos costos de operación y toxicidad de los derivados residuales. Como respuesta a estas problemáticas, se lleva a cabo investigación para el desarrollo de técnicas de desinfección innovadoras, accesibles, eficaces y socialmente aceptables. Entre ellas destacan los procesos avanzados de oxidación; en los cuales, se generan intermediarios altamente reactivos, mismos que pueden provocar la oxidación de contaminantes y promover la desinfección de organismos patógenos residuales en el agua. El presente trabajo se enfoca en los alcances obtenidos en esta área de investigación y pretende dar a conocer la problemática actual del agua, enfatizando las tecnologías emergentes para su desinfección, basadas en procesos avanzados de oxidación.
Palabras clave: desinfección, procesos avanzados de oxidación, radicales libres, reacción de Fenton, fotocatálisis.
Abstract
Availability of safe drinking water is essential for human health maintenance and disease prevention. It is also well documented that its pollution decreases the user´s quality of life. Despite the effectiveness of conventional technologies there are increasing concerns about their high operating costs and residual toxicity of the derivatives generated. Therefore, to these needs, research is held for the development of innovative, accessible, effective and socially acceptable disinfection techniques.These methodologies include advanced oxidation processes, in which, highly reactive intermediates are generated which may cause the oxidation of pollutants and promote disinfection of pathogenic species present in water.This work focuses on achievements in this area of research and disseminates current water issues, emphasizing the emerging technologies for water disinfection based on advanced oxidation processes.
Keywords: disinfection, advanced oxidation processes, free radicals, Fenton reaction, photocatalysis.
*Programa de Doctorado en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: jordanah.castillola@udlap.mx
Introducción
La gestión racional del agua es un tema crucial para el desarrollo de las naciones y su contaminación induce problemas sociales, económicos y de salud que pueden afectar seriamente el desarrollo económico de un pueblo.
La contaminación del agua, por diversos agentes biológicos (microorganismos) o compuestos orgánicos tóxicos, es responsable de la disminución en la calidad de vida de la población. Las deficiencias en los sistemas de distribución de agua son comúnmente asociadas con enfermedades adquiridas por la ingesta de agua contaminada y estas enfermedades son responsables de aproximadamente el 30% de los casos de muerte por enfermedades transmitidas por el consumo de agua en América Latina; seis veces más que el porcentaje reportado en países desarrollados. Según datos de la Organización Mundial de la Salud, alrededor de 80,000 niños mueren cada año en América Latina por enfermedades asociadas a las diarreas que, generalmente, son originadas por las condiciones insalubres del agua (Gisela et al., 2009).
El suministro de agua potable conlleva problemáticas muy complejas que se acentúan por la falta de técnicas efectivas, accesibles y amigables con el ambiente. De aquí se ha derivado la importancia de desarrollar tecnologías innovadoras, simples, eficaces, de bajo costo y socialmente aceptables para la desinfección/potabilización del agua.
En respuesta a la preocupación pública acerca de los problemas de salud generados por la contaminación del agua y a la demanda de agua de calidad por parte de la población, la comunidad científica ha investigado la eficacia de diversas metodologías aplicables al tratamiento de desinfección/potabilización del agua.
En la actualidad se utilizan tecnologías convencionales como la aplicación de cloro y la ozonación para la desinfección del agua.
Sin embargo, debido a sus altos costos de operación, a la creciente preocupación sobre la toxicidad de los derivados residuales y a las desventajas propias de cada tipo de tratamiento, tales como: condiciones de operación y resistencia de los contaminantes, se ha detectado la necesidad de desarrollar métodos alternativos de desinfección capaces de llevar a cabo la generación de agua segura sin las desventajas de los métodos convencionales.
Entre estas metodologías alternativas, los procesos avanzados de oxidación (PAO) han emergido como técnicas prometedoras aplicables en la desinfección del agua. Los PAO son métodos innovadores, eficaces y de bajo costo, basados en catálisis y fotoquímica, en los que recientemente se han conseguido interesantes progresos.
Estas tecnologías se basan en la generación de intermediarios altamente reactivos; radicales hidroxilos, los cuales inician una secuencia de reacciones que provocan la oxidación de compuestos orgánicos y promueven la desinfección.
Entre los PAO se pueden mencionar las reacciones de Fenton, foto-Fenton, fotocatálisis y fotocatálisis heterogénea. Recientemente se ha logrado incrementar la eficacia de estos procesos de desinfección, al utilizar el espectro visible de la radiación solar como fuente para la generación de radicales. Estos intermediarios oxidan y mineralizan los compuestos orgánicos peligrosos e inactivan a los microorganismos patógenos presentes en el agua. Esto ha convertido a los PAO en tecnologías prometedoras para la purificación del agua.
Resulta importante recalcar la existencia de una vasta serie de estudios científicos que demuestran la viabilidad de la destrucción decasi todos los tipos de compuestos peligrosos y microorganismos, mediante la aplicación procesos avanzados de oxidación (Tryba, 2008).
Este trabajo se enfoca en los avances obtenidos en esta creciente área de investigación y da a conocer la problemática actual del agua, haciendo énfasis en los procesos avanzados de oxidación utilizados como metodologías novedosas para la desinfección delagua.
Toda industria que consume agua tendrá algún efluente líquido y la calidad de los efluentes dependerá completamente del proceso industrial (CGIAB, 2010). Por tanto, la gran variedad de procesos industriales genera un amplio abanico de efluentes contaminantes. Entre los efluentes producidos por las principales industrias contaminantes se pueden mencionar (EUPS, 2010):
a) Industria del petróleo. Los efluentes generados presentan sosa, sulfuros, fenoles, compuestos orgánicos disueltos, parafinas, alcoholes pesados, benceno, cianuros, acetonitrilos y metales, entre otros.
Revisión bibliográfica
1. Problemática ambiental del agua
La disponibilidad del agua potable representa un problema importante que enfrenta la humanidad y requiere resolverse adecuadamente. En el sureste de Europa, el Este Medio, Asia Central y África, el agua es un recurso limitado y, debido al cambio climático global, continuan disminuyendo las reservas, mientras que en extensas partes del hemisferio norte grandes cantidades de agua se encuentran disponibles. Además, debido a la pobreza y al crecimiento demográfico, los países en desarrollo resultan especialmente afectados por la falta de agua. De cualquier manera, los problemas no sólo se originan por la falta de este líquido vital, sino por su contaminación (Backhaus et al., 2009).
Mundialmente, existe una gran preocupación por el incremento en los niveles de contaminación de los sistemas de agua por compuestos químicos producidos por las actividades en ciudades, industrias y por los residuos derivados de labores o procesos agrícolas (De la Hozet al., 2007).
b) Tenerías. Este sector industrial emplea taninos vegetales o sales de cromo para los procesos de curtición que se encuentran en sus vertidos. Sus efluentes contienen: proteína, coloides, grasas, pelos y colorantes compuestos con cloro y azufre.
c) Industria textil. Sus efluentes contienen sólidos en suspensión, grasas, sales orgánicas, tintes y colorantes. Las lavanderías generan efluentes con alta contaminación compuesta fundamentalmente de productos de lavado (carbonato sódico, tripolifosfato, jabones, detergentes biodegradables).
d) Industria del acero. Los efluentes generados presentan alto contenido de óxidos, sólidos en suspensión, hidrocarburos insolubles en amoniaco, hierro II, zinc, plomo, ácido sulfúrico, aceites y sólidos en suspensión.
e) Industria automotriz. En general este tipo de agua presenta metales pesados como plomo, cromo VI, detergentes, grasas y sólidos en suspensión.
f) Industria energética. Dentro de este sector se consideran las plantas térmicas y nucleares, los sistemas de limpieza de gases y de gasificación, la minería del carbón y el reprocesado de combustibles irradiados. Los
efluentes presentan contaminación por hidrocarburos, sólidos en suspensión, cianuros, gases ácidos, metales pesados, y compuestos radioactivos.
g) Industria metalúrgica. Incluye la industria del aluminio, oro, uranio, y zinc. Los contaminantes más habituales son: carbono, fluoruros, metales, sosa, cianuros y disolventes.
h) Industria química. Se incluyen sectores de características muy diferentes como la industria del cloro, amoniaco, urea, farmacéutica y de tintes.
i) Industria cosmética. Sus efluentes presentan altos niveles de Demanda Química de Oxígeno (DQO), grasas y detergentes aniónicos y no iónicos.
j) Industria de adhesivos. Genera efluentes con copolímeros vinílicos y alta DQO.
k) Industria de explosivos. Sus efluentes presentan coloración, compuestos no biodegradables y acidez alta.
l) Industria agroalimentaria. Las características principales de la carga contaminante son el alto contenido de materia orgánica, en especial fermentados, azúcares, almidones y otros carbohidratos. También se originan altos contenidos de sólidos no disueltos como huesos, cáscaras y hojas. Las descargas son altas en Sólidos Suspendidos Totales (SST), Demanda Bioquímica de Oxígeno (DBO), coliformes totales y fecales (IMTA, 2010).
2. Importancia de la desinfección del agua
La presencia de microorganismos patógenos y compuestos contaminantes en el agua puede causar enfermedades, es por esto que surge la necesidad de implementar técnicas que
reduzcan los riesgos asociados a esta contaminación.
Los sistemas de desinfección de agua son metodologías que tienen por objetivo reducir la carga de contaminantes muy específicos y microorganismos patógenos presentes en los efluentes que se descargarán en el ambiente.
La desinfección se utiliza sobre todo si se pretende realizar posteriormente una reutilización del agua.
El mejor método para eliminar contaminantes es prevenir su presencia en primera instancia; sin embargo, esto no siempre es posible. Actualmente existe una gran variedad de métodos utilizados para reducir los contaminates y cada uno de ellos presenta diferentes ventajas y desventajas.
Las aguas contaminadas por la actividad humana, en general, pueden ser procesadas eficientemente por plantas de tratamiento biológico, por adsorción de carbón activado u otros adsorbentes, como también por tratamientos químicos convencionales, oxidación térmica, cloración, ozonación, entre otros (De la Hoz et al., 2007).
3. Tecnologías convencionales utilizadas en desinfección de agua
Los métodos tradicionales para reducir la contaminación involucran tratamientos biológicos, químicos y físicos, y la eficacia de cada método depende del tipo de tratamiento, condiciones de operación, corrosión de equipos, fisiología de los microorganismos, concentración y tiempo de exposición a los reactivos, pH, temperatura, y resistencia de los contaminantes.
A continuación se presentan las principales ventajas y desventajas de la cloración y ozonación como metodologías convencionales aplicadas en desinfección de agua:
a) Uso de cloro (hipoclorito, cloruro de sodio acidificado, dióxido de cloro).Son sistemas utilizados comúnmente. No obstante, altas concentraciones de materia orgánica pueden inhibir la eliminación de patógenos y generar subproductos clorados con efectos adversos potenciales para la salud.
También resulta importante considerar que el uso de estos reactivos provoca corrosión de los equipos, son dependientes del pH, sensibles a la temperatura, el aire, los metales y a la concentración de materiales orgánicos, en diferente medida, respecto a cada reactivo clorado. Además, algunas bacterias y huevos de protozoarios son resistentes a esta metodología de desinfección. El ácido hipocloroso es la forma de cloro libre disponible que exhibe la actividad bactericida más alta contra una amplia variedad de microorganismos (Parish et al., 2003).
No obstante, durante los últimos años la capacidad del cloro para inactivar microorganismos patógenos e inhibir su crecimiento ha sido puesta en perspectiva con respecto a sus efectos sobre la salud humana, debido a la generación de subproductos tóxicos. Estos compuestos aparecen durante el proceso de desinfección, cuando el cloro reacciona con la materia orgánica natural presente en la superficie del agua y con la materia orgánica de los efluentes residuales, generándose trihalometanos y ácidos haloacéticos, entre otros compuestos clorados, que exhiben un alto potencial carcinogénico y mutagénico (Backhaus et al., 2009).
b) Uso de ozono. Es una metodología comúnmente utilizada para desinfección de agua. Su uso es efectivo a bajas concentraciones y tiempos de exposición cortos. El ozono es muy reactivo por lo que su espectro es amplio y oxida la mayoría del material orgánico con el que entra en contacto, incluyendo protozoarios, por lo que elimina la mayoría de microorganismos patógenos.
El proceso exhibe buena habilidad de penetración. Por otra parte, entre sus desventajas se puede mencionar la inestabilidad del sistema y que es altamente reactivo; por lo que debe ser producido en su sitio de uso. Otra desventaja del ozono es su alto costo de operación y la necesidad de personal capacitado para operar el sistema, además de provocar corrosión de los equipos (Parish et al., 2003).
4. Procesos avanzados de oxidación como tecnologías emergentes de desinfección de agua
Entre los diversos tratamientos convencionales existentes, el cloro ha sido utilizado ampliamente como agente de desinfección por más de un siglo debido a su bajo costo y alta eficacia.
En años recientes ha aumentado el interés por desarrollar metodologías de desinfección alternativas, que no generen subproductos peligrosos y cuenten con otras características deseables como alta eficacia y bajos costos de operación.
Entre estas metodologías alternativas, los procesos avanzados de oxidación (PAO) emergen como técnicas prometedoras. Los PAO, definidos como aquellos procesos que involucran la generación de radicales hidroxilo para efectuar la purificación del agua (Parsons, 2005; Gottschalk et al., 2000), han demostrado ser eficientes e incrementar la cinética de degradación y el nivel de biodegradabilidad de muchos microorganismos, surfactantes y otros compuestos orgánicos (Metcalf y Eddy, 2003).
Los PAO por lo general se clasifican de acuerdo con la fase en la que se lleva acabo la reacción, siendo homogénea o heterogénea; o de acuerdo al método de generación del radical hidroxilo que puede ser químico, electroquímico o fotoquímico (Peralta et al., 2007).
4.1 Reacción de Fenton
Es un proceso que utiliza H2O2 con la adición de iones Fe2+. La combinación de hierro ferroso y peróxido de hidrógeno promueven una serie de reacciones en cadena, representadas en las ecuaciones 1 a 9.
Fe2+ + H2O2 Fe3++ OH + OH- (Ec. 1)
Fe3+ + H2O2 Fe2+ + HO 2 / O-2+ H+ (Ec. 2)
H2O2+ OH HO 2 / O-2+ H2O (Ec. 3)
Fe3+ + HO 2 Fe2+ + O2+ H+ (Ec. 4)
Fe2+ + OH Fe3+ + OH- (Ec. 5)
Fe2+ + HO 2 + H+ Fe3+ + H2O2 (Ec. 6)
Los radicales pueden reaccionar con el fierro o con cualquier sustancia orgánica presente. El radical hidroxilo (OH) es la especie más oxidante después del flúor; y puede oxidar los compuestos orgánicos más rápido que el ozono.
Además, estas reacciones propagan el ciclo en cadena, mediante la generación de otros tipos de radicales; superóxido y su ácido conjugado; quienes pueden reducir nuevamente el fierro III a fierro II (ecuación 4) o terminar la cadena por la oxidación de Fe II (ecuaciones 5 y 6).
También existen reacciones adicionales que pueden terminar la cadena. Estas reacciones incluyen los caminos de recombinación de los radicales (ecuaciones 7 a 9) (Crittendenet al., 1999; Duesterberget al., 2005).
Cabe señalar que este proceso se lleva a cabo en un intervalo de pH 2-4 (Esquivel, 2008).
4.2 Reacción de foto-Fenton
La reacción de foto-Fenton es una tecnología ambientalmente atractiva para la degradación de contaminantes tóxicos orgánicos (Xiejun et al., 2005). Recientemente se ha demostrado que el uso de Fe III y H2O2, con la aplicación de radiación UV es una alternativa efectiva para la degradación de contaminantes orgánicos (Kusic et al., 2006; Kwan y Chu, 2003).
El proceso se acelera debido a que se facilita la generación de radicales hidroxilo. La descomposición del Fe(OH)2+ incrementa la eficacia del proceso al proveer una fuente adicional de radicales OH (Kusic et al. 2006; Kwan y Chu, 2003) a partir de la reacción convencional de Fenton o por fotólisis de iones Fe III en disolución; como se muestra en la ecuación 10. Estos radicales se han propuesto como las principales especies reactivas para la oxidación y mineralización de varios contaminantes orgánicos presentes en el agua (Xuejun et al., 2005).
Fe(OH) 2++ hv Fe2+ + OH (Ec. 10)
Alternativamente, en presencia de radiación, el peróxido de hidrógeno en disolución puede ser fotolizado liberando OH como se muestra en la ecuación 11 (Kusic et al., 2006; Kwan y Chu, 2003).
H2O2+ hv 2OH (Ec. 11)
La reacción de foto-Fenton ha sido aplicada exitosamente en muchos estudios para la destrucción de residuos orgánicos peligrosos,
como nitrobenceno, colorantes y herbicidas (Xiejunet al., 2005).
4.3
Fotocatálisis
Se ha reportado que la energía solar puede ser utilizada efectivamente en la desinfección de agua, dado que la inactivación de los microorganismos se alcanza, ya sea calentando el agua a altas temperaturas, por arriba de 70°C, o exponiéndola cerca del intervalo UV (300-400nm) del espectro electromagnético (Rodríguezet al., 2007).
Esta radiación provoca daños en diversos componentes celulares y en la estructura genética de los microorganismos patógenos, inhibiendo su reproducción. El uso de la energía solar en procesos de desinfección, resulta muy atractivo por la disponibilidad de esta fuente. Sin embargo, únicamente el 7% del espectro solar está conformado por radiación UV mientras que la región visible representa cerca del 45%.
Serpone y Emeline (2002) definen la fotocatálisis como la aceleración de una fotoreacción por la acción de un catalizador.
La fotocatálisis solar es un proceso avanzado de oxidación que utiliza la radiación solar para la producción de radicales hidroxilo (Malato et al., 2002) y utiliza principalmente dióxido de titanio como fotocatalizador. Uno de los principales usos de esta tecnología está en el tratamiento microbiológico del agua, dado su efecto bactericida (De la Hoz, 2009).
En este esquema, la radiación conduce a la formación de pares hueco-electrón, promoviendo un electrón de la banda de valencia a la banda de conducción del dióxido de titanio (ecuación 12).
TiO2 + hν TiO2 (e- + h+) (Ec. 12)
El hueco en la banda de valencia genera radicales hidroxilo cuando una molécula de agua es adsorbida (ad) en la superficie del catalizador o por oxidación de los iones oxidrilo (ecuaciones 13 y 14).
TiO2 (h+) + H2Oad TiO2 + OHad + H(Ec. 13)
TiO2 (h+) + OH-ad TiO2 + OHad (Ec.14)
Por otra parte, el electrón en la banda de conducción reduce el oxígeno para generar radicales superóxido que pueden ser parcialmente protonados (ecuación 15).
TiO2 (e-) + O2 TiO2 + O•2- (Ec. 15)
O2 + 2e- + 2H+ H2O2 (Ec. 16)
En donde a partir del peróxido de hidrógeno y del radical superóxido se generan radicales libres mediante las ecuaciones 17 a 19.
2O•2+ 2H2O 2•OH+ 2•OH- + O2 (Ec. 17)
H2O2+ O•2-OH- + O2 + •OH (Ec. 18)
H2O2+ e-•OH+•OH- (Ec. 19)
Finalmente, la desinfección tiene lugar cuando los microorganismos son atacados por los radicales OH y O2 conocidos como especies reactivas de oxígeno (ROS).
La velocidad de reacción general del proceso se determina por las tasas de formación de los pares hueco-electrón, de la formación de las ROS a partir de las especies adsorbidas y de la recombinación huecoelectrón y el posible control de la adsorción o transferencia de masa de la solución (Backhauset al., 2009).
Dado que los oxidantes producidos son de alto poder y no discriminan, poseen el potencial de eliminar la mayoría de los microorganismos y de degradar o mineralizar la mayoría de los contaminantes orgánicos presentes en el agua (De la Hoz et al., 2007).
El mecanismo de acción mediante el cual se alcanza la desinfección de los microorganismos aún no se conoce con detalle. Sin embargo, Kiwi y Nadtochenko (2004 y 2005) y Nadtochenko et al. (2004) han reportado diversas modificaciones que tienen lugar en estructuras celulares como la pared y la membrana de los microorganismos. Se ha comprobado que el proceso se basa en la promoción de la oxidación directa de los fosfolípidos poliinsaturados componentes de la membrana. El daño en la pared celular favorece el acceso de los ROS a la membrana y la instrusión de las partículas de titanio al interior de las células. Estas fallas conducen a la muerte de los microorganismos por problemas de la actividad respiratoria, oxidación de enzimas y liberación del contenido celular (Backhaus et al., 2009).
Entre los diversos materiales que se han desarrollado para aplicaciones fotocatalíticas, el dióxido de titanio ha recibido gran atención debido a que no es tóxico y tiene alta actividad fotocatalítica, termoestabilidad y bajo costo (Bakhaus et al., 2009), además de ser inocuo, económico y reciclable. No obstante, debido a su amplia brecha de banda (3.2 eV), este catalizador exhibe actividad únicamente con radiación UV.
Esto es de gran interés debido a que se pueden generar materiales basados en TiO2 modificado, de tal forma que se incremente su sensibilidad a los fotones del espectro solar visible. Si el semiconductor utilizado tiene una separación apropiada entre sus bandas de valencia y conducción, ésta puede ser superada por la energía contenida en un fotón del espectro visible; lo que incrementaría su
actividad fotocatalítica y haría más eficaz el proceso de desinfección.
Por lo antes mencionado, en años recientes ha crecido el interés en aumentar la respuesta óptica del TiO2 del espectro UV al visible, con el fin de incrementar la eficacia de la fotocatálisis por TiO2. Dopar selectivamente el catalizador es una de las estrategias más efectivas para cambiar la estructura intrínseca de la banda de TiO2, lo cual puede promover la actividad fotocatalítica incrementando la sensibilidad a la luz solar.
Actualmente se llevan acabo investigaciones en las que se combinan las reacciones de Fenton y fotocatálisis heterogénea, mediante el diseño de catalizadores compuestos por dióxido de titanio y fierro, entre otros elementos. Los resultados en desinfección de agua se muestran prometedores.
Algunos ejemplos de aplicación de procesos de descontaminación fotocatalítica son el tratamiento de aguas residuales conteniendo formaldehídos provenientes de laboratorios veterinarios (Araña et al., 2004), y el tratamiento de efluentes provenientes de plantas papeleras (Machado et al., 2003). Casos interesantes de mencionar son las experiencias en la Plataforma Solar de Almería (PSA, España) en donde se utiliza fotocatálisis solar para el tratamiento del agua, el desarrollo de dióxido de titanio modificado (Xie y Yuan, 2004) y el acople de tecnologías basadas en radiación solar con tratamientos biológicos (Sarria et al., 2003).
También se destacan las experiencias reportadas por Litter y Mansilla (2003 a y b) en el marco del proyecto OEA AE 141/2001 de la Agencia Interamericana para la Cooperación y el Desarrollo, sobre desinfección solar y remoción de arsénico de aguas en comunidades rurales de América Latina.
Conclusiones
A pesar de los avances alcanzados en tecnologías para desinfección de agua, el incremento constante de sus niveles de contaminación obliga al desarrollo de nuevas metodologías que garanticen la disponibilidad de agua segura para consumo humano.
Considerando las ventajas de utilizar la energía solar en combinación con las reacciones de Fenton, foto-Fenton y fotocatálisis heterogénea para desinfección, durante los últimos años, la investigación y el desarrollo en procesos avanzados de oxidación se han convertido en temas con gran relevancia.
Un punto de interés comprende la generación de nuevos materiales semiconductores para su uso como catalizadores sensibles al espectro solar visible, que incrementen la eficiencia de los procesos fotocatalíticos para ser utilizados en inactivación microbiana y degradación de contaminantes.
Con base en lo antes mencionado se pronostica que la comunidad científica internacional continuará observando el desarrollo y la inversión en esta área, de la cual se posee vasta información, que no obstante, resulta insuficiente aún para su aplicación óptima.
Referencias
Araña, J., Martínez, J. L., Herrera, J. A., Rodríguez, J. M., Pérez, J., Bergasa, O., Álavarez, C. y Méndez, J. 2004. Photocatalytic degradation of formaldehyde containing wastewater from veterinarian laboratories. Chemosphere. 55(6):893-904.
Bakhaus, K., Marugán, J., van Grieken, R. y Sordo, C. 2009. Photocatalytic inactivation of E. faecalis in secondary wastewater plant effluents. ESCET. Universidad Rey Juan Carlos. España. Contaminación de aguas por la industria. http://www.aguabolivia.org/situacionaguaX/Situacio nX/CONTAMINACION.htm, accesada 22/2/2010.
Crittenden, C., Hu, S., Hand, D. y Green, S. 1999. A kinetic model for H2O2/UV process in a completely mixed batch reactor. Water Research. 33(10):23152328.
De la Hoz, F., Rivera, D., Arumi1, J. y Mansilla, H. 2007. Avances en la desinfección de agua de riego por fotocatálisis solar: Desarrollo experimental y resultados preliminares. Gestión Ambiental. 14:1-13.
Duesterberg, C. K., Cooper, W. J. y Waite, T. D. 2005. Fenton-mediated oxidation in the presence and absence of oxigen. Environmental Science and Technology. 39(13):5052-5058.
Esquivel, K. 2008. Desarrollo de un electrodo a base de fibra óptica recubierto con TiO2 incorporado en un reactor fotoelectroquímico para el tratamiento de efluentes acusos contaminados con colorante textil mediante procesos electroquímicos de oxidación avanzada. Tesis de Maestría. Centro de Investigación y Desarrollo Tecnológico en Electroquímica, S. C. CIDETEQ. Qro. México. pp. 98.
Agradecimientos
J. H. Castillo-Ledezma agradece al Consejo Nacional de Ciencia y Tecnología (CONACyT) y a la Universidad de las Américas Puebla, por el financiamiento de sus estudios de posgrado.
EUPS (Escuela Universitaria Politécnica de Sevilla. Grupo Tar). 2010. Tipos de aguas residuales industriales. http://prueba2.aguapedia.org/master/ponencias/mod ulo1/ponencias_modulo01_master_0406/ari_general idades.pdf, accesada 20/2/2010.
Gisela, K., Calderón, G., Schneider, S., Domínguez, W. y Gutiérrez G. 2009. Informe técnico sobre ingeniería agrícola y alimentaria. Organización de las Naciones Unidas para la Agricultura y la Alimentación. ftp://ftp.fao.org/docrep/FAO/011/i0480s/i0480s.pdf, accesada24/2/2010.
Gottschalk, C., Libra, J. y Saupe, A. 2000. Ozonation of water and wastewater.Wiley-VCH, Alemania. pp. 9, 11-18, 30, 148, 149.
IMTA. 2010. Agua para producción de alimentos. Instituto Mexicano de Tecnología del Agua, 2010.http://www.imta.gob.mx/index.php?option=co m_content&view=article&id=180:agua-paraproduccion-dealimentos&catid=52:enciclopediadelagua&Itemid=8 0, accesada 22/2/2010.
Kiwi, J. y Nadtochenko, V. 2004. New evidence for TiO2photocatalysis during bilayer lipid peroxidation. Journal of Physical Chemistry B. 108(45):1767517684.
Kiwi, J. y Nadtochenko, V. 2005. Evidence for the mechanism of photocatalytic degradation of the bacterial wall membrane at the TiO2 interface by ATR-FTIR and laser kinetic spectroscopy. Langmuir. 21(10):4631-4641.
Kusic, H., Koprivanac, N., Loncaric, B. y Selanec, I. 2006. Photo-assisted Fenton type processes for the degradation of phenol: A kinetic study. Journal of hazardous Material. 136(3):632- 644.
Kwan, C. Y. y Chu, W. 2003.Photodegradation of 2,4dichlorophenoxyacetic acid in various iron-mediated oxidation systems. Water research. 37(18):44054412.
Litter, M. y Mansilla, H. 2003a. Desinfección Solar de aguas en Comunidades Rurales de América Latina. Agencia Interamericana para la Cooperación y el Desarrollo.Proyecto OEA AE 141/2001. Documento técnico.
Litter, M y Mansilla, H. 2003b. Remoción de arsénico asistida por luz solar en comunidades rurales de América Latina. Agencia Interamericana para la Cooperación y el Desarrollo. Proyecto OEA AE 141/2001. Documento Técnico.
Machado, A., De Miranda, J., De Freitas, R., Thomas, E., Duarte, F., Ferreira, L., Albuquerque, Y., Ruggiero, R., Sattler, C. y De Oliveira, L. 2003. Destruction of the organic matter present in effluent from a cellulose and paper industry using photocatalysis. Journal of Photochemistry and Photobiology A: Chemistry. 155(1-3):231- 241.
Malato, S., Blanco, J., Vidal, A. y Richter, C. 2002. Photocatalysis with solar energy at a pilotsacle: an overview. Applied Catalysis B: Environmental. 37(1):1-15.
Metcalf y Eddy. 2003. Eastwater engineering. Treatment and reuse. Cuarta edición. MacGraw Hill, NY, EE.UU. pp. 1196-1201.
Nadtochenko, V., Rincón, A., Stanca, S. y Kiwi, J. 2004. Dynamics of E. coli membrane cell peroxidation during TiO2 photocatalysis studied by ATR-FTIR spectroscopy and AFM microscopy. Journal photochemistry and photobiology A: Chemistry. 169(2):131-137.
Parish, M. E., Beuchat, L.R., Suslow, T. V., Harris, L.J., Garrett, E. H., Farber, J. N. y Busta, F. F. 2003. Methods to reduce/eliminate pathogens from fresh and fresh-cut produce. Comprehensive reviews in food science and food safety. 5(2):161-173.
Parsons, S. 2005. Advanced oxidation processes for water and watewater treatment. IWA Publishing. Londres, ReinoUnido. pp. 1-5, 138-139.
Peralta, J. M, Maldonado, M. I., Meas, V., Rodríguez, F.,Godñinez, L. A y Malato, S. 2007. Aplicación de procesos electroquimicos de oxidación avanzada para la degradación de compuestos orgánicos en efluentes acuosos. CIEMAT. Ed. Madrid, España. pp. 17, 23-27, 69-70.
Rodríguez, C. P., Ziolli, R., L. y Guimaraes, J. R. 2007. Inactivation of Escherichia coli in water by TiO2assisted disinfection using solar light. Journal of Brazilian Chemical Society. 18(1):126-134.
Sarria, V., Kenfack, S., Guillod, O y Pulgarín, C. 2003.An innovative coupled solar-biological system at field pilot scale for the treatment of biorecalcitrant pollutants. Journal of Photochemistry and Photobiology A: Chemistry. 159(1):89-99
Serpone, N., Emeline, A. 2002. Suggested terms and definitions in photocatalysis and radiocatalysis. International Journal of Photoenergy. 4(3):89-99.
Tryba, B. 2008. Increase of the Photocatalytic Activity of TiO2 by Carbon and Iron Modifications. International Journal of Photoenergy. Article ID 721824.doi:10.1155/2008/721824.
Xie, Y y Yuan, Ch. 2004. Photocatalysis of neodymium ion modified TiO2 sol under vis- ible light irradiation. Applied Surface Science. 221(1-4):1724.
Xiejun, L., Yiming, X., Kangle, L. y Gencheng, Z. 2005. Photo-assisted degradation of anionic dyes over iron(III)-loaded resin in the presence of hydrogen peroxide. Journal of photochemistry and Photobiology A: Chemistry. 173(2):121-127.

Temas Selectos de Ingeniería de Alimentos 1 – 4 (2010): 84 – 95

Piranoantocianinas: modificaciones estructurales de antocianinas
Ma. del Pilar Guzmán-Figueroa*, Ana E. Ortega-Regules, Cecilia Anaya-Berrios
Departamento de Ingeniería Química, Alimentos y Ambiental. Universidad de las Américas, Puebla. Sta. Catarina Mártir, Cholula, Puebla. 72810. México
Resumen
Las antocianinas son compuestos cuyos alcances han ido más allá de ser sólo pigmentos, ya que proporcionan beneficios a la salud. Sin embargo, su limitada estabilidad ha restringido su uso en alimentos. Esto, aunado al descubrimiento de otros compuestos derivados que exhiben mayor estabilidad ante el pH y la degradación, ha dado paso a la búsqueda de derivados y a su síntesis química. En este artículo se presentan a las piranoantocianinas como modificaciones realizadas a las antocianinas, además su estructura y reactividad.
Palabras clave: antocianinas, piranoantocianinas, modificaciones estructurales, derivados de antocianinas.
Abstract
Anthocyanins have not been just pigments but compounds with certain benefits for health. Nevertheless their weak stability in addition to discovery other derived anthocyanins have give rise to their search and their synthesis. This is mainly due to their major pH and degradation stability. In the present paper, pyranoanthocyanins are presented as anthocyanins-derived and it describes their structure and reactivity.
Keywords: anthocyanins, pyranoanthocyanins, structural transformations, derived anthocyanins.
Introducción
Las antocianinas constituyen una de las familias polifenólicas más grandes en el reino vegetal; éstas pertenecen al grupo de los flavonoides, pero se consideran como una clase diferente debido a su habilidad de formar cationes flavilio (Mazza et al., 2004). Ellas son las responsables de los colores rojo, violeta y azul presentes en muchas frutas
*Programa de Doctorado en Ciencia de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: jordanah.castillola@udlap.mx
(Hillebrand et al., 2004).
En la actualidad, las antocianinas son de interés en la industria de los alimentos debido a que tienen algunas aplicaciones como colorantes naturales (Oliveira et al., 2006). De hecho, pueden ser consideradas como remplazo potencial para los colorantes cuyo uso ha sido cuestionado, ya que las antocianinas tienen colores brillosos y son solubles en agua (Rodriguez-Saona et al., 1998).
En años recientes, numerosos estudios han mostrado que las antocianinas exhiben una gran cantidad de actividades biológicas incluyendo la actividad antiinflamatoria, antimicrobiana, anticancerígena y antioxidante. De hecho, las antocianinas son potentes antioxidantes superiores a los antioxidantes clásicos, como el hidroxibutilanisol (BHA), butil hidroxitolueno (BHT) y α-tocoferol (Mazza, 2007). Debido a esas propiedades antioxidantes, es posible que tengan un papel terapéutico potencial en el cáncer (Hou et al., 2005; Wang y Stoner, 2008) y en enfermedades crónicas degenerativas asociadas con el estrés oxidativo como la arterioesclerosis (Mazza et al., 2004). Además, tienen efectos en los vasos sanguíneos y en las plaquetas, que pueden reducir el riesgo de la enfermedad coronaria cardiaca (Mazza, 2007). Por todo lo anterior, las antocianinas son consideradas como nutracéuticos importantes.
Pese a sus bellos colores y actividades benéficas para la salud, las antocianinas son inestables a ciertos factores. Sin embargo, se han aislado derivados estructurales de las antocianinas que muestran mayor estabilidad, entre los cuales se encuentran las piranoantocianinas. Este artículo presenta una revisión general de las antocianinas, su estructura y reactividad, así como las características estructurales y estabilidad de las piranoantocianinas.
En frutas y vegetales, las antocianinas se encuentran en forma glicosilada, son comunes los 3-monoglucósidos, 3-diglucósidos y 3, 5diglucósidos Sin embargo, muchos de los procedimientos analíticos convierten a los glicósidos en agliconas (antocianidinas); por tal motivo, los datos de las Tablas I y II están reportados como agliconas. Entre diferentes vegetales y/o variedades del mismo vegetal, el contenido total de las antocianinas puede variar considerablemente. Éste puede estar afectado por genes, luz, temperatura y factores agronómicos (Horbowicz et al., 2008). En el 90% de los vegetales se encuentra la cianidina, siendo la antocianidina más abundante, seguida de la delfinidina, peonidina, pelargonidina, petunidina y malvidina (en orden decreciente).
Como se observa en la Tabla I, los alimentos más ricos en antocianinas son la aronia (originaria de EE. UU.), el saúco (origen europeo) y la uva. Los dos primeros no se cultivan en el país, a diferencia de la uva, de cuya producción México ocupó el quinto lugar
Tabla I. Contenido total de antocianinas en algunas frutas y vegetales.
Fruta o vegetalContenido total de antocianinas (mg/kg)
Manzana roja (cáscara)100-2160
Arándano4600
Zarzamora820-1800
Mora azul825-5300
Cereza3500-4500
Aronia5060-10000
Arándano rojo460-2000
Saúco2000-15600
Uva (roja)300-7500
Uva (azul)80-3880
Revisión bibliográfica
1. Antocianinas en los alimentos
Las antocianinas son pigmentos vacuolares presentes en todo el reino vegetal que pueden encontrarse en diversos tejidos incluyendo flores, frutos, hojas, tallos, tubérculos, raíces y cáscaras de semillas (Oliveira et al., 2006; Yoshida et al., 2009).
Naranja sanguina2000
Ciruela19-250
Frambuesa (negra)763-4277
Fresa127-360
Grosella (negra)1300-4000
Grosella (roja)119-186
Col morada250
Berenjena7500
Rábano110-600
Cebolla (roja)<250
Adaptado de Horbowicz et al. (2008)
Tabla II. Contenido de las principales antocianinas en algunas frutas y vegetales (mg/100 g)
EspecieCyPgMvPtPnDp
Manzana
Gala1.5
Goldern delicius2.0
Red delicius6.1
Zarzamora90.30.2
Arándano112.654.451.151.1161.9
Blueberries17.061.426.411.447.4
Aronia435.81.4
Arándano rojo41.80.342.17.7
Grosella (negra)85.61.23.90.7181.1
Grosella (roja)12.9
Saúco785.51.1
Uva (roja)1.51.134.72.92.13.7
Ciruela39.7
Frambuesa (roja) 35.81.90.70.3
Frambuesa (negra)323.5
Cereza75.20.54.5
Fresas2.031.30.3
Frijol (negro)6.59.612
Frijol (rojo)1.22.4
Col morada72.90.1
Berenjena13.8
Lechuga (roja)2.8
Cebolla (roja)6.21.22.3
Rábano25.7
Cy, cianidina; Pg, pelargonidina; Mv, malvidina, Pt, petunidina; Pn, peonidina; Dp, delfinidina
Adaptado de Horbowicz et al. (2008)
a nivel mundial en el año 2005 (Alimentariaonline, 2005). En la uva, a diferencia de la mayoría de las frutas, la antocianina mayoritaria es la malvidina (Rein, 2005) (Tabla II). Y puesto que la uva es la materia prima para la elaboración del vino, las antocianinas también se encuentran presentes en este producto -sus antocianinas son extraídas durante el aplastamiento, prensado y fermentación- (Mazza et al., 1999). Éstas junto con otros flavonoides, juegan un papel muy importante en la calidad del vino, pues contribuyen a las características sensoriales, particularmente al color y astringencia. Además, las interacciones de las antocianinas con otros compuestos fenólicos incoloros, contribuyen al sabor y a otras características químicas.
En el caso de los vinos, la concentración y composición fenólica depende de la especie, variedad y estación de la uva, así como de un amplio rango de factores ambientales (Mazza et al., 1999). La malvidina también es la antocianina más abundante en los vinos, aunque existen vinos en los que predominan otras antocianinas (Jackson, 2008). Casterallin y DiGaspero (2007) afirman que la malvidina es la antocianina más abundante en vinos preparados con variedades donde prevalezcan antocianinas tri-hidroxiladas, mientras que para las variedades en las que dominen las antocianinas di-hidroxiladas, la antocianina predominante será la peonidina.
Las antocianinas se utilizan comercialmente como aditivos en forma de antocianidinas, las cuales se extraen de fuentes como col morada,
fresas, cáscara de uva, mora azul o frambuesa, y pueden adquirirse en forma individual bajo los códigos:
Cianidina CAS#528-58-5
Delfinidina CAS#528-53-0
Malvidina CAS#643-84-5
Peonidina CAS#134-01-0
Petunidina CAS#1429-30-7
Pelargonidina CAS#134-04.3 E163
Aunque también los extractos ricos en antocininas provenientes de frutas y vegetales pueden ser usados como colorantes. Hasta ahora, el bagazo de uva ha constituido el recurso principal de los colorantes basados en antocianinas, producidos comercialmente en Italia desde 1879, con una producción anual de ~65 millones de toneladas. El bagazo de uva constituye una fuente de antocianinas de bajo costo y abundante. Otras frutas como el
4 – 1 (2010): 84 – 95
saúco, el casis o la aronia, también han sido utilizadas como colorantes rojos en alimentos y en bebidas ácidas (Malien-Aubert et al., 2001).
2. Estructura y reactividad de las antocianinas
Estructuralmente, las antocianinas (Fig. 1) son sistemas aromáticos conjugados, derivados hidroxilados o metoxilados del fenil-2benzopirilio o sales de flavilo. Ya que cada antocianidina puede ser glicosilada y acetilada por varios azúcares y ácidos orgánicos en diferentes posiciones, es posible un gran número de combinaciones (Horbowicz et al., 2008). Sin embargo, la mayoría de las variaciones se deben a la sustitución glicosídica en las posiciones 3 y 5. Así pues, mientras que son seis las antocianidinas comunes, existen más de 540 antocianinas (Wrolstad et al., 2005).
Nombre de la antocianidina
max (nm)
PelargonidinaHH494 (naranja)
CianidinaOHH506 (naranja-rojo)
DelfidinaOHOH508 (azul-rojo)
Peonidina OCH3 H506 (naranja-rojo)
Petunidina OCH3 OH508 (azul-rojo)
Malvidina OCH3 OCH3 510 (azul-rojo)
Fig. 1. Estructura general de las antocianidinasy de las antocianinas (Astrid-Garzón, 2008).
En cuanto a la reactividad de éstas, se sabe que los anillos aromáticos de los flavonoides tienen cierta densidad electrónica en sitios específicos, debido a los efectos mesoméricos de los sustituyentes electrodonadores (como los grupos hidroxilos) (Jordheim et al., 2007a).
Estas características dan lugar a que puedan sufrir un ataque nucleofílico en las posiciones cargadas positivamente en C-2 y C-4 del anillo C. Además, son capaces de reaccionar con compuestos electrofílicos a través de C-6 y C8 del anillo A. La existencia del grupo 5-OH es muy importante para la reactividad de estos pigmentos con otros compuestos (Fig. 2).
Ataqueelectrofílico
Ataquenucleofílico
Las antocianinas absorben en el rango visible, por lo que cada una de ellas puede ser representada a través de su color único (Jaldappagari et al., 2008). Las características crómicas de las antocianinas están afectadas de manera significativa por la sustitución en el anillo B. Por ejemplo, el incremento de grupos hidroxilo resulta en un desplazamiento batocrómico. Otros factores importantes son la naturaleza del azúcar, si se encuentra acilado o no, y la posición en la aglicona (DeFreitas y Mateus, 2006).
4 – 1 (2010): 84 – 95
Las antocianinas se degradan durante el procesamiento y almacenamiento de los alimentos, lo cual puede tener un impacto grave en la calidad del color y en las propiedades nutricionales (Wrolstad et al., 2005). Cabe mencionar que la estabilidad depende de la estructura de la antocianina que se trate; la estabilidad se incrementa con el número de grupos metoxilos en el anillo B y decrece al aumentar los grupos hidroxilos. Así, la antocianina más estable es la malvidina, seguida de la peonidina, petunidina, cianidina y delfinina (Li y Jiang, 2007). A continuación se presentan algunos factores externos que afectan la estabilidad.
2.1. pH
En solución acuosa, las antocianinas existen en cuatro diferentes formas en equilibrio (Fig. 3): la base quinoidal (A), el catión flavilio (AH+), el carbinol o pseudobase (B) y la chalcona (C). En soluciones muy ácidas (pH<1) el equilibrio se desplaza hacia el catión flavilio, existiendo sólo esta forma. Al incrementar el pH se reduce la intensidad del color debido a la disminución de concentración de este catión, el cual se convierte en su forma incolora de hemiacetal a través del ataque nucleofílico del agua. Cabe mencionar que las antocianinas pierden cerca del 80% de la intensidad de su color en un intervalo de pH de 1 a 5 como resultado de la formación de la base carbinol (Rentzsch et al., 2007).
2.2. Temperatura
La temperatura induce una destrucción lenta de los pigmentos; cuando ésta se incrementa, las antocianinas pueden transformarse en chalcona, estructura inestable que se degrada en compuestos de color café (Horbowicz et al., 2008). También es posible que las unidades glicosídicas se pierdan por hidrólisis del enlace glicosídico al aumentar la temperatura en un intervalo de pH de 2 a 4, por lo cual las antocianinas pierden el color, ya que las
Fig. 2. Sitios reactivos de la antocianina (Rentzsch et al., 2007).
agliconas son más estables que sus formas glicosídicas originales (Rein, 2005).
2.3. Otros factores
a) Oxígeno. El efecto de deterioro que tiene en las antocianinas ocurre a través de mecanismos de oxidación directa y/o indirecta, en los que los compuestos oxidados del medio reaccionan con las antocianinas, para dar compuestos incoloros o cafés. Las antocianinas también son reactivas a radicales de oxígeno. En estas reacciones las antocianinas se comportan como antioxidantes (Rein, 2005).
b) Agua oxigenada. Es el agente de esterilización de empaques más común, y aunque el procedimiento está diseñado para eliminar totalmente el agua oxigenada, pueden quedar residuos o vapores. Su presencia causa degradación de antocianinas, la cual se potencializa si hay ácido ascórbico presente. Sin embargo, a concentraciones bajas, el ácido ascórbico es capaz de proteger la antocianina de la degradación por agua oxigenada (Ozkan, 2002).
c) Luz. Afecta a las antocianinas de dos formas, ya que, por una parte, la luz es esencial para la biosíntesis de estos compuestos, pero por otro lado, también
Bases quinoidales (Azul)
Carbinol (Incoloro)
Chalcona (Incoloro)
Catión flavilio (Rojo)
Fig. 3 . Equilibrio de las estructuras de la antocianina en solución acuosa (Horbowicz et al. , 2008).
acelera su degradación (Rein, 2005), pues se sugiere que la luz incrementa la conversión hacia el catión flavilio y que en ausencia de luz, la cantidad de chalcona es mayor que la del catión flavilio. Un estudio en cuatro especies de Malus demostró que los pigmentos expuestos a la luz durante 135 días a 20 °C mostraban el 50% de sus pigmentos destruidos, mientras que las muestras que se mantuvieron en la obscuridad presentaban el 30% de destrucción (Bakhshyeshi et al., 2006).
d) Ácido ascórbico. Éste puede propiciar la polimerización de las antocianinas, lo cual las hace incoloras. Aunque también existe la posibilidad de que el ácido reaccione directamente con las antocianinas, con lo cual seguirá un mecanismo de degradación (Rein, 2005).
e) Azúcares. Los azúcares y sus productos de degradación disminuyen la estabilidad de las antocianinas. Es sabido que sacarosa, fructosa, glucosa y xilosa degradan de la misma forma, generando pigmentos poliméricos cafés (Rein, 2005). No obstante, añadir sacarosa protege a las antocianinas de la degradación en el almacenamiento en congelación, y previene el obscurecimiento y la formación pigmentos poliméricos, lo cual es probablemente debido a que inhibe reacciones enzimáticas y hace más lentas a las reacciones de condensación. El efecto del azúcar añadido en la estabilidad de las antocianinas depende de la estructura, concentración y tipo de azúcar (Nikkhah et al., 2007).
f) Dióxido de azufre (SO2). Es usado ampliamente en la elaboración moderna del vino como antioxidante e inhibidor del crecimiento microbiano indeseable. Aunque también es conocido como blanqueador y aclarante del color del vino debido a la formación de antocianin-4-bisulfito, un compuesto incoloro. Es necesario mencionar que una pequeña cantidad de SO2 puede
decolorar grandes cantidades de antocianinas. Es posible hacer un buen vino sin el uso de sulfitos, pero tendrían menos consistencia y estabilidad biológica (Nikkhah et al., 2008).
g) Enzimas. Se han reportado diversos sistemas enzimáticos que afectan la estabilidad de las antocianinas, produciendo colores cafés, entre ellos, la fenolasa, la peroxidasa (POD) y polifenol-oxidasa (PPO) (Calderon et al., 1992). Las últimas dos han sido implicadas en el obscurecimiento enzimático de los tejidos en frutas, aunque la PPO parece ser la enzima principal (Kader et al., 2002).
Se ha sugerido que la PPO no degrada directamente a las antocianinas, sino que son las quinonas formadas durante la oxidación de otros compuestos fenólicos (Calderon et al., 1992). Posteriormente, las quinonas polimerizan a las antocianinas, formando pigmento cafés (Kader et al., 1997). Mientras tanto, el mecanismo de la degradación por la POD permanece aún desconocido (Kader et al., 2002).
3. Modificaciones estructurales
3.1. Importancia de las modificaciones estructurales a las antocianinas
Los cambios de color que sufren las antocianinas representan una desventaja para su uso como colorantes en alimentos en los cuales existan condiciones de pH neutras o que difieran en las expresiones de color. Por ello, diversos grupos de investigación dedicados a la industria alimentaria, se han dado a la tarea de buscar nuevos pigmentos naturales con mayor estabilidad, no sólo frente al pH, sino a factores como el SO2 y la temperatura (Oliveira et al., 2006). De esta forma, el desarrollo de colorantes naturales basados en antocianinas que tengan mejor color y estabilidad es un área de gran interés en la investigación (Wrolstad et al., 2005).
3.2. Piranoantocianinas
Las características del vino dependen de su añejamiento. Se ha establecido que el cambio más importante en el color ocurre durante el primer año de maduración, durante el cual es almacenado a granel. Esta fase es considerada distinta a las “etapas de añejado” posteriores, en las que el vino está embotellado y protegido de cualquier contacto con el aire. El cambio de color durante la maduración del vino es atribuido a la formación de nuevos pigmentos, entre ellos las piranoantocianinas resultantes de la reacción entre antocianinas y otros compuestos fenólicos, (Mateus et al., 2001).
Las piranoantocianinas son derivados de las antocianinas en las cuales el grupo hidroxilo se une a diferentes sustratos formando un anillo pirano. En la literatura, algunos autores suelen agrupar a todas las antocianinas con el anillo del pirano bajo el nombre genérico de piranoantocianinas (Jordheim et al., 2006). Sin embargo, existen diversas clases (Fig. 4): hidroxifenil-piranoantocianinas, vitisinas y portisinas (Rentzsch et al., 2007).
En general, se puede afirmar que las piranoantocianinas difieren de las antocianinas en algunos aspectos analíticos, especialmente en el color. En comparación con las
Ácidoscinámicos Vinilfenol
Acetaldehído
Fig. 4 . Algunas clases derivadas de antocianinas.
Antocianina
antocianinas originales, las piranoantocianinas poseen un desplazamiento hipsocrómico de la absorción máxima, la cual resulta en un color más naranja comparado con el rojo-morado original. Es interesante destacar que debido al nuevo anillo pirano, el color de la piranoantocianina no cambia su intensidad ante cambios de pH. Esto sucede por el efecto protector del nuevo anillo hacia el ataque nucleofílico del agua (Rentzsch et al., 2007).
Otro aspecto que vale la pena enfatizar es que esta clase de pigmentos están ausentes en extractos frescos, y que sus concentraciones aumentan gradualmente con el tiempo, probablemente debido a la reacción de las antocianinas y el ácido p-cumárico en los extractos (Jordheim et al., 2006). Así pues, al contrario de las antocianinas que se encuentran en constante degradación, las piranoantocianinas aumentan su concentración a lo largo del tiempo.
En cuanto a reactividad se refiere, se ha determinado que a diferencia de las antocianinas con centros susceptibles a ataques electrofílicos en C-6 y C-8, las piranoantocianinas carecen de esta susceptibilidad en dichos carbonos. Sin embargo, muestran un nuevo centro en C-4 del anillo D (Jordheim et al., 2007a). No obstante, a pesar de las diferencias en reactividad, las piranoantocianinas siguen exhibiendo propiedades antioxidantes comparables y en algunos casos mayores a las antocianinas originales (Jordheim et al., 2007b).
Aunque es posible que las piranoantocianinas tengan actividades biológicas similares y mayor estabilidad que las antocianinas, hasta el momento no se han encontrado reportes sobre la toxicidad de estos compuestos, por lo que aún se desconoce si podrán ser empleados o no. Sin embargo, es probable que la cantidad de piranoantocianinas necesaria para impartir color sea similar a la
que se encuentra en los vinos; si tal es el caso, no serían tóxicas.
3.2.1. Hidroxifenil-piranoantocianinas
La historia de las hidroxifenilpiranoantocianinas data desde 1996, cuando una nueva clase de pigmentos fue detectada en vinos tintos por Cameira dos santos et al. Dos de estos nuevos pigmentos fueron aislados y poseían características diferentes en el espectro UV/Visible. Un análisis de ESI-LCMS (Cromatográfia líquida acoplada a un espectrómetro de masas de ionización por electrospray) reveló que estos nuevos pigmentos eran el glucósido y pcumaroilglucósido de una aglicona desconocida con una masa molecular superior a la de las antocianinas originales de la uva, por lo que sólo se concluyó que se podía tratar de un derivado de antocianinas. Sin embargo, en el mismo año Fulcrand et al.(1996), presentó una estructura con un anillo de pirano adicional entre el C-4 y el grupo hidroxilo de C-5 de un centro de malvidina y un fragmento fenólico. Más tarde, demostró que esos compuestos eran el resultado de la reacción de la malvidina 3-glucósido y el vinilfenol, no obstante se han sintetizado otras piranoantocianinas con otros centros, como se muestra en la Fig. 5.
En general, las hidroxifenilpiranoantocianinas son el producto de adición entre las antocianinas y ácidos cinámicos o compuestos vinilfenólicos, resultando en la formación de un anillo pirano sustituido en C10 por un fragmento aromático. Recientemente, se han aislado pigmentos análogos de la fresa y la frambuesa después de haber añadido ácidos cinámicos (Jordheim et al., 2006). El mecanismo propuesto para la formación de esta clase de piranoantocianina se muestra en la Fig. 6. El enlace inicial formado entre C-4 de la antocianina y C-2 del ácido, es consistente con la naturaleza fuertemente electrofílica del fragmento
benzopirilio y la nucleofilicidad del carbón α del ácido. El intermediario se estabiliza mediante los efectos electronadores de los grupos unidos al anillo aromático del ácido. Cualquiera de los intermediaros puede sufrir una reacción intramolecular con el grupo hidroxilo y finalmente el producto se forma por oxidación seguida de una descarboxilación (Schwarz y Winterhalter, 2003).
3.2.2. Vitisinas
Un grupo importante de las piranoantocianinas, fue descrito por primera vez en 1997 por Bakker y Timberlake, quienes aislaron el compuesto llamado vitisina A. Ellos asumieron que ésta es el producto de la reacción entre la malvidina 3-glucósido y una molécula desconocida, la cual está ausente en las uvas frescas pero presente en los vinos añejados (Rentzsch et al., 2007).
En cuanto a su color se refiere, tanto la vitisina A como la vitisina B, presentan desplazamientos hipsocrómicos: vitisina A, 18-19 nm y vitisina B, 36-39 nm, dependiendo del disolvente. Esto puede deberse a la carga positiva en el anillo C, la cual puede deslocalizarse por resonancia pasando al anillo D (Fig. 7). También presentan una banda de absorción inusual, la cual es atribuida a la sustitución presente en C-4 (Bakker y Timberlake, 1997).
En los últimos años, derivados de la malvidina sustituidos en C-4 han sido descubiertos en pequeñas cantidades en vinos, en bagazo de uva y en la fresa (Fragaria ananassa) (Andersen et al., 2004).
3.2.3. Portisinas
En el caso de las portisinas, las propiedades espectroscópicas son diferentes a las clases anteriores de piranoantocininas. Están conformadas por una antocianina unida a un flavanol a través de un puente vinílico (Mateus
4 – 1 (2010): 84 – 95
et al., 2004). Éstas poseen un desplazamiento batocrómico con una absorción en el visible cercana a 580 nm, por lo que presentan colores azulados (Rentzsch et al., 2007), lo cual puede deberse a que la conjugación de los electrones π se extiende en las estructuras formadas (Oliveira et al., 2007).
Las portisinas fueron aisladas del vino de Oporto, y en cuanto a su formación, pueden deberse a la reacción entre aductos de antocianina-ácido pirúvico y otros compuestos como los flavanoles, floroglucinol en presencia acetaldehído, o bien, de la reacción directa con vinilfenol (Mateus et al., 2004). Recientemente, se aislaron de un vino tinto donde se forman a través de una reacción entre el 5-carboxipiranomalvidina-3-glucósido (vitisina A) y el vinilfenol (Mateus et al., 2006). Sin embargo, estos pigmentos han sido sintetizados por el grupo de investigación de Mateus, quienes establecieron un protocolo para la obtención de estos compuestos, el cual comienza por la obtención de las antocianinas, que puede ser de cualquier recurso natural, seguida de su reacción con ácido pirúvico. Al aducto formado se le hace reaccionar con (+)catequina, en presencia de acetaldehído (Fig. 8).
Estos pigmentos, al ser de color azul, pueden ser prometedores en la industria alimentaria, ya que a pesar de la gran gama de colores que existe en la naturaleza, los pigmentos azules son escasos.
Conclusiones
Las antocianinas son compuestos que tienen muchas ventajas, sin embargo, su inestabilidad ha propiciado la búsqueda de nuevos pigmentos. Es ahí donde las piranoantocianinas se presentan como una opción para sustituir tanto a los pigmentos sintéticos como a las mismas antocianinas. Sin
M. P. Guzmán-Figueroa et al. / Temas Selectos de Ingeniería de Alimentos 4 – 1 (2010): 84 – 95
embargo, las piranoantocianas no han sido totalmente exploradas, hasta el momento el conocimiento prácticamente se ha limitado a aislarlas y caracterizarlas, por tanto, su síntesis y su uso como aditivo no ha sido estudiado extensamente.
Casterallin, S. D. y DiGaspero, G. 2007. Transcriptional control of anthocyanin biosynthetic genes in extreme phenotypres for berry pigmentation of naturarally occurring grapevines. MBMC Plant Biology 7: 4655.
DeFreitas, V. y Mateus, N. 2006. Chemical transformations of anthocyanins of colours. Environmental Chemistry Letters. 4: 175-183.
Agradecimientos
Se agradece al Consejo Nacional de Ciencia y Tecnología (CONACYT) y a la Universidad de las Américas Puebla (UDLAP) por el apoyo para la realización de este trabajo.
Fulcrand, H., Cameira dos Santos, P. J., SarniManchado, P., Cheynier, P. y Favre-Bonvin, J. 1996. Structure of new anthocyanin-derived wine pigments. Journal of the Chemical Society Perkin Transactions 1: 735-739.
Hendry, G. A. y Houghton, J. D. 1996. "Natural Food Colorants". Gran Bretaña, Chapman & Hall.
Referencias
Alimentariaonline. 2005. Servicio de Delta Enfoque de http://www.alimentariaonline.com/desplegar_n ota.asp?did=945 accesada el 15/04/10.
Andersen, O. M., Fossen, T., Torkangerpoll, K., Fossen, A. y Hauge, U. 2004. Anthocyanin from strawberry (Fragaria ananassa) with the novel aglycone, 5carboxypyranopelargonidin. Phytochemistry 65: 405-410.
Bakhshyeshi, M. A., Khayami, M., Heidari, R. y Jamei, R. 2006. The effects of light, storage temperature, pH and variety on stability of anthocyanin pigments in four Malus varieties. Pakistan Journal of Biological Sciences 9: 428-433.
Bakker, J. y Timberlake, C. F. 1997. Isolation, identificaion and characterization of new colorstable anthocyanins ocurring in some red wines. Journal of Agricultural and Food Chemistry 45: 3543.
Calderon, A. A., Carcía-Florenciano, E., Muñoz, R. y RosBarcelo, A. 1992. Gamay grapevine peroxidase: its role in vacuolar anthocyanindin degradation. Vitis 31: 139-147.
Cameira dos Santos, P. J., Brillouet, J. M., Cheynier, V. y Moutounet, M. 1996. Detection and partial characterization of new anthocyanin-derived pigments in wine. Journal of Science and Food and Agriculcure 70: 204-208.
Hillebrand, S., Schwarz, M. y Winterhalter, P. 2004. Characterization of anthocyanins and pyranoanthocyanins from blood orange [Citrus sinensis (L.) Osbeck] juice. Journal of Agricultural and Food Chemistry 52: 7331-7338.
Horbowicz, M., Kosson, R., Grzesiuk, A. y Debski, H. 2008. Anthocyanins of fruits and vegetables -their ocurrence, analysis and role in human nutrition Vegetable Crops Research Bulletin 68: 5-22.
Hou, D., Tong, X., Terahara, N., Lou, D. y Fuji, M. 2005. Delphinidin 3-sambubiosido, a Hibiscus anthocyanin, induces apoptosis in human leukemia cells through reactive oxygen species-mediated mitochondrial pathway. Archives of Biochemistry and Biophysics 440: 101-109.
Jackson, R. S. 2008. "Wine Science. Principles and applications". San Diego, California, EE.UU., Elsevier.
Jaldappagari, S., Motohashi, N., Gangeenahalli, M. P. y Naismith, J. H. 2008. Topics in heterocyclic chemistry. Berlin, Springer: 49-54.
Jordheim, M., Fossen, T. y Andersen, O. M. 2006. Preparative Isolation and NMR characterization of carboxypyranoanthocyanins. Journal of Agricultural and Food Chemistry 54: 3572-3577.
Jordheim, M., Aaby, K., Fossen, T., Skrede, G. y Andersen, O. M. 2007a. Molar absorptivities and reducing capacity of pyranoanthocyanins and other anthocyanins. Journal of Agricultural and Food Chemistry 55: 10591-10596.
Jordheim, M., Fossen, T., Songstad, J. y Andersen, O. M. 2007b. Reactivity of anthocyanins and pyranoanthocyanins. Studies on aromatic hydrogen-
M. P. Guzmán-Figueroa et al. / Temas Selectos de
deuterium exchange reactions in methanol. Journal of Agricultural and Food Chemistry 55: 8261-8268.
Kader, F., Rovel, B., Girardin, M. y Metche, M. 1997. Mechanism of browing in fresh highbush blueberry fruit (Vaccinium corymbosum L). Role of blueberry polyphenol oxidase, chlorogenic acid and anthocyanins. Journal of Science and Food and Agriculcure 74: 31-34.
Kader, F., Irmouli, M., Nicolas, J. P. y Metche, M. 2002. Involvement of blueberry peroxidase in the mechanisms of anthocyanin degradation in blueberry juice. Journal of Food Science 67: 910915.
Li, J. y Jiang, Y. 2007. Litchi flavonoids: isolation, identification and biological activity. Mocules 12:(745-758).
Malien-Aubert, C., Dangles, O. y Amiot, M. J. 2001. Color stability of commercial anthocyanin-based extracts in relation to the phenolic composition. Protective effects by intra and intermolecular copigmentation. Journal of Agricultural and Food Chemistry 49: 170-176.
Mateus, N., Oliveira, J. y Pissarra, J. 2006. A new vinylpyranoanthocyanin catechin pigment (a portisin). Tetrahedron Letters 45: 3455-3457.
Mateus, N., Oliveira, J., Haettich-Motta, M. y DeFreitas, V. 2004. New family of bluish pyranoanthocyanins. Journal of Biomedicine and Biotechnology 299-305.
Mateus, N., Silva, A. M. S., Vercauteren, J. y DeFreitas, V. 2001. Ocurrence of anthocyanin-derived pigments. Journal of Agricultural and Food Chemistry 49: 4836-4840.
Mazza, G. 2007. Anthocyanins and heart health. Ann 1st Super Sanitá 43: 369-374.
Mazza, G., Cacace, J. E. y Kay, C. D. 2004. Methods of analysis for anthocyanins in plants and biological fluids. Journal of AOAC International 87: 129-145.
Mazza, G., Fujimoto, L., Delaquis, P. y Ewer, B. G. B. 1999. Anthocyanins, phenolics and color of cabernet franc, merlot and pinot noir wines from british columbia. Journal of Agricultural and Food Chemistry 47: 4009-4017.
Nikkhah, E., Khayamy, M., Heidari, R. y Bernousi, I. 2008. Effect of SO2 treatment stability of anthocyanin pigments in berries. Reserch Journal of Biological Sciences 3: 80-84.
de Alimentos 4 – 1 (2010): 84 – 95
Nikkhah, E., Khayamy, M., Heidari, R. y Jamee, R. 2007. Effect of sugar treatment on stability of anthocyanin pigments in berries. Journal of Biological Sciences 7: 1412-1417.
Oliveira, J., DeFreitas, V., Silva, A. M. S. y Mateus, N. 2007. Reaction between hidroxylcinnamic acids an anthocyanin-pyruvic acid adducts yielding new portisins. Journal of Agricultural and Food Chemistry 55: 6349-6356.
Oliveira, J., Fernandes, V., Miranda, C., Santos-Buelga, C., Silva, A., DeFreitas, V. y Mateus, N. 2006. Color properties of four cyanidin-pyruvic acid adducts. Journal of Agricultural and Food Chemistry 54: 6894-6903.
Ozkan, M. 2002. Degradation of anthocyanins in sour cherry and pomegranate juices by hydrogen peroxide in the presence of added ascorbic acid. Food Chemistry 78: 499-504.
Rein, M. 2005. Copigmentation reaction and color stability of berry anthocyanins. Department of applied chemistry and microbiology. Helsinki. University of Henlsinki.
Rentzsch, M., Schwarz, M. y Winterhalter, P. 2007. Pyranoanthocyanins- an overview on structures, ocurrence, and pathways of formation. Trends in Food Science & Technology 18: 526-534.
Rodriguez-Saona, L. E., Giusti, M. M. y Wrolstad, R. E. 1998. Anthocyanin pigment composition of redfleshed potatoes. Journal of Food Science 63: 458465.
Schwarz, M. y Winterhalter, P. 2003. A novel synthetic route to substituted pyranoanthocyanins with unique colour properties. Tetrahedron Letters 44: 75837587.
Wang, L. y Stoner, G. D. 2008. Anthocyanins and thier role in cancer prevention. Cancer Letters 269: 281290.
Wrolstad, R., Durst, R. W. y Lee, J. 2005. Tracking color and pigment changes in anthocyanin products. Trends in Food Science & Technology 16: 423-428.
Yoshida, K., Mori, M. y Kondo, T. 2009. Blue flower color development by anthocyanins: from chemical structure to cell physiology. Natural Products Reports 26: 884-915.
