



















Temas Selectos de Ingeniería de Alimentos Vol. 3 / No. 2
Dra. María Eugenia Bárcenas Pozos
Dra. María Teresa Jiménez Munguía
M. C. Fidel Vergara Balderas
Temas Selectos de Ingeniería de Alimentos

Contenido
Temas Selectos de Ingeniería de Alimentos Vol. 3 / No. 2
Volumen 3 / No. 2 Ago – Dic 2009
Temas Selectos de Ingeniería de Alimentos
Cuerpo editorial …………………………………………………………………………………. i Editorial ………………………………………………………………………………………….. iii
Contribución especial
No more excuses: Eat your fruits and vegetables!
L. Valerio – Junco* ………………………………………………………………………………... 1
Artículo de Revisión
Efecto de la incorporación de estabilizantes en la viscosidad de bebidas lácteas no fermentadas M.O. Ramírez-Sucre* y J. F. Vélez-Ruiz ………………………………………………………… 4
Artículos de Investigación
Evaluación de agentes antioxidantes de un extracto de flor de jamaica microencapsulado
C. Salazar-González*, F.T. Vergara-Balderas, J.A. Guerrero-Beltrán ………………………... 14
Efecto de hidrocoloides en las propiedades de pan recalentado en horno de microondas
G. Pérez-García*, F. Vergara-Balderas y M. E. Bárcenas-Pozos ………………………………. 26
Cinética de deshidratación por liofilización de maíz para la elaboración de botanas
D. Márquez - Aquino*, F. Vergara – Balderas …………………………..………………………. 39
Inactivación de esporas de Aspergilli con radiación UVC y sorbato de potasio en néctar de durazno J.A. Del Campo-Sacre*, D.X. Flores-Cervantes, J.J. Gómez-Díaz, A. López-Malo Vigil, M.T. Jiménez-Munguía y E. Palou-García ……………………………………..……………………… 51
Inactivación de dos levaduras por medio de radiación ultravioleta de onda corta en combinación con reducción de actividad de agua
T. Hernández-Grajales*, E. Palou-García, A. López-Malo

Editorial
Temas Selectos de Ingeniería de Alimentos Vol. 3 / No. 2
Temas Selectos de Ingeniería de Alimentos
El desarrollo del conocimiento es una de las responsabilidades de los estudiantes de posgrado e investigadores que aportan nuevas técnicas, métodos, teorías o aplicaciones en el área de su especialidad. Sin embargo, estas actividades serían insuficientes si no se hiciera un esfuerzo estructurado y formal para la difusión de dichos conocimientos a la comunidad científica.
Es en este contexto que se publica la revista Temas Selectos de Ingeniería de Alimentos (TSIA), cuyos objetivos son el entrenamiento de los estudiantes en la escritura de artículos científicos, así como la difusión de los trabajos de investigación y desarrollo de la Maestría y Doctorado en Ciencia de Alimentos realizados en el Departamento de Ingeniería Química, Alimentos y Ambiental de la Universidad de las Américas Puebla.
En este número se presentan artículos de investigación de los estudiantes de maestría sobre los resultados obtenidos en sus proyectos, se incluye un artículo de revisión realizado por un estudiante de doctorado y un artículo especial de una estudiante de licenciatura que obtuvo el tercer lugar en el “Undergraduate Technical Writing Competition 2009” organizado por el Institute of Food Technologists.
Una revista científica de prestigio es el resultado de la calidad y valor de las publicaciones que aparecen en sus páginas, este reto lo ha tomado el Comité Editorial de la revista TSIA y espero que con el paso del tiempo, con su esfuerzo y compromiso, nuestra revista llegue a ser una referencia en el campo de la Ingeniería de Alimentos.
Dr. René A. Lara Díaz Jefe del Departamento de Ingeniería Química, Alimentos y Ambiental Universidad de las Américas Puebla México

Temas Selectos de Ingeniería de Alimentos
Temas Selectos de Ingeniería de Alimentos 3 – 2 (2009): 1 – 3
No more excuses: Eat your fruits and vegetables!
L. Valerio – Junco*
Departamento de Ingeniería Química y Alimentos, Fundación Universidad de las Américas Puebla. Sta. Catarina Mártir, Cholula, Puebla. C.P. 72820. México
Tercer Lugar del Undergraduate Technical Writing Competition 2009, organizado por el IFT
What's your excuse for not eating your fruits and vegetables? Before you start coming up with reasons to exclude them from your diet, I invite you to continue reading and when you’re done, maybe you’ll finally agree with your mom when she asked you to eat your broccoli, because when it’s best for you: she’s always right! Plus, food science and medical research on the health advantages of fruits and vegetables are on her side.
Since childhood, they taught us that fruits and vegetables can improve our health in a powerful way. But what’s the source of their power? In addition to their vitamins, minerals and fiber content, fruits and vegetables possess phytochemicals that act as natural antioxidants (NA) and have protective effects against cell oxidation (Pellegrini and others 2007). Nowadays, these compounds have gained great attention because of their role in preventing diseases caused by oxidative stress; a process occurring in the body that involves the release of free oxygen radicals (Liu and Finley 2005).
* Estudiante de Licenciatura en Ingeniería de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: larissa.valeriojo @udlap.mx
Free radicals or so called ROS are highly reactive molecules that seek stability by stealing other molecules’ electrons; the attacked molecule is converted into a free radical itself and a chain reaction starts. ROS can be produced naturally by the body or by environmental factors (pollution, radiation, cigarette smoke). Environmental factors can provoke harmful oxidation and serious cellular damages, reducing cells’ potential towards ageing and illnesses if ROS are generated in excess (Kaur and Kappor 2001).
In order to fight against ROS, the body is equipped with a “defense system” including low molecular weight antioxidants that donate one of their own electrons to stop the electronstealing reaction (Liu and Finley 2005). The US Food and Drug Administration (FDA) has recognized the existence of natural (flavonoids, polyphenols, chlorophylls, vitamins A, B, C, E, carotenoids) and synthetic antioxidants (BHT, BHA, TBHQ). Since possible toxic effects of synthetic antioxidants have been presumed, NA have become popular and are assumed as safe, nutritive and even therapeutic (Kaur and Kappor 2001).
Fruits and vegetables rich in NA have been revealed to play a key role in the prevention of cancers, skin ageing, cardiovascular diseases and neurodegenerative disorders, such as Alzheimer’s disease (Singh and others 2008). Scientists have proposed that diet is responsible for about one-third of cancer incidence, as a high fruit intake in childhood has been related to lower adult cancer risk. Therefore, increasing fruit consumption is a logical strategy to enhance antioxidant intake and decrease oxidative stress (Wolfe and others 2008).
The British Committee on Medical Aspects of Food Policy demonstrated that a high fruit and vegetable consumption could reduce risk of colorectal and gastric cancers (Buttriss and others 2002). It’s suggested that people who avoid fruits and vegetables completely or consume very little, are at higher risk of stomach, breast and colon cancers (Terry and others 2001). There’s also plenty of evidence that a diverse diet, rich in vegetables (in particular tomato), can reduce the risk of prostate cancer (Chan and others 2009).
For instance, a case-control study of diet in relation to oesophageal cancer risk cited by Terry and others (2001) demonstrated that individuals with high veggies consumption (46 servings per day) had 40-60% lower risks than those with low consumption (1-2 servings per day); whereas individuals with fewer than 1.5 servings of fruits and vegetables per day had a 65% higher risk of colon cancer (Terry and others 2001).
Besides, fruits and vegetables consumption has also been inversely associated with cardiovascular disease risk (Ruel and Couillard 2007). Moreover, some studies have shown an important association between intake of fruits and vegetables and prevention of diseases like atherosclerosis, diabetes and arthritis (Kaur and Kappor 2001). Furthermore, NA in fruits and vegetables can
have complementary mechanisms of action including: anticarcinogenic, antiinflammatory, antibacterial and antiviral effects (Liu and Finley 2005).
What’s more, it has been proven that reactive oxygen species influence the process of ageing, since the skin is exposed to UVirradiation, a source for oxidative stress (Podda and Grundmann-Kollmann 2001). Additionally, Darvin and others (2007) found that a diet based on high amounts of carotenoid rich foods, increased the concentration of carotenoids in the human skin and slowed down skin ageing.
Concerning fruits, pomegranate and grape commercial juices have been discovered to have the highest antioxidant activity, followed by cranberry, grapefruit, tomato, orange and apple juices (Kaur and Kappor 2001). More analyses of fruits demonstrated that plum, pineapple, date, and kiwi, together with most members of the citrus family and tropical fruits like guava, papaya and mango (Mahattanatawee and others 2006), have potent antioxidant activity. Likewise, blueberries and strawberries are not only delicious, but also a rich source of antioxidant vitamins. Similarly, garlic, asparagus, chili pepper, red cabbage, artichoke, Brussels sprouts, mushrooms, cauliflower, corn, spinach, beets, eggplant and onion are rich sources of NA (Singh and others 2008).
After all, antioxidants act as cell saviors and future studies should concentrate on examining more health attributes of fruits and vegetables, beyond basic nutrition. An adequate and creative combination of these free radical scavengers may be necessary for improving your health and preventing chronic diseases. Even though many questions will still remain, moms certainly have a point when they tell their kids to eat their fruits and vegetables, because it matters.
References
Buttriss, J., Hughes, J., Kelly, C. and Stanner, S. 2002. Antioxidants in food: a summary of the review conducted for the Food Standards Agency. British Nutrition Foundation Nutrition Bulletin, 27, 227236.
Chan, R., Lok, K., Woo, J. 2009. Prostate cancer and vegetable consumption. Molecular Nutrition & Food Research, 53, 201-216.
Darvin, M., Gersonde, I., Albrecht, H., Sterry, W., Lademann, J. 2007. Resonance Raman Spectroscopy for the detection of carotenoids in foodstuffs. Influence of the Nutrition on the Antioxidative Potential of the Skin. Laser Physics Letters, 4, 452456.
Kaur, C. and Kappor, H. 2001. Review: Antioxidants in fruits and vegetables- the millennium’s health.
Podda, M. and Grundmann-Kollmann. 2001. Low molecular weight antioxidants and their role in skin ageing. Clinical and experimental dermatology, 26, 578-582.
Ruel, G. and Couillard, C. 2007. Evidences of the cardioprotective potential of fruits: the case of cranberries. Molecular Nutrition & Food Research, 51, 692-701.
International Journal of Food Science and Technology, 36, 703-725.
Liu, R. and Finley, J. 2005. Potential cell culture models for antioxidant research. Journal of Agricultural and Food Chemistry. 53, 4311-4314.
Mahattanatawee, K., Manthey, J., Luzio, G., Talcott, S., Goodner, K., Baldwin, E. 2006. Total antioxidant activity and fiber content of select Florida-grown tropical fruits. Journal of Agricultural and Food Chemistry, 54, 7355-7363.
Pellegrini, N., Colmbi, B., Salvatore, S., Brenna, O., Galaverna, G., Del Rio, D., Bennett, R., Brighenti, F. 2007. Evaluation of antioxidant capacity of some fruit and vegetable foods: efficiency of extraction of a sequence of solvents. Journal of the Science of Food and Agriculture, 87, 103-111.
Singh, M., Arseneault, M., Sanderson, T., Murthy, V., Ramassamy, C. 2008. Challenges for research on poyphenols from food in Alzheimer’s disease: bioavailability, metabolism and cellular and molecular mechanisms. Journal of Agricultural and Food Chemistry, 56, 4855-4873.

Temas Selectos de Ingeniería de Alimentos 3 – 2 (2009): 4 – 13
Temas Selectos de Ingeniería de Alimentos
Efecto de la incorporación de estabilizantes en la viscosidad de bebidas lácteas no fermentadas
Departamento de Ingeniería Química y Alimentos, Fundación Universidad de las Américas Puebla. Sta. Catarina Mártir, Cholula, Puebla. C.P. 72820. México
Resumen
La leche es un alimento de gran importancia a nivel mundial y su consumo en forma de bebidas lácteas ha ido en aumento en los últimos años. La modificación de propiedades como consistencia o la viscosidad ha permitido generar nuevos productos que son bien aceptados por los consumidores. Estas modificaciones se han logrado gracias a la alteración de la consistencia debida a la acción de distintos aditivos. De aquí que el objetivo de este artículo haya sido realizar una revisión bibliográfica del efecto que tienen distintos aditivos en la modificación de la viscosidad de bebidas lácteas. Estabilizantes como el almidón o la inulina en concentraciones de hasta 10% han mejorado la consistencia. Por otro lado, la carragenina es un estabilizador que incrementa la viscosidad de la leche en concentraciones tan bajas como 0.01%. La viscosidad es una propiedad física de suma importancia en la caracterización de bebidas lácteas, tanto por su manejo industrial como por su efecto sensorial, por lo cual se han evaluado nuevos aditivos que han modificado esta propiedad.
Palabras clave: leche, bebidas lácteas, estabilizantes, viscosidad, consistencia.
Abstract
Milk is a food of great importance worldwide and its consumption as lactic beverages has been increasing in recent years. The modification of properties such as consistency or viscosity has brought further improvements in its quality and its acceptance by consumers. These consistency changes have been achieved by the incorporation of various additives. Therefore, the objective of this paper was to conduct a literature review on how different additives contribute to changes in the viscosity of milk beverages. Stabilizers such as starch or inulin at concentrations up to 10% have modified the milk consistency. On the other hand, carrageenan is a stabilizer that increases the viscosity at concentrations of 0.01%. Viscosity is a property of great importance in the characterization of dairy beverages, in industrial management as in sensory impact, so that new additives that have modified this property have been evaluated recently.
Keywords: milk, milk beverages, stabilizers, viscosity, consistency.
*Programa de Doctorado en Ciencias de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: manuelo.ramirezse@udlap.mx
La leche es uno de los alimentos más nutritivos, ya que está compuesta principalmente por agua, lactosa, materia grasa, proteínas y otros nutrientes como vitaminas y minerales. La leche proveniente de la vaca es la más importante para la dieta humana y la que tiene más aplicaciones industriales (Badui, 2006). El consumo de productos lácteos también ha experimentado, desde la década de 1950, un considerable crecimiento en la demanda mundial que ha llevado a la industria a superar retos tecnológicos importantes (Saxelin et al., 2003).
Las últimas tres décadas de desarrollo en la ciencia y la tecnología dedicada a la leche y los productos lácteos han dado lugar a importantes avances en la mecanización, la automatización, la higiene en la planta, la calidad y la seguridad, la ampliación de la vida útil, y la introducción de nuevos productos que han traído variedad y conveniencia para el consumidor. El consumidor se ha beneficiado enormemente, en especial por la mejora de la calidad y la vida útil de la leche y la diversidad de productos lácteos. Estos treinta años se han caracterizado por la consolidación de la industria de la leche y los productos lácteos. De los 74.3 mil millones de litros de leche producida en los Estados Unidos en 2003, el 39% se consumió como leche fluida. En Canadá, la producción de leche en 2002 se situó en 7.4 mil millones de litros y un 38% se vendió como leche fluida. En 2002, México ocupó el décimo tercer lugar del mundo con un total de leche producida de 9,542 millones de litros. Actualmente, las plantas de producción de leche pasteurizada y las bebidas afines generan volúmenes de hasta 200,000 L/h (Goff y Griffiths, 2006).
Los productos lácteos se pueden dividir en productos sólidos y bebidas lácteas. Las bebidas lácteas son el grupo de alimentos
procesados derivados de la leche, cuya consistencia es líquida o semilíquida y que son altamente perecederos. Las bebidas lácteas pueden presentarse en formas fermentadas como el yogur y el kéfir, así como en formas no fermentadas como leches funcionales y leches saborizadas. El desarrollo de nuevas bebidas lácteas es una alternativa a la producción de leche fluida cruda, ya que como mencionan Yanes et al. (2002), las bebidas lácteas saborizadas para consumo directo son comunes en muchos países y su consumo se fortalece en grupos de personas como jóvenes y ancianos. Varias de las propiedades de estas bebidas han sido modificadas, adicionando fibra, calcio, vitaminas, minerales, ácido linoleico, distintas cepas microbianas (probióticos), prebióticos (fructooligosacáridos), distintos tipos de frutas con altos contenidos de antioxidantes, carotenoides, flavonoides y antocianinas, entre otros.
Aunque todas las propiedades fisicoquímicas de estas bebidas, tales como color, densidad, acidez, entre otras, son muy importantes, una de las principales es su consistencia, misma que puede ser expresada a partir de la viscosidad. La viscosidad es una propiedad física de gran importancia en etapas de control de calidad de ingredientes y producto terminado; en el diseño y evaluación de procesos y para el desarrollo de alimentos debido a que tienen gran impacto en la aceptabilidad del producto por parte del consumidor.
Existen muchas bebidas lácteas en las cuales la viscosidad es afectada por la adición de distintos ingredientes y/o aditivos, entre los que destacan las gomas (Villegas y Costell, 2007; Villegas 2008; Tárrega et al., 2005).
De aquí que el objetivo de este artículo sea hacer una revisión de estudios en los que se haya evaluado la adición de estabilizantes en
la viscosidad de bebidas lácteas no fermentadas.
1. Bebidas lácteas y propiedades reológicas
Las bebidas lácteas se pueden dividir en dos grandes grupos: fermentadas o no fermentadas. Las bebidas lácteas fermentadas son productos líquidos en los que la acción de las bacterias ácido lácticas contribuye de manera sobresaliente en las características de dichas bebidas. El efecto de las bebidas lácteas fermentadas en el organismo humano es restablecer y fortalecer la flora intestinal; además, el proceso de fermentación incrementa la vida útil del lácteo y le proporciona características sensoriales diferentes y agradables.
Por otro lado, las bebidas lácteas no fermentadas son productos derivados de la leche, a los que se les ha modificado el contenido graso, el valor nutricional o el sabor, entre otras características. Entre estos productos están las leches funcionales y las leches saborizadas.
La industria de los productos lácteos está interesada en la incorporación de ciertos elementos, tales como nutrientes, microorganismos y sabores a los productos de la leche, ya que actualmente la fortificación, la funcionalidad y la búsqueda de satisfacción del consumidor son una práctica común (AportelaPalacios et al., 2005).
Mientras que las leches saborizadas se comercializan con sabores como fresa, chocolate, vainilla (vainillina), entre otros, con el objeto de hacer la ingesta de la leche más atractiva a ciertos sectores de la población. Las leches funcionales son aquellas cuyo contenido nutricional natural ha sido alterado
de forma artificial con el objeto de que el producto cubra ciertas carencias nutricionales (Mostproject, 2005).
Por otra parte, las bebidas lácteas de diferentes sabores para el consumo directo son comunes en muchos países. Sus características nutricionales y sensoriales, así como su conveniencia, mayormente cuando se presentan en empaques individuales, favorecen su consumo por grupos de personas como los jóvenes y los ancianos. Las más populares son las bebidas de chocolate. Básicamente son formuladas con leche, glucosa, polvo de cacao y algunos hidrocoloides; estos últimos son adicionados para mejorar la consistencia y prevenir la sedimentación de partículas de cacao. Los sólidos lácteos también son incluidos con frecuencia. Las características particulares de los diferentes ingredientes como el contenido de grasa de la leche, la alcalinidad y el color del polvo de cacao, el tipo y la concentración del hidrocoloide, producen diferencias notables en la composición final y en las propiedades físicas y sensoriales específicas de los productos formulados (Yanes et al., 2002).
En la literatura se encuentran referencias que señalan la dependencia de las propiedades sensoriales de estos productos de los factores composicionales, como el contenido de grasa en la leche (Raats y Shepherd, 1992), el contenido de hidrocoloides, la glucosa y el polvo de cacao (Folkenberg et al., 1999; Houg y Sánchez, 1998). Los efectos del contenido de grasa en el color y la viscosidad y el efecto de los hidrocoloides en las propiedades de flujo (Langendorff et al., 2000) han sido estudiados en leche, el mayor componente de estas bebidas.
El conocimiento de las propiedades reológicas de los productos lácteos es esencial para el manejo del material, para el diseño y operación del equipo de proceso utilizado en la industria y también debido a la relación que
tienen con las propiedades sensoriales. Algunos productos lácteos, cuando se someten a deformación, exhiben “adelgazamiento”, aparentemente debido al rompimiento en su estructura. Sin embargo, la estructura puede reconformarse con el tiempo, cuando al producto se le permite asentarse, y exhibe un comportamiento tixotrópico, una característica de muchos productos alimenticios (Awadhal y Singh, 1985).
La reología de los productos lácteos ha sido estudiada en forma limitada. En ciertas condiciones, como velocidad moderada de deformación, contenidos de grasa por debajo del 40% y temperaturas sobre los 40º C, a la que la grasa es líquida y no existe coagulación por enfriamiento. La leche bronca, la leche concentrada y la crema son fluidos con propiedades reológicas newtonianas. Sin embargo, estos productos lácteos exhiben propiedades reológicas no newtonianas, sobretodo cuando las cremas se mantienen en condiciones por debajo de los 40º C y pequeñas velocidades de deformación (Fox y McSweeney, 1998). La leche condensada y endulzada, la crema y el yogurt muestran comportamiento tixotrópico, es decir, su viscosidad aparente está inversamente relacionada con las velocidades de deformación. La leche concentrada, mantequilla, helado, yogurt y queso son productos que pueden expresar propiedades viscoelásticas (Vélez-Ruiz y BarbosaCánovas, 1997; Penna et al., 2001).
Los agentes estabilizadores mejoran el cuerpo y la viscosidad de los productos lácteos. Estos estabilizadores incluyen compuestos como almidón, carragenina, garrofín, goma xantana, goma guar, pectina, inulina, entre otros (Silverson, 2009). A continuación se presentan las características de algunos, mismos que fueron seleccionados debido a su amplia utilización en la industria láctea (carragenina)
o la adición de otras propiedades como la dulzura (inulina) o a su bajo costo de producción (almidón), además de sus características de agentes estabilizadores modificadores de la viscosidad.
El almidón es un polisacárido de reserva alimenticia predominante en las plantas, que proporciona el 70-80% de las calorías consumidas por los humanos de todo el mundo. Tanto el almidón como los productos de la hidrólisis del almidón constituyen la mayor parte de los carbohidratos digeribles de la dieta habitual. Tanto los almidones nativos como los almidones modificados tienen un número enorme de posibles aplicaciones en los alimentos, que incluyen las siguientes: adhesivo, ligante, enturbiante, formador de películas, estabilizante de espumas, agente anti-envejecimiento de pan, gelificante, glaseante, humectante, estabilizante, texturizante y espesante. Los almidones nativos y modificados se usan comúnmente en los productos lácteos porque incrementan la viscosidad, mejoran la palatabilidad y evitan la pérdida del suero de leche.
Cuando se usa solo o como parte de una mezcla de estabilizadores, el almidón es un buen agente espesante debido a su textura cremosa, la facilidad de procesamiento y bajo costo en comparación con otros hidrocoloides (Foss, 2009). En sistemas con almidón, la interacción con los componentes de la leche puede afectar a la estructura del sistema, influyendo tanto en sus propiedades de flujo como viscoelásticas dependiendo de la naturaleza del almidón (Tárrega et al., 2005).
Las carrageninas pertenecen al grupo de los polisacáridos sulfatados lineales aniónicos. Se componen de residuos de D-galactopiranosa
ligados por enlaces alternados α (1-3) y β (14). Existen tres tipos principales de carrageninas: λ, ι y κ.
Su capacidad de formación de gel se atribuye al hecho de que son capaces de combinarse en doble hélice, para formar enlaces cruzados entre las moléculas en una red tridimensional. La λ-carragenina no forma geles, sólo provoca un aumento de la viscosidad de las soluciones acuosas. Las interacciones entre la carragenina y las proteínas de leche han sido estudiadas en detalle en vista de su amplia aplicación en la industria láctea (Shchipunov y Chesnokov, 2003)
La funcionalidad de la κ-carragenina en sistemas de producción lechera ha sido bien conocida y estudiada por muchos años. En leche tiene la capacidad para inhibir la separación de fases entre las proteínas de la leche y los polisacáridos, aún en concentraciones muy bajas (< 200ppm) (Vega et al., 2004)
Cuando las partículas se hidratan en una dispersión de carragenina, la viscosidad aumenta debido a que las partículas hidratadas ofrecen más resistencia al flujo. Las soluciones muy diluidas, con niveles de alrededor de 200 ppm de carragenina, se usan para estabilizar las leches de chocolate y otras bebidas lácteas.
Algunos de los primeros usos de la carragenina se encuentran en geles de leche y flanes, y en la estabilización de la leche evaporada y mezclas de helado. En estas aplicaciones, la κ-carragenina forma un gel débil en la fase acuosa que también interactúa con los aminoácidos de las proteínas de la superficie de las micelas de caseína. Niveles muy bajos de carragenina (150-250ppm) son suficientes para evitar la separación de suero de leche durante la fabricación y el almacenamiento de una amplia gama de productos lácteos. Estos incluyen el helado y
batidos de leche, queso crema y postres lácteos. En las leches de chocolate, este bajo nivel de carragenina es capaz de evitar la separación de fases y generar una red que mantiene las partículas de cacao en suspensión. El amplio espectro de propiedades espesantes y gelificantes de la carragenina hacen que su uso sea extenso en una amplia gama de productos lácteos (Imeson, 2000)
La inulina es un compuesto que se encuentra de manera natural en muchas especies vegetales y que actualmente se produce a escala comercial por extracción a partir de la raíz de la achicoria. La inulina nativa es una mezcla de cadenas de oligómeros y polímeros con un número variable de moléculas de fructosa, unidas por enlaces β (2→1) que suele incluir en su extremo, una molécula de glucosa (Villegas, 2008). La inulina y sus derivados ofrecen múltiples usos como ingredientes en la formulación de productos ya que tienen la capacidad de formar geles, actúan como agentes emulgentes, como edulcorantes, como sustitutos de grasas, y son capaces de modificar la viscosidad. El grado de polimerización de la inulina es variable, y determina sus propiedades fisicoquímicas y sus aplicaciones como ingrediente en las formulaciones alimenticias (Madrigal y Sangronis, 2007). La inulina de cadena corta u oligofructosa es mucho más soluble y más dulce que la inulina nativa, con un perfil de dulzor similar al de la sacarosa y menor contenido calórico (4200-8400 kJ/kg), aunque con un poder edulcorante inferior (30-35%). Puede ser útil para reemplazar parcialmente a la sacarosa de una formulación o sustituirla totalmente cuando se combina con otros edulcorantes calóricos. La inulina de cadena larga, con grado de polimerización alto (2225), es más estable térmicamente, menos soluble y más viscosa que la nativa (Wada et al., 2005), y tiene una capacidad como sustituto de grasa, que es prácticamente el
doble que la de la inulina nativa (Coussement, 1999). Sus propiedades como sustituto de grasa se atribuyen a su capacidad para formar microcristales que interaccionan entre sí formando pequeños agregados que atrapan gran cantidad de agua, originando una textura cremosa y fina que proporciona una sensación bucal similar a la de la grasa (Bot et al., 2004). En fórmulas de leche de chocolate, la adición de inulina aumenta la viscosidad (Tungland y Meyer, 2002); además, incrementa la dulzura, la oscuridad, el espesor y la cremosidad, y reduce al mínimo la sedimentación de partículas de cacao (Abd, 2009).
Otros agentes estabilizantes como el garrofín, alginatos, goma xantana, goma guar y pectina también se utilizan en bebidas lácteas siendo su efecto estabilizante similar al de la carragenina, almidón o inulina; sin embargo, son utilizados con menor frecuencia.
3. Leche estabilizada
En las leches son sabor pueden utilizarse una gran variedad de estabilizadores. La leche más comercial es la de sabor chocolate y se estabiliza con carragenina, otras gomas, y almidón de maíz (Krautheim, 2008).
4 - 13
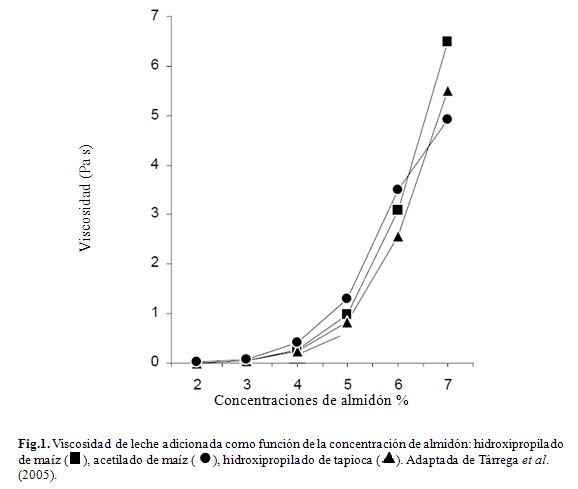
En la Fig. 1 se muestra la viscosidad de dispersiones de tres tipos de almidón que fueron agregados a la leche. Como se esperaba, la viscosidad de la dispersión se incrementó con el aumento de la concentración del almidón, debido, probablemente, al aumento de la fracción volumétrica de los gránulos de almidón en la dispersión. Sin embargo, no se encontraron diferencias significativas entre los tres tipos de almidón y su efecto viscoso (Tárrega et al., 2005). Los altos valores de viscosidad obtenidos son atribuibles a la viscosidad de la fase contínua (leche), debido a la presencia de las caseínas, lactoglobulinas, grasa y otros componentes de la leche y a las posibles interacciones entre estos componentes y el almidón (Vélez-Ruiz y Barbosa, 1997).
Abu-Jdayil et al. (2004) estudiaron el efecto de dispersiones de almidón de trigo en la viscosidad de leche y encontraron que, además de presentar un aumento en la viscosidad aparente, el efecto se hizo más pronunciado con el aumento del contenido graso de la leche.
El comportamiento reológico de mezclas de proteínas de leche comercial con κ-carragenina en solución acuosa fue estudiado por Hemar et al. (2002) con cuatro fuentes de proteína de leche: leche descremada en polvo, concentrado de proteína de leche, caseinato de sodio, y proteína de suero. Para concentraciones de κcarragenina de hasta 0.5%, la viscosidad de la mezcla se incrementó notablemente a bajas velocidades de deformación con la adición de leche descremada en polvo y concentrado de proteína de leche, pero no cambió con la adición de caseinato de sodio o proteína de suero de leche. Para κ-carragenina con concentraciones de 1 a 2.5%, las mediciones reológicas mostraron que se mejoró notablemente la resistencia de los geles.
Anderson et al. (2002) encontraron que la viscosidad en leche descremada con adición de carragenina aumentó significativamente a distintos niveles de concentración (0.005, 0.01, 0.02 o 0.04%), como se esperaba. En otro estudio de Tijssen et al. (2007), la viscosidad de la leche descremada aumentó con la adición de carragenina, de 0.008 a 0.06 Pa s.
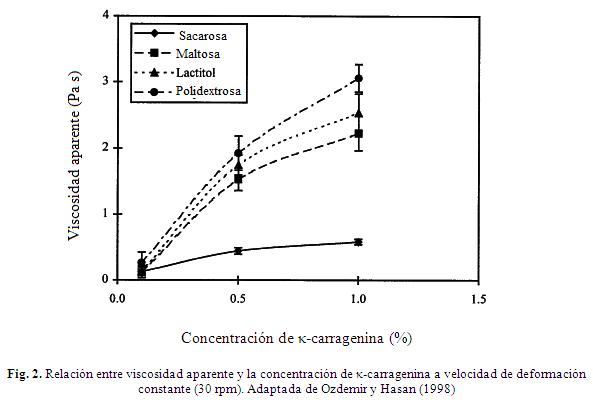
En la Fig. 2 se presenta el efecto de la adición de κ-carragenina en las propiedades reológicas de soluciones a 25º C, que contienen 40% de sustitutos de azúcar. En
2 (2009): 4 - 13
estos sistemas se encontró que la κcarragenina es un factor efectivo de control de la viscosidad aparente ya que dicho parámetro se incrementa proporcionalmente con la concentración de la goma (Ozdemir y Hasan, 1998).
En un estudio de Villegas (2008), se adicionaron tres tipos de inulina a la leche para conocer el efecto de la longitud de ésta en la viscosidad. La inulina de longitud de cadena larga fue la que proporcionó los mayores incrementos de viscosidad instrumental, seguida de la inulina de cadena corta y de la inulina nativa. Paralelamente, se puso de manifiesto que la capacidad de la inulina como sustituto de grasa dependía no sólo de la longitud media de las cadenas, sino también de la concentración de inulina añadida.
En la Fig. 3 Villegas y Costell (2007), presentan el efecto de la inulina sobre la viscosidad de leche. En este estudio no se observaron diferencias significativas entre la viscosidad de las muestras con concentraciones de inulina menores al 6%; sin embargo, se detectaron diferencias significativas en la viscosidad de la leche adicionada con concentraciones de 8 y 10% de inulina. El incremento de las concentraciones de inulina aumentó significativamente
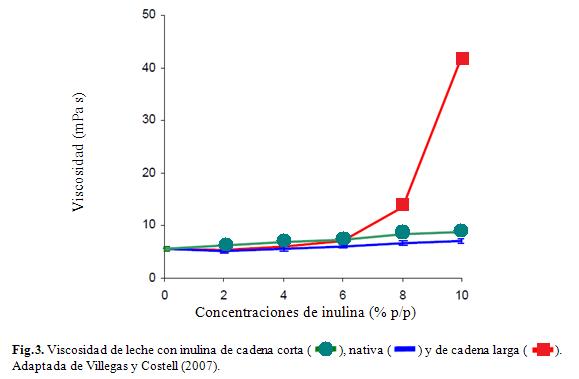
la viscosidad; este efecto resultó más acusado en los sistemas con inulina de cadena larga.
Villegas (2008) concluyó que es necesario añadir inulina de cadena larga a concentraciones de más del 8% a la leche baja en grasa, a fin de obtener bebidas con viscosidad y cremosidad similares a las percibidas en las bebidas elaboradas con leche entera. A concentraciones más bajas (6 y 8%), los tres tipos de inulina estudiadas tienen una viscosidad significativamente menor que la correspondiente a la leche entera. Independiente del grado de polimerización, cuando una concentración de 6% de inulina se ha añadido a la leche descremada, la leche se percibe menos viscosa y menos cremosa que la leche entera. Al añadirse diferentes tipos de inulina con una concentración del 8% la leche baja en grasa se percibe menos viscosa que la leche entera. La influencia de la longitud de la cadena sobre el potencial de sustitución de grasa de la inulina en bebidas, se acentuó con el aumento de la concentración hasta el 10%.
La viscosidad de la muestra con el 10% de inulina de cadena larga no difirió de la viscosidad de la muestra con la leche entera.
Entonces el efecto de la adición de inulina en el comportamiento reológico de la leche y de leche con κ-carragenina, depende
claramente del contenido de materias grasas lácteas y de la longitud de la cadena de inulina en función de la concentración añadida.
La adición de inulina con los diferentes grados de polimerización en una concentración suficientemente alta, aumenta la viscosidad aparente de la leche. Mientras que el comportamiento de la viscosidad de leche adicionada con almidón, principalmente depende tanto del tipo de almidón como de la fracción volumétrica de los gránulos. Lo cual se puede atribuir al aumento en la rigidez de los gránulos de almidón.
Tanto el almidón como la inulina son agentes que confieren consistencia a la leche; no obstante, la inulina es un agente que no sólo confiere estabilidad sino también sabor a las bebidas lácteas. Aunque este compuesto afecta el sabor de la leche, este atributo se ha modificado más claramente mediante la adición de distintos ingredientes como chocolate, vainilla, etc.
Por otro lado, Preston (2007) encontró que otro aditivo, la miel, puede utilizarse en la leche de chocolate mejorando su sabor y viscosidad. Los cambios de la viscosidad en almacenamiento de esta bebida láctea tuvieron valores desde 496.52 mPa s hasta 537.63 mPa
s en un lapso de 14 días, mejorando la viscosidad de la leche de chocolate comercial (525 mPa s). Diversos azúcares, jarabes y mezclas de edulcorantes artificiales se utilizan de igual manera en el mejoramiento del sabor y de la consistencia de bebidas lácteas.
Conclusión
Las bebidas lácteas no fermentadas son de gran importancia a nivel mundial debido al incremento en su consumo, por lo que el mejoramiento de la consistencia mediante la modificación de la viscosidad con diferentes agentes estabilizantes es una práctica que se desarrolla actualmente.
La viscosidad es una propiedad de suma importancia en la caracterización de productos alimenticios y por ende de productos lácteos, por lo cual se han encontrado nuevos aditivos que han mejorado esta propiedad. Ejemplos de estos aditivos son la inulina, el almidón y la carragenina, que se han agregado a bebidas lácteas no fermentadas y que al mejorar la consistencia, han mejorado también su aceptabilidad por parte del consumidor.
Existen aún muchos aditivos por estudiar, que modifiquen la viscosidad de bebidas lácteas. Aditivos innovadores que podrían corregir la consistencia, sin modificar otras propiedades fisicoquímicas.
M.O. Ramírez-Sucre agradece al Consejo Nacional de Ciencia y Tecnología (CONACyT) por el financiamiento de sus estudios de doctorado.
3- 2 (2009): 4 - 13
Abd, E. A. 2009. Optimization of a new version of chocolate milk for endurance performance and postexercise. Research Journal of Agriculture and Biological Sciences. 5(4):482-489.
Abu- Jdayil, B., Mohameed, H. y Eassa, A. 2004. Rheology of wheat starch-milk-sugar systems: effect of starch concentration, sugar type and concentration, and milk fat content. Journal of Food Engineering. 64:207-212.
Aportela-Palacios, A., Sosa-Morales, M. E. y VélezRuiz, J. F. 2005. Rheological and physicochemical behavior of fortified yogurt, with fiber and calcium. Journal of Texture Studies. 36:333-349.
Awadhal, N. K. y Singh, C. P. 1985. A rheological model for milk products. Journal of Food Science. 50:1611-1614.
Anderson, A.D., Daubert, C.R. y Farkas B.E. 2002. Rheological characterization of skim milk stabilized with carrageenan at high temperatures. Journal of Food Science. 67(2):649-652.
Badui, D. S. 2006. Química de los alimentos. Editorial Pearson. 4a. ed. 604 p.
Bot, A., Erle, U., Vreeker, R. y Agterof, W.G. 2004. Influence of crystallization conditions on the large deformation rheology of inulin gels. Food Hydrocolloids. 18(4):547-556.
Coussement, P.A. 1999. Inulin and oligofructose: safe intakes and legal status. American Society for Nutritional Sciences. 129:1412-1417.
Folkenberg, D. M., Bredie, W. L. y Martens, M. 1999. What is mouthfeel? Sensory- rheological relationships in instant hot cocoa drinks. Journal of Sensory Studies. 14:181-195.
Foss, J. W. 2009. How processing affects starch selection for yogurt http://eu.foodinnovation.com/pdfs/process_yogurt.p df, accesada: 05/06/2009.
Fox, P. F. y McSeweeney, P. L. 1998. Dairy Chemistry and Biochemistry. Blackie Academic and Professional. EE.UU. 478 p.
Goff, H. D. y Griffiths. 2006. Major advances in fresh milk and milk products: fluid milk products and frozen desserts. Journal of Dairy Science. 89:1163–1173.
Hemar, Y., Hall, C. E., Munro, P. A. y Singh, H. 2002. Small and large deformation rheology and
microstructure of κ-carrageenan gels containing commercial milk protein products. International Dairy Journal. 12(4):371-381.
Hough, G. y Sánchez, R. 1998. Descriptive analysis and external preference mapping of powdered chocolate milk. Food Quality and Preference. 9(4):197-204.
Imeson, A. P. 2000. Carrageenan En: Phillips, G.O. y Williams P.A. Handbook of hydrocolloids Woodhead Publishing, Cambridge. 87-102 p.
Krautheim, A. 2008. Formulating reduced calorie / reduced sugar flavored milks. National dairy council.
http://www.innovatewithdairy.com/NR/rdonlyres/B6 A0CFA0-7CAF-4EF4-80EF5C4907C7C810/0/FormulatingReducedCalorieRedu cedSugarFlavoredMilks.pdf accesada: 01/03/2009.
Langendorff, V. Cuvelier, G., Michon, C., Launay, B., Parker, A. y De kruif, C. G. 2000. Effects of carrageenan type on the behavior of carrageenan/milk mixtures. Food Hidrocolloids 14:273-280.
Madrigal, L. y Sangronis E. 2007. La inulina y derivados como ingredientes claves en alimentos funcionales. Archivos Latinoamericanos de Nutrición. 57(4):387-396.
Mostproject. 2007. La inulina y derivados como ingredientes claves en alimentos funcionales. Archivos Latinoamericanos de Nutrición. 57(4):387396.
Ozdemir, M. y Hasan, S. 1998. Characterization of rheological properties of systems containing sugar substitutes and carrageenan. International Journal of Food Science and Technology. 33:439-444.
Penna, A. L., Sivieri, K. y Oliveira, M. N. 2001. Relation between quality and rheological properties of lactic beverages. Journal of Food Engineering. 49:7-13.
Preston, M. B. 2007. Honey in chocolate milk-based Beverages. National Honey Board and University of Nebraska-Lincoln Food Processing Center. http://www.honey.com/foodindustry/resourcedb/cho colatemilk.htm, accesada: 15/02/09.
Raats, M. M. y Shepherd, R. 1992. Free-choice profiling of milks and other products prepared with milks of different fat contents. Journal of Sensory Studies. 7:179-203.
Saxelin, M., Korpela, R. y Mäyrä-Mäkinen, A. 2003. Introduction: classifying functional dairy products.
En: Mattila-Sandholm, T. y Saarela, M. Functional dairy products. Valió Ltd, Finlandia. 395 p.
Shchipunov, A. Y. y Chesnokov, A. V. 2003. Carrageenan gels in skim milk: formation and rheological properties. Colloid Journal. 65(1):114123.
Silverson. 2009. Food. Production of flavored milk drinks. Aplicattion report. http://www.silverson.com/USA/SearchResults.cfm, accesada: 01/03/2009.
Tárrega, A., Vélez-Ruiz, J. F. y Costell, E. 2005. Influence of milk on the rheological behaviour of crosslinked waxy maize and tapioca starch dispersions. Food Research International 38(7):759-768.
Tijssen, R. L., Canabady-Rochelle L. S. y Mellema M. 2007. Gelation upon long storage of milk drinks with carrageenan. Journal of Dairy Science. 90(6):2604–2611.
Tungland, B. C. y Meyer, D. 2002. Non-digestible oligosaccharides (dietary fibre): their physiology and role in human health and food. Comprehensive Reviews in Food Science and Food Safety. 3:73-92.
Vega, C., Andrew, R.A., y Goff, H.D. (2004). Serum separation in soft serve ice cream mixes. Milchwissenshaft. 59:284-287.
Vélez-Ruiz, J. F. y Barbosa-Cánovas, G. V. (1997). Rheological properties of selected dairy products. Critical Reviews in Food Science and Nutrition 37:311–359.
Villegas, B. 2008. Efecto de la adición de inulina en las características físicas y sensoriales de batidos lácteos. Tesis Doctoral. Universidad Politécnica de Valencia. Valencia, España.
Villegas, B. y Costell, E. 2007. Flow behaviour of inulin-milk beverages. Influence of inulin chain length and of milk fat content. International Dairy Journal. 17(7):776-781.
Wada, T., Sugatani, J., Terada, E., Ohguchi, M. y Miwa, M. 2005. Physicochemical characterization and biological effects of inulin enzymatically synthesized from sucrose. Journal of Agricultural and Food Chemistry. 53:1246-1253.
Yanes, M., Durán, L. y Costell, E. 2002. Rheological and optical properties of commercial chocolate milk beverages. Journal of Food Engineering. 51:229234.

Temas Selectos de Ingeniería de Alimentos 3 – 2 (2009): 14 – 25
Temas Selectos de Ingeniería de Alimentos
Evaluación de agentes antioxidantes de un extracto de flor de jamaica microencapsulado
Departamento de Ingeniería Química y Alimentos, Fundación Universidad de las Américas Puebla. Sta. Catarina Mártir, Cholula, Puebla. C.P. 72820. México
Resumen
El objetivo de esta investigación fue evaluar los agentes antioxidantes de un extracto de flor de jamaica microencapsulado. Para la obtención de los microencapsulados, se deshidrató un extracto de flor de jamaica mediante secado por aspersión, usando goma de mezquite (1, 2, 3, 4 y 5 g de goma/100 mL de extracto) como agente encapsulante. Las muestras se evaluaron en cuanto al rendimiento, humedad, concentración y estabilidad de compuestos fenólicos, antocianinas monoméricas, capacidad antioxidante y color durante cinco semanas (25°C, sin luz). En términos generales, las pruebas de estabilidad mostraron que el contenido de compuestos fenólicos y antocianinas en los microencapsulados no cambió durante el almacenamiento. Por el contrario, la capacidad antioxidante de los microencapsulados sí mostró diferencias significativas durante el almacenamiento; sin embargo, los cambios observados no presentaron una tendencia definida.
Palabras clave: flor de jamaica, antioxidantes, antocianinas, compuestos fenólicos, microencapsulación.
Abstract
The aim of this investigation was to evaluate the antioxidant agents of a microencapsulated extract of Roselle. To obtain the microcapsules, a Roselle extract was dehydrated by spray drying using mesquite gum (1, 2, 3, 4 and 5 g of gum/100 mL of extract) as wall material. Samples were evaluated as for their yield, moisture content, concentration and stability of phenolic compounds, monomeric anthocyanins, antioxidant capacity and color during five weeks (25°C, without light). In general terms, stability tests showed that the content of phenolic compounds and anthocyanins of the microcapsules did not change during the storage. On the contrary, the antioxidant capacity of the microcapsules showed significant differences during the storage; however, the observed changes did not present a defined trend.
Key words: Roselle, antioxidants, anthocyanins, phenolic compounds, microencapsulation.
* Programa de Maestría en Ciencias de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727 Dirección electrónica1: angel.guerrero@udlap.mx
Introducción
Existe un número convincente de estudios epidemiológicos y estudios in vitro que demuestran que los alimentos que contienen fitoquímicos con actividad antioxidante, tienen un fuerte efecto protector contra ciertas enfermedades crónicas y degenerativas.
En individuos sanos, la producción de radicales libres está controlada por un sistema de defensa balanceado, de tal manera que el estrés oxidativo se genera cuando el balance está a favor de los radicales libres debido a un aumento en su producción o agotamiento de niveles de antioxidantes (Faudale et al., 2008). El daño oxidativo, causado por la acción de radicales libres, puede iniciar y promover la progresión de enfermedades como artritis, enfermedad de Alzheimer y enfermedad de Parkinson, disfunciones gastrointestinales, entre otras.
Los antioxidantes neutralizan la acción de los radicales libres; éstos al interactuar con el radical libre ceden un electrón y se oxidan. Por lo que la reposición de ellos debe ser continua mediante la ingestión de alimentos que los contienen (Yanishlieva, 2001).
La flor de jamaica (Hibiscus sabdariffa L.) conocida también como rosa de Abisinia, Hibisco o Rosella, es una planta silvestre cultivada en regiones tropicales y subtropicales de todo el mundo que pertenece a la familia de las malváceas. Se utilizan los cálices que envuelven al fruto para la obtención de una infusión aromática de color rojo intenso, que puede ser consumida fría o templada. Se emplea también como aromatizante ácido en salsas, jaleas, mermeladas, bebidas y como colorante en alimentos, entre otras aplicaciones (Simonetti, 1994). Diversos autores han reportado la presencia de agentes antioxidantes en la flor de jamaica, tal como la quercetina, el ácido Lascórbico y los compuestos fenólicos
(Hirunpanich et al., 2005, Christian et al., 2006, Yun-Ching et al., 2006, MarquezVizcaino et al., 2007, Prenesti et al., 2007, Reanmongkol y Itharat, 2007). El contenido de sustancias fenólicas en la planta, consiste principalmente de flavonoides y en particular de antocianinas como la delfinifina-3glucósido, delfinidina-3-sambubiósido y cianidina-3-sambubiósido (Pouget et al., 1990; Wong et al., 2002; Ali-Bradeldin et al., 2005; Salazar-González, 2009). Dichos compuestos están asociados con la prevención del cáncer (Garzón, 2008) y las enfermedades coronarias como la aterosclerosis (El-Saadany et al., 1991).
Los compuestos fenólicos son efectivos donadores de hidrógenos. Su potencial antioxidante depende del número y la posición de los grupos hidroxilos, así como de la presencia de electrones donadores en su anillo aromático estructural.
Las antocianinas poseen una estructura química adecuada para actuar como antioxidantes, ya que pueden donar hidrógenos o electrones a los radicales libres o bien, atraparlos y desplazarlos en su estructura aromática (Kuskoski et al., 2004a).
A pesar de los efectos benéficos que presentan los agentes antioxidantes para la salud, su aplicación comercial está limitada, ya que factores como la luz, la humedad, el oxígeno y la temperatura afectan su estabilidad. Por esta razón, el uso de tecnologías para preservar estos compuestos, se vuelve una herramienta útil para obtener productos estables.
La microencapsulación es una forma especial de empacar, en la que las partículas de un material pueden ser cubiertas de manera individual para protegerlo del ambiente y de influencias deletéreas. El secado por aspersión es un método ampliamente usado para encapsular ingredientes alimenticios y es el
más económico. Una de las grandes ventajas de este proceso, además de su simplicidad, es que es apropiado para materiales sensibles al calor, ya que el tiempo de exposición a temperaturas elevadas es muy corto (PedrozaIslas, 2002).
Por lo anterior, en este trabajo se evaluaron los agentes antioxidantes de un extracto de flor de jamaica microencapsulado mediante secado por aspersión. De igual manera, se evaluó la estabilidad de los antioxidantes durante su almacenamiento.
3. Obtención del extracto líquido de flor de jamaica
Materiales y métodos
1. Materiales
Se emplearon cálices de flor de jamaica cultivados en el municipio de Chiautla de Tapia, Puebla. Éstos fueron adquiridos deshidratados en la central de abastos de la ciudad de Puebla. Se empleó como agente encapsulante goma de mezquite, la cual se adquirió en el Centro de Investigación en Alimentación y Desarrollo (CIAD) de Hermosillo, Sonora.
2. Purificación del agente encapsulante para el secado por aspersión
Se empleó la técnica de Beristain et al. (2002) modificada por Salazar-González (2009). Se seleccionaron aquellas porciones con menos impurezas, se adicionó agua destilada y se agitó hasta disolver los cristales de goma. La solución obtenida se filtró y se almacenó en placas en un congelador a -40°C durante 24 h. La muestra congelada se colocó en la cámara de un liofilizador (Labconco, LYPH LOCK6, EE.UU.) a una temperatura de condensación de -50°C y una presión de vacío de 10 micrones de Hg, sin calentamiento. El producto deshidratado se trituró hasta obtener un polvo fino.
Se colocaron cálices de flor Jamaica triturados en disolvente etanol al 96%-agua (50:50). La mezcla se mantuvo en agitación y en la oscuridad a temperatura ambiente durante 2 h. Después se centrifugó (Hermle, Z383K, Alemania) a 4500 rpm. Luego se filtró en un embudo Büchner a través de papel Whatman No. 2. Posteriormente, se llevó a cabo la eliminación del disolvente en un evaporador rotatorio (Büchi, 461, Suiza) a 35°C. El extracto concentrado se ajustó a 18.4 °Bx y se caracterizó con base en la concentración de compuestos fenólicos, antocianinas monoméricas totales, actividad antioxidante y color.
4. Obtención del microencapsulado
Se pesaron 1, 2, 3, 4 y 5 g de goma de mezquite purificada y se añadieron 100 mL de extracto líquido de flor de jamaica. La mezcla se agitó hasta disolver la goma de mezquite y se alimentó en un secador por aspersión (Büchi, Mini spray drier B-290, Suiza) a una temperatura del aire de entrada de 180 ± 2°C y temperatura de aire de salida de 104 ± 2.34°C. La potencia del aspirador fue del 100% (correspondiendo a un flujo de aire de 38 m3/h) y la de la bomba fue del 35% para mantener un flujo de 10 mL/min. El nivel de limpiador de la esprea fue de 1. Los microencapsulados se almacenaron en una incubadora (Lab Line Instruments, Imperial III, India) a 25°C en ausencia de luz, durante cinco semanas y se evaluaron con base en la concentración de compuestos fenólicos, antocianinas monoméricas totales, actividad antioxidante y color. El rendimiento se calculó mediante la relación entre los gramos de polvo obtenidos y los °Bx del extracto con goma.
5. Cuantificación de compuestos fenólicos
Los compuestos fenólicos totales se determinaron por una adaptación al método de Folin-Ciocalteau (Singleton y Rossi, 1965) realizada por Salazar-González (2009), en un espectrofotómetro UV-Visible (Varian Cary 100 Conc., EE.UU.) usando ácido gálico como estándar. El contenido de compuestos fenólicos se expresó como miligramos equivalentes de ácido gálico por 100 mL de extracto de flor de jamaica, mientras que para los extractos en polvo (microencapsulados) se expresó como miligramos equivalentes de ácido gálico en 1 g de sólidos solubles de jamaica.
6. Evaluación de antocianinas monoméricas totales
La determinación de antocianinas monoméricas totales se llevó a cabo mediante el método de pH diferencial descrito por Giusti y Wrolstad (2001), adaptado por SalazarGonzález (2009). La absorbancia se midió en un espectrofotómetro UV-Visible a 520 y a 700 nm usando soluciones buffer a pH 1 y a pH 4.5. Los resultados obtenidos se expresaron como miligramos equivalentes de cianidina-3-glucósido en 100 mL de extracto de flor de jamaica y en los extractos en polvo (microencapsulados) se expresó como miligramos equivalentes de cianidina-3glucósido en 1 g de sólidos solubles de jamaica.
7. Medición de la capacidad antioxidante
La actividad antioxidante se determinó mediante la metodología ABTS desarrollada por Re et al. (1999), modificada por Kuskoski et al. (2004a) y por Salazar-González (2009). Se empleó Trolox (6-hidroxi-2, 5, 7, 8tetrametilcromo-2-ácido carboxílico, SigmaAldrich, México) como antioxidante de referencia. Los resultados de actividad antioxidante se expresaron como μmol
equivalente a Trolox en 100 mL de extracto y en los extractos en polvo (microencapsulados) se expresó como μmol equivalente a Trolox en 1g de sólidos solubles de jamaica.
8. Humedad de los microencapsulados
La humedad de los microencapsulados se determinó por secado y diferencia de pesos de acuerdo al método 934.06 de la A.O.A.C. (2000).
9. Evaluación del color en el extracto líquido y en los microencapsulados de flor de jamaica
La evaluación del color se llevó a cabo en un colorímetro (Gardner-Color, Gardner System 05, Alemania) empleando un aditamento de transmitancia y se midieron los parámetros de Hunter L, a y b. Posteriormente se calculó la pureza (C) y el tono (H). Para los extractos en polvo (microencapsulados), la medición del color se llevó a cabo mediante pruebas de reflectancia (7 g de polvo) y transmitancia (0.1 g de polvo/7.5 mL agua destilada). Se calculó la diferencia neta de color entre el punto inicial y final del almacenamiento de los microencapsulados.
10. Análisis estadístico
Todas las mediciones se realizaron por triplicado y se analizaron mediante un ANOVA usando el paquete Minitab (v.14, Minitab Inc.).
Resultados y discusión
En la Tabla I se muestran las características del extracto líquido empleado en la microencapsulación. Los parámetros de color indicaron una baja luminosidad e inclinación hacia las regiones roja y amarilla.
I. Características del extracto líquido de flor de jamaica empleado en la microencapsulación
Compuestos fenólicos*
Parámetro de color
L1.27 ± 0.00
a3.45 ± 0.00
b0.89 ± 0.00
Tono C0.25 ± 0.00
Pureza H3.56 ± 0.00
*mg de ácido gálico/100 mL de extracto
**mg de cianidina-3-glucósido/100 mL de extracto
*** μmol de Trolox/100 mL de extracto
1. Evaluación de los microencapsulados
1.1 Rendimiento y humedad
Con respecto al rendimiento (Tabla II), se observa que se tienen pérdidas de alrededor del 26% del producto final, mismas que se pueden atribuir al porcentaje de polvo que queda adherido en las paredes del secador. Estudios realizados por Robert et al. (2003), reportaron pérdidas alrededor del 31% en la encapsulación de carotenoides de Rosa Mosqueta mediante secado por aspersión.
Por otro lado, los datos obtenidos de humedad (Tabla II) indicaron que la concentración de la goma de mezquite no tuvo un efecto significativo en la humedad de los microencapsulados, ya que los resultados obtenidos no son estadísticamente diferentes (p>0.05).
II. Rendimiento y humedad de los microencapsulados de flor de jamaica
g goma de mezquite/100 mL extracto Rendimiento (%)% Humedad (b.h) 1
2.99 ± 0.00a
Los resultados del análisis estadístico (Fig. 1) mostraron que no existen diferencias significativas (p>0.05) en el contenido de compuestos fenólicos para cada uno de los microencapsulados; por lo tanto, es posible afirmar que la concentración de goma de mezquite no tuvo un efecto importante en el contenido de compuestos fenólicos y que por consiguiente tuvo el mismo efecto protector. Sin embargo, al comparar los resultados obtenidos con los del extracto líquido empleado, se observó una importante reducción en el contenido de compuestos fenólicos de los microencapsulados. Estas pérdidas se pueden atribuir a la termosensibilidad que pueden presentar ciertos compuestos fenólicos a las altas temperaturas de procesamiento.
Desobry et al. (1997) observaron perdidas del 11% en β-carotenos encapsulados con maltodextrinas. Cardona et al. (2009) reportaron pérdidas del 21.5 % de los compuestos fenólicos de uva Muscadinia en un proceso de secado por aspersión sin agente encapsulante. Al comparar los resultados de los estudios anteriores, es posible afirmar que el uso de un biopolímero protector en el secado por aspersión, puede reducir las pérdidas de los compuestos activos.
1.3 Concentración de antocianinas monoméricas totales
a Letras iguales significan valores estadísticamente iguales, letras diferentes significan valores estadísticamente diferentes al 95% de confianza
En la Fig. 2 es posible observar que en forma distinta de lo que ocurre con los compuestos fenólicos, las muestras presentan diferencias significativas (p<0.05) en el contenido de antocianinas monoméricas totales. De esta manera se podría afirmar que la de goma de mezquite tuvo un mayor efecto protector en ciertos microencapsulados que en otros, ya que los microencapsulados con 5 g de goma
mg de ácido gálico/ g de sólidos solubles
b a a a a a



g de goma de mezquite / 100 mL
Extracto líquido 1
Fig. 1. Concentración de compuestos fenólicos de los microencapsuladosde flor de jamaicacon goma de mezquite (g goma de mezquite/100 mL de extracto)
a,b Letras iguales significan valores estadísticamente iguales, letras diferentes significan valores estadísticamente diferentes al 95% de confianza
tuvieron una concentración de antocianinas significativamente mayor que aquellos con 1 y 2 g de goma. No obstante, estas diferencias se mantienen en un intervalo estrecho.
Por otra parte, se observa que los microencapsulados conteniendo 3, 4 y 5 g de goma de mezquite no presentaron diferencias significativas en su concentración de antocianinas monoméricas totales, con respecto al extracto líquido. Esto puede deberse al efecto protector que ejerce la goma de mezquite sobre las antocianinas de la flor de jamaica. Cardona et al. observaron pérdidas del 30.3% de las antocianinas totales de uva Moscadina en un proceso de secado por aspersión sin el uso de un agente encapsulante.
Los resultados de la actividad antioxidante de los microencapsulados mostraron un comportamiento distinto a los de los compuestos fenólicos y las antocianinas monoméricas totales. La actividad antioxidante de los extractos en polvo resultó ser significativamente mayor que la del extracto líquido (Fig. 3), por lo que puede afirmarse que hubo un efecto protector de la goma de mezquite sobre los compuestos funcionales.
1 2 3 4 5 6 mg de cianidina-3-glucósido/g de sólidos solubles




g de goma de mezquite / 100 mL
Fig. 2. Concentración de antocianinas monoméricas totales de los microencapsulados de flor de jamaicacon goma de mezquite (g gomade mezquite/100 mL de extracto)
a,b Letras iguales significan valores estadísticamente iguales, letras diferentes significan valores estadísticamente diferentes al 95% de confianza
La tendencia apreciada en la Fig. 3, indica que la mayor capacidad antioxidante la muestran los microencapsulados con menor concentración de goma (1 y 2 g de goma de mezquite), mientras que la menor actividad antioxidante la presentan los extractos en polvo con un mayor contenido de goma (4 y 5 g). Esto resulta un tanto contradictorio con los resultados obtenidos para las antocianinas monoméricas totales; sin embargo, es un indicador de que éstos compuestos no son los únicos responsables de la capacidad antioxidante de los microencapsulados.
Con el fin de explicar este comportamiento, se decidió evaluar la capacidad antioxidante de sólo la goma de mezquite, para observar si existía alguna contribución importante por parte de ésta. Para ello, se prepararon dos soluciones de goma de mezquite: una con 1 g de goma y otra con 5 g de goma de mezquite; éstas se deshidrataron mediante secado por aspersión usando las mismas condiciones que se usaron para los microencapsulados, y se realizaron las evaluaciones correspondientes a la capacidad antioxidante.
Se observó que para los polvos con 1 g de goma de mezquite se obtienen concentraciones de 99.22 μmol de Trolox/g de polvo de goma, mientras que para los polvos con 5 g de goma se obtienen concentraciones de 89.11 μmol de Trolox/g de polvo de goma. Con base en estos
3 - 2 (2009): 14 - 25


a Fig. 3. Actividad antioxidantede los microencapsulados de flor de jamaica con goma de mezquite (ggoma de mezquite/100 mL de extracto)
a,b,c Letras iguales significan valores estadísticamente iguales, letras diferentes significan valores estadísticamente diferentes al 95% de confianza
resultados, es posible afirmar que la goma de mezquite presenta cierto tipo de actividad antioxidante, debido a los taninos presentes en su estructura (López-Franco et al., 2006); ya que los taninos forman parte de la familia de los compuestos fenólicos y, por lo tanto, poseen capacidad antioxidante (Vattem et al., 2005).
Con respecto a los resultados de los parámetros de color de los polvos en una prueba de reflectancia, los datos mostraron que no existen significativas (p>0.05) para el parámetro (L). Los microencapsulados se mantienen dentro en un valor promedio de 40.3 ± 0.71. Lo mismo ocurre para el parámetro a, en el que los valores obtenidos son estadísticamente iguales (p>0.05), con un valor promedio de 31.93 ± 0.29, lo que muestra que todos los polvos se mantienen alrededor de un mismo punto de la región roja. Con respecto al parámetro b, sí se observaron diferencias significativas entre las distintas concentraciones de goma; sin embargo, los valores positivos obtenidos para cada uno de los polvos indicaron que todos los microencapsulados presentan una mayor inclinación hacia la región amarilla que hacia la región azul. El tono y la pureza mostraron que los microencapsulados se mantienen dentro del mismo matiz rojo (0.28 ± 0.00) y
dentro de la misma intensidad (33.19 ± 0.3), por lo tanto, la concentración de goma no tuvo efecto alguno en estos parámetros colorimétricos.
Los resultados de las pruebas de transmitancia mostraron el comportamiento de los polvos en solución. Se observó que la mayor luminosidad la presentaron los polvos con 3 y 4 g de goma (30.54 ± 0.05 y 29.19 ± 0.34, respectivamente), mientras que la menor luminosidad correspondió a los polvos con 1 y 5 g de goma (23.96 ± 0.66 y 24.05 ± 3.01, respectivamente). Con respecto al parámetro a, los datos obtenidos indicaron que los polvos se mantienen en la región roja del espectro de color mientras están en solución. El mayor valor de este parámetro lo presentaron los microencapsulados con 2, 3 y 4 g de goma al ser estadísticamente iguales (38.50 ± 0.20, 42.84 ± 0.28 y 40.37 ± 0.39, respectivamente). El menor valor lo presentaron los polvos con 1 y 5 g de goma (36.02 ± 0.84 y 32.83 ± 3.83, respectivamente). Para el parámetro b, se observó que aunque existen ciertas variaciones entre las muestras, éstas se mantienen en la región amarilla. Los valores mayores los presentaron los microencapsulados con 2, 3 y 4 g de goma (16.41 ± 0.09, 18.66 ± 0.08, 17.68 ± 0.21), mientras que se obtuvieron valores de 14.84 ± 0.40 y 14.56 ± 1.77 para los microencapsulados con 1 y 5 g de goma. Los resultados obtenidos para tono indicaron que los polvos se mantienen dentro del mismo matiz en solución, es decir, conservan su color rojo. En cambio, los resultados del parámetro de pureza indicaron que los microencapsulados con 3 g de goma presentan una mayor intensidad, un color más vivo cuando están en solución, mientras que los microencapsulados con 5 g de goma, presentan un menor matiz, ya que tienen un color más opaco cuando están en solución.
3. Estabilidad de los microencapsulados durante el almacenamiento
3.1 Evaluación de los compuestos fenólicos
La Fig. 4 muestra la estabilidad de los compuestos fenólicos con respecto al tiempo de almacenamiento. Los resultados del análisis estadístico indicaron que la concentración de goma afecta el contenido de compuestos fenólicos durante el almacenamiento; sin embargo, los valores se mantienen en un intervalo estrecho. Los resultados también indicaron que el tiempo es una variable que afecta la concentración de compuestos fenólicos, ya que se observan ciertas fluctuaciones en los valores. Sin embargo, comparando los puntos inicial y final de almacenamiento (días 4 y 37), se encuentra que no existen diferencias significativas (p>0.05) para los microencapsulados con concentraciones de 1, 3 y 5 g de goma; y aunque sí las hubo para las muestras con 2 y 4 g de goma, los valores obtenidos variaron en un intervalo estrecho. En términos generales, puede considerarse que las variaciones observadas fueron debidas a la variabilidad propia del trabajo experimental y que los compuestos fenólicos microencapsulados se mantuvieron estables durante el almacenamiento.
3.2 Evaluación de las antocianinas monoméricas totales
En la Fig. 5 se presenta el comportamiento de las antocianinas monoméricas totales de los microencapsulados durante el almacenamiento. Al igual que para los compuestos fenólicos, se observa que existe una variación significativa (p<0.05) en la concentración de antocianinas, debida al contenido de goma, pero que los valores fluctúan en un intervalo estrecho.
En cuanto al tiempo de almacenamiento también tuvo efecto significativo en la
gálico/g de sólidos solubles
tiempo (días)
los
los
tiempo (días)
concentración de antocianinas; sin embargo, se observan ciertos incrementos y decrementos en los valores. Al comparar el contenido de antocianinas de los microencapsulados al inicio del almacenamiento, con el correspondiente al de los del final, se encuentra que no existe diferencia significativa entre ellas; por lo tanto, se puede afirmar que la concentración de todos los microencapsulados no cambió durante del almacenamiento. Esto puede deberse a que el agente encapsulante retarda la degradación de antocianinas (Duangmal et al., 2008).
Ersus y Yurdagel (2007) evaluaron la estabilidad de pigmentos antociánicos de zanahoria negra en polvos microencapsulados con diferentes maltodextrinas mediante secado por aspersión. Los resultados de este estudio mostraron que el contenido de antocianinas disminuyó en un 19% al final de un periodo de almacenamiento de cinco semanas bajo
condiciones similares a las de este trabajo. Por lo tanto, podría considerarse que la goma de mezquite resulta ser más efectiva que algunos agentes encapsulantes convencionales, para la protección de antocianinas durante el almacenamiento.
3.3 Evaluación de la estabilidad de la capacidad antioxidante
La Fig. 6 ilustra el comportamiento de la capacidad antioxidante de los microencapsulados durante el almacenamiento. A diferencia de lo que ocurre con los compuestos fenólicos y las antocianinas, se observan importantes variaciones entre muestras con diferente contenido de goma al inicio del almacenamiento. Así mismo, se aprecia que el tiempo afecta significativamente la capacidad antioxidante de los microencapsulados, observándose fluctuaciones considerables en los valores obtenidos.
Al comparar el punto inicial y final del almacenamiento, los resultados indicaron que el microencapsulado con 2 g de goma posee la misma actividad antioxidante al inicio y al concluir el periodo de tiempo; mientras que para el resto de los microencapsulados, existen diferencias significativas entre ambos valores. También se observa que al finalizar el almacenamiento, la capacidad antioxidante del microencapsulado con 1 g de goma disminuye, contrario a lo que ocurre para las muestras con 3, 4 y 5 g de goma. Por lo tanto, la capacidad antioxidante no mostró una tendencia definida durante el almacenamiento.
Kuskoski et al. (2005b) señalan que la capacidad antioxidante de una mezcla no viene dada sólo por la suma de las capacidades antioxidantes de cada uno de sus componentes; también depende de la interacción de los compuestos entre sí,
tiempo (días)
pudiendo producir efectos sinérgicos o inhibitorios. Por lo tanto, el comportamiento mostrado en los primeros días del periodo de almacenamiento se podría atribuir a las interacciones tanino-antocianinas. Las reacciones de estabilización tienen, la mayoría de las veces, su origen en la formación entre antocianos y taninos para formar pigmentos estables. Las antocianinas bajo su forma catiónica, reaccionan con las posiciones negativas C6 ó C8 de los taninos, formando un flaveno incoloro, el cual, posteriormente se puede colorear de rojo en presencia de oxígeno, estableciéndose un estado de equilibrio entre ambas formas (Bautista, 2005). Por lo que interacciones taninoantocianinas, pudieran estar produciendo una mayor capacidad antioxidante. Laine et al. (2008) observaron ligeros incrementos en la capacidad antioxidante de extractos microencapsulados de Mora de los pantanos durante el almacenamiento.
3.4 Evaluación de la estabilidad del color
De manera general, los resultados del análisis estadístico revelaron que los parámetros L, a y b se ven afectados (p<0.05) por la concentración de goma y por el tiempo. No obstante, estas variaciones se mantuvieron en un margen muy pequeño. Por otra parte, al evaluar la diferencia neta de color (∆E) para todas las muestras, se encontró que los valores oscilaban entre 0.83 y 1.79. De esta manera,
fue posible afirmar que el (∆E) fue poco considerable y que el color de los microencapsulados se mantuvo estable con respecto al tiempo. Duangmal et al. (2008) observaron cambios en la pureza de polvos de flor de jamaica obtenidos por liofilización con maltodextrinas. Así mismo, Ersus y Yurdagel (2007) observaron un color café en los microencapsulados de zanahoria negra al concluir el almacenamiento. En ambos estudios los autores atribuyen dichas alteraciones a la degradación de antocianinas. En este caso las antocianinas se mantuvieron estables al término del almacenamiento, por lo que el color de los microencapsulados no se vio afectado.
Al evaluar el comportamiento de los parámetros colorimétricos al poner los microencapsulados en solución, el ANOVA indicó que los parámetros L, a y b se ven afectados (p<0.05) por la concentración de goma.
Por otro lado, el comportamiento de las soluciones con respecto al tiempo fue evaluado mediante el cálculo de la diferencia neta de color (∆E). Con base en los resultados obtenidos del análisis estadístico, se concluyó que el tiempo no afecta los parámetros colorimétricos de las muestras cuando se colocan en solución.
los microencapsulados no mostró una tendencia definida, mientras que los compuestos fenólicos, y las antocianinas se mantuvieron estables. Para atribuir este comportamiento al efecto protector de la goma de mezquite, sería necesario evaluar la estabilidad de un extracto en polvo no microencapsulado, obtenido por deshidratación a las mismas condiciones que las del extracto microencapsulado. El uso de la goma de mezquite representa una alternativa más económica respecto a los agentes encapsulantes convencionales y una oportunidad de aprovechamiento de un recurso nacional.
Los autores agradecen al Consejo Nacional de Ciencia y Tecnología (CONACyT) por el financiamiento de esta investigación como parte del proyecto "Extracción, caracterización y funcionalidad de compuestos de origen vegetal obtenidos de materiales mexicanos empleados como condimentos. Obtención de agentes antimicrobianos, antioxidantes e ingredientes funcionales".
A.O.A.C. 2000. Official methods of Analysis of A.O.A.C International: Food Composition, Additives, Natural Contaminants. Gaithersburg, Maryland. EE.UU. 2000 p.
Conclusión
Los resultados de este estudio demostraron que el extracto de jamaica microencapsulado con goma de mezquite mantuvo una concentración de antocianinas similar a la del extracto líquido, y presentó una capacidad antioxidante superior. En cambio, los compuestos fenólicos fueron afectados negativamente como consecuencia de la microencapsulación. En cuanto al efecto del almacenamiento, la capacidad antioxidante de
Ali-Bradeldin, H., Al-Wabel, N. y Gerald, B. 2005. Phytochemical, pharmacological and toxicological aspects of Hibiscus sabdariffa L: A review. Phytotheraphy Research. 19:369–375.
Bautista, A.B. 2005. Técnicas enológicas para la obtención de vinos de Monastrell de alto contenido polifenólico. Tesis de Doctorado. Universidad de Murcia. España.
Beristain, C., Azuara, E. y Vernon, E. 2002. Effect of water activity on the stability to oxidation of spraydried encapsulated orange peel oil using mesquite
gum (Prosopis juliflora) as wall material. Journal of Food Science. 67:206-211.
Cardona, J.A., Hee Lee, J. y Talcott S.T. 2009. Color and Polyphenolic Stability in Extracts produced from Muscadine grape (Vitis rotundifolia) pomace. Journal of Agricultural and Food Chemistry. 57:8421-8425.
Christian, K.R., Nair, M.G. y Jackson, J.C. 2006. Antioxidant and cyclooxygenase inhibitory activity of sorrel (Hibiscus sabdariffa). Journal of Food Composition and Analysis. 19:778-783.
Desobry, S., Netto, F. y Labuza, T. 1997. Comparison of spray-drying, drum drying and freeze drying for β-carotene encapsulation and preservation. Journal of Food Science. 62(6):1158-1162.
Duangmal, K., Saicheva, B. y Sueeprasan, S. 2008. Colour evaluation of freeze-dried roselle extract as a natural food colorant in a model system of a drink Food Science and Technology. 41(8):1437-1445.
El-Saadany, S.S., Sitohy, M.Z., Labib, S.M. y ElMassry, R.A.1991. Biochemical dynamics and hypocholesterolemic action of Hibiscus sabdariffa (Karkade). Die Nahrung. 35(6):567–576.
Ersus, S. y Yurdagel, U. 2007. Microencapsulation of anthocyanins pigments of black carrot (Daucus carota) by spray drier. Journal of Food Engineering. 80:805-812.
Faudale, M., Viladomat, F., Bastida, J., Poli, F. y Codina, C. 2008. Antioxidant Activity and phenolic composition of wild, edible, and medicinal fennel from different mediterranean countries. Journal of Agricultural and Food Chemistry. 56:1912-1920.
Garzón, G. 2008. Las antocianinas como colorantes naturales y compuestos bioactivos: revisión. Acta biológica Colombiana. 13(3):27-36.
Giusti, M. y Wroslstad, R. 2001. Characterization and measurement of anthocyanins by UV-Visible Spectroscopy. En: R.E., Wrolstad, T.E., Acree, E.A., Decker, M.H., Penner, D.S., Reid, S.J., Schwart, C.F., Shoemaker, D.M., Smith y P. Sporns (Eds.) Current Protocols in Food Analytical Chemistry. John Wiley and Sons, Inc. EE.UU. pp. F1.2.1F1.2.13.
Hirunpanich, V., Utaipat, A., Morales, N.P., Bunyapraphatsara, N., Sato H., Herunsalee, A. y Suthisisang, C. 2005. Antioxidant effects of aqueous extracts from dried calyx of Hibiscus sabdariffa L (Roselle) in vitro using rat low-density lipoprotein
(LDL). Biological and Pharmaceutical Bulletin 28(3):481-484.
Kuskoski, M., Asuero, A., García-Parrilla, M., Troncoso, A. y Fett, R. 2004a. Actividad antioxidante de pigmentos antociánicos. Ciencia y Tecnología Alimentaria (México). 24(4): 691-693.
Kuskoski, M.E, Asuiero, A.G., Troncoso, A.M., Mancini-Filho, J. y Fett, R. 2005b. Aplicación de diversos métodos químicos para determinar actividad antioxidante en pulpa de frutos. Ciencia y Tecnología Alimentaria (México). 25(4):726-732.
Laine, P., Kylli, P., Heinonen, M. y Jouppila, K. 2008. Storage stability of microencapsulated cloudberry (Rubus chamaemorus) phenolics. Journal of Agricultural and Food Chemistry. 56:11251-11261.
López-Franco, Y.L., Goycoolea, F.M., Valdez, M.A. y Calderón, A.M. 2006. Goma de mezquite: una alterativa de uso industrial. Interciencia. 3(31):183189.
Marquez-Vizcaino, R.L, De La Rosa-Torres, C., Agusto-Rivero, C. y Medina-Montes, M. 2007. Actividad diurética del extracto total acuoso de los cálices de Hibiscus sabdariffa L. administrado en ratas albinas variedad wistar. Scientia et Technica (33)377-381.
Pedroza-Islas, R. 2002. Alimentos Microencapsulados: Particularidades de los procesos para la microencapsulación de alimentos para larvas de especies acuícolas. En: L. E., Cruz-Suárez, D., Ricque-Marie, M., Tapia-Salazar, M.G., GaxiolaCortés y N., Simoes (Eds.). Avances en Nutrición Acuícola VI. Memorias del VI Simposium Internacional de Nutrición Acuícola. Cancún, Quintana Roo, México. Septiembre 2-6.
Pouget, M.P., Vennat, B. y Pourrat, A. 1990. Identification of anthocyanins of Hibiscus sabdariffa L. Lebensmittel Wissenschaft und Technologie 23:101-102.
Prenesti, E., Berto, S., Daniele, P.G. y Toso, S. 2007. Antioxidant power quantification of decoction and cold infusions of Hibiscus sabdariffa flowers. Food Chemistry. 100:433-438.
Re, R., Pellegrini, N., Proteggente, A., Annala, A., Yang, M. y Rice-Evans, C. 1999. Antioxidant activity applying an improved ABTS radical cation decolorization assay. Free Radical Biology Medicine. 26:1231-1237.
Reanmongkol, W. y Itharat A. 2007. Antipyretic activity of the extracts of Hibiscus sabdariffa
calyces L. in experimental animals. Songklanakarin Journal of Science and Technology. 29:29-38.
Robert, P., Carlsson, R.M., Romero, N. y Masson, L. 2003. Stability of spray-dried encapsulated carotenoid pigments from Rosa Mosqueta (Rosa rubiginosa) oleoresin. Journal of the American Oil Chemist’s Society. 80(11):1115-1120.
Salazar-González, C. 2009. Evaluación de agentes antioxidantes en extractos de flor de jamaica y aceite esencial de laurel. Tesis de Licenciatura. Universidad de las Américas, Puebla. México.
Simonetti, G. 1994. Guía de Hierbas y Especias. Ediciones Grijalbo S.A. Barcelona, España. 170 p.
Singleton, V.L. y Rossi, J.A. 1965. Colorimetry of total phenolics with phosphomolybdic-phosfhotungstic acid reagents. American Journal of Enology and Viticulture. 16(3):144-158.
3 - 2 (2009): 14 - 25
Vattem, D.A., Ghaedian, R. y Kalidas, S. 2005. Enhancing health benefits of berries through phenolic antioxidant enrichment: focus on cranberry. Asia Pacific Journal of Clinical Nutrition 14(2):120-130.
Wong, P., Yusof, S., Ghazali, H.M y Che Man, Y.B. 2002. Physico-chemical characteristics of roselle (Hibiscus sabdariffa L.). Nutrition and Food Science. 32(2):68-73.
Yanishlieva, N. 2001. Inhibición de la oxidación. En: J., Pokorny, J., N., Yanishlieva, y M., Gordon. (Eds). Antioxidantes de los Alimentos Aplicaciones Prácticas. Editorial Acribia S.A. Zaragoza. España. pp. 185-189.
Yun-Ching, C., Kai-Xun, H., An-Chun, H., YungChyuan, H. y Chau-Jong, W. 2006. Hibiscus anthocyanins-rich extract inhibited LDL oxidation and oxLDL-mediated macrophages apoptosis. Food and Chemical Toxicology. 44:1015-1023.

Temas Selectos de Ingeniería de Alimentos 3 – 2 (2009): 26 – 38
Temas Selectos de Ingeniería de Alimentos
Efecto de hidrocoloides en las propiedades de pan recalentado en horno de microondas
G. Pérez-García*, F. Vergara-Balderas y M. E. Bárcenas-Pozos
Departamento de Ingeniería Química y Alimentos, Fundación Universidad de las Américas Puebla. Ex hacienda Sta. Catarina Mártir, Cholula, Puebla. CP 72820. México.
Resumen
El recalentamiento del pan en horno de microondas en la actualidad es muy utilizado, sin embargo da lugar a un producto húmedo y demasiado blando, por lo cual en esta investigación se estudió el efecto de la adición de pectina o hidroxipropilmetilcelulosa (HPMC) en dos concentraciones (0.1 ó 0.5% p/p) en la textura evaluada sensorialmente y en otras propiedades medidas de manera objetiva (dureza y humedad) de pan recalentado en horno de microondas. El pan fue almacenado sin empaque y sobre un soporte perforado; fue analizado a temperatura ambiente a las 0, 24 y 48 horas de almacenamiento, tanto recalentado como sin recalentar; además se evaluó un pan testigo. Aunque los resultados obtenidos en la medición de la dureza mostraron que éste disminuye como consecuencia del recalentamiento, las calificaciones obtenidas durante la evaluación sensorial para la textura del pan recalentado no fueron significativamente diferentes (p< 0.05) con respecto a las de los panes que no fueron recalentados. Se concluyó que los jueces no identificaron diferencias en la textura del pan recalentado en horno de microondas, adicionadas con hidrocoloides.
Palabras clave: pan recalentado, microondas, hidroxipropilmetilcelulosa, pectina, evaluación sensorial, dureza.
Abstract
Nowadays, reheating of bread by microwave oven is widely used; however, it results in a product with a higher level of moisture and softness. Therefore, in this investigation the effect of pectin or hydroxypropilmentilcellulose (HPMC) at two levels (0.1 or 0.5% w/w) on the texture through sensory evaluation, and other properties measured in an objective way (hardness and moisture) of bread reheated by microwave were evaluated. The bread, reheated or not, was stored at room temperature, without packaging over a perforated support and analyzed after 0, 24 and 48 hours of storage; besides, a reference sample was also evaluated. Although the results of the hardness measurement showed that it decreases as a result of reheating, the scores obtained during the sensory evaluation for texture of reheated bread were not significantly different (p <0.05) respect to the breads that were not reheated. It was concluded that judges did not identify the differences in texture of reheated bread by microwave added with hydrocolloids.
Keywords: reheated bread, microwave, hydroxypropylmethycellulose, pectin, sensory analysis, hardness.
*Programa de Maestría en Ciencias de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: gabriela.perezg@udlap.mx
El pan de sal posee una vida útil corta, que se atribuye al fenómeno de envejecimiento, el cual implica la presencia de todos los procesos que ocurren durante el almacenamiento del pan, exceptuando los cambios y deterioro provocados por microorganismos. Las principales características del pan envejecido son el cambio de sabor, la pérdida de aroma, la pérdida de agua y, principalmente, el endurecimiento de la miga y el ablandamiento de la corteza. Estos cambios se presentan poco tiempo después de que el pan ha sido sacado del horno (Matz, 1992; Guarda et al., 2004).
El recalentamiento del pan con horno convencional permite revertir el envejecimiento (Rogers et al., 1990; Eliasson y Larsson, 1993). En la actualidad, el calentamiento en horno de microondas es muy popular en el hogar; sin embargo, los productos de panificación recalentados en horno de microondas por lo regular son considerados de mala calidad, debido a que presentan características indeseables como pérdida de sabor, un recalentado heterogéneo, gomosidad, dificultad para romper la corteza, dificultad para masticar la miga, endurecimiento rápido después del recalentado, entre otras (Rogers et al., 1990; Sumnu, 2001; Mandala y Sotirakoglou, 2005).
Para mejorar la calidad de los productos de panificación recalentados en horno de microondas se han probado diferentes formulaciones, enfocadas principalmente en el efecto del gluten, en el uso de emulsificantes y en la combinación de diferentes ingredientes, incluyendo agentes para la retención de agua (Clarke y Farrel, 2000).
Se ha comprobado que el recalentamiento de pan en horno de microondas causa pérdidas de agua, debido a la ebullición interna generada, la cual favorece el endurecimiento del pan. Sin embargo, Mandala y Sotirakoglou
(2005) encontraron que la inclusión de hidrocoloides en la formulación de pan que luego fue congelado, dio lugar a la obtención de un producto recalentado en horno de microondas de mejor calidad que la del pan que no fue adicionado con estos compuestos.
De la O (2008) y Torres (2008) realizaron estudios sobre el efecto de la adición de hidrocoloides en las propiedades físicas de pan recalentado en horno de microondas. Como resultado de dichos estudios se obtuvo pan en el cual fue posible revertir el endurecimiento al calentar en horno de microondas, sin tener cambios significativos en la humedad y fracturabilidad de la corteza, y sin la textura húmeda y blanda, desagradable, antes mencionada. Sin embargo, no se realizó una evaluación sensorial formal del pan obtenido.
La evaluación sensorial ofrece la oportunidad de obtener información de las propiedades que perciben los sentidos de los humanos. Las pruebas afectivas, conocidas como pruebas hedónicas, se realizan con la finalidad de saber el grado de aceptabilidad o gusto por un producto. En este tipo de prueba, el juez expresa su reacción ante el producto, indicando su nivel de agrado (Wilbur, 1993).
El propósito del presente estudio fue conocer cómo afecta la adición de algunos hidrocoloides (hidroxipropilmetilcelulosa y pectina) a la calificación otorgada a la textura evaluada sensorialmente de pan recalentado en horno de microondas, así como a la dureza y la humedad de este mismo producto, con la finalidad de establecer su grado de aceptación y calidad.
Materiales y Métodos
1. Materias primas
Las materias primas utilizadas para la elaboración del pan de sal fueron: harina de
trigo con un contenido proteico de 11 a 12% (Elizondo, México); sal (Comercializadora Salinera de Yucatán, México) y azúcar comercial (Ingenio San Miguel, México); agua purificada y levadura prensada fresca (La Florida, México). Para el caso del pan con hidrocoloides se utilizaron: hidroxipropilmetilcelulosa (Demacol 2208 HK 4M, Demacsa, México) o pectina cítrica de alto metoxilo (Laumann®, México).
2.1 Elaboración, almacenamiento y recalentamiento del pan de sal
El pan fue fabricado utilizando un proceso directo a través de una formulación básica que consistió en: harina, 61%; agua, 36%; sal, 1%; azúcar, 1%; y levadura, 1%. Los hidrocoloides fueron incorporados a la mezcla de ingredientes al iniciar el mezclado en una concentración de 0.1% ó 0.5% (p/p). Todos los ingredientes fueron mezclados y amasados formando una masa, la cual luego fue dividida, boleada y formada en barras de 180 gramos, de acuerdo a un formato tipo “baguette”. Enseguida se permitió la fermentación en una fermentadora industrial (GPG, España) controlando, durante 30 minutos, una temperatura de 35ºC y una humedad relativa del 65%. Posteriormente, el horneado del pan se realizó a 250ºC durante 14 minutos en un horno convencional (GPG, España) y luego el producto horneado se dejó enfriar a temperatura ambiente durante una hora. Para el caso del pan testigo se realizó el mismo procedimiento de elaboración que el utilizado con el pan adicionado, con la diferencia de que sólo se usaron los ingredientes de la formulación básica.
El almacenamiento del pan se llevó a cabo sin empaque, a temperatura ambiente y sobre un soporte perforado de poliestireno (altura, 9.3 cm; diámetro interno, 7.4 cm; diámetro externo, 8.2 cm).
Para el recalentamiento del pan, se utilizó un horno de microondas doméstico (DAE7028G, Naoki, México) con una potencia nominal de 1300 W. El recalentamiento de cada baguette se realizó durante 20 segundos con una potencia efectiva de 600 W, sobre un soporte perforado de poliestireno. Posteriormente, la baguette se dejó enfriar al ambiente, durante 8 minutos, sobre el mismo soporte perforado.
2.2 Análisis del pan
2.2.1 Volumen específico y relación ancho/alto
Para el pan recién horneado se determinó tanto el volumen específico, utilizando una modificación del método 10-05 de la AACC (2000) mediante el desplazamiento de semillas de nabina, como la relación ancho/alto de acuerdo al método reportado por Lainez et al. (2008) a través de la medición directa de las dimensiones ancho y alto en la rebanada central (25 mm de espesor). Ambas mediciones fueron realizadas por triplicado.
2.2.2 Pruebas durante el almacenamiento
En las baguettes recién horneadas y después de cada periodo de almacenamiento, se tomaron dos muestras del mismo tipo y concentración de hidrocoloide, una de las cuales fue recalentada en un horno de microondas y otra permaneció sin recalentar; en ambas muestras se realizó una evaluación por triplicado de los siguientes parámetros:
2.2.2.1Evaluación sensorial de textura
La evaluación sensorial de la textura del pan fue realizada por 21 jueces no entrenados. Las muestras fueron evaluadas de acuerdo a una prueba afectiva de escala hedónica estructurada de nueve puntos, los cuales corresponden a: “me gusta muchísimo”, “me gusta mucho”, “me gusta moderadamente”, “me gusta poco”, “ni me gusta ni me
disgusta”, “me disgusta poco”, “me disgusta moderadamente”, “me disgusta mucho” y “me disgusta muchísimo”, siendo el punto nueve el nivel máximo de agrado (Stone y Sidel, 2004). Los resultados fueron obtenidos del promedio de las calificaciones dadas por los jueces.
2.2.2.2
Para medir la dureza se utilizó una adaptación del método 74-10a de la AACC (2000), la cual consistió en tomar la rebanada central (2 cm de espesor) de la hogaza, a la que le fue removida la corteza. Posteriormente, se determinó la dureza por compresión de la miga, utilizando un texturómetro TA-TX2 (Stable Microsystems, Surrey, EE.UU.) en modo manual y una sonda cilíndrica de plexiglás de 20 mm de diámetro. Para el recorrido de la sonda cilíndrica se programó una velocidad de 1.7 mm/s y una distancia de recorrido del cilindro de 10 mm.
En cuanto a la humedad, la determinación se realizó siguiendo el método 44-15a de la AACC (2000), por secado en dos etapas y diferencia de peso.
2.3 Análisis estadístico de los resultados
El análisis estadístico de los resultados se llevó a cabo usando el programa Statgraphics Plus (v. 5.1, Statistical Graphics Corp.), de acuerdo a una comparación de múltiple efecto, considerando un diseño anidado combinado
con factorial, con un nivel de confianza del 95%. Las variables independientes fueron: el tipo y la concentración de hidrocoloide, el tiempo de almacenamiento y el recalentamiento en horno de microondas; mientras que las variables dependientes fueron: la dureza, el contenido de humedad y la evaluación sensorial de textura.
1. Efecto de la adición de hidrocoloides en el volumen específico y relación ancho/alto del pan
La adición de hidrocoloides en diferentes concentraciones trae consigo un efecto sobre la masa panadera, lo cual da lugar a diversos cambios en parámetros de calidad del pan, tales como el volumen específico y la relación ancho/alto. En la Tabla I se presentan los resultados obtenidos al estudiar el efecto de la adición de hidrocoloides sobre el volumen específico y la relación ancho/alto del pan. De igual forma, se presentan los resultados obtenidos para la medición de ambos parámetros en un pan testigo.
Se observa que la presencia de hidrocoloides aumentó el volumen específico de los panes adicionados con respecto al del pan testigo, con excepción del de los panes con HPMC al 0.1%.
0.07
0.1%4.42 ± 0.501.41 ± 0.05
0.5%3.76 ± 0.141.62 ± 0.10
0.1%3.22 ± 0.281.38 ± 0.10
0.5% 4.06 ± 0.131.51 ± 0.09
a Promedio y desviación estándar de la evaluación de tres panes “barra mediana” tipo baguette.
Se ha comprobado que la adición de hidrocoloides provoca un aumento del volumen específico del pan (Rosell et al. 2001; Guarda et al., 2004; Bárcenas et al., 2005; De la O, 2008; Torres, 2008). Debido a lo anterior, en este estudio se esperaba que la adición de HPMC o pectina, en ambas concentraciones, trajera consigo un aumento en el volumen específico.
De acuerdo con Bárcenas y Rossell (2005), la adición de HPMC al 0.5% mejora el volumen del pan debido a que cuando este hidrocoloide se hidrata y se expone a altas temperaturas, se presenta una interacción importante entre sus cadenas formándose una red temporal, lo cual disminuye la pérdida de gas, favoreciendo, consecuentemente, una expansión mayor de la masa durante el horneado.El bajo volumen específico del pan adicionado con 0.1% de HPMC, pudo deberse a las variaciones propias del proceso de panificación, ya que el gran número de puntos críticos de este proceso lo hacen muy susceptible a las pequeñas alteraciones que pudieran ocurrir durante el mismo.
En cuanto a la relación ancho/alto (Tabla I), se observa que las muestras adicionadas con HPMC o pectina presentaron valores mayores de este parámetro con respecto al pan testigo. Las hogazas adicionadas con pectina o HPMC al 0.5% tuvieron una relación ancho/alto mayor en relación a las adicionadas con concentraciones menores de los hidrocoloides. La relación ancho/alto del pan proporciona información sobre la forma del mismo: una relación ancho/alto mayor indica un pan plano, mientras que una relación ancho/alto menor, corresponde a un pan con mayor altura y mejor proporcionado. El valor de la relación ancho/alto de una hogaza comercial, de peso similar al de las elaboradas en este estudio es de 1.45 (Pérez, 2008).
Tanto Guarda et al. (2004) como De la O (2008), observaron una menor relación
ancho/alto en los panes adicionados con HPMC al 0.5%, respecto a la de los adicionados con HPMC al 0.1%; sin embargo, en este trabajo se observó lo contrario, es decir, los panes adicionados con HPMC al 0.5% presentaron una relación ancho/alto mayor.
Por otra parte, se observó que la adición de pectina tuvo una respuesta similar a la de la adición de HPMC, debido a que al aumentar la concentración de pectina se presentó una relación ancho/alto mayor. Esto no concuerda con lo reportado por De la O (2008), quien observó una relación ancho/alto mayor para los panes adicionados con pectina al 0.1%.
Los resultados obtenidos permiten demostrar que los panes adicionados con hidrocoloides presentaron una forma más plana que la del pan testigo. Es probable que este hecho se deba a la escasa experiencia de los panaderos que elaboraron este producto, para realizar de manera adecuada el boleado de la masa y el formado de las hogazas, dada la importancia del efecto de estas operaciones en el desarrollo del gluten y, consecuentemente, en la expansión de la masa durante la fermentación y el horneado.
2. Dureza de la miga de pan con hidrocoloides y recalentado en horno de microondas
El recalentamiento del pan revierte la retrogradación del almidón y permite obtener un producto cuya miga es suave. Por otra parte, la adición de hidrocoloides retarda el endurecimiento del pan. En este estudio se evaluó la dureza del pan adicionado con hidrocoloides y recalentado en horno de microondas, luego de diferentes tiempos de almacenamiento. Los resultados obtenidos se presentan en la Fig. 1. Se encuentra que la dureza del pan aumentó conforme transcurre el tiempo de almacenamiento, observándose la mayor dureza para todas las muestras sin recalentar a las 48 horas de almacenamiento.
Además, se observa que el recalentamiento de las muestras a los diferentes tiempos de almacenamiento dio lugar a una reducción en la dureza de la miga.
Así mismo, se observa que la presencia de hidrocoloides provocó un aumento en la dureza de la miga, ya que en las hogazas adicionadas recién horneadas se observó una dureza mayor en comparación con la muestra testigo. De igual forma, a las 24 y 48 horas de almacenamiento la dureza de las muestras adicionadas fue mayor que la del testigo.
El efecto de hidrocoloides en la dureza se analizó también después del recalentamiento del pan. A las 24 horas, las muestras adicionadas con pectina al 0.1% y HPMC al 0.1% y 0.5% presentaron una mayor reducción en la dureza de la miga en comparación con el resto de las muestras. De igual forma, a las 48 horas de almacenamiento la muestra adicionada con HPMC al 0.1% tuvo la disminución más notoria en la dureza debida al recalentamiento, con respecto a las demás muestras.
3. Contenido de humedad de pan con hidrocoloides y recalentado en horno de microondas
El envejecimiento del pan es la consecuencia de diversos cambios, entre los que destacan la pérdida y redistribución del agua en el producto (Lineback, 1982; Pyler, 1988; Eliasson y Larsson, 1993; Baik y Chinachoti, 2000). La redistribución del agua consiste en la ganancia de humedad por parte de la corteza y la pérdida de la misma por parte de la miga, debido a la menor aw de la primera respecto a la de la segunda (Eliasson y Larsson, 1993).
Por su parte, los hidrocoloides poseen la capacidad de incrementar la retención de agua de los productos a los que se adicionan (Armero y Collar, 1996; Guarda et al., 2004). En el caso del pan, se sabe que los hidrocoloides ayudan a retener el agua, retardando así el envejecimiento de este alimento. De aquí que en este estudio se haya determinado el contenido de humedad en las muestras adicionadas y en la muestra testigo, a los diferentes tiempos de almacenamiento, así como también en el pan que fue recalentado y en el que permaneció sin recalentar. Los resultados se presentan en la Fig. 2. Se observa que el contenido de humedad disminuyó
S/R 48 h R
2. Contenido de humedad de pan con hidrocoloides y pan testigo, recalentado en horno de microondas (R) y sin recalentar (S/R), a las 0, 24 y 48 horas de almacenamiento.
conforme aumenta el tiempo de almacenamiento. Además, se encuentra que el recalentamiento dio lugar a una disminución en el contenido de humedad de todas las muestras. Esto concuerda con los resultados obtenidos por Rogers et al. (1990), quienes realizaron una medición del contenido de humedad en hogazas de pan recalentadas en horno de microondas, en horno convencional y en un horno con vapor, observando que el recalentamiento de las muestras causó un decremento en el contenido de humedad.
En cuanto al efecto de los hidrocoloides, su adición disminuyó el contenido de humedad en las hogazas recién horneadas. A las 24 horas de almacenamiento se observó que de las muestras evaluadas, las adicionadas con 0.5% tanto de pectina como de HPMC presentaron la menor pérdida de agua. A las 48 horas, la menor pérdida de humedad con respecto a la muestra almacenada durante 24 horas fue presentada por las hogazas adicionadas con pectina al 0.1%.
4. Evaluación sensorial de la textura de pan con hidrocoloides y recalentado en horno de microondas
La evaluación sensorial es un método subjetivo utilizado para medir diversos atributos organolépticos de los alimentos, tales como la textura, sabor, color, aroma, entre
otros. Este método está basado en el juicio de las personas que evalúan las propiedades organolépticas del alimento (Bourne, 2002). Se debe destacar que las personas poseen el criterio más importante, el que determina la elección y la evaluación de las características sensoriales del alimento.
Con el propósito de evaluar el efecto de la adición de hidrocoloides el recalentamiento del pan en horno de microondas y en el tiempo de almacenamiento sobre la textura del pan, se realizó una evaluación sensorial utilizando una prueba afectiva con una escala hedónica estructurada de nueve puntos. En la Fig. 3 se muestran las calificaciones obtenidas en dicha evaluación.
Se observa que las hogazas recién horneadas recibieron calificaciones entre siete y ocho, es decir, entre “me gusta mucho” y “me gusta moderadamente”.
Por otra parte, se encuentra que al incrementarse el tiempo de almacenamiento, la calificación dada a la textura del pan fue menor; además a tiempos de almacenamiento mayores, la presencia de hidrocoloides no mejoró la calificación otorgada por parte de los jueces.
A las 24 horas de almacenamiento las calificaciones dadas para el pan testigo y las
0 h
24 h S/R
24 h R
48 h S/R
48 h R
muestras adicionadas con los hidrocoloides al 0.1%, sin recalentar, fueron entre seis y siete, correspondientes a “me gusta poco” y “me gusta moderadamente”. El resto de las muestras recibió una calificación entre cinco y seis, las cuales en la escala hedónica corresponden a “ni me gusta ni me disgusta” y “me gusta poco”, respectivamente; por tanto, es posible considerar que fueron aceptadas por los jueces (Guarda et al., 2004). A las 48 horas de almacenamiento las calificaciones otorgadas estuvieron por debajo de los cinco puntos, por lo cual puede afirmarse que no fueron aceptadas por los jueces.
Para las muestras recalentadas a las 24 horas de almacenamiento, se obtuvieron calificaciones entre seis y siete, siendo la muestra testigo y la adicionada con pectina al 0.1% las que obtuvieron la calificación más alta. Por otro lado, las muestras recalentadas y con 48 horas de almacenamiento presentaron calificaciones entre cuatro y cinco correspondientes a “me disgusta poco” y “ni me gusta ni me disgusta” respectivamente, por lo cual no existió aceptación por parte de los jueces.
5. Resultados del análisis estadístico
Tomando en cuenta que el efecto de cada hidrocoloide sobre las propiedades del pan depende de la concentración en la que haya sido adicionado, no es posible considerar el efecto de la concentración del hidrocoloide sobre las variables dependientes de manera individual. Entonces se dice que el efecto de la concentración del hidrocoloide está anidado al efecto del tipo de hidrocoloide. El resto de las variables independientes se analizaron utilizando un modelo factorial. De aquí que el análisis estadístico se haya realizado de acuerdo con una comparación de múltiple efecto, considerando un diseño anidado combinado con factorial. En las Tablas II, III y IV se presenta la comparación de múltiple efecto del tipo de hidrocoloide, el recalentamiento y el tiempo de almacenamiento, respectivamente, y sobre la dureza, la humedad, y la calificación otorgada por los jueces a la textura de las hogazas de las muestras adicionadas con hidrocoloides y del testigo.
En la Tabla II se observa que el contenido de humedad fue significativamente (p < 0.05) afectado por el tipo de hidrocoloide, siendo el pan testigo el que tuvo la humedad más alta y el pan con HPMC el que presentó el menor contenido de humedad.
En varios estudios (León et al., 1997; Rojas et al., 1999; Guarda et al., 2004; Ribotta et al.,
TablaII .Comparaciónmúltipledelefectodeltipodehidrocoloidesobre el contenido de humedad, la dureza y la calificación de textura de pan de sal (1,2)
Hidrocoloide
Humedad Dureza (%) (g f )
Calificación
Textura
Testigo30.11 c1617.17 a6.21 a
Pectina27.70 b2967.53 c6.24 a
HPMC26.39 a2433.62 b6.07 a
1 Entrelasmediasseguidasporlamismaletraparacadacolumna,no existe diferencia significativa, con un nivel de confianza del 95%.
2 Promediodetodoslosvaloresobtenidosparacadaunodelos parámetros.
2004) se ha demostrado que la adición de hidrocoloides a la masa panadera da lugar a la obtención de panes con mayor contenido de humedad, respecto a la muestra testigo. Sin embargo, en este estudio no ocurrió así. Una posible causa es el hecho de que algunas formulaciones se prepararon usando diferentes proporciones de agua, ya que los hidrocoloides modifican la cantidad de agua requerida para formar masas con características adecuadas para la panificación. Otra posible explicación es que el tiempo de horneado aplicado a los distintos lotes de pan fabricados, no haya sido exactamente el mismo (Saravacos y Kostaropoulos, 2002).
En la dureza de la miga, se encuentra que las muestras adicionadas con hidrocoloides tuvieron durezas significativamente mayores
(p < 0.05) en comparación con las hogazas no adicionadas.
Se ha comprobado que la adición de diferentes tipos de hidrocoloides da lugar a una disminución en la dureza (Guarda et al., 2004; Bárcenas et al., 2005; De la O, 2008), debido probablemente a que interfieren con la movilidad de las cadenas de amilosa y amilopectina durante el almacenamiento, afectando así la retrogradación del almidón (Bárcenas y Rosell, 2005). Por lo tanto, en este estudio se esperaba que la adición de HPMC o pectina provocara una disminución en la dureza de la miga de las hogazas.
De la O (2008) observó una diferencia significativa (p < 0.05) entre la dureza de hogazas adicionadas con pectina y la de hogazas sin adicionar, encontrando que las muestras adicionadas mostraron una dureza menor. Sin embargo, en este estudio se observó lo contrario.
En el caso de HPMC, De la O (2008) estudió el efecto de su adición sobre la dureza de la miga, observando que la presencia de este hidrocoloide redujo significativamente la dureza en relación a la de las hogazas no adicionadas. Rosell et al. (2001) y Guarda et al. (2004) encontraron que muestras adicionadas con HPMC tuvieron una dureza menor que muestras sin adicionar. Por el contrario, en este estudio la adición de HPMC aumentó significativamente (p < 0.05) la dureza de la miga en relación al testigo.
En general, el pan adicionado con HPMC al 0.5% presentó características muy distintas a las esperadas de acuerdo con lo reportado por otros investigadores (Rojas et al., 1999; Guarda et al., 2004; Bárcenas et al., 2005; Bárcenas y Rosell, 2005), lo cual pudo deberse a que en este estudio el pan fue elaborado por panaderos sin suficiente experiencia, por lo que las etapas de amasado, boleado y formado pudieron no haber sido realizadas
adecuadamente, afectando la formación óptima del gluten y la textura del pan, y dando lugar a un producto con mayor dureza que la del pan no adicionado.
En el caso de las calificaciones otorgadas a la textura por los jueces, no hubo diferencia significativa (p < 0.05) entre las calificaciones recibidas por la textura de los distintos tipos de pan. En este trabajo se esperaba que los panes adicionados recibieran calificaciones más altas debido a que en diversos estudios se ha demostrado que la adición de hidrocoloides aumenta la calidad sensorial del pan (Guarda et al., 2004; Bárcenas y Rosell, 2005).
La comparación múltiple del efecto del recalentamiento se presenta en la Tabla III. En cuanto al contenido de humedad, las muestras que permanecieron sin recalentar presentaron valores significativamente (p < 0.05) más altos en comparación con las muestras que fueron recalentadas en horno de microondas. De la O (2008), Rogers et al. (1990) y Mandala (2005) comprobaron que el recalentamiento del pan en horno de microondas disminuye la humedad. La reducción en el contenido de humedad del pan al ser recalentado en horno de microondas, se debe principalmente a la evaporación del agua como consecuencia del calentamiento (Uzzan et al., 2007).
En el caso de la dureza, se observa una diferencia significativa (p < 0.05) entre las muestras recalentadas y las que permanecieron sin recalentar, siendo menor la dureza del pan recalentado. De la O (2008) y Torres (2008) evaluaron el efecto del recalentamiento en horno de microondas sobre la dureza de la miga en hogazas adicionadas con diferentes hidrocoloides y en muestras no adicionadas; dichos autores observaron una diferencia
significativa entre las muestras recalentadas y las no recalentadas, notando una dureza mayor en las muestras que no fueron recalentadas, lo cual coincide con lo obtenido en este estudio.
El recalentamiento del pan revierte la retrogradación del almidón (Rogers et al., 1990; Eliasson y Larsson, 1993). La disminución de la dureza de la miga de las muestras que fueron recalentadas, se debe a que las estructuras formadas durante la retrogradación de la amilosa y la amilopectina pierden su arreglo al ser sometidas a altas temperaturas, causando que el pan recupere su textura blanda (Hug-Iten et al., 2003).
En la calificación de textura otorgada por los jueces, se observa que no hubo diferencia significativa (p < 0.05) entre las hogazas recalentadas y aquellas sin recalentar, es decir, los jueces no mostraron preferencia por hogazas recalentadas o sin recalentar.
En la Tabla IV se presenta la comparación múltiple del efecto del tiempo de almacenamiento. En el contenido de humedad, se observa que éste disminuyó significativamente (p < 0.05) conforme el tiempo de almacenamiento se incrementó. De la O (2008) observó un efecto significativo del tiempo de almacenamiento sobre la humedad en diferentes puntos de hogazas de pan adicionadas con pectina y HPMC; por tanto, hay concordancia entre lo obtenido en este estudio y lo observado por dicho autor. Además, el comportamiento observado en este estudio, también coincide con lo reportado por Baik y Chinachoti (2000), quienes estudiaron
TablaIII .Comparaciónmúltipledelefectodelrecalentamientoenhornode microondassobreelcontenidodehumedad,ladurezaylacalificacióndetextura de pan de sal (1,2)
Recalentamiento
Humedad Dureza Calificación
(%) (g f ) Textura Sin29.20 b2792.13 b6.12 a Con26.93 a1886.75 a6.23 a
1 Entrelasmediasseguidasporlamismaletraparacadacolumna,noexiste diferencia significativa, con un nivel de confianza del 95%.
2 Promedio de todos los valores obtenidos para cada uno de los parámetros.
TablaIV. Comparaciónmúltipledelefectodeltiempodealmacenamiento sobreelcontenidodehumedad,ladurezaylacalificacióndetexturadepan de sal (1, 2)
Tiempo (horas)
Humedad Dureza
(%) (g f )
Calificación Textura
033.07 c617.70 a7.72 c 2428.32 b2505.01 b6.19 b 4822.81 a3895.60 c4.61 a
1 Entrelasmediasseguidasporlamismaletraparacadacolumna,noexiste diferencia significativa, con un nivel de confianza del 95%.
2 Promedio de todos los valores obtenidos para cada uno de los parámetros.
la redistribución de humedad durante el envejecimiento del pan almacenado con y sin corteza. Piazza y Masi (1995) reportaron que el promedio en el contenido de humedad en la
Debido a que el pan fue almacenado sin envase y expuesto al ambiente, se plantea que la disminución en el contenido de humedad conforme transcurrió el tiempo de almacenamiento se debió a la migración del agua desde el pan hacia el ambiente.
Para el caso de la dureza, se observa que ésta aumentó significativamente (p < 0.05) conforme al tiempo de almacenamiento; este fenómeno ha sido ampliamente estudiado (Armero y Collar, 1998; Hallberg y Chinachoti, 2002; Murat, 2006; Bárcenas y Rosell, 2007). El incremento en la dureza de la miga durante el almacenamiento del pan se debe principalmente a la retrogradación del almidón (Hallberg y Chinachoti, 2002; Bárcenas y Rosell, 2005). Además, la pérdida y redistribución de agua que experimenta el
miga central de la rebanada central, de diferentes formulaciones de pan, disminuye conforme al tiempo, lo cual concuerda con lo observado en este estudio.
pan, también contribuye al endurecimiento de la miga (He y Hoseney, 1990; Piazza y Masi, 1995). En el caso del pan evaluado en este estudio, el haber almacenado el pan sin empaque y en contacto directo con el ambiente, favoreció su endurecimiento.
Finalmente, se observa que las calificaciones otorgadas por los jueces a la textura de las hogazas disminuyeron significativamente (p < 0.05) conforme aumentó el tiempo de almacenamiento. Los panes recién horneados recibieron las calificaciones más altas. El incremento de la dureza y la disminución de la humedad del pan durante el almacenamiento, pudieron haber causado que las calificaciones otorgadas por los jueces a la textura, disminuyeran.
Conclusión
Se observó que la dureza y la humedad del pan adicionada con hidrocoloides disminuyeron debido al recalentamiento. Sin embargo, estas diferencias no fueron detectadas por los jueces en la evaluación sensorial de la textura. Por tanto, se considera necesario llevar a cabo un estudio sensorial más riguroso que incluya la definición de descriptores para evaluar la textura, un método de evaluación apropiado, la participación de jueces entrenados, entre otros aspectos.
Por otra parte, las contradicciones encontradas en varios resultados y atribuidas a la inexperiencia de los panaderos, llevan a proponer que la panificación se realice de forma más escrupulosa.
Agradecimientos
Los autores agradecen a la ingeniera Amalia Alba Torres y a la empresa PABISAN, S.A. de C.V. su apoyo para la realización de este estudio.
baking process with frozen storage. Food Hydrocolloids. 18(2):769-774.
Bárcenas, M. E. y Rosell, C. M. 2005. Effect of HPMC addition on the microstructure, quality and aging of wheat bread. Food Hydrocolloids. 19(6):1037-1043.
Bárcenas, M. E. y Rosell, C. M. 2007. Different approaches for increasing the shelf life of part-baked bread: Low temperatures and hydrocolloid addition. Food Chemistry. 100(4): 1594-1599.
Bourne, M. 2002. Food Texture and Viscosity. Segunda edición. Academic press, EE.UU. 257 p.
Clarke, C. y Farrell, G. 2000. The effects of recipe formulation on the textural characteristics of microwave-reheated pizza bases. Journal of the Science of Food and Agriculture. 80(8): 1237-1244.
De La O, J. 2008. Efecto de la adición de hidrocoloides sobre la calidad y envejecimiento de pan recalentado en horno de microondas y sobre las propiedades de los componentes del pan. Tesis de Maestría. Universidad de las Américas, Puebla.
Eliasson A. C. y Larsson, K. 1993. Cereals in breadmaking: a molecular colloidal approach Tercera edición. Marcel Dekker. EE.UU. 327 p.
Guarda, A., Rosell, C. M. y Galotto, M. J. 2004. Different hydrocolloids as bread improvers and antistaling agents. Food Hydrocolloids 18(2):241247.
Referencias
AACC. American Association of Cereal Chemists. 2000. Approved methods of the AACC. Décima edición. The American Association of Cereal Chemists. St. Paul, MN, EE.UU.
Armero, E. y Collar, C. 1996. Antistaling additive effects on fresh wheat bread quality. Food Science and Technology Internacional. 2(5):323-333.
Armero, E. y Collar, C. 1998. Crumb firming kinetics of wheat breads with anti-staling additives. Cereal Chemistry 28(2):165-174.
Baik, M. y Chinachoti, P. 2000. Moisture redistribution and phase transitions during bread staling. Cereal Chemistry. 77(4):484-488.
Bárcenas, M. E., Benedito, C. y Rosell, C. M. 2005. Use of hydrocolloids as bread improvers in interrupted
Hallberg, L. M. y Chinachoti, P. 2002. A fresh perspective on staling: the significance of starch recrystallization on the firming of bread. Journal of Food Science. 67(3):1092-1096.
He, H. y Hoseney, R. C. 1990. Changes in bread firmess and moisture during long-term storage. Cereal Chemistry. 67(6):603-605.
Hug-Iten, S., Escher, F. y Conde-Petit, B. 2003. Staling of bread: role of amylose and amylopectin and influence of starch-degrading enzymes. Cereal Chemistry. 80(6):654-661.
Lainez, E., Vergara, F. y Bárcenas, M.E. 2008. Quality and microbial stability of partially baked bread during refrigerated storage. Journal of Food Engineering 89:414-418
León, A., Durán, E. y Benedito C. 1997. A new approach to study starch changes occurring in the dough-baking process and during bread storage. Zeitschrift für Lebensmittel Untersuchung und Forschung A, 204(4)316:320.
Lineback, I. 1982. Food Carbohydrates. The Avi Publishing Company. EE.UU. 237 p.
Mandala, I. G. 2005. Physical properties of fresh and frozen stored, microwave-reheated breads, containing hydrocolloids. Journal of Food Engineering. 66(3):291-300.
Mandala, I. G. y Sotirakoglou, K. 2005. Effect of frozen storage and microwave reheating on some physical attributes of fresh bread containing hydrocolloids. Food Hydrocolloids. 19(44):709-719.
Matz, S. 1992. Bakery Technology and Engineering Tercera edición. Pan-Tech International, INC., EE.UU. 154-157 p.
Murat, M. 2006. Effect of baking procedure and storage on the pasting properties and staling of part-baked and rebaked white pan bread. International Journal of Food Properties. 9(4):609-622.
Pérez, G. 2008. Efecto del uso de hidrocoloides en la calidad sensorial y las propiedades de pan de sal recalentado en horno de microondas. Tesis de Licenciatura. Universidad de las Américas, Puebla
Piazza, L. y Masi, P. 1995. Moisture Redistribution throughout the bread loaf during staling and its effect on mechanical properties. Cereal Chemistry 72(3):320-325.
Pyler, E. 1988. Baking Sciende and Technology. Tercera edición. Sosland Publishing Company. Kansas, EE.UU. 815-817 p.
Ribotta, P. D., Pérez, G. T., León, A. E. y Añón, M. C. 2004. Effect of emulsifier and guar gum on microstructural, rheological and baking performance
of frozen bread dough. Food Hydrocolloids. 18:305313.
Rogers, D. E., Doescher, L. C. y Hoseney, R. C. 1990. Texture characteristics of reheated bread. Cereal Chemistry. 67(2):188-191.
Rojas, J. A., Rosell, C. M. y Benedito C. 1999. Pasting properties of different wheat flour-hydrocolloid systems. Food Hydrocolloids. 13:27-33.
Rosell, C. M., Rojas, J. A. y Benedito, C. 2001. Influence of hydrocolloids on dough rheology and bread quality. Food Hydrocolloids. 15:75-81.
Saravacos G. y Kostaropoulos, A. 2002. Handbook of food processing equipment. Kluwer Academic/Plenum Publishers, EE.UU. 412 p.
Stone, H. y Sidel J. L. 2004. Sensory evaluation practices. Tercera edición. Food Science and Technology, International Series. EE.UU. 247 p.
Sumnu, G. 2001. A review on microwave baking of foods. Journal of Food Engineering. 71(2)150:155.
Torres, R. 2008. Efecto de la adición de hidrocoloides sobre las características de pan recalentado con microondas. Tesis de Licenciatura. Universidad de las Américas, Puebla
Wilbur, A. 1993. Total quality assurance for the food industries. Tercera edición. CTI Publicatons, Inc. EE.UU. 95 p.
Uzzan, M., Ramon, O., Kopelman, I. J., Kesselman, E. y Mizrahi, S. 2007. Mechanism of crumb toughening in bread-like products by microwave reheating. Journal Agriculture Food Chemistry. 55(16): 6553-6560..

Temas Selectos de Ingeniería de Alimentos 3 – 2 (2009): 39 – 50
Cinética de deshidratación por liofilización de maíz para la elaboración de botanas
D. Márquez - Aquino*, F. Vergara - Balderas
Departamento de Ingeniería Química y Alimentos, Fundación Universidad de las Américas Puebla. Ex hacienda Sta. Catarina Mártir, Cholula, Puebla. CP 72820. México.
Resumen
Se determinaron las cinéticas de deshidratación por liofilización de granos de maíz salados y acidificados, para la obtención de botanas. Previamente se determinaron las concentraciones necesarias de aditivos para obtener el sabor deseado y se estableció un tiempo de cocción. Se determinó la velocidad de congelación con una y dos capas de espesor de los granos (1 y 2 cm), obteniéndose el menor tiempo de congelación para una capa. Se analizó la cinética de deshidratación de las botanas de granos de maíz usando diferentes temperaturas de calefacción (25, 35 y 45 °C) y distintos números de capa (una y dos). La humedad final del producto liofilizado fue menor al 10 %.
Palabras clave: liofilización, cinética de deshidratación, botanas de granos de maíz, curvas de congelación
Abstract
Corn kernels were treated with freeze drying with the aim to obtain a new product: corn kernels snack with an acid and salty flavor. As pretreatment, the adequate additive concentrations were used in order to obtain the desired flavor, and a cooking time was established. The freezing velocity was determined in trays with kernels with one and two layer thickness (1 and 2 cm each one), achieving the minimum freezing velocity time for one layers thickness. The dehydration kinetic of the corn kernels snacks was analyzed and the best drying time was selected in accordance to the heating plates temperature (25, 35 y 45 ºC) and the layer thickness (one and two layers). The final product moisture was less than 10 %.
Keywords: freeze drying, dehydration kinetic, corn kernels snack, freezing curves
Introducción
*Programa de Maestría en Ciencias de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: daniela.marqueza@udlap.mx
El maíz es un cereal altamente cultivado en el mundo, debido a su capacidad inigualable de cultivo y su elevado consumo. Los principales productores de maíz son: Estados Unidos de América, con un 40 % de la producción total; China con un 19 %; Brasil con un 6 % y México con un 3 % (SIAP, 2007). En México, Temas Selectos de Ingeniería de Alimentos
puesto que el maíz presenta una amplia gama de variedades, se han generado una gran cantidad de productos finales como: tortillas, harina de maíz, masa, aceite de maíz, cereales para el desayuno, jarabes, aceites, botanas, pastas, sémola, almidones, glucosa, fructosa, bebidas sin alcohol, forraje para animales, etanol para bebidas o como insumo en la producción de biocombustible, entre otros (FAO, 1993; FAO, 2001; SIAP, 2007). Pero para los productores de maíz estos productos no son suficientes, así que buscan elaborar nuevos productos que les permitan obtener mayor aprovechamiento de la materia prima y mejores ganancias; por lo que surge la idea de crear botanas salada y ácida de granos de maíz liofilizados.
La liofilización es un proceso que origina productos de alta calidad y conserva la estructura del material; tiene dos características importantes: la ausencia de aire que junto a la baja temperatura previene el deterioro por oxidación; y el secado a una temperatura inferior a la ambiente, lo cual causa un daño mínimo en el producto final (Ibarz y Barbosa-Cánovas, 1999). El proceso de liofilización está constituido por tres fases: congelación, secado primario (sublimación del hielo) y secado secundario (eliminación del agua) (Ibarz y Barbosa-Cánovas, 1999; Tambunan et al.; 2001). La muestra antes de secarse, se congela (Chin et al., 2008). La congelación del producto debe ser rápida para obtener cristales de hielo muy reducidos (amorfos) (Welti-Chanes et al., 2004). El tiempo de congelación del producto depende de la temperatura inicial y final del mismo, de la cantidad de calor que es removido, de las dimensiones del producto (grosor), del calor transferido y de la temperatura del medio (Mallet, 1993). Después, el agua se elimina por sublimación (Marques y Freire, 2005). En diagramas de fases de agua (temperatura, presión), se observa que al disminuir la presión (descender por debajo del punto triple; presión de 627 Pa) y la temperatura del agua
del alimento (por debajo del punto denominado zona de eutexia, donde se consigue el máximo grado de solidificación), se logra la sublimación (Welti-Chanes et al., 2004).
El proceso de liofilización requiere altas cantidades de energía que aumentan el costo y del producto obtenido, aunque se compensa debido a que se conservan las propiedades del alimento (olor, sabor y color) y se aumenta la vida de anaquel. Es un proceso que se considera como una alternativa más que ayuda a la preservación de alimentos (Ratti, 2001; Claussen et al., 2007; Trelea et al., 2007). La calidad de los productos liofilizados se ve afectada por las características de la materia prima (como el grado de madurez), y las condiciones de operación (como la presión de la cámara, la velocidad de calentamiento y la velocidad de congelación) (Grajales-Agudelo et al., 2005). La estructura esponjosa del producto liofilizado permite una rápida rehidratación (de 4 a 6 veces más alta que el secado por aire) (Ibarz y Barbosa-Cánovas, 1999; Ratti, 2001). Los tiempos de secado requeridos para el proceso de liofilización son substancialmente mayores comparados con los métodos de secado convencional por evaporación (Sadikoglu et al., 2006).
En esta investigación se generaron productos de maíz con un alto valor agregado, que contribuyen a diversificar las alternativas de procesamiento de este cereal; en este caso con granos de maíz previamente sometidos a un proceso de cocción con aditivos y luego liofilizados, para obtener botanas salada y ácida. El objetivo general de esta investigación fue determinar la cinética de deshidratación por liofilización de granos de maíz salados y acidificados, para la obtención de botanas.
Materiales y métodos
1. Obtención de los granos de maíz
Se utilizó maíz criollo (Zea mays Linnaeus.) blanco de grano grande. La mazorca se deshojó y se seleccionó de forma subjetiva de acuerdo al tamaño (grande o mediano), ternura media y aspecto de los granos de maíz. Una vez seleccionada la mazorca se desgranó de forma manual.
2. Pretratamiento del grano de maíz para botanas
2.1 Mezcla de aditivos y proceso de cocción
La cocción se realizó de acuerdo a lo recomendado por Pérez-Pérez et al. (2007) (relación de 100 g de maíz en 0.171 L de solución). Se prepararon las soluciones y posteriormente se colocaron los granos para el proceso de cocción de acuerdo a lo mencionado por Márquez-Aquino (2009). Para la botana salada se preparó una solución con una concentración de 0.88 % de sal; y para la botana ácida se preparó una solución al 0.88 % de sal con 0.59 % de ácido cítrico. La mezcla hirvió durante 45 minutos en una estufa de gas. Posteriormente, se filtró la mezcla con una coladera para separar la solución de los granos. Por último, se determinó la humedad de los granos cocidos por diferencia de pesos, secando en una estufa al vacío a 135°C durante ocho horas, de acuerdo al método 7.007 de la A.O.A.C. (1984). Esta determinación se hizo por triplicado.
Los granos de maíz se colocaron en charolas formando una y dos capas, 1.0 y 2.0 cm de espesor, respectivamente. Se instaló un termopar de cobre-constantano en el centro y la orilla de dos diferentes granos para registrar las temperaturas del producto mediante un lector Cole-Parmer (modelo 92800-00,
Scanning Thermocouple Thermometer, EE.UU.). Las charolas se introdujeron en un congelador a -45°C (Revco, EE. UU.) y la temperatura se registró cada 5 minutos para generar las curvas de congelación. La congelación se dio por terminada al observar que la temperatura del grano permanecía constante. Para la obtención de las curvas del porcentaje de agua congelada, se siguió el procedimiento detallado por Heldman y Singh (1981) y Márquez-Aquino (2009).
3. Proceso de liofilización
Se utilizó un liofilizador (modelo Lyph-Lock 6 Freeze System, LABCONCO, EE.UU.) operando con placas calefactoras a 25ºC, 35°C y 45°C, a un nivel de presión de 0.1-0.2 mm Hg y a una temperatura del condensador de -55°C.
3.1 Preparación de las charolas con muestras para liofilizar
Para cada corrida se usaron tres charolas con granos previamente congelados. El peso inicial de las charolas se registró en una balanza (modelo Scout Pro SP2001, Ohaus Corporation, EE. UU.) cuya sensibilidad es de 0.1g. Las charolas con una capa de espesor contienen 0.177±0.024 kg de granos y con dos capas 0.387±0.032 kg. Se calentaron las placas a la temperatura de trabajo y se colocaron las charolas en la cámara del liofilizador.
3.2 Ciclo de liofilización
Una vez introducidas las charolas dentro de la cámara, se hizo vacío hasta una presión de 0.10.2 mm Hg. Cuando se alcanzó dicha presión se verificaron la temperatura del condensador, la presión y la temperatura dentro de la cámara y se inició el proceso de liofilización. Dos horas después, se rompió el vacío y una vez establecida la presión atmosférica, se pesaron nuevamente las charolas. En seguida, las charolas se introdujeron al liofilizador para
continuar con el proceso y se verificaron las condiciones del equipo. El proceso anterior se repitió cada dos horas. El ciclo de liofilización terminó cuando entre dos intervalos de tiempo, la variación del peso fue menor a 0.002 kg y la humedad final fue menor al 10 % (en base húmeda). Al terminar, la muestra fue envasada dentro de bolsas, que luego fueron selladas, y se almacenó en un cajón donde no existían cambios de humedad.
una capa y dos capas de espesor. Los datos obtenidos experimentalmente del termopar en el centro y en la orilla del grano de maíz son similares, por lo tanto, se toma en cuenta el termopar en el centro, ya que es importante asegurar que el grano esté completamente congelado.
Resultados y discusión
1. Pretratamiento de los granos de maíz
Los valores de humedad para las botanas ácida y salada al final de la cocción fueron similares, encontrándose en un intervalo de 79.0 a 81.0% en base húmeda. Comparando con la humedad del grano fresco obtenida experimentalmente (68.27 ± 0.59 %), se observa un aumento de humedad de los granos cocidos en soluciones ácida y salada. Los cambios de humedad se deben a que el grano de maíz es un material poroso que tiene una membrana semipermeable, la cual permite la transferencia de masa en la disolución. El tamaño de los poros es tan minúsculo que deja pasar las moléculas pequeñas pero no las grandes. Las moléculas de agua, sal o ácido son pequeñas, por lo que no tienen problemas para entrar. En el proceso de cocción se produjo un fenómeno de transferencia de masa de la disolución hipotónica (menor concentración- soluciones de sal y ácido) a la disolución hipertónica (mayor concentración- solución en el interior del grano de elote) (Gekas, 1992).
2. Curvas de congelación para las botanas ácida y salada
2.1 Efecto del espesor de la capa de granos sobre el tiempo de congelación
En la Fig. 1 se presentan las curvas de congelación de las botanas salada y ácida con
En la Fig. 1a se observa que la remoción de calor sensible es más rápida en la charola con una capa de granos, ya que el tiempo requerido para alcanzar una temperatura de -0.1°C es de 5 minutos. También se observa una meseta que indica la remoción del calor latente de congelación (calor necesario para el cambio de fase), con una duración de 20 minutos. En la charola con dos capas se alcanza la misma temperatura (-0.1°C) en un tiempo de 28 minutos y la meseta se observa durante 70 minutos. Después de la meseta, la temperatura continúa disminuyendo, por lo que se sigue eliminando calor; a este proceso se le conoce como sub-enfriamiento o reducción a la temperatura de almacenamiento. En este período se remueve gran cantidad de la energía, la temperatura se reduce desde la temperatura en la cual la mayoría del agua congelable ha sido convertida a hielo, hasta la temperatura final prevista; el agua se separa como cristales de hielo puro (Mallet, 1993). La transferencia de energía en la charola con dos capas es más lenta comparada con la de una capa, ya que los granos en la parte inferior del espesor tardan más en transferir energía hacia el medio de congelación (el centro del espesor de capa se enfría más lento) y como consecuencia el tiempo requerido para la congelación es mayor.
Es importante considerar el tamaño de los cristales de hielo, el cual puede afectar subsecuentemente la velocidad de secado; los cristales más pequeños producirán un tamaño de poro más pequeño, lo cual dificultará la salida del vapor de agua. Si los poros son
orilla del grano (una capa) centro del grano (una capa) orilla del grano (dos capas) centro del grano (dos capas) medio de congelación
grandes, existirá mayor flujo másico y los tiempos de secado serán más cortos (Heldman y Singh, 1981; Lewis, 1990; Marques y Freire, 2005; Welti-Chanes et al., 2004). El proceso de liofilización requiere la formación de poros grandes del vapor de agua del alimento (WeltiChanes et al., 2004). En general, el proceso de congelación del grano de maíz, para una o dos capas, presenta una velocidad de congelación lenta y, por lo tanto, se favorece la liofilización.
La curva de congelación de la botana ácida (Fig. 1b) presenta un comportamiento similar a la curva de congelación de la botana salada,
por lo que se confirma que con una capa de espesor la velocidad de congelación es menor.
En la Tabla I se encuentran los datos obtenidos de cada curva de congelación; se presentan los tiempos de congelación de los granos de maíz cocidos, que es el tiempo requerido para que la variación de temperatura en un periodo de dos horas sea mínima (0.1 °C); y la temperatura inicial de congelación observado en las gráficas, la cual corresponde al primer cambio de pendiente en la curva de congelación. Muchos productos contienen diferentes componentes que influyen en la magnitud de la depresión del punto de
Tabla I. Tiempos de congelación a y temperaturas iniciales de congelación para cada botana b Botana b Tiempo (min)Punto inicial de congelación (°C)
1 capa2 capas1 capa2 capas
Ácida 180230-1.1-1.2
Salada 186220-1.4-1.2
a Tiempo que tarda en mantenerse constante la temperatura del grano
b Granos de maíz cocidos en solución de NaCl (salada) o en solución de NaCl y ácido cítrico (ácida)
congelación del alimento respecto a la temperatura de congelación del agua; y es imposible evaluar los componentes que más contribuyen a dicha depresión (Heldman y Singh, 1981).
Se observa que los tiempos de congelación no presentaron diferencia considerable para los dos tipos de botanas. Por otra parte, el punto inicial de congelación para el grano estuvo entre -1.1 y -1.4 °C. Rahman (1995) reporta que la temperatura de congelación del maíz blanco es -1.7 °C. Por lo tanto, los datos obtenidos en este estudio fueron cercanos. Las diferencias de la temperatura inicial de congelación posiblemente se deban a la composición, a la variedad o a la maduración del grano y a que se coció el grano antes de la congelación, a diferencia del grano fresco que se encontró reportado.
2.2 Análisis del porcentaje de agua congelada
La humedad del producto y su punto inicial de congelación son utilizados para la obtención del peso molecular promedio de los solutos efectivos, el cual puede ser usado para calcular el porcentaje de agua congelada existente en el producto a temperaturas por debajo del punto de congelación (Heldman y Singh, 1981). En este estudio se obtuvo el porcentaje de agua congelada a diferentes temperaturas. Se observó que no existe diferencia considerable entre las dos posiciones de los termopares en el porcentaje de agua congelada y que el comportamiento de las dos botanas fue similar.
En la Tabla II se reportan los valores de la temperatura para congelar la mayor parte del agua (alrededor de un 80 %) y la temperatura final alcanzada. Como se observa, la mayor arte del agua está congelada a una temperatura menor a -9.0 °C. Por debajo de esta temperatura el porcentaje de agua congelada es mayor al 80 %. No existe gran diferencia entre las temperaturas finales alcanzadas para las botanas ácida y salada con una y dos capas de granos de maíz, por lo tanto, la temperatura final obtenida estuvo entre -38.9 y -40.7 °C. En la Fig. 2 se observan las curvas del porcentaje de agua congelada para las botanas ácida y salada, para uno y dos espesores de capa con el termopar en el centro del grano de maíz. Para la botana salada con 1 capa el porcentaje de agua congelada a una temperatura de -10.0 °C es del 82.87 % y para 2 capas es del 88.28 %; y para la botana ácida con una capa es del 89.45 % y con dos capas es del 88.28 %. Los porcentajes entre los dos tipos de botanas son muy cercanos. Existe una cierta proporción de agua (alrededor del 10 %) que permanece sin congelar y que corresponde a la fracción de agua más ligada a los compuestos del alimento (Braverman, 1986). Conocer el porcentaje de agua congelada permite establecer las condiciones necesarias para el proceso de congelación, es decir, para determinar la temperatura a la cual debe ser almacenado el alimento para que se mantenga congelada la mayor parte del agua (Heldman y Singh, 1981).
Porcentaje de agua congelada
Tabla II. Temperatura para tener la mayor parte del agua congelada y temperatura final alcanzada en la congelación de botanas a de maíz a Granos de maíz cocidos en solución de NaCl (salada) o en solución de NaCl y ácido cítrico (ácida)
Botanas a
Con la mayor parte de agua congelada (80%) (°C)
Final alcanzada (°C)
1 capa2 capas1 capa2 capas
Ácida -5.9-5.4-38.9-39.5
Salada -8.9-5.7-40.7-40.0
1 capa (botana ácida)
2 capas (botana ácida)
1 capa (botana salada)
2 capas (botana salada)
Temperatura (°C)
Fig. 2. Porcentaje de agua congelada durante el proceso de congelación para lasbotanas ácida y salada con el termopar en el centro del grano de maíz
3. Cinética de deshidratación para los dos tipos de botanas
El proceso de secado es una operación unitaria importante en la industria de alimentos y se define como la eliminación de la humedad de un producto; en la mayoría de las situaciones prácticas la etapa principal del proceso es la transferencia interna de materia (Lewis, 1990).
Una curva de secado se obtiene al representar la humedad del alimento en base seca frente al tiempo de secado (BarbosaCánovas y Vega-Mercado, 1996). En la Fig. 3 se presentan las curvas de secado de las botanas salada (a) y ácida (b). Las curvas de secado permiten conocer la humedad final
obtenida después del proceso de liofilización, la cual es de suma importancia para identificar los cambios en el grano y la estabilidad que presenta el producto final. En la Tabla III se muestran los valores de la humedad final y los tiempos de secado de las dos botanas con una y dos capas de espesor y a tres temperaturas de calefacción (25, 35, 45 °C).
Al terminar el proceso de liofilización, las botanas presentaron contenidos de humedad entre 0.0212 y 0.1611 kg H2O/kg s.s., siendo la mayoría de estos valores inferiores a 0.1111 kg H2O/kg s.s. (10% en base húmeda). El espesor de la capa de granos de maíz sometidos a liofilización y la temperatura de calefacción en las placas del liofilizador, son
Tabla III. Tiempo requerido para la liofilización a y humedad al finalizar el proceso de secado
Temperatura de calefacción Espesor de capa
35 °C
45 °C
Tiempo (horas)
Botana ácidaBotana salada
Humedad (kg H2O/kg s.s.)
Tiempo (horas)
Humedad (kg H2O/kg s.s.)
115.830.028714.500.1611
25 °C a Tiempo al cual la variación del peso de la muestra fue menor a 0.002 kg
229.920.044929.920.073
111.920.02712.080.0712
223.750.056323.750.1180
110.000.065710.000.0315
219.000.095419.000.0212
factores determinantes en el tiempo de secado necesario para el proceso de liofilización.
3.1 Efecto del espesor de capa sobre la cinética de deshidratación
El espesor de la capa es de suma importancia ya que se limita la transferencia de masa en el alimento, aunque sea el mismo peso de granos de maíz en las charolas. El tiempo del proceso de secado del producto (Tabla III) se ve influenciado notablemente por la magnitud del espesor de la capa de granos de maíz. Los tiempos requeridos para la deshidratación botana salada a 25 °C son de 15.83 horas para una capa y 29.92 horas para dos capas; la botana ácida a la misma temperatura necesita 14.50 horas para una capa y 29.92 horas para dos capas.
Se observa que cuando el espesor es de una capa, el tiempo necesario para el secado es menor, que cuando el espesor es más grande (dos capas). Esto se debe a que la transferencia de masa del interior del grano de maíz al medio es más lenta, ya que los granos en la parte inferior están obstruidos por el material que se ubica en la parte superior y se dificulta la salida de agua. El efecto del número de capas sobre el proceso de deshidratación se observa claramente en la Fig. 3, ya que se encuentra que, independientemente de la temperatura, la humedad disminuye más rápido cuando se tiene una capa de maíz, que cuando se tienen dos.
3.2 Efecto de la temperatura de calentamiento sobre la cinética de deshidratación
El mayor tiempo de secado fue a 25°C para las botanas ácida y salada (29.92 horas). A 45°C se presentó el menor tiempo de secado, para las dos botanas, con 2 capas de espesor. El tiempo disminuyó entre 4 y 6 horas al aumentar 10 °C la temperatura de las placas. Por tanto, el tiempo de secado fue menor cuando la temperatura aumentó.
La elevación de la temperatura acelera el proceso de liofilización, ya que se alcanza más rápido la entalpía de cambio de fase y así el agua puede salir del alimento a mayor velocidad. Al utilizar placas calefactoras, los mecanismos de transferencia de calor involucrados son convectivo y conductivo, a diferencia de cuando no se utilizan placas, que sólo es convectivo. Por lo tanto, la transferencia de calor es mayor y ocurre principalmente a través de la capa congelada; en cambio, la transferencia de masa ocurre a través de la capa seca. En las curvas de deshidratación se observa, particularmente e el caso de la deshidratación de una capa de granos, que entre más alta es la temperatura menor es el tiempo requerido para alcanzar un valor de humedad determinado. Shishehgarha et al. (2002) mencionan que al liofilizar fresas incrementando la temperatura de las placas (hasta 40 °C), la humedad se pierde más rápido, por lo que los tiempos de proceso se
25 °C -una capa
35 °C -una capa
45 °C -una capa
25 °C -dos capas
35 °C -dos capas
45 °C -dos capas
W ( k g H 2 O/k g s.s. )
tiempo (h)
tiempo (h) (b)
05101520253035 W (kg agua/kg s.s.)
3. Cinética de deshidratación de la botana salada(a) y ácida (b)a tres temperaturas con una y dos capas de granosde maíz
reducen. A temperaturas más altas en las placas, la reducción del contenido de humedad residual debido al calentamiento fue menos importante.
3.3 Curvas de velocidad de secado
En la Fig. 4 se presentan las curvas de velocidad de secado en función de la humedad para las botanas ácidas con una (Fig. 4a) y dos (Fig. 4b) capas de espesor de granos. Estas curvas ayudan a conocer la rapidez con la que el alimento pierde agua. En las curvas de velocidad de secado generalmente se presentan
dos períodos: de velocidad constante y de velocidad decreciente. El período de velocidad constante no se observa comúnmente en las curvas de secado de alimentos. El período de velocidad decreciente ocurre cuando la velocidad de secado empieza a disminuir, además, la actividad de agua en la superficie del producto se hace menor a la unidad (Heldaman y Singh, 1981; Barbosa-Cánovas y Vega-Mercado, 1996). La cantidad de agua eliminada en este período puede ser baja, mientras que el tiempo requerido para llevar a cabo el proceso de secado puede ser elevado, ya que la velocidad de secado disminuye
(a)
(a)
dW/dt (b)
dW/dt
(Kg agua/Kg s.s.)
0.00.51.01.52.02.53.03.54.04.5
W (kg H2O/kg s.s.)
(Barbosa-Cánovas y Vega-Mercado, 1996; Márquez-Aquino, 2009).
En las curvas de velocidad de secado obtenidas en este estudio (Fig. 4), se observa que la velocidad inicial de secado es alta, ya que la resistencia de los flujos de masa y energía es pequeña. La transferencia de materia desde el frente de hielo se reduce a medida que el espesor de la capa seca aumenta (Babića et al., 2009). Esto se debe a la reducción de la difusión desde la interfaz de sublimación hacia la superficie del producto (Marques y Freire, 2005; Babića et al., 2009). Por lo tanto, la velocidad de secado es más lenta cuando el producto que se está deshidratando ya está más seco por el proceso. En la Fig. 4 también se observa la ausencia del período de velocidad constante y la
considerable reducción que causa el aumento del número de capas en la velocidad de secado, en contraste con el bajo efecto de la temperatura sobre dicha velocidad. Resultados similares fueron obtenidos en el caso de la botana salada.
Conclusión
La determinación de la cinética de deshidratación de botanas salada y ácida elaboradas con granos de maíz confirmó que el tiempo de liofilización depende el espesor de la capa de granos y de la temperatura de calefacción. El menor tiempo de liofilización requerido para obtener una humedad menor al 10 %, correspondió al proceso realizado a 45
°C y una capa de granos. Además, en las curvas de velocidad de secado sólo se observó el período de velocidad decreciente. La formulación de las botanas no influyó en la cinética de deshidratación. Los resultados obtenidos pueden servir de base para establecer las condiciones óptimas para la liofilización de este producto.
A.O.A.C. (Association of Oficial Analytical Chemists). 1984. Official Methods of Analysis. Décimo cuarta edición. A.O.A.C., Washington D.C., EE. UU.
Babića, J., Cantalejob, M. J., y Arroqui, C. 2009. The effects of freeze-drying process parameters on broiler chicken breast meat. Food Science and Technology. 42(8):1325-1334.
Barbosa-Cánovas, G. V. y Vega-Mercado, H. 1996. Dehydration of Foods. Chapman & Hall, Nueva York, EE. UU. 330 p.
Braverman, J. B. S. 1986. Introducción a la Bioquímica de los Alimentos. El Manual Moderno: 1980, México. 358 p.
Chin, S.T., Nazimah, S.A.H., Quek, S.Y., Che Man, Y.B., Abdul Rahman, R. y Mat Hashim, D. 2008. Changes of volatiles' attribute in durian pulp during freeze- and spray-drying process. Food Science and Technology. 41(10):1899-1905.
Claussen, C., Ustad, T. S., Strømmen, I. y Walde, P. M. 2007. Atmospheric freeze drying: a review. Drying Technology. 25(6):957-967.
FAO (Organización de las Naciones Unidas para la Agricultura y la Alimentación). 1993. El maíz en la nutrición humana. Colección FAO: Alimentación y nutrición. No. 25. Roma, Italia. http://www.fao.org/docrep/T0395S/T0395S00.htm, accesada 15/09/2009.
FAO (Organización de las Naciones Unidas para la Agricultura y la Alimentación). 2001. El maíz en los trópicos: mejoramiento y producción. Colección FAO: Producción y protección vegetal. No. 28. Roma, Italia. http://www.fao.org/DOCREP/003/X7650S/x7650s0 8.htm, accesada 12/10/2009
Gekas, V. 1992. Transport Phenomena of Foods and Biological Materials. Ed. CRC Press, Boca Raton, EE.UU. 237 p.
Grajales-Agudelo, L. M., Cardona-Perdomo, W. A. y Orrego-Alzate, C. E. 2005. Liofilización de carambola (Averrhoa carambola L.) osmodeshidratada. Ingeniería y Competitividad 7(2):19-26.
Heldman, D. R. y Singh, R. P. 1981. Food Process Engineering. Segunda edición. Avi Publishing Company, Inc., Westport Conneticut, EE. UU. 415 p.
Ibarz, A. y Barbosa-Cánovas, G. V. 1999. Operaciones Unitarias en la Ingeniería en Alimentos. Technomic Publication, EE. UU. 882 p.
Lewis, M. J. 1990. Physical Properties of Food and Food Processing Systems. Ellis Horwood, Chinchester; International Publishers in Science and Technology, EE. UU. 465 p.
Mallet, C.P. 1993. Frozen Food Technology. Blackie Academic and Professional, Londres, Inglaterra. 339 p.
Marques, L. G. y Freire, J. T. 2005. Analysis of freezedrying of tropical fruits. Drying Technology 23(9):2169-2184.
Márquez-Aquino, D. 2009. Desarrollo de productos de maíz (botanas) por medio de liofilización Universidad de las Américas, Puebla. Tesis de Licenciatura en Ingeniería de Alimentos. 107p.
Pérez-Pérez, E. P., Welti-Chanes, J., Vergara-Balderas, F. y Mejía-Garibay, B. 2007. Desarrollo de Tecnologías para la Elaboración de Maíz. Universidad de las Américas, Puebla. Informe inédito para proyecto Produce, folio: 21-2006-0317.
Rahman, S. 1995. Food Properties Handbook. Ed. CRC Press, Boca Ratón, EE. UU. 430 p.
Ratti, C. 2001. Hot air and freeze-drying of high-value foods: a review. Journal of Food Engineering 49(4):311-319.
Sadikoglu, H., Ozdemir, M. and Seker, M. 2006. Freeze-drying of pharmaceutical products: research and development needs. Drying Technology 24(7):849-861.
Shishehgarha, F., Makhlouf, J. y Ratti, C. 2002. Freezedrying characteristics of strawberry. Drying Technology. 20(1):131–145.
SIAP (Servicio de Información Agroalimentaria y Pesquera). 2007. Situación Actual y perspectivas del Maíz en México 1996-2012. SAGARPA, México. 208 p.
Tambunan, A. H., Yudistira, Kisdiyani y Hernani. 2001. Freeze drying characteristics of medicinal herbs. Drying Technology. 19(2):325-331.
Trelea, I. C., Passot, S., Fonseca, F. y Marin, M. 2007. An interactive tool for the optimization of freeze-
3 – 2 (2009): 39 - 50
drying cycles based on quality criteria. Drying Technology. 25(5):741-751.
Welti-Chanes J., Bermúdez D., Vergara-Balderas F. y Alzamora S.M. 2004. Principles of freezeconcentration and freeze-drying. En: Y. H. Hui, P. Cornillon, L. I. Guerrero, M. H. Lim, K. H. Murrel y W. K. Nip. Handbook of Frozen Foods. Ed. Marcel Dekker, Inc., New York, EE. UU. 13-25p.

Temas Selectos de Ingeniería de Alimentos 3 – 2 (2009): 51 – 58
Temas
Selectos de Ingeniería de Alimentos
Inactivación de esporas de Aspergilli con radiación UVC y sorbato de potasio en néctar de durazno
J.A. Del Campo-Sacre*, D.X. Flores-Cervantes, J.J. Gómez-Díaz, A. López-Malo Vigil, M.T. Jiménez-Munguía y E. Palou-García
Departamento de Ingeniería Química y Alimentos, Fundación Universidad de las Américas Puebla. Sta. Catarina Mártir, Cholula, Puebla. C.P.72820. México.
Resumen
Los procesos no térmicos están siendo estudiados para minimizar la degradación de la calidad de alimentos manteniendo su seguridad. La radiación ultravioleta de onda corta (UVC) se ha sugerido para el procesamiento de alimentos debido a su efecto letal sobre los microorganismos. El objetivo de este trabajo fue la determinación de la eficacia de la radiación UVC para la eliminación de esporas de Aspergillus niger o A. flavus en néctar de durazno, además del tratamiento del néctar con diferentes concentraciones de sorbato de potasio (SK). El efecto de la radiación UVC en las cuentas en placa de los mohos mostró una reducción logarítmica de 3 y 4 ciclos para A. niger y A. flavus, respectivamente, después de 60 minutos de tratamiento, cuando el néctar fue recirculado a 1.36 L/min. El método con sorbato de potasio como antimicrobiano produjo una reducción de más de 3 ciclos logarítmicos a altas concentraciones durante 7 días. Se hizo, también, la modelación con el método Weibull obteniéndose un buen ajuste.
Palabras clave: radiación UVC, sorbato de potasio, Aspergillus flavus, Aspergillus niger.
Abstract
Non-thermal processes are being studied in order to minimize quality degradation in foods while maintaining their safety. Short-wave ultraviolet light (UVC) for food processing has been suggested due to its lethal effect on microorganisms. The objective of the present study was to determine the efficacy of UVC irradiation to eliminate spores of Aspergillus niger or A. flavus in peach nectar and peach nectar with selected potassium sorbate (KS) concentrations. The effect of UVC on standard plate and inoculated mold counts resulted in a 3 and 4-log cycle reduction after a 60 min treatment when the nectar was circulated at 1.36 L/min. The method with KS as antimicrobial produced a reduction of more than 3 logarithmic cycles with high concentrations for 7 days. Weibull modelation was also approached with a good adjustment.
Keywords: UVC radiation, potassium sorbate, Aspergillus flavus, Aspergillus niger.
*Programa de Maestría en Ciencias de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: josea.delcampos@udlap.mx
Introducción
Actualmente, el consumidor está preocupado por contar con productos alimenticios que garanticen la inocuidad microbiana con amplia vida de almacenamiento, manteniendo las características y propiedades nutrimentales de un alimento fresco. La tendencia actual hacia lo mínimamente procesado ha llevado a que se investiguen nuevos procesos de conservación de alimentos, ya que los procesos térmicos que son regularmente utilizados provocan algunos efectos negativos en la calidad de los productos (López-Malo y Palou, 2005).
Dentro de los nuevos procesos estudiados se encuentran las llamadas tecnologías emergentes para el control microbiano, como la radiación ultravioleta de onda corta (UVC), de longitudes de onda entre 200 y 280 nm. La acción letal de la radiación UVC sobre microorganismos ha sido demostrada (López-Malo y Palou, 2005; Rahman, 2007) y, a diferencia de otras tecnologías, es segura, amigable con el medio ambiente y requiere de costos de instalación y operación más bajos que otros métodos. Sin embargo, por su poca profundidad de penetración, se usa generalmente para esterilizar aire y capas delgadas de líquido.
No obstante, desde 1999, la FDA (Food and Drug Administration) de los EE.UU. considera los tratamientos con radiación UVC como una alternativa para eliminar microorganismos patógenos de jugos de frutas, reteniendo sus niveles de vitaminas y llamando al producto “ligeramente procesado” (Food and Drug Administration, 2000). Como la radiación UVC es poco penetrante y los microorganismos deben ser expuestos directamente, aquéllos que estén protegidos por sólidos no serán afectados (LópezMalo y Palou, 2005); este tratamiento se ha usado para controlar el crecimiento de Bacillus stearothermophilus en capas delgadas de azúcar (Weiser, 1962), así como para tratar pescado fresco (Huang y Toledo, 1982), cascarón de huevo (Kuo et al., 1997), y carne (Reagan et al., 1973), entre otros productos. También se ha utilizado para desinfectar agua, asegurando el 99.999% de destrucción microbiana después de un minuto de tratamiento, sin cambiar el color, olor o pH (Snowball y Hornsey, 1988). Actualmente, existe
gran interés en utilizar radiación UVC para reducir la carga microbiana en jugos de frutas y verduras (Bintsis et al., 2000).
López-Malo et al. (2001b) utilizaron radiación UVC en jugo de zanahoria para disminuir la carga microbiana, observándose reducciones importantes con cambios mínimos en las características físicas y, además, sin efectos negativos en los atributos sensoriales. Wright et al. (2000) usaron un equipo de desinfección UVC de capa delgada para tratar sidra de manzana sin previa pasteurización e inoculada con Escherichia coli O157:H7; utilizando varios flujos (de 0.999 a 6.48 L/min) con 94 a 610 J/m2 y encontraron una reducción de 3.81 ciclos logarítmicos. Por otro lado, Farid et al. (2001) realizaron un tratamiento sobre una capa delgada de jugo de naranja cayendo sobre un sistema UV a 214.2 W/m2 y encontraron que el jugo aumentaba su vida de anaquel al doble, sin cambios en el color o sabor.
En jugos de frutas y bebidas, los sorbatos son utilizados normalmente en el periodo de preprocesado, junto con dióxido de azufre y pasteurización, para inhibir el deterioro químico, enzimático o microbiológico (Stopforth et al., 2004). Combinaciones de sorbatos con dióxido de azufre son utilizadas para la conservación de jugos de frutas con pulpa; en este caso, el sorbato actúa como inhibidor microbiológico, y el dióxido de azufre previene la oxidación y el deterioro enzimático (Lück, 1980). Así mismo, el sorbato de potasio y el benzoato de sodio fueron efectivamente utilizados para reducir las concentraciones de levaduras y mohos en jugo de tomate (Bizri y Wahem, 1994). Los sorbatos, en general, pueden ser más adecuados para los productos de frutas que otros conservadores por sus propiedades organolépticas suaves y su sabor neutral. Sin embargo, normalmente se usan los sorbatos en combinación con otros métodos en la conservación de jugos de frutas, inhibiendo el crecimiento de mohos (Stopforth et al., 2004).
Por otro lado, las especies de Aspergillus son contaminantes comunes de varios sustratos orgánicos, regularmente en regiones tropicales y subtropicales. El interés en el estudio de Aspergillus se debe a que ciertas especies son
patógenas y tienen la habilidad de producir metabolitos tóxicos (ácido 3-nitropropiónico, ácido ciclopiazónico y aflatoxinas B). Las aflatoxinas B son la forma más activa de las aflatoxinas (producto de A. flavus) que provocan necrosis hepática, coagulopatía, hemorragias, cáncer y hasta la muerte en humanos, por lo que se debe controlar su nivel en los alimentos para evitar los efectos de la aflatoxicosis (Hayes, 1981; Pier y Richard, 1992). Además, A. niger sintetiza ácidos orgánicos que disminuyen el pH del alimento produciendo sabores y olores indeseables, así como ennegrecimiento en frutas. Conjuntamente, en altas concentraciones, provoca aspergillosis, enfermedad que causa alteraciones pulmonares (MedlinePlus Medical Encyclopedia, 2006).
La importancia de este trabajo se centra en estudiar la eficacia del tratamiento con radiación UVC o con sorbato de potasio para inactivar esporas de A. flavus y A. niger en néctar de durazno.
L/min. El néctar pasa a un vaso de doble pared conectado a un baño termostático (1268-24, Polystat, México) que mantiene la temperatura a 25 ± 1 °C. El volumen total de néctar recirculado es 2.5 L por corrida (1 L por lámpara y 500 mL en el vaso de doble pared y mangueras). Se obtuvieron alícuotas de 1 mL a los 0, 1, 2, 3, 4, 5, 10, 15, 20, 25, 30, 40 y 60 minutos de tratamiento con radiación UVC, las cuales fueron usadas para realizar el análisis microbiológico.
2. Tratamiento con sorbato de potasio (SK)
Frascos previamente esterilizados fueron llenados con 100 mL de néctar, el cual contenía una carga inicial de A. flavus o A. niger de 104 esporas/mL (determinado experimentalmente al tiempo cero) y se les añadió sorbato de potasio en una concentración determinada (0, 250, 500, 1000, 1500 ó 2000 ppm). Se tomaron alícuotas de 1mL de cada sistema cada 24 horas durante 7 días para su siembra y el conteo de esporas subsecuente.
3. Siembra, conteo de esporas y modelación
Materiales y métodos
Se utilizó néctar de durazno pasteurizado con pH de 3.18 ± 0.01, acidez titulable de 0.65 ± 0.06% (ácido málico), 13.40 ± 0.59 °Bx y valores de reflectancia (color) de 27.95 ± 0.04 para L, -0.60 ± 0.06 para a y 16.11 ± 0.03 para b. Cada muestra de néctar de durazno tuvo una carga inicial del orden de 104 esporas/mL (determinado experimentalmente al tiempo cero). Todos los tratamientos fueron realizados por duplicado.
El sistema para dar el tratamiento con radiación UVC consiste de dos lámparas UVC de 1.5 cm de diámetro y 82 cm de largo (40 W, 254 nm, baja presión; G37T6VH, Light Sources, EE.UU.) cada una, protegidas por un cilindro de cuarzo de 2.5 cm de diámetro, que a su vez están localizadas dentro de un tubo de acero inoxidable de 7.5 cm de diámetro. El néctar fluye en el ánulo entre el tubo de acero y el cilindro de cuarzo impulsado por una bomba peristáltica (7553-71, MasterFlex, EE.UU.), manteniendo un flujo constante de 1.36
Las muestras de cada tratamiento fueron sembradas por medio del método de siembra por extensión en superficie, por duplicado y en cajas Petri con agar Dicloran Rosa de Bengala Cloranfenicol DRBC (Becton Dickinson DIFCO, EE.UU.), para después incubarlas a una temperatura de 25°C y hacer el conteo de las esporas después de 5 a 7 días. Se determinaron las curvas de inactivación (log N/No contra tiempo de tratamiento) de cada uno de los microorganismos estudiados con cada tratamiento y se escogieron las que mostraron la pendiente negativa, ya que es un parámetro esencial para la modelación. Se realizó el modelado matemático de estas curvas de inactivación utilizando la ecuación de Weibull y ajustando los datos de cada curva a la forma acumulativa de la distribución de resistencias de Weibull, cuyo modelo es:
log S(t) = - b tn (Ec. 1)
Donde S(t) = N / N0 ; N: población al tiempo t; N0: población inicial; b y n son constantes (Peleg y Cole, 1998). Se determinaron los valores de b y n utilizando KaleidaGraph (3.52, Sinergy Software, EE.UU) con el valor de Chi cuadrada.
4. Comparación de tratamientos y propuesta
A partir de las curvas de inactivación y la modelación, se hicieron comparaciones entre los tratamientos con UVC y con sorbato de potasio. Utilizando las predicciones del modelo que arroje la máxima reducción de esporas, se determinaron las mejores condiciones para el tratamiento de néctar de durazno (Del Campo-Sacre, 2009).
Resultados y discusión
1. Tratamiento con UVC
Se obtuvieron las curvas de inactivación de ambos microorganismos (Fig. 1). Se observó una
reducción de 3.02 ciclos logarítmicos para A. niger y 4.09 ciclos logarítmicos para A. flavus después de 60 minutos de tratamiento. Es importante destacar que A. niger mostró mayor resistencia al tratamiento, ya que presentó una menor reducción de ciclos logarítmicos. Sin embargo, la inactivación fue efectiva para ambos mohos, ya que se observó una reducción importante de los microorganismos. La reducción fue menor a la obtenida por López-Malo et al. (2001a) para inactivar la flora nativa de jugo de zanahoria, la cual fue de cinco ciclos logarítmicos después de 30 minutos de tratamiento con UVC con un sistema vertical. Guerrero-Beltrán y BarbosaCánovas (2005) obtuvieron una reducción de 1.34 ± 0.354 ciclos logarítmicos para Saccharomyces cerevisiae, valor menor a los obtenidos en el presente trabajo; sin embargo, también obtuvieron valores mayores, de 4.29 ± 2.34 y 5.10 ± 1.12 ciclos logarítmicos para Listeria innocua y Escherichia coli, respectivamente, en jugo de manzana (con flujo de 548 mL/min).
2.
Para evaluar la acción antimicrobiana del sorbato de potasio se hicieron tomas de alícuotas de 1 mL de la muestra inoculada y con antimicrobiano, durante 7 días. A. niger presentó una reducción microbiana de 3.3 ciclos logarítmicos con 2000 ppm de antimicrobiano después de dos días y hasta el final del periodo de evaluación (Fig. 2). A una concentración de 1000 ppm de sorbato de potasio, el valor máximo de este atimicrobiano aceptado
para jugos y néctares de frutas en México (Secretaría de Salud, 1994), se observó una reducción de 1.3 ciclos logarítmicos después de siete días de almacenamiento. Las reducciones microbianas observadas a concentraciones de 500 y 250 ppm fueron menores.
Por otro lado, para las esporas de A. flavus con 1500 y 2000 ppm del antimicrobiano, se obtuvo la reducción de 3.1 ciclos logarítmicos en los primeros días de evaluación (Fig. 3). Sin embargo,
01234567
tiempo (días)
01234567
tiempo (días)
con 1000 ppm se logró la misma reducción, después de 4 días de tratamiento. Igual que en el caso de A. niger, la reducción microbiana causada por la adición de 250 y 500 ppm de SK sobre el crecimiento de A. flavus fue muy baja.
Las curvas que mostraron mejor inactivación y pendientes negativas, tanto para A. niger como para A. flavus, fueron las correspondientes a los tratamientos con radiación UVC. Por tanto, dichas
curvas fueron utilizadas al aplicar el modelo de Weibull.
La Tabla 1 muestra los parámetros determinados con el modelo de Weibull (b y n) para cada curva que haya presentado tendencia negativa. Entre más pequeño sea el valor de Chi cuadrada (Chisq) hay mejor aproximación de la predicción a la curva experimental, lo que se puede apreciar en la Fig. 4. Por lo que se puede mencionar que hubo una buena aproximación del modelo a los datos experimentales.
Tabla I. Parámetros del modelo Weibull para el tratamiento con radiación ultravioleta de onda corta (254 nm) aplicado a néctar de durazno inoculado con A. niger y A. flavus
A. niger
A. flavus
b 6.17x10-3 ± 3.1x10-3 6.75x10-5 ± 9.53x10-5
n 1.50 ± 0.129
2.56 ± 0.35
Chisq 0.286 0.339
R 0.983 0.966
Chisq : Chi cuadrada; R : Coeficiente de correlación
(a)
0204060 log N/No tiempo (min)
(b)
0204060 log N/No tiempo (min) (b)
Fig. 4. ModelaciónWeibull del tratamiento con radiación ultravioleta de onda corta (254 nm) para a) A. niger y b) A. flavus (Resultados experimentales; __ Resultados predichos por el modelo)
Para A. flavus, el tratamiento con radiación UVC durante 60 minutos mostró mayores reducciones logarítmicas que aquel con sorbato de potasio a cualquiera de las concentraciones probadas. En el caso de A. niger, sólo la adición de 2000 ppm de sorbato de potasio dio lugar a una reducción similar a la lograda al tratar el néctar con radiación UVC durante 60 min. Por esta razón, se propone el uso de radiación UVC durante 60 minutos para la inactivación de estos microorganismos en néctar de durazno.
Asesoría de Estudiantes de Nivel Licenciatura. También agradecen el financiamiento de Fundación Produce Puebla para el proyecto "Tecnologías para el Procesamiento de Durazno".
Conclusión
El tratamiento con radiación UVC mostró reducciones logarítmicas altas de ambos mohos. Las esporas de A. niger mostraron mayor resistencia que las de A. flavus.
La radiación UVC se puede utilizar como método no térmico para inactivar las esporas de A. niger y A. flavus; sin embargo, se requiere el estudio con otros microorganismos y a diferentes condiciones para obtener productos seguros.
El tratamiento con sorbato de potasio obtuvo reducciones logarítmicas altas a concentraciones mayores a la aceptada por las normas de México para jugos y néctares de frutas.
A partir de lo observado, se propone el posterior estudio del tratamiento combinando radiación UVC y sorbato de potasio, dejando actuar el compuesto antimicrobiano durante mínimo cuatro días, para poder estudiar su efecto sobre los microorganismos.
Referencias
Bintsis, J.R., Litopoulou-Tzanetaki, E. y Robinson, R. 2000. Existing and potential applications of ultraviolet light in the food industry: a critical review. Journal of the Science of Food and Agriculture. 80:637-645.
Bizri, J.N. y Wahem, I.A. 1994. Citric acid and antimicrobials affect microbiological stability and quality of tomato juice. Journal of Food Science. 59:130-134.
Del Campo-Sacre, J.A. 2009. Inactivación de esporas de Aspergilli mediante la combinación de radiación ultravioleta de onda corta y agentes antimicrobianos en néctar de durazno. Tesis de licenciatura. Universidad de las Américas Puebla.
Farid, M.M., Chen, X.C. y Dost, Z. 2001. Ultraviolet sterilization of orange juice. En J. Welti-Chanes, G.V. Barbosa-Cánovas y J.M. Aguilera (Eds). Proceedings of the eighth international congress of engineering and food. Technomic Publishing Co., Inc. Lancaster. pp. 1567-1572.
Food and Drug Administration. 2000. FDA approves the use of ultraviolet radiation for juice. Food safety initiative. Center for food safety and applied nutrition. http://www.cfsan.fda.gov/~comm/iftuv.html, accesada 02/05/2009.
Guerrero-Beltrán, J.A. y Barbosa-Cánovas, G.V. 2005. Reduction of Saccharomyces cerevisiae, Escherichia coli and Listeria innocua in apple juice by ultraviolet light. Journal of Food Process Engineering. 28:437-452.
Hayes, A.W. 1981. Mycotoxin teratogenicity and mutagenicity. En: J.W. Bennet y M.A. Klich (Eds). Aspergillus: Biology and industrial applications Butterworth-Heinemann. Stoneham. pp. 241-243.
Agradecimientos
Los autores agradecen el financiamiento del proyecto al Consejo Nacional de Ciencia y Tecnología (CONACyT), como parte del Apoyo para Investigadores Nacionales para el Fortalecimiento de Actividades de Tutoría y
Huang, Y.W. y Toledo, R. 1982. Effect of high and low intensity UV irradiation on surface microbiological counts and storage-life of fish. Journal of Food Science. 47:1667-1669, 1731.
Kuo, F.L., Carey, J.B. y Ricke, S.C. 1997. UV irradiation of shell eggs: effect on populations of
J.A. Del Campo et al. / Temas Selectos de Ingeniería de Alimentos 3 – 2 (2009): 51 - 58
aerobes, moulds, and inoculated Salmonella typhimurium. Journal of Food Protection. 60:639643.
López-Malo, A. y Palou, E. 2005. Ultraviolet light and food preservation. En: G.V. Barbosa-Cánovas, M.S. Tapia y P. Cano (Eds). Novel Food Processing Technologies. Marcel Dekker, Inc. New York. pp. 405-421.
López-Malo, A., Medrano, A. y Palou, E. 2001a. Shortwave ultraviolet irradiation effects on red beet juice. Tercer Congreso Iberoamericano de Ingeniería de Alimentos (CIBIA III). Valencia, España. Marzo.
López-Malo, A., Palou, E., Arce-García, M.R., Beristain, L., Bermudez-Aguirre, D. y Gómez-Diaz, J.J. 2001b. Short-wave ultraviolet light irradiation effects on carrot juice. Institute of Food Technologists Annual Meeting. New Orleans, EE.UU. Junio.
Lück, E. 1980. Antimicrobial food additives: characteristics, uses, effects. En: P.M. Davidson, J.N. Sofos y A.L. Branen (Eds). Antimicrobials in Food. CRC Taylor and Francis Group. Boca Ratón, EE.UU. pp. 49-90.
MedlinePlus Medical Encyclopedia. 2006. Aspergillosis. U.S. National Library of Medicine and the National Institutes of Health. http://www.nlm.nih.gov/medlineplus/encyclopedia. html, accesada 13/02/2009.
Peleg, M. y Cole, M.B. 1998. Reinterpretation of microbial survival curves. Critical Reviews in Food Science. 38(5):353-380.
Pier, A.C. y Richard, J.L. 1992. Mycoses and mycotoxicoses of animals caused by Aspergilli. En
J.W. Bennet y M.A. Klich (Eds). Aspergillus: Biology and Industrial Applications. ButterworthHeinemann. Stoneham, EE.UU. pp. 241-243.
Rahman, S. 2007. Handbook of food preservation. CRC Press. Boca Raton. Fla. EE.UU.
Reagan, J.O., Smith, C.G. y Carpenter, Z.L. 1973. Use of ultraviolet light for extending the retail caselife of beef. Journal of Food Science. 38:929-931.
Snowball, M.R. y Hornsey, I.S. 1988. Purification of water supplies using ultra-violet light. En R.K. Robinson (Ed) Developments in Food Microbiology-3. Elsevier Applied Science. Londres, Inglaterra. pp. 171-192.
Secretaría de Salud. 1994. Norma Oficial Mexicana NOM-086-SSA1-1994, Bienes y servicios. Alimentos y bebidas no alcohólicas con modificaciones en su composición. Especificaciones nutrimentales. SSA. México.
Stopforth, J.D., Sofos, J.N. y Busta F.F. 2004. Sorbic acid and sorbates. En: P.M. Davidson, J.N. Sofos y A.L. Branen (Eds). Antimicrobials in Food. CRC Taylor and Francis Group. Boca Ratón, EE.UU. pp. 49-90.
Weiser, H.H. 1962. Practical food microbiology and technology. AVI Publishing. Westport, EE.UU.
Wright, J.R., Summer, S.S., Hackney, C.R., Pierson, M.D. y Zoecklein, B.W. 2000. Efficacy of ultraviolet light for reducing Escherichia coli O157:H7 in unpasteurized apple cider. Journal of Food Protection. 63(5):563-567.

Temas Selectos de Ingeniería de Alimentos 3 – 2 (2009): 59 – 66
Temas Selectos de Ingeniería de Alimentos
Inactivación de dos levaduras por medio de radiación ultravioleta de onda corta en combinación con reducción de actividad de agua
T. Hernández-Grajales*, E. Palou-García, A. López-Malo
Departamento de Ingeniería Química y Alimentos, Fundación Universidad de las Américas Puebla. Sta. Catarina Mártir, Cholula, Puebla. C.P. 72820. México
Resumen
El objetivo principal de esta investigación fue evaluar el efecto de la radiación ultravioleta de onda corta (UVC) sobre las levaduras Saccharomyces cerevisiae y Zygosaccharomyces bailii suspendidas en sistemas modelo con diferentes actividades de agua (aw) (0.99, 0.97, 0.95). Durante el tratamiento con radiación UVC, que se llevó a cabo a tres distancias distintas entre la muestra y la lámpara (1, 5, 10 cm), se evaluó la cinética de inactivación de las levaduras para llevar a cabo una comparación entre el comportamiento de cada una de éstas. Se observó que el tiempo requerido para disminuir la población de las levaduras por debajo del nivel de detección (< 10 UFC/ml) varía dependiendo de la aw y de la distancia de la muestra a la lámpara UVC, el sistema modelo con aw de 0.95, a 1 cm de distancia de la lámpara UVC, el más efectivo.
Palabras clave: radiación ultravioleta de onda corta, S. cerevisiae, Z. bailii, actividad de agua, sistema modelo.
Abstract
The main objective of this research was to evaluate the effect of short-wave ultraviolet (UVC) on yeasts of Saccharomyces cerevisiae and Zygosaccharomyces bailii suspended in model systems with different water activities (wa) (0.99, 0.97, 0.95). During treatment with UVC radiation, which was conducted at three different distances between the sample and the lamp (1, 5, 10 cm), the kinetics of inactivation of yeasts were assessed to carry out a comparison between the behavior of each of them. It was noted that the time required to reduce the yeasts population below the detection level varies depending on the wa and the distance of the sample to the UVC lamp, requiring the least time to achieve total inactivation with the model system with wa of 0.95, at a distance of 1 cm between the sample and the UVC lamp.
Key words: UV radiation, S. cerevisiae, Z. bailii, water activity, model system.
*Programa de Maestría en Ciencias de Alimentos
Tel.: +52 222 229 2126, fax: +52 222 229 2727
Dirección electrónica: teresac.hernandezgs@udlap.mx
Introducción
En la actualidad, la aplicación de tratamientos térmicos y el almacenamiento a bajas temperaturas son los métodos de conservación de alimentos más comúnmente utilizados. Los procesos emergentes, que utilizan métodos físicos de destrucción microbiana y/o enzimática, aplicados a la conservación de alimentos sin los efectos colaterales de los tratamientos con calor, están siendo intensamente evaluados (López-Malo y Palou, 2004; López-Malo et al., 2001; 2003). Además, se busca el uso simultáneo de diferentes métodos para disminuir la intensidad de los tratamientos.
Algunas tecnologías emergentes como la aplicación de altas presiones, pulsos eléctricos, pulsos magnéticos, ultrasonido de baja frecuencia y luz ultravioleta, se están estudiando como sustitutos de los tratamientos térmicos (Alzamora et al., 2005; López-Malo y Palou, 2004); no obstante, la mayoría de éstas se encuentran todavía en estudio y su aplicación a alimentos industrialmente es, en muchos casos, aún incierta.
Dentro de los llamados procedimientos emergentes, se encuentra la irradiación de alimentos con radiación ultravioleta de onda corta (UVC); la cual ha sido reportada como un método efectivo para inactivar bacterias que contaminan agua y superficies de diversos materiales. A pesar de esto, la respuesta microbiana en alimentos a esta tecnología emergente está siendo recientemente investigada, por lo que el conocimiento del comportamiento de ciertos microorganismos que crecen en alimentos bajo el efecto de la radiación UVC ayudaría a implementar esta tecnología en la industria alimenticia.
La reducción de actividad de agua (aw) en los alimentos también ha resultado ser una herramienta bastante efectiva para evitar y
reducir el crecimiento de microorganismos en éstos.
La combinación de factores o métodos combinados para la conservación de alimentos también está siendo evaluada. Se basa en inhibir el crecimiento microbiano o inactivar a los microorganismos inicialmente presentes, y en retardar o evitar las reacciones deteriorativas de alimentos, combinando los efectos de varios factores de preservación (Alzamora y López-Malo, 2002), los cuales, al utilizarse por sí solos como métodos de conservación, necesitan ser aplicados a niveles extremos causando, generalmente, una alteración de las características físicas, químicas y sensoriales del alimento. Los nuevos factores de conservación aplicados en combinación requieren de estudios serios y profundos sobre los efectos benéficos que tengan en los alimentos.
Por otro lado, las levaduras están involucradas en el deterioro de varios alimentos, particularmente aquellos que contienen altos niveles de azúcar (Banwart, 1981).
Por lo expuesto anteriormente, se consideró de gran importancia evaluar el efecto de la radiación UVC sobre las levaduras Saccharomyces cerevisiae y Zygosaccharomyces bailii, suspendidas en sistemas modelo con diferentes aw
1. Obtención de microorganismos y preparación del inóculo
Se obtuvieron de la colección del Laboratorio de Alimentos de la Universidad de las Américas Puebla, cepas de las levaduras S. cerevisiae y Z. bailii. Las cepas se mantuvieron en cuñas de agar papa-dextrosa
(PDA) y se resembraron periódicamente (López-Malo, 1995). Para la preparación del inóculo, las levaduras se hicieron crecer en caldo maltosa Sabouraud (Merck, Darmstadt, Alemania) esterilizado a 121°C.
2. Preparación de los sistemas modelo
Se prepararon 100 ml de los sistemas modelo utilizando como base caldo maltosa Saboraud (Merck, Darmastadt, Alemania). Para tener sistemas modelo con aw de 0.95 y 0.97 se ajustó el medio de cultivo utilizando como soluto una determinada cantidad de sacarosa comercial, de acuerdo a la ecuación de Norrish (1966). Para el correspondiente a aw de 0.99 no se agregó ningún soluto al medio de cultivo. Los sistemas modelo se esterilizaron a 121°C y posteriormente se dejaron enfriar. Ya enfriados, los sistemas modelo se inocularon con cada una de las dos levaduras por separado, tomando dos asadas de las cuñas correspondientes a cada microorganismo.
3.
Se empleó una lámpara de radiación UVC (Germicidal Lamp G15T8 Sankyo Denki, Japan) de baja presión cuya longitud de onda mayoritaria es de 254 nm y cuya potencia inicial se reporta de 15 W. Se vertieron 10 ml de cada sistema modelo con su respectiva aw y conteniendo el inóculo en cajas petri, siendo esta cantidad equivalente a un espesor de 4 mm del sistema. Se determinó una población inicial de 107 UFC/ml, aproximadamente. Después se trató por medio de la radiación UVC colocando las cajas a distintas distancias de la lámpara (1, 5 y 10 cm). El tratamiento se llevó a cabo durante siete tiempos diferentes; de 0 a 30 minutos en intervalos de 5 minutos, correspondiendo al control el sistema modelo con un tratamiento de cero minutos. Lo anterior se realizó por triplicado.
Se tomó una muestra de 1 ml de cada uno de los sistemas modelo tratados, así como del control, y se sembró en agar papa-dextrosa (PDA). Las cajas petri se incubaron a 36 °C durante 48 horas (López-Malo, 1995). Después se realizó el conteo en placa.
5. Análisis del comportamiento microbiano
Con los datos obtenidos del conteo microbiano se obtuvieron gráficas de supervivencia, en cuyo eje de ordenadas se representa el logaritmo decimal de la cantidad de microorganismos presentes al tiempo t de tratamiento sobre la cantidad inical de microorganismos (log (N/N0)) y en el eje de abscisas el tiempo de tratamiento. Finalmente se realizó una comparación entre el comportamiento de cada una de las levaduras bajo el efecto de la radiación UVC.
y discusión
1. Efecto de la radiación UVC en S. cerevisae
En cada sistema modelo se observó una disminución de la población microbiana de entre seis y siete ciclos logarítmicos, como consecuencia del tratamiento aplicado. Como ejemplo se presenta la disminución de la población de S. cerevisiae correspondiente al tratamiento del sistema modelo con aw de 0.95, a las tres distancias de la lámpara de UVC (Fig. 1).
Se observó que en todos los casos se logra reducir la población de la levadura por debajo del nivel de detección (<10 UFC/ml). El tratamiento llevado a cabo con los demás sistemas modelo (aw = 0.97, 0.99) también fue efectivo, presentándose un comportamiento en
las curvas similar al que se representa en la Fig. 1. El tiempo requerido para lograr dicha reducción en la población microbiana disminuyó conforme la distancia y la aw disminuyeron. Los ciclos logarítmicos que se lograron reducir y el tiempo que se requirió para obtener una población microbiana menor a 10 UFC/ml en cada caso pueden observarse en la Tabla I.
El efecto de la radiación UVC es mayor mientras más cerca se encuentra la muestra a la lámpara UVC, lo que concuerda con lo observado por Sommer et al. (1996), quienes mencionan que la intensidad de la radiación
Fig. 1. Inactivación de S. cerevisiae en un sistema modelo con aw de 0.95 a las tres distancias de la lámpara UVC en función del tiempo de tratamiento. aw Dist (cm) a Ciclos log b Tiempo (min) c 0.99106.9125
UVC es mayor cuando la lámpara se encuentra a una menor distancia de la muestra a tratar; la reducción en la aw también influye en la disminución de la población microbiana, ya que al inducir a un microorganismo a un factor de estrés, como lo es la aw, se debilita su estructura haciéndolo más vulnerable a otro tratamiento de inactivación microbiana (Vermeulen et al., 2008), como en esta investigación fue la radiación UVC. Debido a lo anterior, el menor tiempo de tratamiento se obtuvo con el sistema modelo con aw de 0.95 a 1 cm de distancia de la lámpara UVC.
Se han realizado diferentes investigaciones en las últimas décadas sobre el efecto de la radiación UVC en varios microorganismos (Harris et al., 1987). Algunas de estas investigaciones se han centrado en analizar el efecto que la radiación tiene sobre las levaduras, principalmente sobre S. cerevisiae. Sommer et al. (1996) trataron medios líquidos conteniendo a S. cerevisiae, logrando una reducción de cuatro ciclos logarítmicos de la población al aplicar radiación UVC. Sin embargo, la reducción microbiana obtenida
Tabla I. Ciclos logarítmicos reducidos de la población de S. cerevisiae en cada uno de los sistemas modelo y tiempo requerido para reducir la población microbiana por debajo del nivel de detección.
a Distancia de la muestra a la lámpara UVC
b Ciclos logarítmicos reducidos
c Tiempo requerido para reducir la población microbiana por debajo del nivel de detección (< 10 UFC/ml)
en el presente trabajo de investigación fue mayor, probablemente debido a la combinación de la radiación UVC con la reducción de aw. Además, los resultados obtenidos en una investigación realizada por Vladislav et al. (2001), en la que se observa una importante inactivación de S. cerevisiae, coinciden en que dicha inactivación se favorece al combinar la radiación UVC con un tratamiento térmico; ya que la radiación UVC tiene un mayor efecto cuando existe algún otro tipo de factor de estrés al que se somete a la levadura, como la reducción de aw
Otro estudio (Legan, 1980) reporta reducciones de 7.3 ciclos logarítmicos para S. cerevisiae al tratar aire mediante radiación UVC conteniendo a esta levadura. Por lo que dicha radiación es un método efectivo para reducir la población microbiana. De acuerdo a Groocock (1984), mientras más translúcido sea un fluido, mayor será la penetración de la radiación UVC. Sin embargo, en este estudio las reducciones microbianas más importantes alcanzaron 7 ciclos logarítmicos a pesar de tratarse de un fluido menos claro que el aire.
2. Efecto de la radiación UVC en Z. bailii
El tratamiento llevado a cabo para inactivar a la levadura Z. bailii también fue efectivo, ya que se observó una población microbiana menor a 10 UFC/ml en cada uno de los sistemas modelo con las diferentes distancias estudiadas de la muestra a la lámpara (UVC). En la Fig. 2 se presenta la disminución de la población de Z. bailii correspondiente al tratamiento del sistema modelo con aw de 0.97, a las tres distancias evaluadas.
Mediante el tratamiento con radiación UVC se logró una reducción microbiana de aproximadamente siete ciclos logarítmicos. La reducción de la población microbiana por debajo del nivel de detección se obtuvo a los diez minutos en el caso de la menor
Tiempo (min)
Fig. 2. Inactivación de Z.bailii en un sistema modelo con aw de 0.97 a las tres distancias de la lámpara UVC en función del tiempo de tratamiento.
distancia (1cm) y a los quince minutos con las otras dos distancias (5 y 10 cm). Un comportamiento de las curvas similar se tiene para el tratamiento de los demás sistemas modelo. El tiempo que se requiere para lograr la inactivación total y los ciclos logarítmicos que se reducen en cada caso se muestran en la Tabla II.
La respuesta de esta levadura fue similar a la de la anterior, ya que con cada tratamiento se observó una población menor a 10 UFC/ml de Z. bailii, y el tiempo se modificó dependiendo de la distancia y de la aw del sistema modelo. Se requirió un menor tiempo para lograr la reducción mencionada conforme se disminuyó la aw y la distancia del sistema modelo a la lámpara UVC. Las condiciones con las que se obtuvo el menor tiempo de tratamiento fueron la distancia de 1 cm de la muestra a la lámpara UVC y la aw de 0.95.
El hecho de que se logre reducir la población de Z. bailii por debajo del nivel de detección indica que la radiación UVC es un método efectivo para inactivar levaduras, debido a que en diferentes investigaciones se ha reportado a Z. bailii como una levadura resistente a varios tratamientos (Martorell et al., 2007), ya que puede crecer a altas temperaturas y a altas concentraciones de azúcar, lo que dificulta el control de su crecimiento (Vermeulen et al., 2008). Por lo
Tabla II. Ciclos logarítmicos reducidos de la población de Z.bailii en cada uno de los sistemas modelo y tiempo requerido para reducir la población microbiana por debajo del nivel de detección.
aw Dist (cm) a Ciclos log b Tiempo (min) c 0.99106.9930 57.7120 17.7010
0.97107.9715
57.8315 16.8910 0.95106.9515 56.9210 16.885
a Distancia de la muestra a la lámpara UVC
b Ciclos logarítmicos reducidos
c Tiempo requerido para reducir la población microbiana por debajo del nivel de detección (< 10 UFC/ml)
anterior, podría proponerse como un método de conservación de alimentos.
3. Estudio comparativo entre las levaduras
Con el fin de comparar la cinética de inactivación entre las dos levaduras, S. cerevisiae y Z. bailli, se obtuvieron sus respectivas curvas de inactivación bajo las mismas condiciones, tanto de aw como de distancia a la lámpara de UVC.
En la Fig. 3 se muestra la inactivación de las levaduras con una aw de 0.99 y a 1 cm de distancia de la lámpara.
El tratamiento de radiación UVC fue efectivo, ya que se logró reducir la población de ambas levaduras por debajo del nivel de detección; sin embargo, para Z. bailli se requiere un tiempo de exposición a la radiación UVC mayor (10 min) que para S. cerevisiae (5 min). En tres casos de los nueve tipos de tratamientos diferentes se requirió el mismo tiempo para reducir la población microbiana por debajo del nivel de detección; en dos casos el tiempo de tratamiento requerido para lograr esa reducción fue menor al tratarse de la levadura S. cerevisiae, mientras que en cuatro casos se requirió un mayor tiempo de tratamiento al tratarse de la
levadura Z. bailii. Debido a que el número de casos en los que el tiempo requerido para reducir la población de la levadura Z. bailii por debajo del nivel de detección fue mayor, dicha levadura podría considerarse como la más resistente de las dos estudiadas, al tratamiento UVC. Existe poca información sobre el tratamiento de Z. bailli con radiación UVC. Sin embargo, Martorell et al. (2007) concluyen que Z. bailii es la levadura más resistente de entre cinco tipos evaluados utilizando distintos antimicrobianos. Por otro lado, Nielsen y Arneborg (2007) concluyeron que la resistencia de la levadura Z. bailii es mayor a la de S. cerevisiae al evaluar diferentes niveles de pH y diferentes tipos de antimicrobianos.
(min)
3. Inactivación de dos levaduras con una aw de 0.99 y a 1 cm de distancia de la lámpara UVC.
Conclusión
La combinación de la radiación ultravioleta de onda corta con la reducción de la aw es un método de desinfección efectivo, ya que en todos los casos se logró reducir la población microbiana por debajo del nivel de detección (<10 UFC/ml). Las reducciones máximas alcanzadas fueron de 7 ciclos logarítmicos. En general la levadura más resistente al tratamiento fue Z. bailii. La efectividad del tratamiento de radiación UVC se aumenta en función de la reducción de la distancia entre la muestra y la lámpara y la disminución de la aw. La aw es un tipo de factor de estrés que favorece la disminución en la población microbiana al combinarse con la radiación UVC.
La combinación de dos técnicas de conservación redujo el tiempo de exposición de los sistemas modelo al tratamiento por lo que podría proponerse su aplicación en la industria alimenticia.
Harris, G. D., Adams, V. D., Sorenson, D. L., y Curtis, M. S. 1987. Ultraviolet inactivation of selected bacteria and viruses with photoreactivation of the bacteria. Water Res. 21:687–692.
Legan, R.W. 1980. UV disinfection chambers. Water and Sewage Works. 1:56-61.
López-Malo, A. 1995. Efecto de diversos factores sobre la capacidad antimicótica de vainillina. Tesis de Maestría Universidad de las Américas-Puebla. México.
López-Malo, A., Palou, E., Arce-García, M.R., Beristain, L., Bermúdez-Aguirre, D. y Gómez-Díaz, J.J. 2001. Short-wave ultraviolet light irradiation effects on carrot juice. 2001 Institute of Food Technologists Annual Meeting. New Orleans, LA. EE. UU.
López-Malo, A., Medrano, A. y Palou, E. 2003. Efectos de la radiación ultravioleta de onda corta en jugo de betabel. En: Fito, P., Mulet, A., Chiralt, A. y A. Andrés (Eds.). Ingeniería de Alimentos: Nuevas Fronteras en el Siglo XXI. Tomo III: Ingeniería de Operaciones y Procesos. Universidad Politécnica de Valencia, España. pp 477-482.
López-Malo, A. y Palou, E. 2004. Ultraviolet light and food preservation. En: Cano, MP y Tapia, MS (Eds.). Emerging Technologies for the Food Industry. Marcel Dekker, Inc., New York, EE.UU. pp 405-421.
Referencias
Alzamora, S.M y López-Malo, A. 2002. Microbial behavior modeling as a tool in the design and control of processed foods. En: Welti-Chanes, J., Barbosa-Cánovas, G. y Aguilera, J. M. (Eds.). Engineering and Food for the 21st Century. CRC Press. EE.UU. pp 631-650.
Alzamora, S.M., Guerrero, S.N., Lopez-Malo, A., Welti-Chanes, J., Tapia, M.S., Palou, E. y Argaiz A. 2005. Combined Preservation Techniques for Fresh Fruit and Vegetables. En: Jongen, W. (Ed.). Improving the Safety of Fresh Fruit and Vegetables. Woodhead Publishing, Ltd., UK. pp 437-454.
Banwart, G.J. 1981. Basic Food Microbiology. 2a Ed. The AVI Publishing Co. Connecticut, EE.UU.
Groocock, N.H., 1984. Disinfection of drinking water by ultraviolet light. J. Inst. Water Engineers and Scientists. 38(2):163-172.
Martorell, P., Stratford, M., Steels, H., FernándezEspinar, M. T., Querol, A. 2007. Physiological characterization of spoilage strains of Zygosaccharomyces bailii and Zygosaccharomyces rouxii isolated from high sugar environments. International Journal of Food Microbiology. 114(2): 234-242.
Nielsen, M. y Arneborg, N. 2007. The effect of citric acid and pH on growth and metabolism of anaerobic Saccharomyces cerevisiae and Zygosaccharomyces bailii cultures. Food Microbiology. 24:101-105.
Norrish, R. S. 1966. An equation for the activity coefficients and equilibrium relative humidities of water in confectionery syrups. J .Food. Technol. 1:25-39.
Sommer, R., Haider, T., Cabaj, A., Heidenreich, E. y Kundi, M. 1996. Increased inactivation of Saccharomyces cerevisiae by protraction of UV irradiation. Applied and environmental microbiology. 62(6):1977–1983.
T. Hernández-Grajales et al. / Temas
Vermeulen, A., Dang, T.D., Geeraerd, A.H., Bernaerts, K., Debevere, J., Van Impe, J. y Devlieghere, F. 2008. Modelling the unexpected effect of acetic and lactic acid in combination with pH and aw on the growth/no growth interface of Zygosaccharomyces bailii International Journal of Food Microbiology. 124:79-90.
de
3 - 2 (2009): 59 - 66
Vladislav, G., Jin Kyu, K., Anastasiya, V. y Zhurakovskayaa, P. 2001. Mitotic recombination and inactivation in Saccharomyces cerevisiae induced by UV-radiation (254 nm) and hyperthermia depend on UV fluence rate. Mutation Research/Fundamental and Molecular Mechanisms of Mutagenesis. 478(2):169-176.