A look at SARS-CoV-2 from nanomedicine
medicina nano SARS-CoV-2 Una mirada al
Por: Jessica A. Flood-Garibay · Miguel A. Méndez-Rojas
RESUMEN

KEYWORDS
Coronavirus · Nanomedicine · Diagnostics · Therapy · Vaccines
INTRODUCCIÓN
ABSTRACT
PALABRAS CLAVE
Coronavirus · Nanomedicina · Diagnóstico · Terapia · Vacunas
Una colisión entre los mundos macroscópico y nanométrico impacta nuestro estilo de vida. Mientras la mitad de la población mundial está confinada en sus casas, la primera gran pandemia del siglo xxi reta a la comunidad científica internacional a buscar soluciones para ganar la batalla a un virus de apenas 120 nanómetros de diámetro; el sars-cov-2 ha puesto en jaque al sistema de salud mundial. En una carrera contra el tiempo, se buscan vacunas y fármacos que permitan tratar de forma efectiva la enfermedad, así como métodos diagnósticos rápidos y precisos, y materiales que sirvan como barreras que disminuyan la propagación y contagio. En este escenario, la nanociencia y la nanotec nología nos ofrecen alternativas interesantes e innovadoras. En este texto analizamos, desde la nanomedicina, algunas de las características más distintivas del sars-cov-2 y su enfermedad asociada, la covid-19, para identificar algunas áreas de oportunidad en su diagnóstico, tratamiento y prevención.
Flood-Garibay J. y Méndez-Rojas M. (2020).Una mirada al sars-cov-2 desde la nanomedicina. Entorno UDLAP. Edición Especial Recibido: 28 de abril de 2020 Aceptado: 25 de mayo de 2020
A collision among the macroscopic and the nanometric worlds is affecting our life style. While half of the world population is quarantined inside their homes, the first great pandemic of the XXI century challenges the international scientific community to search for solutions to successfully confront this virus of barely 120 nanometers in diameter; the sarscov-2 is overwhelming the world’s health system. Vaccines, new drugs that may allow to effectively treating the disease, fast and precise diagnostic tools, as well as barriers and tools to decrease propagation and contagion are being sought worldwide. In this scenario, the Nanoscience and Nanotechnology are offering a unique perspective, offering promising and innovative solutions. Here, we analyze, from the perspective of Nanomedicine, the main characteristics and challenges of the novel sars-cov-2 and its associated disease, covid-19, in order to identify some areas of opportunity for its diagnosis, treatment and prevention.
A finales de diciembre de 2019, China envió una alerta sanitaria a la Organización Mundial de la Salud (oms) respecto a la creciente incidencia de un nuevo agente viral altamente infeccioso que, en la ciudad de Wuhan, localizada en la provincia china de Hubei, estaba enfermando a cientos de sus ciudadanos y que a la fecha se ha extendido a más de 170 países. Ya para enero de 2020 el genoma del virus, obtenido de una muestra de un hombre de 41 años, trabajador de una pescadería de Wuhan, había sido secuenciado. El sars-cov-2 es el miembro más reciente de una familia formada por siete coronavirus humanos (hcov) que causan el síndrome respiratorio agudo severo (sars-cov) o el síndrome respiratorio de coronavirus de Oriente Medio (mers-cov), cuatro de ellos están circulando a nivel mundial y contribuyen aproximadamente un tercio de las infecciones humanas (Lim, 2016). El último coronavirus que está causando la pandemia en este siglo xxi es el denominado sars-cov-2 y es el responsable de la pandemia de la enfermedad conoci-
CUANDO UN VIRUS
ATACA UNA CÉLULA, EL ARN «SECUESTRA» LA MAQUINARIA
CELULAR, FORZANDO
A LA CÉLULA A
HACER COPIAS DEL ARN DEL VIRUS
PARA PRODUCIR
SUS PROTEÍNAS
ESTRUCTURALES.
da como covid-19, misma que al momento de escribir estas líneas ya rebasaba los dos millones de infectados; causando cerca de 130,000 decesos.
La alta capacidad infecciosa del nuevo agente viral pone en riesgo la infraestructura de salud pública de todos los países, ya que podrían colapsar ante un aumento descontrolado de casos con cuadros clínicos severos que requieran hospitalización. Esto ya ocurrió en algunos países de Europa y, previniendo que pueda ocurrir algo similar en el nuestro, resulta necesario realizar acciones emergentes para detectar, mitigar o eliminar el virus sars-cov-2 a partir de esfuerzos multidisciplinarios aprovechando las fortalezas actuales de varios centros de investigación en instituciones públicas y privadas. Para tal fin, es importante desarrollar métodos de detección (biosensores) que puedan servir para el diseño de plataformas diagnósticas de la infección al coronavirus, así como nuevos tratamientos farmacológicos o vacunas, al igual que materiales que puedan ayudar a generar barreras efectivas que impidan el contagio y propagación de la enfermedad. Para alcanzar dichas metas, es imprescindible conocer bien las características físicas y estructurales del nuevo coronavirus.
El virus como una nanoestructura
Los virus pueden describirse como nanopartículas autoensambladas, formadas principalmente por material genético (arn o adn), proteínas (codificadas por el propio virus) y lípidos (tomados por lo regular de la membrana lipídica de la célula infectada); pueden medir entre 20 (parvovirus), 200 (herpevirus) o más nanómetros (virus de la varicela o del ébola).
Por lo regular, la capa superficial (envoltura o cápsula) de un virus está constituida por una doble capa lipídica asociada a glicoproteínas que pueden proyectarse en forma de espigas desde la superficie de la partícula viral hacia el exterior. La bicapa lipídica es el componente más débil de un virus, misma que se ensambla a través de interacciones no-covalentes muy débiles. En el caso de los coronavirus, el material genético viral es arn (que, en
el caso del coronavirus, mide aproximadamente 30,000 nucleótidos). Las proteínas, por otro lado, le sirven al virus para reconocer a la célula blanco, asistir la replicación viral y, en esencia, como bloque estructural. Los lípidos y las proteínas forman un recubrimiento alrededor del virus para protegerlo y ayudarle a su propagación, y en la invasión celular. Cuando un virus ataca una célula, el arn «secuestra» la maquinaria celular, forzando a la célula a hacer copias del arn del virus para producir sus proteínas estructurales. Estas nuevas moléculas de arn y proteínas se autoensamblan al interior de endosomas y luego, al emerger, remueven parte de los lípidos de la membrana de la célula infectada a través de interacciones débiles para formar las nuevas partículas virales. Una vez que el virus inicia el proceso de infección, nuestro sistema inmune busca contrarrestarlo, a través de la acción de células especializadas que atacan al invasor (células dendríticas, macrófagos, células B y T), así como de anticuerpos sintetizados por los linfocitos B (IgG e IgM). Como puede notarse en la figura 1, los tamaños relativos de los sistemas de defensa parecen hacer a ésta una lucha desigual, pero no necesariamente efectiva. El virus es capaz de engañar (por su tamaño y por los azúcares con que superficialmente modifica a sus proteínas en membrana) al sistema de defensa, evitando así ser reconocido y continuando su proceso de infección. Ante la ineficacia de las primeras líneas de defensa inmunológica, la reacción inmune se hace más intensa y, en la segunda fase del proceso infectivo, se activa la «tormenta de citoquinas» que pueden causar el «síndrome de liberación de citoquinas» (crs, por sus siglas en inglés) que genera una reacción muy fuerte proinflamatoria, causando sepsis, trombosis y fallas orgánicas, que en la mayoría de los casos pueden provocar la muerte del paciente infectado. Es por ello que terapias de control de los procesos inflamatorios, como el uso de antinflamatorios no esteroideos, vitamina C (un antioxidante) y antagonistas de interleucina-6 (IL6, un promotor de respuesta inflamatoria), han servido para disminuir el crs, aunque no está comprobada al 100% su efectividad.
1.
Macrófagos 21 μm Células NK 6-7 μm
Primera línea de defensa
Segunda línea de defensa
Células dendríticas 10-15 μm
Células B y Células T 7-10 μm
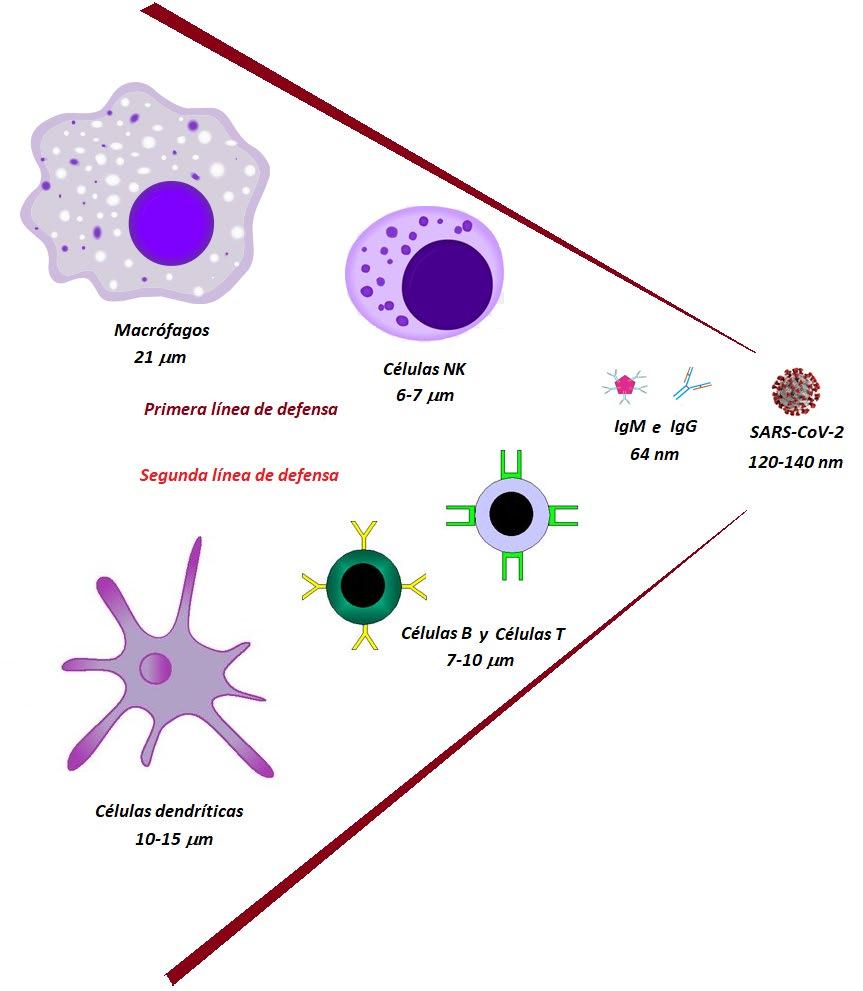
El sars-c o v -2 es un virus relativamente grande, con un diámetro promedio entre 120140 nm y que muestra una estructura esférica con un «halo» coronado, de ahí su nombre: coronavirus. Tiene un volumen de un millón de nanómetros cúbicos (1x106 nm 3) y una masa aproximadamente de 1 fentogramo (1x10-15 g).
Jean Shingelwood y su esposo Peter Medawar, decían en 1977 que un virus no es más que «malas noticias envueltas en proteínas». En ese sentido, el nuevo coronavirus, sars-cov-2, presenta una estructura y composición únicas. El material genético ( arn ) codifica para al menos 29 proteínas distintas (tabla 1). Una de las proteínas características del coronavirus es la proteína de espiga o proteína S (una de las cuatro proteínas estructurales, además de la proteína E de ensamblaje, la M de membrana y la N de protección al arn), la cual se encuentra en la cápsula superficial que protege al arn y que le permite llevar a cabo procesos de
SARS-CoV-2 120-140 nm IgM e IgG 64 nm
Representación esquemática de los tamaños relativos de los componentes efectivos del sistema inmune que nos defienden ante la infección por el sars-CoV-2.
reconocimiento hacia receptores específicos en distintos tejidos (en particular a receptores del tipo de las proteínas ace2, que se encuentran en numerosos tejidos respiratorios humanos). La proteína S forma un trímero, que forma las «puntas» características y que dan nombre a los coronavirus y que es además la estructura responsable del proceso de reconocimiento molecular que ayuda a la infección viral. Otras proteínas «accesorias» (orf 3a, orf 3b, orf 6, orf 7a, orf 8) (tabla 1) ayudan a cambiar el ambiente dentro de la célula infectada para favorecer los procesos de replicación, abren agujeros en las membranas de las células infectadas para permitir el escape de las nuevas partículas virales y desencadenan el proceso inflamatorio, uno de los síntomas más peligroso de la enfermedad. La proteína N, en particular, es importante para la estabilización del arn viral, formando fibras espirales que envuelven y protegen al material genético (figura 2).
2.
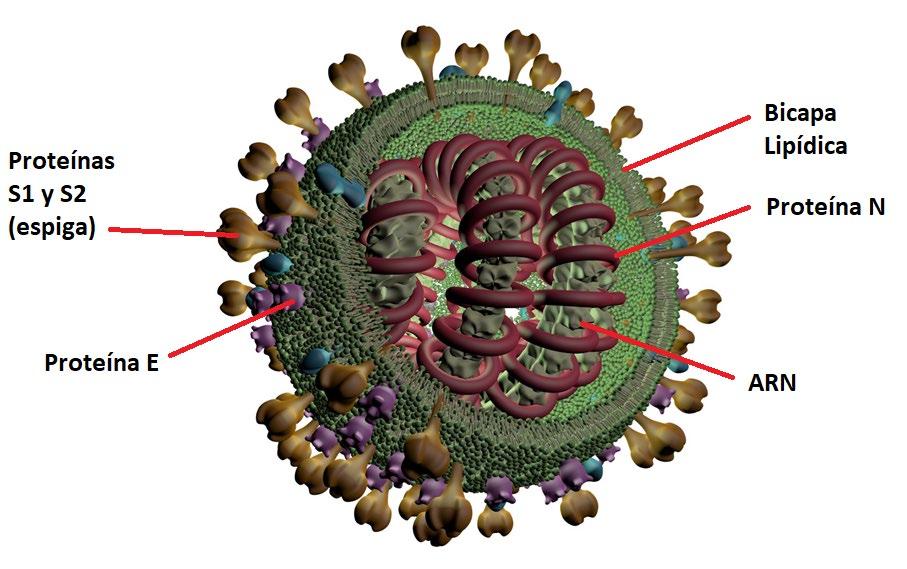
Representación esquemática del sars-CoV-2 y sus distintos componentes estructurales. (Imagen creada por el Dr. M. Eugenio Vázquez, Universidad de Santiago de Compostela, España, y adaptada para este artículo con la autorización del autor).
Fundamentos moleculares de la estabilidad del virus
Una persona infectada puede expulsar hasta tres mil gotitas de secreciones al toser o estornudar, según un estudio de 2009 de la oms. Las gotitas de saliva son expulsadas a velocidades de entre 10 a 50 m/s, alcanzando una distancia de 10 metros. Las gotitas expulsadas al estornudar o hablar se depositan en las superficies y se secan rápidamente. La estabilidad del virus dependerá de las interacciones con las superficies en las que se depositan. El virus puede mantenerse activo e infeccioso cuando se encuentra depositado sobre diferentes tipos de superficies. Cuando se deposita sobre metales, cerámicos y algunos tipos de plásticos como el teflón, las superficies no generan interacciones fuertes con el virus, estabilizándolo y manteniéndolo activo por varias horas o días. Por ejemplo, en superficies de cobre (un material
que se sabe desde hace mucho tiempo tiene actividad antibacteriana y antiviral) se mantiene activo sólo por cuatro horas, mientras que sobre acero inoxidable o vidrio entre 72 y 96 horas (figura 3) (van Doremalen, 2020). Por otro lado, cuando el virus se deposita sobre telas, madera, cartón o plásticos como el polipropileno, se generan interacciones fuertes (por lo regular asociadas a los grupos hidroxilo, -OH, y otros grupos polares superficiales que existen en estos materiales). Sin embargo, en la mayoría de los casos las estructuras altamente rugosas que tienen estos materiales pueden inducir el rompimiento de la estructura viral de forma espontánea, inactivándolo. Es por ello que, sobre papel o cartón, el virus sólo permanece activo entre 3 y 24 horas. Sin embargo, en los billetes (que hoy se fabrican con fibras poliméricas artificiales), la textura lisa y homogénea del material tiene como consecuencia que las inte-
Tabla 1. Nombre y descripción de las proteínas virales encontradas en SARS-CoV-2 (Corum y Zimmer, 2020).
Proteína Nombre Uso
Proteína Nombre Uso
NSP1 Saboteador celular Alentar la producción de proteínas en la célula infectada. NSP14 Corrector
NSP2
NSP3
NSP4
Proteína no caracterizada
Desenganche y corte
Indeterminado. NSP15 Limpiador
Cortar las proteínas virales y alteración de proteínas de la célula infectada. NSP16 Camuflaje extra
Productor de burbujas
Construir burbujas llenas de líquido dentro de las células infectadas. S Proteína espiga
NSP5 Tijeras proteicas
Cortar las proteínas virales para activarlas. ORF3a Artista del escape
NSP6
Productor de burbujas
NSP7 Asistente de copia
NSP8 Asistente de copia
Trabajar con NP4 construyendo burbujas para construir virus dentro de las células infectadas. E Proteína de envoltura
Ayudar a NSP12 a hacer nuevas copias de rna M Proteína de envoltura
Ayudar a NSP12 a hacer nuevas copias de rna ORF6 Bloqueador de señal
NSP9 Al corazón de la célula
Producir pequeños canales en la membrana nuclear de la célula infectada. ORF7a Liberador de virus
NSP10
NSP12
NSP13
Camuflaje genético
Máquina de copiado
Desenrollador de arn
Camuflaje de los genes virales del ataque de la célula infectada. ORF8
Junto con NSP11, construir nuevos genomas víricos (arn). N
Proteína no caracterizada
Proteína de nucleocapside
Proteína no caracterizada
Corregir los errores de copia al arn viral producidos por NSP12.
Destruir el arn viral sobrante para engañar a las defensas de la célula infectada.
Trabajar con NSP10 escondiendo los genes virales de las defensas de la célula infectada.
Proteína estructural, proteger el ARN viral dentro de cápside, interacciona con la membrana celular de la célula infectada.
Producir agujeros en la membrana de las células infectadas para permitir el escape de las nuevas partículas virales.
Proteína estructural que interacciona con proteínas reguladoras del genoma de la célula infectada.
Proteína estructural.
Bloquear señales de la célula infectada hacia el sistema inmune.
Ayudar a las partículas virales nuevas a escapar de las defensas de la célula infectada e induce apoptosis de éstas.
Proteína accesoria, característica de sarsCov-2.
Mantener el arn viral dentro de la cápside viral.
Probable proteína accesoria, característica de sarsCov-2. Flood-Garibay J. y Méndez-Rojas
Desenrollar el arn viral para que otras proteínas puedan copiarlo. ORF10










racciones fuertes pueden estabilizar al virus en su forma infecciosa hasta por 96 horas. Pero es con la piel humana, compuesta por proteínas y ácidos grasos similares a los componentes estructurales del virus, el tipo de superficie con que los coronavirus pueden interaccionar más fuertemente. Al tocar una superficie contaminada con partículas de virus, éstas se adherirán a las manos prácticamente de forma inmediata. Si luego uno se toca el rostro, el virus se transferirá a la cara y podrá alcanzar boca y ojos, por donde puede entrar al organismo e infectarlo. Lavar sólo con agua no es suficiente. Para remover el virus de la piel e inactivarlo hay que añadir jabón al agua, para luego tallar y enjuagar bien durante, al menos, veinte segundos para asegurar que el jabón alcance cada grieta y rincón de la piel que pudiera esconder virus activos. Las moléculas de detergente en el jabón (anfóteras, es decir, con una cabeza polar y otra no polar, de naturaleza lipofílica) interaccionan con los lípidos (grasas) de la membrana del virus, promoviendo su desintegración (figura 4). También es posible emplear productos que contengan alcohol (etanol, isopropanol), que pueden romper la membrana lipídica viral o desnaturalizar las proteínas estructurales: se requerirán entre uno y cinco minutos de contacto. Agentes reductores como el ácido L-láctico o el ácido cítrico, o agentes oxidantes como el ácido peracético, el peróxido de hidrógeno o el hipoclorito de sodio actúan de forma similar, pero además son capaces de reducir u oxidar, respectivamente, algunos componentes estructurales del virus que son críticos para su propagación; dependiendo de la sustancia pueden requerir al menos entre uno y cinco minutos de contacto). En general, los productos basados en alcohol no son tan buenos como el jabón y el agua para esta tarea. Se ha reportado que los coronavirus pueden desactivarse tratando las superficies con etanol al 70%, agua oxigenada al 0.5% o hipoclorito de sodio al 0.1% por un minuto. Es importante inactivar el virus, porque tan sólo algunos cientos de virus son suficientes para infectar a una persona. También es posible inactivar al virus con radiación ultravioleta, la cual puede degradar el material genético viral,
El jabón y el agua rompen la envoltura lipídica del virus.
La luz ultravioleta puede dañar e inactivar el material genético viral. El calor desnaturaliza (rompe) la estructura de la espiga proteica.
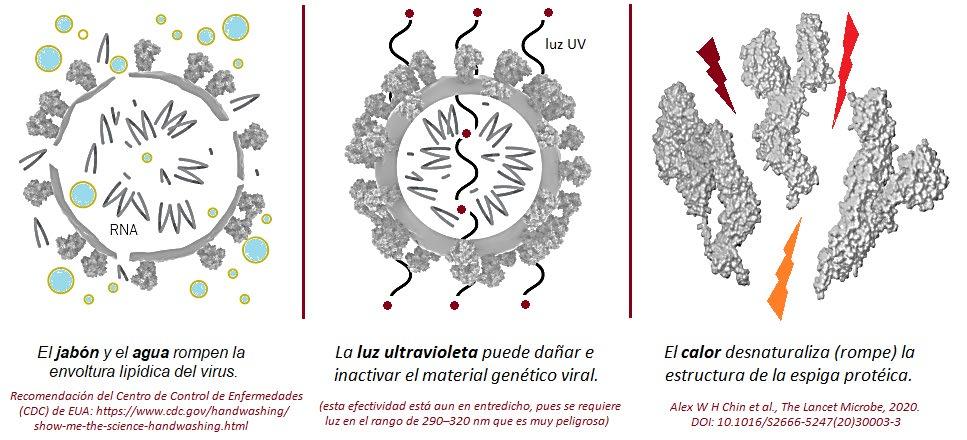
con luz UV y tratamientos térmicos como han reportado investigadores del Centro para Iluminación de Estado Sólido y Electrónica Energética (ssleec, por sus siglas en inglés) de la Universidad de California en Santa Bárbara quienes han diseñado un sistema de iluminación uv-led que puede inactivar hasta el 99.9% de los virus en las superficies irradiadas. El calor también puede inducir cambios en las proteínas estructurales virales (como la S1), rompiendo su estructura e inactivándola; estudios recientes de investigadores de la Universidad de Aix-Marsella en Francia, descubrieron que tratamientos a 56 o 60 °C durante una hora eran ineficaces para inactivar el virus por completo, aunque tratamientos a 97 °C durante quince minutos sí conseguían inactivarlo al 100%.
Desarrollo de nanoplataformas para diagnóstico y detección La detección temprana y el diagnóstico efectivo de individuos contagiados, con o sin síntomas, al menor costo, se ha convertido en una prioridad pues una respuesta rápida permite una intervención oportuna y un tratamiento apropiado, ofreciendo al paciente mayores probabilidades de recuperación, y evitando también que éste se convierta en un agente de contagio para los que le rodean. Los métodos de diagnóstico actuales requieren, primero, tomar un exudado bucofaríngeo con un hisopo, a partir del cual se extrae arn viral. Este material genético se purifica y amplifica utilizando la técnica conocida como pcr o se marca con tintes fluorescentes que se unen al arn. De esta manera la detección puede hacerse mediante corrimiento electroforético del material genético en un gel o mediante un espectrofluorómetro. Aunque las técnicas basadas en detección de arn
viral mediante pcr son consideradas el «estándar de oro», presentan numerosos problemas tales como el costo y escasez de los reactivos que requieren, la velocidad con que se obtienen resultados (una prueba puede tardar varias horas), además de que, si la muestra no se almacena y transporta apropiadamente, puede degradarse generando falsos positivos y negativos. El diagnóstico empleando arn viral funciona apropiadamente para saber si una persona está infectada, pero no nos da información sobre si un individuo asintomático se contagió en el pasado. Para tal fin, la detección serológica de anticuerpos contra el virus es la solución más recomendada. Ya que los anticuerpos se producen por el sistema inmunitario entre siete a diez días posteriores a la infección, su detección puede servir para confirmar estados avanzados de contagio o para determinar población que ha desarrollado inmunidad ante la enfermedad. Un tipo de prueba diagnóstica rápida, actualmente en proceso de desarrollo, busca detectar proteínas virales (como la S1) en sangre, saliva o en exudado bucofaríngeo, y puede servir para detectar infección en etapas tempranas (cuando el individuo es aún asintomático), a un costo mucho menor, aunque con resultados no tan confiables. Para alcanzar tales metas, actualmente se están empleando nanoplataformas diagnósticas que puedan servir para la detección oportuna de la enfermedad en sus primeras etapas (pruebas rápidas), pero también para apoyar estudios epidemiológicos que permitan determinar el grado de contagio en la población en general y determinar los grupos poblacionales que, luego de haber sido expuestos al virus, han desarrollado anticuerpos e inmunidad ante la enfermedad (Méndez-Rojas, 2017).
AUNQUE LAS TÉCNICAS BASADAS EN DETECCIÓN DE ARN VIRAL MEDIANTE PCR SON CONSIDERADAS EL «ESTÁNDAR DE ORO», PRESENTAN NUMEROSOS PROBLEMAS TALES COMO EL COSTO Y ESCASEZ DE LOS REACTIVOS QUE REQUIEREN.

AuNPs Proteína S
AuNP-Proteína S conjugados
UNA APROXIMACIÓN
INNOVADORA SE BASA EN LA DETECCIÓN DE PROTEÍNAS
VIRALES QUE PUEDAN ESTAR PRESENTES EN FLUIDOS
FISIOLÓGICOS DEL PACIENTE ENFERMO
A TRAVÉS DEL USO DE ANTICUERPOS
MONOCLONALES
INMOVILIZADOS EN NANOPLATAFORMAS.
(Zhao, 2020). Este es probablemente un trabajo similar al desarrollado por investigadores de Yachay Tech, Universidad Tecnológica en Ecuador, quienes empleando también nanopartículas magnéticas han logrado triplicar el número de pruebas diagnósticas realizadas en dicho país (Yachay Tech, 2020). Por otra parte, el grupo de nanobiosensores y aplicaciones bioanalíticas de la Dra. Laura Lechuga, en el Instituto Catalán de Nanociencia y Nanotecnología (icn2) se encuentra desarrollando un sistema que emplea nanopartículas de oro (Au) para detectar la presencia de partículas virales en menos de treinta minutos. El biosensor monitorea cambios en el índice de refracción de un láser por la interacción entre anticuerpos inmovilizados sobre la superficie de las nanopartículas de oro y la partícula viral. De forma similar en México, el grupo de investigación de los doctores Tatiana Fiordelisio y Mathieu Hautefeuille, del Laboratorio Nacional de Soluciones Biomiméticas para Diagnóstico y Terapia (LaNSBioDyT) de la unam, se encuentra desarrollando una prueba rápida (dos horas) que emplea nanopartículas magnéticas que «pescan» el arn viral y, mediante técnicas de fluorescencia en dispositivos microfluídicos, promete diagnosticar la infección. La prueba se encuentra actualmente en fase de validación ante el Instituto de Diagnós-
tico y Referencia Epidemiológicos «Dr. Manuel Martínez Báez» (InDRE) y, de acuerdo con los investigadores, no requiere el uso de reactivos costosos ni instrumentación compleja. Una aproximación innovadora se basa en la detección de proteínas virales que puedan estar presentes en fluidos fisiológicos del paciente enfermo a través del uso de anticuerpos monoclonales inmovilizados en nanoplataformas. A través de cambios en el color (plasmón superficial) o mediante el uso de sondas fluorescentes o sistemas de revelado colorimétrico, es posible obtener respuestas que indiquen resultados positivos o negativos, con un cierto grado de confiabilidad. En nuestro grupo de investigación en la udlap hemos investigado el uso de nanopartículas de Au y de magnetita, modificados superficialmente con anticuerpos monoclonales hacía proteínas no específicas de dengue (NS1), que podrían fácilmente adaptarse para desarrollar un biosensor de bajo costo, rápido y de fácil uso para el diagnóstico de infección por sars-cov-2 (figura 5) (Ramírez-Navarro, 2020). Finalmente, muy recientemente Saylan y colaboradores han propuesto el uso de un lab-on-achip (laboratorio-en-un-chip) consistente en un sensor electroquímico incorporado en un cartucho desechable en el que se pone la muestra del paciente; el cartucho entonces se inserta en un dispositivo móvil que en treinta minutos es capaz de realizar una prueba rápida de detección y transmitir el resultado al teléfono celular, permitiendo que la información sea compartida en la nube para propósitos de crear mapas de distribución geográfica de la infección y generar datos sobre la epidemiología y distribución de la enfermedad (Saylan, 2019). Estas tecnologías han sido probadas exitosamente en el pasado para monitorear un brote de dengue en Taiwán en 2018 y del parásito que causa la malaria en Kenia en 2019.
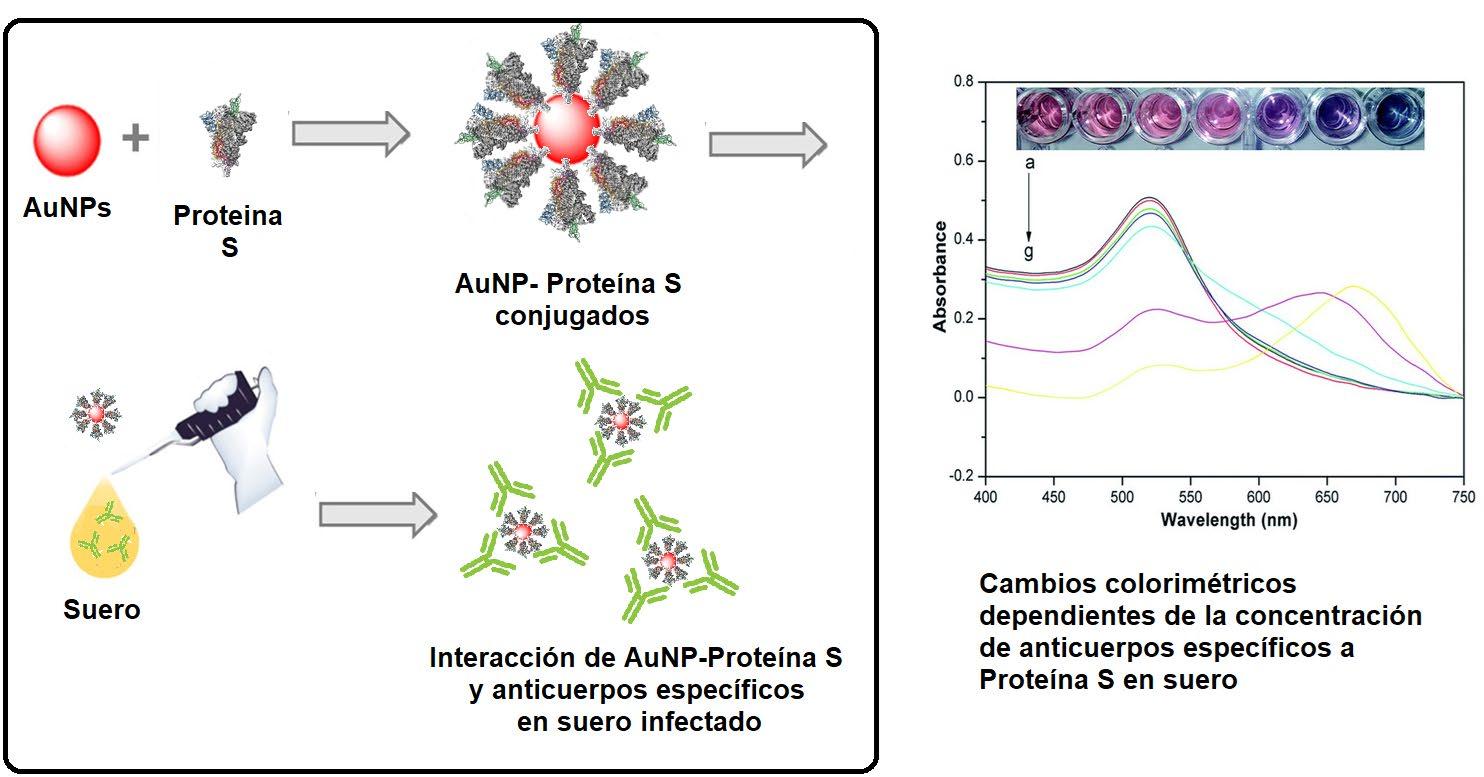
Interacción de AuNP-Proteína S y anticuerpos específicos en suero infectado
Agentes terapéuticos con nanotecnología Diferentes nanomateriales han sido explorados en la búsqueda de nuevos agentes antibacteriales y antivirales (Angulo Molina, 2017; Flood-Garibay, 2019). Entre ellos, las nanopartículas de plata (Ag) y de cobre (Cu) tienen un lugar especial ya que han demostrado ser efectivas para la inactivación de distintos tipos de virus. Nanopartículas de Ag recubiertas de polivinilpirrolidona (pvp), han sido capaces de inactivar el virus de la inmunodeficiencia humana (vih) y virus respiratorio sincitial, mientras que nanopartículas de 4 nm de Ag y Au recubiertas con sulfonato de mercaptoetano o con ácido siálico han hecho lo propio hacia el virus de la influenza y del herpes simple tipo 1 (hsv1). Por otra parte, nanopartículas de Ag recubiertas con polisacáridos han mostrado actividad inhibitoria sobre el virus de la hepatitis B. Recientemente, puntos cuánticos de grafeno funcionalizados con distintos grupos químicos superficiales han sido empleados para bloquear las proteínas S1 de las partículas virales, inhibiendo su capacidad de llevar a cabo procesos de reconocimiento molecular con los receptores ace2 evitando así la infección a las células sanas. Aunque no se conoce con precisión el mecanismo de dicha inactivación, muy probablemente esté asociado a las interacciones superficiales entre las glicoproteínas en la superficie de las partículas virales y los puntos cuánticos, aunque también pueden resultar de
Cambios colorimétricos dependientes de la concentración de anticuerpos específicos a proteína S en suero
la internalización del nanomaterial al interior de la célula, el cual interacciona con el material genético viral, degradándolo o suprimiendo su replicación. También se ha sugerido el uso de nanopartículas que se asemejen a «viriones» desactivados (sin material genético) para el diseño de vacunas que puedan servir para inducir una respuesta inmune moderada y, con ello, generar anticuerpos e inmunidad contra la enfermedad. Como podemos ver, muchas ideas innovadoras empleando nanomateriales se están explorando en esta búsqueda de sistemas terapéuticos efectivos para tratar esta enfermedad. Finalmente, en la búsqueda por medicamentos ya aprobados para su uso clínico en la terapéutica y/o profiláctica contra sars-cov-2 se consideró la posibilidad de que la cloroquina y su derivado, la hidroxicloroquina podrían ser buenos candidatos. Estos fármacos tienen una larga historia como medicamentos seguros y económicos para el tratamiento de la malaria y otras enfermedades autoinmunes. En modelos animales y en cultivos celulares se ha observado que el fármaco tiene actividad terapéutica contra sars-cov, otros coronavirus humanos; sin embargo, su actividad contra virus como el ébola o chikungunya no ha sido del todo exitosa ya en estudios con animales o fases clínicas. De igual forma la cloroquina ha sido usada en el área de la nanomedicina para investigar la absorción (endocitosis) de nanopartículas en células.
Nuevos candidatos profilácticos y terapéuticos podrían ser identificados a partir de los mecanismos precisos a través de los cuales la cloroquina puede actuar para atenuar las infecciones por sars-cov-2 por lo que es de sumo interés llevar a cabo estudios de nanomedicina que proporcionen pistas sobre las alteraciones inducidas por el fármaco durante la captación e internalización celular de sarscov-2 (Hu, 2020). La cloroquina se ha empleado en nanomedicina para reducir la internalización de nanopartículas sintéticas, mediante la inhibición de la expresión de la proteína de ensamblaje de clatrina que se une al fosfatidilinositol (picalm); esta proteína detecta e impulsa la curvatura de la membrana, regulando así la tasa de endocitosis mediada por clatrina. Es posible que uno de los mecanismos responsables de los efectos mediados por la cloroquina contra el sars-cov-2 sea precisamente éste. Sin embargo, es importante mencionar que múltiples mecanismos pueden estar involucrados y que se ha demostrado que la cloroquina muestra actividad antisars-cov en cultivo celular incluso cuando se administra después de la absorción viral. La cloroquina es una base débil que queda atrapada en organelos de pH bajo interfiriendo con su acidificación, lo que conduce, por ejemplo, a un aumento en el pH lisosómico. Esto a su vez dificulta su fusión con vesículas que han sido internalizadas; lo que en el caso de sars-cov-2 detiene el virus en los endosomas inhibiendo la fusión/replicación viral. Además, es probable que la cloroquina presente efectos en el huésped, independientemente de la acción viral directa, atenuando la expresión de factores y receptores proinflamatorios que pueden inducir el síndrome de dificultad respiratoria aguda, que es el principal responsable de la mortalidad asociada al coronavirus.

LA NANOTECNOLOGÍA SE
HA CONVERTIDO EN UNA
ESTRATEGIA CENTRAL
PARA LUCHAR CONTRA EL CORONAVIRUS, EN DONDE LA CONFRONTACIÓN OCURRIRÁ
EN LA MISMA ESCALA DIMENSIONAL, LA ESCALA NANOMÉTRICA. SERÁ UNA LUCHA DIMINUTA, PERO DE PROPORCIONES GLOBALES.
Perspectivas futuras
El nuevo coronavirus sars-cov-2 está mostrando ser todo un reto científico y tecnológico. Pero sin lugar a duda, a través de un cuidadoso estudio de sus características estructurales, del mecanismo a través del cual se propaga e infecta, y mediante el desarrollo de metodologías innovadoras para su detección, diagnóstico y tratamiento, podremos encontrar las soluciones más apropiadas para combatirlo y vencerlo. La nanotecnología se ha convertido en una estrategia central para luchar contra el coronavirus, en donde la confrontación ocurrirá en la misma escala dimensional, la escala nanométrica. Será una lucha diminuta, pero de proporciones globales. Sin duda, triunfaremos.

Miguel Ángel
Méndez Rojas autor de correspondencia Doctor en Química por la Universidad Cristiana de Texas (ee. uu.) y profesor titular senior del Departamento de Ciencias Químico-Biológicas en la udlap desde 2003. Autor de 98 publicaciones en química, nanociencia y nanotecnología; quince capítulos en libros y tres libros de divulgación científica. Es investigador nacional (sni) nivel 2. Premio Estatal de Ciencia y Tecnología 2013 en el área de ciencias exactas y naturales. Miembro de la American Chemical Society, la Royal Society of Chemistry y la Sociedad Química de México. Egresado de la Licenciatura en Química (udlap, 1997). miguela.mendez@udlap.mx

Jessica Flood Garibay
Maestra en Ciencias Químicas por la Universidad de Toronto (2011). De 2012 a 2017 fue profesora de Química en el itesm-ccm Cuenta con cinco publicaciones científicas en el área de química bioinorgánica y nanomedicina. Candidata a doctor en el programa de Doctorado en Biomedicina Molecular en la udlap. Egresada de la Licenciatura en Química (udlap, 2006). jessicaa.floodgy@udlap.mx
• Flood-Garibay, J., Castro-Pastrana, L. I. y Méndez-Rojas, M. A. (2019). Recent advances in the development of mesoporous anti-cancer drug nanocarriers. Frontiers in Anti-Cancer drug discovery, 10, 23-70. DOI: 10.2174/9789811400711119100008
• Hu, T. Y., Frieman, M. y Wolfram, J. (2020). Insights from Nanomedicine into Chloroquine Efficacy against COVID-19. Nature Nanotechnology, 15, 247-249. doi:10.1038/s41565020-0674-9.
Lim Y. X., Ng Y. L., Tam J. P. y Liu D. X. (2016). Human Coronaviruses: A Review of Virus–Host Interactions. Diseases, 4(3), 26.
• Méndez-Rojas, M. A., Angulo Molina, A. y Aguilera-Portillo, G. (2016). Nanomedicine: small steps, big effects. En B. I. Kharisov, O. V. Kharissova y U. Ortiz-Méndez (eds)., CRC Concise Encyclopedia of Nanotechnology
• Méndez-Rojas, M. A., García de la Rosa, L. A., Flood-Garibay, J. y Veloz-Castillo, M. F. (2017). Investigación y desarrollo de nanomateriales para aplicaciones biomédicas. Entorno UDLAP 4(1), 13-21.
• Ramírez-Navarro, H. R., Polesnak, P., Vázquez-Chagoyan, J. C., Pedroza-Montero, M. R., Reyes-Leyva, J. R., Angulo-Molina, A. y Méndez-Rojas, M. A. (2020). Magnetic Immunoconjugate Nanoplatform for Easy Colorimetric Detection of NS1 Protein of Dengue Virus in Infected Serum. Nanoscale Advances. https://doi.org/10.1039/D0NA00251H
• Saylan, Y., Erdem, Ö., Ünal, S. y Denizli, A. (2019). An Alternative Medical Diagnosis Method: Biosensors for Virus Detection. Biosensors (Basel), 9(2), 1-22.
REFERENCIAS
• Angulo-Molina, A. y Méndez-Rojas, M. A. (2017). Nanomedicamentos. En Castro, L. I. (ed.), Retos actuales en Farmacovigilancia. México: Editorial udlap
• Corum, J. y Zimmer, C. (2020). Bad news wrapped in protein: inside the coronavirus genome. The New York Times Recuperado de https://www.nytimes. com/interactive/2020/04/03/science/coronavirus-genome-bad-news-wrapped-in-protein.html
• van Doremalen, N., Bushmaker, T., Morris, D. H., et al. (2020). Aerosol and surface stability of SARS-Cov-2 as compared with SARS-Cov-1. The New England Journal of Medicine
• Yachay Tech (2020). Universidad Yachay Tech desarrolló nanopartículas especiales para que miles de pruebas por Covid-19 se realicen en Ecuador Recuperado de https:// www.yachaytech.edu.ec/noticia/nanoparticulas-covid-19/
• Zhao, Z., Cui, H., Song, W., Ru, X., Zhou, W. y Yu, X. (2020). A simple magnetic nanoparticles-based viral RNA extraction method for efficient detection of SARS-CoV-2. BioRxiv. DOI: 10.1101/2020.02.22.961268.
