SARS-CoV2:
a molecular view

a molecular view
Por: María Fernanda Batiz-Sayavedra · Paola Méndez-Muñoz ·
Irene Vergara-Bahena · Ana Eugenia Ortega-Regules ·
José Daniel Lozada-Ramírez

RESUMEN
A finales de 2019 surgió en Wuhan, China, un nuevo coronavirus denominado sars-cov-2, causante de la enfermedad conocida como covid-19. Ésta se transmite mediante gotas de saliva y moco, así como objetos infectados. La pandemia originada por este virus ha llegado a afectar la salud y la economía mundial. Por esta razón es importante estudiar las características de sars-cov-2 y, de esta manera, avanzar para encontrar posibles tratamientos, tanto para la prevención como para la etapa clínica; así como para ser capaces de prever un nuevo brote de infección por algún miembro de la familia Coronaviridae. Con este propósito, el presente artículo aborda los aspectos moleculares del virus, además de presentar una comparación entre éste y otros virus de la familia. Asimismo, se tratan aspectos sobre el posible origen del patógeno, presentando como mayor probabilidad la zoonosis y se darán las perspectivas en los avances del desarrollo de una vacuna.
PALABRAS CLAVE
Coronavirus · SARS-CoV-2 · COVID-19 · Vacuna · Pandemia
SUMMARY
In late 2019 emerged in Wuhan, China, a novel coronavirus known as sars-cov-2, causing the disease known as covid -19. This is transmitted via saliva droplets and mucus, as well as through infected objects. The pandemic originated by this virus has affected health and economy worldwide. For this, it is important to study the characteristics of sars-cov-2 and thus move towards the discovery of possible treatments, both for prevention and the clinical stage; as well as to be able to foresee a new outbreak of infection by any member of the Coronaviridae family. With this purpose, this article reviews the molecular aspects of the virus, in addition to presenting a comparison between this and other viruses in the family. Furthermore, the possible origin of the pathogen is discussed, presenting as the greater probability zoonosis, and perspectives on the progress of the development of a vaccine are described.
KEYWORDS
Coronavirus ·SARS-CoV-2 · COVID-19 ·Vaccine · Pandemic
Súbitamente, todo cambió El mundo ha cambiado desde la aparición del nuevo coronavirus, sars-cov-2 (Coronavirus del síndrome respiratorio agudo severo 2, por sus siglas en inglés), afectando no sólo la salud a nivel global, sino también la economía de las naciones y su desarrollo. El brote epidémico que ha causado cientos de miles de muertes a lo largo del planeta, provocando alarma y preocupación, lo que hace evidente la necesidad de investigar sobre las enfermedades transmitidas de los animales a los seres humanos (de origen zoonótico), en su atención y tratamiento, en la forma en la que los gobiernos hacen frente a dichas enfermedades y en cómo se destinan recursos en las áreas prioritarias como la investigación y la atención sanitaria de las poblaciones.

La enfermedad causada por sars-cov-2, llamada covid-19, es altamente transmisible y patógena, potencialmente mortal y de gran preocupación mundial (Hassan et al., 2020; Shereen et al., 2020). El tiempo de incubación es de uno a catorce días, aunque hay un gran número de personas infectadas asintomáticas (Ceccarelli et al., 2020). sars-cov-2, al igual que sars-cov, es un b-coronavirus causante de neumonía con lesión alveolar difusa que provoca el síndrome respiratorio agudo severo (Peiris et al., 2004; Pyrc et al., 2007) y lesión aguda en el miocardio y daño crónico del sistema cardiovascular, de aquí la importancia del tratamiento protector del sistema circulatorio (Zheng et al., 2020). Se cree que, junto con diferentes cepas de virus de la influenza, adenovirus, otros coronavirus (229E, NL63, OC43), bocavirus humano, metapneumovirus humano, virus de parainfluenza (1-3), rinovirus y virus sincicial respiratorio (A y B), entrará al grupo de infecciones estacionales. Tanto mers-cov, sars-cov y sars-cov-2 se contagian a humaCORONAVIRUS
Donde aparecieron varios casos con neumonía atípica.
sars-CoV-2: una descripción general Hasta antes de 2002, los coronavirus se asociaban a enfermedades respiratorias leves en aves y mamíferos, aislándose por primera vez en humanos en 1960; durante este tiempo, conocido por causar el resfriado común (catarro). El primer brote de la enfermedad grave en humanos causada por coronavirus se reportó en 2002, en Guangdong China, donde aparecieron varios casos con neumonía atípica (Zuckerman et al., 2004). El nuevo coronavirus 2019-nCoV representa una preocupación y emergencia global (who, 2020a), particularmente por la falta de información cuantitativa y cualitativa sobre sus aspectos genómicos y proteómicos (Hassan et al., 2020). El virus se denomina sars-cov-2 y forma parte del orden Nidovirales, familia Coronaviridae, subfamilia Coronavirinae, siendo que la subfamilia se divide en cuatro géneros que conforman dos clados, uno agrupando los alfa (α)-, delta (δ)- y gamma (γ)-coronavirus y el segundo al género beta (β)-coronavirus (Cui et al. 2019; Shereen et al., 2020). El género β se divide a su vez en cinco linajes; linaje A (Embevirus), B (Sarbecovirus), C (Merbecovirus), D (Nobecovirus) y E (Hibecovirus) (Shereen et al., 2020; Chan et al., 2020a; Wu et al., 2020a, Wu et al, 2020b). Hasta hoy, se conocen siete especies patógenas de humanos, dos de ellas α-coronavirus, HCoV-229E y HKU-NL63, y cinco β-coronavirus, HCoV-OC43 y HCoV-HKU1 (Embevirus); sars-cov, que causó la epidemia de 2002-2003, y sars-cov (Sarbecovirus); y mers-CoV, responsable de la epidemia de 2012 en Medio Orien-
te (Merbecovirus). De los siete, se considera que cuatro, HCoV-229E, Hku-Nl63, sars-cov y mers-cov, se originaron de murciélagos, que son los mayores reservorios de α- y β-coronavirus, por lo que es altamente probable que sars-cov-2 también (Drexler et al., 2014; Cui et al., 2019; Wu et al., 2020a). sars-cov-2 es el más recientemente patógeno humano reconocido y el tercero que ocasiona un síndrome clínico severo, sumándose a sars-cov y a mers-cov1 (Ceccarelli et al., 2020).
El nuevo coronavirus 2019-nCoV representa una preocupación y emergencia global, particularmente por la falta de información cuantitativa y cualitativa sobre sus aspectos genómicos y proteómicos. El virus se denomina sars-CoV-2 y forma parte del orden Nidovirales, familia Coronaviridae, subfamilia Coronavirinae.
nos como infecciones nosocomiales; de igual manera, se ha observado que la transmisión de sars-cov-2 ocurre en el ambiente familiar y por personas cercanas (Guo et al., 2020), a través de gotas pequeñas de saliva y moco con partículas virales y del contacto directo con objetos infectados (Hassan et al., 2020; Ceccarelli et al., 2020).
sars-CoV-2 desde el punto de vista molecular Los coronavirus poseen arn monocatenario positivo asociado a nucleoproteínas, es decir, es de cadena simple y puede ser traducido inmediatamente en la célula infectada. Dicho arn contiene de 26-32 kilo bases (kb) (Shereen et al., 2020; Walls et al., 2020) y comprende de seis a catorce marcos de lectura abierta (orf) (Guo et al., 2020; Wu et al., 2020). Estos virus pleomórficos y envueltos (capa externa lipídica) tienen tamaños entre los 65-125 nm de diámetro, presentando una estructura en forma de corona debida a proyecciones en forma de espigas o espículas de proteína (S) que sobresalen de su superficie, de allí su nombre, coronavirus o virus corona (figura 1). Los genes de los coronavirus codifican las proteínas implicadas en los procesos de su replicación (15 o 16 proteínas relacionadas a la replicasa), así como cuatro o cinco proteínas estructurales (incluyendo la nucleocápside y las espigas) y de 1 a 8 proteínas accesorias (Perlman y Netland, 2009; Boheemen et al., 2012), siendo estas últimas las responsables de la unión a la
La enfermedad causada por sars-CoV-2, es altamente transmisible y patógena, potencialmente mortal y de gran preocupación mundial (Hassan et al., 2020; Shereen et al., 2020).
célula que va a ser infectada. El orf1a/b codifica para la síntesis de proteínas de replicación (incluidas pp1ab y pp1a) y comprende dos tercios (>60%) de su genoma (Perlman y Netland, 2009; Guo et al., 2020). Estas proteínas se sintetizan como una poliproteína (proteína inactiva) que es cortada por proteólisis para dar origen a 15 o 16 proteínas no estructurales: ribosa-2’-O-metiltransferasa (2’OMT); 3’5’ exonucleasa (ExoN); helicasa (Hel); endoribonucleasa específica de uridilato (NendoU); arn polimerasa dependiente de arn (rdrp) y proteína de unión a arn monocatenario (ssrbp). El extremo 3’ del arn viral codifica para cuatro proteínas estructurales: espiga (S), membrana (M), envoltura (E) y nucleocápside (N), además de proteínas accesorias específicas para cada virus (Perlman y Netland, 2009) (figura 1). Específicamente, sars-cov-2 tiene doce (Chan et al., 2020b) o catorce (Wu et al., 2020) orfs y, al igual que para todos los coronavirus, el primer orf (5’3’) es orf1a/b (figura 2). Los genes que se leen río abajo generan las proteínas estructurales y accesorias; S, que se lee a partir del orf2; E (orf4), M (orf5), N (orf9) y las proteínas accesorias (ORF3a/b, orf6, orf7a/b, orf8b, orf9b y orf10 u orf14) (Guo et al., 2020). Se propone que la proteína accesoria codificada por el orf8 de Sarbecovirus de los β-coronavirus, proviene de los coronavirus de murciélago bat-CoVYNLF31C y bat-YNLF34C (Chan et al., 2020b).
Las proteínas S son glicoproteínas triméricas que tienen afinidad por la enzima hACE2
LOS CORONAVIRUS POSEEN ARN MONOCATENARIO POSITIVO ASOCIADO A NUCLEOPROTEÍNAS, ES DECIR, ES DE CADENA SIMPLE Y PUEDE SER TRADUCIDO INMEDIATAMENTE EN LA CÉLULA INFECTADA.
Desarrollador Tipo de vacuna Fase Plataforma base
CanSino Biological Inc./Beijing Institute of Biotechnology Vector adenoviral tipo 5, no replicativo Fase clínica 2 Fase clínica 1 Ébola
Inovio Pharmaceuticals Plásmido de adn Fase clínica 1
Beijing Institute of Biological Products Wuhan Institute of Biological Products
Sinovac
Lassa, Nipah / hiv / Filovirus / HPV / Cancer indications / Zika / Hepatitis B
Virus sars-CoV-2 inactivado Fase clínica 1
Virus sars-CoV-2 inactivado + alum (adyuvante) Fase clínica 1 SARS
Moderna/NIAID mRNA encapsulado Fase clínica 1
WRAIR/U.S. Army Medical Research Institute of Infectious Diseases/ Clover Biopharmaceuticals Inc/GSK Vaxil Bio AJ Vaccines Genrex/EpiVax/ University of Georgia Sanofi Pasteur Novavax Heat Biologics/University of Miami University of Queensland/GSK/ Baylor College of Medicine iBio/CC-Pharming
Subunidad de la proteína S Estudios preclínicos
GeoVax/BravoVax/ Janssen Pharmaceutical Companies/ University of Oxford/ Altimmune/ Greffex/ Vaxart/ ExpresS2ion Vector No replicativo
Estudios preclínicos
Codagenix/Serum Institute of India Virus atenuado Estudios preclínicos
Inovio Pharmaceuticals Takis/Applied DNA Sciences/Evvivax Zydus Cadila adn
Estudios preclínicos
(enzima convertidora de angiotensina humana 2, por sus siglas en inglés), a la que utilizan como receptor y que se expresa en varios tipos de células humanas (figura 3). Estas proteínas S se componen de dos subunidades, S1 y S2, siendo que S1 tiene dos dominios, amino terminal y carboxilo terminal, este último actuando como sitio de unión al receptor (rbd). Este rbd se une débilmente al hACE2, por lo que el virus puede infectar múltiples hospedadores. No obstante, aunque sars-CoV y sars-CoV-2 se unen a hACE2, el mecanismo de reconocimiento entre S y hACE2 es diferente para cada virus. Por ejemplo, para hACE2, el residuo de aminoácido Lys31 establece interacción iónica con Glu35, mientras que Lys353 con Asp38, como resultado de la presencia de Tyr442, Asn479 y Thr487 en el rbd de la proteína S de sars-CoV, siendo distintas a las interacciones que se dan entre hACE2 (únicamente entre Lys353 con Asp38),
Diversas plataformas: ébola, Marburgo, HIV, Zika, influenza, HPV, sars-CoV, etcétera.
debido a una composición de aminoácidos distinta en sars-cov-2, Leu455; Gln493 y Asn501 en el rbd de S (figura 4) (Shang et al., 2020a).
Por lo anterior, se puede decir que la unión de la proteína S de sars-CoV-2 parece estar optimizada para la unión con hACE2 (Andersen et al., 2020; Li et al., 2003; Perlman y Netland, 2009). Otros coronavirus como el NL63 humano (HCoV-NL63), que causa enfermedad leve, también usa hACE2 para ingresar a la célula, uniéndose a otra región y de diferente manera a la que se une S de sars-cov y de sars-cov-2 (Hofmann et al., 2005; Li et al., 2007). hACE2 tiene un papel crucial para la replicación efectiva del virus, siendo que al afectarse este receptor disminuye el número de virus que pueden ingresar a la célula y, por lo tanto, el número de replicaciones virales. Es por esto que se considera que el sistema de angiotensina tiene un rol esencial en la lesión aguda severa del pul-
món; sin embargo, este receptor tiene un papel protector en la insuficiencia pulmonar aguda causada por aspiración de ácido o por sepsis, esto debido a que se ha observado que su dis minución tiene consecuencias negativas en es tos casos (Kuba et al., 2005; Imai et al., 2005). En el virus de influenza aviar, la envoltura contie ne hemaglutinina, que cumple con una función similar a la de la proteína de espiga del CoV-2 (Andersen et al., 2020).
Por otro lado, N es necesaria para la encap sidación del arn del virus, actúa como antago nista del interferón (ifn), por lo tanto, evita su inducción y señalización (Perlman y Netland, 2009). Las proteínas E son integrales de mem brana con función de morfogénesis, ensambla je y gemación del virus, además de canal ióni co para la replicación viral (Wilson et al., sabiéndose que su ausencia causa la inhibición parcial de la liberación del virus (sars-CoV) (Dediego et al., 2006). Finalmente, los genes que codifican las proteínas accesorias están intercalados entre los genes estructurales y se cree que son importantes para la replicación en el hospedero natural (Perlman y Netland, 2009).
son ensamblados en el retículo endoplásmico y el aparato de Golgi de la célula hospedera para generar viriones, para luego ser transportado a través de vesículas al exterior de la célula por exocitosis, y estos viriones infectarán nuevas células (Perlman y Netland, 2009; Shereen et al., 2020; Hoffmann, et al., 2020).
El genoma completo de sars-CoV-2 tiene identidad de secuencia de nucleótidos del 79.6% con relación a la secuencia de los virus sars-CoV BJ01 y Tor2 (ambos sars-CoVs); del 88-89% con los virus bat-SL-CoVZC45 y ZXC21; y del 96% con el RaTG13 (coronavirus de murciélago no relacionado con sars) (Zhou et al., 2020). Esta homología en las secuencias de nucleótidos se traduce en un elevado porcentaje de identidad de aminoácidos de S (77-83%) con los sars-covs y (82%) con bat-SL-CoVZC45 (Wu et al., 2020b, Sardar et al., 2020). Cuando la secuencia genética completa de sars-cov-2 se comparó con la de otros coronavirus se observó que, sorprendentemente, tienen mayor cercanía con los coronavirus de murciélago previamente mencionados, ya sean aquellos relacionados con sars (denominados SL o sars-like) o aquellos que no, que con los sars patógenos de humanos (Wu et al., 2020a, Sardar et al., 2020). Lo anterior proporciona las claves para determinar el origen genético del sars-cov-2 y que la fuente primaria de contagio y evolución es a partir de estos mamíferos (figura 5).
sars-CoV-2, comparado con otros virus Aunque sars-cov-2 tiene una relación más estrecha con los coronavirus que afectan al murciélago, es de gran relevancia comprender cuáles son las similitudes y diferencias con sars-cov (figura 2), ya que ésta es la referencia más cercana en cuanto a coronavirus patógenos de humanos. El análisis de nucleótidos indica que existen dominios altamente conservados entre ambos virus, particularmente en la primera proteína no estructural (nsp1) codificada por orf1a/b y en la subunidad 2 del gen S (S2) por orf2 (Chan et al., 2020b; Wu et al., 2020b). Las principales diferencias genéticas entre sars-cov-2 y sars-covV se encuentran en tres regiones; orf3, orf8 y gen S (Cui et al., 2020). orf3a es genéticamente cercano a los sars-CoVs humanos, sin embargo, la proteína codificada por orf3b es considerablemente más larga en sars-cov (154 residuos de aminoácidos) que la codificada por el mismo orf en sars-cov-2 (22 residuos) (Sheeren et al., 2020; Wu et al. 2020a). También, orf3b de sars-cov-2 codifica para una supuesta pro-
LA INFECCIÓN COMIENZA
CUANDO EL VIRUS TIENE ACCESO AL ORGANISMO A TRAVÉS DE LAS MUCOSAS DEL TRACTO RESPIRATORIO, DONDE EL CICLO DE VIDA DEL VIRUS TIENE LUGAR AL GENERARSE LA UNIÓN DE S, A TRAVÉS DE SU RBD, A hACE2.
teína (putativa) de 4 hélices, la cual no presenta homología a ninguna existente en sars-CoV ni en coronavirus bat-SL (Chan et al., 2020b).
La función de orf3b en sars-cov es antiinterferón (irf), a través de la regulación de la actividad del factor regulatorio de ifn (irf3). Sin embargo, otros coronavirus semejantes a sars, incluyendo sars-CoV-2, tienen truncado el extremo C-terminal de la proteína ORF3b, el cual corresponde a una señal de localización nuclear que es la antagonista de la función ifn. A pesar de ello, se ha demostrado que en algunos virus semejantes a sars-CoV, que poseen la proteína truncada, ésta es capaz de antagonizar ifn a través de mecanismos distintos (Zhou et al., 2012). Sin embargo, otros estudios indican que esta función anti-irf se ha perdido en otros SARS-CoV de murciélagos (Cui, Li y Shi, 2019), y particularmente importante, contra irf tipo I en irf-CoV-2, que muestra cierta sensibilidad ante el tratamiento con este interferón (Lokugamage, Schindewolf y Menachery, 2020).
La segunda diferencia relevante se observa en irf8, irf8a está ausente y irf8b es más larga en sars-CoV-2 (121 residuos contra 84 residuos en sars-CoV) (Shereen et al., 2020; Wu et al., 2020a), aunque se observa por análisis de comparación que el irf8b de sars-Cov-2 sí es genéticamente cercano a los sars-CoVs, incluyendo a los virus bat-SL-CoVZC45 y ZXC21 (Chan et al., 2020b). Por otro lado, sars-CoV-2 comparte 77.2% de aminoácidos idénticos con sars-cov de S, siendo parte de la diferen-
cia que sars-cov-2 tiene cambios en 4 de los 5 residuos de aminoácidos clave (Zhou et al., 2020), además de tener 24 deleciones y que su secuencia es más larga (Ceccarelli et al., 2020). Por ello, sars-cov-2 tiene una S con 1,274 residuos de aminoácidos mientras que la de sarsCoV tiene 1256, compartiendo sus genes una identidad de nucleótidos del 86.9% (Chaterjee, 2020), aunque específicamente la región rbd de S tienen una identidad de aminoácidos de entre el 73-75%. Otras proteínas codificadas por sars-CoV-2 también presentan variaciones, por ejemplo, E de sars-CoV-2 tiene un residuo de aminoácido menos que en sars-cov, un aminoácido más en M (85% de identidad de nucleótidos) y tres residuos menos en N (88.3% de identidad de nucleótidos) (Chaterjee, 2020).
En cuanto a los virus de murciélago, los más cercanos a sars-CoV-2 son bat-SL-CoVZC45 y ZXC21. En filogenias realizadas por Chan et al. (2020a) y Wu et al. (2020b), pertenecen al mismo clado, independientemente del gen comparado; incluyendo el gen S (82.3% de identidad de aminoácidos). S2 está altamente conservada, mientras que S1 tiene identidad de 77%, siendo el rbd el dominio con mayor divergencia. En otros virus de murciélago, tales como bat-SL-CoVRs7327, bat-SL-CoVRs4874 y bat-SLCoVRs4231, las secuencias del RBD tienen una identidad de aminoácidos del 73.8-76.9% comparadas con sars-CoV-2. Además, hay evidencia de recombinación del gen S entre bat-SL-CoVWIV1 y bat-SL-CoVRsSHC014 con sars-CoV-2
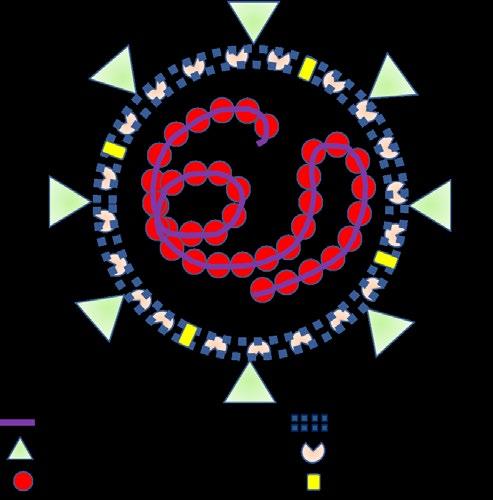
Representación de la estructura del virión de sars-CoV-2 (adaptado de Shereen et al., 2020; Perlman y Netland, 2009).
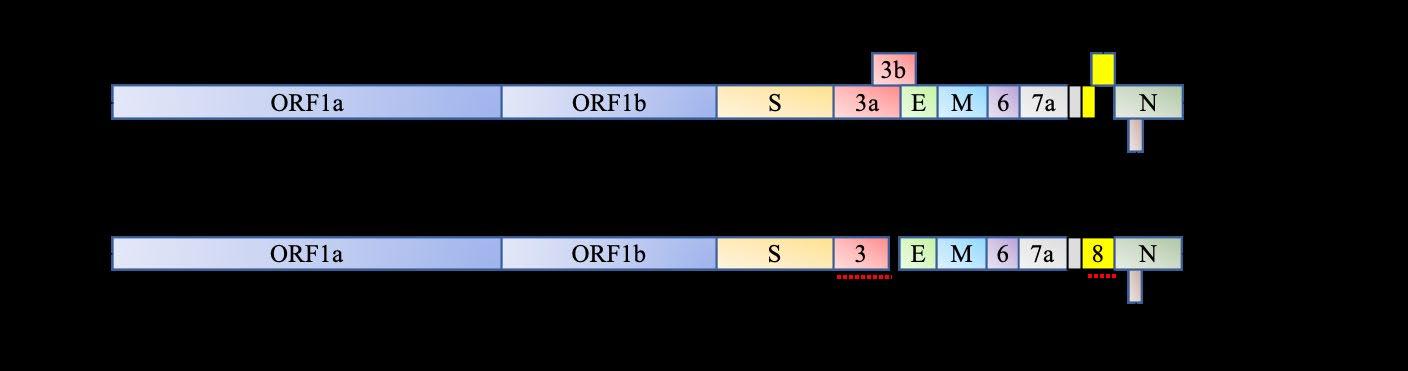
Estructura de los arns de sars-CoV y de sars-CoV-2. Se resalta en líneas punteadas (rojo) las secuencias que generan proteínas con más diferencias (UTR = región no traducida, por sus siglas en inglés) (adaptado de Shereen et al., 2020; Perlman y Netland, 2009).

SARS-COV-2 ESTÁ MUY RELACIONADO A DOS VIRUS DE MURCIÉLAGO, CAUSANTES DEL SÍNDROME RESPIRATORIO AGUDO SEVERO (SARS) (MARRA ET AL., 2003).
(Wuhan-Hu-1), entre los nucleótidos 1029 y 1652, que comprenden al rbd de S. Las regiones restantes (nucleótido 1 al 1029 y 1652 al final de la secuencia) de sars-cov-2 mantienen mayor relación con bat-SL-CoVZC45 y ZXC21 (Wu et al., 2020b). Por ende, bat-SL-CoVWIV1 y RsSHC014 tienen alta probabilidad de ser los otros b-coronavirus de donde proviene el gen S de SARS-CoV-2. Es importante hacer notar que S de bat-SL-CoVZC45 y ZXC21 no reconocen el receptor hACE2, sin embargo, bat-SL-CoVWIV1 y RsSHC014 sí son capaces de reconocerlo. La recombinación de rbd de sars-CoV-2 con estos virus podría ser la clave de por qué reconoce al receptor humano, y puede ser la razón por la cual sars-CoV-2 es más virulento (Sheeren et al., 2020). Por otra parte, hay que considerar que el coronavirus de murciélago no relacionado con sars, bat-CoVRaTG13, tiene una identidad de genoma total de 96.2% con sarsCoV-2 y específicamente de 93% en el gen S. Bat-CoVRaTG13 tampoco es reconocido por el receptor hACE2, y al igual que bat-SL-CoVZC45 y ZXC21, rbd es variable (Zhou et al., 2020). En las filogenias realizadas por Zhou et al. (2020), bat-CoVRaTG13 se encuentra en el mismo clado que sars-cov-2 y conforma un clado hermano del grupo de bat-SL-CoVZC45 y ZXC21, es decir, sars-CoV-2 está más cercanamente emparentado a RaTG13 que a los otros dos virus. Es relevante aclarar que las filogenias realizadas por Wu et al. (2020b) y por Chan et al. (2020a) no incluyen el genoma de bat-CoV-RaTG13.
Rastreando el origen de sars-CoV-2 Las infecciones zoonóticas causadas por virus han ocurrido periódicamente en la historia de la humanidad, tal es el caso del virus de la inmunodeficiencia humana vih el virus del ébola y, presuntamente, el sars-CoV-2 (Sun et al., 2020). Actualmente, esto está altamente acep-
tado ya que, a partir de análisis evolutivos, se ha observado que los α-coronavirus y los β-coronavirus tienen como fuentes primarias roedores y murciélagos (Chan et al., 2020b). Ceraolo y Giorgi (2020) señalan una gran similitud entre las secuencias de los genomas de los CoV2019, algunas de hasta el 99%. Además, existen secuencias que comparten hasta el 96% de identidad, lo cual confirma su origen zoonótico. Dadas las similitudes genómicas y la elevada relación filogenética de sars-CoV-2 con aquellos semejantes a sars de murciélagos (Shereen et al., 2020), además de su gran capacidad recombinante, se ha determinado que la fuente primaria de contagio hacia los seres humanos son los murciélagos (Cui et al., 2019; Lu et al., 2020; Chan et al., 2020a). Adicionalmente, los murciélagos herradura del género Rhinolophus presentan anticuerpos contra sarsCoV, confirmando que son fuente primaria de estos virus (Shi y Hu, 2008). Recientemente se ha establecido la presencia del virus en los géneros de murciélagos Pipisterllus y Perimyotis, evidenciando la importancia de estos organismos como medio de transmisión viral (Annan et al., 2013; Huynh et al., 2012; Lau et al., 2013). sars-CoV-2 está muy relacionado a dos virus de murciélago, causantes del síndrome respiratorio agudo severo (sars) (Marra et al., 2003). A pesar de su origen en murciélagos, estos virus tienden a ser transmitidos a otras especies de mamíferos que permiten su diseminación, fungiendo como intermediarios (vectores) para la infección hacia los seres humanos. Tal es el caso de los β-coronavirus que han causado estragos anteriormente, sars-cov (2002-2003) y mersCoV (2012), que llegaron a humanos usando especies intermediarias, civetas de las palmeras (Paradoxurus hermaphroditus) y camellos (Camelus dromedarius), respectivamente (Cui et al., 2019; Kan et al., 2006), pero ambos con
A PESAR DE SU ORIGEN EN MURCIÉLAGOS, ESTOS VIRUS TIENDEN A SER TRANSMITIDOS A OTRAS ESPECIES DE MAMÍFEROS QUE PERMITEN SU DISEMINACIÓN, FUNGIENDO COMO INTERMEDIARIOS (VECTORES) PARA LA INFECCIÓN HACIA LOS SERES HUMANOS.
origen en murciélagos. Por ello, se ha planteado que el intermediario de sars-CoV-2 sea el pangolín malayo (Manis javanica), además de que varios coronavirus que infectan al pangolín son muy similares (Zhang et al., 2020). Se han observado especies silvestres con diferentes virus de la familia Coronaviridae, muchos de los cuales no han estado en contacto con el ser humano, pero que representan un riesgo, pues podrían ocasionar diferentes enfermedades en el futuro. Por esto, es vital que se dimensionen los riesgos de convivir con especies silvestres, así como de consumir productos derivados de éstas. Según Andersen et al.(2020), este es un tipo de evento de emergencia de enfermedad natural del que se ha advertido durante muchos años.
Algunos consideran que sars-CoV-2 es una creación de laboratorio, tanto un accidente como una creación intencional. Sin embargo, esto es improbable, puesto que la secuencia del rbd de la proteína S no tiene una afinidad óptima para unirse a su receptor, la enzima convertidora de la angiotensina 2 (hACE2). Se considera que esta emergencia de enfermedad natural se había advertido por muchos años, ya que la vida silvestre contiene muchos coronavirus con
el potencial de infectar humanos, por lo que debemos prevenir una próxima emergencia reduciendo la exposición a la vida silvestre (Andersen et al., 2020).
Una vacuna contra sars-CoV-2
El desarrollo de una vacuna es un proceso largo y complejo que involucra estudios preclínicos y clínicos para evaluar su eficacia y seguridad. Las vacunas se desarrollan, aprueban y regulan de manera similar a otros medicamentos. El tiempo que transcurre desde que comienza su desarrollo hasta que está disponible en el mercado es variable, se estima que puede tardar entre ocho y quince años para cumplir con las distintas fases de evaluación y aprobación por las entidades regulatorias (Han, 2015).
La evaluación preclínica toma de uno a dos años, se hacen experimentos in vitro donde se evalúa la capacidad de la vacuna para activar cultivos de células que secretan moléculas de la respuesta inmune, como las citocinas. También, se hacen diversas pruebas en modelos animales (ratones, cobayos y conejos) para medir la inmunogenicidad, los efectos fisiológicos, la toxicidad, diferentes dosis, la formula-
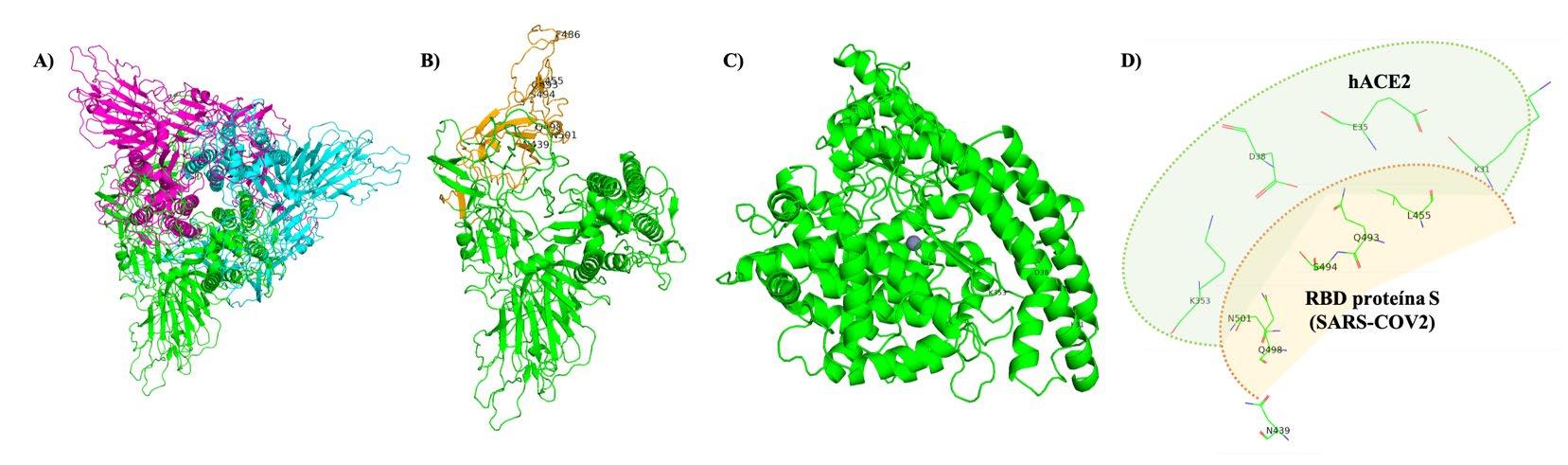
A) Estructura 3-D de tres proteínas S (trímero) de sars-CoV-2 asociadas. Elaboración con base en datos de ncbi y pdb id 6VSB.
B) Una unidad (monómero) de la proteína S de sars-CoV-2, se indican los residuos de aminoácidos implicados en el reconocimiento con hACE2 (Asn439, Leu455, Phe486, Gln493, Ser494, Gln498 y Asn501) y se resalta en anaranjado el rbd (elaboración con base en datos de ncbi y pdb id 6VSB).
C) Receptor hACE2, se indican los residuos de aminoácidos implicados en el reconocimiento con la proteína S de sars-CoV-2 (Lys31, Glu35, Asp38 y Lys353) (elaboración con base en datos de ncbi y pdb id 6M18).
D) Representación del reconocimiento entre el receptor hACE2 (verde) y el rbd de la proteína S de sars-CoV-2 (anaranjado). Se indican los residuos de aminoácidos implicados en el reconocimiento (elaboración con base en datos de ncbi y pdb id 6VW1 y 2AJF).
Para la adquisición de los modelos se utilizaron herramientas bioinformáticas de SWISS-PROT (Waterhouse et al. 2018) y las estructuras se modelaron usando PyMOL (2020) (los autores se basaron en Shang et al. 2020b, Wrapp et al. 2020 y Wan et al. 2020 para la realización de los modelos).
ción y la vía de administración. En laboratorios con alto presupuesto, se utilizan primates no humanos. Los resultados del estudio preclínico definen el avance de la vacuna a la etapa clínica, las que no superan esta etapa, podrían ser modificadas para mejorar su respuesta o disminuir sus efectos tóxicos y se evalúan nuevamente; en algunos casos se descartan por completo (Han, 2015). La etapa clínica se divide en cuatro fases (I, II, III, IV), se realiza en humanos, y está regida por principios bioéticos y rigurosas medidas regulatorias para garantizar la seguridad de los participantes (Gomez et al., 2013).
• FASE I: grupos pequeños de personas adultas sanas (20-100 individuos). Se evalúa la dosis, vía de administración, los efectos biológicos y la seguridad de la vacuna. Si los resultados son positivos, se avanza a la siguiente fase.
• FASE II: participan cientos de personas, entre ellas, puede haber grupos susceptibles a contraer la enfermedad. Se evalúa la capacidad inmunogénica y se determina si se previene la enfermedad, el esquema de vacunación y la forma de administración.
• FASE III: involucra a miles de personas, las pruebas se realizan de forma aleatoria en modalidad «doble ciego», que significa administrar la vacuna experimental en un cierto número de personas y, a la otra parte del grupo, se le da un placebo (una sustancia sin efecto terapéutico o tóxico). El objetivo es evaluar la eficacia y seguridad de la vacuna en un grupo grande de personas.
• FASE IV: la vacuna que haya tenido éxito en la fase III puede iniciar los trámites para la solicitud de registro ante la autoridad sanitaria local o internacional, con fines de comercialización y distribución masiva. Esta fase incluye la vigilancia permanente y el registro de los efectos no deseados asociados a la aplicación de la vacuna, así como efectos que no habían sido observados con anterioridad (Han, 2015; Gomez et al., 2013).
En el caso de epidemias o pandemias el desarrollo de una vacuna es prioritario y se puede
acelerar. Esta carrera contra el tiempo representa un gran reto para investigadores, farmacéuticas y organismos regulatorios, sin embargo, al ser un problema de salud pública, todos los actores se coordinan para tener disponible la vacuna en el menor tiempo posible.
Bajo las circunstancias de la pandemia, se convoca a todos los profesionales que puedan aportar y acelerar el proceso de la investigación, la formulación y las pruebas preclínicas. Por otra parte, las instancias regulatorias como la fda (Food Drug Administration) en Estados Unidos, la ema (European Medicines Agency) en la Unión Europea, o cofepris (Comisión Federal para la Protección contra Riesgos Sanitarios) en el caso de México, trabajan a marchas forzadas en la revisión y en los trámites administrativos para otorgar la licencia de aprobación, si la vacuna superó las pruebas necesarias.
Debido a la urgencia de tener una vacuna contra covid-19 lo antes posible, varias organizaciones se han sumado para coordinar los esfuerzos de los grupos de investigación; entre las que podemos mencionar a la Organización Mundial de la Salud (oms), la cepi (The Coalition for Epidemic Preparedness Innovation), la fundación Bill & Melinda Gates y la organización Wellcome Trust, entre muchas otras. También hay participación importante de la industria farmacéutica, las instituciones de salud y los gobiernos.
A la fecha, al menos setenta grupos de investigación en todo el mundo están tratando de desarrollar una vacuna eficiente contra la covid-19 (Khamsi et al., 2020). Para «ganar» tiempo, algunos investigadores han comenzado a utilizar las plataformas que se usaron en el desarrollo de vacunas contra otros virus como el ébola (2013), influenza H1N1 (2009), coronavirus mers (2012) y los avances para las múltiples vacunas contra vih.
Para el desarrollo de la vacuna contra el sars-CoV-2 hay al menos tres enfoques, de acuerdo con el material que se utiliza como antígeno, 1) el virus inactivado, 2) proteínas recombinantes 3) vacunas de adn o rnam que codifican para la proteína viral S. En este mo-
UNA VEZ QUE LA VACUNA CONTRA LA COVID-19 ESTÉ
LISTA, EL SIGUIENTE RETO ES ABASTECER
LOS MILLONES DE DOSIS QUE SERÁN
NECESARIOS PARA LA POBLACIÓN MUNDIAL.
mento hay registrados dos protocolos en fase clínica I con una vacuna del sars-cov-2 inactivado (tabla 1). Por otra parte, varios grupos de investigación están utilizando vectores replicativos o no-replicativos, donde se inserta la información genética que codifica para una subunidad del trímero de la proteína S; con esta estrategia se busca que las células de la persona sinteticen la subunidad de la proteína S, misma que desencadenará la respuesta inmune. Los protocolos clínicos que hoy tienen el mayor avance (fase clínica II) utilizan un vector no replicativo de adenovirus tipo 5 (Ad-5) con el arnm de una subunidad de la proteína S (tabla 1). Las vacunas que ya están en fases clínicas necesitan demostrar su inmunogenicidad, seguridad y tolerabilidad antes de su aprobación (Zhu et al., 2020).
Una vez que la vacuna contra el covid-19 esté lista, el siguiente reto es abastecer los millones de dosis que serán necesarios para la población mundial.
Una de las preguntas que preocupa a varios gobiernos, instituciones de salud y personas en general, es si habrá acceso equitativo a ella cuando esté aprobada; especialmente en los países en desarrollo, como México. Históricamente, se ha documentado que el acceso a la vacunación no es universal en condiciones normales, y menos aún, en el caso de las pandemias. Pensando en esta problemática, Méxi-
co y otros países han planteado que se haga un acuerdo en el que se establezca el acceso igualitario y oportuno a la vacuna en todo el mundo. También se requiere el financiamiento por parte de los países y organizaciones sin fines de lucro, que permita la producción en gran escala y así asegurar el abasto.
Caracterizar el virus y comprender los eslabones que lo conforman es vital para el conocimiento de éste y a su vez, entenderlo es condicionante para poder desarrollar tratamientos capaces de combatirlo. La elaboración de una vacuna eficiente y accesible para cualquier persona que la requiera es siempre un reto y en el caso de una pandemia como la que vivimos, es una carrera contra el tiempo. Gracias a la colaboración entre científicos y organizaciones alrededor del mundo, es un reto que con seguridad se alcanzará. Esta, como otras pandemias, plantea la oportunidad de reflexionar sobre cómo debemos prepararnos para enfrentar este tipo de retos y, sobre la importancia que tiene apoyar al desarrollo científico y tecnológico. Igualmente, representa una llamada de atención con respecto a la relación existente con la fauna silvestre, es clara la necesidad de regular este tipo de interacciones, puesto que, de no hacerlo, esta no será la última pandemia a la que nos enfrentemos los seres humanos.
Figura 4

Alineamiento de las secuencias de la proteína S de: a) sars-CoV-2 (humano); b) sars-CoV (humano); c) SL-CoVZC45 (murciélago); d) SL-CoVZXC21 (murciélago). Las identidades se muestran resaltadas en gris (*identidades: homologías; semejanzas). Los residuos de aminoácidos del rbd se resaltan en púrpura y los que diferencian el reconocimiento del rbd de S de sars-CoV-2 con hACE2 y del rbd de S de sars-CoV con hACE2, se resaltan en rojo (ver el texto: Asn439 y Arg426; Leu455 y Tyr442; Phe486 y Leu472; Gln493 y Asn479; Ser494 y Asp480; Gln498 y Tyr484; Asn501 y Thr487) (datos obtenidos de ncbi [2020] y de Ou et al., 2020 [pdb id 2AJF]).
Figura 5

Resumen del alineamiento de los genomas completos (arns) de: a) sars-CoV-2 (humano); b) SL-CoVZC45 (murciélago); c) SL-CoVZXC21 (murciélago); d) sars-CoV (humano) (elaboración con datos obtenidos de ncbi [2020]).

María Fernánda Batiz-Sayavedra
Estudiante de la Licenciatura en Bioquímica Clínica en la udlap. Forma parte del Programa de Honores desa rrollando el proyecto de investigación «Estudio de la actividad antituberculosa de maria.batizsa@udlap.mx


Paola Méndez Muñoz
Estudiante de la Licenciatura en Biología en la Forma parte del Programa de Honores desarrollando el proyecto de investigación «Búsqueda y desarrollo de nuevos compuestos antimicrobianos». paola.mendezmu@udlap.mx
Dra. Irene Vergara Bahena
Licenciada en Farmacia por la Universidad Autónoma del Estado de Morelos. Maestra y doctora en Ciencias por la Universidad Nacional Autónoma de México-Instituto de Biotecnología. Miembro del Sistema Nacional de Investigadores Nivel I y coordinadora de la Licenciatura en Químico Farmacéutico Biólogo de la udlap irene.vergara@udlap.mx

Dra. Ana Eugenia Ortega-Regules
Licenciada en Quimicofarmacobiología y Maestra en Biotecnología por la udlap Doctora en Química Enológica por la Universidad de Murcia (España). Posdoctora por la Universidad Autónoma Metropolitana Iztapalapa (UAM-I) y por la udlap. Coordinadora de la Licenciatura en Ciencias de la Nutrición de la udlap de 2018 a la fecha.ana.ortega@ udlap.mx

Dr. José Daniel Lozada-Ramírez
autor de correspondencia
Licenciado en Quimicofarmacobiología y Maestro en Biotecnología por la udlap Doctor en Biología Fundamental (Bioquímica y Biotecnología Enzimática) por la Universidad de Murcia (España). Director del Departamento de Ciencias Químico Biológicas de la udlap de 2012 a 2015 y decano de la Escuela de Ciencias de la udlap de 2015 a la fecha. jose.lozada@ udlap.mx
• Boheemen, S. V., Graaf, M. D., Lauber, C., Bestebroer, T. M., Raj, V. S., Zaki, A. M., … Fouchier, R. A. M. (2012). Genomic Characterization of a Newly Discovered Coronavirus Associated with Acute Respiratory Distress Syndrome in Humans. MBio, 3(6). doi: 10.1128/mbio.00473-12
• Ceccarelli, M., Berretta, M., Venanzi-Rullo E., Nunnari, G. y Cacopardo B. (2020). Differences and similarities between Severe Acute Respiratory Syndrome (sars)-CoronaVirus (CoV) and sars-CoV-2. Would a rose by another name smell as sweet? European Review for Medical and Pharmacological Sciences 24, 2781-2783.
• Ceraolo, C. y Giorgi, F. M. (2020). Genomic variance of the 2019-nCoV coronavirus. Journal of Medical Virology, 92(5), 522–528. doi: 10.1002/ jmv.25700
• Chan, J. F.-W., Kok, K.-H., Zhu, Z., Chu, H., To, K. K.-W., Yuan, S. y Yuen, K.-Y. (2020b). Genomic characterization of the 2019 novel human-pathogenic coronavirus isolated from a patient with atypical pneumonia after visiting Wuhan. Emerging Microbes & Infections, 9(1), 221-236. doi: 10.1080/22221751.2020.1719902
• Chan, J. F.-W., Yuan, S., Kok, K.-H., To, K. K.-W., Chu, H., Yang, J., … Yuen, K.-Y. (2020a). A familial cluster of pneumonia associated with the 2019 novel coronavirus indicating person-to-person transmission: a study of a family cluster. The Lancet, 395(10223), 514-523. doi: 10.1016/s0140-6736(20)30154-9
• Cui, J., Li, F. y Shi, Z.-L. (2018). Origin and evolution of pathogenic coronaviruses. Nature Reviews Microbiology, 17(3), 181-192. doi: 10.1038/ s41579-018-0118-9
• Dediego, M. L., Álvarez Enrique, Almazán Fernando, Rejas María Teresa, Lamirande, E., Roberts, A., … Enjuanes, L. (2006). A Severe Acute Respiratory Syndrome Coronavirus That Lacks the E Gene Is Attenuated In Vitro and In Vivo. Journal of Virology, 81(4), 1701-1713. doi: 10.1128/jvi.01467-06
• Drexler, J. F., Corman, V. M. y Drosten, C. (2014). Ecology, evolution and classification of bat coronaviruses in the aftermath of SARS. Antiviral Research, 101, 45-56. doi: 10.1016/j.antiviral.2013.10.013
• Flint, S. J., Enquist, L. W. (ed.), Racaniello, V. R., Rall, G. F. y Skalka, A. M. (2015). Principles of virology Washington, D. C.: ASM Press.
• Gomez, P. L., Robinson, J. M. y Rogalewicz, J. A. (2013). Vaccine manufacturing. Vaccines 44–57. doi: 10.1016/b978-1-4557-00905.00019-7
• Guo, Y.R., Cao, Q.-D., Hong, Z.-S., Tan, Y.-Y., Chen, S.-D., Jin, H.-J., … Yan, Y. (2020). The origin, transmission and clinical therapies on coronavirus disease 2019 (covid-19) outbreak –an update on the status. Military Medical Research, 7(1). doi: 10.1186/s40779-020-00240-0
• Han, S. (2015). Clinical vaccine development. Clinical and Experimental Vaccine Research, 4(1), 46. doi: 10.7774/cevr.2015.4.1.46
• Hassan, S. S., Rout, R. K. y Sharma, V. (2020). A Quantitative Genomic View of the Coronaviruses: sars-COV2. doi: 10.20944/ preprints202003.0344.v1
• Hoffmann, M., Kleine-Weber, H., Schroeder, S., Krüger, N., Herrler, T., Erichsen, S., … Pöhlmann, S. (2020). sars-CoV-2 Cell Entry Depends on ACE2 and TMPRSS2 and Is Blocked by a Clinically Proven Protease Inhibitor. Cell, 181(2). doi: 10.1016/j. cell.2020.02.052
• Hofmann, H., Pyrc, K., Hoek, L. V. D., Geier, M., Berkhout, B. y Pohlmann, S. (2005). Human coronavirus NL63 employs the severe acute respiratory syndrome coronavirus receptor for cellular entry. Proceedings of the National Academy of Sciences, 102(22), 7988–7993. doi: 10.1073/pnas.040946510
• Huynh, J., Li, S., Yount, B., Smith, A., Sturges, L., Olsen, J. C., … Donaldson, E. F. (2012). Evidence Supporting a Zoonotic Origin of Human Coronavirus Strain NL63. Journal of Virology, 86(23), 12816-12825. doi: 10.1128/jvi.00906-12
• Imai, Y., Kuba, K., Rao, S. et al. (2005). Angiotensin-converting enzyme 2 protects from severe acute lung failure. Nature 436, 112-116. https://doi.org/10.1038/nature03712
• Kan, B., Wang, M., Jing, H., Xu, H., Jiang, X., Yan, M., … Xu, J. (2006). Molecular Evolution Analysis and Geographic Investigation of Severe Acute Respiratory Syndrome Coronavirus-Like Virus in Palm Civets at an Animal Market and on Farms. Journal of Virology, 80(15), 7786–7786. doi: 10.1128/jvi.01072-06
• Khamsi, R. (2020). If a coronavirus vaccine arrives, can the world make enough? Nature, 580(7805), 578–580. doi: 10.1038/ d41586-020-01063-8
• Kuba, K., Imai, Y., Rao, S., Gao, H., Guo, F., Guan, B., … Penninger, J. M. (2005). A crucial role of angiotensin converting enzyme 2 (ACE2) in SARS coronavirus–induced lung injury. Nature Medicine, 11(8), 875–879. doi: 10.1038/nm1267
• Lau, S. K. P., Li, K. S. M., Tsang, A. K. L., Lam, C. S. F., Ahmed, S., Chen, H., … Yuen, K.-Y. (2013). Genetic Characterization of Betacoronavirus Lineage C Viruses in Bats Reveals Marked Sequence Divergence in the Spike Protein of Pipistrellus Bat Coronavirus HKU5 in Japanese Pipistrelle: Implications for the Origin of the Novel Middle East Respiratory Syndrome Coronavirus. Journal of Virology, 87(15), 8638-8650. doi: 10.1128/jvi.01055-13
• Li, W., Moore, M. J., Vasilieva, N., Sui, J., Wong, S. K., Berne, M. A., … Farzan, M. (2003). Angiotensin-converting enzyme 2 is a functional receptor for the SARS coronavirus. Nature, 426(6965), 450-454. doi: 10.1038/nature02145
• Li, W., Sui, J., Huang, I.-C., Kuhn, J. H., Radoshitzky, S. R., Marasco, W. A., … Farzan, M. (2007). The S proteins of human coronavirus NL63 and severe acute respiratory syndrome coronavirus bind overlapping regions of ACE2. Virology, 367(2), 367-374. doi: 10.1016/j.virol.2007.04.035
• Lokugamage K. G., Hage A., Schindewolf, C., Rajsbaum R. y Menachery V. D. (2020). SARS-CoV-2 is sensitive to type I interferon pretreatment. bioRxiv doi: https://doi. org/10.1101/2020.03.07.982264
• Lu, R., Zhao, X., Li, J., Niu, P., Yang, B., Wu, H., … Tan, W. (2020). Genomic characterisation and epidemiology of 2019 novel coronavirus: implications for virus origins and receptor binding. The Lancet, 395(10224), 565-574. doi: 10.1016/s0140-6736(20)30251-8
• Marra, M. A., Jones S. J., Astell C. R., Holt R. A., Brooks-Wilson A., Butterfield Y. S., Khattra J., Asano J. K., Barber S. A., Chan S. Y., … Roper, R. L. (2003). The Genome Sequence of the SARS-Associated Coronavirus. Science 300(5624), 1399-1404. doi: 10.1126/ science.1085953
• National Center for Biotechnology Information (ncbi) (2020). NCBI Visual Data Dashboard.Recuperdo de https://www.ncbi. nlm.nih.gov/labs/virus/vssi/
• National Institutes of Health (nih) (2020). Clinical Trials. Recuperado de https://www.clinicaltrials.gov/ct2/show/record/ NCT00533741
• Ou, X., Liu, Y., Lei, X. et al. (2020). Characterization of spike glycoprotein of sars-CoV-2 on virus entry and its immune cross-reactivity with sars-CoV. Nature Communications, 11 1620. https://doi.org/10.1038/s41467-020-15562-9
• Peiris, J. S. M., Guan, Y. y Yuen, K. Y. (2004). Severe acute respiratory syndrome. Nature Medicine, 10(S12). doi: 10.1038/nm1143
• Perlman, S. y Netland, J. (2009). Coronaviruses post-SARS: update on replication and pathogenesis. Nature Reviews Microbiology, 7(6), 439–450. doi: 10.1038/nrmicro2147
• Protein Data Bank in Europe (PDBe) (2020). Prefusion 2019nCoV spike glycoprotein with a single receptor-binding domain up. Recuperado de https://www.ebi.ac.uk/pdbe/entry/pdb/ 6VSB
• PyMOL. (2020) The PyMOL Molecular Graphics System, Version 2.0 Schrödinger, LLC.
• Pyrc, K., Berkhout, B. y Hoek, L. V. D. (2007). Identification of new human coronaviruses. Expert Review of Anti-Infective Therapy, 5(2), 245-253. doi: 10.1586/14787210.5.2.245
• Shang, J., Ye, G., Shi, K. et al. (2020a). Structural basis of receptor recognition by SARS-CoV-2. Nature https://doi.org/10.1038/ s41586-020-2179-y
• Shang, J., Ye, G., Shi, K., Wan, Y., Aihara, H. y Li, F. (2020b). Structure of SARS-CoV-2 chimeric receptor-binding domain complexed with its receptor human ACE2. Nature. doi: 10.2210/ pdb6vw1/pdb
• Shereen, M. A., Khan, S., Kazmi, A., Bashir, N. y Siddique, R. (2020). covid-19 infection: Origin, transmission, and characteristics of human coronaviruses. Journal of Advanced Research, 24 91-98. doi: 10.1016/j.jare.2020.03.005
• Shi, Z. y Hu, Z. (2008). A review of studies on animal reservoirs of the sars coronavirus. Virus Research, 133(1), 74-87. doi: 10.1016/j.virusres.2007.03.012
• Sun, Z., Thilakavathy, K., Kumar, S. S., He, G. y Liu, S. V. (2020). Potential Factors Influencing Repeated sars Outbreaks in China. International Journal of Environmental Research and Public Health, 17(5), 1633. doi: 10.3390/ijerph17051633
• Walls, A. C., Park, Y.-J., Tortorici, M. A., Wall, A., Mcguire, A. T. y Veesler, D. (2020). Structure, function and antigenicity of the SARS-CoV-2 spike glycoprotein. doi: 10.1101/2020.02.19.956581
• Wan Y., Shang J., Graham R., Baric R. S. y Li, F. (2020) Receptor recognition by novel coronavirus from Wuhan: 3 An analysis based on decade-long structural studies of SARS 4. Journal of Virology, 94(7) e00127-20. doi:10.1128/JVI.00127-20
• Waterhouse, A., Bertoni, M., Bienert, S., Studer, G., Tauriello, G., Gumienny, R., Heer, F.T., de Beer, T.A.P., Rempfer, C., Bordoli, L., Lepore, R. y Schwede, T. (2018). SWISS-MODEL: homology modelling of protein structures and complexes. Nucleic Acids Research 46, W296-W303.
• Wilson, L., Mckinlay, C., Gage, P. y Ewart, G. (2004). SARS coronavirus E protein forms cation-selective ion channels. Virology, 330(1), 322-331. doi: 10.1016/j.virol.2004.09.033
• World Health Organization (WHOa) (2020). Recuperado de https://www.who.int/
• World Health Organization (WHOb) (2020). Immunization, Vaccines and Biologicals.Recuperado de https://www.who.int/ immunization/diseases/en/
• World Health Organization (WHO) (c). DRAFT landscape of covid-19 candidate vaccines. Recuperado de https://www.who. int/blueprint/priority-diseases/key-action/novel-coronavirus-landscape-ncov.pdf
• Wrapp, D., Wang, N., Corbett, K., Goldsmith, J., Hsieh, C., Abiona, O., … Mclellan, J. (2020). Cryo-EM structure of the 2019-nCoV spike in the prefusion conformation. Science, 367(6483),1260-1263. doi: 10.1126/science.abb2507
• Wu, A., Peng, Y., Huang, B., Ding, X., Wang, X., Niu, P., … Jiang, T. (2020a). Genome Composition and Divergence of the Novel Coronavirus (2019-nCoV) Originating in China. Cell Host & Microbe, 27(3), 325-328. doi: 10.1016/j.chom.2020.02.001
• Wu, F., Zhao, S., Yu, B., Chen, Y.-M., Wang, W., Song, Z.-G., … Zhang, Y.-Z. (2020b). A new coronavirus associated with human respiratory disease in China. Nature, 579(7798), 265–269. doi: 10.1038/s41586-020-2008-3
• Zhang, T., Wu, Q. y Zhang, Z. (2020). Probable Pangolin Origin of SARS-CoV-2 Associated with the covid-19 Outbreak. Current Biology, 30(7). doi: 10.1016/j.cub.2020.03.022
• Zheng, Y., Ma, Y., Zhang, J. et al. covid-19 and the cardiovascular system. Nat Rev Cardiol 17, 259–260 (2020). https://doi. org/10.1038/s41569-020-0360-5
• Zhou, P., Yang, X.-L., Wang, X.-G., Hu, B., Zhang, L., Zhang, W., … Shi, Z.-L. (2020). A pneumonia outbreak associated with a new coronavirus of probable bat origin. Nature, 579(7798), 270–273. doi: 10.1038/s41586-020-2012-7
• Zhou, P., Li, H., Wang, H., Wang, L. F. y Shi, Z. (2012). Bat severe acute respiratory syndrome-like coronavirus ORF3b homologues display different interferon antagonist activities. Journal of General Virology, 93(2), 275-281. https://doi.org/10.1099/ vir.0.033589-0
• Zhu, F. C., Li, Y. H., Guan, X. H., Hou, L. H., Wang, W. J., et al. (2020). Safety, tolerability, and immunogenicity of a recombinant adenovirus type-5 vectored covid-19 vaccine: a dose-escalation, open-label, non-randomised, first-in-human trial. The Lancet https://doi.org/10.1016/S0140-6736(20)31208-3
• Zuckerman, A. J., Banatvala, J. E., Pattison, J. R. Griffiths, P. D. y Schoub, B. D. (2004). Principles and practice of clinical virology John Wiley & Sons Ltd.