sars-CoV and sars-CoV-2 3CLpro related inhibitors and their possible utility in the treatment of covid-19 infections.


sars-CoV and sars-CoV-2 3CLpro related inhibitors and their possible utility in the treatment of covid-19 infections.
Por: Jorge Luis Mejía-Méndez • Erwin Josuan Pérez-Cortés
RESUMEN
La replicación y maduración viral de los coronavirus está condicionada por las proteasas PLpro y 3CLpro, respectivamente. El diseño de agentes terapéuticos con actividad inhibitoria de dichas estructuras comenzó durante las infecciones por sars-CoV (2002) y MErs-CoV (2012). Sin embargo, a finales de 2019 se identificó un nuevo coronavirus denominado sarsCoV-2, el cual ha sido responsable de una alta tasa de mortalidad a nivel global como consecuencia de la escasez de tratamientos específicos. De esta manera, y gracias a los avances respecto al entendimiento del ciclo de infección, replicación viral y homología con sars-CoV, múltiples investigaciones alrededor del mundo se han enfocado en retomar la información correspondiente sobre moléculas con potencial inhibitorio, especialmente aquellas dirigidas a la proteasa 3CLpro El progreso realizado en años pasados puede ser de utilidad para el seguimiento terapéutico de la población afectada por la infección covid-19.
PALABRAS CLAVE
COVID-19 · SARS-CoV-2 · SARS-CoV · Inhibidores de proteasa · 3CLpro
ABSTRACT
Proteases are indispensable for the viral life cycle and essential role in viral replication and maturation. Protease inhibitors design started during sars -CoV (2002) and MErs -CoV (2012) infections. Unfortunately, at the end of 2019 a new coronavirus was identified as sars-CoV-2, which has been responsible for a high mortality rate globally as a consequence of the lack of specific treatment. Therefore, the advances in the understanding of the cycle of infection and viral replication obtained in the past, has been useful on multiple investigations around the world which are focused on retaking the existing information on molecules with inhibitory potential, especially targeting protease 3CLpro as a result of its high homology with sars-CoV. The progress made in past years can be useful for therapeutic monitoring of the population affected by the covid-19 infection.
KEY WORDS
COVID-19 · SARS-CoV-2 · SARS-CoV · Protease inhibitors · 3CLpro
INTRODUCCIÓN
Ante un brote viral, es importante establecer rápidamente si éste es causado por un virus nuevo o previamente conocido, ya que esto ayuda a decidir qué enfoques y acciones son más apropiados para detectar el agente causal, controlar su transmisión y limitar las posibles consecuencias de la epidemia. La evaluación de la novedad del virus también tiene implicaciones para definir las prioridades de su investigación en áreas como virología y salud pública. Por lo tanto, se requiere implementar una serie de medidas como las que propone la «Organización Mundial de la Salud» (oMs) destinadas a cuatro áreas críticas, por ejemplo: prepararse y estar listo; detectar, proteger y tratar; reducir la transmisión y finalmente, innovar y aprender (Gorbalenya et al., 2020). El 31 de diciembre de 2019, se identificaron 27 casos de neumonía de etiología desconocida en la ciudad de Wuhan, provincia de Hubei en China cuya población supera los once millones de personas. Estos pacientes se presentaron con síntomas clínicos de tos seca, disnea y fiebre. Los casos se vincularon al mercado de alimentos marinos de la misma ciudad, el cual comercializa pescado y una variedad de especies de animales vivos, incluidas aves de corral, murciélagos, marmotas y serpientes (Smith y Judd, 2020). El 7 de enero de 2020, las autoridades sanitarias chinas confirmaron que este grupo estaba asociado con un nuevo coronavirus, 2019-nCoV. Posteriormente, el virus pasó a llamarse sars-CoV-2, puesto que es similar al virus causante del síndrome respiratorio agudo severo (sars-CoV) mientras que su infección se denominó covid-19 (Sohrabi et al., 2020).
Hasta el 27 de mayo de 2020, como parte de su reporte, la Organización Mundial de la Salud (oMs, 2020) dio a conocer que las infecciones a nivel global por sars-CoV-2 confirmadas son 5,488,825 mientras que 349,095 casos han terminado en muerte. La preocupación y emergencia internacional de dichas cifras han llevado a la comunidad científica al desarrollo de múltiples investigaciones que impulsen el entendimiento estructural del nuevo coronavirus con el objetivo de diseñar nuevos fármacos y/o considerar los ya existentes para el tratamiento de las infecciones covid-19, ya sea a nivel del sistema inmunitario humano o en el bloqueo de
31 de diciembre de 2019, se identificaron 27 casos de neumonía de etiología desconocida en la ciudad de Wuhan, provincia de Hubei en China
El 7 de enero de 2020, las autoridades sanitarias chinas confirmaron que este grupo estaba asociado con un nuevo coronavirus, 2019-nCoV

27 de mayo de 2020, la Organización Mundial de la Salud (oms, 2020) dio a conocer que las infecciones a nivel global confirmadas son 5,488,825 349,095 casos han terminado en muerte

las vías de señalización celular necesarias para la replicación del virus (Wu et al., 2020). De esta manera, se han determinado distintos blancos terapéuticos, en sars-CoV-2 como, por ejemplo, los inhibidores de la proteasa 3CLpro, de la cual ya se han obtenido avances significativos durante el estudio de las infecciones por sarsCoV en años pasados y se ha caracterizado por ser un dominio catalítico altamente conservado y fundamental en el mecanismo de replicación de los coronavirus (Liu et al., 2005). Por ello, su inhibición representa una línea extensa de resultados innovadores que con los análisis correspondientes pueda ser de utilidad para enfrentar la pandemia vivida hasta el momento en el que se escriben estas palabras. Por lo tanto, a continuación, se presenta una revisión bibliográfica sobre el diseño de nuevos agentes terapéuticos especialmente los dirigidos hacia la proteasa viral principal 3CLpro de sars-CoV-2 así como su relación con estudios, ya realizados, con el mismo propósito durante el brote de sars-CoV en 2002.
LOS CORONAVIRUS (CoV) SON UN GRUPO
DIVERSO DE VIRUS
PERTENECIENTES
A LA FAMILIA CORONAVIRIDAE
SUBFAMILIA ORTHOCORONAVIRINAE.
Los coronavirus (CoV) son un grupo diverso de virus pertenecientes a la familia Coronaviridae subfamilia Orthocoronavirinae. Estructuralmente son virus esféricos de 100-160 nm de diámetro, con envoltura y contienen arN monocatenario (ssRNA) de polaridad positiva de entre 26 y 32 kilobases de longitud (Organización Mundial de la Salud, 2020; Lv et al., 2020). Según las características del serotipo y genoma, la subfamilia de coronavirus se divide en cuatro géneros: α, β, γ y δ. Hay seis tipos de coronavirus que se sabe que infectan a los humanos, incluidos 229E, NL63, OC43, HKU1, MErsCoV y sars-CoV. El nuevo coronavirus aislado del tracto respiratorio inferior de pacientes con neumonía no identificada en Wuhan es un nuevo tipo de coronavirus (sars-CoV-2) que pertenece al género β (Centro de Coordinación de Alertas y Emergencias Sanitarias, 2020; Deng et al., 2020). Su identificación fue rápida puesto que las investigaciones moleculares ya realizadas durante el brote de síndrome respiratorio agudo grave (sars) ocasionada por sars-CoV en 2003 facilitaron evidenciar el alto porcentaje de homología en su secuencia genética (Zhang et al., 2020).
En cuanto a su análisis genómico y proteómico se ha evidenciado que sars-CoV-2 codifica aproximadamente 25 proteínas necesarias para llevar a cabo la infección en humanos y consecuentemente, su replicación (Parks y Smith, 2020). Asimismo, el genoma del nuevo coronavirus es similar a otros de la misma familia pues está conformado por al menos diez marcos de lectura abiertos (orFs, por sus siglas en inglés) de los cuales algunos son necesarios para la expresión de poliproteínas involucradas en la formación del complejo replicasa-transcriptasa (rTc, por sus siglas en inglés) cuyo objetivo es favorecer el ensamblaje de proteínas virales en el organismo infectado. No obstante, también codifican proteínas que a pesar de ser consideradas como no esenciales para la replicación, se ha demostrado que confieren cierta ventaja en cuanto a la sobrevivencia del virus en sistemas in vivo (Malik, 2020; Sawicki et al., 2005; Lee y Treanor, 2016). Por otra parte, investigaciones pasadas han demostrado que la mayoría de los CoV requieren de al menos cuatro proteínas estructurales para producir una partícula viral estructuralmente completa (ver figura I), lo que sugiere que algunos CoV pueden codificar proteínas adicionales con funciones compensatorias superpuestas en el ciclo de replicación del virus.
Figura 1. Proteínas estructurales de la partícula viral SARS-CoV-2 y unión de la proteína (S) a la enzima convertidora de angiotensina 2 (ace2, por sus siglas en inglés) (elaboración propia con información de Malik, 2020).
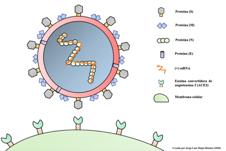
De esta manera, las proteínas estructurales comúnmente reportadas por su importancia estructural son las siguientes: S (espiga), M (matriz), E (envoltura) y N (nucleocápside). Cada una de ellas cuenta con características y propiedades distintivas (ver tabla I) que son reconocidas durante el ciclo de infección de sarsCoV-2 (Tilocca et al., 2020; Wang et al., 2020). Inicialmente, es crucial considerar que la infección covid-19 está condicionada por la expresión de la enzima convertidora de angiotensina 2 (acE2, por sus siglas en inglés) misma que es altamente expresada en la superficie extracelular de distintos orgános como los pulmones, cerebro, corazón, riñones e intestino, lo que a su vez explicaría la fisiopatología sistémica de otros coronavirus (Li et al., 2020; Hamming et al., 2004). Por consiguiente, la subunidad S1 de la proteína viral (S) es el segmento responsable de la unión al receptor acE2 garantizando la entrada celular de sars-CoV-2 en el huésped (Lu et al., 2020; Li et al., 2019). De manera simultánea, la subunidad S2 es activada por la TMPrss2 (proteasa transmembrana de serina 2 asociada a la superficie del huésped). Juntas, estas acciones dan como resultado la fusión completa de la membrana viral y la liberación del genoma de arN en el citoplasma de
la célula huésped. Posteriormente, la maquinaria celular de traducción del huésped es secuestrada para la síntesis de las poliproteínas y proteasas virales esenciales. De las cuales, las poliproteínas (PP1a y PP1ab) se dividen en 16 proteínas efectoras no estructurales mediante las proteasas 3CLpro y PLpro, lo que les permite formar el complejo de replicación junto con la arN polimerasa dependiente de arN, el cual es necesario para cumplir dos funciones: (i) replicar el genoma completo de arN y (ii) generar las plantillas individuales de mARN subgenómico requeridas para la traducción de las proteínas estructurales y accesorias virales (Chen et al., 2020). Las nuevas estructuras proteicas recién sintetizadas son transferidas desde el retículo endoplasmático al aparato de Golgi, donde se ensamblan los nuevos viriones (Fehr y Perlman, 2015). Finalmente, los viriones maduros de sars-CoV-2 se exocitan y se liberan de la célula huésped al ambiente para repetir el ciclo de infección. En este contexto y dentro de los últimos meses, por motivo del desafío global de la pandemia covid-19, la prioridad de diversos laboratorios de investigación se ha enfocado en identificar compuestos químicos que interfieran con la traducción de las proteínas virales del nuevo coronavirus (Amrane et al., 2020;
PROTEÍNA ESTRUCTURAL CARACTERÍSTICAS Y PROPIEDADES
Espiga (S)
Matriz (M)
Estructura con peso molecular aproximado de 150 kDa. Su ensamblaje en homotrímeros en la superficie del virus asemeja a un «pico» y pertenece a la clasificación I de proteínas de fusión. Cuenta con dos dominios funcionales, S1 (facilita la unión al receptor) y S2 (funge como soporte estructural), respectivamente.
Estructura con peso molecular aproximado de 25-30 kDa. Cuenta con tres dominios transmembranales que mantienen la curvatura morfológica característica de los coronavirus y se encuentra unida a la nucleocápside.
Envoltura (E)
Estructura con peso molecular aproximado de 8-12 kDa. Se ha identificado por ser una proteína transmembrana que asemeja la actividad de un canal iónico posiblemente necesario para la patogénesis de SARS-CoV-2. Además, es fundamental para el ensamblaje del virión y liberación del material genético.
Participa en el empaquetamiento del genoma viral al interactuar directamente con la proteína M y nsp3, el cual es uno de los componentes que favorecen su unión al complejo replicasa-transcriptasa (RTC).
SARS-CoV-2
CODIFICA
APROXIMADAMENTE 25 PROTEÍNAS NECESARIAS PARA LLEVAR A CABO LA INFECCIÓN EN HUMANOS Y CONSECUENTEMENTE, SU REPLICACIÓN (PARKS Y SMITH, 2020).
Smith y Smith, 2020; Lee y Treanor, 2016). De ahí que uno de los blancos estructurales bajo investigación es la proteasa 3CLpro (Zhavoronkov et al., 2020).
Proteasas y sus inhibidores
Las proteasas son enzimas cuya actividad es responsable de la hidrólisis de péptidos mediante diferentes mecanismos moleculares, criterio por el cual se clasifican en distintas sub-familias: aspartato, serina, treonina, cisteína, ácido glutámico y metaloproteasas, respectivamente. En la actualidad, un gran número de estas moléculas han sido identificadas, cuyas funciones biológicas son muy diversas, interviniendo en procesos muy dispares. En el caso concreto de agentes infecciosos como los virus, las proteasas permiten la maduración de proteínas víricas a partir de los productos de la traducción de su ARN mensajero, confiriéndoles a las proteínas hidrolizadas su capacidad funcional (Fernández-García, 2015). Su actividad proteolítica puede ser regulada y/o bloqueada en casos de actividad exacerbada mediante inhibidores de proteasas (IPs). Los cuales constituyen importantes herramientas de la naturaleza pues se presentan en múltiples formas (por ejemplo tejidos de animales, plantas y microorganismos) y en diversos procesos fisiológicos normales, al igual que en aquellos de carácter patológico (Cotabarren, 2019).
El diseño de medicamentos a partir de estas estructuras considera las siguientes clasificaciones: (i) inhibidores, que imitan sustratos peptídicos naturales, (ii) e inhibidores basados en moléculas pequeñas obtenidos de modificaciones químicas de IPs existentes que posteriormente son evaluados por técnicas de cribado virtual considerando su estabilidad en términos de su energía mínima libre posible (Khanna et al., 2019). Desafortunadamente, lleva a muchos investigadores a dedicar innumerables horas a la identificación de compuestos biológicamente activos que después resultan inactivos (Berry et al., 2015).
Relación entre los inhibidores de la proteasa 3CLpro de sars-CoV y sars-CoV-2 La proteasa 3CLpro, también conocida como Mpro, es la enzima principal que se requiere para la maduración proteolítica del coronavirus al participar en la escisión de las poliproteínas PP1a y PP1ab. Recordando que otras
proteínas funcionales como la arN polimerasa, la endoribonucleasa y la exoribonucleasa se generan mediante la escisión de dichos péptidos. Por lo tanto, las investigaciones referenciadas demuestran que utilizar a la enzima 3CLpro como blanco terapéutico inhibirá la maduración viral y mejorará la respuesta inmune innata del huésped contra covid-19. Estas hipótesis no habrían sido posibles sin la obtención de la primera estructura cristalina de la proteasa 3CLpro de la cual, inicialmente se reveló que cuenta con tres dominios, pero hay un dominio α-helicoidal adicional que está involucrado en la dimerización de esta misma, mecanismo necesario para su actividad catalítica (Zhang et al., 2020). Adicionalmente, como parte de la investigación realizada por Dai et al (2020) se evidenció que los sitios activos de la proteasa en cuestión son clasificados como S1’, S1, S2 y S4, respectivamente, así como la similitud en cuanto a su alta conservación con otros coronavirus como sars-CoV y MErs-CoV (Chen et al., 2020; Kumar et al., 2016).
El diseño de las moléculas con actividad anti-CoV, surgió para el tratamiento contra los coronavirus HCoV-NL63, por motivo de la severidad de su infección pues repercuten gravemente en el tracto respiratorio superior y, a veces, inferior (Galante et al., 2016).
Sin embargo, no se le dio la prioridad necesaria a continuar las investigaciones correspondientes, a pesar de contar con avances significativos en el estudio de compuestos con tal bioactividad. Por ejemplo, los avances en la elucidación de la estructura cristalina de 3CLpro permitieron que durante la síntesis de las primeras sustancias con actividad inhibitoria -específicamente en sars-CoV- de la proteasa, se considerara grupos funcionales como el aceptor de Michael, epóxidos y cetonas con la capacidad de unirse irreversiblemente con el sitio activo de la proteasa (Akaji et al., 2008). No obstante, fue hasta noviembre de 2002, en que se documentó el primer caso conocido de síndrome respiratorio agudo severo (sars, por sus siglas en inglés) en Foshan, China, que resurgió la necesidad de contar con medicamentos en específico contra las infecciones por coronavirus puesto que, a partir de esa fecha, surgieron nuevos casos en la región continental del mismo país y posteriormente la infección comenzó a propagarse a Hong Kong y de allí
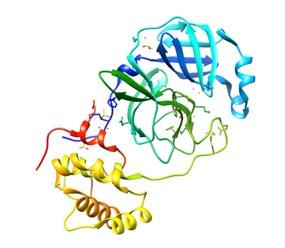
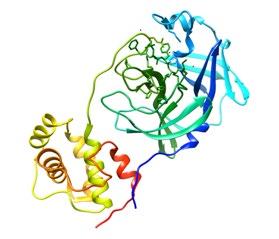
e información de Zhang et al., 2020; Yang et al. 2003). Las estructuras presentadas se obtuvieron de Protein Data Bank (PDB ID: 6M03 y 1UJ1, respectivamente). (A) (B)
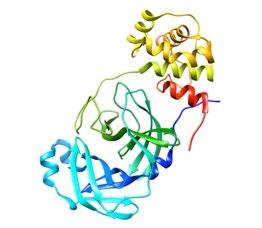
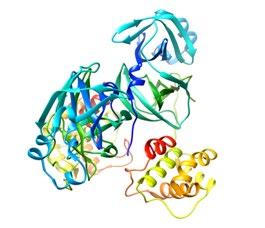
a Vietnam, Canadá y otros países. Ante la urgencia de determinar el agente causal, la oMs estableció una red de laboratorios que a través de un notable esfuerzo lograron la identificación de un nuevo coronavirus en esa fecha y se procedió a denominarlo SARSCoV. El conocimiento adquirido durante y al finalizar la pandemia sars-CoV en 2003, dio pauta para continuar con el análisis de sustancias, que bien pueden ser de distinta naturaleza (p.e. moléculas sintéticas y/o de origen natural), con la capacidad de mitigar la tasa de infección por sars-CoV donde uno de los blancos terapéuticos específicos fue la proteasa 3CLpro (Pillaiyar et al., 2016). De la cual, la evidencia consultada demuestra que al ser un coronavirus del género beta, el mecanismo de replicación e infección es similar al establecido para sars-CoV-2 (de Wit et al., 2016).
Por ello, Hall Jr., y Ji (2020) mediante modelos in silico, analizaron el porcentaje de similitud existente entre la proteasa viral principal (3CLpro) de sars-CoV-2 y su semejante sars-CoV, demostrando que su alineación estructural presenta un 98% de homología (ver figura II). De la misma manera, ul Qamar et al. (2020) a través de la construcción de un modelo 3D evidenciaron la homología de la proteasa 3CLpro entre sars-CoV-2 y otros coronavirus. Sus resultados demostraron que la similitud de dicha estructura con los coronavirus MErs-CoV, HCoV y BCoV es de 87.00%, 90.00% y 90.00%, respectivamente.
Por otra parte, Macchiagodena et al. (2020) señalaron que existen ciertas diferencias en la estructura de 3CLpro entre sars-CoV-2 y sars-CoV, específicamente en doce aminoácidos del sitio activo de la proteasa. A pesar de ello, llevaron a cabo una serie de estudios por acoplamiento molecular que les permitió elucidar la similitud en cuanto a la unión específica de sustratos, especialmente de inhibidores no-covalentes. Por consiguiente, examinaron 93 ligandos 3CLpro utilizando diagramas de correlación entre los coronavirus mencionados y de esta manera, evidenciaron que la energía libre de unión entre los ligandos y la proteasa de sars-CoV sugiere compuestos útiles para aquellos estudios destinados al diseño de moléculas contra la proteasa principal de sars-CoV-2. Por lo tanto, en la tabla II se presenta una lista de moléculas diseñadas y evaluadas en modelos in silico ante la proteasa 3CLpro con la finalidad de demostrar parte de los avances realizados en el área bioinformática de los cuales es relevante considerar que tres de ellos -remdesivir, saquinavir y darunavir- cuentan con la aprobación por la Fda debido a su actividad biológica ya demostrada. Sin embargo, se hace hincapié en considerar que los ensayos con este tipo de herramientas no garantizan necesariamente que la molécula diseñada presente su actividad en modelos in vivo y que, en general, la eficacia farmacológica y recomendaciones a seguir tendrán que estar sujetas a investigaciones futuras para evaluar su seguridad y evitar la probabilidad de que el virus desarrolle resistencia (Chen et al., 2020; International Pharmaceutical Federation, 2020).
NOMBRE DEL COMPUESTO
Diosmina Remdesivir
Hesperidina Saquinavir
MK-3207 Darunavir
Dihidroergocristina Disulfiram
Bolazina Irinotecan
R228 Lumacaftor
Ditercalinium Velpatasvir
Etopósido Eluxadolina
Tenipósido Ledipasvir
UK-432097 Atazanavir
Simeprevir Amprenavir
Indinavir Derivados de flavonoides y cumarinas
Por otra parte, ante la necesidad de contar con métodos rápidos y eficaces para determinar la inhibición de la actividad enzimática de 3CLpro Liu et al. (2005) implementaron análisis complementarios como lo es la transferencia de energía de resonancia de Förster (FrET, por sus siglas en inglés) utilizando un grupo cromóforo donador y otro aceptor a 320 nm (longitud de onda de excitación) y 425 nm (longitud de onda de emisión) para averiguar el potencial anti-sars-CoV de un conjunto de moléculas. A pesar de que sus resultados fueron amplios por la cantidad de sustancias que evaluaron, demostraron que, por este método, el fármaco hexaclorofeno y sus derivados (por ejemplo MFCD00020139, MFCD00152965, MFCD00437158, entre otros) tienen la capacidad de inhibir a la proteasa 3CLpro con una potencia mucho mayor que otros fármacos también evaluados como triclosan y nelfinavir, respectivamente. A partir del mismo fundamento, Jin et al. (2020) con modelos in silico analizaron un poco más de 10,000 compuestos, entre los cuales se encuentran desde medicamentos aprobados por la Fda -disulfiram y carmofur, específicamente- hasta moléculas de origen sintético y natural consideradas como «candidatos» pues continúan siendo evaluadas en fases clínicas (ebselen, shikonina, tideglusib, PX-12, entre otros) (ver figura III). De la misma forma, emplearon espectroscopia de masas con el objetivo de determinar el potencial inhibitorio de los fármacos an-
teriormente mencionados, y de un nuevo inhibidor denominado N3, el cual fue diseñado por el mismo grupo de investigación en publicaciones pasadas ante infecciones por sars-CoV y MErs-CoV. Como parte de los resultados, se reportó que PX-12 y carmofur se unen covalentemente a la proteasa 3CLpro de sars-CoV-2 mientras que el candidato ebselen sólo modificó parcialmente a la proteasa por interacciones no-covalentes. Por otra parte, los análisis cinéticos desarrollados les permitieron elucidar el mecanismo inhibitorio de N3, evidenciando su unión irreversible en dos etapas a la proteasa 3CLpro (ver figura II). Por ello, los autores del mismo estudio decidieron comprobar los resultados obtenidos a diferentes concentraciones de manera in vitro utilizando células Vero E6-infectadas por sars-CoV-2. El bloqueo de la replicación viral fue analizado a través de rT-Pcr, la cual, es importante señalar, es uno de los estándares de oro en el diagnóstico de las infecciones virales como covid-19 (Barrera et al., 2016; Li et al., 2020; Organización Mundial de la Salud, 2020; Zhai et al., 2020). Adicionalmente, se reportó que, mediante curvas de dosis-respuesta, ebselen y N3 mostraron el mayor efecto antiviral a una concentración efectiva de 4.67 µ M y 16.77 µ M, respectivamente. Asimismo, se detalla que su seguridad ya ha sido evaluada en fases clínicas en términos del tratamiento de pacientes con desórdenes bipolares y pérdida auditiva, por lo que sólo se sugiere su utilidad
III. (A) Proteasa 3CLpro de SARS-CoV-2 con el inhibidor carmofur
en el tratamiento de pacientes afectados por sars-CoV-2.
Históricamente, la obtención de principios activos se ha caracterizado por ser un área de inigualable valor para la síntesis de medicamentos como respuesta ante el incremento exponencial de alteraciones fisiológicas en el ser humano. La obtención de sustancias biológicamente activas puede ser a partir de fuentes de distinta índole, como por ejemplo de origen natural, especialmente de plantas medicinales cuya actividad biológica puede ser variada y de utilidad ante infecciones por microorganismos virales. Así pues, Jo et al. (2020) evidenciaron a nivel molecular, la actividad anti-sars-CoV de los flavonoides herbacetin, rhoifolin y pectolinarin, respectivamente. No obstante, llevaron a cabo la expresión de la proteasa 3CLpro en el bacteriófago T7 mientras que su purificación la realizaron por cromatografía de intercambio catiónico. El uso de herramientas por acoplamiento molecular, les permitió establecer la afinidad y mecanismo de unión de los flavonoides por la proteasa, elucidando su unión a los sitios S1 y S2 de la proteasa. Los avances anteriormente mencionados, fueron empleados por ul Qamar et al. (2020) al analizar, por medio de cribado virtual, un total de 32,297 principios activos ya identificados en plantas medicinales chinas, de los cuales la 5,7,3’,4’-tetrahidroxi-2’-(3,3-dimetilalil) isoflavona, extraída de Psorothamnus arborescens se caracterizó por ser la molécula con más alta afinidad por los residuos cys-145 e his-
41 de la proteasa 3CLpro de sars-CoV-2 ocasionando su inhibición. Los principios activos de plantas medicinales tienen el potencial de proporcionar nuevos compuestos químicos para el desarrollo de nuevos productos farmacéuticos. Asimismo, su aplicación también puede ser antimicrobiana, antifúngica, anticancerígena, antioxidante, antiparasitaria, entre otros. Su investigación ha evolucionado respecto al tiempo, pues la evidencia consultada, demuestra que una extensa gama de compuestos obtenidos de fuentes vegetales posee actividades bio/ farmacológicas, y que han sido de utilidad para la síntesis de medicamentos importantes para uso humano (Che y Zhang, 2019).
DISCUSIÓN
Los coronavirus humanos (HCoVs) son agentes patógenos que causan daños tanto en el tracto respiratorio superior como inferior. Desafortunadamente, también se han caracterizado por desancadenar síndromes entéricos y nerviosos (Zhang et al., 2020; Liu et al., 2020), de los cuales, los casos reportados pueden variar por distintos factores, como: la patogenicidad del coronavirus, dificultad de diagnóstico, vulnerabilidad y falta de tratamiento específico para los grupos poblaciones perjudicados (Jin et al., 2020; Zhang et al., 2020; Zhai et al., 2020). Su diagnóstico depende, en parte, de la intensidad de la transmisión, el número de casos y la capacidad del laboratorio, pues sólo un subconjunto de los casos sospechosos puede prio -
CORONAVIRUS HUMANOS (HCoVS) SON AGENTES PATÓGENOS QUE CAUSAN DAÑOS TANTO EN EL TRACTO RESPIRATORIO SUPERIOR COMO INFERIOR.
USUALMENTE, LOS PROYECTOS ENFOCADOS EN EL DISEÑO DE FÁRMACOS CON POTENCIAL ANTIVIRAL PUEDEN TOMAR MÁS DE DIEZ AÑOS.
rizarse para las pruebas correspondientes (Organización Mundial de la Salud, 2020). La incidencia de otros miembros del género Betacoronavirus, como sars-CoV ha expandido el conocimiento a nivel estructural de los mecanismos involucrados en sus procesos de replicación, infección y transmisión, así como en el diseño de agentes terapéuticos que sean de utilidad en el seguimiento terapéutico de las personas infectadas. Los avances tecnológicos y científicos posibilitaron que el 7 de enero de 2020, se identificara a un nuevo coronavirus, sars-CoV-2 y que, poco después, se publicara su primera secuencia genética y se estableciera su similitud con el género de los coronavirus (Konrad et al., 2020). A pesar de su alta mortalidad y morbilidad en el mundo, y de contar con estrategias novedosas como terapias con anticuerpos monoclonales, no se han aprobado vacunas efectivas ni agentes terapéuticos antivirales específicos para tratar la infección covid-19 o cualquier otra infección humana por CoV hasta la fecha (Shanmugaraj et al., 2020).
Pese a ello, y dada la preocupante mortalidad de sars-CoV-2 se ha optado por la administración de interferón, antibióticos de amplio espectro y medicamentos antivirales para reducir la carga viral y sintomatología del paciente.
Además, de acuerdo con la oMs, la confirmación rutinaria de los casos de covid-19 se realiza a partir de las muestras obtenidas de las vías respiratorias superiores e inferiores de los pacientes para, posteriormente, llevar a cabo la detección de secuencias únicas de arN del virus por pruebas de amplificación de ácido nucleico o NaaT (por sus siglas en inglés: nucleic acid amplification tests) donde los genes virales a identificar hasta el momento que realiza la presente revisión son N, E, S y RdRP. Sin embargo, la población en pleno 2020 se ha visto afectada por las consecuencias que trae consigo la investigación científica puesto que, en el 29 de febrero del presente año, mediante ensayos in vitro e in vivo, Gao et al. (2020) reflejaron que la administración de cloroquina era prometedora para el bloqueo de la infección covid-19 mejorando los hallazgos de las imágenes pulmonares y conversión negativa al virus. Durante el transcurso de semanas posteriores, Mehra et al. (2020), a través del análisis multinacional de 671 hospitales localizados en distintos puntos de los continentes, reportaron que los pacientes bajo tratamiento con cloroquina o su coadministración con macrólidos incrementaron la mortalidad y riesgo de arritmias ventriculares en los pacientes infectados por sarsCoV-2. Es alarmante que la complementariedad entre el diagnóstico y propuestas terapéuticas específicas siga siendo insuficiente para reducir y mitigar la infección covid-19. Por ello, se deberá recurrir a la innovación de moléculas con potencial anti-CoV.
El acoplamiento molecular fue diseñado en 1982 con el objetivo de ser rápido (segundos e incluso menos por cada compuesto) lo cual es deseable ante la pandemia covid-19 en la que se requiere de estudiar miles de moléculas en periodos de tiempo cortos. Existen numerosos métodos computacionales como docK Glide, AutoDock, FlexX, icN, PMF, GoLd, entre otros cuya aplicación radica en explorar múltiples conformaciones y orientaciones de ligandos que no necesariamente tienen que estar dirigidos a un receptor en particular, pues el conoci-
miento termodinámico y bioquímico necesario de las especies químicas bajo estudio permiten evaluar miles de interacciones ligando-receptor. Asimismo, son de utilidad para determinar la influencia de moléculas externas (por ejemplo agua, iones, cofactores, entre otros) en la interacción proteína-ligando (Mobley y Dill, 2009). Usualmente, los proyectos enfocados en el diseño de fármacos con potencial antiviral pueden tomar más de diez años, de ahí la necesidad de considerar los avances obtenidos en el pasado durante las infecciones por otros coronavirus, especialmente aquellos con un alto porcentaje de homología a nivel genético, como con sars-CoV. No obstante, en la elucidación de moléculas, los modelos in silico también pueden ser de utilidad para evaluar todos y cada uno de los fármacos con actividad biológica ya demostrada y aprobada en cuanto a sus propiedades farmacocinéticas, farmacodinámicas, efectos adversos e intervalos de dosificación (Srinivasan et al., 2020). Asimismo, la disposición de información en cuanto a los avances realizados se ve facilitada por bases de datos, como «por ejemplo» el Centro Nacional para la Información Biotecnológica (NcBi, por sus siglas en inglés), en el cual se encuentran almacenados los resultados respecto a la secuenciación de aminoácidos que conforman la estructura no sólo del nuevo coronavirus, sino también de otros de ellos. Esto a su vez, favorece que los avances realizados en laboratorios alrededor del mundo en cuanto al diseño de fármacos y modelamiento molecular -especialmente de los dirigidos hacía la proteasa 3CLpro puedan ser consultados en bases de datos como Protein Data Bank (PdB, por sus siglas en inglés), el cual también funge como repositorio del estudio de proteínas y otras macromoléculas de importancia biológica que han sido analizadas por métodos como cristalografía de rayos X, espectroscopia de resonancia magnética nuclear (rMN), criomicroscopía electrónica, por mencionar algunos.
De esta manera, la evidencia consultada demuestra que la conformación y funcionali-
dad viral de la familia de los coronavirus está directamente relacionada con la participación de componentes proteicos como 3CLpro y que su alta conservación en cuanto afinidad por substratos y actividad catalítica posibilita a químicos y biólogos computacionales llevar a cabo la traducción de información sobre la conformación y configuración de estructuras proteicas.
Los avances en el análisis estructural de los coronavirus han permitido a la comunidad científica elucidar y explicar la similitud de los mecanismos involucrados en la patogenicidad de los miembros del género, especialmente sars-CoV y sars-CoV-2. La homología entre ambos coronavirus es observada en distintos componentes estructurales, dentro de los cuales destaca la proteasa 3CLpro. El diseño de fármacos y el uso de herramientas computacionales desempeñó un papel fundamental durante la epidemia sars-CoV en 2002, por ello, se recopilaron y analizaron librerías bastante amplias tanto de compuestos con actividad antiviral como otros aún considerados como experimentales, de los cuales gran parte están dirigidos a la proteasa 3CLpro. La disponibilidad de estructuras cristalizadas y metodologías complementarias ya empleadas en investigaciones pasadas son de utilidad para el diseño de nuevos fármacos ante el incremento exacerbado de las infecciones covid-19. Finalmente, los análisis computacionales fungen como soporte principal de las líneas de investigación dirigidas al descubrimiento de principios activos con la capacidad de que, en futuro cercano, disminuyan la tasa de mortalidad generada por el nuevo coronavirus.

Jorge Luis Mejía Méndez
Licenciado en Ciencias Farmacéuticas por la udLaP. Actualmente es estudiante del Doctorado en Biomedicina Molecular en la misma institución donde su investigación se encuentra dirigida a la obtención, identificación y encapsulación de principios activos de plantas medicinales. jorge.mejiamz@udlap.mx

Erwin Josuan Pérez Cortés autor de correspondencia
Doctor en Ciencias Fisiológicas, participa como revisor del medio de comunicación en fisiología Fisiología DJ. Coordinador del Posgrado de la Escuela de Ciencias de la udLaP erwin.perez@udlap.mx
REFERENCIAS
• Akaji, K., Konno, H., Onozuka, M., Makino, A., Saito, H. y Nosaka, K. (2008). Evaluation of peptide-aldehyde inhibitors using R188I mutant of SARS 3CL protease as a proteolysis-resistant mutant. Bioorganic & medicinal chemistry, 16(21), 9400-9408.
• Amrane, S., Tissot-Dupont, H., Doudier, B., Eldin, C., Hocquart, M., Mailhe, M., ... y Lagier, J. C. (2020). Rapid viral diagnosis and ambulatory management of suspected COVID-19 cases presenting at the infectious diseases referral hospital in Marseille, France,-January 31st to March 1st, 2020: A respiratory virus snapshot. Travel Medicine and Infectious Disease, 101632.
• Barrera, G., Murcia, J., Cerón, J., Cuartas, P., Guzmán, C. y Villamizar, L. (2016). PCR en tiempo real: una metodología útil para la detección y cuantificación de granulovirus. Revista Colombiana de Biotecnología, 18(2), 24-31.
• Berry, M., Fielding, B. y Gamieldien, J. (2015). Practical considerations in virtual screening and molecular docking. Emerging Trends in Computational Biology, Bioinformatics, and Systems Biology; Tran, QN, Hamid, AR, Eds, 487-502.
• Calligari, P., Bobone, S., Ricci, G. y Bocedi, A. (2020). Molecular Investigation of SARS–CoV-2 Proteins and Their Interactions with Antiviral Drugs. Viruses, 12(4), 445.
• Centro de Coordinación de Alertas y Emergencias Sanitarias. Informe técnico. Enfermedad por coronavirus, COVID-19. Ministerio de Sanidad. Recuperado de: https://www.mscbs.gob. es/profesionales/saludPublica/ccayes/alertasActual/nCov-China/documentos/20200317_ITCoronavirus.pdf
• Chen, Y. W., Yiu, C. P. B. y Wong, K. Y. (2020). Prediction of the SARS-CoV-2 (2019-nCoV) 3C-like protease (3CL pro) structure: virtual screening reveals velpatasvir, ledipasvir, and other drug repurposing candidates. F1000Research, 9.
• Che, C. T. y Zhang, H. (2019). Plant natural products for human health. International journal of molecular sciences.
• Cotabarren, J. (2019). Estudio de inhibidores peptídicos de proteasas aislados de alimentos de origen vegetal: potenciales aplicaciones como agentes anticoagulantes, anti-infectivos naturales y capacidad protectora del Factor de Crecimiento Epidérmico.
• Dai, W., Zhang, B., Su, H., Li, J., Zhao, Y., Xie, X., ... y Bai, F. (2020). Structure-based design of antiviral drug candidates targeting the SARS-CoV-2 main protease. Science
• Deng, S. Q. y Peng, H. J. (2020). Characteristics of and public health responses to the coronavirus disease 2019 outbreak in China. Journal of clinical medicine, 9(2), 575.
• Fernández-García, M. (2015). Fármacos inhibidores de proteasas virales. Optimización de su relación estructura-actividad. Recuperado de: http://147.96.70.122/Web/TFG/TFG/Memoria/ MIGUEL%20FERNANDEZ%20GARCIA.pdf
• Fehr, A. R. y Perlman, S. (2015). «Coronaviruses: an overview of their replication and pathogenesis». En Coronaviruses (pp. 1-23). Nueva York: Humana Press.
• Galante, O., Avni, Y. S., Fuchs, L., Ferster, O. A. y Almog, Y. (2016). Coronavirus NL63-induced adult respiratory distress syndrome. American journal of respiratory and critical care medicine, 193(1), 100-101.
• Gao, J., Tian, Z. y Yang, X. (2020). Breakthrough: Chloroquine phosphate has shown apparent efficacy in treatment of COVID-19 associated pneumonia in clinical studies. BioScience Trends
• Gorbalenya, A. E., Baker S. C., Baric R. S, de Groot, R. J., Drosten, C., … y Ziebuhr J. (2020). The species Severe acute respiratory syndrome-related coronavirus: classifying 2019-nCoV and naming it SARS-CoV-2. Nature Microbiology, 1.
• Hall Jr., D. C., y Ji, H. F. (2020). A search for medications to treat COVID-19 via in silico molecular docking models of the SARS-CoV-2 spike glycoprotein and 3CL protease. Travel Medicine and Infectious Disease 101646.
• Hamming, I., Timens, W., Bulthuis, M. L. C., Lely, A. T., Navis, G. J. y van Goor, H. (2004). Tissue distribution of ACE2 protein, the functional receptor for SARS coronavirus. A first step in understanding SARS pathogenesis. The Journal of Pathology: A Journal of the Pathological Society of Great Britain and Ireland, 203(2), 631-637.
• International Pharmaceutical Federation. (2020). Ppdated 26 March 2020. FIP health advisory COVID-19: clinical information and treatment guidelines. Recuperado de: https:// www.fip.org/files/content/priority-areas/ coronavirus/COVID-19-Clinical information-and-treatment guidelines.pdf?fbclid=IwAR2RX9Y7sNIW08JE7V7chEliYLeFjE7n_EkJdOMoMrdjuXgFLvH6WkR7UdA
• Jin, Y. H., Cai, L., Cheng, Z. S., Cheng, H., Deng, T., Fan, Y. P., ... y Han, Y. (2020). A rapid advice guideline for the diagnosis and treatment of 2019 novel coronavirus (2019-nCoV) infected pneumonia (standard version). Military Medical Research, 7(1), 4.
• Jin, Z., Du, X., Xu, Y., Deng, Y., Liu, M., Zhao, Y., y Yang, H (2020). Structure of Mpro from SARSCoV-2 and discovery of its inhibitors. Nature
• Jin, Z., Zhao, Y., Sun, Y., Zhang, B., Wang, H., Wu, Y., ... y Duan, Y. (2020). Structural basis for the inhibition of SARS-CoV-2 main protease by antineoplastic drug Carmofur. Nature structural & molecular biology, 1-4.
• Khanna, V., Ranganathan, S. y Petrovsky, N. (2019). «Rational structure-based drug design». En Encyclopedia of bioinformatics and computational biology (pp. 585-600). Elsevier.
• Konrad, R., Eberle, U., Dangel, A., Treis, B., Berger, A., Bengs, K., ... y Sing, A. (2020). Rapid establishment of laboratory diagnostics for the novel coronavirus SARS-CoV-2 in Bavaria, Germany, February 2020. Eurosurveillance, 25(9).
• Kumar, V., Tan, K. P., Wang, Y. M., Lin, S. W., y Liang, P. H. (2016). Identification, synthesis and evaluation of SARS-CoV and MERS-CoV 3C-like protease inhibitors. Bioorganic & medicinal chemistry, 24(13), 3035-3042.
• Lee, F. E. H. y Treanor, J. J. (2016). Viral infections. Murray and Nadel’s Textbook of Respiratory Medicine 527.
• Li, Y., Zhou, W., Yang, L. y You, R. (2020). Physiological and pathological regulation of ACE2, the SARS-CoV-2 receptor. Pharmacological research 104833.
• Li, Q., Guan, X., Wu, P., Wang, X., Zhou, L., Tong, Y., ... y Xing, X. (2020). Early transmission dynamics in Wuhan, China, of novel coronavirus–infected pneumonia. New England Journal of Medicine
• Li, Z., Tomlinson, A. C., Wong, A. H., Zhou, D., Desforges, M., Talbot, P. J., ... y Rini, J. M. (2019). The human coronavirus HCoV-229E S-protein structure and receptor binding. Elife, 8, e51230.
• Liu, Y. C., Huang, V., Chao, T. C., Hsiao, C. D., Lin, A., Chang, M. F. y Chow, L. P. (2005). Screening of drugs by FRET analysis identifies inhibitors of SARS-CoV 3CL protease. Biochemical and biophysical research communications, 333(1), 194-199.
• Liu, Y., Yang, Y., Zhang, C., Huang, F., Wang, F., Yuan, J., ... y Zhang, Z. (2020). Clinical and biochemical indexes from 2019-nCoV infected patients linked to viral loads and lung injury. Science China Life Sciences, 63(3), 364-374.
• Lobo-Galo, N., Terrazas-López, M., Martínez-Martínez, A. y Díaz-Sánchez, Á. G. (2020). FDA-approved thiol-reacting drugs that potentially bind into the SARS-CoV-2 main protease, essential for viral replication. Journal of Biomolecular Structure and Dynamics (just-accepted), 1-12.
• Lu, R., Zhao, X., Li, J., Niu, P., Yang, B., Wu, H., ... y Bi, Y. (2020). Genomic characterisation and epidemiology of 2019 novel coronavirus: implications for virus origins and receptor binding. The Lancet, 395(10224), 565-574.
• Lv, D. F., Ying, Q. M., Weng, Y. S., Shen, C. B., Chu, J. G., Kong, J. P., ... y Chen, X. Q. (2020). Dynamic change process of target genes by RT-PCR testing of SARS-Cov-2 during the course of a Coronavirus Disease 2019 patient. Clinica Chimica Acta
• Macchiagodena, M., Pagliai, M. y Procacci, P. (2020). Identification of Potential Binders of the Main Protease 3CLpro of the COVID-19 via Structure-Based Ligand Design and Molecular Modeling. Chemical Physics Letters 137489.
• Malik, Y. A. (2020). Properties of Coronavirus and SARS-CoV-2. The Malaysian Journal of Pathology, 42(1), 3-11.
• Mehra, M. R., Desai, S. S., Ruschitzka, F. y Patel, A. N. (2020). Hydroxychloroquine or chloroquine with or without a macrolide for treatment of COVID-19: a multinational registry analysis. The Lancet
• Mobley, D. L. y Dill, K. A. (2009). Binding of small-molecule ligands to proteins: «what you see» is not always «what you get». Structure 17(4), 489-498.
• Organización Mundial de la Salud. (2020). Coronavirus disease 2019 (COVID-19): situation report, 128. Recuperado de: https://www.who. int/docs/default-source/coronaviruse/situation-reports/20200527-covid-19-sitrep-128. pdf?sfvrsn=11720c0a_2
• Organización Mundial de la Salud. (2020). Global surveillance for COVID-19 caused by human infection with COVID-19 virus: interim guidance, 20 March 2020 (No. WHO/2019-nCoV/SurveillanceGuidance/2020.6). World Health Organization.
• Organización Mundial de la Salud. (2020). Laboratory testing for coronavirus disease 2019 (COVID-19) in suspected human cases: interim guidance, 19 March 2020 (No. WHO/COVID-19/ laboratory/2020.5). World Health Organization.
• Parks, J. M. y Smith, J. C. (2020). How to Discover Antiviral Drugs Quickly. New England Journal of Medicine
• Pillaiyar, T., Manickam, M., Namasivayam, V., Hayashi, Y. y Jung, S. H. (2016). An Overview of Severe Acute Respiratory Syndrome–Coronavirus (SARS-CoV) 3CL Protease Inhibitors: Peptidomimetics and Small Molecule Chemotherapy. Journal of medicinal chemistry, 59(14), 6595-6628.
• Sawicki, S. G., Sawicki, D. L., Younker, D., Meyer, Y., Thiel, V., Stokes, H. y Siddell, S. G. (2005). Functional and genetic analysis of coronavirus replicase-transcriptase proteins. PLoS pathogens, 1(4).
• Shanmugaraj, B., Siriwattananon, K., Wangkanont, K. y Phoolcharoen, W. (2020). Perspectives on monoclonal antibody therapy as potential therapeutic intervention for Coronavirus disease-19 (COVID-19). Asian Pacific Journal of Allergy and Immunology, 38(1), 10-18.
• Smith, M. y Smith, J. C. (2020). Repurposing therapeutics for COVID-19: supercomputer-based docking to the SARS-CoV-2 viral spike protein and viral spike
• Smith, J. A. y Judd, J. (2020). COVID-19: Vulnerability and the power of privilege in a pandemic. Health Promot J Austral DOI:10.1002/hpja.333
• Sohrabi, C., Alsafi, Z., O’Neill, N., Khan, M., Kerwan, A., Al-Jabir, A., ... y Agha, R. (2020). World Health Organization declares global emergency: A review of the 2019 novel coronavirus (COVID-19). International Journal of Surgery
• Srinivasan, S., Cui, H., Gao, Z., Liu, M., Lu, S., Mkandawire, W., ... y Korkin, D. (2020). Structural Genomics of SARS-CoV-2 Indicates Evolutionary Conserved Functional Regions of Viral Proteins. Viruses, 12(4), 360.
• Tilocca, B., Soggiu, A., Musella, V., Britti, D., Sanguinetti, M., Urbani, A. y Roncada, P. (2020). Molecular basis of COVID-19 relationships in different species: a one health perspective. Microbes and Infection
• ul Qamar, M. T., Alqahtani, S. M., Alamri, M. A. y Chen, L. L. (2020). Structural basis of SARS-CoV-2 3CLpro and anti-COVID-19 drug discovery from medicinal plants. Journal of Pharmaceutical Analysis
• Wang, F., Chen, C., Tan, W. et al. (2016). Structure of Main Protease from Human Coronavirus NL63: Insights for Wide Spectrum Anti-Coronavirus Drug Design. Sci Rep, 6 22677. DOI: https:// doi.org/10.1038/srep22677
• de Wit, E., van Doremalen, N., Falzarano, D. y Munster, V. J. (2016). SARS and MERS: recent insights into emerging coronaviruses. Nature Reviews Microbiology, 14(8), 523.
• Rabaan, A. A., Al-Ahmed, S. H., Haque, S., Sah, R., Tiwari, R., Malik, Y. S., ... y Rodriguez-Morales, A. J. (2020). SARS-CoV-2, SARS-CoV, and MERSCoV: a comparative overview. Infez Med, 28(2), 174-84.
• Wu, C., Liu, Y., Yang, Y., Zhang, P., Zhong, W., Wang, Y., ... y Zheng, M. (2020). Analysis of therapeutic targets for SARS-CoV-2 and discovery of potential drugs by computational methods. Acta Pharmaceutica Sinica B
• Yang, H., Yang, M., Ding, Y., Liu, Y., Lou, Z., Zhou, Z., ... y Gao, G. F. (2003). The crystal structures of severe acute respiratory syndrome virus main protease and its complex with an inhibitor Nueva York: Protein DataBank.
• Zhavoronkov, A., Zagribelnyy, B., Zhebrak, A., Aladinskiy, V., Terentiev, V., Vanhaelen, Q., ... y Bishop, M. (2020). Potential non-covalent SARS-CoV-2 3C-like protease inhibitors designed using generative deep learning approaches and reviewed by human medicinal chemist in virtual reality.
• Zhai, P., Ding, Y., Wu, X., Long, J., Zhong, Y. y Li, Y. (2020). The epidemiology, diagnosis and treatment of COVID-19. International Journal of Antimicrobial Agents, 105955.
• Zhang, J. J., Dong, X., Cao, Y. Y., Yuan, Y. D., Yang, Y. B., Yan, Y. Q., ... y Gao, Y. D. (2020). Clinical characteristics of 140 patients infected by SARS-CoV-2 in Wuhan, China. Allergy
• Zhang, L., Lin, D., Kusov, Y., Nian, Y., Ma, Q., Wang, J., ... y de Wilde, A. H. (2020). Alpha-ketoamides as broad-spectrum inhibitors of coronavirus and enterovirus replication Structure-based design, synthesis, and activity assessment. Journal of Medicinal Chemistry.
• Zhang, L., Lin, D., Sun, X., Curth, U., Drosten, C., Sauerhering, L., ... y Hilgenfeld, R. (2020). Crystal structure of SARS-CoV-2 main protease provides a basis for design of improved α-ketoamide inhibitors. Science, 368(6489), 409-412.
• Zhang, W., Du, R. H., Li, B., Zheng, X. S., Yang, X. L., Hu, B., ... y Zhou, P. (2020). Molecular and serological investigation of 2019-nCoV infected patients: implication of multiple shedding routes. Emerging microbes & infections, 9(1), 386-389.
• Zhang, B., Zhao, Y., Jin, Z., Liu, X., Yang, H. y Rao, Z. (2020). The crystal structure of COVID-19 main protease in apo form Nueva York: Protein DataBank.
• Zhao, Y., Zhang, B., Jin, Z., Liu, X., Yang, H. y Rao, Z. (2020). The crystal structure of COVID-19 main protease in complex with carmofur. Nueva York: Protein DataBank.
• Zhu, L. y Hilgenfeld, R. (2012). Crystal structures of SARS-Cov main protease complexed with a series of peptidic unsaturated esters. Nueva York: Protein DataBank.