Cannabinoids for the treatment of chronic non-cancer pain: what evidence is there for their effectiveness?


Cannabinoids for the treatment of chronic non-cancer pain: what evidence is there for their effectiveness?

¿qué evidencia existe sobre su efectividad?

Arias Soto K. et al. (2021). Cannabinoides para el tratamiento del dolor crónico no canceroso: ¿qué evidencia existe sobre su efectividad?. Entorno UDLAP, 15
El dolor crónico es un problema de salud pública altamente prevalente que no cuenta con opciones terapéuticas cien por ciento efectivas, por lo que se requiere investigar nuevos tratamientos que reemplacen o complementen los actuales. Debido a la gran cantidad de literatura disponible sobre el tema, el objetivo de esta revisión sistemática cualitativa fue concentrar y analizar los resultados de revisiones sistemáticas previas sobre la efectividad de los cannabinoides en el manejo del dolor crónico no canceroso. Siguiendo la metodología prisma se realizó una búsqueda con términos MeSH en PubMed. El análisis de las nueve publicaciones que cumplieron los criterios de inclusión arrojó que el uso de cannabinoides confiere resultados positivos de alivio del dolor a corto plazo con efectos adversos leves o moderados y generalmente bien tolerados. Sin embargo, la falta de evidencia sobre su uso prolongado permite concluir que los cannabinoides aún no pueden considerarse tratamiento de primera línea para ningún tipo de dolor crónico no canceroso.
Dolor crónico · Dolor crónico no canceroso · Cannabis · cannabinoides · Marihuana
Chronic pain is a highly prevalent public health problem that does not have one hundred percent effective therapeutic options, which is why it is necessary to investigate new treatments that replace or complement the current ones. Due to the large amount of literature available on the subject, the objective of this qualitative systematic review was to concentrate and analyze the results of previous systematic reviews on the effectiveness of cannabinoids in the management of chronic non-cancer pain. Following the PRISMA methodology, a PubMed search was carried out using MeSH entry terms. Analysis of the nine publications that met the inclusion criteria found that the use of cannabinoids confers positive short-term pain relief results with mild or moderate adverse effects and generally well tolerated. However, the lack of evidence on the effects of their long-term use, lead to the conclusion that cannabinoids cannot yet be considered first-line treatment for any type of non-cancer chronic pain.

EN MÉXICO NO SE HAN PUBLICADO FORMALMENTE ESTUDIOS EPIDEMIOLÓGICOS
DE CORTE NACIONAL QUE PERMITAN CONOCER
LA PREVALENCIA DEL DOLOR CRÓNICO EN EL PAÍS, SIN EMBARGO, CONSIDERANDO LA PREVALENCIA DE DIABETES EN MÉXICO Y QUE EL DOLOR NEUROPÁTICO ES SU COMPLICACIÓN
MÁS COMÚN QUE AFECTA HASTA AL 60% DE LOS PACIENTES DIABÉTICOS, SE ESTIMA QUE AL MENOS 28 MILLONES DE MEXICANOS PODRÍAN PADECER DOLOR CRÓNICO (COVARRUBIASGÓMEZ ET AL., 2015; CENETEC, 2013).
chronic pain · chronic non-cancer pain · cannabis · cannabinoids · marijuana
El dolor crónico no canceroso o no relacionado con el cáncer puede definirse como un dolor moderado o severo que dura seis meses o más y en cuya clasificación se incluyen afecciones como el dolor lumbar, dolor por osteoartritis o por artritis reumatoide, dolor neuropático, fibromialgia, esclerosis múltiple, entre otras condiciones (Stannard y Moore, 2016).
El dolor crónico representa una de las principales causas de debilidad y discapacidad, ya que éste tiende a ser de moderado a intenso con un periodo de duración de muchos años, representando una pérdida considerable de la calidad de vida (Andrew et al., 2014). Este padecimiento se ha clasificado ya, por varios autores, como un problema de salud pública porque tiende a ser altamente prevalente en la población y desgraciadamente hay pocas opciones farmacológicas y terapéuticas que además no son 100% efectivas (Andrew et al., 2013; Kalso et al., 2013). En México no se han publicado formalmente estudios epidemiológicos de corte nacional que permitan conocer la prevalencia del dolor crónico en el país, sin embargo, considerando la prevalencia de diabetes en México y que el dolor neuro-


ESTÁN EL TETRAHIDROCANNABINOL (THC) Y EL CANNABIDIOL (CBD), LAS CUALES SE ENCUENTRAN EN SU FORMA ÁCIDA EN LA PLANTA EN ESTADO FRESCO Y REQUIEREN DESCARBOXILARSE PARA «ACTIVARSE» (FDA, 2019; LEVINE Y KERRIGAN, 2020).
pático es su complicación más común que afecta hasta al 60% de los pacientes diabéticos, se estima que al menos 28 millones de mexicanos podrían padecer dolor crónico (Covarrubias-Gómez et al., 2015; cenetec, 2013).
Desde hace varios años el dolor crónico se ha tratado con opioides, paracetamol, analgésicos antiinflamatorios no esteroideos (aines), antidepresivos como la amitriptilina, y con gabapentinoides como la gabapentina y la pregabalina; sin embargo, no se han encontrado terapias farmacológicas de primera línea o complementarias que representen un resultado clínico significativo (Finnerup et al., 2010). De hecho, se presume que la prescripción excesiva de opioides para el tratamiento del dolor crónico no canceroso fue en parte lo que desencadenó la llamada «crisis o epidemia de los opioides» en EE.UU. y Canadá que tantas muertes por sobredosis ha causado (Lake et al., 2019). Además de peligrosos, los opioides son fármacos mucho más costosos (Stannard y Moore, 2016). Por lo anterior, algunas personas han empezado a sustituir el uso de opioides por cannabis para el manejo del dolor y reducir su consumo de opioides (Lake et al., 2019). El miedo a prescribir opioides también ha conducido a una prescripción excesiva de gabapentinoides para cualquier tipo de dolor, a pesar de que se trata de fármacos que causan efectos adversos neurológicos nada triviales y cuyos tratamientos con dosis altas pueden provocar síndrome de abstinencia cuando se interrumpen abruptamente (Goodman y Brett, 2017).
(centrales y periféricos) y cb2 (predominantemente periféricos) del sistema endocannabinoide humano, así como con otros receptores como gpr18, gpr55, gpr119, ppar, receptores de serotonina, receptores opioides y varios canales iónicos. Todos estos receptores y sistemas se encuentran involucrados en la modulación del dolor (Vučković et al., 2018).
El cbd y el thc tienen la misma fórmula química C21H30O2 y derivan de la misma ruta de biosíntesis, pero su estructura molecular y disposición de los átomos difiere y por lo tanto difieren sus efectos como ligando de moléculas endógenas (Levine y Kerrigan, 2020). También difieren en la abundancia con la que se encuentran en las distintas variedades de la planta. Por otra parte, cbd y thc tienen un perfil farmacocinético muy similar cuando se administran por la misma ruta (Vučković et al., 2018).
LA PLANTA DEL CANNABIS CONTIENE MÁS DE CIEN SUSTANCIAS CANNABINOIDES.
La planta del cannabis contiene más de cien sustancias cannabinoides; entre las más comunes se encuentran el tetrahidrocannabinol (thc) y el cannabidiol (cbd), las cuales se encuentran en su forma ácida en la planta en estado fresco y requieren descarboxilarse para «activarse» (fda, 2019; Levine y Kerrigan, 2020). Estos fitocannabinoides interactúan en distintas formas y afinidades con los receptores cb1
En lo que respecta a sus efectos biológicos, el thc tiene efectos eufóricos y psicoactivos porque interactúa con los receptores cb1 del sistema nervioso. El cannabinol (cbn), un metabolito del thc, tiene una acción psicoactiva más leve que éste y actúa principalmente sobre receptores cb2 que predominan en el sistema inmunológico y en la microglia cerebral. Por su parte el cbd presenta baja afinidad directa por los receptores cb1 y cb2, por lo que no tiene efectos psicoactivos ni causa dependencia física, aunque los antagoniza en presencia de thc y actúa en forma sinérgica con éste para contribuir al efecto analgésico. El cbd también regula la percepción del dolor al afectar la actividad de muchos otros receptores como 5-ht1a, trpv1, trpa1, tprm8, glyr, ppar, entre otros (Levine y Kerrigan, 2020; Vučković et al., 2018).
Hoy día existe suficiente evidencia científica básica que vincula al sistema de neurotransmisores cannabinoides con la nocicepción o proceso neuronal de percepción del dolor (Piper et al., 2017; Stockings et al. 2018). Por el contra-
rio, la patogénesis de los distintos tipos de dolor crónico es aún poco comprendida y a esto se le suman la complejidad de sus síntomas y las estrategias farmacoterapéuticas actuales de eficacia variable, con numerosos efectos secundarios, con potencial adictivo y de alto costo (Stockings et al., 2018). Por lo anterior se ha prestado más atención a la manipulación del sistema cannabinoide a través del uso de cannabis natural y sintético como modalidad terapéutica en el manejo del dolor crónico no relacionado con el cáncer.
Sin duda, uno de los grandes retos actuales del cannabis es el tema de su legalización, desde el punto de vista medicinal y recreativo, ya que sigue habiendo múltiples disputas al respecto (Sznitman & Zolotov, 2015; Ware et al., 2003). Uno de los debates principales gira en torno a su utilidad, abuso y seguridad, cuestiones que siguen sin resolverse, específicamente porque en el área de la medicina aún es muy cuestionado por los efectos adversos para la salud a corto y largo plazo (Volkow et al., 2014). Actualmente, el uso más común del cannabis es para el dolor crónico, gracias a que se condona su uso medicinal en muchos países, entre ellos Alemania, Canadá, Colombia, España, Reino Unido, Uruguay y gran parte de EE.UU. (Piper et al., 2017).
Por la relevancia del tema, se han publicado numerosos estudios clínicos y revisiones sistemáticas que evalúan la utilización del cannabis y sus derivados en distintas presentaciones para el manejo de los diferentes tipos de dolor crónico no canceroso. La pregunta común de investigación se centra en explorar si las diferentes sustancias cannabinoides demuestran ser una alternativa terapéutica segura y eficaz para la disminución y tratamiento del dolor crónico.
Debido a la gran cantidad y variabilidad metodológica en los estudios clínicos disponibles en la literatura, el objetivo de este trabajo fue concentrar, sintetizar y analizar cualitativamente los hallazgos y conclusiones de revisiones sistemáticas previas sobre la efectividad de los cannabinoides en el manejo del dolor crónico no canceroso para proporcionar un resumen definitivo que pueda usarse para guiar la práctica clínica.
MÉTODOS
Obtención de los estudios
Se realizó una revisión sistemática cualitativa conforme a los lineamientos prisma (Urrútia
y Bonfill, 2010) de revisiones sistemáticas previas acerca de la eficacia y seguridad de distintos cannabinoides en el tratamiento del dolor crónico por diferentes causas distintas del cáncer. La base de datos utilizada fue PubMed (medline) siendo la última fecha de búsqueda el 24 de junio del 2020. La estrategia de búsqueda incluyó términos MeSH (Medical Subject Headings) para «chronic pain» y «medical marijuana» o «synthetic cannabinoids» o «cannabinoids» utilizándo se la siguiente fórmula: («Chronic Pain»[Mesh]) and (((«Medical Marijuana»[Mesh]) OR synthetic cannabinoids) OR «Cannabinoids»[Mesh]). Los primeros resultados obtenidos de esta búsque da fueron posteriormente filtrados por «revisión sistemática» y «humanos». Los artículos filtrados fueron cribados conforme a los criterios de inclu sión y exclusión para su posterior análisis a tex to completo.
Selección de estudios con base en criterios de inclusión y exclusión
Los siguientes criterios fueron usados para la in clusión de estudios: 1) revisiones sistemáticas con o sin meta-análisis; 2) en idiomas español o inglés solamente; 3) dolor crónico no canceroso como tema central; y, 4) que contaran con algu nos elementos de elegibilidad del método PRIS MA como, 4.1) especificación de las característi cas del estudio con base en el acrónimo PICOS (población, intervenciones, comparación, resul tados y diseño del estudio; 4.2) descripción de las fuentes de información; 4.3) definición de la estrategia de búsqueda; 4.4) descripción de la evaluación del riesgo de sesgo (en caso de me ta-análisis); y 4.5) descripción de resultados. Los criterios de exclusión fueron: sólo abstract sumen disponible, no era una revisión sistemáti ca, o, el estudio no se enfocaba en la eficacia y/o efectos adversos de algún o algunos cannabinoi des en personas con dolor crónico no canceroso.
Extracción de datos Los datos fueron extraídos con ayuda de un for mato de elaboración propia y de manera inde pendiente por cada autor; las discrepancias fue ron resueltas por decisión colectiva. La hoja de extracción de datos incluyó: criterios picos de dolor crónico, número de participantes en la población de estudio, dosis y tipo de cannabinoi de investigados, características de los grupos de control, resultados o no de metaanálisis, bases de datos utilizadas, periodo de tiempo abarcado por las revisiones, resultados de eficacia, tolerancia y seguridad, conclusiones de los autores.


La búsqueda en PubMed arrojó 171 artículos en total, de los cuales se excluyeron 150 que no eran revisiones sistemáticas obteniendo 21 artículos. Finalmente, después del análisis a texto completo, nueve artículos fueron seleccionados tras aplicar los criterios de inclusión y exclusión (ver figura 1).
Los nueve estudios de revisión sistemática seleccionados para este trabajo incluyeron un total de 16,222 pacientes, de los cuales el 60% padecía de dolor neuropático y, el porcentaje restante incluía dolor crónico por fibromialgia, esclerosis múltiple, osteoartritis, artritis reumatoide o dolor crónico mixto. Los distintos cannabinoides investigados en cuanto a su efectividad para el manejo del dolor crónico no canceroso fueron: cannabis natural, extractos estandarizados de cannabis con combinaciones en cantidades específicas de thc y cbd, extracto de thc solo, extracto de cbd solo, nabilona (nab), dronadrn), ácido ajulémico (CT-3) y nabiximol. En la tabla 1 se presentan las características más importantes de cada una de las revisiones sistemáticas analizadas en este trabajo.
NÚMERO TOTAL DE ARTÍCULOS RECUPERADOS DE PUBMED
N=171
NÚMERO TOTAL DE REVISIONES SISTEMÁTICAS CRIBADAS
N=21
NÚMERO TOTAL DE REVISIONES
SISTEMÁTICAS A TEXTO COMPLETO EVALUADAS PARA DECIDIR SU ELEGIBILIDAD
N=14
NÚMERO TOTAL DE REVISIONES
SISTEMÁTICAS INCLUIDAS EN LA SÍNTESIS CUALITATIVA DESPUÉS DE APLICAR CRITERIOS DE INCLUSIÓN/EXCLUSIÓN N=9
Aun cuando el dolor suele definirse como crónico a partir de los 6 meses (Stannard y Moore, 2016), algunas revisiones como las de Andreae et al. (2015) y de Meng et al. (2017) se enfocaron en estudios con pacientes con dolor neuropático de por lo menos 3 meses de evolución.
Una de las intervenciones más comunes consistió en el uso del cannabis natural (planta Cannabis sativa o marihuana) inhalado, fumado o vaporizado, principalmente en forma de cigarrillos preenrollados (Lynch y Campbell, 2011; Andreae et al., 2015; Boychuk et al., 2015; Deshpande et al., 2015; Lynch y Ware, 2015; Mücke et al., 2018; Stockings et al., 2018). También fue frecuente la administración en aerosol oromucosal de la combinación de extractos de thc (figura 2a) con cbd (figura 2b) (Lynch y Campbell, 2011; Lynch y Ware, 2015; Mücke et al., 2018; Stockings et al., 2018); así como de los cannabinoides sintéticos dronabinol (drn, figura 2c) y nabilona (nab, figura 2d) (Lynch y Campbell, 2011; Boychuk et al., 2015; Lynch y Ware, 2015; Fitzcharles et al., 2016; Meng et al., 2017; Mücke et al., 2018; Stockings et al., 2018). Adicional-
ARTÍCULOS EXCLUÍDOS AL APLICAR FILTRO A LA BÚSQUEDA N=150
• NO ERAN REVISIONES SISTEMÁTICAS: 150
• NO ESTUDIOS EN HUMANOS: 0
REVISIONES SISTEMÁTICAS EXCLUÍDAS N=7
• IDIOMA DISTINTO AL INGLÉS O ESPAÑOL: 1
• TÍTULO O ABSTRACT: 6
REVISIONES SISTEMÁTICAS EXCLUÍDAS N=5
• SOBRE OPIOIDES EN GENERAL: 2
• INFORMACIÓN INSUFICIENTE: 2
• MEDICIÓN DE EFECTIVIDAD DEFICIENTE: 1
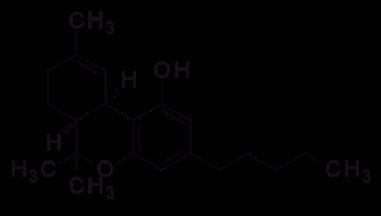
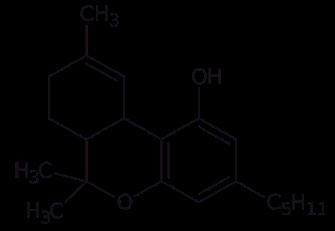
mente, la combinación fija de thc:cbd (2.7:2.5 mg) como extracto estandarizado en solución para pulverización bucal cuya denominación genérica es nabiximol, fue investigada en numerosos estudios (Boychuk et al., 2015; Fitzcharles et al., 2016; Meng et al., 2017; Stockings et al., 2018). En la revisión sistemática más reciente se incluyeron estudios que investigaron todas las modalidades de cannabinoides y vías de administración antes mencionadas (Stockings et al. 2018).
La efectividad de los cannabinoides se comparó principalmente contra placebo, contra un analgésico opioide (dihidrocodeína) (Mücke et al., 2018), contra nabilona e ibuprofeno (Lynch y Ware, 2015) y contra amitriptilina (Fitzcharles et al., 2016); en otras dos revisiones los comparadores fueron placebo o el tratamiento estándar (farmacoterapia, fisioterapia o una combinación de éstos) (Meng et al., 2017 y Stockings et al., 2018). En las restantes cuatro revisiones sólo se comparó contra placebo.
Dentro de los resultados, además del efecto sobre el dolor y su intensidad, se tomó en cuenta el impacto en las actividades de la vida diaria, en la calidad de vida y en la impresión global de cambio, así como los efectos adversos identificados. La mayoría de los estudios emplearon instrumentos estandarizados para medir la intensidad del dolor como la escala de calificación numérica para el dolor (nrs), la escala visual analógica para el dolor (vas), la escala de descriptor diferencial (dds), la escala de dolor neuropático o la escala de dolor McGill.
Dado que las revisiones sistemáticas incluidas en este trabajo se enfocaron en el tipo de
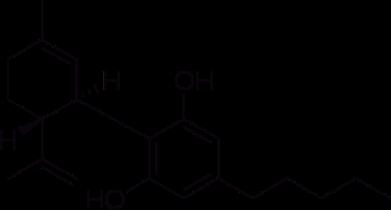
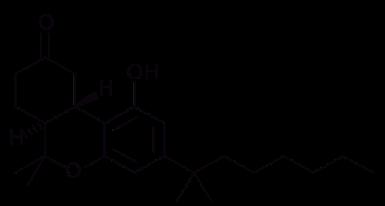
dolor que padecían los pacientes, se observó una gran variabilidad en los cannabinoides estudiados, en sus preparaciones farmacéuticas, en sus vías de administración y en sus dosis. A continuación y como complemento a la información contenida en la tabla 1, se sintetizan los hallazgos más relevantes de cada una de las nueve revisiones sistemáticas analizadas en el presente trabajo, organizadas de la más antigua a la más recientemente publicada.
Lynch y Campbell (2011)
La revisión de Lynch y Campbell tuvo como objetivo examinar sistemáticamente todos los ensayos clínicos controlados aleatorizados (eccas) disponibles en la literatura en los que se probó el uso de cannabinoides en el manejo del dolor crónico (Lynch y Campbell, 2011). Este trabajo incluyó 18 estudios, se probaron distintos cannabinoides por distintas dosis y rutas de administración encontrándose en términos generales una mejoría moderada global, en donde se alivió el dolor crónico y se mejoró la calidad del sueño. En cuanto a efectos adversos, éstos fueron pocos y tolerables, entre ellos: mareo, dolor de cabeza, cansancio, naúseas, somnolencia, sedación, boca seca, disminución de la concentración, ansiedad y efectos psicoactivos como euforia, paranoia y excitación. Por ejemplo, en uno de los ensayos clínicos que evaluaron, la nab demostró una mejora significativa en comparación con el placebo para el tratamiento de la fibromialgia, valorada a través del Cuestionario de Impacto de la Fibromialgia (FIQ, Fibromyalgia Impact Questionnaire). Respecto a los resultados relacionados
2. Estructuras químicas de los principales cannabinoides naturales (a) thc y (b) cbd y, cannabinoides sintéticos (c) drn y (d) nab, investigados en los estudios sobre su efectividad en el dolor crónico no canceroso.
EN PUBMED ARROJÓ 171 ARTÍCULOS EN TOTAL, DE LOS CUALES SE EXCLUYERON 150 QUE NO ERAN REVISIONES SISTEMÁTICAS OBTENIENDO 21 ARTÍCULOS. FINALMENTE, DESPUÉS DEL ANÁLISIS A TEXTO COMPLETO, NUEVE ARTÍCULOS FUERON SELECCIONADOS TRAS APLICAR LOS CRITERIOS DE INCLUSIÓN Y EXCLUSIÓN (VER FIGURA 1).
LOS NUEVE ESTUDIOS DE REVISIÓN SISTEMÁTICA SELECCIONADOS
PARA ESTE TRABAJO INCLUYERON UN TOTAL DE 16,222 PACIENTES, DE LOS CUALES EL 60% PADECÍA DE DOLOR NEUROPÁTICO Y EL PORCENTAJE RESTANTE INCLUÍA DOLOR CRÓNICO POR FIBROMIALGIA, ESCLEROSIS MÚLTIPLE, OSTEOARTRITIS, ARTRITIS REUMATOIDE O DOLOR CRÓNICO MIXTO.
con el nivel de funcionalidad de los pacientes, uno de los estudios demostró una mejoría significativa en comparación con placebo en 125 participantes con dolor neuropático; mientras que otro estudio no observó diferencias significativas con respecto al placebo en 48 participantes con dolor central por lesiones graves del plexo braquial. Dos estudios que utilizaron el índice de Barthel para valorar las actividades de la vida diaria, no observaron una mejora significativa ni con nab para el dolor relacionado con la espasticidad ni con los extractos oromucosales de cannabis para la esclerosis múltiple. Por lo anterior, los autores concluyeron que los cannabinoides son «modestamente eficaces y seguros» para tratar el dolor crónico sobre todo de tipo neuropático, con «evidencia preliminar de eficacia» en fibromialgia y artritis reumatoide. Sin embargo, también resaltaron que se requieren estudios de mayor duración, con muestras más grandes y en poblaciones más homogéneas para poder concluir en forma más precisa sobre la efectividad de estas sustancias. Adicionalmente, sugirieron que también se deben medir y reporta los resultados en la funcionalidad de los pacientes (Lynch y Campbell, 2011).
Esta revisión sistemática se actualizó cuatro años más tarde incluyendo once nuevos estudios y también fue incluida en el presente trabajo (Lynch y Ware, 2015).
Andreae et al. (2015)
El trabajo de Andreae et al. (2015) consistió en una revisión con metaanálisis para determinar si el Cannabis sativa inhalado proporcionó alivio a pacientes con dolor crónico neuropático en comparación con placebo. Se incluyeron eccas donde la causa del dolor fue por diabetes, trauma o relacionada con infección por virus de la inmunodeficiencia humana (vih); excluyéndose la esclerosis múltiple o condiciones del sistema nervioso central como agentes causales del dolor. Se encontró efectividad con dosis altas de cannabis (hasta 96 mg), beneficiando al paciente para el alivio del dolor con reducciones del 30%. Los efectos adversos fueron poco frecuentes, observándose deterioro de la memoria, psicosis o incluso aumento del dolor. También se informaron disminuciones a corto plazo en la atención, el rendimiento psicomotor y el aprendizaje en el grupo de dosis más alta (equivalente a 7% de thc). Sin embargo, los estudios tuvieron tamaños de muestra no idóneos y no se generó evidencia concluyente de los efectos a largo plazo. Con base en la información analizada, los autores determinaron
que el cannabis inhalado puede proporcionar alivio a corto plazo para 1 de cada 5-6 pacientes con dolor neuropático, pero también recomendaron que se necesitan más estudios que evalúen los beneficios y los riesgos a largo plazo de este tratamiento (Andreae et al., 2015).
Boychuk et al. (2015)
Boychuk et al. (2015) revisaron sistemáticamente la literatura con el objetivo de determinar la efectividad de los cannabinoides en el manejo del dolor crónico no canceroso de tipo neuropático. Adicionalmente resumieron la información disponible sobre los eventos adversos presentados en los pacientes. Los autores concentraron los resultados de 13 estudios con distintos cannabinoides. Las diferentes formas de administración de thc (cannabis, thc: cbd y thc solo) con concentraciones de 2.5% a 9.4% de thc demostraron una reducción estadísticamente significativa en la intensidad del dolor en comparación con el placebo, mejora evidenciada a través de la escala vas y de los reportes de incomodidad por el dolor por parte de los pacientes. Por su parte los cannabinoides sintéticos lograron una reducción en la intensidad del dolor mayor al 30%-50% en comparación con placebo. No se observaron efectos adversos graves y entre los más frecuentes se registraron mareos/vértigo, cansancio/somnolencia/fatiga y, boca seca (Boychuk et al., 2015). Sin embargo, los autores también concluyeron que se requieren más estudios de alta calidad para poder medir el impacto de la duración del tratamiento así como las formulaciones y vías de administración más adecuadas.
Deshpande et al. (2015)
El trabajo de Deshpande et al. (2015) tuvo como objetivo determinar si los cannabinoides no sintéticos, fumados o vaporizados fueron capaces de aliviar el dolor crónico no canceroso así como identificar las indicaciones, los efectos en la funcionalidad, las reacciones adversas y las dosis terapéuticas empleadas en los pacientes. No fue posible completar un metaanálisis sobre la efectividad del thc con los resultados de los 6 estudios incluidos en la revisión sistemática debido a la heterogeneidad de las intervenciones y la variabilidad en los resultados. En general se informaron en esta revisión reducciones estadísticamente significativas del dolor frente a placebo con hasta un 61% de los pacientes reportando un beneficio, sin embargo, las poblaciones de estudio fueron pequeñas. Asimismo, los efectos adversos psicoactivos del thc cau-
saron que los pacientes se dieran cuenta a qué grupo de estudio pertenecían, lo cual pudo haber afectado los resultados. Los autores de esta revisión enfatizaron la importancia de realizar más estudios que, además de medir el impacto en el dolor y su intensidad, midan con ayuda de escalas estandarizadas, la funcionalidad y calidad de vida, así como la impresión global de cambio o mejora por parte de los pacientes, de modo que la significancia clínica de la reducción del dolor se haga más evidente. También resaltaron la importancia de promover la realización de estudios prospectivos observacionales para crear registros de pacientes, protocolos de actuación y el reporte obligatorio de los efectos adversos; de lo contrario, al generalizarse el uso medicinal de los cannabinoides, los médicos podrían propagar sin saberlo problemas similares a los que se viven hoy día con los opioides (Deshpande et al., 2015). Los autores de esta revisión ultimaron que, aunque los cannabinoides se toleran bien a corto plazo, los efectos psicoactivos y neurocognitivos a largo plazo se desconocen. Por lo tanto, concluyeron que la evidencia disponible no respalda usar cannabinoides para todos los tipos de dolor crónico no canceroso y que los médicos deben tener cuidado con prescribir estas sustancias en pacientes cuyo dolor no es neuropático, así como considerar el potencial de abuso.
Lynch y Ware (2015)
Lynch y Ware actualizaron su trabajo previo publicado en 2011 y en esta revisión incluyeron todos los eccas que examinaron el efecto de los cannabinoides en el dolor crónico no canceroso en comparación con placebo. En esta revisión sistemática la nab probó ser superior al placebo, demostrando reducción de la intensidad del dolor con mejoras significativas en la evaluación de ansiedad y sueño. Por otra parte, el aerosol oromucosal de cannabis brindó un efecto analgésico significativo con mejoras en el sueño y reducción del dolor en comparación con el placebo al tratar el dolor neuropático. De igual forma, en esclerosis múltiple con espasticidad el extracto de cannabis vía oral (dosis de 5 a 25 mg al día de cbd y entre 29 y 72% de thc) probó que el alivio del dolor por rigidez muscular y el sueño mejoraron dos veces más con el extracto que con el placebo. El cannabis fumado con 4% de thc demostró una significativa antiespasticidad y efecto analgésico en comparación con el placebo, mientras que el cannabis vaporizado demostró una respuesta analgésica significativa en comparación con el
placebo (Lynch y Ware, 2015). Los efectos adversos más frecuentes fueron fatiga y mareo, aunque también se reportaron efectos psicoactivos y neurocognitivos, todos con intensidad de leve a moderada. Se concluyó que los cannabinoides estudiados demostraron en general efectos analgésicos significativos y que los efectos adversos relacionados con el tratamiento fueron generalmente bien tolerados. Los autores afirmaron que los cannabinoides disponibles pueden considerarse analgésicos seguros y moderadamente efectivos en el tratamiento del dolor crónico no canceroso.
Fitzcharles et al. (2016) Fitzcharles et al. (2016) establecieron como objetivo de su revisión sistemática el identificar la evidencia disponible sobre la eficacia, tolerabilidad y seguridad de los distintos tipos de sustancias cannabinoides en comparación con placebo o con cualquier medicamento autorizado. Incluyeron en su trabajo todos los eccas de al menos 2 semanas de duración donde los pacientes participantes fueran de cualquier edad y tuvieran diagnóstico de dolor crónico músculo-esquelético asociado a dolor espinal crónico (cuello y espalda), osteoartritis, artritis reumatoide o fibromialgia. Los autores informaron a partir de su revisión que, en general, con los cannabinoides se observan mejoras estadísticamente significativas, aunque no consistentes entre los estudios, en el dolor, la ansiedad y la calidad de vida relacionada con la salud. Por ejemplo, nab tuvo mejores efectos estadísticamente significativos sobre el sueño que el fármaco amitriptilina y la intensidad del dolor de columna fue significativamente menor con nab que con el placebo. Asimismo, la combinación thc:cbd fue estadísticamente significativa en superioridad frente al placebo para reducir los problemas de sueño y la puntuación de la escala das (Disease Activity Score Calculator for Rheumatoid Arthritis) en pacientes con artritis reumatoide, la cual permite medir reducciones en la actividad de la enfermedad; sin embargo, thc:cbd no logró reducir la rigidez matutina. De los 4 estudios incluidos en la revisión, sólo se informó un evento adverso grave (caída con fractura debido a mareos) asociado con nab y dos eventos adversos graves posiblemente relacionados con el placebo (Fitzcharles et al., 2016). Los autores concluyeron que la información disponible resultaba insuficiente como para poder recomendar cualquier formulación a base de cannabinoides para el manejo sintomático de pacientes con dolor crónico asociado a enfermedades reumáticas.
DENTRO DE LOS RESULTADOS, ADEMÁS DEL EFECTO SOBRE EL DOLOR Y SU INTENSIDAD, SE TOMÓ EN CUENTA EL IMPACTO EN LAS ACTIVIDADES DE LA VIDA DIARIA, EN LA CALIDAD DE VIDA Y EN LA IMPRESIÓN GLOBAL DE CAMBIO, ASÍ COMO LOS EFECTOS ADVERSOS IDENTIFICADOS.
EL USO DE CANNABINOIDES PARA EL TRATAMIENTO DEL DOLOR CRÓNICO NO CANCEROSO DEMOSTRÓ, EN LA MAYORÍA DE LOS ESTUDIOS, RESULTADOS POSITIVOS DE ALIVIO A CORTO PLAZO (ANDREAE ET AL., 2015) Y A LARGO PLAZO (BOYCHUK ET AL., 2015),
Meng et al. (2017)
Por su parte, Meng et al. (2017) establecieron el objetivo de realizar una revisión con metaanálisis sobre la eficacia analgésica y la seguridad de los cannabinoides selectivos drn, nab, y nabiximol en comparación contra placebo o contra el manejo convencional. Únicamente consideraron eccas donde se haya realizado un seguimiento de los pacientes de al menos 2 semanas tras el inicio del tratamiento. Los autores reportaron en su revisión sistemática de 11 estudios, que drn, nab, y nabiximol demostraron superioridad analgésica en comparación con el placebo en función del cambio en las puntuaciones de dolor nrs; así como mejora en la calidad de vida y del sueño. Sin embargo, el impacto en la función física y psicológica no está claro. En general, entre los diferentes cannabinoides selectivos, nabiximol y drn, pero no nab, confirieron un beneficio analgésico. La mayoría de los efectos adversos informados con los cannabinoides selectivos fueron de leves a moderados, entre ellos: mareo, dolor de cabeza, cansancio, somnolencia, boca seca, naúseas, euforia y deterioro de la memoria. Se usó la herramienta Cochrane para asignar la calidad de los estudios y evaluar el riesgo de sesgo y, los datos de 10 ensayos fueron incluidos en el metaanálisis el cual reveló una pequeña reducción de los puntajes de dolor con cannabinoides selectivos en comparación con placebo o dihidrocodeína en pacientes con dolor neuropático (Meng et al., 2017). En esta revisión se encontró evidencia de calidad moderada que sugiere que el nabiximol es efectivo reduciendo el dolor neuropático y que los otros cannabinoides podrían ser efectivos como terapia coanalgésica para el dolor neuropático refractario. Por lo anterior, los autores concluyeron que se requieren estudios más homogéneos, de mejor diseño, mayor tamaño de muestra y aleatorizados para evaluar mejor la dosis específica, la duración del tratamiento y los efectos en la función física y psicológica de los pacientes.
Mücke et al. (2018)
La revisión realizada por Mücke et al. (2018) tuvo como objetivo evaluar la eficacia, tolerabilidad y seguridad de distintas preparaciones farmacéuticas de cannabis (herbolarias, extractos o sintéticas) comparadas contra placebo o contra medicamentos convencionales empleados en el manejo del dolor crónico neuropático en adultos. Esta revisión fue auspiciada por el grupo Cochrane sobre dolor y cuidados paliativos y de soporte e incluyó eccas con una duración mínima del tratamiento de 2 semanas. Los
autores encontraron que el uso de preparaciones a base de cannabis logró disminuir el dolor de los pacientes, mostrando un 50% de mejoría vs. 17% del placebo, pero también se presentaron efectos adversos y por esta razón un 10% decidió suspender el tratamiento. El consenso de los efectos adversos más comunes para todas las formulaciones de cannabis estudiadas fue: somnolencia, sedación, confusión y psicosis. Aun así los beneficios superaron los efectos adversos. Para valorar el posible riesgo de sesgo, Mücke et al. (2018) utilizaron la herramienta de Cochrane para asignar la calidad de los estudios, encontrando que 12 de los 16 estudios analizados fueron de calidad moderada. Por lo anterior, los autores determinaron que no se encontró evidencia de alta calidad en los estudios analizados y que, aunque los beneficios de los cannabinoides probados superan sus posibles daños, se requieren más estudios con tamaños de muestra mayores y mejor diseño metodológico que no excluyan participantes con otras comorbilidades importantes y/o con historial de abuso de sustancias.
Stockings et al. (2018) Por último, la revisión sistemática más reciente hecha por Stockings et al. (2018) también fue la que mayor número de estudios incluyó (ver tabla 1), tanto eccas como estudios observacionales y, además, se realizó metaanálisis de los datos. El objetivo de este trabajo fue examinar la evidencia existente para todos los tipos de dolor crónico no canceroso, todos los tipos de sustancias cannabinoides y considerando todos los tipos de diseño experimental de los estudios incluidos. Los autores emplearon la herramienta Cochrane para asignar la calidad de los estudios y evaluar su riesgo de sesgo. Se encontró una mayor probabilidad de que el tratamiento con cannabinoides logre una reducción del 30% del dolor crónico neuropático o de otros tipos con respecto al placebo; sin embargo, esto sólo ocurrirá en el 29% de los pacientes bajo tratamiento con cannabinoides versus un 25.9% de pacientes en el grupo placebo que también experimentarán esta reducción del 30%. Para 5 estudios que reportaron una reducción del 50%, específicamente del dolor neuropático, el metaanálisis tampoco encontró diferencia significativa entre el tratamiento con cannabinoides y el tratamiento con placebo. En términos generales, sí es posible argumentar una mayor reducción en la intensidad del dolor gracias a los cannabinoides, sobre todo en pacientes con dolor neuropático; así como mejoras menores en el sueño. Sin embargo, no se evidenciaron mejoras en la funcio-
nalidad emocional o física o en la calidad de vida. Finalmente, los pacientes que recibieron cannabinoides tuvieron más probabilidades de informar eventos adversos como, por ejemplo, mareos, alteraciones en la atención, confusión y desorientación. Se concluyó que es poco probable que los cannabinoides puedan considerarse opciones altamente efectivas para el tratamiento del dolor crónico no canceroso. Los autores determinaron que es poco probable que los cannabinoides sean medicamentos altamente eficaces para el dolor crónico no canceroso y que pudieran servir como monoterapia para el tratamiento de esta condición. También concluyeron que se desconocen la eficacia y la seguridad a largo plazo de estas sustancias y que, en general, la evidencia de la efectividad de los cannabinoides en el dolor crónico no canceroso es limitada.
El uso de cannabinoides para el tratamiento del dolor crónico no canceroso demostró, en la mayoría de los estudios, resultados positivos de alivio a corto plazo (Andreae et al., 2015) y a largo plazo (Boychuk et al., 2015), reducción en la intensidad del dolor de un 30% a 50% en administración conjunta con opioides o analgésicos (Andreae et al., 2015; Mücke et al., 2018), y efecto analgésico significativo en el dolor crónico neuropático con eficacia preliminar en fibromialgia y artritis reumatoide (Lynch y Campbell, 2011., Lynch y Ware, 2015). Sin embargo, dos revisiones sistemáticas informaron que la evidencia de los estudios fue de calidad baja a moderada debido a que los resultados son inconsistentes por lo que la fuerza de recomendación es débil para el contexto clínico (Mücke et al., 2018; Meng et al., 2017). Algunos trabajos resaltaron que los beneficios de los cannabinoides son superados por sus posibles daños, no obstante, algunos de sus efectos adversos podrían limitar su utilidad clínica (Mücke et al., 2018). Stockings et al. (2018), cuya revisión es la más reciente y completa, sentencian que es poco probable que los cannabinoides constituyan opciones terapéuticas altamente efectivas para el dolor crónico no canceroso. El nabiximol, en todo caso, podría ser la alternativa con evidencia de grado moderado a alto para la que podría sustentarse su uso como terapia complementaria para reducir el dolor neuropático y el dolor relacionado con la esclerosis múltiple (Meng et al., 2017; Stockings et al., 2018).
En 7 de los 9 artículos abordados en la presente revisión sistemática se reportó que los
efectos adversos ocurrieron incluso a dosis bajas de los diferentes cannabinoides, pero fueron de severidad leve a moderada y generalmente bien tolerados; consistieron principalmente en fatiga, mareos, boca seca, náuseas, somnolencia, trastornos neurocognitivos y déficits psicomotores (Andreae et al., 2015; Deshpande et al., 2015; Meng et al., 2017; Lynch y Campbell, 2011; Lynch y Ware, 2015; Boychuk et al., 2015; Fitzcharles et al., 2016). Sólo en dos revisiones sistemáticas se reportaron altas tasas de abandono debido a los efectos adversos graves (Mücke et al., 2018 y Stockings et al., 2018).
Adicionalmente, todos los estudios enfatizaron la falta de evidencia sobre la eficacia y la seguridad a largo plazo de los cannabinoides, por lo que se sugieren ensayos más grandes y de mayor duración para confirmar las señales de eficacia sugeridas por los estudios antes mencionados y para el monitoreo a largo plazo de pacientes que usan cannabinoides (Lynch y Campbell 2011). Lo anterior es importante porque estas sustancias después de un tiempo podrían producir tolerancia y los efectos adversos delimitarse al inicio de la terapia para después disminuir en intensidad o ceder (Meng et al., 2017). O bien, con su uso prolongado podría alcanzarse el efecto de «techo analgésico», donde hasta cierta dosis se alcanza el efecto máximo posible y posteriores aumentos de dosis no aumentarían su eficacia pero sí sus efectos adversos.
La variabilidad en los resultados obedece en gran medida a que, como se observa en la tabla 1, los tipos de sustancias cannabinoides, las preparaciones farmacéuticas, las rutas de administración y las dosis utilizadas fueron muy variadas en los distintos estudios que se incluyeron en las revisiones sistemáticas analizadas. El eje conductor de todas las revisiones fue el tipo de dolor seguido del tipo de estudio (en su mayoría eccas) y de la duración mínima del tratamiento, pero la mayoría no delimitó el tipo de sustancia o preparación cannabinoide, ni su origen, proporción y contenido en la formulación. Tampoco se acotó el análisis a la vía de administración ni a la dosis, por ejemplo, ajustada a porcentaje o miligramos equivalentes de thc. Lo anterior apunta a la necesidad de realizar subanálisis sistemáticos de la evidencia considerando estos parámetros para evitar subestimar los resultados de eficacia analgésica y de seguridad.
La gran mayoría de las revisiones incluidas en esta revisión concluyen en que se requie-

LA PRESENTE REVISIÓN SISTEMÁTICA COMPRENDE UN NÚMERO RELATIVAMENTE BAJO DE ESTUDIOS, TAMBIÉN DE REVISIÓN SISTEMÁTICA, INCLUIDOS PARA SU ANÁLISIS.
ren más estudios con poblaciones grandes de participantes pero a su vez más homogéneas y enfocadas a cannabinoides específicos. Asimismo, apuntan a que el dolor crónico no canceroso no se puede generalizar por lo que futuros estudios clínicos controlados y observacionales habrán de delimitar también el tipo de dolor específico a investigar. Además del impacto del uso de cannabinoides en el dolor, los autores de las distintas revisiones coinciden en que debe medirse el impacto en la calidad de vida y en la funcionalidad física de los pacientes; así como la frecuencia, severidad e impacto de los efectos adversos que se presenten, sobre todo los de tipo neurocognitivo y psiquiátrico. También resaltaron que futuros estudios deberán investigar la seguridad de los cannabinoides sobre todo en su utilización por periodos prolongados, en su uso como terapia adyuvante junto con otros fármacos del sistema nervioso central y con respecto a su potencial de abuso. Deshpande et al., (2015) y Stockings et al., (2018) fueron los más enfáticos al prevenir sobre los riesgos de que se empiece a generalizar la prescripción de cannabinoides ante evidencia tan preliminar, ya que podría replicarse lo que actualmente está pasando con los opioides.
Más aún, para poder definir el papel de los cannabinoides en el tratamiento del dolor crónico, es necesario compararlos no sólo contra placebo, sino contra las terapias farmacológicas actualmente establecidas para los distintos tipos de dolor, por ejemplo, el dolor crónico asociado con enfermedades reumáticas (Lynch y Campbell, 2011; Andreae et al., 2015; Boychuk et al., 2015; Lynch y Ware, 2015; Fitzcharles et al., 2016). Stockings et al. (2018) enfatizaron que las personas que viven con dolor crónico a menudo tienen otras enfermedades complejas por lo que es probable que se requiera un tratamiento multidisciplinario que incluya terapia física y psicológica en lugar de depender únicamente de medicamentos. Es relevante mencionar que los métodos de administración más nuevos para los cannabinoides resultaron mucho más seguros que fumar el cannabis; por ejemplo, los sistemas de pulverización oromucosal proporcionan niveles sanguíneos más consistentes y, por lo tanto, permiten niveles efectivos de analgesia minimizando los efectos adversos (Boychuk et al., 2015). También proporcionan un nivel de protección contra el abuso al limitar el número de aplicaciones diarias. Por otra parte, Andreae et al. (2015) argumentaron que el cannabis inha-
lado o fumado no representa una carga económica muy grande, debido a que su costo es relativamente bajo y esto podría constituir una ventaja; sin embargo, se tiene que romper con los estigmas y se necesita avanzar en su proceso de regulación jurídica y legal para que en algún futuro pueda llegar a representar una alternativa viable en el tratamiento del dolor crónico. Por lo anterior, es fundamental conocer el estatus legal del cannabis para ser usado con fines médicos y científicos. En países como Uruguay, Canadá, y algunos estados de Estados Unidos ya han regulado el mercado del cannabis con fines lúdicos y medicinales (Pacula, 2017). En México se reformaron diversas disposiciones a la Ley General de Salud y del Código Penal Federal, con la finalidad de regular el uso medicinal de cannabis sativa, índica y americana o marihuana (Cámara de Diputados H. Congreso de la Unión, 2017), sin embargo, la Secretaría de Salud y la cofepris no han emitido los reglamentos y lineamientos para la compra y distribución de la marihuana para su uso medicinal y científico (Senado de la República, 2020). Las Comisiones de Salud, Justicia y Estudios Legislativos del Senado de la República aprobaron en lo general, el 4 de marzo de 2020, el dictamen que busca regular el uso lúdico, medicinal y científico de la marihuana en México. Dicho dictamen se ha retrasado por la pandemia por covid-19, pero deberá ser aprobado en el futuro por el pleno del Senado, por la Cámara de Diputados y finalmente promulgado por parte del poder Ejecutivo (Cámara de Diputados H. Congreso de la Unión, 2020). Sin duda, el contar con leyes que regulen el uso de la marihuana para ser utilizada en investigación clínica es indispensable para generar evidencia con base en el contexto mexicano y con ello determinar si se deberá incorporar a los cannabinoides en las guías de práctica clínica nacionales para el manejo del dolor crónico. Para esto, los riesgos y los beneficios deberán estar bien sustentados en estudios clínicos y habrán de comunicarse efectivamente a los profesionales de la salud y pacientes para promover una toma de decisiones terapéuticas racional, justa y segura. La presente revisión sistemática comprende un número relativamente bajo de estudios, también de revisión sistemática, incluidos para su análisis. Esto puede deberse principalmente a que la búsqueda se delimitó a la base de datos PubMed. Sin embargo, PubMed a diferencia de otros repositorios contiene registros que son seleccionados para su inclusión por humanos en comités con base en criterios académicos y de
calidad científica, los artículos están etiquetados, permiten la aplicación de filtros y son elegidos y clasificados también por contenido (Michigan State University, 2019). Además, el uso de términos MeSH para la búsqueda en PubMed supera la limitante de que los autores pudieran usar diferentes palabras clave o descriptores sobre el tema de interés. Dado que un término MeSH puede formar parte de una o más jerarquías, la indexación en este sistema aumenta la capacidad de descubrimiento de las citas y facilita la búsqueda tanto de lo amplio como de lo acotado simultáneamente (Icahn School of Medicine at Mount Sinai, 2020). Lo anterior permite garantizar la obtención de los artículos más relevantes sobre el tema buscado.
Adicionalmente, dado que el alcance de este trabajo se delimitó a la búsqueda en PubMed, es factible que artículos latinoamericanos hayan quedado excluidos. Por lo anterior se considera importante incluir en futuras actualizaciones de la presente revisión sistemática, la búsqueda en otras bases de datos como Web of Science, embase y lilacs; en particular en esta última para añadir representatividad de publicaciones de la especialidad realizadas en la región de América Latina y el Caribe.
Por otra parte, las revisiones sistemáticas permiten la creación de un resumen sobre un tema de importancia en un solo documento, permitiendo destacar las revisiones de mejor calidad y proporcionando resúmenes definitivos que pueden usarse para guiar la práctica clínica (Smith et al., 2011). Dado que los profesionales de la salud y otros tomadores de decisiones se enfrentan a una gran cantidad de revisiones bibliográficas de calidad y enfoque variables, este tipo de trabajos que comparan y contrastan los resultados de revisiones independientes permiten brindar garantías de que las conclusiones de las revisiones individuales son consistentes o no.
En particular, en lo que respecta al tema central de esta revisión sistemática, el consenso general es que, con base en la evidencia actual, los cannabinoides en sus distintos tipos, preparaciones farmacéuticas y vías de administración presentan beneficios a corto plazo y con moderada eficacia, por lo que aún no pueden considerarse como monoterapia ni como tratamiento de primera línea para ninguna clase de dolor crónico no canceroso. La evidencia revisada tampoco permite concluir en forma precisa y contundente sobre su eficacia y seguridad a largo plazo ni sobre cuáles son los compuestos cannabinoides que mejores resultados han te-
nido para el dolor crónico y cuáles son las dosis y vías de administración más efectivas y seguras.
Asimismo, se recomienda su utilización cautelosa por especialistas en dolor que ya cuenten con experiencia previa con el uso de cannabinoides (Mücke et al., 2018).
El análisis de nueve revisiones sistemáticas sobre la efectividad de los cannabinoides en el tratamiento del dolor crónico no canceroso permite concluir que estas sustancias son un buen recurso para tratar este padecimiento, aunque la evidencia disponible los sitúa como una opción terapéutica de eficacia moderada.
Ante la evidencia actual, no existe consenso sobre cuáles son los compuestos cannabinoides que mejores resultados han tenido para el dolor crónico. Tampoco es posible concluir sobre la duración idónea del tratamiento ni sobre cuáles son las formulaciones, las vías de administración y las dosis o rangos de dosis más efectivas y seguras.
El análisis de la literatura arrojó que, los distintos tipos de cannabinoides:
• No cuentan con evidencia suficiente que permita considerarlos como tratamiento de primera línea para ninguna clase de dolor crónico no canceroso;
• Presentan beneficios moderados a corto plazo, como terapia conjunta con otros analgésicos y cuando los pacientes no responden a otros tratamientos;
• Pueden brindar beneficios para el paciente, sobre todo en dosis elevadas, sin embargo, se debe advertir sobre el posible desarrollo de efectos adversos leves o tolerables y, en menor medida, graves;
• Causan los siguientes efectos adversos más comunes: mareo, dolor de cabeza, fatiga, boca seca, somnolencia, sedación, náuseas; alteraciones psicoactivas como psicosis, euforia, excitación, y alteraciones neurocognitivas como desorientación, confusión, deterioro de la concentración y la memoria y disminución en el rendimiento psicomotor;
• No cuentan con evidencia que permita concluir en forma precisa y contundente sobre su eficacia y seguridad a largo plazo ni sobre su potencial de abuso sobre todo en personas con historial de abuso de sustancias.
Sin duda, resulta apremiante la realización de más estudios con una mayor duración y cantidad de pacientes para evaluar los riesgos potenciales que puedan presentarse a largo plazo. También es necesario recalcar que independientemente del tipo, dosis y vía de administración de los cannabinoides, lo más importante es la calidad de vida del paciente en cuanto a la reducción significativa y segura del dolor crónico de distinta etiología. Ante la futura emisión de los lineamientos que regularán en México el uso medicinal y científico del cannabis, resulta relevante proporcionar un resumen analítico de la evidencia actualmente disponible para que pueda usarse para guiar la práctica clínica.
Revisión sistemática
Lynch y Campbell (2011)
Población de estudio total
Andreae et al. (2015)a
766 participantes en 18 estudios
No se menciona edad
Diagnóstico de dolor crónico no canceroso por: artritis reumatoide, dolor neuropático, fibromialgia y dolor mixto
Cannabinoides probados, dosis y controles
CAN fumado contra placebo (4 estudios: 1% hasta 9.4% THC)
Extractos oromucosales de THC/CBD contra placebo (7 estudios: 5.4 a 9.6 pulverizaciones/día)
NAB contra dihidrocodeína (1 estudio: 2 mg contra 240 mg de dihidrocodeína)
NAB contra placebo (3 estudios: 0.25 mg/día a 2 mg/día)
DRN contra placebo (2 estudios: 10 y 20 mg/día)
CT-3 contra placebo (1 estudio: sin dosis especificada).
178 participantes en 5 estudios
Adultos
Diagnóstico de dolor crónico neuropático de por lo menos 3 meses
CAN inhalado contra placebo (3 estudios: cigarrillos preenrollados, 1 estudio: vaporizador Volcano y 1 estudio: cápsulas de gelatina fumadas a través de una pipa)
Las dosis varían entre cada estudio, y oscilan entre 1.625 mg - 96 mg por día o sesión.
Características del tratamiento
Resultados globales de cada revisión sistemática
Boychuk et al. (2015)
771 participantes en 13 estudios
Diagnóstico de dolor neuropático cronico no canceroso
CAN vaporizado (1 estudio) y fumado (4 estudios) contra placebo con contenidos del 1% al 9.4% de THC Spray oromucosal de nabiximol contra placebo (5 estudios) b Cannabinoides sintéticos DRN, NAB y CT-3 contra placebo (3 estudios) b
La duración media del tratamiento fue de 2.8 semanas (rango de 6 horas a 6 semanas)
No se reporta uso concomitante de medicación analgésica previa.
La duración del seguimiento varió desde horas (5-6 horas) y días (5 días) hasta semanas (2 semanas) No se reporta uso concomitante de medicación analgésica previa.
La duración del tratamiento de los estudios varió de menos de 1 semana a 6 semanas o más. Esta variabilidad no parece haber afectado a los principales resultados de los estudios. No se reporta uso concomitante de medicación analgésica previa.
Se demostró la seguridad del uso de marihuana en distintos dolores crónicos, sin embargo, la eficacia fue moderada. En la mayoría de los estudios se demostró efecto analgésico y mejoras en la calidad del sueño.
El uso de marihuana por inhalación mostró beneficios a corto plazo para la reducción del dolor neuropático crónico en un 30% de acuerdo con escalas de intensidad del dolor. Sin embargo, no hay evidencia concluyente a largo plazo debido al tamaño muestra.
El análisis de los estudios sugirió que los cannabinoides pueden proporcionar analgesia efectiva en dolor neuropático crónico que no responde a otros tratamientos.
226 participantes en 6 estudios
Adultos
Deshpande et al. (2015)
Diagnóstico de dolor crónico no canceroso, de los cuales la mayoría (189) con dolor neuropático crónico
CAN fumado o vaporizado contra placebo, con dosis variables calculadas de THC entre 1.9 mg/día hasta 34 mg/ día.
Todas las sesiones experimentales en los estudios fueron de corta duración (máximo 5 días) No se reporta uso concomitante de medicación analgésica previa.
Sólo tres de seis estudios reportaron resultados positivos en términos de reducción del dolor medida como disminución de 2 puntos en la escala de 0-a10 o como una mejoría del 30% en la intensidad del dolor. En términos generales el CAN medicinal en dosis muy bajas (< 34 mg/día) se asoció con una mejoría del dolor neuropático refractario de gravedad moderada en adultos que usan analgésicos concomitantes.
1185 participantes en 11 estudios
No se menciona edad
Lynch y Ware (2015)
Diagnóstico de dolor crónico no canceroso: neuropatía diabética dolorosa, fibromialgia, esclerosis múltiple, dolor neuropático, esclerosis múltiple con espasticidad, dolor de cabeza por uso excesivo de medicamentos
NABb contra amitriptilina
NABb contra ibuprofeno
NABb + gabapentina contra placebo
NABb contra placebo
CAN fumado 4% THC
Extracto de CAN vía oral (5 mg a 25 mg de CBD y de 29% a 72% de THC)
Aerosol oromucosal de CAN (cada aerosol proporciona 2.7 mg de THC y 2.5 mg de CBD)
CAN vaporizado (1.29% a 3.53% THC)
La duración de los estudios fue variable, de 1 día hasta 14 semanas. No se reporta uso concomitante de medicación analgésica previa.
Se demostraron efectos analgésicos significativos de los cannabinoides estudiados. Se informaron beneficios en el sueño, rigidez muscular y en la espasticidad.
Fitzcharles et al. (2016)
Tabla
159 participantes en 4 estudios
Edad entre 26 y 76 años
La mayoría fueron mujeres
Diagnóstico de dolor crónico no canceroso: fibromialgia, dolor espinal crónico, artritis reumatoide y osteoartritis
Meng et al (2017)a
Mücke et al. (2018)
1219 participantes en 11 estudios
Mayores de edad
Diagnóstico de dolor neuropático de por lo menos 3 meses
NAB contra placebo (2 estudios; la dosis se incrementó progresivamente: 0.25 a 1 mg de una a dos veces al día) NAB contra amitriptilina (1 estudio; 0.5 a 1 mg al día)
Nabiximol contra placebo (1 estudio; administrado en 1 a 6 pulverizaciones del aerosol oromucosal con 2.7 mg THC:2.5 mg de CBD).
DRN (1 estudio: dosis diaria de 2.5 a 10 mg)
NAB (3 estudios: dosis diaria de entre 1 y 4 mg)
Nabiximol (7 estudios: aerosoles con dosis diarias de 22.4 mg de THC y 20.8 mg de CBD)
Todos los estudios con excepción de uno que comparó a la NAB contra dihidrocodeína, compararon al cannabinoide en cuestión contra placebo.
La duración del estudio varió de 2 a 5 semanas. No se reporta uso concomitante de medicación analgésica previa.
Stockings et al. (2018)a
1750 participantes en 16 estudios
Adultos (18 años o más)
Diagnóstico de dolor neuropático
9958 participantes en 104 estudios
Mayores de edad (hombres y mujeres), adolescentes (2 estudios) y niñas
Diagnóstico de dolor neuropático (por esclerosis múltiple y otras causas), fibromialgia, artritis reumatoide y dolor crónico no canceroso
Combinación THC/CBD en aerosol oromucosal (10 estudios: 2.7/2.5 mg, máximo 48 pulverizaciones/día)
NAB (2 estudios: 0.25-5 mg)
CAN herbario fumado (2 estudios (2.59.4% THC)
DRN (2 estudios: 5-10 mg/día).
15 estudios compararon al cannabinoide en cuestión contra placebo y un estudio contra dihidrocodeína (30-240 mg).
CAN (26 estudios) fumado o ingerido (60 mg-2.46g) o vaporizado (9% THC; 13% CBD)
DRN (18 estudios; 7.5 mg-60mg)
Nabiximol (24 estudios; 9.99mg THC; 120mg CBD)
THC:CBD en aerosol oromucosal (3 estudios; 2.5 mg; 120 mg)
NAB (17 estudios; 1 mg-3.05 mg)
Extracto de THC (11 estudios; 2.5 mg120 mg)
Extracto de CBD (2 estudios; 25mg150mg).
La duración del seguimiento varió de 2 a 15 semanas.
En todos los estudios con excepción de uno, los participantes continuaron su terapia analgésica previa.
Todos los estudios incluidos informaron al menos un resultado relacionado con el dolor que indica cierta mejoría con los cannabinoides, aunque un estudio comparativo de NAB contra amitriptilina no mostró diferencias entre los dos tratamientos para el dolor.
En comparación con placebo, los pacientes que recibieron cannabinoides informaron una reducción significativa, pero clínicamente pequeña, en las puntuaciones de dolor de la escala de calificación numérica media.
El uso de cannabinoides selectivos también se asoció con mejoras en la calidad de vida y el sueño sin mayores efectos adversos.
Se demostró un alivio del 50% o más en el dolor crónico neuropático; sin embargo, hubo un aumento de los efectos adversos a nivel del SNC (17% desarrolló un trastorno psiquiátrico).
Duración de tratamiento de al menos 2 semanas hasta 26 semanas.
En términos generales todos los cannabinoides probados fueron mejores que el placebo para la mejora global y para reducir la intensidad del dolor, los trastornos del sueño y la angustia psicológica; pero la evidencia es de calidad muy baja a moderada.
La duración de los tratamientos varió de 1 día a 156 semanas 87 estudios examinaron a los cannabinoides como terapia de segunda línea adicional a la medicación analgésica pre-existente.
Se reportó que no hay diferencia significativa en el uso de los cannabinoides para la reducción del dolor crónico no canceroso en comparación con el placebo. Se encontró evidencia de grado moderado a alto que respalda el uso del nabiximol para lograr reducciones modestas del dolor como terapia complementaria en el dolor relacionado con esclerosis múltiple. Sin embargo, hubo altas tasas de abandono por eventos adversos.
a Revisión sistemática con metaanálisis; b No se especifica la dosis; CAN = cannabis, cannabis sativa o marihuana; CBD = cannabidiol, componente no psicoactivo del cannabis; CT-3 = ácido ajulémico, derivado sintético del THC; DRN = dronabinol, forma sintética del THC; NAB = nabilona, cannabinoide sintético; THC = tetrahidrocannabinol, componente psicoactivo del cannabis.
Karla Andrea Arias Soto

Recién egresada de la Licenciatura en Ciencias Farmacéuticas de la udlap. Participó en el proyecto «Biotecnología para el cultivo de organismos acuáticos tropicales» en la ujat , colaboró como auxiliar farmacéutica en el Hospital Puebla en el área de Farmacia Hospitalaria y Farmacovigilancia. Realizó el curso «Prescription Drug Regulation, Cost, and Access: Current Controversies in Context» impartido por la Universidad de Harvard por la plataforma edX. karla.ariasso@udlap.mx

Paulina López Márquez
Recién egresada de la Licenciatura en Ciencias Farmacéuticas de la udlap. Fue miembro del Programa de Honores de esta institución y desarrolla el proyecto «Moléculas con actividad biológica presentes en venenos de serpientes» dirigido por la Dra. Irene Vergara y para el cual realizó una estancia de investigación en el Instituto de Biotecnología de la unam paulina.lopezmz@udlap.mx

Felicia Villagómez Ocampo
Estudiante de la Licenciatura en Bioquímica Clínica y de la Licenciatura en Ciencias Farmacéuticas de la udlap Colaboró en el proyecto «Aislamiento de bacteriocinas de Pseudomonas aeruginosa para confirmar su actividad antimicrobiana» con el Dr. José Luis Sánchez. Expresidenta de la Mesa Directiva de Biología, Bioquímica Clínica y Químico Farmacéutico Biólogo. Actualmente se encuentra trabajando en el área de Asuntos Regulatorios. felicia.villagomezoo@udlap.mx

Leslie Martínez Hernández
Recien egresada de la Licenciatura en Bioquímica Clínica de la udlap. Actualmente participa en el proyecto «Evaluación de los efectos de diversos productos farmacéuticos a partir del análisis de bases de datos de publicaciones científicas, reportes de seguridad y registros de farmacovigilancia» dirigido por la Dra. Lucila Castro y donde también colabora con investigadores del Instituto Nacional de Salud Pública. leslie. martinezhz@udlap.mx

Lucila Isabel Castro Pastrana
Doctora en Bioquímica Farmacéutica por la Universidad de Tübingen, Alemania. Fue profesora visitante en la Universidad de British Columbia en temas de farmacovigilancia y farmacogenómica. Es autora y compiladora de cuatro libros sobre farmacovigilancia. Se encuentra certificada por trayectoria profesional en el perfil Farmacia por el Colegio Nacional de Químicos Farmacéuticos Biólogos México. Es profesora de tiempo completo de la udlap lucila.castro@udlap.mx
• Andreae, M. H., Carter, G. M., Shaparin, N., Suslov, K., Ellis, R. J., Ware, M. A., Abrams, D. I., Prasad, H., Wilsey, B., Indyk, D., Johnson, M. y Sacks, H. S. (2015). Inhaled Cannabis for Chronic Neuropathic Pain: A Meta-analysis of Individual Patient Data. The journal of pain: official journal of the American Pain Society 16(12), 1221–1232. https://doi. org/10.1016/j.jpain.2015.07.009
• Andrew, R., Derry, S., Taylor, R. S., Straube, S. y Phillips, C. J. (2014). The costs and consequences of adequately managed chronic non-cancer pain and chronic neuropathic pain. Pain practice: the official journal of World Institute of Pain, 14(1), 79–94. https://doi. org/10.1111/papr.12050
• Boychuk, D. G., Goddard, G., Mauro, G. y Orellana, M. F. (2015). The effectiveness of cannabinoids in the management of chronic nonmalignant neuropathic pain: a systematic review. Journal of oral & facial pain and headache, 29(1), 7–14. https://doi.org/10.11607/ofph.1274
• Cámara de Diputados H. Congreso de la Unión. (2017). Diputados aprueban uso medicinal de la cannabis sativa, índica y americana o mariguana (Boletin Nº 3577). Recuperado de http://www5.diputados.gob.mx/index.php/esl/Comunicacion/Boletines/2017/Abril/28/3577-Diputados-aprueban-uso-medicinal-de-la-cannabis-sativa-indica-y-americana-o-mariguana
• Cámara de Diputados H. Congreso de la Unión. (2020). Celebra PRD aprobación, en comisiones del Senado de la República, del uso lúdico de la marihuana (Nota Nº 4528). Recuperado de http://www5. diputados.gob.mx/index.php/esl/Comunicacion/Agencia-de-Noticias/2020/Marzo/05/4528-Celebra-PRD-aprobacion-en-comisiones-del-Senado-de-la-Republica-del-uso-ludico-de-la-marihuana
• cenetec. (2013). Diagnóstico y tratamiento médico del dolor por neuropatía periférica diabética en adultos en el primer nivel de atención. México: Secretaría de Salud. Recuperado de http://www.cenetec.salud.gob.mx/descargas/gpc/CatalogoMaestro/010_GPC_NeuropDiabetica/SSA-010-08_NEUROPATxA_Y_PIE_DIABxTICOEVR.pdf
• Covarrubias-Gómez, A., Guevara-López, U. M., Cantú-Brito, C., Nuche-Cabrera, E. y Guajardo-Rosas, J. A. (2015). Recomendaciones de práctica clínica para el manejo del dolor neuropático: Grupo de interés en dolor neuropático de la Asociación Mexicana para el Estudio y Tratamiento del Dolor. Revista Mexicana de Anestesiología, 38(4), 264-276.
• Deshpande, A., Mailis-Gagnon, A., Zoheiry, N. y Lakha, S. F. (2015). Efficacy and adverse effects of medical marijuana for chronic noncancer pain: Systematic review of randomized controlled trials. Canadian family physician Medecin de famille canadien 61(8), e372–e381.
• Diccionario de Biología. (s. f.). Dosis equianalgésica. Recuperado de https://www.biodic.net/palabra/dosis-equianalgesica/#.Xikczy2b5QI
• Finnerup N. B., Sindrup S. H. y Jensen T. S. (2010). The evidence for pharmacological treatment of neuropathic pain. Pain, 150(3), 573–581. https://doi.org/10.1016/j.pain.2010.06.019
• Fitzcharles, M. A., Baerwald, C., Ablin, J. y Häuser, W. (2016). Efficacy, tolerability and safety of cannabinoids in chronic pain associated with rheumatic diseases (fibromyalgia syndrome, back pain, osteoarthritis, rheumatoid arthritis): A systematic review of randomized controlled trials. Schmerz (Berlin, Germany), 30(1), 47–61. https://doi.org/10.1007/ s00482-015-0084-3
• Food and Drug Administration (2019). FDA Regulation of Cannabis and Cannabis-Derived Products: Questions and Answers. Silver Spring, MD: Food and Drug Administration. Recuperado de https://www.fda.gov/newsevents/public-health-focus/fda-regulation-cannabis-and-cannabis-derived-products-questions-and-answers#approved
• Goodman, C. W. y Brett, A. S. (2017). Gabapentin and Pregabalin for Pain — Is Increased Prescribing a Cause for Concern? New England Journal of Medicine, 377, 411-414. https://doi.org/10.1056/NEJMp1704633
• Icahn School of Medicine at Mount Sinai. (2020). PubMed Tutorial from The Levy Library: MeSH: The Key to Medline. Recuperado de: https://libguides.mssm.edu/pubmed_tutorial/MeSH
• Kalant, H. (2001). Medicinal use of cannabis: history and current status. Pain research & management, 6(2), 80–91. https://doi. org/10.1155/2001/469629
• Kalso, E., Aldington, D. J. y Moore, R. A. (2013). BMJ (Clinical research ed.), 347, f7339. https://doi.org/10.1136/bmj.f7339
• Lake, S., Walsh, Z., Kerr, T., Cooper, Z. D., Buxton, J., Wood, E., et al. (2019). Frequency of cannabis and illicit opioid use among people who use drugs and report chronic pain: A longitudinal analysis. PLoS medicine 16(11), e1002967. https://doi.org/10.1371/journal.pmed.1002967
• Léger, J. M. (1999). Diagnosis of chronic neuropathy. Journal of neurology, 246(3), 156–161. https://doi.org/10.1007/s004150050326
• Levine, B.S., Kerrigan, S. eds. (2020). Principles of forensic toxicology. 5th ed. Cham, Switzerland: Springer Nature Switzerland AG. https://doi. org/10.1007/978-3-030-42917-1
• Lynch, M. E. y Campbell, F. (2011). Cannabinoids for treatment of chronic non-cancer pain; a systematic review of randomized trials. British journal of clinical pharmacology, 72(5), 735–744. https://doi.org/10.1111/j.13652125.2011.03970.x
• Lynch, M. E. y Ware, M. A. (2015). Cannabinoids for the Treatment of Chronic Non-Cancer Pain: An Updated Systematic Review of Randomized Controlled Trials. Journal of neuroimmune pharmacology: the official journal of the Society on NeuroImmune Pharmacology, 10(2), 293–301. https:// doi.org/10.1007/s11481-015-9600-6
• Meng, H., Johnston, B., Englesakis, M., Moulin, D. E. y Bhatia, A. (2017). Selective Cannabinoids for Chronic Neuropathic Pain: A Systematic Review and Meta-analysis. Anesthesia and analgesia, 125(5), 1638–1652. https:// doi.org/10.1213/ANE.0000000000002110
• Michigan State University. (2019). PubMed, Web of Science, or Google Scholar? Recuperado de: https://libguides.lib.msu.edu/pubmedvsgooglescholar
• Mücke, M., Phillips, T., Radbruch, L., Petzke, F. y Häuser, W. (2018).
Cannabis-based medicines for chronic neuropathic pain in adults. The Cochrane database of systematic reviews, 3(3), CD012182. https://doi. org/10.1002/14651858.CD012182.pub2
• Pacula, R. L. y Smart, R. (2017). Medical Marijuana and Marijuana Legalization. Annual review of clinical psychology 13, 397–419. https://doi. org/10.1146/annurev-clinpsy-032816-045128
• Piper, B. J., Beals, M. L., Abess, A. T., Nichols, S. D., Martin, M. W., Cobb, C. M. y DeKeuster, R. M. (2017). Chronic pain patients’ perspectives of medical cannabis. Pain, 158(7), 1373–1379. https://doi.org/10.1097/j. pain.0000000000000899
• Senado de la República. (2020). Proposición con punto de acuerdo por el que se exhorta a la Secretaría de salud y a la comisión federal para la protección contra riesgos sanitarios, para que analicen y, en su caso emitan el reglamento y lineamientos que contengan normatividad sobre el control medicinal de la cannabis (Gaceta: LXIV/2SPR-17/108676). Recuperado de https://www.senado.gob.mx/64/gaceta_del_senado/documento/108676
• Smith, V., Devane, D., Begley, C. M. y Clarke, M. (2011). Methodology in conducting a systematic review of systematic reviews of healthcare interventions. BMC medical research methodology, 11(1), 15. https://doi. org/10.1186/1471-2288-11-15
• Stannard, C. y Moore, A. (2016). Traditional opioids for chronic non-cancer pain: untidy, unsatisfactory, and probably unsuitable. Oxford, UK: The Cochrane Collaboration. https://9sh.re/bio6Yt-DM#2
• Stockings, E., Campbell, G., Hall, W. D., Nielsen, S., Zagic, D., Rahman, R., Murnion, B., Farrell, M., Weier, M. y Degenhardt, L. (2018). Cannabis and cannabinoids for the treatment of people with chronic noncancer pain conditions: a systematic review and meta-analysis of controlled and observational studies. Pain, 159(10), 1932–1954. https://doi.org/10.1097/j. pain.0000000000001293
• Sznitman, S. R. y Zolotov, Y. (2015). Cannabis for therapeutic purposes and public health and safety: a systematic and critical review. The International journal on drug policy 26(1), 20–29. https://doi.org/10.1016/j. drugpo.2014.09.005
• THC structure.svg. (2018). Wikimedia Commons, the free media repository. Recuperado de https://commons.wikimedia.org/w/index.php?title=File:THC_structure.svg&oldid=302586028
• Urrútia, G. y Bonfill, X. (2010) Declaración PRISMA: una propuesta para mejorar la publicación de revisiones sistemáticas y metaanálisis. Medicina Clinica (Barcelona).;135(11):507–511.
• Volkow, N. D., Baler, R. D., Compton, W. M. y Weiss, S. R. (2014). Adverse health effects of marijuana use. New England Journal of Medicine, 370(23), 2219-2227.
• Vučković, S., Srebro, D., Vujović, K. S., Vučetić, Č. y Prostran, M. (2018). Cannabinoids and Pain: New Insights From Old Molecules. Frontiers in pharmacology, 9, 1259. https://doi.org/10.3389/fphar.2018.01259
• Ware, M. A., Rueda, S., Singer, J. y Kilby, D. (2003). Cannabis use by persons living with HIV/AIDS: patterns and prevalence of use. Cannabis Therapeutics
