New uses for existing medicines: drug repurposing and its importance in health crises


New uses for existing medicines: drug repurposing and its importance in health crises



el reposicionamiento de fármacos y su importancia en crisis sanitarias1

1 Se agradece a Jennifer Tamayo Núñez por lectura crítica al manuscrito.


Por: Fernanda I. Saldívar-González · José L. Medina-Franco
Saldívar-González F. y Medina-Franco J. (2020).Nuevos usos a medicamentos existentes: el reposicionamiento de fármacos y su importancia en crisis sanitarias. Entorno UDLAP, 14
Recibido: 25 de agosto de 2020 Aceptado: 8 de enero de 2021
RESUMEN:
Al nuevo uso de medicamentos ya existentes, y que ya han sido probados en estudios clínicos, se le conoce como reposicionamiento de fármacos. Es una estrategia muy útil para proponer y probar fármacos, particularmente en crisis y emergencias sanitarias donde existen pocas o nulas opciones terapéuticas. El reposicionamiento de fármacos ofrece innumerables ventajas sobre los métodos clásicos de desarrollo de fármacos, pero no está exento de riesgos. En este artículo se describen las bases y las estrategias que existen para reposicionar fármacos. También se discuten las ventajas y desventajas de reutilizar medicamentos principalmente en crisis sanitarias como la actual pandemia de covid-19 causada por el virus sars-CoV-2.
PALABRAS CLAVE:
covid-19 · Crisis sanitaria · Reposicionamiento de fármacos · sars-CoV-2
ABSTRACT:
The new use of existing drugs that have already been tested in clinical trials is known as drug repurposing. It is a very useful strategy for proposing and testing drugs, particularly in a health emergency, where there are few or no therapeutic options. Drug repurposing offers myriad advantages over classical drug development methods, it is not risk-free. This article describes the basis and strategies that exist to repurposing drugs. The advantages and disadvantages of reusing drugs, mainly in health crises such as the current covid-19 pandemic caused by the sars-CoV-2 virus, are also discussed.
KEYWORDS:
covid-19 · Health emergency · Drug repurposing · sars-CoV-2


AL
YA
EN ESTUDIOS CLÍNICOS, SE LE CONOCE COMO REPOSICIONAMIENTO DE FÁRMACOS.
La reciente propagación del nuevo coronavirus, sars-CoV-2, ha creado una emergencia mundial de salud pública. En diciembre de 2019, el brote de esta enfermedad emergente (covid-19) comenzó en Wuhan, China. Se extendió rápidamente por el mundo, y la Organización Mundial de la Salud (oms) declaró una pandemia en marzo de 2020. Según el recuento de la Universidad Johns Hopkins en Estados Unidos, hasta el momento de la redacción de este manuscrito (enero 2021), se han reportado más de 85 millones de personas infectadas y más de 1,800,00 muertes en todo el mundo. México ha sido uno de los países más afectados con más de 1,400,000 personas infectadas y más de 127,000 muertes asociadas a covid-19. Desde que se dio a conocer esta emergencia sanitaria hemos escuchado que se han propuesto diferentes medicamentos de uso clínico para tratar esta enfermedad o mitigar sus efectos. Por ejemplo, en Estados Unidos la fda (Food and Drug Administration) que es agencia del gobierno responsable de la regulación de alimentos y medicamentos autorizó, en mayo de 2020, el uso de remdesivir en pacientes con enfermedad severa por sars-CoV-2 y en octubre
del mismo año se convirtió en el primer fármaco aprobado para tratar la enfermedad del covid-19 que requiere hospitalización. Este fármaco fue desarrollado en 2009 inicialmente para atacar el virus del Ébola (Warren et al., 2016). Sin embargo, en estudios clínicos remdesivir mostró poca efectividad. Recientemente, también se anunció que el uso de dexametasona, un glucocorticoide que funciona como antiinflamatorio e inmunosupresor, es efectivo en pacientes graves con covid-19, disminuyendo las muertes en aproximadamente un tercio en los pacientes que requieren ventilación y en un quinto en los que requieren oxígeno suplementario (Horby y Landray, 2020).
A este nuevo uso de medicamentos ya existentes, en una indicación terapéutica distinta para la que se comercializó inicialmente, se le conoce como reposicionamiento de fármacos. Esta definición original se ha ampliado para incluir sustancias activas que fallaron en la fase clínica de su desarrollo debido a su toxicidad o eficacia insuficiente, así como a los medicamentos retirados del mercado debido a problemas de seguridad. Sin embargo, no debe incluirse sustancias que aún no hayan sido sometidas a investigación clínica, es decir, que aún no se hayan probado en humanos (Jourdan et al., 2020).
Glicopirrolato
EPOC (2015) - Hiperhidrosis (2018)
Atomoxetina
Parkinson (2020) - TDAH (2017) Topiramato
Epilepsia (1996) - Migraña (2004)Control de peso (2012)
No. de artículos
Figura 2. Número de publicaciones indexadas en PubMed que contienen los términos «drug repurposing» o «drug repositioning» en su título, resumen o palabras clave, versus año de publicación. Total de publicaciones recuperadas: 6,835 (diciembre 2020).
Aunque esta estrategia está lejos de ser nueva, ha ganado un impulso considerable en la última década. Ejemplos de fármacos aprobados recientemente mediante reposicionamiento de fármacos son el glicopirrolato, aprobado por primera vez por la fda en 2015 para su uso como tratamiento independiente para la enfermedad pulmonar obstructiva crónica (epoc) y que en 2018 se aprobó para el tratamiento tópico de la hiperhidrosis (Abels y Soeberdt, 2019); la atomoxetina, aprobada por primera vez para el tratamiento de la enfermedad de Parkinson y que actualmente está indicada para el tratamiento del trastorno por déficit de atención e hiperactividad (tdah) (Hutchison et al., 2016); y el topiramato, un fármaco antiepiléptico que se utiliza para controlar las convulsiones y prevenir las migrañas y que, desde 2012, su formulación de liberación prolongada combinada con fentermina ha sido aprobada para la terapia crónica de control de peso en adultos (Cosentino et al., 2013) (figura 1). Se estima que aproximadamente un tercio de las aprobaciones en los últimos años corresponden al reposicionamiento de fármacos, y los medicamentos reutilizados actualmente generan alrededor del 25% de los ingresos anuales para la industria farmacéutica (Naylor, 2015). El creciente interés en el reuso de fármacos se puede visualizar en la evolución de publicaciones académicas relacionadas (figura 2). Tan sólo en 2020, se publicaron 2,118 artículos que incluyen el término reposi-
cionamiento de fármacos y de los cuales 779 (36.77%) están relacionados con el nuevo coronavirus sars-CoV-2.
El objetivo de este artículo es discutir las bases del reposicionamiento de fármacos y las estrategias que existen para lograrlo. También se presentan las ventajas y desventajas de reutilizar medicamentos existentes particularmente en crisis sanitarias.
Bases del reposicionamiento de fármacos
La idea de volver a perfilar un medicamento está profundamente relacionada con los fundamentos de la «polifarmacología» que es un concepto que describe la capacidad de un fármaco para interactuar con más de un objetivo molecular. Se estima que un fármaco puede interactuar directamente con entre 6 y 13 dianas terapéuticas en promedio (Vogt y Mestres, 2010). Disciplinas que han emergido y desarrollado con el objetivo de identificar o predecir estas interacciones son la quimiogenómica y la quimiogenómica computacional (Bajorath, 2013; Brown et al., 2013; Rognan, 2013). Mediante la identificación del espacio quimiogenómico, es decir, de todos los posibles ligandos para todas las posibles dianas terapéuticas, es posible detectar candidatos a fármacos que permitan generar rápida y eficazmente nuevos tratamientos para muchas enfermedades. Hoy en día, existe un gran nú-
UN
NÚMERO DE HERRAMIENTAS EN LÍNEA QUE PERMITEN EXPLORAR EL ESPACIO QUIMIOGENÓMICO Y REALIZAR EXPERIMENTOS DE DETECCIÓN VIRTUAL (SINGH ET AL., 2020).


Reposicionamiento de fármacos
mero de herramientas en línea que permiten explorar el espacio quimiogenómico y realizar experimentos de detección virtual (Singh et al., 2020).
Enfoques usados para el reposicionamiento de fármacos
En un principio las observaciones en donde un fármaco podría tener más de una indicación terapéutica se dieron por serendipia o descubrimiento afortunado durante los ensayos clínicos. Quizá uno de los ejemplos más conocidos es el caso del sildenafil. Aún cuando falló demostrar efectividad como antihipertensivo, en los estudios clínicos se encontró que podía ser una terapia efectiva contra la disfunción eréctil (Boolell et al., 1996). Otro ejemplo es el del minoxidil que se usó para tratar la hipertensión antes de que se produjeran los efectos del crecimiento del cabello (Suchonwanit et al., 2019). Incluso los efectos no deseados de un medicamento pueden ser beneficiosos en el contexto de otra indicación. En el trágico caso de la talidomida, su fuerte actividad antiangiogénica resultó ser útil para el tratamiento del mieloma múltiple (Ashburn y Thor, 2004). Estas observaciones dieron pie a que se comenzaran a implementar las búsquedas en la literatura, en
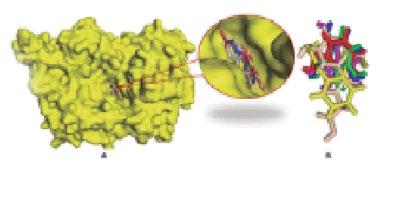
Métodos in silico
donde mediante el conocimiento de la fisiopatología de una enfermedad se buscan fármacos que tengan los efectos deseados. Sin embargo, hoy en día, un enfoque más racional para la identificación de candidatos a fármacos para el reposicionamiento es posible, especialmente utilizando métodos computacionales.
La figura 3 muestra el flujo de trabajo general que se sigue en muchos proyectos de reposicionamiento de fármacos. Este esquema de trabajo consiste en reunir un conjunto de medicamentos conocidos, ya sea como muestras físicas o, en el caso de métodos computacionales, estructuras 2D confiables. Luego, mediante métodos in silico o in vitro se detectan aquellos medicamentos prometedores contra el objetivo en estudio (generación de hipótesis). Posteriormente, se realiza la evaluación mecanicista del efecto del fármaco en modelos preclínicos. Una vez generada la evidencia experimental, la siguiente etapa de reutilización de medicamentos es ingresar a los ensayos clínicos de fase II para la indicación a la que se está reposicionando (suponiendo que haya suficientes datos de seguridad de los estudios de fase I realizados como parte de la indicación original). Es importante mencionar que cualquier cambio en la formulación, dosificación o vía de adminis-
Pruebas preclínicas
Métodos in vitro
Aprobación por agencias regulatorias
Pruebas clínicas fase II/III
tración requerirá un nuevo examen del perfil de seguridad del fármaco bajo estas nuevas condiciones. De las fases mencionadas anteriormente, la más crítica es la detección de medicamentos prometedores contra el objetivo en estudio y es aquí donde los enfoques modernos para la generación de hipótesis cobran mayor importancia. Estos enfoques se pueden subdividir en enfoques computacionales y enfoques experimentales, los cuales se utilizan cada vez más en conjunto. Entre las estrategias computacionales para reposicionar fármacos podemos mencionar la correspondencia de firmas de datos transcriptómicos y proteómicos, aproximaciones de similitud molecular, acoplamiento molecular o docking, mapeo de rutas y el análisis sistemático de historias clínicas electrónicas y datos de ensayos clínicos, así como la vigilancia postcomercialización (Hodos et al., 2016; Loging et al., 2007; Pushpakom et al., 2019). Por otra parte, entre los enfoques experimentales se encuentran los cribados fenotípicos y los ensayos de unión que se realizan mediante técnicas como la cromatografía de afinidad y la espectrometría de masas (Hage, 2017; Hodos et al., 2016; Loging et al., 2007; Pushpakom et al., 2019).
Ventajas y desventajas del reposicionamiento de fármacos
El reposicionamiento de fármacos tiene varias ventajas en comparación con los enfoques tradicionales para el descubrimiento de fármacos. Esta estrategia es atractiva puesto que un fármaco aprobado requerirá de menos tiempo para probar su seguridad, ahorrando tiempo y recursos que se invierten durante las fases preclínicas y clínicas. Se ha mostrado que esta estrategia puede ahorrar hasta el 50% de las inversiones de tiempo y dinero para desarrollar la aprobación de un tratamiento (Paul y Lewis-Hall, 2013). Esto permite un beneficio considerable no sólo para las empresas farmacéuticas, sino también para quienes padecen enfermedades poco comunes o afecciones que tienen pocas o ninguna opción terapéutica. Sin embargo, la reutilización de medicamentos no está exenta de riesgos. Un compuesto aprobado como seguro y efectivo para una indicación puede no ser efectivo ni seguro para otra. Aproximadamente entre 30% y 40% de los medicamentos aprobados por la fda están aprobados con advertencias en recuadro, lo que significa que tienen problemas de seguridad conocidos
e importantes, pero en el contexto de la indicación aprobada, éstos son tolerables y están en el lado apropiado de un análisis de riesgo-beneficio (Oprea y Overington, 2015). Las responsabilidades de seguridad tolerables de un medicamento dependen de manera crucial de la enfermedad objetivo, con una mayor aversión al riesgo en condiciones crónicas comunes como la obesidad y la diabetes, o grupos de pacientes como en entornos pediátricos o de embarazo. Por otro lado, no hay que olvidar que los fármacos suelen ser el resultado de un largo proceso de optimización dirigido a mejorar la afinidad y la selectividad para un objetivo principal determinado. Como consecuencia, los medicamentos pueden no producir un beneficio clínico significativo en la indicación en la que se están reposicionando y si ya se han aprobado otros fármacos para esa indicación, demostrar superioridad con respecto a la eficacia y seguridad en una nueva indicación puede ser un desafío insuperable (Lipworth et al., 2012). Otro problema que se acentúa principalmente en una situación de crisis sanitaria como la que vivimos actualmente por el nuevo coronavirus sars-CoV-2 es que, al estar estos medicamentos disponibles comercialmente, las personas pueden automedicarse, aún cuando no haya evidencia suficiente de su seguridad y eficacia en pacientes con la enfermedad. Balancear los posibles beneficios y riesgos del reposicionamiento de fármacos es una parte integral de las agencias reguladoras de medicamentos de cada país y, por lo tanto, tiene que estar respaldado por evidencia científica. En México, la Comisión Federal para la Protección contra Riesgos Sanitarios (cofepris) es la agencia de gobierno que autoriza los protocolos para realizar estudios clínicos de reposicionamiento de fármacos.
El reposicionamiento de fármacos en crisis sanitarias
Una crisis sanitaria o de salud pública es una situación grave, repentina, en la que ha aparecido un problema de salud, o hay una probabilidad de riesgo para la salud, con una incidencia o letalidad mayor de lo normal y donde no se puede garantizar la dimensión final del problema (Cotanda, 2006). Su gravedad se suele medir por el número de personas afectadas, por su extensión geográfica, y por la morbilidad o mortalidad que ocasiona (Gravitz, 2011). A lo largo de la historia, diversas crisis sanitarias


ESTA ESTRATEGIA ES ATRACTIVA PUESTO QUE UN FÁRMACO APROBADO REQUERIRÁ DE MENOS TIEMPO PARA PROBAR SU SEGURIDAD, AHORRANDO TIEMPO Y RECURSOS QUE SE INVIERTEN DURANTE LAS FASES PRECLÍNICAS Y CLÍNICAS.
han existido y desafortunadamente el panorama actual no es muy alentador. El aumento de la población mundial, el cambio climático, las migraciones masivas, los cambios en los sistemas de producción y distribución de alimentos, entre otras causas, van a promover que aparezcan cada vez más situaciones de crisis en donde la salud de la población se vea comprometida. Ante esta situación, el reposicionamiento de fármacos juega un papel muy importante ya que puede responder de manera más eficiente a una crisis que un proceso clásico de descubrimiento de fármacos. Actualmente se encuentran en marcha diferentes proyectos de reposicionamiento de fármacos para atender las crisis sanitarias como la malaria, o las ocasionadas por el virus del Ébola y el sars-CoV-2. Varias organizaciones como el Centro Nacional para el Avance de Ciencias Transnacionales de Estados Unidos (ncats, por sus siglas en inglés), MRC-AstraZeneca, la Organización Mundial de la Salud (oms) y otros sectores públicos y privados están patrocinando propuestas conceptuales sobre reutilización de fármacos con grandes expectativas de soluciones para problemas sin respuesta en condiciones médicas existentes y fallas terapéuticas (Allarakhia, 2013).
En este contexto, una clasificación a los proyectos de reposicionamiento de fármacos basada en la calidad de la evidencia científica como
la propuesta por Oprea y Overington (2015) se vuelve indispensable (tabla 1). La evaluación distingue cinco etapas del nivel de evidencia de reposicionamiento de medicamentos dada la cantidad y calidad de evidencia disponible (es decir, 0-4). El nivel de confianza aumenta a medida que la evidencia progresa de estudios in vitro a estudios en animales y humanos, asignándose un mayor peso a aquellos datos con relevancia clínica directa.
Esta clasificación se vuelve crucial en un contexto en donde el reciente entusiasmo académico en este campo y el incremento en los recursos informáticos disponibles han llevado a que muchos grupos de investigación realicen predicciones in silico y publiquen, en preprints y en trabajos revisados por pares, listas relativamente largas de fármacos que podrían reutilizarse para diversas indicaciones. En la figura 4 se muestra el número de publicaciones que contienen los términos de reposicionamiento de fármacos y cribado virtual o in silico en su título o palabras clave, en la cual se observa un incremento notable en 2020. Esto por una parte es bueno porque hay compuestos como candidatos concretos para evaluar en un esfuerzo global multidisciplinario. Sin embargo, puede llevar a falsas expectativas y a que las personas se automediquen a partir de información teórica y que no ha progresado a los otros niveles de evidencia que se mencionan en la tabla 1.
Clasificación de los proyectos de reposicionamiento de fármacos según la evidencia científica.
0 Sin evidencia; incluye predicciones in silico sin confirmación.
1 Estudios in vitro con valor limitado para predecir la situación in vivo en humanos.
2 Estudios en animales con relevancia hipotética en el hombre.
3 Estudios incompletos en humanos a la dosis apropiada, por ejemplo, prueba de concepto, muy pocos casos o inferencia de registros médicos, algunos efectos clínicos observados.
4 Puntos finales clínicos bien documentados observados para el fármaco reutilizado a dosis dentro de los límites de seguridad.
Tabla 1. Clasificación de los proyectos de reposicionamiento de fármacos según la evidencia científica.
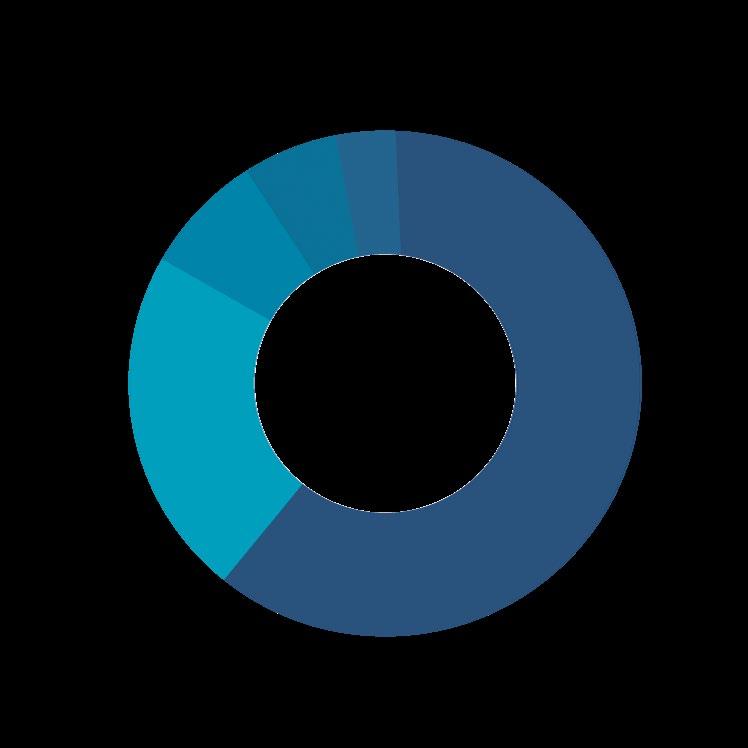
4. Número de publicaciones indexadas en PubMed que contienen los términos «drug repurposing» y cribado virtual «virtual screening» o «in silico» en su título, resumen o palabras clave, versus año de publicación (izquierda). Distribución de los tipos de publicaciones que contienen el término «drug repurposing» y «SARS-CoV-2» (derecha).
El reposicionamiento de fármacos en COVID-19
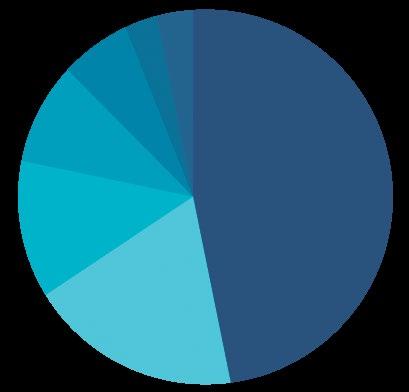
De acuerdo a lo reportado en la página de DrugBank (DrugBank, s. f.), existen registrados 43 tratamientos experimentales y un fármaco aprobado contra covid-19 y, hasta la fecha, se tienen contabilizados 3,275 ensayos clínicos. De estos 44 tratamientos, 34 pertenecen a fármacos ya aprobados o que se investigaron en otra indicación terapéutica. La figura 5 muestra una clasificación para los 34 fármacos que intentan reposicionarse de acuerdo a su indicación original. Como se observa en la figura, se ha priorizado el uso de fármacos antivirales, antiinflamatorios y antineoplásicos.
Las terapias con una eficacia potencial particularmente alta para seguir los pasos del remdesivir y aprobarse para el tratamiento del covid-19 incluyen el antiviral favipiravir, los inmunosupresores tocilizumab, baricitinib y el antiinflamatorio dexametasona (Santos et al., 2020). En las primeras investigaciones, los antivirales dirigidos remdesivir y favipiravir parecen beneficiar a los pacientes al disminuir la replicación viral (Cai et al., 2020); los ensayos clínicos han demostrado que el remdesivir acelera la recuperación del covid-19 (Beigel et al., 2020; Wang et al., 2020). Tocilizumab y baricitinib parecen disminuir la mortalidad al prevenir una tormenta de citocinas severa (Cantini et al., 2020; Mehta et al., 2020). Actualmente existe una autorización por parte de la fda para
usar la combinación de remdesivir y baricitinib en adultos y pacientes pediátricos hospitalizados con covid-19. La dexametasona, por su parte, puede modular la lesión pulmonar mediada por inflamación y, por lo tanto, reducir la progresión a insuficiencia respiratoria y muerte (Ledford, 2020). En la figura 6 se ejemplifican algunos de los medicamentos propuestos para reposicionamiento en covid-19 clasificados de acuerdo a su nivel de evidencia científica (tabla 1).
En el caso de la enfermedad covid-19, al afectar a diferentes grupos de la población, como adultos mayores, personas con obesidad, hipertensión e incluso personas sin una afectación previa, se dificulta que un solo medicamento responda de forma eficiente. Por lo tanto, además de prestar atención en la evidencia científica, será necesario prestar atención en las condiciones en la que el medicamento mostró ser efectivo.
Desafíos en el reposicionamiento de fármacos
· Propiedad intelectual
Un aspecto interesante que involucra medicamentos ya aprobados es el panorama de la propiedad intelectual. Generalmente, se busca que la reutilización de medicamentos sea sobre aquellos cuyos derechos de patente sobre la materia y/o indicación han expirado. Dado que estos medicamentos ya han sido patenta-
CLÍNICOS HAN
DEMOSTRADO QUE EL REMDESIVIR ACELERA
COVID-19 (BEIGEL ET AL., 2020; WANG ET AL., 2020).

Nivel 0 Estudios computacionales
Metisazona, Prulifloxacina, Tegobuvir, etc
Nivel 1 Estudio in vitro
Ivermectina, Nitazoxanida, Auranofina

Nivel 2 Estudio en animales

Nivel 3 Estudios incompletos en humanos
Cloroquina, Hidroxicloquina + Azitromizina
Evidencia científica
Antivirales 46.9%
Antiinflamatorios 18.8%
Antineoplásicos 12.5%
Antiespasmódicos 9.4%
Vacunas 6.3%
Antibióticos 3.05%
Antipalúdicos 3.05%

Nivel 4 Estudios bien documentados en humanos Aprobación
Dexametasona y Remdesivir + Baricitinib
Remdesivir
Ejemplos de medicamentos propuestos para su reposicionamiento en el tratamiento de covid-19. Los compuestos se encuentran clasificados de acuerdo a su nivel de evidencia científica.
dos como una nueva entidad química, los medicamentos posteriores que contengan la misma entidad sólo pueden protegerse mediante una nueva solicitud de patente respaldada por una nueva indicación terapéutica o un nuevo proceso de formulación.
Sin embargo, existen aspectos legales que podrían perjudicar la patente de un nuevo uso médico y/o la aplicación de los derechos de patente. Por ejemplo, algunas legislaciones nacionales, como es el caso de la India, impiden la obtención de una patente para usos médicos secundarios o posteriores. Esta exclusión se basa en la noción de que los nuevos usos no cumplen los criterios clave de patentabili-
dad, como la no obviedad y la novedad. Asimismo, la información publicada en artículos científicos sobre los potenciales usos de fármacos ya existentes, al ser de dominio público, incluso si no se confirma experimentalmente, sigue constituyendo «estado de la técnica». Esto bloquea efectivamente la protección de la propiedad intelectual y la inversión futura en esa combinación particular de medicamentos y dianas o indicaciones clínicas. También, la protección de medicamentos reposicionados son más débiles, en particular ante una posible impugnación legal sobre la base de que la nueva indicación era predecible a partir de los datos de la literatura científica (Cavalla, 2017).
· Espacio de reutilización
Otro argumento que se puede cuestionar en las campañas de reposicionamiento de fármacos está relacionado con el número limitado de candidatos a reutilizar. Afortunadamente, el número de posibles indicaciones de fármacos reposicionados supera la capacidad de detección actual de la mayoría de las empresas. Aunque el auge consumirá a los candidatos más obvios, es probable que sigan presentándose oportunidades de reposicionamiento, aunque posiblemente a un ritmo menor.
OPORTUNIDADES EN EL REPOSICIONAMIENTO DE FÁRMACOS
· Enfermedades desatendidas
Enfermedades como el dengue, leishmaniasis, rabia o la enfermedad de Chagas son ejemplos de enfermedades que afectan principalmente a las poblaciones más pobres y con un limitado acceso a los servicios de salud y que han sido clasificadas como desatendidas u olvidadas (oms, 2015), ya que no han recibido tanta atención como otras enfermedades. Para las industrias farmacéuticas este tipo de enfermedades no suelen ser muy atractivas debido a que están concentradas en pequeñas regiones y el número de personas afectadas suele ser muy pequeño. Por este motivo, académicos y organizaciones sin fines de lucro tienen que buscar alternativas eficientes, que tengan lugar con menos recursos y una mayor tasa de éxito clínico. Dentro de las iniciativas para tratar enfermedades desatendidas una fracción considerable de medicamentos que se someten a ensayos clínicos corresponde a medicamentos reutilizados. Ejemplos de fármacos reposicionados para atender enfermedades desatendidas son el fexinidazol, el fosravuconazol, el tamoxifeno, la eflornitina y la miltefosina (Klug et al., 2016; Swinney y Pollastri, 2019).

CON LOS AVANCES
JUNTO CON UN MAYOR
PODER COMPUTACIONAL, LA
REUTILIZACIÓN DE FÁRMACOS
POTENCIADA POR IA PUEDE
RESULTAR BENEFICIOSA (CHAN ET AL., 2019).
· Avances tecnológicos: inteligencia artificial Con los avances tecnológicos en inteligencia artificial (ia) junto con un mayor poder computacional, la reutilización de fármacos potenciada por ia puede resultar beneficiosa (Chan et al., 2019). Ramas de la ia como el «aprendizaje profundo» y el «aprendizaje de máquinas» pueden reforzar y acelerar el reposicionamiento de fármacos y ayudar en proponer indicaciones terapéuticas no tan obvias para fármacos aprobados. En el caso de enfermedades raras, cuya fisiopatología a menudo está mal caracterizada, estas técnicas ofrecen una forma rápida de identificar hipótesis comprobables que pueden traducirse en la clínica.
CONCLUSIONES
El reposicionamiento de fármacos para una indicación terapéutica distinta de aquella para la que se investigó o comercializó inicialmente es una tendencia creciente que se ha impulsado por el acceso a métodos computacionales


INDICACIÓN TERAPÉUTICA DISTINTA DE AQUELLA PARA LA QUE SE INVESTIGÓ O COMERCIALIZÓ INICIALMENTE ES
UNA TENDENCIA CRECIENTE QUE SE HA IMPULSADO POR EL ACCESO A MÉTODOS COMPUTACIONALES Y BASES DE DATOS.
y bases de datos. Esta estrategia es particularmente atractiva en crisis y emergencias sanitarias, así como en la búsqueda de tratamientos a enfermedades desatendidas ya que puede responder de forma más eficiente y requiere menor inversión que los métodos tradicionales de diseño de fármacos. Un ejemplo exitoso de la aplicación del reposicionamiento de fármacos en crisis sanitarias se encuentra en el fármaco remdesivir, el cual fue aprobado para el tratamiento de covid-19 a menos de un año de la aparición de dicha enfermedad. Para los medicamentos que aún se encuentran en evaluación para su reposicionamiento, es necesario establecer criterios

Fernanda I. Saldívar-González
Maestra en Ciencias Químicas y licenciada en Química Farmacéutico Biológica, ambas por la Universidad Nacional Autónoma de México. Ha participado en diferentes estancias de investigación y congresos nacionales e internacionales relacionados con el diseño de fármacos asistido por computadora. fer.saldivarg@gmail.com
• Abels, C. y Soeberdt, M. (2019). Can we teach old drugs new tricks? Repurposing of neuropharmacological drugs for inflammatory skin diseases. Experimental Dermatology, 28(9), 1002-1009.
• Allarakhia, M. (2013). Open-source approaches for the repurposing of existing or failed candidate drugs: learning from and applying the lessons across diseases. Drug Design, Development and Therapy, 7, 753-766.
• Ashburn, T. T. y Thor, K. B. (2004). Drug repositioning: identifying and developing new uses for existing drugs. Nature Reviews. Drug Discovery, 3(8), 673-683.
• Bajorath, J. (2013). A Perspective on Computational Chemogenomics. Molecular Informatics, 32(11-12), 1025-1028.
de clasificación de acuerdo a la cantidad y calidad de evidencia científica, esto con el fin de evitar generar falsas expectativas hacía medicamentos que no han progresado a evaluaciones experimentales.
Entre los retos que presenta la estrategia de reposicionamiento de fármacos se encuentran la propiedad intelectual y la cantidad limitada de compuestos a reutilizar, no obstante, se espera que el uso de nuevas herramientas como la inteligencia artificial y, en particular, el llamado «aprendizaje profundo», puedan acelerar el proceso y favorecer las colaboraciones entre academia e industrias farmacéuticas.

José L. Medina-Franco
Profesor titular de la Universidad Nacional Autónoma de México (unam). Responsable del grupo de investigación difacquim: Diseño de Fármacos Asistido por Computador de la unam. Su investigación se centra en la quimioinformática y el diseño de fármacos asistido por computadora con aplicaciones en objetivos epigenéticos, productos naturales y péptidos. medinajl@unam.com
• Beigel, J. H., Tomashek, K. M., Dodd, L. E., Mehta, A. K., Zingman, B. S., Kalil, A. C., Hohmann, E., Chu, H. Y., Luetkemeyer, A., Kline, S., Lopez de Castilla, D., Finberg, R. W., Dierberg, K., Tapson, V., Hsieh, L., Patterson, T. F., Paredes, R., Sweeney, D. A. y Short, W. R. (ACTT-1 Study Group Members). (2020). Remdesivir for the Treatment of Covid-19 - Preliminary Report. The New England Journal of Medicine. https://doi.org/10.1056/NEJMoa2007764
• Boolell, M., Gepi-Attee, S., Gingell, J. C. y Allen, M. J. (1996). Sildenafil, a novel effective oral therapy for male erectile dysfunction. In British Journal of Urology, 78(2) 257–261.
• Brown, J. B., Niijima, S. y Okuno, Y. (2013). Compound-Protein Interaction Prediction Within Chemogenomics: Theoretical Concepts, Practical Usage, and Future Directions. In Molecular Informatics, 32(11-12), 906-921.
• Cai, Q., Yang, M., Liu, D., Chen, J., Shu, D., Xia, J., Liao, X., Gu, Y., Cai, Q., Yang, Y., Shen, C., Li, X., Peng, L., Huang, D., Zhang, J., Zhang, S., Wang, F., Liu, J., Chen, L. y Liu, L. (2020). Experimental Treatment with Favipiravir for covid-19: An Open-Label Control Study. In Engineering. https://doi. org/10.1016/j.eng.2020.03.007
• Cantini, F., Niccoli, L., Matarrese, D., Nicastri, E., Stobbione, P. y Goletti, D. (2020). Baricitinib therapy in covid-19: A pilot study on safety and clinical impact [Review of Baricitinib therapy in COVID-19: A pilot study on safety and clinical impact]. The Journal of Infection, 81(2), 318-356.
• Cavalla, D. (2017). Scientific commercial value of drug repurposing. Drug Repositioning--Approaches and Applications for Neurotherapeutics, 3–22.
• Chan, H. C. S., Shan, H., Dahoun, T., Vogel, H. y Yuan, S. (2019). Advancing Drug Discovery via Artificial Intelligence Trends in Pharmacological Sciences, 40(8), 592–604.
• Cosentino, G., Conrad, A. O. y Uwaifo, G. I. (2013). Phentermine and topiramate for the management of obesity: a review. Drug Design, Development and Therapy, 7, 267–278.
• Cotanda, F. L. (2006). Crisis sanitarias y respuesta política. Revista de Administración Sanitaria Siglo XXI, 4(3), 401-406.
• DrugBank. (s. f.). Recuperado el 12 de agosto de 2020 de https://www. drugbank.ca/
• Gravitz, L. (2011). Introduction: a smouldering public-health crisis. Nature, 474(7350), S2-S4.
• Hage, D. S. (2017). Analysis of Biological Interactions by Affinity Chromatography: Clinical and Pharmaceutical Applications. Clinical Chemistry, 63(6), 1083-1093.
• Hodos, R. A., Kidd, B. A., Shameer, K., Readhead, B. P. y Dudley, J. T. (2016). In silico methods for drug repurposing and pharmacology. Wiley Interdisciplinary Reviews. Systems Biology and Medicine, 8(3), 186-210. Johns Hopkins Coronavirus Resource Center. (s. f.). Recuperado de https://coronavirus.jhu.edu/
• Horby, P. y Landray, M. (2020). Low-cost dexamethasone reduces death by up to one third in hospitalised patients with severe respiratory complications of COVID-19 Recuperado de https://www.recoverytrial.net/news/ low-cost-dexamethasone-reduces-death-by-up-to-one-third-in-hospitalised-patients-with-severe-respiratory-complications-of-covid-19
• Hutchison, S. L., Ghuman, J. K., Ghuman, H. S., Karpov, I. y Schuster, J. M. (2016). Efficacy of atomoxetine in the treatment of attention-deficit hyperactivity disorder in patients with common comorbidities in children, adolescents and adults: a review. Therapeutic Advances in Psychopharmacology, 6(5), 317-334.
• Jourdan, J.-P., Bureau, R., Rochais, C. y Dallemagne, P. (2020). Drug repositioning: a brief overview. The Journal of Pharmacy and Pharmacology, 72(9), 1145-1151.
• Klug, D. M., Gelb, M. H. y Pollastri, M. P. (2016). Repurposing strategies for tropical disease drug discovery. Bioorganic & Medicinal Chemistry Letters, 26(11), 2569-2576.
• Ledford, H. (2020). Coronavirus breakthrough: dexamethasone is first drug shown to save lives. In Nature, 582(7813), 469-469).
• Lipworth, W. L., Kerridge, I. H. y Day, R. O. (2012). Wrong questions, wrong answers? Are we getting the drugs we need? Clinical Pharmacology and Therapeutics, 91(3), 367-369.
• Loging, W., Harland, L. y Williams-Jones, B. (2007). High-throughput electronic biology: mining information for drug discovery. Nature Reviews. Drug Discovery, 6(3), 220-230.
• Mehta, P., McAuley, D. F., Brown, M., Sanchez, E., Tattersall, R. S., Manson, J. J., Collaboration, H. A. S. et al.. (2020). COVID-19: consider cytokine storm syndromes and immunosuppression. Lancet, 395(10229), 1033.
• Naylor, D. M. (2015). Therapeutic drug repurposing, repositioning and rescue. Drug Discovery, 57. Recuperado de https://www.researchgate.net/ profile/Stephen_Naylor2/publication/282951546_Therapeutic_drug_repurposing_repositioning_and_rescue_Part_II_Business_review/links/ 568c102208ae71d5cd04abdc/Therapeutic-drug-repurposing-repositioning-and-rescue-Part-II-Business-review.pdf
• oms (2015). ¿Por qué se les dice «desatendidas» a algunas enfermedades tropicales? Recuperado de https://www.who.int/features/qa/58/es/
• Oprea, T. I. y Overington, J. P. (2015). Computational and Practical Aspects of Drug Repositioning. Assay and Drug Development Technologies, 13(6), 299-306.
• Paul, S. M. y Lewis-Hall, F. (2013). Drugs in search of diseases. Science Translational Medicine, 5(186), 186fs18.
• Pushpakom, S., Iorio, F., Eyers, P. A., Escott, K. J., Hopper, S., Wells, A., Doig, A., Guilliams, T., Latimer, J., McNamee, C., Norris, A., Sanseau, P., Cavalla, D. y Pirmohamed, M. (2019). Drug repurposing: progress, challenges and recommendations. Nature Reviews. Drug Discovery, 18(1), 41-58.
• Rognan, D. (2013). Towards the Next Generation of Computational Chemogenomics Tools. Molecular Informatics, 32(11-12), 1029-1034.
• Santos, J., Brierley, S., Gandhi, M. J., Cohen, M. A., Moschella, P. C. y Declan, A. B. L. (2020). Repurposing Therapeutics for Potential Treatment of SARSCoV-2: A Review. Viruses, 12(7). https://doi.org/10.3390/v12070705
• Singh, N., Chaput, L. y Villoutreix, B. O. (2020). Virtual screening web servers: designing chemical probes and drug candidates in the cyberspace. Briefings in Bioinformatics. https://doi.org/10.1093/bib/bbaa034
• Suchonwanit, P., Thammarucha, S. y Leerunyakul, K. (2019). Minoxidil and its use in hair disorders: a review. Drug Design, Development and Therapy, 13, 2777-2786.
• Swinney, D. C. y Pollastri, M. P. (2019). Drug Discovery Strategies for Neglected Tropical Diseases: Repurposing Knowledge, Mechanisms and Therapeutics to Increase Discovery Efficiency. Neglected Tropical Diseases: Drug Discovery and Development, 1-13.
• Vogt, I. y Mestres, J. (2010). Drug-Target Networks. Molecular Informatics, 29(1-2), 10–14.
• Wang, Y., Zhang, D., Du, G., Du, R., Zhao, J., Jin, Y., Fu, S., Gao, L., Cheng, Z., Lu, Q., Hu, Y., Luo, G., Wang, K., Lu, Y., Li, H., Wang, S., Ruan, S., Yang, C., Mei, C., … Wang, C. (2020). Remdesivir in adults with severe COVID-19: a randomised, double-blind, placebo-controlled, multicentre trial. The Lancet, 395(10236), 1569-1578.
• Warren, T. K., Jordan, R., Lo, M. K., Ray, A. S., Mackman, R. L., Soloveva, V., Siegel, D., Perron, M., Bannister, R., Hui, H. C., Larson, N., Strickley, R., Wells, J., Stuthman, K. S., Van Tongeren, S. A., Garza, N. L., Donnelly, G., Shurtleff, A. C., Retterer, C. J. y Bavari, S. (2016). Therapeutic efficacy of the small molecule GS-5734 against Ebola virus in rhesus monkeys. Nature, 531(7594), 381-385.