
MERS-CoV and its relevance for understanding




MERS-CoV and its relevance for understanding

Y SU RELEVANCIA PARA EL ENTENDIMIENTO DE LAS



RESUMEN

ABSTRACT
El coronavirus del síndrome respiratorio de Oriente Medio (mers-CoV) se identificó como un patógeno que causó una enfermedad respiratoria grave en humanos durante el verano de 2012. Pertenece al género Betacoronavirus, al cual también ha sido asignado el nuevo agente viral responsable de la actual catástrofe global e identificado como sars-CoV-2. Ambos coronavirus son de origen zoonótico y han sido identificados en una amplia variedad de huéspedes, incluidos mamíferos y aves. Sin embargo, el mers-CoV cuenta con características intrínsecas que le confieren un grado mayor de virulencia. Los tratamientos reportados para dicho coronavirus pueden ser de utilidad para las investigaciones actualmente realizadas para el manejo terapéutico de pacientes infectados por sars-CoV-2.
PALABRAS CLAVE
Jorge Luis Mejía-Méndez · Lucila Isabel Castro-Pastrana · Erwin Josuan Pérez-Cortés



Neumonía viral · mers-CoV · sars-CoV-2 · COVID-19 · Zoonosis · Pandemia
The Middle East respiratory syndrome coronavirus (MERSCoV) was identified as a pathogen that caused severe respiratory disease in humans during the summer of 2012. It belongs to the genus Betacoronavirus, to which has been assigned the new viral agent responsible for the current global catastrophe and identified as SARS-CoV-2. Both coronaviruses are of zoonotic origin and have been identified in a wide variety of hosts, including mammals and birds. However, the MERS-CoV has intrinsic characteristics that give it a greater degree of virulence. The treatments reported for this coronavirus may be useful for the investigations that are currently being carried out for the therapeutic management of patients infected with SARS-CoV-2.
KEYWORDS
Viral pneumonia · MERS-CoV · SARS-CoV-2 · COVID-19 · Zoonosis · Pandemia










DEL SÍNDROME RESPIRATORIO DE ORIENTE MEDIO (MERS-CoV) SE IDENTIFICÓ COMO UN PATÓGENO QUE CAUSÓ UNA ENFERMEDAD RESPIRATORIA GRAVE EN HUMANOS DURANTE EL VERANO DE 2012.
INTRODUCCIÓN

LA NEUMONÍA ES UNA DE LAS PRINCIPALES CAUSAS DE HOSPITALIZACIÓN EN TODO EL MUNDO Y CONLLEVA A UNA MORBILIDAD Y MORTALIDAD SIGNIFICATIVAS.
La neumonía es una de las principales causas de hospitalización en todo el mundo y conlleva a una morbilidad y mortalidad significativas que difieren según la etiología subyacente. En general, la neumonía viral se considera menos grave en comparación con la neumonía bacteriana. Numerosas clases de patógenos pueden causar neumonía aguda y el riesgo de neumonía aumenta considerablemente en condiciones de defensa pulmonar deteriorada del huésped. El principal patógeno causante de la neumonía adquirida en la comunidad (nac) es la bacteria Gram-positiva Streptococcus pneumoniae, que representa la mayoría de las infecciones bacterianas del tracto respiratorio superior e inferior y es responsable de millones de muertes al año (Dietert et al., 2017).
En los últimos años, las neumonías virales de origen zoonótico han causado brotes marcados por una rápida propagación y alta mortalidad, tal es el caso de la aparición en 2002, del coronavirus del síndrome respiratorio agudo severo (sars-CoV) y de la pandemia de gri-
pe porcina H1N1 en 2009. Su presencia puede ser difícil de predecir a medida que surgen nuevas cepas o resurgen los reservorios zoonóticos (Schindewolf y Menachery, 2019), fenómeno actualmente observado en las infecciones causadas por un nuevo coronavirus, sarsCoV-2 cuya infección es denominada COVID-19 (Whitworth, 2020). Inicialmente, en diciembre de 2019 se ubicó en la región de Wuhan, China, siendo expandido a más de cien países con más de cien mil casos confirmados y más de 3,800 muertes confirmadas en todo el mundo al 11 de marzo de 2020, día en el que la Organización Mundial de la Salud (oms) declaró al COVID-19 como pandemia (Smith y Judd, 2020). Desafortunadamente, el 28 de febrero de 2020, en China se reportó una tasa de mortalidad estimada de ~ 2% (Duan et al., 2020). La velocidad y brusquedad de su diseminación es alarmante, al igual que lo fue con los casos de infección reportados por mers-CoV. Sin embargo, en la última década, la mortalidad relacionada con la neumonía viral ha aumentado sustancialmente por infección del coronavirus del síndrome respiratorio de Oriente Medio (mers-CoV). Hasta julio de 2017, la oms había recibido informes de 27 países de 2,040 casos de mers confirmados por laboratorio y al menos 677 muertes relacionadas que representaban una letalidad del 35%. Se ha descrito que el curso de la enfermedad varía desde una enfermedad viral asintomática hasta insuficiencia respiratoria mortal y el desarrollo del síndrome de dificultad respiratoria aguda (sdra). También se ha informado afectación gastrointestinal y renal en un tercio y la mitad de los casos, respectivamente (Al-Baadani et al., 2019). El virus mers-CoV se informó por primera vez en 2012 en un paciente que vivía en el Reino de Arabia Saudita (Conzade et al., 2018; Hemida et al., 2019), y entre el 1 de septiembre de 2012 y el 15 de junio de 2013, hubo 47 casos confirmados por laboratorio (46 adultos y un niño) con una tasa de mortalidad del 60%. Assiri et al., (2013) habían reportado las características
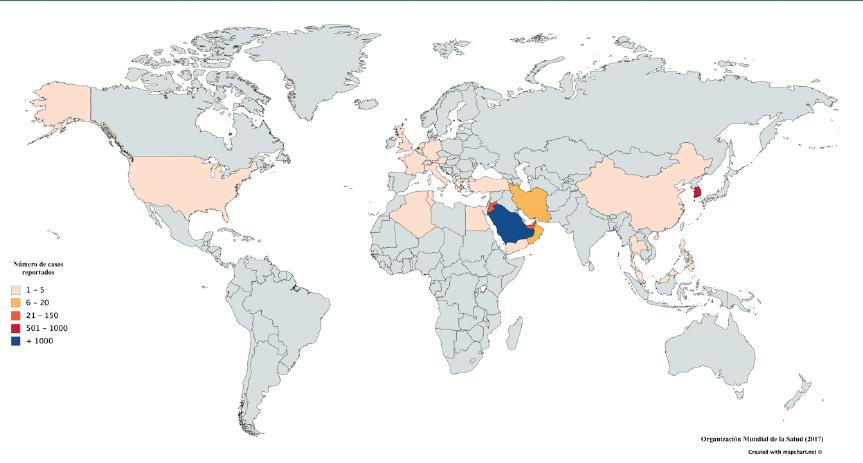
epidemiológicas del mers-CoV en Arabia Saudita, ya sea como casos comunitarios que se ejecutan en grupos dentro de las familias o entre los trabajadores de la salud con o sin contacto directo con los camellos. Durante junio-agosto de 2015, ocurrió un segundo brote de mers-CoV con un total de 130 casos detectados. En general, 96 pacientes (74%) requirieron hospitalización, de ellos 63 (66%) requirieron tratamiento de cuidados intensivos y la tasa de mortalidad fue del 53% (Al-Baadani et al., 2019). Al 31 de julio de 2019, un total de 2,458 casos y 848 muertes han sido reportados a la oms con todos los casos en el Medio Oriente o en viajeros de esta región o sus contactos. La distribución del número de casos reportados alrededor del mundo se presenta en la figura 1. Los casos de mers se dividen en dos categorías, primaria y secundaria. Los casos secundarios, que resultan más comúnmente de la transmisión de persona a persona en los hospitales, fueron más prominentes durante los primeros años del brote. No obstante, debido a que se consideraron medidas estrictas de control de infecciones, una mayor proporción de casos se clasifica como primaria. Se cree que los camellos son la fuente zoonótica de infec-

ciones primarias, pero una gran proporción de pacientes no describen contacto con camellos, lo que plantea la cuestión de cómo adquirieron la enfermedad (Zheng et al., 2019). Por lo tanto, a continuación, se presenta una revisión bibliográfica respecto a la patogenia, epidemiología y tratamiento de pacientes infectados por mers-CoV para, posteriormente, discutir cómo el conocimiento adquirido con este virus puede servir de sustento a las estrategias de mitigación, tratamiento y prevención de la infección con sars-CoV-2 que están sobre la mesa en 2020.
MÉTODOS
Estrategia de búsqueda y selección de artículos
Se llevó a cabo un estudio de revisión bibliográfica utilizando el motor de búsqueda PubMed. Para la evaluación de los estudios consultados se consideró un lapso no mayor a cinco años. Los criterios de inclusión de artículos fueron los siguientes: a) análisis de artículos originales y revisiones sistemáticas publicados en PubMed, b) reporte de datos epidemiológicos sobre la infección por mers-CoV y sars-CoV-2, y c) evaluación de posibles tratamientos.



el sitio online mapchart.net).





Los coronavirus son un gran grupo de virus que causan muchos problemas de salud (síndromes respiratorios, entéricos y nerviosos) en varias especies de animales y humanos. Con el paso de los años y según sus secuencias genómicas, se han clasificado en los géneros de Alfacoronavirus (HCoV-229E y HCoV-NL63) y Betacoronavirus (HCoV-OC43, HCoV-HKU1, sars-CoV y mers-CoV) (Wang et al., 2016). El nuevo sarsCoV-2 muestra un 82% de similitud a nivel de arn con sars-CoV por lo que se le ha situado dentro del género Betacoronavirus (Zhang et al., 2020).
A pesar de ello, el coronavirus del síndrome respiratorio de Oriente Medio (mers-CoV) fue el primero en ser identificado en 2012 tratándose de un virus de arn monocatenario cuya infección conduce a una variedad de resultados clínicos en humanos que van desde infección asintomática y leve hasta lesión pulmonar aguda grave, insuficiencia multiorgánica y muerte. Debido a su alta tasa de mortalidad y su potencial de propagación en todo el mundo, es importante comprender el origen de tal agente viral, así como el estudio de la patogénesis de mers-CoV en modelos animales. Los ratones son las especies de animales de laboratorio más comunes y accesibles utilizadas para la investigación biomédica en general (Algaissi et al., 2020).
Los murciélagos desempeñan un papel fundamental en el mantenimiento de los ecosistemas contando con una gran relevancia como polinizadores y dispersores de semillas de diversas especies de plantas. Representan la única manera natural de combatir grandes cantidades de insectos capaces de transmitir enfermedades mientras que otros están considerados plagas agrícolas. Sin embargo, el origen primario del mers-CoV tanto en humanos como en camellos coincide en la familia de murciélagos denominada Vespertilionidae (Baharoon y Memish, 2019; Cuhna y Poal, 2014). Este dato se puede comparar con lo recientemente reportado para el sars-CoV-2 cuyo origen primario ha sido identificado en la especie de murciélagos Rhinolophus affinis presentando una similitud del 96.2% en su secuenciación genética. Además es importante resaltar que este tipo de mamíferos son conocidos por ser los hospederos de predilección de treinta coronavirus (Xu et al., 2020).
Epidemiología de la enfermedad por mers-CoV


que las personas sin condiciones médicas previas (9.2%). Del mismo modo, los pacientes mayores de sesenta años tuvieron una tasa de mortalidad más alta (38.1%) que los pacientes más jóvenes (6.4%) (Adhikari et al., 2019).
Transmisión camello-humano de mers-CoV
LA ENFERMEDAD SE HA REPORTADO EN 27 PAÍSES DE DIFERENTES CONTINENTES, LA MAYORÍA DE ELLOS ASOCIADOS CON VIAJES RECIENTES A LA PENÍNSULA ÁRABE.
Origen y reservorio de mers-CoV Los murciélagos son el segundo mayor orden de mamíferos, con más de 1,200 especies o aproximadamente el 20% de todas las especies de ellos clasificados en todo el mundo. Se encuentran en todos los continentes, excepto en la Antártida. También fungen como reservorios naturales de muchos patógenos microbianos y su movilidad a través del vuelo, la longevidad y las estructuras sociales contribuyen a la transmisión y propagación de enfermedades zoonóticas (Arai y Yanagihara 2019).
La enfermedad se ha reportado en 27 países de diferentes continentes, la mayoría de ellos asociados con viajes recientes a la península árabe. La transmisión de persona a persona ha sido bien documentada, especialmente en trabajadores de la salud y miembros de la familia, y puede dar lugar a grandes brotes con un impacto significativo en la salud pública como se observa en el Medio Oriente y Corea. Se ha informado que la tasa de mortalidad del paciente varía en gran medida según la edad y las afecciones subyacentes, como diabetes, enfermedades cardíacas y enfermedad pulmonar crónica. En el brote de Corea del Sur, se informó que la tasa de mortalidad general fue del 19.4%. Las personas infectadas con mers que ya estaban hospitalizadas por otras afecciones médicas tuvieron una tasa de mortalidad más alta (33.8%)
MUESTRA UN
Las personas en contacto cercano con los camellos dromedarios, con los pacientes con infecciones por mers-CoV y los trabajadores de la salud que atienden a pacientes con mers-CoV tienen un mayor riesgo de contraer la infección en comparación con la población general. Se cree que la transmisión de mers-CoV de los camellos a los seres humanos se produce por contacto directo con los camellos a través de gotitas respiratorias o saliva, o por el consumo de productos de camellos, como la leche o la carne de camello poco cocida. La transmisión de especies de mers-CoV ha sido confirmada por la secuenciación de arn viral de muestras obtenidas de camellos dromedarios infectados y de pacientes sintomáticos y asintomáticos después de la exposición a camellos infectados (Hui et al., 2018).
Transmisión humano-humano de mers-CoV
Se ha observado que las personas con casos tempranos de infección por mers-CoV tuvieron exposición a camellos dromedarios (Alraddadi et al., 2016). Los seres humanos adquieren principalmente el virus de los camellos, ya sea directamente a través del contacto directo con las secreciones respiratorias de los camellos infectados o indirectamente a través del contacto con personas que han tenido exposición a la misma secreción. Estas infecciones primarias pueden verse desencadenadas al ser transmitidas de persona a persona a través del contacto cercano con secreciones respiratorias humanas infectadas, por lo general, en centros
DE SIMILITUD A NIVEL ARN CON SARS-CoV SE SITÚA DENTRO DEL GÉNERO
BETACORONAVIRUS.
de atención médica. Los pacientes con dicha infección usualmente presentan signos y síntomas respiratorios agudos acompañados de fiebre, tos, dolor de cabeza, mialgia y, a veces, náuseas, vómitos o diarrea. La gravedad de la enfermedad varía ampliamente de casos asintomáticos a resultados fatales (Al-Raddadi et al., 2019).
Comparativamente, la transmisión de sars-CoV-2 de persona a persona se produce principalmente entre miembros de la familia y amigos que contactaron íntimamente con pacientes o portadores del virus. Se suponía que el contacto directo con los animales hospedadores intermedios o el consumo de animales salvajes era la ruta principal de transmisión del sars-CoV-2 (Guo et al., 2020): los mecanismos de transmisión continúan en discusión y revisión.
Características clínicas de mers-CoV
SARS-CoV SE IDENTIFICÓ EN EL
TRATÁNDOSE DE UN VIRUS ARN EN UN PACIENTE QUE VIVÍA EN EL REINO DE ARABIA SAUDITA Y ENTRE EL 1 DE SEPTIEMBRE DE 2012 Y EL 15 DE JUNIO DE 2013, HUBO 47 CASOS CONFIRMADOS POR LABORATORIO.
La media de edad de las personas con infección por mers-CoV confirmada por laboratorio es de 49 años donde el 65% de los pacientes son hombres. El tiempo promedio desde el inicio de la enfermedad hasta la hospitalización es de aproximadamente cuatro días, lo que resulta en una mediana de estadía de 41 días. Actualmente, entre todos los pacientes, la tasa de morbilidad es aproximadamente del 36%. Los hallazgos en la radiografía de tórax y la tomografía computarizada son generalmente consistentes con neumonitis viral y síndrome de dificultad respiratoria aguda. Los resultados de laboratorio incluyen linfopenia, trombocitopenia y niveles elevados de lactato deshidrogenasa (Chafekar y Fielding, 2018; Habib et al., 2019).
Manejo y medidas de prevención Hasta la fecha, no existen vacunas o terapias autorizadas para la prevención o el tratamiento de la infección por mers-CoV y la terapia se centra en la atención de soporte vital para dis-



minuir los síntomas y, en casos más graves, también para apoyar la función de los órganos vitales. Considerando que no hay un tratamiento específico disponible, la terapia de apoyo y el uso de antivirales de amplio espectro son actualmente las opciones de tratamiento. Se ha utilizado una amplia gama de terapias en la clínica para tratar a pacientes infectados con mers-CoV, y su uso se basa en el conocimiento obtenido durante el brote del síndrome respiratorio agudo severo (sars) en 2003 y los casos reportados de influenza en 2009. Además, faltan estudios clínicos completos y sólo se dispone de datos de campo (Leyva-Grado y Behzadi 2019). La cuestión de cómo abordar a estos pacientes para el diagnóstico y el tratamiento continúa evolucionando, ya que, para los pacientes en Estados Unidos, los Centros para el Control y la Prevención de Enfermedades (cdc) actualizan continuamente la información y tienen instrucciones sobre a quién evaluar y el flujo de trabajo a seguir con respecto al manejo de muestras (Guarner, 2020).



no pasteurizada, carne cruda, vísceras y orina (Kandeil et al., 2019). En adición, se ha promovido acelerar el desarrollo de una vacuna de camello dromedario para evaluar el potencial de reducir la transmisión de contagio a los humanos. La aceptabilidad, la rentabilidad y la viabilidad de esta vacuna también deberán evaluarse y compararse con otras estrategias de intervención, como la vacunación humana de grupos de alto riesgo (Aguanno et al., 2018).
(Gong y Bao, 2018). Sin embargo, otras especies animales como los primates (macacos rhesus y titíes comunes), miembros de la familia Camelidae (alpacas y llamas), conejos y cerdos han demostrado ser susceptibles a la infección por mers-CoV (Vergara-Alert et al., 2017).
Por otra parte, el descubrimiento de fármacos comienza con el diagnóstico de una enfermedad con síntomas bien caracterizados.

LA INFECCIÓN
CON MERS-CoV

LOS CORONAVIRUS
SON UN GRAN GRUPO DE VIRUS QUE CAUSAN MUCHOS PROBLEMAS DE SALUD (SÍNDROMES RESPIRATORIOS, ENTÉRICOS Y NERVIOSOS) EN VARIAS ESPECIES DE ANIMALES Y HUMANOS.
Los estudios han descrito demoras en el reconocimiento de casos y el establecimiento de precauciones para el control de infecciones como factores en la transmisión asociada a la atención médica. Las prácticas de triage que resultan en un aislamiento rápido de pacientes sospechosos de mers y la aplicación de precauciones pueden disminuir las oportunidades de infección. Sin embargo, la inespecificidad de los signos y síntomas dificultan la identificación rápida de casos de mers-CoV (Killerby et al., 2020).
Las actuales estrategias de control recomendadas para la infección por mers-CoV en camellos son la vigilancia reguladora, el control del movimiento de camellos en las áreas infectadas, el uso de equipos de protección personal durante el manejo de los camellos, el aumento de la conciencia sobre el virus y los riesgos de exposición a la leche de camello
Áreas de oportunidad en la investigación biomédica para enfrentar a los coronavirus La infección con mers-CoV ha dado como resultado una mayor mortalidad y nuevos síntomas. Por lo tanto, se necesita identificar urgentemente los orígenes de los virus y encontrar formas de tratarlos a través de modelos experimentales en animales, los cuales son los principales estudios que permiten el aumento del conocimiento científico a pasos agigantados, ya que constituyen el primer paso antes de la investigación clínica, observando la fisiopatología, patogenia, tratamiento y prevención de las enfermedades. Sin embargo, en la mayoría de los países latinoamericanos se tiene poca experiencia con el área experimental (Tarrillo et al., 2016). Las diversas formas de neumonía se han reproducido con éxito en modelos murinos específicos siendo inducidas experimentalmente. Estos modelos han contribuido sustancialmente a la comprensión del desarrollo de la neumonía adquirida en la comunidad y en el hospital, así como de las infecciones pulmonares emergentes en todo el mundo, y son indispensables para el desarrollo de nuevas estrategias terapéuticas (Dietert et al., 2017).
Se han presentado una serie de modelos animales dentro de las investigaciones consultadas, así como el daño observado en el mismo organismo una vez que fue inoculado el virus teniendo en cuenta lesiones histopatológicas
Convencionalmente, un medicamento deseable se compondría de una molécula, simple o compleja, o bien de una combinación de químicos capaz de reducir o desaparecer los síntomas sin causar reacciones adversas graves en el paciente. Otras propiedades incluyen la asequibilidad y el beneficio para las compañías farmacéuticas, la baja probabilidad de que se desarrolle resistencia a los medicamentos, lo cual puede conducir a una disminución dramática en el valor comercial del agente terapéutico, entre otros. Por lo tanto, se requieren técnicas bioinformáticas que permitan el diseño y predicción del efecto farmacológico que tendrán este tipo de sustancias. Estas investigaciones son desempeñadas por biólogos moleculares, químicos computacionales y matemáticos (Xia, 2017).
Adicionalmente la progresión tecnológica se refleja en una serie de plataformas de detección molecular con enfoques de biología computacional capaces de proporcionar nuevas ideas para responder rápidamente contra las enfermedades virales emergentes (Tortorici y Veesler2019). El prototipo de estos enfoques incluye el modelo animal in vivo, el modelo de cultivo de tejidos y los estudios de vacunas (Skariyachan et al., 2019). Tal es el caso de la secuenciación genética de todos los CoV conocidos, donde el mayor número de genomas, casi completos, está disponible para sars-CoV y mers-CoV incrementando la posibilidad de conocer el origen y evolución de estos agentes virales (Lau et al., 2017; Liu et al., 2020).
HA DADO COMO RESULTADO UNA MAYOR MORTALIDAD Y NUEVOS SÍNTOMAS.
Discusión
El control de la situación epidémica en 2020 por las infecciones por coronavirus –específicamente aquellas diagnosticadas como COVID-19– es extremadamente urgente y los tratamientos contra COVID-19 son incipientes. El 14 de febrero de 2020, había más de 54,000 pacientes confirmados en la provincia de Hubei, China. Las cifras reportadas hasta la fecha de elaboración de este artículo pueden ser complicadas de consultar puesto que a medida que se realiza la presente revisión la tasa de infección aumenta.
EN LA MAYORÍA DE LOS PAÍSES LATINOAMERICANOS SE TIENE POCA EXPERIENCIA CON EL ÁREA EXPERIMENTAL.

LAS DIVERSAS FORMAS DE NEUMONÍA SE HAN REPRODUCIDO CON ÉXITO EN MODELOS MURINOS ESPECÍFICOS, SIENDO INDUCIDAS EXPERIMENTALMENTE.
Debido a la falta de medicamentos antivirales efectivos, el pronóstico de la evolución de los pacientes depende únicamente de su edad y condición física. La posible mutación adaptativa del sars-CoV-2 dificulta el desarrollo de la vacuna. Por lo tanto, es urgente desarrollar métodos de diagnóstico más sensibles y medicamentos efectivos (Xu et al., 2020). La secuenciación genética de sars-CoV-2 demostró una alta similitud con lo ya sabido respecto a sarsCoV y mers-CoV, por lo que considerar casos ya reportados e información científica extraída de pacientes tratados contra mers-CoV puede ser de alta utilidad para el entendimiento del origen, epidemiología, fisiopatología y posible tratamiento para las infecciones por COVID-19. Aunque se ha demostrado la seguridad clínica de los medicamentos ya disponibles en el mercado, algunos de ellos pueden causar reacciones adversas graves. Por ejemplo, la hidroxicloroquina desencadena como reacción adversa arritmia, que puede conducir a la muerte. Por lo tanto, se debe prestar especial atención a la seguridad de fármacos para estas nuevas indicaciones (Duan et al., 2020).
La aparición de mers-CoV sigue constituyendo un gran desafío para el sistema de salud de Arabia Saudita. Dado que Oriente Medio es un centro de actividades de turismo y negocios, viajar a esta región representa un riesgo para los
viajeros que podrían adquirir y diseminar mersCoV más allá de sus límites. Arabia Saudita, como destino de millones de peregrinos para la costa del Hajj cada año y para Omra durante todo el año, está particularmente bajo un desafío enorme para proteger, no sólo a sus propios ciudadanos y residentes, sino también a la población mundial de esta infección emergente. Si bien se considera que los camellos dromedarios son la fuente del mers humano primario (no nosocomial), la mayoría de los casos de mers no describen la exposición al camello, por lo que es crítico determinar la vía precisa de la transmisión del camello al humano. Aquellas personas que tengan un mayor contacto con camellos tienen un alto riesgo de infección por mers-CoV y podrían servir como conductos para la infección de la población general (Alshukairi et al., 2018).
Se ha registrado un aumento de los casos de infección por mers-CoV adquiridos en la comunidad observados en el periodo comprendido entre marzo y mayo en Arabia Saudita lo cual puede corresponder a un factor estacional como lo es la temporada de parto (diciembre a febrero) para los camellos, incrementando así la exposición que tendrán los humanos. Considerando lo reportado, técnicas moleculares como rt-pcr (reverse transcription-PCR, por sus siglas en inglés) y crispr (Clustered Regularly Interspaced Short Palindromic Repeats, por sus siglas en inglés) han facilitado la detección de mers-CoV en pacientes infectados y, actualmente también de sars-CoV-2.
CONCLUSIONES
Ha habido tres brotes importantes de coronavirus en el siglo 21: sars-CoV (2002), mers-CoV (2012) y sars-CoV-2 (2019). La bibliografía consultada y concentrada en el presente artículo demuestra que mers-CoV sigue siendo un desafío no sólo en términos de diagnóstico y tratamiento, sino también en lo que respecta a la comprensión del origen, formas de transmisión y epidemiología de la enfermedad que causa. Mientras las investigaciones sobre el mers-CoV
siguen en proceso, la humanidad ya tiene ante sí un nuevo reto, el sars-CoV-2 o COVID-19.
Se sabe que el mers-CoV causa frecuentemente infecciones con síntomas muy leves o atípicos, por lo que puede pasar inadvertido, mientras que el número de infecciones por COVID-19 crece de manera desmesurada. Ello sugiere que el personal sanitario deba aplicar precauciones estándar continuamente con todos los pacientes de hospitales en los que se haya diagnosticado algún caso de infección por dicho coronavirus. El implementar medidas profilácticas que impidan la diseminación del virus resulta crucial en la población actual puesto que, de no ser así, SARS-CoV-2 continuará encabezando la catástrofe global a la que nos enfrentamos.
La experiencia de estrategias de detección efectivas y de desarrollo de fármacos es aún emergente por lo que tiene que ser explotada estableciéndose a nivel molecular y en modelos animales lo antes posible. Existen propuestas sumamente interesantes de nuevos agentes terapéuticos para responder a la amenaza de salud pública global que representa el COVID-19, sin embargo, las investigaciones deben acelerarse para ganar el mayor tiempo posible.

Jorge Luis Mejía Méndez
Licenciado en Ciencias Farmacéuticas por la udlap
Actualmente es estudiante del Doctorado en Biomedicina
Molecular en la misma institución donde su investigación se encuentra dirigida a la obtención, identificación y encapsulación de principios activos de plantas medicinales. jorge.mejiamz@udlap.mx

Lucila Isabel
Castro Pastrana
Doctora en Bioquímica Farmacéutica por la Universidad de Tübingen, Alemania. Fue profesora visitante en la Universidad de British Columbia en temas de farmacovigilancia y farmacogenómica. Es autora y compiladora de cuatro libros sobre farmacovigilancia. Se encuentra certificada por trayectoria profesional en el perfil Farmacia por el Colegio Nacional de Químicos Farmacéuticos Biólogos México. Es profesora de tiempo completo de la udlap lucila.castro@ udlap.mx

Erwin Josuán
Pérez Cortés
Doctor en Ciencias Fisiológicas. Coordinador del Posgrado de la Escuela de Ciencias de la udlap erwin.perez@udlap.mx
• Adhikari, U., Chabrelie, A., Weir, M., Boehnke, K., McKenzie, E., Ikner, L., ... y Rose, J. (2019). A Case Study Evaluating the Risk of Infection from Middle Eastern Respiratory Syndrome Coronavirus (MERS-CoV) in a Hospital Setting Through Bioaerosols. Risk Analysis 39(12), 2608-2624.
• Aguanno, R., ElIdrissi, A., Elkholy, A. A., Embarek, P. B., Gardner, E., Grant, R., ... y Wiersma, L. (2018). MERS: Progress on the global response, remaining challenges and the way forward. Antiviral research 159 35-44.
• Ai, J. W., Zhang, Y., Zhang, H. C., Xu, T., y Zhang, W. H. (2020). Era of molecular diagnosis for pathogen identification of unexplained pneumonia, lessons to be learned. Emerging Microbes & Infections, 9(1), 597-600.
• Al-Baadani, A. M., Elzein, F. E., Alhemyadi, S. A., Khan, O. A., Albenmousa, A. H., y Idrees, M. M. (2019). Characteristics and outcome of viral pneumonia caused by influenza and Middle East respiratory syndrome-coronavirus infections: A 4-year experience from a tertiary care center. Annals of Thoracic Medicine 14(3), 179.
• Al-Raddadi, R. M., Shabouni, O. I., Alraddadi, Z. M., Alzalabani, A. H., Al-Asmari, A. M., Ibrahim, A., ... y Madani, T. A. (2019). Burden of Middle East respiratory syndrome coronavirus infection in Saudi Arabia. Journal of Infection and Public Health.
• Alraddadi, B. M., Watson, J. T., Almarashi, A., Abedi, G. R., Turkistani, A., Sadran, M., ... y Albalawi, E. (2016). Risk factors for primary Middle East respiratory syndrome coronavirus illness in humans, Saudi Arabia, 2014. Emerging infectious diseases 22(1), 49.
• Algaissi, A., Agrawal, A. S., Hashem, A. M. y Tseng, C. T. K. (2020). Quantification of the Middle East Respiratory Syndrome-Coronavirus RNA in Tissues by Quantitative Real-Time RT-PCR. In MERS Coronavirus (pp. 99-106). Nueva York: Humana.
• Alshukairi, A. N., Zheng, J., Zhao, J., Nehdi, A., Baharoon, S. A., Layqah, L., ... y Ten Eyck, P. (2018). High prevalence of MERS-CoV infection in camel workers in Saudi Arabia. MBio, 9(5), e01985-18.
• Arai, S. y Yanagihara, R. (2019). Genetic diversity and geographic distribution of bat-borne hantaviruses. Bat-Borne Viruses; Corrales-Aguilar, E., Schwemmle, M., Eds, 59-86.
• Assiri, A., McGeer, A., Perl, T. M., Price, C. S., Al Rabeeah, A. A., Cummings, D. A., ... y Madani, H. (2013). Hospital outbreak of Middle East respiratory syndrome coronavirus. New England Journal of Medicine, 369(5), 407-416.
• Baharoon, S. y Memish, Z. A. (2019). MERS-CoV as an emerging respiratory illness: A review of prevention methods. Travel medicine and infectious disease 101520.
• Chafekar, A. y Fielding, B. C. (2018). MERS-CoV: understanding the latest human coronavirus threat. Viruses 10(2), 93.
• Conzade, R., Grant, R., Malik, M. R., Elkholy, A., Elhakim, M., Samhouri, D., ... y Van Kerkhove, M. D. (2018). Reported direct and indirect contact with dromedary camels among laboratory-confirmed MERS-CoV cases. Viruses 10(8), 425.
• Cunha, C. B. y Opal, S. M. (2014). Middle East respiratory syndrome (MERS) A new zoonotic viral pneumonia. Virulence, 5(6), 650-654.
• Dietert, K., Gutbier, B., Wienhold, S. M., Reppe, K., Jiang, X., Yao, L., ... y Peteranderl, C. (2017). Spectrum of pathogen-and model-specific histopathologies in mouse models of acute pneumonia. PloS one, 12(11), e0188251.
• Duan, Y, H-Liang, Z. y Zhou, C. (2020) Advance of promising targets andagents against 2019-nCoV in China,Drug Discovery Today
• Gong, S. R. y Bao, L. L. (2018). The battle against SARS and MERS coronaviruses: Reservoirs and Animal Models. Animal Models and Experimental Medicine, (2), 125-133.
• Guarner, J. (2020). Three Emerging Coronaviruses in Two DecadesThe Story of SARS, MERS, and Now COVID-19. American Journal of Clinical Pathology.
• Guo, Y. R., Cao, Q. D., Hong, Z. S., Tan, Y. Y., Chen, S. D., Jin, H. J., ... y Yan, Y. (2020). The origin, transmission and clinical therapies on coronavirus disease 2019 (COVID-19) outbreak–an update on the status. Military Medical Research, 7(1), 1-10.
• Habib, A. M. G., Ali, M. A. E., Zouaoui, B. R., Taha, M. A. H., Mohammed, B. S. y Saquib, N. (2019). Clinical outcomes among hospital patients with Middle East respiratory syndrome coronavirus (MERS-CoV) infection. BMC Infectious Diseases, 19(1), 1-6.
Hemida, M. G. (2019). Middle East respiratory syndrome coronavirus and the one health concept. PeerJ, 7, e7556.
Hui, D. S., Azhar, E. I., Kim, Y. J., Memish, Z. A., Oh, M. D. y Zumla, A. (2018). Middle East respiratory syndrome coronavirus: risk factors and determinants of primary, household, and nosocomial transmission. The Lancet Infectious Diseases 18(8), e217-e227.
Kandeil, A., Gomaa, M., Nageh, A., Shehata, M. M., Kayed, A. E., Sabir, J. S., ... y Byarugaba, D. K. (2019). Middle East Respiratory Syndrome Coronavirus (MERSCoV) in Dromedary Camels in Africa and Middle East. Viruses, 11(8), 717.
Killerby, M. E., Biggs, H. M., Midgley, C. M., Gerber, S. I. y Watson, J. T. (2020). Middle East respiratory syndrome coronavirus transmission. Emerging Infectious Diseases 26(2), 191.
Lau, S. K., Wong, A. C., Lau, T. C. y Woo, P. C. (2017). Molecular evolution of MERS coronavirus: dromedaries as a recent intermediate host or long-time animal reservoir? International journal of molecular sciences, 18(10), 2138.
Liu, C., Zhou, Q., Li, Y., Garner, L. V., Watkins, S. P., Carter, L. J., ... y Albaiu, D. (2020). Research and Development on Therapeutic Agents and Vaccines for COVID-19 and Related Human Coronavirus Diseases.
Leyva-Grado, V. H. y Behzadi, M. A. (2019). Overview of current therapeutics and novel candidates against influenza, respiratory syncytial virus and Middle East respiratory syndrome coronavirus infections. Frontiers in Microbiology 10 1327.
Organización mundial de la salud. (2019). Coronavirus causante del síndrome respiratorio de Oriente Medio (MERS-CoV) — Emiratos Árabes Unidos. Recuperado de https://www.who.int/csr/don/31-october-2019-mers-the-united-arab-emirates/es/
Schindewolf, C. y Menachery, V. D. (2019). Middle east respiratory syndrome vaccine candidates: cautious optimism. Viruses 11(1), 74.
Skariyachan, S., Challapilli, S. B., Packirisamy, S., Kumargowda, S. T. y Sridhar, V. S. (2019). Recent aspects on the pathogenesis mechanism, animal models and novel therapeutic interventions for Middle East respiratory syndrome coronavirus infections. Frontiers in microbiology, 10
Smith, J.A. y Judd, J. (2020). COVID-19: Vulnerability and the power of privilege in a pandemic. Health Promotion Journal of Australia
Tarrillo, G. C., Yshpilco, L. B., Murillo-Padilla, J. C. y Cláudio, J. (2016). Importancia de la investigación en modelos Experimental,¿ qué sesgos debemos de evitar para poder publicar?. CIMEL 21(2), 51-54.
Tortorici, M. A. y Veesler, D. (2019). Structural insights into coronavirus entry. Advances in virus research 105 93-116.
Vergara-Alert, J., Raj, V. S., Muñoz, M., Abad, F. X., Cordon, I., Haagmans, B. L., ... y Segales, J. (2017). Middle East respiratory syndrome coronavirus experimental transmission using a pig model. Transboundary and emerging diseases 64(5), 1342-1345.
Wang, F., Chen, C., Tan, W., Yang, K., y Yang, H. (2016). Structure of main protease from human coronavirus NL63: insights for wide spectrum anti-coronavirus drug design. Scientific reports, 6, 22677.
Whitworth, J. (2020). COVID-19: a fast-evolving pandemic, Transactions of The Royal Society of Tropical Medicine and Hygiene traa025.
Xia, X. (2017). Bioinformatics and drug discovery. Current topics in medicinal chemistry, 17(15), 1709-1726.
Xu, J., Zhao, S., Teng, T., Abdalla, A. E., Zhu, W., Xie, L., ... y Guo, X. (2020). Systematic Comparison of Two Animal-to-Human Transmitted Human Coronaviruses: SARS-CoV-2 and SARS-CoV. Viruses 12(2), 244.
Zheng, J., Hassan, S., Alagaili, A. N., Alshukairi, A. N., Amor, N. M., Mukhtar, N., ... y Yaqub, T. (2019). Middle East Respiratory Syndrome Coronavirus Seropositivity in Camel Handlers and Their Families, Pakistan. Emerging infectious diseases, 25(12), 2307.
Zhang, L., Lin, D., Sun, X., Curth, U., Drosten, C., Sauerhering, L., ... y Hilgenfeld, R. (2020). Crystal structure of SARS-CoV-2 main protease provides a basis for design of improved α-ketoamide inhibitors. Science