2025 THRS Annual Conference in Conjunction with Ventricular Arrhythmia Forum and Taipei-Tokyo-Seoul Arrhythmia Joint Conference 會議心得
三軍總醫院心臟內科 張大為醫師
今年的「2025 THRS Annual Conference in Conjunction with Ventricular Arrhythmia Forum and Taipei-Tokyo-Seoul Arrhythmia Joint Conference 」在台北萬豪酒店盛大舉 行,作為一年一度的心律專業盛事,會中匯聚了國內 外頂尖心律學專家、臨床醫師及研究人員。活動橫跨 整個週末,不僅安排了各式專題演講,也舉辦了多項 臨床案例競賽、海報討論及會議,涵蓋最先進的消融 技術以及新穎的心律植入裝置應用,讓與會者在學術 和臨床經驗上都能有所收穫。
海報展覽對於想要一窺時下研究前沿的同好們, 往往是非常富有學習意義的一項學術活動。有機會看到 其他醫學中心正在進行的研究及發現的初步成果,或許 比期刊帶給我們的知識有更即時的創新啟發。台大醫院 的團隊參與展覽的題目探討了時下非常熱門的心房顫動
治療策略,在病友同時有心房顫動及病竇症候群的狀況 下,依照現有的常規治療放置心臟節律器或是優先執行 心房顫動電燒手術,究竟對病友的all cause death是否會 產生影響。研究結果非常的有參考意義,電燒可能帶來 比過去奉行的節律器治療更好的預後,尤其在左心房尚 未擴大、左心收縮功能並未嚴重下降的病友,可能更有 潛力藉由share decision making選擇更適合每位獨立病友 的醫療服務。雖然研究並不是 RCT 研究,而是以 propensity scores校正的data analysis,但也提供了進行 RCT 研究的潛力題材。中國醫藥大學團隊的嶄新 pulmonary vein isolation電燒策略Handcuff,讓臨床醫師 在傳統術式外,多一種可能的治療選擇。此外也有許多 針對Conduction system pacing的研究,都使與會同好有 機會重新思考臨床與研究上可能的未來。
除了參與海報展覽外,我也在師長的支持下報名 了大會的案例競賽,並從報告者演講內容及國內外評 審大師的點評中獲益良多。許多競賽演講者分享了利用 3D 立體電生理標測系統 (3D mapping) 進行心房撲動或 心房顫動消融的實際經驗,包括 roof line 與 posterior line 消融策略的深入討論。其中一位評審專家建議,做 完 pulmonary vein isolation 後若心房顫動仍可誘發且不 再源於肺靜脈,可優先做posterior line ablation。基於後 壁較薄、基質電位較低的特性,若在此區電燒後成功 抑制心房顫動,則不一定要再進行較厚而不易成功的 roof line ablation。此外也有演講者以自身案例提醒與會 者,epicardial conduction永遠是常規的電燒後仍無法成 功終止macro-reentry tachycardia時,必須想到的鑑別診 斷之一。除了常見的成人心律案例外,此次會議也有 涉獵到發生在兒童身上的心律不整治療。演講者分享 了一位患有罕見結構性心臟問題的兒童,其下腔靜脈 並非直接通往右心房下部,而是經由 Azygos vein 匯入 上腔靜脈,才回流到右心房。這樣的結構導致傳統由 大腿股靜脈進入右心房的電生理檢查與消融路線在操 作上異常困難。講者分享了可能的治療策略:例如使 用右側內頸靜脈、肝靜脈,或仍然由奇靜脈遞送電燒 導管。講者最終以精妙的技術,成功經奇靜脈完成電 燒。此外讓人非常驚艷的案例分享,則是替右位心 (dextrocardia)患者進行電燒消融的案例,因整個心臟解 剖鏡像翻轉,消融導管的操作需要完全不同於常規的 觀察與定位;另一位講者則分享其配合 thoracotomy 裝 置左心室輔助裝置時,同步使用HD Grid導管進行心室 心律不整的心外膜 mapping 經驗。此類案例都展現了新 世代電生理檢查儀器的進步與養成成熟技術的重要 性,也提醒臨床醫師面對各種先天或後天心臟結構變
異時,需要更靈活的應對與團隊合作。
除了案例分享外,琳瑯滿目的學術活動也包括研 究 abstract 的報告競賽、國內外大師對新穎治療策略或 儀器操作的心得案例分享,而最讓人感到興奮的,則 是各家參展贊助紛紛提供自家設備的操作模型,讓有 志於學習日新月異治療設備的年輕醫師及技術員,能在 安全的環境下,接受如intracardiac echocardiography、 left bundle branch pacing 心律調節器的 V lead 置放、 leadless 心律調節器置放的模型操作等,含金量滿滿的 動手實作機會。
本屆大會的每個細節安排及學術活動內容,都可 以說是非常精心策劃且成功。與會的外賓如 EHRA (European Heart Rhythm Association) 會長 Helmut Pürerfellner、HRS(Heart Rhythm Society)候任主席 Mina K. Chung 等人,都對本次的安排讚不絕口,並邀請與 會同好有機會能一同參與 Vienna 的 EHRA 及 San Diego 的 HRS 大會,讓人深刻感受全球心律學界攜手並進的 氛圍。
2025 年初的這場大型國際心律學盛會,不僅展現 了全球心律專業的水準與最新的技術發展,也讓台灣 醫界和年輕醫師有機會在世界舞台上發光發熱。從常 規的AF、VT
消融到挑戰性的罕見結構心臟病處理,都 能看見國際之間對於電生理技術的投入與激盪。隨著 國內外專家的熱烈參與,以及會後如火如荼的聯誼交 流,台灣心律學界的國際連結更上層樓。未來若有更 多年輕醫師能夠積極參與類似的學術場合,相信台灣 在心律學研究與臨床實務上的成果將更加豐碩,與國 際齊步邁進。

A 46-year-old male with a clinically short RP tachycardia
臺北榮民總醫院心臟內科 吳政億醫師
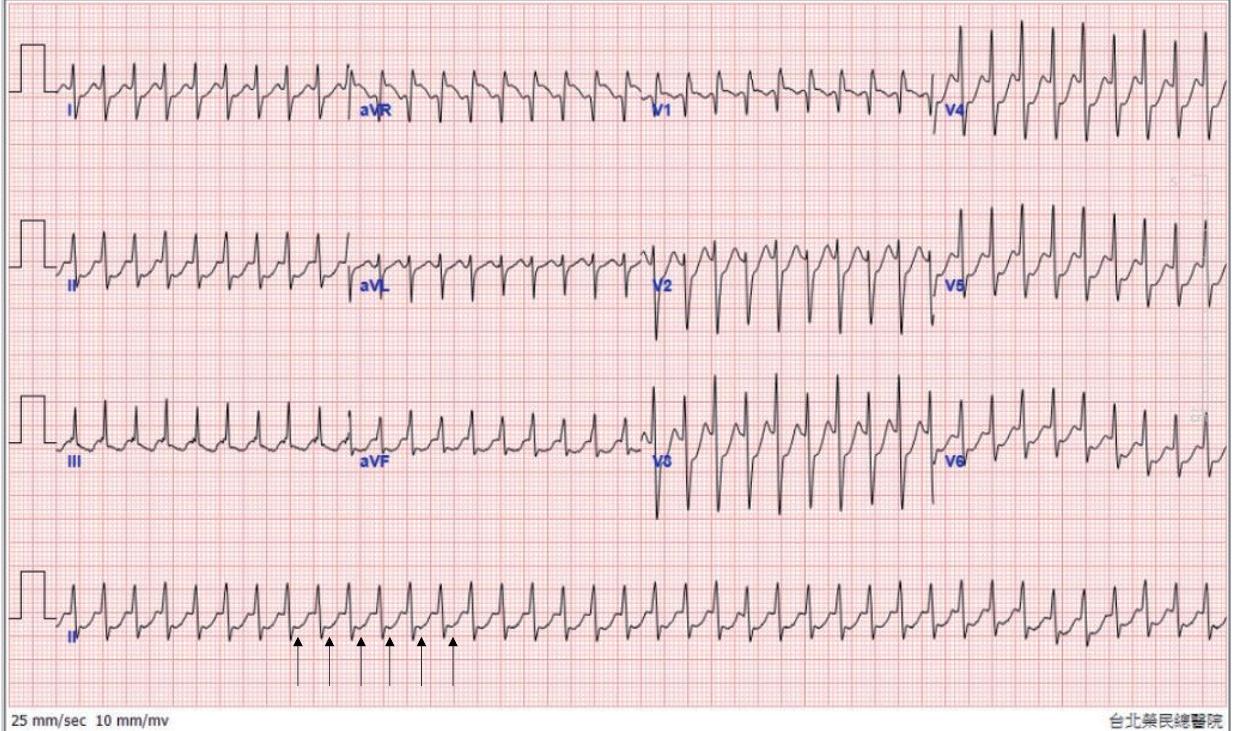
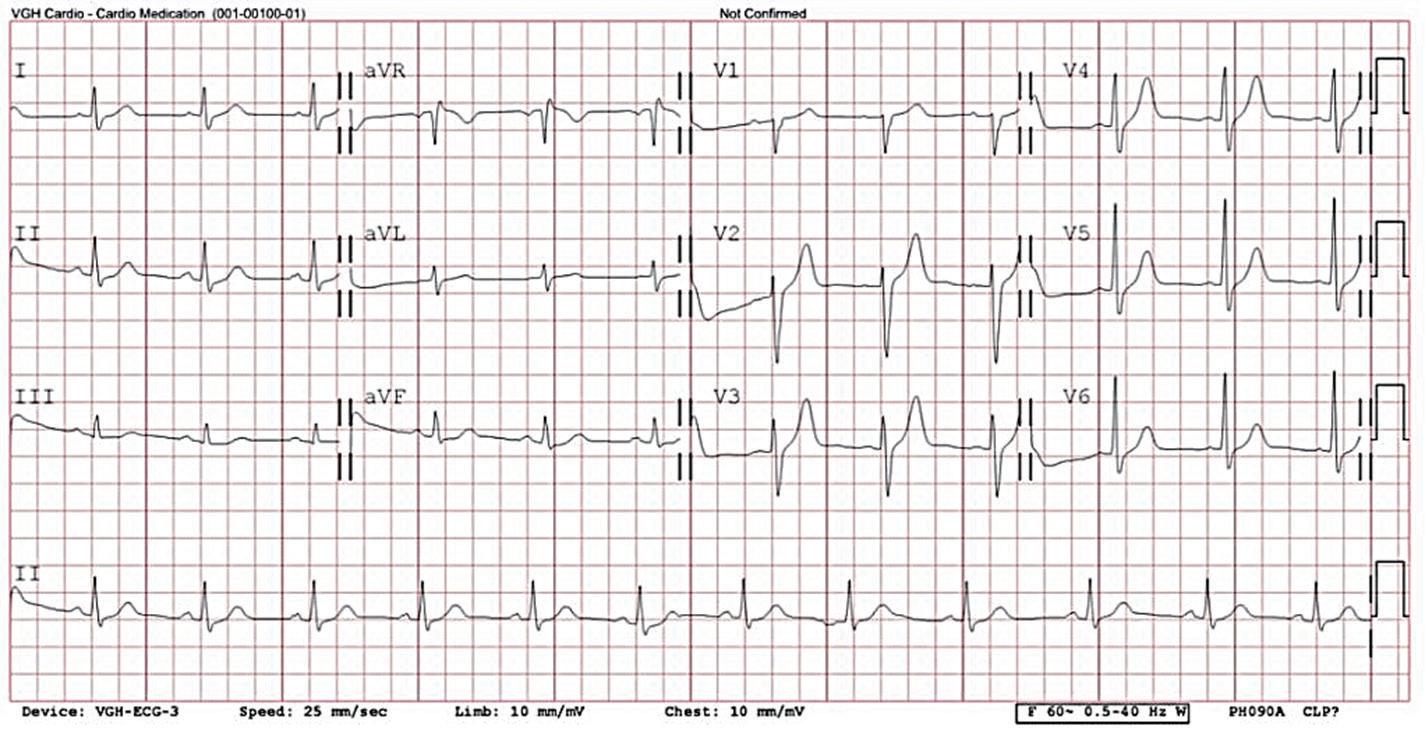
一位 46 歲男性病患去年開始有心悸的症狀。根據 病史詢問,得知患者沒有先天性心臟疾病。因為近日 心悸頻發,所以來到急診求診;發作時的 12 導程心電 圖顯示為short RP tachycardia(HR 220bpm, 如圖一 ),在 急診注射 adenosine 後心律恢復正常, 12 導程心電圖也 沒有異常(圖二)。超音波檢查顯示心臟結構以及左心室 射出分率均正常。經解釋後病患希望接受心臟電生理 檢查併電燒手術。術中放置 CS 導管時, tachycardia 就很容易被導管誘發,根據CS sequence可知為eccentric tachycardia 。放置好診斷管後,電生理檢查發現 RV
S1S1 pacing 時 fast 1 to 1 為 350ms, slow 為 320ms , retrograde fast ERP為280ms,HRA pacing時fast 1 to 1 為
330ms, HRA S1S2 pacing 時 fast ERP 250ms, slow ERP<220ms。Tachycardia很容易被pacing誘發。誘發時 AH 123ms , HA 225ms , AH/HA<1( 圖三 ) , VOP 顯示 為 pseudo VAAV response( 圖四 ) , SA-VA 為 87ms ,
PPI-TCL 為 198ms , His-refractory VPC 顯示 no atrial reset , delta AH 為 37ms 。由以上特徵診斷為 fast-slow AVNRT。在使用RF 50W 50℃ 373 seconds後,fast-slow AVNRT 便無法誘發,術後也未曾復發。根據文獻約有 3% 的 AVNRT 患者同時有 typical AVNRT 和 atypical AVNRT[1],雖然臨床ECG疑似為short RP tachycardia, 但根據電生理檢查,最後仍有可能診斷為 fast-slow AVNRT。
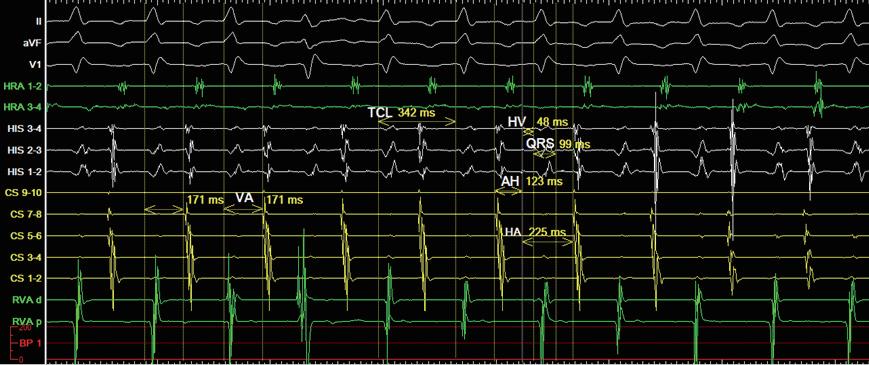
(圖三)、tachycardia時的EGM。
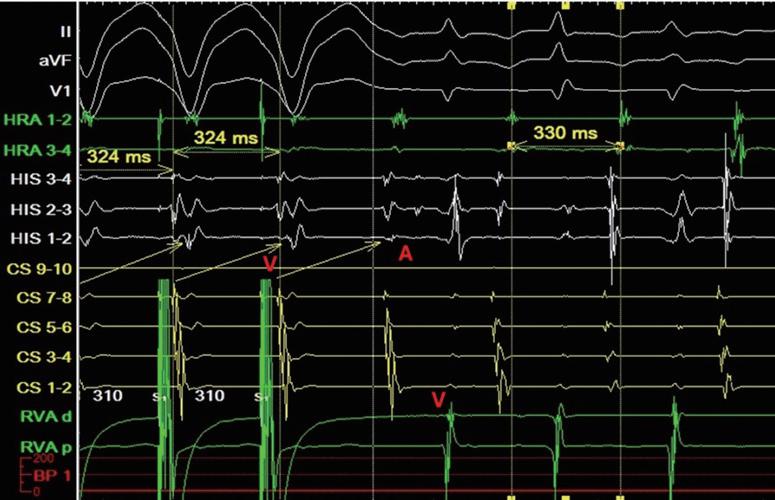
(圖四)、pseudo VAAV response。
Reference:
1. Schernthaner C, Danmayr F, Strohmer B. Coexistence of atrioventricular nodal reentrant tachycardia with other forms of arrhythmias. Med Princ Pract. 2014;23(6):543-50. (
5-Year
Results From the AMPLATZER Amulet Left
Atrial Appendage Occluder Randomized Controlled Trial (AMPLATZER Amulet
左心耳封堵器隨機對照試驗的 5 年追蹤結果)
臺北醫學大學附設醫院心臟內科 陳威達醫師
Amulet IDE trial 在2021年發表於Circulation,是截至目前為止規模最大的比較兩大左心耳封堵器(Amulet V.S. Watchman)的研究。研究團隊又於2023年,在JACC Cardiovascular Intervention上發表三年後的追蹤成果。在2024年 11月,最新的五年成果,又被發表於JACC。本文將此五年後的追蹤成果簡略報告。
Introduction
Amulet IDE trial 是一個跨國,多中心的前瞻性研究,比較 Amulet 以及 Watchman 2.5 對於心房顫動患者的預 防中風成效。相對於Watchman 2.5的單封堵系統(single seal system),Amulet是使用雙封堵系統(dual-seal technology) 來達成左心耳的封堵。
Method
這個研究的收案對象是18歲以上,具有陣發性,持續性,或永久性非瓣膜性的心房顫動患者。CHADS2必須兩 分以上,或是CHA2DS2-VAS三分以上。收案的患者以 1:1 的比例分配給 Amulet 以及 Watchman 2.5 這兩種封堵器。
在Amulet組,病人出院時使用的藥物是由研究者根據病人的狀況選擇dual antiplatelet或是Oral anticoagulation(OAC) 加上aspirin。但如果有超過5mm的血流jet進出左心耳,則必須要使用OAC。在Watchman 2.5組,所有病人出院時, 都是使用OAC加上aspirin。若在術後45天的經食道超音波(TEE)發現血流jet小於5mm,就會停止使用OAC。兩組病 人都會繼續服用dual antiplatelet直到術後六個月,然後就留下aspirin長期使用。
在baseline,手術中,術後45天,術後6個月以及12個月,病人都會接受TEE的檢查。如果病人有發生中風,也會 進行TEE檢查。TEE主要觀察的目標有兩個,一個是device-related thrombus (DRT),另一個是peridevice leak (PDL)。大 於3mm的PDL才會被本次研究納入分析。
本研究案的primary endpoint包含了(1) ischemic stroke,或是(2) systemic embolism之複合式終點。而secondary endpoint則是包含了(1) 中風(梗塞型或是出血型),(2) systemic embolism,或是(3) CV/unexplained death 之複合式終 點。其他的 endpoint 包含了 transient ischemic attack, major bleeding, all-cause death以及CV death。
Results
本研究案共有1878個病人接受隨機分配,扣處掉少數無法裝置封堵器病人後,共有917位病人接受Amulet封堵 器的置放。有916位病人接受Watchman 2.5封堵器的置放。一直到術後五年,Amulet組有89.2%的病人有完成追蹤分 析,而Watchman 2.5組則有83.3%的病人完成追蹤。這些收案病人的平均年齡大約75歲,男性約佔60%,大約55% 的患者是陣發性心房顫動,平均CHA2DS2-VAS為4.6分,平均HAS-BLED為3.3分。其中有27%的病人曾經發生過中 風,TIA或是thromboembolism。在病人的基本資料中,兩組並沒有顯著差異。
在使用OAC方面,因為Watchman 2.5的標準建議為術後前45天必須使用OAC,所以在出院時,Watchman 2.5組 僅 4.2% 病人停止使用 OAC 。相對的, Amulet 組有 78.9% 的病人在出院時,就已經停止使用 OAC 。在後續的每次追 蹤,Amulet組都有較高的比例停止使用OAC。一直到第五年,Amulet組有94%的病人沒有使用OAC,而Watchman 2.5組,則有90.9%的病人沒有使用OAC。(如圖一)
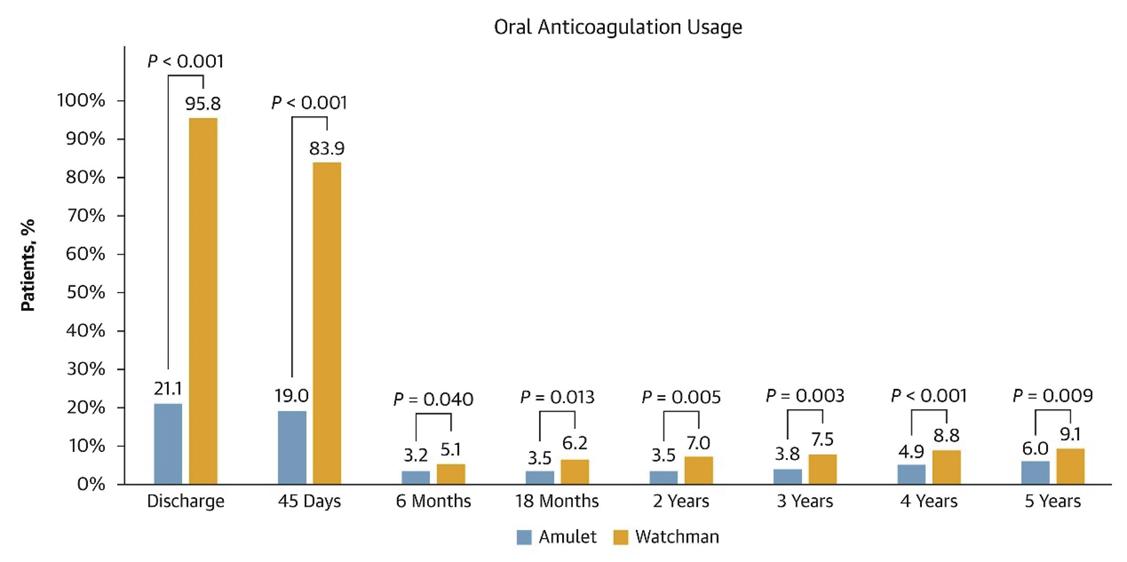
而本研究的primary endpoint,以及其他的臨床結果分析,兩組都沒有達到統計上的顯著差異。不論是缺血性 中風,systemic embolism的發生機率,所有原因的中風,CV相關的死亡率,出血率,以及all-cause death,兩組都 沒有統計上的差異(如圖二)。兩組的每年中風率皆為1.6%。 (圖一)
(圖二
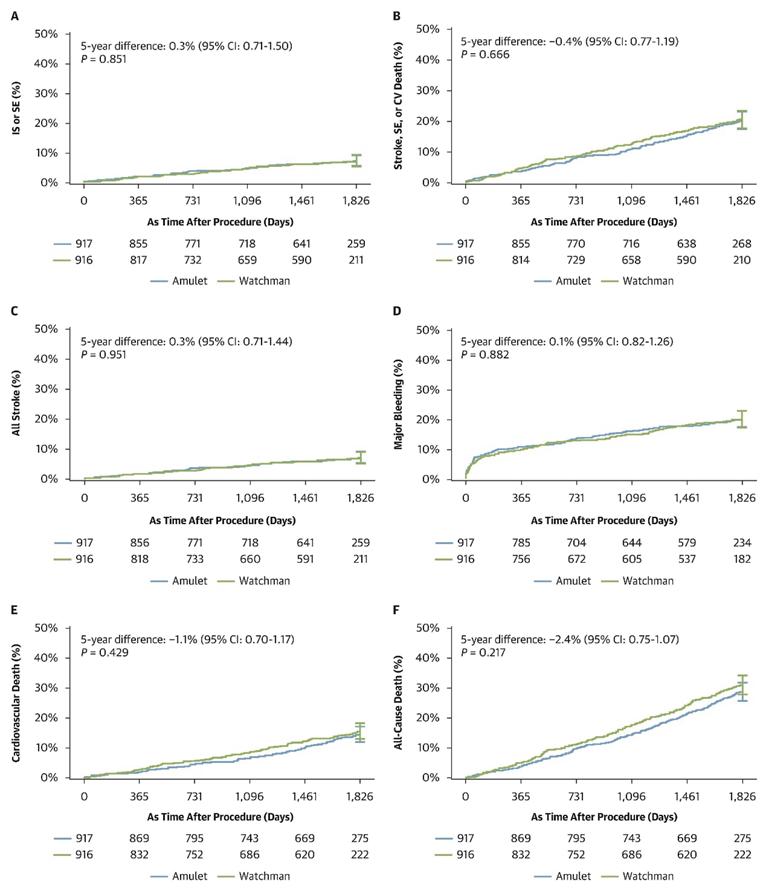

(圖二)
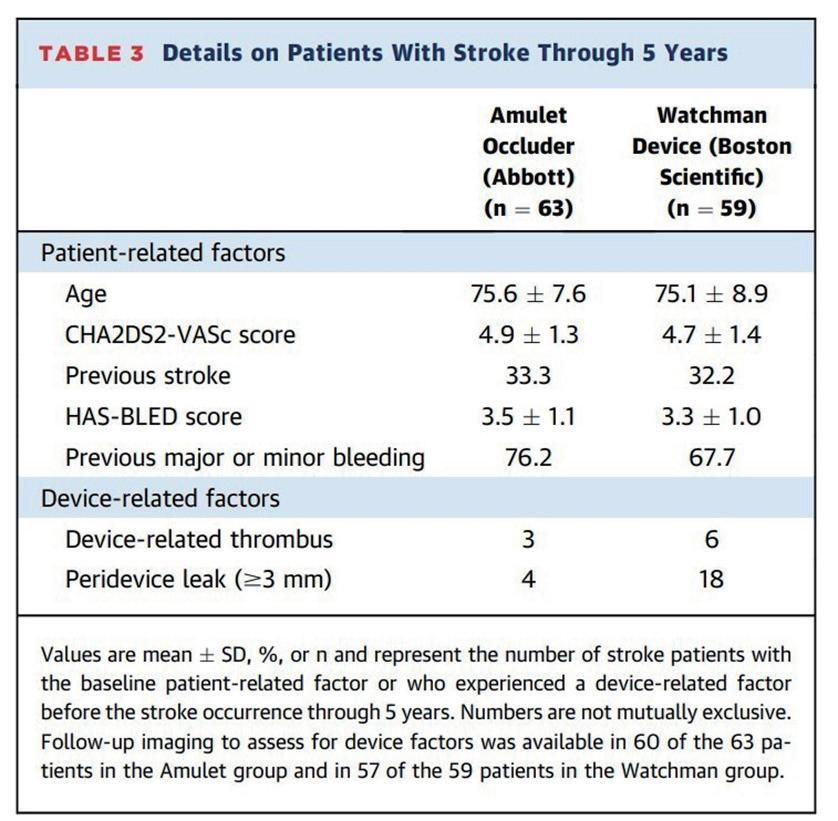
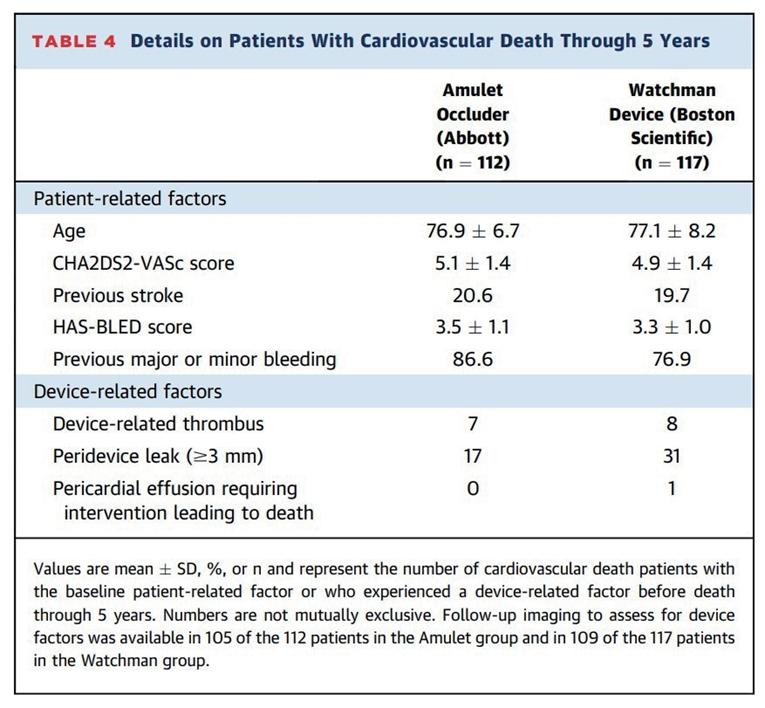
進一步分析, Amulet 組有 63 位病人發生中風,而 Watchman 2.5 組則有 59 位。在中風發生前, Amulet 組有 3 個 病人有DRT,另外有4個病人有PDL。而Watchman 2.5組,則有6位病人有DRT,有18位病人有PDL(如表一)。若討論 到CV相關的死亡病例,Amulet組有112病人死亡,而Watchman 2.5組有117位病人死亡。在死亡病例中,也有類似 中風的DRT以及PDL分布,Amulet組有7位病人有DRT,17位病人有PDL; 而Watchman 2.5組則有8位病人有DRT,有 31位病人有PDL (如表二)。 (表一) (表二)
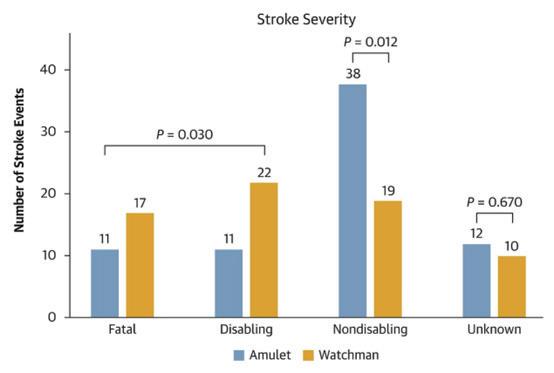
(圖三)
若將中風的嚴重度區分為fatal, disabling, non-disabling來分析,Amulet組有較高的比例的病人為non-disabling, 而 Watchman 2.5 組的病人中風嚴重度則比較高 ( 如圖三 ) 。在較為嚴重的中風病人族群中 (fatal + disabling) , Watchman 2.5組有48.7%的病人有DRT或是PDL;而在Amulet組,此比率則為18.2%。
Discussion
本研究有幾個主要的發現。 1. Amulet 組有較高的比率的病人可以停止使用 OAC ; 2. 兩種左心耳封堵器有類 似的臨床表現; 3. Amulet 組的中風病人嚴重度較低; 4 Watchman 2.5 組有較多的 DRT 以及 PDL 發生在中風或是心 因性死亡前。
Watchman 2.5的原廠建議在術後45天內繼續使用OAC,這使得Watchman 2.5組在出院時,僅有少數病人停止使 用 OAC 。這可以解釋本研究初期發現 Amulet 組有較高比率的病人停止使用 OAC 。然而, Amulet 組的病人停止使用 OAC 的比率,卻在後續每次的追蹤中,都比 Watchman 2.5 組來的高。這可能跟 Watchman 2.5 組有較多的 DRT 以及 PDL有關係。
Watchman 2.5 組有較多的 DRT 以及 PDL ,是否能解釋該組病人的中風嚴重度較高,仍然只是個假設。但若為 真,則DRT以及PDL不僅可能會增加thromboembolism的機會,也可能會影醒中風的嚴重度。
本研究案所使用的Watchman為2.5版本,但目前更新一代的Watchman FLX比Watchman 2.5有更低的DRT以及 PDL發生率。所以若以最新的Watchman FLX來與Amulet相比,研究結果也許會有改變,這仍需要後續的研究來提 供解答。
Conclusion
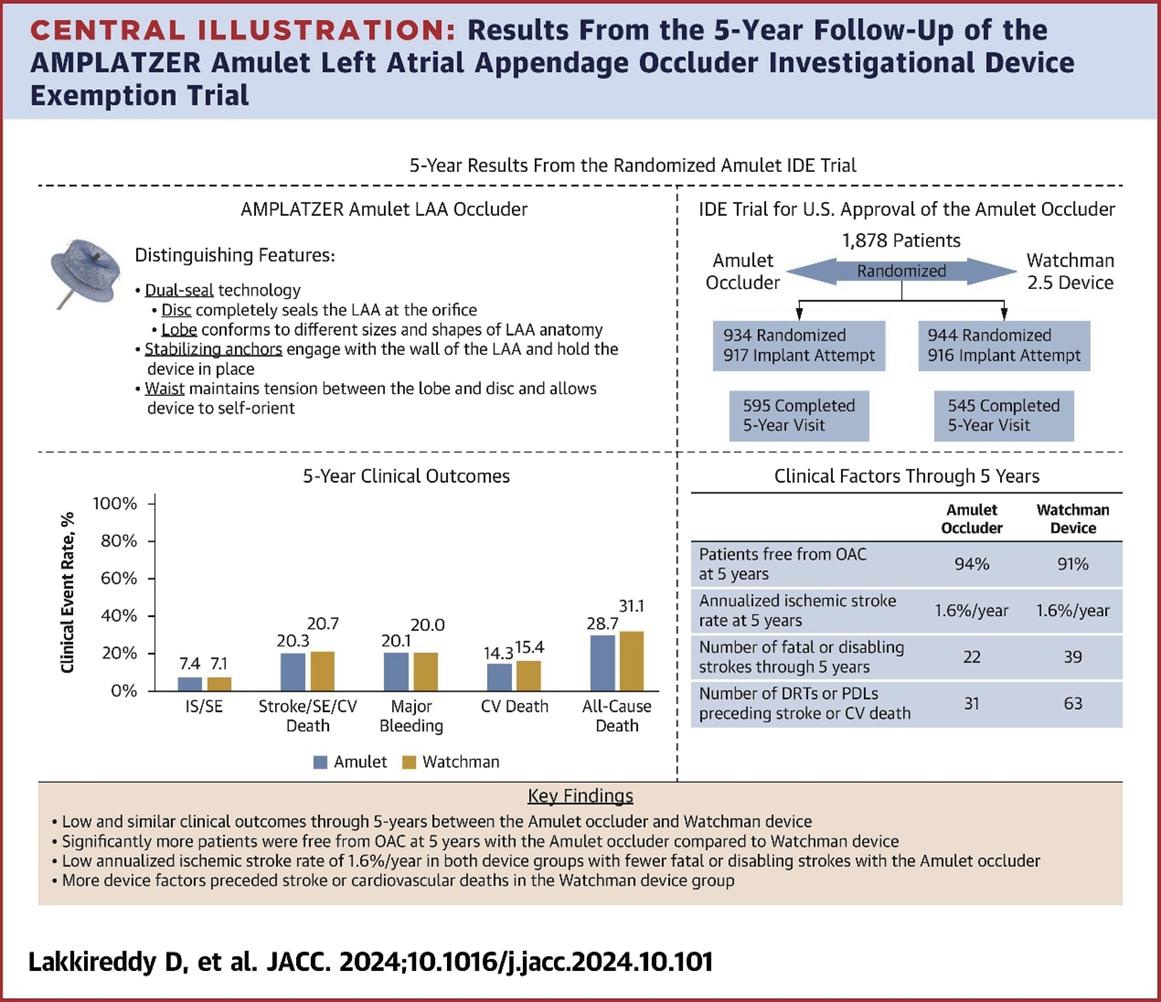
在這個最大的head-to-head比較LAAO的研究中,Amulet的安全性及有效性不亞於Watchman 2.5。而在LAAO的 封堵性方面Amulet則優於Watchman 2.5。(圖四)
Editorial Comment
最後,在本期的JACC中,Editor也特別撰文了一篇editorial comment探討此研究案。除了上述研究案中提到的 發現,此篇 editorial comment 特別指出,目前 Watchman 的最新版本已經是第三代的 Watchman FLX 。而 Watchman FLX 相較於本研究案中所使用的 Watchman 2.5 有較低的 DRT 以及 PDL 率。因此,若是將 Watchman FLX 與 Amulet 相比,研究也許會有不同的結果。
此外不論是Amulet或是Watchman 2.5,都在將術後用藥降接到single antiplatelet之後,有明顯的出血風險下降。 因此,在 LAAO 置放後,盡早將抗凝血以及抗血小板藥物降階至 single antiplatelet ,或許能使 LAAO 的臨床好處 更大,然而這也需要更多的研究來提供數據支持。這個議題近期有一個研究案正在進行中,叫做SIMPLAAFY trial (Watchman FLX Pro Left Atrial Appendage Closure Device With Alternative Post-Implant Monotherapy; NCT06521463)。 Editor建議大家可以密切追蹤這個Trial的結果,可以當作未來LAAO術後用藥的參考指引。
Reference:
1. 5-Year Results From the AMPLATZER Amulet Left Atrial Appendage Occluder Randomized Controlled Trial / JACC. Nov 18, 2024. Epublished.
2. Amulet LAAO 5-Year Outcomes: Best in Class or Class Effect? / JACC. Dec 04, 2024. Epublished. (圖四)
Left Ventricular Summit Arrhythmias
衛生福利部雙和醫院心臟內科 陳俊兆醫師
一、前言
左心室頂點(Left Ventricular Summit, 以下簡稱LVS) 位於左心室基底部與流出道最上緣,在心臟立體構造 中被視為「左心室外膜面」最頂端的區域。近年來臨 床上常見到部分「特發性心室心律不整」 (idiopathic ventricular arrhythmia),尤其是非持續性室性心律不整 (PVC, VT 等 ) ,起源於此處。由於 LVS 區域解剖極其複 雜,緊鄰冠狀動脈主幹及其重要分支,再加上該處通 常存在較厚的脂肪組織,使得臨床電生理醫師在進行 導管消融時,往往面臨定位與安全性的雙重難題。本 文將詳加介紹LVS在解剖層面上的重要性、致心律不整 的機制、臨床上如何透過各種導管或特殊技術完成標 測與消融,並進一步探討新技術與未來趨勢。
二、解剖與定位
1. 位置與定義
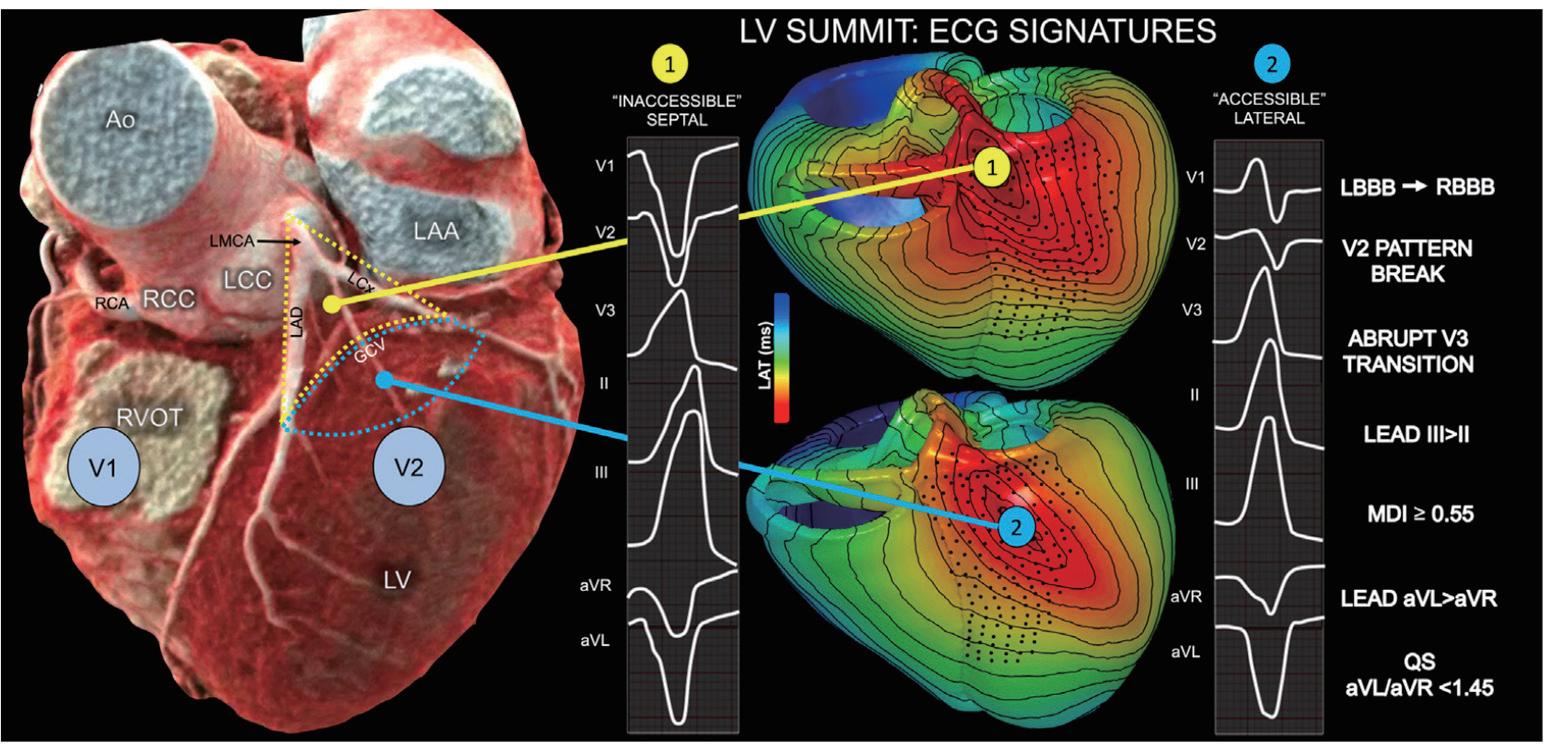
LVS 大致可想像為一個位在左心室流出道最上方的 「三角區域」。此三角常以「左前降支 (LAD) 」與 「左迴旋支(LCx)」的走向作為邊界,向上可延伸到 左冠狀動脈主幹(LMCA)分岔處,其底部則鄰近左心 室基底部與隔膜相接的位置。該區在外膜面可分為 「可及區域」與「不可及區域」:
- 可及區域(Accessible Region):通常位於比較偏下 方且遠離主要冠狀動脈幹與分支的部位,導管在 此能相對安全地接近與施以射頻燒灼。
- 不可及區域 (Inaccessible Region) :多位於更靠近
LAD 與 LCx 以及左冠主幹分岔處的上方,該處常 有厚實脂肪組織與冠脈走行,若要由心外膜面施 以燒灼,則易發生冠狀動脈灼傷或無法達成足夠 能量傳導。
2. 與冠狀動脈/靜脈系統的關係
LVS 周邊佈滿豐富且互相交錯的冠狀血管分支:除 LAD 、 LCx 外,尚可能有斜枝、對角支以及鈍緣支 等。靜脈系統方面,主要由大心靜脈 (Great Cardiac Vein, GCV)及前降靜脈(AIV)分支等交織在此,甚至 可見到通向隔壁穿通靜脈 (septal perforators) 與心前 靜脈。多條血管在此交錯使得導管走向不易,且若 射頻能量靠近主要血管,則可能引發心肌梗塞或冠 脈痙攣等風險。
3. 與鄰近結構的空間分布
LVS緊鄰主動脈根部、肺動脈幹以及左心耳(LAA)。 因此,臨床有時會利用比鄰處如主動脈竇 (aortic cusps)、肺動脈瓣下方或左心耳內側等「反向路徑」 進入或施行燒灼,期待能從不同方位達成足夠能量 傳遞,克服傳統左心室外膜燒不透的限制。
三、心律不整機制與臨床意義
1. 自動性與觸發性
許多 LVS 起源的心律不整屬於「特發性室性期前收 縮 (PVC) 」或「非維持性室性心博 (NSVT) 」;其機 制常被歸因於 automaticity 的提高或延遲後去極化 (delayed afterdepolarization)形成的觸發活動。也有研 究指出,某些LVS ventricular arrythmia 對adenosine 的反應,暗示trigger activity 的機轉。
2. 結構性心臟病的角色
在缺血性心臟病或擴大性心肌病變等患者中,LVS區 域亦可能成為瘢痕基質延伸的重要一環,導致折返性 室頻(re-entrant VT)發生。此時,傳統的消融路徑若無 法有效滲透至瘢痕深處,亦會提升手術難度。
四、十二導程心電圖特徵
1. 正後軸與負向I導程
由於LVS位於左心室基底部外側,心電圖常呈現軸向 朝下,II與III導程多為R波主導;與此同時,I導程較 負向,且aVL多為負波,aVR則相對不那麼負。
2. 左束支型態或右束支型態
根據起源點偏左或偏右, V1 導程可呈現 RBBB 或 LBBB 樣貌。若 LVS 偏右側 ( 靠近 Inaccessible region/ septal site)起源,較常見LBBB圖形;反之,偏左側( 靠近accessible region/lateral site)起源時,則可呈現 RBBB 且早期便出現全胸導程 R 波 (positive concordance) ,且 V3 處容易有「突轉」 (abrupt transition)或「V2 pattern break」。
3. 其他典型指標
因屬於心外膜起源,常可見 pseudo- δ wave(>30-35
ms)、較長RS時間、intrinsicoid deflection延後,以及較大的最大波幅比(maximum deflection index)。這些徵象也常 被應用於預測消融是否需要走心外膜路徑。
五、標測策略
1. 傳統激動順序(activation mapping)
最早期的標測方式是尋找最早的雙極電位峰值與單極 QS 波形,然而 LVS 常同時影響左右心室流出道附近 且存在潛在「深層或中層起源」,使得僅從單一腔室 標測時難以完全掌握真正的起源點。因此,臨床上需 同時評估右心室流出道 (RVOT) 、左心室流出道 (LVOT)與相鄰結構(如冠狀竇、主動脈竇)之電位。
2. 冠狀靜脈系統(Coronary Venous System)標測
若懷疑病灶在心外膜或近中層區域,醫師可於GCV ( 大心靜脈)或AIV(前降靜脈)放置特製小口徑導管,以 更貼近外膜區域觀察電位是否比內膜側更早。若必 要,還可嘗試沿著AIV的穿通靜脈(septal perforator) 以導絲探測,判斷是否為中層(intramural)焦點。
3. 動脈內導絲(Intracoronary Guidewire)標測 更進階的作法,是將經皮冠狀動脈介入術用的細徑 導絲,直接置於左前降支或其分支內,並將導絲接 上電生理系統,進行單極訊號標測或嘗試冷鹽水灌 注試驗、酒精注射等。如此若找到病灶「最早」激 動點或證實酒精注射能立即壓制心律不整,即可反 推最可能的起源深度。然而,此法侵入性高且可能 有血管損傷、痙攣、血栓等風險,必須謹慎評估。
六、消融策略與技術
1. 內膜端與流出道(outflow tract)消融
由於 LVS 常存在「多出口路徑」,並非對準表面最 早激動點就能成功。因此常見做法是「多方標測、 多點嘗試」:包含左心室流出道端、主動脈冠狀竇 ( 特別是左冠竇 LCC 與左 - 右交界 ) 、非冠竇 NCC 與其 下方的膜部室間隔以及右心室流出道高位等處。當 發現電位最早區在內膜就能夠消融到則屬理想,但 若較深層則需進一步策略。
2. 心外膜與冠狀靜脈消融
若確定屬心外膜焦點且位於可及區域,經心包膜下燒 灼可直接處理;但若血管與脂肪阻擋,射頻能量易無 法穿透。另一選擇是在冠狀靜脈分支內以導管施行「 靜脈內消融」,然而必須嚴格監測消融點與主要冠脈 的距離,避免灼傷。此法對於LVS下方較無法從內膜 端接近之病灶,可能提供關鍵性的輔助效果。
3. 高能量消融或新興技術
由於 LVS
常具中層或深層起源,單純射頻若能量深 度不足,易復發。臨床正逐漸應用更高功率、長時 間應用 (high-power, prolonged-duration) 或半能量注 入法,試圖增加消融深度。亦有研究使用冷鹽水灌 注、半導體雷射、超音波消融等先進技術,以期待 能安全又更有效地達到足夠滲透深度。此外,脈衝 場消融(pulsed field ablation)因對心肌外細胞膜有選 擇性破壞效果,且對血管及周邊組織相對安全,也 成為未來相當受到期待的方案。
七、特定狀況與新發展
1. 介入性映射與血管導絲
近年已有數項報告利用冠狀動脈導絲或穿通靜脈導 絲,直接在血管腔內觀察最早激動時間,甚至可以 進行通電測試、酒精注射,若能中斷異常電活動, 即可確立區域性焦點。此法雖具有潛在血管傷害風 險,但對於棘手且傳統方法皆無法奏效的病例,可 能提供成功機會。
2. 脈衝場消融(Pulsed Field Ablation, PFA)
脈衝場消融(Pulsed Field Ablation, PFA)是一種新興的 消融技術,透過電穿孔 (electroporation) 原理作用於 目標心肌細胞,使細胞膜瞬間形成孔洞、喪失細胞 功能,因而達到消融目的。此技術最初應用於房顫 消融,近期逐漸開始用於更具挑戰性的室性心律不 整,尤其對於Left Ventricular Summit等複雜解剖區 域的病灶具有潛在優勢。
相較於傳統射頻(RF)或冷凍消融,PFA最突出的優 點是其具有高度的組織選擇性(tissue selectivity),在理 論上可以保護周圍的血管、神經、食道和氣管等結 構,從而降低併發症發生機率。然而,針對靠近冠狀 動脈的LVS區域消融,仍有研究指出可能引起短暫的冠 脈痙攣,這表示PFA的組織選擇性雖佳,但對冠狀動脈 的影響仍需謹慎評估,術前術中必須密切監測。
病灶深度方面,PFA最大的優勢在於能夠達到較深 的穿透效果。文獻指出,利用不同的消融導管配置 ( 如 單極和雙極導管模式 ) , PFA 可達到超過傳統射頻消融 能量的心肌破壞深度。在動物模型研究中發現,單極 PFA 模式可有效達到約 5-7 毫米深的心肌損傷,而雙極 模式更可將破壞深度延伸至約 10 毫米甚至更深,遠超 過傳統射頻消融 ( 通常約 3-5 毫米左右 ) 。這種深層的穿 透能力,對於位於LVS深層、傳統射頻或冷凍能量難以 有效穿透的中層(intramural)病灶具有特別的潛力,可望 大幅提升此類病灶的長期消融成功率。
儘管如此,現階段的PFA導管與電極設計尚處於早 期階段,距離實際臨床常規應用於深部LVS病灶仍存在 挑戰。例如,如何避免過多的能量傳遞導致鄰近冠脈受 損,引發房室結阻斷(AV block)、心室顫動(ventricular fibrillation)、心外膜出血(epicardium hemorrhage)。如何 精確控制能量輸送的範圍與深度,以及如何確保臨床應 用的穩定性與安全性等,都是需要未來更多臨床研究與 科技發展才能逐步克服的問題。
3. 數位導航與整合成像
隨著三維電解剖標測系統 ( 如 Carto 、 EnSite) 與心臟 CT/MRI的整合,術者可於術前先行建模,了解冠脈 及周邊結構,並在術中即時參考。 ICE( 腔內超音波 ) 更可即時掃描左冠主幹與其分支,確認消融位置與 血管距離,在安全範圍內精準施作。
八、臨床成效與預後
1. 短期成功與復發
LVS 心律不整的導管消融短期成功率在不同文獻中 約為 70%-90% 不等。然而,由於部位深層或多路出 口特性,一次操作的根治率仍有限,不少患者在數 個月或一年內復發。若進行複雜標測並多路徑消 融,一旦觸及關鍵病灶,成功機率將大幅提升。
2. 長期監測與併發症
在可及區域使用安全劑量射頻能量,多數併發症可 控,尤其在精準標測配合冠脈影像評估後,主要風 險如冠脈損傷、心包填塞等相對少見。對深層或中 層病灶,若反覆消融仍無法阻斷,則必須考慮外科 顯露、酒精注射或其他創新方法。
3. 新技術展望
隨著 PFA 等選擇性組織消融模式興起,人們期待未 來能降低對冠脈及周邊結構的潛在傷害,提高對心 肌病灶滲透度;未來亦可能有更微創且高精度的心 外膜輔助裝置或能量源,進一步改善 LVS 區域消融 的挑戰。
九、結論
左心室頂點 (LVS) 心律不整因其特殊且複雜的解剖 位置,成為臨床電生理學上相當具挑戰性的一環。從內 膜到外膜、從冠狀動脈到靜脈系統,皆需綜合性標測與 多重角度燒灼策略,才能獲得理想成效。隨著高階三維 導航、腔內超音波、血管內導絲標測、高能量延時消融 以及脈衝場消融等新技術的發展,我們有機會在安全與 有效性方面取得更佳平衡。雖然目前仍無法一勞永逸地 解決LVS區域的所有消融難題,但臨床與研究領域正持 續積累經驗與證據,未來勢必能讓這塊「高難度地帶」 的心律不整治療更加精準、可靠與成熟。
Reference:
1. Left Ventricular Summit Arrhythmias: State-of-the-Art Review of Anatomy, Mapping, and Ablation Strategies. J Am Coll Cardiol EP. 2024 Nov, 10 (11) 2516–2539.