Arrhythmia News
發行人: 溫明賢 (Ming-Shien Wen)
發行單位: 中華民國心律醫學會 (Taiwan Heart Rhyrhm Society)
地址: 10041台北市中正區忠孝西路一段50號25樓之18
本期摘要
P1. P4. P6. P10. P12. P14.
因性猝死
電話: 886-2-23821530 傳眞: 886-2-23821528 網址: www.thrs.org.tw ISSN: 2223-0130
總編輯 林文裕 Wen-Yu Lin 劉言彬 Yen-Bin Liu 本期主編 陳建鈞 Jien-Jiun Chen 黃鼎鈞 Ting-Chun Huang 編輯
張耀庭 Yao-Ting Chang 顏琨麒 Kun-Chi Yen 劉至民 Chih-Min Liu 莊再庚 Chye-Gen Chin 林柏霖 Po-Lin Lin 廖敏村 Min-Tsun Liao
SEP. 2022 NO.047
How to Achieve Near Zero Fluoroscopy During Cardiac Implantable Electronic Device Implantation 輻射防護技術來減少電燒期間輻射暴露並增加輻射工作人 員的工作壽命 ECG of the Month Role of Stereotactic Radioablation for Refractory Ventricular Arrhythmia Implantable loop recorder (ILR) 在心房顫動 (AF) 及心
(SCD) 病患上臨床的應用 脈動新聞 How to Achieve Near Zero Fluoroscopy During Cardiac Implantable Electronic Device Implantation 近 30 年來,介入性心臟電生理學的領域蓬勃地 發展。傳統上,無論是心律不整的燒灼或是心臟植 入性電子儀器( cardiac implantable electronic devices, CIEDs)的置放,都需要在心導管室內,藉由螢光檢 查(fluoroscopy, X 光透視法)在螢光屏上連續顯示 X 光圖像,判斷導管、導線以及電子儀器放置的位置, 才能順利完成。此技術行之有年,然而螢光檢查只能 提供 2D 平面影像,即使輔助以不同的透視角度,有 時對於導線的空間位置判斷仍會有困難;此外,螢光 檢查以 X 光進行,對於病人本身與心導管室的醫護團 隊,都會增加輻射暴射相關的風險。 輻射暴露對於兒童或是孕婦患者,格外地重要, 目前沒有研究能明確地劃分出輻射暴露的安全劑量範 圍。因此,心導管技術中螢光檢查的使用原則是: 「合理範圍內,以最低劑量執行(as low as reasonably achievable, ALARA) 」為目標。研究顯示,輻射暴露 對於執行的醫護團隊會增加癌症以及白內障發生的風 險 (1,2),長時間穿著鉛衣等護具,也會增加骨骼相關的 職業傷害,包含脊椎或是下肢骨骼的問題 (3)。近年來, 科技的進步,發展出了相當多可以應用於減少輻射暴 露的工具,新近的發展包含心臟內超音波(intracardiac echocardiography , ICE)、心血管核磁共振(cardiac magnetic resonance image)以及 3D 電生理解剖定位系 統(3D electroanatomic mapping system, EAM, 簡稱 3D 定位系統),都被使用於合理地減少介入性心臟電生 理學介入治療中輻射的暴露 (4)。在心律不整導管燒灼 治療的領域,無輻射導管的技術發展較早也較完善, 大部分種類的心律不整,都已在文獻中有完整的無輻 射治療施作步驟與安全效益等資料 (5-7)。然而 CIED 的 置放,在降低輻射部分,尚有待克服的困難,相關技 術與步驟也尚未標準化。 目前國內廣為使用的 3D 定位系統,包含 CARTO 國立臺灣大學醫學院附設醫院 許嘉晏醫師/ 曾偉杰醫師
(Biosense Webster, Irvine, CA) 、 EnSite (Abbott Labs, Abbott Park, IL) 以及 Rhythmia (Boston Scientific, Cambridge, MA),其中前兩者於無輻射 CIED 置放的 技術報告中,較常被使用。CARTO 系統藉由三個不同 頻率的低強度磁場發射線圈產生訊號,利用特殊導管 尖端上的接受器,計算導管在不同位置所得到的不同 訊號,進一步推得導管的位置,定出心臟的結構,進 而繪製出心臟的 3D 立體圖型。EnSite 系統則藉由三個 相互垂直的電極組,於病人胸腔產生低電流,並計算 不同位置的電阻進行定位與心臟圖型的繪製。EnSite 的優勢是可以使用任何具電極的導管或導線執行,不 需使用特定導管,目前 EnSite 也有以外加磁場增加定 位精確度的功能 (4,8,9)。
心臟植入性電子儀器為許多心律不整的治療選 項,包含節律器(pacemaker)、植入式心內去顫器 (implantable cardioverter defibrillator, ICD )以及心 臟再同步治療裝置( cardiac resynchronization therapy device, CRT)。3D 定位系統,在放置心臟植入性電子 儀器的過程,可以看到導管或導線在心臟內的 3D 空 間位置,但此技術仍屬發展階段,還沒有標準化的指 引步驟,對於過程中何時需用螢光檢查、心臟內超音 波或其他儀器輔助,也依照各醫療團隊的習慣、置入 的儀器以及病人狀況而異 (10-13)。
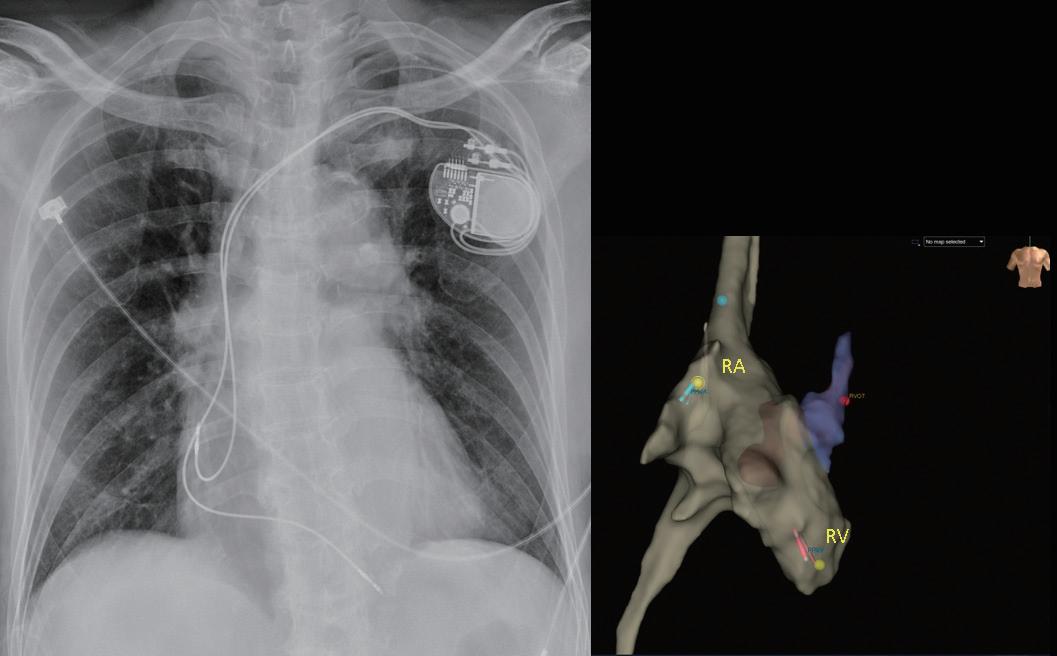
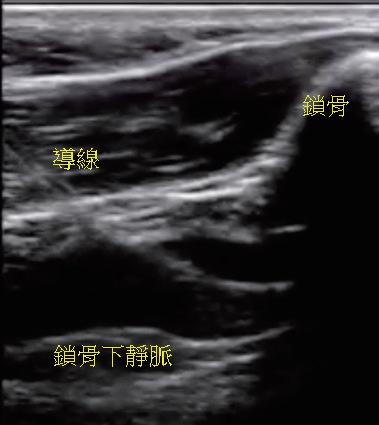
臺大兒童醫院兒童心臟科在吳美環教授與邱舜南 教授的率領下,於 2016 年底開始進行無輻射心律不 整燒灼,並於 2018 年開始發展 EnSite Precision 心臟 定位系統輔助進行無輻射心臟植入性電子儀器放置。 病患在以 propofol 鎮靜和 lidocaine 局部麻醉後,藉由 無菌的超音波即時導引技術,穿刺左鎖骨下靜脈或左 腋靜脈並留置導線(圖一),接著先於鎖骨下區域手
Greco et. al. 於 2017 年發表一篇義大利多中心的研究, 比較 125 位 3D 定位系統導引無輻射心臟再同步治療 裝置與 250 位傳統螢光檢查導引放置,兩者間的成效。 他們使用 EnSite 系統建立靜脈與右心和冠狀靜脈竇的 3D 構造,在 3D 定位系統的引導下,先將右心室導極 置入預期位置,再將另一導管置入 CS 並建立 CS 分枝 的 3D 影像,這個步驟是否使用血管攝影輔助,由執 行醫師當場決定,完成後將左心室導線(LV lead)藉 由 3D 定位系統影像送至目標血管位置,最後才放置 右心房導線。該研究中,有五家醫學中心執行無輻射 心臟再同步治療裝置置放大於十次(共 105 次),其 餘六家醫學中心則皆執行小於十次(總共
中華民國心律醫學會‧ Taiwan Heart Rhythm Soclety ‧中華民國 111 年 9 月出刊
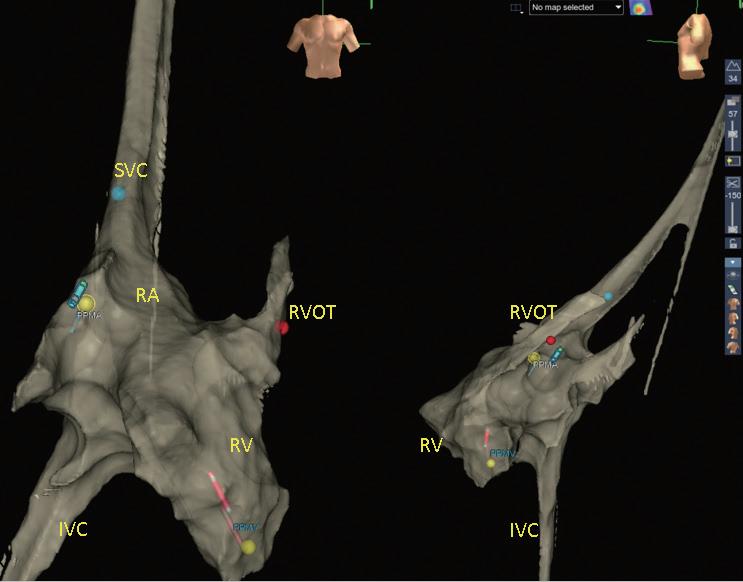
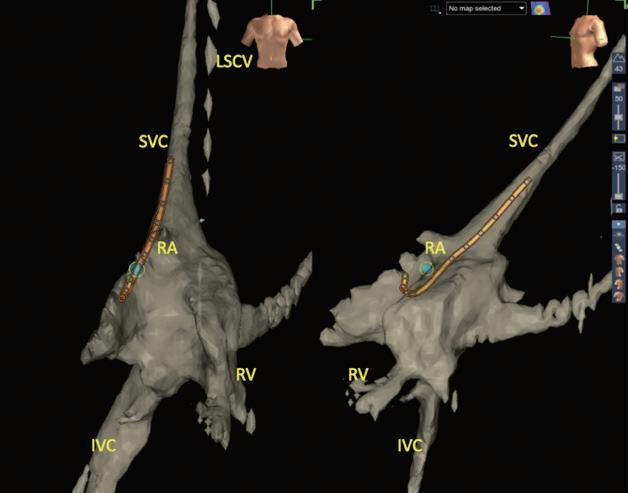
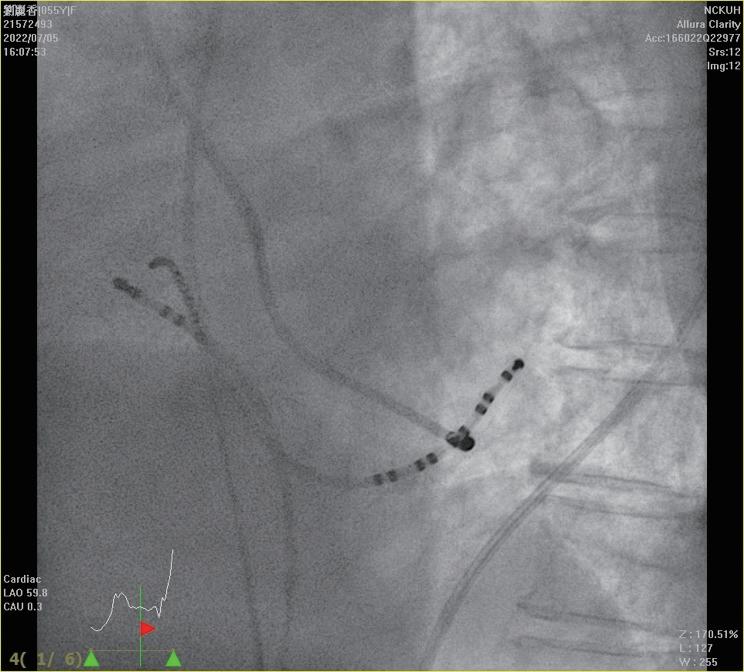
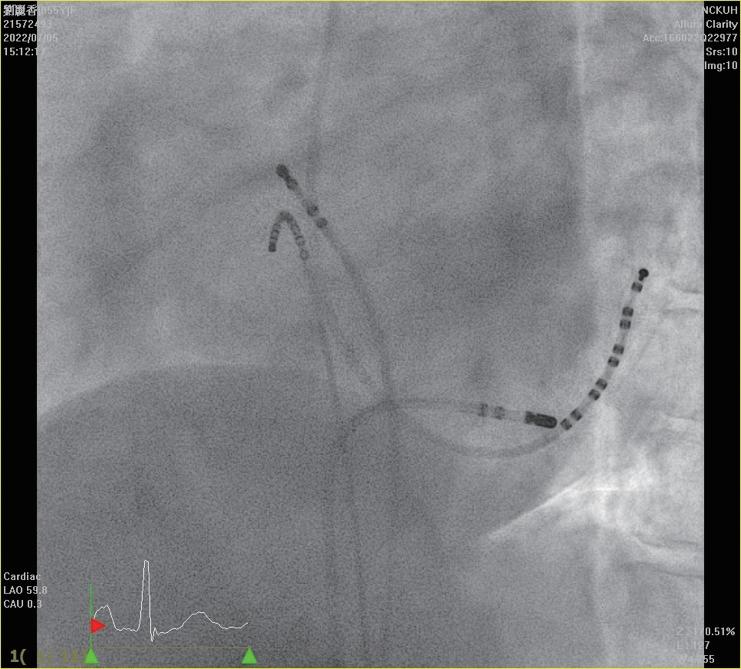
術製造皮下口袋(subcutaneous pocket)後,再以導線 經 Seldinger technique 建立靜脈的通道。接著,藉由 EnSite Precision 心臟定位系統,使用可控式 10 極導管 ( InquiryTM, steerable diagnostic catheter, SJM ), 自左鎖骨下靜脈、頭肱靜脈 , 上、下腔靜脈、右心房 以及右心室等立體結構,進行心血管系統之 3D 繪製 (圖二)。繪製時,會特別著重右心耳、右心尖與右 心室出口的結構與位置,以利後續置放進行。接著, 將心臟植入性電子儀器的導線連結於 EnSite 系統並成 像,在 3D 定位系統導引下,由先前繪製的構造中, 將導線尖端置於目標處(圖三),並進行相關參數測 試。選定適當位置進行導線固定時,由於目前系統無 法將主動固定的螺旋( screw)成像,因此無法確認螺 旋是否確實伸展。我們團隊於此步驟會藉由螢光檢查 檢視螺旋伸展的狀況、評估放置位置是否與預期相符 以及導線鬆弛程度( lead slack)是否適當。調整後, 完成心臟植入性電子儀器放置時,亦會再藉由螢光檢 查確認位置(圖四)。目前臺大單一中心經驗,藉由 3D 定位系統於 13 個病人中放置過 14 個儀器(3 個單 腔節律器、6 個雙腔節律器、4 個植入式心內去顫器及 1 例心臟再同步治療裝置),平均輻射暴露時間約為 0.6 分鐘,相較於傳統方式(平均輻射暴露時間為 10.3 分 鐘)明顯少許多。目前無觀察到相關術後併發症,且 各儀器的追蹤參數與傳統置入的儀器無差別。 相較於置放節律器與植入式心內去顫器,心臟再 同步治療裝置的更為複雜,因為需將導線置於冠狀 靜脈竇(coronary sinus, CS),可能需要藉由顯影劑 讓 CS 顯像,且所需的輻射暴露時間常為前兩者的數 倍 (14),病人與執行醫師的輻射暴露也最強,過去甚至 有研究建議一位醫師單月放置心臟再同步治療裝置數 目勿超過四個,以控制在較安全的輻射曝露量 (15)。
20 次)。相 比之下輻射暴露時間與 CS 血管攝影比率,於經驗較 少的醫學中心皆較高,但整體執行所需時間與成功率 並無顯著差異。綜合十一家醫學中心的結果,無輻射 心臟再同步治療裝置的技巧,可使輻射暴露時間降低 75%(中位數 3 分鐘 vs 11 分鐘 , p<0.001),血管攝影 比率也減少了 70%(21% vs 55%, p<0.001),且成功 率和併發症與傳統技術相比並無差異 (12)。 Patel et. al. 於 2019 年發表較小型的研究,由同一 位資深醫師執行 19 個無輻射導引與 19 個傳統方式放 置 CIED,其中以因為心肌病變導致左心室射出分率 小於 35% 而放置單腔心內去顫器為大宗(無輻射中佔 88%,傳統螢光檢查佔 73%),其餘為雙腔節律器。 兩組住院時間相仿( 1.2 天 vs 1.47 天 , p = 0.1)皆為 手術當天或是隔天出院。執行過程則是無輻射導引組 較長(49 min vs 25 min, p<0.001),但隨著無輻射導 引的執行次數增加,所需時間漸減,逐漸接近傳統組 別。平均輻射暴露時間則是無輻射導引組較低(4.5 秒 2 NO.047
Reference:
1. Venneri L, Rossi F, Botto N et al. Cancer risk from professional exposure in staff working in cardiac catheterization laboratory: insights from the National Research Council's Biological Effects of Ionizing Radiation VII Report. Am Heart J 2009;157:118-24.
2. Stahl CM, Meisinger QC, Andre MP, Kinney TB, Newton IG. Radiation Risk to the Fluoroscopy Operator
and Staff. AJR Am J Roentgenol 2016;207:737-744.
3. Goldstein JA, Balter S, Cowley M, Hodgson J, Klein LW, Interventional Committee of the Society of Cardiovascular I. Occupational hazards of interventional cardiologists: prevalence of orthopedic health problems in contemporary practice. Catheter Cardiovasc Interv 2004;63:407-11.
中華民國心律醫學會‧ Taiwan Heart Rhythm Soclety ‧中華民國 111 年 9 月出刊 ( 圖三 ) ( 圖ㄧ ) ( 圖二 ) ( 圖四 ) vs 101.4 秒 , p<0.001),16 位無輻射導引組執行過 程 的輻射暴露時間 < 1 秒,使用於螺旋旋入後之確認影 像,兩組病人於手術當下、一週與 4 到 6 週的追蹤皆 無併發症,並且於追蹤導線電阻(impedance)、相關 閾值(包括 capture voltage, capture time)等皆無差別, 可謂兩組放置成效相仿 (16)。對於使用無輻射導引置放 CIED 的過程,何時要使用螢光檢查確認,依不同醫學 中心的習慣而異。有個案報告於懷孕婦女中,在術中 以心臟內超音波評估導線鬆弛程度(lead slack);或 以更換不同曲度的探針( stylet)而導線尖端位置維持 不變,做為螺旋順利旋入的間接證據,來達成完全零 輻射暴露的 CIED 置放。然而大部分的中心,仍常規 於螺旋固定後,以螢光檢查影像進行相關確認 (10,11,16)。 當面臨血管解剖構造有變異、導管產生糾結或是冠狀 靜脈竇無法完整繪製的狀況,螢光檢查仍佔重要的輔 助角色 (11)。 3D 定位系統於介入性心臟電生理學的領域,未來將 佔據更重要的角色,對於構造複雜的先天性心臟病患者, 因其血管走向常不典型,過往治療可能造成多處心肌纖 維化或高度累積輻射暴露,以無輻射導引方式進行介入 性心臟電生理治療與儀器置放,有其優勢與必要性 (17)。 現階段因為各國技術上仍未標準化,此技術尚未普及, 也缺乏大型研究分析其成效與安全性,針對長期預後以 及是否符合成本效益,還有賴未來研究證實。不過在執 行數量增加後,執行時間預期可以降低且可大幅度降低 輻射暴露,相信在不久的未來,能為病患與醫療團隊, 建構更安全、有效率的醫療環境。
3NO.047
4. Purtell CS, Kipp RT, Eckhardt LL. Into a Fluoroless Future: an Appraisal of Fluoroscopy-Free Techniques in Clinical Cardiac Electrophysiology. Curr Cardiol Rep 2021;23:28.
5. Tseng WC, Wu MH, Lu CW et al. Zero Fluoroscopy During Ablation of Right-Sided Supraventricular Tachycardia Substrates in a Pediatric PopulationInitial Experience in Taiwan. Acta Cardiologica Sinica 2019;35:476-483.
6. Tseng WC, Wu MH, Lu CW et al. Zero-fluoroscopy ablation of left-sided arrhythmia substrates in children - Mid-term safety and feasibility study from transaortic approach. J Formos Med Assoc 2022.
7. Yang L, Sun G, Chen X et al. Meta-Analysis of Zero or Near-Zero Fluoroscopy Use During Ablation of Cardiac Arrhythmias. Am J Cardiol 2016;118:15111518.
8. Del Greco M, Marini M, Bonmassari R. Implantation of a biventricular implantable cardioverter-defibrillator guided by an electroanatomic mapping system. Europace 2012;14:107-11.
9. DeSena HC, Landis BJ, Moore RA, Spar DS, Whiteside W, Blaxall BC. Future Diagnostic Strategies Pediatric. Cardioskeletal Myopathies in Children and Young Adults, 2017:361-379.
10.Silver ES, Nash MC, Liberman L. Implantation of permanent pacemaker and ICD leads in children using a three-dimensional electroanatomic mapping system as an aid to fluoroscopy. Pacing Clin Electrophysiol 2015;38:448-54.
11.Colella A, Giaccardi M, Colella T, Modesti PA. Zero x-ray cardiac resynchronization therapy device
implantation guided by a nonfluoroscopic mapping system: A pilot study. Heart Rhythm 2016;13:1481-8.
12.Del Greco M, Maines M, Marini M et al. ThreeDimensional Electroanatomic Mapping SystemEnhanced Cardiac Resynchronization Therapy Device Implantation: Results From a Multicenter Registry. J Cardiovasc Electrophysiol 2017;28:85-93.
13.Gianni C, Della Rocca DG, Natale A, Horton RP. Fluoroless 3D mapping-guided pacemaker implant in a pregnant patient. Pacing Clin Electrophysiol 2021;44:1641-1645.
14.Picano E, Vano E, Rehani MM et al. The appropriate and justified use of medical radiation in cardiovascular imaging: a position document of the ESC Associations of Cardiovascular Imaging, Percutaneous Cardiovascular Interventions and Electrophysiology. Eur Heart J 2014;35:665-72.
15.Butter C, Schau T, Meyhoefer J, Neumann K, Minden HH, Engelhardt J. Radiation exposure of patient and physician during implantation and upgrade of cardiac resynchronization devices. Pacing Clin Electrophysiol 2010;33:1003-12.
16.Patel H, Hiner E, Naqvi A, Wrobel J, Machado C. The safety and efficacy of electroanatomical mapping (EAM)-guided device implantation. Pacing Clin Electrophysiol 2019;42:897-903.
17.Paech C, Schnappauf D, Gehre T, Wagner F, Gebauer RA. Use of the Abbott EnSite Precision threedimensional mapping system for the placement of an atrial pacemaker lead in a patient with congenital heart disease. Ann Pediatr Cardiol 2019;12:130-131.
中華民國心律醫學會‧ Taiwan Heart Rhythm Soclety ‧中華民國 111 年 9 月出刊
國立臺灣大學醫學院附設醫院 莊家權放射師/ 陳橙葦放射師 輻射防護技術來減少電燒期間輻射暴露並增加輻射 工作人員的工作壽命 電生理 (Interventional electrophysiology, EP) 發 展至今已超過 20 年,早期利用X光機透視導引下 進行心律不整診斷及燒灼術,近年結合三維 (Three
Dimensional, 3D) 立體定位系結合多方醫療影像,例 如:電腦斷層 (Computed Tomography , CT) 及心臟超 音波(Echocardiography) 等醫學資訊,將其投射在即 4 NO.047
時透視影像系統上提供新心臟解剖結構及定位導管的 位置和方向,因需準確診斷和了解復雜心臟解剖情況, 而造成病人與工作人員的累積輻射曝露量增加,癌症 發生的機率與劑量有關,機率隨劑量的增加而提高, 我們稱此效應為機率效應。另一方面,近期很多新的 儀器設備以及技術來幫助輻射工作人員達到減少輻射 曝露量產生以及無輻射的診斷及電燒治療,以符合
ALARA 原則 ’as low as reasonably achievable’。
當然並不是以無輻射為目標,X光機透視扮演的

中華民國心律醫學會‧ Taiwan Heart Rhythm Soclety ‧中華民國 111 年 9 月出刊
角色及為重要,於複雜的電生理診斷及治療中必須有 效的輻射曝露以及患者安全中取得平衡,基於輻射防 護三原則,正當化、最適化、劑量限度,本文主要目 標能夠在 EP 診斷及治療中,輕鬆實現減少輻射暴露 ( 圖ㄧ ) ( 圖二 ) ( 圖三 ) 在X光機透視系統執行手術中,為擋掉散射輻射 有提供兩個單獨輻射防護設備讓術者使用,一為可移 動手術檯下的鉛屏,每 0.5mm 的鉛屏可減少 90% 的 散射輻射,但往往因礙於手術檯上的移動以及管球推 移影響照射品質而被拆掉,另一個是懸吊上的鉛擋版, 隨者術者打不同角度透視時可自行挪動,輻射操作人 員可以藉由兩保護設備減少輻射暴露量 ( 圖二 )。 治療過程中導管護理師及相關專業人員必須隨時 注意病人狀況而靠近輻射設備,也會協助術者進行導 管介入治療輔助,可能會接受高輻射曝露,必須手術 全程穿著輻射防護裝備,在非必要醫療行為下盡量遠 離透視輻射設備(輻射暴露率與距離平方成反比關 係),及工作行政區盡量在鉛擋板後方 ( 圖三 ),此外 護理師及相關專業人員如需接近患者時在非緊急時刻 發出信號,請術者在可能的情況下暫時先停止輻射透 視。 EP 主要將電訊號極導管放置在心臟腔室及腔室間 的對應位置,甚至可利用 3D 立體定位系統來輔助亦 或是其他醫療影像支援,不需使用高顯像率,可將顯 相率每秒 15 張縮減到每秒 3.75 張,可有效減少輻射 劑量。 最近,CARTO 開發了一種新的 3D 無輻射導引 技術 (CARTO-UNIVU TM Module of CARTO 3 system, Biosense Webster),將透視機器和磁場定位版的位置進 行註冊而得到相對位置,再結合電腦斷層重組影像以 及 3D 畫圖系統提供新心臟解剖結構及定位導管的位 置和方向 ( 圖四 ),就可進行心律不整診斷及燒灼術進 行,特別考慮複雜的燒灼術 (AF 和 VT) 的需求增加, 此研究表明,能夠顯著減少患者及輻射工作人員的輻 射暴露。 同時可以維持影像品質。 導管室輻射工作人員必須穿著的輻射防護裝備, 包括一般穿著鉛衣、鉛裙以及配戴能夠保護甲狀腺的 鉛頸圈和保護眼睛水晶體的鉛眼鏡,因為大部分透視 攝影機器靠近術者的左側,因此部分鉛衣有特製左袖 套防護可以減少散射輻射的曝露量並保護腋下淋巴 ( 圖一 ),個人輻射防護裝備是必須每年定期檢驗。 早期鉛衣厚重,往往造成術者肩膀痠痛 50 肩以 及腰椎椎間盤突出,現今鉛衣發展有無鉛材質的鉛衣, 不但跟鉛衣一樣保護效果,鉛當量也足夠抵擋散射以 外,最重要的是無鉛材質的鉛衣也相對比一般鉛衣輕, 可減少術者在手術過程中長時間不舒服。 5NO.047
Reference:
1. Christoph M, Wunderlich C, Moebius S, Forkmann M, Sitzy J, Salmas J, et al. Fluoroscopy integrated 3D mapping significantly reduces radiation exposure during ablation for a wide spectrum of cardiac arrhythmias. Europace. 2015;17(6):928-37.

2. Heidbuchel H, Wittkampf FH, Vano E, Ernst S, Schilling R, Picano E, et al. Practical ways to reduce radiation dose for patients and staff during device implantations and electrophysiological procedures. Europace. 2014;16(7):946-64.
3. Kato M, Chida K, Munehisa M, Sato T, Inaba Y, Suzuki M, et al. Non-Lead Protective Aprons for the Protection of Interventional Radiology Physicians from Radiation Exposure in Clinical Settings: An Initial Study. Diagnostics (Basel). 2021;11(9).
4. Livingstone RS, Varghese A, Keshava SN. A Study on the Use of Radiation-Protective Apron among Interventionists in Radiology. J Clin Imaging Sci. 2018;8:34.
中華民國心律醫學會‧ Taiwan Heart Rhythm Soclety ‧中華民國 111 年 9 月出刊
國立成功大學醫學院附設醫院 陳昭佑醫師 /黃鼎鈞醫師 ECG of the Month Ablation of Left Postero-septal Accessory Pathway with RA-LV Connection: Tips and Pitfalls ( 圖 四 ) 6 NO.047

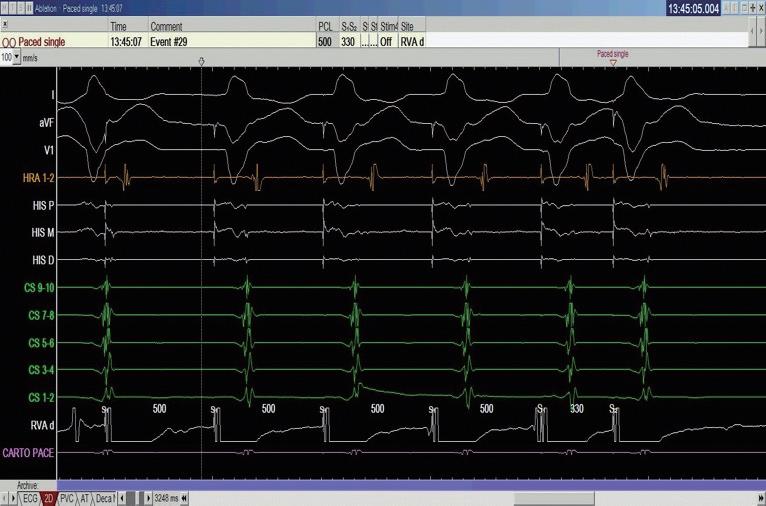
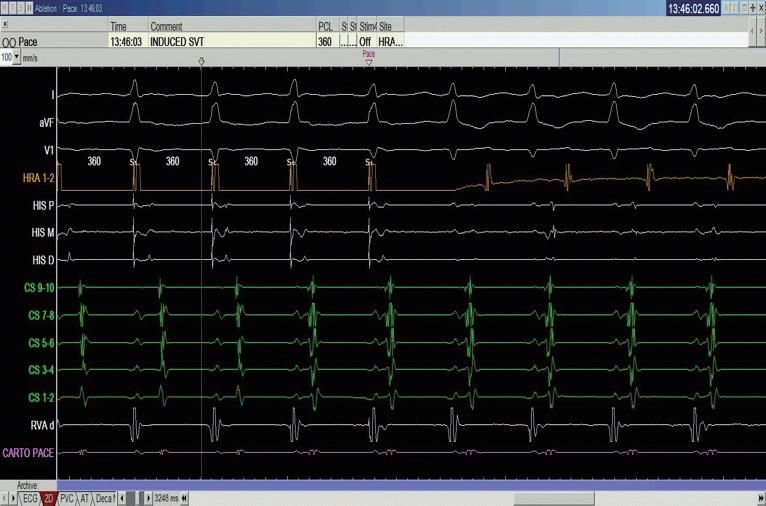
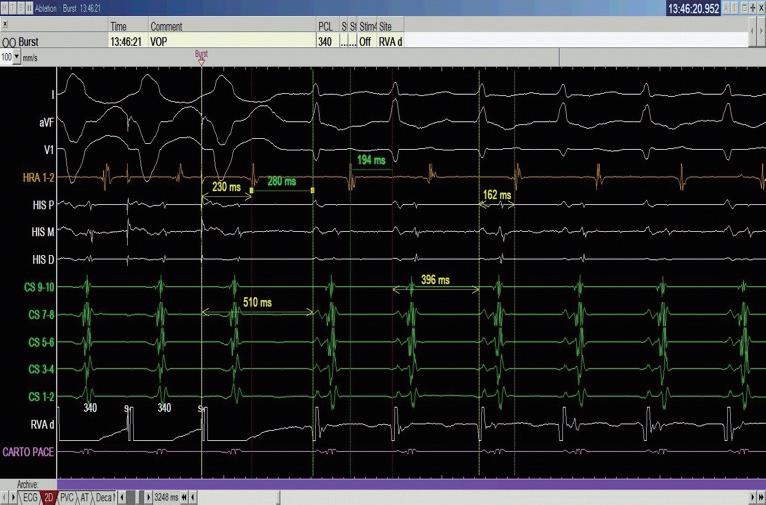
中華民國心律醫學會‧ Taiwan Heart Rhythm Soclety ‧中華民國 111 年 9 月出刊 我們在此報告一個來進行 PSVT 電燒的 55 歲 女性,沒有其他慢性病症,甲狀腺檢查正常,因為 PSVT 前往急診,發作時十二導程心電圖如下 ( 圖一 ) , 看起來是 short-RP 的 tachycardia 並且有 electrical alternans 的現象,第 12 個波組看起來比較不一樣,推測有可能 此時 tachycardia 有短暫的 termination 又被第 13 個波 組的 VPC 重新啟動一輪的 SVT 。 進入 EP lab ,在一開始進行 Ventricular extra stimulus test (VEST) 檢查時,心房訊號的傳導 是中軸傳導 (Concentric atrial activation pattern),而 且我們觀察不到明顯遞減傳導的現象 (Decremental conduction),一般而言正常經過房室結的傳導無論 順向或逆向多半會有 Decremental conduction 的情 況,這讓人懷疑隱藏在著一條在中軸的副傳導路徑 (Accessory pathway)( 圖二 ) 病人的心律不整很容易在右心房用 rapid pacing 誘 發,誘發時會看到心房心室傳導逐漸出現 Wenckebach 的現象,接下來就產生一個 Short-RP 的 tachycardia, 在 tachycardia 時的 atrial activation sequence 在 CS 導 程的表現看起來與我們先前在做 RV pacing 時是一致 的 ( 圖三 ) ( 圖二 ) ( 圖一 ) ( 圖三 ) 7NO.047
HIS refractory VPC 做確認時(圖五),結果又有點出乎 意外,當
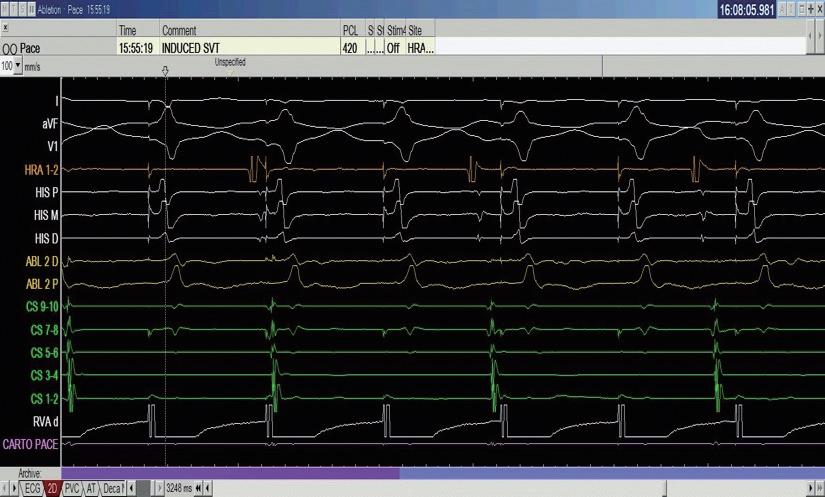

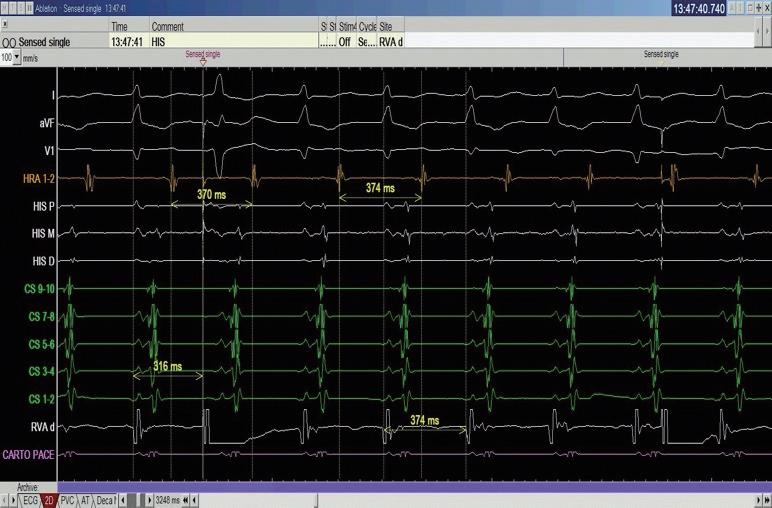
中華民國心律醫學會‧ Taiwan Heart Rhythm Soclety ‧中華民國 111 年 9 月出刊 ( 圖四 ) ( 圖六 ) ( 圖五 ) ( 圖八 ) 我們接著進行 Para-hisian pacing 來證實我們的想 法,我們將原本放在 HRA 的電極放到在 Para-hisian 的 V site,邊做 pacing 邊調降 pacing voltage,一路將 voltage 降到 0.3mV 都可以 capture myocardial 並傳回 atrium 去,其中的 V-A interval 都保持一致,證實這個 accessory pathway 的存在(圖六)。 由於看起來是不管在 RV pacing 或心律不整跳起 來時 Atrial activation 都以 CS 9-10 最早,儘管 CS lead 在 fluoroscopy 的 LAO view 下放得比較深,我們先 在 Tricuspid ring 的 septal site 靠近 CS9-10 的地方進行 電燒。( 圖七 ) 我們在右側電燒時,不管是電燒或者 mechanical bump 的方式,都可以將正在跳的心律不整 終止。這時候心律不整下的 V-A 訊號看起來也比之前 寬,然而類似的心律不整依舊會被誘發。 我們於是考慮這條 accessory pathway 其實比較 broad band,並且牽扯到 LV 的 septum,最終我們成 功在 Mitral subvalvular 的 septal site 將這條 accessory pathway 燒掉,並且達到 complete VA block(圖八), 最終電燒位置即在先前右側電燒點的對面(圖九, 圖中 CS catheter 有外拉,電燒導管位置近似於圖七 CS 9-10)。 這時候為了區分 AVNRT 與使用 septal kent 作 為傳導的 orthodromic AVRT,或者有一個很長 PR interval 的 AT( 儘管在前面的誘發過程較為不像 ),我 們使用 RV 的導管做 overdrive pacing 來 entrain 這個 tachycardia。 在成功 RV entrainment 停止後,我們觀察 tachycardia 傳導回來的方式是 V-A-V response ,這 個反應排除了心房頻脈。接著我們計算 PPI-TCL 以 及 Stimulus-atrial interval minus ventriculoatrial interval (SA-VA),可以看到 PPI-TCL 數值為 114ms, 而 SA-VA 為 68ms。(圖四)PPI-TCL 剛好在一個邊 界值,是嗎?這裡有個小陷阱,我們應該要對 delta A-H 做校正,在本圖中因為 His 的訊號不明顯,所以我們 使用 delta A-V 做校正(假設 HV 為定值不太會變), 可以看到 PPI 的 A-V 因為 decremental properties 的 關係較長(280ms),而平常 tachycardia 在跳的時候 A-V interval 較短(194ms),校正後的 corrected PPITCL 其實是 114-(280-194)= 28ms。 從這樣的檢查代表應該是 septal accessory pathway 造成的 orthodromic AVRT,然而當我們進一步做
RV pacing 在 surface ECG 出現 fusion beat, 足以證實在 HIS refractory phase 時,並沒有 advanced 下一個 A,然而這樣是代表沒有 accessory pathway 存 在嗎?其實並不,因為單一 HIS refractory beat 不見 得真的能比從 His-Purkinjean system 傳下了的訊號更 早到達 accessory pathway,HIS refractory VPC 假設 有 advanced next A or terminate tachycardia 可以代表 有 accessory pathway 的存在,反過來並不能拿來證實 accessory pathway 不存在。 8 NO.047
1. Lebloa,
Pascale,
Endocardium
Discrimination
Posteroseptal Accessory Pathways Ablated
Epicardial
Venous Approach.
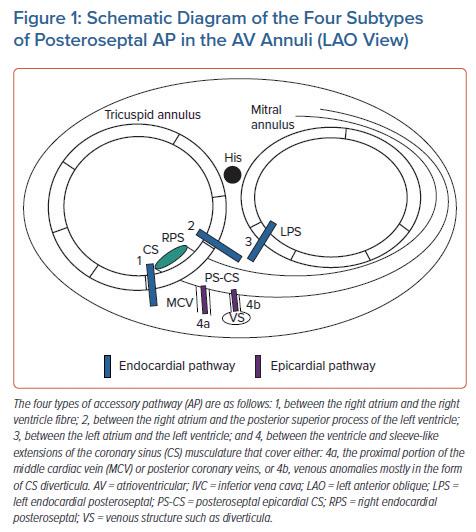
中華民國心律醫學會‧ Taiwan Heart Rhythm Soclety ‧中華民國 111 年 9 月出刊 ( 圖七 ) ( 圖九 ) 根據 Lebloa et al. 在 Arrythmia & Electrophysiology review 的 posteroseptal accessory pathways 的分類, 分為三種 endocardial pathway 跟一種 epicardial pathway,Type 1 是 RA 跟 RV 的 connection,type 2 是 RA 跟 posterior superior process of LV,type 3 是 LA 跟 LV,Type 4 則是 epicardial pathway 牽扯到從 ventricle 延伸到 coronary sinus 內。(圖十)就我們這處理這個 病人的經驗,這個 accessory pathway 的確可能 inserted to 兩邊的腔室,最終需要兩側都做電燒才可以成功。 Reference:
M., &
P. (2022). Preprocedural
of
from the Right
from Those Requiring a Left-sided or
Coronary
Arrhythmia & electrophysiology review, 11, e07. https://doi.org/10.15420/aer.2021.55 ( 圖十 ) 9NO.047
Role
ablation 還要好 1。現今
ablation 已經被證實在 VT burden 和首次 VT 復發有比使用抗心律不整藥還要好, 但對於存活率沒什麼助益。且在經過 RF ablation 之後
的位置難以去接 近。在 refractory VT 的治療方法,除了上述提及的 RF
中華民國心律醫學會‧ Taiwan Heart Rhythm Soclety ‧中華民國 111 年 9 月出刊 國立臺灣大學醫學院附設醫院 陳建倫醫師/ 賀立婷醫師
of Stereotactic Radioablation for Refractory Ventricular Arrhythmia 時至今日,在就算使用了抗心律不整藥物卻依 然發生 recurrent ventricular tachycardia(VT) 而需要使 用心律整流除顫器 (ICD) 的病人,會去考慮使用經導 管射頻燒灼術 (RF ablation)。而在 RF ablation 中,使 用 extensive ablation 的方式的效果明顯比傳統 limited
RF
的復發率依舊有 40%-60%2。復發率這麼高,可能有以 下幾種造成 RF ablation 會失敗的可能因素:產生 VT 的位置可能難以定位,或是造成 VT
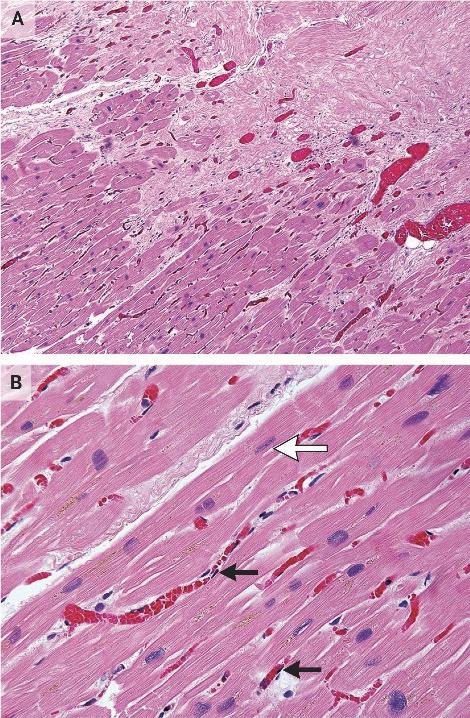
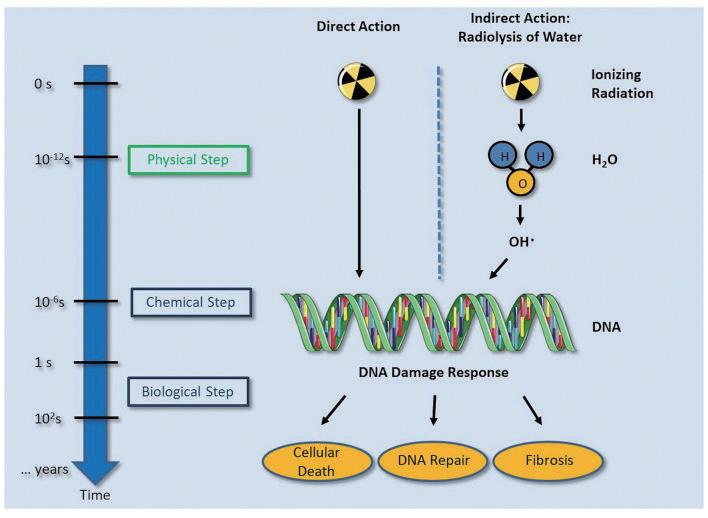
在一位曾經接受過 SBRT 的病患的心肌切片中 ( 圖 二 ),可以看見出現了部分的纖維化。比較特別的是, 這位接受過 SBRT 的心肌沒有出現接受到一般放射線 的心肌常見的急性心肌壞死、出血或是發炎,由此可 見在初次接受 SBRT 的幾週內並不會產生對心臟多餘 的傷害 4 。 在效果上,ENCORE-VT 臨床試驗指出接受過 SBRT 的 19 位病人發生的 VT 以及使用 ICD shock therapy 的次數大幅下降,的次數大幅下降,6 個月以 及 12 個月的存活率分別可達 89% 和 72%,此外整體 ablation 之外,還有較少去施行的外科處置,以及本 篇要探討的全身立體定位放射治療 (stereotactic body radiation therapy, SBRT)。 何謂 SBRT ?顧名思義就是使用高精準度的放射 線去照射我們所標定的目標處,之前為人所知的是用 在不適合開刀的早期肺癌。其原理如圖一所示,人體 細胞在接受到放射線之後,不管是放射線本身還是受 到放射線而裂解出的氫氧自由基都會對 DNA 造成傷 害,在受到傷害之後細胞可能會死亡、DNA 修復或是 纖維化 3 。 ( 圖ㄧ ) ( 圖二 ) 的生活品質也大幅提升 5。在安全性部分,SBRT 這樣 的放射線還是可能對冠狀動脈、心臟傳導系統、瓣膜、 心肌以及心包膜造成後續影響,可能會發生心包膜炎 或是心包膜積液。而更長期的安全性報告則需要更多 的後續研究來證實。 台大醫院的流程是先用核磁共振、電腦斷層以及 心臟電生理定位出 substrate 的位置,接著由放射腫瘤 科,放射診斷科以及電生理科醫師共同擬定 SBRT 計 畫,最後施行放射線治療。以一個病人為例,一位 47 歲的男性,有擴張型心肌病變 (dilated cardiomyopathy) 10 NO.047
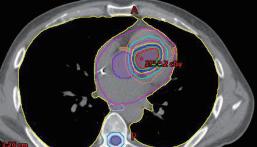
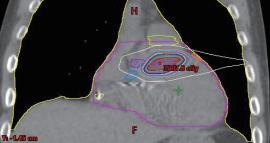
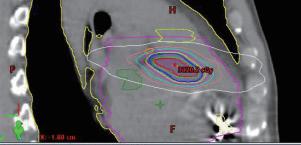

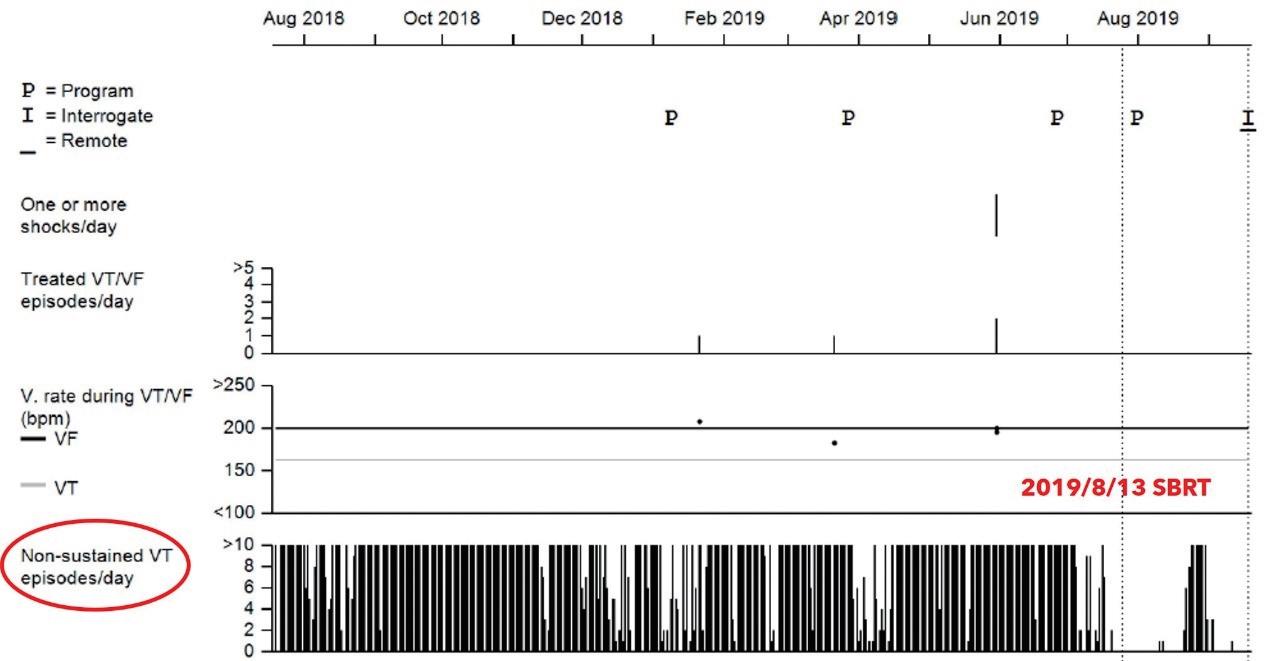
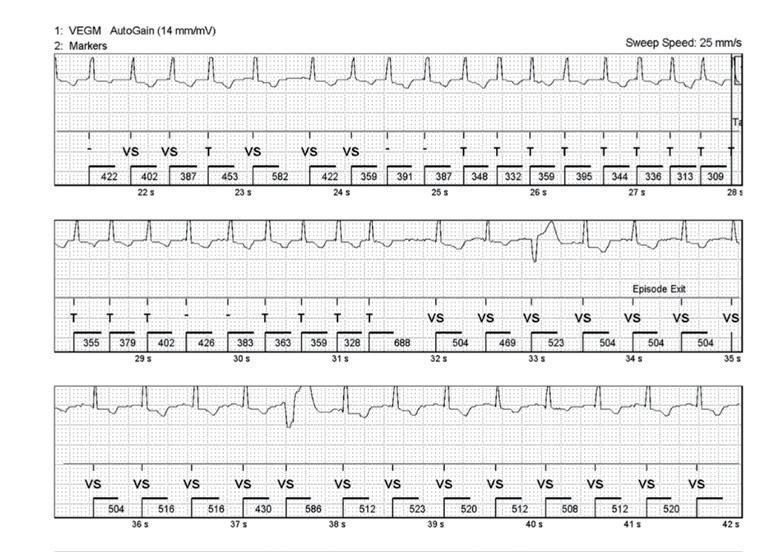
中華民國心律醫學會‧ Taiwan Heart Rhythm Soclety ‧中華民國 111 年 9 月出刊 ( 圖三 ) ( 圖四 ) ( 圖五 ) 和原發於右心室流出道 (right ventricular outflow tract, RVOT) 的 refractory VT。定位的位置是在 RVOT。 SBRT 進行的計畫顯示腫瘤體積 (gross target volume, GTV) 有 4.6 ml,而計畫靶體積 (planning target volume, PTV ) 有 14.4 ml,如 ( 圖三 ) 至 ( 圖五 ) 所表示。SBRT 進行時間為 11.9 秒,由 6 個共平面以及 4 個非共平面的 放射源進行照射,如 ( 圖六 ) 所示。而在進行完 SBRT 後, 病人 VT 的次數以及持續時間皆有顯著的下降 ( 圖七 )。 ( 圖六 ) 綜合上述,在 refractory VT 的病人使用 SBRT 可 以達成不錯的短期效果,顯著降低 VT 的次數和持續 時間,另外安全性的部分至少短期內不會對其他心肌 造成額外的傷害。雖然說長期的安全性與副作用還是 未知,但 SBRT 確實是幫 refractory VT 找到了新的治 療道路。 Reference: 1. Di Biase L, Burkhardt JD, Lakkireddy D, Carbucicchio C, Mohanty S, Mohanty P, Trivedi C, Santangeli P, Bai R, Forleo G, Horton R, Bailey S, Sanchez J, AlAhmad A, Hranitzky P, Gallinghouse GJ, Pelargonio G, Hongo RH, Beheiry S, Hao SC, Reddy M, Rossillo A, Themistoclakis S, Dello Russo A, Casella M, Tondo C, Natale A. Ablation of Stable VTs Versus Substrate Ablation in Ischemic Cardiomyopathy: The VISTA Randomized Multicenter Trial. J Am Coll Cardiol. 2015;66:2872–2882. 2. Tokuda M, Kojodjojo P, Tung S, Tedrow UB, Nof E, Inada K, Koplan BA, Michaud GF, John RM, Epstein ( 圖七 ) 11NO.047
LM, Stevenson WG. Acute failure of catheter ablation for ventricular tachycardia due to structural heart disease: causes and significance. J Am Heart Assoc. 2013;2:e000072.
3. Jumeau R, Ozsahin M, Schwitter J, Elicin O, Reichlin T, Roten L, Andratschke N, Mayinger M, Saguner AM, Steffel J, Blanck O, Vozenin M-C, Moeckli R, Zeverino M, Vallet V, Herrera-Siklody C, Pascale P, Bourhis J, Pruvot E. Stereotactic Radiotherapy for the Management of Refractory Ventricular Tachycardia: Promise and
Implantable loop recorder
Future Directions. Front Cardiovasc Med. 2020;7:108.
4. Cuculich PS, Schill MR, Kashani R, Mutic S, Lang A, Cooper D, Faddis M, Gleva M, Noheria A, Smith TW, Hallahan D, Rudy Y, Robinson CG. Noninvasive Cardiac Radiation for Ablation of Ventricular Tachycardia. NEnglJMed. 2017;377:2325–2336.
5. Robinson CG, et al. Phase I/II Trial of Electrophysiology-Guided Noninvasive Cardiac Radioablation for Ventricular Tachycardia. Circulation. 2019;139:313-321.
ILR (Implantable loop recorder) 為植入式心律紀 錄器,可以在皮下監控心律二到三年的時間,偵測是 否有心律不整,包含心房顫動、心室心律不整或是心 搏過緩,而導致例如心悸、暈厥等等症狀。近年因醫 師以及病患對於心房顫動的重視,ILR 常被使用來偵 測心房顫動。然而在 Lancet 2021 年發表的 The LOOP Study 告訴我們,在相對高齡 (70-90 歲 ),且有中風 風險的病患,利用 ILR 偵測心房顫動並給予抗凝劑 治療,並不會改善中風或是全身性栓塞的風險。由此 可知,ILR 在心房顫動上的應用,是要慎選病患接受 監控,而不是盲目建議病患使用。Embolic stroke of undetermined source (ESUS),是一群可以利用 ILR 偵 測心房顫動,而可能改變治療及預後的病人群。在過 去的許多研究皆發現,使用 ILR 可以增加約三成心房 顫動的偵測率,然而過去的 ILR 紀錄心房顫動的時
間,是大於兩分鐘才會自動記錄。新一代的 ILR,例 如 Abbott 的 CONFIRM Rx ICM,則可以自動記錄大 於 30 秒以上的心房顫動,使得偵測心房顫動可以更靈 敏。在此提出一位病患案例,為 69 歲男性,於 2014 年因 TIA 接受抗血小板藥物治療,在 2020 年因為 acute right MCA posterior M2 occlusion,做了血管內 取栓術。術後詳細的檢查包括 24-hours Holter、胸前 及經食道心臟超音波、頸動脈超音波、顱內血管超音 波以及凝血功能等,結果皆為正常。因此神經科醫師 診斷為 ESUS,並給予 clopidogrel 治療,且建議病患 裝置 ILR。病患於 2021 年 2 月裝置 Abbott CONFIRM Rx ICM,於 2021 年 6 月抓到超過 30 秒鐘的心房顫動 ( 如下圖 ),因此神經科醫師改變治療,將 clopidogrel 改成口服抗凝血劑。
中華民國心律醫學會‧ Taiwan Heart Rhythm Soclety ‧中華民國 111 年 9 月出刊 國立臺灣大學醫學院附設醫院 莊志明醫師/賀立婷醫師/林廷澤醫師
(ILR) 在心房顫動 (AF) 及心因性猝死 (SCD) 病患上臨床的應用
12 NO.047
表示劉先生在前幾天於睡夢中心跳停止過世,未曾再 醒來,嘆息著說早知道當初應該要積極的找出暈厥的 原因。醫師點閱劉先生的病歷資料,發現心臟超音波 的報告打著「肥厚型心肌病變」。一位 40 幾歲的中壯 年男性,突然地心因性猝死,來不及和家人說聲再見… 心因性猝死 (sudden cardiac death) 的定義是因心臟 疾病所引起的非預期性的死亡。男性的發生率高於女 性,平均發生年齡約在 55 到 58 歲,發生率隨著年齡 的增長而增加。例如 50 歲的族群為千分之一,而 75 歲則增加到千分之八。然而,心因性猝死卻占年輕族 群死亡原因的多數,加上突然且非預期性的特性,帶 給社會經濟和家屬心理的重大衝擊。心因性猝死的存 活率不高,約 10-30% 不等。八成以上的心因性猝死, 由心室頻脈或心室顫動所引起,此惡性的心律不整,
75% 肇因於冠狀動脈疾病和心肌梗塞。在猝死的男性 患者中 80% 是患有冠狀動脈疾病,而女性則較多因遺 傳性的心肌病變和心律不整所引起 ( 圖一 )[1]。
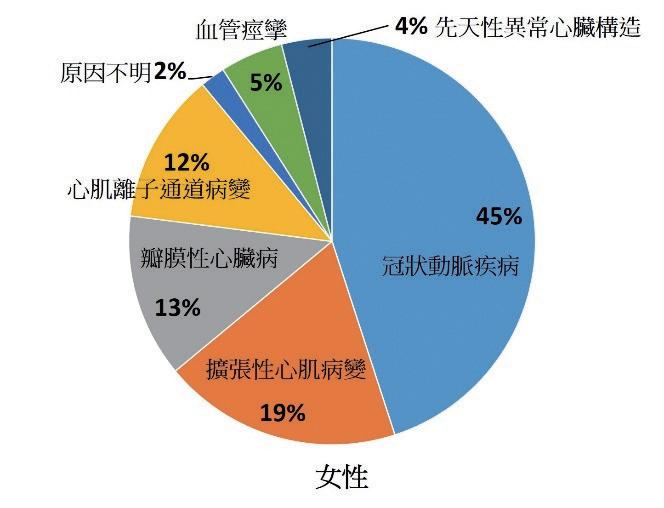
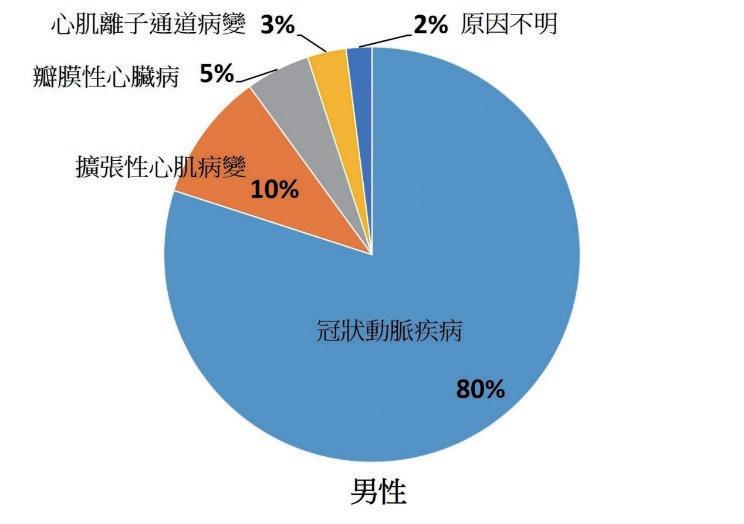
心因性猝死可能是先天遺傳的影響或是後天環境
和行為的改變,主要可分成冠狀動脈疾病、各種心肌 病變和遺傳性離子通道病變等類,有這些高風險疾病
sudden cardiac death
that
Deo R, Albert CM. Epidemiology and genetics of sudden cardiac death. Circulation 2012;125(4):620-37.
Reference:
1. Deo R, Albert CM. Epidemiology and genetics of sudden cardiac death. Circulation 2012;125(4):62037.
2. Elpidoforos S Soteriades , Jane C Evans, Martin G Larson, Ming Hui Chen, et al. Incidence and prognosis of syncope. N Engl J Med. 2002;347:878–885.
3. Ryan J Koene , Wayne O Adkisson , David G Benditt .J Arrhythm. Syncope and the risk of sudden cardiac death: Evaluation, management, and prevention. 2017 Dec; 33(6): 533–544.
4. Jonathan S Steinberg , Niraj Varma , Iwona Cygankiewicz. et al. 2017 ISHNE-HRS expert consensus statement on ambulatory ECG and external cardiac monitoring/telemetry Heart Rhythm.;2017(14):e55–e96.
5. Andrew D. Krahn, George J. Klein, Raymond Yee and Allan C. Skanes . Randomized Assessment of Syncope Trial. Circulation. 2001;104:46–51.
6. D J Farwell , N Freemantle, A N Sulke J. Use of implantable loop recorders in the diagnosis and management of syncope. Eur Heart. 2004;25:1257–1263.
中華民國心律醫學會‧ Taiwan Heart Rhythm Soclety ‧中華民國 111 年 9 月出刊 診間的門一打開,走進一位哭得梨花帶雨的女士, 猛然想起是兩個月前因昏厥求診的劉先生的太太。她
的患者,發生昏厥 (Syncope) 後,其中在一年內有 1830% 的人會發生猝死 [2],也常常與心室頻脈或心室顫 動有關,因此為了能夠提早診斷提早預防,然而昏厥 本身的發生頻率不高,電生理檢查 EPS 及一般的 24 小時心電圖或是 7 天至 14 天的連續型心電圖貼片其診 斷率並不高 [3],因此長時間連續型的體內心電圖紀錄 器 (implantable cardiac monitors [ICM]) 便有其診斷價 值。 ICM 三年的紀錄其間,約 30-50% 的暈厥患者能 夠找到原因 [4]。在兩個隨機分配臨床試驗中發現,與 傳統診斷工具相比 (6~20%),使用長時間連續型的體 內心電圖紀錄器 (ICM),於一年到一年半後能夠達到 43-52% 的診斷效果 [5-6]。在日益進步的醫療儀器中, 許多微小化且方便裝置的連續型的體內心電圖紀錄器 將能夠替暈厥患者帶來更好的診斷效率和治療結果。。 “ The only difference between syncope and
is
in one you wake up." ~ 喬治·L· 恩格爾 ( 圖ㄧ ) 男性與女性的心因性猝死原因 圖片重製於
13NO.047
New-Onset Atrial Fibrillation in Patients
Hospitalized With COVID-19: Results From the American Heart Association COVID-19 Cardiovascular Registry
Circ Arrhythm Electrophysiol 2022 May;15(5):e010666.
COVID-19 住院患者新發生心房顫動之預後 - 美國心臟 學會成果報告
摘要
背景
新發作之心房顫動於 COVID-19 住院患者中曾被報 導為與不佳的預後相關。我們的目標在於了解美國
族群中,新發作之心房顫動於之 COVID-19 住院患 者中之盛行率及預後。
方法
分析美國心臟協會 COVID-19 併心血管疾病註冊 系統中登錄的資料。登錄的患者將被分為有新發作 及無新發作心房顫動兩組。主要評估指標 (Primary endpoint) 為住院中死亡率 (In hospital mortality)。次要 評估指標為重要不良心臟事件 (MACE,major adverse cardiovascular events),包括心因性死亡、心肌梗塞、 中風、心因性休克與心衰竭。新發作之心房顫動與主 要及次要評估指標的關係,使用比例風險回歸模型
(Cox proportional-hazards models) 分析。 結果
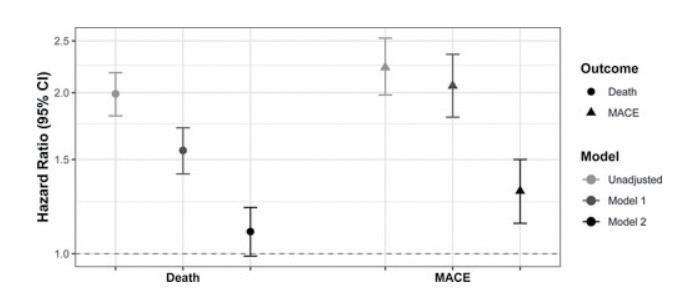
在 30999 位於 120 個美國醫療機構因 COVID-19 住 院的患者中,有 27851 位患者沒有心房顫動的病史。 其中,1517 位患者 (5.4%) 的患者於住院中被發現有 新發作的心房顫動。新發作心房顫動的患者有較高的 死亡率 (45.2% versus 11.9%) 及較高的 MACE (23.8% versus 6.5%)。於校正前的分析中,有新發作心房顫動 的患者,其死亡的風險比為 1.99(95% CI, 1.81–2.18), MACE 的風險比為 2.23 (95% CI, 1.98–2.53)。校正患 者的背景資料、臨床合併症及疾病嚴重度後,死亡 的風險比明顯下降 (hazard ratio, 1.10 [95% CI, 0.991.23]),而 MACE 的風險比則部分下降 (hazard ratio, 1.31 [95% CI, 1.14-1.50])。 結論
於 COVID-19 住院患者中,新發作心房顫動的發生率 為 5.4%。幾乎有一半新發作心房顫動的患者於住院中 死亡。在校正患者的合併症與疾病嚴重度後,新發作 心房顫動與死亡沒有顯著的統計相關性,說明新發作 的心房顫動可能僅是 COVID-19 患者臨床狀況不佳的 指標之一,而非直接的致死因子。關於新發作的心房 顫動與 MACE 之間的關係,尚需進一步的研究加以驗 證。
中華民國心律醫學會‧ Taiwan Heart Rhythm Soclety ‧中華民國 111 年 9 月出刊
國立成功大學醫學院附設醫院 廖瑀 醫師 脈新 動聞 媒體及學會新聞
14 NO.047
Circumferential Pulmonary Vein Isolation Plus Low-Voltage Area Modification in Persistent Atrial Fibrillation: The STABLE-SR-II Trial
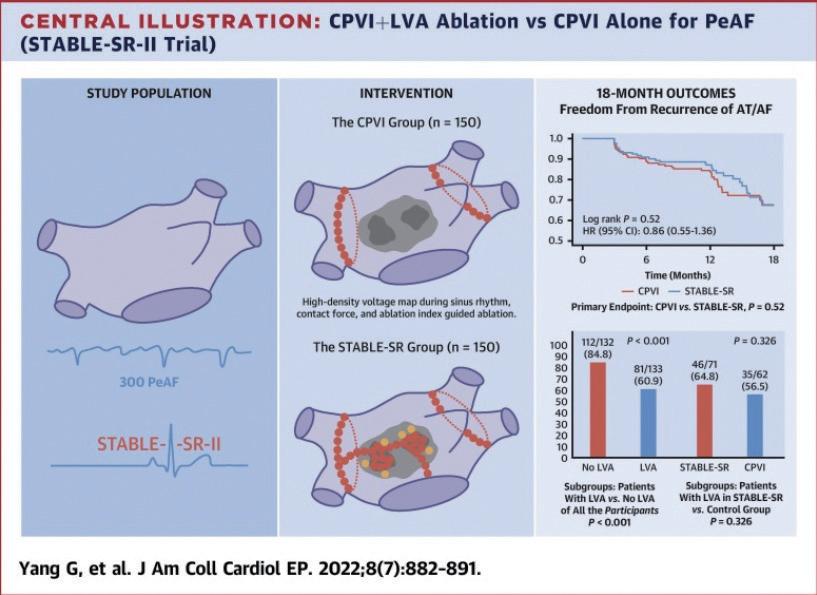
JACC Clin Electrophysiol. 2022 Jul;8(7):882-891 持續性心房顫動患者進行環肺動脈電氣隔離合併低電 位區域電燒手術之成果
摘要
背景 針對持續性心房顫動之電燒治療,環肺動脈電氣隔離 術加上其他輔助性電燒策略相比於單獨使用環肺動脈 電氣隔離術,其帶來的益處並不明確。
目的 此研究目標為於持續性心房顫動之患者,比較環肺動 脈電氣隔離併低電位區域電燒手術與單純使用環肺動 脈電氣隔離手術之臨床成果。
方法
於 2018 年 3 月至 2019 年 8 月期間,共收納 300 位 此前未接受治療的持續性心房顫動患者。患者被隨 機且前瞻性的分為 STABLE-SR 組 (n=150) 與 CPVI 組 (n=150)。CPVI 組接受環肺動脈電氣隔離手術,而
STABLE-SR 組在完成環肺動脈電氣隔離手術後,於 竇性心律下繪製左心房的高密度電位圖 (high density
voltage mapping),並於低電位區域或複雜性電訊區 (complex electrograms) 執行電燒。所有的電燒均參考 電燒指數 (ablation index) 下完成。其主要研究指標為, 於 3 個月的寬容期後 (blanking period),在不使用抗心 律不整藥物下,患者是否有發生超過 30 秒以上的心房 心律不整。 結果
經過 18 個月的追蹤,STABLE-SR 組與 CPVI 組於未 發生心房心律不整 (Atrial-arrhythmia-free survival) 並 無明顯差異 (67.2% vs 67.4%; HR: 0.89; 95% CI: 0.551.36; P = 0.52)。僅有約一半的患者 (50.2%) 被發現有 異常的左心房訊號 (LA substrate),其中低電位區域佔 比之中位數為 4.6%(2.1%-9.5%)。然而,沒有異常左心 房訊號 (LA substrate) 患者,相對於有異常左心房訊號 的患者,其手術成功率有明顯的差異 (84.8% vs 60.9%; P < 0.001)。 結論 合併低電位區域電燒並未增加接受環肺動脈電氣隔離 術之持續性心房顫動患者維持竇性心律的成功率。這 些患者中,將近一半的患者有正常左心房之電訊號。 高密度電位圖 (high density voltage mapping) 可以辨別 出具有正常左心房訊號的患者,這些患者接受單純的 環肺動脈電氣隔離術後能夠很好地維持竇性心律。
中華民國心律醫學會‧ Taiwan Heart Rhythm Soclety ‧中華民國 111 年 9 月出刊
15NO.047
Limitations of Unipolar Signals in Guiding Successful Outflow Tract Premature Ventricular Contraction Ablation
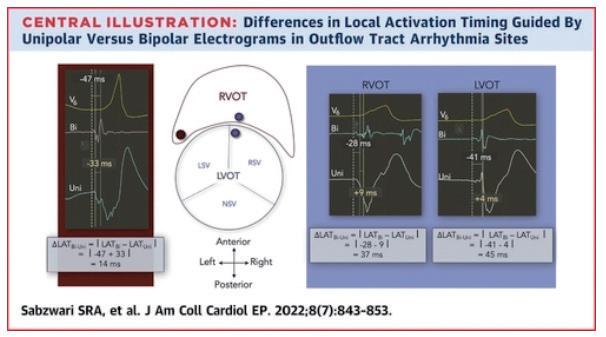
JACC Clin Electrophysiol 2022 Jul;8(7):843-853. 針對心室出口心室早期收縮,以單極訊號導引進行電 燒手術之限制
摘要
背景
單極電訊號 (unipolar electrograms, UniEGMs) 常被用 於標記局部發作型心律不整 (focal arrhythmia) 最早 的電訊號激活點。然而,當心室早期收縮並非發源 於表淺處時,使用單極電訊號 (unipolar electrograms, UniEGMs) 定位將產生侷限。
目的
作者試著比較使用雙極電訊號 (bipolar electrograms, BiEGMs) 與單極電訊號 (unipolar electrograms, UniEGMs) 導引下,進行右心室出口 (right ventricular outflow tract,RVOT) 及心肌內出口型 (intramural outflow tract) 心室早期收縮電燒之成果。作者有以下的假設 (1) 使 用雙極電訊號最早的激活時間點做為電燒導引,將比 使用單極電訊號之訊號單位時間變化量 (UniEGM dV/ dt) 或單極電訊號之 QS 型態為佳 (2) 考慮雙極電訊號 與單極電訊號激活時間差時 ( ΔLAT Bi-Uni) ,心肌內 出口型心室早期收縮的時間差將大於右心室出口心室 早期收縮。
方法 於 2017 年至 2020 年間,將成功接受右心室出口或左 右心室出口 (RVOT+LVOT) 心室早期收縮電燒手術的 患者以回溯式研究分析。作者比較電燒成功處的雙極 電訊號與單極電訊號。
出現的比率為 53%(P<0.016)。左右心室出口均須電燒 的患者,其電燒位置最常見位於右心室出口之後中膈 處 (posteroseptal) 及其相鄰的左心室出口,且 43% 的 位置之單極電訊號並非為 QS 型態。當使用雙極電訊 號與單極電訊號激活時間差 >15 毫秒作為條件時,可 以很好的區辨僅需於右心室出口或須於左右心室出口 電燒的兩組患者。
結論 針對出口型心室早期收縮,使用最早的雙極電訊號激 活時間點做為電燒導引較 使用單極電訊號為佳,尤其是當治療心肌內出口型 (intramural outflow tract) 心室早期收縮時。
中華民國心律醫學會‧ Taiwan Heart Rhythm Soclety ‧中華民國 111 年 9 月出刊
結果 在總數 70 位的病人當中,有 50 人僅需於右心 室出口進行電燒,而有 20 位須於左右心室出口 (RVOT+LVOT) 電燒來達到長期控制心室早期收縮。 對於僅需於右心室出口進行電燒的患者,雙極電訊號 與單極電訊號激活時間差 ( ΔLAT Bi-Uni) 較短 (9.3 ± 6.4 ms vs 17.4 ± 9.9 ms; P < 0.01)。電燒成功處之單極 電訊號中,僅需於右心室出口進行電燒的患者出現 QS 型態的比例為 78%,而左右心室出口均須電燒的患者
16 NO.047
