Arrhythmia News
發行人: 曹玄明 (Hsuan-Ming Tsao)
發行單位: 中華民國心律醫學會 (Taiwan Heart Rhyrhm Society)
地址: 100506台北市中正區忠孝西路一段50號25樓之18
本期摘要
P1. 狹窄與寬QRS波心動過速的電生理診斷
P7. Incremental Benefit of Stepwise Nonpulmonary Vein Trigger Provocation During Catheter Ablation of Atrial Fibrillation
P9. 運用左束支電刺激的心臟再同步化治療 ‒現今證據與未來展望
P13. ECG of the Month
P16. 脈動新聞
電話: 傳眞: 網址: ISSN: 2223-0130
886-2-23821530
886-2-23821528 www.thrs.org.tw
總編輯
洪元 Yuan Hung 林文裕 Wen-Yu Lin
本期主編
黃鼎鈞 Ting-Chun Huang 莊再庚 Chye-Gen Chin
編輯
鄭文涵 Wen-Han Cheng 黃冠智 Kuan-Chih Huang
劉京翰 Ching-Han Liu 黃彥彰 Yen-Chang Huang
潘國利 Kuo-Li Pan 許竹佑 Chu-Yu Hsu
黃世鐘 Shih-Chung Huang
狹窄與寬QRS波心動過速的電生理診斷
大林慈濟醫院心臟內科 李禎元醫師
序言
本文回顧了狹窄與寬 QRS 波心動過速的診斷要 點,根據心臟電激活模式的辨識,結合每個病例的特 定起搏操作來進行討論。
狹窄QRS波心動過速 (Narrow Complex Tachycardias, NCT)
在面對狹窄QRS波心動過速(NCT)時,初步診斷的 線索包括房室 (AV) 關係及心房激活的順序 ( 表 1) 。如果 NCT 伴隨心室 - 心房 (VA) 分離或心室激活快於心房 ( 如 2:1 VA 關係 ) ,這通常由一些不涉及心房的心律不整引 起,例如房室結折返性心動過速 (AVNRT) 、交界性心 動過速 (JT) 以及涉及結 - 束支 (NF) 或結 - 心室 (NV) 傳導徑 路的順行性心動過速。至於心房激活的順序,偏心激 活模式通常可排除 AVNRT 或 JT ,而支持心房性心動過
速 (AT) 或順行性房室折返性心動過速 (AVRT) 的診斷。 為了便於診斷並指導起搏操作,可以將這些心動過速 分為以下幾組:
1. 狹窄QRS波心動過速伴向心性心房激活 這是最常見的激活模式,可能由任何上心室性心 動過速 (SVT) 機制引起。鑑別診斷包括: 1) 房室結折返 性心動過速 (AVNRT) ; 2) 使用中隔房室旁路的順行性 房室折返性心動過速 (AVRT) ; 3) 中隔心房心動過速 (AT) ; 4) 交界性心動過速 (JT) ; 5) 使用隱匿 NF/NV 傳導 徑路的順行性心動過速 (NF/NV 心動過速 ) 。如果中隔 VA 時間(從表面QRS波的起點到最早的心房中隔電位的 時間 ) 在成人中小於 70 毫秒或在兒童中小於 50 毫秒,則 可以排除 AVRT ,因為這是電衝動經心室返回心房所需 的最短時間。
中華民國心律醫學
在這種情況下,合理的第一步是使用心室超速起 搏 (VOP) 來排除AT( 見圖一 ) 。若 VOP 從右心室(RV)引發 VAAV( 或 VAAHV) 反應,則診斷為 AT ;而 VAV(VAHV) 反應則出現在其他情況中。值得注意的是,假性VAAV 反應在非典型 ( 快 - 慢型 )AVNRT 或使用慢傳導遞減性房 室旁路的順行性 AVRT 中常見,這是由於回路中的逆行 肢段存在遞減性傳導。如果心房頻率無法加速至心室 起搏速率,心房超速起搏(AOP)也可能有幫助:如果最 後一個加速的心室搏動後的 VA 間隔與心動過速期間的 VA 間隔相同,這表明心房激動與心室激動相關 (VA 連 結 ) ,因此不太可能是心房心動過速 (AT) 。其他使房性 心動過速 (AT) 不太可能的因素包括:在非早搏的情況 下,心動過速伴隨房室傳導阻滯的持續終止,以及早 期心室搏動 (PVC) 或心室超速起搏 (VOP) 未能傳導至心 房而終止心動過速。
如果心動過速加速至起搏速率且出現 VAHV 反 應,則 VOP 後的超速起搏間隔 (PPI) 可反映起搏位置與 心動過速回路的接近程度,有助於區分 AVNRT 與使用
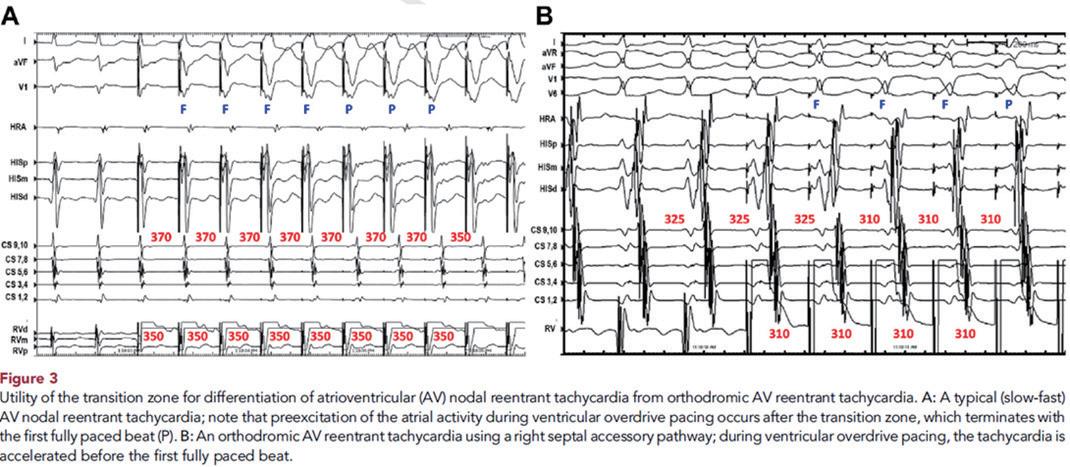
中隔旁路的AVRT 。PPI-TCL小於115 毫秒,且SA-VA小 於 85 毫秒,提示使用中隔旁路的 AVRT ;而 PPI-TCL 大 於 115 毫秒,且 SA-VA 大於 85 毫秒,則可能是使用側向 或遞減旁路的順行性AVRT。在長RP心動過速(RP > PR) 中, PPI-TCL 小於 125 毫秒更有助於區分與旁路相關的 心動過速與非典型 AVNRT 。由於快速起搏可能引起 AV 結遞減性傳導延長PPI(或隱藏於順行肢段),PPI-TCL的 差異可透過減去第一個回歸搏動的 AH 間隔與 SVT 期間 AH 間隔的差異進行校正。在 VOP 期間還需注意的另一 點是心動過速在過渡區的干擾:在順行性 AVRT 中,心 室起搏會在過渡區重置心動過速 ( 即完全起搏搏動之 前,before the first fully paced beat);而在AVNRT中,則 是在過渡區之後(見圖一)。一個新指標是心動過速期間 和心動過速誘導期間局部 VA 時間的差異,這可通過 CS 導管測量;差異小於 40 毫秒可確定為 AVRT ,即使心動 過速終止時該指標仍然有效。
第二步是證實旁路(accessory pathway, AP)的存在, 最有效的操作是引入希氏束不應期的 PVC 。這些 PVC 是在希氏束電位出現後(just after a His potential)或預期 的希氏去極化前 50 毫秒內釋放的。三種反應可以證實 旁路的存在: 1) 提前下一次心房激活並重置心動過 速; 2) 延遲下一次心房激活 ( 延遲重置 ) ; 3) 心律不整中 止於VA block。通常,後兩種反應也能證實旁路參與了 心動過速的回路。然而,希氏束不應期 PVC 也可能通 過隱匿的旁路 (NF/NV 通路 ) 重置或終止 AVNRT 。因
此,正向反應並無法區分 AVRT 、 NF/NV 心動過速或 AVNRT with a bystander NF/NV pathway。要區分AVRT 與結性心動過速 (NF/NV 心動過速及 AVNRT) ,可比較 Atrial entrainment( 或以心動過速周期長度起搏 ) 期間與 SVT 期間的 AH 間隔。對於 AVRT ,由於激活順序相似 ( 心房→房室結→希氏束 ) ,Δ AH(AH entrainment-AH SVT)< 20 毫秒。而在結性心動過速中,Δ AH > 40 毫 秒,因為心動過速期間的 AH 間隔非常短,由於心房與 希氏束幾乎同時 ( 非順序 ) 激活所致。隱匿的 NV 心動過 速與隱匿的 NF 心動過速可以透過心動過速期間的心室 起搏下是否出現 QRS 融合波來區分:有融合波表明心 室參與了NV心動過速的回路,而NF心動過速因其回路 侷限於希氏 - 浦肯野系統,不涉及心室心肌,因此不會 出現QRS融合波。
最後, AVNRT 與 JT 可以通過引入心房早搏 (PAC) 或心房超速起搏(AOP)來區分。如果早期的房性早搏能 夠重現性地終止心動過速,並且提前出現希氏束電 位,或者希氏束不應期的 PACs 擾亂了心動過速 (包括提 前、延遲下一次希氏束電位或終止心動過速 ) ,則可排 除交界性心動過速 (JT) 。其原因是 PAC通過快通道的順 行傳導,讓快通道進入不應期,從而終止 AVNRT 。使 用 AOP 時,如果起搏結束後出現 AHA 反應,證實 AVNRT;而出現AHHA反應則提示為JT。
2. 狹窄複合心動過速伴離心性心房激活 這種情況下的診斷通常不會太困難,因為可能的 機制主要有兩個:1) 心房心動過速(AT);2)順行性房室 折返性心動過速 (AVRT) 。大多數情況下,通過心室超 速起搏(VOP)可以輕鬆區分兩者。心動過速的誘導如果 產生 VAV 反應,提示為 AVRT ;而 VAAV 反應則與 AT 致。最後,希氏束不應期 PVC 對心動過速的影響 ( 心房 提前激動、心房延遲或心動過速終止 ) 可排除 AT ,並確 認存在旁路。
罕見的情況下,使用左側延伸的房室結的非典型 AVNRT 可能會呈現離心性激活模式,其最早的心房激 活可出現在冠狀竇 (CS) 近端,甚至是二尖瓣環的下外 側部位。
3. 狹窄複合心動過速伴VA分離(V > A)
鑑別診斷包括那些不需要心房參與的心律失常機 制,這些是: 1) 房室結折返性心動過速 (AVNRT) ,伴 the upper common pathway的逆行阻滯;2)交界性心動過 速(JT),伴心房阻滯;3) 順行性NF/NV心動過速,伴心
房阻滯。
這種情況下的第一步是排除異位交界性心動過 速,方法是引入提前的希氏束不應期心房早搏 (PAC) 。 隨後,通過引入希氏束不應期 PVC 及 VOP 來區分 AVNRT 與 NV/NF 心動過速,不過第二步操作需要恢復 1:1的VA關係,這可通過異丙基腎上腺素(isoproterenol) 輸注來實現。在 AVNRT 或 JT 中,希氏束不應期 PVC 不 應影響下一次希氏束激活的時間;而希氏束不應期 PVC 提前、延遲下一次希氏束激活或終止心動過速則 提示存在NF/NV通路。如前所述,NF與NV心動過速可 通過穩定VOP誘導後是否出現QRS融合來區分。
此外,還有一些罕見情況需要提及。上隔分支性 室性心動過速(upper septal fascicular VT)可能表現為狹 窄複合心動過速,並且可以通過與竇性節律時相比較 短的 HV 間隔來快速區分。雙重發火型心動過速 (Double fire tachycardia)是由快速與緩慢的房室結傳導 路徑同時前向傳導所引起的一種罕見情況,表現為成 組搏動,並伴隨交替出現不同的RR間隔。
寬QRS波心動過速 (Wide Complex Tachycardias, WCT)
一般來說,寬 QRS 波心動過速 (WCT) 可能由以下 幾種情況引起:室性心動過速 (VT) 、伴異常傳導的室 上性心動過速(SVT)及伴預激的心動過速(見表2)。診斷 的第一線索通常來自 12 導極心電圖,典型的束支傳導 阻滯 (BBB) 圖形提示伴異常傳導的 SVT ,而非典型圖形 則暗示 VT 或伴預激的 SVT 。但有一些例外情況,如束 支折返性心動過速 (BBRT) 和經房束徑路徑的折返性心 動過速(AF-AVRT),這些情況可能會產生典型的BBB圖 形。接下來需要檢查心內電生理記錄中的房室 (AV) 及 希氏束 - 心室 (HV) 關係。如果不存在 1:1 的 AV 關係,可 以排除折返性心動過速,因為在這種情況下,心房和 心室都是心動過速迴路中的必要組成部分。若 QRS 波 之前未見到希氏束電位,也可以排除伴異常傳導的 SVT ,因為此時心室激活並不依賴於希氏 - 浦肯野系 統。在VT和伴預激的SVT中,HV間隔短或為負值;而 在伴異常傳導的SVT及BBRT中,HV間隔正常或延長(≥ 竇性節律 ) 。基於這些考量, WCT 可分為以下三種模 式:
1. 寬QRS波心動過速伴
VA分離
伴有 VA 分離的寬 QRS 波心動過速 (WCT) 幾乎在所 有情況下都是室性心動過速 (VT) 。然而,鑑別診斷時
也應考慮其他不涉及心房的心動過速,這些包括: 1) 伴異常傳導的 AVNRT ; 2) 伴異常傳導 (aberrancy) 的 JT;3) 伴異常傳導的NF/NV心動過速。
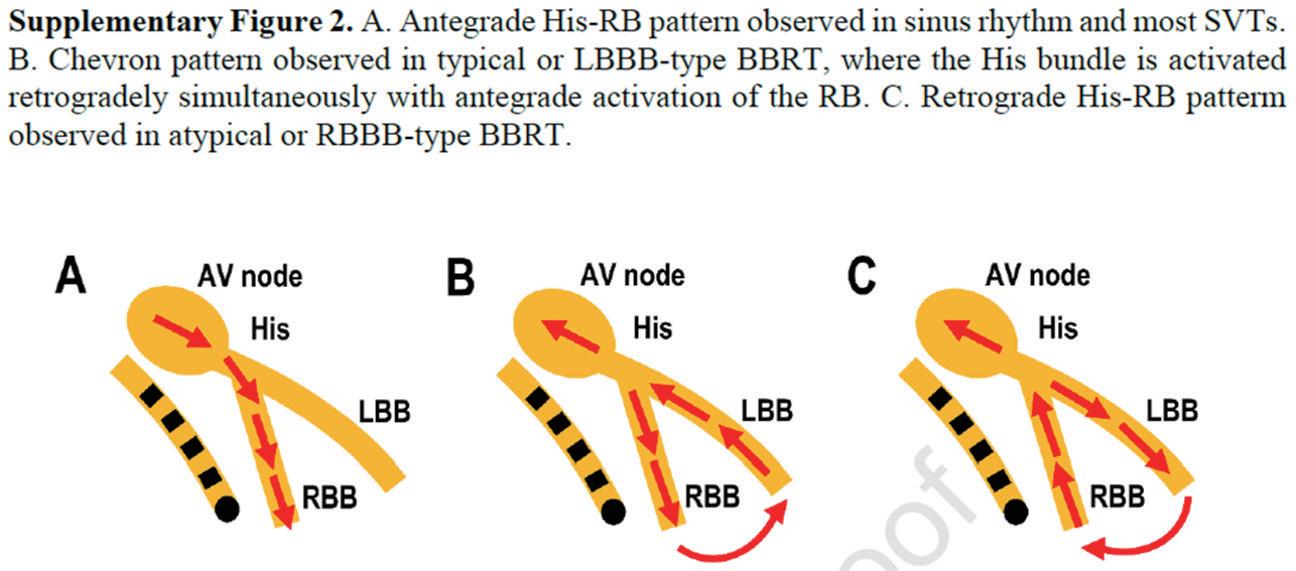
在這種情況下,希氏束電位的時間和激活順序對 於確定心動過速的機制至關重要。在心室性心動過速 ( 如心肌性 VT 或分支束 VT) 中, HV 間隔比竇性節律短或 為負值;而在 BBRT 、 AVNRT 、 JT 和 NF/NV 心動過速 中, HV 間隔應與竇性節律相等或更長。此外,希氏束 至右束支 (RB) 的激活順序在 AVNRT( 希氏束在 RB 之 前 ) 、 JT和NF/NV心動過速中為順行;而在心肌性VT和 BBRT 中則為逆行 (RB 在希氏束之前 ) 。然而,在典型或 左束支傳導阻滯 (LBBB) 型的 BBRT 中,由於 RB 的順行 激活和希氏束的逆行激活同時發生,可能會觀察到V 字 形模式(參見圖二)。
從右心室尖部的過度刺激也可以提供一些有關機 制的見解。如果過度刺激伴隨明顯的融合現象(manifest fusion) ,則可以排除 AVNRT 、 JT 和 NF 心動過速,因為 這些心動過速的迴路局限於希氏束 - 浦肯野系統。此 外,從右心室尖部刺激導致的短 PPI-TCL(<30 毫秒 ) 提 示束支折返性心動過速 (BBRT) ,但也可能見於源自右 心室的心肌性室性心動過速(VT)。
2. 寬QRS波心動過速伴有1:1房室傳導和短或 負HV間期
在1:1的寬QRS波心動過速中,短或負的HV間期提 示心室去極化不依賴於希氏束的激活,可能是因為迴路 局限於心室心肌,或是通過旁路(AP)傳導。因此,在此 情況下可能的心動過速機制包括心肌性 VT 或預激性 SVT,具體包括:1)逆行性房室折返性心動過速(AVRT) ;2) 伴隨AP的AVNRT;3) 伴隨AP的AT;4) 傳導徑對傳 導徑的心動過速 ( 雙折返性 AVRT ,順行通過一條 AV 徑,逆行通過另一條 AV 徑、 NF 徑或 NV 徑 ) 。然而,如 果房性激活呈現偏心性,鑑別診斷範圍就會縮小,因為 可以排除 VT 、逆行性 AVRT 和伴隨 AP 的 AVNRT 。這些 心律失常的QRS波形通常呈現非典型性右束支傳導阻滯 (RBBB) 或左束支傳導阻滯 (LBBB) ,但 atriofascicular pathways通常會產生典型的LBBB。
在這種情況下,一個有用的鑑別診斷手段是通過 AOP 進行心動過速的控制,刺激周期長度比心動過速 的周期短 20-40 毫秒。在房性起搏期間,如果 QRS 波形 發生變化,這提示可能為VT,原因是希氏束-浦肯野系 統的前向捕捉,或較不常見的是旁路的參與 ( 前者希氏 束提前,後者希氏束不變 ) 。此外,在停止起搏後出現
AVVA反應是心室性心動過速的特徵,因為心房的激活 由心室驅動,而出現 AVA 反應則提示為房室結折返性 心動過速 (SVT) 。需要強調的是,這些標準適用於心肌 性 VT ,但不一定適用於束支折返性心動過速 (BBRT) 或 fascicular VT。
排除VT後,下一步是確認是否存在AP並證明其可 能參與了迴路。這可以通過引入心房早期刺激來完成:
z 一個心房早期刺激(PAC)如果能終止心動過速而不使 心室去極化,則可以排除VT。如果在septum A波處 於不應期時發出 PAC(atrial electrogram in the His catheter is not advanced),而心動過速終止,這表明 可能為逆行性AVRT或AT。
z 一個 PAC 如果能提前下一次心室激活而不改變 QRS 波形,則可以排除心肌性VT。如果PAC 在septum A 波處於不應期時發出,下一次心室激活提前則表明 旁路的存在。如果心動過速被重置,則旁路是心動 過速的關鍵組成部分 ( 排除 VT 以及伴隨 AP 的 AVNRT 或 AT) 。如果隨後的心房激活提前而不影響逆行的 希氏束,心房激活序列偏心或希氏束不應激的 PVC 提前並重置心動過速,則懷疑為雙傳導性心動過 速。如果晚期 PAC 延遲了下一次心室激活並重置了 心動過速,則表明使用atriofascicular pathway的逆行 性AVRT。
z 一個 PAC 如果提前下一次心室激活並改變 QRS 波 形,可能是 VT( 希氏束提前 ) 或 a bystander AP( 希氏 束不變 ) 。
3. 寬QRS波心動過速伴有1:1房室傳導和正常 或長的HV間期
大多數這種情況下的心動過速對應於伴有傳導異 常的SVT(SVT with aberrancy),但伴有1:1房室傳導的 BBRT也是一個罕見的可能性(大多數BBRT表現為VA分 離)。在伴異常傳導的SVT中,HV間隔表示從希氏束到 心室的實際傳導時間;而在BBRT中,HV間隔是一個偽 間隔,這是由希氏束逆行傳導和右束支順行傳導所致。
如前所述,希氏束 - 右束支的逆行或“ V ”形激活 模式,以及從RV apex entrainment下的PPI-TCL < 30毫 秒,強烈暗示有 BBRT 。如果在 BBRT 期間記錄右束支 和左束支的電位,激活序列應與涉及希氏 - 浦肯野系統 的宏觀折返一致(左束支傳導阻滯模式下為希氏束-右束 支 - 左束支,右束支傳導阻滯模式下為希氏束 - 左束支右束支 ) 。 AOP 在這種情況下無助於區分 SVT 伴異常傳 導和 BBRT ,因為兩者都可能表現出在刺激過程中 QRS 波形不變並伴有AVA反應。
一旦排除了 BBRT ,具體的 SVT 機制可以通過標準 操作來診斷,包括希氏束不應期的PVC。
結論
逐步應用刺激操作是心動過速電生理評估中的必要 步驟,無論診斷看起來多麼明顯,都應該進行。遵循有 條理的方法可能有助於診斷一些非典型的心律失常或異 常表現。NCT和WCT的建議流程圖見(圖三)和(圖四)。
References:
Enriquez A, Gonzalez R, Kumareswaran R, et al Electrophysiologic diagnosis of narrow and wide complex tachyarrhythmias. Heart Rhythm. 2024 May 10:S1547-5271(24) 02552-9.
(圖一)
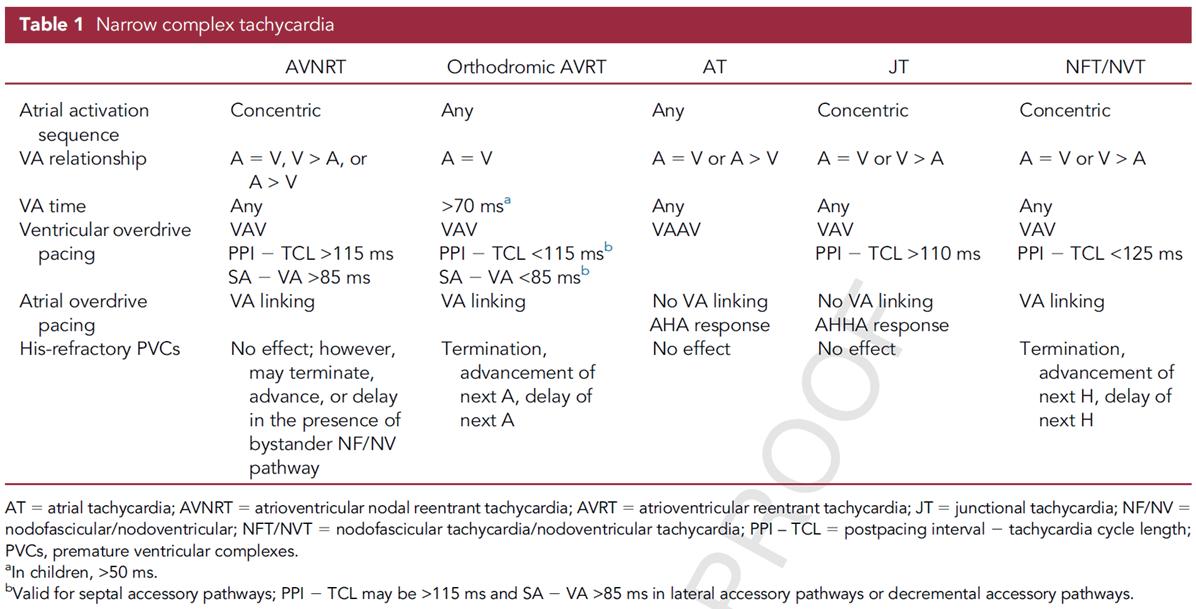
表1)
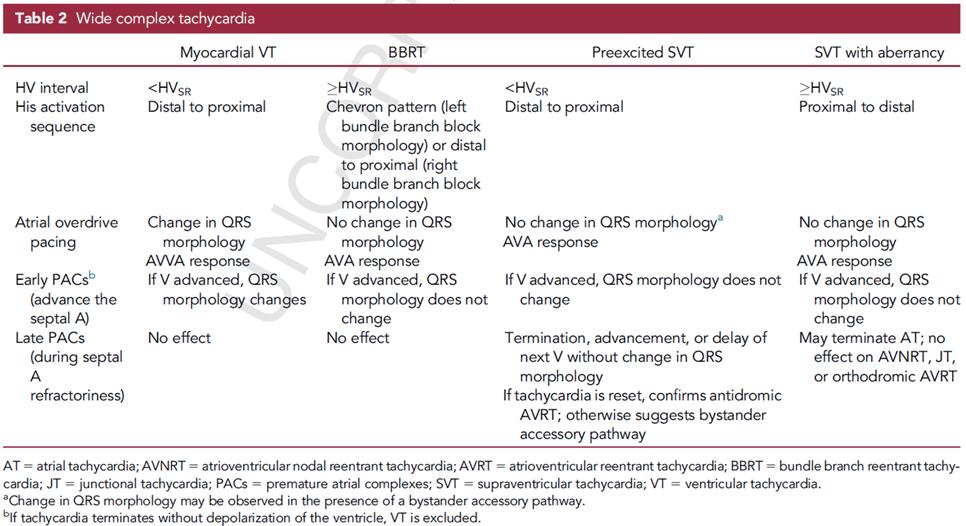
表2)
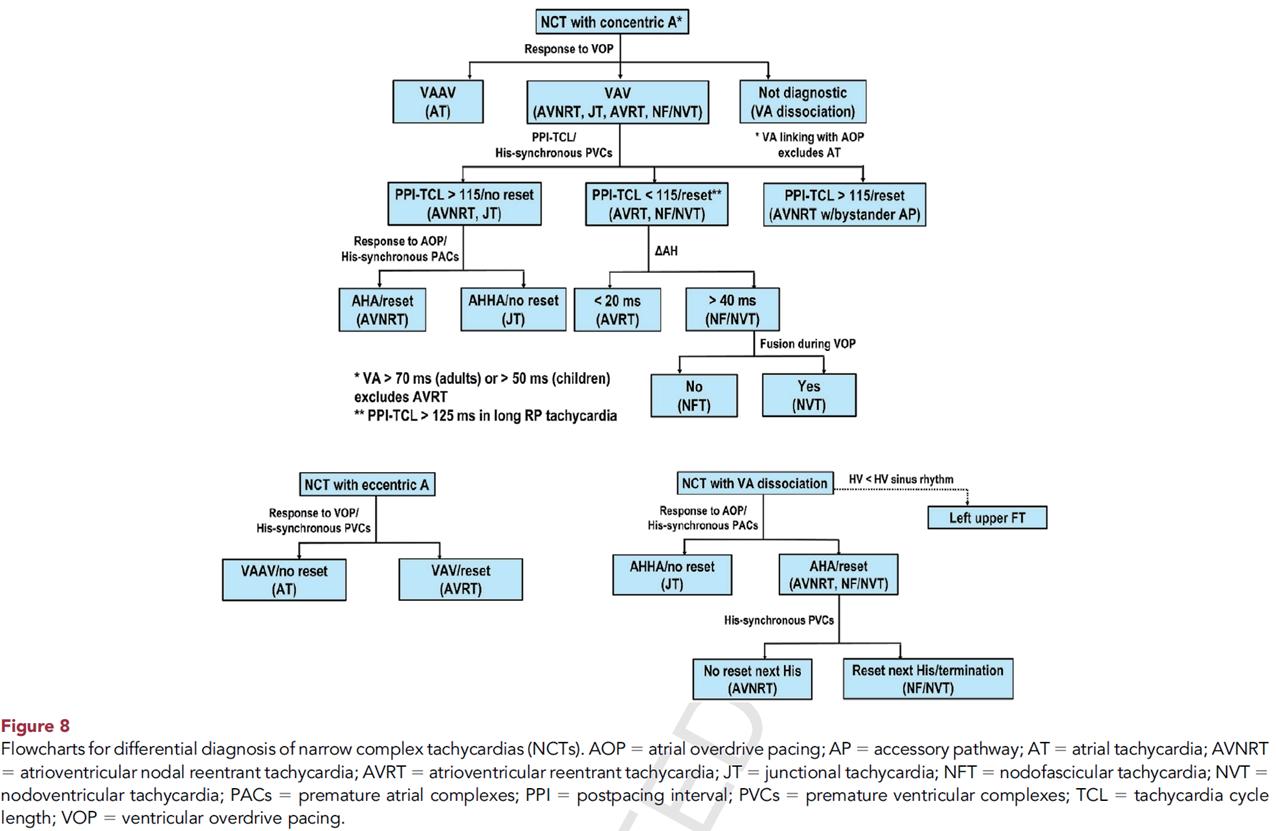



(圖四)
Incremental Benefit of Stepwise Non-pulmonary Vein
Trigger Provocation During Catheter Ablation of Atrial Fibrillation (逐步非肺靜脈觸發之誘發方式在心房顫動 導管消融中的增量效益)
亞東紀念醫院心臟血管內科 張基業醫師
– 本研究探討了非肺靜脈觸發(non-PV trigger)在心房顫 動(AF)中的重要性,並評估了逐步誘發方法的增量效 益。
– 過去的方法主要依賴 spontaneous trigger ,但許多 non-PV trigger 需要誘發才能被識別,這使得其檢測 變得困難。
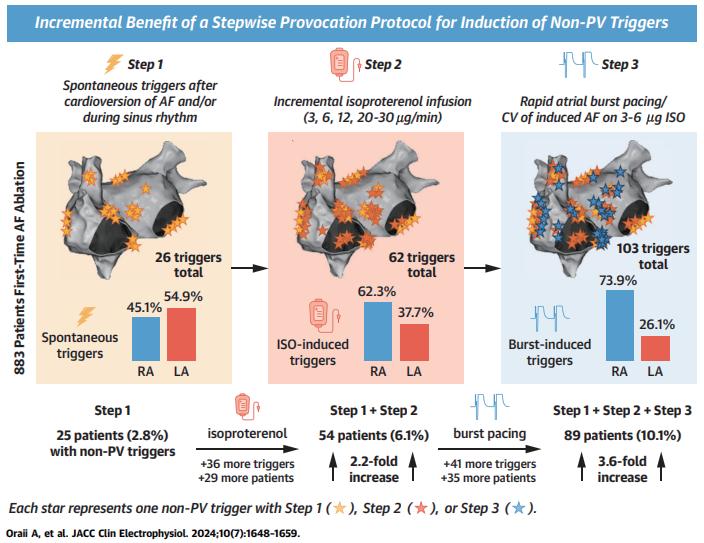
– 本研究提出了一個包括異丙腎上腺素(isoproterenol)注 射和 rapid burst pacing 刺激的 Stepwise Provocation Protocol,以提高non-PV trigger的識別率。
研究設計
此研究前瞻性使用賓州大學附設醫院的 AF 消融登
記系統中所有接受 AF 消融術患者的詳細臨床及程序數 據。研究包括所有在 2020 年1 月至 2022 年12 月之間進行 首次AF消融的成年患者,並排除有心臟移植或外科AF 消融病史的患者。
non-PV trigger定義為引發持續或非持續性AF的心 房早期去極化 (APDs) 或持續的心房頻脈 (AT) 。 AVNRT 和 AVRT 也被視為 non-PV trigger 。然而, macroentry flutter和未能引發AF的單獨頻繁non-PV APDs不被認為 是non-PV trigger。
Stepwise Provocation Protocol
進行首次 AF 消融的患者通常在心臟內超音波 (Intracardiac echocardiography, 簡稱ICE)和X光透視引導 下兩根十極導管在ICE和透視引導下放置,其中一根位 於冠狀靜脈(CS),另一根放置在crista terminalis(CT)上( 最遠端電極延伸至上腔靜脈),以促進non-PV trigger的 明確區域化。之後進行兩次 transseptal puncture ,使多 電極 mapping catheter 和接觸力感測灌流消融導管進入 左心房。在全身麻醉下,患者進行 electroanatomical mapping(EAM),隨後對肺靜脈進行環狀隔離術(PVI)。 在確認PV entrance and exit block後,把多電極mapping catheter 會放置於後壁,消融導管置於左上肺靜脈內, 進行有明確定義的誘發性動作,以識別non-PV trigger。
一旦確認non-PV trigger的位置,multielectrode mapping catheter 和消融導管會移動到可疑的區域進行更詳細的 標測。
步驟簡述
1. 自發性non-PV trigger:在竇性心律下監 控自發性觸發源。
2. 增量異丙腎上腺素 (isoproterenol) 注射: 根據血液動力學和心率反應增量增加異 丙腎上腺素的注射劑量,同時監測患者 的反應。異丙腎上腺素注入步驟需要約 20 分鐘(每個 3、 6、12 和 20-30 mg/min 的注射速率為 3-5 分鐘)
3. 快速心房起博和程序性心房刺激:以 180~250msec 的 cycle length 進行 15 次快 速心房起博以觸發心房顫動或持續性非 肺靜脈心房心跳的誘發。
4. 對誘發的non-PV trigger進行定位和消融。 burst pacing步驟需要約 5 至 10 分鐘。
完整的逐步誘發方案會使總的手術時間增加約 30 分鐘。若誘發到 non-PV trigger ,則需要額外的時間。 另外,根據操作醫師的判斷,部分患者也會接受多次 推注腺苷(adenosine, dosage: 6-18 mg),以排除dormant PV conduction 的存在,然後再繼續進行 non-PV trigger Provocation Protocol。
結果及討論
本研究首次專門調查了在首次心房消融中,逐步 誘發方案對 non-PV trigger 的實用性和增益效果。主要 發現包括:
1. 只有三分之一的非肺靜脈觸發在 Baseline 時表現出 來,其餘需要進行誘發操作才能引發;
2. 實施逐步誘發方案,包括逐漸增加劑量的異丙腎上 腺素注入,隨後進行快速心房突發起搏 / 程式刺激以 及在異丙腎上腺素 infusion 或 washout 期間進行的 electrical cardioversion,結果顯示識別出非肺靜脈觸 發的患者數量增加了大約 3.6 倍;
3. 較多trigger來自右心房結構,而不是左心房結構。
根據此誘發方案所執行的步驟, burst pacing 所帶 來的效益,主要是更能發現持續心房陣動的 non-PV trigger 。把 burst pacing 作為誘發方案的最後一個選擇 可能低估了 burst pacing 的潛在益處。研究意外發現腺 苷注射可發現少數non-PV trigger,而腺苷誘發的trigger 在異丙腎上腺素下無法重現的情況,支持不同誘發操 作對不同心房區域影響不一的假設。以往文獻也有發
現右心房心肌細胞對腺苷的敏感性更高。儘 管腺苷注射對 non-PV trigger 的誘導有益,與 異丙腎上腺素或 burst pacing 操作相比,其附 加價值有限。
研究限制:目前沒有一個GOLD STANDARD 來誘導所有潛在的觸發,無法評估此操作對 識別 non-PV trigger 的敏感性。一部分患者因 病況並未接受完整的逐步誘發方案,這可能 低估了 non-PV trigger 的流行率。研究也並沒 有系統性檢測心房顫動觸發的reproducibility。 最後,腺苷注射並不是觸發誘發方案的一部 分,而是由操作者自行決定,用於評估潛伏 的 non-PV trigger 。儘管研究對 ADENOSINE 施用的附加價值提供了一些見解,但其對非 肺靜脈觸發誘導的實用性還需在未來的研究 中進一步探討。
結論
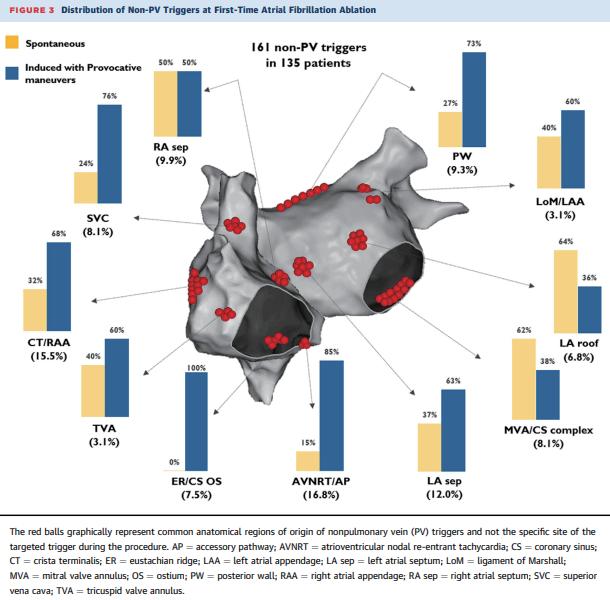
在接受首次 AF 消融治療的患者中,觀察到的大多數 non-PV trigger 需要進行 induction 才能被識別。由漸進式 異丙腎上腺素注射隨後進行 rapid atrial burst pacing 所組成的逐步 trigger 誘發方案,可以使識別到non-PV trigger的 患者數量增加3.6倍。右心房是較為常見的non-PV trigger。通過系統性induction,約10%的患者在首次AF消融期間被 發現有non-PV trigger 觸發因素。
Reference:
Oraii A, Chaumont C, Rodriguez-Queralto O, et al. Incremental Benefit of Stepwise Nonpulmonary Vein Trigger Provocation During Catheter Ablation of Atrial Fibrillation. JACC Clin Electrophysiol. 2024 Jul;10(7 Pt 2):1648-1659
運用左束支電刺激的心臟再同步化治療 –
現今證據與未來展望
Left Bundle Branch Pacing for Cardiac Resynchronization
Therapy: Current Evidences and Further Perspectives
長庚醫療財團法人高雄長庚紀念醫院心臟內科 陳煌中醫師
前言
嚴重心衰竭 (heart failure, HF) 的病人,在接受最佳的藥物治療 3 到 6 個月後,左心室射出率 (left ventricular ejection fraction, LVEF) 仍然小於等於 35% ,合併左束支傳導阻斷,且仍有相關症狀 ( 定義為紐約心臟協會功能
分級 II–IV 級 ) 者,心臟再同步化治療 (cardiac resynchronization therapy, CRT) 是一種發展超過 30 年且成熟的治 療策略。
傳統 CRT 的做法,是從冠狀靜脈竇在左心室心外膜置放一根左心室導線,達成雙心室再同步化收縮 (Biventricular pacing, BiVP) ,儘管多項研究已顯示 BiVP-CRT 可改善生活品質和心臟功能,減少相關心衰竭再 住院率及全因死亡率 [1] ,但還是有需多缺陷存在,包括左心室導線置放失敗 ( 約 3-4%) 、膈神經刺激 ( 約 40%) , 及日後刺激閾值上升 [2] 。然而,有高達 20% 至 30% 的病人裝置 CRT 後無反應 (non-responder) [3] ,主要歸因於 BiVP-CRT 繞過了傳導系統 (conduction system) ,只對左心室心肌做非生理性的刺激;另外,冠狀靜脈竇分支 解剖結構的變異性,及其所限制的電刺激部位,也是治療後無反應重要的原因。
然而, BiVP-CRT 的這些限制,促使了生理性傳導系統電刺激的研究。在西元 2000 年, Deshmukh 等人 [4] 首 次發表希氏束電刺激 (His bundle pacing, HBP) ,對於持續性心房顫動的心衰竭病人有顯著的臨床改善。然而, 其主要缺點包括:導線閾值不穩定和脫落、裝置學習曲線長、長時間的輻射線透視,和早期電池耗損等,阻 礙了 HBP 的後續發展。在西元 2018 年,溫州醫科大學附屬第一醫院的黃偉劍醫師,將導線往下位移並穿進左 心室中膈,成功發展出左束支電刺激 (left bundle branch pacing, LBBP) 的技術 [5] ,之後陸續研究顯示 LBBP 可以 克服 HBP 的許多限制,並有長期穩定的導線參數。現今,各國專家學者已發展出許多實現 CRT 的電刺激技術 ( 圖一 ) [6] 。
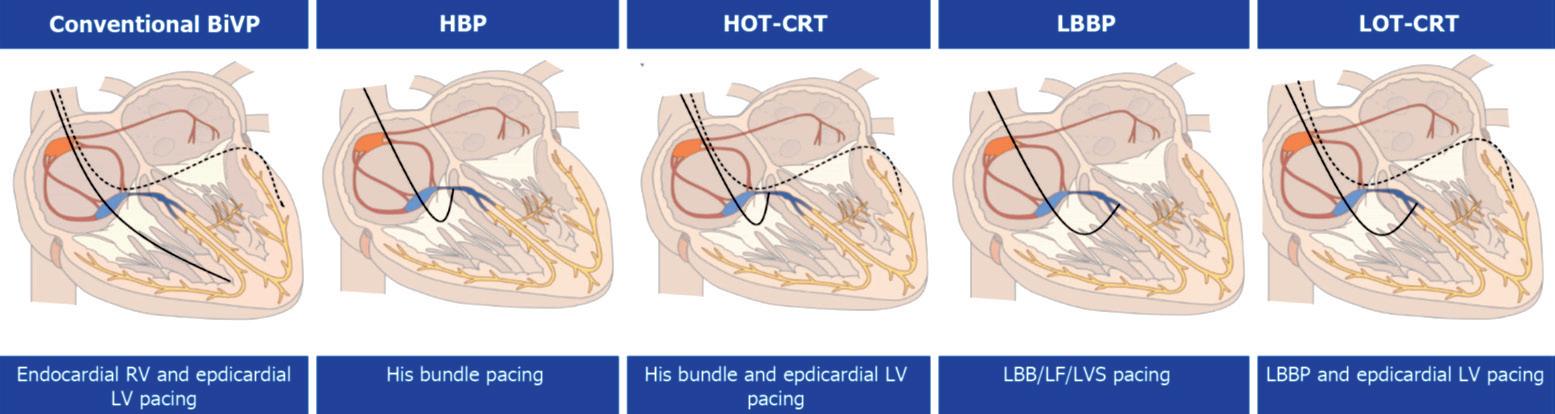
(圖一)、 各種實現心臟再同步化治療(CRT)的電刺激技術[6]。
BiVP:雙心室電刺激;HBP:希氏束電刺激;HOT-CRT: 希氏束優化心臟再同步治療;LBBP: 左 束支電刺激;LF: 左束支分支;LOT-CRT: 左束支優化心臟再同步治療;LVS: 左心室中膈
現今證據與治療指引的建議
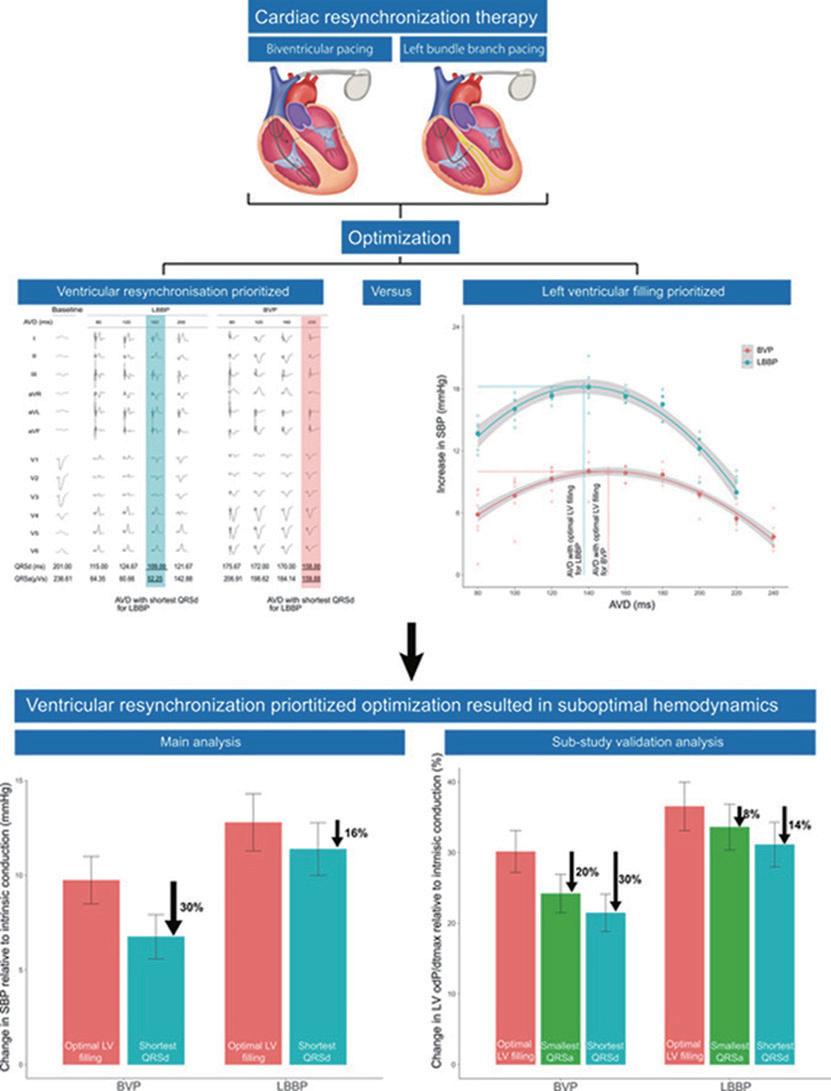
在談論現今證據之前,首先要認識這個有廣泛定義的名詞:左束支區域電刺激(left bundle branch area pacing, LBBAP),包括選擇性LBBP、非選擇性LBBP、和左心室中膈電刺激(left ventricular septal pacing, LVSP) 。由於電刺 激的閾值和重新再同步的效果差異只有很細微的差異,這些術語經常在文獻中被交替使用。早期研究結果顯 示, LBBP-CRT 在心臟血行動力學和改善心臟功能方面至少與 BiVP-CRT 一樣有效。然而,現階段的證據大多 是觀察性的,僅有一項小型隨機分派臨床試驗比較了 LBBP-CRT 和 BiVP-CRT ,結果顯示 LBBP-CRT 在非缺血 性心肌病和左束支傳導阻斷的心衰竭病人中,比 BiVP-CRT 有更顯著的 LVEF 改善 [7] 。
相對來說,目前最有證據力的文獻是由美國 Vijayaraman 醫師等人所發表的大規模觀察性研究 [8] ,收集來 自全球 15 個醫學中心的 1778 名病人,其中 797 位接受了 LBBAP-CRT , 981 位接受了 BiVP-CRT ,平均年齡為 69 ± 12 歲, 32% 為女性,平均 LVEF 為 27% ± 6% 。 LBBAP-CRT 的 pacing QRS 寬度顯著比 BiVP-CRT 短 (128 ± 19 ms vs. 144 ± 23ms, P < 0.001) ;改善 LVEF 顯著大於 BiVP-CRT(13% ± 12% vs. 10% ± 12%, P < 0.001) ;在多 變量回歸分析中,LBBAP-CRT顯著降低主要療效指標(心衰竭再住院率及全因死亡率)(20.8% vs. 28%;HR : 1.495 ; 95% CI : 1.213-1.842 ; P < 0.001) 。由此結果,作者得出結論, LBBAP-CRT 可作為 BiVP-CRT 有效的替代療 法。另外,提供綜述文獻也整理出目前 LBBAP-CRT 與 BiVP-CRT 比較的觀察性研究結果 ( 圖二 ) [9] 。
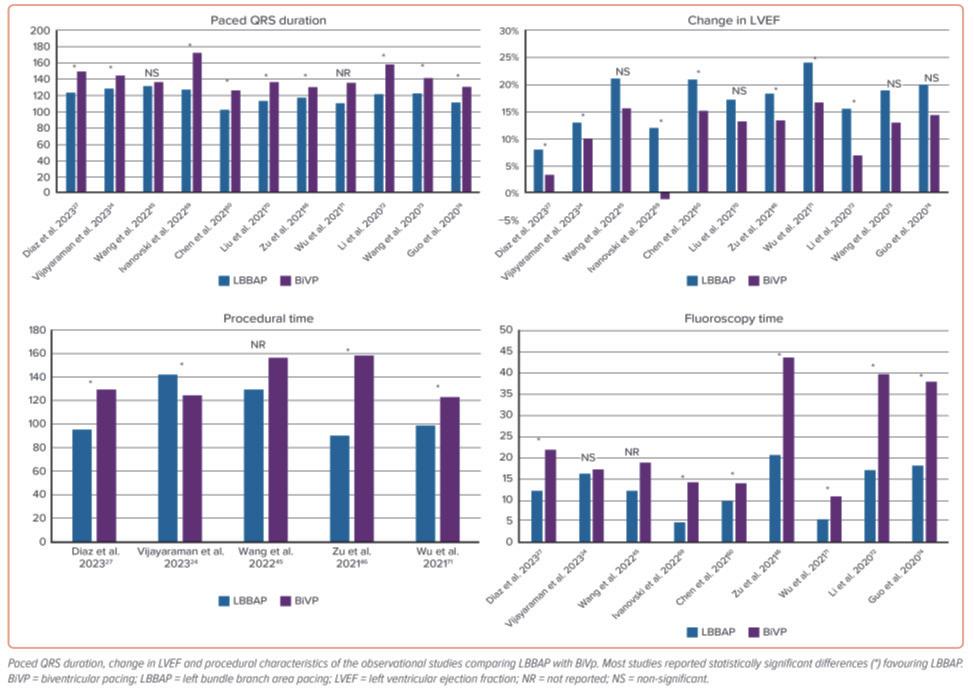
(圖二)、 左束支區域電刺激(LBBAP)與雙心室電刺激(BiVP)的觀察性研究比較[9]。
最近由 Yasmin 等人發表的綜合分析中 [10] ,包含了 6 篇文獻 (1 項隨機分派臨床試驗和 5 項比較觀察性研究 ) , 收錄共 389 名病人,其中 159 人接受 LBBP-CRT , 230 人接受 BiVP-CRT 。該研究結果顯示, LBBP-CRT 在改善 LVEF 、心臟腔室大小、導線閾值以及紐約心臟協會功能分級方面優於 BiVP-CRT 。此外, LBBP-CRT 組在追蹤 期間,相較於 BiVP-CRT ,有顯著降低的 NT-ProBNP 濃度。本篇作者推論, LBBP-CRT 的優勢可能源於較低的 pacing QRS 寬度 (LBBP-CRT 115.4ms vs BiVP-CRT 138.0ms; P < 0.00001) ,以達成更有效的心臟再同步和心臟 收縮,研究結果可能增強 LBBP 運用在 CRT 的證據。儘管目前有正向的分析結果,但仍需謹慎對待。首先,該 綜合分析主要基於觀察數據,這些數據本身容易受到選擇偏倚的影響,可能掩蓋了 LBBP-CRT 組中的一些異常 情況。此外,內文唯一隨機對照試驗僅包含 40 名病人,追蹤時間也只有 6 個月。另外,所有研究均來自中國, 因此結果的普遍適用性尚待確定。還有, LBBP-CRT 的長期導線耐久性尚未確立,須觀察導線植入在心室中隔 長期受到機械壓力後,會不會造成導線斷裂。
儘管現今對 LBBP-CRT 的證據有逐漸增加,但仍迫切需要進行更大規模的研究已證實其療效。到目前為 止,有 4 個大規模的隨機分派臨床試驗正在進行中 ( 圖三 ) [6] ,靜待後續其發表相關成果。
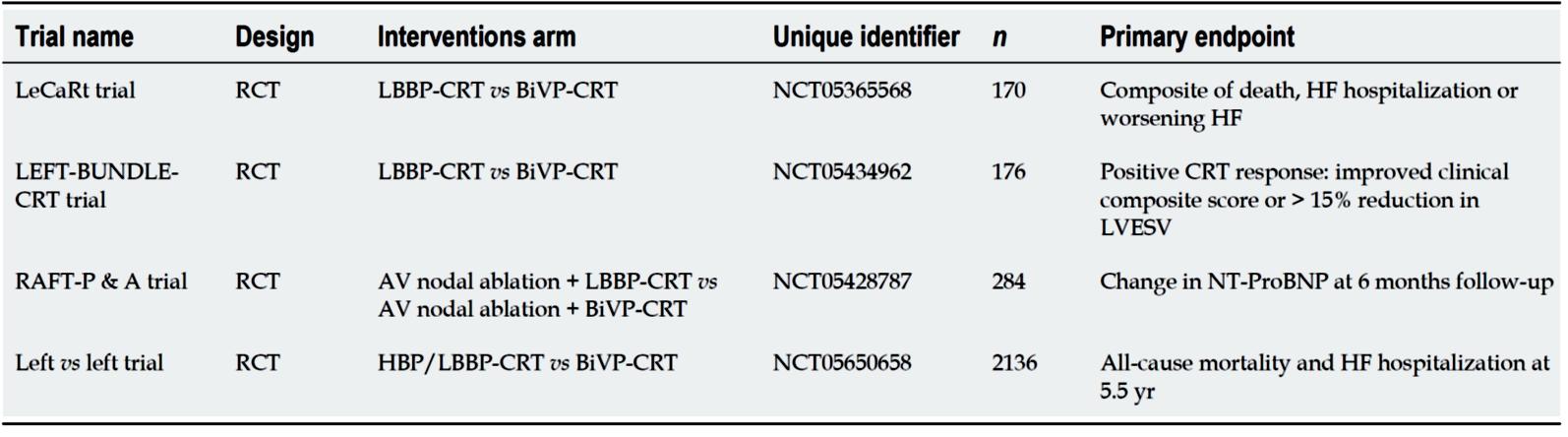
(圖三)、 目前正在進行比較LBBAP-CRT和BiVP-CRT臨床結果的隨機分派臨床試驗[6]。
有關於治療指引的建議,在西元 2023 年,美國 心律學會 / 亞太心律學會 / 拉丁美洲心律學會共同發表 的治療指引,裡面指出無法成功實施 BiVP-CRT 的心 衰竭病人,執行 LBBP-CRT 給予了 2a 等級的推薦。另 外,作為 BiVP-CRT 的替代方案, LBBP-CRT 也被給 予了 2b 等級的推薦。 [11]
達成左束支區域電刺激(LBBAP)的條件
根據文獻,在心衰竭病人成功刺激到左束支的成 功率可達 82%-84% 。最新的傳導系統心臟節律器植入 共識 [12] 提到,如果滿足下列標準中的任何一項則是 LBBP : (1) 在閾值測試時, QRS 型態會過渡到 LVSP 或 選擇性LBBP;(2)V6RWPT <80 ms(在LBBB病人);(3) V6-V1 interpeak interval >44 ms ; (4) 在 programmed stimulation 時, QRS 過渡到選擇性 LBBP 。如果病人的 V6RWPT <100 ms( 在 LBBB 病人中 ) 、 V6-V1 interpeak interval >33 ms 、在 programmed stimulation 時過渡到 LVSP 、或在閾值測試期間 QRS 過渡伴隨 V6RWPT 1014 ms,則病人可能具有LBBP。
不符合上述標準但在 V1 導程有 R 波者,則考慮是 LVSP 。雖然 LVSP 並不直接激活傳導系統,但通過刺 激左心室中膈,產生幾乎同時的兩側心室激活來顯 著減少總心室激活時間。然而,與 LBBP 相比, LVSP 與 V5-V6 的左心室激活時間顯著延長,以及 pacing QRS 寬度較寬,這可能會導致左心室同步性下降。
最新文獻顯示 [13] ,在 259 位心衰竭病人 (68 位 LBBCRT 、 38 位 LVSP-CRT 、 153 位 BiVP-CRT) ,與 BiVP 和 LVSP 相比, LBBP 顯著降低了主要終點的風 險。 LVSP 的調整後全因死亡風險顯著高於 BiVP ,而 LBBP 和 BiVP 之間的風險相當。傾向分數配對後也看 到類似的結果,後續仍需進一步研究以確認這些初
步結果。
總結
目前證據顯示, LBBP 已經成為 CRT 中一個強而 有力替代 BiVP 的方案。 LBBP-CRT 通過生理性刺激 心臟傳導系統所帶來的理論優勢,逐漸在許多文獻 看到比 BiVP-CRT 較好的臨床結果。然而,儘管支持 LBBP-CRT 的證據不斷增加,但仍受限於觀察性研 究。因此,需等候更大規模的隨機分派臨床試驗發 表正向的結果,未來 LBBP 才能站穩在 CRT 中的角 色。
References:
1. Cleland JG, Daubert JC, Erdmann E, et al; Cardiac Resynchronization-Heart Failure (CARE-HF) Study Investigators. The effect of cardiac resynchronization on morbidity and mortality in heart failure. N Engl J Med. 2005 Apr 14;352(15):1539-49.
2. McAlister FA, Ezekowitz J, Hooton N, et al. Cardiac resynchronization therapy for patients with left ventricular systolic dysfunction: a systematic review. JAMA. 2007 Jun 13;297(22):2502-14.
3. Naqvi SY, Jawaid A, Goldenberg I, Kutyifa V. Non-response to Cardiac Resynchronization Therapy. Curr Heart Fail Rep. 2018 Oct;15(5):315-321.
4. Deshmukh P, Casavant DA, Romanyshyn M, et al; Permanent, direct His-bundle pacing: a novel approach to cardiac pacing in patients with normal His-Purkinje activation. Circulation. 2000 Feb 29;101(8):869-77.
5. Huang W, Su L, Wu S, et al. A Novel Pacing Strategy With Low and Stable Output: Pacing the Left Bundle Branch Immediately Beyond the Conduction Block. Can J Cardiol. 2017 Dec;33(12): 1736.e1-1736.e3.
6. Batta A, Hatwal J. Left bundle branch pacing set to outshine
biventricular pacing for cardiac resynchronization therapy?
7. Wang Y, Zhu H, Hou X, et al; LBBP-RESYNC Investigators. Randomized Trial of Left Bundle Branch vs Biventricular Pacing for Cardiac Resynchronization Therapy. J Am Coll Cardiol. 2022 Sep 27;80(13):1205-1216.
8. Vijayaraman P, Sharma PS, Cano Ó, et al. Comparison of Left Bundle Branch Area Pacing and Biventricular Pacing in Candidates for Resynchronization Therapy. J Am Coll Cardiol. 2023 Jul 18;82(3):228-241.
9. Diaz JC, Duque M, Aristizabal J, et al. The Emerging Role of Left Bundle Branch Area Pacing for Cardiac Resynchronisation Therapy. Arrhythm Electrophysiol Rev. 2023 Dec 1;12:e29.
10. Yasmin F, Moeed A, Ochani RK, et al. Left bundle branch pacing vs biventricular pacing in heart failure patients with left bundle branch block: A systematic review and metaanalysis. World J Cardiol. 2024 Jan 26;16(1):40-48.
11. Chung MK, Patton KK, Lau CP, et al. 2023 HRS/APHRS/ LAHRS guideline on cardiac physiologic pacing for the avoidance and mitigation of heart failure. J Arrhythm. 2023 Aug 2;39(5):681-756.
12. Burri H, Jastrzebski M, Cano Ó, et al. EHRA clinical consensus statement on conduction system pacing implantation: endorsed by the Asia Pacific Heart Rhythm Society (APHRS), Canadian Heart Rhythm Society (CHRS), and Latin American Heart Rhythm Society (LAHRS). Europace. 2023 Apr 15;25(4):1208-1236.
13. Zhu H, Qin C, Du A, et al. Comparisons of long-term clinical outcomes with left bundle branch pacing, left ventricular septal pacing, and biventricular pacing for cardiac resynchronization therapy. Heart Rhythm. 2024 Aug;21(8): 342-1353.
A 50-year-old
female with a short RP tachycardia
臺北榮民總醫院心臟內科 吳政億醫師
一位 50 歲女性, 6 年前開始有心悸的症狀。病患沒 有先天性心臟疾病。因為近日心悸頻發,所以來到門 診求診。做了 12 導程心電圖並沒有看到特別的異常 ( 圖 ) 。超音波檢查結果顯示心臟結構以及心室收縮率均 正常。Event recorder則是檢測出short RP tachycardia, 心跳介於 120 到 150bpm( 圖二 ) 。經解釋後病患希望接受 心導管電生理檢查並電燒處理。診斷管放置位置如 ( 圖 三 ) , retrograde 傳導測試發現 VA 傳導功能差, RVS1S1 無法達到VA 1 to 1,VERP則是250ms。Anterograde傳 導測試發現dual AV conductive property;fast AV 1 to 1
是 750ms , slow AV 1 to 1 為 500ms , AV fast ERP 為 680ms , AV slow 1 ERP 為 320ms , AV slow 2 ERP 為 300ms 。 pacing 誘發測試無法誘發 tachycardia ,所以我
們加上 isuprel 併作誘發測試。但加上 isuprel 後 VA 傳導
功能仍然不佳,而且也仍然無法誘發 tachycardia 。 於是加上了 atropine 測試;加了 atropine 後 long RP tachycardia 被誘發,速度為到 120-140bpm 和臨床表現 相符。此時V pacing仍然顯示VA dissociation,A pacing可 知delta AH為6,且比較心電圖可見SR時II、aVL為+, III 、 V1 為 +/- , tachycardia 時 II 、 III 為 + , aVL 為 flat , V1為+(圖四)。由以上特徵推測為atrial tachycardia(AT)。 因此使用 3D 定位找出 AT 最早的位置在上腔靜脈 (SVC) 的 anteroseptal area( 圖五 ) 。在使用 RF 45W 50C 160 seconds 後, AT 便無法誘發,術後也未曾復發。最後的 診斷為 anterosetpal SVC atrial tachycardia with slow pathway ;由於患者發作的時候, anterograde 傳導跳到 了 slow pathway ,所以 event recorder 的心電圖表現為 short RP tachycardia。
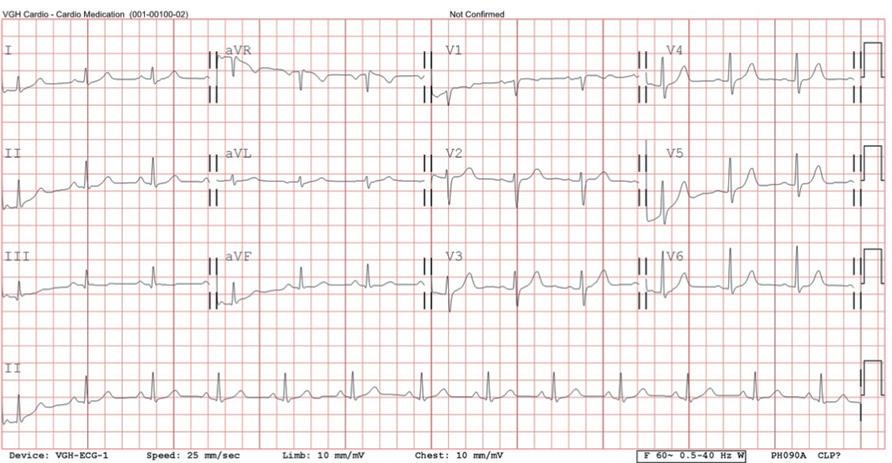
(圖一) ECG
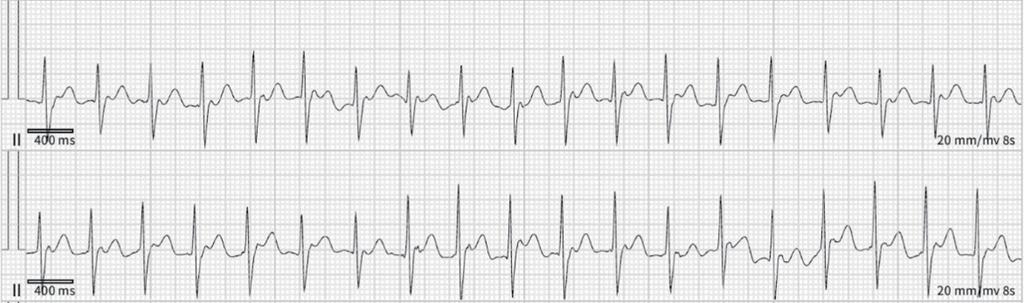
(圖二) event recorder記錄到的short RP tachycardia。箭頭所指為p wave
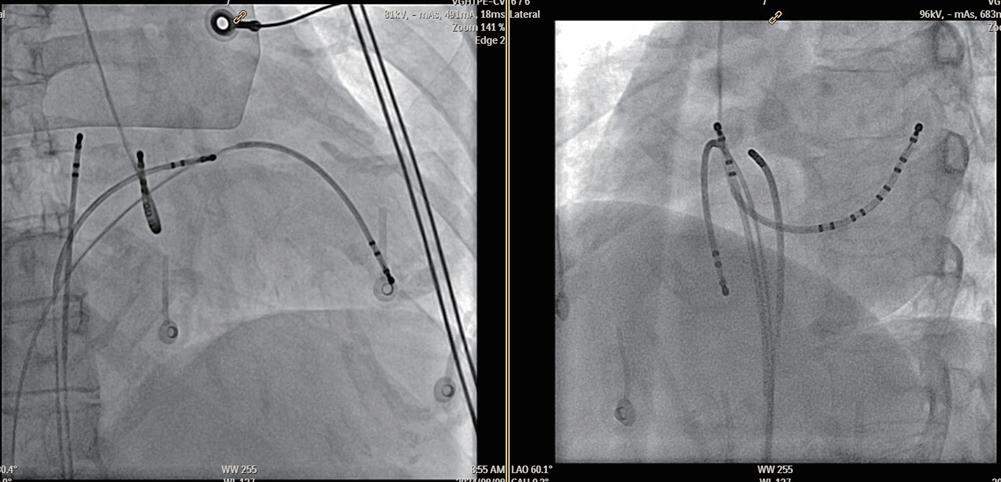
(圖三) 診斷管放置的位置
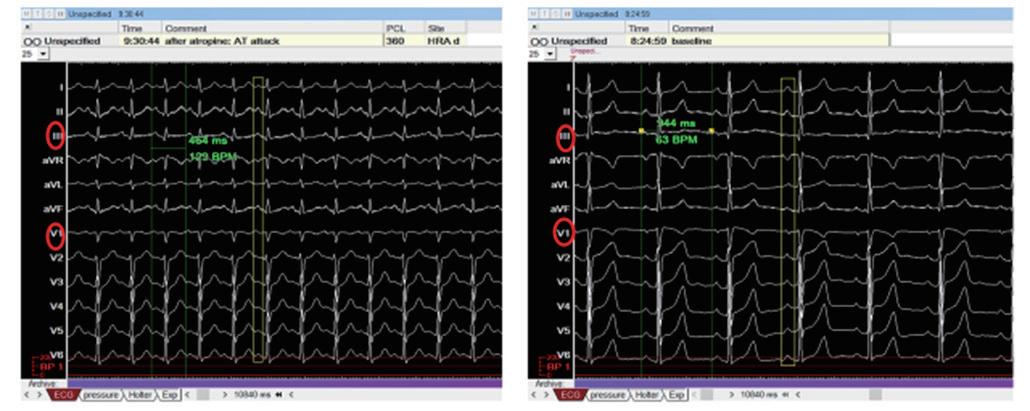
(圖四) 左側為tachycardia,右側為SR
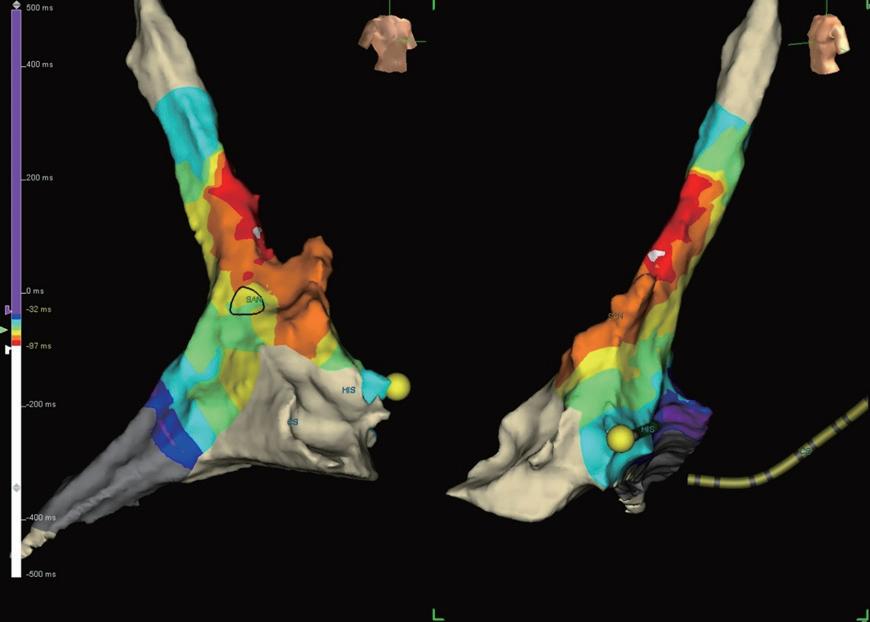
(圖五) AT發作的位置如白色點所示,黑色圈為sinus node