Arrhythmia News
發行人: 曹玄明 (Hsuan-Ming Tsao)
發行單位: 中華民國心律醫學會
(Taiwan Heart Rhyrhm Society)
地址: 100506台北市中正區忠孝西路一段50號25樓之18
本期摘要
P1. 脈衝消融手術的簡介
P3. ESC指南: 心室性心律不整管理與預防突發性 心臟死亡
P6. 人工智慧在心房顫動電燒手術的進展
(The Advance of AI in Catheter Ablation of Atrial Fibrillation)
P9. 脈動新聞
電話: 傳眞: 網址: ISSN: 2223-0130
886-2-23821530
886-2-23821528
www.thrs.org.tw
總編輯
洪元 Yuan Hung 林文裕 Wen-Yu Lin
本期主編
劉京翰 Ching-Han Liu 黃彥彰 Yen-Chang Huang
編輯
潘國利 Kuo-Li Pan 許竹佑 Chu-Yu Hsu
黃鼎鈞 Ting-Chun Huang 莊再庚 Chye-Gen Chin
鄭文涵 Wen-Han Cheng 黃冠智 Kuan-Chih Huang
黃世鐘 Shih-Chung Huang
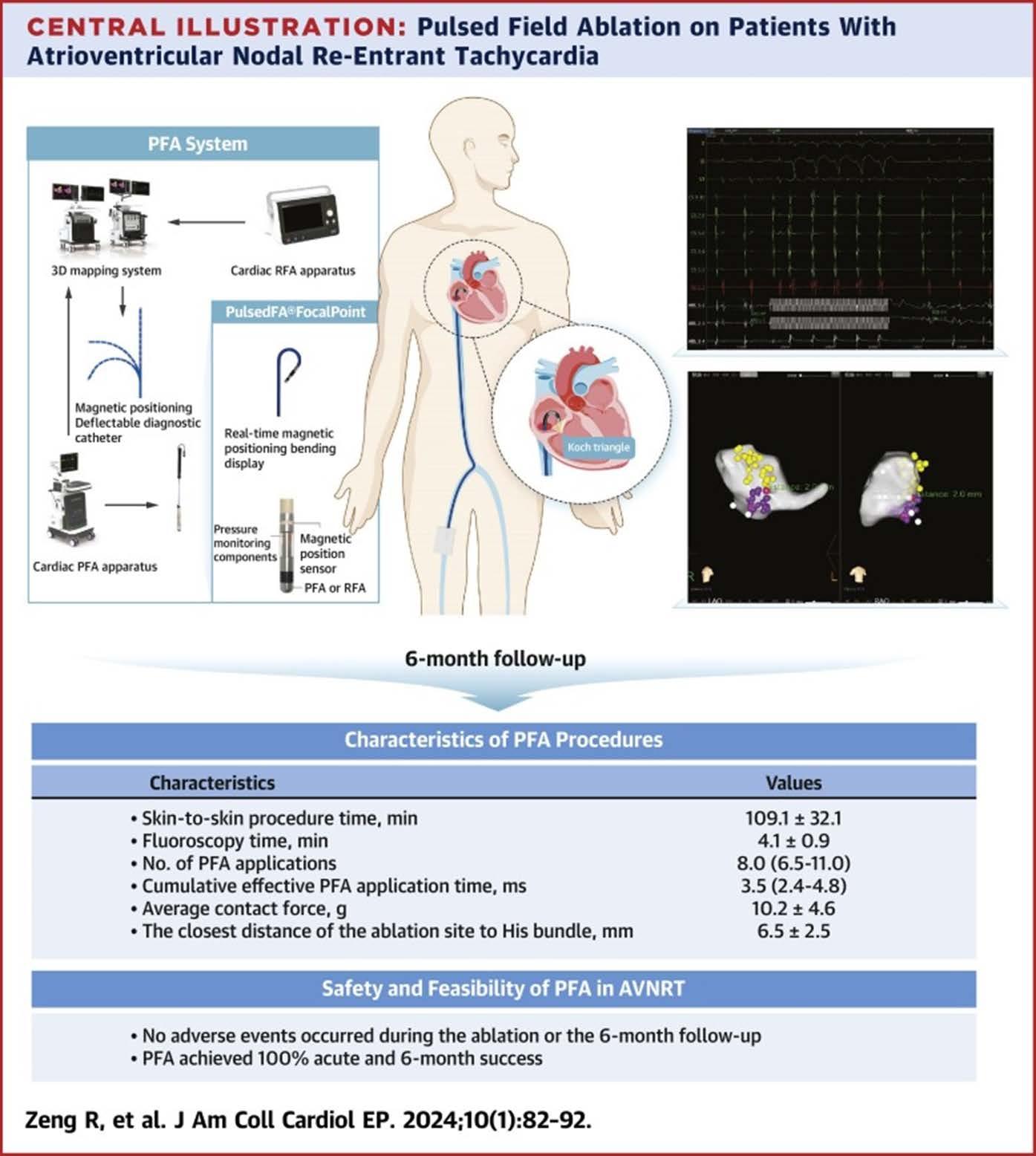
脈衝消融手術的簡介
臺北榮民總醫院 劉馨惠醫師
背景介紹
隨著不可逆之電流穿孔技術的問世,脈衝消融手 術 (pulse-field ablation, PFA) 的應用將使得心律不整導 管電氣燒灼手術迎來新的時代。在 2023 年 12 月,美 國食品和藥物管理局 (FDA) 批准了第 1 個 PFA 系統 (PulseSelect, Medtronic) 用於治療陣發性和持續性心房 顫動 (atrial fibrillation, AF) 。這項技術與專利先前在歐 洲國家已獲得批准且預計不久將在美國上市。同一 月份, Cleveland Clinic 開始招募第 1 批隨機臨床試驗
AVANT GUARD 的病患。這臨床試驗將分析比較
FARAPULSE PFA系統 (Boston Scientific) 與抗心律不整 藥物治療對於持續性AF在第1線治療的效果。這項臨床 試驗是 PFA 系列中第 1 個隨機臨床對照研究。目前臨床 證據顯示,這項非電氣的燒灼手術具有良好的持久 性,手術時間比傳統電氣燒灼手術更快,且對相鄰心
臟結構破壞風險較低。在Cleveland Clinic心臟電生理學 部 Oussama Wazni 主任的帶領之下,於 JACC Clinical Electrophysiology 雜誌中發表完整 PFA 技術的基礎與臨 床研究相關探討 (JACC Clin Electrophysiol. 2023 Sep; 9(9):2008-2023)。Wazni博士的團隊表示「PFA技術是一 種非常前瞻性治療及控制AF的方法,且不失其安全性。 期望透過PFA技術的普及化,使能得到廣泛應用」。
電流穿孔技術是甚麼?
PFA 的手術涉及電流穿孔技術,將快速且高電壓 的脈衝電磁場傳送到心臟組織中,使心肌細胞膜變得 更具通透性而穿孔。根據PFA技術應用的不同強度,導 致細胞膜中出現可逆或不可逆的孔隙並引發心肌細胞 凋亡。本項技術最大的特色是可根據電磁場的強度調 節,使PFA技術僅破壞心肌細胞而不損傷周圍不相關的 組織細胞,包括食道、肺靜脈和橫膈神經等。這些周
圍不相關的組織或結構對於電流穿孔技術的損傷有較 高的閾值,因此讓 PFA 技術更具安全性。 Wazni 博士的 團隊表示PFA技術與傳統電氣燒灼手術比較之下,不可 逆的電流穿孔技術,能提供針對心房或心室心律不整 相關心肌細胞的治療專一性,且具更低的副作用。
安全性和有效性的臨床證據
目前豬和狗的基礎研究在心房、心室及心外膜進 行了多項臨床前體外和體內的探討,並為病患奠定臨 床試驗的基礎。 Wazni 博士的團隊發現在豬模型中使用 傳統電氣燒灼手術後再使用PFA技術有良好成效,故針
對AF復發病患再予以追加使用PFA技術可以達到良好療 效 (JACC Clin Electrophysiol. 2024 Feb;10(2):222-234) 。
目前為止,PFA技術已完成至少10項有關陣發性或持續
性 AF 的臨床試驗,並收案超過 1,200 名病患。其
中,PULSED AF臨床試驗利用PulseSelect PFA系統於陣 發性 (n=150) 或持續性 (n=150) AF病患,發現PFA技術 的療效與傳統電氣燒灼手術相當,更重要的是PFA技術 的不良事件發生率更低。另一項跨國臨床試驗
MANIFEST-17K ,收案 106 個醫學中心中 17,000 名病患 的研究顯示使用CE認證的FARAPULSE PFA系統的1年 後,陣發性和持續性AF的整體治癒率分為73%和58%, 主要不良事件發生率低於1%。
基礎研究在PFA的證據
目前傳統電氣燒灼手術仍是心房顫動的重要治療 技術。儘管近年來在技術上取得進展,但依舊有20%的 復發率,並且有相當數量的病患需要進行重新電氣燒 灼手術。近期於JACC: Clinical Electrophysiology雜誌中 分析PFA在傳統電氣燒灼手術後病患的電燒狀況 (JACC Clin Electrophysiol. 2024 Feb;10(2):222-234)。研究發 現,使用線性PFA作用在經傳統電氣燒灼手術後有多個 復發間隙進行脈衝消融,導致右心房內形成了清晰、 連續且均勻的電燒組織。豬的心臟模型檢查中,部分 使用傳統電氣燒灼手術處理的肺靜脈 (模擬重新消融環 境) 中,使用花瓣型PFA導管進行重新消融導致肺靜脈 和後壁消融部分可形成完整電燒組織。心室中,應用 於傳統電氣燒灼手術後而以PFA技術補強的狀況,與在 健康心肌上的PFA電燒組織病變相似且比傳統電氣燒灼 手術的電燒組織範圍更大。總結來說,在實驗性重新 消融環境中,心房 (右心房和左心房) 中的PFA消融產生 持久且寬的病變。此外,左心室中的PFA技術消融在先
前傳統電氣燒灼手術後的重新消融中,表現優於原先 的電氣燒灼。重要的是PFA技術產生的電燒組織病變與 傳統電氣燒灼手術的消融不同,不會受先前傳統電氣 燒灼手術造成的瘢痕的顯著影響。另一項基礎研究, 更是將PFA技術與contact force (CF) 之間的關聯性在豬 隻的心室進行分析研究 (Circ Arrhythm Electrophysiol. 2024 Feb 23:e012717)。這項研究利用 PFA 技術透過
OMNYPULSE 導管的 CF 進行探討後,發現 PFA 技術在
CF 的作用之下造成的電燒組織平均病變深度和寬度分 別為3.5±1.2和12.0±3.5 mm且PFA電燒指數 (PF index) 與電燒組織深度有關 (r2=0.66,P<0.001)。由此可見, PFA 技術結合 CF 的應用有關鍵性作用,但仍需進一步 探討最佳的參數組合。此外,當兩種技術結合應用於 心房疾病組織仍需更多研究驗證。
PFA技術的挑戰
PFA 技術仍有許多疑問需要在臨床試驗中進一步 驗證。 PFA 技術的挑戰包含目前尚未確定能量強度 ( 電 壓 ) 、脈衝持續時間和脈衝持續頻率、雙相脈衝與單相 脈衝的傳遞、不同的電極配置、多種設備設計和病患 特徵的選擇。此外,PFA技術仍需要研究電流穿孔導致 的周邊血管痙攣、肺動脈出血、橫膈神經受損、潛在 的消融範圍過度深層或針對曾經歷經傳統電氣燒灼手 術的病患是否合適等諸多問題,仍須制定相關策略以 防止這些嚴重的併發症。最後,傳統電氣燒灼手術與 PFA 的技術轉換成本和效益必須持續評估,畢竟 PFA 技 術新穎且昂貴。
Reference:
1. Pulsed Field Ablation for the Treatment of Atrial Fibrillation: PULSED AF Pivotal Trial. Circulation. 2023;147:1422–1432.
2. Pulsed Field or Conventional Thermal Ablation for Paroxysmal Atrial Fibrillation. JACC Clin Electrophysiol. 2023 Sep;9 (9) :2008-2023.
3. Catheter-Based Electroporation: A Novel Technique for Catheter Ablation of Cardiac Arrhythmias. JACC Clin Electrophysiol. 2023 Sep;9(9):2008-2023.
4. Efficacy of Pulsed Field vs Radiofrequency for the Reablation of Chronic Radiofrequency Ablation Substrate: Redo Pulsed Field Ablation. JACC Clin Electrophysiol. 2024 Feb;10 (2) :222-234.
5. Pulsed Field Ablation Index-Guided Ablation for Lesion Formation: Impact of Contact Force and Number of Applications in the Ventricular Model. Circ Arrhythm Electrophysiol. 2024 Feb 23:e012717.
ESC 指南: 心室性心律不整管理與
預防突發性心臟死亡
臺北市立萬芳醫院 莊再庚醫師
心血管疾病一直是全球主要死亡原因,突發性心 臟死亡 (sudden cardiac death, SCD) 佔所有死亡的 10-20% 。為了有效管理心室性心律不整 (ventricular arrhythmia, VA) 並預防SCD,ESC最新發布的指南融合 了最新科學證據,更新了 2015 年的版本。這份超過 130 頁的新指南增加了許多新建議和章節,特別強調了公眾 基礎生命支援 (BLS) 和自動體外除顫器 (AED) 的可及
性,以提高醫院外心臟驟停 (OHCA) 受害者的生存率。
該指南獨立章節著重於旁觀者立即進行CPR的重要性,
推動社區基礎生命支援訓練,並透過電話通知訓練有素 的旁觀者協助附近的OHCA受害者,旨在增強公眾對緊 急情況下救助能力的認識。此外,指南介紹了新的診斷 工具和VA/SCD風險分級的系統性概述,包括五種VA首
次出現的臨床場景及其基於證據的診斷評估建議。

與2015年ESC指南相比,2022年ESC關於心室性心律不整和突發性心臟死 亡指南的10個新要點概覽。
管理電氣風暴的新焦點
2022 年 ESC 指南首次專設一章討論電氣風暴管 理,定義為 24 小時內發生三次以上需干預終止的獨立 持續性心律不整。鑒於電氣風暴不僅與心理壓力大為
有關,還與死亡率增加相聯,其治療顯得極為重要。
新指南對電氣風暴的管理方法進行了顯著修訂,提出了 一個根據心律不整類型 (多形性vs.單形性) 和潛在的結構 性心臟病 (SHD) 或誘發條件的綜合算法,以指導診斷和 治療。新指南特別強調多維治療方法 (multi-dimensional
therapy) ,包括 ICD 查詢與重新編程、抗心律不整藥物 (AAD) 治療、心室性心搏過速 (VT) 觸發性 (triggering) 的
心室早期收縮的導管消融,以及在心因性休克情況下的 鎮靜、自主調節和機械循環支持。對於患有SHD和電氣 風暴的患者,首選治療為胺碘酮 (amiodarone) 和非選擇 性β-阻斷劑,並建議輕至中度鎮靜來處理升高的交感神 經張力。反覆出現的電氣風暴情況下,建議在經驗豐富 的中心進行導管消融,優於深度鎮靜、自主調節和機械 循環支持。這些建議顯示,電氣風暴患者如需額外治 療,應轉診至專業中心。
遺傳諮詢與檢測的新進展
隨著臨床數據增加和大規模平行測序技術 (massive parallel sequencing) 的進步,遺傳檢測成本的降低,使 遺傳諮詢和檢測在 VA 患者的診斷評估和風險分層中的 重要性大幅提升。新ESC指南提高了遺傳諮詢和檢測的 優先級,將其作為患有遺傳性心肌病和心律不整綜合 症患者護理的常規部分。這些改變不僅體現在遺傳檢 測作為獨立診斷工具章節的增加,也通過在不同情境 下明確推薦遺傳諮詢和檢測來展示。新指南推薦,在 診斷出可能具遺傳基礎且有心律不整和 SCD 風險的狀 態時進行遺傳檢測。對於患有擴張型心肌病 (DCM) /低 動力非擴張型心肌病 (HNDCM) 且有其他風險因素或家 族史的患者,建議進行遺傳檢測。此外,對於疑似有 遺傳病因的孤立病例也推薦進行遺傳檢測,因為高達
50% 的 DCM/HNDCM 患者可以發現遺傳原因,這對預 後和治療有顯著影響。
新指南還強調了對心律不整性右室心肌病 (ARVC)、 肥厚型心肌病 (HCM)、臨床診斷的長QT綜合症 (LQTS)、 安德森 - 陶維爾綜合症 (Andersen-Tawil syndrome) 以及 布魯加達綜合症 (BrS) 和兒茶酚胺敏感性多形性心室性 心搏過速等疾病的病人,進行針對性的遺傳檢測。這 些更新體現了向更加個性化醫療的轉型,並對未來的 臨床實踐提出了新的挑戰和機遇。
心臟磁共振造影與抗心律失常藥物治療新 進展
最新 ESC 指南顯著提升了心臟磁共振造影 (CMR) 在診斷和風險分層中的作用,特別是決策初級預防性 植入式心臟去顫器 (ICD) 治療時。此外,指南首次包含 了針對使用鈉通道阻斷劑和 QT 延長藥物患者的治療演 算法,旨在提高 AAD 治療的安全性。這些進展對歐洲 的醫療系統提出了挑戰,因為這涉及到限制資源和高 昂的成本。新指南強調了導管消融在 VA 治療中的重要 性提升,無論是特發性VA還是源自SHD的VA。對於心 臟核磁共振造影,除了 2015 年指南中已提及的應用 外,現在更加強調對所有無明確原因的突發性心臟驟 停存活者進行 CMR ,並提高了對特定 SHD 患者的 CMR 推薦等級。同時,新指南提倡在更多情境下應用 CMR ,包括但不限於 ARVC 和 HCM 患者,進一步細化 了心臟疾病診斷和風險評估。這代表了對心臟影像技 術和抗心律不整治療策略的深入發展,促使臨床實踐 朝著更加個人化和精準的方向邁進。
心室性心律不整管理中導管消融的角色 增加
2022 年 ESC 指南強調,導管消融在 VA 管理中的重 要性有顯著提升。這種治療方式現已成為有無 SHD 患 者中VA的首選策略,特別是對於症狀性特發性VT和來 自右心室流出道 (RVOT) 及左心室束支的PVC患者。對 於PVC相關的心肌病 (CM) 患者,不論PVCs/VT的假設
起源,導管消融同樣成為首選治療 (由2015年的IIa級提 升至I級) 。新指南也首次探討了對PVC負荷高於20%的 無症狀患者進行導管消融的可能性,儘管這方面的預 後益處尚未證明,因此給出了 IIb 級的推薦。此外,針
對有 SHD 和 VA 的患者,導管消融在治療上的重要性增 加,特別是在長期 AAD 治療失敗的情況下,雖然導管 消融治療 VA 的預後角色證據仍不足。在缺血性心臟病 (IHD) 患者中,尤其在首次VT發作後立即或在ICD植入 前後,建議進行“早期”導管消融 (IIb 級推薦 ) ,但最 佳時機仍有待確定。針對 DCM 患者,新指南對藥物難 治性、有症狀、反復發生的SMVT進行導管消融提出了 IIa 級推薦。此外,對於 BrS 患者和反復出現適當 ICD 電 擊的藥物難治性患者,更強烈地推薦進行觸發 VF 的 PVCs 和 / 或特發性 RVOT 心外膜基質的導管消融 ( 從 IIb 級提升至IIa級)。這些更新反映了對專門進行VT消融治 療的中心的需求,顯示出導管消融在心律不整管理中 的角色越來越重要,同時也指出了在這一領域仍有許 多未知和挑戰。
SCD風險分層的變化
確定最高風險SCD患者進行成功的初級預防性ICD 治療一直是挑戰,也是 2015 年與 2022 年指南中最具爭 議和廣泛討論的議題。 2022 年的更新提供了更多針對 特定疾病的 SCD 風險分層建議,新識別的風險指標不 僅適用於 SHD 患者,也適用於原發性電生理疾病患 者。儘管過去以左心室功能不全 ≤35% 和症狀性心衰竭 作為SHD患者SCD風險增加的標誌,但基於DANISH試 驗結果,新指南對 DCM 患者的 ICD 植入建議由一級降 為 IIa 級。此外,新指南納入了未解釋暈厥、 SMVT 的 可誘導性等新風險標誌,並將MRI上的LGE和特定基因 變異作為風險評估標準。這些更新體現了從過分依賴 左心室功能轉向考慮“新”風險標誌的趨勢,旨在為 中等風險患者提供更精細化的 SCD 風險評估。然而, 仍存在許多關於 SCD 風險分層的未知領域,特別是在 左心室功能保留的患者中。此外,隨著患者群體的變
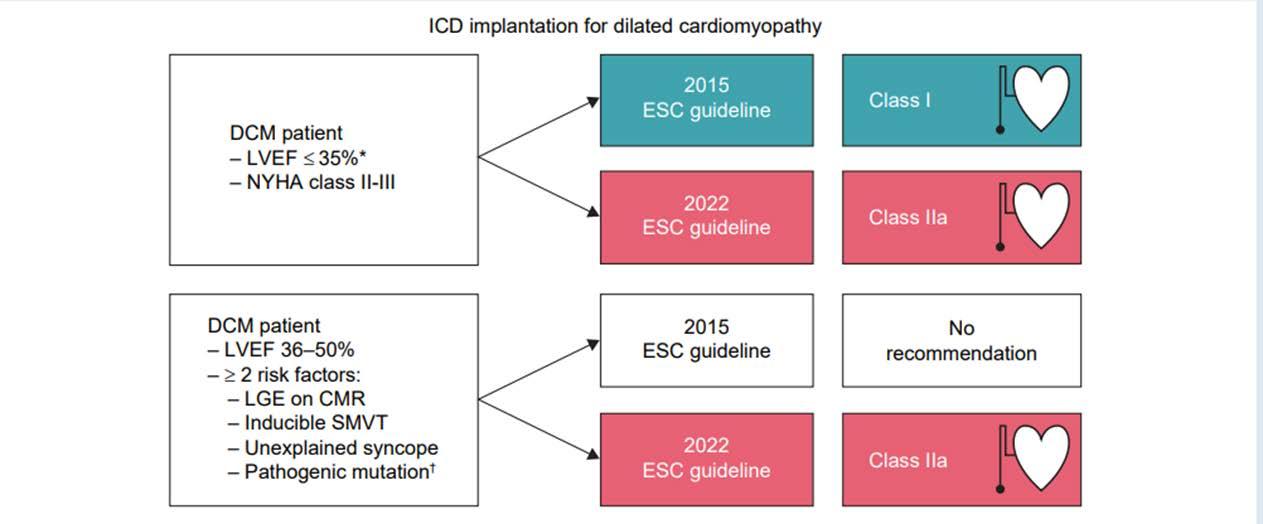
2015年與2022年ESC指南中,關於選定擴張型心肌病患者一級預防性 ICD治療的不同建議的示例
化和心衰竭治療的顯著改進,初級預防性ICD治療的角 色問題仍待解答。
風險評分與風險計算器的實施
風險計算器提供的預後資訊有助於識別最高風險 的VA和SCD患者。2015年指南首次根據HCM風險-SCD 計算器估算的 5 年 VA 和 SCD 風險,為 16 歲及以上的 HCM 患者的 ICD 治療提出建議。近年來,預測模型領 域進展顯著,提出了多個經過細致方法學評估的新風 險計算器。因此,最新指南採用了其他風險計算器, 針對不同遺傳性心律失常疾病中的 VA 和 SCD 風險進行 評估。對於 16 歲以下 HCM 患者的初級預防性 ICD 治療 建議,採用了經過驗證的 HCM 風險 - 兒童評分。攜帶 LMNA 基因突變且患有 DCM 的患者的 ICD 治療建議, 則由基於 5 年內危及生命 VA 風險的另一風險計算器指 導,並考慮了如NSVT、LVEF<50%或AV阻滯等心臟表 型。此外,對於無症狀的長 QT 綜合症 (LQTS) 患者的 初級預防性 ICD 治療建議,考慮了最近驗證的 1-2-3-LQTS-Risk 計算器,用於識別基於基因型和 QTc 時長的高風險患者。風險模型和計算器的侷限性在 於,它們源自可能不具代表性、相對較小、過於同質 化的患者隊列,或缺乏外部驗證。此外,風險模型採 用的不同組合終點不等同於 SCD 。將嚴格的數學模型 應用於異質性心臟病患者存在困難,因此風險計算器 結果只能作為共同決策過程的一部分。同時,仍缺乏 系統性研究探討在β - 阻斷劑和基因型特異性治療之 外,保留射出分率或僅輕度降低射出分率的 SHD 患者 和LQTS患者的初級預防性ICD治療的作用。
在原發性電氣疾病領域中的重要變化
2022 年 ESC 指南針對原發性電氣疾病引入了重要 更新,包括早期去極化模式和早期去極化綜合症的特 定標準,以及特發性 VF 的區分診斷標準。此外,對布 魯加達症候群 (BrS) 的診斷要求更加嚴格,需要臨床因 素如存活的心臟驟停、陽性家族史或心律失常性暈厥 史。短QT綜合症 (SQTS) 的診斷標準也調整,除了QTc 間隔 ≤360 毫秒外,還要求具有特定致病基因突 變、SQTS家族史或因VT/VF存活的SCD 家族史。β-阻 斷劑繼續是治療 CPVT 和 LQTS 患者的重要藥物,新指 南特別推薦非選擇性β-阻斷劑,如那多洛 (nadolol) 和 普萘洛爾 (propranolol)。針對LQTS 3型患者,首次提及 mexiletine 作為 I 級推薦的基因型特異性治療。對於 CPVT 患者,建議在β - 阻斷劑治療基礎上加用氟卡尼 (flecainide) ,以治療多形性或雙向 VT 、持續運動性 PVCs 或反復暈厥。此外,指南在 SCD 風險分層方面提 出創新,對於無症狀但自發表現為一型布魯加達 ECG 的患者,可考慮進行程式化電刺激 (PES) 進行風險評 估。植入式循環記錄器亦可用於幫助對年輕的 SQTS 患 者和有額外風險特徵的ERP患者進行風險分層。值得注 意的是,安德森-塔維爾綜合症首次被從其他LQTS形式 中單獨區分開來。
這些變化反映了對原發性電氣疾病更深入的理解 和管理,指南提供了更詳細的診斷標準和治療建議, 以期改善患者預後並降低 SCD 風險。這不僅提高了臨 床實踐的精準性,也強調了多學科治療方法的重要 性,為患者提供更全面、個人化的治療方案。
人工智慧在心房顫動電燒手術的進展
(The Advance of AI in Catheter Ablation of Atrial Fibrillation)
臺北榮民總醫院 劉至民醫師
在治療心律不整時,我們通常能夠透過觀察心臟 內的電氣訊號來引導電燒手術,這對於大多數心律不 整的治療來說是有效的。早期嘗試定位和電燒心房內 特別混亂的電信號—複雜分散的心房電圖 (complex fractionated atrial electrograms; CFAE)—在某些情況下確 實有效,但往往結果不一,有時並不帶來預期的改 善。 STAR AF II 的結論是,執行超出肺靜脈隔離手術 (pulmonary vein isolation; PVI)的額外電燒方式並不會帶 來改善的長期結果。在目前的標準肺靜脈隔離手術之
後,倘若顫動心律沒有轉成竇性心律,左右心房內的 雜亂電氣訊號卻不那麼容易分析處理。這些混亂的電 氣訊號通常是透過在心臟特定點位的電極捕捉到的, 而當使用更多電極進行捕捉時,我們可以得到更多關 於這些電氣訊號性質的信息。透過分析心臟內的電氣 訊號,史丹佛大學 Sanjiv Narayan 醫師團隊描繪出心房 顫動的驅動子 (rotor drivers) 進行電燒,可以終止心房 顫動的進行。法國醫師Julien Seitz於2019年發現,這些 混亂電信號不僅僅是隨機出現的;它們在空間上有一 定的分佈模式,並且其時間變化也遵循某種規律。在 鄰近的電極位置發生的非同時分散 ( 時間分散; time dispersion) 以及在明確定義的群集中組織化的分散 (空 間分散; spatial dispersion) ,這種空間時間分散模式 (spatiotemporal dispersion ;圖一 ) 暗示存在潛在的心 房顫動的驅動子 (drivers)。在空間時間分散模式區域進 行的電燒治療使得 105 名患者中有 95% 的心房顫動終 止。經過 18 個月的追蹤後,每位患者平均經歷 1.4 ±0.5 次手術的任何心房心律不整復發率為15%;而在對照組 中,每位患者平均經歷 1.5 ± 0.5 次手術的任何心房心律 不整復發率為41% (Log-rank p <0.001) 。
隨著人工智慧技術的引入,基於人工智慧分析心 內電氣訊號的模組,經專家訓練,能在手術中即時分 析這些混亂的電氣訊號,透過這種創新技術來標準化 治療方法,以更精準地識別和電燒那些可能引起心房 顫動的心臟區域,提高治療效果,並減少因為不同手 術醫師之間的技術差異所造成的個人影響。
在2022年的Heart Rhythm Society Conference大會 上,一個使用人工智慧導引的心房顫動電燒模組 (Volta
VX1) 被提出 ( 圖二 ) ,該演算法被訓練用於分析多極心 內膜電氣訊號圖內的空間時間分散模式。一項前瞻 性、多中心、非隨機化研究,在 85 名持續性心房顫動 患者中進行,其中有 29% 是長期持續性心房顫動 (longstanding persistent AF),共有法國的8個中心和17名醫師 參與,比較主要和衛星中心進行電燒後的急性和長期 預後。同時,也與通過訓練有素的醫師視覺指導進行 電燒的對照組進行了結果比較。 VX1 能夠在所有患者 中通過17名醫師操作者使用三種3D導航設備 (Carto® 3, Biosense Webster; EnSite PrecisionTM, Abbott; Rhythmia HDxTM, Boston Scientific) 和六種多極導管(PentaRay® catheter spacing 2 6 2 [Biosense Webster], AdvisorTM HD Grid [Abbott], ReflexionTM HD [Abbott], AdvisorTM FL [Lasso 10 pole; Abbott], Lasso® Nav Eco catheter [Biosense Webster], Intellamap OrionTM [Boston Scientific]) 構建標 準化的分散圖,並針對具有有標示病灶的心內圖區域 進行電燒(圖三),並附加或無肺靜脈隔離術。研究結果 發現, VX1 的使用在主要和衛星中心之間沒有統計學 上顯著的差異,心房顫動在主要和衛星中心的患者中 分別有92%和83%的心房顫動電燒終止率 (p=0.31) 。經 過 13.5 ± 3.2 個月的追蹤,在單一電燒手術後,無論是 否使用抗心律不整藥物,無心房顫動的比率為86%,在 平均每位患者進行1.3次電燒手術後提升至89% (p=0.4)
。在單次電燒手術後與平均每位患者接受 1.3 次電燒手
術後,無論是否使用抗心律不整藥物,無任何心房性心 律不整的比率分別為54%和73%(p <0.001) 。對於一次 (p=0.8) 或多次電燒手術 (p=0.4) (圖四),以及整個研究 族群與控制組之間的結果 (p>0.2) ,未觀察到主要與衛 星中心之間結果的統計學上顯著差異,代表即使新上手 的醫師沒有任何使用VX1的經驗,依然可以複製電燒的 良好效果,不因手術醫師的差異而不同。VX1目前已經 通過美國FDA與歐盟CE Mark。
近期的前瞻性研究於 2021 年 5 月至 2023 年 1 月在德 國慕尼黑的德國心臟中心進行,為單一中心研究,共 收納了 50 名連續案例。有別於以往的研究,這些患者 全部為長期持續性心房顫動進行導管電燒治療,並且 於手術一開始先進行肺靜脈隔離術。在實施肺靜脈隔
離術之後,對展現心內圖DISPERS區域 (spatiotemporal dispersions) 的左心房和右心房進行電燒,使心房顫動週 期長度從平均 162.0 ± 16.6 ms 增加到 202.2 ± 21.6 ms , 並且在 12 名患者 (24%) 中心房顫動終止轉為心房過速 (atrial tachycardia) 或竇性心律。在平均追蹤期為363.14 ±187.42天之後,共22名患者接受了再次電燒手術。經 過平均 1.46 ± 0.68 次的電燒手術後,有 82% 的患者維持 穩定的竇性心律。整體來看,使用人工智慧導引的 DISPERS 電燒策略在長期持續性心房顫動患者中展示 了高度的成功率。即使電燒時間延長,但併發症的發 生率仍然維持在低水平。
在臺北榮民總醫院的研究中,陳適安教授與林彥 璋教授使用心內圖電氣訊號的遞迴圖 (recurrence plot) 進 行人工智慧訓練 (DeePRISM),並已在2022 Heart Rhythm
Society Conference發表,獨立測試族群準確度 (AUC) 可 達0.87,使用人工智慧模組進行電燒患者並有較好的預 後效果,目前已進行前瞻性臨床實驗,期待進一步的 結果發表。
總結而言,在持續性心房顫動心律不整的治療過 程中,透過觀察心臟內部電氣訊號引導的電燒手術是一 項有效的策略。雖然早期嘗試對心房內的複雜分散心房 電圖進行定位和電燒有時能夠帶來改善,但結果往往不 一致。隨著人工智慧技術的引入,這些雜亂的電氣信號 可以被即時且精確分析,從而提高電燒治療的效果,並 減少手術間的變異性。利用AI來引導心房顫動電燒的新 方法,已在多中心研究中展示其對於提高治療效果的潛 力。這突顯了人工智慧在心律不整治療領域的創新應 用,為臨床實踐帶來了新的希望和方向。
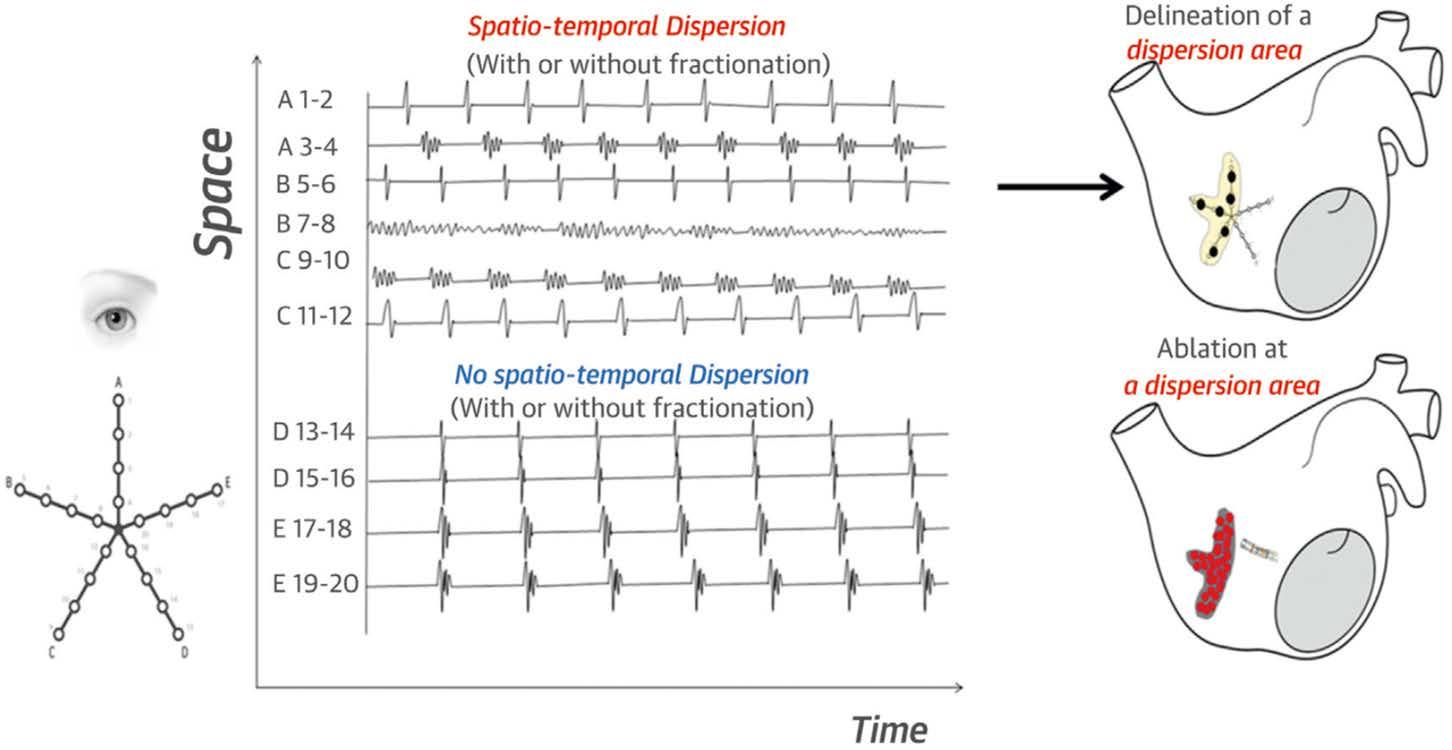
(圖一) 多極心內電氣圖的時空分散 (spatiotemporal dispersion) 模式。
(圖二) VX1 模式流程。

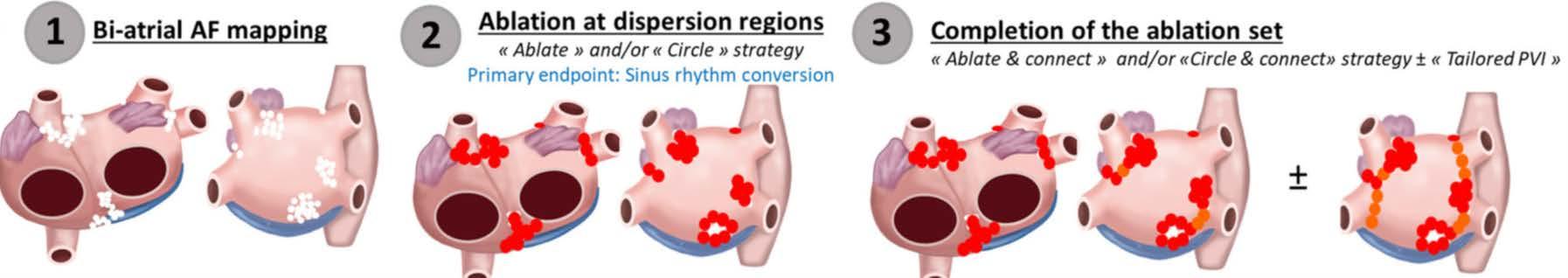
(圖三) VX1 模組電燒部位。

(圖四) 長期持續性心房顫動使用 VX1 一年電燒結果。左圖:單一手術;右圖:多次手術。
References
1. Chen SA, Hsieh MH, Tai CT, Tsai CF, Prakash VS, Yu WC, Hsu TL, Ding YA, Chang MS. Initiation of atrial fibrillation by ectopic beats originating from the pulmonary veins: electrophysiological characteristics, pharmacological responses, and effects of radiofrequency ablation. Circulation. 1999;100:1879-1886.
2. Nademanee K, McKenzie J, Kosar E, Schwab M, Sunsaneewitayakul B, Vasavakul T, Khunnawat C, Ngarmukos T. A new approach for catheter ablation of atrial fibrillation: mapping of the electrophysiologic substrate. JournaloftheAmericanCollegeofCardiology 2004;43:2044-2053.
3. Verma A, Jiang CY, Betts TR, Chen J, Deisenhofer I, Mantovan R, Macle L, Morillo CA, Haverkamp W, Weerasooriya R, et al. Approaches to catheter ablation for persistent atrial fibrillation. The New England journal of medicine. 2015;372:1812-1822.
4. Lin YJ, Tai CT, Kao T, Chang SL, Wongcharoen W, Lo LW, Tuan TC, Udyavar AR, Chen YJ, Higa S, et al. Consistency of complex fractionated atrial electrograms during atrial fibrillation. Heart Rhythm. 2008;5:406-412.
5. Lin YJ, Suenari K, Lo MT, Lin C, Hsieh WH, Chang SL, Lo LW, Hu YF, Cheng CC, Kihara Y, et al. Novel assessment of temporal variation in fractionated electrograms using histogram analysis of local fractionation interval in patients with persistent atrial fibrillation. Circulation Arrhythmia and electrophysiology. 2012;5:949-956.
6. Narayan SM, Krummen DE, Shivkumar K, Clopton P, Rappel WJ, Miller JM. Treatment of atrial fibrillation by the ablation of localized sources: CONFIRM (Conventional Ablation for Atrial Fibrillation With or Without Focal Impulse and Rotor Modulation) trial. Journal of the American College of Cardiology. 2012;60:628-636.
7. Seitz J, Bars C, Théodore G, Beurtheret S, Lellouche N, Bremondy M, Ferracci A, Faure J, Penaranda G, Yamazaki M, et al. AF Ablation Guided by Spatiotemporal Electrogram Dispersion Without Pulmonary Vein Isolation: A Wholly Patient-Tailored Approach. Journal of the American College of Cardiology. 2017;69:303-321.
8. Seitz J, Durdez TM, Albenque JP, Pisapia A, Gitenay E, Durand C, Monteau J, Moubarak G, Théodore G, Lepillier A, et al. Artificial intelligence software standardizes electrogram-based ablation outcome for persistent atrial fibrillation. Journal of cardiovascular electrophysiology. 2022;33:2250-2260.
9. Bahlke F, Englert F, Popa M, Bourier F, Reents T, Lennerz C, Kraft H, Martinez AT, Kottmaier M, Syväri J, et al. First clinical data on artificial intelligence-guided catheter ablation in long-standing persistent atrial fibrillation. Journal of cardiovascular electrophysiology. 2024;35:406-414.