Arrhythmia News
發行人: 謝敏雄 (Ming-Hsiung Hsieh)
發行單位: 中華民國心律醫學會 (Taiwan Heart Rhyrhm Society)
地址: 100506台北市中正區忠孝西路一段50號25樓之18
本期摘要
P1. 無導線心律調節器的十年旅程與未來展望
P5. ECG of the Month
P8. Left Atrium Appendage Occlusion (LAAO) 臨床實證與展望
P13. 脈動新聞
電話: 傳眞: 網址: ISSN: 2223-0130
886-2-23821530
886-2-23821528 www.thrs.org.tw
總編輯
林廷澤 Ting-Tse Lin 黃嵩豪Sung-Hao Huang
本期主編
林柏霖Po-Lin Lin 陳韋翔Wei-Siang Chen
編輯
陳威達Wei-Ta Chen 黃于珊Yu-Shan Huang
黃冠智Kuan-Chih Huang 鍾偉信Wei-Hsin Chung 吳宏彬Hung-Pin Wu 陳力瀚Li-Han Chen
無導線心律調節器的十年旅程與未來展望
新竹馬偕紀念醫院 心臟內科 林柏霖醫師
過去十年間,無導線心律調節器 (Leadless Pacemaker, LP) 的發展,為心律治療領域帶來了革命 性的改變。 2016 年,美敦力的 Micra 經導管心律調節系 統 (TPS) 首度獲得美國 FDA 核准,標誌著臨床應用的重 要里程碑(圖一)。這種完全植入心內、無需導線與皮下 囊袋的起搏方式,不僅降低了感染風險,也改善了許 多傳統導線式 (Transvenous Pacemaker, TV-PPM) 的長 期問題。
臨床研究的累積證據
在臨床實證方面, Micra 最初的 IDE 試驗已確認其 安全性與有效性[1],隨後的PAR(post-approval registry, 上市後登錄研究 ) 進一步提供長期追蹤數據 [2] 。約 1800 位接受植入的患者在五年追蹤中顯示:無需因裝置相 關感染而取出 ( 表 1) 。僅 4.9% 病人需要更換或升級 ( 圖 2) 。儘管起搏比例中位數達 80% ,僅 2% 病人需升級至 心臟再同步治療 (CRT)( 圖 3) 。這些結果顯示 Micra 在安
全性及長期耐用性上均有優勢。
另一方面, CED (Coverage with Evidence Development) 研究對美國Medicare患者進行比較,結果 證實無導線節律在降低再手術(圖4B)與併發症(圖4A)發 生率上,優於傳統導線式節律器[3]。
新一代無導線起搏器的進展
在技術發展方面,第一代 Nanostim 因電池提前耗 盡而未能獲批,但後續的AVEIR-VR解決了此問題,並 於 2022 年獲得 FDA 核准,進一步擴展了單腔無導線起 搏的選項。
此外,藉由內建的三維加速度感測器 ( 圖 5) [4] , Micra 能夠偵測心房機械收縮訊號並追蹤心房活動,進 而發展出 Micra AV ,能提供部分房室同步起搏。雖然 在高心率下房室同步仍有限制,但其追蹤速率已提升 至135次/分鐘,讓更多病患能從無導線起搏中獲益。
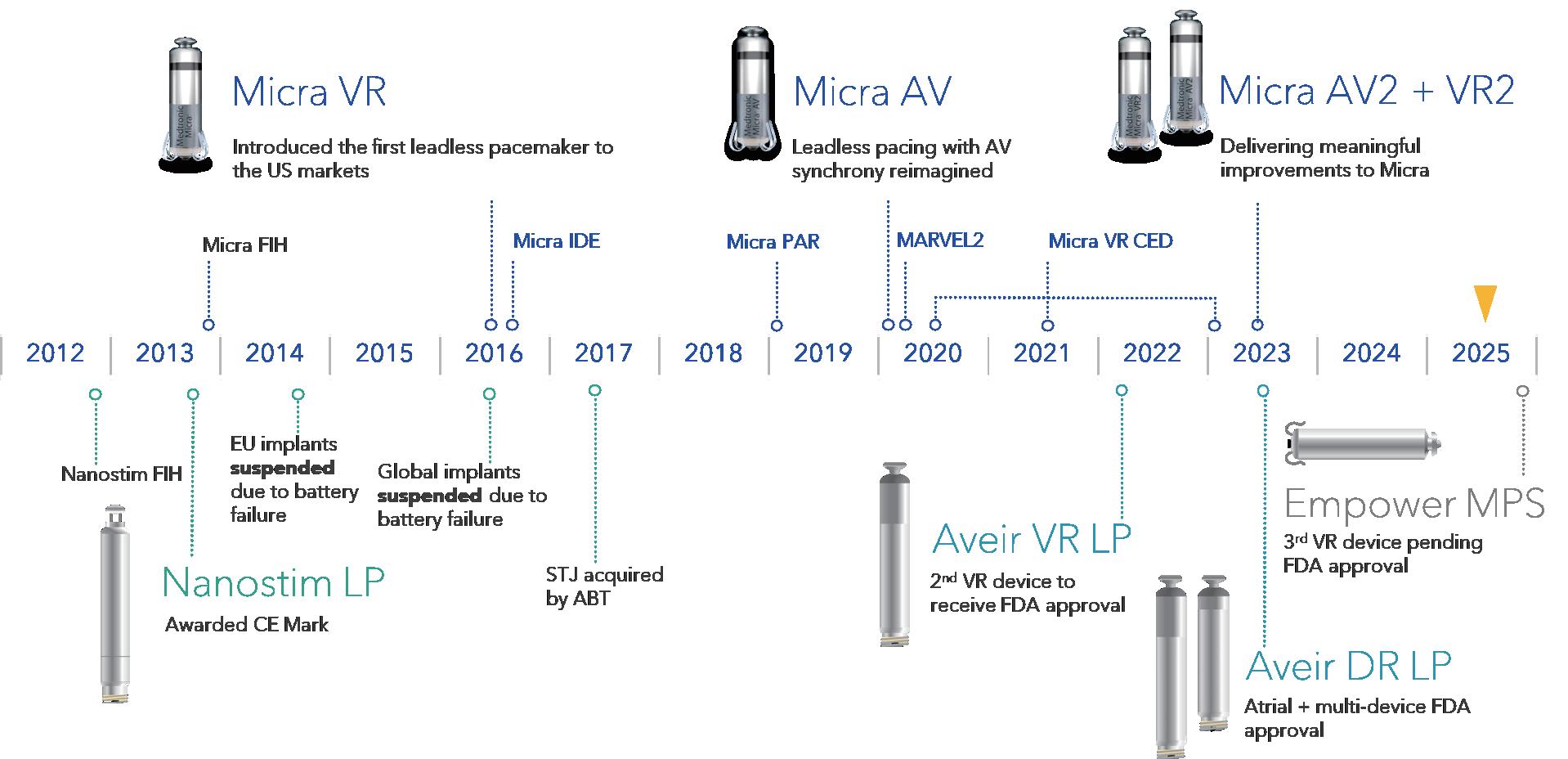
(圖一)、 無導線心律調節器 (Leadless Pacemaker, LP) 發展。
( 表 1) 、 在 Micra VR 植入患者中的感染事件 (Infection Events) 。
資料來源: Leadless pacemakers at 5-year follow-up: the Micra transcatheter pacing system post-approval registry. (2024) Table 3 [2]
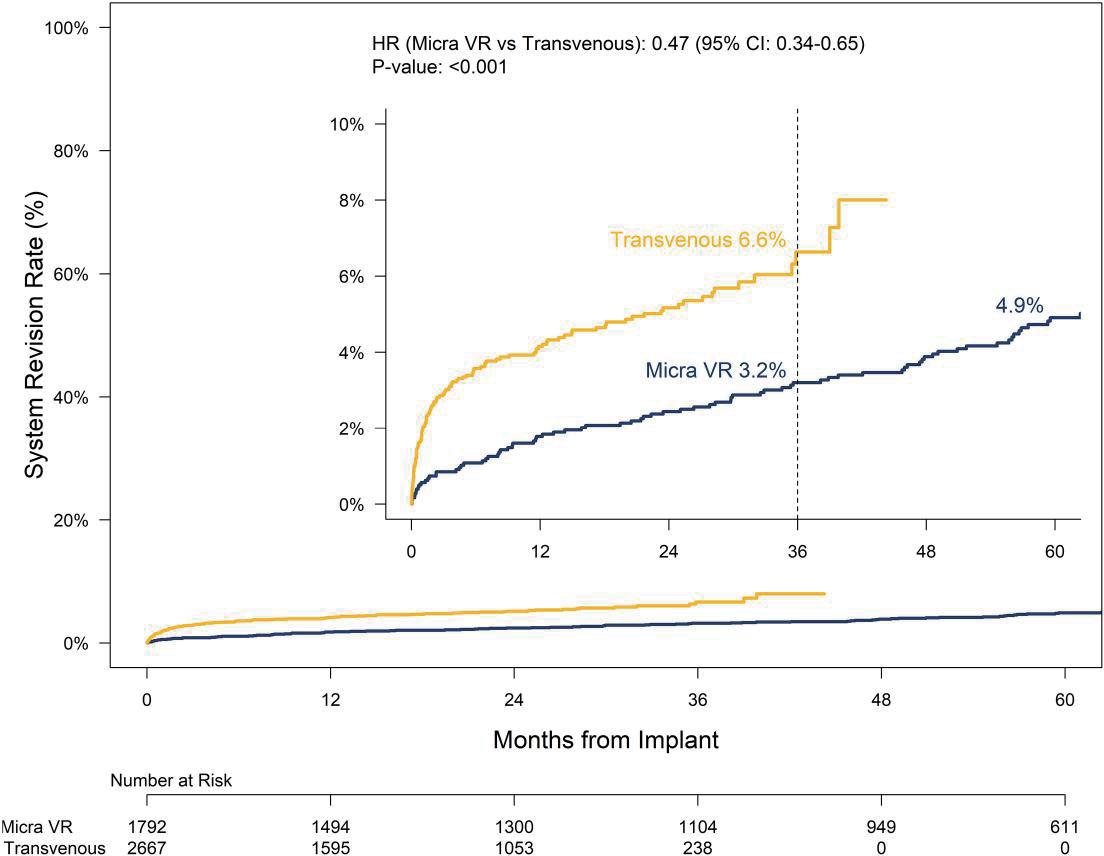
( 圖 2) 、裝置 Micra 的病人術後 60 個月追 蹤,僅 4.9% 需要更換或升級。
資料來源: Leadless pacemakers at 5-year follow-up: the Micra transcatheter pacing system post-approval registry. (2024) Figure 4 [2]
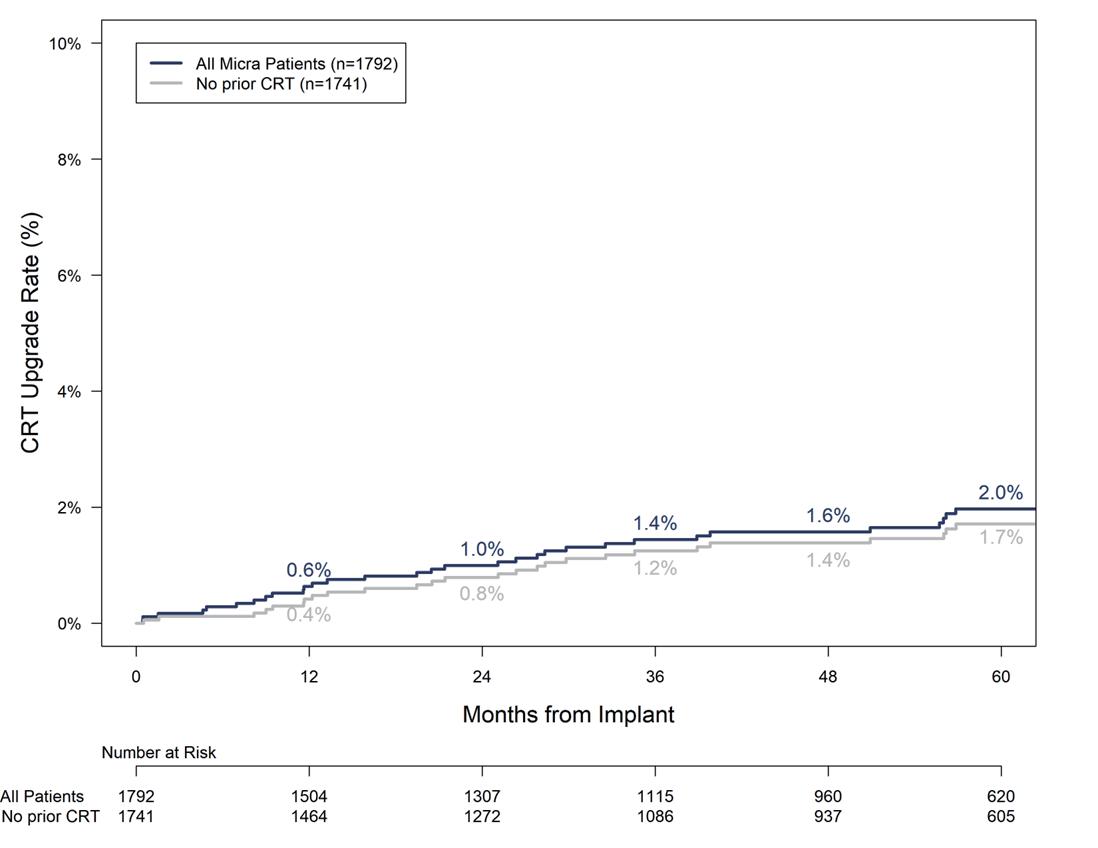
( 圖 3) 、 所有 Micra 植入患者升級心臟 再同步治療的比率為 2.0% 。
資料來源: Leadless pacemakers at 5-year follow-up:the Micra transcatheter pacing system post-approval registry.(2024) Supplementary Figure S2 [2]
( 3
(Cumulative Incidence
資料來源: up of the Micra CED study. (2023) Figure 1

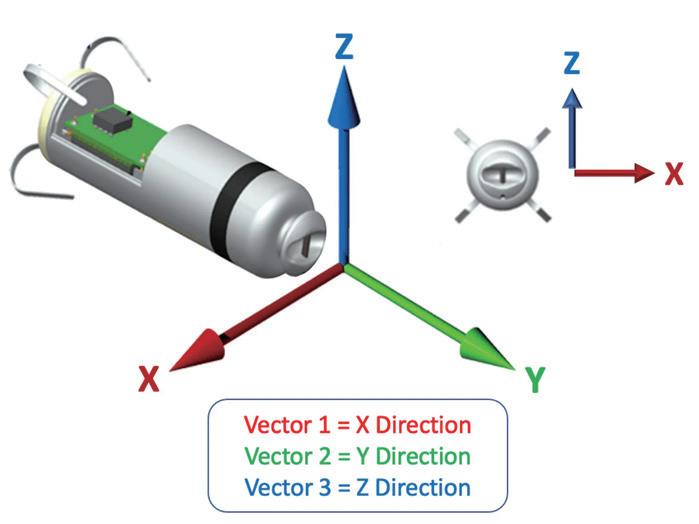
Atrioventricular synchronous leadless pacemaker: state of art and broadened indications (2021) Figure 2 [4]
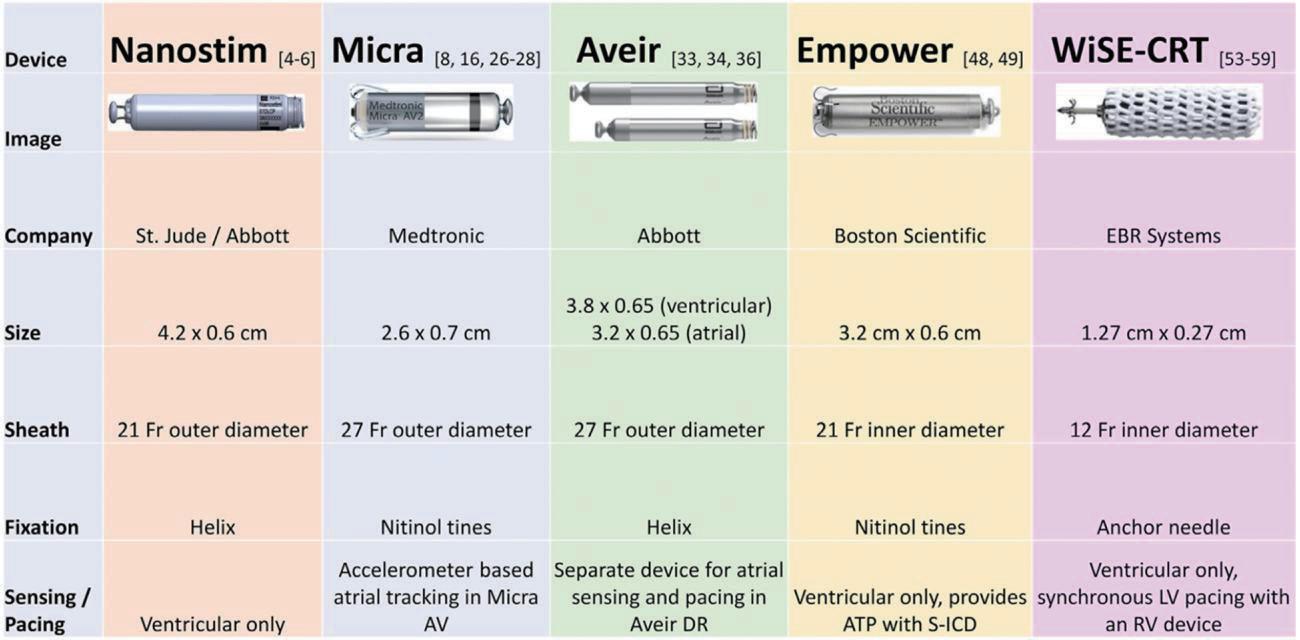
(圖6)、無導線節律器與特色。
資料來源:European Heart Journal Supplements (2025) Figure 1 [5]
更進一步,AVEIR DR作為全球首款獲得FDA核准 的雙腔無導線起搏器,成功拓展了適應症至竇房結功 能不全的病患,成為另一重大突破。而波士頓科學所 研發的EMPOWER LP能與皮下型心臟去顫器(S-ICD)互 相通訊,實現抗心動過速起搏,展現無導線裝置與其 他電療技術結合的潛力(圖6)[5]。
臨床證據與臨床定位
至今,Micra相關的三大研究(IDE、PAR、CED)已 涵蓋近 9000 名患者, AVEIR 則累積約 210 名受試者的數 據(表2) [1] [2] [3] [6]。這些大量臨床證據已充分證明單腔無 導線起搏的可靠性與優勢,使其成為傳統導線式起搏 器的可行替代方案。臨床醫師在與患者討論時,應透 過共同決策,權衡傳統與無導線節律的利弊。
Micra AVEIR
IDE PAR CED IDE N=725 N=1,817 N=6,219 N=210 (表2)、Micra、AVEIR臨床研究涵蓋患者
未來的方向與挑戰
展望未來,無導線起搏的發展可能走向模組化概 念。例如:竇房結功能不全的患者僅需心房起搏器, 而房室傳導阻滯且竇房結功能正常的患者,則可選擇 具「 VDD 」功能的無導線裝置。若能進一步整合為單 一裝置,同時感測並起搏心房與心室,甚至與傳導系 統結合以實現生理性起搏,將是臨床的理想目標,也 被認為是起搏領域的「聖杯」。
結語
十年間,無導線心律調節器從單腔裝置起步,逐 步演進至具房室同步功能與雙腔設計,並展現與其他 心律裝置結合的潛能。隨著臨床數據的累積與技術持 續創新,無導線起搏已不僅是傳統起搏器的補充,而 正逐步走向主流選擇。未來,如何在「最小化心臟內 硬體」與「最大化治療效益」之間取得平衡,將是推 動此技術持續前進的關鍵。
參考文獻
1. REYNOLDS, Dwight, et al. A leadless intracardiac transcatheter pacing system. New England Journal of Medicine, 2016, 374.6: 533-541.
2. EL-CHAMI, Mikhael F., et al. Leadless pacemakers at 5-year follow-up: the Micra transcatheter pacing system post-approval registry. European Heart Journal, 2024, 45.14: 1241-1251.
3. CROSSLEY, George H., et al. Leadless versus transvenous single chamber ventricular pacemakers: 3 year follow up of the Micra CED study. JournalofCardiovascularElectrophysiology, 2023, 34.4: 1015-1023.
4. MITACCHIONE, Gianfranco, et al. Atrioventricular synchronous leadless pacemaker: state of art and broadened indications. Reviews in cardiovascular medicine, 2021, 22.2: 395-401.
5. Laurence M Epstein, Mikhael F El-Chami, Clemens Steinwender, Kyoko Soejima, Ten years of leadless pacing, European Heart Journal Supplements, Volume 27, Issue Supplement_2, March 2025, Pages ii3–ii7
6. REDDY, Vivek Y., et al. 1-Year outcomes of a leadless ventricular pacemaker:the LEADLESS II(phase 2) trial. Clinical Electrophysiology, 2023, 9.7_Part_2: 1187-1189
7. EL-CHAMI, Mikhael F.; STEINWENDER, Clemens. The exciting and evolving journey of leadless pacing. European Heart Journal Supplements, 2025, 27.Supplement_2: ii1-ii2.
A 76-year-old woman with multiple circuits of atypical flutters
奇美醫院 心臟血管內科 黃沛頡醫師
一位 76 歲女性,有高血壓以及陣發性心房顫動病史,規律於心臟科門診服用抗心律不整藥物 (flecainide) 以 及抗凝血劑 (apixaban) 以控制慢性病。然而,病人最近數月來感到間歇性胸悶與心悸,且症狀逐漸加重。經血 管介入專家排除冠狀動脈狹窄阻塞之問題後,判斷此病人之不適與多種嚴重心律不整有關 ( 如圖一與圖二 ) ,包 含可能源自於左心房的心房撲動 (atypical atrial flutters) 。經詳細解釋與討論,病人決定入院接受電氣生理檢查 與電氣燒灼治療。術前電腦斷層顯示左心房及左心耳無血栓,左心房有擴大 ( 約為 160 毫升 ) 。手術當日,病人心 律為 counter-clockwise isthmus-dependent atrial flutter( 如圖三 ) ,利用 entrainment method ,冠狀竇近端比遠端更 近 flutter circuit , 3 維傳播路徑圖為逆時針旋轉路徑。但是在 cavo-tricuspid isthmus 阻斷後, flutter 並未停止,發 生了訊號序列以及 cycle length 的變化,此時右側心房沒有辦法找到合適 entrainment 位置,經兩心房 3 維傳播路 徑圖判定病人之心律不整已轉變為源自左心房後壁之 atypical atrial flutter ,但是在左心房後壁阻斷後, flutter circuit 和 cycle length 仍不斷改變。在左心房經歷如同警匪追逐戰一般的多次阻斷以及訊號序列轉變後 ( 如圖四至 圖六 ) ,終於在冠狀竇 (coronary sinus) 遠端完成此病人的心律不整電氣燒灼手術 ( 如圖七 ) ,且無法再誘發。此病 人之心房撲動訊號序列變化與燒灼相關整理如圖八。術後病人恢復良好,胸悶心悸感已完全消除,固定於門診 領取抗凝血劑與低劑量抗心律不整藥物持續服用併追蹤。
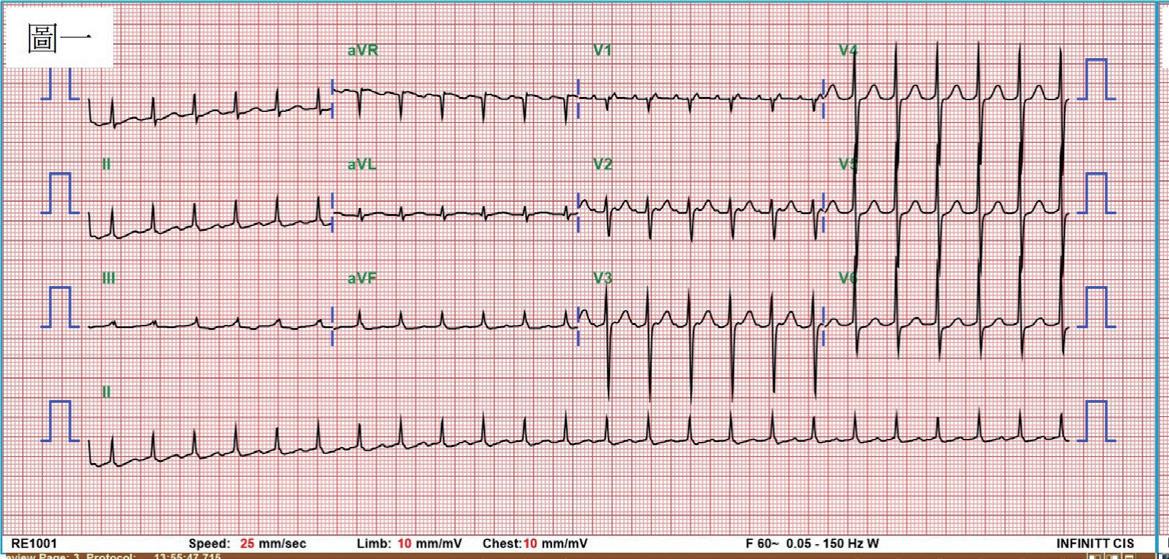
(圖一)、 病人臨床上偵測到的第一種心房撲動,雖然下壁導極有鋸齒狀之表現 (saw-tooth appearance), 但細看可發現其特徵並不是典型之表現。搭配V1導極之正向波,可能仍是一種源自左心房之 atypical atrial flutter?
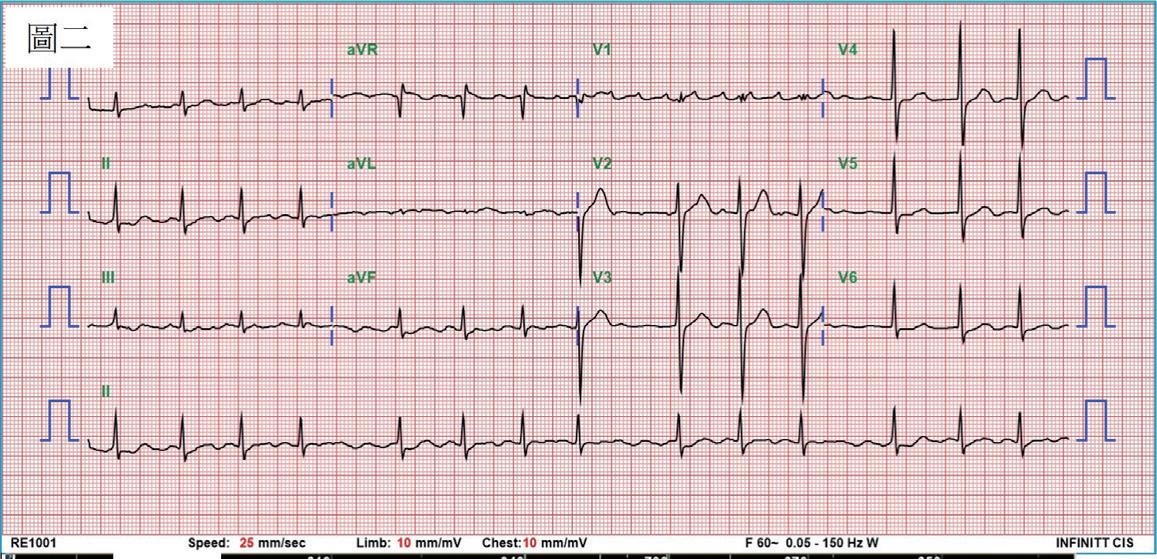
(圖二)、 病人臨床上偵測到的第二種心房撲動,心房之cycle length較第一種心房撲動略慢。下壁導極沒 有典型之鋸齒狀特徵,而且V1導極是正向波,應為一種源自左心房的atypical atrial flutter。
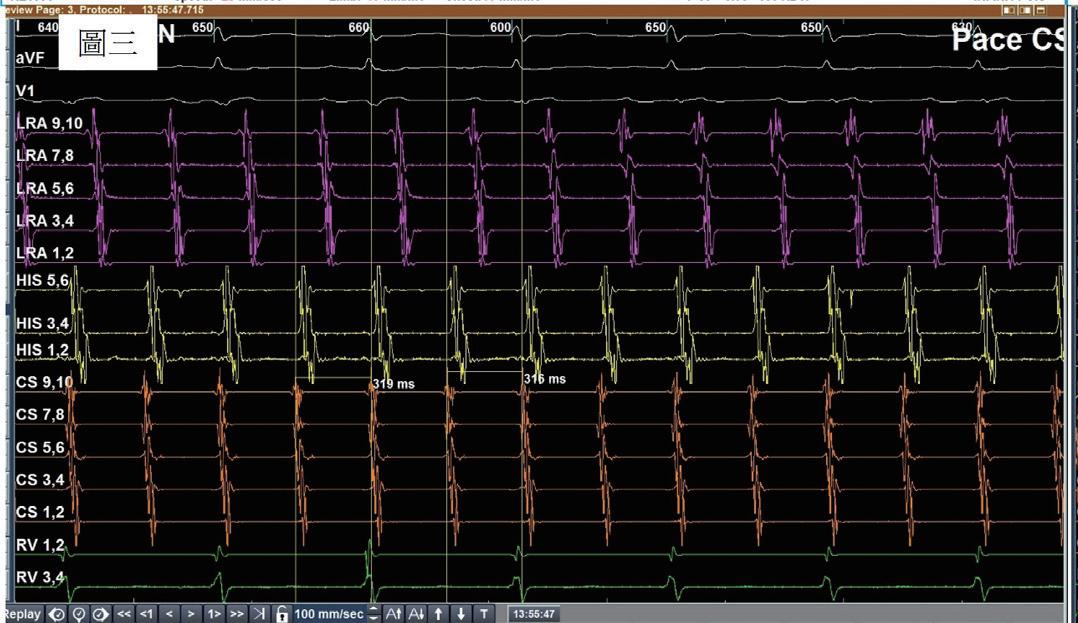
(圖三)、
病人接受電氣燒灼手術當天的 baseline rhythm 。為一個 counter-clockwise atrial flutter。透過entrainment method得知冠狀 竇近端較冠狀竇遠端更靠近flutter circuit。
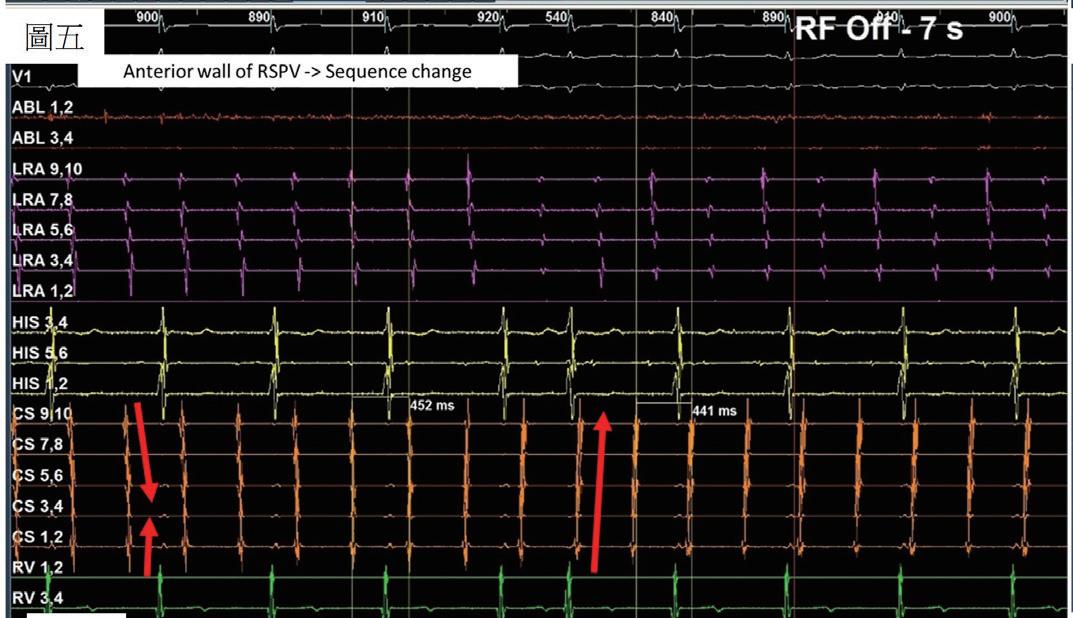
(圖五)、 Mapping後判斷可能之critical isthmus位 於right superior pulmonary vein開口之後 側與前側。針對這兩個位置電燒後,發 生第二次訊號序列變換,轉變為CS 1,2往 CS 9,10之走向。
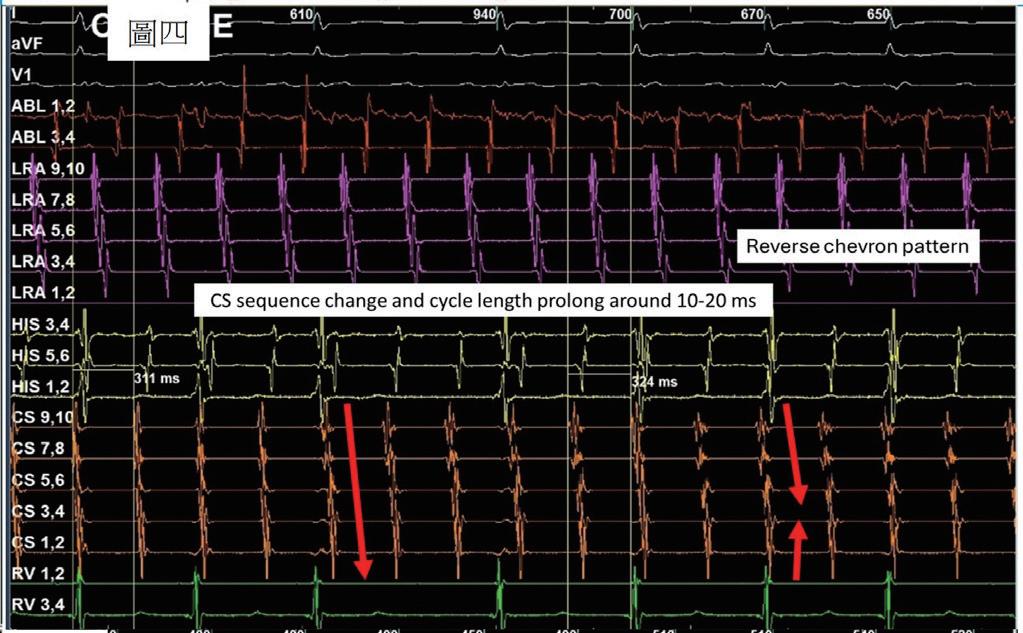
(圖四)、 病人接受cavo-tricuspid isthmus阻斷後發生 第一次sequence change。病人在CS的訊號序 列呈現“reverse chevron pattern”。而且右 心房無法順利 entrainment 。於是進行心房 中膈穿刺,前往左心房繼續治療心房撲動。
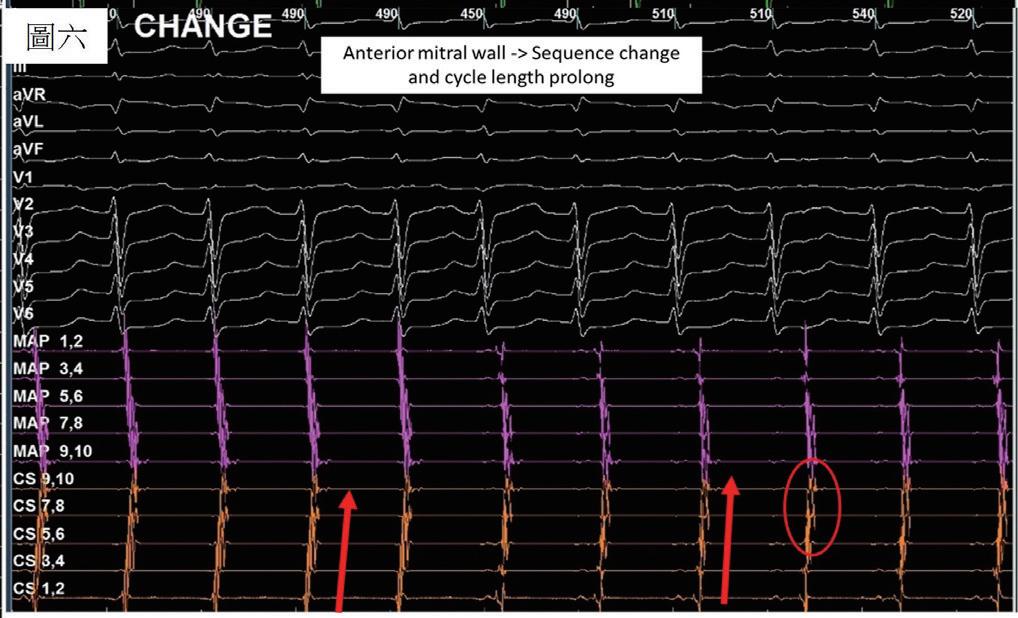
(圖六)、 Mapping後判斷轉為mitral flutter,於是先 針對anterior mitral line進行電燒。然而在 電燒過程中,訊號再次出現細微變化, CS 7,8,9,10出現一些碎裂分岔的訊號。
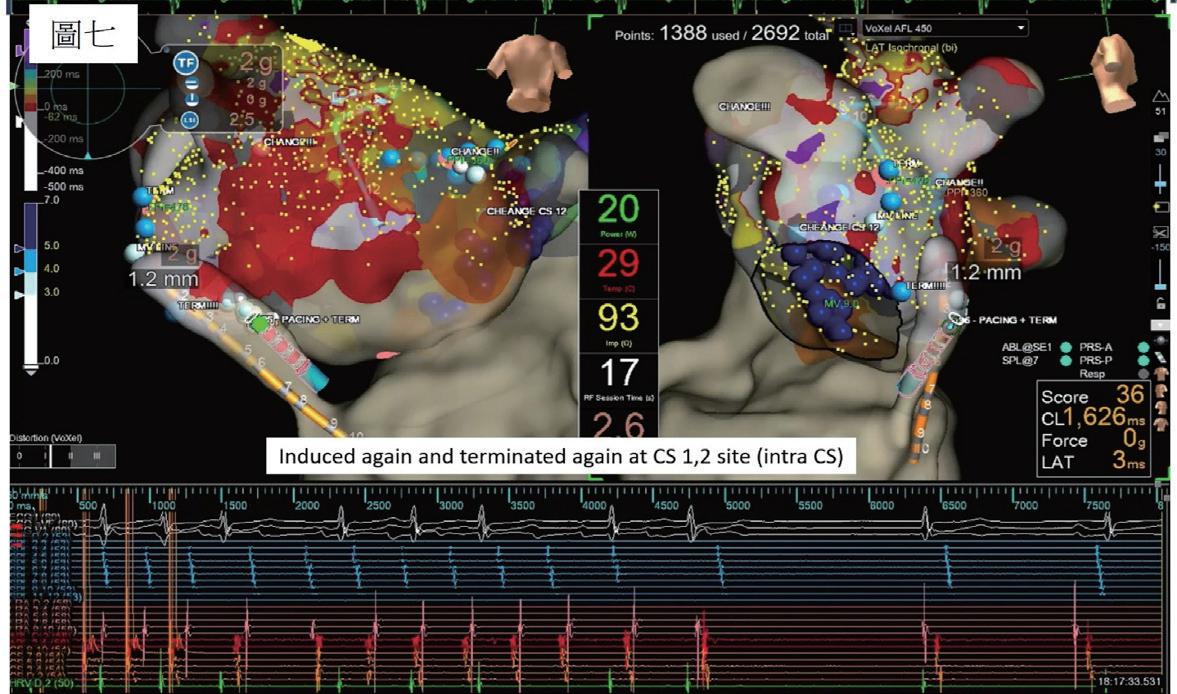
(圖七)、 冷靜下來後重新出發,判斷此時的心房撲動於 左心房側壁至 CS 1,2 之間是重要的 isthmus 。經歷 posterior mitral line 電燒,以及往 CS 1,2 延長電燒 範圍,最後將電燒管伸進冠狀竇,於CS 1,2位置進行 epicardium 電燒,順利終止病人的心律不整。
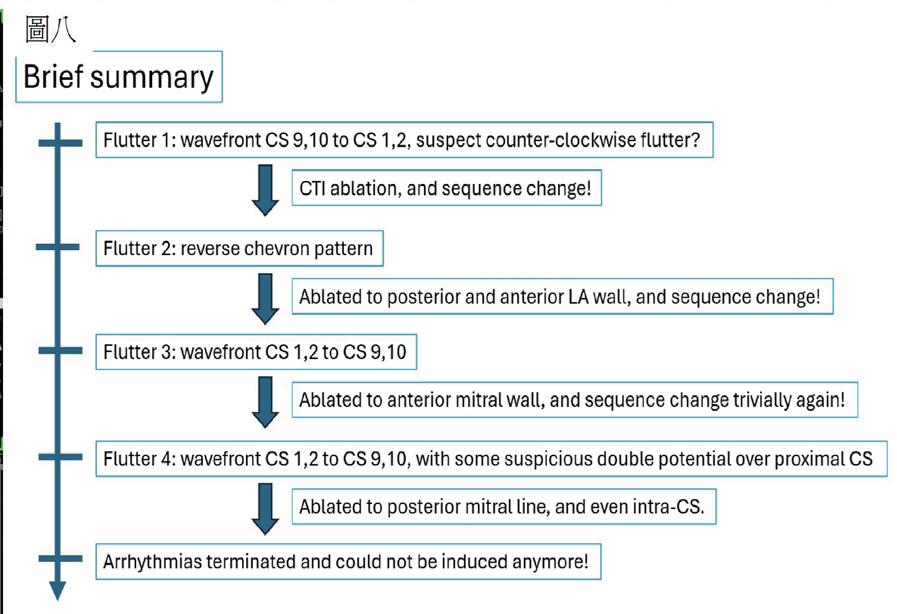
(圖八)、 病人於此次電氣燒灼手術中,發生 序列變化與電氣燒灼位置整理圖 表。
A
69-year-old man with "painful left bundle branch block syndrome"
高雄長庚紀念醫院 心臟血管內科 鄭又誠/陳煌中醫師
一名 69 歲男性,有高血壓及高血脂病史,因胸悶合併心悸至本院急診就診,心電圖顯示新發生的左束支傳 導阻斷 (left bundle branch block, LBBB) ( 圖一 ) 。病人曾接受多切心臟電腦斷層掃描顯示無明顯冠狀動脈狹窄, 且心臟超音波顯示左心室收縮功能正常且無心室肥厚,排除急性冠心症後返回門診追蹤。病人自述胸悶且心搏 過速時,智慧型手錶會顯示寬的 QRS 波心電圖,當回復窄的 QRS 波時症狀即緩解,臨床診斷懷疑是 painful LBBB症候群。初期以乙型阻斷劑控制症狀,但日常活動時仍間歇發作,後續嘗試以茶鹼(theophylline 100mg BID) 治療後,目前症狀緩解未再復發,後續心電圖並未有 LBBB 之情形 ( 圖二 ) ,且智慧型手錶顯示寬的 QRS 波心電圖 頻率也大幅下降。
LBBB 可見於多種心臟病理或隨年齡增加而出現,但大多不伴隨典型胸痛,而 painful LBBB 症候群定義為 每當 LBBB 發生就伴隨胸痛,通常與速率相關,且須排除心臟缺血。機轉推測為心室不同步收縮導致心肌張力 與牽張改變,而引起胸痛症狀。與慢性 LBBB 有所區別,文獻中提及 painful LBBB 症候群的心電圖胸前導程會呈 現極低的 S/T wave ratio(<1.8) 及 inferior QRS axis ,本個案有低的 S/T wave ratio 為 1.43 。此症候群多為速率相關 ( 如運動、情緒或心率上升時出現 ) ,常導致病人被延誤診斷,或反覆至急診就診或接受檢查。文獻建議首選為心 率控制 ( 乙型阻斷劑或 ivabradine) ,另可藉運動訓練提高出現 LBBB 的心率閾值,亦有茶鹼 (theophylline) 治療成 功之個案報告。當藥物治療失敗時,有報導指出傳導系統刺激 (Conduction System Pacing) 如 His bundle pacing 與 left bundle branch area pacing 可恢復生理性心室去極化來緩解症狀。本個案因無適應症裝置心臟節律器,經向 病人說明後使用茶鹼控制症狀,目前於心臟內科門診穩定追蹤中。
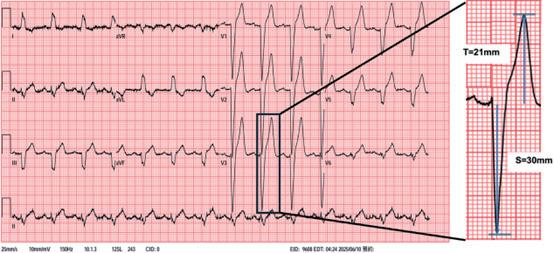
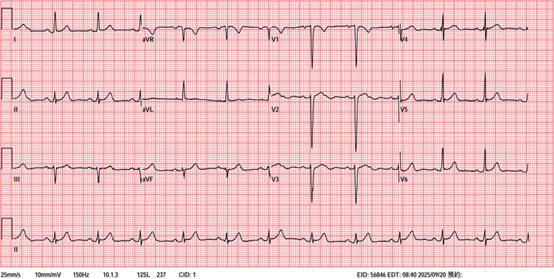
(圖一)、 急診時12導程心電圖顯示左束支傳導阻斷, 其V3 S/T ratio為1.43 (<1.8) (圖二)、 後續於門診接受茶鹼 (theophylline) 治 療後LBBB未再復發
Reference:
1. Anyaso CJ, et al. Painful Left Bundle Branch Block Syndrome Diagnosed in the Emergency Department. J Emerg Med. 2025 Aug;75:218221. doi: 10.1016/j.jemermed.2025.02.017
2. Konstantinou CS, et al. Painful left bundle branch block: A syndrome with a particular clinical significance. J Cardiol Cases. 2020 Jul 29;22(6):273-275. doi: 10.1016/j.jccase.2020.07.003
3. Shvilkin A, et al. Painful left bundle branch block syndrome: Clinical and electrocardiographic features and further directions for evaluation and treatment. Heart Rhythm. 2016 Jan;13(1): 226-32. doi: 10.1016/j.hrthm.2015.08.001
4. Amir R, et al. Oral theophylline for treatment of painful left bundle branch block. HeartRhythm Case Rep. 2023 May 18;9(6): 342-346. doi: 10.1016/j.hrcr.2023.02.017
Left Atrium Appendage Occlusion (LAAO)
臨床實證與展望
基隆長庚紀念醫院 心臟內科 陳韋翔醫師
左心耳(left atrium appendage,LAA)的致血栓性
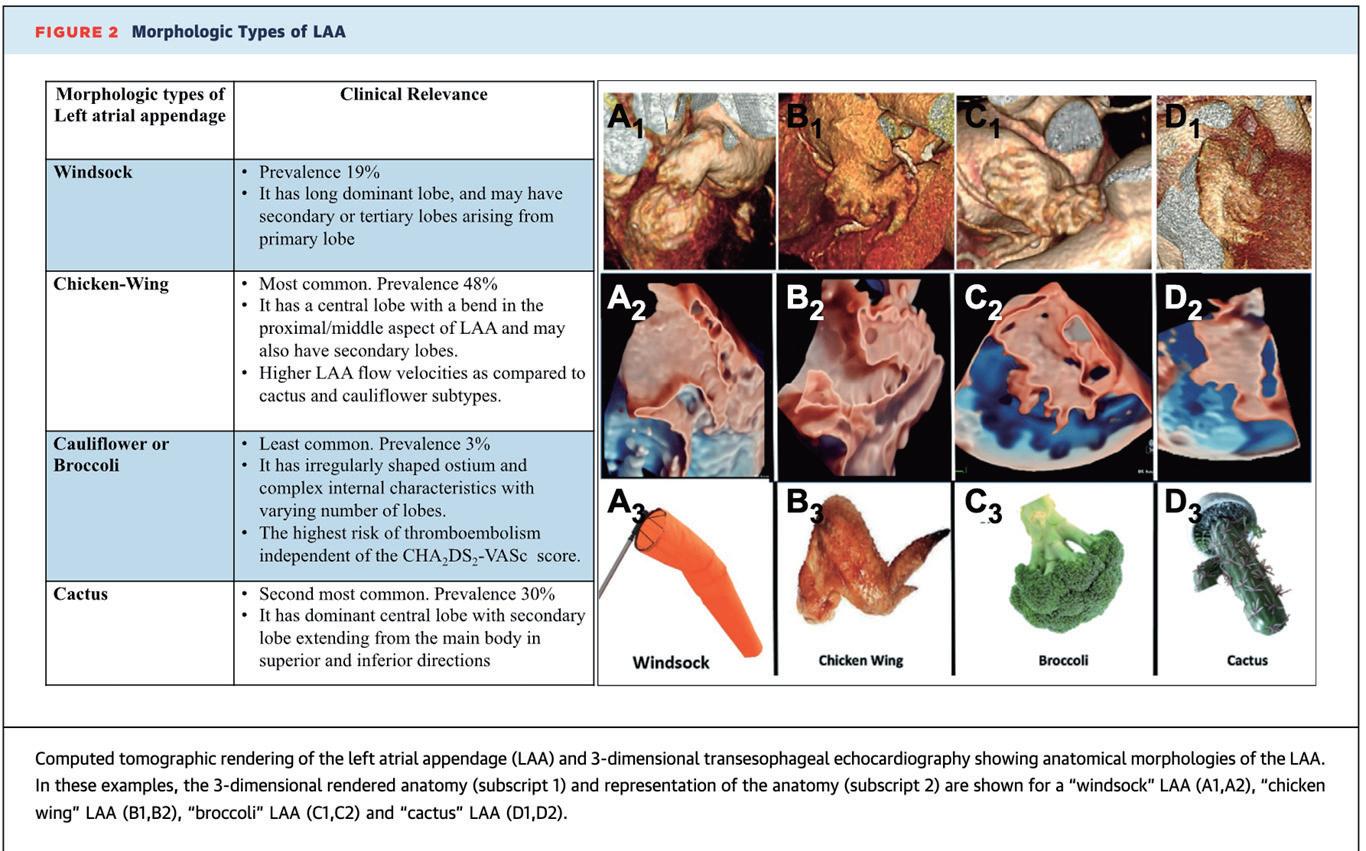
LAA 是形成 90% 非瓣膜性心房顫動血栓 (non-valvular AF) 與 57% 瓣膜性心房顫動血栓 (valvular AF)1。心房顫動 患者的血小板活化與凝集會加強,再合併內皮細胞功能異常,導致血栓形成的活性增強2。臨床上有幾種常見的型 態,包括風向袋(windsock)、雞翅(chicken-wing)、花椰菜(cauliflower)與仙人掌(cactus)3。
SURGICAL LAA EXCLUSION. 外科手術左心耳閉合。
AtriClip LAA exclusion system(AtriCure)左心耳閉夾鉗合器,在開心手術時同時執行4。
LARIAT LAA EXCLUSION, epicardial suture ligation,心包膜表面縫合結紮器5。
ENDOCARDIAL LAA EXCLUSION經心內左心耳閉合。
2005年PLAATO system的使用,開啟了經皮經心內左心耳閉合的時代6。時至今日,波士頓科技的Watchman與亞培 公司的Amulet均被核准在市場上使用。
PATIENT SELECTION病患選擇
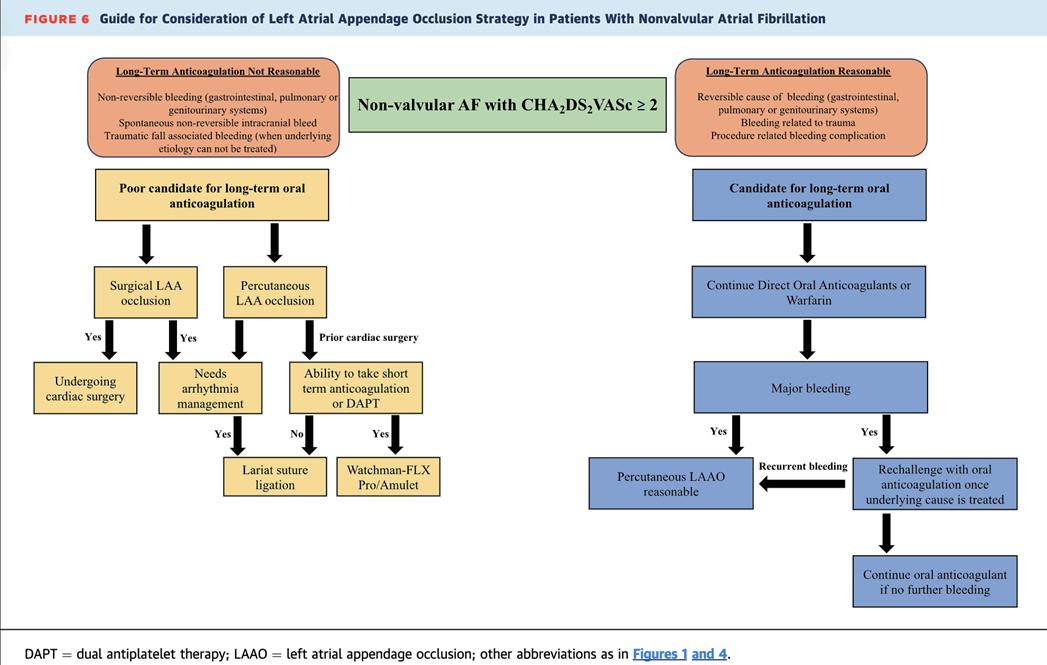
根據治療指引建議(2023 ACC/AHA/HRS guideline for AF management),CHA2DS2-VA大於等於2分應行口服抗凝 血劑治療,但如果同時HAS-BLED大於等於3分又有高出血風險。因此,在非瓣膜性心房顫動患者考慮左心耳閉合術 應有以下幾個考量:1.依據CHA2DS2-VA評估患者的全身血栓與中風風險,以及是否有不可逆的長期服用抗凝血藥 禁忌症7。2.重大出血病史。3.患者整體情況,包含慢性共病,跌倒風險,預期餘命,患者偏好與抗凝藥的順從性8。
以下圖示可作為LAAO的策略選擇。
PREPROCEDURAL IMAGING術前影像學
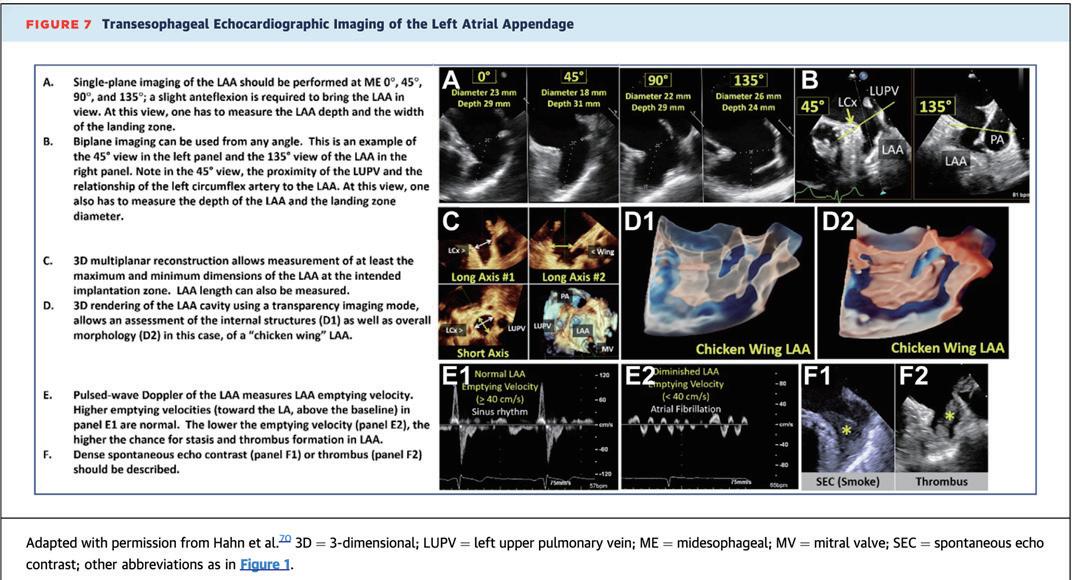
術前影像學評估包含經食道超音波 (TEE) 與電腦斷層血管攝影 (CTA) 能有很大幫忙。主要能了解: 1. 左心耳是 否有血栓。
2. 左心耳構造與大小,用於導引閉合器尺寸選擇。
3. 評估周邊構造,如左心房,左迴旋冠狀動脈,心 房中隔,並決定適當的心房中隔穿刺角度。
至少128切的CTA被推薦使用,腎絲球濾過率<30 mL/min的患者應謹慎評估CTA。運用立體重組與軟體運算, 可以與手術中3D TEE有很好的相關性,決定LAA開口,閉合器施放處,且預估閉合器滲漏(peri-device lead, PDL) 9。
PERIPROCEDURAL IMAGING術中影像學
術中最重要的影像學當數TEE或心內超音波(ICE),TEE仍然是黃金標準,尤其在手術開始前確認LA或LAA有 無血栓,並在3D TEE的應用下,將影像調整至解剖學或手術視野10。
ICE的使用,吸引了許多注目。主要在於可以單一手術醫師完成,並且不需要全身麻醉,進一步改善了手術效 率。ICE導引的LAAO必須將ICE放到LA,所以需要擴張心房中隔甚至2次穿刺心房中隔;整體而言,使用ICE執行 LAAO 需要更多手術經驗 11 。傳統 ICE 缺乏多角度視野與立體影像,因此新一代 4D ICE 被發展出來 (NuVision ICE, Biosense Webster, and VeriSight Pro ICE, Philips)。
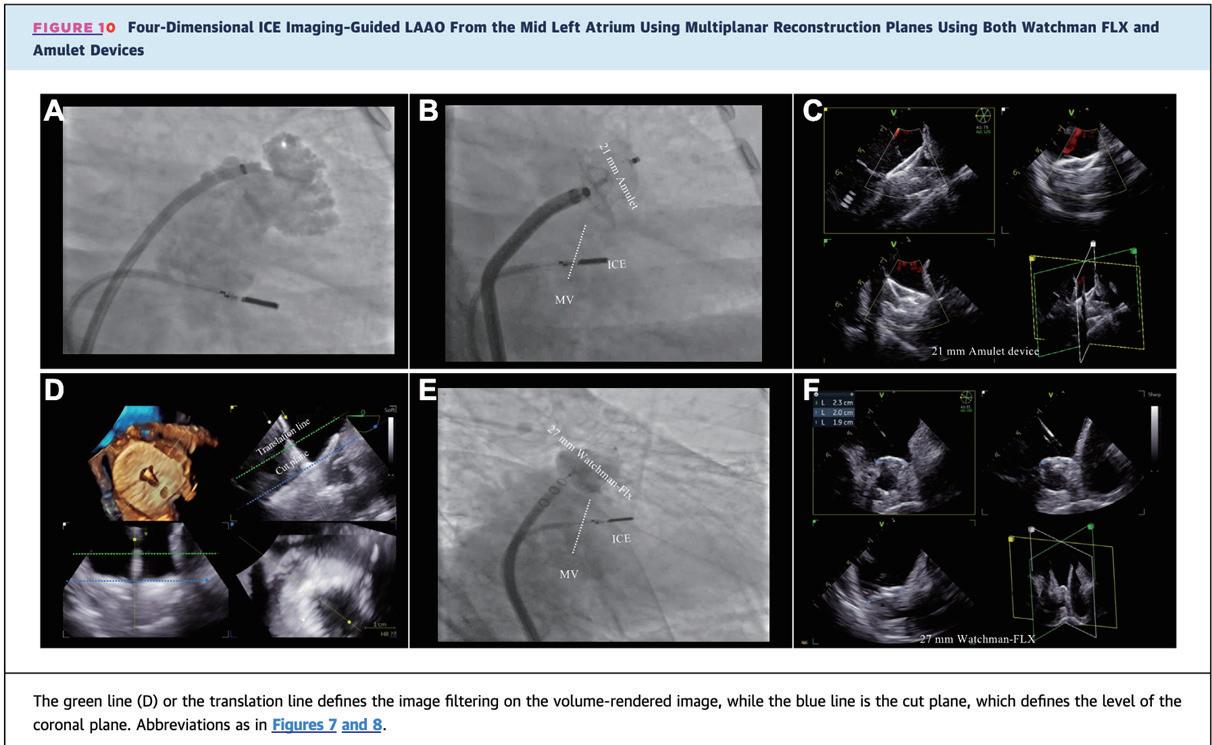
Percutaneous LAAO procedure:
1. 右股靜脈穿刺,在超音波導引下; 術後止血可採用直接加壓,8字型縫合法(figure of 8)或血管止血器(如Perclose, Abbott)。
2. 心房中隔穿刺(TSP, transeptal puncture )在TEE或ICE指引下,應朝後下(inferoposteriorly),朝上的方位應該避免。
3. 在豬尾巴導管的導引下將閉合器的輸送導鞘送至LAA。此舉可降低LAA破裂風險。輸送導鞘應仔細進行空氣的 排空,避免空氣栓塞12。
4. 閉合器尺寸選擇根據術前與術中的影像學測量,特別是術中測量應在LA壓力大於等於12mmHg的條件下。
5. 依據不同的閉合器,有預設的符合可施放標準。Watchman FLX, PASS criteria: position, anchor, size, seal。Amulet , CLOSE criteria: circumflex, lobe, orientation, separation, ellipitical。
LAAO併發症
嚴重的狀況包含了心包膜填塞(PE),閉合器脫離(device embolization)與術中中風。心包膜填塞(PE)在早期的嚴重 追蹤有4.8%,而在更近期的文獻中逐年下降至0.5~1%。通常24小時內發生的心包膜填塞與病患一年死亡率相關13。 早期發現,搶救,甚而第一線手術介入有機會減少死亡率。
閉合器脫離是另一個造成高死亡率的合併症,最常在置放後的 5 分鐘內發生。施放閉合器後可以考慮觀察 5 分 鐘。
術中血栓中風常在 24 小時內發生。可能是空氣栓塞,術中凝血控制不足 (ACT<250~300 秒) 或 LA 血栓。故適當 準備輸送導鞘與監控凝血時間可減少此問題。
PDL閉合器旁滲漏
事實上關於 PDL 並沒有明確定義,但一般指閉合器術後 LA 與LAA 仍有溝通。 TEE 常用來做術後追蹤,而對於 明確的心臟內皮細胞覆蓋閉合器,無法明確偵測。
CTA
漸漸成為客觀的追蹤影像檢查,可以分辨滲漏位置,有無 血栓14。根據PRAGUE-17 trial,PDL小於3mm被認為可接受15。而有趣的是PROTECT AF trial中,1~3mm滲漏相較 於 3mm 以上滲漏,有較高的缺血性中風與全身血栓。或許最好的處理方式為藉由良好的事前準備,改善手術經驗 與新一代閉合器設計,不要產生PDL。
中華民國心律醫學
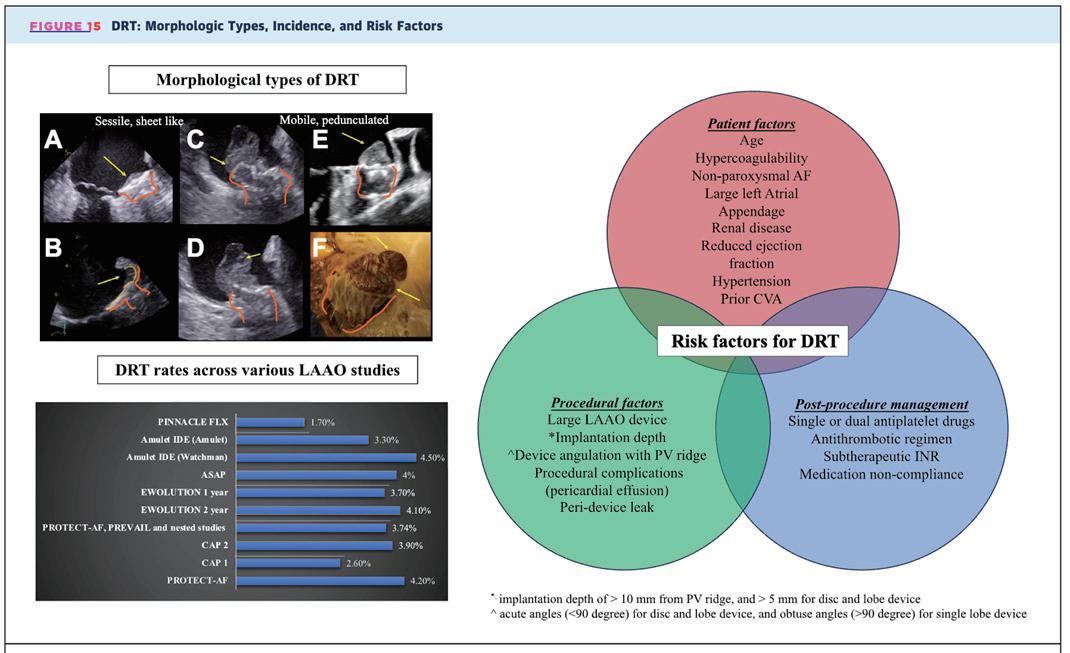
DRT (DEVICE-RELATED THROMBUS) 閉合器血栓
DRT 的發生率在不同研究與追蹤時間中,盛行率為 1.7~4.5% 。圖示為可能的風險因子。 DRT 會同時增加死亡 率,缺血性中風;並且必須重啟抗凝血藥物而增加出血性中風 16 。立刻開始使用抗凝血藥為直覺反應,但有個問 題:許多患者是抗凝藥耐受不良而選擇閉合器手術,或就算使用抗凝藥仍有 20~25% 持續有 DRT 。再者,即使第一 次DRT緩解,更有35%復發。DRT的發生仍是一個待解決的問題。
LAAO術後的抗血栓藥物處方
最理想的處方仍無定論,最早是warfarin加aspirin 45天,降階為aspirin加clopidogrel 6個月,然後終生aspirin。 在PINNACLE-FLX研究中演變為direct oral anti-coagulation(DOAC)加 aspirin 45天。歐洲的研究中,則大多使用雙 重抗血小板藥物。然而,部分病人即使是短期抗凝藥或雙重抗血小板藥物都發生流血事件,此類病人應該使用單 一抗血小板藥物或完全不用藥還沒有定論,當然是因為DRT可能發生。
LAAO與warfarin,DOAC,ablation
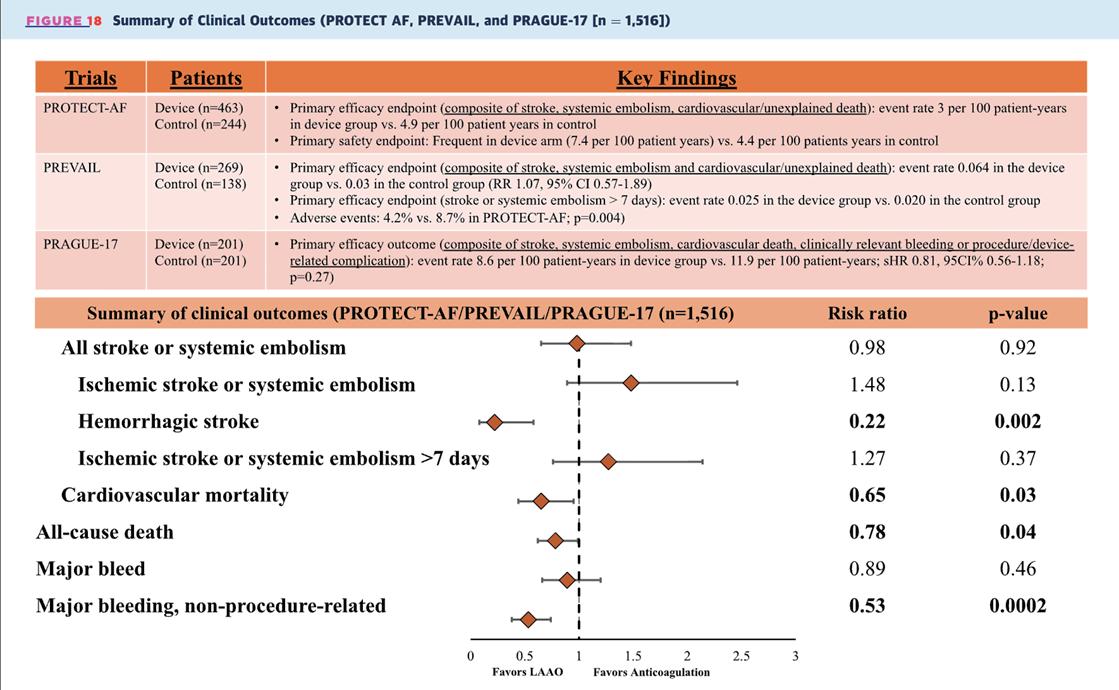
在PROTECT AF與PREVAIL研究中,LAAO相較於warfarin有效減少出血性中風,失能/致死性中風以及全因死 亡率。在 PRAGUE-17 研究中, LAAO 在死亡,全身血栓,心血管死亡,重大出血的綜合總和試驗終點,達到不輸 於DOAC的效果。
OPTION trial,此臨床試驗評估心房顫動患者,接受電燒手術後,持續服用抗凝血藥與進行LAAO的隨機對照 試驗。 LAAO 組在重大出血試驗終點贏過抗凝藥組,在死亡率 /全身血栓 /中風的總和終點與抗凝藥組相當。暗示著 電燒手術與LAAO的結合,能降低出血事件與有效減少中風17。
總結:LAAO在2023年ACC/AHA的AF治療指引第一次拿到class IIa indication,建議在無法長期耐受抗凝藥患 者使用。而2024年ESC 的AF治療指引仍停在class IIb indication,主要的理由在安全顧慮,如前所述 PDL與DRT的發 生。閉合器的改善,手術醫師的經驗累積與臨床實證的累積,使得心房顫動患者的中風預防,在藥物以外,LAAO 仍有其角色存在。未來,將有更多的臨床試驗結果,包含洗腎患者的應用, LAAO 術後單一抗血小板藥物的實 證,LAAO直接對決DOAC等等。精彩可期。
Reference
1. Blackshear, Joseph L., and John A. Odell. "Appendage obliteration to reduce stroke in cardiac surgical patients with atrial fibrillation." The Annals of thoracic surgery 61.2 (1996): 755-759.
2. Tilly, Martijn J., et al. "The association of coagulation and atrial fibrillation: a systematic review and meta-analysis." Europace 25.1 (2023): 28-39.
3. Di Biase, Luigi, et al. "Does the left atrial appendage morphology correlate with the risk of stroke in patients with atrial fibrillation? Results from a multicenter study." Journal of the American College of Cardiology 60.6 (2012): 531-538.
4. Ailawadi, Gorav, et al. "Exclusion of the left atrial appendage with a novel device: early results of a multicenter trial." The Journal of thoracic and cardiovascular surgery 142.5 (2011): 1002-1009.
5. Bartus, Krzysztof, et al. "Percutaneous left atrial appendage suture ligation using the LARIAT device in patients with atrial fibrillation: initial clinical experience." Journal of the American College of Cardiology 62.2 (2013): 108-118.
6. Ostermayer SH, Reisman M, Kramer PH, et al. Percutaneous left atrial appendage transcatheter occlusion (PLAATO system) to prevent stroke in high-risk patients with non-rheumatic atrialfibrillation: results from the international multicenter feasibility trials. J Am Coll Cardiol. 2005;46(1):9–14.
7. Joglar, José A., et al. "2023 ACC/AHA/ACCP/HRS guideline for the diagnosis and management of atrial fibrillation: a report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines." Journal of the American College of Cardiology 83.1 (2024): 109-279.
8. Daimee, Usama A., et al. "Indications for left atrial appendage occlusion in the United States and associated in-hospital outcomes: results from the NCDR LAAO registry." Circulation: Cardiovascular Quality and Outcomes 15.8 (2022): e008418.
9. Korsholm, Kasper, et al. "Expert recommendations on cardiac computed tomography for planning transcatheter left atrial appendage occlusion." Cardiovascular Interventions 13.3 (2020): 277-292.
11. Velagapudi, Poonam, et al. "Intracardiac vs transesophageal echocardiography for percutaneous left atrial appendage occlusion: a meta analysis." Journal of Cardiovascular Electrophysiology 30.4 (2019): 461-467.
12. Kewcharoen J, Shah K, Bhardwaj R, et al. Adverse events associated with Amplatzer left atrial appendage occlusion delivery system: a Food and Drug Administration MAUDE database study. J Cardiovasc Electrophysiol. 2023;34(11): 2382–2385.
13. 84. Galea R, Bini T, Krsnik JP, et al. Pericardial effusion after left atrial appendage closure: timing, predictors, and clinical impact. JACC Cardiovasc Interv. 2024;17(11):1295–1307.
14. Rajiah P, Alkhouli M, Thaden J, Foley T, Williamson E, Ranganath P. Pre- and postprocedural CT of transcatheter left atrial appendage closure devices. Radiographics. 2021;41(3):680–698.
15. Osmancik P, Herman D, Neuzil P, et al. Left atrial appendage closure versus direct oral anticoagulants in high-risk patients with atrial fibrillation. J Am Coll Cardiol. 2020;75(25):3122–3135.
16. Dukkipati SR, Kar S, Holmes DR, et al. Devicerelated thrombus after left atrial appendage closure: incidence, predictors, and outcomes. Circulation. 2018;138(9):874–885.
17. Wazni OM, Saliba WI, Nair DG, Marijon E, Schmidt B, Hounshell T, Ebelt H, Skurk C, Oza S, Patel C, Kanagasundram A, Sadhu A, Sundaram S, Osorio J, Mark G, Gupta M, DeLurgio DB, Olson J, Nielsen-Kudsk JE, Boersma LVA, Healey JS, Phillips KP, Asch FM, Wolski K, Roy K, Christen T, Sutton BS, Stein KM, Reddy VY; OPTION Trial Investigators. Left Atrial Appendage Closure after Ablation for Atrial Fibrillation. N Engl J Med. 2025 Apr 3;392(13):1277-1287. doi: 10.1056/ NEJMoa2408308. Epub 2024 Nov 16. PMID: 39555822.
18. Garg J, Kabra R, Gopinathannair R, Di Biase L, Wang DD, Saw J, Hahn R, Freeman JV, Ellis CR, Lakkireddy D. State of the Art in Left Atrial Appendage Occlusion. JACC Clin Electrophysiol. 2025 Mar;11(3):602-641. doi: 10.1016/j.jacep.2024.10.024. Epub 2025 Jan 8. PMID: 39797854.
10. Hahn, Rebecca T., et al. "Recommended standards for the performance of transesophageal echocardiographic screening for structural heart intervention: from the American Society of Echocardiography." Journal of the American Society of Echocardiography 35.1 (2022): 1-76.