Analizador Multiparamétrico
Totalmente Automatizado
Dispositivo individual de un solo uso que contiene
todos los reactivos necesarios para realizar el ensa
Capacidad multiparamétrico: Procesa hasta 30 diferentes pruebas por corrida.
La velocidad permite obtener resultados simultáneos de diferentes paneles.
El primer resultado se obtiene antes de 90 minutos.
Volumen de muestra:
La muestra se dispensa manualmente ELISA:
Mínimo de muestra 60 uL.
Enfermedades Infecciosas
ADENOVIRUS IgA
ADENOVIRUS IgG
BORDETELLA PERTUSSIS IgA
BORRELIA IgG
BORRELIA IgM
BRUCELLA IgG
BRUCELLA IgM
CHIKUNGUNYA IgG
CHIKUNGUNYA IgM
CHLAMYDOPHILA PNEUMONIAE IgA
CHLAMYDOPHILA PNEUMONIAE IgG
CHLAMYDOPHILA PNEUMONIAE IgM
CLOSTRIDIUM DIFFICILE A/B TOXINS
CLOSTRIDIUM DIFFICILE GDH
COXACKIE VIRUS A MIX
COXACKIE VIRUS B MIX
CYTOMEGALOVIRUS IgG
CYTOMEGALOVIRUS IgG AVIDITY
CYTOMEGALOVIRUS IgM
DENGUE IgG
DENGUE IgM
DIPHTERIA IgG
ECHINOCOCCUS IgG
ECHO VIRUS N MIX
ECHO VIRUS P MIX
EPSTEIN-BARR EARLY ANTIGEN IgG
EPSTEIN-BARR EARLY ANTIGEN IgM
EPSTEIN-BARR EBNA IgG
EPSTEIN-BARRVCA IgG
EPSTEIN-BARR VCA IgM II
HELICOBACTER PYLORI IgA
HELICOBACTER PYLORI IgG
HSV1 SCREEN
HSV2 SCREEN
HERPES SIMPLEX 1 IgG Recombinant
HERPES SIMPLEX 1+2 IgM
HERPES SIMPLEX 2 IgG Recombinant
INFLUENZA A IgA
INFLUENZA A IgG
INFLUENZA B IgA
INFLUENZA B IgG
LEGIONELLA PNEUMOPHILA
LEGIONELLA PNEUMOPHILA 1 IgG
LEGIONELLA PNEUMOPHILA 1-6 IgG
LEGIONELLA PNEUMOPHILA IgM
LEGIONELLA URINARY ANTIGEN
LEPTOSPIRA MIX
LISTERIA MONOCYTOGENES
MEASLES IgG
MEASLES IgM
MUMPS IgG
MUMPS IgM
MYCOPLASMA PNEUMONIAE IgA
MYCOPLASMA PNEUMONIAE IgG
MYCOPLASMA PNEUMONIAE IgM
PARAINFLUENZA MIX
Parvovirus B19 IgG
Parvovirus B19 IgM
POLIOVIRUS IgG
Q FEVER
RESPIRATORY SYNCYTIAL IgA
RESPIRATORY SYNCYTIAL IgG
RUBELLA IgG AVIDITY
RUBELLA IgG
RUBELLA IgM
SYPHILIS SCREEN RECOMBINANT
TETANUS IgG
TICK-BORNE ENCEPHALITISVIRUS
TOXOPLASMA IgG
TOXOPLASMA IgM
TRACHOMATIS IgA
TRACHOMATIS IgG
TREPONEMA IgG
TREPONEMA IgM
VARICELLA IgG
VARICELLA IgM
25 OHVITAMIN DTOTAL
TICK-BORNE ENCEPHALITIS VIRUS IgM
TIROGLOBULIN HIGH SENSITIVITY
TOSCANAVIRUS IgG
TOSCANAVIRUS IgM
TOXOCARA IgG
TOXOPLASMA IgA
TOXOPLASMA IgG AVIDITY
ANA-8
ANA-SCREEN
ENA-6 S
SM
SS-A
SS-B
Scl-70
Cenp-B
Jo-1
ds-DNA-G
ds-DNA-M
snRNP-C
U1-70 RNP
anti-CCP
RF-G
RF-M
CALPROTECTIN
CALPROTECTIN K
CARDIOLIPIN-G
CARDIOLIPIN-M
BETA 2-GLYCOPROTEIN-G
BETA 2-GLYCOPROTEIN-M
DEAMIDATED GLIADIN-A
DEAMIDATED GLIADIN-G
GLIADIN-A
Editorial
La actualización permanente y la difusión del conocimiento constituyen pilares esenciales para el desarrollo de la bioquímica clínica y del laboratorio como herramientacentralenlatomadedecisionesensalud. Enestaediciónpresentamosunainvestigaciónqueaborda los desafíos diagnósticos de la anemia hemolítica autoinmune con prueba de Coombs negativa, destacando el aporte de la citometría de flujo para detectar autoanticuerpos eritrocitarios y mejorar la precisión diagnósticaensituacionescomplejas.
Otro estudio analiza la frecuencia de factores de riesgo cardiovascular en mujeres durante la perimenopausia y la posmenopausia, evidenciando una elevada prevalencia de sedentarismo, exceso de peso y otros determinantes asociados a enfermedad cardiovascular.
Asimismo, se exploran los desafíos emergentes vinculados al uso de inteligencia artificial en medicina de laboratorio, destacando la necesidad de marcos de evaluación que garanticen la precisión, fiabilidad y calidad de la información generada por modelos de lenguaje comoChatGPT
Estos trabajos reflejan el compromiso permanente con la investigación, la innovación y la actualización profesional, pilares fundamentales para fortalecer el rol dellaboratorioclínicoenelsistemadesalud.
Agradecemos a nuestros lectores por acompañarnos en este espacio de intercambio científico y los invitamos a seguir compartiendo conocimiento. Nos reencontramos en la próxima edición de Revista Bioanálisis.
Dra. Paola Boarelli Directora de Contenidos
Staff Revista Bioanálisis
Teléfono: (54 261) 681-6777 - Horario de Atención: de 9 a 17 hs.
Dirección General: Lic. Daniela Lamy I dlamy@revistabioanalisis.com
Directora de Marketing: Elda Bordin I mkt@revistabioanalisis.com
Directora de Contenidos: Dra. Paola Boarelli I contenidos@revistabioanalisis.com
de flujo en pacientes con anemia hemolítica autoinmune caliente con prueba de Coombs negativa Pág. 8.
Hipertensión arterial secundaria a feocromocitoma de causa genética e hipoatrofia renal en edad pediátrica
Pág. 18.
Formación de Posgrado. Pág 60
BioAgenda // Empresas. Pág 62 >> >>
Factores de riesgo cardiovascular en mujeres en etapa de perimenopausia y postmenopausia
Pág 28.
Aplicaciones y retos de ChatGPT en la medicina de laboratorio
Pág 38.
Citometría
de flujo en pacientes con anemia
hemolítica
autoinmune caliente con prueba de Coombs negativa
Este artículo destaca la utilidad de la citometría de flujo para diagnosticar con precisión la anemia hemolítica autoinmune caliente con prueba de Coombs negativa, facilitandodiagnósticosmássensiblesyconfiables.
>>> AUTORES
1*
1 Yisenia Romero Díaz , Mariela Forrellat Barrios , Alexis 2 MoránFernández
1 Ins�tuto de Hematología e Inmunología, La Habana, Cuba,
2 Hospital Pediátrico Docente Juan Manuel Márquez, La Habana,Cuba
Correspondencia:yisi2801@gmail.com
Fuente: Revista Cubana de Hematología, Inmunología y Hemoterapia.2025;41:e2219
RESUMEN
Introducción: La anemia hemolí�ca autoinmune es una enfermedad caracterizada por la presencia de an�cuerpos dirigidos contra an�genos eritrocitarios propiosdelpaciente.Eldiagnós�coinmunohematológico se basa fundamentalmente en la evidencia de autoan�cuerpos en los eritrocitos mediante la prueba de an�globulina directa (PAD); sin embargo, en ocasiones estaresultanega�va.
Obje�vo: Aplicar la técnica de citometría de flujo
al diagnós�co de las anemias hemolí�cas autoinmunes calienteconPADnega�vaenelIns�tutodeHematologíae Inmunología.
Métodos: Se realizó un estudio exploratorio, transversal de �po inves�gación desarrollo y evaluación de tecnología. Se analizó la suspensión de eritrocitos de 72 pacientes con sospecha de anemia hemolí�ca autoinmune, en el Ins�tuto de Hematología e Inmunologíaentre2020y2024.
Resultado: De las 72 muestras estudiadas, 35 (48,6 %) correspondían al sexo femenino y 37 (51,4 %) al sexo masculino. Se detectaron autoan�cuerpos en 39 muestras, 54,16 % del total estudiado, de ellas 28 presentaron fluorescencia para el iso�po IgG, 8 para el iso�poIgMy3paraeliso�poIgA
Conclusiones: La citometría de flujo es una herramientaqueproporcionacertezaeneldiagnós�code las anemias hemolí�cas autoinmunes caliente PAD nega�va, la que usualmente es un desa�o para el diagnós�coclásico.
Palabras clave: citometría de flujo; anemias hemolí�cas autoinmunecaliente;pruebaan�globulinadirecta.
INTRODUCCIÓN
Lasanemiashemolí�casautoinmunes(AHAI)son elresultadodelareduccióndelavidamediadeleritrocito por mecanismos inmunológicos y el incremento de la hemólisis.Elcuadroanémiconosiempreestápresente,ya que la médula ósea �ene la capacidad de aumentar la produccióndeeritrocitosquecompensaladestrucción;lo que resulta en un estado hemolí�co sin anemia.(1) Se caracteriza por la producción de an�cuerpos dirigidos contralosglóbulosrojospropioscomoconsecuenciadela existencia de autoan�cuerpos (auto-Ac) dirigidos contra elementos an�génicos de la membrana eritrocitaria
Dado que, en general, los auto-Ac se dirigen contra an�genosdealtaincidencia,amenudotambiénmuestran reac�vidad contra los glóbulos rojos alogénicos. La AHAI es un trastorno poco común, con es�maciones de incidencia de 1 a 3 casos por 100 000 por año. (2,3)
E�ológicamente, se pueden clasificar en AHAI secundariasyprimariasoidiopá�cas.
La AHAI de �po caliente es la más frecuente y aparece, generalmente, después de los 40 años de edad. Las enfermedades que con mayor frecuencia se asocian con AHAI son las linfoprolifera�vas, el lupus eritematoso sistémico, la artri�s reumatoide y la coli�s ulcera�va. En este�pode AHAI predominanlosan�cuerposde�poIgG yocasionalmenteIgA (4,5,6,7)
Su incidencia anual es de 1/25 000 - 1/ 80 000 casos/año, aunque es probable que estos datos subes�man su incidencia debida, en parte, a las dificultades en la comprensión de los estudios diagnós�cos; por lo que la no disponibilidad de un protocolo definido, origina demoras innecesarias e inexac�tudes en la definición del sub�po de la enfermedadysucausa.(5,6,7,8)
La prueba de an�globulina directa (PAD) mediante la técnica en tubo o prueba de Coombs directa es el método más comúnmente u�lizado y la prueba de referencia para el diagnós�co de AHAI Sin embargo, una PAD nega�va no excluye el diagnós�co de esta enfermedad, ya que entre el 2 y el 10 % de los pacientes con las caracterís�cas clínicas de AHAI, exhiben una PAD nega�va. El diagnós�co de AHAI PAD nega�va se basa en el método de exclusión de otras posibles causas. Estos factores incluyen: la existencia de inmunoglobulina G (IgG) unida a glóbulos rojos en niveles demasiado bajos para ser detectados con los métodos estándar; la unión rela�vamentedébildelaIgG;lafaltadeuneluidoposi�vo por los métodos estándares y; la presencia de inmunoglobulina A(IgA) unida a glóbulos rojos. En un intento de aumentar la sensibilidad de la PAD, se ha iniciado el uso de la citometría de flujo en el diagnós�co de AHAI, aunque aún no se realiza de forma ru�naria. (710) La citometría de flujo, es una técnica de gran
sensibilidad y especificidad que puede contribuir al diagnós�co eficaz de los pacientes con niveles bajos de auto-Ac Sus principales ventajas son la rapidez, el número de parámetros evaluables, la sensibilidad y la capacidad de cuan�ficar un gran número de células para un criterio par�cular (9, 10,11,12) Este trabajo �ene como obje�vo aplicar la técnica de citometría de flujo al diagnós�co de las anemias hemolí�cas autoinmunes calienteconPADnega�vaenelIns�tutodeHematologíae Inmunología.
MÉTODOS
Se realizó un estudio exploratorio, transversal de �po inves�gación desarrollo y evaluación de tecnología. La información se obtuvo a par�r de la revisión de las órdenes de estudio de AHAI de pacientes con sospecha de anemia recibidas en el Laboratorio de Inmunohematología del Ins�tuto de Hematología e Inmunologíaduranteelperíodo2020-2024.
La muestra quedó conformada por 72 muestras de sangre de pacientes con sospecha de AHAI caliente con PAD nega�va seleccionadas por muestreo no probabilís�co intencional Se incluyeron todos los pacientes que potencialmente presentan sospechas de AHAI caliente con PAD nega�va. Se excluyeron aquellos conPADnega�vaylatécnicadeeluciónposi�va.
Para la citometría de flujo se seleccionaron los valores de voltaje que permi�eron situar la población de eritrocitos en la región inferior izquierda del dotplot FSCSCC, correctamente separados de los detritos celulares. Se trabajó con suspensiones al 1, 2 y 3 % de muestras de sangre total con an�coagulante EDTA; con diferentes concentraciones de los reac�vos de detección (an�-IgM, IgG,IgAconjugadaconFITC,an�-IgMconjugadaconFITC, an�-IgA conjugada con FITC y fracción (Fab)2 de an�-IgG humano obtenida en conejos conjugada con FITC), se escogió la menor concentración que produjo una señal adecuada. Todos los reac�vos fueron de la marca DAKO. Se u�lizó el reac�vo hemoclasificador an�-D (LABEX, San�ago de Cuba), como control posi�vo para la IgM; y el suero de una embarazada aloinmunizada con un �tulo de an�cuerpos an�-D mayor que 16, como control de la IgG; ambos se enfrentaron mediante prueba an�globulina indirecta (PAI) a una célula O posi�vo conocida. Para el controlnega�voseu�lizaroncélulasOposi�vosinmarcar.
Lasuspensióndeeritrocitosdondeseobtuvouna señal adecuada de marcaje fue del 1 %, con una dilución del reac�vo en PBS de 1/5 y se consideró como un resultado posi�vo un porcentaje de dispersión de la fluorescencia hacia la derecha del gráfico igual o superior alamediamástresdesviacionesestándardeloscontroles nega�vos.
Las variables que se tuvieron en cuenta para el estudiofueron:sexo,edad,grupo ABO yRhDparalasque sedeterminaronlasfrecuenciasabsolutasyrela�vas.
La inves�gación cumplió con los principios de la Declaración de Helsinki para la inves�gación en seres humanos (13) y para su realización contó con la aprobación del Comité de É�ca de la Inves�gación y el ConsejoCien�ficodelains�tución.
RESULTADOS
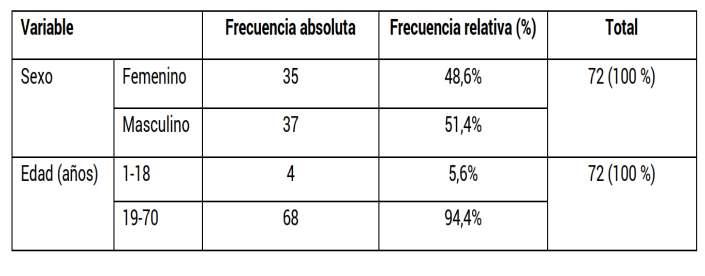
De las 72 muestras estudiadas, 35 (48,6 %) correspondían al sexo femenino y 37 (51,4%) al masculino.Elnúmerodemuestrascorrespondientesalos pacientesadultosfuede68(94,4%),edadesentre39a70 años, y una edad promedio de 56,2 años. Solo 4 (5,6 %) muestraspertenecieronalaedadpediátrica(tabla1).
Tabla 1. Distribución según edad y sexo de los pacientes con anemia hemolí�ca autoinmune caliente con prueba de Coombs nega�vas en el Ins�tuto de HematologíaeInmunología,2020–2024
Se detectaron auto-Ac por citometría de flujo en 39 muestras (54,16 %) De ellas, 28 presentaron fluorescencia para el iso�po IgG, 8 para el iso�po IgM y 3 paraeliso�poIgA.
En relación con el grupo ABO se observó una mayor prevalencia del grupo O (n=31), seguido por el grupoA(n=20),B(n=18)yAB(n=3).Paraelan�genoDdel sistema Rh se encontró un mayor número de muestras RhD posi�vas (n=68) con respecto a las muestras RhD nega�vas (n=4); todas las muestras donde se detectaron auto-Ac mediante citometría de flujo resultaron ser Rh D posi�vas.
Se detectaron an�cuerpos en 39 muestras (54,16 % del total estudiado); de ellas, 28 presentaron
fluorescencia para el iso�po IgG, 8 para el iso�po IgM y 3 para el iso�po IgA. El resto de las muestras analizadas fueron nega�vas, por lo que no fueron válidas para el estudio ya que no presentan anemia por auto-Ac
DISCUSIÓN
Las AHAI se caracterizan principalmente por la hemólisis asociada a la presencia de inmunoglobulinas de la clase IgG, IgM e IgA o fragmentos del sistema del complemento que opsonizan la membrana de los eritrocitos.
El diagnós�co de las AHAI se realiza teniendo en cuenta la condición clínica del paciente, la posi�vidad de la prueba de Coombs directa y la detección de (auto-Ac) presentes en el suero del paciente. Muchos autores plantean que a mayor intensidad de aglu�nación de la PAD mayor es el grado de destrucción de los glóbulos rojos;(2) sin embargo, se ha demostrado una pobre relación entre la intensidad de la aglu�nación y la hemólisis.(2,3,4)
Los glóbulos rojos opsonizados por auto-Ac calientes son secuestrados y fagocitados por los macrófagos, principalmente en el bazo. Los macrófagos expresan en su superficie receptores para la región Fc de las inmunoglobulinas, lo que permite una captura y fagocitosis de los glóbulos rojos opsonizados. En ocasiones la fagocitosis es incompleta y resulta en la formación de esferocitos; esto ha sido explicado por la remoción de más membrana que volumen. (2) Además, las ectoenzimas en la superficie del macrófago causan microperforacionesenlamembranadeleritrocito,loque incrementasupermeabilidad.Deestamanerapropiciala transición de una forma bicóncava de la célula a una forma esférica, y lo hace más propensos a la destrucción, durante el paso a través del bazo. Esto se relaciona con la gravedaddelahemólisisconlaesferocitosis,peronocon laintensidaddelaaglu�nación.(12,13,14,15)
A principios de la década de 1970, se enfa�zó en que la can�dad de an�cuerpos encontrada en los eritrocitos de pacientes con AHAI puede ser insuficiente para detectarlos con reac�vos para técnicas convencionales. Se propuso que la distribución de los an�cuerpos IgG en los glóbulos rojos circulantes no era uniforme.
Los eritrocitos acumulan IgG a medida que envejecen,loquedalugaraunamayorproporcióndeIgG en los eritrocitos más viejos en comparación con los más jóvenes.(10,11)
Alrededor del 3–10 % de los pacientes con una AHAI por an�cuerpos calientes presentan una PAD nega�va. Por lo que, a pesar de que la PAD es la técnica
clave para el diagnós�co; esta no es totalmente sensible, ya que otras variables influyen en su nega�vidad o posi�vidad como el rango de detección del reac�vo poliespecífico an�globulina humana o el �po de inmunoglobulina presente. Por ello, en ocasiones, se ob�ene un resultado de laboratorio nega�vo, a pesar de laclínicaelpacientepresentemanifestacionespropiasde laenfermedad.
Una mayor complejidad para interpretar correctamente la PAD reside en la capacidad de los autoAc para ac�var el complemento. Las IgM son potentes ac�vadores de la vía clásica del complemento Sin embargo, pueden desprenderse de la célula durante los procedimientos de lavado o incluso in vivo, y dar un resultado nega�vo. En este caso, las fracciones del complemento (principalmente C3d) permanecen en la superficie de los eritrocitos, lo que permite una PAD posi�vaconan�suerosan�complemento.
En un intento de aumentar la sensibilidad de la PAD en tubo, se ha introducido la técnica de citometría de flujo, aunque todavía no se u�liza de forma ru�naria en el diagnós�co de AHAI En un estudio de la Universidad de Cataluña reportaron que 5 de 50 AHAI PAD nega�vas en tubo, diagnos�cadas clínicamente, fueron posi�vas por citometría de flujo. Los autores tambiénabordaronlacues�óndelvalordecortedelnivel de IgG unida a los glóbulos rojos, que se desarrolló con más detalle en un estudio más reciente. Por su parte, en un estudio del año 2023 se evaluaron 64 pacientes con AHAI PAD nega�vas y demostraron una sensibilidad del 71,4 % y una especificidad del 87,8 % con respecto a la técnica convencional en tubo Además, la detección mediante este método permite descubrir an�cuerpos IgM calientes unidos a los glóbulos rojos, que no pueden ser revelados por los métodos estándar y pueden causar AHAIgrave.(14,15,16)Porestarazón,cadavezseu�lizan técnicas más sensibles, como la citometría de flujo, para caracterizar las inmunoglobulinas unidas a los glóbulos rojos debido a su mayor precisión, reproducibilidad y sensibilidad.
Con respecto al sexo, los resultados del presente estudio no coinciden con la literatura, donde se reporta que la AHAI es más frecuente en mujeres que hombres, estopuededebersealacasuís�caobtenidaenelperíodo deestudio.
Según la literatura la AHAI caliente aparece generalmente después de los 40 años y su incidencia aumenta con la edad debido a su relación con las enfermedades linfoprolifera�vas Predomina en los adultos donde la enfermedad es más grave, dato que coincide con los resultados del estudio; y requiere de tratamientoinmunosupresoralargoplazo.(6)

La frecuencia de muestras posi�vas por citometríadeflujoparaIgG,coincideconloplanteadoen laliteratura.(15)Losautorescoincidenenquehastaenel 90 % de los pacientes con AHAI presentan an�cuerpos an�-IgG. Además, en ellos se detecta el fragmento C3b del complemento. (14,15,16) Ambos mecanismos contribuyen a la hemólisis pues los eritrocitos recubiertos con IgG se destruyen en el bazo y los opzonizados por C3 son secuestrados en hígado y en bazo. Los macrófagos del hígado con receptores para el fragmento C3b no son eficientes en la destrucción de eritrocitos con C3b unido sin IgG. Estos macrófagos inmovilizan los eritrocitos a través de los receptores para C3b y posteriormente deben atrapar las células por el receptorparaelfragmentoFcdelaIgG.(15)
Por otra parte, aunque el iso�po de inmunoglobulina predominante es del �po IgG, se detecta con menor frecuencia inmunoglobulinas de las clases IgA e IgM. Las inves�gaciones previas informan que la iden�ficación de auto-Ac IgG acompañados de auto-Ac IgA, IgM o de ambas inmunoglobulinas es la causa principal de la gravedad de la hemólisis autoinmune.(15,16,17)
En el 14 % de las AHAI por an�cuerpos calientes el an�cuerpo que está presente en los hema�es es de la clase IgA. El mecanismo por el cual ocurre la destrucción de los hema�es por esta inmunoglobulina, es similar al que ocurre cuando están presentes an�cuerpos de la clase IgG, lo que podría explicar las similitudes clínicas entre las AHAI mediadas por estos auto-AC. (2,3,4,5,6) Algunos estudios sugieren que los auto-Ac pueden ser capaces de ac�var el complemento, aunque esto aún es un tema poco definido. (7,8,9)
Los auto-Ac de la clase IgM, generalmente son responsables de la variante fría de las AHAI ya que presentan una temperatura óp�ma de reacción de 4oC, que causa hemólisis intravascular y en menor medida hemólisis extravascular asociado a C3d. Sin embargo, la amplitudtérmicadereaccióndeestosan�cuerpospuede variar de 0 a 34oC, por lo que también puede estar asociado a formas graves de AHAI por an�cuerpos calientes, sobre todo si se encuentra concomitando con unaIgA (2,3,4,5,6)Segúnlaliteratura,enlasvariantesde AHAI por an�cuerpos calientes donde la IgM no sea detectada por la PAD, podría estar presente una IgM monomérica incapaz de ac�var el sistema del complemento, lo cual impide su detección con el suero poliespecífico an�globulina humana, que con�ene an�IgGyan�-C3.(8)
En relación con el grupo ABO, el predominio del
grupo O, no se ha relacionado con la predisposición a padecerAHAIoacursarformasgravesdelaenfermedad; pero si se relaciona con la frecuencia feno�pica de la población cubana debido al gran mes�zaje con la que estacuenta.(18)
Según lo planteado en la literatura los auto-Ac calientes que provocan AHAI reconocen a los Ag del sistema Rh, elemento que coincide con lo obtenido en el estudio pues todas las muestras posi�vas mediante citometría de flujo son RhD posi�vas. En par�cular, el Ag RhD es una diana común, tanto para respuestas inmunes autoagresivas como convencionales, por lo que es el auto-Ag u�lizado para la caracterización de los defectos en los mecanismos de tolerancia en diferentes individuos. Hasta este momento, el sistema de grupo sanguíneoRhno sehadetectado enotro�po celular,por lo que es específico de los eritrocitos. Este sistema es un complejo molecular formado por el ensamblaje de la proteína Rh en asociación directa con el sistema RhAG, imprescindibleparalaexpresióndelaAgRh.(2,18)
Esteestudiodemuestraquelacitometríadeflujo es una herramienta que proporciona certeza en el diagnós�co de las AHAI caliente PAD nega�va, la que usualmenteesundesa�oparaeldiagnós�coclásico.
D E C L A R A C I Ó N D E C O N F L I C TO D E INTERESES
Los autores declaran que no existe conflicto de intereses
CONTRIBUCIÓNDEAUTORÍA
Conceptualización: Yisenia Romero Díaz, Mariela Forrellat Barrios
Curacióndedatos:YiseniaRomeroDíaz,AlexisMoránFernández
Análisis formal: Yisenia Romero Díaz, Mariela Forrellat Barrios, Alexis MoránFernández.
Inves�gaciónYiseniaRomeroDíaz,MarielaForrellatBarrios
Metodología:YiseniaRomeroDíaz
Validación:YiseniaRomeroDíaz
Redacción – borrador original: Yisenia Romero Díaz, Mariela Forrellat Barrios,AlexisMoránFernández
Redacción – revisión y edición: Yisenia Romero Díaz, Mariela Forrellat Barrios
REFERENCIASBIBLIOGRÁFICAS
1. Loriamini M, Cser�-Gazdewich C, Branch DR
Autoimmune Hemoly�c Anemias: Classifica�ons, Pathophysiology, Diagnoses and Management. Int J Mol Sci. 2024;25(8):4296.DOI:h�ps://doi.org/10.3390/ijms25084296
2. Soler Noda G. Anemia hemolí�ca autoinmune:
mecanismos de inducción de autoinmunidad e inmunobiología. Rev Cubana Hematol Inmunol Hemoter 2022
[citado 15/01/25];38(4):e1724 Disponible en: h�ps://revhematologia.sld.cu/index.php/hih/ar�cle/view/17 24
3. Bandikatla S, Zhang Y, Jaglal M Autoimmune Hemoly�c Anemia. In: Sokol L., Zhang L. (eds) Non-Neoplas�c Hematologic Disorders. Springer, Cham; 2024. DOI: h�ps://doi.org/10.1007/978-3-031-62373-8_16
4. Alfonso Valdés ME, Bencomo Hernández A, Espinosa
Mar�nez E, Guerrero Calderón R, Guerra Borrego E, Guerrero Calderón AI. Caracterización de pacientes adultos con anemia hemolí�ca autoinmune atendidos en el Ins�tuto de Hematología e Inmunología. Rev Cubana Hematol Inmunol Hemoter 2009 [citado 20/03/25]; 25(3): Disponible en: h�p://scielo.sld.cu/scielo.php?script=sci_ar�ext&pid=S086402892009000300005&lng=es.
5. Zantek N, Koepsell S, Tharp Jr D, Cohn C. The direct an�globulin test: A cri�cal step in the evalua�on of hemolysis.
A m J H e m a t o l . 2 0 1 2 . 8 7 : 7 0 7 - 9 . D O I : h�ps://doi.org/10.1002/ajh.23218.
6. Soler Noda G. Anemia hemolí�ca autoimmune caliente y eriptosis. Rev Cubana Hematol Inmunol Hemoter 2022 [citado 16/09/23];38(1). Disponible en: h�ps://revhematologia.sld.cu/index.php/hih/ar�cle/view/16
79
7. Vasilchenkova PI, Galtseva IV, Lukina E A
Autoimmune hemoly�c anemia: the current state of the issue.
O n c o h e m a t o l 2 0 2 3 ; 1 8 ( 2 ) : 6 0 - 7 D O I : h�ps://doi.org/10.17650/1818-8346-2023-18-2-60-67.
8. Scheckel CJ, Go RS Autoimmune Hemoly�c Anemia: Diagnosis and Differen�al Diagnosis. Hematol Oncol Clin North
A m 2 0 2 2 ; 3 6 ( 2 ) : 3 1 5 - 2 4 D O I : h�ps://doi.org/10.1016/j.hoc.2021.12.001.
9. Ascoli Bartoli T, Lepore L, D'Abramo A, Adamo G, Corpolongo A, Scorzolini L, et al. Systema�c analysis of direct an�globulin test results in post-artesunate delayed h a e m o l y s i s M a l a r J 2 0 2 1 ; 2 0 ( 1 ) : 2 0 6 D O I : h�ps://doi.org/10.1186/s12936-021-03735-w.
10. Rodberg K DAT-Nega�ve Autoimmune Hemoly�c Anemia. Hematol Oncol Clin North Am. 2022;36(2):307-313. DOI:h�ps:doi.org/10.1016/j.hoc.2021.11.004.
11. Roumier M, Loustau V, Guillaud C, Languille L, Mahevas M, Khellaf M, et al. Characteris�cs and outcome of warm autoimmune hemoly�c anemia in adults: New insights based on a single-center experience with 60 pa�ents. Am J H e m a t o l 2 0 1 4 ; 8 9 ( 9 ) : E 1 5 0 - 5 D O I : h�ps://doi.org/10.1002/ajh.23767.
12. Chaudhary R,Das SS Applica�onofflowcytometryin transfusion medicine: The Sanjay Gandhi Post Graduate Ins�tuteofMedicalSciences,Indiaexperience.AsianJTransfus
S c i . 2 0 2 2 ; 1 6 ( 2 ) : 1 5 9 - 6 6 . D O I : h�ps://doi.org/10.4103/ajts.ajts_61_22.
13. World Medical Associa�on. Declara�on of Helsinki. Ethical Principles for Medical Research Involving Human Par�cipants. JA M A. 2024;23(18):e21972. D O I: h�ps://doi.org/10.1001/jama.2024.21972
14. Theis SR, Hashmi MF. Coombs Test. [Updated 2022 Sep 12] In: StatPearls [Internet] Treasure Island (FL): StatPearlsPublishing;2025Jan–.[citado20/03/25].Disponible en:h�ps://www.ncbi.nlm.nih.gov/books/NBK547707/
15. Barcellini W, Fa�zzo B. Strategies to overcome the diagnos�c challenges of autoimmune hemoly�c anemias
h�ps://doi.org/10.1080/17474086.2023.2216930.
16. Barcellini W, Fa�zzo B. Autoimmune Hemoly�c Anemias: Challenges in Diagnosis and Therapy Transfus Med H e m o t h e r 2 0 2 4 2 7 ; 5 1 ( 5 ) : 3 2 1 - 3 1 D O I : h�ps://doi.org/10.1159/000540475.
17. Fayek MH, Saad AA, Eissa DG, Tawfik LM, Kamal G. Role of gel test and flow cytometry in diagnosis of Coombs' nega�ve autoimmune haemoly�c anaemia. Int J Lab Hematol. 2012;34:311-9 DOI: h�ps://doi org/10 1111/j 1751553X.2011.01397.
18. SolerNodaG,RomeroDíazY,GonzálezDíazI,Forrellat BarriosM,LamDíazRM,CabreraCarballosaCC,etal Infección por SARS-CoV-2 y grupos sanguíneos en pacientes cubanos diagnos�cados con la COVID-19. Rev Cuba Med. 2023 [citado
2 0 / 0 9 / 2 4 ] ; 6 2 ( 2 ) D i s p o n i b l e e n : h�p://scielo.sld.cu/scielo.php?script=sci_ar�ext&pid=S003475232023000200006&lng=es.
Hipertensión arterial secundaria a feocromocitoma de causa genética e hipoatrofia renal en edad pediátrica
La hipertensión arterial en pediatría puede deberse a causas poco frecuentes como el feocromocitoma del presente caso. Este tipo de situaciones son las que requieren de un diagnóstico temprano y manejo multidisciplinario para prevenir los dañosalargoplazo.
AUTOR
1 2
Mariana Dufort y Álvarez , Margarita Halty , Mónica
3 4 Rodríguez , Gustavo Dufort y Álvarez , Rosario
5 6 Gueçaimburu ,WalterPérez
1.NefrologaPediatra.MP HospitalBritánico.
2 Prof Adj Clínica Pediátrica Facultad de Medicina UDELAR. Nefróloga Pediatra. MP. Nefróloga Pediatra. CHPR
3 Ex Asist Clínica Pediátrica Facultad de Medicina
UDELAR.Pediatra.MP. 4.Medico.Pediatra.MP.
5 Medico Pediatra Neonatologa Gene�sta Hospital Británico.
6.Prof.ClínicaPediátrica.FacultaddeMedicina. UDELAR. DirectorTécnico.MP MedicinaPersonalizada. Correspondencia:margahalty@gmail.com
Fuente:ArchivosdePediatríadelUruguay2025;96(1)
RESUMEN
La hipertensión arterial (HA) �ene tendencia creciente en pediatría. El diagnós�co y tratamiento oportunos pueden solucionar una eventual causa subyacente y evitar daños agudos y alejados Feocromocitomas y paragangliomas son causa infrecuentedeHAenniños. El obje�vo es comunicar un caso de HA secundaria a un feocromocitoma de causa gené�ca, y atrofiadelriñónipsilateral.
Se presenta una escolar de 9 años asintomá�ca con HA severa, crónica, función renal normal y sin daño de órganos blanco. La ecogra�a y la angiorresonancia mostraron un nódulo en topogra�a suprarrenal derecha; enelcentellogramaconDMSAtenía12%decaptaciónen el riñón derecho Las metanefrinas urinarias y la reninemiaestabanmuyelevadas.ElPETfueposi�vopara feocromocitoma sin diseminación. Luego del descenso lento de la presión arterial, se realizó la resección quirúrgica; la anatomía patológica confirmó el
diagnós�co y la naturaleza benigna. El estudio gené�co detectó la variante patogénica c 72+1G›A en el gen
SDHB En el posoperatorio persis�ó con HA, las metanefrinas se normalizaron, el eco Doppler mostró hipovascularización en la mitad superior del riñón y la función en el DMSA descendió a 9% Se realizó la nefrectomía. Normalizó las cifras tensionales en el consultorio, el monitoreo ambulatorio fue aún patológico.
Es esencial el monitoreo mul�disciplinario de esta paciente monorrena, con posibilidad de recidiva tumoralmalignización.
Palabrasclave:Hipertensión,Feocromocitoma,Niño
INTRODUCCIÓN
La hipertensión arterial (HA) es una condición relevante en todas las edades. Su definición en pediatría sebasaenladistribucióndelosvaloresdepresiónarterial (PA) en niños sanos, de acuerdo a sexo, edad y estatura. En las úl�mas norma�vas de la American Academy of Pediatrics(AAP)de2017,enlaconfeccióndelastablasno se incluyeron niños con índice de masa corporal >
percen�l 85(1). De acuerdo a estas guías, se diagnos�ca HA convaloresde PA ≥percen�l95(p95)parasexo,edad y talla en tres mediciones separadas en el �empo. Si las cifras son muy elevadas, o hay compromiso de órganos blanco, una sola medición es suficiente para el diagnós�co(1).
SedefinelaHAestadio1cuandolosvaloresdePA son ≥ p95 y < p95 +12 mmHg, o entre 130/80 y 139/89 mmHg (el valor que sea menor). En el estadio 2 la PA es ≥ p95+12mmHgo≥140/90mmHg(1).
La prevalencia actual de la HA en niños y adolescentes es de 3,5% con una tendencia creciente en las úl�mas décadas (1). La HA en edades tempranas determinadañovascularaceleradoeincrementanotoriamente el riesgo de padecerla en la edad adulta y de asociarsíndromemetabólico(2).
A diferencia de la esencial o primaria, la HA es secundaria cuando es posible iden�ficar una causa subyacente que determina el ascenso persistente de las cifras tensionales (3,4). La HA primaria está fuertemente
asociada a sobrepeso / obesidad infan�l y adolescente (1,2,4).
La frecuencia de HA secundaria es de hasta 75%85% en niños pequeños (2) Dentro de las causas secundarias, la enfermedad renal y la renovascular representan 34%-79% y 12%- 13% respec�vamente, en niños y adolescentes, con variaciones de acuerdo a la edad (1). La e�ología endocrinológica, resultado de la producción excesiva de hormonas, es poco frecuente, entreel0,05%-6%(1).
Los tumores neuroendócrinos, secretantes de catecolaminas, son responsables de HA con una incidencia en la población de 2-6 casos/millón/año (5,6). El 10%- 20% se desarrollan en la edad pediátrica y son responsables del 0,5%-2% de los casos de HA en niños (5,7).
Los tumores que derivan de células cromafines de la médula suprarrenal se conocen como feocromocitomas (FCC), mientras que los tumores morfológica- mente idén�cos que surgen en otros si�os se conocen como paragangliomas (PGL), éstos, a su vez, sesubdividenensimpá�cosyparasimpá�cos(5,6,8,9).
Los FCC y los PGL son hereditarios en 80% de los casos (5-7), la mayoría debido a mutaciones en la línea germinal, y su herencia es autosómica dominante con penetrancia variable (5,8) Pueden formar parte del síndrome FCC/PGL familiar, Von Hippel-Lindau (VHL), neoplasia endócrina múl�ple �po 2, neurofibromatosis �po 1, Carney Stratakis. Múl�ples genes han sido iden�ficados; diferentes variantes patogénicas en genes de la enzima Succinato Deshidrogenasa (SDH) se asocian al síndrome FCC/PGL familiar y presentan altas tasas de recurrencia, tumores mul�céntricos y enfermedad maligna(5,6,8).
La importancia del diagnós�co y tratamiento oportunos de la HA radica en mi�gar los daños agudos, solucionar la causa subyacente si existe y evitar las consecuenciasalargoplazo.
Elobje�vodelapublicaciónescomunicaruncaso de HA severa secundaria a un FCC de causa gené�ca, asociado a hipo/atrofia del riñón homolateral al tumor. Analizamoselcasoalaluzdelabibliogra�aactualizada.
Aspectos é�cos: se solicitó el consen�miento informado a la familia para la publicación de este caso clínico y la autorización a la dirección técnica de la ins�tución de asistencia. Se contó con el aval del Comité deÉ�caenInves�gacióndelains�tución.
CASOCLÍNICO
Se presenta el caso de una escolar de 9 años sin ante- cedentes patológicos, con el antecedente familiar de hermana nefrectomizada al año de vida por estenosis severa de una arteria renal, con buena evolución a los 23 añosdeedad.
En un control de salud, estando la paciente asintomá�ca, al examen �sico se constató sobrepeso, índice de masa corporal (IMC) p86, z score +1,06 y cifras de PA 150/110 mmHg (p95: 117/77). Se hospitalizó para su estudio y tratamiento Los estudios inicia- les mostraron una alcalosis metabólica (HCO3 30,3 mmol/l), hipopotasemia (2,7 mEq/l); azoemia 28 mg/ dl, crea�ninemia 0,43 mg/dl; el hemograma, orina, albuminuria, ecocardiograma y fondo de ojo fueron normales. La ecogra�a renal y suprarrenal evidenció un nódulo sólido en topogra�a suprarrenal derecha de 23 x 18 mm, de ecoestructura heterogénea, vascularizada. Ambos riñones eran de tamaño y ecogenicidad habituales, el eco Doppler de vasos renales mostró índices reno/aór�cos normales, la arteria renal derecha no se observó en su tercio medio por interposición de gases. Las metanefrinas fraccionadas en orina 24 hs estaban elevadas (normetanefrina: 1542 µg/24 hs (valor normal 29-145 µg/24 hs), metanefrinas totales: 1668 µg/24 hs (57-210 µg/24 hs); ac�vidad de renina plasmá�ca 73 ng/ml/h (0,8-2,0 ng/ml/h). La angiorresonancia mostró el riñón derecho levemente máspequeñoendiámetrosanteroposteriorytransversal, descendidoymalrotado,conalteracióndelaseñalenT2; evidenció una tumoración en contacto con el polo superior del riñón derecho y la pared posterior de segundaporcióndeduodeno.Elnóduloseencontrabaen ín�mo contacto con la vena cava inferior a la que comprimía. A nivel vascular presentaba doble vena renal rodeando la lesión, el sector proximal de la arteria renal derechadecalibrefino,2mm,englobadaporlalesión;no se iden�ficó su sector distal. El diagnós�co fue tumor suprarrenal derecho, probable FCC El centellograma renal con DMSA evidenció a derecha captación únicamente en el polo inferior con aporte funcional rela�vo de 12%. El PET mostró una imagen nodular en la logia suprarrenal derecha con intensa expresión de receptoresdesomatosta�na,sinextensiónlesional.
Con el planteo de HA secundaria a FCC suprarrenal derecho y posible asociación con causa renovascular homolateral, se inició tratamiento médico con dieta hiposódica, enalapril y nifedipina; las cifras tensionales descendieron progresivamente a valores de 120- 130/70-80 mmHg, con buena tolerancia, previo a la cirugía. El abordaje fue mul�disciplinario con pediatra, nefrólogo, oncólogo, gene�sta, cirujano pediátrico, cirujano vascular, endocrinólogo y anestesista El

tratamiento quirúrgico consis�ó en la resección de la tumoración en su totalidad, junto con la glándula suprarrenal homolateral Durante la manipulación tumoral en el intraoperatorio tuvo un pico hipertensivo de 220/136 mmHg, PA media 160 mmHg, por lo que recibió nitroprusiato de sodio. La biopsia extemporánea mostró una proliferación celular compa�ble con FCC, sin elementos de malignidad. Dado que a la exploración el hiliorenalyelriñónderechoimpresionabannormales,no se realizó ninguna intervención vascular ni nefrectomía. Cursóelposoperatorioinmediatoencuidadosintensivos, presentócifrastensionales>p95(120-125/70-80mmHg) que se controlaron con enalapril oral. La medicación se mantuvoalaltaadomicilioyenlaevoluciónalejada.
La anatomía patológica defini�va confirmó el diagnós�co de FCC Se trataba de un tumor suprarrenal de 2,5 x 2 x 3 cm, con una proliferación celular sólida, lobulada, muy vascularizada, con nódulos con patrón de Zellballen conteniendo células poligonales de citoplasma amplio y núcleos de tamaños variados con croma�na finamente granular y nucléolo conspicuo. Pre- sentaba extensas áreas de hemorragia y depósitos de hemosiderina. La inmunohistoquímica mostró: Ki67 bajo 10%, cromogranina citoplasmá�ca intensamente posi�va.SDHBnega�vo.
El estudio gené�co detectó la variante patogénicac.72+1G›A,enheterocigosis,enelgenSDHB.
Al mes de la cirugía, las metanefrinas fraccionadas en orina habían descendido: 287 µg/24 hs (57-210 µg/24 hs); los valores se normalizaron al cuarto mes: 138 µg/24 hs. La ac�vidad de renina plasmá�ca se mantuvo elevadaconvaloresde22ng/ml/h(0,8-2,0ng/ml/h).
Al mes y a los seis meses del posoperatorio el monitoreo ambulatorio de presión arterial (MAPA) evidenció HA estadio 2 en sueño y vigilia con dip nocturno, a pesar del ajuste de enalapril. El ecocardiograma Doppler fue normal El seguimiento ecográfico constató una hipo/atrofia de la mitad superior de riñón derecho, el centellograma con DMSA un aporte funcionalrela�vodelriñónderechode9%,elecoDoppler renal mostró en la arteria renal derecha velocidades circulatorias e índices resis�vos normales, y la vascularizaciónparenquimatosadifusamentedisminuida aniveldelamitadsuperiordedichoriñón.
Alañodelposoperatorioserealizólanefrectomía derecha sin incidentes. En la anatomía patológica se encontró una hipoplasia de la mitad superior del órgano, fibrosis, infiltrado inflamatorio y lesiones arteriales severas con paredes gruesas y tortuosas; no había alteraciones de la arteria renal principal. Luego de la cirugía la paciente estaba asintomá�ca, con sobrepeso y
con cifras de PA en consultorio entre p75- p90. A los dos meses de la nefrectomía, el MAPA informó HA sistodiastólica estadio I, y al año HA sistólica diurna en valor límite. Recibió seguimiento con nutricionista y se mantuvo con enalapril a 5 mg/día. El ecocardiograma y fondo de ojo fueron normales, la proteinuria y albuminuria nega�vas, los valores de crea�nina 0,51 y urea 21 mg/dl (a los dos años de la cirugía inicial y al año delanefrectomía).
Luego de realizado el diagnós�co e�ológico, surgió el antecedente familiar de dos �os por línea maternaquehabíanpresentadounparaganglioma.
DISCUSIÓN
El diagnós�co de HA estadio 2 en una escolar asintomá�ca fue posible gracias a la conducta pediátrica acorde con las guías vigentes de la AAP que recomienda el control anual de la PA con el control de salud (1). Planteamosqueeracrónicadebidoalabuenatolerancia, con una evolución no muy prolongada, ya que los controlesanualesprevioshabíansidonormalesynotenía repercusión en órganos blanco. Debido a la severidad de los valores, se interpretó como HA secundaria y se inició de inmediato la búsqueda exhaus�va de la patología causal. El hallazgo de una tumoración a nivel suprarrenal en el contexto de una HA severa, la elevación de las metanefrinas fraccionadas en orina y los estudios de imagen, orientaron al planteo de un tumor secretor de catecolaminas: FCC cuyo diagnós�co fue confirmado por laanatomíapatológica.
Se calcula que hasta 30% de todos los casos de FCC/PGL son familiares. En niños con mutaciones en la línea germinal la media de edad al diagnós�co de FCC/PGL es de 13 años (9-12). Estos tumores se caracterizan por manifestaciones proteiformes; la hipertensión puede ser �picamente paroxís�ca y sintomá�ca, pero también prolongada y sostenida (5,6), como en el caso de esta paciente, que estuvo asintomá�ca.Losepisodiosdesudoración,palpitaciones, taquicardia y cefalea se reportan en 50%-80% de los casos. Con menor frecuencia se observan dolor abdominal o lumbar, desórdenes psiquiátricos (crisis de pánico), hipotensión ortostá�ca, polidipsia, poliuria y hematuria(6,9,12).
Anivelbioquímico,50%delostumoresproducen una mezcla de norepinefrina y epinefrina, la mayoría restantesolonorepinefrinayraravezdopamina(9).
El estudio de las catecolaminas en orina de 24 horas �ene una sensibilidad de 86% para el diagnós�co de FCC/PGL. Los falsos nega�vos pueden explicarse por una función renal alterada y/o la rápida metabolización
de las catecolaminas circulantes (9,11). La medición de metanefrinas fraccionadas en sangre y orina (metanefrina y normetanefrina) son la herramienta diagnós�ca de elección, con una sensibilidad y especificidadenpacientessintomá�cosde98%(6,15).La velocidad de eritrosedimentación y la proteína C reac�va pueden estar elevadas, así como la glicemia, por el alto nivel de hormonas contrarreguladoras de la insulina (6,8,9,13,14). Con respecto a los estudios de imagen, la resonancia magné�ca mostró la imagen �pica hiperintensa en T2, caracterís�ca de los tumores cromafines, siendo la sensibilidad 90%-100% para el diagnós�co(8,9,11,13,15).
El PET y el centellograma con 123/131I-MIBG �enen igual desempeño para el diagnós�co de tumo- res no metastásicos, siendo superior el PET para los metastásicos. Este u�liza marcadores de ac�vidad de s o m a t o s t a � n a ( G a - 6 8 D O T A T A T E , 1 8 Ffluorodexiglucosa), cuya expresión es intensa en estos tumores(6,9,13,15).
La anatomía patológica evidenció el clásico patrónhistológicodenominadoZellballen(16).
La inmunohistoquímica fue coincidente detectando posi�vidad al marcador neuroendócrino cromogranina. La nega�vidad por inmunohistoquímica de SDHB refleja una mutación a nivel de la SDH, estando ausenteenlascélulastumorales(17).
En relación con el aspecto gené�co, se encontró una variante patogénica c.72+1G›A en heterocigosis, en el gen SDHB, que codifica la subunidad B de enzima SDH Esta mutación determina un cambio de secuencia que afectaalsi�odecorteyempalmedel ARN conduciendoa lapérdidadefuncióndelaproteína(PMID:16199547).El complejoSDH-mitocondrialestáimplicadocomoenzima en el ciclo de Krebs y en el transporte de electrones y metabolismo oxida�vo de la cadena respiratoria. Las dis�ntassubunidadesdelaSDH(A,B,C,D)yotraproteína codificada por un quinto gen(SDHAF2),necesariaparala flavinación de la subunidad A, son conocidos como SDHx yestánrelacionadosconlasupresióntumoral(6,9,12).
La presencia familiar de mutaciones en SDHx causa los síndromes FCC/PGL heredados al no exis�r la supresión o inhibición tumoral Se iden�fican tres subgrupos moleculares de tumores con caracterís�cas clínicas,bioquímicasydeimagenpar�cularesqueayudan
ENFERMEDAD CELIACA Y OTROS DESÓRDENES ASOCIADOS
Diagnóstico de Laboratorio paso a paso
a orientar el tratamiento y el seguimiento de los pacientes: grupo 1 (A y B) relacionado con la pseudohipoxia; grupo 2, relacionado con la señalización delascinasas;grupo3,relacionadoconlaseñalizaciónde WNT (5,11,12). El subgrupo 1, al cual corresponde la mutación de la paciente, se asocia a presentación en edadesmástempranas,tumoresmúl�plesyrecurren-tes conpotencialdiseminaciónmetastásica(5,6,12).
El tratamiento de los FCC/PGL secretores es médico y quirúrgico. Inicialmente es imprescindible el control de la HA. Una rápida reducción de la HA severa hacia un valor normal conllevaría un riesgo significa�vamente mayor de daño neurológico o muerte que una reducción controlada y paula�na (18). En el caso clínico comentado, el tratamiento con calcioantagonistas asociado a inhibidores de la enzima conversora de angiotensina,redujolascifrasdeformalenta,fueefec�vo y bien tolerado, sin lograr la normalización de los valores. Los an�hipertensivos recomendados de primera línea son los alfabloqueantes (7-14 días previos a la cirugía), seguidosporbetabloqueantessiesnecesario,siendouna alterna�va válida el uso de calcioantagonistas o la me�rosina (bloqueador de la �rosina hidroxilasainhibidor de la síntesis de catecolaminas) (15,19,20). La expansión de volumen es una medida recomendada debido a que existe una disminución del volumen plasmá�co circulante secundaria a vasoconstricción mediadaporlosreceptoresadrenérgicosα1(9,19,20).
La intervención quirúrgica sin preparación previa puede elevar significa�vamente la morbilidad y mortalidad(8,19,20).
La tumorectomía puede realizarse por cirugía convencional o laparoscópica incluyendo o no la adrenalectomíaipsilateral(13,20).Lascomplicacionesen el acto quirúrgico pueden ser: crisis hipertensiva o arritmiasmalignasyenelposoperatoriolahipotensión.El riesgo es mayor a mayor ac�vidad adrenérgica previa y aumenta con el tamaño tumoral. Una cirugía exitosa debería restaurar la PA normal dentro de la primera semanadelposoperatorio(15,16,19,20).
En el caso comentado la HA persis�ó en el posoperatorio inmediato y alejado, sin repercusión en órganos blanco. Tuvo una respuesta excelente a los inhibidores de la enzima de conversión (IECA), lo que se explica por la hiperreninemia persistente. Luego de la nefrectomía, la HA presentó una clara mejoría, persis�endoaúnvaloresennivellímite.
La escisión del tumor puede curar la HA causada por la compresión extrínseca o por pseudoestenosis vascular. En otros pacientes, la compresión crónica conduce a la proliferación de la mioín�ma arterial, lo que
provoca estenosis luminal persistente y resulta en hipertensiónpersistente(3,10,21).
La aparición simultánea de FCC e HA de e�ología renal o renovascular es rara. El estudio de Gill y colaboradores describió 87 casos, y posteriormente se reportaroncasosesporádicos(5,7,8,10,21,22).
Se han propuesto diferentes mecanismos fisiopatológicos: isquemia renal por compresión directa del parénquima o del hilio, �stula arterio venosa renal, obstrucción ureteral, aumento local prolongado de las catecolaminas induciendo un vasoespasmo arterial con “pseudoestenosis”, adherencia periarterial persistente luego de la resección del tumor, o displasia neuroectodérmica generalizada con FC C y neurofibromatosis asociadas (5,8,10,21,22). También se ha descripto la ocurrencia simultánea pero independiente de lesiones estenó�cas de la arteria renal [por ejemplo, aterosclerosis, displasia fibromuscular que aumentan la ac�vidad del sistema renina-angiotensinaaldosterona (SRAA)] (7). En algunas situaciones, la hiperreninemia puede generarse por disminución del volumenplasmá�co,restricciónsalinayusodediuré�cos para el control de la HA o posible efecto es�mulador directo de catecolaminas. Por tal mo�vo, la medición de la ac�vidad de la renina plasmá�ca en vena periférica no siempre significa la presencia de estenosis arterial renal (11,21,22).
Si bien la compresión extrínseca de la arteria renal parece ser la asociación más común, en el caso presentado, la compresión del parénquima renal por la masa tumoral parece tener un rol patogénico El centellograma demostraba ausencia de parénquima renal funcionante en polo superior del riñón, seguramente secundario a isquemia renal en ese sector. El riñón siguió evolucionando a una hipoatrofia renal poscirugía, confirmado por la anatomía patológica renal, sin hallarse estenosis anatómica de la arteria renal. La literatura reporta algunos informes de hipertensión por compresión tumoral; en tres de éstos, la angiogra�a no evidenciaba imagen de oclusión arterial o estenosis circunscritaalhiliorenal(21,22).
Luego de las dos cirugías la niña mantuvo cifras de PA normales en el consultorio, pero levemente elevadas en el MAPA, lo que cons�tuye una HA enmascarada (23). La paciente es monorrena quirúrgica, con función renal normal, siendo portadora de una enfermedad renal crónica (ERC) estadio 1. La HA es un problema frecuente en todos los estadios de la ERC, cons�tuyendo a su vez un mecanismo de progresión, entrelosqueseencuentraelroldel SRAA.Portalmo�vo, los antagonistas del SRAA son drogas de primera opción en estos casos, y el obje�vo de PA se encuentra entre los

percen�les 50 y 75 para lograr una óp�ma nefroprevención y salud cardiovascular El MAPA es una guía para lograr el nivel de PA deseado, agregando precisiónparalaevaluaciónyelmanejodela HA enniños y jóvenes (23,24). En este caso, además, no debemos dejar de lado un pilar esencial en el manejo de la HA, que es el tratamiento higiénico-dieté�co: dieta hiposódica, con aporte calórico adecuado para rever�r el sobrepeso, supervisadaconnutricionistayejercicioreglado(25).
Con respecto a la evolución tumoral alejada, el riesgo de un segundo tumor primario puede llegar a 50% en 30 años y es mayor en la enfermedad hereditaria (6,9,12).Laslesionesmetastásicas�enenunahistologíay bioquímica iguales al tumor benigno diferenciándose en su capacidad de invasión regional y diseminación a distancia. Los tumores son de crecimiento rela�vamente lento, lo que explica la necesidad de un seguimiento prolongado (12). En un estudio de Jochmanova I. y colaboradores (26), en 64 pacientes con mutaciones en SDHB,el70%presentómetástasisconunamedianade16 años luego del tumor inicial, la mayoría de éstas se iden�ficarondurantelosdosprimerosañosposterioresal diagnós�co. La tasa de supervivencia calculada a cinco añosfuede100%,alos20añosde77,7%(12).
La importancia de conocer la gené�ca en este caso radica en los controles futuros que requerirá la paciente y el riesgo de los familiares de primer grado de padecer condiciones autosómicas dominantes relacionadas y de ser portadores de enfermedades autosómicasrecesivasrelacionadascongen SDHB,porlo cualdebenserestudiados(27,28).Enunfuturoalejado,la paciente deberá recibir consejo gené�co cuando planifiqueunembarazo.
No encontramos en la bibliogra�a una vinculación entre el antecedente de la hermana con HA renovascularyelcasodescripto(29,30).
CONCLUSIONES
Describimos el caso de una escolar con diagnós�co de HA severa, sin daño de órganos blanco, secundaria a un feocromocitoma de causa gené�ca, tratado exitosamente. A ésta se asoció otra causa de HA, una hipotrofia renal homolateral, probablemente a consecuencia del tumor por diferentes mecanismos, con compro- miso vascular de ramas intrarrenales. Por tal mo�vo, requirió una segunda cirugía, siendo nefrectomizada. Actualmente es una paciente monorrena, con función renal normal e HA leve enmascarada, y portadora de una mutación gené�ca. Deberá recibir un seguimiento mul�disciplinario, con medidas de nefroprevención, y monitorización por el riesgoderecidivatumoralydemalignización.
Trabajoinédito.
Declaramosnotenerconflictosdeintereses.
Disponibilidaddedatos
El conjunto de datos que apoya los resultados de este estudio NO se encuentra disponible en repositorios de accesolibre.
CONTRIBUCIÓNDELOSAUTORES
Todoslosautoresdeestemanuscritohancontribuidoala concepción y revisión crí�ca, y realizaron la aprobación finaldelaversiónapublicar.
REFERENCIASBIBLIOGRÁFICAS
1.FlynnJ,KaelberD,BakerC,BloweyD,CarrollA,DanielsS,etal;Subcommi�ee on Screening and Management of High Blood Pressure in Children. Clinical prac�ce guideline for screening and management of high blood pressure in children and adolescents Pediatrics 2017; 140(3): e20171904 doi: 10.1542/peds.2017-1904.Erratumin:Pediatrics2017;140(6):e20173035.doi: 10.1542/peds.2017-3035.Erratumin:Pediatrics2018;142(3):e20181739.doi: 10.1542/peds.2018-1739.
2.Lurbe E, Agabi� E, Cruickshank J, Dominiczak A, Erdine S, Hirth A, et al. 2016 European Society of Hypertension guidelines for the management of high blood pressure in children and adolescents. J Hypertens 2016; 34(10):1887920.doi:10.1097/HJH.0000000000001039.
3.Caggiani M, Farre Y 3er Consenso uruguayo de hipertensión arterial en el niñoyeladolescente.ArchPediatrUrug2006;77(3):300-5.
4.BoggiaJ,LujambioI,NoboaA.Hipertensiónarterial.En:BoggiaJ,MalacridaL, Luzardo L Fisopatología: mecanismos de las disfunciones orgánicas Montevideo:BiblioMédica,2017:137-58.
5.Pamporaki C, Hamplova B, Peitzsch M, Prejbisz A, Beus- chlein F, Timmers H, et al Characteris�cs of pediatric vs adult pheochromocytomas and paragangliomas J Clin Endocrinol Metab 2017; 102(4):1122-32 doi: 10.1210/jc.2016-3829.
6.Neumann H, Young WJr, Eng C. Pheochromocytoma and Paraganglioma. N EnglJMed2019;381(6):552-65.doi:10.1056/NEJMra1806651.
7.Kota S, Kota S, Meher L, Tripathy P, Sru� J, Modi K. Pheochromocytoma with renal artery stenosis: a case-based re- view of literature. J Cardiovasc Dis Res 2012;3(1):36-9.doi:10.4103/0975-3583.91601.
8.Chandra V, Thompson G, Bower T, Taler S. Renal artery stenosis and a func�oning hilar paraganglioma: a rare cause of renovascular hypertension-a case report Vasc Endovascular Surg 2004; 38(4):385-90 doi: 10.1177/153857440403800413.
9 Bholah R, Bunchman T Review of pediatric pheochromocytoma and paraganglioma.FrontPediatr2017;5:155.doi:10.3389/fped.2017.00155.
10.Sarathi V, Bandgar T, Lila A, Deshpande A, Dalvi A, Patwardhan S, et al. Coexistence of pheochromocytoma/praganglioma and renal artery stenosis. Indian J Endocrinol Metab 2012; 16(6):1009-11 doi: 10 4103/22308210.103022.
11.Rednam S, Erez A, Druker H, Janeway K, Kamihara J, Kohlmann W, et al. Von Hippel-Lindauandhereditarypheochromocytoma/paragangliomasyndromes: clinicalfeatures,gene�cs,andsurveillancerecommenda�onsinchildhood.Clin CancerRes2017;23(12):e68-e75.doi:10.1158/1078-0432.CCR-17-0547.
12.Ins�tuto Nacional del Cáncer Feocromocitoma y paragangliom: versión para profesionales de salud Bethesda, MD: INC, 2023 Disponible en: h�ps://www.cancergov/espanol/�pos/ feocromocitoma/pro. [Consulta: 21 noviembre2023].
13.Lenders J, Eisenhofer G, Mannelli M, Pacak K. Phaeochromocytoma. Lancet 2005;366(9486):665-75.doi:10.1016/S0140-6736(05)67139-5.
14.Januszewicz P, Wieteska A, Wyszyńska T Pheochromocytoma in children: difficul�es in diagnosis and localiza�on. Clin Exp Hypertens A 1990; 12(4):5719.doi:10.3109/10641969009073485.
15.Oleaga A, Goñi F Feocromocitoma: actualización diagnós�ca y terapéu�ca. EndocrinolNutr2008;55(5):202-16.doi:10.1016/S1575-0922(08)70669-7.
16.Achilli L, Bertoglio V Feocromocitoma. Rosario, ARG: UNR, Cátedra de Anatomía y Fisiología Patológicas, Unidad de ciencias médicas, 2011
Disponibleen:h�p://www.patologia-fcm.com.ar/feocromocitoma.[Consulta: 21noviembre2023].
17.van Nederveen F, Gaal J, Favier J, Korpershoek E, Olden- burg R, de Bruyn E, et al An immunohistochemical procedure to detect pa�ents with paragangliomaandphaeochromocytomawithgermlineSDHB,SDHC,orSDHD gene muta�ons: a retrospec�ve and prospec�ve analysis. Lancet Oncol 2009; 10(8):764-71.doi:10.1016/S1470-2045(09)70164-0.
18.Coulthard M. Managing severe hypertension in children. Pediatr Nephrol 2023;38(10):3229-39.doi:10.1007/s00467-023-05896-z.
19. Vaca L, Zayas H, García M, Granados J Manejo anestésico de emergencia hipertensiva perioperatoria secundaria a tumores neuroendocrinos.RevFacMed(Méx)2016;59(6):27-31.
20. Mamilla D, Araque K, Brofferio A, Gonzales M, Sullivan J, Nilubol N, et al. Postopera�ve management in pa�ents with pheochromocytoma and p a ra ga n g l i o m a C a n c e rs ( B a s e l ) 2 0 1 9 ; 1 1 ( 7 ) : 9 3 6 d o i : 10.3390/cancers11070936.
21. Weidmann P, Siegenthaler W, Ziegler W, Sulser H, Endres P, Werning C. Hypertension associated with tumors adjacent to renal arteries. Am J Med 1969;47(4):528-33.doi:10.1016/0002-9343(69)90183-1.
22. Hermida A, Lazaré H, López J, Calvo C. Hipertensión renovascular secundaria a feocromocitoma, Rev Clin Esp 2012; 212(9):467-73 doi: 10.1016/j.rce.2012.03.005.
23. Mitsnefes M, Wühl E Role of hypertension in progression of pediatric CKD. Pediatr Nephrol 2023; 38(11):3519-28. doi: 10.1007/s00467023-05894-1.
24. Flynn J, Urbina E, Brady T, Baker C, Daniels S, Hayman L, et al. Ambulatory blood pressure monitoring in children and adolescents: 2022 update: a scien�fic statement from the Ameri- can Heart Associa�on Hypertension2022;79(7):e114-24.doi:10.1161/HYP.0000000000000215.
25. Perrin E, Ravi H, Borra G, South A. Prevalence and risk factors of disordered ea�ng behavior in youth with hypertension disorders. Pediatr Nephrol2023;38(11):3779-89.doi:10.1007/s00467-023-05921-1.
26. Jochmanova I, Abcede A, Guerrero R, Malong C, Wesley R, Huynh T,
et al Clinical characteris�cs and outcomes of SD- HB-related pheochromocytoma and paraganglioma in children and adolescents. J Cancer ResClinOncol2020;146(4):105163.doi:10.1007/s00432-020-03138-5.
27. Strajina V, Dy B, Farley D, Richards M, McKenzie T, Bible K, et al. Surgical treatment of malignant pheochromocytoma and paraganglioma: retrospec�ve case series Ann Surg Oncol 2017; 24(6):1546-50 doi: 10.1245/s10434-016-5739-5.
28. Children's Oncology Group. Long-term follow-up guidelines for survivors of childhood, adolescent, and young adult cancers. Version 6.0 (October 2023) Disponible en: h�p://www survivorshipguidelines org [Consulta:21noviembre2023].
29. WeingartenT,WelchT,MooreT,WaltersG,WhippleJ,CavalcanteA, et al Preopera�ve levels of catecholamines and metanephrines and intraopera�vehemodynamicsofpa�entsundergoingpheochromocytomaand paragangl
10.1016/j.urology.2016.10.012.
30. ButzJ,WeingartenT,CavalcanteA,BancosI,Young WJr,McKenzieT, et al. Periopera�ve hemodynamics and outcomes of pa�ents on metyrosine undergoingresec�onofpheochromocytomaorparaganglioma.IntJSurg2017; 46:1-6.doi:10.1016/j.ijsu.2017.08.026.
Factores de riesgo cardiovascular en mujeres en etapa de perimenopausia y postmenopausia
Esteestudioanalizacómolareduccióndeestrógenosdurantelaperimenopausia y la posmenopausia incrementa los riesgos de hipertensión, diabetes, obesidad, tabaquismo,ysedentarismo.
AUTOR
1 Ana Mary Fernández Milán , Georgia Díaz-Perera
2 3 Fernández ,DaysiAntoniaNavarroDespaigne
1 Centro de Inves�gaciones y Referencias de Aterosclerosis. Policlínico Universitario 19 de, La Habana, LaHabana,Cuba
2 Centro de Inves�gaciones y Referencia de Aterosclerosis,LaHabana,LaHabana,Cuba
3 Ins�tuto Nacional de Endocrinología, Universidad de CienciasMédicasdeLaHabana,Cuba
Correspondencia:afernandezmilan@gmail.com
F u e n t e : R e v i s t a F i n l a y 2 0 2 6 , 1 6 ( 0 ) h�ps://revfinlay.sld.cu/index.php/finlay/ar�cle/view/16 22
RESUMEN
Fundamento: las mujeres durante la edad reproduc�va presentan un factor protector frente a la enfermedad cardiovascular debido al efecto de los
estrógenos sobre el endotelio vascular, pero durante la perimenopausiay laposmenopausia, ocurren estados de hipoestrogenemia que ocasionan un incremento en el riesgodeenfermedadcardiovascularylamuerte.
Obje�vo: determinar la frecuencia de los principales factores de riesgo cardiovascular en mujeres perimenopáusicasyposmenopáusicas.
Método: se realizó un estudio de corte transversalen332mujeresqueacudieronalaconsultade climaterio y menopausia del Policlínico Universitario 19 de Abril del municipio Plaza de la Revolución, durante el período 2018-2020 Las variables estudiadas fueron: hipertensión arterial, diabetes mellitus �po 2, sobrepeso y obesidad, obesidad abdominal, hipercolesterolemia tabaquismo, sedentarismo, perimenopausia y posmenopausia. Se determinó la media y la desviación estándar en las variables que lo requerían y las �picas medidas de asociación (Odds Ra�os y coeficientes de con�ngencia)paraevaluarlasasociacionesbinariasentre lasvariables.
Resultados: los factores de riesgo cardiovascular
�enen una elevada frecuencia en la etapa de posmenopausia con respecto a la etapa de perimenopausia, con prevalencia del sedentarismo con 214 pacientes (78,7 %), seguido del exceso de peso con 179 pacientes (65,8 %). Las pacientes que tuvieron 3 factores de riesgo, representaron el 82,1 % de las pacientes, mientras las que tuvieron 7, representaron el 94,7%enetapadeposmenopausia.
Conclusión: la alta prevalencia de factores de riesgo ateroscleró�co en etapa de posmenopausia, resalta la necesidad de estrategias preven�vas específicas para reducir la carga cardiovascular en mujeresclimatéricas.
Palabras clave: mujeres, factores de riesgo de enfermedad cardiovascular, menopausia, posmenopausia,perimenopausia
INTRODUCCIÓN
La enfermedad cardiovascular es la principal causa de muerte en hombres y mujeres en todo el mundo,enlasmujeresmenoresde50años,suincidencia es muy baja e inferior a las que se dan en hombres de la mismaedad.Despuésdelos50años,se�endeacoincidir con el climaterio, la incidencia se nivela y se presenta una alta morbilidad y mortalidad. El aumento observado es mayor que el percibido a la misma edad en los hombres, lo que sugiere a la menopausia como un factor de riesgo potencial para la enfermedad cardiovascular independientedelenvejecimiento.(1,2,3)
Las enfermedades cardiovasculares son la principalcausademortalidadenlasmujeresyestoocurre a más féminas que todas las formas de cáncer combinadas y, aun así, solo el 44 % de ellas, reconocen que la enfermedad cardiovascular es su mayor amenaza para la salud, una de cada tres mujeres muere cada año por esta causa. Muchas priorizan enfermedades como el cáncer de mama o la osteoporosis, aunque estas �enen unmenorimpactoentérminosdemortalidad.(4,5,6)
Las enfermedades cardiovasculares en Cuba estuvieron entre las principales causas de muerte según sexo entre el año 2022 y 2023. Las enfermedades cardiovasculares fueron la primera causa de muerte en la mujerenesosaños.(7)
LaesperanzadevidaalnacerenCuba,seubicóen el periodo 2018-2020 en los 77,70 años, el indicador calculadoexpresaenlasmujeresunaesperanzadevidaal nacer de 80,15 años y en los hombres de 75,33 años. (8) Estos valores hacen que se reconozca entre los países del mundo de más alta esperanza de vida al nacer En la poblaciónfemeninaestosignificaquecasilaterceraparte desuvidatranscurredespuésdelamenopausia.
Es un hecho incues�onable, que las mujeres están protegidas de las enfermedades cardiovasculares debido a los estrógenos, hormonas sexuales con diversos efectos beneficiosos. Durante la perimenopausia y posmenopausia, la disminución de estrógenos genera cambios metabólicos que favorecen un perfil lipídico aterogénico,aumentodelapresiónarterialyalteraciones en la función endotelial. Estos cambios incrementan la suscep�bilidad a la formación de placas ateroscleró�cas. Además, factores de riesgo clásicos como: el sedentarismo, la obesidad, la hipertensión y el tabaquismo son altamente prevalentes en esta población. Los estrógenos logran explicar, en parte, el rol protector frente al desarrollo de la enfermedad cardiovascular en las mujeres durante la edad fér�l, y su déficitenlamenopausiaylaposmenopausia explicaríael aumento de dichas enfermedades en este grupo poblacional.(1,6)
Comprender la distribución y el impacto de estos factores de riesgo cardiovascular en mujeres perimenopaúsicasyposmenopaúsicasesprimordialpara trazar intervenciones efec�vas de prevención cardiovascular, por tanto, se realiza este estudio con el obje�vo de: determinar la frecuencia de los principales factores de riesgo cardiovascular en mujeres perimenopáusicasyposmenopáusicas.
MÉTODOS
Se realizó un estudio de corte transversal, con el obje�vo de determinar la frecuencia de los principales factores de riesgo cardiovascular en mujeres perimenopáusicas y posmenopáusicas de 40 a 64 años que acudieron a la consulta de climaterio y menopausia del Policlínico Universitario 19 de Abril del municipio Plaza de la Revolución, en La Habana, en el periodo de enero2018aenero2020.
El universo del estudio estuvo representado por 332 pacientes de 40 a 64 años, que acudieron a la consulta en ese periodo de �empo, aceptaron par�cipar enlainves�gaciónycumplieronloscriteriosdeinclusión: residir en el área de salud del policlínico. Se consideró criteriodeexclusión,padecerdiabetes�pomellitus�po1 y estar o haber estado bajo tratamiento con terapia hormonaldereemplazo.
Serecogieronlassiguientesvariables:
-Edad.
-Factores de riesgo de la aterosclerosis (FRA): sobrepeso/obesidad, obesidad abdominal, hipertensión arterial (HTA), diabetes mellitus �po 2 (DM2), hipercolesterolemia,tabaquismo,sedentarismo.
-Indicadores antropométricos: índice de masa corporal
(IMC).Circunferenciadelacintura(CC).
-Perimenopausia.
-Posmenopausia.
A las mujeres que aceptaron par�cipar en el estudio, se les aplicó en la consulta el modelo de recolección del dato primario validado por el Centro de Inves�gaciones y Referencias de Aterosclerosis de la Habana (CIRAH), que se u�liza para facilitar las inves�gaciones de aterosclerosis en inves�gaciones en la comunidad.
Las variables estudiadas fueron: hipertensión arterial, diabetes mellitus �po 2, hipercolesterolemia, tabaquismo (se exploraron según antecedentes personales) sobrepeso, obesidad, obesidad abdominal (según medidas antropométricas) y sedentarismo (se consideraron sedentarias aquellas mujeres que trabajan sentadas o de pie y no realizan ninguna ac�vidad �sica complementaria, el cálculo no está exento de errores, perobrindaunaideadeaquellasmujeresque�enenpoca o ninguna ac�vidad �sica, es decir, sedentarias e hipociné�cas).
Para la evaluación de la acumulación y distribucióndetejidoadipososeu�lizóel IMC oíndicede Quetelet,quesedefinecomoelpesoenkgdivididoporla talla expresada en metros y elevada al cuadrado. Según Garrow,sepuedeclasificaralossujetosencuatrogrados, deacuerdoalIMC (9)
-Normopeso-Grado0:(IMC:20-24,9kg/m2).
-Sobrepeso-GradoI:(IMC:25-29,9kg/m2).
-Obesidad-GradoII:(IMC:>=30-39.9kg/m2).
-Obesidad-GradoIII(IMC>40kg/m2).
Las mediciones antropométricas se realizaron por la inves�gadora principal, con equipos calibrados y supervisados antes de comenzar el estudio y durante este.
La CC se tomó con una cinta métrica flexible, se solicitó a la paciente despejar esta zona. Se marcó un punto intermedio, entre el margen costal inferior y la espina ilíaca anterosuperior, en bipedestación y en un plano paralelo al suelo tras una espiración poco profunda y luego se colocó la cinta métrica en el punto intermedio, alrededor de la cintura y se midió la circunferencia. Se
considerarán valores normales ≤ 88 cms según los criterios del Na�onal Colesterol Educa�on Program /Adult Treatment Panel III (NCEP/ATP III), (por sus siglas eninglés).
Lavariableperimenopausiayposmenopausia,se evaluó según III Consenso Cubano sobre Climaterio y Menopausia:(10)
-Perimenopausia: desde el inicio de los síntomas climatéricos hasta la menopausia, se define por la aparición de cambios en el patrón menstrual acompañados o no de síntomas vasomotores y/o psicológicos.
-Posmenopausia: etapa que se ex�ende desde la menopausia(amenorreamayorde12meses)hastalos64 años,queasuvezsesubdivideen:
-Etapa temprana: se refiere a los 5 primeros años de posmenopausia.
-Etapa tardía: desde 5 años después de la menopausia hastalos64años.
ElestudiofueaprobadoporelComitédeÉ�cadel área de salud, se tomaron en consideración los criterios é�cos para la inves�gación en seres humanos. Se le solicitó a cada paciente su consen�miento informado, antes de ser incluida en la inves�gación. Se explicaron los obje�vos del estudio y la garan�a de la confidencialidad de los datos, así como la posibilidad de abandonar el estudio,sinconsecuenciaparasuatenciónposteriorenel áreadesalud.
Con la información obtenida se creó una base de datos en Microso� Excel que fue posteriormente exportada a SPSS (Sta�s�cal Package for the Social Sciences) (por sus siglas en inglés) versión 27.0, para Windows.Secrearontablasdedistribucióndefrecuencia con valores absolutos (número de casos) y rela�vos (porcentajes). Se determinó la media y la desviación estándar en las variables que lo requerían para su presentación resumida en la población de mujeres de 40 a64añosylas�picasmedidasdeasociación(OddsRa�os y coeficientes de con�ngencia) para evaluar las asociacionesbinariasentrelasvariables.
RESULTADOS
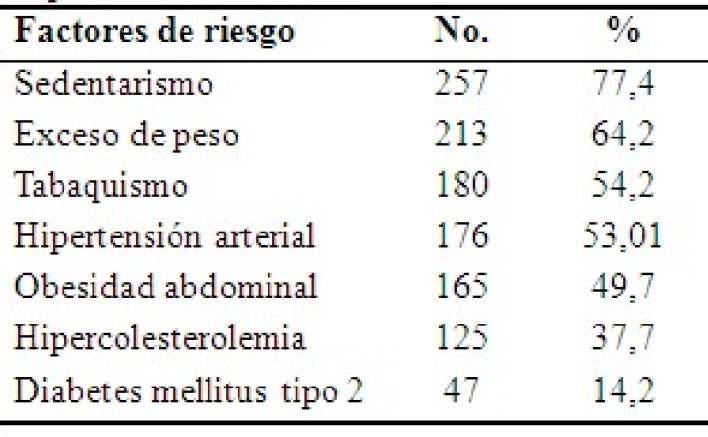
El rango de edades que predominó fue el de 50 a 54añosparauntotalde135(40,7%).Lamediadelaedad fue de 53,40 años, el color de la piel blanca y el grado de escolaridaduniversitario.Enetapadeperimenopausiase encontraban 60 pacientes (18,1 %) y en etapa de posmenopausia (272) 81,9 %. El sedentarismo fue el factor de riesgo cardiovascular que prevaleció, 257 pacientes para el 77,4 %, seguido del exceso de peso 213 (64,2%)ydeltabaquismo180(54,2%).(Tabla1).
Tabla 1. Distribución de los factores de riesgo en lapoblaciónestudiada
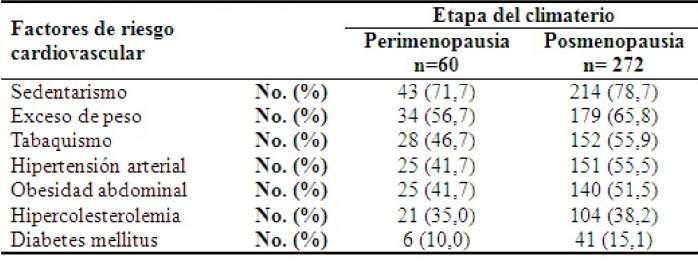
A con�nuación, se observa cómo los factores de riesgo cardiovascular tuvieron una elevada frecuencia en la etapa de posmenopausia con respecto a la etapa de perimenopausia, con prevalencia del sedentarismo con 214 pacientes (78,7 %), seguido del exceso de peso con 179pacientes(65,8%).(Tabla2).
Tabla 2. Distribución de los factores de riesgo cardiovascular según etapa de perimenopausia y posmenopausia
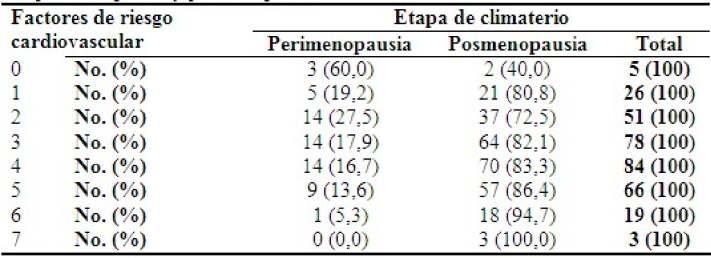
Al agrupar los factores de riesgo cardiovascular, seobservacómoenlaetapadeposmenopausiaaumentó el porcentaje de los factores de riesgo agrupados con respecto a la etapa de perimenopausia, por ejemplo, las pacientes que tuvieron 3 factores de riesgo, representaronel82,1%delaspacientes,mientraslasque tuvieron 7, representaron el 94,7 % en etapa de posmenopausia.(Tabla3).
Tabla3.Distribuciónsegúnelnúmerodefactores de riesgo de aterosclerosis y etapa de perimenopausia y posmenopausia
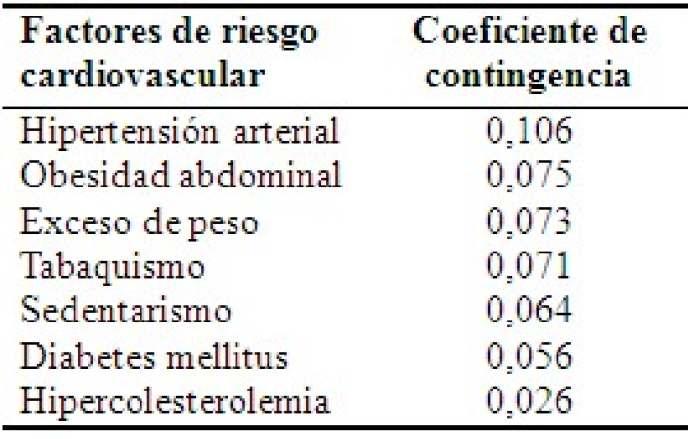
Al analizar los coeficientes de con�ngencia, que aportanunamedidadelaasociaciónentrelosfactoresde riesgo cardiovasculares y la etapa de posmenopausia, se
observó la mayor asociación con la hipertensión arterial, seguidodelaobesidadabdominal.(Tabla4).
Tabla 4. Asociación de la posmenopausia con los factoresderiesgodeenfermedadcardiovascular.
DISCUSIÓN
Lasenfermedadescardiovascularessonungrupo dedesórdenesdelcorazónydelosvasossanguíneos,que desde hace más de 20 años se man�enen como la primera causa de muerte en todo el mundo Generalmente, se producen debido a la presencia de una combinación de factores de riesgo cardiovascular, que son un es�lo de vida o caracterís�ca biológica cuya presencia incrementa la probabilidad de desarrollar o morir como consecuencia de una enfermedad cardiovascular en aquellas personas que lo presentan. (11)
Existen diferencias entre hombres y mujeres, en cuanto a estos factores de riesgo, los factores de riesgo cardiovascular exclusivos del sexo femenino son, en la mujer joven, el síndrome de ovario poliquís�co, tratamiento con an�concep�vos hormonales y la menarquia precoz; en la mujer embarazada, la diabetes gestacional, la hipertensión gestacional y el parto prematuro; y en la mujer adulta, la terapia de reemplazo hormonalylamenopausia.(11)
Las enfermedades cardiovasculares representan la principal causa de muerte de las mujeres en todo el mundo, tanto en edad fér�l como después de la menopausia y cons�tuyeron alrededor del 30 % del total de muertes en mujeres en 2021. Las mujeres, durante la menopausia, experimentan un riesgo mayor de muerte por enfermedades cardiovasculares, porque el efecto protector de los estrógenos en esta etapa de la vida se pierde y esto a su vez se asocia a una mayor prevalencia de factores de riesgo cardiovascular como: la diabetes mellitus, el síndrome metabólico, la redistribución de la grasa corporal, el aumento de peso, la dislipidemia y la sensibilidadinsulínica,porlotanto,lapostmenopausiase
ha conver�do en un factor de riesgo cardiovascular muy importante y hace que las mujeres estén predispuestas, no solo a una mayor mortalidad por esta causa, sino también a presentar otras enfermedades o condiciones que incrementan de forma adicional el riesgo cardiovascular (1,5,12)
Enlamenopausiaconfluyenunaseriedefactores que hacen que el riesgo de enfermedades cardiovascularespuedaagudizarse.Alrededordeun60% de las mujeres menopaúsicas padecen alguna enfermedad crónica, y son las enfermedades cardiovasculares las que mayor tasa de morbilidad y mortalidadproducenapar�rdeestaépoca,afinesconlos cambios metabólicos que ocurren durante la transición deperimenopausiaamenopausiayaestablecida.(13)
La menopausia se asocia con un aumento del colesterol de lipoproteínas de baja densidad, lo que contribuye a la dislipidemia aterogénica, por otra parte, las mujeres en la posmenopausia a menudo experimentan un aumento de la presión arterial sistólica, la pérdida de los efectos vasodilatadores de los estrógenoscontribuyealincrementodelarigidezarterial y la hipertensión, lo que agrava el riesgo cardiovascular Además, durante esta etapa, la obesidad abdominal, se puedeincrementardebidoaloscambioshormonalesque conducen a un aumento de la masa grasa total y grasa visceral, lo cual está relacionado con complicaciones metabólicasasociadas.(3,14,15)
Al mismo �empo, la menopausia está vinculada con un aumento del estrés oxida�vo y la inflamación sistémica, procesos que están implicados en la patogénesis de la aterosclerosis y otras condiciones cardiovasculares. En cuanto a los trastornos metabólicos, la prevalencia del síndrome metabólico, caracterizado por un metabolismo alterado de la glucosa y resistencia a la insulina, es mayor, lo que acrecienta el riesgo de desarrollar diabetes �po 2 y enfermedades cardiovasculares.(14,15)
Durante la transición menopáusica, las mujeres muestran numerosos cambios metabólicos, independientes del envejecimiento, que podrían explicar el aumento de los eventos cardiovasculares asociados conmenopausia.
Una inves�gación realizada en un total de 97 mujeresdelBiobankdeOxford,unestudioprospec�voen mujeres premenopáusicas y posmenopaúsicas que se some�eron a absorciometría dual de rayos X, bioquímica sanguínea y lecturas de presión arterial antes y después de la menopausia, proporciona evidencia de que a lo largo de la transición menopáusica, se observan cambios en la distribución de la grasa corporal hacia una
distribución más similar al androide, junto con un empeoramiento de los factores de riesgo cardiovascular durante este mismo período. (3) Ambos estudios con diferentes métodos de recolección de los datos, evidencian, el aumento de los factores de riesgo cardiovascularenlaposmenopausia.
En estudio realizado en la consulta externa del Servicio de Ginecología del Hospital General San FranciscodelIESS(QuitoEcuador),(12)conelobje�vode determinar el riesgo cardiovascular en mujeres perimenopaúsicas y posmenopaúsicas, mediante la aplicación de la escala de Framingham se estudiaron 350 mujeres,conedadmedia56,1años;delascuales67,43% correspondieron a pacientes postmenopáusicas y 32,57 % a pacientes perimenopáusicas. En el estudio se paten�za que los factores asociados a las mujeres perimenopaúsicas y postmenopáusicas, clasificados según grados de riesgo cardiovascular de Framingham incluyeron: obesidad, falta de ac�vidad �sica, diabetes, osteoporosis,dislipidemiaeHTA
En el proyecto MENOVASC (11) un estudio realizado en solo 18 mujeres entre 45 y 55 años perimenopaúsicas, asistentes a una farmacia comunitaria, en Murcia, España, a las cuales se les tomó los niveles de colesterol y tensión arterial, el 38,9 % tenía hipertensión arterial y el 44,4 %, niveles de colesterol elevados, el 61 % presentaba sobrepeso y el 77,8 % realizaba ac�vidad �sica. En esta inves�gación se trabajó según antecedentes patológicos personales, pero las cifras no difieren en gran medida de las halladas en el Proyecto, salvo la ac�vidad �sica, que en este estudio un granporcentajedemujereslarealizaban.
En una inves�gación ejecutada en Valencia, España, por Romero Alonso (13) en pacientes que acudieronaunaconsultaprivadademedicinageneral,se observa, según las encuestadas, que el 11,7 % tenía diagnos�cada hipertensión arterial (5,5 % de las perimenopáusicasvs16,9%posmenopaúsicas);el21,1% decían tener hipercolesterolemia (5,6 % perimenopáusicas vs 33,3 % posmenopáusicas) La prevalencia de diabetes �po 2 fue del 3,7 % y la de obesidad del 27 % en ambos casos sin diferencias según estatusdemenopausia,eranfumadorasyel17,8%delas perimenopaúsicas vs 25,6 % de las posmenopaúsicas, el ejercicio �sico lo realizaba el 54,8 % de las perimenopaúsicas vs el 66,7 % de las posmenopaúsicas, el 31,5 % de las perimenopaúsicas vs el 30 % de las posmenopáusicas tenían exceso de peso, resultados que engeneraldifierenconlosdeestainves�gación.
Un estudio coreano(4) observacional retrospec�vo con análisis secundario, que u�lizó los datos de cohortes nacionales extraídos del Korean
Genome and Epidemiology Study, (KoGES) que tuvo como obje�vo examinar la incidencia y los factores de riesgo de las enfermedades cardiovasculares y cerebrovasculares entre las mujeres menopáusicas de 40 a64años(edadmediadelaspar�cipantesde54,57±6,15 años), un seguimiento de 14 años, halla que el 69,5 % �enesobrepeso,el4%fuma,el5,8%esdiabé�ca,el39,8 % es hipertensa, el 35,3 % �ene una obesidad abdominal (≥ 85 cm) y un 36,6 % el low-density lipoprotein (LDL) elevado.
Enelaño2023serealizaenfarmaciasitalianas(5) una campaña de prevención cardiovascular para evaluar la eficacia de las ac�vidades de cribado ofrecidas por las farmacias y aumentar la conciencia sobre el estado de salud cardiovascular en mujeres italianas mayores de 40 años, que acuden de forma voluntaria; como resultado, se evaluaron 1510 mujeres, el 84,7 % menor de 70 años; el factor de riesgo cardiovascular más prevalente fue el es�lo de vida sedentario (57,9 %), seguido de sobrepeso/obesidad (44,3 %), hipercolesterolemia (37,9 %), hipertensión (31,3 %), tabaquismo (20,6 %) y diabetes (5 %), 1 de cada 4 mujeres fue clasificada como con mayor riesgo cardiovascular Aunque la metodología de este estudio es diferente a la de este, es de destacar que coinciden el sedentarismo y el exceso de peso, como losfactoresderiesgoprevalentes.
Los resultados confirman la alta prevalencia de factores de riesgo ateroscleró�co en mujeres en posmenopausia, resultados que coinciden con los de estudios previos que evidencian el impacto del déficit estrogénicoenlasaludcardiovascular.Elsedentarismo,el exceso de peso, el tabaquismo son factores modificables que deben abordarse prioritariamente con estrategias preven�vas La hipertensión común en esta etapa, requieren vigilancia y tratamiento oportuno para evitar complicaciones. Estos hallazgos subrayan la importancia de programas integrales de salud dirigidos a mujeres climatéricas, que incluyan educación, promoción de es�losdevidasaludablesycontrolmédicoregular.
Se observó una mayor prevalencia de factores de riesgo en mujeres posmenopáusicas comparadas con perimenopáusicas. La posmenopausia se asocia con una elevada frecuencia de factores de riesgo ateroscleró�co, especialmente, hipertensión arterial y obesidad abdominal. La iden�ficación temprana y el manejo adecuado deestosfactoresson esencialesparareducirla cargacardiovascularenmujeresclimatéricas.
CONFLICTODEINTERESES
Lasautorasdeclaranlanoexistenciadeconflictos deinteresesrelacionadosconelestudio.
LOSROLESDEAUTORÍA
1.Conceptualización:AnaMaryFernándezMilán. 2.Curacióndedatos:AnaMaryFernándezMilán.
3.Análisis formal: Ana Mary Fernández Milán, Georgia Díaz-PereraFernández.
4.Adquisición de fondos: Esta inves�gación no contó con adquisicióndefondos.
5.Inves�gación:AnaMaryFernándezMilán.
6 Metodología: Ana Mary Fernández Milán, Daysi Antonia Navarro Despaigne, Georgia Díaz-Perera Fernández.
7 Administración del proyecto: Ana Mary Fernández Milán.
8.Recursos:AnaMaryFernándezMilán.
9.So�ware:AnaMaryFernándezMilán.
10 Supervisión: Daysi Antonia Navarro Despaigne, GeorgiaDíaz-PereraFernández.
11.Validación:AnaMaryFernándezMilán.
12.Visualización:AnaMaryFernándezMilán.
13.Redacción del borrador original: Ana Mary Fernández Milán, Daysi Antonia Navarro Despaigne, Georgia DíazPereraFernández.
14.Redacción, revisión y edición: Ana Mary Fernández
Milán, Daysi Antonia Navarro Despaigne, Georgia DíazPereraFernández.
REFERENCIASBIBLIOGRÁFICAS
1. Hurtado L, Saldarriaga CI, Jaramillo LI, Hormaza MP
Riesgo cardiovascular durante la menopausia: una visión del cardiólogo y del ginecólogo. Rev Colomb Cardiol[Internet]. 2022[citado10/8/2023];29(1):[aprox.8p.].
Disponible e n : h�ps://www.scielo.org.co/pdf/rcca/v29n1/0120-5 633-rcca29-1-7.pdf
2. Sariol Y, Navarro D, Álvarez R, García JK, Domínguez E. Intensidaddelsíndromevasomotorysurelaciónconlafunción endotelial en mujeres de edad mediana Rev Cubana Endocrinol[Internet]. 2 0 2 1 [ c i t a d o 16/3/2022];32(1):[aprox.10p.].
D i s p o n i b l e e n : h�ps://revendocrinologia sld cu/index php/endocr inologia/ar�cle/view/264/291.
3. Dehghan A, Vasan SK, Fielding BA, Karpe F. A prospec�vestudyoftherela�onshipsbetweenchangeinbody composi�on and cardiovascular risk factors across the
menopause.Menopause.2021;28(4):400-6.
4. Park JH, Seo EJ, Bae SH Incidence and Risk Factors of Cardio-Cerebrovascular Disease in Korean Menopausal Women:ARetrospec�veObserva�onalStudyusingtheKorean Genome and Epidemiology Study data. Asian Nurs Res. 2021;15(4):265-71.
5. Del Pinto R, Vitale M, Morreale ME, Mo�nelli C, Muiesan ML, Volpe M, et al. Cardiovascular risk factors and diseasesandawarenessofrelatedburdeninwomen:Resultsof a survey in italian pharmacies. High Blood Press Cardiovasc Prev 2025;32(2):191-8.
6. Sambola A, Campuzano R, Castro A, Goya M, Coronado P, Fernández R, et al Primary and secondary cardiovascular preven�on through life cycles in women Consensus document of the SEC-GT CVD in Women, ACP-SEC, SEGO, AEEM, SEEN,semFYC, SEMERGEN, AEP,and AEM Rev Esp Cardiol[Internet]. 2025[citado 20/10/2025];78(7):[aprox. 12p ] Disponible en: h�ps://www revespcardiol org/enprimary-and-se condary-cardiovascular-pre-ar�culoS1885585725000222-pdf-file.
7. Ministerio de Salud Pública. Anuario Estadís�co de Salud 2024[Internet] La Habana: MINSAP;2025[citado 20/5/2025]. Disponible en: h�ps://bvscuba.sld.cu/anuarioestadis�co-de-cuba/.
8. FariñasL,CarmonaE.Cubaendatos.Envejecimientoy esperanza de vida, ¿qué dicen los indicadores demográficos? [Internet]. La Habana: Cubadebate;2023[citado 27/7/2024]. Disponible e n : h�ps://www cubadebate cu/especiales/2023/06/0 2/cubaen-datos-envejecimiento-y-esperanza-de- vida-que-dicen-losindicadores-demograficos/.
9. González NL, Tejeda AA, Quin�n E Indicadores antropométricos y es�los de vida relacionados con el índice aterogénico en población adulta. Cienc Ergo-sum[Internet]. 2020[citado 1/2/2024];27(1):[aprox 10p ] Disponible en: h�ps://www.redalyc.org/journal/104/10461231003/html/.
10. Sociedad Cubana de Ginecología y Obstetricia. III Consenso Cubano sobre Climaterio y Menopausia. 3ra ed. La Habana:CENESEX;2021.
11. Palazón A, Sánchez DP. Programa piloto de cribado de riesgo vascular en la mujer perimenopaúsica desde la farmacia comunitaria:proyecto MENOVASC F a r m Comunitarios[Internet]. 2022[citado 15/9/2025];14(Suppl 1 ) : [ a p r o x . 7 p . ] . D i s p o n i b l e e n : h�ps://www farmaceu�coscomunitarios org/es/sy stem/files/journals/3475/ar�cles/fc23-15-03-03-m enovasc.pdf
12. Mosquera D, Díaz A. Factores de riesgo asociados al riesgo cardiovascular en mujeres Peri y Postmenopaúsicas atendidasenlaconsultaexternadelServiciodeGinecologíadel Hospital General San Francisco del IESS en el periodo marzo 2015 hasta marzo 2019[Internet]. Quito:Repositorio Nacional PUCE;2020[citado15/9/2025]. Disponible e n : h�ps://repositorio.puce.edu.ec/items/bf630784-6 5a8-410c8f87-361aa3e9d166/full.
13. Romero A Factores de riesgo en mujeres en situación de perimenopausia y posmenopausia y su prevención
[Internet]. Valencia:Universidad de Valencia;2023 [citado 15/9/2025].
D i s p o n i b l e e n : h�ps://webges uv es/public/uvEntreuWeb/tesis/tesis2544468-AT9057LL24M17EG5.pdf.
14. Anagnos�sP,Stevenson JC Cardiovascularhealthand the menopause, metabolic health Best Pract Res Clin EndocrinolMetab.2024:38(1):101781.
15. Song DK, Hong YS, Sung YA, Lee H. The effect of menopause on cardiovascular risk factors according to body mass index in middle-aged Korean women PLoS One 2023;18(3):e0283393.
Aplicaciones y retos de ChatGPT en la medicina de laboratorio
EsteartículorevisaelusodeChatGPTyotroschatbots,destacandotantoventajas como limitaciones. Enfatiza la necesidad de evaluar la fiabilidad y veracidad de la información generada con herramientas específicas que garanticen la calidad de la información.
AUTOR
Zhili Niu, Xiandong Kuang, Juanjuan Chen, Xin Cai y PinganZhang*
Servicio de Análisis Clinicos, Ins�tute of Transla�onal Medicine, Renmin Hospital of Wuhan University, Wuhan, HuBeiProvince,Hubei,China
Correspondencia:zhangpingan927@163.com
Fuente: Adv Lab Med 2025; 6(4): 397–410. h�ps://doi.org/10.1515/almed-2025-0158
RESUMEN
La rápida evolución de la inteligencia ar�ficial ha permi�do desarrollar chatbots con un enorme potencial en campos como el de la medicina, especialmente en el laboratorio clínico. Realizamos un análisis sistemá�co de lasventajaseinconvenientesquesuponelau�lizaciónde chatbots en este campo, profundizando en sus posibles aplicaciones para el diagnós�co de enfermedades. La fiabilidad y veracidad cien�fica de los chatbots se ven
determinadas por diversos factores, entre los que se encuentran la calidad de los datos, los sesgos de los modelos, la protección de la privacidad, y los requisitos de retroalimentación del usuario. Sin embargo, el marco jurídico existente, como la Ley sobre inteligencia ar�ficial (IA) de la UE, no garan�za por sí solo la veracidad y fiabilidad de los contenidos, por lo que no podemos depender únicamente del mismo, haciendo necesario el empleo de dos herramientas de evaluación, METRICS y CLEAR, herramientas diseñadas para evaluar de manera integral la calidad de la información relacionada con la saludgeneradaporIA.
Palabras clave: ChatGPT; chatbots; laboratorio clínico; ventajas;desventajas
INTRODUCCIÓN
La inteligencia ar�ficial (IA) fue conceptualizada por primera vez en 1950 por la pregunta fundamental planteada por Alan Turing “¿Pueden pensar las máquinas?”, que sentó los fundamentos teóricos de este
campodeconocimiento(1).
El término “inteligencia ar�ficial” fue oficialmente acuñado en 1956 por John McCarthy et al. en la Conferencia de Dartmouth, dando así lugar al nacimiento de la IA como una disciplina cien�fica propia (1).
La IA abarca un amplio espectro, desde la inteligencia ar�ficial general (IAG), que trata de replicar la inteligencia humana, hasta la inteligencia ar�ficial estrecha (IAE) o débil, centrada en tareas específicas. En un principio, la IA empleaba algoritmos basados en reglas, como las reglas “si… entonces”, siendo estos sistemas no adapta�vos aún empleados actualmente en muchos entornos clínicos. Sin embargo, los avances tecnológicos han permi�do desarrollar métodos más sofis�cados de IA, entre los que se encuentran los algoritmos de aprendizaje automá�co (ML, del inglés, machine learning) y de aprendizaje profundo (DL, del inglés, deep learning), mejorando así el análisis de datos, el reconocimiento de imágenes y la predicción de enfermedadeseneldiagnós�coclínico.
Comoresultadodelaautoma�zacióngradualdel laboratorio clínico, se generan a diario enormes volúmenes de datos de extrema complejidad, sobrepasando la capacidad de procesamiento del cerebro humano, y haciendo cada vez más necesaria la u�lizacióndela IA Enellaboratorioclínico,la IA escapaz deanalizardatosestructuradosdegrancalidad,loqueha revolucionadolosmétodosdiagnós�cos(2).Losmodelos básicos de IA genera�va simplifican los flujos de trabajo, mejoran la eficiencia y reducen los costes sanitarios, impulsadoademáslamedicinapersonalizada,alpermi�r predecir el riesgo de enfermedades y sus resultados clínicos con mayor precisión. Así mismo, estos modelos de IA han mejorado la alfabe�zación en salud pública, empoderando a los pacientes al proporcionarles información sanitaria comprensible que les permite una mejorautoges�óndesusenfermedades(3).
En los úl�mos años, el desarrollo de los grandes modelosdelenguaje(LLM,porsussiglaseninglés),como los trans- formadores pre-entrenados (GPT), BERT y el modelo de lenguaje Pathways (PaLM) ha tenido un gran impactoendiversoscampos,entrelosqueseencuentran la generación de textos, la traducción automá�ca y el

diseño crea�vo de contenidos. Los LLM han revolucionado la interacción médico-paciente al simular las conversaciones humanas, lo que ha modificado los patronesdecomunicacióntradicionalesenelcampodela salud (4). Aunque los chatbots de IA pueden mejorar la alfabe�zación en salud, responder con rapidez a preguntas frecuentes sobre pruebas analí�cas y ayudar a interpretar los resultados de las mismas, sus aplicaciones siguen encontrándose en fase inicial y los riesgos y dificultades asociados a los mismos precisan ser abordados (5, 6). Cuando a los pacientes no se les proporciona con pron�tud una explicación de los resultados de las pruebas analí�cas, estos suelen recurrir a internet para buscar información, lo que puede derivar en desinformación y riesgos para la salud (7–9). Además, elrendimientodelosdiferentesmodelosdechatbotvaría significa�vamente, influenciado por factores como las configuraciones del modelo, la diversidad de las indicaciones y las metodologías de evaluación (10–12). Los chatbots de IA �enen la capacidad de generar información aparentemente creíble pero imprecisa en realidad, por lo que es necesario que tanto los médicos como el personal del laboratorio sean conscientes de las ventajasylimitacionesdeestasherramientas(13,14).
El propósito de la presente revisión es realizar una síntesis de las ventajas y limitaciones de emplear chatbots en el laboratorio clínico, así como analizar las dificultades que esta prác�ca plantea y dar orientación para futuras inves�gaciones en el contexto del laboratorio clínico. Así mismo, proporcionamos algunas referencias de gran u�lidad sobre el empleo de chatbots, dirigidas al personal de laboratorio, favoreciendo de esta formalaintegracióndelaIAenlamedicina.
Necesidadesyestadoactualdelainteligenciaar�ficial
Los informes de medicina de laboratorio son determinantes en la toma de decisiones clínicas, ya que influyendemanerasustancialeneldiagnós�coyelección de tratamientos, jugando un papel crucial en el manejo de los pacientes. Sin embargo, la complejidad de dichos informessuelehacerqueestosresultenconfusosparalos legos en la materia, llevando a no pocos pacientes a buscar información en los chatbots cuando presentan problemasdesalud.Algunosestudiosseñalanqueel78% de los usuarios de ChatGPT �enden a emplearlo para realizarunautodiagnós�co,loquesubrayalasignifica�va demanda existente de fuentes fiables de información sanitaria (15). Según el estudio realizado por Giardina et al.,el46%delospacienteshacenusodelasbúsquedasen internet para interpretar los resultados de sus pruebas analí�cas, lo cual también refleja la dificultad que estos encuentran a la hora de evaluar la gravedad de los resultados (5). La ausencia de información clara en un plazo razonable de �empo puede agravar la
preocupación y dificultad de los pacientes para interpretarlosresultados.Asímismo,elestudiorealizado por Kopanitsa revela una mayor probabilidad de que los pacientes que reciben explicaciones generadas automá�camente presenten una mejor adherencia al seguimiento (71 %), en comparación con aquellos a los que únicamente se les proporcionan los resultados de las pruebas(49%).Lospacientessuelenapreciarlapron�tud de dichas aclaraciones, lo que evidencia el enorme potencial de los nuevos métodos de comunicación para mejorar notablemente la experiencia del paciente, así comolosresultadosclínicos(16).
Se han observado caracterís�cas jerárquicas significa�vas en la percepción y aceptación de la IA por parte del personal clínico (17–19). La mayoría de los encuestados abogan por el uso de la IA como una herramienta complementaria, valorando especialmente su u�lidad para el análisis de datos. En las autoevaluaciones, los médicos más jóvenes (<45 años) evidencian un menor conocimiento de la IA en comparación con sus colegas, si bien manifiestan una mayordisposiciónhaciaelaprendizajecon�nuo.Porotro lado,elniveldeformaciónesdeterminanteenlosniveles deansiedad,yaquelospacientesconestudiossuperiores manifiestan una menor preocupación por los errores de la IA, debido a su mayor capacidad para comprender aspectostécnicos.
Cabe señalar que el personal de laboratorio muestra una profunda preocupación por la pérdida de empleos (32 %), frente aquellos que ocupan puestos de direcciónquepresentanunamenorinquietudalrespecto (25 %). Los modelos mul�modales de IA pueden mi�gar las limitaciones de alfabe�zación en IA del personal de laboratorio integrando diversos �pos de datos (p ej imágenes morfológicas, biomarcadores celulares, y parámetros bioquímicos) en un marco analí�co unificado (20).Lossistemasmul�modalessoncapacesdecombinar redesneuronalesconvolucionales(CNN,porsussiglasen inglés) para extraer las caracterís�cas espaciales de los fro�s de sangre, con modelos basados en grafos para analizar las redes de interacción celular y con algoritmos de regresión para interpretar las tendencias en los parámetros bioquímicos (21, 22) Esta integración evitaría tener que sinte�zar manualmente los datos, automa�zando tareas de elevada complejidad, como la iden�ficación de células displásicas en la leucemia, y determinando la correlación entre las anomalías morfológicas y las alteraciones en los parámetros bioquímicos (p.ej. niveles elevados de lactato deshidrogenasa) Para mejorar la accesibilidad, se pueden integrar estos modelos en plata- formas sencillas con interfaces intui�vas que incluyan funciones como cargar imágenes arrastrándolas y soltándolas y la generación automá�ca de informes obviando
complejidades técnicas. Así mismo, la incorporación de componentes de IA (XAI, por sus siglas en inglés) como los mapas de calor que resaltan caracterís�cas celulares esenciales o los resúmenes en lenguaje natural de correlaciones bioquímicas, permite al personal de laboratorio validar los resultados sin que ello requiera un elevado nivel de cono- cimientos técnicos. Al agilizar los flujos de trabajo y proporcionar información contextualizada, los modelos mul�modales salvan la brechaentrelascapacidadesdelaIAylastareasprác�cas de laboratorio, reforzando la confianza y la adopción de esta tecnología incluso entre aquellos con una formación limitadaenIA
Actualmente, las plan�llas de los laboratorios cuentan con una formación en IA alarmantemente insuficiente, habiendo demostrado unas competencias sólidasen IA soloel10,8%deestosprofesionales,siendo la proporción aún menor entre los informá�cos de los hospitales terciarios, en comparación con los centros sanitarios privados. Estas diferencias notables quedan evidenciadas por el hecho de que el 89,7 % de los encuestados haya declarado necesitar urgentemente formación en IA Sin embargo, el 47,2 % de los laboratorios encuentran dificultades significa�vas a la hora de implementar con eficacia las tecnologías de IA, principalmente debido a la falta de equipos de asistencia técnicaadecuados(23).
Existen discrepancias significa�vas entre los agentes implicados, rela�vas a la asignación de responsabilidades en los errores médicos relacionados conelusodeIA(24–26).Lasencuestasindicanqueel66,7 % de los encuestados abogan por una responsabilidad compar�da entre los usuarios y los fabricantes, frente a algunos que consideran que toda la responsabilidad por los productos con fallos de diseño debería recaer exclusivamente sobre el fabricante Los médicos se inclinan por asignar una responsabilidad compar�da entre los fabricantes y las ins�tuciones sanitarias, afirmando que los fabricantes deberían ser los que asuman la principal responsabilidad si las herramientas de IA han sido some�das a un proceso riguroso de validación y cumplen con los requisitos de calidad aplicables(26,27).
Integración de las interfaces HL7- FHIR/LIS y aspectos relacionadosconlaprivacidadylaseguridad
Para conseguir una implementación prác�ca de los chatbots de IA en el laboratorio, es necesario integrarlos de forma sólida en la infraestructura existente, especialmente a través de interfaces estandarizadas como Health Level 7 Fast Healthcare Interoperability Resources (HL7-FHIR) y Laboratory Informa�on Systems (LIS) (28, 29). HL7-FHIR permite el
intercambio
interoperable de datos entre el modelo de IA y la base de datos del laboratorio, garan�zando el acceso en �emporealalosresultadosestructuradosdelaspruebas, el historial de los pacientes, y los criterios diagnós�cos (28–31) La interpretación de perfiles bioquímicos mediante la aplicación de la IA se podría mejorar a través de la comunicación bidireccional con los LIS, lo que permi�ría generar alertas sobre valores crí�cos o realizar un análisis contextual de datos longitudinales (31). Sin embargo, dicha integración requiere de la aplicación de robustos protocolos de ciberseguridad des�nados a salva- guardar datos clínicos sensibles Entre los requisitos básicos de confidencialidad y seguridad se encuentran el cifrado de extremo a extremo de las transmisiones de datos, controles de acceso por funciones que cumplan la legislación vigente, como el Reglamento General de Protección de Datos (RGPD) y la Ley de Portabilidad y Responsabilidad del Seguro Médico (HIPAA), así como la realización de auditorías periódicas des�nadasadetectarposiblesvulnerabilidades.
Aplicación de chatbots a la inteligencia ar�ficial en la medicinadelaboratorio
Actualmente, el empleo de la IA se ha extendido a disciplinas como la radiología, para el reconocimiento de imágenes, si bien su u�lización en la medicina de laboratorio se encuentra en fase inicial. Esto se debe principalmente al hecho de que la interpretación de los informes de laboratorio implica un enorme número de variables cuan�ta�vas y cualita�vas, tales como los síntomas, el historial médico, y los resultados analí�cos (32), lo cual exige una aún mayor complejidad y precisión de los modelos de IA. Desde el lanzamiento de ChatGPT en 2022, este ha atraído el interés de la comunidad médica, habiéndose realizado importantes estudios sobre su rendimiento en los exámenes de habilitación médica, su viabilidad a la hora de responder a las preguntas de los pacientes, y su capacidad para ayudar a los médicos en la resolución de problemas clínicos, evidenciado su potencial aplicación en la medicina de laboratorio(33–35).
CapacidadesdeChatGPTenlamedicinadelaboratorio
Si bien no ha sido entrenado específicamente para procesar datos clínicos, se ha demostrado la viabilidad de emplear ChatGPT en la medicina. MunozZuluaga et al. llevaron a cabo un estudio en el que le realizaron 65 preguntas a ChatGPT rela�vas a múl�ples temas para evaluar sus capacidades y veracidad a la hora de responder a preguntas relacionadas con la medicina de laboratorio (36). Según los resultados obtenidos, ChatGPT contestó correctamente al 50,7 % de las
preguntas, dio una respuesta incompleta o parcialmente correcta al 23,1 % de las preguntas, ofreció información incorrecta o engañosa en el 16,9 % de las preguntas, y proporcionó una respuesta irrelevante al 9,3 % de las cues�ones. Cabe mencionar que las respuestas correctas solían referirse a preguntas relacionadas con conocimiento médicos o técnicos básicos (59,1 %), mientras que los errores se solían producir en las preguntas relacionadas con procedimientos o reglamentossobreprocedimientosdelaboratorio(31%). AunqueGPT-4presentamejorassignifica�vasenrelación a su veracidad, aún siguen siendo evidentes sus limitacionesenalgunoscampos.Girtonetal.evaluaronla capacidad de ChatGPT para responder a 49 consultas reales realizadas por pacientes en plataformas de redes sociales como Reddit y Quora rela�vas a sus pruebas analí�cas, y comparó las respuestas con aquellas proporcionadas por estudiantes de medicina (37). Los revisores tendían a preferir las respuestas de ChatGPT por encima de las aportadas por los profesionales médicos.EstehallazgosubrayalaevolucióndeChatGPT a la hora de manejar cues�ones clínicas complejas, revelando así mismo carencias en la formación de los profesionalesmédicosenestecampo.Aproximadamente la mitad de las respuestas de los estudiantes de medicina fueron calificadas como “inadecuadas”, frente a menos del 10 % de las respuestas de ChatGPT (37). La escasa atenciónprestadaalamedicinadelaboratoriodurantela formación médica podría contribuir a que incluso a los médicos más experimentados les resulte di�cil proporcionarrespuestasdecalidadapreguntasreales.
Otroestudiocomparólasrespuestasdetreschatbots
(ChatGPT, Gemini y Le Chat) con las proporcionadas por médicos colegiados en consultas online (38). En términos generales, los chatbots fueron superiores a los médicos en las consultas online a la hora de interpretar los resultados del laboratorio. Aunque los médicos online quedaron en primer lugar en el 60 % de los casos, Gemini recibió una puntuación inferior en solo el 39 % de los casos. ChatGPT presentó una calidad y veracidad similares a los de los médicos humanos. Sin embargo, los chatbots mostraron una mayor tendencia a sobrees�mar la gravedad clínica (incidencia del 22–33 %) frente a una tasa de sobrees�mación de 1,0 % entre los médicos. Esto evidencia la dificultad de los chatbots a la hora de procesar información contextual compleja e interpretar datos analí�cos, pudiendo la ausencia de patrones de referencia unificados dar lugar a interpretaciones incongruentes de los datos analí�cos de lospacientes(38).
Implementación de los chatbots para el diagnós�co en el laboratorioclínico
Los recientes avances en el campo de la inteligencia ar�ficial han animado a la comunidad cien�ficaaanalizarsucapacidadparalainterpretaciónde datos bioquímicos. Ka�an AN et al. demostraron la heterogeneidad en los niveles de veracidad de los modelos de IA (Copilot, Gemini) en el análisis de datos bioquímicos (39) Copilot mostró un rendimiento superior en todas las métricas de evaluación, logrando ventajas estadís�camente significa�vas en la interpretación de parámetros bioquímicos, frente a otros modelos Esto indica que su capacidad superior de procesamiento de datos radica en su sofis�cada arquitectura algorítmica. Aunque el rendimiento de los otros modelos fue inferior al de Copilot, sus capacidades en campos especializados siguen haciendo de ellas herramientas ú�les para su aplicación en tareas clínicas específicas(39).
La precisión diagnós�ca y el rápido procesamiento de datos que la microbiología exige confieren a esta disciplina un valor estratégico especial a la hora de integrar la inteligencia ar�ficial (IA) en la prác�ca clínica. La IA ha demostrado poseer una gran capacidad para mejorar la eficiencia en la toma de decisiones clínicas y op�mizar el manejo de enfermedades infecciosas, redundando en mejores resulta- dos clínicos. Sin embargo, es necesario seguir mejorando los sistemas de IA en el manejo de escenarios clínicos complejos y la generación de respuestas contextualmente apropiadas, con el fin de garan�zar su relevancia clínica (40). Cabe señalar que ChatGPT-4.0 presenta unas limitaciones notables a la hora de responder a consultas relacionadas con las pruebas de suscep�bilidadalosan�microbianos (41,42).Demanera errónea, el modelo recomendó el uso de la clindamicina para las infecciones por enterococo y no incluyó las metodologías estándar para la evaluación de la suscep�bilidad a la polimixina. Una información errónea podría inducir a errores en la prác�ca clínica, dando lugar a regí- menes terapéu�cos ineficaces y a un posible perjuicioparalospacientes.
Li Y et al. realizaron una evaluación sistemá�ca delrendimientodedos LLM,ChatGPT yGoogleGemini,a la hora de abordar consultas clínicas relacionadas con el VHB (43) ChatGPT-4.0 tuvo un rendimiento general superior, habiendo logrado una veracidad del 80,8 % en las preguntas basadas en la evidencia, frente a Google Gemini (73,1 %). El análisis por especialidad reveló una mayor u�lidad diagnós�ca de ChatGPT-4 0 en la interpretaciónserológicadel VHB,sibienGoogleGemimi proporcionó descripciones más completas de sus manifestaciones clínicas. Todos los modelos presentaron importantes limitaciones a la hora de ofrecer estrategias para la prevención de la infección por VHB, especialmente en lo rela�vo a la vigencia de la
información sobre vacunas. Así, únicamente Google Gemini hizo referencia al consenso actualmente existente, por el cual se recomienda la vacunación neonatal contra la hepa��s B en las 12 horas posteriores alnacimiento.
Además, a pesar de las variaciones en la veracidad, tanto ChatGPT como Gemini incumplieron la instrucción de que el nivel de legibilidad de la respuesta estuviera adaptado un nivel de 8° grado (13/14 años) (Flesch-Kincaid 10,2–11,4 grado), lo que dificulta su comprensión por parte de los pacientes. Estos hallazgos subrayanlanecesidaddequelosresultadosofrecidospor los LLM sean verificados por un médico, con el objeto de garan�zar tanto su interpretabilidad como la validez clínica. El presente estudio compara�vo aporta información crucial sobre las ventajas e inconvenientes de los modelos en relación a su implementación en la clínica.
Inconvenientes mul�dimensionales de los chatbots de saludenlaprác�caclínica
Aunque los chatbots fueron diseñados y presentados como herramientas conversacionales más que como herramientas para consultas sobre salud o de apoyo a la toma de decisiones clínicas, han demostrado poseer una capacidad asombrosa para detectar en interpretar alteraciones analí�cas. Esta capacidad se evidencia en su eficacia para el procesamiento y análisis de grandes volúmenes de datos, una capacidad especialmente notable de los grandes modelos de lenguaje como ChatGPT. Sin embargo, dicho potencial se ve limitado por algunas deficiencias, especialmente porque estos modelos no han sido específicamente entrenados ni op�mizados para su uso en la generación deinformesdemedicinadelaboratorio.
Dificultades en la aplicación de ChatGPT en la interpretacióndedatosanalí�cos
La evaluación del grupo de trabajo de la Federación Europea de Química Clínica y Medicina de Laboratorio(EFLM)revelaimportanteslimitacionesenel uso clínico de ChatGPT a pesar de su capacidad para generar “análisis de datos analí�cos correctos en términos generales y relevantes para la seguridad” (44). Por otro lado, ChatGPT no iden�ficó marcadores de enfermedad subclínica con valores en los límites de normalidad. Por ejemplo, no tuvo en cuenta que los niveles elevados de GGT no �enen por qué ser necesariamente indica�vos de daño hepá�co, ni que una distribución normal de la subpoblación de leucocitos no garan�za la integridad del sistema inmunológico. Dicho análisis por parámetros corre el riesgo de pasar por alto indicadores de patología incipiente. Así mismo, en el
reconocimiento de factores preanalí�cos surgen deficiencias importantes Aunque ChatGPT advierte correcta- mente del riesgo de diabetes ante la presencia de niveles elevados de glucosa y HbA1c, omite variables esencialespreviasalatomademuestras(p.ej.obtención en ayunas) a la hora de interpretar resultados discordantes(nivelesnormalesdeglucosaconcurrentesa nivelesnormalesdeHbA1c).
Además, ChatGPT realiza una síntesis incorrecta de los perfiles mul�analitos, y la interpretación de los marcadores de función hepá�ca (ALT, AST, bilirrubina, GGT)nointegraelcontextoclínico,queresultaesenciala la hora de obtener un razonamiento diagnós�co completo (44). Por otro lado, ChatGPT no analiza en profundidad los riesgos asociados a los resultados analí�cos. Por ejemplo, en los casos de anemia severa o de alteraciones en el perfil lipídico, se limita a aconsejar a los pacientes que consulten a un médico, pero no les informadelaposiblegravedadclínicadeestaspatologías, lo que podría poner en riesgo la salud de los pacientes. Por úl�mo, ChatGPT no es capaz de dis�nguir eficazmenteentrelosvaloresa�picosylosvaloresumbral crí�cos.Estalimitaciónpodríaderivarenerroresmédicos en escenarios clínicos crí�cos La incapacidad para diferenciarentrevaloresanormalesyvaloresclínicosque requieren atención médica urgente resulta especialmente preocupante, ya que dicha dis�nción resulta crucial para garan�zar una intervención médica adecuada.
Diversidadyvariabilidadentrechatbots
En el ecosistema actual de chatbots, la significa�va variabilidad entre los diferentes modelos dificulta considerablemente la realización de estudios compara�vos. Los modelos de IA genera�va están diseñados con diferentes arquitecturas, entornos y obje�vos,porloquesurendimientoycalidadalahorade generar contenido difieren sustancialmente. Así, su arquitectura y capacidades influyen directamente en la veracidad y efec�vidad de sus resultados. En algunas tareas concretas, existen diferencias significa�vas en el rendimiento de los dis�ntos modelos de IA genera�va. Por ejemplo, se ha demostrado que Bing es el que presentamayorveracidadyespecificidadenlapredicción deinteraccionesentrefármacos,superandosignifica�vamente a Bard y ChatGPT-4, lo que evidencia que algunos modelos podrían presentar algunas ventajas para aplicacionesespecíficas(45).
Así mismo, no debemos obviar la variabilidad del propio modelo, ya que el mismo modelo puede generar resultados incongruentes cuando se emplean diferentes configuraciones, datos de entrada o estrategias de generación, lo cual es especialmente relevante en el
campo de la salud pública, donde dicha inconsistencia puede tener importantes implicaciones en la toma de decisiones (45, 46). La heterogeneidad en el rendimiento de un modelo no afecta únicamente a la efec�vidad de la divulgación de la información, sino que también influye directamente en la experiencia y sa�sfacción del usuario. Por ejemplo, se ha demostrado que Bard proporciona información más comprensible sobre la rinoplas�a, seguido de ChatGPT y Bing (47). De este modo, tanto los inves�gadores como los usuarios deben ser cautelosos y seleccionar el modelo de IA genera�va con mejor rendimiento en tareas concretas y que sa�sfaga las necesidadesdelpropiousuario.
Riesgos asociados a la actualización de las versiones de loschatbots
Aunque el fin úl�mo de las actualizaciones de los chatbotsesmejorarsuscapacidadesyrendimiento,estas también plantean algunas dificultades rela�vas a la coherencia, calidad y fiabilidad de los datos Las actualizacionesdelosmodelospuedenintroducirnuevos conocimientos, con el riesgo de hacer referencia a datos obsoletos, especialmente en campos que evolucionan rápidamente, como es el caso de la medicina Por ejemplo, los datos empleados para entrenar ChatGPT no incluíanlosúl�mosvaloresdereferenciaparaelplomoen sangre de 3,5 μg/dL en los hemogramas de pacientes pediátricos. Por el contrario, CopyAI proporcionó valores de referencia exactos para el plomo en sangre, lo que indica que las diferencias en la actualización de datos de entrenamiento entre los dis�ntos chatbots pueden derivarenresultadosdeimpresiónclínicadiferentes(48). Además, el rendimiento no siempre mejora con las actualizaciones, pudiendo disminuir su veracidad en algunastareas.Unestudiorealizadoporlasuniversidades de Stanford y California, Berkeley, reveló que si bien GPT4.0 proporciona información más completa en algunas áreas, su veracidad en tareas como las matemá�cas, la codificaciónyelrazonamientovisualdisminuyó(49).Este fenómeno evidencia la importancia de evaluar con�nuamente el rendimiento de los LLM, especialmente en campos como la medicina de laboratorio,dondelaprecisiónresultacrucial.
Problemas de coherencia en la generación de contenidos aplicandomodelosdeIAgenera�va
La consistencia de los resultados de los chatbots enlageneracióndecontenidosmereceespecialatención, especialmente en campos especializados como la medicina. Los estudios indican que pequeñas diferencias en la redacción de los prompts o en la información contextual pueden provocar variaciones significa�vas en el contenido generado, pudiendo afectar a su fiabilidad a la hora de darle una aplicación prác�ca a dicha
información (10, 50, 51). Un estudio llevado a cabo por Kochanekycol.revelóunaconsistenciadel85–88%entre las respuestas de GPT-4.0 a la misma pregunta en el transcurso de cuatro días, lo que demuestra la influencia de la incer�dumbre en la generación de contenidos (52). En el campo de la medicina, donde es esencial que los resultados sean coherentes, la heterogeneidad en las respuestas podría plantear riesgos considerables. Es necesario con�nuar evaluando la reproducibilidad y precisión de ChatGPT en el campo de la medicina de laboratorio, con el fin de poder garan�zar su fiabilidad comofuentedereferenciaenaplicacionesclínicas(37).
Además,losmodelosde IA genera�vasepueden ver influidos por sesgos culturales y socioculturales inherentes a los datos de entrenamiento empleados, lo que puede provocar incoherencias en el contenido generado, dependiendo del contexto cultural o lingüís�co. Por ejemplo, Want y col. observaron que ChatGPT mostró un rendimiento significa�vamente superior en inglés que en chino durante el examen de habilitación en farmacia de Taiwán (53). Por otro lado, Alfertshofer y col. determinaron que el rendimiento de ChatGPT varió sustancialmente en los exámenes de habilitación en medicina de seis países, lo que evidencia la influencia de los factores nacionales y lingüís�cos (54). Estos hallazgos indican la necesidad de realizar estudios en profundidad, así como de op�mizar los modelos de IA genera�va en entornos mul�lingües y mul�culturales, con el fin de mejorar su adaptabilidad y precisión en dis�ntosescenarios.
Calidadlimitadadelainformaciónsanitaria
Loschatbotsestánadquiriendounpapelcadavez más importante en la divulgación de información sanitaria, aunque la claridad, concisión y relevancia de sus respuestas deben ser contempladas con cautela (37). En aras de la claridad, es preciso que el contenido generado sea fácil de entender, por lo que debe evitarse el empleo de jerga médica complicada para garan�zar que la población general pueda entender fácilmente los puntos clave. A su vez, para garan�zar la concisión de la información es necesaria una comunicación directa que no se ex�enda innecesariamente, lo que mejora la per�nencia de la información sanitaria y ayuda al público a mejorar su alfabe�zación en salud, permi�éndole así adoptar decisiones informadas sobre su salud. Por otro lado, resulta esencial que el contenido generado con IA sea relevante, ya que el acceso a información precisa y per�nente evita malentendidos, especialmente en escenariosenlosqueelpacientenopuedepreguntarasu médico en una consulta presencial, lo que evita situacionesdepreocupacióninnecesariaoriesgosparala salud causados por la desinformación (55). Dar prioridad a la relevancia de la información evita la sobrecarga de
información, garan�zando la emisión clara de mensajes importantes sobre salud. La información no relacionada con las consultas sobre salud puede dificultar la comprensión de las patologías por parte de la población, lo que agrava su confusión a la hora de manejar sus problemasdesalud.
Sin embargo, la divulgación de información sanitaria a través de la IA debe establecer un equilibrio entre las diversas necesidades de los pacientes y los faculta�vos. Los pacientes suelen preferir respuestas breves y directas para entender información clave, lo que contrasta con la tendencia por parte de los médicos a ofrecer respuestas detalladas y exhaus�vas Esta divergenciadenecesidadesesunaespadadedoblefilo:si bien la abundancia de información ayuda a los profesionales a realizar análisis en profundidad, puede sobrepasar al usuario, provocando dificultades de comprensión y preocupación. Independientemente del método de presentación empleado, es crucial que se proporcioneinformacióncompleta,yaquelaausenciade detallesnecesariospuedellevaraundiagnós�coerróneo o a un autodiagnós�co inexacto, aumentando los riesgos paralasalud.
A modo ilustra�vo, los pacientes con una alfabe�zación en salud limitada pueden encontrar dificultades a la hora de interpretar los resultados analí�cos con precisión, tales como iden�ficar los niveles altos de colesterol en el perfil lipídico, lo que puede derivar en graves problemas de salud como un infarto de miocardio o un accidente cerebrovascular (44). De este modo, mejorar la capacidad de los pacientes para entender los resultados de sus pruebas analí�cas resulta degranimportancia.
Riesgosderivadosdelas“alucinaciones”deloschatbots
El uso de chatbots para la divulgación de información sanitaria se está extendiendo, suscitando inquietud por el riesgo que puede conllevar la desinformación. Aunque las herramientas de IA como GPT presentan algunas ventajas a la hora de acceder a la información,suincapacidadparaexplicarsusprocesosde toma de decisiones impide que se puedan iden�ficar y corregir los sesgos o errores del propio modelo. En el campo de la medicina, la desinformación generada por la IA puede tener graves consecuencias, como un autodiagnós�coerróneo,atenciónmédicapostergada,la expansión de enfermedades potencialmente peligrosas,







insuficientes, y los sesgos inherentes a los datos básicos (63). Si los datos de entrenamiento son más an�guos, se pueden ver amplificados los posibles sesgos y errores en las respuestas de los modelos (64). Este fenómeno se torna especialmente evidente en los ar�culos existentes, especialmente en áreas clave como el diseño aleatorizado, lo que evidencia los posibles sesgos en los procesosdeseleccióndelasconsultas.
La Ley de IA de la UE y la Guía de apoyo a la toma de decisionesclínicasdelaFDA
La Ley de Inteligencia Ar�ficial de la Unión Europea (Ley IA), vigente desde el 12 de julio de 2024, cons�tuye el primer marco jurídico regulatorio integral de la IA, y prioriza el desarrollo é�co, la protección de los derechos fundamentales, y la innovación centrada en las personas (65). Adoptando un enfoque basado en los riesgos, la Ley clasifica los sistemas de IA en cuatro niveles: riesgo inaceptable (prohibido); riesgo elevado (p.ej. diagnós�co médico, sujeto a estrictos criterios de seguridad, transparencia y responsabilidad); IA general con riesgos sistémicos (obligación de transparencia); y riesgo bajo o sin riesgo (regulación mínima) (66). En el ámbito de la salud, la estricta norma�va sobre el uso de IA de riesgo elevado en contextos clínicos exige la realización de pruebas rigurosas, la mi�gación de sesgos, y el seguimiento post-comercialización, aunque siguen persis�endo algunas lagunas en relación a los derechos de los pacientes y la responsabilidad sobre las aplicaciones de riesgo bajo. Entre las dificultades, se encuentran una implementación desigual entre los estados miembro, marcos de responsabilidad civil ambiguos, y limitaciones cambiantes a la hora de detectar contenido generado con IA (67). La Ley también aborda aspectos relacionados con los derechos de protección de la IA, exigiendo transparencia sobre la u�lización de datos de entrenamiento y salvaguardando la propiedad intelectual, aunque exceptúa la inves�gación anterior a la comercialización (66) Se esperaqueestaLeytengaun impactoenotrosterritorios similaralquetuvolaRGPD,remodelandolasprác�casde IA a nivel mundial, y haciendo precisa una formación en é�ca de la IA Con el fin de establecer un equilibrio entre la regulación y la innovación, la Ley de IA promueve el desarrollo de una IA fiable, pero exige unas guías más claras, la colaboración de todos los agentes implicados, y la implementación de normas sanitarias adaptadas, con el fin de garan�zar el acceso a la IA en condiciones de igualdadyseguridadparalospacientes.
Hasta la fecha, la FDA no ha aprobado ningún modelo de LLM para la toma de decisiones clínicas. Se han realizado algunos estudios para evaluar si los LLM se pueden adherir a las regulaciones en el contexto de las urgenciasmédicas.Losresultadosobtenidosrevelanque,
aunque las recomendaciones sobre prevención proporcionadas por los LLM son adecuadas, el 100 % de las respuestas de GPT-4 y el 52 % de las respuestas de Llama-3 no se ajustaban a un escenario de urgencias, ofreciendounsoportecomparablealdeundisposi�vo,al sugerir diagnós�cos y tratamientos concretos (68). Aunque los prompts estuvieran basados en la guía de la FDA, no se logró que se ajustara a ella de manera uniforme Estos resultados evidencian la necesidad urgente de desarrollar nuevos marcos regulatorios que aborden la problemá�ca que el empleo de IA genera�va plantea en el ámbito de la salud, dado que las guías actuales resultan insuficientes a la hora de evitar que los LLM ofrezcan de manera no autorizada resultados que corresponderían a los de un disposi�vo médico autorizado.
Establecimiento de un marco integral de evaluación para abordar las limitaciones de los chatbots deIAenelcampodelasalud
A la luz de los riesgos que plantea el uso de chatbots de IA en la medicina, es impera�vo desarrollar un marco integral de evaluación. El primer paso para garan�zarlacalidaddelosresultadosgeneradosporla IA consiste en establecer unos criterios estrictos de evaluación que aborden la precisión, fiabilidad y relevancia de la información. Además, la evaluación periódica del rendimiento de los modelos permite iden�ficar fallas del sistema, garan�zando que todos los modelos de IA sean coherentes con la información más reciente en el campo de la medicina. Los mecanismos de retroalimentación, que reúnen información proporcionada por usuarios y profesionales, aportan datos de gran u�lidad para la mejora con�nua de los modelos La inclusión de mecanismos de revisión profesionales resulta igualmente crucial. La par�cipación de médicos expertos mejora aún más la fiabilidad e integridad cien�fica de los sistemas de IA, lo que garan�za que la información generada se ajuste a los criteriosdeé�cayprác�camédica.
Para tal fin, se han desarrollado diversas herramientas y guías para facilitar la evaluación y mejora de la calidad de la información en salud (69–71). Sin embargo, las herramientas actuales de evaluación de informaciónsanitarianohansidoadaptadasparaevaluar específicamente la calidad de la información en salud generada por los modelos de IA. Para poder garan�zar la fiabilidad y precisión de la IA en el campo de la medicina de laboratorio, es preciso disponer de herramientas devaluación estandarizadas. Actualmente, las herramientas“METRICS'y“CLEAR'”cuentan con amplia aceptación como métodos eficaces para evaluar informaciónensaludgeneradamedianteIA(72,73).
y la pérdida de confianza por parte de la población en los profesionaleseins�tucionessanitarias.Porejemplo,GPT ha proporcionado descripciones inexactas de los disposi�vos analí�cos aprobados por la FDA para la determinación de la troponina de alta sensibilidad en el lugar de atención Dichas “alucinaciones” no son incidentes aislados, lo que subraya las limitaciones de los modelos de IA genera�va a la hora de garan�zar la precisión de la información (56, 57). De este modo, resulta vital poder asegurar la precisión, fiabilidad y veracidad de la información médica generada por la IA. A la hora de diseñar y entrenar los modelos de IA, los desarrolladoresdebendarprioridadaesteobje�vo,dado que algunos estudios revelan que la generación de información imprecisa es un fenómeno muy extendido entredichasherramientas.
Implicaciones jurídicas y é�cas del empleo de datos para elentrenamientodechatbots
Lasimplicacionesjurídicasyé�casqueconllevala u�lización de datos para el entrenamiento de chatbots durante el desarrollo de modelos de inteligencia ar�ficial genera�va son mo�vo de preocupación (58–61). Estos aspectos no están relacionados únicamente con los
datos, sino también con su uso y aceptabilidad, lo que afecta directamente a la transparencia y credibilidad del modelo. La transparencia de los datos resulta de especial relevancia, ya que garan�za que tanto usuarios como inves�gadores conozcan los métodos empleados para la obtenciónylau�lizacióndedatos,pudiendoasívalidarla fiabilidad e integridad cien�fica del modelo. Así mismos, no debemos obviar los aspectos é�cos, especialmente cuando se u�lizan materiales y datos clínicos sujetos a derechos, dado que es impera�vo garan�zar la legalidad del proceso de obtención y u�lización de datos, a la vez que se salvaguardan los derechos de privacidad de los proveedoresdedatos.
Los modelos de IA genera�va como ChatGPT están entrenados con datos extraídos de internet, heredando inevitablemente los sesgos que dicha información con�ene, lo que se refleja en las respuestas de estos modelos (62). En diversos estudios, se han iden�ficado sesgos en los LLM en relación al género, la raza y otros factores sociales, lo cual no solo puede derivar en respuestas poco justas, sino que también puede exacerbar las desigualdades sociales. Dichos sesgos están ín�mamente relacionados con aspectos como las lagunas de datos, tamaños muestrales
Tabla1:EntradasenMETRICS.
Tabla2:EntradasenCLEAR
La lista de comprobación METRICS proporciona un marco para diseñar y comunicar estudios estandarizados sobre IA, abarcando nueve temas clave: Modelo, Evaluación, Temporalidad, Rango, Aleatorización, Recuento, y Especificidad de las indicacionesyellenguaje.Estostemasestánorientadosa analizar de manera exhaus�va el diseño y estado opera�vo de los modelos de IA, garan�zando el rigor cien�fico y la solidez de sus resultados. Por otro lado, la herramienta CLEAR se centra en la evaluación sistemá�ca de múl�ples dimensiones de contenido generado con IA, entre los que se incluyen cinco criterios clave: Integridad del con- tenido, Ausencia de informaciónfalsaenelcontenido,Evidenciaquerespalde el contenido; Per�nencia del contenido, y Relevancia. En la Tabla 1 se detalla el significado concreto de cada criterio, mientras que la Tabla 2 ofrece a los evaluadores
una guía clara para garan�zar que el contenido generado conIAcumpleunoscriteriosdecalidadpredefinidos.
Malik Sallam et al. evaluaron tres modelos de IA genera- �va (ChatGPT, Microso� Bing, y Google Bard) mediante el empleo de la herramienta METRICS (72). La puntuación total media de los tres modelos según METRICS fuede3,0(SD 0,58).Alanalizarloscriteriospor separado, el criterio “Modelo” fue el que recibió una puntuación media más alta, seguido de “Especificidad” Por otro lado, los criterios que obtuvieron puntuaciones más bajas fueron “Aleatorización” (clasificada como subóp�ma) y “Factores individuales” (clasificado como sa�sfactorio). En otro estudio, los cinco modelos de IA se evaluaron por separado empleando la herramienta CLEAR en relación a cinco temas diferentes (73). Microso� Bing fue el que obtuvo una puntuación CLEAR más alta (media 24,4±0,42), seguido de ChatGPT-4 (media: 23,6±0,96), Google Bard (media: 21,2±1,79), y finalmentedeChatGPT-3.5(media:20,6±5,20).
Si bien METRICS y CLEAR han facilitado la evaluación de contenidos generados con IA, también presentanalgunaslimitaciones(detalladasenlastablas1 y 2). Por ejemplo, es posible que estas herramientas no abarquen todas las variables en contextos concretos o tengan una aplicación limitada en algunos campos especializados. Estas limitaciones precisan ser validadas en estudios que confirmen su efec�vidad y adecuación para su aplicación en la prác�ca. La iden�ficación y resolución de dichas limitaciones nos permi�ría mejorar la credibilidad de la información en salud generada con IA,loquecontribuiríaaestablecerunabasesólidaparala tomadedecisionesclínicas(Figura1).
Figura1:Diagramadeventajaseinconvenientes.
La formación en medicina es un proceso que requiere �empo y se actualiza lentamente, lo que dificulta que los estudiantes asimilen todos los aspectos esenciales. De este modo, los chatbots de IA presentan granpotencialcomoimportantesherramientasauxiliares
en la formación médica, lo que contribuye a cubrir lagunasenlaadquisicióndeconocimientos.Sinembargo, la resolución crea�va de problemas sigue siendo una capacidad exclusiva del ser humano. Para aprovechar al máximo el potencial de la IA en la medicina, resulta esenciar contar con la colaboración de los desarrolladoresdeIAylosprofesionalesdelamedicina.
La medicina de laboratorio es un campo en rápida evolución, ya que surgen con�nuamente nuevas tecnologías y métodos analí�cos que se van integrando en la prác�ca clínica. Si resolviéramos eficazmente las limitaciones de los chatbots de IA, estos se conver�rían enherramientasindispensablesparalosfaculta�vosylos técnicos de laboratorio en la prác�ca ru�naria. Superar las dificultades existentes podría redundar en una mayor precisión diagnós�ca, una mejor calidad en la atención a los pacientes, y en la promoción de la medicina personalizada. La colaboración entre la IA y los médicos expertos humanos sentará las bases para el futuro desarrollodelamedicinadelaboratorio.
APROBACIÓNÉTICA
Noprocede.
CONSENTIMIENTOINFORMADO
Seobtuvoelconsen�mientoinformadodetodos lospar�cipantesdeesteestudio.
CONTRIBUCIÓNDELOSAUTORES
Zhili Niu y Xiandong Kuang contribuyeron por igualaestetrabajo.
Todos los autores han aceptado la responsabilidad de todo el contenido de este manuscrito yhanaprobadosupresentación.
Uso de modelos de lenguaje, IA y herramientas deaprendizajeautomá�co:Paramejorarlaredacción.
CONFLICTODEINTERESES
Losautoresdeclarannotenerningúnconflictode intereses.
FINANCIACIÓNDELPROYECTO
Ningunodeclarado.
DISPONIBILIDADDELOSDATOS
Noprocede.
REFERENCES
1. Kaul V Enslin S, Gross SA History of ar�ficial intelligence in medicine. Gastrointest Endosc 2020;92:807–12.
2. Ferraro S, Panteghini M. The role of laboratory in ensuring appropriate test requests. Clin Biochem2017;50:555–61.
3. Lavoie-Gagne O, Woo JJ, Williams RJ3rd, Nwachukwu BU, Kunze KN, Ramkumar PN Ar�ficial intelligence as a tool to mi�gate administra�ve burden, op�mize billing, reduce insurance and creden�aling-related expenses, and improve quality assurance within healthcare systems. Arthroscopy 2025;41:3270–5.
4. JohriS,JeongJ,TranBA,SchlessingerDI,WongvibulsinS, BarnesLA etal.Anevalua�onframeworkforclinicaluseof largelanguagemodelsinpa�entinterac�ontasks.NatMed2025;31:77–86.
5. Giardina TD,BaldwinJ,Nystrom DT,Si�g DF,SinghH.Pa�entpercep�onsofreceivingtest resultsviaonlineportals:amixed-methodsstudy JAmMedInformAssoc2018;25:440–6.
6. Bar-Lev S, Beimel D Numbers, graphs and words - do we really understand the lab test resultsaccessibleviathepa�entportals?IsrJHealthPolRes2020;9:58.
7. Chu SKW, Huang H, Wong WNM, Ginneken WFV, Hung MY Quality and clarity of health informa�ononQ&Asites.LibrInfSciRes2018;40.
8. He Z, Bhasuran B, Jin Q, Tian S, Hanna K, Shavor C, et al. Quality of answers of genera�ve largelanguagemodelsversuspeerusersforinterpre�nglaboratorytestresultsforlaypa�ents:evalua�on study JMedInternetRes2024;26:e56655.
9. WillChatGPTtransformhealthcare?.NatMed2023;29:505–6.
10. Meskó B. Prompt engineering as an important emerging skill for medical professionals: tutorial.JMedInternetRes2023;25:e50638.
11. Eysenbach G. The role of ChatGPT, genera�ve language models, and ar�ficial intelligence inmedicaleduca�on:aconversa�onwithChatGPTandacallforpapers.JMIRMedEduc2023;9:e46885.
12. Hris�dis V Ruggiano N, Brown EL Ganta SRR Stewart S. ChatGPT vs google for queries related to demen�a and other cogni�ve decline: comparison of results J Med Internet Res 2023;25:e48966.
13. Sallam M. ChatGPT u�lity in healthcare educa�on, research, and prac�ce: systema�c review on the promising perspec�ves and valid concerns. Healthcare 2023;11. h�ps://doi.org/10.3390/ healthcare11060887.
14. Rajpurkar P Chen E Banerjee O Topol EJ AI in health and medicine Nat Med 2022;28:31–8.
15. Shahsavar Y, Choudhury A. User inten�ons to use ChatGPT for self- diagnosis and healthrelatedpurposes:cross-sec�onalsurveystudy JMIRHumFactors2023;10:e47564.
16. Kopanitsa G. Study of pa�ents' a�tude to automa�c interpreta�on of laboratory test resultsanditsinfluenceonfollow-uprate.BMCMedInformDecisMak2022;22:79.
17. SarwarS,DentA,FaustK,RicherM,DjuricU VanOmmerenR,etal.Physicianperspec�ves onintegra�onofar�ficialintelligenceintodiagnos�cpathology NPJDigitMed2019;2:28.
18. ArdonO,SchmidtRL Clinicallaboratoryemployees'a�tudestowardar�ficialintelligence. LabMed2020;51:649–54.
19. Oh S, Kim JH, Choi SW, Lee HJ, Hong J, Kwon SH, et al. Physician confidence in ar�ficial intelligence:anonlinemobilesurvey JMedInternetRes2019;21:e12422.
20. Tarmissi K, Alsamri J Maashi M, Asiri MM Yahya AE Alkharashi A, et al. Mul�modal representa�onsoftransferlearningwithsnakeop�miza�onalgorithmonbonemarrowcellclassifica�on usingbiomedicalhistopathologicalimages.SciRep2025;15:14309.
21. Matek C,Krappe S,Münzenmayer C,HaferlachT Marr C. Highlyaccurate differen�a�on of bone marrow cell morphologies using deep neural networks on a large image data set. Blood 2021;138: 1917–27.
22. Durant TJS, Olson EM, Schulz WL, Torres R. Very deep convolu�onal neural networks for morphologicclassifica�onoferythrocytes.ClinChem2017;63:1847–55.
23. CadamuroJ,CarobeneA,CabitzaF,DebeljakZ,DeBruyneS, van Doorn W et al. A comprehensive survey of ar�ficial intelligence adop�on in European laboratory medicine:currentu�liza�onandprospects.ClinChemLabMed2025;63:692–703.
24. Yu S, Jeon BR, Liu C, Kim D, Park HI, Park HD, et al. Laboratory prepara�on for digital medicine in healthcare 4.0: an inves�ga�on into the awareness and applica�ons of big data and ar�ficial intelligence.AnnLabMed2024;44:562–71.
25. Khullar D, Casalino LP, Qian Y, Lu Y, Chang E, Aneja S, et al. Public vs physician views of liabilityforar�ficialintelligenceinhealthcare.JAmMedInformAssoc2021;28:1574–7.
26. Abràmoff MD, Tobey D, Char DS Lessons learned about autonomous AI: finding a safe, efficacious,andethicalpaththroughthedevelopmentprocess.AmJOphthalmol2020;214:134–42.
27. Bazoukis G, Hall J Loscalzo J Antman EM Fuster V Armoundas AA et al. The inclusion of augmented intelligence in medicine: a framework for successful implementa�on. Cell Rep Med 2022;3:100485.
28. Wen Y, Choo VY, Eil JH, Thun S, Pinto Dos Santos D, Kast J, et al. Exchange of quan�ta�ve computed tomography assessed body composi�on data using fast healthcare interoperability resources as a necessary step toward interoperable integra�on of opportunis�c screening into clinical prac�ce: methodologicaldevelopmentstudy JMedInternetRes2025;27:e68750.
29. Dolin RH, Heale BSE, Alterovitz G, Gupta R, Aronson J, Boxwala A, et al. Introducing HL7 FHIR genomics opera�ons: a developer- friendly approach to genomics-EHR integra�on. J Am Med InformAssoc2023;30:485–93.
30. Vorisek CN, Lehne M, Klopfenstein SAI, Mayer PJ, Bartschke A, Haese T, et al. Fast healthcare interoperability resources (FHIR) for interoperability in health research: systema�c review JMIRMedInform2022;10:e35724.
31. Tran DM,ThanhDungN,MinhDucC,NgocHonH,MinhKhoiL,PhucHauN,etal.Statusof digitalhealthtechnologyadop�onin5Vietnamesehospitals:cross-sec�onalassessment. JMIR FormRes 2025;9:e53483.
32. Burnside ES, Grist TM, Lasarev MR, Garre� JW, Morris EA Ar�ficial intelligence in radiology:aleadershipsurvey JAmCollRadiol2025;22:577–85.
33. TakagiS,WatariT ErabiA,SakaguchiK.PerformanceofGPT-3.5andGPT-4ontheJapanese medicallicensingexamina�on:comparisonstudy JMIRMedEduc2023;9:e48002.
34. Wang H, Wu W, Dou Z, He L, Yang L. Performance and explora�on of ChatGPT in medical examina�on records and educa�on in Chinese: pave the way for medical AI Int J Med Inf
2023;177:105173.
35. Lim ZW, Pushpanathan K, Yew SME, Lai Y, Sun CH, Lam JSH, et al. Benchmarking large language models' performances for myopia care: a compara�ve analysis of ChatGPT-3.5, ChatGPT-4.0, andgooglebard.EBioMedicine2023;95:104770.
36. Munoz-Zuluaga C, Zhao Z, Wang F, Greenbla� MB, Yang HS Assessing the accuracy and clinicalu�lityofChatGPTinlaboratorymedicine.ClinChem2023;69:939–40.
37. Girton MR, Greene DN, Messerlian G, Keren DF, Yu M. ChatGPT vs medical professional: analyzingresponsestolaboratorymedicineques�onsonsocialmedia.ClinChem2024;70:1122–39.
38. Meyer A, Soleman A, Riese J Streichert T Comparison of ChatGPT Gemini, and Le Chat with physician interpreta�ons of medical laboratory ques�ons from an online health forum. Clin Chem LabMed2024;62:2425–34.
39. Ka�anAN HussainMK NaserFH ResponseaccuracyofChatGPT3.5copilotandgeminiin interpre�ngbiochemicallaboratorydataapilotstudy SciRep2024;14:8233.
40. Sallam M, Al-Salahat K, Al-Ajlouni E ChatGPT performance in diagnos�c clinical microbiologylaboratory-orientedcasescenarios.Cureus2023;15:e50629.
41. Carey RB, Bha�acharyya S, Kehl SC, Matukas LM, Pentella MA, Salfinger M, et al. Prac�cal guidance for clinical microbiology laboratories: implemen�ng a quality management system in the medicalmicrobiologylaboratory ClinMicrobiolRev2018;31.h�ps://doi.org/10.1128/cmr.00062-17.
42. Genzen JR, Tormey CA Pathology consulta�on on repor�ng of cri�cal values. Am J Clin Pathol2011;135:505–13.
43. Li Y Huang CK Hu Y Zhou XD, He C, Zhong JW et al. Exploring the performance of large language models on hepa��s B infec�on-related ques�ons: a compara�ve study. World J Gastroenterol 2025;31:101092.
44. Cadamuro J Cabitza F Debeljak Z, De Bruyne S, Frans G, Perez SM et al. Poten�als and pi�allsofChatGPT andnatural-languagear�ficialintelligencemodelsfortheunderstandingoflaboratory medicine test results. An assessment by the european Federa�on of clinical chemistry and laboratory medicine(EFLM)workinggrouponar�ficialintelligence(WG-AI).ClinChemLabMed2023;61:1158–66.
45. Al-Ashwal FY, Zawiah M, Gharaibeh L, Abu-Farha R, Bitar AN Evalua�ng the sensi�vity, specificity, and accuracy of ChatGPT-3.5, ChatGPT-4, bing AI, and bard against conven�onal drug-drug interac�onsclinicaltools.DrugHealthcPa�entSaf2023;15:137–47.
46. Baglivo F, De Angelis L, Casigliani V, Arzilli G, Privitera GP, Rizzo C, et al. Exploring the possibleuseofAIchatbotsinpublichealtheduca�on:feasibilitystudy JMIRMedEduc2023;9:e51421.
47. Seth I, Lim B Xie Y Cevik J Rozen WM Ross RJ, et al. Comparing the efficacy of large language models ChatGPT, BARD, and bing AI in providing informa�on on rhinoplasty: an observa�onal study AesthetSurgJOpenForum2023;5:ojad084.
48. AbusogluS,SerdarM,UnluA,AbusogluG.Comparisonofthreechatbotsasanassistantfor problem-solvinginclinicallaboratory ClinChemLabMed2024;62:1362–6.
49. Lingjiao Chen MZ, James Z. How is chatgpt's behavior changing over �me_.pdf Harv Data SciRev2023;2024:2.
50. Giray L. Prompt engineering with ChatGPT: a guide for academic writers. Ann Biomed Eng 2023;51:2629–33.
51. Khlaif ZN MousaA,Ha�ab MK ItmaziJ Hassan AA SanmugamM,etal.Thepoten�aland concerns of using AI in scien�fic research: ChatGPT performance evalua�on. JMIR Med Educ 2023;9: e47049.
52. Kochanek K, Skarzynski H, Jedrzejczak WW Accuracy and repeatability of ChatGPT based onasetofmul�ple-choiceques�onsonobjec�vetestsofhearing.Cureus2024;16:e59857.
53. Wang YM, Shen HW, Chen TJ Performance of ChatGPT on the pharmacist licensing examina�oninTaiwan.JChinMedAssoc2023;86:653–8.
54. Alfertshofer M, Hoch CC, Funk PF, Hollmann K, Wollenberg B, Knoedler S, et al. Sailing the sevenseas:amul�na�onalcomparisonofchatgpt'sperformanceonmedicallicensingexamina�ons.Ann BiomedEng2024;52:1542–5.
55. Zikmund-Fisher BJ,Scherer AM,Wi�eman HO,Solomon JB,Exe NL,FagerlinA,etal.Effect of harm anchors in visual displays of test results on pa�ent percep�ons of urgency about near-normal values:experimentalstudy JMedInternetRes2018;20:e98.
56. van Dis EAM, Bollen J, Zuidema W, van Rooij R, Bock�ng CL ChatGPT: five priori�es for research.Nature2023;614:224–6.
57. SandersonK.GPT-4ishere:whatscien�ststhink.Nature2023;615:773.
58. MurdochB.Privacyandar�ficialintelligence:challengesforprotec�nghealthinforma�on inanewera.BMCMedEthics2021;22:122.
59. Mijwil MM Aljanabi M, Ali AH ChatGPT: exploring the role of cybersecurity in the protec�onofmedicalinforma�on.MesopotamianJCyberSecurity2023;2023.h�ps://doi.org/10.58496/ mjcs/2023/004.
60. Chen Z. Ethics and discrimina�on in ar�ficial intelligence-enabled recruitment prac�ces. PalgraveCommun2023;9:12.
61. Wang C, Liu S, Yang H, Guo J, Wu Y, Liu J, et al. Ethical considera�ons of using ChatGPT in healthcare.JMedInternetRes2023;25:e48009.
62. Liang P, Wu C, Morency LP, Salakhutdinov R. Towards understanding and mi�ga�ng social biasesinlanguagemodels.PMLR2021;139:2640–3498.
63. Gianfrancesco MA, Tamang S, Yazdany J, Schmajuk G. Poten�al biases in machine learning algorithmsusingelectronichealthrecorddata.JAMAInternMed2018;178:1544–7.
64. Tianyu Gao HY, Jiatong Y, Danqi C. Enabling large language models to generate text with cita�ons.pdf ArXiv2023.h�ps://doi.org/10.48550/arXiv.2305.14627.
65. GasserU AnEUlandmarkforAIgovernance.Science2023;380:1203.
66. März M, Himmelbauer M, Boldt K, Oksche A. Legal aspects of genera�ve ar�ficial intelligenceandlargelanguagemodelsinexamina�onsandtheses.GMSJMedEduc2024;41:Doc47. 67. AlvaradoA.LessonsfromtheEUAIact.Pa�erns(NY)2025;6:101183.
68. Weissman G, Mankowitz T, Kanter G. Large language model non- compliance with FDA guidance for clinical decision support devices Res Sq 2024 h�ps://doi org/10 21203/rs 3 rs4868925/v1.
69. Charnock D, Shepperd S, Needham G, Gann R. DISCERN: an instrument for judging the quality of wri�en consumer health informa�on on treatment choices. J Epidemiol Community Health 1999;53:105–11.
70. Baur C, Prue C. The CDC clear communica�on index is a new evidence- based tool to prepareandreviewhealthinforma�on.HealthPromotPract2014;15:629–37.
71. DeWalt DA, Broucksou KA, Hawk V, Brach C, Hink A, Rudd R, et al. Developing and tes�ng thehealthliteracyuniversalprecau�onstoolkit.NursOutlook2011;59:85–94.
72. Sallam M, Barakat M, Sallam M. A preliminary checklist (METRICS) to standardize the designandrepor�ngofstudiesongenera�vear�ficialintelligence-basedmodelsinhealthcareeduca�on andprac�ce:developmentstudyinvolvingaliteraturereview InteractJMedRes2024;13:e54704.
73. SallamM, Barakat M,SallamM.Pilottes�ng of a tool to standardize the assessment of the qualityofhealthinforma�ongeneratedbyar�ficialintelligence-basedmodels.Cureus2023;15:e49373.