L’innovation au cœur de l’évolution des pratiques



Une offre pour étudiants en imagerie médicale, en radio‑oncologie et en électrophysiologie médicale.
bnc.ca/specialiste-santé

L’innovation au cœur de l’évolution des pratiques



Une offre pour étudiants en imagerie médicale, en radio‑oncologie et en électrophysiologie médicale.
bnc.ca/specialiste-santé

L’innovation au cœur de l’évolution des pratiques
Mot du président 4
Les technologues se doivent d’influencer, de comprendre et de mettre l’évolution technologique au service des patients et du réseau.
Pratique professionnelle 6
Harmonisation de l’inspection
Déontologie 9
Top 5 des décisions disciplinaires chez les technologues
DOSSIER SPÉCIAL 14
L’intelligence artificielle en imagerie médicale : où en sommes-nous au Québec ?
Articles
Injection de PRP
guidée par échographie musculosquelettique
Une entrevue avec Julie Robillard et Dr Étienne Cardinal
La scintigraphie
16
22 de Meckel revisitée : mise à jour des protocoles de préparation et d’imagerie, pièges diagnostiques
Innovation technologique
32 et traitement des métastases cérébrales
Medscint : quand
38 l’innovation québécoise révolutionne la dosimétrie en radio-oncologie
Tout savoir 45 sur l’angio-mammographie
Comprendre cette technique et son application concrète en milieu clinique
L’IA en échocardiographie 51 Quand les robots prennent la sonde
L’ÉchoX, la revue de l’Ordre des technologues en imagerie médicale, en radio-oncologie et en électrophysiologie médicale, est publié depuis 1964. Elle est disponible en format numérique sur le site de l’Ordre. • COLLABORATEURS AU CONTENU Karine Audet, t.r.o.; Mathieu Bergeron, t.r.o.; Raphaëlle Breault, Étudiante au Barreau du Québec; Audrey Charbonneau, Conseillère aux communications; Vincent Dubé, t.i.m. (MN); Geneviève Dupuis, t.i.m. (RD); Sandie Guénette-Dubois, t.i.m. (RD); Brigitte Joyal, t.i.m. (RD); Étienne Cardinal, MD-radiologiste; Julie Robillard, t.i.m. (RD); Samia Guerboukha, t.i.m. (RD); Julie Lanctôt Bédard, MD, Kelly Chouinard, t.i.m. (RD) • RÉVISION ET CORRECTION Dominique Gaucher • PUBLICITÉ OTIMROEPMQ • DESIGN GRAPHIQUE Bunka • PLATEFORME DE DIFFUSION ISSUU • ABONNEMENTS communications@otimroepmq.ca • POLITIQUE D’ABONNEMENT Les membres reçoivent l’ÉchoX deux fois par année par infolettre. • POLITIQUE ÉDITORIALE Sauf indications contraires, les textes et les photos publiés n’engagent que les auteurs. Toute reproduction doit mentionner la source, après autorisation préalable de l’Ordre.
6455, rue Jean-Talon Est, bureau 401, Saint-Léonard, Montréal (Québec) H1S 3E8 514 351-0052 ou 1 800 361-8759 • otimrœpmq.ca
DÉPÔT LÉGAL Bibliothèque nationale du Québec et Bibliothèque nationale du Canada ISSN 0820-6295

Au-delà de suivre l’évolution technologique, les technologues se doivent de l’influencer, de la comprendre et de la mettre au service des patients et du réseau.
L’importance de l’innovation dans nos professions ne fait plus de doute. Dans des domaines où les besoins sont grandissants et les attentes de plus en plus élevées, il nous incombe de développer les outils qui nous permettront d’offrir les solutions aux enjeux contemporains du système de santé québécois. Cet engagement passe par un leadership fort de l’Ordre, mais surtout des technologues en imagerie médicale, en radio-oncologie et en électrophysiologie médicale. Un leadership que l’on voit s’incarner à de multiples occasions, comme c’est le cas dans cette édition de l’ ÉchoX qui met en lumière des projets inspirants portés par des technologues engagés.
S’approprier l’innovation
C’est dans cet esprit que l’Ordre a apporté des modifications à son règlement sur la formation continue. Nous souhaitons encourager l’implication des technologues dans le développement de leur profession. Cette démarche ne se résume pas à suivre l’évolution technologique : il consiste à l’influencer, à la comprendre en profondeur, et à la mettre au service des patients et du réseau. En insistant sur l’importance des activités de formation continue qui favorisent l’innovation, l’analyse critique, la collaboration interdisciplinaire ou la diffusion des connaissances, nous affirmons que chaque technologue peut être un acteur de changement.
L’innovation n’est pas un geste isolé ni un privilège réservé à quelques personnes. Elle peut prendre mille formes. Elle peut émerger d’un projet de recherche clinique mené dans un centre hospitalier universitaire, mais aussi d’une optimisation ingénieuse faite sur le terrain qui permet d’améliorer les flux de patients, de réduire les temps d’attente ou d’augmenter la qualité des images. Elle peut se traduire par l’adoption d’une nouvelle technologie, mais également par une manière renouvelée d’aborder un enjeu éthique, de communiquer avec un patient anxieux ou de collaborer avec l’équipe médicale.
C’est pour cela que l’Ordre souhaite valoriser l’ensemble de ces initiatives, qu’elles soient grandes ou modestes. Chacune contribue, à sa façon, à faire progresser la profession et à solidifier notre rôle incontournable dans le continuum de soins.
En reconnaissant plus explicitement ces contributions dans le cadre de la formation continue, nous voulons créer un environnement où l’innovation est encouragée, soutenue et célébrée.
La transformation du système de santé québécois exige une capacité d’adaptation exceptionnelle. Les pressions sont nombreuses : augmentation des besoins en soins diagnostiques et thérapeutiques, complexification des cas, exigences accrues en matière de radioprotection, avancées rapides de l’intelligence artificielle, pénurie de main-d’œuvre, préoccupations
concernant la qualité et la sécurité des actes. À cela s’ajoutent les attentes élevées des patientes et patients, qui souhaitent des soins à la fois accessibles et humains.
Face à ces réalités, nos professions ne peuvent pas demeurer statiques. Heureusement, les technologues du Québec démontrent quotidiennement une créativité, un engagement et une rigueur remarquables. Plusieurs participent à des groupes de travail provinciaux, élaborent des protocoles, contribuent à des programmes de formation, ou collaborent à des projets d’intégration de nouvelles technologies comme l’IA, la dosimétrie avancée ou les outils de monitorage cardiaque à distance.
Innovation, sécurité et leadership professionnel
Le rôle de l’Ordre, dans ce contexte, est double : d’une part, soutenir, encadrer et outiller les technologues pour qu’ils puissent contribuer à ces changements ; d’autre part, assurer que ces innovations se déploient dans un cadre éthique, sécuritaire et conforme à la mission première de protection du public.
Ce nouvel équilibre entre innovation, sécurité et leadership professionnel est au cœur de notre vision. Nous voulons que les technologues se sentent autorisés à proposer des solutions, à faire avancer les pratiques et à participer activement à la réflexion collective. Mais nous voulons aussi qu’ils disposent des repères nécessaires pour agir avec confiance et compétence dans un monde en transformation.
C’est également dans cet esprit que nous avons souhaité mettre en valeur, dans cette édition de l’ÉchoX, des projets menés par des technologues qui repoussent les limites de ce qui est possible. Leur créativité et leur détermination sont une source d’inspiration pour toute la communauté professionnelle. Ces initiatives ne sont pas seulement des réussites individuelles : elles témoignent de ce que notre profession peut accomplir lorsqu’elle est soutenue, reconnue et mobilisée.
À travers ces exemples, nous voyons peu à peu se dessiner le futur de la profession : un futur où les technologues jouent un rôle accru dans le développement de s
Un futur où la formation continue n’est pas perçue comme une obligation administrative, mais comme une occasion de croissance, de collaboration et de contribution.
pratiques cliniques, dans l’intégration des technologies émergentes et dans la recherche appliquée. Un futur où l’on reconnaît pleinement l’expertise unique qu’ils apportent au système de santé. Un futur où la formation continue n’est pas perçue comme une obligation administrative, mais comme une occasion de croissance, de collaboration et de contribution. Finalement, l’innovation n’est pas une fin en soi. Elle est un moyen : un moyen d’améliorer la qualité des soins, de soutenir la sécurité des patientes et patients, d’optimiser les pratiques, et de renforcer la place de nos professions dans un système de santé qui a besoin de nous plus que jamais. Et ce moyen, nous l’avons entre nos mains. Ensemble, continuons de façonner un avenir où notre expertise, notre créativité et notre leadership feront la différence.

Vincent Dubé, t.i.m. (MN) Président de l’OTIMRŒPMQ



PRÉSENTATION DU NOUVEAU PROCESSUS
D’INSPECTION PROFESSIONNELLE

Cinq années après la mise en œuvre des programmes d’inspection, le moment est venu d’en dresser le bilan. Le service d’inspection professionnelle (SIP) a analysé les succès obtenus ainsi que les enjeux rencontrés. À l’issue de cette réflexion approfondie, l’Ordre des technologues en imagerie médicale, en radio-oncologie et en électrophysiologie médicale du Québec (l’Ordre) a décidé d’harmoniser et de réviser ses programmes.
Il convient de rappeler que la mission fondamentale de l’Ordre demeure la protection du public. Pour atteindre cet objectif, l’Ordre s’assure que ses membres exercent leurs activités professionnelles conformément aux lois, aux règlements et aux normes de pratique en vigueur. Cette vérification s’effectue notamment par le moyen d’inspections professionnelles menées dans les divers domaines de pratique.
Déroulement du processus d’inspection
Afin de simplifier nos processus, de maximiser l’atteinte des objectifs et de soutenir l’amélioration continue de la pratique professionnelle
de nos membres, l’ensemble des programmes d’inspection, soit le programme de surveillance générale, le programme de surveillance de la pratique autonome et le programme de surveillance de la mammographie, seront désormais harmonisés et suivront les mêmes phases.
L’évaluation professionnelle
À partir des constats issus des programmes précédents, le SIP a procédé à une révision des questionnaires, initialement conçus de manière plus générale. Afin de mieux cerner les besoins en formation et d’évaluer l’état des connaissances techniques de ses membres, l’Ordre introduira des questionnaires plus
Il importe de rappeler que ce processus ne se résume pas à une simple démarche de surveillance : il s’agit avant tout d’un accompagnement structuré, centré sur le développement et le rehaussement des compétences de chacun.
spécialisés et orientés vers les aspects techniques. Conscient que certaines notions fondamentales peuvent s’atténuer avec le temps et l’expérience, l’Ordre souhaite mettre l’accent sur le maintien et le renforcement des bonnes pratiques professionnelles. À la fin de cette phase, chaque membre recevra une note l’orientant vers les aspects à améliorer dans sa pratique.
La visioconférence
Une des phases des programmes d’inspections professionnelles prendra la forme d’une visioconférence entre le membre et l’inspecteur. Elle constitue un moment privilégié pour clarifier les réponses aux questionnaires, échanger sur les méthodes de travail, les outils et les mécanismes propres au centre, et offrir un accompagnement personnalisé. Dans ce cadre, le membre devra avoir préalablement transmis des images d’examens qu’il aura réalisés ainsi que les documents utilisés dans son établissement, tels que les formulaires. L’inspecteur pourra ainsi analyser ces éléments et orienter la visioconférence en fonction des particularités du contexte de travail du technologue.
Cette phase consiste à évaluer les compétences professionnelles du membre inspecté. À cette fin, un inspecteur nommé se déplace dans l’établissement où exerce le membre. Cette présence sur le terrain favorise une compréhension exhaustive des méthodes utilisées, des équipements disponibles et des mécanismes propres à l’établissement. Cette rencontre vise non seulement à assurer le respect des lois, règlements et normes de pratique, mais également à offrir un accompagnement constructif et positif. Elle permet de mettre en lumière les bonnes pratiques déjà en place et de déterminer les aspects pouvant être améliorés, toujours dans l’optique de protéger le public et de soutenir le développement professionnel des membres.
L’inspection : un cycle structuré et flexible
Le SIP a pour mandat d’inspecter l’ensemble des membres sur un cycle de cinq ans, ce qui représente environ 20 % des membres par année. Les membres sont choisis de la manière suivante : les deux tiers sont
sélectionnés au hasard, tandis que le tiers restant l’est en fonction de critères de risque établis par le conseil d’administration de l’Ordre. Dans des situations particulières (p. ex. signalement, plainte), il est possible qu’un membre soit ajouté à l’un ou l’autre des programmes d’inspection en cours.
De manière générale, les différentes phases de l’inspection suivent une progression linéaire. Toutefois, selon les besoins déterminés ou en fonction de la période de l’année, il est possible que certaines phases soient réalisées de façon partielle ou non séquentielle. Cette flexibilité permet d’intégrer un membre en cours de programme et d’adapter le processus aux objectifs poursuivis.
À la fin de chaque phase, le technologue reçoit une communication l’informant de la fin de son inspection ou de la poursuite de son inspection à une autre phase.
Toutes les communications (p. ex. avis d’inspection, dépôt de documents dans le dossier d’inspection) en lien avec l’inspection professionnelle se font par courriel. Il est donc primordial que les coordonnées de chaque membre soit mises à jour dans le Portail de l’Ordre.
Finalement, à l’issue de la visioconférence ou de la visite, un rapport d’inspection comprenant des recommandations est envoyé au membre
inspecté. Ce dernier devra ensuite s’engager à mettre en place des éléments d’amélioration dans sa pratique professionnelle.
Engagé dans la qualité de votre pratique
L’harmonisation des programmes d’inspection professionnelle représente une étape importante dans l’évolution de nos pratiques au sein de l’Ordre. Il importe de rappeler que ce processus ne se résume pas à une simple démarche de surveillance : il s’agit avant tout d’un accompagnement structuré, centré sur le développement et le rehaussement des compétences de chacun. Si la protection du public demeure au cœur de notre mission, l’inspection professionnelle se veut également un outil de soutien positif et constructif, pensé pour valoriser les bonnes pratiques déjà en place et guider les technologues vers une excellence professionnelle continue.
Nous vous encourageons à aborder ce processus avec ouverture, en le considérant comme une occasion d’échange et de croissance professionnelle. Le service d’inspection professionnelle demeure disponible pour répondre à toutes vos questions et vous accompagner tout au long des différentes phases. N’hésitez pas à communiquer avec nous : votre participation active et vos échanges sont essentiels à la réussite de cette démarche collective.

Par leur serment professionnel, les technologues en imagerie médicale, en radio-oncologie ou en électrophysiologie médicale (ci-après « le technologue ») s’engagent à exercer leur profession avec conscience, loyauté, intégrité et dignité, à respecter le secret professionnel et à se conformer au Code des professions1 , à la Loi sur les technologues en imagerie médicale, en radio-oncologie et en électrophysiologie médicale2 (ci-après « Loi sur les technologues »), ainsi qu’aux règlements de l’Ordre, dont le Code de déontologie3 .
Au cours des dix dernières années, le conseil de discipline de l’Ordre a été saisi de plusieurs plaintes disciplinaires, dont certaines de même nature. Le présent texte propose une synthèse des décisions disciplinaires les plus marquantes, regroupées selon les infractions les plus fréquemment sanctionnées.
1. La consultation de dossiers sans autorisation
La curiosité professionnelle, lorsqu’elle n’est pas encadrée par une justification, peut entraîner des conséquences sérieuses pour le professionnel. La jurisprudence récente illustre cette réalité : près d’une dizaine de décisions ont été rendues par le Conseil de discipline de l’Ordre à l’encontre de technologues ayant consulté des dossiers médicaux sans autorisation.
Un tel comportement contrevient à plusieurs dispositions législatives visant la protection de la vie privée et des renseignements personnels 4. En effet, la consultation d’un dossier-patient, lorsqu’elle n’est ni justifiée ni autorisée, constitue une atteinte au droit au respect de la vie privée 5
À titre indicatif, dans l’affaire Jourdain-Simard 6 , une technologue en électrophysiologie médicale a consulté, sans autorisation et justification professionnelle valable, le dossier de deux patients, pour approfondir ses connaissances, et ce, considérant qu’il s’agissait, selon elle, de cas inédits. Considérant sa conduite, le Conseil de discipline lui a imposé une période de radiation d’une semaine. Pour déterminer la sanction, plusieurs facteurs atténuants ont été considérés, dont le peu d’expérience de l’intimée, la suspension sans solde, les formations effectuées et le plaidoyer de culpabilité.
Il importe de rappeler que le simple fait d’être employé au sein d’un établissement ne confère aucun droit de consultation des dossiers contenant des renseignements personnels. Toute consultation doit être justifiée, autorisée et conforme aux exigences légales applicables. Les sanctions imposées pour ce type d’infraction varient selon la gravité des faits et le contexte, allant de la réprimande7 à l’amende 8, voire à la radiation temporaire9
Les autres ordres professionnels œuvrant dans le domaine de la santé et des


Directrice des affaires juridiques et secrétaire adjointe
services sociaux adoptent une approche similaire. À titre d’exemple, une infirmière a consulté, entre 2014 et 2020, les dossiers médicaux de proches de personnalités publiques, de collègues de travail, de leurs enfants ainsi que de membres de sa famille. Considérant la gravité du geste, le conseil de discipline lui a imposé une radiation de deux mois10
De même, en 2012, un travailleur social a consulté 2 645 dossiers sur une période de 79 jours, principalement pour « occuper son temps », disait-il. Ce comportement lui a valu une radiation temporaire d’un mois et une amende de 1 500 $11
2. Manque de diligence ou erreur dans la réalisation d’un examen
Il est admis que l’erreur est inhérente à toute activité humaine. Toutefois, lorsqu’elle découle d’un manque de rigueur ou de diligence, ou même de négligence, elle cesse d’être une simple maladresse pour s’inscrire dans le champ de la faute disciplinaire.
Dans l’affaire Therrien12, un technologue a été reconnu coupable d’un manquement à son devoir de diligence à la suite de plusieurs erreurs commises lors de la réalisation d’examens radiologiques. Bien que l’erreur soit possible, les professionnels sont tenus à un haut standard de qualité13. En l’espèce, le technologue avait notamment irradié le mauvais membre, versé les images dans un dossier-patient erroné et procédé à des radiographies de régions non visées par l’ordonnance médicale. Ces manquements ont été jugés suffisamment graves pour justifier une radiation d’un mois.
Dans une affaire comparable14 mettant en cause la négligence d’une technologue, le Conseil de discipline a imposé plusieurs périodes de radiation purgées concurremment. La professionnelle avait notamment omis d’assurer le remplacement quotidien des solutés et d’effectuer les prélèvements requis, et négligé de s’assurer que l’examen avait été réalisé de manière complète. Ces omissions, bien qu’à première vue elles puissent paraître techniques, ont été considérées comme compromettant directement la qualité et la sécurité des soins offerts.
Également, le technologue sera aussi sanctionné pour omettre de corriger ses erreurs dans le dossier de son client 15 ou de se conformer à l’ordonnance médicale émise16. Quant à la disponibilité, des professionnels ont été sanctionnés pour avoir, par exemple, causé des retards ou des délais inutiles pour les patients17
Un tel manquement disciplinaire peut également faire l’objet d’un recours parallèle en responsabilité civile si une faute causale des dommages est établie. Le technologue doit donc s’assurer de respecter les normes de pratique et agir selon les règles de l’art.
3. Usage d’un médicament ou réalisation d’un examen à des fins personnelles
Les articles 7 et 11.1 de la Loi sur les technologues définissent de manière précise les activités réservées aux technologues. Ces activités doivent être exercées exclusivement « à des fins diagnostiques ou thérapeutiques ». Toute activité exercée en dehors de ces finalités soulève inévitablement des enjeux liés à la compétence, à l’aptitude professionnelle et, plus largement, à l’intégrité de la profession.
Ainsi, dans une décision récente, le Conseil de discipline a imposé une radiation de neuf mois à une technologue qui avait administré de l’ANCEF à une représentante médicale dans le but de « guérir » une infection à l’œil. Le Conseil a alors souligné que ce geste excédait clairement le champ des activités autorisées et qu’il contrevenait aux valeurs fondamentales de la profession :
Par ailleurs, l’administration de l’ANCEF, […] sans respecter les limites de ses aptitudes […], est un comportement dangereux et téméraire.
[…]
Par son expérience, l’intimée doit agir avec sollicitude et empathie ainsi que veiller au bien-être et à la sécurité d’un patient. Or, son comportement va à l’encontre de ces valeurs18
Dans des circonstances comparables, des infirmières et infirmiers ont fait l’objet de sanctions sévères pour s’être approprié des médicaments à des fins personnelles19. Le Conseil de discipline a alors imposé des périodes de radiation allant jusqu’à neuf mois et, parfois même, assorties d’une limitation temporaire du droit d’exercice.
Le conseil de discipline a également jugé contraire à l’intégrité de la profession le fait de réaliser des examens à des fins personnelles, notamment sur des membres de la famille ou des proches. Le conseil a rappelé que le titre professionnel constitue un privilège et non un droit absolu. Selon le conseil, ces gestes sont qualifiés d’abus de pouvoir, et le professionnel « fait fi des règles d’admissibilité aux services et ressources publics, les utilise à mauvais escient et abuse de la confiance de son employeur et de ses
collègues de travail 20 ». Pour ces manquements, le technologue s’est vu imposer une radiation de deux semaines, la publication d’un avis de radiation à ses frais ainsi que le paiement des déboursés.
Qu’il s’agisse de radiographier l’avant-bras d’un petit-fils 21 , de réaliser une échographie pour permettre à une fille enceinte de connaître le sexe de son enfant 22 ou encore d’effectuer un examen d’imagerie sur une conjointe présentant des antécédents familiaux d’anévrisme23, le conseil de discipline a systématiquement conclu à un manquement déontologique. Pour l’ensemble de ces cas, les technologues visés se sont vu imposer, au minimum, une période de radiation d’un mois.
4. Violence verbale ou à caractère sexuel
Aucune forme de violence n’est tolérée dans l’exercice de la profession. Le Conseil de discipline applique ce principe avec rigueur, en imposant des sanctions sévères afin d’assurer la protection du public et de remplir l’objectif de dissuasion.
Conformément au deuxième alinéa de l’article 156 du Code des professions, tout geste à caractère sexuel commis pendant la relation professionnelle, y compris des propos abusifs à caractère sexuel, doivent minimalement faire l’objet d’une radiation de cinq ans ainsi que d’une amende d’au moins 2 500 $. Ces sanctions minimales traduisent clairement la volonté du législateur d’encadrer sévèrement les inconduites sexuelles commises par des professionnels.
À cet égard, en 2024, un technologue a été reconnu coupable24 d’avoir palpé des régions intimes d’une patiente lors d’un examen demandant des radiographies dorsales, lombaires et abdominales. Le tribunal a rappelé que, dans un tel contexte, le professionnel se trouve en position de force devant une cliente vulnérable et qu’il a clairement abusé de cette relation de confiance25. En conséquence, le technologue s’est vu imposer une radiation de cinq ans ainsi qu’une amende de 2 500 $.
En ce qui concerne la violence verbale, la Cour suprême du Canada a reconnu que la notion de violence ne doit pas être définie uniquement par le recours à la force physique, mais plutôt en fonction du préjudice causé. Une interprétation large doit donc être retenue, notamment dans le contexte disciplinaire, afin de préserver l’objectif de protection du public 26
Dans cette optique, plusieurs décisions rendues par le conseil de discipline de l’Ordre ont sanctionné
des technologues pour avoir tenu des propos agressifs, menaçants ou violents. Ces comportements contreviennent à l’obligation fondamentale d’agir avec honneur et dignité :
Les professionnels doivent tous adopter, à tout moment et dans tous les aspects de l’exercice de leur profession, un comportement digne, modéré et intègre. En effet, le public, incluant les usagers et les collègues de l’intimé, doit pouvoir s’attendre à faire affaire avec un professionnel qui ne risque pas de s’emporter ou perdre patience violemment. Le public recherche le respect, l’empathie et la compassion, surtout dans le domaine de la santé27
Ainsi, une technologue a été radiée pour une période de trois mois pour avoir crié des insultes, proféré des menaces et lancé un objet en direction d’une collègue28. Dans une autre affaire, une technologue a reçu une radiation de quatre mois pour avoir haussé le ton, crié à l’endroit de collègues et proféré des insultes, lesquelles ont été entendues par un usager29
Le Conseil de discipline applique ce principe avec rigueur, en imposant des sanctions sévères afin d’assurer la protection du public et de remplir l’objectif de dissuasion.
Dans une autre affaire, un infirmier a été sanctionné par une période de radiation de 18 mois pour avoir insulté à répétition plusieurs patients. Les commentaires reprochés traduisaient de la brusquerie, de l’impatience et une agressivité incompatible avec le devoir de protection des personnes vulnérables 30
L’ensemble de cette jurisprudence illustre clairement l’intention de sanctionner fermement ces comportements afin de préserver la confiance du public et de maintenir les standards élevés dans les professions de la santé.
5. Consommation de substances illicites
Conformément à son Code de déontologie, le technologue doit « s’abstenir d’exercer sa profession dans un état ou des conditions susceptibles de compromettre la qualité de ses services ou la dignité de la profession31 ».
Plusieurs décisions rendues par le Conseil de discipline de l’Ordre font état de technologues ayant consommé de l’alcool ou du cannabis sur les lieux de travail, y compris durant les pauses. Au cours des dix dernières années, les technologues reconnus coupables de tels manquements se sont tous vu imposer minimalement une période de radiation.
La jurisprudence faisait alors ressortir une tendance claire vers des périodes de radiation oscillant entre neuf et dix mois 32
Dans l’affaire Tardif 33, une infirmière a été retrouvée dans la salle de pause, incapable de se lever seule et dégageant une forte odeur d’alcool. Elle était alors dans l’impossibilité d’assumer les responsabilités qui lui incombaient à titre d’infirmière responsable. Compte tenu de la gravité des faits et du risque élevé de récidive, le Conseil de discipline a prononcé la radiation permanente de l’intimée.
Pour conclure, les technologues sont soumis à des standards professionnels élevés en raison des risques inhérents à l’exercice de leur profession. Leurs obligations professionnelles et déontologiques les suivent en tout temps, qu’ils soient dans le cadre de leur fonction ou dans leur quotidien.
Il importe également de rappeler que la responsabilité du technologue ne se limite pas au cadre disciplinaire. Les politiques internes des établissements de santé, l’exercice du droit de gérance de l’employeur ainsi que les règles de la responsabilité civile peuvent s’appliquer parallèlement. Ainsi, une même conduite fautive est susceptible d’engager la responsabilité sur plusieurs fronts.
RÉFÉRENCES
1 – RLRQ, c. C-26.
2 – LRQ, c. T-5.
3 – Code de déontologie des technologues en imagerie médicale, en radio-oncologie et en électrophysiologie médicale, RLRQ, c. T-5, r. 5.
4 – Notamment : Loi sur les renseignements de santé et de services sociaux, LRQ, c. R-22.1, Loi sur la gouvernance du système de santé et de services sociaux, LRQ, c. G.1-1.021, Loi sur la protection des renseignements personnels dans le secteur privé, LRQ, c. p-39.1.
5 – Charte des droits et libertés de la personne, LRQ, c. C-12, art. 5 et 9, Code civil du Québec, c. CCQ-1991, art. 3.
6 – Technologues en imagerie médicale, en radio-oncologie et en électrophysiologie médicale du Québec (Ordre des) c. Jourdain-Simard, 2025 QCCDTIMROEM 1.
7 – Technologues en imagerie médicale, en radio-oncologie et en électrophysiologie médicale (Ordre professionnel des) c. Noël, 2019 QCOTIMRO 113563.
8 – Technologues en imagerie médicale, en radio-oncologie et en électrophysiologie médicale (Ordre professionnel des) c. Pouliot, 2018 QC OTIMRO 100227 (amende de 2 500 $ pour le chef d’infraction lié à la consultation illicite); Technologues en imagerie médicale, en radio-oncologie et en électrophysiologie médicale (Ordre professionnel des) c. Dumontier, 2021 QCCDTIMROEM 3 (amende de 3 000 $).
9 – Technologues en imagerie médicale, en radio-oncologie et en électrophysiologie médicale (Ordre professionnel des) c. Ekongolo, 2020 QCCDTIMROEM 3 (radiation temporaire de deux semaines sur chacun des deux chefs d’accusation).
10 – Infirmières et infirmiers (Ordre professionnel des) c. Bouchard, 2023 QCCDINF 13.
11 – Travailleurs sociaux (Ordre professionnel des) c. Rochette, 2012 QC OTSTCFQ 99569.
12 – Technologues en imagerie médicale, en radio-oncologie et en électrophysiologie médicale (Ordre professionnel des) c. Therrien, 2022 QCCDTIMROEM 1.
13 – Tremblay c. Dionne, 2006 QCCA 1441.
14 – Technologues en imagerie médicale, en radio-oncologie et en électrophysiologie médicale (Ordre professionnel des) c. Altidor, 2021 QCCDTIMROEM 4.
15 – Technologues en imagerie médicale, en radio-oncologie et en électrophysiologie médicale (Ordre professionnel des) c. Pouliot, 2018 QCCDTIMROEM 10027.
16 – Technologues en imagerie médicale, en radio-oncologie et en électrophysiologie médicale (Ordre professionnel des) c. Lapierre, 2016 QCCDTIMROEM 1.
17 – Technologues en imagerie médicale, en radio-oncologie et en électrophysiologie médicale (Ordre professionnel des) c. Lapierre, 2016 QCCDTIMROEM 103885; Technologues en imagerie médicale, en radio-oncologie et en électrophysiologie médicale (Ordre professionnel des) c. Pomerleau, 2025 QCCDTIMROEM 2.
18 – Technologues en imagerie médicale, en radio-oncologie et en électrophysiologie médicale (Ordre professionnel des) c. Martin, 2024 QCCDTIMROEM 3, par. 36 et 40.
19 – Infirmières et infirmiers (Ordre professionnel des) c. Aussant, 2010 QC CDOII 40630; Infirmières et infirmiers (Ordre professionnel des) c. Trottier, 2021 QCCDINF 3; Infirmières et infirmiers (Ordre professionnel des) c. Fillion, 2011 QC CDOII 41222.
20 – Technologues en imagerie médicale, en radio-oncologie et en électrophysiologie médicale (Ordre professionnel des) c. Vallières, 2022 QCCDTIMROEM 2, par. 41.
21 – Technologues en imagerie médicale, en radio-oncologie et en électrophysiologie médicale (Ordre professionnel des) c. Baril, 2019 QCCDOTIMROEM 37956.
22 – Technologues en imagerie médicale, en radio-oncologie et en électrophysiologie médicale (Ordre professionnel des) c. Côté, 2019 QCCDTIMROEM 80288.
23 – Technologues en radiologie (Ordre professionnel des) c. Paris, 2012 QCOTIMRO 78320.
24 – Technologues en imagerie médicale, en radio-oncologie et en électrophysiologie médicale (Ordre professionnel des) c. Bono, 2024 QCCDTIMROEM 1.
25 – Ibid., par. 45 et 46.
26 – R. c. C.D.; R. c. C.D.K., 2005 CSC 78; Infirmières et infirmiers (Ordre professionnel des) c Brunelle, 2007 CanLII 82910 (QC CDOII), par. 136-138.
27 – Ibid., Par. 39.
28 – Technologues en imagerie médicale, en radio-oncologie et en électrophysiologie médicale (Ordre professionnel des) c. Lavergne, 2023 QCCDTIMROEM 1.
29 – Technologues en imagerie médicale, en radio-oncologie et en électrophysiologie médicale (Ordre professionnel des) c. Descôteaux-Simard, 2021 QCCDTIMROEM 1.
30 – Infirmières et infirmiers auxiliaires (Ordre professionnel des) c. Raymond, 2010 CanLII 100017 (QC OIIA). (À noter que l’intimé ne s’est pas présenté à son audience. Le Conseil estime que la preuve présentée par le plaignant le décharge de son fardeau de preuve.
31 – Note 3, art. 8.
32 – Technologues en imagerie médicale, en radio-oncologie et en électrophysiologie médicale (Ordre professionnel des) c. Vallejos, 2025 QCCDTIMROEM 2; Technologues en imagerie médicale, en radio-oncologie et en électrophysiologie médicale (Ordre professionnel des) c. Descoteaux-Simard, 2025 QCCDTIMROEM 1; Technologues en imagerie médicale, en radiooncologie et en électrophysiologie médicale (Ordre professionnel des) c. St-Gelais, 2021 QCCDTIMROEM 1.
33 – Infirmières et infirmiers (Ordre professionnel des) c. Tardif, 2011 CanLII 41221 (QC CDOII).
UNE CONVERSATION QUI SE POURSUIT…
L’intelligence artificielle s’est imposée comme l’un des sujets les plus discutés dans nos milieux de pratique. Depuis quelques années, la revue ÉchoX et notre balado Fréquences et images vous ont proposé plusieurs éclairages sur cette réalité en pleine transformation. Vous avez pu y entendre des experts, des collègues et des chercheurs explorer les promesses, mais aussi les défis concrets que pose l’IA dans votre quotidien professionnel.
Aujourd’hui, cette conversation prend une nouvelle dimension. L’Institut national d’excellence en santé et en services sociaux (INESSS) vient de publier un état des connaissances complet, commandé par le ministère de la Santé et des Services sociaux (MSSS), qui dresse un portrait structuré des solutions d’IA disponibles ou prometteuses en imagerie médicale –et qui balise les conditions d’un déploiement réussi au Québec.
Nous vous invitons à prendre connaissance de ce document de référence. En attendant, voici quelques faits saillants qui nous parlent directement.


Ce que révèle l’INESSS : 5 faits à retenir

1
2
Deux grands champs d’application. L’IA en imagerie se décline en applications non interprétatives (optimisation des flux de travail, gestion des examens, qualité d’acquisition des images) et interprétatives (aide à la détection et à la caractérisation des anomalies). Ce sont les deux versants de notre pratique quotidienne.
La détection du cancer du sein et des fractures aux urgences figurent parmi les applications jugées les plus prometteuses à court terme par les experts consultés. Des revues systématiques montrent que l’IA améliore la sensibilité de détection tout en maintenant une spécificité comparable aux méthodes conventionnelles.
3
4 5
La FDA a approuvé ou autorisé environ 700 solutions d’IA en santé, dont 76 % concernent la radiologie. Au Canada, cinq de ces solutions évaluées par le NICE britannique sont déjà homologuées — notamment pour la détection de fractures et la planification en radiothérapie.
Au Québec, plusieurs projets pilotes sont en cours. Du CHU de Québec au CHUM, en passant par l’Hôpital général du Lakeshore et le CUSM, des établissements testent déjà des outils d’IA pour la détection de fractures, le dépistage de la rétinopathie diabétique, la détection de nodules pulmonaires et l’optimisation des IRM.
Des conditions clés s’imposent pour un déploiement réussi : une validation clinique rigoureuse, une formation adaptée, l’interopérabilité des systèmes (uniformisation des PACS en cours), une gouvernance solide, la protection des données et une attention aux biais algorithmiques. Notre rôle comme technologues est central dans chacune de ces étapes.
Lire le rapport complet de l’INESSS
Intelligence artificielle en imagerie médicale — Champs d’application et considérations pour son déploiement au Québec (INESSS, novembre 2025).
L’IA ne remplacera pas votre jugement clinique ni votre expertise — elle viendra le compléter.
Échographie médicale

Une entrevue avec Julie Robillard, t.i.m., et le Dr Étienne Cardinal, M.D. FRCPC, nous a permis d’explorer en profondeur les multiples facettes de l’injection de plasma riche en plaquettes (PRP) guidée par échographie musculosquelettique. De la biologie des plaquettes aux protocoles cliniques, en passant par le cadre réglementaire québécois, cet échange met en lumière le rôle croissant de cette approche régénératrice dans la pratique de l’imagerie médicale interventionnelle.


Principe biologique et applications cliniques du PRP
Pouvez-vous expliquer de façon simple le principe biologique du PRP et la manière dont les facteurs de croissance contenus dans les plaquettes favorisent la régénération tissulaire, dans le cas des tendinopathies et de l’arthrose ?
Les plaquettes attirent les facteurs de croissance et les fibroblastes au site de l’injection pour démarrer une cascade inflammatoire qui stimule le processus de guérison. Dans les cas d’arthrose, les zones endommagées du cartilage sont remplies par du fibrocartilage (cartilage cicatriciel), et, dans les tendons, les fibroblastes aident à la cicatrisation des déchirures.
Quelles sont actuellement au Québec les principales indications musculosquelettiques pour lesquelles vous recommandez une injection de PRP guidée par échographie ?
Les cas les plus fréquents traités par le PRP dans nos cliniques sont l’arthrose du genou, l’épicondylite du coude (souvent avec déchirures) et les déchirures partielles du tendon d’Achille, du fascia plantaire et de la coiffe des rotateurs.
L’efficacité du PRP dans l’arthrose du genou semble bien documentée dans la littérature récente. Pouvez-vous nous expliquer pour quels stades d’arthrose le PRP est le plus efficace et comment vous évaluez si un patient est un bon candidat pour l’injection ?
Le PRP peut être efficace pour les cas d’arthrose de légère à modérée. Il est moins indiqué dans les cas d’arthrose sévère, puisque le cartilage est déjà très abîmé, voire absent.
Procédé de prélèvement et de préparation du PRP
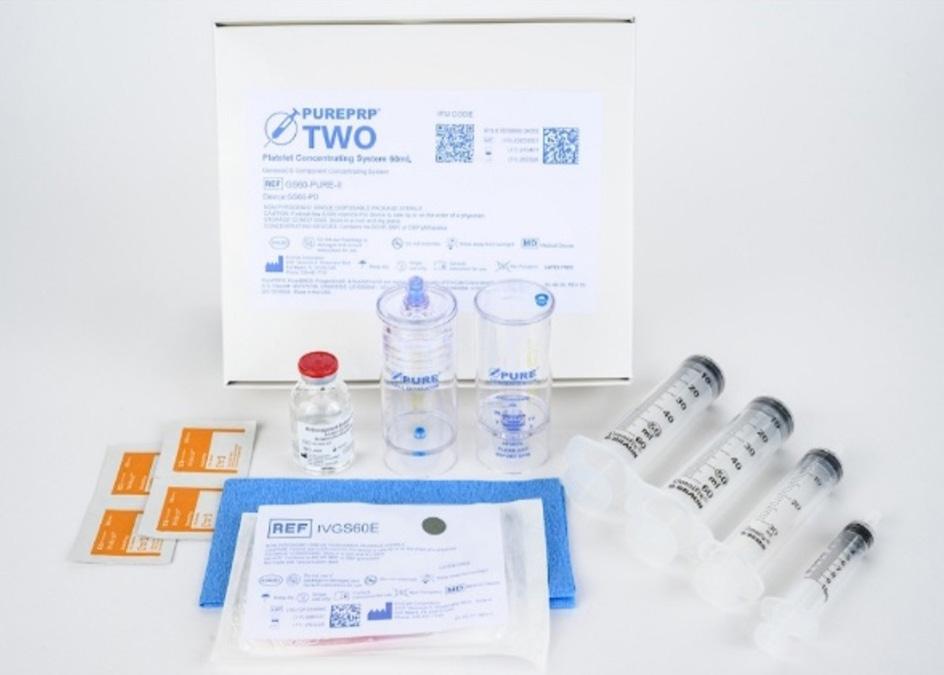
Pouvez-vous nous décrire étape par étape le protocole complet d’une séance de PRP, du prélèvement sanguin initial jusqu’à l’injection finale ? Combien de temps dure l’ensemble de la procédure ?
La procédure demande environ 30 minutes. Le patient est accueilli en échographie, et des images de la région à traiter sont prises par le radiologiste ou la technologue autonome assistant le radiologiste. Ensuite, le radiologiste rencontre le patient pour confirmer la pertinence du traitement et discuter des précautions à prendre dans les jours ou semaines qui suivent (limitation du sport, usage de béquilles, etc.).
Le prélèvement sanguin est effectué par le radiologiste, une infirmière ou la technologue détenant l’attestation émise par l’OTIMROEPMQ. Le prélèvement se fait avec un papillon dans une seringue contenant une petite quantité d’anticoagulant (10 % du total de sang prélevé). Le sang est ensuite transféré dans un contenant stérile destiné à la centrifugeuse. À noter que les protocoles peuvent varier selon le type de matériel utilisé. Dans notre protocole, un premier spin est effectué pour séparer le plasma des globules rouges. Le plasma est ensuite transféré dans un deuxième contenant stérile pour un deuxième spin. Ce dernier a pour effet de séparer les plaquettes, qui vont se déposer au fond du contenant par la force centrifuge (4 400 rpm). Une partie du plasma pauvre en plaquettes est ensuite retirée, puis les plaquettes au fond du contenant sont remises en suspension dans la quantité de plasma restante, ce qui en fait un plasma riche en plaquettes. L’injection de plasma est une procédure stérile guidée sous échographie. Certains ensembles/kit ne requièrent qu’un seul spin.
Quelle quantité de sang prélevez-vous généralement pour obtenir une quantité suffisante de PRP ?
Comment cette quantité influence-t-elle le volume définitif de PRP obtenu ?
Il est maintenant établi que plus que la concentration de plaquette, c’est la quantité totale de plaquettes injectées qui est le facteur déterminant pour obtenir un résultat clinique satisfaisant. Selon le site à injecter, de 30, 60 ml ou 120 ml de sang est prélevé. La quantité optimale de plaquettes visée est de minimum 3,5 milliards, mais généralement au-dessus de 10 milliards. La quantité de sang à prélever doit tenir compte du pourcentage d’extraction plaquettaire du kit (certains kits ont une efficacité de plus de 80 %, alors que d’autres oscillent autour de 60 %). De plus, avec l’âge, la concentration en plaquettes dans le sang diminue. Cela peut être compensé par un prélèvement d’une plus grande quantité de sang pour s’assurer d’avoir une quantité suffisante de plaquettes à injecter pour obtenir le meilleur résultat possible. Idéalement, connaître le décompte plaquettaire du patient permet de s’assurer d’injecter une dose thérapeutique.
Au Québec, qui est légalement autorisé à effectuer le prélèvement sanguin pour le PRP ?
Les infirmières, médecins, radiologistes et technologues en imagerie médicale détenant l’attestation émise par l’OTIMROEPMQ peuvent effectuer un prélèvement sanguin.
Au Québec, les infirmières, médecins, radiologistes et technologues en imagerie médicale détenant l’attestation émise par l’OTIMROEPMQ peuvent effectuer un prélèvement sanguin.

Quel type de tubes utilisez-vous pour le prélèvement sanguin du PRP ? S’agit-il de tubes spéciaux pour PRP avec gel séparateur et anticoagulant, ou utilisez-vous des tubes de prélèvement sanguin standard ?
Le sang est prélevé dans une seringue stérile avant d’être transféré dans les contenants stériles destinés à la centrifugeuse..
Pourquoi est-il essentiel d’utiliser un anticoagulant lors du prélèvement ? Que se passerait-il si le sang coagulait avant la centrifugation ?
L’anticoagulant permet la séparation du plasma des globules rouges au moment de la centrifugation. Si le sang coagule, il n’est plus possible de séparer adéquatement les différentes parties du sang, car elles seront agglomérées et gélatineuses (figure 1 ).
Processus de centrifugation et séparation des composants sanguins
Pouvez-vous expliquer le principe physique de la centrifugation pour séparer les composants sanguins ? Comment la force centrifuge permet-elle de séparer les globules rouges, les plaquettes et les globules blancs, et le plasma ?
Sous l’effet de la force centrifuge, les composantes plus denses du sang sont déplacées vers l’extérieur par rapport aux autres; vers l’extérieur, cela signifie qu’elles se déposent au fond du contenant. Plus les composantes du sang sont denses et volumineuses, plus leur mouvement sera grand. À titre d’exemple, la concentration approximative des globules rouges est d’environ 1,1 g/ml, alors que celle des plaquettes est de 1.05 g/ml. Le plasma et les plaquettes étant plus légers et moins concentrés, ils seront dans la partie supérieure du contenant à la suite du processus de centrifugation.
Pouvez-vous décrire les deux étapes de la centrifugation double ?
La première centrifugation sépare le sang en trois couches distinctes :
■ Plasma (couche supérieure);
■ Couche leucoplaquettaire (couche moyenne, appelée « buffy coat », qui renvoie à sa couleur beige);
■ Globules rouges (couche inférieure).
La deuxième centrifugation a pour but de provoquer le dépôt des plaquettes dans le fond du contenant. Grâce à cette étape, le radiologiste peut enlever aisément une partie du plasma, ce qui permet de remettre les plaquettes en suspension dans un plus petit volume (en brassant manuellement le contenant), afin que le volume injecté soit adapté au site d’injection (p. ex. 2-3 ml pour un tendon, 10 ml pour un genou) (figure 2).












Comment prélevez-vous spécifiquement la fraction de PRP (couche riche en plaquettes) sans aspirer les globules rouges en dessous ni le plasma pauvre en plaquettes (PPP) au-dessus ?
Le prélèvement est fait à la main dans une seringue stérile.
Quelle concentration plaquettaire visez-vous dans votre PRP final ?
La quantité injectée est une valeur plus importante qu’une concentration donnée, qui pourrait varier d’un patient à l’autre. Avec nos doubles spins et une plus grande quantité de sang prélevé, une quantité minimale de 3,5 milliards de plaquettes est visée pour avoir une réponse efficace au traitement. Cependant, pour une plus grosse articulation comme le genou, un minimum de 10 milliards est souhaité.
Asepsie et stérilité du processus
Comment assurez-vous la stérilité absolue du prélèvement sanguin et de toute la chaîne de préparation du PRP, sachant que ce produit autologue sera réinjecté dans le corps du patient quelques minutes plus tard ?
Le sang est prélevé dans une seringue stérile, et transféré dans un contenant stérile, toujours en assurant une bonne désinfection des bouchons ou connecteurs. Ensuite, le radiologiste porte des gants stériles pour manipuler les seringues et les aiguilles qui serviront à l’injection. L’assistante ou la technologue prépare le champ stérile ainsi que le matériel nécessaire en respectant les règles d’asepsie (ouverture des paquets, respect des bordures du champ, etc.). Elle présente le contenant de PRP au radiologiste en ayant désinfecté l’embout : celui-ci connecte sa seringue sans toucher l’extérieur du contenant pour faire le prélèvement.
Quel est votre protocole de préparation de la salle d’échographie pour une injection de PRP ? Y a-t-il des différences en matière d’asepsie par rapport à d’autres procédures interventionnelles comme les infiltrations de corticostéroïdes ?
La procédure est la même : port du masque, préparation du matériel et ouverture du champ par une personne non gantée. L’intérieur du champ, les seringues et les aiguilles ne sont touchés que par le radiologiste qui porte masque et gants stériles. La peau est désinfectée avec de la chlorhexidine. Il en va de même pour la sonde échographique. Du gel stérile est utilisé lors de la procédure. Le tout se fait en présence du patient.
Utilisez-vous systématiquement une gaine stérile pour la sonde échographique et du gel stérile lors des injections de PRP? Y a-t-il une différence de protocole selon que l’injection est intraarticulaire ou intratendineuse ?
Dans nos centres, l’utilisation de la gaine ou membrane stérile dépend de la préférence du radiologiste effectuant la procédure. Si une gaine stérile n’est pas utilisée, la sonde est stérilisée au préalable avec de la chlorhexidine et nettoyée ensuite avec une lingette virucide et bactéricide.
Pour les injections intratendineuses, la douleur postprocédure peut être plus incommodante dans les jours suivants, puisque plusieurs passages avec l’aiguille sont effectués dans le tendon à traiter (dépôt de PRP à plusieurs endroits). Le radiologiste va donc offrir au patient une ordonnance d’antidouleurs plus puissants que de l’acétaminophène, ce qui n’est pas nécessaire pour les injections intra-articulaires. Cela peut être
Il existe un intérêt à élargir l’utilisation du PRP aux déchirures musculaires aiguës et aux lésions ligamentaires.
requis dans les premiers jours, puisqu’il n’est pas recommandé de mettre de la glace (vasoconstriction) ou de prendre de l’ibuprofène (inhibe le processus inflammatoire) dans les deux semaines suivant la procédure. De plus, pour les procédures impliquant un tendon du membre inférieur (p. ex. tendon d’Achille) ou le fascia plantaire, l’usage de béquilles ou d’une botte de marche est recommandé afin d’éviter une mise en charge sur le membre traité quelques jours (jusqu’à une semaine selon les cas) après le traitement.
Optimisation de l’imagerie échographique
Quels sont les signes échographiques que vous recherchez spécifiquement lors de l’évaluation préinjection pour caractériser une tendinopathie chronique ? Pourquoi cette évaluation échographique détaillée est-elle importante pour déterminer si le patient est un bon candidat au PRP ?
La tendinopathie chronique se voit par une perte de l’aspect fibrillaire du tendon à l’échographie. Celui-ci peut aussi présenter des déchirures partielles (images anéchogènes) à l’intérieur du tendon ou transfixiantes (déchirure traversant l’épaisseur complète du tendon). Certaines tendinopathies s’accompagnent aussi d’une hypervascularisation locale, visible grâce au Doppler couleur (souvent visualisée dans les cas d’épicondylite du coude et de tendinopathie du tendon d’Achille).
Quelle approche échographique utilisez-vous pour l’injection intra-articulaire du genou ?
Pourquoi privilégiez-vous cette approche ?
Le genou est positionné en légère flexion, et une approche latérale externe ou médiale est utilisée pour déposer le bout de l’aiguille sur le cartilage de la trochlée fémorale. La flexion légère du genou comprime les récessus fémoro-patellaires latéraux et mobilise le liquide articulaire vers le récessus supra-patellaire, ce qui offre une cible plus facile au moment de l’injection. S’il existe un épanchement important, il est recommandé de l’aspirer avant de procéder à l’injection de PRP.
Comment différenciez-vous échographiquement le liquide synovial inflammatoire du PRP injecté (peut apparaître légèrement hyperéchogène) durant et après l’injection ?
Les deux sont anéchogènes. On visualise un mouvement des fluides lors de l’injection, mais c’est surtout une absence de résistance qui permet au radiologiste de confirmer qu’il est bien positionné.
Particularités du PRP versus d’autres injections
Pouvez-vous expliquer pourquoi les antiinflammatoires non stéroïdiens (AINS) doivent être arrêtés environ 7 à 15 jours avant l’injection de PRP et évités pendant plusieurs semaines après (souvent six semaines) ?
Les AINS inhibent la cascade inflammatoire nécessaire à l’obtention des résultats désirés à la suite du traitement (facteurs de croissance et fibroblastes attirés au site d’injection par le dépôt des plaquettes).
Comment cette contrainte a-t-elle un impact sur la gestion de la douleur chez vos patients, surtout dans les premiers jours post-injection, qui peuvent être plus douloureux que la douleur de base ? Que recommandez-vous comme solution ?
Il est recommandé de prendre de l’acétaminophène au besoin. La glace et les AINS sont contre-indiqués dans les deux semaines suivant le traitement. Le radiologiste peut prescrire un médicament un peu plus efficace pour les procédures plus douloureuses, telles que les injections intratendineuses (p. ex. Tramacet).
Quelles sont les contre-indications absolues au PRP que les technologues devraient connaître avant de préparer une salle d’échographie pour ce type d’intervention? Par exemple :
■ Infection active (locale ou systémique) ?
■ Cancer actif ou antécédents récents de cancer ?
■ Thrombocytopénie sévère (< 100 000 plaquettes/μL) ?
■ Troubles de la coagulation non contrôlés ?
■ Prise d’anticoagulants (Warfarine, nouveaux anticoagulants oraux) ?
Il n’y a aucune contre-indication absolue au traitement de PRP.
Effectuez-vous systématiquement une échographie de contrôle immédiatement après l’injection de PRP ?
Des images échographiques sont prises avant, pendant et après l’injection de PRP pour vérifier la bonne distribution du produit.
À quels intervalles effectuez-vous des échographies de suivi après une injection de PRP ? Ces suivis sont-ils systématiques ou les fait-on seulement si la condition du patient ne s’améliore pas cliniquement ?
Il n’y a aucun suivi échographique systématique effectué. L’efficacité du traitement est évaluée en fonction du tableau clinique (amélioration de la mobilité, réduction des douleurs, etc.). Toutefois, un suivi peut être demandé par le médecin traitant si les douleurs augmentent dans les semaines suivant la procédure. On constate généralement l’efficacité du PRP dans les quatre à six semaines, mais l’effet du traitement se prolonge pendant plusieurs mois. Si le patient a eu une réponse partielle au traitement, et si un deuxième PRP est envisagé, cela se fait généralement de quatre à six mois après la première injection.
Contexte et avenir
Au Québec, comment se déroule habituellement la prise en charge financière des injections de PRP ? Étant donné que ce traitement n’est généralement pas couvert par la RAMQ, quel est le coût typique pour les patients ?
Le coût varie entre 500 $ et 900 $, et peut être influencé par le système/kit utilisé. Certaines cliniques facturent une partie des frais d’échographie à la RAMQ.
Comment voyez-vous l’avenir du PRP en imagerie musculosquelettique au Québec dans les cinq à dix prochaines années ?
Nous pouvons être portés à croire qu’il continuera d’y avoir une augmentation de l’intérêt pour une médecine régénérative, comme le PRP qui potentialise une guérison, et une baisse du recours aux injections de cortisone qui soulagent pour peu de temps et qui ne contribuent pas à accélérer la guérison (un « bandaid », comme le disent les patients). De plus, il y a une prise de conscience de complications potentielles de la cortisone (p. ex. insuffisance surrénalienne, chondrotoxicité, etc.) qui porte à éviter de procéder à des infiltrations à répétition.
Y a-t-il de nouvelles applications ou indications émergentes du PRP que vous envisagez d’intégrer dans votre pratique ?
Il existe un intérêt à élargir l’utilisation du PRP aux déchirures musculaires aiguës et aux lésions ligamentaires. Certaines études préconisent l’injection concomitante de PRP et d’acide hyaluronique, mais ces études récentes méritent d’être validées avant de les reconduire à grande échelle.
Cet échange illustre bien la complémentarité des expertises en imagerie médicale interventionnelle et la place grandissante que la médecine régénératrice occupe dans les pratiques cliniques au Québec. Le PRP guidé par échographie représente une avenue prometteuse, et la collaboration entre technologues et radiologistes en demeure un pilier essentiel.
FIGURES
1 – Propriété de emcyte.com
2 – Propriété de accelleratedbiologics.com
Médecine nucléaire

Introduction
Le diverticule de Meckel est l’anomalie congénitale la plus fréquente du système gastro-intestinal. La scintigraphie au 99mTc-Pertechnétate (99mTc-PS), aussi nommée scintigraphie de Meckel, est utilisée en médecine nucléaire depuis de nombreuses années, pour la détection de la muqueuse gastrique ectopique. Le but de cet article est de revoir l’épidémiologie et pathophysiologie du diverticule de Meckel, sa présentation clinique et sa mise en image incluant la préparation pharmacologique et l’utilisation de la scintitomographie avec tomodensitométrie à faible dose.
Epidémiologie et pathophysiologie
Le diverticule de Meckel résulte de la persistance du canal omphalo-mésentérique après la période de développement fœtal. D’autres variantes anatomiques de cette persistance existent, soit des bandes fibreuses et le résidu prédisposant aux obstructions intestinales, des kystes omphalomésentériques et des fistules omphalomésentériques qui drainent au niveau de l’ombilic. La prévalence estimée dans la population générale est entre 0,3 à 2,9 %. Il n’y a pas d’évidence
de prédisposition familiale. La règle des 2 est comme suit : affecte 2 % de la population; le ratio homme-femme est de 2:1; se situe à 2 pieds de la valve iléo-caecale; mesure 2 pouces et 2 à 4 % des patients développent des complications souvent avant l’âge de deux ans1,2
Les duplications intestinales sont rares, se présentant dans la première année de vie pour la majorité. Elles peuvent se situer à tous les niveaux du tractus digestif, le plus fréquemment au niveau de l’iléon, versant mésentérique et généralement ne communiquent pas avec la lumière digestive. Elles peuvent contenir du tissu gastrique3,4
Présentation clinique
Les diverticules de Meckel demeurent asymptomatiques dans la majorité des patients et la présence de symptômes va être reliée à la présence de muqueuse gastrique ectopique. Dans une étude portant sur quasiment 8 000 appendicectomies, des diverticules de Meckel asymptomatiques avaient été découverts chez 233 patients et réséqués à la discrétion du chirurgien dans 188 cas. Seulement deux étaient porteurs de muqueuse gastrique ectopique5. Dans d’autres
études comparant les caractéristiques des diverticules de Meckel réséqués suite à la présence de symptômes versus ceux identifiés lors de chirurgies abdominales pour d’autres indications, la présence de muqueuse gastrique ectopique était trouvée dans 50-76 % des patients du premier groupe, dans des diverticules plus longs et plus larges, versus 12-20 % du second6,7
La présentation clinique la plus aigüe est un saignement non douloureux, causé par l’ulcération du petit intestin en lien avec la sécrétion d’acide par la muqueuse gastrique ectopique au sein du diverticule. Le site de l’ulcération et du saignement est adjacent ou juste en aval du diverticule. Le saignement non douloureux est présent dans 30 à 75 % des enfants mais peut également être retrouvé dans environ 30 à 50 % des adultes8-10
Le second type de présentation aigüe est celui d’une obstruction intestinale, causée par intussusception, volvulus, torsion, inversion, herniation ou inflammation du diverticule dans environ 40 % des patients tant adultes que pédiatriques8-10
Les facteurs de risque de développer des symptômes qui ont été identifiés dans une étude de 1 476 patients suivi sur 50 ans étaient : âge < 50 ans (OR 3.95, 95 % CI 2.6-4.8); sexe masculin (OR 1.8, 95 % CI 1.32.4); longueur du diverticule de plus de 2 cm (OR 2.2, 95 % CI 1.1-4.4); présence histologique de tissus anormal (OR 13.9, 95% CI 9.9-19.6)8
Dans une revue de 600 patients symptomatiques, le diverticule de Meckel était retrouvé en moyenne à 34 cm de la valvule iléo-caecale chez les patients âgés de moins de 2 ans, 46 cm pour ceux entre 2 et 20 ans et 66 cm chez les patients plus vieux. De la muqueuse gastrique était identifiée dans 62 % des cas, pancréatique dans 16% et une combinaison des deux dans 5 %9
Certains enfants peuvent présenter des symptômes plus chroniques comme douleurs abdominales mal définies nausées, vomissements ou retard staturopondéral. La scintigraphie est plus fréquemment positive chez les patients avec saignement qu’avec d’autres symptômes non-spécifiques (26 % versus 2 %)10
Un diverticule de Meckel doit donc être soupçonné chez les enfants particulièrement en bas de 10 ans avec saignement digestif bas sans signe de gastro-entérite ou de maladie inflammatoire de l’intestin, chez les adultes (particulièrement en bas de 40 ans) avec saignement digestif sans source de saignement
identifié à l’endoscopie et à l’imagerie radiologique conventionnelle et chez les patients avec intussusception surtout si récurrent ou atypique.
Scintigraphie au Pertechnétate de Tc99-m (99mTc-SP)
La scintigraphie au Pertechnétate de Tc99m est le test de choix pour identifier la muqueuse gastrique ectopique chez les patients dont la suspicion clinique est élevée. Cependant, quoique le diverticule puisse potentiellement être identifié sur la TDM faible dose si effectuée, s’il n’y pas de muqueuse gastrique ectopique ou cause de faux positif, l’étude scintigraphique par elle-même sera négative. Dans la scintigraphie au 99mTc-Pertechnétate, la captation du traceur est principalement au niveau des cellules sécrétrices de mucine mais son élimination est influencée par les cellules pariétales11,12. Sans manipulation pharmacologique, il y a élution du traceur de l’estomac vers le duodénum et le grêle en cours d’étude. Il est également visualisé l’élimination physiologique par les reins vers la vessie (figure 1 ).
Dans la population pédiatrique la sensibilité de 99mTc-SP est de 80-90 %, sa spécificité de 95 %, son exactitude de 90 % mais ces valeurs sont moindres chez l’adulte, soit 62 %, 9 % et 46 % respectivement 13 Une revue systématique et méta-analyse pédiatrique en 2023 incluant 16 études effectuées entre 1974 et 2018, chez 1 115 enfants a démontré une sensibilité combinée de 0.8 (95 % CI 0.73-0.86) et une spécificité combinée de 0.95 (95 % CI 0.85-0.90)14. Il n’y a cependant pas d’études avec utilisation systématique de l’acquisition tomographique (SPECT) avec ou sans tomodensitométrie (TDM).
La TDM avec produit de contraste est une méthode alternative diagnostique de plus en plus utilisée et peut mettre en évidence l’extravasation du produit de contraste en cas de saignement actif 15
La préparation du patient consiste en un jeûne de 4 à 6 heures avant l’examen, à l’exception de ceux âgés de moins de 2 ans pour lequel un jeûne de 3 heures avant est demandé. Le patient ne doit pas avoir reçu du sodium perchlorate ou une étude avec baryum dans les 3 à 4 jours précédant l’examen16-18
Il ne doit pas avoir eu une étude aux globules rouges marqués avec un marquage in vivo avant la
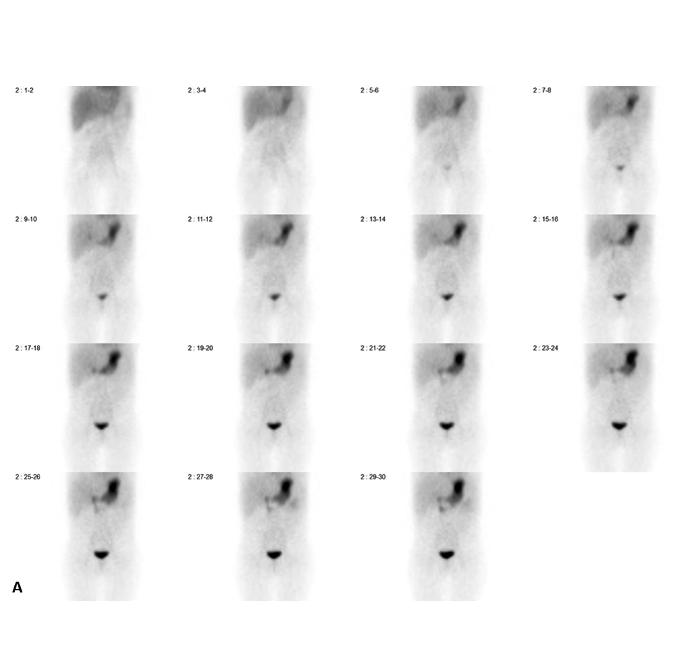
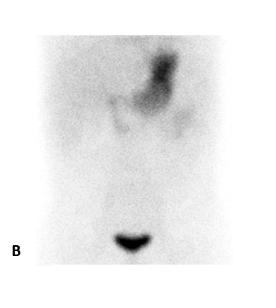
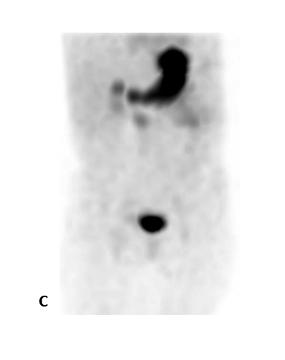
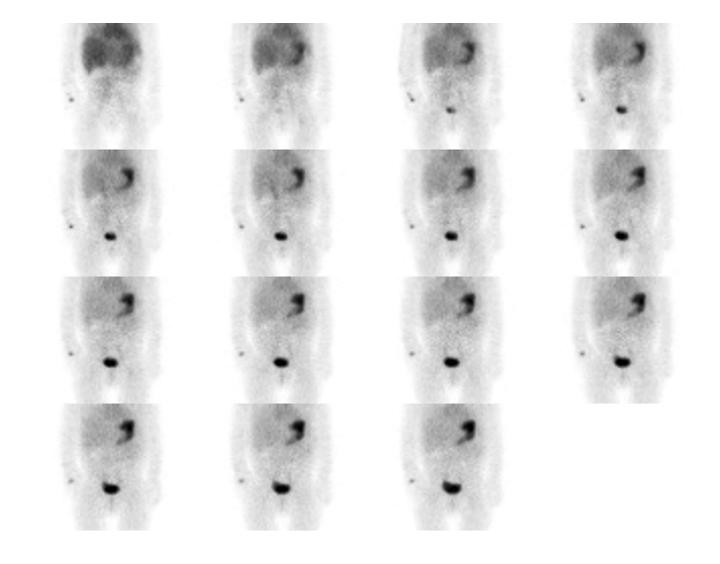
Figure 1 : Examen effectué sans préparation pharmacologique et avec SPECT simple chez un patient de 4 ans avec rectorragies. Mise en évidence d’une élution du traceur en cours d’étude avec visualisation du duodénum et du grêle. Acquisition dynamique ( A ), cliché statique à 30 minutes post injection (B) et rendu 3D de l’acquisition tomographique (C)
scintigraphie au Tc99m04- car les globules rouges restent potentiellement sensibilisés. Cependant, il est possible de procéder après un marquage in vitro (figure 2)19,20
Il est recommandé que le patient fasse des mictions avant et pendant l’examen.
En ce qui concerne la préparation pharmacologique, la pentagastrine et le glucagon étaient auparavant utilisés pour augmenter la captation, mais il y a eu retrait du marché de la pentagastrine aux États-Unis en raison d’effets secondaires graves. Ceci a laissé place à une préparation avec les antagonistes des récepteurs à l’histamine de type 2, qui augmentent la captation du Pertechnétate en inhibant son élution par la muqueuse gastrique. La Cimétidine (Tagamet®) n’est plus disponible. La ranitidine (Zantac®) per os a été retirée du marché. Le dosage était 2 mg/kg BID pour deux jours avant l’examen (figure 3). En ce qui concerne la forme IV, la dose est de 1mg/kg (maximum 50mg), infusé sur 20 minutes, avec mise en image 60 minutes après (figure 4).
Pour une préparation avec la famotidine (Pepcid®) per os, la dose est 0.5 mg/kg/dose die (maximum 40 mg) si le patient est âgé de plus de 2 mois et 0.5 mg/kg/dose die si 2 mois et moins, administré avant le coucher pendant 2 jours avant la scintigraphie. En pratique, à moins d’avoir accès à une préparation magistrale, la préparation per os n’est possible que pour les enfants en haut de 20 kg, la forme disponible étant des comprimés de 10 mg. Pour la forme IV, il y a administration de 0,25 mg/kg, infusé sur 20 minutes, 60 minutes avant le début des images16-18 (figure 5).
Une étude animale et une étude humaine récentes ont démontré qu’un inhibiteur à pompe à protons (IPP) comme esomeprazole (Nexium ®) intraveineux 30 minutes avant la scintigraphie étaient une alternative valide à la ranitidine20,21. Cependant il n’y a pas d’études en ce qui concerne la forme orale.
Dans notre expérience, aucune préparation soit Ranitidine po, Ranitidine iv, Famodine po, Famotidine iv ou IPP po n’empêche l’élution durant l’examen. Elle se
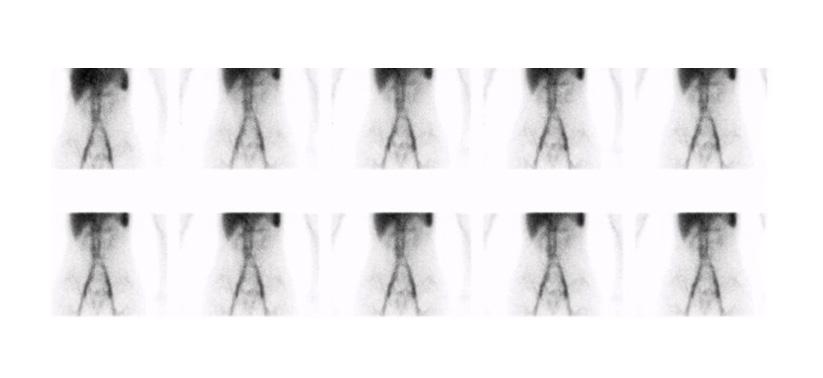
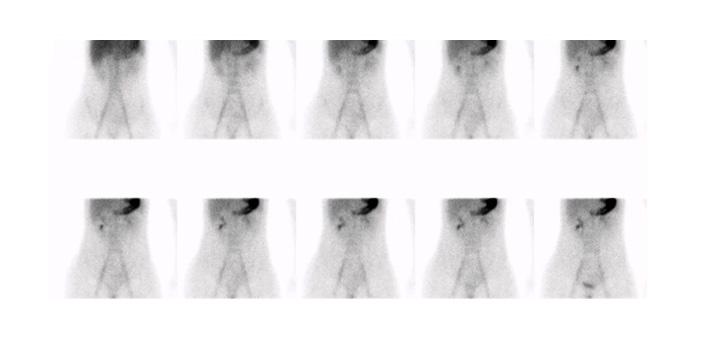
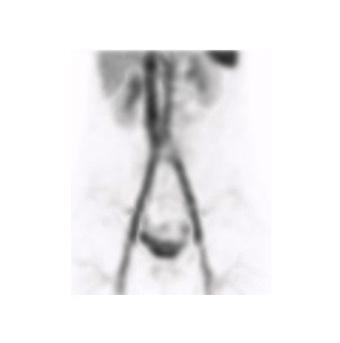
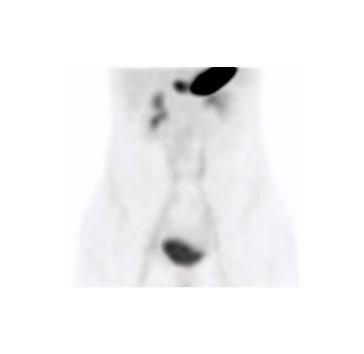
Figure 2 : Étude aux globules rouges avec marquage in vitro (UltratagTM) chez adolescente avec saignement occulte entrainant une anémie sévère. Acquisition dynamique ( A ) et rendu 3D de l’acquisition tomographique (B). Scintigraphie de Meckel sans interférence effectuée 12 jours plus tard. Acquisition dynamique ( C ) et rendu 3D de l’acquisition tomographique ( D ). Les deux études se sont avérées négatives et malgré une investigation extensive, la source du saignement n’a pas été identifié.
produit dans environ 1/3 des patients sous Ratidine, 50 à 60 % des patients sous Famotidine et 70 % des patients sous IPP. Cependant, l’élution est plus tardive, autour de 20 minutes avec la Famotidine IV.
Acitivité administrée et acquisition
La dose administrée chez les enfants et de 0,05 mCi/kg (1,85 MBq/kg), avec une dose minimale de 0,25 mCi (9,25MBq) IV et maximale de 8 mCi (296 MBq) IV. Pour les adultes, la dose administrée est de 5 à 10 mCi (185-370 MBq) IV 16,22
L’acquisition est réalisée avec une gamma-caméra grand champ, avec un collimateur basse énergie, tout usage ou haute résolution en acquisition antérieure et postérieure. Le patient est positionné en décubitus dorsal avec l’appendice xiphoïde jusqu’à la symphyse pubienne dans le champ d’acquisition.
Elle consiste en une étude de flot de 60 secondes, si possible 1 seconde par cadre suivie d’une étude
dynamique aux minutes pendant 30 minutes. Certains protocoles effectuent l’étude dynamique sur 60 minutes mais notre expérience est que même avec une préparation pharmacologique, l’élution peut se produire à partir de 20 minutes. Par la suite des images statiques en incidences antérieure, postérieure, latérales droite et gauche si possible post-miction sont réalisées. Les incidences latérales permettent de séparer un foyer de muqueuse ectopique, antérieure de l’activité rénale postérieure. Les clichés post-miction de même que l’acquisition SPECT-TDM permettent une meilleure visualisation des régions adjacentes à la vessie et parfois le diverticule est visible sur la composante TDM faible dose (figure 6)12, 16-18, 23
Dans notre expérience, l’étude SPECT-TDM faible permet de confirmer les trouvailles planaires et de mieux le localiser par rapport aux structures normales pour la planification opératoire (figure 7 ). Dans notre expérience également, quoiqu’aucun diverticule de Meckel n’ait été identifié uniquement sur l’étude
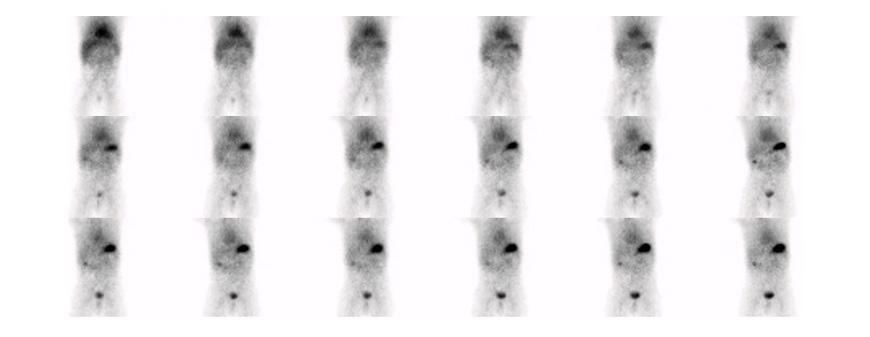
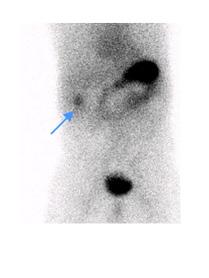
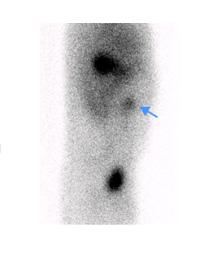

Figure 3 : Patient de 2 ans avec rectorragies intermittente depuis 7 mois et anémie. Examen effectué avec préparation pharmacologique de type ranitidine per os. Étude dynamique ( A ) et statique ( B ) en incidence antérieure démontrant un foyer pouvant potentiellement être d’origine rénale au niveau de l’hypochondre droit (flèche). Position antérieure du foyer de captation démontré par l’incidence latérale droite (C) et confirmé par la triangulation en SPECT ( D) et le rendu 3D (E). Mise en évidence d’un diverticule de 2cm contenant de la muqueuse gastrique ulcérée et de la muqueuse pancréatique.
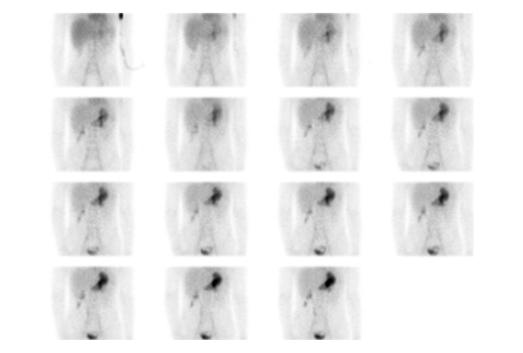
2 : 15-16
2 : 13-14
2 : 11-12
2 : 9-10
2 : 17-18
2 : 19-20
2 : 21-22
2 : 23-24
2 : 25-26
2 : 27-28
2 : 29-30
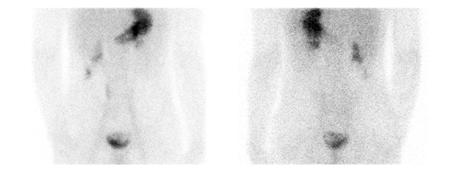
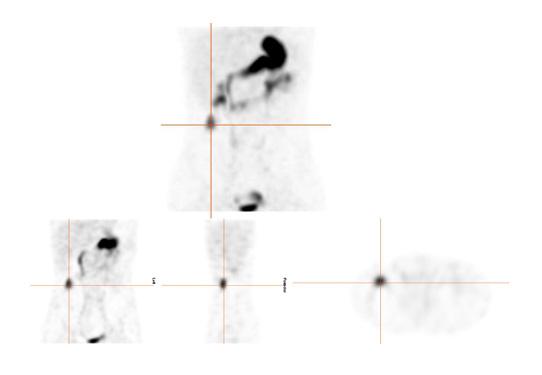
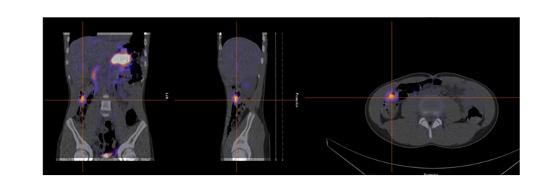
Figure 4 : Patient de 13 ans. Rectorragies avec chute de l’hémoglobine. Administration de Zantac IV deux heures avant la scintigraphie. Mise en évidence d’élution au niveau du duodénum et du grêle mais également d’un diverticule de Meckel au flanc droit, près du rein, mieux identifié sur l’étude tomographique. Étude dynamique ( A ) et statique (B) en incidence antérieure, rendu 3D du SPECT (C) et image de fusion (D).
2 : 9-10
2 :
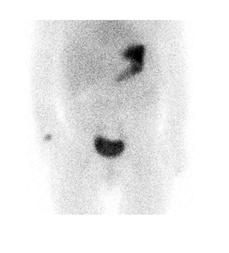
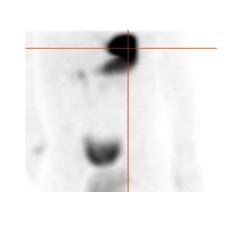
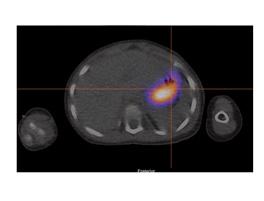
Figure 5 : Patiente de 19 mois avec deux épisodes de méléna. Scintigraphie effectuée après préparation avec Famotidine IV incluant une étude SPECT-TDM négative. Excellent blocage de l’estomac. Étude dynamique ( A ) et statique (B) en incidence antérieure, rendu 3D du SPECT (C) et image de fusion au niveau de l’estomac (D).
Dans notre expérience, bien qu’aucun
Meckel n’ait été détecté uniquement sur SPECT, le SPECT/TDM a offert une meilleure localisation, une clarification des résultats douteux sur l’imagerie planaire et pour certains un diagnostic alternatif.
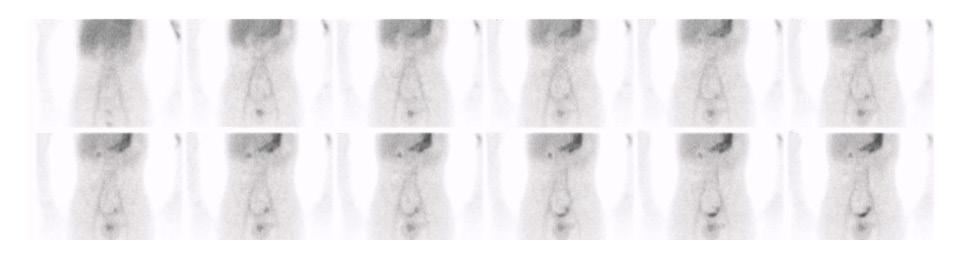
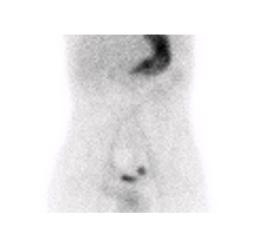
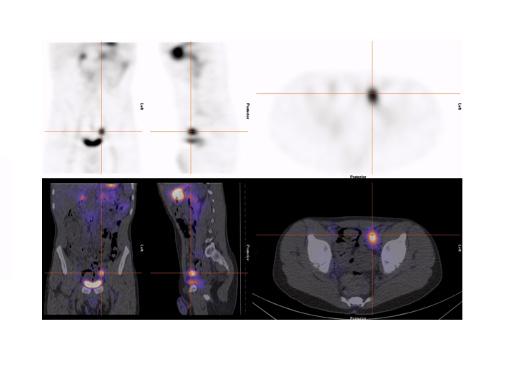
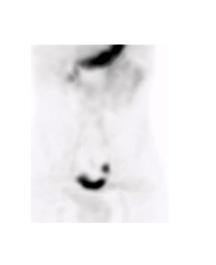
Figure 6 : Patient de 13 ans avec douleurs abdominales mais sans rectorragies. Mise en évidence sur la TDM diagnostic d’une image anormale à la fosse iliaque gauche. Scintigraphie effectuée avec préparation préalable avec famotidine po pendant 2 jours. Sur l’étude dynamique ( A ) apparition d’un foyer au niveau de la fosse iliaque gauche (flèche) de façon concomitante à l’estomac, soit vers la deuxième minute, avant les reins et la vessie qui sont démontrés respectivement à 5 et 9 minutes. Foyer (flèche) en augmentation sur le cliché planaire post miction ( B), confirmé avec la triangulation de l’étude SPECT-TDM où le diverticule est visualisé (C) et le rendu 3D (D).
SPECT-TDM, celle-ci permettait d’identifier d’autres pathologies comme des œsophagites, des saignements actifs et des segments inflammatoires. Quoique recommandée dans des cas équivoques, elle n’est pas utilisée de façon systématique dans la littérature24
Interprétation
Le diverticule de Meckel apparait comme une captation focale le plus souvent au quadrant inférieur droit (figure 8). La captation apparait souvent dans les 5 à 10 minutes après l’injection en parallèle avec l’estomac et peut apparaitre dès la première minute. La captation augmente en intensité avec le temps, typiquement au même rythme que la captation gastrique alors que l’activité rénale démontrée dans les 2-3 premières minutes va diminuer (figure 9).
Les causes de faux négatifs sont : une technique inadéquate, une dilution et délavage du Pertechnétate en présence de saignement actif, un délavage rapide du Pertechnétate secrété, surtout en l’absence de préparation pharmacologique, une absence de muqueuse gastrique dans le diverticule, un diverticule
de petite taille surtout chez les patients en bas de 1 an (figure 10), une localisation rétrovésicale sans complément d’étude tomographique ou acquisition post-miction et une altération de l’apport sanguine au diverticule, par exemple suite à une intussusception12
Les causes de faux positifs sont les foyers d’activité urinaire, les malformations vasculaires, les maladies inflammatoires digestives, les tumeurs malignes, les kystes de duplication dont certains peuvent contenir de la muqueuse gastrique, l’œsophage de Barrett, le tout avec ou sans saignement 12
Conclusion
En résumé la scintigraphie au Pertechnétate de Tc99m continue à jouer un rôle important dans la détection de la muqueuse ectopique. Une préparation adéquate incluant l’utilisation de la famotidine IV et une mise en image complète incluant le SPECT-TDM permet d’optimiser la technique. Dans notre expérience, bien qu’aucun Meckel n’ait été détecté uniquement sur SPECT, le SPECT/TDM a offert une meilleure localisation, une clarification des résultats douteux sur l’imagerie planaire et pour certains un diagnostic alternatif.
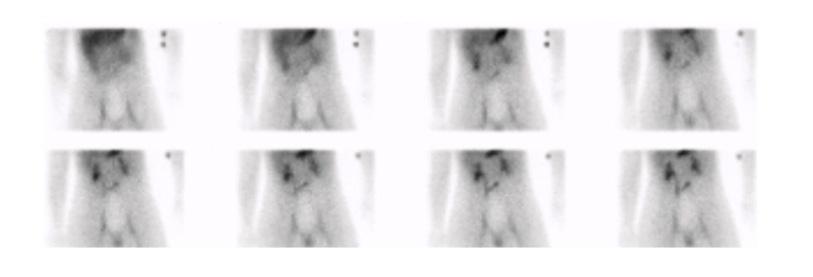
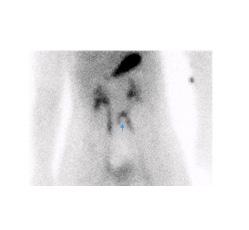
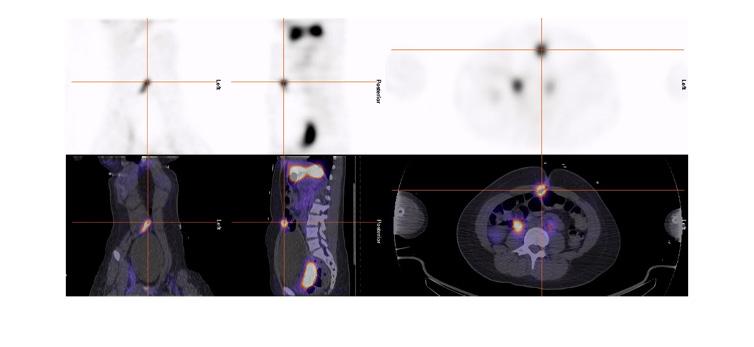
Figure 7 : Adolescente admise avec hémorragie basse massive. Préparation avec famotidine intraveineuse. Mise en évidence sur l’étude dynamique ( A ) puis sur le cliché statique ( B ) d’un foyer ombilical augmentant en intensité et en taille (flèche). La relation du diverticule contenant de la muqueuse gastrique avec l’ombilic est bien démontrée sur le SPECT-TDM (C). La pathologie de la chirurgie effectuée dans la foulée via laparotomie et non laparoscopie étant donné les trouvailles a démontré un Meckel de 6 x 2 cm contenant de la muqueuse gastrique, avec aspect perforé associé à un canal omphalomésentérique de 0,5 x 0,5 x 0,5 cm. Moins de 4 heures se sont écoulées entre l’arrivée de la patiente à l’urgence et la chirurgie.
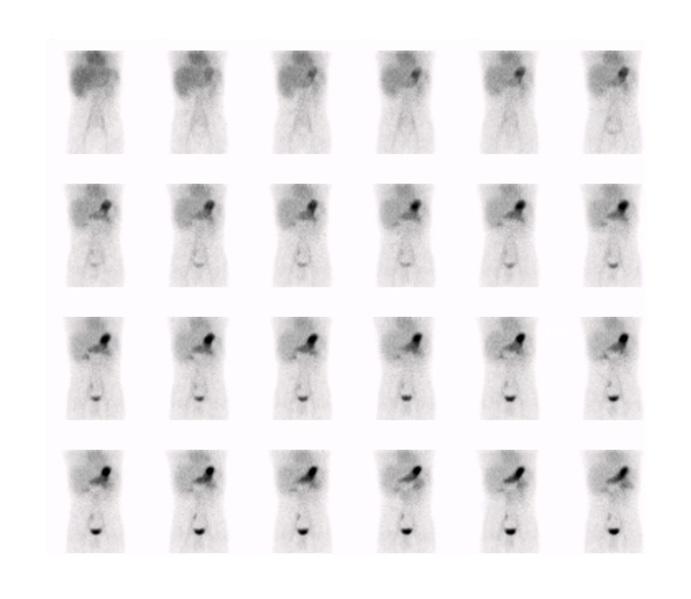
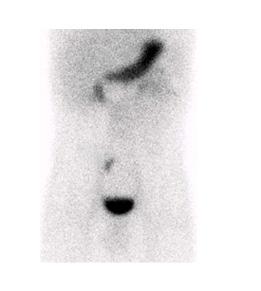
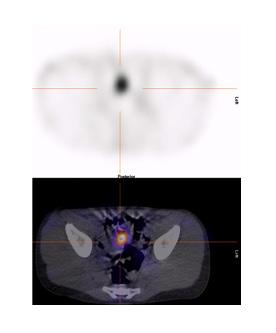
Figure 8 : Patient de 8 ans avec douleur abdominale, rectorragie, lipothymie. Examen effectué après préparation préalable avec Ranitidine IV. L’étude dynamique ( A ) puis le cliché statique ( B ) révèle un foyer de captation près des vaisseaux iliaques droits qui augmente au cours du temps (flèche). Le diverticule et la captation du traceur sont revus sur l’étude SPECT-TDM (C). Un Meckel de 5 cm contenant de la muqueuse grêle et gastrique a été trouvé à la chirurgie.
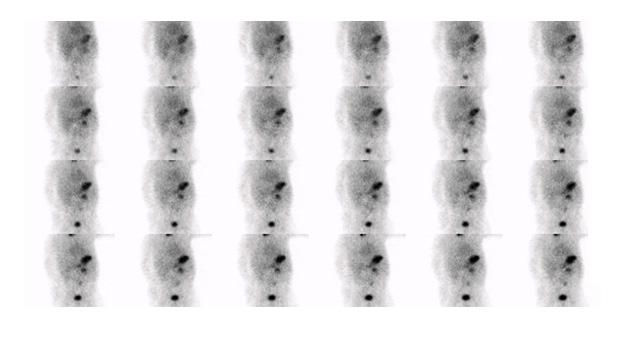
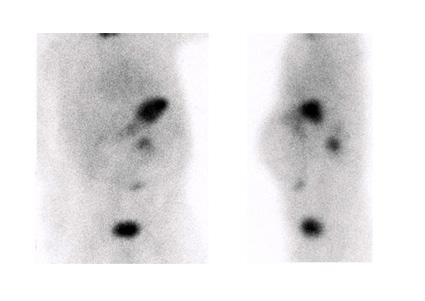
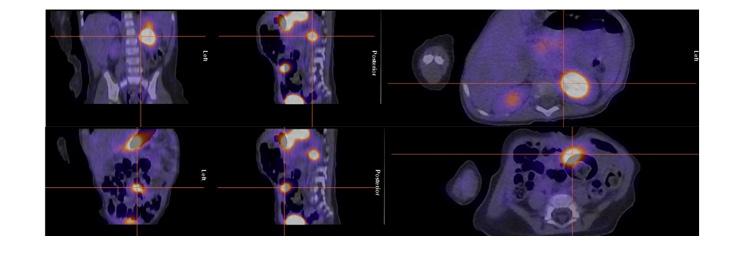
Figure 9 : Patiente de 8 mois avec épisodes de méléna et un épisode de rectorragie amenant une consultation à l’urgence. Deux foyers de captation dont un est rénal, mieux identifié sur le cliché latéral (flèche mince), qui diminue au cours du temps et le second est suspect malgré sa localisation paramédiane gauche (flèche épaisse), qui augmente en parallèle avec l’ estomac. Opérée le jour même avec résection d’un Meckel proche de l’ombilic. Étude dynamique ( A ) et statiques (B) en incidences antérieure et latérale gauche, et images de fusion SPECT-TDM (C).
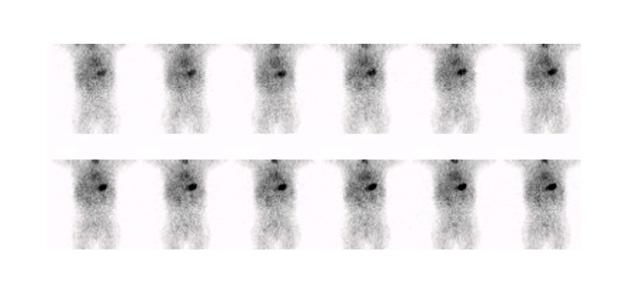
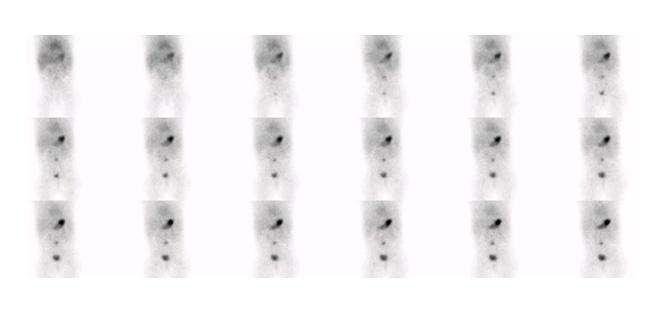
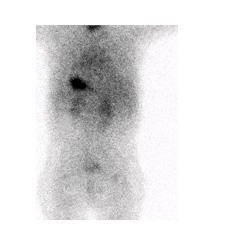
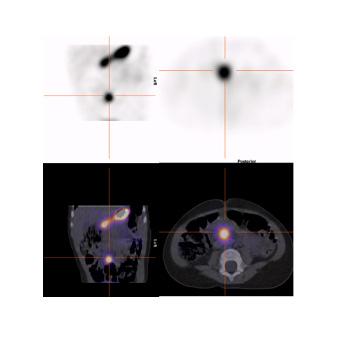
Figure 10 : Patiente présentant des épisodes de vomissements récidivants depuis l’âge de 2 mois, diminué sous ranitidine. Première scintigraphie en phase dynamique ( A ) et statique ( B ) à l’âge de 7 mois sous prise chronique de Ranitidine démontrant un foyer pouvant être un Meckel versus élution à l’hypochondre droit (flèche). SPECT-TDM non diagnostic. Seconde étude également sous prise chronique de Ranitidine à l’âge de 9 mois, douteuse au même site versus négative (non montrée). À l’âge de 14 mois la patiente se représente avec un épisode de rectorragie aigue. Étude dynamique (C) et SPECT-TDM (D) effectués avec administration préalable de Ranitidine intraveineuse démontrant un foyer de captation de localisation différente des études précédentes (flèche). Mise en évidence à la chirurgie d’un diverticule de Meckel de 24 mm avec muqueuse gastrique et inflammation chronique.
1 – An J, Zabbo CP. Meckel Diverticulum. StatPearls, Treasure Island (FLO StatPearls Publishing, 2025), PubMed.
2 – Uppal K, Tubbs RSM, Matusz P, et al Meckel’s diverticulum: a review. Clin Anat. 2011; 24(4):416-422. doi:10.1002/ca.21094
3 – Anand S, Aleem A. Duplication Cyst. StatPearls, StatPearls Publishing, 2025. PubMed.
4 – Scagnol I, Detry O, De Leval L, et al Confrontation anatomo-clinique: duplication caecale [Anatomo-clinical comparison: caecal duplication cyst], Rev Med Liege. 2007 Feb; 62(2):118-21. French. PMID:17461302.
5 – Ueberrueck T, Meyer L, Koch A, et al The significance of Meckel’s diverticulum in appendicitis-a retrospective analysis of 233 cases, World J Surg 2005; 29:455.
6 – Slívová I, Vávrová Z, Tomášková H, et al Meckel’s Diverticulum in Children-Parameters Predicting the Presence of Gastric Heterotopia, World J Surg 2018; 42:3779.
7 – Lohsiriwat V, Sirivech T, Laohapensang M, et al Comparative study on the characteristics of Meckel’s diverticulum removal from asymptomatic and symptomatic patients: 18-year experience from Thailand’s largest university hospital, J Med Assoc Thai 2014; 97:506.
8 – Park JJ, Wolff BG, Tollefson MK, et al Meckel diverticulum: the Mayo Clinic experience with 1476 patients (1950-2002) Ann Surg 2005; 241:529.
9 – Yamaguchi M, Takeuchi S, Awazu S. Meckel’s diverticulum. Investigation of 600 patients in Japanese literature, Am J Surg 1978; 136:247.
10 – Sinha CK, Pallewatte A, Easty M, et al Meckel’s scan in children: a review of 183 cases referred to two paediatric surgery specialist centres over 18 years. Pediatr Surg Int 2013; 29:511.
11 – Chaudhuri T, Polak JJ. Autoradiographic studies of distribution in the stomach of 99mTc-Pertechnetate, Radiology, 1977; 123:223-4.
12 – Emamian SA, Shalaby-Rana E, Majd M. The Spectrum of Heterotopic Gastric Mucosa in Children Detected by Tc-99m Pertechnetate Scintigraphy. The Spectrum of Heterotopic Gastric Mucosa in Children Detected by Tc-99m Pertechnetate Scintigraphy, Clin Nucl Med 2001; 26:529-535.
13 – Sagar J, Kumar V, Shah DK. Meckel’s diverticulum: a systematic review, J R Soc Med, 2006; 99:501-5.
14 – Yan P, JianG S. Tc-99m scan for pediatric bleeding Meckel diverticulum: a systematic review and meta-analysis, J Pediatr (Rio J) 2023; 99:425.
15 – García-Blázquez V, Vicente-Bártulos A, Olavarria-Delgado A, et al Accuracy of CT angiography in the diagnosis of acute gastrointestinal bleeding: systematic review and meta-analysis, Eur Radiol 2013; 23:1181.
16 – Stephanie E. Spottswood (Chair), Thomas Pfluger (Cochair), Stephen P. Bartold, et al SNMMI and EANM Practice Guideline for Meckel Diverticulum Scintigraphy 2.0, J Nucl Med Tech 2014; 42:163-169.
17 – Chin J, Vali R, Charron M, Shammas A. Update on Pediatric Nuclear Medicine in Acute Care, . Semin Nucl Med. 2023; 53:820-839.
18 – Kwok CG, Lull RJ, Yen CK, et al Feasibility of Meckel’s scan after RBC gastrointestinal bleeding study using in-vitro labeling technique, Clin Nucl Med. 1995; 20:959-61.
19 – Yen CK, Lanoie Y. Effect of stannous pyrophosphate red blood cell gastrointestinal bleeding scan on subsequent Meckel’s scan, Clin Nucl Med, 1992; 17:454-6.
20 – Gültekin A, Şengöz T, Demirezen S, et al Can Pantoprazole be Used for Premedication in Meckel Scintigraphy? Mol Imaging Radionucl Ther. 2024; 33:90-93.
21 – Ververs TF, Lobbezoo AH, Hobbelink MG, et al Patient Preparation with Esomeprazole Is Comparable to Ranitidine in Meckel Diverticulum Scintigraphy, J Nucl Med Technol. 2023; 51(3):211-214.
22 – 2024 Update of the North American Consensus Guidelines for Pediatric Administered RP Activities. Consulté le 25 février 2025.
23 – Pirayesh E. Obscured Meckel’s, Diverticulum by the Urinary Bladder: The Value of Lateral View and Post Void Images Clin Nucl Med. 2020; 45(6):487-488.
24 – Koç ZP, Özcan PP, Tuncel F, et al SPECT/CT in the Diagnosis of Ectopic Gastric Mucosa-Meckel’s Diverticulum World J Nucl Med. 2024 Jun 11; 23(3):176-179.
FIGURES
1 à 10 – Banque du CHU Ste-Justine.
Radiooncologie
LES AVANCÉES TECHNOLOGIQUES ET LA VISION DE NOTRE ÉQUIPE MÉDICALE A PERMIS D’OFFRIR UN TRAITEMENT DE POINTE AUX PATIENTS DE NOTRE RÉGION

Quiconque travaille en radio-oncologie vous dira que les innovations technologiques sont chose commune. L’augmentation de la vitesse des calculs grâce à l’informatique y est pour beaucoup. Il n’y a pas si longtemps encore, on validait les temps d’irradiation avec des calculs manuels en un point, directement à la salle de traitement.
Puis les scans ont fait leur entrée en radio-oncologie, avec l’amélioration des planificateurs de traitement, qui pouvaient prendre en charge ces images et associer une densité aux pixels, permettant ainsi d’être plus précis quant à la dose déposée dans toute la zone irradiée.
S’en est suivi l’ajout de l’imagerie à même les accélérateurs linéaires, augmentant la précision du traitement, amenant la réduction des marges et l’augmentation des doses de radiation, pour un meilleur contrôle local et une baisse des effets secondaires.
Malgré tout, certains types de traitements n’étaient disponibles que dans les centres universitaires, en raison de leur complexité et des calculs à faire. C’était le cas pour le traitement des métastases cérébrales.
Voyons d’abord ce que sont les métastases cérébrales. Il s’agit de tumeurs secondaires dans le cerveau, provenant d’un cancer situé ailleurs dans le corps. Les deux principaux cancers aptes à générer des métastases au cerveau sont : les cancers du poumon et les cancers du sein (figure 1 ).
Ces deux types de cancers sont assez communs. De nos jours, beaucoup de traitements, soit par chirurgie, chimiothérapie, immunothérapie ou radiothérapie, sont disponibles, assurant un contrôle local ou systémique de la maladie.
Malgré un meilleur contrôle de ces cancers, il arrive que les patients développent des métastases cérébrales.
Pour les patients atteints d’un cancer pulmonaire ou du sein, un suivi régulier est mis en place, soit par une surveillance des symptômes ou par des IRM cérébrales aux trois à six mois. C’est de cette façon qu’on réussit à détecter les tumeurs secondaires rapidement.
Comment traite-t-on les métastases cérébrales ?
Les traitements habituellement offerts sont la chirurgie ou la radiothérapie. La chirurgie étant réservée à une métastase unique et chirurgicalement bien placée, la radiothérapie est disponible pour les métastases multiples. Les métastases cérébrales se traitent en radio-oncologie depuis un bon moment déjà. La technique standard était de placer deux champs parallèles et opposés (deux latéraux) et d’y inclure tout l’encéphale, en évitant les yeux ainsi que la bouche (figure 2 ).
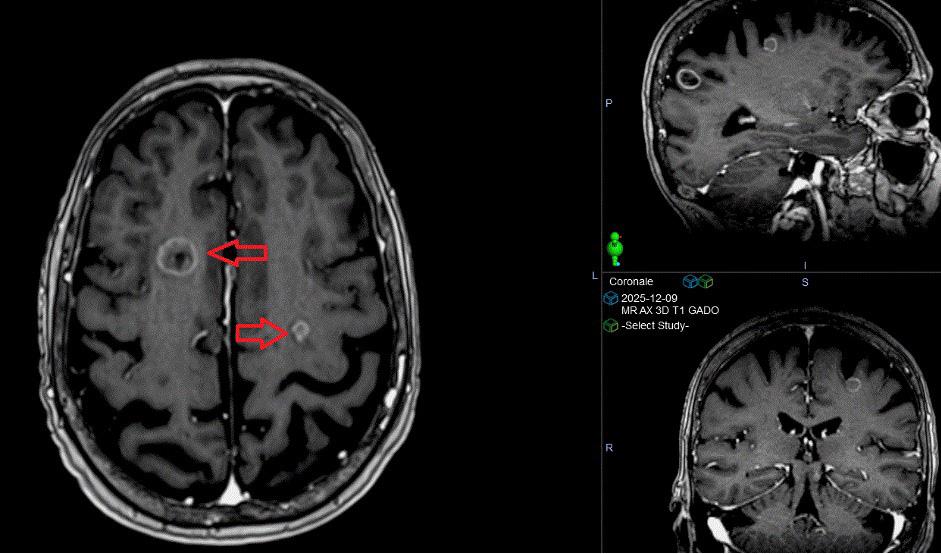
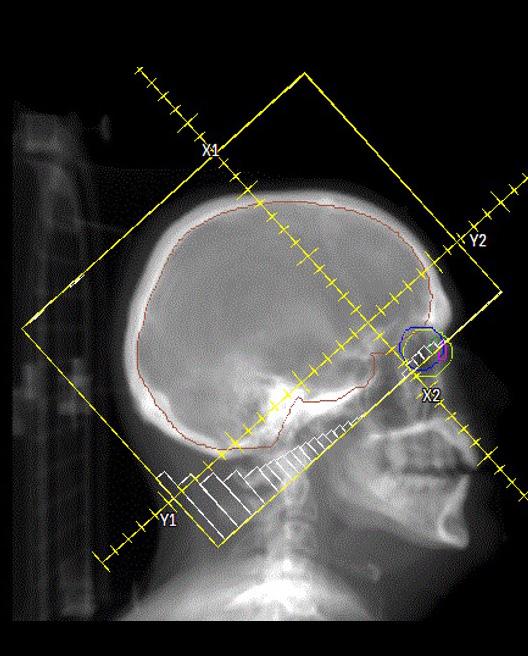
Avec le temps, les moyens de contention du patient se sont améliorés, en passant d’un ruban adhésif sur le front à un masque personnalisé de thermoplastique (ou Kevlar).
À la fin des années 1990, en radio-oncologie, certains centres universitaires ont commencé à développer le traitement des métastases uniques. En région, comme la nôtre, peu de nos patients acceptaient de s’exiler pour recevoir ce type de traitement. Bien que les effets secondaires sont moindres et que l’espérance de vie a légèrement augmenté, cela ne parvenait pas à les convaincre.
Quels sont au juste les effets secondaires d’une irradiation complète de l’encéphale ? Les effets trouvés sont une fatigue importante, des nausées et parfois des vomissements, la perte de cheveux et la possibilité de voir augmenter des symptômes neurologiques à cause des tumeurs. De plus, à moyen terme peuvent s’ajouter des troubles cognitifs. Tous ces effets ne sont pas à négliger, et il était pertinent pour nous de pouvoir offrir un traitement plus ciblé, plus efficace générant moins d’effets secondaires.
Il y a quelques années déjà, grâce au travail minutieux de l’équipe de physique et de l’équipe médicale, nous avons mis au point un traitement ciblé des métastases cérébrales. Avec l’équipement dont nous disposions, il nous était cependant difficile de réussir à traiter plus de trois métastases à la fois, et nous ne pouvions traiter une métastase avec un diamètre inférieur à 8 mm.
Les accélérateurs que nous possédions n’étaient pas munis d’une table à correction 6D pour ajuster le positionnement du patient; ainsi, chaque métastase devait avoir son propre isocentre (axe de rotation du faisceau) et devait être irradiée individuellement. Cela augmentait le temps du traitement de façon très significative et complexifiait le calcul, car nous devions considérer l’apport de dose d’une tumeur à l’autre.
De plus, les marges sécuritaires à un bon traitement étant de 3 mm, cela augmentait le risque de radionécrose. Pour réduire ce risque, la dose était délivrée en cinq fractions.
Toutefois, le gain était quand même très intéressant pour les patients, soit une diminution des effets secondaires, un contrôle local plus efficace et, surtout, une amélioration de leur qualité de vie. À ce moment, c’était la possibilité la plus intéressante que nous pouvions offrir à nos patients qui désiraient rester en région. Puis vint le temps de changer notre flotte d’accélérateurs. Avec l’arrivée de nouveaux accélérateurs et d’un nouveau logiciel de planification de traitements, nous avons vu là l’occasion d’améliorer notre offre de traitements.
Certains investissements ont dû être faits, soit l’achat d’une table 6D, un système de contention Encompass, l’obtention de la licence HyperArc pour le logiciel de planification, l’ajout du système de guidage de surface Identify, ainsi que du temps
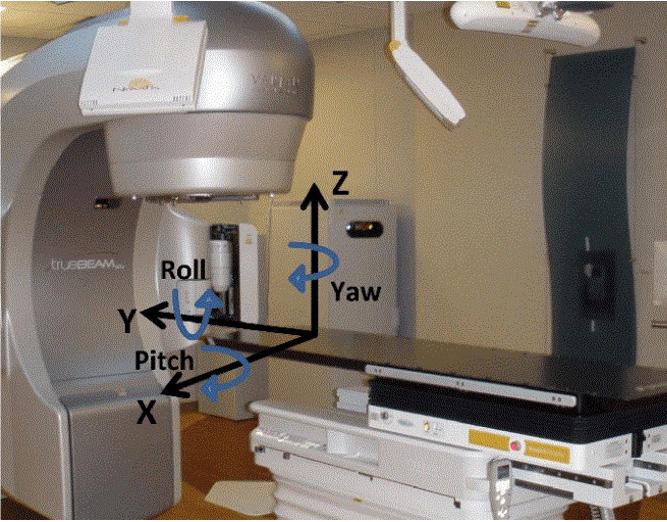
de mesure aux appareils par l’équipe de physique pour mettre en service les très petits champs (figure 3).
En quoi ces investissements ont-ils amélioré notre offre de services ? La table 6D permet, en plus des mouvements habituels de translation latérale, longitudinale et verticale, des mouvements de rotation gauche-droite (roulis), ainsi que de tête-pied (tangage). Elle permet ainsi de corriger la position du patient lors du traitement, pour identique à la position lors du SCAN de planification.
Le système d’immobilisation de la tête et du cou non invasif Encompass, hautement rigide et de haute précision, permet une précision sous-millimétrique et il est essentiel pour l’utilisation du planificateur HyperArc. C’est une feuille de Kevlar, munie d’un arceau chauffé; ainsi ramollie, elle épouse la forme de la tête du patient, et obtient de cette manière un moyen de contention confortable et efficace (figure 4).
Le système de guidage de surface utilise des caméras orientées vers le patient et qui surveillent ses mouvements volontaires ou involontaires. En cas de mouvement, le système avise l’équipe de technologues, qui peuvent ainsi arrêter l’irradiation, imager de nouveau avant de reprendre le traitement (figure 5).
Finalement, la licence HyperArc s’ajoute au système de planification Eclipse, qui, avec l’utilisation obligatoire du système Encompass, détecte le patient dans son environnement et place les faisceaux (arcs) d’irradiation de façon à éviter les collisions, en plus de déterminer leurs parcours angulaires, de sorte que la dose soit distribuée de façon efficace, en étant très
La table 6D
permet, en plus des mouvements habituels de translation latérale, longitudinale et verticale, des mouvements de rotation gauche-droite (roulis), ainsi que de tête-pied (tangage).
conforme à la tumeur et en évitant de doser le reste du cerveau sain et les autres organes (figure 6).
La mise en service de ces nouveautés nous a permis d’améliorer l’offre de traitements pour les patients atteints de métastases cérébrales, uniques et multiples. Avec HyperArc, on a la possibilité d’inclure de multiples métastases, peu importe leur grosseur, dans un même plan (figure 7 ).
Un seul isocentre englobe les métastases; les mâchoires de l’appareil s’adaptent à l’ouverture des lames du collimateur. Jadis, on se limitait à un maximum de trois ou quatre métastases, car cela nécessitait plusieurs dosimétries (plan de calcul). Il fallait concilier la somme de tous ces plans, sans oublier le temps du traitement pour le patient, qui pouvait facilement passer plus de deux heures immobilisé sur la table de traitement.
Ces nouvelles précisions ont permis à l’équipe médicale de réduire les marges de sécurité (PTV). Nous sommes partis des marges de 3 mm à des marges de 1 mm pour le traitement des métastases uniques, et de 1 à 2 mm pour le traitement de multiples métastases. Cette réduction des marges a pour but de diminuer les risques de radionécrose, et permet aussi d’augmenter la dose et de passer de cinq à trois, et même à une fraction de dose. En décidant de réduire les marges, nous avons aussi mis en place un protocole 48 heures. Cela signifie que 48 heures doivent au maximum s’écouler entre l’imagerie de planification et le traitement. Avec une marge de PTV de 1 à 2 mm, on ne veut pas risquer que la ou les métastases augmentent de volume entre la planification et le traitement.
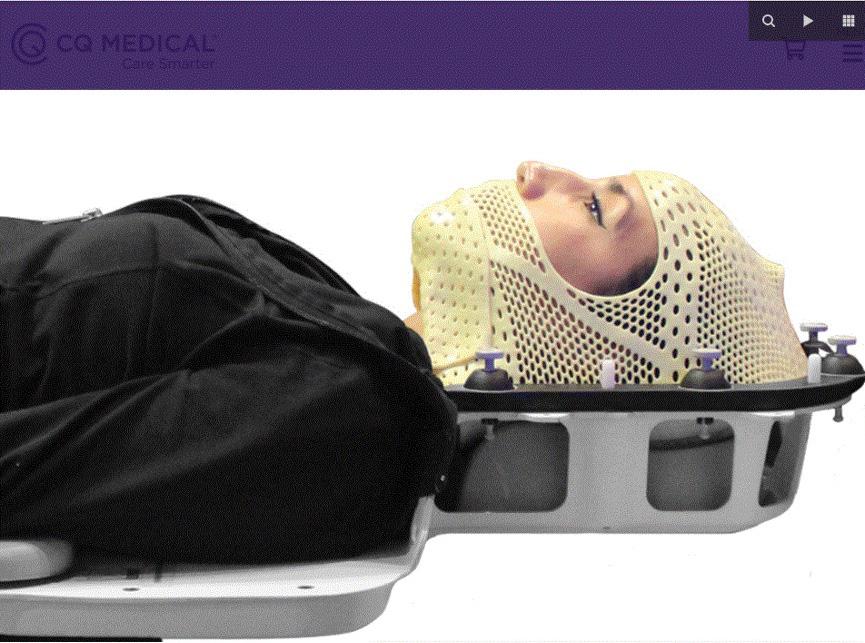

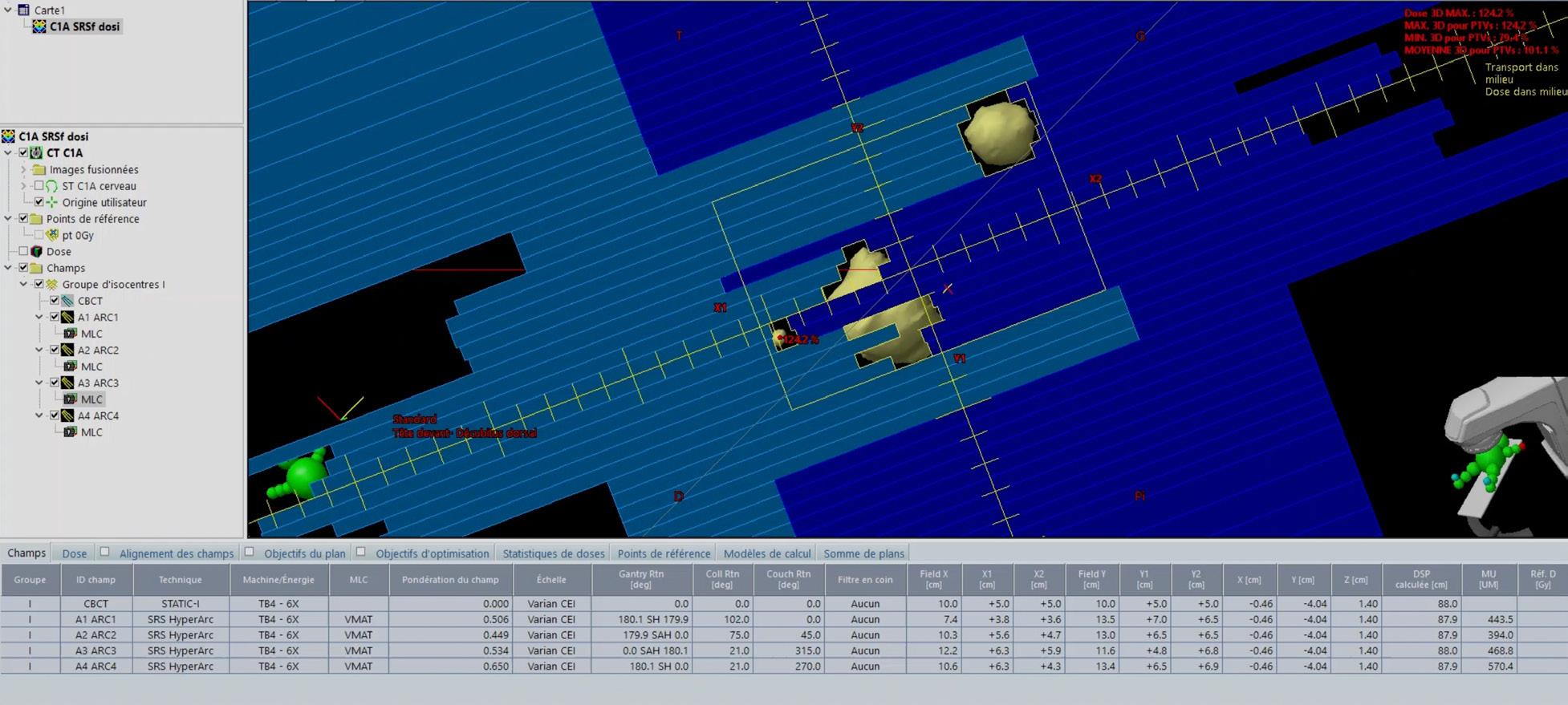
Grâce à la participation du Département de l’imagerie médicale, une plage horaire nous est consacrée chaque semaine. Le protocole en place va comme suit : d’abord le scan de planification, suivi d’une IRM cérébrale, de la dosimétrie (planification de la dose), de la vérification du plan, et pour finir, de la mise en traitement, le tout en moins de 48 heures.
Avec l’utilisation d’HyperArc pour la planification, tout ce qui se passe à l’appareil de traitement se trouve aussi optimisé. Une fois le patient installé sur la table
de traitement, le positionnement fait à partir du CBCT (Scan à partir d’un accélérateur) et corrigé avec les mouvements en 6D, la fonction HyperArc s’enclenche, c’est-à-dire que tous les arcs de radiation se suivent, l’un après l’autre, de façon automatique. Les technologues surveillent les informations fournies par Identify, portant sur les modifications du contour externe du patient, pouvant ainsi arrêter le traitement advenant un mouvement volontaire ou involontaire de sa part.
Pour une métastase unique, toutes ces nouveautés ont augmenté la rapidité du traitement, passant de 60 min à plus ou moins 20 min. Mais c’est surtout pour les multiples métastases que la rapidité du traitement est surprenante, passant de plus de 2 h à moins de 30 min.
Il ne faut surtout pas oublier que le principe d’inclure plusieurs métastases dans un même plan, en plus de l’automatisation, a réduit considérablement le temps à passer sur la table de traitement. Pour une métastase unique, toutes ces nouveautés ont augmenté la rapidité du traitement, passant de 60 min à plus ou moins 20 min. Mais c’est surtout pour les multiples métastases que la rapidité du traitement est surprenante, passant de plus de 2 h à moins de 30 min.
Nous pouvons dire : « mission accomplie ». Maintenant, nous disposons d’un traitement qui va améliorer la qualité de vie, beaucoup moins invasif et pratiquement sans effets secondaires.
Tout cela a été possible grâce à une vision d’avenir des équipes médicale, de physique, technique ainsi que de l’administration, qui a su voir la possibilité d’une amélioration de la qualité des soins par l’achat de quelques modules supplémentaires, lors de l’acquisition de nouveaux équipements.
Grâce aux avancées technologiques, nous pouvons maintenant offrir un service à la fine pointe de la technologie pour les patients de notre région.
REMERCIEMENTS
Merci à l’équipe médicale de vouloir offrir des traitements de pointes, à l’équipe de physique de tout mettre en œuvre pour y arriver, aux coordonnateurs de traitements pour arrimer le tout et à tous les technologues de toujours vouloir être à la hauteur des multiples défis, tout ça pour le bien être de notre population.
RÉFÉRENCES
1 et 2 – Banque personnelle de l’Hôpital de Chicoutimi.
3 – Journal of Applied Clinical Medical PhysicsOpen Access 17(3): p 111-127, May 2016., consulté le 06-03-2026.
4 – Image publicitaire de CQ MEDICAL , consulté le 06-03-2026.
5 – Image publicitaire de VARIAN, consulté le 06-03-2026.
6 et 7 – Simulation local d’HypeArc.
Radiooncologie
COMMENT UNE STARTUP NÉE DANS LES LABORATOIRES DE L’UNIVERSITÉ LAVAL SE HISSE AU SOMMET MONDIAL DE LA DOSIMÉTRIE PAR SCINTILLATION


Dans un contexte où la radiothérapie évolue vers des traitements toujours plus précis et personnalisés, les outils d’assurance qualité doivent suivre la cadence. Medscint, une entreprise 100 % québécoise, fondée à Québec en 2018, s’est positionnée comme chef de file mondial dans le développement de solutions de dosimétrie par scintillation. Pour les centres de radio-oncologie du Québec, cette innovation représente bien plus qu’une avancée technologique : c’est une fierté locale qui contribue directement à la recherche dans le domaine de la radiothérapie et à l’amélioration des traitements qui y ont cours.
Une startup née de la recherche en physique médicale
Medscint est le fruit de plusieurs années de recherche en physique médicale, menée à l’Université Laval-CHU de Québec et à l’Université du Texas-MD Anderson Cancer Center, particulièrement autour de la dosimétrie par scintillation en radiothérapie. L’entreprise est directement issue des travaux doctoraux de son cofondateur, président et CEO François Therriault-Proulx, Ph. D., axés
sur une nouvelle manière de mesurer la dose de radiation en temps réel grâce à la technologie des scintillateurs.
François a cofondé l’entreprise avec Simon Lambert-Girard, Ph. D., ing. et Jonathan Turcotte, ing. MBA, en 2018, avec pour mission de commercialiser cette innovation afin d’améliorer la précision des traitements par radiothérapie, tout en simplifiant la vie des physiciens médicaux en clinique et dans leurs projets de recherche. La vision de l’entreprise va plus loin encore : faire croître Medscint à l’échelle mondiale pour en faire un véritable fleuron technologique canadien dans le domaine du contrôle de la qualité en radio-oncologie.
Une présence mondiale — et déjà ancrée au Québec
La reconnaissance internationale de Medscint ne s’est pas fait attendre. Leurs solutions sont aujourd’hui utilisées par des chercheurs en radiothérapie dans 15 pays. L’enregistrement clinique obtenu à l’automne 2025 auprès de la Food and Drug Administration américaine – les États-Unis étant le plus

Figure 1 : Medscint compte aujourd’hui une douzaine d’employés et de multiples collaborateurs universitaires. Voici un portrait d’une partie de l’équipe présente sur le site lors de la visite d’ÉchoX. De gauche à droite : Raphaël Brodeur, François Therriault-Proulx, Alec Vincent, Yoan LeChasseur, Raphaël Larouche, Boby Lessard, Jonathan Turcotte, Louis Archambault et Simon Lambert-Girard.
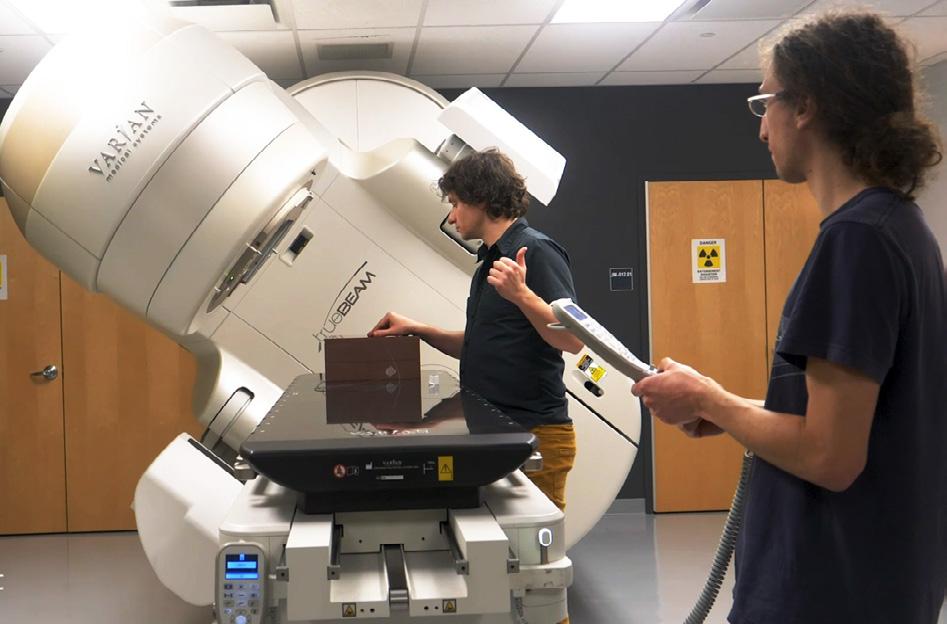
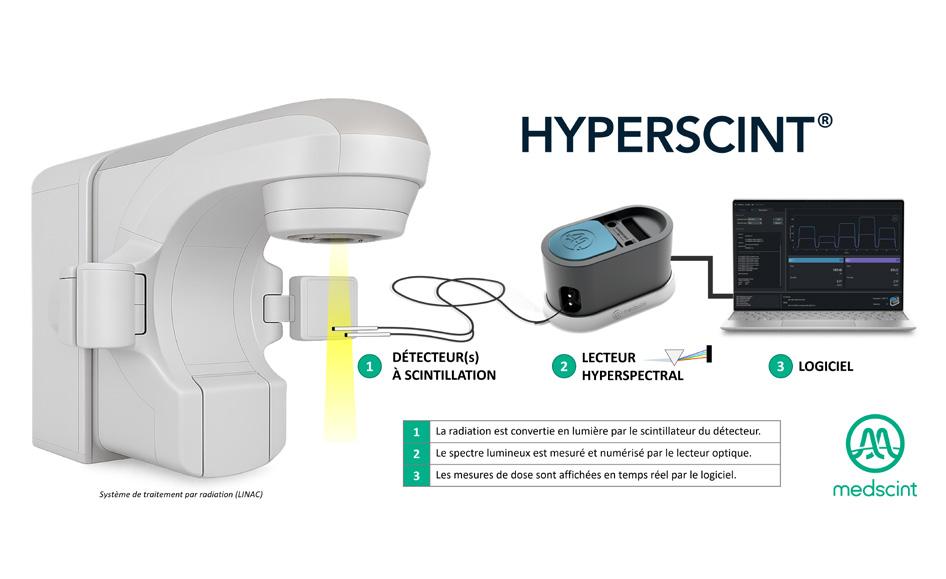
3 : Schéma explicatif de la solution de dosimétrie HYPERSCINT développée par Medscint pour la radiothérapie.
grand marché de la radiothérapie au monde – ouvre la porte à une commercialisation élargie aux États-Unis, au Japon et en Corée du Sud. Le Canada et les pays européens sont également dans la mire de l’entreprise, qui travaille en parallèle avec des partenaires réglementaires pour obrir le plus rapidement possible ses solutions à ses compatriotes canadiens.
À l’échelle provinciale, la moitié des 14 centres de radiothérapie du Québec ont déjà fait l’acquisition de la technologie HYPERSCINT. Cette adoption témoigne de la confiance et du soutien de la communauté scientifique envers cette innovation d’ici.
La collaboration entre Medscint, le CHU de Québec et le Cégep de Sainte-Foy illustre bien cette synergie entre industrie, clinique et enseignement. Les équipements de pointe du Cégep, dont un accélérateur linéaire à la fine pointe de la technologie, ont permis à l’entreprise de tester et de développer sa technologie dans des conditions similaires à celles des plus grands centres du monde. L’équipe multidisciplinaire du Cégep a également apporté un soutien précieux au projet, notamment en obrant des formations en radioprotection, en prodiguant des conseils sur l’utilisation des équipements et les pratiques du milieu et en soutenant des projets de recherche utilisant les technologies de Medscint. L’accès privilégié à cet accélérateur linéaire, moins sollicité que dans une clinique conventionnelle, a constitué un avantage déterminant. Le Centre collégial de transfert de technologie (CCTT) du Cégep a de surcroît contribué au développement logiciel de la solution, un exemple remarquable de partenariat entre l’industrie et le secteur de l’enseignement.
La technologie expliquée : les détecteurs à scintillation fibrés
Le principe de la dosimétrie par scintillation se distingue par la simplicité de sa conception : lorsqu’un scintillateur est stimulé par un rayonnement ionisant, il émet instantanément, en quelques nanosecondes, une quantité de photons optiques proportionnelle à l’énergie reçue. Ces photons sont ensuite acheminés par fibre optique vers un système de mesure de précision.
Ce qui distingue Medscint, c’est non seulement le design unique de ses détecteurs à scintillation, mais aussi l’utilisation d’un mode de lecture brevetée – dit « hyperspectral » – de la lumière. Par une analyse spectrale évoluée, basée sur un assemblage optomécanique, électronique et logiciel innovant développé
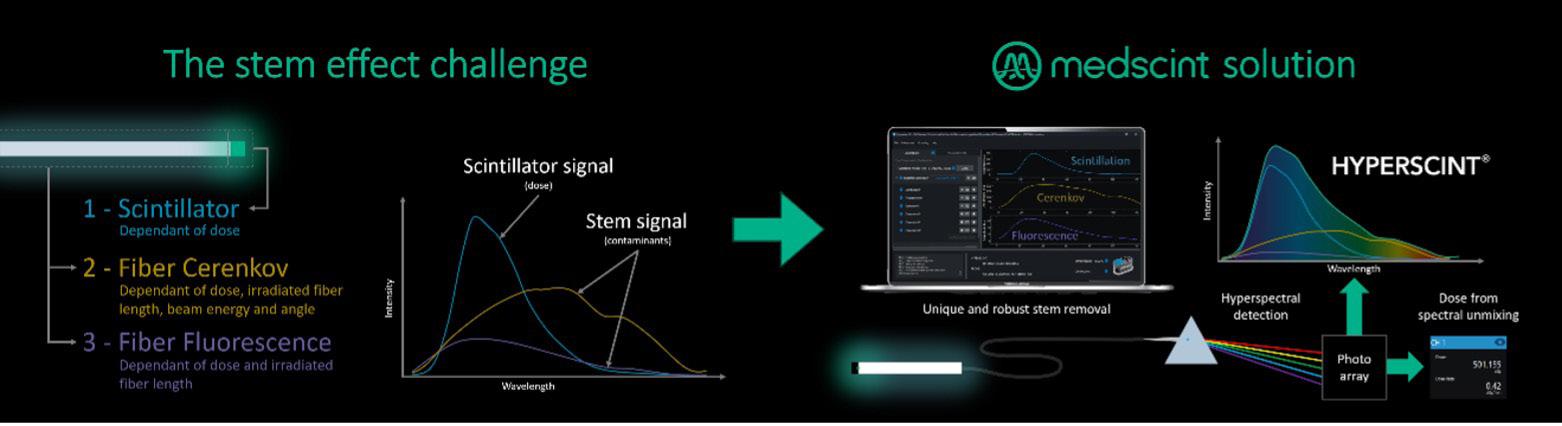
Figure 4 : Schéma descriptif du défi d’isoler les signaux optiques d’un détecteur à scintillation ( stem effect challenge) et la solution brevetée dite « hyperspectrale » développée par Medscint (à droite).
par Medscint, HYPERSCINT sépare mathématiquement la lumière du scintillateur – proportionnelle à la dose – de la lumière Cerenkov* provenant de la fibre optique – signal indésirable. Grâce à cette déconvolution spectrale, Medscint obtient en temps réel une mesure de dose pure, précise, indépendante de la géométrie et parfaitement adaptée aux techniques modernes de radiothérapie, là où les détecteurs traditionnels atteignent leurs limites.
* Cerenkov Radiation (souvent écrit Tcherenkov en français) est un phénomène physique où une lumière bleutée est émise lorsqu’une particule chargée (comme un électron) traverse un milieu plus vite que la vitesse de la lumière.
Finalement, contrairement aux autres approches de dosimétrie par scintillation développées au fil des dernières années, l’approche spectrale brevetée de Medscint permet d’utiliser une seule calibration pour gérer la grande majorité des cas d’irradiation en radiothérapie. Elle est de loin plus robuste, polyvalente et précise tout en étant simple d’utilisation.
Cinq avantages qui changent la donne
Les détecteurs HYPERSCINT se distinguent des outils traditionnels par cinq caractéristiques fondamentales :

Figure 6 : Image radiographique haute résolution comparant le design unique, entièrement plastique et quasi « radio-transparent » d’une sonde Medscint avec celui de détecteurs électroniques traditionnels couramment utilisés en radiothérapie.
1. Équivalence à l’eau
Le design entièrement plastique utilise des matériaux dont les propriétés physiques sont quasi équivalentes à l’eau. Ce design unique ne perturbe pratiquement pas le faisceau de rayonnement. Les mesures reflètent ainsi fidèlement la dose déposée dans les tissus – une condition essentielle pour des mesures cliniques réalistes.
2. Taille millimétrique, précision maximale Avec un volume sensible de détection sous le 1 mm³, le détecteur HYPERSCINT offre une
précision spatiale exceptionnelle – particulièrement critique dans le contexte des techniques modernes de radiochirurgie et de radiothérapie stéréotaxique, qui font aujourd’hui partie du quotidien en radio-oncologie.
3. Indépendance énergétique et angulaire
Contrairement aux détecteurs traditionnels, comme les diodes, dont la réponse varie grandement selon l’angle d’incidence, les détecteurs
HYPERSCINT maintiennent une réponse uniforme et acceptable, quelle que soit l’orientation ou l’énergie du faisceau provenant d’un LINAC conventionnel haute-énergie (MV). Fini les corrections complexes : les mesures sont fiables d’emblée.
4. Dosimétrie à de multiples points
La solution HYPERSCINT permet de mesurer la dose à plusieurs emplacements simultanément grâce à la lecture parallèle de dibérents canaux d’acquisition. Cet avantage unique obre aux utilisateurs une vue détaillée, améliorant ainsi la précision du contrôle qualité pour des plans comportant plusieurs cibles ou régions d’intérêt.
5. Dosimétrie en temps réel
Avec une réponse de l’ordre de quelques nanosecondes, le détecteur assure une acquisition continue durant l’irradiation. Le physicien bénéficie ainsi d’un retour immédiat tout en intégrant la dimension temporelle à ses mesures, ce qui améliore la compréhension du faisceau et optimise l’évaluation dosimétrique. Cela constitue un atout majeur dans le contexte des pratiques adaptatives de plus en plus présentes en clinique.
Pour bien comprendre ces avantages, il est essentiel de reconnaître les limites des détecteurs traditionnels. Les diodes et chambres d’ionisation, par exemple, reposent sur la mesure de charges électriques par des composantes métalliques qui perturbent inévitablement le faisceau dans le milieu de mesure. Cette interaction impose aux physiciens l’application de nombreux facteurs de correction dépendant à la fois du design du détecteur (p. ex. volume sensible, matériaux, etc.) et des conditions d’irradiation (p. ex. angle d’incidence, énergie, température, pression atmosphérique, etc.). Quant aux détecteurs passifs, comme les films Gafchromic, leur précision est fortement influencée par les conditions de conservation, de calibration et de lecture, en plus d’exiger des délais d’analyse pouvant aller jusqu’à plusieurs jours avant d’obtenir un résultat exploitable.
Là où les détecteurs traditionnels exigent des corrections souvent complexes, le dosimètre
HYPERSCINT de Medscint offre une mesure rapide, précise et directement exploitable.
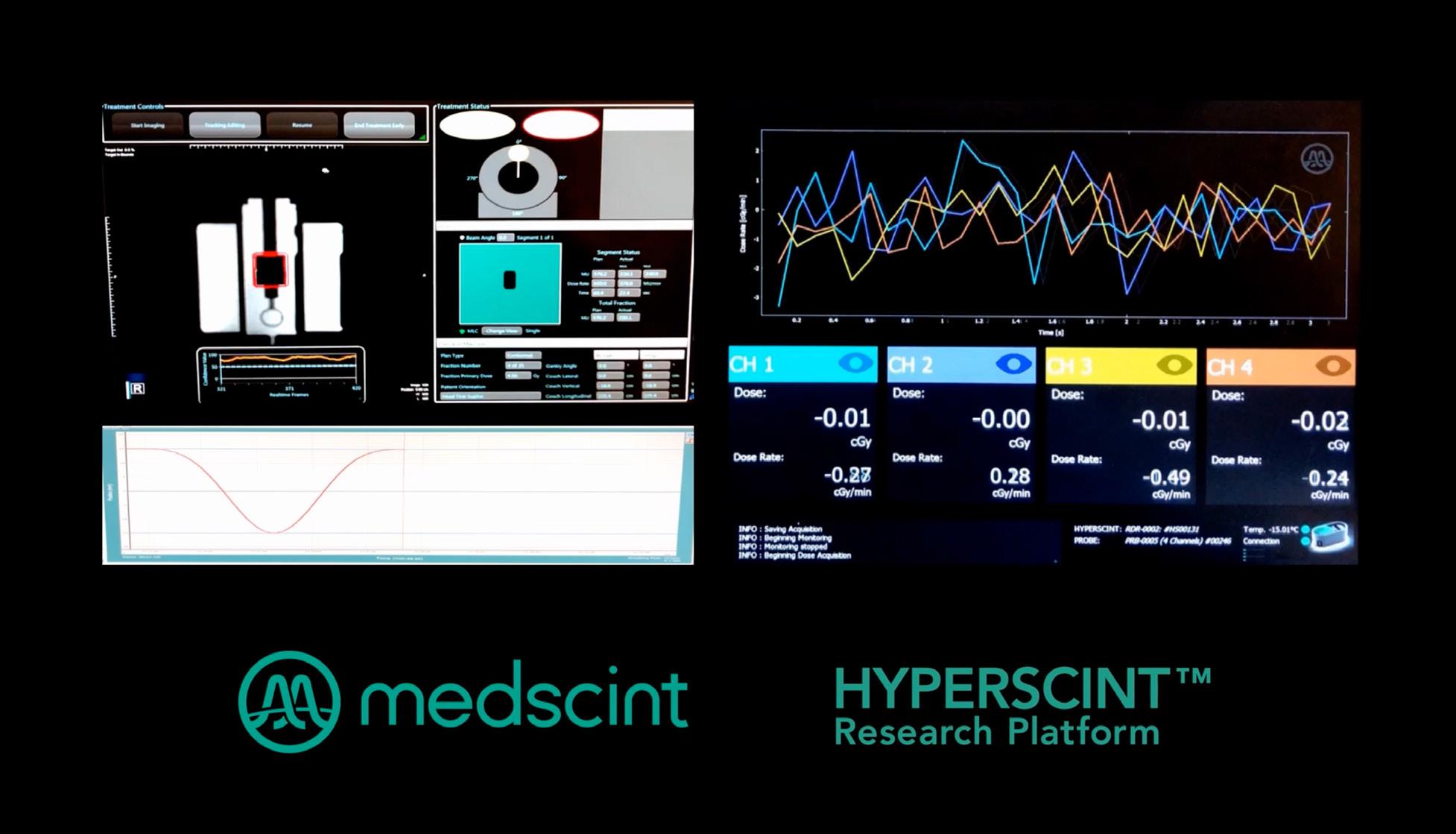
Dans les techniques modernes, comme l’IMRT, la VMAT, les petits champs (simples ou multimétastases) ou les appareils de type MRLinac, la complexité de la méthode amplifie l’influence du design du détecteur sur la mesure. Elle augmente ainsi le risque d’erreurs liées à la directionnalité, au volume sensible ou aux matériaux utilisés. Ces limitations imposent des analyses plus longues et contribuent à accroître l’incertitude globale des mesures de contrôle qualité.
La technologie optique développée par Medscint élimine la plupart de ces contraintes. Faite de plastique et dépourvue de composante électronique, elle perturbe minimalement le faisceau et ne nécessite aucun facteur de correction. Compact et précis, le détecteur HYPERSCINT est également indépendant de l’angle et de l’énergie, tout en obrant des mesures multipoints en temps réel – une combinaison idéale pour les irradiations complexes. Le bénéfice est tangible : un contrôle de qualité plus rapide, plus fiable et associé à des incertitudes nettement réduites, particulièrement avantageux pour des systèmes avancés obrant des modalités de radiochirurgie (p. ex. SRS/SBRT ou les CyberKnife et GammaKnife), les MRLinac, ou encore pour optimiser les approches modernes à multiples cibles ou adaptatives. Sans perturbation du faisceau. Sans facteur de correction. En temps réel. Trois réalités qui redéfinissent ce que le contrôle qualité peut offrir en radio-oncologie.
Sans perturbation du faisceau.
Sans facteur de correction.
En temps réel. Trois réalités qui redéfinissent ce que le contrôle qualité peut obrir en radio-oncologie.

Figure 8 : Exemple de collaboration avec l’institution médicale académique
UMC Utrecht (Pays-Bas) et l’entreprise IBA Dosimetry (Allemagne) pour le contrôle de la qualité en temps réel sur phantom à de multiples points lors de la délivrance d’un traitement avec gestion du mouvement sur un MRLinac (Elekta Unity, Sweden).
Des défis dosimétriques relevés pour les techniques avancées
Les techniques modernes de radiothérapie posent des défis particuliers en dosimétrie, et le HYPERSCINT peut aider à faire face à plusieurs de ces défis.
Par exemple, une équipe souhaitant intégrer la radiothérapie stéréotaxique dans son obre de soins doit impérativement bien contrôler les paramètres physiques des petits champs (faisceaux de quelques millimètres de diamètre) de sa machine avant de traiter des patients; particulièrement si l’hypofractionnement est envisagé. Pour ce faire, le détecteur de Medscint est tout indiqué, car sa composition équivalente à l’eau et sa taille millimétrique minimisent la perturbation et le moyennage volumétrique, pour des résultats hyper précis.
Pour les traitements dynamiques, comme la VMAT ou l’IMRT, la taille et l’indépendance angulaire et en énergie du détecteur HYPERSCINT constituent un atout majeur. Pour les applications où on ajoute une portion adaptative, l’aspect « temporellement résolu » du détecteur permet de contrôler la qualité du traitement là et quand il est appliqué. Par exemple, le détecteur de Medscint est utilisé par des équipes au Canada, aux États-Unis et en Europe, conjointement avec des fantômes mécanisés, pour valider les performances de dibérents algorithmes de tracking.
La configuration multipoints représente un autre avantage distinctif. Les détecteurs de la gamme PRO Series sont oberts en modèles à 1, 2 ou 4 canaux, chaque canal étant une tête indépendante au bout d’une fibre optique, avec les mêmes performances que les autres canaux. Le système reconnaît le signal de chaque canal pour livrer une mesure de dose précise, en temps réel et à plusieurs points simultanément – particulièrement
utile pour valider des plans de traitement stéréotaxiques impliquant plusieurs cibles, comme des métastases, ou pour évaluer simultanément la dose à un organe à risque et au volume cible planifié (PTV).
Medscint a également développé plusieurs familles de sondes pour répondre à des besoins spécifiques : la MICRO Series, pour une précision redéfinie dans les ultrapetits champs; la FLEX Series, pour un design compact et polyvalent; la FLASH Series*, conçue pour résister aux accumulations de doses élevées; et les Dosimetry Modules, pour une intégration transparente dans les flux de travail existants.
Qui utilise ces détecteurs et comment ?
Actuellement, ce sont les physiciens médicaux qui gèrent les équipements HYPERSCINT dans les centres de radiothérapie. Leur expertise en physique des rayonnements et en métrologie est sollicitée pour l’utilisation de ces
* La FLASH-thérapie est une technique émergente en radiothérapie qui consiste à délivrer la dose de rayonnement à un débit extrêmement élevé, en quelques millisecondes, plutôt que sur plusieurs secondes ou minutes, comme en radiothérapie conventionnelle.
Avantages potentiels : réduction des toxicités normales; possibilité d’augmenter la dose tumorale; traitement beaucoup plus rapide (quelques millisecondes).
détecteurs sophistiqués. La formation initiale se fait entièrement en ligne, en deux séances de deux heures chacune : une première pour présenter la technologie, le logiciel et la solution dans son ensemble, et une seconde pour accompagner le client lors de sa première utilisation à l’accélérateur linéaire.
Dans les protocoles cliniques, le HYPERSCINT QA est principalement utilisé pour le contrôle de qualité des appareils, notamment lors de la mise en service d’un nouvel accélérateur, au moment des vérifications annuelles et après les maintenances nécessitant de refaire le contrôle de qualité annuel, ainsi que pour la validation des plans de traitement des patients, en particulier dans les programmes de radiothérapie stéréotaxique (SRS/SBRT). En raison de sa nature millimétrique, de son équivalence à l’eau et de l’absence de facteur de correction, le détecteur est particulièrement efficace pour la validation de plans de traitement sur tous types de fantômes, qu’ils soient anthropomorphiques ou non, statiques ou dynamiques.
Dans les prochaines étapes, Medscint poursuit activement le développement de solutions de dosimétrie in vivo pour mesurer la dose directement sur le patient durant le traitement. Dans ce contexte, et selon les protocoles en place dans chaque établissement, les technologues en radio-oncologie pourraient être appelés à participer activement au processus : installation des détecteurs sur le patient et enregistrement des données dans le dossier patient.
L’excellence québécoise au service du patient
Medscint incarne l’excellence de l’innovation québécoise dans un domaine hautement spécialisé. En développant une technologie qui se positionne au sommet mondial, l’entreprise contribue non seulement au rayonnement du Québec sur la scène internationale, mais surtout à l’amélioration concrète des traitements de radiothérapie oberts aux patients.
La vision de Medscint pour l’avenir est claire : développer un réseau de collaborateurs de proximité, des experts de la radiothérapie avec qui concevoir les solutions de dosimétrie optique de demain. Avec une présence dans plus d’une cinquantaine de centres d’excellence à travers le monde, Medscint travaille déjà avec ses partenaires sur les modalités les plus émergentes, comme la radiothérapie à débits de dose ultra-élevés (UHDR ou FLASH), la protonthérapie et des concepts novateurs, comme les Very High Energy Electron (VHEE)*

Figure 9 : Comparaison de la taille d’un détecteur Medscint de la gamme FLEX Series avec un stylo.
Alors que la radiothérapie continue d’évoluer vers des approches toujours plus personnalisées et ciblées, les outils d’assurance qualité doivent suivre le rythme. Simple d’utilisation, performant et polyvalent, le système HYPERSCINT de Medscint propose une solution qui répond aux défis actuels, tout en étant prête à relever ceux de demain. Une chose est certaine : l’avenir de la dosimétrie en radio-oncologie se dessine ici, au Québec.
* Pour les débits de dose ultra-élevés, comme ceux utilisés en radiothérapie FLASH, la technologie Medscint livre des mesures dosimétriques précises, même à d’immenses débits de dose. Cette performance est validée par plus d’une quinzaine de groupes experts en radiothérapie FLASH dans une dizaine de pays. La technologie est également utilisée dans d’autres modalités émergentes, comme la radiothérapie focalisée et les très hautes énergies électroniques (VHEE).
REMERCIEMENTS
Nous tenons à remercier chaleureusement les personnes qui ont rendu cet article possible. Merci à François Therriault-Proulx, Ph. D., PDG et cofondateur de Medscint, ainsi qu’à Jonathan Turcotte, ing. MBA, ingénieur en physique, cofondateur et directeur ventes et du marketing, pour leur disponibilité et la générosité avec laquelle ils m’ont communiqué leur expertise et leur vision. Un merci tout particulier à Mathieu Bergeron, t.r.o. et enseignant au programme de radio-oncologie du Cégep de Sainte-Foy, dont la collaboration a été précieuse pour ancrer cet article.
RÉFÉRENCES
Pour en savoir plus : medscint.com
MIEUX COMPRENDRE CETTE TECHNIQUE ET SON APPLICATION
CONCRÈTE EN MILIEU CLINIQUE
L’angio-mammographie ou mammographie de contraste représente une avancée prometteuse dans le diagnostic du cancer du sein. Pour mieux comprendre cette technique et son application concrète en milieu clinique, nous nous sommes entretenus avec Kelly Chouinard, technologue expérimentée qui pratique régulièrement cet examen. Voici ce qu’elle nous a communiqué.
Aspects techniques de l’examen
Quel est le protocole technique standard utilisé dans votre établissement pour l’angio-mammographie ?
Pour une angio-mammaire, chaque vue nécessite deux expositions. Nous avons la basse énergie (34 kV, 80 mAs) et ensuite la soustraction en haute énergie, avec le colorant (49 kV, 140 mAs).
Quelles sont les incidences réalisées ?
Incidences de base comme mammo régulière ?
Nous procédons à une mammographie standard, soit CC, MLO et CCX ou spot infra, au besoin.
Quels sont les paramètres d’injection du produit de contraste (type, volume, débit) ?
1.5 ml/kg à 3cc/sec. La dose maximale administrée peut varier selon le centre, mais les études disent souvent un maximum de 150cc. Nous ne pouvons pas réduire le débit, donc l’étanchéité de la veine est très importante.
Utilisez-vous un injecteur automatique ?
Si oui, lequel ?
Oui, nous utilisons le système d’injection Empower CTA+ de la compagnie BRACCO, un injecteur automatique portable.


Quel produit de contraste utilisez-vous ?
Nous utilisons du Isovue 370. Éventuellement, nous devrons détenir une deuxième sorte de produit de contraste pour les patientes allergiques à l’iode, mais rien n’est encore fait.
Quel est le délai optimal entre le début de l’injection et la prise de vue ?
Nous devons attendre 2 minutes entre le début de l’injection et la première image. Selon la quantité d’iode injectée, en général, il reste un peu moins d’une minute à la patiente pour retirer sa jaquette, mettre les plombs aux mamelons et se placer devant l’appareil de mammographie. Par la suite, nous avons 5 minutes pour faire l’examen complet.
Le matériel de mammographie utilisé nécessitet-il des adaptations spécifiques (post-traitement, filtres, compression) ?
Pour procéder à une angio-mammographie, vous devez avoir un programme CESM dans la console de mammographie, qui fera l’image soustraite avec le colorant. L’angio-mammographie ne peut pas être faite avec une palette souple.
Comment l’exposition aux rayonnements est-elle optimisée pour cet examen combiné ?
Cette sorte de mammographie donne une dose légèrement plus élevée de rayons (1.2 fois plus élevée), mais elle permet de déceler des lésions dans un sein très dense, qui seraient difficiles à déceler autrement.
Est-ce que la tomosynthèse est nécessaire ou l’image 2D est-elle suffisante ?
Nous ne pouvons pas faire de tomosynthèse avec l’angio-mammographie. L’image 2D et la soustraction sont suffisantes.
Est-ce que vous avez besoin d’une 2e technologue ?
(En France, elles sont 2 pour l’angio-mammographie)
Préférablement, cet examen se fait à 2 technologues, mais il est possible de la faire seule si on possède un injecteur avec une manette qui permet de déclencher l’injection à distance.
Est-ce que vous pouvez faire des angiomammographie sur des spots demandés par le radiologiste à la suite d’une mammographie que la patiente aurait passée (avec ou sans angio) ?
Non, nous faisons des mammographies unilatérales ou bilatérales pour profiter de l’injection. Les patientes qui
possèdent des prothèses mammaires peuvent faire l’examen, mais la partie contenant la prothèse est faite avant l’injection. Seule la portion EKLUND peut être faite en angio-mammographie.
Quelle est la durée complète (temps alloué) pour un examen d’angio-mammographie ?
(sachant qu’une mammo standard dure +/-15 minutes dans la majorité des centres)
Dans notre centre, nous faisons des journées complètes. Notre première patiente de la journée se voit allouer 45 minutes, pour donner le temps à la technologue de monter l’injecteur. Par la suite, nous consacrons 30 minutes à chaque angio-mammographie. La procédure en tant que telle doit durer 5 minutes, temps où le colorant subsiste dans les seins. Cependant, nous avons plus de temps pour revoir le questionnaire d’injection, ainsi que le questionnaire de mammographie, peser la patiente au besoin, installer un cathéter et procéder à l’injection.
L’angio-mammographie est préférable à l’IRM mammaire, puisqu’elle est plus accessible, les délais sont moins longs et l’examen est également moins long.
Si la patiente est allergique à l’iode (réaction allergique sévère), celle-ci sera redirigée vers l’IRM mammaire.
Indications cliniques et place dans le parcours diagnostique
Quelles sont les principales indications de l’angio-mammographie aujourd’hui ?
Une angio-mammographie est prescrite pour la détection des lésions néoplasiques. Il s’agit d’un examen complémentaire à la mammographie et à l’échographie mammaire.
À quelles patientes ne recommanderiez-vous pas cet examen ?
Les patientes souffrant d’une allergie sévère à l’iode ne peuvent pas bénéficier de cet examen, il s’agit de la seule contre-indication absolue. Cet examen pourrait ne pas être possible chez les patientes à mobilité réduite, puisqu’il nous est impossible de les positionner pour une mammographie. Sinon, il est recommandé pour toutes les femmes.
Dans quels cas préférez-vous l’IRM mammaire ?
Et dans quels cas l’angio-mammographie est-elle préférable ?
L’angio-mammographie est préférable à l’IRM mammaire, puisqu’elle est plus accessible, les délais sont
moins longs et l’examen est également moins long. Si la patiente est allergique à l’iode (réaction allergique sévère), celle-ci sera redirigée vers l’IRM mammaire.
Est-ce que cet examen est utilisé en situation de dépistage, ou uniquement dans un contexte diagnostique ?
Pour l’instant, il est utilisé plus en diagnostic et en contrôle d’une lésion qui rehausse.
Comment communiquez-vous les indications au technologue en amont ?
Au besoin, nous laissons des commentaires dans Radimage et dans l’onglet d’allergie.
Rôle et responsabilités du technologue
Quelles compétences spécifiques sont nécessaires pour un technologue qui réalise une angio-mammographie ?
Sans parler de la spécialisation en mammographie, la technologue doit avoir les connaissances pour installer un cathéter au patient, ainsi que les connaissances reliées à une injection de contraste (les effets, les contre-indications et l’aptitude à réagir rapidement en cas d’extravasation). De plus, la technologue doit avoir de l’expérience, ainsi qu’une rapidité d’exécution pour avoir le temps de faire la mammographie au complet dans le petit délai de 5 minutes.
Une formation complémentaire est-elle requise ou recommandée ?
La technologue doit bien connaître son appareil ainsi que le module d’angio-mammographie (CESM). La technologue doit avoir de l’expérience pour faire des mammographies et bien comprendre le fonctionnement de l’angio-mammographie pour être à l’aise lors de l’examen.
Quelles précautions doivent être prises lors de l’installation de la patiente ?
Nous devons nous assurer que la patiente a rempli le questionnaire d’injection, le questionnaire de mammographie et qu’elle ait une voie ouverte résistante à l’injection.
DOCUMENTS À CONSULTER
Questionnaire d’allergies
Questionnaire Angio-mammographie
Quelle est la procédure de préparation de la patiente (questions préalables, questionnaire iodé, consentement) ?
Tout d’abord, la secrétaire pose les questions relatives au questionnaire d’injection. Si la patiente répond oui à une des questions, elle devra arriver plus tôt pour avoir une prise de sang afin de s’assurer que les reins peuvent filtrer l’iode. Si la patiente a eu une légère réaction allergique à l’iode dans le passé, une préparation d’allergie est faite avant l’examen. La patiente devra être à jeun 2 h avant l’examen. Les consignes sont les mêmes que pour la mammographie standard, soit : pas de déodorant, crème, poudre ou parfum. Une fois en salle, la technologue revoit le questionnaire d’injection, qui avait été administré au téléphone, le signe et fait signer la patiente. Elle s’assure que le poids de la patiente est exact, sinon une balance est mise à la disposition. Le questionnaire de mammographie est aussi révisé. Nous prenons le temps de bien expliquer à la patiente le déroulement de l’examen, ainsi que les effets secondaires de l’iode, puisque à la suite de l’injection, l’examen est très rapide, et nous ne voulons pas brusquer la patiente. À la fin de l’examen, nous lui rappelons de boire beaucoup d’eau pour aider les reins à éliminer l’iode, nous retirons le cathéter et nous expliquons les délais de lecture. Nous gardons les patientes 15 minutes post-injection, s’il s’agit d’une première injection.
Quelle est l’importance du dialogue technologuepatiente dans ce contexte ?
Il est primordial d’avoir une bonne communication, de bien expliquer l’examen et de demander si la patiente a des questions pour avoir la meilleure collaboration qui soit de sa part lors de l’angio-mammographie.
Interprétation et qualité des images
Quelles anomalies ou lésions l’angio-mammographie met-elle en évidence de façon plus fiable ?
L’angio-mammographie est un excellent examen pour la détection des lésions néoplasiques. Son degré de détection est comparable à celui de l’IRM.
Quel est l’intérêt de la cartographie vasculaire mammaire dans la détection tumorale ?
Les lésions néoplasiques sont hypervascularisées, car elles génèrent une néovascularisation, qui se traduit par un rehaussement significatif à l’angio-mammographie, d’où l’intérêt de la cartographie vasculaire.
Existe-t-il des limitations dans l’interprétation des résultats (artefacts, contrastes mal répartis) ?
Tout comme dans chaque examen radiologique, il y a des artéfacts. Les radiologistes sont très familiers avec ceux-ci, qui sont rarement un enjeu dans la détection des lésions. Les artéfacts les plus couramment observés sont l’artéfact de halo, l’artéfact de « ghosting » et l’artéfact d’éclaboussement du produit de contraste, en plus de ceux connus lors de la mammographie standard, tel que l’artéfact du pli, du mouvement, celui lié au déodorant...
Comment jugez-vous la performance de cette modalité (sensibilité, spécificité, valeur prédictive) ?
L’angio-mammographie est un excellent outil. Elle possède une sensibilité d’environ 96 % et une spécificité d’environ 80 % (car les lésions bénignes peuvent parfois rehausser).
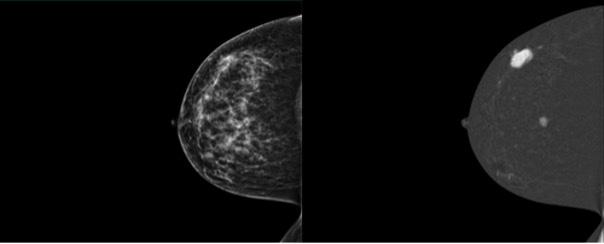
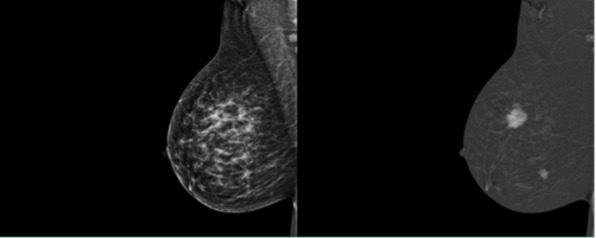
Conclusion
« En plus de la masse néoplasique au quadrant supéro-externe du sein droit observée à l’échographie, on note une seconde masse BIRADS 5 à la jonction des quadrants inférieurs du sein droit. Cette lésion sera recherchée lors de l’échographie pré-biopsie. Les deux lésions devront faire l’objet d’une biopsie. Ganglion probablement suspect axillaire droit. BIRADS 5. Veuillez-vous référer au rapport de biopsie qui suivra. »
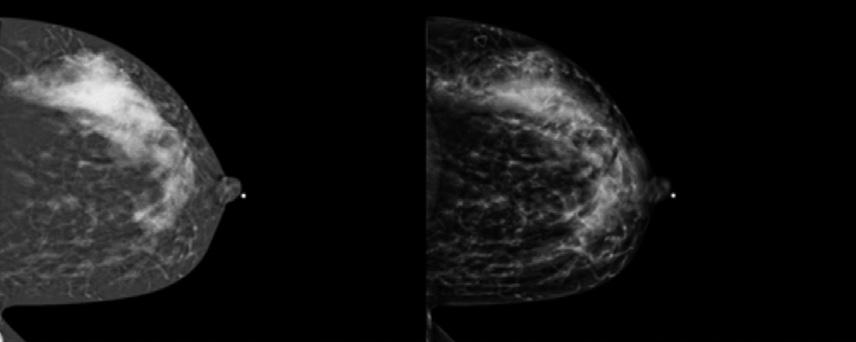
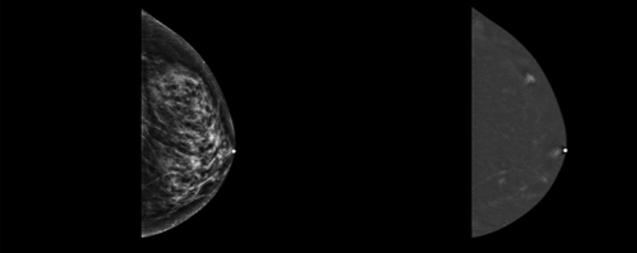
Conclusion
« Suspicion d’un processus néoplasique inflammatoire du sein gauche. La masse circonscrite au quadrant supéro-externe gauche est volumineuse et atteint jusqu’à 6 cm. Il y a un rehaussement nonmasse qui englobe cette masse et touche la totalité du quadrant supéro-externe, débordant en inféro-externe et en supéro-interne. Cela devra être réévalué par échographie. Nous procéderons à la biopsie de la masse principale au quadrant supéro-externe et nous déterminerons à l’échographie s’il y a une autre zone à biopsier afin de prouver l’atteinte multicentrique du sein gauche. Nous procéderons également à biopsier un des ganglions pathologiques axillaires gauches. Nous réévaluerons le sein droit afin de déterminer l’étiologie des rehaussements non-masses qui sont a priori physiologiques. »
Sécurité et effets secondaires
Quels sont les principaux risques liés à l’examen ?
Le risque principal relié à cet examen est l’injection de produit de contraste et la réaction de la patiente.
Quelles contre-indications absolues ou relatives doivent être évaluées ?
Une réaction allergique sévère à l’iode est une contreindication absolue pour l’angio-mammographie. Comme pour la mammographie standard, nous devons attendre six mois post chirurgie.
Comment gérez-vous les réactions au produit de contraste ?
Nous avons toujours un soluté prêt et le cabaret d’urgence à la disposition. Nous allons chercher la

Conclusion
« On confirme la présence d’un rehaussement masse catégorisé BI-RADS 4C au quadrant supéro-externe du sein gauche. Il y a un second rehaussement en supéro-interne du sein gauche qui devra être réévalué par échographie. S’il n’y a pas de correspondance, nous le biopsierons sous guidage stéréotaxique puisqu’il s’agit du site des microcalcifications. À droite, découverte fortuite d’une masse suspecte au quadrant supéroexterne catégorisée BI-RADS 4C invisible à la mammographie. Cette lésion sera également biopsiée sous guidage échographique. »
radiologiste du jour pour qu’elle évalue la patiente, nous avons un moniteur à signes vitaux et une infirmière proche, à la clinique du sein. Au besoin, nous avons accès à l’urgence.
Y a-t-il un protocole de surveillance post-examen ?
Tout dépend de la réaction de la patiente. Si c’est une réaction légère, aucune surveillance. Si la réaction est plus prononcée, nous pouvons la diriger vers l’urgence. Pour les patientes qui ont leur première injection d’iode lors de l’angio-mammographie, nous les gardons dans le département de la mammographie avec le cathéter en place 15 minutes après l’examen, pour être certaines qu’il n’y a aucune réaction tardive.
Avez-vous déjà rencontré des effets secondaires notables ? Si oui, comment ont-ils été pris en charge ?
Nous avons déjà eu une réaction allergique à la suite d’un protocole d’allergie. Nous avons emmené la patiente à l’urgence, et elle a été prise en charge. Une note à son dossier a dû être inscrite pour qu’elle n’ait plus d’injection d’iode, et ce, malgré le protocole d’allergie fait préalablement avant l’examen.
Perspectives et innovations
Comment voyez-vous l’évolution de l’angiomammographie dans les années à venir ?
Dans notre centre, nous faisons des journées entières d’angios-mammographies et nous offrons également la biopsie par aspiration en stéréotaxie avec l’angiomammographie. Nous sommes le premier centre au Québec à faire ce type de biopsie. Nous croyons que le nombre d’angios-mammographies va augmenter dans les années qui viennent, surtout pour les patientes qui ont une grande densité mammaire. Nous espérons que cet examen deviendra accessible à toutes les patientes, par son implantation dans de multiples hôpitaux.
Est-ce que des études locales ou nationales sont en cours dans votre centre ?
La compagnie GE Santé souhaiterait faire une étude sur l’injection d’iode et l’intelligence artificielle, mais rien n’est conclu pour le moment.
Cette technique pourrait-elle, selon vous, être intégrée un jour au dépistage organisé ?
Absolument, l’angio-mammographie permet de déceler les lésions qui sont difficiles à voir pour une femme dont les seins sont denses.
Quels sont les freins actuels à une adoption plus large ?
L’équipement et la formation sont des freins actuels. Avec toutes les coupures dans le milieu de la santé, le changement et l’ajout d’équipement ne sont pas toujours une priorité. Le centre doit avoir un appareil qui offre la mammographie à la suite de l’injection de contraste (CESM). Il doit également détenir un injecteur automatique et son personnel doit avoir une formation adéquate et l’expérience en mammographie pour faire ce type d’examen. Le centre doit aussi disposer d’un radiologiste formé pour lire cet examen.
Que recommanderiez-vous à une qui souhaite se former à cette nouvelle pratique ?
Je lui dirais de se faire confiance et de ne pas craindre le délai de réalisation. Cela peut-être stressant de
savoir que vous avez seulement 5 minutes pour faire une mammographie complète, mais, avec le temps, on finit par aimer cet examen. C’est satisfaisant et impressionnant parfois de voir apparaître une lésion rehaussée qu’on n’aurait pas soupçonnée ou de voir l’étendue réelle d’un cancer dans le sein. Il y a un sentiment de satisfaction d’avoir découvert des lésions qui rehaussent.
Pour approfondir votre compréhension de ces avancées technologiques, nous vous invitons à écouter l’épisode 3 de notre Balado Fréquences et Images : « Avancées pour le dépistage du cancer du sein ». Dans cet épisode, l’animateur Dominic Arpin reçoit Kelly Chouinard, t.i.m., ainsi que Dr Rémi Poirier, radiologiste, MD, FRCPC.
Ensemble, ils explorent comment le dépistage évolue pour devenir plus précis, moins invasif et plus rassurant, et comment la technologie transforme la mammographie et la biopsie mammaire.

Nous tenons à remercier chaleureusement Kelly Chouinard pour sa générosité et la richesse de son témoignage. Merci également à Mélanie Labarre, t.i.m. et Nancy Roy, t.i.m. pour leur précieuse collaboration à la réalisation de cet article. Leur expertise et leur engagement envers l’avancement de la pratique en mammographie sont une source d’inspiration pour toute la communauté des technologues en imagerie médicale.
QUAND LES ROBOTS PRENNENT LA SONDE : MENACE OU PARTENAIRE DES TECHNOLOGUES ?
L’idée selon laquelle l’intelligence artificielle pourrait un jour remplacer les technologues suscite à la fois curiosité et inquiétude. Si cette perspective paraît peu probable à court terme, l’intégration progressive de l’intelligence artificielle en échocardiographie est, quant à elle, bien réelle. La question n’est donc plus de savoir si l’intelligence artificielle fera partie de notre pratique, mais plutôt comment elle transformera notre manière de pratiquer, ainsi que de comprendre les défis associés à son implantation.
Contexte clinique
Dans les laboratoires d’échocardiographie, la charge de travail ne cesse d’augmenter. Les examens sont de plus en plus nombreux, souvent plus complexes, et leur acquisition, comme leur interprétation, exige un temps considérable. À cela s’ajoute une variabilité entre les opérateurs susceptible d’influencer la cohérence des résultats et, par conséquent, l’efficacité de l’émission d’un diagnostic juste.
Dans ce contexte, l’IA apparaît comme un outil prometteur pouvant améliorer la standardisation, la reproductibilité et l’efficience des examens échocardiographiques.
Principes généraux de l’intelligence artificielle
Les principes de l’intelligence artificielle reposent sur un ensemble de méthodes informatiques permettant à une machine d’apprendre à partir de données, de reconnaître des schémas complexes et d’effectuer des tâches particulières de manière autonome.
Ces systèmes sont entraînés sur de vastes bases de données annotées par des experts. L’IA teste différentes analyses sur ces banques de données et reçoit une rétroaction sur la précision de ses mesures, ce qui lui permet d’améliorer ses performances au fil du temps.
Quand l’image est complexe, comme en échocardiographie, on peut recourir à l’apprentissage profond qui utilise des réseaux de neurones complexes pour extraire des mesures, telles que la fraction d’éjection ou la déformation myocardique longitudinale du ventricule gauche, communément appelée « strain ».
Électrophysiologie médicale
L’IA apparaît comme un outil prometteur pouvant améliorer
la standardisation, la reproductibilité et l’efficience des examens échocardiographiques.
Intégration de l’IA au processus échocardiographique

Enseignante en échographie médicale
Collège Ahuntsic
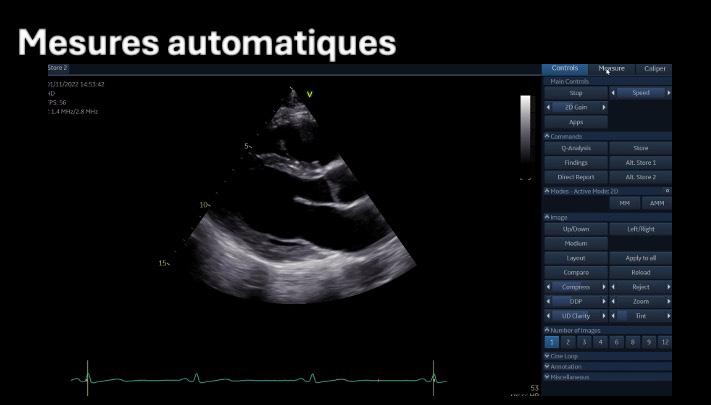
L’intelligence artificielle peut intervenir à chaque étape du processus échocardiographique, depuis l’acquisition des images à leur analyse et de la révision jusqu’à la génération du rapport et l’exploitation des données pour des analyses approfondies.
L’un des objectifs principaux de l’intégration de l’IA en acquisition d’images est d’optimiser le temps du praticien et d’assurer une meilleure uniformité des mesures. Les principaux fabricants d’équipements d’échographie investissent de manière significative dans le déploiement de ces nouvelles technologies, tandis que de nouvelles entreprises émergentes se consacrent spécifiquement au développement de stations de lecture assistées par l’intelligence artificielle.
Par exemple, la mesure automatisée des dimensions du ventricule gauche réduit les interventions manuelles et améliore la reproductibilité des suivis. Tout en étant un soutien à l’opérateur, cette technologie lui offre la possibilité d’ajuster les contours au besoin ( média 1 ).
De même, certains algorithmes sont capables de reconnaître et de tracer automatiquement les spectres Doppler. Ils peuvent analyser plusieurs cycles cardiaques, en effectuer une moyenne et ainsi améliorer
la précision des mesures, y compris en présence de rythmes irréguliers (média 2).
À cela s’ajoute la capacité de l’IA à simplifier l’utilisation de l’équipement grâce à une automatisation avancée, détectant systématiquement le spectre Doppler sans qu’il soit nécessaire de le sélectionner manuellement au préalable. Il suffit d’activer le mode « mesure » de l’échographe, et le logiciel détecte automatiquement le spectre Doppler et la mesure sans que l’on ait besoin de la sélectionner ( média 3).
Analyse automatisée des images
En matière d’analyse des images, l’intelligence artificielle est en mesure de faire l’analyse automatisée de la cinétique segmentaire des parois myocardiques en reconnaissant les vues échocardiographiques, en segmentant le myocarde et en évaluant la contraction de chaque segment. Un score global quantitatif est ensuite généré, accompagné d’un indicateur de qualité. Une étude parue dans le Journal of the American Society of Echocardiography, en 2024, avait pour but de valider l’utilisation d’un modèle d’intelligence artificielle capable de détecter les anomalies régionales de la contractilité des parois du muscle cardiaque sur les échocardiographies et de comparer sa performance à celle de lecteurs humains, experts et novices. Cette étude visait à évaluer la capacité de l’IA
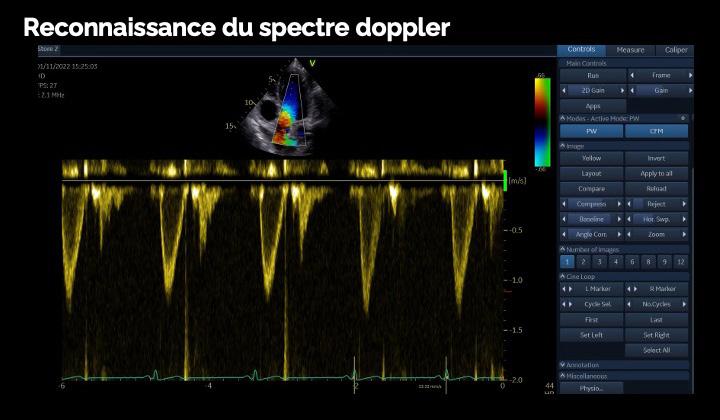
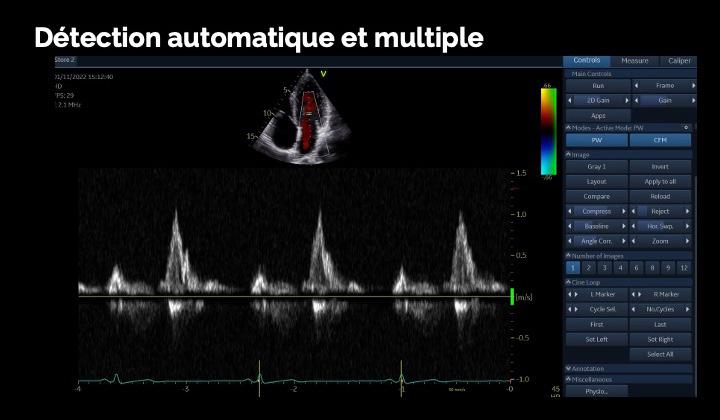
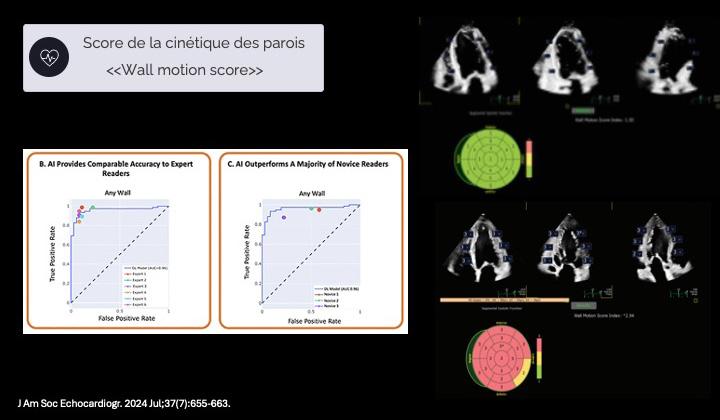
à égaler ou à surpasser les cardiologues dans cette tâche. Les performances de ce système se sont révélées comparables à celles de cliniciens experts, et supérieures à celles de lecteurs moins expérimentés ( média 4).
L’algorithme de détection automatique de région d’intérêt, fondé sur l’intelligence artificielle, permet une mesure entièrement automatisée de la fraction d’éjection, ne nécessitant qu’une interaction minimale de l’utilisateur pour lancer l’analyse et valider les résultats. Cela fonctionne aussi bien en 2D qu’en 3D, avec des corrélations très satisfaisantes dans les études comparant l’IA à des opérateurs expérimentés. Une étude de Asch et coll., en 2019, a testé un algorithme d’apprentissage automatique capable d’estimer la fraction d’éjection du ventricule gauche, en analysant des images échocardiographiques, sans avoir recours à des mesures volumétriques classiques. L’algorithme a montré des résultats proches de ceux d’experts humains et une bonne capacité à détecter les dysfonctions sévères. Cette approche automatisée pourrait faciliter et standardiser l’évaluation clinique de la fraction d’éjection ventriculaire gauche. Il existe également le 3D-dynamic heart model , créé par Philips, un outil de quantification 3D intégré aux échographes, qui permet de mesurer automatiquement les volumes du ventricule et de l’oreillette gauche. Grâce à l’intelligence artificielle, il devient capable de reconnaître les cavités cardiaques, de suivre les contours endocardiques tout au long du cycle cardiaque et de mettre à jour le modèle en temps réel selon l’image, pour que le tout puisse fonctionner. Puisqu’il agit en 3D, il ne repose donc pas sur des
hypothèses géométriques simplifiées, ce qui le rend plus fidèle à la réalité anatomique du ventricule gauche (figure 1 ).
L’intelligence artificielle peut aussi réaliser la segmentation automatique de structures plus complexes, telles que la valve mitrale. À partir d’images échographiques 3D, elle peut modéliser une fuite mitrale de façon dynamique et plus précise que la méthode PISA classique, qui repose sur de nombreuses hypothèses souvent non trouvées chez nos patients. Grâce à l’analyse des données Doppler, couleur 3D, le flux régurgitant est quantifié de manière continue sur l’ensemble de la systole, offrant une évaluation complète du jet. Contrairement à la méthode PISA classique, qui repose sur une mesure ponctuelle au cours du cycle cardiaque et une géométrie simplifiée de l’orifice, cet algorithme permet une analyse volumique et dynamique tout au long du cycle cardiaque, moins dépendante de l’opérateur. Cette approche améliore la précision, la reproductibilité et la standardisation de la quantification de la régurgitation mitrale. Cet outil a été conçu pour répondre aux limites que l’on rencontre souvent dans l’évaluation du volume de régurgitation mitrale. Tel que démontré à la figure 2
Reconnaissance des vues et sélection automatique
L’IA peut aussi faire une reconnaissance automatique des vues, et choisir les meilleurs clips avant d’effectuer l’analyse. Ce type d’algorithme combine les informations de la vue avec la fréquence cardiaque et la cadence d’acquisition pour sélectionner automatiquement un trio d’images apicales
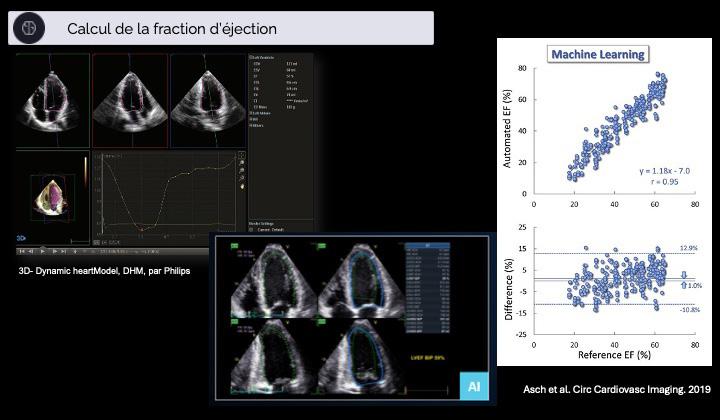
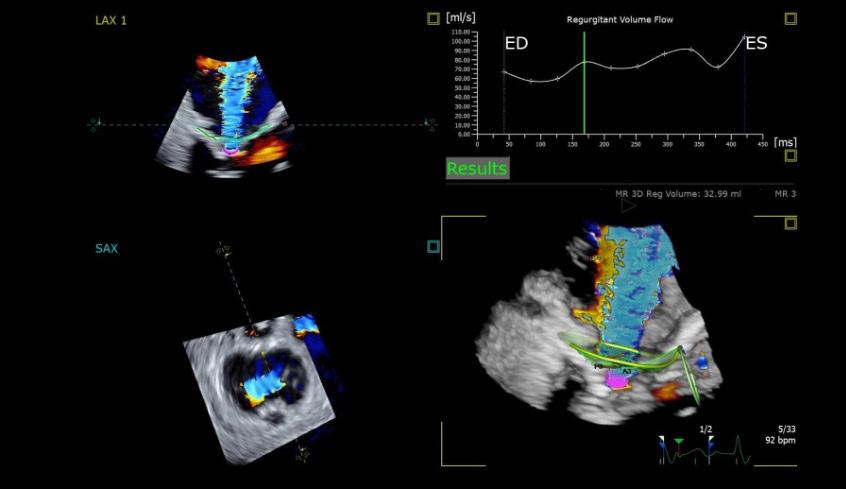
Grâce à l’intelligence artificielle, il devient capable de reconnaître les cavités cardiaques, de suivre les contours endocardiques tout au long du cycle cardiaque et de mettre à jour le modèle en temps réel selon l’image, pour que le tout puisse fonctionner.
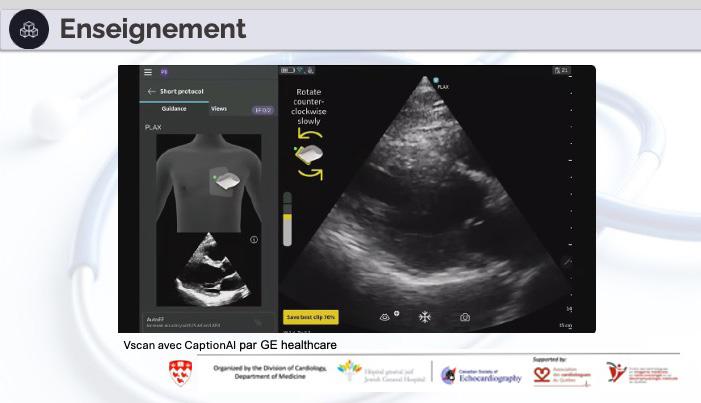
optimal avant, par exemple, de calculer le « strain ». Hormis le déclenchement de l’outil et la validation finale, aucune intervention manuelle n’est requise.
Évaluation du « strain »
L’évaluation du « strain » a aussi grandement été facilitée par l’intelligence artificielle. Elle a permis de développer sa mesure dans de nouvelles cavités, comme le ventricule droit et l’oreillette gauche. Une étude récente de Sverić et coll., publiée en 2024, dans European Heart Journal – Imaging, a testé une intelligence artificielle capable de calculer automatiquement le « strain » global du ventricule gauche à partir d’images échocardiographiques, sans qu’aucune correction ne soit apportée par l’opérateur. Les mesures obtenues par l’IA se sont révélées fiables et concordantes avec celles d’un expert, et, grâce à l’IA, même un débutant a pu obtenir des
résultats comparables à ceux d’un expert. En laissant l’outil travailler seul, on voit que cette technologie peut standardiser les mesures, réduire la variabilité entre les opérateurs et rendre le suivi des patients plus rapide et homogène.
L’intelligence artificielle ouvre également de nouvelles perspectives innovantes en matière d’enseignement. Des échographes portables intégrant un assistant intelligent peuvent analyser les images en temps réel, proposer des annotations automatiques et fournir un indicateur de qualité tout au long de l’acquisition. Le Vscan, offert par GE HealthCare, combiné à Caption AI, permet de réaliser des échographies portables sur son téléphone avec un assistant d’IA intégré, qui analyse les images en temps réel et propose automatiquement des légendes ou annotations sur la structure visualisée. L’outil calcule simultanément la fraction d’éjection et fournit un indicateur de qualité, qui évalue la qualité de l’acquisition. L’option « Save Best Capture » enregistre automatiquement l’image de meilleure qualité de la séquence, facilitant la documentation et réduisant la nécessité de sélectionner les images manuellement. Cette technologie peut être particulièrement intéressante pour les opérateurs novices, entre autres (voir média 5).
De la même manière, un autre échographe portable, développé par EchoNous, comporte une intelligence artificielle pour guider la sonde, optimiser la qualité de l’image et mesurer automatiquement des paramètres cardiaques, tels que la fraction d’éjection, permettant ainsi une évaluation
Plutôt qu’un substitut au technologue, l’intelligence artificielle devrait être considérée aujourd’hui comme un outil complémentaire susceptible d’optimiser la pratique à condition qu’elle soit intégrée au travail de manière réfléchie et encadrée.
1 – Roberto M. Lang, MD et coll., 2015, Recommendations for Cardiac Chamber Quantification by Echocardiography in Adults: An Update from the American Society of Echocardiography and the European Association of Cardiovascular Imaging
2 – Amro Sehly et coll., 2022, Artificial Intelligence in Echocardiography: The Time is Now, National Library of Medicine.
3 – Jimmy Su et coll., Philips White paper, 2024, Dynamic quantification of mitral regurgitation
4 – Michal Yaacobi et coll., Philips White paper, 2024, First-of-kind automated segmental wall motion assessment of the left ventricle
5 – Kristin McLeod, GE White paper, 2021, The Role of Artificial Intelligence in Streamlining Echocardiography Quantification.
6 – Philips White paper, 2024, The next dimension in echocardiography.
7 – Akhil Narang et coll., European heart journal –cardiovascular imaging, 2018, Machine learning based automated dynamic quantification of left heart chamber volumes.
rapide du cœur au chevet du patient. Il rend là encore l’échocardiographie accessible même aux utilisateurs moins expérimentés (voir média 6).
Conclusion
L’intelligence artificielle constitue un outil prometteur en échocardiographie. Elle permet d’automatiser certaines analyses, d’améliorer la reproductibilité des mesures et de soutenir la formation des opérateurs. Toutefois, elle peut comporter des pièges si elle est utilisée sans vigilance. Plutôt qu’un substitut au technologue, l’intelligence artificielle devrait être considérée aujourd’hui comme un outil complémentaire susceptible d’optimiser la pratique, à condition qu’elle soit intégrée au travail de manière réfléchie et encadrée. Elle doit donc s’accompagner d’un encadrement rigoureux, d’une validation continue et d’une supervision par des professionnels formés.
8 – Verena Roediger, Site internet Philips, 2025, Automated « strain » measurements with Auto « strain » LV/RV/LA
9 – Hila Best et coll., GE White paper, 2021, Venue™ Family Real-Time EF
10 – GE HealthCare, 2022, vidéo YouTube.
11 – GE HealthCare, 2022, Vivid E95 customer presentation, Ultra edition.
12 – GE HealthCare, 2026, Caption AI Vscan Air SL- Cardiac Guidance and Interpretation, vidéo YouTube.
13 – Kosmos by EchoNous, 2024.
14 – Jimmy Su, PhD, Philips, 2024, Dynamic quantification of mitral regurgitation, Philips white paper.
15 – Sverić KM, et coll., 2024, The role of artificial intelligence in standardizing global longitudinal « strain » measurements in echocardiography. Eur Heart J – Imaging Methods Pract.
16 – Asch FM et coll., 2019, Automated echocardiographic quantification of left ventricular ejection fraction without volume measurements using a machine learning algorithm mimicking a human expert, Cardiovascular Imaging.




Vous renouvelez votre police d’assurance dans moins de 90 jours ?
Automobile
Habitation
Bateau
Motoneige
Véhicule récréatif
Appelez-nous pour une soumission dès aujourd’hui !
Appliquez le Code Promo Z00088
