Sede
Porlamar

Sede
Porlamar
Tipos de diagramas, métodos, ejercicios, etc.


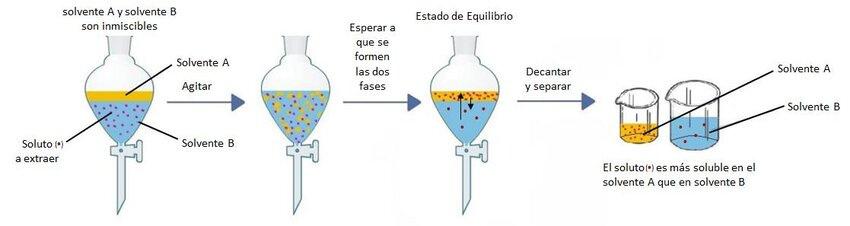
La extracción líquido-líquido, también conocida extraccióndesolvente,esunprocesoquímicoempleado para separar componentes en solución mediante su distribuciónendosfasesliquidasinmiscibles.
Este proceso también se le conoce como extracción liquida o extracción con disolvente En esta extracción líquido-líquido se ven involucrada la transferencia de masa de una fase líquida a una segunda fase líquida inmiscible, el proceso se puede realizar en varias formas El ejemplo más sencillo involucra la transferencia de un componente de una mezcla binaria a una segunda fase liquida inmiscible Un ejemplo es la extracción líquido-líquido de una impureza contenida en el agua de desperdicio mediante un disolvente orgánico Esto es similar al agotamiento o absorción en la que se transfiere masa de una fase a otra
El factor de separación es una razón de distribución dividida por otra, es una medida de la habilidad del sistema para separarse en dos solutos
Por ejemplo si la distribución de la razón para el níquel (DNi) es 10 y la distribución de la razón para la distribución de la plata (DAg) es 100, entonces el factor de separación plata/níquel (SFAg/Ni) es igual a DAg/DNi = SFAg/Ni = 10
K =

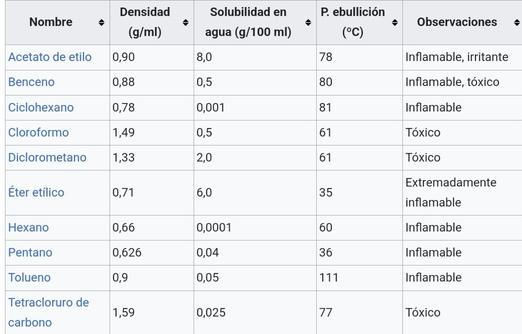
En la extracción líquido-líquido, son empleados dos disolventesinvisiblesentresí,enlamayoríadeloscasos uno de estos es agua o una disolución actuosa y el otro componente suele ser un disolvente orgánico de muy bajapolaridad..
Tabla con disolventes orgánicos de uso más frecuente en las operaciones de extracción líquido-líquido

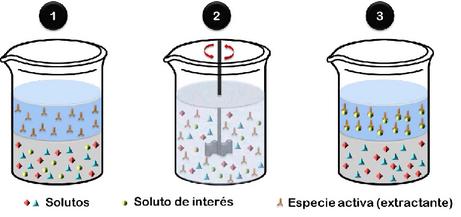
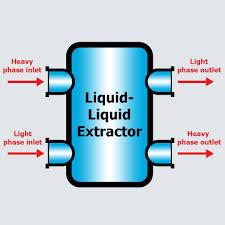
La extracción líquido-líquido se viene utilizando tanto a pequeña escala, a nivel de laboratorio de química, como a gran escala,enprocesosindustriales
La presión y la temperatura afectan la solubilidad mutua de los líquidos, lo quepuedeinfluirenlaextracciónlíquido-líquido.
Gracias a que la presión y la temperatura afectan a la solu mientras que mayor sea la temperatura las partícbilidad de los gases existe un efecto importante en la reacción Mientras mayor sea la temperatura las partículas de absoluto y solvente están en un movimiento más rápido, eso produce que se debiliten las fuerzas intermoleculares y claro que esto también hace que se afecte la solubilidad de ambos productos.
E f e c t o d e l a p r e s i ó n
C u a n d o c o n t a m o s c o n
b a j a s p r e s i o n e s l o s
e f e c t o s s o n p e q u e ñ o s p o r
l o q u e p u e d e n t o m a r s e
i m p e r c e p t i b l e s y
d e s e c h a r s e . E s
i m p o r t a n t e m e n c i o n a r q u e
p a r a m a n t e n e r e l
e q u i l i b r i o d e l a f a s e
l í q u i d a s e d e b e n u t i l i z a r
p r e s i o n e s m á s a l t a s a l a s
p r e s i o n e s d e v a p o r d e
c a d a s o l u c i ó n , p a r a q u e
d e e s t a m a n e r a s e
m a n t e n g a u n s i s t e m a
c o n d e n s a d o , e v i t a n d o a s í
q u e s e d e s e q u i l i b r e l a
r e a c c i ó n a p a r e c i e n d o u n a
f a s e d e v a p o r e n l a f a s e
l í q u i d a .
E f e c t o d e l a t e m p e r a t u r a
E s t a t i e n e u n e f e c t o
d i r e c t o e n l a s o l u b i l i d a d ,
p a r a e s t e t i p o d e
s i s t e m a s e n e l q u e
c o n t a m o s c o n l í q u i d o
l í q u i d o a l a u m e n t a r l a
t e m p e r a t u r a s e
i n c r e m e n t a l a s o l u b i l i d a d
d e a m b o s s i s e c u e n t a
c o n u n a t e m p e r a t u r a
c r í t i c a p u e d e l l e g a r a l .
d e d i s o l v e r s e l a r e a c c i ó n
p o r l o q u e e s i m p o r t a n t e
m a n t e n e r u n c o n t r o l e n l a
t e m p e r a t u r a d e l a m i s m a .
e s i m p o r t a n t e m e n c i o n a r
q u e l a s p a r e d e s s o l t ó
d i l u n t e y s o l v e n t e
d i l u e n t e t a m b i é n s e v e n
a f e c t a d a s p o r l a
t e m p e r a t u r a .


Los diagramas a mencionar son esenciales para el diseño y la optimización de procesos de extracción líquido-líquido,yaqueproporcionaninformaciónvisual
clara sobre el equilibrio de fases y la eficiencia de separaciónramas de equilibrio ternario son los más utilizadosenlaextracciónlíquido-líquido.

c l a b i n a r i a .
Ejes: Las concentraciones de los componentes en cada fase.
Curvas de Equilibrio: Representan la distribución de los componentes entre las dos fases.
Uso: Ayuda a determinar las composiciones de las fases en equilibrio y la eficiencia de separación.
D i a g r a m a d e P u r i f i c a c i ó n
E s t e d i a g r a m a s e u t i l i z a p a r a
r e p r e s e n t a r e l p r o c e s o d e
p u r i f i c a c i ó n d e u n
c o m p o n e n t e e s p e c í f i c o e n l a f a s e e x t r a c t a n t e .
E j e s : P u r e z a d e l
c o m p o n e n t e e n c a d a f a s e .
C u r v a s d e E q u i l i b r i o :
I n d i c a n c ó m o v a r í a l a
p u r e z a d e l c o m p o n e n t e e n
l a s d o s f a s e s .
U s o : P e r m i t e e v a l u a r l a
e f i c i e n c i a d e l a
p u r i f i c a c i ó n y o p t i m i z a r e l
p r o c e s o .
D i a g r a m a d e T r i á n g u l o ( D i a g r a m a
T e r n a r i o )
E s u n o d e l o s d i a g r a m a s m á s
c o m u n e s y ú t i l e s e n l a
e x t r a c c i ó n l í q u i d o - l í q u i d o ,
e s p e c i a l m e n t e p a r a s i s t e m a s
t e r n a r i o s ( t r e s c o m p o n e n t e s ) .
E j e s : C a d a v é r t i c e d e l t r i á n g u l o
r e p r e s e n t a u n c o m p o n e n t e p u r o , y
c u a l q u i e r p u n t o d e n t r o d e l t r i á n g u l o
r e p r e s e n t a u n a m e z c l a d e l o s t r e s
c o m p o n e n t e s .
C u r v a s d e E q u i l i b r i o : I n d i c a n l a s
c o m p o s i c i o n e s d e l a s f a s e s e n
e q u i l i b r i o .
l a m e z c l a e s h o m o g é n e a
R e g i ó
Diagrama de McCabe-Thiele
Aunque es más común en la destilación, también puede aplicarse a la extracción líquido-líquido para sistemas binarios.
Ejes: Concentración de un componente en una fase frente a su concentración en la otra fase.
Líneas de Operación: Representan las etapas de contacto entre las dos fases.
Curva de Equilibrio: Indica el equilibrio entre las fases.
Uso: Ayuda a determinar el número de etapas necesarias para lograr la separación deseada.
Í Q
Extracción en Etapas Múltiples: Este método consiste en realizar varias etapas de contacto entrelafasedealimentaciónyelsolventepara mejorar la eficiencia de la extracción. En cada etapa, las fases se separan y el extracto se someteaunnuevocontactoconunafasefresca desolvente.

ExtracciónContracorriente:
En este método, la fase de alimentación y el solvente se ponen en contacto en contracorriente.Estosignificaquelafasericaen solutoyelsolventefrescofluyenendirecciones opuestasatravésdemúltiplesetapas.
ExtracciónCentrífuga:
En este método, se utilizan fuerzas centrífugas para mejorarlaseparacióndelasfaseslíquidas.Lasfasesse introducenenunacentrífuga,dondeseseparandebidoa lasdiferenciasendensidad.
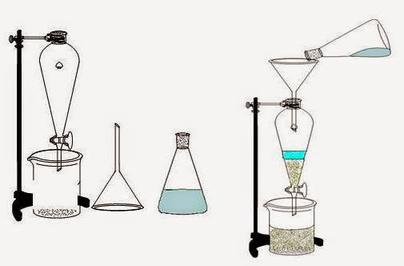
ExtracciónenColumna:
Estemétodoutilizaunacolumnadeextracción dondelasfaseslíquidasseponenencontacto continuo mientras fluyen en direcciones opuestas (contracorriente) o en la misma dirección(corrienteparalela).


S M É T O D O S
ExtracciónenEtapasMúltiples:




ExtracciónContracorriente:
Unaalimentaciónde100gdesoluciónacuosadeAdebeserextraídacon100gdesolventeorgánicoBen unaoperacióncontracorrientedetresetapas.Elcoeficientedereparto
Laalimentaciónseponeencontactoconelsolventefresco,yalequilibrio����=2×����. Sisesuponequelamismamasasedistribuye,entonceselsolventecontendráunamayorconcentración deA.
El solvente que sale de la primera etapa actúa como el solvente fresco para la segunda, y así sucesivamente.
M É T O D O S

ExtracciónenColumna:
Unacolumnadeextraccióntieneunaalimentaciónacuosade1kgdesoluciónquecontiene0.1 kgdecompuestoCyusa1kgdesolventeDporetapa,conuncoeficientederepartoK=3

Lafaseinferior(ahoradisminuidaencontenidodeC)pasaalasiguienteetapadecontacto,yelproceso serepiteencadaetapa.
ExtracciónCentrífuga:
Unamezclalíquidade500gcontieneunsolutoSal20%.Lacentrifugacióncon500gde unsolventePdalugaraunaeficienciadeextraccióndel90%
LamasadesolutoSenlaalimentacióniniciales500×0.2=100g.
Conunaeficienciadel90%,seextrae100x0.90=90gdeSalsolventeP.
EnelsolventePseobtendrán90gdeS,yquedarán10gdeSenlafaseresidual.
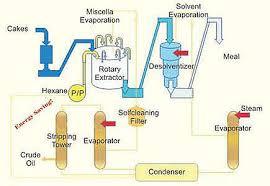
E C U P E R A C I Ó N D E S O L V E N T E S P O R E X T R A C C I Ó N .
Larecuperacióndesolventesporextracciónesunprocesoimportanteenlaindustria químicapararecuperaryreutilizarsolventesdemezclascomplejas,reduciendocostosy minimizandoelimpactoambiental.
Implicalaseparacióndeunsolventedeseadodeunamezclalíquidamedianteelusode unsegundosolventeinmiscible.Elobjetivoestransferirelsolventedeseadoaunanueva faseparapoderreutilizarlo.

S


Laseleccióndedisolventesenlosprocesosdeextracciónlíquido-líquidoesunaetapa críticaparaasegurarlaeficienciayeficaciadelproceso.
C r i t e r i o s
S e l e c t i v i d a d : C a p a c i d a d d e l
d i s o l v e n t e p a r a s e p a r a r e l
c o m p o n e n t e d e s e a d o d e l a m e z c l a .
S o l u b i l i d a d : C a p a c i d a d d e l
d i s o l v e n t e p a r a d i s o l v e r e l s o l u t o .
E l s o l u t o d e b e s e r a l t a m e n t e
s o l u b l e e n e l d i s o l v e n t e , m i e n t r a s
q u e l a s i m p u r e z a s d e b e n s e r p o c o
s o l u b l e s .
I n m i s c i b i l i d a d : C a p a c i d a d d e l
d i s o l v e n t e p a r a n o m e z c l a r s e c o n
l a f a s e o r i g i n a l .
D e n s i d a d : D i f e r e n c i a e n l a d e n s i d a d
e n t r e e l d i s o l v e n t e y l a f a s e
o r i g i n a l .
T o x i c i d a d y S e g u r i d a d : I m p a c t o d e l
d i s o l v e n t e e n l a s a l u d h u m a n a y e l
m e d i o a m b i e n t e .
V o l a t i l i d a d : T e n d e n c i a d e l
d i s o l v e n t e a e v a p o r a r s e .
Supongamos que deseas extraer un compuesto orgánico A de una solución acuosa. Aquí tienes cómopodríasseleccionarundisolvente:
EvaluarlaSolubilidaddeA VerificarlaInmiscibilidadconAgua
ConsiderarlaToxicidadySeguridad CostoyDisponibilidad
Siguiendoestoscriterios,podríasoptarporacetato deetilosiAessolubleenélycumpleconlosotros requisitosdeinmiscibilidad,seguridadycosto
C a r a c t e r í s t i c a s d e l o s
D i s o l v e n t e s C o m u n e s
Éter Dietílico:
Selectividad:Altaselectividadparamuchoscompuestos orgánicos.
Solubilidad:Buenasolubilidadparasolutosorgánicos
Inmiscibilidad:Inmiscibleconagua
Densidad:Menordensidadqueelagua
ToxicidadySeguridad:Inflamableytóxico
Volatilidad:Altavolatilidad.
Costo:Moderado.
AcetatodeEtilo:
Selectividad:Buenaselectividadparacompuestosorgánicos polaresynopolares.
Solubilidad:Buenasolubilidadparasolutosorgánicos. Inmiscibilidad:Inmiscibleconagua.
Densidad:Menordensidadqueelagua
ToxicidadySeguridad:Moderadamentetóxicoeinflamable Volatilidad:Altavolatilidad
Costo:Bajo.
Hexano:
Selectividad:Buenaselectividadparacompuestosnopolares.
Solubilidad:Solubilidadlimitadaparasolutospolares.
Inmiscibilidad:Inmiscibleconagua.
Densidad:Menordensidadqueelagua.
ToxicidadySeguridad:Inflamableytóxico
Volatilidad:Altavolatilidad
Costo:Bajo
Cloroformo:
Selectividad:Altaselectividadparacompuestosorgánicos.
Solubilidad:Buenasolubilidadparasolutosorgánicos. Inmiscibilidad:Inmiscibleconagua.
Densidad:Mayordensidadqueelagua.
ToxicidadySeguridad:Tóxicoypotencialmentecancerígeno. Volatilidad:Moderadavolatilidad.
Costo:Moderado