Une publication de l’International Myeloma Foundation
Top
10 des actualités de la
recherche de l’ASH sur le myélome
La réunion annuelle de l’American Society of Hematology met en avant des résumés prometteurs sur la recherche sur le myélome

Le groupe de travail international sur le myélome de l’IMF et l’équipe de direction de l’IMF œuvrent à faire progresser la recherche dans le domaine du myélome lors du forum majeur des hématologues
Scientifique et clinique
Les 10 meilleurs résumés de la réunion
Par le Dr Joseph Mikhael
Directeur médical au sein de l’IMF
Près de 30 000 membres de la communauté des maladies du sang se retrouvent chaque année en décembre à l’occasion de la réunion annuelle de l’American Society of Hematology (ASH) et de son exposition visant à présenter les données récentes les plus significatives en matière de recherche et à en discuter. Cette année, plus de 9 000 résumés de recherche ont été soumis à l’ASH pour examen et plus de 8 000 ont été sélectionnés en vue d’une présentation. Il est intéressant de noter que parmi tous ces résumés présentés, plus de 1 500 concernaient le myélome multiple !
Le myélome reste le sujet qui suscite le plus d’intérêt lors des réunions de l’ASH. Il est très encourageant de voir les progrès réalisés dans la recherche sur le myélome, lesquels sont très prometteurs pour nos patients et leurs proches. Je partage ci-dessous mon Top 10 personnel des résumés consacrés au myélome, répartis en deux groupes. Cinq résumés portent sur la thérapie par cellules T à récepteurs antigéniques chimériques (CAR) et cinq autres sur les thérapies par anticorps bispécifiques. Thérapie par cellules CAR-T
Ces cinq résumés nous donnent ensemble un réel espoir de pouvoir proposer à nos patients une thérapie par cellules CAR-T plus facilement, plus efficacement et de façon plus sécurisée.
LBA-1 :
Cellules CAR-T in vivo
Ce tout nouveau résumé est l’un des six seulement à présenter des résultats tout juste découverts. Il faisait état des trois premiers patients traités par cellules CAR-T in vivo, c’est-àdire selon un procédé qui se déroule à l’intérieur du patient. Habituellement, la thérapie CAR-T est réalisée ex vivo : des cellules T sont prélevées dans le sang du patient, modifiées en laboratoire, puis réinjectées dans le corps du patient après « ingénierie ». Le nouveau médicament CAR-T in vivo est administré directement au patient, transformant les
son organisme, sans qu’il soit nécessaire de prélever, de modifier, de fabriquer, puis de réinjecter les cellules CAR-T au patient. L’approche CAR-T in vivo est un concept remarquable. Elle pourrait faciliter considérablement l’accès à la thérapie par cellules CAR-T, qui constitue actuellement un véritable défi et une forte inégalité d’accès au traitement du myélome. Les patients traités par la méthode CAR-T in vivo dans le cadre de l’essai clinique, tous atteints d’un myélome multiple à haut risque (HRMM) et ayant été lourdement prétraités, ont obtenu une négativité de la MRD au cours du premier mois et ont subi moins d’effets secondaires que ceux que l’on observe habituellement dans le cadre d’une thérapie CAR-T ex vivo. La thérapie CAR-T in vivo est un grand pas en avant pour rendre accessible à nos patients la thérapie la plus efficace contre le myélome, et ce dans un contexte plus sûr.
Résumé 94 :
Suivi à long terme des patients à risque standard, traités par Carvykti Carvykti® (ciltacabtagene autoleucel, « cilta-cel ») est la thérapie par cellules CAR-T actuellement utilisée dès la première rechute du myélome (traitement de deuxième ligne). Deux essais cliniques importants ont évalué son utilisation chez des patients : l’étude CARTITUDE-1 auprès de patients ayant reçu plus de 4 (en moyenne 6) lignes de traitement et l’étude CARTITUDE-4 auprès de patients ayant reçu 1 à 3 lignes de traitement antérieures. Le suivi à long terme des patients à risque standard dans ces études a montré des résultats que nous n’avions jamais observés auparavant.
En cas de rechute précoce, la survie sans progression (PFS) à 30 mois était de 80 %. En cas de rechute tardive, la PFS était de 60 %. Historiquement, la thérapie CAR-T était utilisée de préférence chez les patients à haut risque, mais nous observons aujourd’hui des résultats très impressionnants chez les patients à risque standard, avec des durées de rémission sans précédent. L’étude CARTITUDE nous fournit également des données plus spécifiques à partager avec les patients à risque standard lorsqu’il s’agit de décider d’une thérapie par cellules CAR-T.
Élimine la déplétion lymphatique de conditionnement
Logistique grandement simpli ée pour élargir l’accès
Aucune culture ex vivo ne peut augmenter la capacité fonctionnelle des cellules T
Perfusion directe
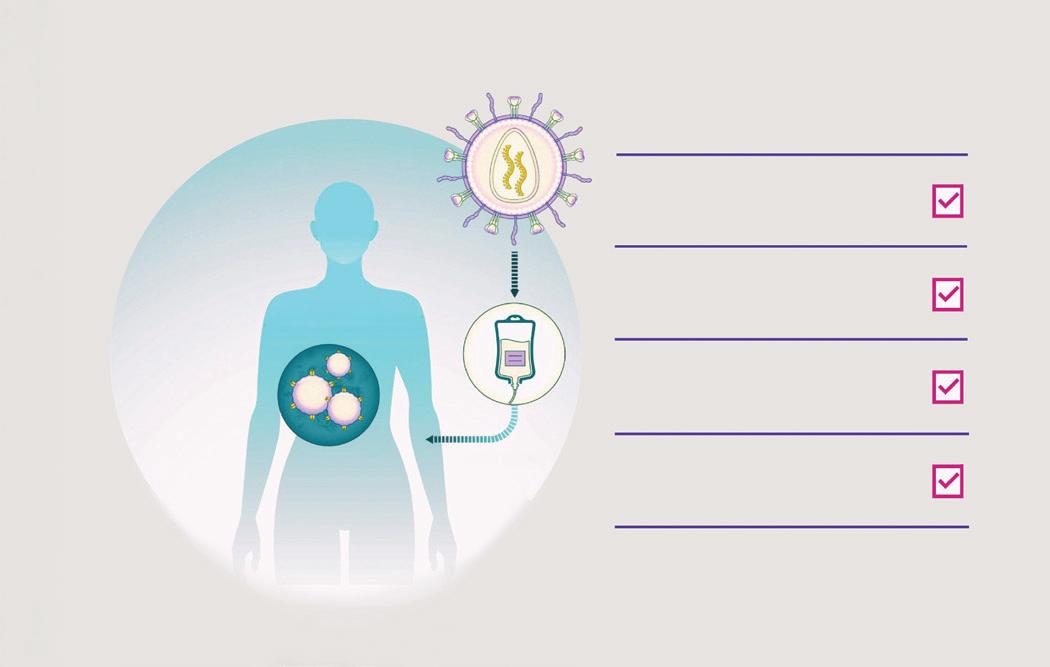
Réduction du coût des biens et de la fabrication
Résumé 1034 :
Améliorer la sécurité de Carvykti
L’un des défis que pose Carvykti concerne les effets indésirables neurologiques retardés, une neurotoxicité qui survient généralement un mois ou davantage après le traitement. Elle peut être assez sévère, avec notamment des syndromes de type parkinsonien et de type Guillain-Barré. Prévenir ou réduire ces neurotoxicités rares est essentiel si nous voulons administrer ce traitement très efficace de manière plus sûre.
de l’American Society of Hematology
Cette étude a suivi plus de 750 patients traités avec Carvykti et a abouti à deux conclusions importantes. Premièrement, nous pouvons réduire le risque de neurotoxicités en administrant une « thérapie relais » efficace, c’est-à-dire le traitement donné après le prélèvement des cellules T, mais avant leur réinjection. Deuxièmement, une augmentation du nombre absolu de lymphocytes (ALC) peut prédire un risque plus élevé de neurotoxicité et des stratégies visant à réduire l’ALC peuvent s’avérer utiles.
Résumé 258 :
Double ciblage BCMA et CD19 FasTCAR-T
Alors que nous cherchons à rendre la thérapie par cellules CAR-T encore plus efficace, une approche CAR-T ciblant deux antigènes à la surface des cellules de myélome est conçue pour se fixer de manière plus spécifique sur les cellules myélomateuses. Cette approche est étudiée avec la molécule GC012F/AZD0120, qui a également été testée chez des patients présentant un myélome multiple récemment diagnostiqué (NDMM). Cette approche s’est révélée très efficace : 100 % des 30 patients ont répondu au traitement et aucun cas de neurotoxicité retardée n’a été observé. Nous avons besoin d’un peu plus de recul et d’un plus grand nombre de données, mais cela pourrait être le signe de l’avènement d’une thérapie par cellules CAR-T encore plus efficace et plus sûre.
Résumé 256 :
Une thérapie CAR-T innovante avec anito-cel
Dans le cadre d’une autre approche visant à améliorer l’efficacité et la sécurité de la thérapie par cellules CAR-T, la nouvelle molécule anito-cel a été testée chez des patients atteints d’un
myélome récidivant. Anito-cel se distingue par un mode de liaison inédit entre les cellules CAR-T et la cellule de myélome, via une liaison par « domaine D » qui pourrait être plus précise. Presque tous les patients de cette étude ont répondu au traitement, avec un taux de réponse global (ORR) de 97 % et aucun cas de neurotoxicité retardée n’a été observé après plus d’un an de suivi chez plus de 100 patients inclus dans l’étude. Il est fortement souhaitable de disposer d’une thérapie à base de cellules CAR-T très efficace, avec un risque minimal, voire nul de neurotoxicité retardée.
Anticorps bispécifiques
Les résumés suivants montrent clairement que l’utilisation d’anticorps bispécifiques dans le myélome nous réserve encore de nombreuses avancées. Ces études sur les anticorps bispécifiques portent notamment sur leur utilisation en association, le traitement des patients à un stade plus précoce de la maladie, leur utilisation à titre de consolidation et leur utilisation en fonction de la MRD afin d’approfondir les réponses.
LBA-6 :
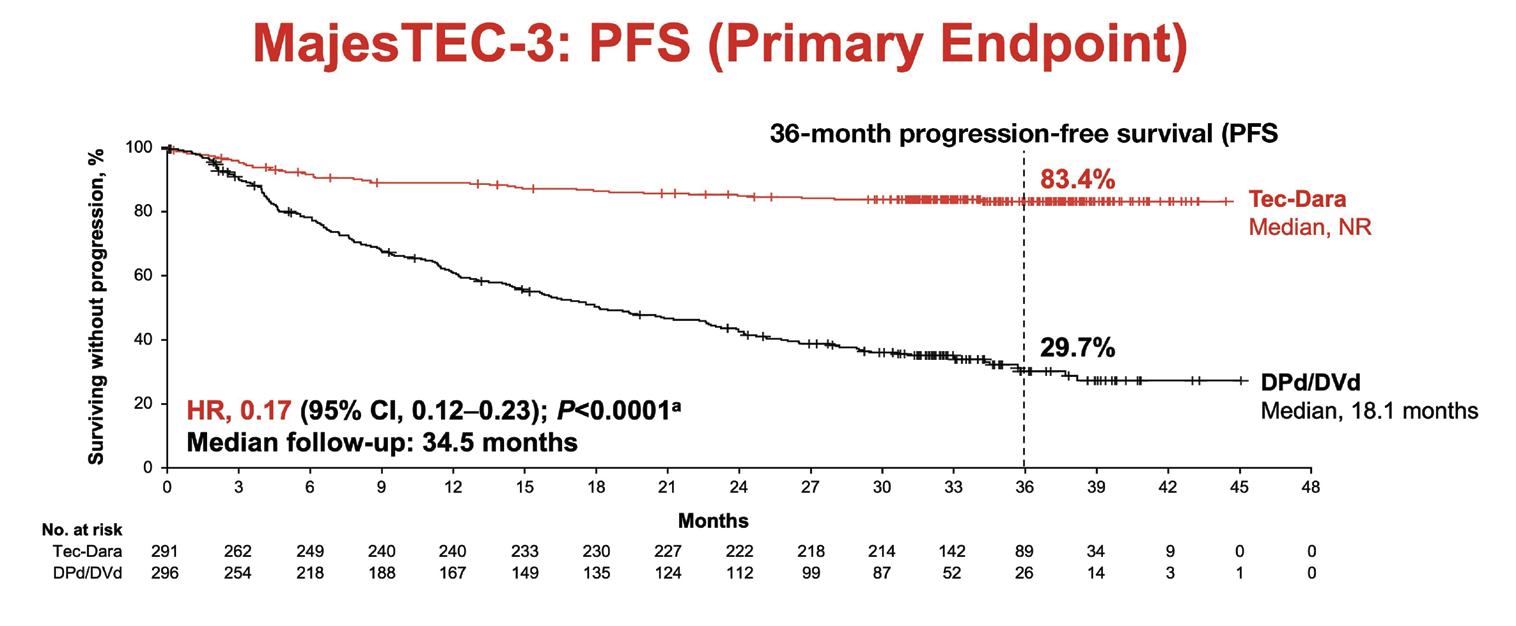
Tecvayli et Darzalex en cas de rechute précoce Il s’agit du résumé très attendu de l’essai clinique de phase III MajesTEC-3, qui compare l’association de l’anticorps bispécifique Tecvayli® (teclistamab-cqyv) et de l’anticorps monoclonal Darzalex® (daratumumab) à l’approche standard d’une triple association (3 médicaments) chez les patients ayant reçu 1 à 3 lignes de traitement antérieures.
Le LBA-6 est sans doute le résumé le plus discuté dans le cadre du myélome ; les résultats sont véritablement impressionnants. Au bout de 3 ans, 83 % des patients traités par l’association



Le groupe de travail international sur le myélome (IMWG), une entité de recherche clé de l’IMF, organise tous les ans un petit-déjeuner pour les membres présents à l’ASH afin de discuter des principales études sur le myélome qui sont présentées
LES 10 MEILLEURS RÉSUMÉS DE L’ASH − SUITE DE LA PAGE 3
Tecvayli + Darzalex étaient toujours en rémission, contre seulement 30 % des patients traités par triple association. La survie globale s’est également améliorée à 3 ans (83 % contre 65 %). De plus, les patients ont reçu moins de Tecvayli que ce qui était utilisé auparavant, car le schéma a été aligné sur celui de Darzalex : une fois par semaine pendant 8 semaines, puis une semaine sur deux pendant 16 semaines, puis une fois toutes les 4 semaines.
Il y avait toutefois un signal préoccupant quant aux infections, puisque 4 % des patients sont initialement décédés d’une infection. Mais les investigateurs de l’étude ont modifié le protocole afin de renforcer les mesures de prévention des infections, notamment par le recours aux immunoglobulines intraveineuses (IVIG). Par la suite, le nombre d’infections a diminué de manière significative. Les données issues de cette étude conduiront très certainement à une utilisation plus précoce des anticorps bispécifiques au cours de la maladie. L’utilisation d’anticorps bispécifiques dans le cadre du myélome n’est actuellement autorisée qu’après 4 lignes de traitement.
Résumé 367 :
Tecvayli et Darzalex en traitement de première ligne
La même combinaison Tecvayli + Darzalex a été testée en traitement de première ligne auprès de patients nouvellement diagnostiqués et non éligibles pour une transplantation. Il s’agissait d’un essai français qui associait Tecvayli à l’agent immunomodulateur Revlimid® (lénalidomide) dans une cohorte (groupe de patients) et Tecvayli + Darzalex dans une autre cohorte. Bien qu’il n’ait été utilisé que chez 37 patients, le taux de réponse a été de 100 % et aucun d’entre eux n’a encore rechuté après 10 mois de suivi ! Il s’agit d’une combinaison importante à surveiller, car elle pourrait conduire à l’utilisation en première ligne d’anticorps bispécifiques et remettre en question notre recours actuel à des thérapies combinées triples et quadruples (4
Survie sans progression, %
Résumé 248 : Lynozyfic pour obtenir une négativité de la MRD en première ligne J’ai intégré ce résumé dans mon Top 10 en raison de la conception novatrice de cet essai clinique. L’étude a évalué des patients atteints de myélome ayant bénéficié d’une thérapie d’induction standard (phase initiale du traitement) pour obtenir une rémission, mais qui restaient néanmoins positifs pour la maladie résiduelle minimale (MRD). Les patients ont reçu 4 cycles de l’anticorps bispécifique Lynozyfic™ (linvoseltamab-gcpt) afin d’évaluer s’il était possible d’approfondir la réponse jusqu’à une négativité de la MRD ; et, en effet, tous les patients y sont parvenus.
L’importance du statut de la MRD a été bien établie. Afin d’approfondir la réponse au traitement, l’approche originale de cette étude a consisté à ajouter un anticorps bispécifique ciblant l’antigène de maturation des lymphocytes B (BCMA), une protéine exprimée à la surface des cellules du myélome. Cette forme de traitement n’est actuellement pas utilisée pour la thérapie d’induction. Cette étude est importante, car elle élargit l’utilisation potentielle des anticorps bispécifiques, utilise la MRD pour guider la thérapie et fournit un autre mécanisme d’action pour contrôler le myélome.
Résumé 699 :
Consolidation par le cevostamab après une thérapie par cellules CAR-T
Une approche potentielle pour améliorer l’efficacité d’une thérapie par cellules CAR-T consiste à enchaîner le traitement avec un anticorps bispécifique ayant une cible différente de la thérapie par cellules CAR-T. Actuellement, la thérapie par cellules CAR-T cible l’antigène BCMA à la surface des cellules du myélome. Le cevostamab est un nouvel anticorps bispécifique en développement, conçu pour cibler un antigène
Figure 2. L’étude MajesTEC-3 sur Tecvayli plus Darzalex montre une amélioration significative de la PFS
Survie sans progression (PFS) à 36 mois
Tec-Dara
Médiane, NR
à risque
HR, 0,17 (IC à 95 %, 0,12-0,23) ; P<0,0001a
Suivi médian : 34,5 mois
DPd/ DVd
Médiane, 18,1 mois
Dans cette étude, les patients ont reçu une thérapie par cellules CAR-T, suivie de cevostamab pendant environ 6 mois. À ce stade, le traitement a été arrêté chez les patients MRD négatifs, tandis qu’il a été poursuivi chez les patients MRD positifs. Les résultats complets sont encore attendus. La conception de l’étude est fascinante, car elle vise à prolonger la durée du bénéfice de la thérapie par cellules CAR-T grâce à un nouvel anticorps bispécifique avec une cible différente à la surface des cellules du myélome. Guidée par la MRD, cette approche pourrait faire partie de l’avenir de la thérapie par cellules CAR-T dans le domaine du myélome.
Résumé 698 :
Talvey + Tecvayli chez des patients présentant une EMD
L’une des formes les plus difficiles du myélome est celle où la maladie se développe en dehors de la moelle osseuse. C’est ce que l’on appelle la maladie extra-médullaire (EMD). Historiquement, les patients atteints de myélome avec maladie extramédullaire (EMD) présentaient des taux de réponse plus faibles aux traitements et, en particulier, des durées de rémission très courtes, la maladie évoluant de façon agressive. Cette étude combine deux anticorps bispécifiques différents qui ont des cibles différentes sur la cellule myélomateuse. Talvey® (talquetamab) cible GPRC5D et Tecvayli cible BCMA.
Les données de l’étude ont mis en évidence un taux de réponse de 80 %, soit près du double par rapport à celui observé avec les traitements antérieurs, avec une durée moyenne dépassant 12 mois. Cette étude pourrait également déboucher sur une nouvelle utilisation des anticorps bispécifiques en les combinant, en particulier pour les formes de myélome difficiles à traiter.
En conclusion
Nous vivons une période vraiment passionnante dans le domaine de la recherche sur le myélome, qui débouche sur des traitements plus efficaces et plus sûrs pour nos patients et qui nous donne un véritable espoir alors que nous nous rapprochons de plus en plus d’un remède. MT
RESTEZ INFORMÉS ! Contactez la ligne d’information de l’IMF pour poser vos questions sur le myélome à l’adresse suivante InfoLine@myeloma.org ou consultez le site myeloma.org pour obtenir plus d’informations.
