Herausgegeben von der International Myeloma Foundation
ASH: Die Top-Ten-News aus der Myelomforschung
Die Jahresversammlung der American Society of Hematology präsentiert spannende Abstracts aus der Myelomforschung

Die International Working Group und das Leadership Team der IMF setzen sich im Rahmen des führenden Hämatologie-Forums für Fortschritte in der Myelomforschung ein
Diese Ausgabe von Myeloma Today wird unterstützt von AbbVie Oncology • Johnson & Johnson
Sanofi
Takeda Oncology
Die Top-Ten-Abstracts der Tagung
Von Dr. Joseph Mikhael, Chief Medical Officer der IMF
Jeden Dezember nehmen bis zu 30.000 Fachleute der Hämatologie-Community am Jahresmeeting der American Society of Hematology (ASH) teil, um die wichtigsten neuen Erkenntnisse und Forschungsdaten zu präsentieren. Dieses Mal wurden bei der ASH über 9.000 Forschungs-Abstracts eingereicht, von denen über 8.000 zur Präsentation ausgewählt wurden. Interessanterweise hatten 1.500 dieser Präsentationen das multiple Myelom zum Thema.
Das Myelom ist bei den ASH-Events nach wie vor jener Fachbereich, der am meisten an Interesse gewinnt. Die großen Fortschritte, die wir bisher in der Myelomforschung erzielen konnten, sind äußerst vielversprechend und sollen Patienten und ihren Familien Zuversicht und Hoffnung vermitteln. Hier finden Sie meine 10 Favoriten unter den vorgestellten Abstracts zum Thema Myelom, die ich in zwei Gruppen unterteilt habe. Fünf dieser Abstracts behandeln die chimäre Antigenrezeptor (CAR)-T-Zelltherapie, die fünf anderen Therapien mit bispezifischen Antikörpern.
CAR-T-Zell-Therapie
Die folgenden fünf Abstracts erläutern, wie wir die CAR-T-ZellTherapie zugänglicher und potenziell effektiver und sicherer machen können.
LBA-1:
In-vivo-CAR-T-Zell-Therapie
Dieser sogenannte „Late-Breaking-Abstract“ (LBA) war einer von insgesamt nur sechs Abstracts mit neuen Forschungsergebnissen. Hier werden die ersten drei Fälle einer angewandten In-vivo- CAR-T-Zell-Therapie beschrieben, ein Prozess, der direkt im Körper des Patienten stattfindet. Bei der traditionellen CAR-T-Zell-Therapie werden die Zellen ex vivo verändert, also außerhalb des Körpers. Dabei werden T-Zellen aus dem Blut extrahiert, im Labor modifiziert und anschließend
re-infundiert. Im Rahmen der neuartigen In-vivo-Therapie wird der Wirkstoff, der die T-Zellen verändert, dem Körper direkt zugeführt. Dadurch entfallen die Blutentnahme, das Harvesting, das Engineering und das Re-Infundieren der CAR-T-Zellen.
Die In-vivo- CAR-T-Zell-Therapie ist ein sehr vielversprechendes Konzept. Diese neue Entwicklung könnte die CAR-T-Zelltherapie einer größeren Patientenpopulation zugänglich machen, was derzeit eine der Herausforderungen im Bereich der MyelomBehandlung darstellt und zu großen Ungleichheiten führt. Im Rahmen einer klinischen Studie erhielten Teilnehmende eine In-vivo- CAR-T-Zelltherapie und erreichten innerhalb eines Monats einen negativen MRD-Status, während gleichzeitig weniger Nebenwirkungen als bei der traditionellen Ex-vivoTherapie beobachtet wurden. Alle Teilnehmenden hatten multiples Myelom mit hohem Risiko (HRMM) und waren stark vorbehandelt. Die In-vivo- CAR-T-Zell-Therapie ist eine hocheffektive, sichere und zugängliche Art der Myelomtherapie und daher wegweisend für die Zukunft.
Abstract Nr. 94:
Carvykti: Langzeitnachbeobachtung von Patienten mit Standardrisiko Carvykti® (Ciltacabtagen-Autoleucel, auch „Cilta-Cel“) ist eine CAR-T-Zell-Therapie, die derzeit als Zweitlinientherapie eingesetzt wird (frühestens beim Auftreten des ersten Rezidivs). Die Therapie wurde in folgenden beiden Studien untersucht: CARTITUDE-1 mit Teilnehmenden, die mit über 4 (im Durchschnitt 6) Therapielinien vorbehandelt waren, sowie CARTITUDE-4 mit Teilnehmenden, die mit 1 bis 3 Therapielinien vorbehandelt waren. Bei Patienten mit Standardrisiko waren die Ergebnisse der Langzeitnachbeobachtung besonders interessant.
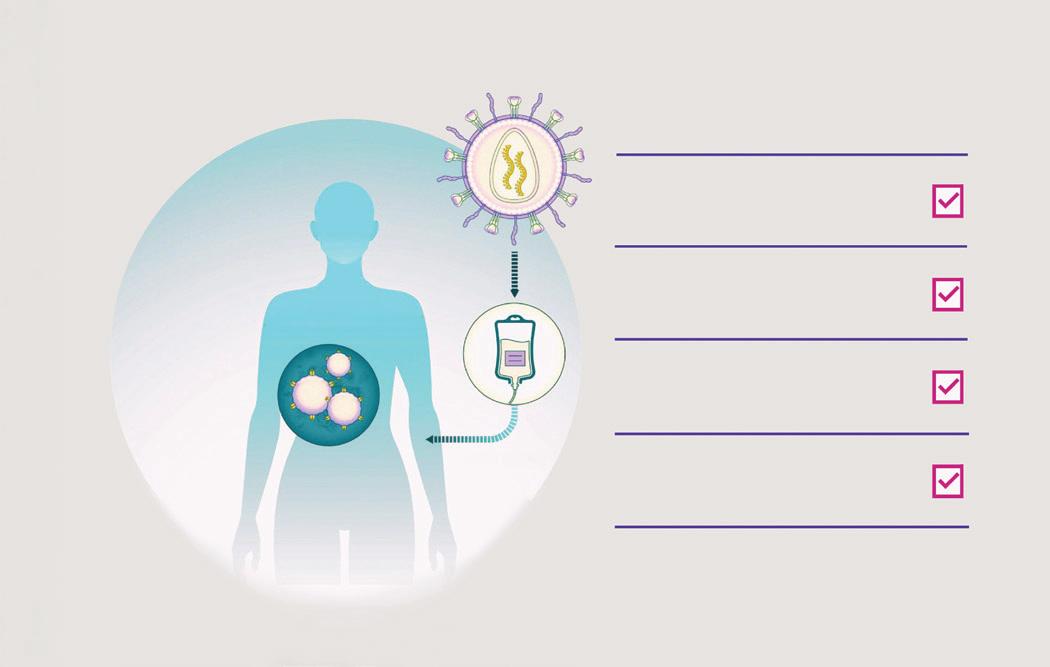
Direktinfusion
Die Vorbehandlung zur Lymphozytendepletion entfällt
Beim frühen Rezidiv betrug das progressionsfreie Überleben (PFS) nach 30 Monaten 80 %. Beim spät auftretenden Rezidiv betrug das PFS 60 %. Die CAR-T-Zelltherapie wird üblicherweise bei Hochrisikopatienten eingesetzt, jedoch sehen wir mittlerweile auch bei auch bei Patienten mit Standardrisiko neue, sehr überzeugende Remissionsdaten. Dank der CARTITUDE-Studie stehen uns nun sehr spezifische Daten zur Verfügung, die bei Patienten mit Standardrisiko in die Behandlungsentscheidung bezüglich einer CAR-T-Zell-Therapie einbezogen werden sollten.
Vereinfachte Logistik –höhere Verfügbarkeit
Keine ex vivo-Kultur –potenziell bessere T-Zell-Qualität
Reduzierte Kosten für Rohsto e und Fertigung
Abstract Nr. 1034:
Verbesserung der Sicherheit von Carvykti Eine große Herausforderung bei der Behandlung mit Carvykti sind verzögerte Nebenwirkungen neurologischer Art, d. h. eine Neurotoxizität, die typischerweise einen Monat nach der Behandlung oder sogar später auftreten kann. Diese Effekte können durchaus schwerwiegend ausfallen und Symptome verursachen, die einer
der American Society of Hematology
Parkinson-Erkrankung oder dem Guillain-Barré-Syndrom ähneln. Die Kontrolle dieser seltenen Neurotoxizität ist ein Schwerpunkt unserer Forschung, während wir daran arbeiten, die Sicherheit und Wirksamkeit unserer Behandlungsoptionen sicherzustellen. Mehr als 750 Teilnehmende wurden in einer klinischen Studie mit Carvykti behandelt und es konnten zwei maßgebliche Schlussfolgerungen gezogen werden. Erstens: Die Risikofaktoren für das Auftreten einer Neurotoxizität lassen sich durch eine gezielte „Bridging-Therapie“ besser kontrollieren; diese wird nach der Entnahme der T-Zellen und vor dem Re-Infundieren der Zellen verabreicht. Zweitens: Die absolute Lymphozytenzahl (ALC) ist ein potenzieller Risikoindikator hinsichtlich des Auftretens einer Neurotoxizität, d. h. eine geeignete Strategie zur ALC-Reduktion könnte sinnvoll sein.
Abstract Nr. 258:
Doppelte CAR-T-Zelltherapie mit BCMA- und CD19-Targets (FasTCAR-T)
Um die Behandlung noch wirksamer zu gestalten, wird derzeit eine CAR-T-Zelltherapie mit zwei Antigen-Targets untersucht, die spezifischer an Myelomzellen binden kann. Dazu wurde das Molekül GC012F/AZD0120 getestet, unter anderem bei Patienten mit neu diagnostiziertem multiplem Myelom (NDMM). Die Behandlung erwies sich als hochwirksam: Die Ansprechrate betrug bei den 30 Teilnehmenden 100 %, und es kam zu keinem einzigen Fall einer verzögerten Neurotoxizität. Diese neue Behandlungsoption muss natürlich mit größeren Datenmengen und über einen längeren Zeitraum hinweg genauer evaluiert werden, jedoch könnte sich daraus eine sehr wirksame und sichere CAR T-Zell-Therapie mit viel Zukunftspotenzial entwickeln.
Abstract Nr. 256:
Eine neuartige CAR-T-Zelltherapie mit Anito-cel Ein weiterer Ansatz zur Verbesserung der Wirksamkeit und Sicherheit der CAR-T-Zelltherapie umfasst das neue Anito-celMolekül zur Behandlung des rezidivierten Myeloms. Anito-cel ist eine CAR-T-Zelltherapie mit „D-Domain“-Binder, die potenziell präziser ist. In einer dazu durchgeführten klinischen Studie mit über 100 Teilnehmenden und einer Nachbeobachtungsdauer von mehr als einem Jahr kam es zu einer Gesamtansprechrate von 97 % ohne Auftreten von verzögerter Neurotoxizität. Ziel ist eine hochwirksame CAR-T-Zell-Therapie, die mit einem minimalen Neurotoxizitätsrisiko verbunden ist.
Bispezifische Antikörper
Die folgenden Abstracts zeigen, dass wir in Sachen bispezifische Antikörper noch viele Neuerungen in der Myelom-Therapie erwarten können. Diese Studien zu bispezifischen Antikörpern befassen sich unter anderem mit Kombinationstherapien, einem früheren Behandlungsbeginn, Konsolidierungstherapien sowie MRD-zentrierte Therapien, um das Ansprechen insgesamt zu verbessern.
LBA-6:
Tecvayli und Darzalex beim frühen Rezidiv
Der mit Spannung erwartete brandneue Abstract der Phase-IIIStudie MajesTEC-3 vergleicht eine Kombinationstherapie (bispezifischer Antikörper Tecvayli® (Teclistamab-cqyv) plus monoklonaler Antikörper Darzalex® (Daratumumab)) mit der Standardbehandlung (Triplet-Kombination) bei Teilnehmenden, die zuvor 1 bis 3 Therapielinien erhalten haben.



Die International Myeloma Working Group (IMWG), eine der zentralen IMF-Forschungsgruppen, lädt lädt ihre Mitglieder auf der ASH zu einem zu einem jährlichen Breakfast-Event ein, um die wichtigsten Studien vorzustellen.
DIE TOP-TEN-ABSTRACTS DER ASH – FORTSETZUNG VON SEITE 3
LBA-6 ist vermutlich der meistdiskutierte Abstract zum Thema Myelom; die enthaltenen Erkenntnisse sind bemerkenswert. Nach 3 Jahren waren 83 % der Teilnehmenden unter Tecvayli plus Darzalex noch immer in Remission, im Vergleich zu 30 % in der Triplet-Gruppe. Auch die Gesamtüberlebensrate war nach 3 Jahren im Vergleich besser (83 % gegenüber 65 %). Außerdem war Tecvayli geringer dosiert als üblich, da die Intervalle wie folgt an das Darzalex-Dosierschema angepasst wurden: 8 Wochen lang einmal wöchentlich, dann 16 Wochen alle zwei Wochen und anschließend alle 4 Wochen einmal.
Es gab jedoch ein besorgniserregendes Sicherheitssignal: 4 % der Teilnehmenden erkrankten an einer Infektion mit tödlichem Verlauf. Daraufhin wurde jedoch der Prüfplan modifiziert, um das Infektionsrisiko zu verringern, unter anderem durch die Verabreichung von Immunglobulin i.v. (IVIG). Dies führte zu wesentlich geringeren Infektionsraten. Die Daten aus dieser Studie sprechen im Wesentlichen für einen frühen Einsatz von bispezifischen Antikörpern. Derzeit sind bispezifische Antikörper in der Myelom-Behandlung jedoch erst nach vier Therapielinien zugelassen.
Abstract Nr. 367: Tecvayli und Darzalex als Erstlinientherapie
Die Kombination aus Tecvayli und Darzalex wurde bei neu diagnostizierten Patienten, für die eine Transplantation nicht in Frage kam, als Erstlinientherapie getestet. Dies fand im Rahmen einer französischen Studie mit zwei Behandlungsgruppen statt: Kohorte 1 mit Tecvayli und dem Immunmodulator Revlimid® (Lenalidomid) und Kohorte 2 mit der Kombinationstherapie Tecvayli plus Darzalex. Die Ansprechrate dieser neuen Kombinationstherapie, die an 37 Teilnehmenden getestet wurde, betrug 100 %. Die Nachbeobachtung läuft seit 10 Monaten und es kam bislang zu keinem Rezidiv! Diese Kombinationstherapie sollten wir im Auge behalten, denn sie könnte dazu führen, dass bispezifische Antikörper bald in der Erstlinie zum Einsatz kommen und sich die Rolle von Triplet- und Quadrupeltherapien drastisch verändert.
Abstract Nr. 248:
Negativer MRD-Status mit Lynozyfic in der Erstlinie
Dieser Abstract steht wegen des interessanten neuen Studiendesigns auf meiner Top-Ten-Liste. Die Studie untersuchte Myelom-Patienten, die nach der Standardinduktionstherapie (also nach der ersten Behandlungsphase) eine Remission erreichten, aber weiterhin einen positiven MRD-Status (minimale Resterkrankung) aufwiesen. Die Teilnehmenden erhielten 4 Behandlungszyklen mit dem bispezifischen Antikörper Lynozyfic™ (Linvoseltamab-gcpt) und alle konnten ihren negativen MRD-Status aufrechterhalten.
Es ist unbestritten, dass der MRD-Status ein wichtiger Faktor ist. Um das Ansprechen zu verstärken, wurde in dieser Studie zusätzlich ein bispezifischer Antikörper eingesetzt, dessen Target das B-Zell-Reifungsantigen (BCMA) ist, ein Protein, das auf der Oberfläche von Myelomzellen zu finden ist. Diese Art der Behandlung wird in der Induktionsphase derzeit nicht verwendet. Die Studie ist von großer Bedeutung, da sie das Einsatzfeld bispezifischer Antikörper erweitert, den MRDStatus stärker in den Mittelpunkt rückt und einen zusätzlichen Wirkmechanismus zur Bekämpfung des Myeloms erschließt.
Abstract Nr. 699:
Cevostamab-Konsolidierungstherapie nach CAR-T-Zell-Therapie
Um die Wirksamkeit der CAR-T-Zelltherapie zu steigern, könnte im Anschluss daran ein bispezifischer Antikörper eingesetzt werden, der auf ein anderes Target abzielt. Derzeit zielt die CAR-T-Zelltherapie auf das BCMA-Antigen auf der Oberfläche der Myelomzelle ab. Cevostamab ist ein neuer bispezifischer Antikörper, der auf das Antigen FcRH5 abzielt.
Die Teilnehmenden erhielten in dieser Studie eine CAR-TZelltherapie, gefolgt von einer etwa sechsmonatigen Cevostamab-Behandlung. Danach setzten lediglich die Teilnehmenden mit MRD-positivem Status die Behandlung
Abbildung 2. Die Studie MajesTEC-3 mit Tecvayli plus Darzalex zeigt eine signifikante PFS-Verbesserung
Progressionsfreies Überleben (PFS): 36 Monate
Tec-Dara
Median, NR
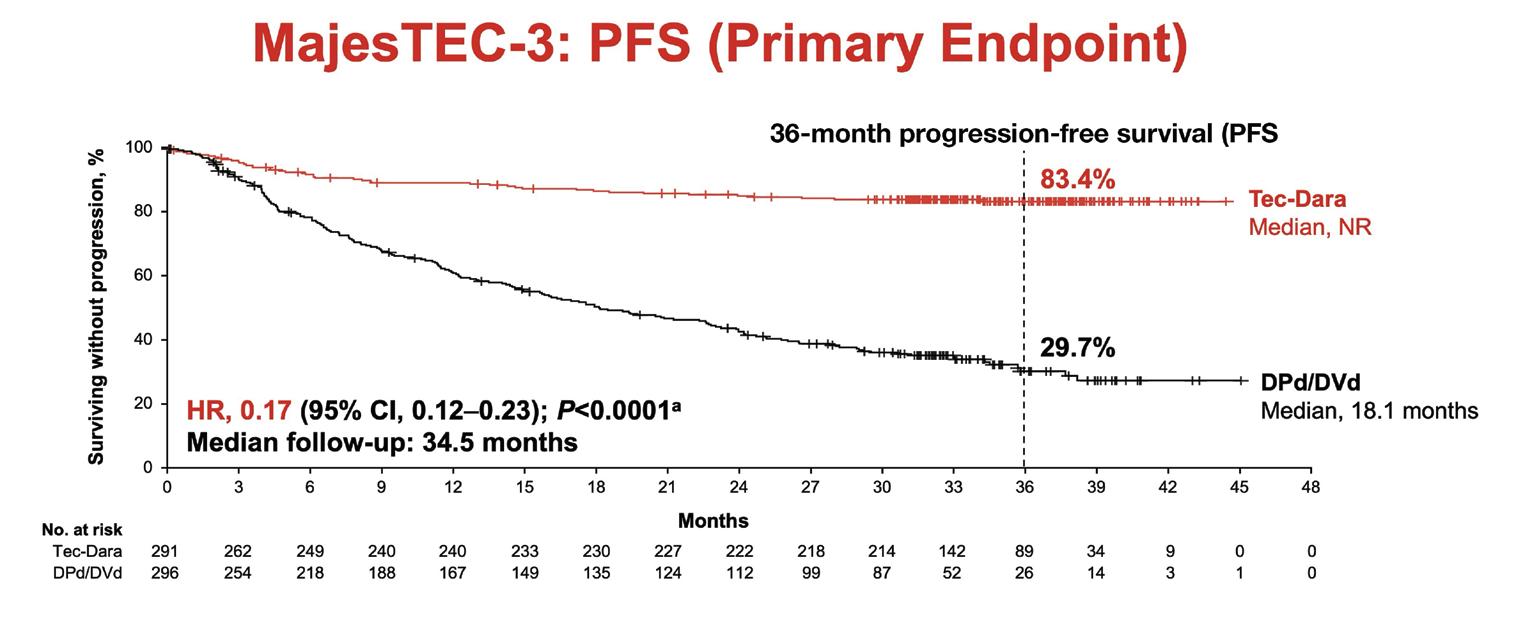
Anz. d. Risikopat.
HR, 0,17 (95%-KI: 0,12-0,23); p<0,0001a
Medianes Follow-up: 34,5 Monate
DVd Median; 18,1 Monate
Behandlung abgebrochen. Die vollständigen Studienergebnisse sind noch nicht verfügbar. Das Studiendesign ist besonders interessant, da es darauf abzielt, die Wirkungsdauer der CAR-TZelltherapie durch den Einsatz eines neuen bispezifischen Antikörpers zu verlängern, der ein anderes Target hat. Mit dem Fokus auf dem MRD-Status könnte diese neue Behandlungsoption die CAR-T-Zell-Therapie revolutionieren.
Abstract Nr. 698:
Talvey plus Tecvayli bei EMD
Eine der größten Herausforderungen bei der Behandlung des Myeloms liegt vor, wenn sich die Erkrankung außerhalb des Knochenmarks manifestiert. Dies wird als extramedulläre Erkrankung (EMD) bezeichnet. Bei der Behandlung des Myeloms mit EMD sehen wir in der Praxis generell ein geringeres Ansprechen und eine verkürzte Remissionsdauer, denn diese Art der Krankheit ist sehr aggressiv. Diese Studie kombiniert zwei verschiedene bispezifische Antikörper mit unterschiedlichen Targets auf der Oberfläche der Myelomzellen. Talvey® (Talquetamab) zielt auf GPRC5D ab, Tecvayli auf BCMA.
Die Gesamtansprechrate betrug in dieser Studie 80 % (fast doppelt so hoch wie die bisherigen Ansprechraten mit anderen Medikamenten) und die Dauer des Ansprechens belief sich auf über 12 Monate. Dies sind bemerkenswerte Ergebnisse. Die Studie könnte zu einer neuartigen Kombination von bispezifischen Antikörpern führen, insbesondere für schwer zu behandelnde Formen des Myeloms.
Fazit
Es ist eine spannende Zeit in der Myelomforschung, in der immer wirksamere und sicherere Therapien entwickelt werden. Dies gibt Hoffnung, da wir einer Heilung Schritt für Schritt näher kommen. MT
BLEIBEN SIE INFORMIERT Wenden Sie sich mit Ihren Fragen und Anliegen zum Myelom an die IMF-InfoLine unter InfoLine@myeloma.org oder besuchen Sie myeloma.org für weitere Informationen.
