MEDICIÓN DIRECTA DE LA CINEMÁTICA DE LA NATACIÓN Y EL BUCEO del atún rojo del atlántico gigante (thunnus thynnus)
VISÍTENOS EN CONACUA ‘19, 27 Y 28 DE NOVIEMBRE STAND A5 SALÓN FIGLOS, LOS MOCHIS, SINALOA. EL MICROBIOMA, LA ACUAPONIA y el futuro de los alimentos
ESTÁNDARES DE BIODEGRADABILIDAD PARA BOLSAS DE TRANSPORTE Y PELÍCULAS plásticas en ambientes acuáticos: una revisión crítica. EL KRILL, SUPER INGREDIENTE DE ALTO VALOR NUTRICIONAL Y FUNCIONAL en la alimentación de camarones
Vol. 15 No. 5 JULIO 2019 www.industriaacuicola.com




El microbioma, la acuaponia y el futuro de los alimentos.
Beijing respalda la revolución verde de la acuicultura.
Medición directa de la cinemática de la natación y el buceo del atún rojo del Atlántico gigante (Thunnusthynnus)
La Importancia de la digestibilidad en los alimentos para acuacultura.
Estándares de biodegradabilidad para bolsas de transporte y películas plásticas en ambientes acuáticos: una revisión crítica.
El Krill, super ingrediente de alto valor nutricional y funcional en la alimentación de camarones.
Incremento de producción en granja de engorda de tilapia por aplicación de SoluVet Acuícola.
Se abre convocatoria al Premio Nacional de Innovación Pesquera y Acuícola 2019.














Los probLemas de La
contaminación
de Los mares por pLásticos y su consumo
Los plásticos en su momento revolucionaron la industria y las economías mundiales, se descubrió para bajar costos y hacer más práctico el uso de innumerables productos y accesorios, pero esto hoy en día se salió de control, aquel material maravilloso hoy nos está matadando, nos envenena poco a poco y los océanos son la primera víctima, con ellos todos. Por el momento, despertemos nuestra conciencia sobre la contaminación de nuestros océanos: 5 zonas de acumulación en los océanos: O. Índico, O. Atlántico, O. Pacífico, 5,000 metros aproximadamente es la profundidad a la que se han encontrado restos de plásticos, 5% - 9% de todo el plástico producido hasta la actualidad a nivel mundial, se ha reciclado, 2.1 millones de toneladas anuales de plástico se producía en 1950, 147 millones en 1993 y más de 400 millones de toneladas anuales en 2015, 8 - 13 millones de toneladas de plástico terminan acumulándose en los océanos cada año, 12% se ha incinerado, 79% de los plásticos producidos, terminan en vertederos ó en el medioambiente en general; En Océanos: 80% de los residuos plásticos proviene de actividades antropocéntricas en los continentes y el 20% restante de la actividad marítima. 5 años tiempo de degradación de las colillas de cigarros, 10-20 años las suelas de zapatos, 55 años bolsas, 65-75 años vasos desechables, 100 años encendedores, 400 años cubiertos (cucharas, cuchillos, tenedores) 500 años botellas, 600 años hilo de pescar, por ejemplo. >1,000,000 de muertes de aves, asociado a plásticos, al año; 100,000 mamíferos marinos mueren al año a consecuencia de los plásticos, 60-80% de la composición de deshechos marinos son plásticos de menos de 5mm, o “microplásticos” no biodegradables y tóxicos, Disruptores endócrino,:Parte de la toxicidad propia del plástico, provocada por compuestos químicos del tipo bisfenol, empleado en la producción de policarbonato y otros plásticos y conocido como potente cancerígeno; pero además, los plásticos tienen la propiedad de atraer y acumular contaminantes hidrofóbicos (del tipo aceitosos) presentes en el agua de mar como contaminantes también, por ejemplo DDT y PCB`s, provenientes de actividades económicas del hombre. Cuando estos microplásticos y nanopartículas son ingeridas por algún organismo marino, la cadena alimentaria marina queda contaminada llegando hasta el consumidor final, el hombre. Es fácil pensar que la “red trófica” de la que depende el hombre, está contaminada. Desde los seres marinos que componen el plancton consumen microplásticos y nanopartículas, incluso por organismos filtradores como ciertos moluscos y otros organismos que se alimentan de ellos, están ingiriendo los fragmentos de plástico. El impacto de estos contaminantes es directo en peces, moluscos, crustáceos, mamíferos marinos, aves y al ser humano. El plástico no es malo, lo malo es la poca ó nula conciencia de la población mundial por el manejo responsable de los plásticos.
Por nuestra parte qué podemos hacer ó debemos estar haciendo?
*Dejar de usar tanto plástico si es que no tenemos la conciencia de su correcto manejo,
*No usar artículos y envases de un solo uso: vasos desechables, contenedores de comida (para llevar) bolsas de plástico, etc.
*Educar desde la escuela y la familia, despertando la conciencia de respeto al medio ambiente y uso responsable de productos plásticos.
*Impulsar proyectos de investigación y desarrollo de plásticos biodegradables y programas de reciclaje, aunque no todo lo reciclable es Biodegradable, hasta en la industria aeronáutica y automovilística hay plásticos reciclados reforzados con fibra de carbono.
Nosotros en la industria acuícola en su conjunto, cuándo empezaremos a usar plásticos biodegradables? Solo por mencionar un ejemplo, en aquellos casos en los que el transporte de larva de crustáceos y alevines de peces, para su transporte, se hace en bolsas de plástico, hasta en los negocios de mascotas, en donde compré el pececito rojo para la pecera de mi hija, te los entregan en bolsas de plástico. La próxima vez que nos leamos, platicaremos de la relevancia del KRILL, mientras tanto, ya estás pensando cómo vas a contribuir para reducir la contaminación de tus mares y dejar un ecosistema saludable a las próximas generaciones?
DIRECTORIO
DIRECTOR
Daniel Reyes Lucero daniel.reyes@industriaacuicola.com
ARTE Y DISEÑO
LDG. Verónica Analy Medina Vázquez areacreativa@industriaacuicola.com
VENTAS
Verónica Sánchez Díaz ventas@industriaacuicola.com
SUSCRIPCIONES
Jannet Aguilar Cobarruvias suscripciones@industriaacuicola.com
REPORTAJES
Verónica Sánchez Díaz ventas@industriaacuicola.com
CONTABILIDAD Y FINANZAS
C.P. Alejandrina Zavala Osuna administracion@industriaacuicola.com
COLABORADORES
PhD. Ricardo Sánchez Díaz Roberto Lopéz Trinidad Virginia Ibarra Rojas
COMENTARIOS Y SUGERENCIAS
daniel.reyes@industriaacuicola.com
OFICINAS
MATRIZ
Av. Carlos Canseco No. 6081-1 Mediterraneo Club Residencial C.P. 82113 Mazatlán, Sinaloa. Tel/Fax (669) 981-8571
SUCURSAL
Coahuila No. 155-A Norte Col. Centro C.P. 85000 Cd. Obregón, Sonora, México Tel/Fax (644) 413-7374
INDUSTRIA ACUICOLA, Año 15, No. 5 - Julio 2019, es una publicación bimestral editada por Aqua Negocios, S.A. de C.V. Av. Carlos Canseco No. 6081-1 Mediterraneo Club Residencial Mazatlán, Sinaloa. C.P. 82113. Teléfono (669) 981 85 71 www.industriaacuicola.com editor responsable: Daniel Reyes Lucero daniel.reyes@industriaacuicola.com Número de Certificado de Reserva otorgado por el Instituto Nacional del Derecho de Autor: 04-2012-051010450800-102. Número de Certificado de Licitud de Contenido: 11574 y número de Certificado de Licitud de Título: 14001, emitidos por la Comisión Calificada de publicaciones y Revistas Ilustradas de la Secretaría de Gobernación. Registro Postal PP25-0003. Permiso SEPOMEX No. PP25-0003, Impresión Celsa Impresos, Cuencamé 108, 4a Etapa Parque Industrial Lagunero Gómez Palacio, Dgo. 35070 México. www.celsaimpresos.com.mx La publicidad y promociones de las marcas aquí anunciadas son responsabilidad de las propias empresas. La información, opinión y análisis de los artículos contenidos en esta publicación son responsabilidad de los autores y no refleja, necesariamente, el criterio de esta editorial. Queda estrictamente prohibida la reproducción total o parcial de los contenidos e imágenes de la publicación sin previa autorización.

¿De dónde vienen los ingredientes de su cena? ¿Una granja en Iowa, tal vez, o el Océano Atlántico?
¿Y si se trata de un laboratorio, una computadora o una granja de insec- tos? Estos nuevos sistemas agrícolas están proliferando, cambiando el có- mo y dónde producimos alimentos.
Los avances científicos también están transformando profundamente la producción de alimentos. Entre los más poderosos se encuentra nuestra profunda comprensión del microbioma, y su papel a menudo oculto en nuestro sistema alimentario, desde el suelo hasta el intestino.
Una empresa que está innovando con estos modelos y descubri- mientos es Edenworks, una granja de acuaponia cubierta en la ciudad de Nueva York. Platicando con el CEO y cofundador Jason Green sobre el microbioma, los enfoques de ecosistemas completos y el futuro de la acuaponia.
¿Qué hace Edenworks?Edenworks (Jason Green) es la granja cubierta con mayor biodiversidad del mun-

do. Nuestra misión es reemplazar el suministro de alimentos globaliza- do de hoy, con productos que sean locales, orgánicos y de bajo costo. Diseñamos y operamos granjas ver- ticales en las que cultivamos productos como hojas verdes, salmón y camarones a través de la acuaponia.
¿Qué quiere decir con "acuaponia" y cuáles son sus beneficios?
La acuicultura es acuicultura, ya sea en tanques en tierra, como lo estamos haciendo en Brooklyn, o en jaulas en los fiordos noruegos, o en los estanques tailandeses. Ese es el "aqua" en la primera mitad de la acuaponia. La otra mitad es hidropónica: cultivar plantas mediante el suministro de fertilizantes a través de su agua de riego.
Creemos que la acuaponia propor- ciona un mejor modelo para nosotros, el consumidor y el planeta. Nuestros rendimientos son más del doble del promedio para la agricul- tura vertical, y lo hacemos al mismo tiempo que reducimos los niveles de fertilizantes en un 90%. Nuestro enfoque elimina las bacterias dañinas
como la E. coli y otros patógenos que son motivo de gran preocupación para los consumidores: los vegetales de hoja verde represen- tan solo el 22% de todos los casos de enfermedades transmitidas por los alimentos en los EE. UU., la tasa más alta para un solo alimento. La forma en que estamos creciendo es un proceso más seguro. Y, en términos de sostenibilidad, no usamos fertilizantes agregados ni químicos, y no generamos escurrimientos de nuestra agricultura o piscicultura.


¿Por qué se le llama la granja cubierta con mayor biodiversidad del mundo?
La clave de la biodiversidad es construir redes alimentarias. Hasta la fecha, hemos cultivado cuatro especies de peces, más de 80 va- riedades de hojas verdes y todo, desde tomates hasta nabos. Pero la biodiversidad no es simplemente la cantidad de verdes que puedo cultivar, sino la cantidad de capas que puedo construir en mi red alimenticia. De eso se tratan los ecosistemas. No solo estamos cultivando peces y plantas; También estamos cultivando el microbioma.
¿Cómo Podría describir el microbioma y cómo se relaciona con nuestros sistemas alimentarios?
El microbioma es la capa invisible de bacterias y hongos en cada ser vivo. Como consumidor, uno podría estar familiarizado con el microbioma intestinal. Muchas de nuestras funciones biológicas bá- sicas como la digestión de alimen- tos, la absorción de nutrientes y la regulación de las hormonas están a cargo de las bacterias que nos colonizan. Antes, todas las bacterias se trataban como malas, pero ahora entendemos que el microbioma desempeña una función esencial en nuestro sistema inmunológico. In- cluso la salud de nuestros cerebros es impulsada por las bacterias en nuestras entrañas, y las condiciones como la depresión ahora están vinculadas a trastornos digestivos. Las plantas tienen un microbioma como los humanos. Mientras que la ciencia de las plantas se ha cen- trado principalmente en productos que suprimen el microbioma, ahora sabemos que el microbioma de las plantas es lo que permite la absor- ción de nutrientes y la resistencia

a las enfermedades, que a su vez impulsan el rendimiento. La única forma de obtener ese beneficio es a través de ecosistemas completos. No se puede cultivar un microbioma saludable en un monocultivo. El uso intensivo de fertilizantes y pesticidas reduce tanto la cantidad como la diversidad de microbios en el ambiente. Un gramo de suelo de una granja saludable tiene de 100 millones a mil millones de células bacterianas, en comparación con solo unos 10,000 en suelos muy degradados que se han cultivado y se les han aplicado productos químicos repetidamente.
¿Cómo han estado cambiando los descubrimientos de microbiomas en la industria alimentaria, incluida su propia empresa?
El microbioma ha sido llamado la mitad oculta de la naturaleza. Es el área más apasionante de la ciencia y la tecnología de hoy. Se están haciendo descubrimientos sobre los fundamentos de la salud humana; y es la vertical mejor financiada dentro de la tecnología agrícola. Indigo Ag, por ejemplo, es la empresa con mayor financiación en el sector: ha recaudado más de $ 600 millones en el desarrollo de semillas que cubren con microbios que pueden mejorar los rendimientos en un 10% a un 15% en el campo.
En Edenworks, estamos demostrando que cultivar un ecosistema robusto y saludable en interiores, optimizando para la salud del mi- crobioma, es aproximadamente 50 veces más poderoso que producir en el amplio acre rociando fertili- zante. Al cultivar peces y utilizar sus desechos para fertilizar nuestras plantas, nuestra estrategia de biodi- versidad logra interacciones no solo entre las plantas y los animales, si-
no también dentro del microbioma en sí, que regula todo el sistema. ¿Los productos acuaponicos son accesibles para la mayoría de los consumidores? ¿Cómo están cambiando las estructuras de costos?
Para que la agricultura de interior se amplíe, debe ser a la paridad de cos- tos con la producción de campo. Las estructuras de costos están cambiando a favor del cultivo en interiores: comprar nuestros vegetales lavados, empacados y listos para comer en Whole Foods es realmente menos costoso que comprar microgreens sin lavar a granel del distribuidor de productos al por mayor más grande de la ciudad de Nueva York. Esa es una transformación dramática.
Crecer en campos tradicionales está bajo una enorme presión. El trabajo se está volviendo más caro. Los rendimientos pueden oscilar en un 25% o más entre cada cosecha. Todo eso tiene un impacto en el balan- ce final de las granjas. Al crecer en interiores, tenemos un proceso de producción predecible. También nos estamos beneficiando de una curva de costos de tecnología ma- siva. Por ejemplo, los duros costos de la iluminación con LED se han reducido drásticamente: el costo de un diodo se ha reducido en un 90% en los últimos cinco años. Al mismo tiempo, la automatización se está volviendo mucho menos costosa. Y con el desarrollo de nuevas herramientas genéticas, podemos cuantificar lo que hay en nuestro microbioma para mejorar continuamente la calidad, aumentar los rendimientos y reducir los costos. ¿Cree que la agricultura de interior, y en particular la acuapónica, es un modelo escalable en los Esta-
dos Unidos y en todo el mundo? Si. La proporción de peces cultivados ahora es más grande que los peces silvestres a nivel mundial. Estamos viendo una explosión de agricultura de interior. Se están construyendo proyectos en los Estados Unidos por una suma de 500 millones de dólares. La mayor empresa camaronera del mundo, en Tailandia, está trasladando el 100% de su producción al interior en los próximos cinco años. Nuevas empresas de interior están surgiendo en lugares como China, especialmente en megaciudades. Parte de esto se debe a inquietudes sobre la seguridad alimentaria: el legado de la fabricación en China provocó la contaminación de meta- les pesados en el suelo, por lo que muchos han estado trasladando la producción de frutas y verduras a invernaderos y granjas verticales.
¿Cómo ve el futuro de esta industria?
Dentro delos EE. UU., estamos preparados para un crecimiento masivo en la acuicultura. Los EE. UU. es el tercer mayor consumidor de maris- cos del mundo después de China y Japón, y actualmente importamos el 90% de los mariscos que comemos. Así que hay un imperativo tan- to económico como de seguridad alimentaria. Y ahora EE. UU. tiene los costos más bajos de electricidad industrial en el mundo: es más barato comprar electricidad industrial en muchas partes de los EE. UU., que en las principales zonas de fa- bricación de China, y más barato construir una instalación de acuicultura en tierra en los EE. UU., que en cualquier otro lugar del mundo.
Ha habido una explosión de proyectos a nivel mundial, pero aún no están a escala. Tan pronto como alguien pueda llegar allí con la tecnología adecuada, y pueda demostrar rentabilidad, ese es el
punto de inflexión. Hay una gran competencia en el mercado para la agricultura y la acuicultura en in- teriores. El capital está fluyendo. Tenemos personas muy inteligentes que trabajan en estos problemas. Creo que estamos dentro de los cin- co años de ese punto de inflexión.
Esta entrevista es parte de una serie sobre cómo la tecnología y cómo la innovación están transformando los sistemas alimentarios y ecológi- cos, y cómo hacerlo bien para las personas y el planeta. La entrevista fue editada por claridad y duración.
Crédito Lorin Fries
Como muchos de ustedes saben, estoy fascinado por las transformaciones en curso en la revolución tecnológica actual. Sin embargo, pocos de ellos abordan los mayores desafíos sociales y ambientales de nuestro tiempo. La mitad de la población mundial está desnutrida. El cambio climático continúa a buen ritmo. Mi serie se basa en ideas de empresas, gobiernos e instituciones sociales, explorando cómo podemos diseñar y escalar la innovación centrada en el ser humano con el "propósito" en el centro, y hacer las preguntas correctas en el camino. He centrado mi carrera en los sistemas alimentarios mundiales y la sostenibilidad ambiental, recientemente como Directora de Colaboración de Sistemas Alimentarios con el Foro Económico Mundial, y anteriormente con la Iniciativa de Responsabilidad Social Corporativa de la Universidad de Harvard, la Agencia de los Estados Unidos para el Desarrollo Internacional y Save the Children en Uganda. Vivo en el Área de la Bahía de San Francisco y he trabajado en África, Asia y América Latina. Recibí una maestría de la Harvard Kennedy School.
Fuente: https://www.forbes.com/ sites/lorinfries/2019/04/03/themicrobiome-aquaponics-and-thefuture-of-food/#21c065051b3b


El anuncio acumuló 30,000 visitas en un sitio web de la industria china y las fuentes en el país lo descri- bieron como "enorme". El jefe del Departamento de Pesca del Minis- terio de Agricultura de China, Zhang Xianliang, dijo que "no tiene precedentes" y que sería " muy importante "para el sector acuícola de China" en los próximos dos a tres años".
Wang Songlin, presidente de la Sociedad de Conservación Marina de Qingdao, informó que habrá claros ganadores. Muchos productores de camarón de la región de China que utilizan sistemas de cultivo intensivo y de baja tecnología en áreas costeras, posiblemente enfrentan una mayor presión reguladora, dijo. El documento titulado inocuamente “Ideas para Acelerar el Desarrollo Verde del Sector Acuícola de China no se destaca de inmediato.
Pero es el sello del Consejo de Estado de China, el cuerpo admi- nistrativo principal del gobierno chino, integrado por un selecto grupo de 35 funcionarios y presi- dido por el primer ministro de Chi- na, Li Keqiang, lo que ha genera- do entusiasmo entre los ejecutivos de la industria, los productores y los académicos dentro del masivo sector de la acuicultura China. "El Consejo de Estado nunca se ha dirigido individualmente al sector de la acuicultura", comentó Zhang, mi-
nistro de pesca, en el Foro Mundial de Acuicultura celebrado en Zhuhai, provincia de Guangdong, en mayo. "Este es un acuerdo muy importante para la industria acuícola de China. Muestra que el gobierno se lo está tomando muy en serio ", dijo a Jiang Undercurrent, Xin Jiang, gerente de Shandong Ocean Oriental Sci-Tech y experto en cría de salmón en China.

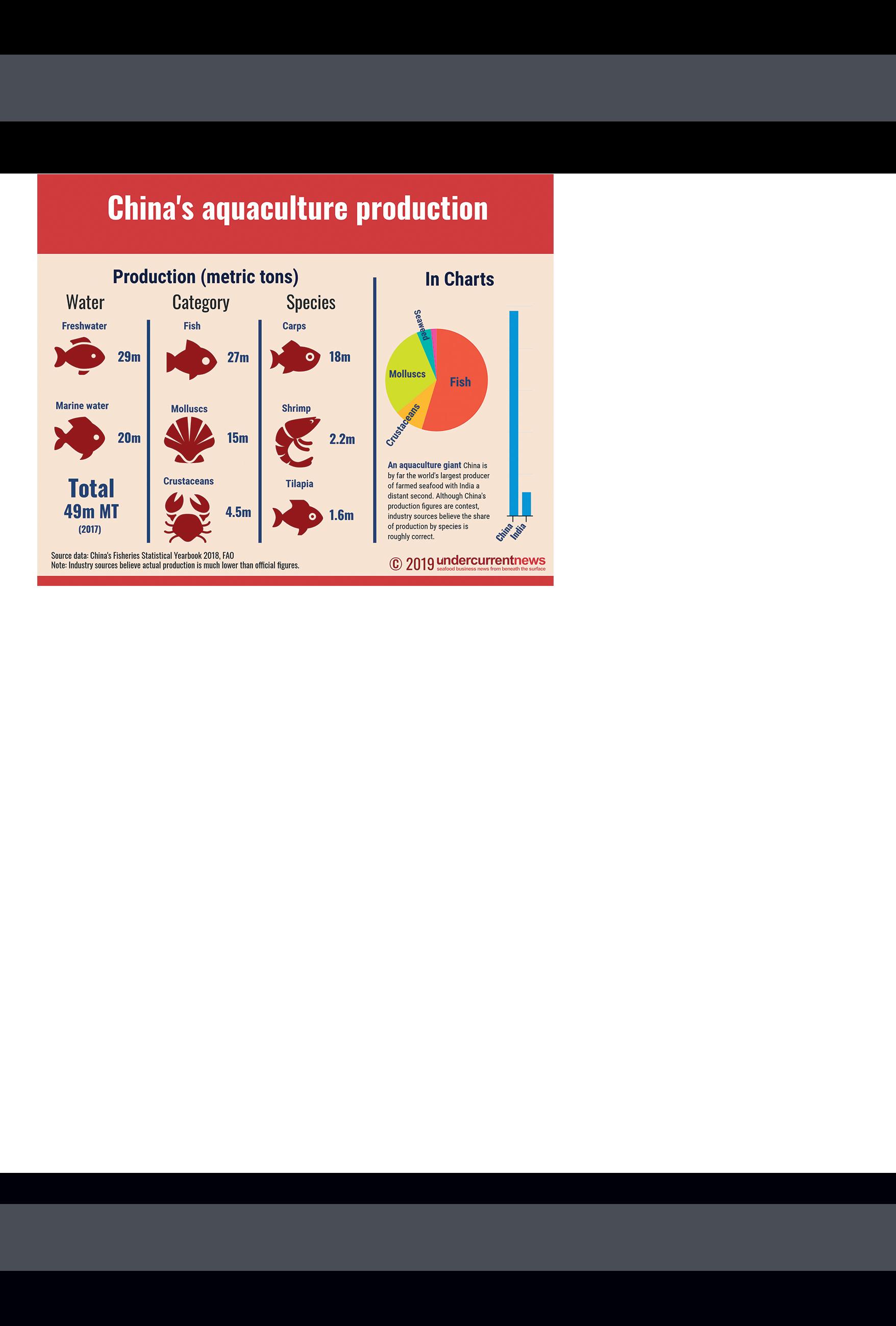
tante., segundo con 5.7 millones de toneladas métricas en 2017, según cifras de la Organización de las Na- ciones Unidas para la Agricultura y la Alimentación (ver infografía uno). Según cifras chinas, 4,9 millones de ciudadanos se dedican a la producción acuícola en el país.
Sin embargo, las preocupaciones

China es el mayor productor mun- dial de peces de cultivo y animales acuáticos. En 2017, el país produjo una cantidad masiva de 49.1 millones de toneladas métricas de productos marinos y acuáticos culti- vados (incluyendo algas marinas), según el Anuario Estadístico de Pesquerías de China 2018. Aunque las cifras de China están en disputa, India, el segundo productor más grande del mundo, es un país dis-
sobre la contaminación de la acuicultura que han afectado al sector en otros países aparecen con mayor frecuencia en los pronunciamientos del gobierno en China. Según las ci- fras en China presentadas en el Foro Mundial de Acuicultura, cerca del 5% de la contaminación en las vías navegables de China proviene de la acuicultura. Hoy en día, las figuras de la industria china lamentan la proliferación de algas rojas y azules.





















El documento del Consejo de Esta- do, trata de abordar lo siguiente: Comienza señalando el "notable éxito del sector de la acuicultura de China en el suministro de proteínas de alta calidad", pero dice: "el sector tiene problemas como el diseño y la estructura de la industria, y una alta densidad de reproducción en algunas áreas".
El resto del documento se lee como el manifiesto de un grupo ambientalista.
La palabra "verde" aparece 28 ve -
ces en el documento, que tiene solo cuatro páginas impresas. Un docu- mento señala que un sector acuí- cola fuerte, puede reducir la presión sobre las pesquerías silvestres.
En 26 artículos se resumen princi- pios, objetivos e ideas, algunos de los cuales son audaces, incluso extravagantes, que cubren todos los aspectos de la visión ecológica del Consejo de Estado para la industria acuícola de China. Esto incluye todo, desde harina de pescado y alimento hasta logística de cadena de frío.

El artículo dos, por ejemplo, titula- do "Principios Rectores", exige el desarrollo de "productos acuáticos ecológicos, distintivos y de alta ca- lidad". También hay un papel más importante para el libre mercado.
Los funcionarios de los estados del Artículo seis, deberían alentar el policultivo de arroz y pescado y, en un gesto de aprobación al creciente sector de la acuicultura en alta mar de China, "apoyar el desa- rrollo de la acuicultura en la costa y la construcción de plataformas de acuicultura inteligentes en la costa".
El artículo 13 exige una gestión más estricta de los desechos y la elimi- nación de los productos de desecho de los equipos de acuicultura, tales como flotadores, redes y bouys. (Aquellos que han visitado las granjas acuícolas cercanas a la costa de China a menudo se sorprenden por la cantidad de boyas de poliestireno desintegradas y des- echadas por el muelle, ver fotos).

Otro artículo establece el objetivo de 7.000 "granjas de demostración de acuicultura saludable a nivel nacional" y 550 "áreas de protec- ción de germoplasma de acuicul- tura a nivel nacional" para 2020. El artículo 21 exige más investigación sobre los sustitutos de la harina de pescado. Existe una dimensión de política ex- terior, con el artículo 19 alentando a los institutos de investigación y universidades a establecer proyec- tos de demostración y promover la tecnología de la acuicultura de Chi- na en el exterior. También menciona

el apoyo a "compañías de acuicul- tura a gran escala" para ayudar a cumplir con la política de China en materia de periferia y carreteras.
Continuando una tendencia
Como es típico de los pronunciamientos de este tipo en China, hay poca información real sobre el documento, sin presupuestos, nuevas leyes o regulaciones, o políticas concretas delineadas.
Pero en el sistema político de Chi- na, los funcionarios están muy en sintonía con la interpretación de la voluntad de Pekin. Por lo tanto, Wang de la Sociedad de Conserva- ción Marina de Qingdao dijo que apoya el "espíritu de este documen- to" y que apunta en una "dirección muy prometedora". Las nuevas políticas del gobierno central y local que cumplan con los objeti- vos del documento deben seguir.
Además, el trabajo para mejorar las credenciales medioambientales de la industria acuícola de China ya es evidente, y los organismos de certi- ficación “Mejores prácticas de acuicultura” y Consejo de administra- ción de acuicultura están ganando terreno entre los gigantes chinos de comercio electrónico JD.com y Ali- baba. La producción acuícola se está volcando en algunas partes del país.
En enero de este año, por ejemplo, antes del anuncio del Consejo de Estado, Cui He, el presidente de la Alianza de Procesamiento y Comer- cialización de Productos Acuáticos de China (CAPPMA), comentó que continuará una campaña de cierre de las granjas acuícolas que conta- minan el medio ambiente. Después de un año marcado por escenas de excavadoras desmantelando tuberías que descargan aguas residuales directamente al mar en Hainan y enterrando estanques de acuicul- tura ilegales con tierra en Jiangsu.
Cui He informó que como resultado de la represión, la producción de acuicultura china de las granjas del interior podría disminuir en 2019. De hecho, el impulso ecológico de Chi- na podría tener ramificaciones para los mercados mundiales de produc- tos pesqueros, con las importaciones de productos pesqueros chinos a 11.9 mil millones de dólares en 2018 y Los Estados Unidos en 2019.
Ganadores y perdedores Wang reconoce que algunos de los productores de camarón de China, muchos de los cuales

cultivan camarón en áreas rurales pobres, podrían enfrentar una mayor presión reguladora.
China afirma ser el mayor productor mundial de camarón de cultivo, aunque, al igual que con las cifras de producción en general, las cifras proporcionadas son controvertidas. Según Wang, los productores de camarón que utilizan estanques recuperados de áreas costeras con manglares o marismas intermarea- les "ciertamente serán los perdedores [de la política]". Más de la mitad de la producción china de camarón Vannamei, la especie de
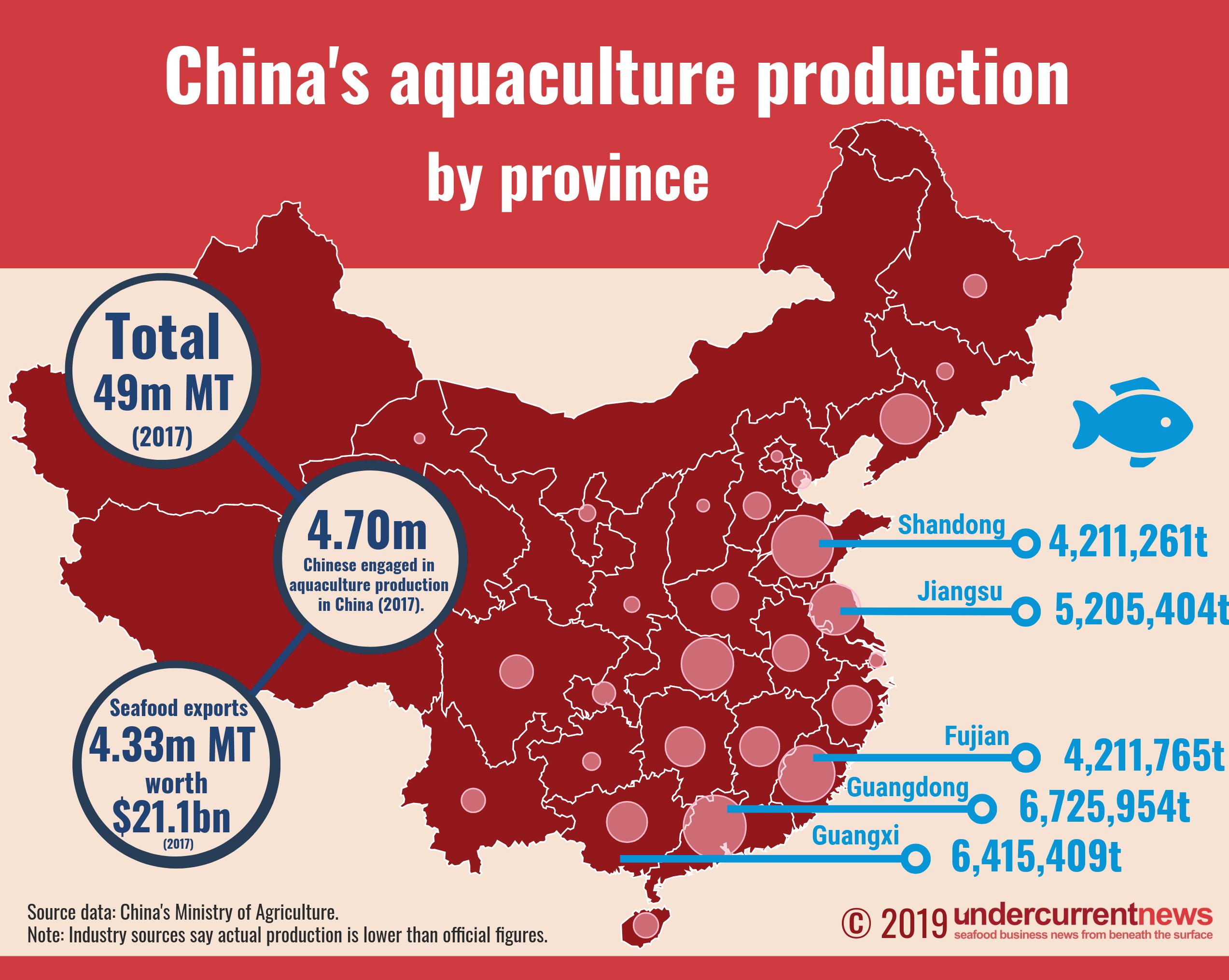
Producción acuícola de China por provincias. camarón más cultivada en China, se produce en las zonas costeras. Los productores chinos de pepinos de mar, que producen de lejos la mayor parte de la producción mun- dial de pepinos de mar, pueden verse presionados por razones si- milares, dijo; Los pepinos de mar se suelen cultivar en humedales recuperados en el norte del país, anotó. Entre otros sectores económicamente valiosos que podrían verse atrapa-

dos por las políticas verdes, está el enorme sector de tilapia de China. "Hay un fuerte llamado [en el documento] para que los productores y el gobierno intervengan, si es necesario, para fomentar la produc- ción hacia arriba o hacia abajo de acuerdo con las necesidades del mercado y del consumidor", dijo Wang. "La tilapia podría ser un caso; hay un exceso de capacidad que conduce a precio más bajo. Este es un llamado muy oportuno para el reajuste de la capacidad y la evaluación de acuerdo con el desempeño ambiental y social".
Dijo que los productores deberían recibir una compensación adecuada si se ven obligados a cerrar. "Tengo la esperanza de que esos profesionales puedan mejorar su prác- tica o recibir una compensación justa si abandonan el mercado".
Sin embargo, Wang dijo que no todos los productores de acuicultura saldrían perdiendo.
Los productores de camarones ecológicos, como los que cultivan camarones en estanques de sal, en densidades muy bajas y con poco o ningún uso de drogas, "se beneficiarían", dijo. Lo mismo ocurre con las empresas con una gran base de capital que podrían invertir en instalaciones de tratamiento de aguas residuales y utili- zar reproductores de camarones específicos sin patógenos (SPF).
"Los productores más pequeños que usen modelos de cultivo tradicionales amigables con el medio ambien- te, o que modernicen modelos tradi- cionales, como el cultivo de arroz-

Una granja de camarones en sistema RAS en el interior del condado de Zhanjiang, provincia de Guangdong, sur de China, 2017. Wang Songlin, presidente de la Sociedad de Conservación Marina de Qingdao, reconoce que los sistemas de producción avanzados como este recibirán la aprobación del gobierno. Crédito: Louis Harkell / Undercurrent News arroz con carpa y policultivos con especies múltiples o con cultivos de hortalizas, también se beneficiarían".
Políticas verdes roban el espectáculo. En el Foro Mundial de Acuicultura celebrado en Zhuhai, funcionarios y académicos chinos del sector acuícola de China se alinearon pa- ra abordar cómo China podría ex- pandir la acuicultura responsable y respetuosa con el medio ambiente. Lifeng Cui, director de la Estación Nacional de Extensión de Tecnología Pesquera de China (NFTES, por sus siglas en inglés), que cuenta con más de 35,000 empleados, dijo que el objetivo principal de NFTES actualmente es alentar a los acuicultores a reducir el uso de drogas. En una sesión titulada "Impulsar el desarrollo ecológico de la industria de la acuicultura de China", Ge Xianping, de la Academia China de Cien- cias de la Pesca, destacó nueve sistemas de acuicultura de agua dulce respetuosos con el medio ambien- te que quiere que los productores adopten siempre que sea posible.
Xu Hao, de la Academia China de Ciencias de la Pesca, detalló varios proyectos en alta mar que involu- cran embarcaciones de acuicultura. Wang informó que el documento "señala acertadamente que ahora, en China, para mejorar aún más la producción acuícola, el enfoque debe estar en la calidad en lugar de la cantidad".
"También está fomentando modelos y prácticas de producción más respetuosos con el medio ambien-

te y haciendo hincapié en que los productos del mar de mayor cali- dad deben satisfacer la nueva demanda de los consumidores chinos y también de los compradores internacionales en el mercado".
Soporte no universal
“El impulso ecológico de China ya está afectando significativamente el sector acuícola de China. Sin embargo, menos que cautivados son los agricultores chinos, muchos de los cuales viven en áreas rurales pobres como la provincia de Guangxi. Un productor que escribe bajo el nombre de la empresa Henan Si- fang Fisheries describe vívidamente un cambio de sentido en la
política del gobierno, que el autor condena como "descarado". "Hace unos años, cuando fuimos a Shanxi y Shaanxi [provincias] para dedicarnos a la acuicultura, ¡el gobierno lo apoyó! Hoy en día, todos se han vuelto hostiles. No solo se están desmantelando los estanques de peces, las carreteras de suministro, las viviendas en el lugar, los almacenes y otras instalaciones, y sin compensación. Lo que es aún más irritante es ser etiquetado como 'invasores que ocupan ilegalmente'.
No puedo entender por qué, en julio y agosto de 2018, ¡más de 100 personas enviadas por el gobierno del condado vinieron a visitar nuestra compañía para observar el proyecto! ¿Cómo es que bajo la sabia orientación del gobierno ahora puede ser ilegal?
Cuando la granja estaba en desa- rrollo por primera vez, el gobierno del condado celebró una reunión de coordinación en el lugar. La reunión solicitó a los departamentos pertinentes de la Oficina de Pesca, Silvicultura, Industria y Comercio, Impuestos, Protección del Medio Ambiente, Transporte, Seguridad Pública y varios municipios que apoyan plenamente el proyecto. Ahora, ellos están diciendo descaradamente que el liderazgo ha cambiado y la política ha cambiado. ¡Si quitas la escalera te caes bajo tu propio riesgo! "
El comentario, publicado en la ver- sión inédita del documento del Consejo de Estado de China de la revista China Aquaculture, ha recibido la mayor cantidad de "me gusta" (likes).

Fuente: https://www.undercurrentnews.com/2019/06/17/beijingbacks-green-aquaculture-revolution/

Los atunes poseen una gama de adaptaciones fisiológicas y mecánicas orientadas a la natación de alto rendimiento que son de gran interés para los fisiólogos, ecólogos e ingenieros. Los avances en biologging han proporcionado mejoras signi- ficativas en la comprensión de las migraciones de atún y los patrones de movimiento vertical, pero nues- tra comprensión de la locomoción y la mecánica de natación de estos peces en condiciones naturales es limitada. Equipamos atún rojo del Atlántico (Thunnus thynnus) con etiquetas sensibles al movimiento y cámaras de video para cuantificar la marcha y la cinemática utilizadas por los peces salvajes. Nuestros datos revelan una variedad significativa en la cinemática locomotora del atún rojo del Atlántico, que va desde la locomoción continua a dos tipos de locomoción intermitente. El atún mantuvo velocidades de natación superiores a 1,5 ms −1.(0.6 longitudes de cuerpo s −1 ), mientras golpean su cola a una frecuencia de aproximadamente 1 Hz. Mientras se buceaba, algunos descensos se componían en su totalidad de desli- zamientos pasivos, con velocidades de descenso más lentas y más desli- zamientos, mientras que los ascen- sos se componían principalmente de natación activa. El comportamiento de natación observado del atún rojo del Atlántico es consistente con los modelos teóricos que predicen que tal locomoción intermitente dará como resultado ventajas mecánicas y fisiológicas. Nuestros resultados confirman que el atún rojo del Atlántico posee especializaciones de comportamiento para aumentar su rendimiento locomotor, que junto con su fisiología única mejoran su capacidad para utilizar hábitats pelágicos y mesopelágicos.
Introducción
Los atunes son peces endotérmicos conocidos por sus elevadas tasas metabólicas y su rendimiento úni- co en natación [ 1 - 3 ]. Además de sus tejidos endotérmicos, los atunes también presentan adaptaciones morfológicas para la natación de
alto rendimiento, como una cola lunada y un sistema musculoesquelético que transfiere el poder de las fibras musculares "rojas" de contracción lenta ubicadas anteriormente a la cola. Esta disposición mecánica da como resultado un estilo rígido de natación, llamado locomoción thunniform [ 1 , 2 , 4 , 5 ]. Los atunes rojos, con su distribución templada y subpolar de peces adultos, presen- tan una fisiología cardíaca única y una gran capacidad aeróbica, dadas las bajas temperaturas que habitan [ 6- 8 ]. Las especializaciones fisiológicas y biomecánicas se asocian con el comportamiento migratorio extraordinario de los atunes rojos, que regularmente realizan migra- ciones transoceánicas y latitudinales de terrenos de forraje productivos a menudo templados a áreas de des- ove más cálidas [ 9 - 11 ]. Debido a su gran tamaño como adultos, las grandes distancias recorridas en los hábitats pelágicos han supuesto un desafío importante para el estudio de la locomoción del atún rojo. Sin embargo, la comprensión de la biomecánica y la actividad locomotora de los atunes rojos es crucial, da- dos sus altos índices metabólicos y sus presas distribuidas de forma irregular en el océano abierto, en gran parte oligotrófico [ 12 , 13 ].
A pesar de los grandes intereses en las adaptaciones biomecánicas y fisiológicas de la natación del atún [ 14 ], sus cinemáticas se han estudiado históricamente en túneles de natación y pequeños tanques, lo que pone serias limitaciones en la forma en que estos peces oceánicos pueden moverse. Esto ha resultado en el estudio de peces juveniles y puede no resaltar la complejidad de su comportamiento locomotor [ 15 ], especialmente porque los peces que nadan en condiciones forzadas a menudo pueden mostrar patrones locomotores significativamente diferentes en comparación con aquellos que nadan de forma voluntaria [ 16].]. Los modelos teóricos han demostrado durante mucho tiempo que las diferentes formas de locomoción intermitente, don-
de los animales se entremezclan en natación activa con deslizamiento pasivo, pueden generar ventajas energéticas, reduciendo el trabajo mecánico de nadar hasta en un 50% [ 17 , 18 ]. Teniendo en cuenta que la locomoción puede comprender aproximadamente el 50% del meta- bolismo de rutina en atunes [ 2 , 19 ], es imperativo entender la actividad locomotora de los peces silvestres para refinar las estimaciones de la demanda de energía obtenida de los túneles de natación [ 20 ].
La llegada de las etiquetas sensibles al movimiento (acelerómetros, mag- netómetros, giroscopios) y su aplica- ción en el estudio del movimiento de animales en libertad [ 21 - 23 ] ha eliminado estas barreras. El trabajo reciente ha revelado estrategias de movimiento de acuerdo con estas predicciones en unos pocos taxones seleccionados; los tiburones ballena (Rhincodon typus) y los tiburones blancos (Carcharodon carcharias) usan deslizamientos pasivos para descender, mientras nadan activamente con estocadas de la cola durante los ascensos [ 24 ] para optimizar su locomoción debido a la flotabilidad negativa, mientras que dos especies de tiburones de aguas profundas hacen Lo contra- rio debido a la flotabilidad positiva [ 25 ]. Ambos escenarios corroboran el modelo de locomoción en dos etapas de Weihs [ 17], al demostrar que muchos animales marinos utilizan fuerzas flotantes para deslizarse y reducir el trabajo mecáni- co realizado durante movimientos verticales, con algunas excepciones notables [ 26 , 27 ]. Se ha demostrado que los tiburones ballena y los ti- burones de punta blanca oceánicos utilizan geometrías de buceo que minimizan el costo del transporte [ 28 , 29 ] y modifican el comportamiento del buceo en respuesta a las condiciones ambientales [ 30 ].
A pesar de la gran promesa de las nuevas tecnologías de biologging, su participación en el estudio de los peces teleósteos se ha retrasado en el trabajo con los vertebrados mari-


nos y los peces de elasmobranquios [ 24 , 25 , 31 , 32 ]. De hecho, debido a su gran tamaño y prominentes ale- tas dorsales, gran parte del trabajo sobre las etiquetas de bioetiquetado sensibles al movimiento provino de peces elasmobranquios debido a la relativa facilidad de adherir los regis- tradores de datos [ 33 - 37 ], mientras que la morfología del pez teleósteo pelágico Proporciona desafíos extraordinarios para la unión firme de los madereros. El trabajo inicial con etiquetas acústicas de sensores múltiples ha demostrado cierto éxito en peces teleósteos grandes, como la aguja azul (Makaira nigricans). Se descubrió que la aguja azul con sensores de velocidad usa dos marchas, nadando a velocidades bajas de 0.15–0.25 ms −1 , con períodos distintos de mayor actividad y velocidades de 0.8–1.2 ms −1 [ 38 ], considerablemente más lento que las estimaciones recientes de natación Velocidades por pez vela (Istiophorus platypterus), que navegan a aproximadamente 2 ms −1 y nadan en ráfagas que superan los 6 ms −1 [ 39]. Además, la nueva información sobre las tasas de buceo proviene de las etiquetas de archivo colocadas en atunes en libertad. Estas etiquetas tienen una resolución temporal relativamente baja (1–60 s) para capturar eventos cinemáticos y están programadas principalmente para despliegues a largo plazo pa- ra adquirir datos de sensores para estimar la posición geográfica y los comportamientos verticales duran- te períodos prolongados (meses- años) hasta que el pez está Captu- rado y la etiqueta se recupera. Los conjuntos de datos de archivo han demostrado hasta la fecha que los atunes tienen un comportamiento de buceo variable y responden a condiciones ambientales cambiantes [ 40 - 43 ]. Las inmersiones notables se han medido con velocidades verticales superiores a 6–8 ms- 1 y a profundidades superiores a 2000 m.
Los datos de marcado de archivo han destacado dos formas prominentes de movimiento vertical presentes en la mayoría de las especies de peces pelágicos; migraciones verticales de diel (DVM) y buceo oscilatorio repetido [ 24 , 44 - 46 ]. Mientras que los cambios de diel en la distribución vertical de muchas especies de atunes (y otros depredadores pelágicos) se mostraron relacionados con los cambios de diel en la distribución de presas, tales argumentos no explican el buceo repetido desde la superficie hasta la profundidad. El uso de etiquetas
de archivo o acústicas que miden la temperatura tanto en las vísceras como en la temperatura ambiente del agua ha demostrado convincen- temente la termorregulación como impulsor de repetidas excursiones verticales, con ejemplos particular- mente convincentes para el atún de ojo grande (Thunnus obesus). Aquí, el atún realiza ascensos rápidos a través de la termoclina para recalentarse en las aguas superficiales antes de regresar al forraje debajo de la termoclina [ 47 , 48 ]. Patrones similares se demostraron recientemente para Mola mola [ 49 ]. Si bien se ha acumulado evidencia significativa para respaldar la termorregulación y la búsqueda de presas como fac- tores importantes que configuran el comportamiento de buceo repetido de los atunes, poca evidencia (pero ver [ 50 ]) apoya las hipótesis de que las inmersiones se realizan para mejorar el rendimiento locomotor y, por extensión, reducen el gasto energético , a pesar de que muchos investigadores sugieren que puede ser un factor importante [ 50 ]. El uso creciente de acelerómetros en peces ha revelado cómo las di- ferentes circunstancias ecológicas afectan la cinemática de la natación de los peces. El despliegue de marcas de acelerometría a corto plazo desplegadas en peces delfín (Coryphaena hippurus) y anguillid eels (Anguilla celebesensis y Anguilla marmorata) reveló patrones similares a los tiburones en su comportamiento de buceo [ 45 , 51 ]. Se encontró que los peces delfín des- cendían deslizándose, con la proporción de descensos pasivos relacionados con la profundidad de
la capa mixta; esto se sugirió como una adaptación para un forrajeo eficiente [ 45]. Igualmente, las anguilas anguilidas realizaron buceos repetitivos con descensos pasivos y poco profundos y ascensos más empinados activos. Sin embargo, se sugirió que la función de estas inmersiones estaba relacionada principalmente con preparar a los peces para su larga migración sin desperdiciar cantidades sustancia- les de energía [ 51 ]. Sin embargo, queda mucho por aprender acerca de los peces teleósteos y los atunes de alto rendimiento en particular (ver [ 45 , 52 , 53 ]). Algunas de estas brechas se han llenado recientemente a través de experimentos en cautiverio. La dinámica de fluidos computacional y experimental ha demostrado el potencial del desli- zamiento pasivo para disminuir el costo horizontal del transporte de atún rojo del Pacífico cautivo (Thunnus orientalis) [ 54]. En un estudio separado que utiliza tecnología de biologging, Noda et al. [ 55 ] demostraron que los peces más pequeños en escuelas mixtas de atún de aleta azul del Pacífico se beneficiaron menos de la natación intermitente en comparación con los peces más grandes dentro de la misma escuela. Aquí, informamos las primeras mediciones directas de la actividad locomotora del atún rojo del Atlántico (Thunnus thynnus) en el golfo de San Lorenzo equipado con acelerómetros y cámaras para ani- males que utilizan una novedosa técnica de acoplamiento para etiquetas de bioetensado. Nuestros datos confirman que el atún rojo del Atlántico posee una flexibili -
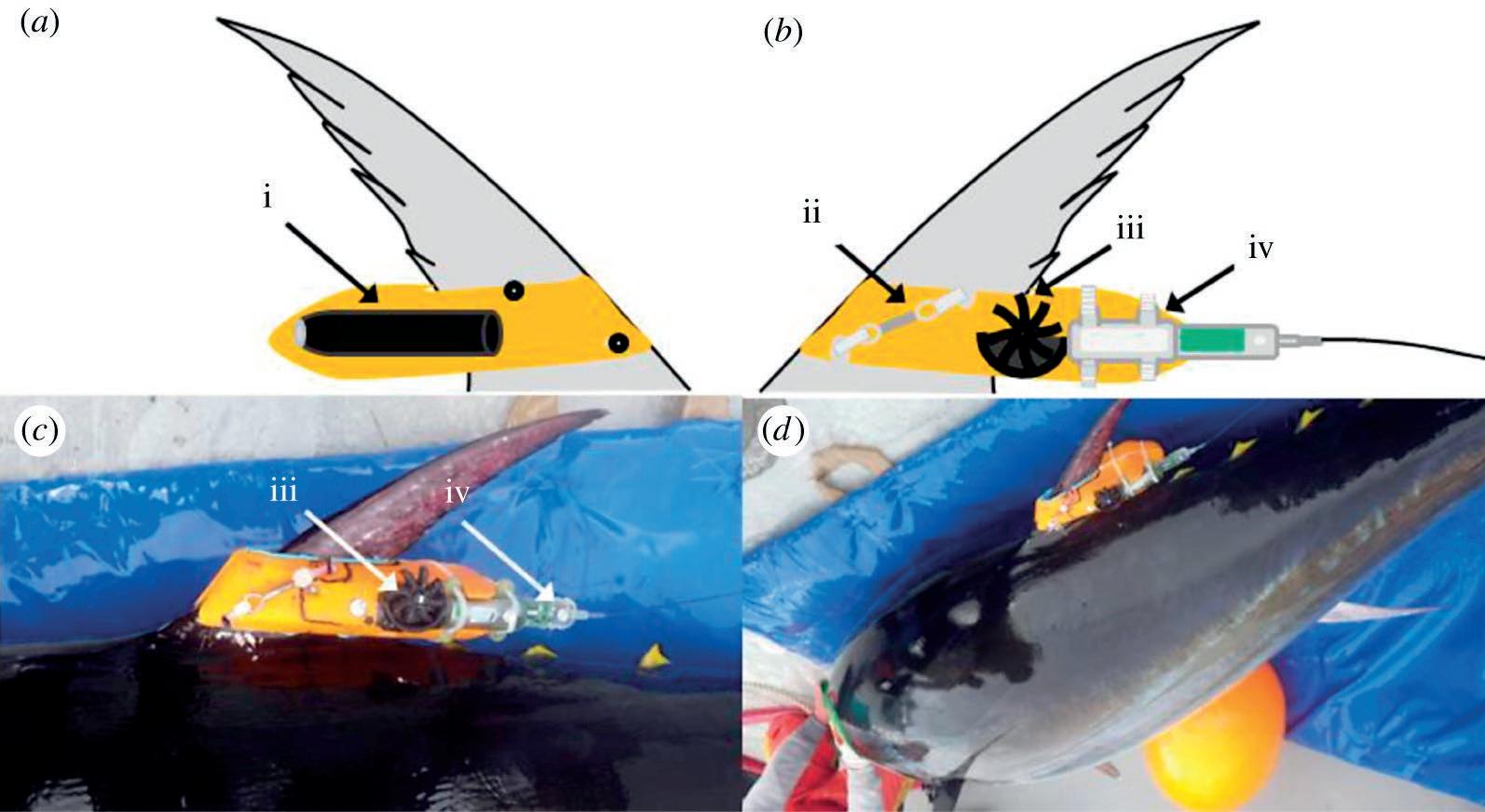
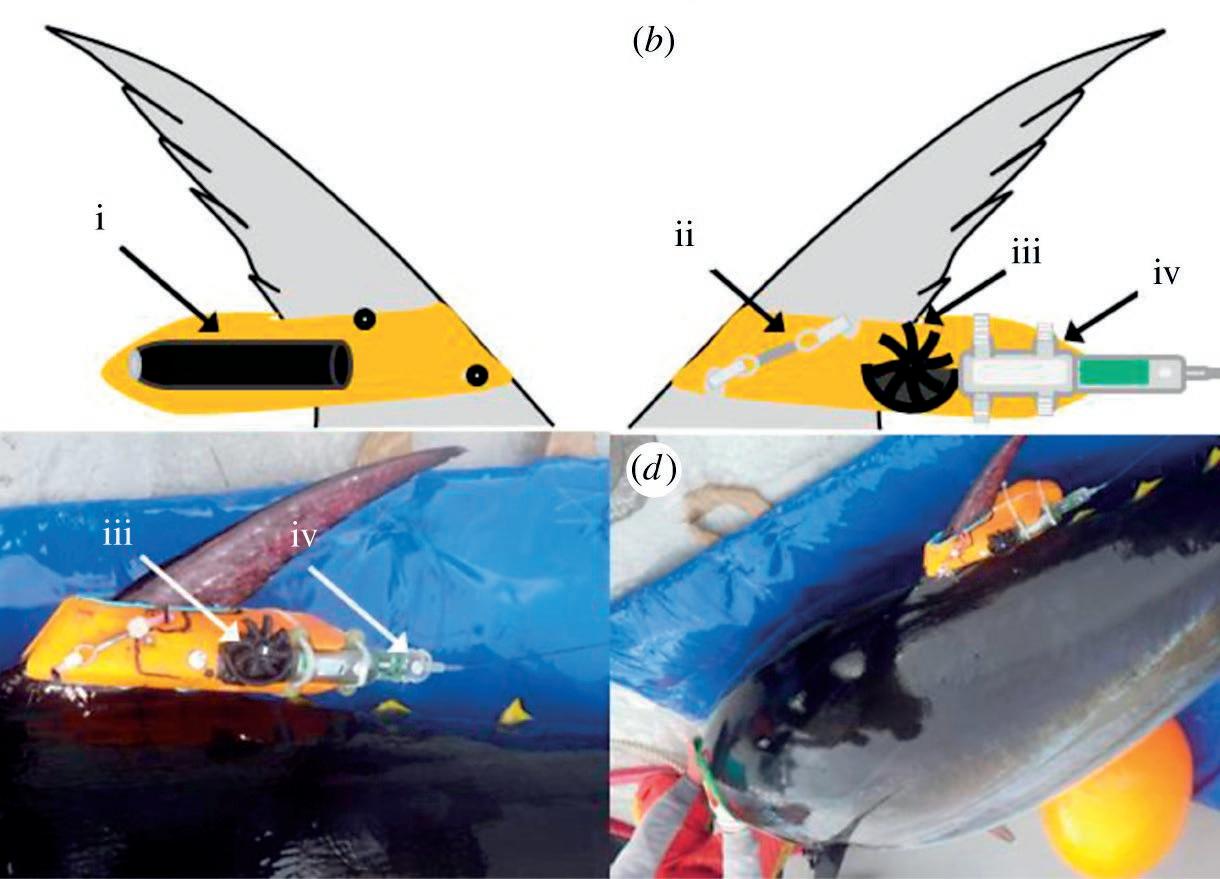
Figura 1. Implementación de una etiqueta de registro de datos de video CATS en un atún rojo del Atlántico. ( a ) Esquema de la etiqueta unida a la segunda aleta dorsal de un atún rojo que muestra la cámara (i) unida al lado derecho del cuerpo de flotación naranja que contiene el sistema de registro de datos. ( b ) El lado izquierdo de la misma etiqueta que muestra la liberación sincronizada galvánica (GTR) (ii) incorporada en la carcasa. ( c ) El mismo lado de la etiqueta adherida a un atún

dad considerable en sus patrones locomotores, de manera consistente con los modelos teóricos que predicen ventajas biomecánicas sobre la locomoción continua.
2. Métodos
Todo el trabajo se realizó de acuer- do con el Comité Institucional de Cuidado y Uso de Animales de la Universidad de Stanford (Protocolo 13865) y el etiquetado satelital se realizó bajo el permiso del Departa- mento de Pesca y Océanos de Canadá (permiso no. SG-GNS-14-132A).
2.1. Despliegue de etiquetas
Los experimentos de marcado elec- trónico se realizaron en las aguas del golfo de San Lorenzo en Port Hood, en la isla de Cabo Bretón, Nueva Escocia, en octubre de 2014 (material complementario electrónico, figura S1). El atún de aleta azul del Atlántico fue capturado en caña y carrete (Penn 130) con caballa fresca o cebos de arenque. El tackle terminal fue líder de 300 libras con un gan- cho de círculo. El atún capturado en el gancho y la línea se enrollaron en la parte posterior del barco y se llevaron a bordo del barco de marcado con un gancho especial de titanio especialmente diseñado que per- mitía tirar del pescado a través de la puerta del travesaño del barco hasta una esterilla de vinilo que estaba resbaladiza y húmeda. El uso de una esterilla de vinilo húmeda permi- tió que el pez se deslice fácilmente sin fricción o daño al cuerpo. Una manguera de agua salada se insertó inmediatamente en la boca del pez para oxigenar las branquias.® ) se colocó sobre los ojos para mantener la calma del pez. Los peces se midieron para determinar la longitud de la horquilla curva (CFL), se tomaron muestras para determi- nar la genética, se marcaron y se liberaron en 1 a 2 min de captura. Las imágenes de la posición de la etiqueta se obtuvieron en el momento del lanzamiento ( figura 1 ).
2.2. Especificaciones de etiqueta y despliegue
Una vez que el atún estuvo en la cu- bierta y bien irrigado, las etiquetas se unieron colocando dos agujeros pequeños (1 cm de diámetro) en la porción ósea de la aleta utilizando una plantilla correspondiente a las ranuras en la etiqueta y un pequeño taladro. Las técnicas de implementación difirieron ligeramente entre los dos tipos de etiquetas utilizadas (etiqueta personali- zada de soluciones de etiquetado de animales (CATS) (ver figura 1 )
y un CEFAS G6a (ver [ 33 ] y tabla 1para detalles del sensor de etiquetas). Ambos tipos de etiquetas esta- ban encerrados en una espuma de flotación positiva para permitir la flotación después del arranque, lo que podría alterar la flotabilidad de su portador. Durante el proceso de diseño, se minimizó la flotabilidad positiva excesiva para reducir este efecto. Las etiquetas completamen- te ensambladas solo mostraron una flotabilidad positiva marginal, como lo demuestra una pequeña fracción de las etiquetas que sobresalen de la superficie del agua mientras flotan.
2.2.1. Etiqueta
CATS
La electrónica estaba contenida dentro de una carcasa impresa tri- dimensional llena de microesferas flotantes y resistentes a la presión: mezcla de epoxi. La velocidad de natación se midió a través de una rueda de paletas externa también construida con plástico impreso tri- dimensional. La parte posterior de la etiqueta contenía una ranura que fue diseñada para adaptarse a una etiqueta SPOT de Wildlife Compu- ters (Wildlife Computers, Redmond, WA, EE. UU.). Ajustamos la flotabilidad de la etiqueta de tal manera que la etiqueta flotó sobre la superficie del agua después de que la etiqueta se desprendiera. Las etiquetas CATS de este primer despliegue fueron diseñadas específicamente para que el atún rojo del Atlántico gigante se monte en la segunda aleta dorsal, manteniendo el paquete a granel detrás de la aleta, reduciendo la resistencia del perfil. La parte anterior de la etiqueta contenía una ranura abierta con un ancho del grosor de la cuerda de la base de la segunda aleta dorsal de un atún rojo del At- lántico, el interior de la ranura también estaba forrado con una espuma hipoalergénica (Poron Blue de 5 mm, Algeos). , REINO UNIDO). Las mediciones se obtuvieron de la segunda aleta dorsal de peces captu- rados por pescadores comerciales antes de diseñar la montura para todas las marcas. Se perforaron dos pequeños orificios en la aleta (diámetro inferior a 10 mm) utilizando una plantilla, y la etiqueta se deslizó sobre la aleta. Dos bridas atadas a los dos orificios para los ojos en una descarga de tiempo galvánico (GTR, Se perforaron dos pequeños orificios en la aleta (diámetro inferior a 10 mm) utilizando una planti- lla, y la etiqueta se deslizó sobre la aleta. Dos bridas atadas a los dos orificios para los ojos en una descarga de tiempo galvánico (GTR, Se perforaron dos pequeños orificios
en la aleta (diámetro inferior a 10 mm) utilizando una plantilla, y la eti- queta se deslizó sobre la aleta. Dos bridas atadas a los dos orificios para los ojos en una descarga de tiempo galvánico (GTR,http://www.neptunemarineproducts.com/galvanictimed-releases/) fueron alimentados a través de los orificios y se sentaron en dos ranuras de 1 cm de profundi- dad de la etiqueta. Ambos extremos de la cremallera se alimentaron a través de los dos orificios perforados en la aleta utilizando una plantilla y se fijaron con la caja abierta de una tercera brida de la cremallera pegada a una arandela de nylon de 4 cm de diámetro exterior y 1,5 cm de diámetro interior (Home Depot, EE. UU.) ). La superficie de la carcasa de flotabilidad y los lados de las arandelas de nylon en contacto con la aleta también se recubrieron con espuma hipoalergénica (3 mm de espesor, PoronBlue, Algeos, Reino Unido) para evitar el roce. Después de la corrosión del GTR, se esperaba que las bridas se aflojaran y la etiqueta se soltara y flotara hacia la superficie. Etiquetas CATS muestreadas aceleración triaxial, profun- didad y temperatura (y otros datos de sensores adicionales que no se utilizan aquí) a 40 Hz. Además de su traje de sensores, Las etiquetas CATS contenían una cámara digital que mira hacia la parte posterior del pez para validar las señales de los acele- rómetros y documentar el entorno del pez. El sistema de la cámara era una cámara de acción Replay Mini, que se ajusta a la medida en una carcasa hidrodinámica. La cámara tenía una velocidad de fotogramas de 30 fps y una resolución de 720 p. 2.2.2. CEFAS
G6A G6as (CEFAS Technology, Lowestoft, EE. UU.) Se encajonaron en una carcasa positivamente flotante y se acoplaron con un transmisor VHF (transmisor de 3 etapas ATS, Insanti, MN, EE. UU.) Descrito en detalle en Whitmore et al. [ 33 ]. El paquete de etiquetas se fijó a la aleta utilizando los mismos materiales que se describen para nuestras etiquetas CATS y usaba los mismos GTR como mecanismos de liberación. Una vez que el GTR se corroería por completo, el enlace entre los dos tirantes se rompería y la etiqueta se liberaría del pez y flotaría a la superficie para comenzar a transmitir su señal VHF para su recuperación. El conjunto de sensores CEFAS G6a contenía acelerómetros triaxiales muestreados a 30 Hz aquí, así como temperatura y profundidad muestreadas a 1 Hz.

2.3. Datos del sensor
Calibramos los acelerómetros de todas las etiquetas a g (9.81 ms −2 ) de acuerdo con Wilson et al . [ 57]. Los datos de aceleración constan de dos señales, una está relacionada con la actitud de la etiqueta en relación con el campo gravitacional (denominada aceleración estática o gravi- tacional) y la otra con el movimiento (aceleración dinámica). Estas señales pueden estimarse mediante diversas técnicas de suavizado para eliminar el componente gravitacional de la aceleración bruta. Sobre la base de la evaluación visual iterativa, encontramos que un filtro Sovitzky- Golay de segundo orden de 1,5 s capturaba la dinámica de la manera más apropiada. Este filtro se aplicó a los tres ejes del acelerómetro. La aceleración creciente se utilizó para calcular el ángulo de cabeceo del atún (el ángulo entre el eje longitu- dinal del pez y el horizonte), a través de una transformación de arcoseno. Como ninguna etiqueta puede alinearse perfectamente con el eje longitudinal del animal, es necesario calcular un desplazamiento entre el ángulo de la etiqueta y el del ani- mal. Para ello, utilizamos el método de Kawatsu.et al . [ 58 ] y retrocedió la velocidad vertical y el ángulo de inclinación; la intersección de esta relación corresponde a este desplazamiento; es decir, cuando los peces nadan de manera nivelada (VV = 0 ms −1 ), la etiqueta tendrá una orientación diferente a la horizontal. Este desplazamiento puede sim- plemente restarse de todo el conjunto de datos (ver también [ 29 ]).
Las aceleraciones dinámicas laterales corresponden a los golpes de cola de los peces. Para estimar el esfuerzo locomotor de los peces, calculamos la frecuencia de batido de la cola de la aceleración lateral dinámica y realizamos una transfor- mada de wavelet continua (CWT) en estos datos para estimar las frecuencias dominantes en Ethogra- pher [ 59] implementado en IgorPro (Wavemetrics, Lake Oswego, OR, EE. UU.). Esto produjo una serie de tiempo de frecuencias de batido de cola con una resolución temporal de 1 s. Por separado, utilizamos un algoritmo personalizado para iden- tificar los deslizamientos pasivos, ya que nuestra CWT perdió una can- tidad considerable de segmentos que se clasificaron como natación activa, a pesar de que no era visi- ble un latido de la cola claramente discernible. Brevemente, los datos
de aceleración dinámica lateral se suavizaron primero utilizando un filtro Sovitzky-Golay de segundo orden. Luego, los datos se agruparon en intervalos de 120 s consecutivos y se calcularon las sumas de la raíz de los cuadrados (RSS) para cada intervalo para cuantificar la variación en la amplitud de la señal con el tiempo. Los valores RSS específicos del tiempo multiplicados por un escalador constante se usaron luego como un umbral para diferenciar la natación frente al deslizamiento en función de los valores RSS para una ventana deslizante de 15 puntos. Los valores por encima del umbral se clasificaron como natación, mientras que los siguientes se categori- zaron como deslizamiento. Los dos conjuntos de datos se combinaron para producir una sola serie de tiempo; cualquier paso de tiempo definido como pasivo en nuestro código de deslizamiento se usó para sobrescribir la frecuencia correspon- diente en el conjunto de datos CWT.
2.3.1. Medida de la velocidad
Las velocidades se calcularon a partir del número de revoluciones registradas por una pequeña rueda de paletas unida al exterior de la etiqueta. La rueda de paletas contenía dos pequeños imanes de polaridad opuesta, fijados a dos paletas opuestas. La rotación en la rueda de paletas dio lugar a pequeñas oscilaciones en los datos del magnetómetro de etiquetas, cuantificado utilizando un CWT en el paquete de Ethographer [ 60].
Estos datos produjeron un conjunto de datos por separado de revoluciones de la rueda de paletas por segundo, que se usó en el procedimiento de calibración. Para estimar las velocidades de natación, utilizamos las medidas de profun- didad y inclinación del atún de bu- ceo para estimar la velocidad de natación. Dado que los sensores de presión proporcionan datos muy precisos, uno puede calcular una velocidad cuando el animal está nadando verticalmente (inclinación = 90 °); Sin embargo, esto no suele ser el caso. En su lugar, utilizamos trigonometría para calcular una velocidad basada en el tono y la velocidad vertical [ 61]. Las estimaciones de la trigonometría tendrán errores cada vez más grandes (acer- cándose al infinito en el tono = 0) en ángulos poco profundos, por lo que restringimos el procedimiento de calibración a secciones de datos donde el ángulo era mayor de 20 °.
Encontramos que las rotaciones de la rueda de paletas aumentaron con nuestra velocidad estimada de natación, pero encontramos alguna va- riación en la relación, que se espera en base al error en la estimación de la velocidad desde el paso. Sobre la base de los gráficos de rotación estimada / velocidad estimada, se hizo evidente que se requería un ajuste no lineal para capturar la dinámica de manera apropiada, especialmen- te a bajas velocidades. Utilizamos un polinomio de cuarto orden para la calibración, que explica el 61% de la variación de la relación (99% para los datos agrupados). Las funciones más simples no pudieron capturar la dinámica a velocidades lentas y ha- brían resultado en una sobreestimación de la velocidad. Posteriormente, aplicamos la calibración a todo el conjunto de datos. No registramos ningún bloqueo de baja velocidad en el sensor, pero alcanzamos una velocidad máxima de resolución de aproximadamente 3.25 ms−1 (ver material complementario electrónico, figura S2). Esto se debió a que las rotaciones de la rueda de paletas alcanzaron los 20 Hz a esta velocidad, equivalente a la frecuencia de Nyquist del régimen de muestreo en el magnetómetro (40 Hz).
3. Resultados
3.1. Despliegue y recuperación de tags acelerometría.
Se desplegaron cuatro etiquetas de biologado para obtener las primeras grabaciones de velocidad y acelerometría del atún rojo del Atlántico (T. thynnus); Dos etiquetas de cáma- ra CATS y dos CEFAS G6as ( figura 1 y tabla 1). Dos etiquetas no fueron recuperadas. Las etiquetas de la cá- mara CATS no se lanzaron a la hora de salida esperada. Ambas etiquetas aparecieron aproximadamente 60 días a partir de la hora prevista de lanzamiento, aproximadamente 100 millas de la costa de Nueva Escocia, cerca de la Isla Sable (material electrónico complementario, figura S1). Una de las etiquetas fue recupe- rada por el barco y la tripulación con un receptor ARGOS de mano. La segunda etiqueta CATS también apareció en la misma vecindad, pero debido al clima severo y la dis- tancia desde la costa, no se pudo recolectar antes de que la batería del PTT se agotara y la transmisión cesara. Se desconoce el motivo de la demora, pero especulamos que las tiras rígidas se atascaron en los surcos de la etiqueta y la aleta y solo se aflojaron después de un período prolongado en libertad. El G6a que solo contenía un transmisor VHF
fue encontrado por un miembro del público cerca de la calzada entre la isla de Cabo Bretón y el continente de Nueva Escocia en la primavera si- guiente. El escaneo inicial de los da- tos reveló que el G6a se desprendió después de 72 h (en lo sucesivo, pez nº 1), mientras que el diario CATS (en lo sucesivo, pez nº 2) se registró mientras estaba conectado al pez durante 48 h. Hasta que las bate- rías de los registradores de datos se agotaron. En conjunto, estos datos proporcionaron 5 días de datos ci- nemáticos sobre atún rojo del Atlán- tico adulto que nadaba libremente con una limitación de la plataforma batimétrica, mientras que el diario CATS (en lo sucesivo, peces nº 2) se registró mientras estaba conectado a los peces durante 48 h, hasta que se agotaron las baterías de los regis- tradores de datos. En conjunto, estos datos proporcionaron 5 días de da- tos cinemáticos sobre atún rojo del Atlántico adulto que nadaba libre- mente con una limitación de la pla- taforma batimétrica, mientras que el diario CATS (en lo sucesivo, peces nº 2) se registró mientras estaba co- nectado a los peces durante 48 h, hasta que se agotaron las baterías de los registradores de datos. En con- junto, estos datos proporcionaron 5 días de datos cinemáticos sobre atún rojo del Atlántico adulto que nadaba libremente con una limitación de la plataforma batimétrica.
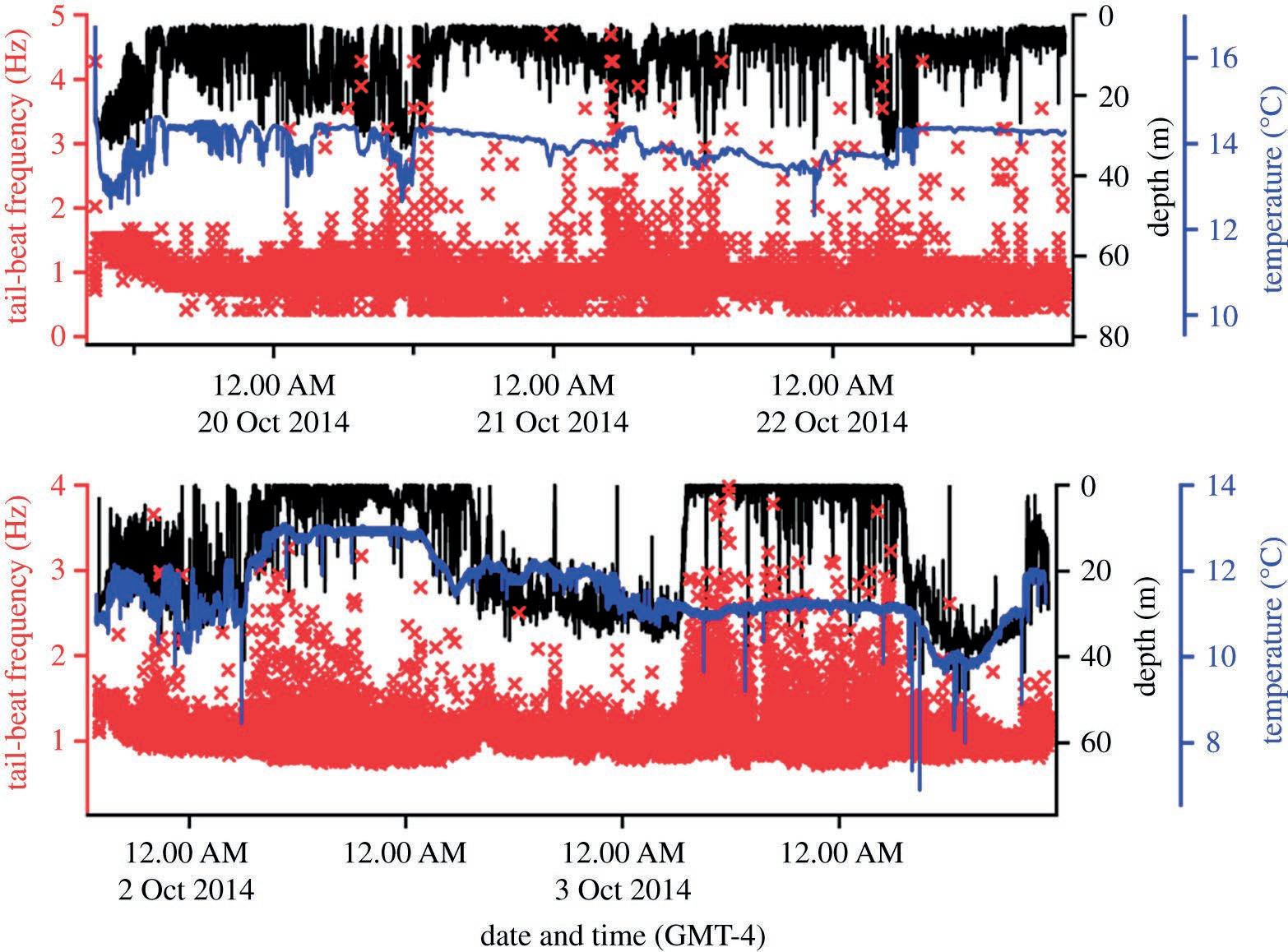
los procedimien- tos de despliegueutilizando técnicas establecidas. En ambos casos, después de la liberación, el pez se zambulló y exhibió un descenso deslizante (sin batir la cola) a pro- fundidades de 20 a 30 m. Ambos peces mostraron una fuerte actividad de batir la cola con una mayor frecuen- cia de batido de la cola de más de 1.5 Hz durante varias horas (ver figura 2 ), seguido de una dis- minución gradual

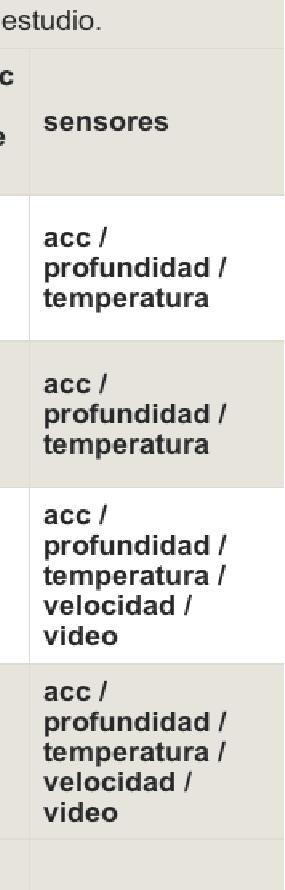
Una longitud de horquilla curva. - b Estimado utilizando una conversión de longitudlongitud y longitud-peso [ 56 ]. - c etiqueta recuperada.
El atún rojo del Atlántico se introdu- jo en la cubierta para el etiquetado electrónico y se soltó de la cabeza primero desde el barco siguiendo
a 30 a 35 m y las temperaturas en- contradas oscilaron entre 12 y 14 ° C. Pescado no. 2 también realizó un DVM mientras encontraba temperaturas de 8–12 ° C ( figura 2 ). A diferencia de los DVM asociados con el buceo, los peces mostraron patrones diel contrastantes en su actividad locomotora, con peces no. 1 actividad principalmente en aumento durante la noche y el pes- cado no. 2 durante el día ( figura 2 ).
3.3. Rendimiento cinemático y natación durante la locomoción horizontal.
2. Visión general de los DVM y los patrones de actividad de los dos atunes rojos del Atlántico gigantes marcados en el Golfo de San Lorenzo, Canadá. hacia un nivel de actividad más sostenido de menos de 1 Hz después de aproximadamente 6 h. En el pez único (pez no. 2) para el que se midió directamente la velocidad de nado, los datos se caracterizaron por una respuesta posterior a la libe- ración de velocidades de natación rápidas de aproximadamente 2,5 ms −1 (aproximadamente 1 longi- tudes de cuerpo s −1), seguido de una reducción a una velocidad de rutina superior a 1,5 ms −1 (aprox. 0,75 longitudes de cuerpo s −1 ) en el transcurso de 6 h. El atún realizó DVM regulares en un ambiente
Durante los episodios de natación horizontal, definidos como el atún que tiene una velocidad vertical absoluta inferior a 0,1 ms −1 y que no realiza movimientos verticales mayores de 10 m, la velocidad de natación mostró una relación lineal con la frecuencia de batido de la cola para el pez no. 2 ( figura 3). Ambos atunes mostraron distribuciones de frecuencia en gran medida sesgadas de la frecuencia de batido de cola, con las frecuencias más utilizadas cerca de la más baja registrada; Las frecuencias modales fueron 0.80 y 0.95 Hz para peces no. 1 y no. 2, respectivamente. En ambos atunes, las frecuencias de latido de cola sostenidas cercanas a 2 Hz estuvieron presentes, pero solo se observaron raramente durante la natación sostenida (definida aquí como la fre- cuencia de batido de cola media en un intervalo de 2 minutos) y se res- tringieron en gran medida al inicio de los despliegues cuando los peces probablemente fueron estresados, aunque los registros aislados de tan alta frecuencia de batido de cola estuvieron presentes más adelan- te. Es importante destacar que, una 3.2. Comportamiento después de la captura
batimétricamente limitado (aprox. 30–40 m); pez no 1 ocurrió a pro- fundidades de alrededor de 30 a 40 m durante el día y pasé la noche principalmente cerca de la super- ficie con inmersiones ocasionales
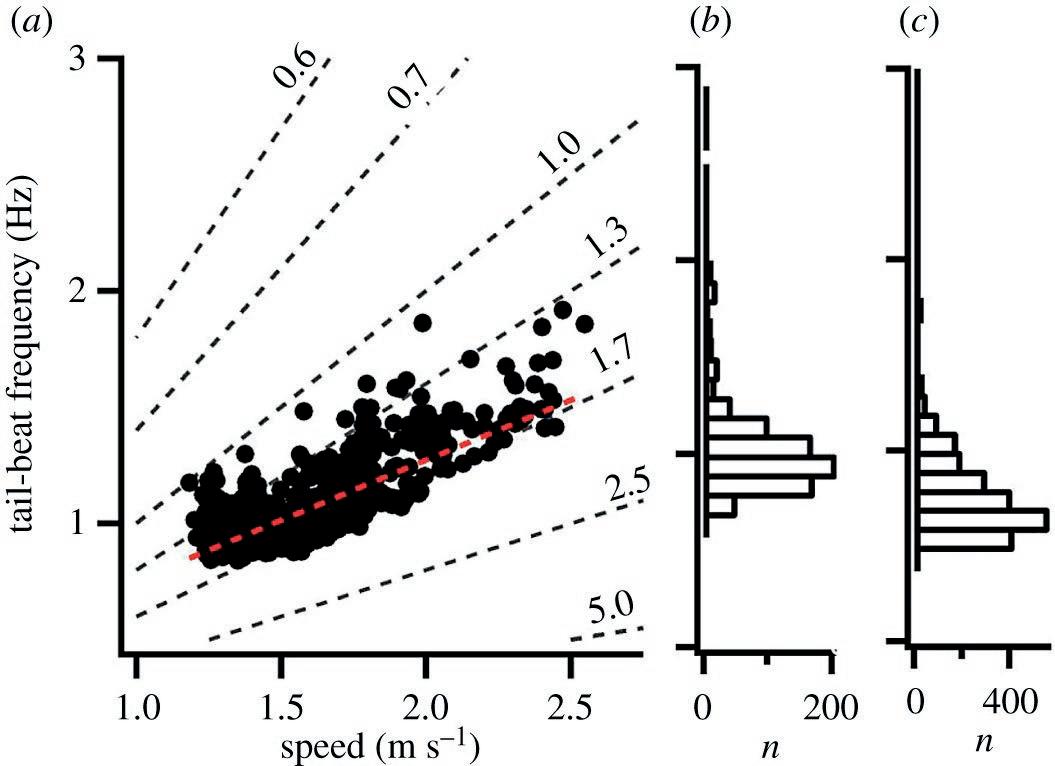
Figura 3. Frecuencias de batido de cola durante la natación horizontal de atún rojo del Atlántico. Relación entre la frecuencia de batido de la cola y la velocidad de natación para nadar a nivel en peces no. 1, la línea roja punteada muestra el ajuste lineal ( r 2 = 0.59) ( a ) y las respectivas distribuciones de frecuencia de las frecuencias de batido de la cola para el mismo pez ( b ) y pez no. 2 ( c ) durante la natación de nivel durante toda la duración. Revelando que los peces pasaron la gran mayoría en frecuencias de batido de cola por debajo de 1 Hz, equivalente a una velocidad de natación de menos de 1,75 ms- 1 o menos de 0,7 longitudes de cuerpo s- 1 . Las líneas punteadas representan longitudes de paso constantes en metros.
observación principal de nuestros datos cinemáticos de peces silves- tres es que la mayoría de las veces, ambos atunes no mostraban latiga- zos continuos, pero mostraban una mezcla de locomoción continua e intermitente ( figura 4), según lo determinado por los acelerómetros y Video adjunto de grabaciones de peces no. 2. A la velocidad de rutina de menos de 1.5 ms −1 , no de pescado. 2 nadaron en gran medida de forma continua, aunque aún se notaron breves períodos de deslizamiento, pero estos no parecían tan estereotipados como la locomoción intermitente después de la liberación del recipiente de marcado o durante movimientos verticales.
3.4. Rendimiento cinemático y na- tación durante movimientos verticales.
Los atunes realizaron movimientos (inmersiones) verticales a gran escala, definidos aquí como movimientos de profundidad con una velocidad vertical continua superior a 0,1 ms −1 con un cambio mínimo en la profundidad de 10 m. Debido a la naturaleza poco profunda del golfo de San Lorenzo (menos de 50 m en la región donde se liberaron los peces), estas inmersiones en las primeras 48 h posteriores a la liberación son probablemente

batimétricamente limitadas, como se evidencia en el registro de video de los peces. llevando una camara de video. Las inmersiones eran tí-
picamente de forma asimétrica; los descensos de atún se caracterizaron por ángulos de inclinación más ba- jos alrededor de aproximadamen- te -9 °, mientras que los ascensos fueron más típicos de aproximadamente 17 ° ( tabla 2). Los descensos se componían principalmente de deslizamientos y solo aproximadamente entre un 30 y un 40% de eventos de natación activos y frecuencias de batido de cola entre 1 y 2 Hz. El deslizamiento estuvo casi ausente en los ascensos, ya que los ascensos están compuestos por más de 90% de natación activa y frecuencias de batido de cola de 1 a 2 Hz, según la velocidad de natación ( tabla 2 ; material complementario electrónico). Pescado no. 2, para las cuales las velocidades de nado estaban disponibles, viajaron a una velocidad media de 1,6 ms −1durante los descensos y de 1,75 m −1 durante los ascensos ( tabla 2 ).
Las correlaciones de momento del producto de Pearson revelaron que la frecuencia de batido de la cola estaba estrechamente relacionada con la velocidad de nado durante los ascensos, pero en menor medida en los descensos ( figura 5 y tabla 3 ). La proporción de tiempo dedica- do a la natación activa, a diferencia del deslizamiento, mostró una tendencia opuesta, ya que la velocidad
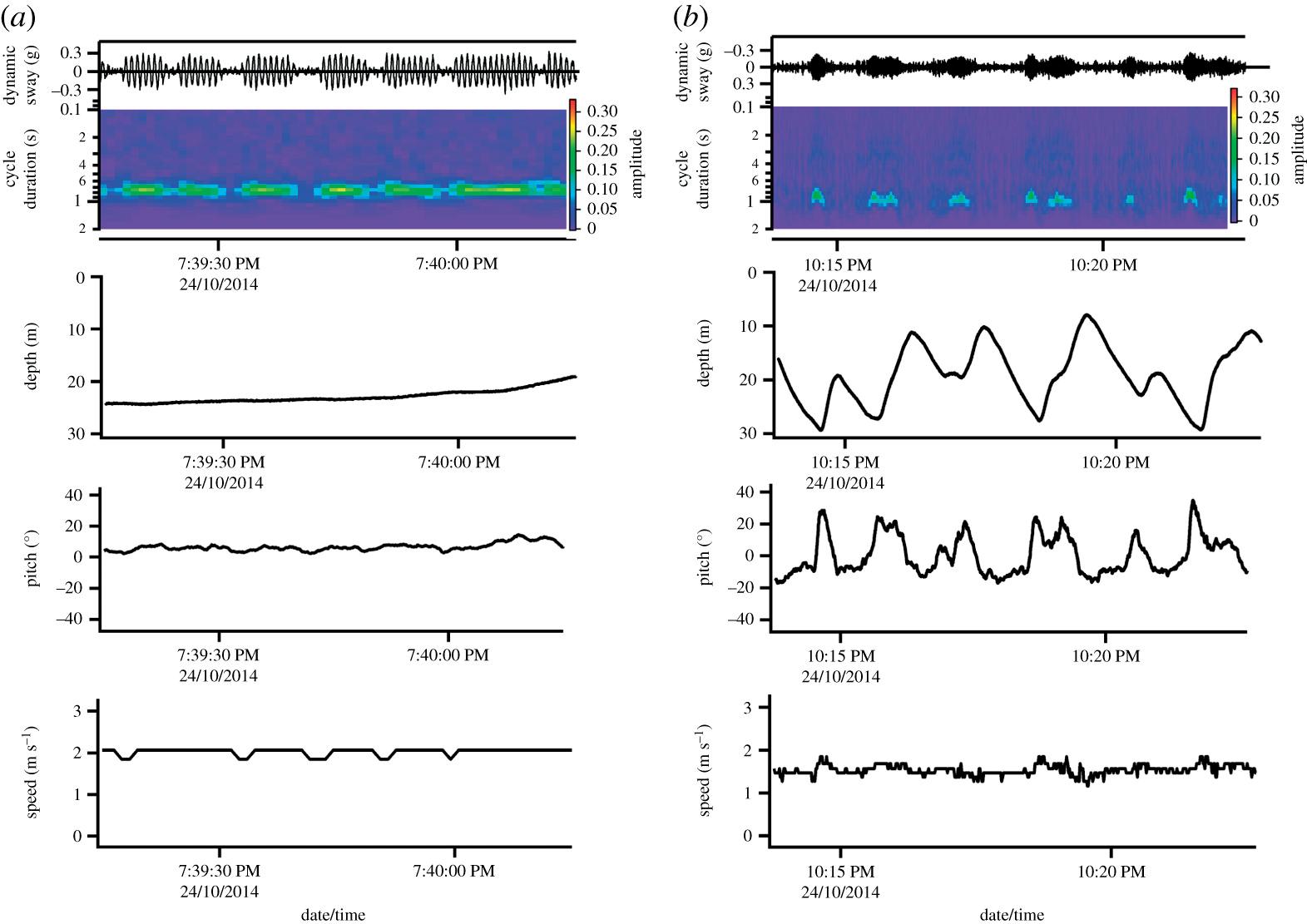
Figura 4. Patrones de locomoción intermitente observados en atún rojo del Atlántico gigante. ( a ) Natación ráfaga-costa clásica [ 18 ], donde la natación rápida enérgica se entremezcla con breves períodos de deslizamiento (vea también el material electrónico complementario) casi en la orientación horizontal del cuerpo. ( b ) La locomoción clásica en dos etapas según lo propuesto por Weihs [ 17 ] para peces con flotabilidad negativa. Los movimientos verticales se realizan a velocidades relativamente bajas y la locomoción intermitente surge principalmente de períodos prolongados de deslizamiento durante descensos poco profundos (aprox. 20 °) y ascensos poco profundos (aprox. 15 °) que comprenden natación activa. Consulte los archivos de video complementarios para ver ejemplos de los diferentes patrones de marcha empleados por este pez.
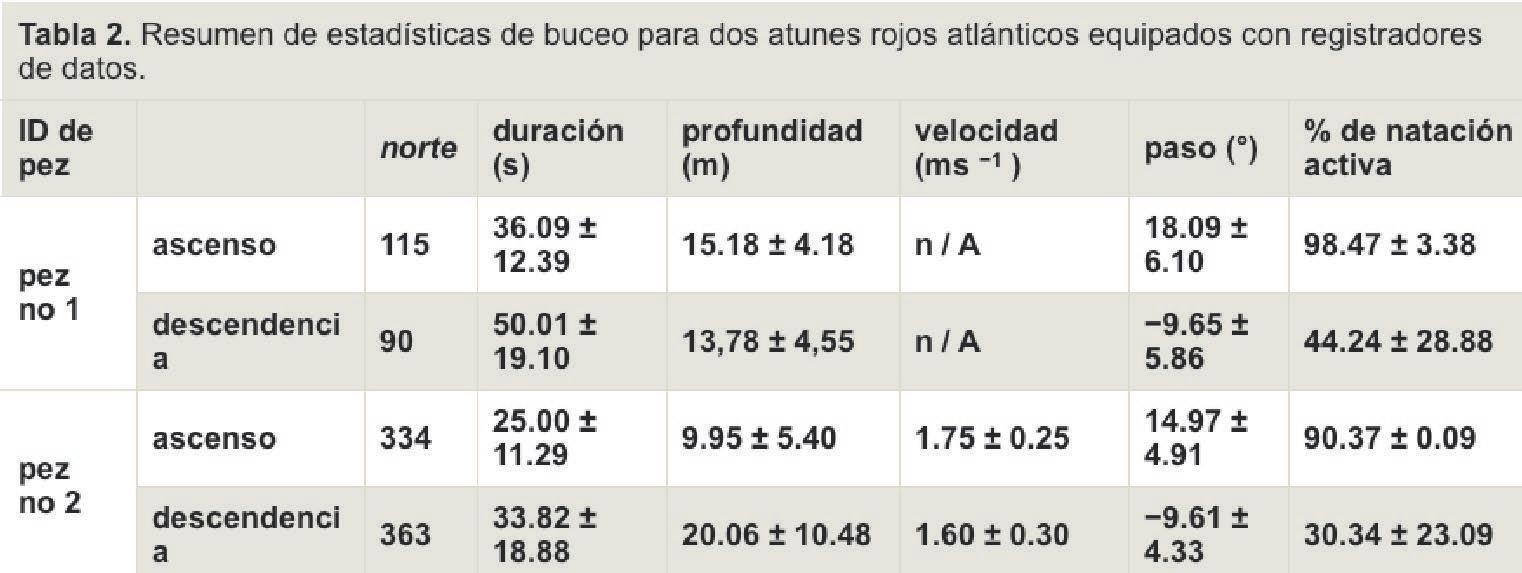
Tabla 3. Correlaciones del momento del producto de Pearson entre cinco parámetros cinemáticos del atún rojo del Atlántico durante excursiones verticales (más de 10 m). Datos de 448 ascensos y 452 descensos. Cada par de valores representa la r de Pearson para ascensos (valor superior) y descensos (valor inferior) de los parámetros emparejados. Las correlaciones significativas están indicadas por el asterisco. Tenga en cuenta que solo un atún llevaba un sensor de velocidad y, por consiguiente, había menos inmersiones disponibles para correlaciones de velocidad (334 ascensos y 363 descensos).
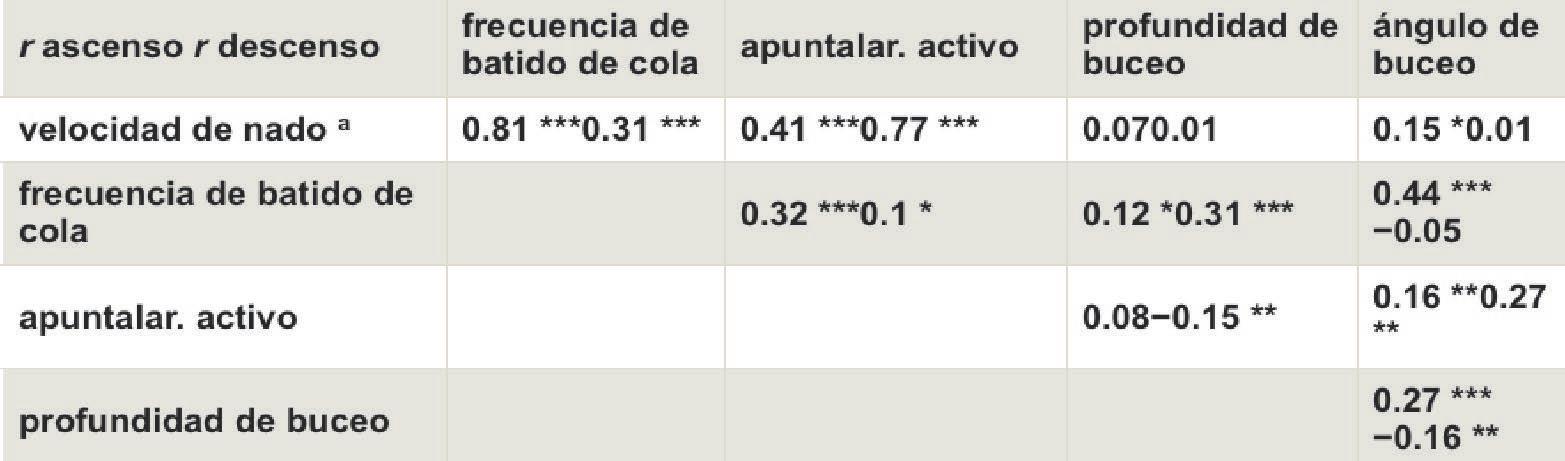
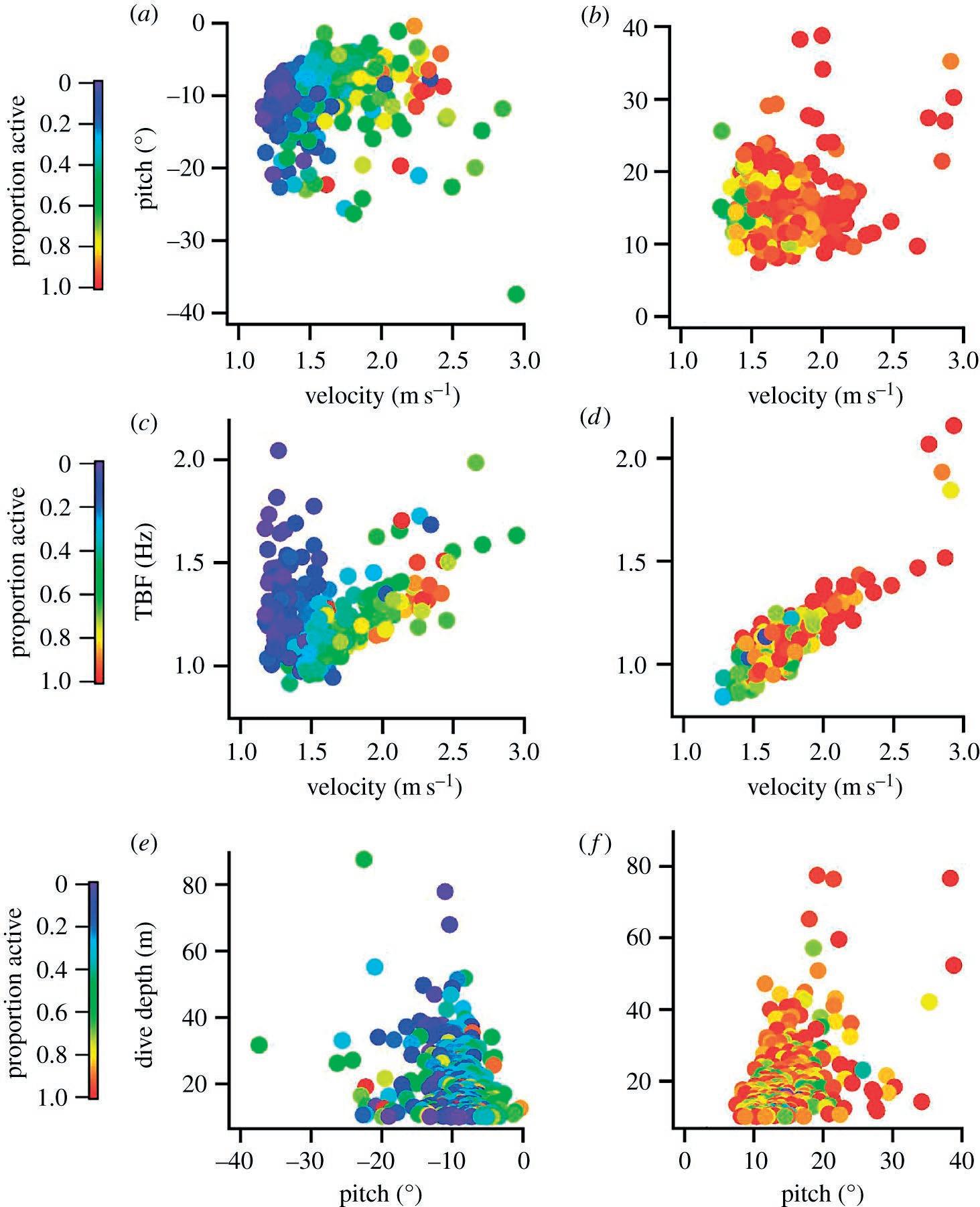
Figura 5. Parámetros cinemáticos para un atún rojo del Atlántico durante el descenso prolongado (más de 10 m) ( a , c , e ) y ascensos ( b , d , f ). Se encontraron relaciones defi cientes para la mayoría de los parámetros cinemáticos ( tabla 3 ), con la excepción de la velocidad de natación, la frecuencia de batido (TBF) y el% de tiempo dedicado a la natación activa (proporción activa en leyenda) que muestra relaciones moderadas a fuertes

de nado y el porcentaje de tiempo de la cola activa se correlacionaron positivamente con los descensos y en menor grado en ascensos ( tabla 3 ). Las profundidades de inmersión mostraron una correlación pobre o nula con otros parámetros, ade- más de una modesta correlación positiva con la frecuencia de bati- do de cola durante los descensos ( tabla 3 ). Los ángulos de buceo también mostraron correlaciones moderadas con la frecuencia de batido de la cola durante los ascensos, pero no los descensos ( tabla 3 ).
*p <0.05; ** p <0,005; *** p <0,0 005.
a Datos solo disponibles para un pez.
Pescado no. 2 con un sensor de velocidad de natación directa mostró que la frecuencia de batido de la co- la estaba estrechamente correlacionada con la velocidad de natación en ambos ascensos y descensos (ANCOVA, F 2.623 = 594.3, r 2 = 0.67, p <0.0001), con una frecuencia de latido de la cola de ascenso ligeramente superior a una velocidad de nado de- terminada (p <0,0001; figura 6), sin interacción significativa ( p = 0,11). Sin embargo, los descensos presentaron una mayor proporción de deslizamientos (tabla 2). Para incorporar la di- ferencia en la cantidad de deslizamiento entre ascensos y des- censos, calculamos una métrica adicional del rendimiento de natación, la tasa de batido de cola, como el número promedio de latidos de cola por segundo para incorporar el deslizamien- to en nuestras estimaciones de la actividad locomotora gene- ral. . Esto reveló una actividad drásticamente menor para los descensos (ANCOVA, F 3,621 = 592,1, r 2 = 0,78, p <0,0001), especialmente a velocidades más bajas, que estaban com- puestas principalmente por deslizamientos (figura 6). La dife- rencia entre ascender y descender disminuyó a velocidades más rápidas, con una interacción significativa entre el ritmo de la cola, la velocidad de natación y si el pez estaba ascen- diendo o descendiendo ( p<0,0001,figura 6 ). Aunque faltan los datos de velocidad de nado, el aleta azul no. 2 mostraron patrones cualitativamente similares con respecto a su com- portamiento de deslizamiento durante ascensos y descensos. 4. Discusión
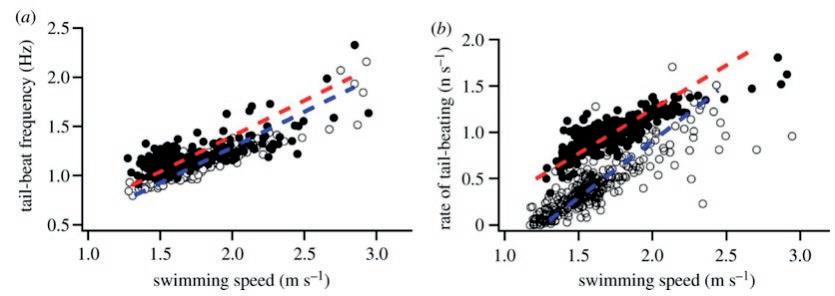
Figura 6. Relación entre la frecuencia de batido de la cola y la velocidad de nado del buceo del atún rojo del Atlántico. ( a ) Cuando el batido de cola activo (número de latidos de cola / tiempo de batido de cola activo), las frecuencias durante el ascenso (círculo relleno, línea discontinua roja) se elevaron ligeramente en comparación con el batido de cola durante el descenso (círculo abierto, línea discontinua azul ). ( b ) Al incorporar la proporción de tiempo que los peces no batieron su cola y se deslizaron activamente, la velocidad de batido de cola (número de latidos de cola / (tiempo de batir de cola activamente + tiempo de deslizamiento pasivo)) se reduce significativamente en los descensos comparados a los ascensos, acercándose a cero golpes de cola en descensos lentos con velocidades de natación de 1.25 ms −1. A velocidades mayores, la diferencia en el esfuerzo locomotor entre ascensos y descensos disminuye cada vez más.

Las etiquetas biológicas están me- jorando rápidamente nuestra ca- pacidad para cuantificar muchos aspectos de la biología de los ani- males que ocupan los lugares más inaccesibles de nuestro planeta. Las etiquetas electrónicas han permi- tido históricamente la elucidación de los patrones espacio-tempora- les en el comportamiento de di- versos taxones, incluido el atún, como las migraciones estaciona- les o los cambios en el comporta- miento y el uso del hábitat [ 10 ].
El avance de las capacidades senso- riales y el aumento de la memoria de las etiquetas biológicas ahora ofrecen una visión revolucionaria similar en los campos de la fisiología comparativa y la biomecánica de in- cluso los animales más enigmáticos en la naturaleza [ 60 , 61 , 62]]. El atún rojo es un atleta extremo con la capacidad de viajar rápidamente a través de las cuencas oceánicas, con migraciones notablemente rápidas desde terrenos de deso- ve de baja latitud a terrenos de forrajeo de alta latitud [ 63 ], res- paldados por adaptaciones fisioló- gicas y biomecánicas únicas [ 1 ].
Si bien los registros de marcas de archivo han revelado las profun- didades notables a las que estos peces pueden bucear y su uso de la columna de agua, este estudio proporciona un primer esfuerzo para examinar la cinemática de la natación en atún salvaje. El uso de una etiqueta biologging de alta re- solución junto con un dispositivo de video ha revelado que además de las especializaciones morfoló- gicas para la natación de alto ren- dimiento, el atún de aleta azul del Atlántico también mostró un reper- torio considerable de patrones de natación que se hipotetizan para mejorar su rendimiento locomotor.
4.1. Locomoción intermitente y rendimiento locomotor.
Se ha planteado la hipótesis de que varios tipos de locomoción inter- mitente aumentan la economía del movimiento en los peces: aquí, proporcionamos evidencia empí- rica de trabajos teóricos anteriores y confirmamos lo que se ha plan- teado durante décadas en atún en libertad [ 17 , 18 ]. En primer lugar, el atún rojo del Atlántico utiliza su flotabilidad negativa y las super- ficies de elevación proporciona- das por sus aletas para deslizarse
durante largos periodos durante el descenso y hacerlo en ángulos muy poco profundos, lo que traduce las fuerzas verticales en una distancia horizontal. Esto representa un as- pecto importante del modelo de locomoción de dos etapas de Weihs [ 17 , 64], sugiriendo que se podrían realizar algunas inmersiones para aumentar la economía de los movimientos horizontales, lo que con- cuerda en gran medida con el tra- bajo cautivo en atún rojo [ 54 , 55 ].
Lo más probable es que las bajas velocidades de natación durante esas inmersiones también sean cruciales para aumentar la eficiencia, ya que descender a velocidades más altas parece requerir que los peces pasen más tiempo activamen- te nadando, ya que las fuerzas hi- drostáticas de flotabilidad negativa no son suficientes para vencer la resistencia a esas velocidades más altas. Sorprendentemente, gran parte del video una vez que el pez estuvo en calma luego de su lan- zamiento, reveló que el atún rojo solo usaba una actividad locomotora menor, a pesar de que toda- vía navega a velocidades aprecia- bles (aproximadamente 1.5 ms- 1).
La conservación de la actividad muscular es clara en estas largas secuencias de deslizamiento con latidos intermitentes de la cola (ver video complementario). Las inmer- siones también presentan geome- trías ligeramente asimétricas, los ascensos son más rápidos y más empinados que los descensos, lo que disminuye el tiempo dedica- do a la parte energéticamente ca- ra de una inmersión y aumenta la cantidad de tiempo dedicado a las fases de deslizamiento en ángulos poco profundos, lo que aumen- ta la distancia horizontal recorrida por unidad energía. Holanda y otros han observado geometrías similares. [ 50] para el atún de ojo grande calculado a partir del rastreo acústico activo de peces con marcas sensibles a la profundidad, que solo brindó ahorros modestos basados en las trayectorias observadas, que fueron muy superficiales a apro- ximadamente 6 ° para ascensos y descensos, en comparación con las geometrías de buceo más pronun- ciadas de aproximadamente 10–15 ° registrado para el aleta azul aquí.
Las geometrías calculadas a partir del seguimiento acústico activo, sin em- bargo, sufren errores que no se han tenido en cuenta, es decir, la inexac-
titud en la ubicación de los peces y no tienen en cuenta las corrientes oceánicas que alterarían los ángulos calculados. Los cálculos de los ángulos de inclinación de los aceleró- metros no sufren los mismos sesgos.
Es importante destacar que la lo- comoción intermitente no se limitó a los descensos durante los movimientos verticales, sino que también se incluyó en la locomoción hori- zontal. Sin embargo, se reservó en gran parte para el inicio del desplie- gue, mientras que la última parte del registro contó con una locomoción más continua a velocidades comparables de natación. Sin embargo, tales velocidades rápidas de nata- ción solo se presentaron esporádi- camente más adelante en el registro.
Está bien establecido que los peces cambian de la marcha de natación continua a la de la costa cuando la velocidad de contracción del músculo aeróbico es insuficiente para lograr una natación eficiente a altas velocidades [ 18 , 65]]. Se requieren más registros de mayor duración para comprender mejor la cinemática del atún, especialmente durante velocidades de nado más altas que rara vez se registraron en despliegues de corta duración.
4.2. Cinemática del buceo
Los novedosos datos de etiqueta- do proporcionados a partir de las etiquetas de acelerometría y video biológico brindan nueva informa- ción sobre cómo los atunes rojos pueden modular la velocidad de na- tación durante el buceo y comien- zan a responder algunas preguntas de larga data sobre la biomecánica de estos peces en la naturaleza.
A partir de estos datos iniciales, hemos aprendido que el atún rojo del Atlántico modifica tanto la frecuencia de su ritmo de cola como la cantidad de tiempo que se pasa deslizándose pasivamente. En la locomoción asistida por gravedad, es decir, cuando el atún desciende debido a su fl otabilidad nega- tiva [ 66 ], la velocidad se modula principalmente por la cantidad de tiempo que se pasa deslizándose pasivamente, especialmente a ve- locidades más bajas, mientras que a velocidades más altas (más de 1.75 ms- 1)), la frecuencia de batido de cola es cinemáticamente más importante ya que el tiempo que pasan los peces para deslizarse se redu- ce a aproximadamente el 40%. La





















velocidad de natación durante los ascensos está determinada en gran medida por la frecuencia de batido de la cola y, en menor medida, por la cantidad de deslizamiento. La clara dicotomía entre la modulación de la velocidad entre ascensos se deriva de dos principios básicos; la flotabilidad negativa del atún rojo se tradu- ce en movimiento hacia adelante a través de la producción por elevación de las aletas pectorales, lo que permite que el atún se deslice du- rante duraciones prolongadas [ 67].
En el ascenso, el atún rojo debe su- perar esta flotabilidad negativa, lo que significa que se debe generar más empuje. Por lo que sabemos, no hay datos disponibles sobre la flotabilidad de ningún atún rojo; sin embargo, según los datos de otros atunes verdaderos, como el ojo grande y el aleta amarilla, con vejiga de gas igualmente pequeña y tejido denso [ 66 , 67 ], el atún rojo es negativamente flotante (BAB 2014, observación personal).
Las mayores cantidades de deslizamiento pasivo durante los descensos del atún estudiado aquí lo respaldan [ 29 , 31 ]. La comparación de la cinemática entre las dos fases del buceo (ascenso y descenso) reveló patrones interesantes; Las diferencias relativamente menores en la frecuencia de batido de cola del atún durante los ascensos y descensos a una velocidad de natación dada fueron sorprendentes. De primera mano, esto puede sugerir que superar las fuer- zas de flotación (es decir, el cambio en la energía potencial) representa un componente menor de la potencia requerida para nadar. Sin embargo, el atún se desliza significativamente más cuando la flotabilidad asistida (descendente) que la flotabilidad impedida (ascendente).
Al incorporar el porcentaje de tiem- po dedicado a planear en nuestra aproximación del esfuerzo locomotor, el descenso con asistencia de la gravedad y el ascenso con el impedimento de la gravedad mues- tran diferencias claras. De manera importante, se encontró que la di- ferencia en la actividad locomotora entre la natación ascendente y des- cendente disminuye a medida que aumenta la velocidad de natación.
Este es un patrón esperado basado en los primeros principios; el arrastre inducido de una superficie que produce sustentación, como la aleta
pectoral de un atún [66 ] está inversamente relacionado con el cuadrado de la velocidad de natación, mientras que el arrastre del cuerpo de los peces (parásito) es propor- cional a la velocidad de natación al cuadrado [ 68 , 69]. Por lo tanto, a velocidades más rápidas, el costo relativo de contrarrestar la flotabilidad negativa se vuelve cada vez más insignificante en comparación con los costos relacionados con la resistencia del parásito; posterior- mente, a las velocidades más altas, esperaríamos que hubiera poca di- ferencia entre los costos energéticos de ascensos y descensos más allá de la diferencia en energía potencial.
Además, las velocidades más rápi- das también incurren en una mayor resistencia hidrodinámica y, por lo tanto, los peces tienen que aumentar la proporción de tiempo nadando activamente en lugar de deslizarse. Por lo tanto, la reducción relativa en el trabajo mecánico por el buceo repetido disminuye a medida que aumentan las velocidades de natación, como se demuestra en la teoría original de Weihs [ 17 ].
Sin embargo, la similitud entre la frecuencia de batido de cola durante el ascenso y el descenso (antes de tener en cuenta el porcentaje de deslizamiento) puede representar más que un artefacto, ya que sugiere que la velocidad de natación y no la flotabilidad representan el parámetro clave que gobierna la fre- cuencia del batido de cola. La razón de esto puede estar relacionada con el engranaje del músculo y las propiedades hidrodinámicas de la cola [ 70 , 71]. Las propiedades hidrodinámicas de los sistemas musculoesquelético e hidrodinámico probablemente están optimizadas para proporcionar un empuje óptimo a una velocidad de nado determinada y el movimiento fuera de este ran- go puede resultar en una pérdida de eficiencia, similar a manejar una bicicleta en la marcha incorrecta.
Al intercalar los deslizadores con el batido activo de la cola, el atún extiende efectivamente esta relación de engranaje, en lugar de usar frecuencias de batido de la cola que pueden implicar una menor eficiencia cuando se requiere menos empuje. Se ha demostrado que una teoría similar se aplica al vuelo intermitente de aleteo en aves [ 72]. Por supuesto, los peces pueden alterar otros parámetros cinemáticos que los acelerómetros no
pueden aludir fácilmente, a saber, la amplitud del latido de la cola o la rigidez de la región caudal, que puede alterarse en respuesta a los cambios en su entorno hidrodinámico. Los cambios en la amplitud pue- den explicar la diferencia marginal en la frecuencia de batido de cola entre ascensos y descensos aquí.
Cabe destacar que nuestras discu- siones relacionadas con los movimientos verticales que brindan un ahorro de energía para los peces se basan en un supuesto importante en la teoría de Weihs [ 17 ], a saber, que la eficiencia de la transformación de la energía química en trabajo mecánico debe diferir entre el ascenso y el descenso [ 27 ].
Originalmente, propusimos que el arrastre incurrido por un pez que nada con ondulaciones laterales debería ser de dos a tres veces más grande que el de un pez rígido y deslizante. Por lo tanto, si un pez puede impulsarse a sí mismo de for- ma pasiva utilizando la gravedad durante el descenso, incurriría en una resistencia sustancialmente menor que si nadara continuamente.
Takagi et al. [ 54], al utilizar la dinámica de fluidos computacional, cuantificó y confirmó que el coeficiente de resistencia al atún rojo ju- venil del Pacífico era mayor durante la natación ondulatoria que por el deslizamiento en un factor de dos, lo que apoya aún más que el atún pue- da ahorrar energía a través del buceo repetido. Se debe tener precaución al traducir estos datos a otros peces, ya que este efecto puede no ser uni- versal y puede depender de la cinemática de la especie en cuestión.
Nuestro análisis ha considerado que las fuerzas y las respuestas cinemá- ticas del atún son algo constantes durante el ascenso y el descenso. Esto, sin embargo, no es estrictamente cierto; a pesar de que las vejigas de gas de atún rojo son pequeñas para su tamaño corporal [ 67], propor- ciona una cantidad apreciable de fuerza hidrostática. Especialmente para los peces que realizan movi- mientos verticales, estas fuerzas hidrostáticas cambian con la profundidad, debido al aumento de la presión ambiental y la reducción del volumen de la vejiga de gas siguiendo la Ley de Boyle. Encontramos algunas pruebas de que la profundidad de las inmersiones (y, por extensión, la cantidad de fuerzas hidrostáticas proporcionadas por la

vejiga) influye en el buceo de estos peces. El atún que asciende desde profundidades más profundas batió sus colas más rápido en compara- ción con las inmersiones menos profundas; sin embargo, también se zambulleron en un ángulo más pronunciado, lo que dificulta la distinción entre la influencia de las fuerzas hidrostáticas cambiantes o la geometría de buceo cambiante.
No observamos los cambios drásticos en el esfuerzo locomotor que se han observado en otras especies con vejigas más grandes, como el esturión o el bagre [ 73 ,74 ]. Esto puede deberse a que los cambios en las fuerzas hidrostáticas durante el movimiento vertical en el atún son algo más pequeños que aquellas especies que tienen grandes vejigas de gas y flotabilidad casi neutral en su profundidad de residencia [ 67 ].
Nuestra discusión se ha enfocado hasta ahora en las consecuencias energéticas del comportamiento del buceo; sin embargo, esto no debe implicar necesariamente que estos atunes se zambullen con el fin de mejorar su rendimiento locomotor, sino de una manera que mejoró su rendimiento locomotor. Se ha demostrado que los peces bucean por una variedad de razones y que las funciones de estas excursiones verticales no se excluyen mutuamente y pueden cambiar diariamente [ 30 , 44 , 75 ].
Ciertamente para el atún rojo del Atlántico y otras especies de atunes, la termorregulación ha sido una explicación prominente para las excursiones verticales, permi- tiendo que los peces se alimenten por debajo de la termoclina mien- tras mantienen elevadas temperatu- ras musculares [ 48 , 49]; el buceo con atún de ojo grande para fines de termorregulación generalmente presenta velocidades verticales muy altas (aproximadamente 1–2 ms- 1 ) [ 48 ], lo que sugiere que los peces se sumergen más que el atún rojo en nuestro estudio.
De hecho, las aguas relativamente poco profundas del golfo de San Lorenzo están bien mezcladas y ofrecen pocas oportunidades para la termorregulación. En cambio, el atún probablemente realiza movimientos verticales repetidos con el propósito de ubicar a sus presas de escolarización.
En general, se piensa que el atún rojo
del Atlántico se reúne anualmente en el Golfo de San Lorenzo para alimentarse de arenque del Atlánti- co (Clupea harengus) y caballa del Atlántico (Scomber scombrus) y la evidencia anecdótica de los pesca- dores comerciales sugiere que los peces ganan una masa sustancial du- rante su residencia de verano (ACG y RJS 2014, comunicación personal).
Las investigaciones futuras deberían implementar etiquetas simila- res en áreas donde el comportamiento de buceo de los peces esté limitado por las condiciones ambientales, como temperaturas muy bajas por debajo de la termoclina o estratificación vertical en la concentración de oxígeno, ya que la cinemática del buceo puede verse drásticamente alterada por cambios en la temperatura y / o el oxígeno.
Nuestro trabajo demuestra que el atún utiliza una serie de estrategias que son consistentes con los modelos teóricos de la economía del movimiento, lo que confirma las hipótesis de larga data sobre la manera en que se mueve el atún en libertad. Estos conocimientos se derivan en gran parte de nues- tros avances metodológicos en la conexión externa de los registradores de datos al atún utilizando su aleta dorsal pequeña pero rígida y un diseño de etiqueta optimizado.
Nuestros resultados prestan un ma- yor apoyo a la teoría de la fuerte convergencia en la evolución de la cinemática de la natación en todos los medios fluidos; donde se han demostrado patrones de locomoción intermitente junto con movimientos verticales en una gama de clados relacionados de manera distante, como aves, fócidos, misticetos y peces elasmobranquios [ 24 , 72 , 76].
Esto sugiere que las fuerzas físicas que actúan sobre los animales en movimiento están bajo una fuer- te presión selectiva y dan como resultado la evolución generalizada de comportamientos y mor- fologías que reducen el gasto de energía innecesario [ 24 , 32 ].
Ética
Los atunes se marcaron con per- miso del Departamento de Pesca y la Región del Golfo del Océano, Canadá (SG-GNS-14-132A). Todos los procedimientos fueron aproba- dos por el Comité Institucional de Cuidado y Uso de Animales de la
Universidad de Stanford (13865).
Accesibilidad de datos Disponibles en el repositorio digital de Dryad: org/10.5061/dryad.7vp288fhttps://doi. [ 77 ].
Contribuciones de los autores ACG y BAB concibieron el estudio. ACG, RJS y SGW realizaron el trabajo de campo. ACG y JJD analiza- ron los datos. ACG redactó el manuscrito con todos los autores contribuyendo y aprobando la versión final. Conflicto de intereses: Declaramos que no tenemos intereses en competencia.
Fondos: El trabajo fue financiado por la Oficina de Investigación Naval. Agradeciemientos:
Nos gustaría agradecer a Gil Iosi- levskii, Denise Greig y un colaborador anónimo cuyos comentarios mejoraron enormemente este manuscrito. También nos gustaría agradecer a Dennis Cameron, Lloyd MacInnes, Duncan Sutherland, la Cooperativa de Pescadores de Ceilidh, el Departamento de Pesca y Océanos, el Dr. Michael Stokesbury y la comunidad de Port Hood por apoyar nuestro trabajo. Nos gustaría agradecer a Nicholas Whit- ney por proporcionar flotadores para G6as y Mike Castleton por producir material complementario electrónico, figura S1. Agradecemos a la Fundación TAG A Giant of the Ocean por su apoyo.
Notas adicionales: El material complementario electrónico está disponible en línea en https://dx.doi.org/10.6084/ m9.figshare.c.4482188
© 2019 Los Autores. Publicado por la Royal Society bajo los términos de la licencia de atribución de Creative Commons http://creativecommons.org/licenses/by/4.0/, que permite el uso sin restricciones, siempre que el autor original y la fuente sean acreditados.
https://royalsocietypublishing.org/doi/ full/10.1098/rsos.190203#RSOS190203F1
Adrian C. Gleiss, Robert J. Schallert, Jonathan J. Dale, Steve G. Wilson y Barbara A. Block
Publicado: 8 de mayo de 2019 https://doi.org/10.1098/rsos.190203
La acuacultura es una actividad económica muy importante en la de producción de alimentos, de materias primas de uso industrial, farmacéutico y organismos vivos para repoblación, ornato o alimento. En 2014 se registró el gran logro de que la actividad acuícola superó por primera vez a la pesca de captura en el medio natural, en el suministro de pescado para consumo huma- no (FAO, 2018). En 2016 se alcanzó una producción acuícola mundial de 80,0 millones de toneladas de pescado comestible (FAO 2018). En los sistemas de producción acuí- cola, el factor de la nutrición es esencial para obtener un producto de alta calidad y económicamente rentable.
Generalmente, la nutrición representa hasta un 50% de los costos de producción en un sistema acuí- cola. Por lo que los esfuerzos en el tema de la nutrición, han llevado a desarrollar nuevas y específicas formulaciones balanceadas que promueven óptimos y saludables crecimientos de los organismos cultivados y de la diversificación a nuevas especies en la industria de la acuacultura, que demanda productos cada vez más seguros y de alta calidad (Craig, S. 2017).
La investigación de la nutrición en un sistema acuícola, se hace necesario formular adecuadamente una dieta balanceada e imprescindible evaluar la calidad no solo de ésta sino de los ingredientes que la componen. Para lo cual, es impor- tante contemplar varios factores, que incluyen información sobre digestibilidad, palatabilidad, así como utilización e interferencia de nutrientes (Glencross et al., 2007).

Un alimento o un ingrediente ali- menticio puede ser una excelente fuente de nutrientes, pero a la vez ser de bajo valor nutrimental al no ser digerido y absorbido por la especie que lo requiera. Por lo que es altamente deseable conocer la digestibilidad de los nutrientes, para asegurar la efectividad nutri- mental de un alimento balanceado (Köprücü y Özdemir, 2005).
La actividad de las enzimas diges- tivas de los organismos acuícolas cultivados promueve su capacidad digestiva, por lo que entender los mecanismos de digestión, lleva a elegir los ingredientes y alimentos con más alto valor nutritivo para ca- da especie (Cruz-Suárez et al., 2002).
La harina de pescado ha sido el ingrediente proteico de más alta demanda en el crecimiento sostenido de la acuacultura, hasta hace una década, por su alto contenido proteico, sus buenos perfiles de aminoácidos y de ácidos grasos de la familia omega-3 (ó n-3), así como por su alta digestibilidad y palatabilidad (Hardy y Tacon, 2002).
Esa alta demanda como ingrediente en la acuacultura, además en dietas de ganado y aves de corral, ha dado como resultado que es la fuente de proteína más cara en dietas balanceadas.
Lo anterior ha llevado a investigar alimentos y/o ingredientes que sean más factibles económicamente y que presenten características nutrimen- tales adecuadas y efectivas para el éxito de los sistemas de cultivo de organismos acuícolas (El-Sayed, 2004).
En la investigación de ingredientes
alternativos a la harina de pescado, se hace importante conocer no solo la composición química de éstos, sino de manera muy especial su di- gestibilidad con el fin de medir el aprovechamiento o disponibilidad de los nutrimentos, así como de reducir la contaminación al ambiente. Factores esenciales de la alimentación en un sistema acuícola, son la digestibilidad y la estrategia de alimen- tación, para proveer de los nutrientes y la energía necesaria para el creci- miento eficiente de las especies cultivadas Carrillo-Farnés et al., 2007).
Desgraciadamente, para llevar a cabo estudios de digestibilidad se requieren organismos vivos a los cuales se les administra un alimento por determinado tiempo y se va registrando su aumento en peso. Este tipo de experimentos son los más certeros en cuanto al valor nutrimental de un alimento que se refleja en aumento de tejido o músculo. Como se podrá advertir, estos experimen- tos requieren tiempo, instalaciones adecuadas y suficiente alimento de prueba, sin olvidar el adecuado adiestramiento del personal que mantiene a los organismos de prueba en las condiciones apropiadas.
¿Qué tan adecuado sería llevar a cabo una prueba en poco tiempo simulando el sistema digestivo del organismo en estudio? En la década de los 60´s del siglo pasado se empezó a experimentar justamente con la digestibilidad “in vitro”, es decir, una simulación en el laboratorio de lo que ocurre en la digestión “in vivo”, es decir, en un organismo viviente. Dado el interés por la alimentación humana, estas pruebas de digestibilidad in vitro, fueron llevadas a cabo en un sistema que

utilizó 3 enzimas clave en la diges- tión humana: la tripsina, la quimio- tripsina y una peptidasa bacteriana, en una prueba diseñada por Hsu y colaboradores en 1977, en la cual se utilizaban las condiciones adecuadas de pH, salinidad y temperatura para cada enzima. Al final se ob- tenía una idea bastante cercana de la hidrólisis del alimento durante la digestión humana. Estos porcentajes de hidrólisis se traducían en % de digestibilidad del alimento mediante ecuaciones obtenidas al repetir el experimento con una gran cantidad de alimentos y relacionándolas con digestibilidades obtenidas “in vivo”. Posteriormente el mismo grupo de investigación, incorporó una enzi- ma más, una alcalasa, obteniendo mejores aproximaciones a una di- gestibilidad “in vivo”. A éste pro- cedimiento se le conoció como el “ensayo de las cuatro enzimas” que se convirtió en el estándar para esti- mar la digestibilidad de un alimento.
La industria de alimentos para ani- males no tardó en adoptar este tipo de ensayos para la formulación de sus dietas y la acuacultura siendo una industria en la cual sus princi- pales insumos son los alimentos, ciertamente no fue la excepción y adoptó estos ensayos para la elabo- ración de dietas. El ensayo de las 4 enzimas parte de un coctel de en- zimas comerciales, las cuales son básicamente enzimas obtenidas por fermentación en microorganismos. Pero, ¿Qué tal si en lugar de ésas, se usaran las enzimas del organismo al cual están dirigidas las dietas?; así fue que justamente es lo que suce- dió en la década de los 80´s y 90´s, se empezó a obtener preparaciones
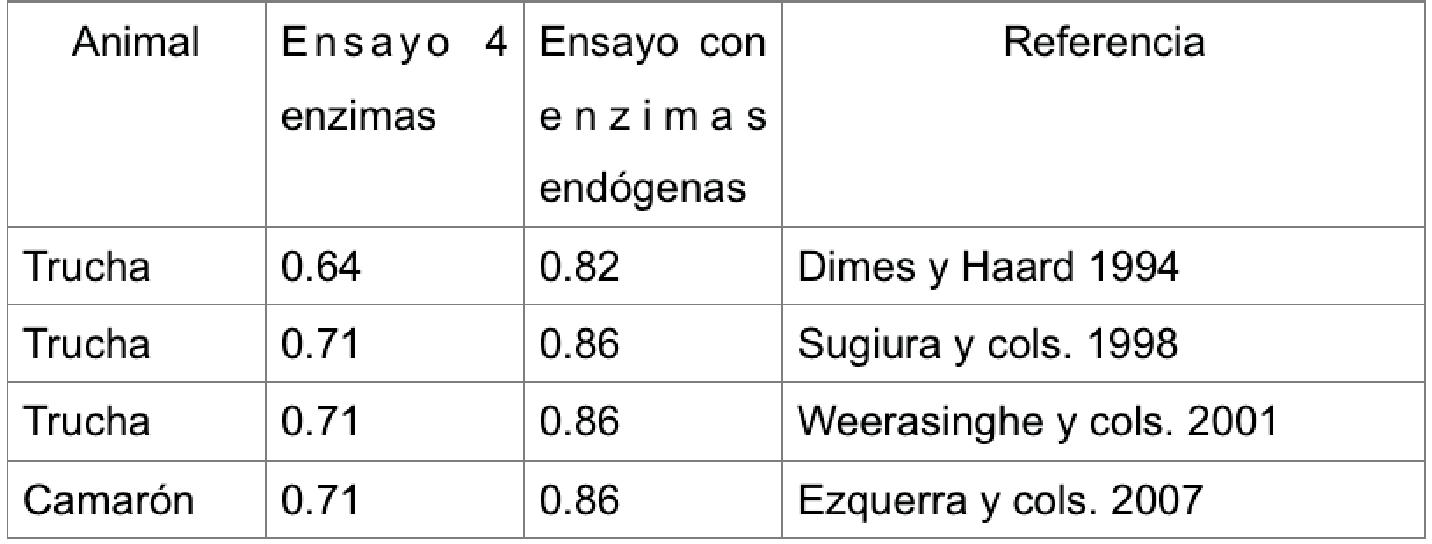
Tabla 1. Comparación del coeficiente de determinación (r2) entre la digestibilidad aparente in vitro y el grado de hidrólisis medidos con la técnica de pH stat, usando la técnica de las 4 enzimas y las enzimas endógenas del organismo en estudio.
enzimáticas de los organismos en estudio (salmón, trucha, camarones, etc.) y se hicieron a la par estudios de digestibilidad in vivo para fines de comparación (Dimes y Haard, 1994). Estas comparaciones mos- traron que la digestibilidad estima- da se incrementaba el coeficiente de correlación de manera signifi - cativa, es decir el ensayo usando enzimas endógenas del organismo en estudio era mucho más cercano a la digestibilidad in vivo y por lo tanto un estimador mucho más confiable del valor de la dieta para incrementar el tejido o músculo del organismo, lo cual se evidencia en la Tabla 1. En esta tabla se puede observar que en todos los casos el coeficiente de determinación (r2) entre la digestibilidad in vitro y el grado de hidrólisis, que es la forma de medir la acción de las enzimas proteolíticas, se incrementa cuando se usan las enzimas endógenas en lugar de las enzimas comerciales. En todas estas publicaciones se usó la misma técnica de medir el grado de hidrólisis, con el aparato pH stat. Actualmente, todas las grandes

compañías que elaboran alimen- tos balanceados tanto para ganado como para la acuacultura, llevan a cabo estimaciones de la digestibili- dad mediante pruebas de digestibi- lidad in vitro. Sin embargo, dada la dinámica de la acuacultura, donde nuevas especies se siguen incorpo- rando a cultivo, la experimentación con enzimas digestivas endógenas debe mantenerse al parejo, ya que las ventajas en la estimación de la di- gestibilidad “verdadera” serán siem- pre mayores, lo cual a finalmente redituará en ahorros en alimento balanceado, así como en mejores pro- ducciones (Moyano, y cols., 2015).
Por todo lo anterior, en el pano- rama regional, las empresas acuí- colas pueden beneficiarse de este tipo de técnicas acudiendo a los investigadores en enzimas ya sea de las Universidades o de Centros de investigación para obtener mejores estimaciones de digesti- bilidad ya sea de los ingredientes que utilizan como insumos o de las dietas que formulan y elaboran.
Referencias
Olimpia Carrillo-Farnés, Alina Forrellat-Barrios, Saúl Guerrero-Galván and Fernando Vega-Villasante. 2007. A Review of Digestive Enzyme Activity in Penaeid Shrimps. Crustaceana. 80 (3). pp. 257-275.
Craig, S. (2007). Understanding Fish Nutrition, Feeds, and Feeding. Virginia Cooperative Extension. Virginia Tech. Virginia State University. Publication 420-256.
Cruz-Suárez, L.E., D. Ricque-Marie, M. Tapia-Salazar, L.F. MarínZaldívar, C. Guajardo-Barbosa, M. NietoLópez & A. Salinas-Miller. 2002. Historia y estatus actual de la digestibilidad y algunas características fisicoquímicas de los alimentos comerciales para camarón usados en México. In: L. Cruz-Suárez, D. Ricque-Marie, M. Tapia-Salazar, G. Gaxiola-Cortés & N. Simoes (eds.). Avances en Nutrición Acuícola. VI Memorias del VI Simposio Internacional de Nutrición Acuícola. Cancún, Quintana Roo, pp. 1-22
Dimes L.E. y Haard, N.F. (1994) Estimation of Protein Digestibility. Comparative Biochemistry and Physiology Part A: Physiology. 108 (2): 349-362.
El-Sayed. El-Sayed, A.F.M 2006. Tilapia culture. CABI Pub.USA. Ezquerra, J.M., García Carreño, F.L. y Haard, N.F. (2007) Effects of Feed Diets on Digestive Proteases from the Hepatopancreas of White Shrimp (2007) Journal of Food Biochemistry 21(2): 401-419. Glencross, B., Booth, M. and Allan, G. (2007), A feed is only as good as its ingredients – a review of in-
gredient evaluation strategies for aquaculture feeds. Aquaculture Nutrition, 13: 17-34.
Hardy,R.W. y Tacon, A.G.J. (2002). Fish meal historical

uses, production trends and future Outlook for sustainable supplies. En R.R. Stickney (Ed.). Sustainable Aquaculture. New York: CABI.
Hsu, H.W., Vavak, D.L., Saterlee L.D. y Miller, G.A. (1977) A Multienzyme technique for estimating protein digestibility. Food Science, Vol 42 (5): 1269-1273.
Hassan, A.S., Seden, M.E., Amer, T.N. y El-Tawil, N.E.(2013). Substituting fish meal with smoked fish waste meal in diets for African catfish (Clarias gariepinus). Abvassa Int. J. Aqua. 6 (2): 46-63.
Moyano F.J., Daénz de Rodrigáñez, M.A. Díaz, M. y Tacon, A.G.J. (2015) Application of in vitro digestibility methods in aquaculture: constraints and perspectives. Reviews in Aquaculture 7:223-242 Kenan Köprücü ̈*,YaYar Özdemir. (2005). Apparent digestibility of selected feed ingredients forNile tilapia (Oreochromis niloticus). Aquaculture. 250. 250. 308–316 Sugiura S.H., Dong F.M., Rathbone C.K., Hardy R.W. (1998). Apparent protein digestibility and mineral availabilities in various feed ingredients for salmonid feeds. Aquaculture 159: 177-202.
Weerasinghe V, Hardy R.W., Haard N.F. (2001). An in vitro method for phosphorus digestibility of trout (Oncorhnychus mykiss) feed. Aquaculture Nutrition 7(1): 1-9.
Bringas-Alvarado, L1., y CárdenasLópez, J.L2. 1 Depto. de Investigaciones Científicas y Tecnológicas. D.I.C.T.U.S. 2 Depto. de Investigación y Posgrado en Alimentos. D.I.P.A.


Estándares de biodegradabilidad para bolsas de transporte y películas plásticas en ambientes acuáticos: una revisión crítica
La basura plástica se encuentra en los ecosistemas acuáticos de todo el mundo, incluidos los entornos polares y las profundidades mari- nas. Para mitigar los impactos socia- les y ecológicos adversos de estos residuos, se ha debatido si los materiales 'biodegradables' deberían recibir exenciones de las prohibi- ciones y gravámenes de las bolsas de plástico. Sin embargo, se debe tener mucho cuidado al tratar de definir este término, debido a la amplia y compleja gama de condicio- nes físicas y químicas encontradas en los ecosistemas naturales. Aquí, revisamos los estándares industriales internacionales existentes y los métodos de prueba regionales pa- ra evaluar la biodegradabilidad de los plásticos en entornos acuáticos (aguas residuales, hábitats de agua dulce y marinos no gestionados). Ar- gumentamos que los estándares actuales y los métodos de prueba son insuficientes en su capacidad para predecir de manera realista la biodegradabilidad de las bolsas de transporte en estos entornos, debido a varias deficiencias en los procedi- mientos experimentales y la escasez de información en la literatura científica. Además, los estándares de biodegradabilidad existentes y los métodos de prueba para ambientes acuáticos no implican pruebas de toxicidad ni tienen en cuenta los impactos ecológicos potencialmente adversos de las bolsas de transporte, los aditivos plásticos, los productos de degradación de polímeros o las pequeñas partículas de plástico (mi- croscópicas) que pueden surgir a tra- vés de la fragmentación. El hecho de abordar con éxito estas lagunas de
conocimiento es un requisito clave para desarrollar nuevos estándares de biodegradabilidad para bolsas de transporte livianas. Debido a varias deficiencias en los procedimien- tos experimentales y la escasez de información en la literatura científica. Además, los estándares de biodegradabilidad existentes y los métodos de prueba para ambientes acuáticos no implican pruebas de toxicidad ni tienen en cuenta los impactos ecológicos potencialmente adversos de las bolsas de transporte, los aditivos plásticos, los productos de degradación de polímeros o las pequeñas partículas de plástico (mi- croscópicas) que pueden surgir a tra- vés de la fragmentación. El hecho de abordar con éxito estas lagunas de conocimiento es un requisito clave para desarrollar nuevos estándares de biodegradabilidad para bolsas de transporte livianas. Debido a varias deficiencias en los procedimien- tos experimentales y la escasez de información en la literatura científica. Además, los estándares de biodegradabilidad existentes y los métodos de prueba para ambientes acuáticos no implican pruebas de toxicidad ni tienen en cuenta los impactos ecológicos potencialmente adversos de las bolsas de transporte, los aditivos plásticos, los produc- tos de degradación de polímeros o las pequeñas partículas de plástico (microscópicas) que pueden surgir a través de la fragmentación. El hecho de abordar con éxito estas lagunas de conocimiento es un requisito clave para desarrollar nuevos es- tándares de biodegradabilidad para bolsas de transporte livianas. Pro- ductos de degradación de polímeros



o pequeñas partículas de plástico (microscópicas) que pueden surgir a través de la fragmentación. El hecho de abordar con éxito estas lagunas de conocimiento es un requisito clave para desarrollar nuevos es- tándares de biodegradabilidad para bolsas de transporte livianas. Pro- ductos de degradación de polímeros o pequeñas partículas de plástico (microscópicas) que pueden sur- gir a través de la fragmentación. El hecho de abordar con éxito estas lagunas de conocimiento es un re- quisito clave para desarrollar nuevos estándares de biodegradabilidad para bolsas de transporte livianas.
1. Introducción
Con una estimación global de más de 300 millones de toneladas de plástico y un billón de bolsas de plástico producidas anualmen- te, la bolsa de un solo uso es un embajador curiosamente icónico para los productos de polímeros [ 1 , 2 ]. Además de mostrar un alto rendimiento de vida útil en términos de resistencia a la tracción y costos por unidad de peso, las bolsas de transporte a menudo se consideran un símbolo no deseado de contaminación plástica. Esta contaminación es tan ubicua que su presencia puede usarse para marcar el posible comienzo de una nueva época geológica llamada el Antropoceno [ 3 ]. La mayor parte de esta contaminación llega a los am- bientes marinos a través de vías que incluyen vías navegables interiores [ 4 , 5]]. Investigaciones recientes sugieren que hay cinco billones de piezas de plástico flotando en los océanos del mundo que pesan co-

lectivamente más de 250 000 toneladas métricas, y la fragmentación de los artículos más grandes es una fuente primaria de partículas microplásticas (menos de 5 mm) [ 6 ]. El plástico a menudo también se iden- tifica como el contaminante físico más abundante en el fondo marino. Por ejemplo, una encuesta costera de Ioakeimidis et al. [ 7 ] encontraron que las bolsas representan aproximadamente un tercio de este tipo de basura en términos de abundancia de artículos. Además de las preocupaciones relacionadas con la abundancia de basura plástica, la imagen ambiental negativa de las bolsas de transporte proviene de la evidencia de las consecuencias perjudiciales de los plásticos en los ecosistemas abiertos (no gestionados) [ 8 ]. Además de las mortalidades causadas por enre- dos y asfixia, los plásticos ingeridos pueden transferir contaminantes orgánicos a las redes alimentarias [ 9 - 12 ]. Además del creciente reconocimiento de los efectos ambientales negativos de los artículos de plástico, los últimos 40 años han implicado un movimiento hacia el desarrollo de plásticos 'biodegra- dables' (§2 y [ 13 , 14]). Una ventaja de los polímeros de base biológica es que pueden proporcionar una alternativa a los plásticos derivados de combustibles fósiles. Dadas las condiciones adecuadas, también pueden ser relativamente fáciles de descomponer en agua, biomasa y gas. Sin embargo, su aplicación como alternativa a los polímeros tradicionales no está exen- ta de desafíos [ 15].]. Las películas de base biológica tienen costos más altos asociados con la producción y propiedades mecánicas reducidas en comparación con los plásticos convencionales. También se ha su- gerido que el uso generalizado de bolsas de plástico biodegradables en el mejor de los casos no tendría ningún efecto sobre la basura y en el peor de los casos podría exacerbar el problema al introducir materiales parcialmente descompuestos en el medio ambien- te, así como a reducir la responsabilidad social, por ejemplo, al reforzar la percepción que el uso de estos productos minimiza o incluso anula los impactos am- bientales negativos de los residuos plásticos [ 16 - 18 ].
Además de los problemas medioambientales, los productos de origen biológico deben ser compatibles con los procesos de recuperación y tratamiento de re-




siduos. Sin embargo, los polímeros de base biológica no son universal- mente compatibles con estos. Por ejemplo, mientras que el poli (ácido láctico) se degrada lo suficientemente bien como para incorporarlo en el compost, en condiciones de diges- tión anaeróbica mesófila permanece en gran parte intacto [ 19 , 20 ]. Los polímeros de base biológica son igualmente problemáticos para las operaciones de reprocesamiento de películas plásticas donde su detec- ción y separación siguen siendo im- posibles [ 21 , 22]. La introducción de películas biodegradables, por lo tanto, requiere una evaluación de su biodegradabilidad, tanto en entornos gestionados como naturales, utilizando criterios de evaluación armonizados. Sin embargo, en comparación con los entornos gestionados, pocos estudios han in- vestigado la biodegradabilidad de los plásticos en ecosistemas abiertos (por ejemplo, [ 23 - 25 ]). Además, se han desarrollado pocos estándares de biodegradabilidad con respecto a la basura plástica depositada en entornos naturales no gestionados. El trabajo inicial sobre la estanda- rización de los métodos de prueba de biodegradabilidad se llevó a cabo en la década de 1980, por ejemplo, por parte de la Organización para la Cooperación y el Desarrollo Económicos (OCDE) [ 26 ]. En 1996, la Comisión Europea ordenó al Comité Europeo de Normalización (CEN) que desarrollara están- dares para el envasado, incluidos los de compostabilidad (Mandato M / 200). Este mandato estaba vinculado a la Directiva 94/62 / CEE y llevó al establecimiento de la norma BS EN 13432: 2000 [ 27 ]. BS EN 13432: 2000 [ 27 ] incluye un requisito para medir la evolución del gas respira- torio microbiano para determinar la biodegradación e incluye pruebas de desintegración del material de prueba, una evaluación de las con- centraciones de metales pesados y una prueba de ecotoxicidad de la planta. Aunque BS EN 13432: 2000 [27 ] fue fundamental para establecer un sistema de estandarización, certificación de productos y cumplimiento, no existen equivalentes a este estándar de biodegradabilidad para entornos naturales no gestio -
nados. De hecho, evaluar la biodegradabilidad de los plásticos dentro de ecosistemas no gestionados es un gran desafío, especialmente porque ese trabajo idealmente debería ir acompañado de información sobre los impactos ambientales a largo plazo del producto en cuestión. Se ha debatido si las exenciones fiscales para los materiales biodegradables deben otorgarse a partir de las prohibiciones y gravámenes de las bolsas de plástico para que, junto con las medidas de reducción de las bolsas de plástico, puedan apoyarse las oportunidades para establecer materiales fílmicos con mejores credenciales ambientales. Esto fue considerado pero rechazado en Irlanda del Norte [ 28 ], y ha sido considerado en Inglaterra [ 29 ]. Al considerar la posibilidad de un estándar de biodegradabili- dad para películas plásticas en un entorno abierto, la confianza en una evidencia sólida es crítica, ya que un estándar tan innovador puede influir en las expectativas de estandarización para otros productos. Por ejemplo, aproximadamente la mitad de los productos plásticos actuales son desechables [ 21]. También hay un interés considerable en muchos otros productos degradables que probablemente encuentren su cami- no hacia el medio ambiente. Se han realizado esfuerzos, por ejemplo, para desarrollar estándares sobre la biodegradabilidad de los biolu- bricantes [ 30 ]. Otros ejemplos de productos potencialmente biodegradables incluyen botellas, cubier- tos, productos de higiene, equipos agrícolas y artes de pesca [ 31 , 32 ]. Tanto desde el punto de vista de la estandarización como de la conservación de la naturaleza, la diversidad de productos potencial- mente biodegradables subraya la necesidad de pisar con cuidado. Un incentivo para aumentar la distribu- ción de un tipo de producto considerado ambientalmente seguro probablemente será seguido por llamadas para aprobar otros materiales y productos. Sería arriesga- do dar la impresión a través de un estándar formal de que la biodegradación plástica en el ambiente abierto es manejable si nuestro conocimiento subyacente todavía tie -
ne brechas significativas. Hay varias preguntas que deben ser considera- das en este contexto, incluyendo:
•- ¿Existen normas que podrían establecer el rendimiento del producto de biodegradabilidad y las credenciales ambientales seguras para películas y bolsas de plástico que podrían estar cubiertas de manera involuntaria?
•- ¿Cuáles son las fortalezas y debilidades de los estándares y especificaciones de biodegradabilidad actuales para películas plásticas?
•- ¿Qué resultados y conclusiones se pueden (o no) extrapolar de las pruebas de laboratorio di- señadas para simular las condiciones en un entorno abierto?
•- ¿Qué tendría que suceder para permitir el desarrollo de una especificación estándar de biodegradabilidad y un sistema de cum- plimiento y certificación para una nueva generación de bolsas de plás- tico que dicen ser biodegradables en todos los ambientes abiertos?
•- ¿Están todos los entornos abiertos igualmente bien respaldados por estándares de biodegradabili- dad y conocimiento científico, o están mejor atendidos que otros?
Aquí, revisamos lo que se sabe sobre la biodegradabilidad de los plásticos para tratar de responder estas preguntas, centrándonos en los entornos acuáticos que sirven como vías de transporte y sumideros para la acumulación de desechos plásticos [ 4 , 5]]. Discutimos la situación actual con respecto a los estándares de biodegradabilidad y destacamos las brechas de conocimiento que podrían influir en el desarrollo de una especificación de biodegradabilidad plástica para el ambiente abierto. Se revisaron las normas y especificaciones existentes desarrolladas por varias autori- dades (ASTM International; British Standards Institution, BSI; Organi- zación Internacional de Normalización, ISO; y Asociación Francesa de Normalización, AFNOR). También se revisó la literatura científica sobre la biodegradabilidad de los plásticos, particularmente cuando es relevante para la biodegradación en ambientes abiertos. Varios otros canales de investigación, a través de


la industria y las autoridades de estandarización, permitieron una comprensión más completa de la situación de los materiales plásticos y su rendimiento de biodegradabilidad. 2. Definiciones de biodegradabilidad. La ciencia y los estándares de biodegradabilidad plástica no pueden con- siderarse sin una comprensión de las definiciones que conforman el desarrollo de estándares y especificaciones de biodegradabilidad. Una debilidad clave del término 'biodegradable' es que no contiene ninguna información sobre la ubicación, el calendario y el alcance del proceso de descomposición. De hecho, la biodegradabilidad a menudo se define en relación con el propósito o las condiciones de interés, y se han desarrollado estándares y métodos de prueba separados para aguas residuales aeróbicas y anaeróbicas, entornos de agua dulce y hábitats marinos (§3.1.1 y §3.1.2). Existen varias clasificaciones de la OCDE para la biodegradabilidad,33 ]). También existe una gran incertidumbre pública sobre el significado exacto de este término. Con frecuencia se combina con 'compostable' y 'bio-based', con el etiquetado del producto a menudo como causa de confusión adicional (ver [ 14 ] para una discusión detallada). Al considerar los procesos de biodegradación gestionados, como el compostaje industrial, se puede al- canzar una definición suficiente de biodegradabilidad con relativa facilidad porque las condiciones del proceso pueden acordarse y estandarizarse. Sin embargo, se debe tener mucho cuidado al tratar de definir la biodegradabilidad en entornos abiertos, donde generalmente se encuentra una amplia y compleja gama de condiciones físicas y químicas [ 14 ]. Para los fines de esta revisión, definimos un compuesto biodegradable como uno que se utiliza completamente como fuente de carbono para el crecimiento microbiano (basado en la definición de "biodegradabilidad definitiva" de la OCDE). En condiciones aeróbicas, el proceso de degradación da como resultado la producción de dióxido de carbono, agua, sales minerales y nueva biomasa. Bajo condiciones anaeróbicas, también se pueden producir metano y / o ácidos de baja masa molecular.
3. Biodegradabilidad en ambientes acuáticos.
3.1. Ciencia y normas
3.1.1. Ambientes de agua dulce y aguas residuales. Los hábitats de agua dulce incluyen ambientes como ríos, arroyos, lagos y humedales. Según nuestro conocimiento, no se han publicado estándares activos de biodegrada- bilidad a nivel regional o internacional con referencia al plástico en estos entornos, incluida la columna de agua y los sedimentos. De manera similar, no se han establecido especificaciones de biodegradabilidad con criterios de aprobación o falla para la eliminación de artículos de plástico en ecosistemas abiertos de agua dulce, aunque sí una marca de conformidad (Vinçotte OK Biodegradable WATER [ 34]) ha sido desarrollado. Los productos que cumplen con esta marca de conformidad se describen como biodegradables "en un entorno natural de agua dulce", y los productos acep- tados deben mostrar una tasa de biodegradación del 90% a temperaturas de 20–25 ° C y dentro de los 56 días de la incubación. Los estándares de biodegradabilidad utilizados como parte de esta certificación se basan en pruebas que emplean lodos activados, compost o suelo como inóculo (a diferencia de las cepas microbianas o de agua dulce recolec- tadas en el campo aisladas de ambientes de agua dulce). Por lo que sabemos, actualmente no se están desarrollando nuevos estándares para evaluar la biodegradabilidad de los plásticos en cuerpos de agua interiores no gestionados. En contraste con las aguas dulces no gestionadas, se han desarrollado varios estándares de biodegradabilidad y métodos de prueba para plásticos dentro de aguas residuales aeróbicas y anaeróbicas. Existen dos estándares internacionales actualmente activos para evaluar la biodegradabilidad de los plásticos dentro de las aguas residuales aeróbicas


Tabla 1. Estándares de biodegradabilidad actualmente activos para materiales plásticos dentro de aguas residuales y lodos de depuradora.
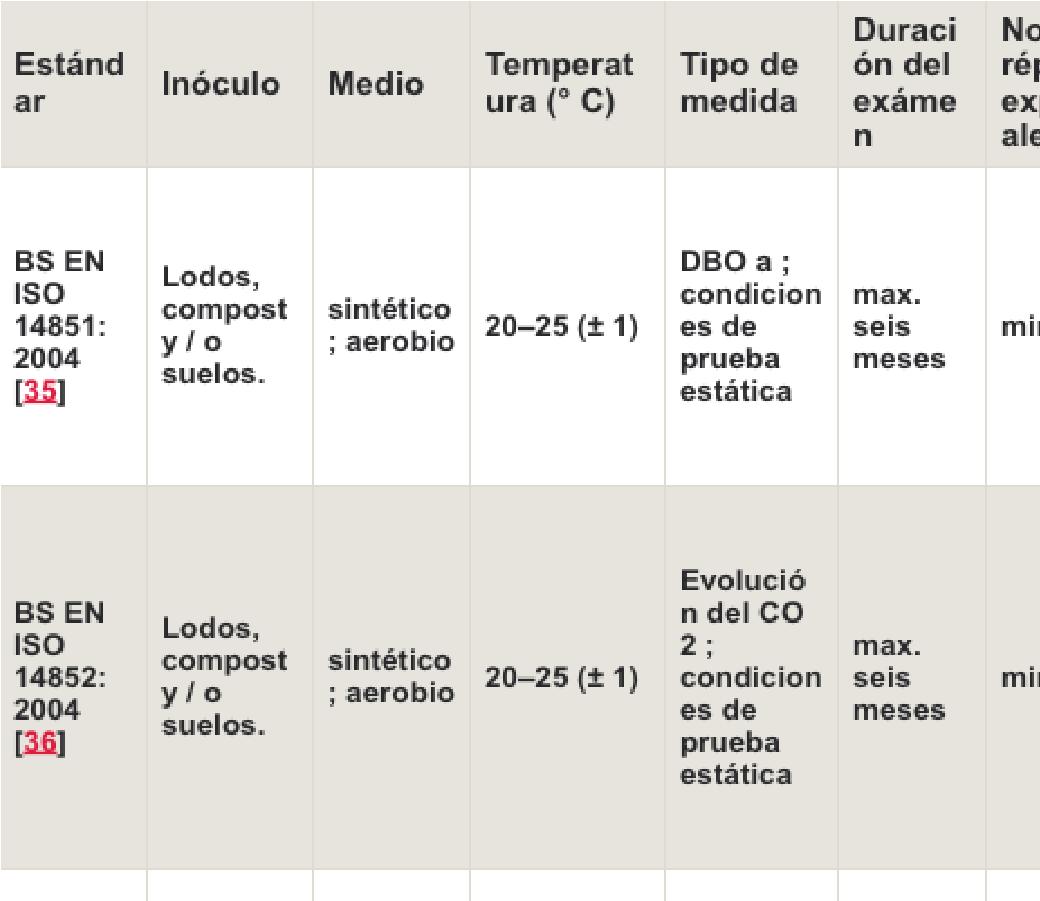

y los lodos de depuración: BS EN ISO 14851: 2004 [ 35 ] y BS EN ISO 14852: 2004 [ 36 ] ( tabla 1 ). Estas normas se utilizan como parte de la marca de conformidad de agua biodegradable Vinçotte OK [ 34 ] y la especificación BS EN 14987: 2006 [ 39 ], que comparten los mismos requisitos para que un material se defina como biodegradable. Ade- más de estos, los métodos de prueba retirados ASTM D5209-92 [ 40 ], D5271-02 [41 ] y D6340-98 (2007) [ 42 ] se desarrollaron para evaluar la biodegradabilidad de los plásticos en presencia de aguas residuales ae- róbicas y lodos de aguas residuales. La norma ASTM D5209-92 [ 40 ] era similar a la norma EN ISO 14852: 2004 [ 36 ] e involucraba la obtención de lodos de aguas residuales ac- tivadas en una planta de tratamiento de aguas residuales municipales y la preparación del inóculo, exponien- do el material plástico al inóculo aireado, [y] midiendo el carbono El dióxido evolucionó en función del tiempo, el contenido de carbono or- gánico soluble (SOC) y el peso resi- dual del polímero. ASTM D5271-02 [ 41 ] fue equivalente a BS EN ISO 14851: 2004 [ 35 ], mientras que ASTM D6340-98 (2007) [ 42 ] involucró mediciones de 14 CO 2evolución a partir de plásticos marcados con radioisótopos con ensayos reali- zados a una temperatura de 58 ± 5 ° C. Por lo que sabemos, actualmente no se están desarrollando nuevos estándares de biodegradabilidad o

métodos de prueba para evaluar la biodegradación de plásticos den- tro de aguas residuales aeróbicas y / o lodos de aguas residuales. Una demanda biológica de oxígeno. b Carbón inorgánico disuelto.
Además de los estándares y méto- dos de prueba desarrollados para aguas residuales aeróbicas, existen dos estándares internacionales de biodegradabilidad para plásticos dentro de aguas residuales anaeró- bicas y lodos de aguas residuales: BS ISO 13975: 2012 [ 37 ] y BS EN ISO 14853: 2016 [ 38 ] ( tabla 1 ). También se ha publicado un método de prue- ba regional único retirado, ASTM D5210-92 (2007) [ 43 ]. Este método de prueba fue similar al BS EN ISO 14853: 2016 [ 38 ], con la excepción de la medición de concentraciones de SOC y masa de polímero. Los estándares activos y retirados y los métodos de prueba desarrollados para evaluar la biodegradabilidad de los plásticos dentro de las aguas dulces generalmente tienen como objetivo evaluar la biodegradabili- dad final, que involucra mediciones de la evolución de CO 2 y CH 4 . Las pruebas se realizan bajo condicio- nes de laboratorio controladas, que con frecuencia involucran la expo- sición del material de prueba a un medio inoculado artificialmente en un rango de temperatura específico (temperaturas de prueba mínimas y máximas de 19 ° C y 63 ° C, res- pectivamente). Como parte de un
único estándar (BS ISO 13975: 2012) [ 37 ], el polímero está directamente expuesto al inóculo (es decir, no se utiliza ningún medio de crecimiento sintético). Todos los procedimien- tos descritos para entornos de agua dulce se completan utilizando con- diciones de exposición estática, en lugar de flujo continuo o Condicio- nes in situ. Se utilizan las duraciones máximas de prueba de seis meses, aunque no se da una duración máxima en ASTM D5210-92 (2007) [ 43 ].
Los inóculos especificados en los procedimientos de prueba para am- bientes de agua dulce provienen de varias fuentes, desde aguas residua- les y lodos recolectados en el cam- po o preparados en el laboratorio hasta el suelo, compost, heces de ganado o "desechos orgánicos" no específicos ( tabla 1 ). El inóculo pue- de involucrar una o varias fuentes ambientales, y puede modificarse (por ejemplo, lavarse o ajustarse a un número deseado de unidades formadoras de colonias, UFC) y / o exponerse al material de prueba antes de su uso. Si bien la mayoría de los estándares y métodos de prueba para estos entornos no recomien- dan el uso de una densidad celular específica, los recuentos de UFC de 10 3 –10 6 ml- 1 han sido recomendados por dos estándares: BS EN ISO 14851: 2004 [ 35 ] y 14852: 2004 [36 ]. Para un solo método de prueba (ASTM D6340-98 (2007)) [ 42 ], no se proporcionan pautas con respec- to al número requerido de réplicas experimentales. Tres de las normas desarrolladas para aguas residuales [ 35 - 37 ] requieren un mínimo de dos réplicas con referencia al ma- terial de prueba. Los procedimien- tos de prueba restantes implican al menos tres repeticiones. La mayo- ría de los protocolos recomiendan el uso de plástico en polvo, pero también se aceptan otros tipos de muestras (como películas, piezas y fragmentos). Además, aunque cier- tos protocolos recomiendan el uso de plásticos libres de aditivos, los estándares y los métodos de prue- ba generalmente se consideran adecuados para una amplia gama de materiales de prueba (incluidos copolímeros y mezclas de políme- ros, plásticos que contienen aditi- vos y polímeros solubles en agua).
3.1.2. Ambientes marinos
Los ambientes marinos cubren dos tercios del área de la superficie de la Tierra y abarcan una gran diversidad de hábitats, incluidos los ecosistemas de océanos abiertos y costeros (co- mo los sitios de estuarios y mareas), así como los ambientes de aguas profundas. Se han publicado dos estándares internacionales activos con referencia a la biodegradación aeróbica de plásticos en la interfaz entre el agua de mar y el sedimento marino arenoso (ISO 18830: 2016 [ 44 ] e ISO 19679: 2016 [ 45 ]; tabla 2 ). Estos estándares implican pruebas de biodegradación basadas
en el laboratorio que utilizan medi- ciones de la demanda de oxígeno o la evolución de CO 2. Además, se han desarrollado dos métodos de prueba regionales activos para evaluar la biodegradabilidad de los materiales plásticos en el agua de mar aeróbica: ASTM D6691-09 [ 46] y D7473-12 [ 47 ] ( tabla 2 ). La norma ASTM D6691-09 [ 46 ] emplea mediciones de la evolución de CO 2 en condiciones controladas, y la norma ASTM D7473-12 [ 47 ] se basa en la evidencia visual de la biodegradación y la pérdida de masa de polímero (%) luego de la exposición al agua de mar en un sistema de flujo continuo. ( tabla 2 ). El último método de prueba se considera insuficiente para esta- blecer la biodegradabilidad por sí mismo, y solo se completa para los materiales que logran al menos un 30% de biodegradabilidad en ASTM

D6691-09 [ 46 ]. También se ha pu- blicado un método de prueba para medir la biodegradabilidad aeróbica de los plásticos en condiciones que simulan el entierro en sedimentos de marea arenosa, utilizando mediciones de CO2 evolución (ASTM D7991-15 [ 48 ]; tabla 2 ). En este método de prueba, el plástico se expone a sedimentos recolectados en el campo y al agua de mar que se han almacenado en el laboratorio hasta cinco semanas antes de su uso. Una demanda biológica de oxígeno.
b No especificado.
c Aunque la norma ASTM D7473-12 establece que los 'procesos anaeró- bicos (por ejemplo, la reducción de sulfato) pueden desempeñar un papel en la biodegradación', el material de prueba se coloca en la superficie del sedimento (que está en contacto di- recto con el agua de mar oxigenada).
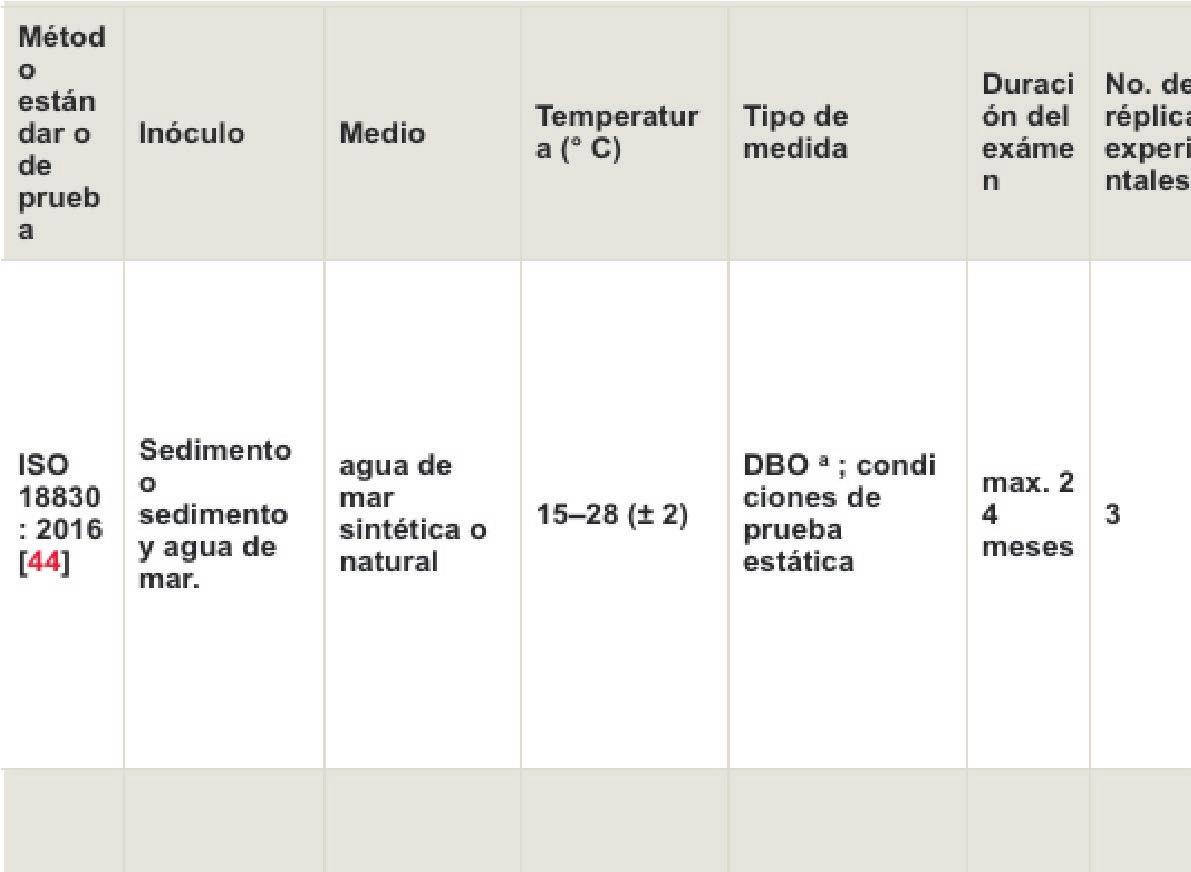
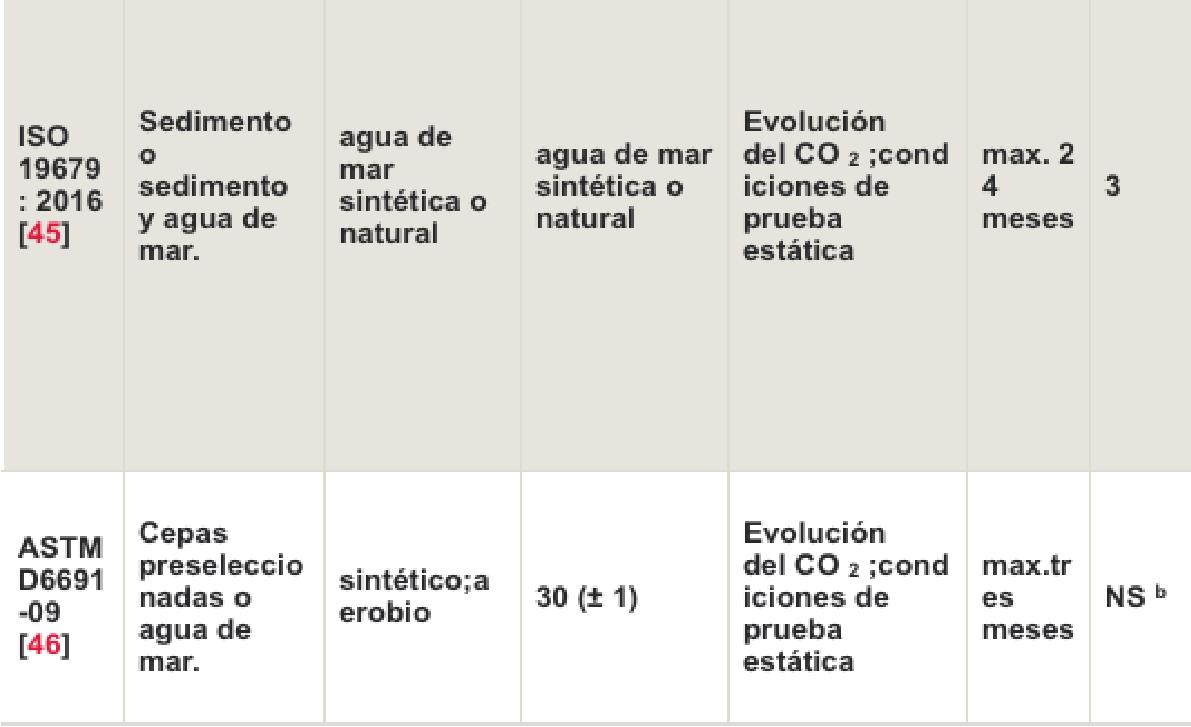


El método de prueba retirado ASTM D6692-01 [ 49 ] se desarrolló para evaluar la biodegradabilidad aeróbi- ca de los plásticos en el agua de mar midiendo la evolución de 14 CO 2 a partir de polímeros marcados con radioisótopos. Además, la especi- ficación retirada ASTM D7081-05 [ 50 ] se diseñó para plásticos en va- rios entornos marinos y se estableció que cubría el agua de mar aeróbica y los sedimentos anaeróbicos. Los requisitos dentro de la especifica- ción incluían criterios para el grado de desintegración plástica durante la degradación, tasas de biodegra- dación y pruebas ecotoxicológicas (pruebas de toxicidad que emplean microorganismos, peces, Dafnia). sp. o algas). También se ha desa- rrollado una marca de conformidad para los productos descritos como biodegradables en agua de mar (Vinçotte OK Biodegradable MARINE [ 51 ]). El componente de biodegradabilidad de este certifi - cado se basa en ASTM D7081-05 [ 50 ], y los productos aceptados deben presentar una tasa de biode- gradación del 90% después de seis meses de exposición. También se incluyen los requisitos para prue- bas de desintegración y toxicidad del material de prueba, basadas en ASTM D7081-05 [ 50 ]. Se requiere un período de incubación de tres meses antes de las pruebas de toxi- cidad, con un requisito adicional de que "menos del 90% de los orga- nismos analizados" estén afectados. En general, los métodos de prueba existentes para ambientes marinos son similares a los publicados para aguas residuales y aguas residuales, ya que se dirigen principalmente a evaluar la biodegradabilidad fi - nal (§3.1.1). Los inóculos de prueba pueden consistir en cepas o taxo- nes preseleccionados naturalmen- te presentes en el ambiente, y las exposiciones directas a los inócu- los se incluyen como una opción o un requisito en los métodos de prueba actuales ( tabla 2 ). De ma- nera similar a los procedimientos publicados para hábitats de agua dulce, los inóculos utilizados pa- ra las pruebas de biodegradación marina pueden originarse de una o varias matrices ambientales, con una selección limitada de estándares que recomiendan recuentos de UFC de 10 3 –10 6 ml −1para usar. Se emplean temperaturas de prueba mínimas y máximas de 13 y 30 ° C, respectivamente, y la mayoría de los métodos de prueba emplean dura- ciones de exposición máximas de seis meses (aunque la norma ASTM D7991-15 [ 48 ], BS ISO 18830: 2016 [ 44 ] y BS ISO 19679: 2016 [ 45 ] implican una duración máxima de 2 años; tabla 2 ). Además, los métodos de prueba desarrollados para ambientes marinos son ampliamen- te comparables con los publicados para aguas residuales y aguas re- siduales en términos de sus requi- sitos para la replicación y validez

experimental, así como los tipos de polímeros y la morfología ( tabla 2 y §3.1.1). Sin embargo, la norma ASTM D7991-15 [ 48 ] recomienda evaluar los materiales de prueba como películas en lugar de como polvos. Si bien se han publicado estándares de biodegradabilidad y métodos de prueba para plásticos depositados en la interfaz agua-sedimento del mar y dentro de la arena aeróbica ( tabla 2 ), no hay estándares o es- pecificaciones actuales dirigidos específicamente a evaluar la biodegradabilidad de los plásticos en hábitats marinos anaeróbicos, marismas, aguas salobres. , o ambientes de aguas profundas frías y pobres en nutrientes. Si bien los ambientes con bajo nivel de oxígeno se in- cluyeron nominalmente en ASTM D7081-05 [ 50 ], los procedimientos enumerados en este documento se basaron en la adición de inóculos en medios acuosos acuosos, en lugar de usar condiciones de exposición estrictamente anaeróbicas. 3.2. Problemas de estandarización Si bien se han desarrollado varios estándares y métodos de prueba para medir la biodegradabilidad de los polímeros en ambientes acuáticos, varios problemas pueden limitar su confiabilidad cuando se intenta predecir las tasas de biodegra- dación in situ. Estos problemas se pueden resumir como incertidum- bres que se originan en (i) enfoques para la preparación del inóculo y condiciones de prueba, (ii) falta de pautas específicas para emplear diferentes materiales de prueba, (iii) replicación estadística insufi- ciente, (iv) falta de procedimientos adecuados para entornos acuáticos no gestionados, y (v) deficiencias en las pruebas de toxicidad y nues- tra comprensión de los impactos más amplios de la basura plástica en los ecosistemas acuáticos. 3.2.1. Preparación de inóculos y condiciones de ensayo. Las fuentes de inóculos recomendadas para las pruebas de biodegradabilidad acuática son diversas y, a menudo, inespecíficas. El tipo de inóculo y la forma en que se prepara pueden afectar significativamente las tasas de biodegradación [ 52 - 56 ]. Por ejemplo, la filtración puede alterar la diversidad taxonómica de un inóculo, lo que puede reducir la confiabilidad de la prueba y dificultar la extrapolación de datos basados en laboratorio a patrones de biodegradabilidad en ambientes naturales [ 55 ]. Los tiempos de almacenamiento del inóculo especificados por los procedimientos de prueba actuales a menudo tampoco son claros, a pesar de la posibilidad de que el almacenamiento prolonga- do de la muestra produzca un sesgo experimental [ 57 - 59]]. Además, con frecuencia se proporciona poca
información sobre las densidades celulares recomendadas, a pesar de la evidencia de que la concen- tración del inóculo en relación con el material de prueba puede afec- tar los resultados de las pruebas de biodegradabilidad [ 54 , 56 ]. El uso de cepas preseleccionadas o precondicionadas, así como los medios sintéticos y las condiciones de exposición estática, constituyen otras fuentes de incertidumbre cuando se emplean procedimientos de prueba existentes para evaluar la biodegradabilidad de los plásti- cos en ambientes acuáticos abiertos. Estas incertidumbres son bien reconocidas en la literatura científica [ 60 , 61 ], y varios autores [ 55 , 56 , 62 , 63 ] destacaron la necesidad de procedimientos de prueba actualizados Solo un número limitado de procedimientos de prueba de biodegradabilidad existentes para hábitats acuáticos implica la exposición directa del material de prueba al inóculo y / o las condiciones de flujo.
Los rangos de temperatura emplea- dos por las pruebas y directrices de biodegradabilidad publicadas son limitados y, por lo general, no tienen en cuenta las fluctuaciones estacionales en las condiciones ambientales que pueden influir en la composición y las actividades de los microorganismos asociados al plástico [ 64 - 68 ] (pero consulte la norma ASTM D7473-12 [ 47 ]; tabla 2 ). Como tal, es probable que las temperaturas empleadas por los procedimientos existentes no sean adecuadas para evaluar la biodegra- dabilidad de los plásticos en aguas no gestionadas (templadas), donde las temperaturas pueden ser considerablemente inferiores a 13 ° C (el límite de temperatura más bajo para los procedimientos de prueba actuales; ISO 18830: 2016 [ 44 ] y ASTM D7991-15 [ 48 ] en la tabla 2). Es probable que las bolsas de transporte exhiban tasas más bajas de biodegradación en aguas no gestionadas en comparación con las aguas residuales y los entornos como el compost (debido a las di- ferencias tanto en las condiciones ambientales como en los taxones presentes), y se pronostica que cier- tos tipos de polímeros requerirán décadas o siglos para convertirse Completamente biodegradado dentro de los ecosistemas marinos [ 17 , 23 , 61 , 69 , 70 ]. Por lo tanto, es probable que las duraciones máxi- mas de las pruebas de biodegrada- bilidad actuales sean insuficientes para evaluar la biodegradación de polímeros en varios hábitats (por ejemplo, fondos lacustres y hábitats de aguas profundas caracterizados por bajas temperaturas, así como bajas disponibilidades de oxígeno, nutrientes y luz) [ 23 ,61 , 71 , 72 ].
3.2.2. Falta de lineamientos específicos para diferentes materiales de prueba. La mayoría de los procedimientos de prueba descritos para ambientes acuáticos se consideran adecuados para materiales compuestos, inclui- das mezclas de polímeros y plásti- cos que contienen aditivos. Aun así, aunque las tasas de biodegradación pueden variar considerablemente entre los tipos de polímeros [ 73 ], ninguno de los procedimientos pu- blicados proporciona instrucciones claras para explicar esto o los impactos de los aditivos en las tasas de biodegradación. La última cuestión, sin embargo, está reconocida por las normas BS EN ISO 14851: 2004 [ 35 ] y 14852: 2004 [ 36 ]. Muchos de los procedimientos de prueba también se basan en métodos de medición únicos, que pueden conducir a resultados poco fiables al evaluar la biodegradabilidad de los materiales compuestos [ 74 ]. Aunque las mediciones emplean 14Los polímeros marcados con C pueden evitar estos problemas [ 75 , 76 ], es probable que no sean adecuados para el uso a gran escala debido al alto costo de los materiales etiquetados con radioisótopos y los posibles problemas relacionados con la concesión de licencias y / o la eliminación de desechos [ 75 ] Además de estos inconvenientes, las normas actuales y los métodos de prueba para entornos acuáticos no proporcionan directrices claras para evaluar la biodegradabilidad de materiales de diferentes formas y tamaños, a pesar de que se ha reconocido que son importantes (BS EN ISO 14851: 2004 [ 35 ] y 14852 : 2004 [ 36 ]). Se ha demostrado que los materiales con una relación relativamente alta de área de superficie a volumen (por ejemplo, polvos) ex- hiben mayores tasas de biodegrada- ción que otros materiales (incluidas las películas), lo que puede resultar en una sobreestimación de las tasas de biodegradación [ 77 ]. Como una fuente adicional de incertidumbre, la relación entre la forma y el tamaño de un material y su biodegradabilidad puede variar entre los tipos de polí- meros y las condiciones de prueba [ 77]. Fundamentalmente, las propiedades superficiales de un material (como su rugosidad) también pueden influir en los resultados de las pruebas de biodegradabilidad [ 66 , 67 ]. 3.2.3. Insuficiente replicación estadística. Muchos de los estándares de biodegradabilidad desarrollados para am- bientes acuáticos se caracterizan por la falta de información sobre el nivel de replicación estadística requeri- da o implican mediciones realiza- das por duplicado (tablas 1 y 2 ). Se requiere un mínimo de mediciones por triplicado para garantizar la validez estadística y la reproducibilidad como parte de un están -
dar de biodegradabilidad dado. 3.2.4. Falta de procedimientos ade- cuados para ambientes acuáticos no gestionados.
Faltan normas y métodos de prueba para evaluar la biodegradabili- dad de los materiales plásticos en los ecosistemas de agua dulce no gestionados (incluidos lagos, arroyos y ríos) y en la mayoría de los entornos marinos [ 63 ]. Las temperaturas de prueba utilizadas por los procedimientos existentes, como se discutió anteriormente, son frecuentemente más altas que las encontradas en ambientes acuáticos (templados), a pesar de la capacidad de la temperatura para influir fuertemente en la composición taxonómica y las actividades metabólicas de las comunidades microbianas [ 61 , 66 , 67 , 78]. Además, es probable que las duraciones máximas de prueba de los procedimientos de prueba publicados sean demasiado bajas para evaluar la descomposi- ción de ciertos tipos de polímeros dentro de varios ecosistemas acuáticos no gestionados, debido a que las tasas de biodegradación son compa- rativamente bajas en estos entornos (aunque se incluyen exposiciones máximas de 2 años como parte de tres normas marinas y métodos de prueba; tabla 2 ). De hecho, las limitaciones de los procedimientos de prueba basados en laboratorio para estimar la biodegradabilidad de los plásticos en ecosistemas no gestionados se reconocen explícitamente en ASTM D6691-09 [ 46]: 'se debe reconocer que es difícil predecir el destino y los efectos ambientales a largo plazo a partir de los resulta- dos de la exposición a corto plazo a un entorno marino simulado. Por lo tanto, se debe tener precaución al extrapolar los resultados obtenidos de esta o cualquier otra prueba de ambiente controlado para su eliminación en el ambiente natural".
Como ejemplo de las tasas de biodegradación plástica estimadas para ambientes acuáticos abiertos, se ha calculado una vida útil de aproxima- damente 10 años para botellas polihidroxibutirato-polihidroxivalederato (PHBV) en la superficie de sedimentos lacustres a una profundidad de 85 my a 6 ° C [ 79 ]. En este mismo estudio, las tasas de biodegradación en la superficie del sedimento también se encontraron aproximadamente dos veces más bajas que las de una profundidad de agua de 20 m (medida como pérdida de masa). Además, un análisis de los frag- mentos de plástico recuperados de los sedimentos del lago Ontario (Ca- nadá) sugiere que estos materiales se han estado acumulando en el lecho del lago durante aproximadamente 40 años [ 80]. Dada esta evidencia de la conservación en múltiples decenales del plástico en los sedimen-

tos de agua dulce, es probable que varios tipos de polímeros, inclui- dos los bioplásticos, requieran una cantidad de tiempo sin precedentes para biodegradarse dentro de estos y varios otros hábitats bénticos. De hecho, las tasas de biodegradación de polímeros dentro de los ecosis- temas marinos a menudo han sido más bajas que las estimadas tanto para el agua dulce como para los ambientes terrestres [ 23 , 61 , 81 ]. 3.2.5. Pruebas de toxicidad e impactos ambientales más amplios. Con la excepción de la marca de conformidad MARINE biodegradable [ 51 ] de Vinçotte OK , las pruebas de toxicidad para plásticos, aditivos plásticos o productos de degradación de polímeros no se in- cluyen como parte de estándares de biodegradabilidad activa o métodos de prueba desarrollados para ecosistemas acuáticos [ 14 ]. Cuando se requieren ensayos de toxicidad, estos se basan en metodologías de prueba única. Además, una de las pruebas de toxicidad recomendadas por la etiqueta MARINE biodegra- dable de Vinçotte OK [ 51 ] (así como la especificación retirada ASTM D7081-05 [ 50 ]) se basa en Daph- niasp., un género de crustáceos de agua dulce, a pesar de que esta mar- ca de conformidad ha sido desarrollada para ambientes marinos. Los impactos de la basura plástica en comunidades multiespecíficas y procesos biogeoquímicos, como los ciclos elementales, no se abordan en los procedimientos de prueba existentes [ 64 , 82 ]. Además, los ensayos de toxicidad requeridos por la etiqueta OK Biodegradable MARINE [ 51 ] no explican explícita- mente la capacidad de las partículas plásticas micro o nanoscópicas para

afectar adversamente a los organismos acuáticos. Por ejemplo, se ha encontrado que la presencia de microperlas poliméricas convencionales (polietileno y poli (cloruro de vinilo)) y de base biológica (poli (ácido láctico)) afecta el comporta- miento de alimentación del gusano Arenicola marina [ 82 ,83]. Se ha demostrado que la exposición a nanoplásticos de poliestireno redu- ce el crecimiento de la población en la especie de algas Scenedesmus oblicua y afecta el tamaño corporal y el comportamiento reproducti- vo de Daphnia magna [ 84 ]. Además, se ha descubierto que la exposición a microplásticos de poliestireno influye en el comportamiento de alimentación y el ren- dimiento reproductivo del copépodo Calanus helgolandicus [ 85 ]. 3.3. Brechas de conocimiento Hemos identificado varios vacíos de conocimiento con referencia a la biodegradabilidad de los plásti- cos en ambientes acuáticos, que se resumen a continuación. Donde sea posible, también se proporcionan recomendaciones para desarrollar nuevos estándares de biodegradabi- lidad para bolsas de plástico livianas.
Brecha de conocimiento 1: relación de datos basados en laboratorio con patrones de biodegradabilidad en entornos acuáticos abiertos
La mayoría de los estándares y métodos de prueba existentes para evaluar la biodegradabilidad de los materiales plásticos en ambientes acuáticos se basan en experimentos de laboratorio que utilizan mediciones respirométricas en condiciones idealizadas. Las mediciones de la evolución de CO 2 y CH 4 pue -

den proporcionar estimaciones confiables de biodegradación en estos y otros entornos, siempre que se tenga en cuenta la evolución del gas a partir de materia orgánica y otras fuentes potenciales de incer- tidumbre [ 86 - 88 ]. Sin embargo, los procedimientos actuales son insuficientes para simular las condiciones encontradas en ambientes naturales, así como la capacidad de estas condiciones para variar es- tacionalmente y geográficamente. Muchos de los protocolos publica- dos para ambientes marinos sí tienen en cuenta escenarios de exposición relativamente complejos, como los que involucran condiciones de flujo continuo, temperaturas in situ y / o exposición a agua o sedimentos recolectados en el campo ( tabla 2). Ciertos aspectos de estos procedimientos de prueba podrían proporcionar un punto de partida para nuevos enfoques metodológicos que imiten las condiciones físicas y químicas clave encontradas en ambientes acuáticos (por ejemplo, experimentos de mesocosmos que involucran bajas temperaturas y / o concentraciones de nutrientes). Los taxones microbianos y las abundan- cias utilizadas en tales pruebas de biodegradabilidad deben ser simi- lares a las presentes en el entorno de interés, y se recomiendan exposiciones directas al inóculo además de los experimentos estrictamente controlados que involucran medios sintéticos. Los inóculos también deben usarse lo antes posible después de su recolección, y se recomienda que cualquier material se analice como destinado para uso público (por ejemplo, como bolsas de transporte intactas; cuando esto sea imposi- ble, se debe intentar predecir la vida útil del producto intacto).14 , 74 ].
Dadas las tasas extremadamente lentas de biodegradación de políme- ros informadas por varios estudios de campo (por ejemplo, [ 69 , 79 ]), es probable que las duraciones de las pruebas especificadas actual- mente sean insuficientes para evaluar la biodegradabilidad de los polímeros en muchos hábitats acuáticos no gestionados. Las tasas de biodegradación dependen en gran medida de las condiciones ambientales circundantes, y se necesita una investigación más amplia sobre el destino a largo plazo de los materiales plásticos en entornos como las aguas marinas profundas y pobres en nutrientes, y los sedimentos sometidos a temperaturas frías [ 89 ].
Brecha de conocimiento 2: Ausencia de estándares de biodegrada- bilidad y métodos de prueba para entornos acuáticos no gestionados
A pesar de los registros de residuos plásticos en ríos, lagos,
aguas costeras y sedimentos, aguas polares y aguas profundas [ 6 , 18 , 80 , 90 , 91 - 95 ], no existen estándares ni métodos de prueba para evaluar la biodegradabilidad de polímeros en sistemas no gestionados. Entornos acuáticos distintos del agua de mar abierta y los sedimentos arenosos ( tabla 2 ). Como los sedimentos represen- tan un importante sumidero para la acumulación de basura plástica, incluidos los materiales que pier- den su flotabilidad con el tiempo [ 18 , 90 , 91], existe una necesidad particular de desarrollar estándares adicionales para ambientes acuá- ticos bentónicos. Como las tasas de biodegradación en la superficie del sedimento pueden no ser representativas de las que se encuen- tran dentro del sedimento [ 72 ], esto también debe ser considerado por cualquier estándar nuevo (s).
Brecha de conocimiento 3: Falta de investigación más amplia de laboratorio y de campo sobre la biodegradación de polímeros en varios entornos acuáticos
El éxito en el diseño y la implementación de nuevos estándares de biodegradabilidad para hábitats marinos y de agua dulce se ve gra- vemente obstaculizado por la falta de investigación primaria relevante [ 63 ]. Por ejemplo, existe la necesi- dad de realizar investigaciones adi- cionales sobre la biodegradación plástica en escenarios de exposición que involucren bajas temperaturas y disponibilidad de nutrientes, así como también condiciones anaeróbicas. Para caracterizar completamente la biodegradabilidad de los polímeros en entornos abiertos, se requerirá una combinación de investigación de laboratorio y de campo. Una forma potencialmente útil de abordar este tema podría involu- crar el cálculo de valores de 'pará- metros degradables ambientalmen- te' (Ed K ) para varios tipos de plás- tico expuestos a una amplia gama de condiciones ambientales [ 73 ].
Brecha de conocimiento 4: Pruebas de toxicidad e investigación sobre los impactos más amplios de los materiales plásticos en los ecosistemas acuáticos
Se requerirá investigación sobre los impactos ambientales toxicológicos y más amplios de un material de prueba dado para identificar marcos de tiempo aceptables para la biodegradación de desechos plásti- cos en hábitats abiertos (incluyendo acuáticos). Si bien algunas de las pruebas de toxicidad especificadas por el certificado MARINE biodegradable de Vinçotte OK [ 51 ] podrían ser útiles para desarrollar uno o más estándares de biodegradabi-
lidad para bolsas ligeras, se centran en un rango limitado de especies y se realizan en la población (en lugar de nivel de la comunidad.
Se requiere investigación toxicológi- ca adicional, particularmente con re- ferencia a las especies que se ha en- contrado que ingieren partículas de plástico, incluidos los invertebrados que se depositan y se alimentan por filtración en la base de las redes alimenticias acuáticas [ 83 - 85 ]. También se requiere evaluar los impactos de los artículos de plástico desechados en múltiples especies y procesos a nivel de la comunidad (como el ciclo elemental mediado por microbios) para comprender completamente las implicaciones ambientales de la contaminación plástica acuática. De hecho, a pesar de varios estudios recientes sobre la formación de biopelículas en resi- duos plásticos en ambientes mari- nos y de agua dulce [ 68 , 96 - 99 ], aún se sabe poco sobre cómo estos residuos afectan el funcionamiento del ecosistema (ver [ 82 ]). 4. Métodos de ensayo alternativos para medir la biodegradabilidad.Procedimientos de ensayo para medir la biodegradación del polímero se basan comúnmente en mediciones de la demanda biológica de oxígeno o la evolución de CO 2y / o CH 4 (tablas 1 y 2 ). Se ha propuesto un método alternativo basado en mediciones de ATP para analizar la biodegradabilidad de las películas de polímero "oxo- degradables" [ 100 ]. Investigación relacionada con el Proyecto ANR OXOMAR DS0103 (Degradación y toxicidad abióticas y bióticas de plásticos oxo-biodegradables en aguas marinas)) está apuntando ac- tualmente a adaptar esta prueba al ambiente marino. Los métodos de prueba más simples que utilizan los cambios en las propiedades físicas de los polímeros como indicadores de la biodegradación también se usan ampliamente en la literatura de investigación y estos métodos son / fueron recomendados por una selec- ción de métodos de prueba ASTM:
•- Los cambios en la apariencia visual se evalúan como parte de ASTM G21-15 [ 101 ] y el método de prueba retirado G22-76 (1996) [ 102 ] para evaluar la resistencia de los materiales plásticos a hongos y bacterias, y en D7473-12 [ 47 ] para evidencia visual de biodegradación en agua de mar, o agua de mar y sedimentos ( preferiblemente lodosos ).
•- Los cambios en la masa se monitorean en los métodos de prueba ASTM retirados D5247-92 [ 103 ] y D6003-96 [ 104 ], así como en la norma ASTM D7473-12 [ 47 ].
•- Los cambios en las propiedades mecánicas también se evalúan como parte de ASTM D5247-92 [ 103 ].
Estos cambios tienen lugar durante diferentes etapas de la biodegrada- ción y, por lo tanto, es importante identificar las etapas en las que dichos cambios físicos son mejores para medir, y qué información adecuada pueden proporcionar sobre la descomposición de di- ferentes polímeros. El proceso de biodegradación a menudo se di- vide en tres fases. Cuando se utilizan mediciones de la evolución de CO 2 o CH 4 , la evolución del gas es despreciable durante las etapas iniciales de la biodegradación (fa- se de retraso) y, posteriormente, muestra un aumento sustancial (fase de biodegradación), seguida de una fase de meseta cuando la biodegradación está cerca de com- pletarse. Estas fases corresponden aproximadamente a distintos pa- sos involucrados en el proceso de degradación, como se describe en Lucas et al. [ 76 ] y Eubeler et al.. [ 89 , 105 ]. La etapa de biodeterioro está dominada por la des- polimerización del material por hidrólisis enzimática (por ejemplo, enlaces éster y amida) o por la peroxidación de polímeros de cadena carbonada. La etapa de biofragmentación da como resultado la desintegración y la frag- mentación del material sin una evolución significativa del gas. Finalmente, la etapa de asimilación
se acompañan de cambios en el aspecto visual y en la pérdida de masa a medida que avanza la biodegradación, lo que proporciona una estimación de primer orden de la biodegradación ( figura 1 ). A pesar de que tales pruebas físicas son útiles debido a su bajo costo y simplicidad, varios problemas limitan su capacidad para propor- cionar información concluyente sobre la biodegradabilidad de los materiales plásticos. La inspección visual es cualitativa y está sujeta a un error humano considerable (por ejemplo, debido a la variación en la experiencia). Además, la evidencia de cambios en la morfología de la superficie o el grado de unión microbiana no es indicativa de la biodegradación por derecho propio [ 105]]. En contraste con la inspec- ción visual, las mediciones de pérdida de masa son cuantitativas y, en general, se correlacionan bien con la evolución de CO 2 [ 106 ]. Sin embargo, como las mediciones de pérdida de masa se realizan a intervalos de tiempo específicos (en lugar de de manera continua) y están sujetas a sesgos inherentes (que se detallan a continuación), esta correlación es comparativa- mente pobre durante la fase de retraso temprana ( figura 1 ). Con frecuencia, se supone que los ma- teriales que exhiben más del 90% de la pérdida de masa están casi completamente biodegradados.
Métodos de prueba físicos para la evaluación de la biodegradación plástica, y su relación con las diferentes etapas de descomposición del polímero y las etapas correspondientes observadas mediante pruebas de evolución de gases (CO 2 y CH 4).
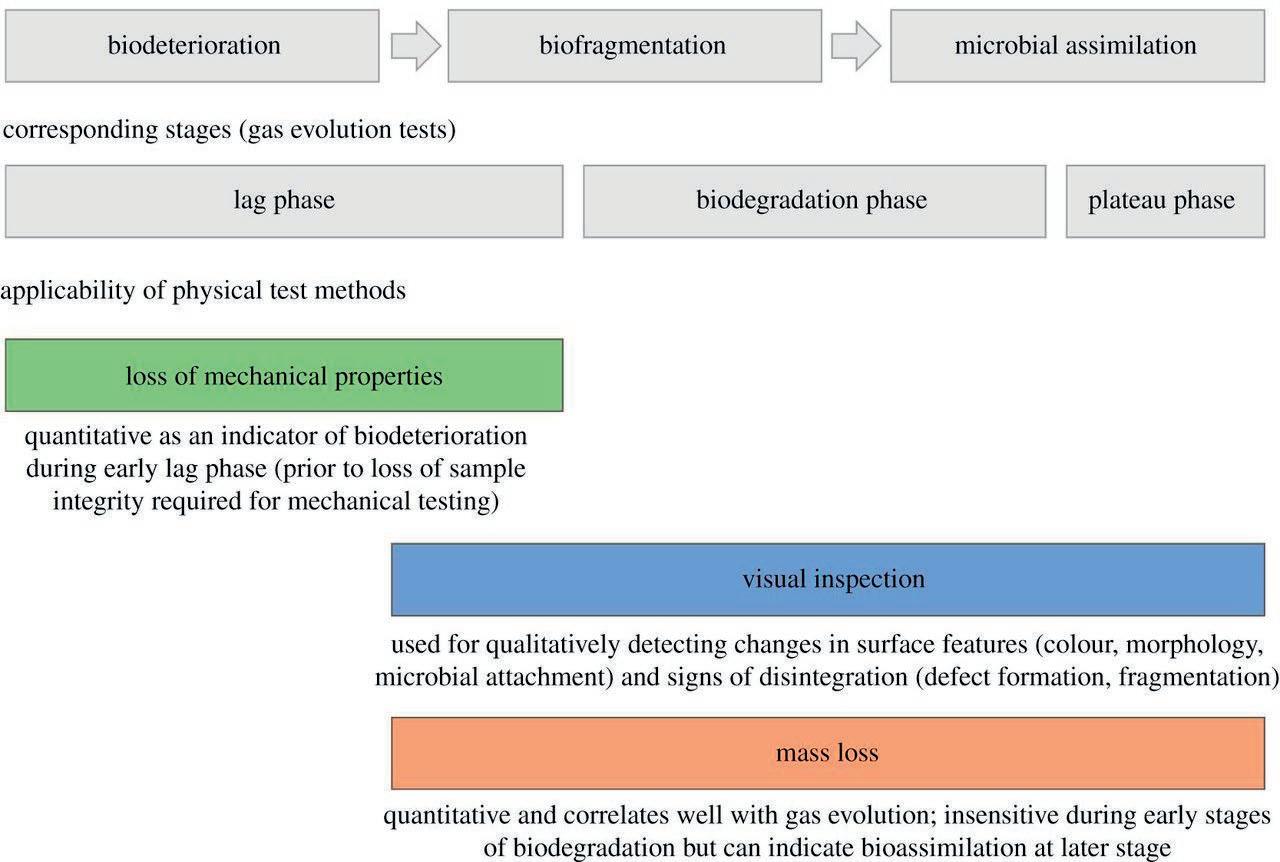
microbiana corresponde a la diges- tión de las especies de bajo peso molecular producidas durante las etapas anteriores, lo que resulta en una importante evolución de los gases y en la mineralización. Los cambios en las propiedades mecánicas de un material a menudo ocurren durante la etapa de biodeterioro y el inicio de la fragmentación ( figura 1 ). Estos

Métodos de prueba físicos para la evaluación de la biodegradación plástica, y su relación con las diferentes etapas de descomposición del polímero y las etapas correspondientes obser- vadas mediante pruebas de evolución de gases (CO 2 y CH 4).
Si bien las mediciones de pérdida
de masa son fáciles de realizar en comparación con los métodos de evolución del gas, se debe tener cuidado con respecto a varios aspectos. Muchos bioplásticos, par- ticularmente aquellos basados en almidón, son higroscópicos y la influencia de los cambios en la humedad en la pérdida de masa debe eliminarse secando la muestra antes de las mediciones. Como el nivel de humedad es crucial para la actividad microbiana, la etapa de secado puede interrumpir la biode- gradación cada vez que se procesa una muestra para su análisis. Esto puede ser mitigado por un régimen de muestreo sacrificial en el que se analizan muestras separadas en ca- da intervalo de muestreo. Durante la degradación, la fragmentación de los materiales puede conducir a la liberación de partículas al medio circundante [ 14].]. También puede ocurrir la absorción de di- versos compuestos de matrices ambientales o del medio de crecimiento. Si bien estos pueden in- fluir en los cambios en la masa, se pueden contrarrestar parcialmente mediante el uso de contenedores (como bolsas de malla de nylon) [ 106 ] para separar los materiales sin evitar la migración de la humedad y las células microbianas.
Al igual que las alteraciones en la apariencia visual y la masa de un material dado, los cambios en las propiedades mecánicas (por ejem- plo, la resistencia a la tracción, el módulo elástico y la elongación a la rotura) son simples de medir en comparación con la evolución del gas. Estos cambios pueden atribuirse a una reducción en el peso molecular debido a la hidrólisis u oxidación enzimática y, por lo tanto, se utilizan como un indicador del inicio de la biodegradación. Sin embargo, incluso antes de una fragmentación significativa inducida biológicamente, la formación de grietas e irregulari- dades de la superficie debido a procesos abióticos puede comprometer gravemente la fiabilidad de los resultados de las pruebas mecánicas. Por ejemplo, ciertos bioplásticos (por ejemplo, basados en almidón) pueden volverse frági- les con el tiempo debido a un cam- bio en la cristalinidad [ 107]. La exposición a la radiación UV y al calor también puede afectar las propiedades mecánicas. Esto puede dificultar la correlación de los cambios en las propiedades mecánicas con la biodegradación.
Para superar las limitaciones de los métodos físicos descritos anteriormente, se pueden combinar con otras técnicas analíticas y enfoques para confirmar los cambios en la estructura molecular de los políme-
ros durante la biodegradación. Estas incluyen mediciones de hidrólisis de superficie, análisis cromatográficos y varias técnicas espectrométricas ( tabla 3 ). La microscopía óptica y de
Tabla 3. Técnicas analíticas y enfoques que pueden utilizarse para complementar los métodos de prueba físicos para evaluar la biodegradabilidad de los polímeros. Industria Acuícola
experimentales descritos en los estándares de biodegradabilidad y métodos de prueba (tablas 1 y 2 ) se han utilizado en la investigación primaria. Algunos estudios han sido
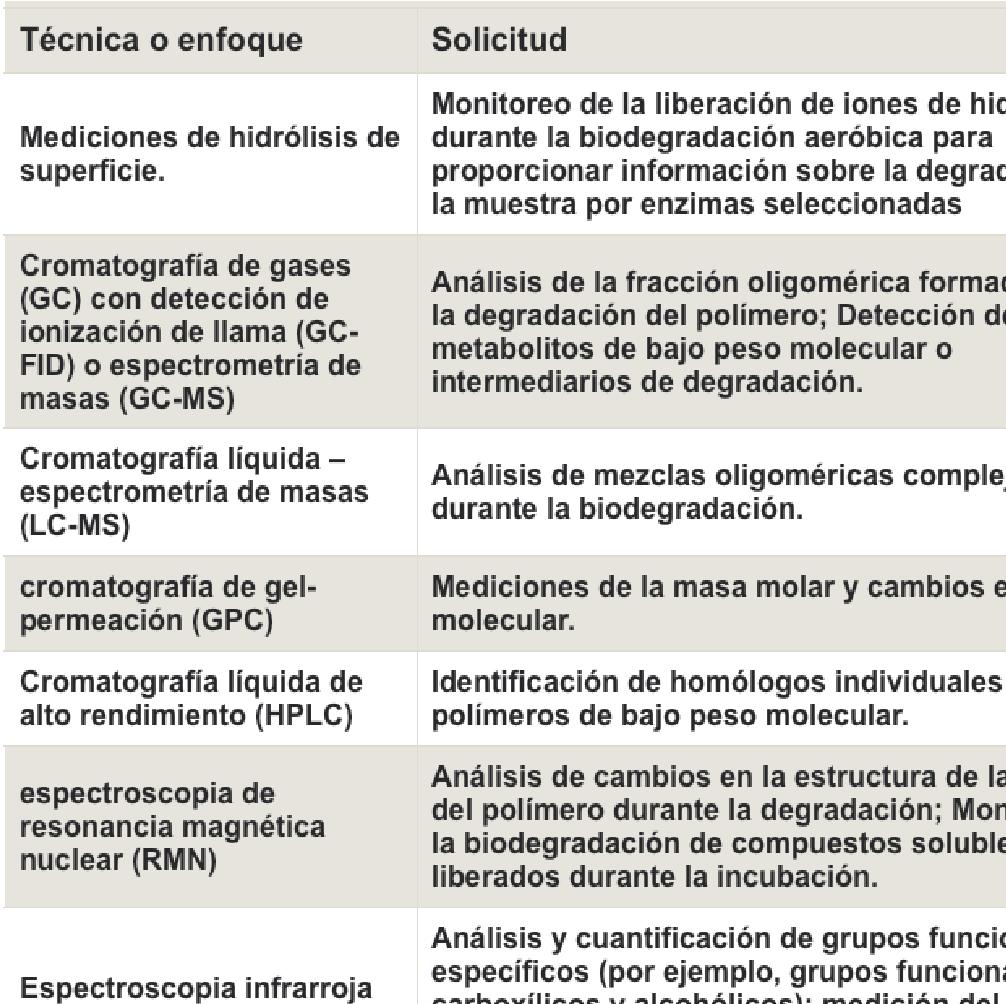

barrido electrónico (SEM) también se puede utilizar para evaluar el bio- deterioro de la superficie debido a la actividad microbiana o la formación de biofilm [ 115 , 117 ]. Aunque la microscopía óptica y la SEM no son cuantitativas, la microscopía de fluo- rescencia se puede usar para cuan- tificar la colonización microbiana de la superficie del polímero [ 119 ]. En Lucas et al. Se proporciona in- formación adicional sobre técnicas analíticas para evaluar los procesos de degradación inducidos por abió- ticos y biológicos. [ 76 ] y Koutny et al. [ 117]. Una limitación de muchos de los métodos descritos anteriormente es que pueden ser costosos de realizar de forma rutinaria. Las mediciones de la oxidación de la superficie basadas en el índice carbo- nilo no se pueden realizar para todos los tipos de polímeros, ya que cier- tos materiales plásticos están poco predispuestos a la oxidación. Ade- más, los cambios en el grado de oxidación de la superficie pueden deberse a procesos abióticos (quí- micos, fotoquímicos y térmicos) y / o bióticos (enzimáticos). Al evaluar la biodegradabilidad de los plásticos en entornos complejos, es probable que las pruebas físicas y mecánicas (así como las mediciones del índice de carbonilo) deban complemen- tarse con otros enfoques, como las mediciones de la evolución del gas.
5. Uso de estándares de biodegra- dabilidad en la literatura de investigación. Muchos de los enfoques


comparativos, e incluyen una va- riedad de materiales o una compa- ración de métodos estandarizados [ 53 , 120 , 121 ]. Sin embargo, a nuestro entender, el único estudio realizado hasta la fecha que ha inten- tado extender los procedimientos de prueba estándar al ambiente abierto fue realizado por Tosin et al. [ 63], quienes desarrollaron nuevos méto- dos para evaluar la biodegradación de polímeros en sedimentos inter- mareales y en sedimentos cercanos a la costa inundados permanente- mente. En el primer método, los se- dimentos arenosos recolectados en el campo y el agua de mar se alma- cenaron dentro de una caja sellada de polipropileno con salidas de ai- re. Las muestras de la película Mater- Bi® se enterraron en el sedimento, seguido de una evaluación visual de la biodegradación. El último método fue una modificación de la norma BS EN ISO 14851: 2004 [ 35 ] ( tabla 1 ), con los recipientes de prueba que contenían 15 g de sedimento húme- do cubiertos con 75 ml de agua de mar artificial. Se colocaron muestras de película sobre el sedimento y se monitorizó el consumo de oxíge- no mediante respirometría. Ambas pruebas se realizaron a temperatura ambiente. Usando estas condiciones de exposición, Mater-Bi ®se demostró que se desintegraba en nueve meses (simulación de la zona intermareal) y mostraba una tasa de biodegradación del 69% en apro- ximadamente 240 días (sedimento inundado) [ 63 ]. Sin embargo, las
condiciones de prueba empleadas en este trabajo no reflejaron muchas de las condiciones que se encuen- tran a menudo en el ambiente marino (como las temperaturas frías), y no tenemos conocimiento de ningún estudio que ofrezca un protocolo completamente sólido para aplicar los estándares existentes para eva- luar la Biodegradabilidad de plásti- cos en ecosistemas no gestionados.
Incluso cuando la biodegradación en un entorno determinado se ha demostrado en parte, muchos in- vestigadores aún consideran la biodegradación a largo plazo (com- pleta) como un problema sin re- solver [ 62 , 122 ]. Los estándares y especificaciones diseñados para medir la biodegradabilidad en si- mulaciones ambientales a menudo incluyen una advertencia sobre la necesidad de estudios adicionales que demuestren un grado acep- table de biodegradabilidad en el entorno abierto. Sin embargo, no parece que ninguna norma brinde orientación sobre cómo se debe completar ese trabajo corroborativo. 6. Conclusión
La conclusión de esta revisión es que las normas internacionales actuales y los métodos de prueba regionales son insuficientes en su capacidad para predecir de manera realista la biodegradabilidad de las bolsas de transporte dentro de las aguas resi- duales, aguas interiores (ríos, arroyos y lagos) y ambientes marinos. Esto se debe a varias deficiencias en los pro- cedimientos de prueba existentes, a la ausencia de estándares relevantes para la mayoría de los hábitats acuá- ticos no gestionados, así como a la escasez de investigaciones más am- plias sobre la biodegradación de ma- teriales plásticos en estos entornos. Si bien la mayoría de los procedi- mientos de prueba existentes em- plean un método confiable para determinar la biodegradabilidad (es decir, las mediciones de la evolución de CO 2 y CH 4 ; tablas 1 y 2), los datos obtenidos por los estánda- res actuales, los métodos de prue- ba y las especificaciones pueden subestimar significativamente las duraciones requeridas para la bio- degradación de polímeros dentro de los ecosistemas naturales. Esto se debe en parte a los sesgos aso- ciados con la preparación de inó- culos experimentales y las propias condiciones de prueba, incluido el uso de cepas preseleccionadas y / o preacondicionadas, inóculos modi- ficados artificialmente, materiales de prueba en polvo, medios sintéticos ricos en nutrientes y temperaturas de prueba que son Con frecuencia más alto que los encontrados en el medio ambiente. Un problema me- todológico clave asociado con los procedimientos existentes es la falta de directrices claras para el análisis
de diferentes tipos de polímeros, incluidos los materiales compues- tos y plásticos que contienen aditivos. También hay una escasez de directrices para materiales de diferentes formas y tamaños y, en ciertos casos, los procedimientos de prueba carecen de un nivel suficiente de replicación estadística. Además, no se han publicado estándares de biodegradabilidad o métodos de prueba para plásticos para entornos no ges- tionados de agua dulce, o hábitats marinos que no sean agua de mar abierto, sedimentos aeróbicos arenosos y la interfaz agua-sedimento.
Sobre la base de investigaciones publicadas anteriormente sobre la biodegradación de plásticos en ambientes acuáticos, los plazos requeridos para la degradación del polímero son muy variables y dependen de las condiciones ambien- tales (incluida la temperatura y la disponibilidad de nutrientes). Por ejemplo, si bien es probable que la degradación completa de ciertos bioplásticos requiera varios meses dentro de las instalaciones de tratamiento de aguas residuales, pueden requerirse años o incluso décadas para que las botellas de PHBV se sometan a una biodegradación completa luego de su deposición en ambientes de lagos profundos [ 79]. Las tasas de biodegradación de polímeros dentro de los hábitats acuáticos generalmente se han esti- mado utilizando métodos indirectos (como la pérdida de masa), y hay una falta de investigación sobre este tema con referencia a varios entornos (incluyendo agua de mar profunda y sedimentos marinos fríos). Dada la acumulación a escala mundial de residuos plásticos en ríos, lagos, aguas costeras y sedimentos, aguas polares y aguas profundas, se requieren datos experimentales adi- cionales sobre la biodegradación de polímeros en la mayoría de los ecosistemas acuáticos no gestionados.
Además de estos problemas, los im- pactos toxicológicos y ambientales más amplios de los desechos plásti- cos acuáticos no se comprenden su- ficientemente, a pesar del requisito de pruebas de toxicidad de la marca de conformidad MARINE biodegra- dable de Vinçotte OK [ 51 ]. De hecho, ninguna norma o método de prueba actual tiene en cuenta los posibles impactos adversos de los plásticos, los aditivos plásticos y / o los productos de degradación de polímeros en los organismos que se depositan en la base de las redes alimenticias acuáticas (como los gusanos marinos [ 83]), o procesos ecológicos como el ciclismo elemental mediado por microbios. Para facilitar el desarrollo de un nuevo estándar (s) de biodegradabilidad para materiales plásticos, se necesitan

metodologías experimentales mejoradas que simulen propiedades clave de los ecosistemas acuáticos (incluidas las bajas temperaturas y la disponibilidad de nutrientes). Por ejemplo, ISO 9887: 1992 [ 123 ], ISO 14592-2: 2002 [ 124 ] y ASTM D7473-12 [ 47 ] implican el uso de un método de flujo de lodo activado semicontinuo o un sistema de flujo continuo y se pueden adaptar para un mayor desarrollo del método. , incluido el diseño de ensayos de biodegrada- bilidad para ambientes acuáticos no considerados por los estándares y métodos de prueba actuales. Finalmente, la naturaleza interconectada de los ecosistemas marinos y de agua dulce debe tenerse en cuen- ta al desarrollar nuevos enfoques para evaluar la biodegradabilidad de los materiales plásticos. Como los entornos como las instalaciones de tratamiento de aguas residuales y los ríos actúan como importantes conductos para el transporte de ba- sura plástica a los hábitats marinos [ 5 ], el tiempo de retención previsto del material de prueba dentro del entorno de interés será un tema clave a considerar cuando se determine un adecuado duración de la prueba (§3.3). Los productos que pasan una prueba de biodegradabilidad que se ha desarrollado exclusiva- mente para entornos de agua dulce pueden presentar tasas de biodegradación extremadamente lentas si se depositan en hábitats marinos, con repercusiones directas por su impacto ambiental y destino [ 16]. Accesibilidad de datos: No se han generado nuevos datos para los

fines de este artículo de revisión, y todos los datos de esta revisión están disponibles en las fuentes a las que se hace referencia.
Contribuciones de los autores: KO y JPH concibieron y diseñaron el estudio. Todos los autores revisaron los productos y definieron conclusiones clave, y contribuyeron con entradas clave. JPH preparó el documento con contri- buciones de todos los coautores. Conflicto de intereses: Declaramos que no tenemos intereses en competencia. Fondos: Este artículo se basa parcialmente en un informe del Grupo de Asesoramiento Técnico encargado por el Departamento de Medio Ambiente, Alimentación y Asuntos Rurales del Reino Unido (ver [ 29 ] para un documento resu- men entregado al Parlamento del Reino Unido en diciembre de 2015).
Agradecimientos: Agradecemos al profesor Richard Murphy y al profesor Edward Kosior por sus valiosos comentarios y sugerencias. Notas al pie: © 2018 Los Autores. Publicado por la Royal Society bajo los términos de la licencia de atribución de Creative Commons http://creativecommons.org/licenses/ by/4.0/ , que permite el uso sin restricciones, siempre que el autor original y la fuente sean acreditados. Publicado: 23 de mayo de 2018 https://doi.org/10.1098/rsos.171792
Fuentes: Jesse P. Harrison, Carl Boardman, Kenneth O’Callaghan, Anne-Marie Delort y Jim Song
Desafíos para el cultivo de camarones
El crecimiento continuo de la acuacultura ha incrementado la necesidad de utilizar ingredientes sustentables en alimentos para peces y camarones. Las harinas de pescado son ingredientes ideales por sus perfiles nutricionales, pero son de producción limitada. Esta limitación en producción dificulta el suministro de la creciente demanda de alimentos acuícolas, por lo que la tendencia es reducir su inclusión suplementando con otras fuentes de proteínas más económicas y disponibles, como lo es la harina de soya.
La soya es una alternativa sustentable y costo eficiente, pero tiene desventajas asociadas con los alimentos basados en ingredientes vegetales; como el consumo reducido de alimento y factores anti-nutricionales asociados con bajos crecimientos. De igual manera, son deficientes en nutrientes esenciales; como minerales y ácidos grasos omega-3 de cadena larga. Alimentos basados en ingredientes vegetales contienen mayor concentración de ácidos grasos omega-6 con comprobado efecto inflamatorio.
Otro ingrediente alternativo que se ha venido utilizando es la harina de subproductos avícolas, que provee buenos niveles de proteína pero que contiene un perfil graso que debe ser complementado con omega-3. Al igual que la harina de soya, requieren ser suplementados con ingredientes atractantes que inciten al consumo del alimento.
Ingredientes innovadores como los son las proteínas unicelulares, harinas de algas y harinas de insectos, entre otros, tienen gran potencial, pero deben lograr ser económico efectivas, escalables y estar disponibles para

su uso. Todas ellas presentan beneficios, pero presentan deficiencias que pueden ser complementadas con harinas de origen marino como el krill.
Los ingredientes de origen marino son una rica fuente de omega-3 de cadena larga que tiene la capacidad de mitigar la inflamación. Cuando, por razones económicas, se utilizan alimentos con baja inclusión de harina de pescado, el krill puede ser incluido para suplir compuestos únicos como son: fosfolípidos ligados omega-3, proteínas de alta calidad, nucleótidos, péptidos solubles, quitina y astaxantina. Estos compuestos proveen demostrados beneficios, los cuales incluyen: mejora en el consumo del alimento, aceleración del crecimiento, reducción de costos, tolerancia a estrés, mejora del sabor y coloración de los camarones cosechados.
¿Por qué Krill?
El krill es un crustáceo zooplanctónico que habita en todos los océanos, pero se concentra en grandes aglomeraciones en las aguas del océano Antártico, donde CCAMLR estima una biomasa de 379.000.000 toneladas. Es muy importante en la cadena alimenticia porque se alimenta principalmente de fitoplancton y hace disponible los nutrientes para otros animales que lo consumen. Por esta razón es una especie clave en el ecosistema Antártico. Best Aquaculture Practices (BAP) aprueba el uso de krill en alimentos para camarón. Con una biomasa en muy buena condición, Sustainable Fisheries Partnership califica al krill en clase “A”, perfilándolo como la pesquería de más alta puntuación en aspectos de sostenibilidad. De igual manera es certificado MSC.
El krill tiene un enorme valor nutricional y funcional, que ha demostrado en innumerables investigaciones mejoras del
desempeño de los alimentos acuícolas tanto en peces como en camarones.
Beneficios nutricionales del Krill
El krill es un recurso único rico en proteínas de muy buena calidad, de alta palatabilidad, que contiene pigmentos naturales y un excelente perfil de ácidos grasos y minerales.
Omega-3s
El krill es rico en omega-3s, y principalmente en ácido eicosapentaenoico (20:5n-3) y docosahexaenoico (22:6n3). La salud y crecimiento del camarón está estrechamente relacionada con la dieta. El camarón tiene una capacidad limitada de sintetizar omega-3s y fosfolípidos, por lo que estos deben ser incluidos en el alimento. Utilizando krill en los alimentos se mejora el contenido de omega-3 en el camarón, promoviendo su normal desarrollo y resistencia, ganancia de peso y sobrevivencia. A su vez, el perfil graso del krill ha demostrado grandes beneficios en el desempeño reproductivo y en el desarrollo larval.
Fosfolípidos y triglicéridos
Los ácidos grasos omega-3s pueden enlazarse entre ellos formando triglicéridos o fosfolípidos. En el krill la mayoría de omega-3s se encuentra en forma de fosfolípidos (fosfatidilcolina), mientras que en el aceite de pescado se encuentran en forma de triglicéridos. Los fosfolípidos omega-3 son importantes ya que conforman los bloques de construcción de las membranas celulares. Los triglicéridos omega-3s en cambio, deben ser primero convertidos a fosfolípidos, antes de que puedan ser tomados por la membrana celular.
Los triglicéridos omega-3 pueden ser usados por el cuerpo como una fuente de energía o depositados como grasa, por esta razón una me -
nor proporción de omega-3 irá a las membranas. Por el contrario, en forma de fosfolípidos son fácilmente tomado por los órganos, dando al camarón mayor omega-3s en sus membranas y resultando en una mejor biodisponibilidad, mejorando a su vez la salud y calidad en cosecha. Los fosfolípidos aseguran que se almacene suficiente energía y que las grasas puedan ser movilizadas por transporte a los tejidos. Esto es particularmente importante para superar la muda de exoesqueleto y condiciones estresantes como híper-salinidad, variaciones de temperatura y bajas concentraciones de oxígeno.
Antioxidante natural
El krill es rico en astaxantina, un poderoso antioxidante natural, secuestrador de moléculas de oxígeno y se ha demostrado que tiene un papel protector contra la acción de los radicales libres. Mejora la sobrevivencia, crecimiento, capacidad reproductiva, tolerancia al estrés, así como la expresión de genes relacionados con inmunidad y resistencia al estrés y a enfermedades. Este compuesto es justamente el responsable de la coloración del camarón que es apreciada en el mercado, mejorando la calidad y precio del producto.
Otros compuestos
El krill es rico en quitina, que es el componente estructural del exoesqueleto de los crustáceos. Varios estudios han demostrado el mejoramiento de la respuesta inmune de los camarones a patógenos cuando se suministra quitina en la dieta. Krill es rico en nucleótidos, péptidos solubles y óxido de trimetilamina, que son promotores del consumo de alimento, aspecto muy importante en la alimentación de los camarones. De igual manera, se ha demostrado que los nucleótidos y péptidos de cadena corta proveen efecto inmunoestimulante, que mejora los mecanismos de defensa en el tracto digestivo del camarón contra patógenos, incrementando sobrevivencia y crecimiento.
Nucleotides (NT) are ubiquitous intracellular compounds of crucial importance to cellular, function and metabolism (Cosgrove 1998). As the basic building blocks of DNA and RNA, nucleotides play an important role in many metabolic processes (Carver 1994; Jyonouchi 1994; Navarro et al. 1996), such as synthesis of DNA and RNA, activating biosynthetic pathways, transferring chemical energy, as coenzyme component and as biological regulators (Cosgrove 1998; Swick et al. 1995). Meanwhile, previous studies showed that aquatic animals fed with nucleotides supplemented diets experienced beneficial effects on the growth, performance (Abtahi et al. 2013; Lin et al. 2009), immune response (Ramadan et al. 1994), gut flora (Gil et al. 1986), gastrointestinal physiology and morphology (Burrells et al. 2001a;Carver 1994) and disease resistance (Burrells et al. 2001a; Leonardi et al. 2003).
El colesterol es un muy importante compuesto graso que no puede ser sintetizado por los camarones y que se encuentra presente en el krill. Deficiencias de colesterol en las dietas de camarones pueden resultar en disminución de crecimiento. No obstante, la combinación de fosfolípidos y colesterol en el krill, al ser incluido en los alimentos de camarón, permite que no se requieran suplementarlos con colesterol.
Minerales como el cobre y vitaminas A, C y E presentes en el krill son igualmente necesarios en el metabolismo del camarón.
En general podemos concluir que el krill en forma de harinas y aceites es un super ingrediente que brinda enormes beneficios en los alimentos de camarones y pueden ser utilizados de forma costo eficiente para mejorar el desempeño de los cultivos.

Geronimo Leonardi - Director de Ventas – QRILL Latin America / Aker BioMarine Cell: +1 786 806 6898















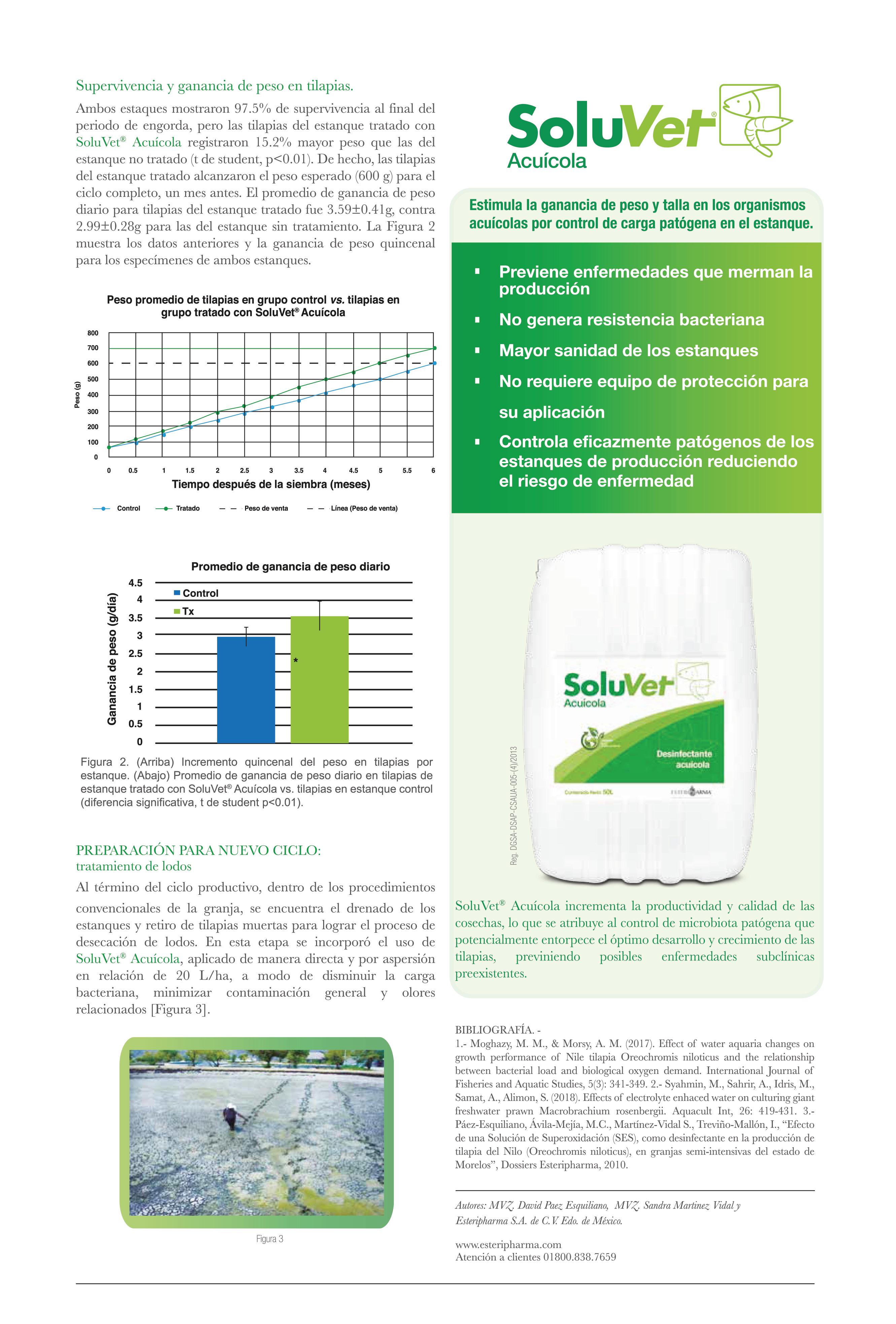
Mazatlán, Sinaloa
Tras el caso de éxito en su edición anterior, Expo Innovación Pesca y Acuacultura 2019 lanza convocatoria para estudiantes y empresas que quieran ser partícipes al premio.
El Premio Nacional de Innovación Pesquera y Acuícola es para personas, organizaciones, empresas, estudiantes y académicos que, a través de sus conocimientos, han desarrollado procesos para resolver problemas o, creado produc- tos con valor agregado, con la intención de lograr negocios más redituables dentro de la industria pesquera.
Las propuestas que se pueden presentar como candidatos a ganar son “aquellos proyectos enfocados en innovación de productos, valor agregado, tec- nología aplicada en la industria acuícola y pesquera; que tengan un impacto económico, ambiental o social, en beneficio del sector en México” dijo Guillermo Cevallos Hemke, director General de Expo Innovación Pesca y Acuacultura 2019.
En su edición de 2018 el ganador fue Enrique Espinoza, quien presentó su producto: Salchichas de Atún Rosso -

nero, el cual llevo al éxito al empresario y se llevó el gran galardón. “Nuestros clientes y amigos fueron los mayores motivadores. Nos comentaban que nuestra salchicha de atún era un producto innovador ya que no había nada igual en el mercado.”
A un año de haber logrado este premio, el emprendedor y propietario de la empresa Rossonero Foods, nos platica de su experiencia al participar en el premio y cómo ha cambiado su vida desde entonces, “fue una grata sorpresa ver el talento y esfuerzo de los participantes, muchos de ellos ofrecían soluciones novedosas. Y es un honor haber sido seleccionados como los ganadores al premio”.
El emprendedor nos cuenta como su producto ha crecido en el mercado: “Ahora contamos con una validación de nuestra propuesta en el mercado, inversionistas, distribuidores y clientes que creen en nuestro producto. Cerramos el mes pasado con 400 puntos de venta a nivel nacional, distribuidor en Estados Unidos y representación en Europa. Creo que va- mos por buen camino” dijo el empresario.
Enrique les da un consejo a todos aquellas personas que tienen un proyecto y quieren
empezar a hacerlo realidad “No hay malas ideas, hay malas ejecuciones. Cree en ti y eventualmente los demás creerán en tu proyecto. Jamás dejes de aprender. Aprende a pedir ayuda y ayuda a los que te rodean. México es el país de los emprendedores, ¡si se puede! No depende de tu gobierno, escuela o calidad socioeconómica, sólo de tus ganas de dar la mejor solución a tu cliente”
Al mismo tiempo, los alumnos David Alejandro Salinas Rodrí- guez, Carlos Ernesto Alvarado Suarez y Rafael Gallardo de la Rosa, del Instituto Tecnológico de Mazatlán, fueron parte de este acontecimiento, quienes ganaron el segundo lugar del Premio Nacional de Innovación Pesquera y Acuícola 2018, con el proyecto de la elaboración de una tostada casera hecha a base de subproductos de camarón.
“Como ingenieros pesqueros, no era nuestro fuerte hablar de procesos, pero sabiendo la problemática pesquera actual y con apoyo de nuestros profesores, asesores e incluso compañeros bioquímicos se llevó aca- bo. Independientemente de no haber ganado el primer lugar, fue el que más impacto tuvo y tuvimos propuestas comerciales en ese mismo momento”.
La idea de su producto nace de una vista de trabajo a Naya- rit, donde descubrieron que la gente usaba polvo de camarón como sazonador. A demás de tener conocimiento que algunos elementos del crustáceo se desechan. En ese momento, Rafael y su equipo ven una oportunidad para desarrollar un subproducto comestible de camarón, darle un segundo uso y un mejor aprovechamiento.
“El objetivo de este proyecto, es ayudar al sector pesquero, trabajamos ahí y convivimos con ellos.
Como ingenieros tenemos una responsabilidad de cumplir con nuestro sector, y que mejor, que darnos la oportunidad por medio de este Premio” el egresado también agregó: “El proyecto es sustentable y ami- gable con el medio ambiente. Es un problema real que todos debemos atender”.
Ahora, a un año de haber par- ticipado, Rafael comenta que una de sus prioridades es poder seguir con el proyecto y hacerle las mejoras necesarias para poder comercializar su producto, ya que cree firmemente que es una fuente de ingresos y empleos para las familias mexica -
nas que viven de este sector. “Recomiendo ampliamente participar y sobretodo promover este tipo de eventos.
Hay muchos jóvenes estudiantes con buenas ideas y maestros que tienen ganas de impulsar- los, quienes también transmiten sus ideas a través de sus alumnos, así que todos debemos de participar sin miedo a perder”.
La convocatoria se cierra el día 18 de Septiembre de este año

y la ceremonia de premiación se llevará a cabo dentro de las actividades de Expo Innovación Pesca y Acuacultura 2019 que se realiza 24 y 25 de Octubre en Mazatlán, Sinaloa.
Las bases del Premio Nacional de Innovación Pesquera y Acuí- cola 2019 se pueden consultar a través de la página: www.expoinnovacion.org/premio


LA PAZ, BCS .-
2 Julio 2019
Convocan a productores acuícolas al programa de acuacultura rural 2019

La inversión para el presente ejer- cicio es de 5 millones de pesos.
El Gobierno del Estado y la Comi- sión Nacional de Acuacultura y Pes- ca (CONAPESCA), convocan a los productores acuícolas de los cinco municipios de la entidad a ingresar sus proyectos al Programa de Acua- cultura Rural 2019, en el que ambos niveles de Gobierno canalizan una inversión de 5 millones de pesos, que se potencializa a 6 millones con la aportación de los beneficiados.
Así lo informó el subsecretario estatal de Pesca y Acuacultura, Fer- nando García Romero, al establecer este programa ofrece 2 vertientes
TAMAULIPAS .-

de apoyo, el primero en infraestruc- tura y equipo que contempla conceptos como bombas, aireadores, tinas, bolsas y canastas ostrícolas, cabos y boyas por mencionar algu- nos, en donde la aportación guber- namental será del 80 por ciento en proyectos de hasta 500 mil pesos.
Del mismo modo, el funcionario de la Secretaría de Pesca, Acuacultura y Desarrollo Agropecuario (SEPADA), agregó que la segunda vertiente es para la adquisición de crías (semillas y alevines), en la que la aportación del Gobierno Estatal y la CONAPESCA es también del 80 por ciento en proyectos de hasta 50 mil pesos.
También te puede interesar.
Máxima autoridad católica en BCS pide el veto al Gobernador sobre el matrimonio igualitario. Sorprendió a hombre queriendo robar y fue atacado con una navaja; esto en La Paz BCS. Una menor de 14 años está desaparecida en La Paz, BCS. García Romero estableció que la ventanilla del Programa Acuacul- tura Rural 2019 estará abierta hasta el 31 de julio y que los productores interesados pueden consultarlas en las páginas electrónicas oficiales del Gobierno del Estado y la SEPADA, o bien acercarse a las oficinas de la instancia estatal y federal en cada uno de los municipios a fin de recibir orientación sobre sus proyectos.
Finalmente, el funcionario estatal valoró el impacto que este progra- ma ha tenido en los últimos años en el aumento de la producción acuícola de nuestra entidad, el número de familias que hoy dependen de la actividad, así como el papel preponderante que actual- mente ésta tiene en la producción de pescados y mariscos en comparación con la pesca extractiva.
14 De Junio 2019 FUENTE:
En Tamaulipas van por mayor cultivo en granjas acuícolas
En Tamaulipas se proyecta incrementar el cultivo de especies marinas como el camarón y el ostión mediante granjas acuícolas.
En Tamaulipas se proyecta incrementar el cultivo de especies marinas como el camarón y el ostión mediante granjas acuícolas.
“Se estima una oportunidad de desarrollo acuícola de Tamaulipas cuenta con 11 principales cuerpos de agua, que representan 135,000 hectáreas, de las cuales se estima que 1, 740,000 son susceptibles para el desarrollo de la acuacultura de peces, ostiones y macroalgas“, señaló Raul Ruiz, titular de Pesca.
El potencial acuícola para la producción de moluscos bivalvos (ostión), es de 231 mil hectáreas de lagunas coste -
ras para la producción de ostión y macroalgas, estimando aproximadamente 1, 800,000 ton anuales de producto.
Hay 451,000 hectáreas susceptibles para el cultivo de camarón, la Secretaria de Pesca en el estado proyecta
incrementar el cultivo en granjas.
Comentó que recientemente se hizo un recorrido por los laboratorios, plantas de proceso y granjas de producción ostrícola y piscícola de Baja California.

LOS MOCHIS, SINALOA.-
23 DE JUNIO DE 2019















































