

IMPLANTOLÓGIA
A FOGÁSZAT INFORMÁCIÓS
„A pécsi fogorvosképzés sorsának alakulása nagyon fontos számomra…”
Irányított sebészi munkafolyamat a kiszámítható tervezéstől az implantációig
Háromtagú moláris híd készítése
Két különböző csatlakozású implantátumtípus klinikai és radiológiai analízise
















































































Tisztelt Olvasó!
A fogászati szakma folyamatos megújulásban él: technológiai fejlődés, digitalizáció, új terápiás protokollok és egyre tudatosabb páciensek formálják mindennapjainkat. Az elmúlt évek kihívásai után a szektor ma már egyértelműen a stabilizáció és a szakmai előrelépés időszakát éli, ahol a minőség, a hatékonyság és az innováció kerültek a fókuszba.
A rendelők és fogtechnikai laborok működésében egyre hangsúlyosabb szerepet kapnak a korszerű eszközök, az új anyagok, valamint a digitális megoldások. A fejlesztések iránti igény töretlen, a piaci szereplők pedig aktívan keresik azokat a lehetőségeket, amelyek hosszú távon is versenyképesebbé tehetik praxisukat. Ebben a környezetben különösen felértékelődik a naprakész, hiteles szakmai információ szerepe.
Kiadóként célunk változatlan: olyan tartalmakat kínálni, amelyek valódi segítséget nyújtanak a mindennapi munkában, inspirációt adnak a fejlődéshez, és eligazítást nyújtanak a gyorsan változó szakmai környezetben. Nagy öröm számunkra, hogy megújult e-Journal kiadványaink pozitív fogadtatásra találnak, és egyre többen tekintenek rájuk szakmai tudástárként. A dental.hu oldalon továbbra is díjmentesen elérhetők korábbi tematikus lapszámaink, egyfajta online könyvtárként szolgálva Olvasóink számára.
Jelen számunkban az általános fogorvosi eljárások mellett kiemelt figyelmet szentelünk az implantológia aktuális kérdéseinek, gyakorlati tapasztalatainak és jövőbeni irányainak.
Bízunk benne, hogy összeállításunk értékes gondolatokat, hasznos ismereteket és új nézőpontokat kínál minden Olvasónk számára.
Tartalmas és inspiráló olvasást kívánok!

Tamás, felelős kiadó
Laczkó
E-Journal IX. évfolyam, 2026. 2. szám
Kiadja: Event Organizer Hungary Kft. 1012 Budapest, Kuny Domokos u. 9.
Felelős kiadó: Laczkó Tamás
Előkészítés:
Event Organizer Hungary Kft., Sárközi András e-mail: andras.sarkozi@dentalworld.hu
Információ, hirdetésfelvétel: Kolozsi Tímea telefon: 06-30-472-0030
Az újság e-mail címe: info@dental.hu
Az újság internetcíme: www.dental.hu
Terjesztés: E-mail hírlevél formájában.
A tudományos közleményeket a szerkesztőség lektoroknak adja át véleményezésre. Közlés csak egyetértő lektori vélemény, illetve a javasolt módosítások elvégzését követően lehetséges. A cikkek szerzői vállalják, hogy az általuk elküldött írás saját forrásból származik, illetve a felhasznált anyagokat (publikációkat, illusztrációkat, képeket stb.) mindenkor pontosan feltüntetik. Írásaiknak jogi és egyéb adatvédelmi kérdéseiben felelősséget vállalnak.
A német nyelvű szakmai cikkeink magyar fordítását az Oemus Media AG Kiadó engedélyével szerkesztettük lapunkba. A fel nem használt kéziratokat, fotókat nem őrizzük meg, és nem küldjük vissza.
A hirdetések tartalmáért nem vállalunk felelősséget. A gyártó, illetve forgalmazó cégek kérésére közzétett cikkeket keretbe foglalva közöljük és (x)-szel jelöljük, azok szakmai tartalmáért a szerkesztőbizottság nem vállal felelősséget.






Dr Claudia Pinter

Dr Filippo Cardinali

Prof Eric Liou

Dr Riccardo Tonini
U D A P E S T








WORLD DENTAL
2 0 2 6 . O K T Ó B E R 8 - 1 0 .
Dr Ricardo Kern
Dr Pierre Dimitrov
Prof Markus Hürzeler
Mdt Edris Rasta
Dr Jun Iwata
Dr Michael Melkers
Dr Joseph Choukroun
Dr Marco Maiolino
Dr Omar Ikram
Dr Dan Lazar
Dr Valentina Lanteri
Prof Adam Nulty
Dr. Riba Magdolna
„A PÉCSI FOGORVOSKÉPZÉS SORSÁNAK ALAKULÁSA NAGYON FONTOS SZÁMOMRA…”
Prof. dr. Szalma József egyetemi tanár, a Pécsi Tudományegyetem Fogászati és Szájsebészeti Klinika igazgatója, az Arc-, Állcsont- és Szájsebészeti Tanszék vezetője, a fog- és szájbetegségek, a dentoalveoláris sebészet, valamint az orális implantológia szakorvosa. A Klinikai Orvostudományok Doktori Iskolájában témavezető, 2021 óta pedig az MTA doktora. A Fogorvosi Szemle, a Journal of Cranio-Maxillofacial Surgery lapok szerkesztőbizottsági tagja, utóbbinak dentoalveoláris sebészet és implantológia rovatszerkesztője, és számos nemzetközi folyóirat rendszeres bírálója. A Béres Károly Alapítványi díj, a Körmöczi-díj, a Regöly-Mérei-díj, illetve az MTA Bolyai-plakett kitüntetés birtokosa. A Magyar Arc-, Állcsont- és Szájsebészeti Társaság elnöke, illetve a Magyar Fogorvosok Egyesülete elnökségének, valamint számos nemzetközi szakmai egyesületnek is tagja.

Prof. dr. Szalma Józseffel néhány évvel ezelőtt már beszélgettem addigi életútjáról, szakmai tevékenységének alakulásáról, most elsősorban a fontosabb változásokról, eredményekről és a terveiről kérdezem.
Professzor Úr! 2026-tól a Pécsi Fogászati és Szájsebészeti Klinika igazgatójának nevezték ki. Milyen tervek és célok fogalmazódtak meg Önben, amikor elvállalta ezt a rangos feladatot?
Tulajdonképpen hallgató korom óta a klinika polgára vagyok, így hallgatóként már láttam és emlékszem arra, amikor Szabó Gyula professzor úr vette át a klinika irányítását, majd 2001-től immár beosztottjaként, 9 évet dolgozhattam vezetése alatt. Szabó professzor úrral 2022-es elhunytáig nagyon jó kapcsolatot ápoltam, mindig a legnagyobb szeretettel gondolt és beszélt egykori kollégáiról, és tenni akarásához sosem fért kétség.
Ezután 2009 őszétől Nagy Ákos lett a klinika igazgatója, akitől 2026-ban én vettem át az irányítást. Így két elődöm működését, módszereit, mentalitását láttam, amiből igyekszem a leginkább előremutató dolgokat megtartani.
Ahogy említettem, lassan már 30 éve folyamatosan, megszakítások nélkül a klinika része vagyok, így elmondhatom, hogy a pécsi fogorvosképzés sorsának alakulása nagyon fontos számomra. Csak egy jól működő klinika, motivált és kvalifikált oktatói kollektíva teremthet stabil alapot a „karosodási” folyamatainknak. Fontosnak tartom a valós működésünket hűen tükröző, nem önálló tanszéki struktúra kialakítását. Emellett elsődleges célom az, hogy a klinika valamennyi alkalmazottja és oktatója a napi működés minden elemében a megbecsülést, a kiszámíthatóságot és következetességet érezze. Az egyetemi közéletben kiemelten fontosnak tartom, hogy mind az Általános Orvostudományi Karral és a Klinikai Központ vezetésével fenntartsuk a harmonikus együttműködésünket, valamint mindent el fogok követni, hogy egyetemünk nemrég megválasztott új rektorával a legnagyobb tisztelet hangján konstruktív, értékteremtő és jövőbe mutató közös célokat valósíthassunk meg. Említette az előzőekben, hogy 2001-től már a Pécsi Fogászati és Szájsebészeti Klinikán dolgozik. Az itt töltött 25 esztendő alatt melyik időszakot tekinti meghatározónak a karrierje szempontjából?
A rezidensi éveimben az akkor még fog- és szájbetegségek szakképzés szerves része volt, hogy egy teljes éven át minden részlegen meg kellett fordulnunk. Így betekintést nyerhettem a fogorvosi tevékenység minden területébe. Már ekkor láttam, hogy a dentoalveoláris sebészet lesz számomra az igazi. Természetesen a fog- és szájbetegségek szakvizsga után, az akkor „ráépített” dentoalveoláris sebészet klinikai szakképzésbe kerüléshez szerencse is kellett. A klinikai alkalmazásomhoz nagymértékben hozzájárult, hogy társaim között kiemelkedő pontszerzést teljesítettem rezidensként. Ezek után, 2006-ban sikeres szakvizsgát tettem dentoalveoláris sebészetből, majd nagyon nehéz időszak következett az életemben. A dentoalveoláris sebészet részlegvezetőjeként – egészen 2012 őszéig – egyedüli szakorvosként tevékenykedtem a részlegen. Számos szakirányú rezidenst képeztem ugyan, de megtartásukhoz valahogy nem kaptam támogatást. Így már akkor eldöntöttem, hogy egy sikeres részleghez mindenképpen nagyobb létszámú csapatért kell harcolnom. Jelenleg már hét szakorvostársammal látjuk el a feladatainkat. 2011-től aztán egyetemi adjunktusként, 2017-től egyetemi docensként vezettem a részleget, illetve 2015-től már az Arc-, Állcsont- és Szájsebészeti Tanszék vezetőjeként a tanszéket is irányíthattam. 2018-tól 2021-ig a Klinika igazgatóhelyettese voltam, és 2023-tól már egyetemi tanárként vezetem a tanszéket.
Korábbi interjúnk során említette, hogy a kutatómunka magától értetődő volt az Ön számára. Hogyan folytatódott, alakult kutatómunkája és publikációs tevékenysége az utóbbi esztendők során?
Szabó Gyula professzor 2005 tavaszán egyik nap bejött a szájsebészet részlegre és megkérdezte, hogy van-e a látókörömben olyan dokumentált beteganyag, amiből közleményt tudnék írni. Látta rajtam, hogy nagyon váratlanul ért a kérdése, így finoman „lekorholt”. Utána azt javasolta, hogy legyen egy „kockás” füzetem, amiben rendszeresen vezetem a vizsgálati céloknak megfelelő adatokat, mert még egy egyszerű retrospektív vizsgálatot is így tudunk megalapozni. Így ezután lett egy kockás füzetem – amelyet a mai napig őrzök –, és két betegcsoportot kezdtem abban vezetni. Az egyik csoport a nyálköves és nyálmirigy-gyulladásos betegek voltak, a másik pedig az idegsérülést elszenvedő bölcsességfog miatt műtött betegek. Előbbiből készült életem


első tudományos kongresszusi előadása 2005 őszén egy Hévízi MAÁSZT kongresszuson, illetve az első magyar nyelvű, a Fogorvosi Szemlében publikált közleményem. Utóbbiból pedig megírtam életem első nemzetközi közleményét. Ezen közlemény teremtett lehetőséget a PhD fokozat megszerzésére, illetve több mint 170 idézéssel a legidézettebb közleményem lett.
A tudományos munka tehát azért is lett számomra teljesen magától értetődő, mert olyan klinikai kérdésfelvetéseim adódtak folyton, amelyek elsősorban a napi munkámból, ténykedésemből adódtak. Ilyen volt a bölcsességfogak eltávolításánál sajnálatosan előforduló nervus alveolaris inferior (IAN) idegsérülés előrejelzésének a kérdésköre is. Sokat olvastam ebből a témakörből, és ha nem kaptam esetleg választ, vagy az nem volt számomra meggyőző, akkor saját



PTE Ünnepi Szenátusi Ülés, 2023
vizsgálatot terveztem, és kitartóan végig is vittem. Ebben a témakörben mind a mai napig publikálok, és fontosnak tartom megjegyezni, hogy ezt a betegcsoportot tevékenyen el is kellett látnom, nem csupán a röntgenfelvételeket elemezgetni.
Az előbb említett kutatómunka eredményei – a későbbiek során – segítették szakmai útjának az alakulását?
Az első két nemzetközi közleményem megadta a PhD értekezésem alapját, mely fokozatot 2011-ben szereztem meg. Ebben az időben Olasz Lajos professzor úr már a nagydoktori anyagán dolgozott, és észrevette, hogy bennem hasonló motivációs elemeket lát. Így felhívta figyelmemet, hogy az nagyon előremutató lenne, ha va -
lamiféle egymásra épülést, kohéziós rendező erőt tudnék a kutatásaim között fenntartani. Tulajdonképpen már Olasz professzor nagydoktori védésén tudtam 2013-ban, hogy ezt én is nagyon szeretném. Időközben, 2016-ban megpályáztam a Magyar Tudományos Akadémia Bolyai ösztöndíját, és sikerült is elnyernem. Nagyon szerettem volna méltón helytállni, rengeteg energiát mozgósítottam magamban, így ez a támogatott időszak nagyot lendített a kutatási eredményeimen. A helytállás azután olyan jól sikerült, hogy 2019-ben – fogorvosként, elsőként – Bolyai-plakettel díjazták a kimagasló pályázati teljesítést. Erre nagyon büszke voltam, hiszen az MTA testületeinél általános módon, a Bolyai-kollégium is az egyik legobjektívebb tudománytámogató testület. Ha szabad, itt fűzném hozzá, hogy feleségem, Lempel Edina professzor volt a második Bolyai-plakettet kiérdemlő fogorvos napjainkig. 2021-ben ezután sikeresen MTA doktora fokozatot szereztem, mely nem meglepő módon szintén a bölcsességfogak témakörében publikált eredményeken alapult. Részben egyéni előrehaladásomnak, részben környezetemben tapasztalható katalitikus hatásnak volt ezután köszönhető, hogy érdemben elkezdhettem dolgozni egy Klinikai Fogorvostudományok Doktori Iskola alapításán.
Doktori értekezését „A bölcsességfogak ellátásának szájsebészeti és fogorvosi szempontjai, valamint a szövődmények megelőzésének a lehetőségei” témakörében védte meg a Magyar Tudományos Akadémián. Dolgozatának mely érdemeit emelné ki, és az azóta kitűzött kutatási céljai közül melyeket sikerült eredményesen folytatni?
A nagydoktori munka érdemei között kiemelném a bölcsességfogakhoz társuló idegsérülési jelek 2 és 3 dimenziós képalkotáson alapuló kutatásait, a koronektómia klinikai és experimentális kutatásait, valamint a dentoalveoláris sebészetre jellemző csontelvételi módok hőtani vizsgálatait. Emellett vizsgáltam a bölcsességfogak hatásait a mandibula töréseknél, illetve a kompozit restaurációk hosszú távú sikerességének megfigyelésével becsültük az előtört, de szuvas bölcsességfogak panaszmentes megtartásának az esélyeit. Az értekezésben bemutatott és megkezdett munka természetesen azóta is aktívan folyik. Így fontos, azóta született eredménynek találom – a COVID-fertőzések apropóján – az effektív aeroszol redukcióval járó restaurációs mód kidolgozását. Emellett egyik PhD hallgatómmal meghatároztuk, hogy mely radiológiai jelekkel azonosíthatjuk és találhatjuk meg – legnagyobb valószínűséggel – a canalist átölelő gyökér-konformációjú bölcsességfogakat már a panorámaröntgen-felvételek segítségével is. Másik PhD hallgatómmal validáltuk a 2019-ben leközölt fúróhüvellyel támogatott koronektómia fogszekciós eljárásunk valós klinikai értékét és használhatóságát. Ugyancsak egy PhD hallgatómmal derítettük ki, milyen klinikai paraméterekkel érdemes használni az autológ csontgyűjtő fúrókat. Emellett meg kell említenem, hogy aktív szereplőivé váltunk négy multicentrikus európai vizsgálatnak is, mely kutatási vérkeringésbe való csatlakozás, nemzetközi láthatóságunk nélkül lehetetlen lett volna.
2024-ben a Magyar Arc-, Állcsont- és Szájsebészeti Társaság elnökének választották. Ez a magas tisztség milyen kihívásokkal és tennivalókkal jár?
Novák Katalin köztársasági elnökkel 2023-ban az egyetemi tanári kinevezéskor.
Dentoalveoláris sebészként ez nagyon nagy meglepetés volt, hiszen társaságunknak eddigi elnökei mind arc-, állcsont-, szájsebész kollégák voltak. Habár tudom, hogy 320 tagunk között többen vannak a „dentós” kollégák, mégis nagyon örültem a választási eredménynek. Tulajdonképpen az elnöki pozícióhoz kiváló előképzést jelentett a 2018 óta már két ciklusban betöltött főtitkári tisztség, miáltal a társaság mindennemű ügyvitelét megismerhettem. Főtitkári időszakomból alapszabályunknak 6 pontban történő módosítását, társasági vagyonunknak 250%-kal történő növelését és tagsági adatbázisunk naprakészre frissítését, továbbá társasági emlékérmünk megújítását tudom említeni. Napjainkban éppen a MAÁSZT alapításának 30 éves jubileumi rendezvényére készülünk, prominens külföldi, nemzetközi meghívott előadókkal, remélem sikeres lesz az idei rendezvényünk is!
Igen gazdag munkásságát kitüntetések, elismerések sora is fémjelzi: a Béres Károly Alapítványi díj (2007; 2008; 2011), a Körmöczi-díj (2012), a Regöly-Mérei-díj (2016), illetve az MTA Bolyai-plakett (2019) kitüntetés. Egyetemén többszörös Kiváló Gyakorlatvezető (2014; 2020) és Előadó (2018; 2019; 2020; 2021; 2022; 2023; 2024; 2025). Mit jelentettek, jelentenek Önnek ezek az elismerések?
Az elismerések és kitüntetések visszajelzések az elvégzett munkáról, az mindig jó érzés, ha az mások szerint így értékelendő. Habár célként sosem a díjak és kitüntetések lebegnek a szemem előtt, csak a tisztes helytállás, de valótlant mondanék azzal, hogy nem örülök ezeknek. Az oktatásért járó elismeréseknek is nagyon örülök, mert tudom, hogy például a „Kiváló előadó" elismerést úgy adják, hogy a végzős hallgatóktól azt kérdezik, egyetemi tanulmányaik egészét tekintve, kit tartanak a legjobb előadójuknak.
Hogyan foglalná röviden össze „ars poeticáját” – orvosi hitvallását?
Azt hiszem, erre a kérdésre nem tudok igazán velőset vagy frappánsat mondani.

Ahogy korábbi interjúmban is említettem, feleségem, Lempel Edina professzor, az MTA doktora, esztétikai és helyreállító fogászattal foglalkozik a klinikánk Konzerváló Fogászat Tanszékén. Nagyon hasonló attitűddel álltunk, állunk hivatásunk kihívásaihoz, ami óriási támogatás. Mindketten úgy gondoljuk, hogy saját előmenetelünk, a publikációkkal megszerzett impaktfaktorok, a támogatott TDK és PhD hallgatók országos sikere vagy sikeres fokozatszerzése, továbbá aktív közéleti tevékenységünk, elnyert pályázataink mind hozzájárulnak saját képzőhelyünk minőségi mutatóihoz. Ezáltal a harmonikus családi élethez szükséges megértés, karrierünk rokon vonásai miatt teljes mértékben jelen lehet.
Zsófia lányom által a lovarda és a lovak is az életünk része lett. Nagyon szeretek dartsozni, az akváriumaimmal bíbelődni, és ha van időm, összedugom a gitárt az effektpedállal. De az örök rajongás, a motorozás is velem marad, amíg csak lehet! Ha minden jól alakul, tavasszal talán sikerül az első orvoskari motorostalálkozót is megszervezni!
Professzor Úr! Ismételten köszönöm ezt a rengeteg információt adó, igen tartalmas beszélgetést, most is sok mindent megtudhattunk életútjának utóbbi esztendőiről, példaértékű kutatói tevékenységéről.
Szerkesztőségünk nevében gratulálunk klinikaigazgatói kinevezéséhez, további eredményes munkát és sikereket kívánunk!
betartását.
A betegek ellátása során igyekszem mindenkit úgy kezelni, mintha közeli hozzátartozóm lenne, ezt időnként nem árt magunkban újra és újra tudatosítani.
A sok-sok feladat, teendő mellé hogyan illeszthető a harmonikus családi élet? Mivel tölti legszívesebben a szabadidejét?

Szakmai rendezvény megnyitó, 2026

É V E S E L Ő F I Z E T É S

4 1 0 0 0 F T 2 5 0 0 0 F T

DENTAL PRESS





ÁLLÁSOK KURZUSOK
CÉGEK
ELADÓ, KIADÓ RENDELŐK
HASZNÁLT TERMÉKEK, BERENDEZÉSEK
DENTAL PRESS
FOGORVOS KERESŐ
Dr. Sean Chiu (Amerikai Egyesült Államok)
AZ IMPLANTÁCIÓ SIKERESSÉGÉNEK NÖVELÉSE
AZ ALVEOLUS KETTŐS
HULLÁMHOSSZÚ LÉZERES
ELŐKEZELÉSÉVEL
Jelen esettanulmányban szeretnénk az általunk használt kettős hullámhosszú lézer módszer (2940 nm-es Er:YAG és 1064 nm-es Nd:YAG) alkalmazási területeire összpontosítani, illetve bemutatni hatékonyságát és kedvező hatását az implantáció sikerességére. Egy implantáció akkor sikeres, ha csökkenteni tudjuk az implantátum körül kialakuló gyulladások (periimplantitis, periimplantáris mucositis), az implantációs sikertelenség és a posztoperatív szövődmények kockázatát, illetve ha növelni tudjuk a csontba behelyezett implantátum hosszú távú stabilitását.
Az Er:YAG lézerről korábban már kimutatták, hogy eredményesen lehet használni granulációs szövet eltávolítására mind lágyszövetben, mind csontban, valamint az implantáció helyének fertőtlenítésére is. Ezen felül alkalmas az osteotomia felszínének felérdesítésére, amely növeli a sejtek adhézióját és ezáltal elősegíti a gyógyulást.
Az implantátumot körülvevő csont dekortikálása Er:YAG lézerrel serkenti a vérkeringést, a gyógyulást, illetve a különböző graftok megtapadását. Az Er:YAG lézer használatakor kicsi a csontszövet túlmelegedésének és karbonizációjának veszélye, mivel csupán a felszíni rétegekben fejt ki ablációs hatást, illetve a vízhűtés is tovább csökkenti
a fejlődő hő mennyiségét. Azt is megállapították erről a lézerről, hogy felszíni fotobiomoduláló hatással bír.
Az Nd:YAG lézer mélyebb fertőtlenítésre alkalmas; csökkenti a parodontopatogén csíraszámot a kortikális csontban fogeltávolítást követően, illetve ha a csontból és az alveolusból nem sikerül teljesen eltávolítani a sarjszövetet. Számos tanulmány támasztja alá azt a megfigyelést, hogy a hagyományos fúróhasználat lézerekhez képest fokozottabb hőképződéssel jár. Emiatt nő a csontnekrózis veszélye, lassul a csont gyógyulási sebessége és a titániumimplantátumok osszeointegrációja, fokozódik a gyulladás, és csökken az implantátumok mechanikai és biológiai stabilitása.
Esetbemutatás
A páciensnek enyhe fokú magas vérnyomása volt, amelyre a következő gyógyszereket szedte: ramipril (angiotenzin-konvertáló enzimgátló), propranolol (béta-blokkoló) és amlodipin (kalcium-csatorna blokkoló). Ezen felül Parkinson-kórban is szenvedett, amelyre levodopa/carbido -
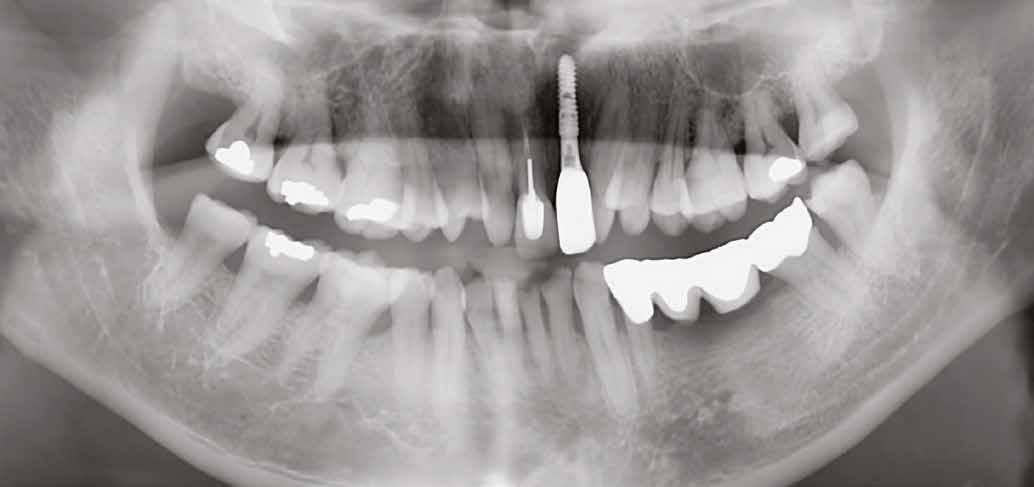
1. ábra: Kiindulási panorámaröntgen.
pat kapott. Korábban számos fogászati kezelésen esett már át (1. ábra) . A páciens szájhigiénéje kielégítő volt, naponta kétszer mosott fogat, fogselymet azonban csak hetente egyszer-kétszer használt. Generalizált, krónikus parodontitisben szenvedett. A klinikai tapadás növelésére, a tasakmélységek csökkentésére és a parodontális csont regenerációjának elősegítésére a páciensnél TwinLight lézer-asszisztált parodontális tisztítást végeztünk, amely módszer ötvözi az Er:YAG és az Nd:YAG lézerek használatát (Fotona).
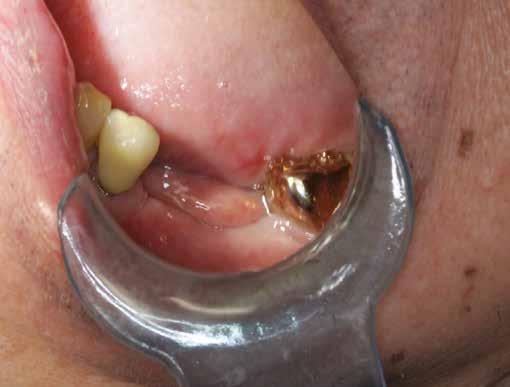
A 34–37 fogak között egy több mint tíz éve készült híd volt, amelyet a distalis pillér kiterjedt szekunder mesialis cariese miatt kellett cserélni (2. ábra) . A páciens kívánságára a régi hidat a mesialis pillér mögött átvágtuk és eltávolítottuk, megtartva a 34 fogon a korábbi koronát. A 37 fog, megfelelő tisztítást és előkészítést követően egy új öntött aranykoronát kapott, a korábbi foghiányok (35 és 36) területére pedig két implantátum beültetését kérte a páciens. A kezelési terv alapján a beültetés előtt Er:YAGés Nd:YAG-lézer kezeléssel elvégeztük az osteotomiák degranulációját, felszínmódosítását és fertőtlenítését.
A kezelés
A páciens a műtétet megelőző napon antibiotikus profilaxisban (2 g amoxicillin szájon át) részesült, valamint 0,12%os klórhexidin oldattal öblített közvetlenül a beavatkozás előtt. A bal oldali n. alveolaris inferiorhoz vezetéses érzéstelenítést (egy ampulla 4% artikain-hidroklorid és 1:200 000 adrenalin), a beavatkozástól lingualisan és buccalisan helyi érzéstelenítést (egy-egy ampulla 2% lidokain és 1:100 000 adrenalin) adtunk. A pácienstől a helyszínen vért vettünk, amelyből előállítottunk három cső L-PRF (leukocytában és vérlemezkében gazdag fibrin; 2700/perc fordulatszámon 12 percig centrifugálva; EBA 200, Hettich) és egy fehér cső F-PRF (hajtogatott PRF; 155/perc fordulatszámon 3 percig centrifugálva) készítményt.
Egy 15-ös szikepengével gerincéli metszést ejtettünk, majd segédmetszés nélkül, teljes vastagságban (mucope -
riostealisan) lebenyt preparáltunk a 34-től a 37-es fogig. Az implantátumok helyét egy előzetesen elkészített sebészi sablon segítségével határoztuk meg és készítettük elő a megfelelő előfúrókkal 800/perc fordulatszámon, közepes fiziológiás sóoldatos vízhűtés mellett. A 35 helyén egy hagyományos átmérőjű jelölőfúróval fúrást ejtettünk, majd tovább tágítottuk az osteotomiát 3,5 és 4,0 mm átmérőig, 7 mm mélységben. A 36 helyén széles átmérőjű jelölőfúróval kezdtük a preparálást, majd folytattuk 3,5 és 4,5 mm átmérőig, 7 mm mélységben. Az implantátumok behelyezése előtt mindkét furatot lézerrel kezeltük elő.
Lézer paraméterek
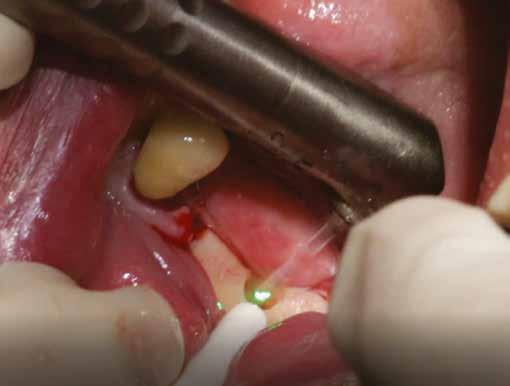
A következőkben bemutatjuk az itt használt Er:YAG és Nd:YAG lézer rendszert (LightWalker AT S, Fotona). A furatok körül a felszíni granulációs szövet eltávolítására, illetve a lágy- és a keményszövetek ablációjára és fertőtlenítésére az Er:YAG H14 kézidarabot használtunk, amelyhez egy cilindrikus 12/1,3 száloptikás fej csatlakozott. A készüléket SP (short pulse, rövid pulzálás) módban, 160 mJ és 20 Hz beállítás és 5:4 víz–levegő arányú hűtés mellett alkalmaztuk (3. ábra) . A degranulációnak köszönhetően a csontból és annak környezetéből minden lágyszövetet eltávolítottunk. Ezt követően ugyanazt a készüléket (Er:YAG H14 kézidarab, cilindrikus 12/1,3 szál optikás fej) használtuk, de MSP (micro-short pulse, mikro-rövid pulzálás) módban, 50 mJ és 30 Hz beállítás és 5:4 víz–levegő arányú hűtés mellett. Fertőtlenítettük az osteotomia belső felszíneit, egyidejűleg konzervatív módon megnyitva a szivacsos csontállomány lacunáit a falak mentén. Ez utóbbi kíméletes beállításával nem fenyeget annak veszélye, hogy szivacsos csontot távolítunk el, amely kockáztatná az implantátum stabilitását és behelyezhetőségét. Csökken a gyulladás veszélye, gyorsul a sebgyógyulás, nagyobb csont–implantátum kontaktust (BIC, bone-to-implant contact) és primerstabilitást érhetünk el, illetve módosítani tudjuk a felszínt, elősegítve ezzel a sejtek tapadását. A mélyebb fertőtlenítésr e Nd:YAG lézert alkalmaztunk : 300 μm-es száloptikás véget MSP módban, 2 W és 20 Hz beállítás mellett (4. ábra) . Segítsé -
2. ábra: A beavatkozás helye a műtét előtt. – 3. ábra: Az implantátum helyének degranulációja Er:YAG lézerrel.
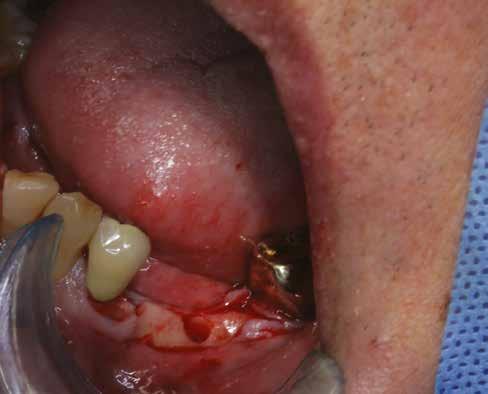
4. ábra: Az osteotomia helye közvetlenül a lézeres kezelést követően.
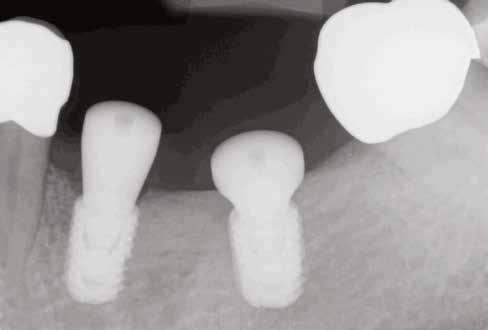
5. ábra: Kontrollröntgen 45 nappal a beavatkozást követően.
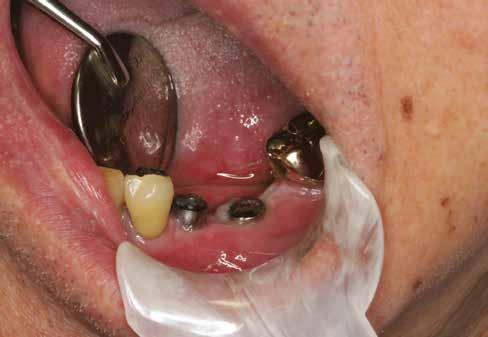
6. ábra: A lágyszövet primer záródása a 45. napon szinte teljes.
gével csökken a parodontopatogén baktériumok száma, amelyek egyébként gátolhatják az osszeointegrációt. Az osteotomiáknál ügyeltünk a vér elszívására, hogy ne zavarja az Nd:YAG lézer működését. Mivel az előfuratokból bő vérzést tapasztaltunk, lézeres dekortikalizációt külön már nem végeztünk. A fenti lépések lehetővé tették, hogy kihagyjuk a hagyományos fizikális kürettázst, így időt spóroltunk és a páciens számára is komfortosabb volt a beavatkozás.
Sebészi sablon segítségével a 35 fog helyére 4,5 ×7,0 mm méretű, a 36 fog helyére 5,0 ×7,0 mm méretű Hiossen ETIII SA (Osstem Implant) implantátum került behelyezésre. A 35-re hosszú nyakú 5×5 mm-es, a 36-ra 6×5 mm-es Hiossen gyógyulási fejek kerültek, amelyeket kézzel húztunk meg. Előzetesen a gyógyulási fejek alá mindkét implantátumnál L-PRF került. A sebet Cytoplast PTFE (politetrafluoretilén, teflon) varratokkal zártuk.
Posztoperatív
utasítások és fájdalomcsillapítás
A sebek gyógyulásának serkentésére és a fájdalom csillapítására fotobiomodulációs kezelést végeztünk a páciensnél két alkalommal, két nap kihagyással. Ehhez a Genova Nd:YAG lézer készüléket használtuk 1-1 percig MSP módban (0,5 W/cm 2 és 10 Hz beállítás) figyelve, hogy az implantátumokhoz közvetlenül ne érjünk.
A műtétet követően a páciens egy hétig szedett antibiotikumot (500 mg amoxicillin) és öblített 0,12% klórhexidin oldattal. Fájdalomcsillapítóra (400 mg ibuprofen) csupán a műtétet követő két napban, összesen két alkalommal volt szükség.
Megfigyelések és eredmények
A páciens a műtét teljes ideje alatt panasz- és fájdalommentes volt. A gerincéli metszés, illetve a lebeny preparációja enyhe vérzéssel járt. A hagyományos előfúrást követően az osteotomiák helyén mérsékelt volt a vérzés. Az Er:YAG lézerrel végzett degranuláció és felszínmódosítás már fokozottabb vérzést eredményezett a csont felszínén. A vérzés végül az implantátumok behelyezésekor alábbhagyott, az L-PRF membránok és a gyógyulási fejek felhelyezésével teljesen megszűnt.
A páciens a műtétet követően két napig tartó enyhe idült fájdalomról és duzzanatról számolt be, ami idővel folyamatosan oldódott. A második fotobiomodulációs kezelés, két nappal a műtétet követően, tovább enyhítette a gyulladást és a fájdalmat. Ekkor már a seb per primam záródása is megkezdődött. A varratokat három hét elteltével távolítottuk el, ekkor már se duzzanat, se vérzés nem volt tapasztalható. Negyvenöt nap elteltével a lágyrészek még mindig gyógyulófélben voltak, a per primam záródás majdnem teljesen lezajlott, a páciensnek panasza nem volt (5–6. ábra).
Összefoglalás
A kettős hullámhosszú, Er:YAG és Nd:YAG lézer módszer elengedhetetlen az implantáció hosszú távú sikeréhez, mivel elősegíti az osteotomia degranulációját, felszínmódosítását, fertőtlenítését és fotobiomodulációját.
Forrás: Implants 2023/1

Dr. Beat R. Kurt (Svájc)
IRÁNYÍTOTT SEBÉSZI MUNKAFOLYAMAT
A KISZÁMÍTHATÓ TERVEZÉSTŐL
AZ IMPLANTÁCIÓIG
A 62 éves férfi páciens ajánlás útján érkezett rendelőnkbe. Négy felső metszőfogával voltak panaszai, amelyek egy 30 évvel korábbi balesetből kifolyóan gyökérkezelésen, illetve különböző protetikai beavatkozásokon estek át. Mind a négy fog panaszos volt, a 2.1-es fognál mobilitást tapasztaltunk, amelyet a páciens is megerősített (1. a–b ábra)
Először egy Cone Beam CT-felvétel (CBCT) készült a felső fogívről, amelyen látszott a 1.2–2.2 fogak periapikális gyulladása (2–3. ábra) . Ezenfelül a 2.1-es fog bukkális oldalán kiterjedt csonthiány, valamint a gyökércsúcs felett egy kis darab amalgám is látható volt, amely feltehetően a 2.1-es fogból származott. A felvételek alapos elemzését követően úgy döntöttünk, hogy a kezelés során eltávolítjuk a 1.2–2.2-es fogakat és alveolus prezervációt végzünk, hogy minimalizáljuk a fogeltávolítás következtében fellépő csonthiányt.
A rendelőnkben szokásos protokoll szerint digitális lenyomatot vettünk az alsó és felső állcsontokról a DEXIS IS 3800 intraorális szkennerrel (4. a–c ábra). A kiindulási állapot rögzítésére szájfotókat is készítettünk. Az ideiglenes kivehető fogpótlás ezekre a digitális mintákra készült.
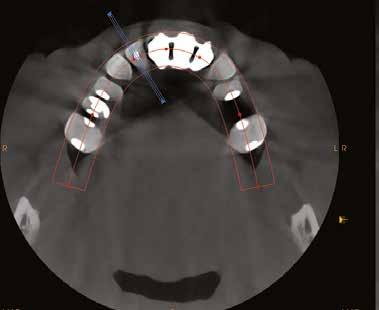
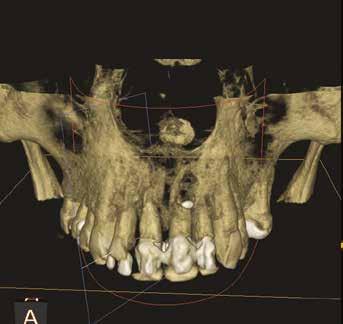
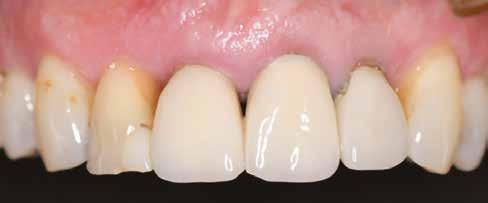
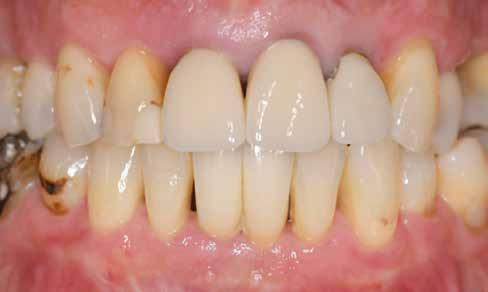
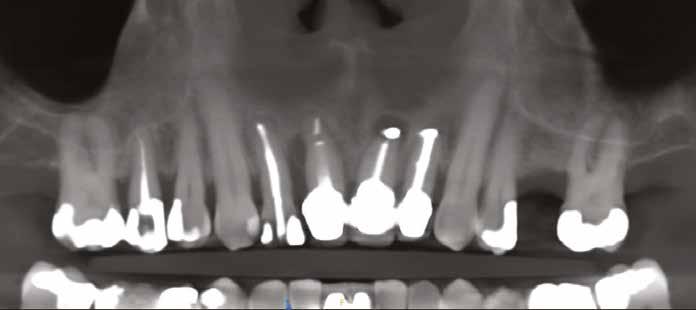
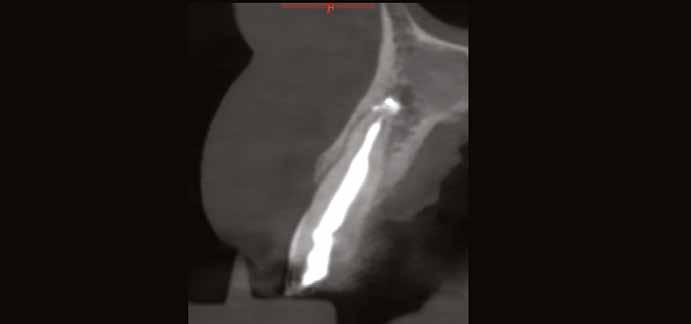
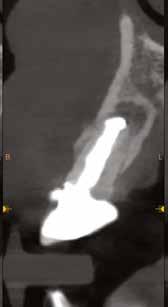
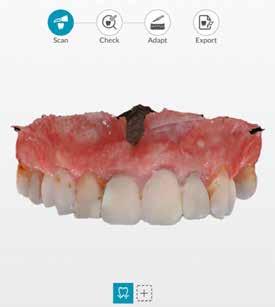
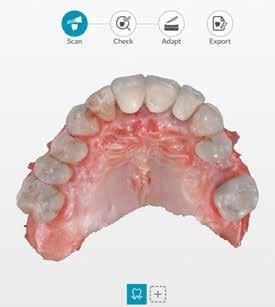
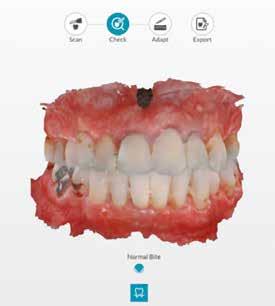
3. ábra: Kiindulási CBCT, a 21-es fognál koronális nézetből jól látszik a bukkális csonthiány. – 4. a–c. ábra: A kiindulási állapotról készült digitális lenyomatok.
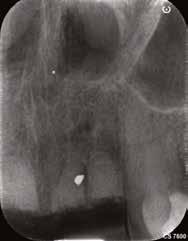
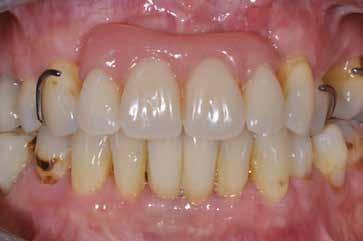
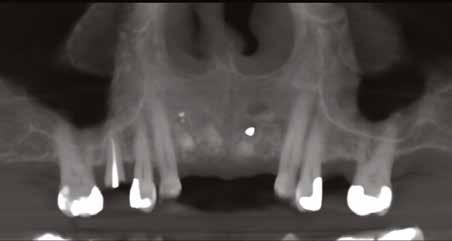
5. ábra: A fogeltávolítást és alveolus prezervációt követő kontrollröntgenek. – 6. ábra: A szájba helyezett ideiglenes fogpótlás. 7. ábra: A fogeltávolítást követően készült CBCT-felvétel.
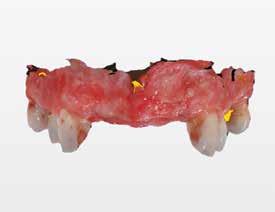
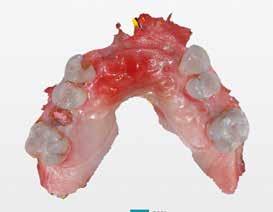
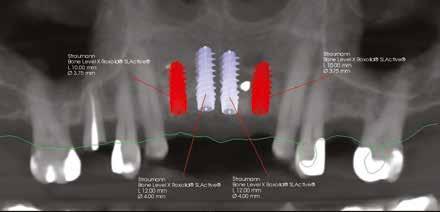
8. a–b. ábra: A fogeltávolítást követően készült digitális lenyomatok. – 9. ábra: A négy lehetséges implantátumpozíció elemzése.
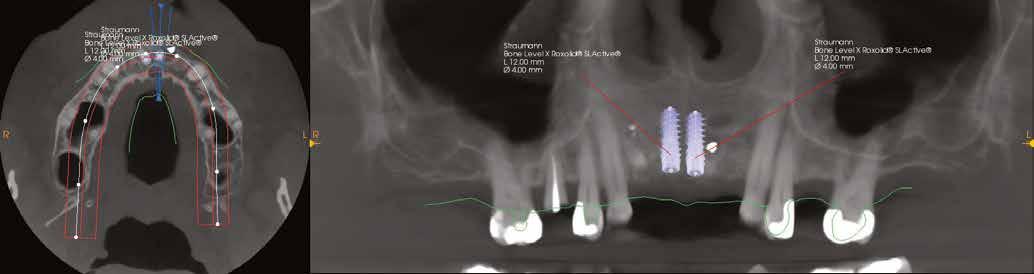
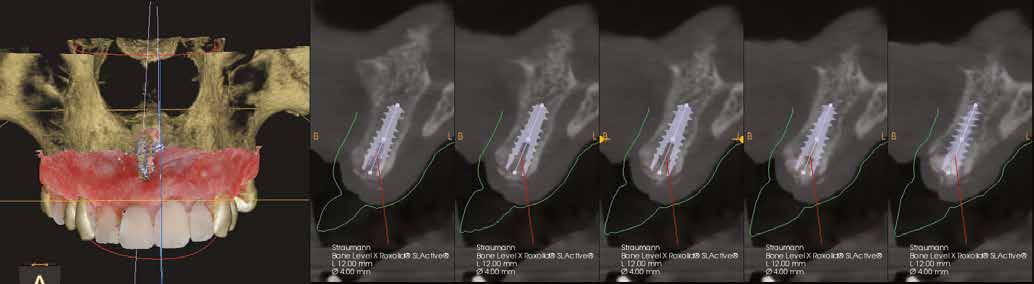
10. ábra: Végső tervezés: a két implantátum pozíciójának meghatározása a CBCT és a digitális lenyomatok egymásra vetítésével.
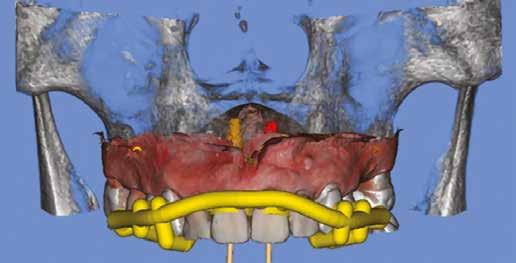
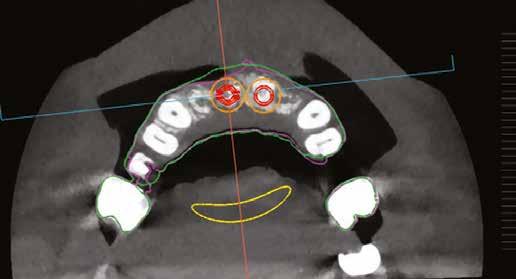
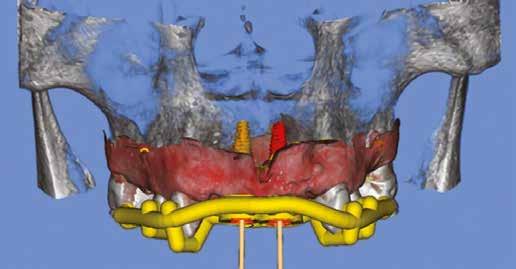
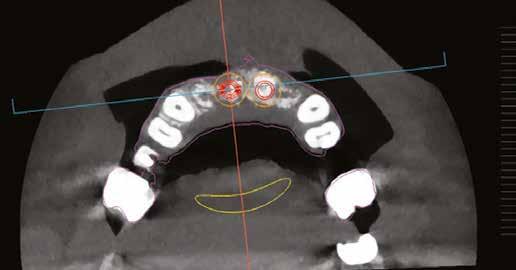
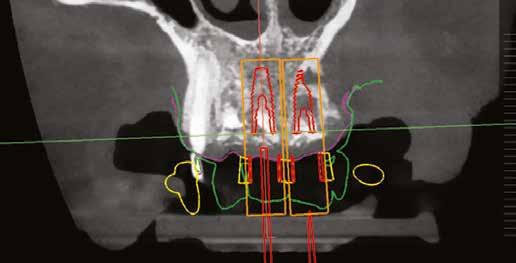
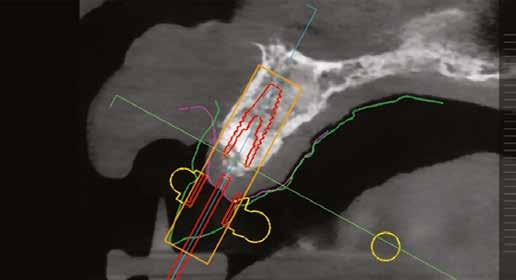
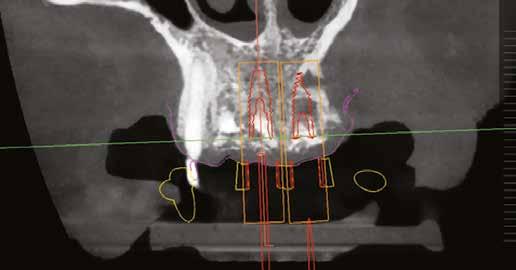
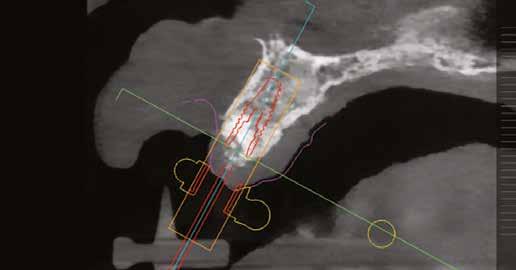
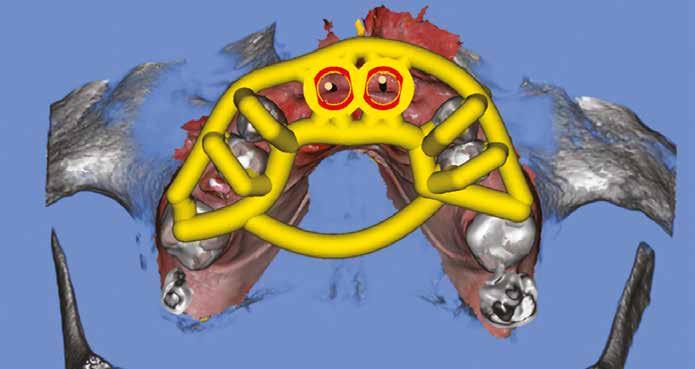
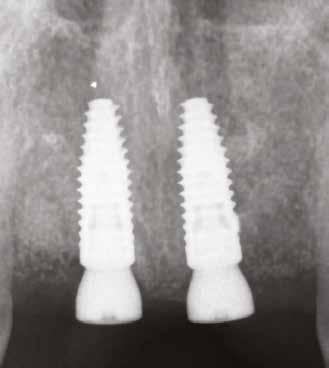
11. a–c ábra: Az implantátumok pozicionálása és a sebészi sablon megtervezése. – 12. ábra: Kontrollröntgen a behelyezett implantátumokról.
11a
11b
11c 12
Miután a páciens egészségbiztosítója jóváhagyta a kezelési tervet, a négy frontfog eltávolításával megkezdtük a terápiát. Miután ez megtörtént, az alveolusokat EthOss degranulációs fúrók segítségével alaposan kitisztítottuk, majd EthOss csontpótlóval töltöttük ki a gyökerek helyeit, hogy segítsük a seb primer záródását és a gyógyulását (5. ábra).
Annak érdekében, hogy a fogeltávolítás és a végleges pótlás átadása közti időben biztosítani tudjuk a páciens számára az esztétikus megjelenést és a funkcionalitást, ideiglenes, kivehető fogpótlást készítettünk (6. ábra) Mivel a pácienst beküldő fogorvos szintén évek óta digitális eszközökkel dolgozott, az ideiglenes pótlások digitális lenyomatokra és 3D nyomtatott mintákra készültek.
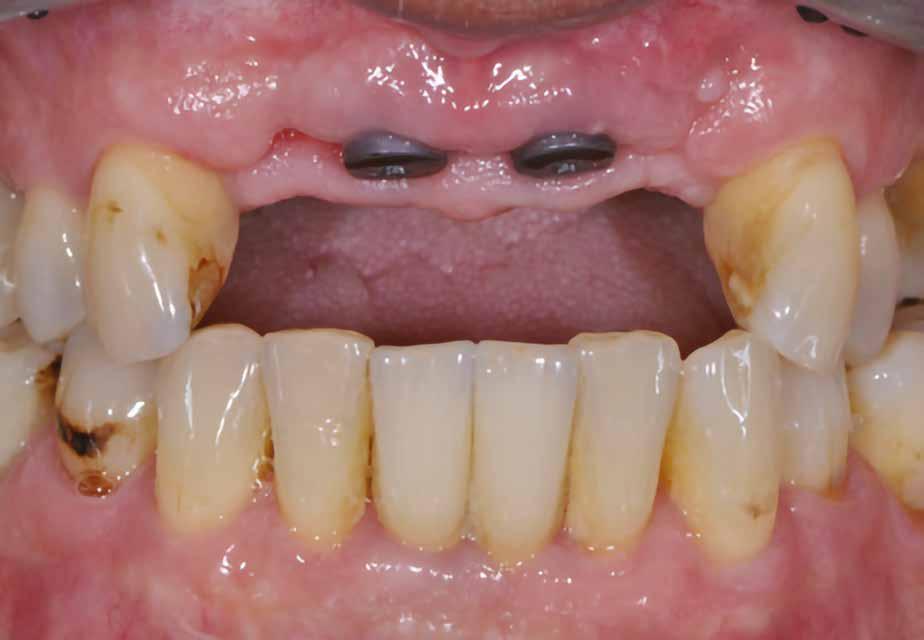
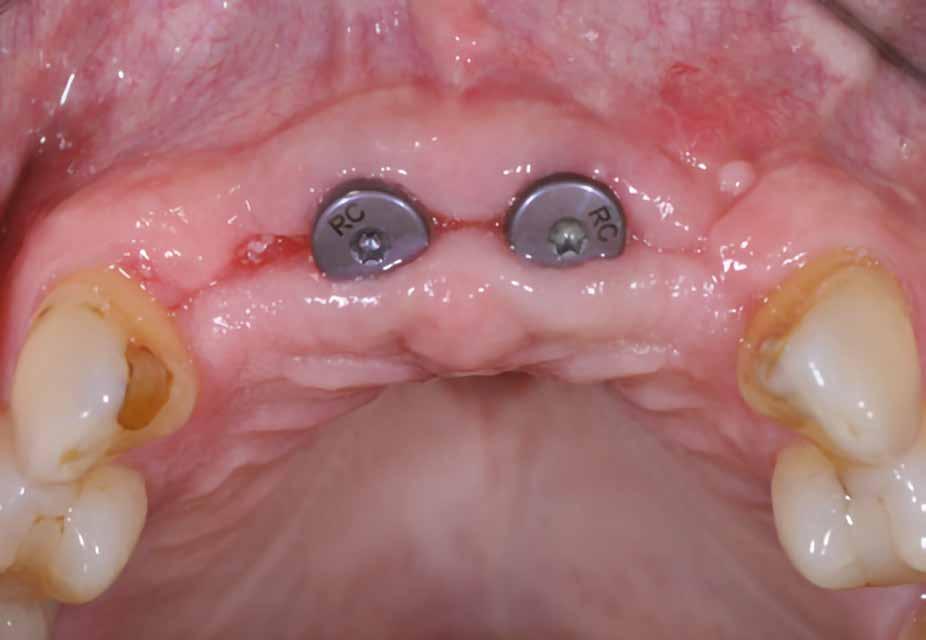
Két hónappal a fogeltávolítást követően készült egy újabb CBCT a felső állcsontról (7. ábra), illetve ismét vettünk egy digitális lenyomatot a DEXIS IS 3800 intraorális szkenner segítségével (8. ábra) . Ezek a lépések nélkülözhetetlenek az implantátumok helyének megtervezéséhez, illetve a sebészi sablon elkészítéséhez. A 3D szoftveres tervezés során az implantátumok pozícióinak meghatározása elsősorban a protetikai szempontok szerint történt (9–10. ábra). A sebészi fúrósablont is ennek megfelelően, egy sebészi sablonok tervezésére alkalmas szoftverrel terveztük meg és készítettük el (11. a–c ábra) . Mind a négy hiányzó fog területét megvizsgáltuk, majd kiválasztottuk azokat a legoptimálisabb és legjobban hozzáférhető területeket, ahova két implantátum és egy hídpótlás kerülhet.
13. a–b ábra: A behelyezett implantátumok és a gyógyulási fejek intraorális nézetből.
megfelelő gyógyulása és integrációja érdekében a bukkális csontot ismét augmentáltuk EthOss csontpótlóval, majd zártuk a sebet úgynevezett félig zárt (semi-submerged) technikával (13. a–b ábra)
A tervezési fázist követően egy sebészi fúrósablont készíttettünk Stratasys 3D nyomtatóval, MED610 rezinből (Stratasys). Ezt követően behelyezésre került két implantátum (4,1 x 12,0 mm, Straumann Bone Level, Tapered, Regular CrossFit, SLActive, Roxolid), a precizitást a Straumann Guided Surgery szettje biztosította. A 2.1es fog gyökércsúcsa feletti csontban található amalgámdarabot óvatosan eltávolítottuk, egy apró szemcse maradt csupán az ínyben (12. ábra) . Az implantátumok
A tízhetes gyógyulási idő leteltével ellenőriztük az implantátumok stabilitási hányadosát (ISQ). A következő lépés a végleges fogpótlás elkészítése, amelyet a páciens beküldő fogorvosa fog végezni. A csavarral rögzülő monolitikus hídpótláshoz a lenyomat intraorális szkennerrel készül, valamint a fogtechnikai lépéseknél is törekedni fognak a lehető legnagyobb mértékű digitalizálásra.
Forrás: Implants 2023/4
Dr. Cosmin Dima, Iulia Florea (Románia)
IMPLANTÁTUM KÖRÜLI LÁGYSZÖVET-
DEFEKTUS KEZELÉSE A „SNAKE
TECHNIQUE” ALKALMAZÁSÁVAL
Az implantátum körüli lágyszövetdefektusok (papilla hiánya, csökkent lágyszövettérfogat, ínyrecesszió, dehiszcencia, színeltérés) kialakulása viszonylag gyakori komplikációnak számít és befolyásolja az implantátum hosszú távú stabilitását, valamint az esztétikai eredményt (1, 2). Számos tényező befolyásolhatja az ilyen defektusok kialakulását. Csontvesztés a faciális falon, illetve a vékony biotípus elősegítheti egy esetleges implantátum körüli recesszió kialakulását (3). A két milliméternél vékonyabb lágyszövet pedig fokozottabb marginális csontvesztést okozhat (4, 5), amelynek következményeképpen az implantátum szabaddá válhat. Ha az ínyrecesszió mellett nem elegendő a keratinizált íny mennyisége, úgy nehezebb azt megfelelően tisztítani, ami gyulladáshoz és esztétikai problémákhoz vezethet (6). Lágyszövet-augmentációt alkalmazhatunk az implantátum felszabadításakor, azonnali implantációval együtt, papillák rekonstrukciójához, keratinizált ínyszélesítéshez, biotípus-vastagításhoz és a gerinckontúr helyreállításához egyaránt (7).
Egyre nagyobb az igény az implantátum körüli lágyszövetdefektusok kezelésére, mivel azonnali implantáció után gyakran alakulhat ki ínyrecesszió, a szövetek átépülése miatt. Vékony lágyszövet (< 2 mm) esetén szürkésen áttűnhet az implantátum vagy a felépítmény, illetve a lágyszövet hegesen gyógyulhat, ami egyaránt lágyszövet-korrekciót tehet szükségessé (8, 9, 10).
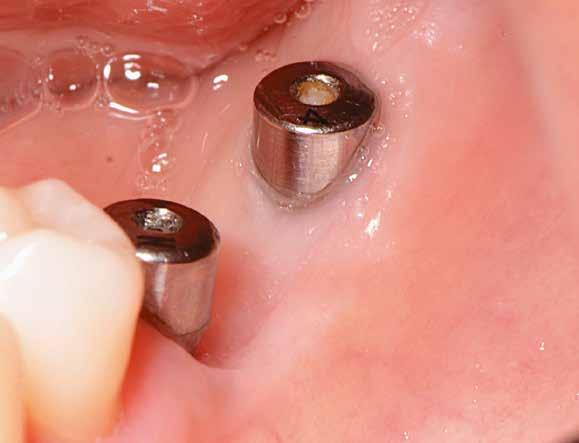
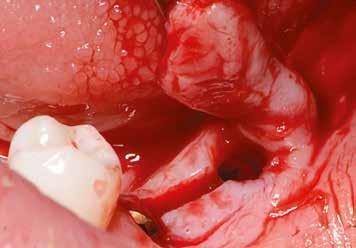
1. ábra: A műtét előtti szituáció, megfigyelhető az implantátumok közötti konkáv terület, ahova könnyen beragad az ételmaradék, és könnyen kialakul a periimplantitis.
Számos sebészi technikát, valamint sebészi és protetikai módszerek kombinációját leírtak már az ilyen defektusok kezelésére. Sok érvet találhatunk, amely az implantátum felszabadításakor (second-stage surgery) a periimplantáris nyálkahártyán végzett beavatkozások mellett szól. Az irodalmi áttekintés leszögezi, hogy esztétikai régióban, illetve a megfelelő plakk-kontroll érdekében szükséges a keratinizált íny regenerációja, hogy az implantátum körüli szövetek stabilitása biztosított legyen (11). A lebeny kialakítása a következőktől függ: az ínyrecesszió kiterjedése, a vesztibulum mélysége, a nem elmozduló nyálkahártya szélessége és az interproximális szövetek térfogata (1). A klasszikus sebészi módszereknél általában apikálisan vagy laterálisan eltolt lebenyeket használunk az implantátum felszabadításakor. Ezeket a technikákat kombinálhatjuk szabad ínylebeny (free gingival graft) átültetéssel, amikor a keratinizált mukóza szélessége minimális. Az apikálisan eltolt lebeny vagy vesztibulumplasztika kombinálása szabad ínylebennyel vagy szubepiteliális kötőszöveti grafttal az egyik legjobban kutatott technika. Az eredmények alapján 1,15 ± 0,81 mm és 2,57 ± 0,50 mm közötti keratinizált ínyszélesség nyerhető, valamint megfelelően fedhető a szabaddá vált implantátumfelszín (12). A keratinizált íny szélesítéséhez apikálisan eltolt lebeny kollagén mátrixszal kombinálva kisebb morbiditást jelent és a műtét ideje is rövidebb, illetve szinte ugyanolyan hatékony, mint a szabad ínylebennyel végzett műtétek (13). Szuprakresztális és/vagy dehiszcencia típusú defektusok esetén is alkalmazhatóak a szabad autológ epiteliális graftok (14). Az autológ graftot alkalmazó módszerek sokkal hatékonyabbak az implantátum körüli lágyszövet-vastagításban és az esztétika javításában, mint a graft nélküli eljárások (15, 16). Egy szisztematikus irodalmi áttekintés megállapította, hogy az ínyvastagításra alkalmazott autológ graftok jelentősen csökkentik a marginális csontvesztést hosszú távon, valamint apikálisan eltolt lebennyel kombinálva megnövelik a keratinizált íny szélességét, ami jobb szondázási vérzésindexet eredményez és a marginális csontszintváltozás sem lesz annyira drasztikus (17). Az imént leírt technikákkal kiváló eredmény érhető el az implantátumok körül, azonban figyelembe kell vennünk a velük járó morbiditást (seb a donorterületen, ami leggyakrabban a szájpadlást jelenti), a dinamikus lágyszöveti változásokat (recidíva) és a hosszabb gyógyulási időt. Ezekkel a technikákkal kompenzálható a volumenveszteség és kezelhetők a kisebb recessziók, azonban kevésbé egyértelmű mélyebb vagy nagyobb recessziók és a papillavesztések kezelése (1). Ezeket a nehézségeket elkerülhetjük nyeles epitelizált vagy nyeles kötőszöveti lebenyekkel kollagén mátrix alkalmazásával vagy anélkül (18). A
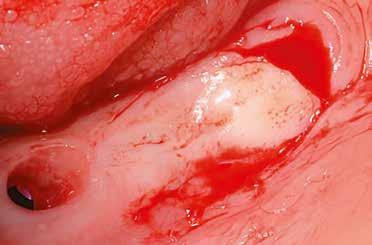
nyelezett lebeny technikák egy viszonylag új, minimálinvazív eljárásnak minősülnek. Ilyen műtétet el lehet végezni az implantációkor vagy a felszabadításkor, egy vagy több implantátum esetén is és front- vagy hátsó területen egyaránt (18). A nyelezett lebeny azoknál az eseteknél javasolt főleg, ahol már volt valamilyen sikertelen implantációs kezelés, illetve teljesen fogatlan pácienseknél, ahol több implantátum mellett is szükséges kötőszövet-átültetést végezni (18). Pandolfi leír egy módosított lebenykialakítást (ómega görgetett borítéklebeny), ahol kombinálja a görgetett lebenyt a módosított zsebtechnikával, hogy korrigálja a helyi horizontális gerincdefektust, és hogy megnövelje az implantátum körüli lágyszövet vastagságát (20). Ezzel az eljárással elkerülhető az autológ kötőszövetvétel, így nincs szükség donorterületre, azáltal, hogy az implantátum feletti szuprakresztális kötőszövetet használjuk fel. Tabanella leír egy bukkális nyelezett lebeny technikát, ami mind front-, mind moláris területen használható legalább két szomszédos implantátum esetén (18). Ez a technika egy lingválisan/palatinálisan vezetett parakresztális metszéssel indul, majd egy-egy paraszulkuláris metszéssel folytatódik meziálisan és disztálisan.
Ezután félvastag lebenyt preparálunk, amit apikálisan eltolunk, így a szövettöbblet egy kissé felgyűrődik, ezáltal vastagítva a bukkális szövetet.
Moreno Rodriguez és Caffesse egy ún. laterális elforgatott lebenyt javasol a defektusok fedésére (21). A technika magába foglalja egy recipiens terület kialakítását a bukkális
defektustól apikálisan, ezt követően az ettől disztálisan és kresztálisan lévő keratinizált ínyt forgatjuk be kb. 90 fokkal (diszto-palatinális irányból), majd rögzítjük az implantátum bukkális oldalán (21, 22). Az alábbi írás célja, hogy bemutasson egy új sebészi eljárást, a „Kígyó” módosított nyelezett lebenyt, az implantátum körüli lágyszövet-kondicionálásra osszeointegrálódott implantátumok körül, a mandibula hátsó részén.
Esetleírás
Egy 47 éves páciens jelentkezett nálunk egy alsó, hátsó foghiánnyal, ahol jelentős csontfelszívódást tapasztaltunk a moláris fogak korábbi eltávolítása miatt (1. ábra). Két implantátum körül is volt ínyrecesszió, illetve a keratinizált íny mennyisége minimális volt (kevesebb mint 1 mm). 4 hónappal az implantációt követően ínykorrekciót végeztünk.
Sebészi technika
Helyi érzéstelenítést végeztünk a műtéti területen artikain és 1:100 000 adrenalin segítségével. A recipiens területet előkészítettük, élesen disszekciót végeztünk, hogy egy izomtapadástól mentes periosteum ágyat képezhessünk. Ettől disztálisan két párhuzamos parakresztális metszést végeztünk egy 15C-s szikepengével, majd a metszéseket egy
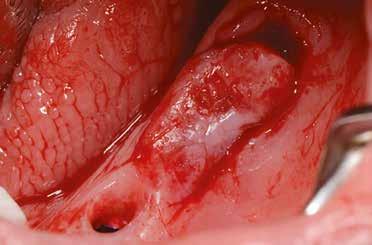
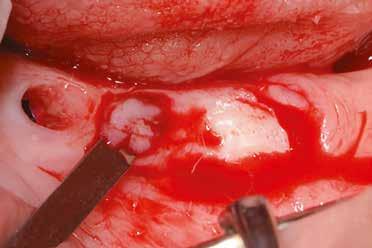
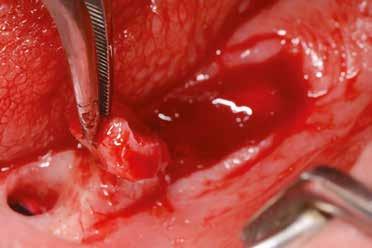
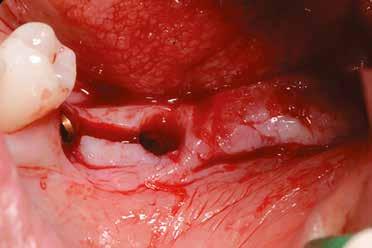
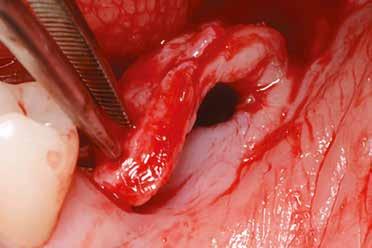
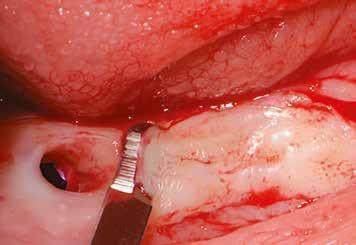
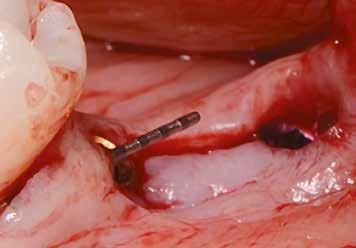
2–5. ábra: A metszések és a deepitelizáció. – 6–9. ábra: Félvastag lebeny. – 10. ábra: A nyelezett ínylebeny „bepróbálása”.
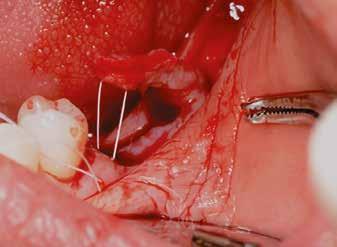
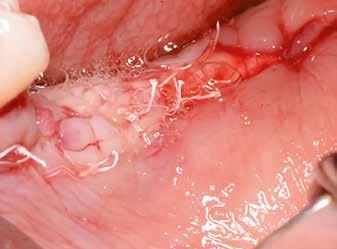
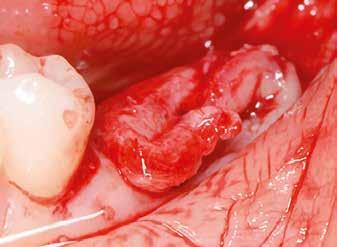
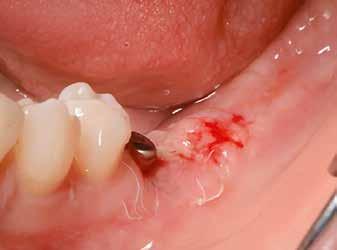
horizontális metszéssel kötöttük össze (2–5. ábra). A metszések hosszát és a köztük lévő távolságot minden esetben a lágyszövet-augmentációhoz szükséges keratinizált szövet határozza meg. A lebeny deepitelizációját egy 15C-s szikepengével végeztük (6. ábra). Ezt követően félvastag lebenyt preparáltunk (7. ábra). A lebenyt apikálisan, az alapjáról belső, felületes metszéssel felszabadítottuk, hogy passzívan áthelyezhessük és rögzíthessük, feszülés nélkül. Meziális irányba 180 fokkal átforgattuk (8–9. ábra). A meziális papillát alagúttechnikával (tunnelling technique) készítettük elő a graft befogadására (10. ábra). Az így kialakított lebenyt a recipiens ágyban rögzítettük az újonnan kialakított vesztibulum alapjánál 5-0 nem felszívódó PTFE (Coreflon, IMPLACORE) varratokkal. A graftot behajtottuk az ínyszél alá és meziális oldalon rögzítettük PTFE varratokkal (11–14. ábra) A műtétet követően napi kétszeri, 0,12%-os klórhexidin tartalmú szájvízzel történő öblögetést javasoltunk a páciensnek, két héten keresztül. Gyulladáscsökkentésre 8 óránként 400 mg Ibuprofént javasoltunk, három napon keresztül. A páciens elmondása szerint sem fájdalmat, sem különösebb diszkomfortot nem tapasztalt. Ezt követően, további 4 héten keresztül, 0,2%-os klórhexidin tartalmú szájvízzel történő öblögetést javasoltunk a betegnek és instruáltuk, hogy lehetőleg ne mossa fogkefével az érintett területet. A varratokat egy héttel később távolítottuk el. A donor- és a recipiens terület – 10 nappal a műtétet követően – kiválóan gyógyult (15–16. ábra). Az ezt követő kontrollokat a következő időpontokban ejtettük meg: kettő, illetve négy héttel a műtét után, majd három, hat és tizenkét hónappal később, ezt követően pedig félévente (17–20. ábra). Minden kontroll alkalmával professzionális fenntartó kezelést végeztünk a területen.
Klinikai mérések
Implantátum körüli szondázási mélységet mértünk az interproximális oldal középső pontjánál, a legmagasabb értéket figyelembe véve az ínyszél és a periimplantáris sulcus alja között. Az implantátum körüli lágyszövet bukkális vastag-
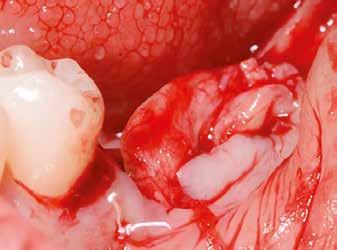
11. ábra: A Kígyó lebeny (varratok disztális részén).
12. ábra: A graftot a meziális oldalon rögzítettük PTFE varrattal.
13. ábra: A graft az ínyszél alá húzva.
14. ábra: Közvetlenül a műtét utáni kép, az utolsó öltések lenyomják a lebenyt, hogy ne maradjon szabad terület.
15. ábra: Tíz nappal a műtét után készült kép, kiválóan gyógyult mind a donor-, mind a recipiens terület.
ságát egy ISO #15-ös endodonciai fájllal mértük 2 mm-re a marginális ínyszéltől meziálisan, disztálisan, illetve az implantátum tengelyében (mint referenciapont). A keratinizált íny szélességét parodontológiai szondával regisztráltuk a kiindulás és a kontrollvizsgálatok alatt. A méréseket elvégeztük a műtét előtt, közvetlenül utána, 4 héttel később, majd egy és két év elteltével. A klinikai paramétereket (keratinizált íny szélessége, lágyszövetvolumen és recessziófedés) regisztráltuk a kiinduláskor és az utánkövetés időpontjai alatt. Kiinduláskor a feszes íny szélessége minimális volt (1 mm). A keratinizált ínyszélesség terén négy hétnél 2 mm-t sikerült nyerni, egy évnél 3 mm-t és öt év alatt 5 mm-t. A recessziót 100%-osan sikerült fedni 4 hét után, és ez nem változott sem egy év, sem öt év után.
Megbeszélés
A kutatások az implantátumok körüli lágyszövetek egészségére fókuszálnak, mivel kulcsfontosságú a megfelelő feszes ínyszélesség és a megfelelő ínyvastagság a biológiai komplikációk és a marginális csontvesztés megelőzésében (4, 5). Nem elmozduló, feszes szövetek szükségesek az implantátum körül, hogy ne alakulhasson ki periimplantitis és megtartható legyen a csontszövet (24, 25). Az implantátumok körüli lágyszövetek kondicionálására szolgáló technikák javasoltak azokban az esetekben, ahol bizonyos tényezők (konvex pótlás-implantátum kontúr, vékony íny, 3 mm-nél nagyobb implantátum platform-csontszint távolság, interproximális szövetvesztés, nem optimálisan pozicionált implantátum) befolyásolhatják a szövetek stabilitását (1). Az implantátum körüli lágyszövethiányok kezelésével kapcsolatban nem sok irodalmi bizonyíték áll rendelkezésre (1.). Keratinizált ínyszélesítés területén egy szisztematikus áttekintés az apikálisan eltolt félvastag lebennyel és szabad ínylebenyátültetéssel végzett technikát hasonlította össze a szubepiteliális kötőszöveti grafttal vagy xenogén lágyszövetpótló anyaggal (12). Ugyanez az áttekintés átlag 28,0% és 96,3%-os recessziófedést írt, amikor koronálisan eltolt
lebenyt szubepiteliális kötőszöveti grafttal vagy allogén lágyszövetpótló anyaggal alkalmaztak, illetve félvastag lebennyel és szubepiteliális kötőszöveti grafttal végzett műtét esetén (12).
A klasszikus apikális vagy laterálisan eltolt lebeny technika (epitelizált grafttal kombinálva) megbízhatósága ellenére számos komplikációt jelentettek (graftelhalás, zsugorodás, recesszió recidívája) (17). Ezenfelül a kötőszöveti graftot vagy kollagén mátrixot alkalmazó technikák is eredményezhetnek mobilis implantátum körüli szöveteket, ezáltal veszélyeztetve az implantátum és a körülötte lévő szövetek stabilitását, ami biológiai komplikációkhoz vezethet (26).
Ezek a lágyszövet-korrekciós technikák többnyire invazív jelleggel és morbiditással bírnak, ezért számos nyelezett lebeny technikát javasolnak különböző szituációban. Ezeket általában esetleírások kapcsán láthatjuk sematikus ábrázolással szemléltetve (18, 20–22).
Moreno Rodriguez és mtsai. az esetbemutatást egy kísérleti tanulmánnyal ötvözték (22). A tesztcsoportban olyan páciensek szerepeltek, akik a felső állcsontba már korábban kaptak implantátumokat és valamilyen lágyszövetdefektussal (keratinizált íny hiánya vagy 2 mm-nél kisebb ínyvastagság és/ vagy -szélesség) rendelkeztek az osszeointegrálódott implantátumok körül és a plakk és vérzési index 30% alatti volt. A kutatók átlagosan 1,37 mm-es bukkális tapadás nyereségét, 3,06 mm-es lágyszövet-vastagodást és 4,69 mm-es keratinizált ínyszélesítést jelentettek. Más kutatók is alkalmaztak nyelezett lebeny technikákat olyan pácienseknél, ahol az ínyvastagság és/vagy -szélesség nem érte el a 2 mm-t. Eredményeik alapján mind a keratinizált ínyszélességben, mind az
ínyvastagságban legalább 2 mm-t sikerült nyerniük (18, 20).
A rövid és középtávú eredményeket figyelembe véve, egy tanulmány javulást mutatott be az első három hónap alatt a lágyszövettérfogat és a keratinizált íny esetében, azonban az 1 éves kontrollon 42,4%-os térfogatveszteséget regisztráltak (14). Szisztematikus irodalmi áttekintések nem találtak elegendő adatot azzal kapcsolatban, hogy melyik technika lenne a legideálisabb vagy milyen lebenyt és graftot kellene alkalmazni lágyszövet augmentációhoz (15–17, 27).
A Kígyótechnika abból az elhatározásból született, hogy a lehető legkisebb traumával járó módszert ajánlhassuk pácienseink részére, akik vékony, sérülékeny implantátum körüli lágyszövettel rendelkeznek. Én mindig is úgy gondolok mind a kezelési tervre, mind a kezelésre, mintha én magam lennék a páciens, és ha én lennék a páciens, szeretném, ha lehetőleg csak egy műtéten kellene átesnem, ami nem jár nagy fájdalommal és minél gyorsabban gyógyul a műtét után. A Kígyótechnikának pontosan ezek az előnyei, és van még egy további előnye: csak egy sebbel jár, nem pedig kettővel. Látva az augmentálandó terület melletti keratinizált szövet mennyiségét és minőségét, azon gondolkodtam, hogy miért vennék szövetet a szájpadlásból, amikor a közvetlenül rendelkezésre álló szövetet is felhasználhatom az augmentációhoz. Amikor a palatumból veszünk valamilyen graftot, annak mindig megszakítjuk a vaszkularizációját, ezzel szemben a Kígyó graft mindig vaszkularizált marad, ami jelentősen csökkenti a graftelhalás kockázatát. A disztális donorterület – ahonnan a lebenyt leválasztjuk az alapjáról – biztosítja a recipiens terület augmentációjához szükséges keratinizált szövetet és kötőszövetet (28).
16
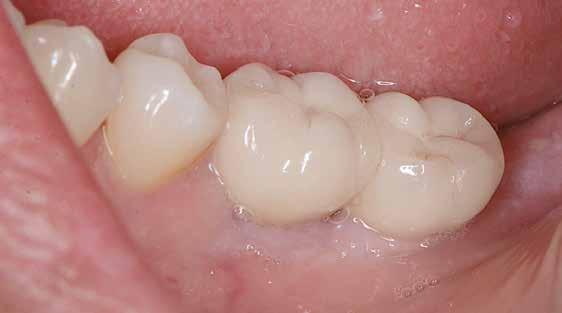
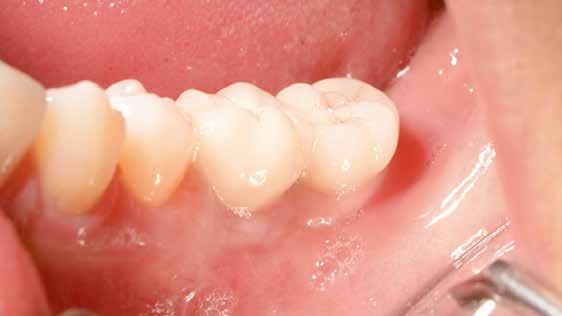
18 17 19
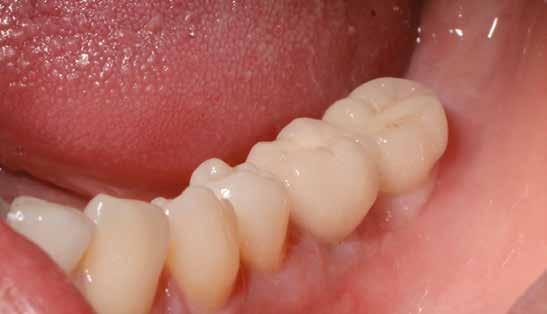
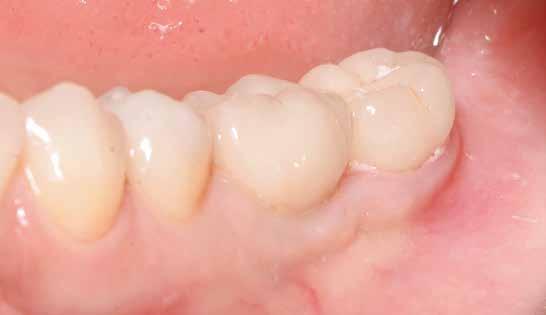
16. ábra: Klinikai kép az implantátumok körüli lágyszövetről a végleges pótlásátadás után. – 17. ábra: Klinikai kép az implantátumok körüli lágyszövetről egy évvel az átadást követően. – 18. ábra: Klinikai kép az implantátumok körüli lágyszövetről két évvel az átadást követően. – 19. ábra: Klinikai kép az implantátumok körüli lágyszövetről öt évvel az átadást követően.
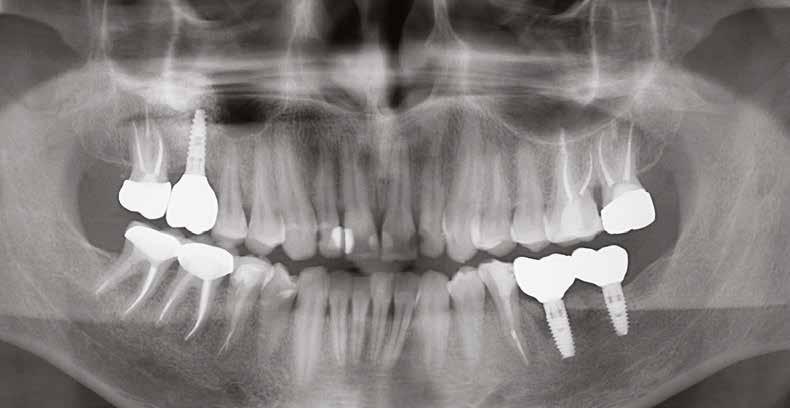
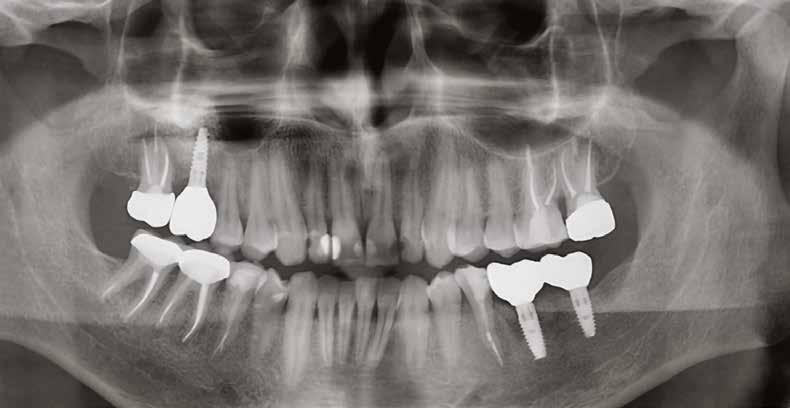
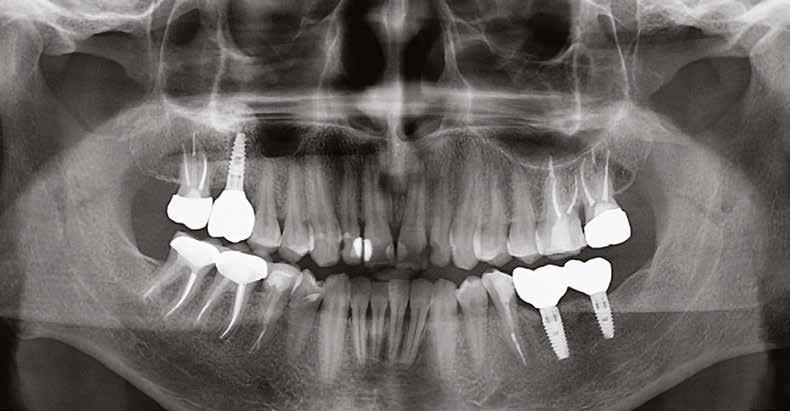
20–22. ábra: 2017-es, 2019-es és 2022-es panorámaröntgen-felvételek.
A lebeny 180 fokos elforgatásával mobilizáljuk azt anélkül, hogy csökkenne a vesztibulum mélysége vagy az izmokat akadályoztatnák, mindez alatt a meziális implantátum körüli terület vérellátása akadálytalan (22). A félvastag lebeny technika biztosítja a flexibilitást, ami által megnövelhető a lágyszövet térfogata, és segít egy esetleges implantátum körüli áltasak kialakulásában, ami bakteriális kolonizáció
kockázatát hordozná magával (18).
A páciens mobilis implantátum körüli lágyszövettel rendelkezett, a keratinizált íny szélessége kevesebb volt, mint 1 mm és a nyálkahártya vastagsága nem érte el a 2 mm-t. Az ínyszél az implantátum platform vonalában volt. Az alábbi műtéti technikával jelentős javulást sikerült elérnünk az implantátum körüli lágyszövetek minőségében és a nem elmozduló keratinizált szövet szélesedett 4 mm-rel. A Kígyótechnikánál alkalmazott elforgatott lebeny a szabad keratinizált ínylebeny előnyeivel növeli a nem elmozduló nyálkahártya szélességét az implantátum körül. Biztosítja továbbá a jó vérellátást és a nyeles lebeny stabilitását, ami kisebb mértékű zsugorodást eredményez, mint egy szabad lágyszövet lebenyátültetésnél (29).
Konklúzió
Az implantátum körüli lágyszövetdefektusok teljes rehabilitációját sikeresen elérhetjük egy második műtéttel elvégzett lágyszövetaugmentációval. A javasolt módosított, nyelezett Kígyó lebeny technika jelentősen javított az implantátum körüli lágyszöveteken, mind szélesség, mind vastagság tekintetében egy, kettő és öt évvel a műtét után is egyaránt tartós maradt az eredmény. Az előnyei a következők: nincs szükség második sebre (távoli donorterületre), jobb a vaszkularizáció, nincs nekróziskockázat, gyorsabb a gyógyulás mind a donor-, mind a recipiens területen, nincs nagyobb fájdalom vagy diszkomfort. Hosszú távú utánkövetéses, randomizált kontrolltanulmányokra van szükség ahhoz, hogy megállapítsuk, hogy valóban egy tartós, megbízható módszerről van szó.
Forrás: Implants 2022/4








PRÉMIUM







BEFEKTETÉS 20+ ÉVRE PRÉMIUM GARANCIÁVAL!
Legalacsonyabb üzemeltetési költség (1,97%) Leghosszabb garancia (10 év) Stabil, folyamatos, megbízható működés - digitális vagy más fejlesztések stabil háttere










A-dec/NSK elektromos, nyomaték szabályozott LED-es, ENDO funkciós mikromotor, rpm 100-40000
























Ebben az A-dec páratlan!
10 év garancia
Varrott kárpit
Varrás nélküli kárpit
Érintés nélkül is működik








KIZÁRÓLAGOS MAGYARORSZÁGI FORGALMAZÓ




Kónuszos felépítmény kapcsolat
Kisebb mikromozgás

Erősebb és egyenletesebb csatlakozás

Platform switching
Prof. Curd Bollen, prof. Martin Jörgens (Hollandia)
EGY- ÉS KÉTRÉSZES KERÁMIA-
IMPLANTÁTUMOK A FOGÁSZATBAN
A kerámiaimplantátumok manapság már nem csupán divatos alternatívák, épp ellenkezőleg, a napi gyakorlatban hasznos kiegészítői az implantációs palettának. Esztétikai tulajdonságaik mellett a teljes fémmentesség is egy fontos előnyük, főleg olyan páciensek esetében, akiknél igazolt az allergia a titánnak azon ötvözeteire (5. osztály), amelyek tartalmaznak vanádiumot és alumíniumot, mivel ezek allergizáló hatása igen erős.
Ezenfelül tovább erősíti a használatuk melletti érveket, miszerint a kerámiaimplantátumok körül ritkábban tapasztalható periimplantitis.
Korábban a cirkonimplantátumok egyrészes (egyfázisú) kialakításban voltak csak elérhetők. Ma már azonban léteznek kétrészesek (kétfázisú, ún. hibrid-koncepció) is, amelyeket széles körben használnak a hiányzó fogak pótlására.
Cikkünk az egy- és kétrészes kerámiaimplantátumok előnyeit és hátrányait klinikai, tudományos, valamint páciensközpontú szempontok alapján hasonlítja össze.
Végezetül említünk néhány, általános ajánlást a kerámiaimplantátumok mindennapi használatával kapcsolatban.

1. ábra: Egy- és kétrészes kerámia- (cirkónium-dioxid) implantátumok (Z-Systems: Z5m & Z5-BL).
Bevezetés
A kerámiaimplantátumok, amelyek manapság cirkónium-dioxidból (ZrO2) készülnek, viszonylag új tagjai a fogászati implantátumok családjának.1 Korábban főleg alumínium-dioxidot használtak erre a célra, de ez az anyag túl rigidnek bizonyult és ez rengeteg töréshez vezetett, stigmatizálva ezzel a kerámiaimplantátumokat. 2
Manapság, esztétikus megjelenésük és biokompatibilitásuk miatt egyre nagyobb népszerűségnek örvendenek.3,4 A hagyományos titánimplantátumokhoz képest hatalmas előnyük, hogy fehéres színükkel tökéletesen illeszkednek a maradék fogazatba, különösen vékony biotípus esetén, ahol a titán szürkés áttetszése az ínyen és egy esetleges magas mosolyvonal esztétikai kudarcot eredményezne.5
A kerámiaimplantátumok hipoallergén tulajdonságaik miatt azok számára is jó megoldást nyújtanak, akiknél bizonyított a fémallergia.6 A titánallergia jeleit számos esetben látjuk a pácienseknél, holott az előfordulása becsült adatok alapján meglehetősen alacsony (0,6%). Nagyobb az allergia kockázata azoknál a betegeknél, akik a beültetést követően valamilyen allergiához társuló tünetet észleltek, illetve akiknél megmagyarázhatatlan okokból sikertelen volt az implantáció.7
A fémimplantátumoknál jelentősen kisebb hővezető képességük miatt a kerámiaimplantátumok esetében ritkább a szájban fellépő hőhatások okozta érzékenység és kellemetlenség.8
Az egy- és kétrészes implantátumok közti választás lehetősége már egy újabb jelenség. A kerámiaimplantátumok hajnalán csupán egyrészes, monoblokk rendszerek léteztek, a fej és az implantátum egy egységet képeztek 9 (1. ábra).
Az implantológiában a mai napig vita tárgya a kerámiaimplantátumok helye a foghiányok (teljes vagy részleges) ellátásában.
A szakma egy része továbbra is úgy tekint a témára, mint múló jelenségre, míg mások igazi áttörést látnak benne.10 Mindemellett a kutatási eredmények azt mutatják, hogy az implantológiában a kerámia értékes alternatívája a titánnak.
Mivel sokkal régebben van forgalomban, az egyrészes implantátumokról több tanulmány született. Sammy Sandhaus és Thomas Driskell már a hetvenes években publikáltak róla. Mindketten, egymástól függetlenül igazolták az egyrészes kerámiaimplantátumok nyújtotta kiváló lehetőségeket.11, 12 A kétrészes kerámiaimplantátumok csak nemrég jelentek meg a piacon (1. táblázat).
Csavaros fej Átmenőcsavar anyaga
Z-Systems Z5-BL/Z5-TL nem igen kerámia vagy titán
Zeramex XT/P6 nem igen karbon
Nobel Biocare NobelPearl nem igen karbon
Straumann Pure nem igen titán
Zircon Medical Patent igen nem –
WITAR AWI nem igen direkt rögzülő*
Neodent Zi nem igen titán
Camlog Ceralog nem igen titán vagy arany
SDS Bright/Value igen igen PEEK (poliéter-éter-keton)
TAV W nem igen titán
1. táblázat: Részletes áttekintés a kétrészes kerámiaimplantátumokról és hozzájuk tartozó protetikai elemekről. *A fej maga kerül becsavarozásra az implantátumba.
Emiatt a kétrészes implantátumokról kevesebb, csupán az elmúlt évtizedet felölelő irodalmi adat áll rendelkezésünkre.13,14 Habár a középtávú (5-6 éves) eredmények kiválóak, a Német Implantológiai Társaság (DGI, Deutsche Gesellschaft für Implantologie) a legutóbbi S3 iránymutatásukban figyelmeztet a használatukkal kapcsolatban.15, 16 Thien és munkatársai megerősítették, hogy az egyrészes cirkonimplantátumok jól alkalmazhatók a titánimplantátumok kiegészítésére és alternatívájaként. Azonban a kétrészes kerámiaimplantátumokkal kapcsolatban nem vonhatunk le következtetéseket a meglevő adatokból. A DGI ezért azt javasolja, hogy részletesen tájékoztassuk a pácienseket a kétrészes kerámiaimplantátumok hosszú távú klinikai tapasztalatainak hiányáról.
Szempontok
Az egy- és kétrészes implantátumok közötti különbségeket, előnyeiket, valamint hátrányaikat nyolc vizsgálati szempont mentén mutatjuk be.
1. Kialakítás
Az egyrészes rendszereknél az implantátum és a fej egy egységet képeznek, így nincs bakteriális szivárgás, ellenben a kétrészes implantátumokkal, ahol az illesztés mentén mindig van egy minimális rés.17 Természetesen ez azt is jelenti, hogy az egyrészes implantátumokon a felépítmény (ideiglenes és végleges egyaránt) csak cementtel rögzíthető. Többféle ilyen implantátum is van forgalomban (2. táblázat).
Az ennél összetettebb, kétrészes implantátumok kettő vagy három darabból épülnek fel: magából az implantátumból, a protetikai fejből és a fejet rögzítő átmenőcsavarból. Amenynyiben a fej cementtel rögzül az implantátumban, nincs átmenőcsavar. A csavar készülhet titánból, aranyból, karbonból vagy cirkóniumból (2. ábra).
Nagyon fontos, hogy mindig kövessük a gyártó utasításait és ne húzzuk meg a kelleténél nagyobb nyomatékkal ezeket a csavarokat! Az ajánlott nyomatékok: 25 Ncm titán, 25 Ncm karbon, 12 Ncm cirkónium és 15 Ncm arany esetében. Jelenleg csupán néhány kétrészes implantátum érhető el a kereskedelmi forgalomban (2. táblázat).
Egyrészes kerámiaimplantátumok Kétrészes kerámiaimplantátumok
Z-Systems: Z5m/Z5m(t) Z-Systems: Z5-BL/Z5-TL
Straumann: Pure Monotype
Straumann: Pure
Camlog: Ceralog Monobloc Camlog: Ceralog Hexalobe
Zircon Medical: Patent 1-piece
Zircon Medical: Patent 2-piece
SDS: Bright SDS: Bright/Value
TAV: W-1
TAV: W-2
Witar: AWI 1-piece Witar: AWI 2-piece
ZiBone ZiBone
Medical Instinct: Bone Trust
Neodent: Zi
Fair Implant: Fair White Zeramex: XT/P6
Ceraroot Nobel Biocare: NobelPearl
Tree Oss Ceramic SIC: SIC White
Bredent: WhiteSky
2. táblázat: Egy- és kétrészes implantátum rendszere.

2. ábra: Különböző átmenőcsavarok a protetikai fejekhez: titán (Neodent) – karbon (Zeramex) – cirkónium (Z-Systems) – arany (Camlog).
2. A műtét
A műtét első része, az implantátum helyének előkészítése, mindkét implantátumtípusnál azonos, bár az egyrészes implantátumoknál a lebenymentes előkészítés is megfelelhet, amely azonban jelentősebb (statisztikailag szignifikáns) csontvesztéssel és a későbbiekben további problémákkal is járhat.18
Gyártó Termék Ragasztott fej

3. ábra: PEEK (poliéter-éter-keton) sapkák egyrészes implantátumok számára (Z-Systems, Z5m).
A kétrészes implantátumoknál egy második műtét során kerül be az ínyformázó, amelynek anyaga lehet PEEK (poliéter-éter-keton) vagy PEKK (poliéter-keton-keton). Mivel az egyrészes cirkonimplantátumokat a behelyezést követően módosítani (csiszolni) már nem tudjuk (ellenőrizzük a gyártó ajánlásait!), a tökéletes pozícióra beültetéskor kell ügyelni.19
Annak érdekében, hogy elkerülhessük a pozicionálási hibákat (a fej elégtelen dőlésszöge), javasolt eleinte sablonnal végezni ezeket a beültetéseket.20 A kétrészes rendszereknél ez a hibaforrás nem ennyire jelentős, mivel a legtöbb gyártó kínál tengelykorrekciós vagy csiszolható fejeket. Függetlenül attól, hogy egy- vagy kétrészes rendszerrel dolgozunk, az előfúrást – bőséges vízhűtés mellett – alacsony fordulatszámon végezzük. A kerámiából készült fúrók a rossz hővezetés miatt nagyon hamar túlmelegíthetik a környező csontot.21 A csont túlmelegedése nem veszélyezteti az implantátum túlélését, viszont jelentősebb marginális csontfelszívódást és ezzel együtt kisebb csont–implantátum kontaktfelszínt (BIC, bone-to-implant conact) eredményez.22 Az első előfúrót 800/perc, az utolsót folyamatos csökkenés mellett 400/perc fordulaton használhatjuk. A nyaki süllyesztő fúrókat a kortikális előkészítésekor csonttípustól függetlenül (D1-D3) csak 15/perc fordulatszámon javasolt használni.23
Mielőtt elkezdünk használni egy fúrósorozatot, rendkívül fontos ellenőrizni az adott gyártó ajánlásait.
3. Terhelés
Mivel a kerámiaimplantátumoknál szinte mindig szükség van a kortikális megtágításra az előkészítés végén, az azonnali terhelés sokszor nem lehetséges.24 Ezért a késői vagy késleltetett terhelés többnyire a kétrészes kerámiaimplantátumoknál javasolt. Sőt, Suchetha és munkatársai kimutatták, hogy a kétrészes technika még javíthatja is a frontterület lágyrészesztétikáját.25
Az egyrészes implantátumokat, kialakításuknál fogva, minden esetben azonnal terheljük. A legtöbb gyártó forgalmaz olyan szilikon- vagy PEEK sapkákat, amelyeket a fejekre helyezve csökkenthetjük a terhelés mértékét. Ezek a stresszelnyelők az íny burjánzásától is megóvják a fejeket a gyógyulás ideje alatt (3. ábra).
4. Felépítmény
Az egyrészes rendszerek protetikai ellátása gyakorlatilag azonos a természetes fogakra készülő koronák munkamenetével. A lenyomatot vehetjük analóg vagy digitális módon is. Az implantátumok körüli lágyszövetek eltartására retrakciós fonalat, vagy valamilyen lézert (dióda lézer) használhatunk.26 Implantátum analógra nincs szükség ebben az esetben. A kétrészes kerámiaimplantátumok protetikai ellátása hasonló a kétrészes titánimplantátumokéhoz: analóg (nyitott vagy zárt kanalas) vagy digitális lenyomatvétel. Minden gyártónak van saját szkennelhető lenyomati feje, illetve a kétrészes rendszereknél mindig szükséges analóg használata a labormunkához. Fontos, hogy a gyártók által biztosított eredeti analógokat használjuk, mivel a 3D nyomtatott analógok nem elég pontosak.27
5. Méretek
A kerámiaimplantátumokból rendelkezésre álló méretek korlátozottak. A 3. táblázatban feltüntettük a leggyakrabban használt átmérő- és hossztartományokat: az átmérők 3,3 mm (Straumann) és 7 mm (SDS), míg a hosszok 6 mm (SDS) és 16 mm (Bredent) között változnak. Az átlagos átmérő 4,2 mm, az átlagos hosszúság pedig 10,8 mm. Ezekkel a paraméterekkel gyakorlatilag valamennyi indikáció lefedhető. Cilindrikus és kúpos formák léteznek, meneteik általában nem önmetszőek, amely szinte mindig szükségessé teszi a kortikális túltágítását behajtás előtt.
A kétrészes rendszerek közt több olyan is van, amely belső kapcsolatos, ezeknek azonban eltérő a stabilitásuk (4. ábra).
6. Költségek
Az egyrészes implantátumok viszonylag olcsóbbak, mivel a cementtel rögzülő kerámiakoronán kívül más protetikai elemet nem igényelnek. A kétrészes implantátumok felépítményéhez minden esetben több elem szükséges: a protetikai fej és az azt rögzítő átmenőcsavar. Az elemek nemcsak gyártói oldalról jelentenek pluszköltséget, hanem a fogtechnikai munkafolyamatokat is összetettebbé teszik, ami végső soron sokkal drágábbá teszi a kétrészes kerámiaimplantátum ellátását az egyrészeshez képest.
7. Szövődmények
A fogászati implantológia legfőbb szövődménye az elégtelen, vagy hiányzó osszeointegráció. A cirkónium-dioxid kerámia és titánimplantátumok sikeraránya összemérhető, mivel hasonló mértékben integrálódnak a lágy- és keményszövetekbe. A titánimplantátumok viszont sokkal gyorsabb osszeointegrációt mutatnak a gyógyulás kezdeti fázisában a kerámiához képest. Mára az is egyértelmű, hogy a cirkónium-dioxid implantátumok nem mutatnak jobb klinikai eredményeket e tekintetben, mint a titánimplantátumok28, 29, a két rendszer eredményei hasonlók.
Az egyrészes implantátumokon rögzített koronák ragasztócementje bepréselődhet az ínyszél alá, amely könnyen vezethet periimplantitis kialakulásához, ha nem kerül eltávolításra.30 A cementfelesleg eltávolítására emiatt kiemelt figyelmet kell fordítani ragasztást követően.31
Mint korábban említettük, a nem megfelelő szögben behelyezett egyrészes implantátum (utólagos tengelykorrekcióra nincs lehetőség) komoly problémákhoz vezethet, amelyekre az egyetlen megoldás az explantáció.
A Legacy Of Performance
A
TSX® Implant System
1. A TSX implantátum kompatibilis a TSV, a Driva Gold fúrókkal és az Eztetic sebészeti műszerekkel és protetikai alkatrészekkel.
2. EXTRAKCIÓS STABILITÁS
A mély apikális menetek és az extrakciós protokoll megkönnyíti az azonnali behelyezést (> 35 Ncm az in vitro extrakciós tesztek során).

3. PERIIMPLANTÁRIS EGÉSZSÉGI ZÓNA
Hibrid felszín: Koronális 1,5 mm, szabadalmaztatott kettős savmaratott (DAE) textúrával, vonzó a csont és nem a baktériumok számára.
4. ELVÁRT AZONNALISÁG
Progresszív szálak és kúp követik az előkészített oszteotómiát a beültetés kiszámíthatósága és nagy stabilitása érdekében (> 70 ISQ in vitro sűrű csontban).
5. OSZSZEOINTEGRÁCIÓS ZÓNA
Saját fejlesztésű MTX™ felület, magas oszteokonduktív potenciállal és több mint két évtizedes klinikai sikerrel.


• Ismert a primer stabilitásáról és az azonnali terhelhetőségéről.
• Megbízható a belső hatszög frikciós illeszkedésű csatlakozásáról.
• Elismert a 98,7%-os kumulatív túlélési arány miatt.



Operációs idő megtakarítása
Szövet megőrzés
Magas primer stabilitás BIC és oszteokonduktív képesség All-in-One megoldás




mm
mm 8–14 mm
3,75–4,3 mm 10–13 mm
Összefoglalás
Az implantológiában mára az egyrészes és kétrészes implantátumokkal hasonló prognózist lehet elérni. A legfrissebb kutatások egyértelműen azt mutatják, hogy kiváló klinikai eredmények érhetők el az egy- és kétrészes kerámiaimplantátumokkal is. Viszont a kétrészes kerámiaimplantátumok esetében még nem áll rendelkezésre elegendő hosszú távú tudományos adat, amely alátámasztaná mindennapi használatukat. Ezért kiemelten fontos, hogy ilyen implantátumok beültetése előtt a pácienst teljeskörűen tájékoztassuk, és ezt követően egyezzen csak bele a kezelésbe.
3. táblázat: A kereskedelemben kapható kerámiaimplantátumok hosszai és átmérői.
A kétrészes implantátumoknál másfajta problémák merülhetnek fel: az átmenőcsavarok lazulása, illetve törése.32 Hogy ezeket megelőzhessük, fontos betartani a gyártói előírásokat és megfelelő nyomatékkal meghúzni ezeket a csavarokat a koronák rögzítésekor. Minél több protetikai elemből áll a rendszer, annál nagyobb a szövődmények kockázata.
A tényleges irodalmi adatok azt mutatják, hogy a kerámiaimplantátumok körül kevésbé jellemző a periimplantitis kialakulása, mint a titánból készülteknél.33, 34 Ennek a jelenségnek az okát jelenleg is kutatják.
8. Páciens szempontok
A mindennapi klinikai gyakorlatban ezeket a szempontokat sokszor alábecsüljük és a kelleténél kisebb hangsúlyt fektetünk rájuk. A páciensek oldaláról elvárás, hogy a kezelések minél kevésbé legyenek invazívak, minél kisebb legyen a morbiditás, kevesebb kezelési alkalom legyen és ne kerüljön sokba. Az egy- és kétrészes implantátumokat összehasonlítva egyértelműen látszik, hogy a páciensek szemszögéből az egyrészes rendszerek több előnnyel bírnak.
A Német Implantológiai Társaság a legutóbbi iránymutatásában (S3) figyelmezteti a fogorvosokat, hogy tájékoztassák pácienseiket, a kétrészes kerámiaimplantátumok korlátlan használatával kapcsolatban igen kevés tudományosan megalapozott ismeret áll rendelkezésre.16 A páciensnek mindig tájékozott beleegyezést kell adnia egy ilyen beavatkozás előtt.
Sokoldalú felhasználhatóságuk miatt a kétrészes kerámiaimplantátumok a jövőben egyre nagyobb teret fognak nyerni az egyrészes implantátumok rovására. Természetesen ez a sokoldalúság azt is jelenti majd, hogy drágábbak lesznek mind a fogorvosok, mind a páciensek számára.
A jövőben randomizált kontrollált vizsgálatokkal meg kell erősíteni a kétrészes cirkonimplantátumok ígéretes eredményeit.
Forrás: EDI Journal 2023/3
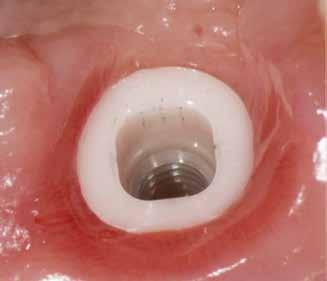
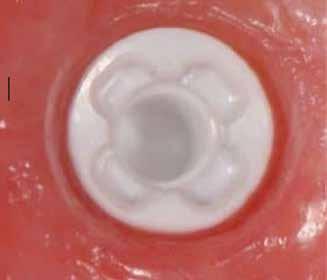
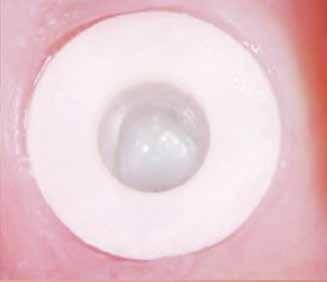
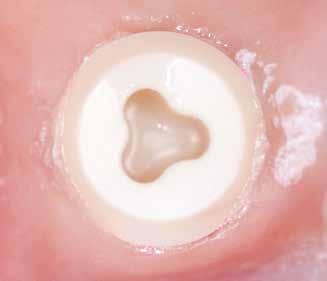
4. ábra: Különböző kétrészes kerámiaimplantátum-platformok (óramutató járásának megfelelően): Pure (Straumann) – Z5c (Z-Systems) – Patent (Zircon Medical) – Zeramex (DentalPoint)











Dr. Ronald Möbius (Németország)
AZ IMPLANTOLÓGIÁT SÚJTÓ SZÖKŐÁR
A periimplantitis tünetei a gyulladás és a csontfelszívódás. A gyulladás megfékezése fontos, elengedhetetlen feltétele a kezelésnek, de a csontanyagcsere helyreállításához nem elég.
Amikor a csont metabolikus folyamatai negatív irányba billennek, felszívódás lép fel, amely végül csontveszteségként fog megnyilvánulni.
A probléma nem a gyulladás, hanem a csont negatív metabolizmusa. A periimplantitis kezelésekor nem elég csupán a gyulladást megszüntetni, hiszen az implantátum meglazulásáért az anyagcsere-egyensúly felborulása felelős.
Az aktivált osteoclastok túlsúlya csontfelszívódással jár. Ugyanakkor nincs olyan mikroorganizmus, amely képes lenne csontbontásra, hiszen egy száz éve eltemetett csontot sem tudnak a földben levő mikroorganizmusok lebontani.
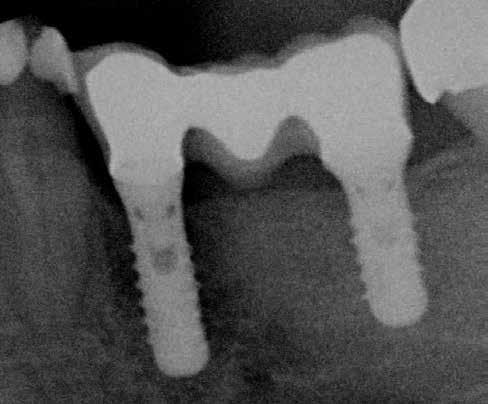
1. ábra: A kezelés előtt.
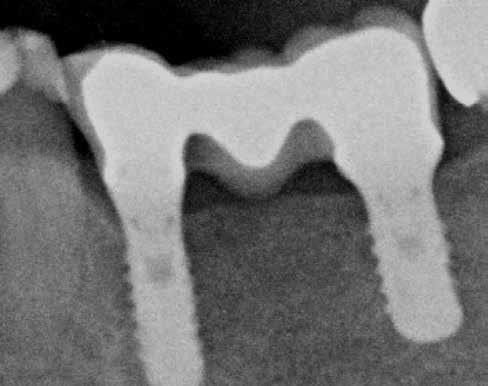
2. ábra: Kilenc hónapos kezelést követően.
Jelen esetben a csontfelszívódást a mikroorganizmusok által kiváltott gyulladás és az azt követő osteoclast-aktiváció okozza, emiatt a kiváltó oknak megfelelően terápiát kell kiválasztani.
Hogyan kezelhető a csontmetabolizmus felborulása? Negatív metabolizmusról akkor beszélünk, ha több csont bomlik le, mint amennyi képződik. Az implantátum elvesztése történhet nagyon gyorsan, vagy akár hosszú évek leforgása alatt is. Ez attól függ, hogy mennyire tolódik el a lebomlás irányába a metabolizmus.
Az osteoblastok és osteoclastok aktivitása, száma és funkciója terápiás eszközökkel befolyásolható. Az osteoclastok például reverzibilisen inaktiválhatók, függetlenül attól, hogy mi volt az aktiválás forrása.
A parodontális gyulladások kezelésére számos lehetőség ismert. A csontmetabolizmus kezelése azonban egy kevésbé ismert és még kevésbé alkalmazott módszer. Korábban a periimplantitis kezelése csupán a gyulladás megszüntetésére összpontosított. Ezeknél a pácienseknél a csont lebomlása túlsúlyban van a képződés rovására. Az átépülés (bone remodelling) kötelező egyensúlya a lebomlás irányába tolódik el. A csontok egyik alapanyaga az 1-es típusú kollagén, amelynek metabolizmusa jól mérhető digitális eszközökkel. Ez az ún. aMMP-8 teszt, ahol a 10 ng/ml alatti kollagénértékeket tekintjük normálisnak, a 10–20 ng/ml közötti értékek elfogadhatóak, míg a 20 ng/ml feletti érték fokozott kollagénlebomlást jelez, amely kezelést igényel. Mindemellett a negatív csontmetabolizmus jelei gondos megfigyeléssel is észrevehetők.11
Az implantátum voltaképpen egy idegen test, ennek megfelelően mindenképpen kivált egy minimális idegentest-reakciót.5 A fogakkal ellentétben, az implantátumok közvetlenül és mereven kötődnek az őket körülvevő csonthoz, amelynek kiegyensúlyozott metabolizmusa biztosítja az implantátum stabilitását.
Számos olyan folyamatot ismerünk, amely fokozott osteoclast-aktivációhoz és csontlebomláshoz vezet. Testünk elöregedése 35 éves kor felett kezdődik meg, és mivel az implantált páciensek többsége ennél idősebb, ez egy alapvető probléma. A kor előrehaladtával csökkenésnek indul a haj mennyisége, a bőr rugalmassága, az izomtömeg és az újonnan képződő csonttömeg is. A csontlebomlás dominanciája csak látszólagos, valójában az új csont képződése is csökken. Ahogy az emberi test öregszik, úgy lassul le minden
élettani folyamat, beleértve a csontképződést is.
• A gyulladást különböző patogének váltják ki.
• A csont lebomlásáért az osteoclastok felelősek.
Az osteoblastok aktivitásának csökkenése, illetve az ezzel arányosan emelkedő osteoclast-aktivitás miatt romlik a csont minősége és szilárdsága. Ráadásul az ásványianyag-tartalma is alacsonyabb lesz, ez pedig nagyban befolyásolja a csontszilárdságot. A rágómozgás csavaró erőt fejt ki az implantátumra, amelynek tengelye az implantátum középpontjában található, a maximális elhajlás és terhelés pedig az implantátum felszíne mentén helyezkedik el. Ennek helyét jelzi a periimplantitis során fellépő marginális csontfelszívódás és csontos tasakképződés. Ezekben a tasakokban megváltozik a mikrobiális környezet, a szupragingivális aerob flóra helyét átveszik a szubgingivális, anaerob, patogén baktériumok. Az implantátum transzgingivális része körüli lágyszövet szerkezetileg hasonlít a természetes fogakat körülvevő ínyhez.12 A biológiai szélesség implantátumok körül átlagosan 3,0 mm (Herman és mtsai.).4 A természetes fogak a fentiektől eltérően, rostos kötőszövetből felépülő szalagrendszerrel kapcsolódnak a csonthoz és a szomszédos többi foghoz.14 Az implantátum–csont kapcsolatát viszont csupán hemidezmoszómák biztosítják.3 Habár ez az úgynevezett „szervült osteogenesis” tekinthető az elérhető legjobb csont–implantátum kapcsolati formának, az esetek nagy részében a titánfelszín és a csont kapcsolata csak „kontakt osteogenesis”-nek felel meg. 13
Különböző okok
Gyulladás
Parodontális csontpusztulás
Különböző kezelések
Gyulladáscsökkentő kezelés
Csont remodellációs terápia
3. ábra: Paradigmaváltás az orális implantológiában.
Kalciumfelszívódás
Felszívódás a gyomorból
Szállítás a véráram útján a magas szérum kalciumszint elősegíti az atherosclerosis kialakulását
A D-, A-, K2-vitaminok és a magnézium jelenléte nélkül:
A kalcium eljut és raktározódik a lágy szövetekben
A szövetek megkeményednek, merevvé válnak, funkciójuk romlik, ráncok alakulnak ki, megkezdődik az elöregedés, az érelmeszesedés, szívroham, stroke léphetnek fel
A kalcium nem tud beépülni a csontokba osteoporosis, parodontitis, a fogak hipomineralizációja – MIH, periimplantitis alakulhatnak ki
4. ábra: Kalciumfelvétel: a „kalcium-paradoxon.”
A természetes fogak körüli tasakokat védi a folyamatosan áramló sulcusfolyadék, amely egy, a szérumból származó, transz- és exudátum. Egy 5 mm mély tasakban átlagosan negyvenszer cserélődik óránként.7 Az implantátum körüli sulcusban nincs ilyen folyadékáramlás, a nyál állandóan pang. Egy virágos vázában, ha sokáig nem cseréljük a vizet, állottá válik. Hasonlóan, az implantátumok körül is pangani kezd a folyadék. Az implantátumok körüli „sulcusfolyadék” egy megbízható indikátora a periimplantitisnek.1,2 Antoine Béchamp (1816–1908) francia professzort idézve: „Megfelelő környezet nélkül nincsenek mikrobák.” A kezelés tartós sikerének érdekében módosítanunk kell a miliőt, a bakteriális környezetet, illetve serkentenünk kell a regeneratív mikroorganizmusok proliferációját.
A periimplantáris csont anyagcseréje nem elemezhető pusztán a szájüreg vizsgálatával. A korai fázisban a röntgenfelvételeken sem láthatóak a negatív csontanyagcsere jelei. Ebben lehet nagy segítségünkre az aMMP-8 vizsgálat, amely jelenleg az egyetlen vizsgált paraméter, amely képes kimutatni a kollagén lebomlását annak megkezdődése előtt. Ennek köszönhetően, már a tünetek megjelenése előtt elkezdhetjük a megfelelő kezelést. Ilyenkor még elegendő a csontanyagcsere kezelése, tulajdonképpen a negatív anyagcsere megelőzése – restitutio ad integrum (az eredeti állapot visszaállítása).
Egyik bakteriális teszt sem szolgálhat segítségül, hiszen a flórában csak akkor mutathatók ki a korábban említett változások, ha ehhez a megfelelő környezet (csontfelszívódás, horizontális csontpusztulás) már létrejött. Ebben az esetben a csontanyagcsere kezelésével maximálisan elérhető terápiás eredmény a restitutio cum defectu (tökéletlen, nem teljes gyógyulás).
A csont anyagcseréje mindenhol, az állkapcsokban, a gerincben, a térdben is egyforma. Tehát a periimplantitis csupán a negatív csontanyagcsere szájüregi megjelenése. Fő okai: mozgásszegény életmód, oxigénhiány, folyadékhiány, kevés jótékony baktérium jelenléte, túlzott szénhidrátfogyasztás; illetve a D3-, K2-, A-vitaminok, kalcium, jód, magnézium és számos más tápanyag elégtelen bevitele. Összegezve: a csont élettani terhelésének hiánya, a tüdők edzetlensége, folyadékhiány és a létfontosságú tápanyagok elégtelen bevitele.
Ezeken mind lehetne változtatni, ez azonban drasztikus életmódbeli változtatásokat követelne meg. A tapasztalat azt mutatja, hogy a páciensek csak komoly általános megbetegedések megjelenését követően hajlandók ezekre a változtatásokra. Természetesen azokat a pácienseket, akik hajlandóak az együttműködésre, érdemes jobb útra terelni.
A kezelés csak akkor lehet hatékony, ha az azt végző fogorvos tisztában van a szisztémás csontanyagcsere folyamataival. Féligazságok és találomra hozott döntések nem vezetnek sikerhez. A csontanyagcsere kiemelten fontos, hiszen a csontnak nem csupán tartó és támasztó szerepe van, hanem a kalciumháztartás közvetlen kapcsolódik a csontok
Osteoclastok
Osteoblastok
Lokális terápia
Osteoclastok A kezelés célja: A kezelés célja: magas szintű egyensúly magas szintű egyensúly
Osteoblastok
Lokális terápia
5. ábra: A lokális és szisztémás csontanyagcsere különbségei.
anyagcseréjével, ezáltal befolyásolja szinte valamennyi életfolyamatot, hiszen valamennyi sejtnek, izomnak, idegsejtnek szüksége van kalciumra a működéséhez. A szervezetben a kalcium az egyik legbőségesebben jelen levő ásványi anyag, amely sokakat félrevezet. Manapság egyre kevesebb kalciumot viszünk be, amely az úgynevezett kalcium-paradoxon kialakulásához vezetett.
Bizonyos szövetekben (lágy szövetek, -szervek, erek, agy), ahol nincs rá szükség, túl sok a kalcium. Máshol, ahol szükség lenne többre (fogak-hypomineralizáció, csontok-csontritkulás), hiány van belőle.
A csontoknak egyéb szerepe is van. A vér alakos elemei 120 napos életciklusukat követően lecserélődnek. Az új vérsejtek, az immunrendszer egyes sejtjei, a daganatölő sejtek, és sok más, amelyek mind az egészségesen működő vörös csontvelőből származnak.
Ez az ismeretanyag nem képezi az alap fogorvosi képzés részét, ezért ajánlom, hogy azok a kollégák, akik szeretnének jobban elmélyedni a témában, vegyenek részt a Szászországi Fogorvosi Szövetség (Saxony State Dental Association) által szervezett továbbképzések egyikén.
Implantátumok
– a probléma meghatározása
1. A csontanyagcsere helyi kezelése – tüneti terápia
Az osteoclastok aktivitásának és számának csökkentésével alkalmazkodhatunk az osteoblast-aktivitás csökkent szint-
jéhez. Ezzel elérhetjük, hogy a képződő és lebomló csont mennyisége egy alacsonyabb aktivitási szinten kiegyenlítődjön.
2. A csontanyagcsere szisztémás kezelése – oki terápia Nem az osteoclastok száma és a csontlebomlás hirtelen megnövekedése a negatív anyagcsere legfőbb problémája. Sokkal inkább a nem megfelelő struktúra és mineralizáltság, amely tévesen úgy tűnhet, mintha túlzott csontfelszívódás menne végbe. A szisztémás kezelés aktiválja az osteoblastokat, stimulálja az új csont képződését és mineralizációját, létrehozva egy magas szintű egyensúlyt képződés és lebomlás között.
A periimplantitis kezelése
A kezelés során az implantátum nyaka körüli kötőszövetes gallér ismét feszessé válik, amelynek következtében a tasak teljesen megszűnik és a pangó sulcusfolyadék nem tud felgyülemleni az implantátum körül. Ezzel párhuzamosan az osteoclastokat reverzibilisen inaktiváljuk; az osteoblastokat, illetve a kalcium anyagcseréjét, szállítását és tárolását pedig aktiváljuk. A csont érésének maximális időtartama 9 hónap.
A kezelést részletesen a Dental Barometer c. folyóiratban írtuk le. 8-10
Sajnos csupán kevés rendelő van felszerelve a periimplantitis és a biofilm kezeléséhez szükséges megfelelő eszközökkel:
1. Alkalmazhatunk-e ultrahangos és szónikus eszközöket olyan implantátumoknál, amelyeknek sérült az osszeointegritása – TILOS!
2. Megtisztíthatjuk-e a szabaddá vált csavarmeneteket kézi eszközökkel – Kétes siker. (Koch)
3. A homokfúvó eszközök penetrációs mélysége a tasakba csupán 2 mm – Elégtelen.
4. Forgó műszerek használata – Kerülendő.
Összefoglalás
A terápiás megközelítés ismeretei nélkül nehezen magyarázhatóak az elmúlt 30 év bevált kezelési módszerei. A gyulladás csökkentése és a csontfelszívódás megfékezése két külön folyamat. Jelenlegi kezeléseink csupán a gyulladásra összpontosítanak, amelyekért mikroorganizmusok felelősek. Ám nem ismerünk olyan mikroorganizmust, amely képes lenne csontot bontani. Minél gyorsabb és hatékonyabb a gyulladás kezelése, annál jobban eltolódik a csont anyagcsere-egyensúlya a negatív irányba, hiszen az antibiotikumok kiirtják a baktériumokat, amelyeket aztán a szervezet saját tisztogató sejtjei fognak felszámolni. A fagocitáló sejtek úgy tudnak a helyszínre migrálni, hogy jelentős men ynyiségű aMMP8-at szabadítanak fel, amely bontja a kollagént.
A végeredmény egy klinikailag még látszólag egészséges környezet, azonban a csont anyagcseréje tovább sodródik negatív irányba.
Forrás: EDI Journal 2023/3










alphaimplant.
Dr. Sergio Piano (Olaszország)
HÁROMTAGÚ MOLÁRIS HÍD KÉSZÍTÉSE
A digitális munkafolyamatok számos előnnyel járhatnak, pontosabb és minőségibb munkát végezhetünk velük. Azonban az anyagok minőségének és kialakításának helyes megválasztása legalább olyan fontos, mint az átfogóan megtervezett kezelési stratégia és a munkamenet. Jelen cikkünkben egy teljes mosolyátalakítást mutatunk be egy hölgypáciensnél, akinek igen magasak voltak az esztétikai elvárásai. Szeretett volna implantátumokat azonnali terheléssel és a munkafolyamatok digitális kivitelezését is preferálta. A páciens elvárásainak sikerült megfelelnünk egy hatékony implantációs protokollal, valamint az esztétikus, ideiglenes és végleges fogpótlással. A Straumann® BLX (Roxolid®) implantátumot választottuk, amely SLActive® felülettel rendelkezik és alkalmas a digitális munkamenetre.

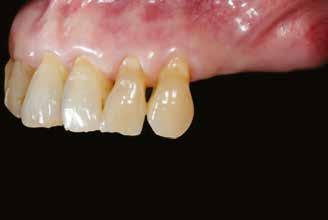
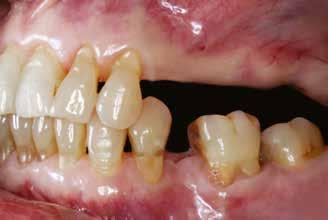
Kiindulási helyzet
Az 58 éves női páciens azzal a panasszal keresett fel minket, hogy a bal oldalon képtelen rágni, illetve szeretett volna egy szebb mosolyt. A páciens kifejezett kívánsága volt, hogy ne legyen kivehető pótlása a kezelés semelyik fázisában. Korábbi fogászati kezelések alkalmával kellemetlen élményei voltak, ezért kérte, hogy amennyire lehet, mellőzzük az invazív beavatkozásokat. A páciensnek közepesen magas volt a mosolyvonala, a hiányzó kis- és nagyőrlők miatt a második kvadránsban mosolygáskor sötét területek látszottak (1. ábra).
A páciens felső állcsontja részlegesen fogatlan volt, hiányoztak a 14, 17, 24–27 fogai, illetve sötét háromszögeket tapasztaltunk a metszők között (2. ábra). A Kennedy-osztályozás szerint a maxillán féloldali sorvégi foghiányt látunk (Kennedy II. osztály, Applegate I. módosítással, 3. ábra). Az oldalról készült képeken látszik, hogy vertikálisan kellő mennyiségű
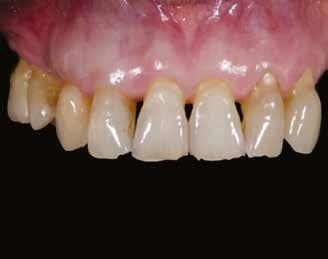
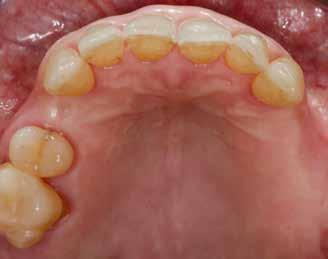
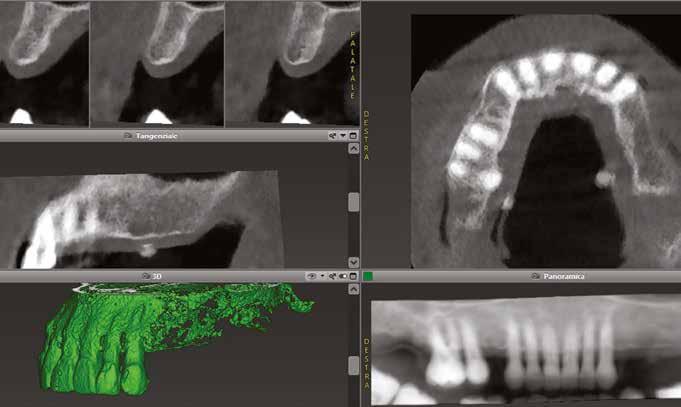
Sebészi besorolás
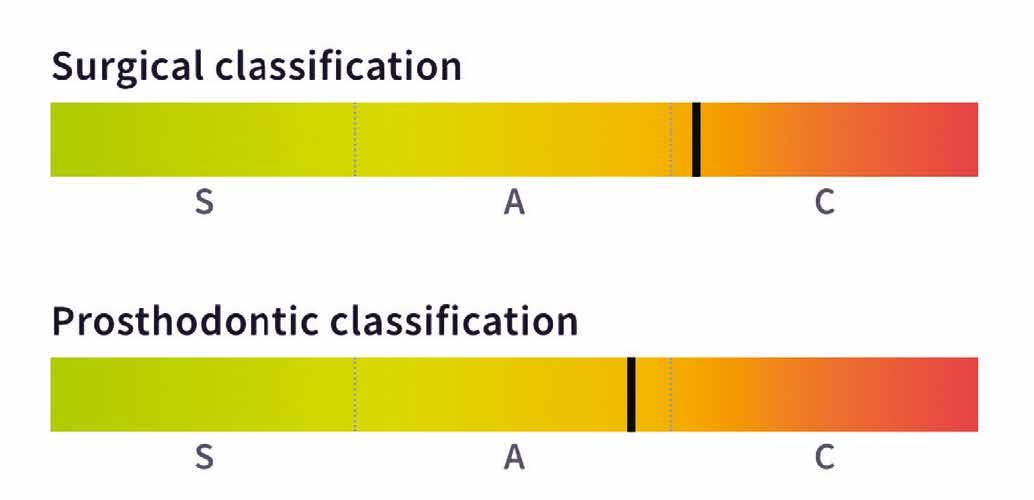
Protetikai besorolás
csont állt rendelkezésre (4. ábra). A bal oldalon, az antagonista fogívben 34 és 36 fogak elongálódtak (5. ábra).
A fogatlan területen rendelkezésre álló csont mennyiségét és minőségét CBCT-felvételen a coDiagnostiX® szoftver segítségével vizsgáltuk (6. ábra). A felvételeken látszott, hogy a 24–26 területen horizontálisan és vertikálisan is elegendő csont áll rendelkezésre az implantációhoz.
Kezelési terv
A kezelés céljait a páciens kívánságainak szem előtt tartása mellett tűztük ki:
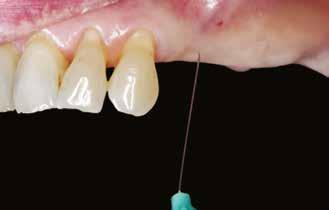
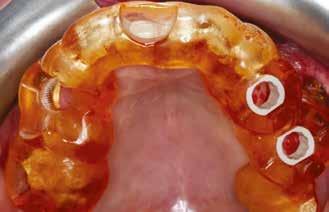
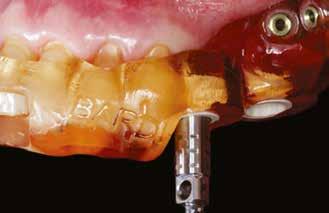
• Háromtagú rögzített hídpótlás készítése a 24 és 26 pozíciókban elhelyezett implantátumokra.
• Amennyiben kielégítő az implantátumok primer stabilitása, azonnali ideiglenes pótlás készítése. Így kielégítő esztétikai eredményt tudunk biztosítani a páciens számára a kezelés teljes ideje alatt.
• Az invazivitás csökkentésére az implantátumok helyének számítógépes megtervezése, a lebenyes feltárás elkerülése és a protetikai munkafolyamatok leegyszerűsítése.
A fenti szempontok alapján tájékoztattuk a pácienst a kezelési lehetőségekről:

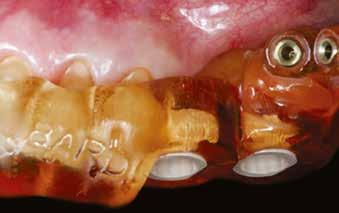
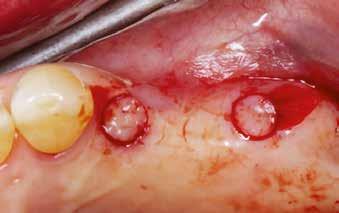

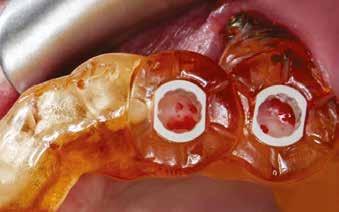
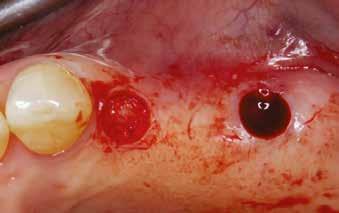
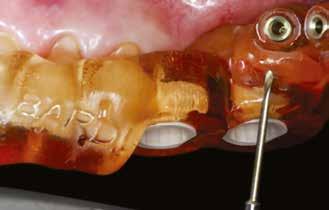
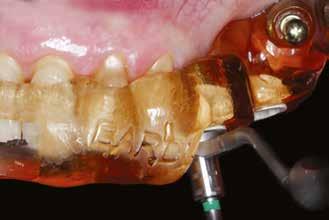
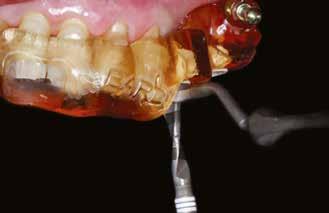

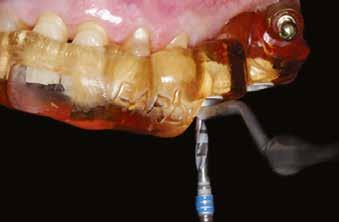

1. Implantátumok behelyezése a 24 és 26 pozíciókba, terhelésmentes gyógyulás ideiglenes pótlás nélkül. A gyógyulási idő leteltével egy háromtagú, implantátumokon elhorgonyzott híd készítése a 24–26 területre.
2. Implantátumok behelyezése a 24 és 26 pozíciókba és amennyiben a primer stabilitás optimális, azonnali ideiglenes híd készítése az implantátumokra. A gyógyulási idő leteltével egy háromtagú, implantátumokon elhorgonyzott híd készítése a 24–26 területre.
3. Az implantátumok behelyezése sebészi sablon segítségével a 24 és 26 pozíciókba és megfelelő primer stabilitás esetén az implantátumokon elhorgonyzott, azonnali ideiglenes híd készítése. A gyógyulási idő leteltével egy háromtagú, implantátumokon elhorgonyzott híd készítése a 24–26 területre.
Az ITI SAC-besorolását (International Team for Implantology, SAC v2.0) alkalmazva kiértékeltük a kezelési terv öszszetettségét és a lehetséges kockázatokat (7. ábra).
A végleges döntés előtt mérlegeltük az irányított sebészi beavatkozás és az azonnali ideiglenes híd (24–26 háromtagú híd) készítésének előnyeit és hátrányait.
A pácienssel átbeszéltük mindhárom kezelési lehetőséget, az előnyöket és a kockázatokat. Ezt követően a páciens korát, általános egészségi állapotát és elvárásait is számításba véve, a harmadik kezelési lehetőség mellett döntöttünk. A számítógépes tervezés során a páciens számára Straumann® BLX implantátumokat választottunk a szoftverben, megterveztük a sebészi sablont és a háromtagú azonnali ideiglenes hidat is.
A következő érvek szóltak a kezelés mellett:
• A páciens nem szeretett volna kivehető ideiglenes fogpótlást.
• Az azonnali ideiglenes híddal esztétikailag kielégítő eredményt tudunk elérni már a kezelés legelejétől.
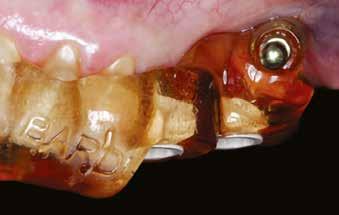
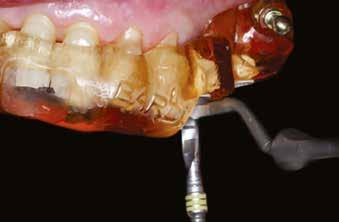

• A BLX implantátumok speciális formájának köszönhetően a primer stabilitás kellően nagy az azonnali terheléshez.
• A számítógépes tervezés csökkenti a sebészi beavatkozások invazivitását és egyszerűbbé teszi a protetikai munkát.
• A megfelelő mennyiségű feszes íny segíti a lebenyes feltárás elkerülését, tovább enyhítve a sebészi beavatkozás esetleges hatásait.
• Az esztétikai jellegű szövődmények esélyét csökkenti az előnyös anatómiai elhelyezkedés, megfelelő mennyiségű csont- és lágyszövet jelenléte.
A kezelés pontos menete
1. Diagnosztikus adatgyűjtés a kezelés megkezdése előtt: intra- és extraorális fotót készítettünk, lenyomatokat vettünk, diagnosztikus CT-sablont, majd azzal CBCT-felvétel készült.
2. A tanulmányi gipszmintákra helyezett diagnosztikus sablont beszkenneltük. STL-fájlokat hoztunk létre a szkennelt adatokból és digitális fogfelállítás történt (wax-up).
3. Az implantátumok pontos helyét megterveztük a coDiagnostiX® szoftverben a korábbi Dicom (CBCT) és STL-fájlok (felső tanulmányi minta, CT-sablon és wax-up) alapján.
4. A coDiagnostiX® terv alapján elkészíttettük a sebészi sablont.
5. A digitális wax-up alapján a fogtechnikus elkészítette az ideiglenes háromtagú hidat (a munkaminta 3D nyomtatott anyagból készült).
6. A műtét: az implantátumokat a sablon segítségével beültettük, majd szájba helyeztük az ideiglenes pótlást.
7. A gyógyulási idő leteltével a páciens kapott egy csavarral rögzülő, háromtagú hidat az implantátumokra.
A sebészi fázis
A műtét napján a páciens 0,12%-os klórhexidin-glükonát oldattal öblögetett. A beavatkozás előtt a műtéti területet (24–25 fogatlan gerincrész menti terület) az áthajlásba adott 2%-os lidokain injekcióval (1:100 000 adrenalin tartalommal) érzéstelenítettük (8. ábra).
A beavatkozáshoz a BLX rendszer irányított műtétekhez való eszközeit használtuk (9–10. ábra).
A sebészi sablont szájba helyeztük, majd ellenőriztük a fogaknak helyein kihagyott ablakoknál, hogy a megfelelő helyen van-e (11. ábra). Oldalnézetből láthatóak azok a hüvelyek, amelyeken keresztül pinekkel rögzíthető a sablon (12. ábra). Erre azért van szükség, hogy fúráskor a sablon tökéletesen stabil legyen. A rágósík felől jól látszik a sablon furatain keresztül a feszes íny kiterjedése, így lehetséges lebenymentes feltárásból dolgozni (13. ábra).
Az előfúrások előtt a sablonon keresztül egy körtrepánnal távolítottuk el az ínyt. Ebben a fázisban még nincs szükség a sablon rögzítésére (14. ábra). A sablont ezután kivettük és ellenőriztük, hogy megfelelő helyen készítettük elő az ínyt (15. ábra), majd a „gingiva pogácsákat” eltávolítottuk (16. ábra). Folyamatosan figyelve a sablon pontos pozíciójára, a fúróvezetőkön keresztül előfúrtuk az implantátumok helyeit (17–18. ábra).
A pinek (mindegyik saját furattal rendelkezik a sablonban) pontosan rögzítik a sablont a helyén és biztosítják a precíz és biztonságos előfúrást. A sablon fixálását követően (19. ábra) először egy maró fúróval (milling cutter) kiegyenlítettük a gerincéli csontot, hogy a további fúrókat biztonsággal tudjuk vezetni. A fúróvezető hüvelyek átmérőjét folyamatosan
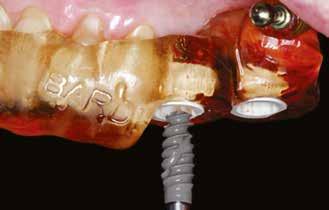

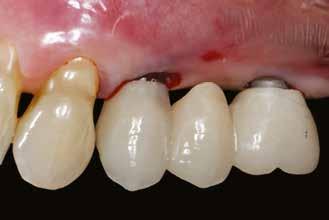
az adott fúrószárhoz igazítottuk. A felhasznált fúrók közül a milling cutter az egyetlen, amelyiken nincs stop (20. ábra). Az előfúrás bő, steril vízhűtés mellett történt, folyamatos, vertikális mozgatás mellett, hogy elkerüljük a csont túlmelegedését. A fúrók szekvenciája a következő volt: 2,2 mm átmérőjű jelölőfúró (21. ábra), ezután 2,8 mm, majd 3,5 mm átmérőjű előfúrók (22–23. ábra).
A coDiagnostiX® tervei alapján, a csontkínálatnak megfelelően, a 24 fog helyére egy 4,5 mm átmérőjű és 12 mm hosszú BLX implantátum került (24. ábra). Az implantátumot a gyártó utasításait követve távolítottuk el a fiolából (25. ábra).
Ezután az implantátumot a sablon vezetőhüvelyén keresztül behelyeztük (26. ábra). A BLX behelyezője és az implantátum akkor van megfelelő végpozícióban, ha a fekete vonal eléri a hüvely szélét (27. ábra). A 26 implantátum helyét ugyanúgy készítettük elő, mint a kisőrlőnél. Mivel a csont minősége rosszabb volt itt, mint az előző helyen, a 2,8 mm átmérőjű fúró volt az utolsó előfúró, amelyet használtunk. Itt is a korábbi coDiagnostiX® tervezés alapján választottuk ki az implantátum méretét: BLX 4,5 mm átmérő, 8 mm hosszúság.
A behelyezést követően ellenőriztük a behajtási nyomatékot és a primer stabilitást. Mindkét implantátumnál elegendőnek bizonyult az azonnali terheléshez (28–29. ábra).
A behelyezett implantátumokat a rágósík irányából szemügyre véve láthattuk, hogy térbeli elhelyezésük ideális (30. ábra). Ezt követően felhelyeztük az implantátumokra a technikus által individualizált ideiglenes protetikai fejeket (31. ábra), majd ellenőriztük az ideiglenes híd illeszkedését a fejeken (32. ábra). Látható, hogy az illeszkedés a precíz terve-
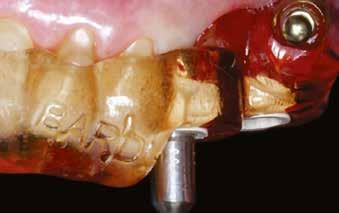
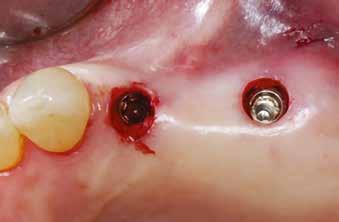
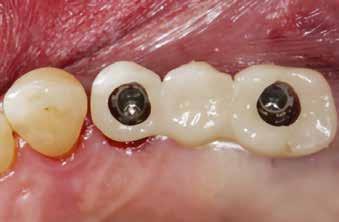
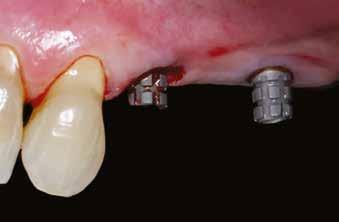
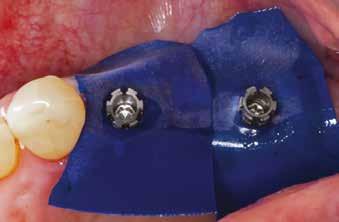
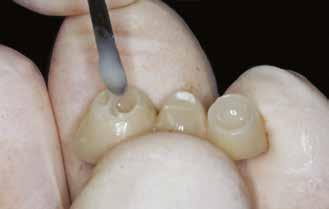
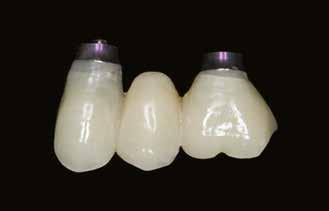
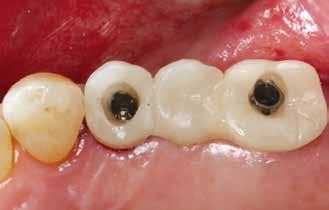
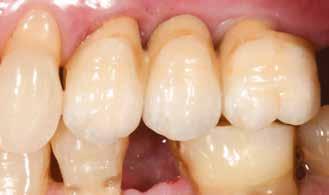
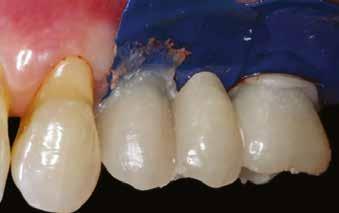
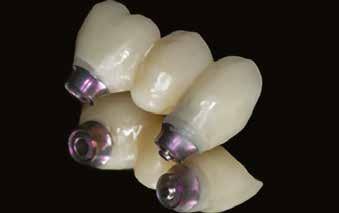
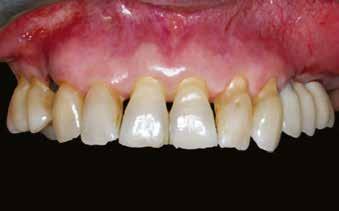
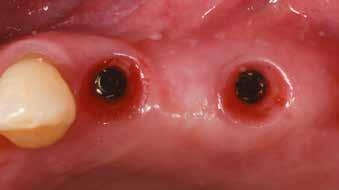
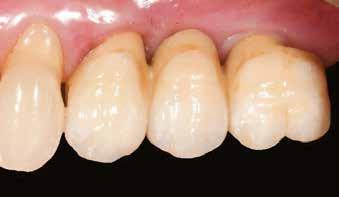
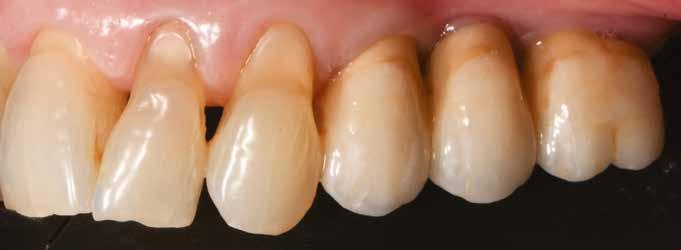
zésnek és kivitelezésnek köszönhetően tökéletes összhangban van a protetikai tervvel (33. ábra).
A műtéti területet izoláltuk kofferdam gumi segítségével, majd önkötő akriláttal rögzítettük a hidat a fejeken. Az izoláció főként lebenyes feltárások esetén nagy se -
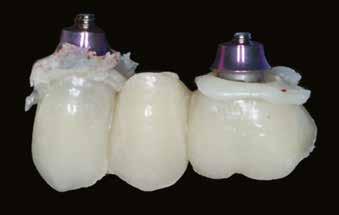
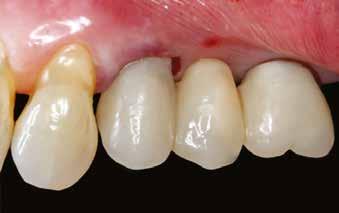
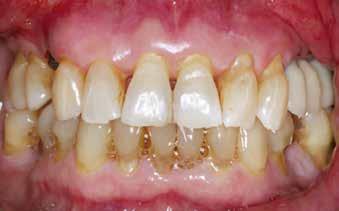
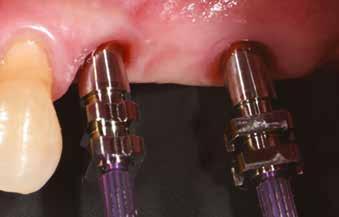
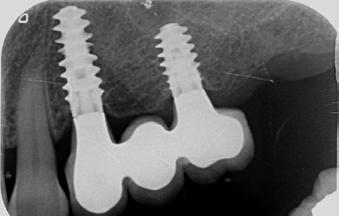
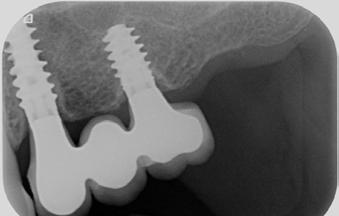
gítség, amikor nehezebb biztosítani az ideális viszonyokat a polimerizációhoz (34. ábra). Az ideiglenes hídra felvittünk egy vékony réteg akrilátot (35. ábra)
A felesleges műanyag eltávolítása után láthatjuk, milyen pontos az illeszkedés (36. ábra). A hidat ezután eltávolítottuk
a szájból a fejekkel együtt és teljesen kitöltöttük a fennmaradt réseket a fejek és a pótlás között, majd polimerizációt követően kidolgoztuk a felszíneket (37. ábra).
Először egy karbidfúró, majd egy előpolírozó gumi, és végül egy polírkorong segítségével dolgoztuk ki. A lágyrészekkel érintkező területeknél ügyeltünk arra, hogy minél simább és megfelelően domború felszíneket érjünk el ( 38. ábra). Gingivális nézetből látszik a helyes emergencia profil kialakítása, amely lehetővé teszi, hogy már a gyógyulás ideje alatt elkezdjük a lágy szövetek kondicionálását (39. ábra).
Az ideiglenes hidat átmenőcsavarokkal rögzítettük az implantátumokon (40–41. ábra)
A csavarnyílásokat zártuk és ellenőriztük a fogpótlás illeszkedését a maradék fogazatban, illetve a mosolyban (42. ábra). A hidat a harapásból kivettük, hogy a gyógyulás idejére ne terheljük túl az implantátumokat (43. ábra). A páciens mosolya közvetlenül a beavatkozást követően (44. ábra)
A páciens elégedett volt az esztétikai és a sebészi végeredménnyel is.
A protetikai fázis
A három hónapos kontroll alkalmával a páciensnek nem volt panasza és az ideiglenes fogpótlással elégedett volt. Az intraorális vizsgálat során látszott, hogy a formálásnak köszönhetően a lágyrészek lefutása harmonikus és természetes. A végleges lenyomatvételhez az ideiglenes hidat eltávolítot-
tuk és ellenőriztük az ínyt. Az implantátumok körüli feszes íny egészséges, az emergenciaprofil optimális (45. ábra). Ezt követően hagyományos analóg lenyomatokat vettünk (46. ábra).
A végleges pótlást átmenőcsavarokkal rögzítettük az implantátumokon (24 és 26), illetve az antagonista fogakra is új fogpótlás készült, hogy a harapást korrigáljuk (47–48. ábra).
A végső kontrollröntgenen látszik, milyen szépen integrálódtak az implantátumok és milyen pontos a végleges híd illeszkedése (49. ábra).
A kezelés eredménye
A kezelés végeredménye minden szempontból kielégítőnek bizonyult a páciens számára, sőt elmondása szerint jobb lett az életminősége. A fenntartó kezelés keretei között évente visszahívtuk kontrollra. Két év elteltével a páciens még mindig nagyon elégedett, az implantátumok körüli szövetek pedig szépen megtartottak (50–51. ábra).
Összegzés
Megfelelő indikáció esetén az azonnali implantáció és az azonnali terhelés csökkentheti a kezelés idejét és költségeit, valamint segíthet megőrizni a lágy szöveti adottságokat és kellemesebbé teheti a kezelést a páciens számára.
Forrás: EDI Journal 2023/3


SurgiTel® – mindennapi munkáját a világ egyik legfejlettebb eszközével támogatjuk. Az amerikai SurgiTel 1934 óta fejti ki professzionális tevékenységét az optikák világában. Legújabb nagyítós szemüveg modellje a SurgiTel ergo IQ a világ egyik vezető gyártójától.
• Extra széles munkatáv, tökéletes belátás a munkaterület egészén
• Minőségi optikai megoldások - maximális élesség, kristálytiszta kép kompromisszumok nélkül
• Ergonómikus kialakítás, terhelésmentesen a nyaknak, hátnak
• Brutális teljesítmény, parádés árakon.
06 30 942 7560 | dental@harmonycom.hu | www.harmonycom.hu
Dr. Révay András
A SIKER KULCSA A KIVÁLÓ CSAPAT
Szerényen, minden hivalkodó cégtábla nélkül működik Budapesten, a VII. kerületi Madách Imre út 11. szám alatt a VIP Dental diagnosztikai központja. Központi elhelyezkedése ellenére nem harsány jelenléttel, hanem szakmai reputációval vívta ki helyét a hazai fogászati diagnosztikában. A cég 20 éves fennállása alkalmából beszélgettünk Vékony Tiborral, aki sportolóból lett vállalkozó, majd egy országos hálózat vezetője.

Valóban érdekes életút. Hogyan indult mindez?
Szerencsés vagyok, mert egy olyan családból jövök, ahol a munka, a felelősség és a teljesítmény természetes érték volt. Édesapám sikeres vállalkozóként mindig példát mutatott. Már gyerekként láttam, mit jelent döntéseket hozni és hoszszú távon gondolkodni. Édesanyám az egészségügyben dolgozott aneszteziológiai asszisztensként, tőle az emberséget és a precizitást tanultam.
A sport szintén meghatározó volt az életemben. Harcművészetek, motorversenyzés, siklóernyőzés – mindig vonzott a kihívás. A Testnevelési Főiskolán tanultam tovább, később gazdasági tanulmányokat is folytattam. Ma már látom, hogy a fegyelem és a gazdasági szemlélet együtt alapozta meg a vállalkozói gondolkodásomat.
Ez valóban érdekes, de hogyan vezetett az út az autókereskedéstől a fogorvosokig?
Az első vállalkozásaim még nem az egészségügyhöz kö-
tődtek. Autókereskedelemmel és vendéglátással foglalkoztam. A fordulópont 2006-ban jött el, amikor édesapámmal felismertük: a hazai fogászati diagnosztikában komoly hiány mutatkozik modern, magánkézben működő 3D képalkotás terén.
Hosszas kutatás után az amerikai i-CAT CBCT technológia mellett döntöttünk. Nem csupán egy berendezést hoztunk be – egy új diagnosztikai szemléletet vezettünk be.
Mit szólt ehhez a szakma?
A 2D filmalapú diagnosztikáról 3D digitális rendszerre váltani szemléletváltást igényelt. Az első évek edukációval teltek, személyesen kerestem fel fogorvosokat, bemutattam a rendszert és segítettem az értelmezésben.
Az implantológiai beavatkozások számának növekedése és a fogászati turizmus fellendülése gyorsan igazolta a döntés helyességét. A CBCT felvételek szakmai és jogi biztonságot is jelentettek a kezelőorvosok számára.
Jártak-e különleges páciensek a rendelőkben?
A titoktartási kötelezettség elsődleges. Annyit azonban elmondhatok, hogy az elmúlt két évtizedben számos ismert közéleti és művészeti szereplő fordult meg nálunk. Ez számunkra elsősorban felelősséget jelentett.
Miért nem terjeszkedtek a nyugati határszél irányába?
A terjeszkedési döntéseket mindig szakmai és piaci alapon hozzuk meg. Miskolcon, Debrecenben és Székesfehérváron is központokat nyitottunk, hogy országos lefedettséget biztosítsunk.

Közben megérkezett a digitalizáció és a mesterséges intelligencia korszaka is. Hogyan hatott ez a munkára?
A digitális átállás minőségi ugrást hozott. A felvételek perceken belül eljutnak a partner fogorvosokhoz, a munkafolyamat gyorsabb és pontosabb lett.
A mesterséges intelligencia támogató eszközként segíti a diagnosztikai biztonságot, de nem helyettesíti az orvosi döntést.
Nem kellene az eddig felhalmozott tudást továbbadni?
Kreditpontos továbbképzéseket szervezünk, ahol a résztvevők saját számítógépen gyakorolják a digitális kiértékelést. Együttműködünk dr. Dobai Adrienne PhD radiológussal.
Mennyire elégedettek az orvosok és a páciensek?
Több ezer visszajelzés alapján 4,9-es Google-átlaggal működünk, ami a következetes minőségbiztosítás visszaigazolása.


Milyen tervei vannak a jövőre nézve?
Folyamatosan figyeljük a nemzetközi trendeket, és integrált diagnosztikai szolgáltatásainkat tovább bővítjük. Ennek részeként a Madách Imre úti központunkban elindítottuk vérvételi szolgáltatásunkat is, amel ylyel célunk, hogy a fogászati és általános diagnosztikai igényeket egy helyen, magas szakmai színvonalon tudjuk kiszolgálni. A szolgáltatást hamarosan debreceni központunkban is bevezetjük, így partnereink és pácienseink számára még komplexebb ellátást tudunk biztosítani.
A cél változatlan: biztonságot és pontosságot adni az orvosok kezébe a lehető legmodernebb technológiával.
Hogyan lehet ekkora terhelés mellett egyensúlyt tartani?
A család számomra stabil alap. A feleségemmel és kisfiammal töltött idő, valamint a sport biztosítja azt az egyensúlyt, amely nélkül hosszú távon nem lehet felelősen vezetni egy szervezetet.
BUDA
1027 - Budapest, Feketesas u. 3/b.
E-mail: info@vipdental.hu
Tel: 06-1-336-1168
Mobil: 06-30-680-8673
hétfő-péntek: 7.00 - 19.00 óráig
szombat: 8.00 - 13.00 óráig
PEST
1075 - Budapest, Madách Imre út 11.
E-mail: madach@vipdental.hu
Tel: 06-1-789-9755
Mobil: 06-20-513-0008
hétfő-péntek: 7.00 - 19.00 óráig
szombat: 8.00 - 13.00 óráig
DEBRECEN
4026 - Debrecen, Péterfia u. 31.
E-mail: debrecen@vipdental.hu
Tel: 06-52-531-933
Mobil: 06-20-364-2122
hétfő-péntek: 7.00 - 19.00 óráig szombat: 8.00 - 13.00 óráig
SZÉKESFEHÉRVÁR
8000 - Székesfehérvár, Seregélyesi út 17.
E-mail: fehervar@vipdental.hu
Tel: 06-22-612-040
Mobil: 06-20-974-9440
hétfő-péntek: 8.00-20.00 óráig
szombat: 8.00-13.00 óráig
Emilio Corvino, Paolo Pesce, Francesca Camodeca, Ofer Moses, Giuliano Iannello, Luigi Canullo (Olaszország)
KÉT KÜLÖNBÖZŐ CSATLAKOZÁSÚ IMPLANTÁTUMTÍPUS KLINIKAI ÉS
RADIOLÓGIAI ANALÍZISE: RANDOMIZÁLT, KONTROLLÁLT VIZSGÁLAT
Kulcsszavak
Implantátumcsatlakozás, implantátum mikrogeometria, implantátumstabilitás, implantátumstabilitás hányados, marginális csontszint, neurális hálózat, randomizált, kontrollált vizsgálat, váll nélküli preparáció, cirkóniumfelépítmény
Absztrakt
Bevezetés: A periimplantáris, marginális csontveszteséget az implantátum–felépítmény együttes és a szövetek közötti kölcsönhatások befolyásolják. Az implantátum és a felépítmény közötti kapcsolat geometriája a periimplantáris csontátépülés egyik legrelevánsabb faktorjának számít. Célkitűzések: Az elsődleges cél az azonos makrogeometriájú, de két különböző kapcsolattal rendelkező implantátumok radiológiai és klinikai összehasonlítása volt. A másodlagos cél az implantátumok túlélési és sikerrátájának, a primer és szekunder stabilitásnak, illetve a marginális csontszint és a klinikai változók közötti korrelációjának vizsgálata volt. Ezenfelül létrehoztunk és vizsgáltunk egy neurális hálózatot annak előrejelzésére, hogy milyen hatással van a behelyezési nyomatékgörbe a marginális csontvesztésre. Anyagok és módszerek: A páciensek, akiknek a posterior régióban legalább 2 implantátumbeültetése volt indikált, random módon lettek két csoportra osztva. Az azonos mikro- és makrotopográfiával rendelkező implantátumok különböző belső kapcsolattal rendelkeztek: kónuszos standard (conical standard, „CS”) vagy belső hexagonális (internal hex „IH”). Az implantátum beültetésekor (T0) vizsgáltuk a behelyezési nyomatékot, az implantátum stabilitását (az implantátumstabilitás hányados értékét rezonanciafrekvencia-analízissel mértük), a lágyszöveti magasságot és a keratinizált gingiva mennyiségét. A stabilitást újra vizsgáltuk a „one-abutment one-time” koncepció szerint és teljes mértékben digitális munkafolyamatban végzett protetikai csatlakoztatás időpontjában (második fázisú műtét). Az implantátum terhelése után 6 hónappal és 1 évvel értékeltük a parodontális paramétereket, és periapikális röntgenfelvételeket készítettünk. A két csoport és a különböző változók közötti különbségek vizsgálatára páros t-próbát és az általánosított becslési egyenlet modelleket alkalmaztuk. Klaszteranalízist alkalmaztunk a behelyezési nyomaték/klinikai profil és a marginális csontszint változása közötti korreláció értékelésére.
Eredmények: Összesen 33 páciens (17 férfi, 16 nő, átlagéletkor 67,4 ± 14,5 év) vett részt a kutatásban. Kizárásra nem került sor. 53 implantátumot (26 CS és 27 IH) ültettünk a maxillába és 15-öt (8 CS és 7 IH) a mandibulába. Minden egyes implantátumbeültetés sikeres volt. A marginális csontveszteség a protetikai terhelés után 6 hónappal a CS kapcsolat esetében 0,33 ± 0,34 mm, az IH esetében 0,43 ± 0,37 mm volt (p=0,125); 1 év után pedig 0,48 ± 0,18 mm volt a CS kapcsolat esetében és 0,57±0,24 mm az IH csoportban. Szignifikáns különbség volt kimutatható a teszt- és a kontrollcsoport implantátumstabilitás hányados értékei között az implantátum beültetésekor (p=0,03) és a második fázisú műtétnél (p=0,000122). Az általánosított becslési egyenlet modell azt mutatta, hogy a lágyrészek magassága (p=0,012), a keratinizált gingiva (p=0,05) és a behelyezési nyomaték (p=0,042) szignifikáns hatással volt a marginális csontvesztésre, míg a többi változó esetében nem mutatkozott statisztikai különbség. A neurális hálózat érzékeny, pontos, precíz és specifikus volt.
Következtetések: Jelen kutatás kimutatta, hogy a különböző implantátum–felépítmény kapcsolatok azonos implantátum makrogeometria mellett szignifikáns hatással vannak a marginális csontvesztésre. A CS csoportban jobb eredmények mutatkoztak az IH csoporthoz képest. A marginális csontveszteséget különböző egyéni és klinikai tényezők is befolyásolják.
Összeférhetetlenségi nyilatkozat: A szerzők nyilatkoznak, hogy a kutatáshoz kapcsolódó összeférhetetlenség nem áll fenn.
Bevezetés
A periimplantáris lágyszövetek és a csontkontúrok stabilitása az implantátumokon elhorgonyzott fogpótlások hosszú távú egészségének, funkciójának és esztétikájának feltétele [1], habár az implantátumok bizonyos mértékű csontreszorpcióval járnak [2].
A periimplantáris marginális csontszint (marginal bone level, „MBL”) változása az élő lágy- és keményszövetek és az implantátum–felépítmény egysége közötti interakciók eredménye, bizonyos időpontokban. Elsőként a sebészi fázis során történhet csontvesztés, úgymint a lebenyképzés [3], a csontfúrás [4], az implantátum behelyezésével járó csontkompresszió [5–6] és az implantátum háromdimenziós pozicionálása során [7–8].
A csontintegrációt követően, a periimplantáris szövetek a protetikai protokolloknak megfelelően, folyamatos átalakuláson mennek keresztül. Úgy tűnik, hogy ez a fázis leginkább az implantátum–felépítmény morfológiájával, illetve felületével [9–11] és az implantátum és felépítmény közötti kapcsolat (implant-abutment junction, „IAJ”) kontaminációjával mutat összefüggést [12]. E mikrohézag bakteriális inváziója a periimplantáris szövetekben a „biológiai szélesség helyreállításának” nevezett reakciót idézheti elő, amely klinikailag és radiológiailag az első év során mutatkozik [13–15]. Az okkluzális terhelés [16–17] (habár még nem bizonyították), a marginális csont további remodellációjához vezethet. Ezen felül a vertikális lágyszöveti vastagság [18–19] és a protetikai fej magassága [20–21] is befolyásoló tényezők lehetnek a korai csontvesztésben. Természetesen a csontveszteség szoros kapcsolatban áll a páciensre jellemző gyulladásos válasszal is [22–23]. Egészséges körülmények között azonban ez egy stabil állapot, amelyet egyes szerzők úgy emlegetnek, mint a gazdatest idegen testhez való alkalmazkodása [24].
Az implantátum és a felépítmény közötti kapcsolat stabilitása az implantátumon elhorgonyzott fogpótlások sikerének egyik kulcstényezője [25–27]. Az implantátum és a felépítmény közötti bakteriális „mikroszivárgás” a csontszintű implantátumok gyenge pontját jelentheti, az implantátum körüli szövetek esetleges kontaminációja miatt [28]. Tekintettel arra, hogy egyik típusú implantátumcsatlakozásról sem bizonyosodott be, hogy megakadályozná a bakteriális kontaminációt [29], az IAJ biomechanikai stabilitása szignifikáns korrelációt mutat a két komponens közötti háromdimenziós pontossággal és illeszkedéssel [30]. Ez pedig szoros összefüggést mutat a biomechanikával az ionos oldatként ható nyál jelenlétében [31–32].
A csont átalakulása azonban nem csak a csontszövet és az implantátum–felépítmény egysége közötti kölcsönhatás közvetlen következménye; úgy tűnik, hogy a lágyrész management is része ennek a folyamatnak. A hagyományos protetikai munkafolyamat az implantátum felszabadítását követően 2 héttel lenyomatvételt, majd további 2 hét után ideiglenes fogpótlás elkészítését foglalja magában. Ezen eljárások a gyógyulás granulációs/kontrakciós és érési fázisában történnek [33]. Szövettani szempontból tehát a protetikai komponensek ismételt szét- és visszacsatlakoztatása – ahogyan az általában a hagyományos protetikai eljárások esetében történik – károsíthatja a kötőszöveti zárást, ez pedig klinikailag, már korai stádiumban is nyilvánvaló, hámszöveti leépüléshez vezethet [34–36].
Mind a klinikusok, mind pedig az irodalomban leírtak szerint, a második műtéti eljárás során alkalmazott definitív felépítmény használata („one-abutment one-time” protokoll) minimalizálhatja a periimplantáris csont-remodellinget [37–39].
A kutatás céljai
A kutatás elsődleges célja volt az azonos mikro- és makroszerkezettel, de eltérő csatlakozással rendelkező implantátumok klinikai és radiológiai paramétereinek összehasonlítása 1 év után. A „one-abutment one-time” protokollt alkalmaztuk,
hogy minimalizáljuk a sebészeti és protetikai fázisokkal járó torzításokat, illetve, hogy maximalizáljuk a csatlakozások marginális csontszint változásaira kifejtett hatását.
A másodlagos cél az implantátum sikerességi rátájának, illetve primer és szekunder stabilitásának mérése volt (csontszintű röntgenfelvételekkel és a stabilitás hányados – Implant Stability Quotient, „ISQ” – értékeivel). Célunk volt továbbá kifejleszteni és vizsgálni egy neurális hálózatot annak érdekében, hogy a betekerési nyomatékgörbe marginális csontvesztésre kifejtett hatása előrejelezhető legyen.
Anyagok és módszerek
Jelen kutatás randomizált, kontrollált vizsgálat volt. A beválasztási kritériumok az alábbiak voltak:
• tájékoztató és beleegyező nyilatkozat aláírása;
• 25 év és afeletti életkor;
• legalább 2 szomszédos implantátumon elhorgonyzott korona indikációja az alsó vagy felső állcsontban;
• Kennedy I., II. és III. osztályú foghiány;
• az implantálás előtt legalább 6 hónappal történt a fogeltávolítás;
• elégséges csontmennyiség az implantáláshoz, augmentáció nélkül.
Kizárási kritériumok:
• várandósság vagy szoptatás;
• erős dohányzás (több mint 10 szál cigaretta/nap);
• antikoaguláns kezelés (INR 1.8 alatt), biszfoszfonát, szteroid vagy antikonvulzív terápia;
• regenerált csont;
• azonnali terhelésű implantátumok;
• kezeletlen parodontológiai betegség, vagy ha megoldhatatlan a vizsgálati követelményeknek megfelelő, optimális szájhigiénia fenntartása (plakk-index > 30%);
• az anamnézisben szereplő alkohol, narkotikum vagy drog abúzus (alkoholizmus: több mint 2 korsó sör/nap);
• folyamatban lévő radioterápia, kemoterápia vagy egyéb immunszuppresszív terápia, illetve az elmúlt 5 évben kapott sugárkezelés (a fej-nyaki régiót érintő sugárkezelés minden esetben kizárásra került függetlenül a kezelés időpontjától);
• metabolikus csontbetegségek;
• kontrollálatlan vérzészavar, úgymint hemofília, trombocitopénia, granulocitopénia;
• degeneratív betegségek;
• az anamnézisben szereplő oszteonekrózis az állcsontban;
• veseelégtelenség;
• szervátültetésen átesett páciensek;
• HIV-pozitvitás;
• rosszindulatú elváltozás;
• immunhiánnyal járó betegség;
• kezeletlen diabetes mellitus (glikált hemoglobin 6,5 felett);
• kezeletlen endokrin betegségek;
• pszichotikus zavarok;
• túlérzékenység az implantátum valamelyik összetevőjével, különösen a titánnal szemben;
• kooperáció hiánya;




1. a–d ábra: A két alkalmazott implantátum–felépítmény csatlakozási típusok: kónikus (a–b) és belső hexagonális (c–d).
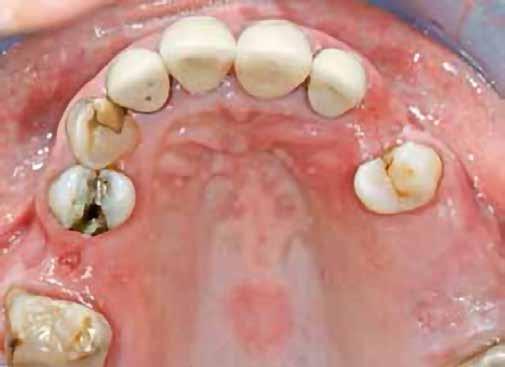
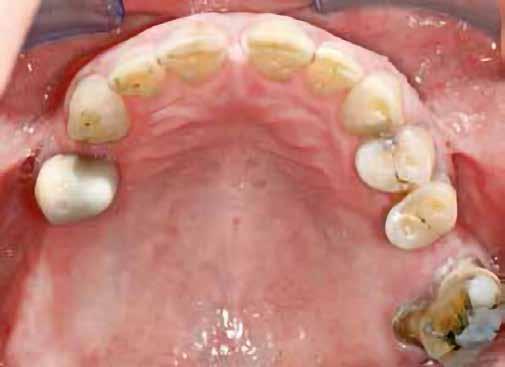
2. a–b ábra: A preoperatív állapot okkluzális nézete a belső hexagonális (IH) csoportban (a) és a kónikus standard (CS) csoportban (b).
• parafunkciók, például bruxizmus vagy temporomandibuláris ízületi elváltozások;
• a szájnyálkahártya különböző elváltozásai, úgymint jóindulatú nyálkahártya pemphigoid, desquamatív ínygyulladás, erozív lichen planus, a szájüreg malignus elváltozásai és a szájnyálkahártya bullózus, erozív elváltozásai;
• lebenyképzés nélküli beavatkozás;
• 5-ös csontdenzitás érték (CT: <150 Hounsfield érték).
A beválasztott pácienseket felkértük a vizsgálatban való részvételre és a vizsgálati protokoll bemutatását követően írásbeli beleegyezésüket adták. A páciensek toborzása és kezelése egy magánrendelőben történt Rómában, Olaszországban, 2018. január és 2018. október között. A vizsgálatot a Helsinki Nyilatkozatban foglalt elvek szerint végeztük.
Randomizálási eljárás
Tekintettel arra, hogy jelen kutatás prospektív megfigyeléses vizsgálat volt, a minta méretének kalkulációja a G*Power 3.1.3 programmal történt (v. 10.7.2; Düsseldorfi Egyetem, Düsseldorf, Németország, http://www.psycho.uni-duesseldorf.de/ abteilun- gen/aap/gpower3/), amely a dz=0,5 hatásméret, α hibavalószínűség=0,05 és teljesítmény=0,80 (1-β hibavalószínűség) mellett a 34-es betegszámot eredményezte.
A betegek randomizálásához a Random Number Generator Pro (v. 1.91; Segobit Software, Moszkva, Oroszország, http:// www.segobit.com) segítségével véletlen számsorozat lett létrehozva. Az áttekinthetetlen borítékokat a generált lista szerint számoztuk meg. Minden egyes borítékot egy független harmadik fél készített elő, és minden pácienst véletlenszerűen osztottunk be a két implantátumcsoport egyikébe (1. ábra).
Preoperatív vizsgálatok
A műtét előtt 1-2 héttel, preoperatívan, az összes, a vizsgálatba bevont betegről szájfotókat készítettünk (2. ábra), és az alsó és felső állcsontról intraorális szkenner (CS 3600, Carestream Dental, Atlanta, GA, USA) segítségével lenyomatot vettünk. Ezt követően a CBCT-felvételek elemzése történt, amelyhez irányított sebészeti szoftvert is alkalmaztunk (Implant 3D, Media Lab, Milánó, Olaszország). A digitális projektet ezután elküldtük Bionovába (Genova, Olaszország) a sebészi sablonok elkészítésének céljából. Ennek a lépésnek az volt a célja, hogy elkerüljük a rendellenes okkluzális terhelési mintázattal és a végleges fogpótlás természetellenes emergenciaprofiljával kapcsolatos torzításokat, amelyek befolyásolhatják az orálhigiénia fenntartását. Szükség esetén parodontológiai kezelést végeztünk.
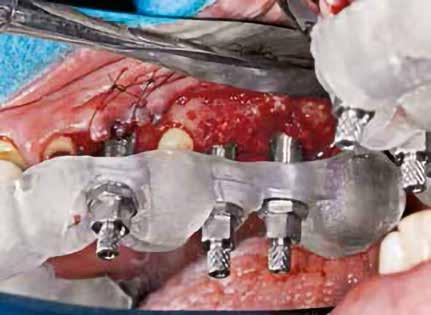
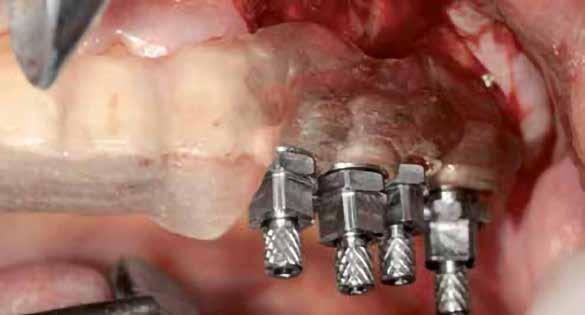
tervezett sebészi sablon és implantátumbeültetés az IH (a) és a CS (b) csoportban.
Sebészeti fázis
Tapasztalt sebész (LC) végzett minden beavatkozást. A páciensek 0,2% klórhexidines szájöblögetést (GUM Paroex 0.2%, Sunstar Suisse, Etoy, Svájc) végeztek naponta 2x, az implantátum beültetése előtt 3 nappal kezdődően és 1 hétig folytatva a műtét után; illetve a beavatkozás előtt 1 órával 2 g antibiotikumot kaptak profilaktikus célból (875 mg amoxicillin és 125 mg klavulánsav, Augmentin, Glaxo SmithKline, Verona, Olaszország).
A helyi érzéstelenítés 4% articain 1:100 000 adrenalin oldattal történt (Ubistesin, 3M ESPE, Seefeld, Németország). Kis méretű lebenyt képeztünk, hogy megelőzzük a periosteum sérülését és megőrizzük a műtéti terület vérellátását a gyógyulási időszak alatt. A lebenyképzést követően felhelyeztük a sebészi sablont és előkészítettük az implantátum helyét a gyártó előírása szerint (3. ábra).
A lebenyképzés után közvetlenül egy asszisztens (EC) jelezte, hogy melyik implantátumot kell behelyezni a sorszámozott borítékban szereplő instrukciók alapján.
A randomizációs eljárás alapján a pácienseket vagy a tesztcsoportba (2 vagy több implantátum kónikus kapcsolattal; NeO Conical Standard [CS], Alpha-Bio Tec, Petah Tikva, Izrael), vagy a kontrollcsoportba (2 vagy több implantátum belső hexagonális kapcsolattal; NeO Internal Hex [IH], Alpha-Bio Tec) osztottuk. Mindkét csoportban ugyanaz a mak-
rotopográfia volt megfigyelhető: az implantátum nyakának koronális része egyenes, mikromenetekkel és homokfúvott, savval maratott felület (NanoTec Implant Surface, Alpha-Bio Tec) egészen a legfelső részig. A koronális vágófuratok segítik a csontszövet átvágását, ezáltal csökken az implantátumágyra gyakorolt nyomás. A menetek kialakítása az implantátum hossza mentén változó, 2,4 mm-es éles sarkos menettel kezdődik, a főmenetek között két mikromenettel. Az implantátumnak kónikus a belső csavarmenete és az apexe, illetve enyhén kónikus a teste. Maga az apex keskeny (2,9 mm), éles menettel, csontkondenzáló furatokkal és szabadalmaztatott centrálási funkcióval.
Az IH platform 2,5 mm-es belső hatszögletű, 45 fokos kúpossággal és 3,5 mm-es platformátmérővel, míg a CS platform 2,5 mm-es belső hatszögletű, 11 fokos kúpossággal és 3,1 mm-es platformátmérővel (1. ábra). Mindkét implantátumrendszer esetében platform switchinget alkalmaztunk, a CS rendszer esetében nagyobb eltéréssel. Valamennyi implantátum 10 mm hosszú és 3,75 mm átmérőjű volt, és az implantátumokat 0,5 mm-rel szubkresztálisan helyeztük be, a gyártó ajánlásait követve. A csontszintet parodontális szondával mértük.
A behelyezési nyomatékértékeket az Elcomed SA-310 készülékkel (W&H, Bürmoos, Ausztria) mértük. A behelyezést követően a SmartPegs készülékkel (Osstell, Gothenburg, Svédország) mértük az implantátumok primer
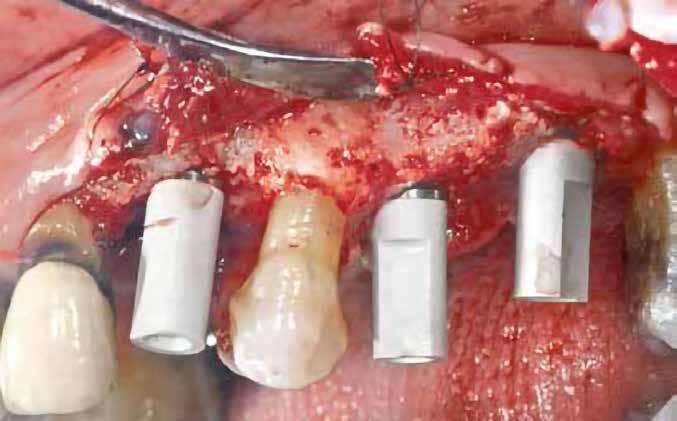
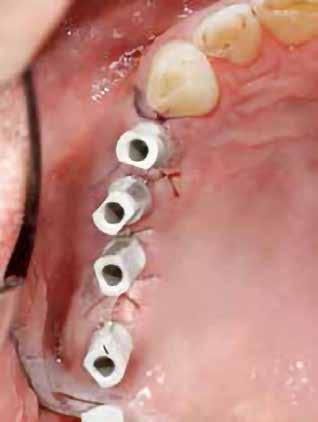
a–b
Az intraoperatív lenyomatvételhez szükséges „scan body”-k az IH (a) és a CS (b) csoportban.
3. a–b ábra: Számítógéppel
4.
ábra:
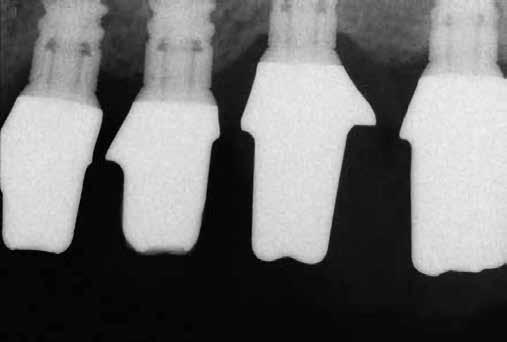
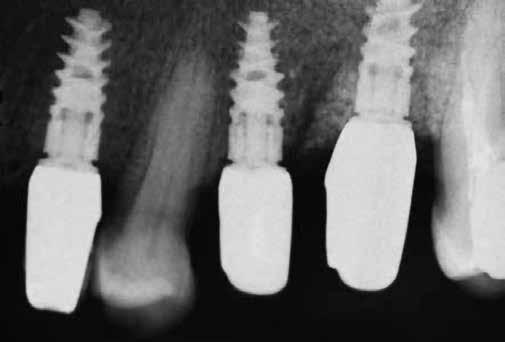
5. a–b ábra: Intraorális röntgenfelvételek, amelyeken a cementtel rögzített ideiglenes koronák láthatók az IH (a) és CS (b) csoportban.
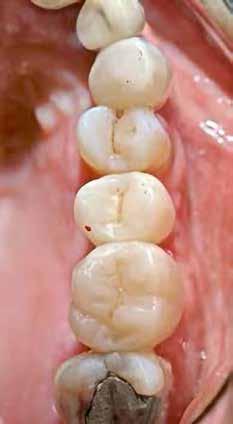
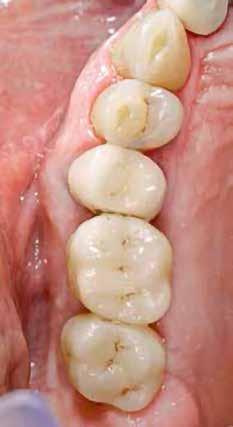
6. a-b. ábra A végleges cirkóniumrestaurációk okkluzális nézete az IH (a) és a CS (b) csoportban.
stabilitását. Ezt követően egy speciális, digitális lenyomatvételre szolgáló fejet csatlakoztattunk az implantátumhoz (4. ábra), és digitális lenyomatot vettünk [40]. Kétfázisú eljárást alkalmaztunk, amely azt jelenti, hogy a beültetett implantátumot lefedve, a sebet egyszerű csomós öltésekkel zártuk (Cytoplast nem felszívódó politet -
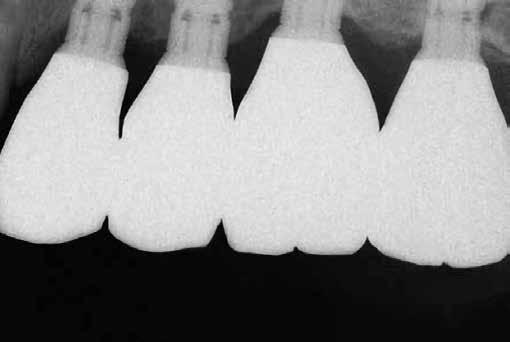
rafluoroetilén [PTFE] varratok, Osteogenics Biomedical, Lubbock, TX, USA; PTFE varratok, De Ore Biomaterials, Negrar, Olaszország).
Posztoperatív instrukciók a betegek számára
Negyven napig tartó kímélő étrendet és puha fogkefe használatát javasoltuk. Fájdalomcsillapításra 600 mg Ibuprofent írtunk fel, 6–8 óránként szedve, 1 héten keresztül. A varratokat a műtét után 2 héttel távolítottuk el.
Protetikai fázis
Az implantátumokat a mandibulából 8, a maxillából 12 héttel a beültetés után szabadítottuk fel (második fázisú műtét). A szekunder stabilitás értékelésére meghatároztuk az ISQ értékeket.
A végleges, CAD-CAM cirkóniumfejet 30 Ncm-rel a Torq Control nyomatékkulccsal (Anthogyr, Sallanches, Franciaország) húztuk meg.
Szájba helyezés előtt minden pótlás és átmenőcsavar antiszeptikus ultrahangfürdőbe került 10 percre, majd 90%-os alkohololdatba 20 percig tisztítás és fertőtlení-
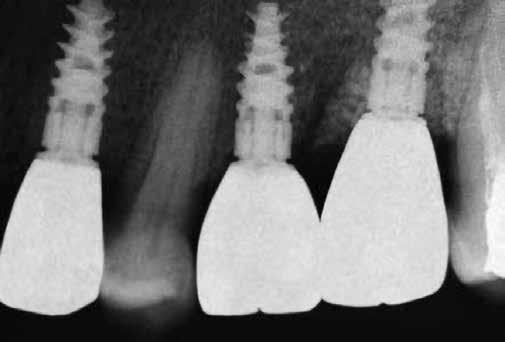
7. a–b. ábra: Intraorális röntgenfelvételek a végleges, cementtel rögzített részleges, lemezes fogpótlásról, 1 évvel a terhelés után az IH (a) és a CS (b) csoportban.
tés céljából [41]. Az implantátumcsatlakozásokat szintén fertőtlenítettük, ezt klórhexidin-diglukonáttal végeztük 1 percig. A rögzítést követően a cirkónium-dioxid felépítményeket véglegesítettük; az átmenőcsavarok nyílásait PTFE szalaggal zártuk le és kompozittal töltöttük ki (5. ábra). Minden páciens ideiglenes, cementrögzítésű koronákat kapott (Temp-Bond, Kerr Dental, Pomona, CA, USA).
A végleges cirkóniumkoronákat ideiglenes cementtel rögzítettük, 1 hónappal a felépítmény behelyezése után (6. ábra). A fogpótlás átadásakor az okklúzió is beállításra került.
A pácienseket 6 és 12 hónap múlva kontrollvizsgálatra hívtuk vissza, amelyek során periapikális röntgenfelvételeket készítettünk (7. ábra).
Vizsgálati eredmények
Az elsődleges vizsgált paraméter a periimplantáris csontveszteség volt, amelyet az implantátum beültetésekor (kiindulási állapot, T0), a 6 hónapos (T1) és az 1 éves (T2) kontrollvizsgálat során készült digitális periapikális röntgenfelvételek alapján számítottunk ki.
Egy független értékelő egyedi röntgenfelvétel-tartó és párhuzamos technika segítségével készítette az intraorális röntgenfelvételeket. Minden röntgenfelvételt egy képelemző szoftver által (Auto-CAD 2019 23.0, Autodesk, San Rafael, CA, USA) egy 24 inch méretű, folyadékkristályos kijelzőn (iMac, Apple, Cupertino, CA, USA) jelenítettünk meg, és standardizált körülmények között (ISO 12646:2004) értékeltünk ki.
Az MBL-változások mérésére elfogadott protokollt Canullo és munkatársai írták le [42]. A különböző időpontokban bekövetkezett MBL-változások közötti különbséget tekintettük csontvesztésnek.
Egy független fogorvos (FC) – aki addig nem vett részt a kutatásban – végezte a csontmagasságméréseket.
A másodlagos vizsgálati paraméterek az alábbiak voltak: a fogpótlásokat és az implantátumokat érintő olyan rendellenességek, amelyek az eltávolításukat tették szükségessé; a teljes követési időszak alatt bekövetkezett sebészeti és protetikai komplikációk; a rezonanciafrekvencia-analízis (RFA) értékei az implantátum behelyezésekor és terhelést követően (8 hét a mandibula és 12 hét a maxilla esetében); valamint a behelyezési nyomatékgörbe és a csontveszteség közötti összefüggés.
Az ISQ-értékeket RFA segítségével rögzítettük. Egy független eredményértékelő (FC) végezte az RFA-méréseket, aki nem vett részt a kutatás klinikai részében.
Az értékeket az Osstell Mentor készülékkel (Osstell) regisztráltuk. Minden implantátum esetében két mérést végeztünk: egyet buccopalatinalisan a buccalis oldalról, egyet pedig mesiodistalisan a mesialis oldalról. Az eredményeket a készülék ISQ-egységekben jelenítette meg 1 és 100 között, és e mérések átlagát használtuk.
A betekerési nyomatékgörbék hatásának értékeléséhez kiszámítottuk a görbék alatt lévő területet. A lágy szövetek vertikális vastagságát parodontális szondával mértük T0 időpontban, azaz az implantátum behelyezése előtt. A keratinizált gingivát buccalisan, a buccalis széltől a mucogingivális átmenetig mértük a végleges fogpótlás beragasztásakor. Az utolsó kontrollvizsgálat alkalmával, parodontális szondával (PCP15, Hu-Friedy, Chicago, IL, USA) vizsgáltuk a szondázási vérzést (BoP) és a plakkindexet (PI). A BoP-t minden implantátum körül négy pontban vizsgáltuk (mesialisan, distalisan, buccalisan és lingualisan). A PI-t, amely a felépítmény–restauráció egységén lévő plakk jelenlétét jelöli, úgy pontoztuk, hogy a parodontális szondát az implantátum körül, a felépítmény felszínével párhuzamosan vezettük.
Statisztikai kiértékelés
A statisztikai analízist a numerikus paraméterek, úgymint az MBL-változás, a csontveszteség és az ISQ-értékek tekintetében SPSS program (v. 18.0; SPSS, Chicago, IL, USA) segítségével végeztük. A leíró elemzést átlag 1 standard deviáció (medián és 95%-os konfidenciaintervallum) segítségével végeztük. A páciensek voltak az elemzés statisztikai egységei. Az egyes időpontok közötti összehasonlításokat minden csoport esetében páros t-próbával végeztük azért, hogy az utánkövetés során a periimplantáris MBL-ben bekövetkezett változásokat kimutassuk. A folyamatos eredmények (röntgenen látható MBL-változások és ISQ-értékek) csoportonkénti átlagainak különbségeit páros t-próbával hasonlítottuk össze.
Neurális hálózat
A vizsgálatba bevont 68 implantátumból 48-at használtunk fel a neurális hálózat kifejlesztéséhez. A 10 másodperces időközönként rögzített nyomatékgörbe-értékeket használtuk bemeneti változóként. Összesen 24 implantátumot választottunk ki véletlenszerűen gyakorlatra, a maradék 24-et pedig tesztelésre használtuk. A gyakorlati készletet a neurális hálózat paramétereinek
2. táblázat: A regresszió-analízis eredménye. df = szabadságfok; F=mintaátlagok/minták közötti eltérés; MS = tapasztalati szórásnégyzet; SS = négyzetösszeg *Az jelölt területet az x-tengely (idő) és a nyomatékgörbe határolja.
beállítására, a tesztkészletet pedig a modell teljesítményének értékelésére használtuk. A neurális hálózat osztályozási képességét a bináris osztályozás eredményeként kapott négy eredményből képzett hibamátrix segítségével mértük.
Eredmények
Harminchárom pácienst (17 férfi, 16 nő, átlagéletkor 67,4 ± 14,5 év) kezeltünk, akiknek legalább két implantátumon elhorgonyzott koronára volt szükségük. Összesen 68 implantátumot ültettünk be (34 CS és 34 IH), 53-at (26 CS és 27 IH) a maxillába és 15-öt (8 CS és 7 IH) a mandibulába. Nem volt sikertelen implantátumbeültetés, és egy beteget sem zártunk ki a vizsgálatból a műtétet követő első évben.
A műtét előtti függőleges, lágyszöveti magasság 2,71 mm (SD: 1,1) volt. A preoperatív vastagság (függőleges magasság) 2,78 mm (SD: 0,999) volt a kontrollcsoportban és 2,65 mm (SD: 1,23) a tesztcsoportban. Statisztikailag nem volt szignifikáns különbség a két csoport között. A demográfiai adatokat az 1. táblázat foglalja össze.
szignifikáns szerepet (2. táblázat). Regresszió-analízis
Marginális csontveszteség
A marginális csontveszteség 6 hónap után 0,33 ± 0,34 mm volt a CS csoportban, és 0,43 ± 0,37 mm az IH esetében (p=0,125). 1 év után 0,48 ± 0,18 mm volt a CS és 0,57 ± 0,24 mm az IH esetében (8. ábra), statisztikailag szignifikáns különbséget eredményezve a csoportok között (p=0,043). A csoportokon belüli különbségek a 6 hónapos és az 1 éves kontrollvizsgálatok között statisztikailag szignifikánsak voltak (p=0,014 a CS csoportban és p=0,036 az IH esetében).
A regressziós modell, amelyet annak meghatározására alkottak meg, hogy a nem, az életkor, a fogeltávolítás oka, az implantáció helye, a biotípus, a lágyrész magassága, a keratinizált gingiva, a csatlakozás, a legnagyobb behelyezési nyomatékérték és a behelyezési nyomatékgörbe alatti terület hogyan befolyásolja az MBL-t, p=0,018 és R2=51% eredményt adott, így megállapítható, hogy ez a modell jól alkalmazható. A regressziós együtthatók értelmezése azt mutatja, hogy a nem (p=0,05), a keratinizált gingiva (p=0,05), a csatlakozás (p=0,029) és a behelyezési nyomatékgörbe alatti terület (p=0,019) jelentősen befolyásolhatja az MBL-t, míg a többi változó nem játszott























Implantátum/protetikai sikertelenség és sebészeti/ protetikai komplikációk
Nem fordult elő a fogpótlások és az implantátumok olyan hibája a teljes követési időszak alatt, amely az eltávolításukat tette volna szükségessé, illetve műtéti vagy protetikai komplikáció sem lépett fel.
Implantátumstabilitás
Statisztikailag szignifikáns különbség volt a teszt- és a kontrollcsoport ISQ-értékei között a T0 időpontban (p=0,03) és a második műtétkor (p=0,000122), valamint az implantátum behelyezésekor (T0) (70,5 ± 9,7) és a második műtét alkalmával mért értékek között (76,1 ± 7,2), függetlenül a csatlakozás típusától (p=0,000523) (8. ábra).
Az ISQ-érték T0-ban 68,6 ± 9,1 mm volt a CS és 73 ± 9,8 mm az IH csoportban, a 3 hónapos kontrollon pedig ez az érték 72,9 ± 7,5 mm volt a CS esetében és 79,3 ± 5,2 mm az IH esetében.
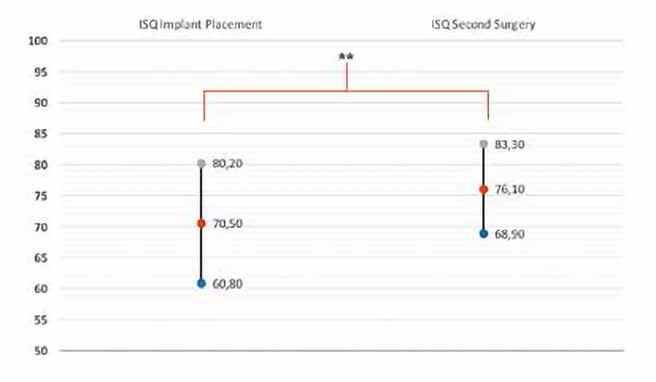
8. ábra: ISQ értékek: átlagértékek és szórás az implantátum beültetésekor és a második műtétkor.
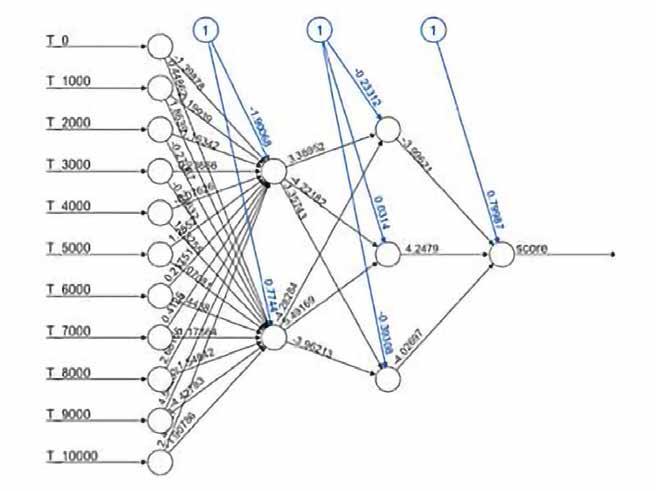
9. ábra: Az „R neuralnet library” (R Foundation for Statistical Computing, Bécs, Ausztria) segítségével létrehozott és az R plot funkcióval megjelenített neurális hálózati modell grafikus ábrázolása. A bal oldalon a T_ttt tizenegy bemeneti csomópont látható. Minden egyes általános T_ttt csomópont a ttt/100 mp időpontban vett mintát jelenti, a belső csomópontok a hálózat rétegét jelentik, a jobb szélső csomópont (score) pedig a hálózat által előállított kategorikus kimenetet jelöli. A fekete vonalak az egyes rétegek közötti kapcsolatokat mutatják (minden kapcsolat a hozzá tartozó súlyokkal van jelölve), míg a kék vonalak a hálózat aktiválási funkciójához a legjobb illeszkedés javítása érdekében hozzáadott torzító kifejezést mutatják.
BoP és PI
Az utolsó kontrollvizsgálat alkalmával az átlagos PI 1, az átlagos BoP pedig 0,6 volt. A két csoport között nem találtunk különbséget.
Neurális hálózat
A neurális hálózat teljesítményét a bináris osztályozás eredményeként kapott négy eredményből képzett hibamátrix segítségével mértük, amely jó érzékenységet (0,917) és pontosságot (0,833), valamint viszonylag jó precizitást (0,786) és specifikusságot (0,750) mutatott. A modell grafikus ábrázolása a 9. ábrán látható.
Megbeszélés
Számos tanulmány vizsgálta a marginális csontveszteség és az implantátum–felépítmény csatlakozása közötti összefüggést. Ezen kutatások különböző implantátumrendszereket [43], felépítményszintű vagy implantátumszintű protetikai kapcsolatot [44], belső és külső kapcsolatot [45], különböző implantátumnyak-morfológiát [46] és különböző felépítménymorfológiákat [41–47] vizsgáltak. Nagy részükben két, vagy több változó is befolyásolhatta a marginális csont reakcióját. Csupán néhány kutatás volt, amely a két különböző belső kapcsolattal és azonos makro- és mikromorfológiával rendelkező implantátumok körüli marginális csontveszteséget vizsgálta. Jelen vizsgálatban a két csoport között statisztikailag szignifikáns különbséget találtunk a marginális csontveszteségben a 6 hónapos és az 1 éves protetikai terhelést követően, bár a csontveszteség mennyisége az egyes csoportokban

minimális klinikai jelentőséggel bírhat. A csontreszorpcióban mutatkozó különbség többféleképpen magyarázható. A CS típusú csatlakozás jobb folytonosságot mutatott a folyáshatár tekintetében és nagyobb merevséget kisebb szivárgásveszéllyel [49]; míg az IH kapcsolatnál a csontgerinchez közeli implantátumnyak első milliméterénél mutatkozott a legnagyobb feszültség. A két csatlakozási forma eltérő platform switching távolságot mutatott, az IH esetében 3,5 mm-es, a CS esetében 3,1 mm-es platformmal, és úgy tűnt, hogy a marginális csontszint jobban megmaradt, ha az implantátum–felépítmény kapcsolat és a csontgerinc közötti távolság nagyobb volt [41–47].
Az implantátumok RFA-val mért stabilitása nem mutatott különbséget a vizsgálati csoportok között. Ennek oka lehet, hogy a két implantátumtípus morfológiája és felületi tulajdonságai azonosak; míg a megnövekedett ISQ értékek a második műtéti szakaszban az implantátum beültetésekor mért értékekhez képest a mechanikai stabilitásról a biológiai stabilitásra való áttéréssel magyarázhatók [50].
A behelyezési nyomaték és a marginális csontveszteség közötti összefüggést már korábban is vizsgálták, és azt feltételezték, hogy a magas behelyezési nyomaték mikrotörést és csontkompressziót okoz, amelyek negatív hatással vannak a csont vaszkularizációjára [51]. A magas, normál és alacsony behelyezési nyomaték meghatározásához alkalmazott küszöbértékek nem standardizáltak, az egyes tanulmányokban eltérő értékeket vettek figyelembe. A marginális csontveszteség klinikai vonatkozásai nem egyértelműek, különböző tanulmányok ellentmondásos eredményekről számoltak be [50].
Ezek az ellentmondásos eredmények korrelációt mutathatnak a vizsgált implantátumok eltérő morfológiájával, az eltérő feszültségeloszlással a marginális csontban, valamint a különböző típusú kutatási tervekkel és az eltérő küszöbértékekkel. Jelen vizsgálat nem mutatott ki összefüggést a magas behelyezési nyomatékérték (> 70 Ncm) és a marginális csontveszteség között, de összefüggést talált a behelyezési nyomatékgörbe alatti terület és a csontreszorpció között. Az implantátum behelyezése során folyamatosan növekvő nyomatékérték esetében kisebb marginális csontveszteség jelentkezett, mint az oszcilláló, változó értéknél. Ez azzal magyarázható, hogy bár mindkét esetben magas behelyezési nyomatékot értünk el, ha a behelyezési nyomaték fokozatosan növekszik, az implantátummal érintkező csontot érő terhelés nem a marginális csontra koncentrálódik, hanem az implantátum teljes hosszában oszlik el. Emellett hangsúlyoznunk kell, hogy az ISQ-értékek és a behelyezési nyomaték két független és nem összehasonlítható változó a mechanikai [52] stabilitás értékelésére, és nem mindig lineárisan korrelálnak egymással [53].
A mesterséges intelligencia (AI) klinikai diagnosztikai alkalmazása az egészségügyben folyamatosan fejlődik. A gépi tanulás a számítógép azon képességét jelenti, hogy az emberi agyi folyamatokat imitáló mély tanulási algoritmusok alapján tapasztalatból tanuljon, és neurális hálózatokon keresztül modelleket hozzon létre a döntéshozatalhoz. A mesterséges neurális hálózat (artificial neural network, „ANN”) egy nemlineáris, statisztikai adatmodellező eszközökön ala-
puló matematikai modell, amelyben korrelációk vannak a bemenetek és a kimenet között többszörös hálózatban. Ez a folyamat az emberi agyi folyamatokat szimulálja, és neurális hálózatokon keresztül modelleket hoz létre a döntéshozatali folyamatban való felhasználásra. Az ANN-ben az adatokat az algoritmusok egy csoportjába vezetik be, majd annak eredményeit egy másik algoritmuscsoportba, hogy megkapják a végleges kimenetet [54].
Az AI-t a radiológiában, az onkológiában és a kardiológiában alkalmazzák, habár néhány vizsgálat beszámolt a fogászatban és az implantológiában való alkalmazásáról is. A páciensek kezeléséhez ma már számos implantátumrendszer, protetikai komponens és sebészi eljárás áll rendelkezésre, és az AI hasznos lehet az implantációs betegek kezelésében, hogy közép- és hosszú távon a lehető legjobb eredményt lehessen elérni. Jelen vizsgálatot neurális hálózattal egészítettük ki, annak felmérésére, hogy az implantátum behelyezési módja a marginális csontveszteség lehetséges prediktív tényezőjének tekinthető-e. Az eredmények szerint a behelyezési nyomaték (különösen, ha több értéket tartalmazó görbeként mérjük) valóban előre jelzi a marginális csontvesztést.
Meg kell említenünk jelen vizsgálat néhány limitációját. Mindenekelőtt eltérő illesztési méreteket használtunk a CS csoportban (0,6 mm) és az IH csoportban (1 mm). Egy nemrégiben megjelent metaanalízis kimutatta, hogy a csontveszteség fordítottan korrelált az implantátum platformja és a felépítmény közötti illeszkedés növekedésével (P = 0,001)55. Ha a CS és az IH csoportok illeszkedései azonosak lettek volna, a köztük lévő különbségek még jelentősebbek lettek volna. Ezen felül elméletileg a cementrögzítésű restaurációk alkalmazása befolyásolhatja az MBL-t, amennyiben cementmaradványok maradnak a periimplantáris sulcusban [56–58], annak ellenére, hogy egy korábbi metaanalízis nem mutatott ki ilyen összefüggést [59], és a felesleges cementet gondosan eltávolították. Ezen túlmenően jelen vizsgálatban változó magasságú felépítményeket használtunk: az alacsony felépítmények negatívan befolyásolhatták az MBL-t a biológiai szélesség helyreállítása során [21,60].
Jelen tanulmány eredményei, bár kisszámú betegre korlátozódtak, a szerzők tudomása szerint a neurális hálózat első olyan alkalmazását mutatják, amely a behelyezési nyomatékgörbe alapján előre jelzi az implantáció alatt álló betegek marginális csontvesztésének tendenciáját.
Következtetések
A vizsgálat limitációt figyelembe véve következtetésként levonható, hogy az 1 éves utánkövetés során az azonos makrogeometriával, de különböző implantátum–felépítmény kapcsolattal rendelkező implantátumok szignifikánsan jobb MBL eredményeket mutattak a CS csoportban, mint az IH csoportban. Az MBL-t úgy véljük, egyéni különbségek és klinikai faktorok is befolyásolják.
A hivatkozott iroddalomjegyzék listája szerkesztőségünkben elérhető.
Forrás: Int J Oral Implantol 2020;13(4):1–14



Dr. Tzovairis Alexander (Belgium), dr. Van Someren Brand Remco (Hollandia), dr. Rossi Roberto (Olaszország)
SZÓLÓIMPLANTÁTUMOK
MELLETT TÖRTÉNŐ EGYFÁZISÚ
KEMÉNY- ÉS LÁGYSZÖVETI
AUGMENTÁCIÓ
A Poncho Lamina technika bemutatása
Absztrakt
A szakirodalomban már számtalan olyan publikációval találkozhattunk, amelyben az implantátumok körül található kemény- és lágyszövetek augmentációjának lehetséges módszerei kerülnek ismertetésre. Az implantátumok hosszú távú stabilitását és funkcióképességét az egyes implantátumokat megfelelő szélességben körülvevő csontszövet jelenléte, valamint a megfelelő lágyrészlefutás, az elegendő volumenben rendelkezésre álló feszes íny és a fogpótlások oly módon történő kialakítása, hogy az azokat körülvevő íny a természetes fogaknál megfigyelhető helyzetet utánozza, biztosítja. A fentiek rendelkezésre állása mind-mind kedvezőbbé teszik az implantátumok hosszú távú prognózisát. Ugyanakkor az előbbiekben leírt optimalizált állapot eléréséhez sokszor invazív sebészi beavatkozások sorozatának elvégzésére van szükség. Ezek pedig mind hozzájárulnak a kezelési idő hoszszának növeléséhez, valamint minden egyes sebészi beavatkozás tovább növeli a műtéti területen jelenlévő hegszövet mennyiségét. Ebben az esetbemutatásban egy olyan újszerű módszert szeretnénk ismertetni, amely alkalmazásával képesek vagyunk a rendelkezésre álló kemény- és lágyszövetek mennyiségének egyidejű megnövelésére. A cikkben bemutatott technika alkalmazása során a már sokak által jól ismert kortikális membránt használjuk a szöveti volumen megnövelésére, míg a megfelelő lágyrészprofil kialakítását az ezzel egyidejűleg behelyezett egyéni ínyformázó felépítmény segítségével biztosítjuk. Két esetet mutatunk majd be, amelyben egy-egy szólóimplantátum került behelyezésre. Az esetek ellátása során analóg vagy digitális módon kialakított egyedi ínyformázók és az ezek segítségével rögzített laminamembránok kerültek felhasználásra. Mindkét esetben egy legalább 4 hónapos gyógyulási időszakot követően végzett kiértékelés során, a kiindulási állapothoz képest kedvezőbb kemény- és lágyszöveti konfigurációt találtunk. Véleményünk szerint további vizsgálatok szükségesek a fogatlan állcsontgerincszakaszoknak megfelelően történő implantátumbehelyezéssel egyidejűleg, az általunk javasolt klinikai protokoll szerint végzett szimultán kemény- és lágyszöveti augmentáció hatékonyságának kiértékelésére.
Kulcsszavak: laminamembrán, egyéni felépítmény, csontpótlás, emergenciaprofil, fogászati implantátum
Bevezetés
Az implantátumokon elhorgonyzott fogpótlásokkal foglalkozó szakirodalomban már többször kitértek az implantátumok körül található jól kialakított emergenciaprofil és az implantátumok mellett megfelelő szélességben rendelkezésre álló feszes íny jelentőségére. Ezek a faktorok biztosítják, hogy: 1. a későbbiekben behelyezésre kerülő fogpótlás számára megfelelő lágyrészviszonyok álljanak fent; 2. valamint ezek biztosítják az implantátumok hosszú távú sikerességéhez szükséges stabil lágyrészviszonyok eléréséhez nélkülözhetetlen feltételeket.
Számtalan olyan technika és eljárás áll rendelkezésünkre, amelyek alkalmazásával lehetőségünk van a meglévő lágyrészvolumen megnövelésére és a feszes íny szélesítésére. Ezek a beavatkozások lehetővé teszik a fogatlan állcsontgerincszakaszoknak megfelelően található lágyrészek mennyiségének és minőségének optimalizálását. Ezt a folyamatot lágyrészmenedzsmentnek nevezzük. Ugyanakkor azt sem szabad elfelejteni, hogy a lágyrész-augmentáció során a megfelelő mennyiségben és pozícióban jelenlévő keményszövetek biztosítják a beavatkozás sikeréhez szükséges stabil feltételeket. A jelenleg általánosan elterjedt klinikai gyakorlatban két- vagy háromfázisú protokollokat alkalmaznak az egyéni ínyformázó felépítmények behelyezésével történő emergenciaprofil formázással kiegészített kemény- és lágyszöveti augmentáció során. Ezek az esetek többségében azt jelentik, hogy az egyes pácienseknek két vagy három műtéti beavatkozáson és a rendelkezésre álló feszes íny szélesítése érdekében, sokszor az ezeket kiegészítő szabad ínylebenyátültetésen kell átesniük. Ezeknek a beavatkozásoknak az elvégzésére legtöbbször az alsó állcsontokba helyezett implantátumok körüli lágyrészek optimalizálásának érdekében van szükség. A két- vagy háromfázisú implantációs protokolloknak az alkalmazása (csontpótlás és azzal egyidejűleg
vagy attól eltérő alkalommal történő implantátumbehelyezés, valamint az implantátumfelszabadítással egyszerre végzett lágyrész-optimalizáció) hegszövet kialakulásához, az eredetileg meglévő feszes íny mennyiségének csökkenéséhez és a kezelés befejezéséhez szükséges idő növekedéséhez vezethet.
Jelen cikkben egy olyan módszert szeretnénk bemutatni, amely segítségével lehetőségünk van a szólóimplantátumok körül található kemény- és lágyszövetek egy beavatkozás keretein belül történő augmentálására. Ezt az eljárást One-Step Optimisationnak (O.S.O., egyfázisú optimalizáció) nevezzük. A beavatkozás során kortikális membránt (Soft Lamina-Osteobiol, Tecnoss) használunk. Ezt a már jól ismert tulajdonságokkal rendelkező felszívódó membránt egy egyéni felépítmény segítségével rögzítjük. A felépítmény a membrán rögzítésén kívül az optimális emergenciaprofil kialakításában is részt vesz. Az alábbiakban két eset bemutatásán keresztül egy innovatív egyfázisú sebészi protokollt kívánunk ismertetni. A protokoll egyaránt beilleszthető az analóg vagy a digitális munkafolyamatokba.
Esetbemutatás
Az esetek bemutatása során két páciens ellátását fogjuk ismertetni. A esetbemutatások közé történő beválasztás kritériumai az alábbiak voltak:
A Az ellátásra jelentkező páciens életkora érje el, vagy haladja meg a 18 éves kort.
B A páciens a tájékoztatást követően aláírta a beleegyező nyilatkozatot és vállalta, hogy követi a műtét utáni utasításokat, valamint elfogadja a kezelési tervben leírtakat.
C A páciens jó általános szájhigiénével rendelkezik, és nem szenved parodontális elváltozásoktól (25% alatti plakk index, az első vizsgálat során nem észleltünk parodontális tasakok jelenlétére utaló jeleket, az ínybarázda szondázását követően a vérzési index nem érte el a 25%-ot [BOP<25%]).
D Az ellátásra kerülő jelenleg még fogatlan állcsontgerincszakaszoknak megfelelően legalább 4 mm széles feszes íny jelenléte.
A bemutatásra kerülő esetek közül kizárásra kerültek azok a páciensek, akik:
a) Olyan alapbetegséggel rendelkeztek, amely megváltoztatja a csontállomány metabolizmusát vagy hatással van a sebgyógyulásra.
b) Terhesek vagy szoptatnak az implantátumok beültetése, valamint a gyógyulási fázis alatt.
c) Dohányoznak.
Első esetbemutatás –digitális munkafolyamat
Egy 58 éves hölgypáciens azzal a kéréssel kereste fel a rendelőnket, hogy segítsünk a hiányzó bal alsó második kisőrlőfogának (35) a pótlásában. A páciens jó általános egészségi állapottal rendelkezett, nem dohányzott, és nem szenvedett parodontális betegségektől. A kiindulási állapotról egy
CBCT-felvétel (Cone Beam Computed Tomography) készült. Az elkészült felvétel kiértékelése során megállapítottuk, hogy nem áll rendelkezésre elegendő csontvolumen a 35-ös fog pozíciójába történő implantátumbehelyezés elvégzéséhez. A meglévő állcsontgerinc-szélessége elégtelennek bizonyult (1. ábra) Ezenfelül a szomszédos 36-os pozícióban lévő implantátum (Straumann Tissue Level) körül is csontos dehisszenciát észleltünk (2. ábra) A dehisszencia vélelmezhetően a meglévő csontállomány gyulladásmentes leépülé-
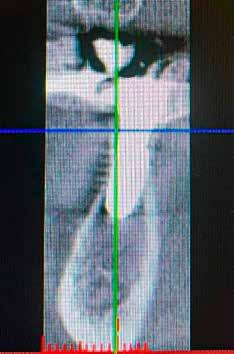
1. ábra: Kiindulási CBCT-felvétel. A bal alsó második kisőrlőfognak (35) megfelelő fogpozícióról készült keresztmetszeti kép.
2. ábra: Kiindulási CBCT-felvétel. A bal alsó első nagyőrlőfognak (36) megfelelően behelyezett implantátumról készült keresztmetszeti kép.
se során alakult ki. A vizsgált területen lévő csontállomány megállapításunk szerint D3-as keménységgel rendelkezett. A fogatlan állcsontgerincszakasznak megfelelően elegendő csontmagasság állt rendelkezésre egy implantátum behelyezéséhez. A mérés során az állcsontgerinc szájüreg felé mutató felszíne (bukkális kortikális) és a canalis mandibulae cranialis fala közti távolságot vizsgáltuk. A pácienst tájékoztattuk a 36-os pozícióban lévő implantátumon található korona cseréjének szükségességéről, de ő ezt elutasította. A klinikai vizsgálat során a 35-ös fog pozíciójának helyén található fogatlan állcsontgerincszakasznak megfelelően 4 mm széles keratinizált ínyt találtunk (3. ábra). A 36-os pozícióban lévő implantátum mellett végzett szondázás során nem találtunk tasakok jelenlétére utaló jeleket, valamint a szondázást követő vérzés kialakulását sem észleltünk.
A páciens ellátása során a 35-ös pozícióba történő implantátumbehelyezést követően, az egyfázisú optimalizációs (One-
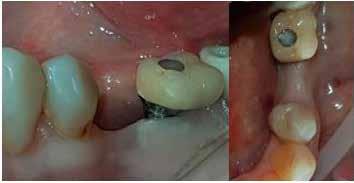
3. ábra: Kiindulási állapot. A 35-ös fogpozíciónak megfelelő területről készült szájüregi felvételek.
Step Optimalization) protokollnak megfelelően alkalmazott Poncho Lamina technikát használtuk. A beavatkozás során egy darab V3 MIS implantátum (MIS Implants Technologies, BAR-LEV, Izrael) került beültetésre. A laterál augmentáció során folyékony S-PRF-fel (Process For PRF, Nizza, Franciaország) összekevert Biogen 0,5 Xenograftot (Biogen 0,5 gr-Bioteck, Torino, Olaszország) használtunk és az egészet egy 25x25-ös Soft Lamina membránnal fedtük. Az emergenciaprofil kialakításában részt vevő egyéni felépítményt a VPI Cervico rendszer (VP Innovato Holdings LTD, Ciprus) segítségével terveztük meg. Ezt az egyéni fejet az implantátumba helyezett connect abutmenten rögzülő ideiglenes felépítmény (temporary cilinder) (MIS Implants Technologies, BAR-LEV, Izrael) segítségével rögzítettük.
Az eset ellátásához szükséges munkafolyamatokat két fő részre lehetett osztani:
A fogtechnikai fázis: Az emergenciaprofil kialakításához szükséges egyéni felépítmény digitális megtervezése és fogtechnikai laboratóriumban történő elkészítése, illetve a membrán megformázásához használt sablon elkészítése. A sablon használatával a sebész pontosan meg tudta határozni a későbbiekben az egyéni felépítménnyel rögzített membrán dimenzióit.
A sebészi fázis: A sebészi beavatkozás során megtörtént az implantátum és a csontpótló anyag behelyezése, valamint a membrán és a környező lágyrészek óvatos egyedi felépítmény köré történő adaptációja.
Digitális fogtechnikai fázis
Emergenciaprofil kialakítása
A sebészi beavatkozás megkezdése előtt egy intraorális szkenner (3Shape Trios) segítségével digitális lenyomatot vettünk az alsó állcsontról, és az így készült STL-fájlt elküldtük a fogtechnikai laboratóriumba. Ezt követően a fogtechnikusok megkezdték az emergenciaprofil és a sablon digitális tervezését. Ezt a fájlt először az Exocad szoftverbe importálták, majd az ellátásra szoruló fogpozíciónak és a hiányt határoló fogak által meghatározott szélességnek megfelelő digitális VPI Cervico emergencia profil sablont is átemeltük ebbe a programba (4. ábra). A VPI Cevico öntőforma Ceramill Map 400 digitális szkennerrel történő (Amann Girrbach) szkennelését követően kialakítottuk az egyedi fej digitális emergencia profil sablonnak megfelelő ínyszél alatti dimenzióit. A VPI Cevico öntőforma digitális másolatát (a majdani implantátum tervezett pozíciójának megfelelően) 3 mm-rel subgingiválisan helyeztük el. A digitális tervet elküldtük a beavatkozást végző sebésznek, majd az ő jóváhagyását követően az egyedi ínyformázó felépítmény digitális tervén az ínyszél magasságának megfelelően, egy 1 mm széles és 0,5 mm mély körkörös vájulatot hoztunk létre (5. ábra). Az ínyformázót ezt követően egy Asiga 3D max háromdimenziós nyomtató segítségével Free print temp A2 resin anyagból kinyomtattuk. Az elkészült ínyformázót 99%-os izopropil alkohollal lemostuk, majd nitrogénben gazdag környezetben egy Otoflash G171 polimerizációs készülékkel elvégeztük az utópolimerizációját. A polimerizáció befejezését követően eltávolítottuk az alátámasztást biztosító csapokról és egy gőzborotvával megtisztítottuk.
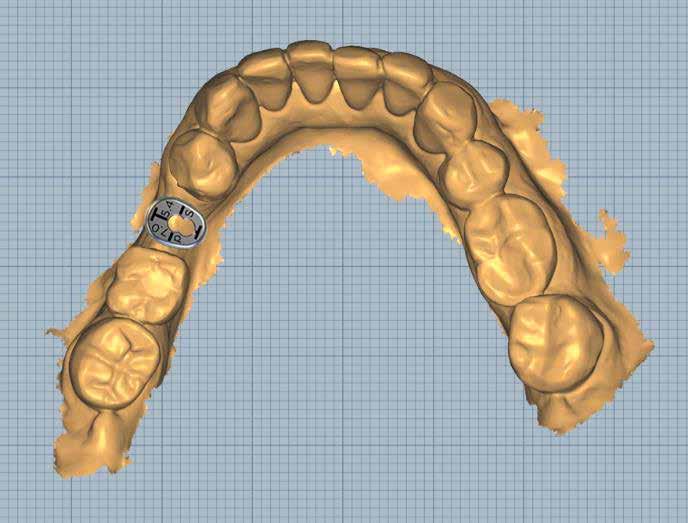
4. ábra: Az Exocad modellen látható állapotnak megfelelő VPI digitális sablon kiválasztása.
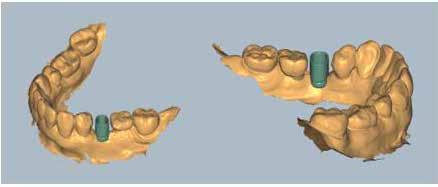
5. ábra: Az ínyszél magasságában elhelyezkedő retenciós barázda virtuális kialakítása.
Sablon elkészítése
Az emergenciaprofilt tartalmazó STL-fájlt a Blender 3D programba (www.blender.org) importáltuk és a membrán későbbi megformázásának elősegítése érdekében létrehoztunk egy 45x45x3 mm-es sablont. Az emergenciaprofilt tartalmazó adatokat és a sablont ezt követően egy fájlban egyesítettük, és az ínyformázó csavar leendő pozíciójának helyén, a sablonon az ínyformázó körvonalának megfelelő mérethű jelölést hoztunk létre. Később ennek a jelölésnek megfelelően a sablont kivágtuk és így megkaptuk az egyedi ínyformázó csavar pontos és méretazonos nyaki formáját. A nyomtatás előtt a sablon digitális tervét némileg módosítottuk. A lemez vastagságát először megnöveltük, majd a sablonra vonatkozó STL-fájlt egy Formlabs Form 2 (Formlabs) 3D nyomtatóra továbbítottuk. A sablont Dental LT resin anyagból nyomtattuk, majd a rezinfeleslegek 99%-os izopropil alkoholban történő lemosását követően egy BB Cure utópolimerizáló készülékben végpolimerizáltuk. Az így elkészült munkadarabot egy gyémántfúró segítségével eltávolítottuk az alátámasztást biztosító csapokról és egy gőzborotva segítségével megtisztítottuk. A kidolgozás utolsó lépéseként a sablon eredetileg 3 mm-es vastagságát egy nedves gipszcsiszoló segítségével 1 mm-re redukáltuk.
Sebészi fázis
A műtéti terület helyi érzéstelenítővel történő infiltrálását követően (articain, adrenalin) egy 15C szikepengével buccalisan és linguálisan intrasulcularisan vezetett metszést végeztünk a 33-as fog disztális felszínétől a 37-es fog meziális felszínéig. A 35-ös fogpozíciónak megfelelően található fogatlan állcsontgerincszakaszon a metszésvonalat a gerincélen ve-
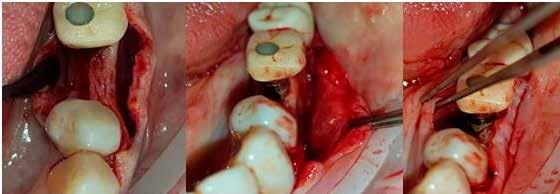
6. ábra: A lebenyképzést és lebenynyújtást követően látható állapot.
zettük. A metszésvonal által érintett papilláknak megfelelően félvastag lebenyt alakítottunk ki, majd a kortikálist elérve mind bukkálisan, mind linguálisan teljes vastagságban folytattuk. A lebenyek kialakítását követően, a lebenyek nyújtását bukkálisan a perioszteumot átmetszésével biztosítottuk, míg linguálisan a musculus mylohyoideus rostjait a lebenyről egy raspa segítségével leválasztottuk (6. ábra).
Az állcsontgerinc tágítását a gyártó által kiadott protokollnak megfelelően Densah fúrók segítségével végeztük (Versah LLC, Michigan, USA), majd a 35-ös pozícióba szubkresztálisan egy 3,9x10 mm-es MIS V3 implantátumot (MIS Implants Technologies, BAR-LEV, Izrael) helyeztünk. A behelyezés során 25 Ncm primer stabilitást mértünk. Ezt követően az implantátumba egy 4 mm átmérőjű, 2 mm magas egyenes felépítményt (connect abutment, MIS Implants Technologies, BAR-LEV, Izrael) rögzítettünk. A felépítményt 30 Ncm-es nyomatékkal húztuk meg (7. ábra)
A fogtechnikai labor által készített emergencia profil formázó felépítmény rögzítését az egyenes felépítménybe (connect abutment) rögzülő, ideiglenes felépítmény (temporary cylinder for connect abutment (MIS Implants Technologies, BAR-LEV, Izrael) segítségével biztosítottuk. Az ideiglenes felépítmény egy átmenőcsavar segítségével rögzült, és az emergencia profil formázó felépítmény stabilitását is ez a csavar biztosította. Az emergencia profil formázó felépítményt intraorálisan polimerizált flow kompozit felhasználásával rögzítettük az ideiglenes felépítményhez. A megvilágítást követően az ideiglenes felépítményhez rögzített emergencia profil formázó felépítményt eltávolítottuk, és szájon kívül tovább formáztuk, majd végül magas fényre políroztuk. A műtéti terület előkészítését és az implantátum behelyezését követően egy kortikális laminamembránt (Soft Lamina 25x25
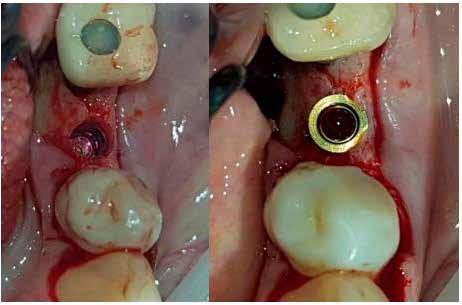
7. ábra: A szubkresztálisan behelyezett implantátumról és az implantátumba helyezett köztielemről készült intraoperatív felvételek.
mm Osteobiol by Tecnoss SRL, Torino, Olaszország) 5 percre fiziológiás sóoldatba helyeztünk. A membrán hidratációja után, a fogtechnikai labor által készített, és a műtét előtt megtisztított (BlueM fertőtlenítő oldatba helyezett, majd steril fiziológiás sóoldattal lemosott) sablont a membránra helyeztük, és az ínyformázó felépítmény leendő pozícióját jelölő nyílásnak megfelelően egy mikro szikepenge (SM67 Swann Morton) segítségével egy nyílást alakítottunk ki. Ezt követően egy 15C-s szikepenge és ollók segítségével a membránt a műtéti terület által adott helyviszonyoknak megfelelő formára alakítottuk. A membrán formázása során kiemelt figyelmet fordítottunk arra, hogy a membrán az ínyformázó felépítményen digitálisan kialakított vájulatba szorosan és pontosan illeszkedjen (8. ábra) Az ínyformázó felépítmény-membrán egység implantátumba történő illesztése előtt az augmentálni kívánt területre
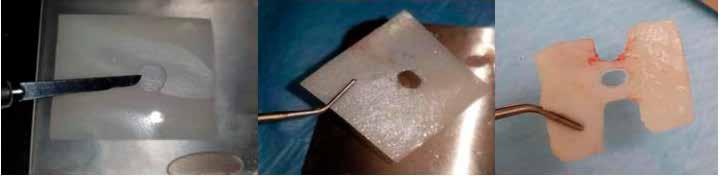
8. ábra: A laminamembrán előkészítése és formázása a 3D nyomtatóval készült sablon igénybevételével történt.
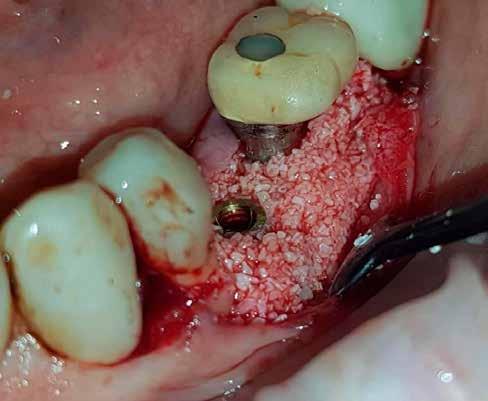
„Sticky bone”-t helyeztünk. A „Sticky bone”-t az SPRF folyadék (Process For PRF, Nizza, Franciaország) és 2 gramm xenogén csontpótló anyag (Biogen 0,5 gr-Bioteck, Torino, Olaszország) összekeverésével hoztuk létre. A csontpótló anyag bukkális és linguális oldalon történő elrendezését követően (9. ábra) a lebenyszéleket óvatosan felemeltük és az ínyformázó felépítmény-membrán egységet finoman a csontpótló anyagra helyeztük. Az egyedi ínyformázó felépítmény egyenes felépítménybe (connect abutment) történő helyezését követően a rögzítőcsavart 20 Ncm-rel meghúztuk. Az ínyformázó rögzítését követően a felépítmény okkluzális felszínét redukáltuk. Erre azért volt szükség, hogy elkerüljük a rágómozgások során a felső fogakkal való érintkezések kialakulását. Az ínyformázó felépítmény rögzítésére szolgáló átmenőcsavarhoz vezető csavarcsatornát teflonszalag és flow kompozit segítségével ideiglenesen lezártuk.
A lebenyek zárása 3 rétegben történt:
Egy 4-0-s felszívódó monofil varróanyaggal (Glycolon, Resorba, Nuremberg, Németország) készült középső réteg, amely a mucogingivális határ alatt 1-2 mm-rel lett behelyezve. Ennek a varratsornak az volt a szerepe, hogy segítsen a lebenyszélek közelítésében és ezáltal lehetővé tegye a felszínes varratsorral megvalósítani kívánt feszültségmentes zárást, valamint a behelyezett membrán stabilizálásában és leszorításában is részt vett.
A felszínes varratsor 5-0-s Glycolon varróanyaggal készült. Ebben a rétegben vertikális matrac- és egyszerű csomós öltéseket készítettünk. A behelyezett varratsor célja a papillák stabilizálása és a lebenyszélek feszülésmentes zárása volt. Egy 5-0-s Glycolon varróanyaggal készült mély varratsor. A lebeny megnyújtása során átmetszett periosteumtól apikálisan gyakorlatilag az eddig teljes vastagságú lebenyből egy félvastag lebenyt hoztunk létre. A varratsor célja ennek a „félvastagon preparált” apikális rész stabilizálása volt. A varratokkal a félvastagon preparált rész szélét ismét a periosteumhoz rögzítettük annak érdekében, hogy megakadályozzuk a környező szövetekben tapadó izmok és a lebenyszél elmozdulása által kifejtett húzóerők lebenyünkre gyakorolt hatásának megjelenését.
A beavatkozás befejezését követően a pácienst tájékoztattuk a műtét utáni teendőkről. Utasítottuk, hogy egy hónapon keresztül naponta kétszer egy fertőtlenítő hatású szájvízzel (Blue®M Mouthwash, Blue®M Oral Care) óvatosan öblögessen, valamint arra kértük, hogy a varratok felszívódásáig kerülje a műtéti terület fogkefével való tisztítását. A műtétet követően antibiotikumot (Augmentin 875 mg/125 mg) és fájdalomcsillapítót (Ibuprofén 600 mg) is elrendeltünk számára. Az antibiotikumot 7 napon keresztül, a fájdalomcsillapítót pedig 5 napon keresztül napi kétszer kellett bevennie. A pácienst 2 hét, 1 hónap, valamint 2, 3 és 4 hónap múlva kontrollvizsgálat céljából visszarendeltük.
Második esetbemutatás –Analóg munkafolyamat
Egy 54 éves hölgypáciens azzal a céllal kereste fel a rendelőnket, hogy a hiányzó bal felső szemfogát (23) implantátumon rögzülő korona segítségével pótoltassa. A foghiánynak megfelelően 4 hónappal ezelőtt csontpótló beavatkozást végeztek (guided bone regeneration, GBR, irányított csontregeneráció), amely végül sikertelennek bizonyult. A páciens jó általános egészségi állapottal rendelkezett, nem dohányzott, és nem szenvedett parodontális betegségektől. A vizsgálatunk részeként készített CBCT-felvételen a 23-as fogpozíciónak megfelelően elégtelen horizontális csontszélesség ábrázolódott, ellenben a vertikális csontmagasság megfelelőnek bizonyult (az orralaptól az
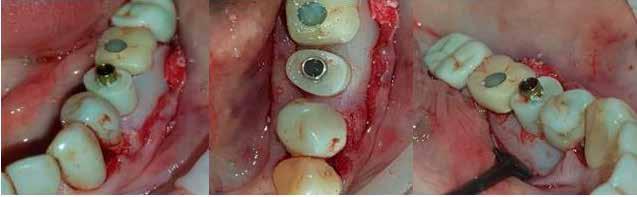
9. ábra: A túldimenzionált csontpótló anyagról készült felvétel (Sticky Bone; SPRF/Xenograft).
10. ábra: Az egyéni ínyformázó felépítményhez rögzített laminamembrán behelyezése.
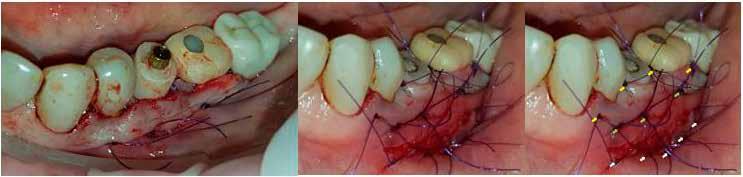
11. ábra: A sebszélek egyesítése során a varratok három rétegben kerültek behelyezésre. A, Felszínes réteg: Sárga nyilak; B, Középső réteg: Zöld nyilak; C, Mély réteg: Fehér nyilak
állcsontgerinc legkoronálisabban elhelyezkedő pontja között mért távolság) egy implantátum behelyezéséhez (11. ábra). A felvétel alapján a páciens D3-as csontkeménységgel rendelkezett. A klinikai vizsgálat során megállapítottuk, hogy a páciensnek alacsony a mosolyvonala, valamint a fogatlan állcsontgerincszakasznak megfelelően (23) elegendő a feszes íny szélessége (12. ábra). Az eset ellátása során ugyanazok az anyagok kerültek felhasználásra, mint az előbbiekben bemutatott digitálisan megtervezett esetnél. A két eset között a legfőbb különbséget az jelentette, hogy itt az egyedi ínyformázó felépítményt a sebészi beavatkozás során a rendelőben készítettük el, valamint a membrán rögzítésére szolgáló nyílást is szabadkézzel hoztuk létre.
Sebészi fázis
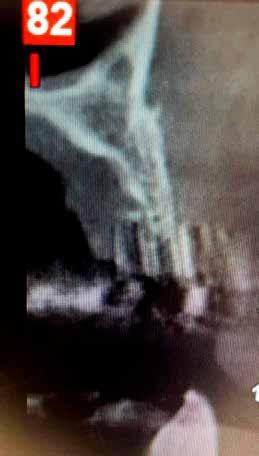
12. ábra: Kiindulási CBCTfelvétel. A bal felső szemfog pozíciójának (23) megfelelően készült keresztmetszeti kép.
A műtéti terület helyi érzéstelenítővel történő (lidocain, adrenalin) infiltrációját követően az első esetbemutatásnál leírt lépéseket követve végeztük el a beavatkozást. Az előkészített implantátumfészekbe egy 3,9x10 mm-es MIS V3 implantátumot helyeztünk, amelyre egy 4 mm széles és 2 mm magas egyenes felépítményt helyeztünk (connect abutment). Az implantátumot és az egyenes felépítményt is 35 Ncm-rel rögzítettük. Ezt követően az augmentálni kívánt területre 2 gramm xenogén csontpótló anyag (Biogen 0,5 gr) és SPRF folyadék keverékéből készült „Sticky
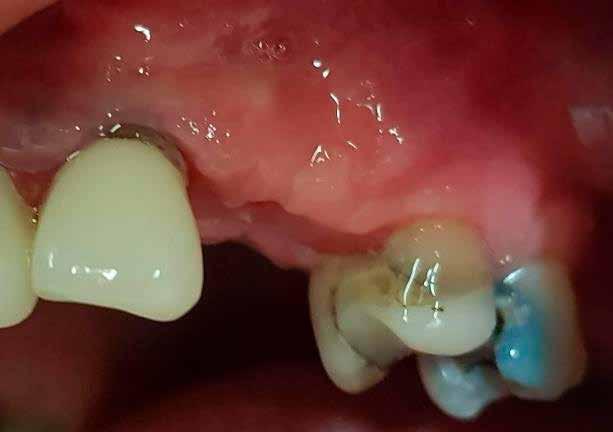
13. ábra: Kiindulási állapot. A bal felső szemfog pozíciójának megfelelően található foghiányról készült szájüregi felvétel.
bone”-t helyeztünk. A lebeny zárása során 5-0-s, és 4-0-s Glycolon varróanyagot alkalmaztunk.
Analóg (rendelői) egyéni ínyformázó felépítmény készítése és membránadaptáció Az egyéni ínyformázó fej készítése során egy nagy méretű front (anterior large) VPI Cervico felépítmény (aL, Dimensions 7,5x6,5 mm) méreteiből indultunk ki. Először a fent említett felépítménnyel megfelelő méretű VPI Cervico öntőforma segítségével folyékony nano-hibrid kompozit felhasználásával létrehoztuk a kiindulási ínyformázó felépítményt. A folyamat során a felépítmény bázisául egy 4 mm-es szélességű egyenes felépítményhez való elfordulásgátolt MIS ideiglenes fejet használtunk (MIS engaged temporary cylinder for 4 mm diameter Connect single unit abutment).
Az ínyformázó felépítmény elkészítését követően, az ideiglenes fej bázisának szélétől 3 mm-re koronálisan egy 1 mm mély körkörös vájulatot alakítottunk ki egy gömbfúró segítségével (13. ábra) . Ennek a barázdának az volt a célja, hogy a későbbiekben a segítségével rögzítsük a membránt. Mivel a nagy méretű front VPI Cervico felépítmény (aL, Dimensions 7,5x6,5 mm) körkörösen 1 mmrel redukált dimenziói megegyeznek a közepes méretű front (anterior medium) VPI Cervico felépítmény (aM, Dimensions 6,5x5,5 mm) méreteivel, ezért egy aM méretű
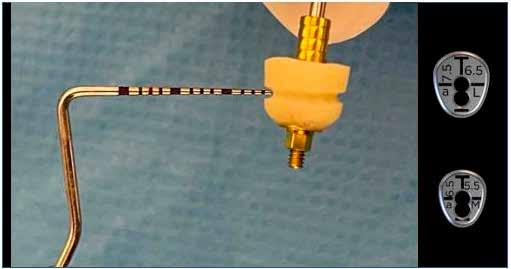
14. ábra: Az aM felépítmény körvonala megegyezik az aL felépítményen, az ínyformázó bázisától 3 mm-re koronális irányba kialakított 1 mm mély barázda körvonalával.

15. ábra: A laminamembrán előkészítése az előzetesen kiválasztott VPI Cervico sablon alapján történt.
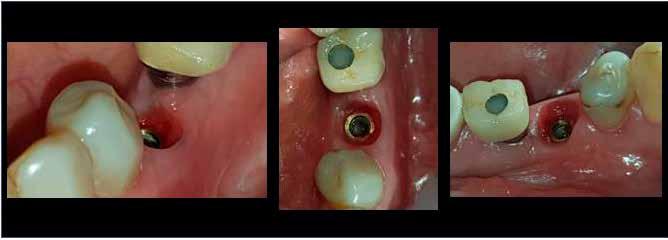
16. ábra: A sebészi beavatkozást követően 4 hónappal történő ínyformázó eltávolítása során készült szájüregi felvételek. (Bal alsó második kisőrlőfog; 35).
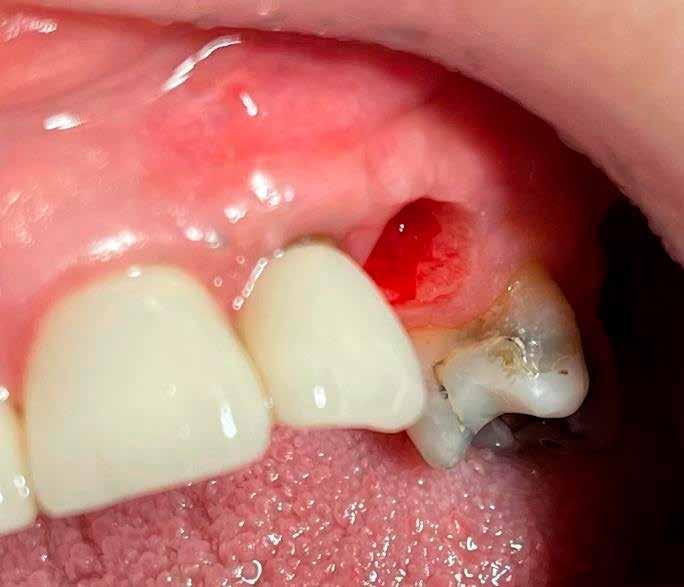
17. ábra: A sebészi beavatkozást követően 4 hónappal történő ínyformázó eltávolítása során készült szájüregi felvételek. (Bal felső szemfog; 23).
VPI Cervico sablont használtunk a Soft Lamina membránon kialakítandó nyílás szikepengével történő létrehozása során (14. ábra) . Ennek köszönhetően a nyílás mérete pontosan követte az aL felépítmény 1 mm-rel redukált
körvonalait. A nyílás elkészítését követően, a membrán nagyságát 15C-s szikepenge és ollók segítségével a műtéti területnek megfelelő méretűre redukáltuk. A folyamat során kiemelt figyelmet fordítottunk arra, hogy az egyéni ínyformázó felépítményen kialakított barázdába helyezett membrán szorosan és stabilan rögzüljön a felépítményhez (15. ábra) . A páciens az előbbiekben bemutatott esetnél (első esetbemutatás) elhangzottakkal megegyező utasításokat kapott a műtét utáni teendőkkel kapcsolatban, valamint ugyanazok a gyógyszerek kerültek elrendelésre. A pácienst 2 hét, valamint 1, 2, 3 és 4 hónap múlva rendeltük vissza kontrollvizsgálatra.
Eredmények
Mindkét eset újraértékelését a beavatkozás elvégzését követően 4 hónappal végeztük el. A 4 hónapos kontroll során a kialakított emergenciaprofil tulajdonságait vizsgáltuk.
Az első esetnél az állcsontgerinc bukkális és linguális oldalán is sikerült megőrizni az eredetileg rendelkezésre álló feszes íny szélességét. A kialakított ínykehely bukkális oldalán 5 mm-es ínymagasságot sikerült elérni, az implantátumhoz rögzülő egyenes felépítmény (connect abutment) 2 mm-es
magassággal rendelkezett, továbbá az egyenes felépítmény legkoronálisabb pontja fölött még 3 mm-es ínymagasságot mértünk (2+3=5). A linguális oldalán 6 mm állt rendelkezésre (az egyenes felépítmény 2 mm-es magasságához szintén hozzáadtuk a felépítmény legkoronálisabb pontjától mért 4 mm-es ínymagasságot [2+4=6]), (16. ábra). A mérések elvégzéséhez parodontális szondát használtunk.
A második eset vizsgálata során szintén megállapíthattuk, hogy az eredetileg rendelkezésre álló feszes ínyt teljes szélességében sikerült megőrizni. Az implantátum bukkális és linguális oldalán mért ínymagasság megegyezett az első esetnél mért értékekkel (17. ábra)
A posztoperatív CBCT-felvételeken mindkét esetben az implantátumok megfelelő osszeointegrációjára utaló radiológiai jeleket észlelhettünk.
Az első esetnél a beavatkozások befejezését követően 10 hónappal készített felvételen a 35-ös pozícióban lévő implantátum körül megfelelő mennyiségű csontvolumen ábrázolódott. A 36-os pozícióban lévő implantátum körüli terület is profitált az elvégzett beavatkozásokból. A kiindulási CBCT-felvételen az implantátum bukkális oldalán egyértelműen megfigyelhető csontos dehisszencia mértéke jelentősen csökkent. A korábban behelyezett implantátum bukkális felszínének megfelelően új csontállomány képződésére utaló radiológiai jeleket lehetett látni (18. ábra)
A második esetről 4 hónappal később készített posztoperatív CBCT-felvételen az implantátum körül megfelelő mennyiségű csont ábrázolódott, valamint az állcsontgerinc szélességét is kielégítőnek ítéltük (19. ábra).
Megbeszélés
A cikk megírása során az volt a célunk, hogy bemutassunk egy olyan újszerű és innovatív eljárást, amely alkalmazásával lehetőségünk van a szólóimplantátumok mellett végzett kemény- és lágyszöveti augmentációt az implantátumok behelyezésével egyidejűleg elvégezni (egyfázisú augmentáció; One-Step Augmentation, O.S. A.). Az eljárás során kortikális laminamembrán és egyéni ínyformázó felépítmények kerülnek felhasználásra. Ennek az eljárásnak köszönhetően lehetőségünk van a kezelési idő és a kezelés befejezéséhez szükséges beavatkozások számának csökkentésére. Ebben a cikkben egy-egy példán keresztül lépésről lépésre ismertettük a digitális és az analóg (rendelői) megközelítés esetén alkalmazott munkafolyamatokat. Ugyanakkor fel szeretnénk hívni az olvasók figyelmét néhány olyan szempontra, amelyet mindenképpen figyelembe kell vennünk, ha a beavatkozás elvégzése mellett döntenénk:
• A műtét során képzett borítéklebenynek elég lazának kell lennie ahhoz, hogy a laminamembránt könnyen és egyszerűen a behelyezett csontpótló anyagra tudjuk helyezni. Véleményünk szerint ehhez a lebenyképzés során a metszésvonalat intrasulculárisan a foghiányt disztálisan határoló fog (vagy implantátum) disztoapproximális felszínéig kell vezetni. Amennyiben sorvégi foghiányról van szó, úgy a gerincélen vezetett metszésvonalunkat megfelelő távolságra kell kiterjeszteni.
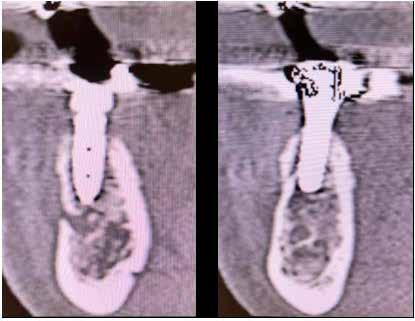
18. ábra: A sebészi beavatkozást követően 10 hónappal készült posztoperatív CBCT-felvételből a 35-ös (bal) és a 36-os (jobb) pozícióban lévő implantátumokról készített keresztmetszeti képek.
• A lebenyek megnyújtása során biztosítanunk kell, hogy a sebszéleket a csontpótló anyagot fedő laminamembrán fölött feszülésmentesen tudjuk egyesíteni. Amennyiben ezt nem tudjuk teljes mértékben megvalósítani, úgy a behelyezett csontpótló anyag korai reszorpciójára számíthatunk.
• Véleményünk szerint a lehető legnagyobb csont–implantátum kapcsolat (bone to implant contact) kialakítása érdekében az implantátumokat mindig javasolt enyhén szubkresztálisan elhelyezni. Ebben az esetben a behelyezés során jó (közel 30 Ncm-es) primer stabilitásra számíthatunk. A behelyezett csontpótló anyagnak elsősorban a meglévő saját csontállományt kell fednie, ugyanakkor az sem jelent problémát, ha az implantátumbehelyezést követően esetlegesen kialakult kis méretű bukkális csontdehisszencia fedésére alkalmazzuk (azaz a csontpótló anyag egy kis felületen közvetlenül az implantátum felszínével kerül érintkezésbe). A D3-as és D4-es keménységű csontban történő implantátumfészek kialakítása során javasolt lehet az osszeodenzifikáló fúrók (pl.: Densah) alkalmazása. Ezek segítségével a lehető legnagyobb mértékben tudjuk megőrizni a meglévő saját csontállományt. Azonban az osszeodenzifikáló fúrók használata a D3-nál keményebb csontállományban kifejezetten kontraindikáltnak számít.
• Az egyéni ínyformázó felépítmény behelyezése előtt mindkét esetben egy-egy köztielemként (mezostruktúra) funkcionáló egyenes felépítményt (connect abutment) rögzítettünk az implantátumokba. Ezen köztielemként funkcionáló felépítmények előzetes behelyezésével meg tudjuk akadályozni, hogy a csontpótló anyag az implantátumok platformja fölé kerüljön, és azt részlegesen fedve a későbbiekben esetlegesen megakadályozza a lenyomatvételi fejek pontos és feszülésmentes behelyezhetőségét.
• Azt javasoljuk, hogy a membrán fixálására szolgáló retenciós barázdát maximum 3 mm-es távolságra helyezzük el az egyéni ínyformázó felépítmény legapikálisabb pontjához (bázisához) képest. Ennek a körkörös vájulatnak a szé-
lessége ne haladja meg az 1 mm-t és a mélysége se legyen nagyobb 0,5–1 mm-nél. Ezen értékek mellett biztosíthatjuk a laminamembrán pontos és feszülésmentes rögzítését. Ez azért fontos, mert a membrán egyedi ínyformázó felépítményre való helyezése közben jelentkező túl nagy mértékű erőhatások könnyen a membrán ruptúrájához vezethetnek.
• Fontos, hogy az augmentálni kívánt területet minden esetben töltsük túl csontpótló anyaggal. A csontpótló anyag túldimenzionálásának jelentősége abban rejlik, hogy ezáltal biztosak lehetünk benne, hogy nem maradnak üres területek a csontpótló és a membrán között. Továbbá a megfelelő mennyiségben jelenlévő csontpótló anyag stabil alátámasztást nyújt a ráhelyezett membrán számára. Ez azért fontos, mert így jobban ellen tud állni az egyesített lebenyszélek által kiváltott apikális irányba mutató erőhatásoknak. A „Sticky bone”-ként felhelyezett csontpótló anyag sokkal stabilabban ül az augmentálni kívánt területen. További előnye, hogy így a csontpótló szemcsék nem szélednek szét a műtéti területre a laminamembrán felhelyezése során.
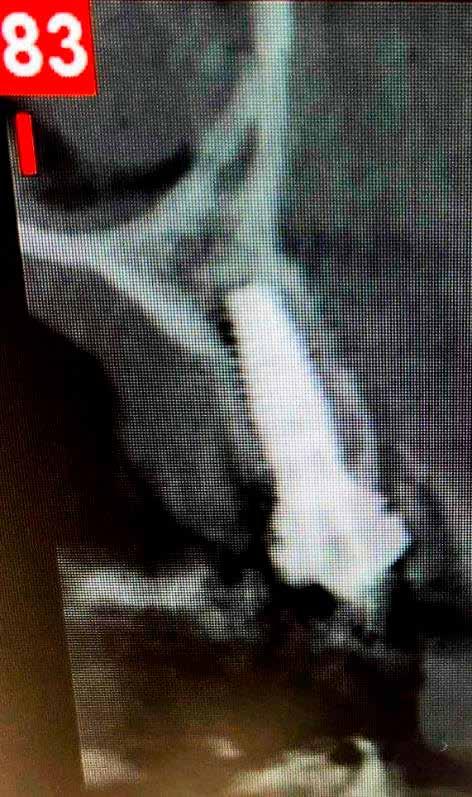
19. ábra: A sebészi beavatkozás után 4 hónappal készült CBCT-felvételből készített keresztmetszeti kép (bal felső szemfog; 23).
• A bemutatott esetek ellátása során a sebszélek egyesítését három rétegben végeztük el. A harmadik (mély) rétegben elhelyezett varratok behelyezése opcionálisnak számít. A céljuk, hogy a felszabadított lebenyt apikálisan is rögzítsék. Ennek a rögzítésnek a jelentősége abban rejlik, hogy így megakadályozhatjuk, hogy a periosteumhoz és a lebenyhez tapadó izmok által kiváltott húzóerők feszülést váltsanak ki az augmentált területnek megfelelően. A fentiek ismeretében minden esetben javasoljuk a harmadik varratsor behelyezését.
• Úgy véljük, ha a cikkben ismertetésre kerülő beavatkozást a fentiekben felsorolt szempontok figyelembevételével és a kurrens klinikai elveknek megfelelően alkalmazzuk, akkor képesek vagyunk az egyidejű kemény- és lágyszöveti augmentáció és optimalizáció elvégzésére. A bemutatott eljárás alkalmazásából fakadó egyedülálló előnyöket a laminamembrán specifikus felhasználási módjának köszönhetjük. A stabilizálását és rögzítését részben az egyéni ínyformázó felépítmény segítségével biztosítjuk.
A membrán a környező lágyrészek szintjében, az ínyformázó bázisához képest 3 mmrel koronálisabb pozícióban rögzül. Ezáltal elegendő teret biztosít a behelyezett csontpótló anyag számára, valamint köpenyszerűen beborítja és védi is. Ezenfelül a membrán a 4 hónapos gyógyulási időszak alatt fokozatosan bekövetkező felszívódásával egyidejűleg megkezdődik a behelyezett csontpótló anyag átépülése. A behelyezett anyag csontnívó felett elhelyezkedő koronális része a lágyrészvolumen növekedését indukálja, míg az állcsontgerinc nívója alatt lévő apikális része, a keményszövetek mennyiségének növekedéséhez járul hozzá. Ugyanakkor az egyéni ínyformázó felépítmény egy „emergencia profil benyomatot” biztosít az íny megfelelő konfiguráció szerinti gyógyulásához. Az ínyformázó felépítmény ezenfelül a membrán stabilizálásában és a csontpótló anyag számára történő helybiztosításban (tenting) is részt vesz.
A cikkben leírtak megfelelő módon alátámasztják, hogy a Poncho Lamina technika alkalmas a szólóimplantátumok mellett történő egyfázisú kemény- és lágyszöveti optimalizáció és augmentáció elvégzésére, illetve egy olyan újszerű egylépéses eljárás is ismertetésre került, amelyben az implantátumbehelyezés, a csontpótlás, a feszes íny szélességének megőrzése és az emergenciaprofil formázása kombináltan történt. A Poncho Lamina technika jelenleg széleskörűen alkalmazott implantológiai gyakorlatba történő további integrációja révén lehetőségünk adódhat a kezelési idő és a műtéti területnek megfelelően végzett egyéb sebészi beavatkozások számának csökkentésére. Ezáltal az implantológiai ellátás invazivitása jelentős mértékben csökkenhet. A cikk szerzői célszerűnek látják a jövőben más prospektív és randomizált vizsgálatok elvégzését, amelyek segítségével pontosabban meg lehetne ítélni az ismertetett eljárás hatékonyságát és az alkalmazásának indikáltságát.
(A cikk megírása során felhasznált szakirodalmi hivatkozások teljes jegyzéke elérhető a szerkesztőségünkben.)
Forrás: Modern Research in Dentistry 2022; Vol. 7, Iss. 2. 705-712


KÉTRÉSZES IMPLANTÁTUMRENDSZER
NÉLKÜL: TOVÁBBI
HOSSZÚ TÁVÚ BIZONYÍTÉKOK
A
Grazi Orvostudományi Egyetem friss 5–12 éves távú eredményei
• A kétrészes Patent™ fogászati implantátumok körül 12 év elteltével sem találtak periimplantitist [1]
• Még a veszélyeztetett betegeknél is csak kisebb biológiai szövődmények jelentkeztek, és nem fordultak elő protetikai komplikációk
• Hosszú távú vizsgálati adatok igazolták a kétrészes Patent™ fogászati implantátumok klinikai eredményességét [1, 2]
Tizenkét év után sem fordult elő periimplantitis – ez a Grazi Orvostudományi Egyetemen végzett új, hosszú távú vizsgálat legkiemelkedőbb eredménye, amelyet a közelmúltban publikáltak az International Journal of Oral and Maxillofacial Implants című szakfolyóiratban. A független és saját finanszírozású kutatás ismét igazolta a kétrészes Patent™ fogászati implantációs rendszer (Zircon Medical Management AG; 1. ábra) klinikai teljesítményét. [1] A dr. Sofia Karapataki vezetésével dolgozó csoport 39,91 implantátummal rendelkező beteget vizsgált 5-től akár 12 évig tartó időtartam során biológiai szövődményeket keresve.
A biológiai szövődmények, mint például az implantátumokat körülvevő lágy és szilárd szövetek fertőzései széles körben elterjedtek: A periimplantáris muscositis a betegek 43%–47%-ánál és az implantátumok 29%-ánál fordul elő, és az esetek mintegy 50%-ában periimplantitis irányába progrediál. [3, 4] Ha egyszer kialakul, a periimplantitis nehezen kezelhető, és sok esetben az implantátum elvesztésével végződik. [5]
Dr. Karapataki és munkatársai vizsgálati eredményei szöges ellentétben állnak a periimplantitis általános előfordulási gyakoriságával. Ráadásul megerősítik a Clinical Oral Implants Research című tudományos folyóiratban 2022 végén közzétett, 9 éven át tartó hosszú távú klinikai vizsgálat eredményeit is, amely szintén nem talált periimplantitist a kétrészes Patent™ implantátumok körül. [2]
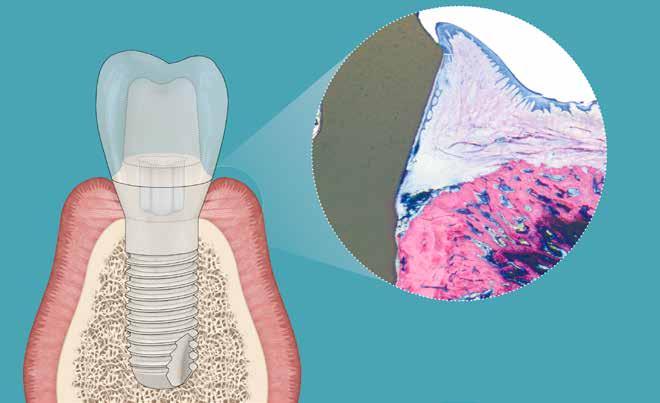
1. ábra: Hogyan előzheti meg a Patent™ a periimplantitist: A lágy szöveti szintű kialakítás, a speciális felületi topográfia és az exkluzív anyagösszetétel célzott kombinációjának köszönhetően a kétrészes Patent™ implantátum szoros érintkezést biztosít a transzmukózális felület és a lágy szövet között. Az így létrejövő biológiai határfelület egyfajta „záró lágy szövetként” működik, és képes megakadályozni, hogy a baktériumok behatoljanak az implantátum körüli lágy és szilárd szövetekbe. Az implantátum kialakításának köszönhetően kritikus szinten küszöböli ki a mikrohézag kialakulásának veszélyét, mind epicrestalisan, mind pedig supracrestalisan, ahol a baktériumok potenciálisan felhalmozódhatnak. Ehelyett a korona pereme a lezárt protetikai illesztéssel együtt equigingiválisan helyezkedik el, így ápolás és szájhigiénia szempontjából könnyen hozzáférhető marad. Ezek a tényezők elengedhetetlenek ahhoz, hogy a krónikus szöveti gyulladás, például a periimplantitis hosszú távon elkerülhető legyen.
100%-os sikerességi mutatók
A 91 implantátum közül egyet sem kellett eltávolítani. Az implantátum beültetése után 5–12 évvel sem alakult ki periimplantitis. Protetikai komplikációk nem fordultak elő, és csak kisebb biológiai szövődményekről számoltak be. Csak három betegnél (7,7%; 9 implantátum) jelentkeztek periimplantáris mucositis tünetei. Harminchat betegnél figyeltek meg egészséges lágy részeket (81 implantátum; 2. ábra). Nyolcvanöt implantátum esetében nem volt marginális csontvesztés, vagy csupán enyhe csontelváltozás (< 0,7 mm) volt megfigyelhető. Hat implantátum esetében a csontvesztés meghaladta a 0,7 mm-t; a legnagyobb marginális csontvesztés 1,67 mm volt. Az implantátumrendszer tehát 100%-os túlélési és sikerességi arányt mutatott. [6, 7]
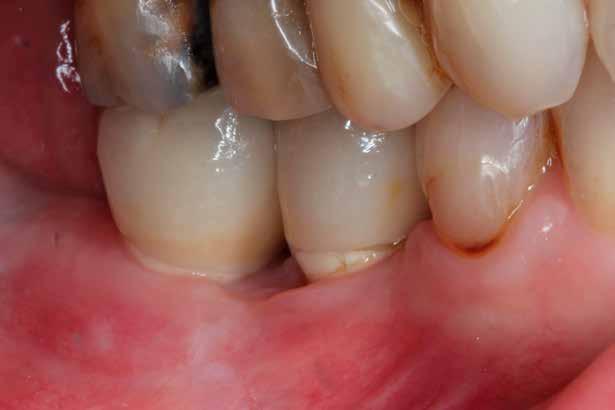
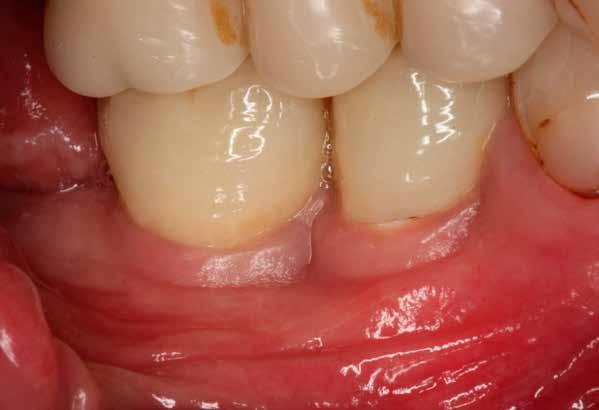
2. ábra: Két Patent™ implantátum a kiindulási állapotban (balra) és klinikailag stabil szövetszintek – a lágy részek térfogatának növekedésével – a 7 éves kontrollvizsgálaton (jobbra; © Karapataki et al. 1).
Alkalmazhatóság a mindennapi gyakorlatban
Az eredmények könnyedén átültethetők a mindennapi implantációs gyakorlatba. Minden sebészeti és protetikai kezelési eljárást, valamint az utóvizsgálatokat is két magánrendelőben (Athénban és Bécsben) végezték. A 18 éves alsó korhatártól eltekintve nem voltak kizáró feltételek. Következésképpen a vizsgálatba bevonásra kerültek általános egészségi állapotú, de betegségekben szenvedő (pl. Down-szindrómával élő vagy daganatos), illetve megfelelő kezelésben részesülő (pl. vérnyomáscsökkentők, antidepresszánsok vagy immunszuppresszánsok) és parodontitisben szenvedő vagy vékony íny biotípusos betegek, valamint dohányosok is. A javallatokat sem korlátozták semmilyen módon: Az implantátumok a felső és alsó állkapocsban, valamint az elülső és a hátsó régióban kerültek beültetésre, illetve szükség esetén egyidejűleg augmentációra is sor került.
Irodalom
Az implantátumokat 2009 és 2016 között helyezték be, a legutolsó nyomonkövetési vizsgálatra pedig 2021 májusában került sor. Induláskor 47 beteget kezeltek 108 implantátummal. Közülük 39-en, összesen 91 implantátummal álltak rendelkezésre a záró vizsgálat elvégzéséhez. Az implantátum beültetésekor és az utolsó kontrollvizsgálat alkalmával rögzítésre került a marginális csontvesztés, a tasakmélység, négy helyen (mesialis, distalis, bukkális, lingualis) a szondázásra történő ínyvérzés, valamint a szájhigiénia (egyszerűsített oralhigiénés index) [8].
Dr. Karapataki végül az alábbi következtetést vonta le: „A hosszú távú tanulmány a vizsgált implantátumrendszerrel elért kiemelkedő eredményeket dokumentálja egy hosszabb, akár 12 éves megfigyelési időszak alatt – olyan »valós« betegeket is beleértve, akiket a praxisomban napi szinten kezelek. Az eredmények azt mutatják, hogy a periimplantitisz nélküli implantációs kezelések a mindennapi implantációs gyakorlatban is megvalósíthatók.”
További információért látogasson el a www.mypatent.com weboldalra.
1. Karapataki S, Vegh D, Payer M, Fahrenholz H, Antonoglou GN. Clinical performance of two-piece zirconia dental implants after 5 and up to 12 years. Int J Oral Maxillofac Implants. 2023. december 12.;38(6):1105–114. doi: 10.11607/jomi.10284. PMID: 38085741.
2. Brunello G, Rauch N, Becker K, Hakimi AR, Schwarz F, Becker J. Two-piece zirconia implants in the posterior mandible and maxilla: a cohort study with a follow-up period of 9 years. Clin Oral Implants Res. 2022. december;33(12):1233–44. doi: 10.1111/clr.14005. PMID: 36184914.
3. Derks J, Tomasi C. Peri-implant health and disease. A systematic review of current epidemiology. J Clin Periodontol. 2015. április;42 Suppl 16:S158–71. doi: 10.1111/jcpe.12334. PMID: 25495683.
4. Lee CT, Huang YW, Zhu L, Weltman R. Prevalences of peri-implantitis and peri-implant mucositis: systematic review and meta-analysis. J Dent. 2017. július;62:1–12. doi: 10.1016/j.jdent.2017.04.011. PMID: 28478213.
5. Abdelhay N, Prasad S, Gibson MP. Failure rates associated with guided versus non-guided dental implant placement: a systematic review and meta-analysis. BDJ Open. 2021. augusztus 18.;7(1):31. doi: 10.1038/s41405-021-00086-1. PMID: 34408127; PMCID: PMC8373900.
6. Buser D, Weber HP, Lang NP. Tissue integration of non-submerged implants. 1-year results of a prospective study with 100 ITI hollow-cylinder and hollow-screw implants. Clin Oral Implants Res. 1990 Dec;1(1):33–40. doi: 10.1034/j.1600-0501.1990.010105.x. PMID: 2099210.
7. Kohal RJ, Knauf M, Larsson B, Sahlin H, Butz F. One-piece zirconia oral implants: one-year results from a prospective cohort study. 1. Single tooth replacement. J Clin Periodontol. 2012. június;39(6):590–7. doi: 10.1111/j.1600-051X.2012.01876.x. PMID: 22519944.
8. Greene JC, Vermillion JR. The simplified oral hygiene index. J Am Dent Assoc. 1964. január;68:7–13. doi: 10.14219/jada.archive.1964.0034. PMID: 14076341.
Könyvajánlataink

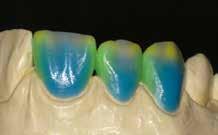










Ennek a könyvnek a kiadásával célkitűzésünk volt áttekinteni fogászati implantológiában hagyományosan alkalmazott csontmegmunkáló eljárásokat (kézi eszközök, forgóeszközök), összehasonlítva őket az új (piezo, lézer, mágneses kalapács /magnetic mallet = MM) módszerekkel, valamint bemutatni a csontpótló anyagokat és köztük az újnak számító BoneAlbumint.
Mind a mágneses kalapács, mind a BoneAlbumin a nemzetközi irodalomban is rendkívül újnak számít, egyelőre kevés vagy egyáltalán nincs sokéves tapasztalat, így fontos, hogy az eddigi ismereteket, technikákat, az elért eredményeket kellő kritikával, önkritikával kezeljük, és reálisan próbáljuk helyüket és szerepüket meghatározni a fogászati implantológiában.
Dr. Gáspár Lajos
Könyvem megszületését elsősorban dr. Forrai Judit professzor asszonynak köszönhetem. Az ő inspirálására született meg ez a történeti visszatekintés. 2014 februárjában a Semmelweis Egyetem Népegészségügyi Intézetének a tantermében megalakult a Magyar Orvostörténeti Társaság részeként a Fogászattörténeti Kör. Az alakuló ülésen érdekes előadások hangzottak el, majd azok befejeztével Forrai Judit tanárnő felkért, hogy tudnék-e az őszi program keretében a fogászati implantológia történetéről előadást tartani. Természetesen szívesen elvállaltam. Az orvoslás, a fogorvoslás történeti vonatkozásai mindig is érdekeltek, és a fogorvostan-hallgatóknak az érzéstelenítésről, az implantológiáról szóló előadásaimban állandóan próbáltam történeti vonatkozásokat is beépíteni. Engem elsősorban a gyógyító eljárások fejlődése érdekelt. Mi volt a régi gyógymódok – az akkori ismeretek szerinti – élettani, patológiai vagy akár vallási háttere?
Dr. Divinyi Tamás
A fogászat és különösen az implantológia fejlôdése az elmúlt évtizedekben az érdeklődés középpontjába került. Magyarországon napjainkban évi közel 60 000 darab fogászati implantátumot helyeznek be, ami mintegy évi 12 milliárd forint forgalmat generál az orvosi és fogtechnikai költségekkel együtt.
Az Implant Index című kézikönyv nemcsak a tudományos és szakmai ismeretek jelentős lexikális anyagát összegzi, hanem talán elsőként mutatja be az implantológiai piac jellemző vonásait, gazdasági elemzéseket, múltra, jelenre és jövőre vonatkozó adatokat, fejlődési tendenciákat. Ugyancsak új témának számít az implantációs betegek gondozását bemutató fejezet is. A könyv fejezeteiben először az adott témakör rövid, áttekintő bevezetésére kerül sor, majd ezt követi a lexikális ismeretanyag táblázatokban, majd elsősorban a mindennapi gyakorlatot segítő írások, cikkek következnek.
Dr. Gáspár Lajos és dr. Toldi Ferenc
Az implantológia a fogorvostudomány egyik legintenzívebben változó, fejlődő szakterülete. A foghiányok pótlásának szándéka - valamilyen csontba épített eszköz, anyag segítségével - több évezredes múltra tekint vissza. Az implantációs kísérletek azonban hosszú időn át - a nem megfelelő biológiai, anyagtani stb. feltételek hiánya miatt- többnyire nem jártak sikerrel. A nagy „előrelépést" a 20. század, annak is különösen a második fele hozta meg. Ezekben az évtizedekben számtalan próbálkozásról, kísérletről olvashattak az érdeklődők a hazai és a nemzetközi szakirodalomban egyaránt. A dentális implantológia mára már a fogorvoslás nélkülözhetetlen területe lett. A mindennapi gyakorlatban szükség van az ismeretek permanens bővítésére, frissítésére, hiszen egyre újabb és újabb implantációs rendszerek, fejlesztések, eszközök és eljárások megjelenésével szembesülnek - szinte naponta - a szakemberek.
Dr. Urbán István

Viz Dental Implant Kft. 1052 Bp., Váci utca 23. 1. em. 1/a Tel.:/fax: 06-1-318-4939, E-mail: office@vizdental.hu, www.vizdental.hu


SGS International Ltd. European Logistic Center 1047 Budapest, Károlyi István u. 1–3.
Tel.: +36 1 328 0427
Fax: +36 1 348 0428
E-mail: info@sgs-dental.com www.sgs-dental.com


Implant Solution
Tel.: 06-20-326-0579
e-mail: info@implantsolution.hu Web: www.cowellmedi.hu




info@alphaimplant.hu +36 1 353 9090 www.alphaimplant.hu

Dent-East Kft. 1112 Budapest, Rétkerülő út 51 www.dent-east.com • mail@dent-east.com


















klinikai tapasztalat és tudományos háttér. Folyamatos fejlesztés 16 éve. A LEGINNOVATÍVABB, PIACVEZETŐ


Kompressziós és bikortikális egyfázisú implantátumok választhatóan multiunit fejjel. Csavarozható stégekhez, overdenture felépítményekhez. Azonnali implantáció és azonnali terhelés meghatározott szakmai protokoll szerint. Folyamatos, többlépcsős kurzusok, praxistréning, felhasználótalálkozók. ISO, CE, nemzetközi klinikai tapasztalat és tudományos háttér. Folyamatos fejlesztés 16 éve.




CS 3700 CAD/CAM a piacvezető oralkamera Szkennelés kompromisszum nélkül Kompressziós





Bővebb felvilágosítás és






web: www.sofortimplant.com



