




Droits d’auteur
Il est interdit de reproduire, de traduire ou d’adapter cet ouvrage sans l’autorisation écrite du Centre de référence en agriculture et agroalimentaire du Québec (CRAAQ) afin de respecter les droits d’auteur et d’encourager la diffusion de nouvelles connaissances.
Avertissements
Les marques de commerce mentionnées dans ce guide le sont à titre indicatif seulement et ne constituent nullement une recommandation de la part des auteurs ou de l’éditeur.
Au moment de sa rédaction, l’information contenue dans le présent guide était jugée représentative du secteur de la production vache-veau au Québec. Son utilisation demeure sous l’entière responsabilité du lecteur. Certains renseignements pouvant avoir évolué de manière significative depuis la rédaction de cet ouvrage, le lecteur est invité à en vérifier l’exactitude avant de les utiliser.
Dans le présent document, le masculin englobe le féminin et est utilisé uniquement pour alléger le texte.
Le CRAAQ remercie ses membres partenaires :
Centre de référence en agriculture et agroalimentaire du Québec
Édifice Delta 1, 2875,boulevard Laurier, 9e étage
Québec (Québec) G1V 2M2
Téléphone : 418 523-5411
Télécopieur : 418 644-5944
Courriel : client@craaq.qc.ca
Site Internet : www.craaq.qc.ca
© Centre de référence en agriculture et agroalimentaire du Québec,2018
PBBO0102
ISBN 978-2-7649-0572-2 (version imprimée)
ISBN 978-2-7649-0573-9 (PDF)
Dépôt légal
Bibliothèque etArchives Canada,2018
Bibliothèque etArchives nationales du Québec,2018
Le CRAAQ remercie toutes les personnes ayant contribué de près ou de loin à la réalisation de cette publication.
Rédaction (2007)
Carole Déziel, médecin vétérinaire, Bureau Vétérinaire L’Islet, Saint-Jean-Port-Joli
Gilles Laverdière, agronome, M.Sc., professeur en production bovine, ITA La Pocatière
C. Déziel (1999)
G. Huneault, D. Bousquet, M. Ibrahim, D.P. Ménard et D. Vaillancourt (1994)
Révision
Rémi Laplante, DMV, vétérinaire-conseil, Les Producteurs de bovins du Québec
Édition
Barbara Vogt, éditrice et traductrice, CRAAQ
Conception graphique et mise en page originale
Communications Science-Impact
Conception graphique de couverture et mise en page (3e édition)
Véronique Michaud, graphiste, CRAAQ
Carole Déziel1
Gilles Laverdière1
Révisé par : Rémi Laplante
1. 2e édition (2007).
1re édition (1999) : Carole Déziel. Basée sur le document de G. Huneault, D. Bousquet. M. Ibrahim, D.P. Ménard et D. Vaillancourt (1994)
La vocation d’une vache de boucherie est de produire un veau vivant par année. Le but premier d’une exploitation vache-veau est de maximiser le nombre de kilogrammes de veau sevré par vache, au meilleur coût possible, tout en considérant l’amélioration du potentiel génétique. Une des conditions essentielles à l’atteinte de ce but est un programme de reproduction adéquat. En production bovine, les problèmes de reproduction représentent de 40 à 60 % des réformes chez les vaches, particulièrement chez les primipares (premier vêlage), en raison d’un diagnostic de gestation négatif au sevrage ou d’une gestation trop tardive en fin de saison de reproduction (vêlages tardifs moins rentables).
Un tel programme nécessite la définition des objectifs de production et de reproduction de l’exploitation, c’est-à-dire des résultats que l’on veut atteindre. Ces points de référence serviront ultérieurement au gestionnaire pour mesurer l’efficacité de son entreprise et apporter des correctifs au besoin.
Les objectifs sont les suivants :
un veau par vache par année;
âge au premier vêlage : entre 22 et 24 mois, avec une moyenne à 23 mois;
poids de la femelle à 13 mois : de 65 à 70 % du poids adulte, prête à se reproduire; vêlages regroupés;
70 % des vêlages dans les 20 premiers jours de la période de vêlage;
intervalle moyen entre les vêlages : 360 à 370 jours; sevrage de 95 % des veaux nés; le poids total des veaux sevrés doit représenter 40 % du poids du troupeau reproducteur, c’est-àdire les vaches, les taureaux et les sujets de remplacement;
taux de mortalité présevrage inférieur à 2 %; taux de mortalité post-sevrage inférieur à 1 %;
taux de mortalité annuel chez les vaches inférieur à 0,5 %;
taux de réforme des sujets reproducteurs : 15 %; période de reproduction ne dépassant pas 63 jours et comportant 3 opportunités de conception pour les vaches et les génisses;
saison d’accouplement des génisses débutant 3 à 4 semaines avant celle des vaches.
Pour réaliser ces objectifs, il faut choisir minutieusement les géniteurs. Cette sélection nécessite de sérieuses réflexions, basées en partie sur les connaissances présentées dans ce chapitre (voir aussi le chapitre Génétique).
Anatomie
L’appareil génital mâle est composé essentiellement des testicules, de glandes accessoires et de canaux (Figure 6.1). Les testicules sont les organes sexuels primaires. Les glandes accessoires et les canaux sont les organes sexuels secondaires.
Figure 6.1
Appareil génital mâle
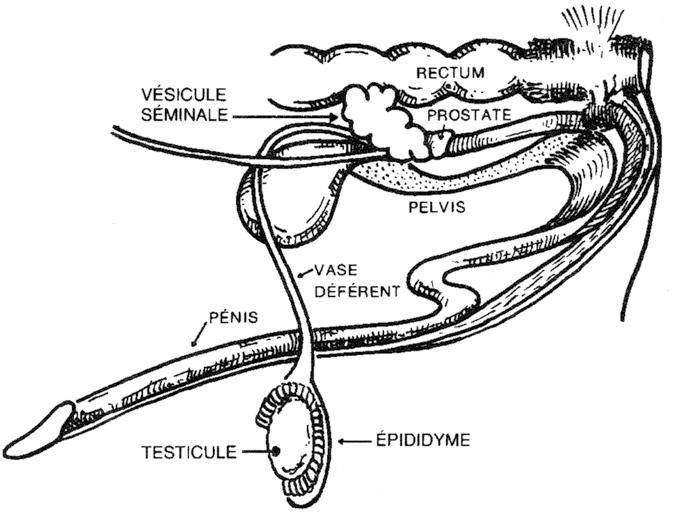
Chez le mâle, la reproduction est influencée par certains éléments du milieu extérieur tels que la température, l’alimentation et les phénomènes sensoriels. Tous ces éléments contribuent à stimuler une partie du cerveau, l’hypothalamus, qui à son tour stimule l’hypophyse (petite glande située à la base du cerveau). Celleci répond au stimulus en sécrétant les gonadotrophines (hormones FSH et LH). Ces hormones atteignent les testicules par la voie sanguine; elles stimulent la production de testostérone et autres hormones mâles, de même que la spermatogenèse (processus de formation des spermatozoïdes).
La testostérone, hormone sécrétée par les cellules de Leydig situées dans le tissu interstitiel des testicules, est nécessaire au développement des organes sexuels. Elle est aussi responsable du développement des caractéristiques sexuelles secondaires mâles : forte carrure, voix, libido, érection, éjaculation.
Chez le taureau, la spermatogenèse dure environ 41 jours (Figure 6.2). Au terme de leur formation, les spermatozoïdes s’acheminent vers l’épididyme où ils subissent une maturation. C’est à cet endroit qu’ils sont recouverts d’une pellicule protéique protectrice. Leur séjour dans l’épididyme dure de 8 à 20 jours selon l’espèce animale et la fréquence de l’éjaculation. Chez le taureau, la spermatogenèse et le transit dans l’épididyme durent au total de 50 à 60 jours.
Un taureau adulte produit environ 13 milliards de spermatozoïdes par jour, la production variant en fonction du nombre de cellules germinales, donc du volume testiculaire. Le sperme est essentiellement une suspension de spermatozoïdes dans un milieu appelé plasma séminal, composé de sécrétions provenant des épididymes, des ampoules déférentielles, des vésicules séminales, de la prostate, des glandes de Cowper et des quelques glandes situées dans l’urètre. Ces sécrétions servent de milieu nutritif et de véhicule aux spermatozoïdes. Le volume éjaculé se situe entre 2 et 10 ml (moyenne de 6 ml) et peut contenir quelques centaines de mil-
Figure 6.2
Coupe transversale d’un tube séminifère illustrant la formation des spermatozoïdes
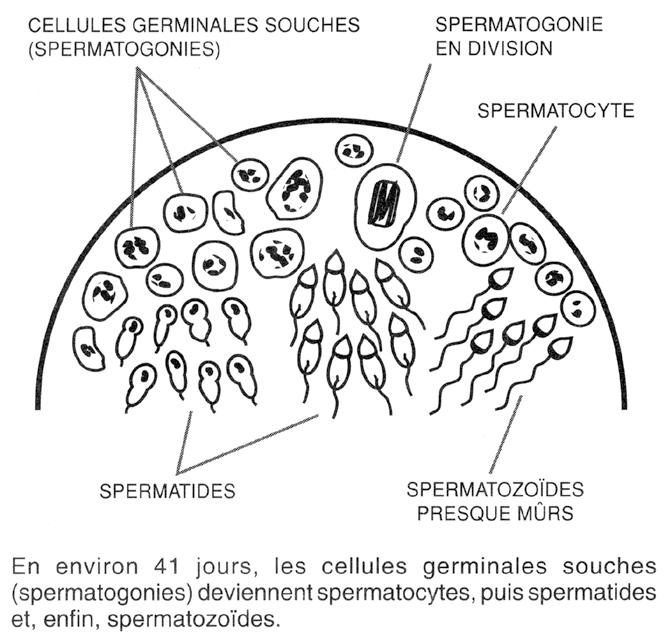
lions voire jusqu’à 10 milliards de spermatozoïdes. La moyenne serait de 7,2 milliards.
La puberté se signale par l’apparition des caractéristiques sexuelles secondaires et du désir sexuel, par la capacité de copuler et par la présence de spermatozoïdes viables dans le sperme. La plupart des taureaux atteignent la puberté vers l’âge de 9 à 12 mois, mais celleci peut survenir entre 6 et 18 mois. Des diètes planifiées et des facteurs génétiques, et particulièrement les différences entre les races, peuvent expliquer ces variations. En général, certaines races de boucherie, notamment le zébu (Bos indicus), atteignent la maturité sexuelle moins rapidement que les races laitières. Le plein potentiel génital est atteint vers l’âge de 3 à 5 ans.
Pour une efficacité optimale, le choix d’un taureau doit reposer sur les critères suivants : développement testiculaire optimal; production maximale de semence; conformation adéquate du scrotum; conformation générale typique de la race et compatible avec la monte; libido supérieure.
Développement testiculaire optimal
Le volume testiculaire est un indicateur de la quantité de tissus pouvant produire des spermatozoïdes. Dans des conditions normales, la mesure de la circonférence scrotale est proportionnelle au volume testiculaire; elle s’avère donc, dans la majorité des cas, un indice fiable du potentiel reproducteur d’un taureau.
Le taureau affichant une circonférence scrotale supérieure procure à ses descendants femelles les avantages suivants :
une puberté précoce; une activité cyclique régulière; une fertilité accrue.
Ses descendants mâles hériteront, pour leur part, des particularités suivantes :
une circonférence scrotale supérieure;
une fertilité accrue.
Mesure de la circonférence scrotale
Trois instruments peuvent être utilisés pour mesurer la circonférence scrotale : le ruban métallique, le ruban Coulter (n’est plus disponible sur le marché cependant) et le nouveau ruban ReliaBull. Tous trois sont conçus spécialement à cette fin et donnent des mesures exactes s’ils sont bien utilisés. La différence entre les trois types de ruban réside dans l’ajustement du ruban autour du
scrotum : l’ajustement se fait manuellement dans le cas du ruban métallique et à l’aide de la poignée dans le cas des rubans Coulter et ReliaBull. Le ruban Coulter a été utilisé dans les stations d’épreuve jusqu’en 2005; il a été remplacé depuis par le ruban ReliaBull.
Pour mesurer la circonférence scrotale avec le ruban métallique, d’une main, on retient fermement les testicules à l’extrémité inférieure du scrotum en prenant soin de les aligner côte à côte. De l’autre main, on glisse le ruban autour du scrotum. On effectue la lecture après avoir bien serré le ruban à l’endroit où le diamètre est le plus grand (Figure 6.3). Une mauvaise technique peut conduire à des lectures erronées; ainsi, la circonférence peut être surévaluée si le ruban n’est pas serré suffisamment. Une température ambiante froide de même que les dépôts de gras chez les sujets ayant un état de chair excessif peuvent également influencer la lecture.
Figure 6.3
Mesure de la circonférence scrotale à l’aide du ruban métallique (Rubans Coulter et ReliaBull)
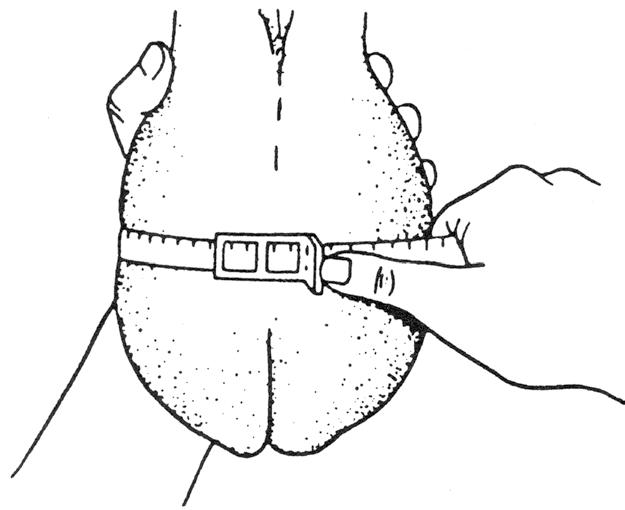
Après avoir bien immobilisé le taureau, il faut palper les testicules et les faire descendre dans le scrotum. On tient les deux cordons spermatiques (la portion au–dessus des testicules dans le scrotum) afin d’éviter qu’ils ne remontent. De l’autre main, on saisit le ruban par la
poignée et on insère le scrotum à l’intérieur du ruban. La mesure doit être prise à l’endroit le plus large. Il faut éviter de comprimer les testicules. Par la suite, on relâche la tension du ruban sur le scrotum. Une fois bien adapté autour du scrotum, le ruban est enlevé pour faire la lecture. On répète deux autres fois pour vérifier la mesure. Dans les stations d’épreuve au Québec, cette

mesure est effectuée par un médecin vétérinaire. Pour en savoir davantage sur le ruban ReliaBull ou pour le commander, consulter la page : www.lane-mfg.com/ scrotaltapenew.html
Les circonférences scrotales minimales recommandées par la Society of Theriogenology (société vétérinaire américaine pour l’étude de la reproduction) sont présentées au Tableau 6.1. Les sujets marginaux ou inférieurs peuvent occasionnellement produire du sperme en quantité et qualité acceptables. Cependant, la majorité de ces taureaux ne peut satisfaire aux exigences d’un programme de reproduction intensif. Conséquemment, il est recommandé de choisir un taureau dont les mensurations sont substantiellement supérieures à ces minimums.
Le lecteur est invité à consulter la section Taureau de génétique supérieure du chapitre Génétique afin de connaître, pour le Québec, les exigences (seuils minimaux) auxquelles chaque race doit satisfaire pour être admissible à une attestation.
La qualité du sperme est intimement reliée à la circonférence scrotale. Habituellement, la production et la qualité augmentent d’une façon rapide jusqu’à ce que
Tableau 6.1
Circonférences scrotales minimales recommandées par la Society of Theriogenology (cm)
Âge (mois) Simmental
Source : Coulter, Mapletoft, Kozub et Cates, 1987
Angus, Charolais, Hays Converter Maine Anjou Hereford, Shorthorn
Blonde d’Aquitaine, Highland, Limousin, Salers et autres races
la circonférence scrotale atteigne 38 cm. Le Tableau 6.2 présente les résultats d’une étude effectuée en Saskatchewan sur des taureaux de plus de 24 mois. L’étude a également démontré que la qualité séminale ne s’améliore que très peu au-dessus de 38 cm de circonférence scrotale.
contractions et les relâchements du scrotum contribuent à garder les testicules à une distance du corps qui permet de maintenir la bonne température. Lorsqu’il fait chaud, les testicules sont éloignés du corps; à basse température, ils tendent à s’en rapprocher.
Tableau 6.2
Relation entre la circonférence scrotale et la production de sperme
Nombre de taureaux évalués
Adapté de Wenkoff, 1987
Circonférence scrotale (cm)
Les testicules sont contenus dans le scrotum. Celui-ci supporte et protège les testicules, mais joue aussi un rôle important dans la régulation de leur température. Les cellules spermatiques se forment seulement à une température inférieure de 4 à 5 °C à celle du corps. Les
Nombre et proportion de taureaux produisant du sperme de qualité satisfaisante
(13 %)
(88 %)
Les dépôts de gras à la partie supérieure du scrotum interfèrent avec la remontée testiculaire, exposant ainsi les organes aux basses températures. Cela a pour effet de ralentir le développement testiculaire, ou même d’en favoriser la dégénérescence. Les lésions provoquées sont parfois irréversibles. C’est le cas du scrotum aux côtés droits et parallèles (Figure 6.5A) fréquemment rencontré chez les taureaux trop gras lorsqu’ils sont jeunes.
6.5
Types de conformation du scrotum
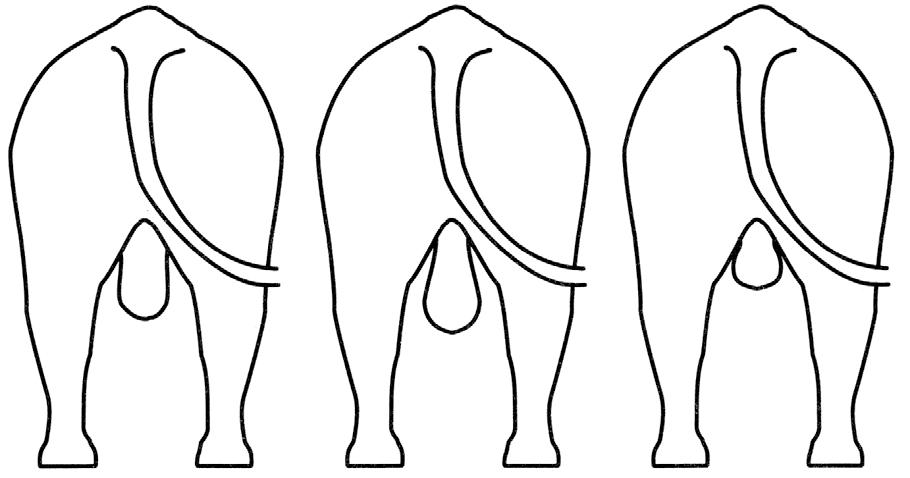
Un scrotum de forme triangulaire, pointant vers le sol, contient de petits testicules qui sont en contact étroit avec la paroi de l’abdomen. La température ambiante est trop élevée pour favoriser une spermatogenèse acceptable (Figure 6.5 C).
Le meilleur développement testiculaire est obtenu chez un taureau dont la partie supérieure du scrotum présente une nette démarcation, favorisant ainsi l’action des mécanismes thermorégulateurs (Figure 6.5 B).
Un taureau doit mériter une cote supérieure de conformation, particulièrement pour les pieds et les membres postérieurs. La monte répétée exige de solides membres postérieurs. Un taureau doté d’une conformation de bouvillon risque d’avoir un système hormonal de bouvillon, lequel est inutile dans un programme de reproduction. Lorsqu’on sélectionne un taureau pour produire des femelles d’élevage, il est opportun de choisir d’abord une race maternelle non déjà présente dans la mère (Angus, Hereford, Gelbvieh, Salers, Shorthorn et Simmental), mais il faut également penser aux pieds et aux membres si l’on souhaite que ces futures femelles restent longtemps dans le troupeau, pendant 15 ans par exemple.
La libido se définit comme le désir d’effectuer la monte, et l’habileté à effectuer l’accouplement est consécutive à la libido. Ces deux facteurs ont de toute évidence un impact certain sur le nombre de gestations obtenues à la fin d’une courte période de saillies.
Un producteur sérieux suit les règles de base suivantes :
Acheter un taureau d’un éleveur réputé, possédant un troupeau qui a fait ses preuves, ou encore d’un encan qui fournit des certificats d’évaluation du potentiel de reproduction;
Avant de conclure l’achat, s’enquérir de la fertilité du père et de la mère du sujet (dossiers);
Acheter un taureau dont la performance de gain de poids post-sevrage a été éprouvée, et dont l’indice est au moins supérieur à la moyenne;
Acheter un taureau dont la circonférence scrotale excède le minimum requis; ne retenir que les taureaux dont la circonférence scrotale correspond au moins à la moyenne de la race à son âge;
Acheter un taureau dont le scrotum présente une nette démarcation à sa partie supérieure (en forme de bouteille). Cette notion est particulièrement importante pour les sujets de 2 ans;
Acheter un taureau ne présentant pas d’excès de gras;
Acheter un taureau possédant de bons pieds, de bons membres et une bonne vision. Des yeux clairs et vifs sont un indice de bonne santé;
Avant la saison d’accouplement, faire subir à chaque taureau un examen du potentiel de reproduction : examen général, circonférence scrotale et examen du sperme (Breeding Soundness Evaluation, Society of Theriogenology);
Acheter un taureau de charpente moyenne;
Acheter un taureau ayant une musculature supérieure (cote de 7,0 ou plus), tout particulièrement s’il s’agit d’un taureau terminal ou d’une race paternelle;
Acheter un taureau d’une race en fonction de l’objectif de production visé : produire des veaux pour les parquets d’engraissement ou produire de futures femelles d’élevage;
Acheter un taureau d’une race permettant de profiter au maximum de la vigueur hybride chez les descendants.
Bref, si on a peu de contrôle sur la quantité de spermatozoïdes produite par le taureau, on a un excellent contrôle sur le pourcentage de cellules spermatiques présentes dans la récolte. L’utilité d’un taureau de
reproduction dont le seul produit est le sperme se mesure à la quantité de cellules spermatiques récoltées.
Anatomie
L’appareil génital femelle (Figure 6.6) est le siège de la fécondation, de la gestation et de la parturition. La vulve, partie la plus externe, est composée de muscles élastiques qui sont responsables de la fermeture normale de cette extrémité de l’appareil génital.
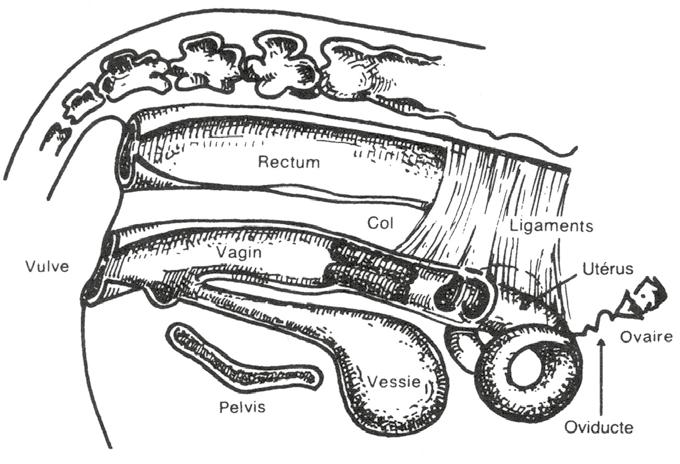
Le vagin est un organe tubulaire, également soumis à des changements au cours du cycle œstral. Ses parois très élastiques permettent le passage du veau lors du vêlage. La paroi interne est parsemée de glandes muqueuses. Leurs sécrétions sont le miroir de l’activité ovarienne, elles sont donc sujettes à divers changements au cours du cycle œstral.
L’utérus est composé d’un col, d’un corps et de deux cornes utérines. Le col utérin est un organe cylindrique formé d’anneaux généralement rigides qui se relâchent légèrement lors de l’œstrus pour permettre le passage du sperme jusqu’aux oviductes. Pendant la gestation, un bouchon muqueux en assure l’étanchéité. Lors du vêlage, le col se dilate suffisamment pour permettre le passage du veau.
Les oviductes sont de minuscules tubes reliant chaque corne utérine à l’ovaire correspondant. C’est le site de la rencontre des spermatozoïdes et de l’ovule (fécondation). Chaque oviducte se termine en entonnoir (pavillon), lequel recueille l’ovule libéré par le follicule mature à la surface de l’ovaire.
Au nombre de deux, les ovaires sont situés à l’extrémité des oviductes. Leur forme ressemble à celle d’une fève et leurs dimensions approximatives sont de 2 à 3 cm de longueur et de 1 à 1,5 cm de diamètre chez la vache adulte. Les principales fonctions ovariennes sont la production d’ovules (gamètes femelles) par les follicules et la production d’hormones, plus particulièrement les stéroïdes tels que la progestérone sécrétée par le corps jaune et l’œstrogène sécrété par le follicule.
Les concepts fondamentaux de la reproduction tels que les variations hormonales, la fécondation et le développement embryonnaire sont relativement complexes et ne cessent de faire l’objet de recherches fondamentales et appliquées.
Les principaux phénomènes et étapes de la reproduction chez la vache sont la puberté, le cycle œstral, l’accouplement ou l’insémination artificielle, la fécondation, la gestation, la parturition et la période post-partum.
La puberté est la période où les organes de la reproduction deviennent fonctionnels, permettant ainsi à l’animal de se reproduire. Le cycle œstral, comprenant les variations hormonales et l’ovulation, se produit alors comme chez l’adulte. L’âge de la puberté est le même chez le taureau et chez la génisse et varie de 200 à 400 jours selon, entre autres, la race, le développement corporel (poids) de l’animal, certains facteurs héréditaires et l’environnement, autant de facteurs sur lesquels le producteur exerce un certain contrôle. De façon générale, la femelle d’une race de petite taille atteint la puberté plus rapidement que la femelle
appartenant à une race de grande taille. Par contre, aucune génisse ne devrait être accouplée ou inséminée avant d’avoir atteint un développement corporel suffisant (en moyenne 65 % du poids adulte).
Le producteur peut influencer l’âge de la puberté par l’entremise de l’alimentation et le gain de poids des jeunes sujets reproducteurs, notamment par l’intermédiaire d’un traitement antiparasitaire et l’usage d’additifs alimentaires (ionophores). Les ré-
régulier et, lors d’une gestation, les cycles œstraux sont interrompus.
La durée moyenne du cycle œstral est de 21 jours, mais le cycle peut varier de 17 à 24 jours (Figure 6.7).
On divise généralement le cycle œstral en deux phases distinctes : la phase lutéale et la phase folliculaire, qui se divisent, à leur tour, en deux sous-phases (Tableau 6.4).
Âge et poids à la puberté en fonction de l’usage de vermifuge et/ou d’additif alimentaire
Conversion alimentaire Âge à la puberté (jours) Poids à la puberté
Source : Beef (1997), cité dans Bovins du Québec, printemps 1997
sultats présentés au Tableau 6.3 démontrent que les génisses vermifugées et/ou recevant des ionophores atteignent la puberté plus rapidement et à un poids moindre que celles ne recevant aucun traitement de vermifuge ni d’ionophore. De plus, cette même étude démontre que les génisses vermifugées ou recevant des ionophores parviennent à une première conception plus rapidement que les génisses ne recevant aucun traitement.
La vache est polyœstrienne puisqu’elle vient en œstrus (chaleur) à intervalles réguliers durant toute l’année. En présence de stress anormaux (malnutrition, maladie grave, etc.), la vache cesse d’avoir un cycle œstral
Figure 6.7
Variations hormonales au cours du cycle œstral
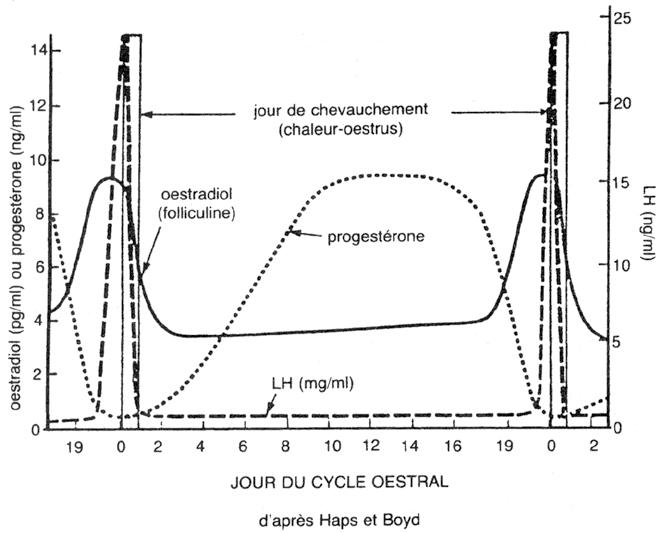
Tableau 6.4
Description
Phase lutéale (jour 1 à jour 17)
• Post-œstrus (jour 1 à jour 5) Période qui suit immédiatement l’œstrus et qui correspond à l’ovulation (libération d’un ovule par un follicule, lequel se transforme ensuite en corps jaune). L’ovulation survient entre 10 et 12 heures après la fin de la chaleur ou de 24 à 36 heures après le début de la chaleur.
Développement progressif du corps jaune. Augmentation graduelle de la production de la progestérone par le corps jaune.
• Diœstrus (jour 6 à jour 17) Production élevée de progestérone par le corps jaune mature. Forte progression de la quantité de récepteurs de prostaglandine F2a (PGF) sur le corps jaune jusqu’au jour 8.
Au début de la période, l’embryon passe de l’oviducte à l’utérus en 2 à 4 jours. Sous l’influence de la progestérone, la muqueuse utérine (endomètre) sécrète des éléments essentiels au développement embryonnaire durant les premières semaines de gestation. La présence de l’embryon dans l’utérus prolonge la survie du corps jaune, pour toute la durée de la gestation. Chez la vache non gravide, vers la fin de la période, certaines cellules de l’endomètre sécrètent des prostaglandines qui font régresser le corps jaune débutant ainsi un nouveau cycle œstral.
Phase folliculaire (jour 17 à jour 21)
• Proœstrus
Période de régression du corps jaune (2 à 4 jours) et de croissance du follicule.
Signes extérieurs
Refus de monte, écoulement de sang, de 24 à 48 heures après la fin de l’œstrus, observé seulement chez 50 % des vaches et 90 % des génisses. La perte de sang provenant de l’utérus ne donne aucune indication du succès ou de l’échec de la fécondation et même de l’ovulation. En production bovine, l’écoulement de sang est difficile à observer parce que les femelles sont souvent gardées en stabulation libre ou au pâturage.
Durant le diœstrus, la femelle ne démontre pas d’intérêt sexuel.
• Œstrus (jour 0)
Période du rut, de réceptivité (chaleur) d’une durée de 6 à 24 heures (18 heures en moyenne).
Correspond au démarrage d’un nouveau cycle. Hormone dominante : œstradiol.
Accouplement des génisses et planification du premier vêlage
Avec une alimentation et une gestion adéquates, les génisses doivent être aptes à se reproduire vers l’âge de 13 à 15 mois pour obtenir un premier vêlage entre 22 et
Apparition de nervosité, de piétinement, d’agitation, de beuglement, écoulement de mucus plus ou moins blanchâtre, tentative de monte sur d’autres vaches. Signes visibles pendant 5 à 15 heures (10 heures en moyenne).
La femelle se laisse monter, écoulement de mucus clair, plus abondant et filant, vulve rosée et enflée.
24 mois, avec une moyenne à 23 mois. Il faut permettre à la génisse de poursuivre sa croissance et d’avoir une gestation et un vêlage normaux. Il a été démontré que la génisse soumise à un programme d’alimentation équilibré, répondant à ses besoins de croissance, est capable de concevoir entre 13 et 15 mois et de mettre bas
à 23 mois en moyenne tout en continuant à se développer normalement. Traditionnellement, les producteurs craignent d’accoupler leurs génisses trop tôt, ce qui occasionne des pertes de productivité et des répercussions importantes dans l’intégration de celles-ci à la production dans un troupeau vache-veau.
La période d’accouplement des génisses doit obligatoirement débuter trois à quatre semaines avant celle des vaches du troupeau afin de permettre une intégration harmonieuse des génisses à la production. Les avantages exhaustifs d’une telle pratique sont les suivants (Laverdière, 2002) :
meilleure sélection pour la fertilité et la précocité;
vêlage des primipares dans des conditions plus salubres;
plus de temps à consacrer aux primipares et à leur veau;
repos additionnel de 2 à 4 semaines avant la deuxième conception par rapport aux vaches;
augmentation du taux de fertilité et du taux de gestation des primipares1; moins de primipares non gestantes au sevrage (évite la réforme à 3 ans);
évite l’étalement des vêlages dès la seconde année; meilleure intégration de la relève comme vache à vêlage hâtif (plus rentable);
facilitation du regroupement des vêlages; augmentation de la longévité et de la productivité à vie des vaches;
veaux au sevrage : plus âgés, plus lourds, plus uniformes.
1. Taux de fertilité (ou taux de conception) (%) = 100 x nombre de femelles gestantes/nombre de femelles mises à la reproduction. Taux de gestation (%) = 100 x nombre de femelles gestantes/nombre total de femelles.
Le taux de conception d’un troupeau est très étroitement lié à des facteurs héréditaires, alimentaires et sanitaires, à l’influence du milieu et à la gestion du cheptel. Pour atteindre un taux de conception de 70 % à la première saillie ou insémination et un taux de gestation de 95 % au cours d’une courte saison d’accouplement, on se doit d’apporter une attention particulière aux facteurs suivants : la fertilité du taureau; la fertilité des vaches et des génisses; la gestion de la reproduction; l’alimentation;
l’hygiène de l’environnement; la santé du troupeau.
Fertilité du taureau
Compte tenu des qualités que doit posséder un bon taureau reproducteur, on considère généralement que 1 ou 2 taureaux sur 5 ne peuvent satisfaire aux exigences des programmes modernes de reproduction, à cause d’une production insuffisante de sperme, d’une production de sperme de qualité inférieure, de défauts physiques interférant avec la monte ou d’une libido déficiente.
On peut s’assurer du potentiel de fertilité d’un taureau en procédant à un examen, 1 à 2 mois avant le début de l’accouplement, pour évaluer :
l’état de santé général; le système locomoteur; la vue et les yeux;
l’appareil génital externe (fourreau, pénis, scrotum et son contenu);
l’appareil génital interne (glandes accessoires, canaux et anneaux inguinaux);
période de vêlage contribue à réduire l’intervalle moyen entre les vêlages. La période de vêlage désirée ne sera pas nécessairement la même pour toutes les entreprises.
Les génisses vêlant au tout début de la période de vêlage ont tendance à vêler tôt chaque année. Bien développer les génisses de remplacement favorise une puberté précoce, augmente la fertilité et, par conséquent, permet d’obtenir les premiers vêlages entre 22 et 24 mois d’âge.
Le contrôle des maladies contagieuses particulières à chaque région est essentiel (exemple : leptospirose). Un programme de vaccination adapté aux besoins de chaque troupeau et résultant d’une concertation entre le producteur et son vétérinaire praticien doit être élaboré.
Il faut mesurer la circonférence scrotale de tous les taureaux âgés entre 12 et 24 mois et ne retenir que les taureaux affichant une mesure supérieure à la moyenne.
Il faut porter une attention toute particulière, pour les génisses et même les primipares, au choix de la race du taureau utilisé ainsi qu’aux ÉPD pour la facilité de vêlage et le poids à la naissance pour minimiser les difficultés potentielles au vêlage (voir chapitre Génétique).
Ball, L., R.S. Ott, R.G. Mortiner et J.C. Simons. 1983. Manual for breeding soundness examination of bulls. Journal of the Society for Theriogenology, (février).
Bousquet, D. 1995. Le transfert embryonnaire : nouvelle génération. 19e Symposium sur les bovins laitiers. CPAQ.
Cates, W.F., H.H. Nocholson, G.H. Crow et E.D. Janzen. 1981. Testicular development in record of performance bulls. Proceedings of Society for Theriology, p. 16-30
De Fontaubert, Y. 1986. La maîtrise des cycles sexuels chez les bovins : le point en 1986. Bulletin technique de l’insémination artificielle, no 42 (décembre).
Deutscher, G.H. 1988. Pelvic measurements: key to reducing incidence of bovine dystocia. Norden news. Summer.
Déziel, C. 1999. (1e édition : G. Huneault et al., 1994). Reproduction. Guide Vache-veau. Conseil des productions animales du Québec, 216 p.
Déziel, C. 1996. Votre guide de régie du troupeau. CIAQ.
Etherington, W.C., et al.1984. Reproductive performance in dairy cows following postpartum treatment with GnRH and/or prostaglandin: a field trial. 10th International Congress on Animal reproduction and A.l. p. 317.
Flechon, J.E., et al. 1980. Blastographie du développement de l’embryon bovin surovulé. Élevage et insémination, 178: 1-28.
Hafez, E.S.E. 1980. Reproduction in farm animals. 4th Edition, Lea & Febiger, Philadelphia.
Hodges, R.J. et al. 1988. A randomized clinical trial of the effect of the time of administration of cloprostenol on detection of estrus in dairy cattle. Revue vét. canadienne 29: 343.
Laverdière, G. 1994. Effets d’analogues de la prostaglandines F2A et de deux programmes de synchronisation de l’œstrus sur la reproduction des vaches de boucherie en période postpartum. Mémoire de maîtrise. Faculté des études supérieures. Département des sciences animales, FSAA. Université Laval. 120 p.
Laverdière, G. 1997. Nouveau programme pour synchroniser les ovulations et inséminer une seule fois à temps fixe. Bovins du Québec, vol. 11, no 4, p. 8-11.
Laverdière, G. 1998. Demandez au taureau de rendre compte de son travail. Le licou marqueur : un outil de gestion à découvrir! Bovins du Québec, vol. 12, no 1, p. 18-19.
Laverdière, G. 2002. Stratégies d’intégration des génisses à la production, une clé de productivité et de rentabilité. Congrès du bœuf, Victoriaville, 11 au 13 octobre. CRAAQ.
Laverdière, G., et al. 1997. Simplifier la gestion des accouplements avec une seule insémination artificielle à temps fixe : un succès bœuf. Congrès du Bœuf, CPAQ, p. 69-80.
Laverdière, G. et G. L. Roy. 1995. Pourquoi synchroniser les chaleurs en production bovine? Bovins du Québec, vol. 9, no 4, p. 7-9.
Laverdière, G., G. L. Roy, N. Pouliot et J. Labbé. 1996. Comment faire pour synchroniser les chaleurs de vos vaches? Bovins du Québec, vol. 10, no 1, p. 10-13.
Laverdière, G., G. L. Roy, J. Proulx, et J. J. Dufour. 1995. Une méthode simple et efficace pour synchroniser les chaleurs chez les vaches de boucherie. Le médecin vétérinaire du Québec, 25: 115-119.
Laverdière, G., G. L. Roy, J. Proulx, D. Lavoie et J. J. Dufour. 1994. Comparaison de l’effet de deux analogues de la prostaglandines F2a sur la synchronisation de l’œstrus chez la vache de boucherie. Can. J. Animal Science 74: 29-36.
Laverdière, G., G. L. Roy, J. Proulx, D. Lavoie et J. J. Dufour. 1995. Estrus synchronization efficiency of PGF2a injection in Shorthorn-Hereford and crossbred Charolais cattle not having exhibited estrus at 4 or 7 days prior to treatment. Theriogenology, 43:899-911.
Paradis, G. 1998. Les facteurs qui influencent les performances en reproduction. Bovins du Québec. Vol. 12, no 2, p. 20-21.
Penner, P. 1991. Manuel technique d’insémination artificielle bovine. CAAB.
Rice, L.E. 1988. Development of replacement heifers. Cont. Educ. 10 (4), (avril).
Rice, L.E. 1980. Reproduction health management in beef cows. Dans : Morrow, D.A., Current therapy in theriogenology, W.B. Saunders, Toronto.
Shea, B.F. 1981. Evaluating the bovine embryo. Theriogenology 15:31-42.
Turner, T.B. et al. 1987. Synchronisation of estrus in beef cows and heifers with Fenprostalene, Cloprostenol sodium and prostaglandin F2 alpha. Theriogenology 28: 15.
Twagiramungu, H., L. A. Guilbault, et J. J. Dufour. 1995. Synchronization of ovarian follicular waves with a Gonadotropin-Releasing Hormone agonist to increase the precision of estrus in cattle: a review. J. Anim. Sci. 73:3141-3151.
Twagiramungu, H., G. L. Roy, G. Laverdière et J. J. Dufour. 1995. Fixed time insemination in cattle after synchronisation of estrus and ovulation with gonadotropin-releasing hormone (GnRH) and prostaglandin Theriogenology 43: 431 (Abstract).
Twagiramungu, H., J. J. Dufour, G. L. Roy, G. Laverdière et A. L. Guilbault. 1996. La GnRH pour une meilleure maîtrise de la synchro-insémination bovine. Journées de recherche et Colloque en zootechnie. CPAQ. p. 59-78.
Vaillancourt, D., L.A. Guilbault, P. Guay, P. Lamothe et Tremblay. 1987. Reproduction et fertilité : endocrinologie en période post-partum. Symposium sur les bovins laitiers. CPAQ.
Wenkoff, M.S. 1987. The evaluation of bulls for breeding soundness. ACV.
Wenkoff, M.S. 1987. The management of drug-induced manipulation of the estrus cycle in normal cows and heifers. Revue vét. canadienne 28: 366.
Whittier, J.C. et al. 1986. Progestin and prostaglandin for estrus synchronization in beef heifers. J. Anim. Sci. 63: 700-704.
