39 -1 2026

Tumorlysesyndrom – en klinisk utforing for anestesileger
«Can intubate, cannot ventilate» – revidert versjon av flytskjema
The airway is not the problem – teamwork in airway emergencies

39 -1 2026

Tumorlysesyndrom – en klinisk utforing for anestesileger
«Can intubate, cannot ventilate» – revidert versjon av flytskjema
The airway is not the problem – teamwork in airway emergencies

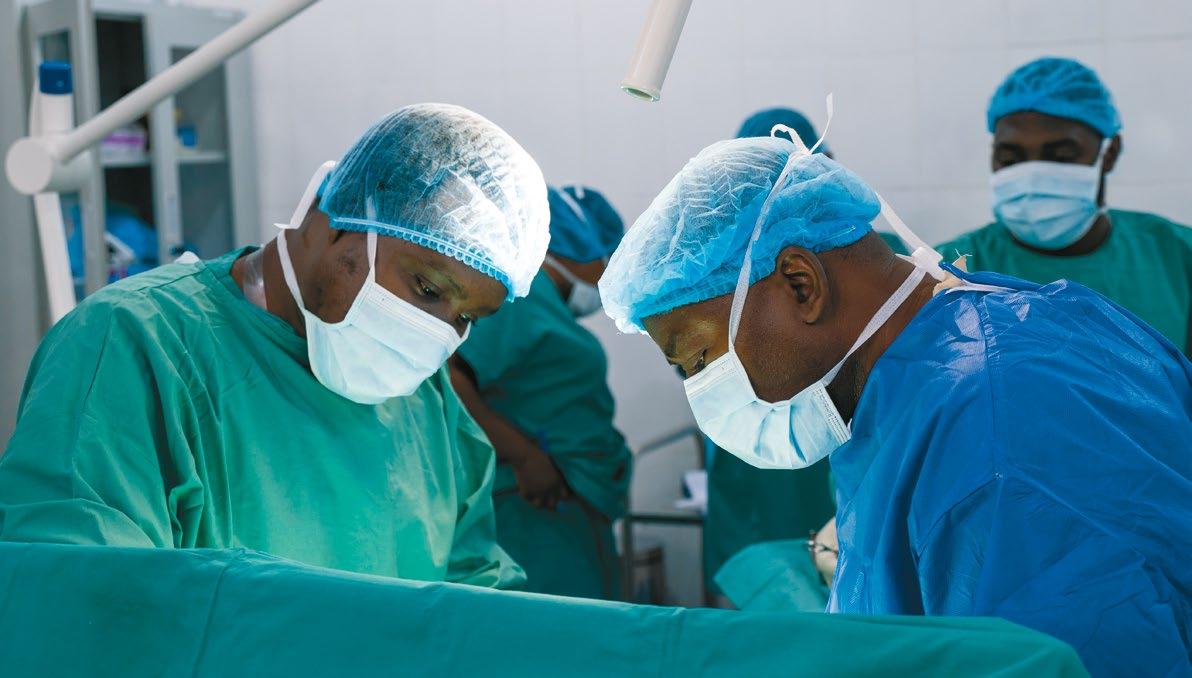
Vi har behov for anestesileger og anestesisykepleiere. Kan det være deg?
For mer informasjon om hva vi trenger, scan QR-koden eller gå til: legerutengrenser.no/jobb-for-oss
Har du spørsmål? Kontakt oss på epost: rekruttering@legerutengrenser.no

Tidsskrift for Norsk anestesiologisk forening
NAForum er et uavhengig tidsskrift. Meninger og holdninger avspeiler ikke nødvendigvis den offisielle holdning til styret i NAF eller Dnlf. Signerte artikler står for forfatterens egen regning. Kopiering av artikler kan tillates etter kontakt med ansvarlig redaktør og oppgivelse av kilde.
STYRETS SAMMENSETNING
Leder Svein Arne Monsen Nordlandssykehuset svein.arne.monsen@legeforeningen.net
Nestleder Randi Marie Mohus St Olavs hospital randi.marie.mohus@legeforeningen.net
Kontakt mot Anestesiutvalget
Kasserer Erling Haug Holen Stavanger universitetssjukehus erling.haug.holen@legeforeningen.net
Kontakt mot Smerteutvalget
Sekretær Ingrid Fæhn Brekke Oslo universitetssykehus Ullevål ingrid.fahn.brekke@legeforeningen.net Kontakt mot Akuttutvalget
Medlemssekretær Vegard Tørå Dokka Sørlandet sykehus Arendal vegard.tora.dokka@legeforeningen.net
Høstmøtesekretær Oda Uhlin Husebekk UNN Tromsø oda.uhlin.husebekk@legeforeningen.net
Styremedlem Kirsten Brun Kjelstrup UNN Tromsø kirsten.brun.kjelstrup@legeforeningen.net Kontakt mot Intensivutvalget
Styremedlem Markus Heiskanen Sørlandet sykehus majheiskanen@gmail.com
Kontakt mot FUNAF
Design/layout
Apriil Media
www.apriil.no
Annonser
Apriil Media
www.apriil.no media@apriil.no
Forsidebilde Sherpa. Foto: Øyvind Arvola, kommunikasjonsrådgiver, Harstad kommune
NAForum på internett www.nafweb.no

Rolf Arne Iversen REDAKTØR UNN Harstad rolf.arne.iversen@icloud.com

Camilla Christin Brathen Sykehuset Innlandet Elverum camilla.brathen@gmail.com

Ahmed Chaudhary Førde sentralsjukehus ahmed-9504@hotmail.com
REDAKSJONEN

Jarl Magnus Moen Sykehuset Telemark HF, Skien jarlmagnus@hotmail.com

Kristin Fagereng Stavanger universitetssjukehus kristinfagereng@hotmail.com

Anne Berit Guttormsen Haukeland universitetssykehus og Uib abgu@ihelse.net

Erling Haug Holen St.Olavs Hospital erling.haug.holen@ legeforeningen.net

Stian Hallen Oslo universitetssykehus, Ullevål stian.hallen@gmail.com

Svein Arne Monsen Leder, Norsk anestesiologisk forening leder@nafweb.no
Lederen har ordet
Jannicke Mellin-Olsen hadde et stort hjerte og mange hjertebarn. Ett av dem var hvordan vi tar vare på hverandre etter hendelser som oppleves som spesielt belastende. Slike hendelser omtales ofte som uønskede hendelser – gjerne med en underliggende oppfatning av at det ikke burde ha skjedd. Jannicke var sentral i utarbeidelsen av Helsedirektoratets veileder «Guide for ivaretakelse av pasienter, brukere, pårørende og medarbeidere ved uønskede hendelser», utgitt høsten 2024. Jeg har overtatt Jannickes plass i en ressursgruppe som på vegne av Helsedirektoratet skal arbeide for at veilederen tas i bruk. Jeg deler hennes engasjement: denne guiden bør ligge fremme på alle anestesiavdelinger og faktisk brukes. Vi jobber i en spesialitet med sterke inntrykk og stor fallhøyde.
Jeg har også mine dyrekjøpte erfaringer. Jeg har ligget våken om natten og tenkt at om jeg hadde handlet annerledes, ville det kanskje ikke gått så galt. Vi er ofte urettferdige mot oss selv. Den våkenatten er likevel en normal reaksjon på en unormal hendelse. Jeg vet at disse opplevelsene har gjort meg til en bedre og tryggere helsearbeider – og jeg tror det samme gjelder for de fleste av oss. En forutsetning er at vi jobber i et miljø med kultur for å ivareta slike situasjoner. Jeg har vært heldig som har jobbet på slike arbeidsplasser. Derfor er Helsedirektoratets guide så viktig.
Guiden er konkret og praktisk – nesten en kokebok for hvordan vi skal ta vare på hverandre etter slike hendelser. Den skisserer i kronologisk rekkefølge ti viktige punkter i oppfølgingen. Det viktigste er at vi som har stått i stormen får mulighet til å sette oss ned sammen i etterkant. Dette er en opplevelse vi har delt. At vi raskt får oversikt bidrar til å dempe den forventede uro. Ikke minst skaper det fellesskap. Dette visste vi var viktig fra før, men det kan være vanskelig i praksis. Vi må bygge kulturer som prioriterer dette, selv om det betyr at noe annet må utsettes eller at ekstra personell må kalles inn. Vi må huske alle involverte – en LIS1 eller en portør som hadde en liten rolle kan allikevel sitte igjen med de sterkeste inntrykkene.
Guiden er på forbilledlig norsk. Fremmedord som defuse og debrief er byttet ut med samtale og gjennomgang. Guiden har bokstavelig talt satt en rød strek over den psykologiske debriefen – hvordan kunne den leve videre så lenge etter at den er tatt ut av alle anbefalinger? Den kan til og med ha negativ effekt. Dette er normale reaksjoner på unormale hendelser.
Vi skal ikke mane fram sterke følelsesmessige reaksjoner. Jeg har sett hvordan varme hjerter har ført til at involvert helsepersonell ble henvist til psykolog allerede i de første døgnene etter en hendelse. Det er ikke riktig. Tvert imot: vi bør dyrke Antonovskys salutogenese, både for enkeltmennesket og i miljøet. Det fremmes gjennom god og akkurat passe omsorgsfull ledelse, god kollegastøtte og tydelig informasjon. Alt dette beskrives godt i guiden.
Vi må også ha en god kultur for å melde til tilsynsmyndighetene – og skape trygge rammer rundt det. Derfor er jeg glad i erfaringslæringen. Den gjennomføres ofte som hendelsesgjennomgang, og disse seansene er avgjørende for å identifisere tiltak som kan hindre at vi gjør unngåelige feil. For vi gjør feil. En annen fin ting er at hendelsesgjennomgangen alltid skal fokusere på hva vi kan lære på systemnivå. Det er ofte med på å løfte ansvaret fra den enkelte helsearbeiders skuldre.
Guidens første kapittel beskriver hvordan vi skal ivareta pasienter og pårørende etter uønskede hendelser. Følger vi dette, bidrar det til tillit og forståelse – og det forebygger medieoppslag som springer ut av det motsatte. Vi skal alltid møte pasienter og pårørende med medfølelse og beklagelse. Når det er på sin plass, skal vi be om unnskyldning – og vi skal mene det. Det er tankevekkende at vi trenger et eget kapittel om hvordan vi skal gi en oppriktig unnskyldning.
Lev vel! Svein Arne

Rolf Arne Iversen Overlege UNN Harstad rolf.arne.iversen@unn.no
Forsidebildet «Sherpaen» er grafitti laget av «Rampestrek» på Harstad Rådhus. Bakgrunnen er en hendelse fra 2017 der en norsk fjellklatrer ble rammet av høydesyke. En lokal sherpa gjenkjente symptomene og fikk fraktet den norske klatreren til lavlandet. Mens han ventet på å bli frisk nok til å dra hjem, oppdaget han hvor dårlig det stod til med skolene i Nepal og ønsket å gjøre noe med saken. Det ble startet et skoleprosjekt bl.a med kunstutstilling til inntekt for saken. «Alle byer trenger sin egen sherpa. En bauta i livet som tar vare på deg og viser veg» uttalte han til lokalavisen. Verket skal minne oss på at andre har det verre enn oss og at man skal bidra til fellesskapet. At kommunens rådhus benyttes til grafitti er også en anerkjennelse av kunstformen street-art.
Det er fellesskapet som er fundamentet i faget, foreningen og bladet vårt. Artikkelen om Squeeze-studien viser hvor viktig det faglige fellesskapet er. I foreningsarbeidet følger styret opp årsmøtets vedtatte strategidokument og jobber bl.a videre for å få flere nasjonale faglige veiledere. Bidrag fra miljøene som kjenner faget best er helt avgjørende for sluttproduktet. Barneanestesi er et fagområde som engasjerer mange. Neste utgave av NAForum som kommer ut før sommeren blir temanummer barneanestesi. Det barneanestesiologiske miljøet er allerede godt i gang med arbeidet. Redaksjonskomiteen er kontaktpunkt for de som har ønsker og innspill. Derfor er navn, bilde og kontaktinformasjon plassert ved siden av innholdsfortegnelsen slik at vi er lett tilgjengelig for dere.

• Fullt betalende medlemmer (spesialister) kr 9 990
• Medlemmer uten spesialistgodkjenning: kr 8 830
• Nyutdannede leger i tre år etter avlagt embetseksamen: kr 7 500
• Stipendiater i full stilling: kr 7 500
• Medlemmer bosatt i utlandet: kr 503
• Studentmedlemmer: kr 760
www.legeforeningen.no/medlem/medlemskap/kontingent/
I dette nummeret får du en forsmak på innholdet i Høstmøtet 2026 som arrangeres av Ahus. Som oppfølging etter Høstmøtet i Trondheim har kollegene der revidert figuren «can intubate, can’t ventilate». I tillegg er Ahus representert med en interessant artikkel om trafikklysmodellen for luftvei. Foreningens stipendordning til forskning er viktig og mottakerne av de siste stipendene har beskrevet sine prosjekter. Reisebrev fra Tanzania underbygger budskapet i forsidebildet.
Vi opplever en stor aktivitet og engasjement i foreningen som vi ønsker å gjenspeile i NAForum. Det er medlemmene i NAF som er motoren i arbeidet. Et årshjul går fort rundt og etter temanummer barneanestesi kommer høstmøtenummeret 3.26. Deretter er veien forholdsvis åpen og vi trenger gode bidrag og forslag fra dere på enkeltsaker og tema. Annonsesalg er en viktig faktor i finansieringen av NAForum. Interessekonflikter skal alltid være avklart i våre publikasjoner. Saker som kan skape interesse for våre annonsører er ønskelig.
Tilbake til sherpaen på forsidebildet så har street-art vært et gjennomgående tema de siste årene. Vi ønsker å utfordre alle til å bidra i fellesskapet med gode bilder av anestesilegelivet som vi kan benytte til forsider og i bladet. Kontaktinfo til oss i redaksjonen finner du fremst i bladet. Vi gleder oss til å høre fra dere. God lesing!
Nr. Utgivelse Deadline Hovedtittel 1-26 Mars 12. februar Vinter 2-26 Juni 22. mai Tema: Barn 3-26 September 18. september Høstmøte 4-26 Desember 23. november Jul





Kirsten Kjelstrup Styremedlem kirsten.brun.kjelstrup@legeforeningen.net


Faglige veiledere – et viktig verktøy
Mange av våre medlemmer, både erfarne og mindre erfarne kolleger, etterlyser at NAF tar ansvar for å utgi faglige veiledere. Alle som har ikke har prøvd, tror det er en enkel jobb å lage sånne veiledere. Anestesiologiens natur gjør faget godt egnet for standardisering. Jo større grad av hast, jo mindre rom er det for individuelle vurderinger. Tiden mellom unnfangelse til en nasjonal veileder eventuelt ser dagens lys er imidlertid ofte veldig lang. For eksempel metodebok i fødselsanestesi som ble publisert på metodebok.no i fjor. Det har kommet flere henvendelser fra dere med ønske om metodebok i anestesi og intensivmedisin, barneanestesi og smertebehandling. En metodebok må være skrevet av forfattere med høy faglig legitimitet og tillit i miljøet. Den må også reflektere en felles metode som er gjenkjennelig uansett hvor du jobber. Vi håper flere vil melde seg når vi skal rekruttere metodebokforfattere.
Kvalitet og læring av hendelser
Et annet tema som engasjerer medlemmene våre, er kvalitet. I dag har vi ikke et nasjonalt register for uønskede hendelser i anestesien. Når det oppstår problemer, for eksempel med luftveien, registreres dette ofte ulikt i pasientjournalene. Enkelte hendelser kan nå kjernejournalen. Men hvordan skal hendelser i én pasients journal kunne fanges opp dersom problemet ikke er pasienten, men systemet?
Foretakene har plikt til å ha systemer for å rapportere avvik og hendelser utenfor journalsystemet. Disse kan i beste fall bidra til læring i et lokalt fagmiljø, men i verste fall blir hendelsene aldri fulgt opp. Og hva med alle nesten-hendelsene som ikke når terskelen for å bli rapportert? Mange leger utvikler egne rutiner for å unngå at det samme skjer igjen, men kollegiet går glipp av denne verdifulle læringen.
«Vi trenger mer åpenhet om hendelser», sier medlemmene våre. Minst like viktig er det at vi lærer av nesten-hendelsene. Derfor følger vi spent med på oppdraget fra Helsedirektoratet til Folkehelseinstituttet om å legge grunnlaget for et nasjonalt register for alvorlige hendelser og nesten-hendelser. Her er det naturlig at anestesilegene bidrar aktivt i utviklingen.
Innspill til ny helsereform
Norsk anestesiologisk forening har nylig levert innspill til Legeforeningens arbeid med en ny helsereform. Vi støtter Legeforeningens klare budskap om at faget må settes i førersetet i helsetjenesten. Våre medlemmer opplever at dagens system lider under en ubalanse mellom administrasjon og fagfolk, og at ansatte ofte ikke blir involvert i viktige beslutninger.
Vi har særlig understreket behovet for at leger må inkluderes i utvikling og implementering av IKT-verktøy. Videre mener vi at forskning, fagutvikling og utdanning må prioriteres like høyt som pasientbehandling.
For å sikre likeverdige helsetjenester må det etableres klare minimumsstandarder for hvilke funksjoner som skal tilbys ved ulike sykehus, basert på faglige vurderinger. Vi ser også behovet for faglig forpliktende nettverk mellom sykehusnivåene. Dette kan blant annet styrkes gjennom digitale løsninger som gir økt beslutningsstøtte, både i akuttmedisinske situasjoner og i avansert elektiv virksomhet. Eksempler på dette kan være virtuelle visitter eller felles indremedisinsk bakvaktsfunksjon.
NAF mener at en ny helsereform må legge til rette for bærekraftige løsninger som ivaretar både pasientenes behov og helsepersonellets arbeidsvilkår – også i krisetider.

Ingrid Fæhn Brekke Styremedlem ingrid.fahn.brekke@legeforeningen.net
Etter fjorårets vellykkede heldagsmøte for styret i Norsk anestesiologisk forening (NAF) og tilhørende utvalg, ble alle utvalg igjen invitert til en felles samling – denne gangen på en iskald vinterdag i februar. Kuldegradene utenfor sto i kontrast til engasjementet inne på Legenes hus, hvor representanter fra foreningens utvalg møttes.
Til stede var representanter fra Smerteutvalget, Forskningsutvalget, Intensivutvalget, NAFWeb, Akuttutvalget, Anestesiutvalget, FU NAF, og UPK (Utvalg for pasientsikkerhet og kvalitet). En samling som utgjorde et utmerket tverrsnitt av foreningens faglige styrke.
Fra strategi til handling
Mens fjorårets møte hadde utarbeidelsen av NAFs strategidokument som hovedformål, var årets samling viet neste steg i prosessen: å konkretisere målene vi har satt oss, og drøfte hvordan vi faktisk skal arbeide for å nå dem.
Hvordan omsetter vi overordnede formuleringer til praktisk foreningsarbeid? Hvilke tiltak skal prioriteres først? Dette var spørsmål som dannet rammen for dagens program. Møtet bar preg av gode plenumsdiskusjoner, aktivt gruppearbeid og presentasjoner. Engasjementet var stort, og strategien oppleves som et felles prosjekt.

Et styrket fundament for videre arbeid
Dagen ga ikke bare konkrete innspill til det videre strategiarbeidet – den bidro også til å styrke samarbeidet på tvers av utvalgene. Å samle så mange sentrale aktører rundt samme bord gir også anledning til å diskutere andre problemstillinger som foreningen står overfor på tvers av utvalg.
Takk til alle som bidro til en inspirerende og engasjerende dag. Vi i NAF-styret har stor tro på at denne typen samlinger er
viktige for å styrke fellesskapet og knytte foreningen tettere sammen på tvers av utvalg. Når vi møtes ansikt til ansikt, deler erfaringer og blir bedre kjent med hverandres arbeid, legger vi et godt fundament for videre innsats – både i det enkelte utvalg og i samarbeidet mellom utvalgene.
Vi håper at denne formen for felles heldagssamling kan bli en tradisjon vi tar med oss videre – til beste for både faget og foreningen.

Signe Søvik
Anestesi og Intensivavdelingen, Akershus universitetssykehus signe.sovik@medisin.uio.no

Felix Haidl
Anestesi og Intensivavdelingen, Akershus universitetssykehus frans.felix.haidl@ahus.no
Onsdag 21. oktober
Utfordringer ved sortering i et stort akuttmottak: Hvordan kan teknologistøttet triage, diagnostikk og behandling bedre vår håndtering?
Fridtjof Heyerdahl, Prehospital divisjon Oslo universitetssykehus
Blodberedskap i lokalt, nasjonalt og europeisk perspektiv
Torunn Oveland Apelseth, Haukeland universitetssjukehus
Kontinuerlig hemodialyse hos pasienter med elektrolyttforstyrrelser – Clinical pearls & nye protokoller
Ole Kristian Fossum, Akershus universitetssykehus
PRT: Nonfarmakologisk reprogrammering av kronisk smerte
Silje Endresen Reme, Mind Body Lab, Oslo universitetssykehus & Akershus universitetssykehus
Ulike opioider – ulike personer
Siri Leknes, Leknes Affective Brain Lab, Universitetet i Oslo
Badstue & Bar downtown Oslo
Torsdag 22. oktober
Peripartum kardiomyopati og andre kritiske hjertetilstander hos fødende Kristina Hermann Haugaa, Universitetet i Oslo
Preeclampsia– a new look Gynekolog Jakob Lykke, Rigshospitalet København
Waking up from anesthesia: Can we speed up the process?
Ken Solt, Professor of Anaesthesia, Pharmacology and Innovation, Harvard Medical School, Boston USA
Kvalitet i utdanningen av nye anestesiologer i Norge
Hanna Chin, Sahlgrenska Universitetssjukhuset, Göteborg; Lill Anette Øyen og Ingvild Seem, Akershus universitetssykehus; Lovisa Hasselberg, OUS.
Kirurgisk nødluftvei på lammestruper Praktisk drop-in trening, med høy puls etter max ergometersykling
Festmiddag med prisutdeling for beste frie foredrag og beste cricothyroido-tomiker
Anestesiavdelingen på Akershus universitetssykehus ønsker velkommen til årets høstmøte, som vil fokusere på cutting edge utvikling av faget vårt og på utdanningen av fremtidige faglige utøvere. Her er noen smakebiter fra programmet.

Fredag 23. oktober
Paneldebatt: Underkapasitet og overkapasitet i LISutdanningen: Hvordan sikre anestesiologisk kompetanse og beredskap i hele landet?
Chair: Felix Haidl
Year in review

Jørund Asvall
Avdeling for anestesi, intensiv og operasjon. Radiumhospitalet. Akuttklinikken, OUS joeasv@ous-hf.no

Marianne Brodtkorb
Avdeling for Kreftbehandling, Kreftklinikken, OUS meide@ous-hf.no

Ulf E. Kongsgaard
Avdeling for anestesi, intensiv og operasjon. Radiumhospitalet. Akuttklinikken, OUS u.e.kongsgaard@medisin.uio.no
Tumorlysesyndrom (TLS) er en alvorlig og potensielt livstruende komplikasjon (1-3) som oppstår når store mengder tumorceller brytes ned over kort tid. Dette fører til frigjøring av intracellulære komponenter (elektrolytter, nukleinsyrer og enzymer) og resulterer i karakteristiske elektrolytt- og metabolske forstyrrelser. Tilstanden betegnes av hyperkalemi, hyperfosfatemi, hyperurikemi, og er ofte ledsaget av forhøyet laktatdehydrogenase (LD), samt forhøyet kreatinin og urinstoff som tegn på nyresvikt. Problemet ses oftest ved akutte leukemier, lymfoblastlymfom og Burkitts lymfom, relativt ofte ved andre aggressive B- og T-cellelymfomer mindre hyppig ved testikkelkreft, småcellet lungekreft og andre krefttyper og fortrinnsvis der det foreligger store tumormasser. Det kan også forekomme ved indolente lymfomer med massiv leukemisering ved oppstart av tumorrettet behandling. Ved de mest aggressive lymfomene og leukemiene kan TLS oppstå spontant før behandling påbegynnes. Ved andre aggressive lymfomer, testikkelkreft og andre krefttyper, ses tilstanden hovedsakelig i forbindelse med oppstart av behandling (4). Man bør være oppmerksom på at det også kan utløses ved start av steroider alene. Nyere behandlingsformer som immunterapi og målrettet
behandling kan utløse TLS, også hos pasienter som tidligere ble ansett å ha lav risiko. Andre risikofaktorer for utvikling av TLS er forhøyet baseline urinsyre eller fosfat, nedsatt nyrefunksjon, dehydrering og hypotensjon.
Forstyrrelsene kan utvikle seg raskt, ofte innen timer til få dager etter oppstart av cytotoksisk behandling, men TLS kan også oppstå spontant ved aggressive maligniteter med høy tumorbyrde. For anestesileger er TLS særlig relevant i sammenheng med akuttmedisin, intensivbehandling og perioperativ håndtering av pasienter med kreftsykdom. Tidlig gjenkjennelse og rask behandling er avgjørende for prognosen.
Ved rask tumorcellelyse frigjøres store mengder kalium, fosfat og nukleinsyrer til sirkulasjonen. Nukleinsyrer metaboliseres til urinsyre, som har lav løselighet og kan utfelles i nyretubuli. Dette kan føre til akutt urinsyrenefropati og redusert nyrefunksjon. Nyresvikt ved TLS kan både være en konsekvens av, og en forsterkende faktor for, elektrolyttforstyrrelsene. TLS deles i laboratorie-TLS og klinisk TLS. LaboratorieTLS defineres ved biokjemiske avvik som hyperkalemi, hyperfosfatemi, hypokalsemi og hyperurikemi. Klinisk TLS foreligger når
disse forandringene gir kliniske konsekvenser som akutt nyresvikt, arytmier, kramper eller plutselig død. Sentrale biokjemiske parametre er kalium, fosfat og urat. Tidlig forhøyet LD skyldes direkte frigjøring fra lyserte celler og indikerer økt sannsynlighet for utvikling av klinisk TLS og bør utløse tettere monitorering. Urat over øvre referanseverdi er vanligvis indikasjon for oppstart rasburikasebehandling. Rasburikase brukes for øvrig liberalt ved høy risiko for TLS.
Viktige kliniske manifestasjoner av betydning for anestesiologer
1) Kardiovaskulære komplikasjoner
Hyperkalemi er den mest akutt livstruende forstyrrelsen ved TLS. Den kan gi raske EKG-forandringer og alvorlige arytmier, inkludert ventrikkelflimmer og asystoli. Hypokalsemi og acidose kan forsterke den arytmogene effekten av hyperkalemi. Anestesiologier vil ofte være involvert i EKG-vurdering og behandling av livstruende arytmier samt sirkulatorisk kollaps.
2) Nevrologiske symptomer
Hypokalsemi kan gi parestesier, tetani, kramper og redusert bevissthetsnivå. Uremi og acidose kan bidra til encefalopati. Kramper ved TLS kan være refraktære
Tidsskrift for Norsk anestesiologisk forening, DNLF
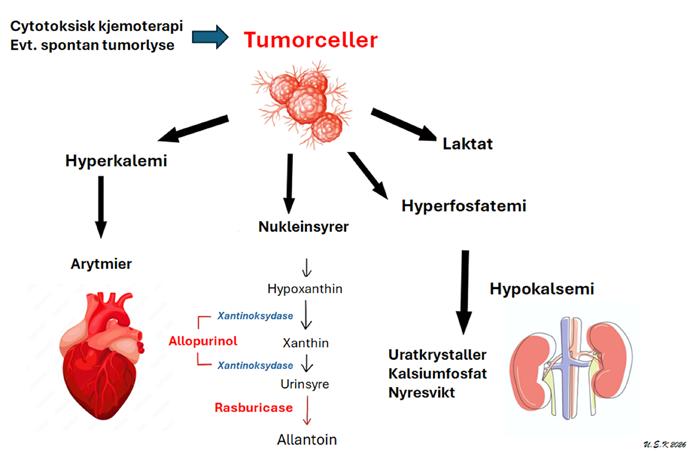
Figur 1. En skjematisk oversikt over patofysiologi, kliniske manifestasjoner og behandlingsprinsipper ved tumorlysesyndrom.
dersom elektrolyttforstyrrelsene ikke korrigeres raskt. Anestesiologer må vurdere behov for overvåking og luftveissikring hos pasienter med kramper eller redusert bevissthet.
Nyresvikt er et sentralt element i klinisk TLS og skyldes både utfelling av uratkrystaller, kalsiumfosfat-avleiring og hemodynamiske faktorer. Redusert nyrefunksjon fører til akkumulering av kalium, fosfat og urat og kan raskt gjøre tilstanden dialysekrevende. Hydrering /væskebehandling og elektrolyttregulering er helt sentralt. Anestesiologers rolle vil dessuten kunne innebære etablering av dialysekateter og hemodynamisk støtte i forbindelse med kontinuerlig nyreerstattende behandling.
Forebygging og behandling
Forebygging av TLS er avgjørende og
baserer seg på identifisering av risikopasienter før oppstart av kreftbehandling (5). Aggressiv hydrering er hjørnesteinen i profylaksen og har som mål å opprettholde høy diurese og redusere konsentrasjonen av urinsyre og fosfat i nyrene.
Farmakologisk profylakse mot tumorlysesyndrom består av allopurinol 300-600 mg/d og forsert diurese ved bruk av loop-diuretika og IV hydrering. Man tilstreber en diurese på 2-3 l per døgn (80-120 ml/time) (4, 5), ved aktiv tumorlysesyndrom økes diurese til 4–6 l per døgn (200-250 ml/time) de første 2–3 døgn. Utviklingen av TLS må følges nøye gjennom blodprøver 1-2 ganger daglig. Ved biokjemisk tegn til tumorlyse, eller høy risiko for TLS ved oppstart kreftbehandling, gis rasburikase for å senke urat. Rasburikase (Fasturtec®) hindrer og reduserer hyperurikemi (4, 5). Man vil ofte komme til målet
med en tredjedel av den anbefalte dose, ev. gjentatt. Mange vil anbefale det brukt ganske liberalt ved de mest aggressive lymfomer (stor tumorbyde), og man bør da gi dette som profylakse som alternativ til allopurinol (5).
Mens allopurinol hemmer nydannelse av urat fra nukleinsyrer, er rasburikase et enzym som gir rask og svært effektiv nedbrytning av eksisterende urat. En dose på 4,5 mg IV er som regel tilstrekkelig og kan gjentas når S-urat begynner å stige igjen. Kontrollblodprøver må holdes på is frem til analyse (og det må spesifiseres i rekvisisjon at rasburikase er gitt) for at urat-verdien ikke skal bli falsk for lav etter at rasburikase er administrert. Alkalisering av urin kan også redusere dannelsen av uratkrystaller, men gir samtidig økt risiko for presipitasjon av kalsiumfosfatkrystaller i nyrene, og er sjelden nødvendig ved bruk av rasburikase.(4). Alkalisering kan vurderes ved metabolsk acidose når rasburikase ikke er tilgjengelig (1).
Det kan i sjeldne tilfeller bli nødvendig med hemodialyse, og man bør informere nefrolog om pasienter med etablert TLS. Alvorlige elektrolyttforstyrrelser (hyperkalemi og hyperfosfatemi), stigende kreatinin og fallende diurese kan være indikasjoner for akutt hemodialyse (se også avsnitt under).
Akutt behandling – anestesiologisk perspektiv
Ved etablert TLS er behandlingen rettet mot rask korreksjon av livstruende metabolske forstyrrelser og støtte av vitale funksjoner. Hyperkalemi vil i de fleste tilfeller korrigeres ved bruk av loop-diuretika og kan i tillegg behandles etter etablerte prinsipper med insulin og glukose,
beta-agonister og eventuelt natriumbikarbonat. Hydrering er viktig (se over). Man bør være tilbakeholden med tilførsel av kalsium for membranstabilisering eller på andre indikasjoner grunnet risikoen for kalsium-fosfatutfelling. Dialyse kan være nødvendig ved refraktær hyperkalemi, hyperforsfatemi, alvorlig acidose eller nyresvikt. Hypokalsemi behandles kun ved kliniske symptomer, da rutinemessig kalsiumtilførsel kan øke risikoen for kalsiumfosfatutfelling. Dette krever nøye klinisk vurdering. Hyperfosfatemi kan om nødvendig korrigeres med orale fosfatbindere, for eksempel kan gjerne sevelamerkarbonat (Renvela®) vurderes, ev. etter råd fra nefrolog (5). Om produktet av fosfat og total-kalsium nærmer seg 7, bør det diskuteres med nefrolog om hemodialyse er aktuelt (6).
Anestesileger må ofte håndtere disse pasientene i en akutt og ustabil fase med behov for invasiv monitorering, sentralvenøs tilgang og tett laboratorieoppfølging.
Perioperativ håndtering
Pasienter med aktivt eller nylig gjennomgått TLS kan trenge akutte kirurgiske inngrep. Preoperativ vurdering bør fokusere på elektrolyttstatus, nyrefunksjon, acidose og hemodynamisk stabilitet. Hyperkalemi må korrigeres før anestesi dersom mulig, og suksametonium er kontraindisert.
Valg av anestesimidler bør ta hensyn til nedsatt nyrefunksjon og risiko for akkumulering av metabolitter. Man bør generelt være forsiktig ved bruk av aminoglykosider etter 1. kur ved aggressive lymfomer der faren for tumorlyse er stor (4).
Tverrfaglig samarbeid og konklusjon
Tumorlysesyndrom er en akuttmedisinsk og intensivmedisinsk utfordring med høy
Tidsskrift for Norsk anestesiologisk forening, DNLF
mortalitet dersom det ikke behandles raskt (2, 3). For anestesileger er inngående kunnskap om patofysiologi, kliniske manifestasjoner og behandlingsprinsipper avgjørende. Tidlig gjenkjennelse, tett monitorering og rask korreksjon av elektrolyttforstyrrelser kan være livreddende. Med økende bruk av effektiv kreftbehandling vil TLS forbli en viktig problemstilling i anestesiologisk praksis, der tett tverrfaglig samarbeid er avgjørende for god pasientbehandling.
Referanser
1. Adeyinka A, Kaur A, Bashir K. Tumor Lysis Syndrome, in StatPearls. 2025, StatPearls Publishing.Copyright © 2025, StatPearls Publishing LLC.: Treasure Island (FL).
2. Larson RA, Pui C-H. Tumor lysis syndrome: Prevention and treatment. UpToDate 2025 July 24, 2025; Available from: https://www.uptodate. com/contents/tumor-lysis-syndrome-preventionand-treatment. (lastet ned 08.02.2026).
3. Molyneux K, Beck-Esmay J, Koyfman A, Long B. High risk and low incidence diseases: Tumor lysis syndrome. Am J Emerg Med, 2025; 98: 283–288.
4. Helsedirektoratet. Tumorlysesyndrom. 2025; Tilgjengelig fra: https://www.helsedirektoratet. no/retningslinjer/lymfekreft-handlingsprogram/ tumorlyse-syndrom. (lastet ned 04.02.2026)
5. eHåndbok, O. Tumorlysesyndrom - forebygging og behandling. 2024; Tilgjengelig fra: https:// ehandboken.ous-hf.no/document/46996. (lastet ned 04.02.2026).
6. Lupușoru, G, Ailincăi I, Frățilă G, et al. Tumor Lysis Syndrome: An Endless Challenge in Onco-Nephrology. Biomedicines 2022; 10: 1012.

Ib Jammer
Overlege, Kirurgisk serviceklinikk, Haukeland Universitetssjukehus, Bergen ib.jammer@helse-bergen.no
Det startet med en enkel observasjon på vår egen avdeling. Noen pasienter kom fra operasjonsstuen med vasopressorinfusjoner, andre ikke, selv når de tilsynelatende var like syke. Når jeg diskuterte dette med kollegaer fra andre sykehus, både i Norge og internasjonalt, fikk jeg samme tilbakemelding: «Hos oss gjør vi det slik…». Men «slik» var forskjellig fra sted til sted.
Spørsmålet jeg hadde var: Hvor mange pasienter får vasopressorer postoperativt? Er det en variasjon og hvis ja, skyldes variasjonen i bruk av postoperativ vasopressor at pasientene er forskjellige, eller er det vi som anestesileger som praktiserer forskjellig?
Dette ble starten på SQUEEZE-studien, en av de største observasjonsstudiene innen anestesiologi, som nylig ble publisert i British Journal of Anaesthesia (1).
En global dugnad
Studiedesignet var bevisst holdt enkelt. Vi ville ha et realistisk bilde av hverdagen, ikke en idealisert versjon. Derfor ba vi hvert sykehus registrere alle voksne pasienter som gjennomgikk ikke-hjertekirurgi i løpet
av én uke (kohort A), samt opptil 30 pasienter som mottok postoperativ vasopressor (kohort B). Ingen ekstra utstyr, ingen spesielle protokoller, bare dokumentasjon av det som faktisk skjedde.
Å koordinere og motivere deltakelse i en internasjonal studie er ingen liten oppgave, men responsen var overveldende. Kollegaer fra Canada til Australia, fra Brasil til Norge, meldte seg på. Nesten 1000 anestesileger ville være med på å kartlegge denne praksisen.
Hvorfor? Kanskje fordi vi alle kjente på den samme usikkerheten: Når skal vi egentlig starte vasopressorer postoperativt? Hvilke pasienter trenger dem? Og hvordan skal vi vurdere behovet?
Tallene som overrasket oss
Total deltok 228 sykehus fra 42 land med til sammen 25.675 pasienter. I Kohort A, de 19.768 pasientene som representerte en «vanlig» uke ved hvert sykehus, var det 3,9 % som mottok postoperative vasopressorinfusjoner. Det høres kanskje ikke så mye ut, men det var variasjonen som virkelig slo meg:
Andelen pasienter som fikk vasopressorer varierte fra 0 % til 18 % mellom sykehusene.
La det synke inn: Ved noen sykehus fikk ingen pasienter postoperativ vasopressorinfusjoner i løpet av hele registreringsuken. Ved andre sykehus fikk nesten hver femte pasient slik behandling.
Som forsker var min første tanke: «Dette må jo skyldes forskjell i pasientpopulasjonen!»
Men da vi justerte for alt vi har målt, f.eks. alder, komorbiditet, type kirurgi, ASA-klasse, akuttgrad osv., forsvant ikke variasjonen. Den var like stor etterpå. Median odds ratio var 2,30, som statistisk betyr at variasjonen mellom sykehus var enorm og uforklart.
Det var et litt ubehagelig aha-øyeblikk.
Det vi ikke gjorde, og kanskje burde gjort
Her kommer det som kanskje overrasket meg mest, og som jeg tror er det viktigste budskapet fra SQUEEZE.
På konferanser som Euroanaesthesia, ASA, eller vårt eget NAF-høstmøte, snakker vi mye om målrettet hemodynamisk
behandling. Vi ser presentasjoner om cardiac output-monitorer, stroke volume variation, og fysiologisk basert væske- og vasopressorbehandling. Industrien viser oss imponerende teknologi. Lærebøkene våre anbefaler objektiv monitorering.
Men hva viste SQUEEZE-dataene?
Av pasientene som fikk vasopressorinfusjoner postoperativt, var bare 6,2 % vurdert med cardiac output-monitorering før beslutningen ble tatt. Bare 6 %!
I kontrast ble nesten tre ganger så mange (18,4 %) vurdert med klinisk skjønn alene. Uten dokumenterte objektive målinger. Uten cardiac output-data. Bare blodtrykk, puls, urinproduksjon, og klinisk erfaring.
Ytterligere 64,6 % kom fra operasjonsstuen med vasopressorinfusjon allerede i gang, så beslutningen var tatt intraoperativt. Men også her må vi anta at de fleste beslutningene ble tatt uten avansert hemodynamisk monitorering.
Som kliniker og forsker må jeg stille spørsmålet: Hvorfor bruker vi ikke de verktøyene vi lærer om?
Gapet mellom det vi vet og det vi gjør
Noen ganger er svaret enkelt: Utstyret er ikke tilgjengelig. Sensorene er dyre. Arbeidstiden strekker ikke til. Det er en realitet ved mange sykehus, også i Norge.
Men jeg tror det er mer enn det. Jeg tror vi som fagmiljø ikke har klart å definere tydelig nok når og for hvem avansert monitorering faktisk gjør en forskjell. Vi har teknologien, men mangler de klare indikasjonene.
Tidsskrift for Norsk anestesiologisk forening, DNLF
Og så er det kliniske erfaringen som vi alle utvikler gjennom årene. Den pasienten som «ikke ser bra ut», selv om tallene muligens ikke er så ille. Den intuisjonen er verdifull, men den er også subjektiv og varierer fra kliniker til kliniker.
Resultatet? En enorm variasjon i praksis som ikke kan forklares av medisinske faktorer.
Hva med pasientene?
Her kommer den vanskelige delen. Pasienter som mottok vasopressor etter kirurgi hadde betydelig høyere dødelighet: 15,5 % døde på sykehuset. De hadde også høyere forekomst av organsvikt og lengre liggetid.
Vi kan ikke påstå at vasopressorene forårsaket dårligere utfall. Det er mest sannsynlig at disse pasientene var sykere fra starten av, og at vasopressorbruken er en markør for alvorlighetsgrad snarere enn en årsak til dårlig prognose.
Likevel minner det oss om at de beslutningene vi tar, når vi starter vasopressorer, hvilket preparat vi velger, hvordan vi titrerer dem, har konsekvenser for ekte mennesker.
Valg av vasopressor: nasjonale tradisjoner
Et annet interessant funn var hvilke vasopressorer som ble brukt. Noradrenalin dominerte klart: 79,3 % av pasientene fikk dette på operasjonsdagen. Men så var det Metaraminol, som 12,9 % fikk. Dette var nesten utelukkende i Storbritannia og Australia, hvor Metaraminol har en lang tradisjon.
I Norge bruker vi ikke Metaraminol. Våre kolleger i UK ville neppe kunne tenke seg en dag uten det.
Dette illustrerer noe grunnleggende: Mye av det vi gjør er basert på tradisjon og lokal praksis, ikke nødvendigvis på evidens. Vi arver praksisen fra våre lærere, som arvet den fra sine. Det er ikke nødvendigvis galt, men det er heller ikke gunstig.
Hvorfor observasjonsstudier er viktige
Jeg skal være ærlig: SQUEEZE er ikke den mest spennende studien å presentere på et kurs. Det er ingen ny behandling, ingen dramatisk intervensjon, ingen statistisk signifikant reduksjon i mortalitet. Det er «bare» en observasjonsstudie som viser hvordan vi praktiserer behandlingen etter kirurgi. Men akkurat derfor er den viktig: Før vi kan forbedre noe, må vi vite hvor vi står. SQUEEZE gir oss det grunnlaget, den viser at:
1. Vi praktiserer svært forskjellig
2. Forskjellene kan ikke forklares av pasientfaktorer
3. Vi bruker sjelden objektive målinger til å veilede behandlingen
4. Det er rom for forbedring
Hva nå?
SQUEEZE reiser flere spørsmål enn den besvarer, og det er faktisk meningen.
Som klinikere må vi spørre oss: Hvordan kan vi standardisere praksisen vår der det er hensiktsmessig? Bør vi utvikle lokale protokoller for når vasopressorer skal vurderes? Hvis objektiv monitorering er viktig (og jeg tror den er det) må vi gjøre den tilgjengelig og lære folk å bruke den riktig.
For forskere er behovet for randomiserte studier åpenbart. Vi trenger studier som kan svare på: Hva er optimalt blodtrykks-
mål postoperativt? Når bør vi starte vasopressorer? Hvilken rolle har cardiac output-monitorering? Her jobber vi videre med SQUEEZE-nettverket.
En personlig refleksjon
Etter flere år med SQUEEZE, fra idé til protokoll til datainnsamling til analyse og publikasjon, sitter jeg igjen med ydmykhet.
Ydmykhet over hvor kompleks klinisk praksis er. Over hvor mange faktorer som påvirker beslutningene vi tar. Over hvor vanskelig det er å standardisere noe så komplekst som postoperativ hemodynamisk behandling.
Tidsskrift for Norsk anestesiologisk forening, DNLF
Men jeg er også optimist. Ingen forsker gjør noe alene. SQUEEZE var mulig takket nesten 1000 anestesileger fra hele verden. Og hvis vi kan samarbeide om å kartlegge denne praksisen, kan vi også samarbeide om å forbedre den. Neste skritt er å finne ut hvor vi skal, og hvordan vi kommer oss dit.
Ib Jammer er overlege ved Avdeling for Anestesiologi, Haukeland universitetssjukehus, Bergen. Han er hovedforfatter av SQUEEZEstudien og har forsket på perioperativ medisin i over 20 år. Kontakt: ib.jammer@helsebergen.no


Referanser
1. Jammer I, Martin P, Wunsch H, Debouche S, Harlet P, Moonesinghe R, Forni L, Creagh-Brown B; Writing committee for the Squeeze investigators. Vasopressor use after noncardiac surgery: an international observational study. Br J Anaesth. 2025 Dec;135(6):1609-1617. doi: 10.1016/j. bja.2025.07.034.


4–6 November 2026 Oslo, Norway


Marianne Myhre
Cand.med., PhD, Avdeling for anestesi og intensivmedisin, Akuttklinikken, OUS-HF mknutson@ous-hf.no
Vi takker for forskningsstipend på 30 000 NOK til PhD-prosjektet «The bradykinin B2 receptor antagonist icatibant and its analgesic efficacy on propofol injection pain and acute nociceptive pain in experimental human pain models».
Stipendet vil bli brukt til innkjøp av 1 stk. elektronisk tourniquet-maskin AT4™ Electronic Tourniquet System (0–600 mmHg) med en tilhørende flergangs overarmsmansjett.
Prosjektet tar utgangspunktet i propofolindusert smerte (PIP) som kan gi moderate til alvorlig smerter ved injeksjon av medikamentet. Medikamentet er et av våre vanligste anestesi-midler og brukes daglig i vår klinikk for å sikre barn og voksne sedasjon ved smertefulle prosedyrer og til narkoser. Vi ønsker å studere bradykinins rolle i PIP / akutt smerte i to eksperimentelle modeller; propofol-indusert smerte og cold pressor test. I to av studiene vil vi ta i bruk en bradykinin B2 reseptor antagonist, icatibant, for å studere bradykinins rolle på venøse nociceptorer. Icatibant er i dag etablert i behandling av hereditært angioødem.
Over 100 forsøkspersoner skal testes flere ganger i en ny eksperimentell smertemodell der venetrykket i underarmen skal holdes konstant på ca 60 mmHg i 5 minutter før trykket reduseres gradvis. Det tiltenkte apparatet AT4™ leverer trygg og konstant venestase i hele området 0-60 mmHg over ønsket tid. Dette er en nødvendig del av smertemodellen og sikrer gradvis nedregulering av stasen slik at forsøksmedisiner ikke når systemsirkulasjonen for raskt eller før tilsiktet tid.
Søknaden om forskningsstipend fra NAF anses som et viktig bidrag til innkjøp av apparatet. De to første studiene i prosjektet innehar alle nødvendige godkjenninger (CTIS 2024-514307-34-01/2025-52135442-00) og første studie startet opp i september 2025. Begge studiene er planlagt gjennomført innen 2. kvartal 2026. Apparatet vil kunne lånes ut til andre forskningsgrupper når det ikke er i bruk i prosjektet.
Klinisk stipendiat: Cand.med. Bjarte Onsrud, Akuttklinikken, Oslo universitetssykehus og Institutt for klinisk medisin UiO.
Hovedveileder: Cand.med. PhD. Marianne Myhre, Akuttklinikken, Oslo universitetssykehus. Biveiledere: Prof. Audun Stubhaug, Oslo universitetssykehus og Institutt for klinisk medisin UiO og Prof. Erik Waage Nilsen, Nordlandssykehuset og Institutt for klinisk medisin UiO. Forsøket vil foregå på Akuttklinikken, OUS-HF Rikshospitalet.

Magnus Salomonsen
Anestesiavdelingen St.Olavs Hospital, Prehospital klinikk Helgelandssykehuset magnus.salomonsen@stolav.no

Kjetil Fosse
Anestesiavdelingen St.Olavs Hospital kjetil.fosse@stolav.no
Fosse et al. Can Intubate, Cannot Ventilate: A Proposed Algorithm to Handle Problems With Ventilation and Oxygenation After Intubation. Acta Anaesthesiologica Scandinavica 22. Desember 2025 https://doi.org/10.1111/aas.70175
Tusen takk for innspill og engasjement etter foredraget vårt på høstmøte. Takket være tilbakemeldinger har vi utarbeidet en revidert versjon av flytskjemaet (figur 1) for postintubasjonshypoksi. Den reviderte utgaven er publisert i Acta.
Vi ønsker å presisere at algoritmen er ment å anvendes når første forsøk på å korrigere utilstrekkelig EtCO₂, ventilasjon og/ eller oksygenering har mislyktes hos en intubert pasient.
I boksen «Intubasjon av trakea» har vi fjernet direkte laryngoskopi (DL) som metode for bekreftelse av tubeposisjon. Vi anbefaler nå bruk av videolaryngoskopi (VL) som den andre modaliteten for verifisering av korrekt trakeal tubeplassering (1). Som nevnt i artikkelen, «kan teammedlemmer vurdere plassering via en delt skjerm, noe som vil lette beslutningstaking og øke teamets tillit til korrekt plassering av trakealtuben».
Vi har flyttet boksen «BE OM HJELP» opp til «Can intubate, cannot ventilate», ettersom erklæring av denne situasjonen krever mer personell og utstyr.
I boksen «Før et sugekateter med aktivt sug gjennom TT» har vi endret fra «Bedring?» til «Obstruksjon?», da dette gjenspeiler det kliniske formålet. Dersom obstruksjon bekreftes, har vi lagt til «vurder ekstubasjon». Valget om å ekstubere pasienten vil avhenge av den kliniske settingen.
Vi har laget et trafikklys ved boksen «Før et fiberoptisk skop gjennom TT». Fiberoptisk skop representerer den tredje modalitet for bekreftelse av trakeal intubasjon og utelukke øsofagal intubasjon. Dersom trakeale strukturer, carina eller hovedbronkier ikke visualiseres, vil dette føre til ekstubasjon under fiberoptisk veiledning. Selv om fiberoptisk bekreftelse ble omtalt i artikkelen, var dette ikke presisert godt nok i flytskjemaet.
Trafikklyset reflekterer det kritiske beslutningspunktet mellom å ekstubere pasienten eller å stole på utstyret. Denne tilnærmingen skiller seg vesentlig fra Project for Universal Management of Airways (PUMA) algoritmen «Failure to satisfy sustained
exhaled CO₂ after intubation» (2). Dersom en korrekt plassert åpen tube i luftrøret ikke klarer å ventilere eller oksygenere, så er det lite sannsynlig at reintubering eller andre tiltak som maskeventilasjon eller larynksmaske vil hjelpe.
Vi har lagt til «Trakeoøsofagal fistel» som en mulig diagnose i boksen som besvares «Ja» på synlig årsak.
Vi håper at den reviderte Figur 1 kan være til hjelp for personell som driver med luftveishåndtering, samt øke pasientsikkerheten.
Referanser
1: Azam S, Khan Z Z, Shahbaz H, et al. (January 05, 2024) Video Versus Direct Laryngoscopy for Intubation: Updated Systematic Review and Meta-Analysis. Cureus 16(1): e51720. doi:10.7759/cureus.51720
2: Chrimes N et al. Preventing unrecognised oesophageal intubation: a consensus guideline from the Project for Universal Management of Airways and international airway societies. Anaesthesia 2022 https://doi.org/10.1111/ anae.15817
Ekstuber pasienten
Luftvei ikke verifisert, ekstuber under fiberoptisk veiledning
(øsofagal intubasjon)
Bronkospasme?
Anafylaksi?
Klinikk for Anestesi og Intensivmedisin, St.Olavs Hospital, Trondheim, Norge
IKKE verifisert
Intubasjon av trakea (verifisert med EtCO2 eller VL)
Can Intubate
Cannot Ventilate
Koble filter fra trakeal tube (TT)
Koble til Lærdalsbag og ventiler med 100% O2
Bedring?
Før et sugekateter med aktivt sug gjennom TT
Obstruksjon?
Før et fiberoptisk skop gjennom TT
Luftvei verifisert? Synlig årsak?
INGEN synlig årsak
TT og trakea er ikke obstruert
Medisinsk og/eller kirurgisk problem?
Pneumothoraks?
Avlast pneumothoraks
Kirurgisk årsak?
Vurder ENlungeventilasjon ved lungeskade, thoraks traume eller mediastinale masser
Vedvarende alvorlig hypoksemi eller sirkulatorisk sjokk?
Fortsett ventilering med 100% oxygen
Hjertelungeredning (HLR) om indisert
Problem i ventilator / slanger / filter
TT knekt eller obstruert (mucus / blod)
Vurder ekstubasjon
Fremmedlegeme / mucus / blod i trakea / hovedbronkus
Utilsiktet endobronkial intubasjon
TT obstruert av trakealveggen eller åpningen er dekt av cuffen
Trakeoøsofagal fistel
Problem med intrapulmonal gassutveksling?
V/Q mismatch?
Aspirasjon, lungeødem, ARDS, sirkulatorisk kollaps?
Optimaliser
respiratorinnstillinger. Korriger årsaker til hypotensjon
Vurder eksplorativ thorakotomi eller ECMO om indisert

Nicholas Percy Barlow Overlege Anestesi/Intensiv Akershus Universitetssykehus Nbar@Ahus.no
"Rules are for the obedience of fools and the guidance of wise men" – or «Regler er ment for dårers lydighet og de klokes veiledning», if one can say that in a clear 1940s British accent.
The quote is attributed to Wing Commander Harry Day, war hero, planner of The Great Escape from Stalag Luft III, and the all-round jolly good fellow we would all like to resemble when things go badly wrong. Calm, resilient, and resourceful, he is the sort of person you would want beside you when the plan has failed and everyone else is losing their cool.
Many of us like to imagine ourselves in that role. In our professional lives we can become the James Bonds of the hospital corridor, dropping into crises with decisive clarity, sweeping everyone off their feet, and then swanning back to the coffee room or operating theatre once order has been restored. We are often at our best when others are losing their composure.
But airway management has a way of puncturing that fantasy. Despite hundreds of uneventful inductions and intubations, sometimes the patient does not behave as expected. Instead of following the script,
the airway becomes like a bad-tempered djinn: desaturation, regurgitation, distorted anatomy, and an unsettling darkness that nothing is working. In those moments, heroism is not what saves you. Systems, teamwork, and shared understanding do.
“There is no such a thing as a difficult airway, and having a whole society devoted to it is a waste of time”. So said an ex-president of the Association of Anaesthetists over a beer and curry after some 150 km bicycling out from London. The logo of the association is an orange ring meant to represent Papaver somniferum, but we preferred to think it was a bicycle wheel. “What next, the difficult venflon society?” (it now exists).
There is some truth in his provocation. We have an excess of guidelines for almost everything, and when surrounded by too many choices, piles of carrots, even a donkey can starve. Yet when things go wrong, having no strategy at all is worse. We do not train for when everything works; we train for when it does not, when panic begins to creep in and time starts to distort.
When I began my anaesthetic career in 1997, the algorithm for unexpected difficult
intubation was simple: try a gum elastic bougie, try a McCoy laryngoscope, and if that failed, turn the patient lateral and wake them up. I have done this more than once. In 2004 the Difficult Airway Society published its first guidelines, incorporating supraglottic airways and ending with emergency surgical airways. There was a cricothyrotomy kit on the theatre wall, but no one had shown me how to use it. I eventually performed one nearly twenty years later, despite NAP41 showing how poorly many such devices worked in practice. It reminded me of another consultant’s mantra: “I don’t bother assessing airways; I just get good at managing them when they go wrong.” Steve Yentis, another extremely bright ex-president of the Association, later crystallised this into his memorable difficult airway test: they are all easy2
The year 2011 forced us to look more closely. NAP4 was published after the death of Elaine Bromley, a 37-year-old mother admitted for elective sinus surgery who died from a mismanaged airway, and in that same year we lost Camilla, a 20-yearold woman scheduled for tonsillectomy. She was septic, and every stage of her care—from admission to induction—was
marked by cognitive errors that culminated in catastrophe.
The Norwegian Board of Health’s conclusion was bleak: she had not received care that met professional standards. Warning signs were missed. Senior anaesthetic and surgical airway expertise was not present. Communication and escalation failed, especially during handover and prioritisation of simultaneous demands. Of the six doctors involved, three never returned to that specialty—the ‘second victim’ effect made painfully real.
In response, our airway management group was forced into existence. NAP4, the largest study of major complications of airway management ever performed, had already shown that human factors contributed to failure in most major airway disasters. We were instructed to rationalise our equipment, procedures, communication, and
Tidsskrift for Norsk anestesiologisk forening, DNLF
training. Management gave us four days twice a year with a full operating team. We had the 2004 DAS guidelines and the weight of NAP4 behind us. What we did not have was any real understanding of what ‘working as a team’ meant.
Our early training reflected this. Everyone sat through a lecture on difficult airways, then the doctors practised surgical airway skills on plastic necks while nurses learned where equipment was kept. We talked about crew resource management, even though the language barely translated. The simulation scenarios were enjoyable, but there was still confusion. The alphabetic A–B–C–D algorithm looked neat on paper but made little sense when people entered it at different points under stress.
Our first real breakthrough came when we introduced a traffic-light system for airway risk before anaesthesia. Proposed by a

senior colleague, it was initially criticised—“no one knows what a yellow airway is”—but operating nurses adopted it avidly; when an airway colour was announced as the patient arrived in theatre, ears pricked up. Patients also found it less alarming to be told their airway was ‘Yellow’ or ‘Red’ rather than ‘difficult’.
One colour now told everyone whether we could proceed as normal, pause to prepare, or focus entirely on the airway. It was not a diagnosis but a shared preparation code. Anaesthetists still discussed Mallampati scores and thyromental distance, because detail guides management, but the colour told the team what sort of day this airway was going to provide.
The logic is simple: if an airway is not ‘easy', ie Green, then it is ‘not-easy’, that is to say Yellow or Red, and the standard airway management has to be adjusted to take
account of whatever the deviation from normality was present. Jaydeep Pandit explains this eloquently and emphatically in an editorial in Anaesthesia3. There is no such thing as a ‘green airway with aspiration risk’. Normal anatomy with abnormal physiology still demands change. Do we decompress the stomach? Tilt the table? Prepare suction? Alter Plan B? The same applies when anatomy and physiology are normal but the cricothyroid membrane cannot be felt.
I ask trainees whether they would jump from an aeroplane if they were not sure their parachute would open. The analogy to mask ventilation is obvious. The follow-up question—would you jump without a reserve parachute?—gets the same answer. Yet we still induce anaesthesia in patients we cannot rescue surgically. The
Tidsskrift for Norsk anestesiologisk forening, DNLF
2025 DAS update finally addresses this by forcing clinicians to decide in advance whether emergency front-of-neck access will be a stab or a vertical incision, deliberately engaging the psychologist Daniel Kahneman’s time and energy consuming ‘System 2’ approach to a problem4.
The 2015 DAS guidelines5 were a remarkable synthesis of evidence and expertise, yet we still struggled to teach teams how to think. We standardised surgical airway equipment along UK lines and removed devices that failed in practice, but people remained bound by the algorithm alphabet.
So we extended the pre-op traffic-light system into the peri-induction airway. A Yellow airway meant controlled difficulty needing help; Red meant immediate
assistance. For nurses acting as intermediaries, this clarity mattered. “The LMA is leaking” and “the saturations are falling” do not have the same urgency. If a Yellow or Red airway is declared assistants now fetch the trolley and call for help without waiting to be told.
Human-factors thinking teaches that systems should make the right action easy, and it is a useful insight that actions also define the airway code and colour. In the same way that asking for a defibrillator could reasonably be met by the question “has the patient arrested?”, asking for a bougie raises the question “is this an unexpected Yellow airway?” and prompts the help that follows. Fetching the trolley, attempting a second intubation, or moving to four-hand ventilation are themselves signals of trouble, and we teach graded
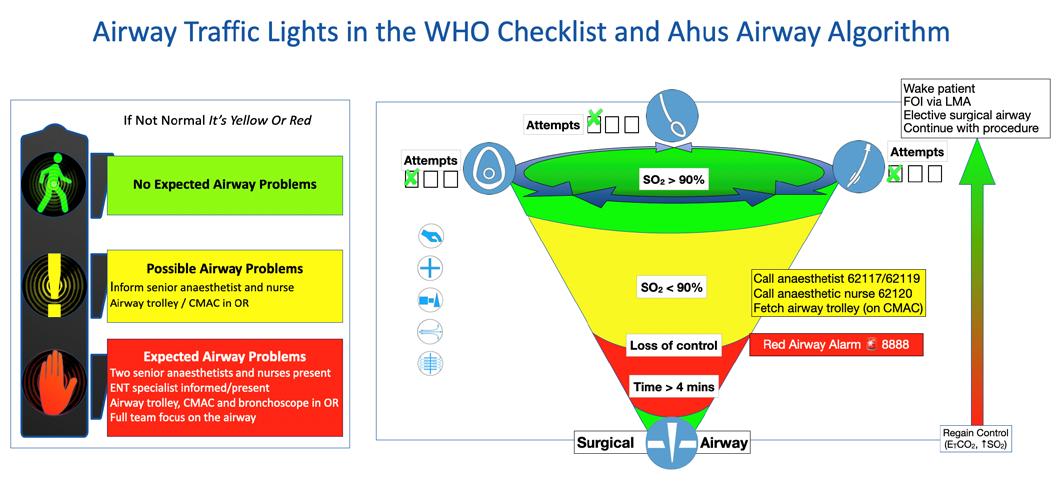
assertiveness: “Do you need help?”; “Shall we call for help?”; “Is this an unexpected Red airway?”. These phrases trigger team roles and movement.
Huitink6 in 2017 showed how often saturations fall below 93% during induction. That may not sound dramatic, but every fatal airway event crosses that threshold. The same applies to repeated attempts or failing modalities; difficulty predicts disaster. Defining the airway ‘Yellow’ early gives teams permission to escalate before it is too late, and early difficulty of almost any kind may in fact be the Gods of Anaesthesia tapping you lightly on the shoulder and saying ‘pay attention to this one!’.
Around this time we realised something more fundamental: the DAS algorithm describes the ideal management of the ideal unexpected difficult intubation, but real airways fail everywhere—mask, supraglottic airway, or tube. Nick Chrimes’ Vortex model7 captured this reality. It was intuitive, much closer to everyday reality, and integrating it transformed our teams understanding of airway management overnight. We removed the handcuffs from the algorithm and allowed people to use is at a tool.
We also changed how we trained. Nurses and doctors now sit together for all of the teaching. Everyone is certified to perform an emergency surgical airway, not because everyone will, but because everyone has to know what it’s like to declare an “unexpected red airway” and support the person with the scalpel. On the manikin, nearly everyone freezes for a moment, and recognising that moment in oneself makes it easier to recognise it in others. That is what team training really means.
Tidsskrift for Norsk anestesiologisk forening, DNLF
In 2019 we introduced a single emergency airway call – Rød Luftveis Alarm. Instead of five phone numbers and the following problem: “Whom shall I call; what is their number, what do I tell them; and how do I explain the urgency?”, one call summons the airway team: anaesthetists, nurses, and ENT.
We now use our training days not just to practise but to critique and keep us updated with changes in all of the different units and wards. A single-page poster hangs in every theatre. Equipment is standardised and we are moving forward to a devoted list for elective awake videoscopic intubation, and more high flow devices for peri-oxygenation.
Ex malo bonum? Can good come from a tragedy? People have asked whether they too ‘need a death’ in order to set up the airway training course that we have. They should not have to: The Helsetilsynet’s report8 is linked at the end of this article and I recommend reading it thoroughly as well as any other coroner’s or similar reports you can find from any country in the world. We have to stop repeating the same mistakes.
I agree with the ex-president: there is no such thing as a difficult airway. Every hand can be a winner and every hand a loser, and one can mess up simple airways with bad planning just as one can manage extreme cases easily with the correct preparation. Even the world’s top airway expert will fail if the team don’t understand each other. What we have developed, is a common language that can help everyone in the room describe what is happening, what it means, and how to help.
1. Cook TM, Woodall N, Frerk C, et al. Major complications of airway management in the UK: results of the Fourth National Audit Project of the Royal College of Anaesthetists and the Difficult Airway Society. Br J Anaesth 2011; 106: 617–631.
2. Yentis SM. Predicting difficult intubation— worthwhile exercise or pointless ritual? Anaesthesia 2002; 57: 105–109. doi:10.1046/j.0003-2409.2001.02515.x
3. Pandit JJ, Heidegger T. Putting the “point” back into the difficult airway. Anaesthesia 2002; 57: 105–109.
4. Kahneman D. Thinking, Fast and Slow. London: Penguin Books; 2011.
5. Frerk C, Mitchell VS, McNarry AF, et al. Difficult Airway Society 2015 guidelines for management of unanticipated difficult intubation in adults. Br J Anaesth 2015; 115: 827–848.
6. Huitink JM, Lie PP. A prospective, cohort evaluation of major and minor airway management complications during routine anaesthetic care at an academic medical centre. Anaesthesia 2017; 72: 42–48. doi:10.1111/anae.13640
7. Vortex Approach. The Vortex Approach: a cognitive aid for airway management. https:// www.vortexapproach.org/
8. Statens helsetilsyn. https://www.helsetilsynet. no/historisk-arkiv/avgjoerelser-i-tilsynssaker-og-rapporter-etter-alvorlige-hendelser/ avgjorelse-i-tilsynssak-brudd-pa-helselovgivningen/
Norepinephrine as first-line vasopressor therapy
Septic shock remains a time-critical condition in which both the choice of vasopressor and the timing of its initiation may influence outcomes. Current Surviving Sepsis Campaign (SSC) guidelines recommend norepinephrine (NE) as the first-line vasopressor in patients with septic shock, exerting its effects primarily through α1-adrenergic receptor activation. Treatment with NE is well established to be associated with lower mortality (Shi et al 2025) and a reduced risk of arrhythmias compared with dopamine. In addition, NE administration may increase cardiac output, improve microcirculation, and reduce harmful afterload.
However, in some patients, vascular responsiveness to catecholamines becomes impaired. Catecholamine hypo-responsiveness, partly related to lactic acidosis and downregulation or decoupling of α1-adrenergic receptors, may limit the effectiveness of further dose escalation. In such situations, vasopressors with alternative mechanisms of action may be required to restore vascular tone and blood pressure. Current SSC guidelines therefore recommend adding vasopressin (AVP), a non-catecholaminergic vasopressor, as a second-line agent rather than further increasing the NE dose in patients requiring NE base doses >0.25–0.50 µg/kg/min, after exclusion of persistent hypovolemia and cardiac dysfunction.
Clinical considerations before initiating vasopressin
• Exclude alternative causes of hypotension. The presence of hypovolemia or intracavitary left ventricular obstruction should be ruled out.
• Assess contributing risk factors. These include fever, sedation, blood glucose abnormalities, calcium imbalance, and acidosis.
• Evaluate left ventricular function. In patients with left ventricular dysfunction, alternative strategies such as dobutamine, epinephrine, or venoarterial extracorporeal membrane oxygenation (VA-ECMO) may be considered.
Vasopressin and the concept of decatecholaminization
AVP is a peptide hormone that induces vasoconstriction via activation of the arginine vasopressin V1 receptor. Early combination therapy using moderate doses of vasopressors with complementary mechanisms of action may help avoid the toxicity associated with high doses of a single agent. By adding AVP, the required NE dose can often be reduced, which may in turn lower the risk of complications associated with high catecholamine exposure. This approach is referred to as decatecholaminization.
The overall treatment goal of AVP therapy is to achieve the targeted mean arterial pressure (MAP) while reducing or maintaining the NE dose needed to sustain adequate perfusion. When should AVP be introduced? Still, a key clinical question remains unresolved: should AVP be introduced only after a predefined NE dose is reached, or could earlier initiation at lower NE doses and earlier in the course of shock offer advantages? Recent observational data, survey results, and model-based analyses suggest that timing may be as important as dose when integrating AVP into vasopressor therapy.
The PRESS Survey, an international survey endorsed by the European Society of Intensive Care Medicine, assessed the current use of AVP and terlipressin in patients with septic shock (Jozwiak et al 2025). The survey was completed by 1919 intensivists from 124 countries. The primary indication for use was refractory septic shock, with the main treatment goals being blood pressure stabilization and reduction of catecholamine load. AVP was used by the majority of respondents (96%), whereas terlipressin was used by only 2%, as it is not currently recommended by SSC guidelines for septic shock. Nevertheless, terlipressin may be of interest in specific subgroups, such as patients with septic shock and cirrhosis or acute-on-chronic liver failure, given its established role in the management of variceal bleeding through effects on portal venous pressure.
This article is an advertisement prepared by AOP Health and is intended as promotional material for healthcare professionals.
The survey demonstrated substantial heterogeneity in dosing strategies. Initial doses of 0.01 or 0.03 U/min were used by 50% of respondents. Mean arterial pressure triggered tapering of AVP or terlipressin for 88% of respondents. Discontinuation was initiated after the dose of the first-line vasopressor had been reduced below a predefined threshold for 43% of respondents and was progressive for 89% of respondents. Further insight is provided by an AI-driven model, which suggests that favorable outcomes are achieved when AVP is initiated earlier and at lower NE base doses, around 0.20 µg/kg/ min, with a median initiation time of approximately four hours after shock onset (Kalimouttou et al., 2025). Findings from the PRESS Survey align with these results: for 78% of respondents, both NE dose and duration influenced the decision to initiate AVP or terlipressin, with the most common trigger being NE base doses >0.25 or >0.50 µg/kg/min sustained for more than 2–6 hours.
Septic shock remains a complex hemodynamic syndrome in which loss of vascular tone and catecholamine hypo-responsivity pose major therapeutic challenges. While NE continues to be the cornerstone of first-line vasopressor therapy, accumulating evidence supports an earlier, multimodal vasopressor strategy that limits excessive catecholamine exposure.
The addition of vasopressin as a second-line agent, particularly when introduced at lower norepinephrine doses and earlier after shock onset, may represent a more physiologically tailored approach to restoring vascular tone and stabilizing blood pressure while limiting cumulative catecholamine exposure. These data invite renewed reflection on how vasopressor strategies are applied in everyday clinical practice, with increased attention to both timing and overall vasopressor load.
VASA_12_022026_NO
Evans L, Rhodes A, Alhazzani W, et al. Surviving sepsis campaign: international guidelines for management of sepsis and septic shock 2021. Intensive Care Med. 2021 Nov;47(11):1181–1247.
Khanna AK, Kinoshita T, Natarajan A, et al. Association of systolic, diastolic, mean, and pulse pressure with morbidity and mortality in septic ICU patients: a
nationwide observational study. Ann Intensive Care. 2023 Jan 21;13(1):9.
Jozwiak M, Cousin VL, De Backer D, et al. Vasopressin use across shock states: international insights from an international ESICM-endorsed survey: the PRESS Survey. Crit Care. 2025 Jul 3;29(1):273.
Shi R, Braïk R, Monnet X, et al. Early norepinephrine
Empressin «argipressin» konsentrat til infusjonsvæske, oppløsning 20 IE/ml Reseptgruppe C Indikasjoner: Behandling av katekolaminresistent hypotensjon etter septisk sjokk hos pasienter >18 år. Dosering: Administreres kun under tett og kontinuerlig overvåkning av hemodynamiske og organspesifikke parametere. Behandlingen skal helst startes innen 6 timer etter utbrudd av septisk sjokk, eller innen 3 timer etter utbrudd hos pasienter som er på høye doser katekolaminer. Skal gis som en kontinuerlig i.v. infusjon av 0,01 IE/min argipressin vha. en infusjonspumpe. Brukes kun i tillegg til konvensjonell vasopressorbehandling med katekolaminer. Avhengig av klinisk respons, kan dosen økes hvert 15.-20. minutt opp til 0,03 IE/minutt. Doser >0,03 IE/minutt skal kun benyttes som akuttbehandling, da det kan gi tarm- og hudnekrose, samt øke risiko for hjertestans. Behandlingsvarighet skal vurderes mht. klinisk tilstand, men bør helst vare i minst 48 timer. Behandlingen skal ikke avsluttes brått, men gradvis nedtrappes i samsvar med klinisk forløp. Se SPC for infusjonshastighet iht. anbefalte doser og tilberedning/håndtering. Spesielle pasientgrupper: Barn: Anbefales ikke. Kontraindikasjoner: Overfølsomhet for innholdsstoffene. Forsiktighetsregler: Skal ikke brukes vekselsvis med andre argipressinpreparater med styrke angitt i andre enheter. Skal ikke gis som bolus ved behandling av katekolaminresistent sjokk. Behandlingen skal kun startes dersom tilstrekkelig perfusjonstrykk ikke kan oppnås til tross for adekvat volumsubstitusjon og bruk av katekolaminerge vasopressorer. Skal brukes med særlig forsiktighet ved hjerte- og karsykdom. Tilførsel av høye doser ved andre indikasjoner har gitt myokard- og tarmiskemi, myokard- og tarminfarkt, samt redusert perfusjon av ekstremiteter. Kan i sjeldne tilfeller gi vannforgiftning. Tidlige symptomer som døsighet, tiltaksløshet og hodepine bør gje kjennes i tide for å forhindre terminal koma og kramper. Skal brukes med forsiktighet ved epilepsi, migrene, astma, hjertesvikt eller en hvilken som helst tilstand hvor rask økning av ekstracellulær væske kan medføre skade på et allerede overbelastet system. Interaksjoner: For utfyllende informasjon om relevante
for patients with septic shock: an updated systematic review and meta-analysis with trial sequential analysis. Crit Care. 2025 May 6;29(1):182.
Kalimouttou A, Kennedy JN, Feng J, et al. Optimal vasopressin initiation in septic shock: the OVISS reinforcement learning study. JAMA. 2025 May 20;333(19):1688–1698.
Less than 10 minutes effective half-life provides a high degree of control 3,5 while maintaining mean arterial pressure 3,4 in catecholamine refractory septic shock 1,2
interaksjoner, bruk interaksjonsanalyse. Samtidig bruk av karbamazepin, klorpropamid, klofibrat, karbamid, fludrokortison eller TCA, kan forsterke argipressins antidiuretiske effekt. Samtidig bruk av demeklocyklin, noradrenalin, litium, heparin eller alkohol kan redusere argipressins antidiuretiske effekt. Ganglionblokkerende midler kan øke følsomheten overfor pressoreffekten til argipressin. Tolvaptan og argipressin kan begge redusere hverandres diuretiske og antidiuretiske effekter. Blodtrykksøkende legemidler kan forsterke argipressins blodtrykksøkende effekt, mens blodtrykkssenkende legemidler kan redusere den. Graviditet og amming: Graviditet: Skal ikke brukes med mindre det er helt nødvendig. Amming: Overgang i morsmelk og påvirkning på barnet er ukjent, forsiktighet må utvises. Bivirkninger: Vanlige: Tarmiskemi, abdominale kramper, angina pectoris, arytmi, hjerteiskemi, digital iskemi, hudnekrose, nekrose, perifer vasokonstriksjon, perioral pallor. Mindre vanlige: Tarmnekrose, kvalme, oppkast, flatulens, hjertestans, livstruende arytmi, redusert hjerteminuttvolum, bronkokonstriksjon, tremor, vertigo, hodepine, hyponatremi, svetting, urtikaria, trombocytopeni, økt bilirubin, økte transaminaser. Sjeldne: Anafylaktisk reaksjon. Overdosering/Forgiftning: Ved vannintoksikasjon skal ingen væske gis og argipressinbehandling kan midlertidig avbrytes inntil polyuri oppstår. I alvorlige tilfeller kan osmotisk diurese utføres ved bruk av mannitol, hypertonisk dekstrose, karbamid med eller uten furosemid. For mer informasjon, se Felleskatalogteksten eller preparatomtalen (SPC) Innehaver av markedsføringstillatelsen: Orpha-Devel Handels und Vertriebs GmbH, Østerrike. Kontaktinformasjon: Telefon: +46 70 578 61 00 E-post: medinfo.no@aop-health.com
Basert på SPC godkjent av SLV/EMA: 11.12.2023
Pakninger og priser per 22.03.2024: 10 stk. (amp. 2 ml 20 IE/ml), kr 9888,20. (priser og ev. refusjon oppdateres hver 14. dag).
Utarbeidet 03/2024
References: 1. Evans L, Rhodes A, Alhazzani W et al.: Surviving sepsis campaign: international guidelines for management of sepsis and septic shock 2021. Intensive Care Med (2021) 47:11811247 2. Dünser M.W.: Arginine vasopressin in advanced vasodilatory shock: a prospective, randomized, controlled study; Circulation.2003 May 13;107(18):23139.17. 3. Summary of Product Characteristics, Empressin. 11.12.2023. 4. Dalimonte MA, DeGrado JR, Anger KE. Vasoactive Agents for Adult Septic Shock: An Update and Review. J Pharm Pract. 2020;33(4):523-532. doi:10.1177/0897190019844124. 5. Tanja A. Treschan, Jürgen Peters; The Vasopressin System: Physiology and Clinical Strategies. Anesthesiology 2006;105(3):599-612.
AOP Orphan Pharmaceuticals Sweden AB Member of the AOP Health Group +46 70 578 61 00 office.se@aoporphan.com www.aop-health.com

Elisabeth
Holmboe
Overlege, Anestesiavdelingen, AHUS og spesialist i barnesykdommer elisabethholmboe@yahoo.no
Livet er fullt av dårlige nyheter – store og små. Å fortelle barna sine at mamma og pappa skal skilles. Å si nei når barnet vil ha sjokolade midt i uka. Å si til 16 -åringen at hun ikke får dra på interrail med en venninne. Helsevesenet er også fullt av dårlige nyheter. Du trenger en ny arteriekran. Mannen din må holdes på respirator noen dager lenger. Den legen dere kjenner best er ikke på jobb i dag. Og i ytterste enden av skalaen: Deres kjære har en alvorlig sykdom, vi vet ikke om han overlever dette. Hvordan kan vi som helsepersonell kommunisere dårlige nyheter på en best mulig måte for pasienten og pårørende? Og hvordan håndterer vi følelsene det utløser? Det finnes nemlig en metode.
Pasienter og pårørende er ofte sårbare. Informasjon som for oss virker nøytral, kan for dem oppleves som en liten katastrofe. Hvis vi øver oss på å gi all informasjon rolig, bit for bit, så får vi med oss reaksjonene som kommer.
Det som er sikkert når du gir noen en dårlig nyhet, er at det kommer vonde følelser. Smerte, skuffelse, sorg, fortvilelse og frykt. Andres vonde følelser kan være ubehagelig fordi det kan vekke negative følelser i oss selv som vi ikke er komfortable med. For mange er negative følelser så skummelt at vi gjør alt for å unngå dem.
Du har helt sikkert både sett eksempler på det og gjort det selv – mange ganger:
• Avlede med å forte seg å snakke om noe annet (Gjerne gi masse medisinsk informasjon, fordi der er vi på trygg grunn).
• Unnvike det ubehagelige med å ikke egentlig si det rett ut («vi har funnet forandringer i prøven»).
• Forsøke å sukre pillen («det kunne vært verre»).
Vi blir stresset og keitete. Det er ubehagelig for pasienten. For da må pasienten ta ansvar i samtalen, og ivareta legen, i stedet for motsatt.
Derfor bør du lære deg å gjenkjenne og tåle følelser, og å stå i dem. Pasientenes og ikke minst dine egne. Det er så lett som det er vanskelig – og livet ditt vil bli mye rikere og enklere. Det blir mye lettere å få til gode samtaler med pasientene. Du blir tryggere som lege. Og du blir et bedre medmenneske for dem rundt deg.
Så hvordan skal man gjøre det da? Oppskriften er verdens enkleste, egentlig.
En stjernefortelling
Klokka var 1445. Jeg hadde gått visitt på en jente innlagt med diffuse smerter i et ben. MR-svaret hadde kommet, og det var mest sannsynlig et sarkom. Jeg visste at moren var veldig nervøs for svaret. Fordi jeg bare var LIS, ønsket jeg at barneonkologen på avdelingen skulle fortelle det. Han hadde aldri møtt pasienten eller moren og var egentlig på vei hjem, men ble med meg. Vi gikk inn til dem, hilste og satte oss ned. Så sa han: «Det jeg skal si nå gjør utrolig vondt å si». Deretter trakk han pusten, før han sa: «MRbildene viser det vi tror er en kreftsvulst i skjelettet». Det var så vidt stemmen bar. Så samlet han seg og tok en pause, før han sa noen setninger om den umiddelbare planen videre, og rundet av. Han og jeg dro hjem til våre friske familier, mens mor og pasient fikk livet snudd på hodet. Det er det råeste jeg har sett, og det er akkurat sånn det skal gjøres. Og det tok cirka fem minutter.
Oppskriften er altså:
• Forbered deg.
• Hopp over smalltalken.
• Koble deg på emosjonelt.
• Gi et forvarsel.
• Si det du skal formidle kort og tydelig.
• Ta en pause, vis og kjenn empati.
• Rund av samtalen når du har ivaretatt pasientens følelser og reaksjoner og gitt kort informasjon om neste umiddelbare steg videre.

Being with Etter du har sagt det du skal si rett ut, kort og tydelig, så vær stille og empatisk. Hvordan viser man empati?
Det kommer ofte en trang til å bli aktiv, gjøre noe eller si noe. I nære relasjoner er vi vant med å gi en klem eller å ta på den andre. Med pasienten er det mye god empati i å reise deg og finne et papir de kan tørke tårene med. Resten må du gjøre inni deg. Med hovedfokus på kroppen og pusten.
Empati er medfølelse som du kjenner i din egen kropp. Det fordrer at du har kontakt med dine egne følelser. Din egen tristhet, skuffelser, frykt, savn og sorg.
Du kan fokusere på å være rolig i kroppen, puste (dype pust holder parasympatikus aktivert) og holde deg «åpen og varm». Kjenne at alt som nå kan komme av reaksjoner er ok for deg. For nå må du vente helt til pasienten sier noe. Den stille tiden – tålmodigheten, følelsen pasienten får av at du kan sitte der stille hele dagen og være tilgjengelig for det som måtte komme. Den tiden kan ganges med tusen og veies i gull. Pasienten kan bli fortvilet, sint, lei seg, stille, eller bli veldig aktiv og stille spørsmål. Nå er det pasienten som skal stake ut kursen videre i samtalen.
Det kan skje at du venter lenge og ser at pasienten er klar til å gå videre, men ikke vet hva de skal si. Da bør du ha et par setninger klare for å hjelpe dem videre, uten å begynne å bable. For eksempel: «Hvordan går det med deg?» Eller: «Nå har du sikkert mange tanker og spørsmål, hvor vil du begynne?». Husk da å stoppe på nytt, vent og pust. Det kan være veldig uvant for pasienten at legen stopper opp på denne måten. Men bare stå rolig. Så vil de etter hvert forstå at du ikke har noen travel agenda. At dette er pasientens tid. Du bare er der med dem i deres følelser. Med dine egne følelser. Being with heter det på fagspråket1.
Når du er emosjonelt til stede, kan det hende du begynner å gråte. Det er helt normalt, og empati på sitt beste. Faren til en av jentene som mistet livet da de ble påkjørt med ponni og vogn for noen år siden, skrev i sin bok «Pass på liten og på stor»2:
«Å oppleve at også de profesjonelle hjelperne felte fortvilte tårer, ble for meg uttrykk for den største solidaritet og medfølelse. Legene og pleierne rygget ikke for min smerte, men ble stående sammen med meg der jeg hadde det som vondest. De og jeg, like hjelpeløse da døden krevde sitt.
At legene kunne sitt fag, var jeg trygg på. At de også ville gå den ekstra milen med meg inn i smerten, kom – det må jeg med skam innrømme – som en overraskelse på meg. Det var imidlertid den beste medisin som var å oppdrive for det knuste pappahjertet.»
De dårlige nyhetene er der. Du kan ikke unngå hverken dem eller de vonde følelsene. Følelser er ikke farlige, de er bare følelser. Lær deg å elske følelsene, de er ditt viktigste verktøy i kontakt med pasienten.
Referanse
1. SPIKES—A Six-Step Protocol for Delivering Bad News: Application to the Patient with Cancer Purchased. Walter F. Baile , Robert Buckman , Renato Lenzi , Gary Glober , Estela A. Beale , Andrzej P. Kudelka. The Oncologist, Volume 5, Issue 4, August 2000, Pages 302–311, https:// doi.org/10.1634/theoncologist.5-4-302. Published: 01 August 2000. https://academic. oup.com/oncolo/article/5/4/302/6386019
2. Sitatet fra boken «Pass på liten og på stor» er gjengitt med tillatelse fra forfatteren Jostein H. Sandsmark.

John Reidar Eriksen
Overlege KSK, Haukeland Universitetssykehus. Consultant anesthesiologist, Kilimanjaro Christian Medical Center. Children’s Burn and Wound Care Foundation jreriksen@gmail.com

Children’s Burn and Wound Care Foundation:
Tidsskrift for Norsk anestesiologisk forening, DNLF
I mars 2024 reiste jeg med familie, kone og 3 barn, til Moshi i Tanzania etter å ha signert en ettårskontrakt med KCMC, med mulighet for forlengelse. Nå er snart 2 år gått og min tid som voluntary consultant går mot slutten – for denne gang. NAForum har utfordret meg til å skrive litt om hva jeg egentlig holder på med her nede. Jeg skal prøve å fatte meg i korthet.
Tanzania
Man tenker umiddelbart på Serengeti, Ngorongoro og Zanzibar. Det er et yndet land for turister, og med god grunn. Dessuten er det et fredelig land, det er relativt trygt å reise rundt, og med et trafikkbilde som krever at du er våken hele tiden. Dessverre har de siste par måneder sjokkert mang en Tanzanianer i møte med landets ledelse som nå har kneblet reell opposisjon, og møter demonstrasjoner med brutalitet. Man spør seg om landet noen gang vil kunne leges etter presidentvalget i oktober.
Helse og anestesi
Størsteparten av landets 70 millioner innbyggere er fattige. Helsetilbudet holder lav standard og kan du ikke betale, får du ikke hjelp. Det finnes forsikringsordninger. Mange har ikke råd. Totalt finnes det ca 60 anestesileger, der en tredjedel av disse enten er i administrative stillinger eller i ferd med å gå av med pensjon. Møter du opp på en helsestasjon for sectio eller annen kirurgi er sannsynligheten for å møte på en anestesilege svært liten. Stort sett er det CMOs (clinical medical officers) som setter spinalen. Likevel ser man at det satses på utvikling av anestesi i landet og det finnes en egen tanzaniansk anestesilegeforening (SATA) med årlige landsmøter.
KCMC
KCMC er et stort regionssykehus med nedslagsfelt på ca 15 millioner mennesker. Det ligger nydelig til ved foten av
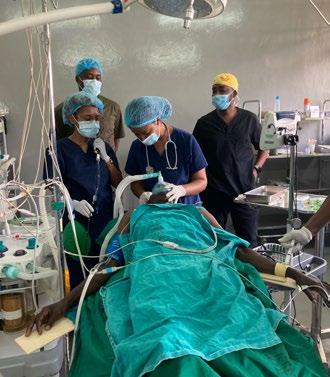
I front: 3 av de mest erfarne anestesilegene på KCMC. Her gjøres fiberoptisk intubasjon videoskopassistert.
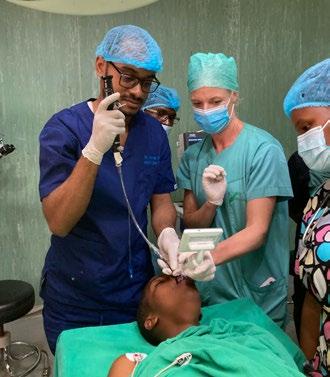
Kilimanjaro. Her er det alltid grønt og skjønt, med godt klima og lite malaria. KCMCs bygningsmasse gjenspeiler ikke omgivelsene. Den bærer preg av forfall og fortid. Tunge mørke ganger og operasjonssaler slik det var populært på 70-ta llet da sykehuset ble bygget, tenker jeg. En nyoppusset hjemmeside skaper et glansbilde av hvor høyteknologiske vi er her på KCMC og hvilken state-of-the-art behandling man får bare man kommer innenfor veggene. Sannheten er en helt annen. Gammelt utstyr. Ødelagt utstyr. Manglende utstyr. Manglende evne til å bruke utstyr. Det er virkeligheten. KCMC drives av Good Samaritan Foundation, en lokal stiftelse. Men den gode samaritan er ikke å se. Betaler du ikke, får du ikke behandling. Om du likevel får hjelp da ting virker litt kritisk, så må du likevel betale før du får forlate sykehuset. For sykehuset har ikke penger. Men mange pasienter har heller ikke det.
Videre på hjemmesiden leser man om alle tilbudene man kan velge i. Blant de kirurgiske disiplinene finnes det nevrokirurgi, øre-nese-hals, urologi, pediatrisk kirurgi, ortopedi, gynekologi/obstetrikk, brannskadekirurgi, endokrinkirurgi og kjevekirurgi. Og sant skal sies: noen av spesialistene er virkelig flinke. Jeg tar av meg hatten. For andre tar jeg hatten på igjen.
Det finnes en blodbank som ofte, men ikke alltid, klarer å skaffe til veie blod om det virkelig er nødvendig. Det finnes kirurgisk og medisinsk intensivavdeling, pediatrisk intensiv og nyfødt intensiv. Jeg skal ikke utale meg om nyfødt intensiven, men de øvrige er et trist kapittel. Og det finnes ingen oppvåkningsavdeling. Og ingen blodgassmaskin.
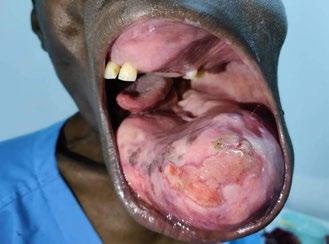
Anestesiavdelingen og min rolle
Leseren spør seg sikkert: hvorfor reiste du ned til dette? Det har vært flere ting som har motivert meg, og en viktig motivasjonsfaktor er at KCMC University i snart 4 år har utdannet anestesileger og anestesisykepleiere: legene går et 4-årig resident program, mens sykepleierne går et ettårig diploma program. Jeg har fått en fantastisk utdannelse hjemme. Det har gitt mening å gi noe videre ved å støtte dette programmet.
I mange år har avdelingen vært drevet av nevnte CMOs, men de siste årene har en nyutdannet anestesilegespesialist hatt jobben som sjef, med 4-5 andre spesialister rundt seg. Alle er utdannet i Dar Es Salaam. De er ferske og uerfarne, men likevel et stort steg i riktig retning. Per nå har vi en LIS-legestab på ca 20 leger, så tidene forandres. Sakte. Det er ikke rosenrødt. Spesialistene er sjelden å se på stuene. LIS-legene er stort sett alltid overlatt til seg selv for å finne ut av hvordan anestesi skal gjøres. Det er minimal oppfølging og veiledning å få. Og å ta kontakt med bakvakt om natta, det gjør man bare ikke!
Så hva har min rolle vært? Den har jeg måttet definere selv. Jeg signaliserte allerede før jeg ankom KCMC at jeg ikke ville
Tidsskrift for Norsk anestesiologisk forening, DNLF
involveres i akuttmottak eller på intensiv. Kun dagarbeid, ingen helg, ingen natt. Det valget er jeg glad for at jeg tok. Det ville blitt for mye, både for meg selv og familien. Fokus på ren anestesi har vært mer enn nok og det ble tidlig klart for meg hva mitt hovedfokus skulle være: pasientsikkerhet – fra pasienten kommer til pasienten trilles ut igjen. Det har vært mye å ta tak i. Mesteparten av tiden har jeg vært opptatt med en-til-en-undervisning på stuene av LIS-er og anestesisykepleiestudenter om det helt grunnleggende. Vi har stort sett det vi trenger av medikamenter, tuber, nåler og annet utstyr. Det er ikke der skoen trykker. Det er konvertering av teoretisk kunnskap over i praktisk håndtering det skorter. Og den teoretiske kunnskapen må veldig ofte korrigeres den også.
Internasjonalt samarbeid
I tillegg har jeg satt i gang en rekke kvalitetsforbedringsprosjekter: utvikling av Safe Anesthesia Checklist, avansert luftveishåndtering, innføring av nevromonitorering etter paralyse, epiduralopplæringsprogram og utarbeidelse av metodebok i non-obstetrisk anestesi (obstetrisk metodebok er på vei). Om ikke alt har kommet helt i mål så har vi nådd langt på to år, mye takket være velvillige og motiverte kolleger fra Norge som har kommet for å bidra, samt donatører fra inn- og utland. Den første som skal nevnes er anestesisykepleier Øystein Myrstad fra Stavanger som sammen med familien flyttet ned omtrent samtidig med oss og var en uvurderlig støtte det første året før de returnerte hjem. I tillegg har seks kollegaer fra Haukeland og en fra Molde besøkt avdelingen med det resultat at en overlege og en LIS-lege nå har blitt ganske kompetente på vurdering og håndtering av vanskelig luftvei med fiberoptikk/ videoskopi. Tre LIS og en overlege har blitt
kompetente på ikke-obstetrisk epiduralanestesi og -analgesi. Dette er nytt i Tanzaniansk sammenheng. Det finnes knapt et etablert epiduraltilbud i landet. Det internasjonale samarbeidet strekker seg lenger enn til Norge. Jeg har vært heldig å være en del av et større nettverk av europeere og amerikanere som i mange år har vært engasjert i utviklingen av anestesiavdelingen på KCMC, faglig og strukturelt. Disse har kun kommet på ukesopphold 1–2 ganger i året. Jeg er glad jeg har kunnet bidra med kontinuitet i samarbeid med disse.
Nareshkumar underviser i våkenintubasjon.
Nareshkumar innførte skalpblokade under sitt besøk. Nå underviser LIS-legene hverandre, og blokaden har vist seg svært nyttig per- og postoperativt i en setting som dette.
Tidsskrift for Norsk anestesiologisk forening, DNLF

Torstein Lyngøy underviser i epiduralteknikk. Et egnet post-operativt areal har blitt dedikert til programmet for å kunne gi analgesi 24-48 timer postoperativt før pasienten går til sengepost.
Oppfordring til NAF
Nå ser jeg fram til å komme hjem igjen til Haukeland, men jeg håper å komme tilbake til Moshi. Det har vært utfordrende å være her, men mest av alt veldig meningsfullt. Jeg tror det er flere der hjemme som kan tenke seg å gjøre noe liknende. NAF har søsterorganisasjoner internasjonalt med sterkt bistandsfokus. Irland og Canada er gode eksempler. Jeg oppfordrer NAF til å tenke i samme gate: utvikle ordninger for å støtte kolleger som vil bidra til utdanning der det trengs. Jeg snakker ikke om «missions». Jeg tenker på langtidsengasjement som sikrer kontinuitet. Det tar tid å bygge tillit. Det tar tid å snu ei skute. Så herved er utfordringen gitt.
Takk til
Det har i høyeste grad vært et fellesprosjekt det jeg har fått være med på i Moshi. Mange skal ha takk. Uten mine sjefer på KSK Haukeland, Elin Bjørnestad og Elin Kryvi, ville dette aldri blitt noe av. En stor takk til dem! Jeg har hatt deres støtte 100 % hele veien.
Pancuron er dessverre svært mye brukt, uten kunnskap om farmakologiske egenskaper. Innføring av TOF har avverget mange restparalyser fra å gå direkte til sengepost. Disse TOF-apparatene har blitt donert av Haukeland.
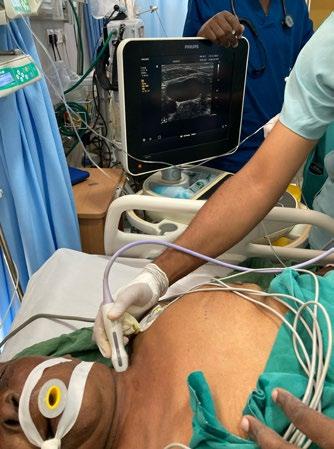
Operasjonskapasiteten er svært begrenset, og pasienter venter i dagevis på operasjon, uten å få antikoagulasjon. Her et bilde post ROSC mest sannsynlig grunnet lungeemboli. Ultradlydapparatet er donert av Haukeland, og er flittig i bruk. Bildet viser en struttende jugularis interna. Vi har ikke kardiolog, ikke trombolyse, og pasienten døde etter kort tid.
Takk til Children’s Burn and Wound Care Foundation som har fungert som min arbeidsgiver her i Moshi.
KSK, fagsykepleiere og Medisinsk teknisk avdeling skal også ha en stor takk for donasjon av en stor mengde utstyr. Den samme takken går også til Haraldsplass Diakonale Sykehus.
Takk til velvillighet i industrien som har donert utstyr:
• Philips Norge
• Braun Medical Norge
• Medtronic Norge
• BD Norge
• Mediplast Norge
• VingMed Danmark
• BoneFoam USA
• Ambu
Takk til alle dere som har kommet på besøk for å støtte, oppmuntre og hjelpe til: Nina Vietheer, Nareshkumar Pathmanathan, Torstein Lyngøy, Bjarte Toppe, Åsmund Øpstad, Lars Olav Sandnes (Haukeland) og Ingvild Haram Stige (Molde Sykehus). Takk til Jonathan Mathers, Gjermund Galleberg og Christopher Bjerkvig (Haukeland) som har bidratt til et virtuelt undervisningsopplegg av LIS-legene ved KCMC.
Til slutt: Kan du hjelpe meg?
Metodeboken jeg har utarbeidet blir i første omgang distribuert på en Whatsapp-gruppe, men målet er å lage en app av metodeboken. Appen må være gratis og helst kunne fungere off-line. Tanken er at den først og fremst skal serve avdelingen her på KCMC, men et overordnet mål er å kunne stimulere til standardisering av anestesi i hele Tanzania. Pr i dag er det ingen standard. Er det noen som kan tenke seg å hjelpe meg med å utvikle dette på frivillig grunnlag, ta gjerne kontakt.
Kandidat
Eva Gravdahl
Avhandlingen utgår fra Institutt for klinisk medisin, Universitetet i Oslo
Arbeidet er utført ved: Palliativ forskningsgruppe, Kirurgisk forskningsavdeling, Akershus universitetssykehus HF
Veiledere
Hovedveileder: Professor Olav Magnus Fredheim, Universitetet i Oslo
Biveiledere: Overlege Siri Steine, Akershus universitetssykehus
Professor Knut Magne Augestad, Universitetet i Oslo
Bedømmelseskomité
1. opponent: Professor Reino Pöyhiä, University of Eastern Finland
2. opponent: Professor Anne Berit Guttormsen, Universitetet i Bergen
Komitéleder: Professor Ulf Erik Kongsgaard, Universitetet i Oslo
Sammendrag
Effektiv lindring av kreftsmerte hos palliative pasienter kan være utfordrende, særlig når perorale opioider ikke gir tilstrekkelig effekt eller gir uakseptable bivirkninger. Ved utilstrekkelig effekt av perorale opioider kan subkutan (s.c.) eller intravenøs (i.v.) administrasjon være aktuelt. Ifølge gjeldende retningslinjer er s.c. administrasjon førstevalg, blant annet fordi tilgangen er enkel å etablere og vedlikeholde. Samtidig har økt bruk av perifert innlagte sentrale venekatetre (PICC) og midline-katetre (MC) gjort i.v. behandling mer tilgjengelig, også utenfor sykehus. I.v. administrasjon har teoretiske fordeler som raskere opptak og mer forutsigbar farmakokinetikk, men kunnskapen om kliniske forskjeller mellom i.v. og s.c.

Eva-Kristin Norum Gravdahl Overlege
Eva-Kristin.Norum.Gravdahl@ahus.no
morfin hos palliative pasienter er begrenset, særlig ved bruk av kontinuerlig infusjon kombinert med behovsdoser via pasientkontrollert analgesi (PCA).
I avhandlingen undersøkte vi kliniske indikasjoner, bruksmønster og sikkerhet ved bruk av PICC og MC, farmakokinetiske forskjeller mellom s.c. og i.v. behovsdoser av morfin, samt den smertelindrende effekten av s.c. og i.v. morfin administrert som kontinuerlig infusjon med behovsdoser via PCA hos palliative pasienter med kreftrelatert smerte.
Resultatene viser at PICC og MC brukes til symptomlindring sent i sykdomsforløpet og er forbundet med lav komplikasjonsrate. Farmakokinetisk ga i.v. bolusdoser raskere og høyere serumkonsentrasjoner av morfin enn s.c. administrasjon, men uten forskjell i total systemisk eksponering første time (AUC₀–₆₀). I den randomiserte studien ble det ikke påvist statistiske eller klinisk signifikante forskjeller mellom s.c. og i.v. administrasjon når det gjaldt tid til stabil infusjonsrate, tid til smertelindring etter bolusdose, smerteintensitet, opioidforbruk, bivirkninger, symptomskår eller livskvalitet over 48 timer.
Avhandlingen konkluderer med at både s.c. og i.v. morfin er trygge og effektive alternativer ved parenteral opioidtitrering i palliativ fase. Valg av administrasjonsvei kan
derfor baseres på klinisk situasjon, tilgjengelig venetilgang og praktiske hensyn, snarere enn forventning om forskjeller i effekt eller sikkerhet.
Artiklene som inngår i avhandlingen
1. Gravdahl E, Steine S, Augestad KM, Fredheim OM. Use and safety of peripherally inserted central catheters and midline catheters in palliative care cancer patients: a retrospective review. Supportive Care in Cancer. 2023;31(10):580.
2. Gravdahl E, Dale O, Šaltyté Benth J, Steine S, Augestad KM, Fredheim OM. Pharmacokinetics of subcutaneous and intravenous bolus doses of morphine in palliative care cancer patients receiving infusion of morphine: a pharmacokinetic substudy of a randomized controlled trial. British Journal of Clinical Pharmacology. 2025;91(12):3422–3431.
3. Gravdahl E, Steine S, Šaltyté Benth J, Augestad KM, Fredheim OM. Subcutaneous versus intravenous route switch from oral to parenteral morphine in patients with cancer: randomised controlled trial. BMJ Supportive & Palliative Care. 2025 Jun 12:spcare2025-005593.
Kandidat
Sigurd Mydske
Avhandlingen utgår fra Klinisk institutt 1, Universitetet i Bergen Arbeidet er utført ved: Fjellmedisinsk forskningsgruppe, Stiftelsen Norsk Luftambulanse, Kirurgisk Serviceklinikk, Helse Bergen HF
Veiledere
Hovedveileder: Førsteamanuensis Øyvind Thomassen, Universitetet i Bergen
Biveiledere: Seniorforsker Jörg Aßmus, Helse Bergen HF
Professor Guttorm Brattebø, Universitetet i Bergen
Seniorforsker Øystein Wiggen, SINTEF
Bedømmelseskomité
1. opponent: Førsteamanuensis Knut Fredriksen, Universitetet i Tromsø 2. opponent: Førsteamanuensis Kristin Tønsager, Universitetet i Stavanger
Komitéleder: Professor Anne Berit Guttormsen, Universitetet i Bergen
Sammendrag
Redusert kroppstemperatur (hypotermi) er en farlig tilstand i seg selv, og spesielt farlig dersom det oppstår i kombinasjon med alvorlig skade eller sykdom. Rask og effektiv behandling av denne tilstanden kan bidra til å reversere de skadelige konsekvensene av hypotermi, og den pre hospitale behandlingen av disse pasientene bør derfor være så effektiv som mulig.
Disse pasientene håndteres i stor grad av ambulansetjenesten, luftambulansetjenesten, redningshelikoptertjenesten og den frivillig redningstjenesten. Avhandlingen har derfor tatt utgangspunkt i

Sigurd Mydske
Stipendiat, Stiftelsen Norsk Luftambulanse sigurd.mydske@norskluftambulanse.no
internasjonalt anerkjente metoder som brukes av disse tjenestene, med mål om å undersøke effekten av dagens behandling.
Avhandlingen bygger på fire arbeider fra tre studier som utgår fra Haukeland Universitetssjukehus: to randomiserte kontrollerte studier der den ene er opphav til to artikler og en eksperimentell laboratoriestudie.
Resultatene viser at det å tilføre varme til personer med lav kroppstemperatur bidrar overraskende lite til å øke kjernetemperaturen. Det bidrar imidlertid til et redusert fall i kjernetemperatur ved bevegelse, såkalt «afterdrop».
Videre viser avhandlingen at bruk av en «dampsperre» som det innerste laget i en innpakkingsmodell kan bidra til raskere oppvarming av hudtemperatur, samt at de andre materialene i modellen holdes tørre og dermed fungerer bedre.
Avhandlingen viser også at flere tilgjengelige varmetepper har potensiale til å bli så varme at de potensielt kan påføre brannskade dersom de plasseres direkte på huden.
Artiklene som inngår i avhandlingen
1. Mydske S, Helland AM, Borasio N, Brattebø G, Østerås Ø, Wiggen Ø, Aßmus J, Strapazzon G, Thomassen Ø. Effect of active external rewarming on esophageal temperature in simulated prehospital
accidental hypothermia: a randomized crossover trial. Scand J Trauma Resusc Emerg Med. 2026;8 (34).
2. Mydske S, Helland AM, Borasio N, Brattebø G, Østerås Ø, Wiggen Ø, Aßmus J, Strapazzon G, Thomassen Ø. Reduction of Afterdrop by Using Active External Warming During Treatment of Accidental Hypothermia—A Randomized, Crossover Trial. Acta Anaesthesiol Scand. 2026; 70(1):e70162.
3. Mydske S, Brattebø G, Østerås Ø, Wiggen Ø, Aßmus J, Thomassen Ø. Effect of a vapor barrier in combination with active external rewarming for coldstressed patients in a prehospital setting: a randomized, crossover field study. Scand J Trauma Resusc Emerg Med. 2024;32(1):35.
4. Mydske S, Brattebø G, Helland AM, Wiggen Ø, Aßmus J, Thomassen Ø. Treatment of accidental hypothermia: Impact of insulation placement above or below an active external rewarming device on temperature and burn risk. J Therm Biol. 2025:104126.

Niroshee Gunasingam Bronebakk Overlege og PhD stipendiat Intervensjonssenteret, OUS og UiO NIRBRO@vestreviken.no
Med støtte fra NAFs forskningsstipend deltok jeg på European Delirium Association Kongress i Hamburg i november 2025. Denne rapporten beskriver hva jeg fikk ut av møtet og hvorfor jeg mener reisen var verdifull.
En tverrfaglig innsats
Kongressen samlet geriatere, psykiatere, nevrofysiologer, farmasøyter, anestesileger og grunnforskere – alle med ulike tilnærminger til delirium. Mye av arbeidet deres er direkte relevant for det vi gjør i anestesi.
En gruppe fra University College London Hospitals presenterte sitt arbeid med å kartlegge hjernen hos pasienter med delirium og demens ved hjelp av EEG. De var forfriskende ærlige om de praktiske utfordringene – å få deliriske pasienter til å ha på seg EEG-hetten lenge nok og ligge stille er genuint vanskelig. De har lykkes med å kartlegge hypoaktivt delirium, men ikke hyperaktivt delirium, av åpenbare grunner.
Professor Arjen Slooter fra Nederland viste EEG-data som demonstrerte at den deliriske hjernen gjennomgår endringer som ligner på dem vi ser under anestesi – spesifikt en nedgang over alle frekvenser med relative økninger i delta- og theta-aktivitet. Dette fanget min oppmerksomhet gitt
implikasjonene for å forstå hvordan et pre-operativ EEG av en pasient med delir ser ut.
Jeg var også interessert i å lære om robuste musemodeller for delirium. Kognitiv vurdering ved hjelp av labyrinter og redebyggingsatferd viser seg å være både robust og repeterbar. Noen sentre filmer musene og bruker maskinlæring til å kvantifisere de kognitive vurderingene, noe som virker som en smart tilnærming.
Pedagogisk innhold
Safe Brain Initiative holdt hovedforelesningen om paradigmeskifter i medisinen. Professor Finn Radtke brukte Picassos dramatiske stilendring – fra «The Family of Saltimbanques» til «Les Demoiselles d'Avignon» på bare to år – som en analogi for hvordan fremskritt noen ganger krever at man bryter med tradisjonen, selv når det skaper uenighet.
Han undersøkte deretter et konkret medisinsk eksempel: ulcusbehandling som gikk
fra kirurgi til antibiotika etter oppdagelsen av H. pylori. Rundt 1997 begynte retningslinjer å anbefale antibiotikabehandling, men likevel ble det fortsatt utført cirka 250 000 operasjoner globalt hvert år. Dette tallet nådde først null i 2005. Han beskrev denne forsinkelsen som en overgang fra akseptert praksis til uaktsomhet, og til slutt til klar skade. Parallellen til vårt felt gikk ikke publikum hus forbi. Han fortsatte med å beskrive hvordan Safe Brain Initiative bruker behandlingspakker som inkluderer EEG og tilbakemeldingssløyfer for å forebygge postoperativt delirium, og at dette innebærer å utfordre tradisjonelle synspunkter.
Dr. Matthias Kreuzer, nevrofysiolog og ekspert på perioperativ EEG, holdt flere praktiske forelesninger om burst suppression, alfabåndsaktivitet, begrensninger ved prosesserte indekser og viktigheten av langsom induksjon og oppvåkning. Disse var genuint nyttige for å tenke gjennom hvordan man tolker det vi ser på monitoren.
I kaffepausene var det betydelig diskusjon om hvorfor de store studiene som ikke viste nytte av EEG-veiledet anestesi kan ha vært metodologisk utilstrekkelige, og hvorfor European Society of Anaesthesia and
Intence Care (ESAIC) likevel valgte å anbefale EEG-monitorering. Disse uformelle samtalene var like verdifulle som de formelle sesjonene.
Annet arbeid av interesse
Professor Dr Leah Acker fra Duke University Hospital presenterte arbeid om hjerne-hjerte-immun-aksen mediert av vagusnerven. I hennes studie bar deltakerne klokker før kirurgi, og de som utviklet postoperative kognitive problemer hadde lavere preoperativ hjertefrekvens-variabilitet og høyere inflammasjonsmarkører. Dette reflekterer en svakere hjerne-hjerte-immun-akse – en interessant måte å tenke om preoperativ risiko på.
Professor Dr Yiying Zhang fra Massachusetts General Hospital delte arbeid om tarm-hjerne-mikrobiome. Hos mus mildnet prebiotika atferdsendringer indusert av anestesi og kirurgi. Jeg er nysgjerrig på hvor denne forskningslinjen går.
Professor Dr Sarah Saxena, ESAIC-leder for deliriumgruppen, holdt en presentasjon om kjønnsforskjeller ved delirium – nok et område hvor vi har mer å lære.
Presentasjon av eget arbeid
Et av mine hovedmål var å få tilbakemelding fra erfarne forskere mens jeg fortsatt kan gjøre endringer i prosjektdesignet. Jeg presenterte to postere om planlagt arbeid, og begge genererte betydelig interesse.
Den første beskriver et kvalitetsforbedringsprosjekt ved Bærum sykehus, med lignende tilnærming som Safe Brain Initiative. Vi har målt baseline deliriuminsidens, propofolforbruk, og væske- og vasopressorbruk. Vi har nå begynt å introdusere EEG-monitorer med
Tidsskrift for Norsk anestesiologisk forening, DNLF
tetthetsspektral array og vil se etter endringer i disse parameterne.
Den andre skisserte en fremtidig randomisert studie som undersøker alfabåndsbevaring som mål for EEG-veiledet anestesi hos pasienter over 60 år. Å få innspill på designet på dette stadiet var akkurat det jeg håpet på.
Nettverksbygging
Jeg hadde muligheten til å representere Norge, Bærum sykehus og Intervensjonssenteret på et internasjonalt forum. Professor Dr Basak Meco fra Safe Brain Initiative har tilbudt seg å støtte implementeringen av vår audit ved Bærum, noe som er et konkret og nyttig utfall. Gjennom posterdiskusjonene har jeg etablert kontakt med Professor Dr Sarah Saxena og Dr Matthias Kreuzer, med uformelle avtaler om fremtidig samarbeid.
Hva jeg fikk ut av det
Oppsummert muliggjorde støtten fra forskningsstipend:
• Eksponering for aktuell forskning på EEG-monitorering og delirium som er direkte relevant for perioperativ praksis
• Eksperttilbakemelding på to norske forskningsprosjekter på et stadium hvor endringer fortsatt kan gjøres
• Et konkret tilbud om støtte fra Safe Brain Initiative
• Internasjonale kontakter for fremtidig samarbeid
EDA-kongressen 2026 i Oslo
Neste års kongress vil bli holdt i Oslo fra 4.–6. november 2026 – så ingen reise er nødvendig for norske kolleger. Kongressen arrangeres av Oslo Delirium Research Group (ODRG), en av svært få forskningsgrupper
internasjonalt som har delirium som hovedfokus. Gruppen har initiert internasjonalt ledende studier innen patofysiologi (ved bruk av cerebrospinalvæske fra hoftebruddpasienter, samlet inn av anestesileger), epidemiologi (populasjonsbaserte data for å utforske sammenhenger mellom skrøpelighet, delirium og demens), samt en nasjonal multisenterstudie av deksmedetomidin mot klonidin mot placebo for å redusere postoperativt delirium etter hjertekirurgi (ALPHA2PREVENT). Gruppen har sterke nasjonale og internasjonale samarbeid.
Hovedforedragsholderen vil være professor Evandro Fang, en internasjonalt anerkjent ekspert på aldring. Jeg vil oppfordre kolleger til å vurdere å delta og sende inn abstrakter. Delirium er vanlig på tvers av medisinske og kirurgiske spesialiteter, og både EDA og ODRG illustrerer verdien av tverrfaglig samarbeid – geriatere, grunnforskere, anestesileger og demenseksperter arbeider sammen mot felles mål. Innholdet er svært relevant for anestesipraksis.
Jeg vil takke Legeforeningen, Norsk Anestesiologisk Forening, Bærum sykehus og Intervensjonssenter for teknologi og innovasjon for å ha gjort det mulig å delta.

Godkjent for bruk hos barn som er 6 år eller eldre1
For akutt smertelindring ved moderate til sterke smerter som følge av traume hos pasienter i alderen 6 år og eldre som er ved bevissthet.2
Rask effekt etter 6-10 inhalasjoner. Hos barn kan ytterligere inhalasjoner være nødvendig.1
Opioidfri behandling3 Til inhalasjon1
Penthrox 99,9%, 3 ml væske til inhalasjonsdamp (metoksyfluran).
Vennligst referer til sammendraget av produktegenskaper (SPC) før du forskriver.
Forkortet forskrivningsinformasjon
Indikasjon: Akutt smertelindring ved moderate til sterke smerter som følge av traume hos pasienter i alderen 6 år og eldre som er ved bevissthet.
Dosering og administrasjonsmåte: Penthrox bør selvadministreres, ved å inalere gjennom den håndholdte Penthrox-inhalatoren, under tilsyn av lege, sykepleier, akuttpersonell eller helsepersonell som er opplært i å administrere legemiddelet. En flaske gis som én enkeltdose. En flaske nummer to bør kun brukes ved behov. Det anbefales ikke mer enn 6 ml daglig eller administrering over flere påfølgende dager. Den totale dosen til en pasient i løpet av én uke bør ikke overstige 15 ml. Pasienter bør instrueres i å inhalere periodevis for å oppnå adekvat smertestillende effekt. Sjekk for fremmedelementer, ødelagte eller skadede deler før bruk.
Kontraindikasjoner: Bruk som anestetikum. Overfølsomhet for innholdsstoffene eller fluorinerte anestetika. Malign hypertermi, samt ved kjent eller mistenkt genetisk predisponering. Alvorlige bivirkninger (inkl. i familieanamnese) etter tidligere inhalasjonsanestetika. Tidligere tegn på leverskade etter tidligere bruk av metoksyfluran eller halogenerte anestetika. Klinisk signifikant nedsatt nyrefunksjon. Endret bevissthetsnivå av enhver årsak, inkl. hodeskade, legemidler eller alkohol. Klinisk påvist kardiovaskulær ustabilitet eller respirasjonsdepresjon. Forsiktighetsregler: Bruk den laveste effektive dosen for å kontrollere smerte, brukes med forsiktighet hos eldre eller andre pasienter med kjente risikofaktorer for nyresykdom. Brukes med forsiktighet hos pasienter diagnostisert med kliniske tilstander som kan predisponere for nyreskade. Risikoen for at metoksyfluran forårsaker toksisitet kan øke med faktorer som øker metaboliseringshastigheten. Penthrox må ikke brukes hos pasienter som har vist tegn på leverskade i anamnesen etter tidligere bruk av metoksyfluran eller halogenerte anestetika. Penthrox bør brukes med forsiktighet hos pasienter med underliggende levertilstander eller med risiko for leverdysfunksjon. Nøye klinisk vurdering bør gjøres når Penthrox skal brukes hyppigere enn hver 3. måned. Det bør utvises forsiktighet hos eldre på grunn av en mulig reduksjon i blodtrykket. Potensielle CNS-effekter som sedasjon, eufori, amnesi, konsentrasjonsevne, endret sensorimotorisk koordinasjon og endret humør er også kjente klasseeffekter. Respirasjonsdepresjon har blitt rapportert også ved analgetiske doser. Respirasjonen skal overvåkes på grunn av risikoen for respirasjonsdepresjon og hypoksi. Penthrox er ikke egnet for lindring av gjennombruddssmerter/forverringer ved kroniske smertetilstander. Penthrox er heller ikke egnet for lindring av nært gjentatte smerteepisoder som følge av traume hos den samme pasienten. Hjelpestoffet butylhydroksytoluen (E 321)
POA Pharma Scandinavia AB (A Galen Company) Tel: +45 3117 4300. Info@poaab.com www.galen-pharma.com
kan forårsake lokale hudreaksjoner, eller irritasjon i øyne og slimhinner. Helsepersonell som jevnlig eksponeres for pasienter som bruker Penthrox-inhalatorer bør være oppmerksom på relevante helse-, miljø- og sikkerhetsrutiner for bruk av inhalasjonsmidler. For å redusere yrkeseksponering for metoksyfluran, bør Penthrox-inhalatoren alltid brukes med kammeret med aktivert karbon (AC) som adsorberer metoksyfluran som pustes ut. Pasienter skal instrueres om å puste ut i Penthrox-inhalatoren. Det har vært rapporter om ikke-alvorlige og forbigående reaksjoner, slik som svimmelhet, hodepine, kvalme og sykdomsfølelse, samt rapporter om overfølsomhetsreaksjoner overfor metoksyfluran eller andre innholdsstoffer, hos helsepersonell eksponert for Penthrox.
Interaksjoner: Samtidig bruk med CYP450-induktor (inkl. alkohol) kan øke risikoen for toksisitet, og bør unngås. Samtidig bruk med nyretoksiske legemidler (f.eks. kontrastmidler, noen antibiotika) bør unngås. Anbefales det å unngå anestesi med sevofluran etter smertelindring med metoksyfluran. Dette skyldes at sevofluran øker serumnivåene av fluorid, og nefrotoksisitet av metoksyfluran er relatert til økt serumfluorid. Samtidig bruk med CNS-depressiver som opioider, sedativer eller hypnotika, generell anestesi, fentiaziner, muskelrelakserende, sederende antihistaminer og alkohol, kan gi depressive tilleggseffekter. Pasienten bør overvåkes nøye ved samtidig bruk av opioider.
Graviditet/amming: Forsiktighet bør utvises når metoksyfluran administreres under graviditet, spesielt under første trimester, og til ammende mødre.
Bivirkninger: Svært vanlige og vanlige bivirkninger er svimmelhet, euforisk humør, hodepine, søvnighet, dysgeusi, hoste, kvalme, fatigue, føle seg full.
Reseptpliktig: Ja Utleveringsgruppe: C Blå resept: Nei
Maksimal utsalgspris for apotek (kr): 399.50 (flaske 3 ml, inhalator 1 stk).
Innhaver av Markedsføringstillatelsen: Medical Developments NED B.V., Strawinskylaan 1647, Tower 7, 1077 XX Amsterdam, Nederland.
Full forskrivningsinformasjon tilgjengelig fra: POA Pharma Scandinavia AB, info@poaab. com.
Dato for forberedelse: Februar 2026. Basert på Penthrox SPC 03.09.2025.
For mer utfyllende informasjon, se Penthrox SPC.
Melding av mistenkte bivirkninger
Det er viktig å rapportere mistenkte bivirkninger. Helsepersonell oppfordres til å melde enhver mistenkt bivirkning. Dette gjøres via meldeskjema som finnes på nettsiden til Direktoratet for medisinske produkter : www.dmp.no/meldeskjema. Bivirkninger bør også rapporteres til POA Pharma via info@poaab.com
THIS IS NOT A TIME FOR COMPROMISE

* Full list of Chemical Warfare Agents and Organophosphate Pesticides can be found here: The RSDL® (Reactive Skin Decontamination Lotion) Kit is intended to remove or neutralize the following chemical warfare agents from the skin:
V-Series Nerve Agents (VX, VR), G-Series Nerve, Agents [Tabun (GA), Soman (GD), Sarin (GB), Cyclohexyl Sarin (GF)], Mustard Gas (HD), T-2 Toxin, and organophosphate pesticides (malathion, parathion, paraoxon, paraoxon-methyl and malaoxon). RSDL® is a CE Marked Class IIA medical device, and it is cleared by the US Food and Drug Administration (FDA) and licensed by Health Canada, the Israeli Ministry of Health and the Australian Therapeutic Goods Administration. Indications may vary across countries. RSDL® is registered under MDD regulation in EU, complies with ISO 13485 and bears the CE mark. Important Safety Information: For external use only by trained individuals. Use only if chemical agent exposure is suspected. Do not use if packet seal is compromised. CAUTION: Allow RSDL to remain on skin for at least two minutes. Avoid prolonged skin contact. Avoid contact with eyes and mucous membranes. Remove RSDL with water when conditions permit. Common side effects include itching and increased heart rate. WARNINGS: Not for prophylactic use or whole body decontamination. Fire hazard. Combustion may occur upon contact with strong oxidising chemicals (e.g., HTH, super tropical bleach). Do not discard used RSDL components into strong oxidising chemicals or their containers.
Three 21 ml individual use packets are supplied in a suitable opaque olive-green pouch. Each packet contains a pad that has 21 ml of lotion.
1. Tear open packet. 2. Remove pad. 3. Scrub exposed skin thoroughly. 4. Discard packet and pad after a single use. Discard packet and pad after use. Discard after use in accordance with unit or local regulations.1 Refer to the Instruction For Use on the packaging for more information.
Suspected Adverse Events, Product Complaints & Product Inquiries: serbmedinfo@serb.com US number: 877-377-3784 / Toll call outside US: +1-303-389-1204 For more information on RSDL, please contact: SERB MEDICAL SOLUTIONS INC. / 300 Four Falls Corporate Center 300 Conshohocken State Road, Suite 300 West Conshohocken, PA, 19428-3820 adv@serb.eu / RSDL.Enquiries@serb.com The artworks are not contractual. References: 1. RSDL® Technical Data Sheet 2025. RSDL ® IS INTENDED TO REMOVE OR NEUTRALIZE CHEMICAL WARFARE AGENTS, T-2 TOXIN, AND ORGANOPHOSPHATE PESTICIDES * FROM THE SKIN. 1 2797 NO–RSDL-2500015 / Date: 17.09.25