

Revolutionize Your Surgical Microscopy
4K image resolution combined with true 3D depth perception — at the same time.
· Complete surgical team integration for improved surgical workflow.
· Freedom from the constraints of traditional microscopes improves surgeon ergonomics.
White light, blue light, infrared light and Narrow Band Imaging (NBI) for improved visualization of anatomical structures. Time-saving and versatile setup and interdisciplinary use.

TEMAER I 2026:
Nr 1. Artroskopisk kirurgi
Nr 2. Barnekirurgi
Nr 3. Robotassistert kirurgi
INNLEVERINGSFRISTER 2026:
Nr 1. Artroskopisk kirurgi: 24/1-26
Nr 2. Barnekirurgi: 24/4-26
Nr 3. Robotassistert kirurgi: 24/8-26
Kirurgen ønsker å være en nasjonal plattform for kirurgi ved å inspirere til faglig kompetanseheving, bedre utdanning og opplæring av unge kirurger, samt øke interessen for kirurgisk forskning. – VISJON, KIRURGEN
UTGIVER
Norsk Kirurgisk Forening Pb 17 Kjelsås, 0411 Oslo ISSN 1504-88 88
REDAKSJON
Tobias Hauge (redaktør) OUS Ullevål tobias@kirurgen.no
Marte Bliksøen (redaksjonsmedlem)
OUS Rikshospitalet marte@kirurgen.no
Saira Mauland Mansoor (redaksjonsmedlem) OUS Ullevål saira@kirurgen.no
David Hui (redaksjonsmedlem)
OUS Rikshospitalet david@kirurgen.no
Øystein Njølstad Skandsen (redaksjonsmedlem) UNN Harstad oystein@kirurgen.no
Maren Baarlid (redaksjonsmedlem) Sykehuset Østfold maren@kirurgen.no
Kristin Read (redaksjonsmedlem) OUS Ullevål kristin@kirurgen.no







og bakre
ØNSKER DU IKKE Å FÅ TILSENDT KIRURGEN LENGRE? medlemsservice@kirurgen.no
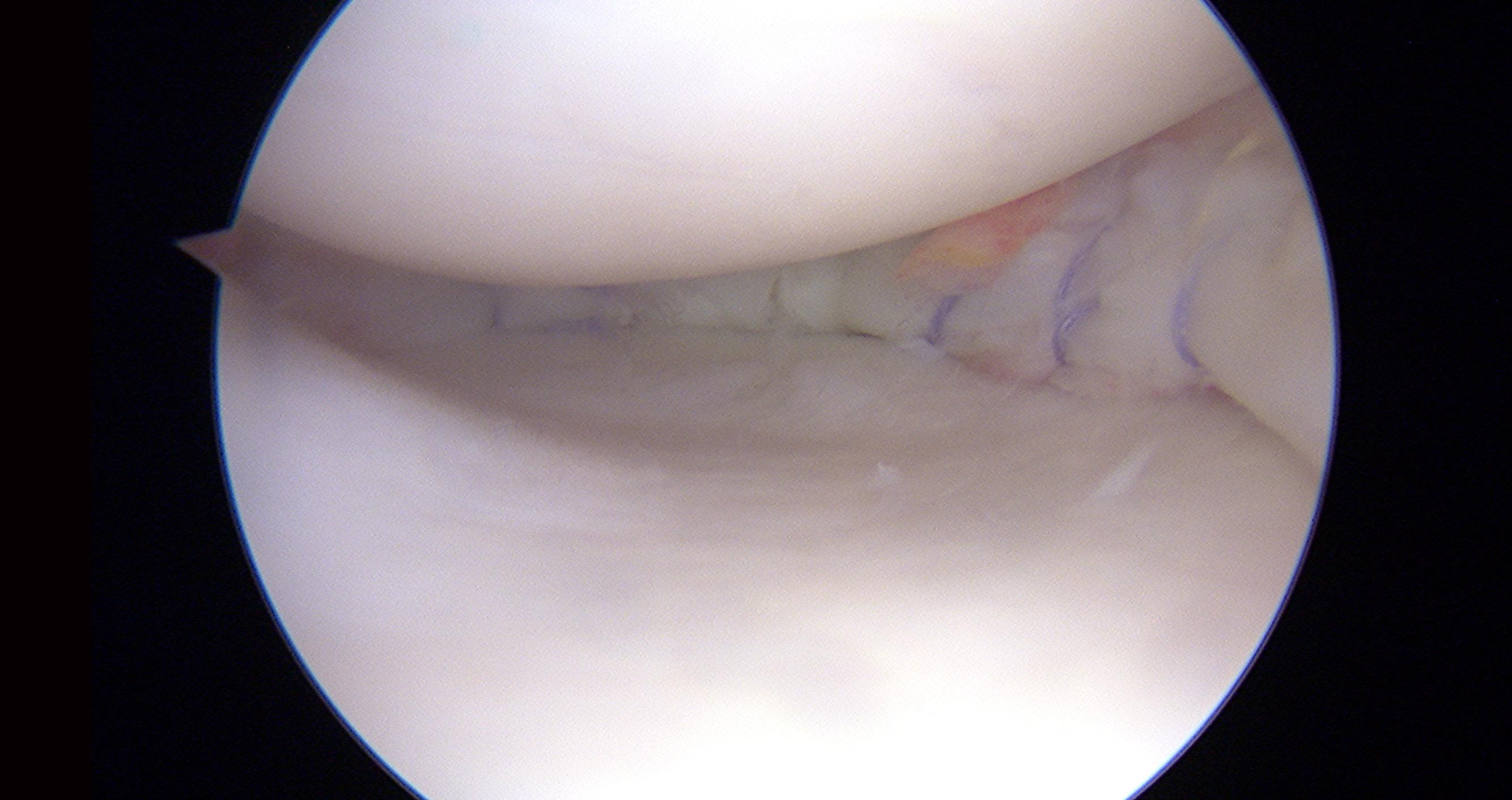
FORSIDEBILDET: Sutur av menisk. Foto: Berte Bøe
LAYOUT, PRODUKSJON OG ANNONSESALG Apriil Media AS www.apriil.no
Annonsesalg ragnar.madsen@apriil.no Tlf.: 92 84 84 02

For behandling av voksne pasienter med fremskreden hormonsensitiv prostatakreft2
ADT= Androgen Deprivation Therapy
*Behandling av avansert hormonavhengig prostatakreft. Refusjonskoder: ICPC Y77: Ondartet svulst i prostata. ICD C61 Ondartet svulst i blærehalskjertel. Vilkår 9: Behandlingen skal være instituert i sykehus, sykehuspoliklinikk eller av spesialist i vedkommende disiplin.


Referanser: 1. Shore ND, et al. N Engl J Med. 2020;382(4):2187–2196. 2. Preparatomtale Orgovyx (relugoliks), seksjon 4.1 og 5.1. www.felleskatalogen.no.
Dette legemidlet er underlagt særlig overvåking. Orgovyx (relugoliks) 120 mg filmdrasjerte tabletter, ATC-nr.: L02BX04, Reseptgruppe: C. Reseptbelagt. Indikasjon: Behandling av voksne pasienter med fremskreden hormonsensitiv prostatakreft. Dosering og administrasjonsmåte: Behandling med Orgovyx skal startes og overvåkes av spesialleger med erfaring innen medisinsk behandling av prostatakreft. Behandling med Orgovyx skal innledes med en startdose på 360 mg (tre tabletter) på den første dagen, etterfulgt av en dose på 120 mg (én tablett) som tas én gang daglig på omtrent samme tid hver dag. Orgovyx kan tas med eller uten mat. Tablettene bør tas med litt væske etter behov, og skal svelges hele. Kontraindikasjoner: Overfølsomhet for innholdsstoffene. Advarsler og forsiktighetsregler: Androgen deprivasjonsterapi kan forlenge QT-intervallet. Hos pasienter med en historie med eller risikofaktorer for QT-forlengelse samt hos pasienter som samtidig får legemidler som kan forlenge QT-intervallet, må man nøye evaluere samtidig bruk av Orgovyx med legemidler kjent for å forlenge QT-intervallet, eller legemidler som kan indusere torsades de pointes, slik som klasse IA (f.eks. kinidin, disopyramid) eller klasse III (f.eks. amiodaron, sotalol, dofetilid, ibutilid) antiarytmika, metadon, moksifloksacin, antipsykotika osv. Hjerte- og karsykdom slik som myokardinfarkt og slag har blitt rapportert for pasienter som fikk androgen deprivasjonsterapi. Derfor bør alle risikofaktorer for hjerte- og karsykdom tas med i beregningen. Redusert bentetthet kan forekomme. Redusert bentetthet, hos pasienter med ytterligere risikofaktorer, kan føre til osteoporose og økt risiko for benfraktur. Overvåkning av leverfunksjon hos pasienter med kjent eller mistenkt leversykdom er tilrådelig under behandling, da det er observert lette forbigående økninger i ALAT og ASAT. Forsiktighet ved alvorlig nedsatt nyrefunksjon. Eksponeringen for relugoliks hos pasienter med alvorlig nedsatt nyrefunksjon kan være økt med opptil 2 ganger. Det må utvises forsiktighet hos pasienter med alvorlig nedsatt nyrefunksjon ved administrasjon av en 120 mg dose med relugoliks én gang daglig. Effekten av Orgovyx skal overvåkes via kliniske parametere og nivåer av prostataspesifikt antigen (PSA) i serum. Interaksjoner: P-gp-hemmere: Samtidig administrasjon av Orgovyx og orale P-gp-hemmere anbefales ikke. Legemidler som er orale P-gp-hemmere inkluderer visse legemidler mot infeksjon (f.eks. azitromycin, erytromycin, klaritromycin, gentamicin, tetracyklin), antimykotika (ketokonazol, itrakonazol), antihypertensiva (f.eks. karvedilol, verapamil), antiarytmika (f.eks. amiodaron, dronedaron, propafenon, kinidin), antianginale legemidler (f.eks. ranolazin), cyklosporin, humant immunsviktvirus (hiv)- eller hepatitt C-virus (HCV)-proteasehemmere (f.eks. ritonavir, telaprevir). Hvis samtidig administrasjon med orale P-gp-hemmere én eller to ganger daglig er nødvendig, skal Orgovyx tas først og den orale P-gp-hemmeren tas 6 timer senere, og pasientene skal overvåkes hyppigere for bivirkninger. Alternativt kan behandling med Orgovyx avbrytes i opptil 2 uker for en kort behandlingsperiode med en P-gp-hemmer. Hvis behandling med Orgovyx avbrytes i mer enn 7 dager, skal administrasjon av Orgovyx gjenopptas med en startdose på 360 mg på den første dagen etterfulgt av 120 mg én gang daglig. Kombinerte P-gp- og sterke CYP3A-induktorer: Samtidig administrasjon av Orgovyx med kombinerte P-gp- og sterke CYP3A-induktorer anbefales ikke. Legemidler som er kombinerte P-gp- og sterke CYP3A4-induktorer inkluderer den androgene reseptorinduktoren apalutamid, visse antikonvulsiva (f.eks. karbamazepin, fenytoin, fenobarbital), legemidler mot infeksjon (f.eks. rifampicin, rifabutin), johannesurt (Hypericum perforatum), hiv- eller HCV-proteaseinduktorer (f.eks. ritonavir) og ikke-nukleoside reverstranskriptaseinduktorer (f.eks. efavirenz). Hvis samtidig administrasjon er nødvendig, skal Orgovyx-dosen økes. Etter seponering av den kombinerte P-gp- og sterke CYP3A-induktoren skal den anbefalte dosen Orgovyx gjenopptas én gang daglig. Fertilitet, graviditet og amming: Legemidlet er ikke indisert for kvinner i fertil alder. Det skal ikke brukes hos kvinner som er eller kan være gravide eller som ammer. Bivirkninger: Noen mindre vanlige bivirkninger kan være alvorlige, og lege kontaktes umiddelbart dersom symptomer på urtikaria eller angioødem utvikles (kan forekomme hos opptil 1 av 100 personer). De vanligste bivirkningene under behandling med relugoliks er fysiologiske effekter av testosteronsuppresjon, inkludert hetetokter (54 %), muskel- og skjelettsmerter (30 %) og fatigue (26 %). Andre svært vanlige bivirkninger inkluderer diaré og forstoppelse (12 % hver). Svært vanlige: Karsykdommer: hetetokter. Gastrointestinale sykdommer: diaré, forstoppelse. Sykdommer i muskler, bindevev og skjelett: muskel- og skjelettsmerter. Generelle lidelser og reaksjoner på administrasjonsstedet: fatigue. Vanlige: Sykdommer i blod og lymfatiske organer: anemi. Endokrine sykdommer: gynekomasti. Psykiatriske lidelser: insomni, depresjon. Nevrologiske sykdommer: svimmelhet, hodepine. Gastrointestinale sykdommer: kvalme. Hud- og underhudssykdommer: hyperhidrose, utslett. Lidelser i kjønnsorganer og brystsykdommer: redusert libido. Undersøkelser: vektøkning, økt glukosed, økt triglyserid, økt blodkolesterol. Mindre vanlige: Hjertesykdommer: myokardinfarkt. Hud- og underhudssykdommer: urtikaria, angioødem. Sykdommer i muskler, bindevev og skjelett: osteoporose/ osteopeni. Undersøkelser: økt aspartataminotransferase, økt alaninaminotransferase. Ikke kjent frekvens: Hjertesykdommer: forlenget QT-tid. Pakningsstørrelser og pris: Orgovyx Filmdrasjert tablett, 120 mg: 30 stk. flaske: 1674,6 kr. Blå resept: Ja. Refusjonsberettiget bruk: Behandling av avansert hormonavhengig prostatakreft. Refusjonskoder: ICPC Y77: Ondartet svulst i prostata. ICD C61 Ondartet svulst i blærehalskjertel. Vilkår 9: Behandlingen skal være instituert i sykehus, sykehuspoli-klinikk eller av spesialist i vedkommende disiplin. Basert på SPC godkjent av DMP/EMA: 13.06.2025. Innehaver av markedsføringstillatelse: Accord Healthcare S.L.U., World Trade Center, Moll de Barcelona, s/n, Edifici Est 6ª planta, 08039 Barcelona, Spania. Tel: +34 93 301 00 64. Les preparatomtale (SPC) for ytterligere informasjon, se www.felleskatalogen.no NO-Onc-Org-01454

Kjære leser, i løpet av de litt over to årene jeg har sittet som redaktør, har redaksjonen fått til mye som vi er stolte av og som jeg håper at du som leser også har satt pris på. Å sørge for at Kirurgen har tilfredsstillende økonomi er en utfordring. Det skal utvikles, trykkes og distribueres til ca. 4.000 medlemmers private postkasser fire ganger årlig. Det redaksjonelle arbeidet gjør redaksjonen frivillig, på kvelder, helger og netter, men å utgi et kvalitetsblad som Kirurgen koster og det hadde ikke vært mulig uten støtten fra industrien. I samarbeid med vår nye tjenesteleverandør Apriil Media er vi er på god vei til å sikre en bedre økonomi for Kirurgen. Samtidig er det min jobb som redaktør å påse at en slik avtale ikke går på bekostning av vårt hovedfokus: å gi ut et godt faglig godt tidsskrift.
Jeg er spesielt stolt av at vi har hatt mer fokus på spalten «Min PhD». «Min PhD» er en fast spalte som formidler en smakebit av det enorme arbeidet som ligger bak en doktorgrad og ikke minst er spalten en fin måte å hedre kirurger som ofrer tid, søvn og ikke minst tid på operasjonsstuen, for å bringe faget vårt videre.
Jeg er også svært stolt over fokuset vi har hatt på originalartikler. De siste to årene har vi publisert et økende antall originalartikler hvor data fra norske sykehus har vært presentert, inkludert en multisenterstudie, i tillegg til flere pasientkasuistikker.
Sosiale medier har vært et annet satsningsområde. Nå publiseres alt dere skriver både på Facebook og på våre nettsider. Det gjør at enda flere får glede av artiklene deres.
Til slutt ønsker jeg å takke alle forfattere og ikke minst temaredaktører jeg har jobbet med de siste årene. Gjennom å dele deres kunnskap, gir dere kirurger på tvers av alle spesialiteter, en unik mulighet til økt kunnskap, inspirasjon og underholdning i hverdagen.
Både i Kirurgen og i NKF foregår det store endringer. Kristin Read, ved Gastrokirurgisk avdeling, OUS Ullevål, tar nå over som ny redaktør og Lars Martin Bjerke, gastrokirurg ved UNN Harstad, har fra nyttår tatt over som leder i NKF. Med dette er både Kirurgen og NKF i de beste hender. Jeg ønsker dere begge masse lykke til! Samtidig vil Kirurgen gå ned til tre utgivelser årlig. Jeg er overbevist om at dette er et positivt tiltak, ikke minst ved at det bidrar til å heve kvaliteten ytterligere på hver enkelt utgivelse.
Tema for denne utgivelsen er artroskopisk kirurgi. Nesten halvparten av de som mottar Kirurgen, er ortopeder, og i dette nummeret venter dere syv meget velskrevne og informative artikler som også bløtdelskirurger vil ha stor glede av. Jeg ønsker dere god lesning.

CAPVAXIVE® er en pneumokokkvaksine for voksne inkludert i de nasjonale anbefalingene.1
Norske overvåkingsdata fra 2015–2023 viste forskjeller mellom serotypene hos personer over 65 år og serotypene som inngår i de nå tilgjengelige pneumokokkvaksinene.3
Indikasjon for CAPVAXIVE® er forebygging av invasiv sykdom og pneumoni forårsaket av Streptococcus pneumoniae hos personer 18 år og eldre.2
Bivirkninger: De vanligste bivirkningene etter vaksinering er lokale reaksjoner som smerte på injeksjonsstedet, tretthet, hodepine og myalgi.
De fleste bivirkninger var milde til moderate og forbigående (≤3 dager). Alvorlige hendelser forekom hos ≤1 % av voksne.² Hyppigheten og typen bivirkninger kan variere med alder og tidligere vaksinasjonsstatus.2
Beregnet serotypedekning (%) for perioden 2015–2023*


Prevenar 20 (PKV20) CAPVAXIVE® (PKV21) Pneumovax 23 (PPV23)
Disse tre vaksinene er inkludert i anbefalingene

Dosering: Én enkel dose (0,5 ml) administreres intramuskulært.2
Kontraindikasjoner: Overfølsomhet overfor virkestoffene eller noen av hjelpestoffene.2
Bruk hos spesielle pasientgrupper: Sikkerhet og effekt hos personer under 18 år er ikke fastslått.2 Data for bruk under graviditet og amming er begrensede.
Produktinformasjon: CAPVAXIVE® (PKV21) pneumokokkonjugatvaksine, 21-valent, Reseptpliktig legemiddel. Pakninger: Ferdigfylt sprøyte, 1 x 0,5 ml. Maksimal utsalgspris AUP 1 369 NOK. Reseptgruppe: C
Referanser: 1. FHI.no [Internet]. Folkehelseinstituttet. 2026 cited 2026 Jan 14]. Available from: https://www.fhi.no/va/vaksinasjonshandboka/vaksiner-mot-de-enkeltesykdommene/pneumokokkvaksinasjon/ 2. CAPVAXIVE® (PKV21) – preparatomtale. Publisert 31.03.25. Tilgjengelig fra: ema.europa.eu 3. Tidsskriftet for Den norske legeforening, Berild JD, Kristoffersen AB, Winje BA. Invasiv pneumokokksykdom i Norge 2004–23 og valg av vaksiner til eldre. Tidsskr Nor Legeforen. 2025;145. Tilgjengelig fra: https://tidsskriftet.no/2025/03/originalartikkel/invasiv-pneumokokksykdom-i-norge-2004-23-og-valg-av-vaksiner-til-eldre *Verdien er basert på epidemiologiske data fra Berild et al. (2025)3 og gjenspeiler ikke effekten til de respektive vaksinene. Det finnes for øyeblikket ingen studier som sammenligner effekten til CAPVAXIVE® (PKV21), Prevenar 20 (PKV20) og Pneumovax 23 (PPV23)
MSD (Norge) AS, Haakon VII Gate 5, 0161 Oslo. Copyright © 2026 Merck & Co, Inc., Rahway, NJ, USA and its affiliates. All rights reserved. PM-nr: NO-PCN-00005 02/2026


Som ny leder av Norsk Kirurgisk Forening er det en stor glede å ønske dere alle et godt 2026. Det nye styret i NKF er nå på plass, og vi er godt i gang med arbeidet. Det var svært hyggelig å se igjen kjente ansikter og samtidig ønske nye medlemmer velkommen. Flere foreninger har fått nye ledere fra årsskiftet: Hildur Skuladottir er ny leder i Norsk plastikkirurgisk forening, Alexander Lott i Norsk karkirurgisk forening, Torbjørn Berge Kristensen i Norsk ortopedisk forening, Peter Majak i Norsk thoraxkirurgisk forening, Nina Obad i Norsk nevrokirurgisk forening og Ole Nelvik Bruseth i Norsk barnekirurgisk forening. NKF har også fått ny påtroppende leder i Trygve Thorsen. Jeg vil benytte anledningen til å ønske dere alle lykke til i viktige verv.
NKF er en overbyggende forening for alle norske kirurger og teller nå mer enn 3600 medlemmer. Dette gjør oss til en viktig og sterk aktør og forkjemper for de kirurgiske fagene. Det er mange ting som forener oss kirurger og det er spesielt noen saker som har stor felles interesse og som blir viktige for oss å jobbe sammen for framover.
En av disse sakene er rekruttering og utdanning av kirurger i Norge. Mangelen på rekruttering til kirurgiske LISstillinger er alvorlig. Uten kirurger stopper operasjonsaktiviteten og vår totale beredskap svekkes. Kirurgi er krevende arbeid som forutsetter dedikerte fagfolk med høy kompetanse og motivasjon. For å kunne gi likeverdig og best mulig behandling til pasienter over hele landet, må vi sikre gode fagmiljøer og stabile bemanningsforhold.
Som kirurger skylder vi våre kolleger (yngre som eldre), pasientene og hele befolkningen å jobbe for å rekruttere flinke folk til fagene våre. Da må vi jobbe for at man som kirurg opplever yrkeslivet som godt. Dette forutsetter at vi arbeider for gode arbeidsforhold, faglig autonomi og reell opplevelse av mening og mestring i arbeidshverdagen. Å trives i jobben er ikke bare et mål i seg selv, men en forutsetning for kvalitet, trygghet og faglig utvikling. Det hviler et stort ansvar på oss for å formidle de gode sidene ved yrket vårt på en realistisk måte uten at vi utelater de belastende og krevende sidene av kirurglivet. Vi skal være ærlige og etterrettelige ovenfor studenter, LIS 1 og yngre kolleger. Men vi må ikke glemme å inspirere, oppmuntre, utfordre og rose når noe er bra!
Jeg synes det passer bra å avslutte denne lederen med et kort dikt av lyriker og psykolog Erling Indreeide. Vi skal bestrebe oss i å være den riktige kloke fordi det gjør oss til bedre kirurger!
Det er ein som er så klok at i lag med han skjønar eg kor dum eg er
Så er det ein annan som er så klok at i lag med han er eg klok eg òg
Med ønsker om et godt 2026!

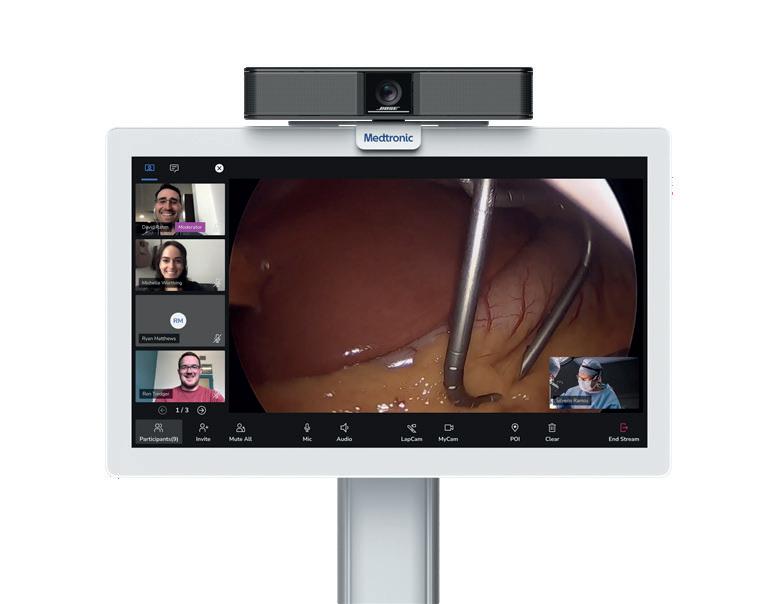

Artroskopisk kirurgi er i kontinuerlig utvikling og favner i dag store deler av det ortopediske fagfeltet fra elektiv presisjonskirurgi til akutte inngrep på vakt. I dette temanummeret presenteres erfaringer og perspektiver fra flere ledd, med artikler som spenner fra basal vaktkirurgi til avanserte elektive prosedyrer. Målet er å inspirere til refleksjon, læring og videre lesning, uavhengig av erfaring og spesialitet.
BERTE BØE
SEKSJONSLEDER, ARTROSKOPISEKSJONEN. ORTOPEDISK AVDELING AKER, OUS. 2ND VICE PRESIDENT ESSKA
KORRESPONDANSE: BERTE2 @ MAC.COM

Artroskopisk kirurgi har på få tiår gått fra å være et nisjeverktøy til å bli en bærebjelke i moderne ortopedisk praksis. Med stadig bedre optikk, instrumenter og biologisk forståelse har vi fått mulighet til å behandle komplekse tilstander med mindre invasivitet, raskere rehabilitering og mer presise inngrep. Samtidig stiller artroskopien store krav til kirurgens ferdigheter, dømmekraft og evne til kontinuerlig læring.
Artroskopiseksjonen ved Oslo Universitetssykehus (OUS) har eksistert siden 1996 og de første årene var det artroskopi i kne og skulder som ble utført i Legevaktsbygget i Storgata. I 2023 flyttet all kirurgisk aktivitet fra Storgata og vi ble til ortopedisk avdeling Aker sammen med Fot og ankelseksjonen og Håndseksjonen. Vi ønsker i dette temanummeret å gi et bredt, praksisnært og inspirerende innblikk i artroskopisk kirurgi slik den utøves i dag. Artiklene spenner fra elektiv kirurgi til akutte situasjoner, fra etablerte metoder til pågående utvikling, og viser hvordan artroskopien har funnet sin plass i store deler av det ortopediske fagfeltet.
Ortopedisk avdeling Aker presenterer artikler som reflekterer både bredde og hverdag. Hofteartroskopi representerer et felt i rask utvikling, der bedre forståelse av patologi og biomekanikk har endret både indikasjoner
og resultater. Rotatorcuffskader i skulderen er blant våre vanligste problemstillinger, men fortsatt fulle av nyanser når det gjelder pasientseleksjon, teknikk og rehabilitering. I begynnelsen ble albueartroskopi brukt nesten utelukkende til diagnostikk, men metoden har utviklet seg til et terapeutisk verktøy med et bredt spekter. Artroskopi av håndledd kombineres i mange sammenhenger med åpen teknikk for å bedre pasientbehandlingen med en mer skånsom tilnærming. Leddene i fot og ankel gjør en stor jobb der de bærer hele kroppsvekten. Da blir det spesielt viktig å kontrollere leddreposisjonen i forbindelse med skader slik at pasientene unngår slitasjeutvikling og senskader. Forekomsten av bløtdelskomplikasjoner blir langt færre med mindre incisjoner.
Til sist retter vi blikket mot en ofte undervurdert del av praksisen: artroskopi av kne og skulder i vaktsituasjon – der tidspress, ufullstendig informasjon og begrensede ressurser setter både ferdigheter og beslutninger på prøve.
Vi som har bidratt til dette temanummeret, jobber ved Ortopedisk avdeling Aker, Oslo universitetssykehus. Etter flyttingen til nye lokaler i august 2023 har vi fått en moderne ramme rundt klinisk virksomhet, undervisning og fagutvikling. Det har gitt rom for refleksjon rundt hvordan vi lærer bort, deler erfaringer og videreutvikler artroskopisk kirurgi, på tvers av seksjoner, generasjoner og erfaringsnivå.
Vårt håp er at artiklene ikke bare formidler kunnskap, men også vekker nysgjerrighet: på teknikkene, på vurderingene bak dem, og på gleden ved presis kirurgi utført gjennom små snitt, men med stor betydning for pasienten.
God lesning.
Ankelleddet er et relativt lite ledd som gjør en stor jobb. En kontaktflate på 4–5 cm² mellom tibia og talus bærer hele kroppsvekten og skal håndtere alt fra spaserturer til sprint, fra hopp på fotballbanen til små glipptak på isen. Åpen ankelkirurgi kan innebære store snitt, lange arr og lang rehabilitering. Ankelskopiske teknikker har imidlertid gitt økte muligheter, og det utvikles stadig nye og bedre metoder. Ankelskopi er i prinsippet det samme som kikkhullskirurgi vi kjenner fra kne, skulder eller hofte. Med små kameraer, fine instrumenter og stor presisjon kan vi se inn i leddet uten å åpne det fullt. Dette gjør inngrepet tryggere, raskere og ofte langt mindre ubehagelig for pasienten. Men, som med mange teknologiske nyvinninger tok det tid før ankelskopi ble en del av daglig klinisk praksis.
ESPEN S. LAUDAL 1, INGRID KVELLO STAKE 1, ANDREAS DØBLE 1, ELISABETH ELLINGSEN HUSEBYE 1 1 ORTOPEDISK KLINIKK, AKER, OSLO UNIVERSITETSSYKEHUS
KORRESPONDANSE: ESPEN S. LAUDAL – ESLAUD @ OUS - HF.NO
FRA RISIKOSPORT TIL RUTINE
På begynnelsen av 1930tallet ble ankelleddet ansett som uegnet for artroskopisk kirurgi, hovedsakelig på grunn av anatomiske forhold. Leddet er trangt, lite og kongruent (1). Til tross for dette ble en systematisk artroskopisk undersøkelse av ankelleddet beskrevet allerede i 1933 (2).
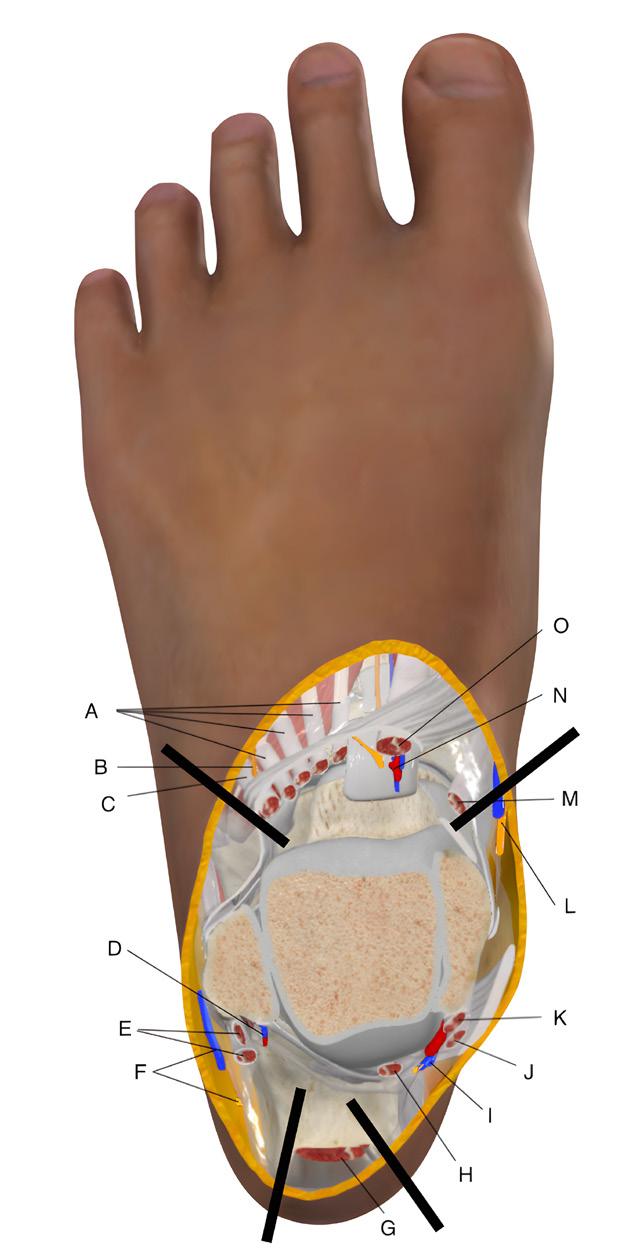
På 1970 og 1980tallet utviklet teknikken seg, men ankelskopi ble fremdeles betraktet som en vanskelig prosedyre med stor risiko for å skade nerver og blodkar, og mange mente at nytteverdien var begrenset. De første årene ble ankelskopi mest brukt til diagnostikk: å kikke inn i leddet for å se hva som foregikk. Litt som å titte gjennom nøkkelhullet i stedet for å åpne døren. Utviklingen av distraksjonsutstyr og mindre skop og instrumenter gjorde visualiseringen enklere, tryggere og mer fullstendig, og indikasjonene utviklet seg til å inkludere mer krevende prosedyrer. Problemet var at dette nøkkelhullet ikke alltid var trygt. Ankelen er et trangt ledd, og både foran og bak ankelleddet er det tettpakket med kritiske strukturer (nerver, sener og blodkar) (Figur 1).
På 1990tallet utviklet van Dijk og medarbeidere en toportalsteknikk for fremre ankelskopi, der man gikk bort fra peroperativt strekk og fokuserte på dorsalflek
sjon for å beskytte brusken ved entring av leddet (3). Ved maksimal dorsalfleksjon i ankelleddet vil brusken på talus gjemme seg under tibia, og man kan dermed gå inn i leddet uten å skade brusken. Dette førte til en tryggere tilgang ved fremre ankelskopi. Etter at de samme forfatterne i år 2000 beskrev en toportalsteknikk for bakre ankelskopi, ble også prosedyrer som inkluderte bakre ankelskopi mer vanlig (4). Med inngående anatomisk kunnskap og en systematisk tilnærming viste de at man kan entre ankelleddet – trygt og effektivt – gjennom to små “porter”. Dette var en “gamechanger”. Fra å være en metode de fleste var skeptiske til, ble ankelskopi gradvis en standardbehandling for en lang rekke ankelplager.
I dag regnes ankelskopi som en trygg, forutsigbar og effektiv prosedyre – forutsatt korrekt indikasjon og teknikk. Van Dijk viste også at ved diagnostisk ankelskopi uten klar formening om årsak til plagene, vil pasienten ha liten effekt av inngrepet (3). Vi må ha en idé om hva som er bak døren før vi går inn, og vi skal ha en plan om hva vi skal gjøre når vi er der inne.
FREMRE ANKELSKOPI - INNGANGSDØREN TIL FORSIDEN
Tilgangen gir kirurgen mulighet til å se og behandle det som skjer i den fremre delen av ankelleddet. Pasienten
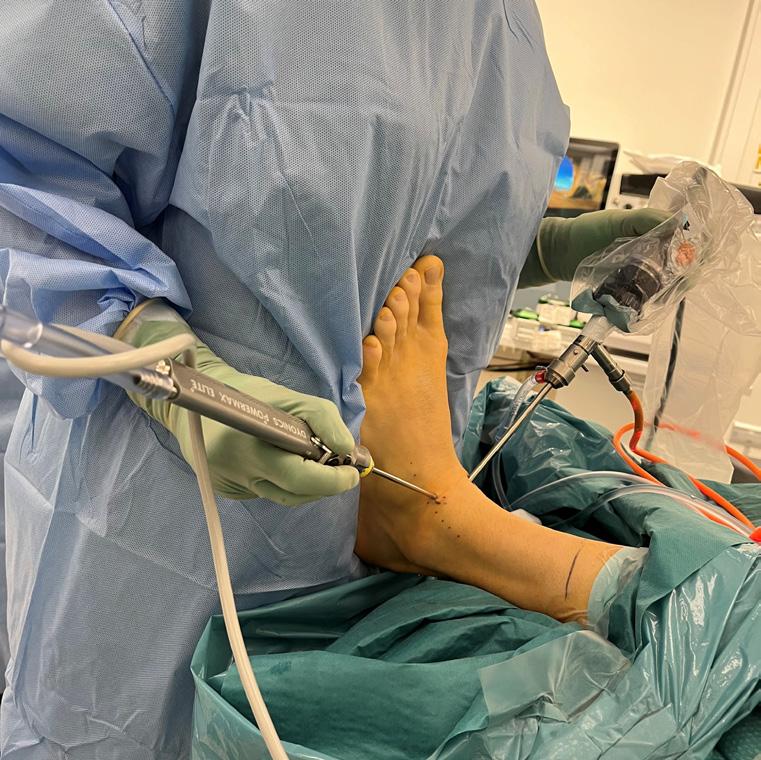
FIGUR 2. Figuren viser fremre ankelskopi med dorsomedial og dorsolateral portal. Ankelen dorsalflekteres ved at kirurgen lener seg mot foten. Nervus peroneus superficialis er markert like ved den dorsolaterale portalen. Samtykke er innhentet fra pasienten.
FIGUR 1. Figuren viser et tverrsnitt gjennom ankelleddet med anatomiske strukturer og fremre og bakre portaler (svarte streker). A) m. ekstensor digitorum longus, B) n. peroneus superficialis, C) m. fibularis tertius, D) a. og v. fibularis, E) m. peroneus longus og brevis, F) v. saphena parva og n. suralis, G) akillessenen, H) m. fleksor hallucis longus, I) n. tibialis, a. tibialis posterior og v. tibialis posterior, J) m. fleksor digitorum longus, K) m. tibialis posterior, L) n. saphenus og v. saphena magna, M) m. tibialis anterior, N) n. peroneus profundus, a. tibialis anterior og v. tibialis anterior, O) m. ekstensor hallucis longus. (Image courtesy of Complete Anatomy)
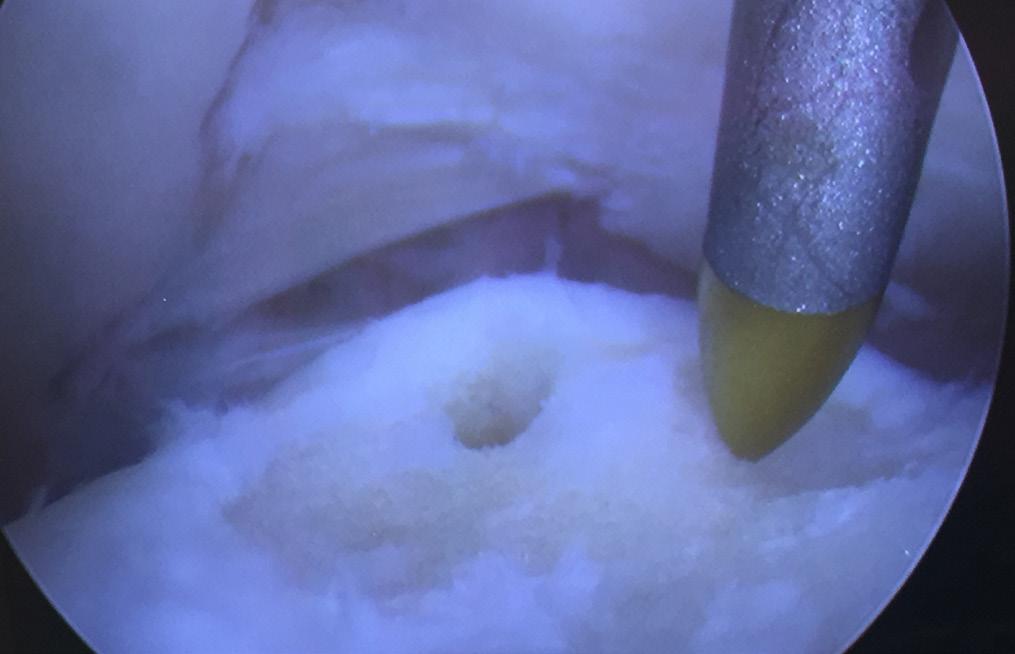
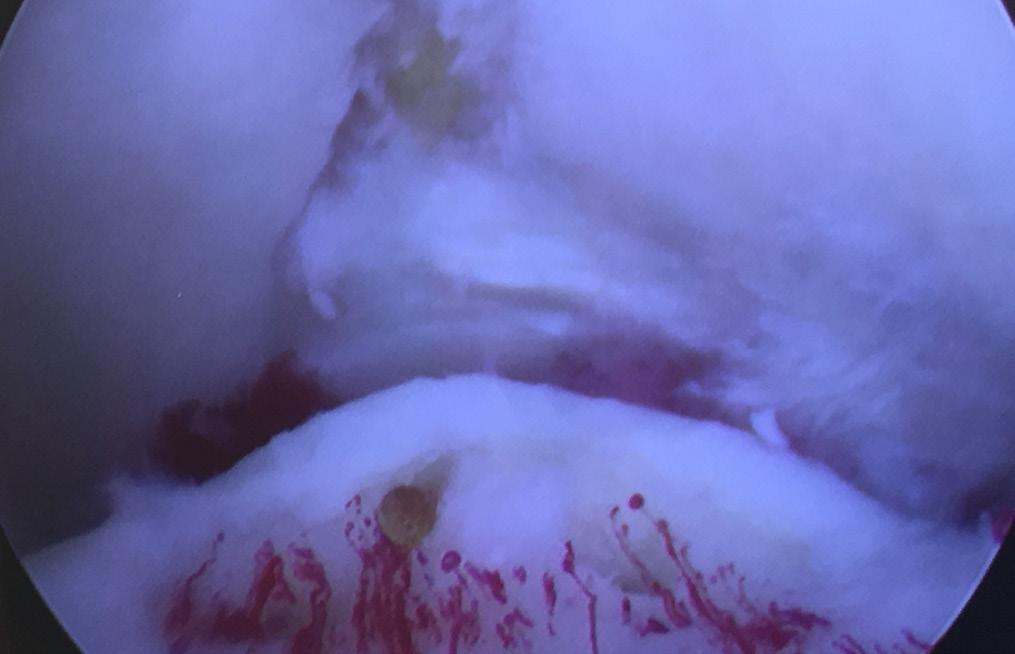
FIGUR 4A og 4B. Figuren viser en brusklesjon i talus med mikrofrakturering (4A) og blødning fra bein etter mikrofrakturering (4B). Samtykke er innhentet fra pasienten.
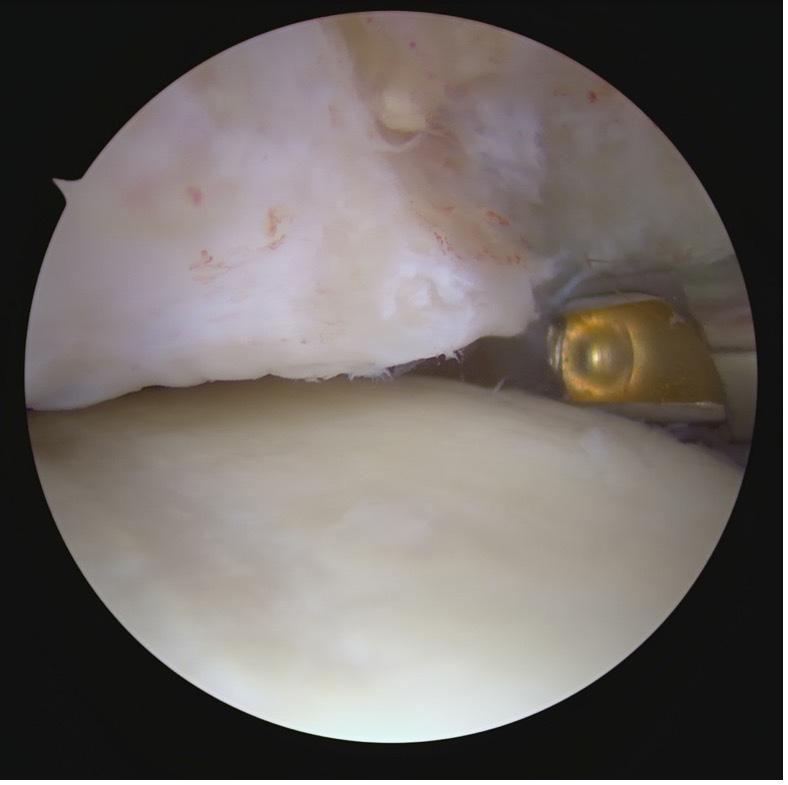
FIGUR 3. Figuren viser ankelleddet ved fremre ankelskopi. Talus sees i nedre del av bildet, mens tibia sees i øvre del av bildet. På nedre fremre kant av tibia er det en nokså spiss kant som representerer osteofytter. Dette er et tidlig tegn på artrose. Samtykke er innhentet fra pasienten.
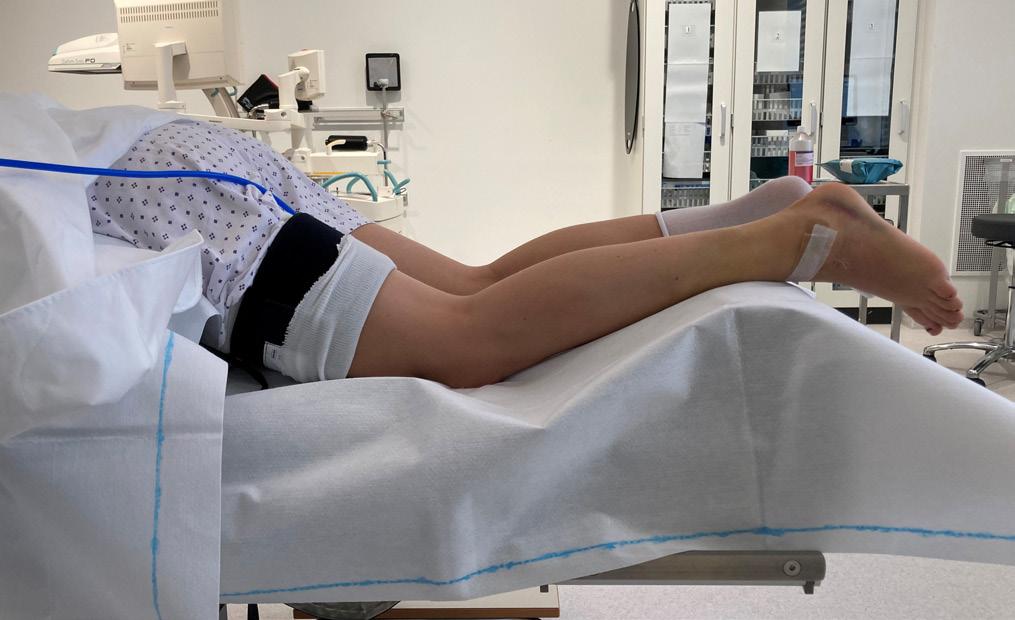
FIGUR 5. Figuren viser leiring ved bakre ankelskopi. Det er viktig å kunne dorsal- og plantarflektere i ankelen under operasjonen. Samtykke er innhentet fra pasienten.
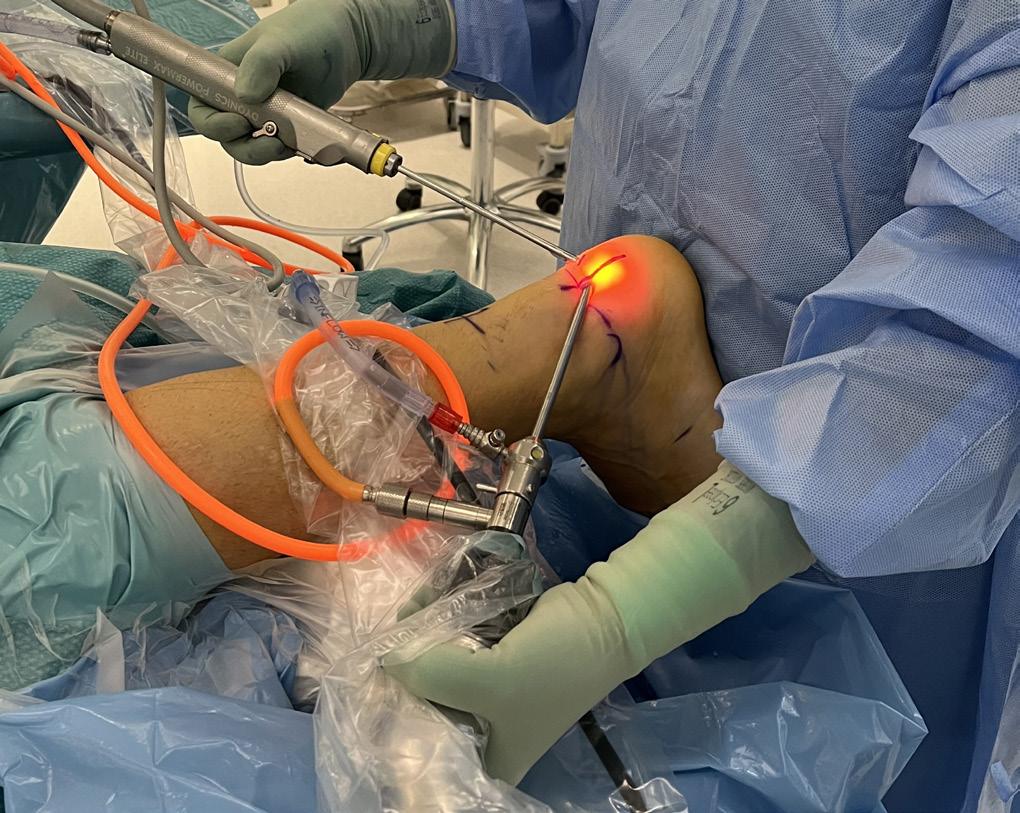
FIGUR 6. Figuren viser bakre ankelskopi med posteromedial og posterolateral portal. Samtykke er innhentet fra pasienten.
ligger i ryggleie med hælen akkurat innenfor operasjonsbordet (Figur 2) (5). På den måten kan kirurgen dorsalflektere ankelleddet ved å lene seg mot pasientens fotsåle. Den anteromediale portalen etableres først, i “soft spot” medialt for tibialis anteriorsenen. Den anterolaterale portalen etableres deretter, like lateralt for peroneus tertiussenen. I dette området forløper peroneus superficialis-nerven, som lokaliseres og markeres før kirurgistart for å unngå at den skades. Nervens forløp kan vanligvis visualiseres ved å plantarflektere 4. tå. En skopiportal og en arbeidsportal er nå etablert. Ved maksimal plantarfleksjon i ankelleddet kan omtrent 2/3 av leddflaten på talus visualiseres.
Hva kan behandles gjennom fremre ankelskopi?
Fordelen med fremre ankelskopi er at det gir oversikt og tilgang til strukturer som ofte er vanskelige å nå på andre måter – uten store snitt. Indikasjonene er mange (Tabell 1) (68).
Fremre impingement: Bløtdeler eller ben vokser inn mot fremre del av ankelleddet og “kiler seg fast”, og kan gi smerter og nedsatt bevegelighet (Figur 3). Vanlig hos idrettsutøvere som belaster ankelen hardt. Bløtdelene eller benet fjernes.
Brusklesjoner: Skader eller defekter i brusken og eventuelt underliggende bein, typisk på talusdomen. Brusklesjonen revideres med fjerning av løs brusk og det gjøres
Tilgang Hva kirurgen ser Hvilke tilstander som behandles
Fremre ankelskopi Forsiden av ankelleddet (fremre 2/3) Fremre impingement
Brusklesjoner
Synovitt
Osteofytter
Artrose
Artrofibrose
Løse legemer
Ankelligamentskader medialt og lateralt
Syndesmoseskader
Adjuvans
Bakre ankelskopi
Baksiden av ankelleddet og bakfoten
Bakre impingement
Os trigonum
Retrocalcaneal bursitt og Haglunds hæl
FHL-tendinopati
Kronisk akillesseneruptur
Subtalar artritt og koalisjoner
Frakturer i talus og calcaneus
Artrose
Brusklesjoner
TABELL 1. Indikasjoner for ankelskopi
eventuelt mikrofrakturering av gulvet i lesjonen for å stimulere tilheling (Figur 4).
Synovitt: Betennelse i leddhinnen som kan oppstå ved revmatiske sykdommer eller etter skade. Synovitt fjernes. Osteofytter: Slitasjeforandringer hvor det er påleiringer fortil i ankelleddet. Osteofyttene fjernes (Figur 3).
Artrose: Dersom det er uttalte slitasjeforandringer i ankelleddet, kan leddet avstives med artroskopisk fjerning av resterende brusk før leddet stabiliseres med perkutane skruer.
Artrofibrose: Unormalt mye arrvev inne i eller rundt ankelleddet som gir stivhet, smerter og redusert bevegelighet. Fibrotisk vev fjernes.
Løse legemer: Små brusk eller benbiter som ligger og flyter rundt i leddet og lager mekaniske plager. Disse fjernes.
Ankelligamentskader: Laterale og/eller mediale ligamentskader. Ankelligamentene sutureres med artroskopisk teknikk.
Syndesmoseskader: Spesielt kroniske syndesmoseskader hvor man gjør en artroskopisk revisjon før syndesmoseskaden fikseres perkutant med skruer eller sutur button.
Adjuvans: Noen ganger får man ikke helt klarhet i hvordan forholdene i ankelleddet er ut fra tilgjengelig billeddiagnostikk, og man gjør gjerne en ankelskopi før man går videre med den åpne prosedyren. Et eksempel kan være ved større brusklesjoner (gjerne over 15 mm) der man skal gjøre hovedprosedyren åpen, men man ønsker å kartlegge leddet først for generell slitasje. Dette kan endre indikasjonen til at det trolig er bedre med en artrodese eller ankelprotese.
Septisk artritt: Ved leddinfeksjon i ankelen er det mye mer skånsomt og effektivt å kunne skylle leddet artroskopisk fremfor med åpen teknikk. Man har da også muligheten til å kartlegge leddbrusken og kunne ta biopsier til dyrkning.
BAKRE ANKELSKOPI - BAKDØREN TIL ANKEL OG BAKFOT Når det er problemer baktil i ankelleddet, hjelper det ikke å banke på inngangsdøra foran. Da må man inn bakveien. Og bakre ankelskopi muliggjør nettopp dette. Ved denne tilgangen har man mulighet til å behandle tilstander både i ankelleddet og i subtalarleddet. Pasienten ligger i mageleie (Figur 5 og Figur 6) (5). Portalene etableres på hver sin side av akillessenen, i nivå med tuppen av fibula. Man etablerer først posterolaterale portal ved å gå blindt inn i retning av 1. web space (mellom 1. og 2. tå). Dette er en trygg bane. Deretter etableres posteromediale portal ved at man fører en peang ventralt for akillessenen og i lateral retning til man treffer skopet. Videre triangulerer man til man ser peangen, mens man fortsatt holder skopet i retning av 1. web space. Shaver introduseres i pean
gens kanal. På den måten vet man at shaveren holder seg unna nerve-karstrengen, som ligger medialt for fleksor hallucis longus (FHL)senen. Man kan nå trygt starte å shave bort fettet for å lage seg et rom å arbeide i, så lenge man holder seg lateralt for FHLsenen. Etter hvert vil man få fin tilgang til både ankelleddet og subtalarleddet.
Hva kan behandles gjennom bakre ankelskopi?
Bakre ankelskopi har gjort det mulig å behandle mange tilstander som tidligere krevde store og krevende åpne operasjoner (Tabell 1) (6,8-9).
Bakre impingement: Bløtdeler eller ben vokser inn mot bakre del av ankelleddet. En av de vanligste årsakene til bakre ankelsmerter, særlig hos dansere, fotballspillere og andre som ofte står på tå. Bløtdelene eller benet fjernes.
Os trigonum: En liten ekstra benbit bak talus som kan bli smertefull. Os trigonum fjernes.
Retrocalcaneal bursitt og Haglunds hæl: Betennelse og benpåleiring ved hælen, ofte kombinert med smerter når skoen gnisser. Betent vev og benpåleiringer fjernes.
FHL-tendinopati: Problemer med senen til stortåbøyeren (fleksor hallucis longus), som kan bli irritert, hoven eller til og med revne. Senen revideres, eventuelle trange partier som hindrer fri bevegelse av senen fjernes.
Kronisk akillesseneruptur: Her kan man bruke FHLsenen som “standin” for å erstatte en skadet akillessene, eller bruke Semitendinosus som fritt graft mellom proksimale akillessenestump og calcaneus.
Subtalar artritt og koalisjoner: Inflammasjon eller sammenvoksninger i subtalarleddet. Synovitt og fibrotisk vev fjernes.
Frakturer: For enkelte brudd oppnås bedret fraktur reposisjon/bedret kontroll over reposisjon med artroskopisk assistanse, eksempelvis noen brudd i talus og calcaneus.
Artrose: Ved uttalt slitasje i subtalarleddet kan resterende brusk fjernes, og leddet stives av med perkutane skruer fra calcaneus og opp i talus. Man kan også behandle artrose i ankelleddet og subtalarleddet kombinert der man kan fjerne resterende brusk i begge ledd, og deretter fiksere begge ledd med en margnagle satt fra fotsålen opp gjennom calcaneus, talus og distale del av tibia.
Brusklesjoner: Noen brusklesjoner ligger helt på bakre kant av talus og kan være lettere å nå gjennom bakre ankelskopi enn ved fremre ankelskopi.
Peroneusseneluksasjoner: Ved bakre ankelskopi kan sulcus retromalleolaris fordypes for å øke stabiliteten av peroneussenene.
FREMRE VERSUS BAKRE TILGANG - TO DØRER, ETT HUS
Noen ganger kan man bruke hoveddøren foran, andre ganger må man inn bakdøren – og av og til må man bruke
begge. For kirurgen er det viktig å planlegge nøye hvilken tilgang som gir best oversikt og arbeidsforhold – og noen ganger kombinere begge i samme operasjon.
Fremre tilgang er best når problemet sitter foran i leddet: fremre impingement, brusklesjoner, synovitt, artrose, løse legemer eller ligamentskader (syndesmosen, laterale ankelligamenter og deltoid).
Bakre tilgang gir oversikt og mulighet til å reparere det som sitter bak: os trigonum, Haglunds hæl, FHL eller akillesseneproblemer, subtalar artritt og koallisjoner, og enkelte frakturer.
HVA MED KOMPLIKASJONER?
Ingenting i kirurgi er 100 % risikofritt. Også ankelskopi kan gi komplikasjoner, men tallene er relativt lave (10–15). En systematisk tilnærming kombinert med respekt for anatomien er avgjørende for å redusere risikoen for komplikasjoner.
Vanlige, men som regel forbigående problemer kan være hevelse og ømhet i relasjon til portaler, stivhet eller stramhet i akillessenen, og nummenhet eller prikking i foten, ofte på grunn av irritasjon av calcaneale nervegrener og trykk eller skade på nervus peroneus superficialis.
Sjeldnere komplikasjoner kan være overfladisk og/eller dyp infeksjon, seneskader (særlig på FHL ved fjerning av os trigonum), karskade, fisteldannelser i relasjon til portaler, dyp venetrombose eller CRPS (komplekst regionalt smertesyndrom).
HVORFOR ANKELSKOPI ER FREMTIDEN
Den store fordelen med ankelskopi er kombinasjonen av presisjon og små tilganger. Ved ankelskopi får man oversikt over intraartikulære strukturer uten å lage en større tilgang eller gjøre osteotomi av malleolene. Skopiske teknikker åpner stadig nye dører. Små instrumenter, bedre kameraer og mer erfaring gjør at indikasjonene utvides år for år.
Kort sagt: Ankelskopi – enten forfra eller bakfra – gir kirurgen flere muligheter og pasienten en lettere vei tilbake på beina.
REFERANSER : Se bakerst i nettutgaven på kirurgen.no
Hofteleddsartroskopi har de siste to tiårene gjennomgått en betydelig utvikling, både teknisk og klinisk. Fra å være en eksperimentell metode for diagnostikk av intraartikulære tilstander, har den utviklet seg til et etablert behandlingstilbud for utvalgte pasienter med femoroacetabulær impingement syndrom (FAIS), labrumrupturer og enkelte andre intraartikulære lidelser. Samtidig har antallet inngrep økt eksponentielt i mange land, særlig i Nord-Amerika og Skandinavia, uten at indikasjonene alltid har vært klart definert. I dag foreligger det økende evidens for hvilke pasientgrupper som faktisk har nytte av hofteleddsartroskopi, men dokumentasjonen understreker også behovet for nøktern pasientseleksjon.
KRISTIAN MARSTRAND WARHOLM, SVERRE LØKEN
ORTOPEDISK KLINIKK, OSLO UNIVERSITETSSYKEHUS
KORRESPONDANSE: KRISTIAN MARSTRAND WARHOLM - KRMARS @ OUS - HF.NO
KLINISK VURDERING OG UTREDNING
Ved hoftesmerter er det avgjørende å skille mellom intraartikulære og ekstraartikulære årsaker. Smerter lokalisert til lysken peker oftest mot intraartikulær patologi, mens smerter lateralt eller posteriort kan skyldes affeksjon av gluteale sener, hamstring sener, iliopsoassenen, trochanterbursitt eller referert smerte fra lumbalcolumna eller sakroiliakalledd. Typiske intraartikulære symptomer er låsninger, sviktfølelse og mekaniske smerter ved fleksjon og rotasjon.
En positiv impingement-test (smerte i lysken ved fleksjon, adduksjon og innadrotasjon) indikerer mulig intraartikulær patologi (sensitivitet 86 %), men testen er uspesifikk (spesifisitet 22 %) og bør alltid tolkes i sammenheng med klinikk og billeddiagnostikk. Før MR bør man starte med røntgenundersøkelse: anteroposterior bekken, samt Dunn 45° eller Lauensteinprojeksjon. Dette kan avdekke morfologiske avvik som cam eller pincerimpingement, samt utelukke artrose, dysplasi og andre ossøse morfologier (f.eks. Calvé-Legg-Perthes' sykdom). Dersom røntgen viser normale leddforhold uten artrose, kan MR eller MRartrografi benyttes for vurdering av labrum og brusk. Røntgen eller ultralydveiledet diagnostisk injeksjon av lokalbedøvelse i leddet kan være nyttig for å bekrefte at smerten stammer fra selve hofteleddet. CT er særlig aktuelt ved planlegging av kirurgi ved uttalte benete deformiteter.
OPERASJONSTEKNIKK
Hofteleddsartroskopi kan utføres i rygg eller sideleie. Det er nødvendig med en del spesialutstyr, herunder eg
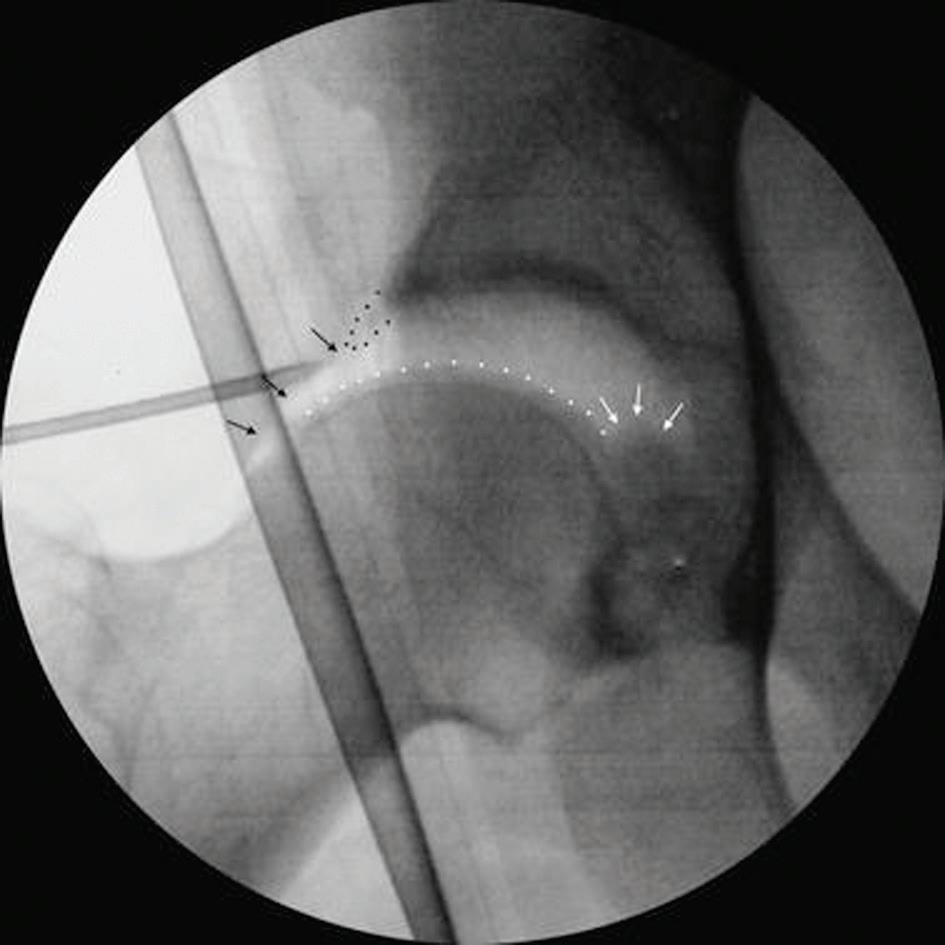
net strekkbord, røntgengjennomlysning og lange artroskopiinstrumenter. Visualisering gjøres med 70° optikk, og det finnes i dag kurvede instrumenter som muliggjør god tilgang rundt caput. Det skilles mellom sentralt kompartment – selve leddspalten mellom caput femoris og acetabulum – og perifert kompartment, som ligger utenfor acetabulum, men innenfor kapselen. For tilgang til det sentrale kompartment kreves distraksjon på 10–15 mm (Figur 1). Trykk mot perineum bør fordeles med bred støtte (>20 cm) for å unngå nerveskader/decubitus, og strekktiden holdes så kort som mulig. Alternativt kan man oppnå strekk uten trykk mot perineum ved at pasienten ligger på en spesialmadrass med høy friksjon kombinert med tipping av operasjonsbordet (hodet lavt).
Tilgangen etableres vanligvis gjennom to til tre portaler (fremre, anterolateral og eventuelt posterolateral). Den tykke kapselen og bløtdelsbroen mellom hud og ledd begrenser instrumentmobilitet, og en moderat kapsulotomi er ofte nødvendig. Store kapselreseksjoner kan gi postoperative smerter og instabilitet, og bør unngås. Sutur av leddkapselen anbefales når det er teknisk mulig.
INDIKASJONER OG PASIENTSELEKSJON
Treningsterapi under veiledning av fysioterapeut skal alltid være første behandlingsvalg ved hoftesmerter. Dersom symptomene vedvarer etter minst tre måneder med strukturert, målrettet trening, og det ikke foreligger radiologisk artrose eller dysplasi, kan pasienten vurderes for artroskopisk behandling. Den vanligste indikasjonen er FAIS med tilhørende labrumlesjon.
LABRUMSKADER
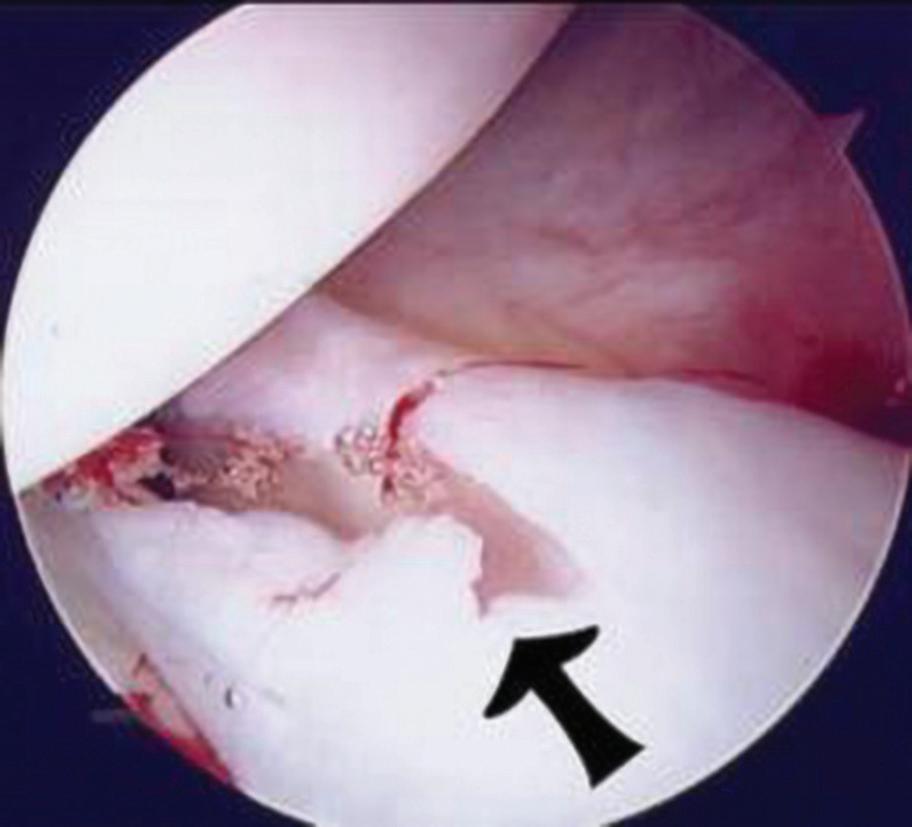
Labrum acetabulare spiller en sentral rolle i hofteleddets stabilitet og væskebalanse ved å opprettholde et intraartikulært «vakuum» som fordeler trykk og bevarer leddets kontaktflate. Labrumrupturer er den hyppigste diagnosen ved hofteleddsartroskopi, oftest lokalisert anterosuperiort (Figur 2). Skaden kan være traumatisk, men utvikles oftest gradvis som følge av mekanisk overbelastning og impingement. Den høye tettheten av smertereseptorer i labrum gjør at slike skader ofte er smertefulle. Smertebildet kan også forsterkes av assosierte paralabrale cyster, som gir økte symptomer ved aktivitet.
MR-artrografi har høyere sensitivitet (91 %) enn konvensjonell MR (63 %) for å påvise slike rupturer, men funn må alltid ses i klinisk sammenheng, ettersom labrum
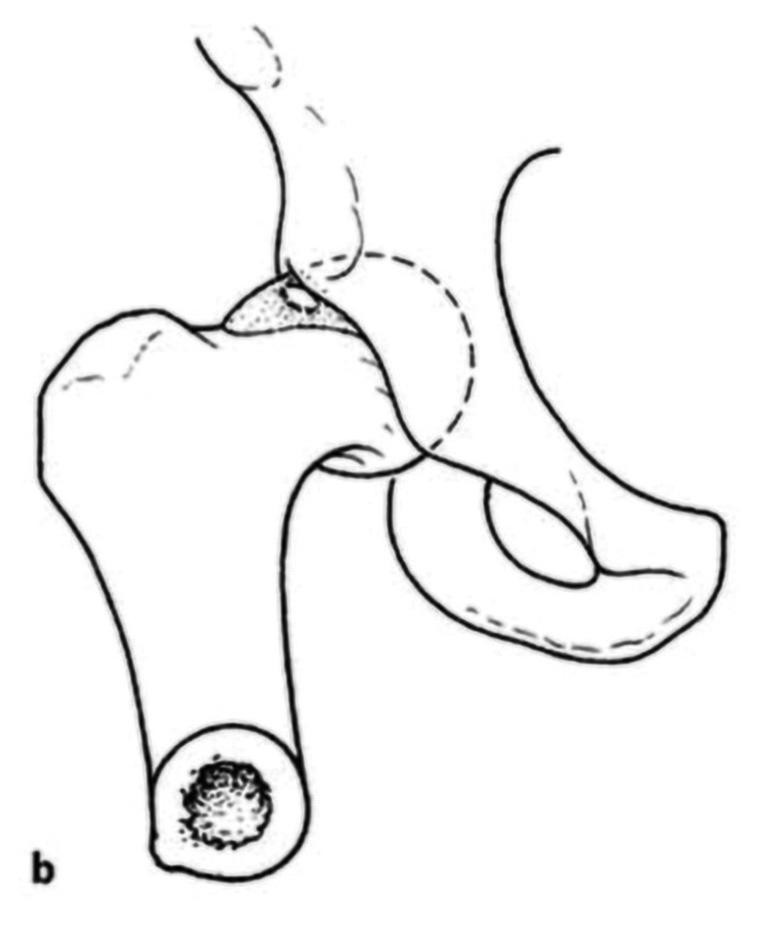
forandringer er vanlige også hos asymptomatiske individer og forekomst øker med alder. Tidligere ble rupturer ofte behandlet med reseksjon, men flere studier har vist at bevaring og sutur av labrum gir bedre resultat både biomekanisk og klinisk som ved meniskskader i kne. Ved irreparerbare skader kan labrumrekonstruksjon vurderes, med gode korttidsresultater i nyere studier (1–3).
FEMOROACETABULÆR IMPINGEMENT SYNDROM ( FAIS ) FAIS beskriver symptomgivende kollisjon mellom femur og acetabulum, typisk ved fleksjon og innadrotasjon. Den vanligste formen er camimpingement, forårsaket av en fortykket overgang mellom caput og collum femoris, mens pincerimpingement skyldes overdekning av acetabulum, som ved retroversjon eller dyp leddskål. Mange pasienter har en kombinasjon av begge (Figur 3).
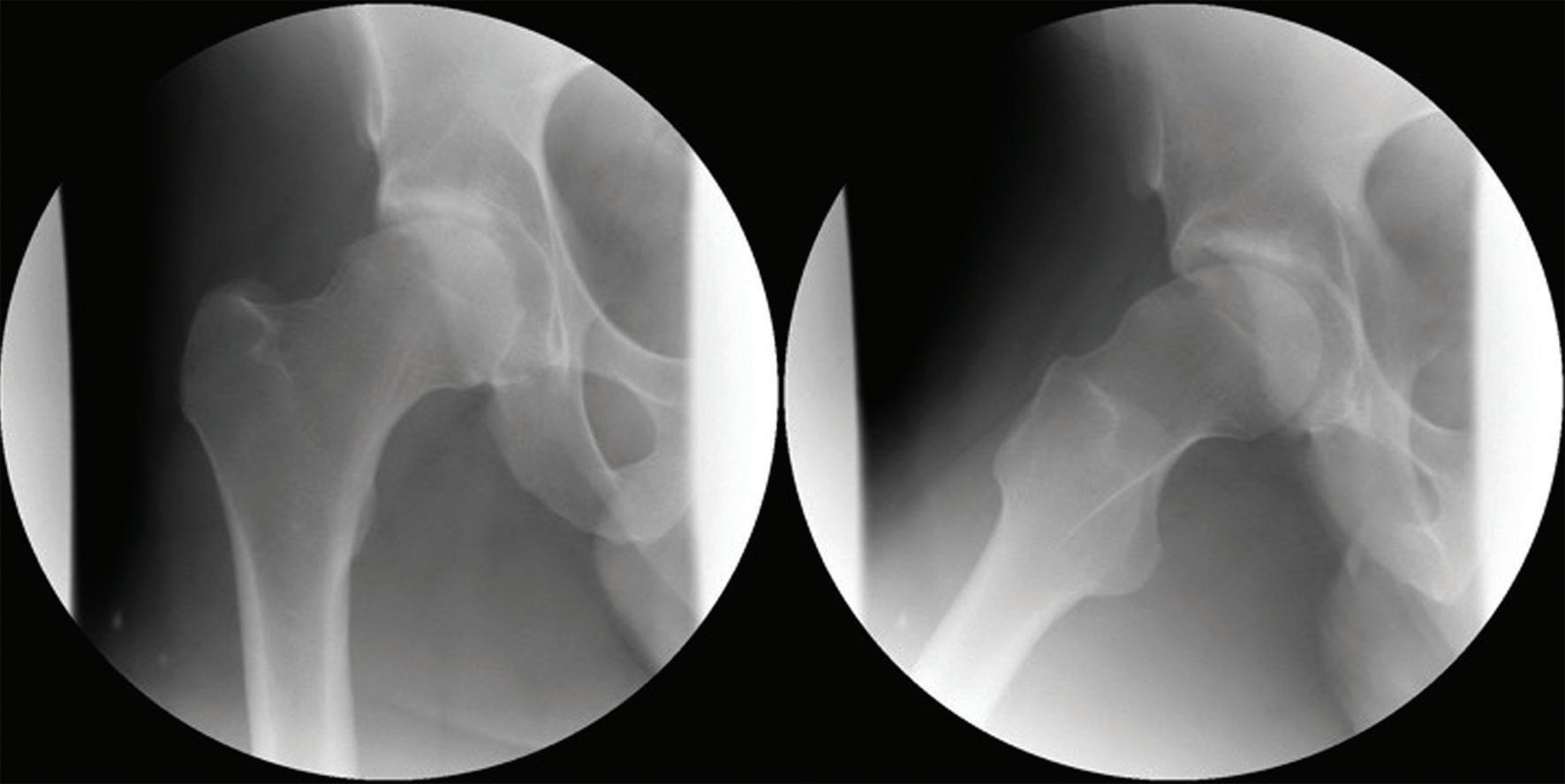
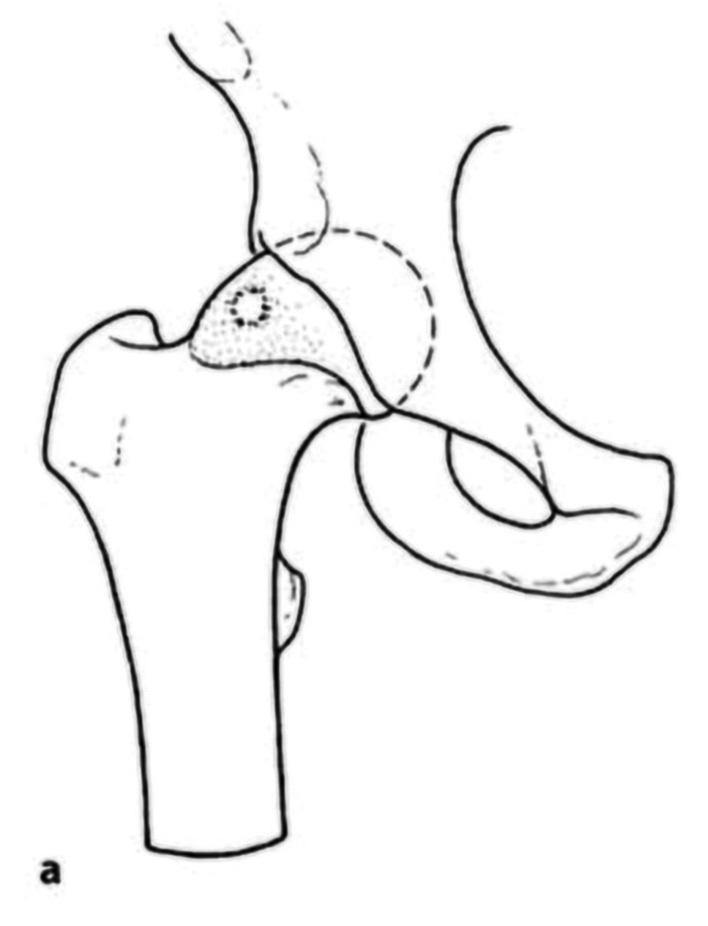
Cammorfologi oppstår ofte i ungdomsårene og er hyppigst hos gutter og idrettsutøvere innen fotball, ishockey og kampsport. Dette skyldes trolig repeterte belastninger mot vekstsonen i caput femoris fra 12årsalderen og frem til man er utvokst. (Figur 4). Flere studier har vist en klar sammenheng mellom FAIS og økt risiko for tidlig artroseutvikling (4–7).
Kirurgisk behandling innebærer reseksjon av benete prominenser for å gjenopprette normal bevegelighet og redusere labrumbelastning. Ved camresesjon arbeider man fra perifert kompartment uten strekk, mens pincerbein fjernes fra acetabularkanten ofte med samtidig labrumrefiksasjon (8,9).
BRUSKSKADER OG ARTROSE
Bruskskader forekommer ofte i kombinasjon med FAI og labrumlesjoner. Behandlingen kan inkludere debridement, vanligvis som tilleggsprosedyre, eller brusktransplantasjon fra samme ledd. Mikrofrakturering har sannsynligvis ikke noen reell plass lenger. Ved etablert artrose med redusert leddhøyde har artroskopi liten eller ingen dokumentert effekt, og totalprotese er ofte et bedre alternativ uavhengig av alder. En systematisk oversikt av Domb et al. viste at pasienter med artrose mer enn Tönnis grad 1 hadde betydelig dårligere resultater etter artroskopisk kirurgi (10).
ANDRE TILSTANDER
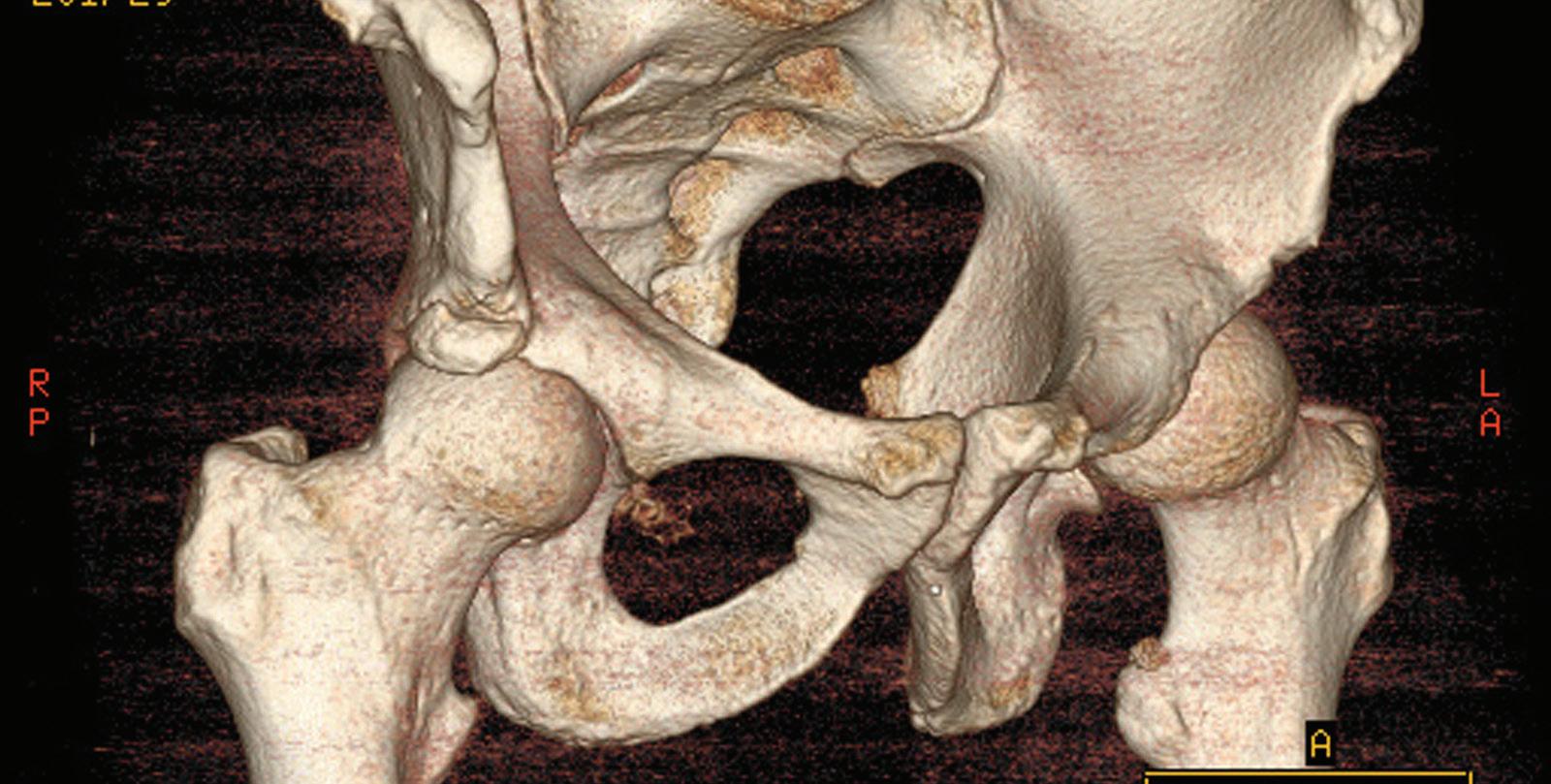
Os acetabuli er et benfragment langs acetabularkanten, ofte som følge av stressfraktur ved impingement (Figur 5). Små fragmenter kan fjernes, mens større frag
menter som omfatter leddflaten bør fikseres, og kan fint gjøres skopisk.
Hofteartroskopi kan også brukes ved synoviale tilstander som synovial kondromatose, pigmentert villonodulær synovitt og ved revmatiske leddlidelser, hvor inngrepet kan gi både diagnostisk og terapeutisk gevinst.
Ruptur av ligamentum teres kan i enkelte tilfeller gi smerte eller låsning og behandles med debridement.
ANDRE KONTRAINDIKASJONER
Artroskopi er ikke egnet ved hofteleddssykdommer med betydelig benavvik eller redusert kongruens. Pasienter med dysplasi (lateral senter–kantvinkel < 20°) bør vurderes for periacetabulær osteotomi før eventuell artroskopi. Også artrose, stivhet (artrofibrose) og heterotop ossifikasjon utgjør kontraindikasjoner.
REHABILITERING
Etter inngrepet anbefales delbelastning til smertegrensen med krykker i to til tre uker, og det gjøres gradvis opptrening under veiledning av fysioterapeut med fokus på bevegelighet, styrke og kontroll. Full idrettsdeltakelse kan vanligvis vurderes etter seks måneder. Ved labrumeller bruskreparasjoner forlenges opptreningen med restriksjoner på rotasjon og dyp fleksjon de første ukene.
KOMPLIKASJONER
Komplikasjonsraten etter hofteartroskopi varierer fra 0,5 til 8 % i større serier (11,12). De fleste er forbigående, men nerveskader (n. pudendus, n. cutaneus femoris lateralis,
n. femoralis) og kapsulær instabilitet forekommer. Bruskog labrumskader kan oppstå iatrogent under inngrepet. Infeksjon og osteonekrose er sjeldne, men alvorlige komplikasjoner. Pasientene må informeres om at selv ved vellykket kirurgi opplever rundt 20–25 % begrenset eller ingen vedvarende symptomforbedring (13,14).
RESULTATER OG EVIDENSGRUNNLAG
De fleste publiserte studier på hofteartroskopi er observasjonsstudier (nivå IV), men de siste årene har flere randomiserte, kontrollerte studier gitt bedre evidensgrunnlag.
Systematiske oversikter viser gjennomsnittlig forbedring i pasientrapporterte utfallsmål som iHOT33 og modified Harris Hip Score på 20–30 poeng etter artroskopisk FAI-behandling, med størst effekt hos yngre pasienter uten artrose (15,16).
Randomiserte studier som FASHIoN (Lancet 2019) og FAIT (BMJ 2018) har vist at kirurgi gir større symptomforbedring enn fysioterapi alene, men også at begge grupper oppnår klinisk relevante forbedringer (17,18).
Den internasjonale HIPARTIstudien, ledet fra Oslo universitetssykehus, sammenligner artroskopisk kirurgi med shamoperasjon i et dobbeltblindet design, og vil kunne gi viktig informasjon om faktisk behandlingseffekt (19).
Nasjonale hofteartroskopiregistere med oversikt over alle typer pasienter er et viktig supplement til randomiserte
kontrollerte studier som ofte har smale inklusjonskriterier. Det er etablert nasjonale hofteartroskopiregistre i flere land, også i Norge.
KLINISK TILNÆRMING FØR HENVISNING
Utredning av hoftesmerter bør starte med grundig klinisk vurdering og røntgenbilder for å utelukke artrose eller dysplasi. Pasienten skal ha gjennomført minst tre måneders målrettet fysioterapi. Først ved vedvarende symptomer til tross for gjennomført treningsterapi og funn forenlige med FAIS eller labrumlesjon uten tegn til degenerasjon, bør pasienten henvises til vurdering med tanke på artroskopisk kirurgi.
KONKLUSJON
Hofteleddsartroskopi er nå etablert som et nyttig verktøy med god effekt i behandlingen av pasienter med FAIS, labrumskader og enkelte andre intraartikulære lidelser. Riktig pasientseleksjon, grundig utredning og nøktern forventningsstyring er avgjørende for gode resultater. De beste resultatene oppnås hos yngre pasienter uten tegn til artrose eller dysplasi.
Videre forskning, både gjennom randomiserte kontrollerte studier og registerstudier, er nødvendig for å studere langtidseffekter og for å kunne anbefale best mulig behandling tilpasset den enkelte pasient.
REFERANSER : Se bakerst i nettutgaven på kirurgen.no
Håndleddsartroskopi har etablert seg som et svært viktig supplement til tradisjonell åpen kirurgi i håndledd og håndrot. I løpet av de siste tiårene har teknikken utviklet seg fra kun å være et diagnostisk hjelpemiddel til å muliggjøre artroskopisk behandling av flere tilstander. I mange sammenhenger kombineres artroskopi med åpen teknikk for å bedre pasientbehandlingen med en mer skånsom tilnærming.
AUDUN TANGERUD 1, ENDRE SØREIDE 1, ELLISIF JENSEN 1, ANNE MARI ROSENLUND 1 , HALLGEIR BRATBERG 1, OLE A. K. FOSSE 1, SONDRE HASSELLUND 1 1 SEKSJON FOR HÅND - OG ALBUEKIRURGI, OUS AKER
KORRESPONDANSE: AUDUN TANGERUD - AUDTAN @ OUS - HF.NO
INNLEDNING
Artroskopi av håndleddet er en presis metode for diagnostikk og behandling av intraartikulær patologi i håndleddet og håndrot. Man får ofte bedre oversikt over leddet med artroskopi enn med åpen tilgang, særlig i radiokarpal og midtkarpalleddet, hvor artroskopi muliggjør direkte vurdering av ligamentintegritet og stabilitet i tillegg til brusk. Dette gjør artroskopi spesielt velegnet ved triangulærbruskskader (TFCCskader), skafolunær (SL) og/eller lunotrikvetral (LT)instabilitet. Ved intraartikulære distale radiusbrudd og brudd i skafoid, kan man artroskopisk vurdere reposisjon, stepp og eventuell skruepenetrasjon. Tilstander som tidligere krevde åpen prosedyre, kan nå håndteres artroskopisk som for eksempel skafoidpseudartrose. Sammenlignet med åpen kirurgi gir håndleddsartroskopi mindre bløtvevstraume, lavere infeksjonsrisiko og ofte redusert rehabiliteringstid.
Vi ønsker å presentere teknikk, utstyr og noen av de mulighetene artroskopisk tilnærming gir i vurdering og behandling av håndleddsproblematikk, med særlig vekt på hvilken rolle artroskopi har ved behandling av brudd og ligamentskader i håndledd og håndrot.
ANATOMI OG TEKNISKE FORHOLD
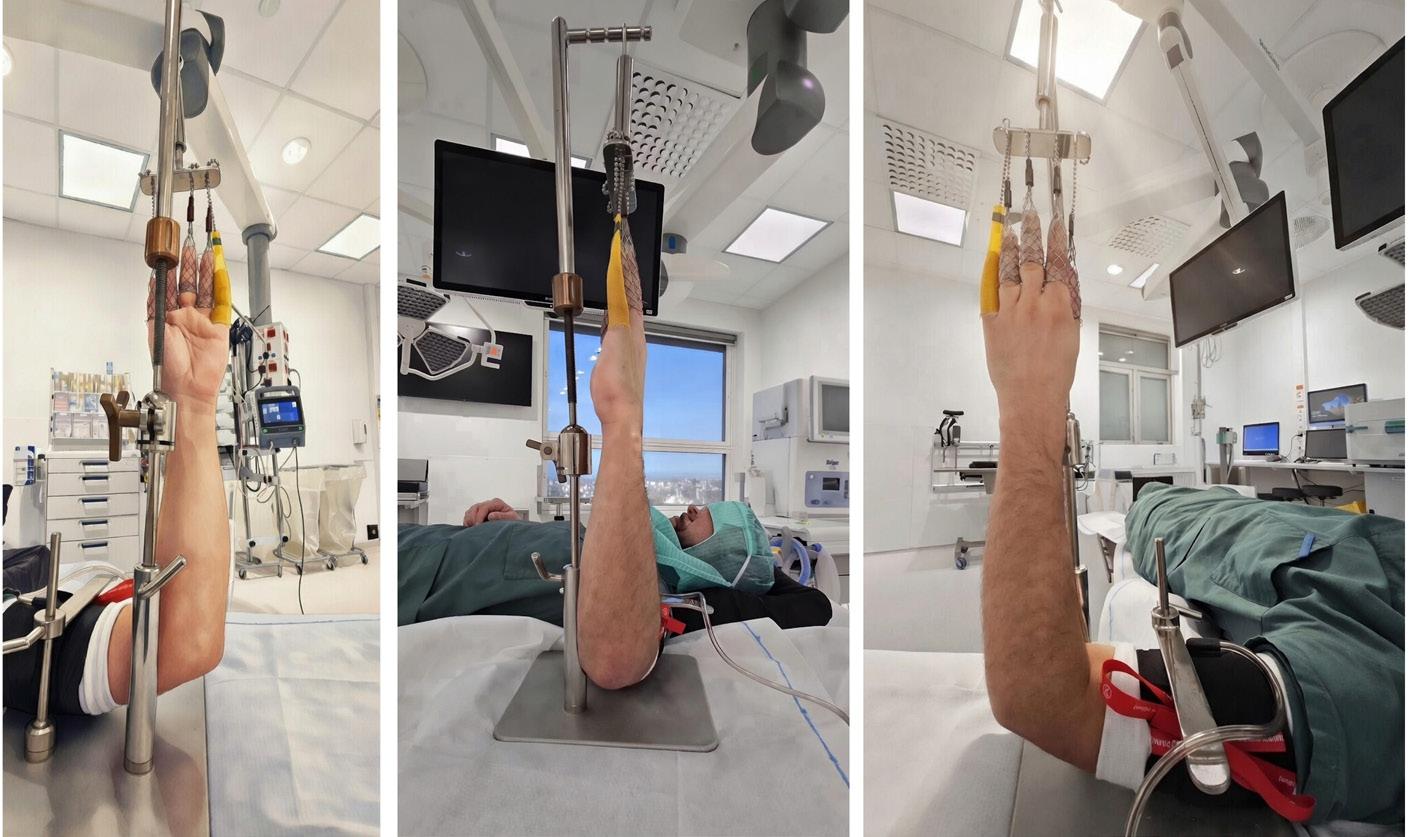
I vår seksjon benytter vi et standardisert oppsett ved håndleddsartroskopi. Pasienten er i ryggleie, vi benytter armbord og traksjonstårn (WristFastTrac) (Figur 1).
Inngrepet utføres i generell eller regional anestesi. Pasienten posisjoneres med skulderen abdusert og albuen i 90 graders fleksjon. Det legges blodtomhetsmansjett på overarmen, og distraksjon oppnås med fingerfeller og ca. 5 kg traksjon (Figur 1). Dette gir gode arbeidsforhold for kirurgen, med god oversikt og tilgang til standard portalplassering.
Håndleddsartroskopi ble tidligere utført med standard kontinuerlig vanngjennomskyll og pumpe. Imidlertid har man sett fordelene ved tørr artroskopiteknikk, hvor man får mindre ødem i bløtdelene som muliggjør lengre prosedyrer, der det er enklere å entre leddet, og i tillegg gir det en betydelig bedre visuell fremstilling (1). Håndleddet har et lite volum, så den ekspanderende effekten av vanntilførsel med gitt trykk er uansett begrenset, og traksjon er viktigere for å skape arbeidsrom. Standardutstyr inkluderer 2.4 eller 2.7 mm artroskop (vanligvis 30° optikk), shaver (3.0 og 3.5 mm), burr (3.0 mm), krok, minifattetenger og eventuelt radiofrekvensprobe. Vi har også 1.9 mm artroskop tilgjengelig som benyttes ved artroskopi i håndledd hos barn, eventuelt ved artroskopi i mindre ledd som karpometakarpalledd eller metakarpofalangialledd (1, 2).
En artroskopisk undersøkelse av håndleddet innebærer både radiokarpal og midtkarpal skopi. Radiokarpalt får man oversikt over leddflatene på radius, samt proksimale skafoid, lunatum og triquetrum. I tillegg visualiseres
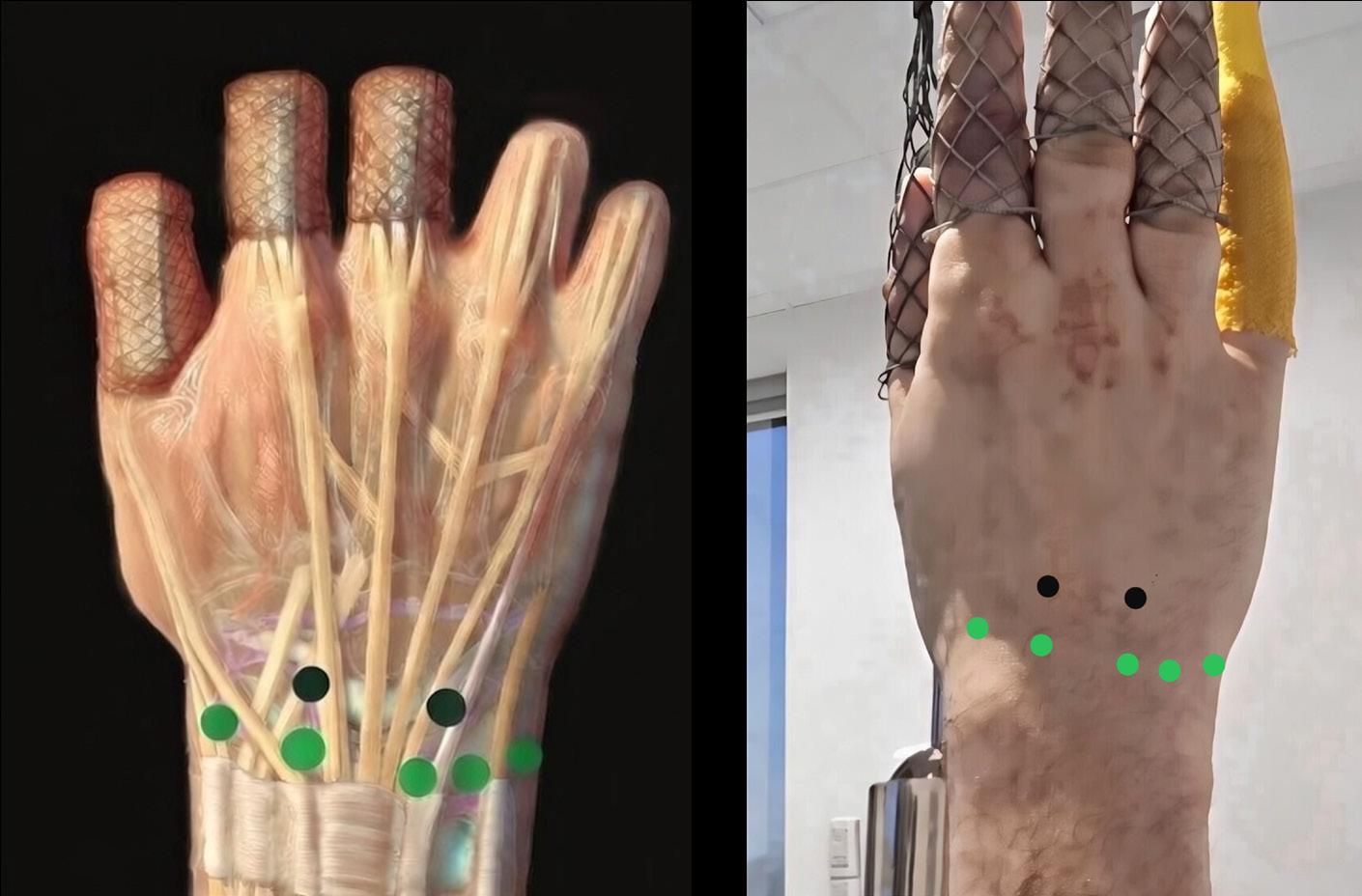
TFCC, volar kapsel, volare ekstrinsiske ligamenter og delvis de dorsale ekstrinsiske ligamentenes innfestning. Fra radiokarpalt har man god oversikt over den membranøse delen av SLligamentet. Bedre vurdering av stabiliteten mellom skafoid–lunatum og lunatum–trikvetrum oppnås imidlertid via midtkarpal skopi, altså i leddet mellom proksimale (skafoid/lunatum/trikvetrum) og distale (kapitatum/hamatum/trapezoid/trapezium) håndrotsrekke. Skafoidtrapeziumtrapezoid(STT) og trikvetrumpisiformleddet er også tilgjengelig for artroskopisk diagnostikk og prosedyrer.
Portalplasser er viktig i håndleddsartroskopi for å sikre god tilgang til leddet og ønskede strukturer (Figur 2) (3). De dorsale og radiale portalene navngis etter strekkesenekulissene, og volare portaler brukes av og til. Det er også beskrevet egne portaler til distale radioulnarledd som spesielt er nyttig ved vurdering av integritet til innfestning av TFCC, i tillegg til generell leddstatus. Den van
FIGUR 1: Leiring av pasient i strekktårn. Mothold over overarmen som ligger over blodtomhetsmansjett, fingerfeller som festes i tårnet.
FIGUR 2: De vanligste portalene avmerket. Radiokarpale portaler i grønt fra venstre: 1-2, 3-4, 4-5, 6R, 6U. I Svart fra venstre midtkarpale portaler; MCU og MCR. (Illustrasjon O.A.K. Fosse)
ligste startportalen er 3–4portalen, ofte i kombinasjon med 6R (portal på radialsiden av 6. strekkesenekulisse). Midtkarpalt brukes normalt to portaler: en ulnar og en radial (Figur 2) (3)
ARTROSKOPISK ( ASSISTERT ) BRUDDBEHANDLING
Artroskopi i behandlingen av distale radiusbrudd Ved intraartikulære distale radiusbrudd er håndleddsskopi et nyttig supplement til åpen reposisjon og intern fiksasjon. Artroskopi muliggjør direkte vurdering av leddkongruens, bruskdefekter og identifisering av samtidig ligamentpatologi. Brudd som kan være aktuelle for artroskopiassistert behandling er intraartikulære brudd, hvor trinndannelse og/eller diastase i leddflaten bør vurderes og reponeres. I tillegg er artroskopi nyttig ved brudd med mistenkt SLskade, enten grunnet økt SLavstand, eller et sagitalt bruddmønster i SLovergangen eller ved et ustabilt DRUledd der vurdering/behandling av TFCC er ønskelig (4, 5).
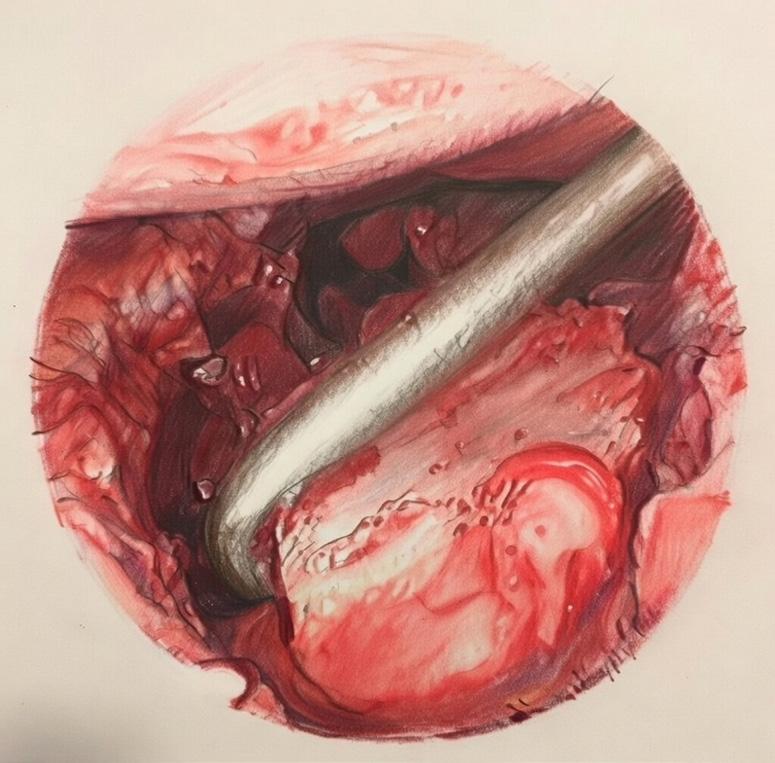
FIGUR 3: Reposisjon av intraartikulær distal radiusfraktur med krok. Etter reposisjon vil man oftest midlertidig pinne opp midlertidig for å fiksere med plate og skruer. (Illustrasjon O.A.K. Fosse)
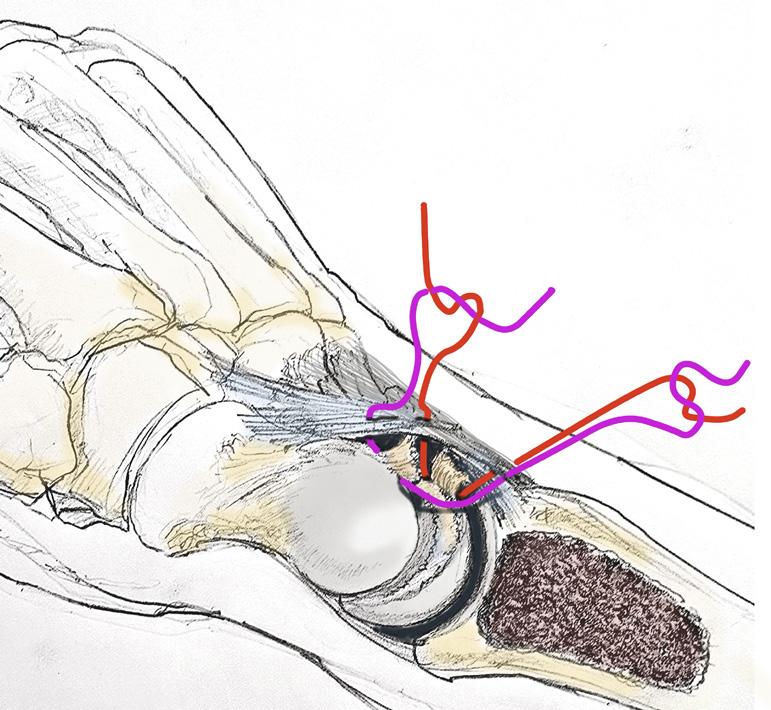
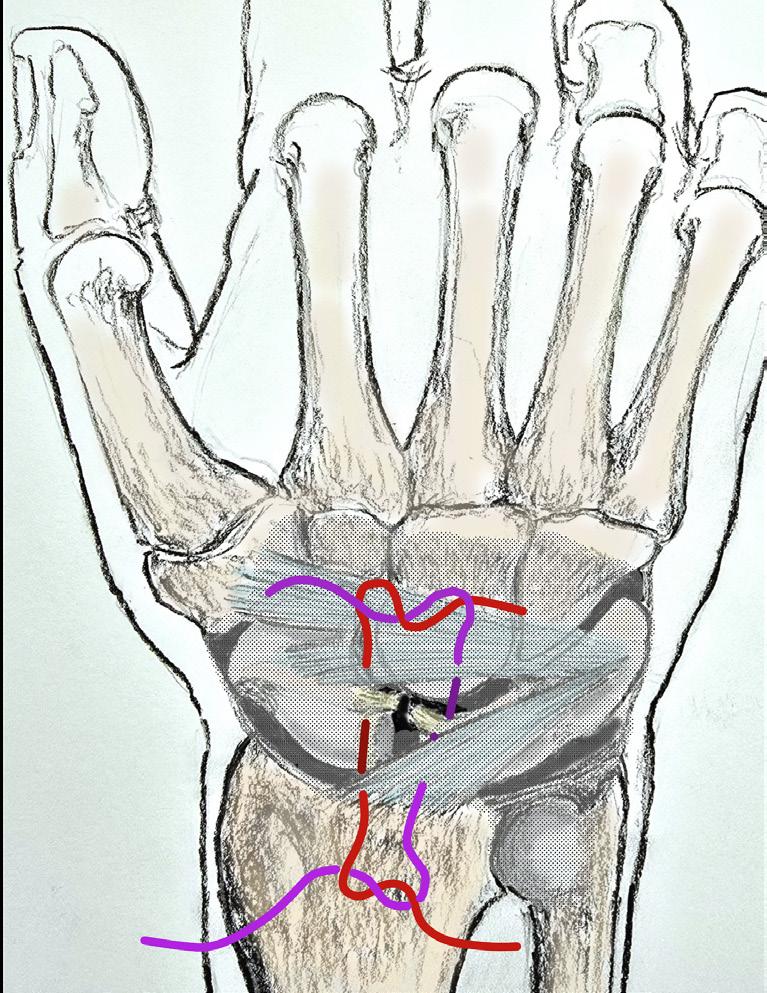
4: Skisse av kapsulo-ligamentær reparasjon am Matoulin. Kapsel og ligamentrestene etter SL-skaden strammes opp, man vil skopisk kunne se en oppstramming av SL-intervallet. Immobiliseres i gips i etterkant. (Illustrasjon O.A.K. Fosse)
Det anbefales å begynne med enklere intraartikulære brudd, for eksempel radiale styloidfrakturer, også kalt «sjåførfraktur». Disse bruddene kan være vanskelig å reponere lukket og artroskopisk får man vanligvis utmerket oversikt og det er lettere å finne riktig rotasjon (Figur 3). Siden stabilitet ulnart i leddet er bevart vil ikke kameraet fra ulnarsiden dislosere bruddet. Med mer erfaring kan man også håndtere mer kominutte brudd, men samtidig vil noen brudd være så knuste at det ikke er så mye å hente på å forsøke å reponere anatomisk skopisk assistert.
Artroskopisk behandling av brudd i skafoid
Det er en klar trend mot økende bruk av artroskopisk assistert behandling av skafoidbrudd de siste årene. Dette gjelder spesielt ved brudd i midtskaft og proksimale pol, og ved pseudartroser. Artroskopi gir direkte visualisering av bruskflater og bruddspalte, og gjør det mulig å reponere og sikre reposisjon med perkutan skruefiksasjon av bruddet. Fordelen sammenlignet med åpen kirurgi er antatt mindre forstyrrelse av blodforsyningen til skafoid og at man kan vurdere og behandle samtidige skader for eksempel SLligamentskade. Samtidig ligamentpatologi forekommer hyppigere enn tidligere antatt, og kan påvirke prognosen for pasientene.
Man etterstreber å få best oversikt over og tilgang til bruddspalten, oftest via egen direkte portal over skafoid midtkarpalt sammen med MCRportalen. Traksjon via traksjonstårnet bidrar ofte til reposisjon av bruddet, som så kan finjusteres med en krok, før man fikserer temporært med perkutan kirschnerpinne. Endelig fiksasjon tilstrebes med en hodeløs kompresjonsskrue, som plasseres under kombinert artroskopisk og radiologisk kontroll.
Studier viser høy tilhelingsrate, gode funksjonelle utfall og lav komplikasjonsrate når artroskopi brukes ved selekterte brudd i skaphoid (3, 4). Etter akutte skaphoidfrakturer er avlastning viktig, men ved god stabilitet etter skruefiksasjon er vanligvis ikke immobilisering nødvendig. Dersom det har vært forsinket tilheling immobiliseres disse skadene oftest i 8 uker, CT brukes til å vurdere tilheling.
ARTROSKOPISK ASSISTERT BEHANDLING
AV LIGAMENTSKADER
Artroskopisk behandling av leddbåndskader i håndroten har blitt stadig mer utbredt de siste årene, og representerer i dag en sentral modalitet for både diagnostikk og behandling av slike skader (3, 68). Skade av SL og LTligamenter og TFCC er blant de vanligste i håndroten, hvor oversett skade eller forsinket behandling kan føre
til kronisk instabilitet og utvikling av symptomatisk artrose. Håndleddsartroskopi gir mulighet for direkte visualisering av intraartikulære strukturer, vurdering av skadeomfang med stabilitetstesting og målrettet behandling med minimal invasivitet og lav morbiditet.
Skafolunære og lunotrikvetrale skader
Akutte leddbåndskader i håndroten oppstår i forbindelse med traume hvor vanligste skademekanisme er fall mot pronert utstrakt arm. Også vridningstraume kan gi disse skadene. Leddbåndskader kan oppstå isolert, da hyppigst på skafolunærligamentet, men også sammen med brudd og/eller luksasjon i karpus, for eksempel håndleddsbrudd, perilunær luksasjon eller radiocarpal frakturluksasjon. Akutte ligamentskader i håndroten presenterer seg ofte med smerte, hevelse og funksjonsnedsettelse, men symptomene kan være subtile. Palpasjonsømhet over karpus, smerter ved passiv bevegelse og nedsatt kraftgrep er vanlig. Det benyttes spesifikke tester for å vurdere SLintervall og LTintervall, i tillegg til en generell håndundersøkelse. Radiologisk diagnostikk starter med røntgen front og side, samt håndrotserie for å identifisere brudd og eventuelle feilstillinger. Økt avstand og/ eller endret konfigurasjon i karpus er indirekte tegn på leddbåndskade. Det er ofte aktuelt å supplere med CT for å utelukke fraktur, eventuelt MR. Suspekte radiologiske funn gir indikasjon for artroskopi av håndleddet, men negativ radiologi utelukker ikke skade dersom anamnese og klinikk er typisk. Artroskopi regnes som gullstandard for å påvise mindre ligamentskader. Ved akutte SL eller LTskader, anbefales artroskopi for vurdering av stabilitet og eventuelt sutur eller pinnefiksasjon der det foreligger synlig skade. Teknikken gjør det mulig å bevare intakt vev og gir raskere rehabilitering.
En del isolerte leddbåndskader blir tolket som distorsjon. Dette gir forsinket diagnostikk og dermed behandling. En oversett akutt ligamentskade kan gi klikking, pseudolåsninger og vedvarende smerter. Ved vedvarende smerter etter håndleddstraume kan leddbåndsskade foreligge til tross for normal røntgen, CT eller MR. I slike tilfeller gir håndleddsartroskopi mulighet for sikker diagnostisk avklaring, vurdering av skadeomfang og stabilitet, samt artroskopisk assistert intervensjon ved behov. Ved subakutte reponerbare leddbåndskader i karpus, som SL og LTinstabilitet, vil kapsuloligamentær reparasjon eller kapsulodeser kunne gi godt resultat (Figur 4).
Man tar da sikte på en oppstramming av omkringliggende strukturer, inkludert det dorsale radiokarpalligamentet (DRC) og dorsale interkarpalligamentet (DIC). Dette kan suppleres med volar kapsulodese, hvor man ved
artroskopisk assistert teknikk strammer opp de volare radiokarpale ligamentene. Dette vil motvirke lunatums tendens til å gå i en dorsal feilstilling samtidig om intervallet mellom skafoid og lunatum strammes opp. Det er publisert lovende resultater med denne type teknikker (6, 7).
Tidligere benyttet man i større grad åpne teknikker hvor man brukte senegraft i bentunneler til å rekonstruere leddbåndene i karpus. Studier viser at kapsulodeseteknikker kan gi tilsvarende kliniske resultater hos mange noe som er fordelaktig siden borrekanaler er forbundet med risiko for brudd og sammenfall av de små håndrotsknoklene. Uttalt instabilitet kan imidlertid fortsatt kreve åpen ligamentrekonstruksjon (3).
Triangular Fibrocartilage Complex-skader
TFCCskader kan opptre i ulike kliniske situasjoner, og håndtering avhenger av om skaden oppstår samtidig med en distal radiusfraktur, om den er en isolert akutt skade, eller om pasienten presenterer med vedvarende, kroniske ulnare håndleddsplager etter tidligere skade.
TFCCskader oppstår ofte i forbindelse med distale radiusfrakturer, særlig ved disloserte brudd. De fleste tilheler uten spesifikk behandling, men hos noen pasienter ser man uttalt instabilitet i distale radioulnarledd eller redusert rotasjon etter reponering. I slike tilfeller bør artroskopisk undersøkelse vurderes. Artroskopi kan avdekke TFCCinterponat som kan reponeres og ofte sutureres. Ved større DRUJinstabilitet må man vurdere stabilisering med pinner mellom radius og ulna, eventuelt i tillegg til artroskopisk sutur.
Isolerte TFCCskader kan være vanskelig å oppdage. Radiologisk utredning omfatter vanligvis røntgen for å utelukke brudd og MR for å påvise eller utelukke TFCCskade. Isolerte akutte TFCCskader behandles stort sett konservativt initialt med immobilisering i gips eller ortose i 4–8 uker.
TFCCskade er samtidig en viktig årsak til senere ulnare håndleddsmerter. Utredning inkluderer grundig anamnese og klinisk undersøkelse. Typiske tester inkluderer ballottementtest for vurdering av DRUJstabilitet og palpasjon ulnart med positiv «fovea sign». MR har moderat sensitivitet og spesifisitet, og ved vedvarende klinisk mistanke kan artroskopi være avgjørende for diagnosebekreftelse, vurdering av skadens omfang og samtidig behandling. Behandlingsvalg avgjøres av skadegrad og type. Artroskopisk debridement er aktuelt ved sentrale
degenerative forandringer, mens perifer eller ligamentær ruptur behandles med artroskopisk sutur/reinserering. Ulnaforkortning eller waferprosedyre vurderes ved positiv ulnar varians, særlig ved kroniske degenerative forandringer.
Rehabilitering etter artroskopisk behandling av leddbåndskader er vesentlig for et godt resultat og innebærer gradvis mobilisering samt tverrfaglig oppfølging mellom lege og fysioterapeut/håndterapeut. Postoperativt immobiliseres pasientene vanligvis i gips i 68 uker før man starter opptrening. Det er vanligvis relativt uttalt stivhet i håndleddet ved oppstart av rehabilitering, og det er vesentlig for prognosen at pasientene utfører gradvis mobilisering og systematisk fysioterapi/ergoterapi. Full belastning anbefales ikke før ca. 3 måneder postoperativt.
Håndrot- og håndleddluksasjoner Håndrot og håndleddluksasjoner, med eller uten fraktur, oppstår som regel etter høyenergitraumer og er ofte kombinert med andre skader. Radiologiske undersøkelser gir ikke alltid et fullstendig bilde av skadeomfanget i karpus, og både brusk, kapsel og leddbåndskader kan være vanskelig å identifisere fullt ut. I slike situasjoner kan håndleddsartroskopi være et nyttig supplement til åpen kirurgi, både for diagnostikk og behandling.
Perilunære frakturluksasjoner har tradisjonelt blitt behandlet med åpen tilgang dorsalt, eventuelt kombinert med en volar tilgang. Hvis ikke lukket reposisjon lykkes, vil man oftest kunne reponere artroskopisk. Videre kan man artroskopisk avklare skadeomfang, fjerne interponat og sikre nøyaktig reposisjon mens man plasserer nødvendig osteosyntesemateriell uten åpen tilgang (4).
Radiokarpale frakturluksasjoner involverer skade av de radiokarpale ligamentene, slik at hele karpus forskyves fra radius’ leddflate, oftest gjennom avulsjon av ligamentinnfestningen på distale radius. Disse skadene er sjeldne, men alvorlige, og lukket reposisjon er som regel utilstrekkelig. Frakturkomponenten av skaden må reponeres eksakt og fikseres, oftest gjennom åpen tilgang. Artroskopi kan bidra til dette ved å gi direkte visualisering av leddflaten slik at reposisjon av spesielt styloidfragmentet kan kontrolleres og justeres før fiksasjon. Artroskopi gjør det også mulig å fjerne løse brusk og benfragmenter, samt identifisere interponerte ligamentstrukturer som kan påvirke både stabiliteten og resultatet av osteosyntesen (5).
Selv om disse skadetypene forekommer relativt sjelden, er det ikke uvanlig at det samtidig foreligger andre skader
i håndroten som ikke fullt ut fremkommer radiologisk. En systematisk artroskopisk gjennomgang av håndledd og håndrot kan derfor være avgjørende for å kartlegge det totale skadeomfanget og sikre en målrettet og komplett behandling.
LÆRINGSKURVE, KOMPLIKASJONER OG
ORGANISATORISKE FORHOLD
Håndleddsartroskopi har en lang læringskurve. Det begrensede leddvolumet, behov for høy instrumentpresisjon og anatomiske variasjoner gjør teknikken krevende for uerfarne kirurger. Studier viser at erfaring påvirker både diagnostisk nøyaktighet og komplikasjonsrate. Systematisk opplæring gjennom kadaverlaboratorier, simulering, mentorbasert supervisjon og gradvis progresjon fra diagnostiske til terapeutiske prosedyrer anbefales. Komplikasjoner som iatrogen bruskskade og seneskade forekommer nesten utelukkende tidlig i læringskurven, mens infeksjon, stivhet og nerveskade generelt er sjeldne ved artroskopiske inngrep (9,10). Enkelte brudd og leddbåndskader ender likevel med vedvarende instabilitet eller artroseutvikling tross adekvat initial behandling.
En organisering som legger til rette for artroskopi på operasjonsstuer brukt til akutt håndskadebehandling er nyttig. Tilgjengelighet av skopi gjør planlegging av inngrep enklere og gir mulighet til å bruke artroskopi når indikasjonen er til stede. Dette bidrar samtidig til erfaring og kompetansebygging, men indikasjonen må alltid styres av skadebildet snarere enn av tilgjengelig utstyr.
Tidlig og korrekt diagnostikk, konservativ behandling eller målrettet kirurgi – inkludert håndleddsartroskopi – gir best mulig prognose for å gjenvinne funksjon etter håndrot og håndleddsskader. Man vil oftest kunne oppnå god funksjon, høy pasienttilfredshet og lav risiko for artroseutvikling dersom skaden behandles tidlig og adekvat.
REFERANSER :
Se bakerst i nettutgaven på kirurgen.no
Kan det være deg? For mer informasjon om hva vi trenger, scan QR-koden eller gå til: legerutengrenser.no/jobb-for-oss
Har du spørsmål? Kontakt oss på epost: rekruttering@legerutengrenser.no
Rotatorcuffpatologi er blant de vanligste årsakene til skulderplager, men sammenhengen mellom strukturelle funn og kliniske symptomer er ofte uklar. En betydelig andel rupturer er asymptomatiske, noe som stiller høye krav til klinisk vurdering og behandlingsvalg. De senere årene har flere sentrale publikasjoner, inkludert bidrag fra ledende norske forskere, bidratt til økt forståelse av hvilke faktorer som bør vektlegges. Denne artikkelen gjennomgår aktuelle prinsipper for diagnostikk og behandling med særlig fokus på pasientseleksjon for kirurgi versus konservativ behandling.
THORA KRISTIN YTREHUS JØRGENSEN, BERTE MARIE BØE ORTOPEDISK KLINIKK, OSLO UNIVERSITETSSYKEHUS
KORRESPONDANSE: THORA KRISTIN YTREHUS JØRGENSEN - KRYTRE @ OUS - HF.NO
RELEVANTE ANATOMISKE FORHOLD
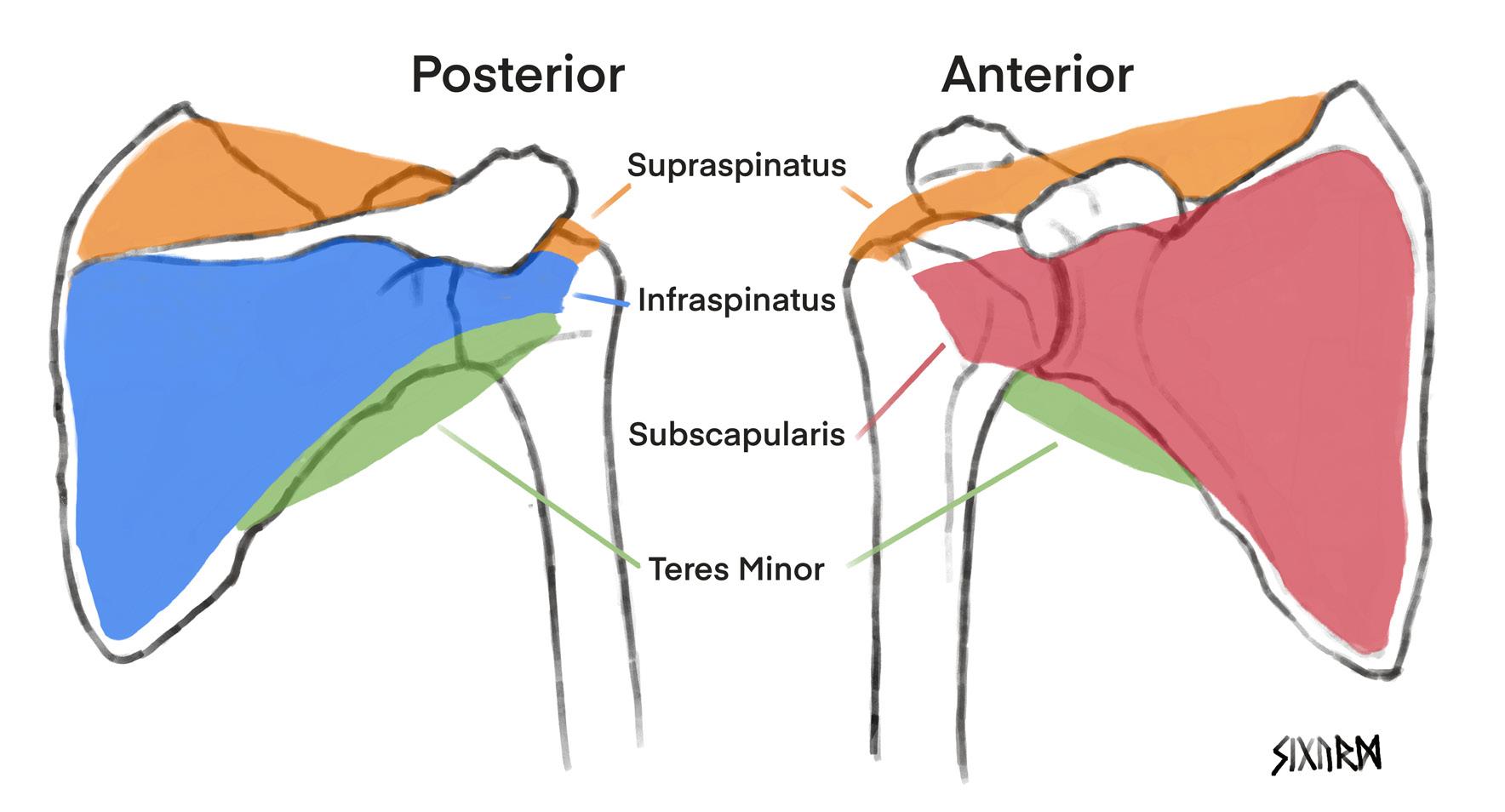
Skulderleddet er den menneskelige kroppens mest bevegelige ledd. Ulempen ved dette er at det også er kroppens mest ustabile ledd. Rotatorcuffen (RC), eller «skuldermansjetten», består av de 4 musklene supraspinatus, infraspinatus, subscapularis og teres minor som abduserer, utadroterer og innadroterer skulderen (Figur 1, Bilde 1). I tillegg har de en viktig funksjon som dynamiske stabilisatorer. Deres primære biomekaniske funksjon er å stabilisere glenohumeralleddet ved å komprimere humerushodet mot glenoid.
ETIOLOGI OG SYKDOMSUTVIKLING
Årsaken til RCpatologi er multifaktoriell. Rupturer kan komme etter et adekvat traume som ved skulderluksasjon, men vi vet også at andre faktorer spiller inn. Alder, genetikk og komorbiditeter, som diabetes mellitus type 2 og bindevevssykdom, påvirker rotatorcuffen. Disse faktorene både øker sjansen for degenerative endringer samt påvirker tilheling ved kirurgisk behandling av rupturer. RCpatologi er et sykdomsspektrum som spenner seg fra
tendinose til delrupturer, videre til fullruptur av en sene til massive rupturer av hele rotatorcuffen. Til slutt ser vi senkomplikasjoner (cuff-artropati) som kommer i kjølvannet av en massiv RCruptur (Bilde 2). Selve mekanismen bak denne progresjonen er ennå ikke godt kartlagt. Inflammasjon antas å spille en viktig rolle og kan bidra til å forklare hvorfor pasienter med diabetes mellitus har økt forekomst, siden sykdommen skaper et mer proinflammatorisk miljø i kroppen (1).
DEGENERATIVE VERSUS TRAUMATISKE RUPTURER
Det foreligger per i dag ingen entydig konsensus for klassifikasjon av RC-skader. En praktisk og klinisk anvendbar inndeling, basert på rupturens morfologi og skademekanisme, gir imidlertid et godt grunnlag for både beskrivelse og behandlingsvalg. Det er vanlig å skille mellom degenerative rupturer, traumatiske rupturer og en tredje gruppe betegnet «akutt på kronisk ruptur». Disse gruppene vurderes forskjellig med hensyn til behandling, ettersom kirurgisk resultat varierer betydelig mellom dem. Behandlingsstrategien for en 78 år gam
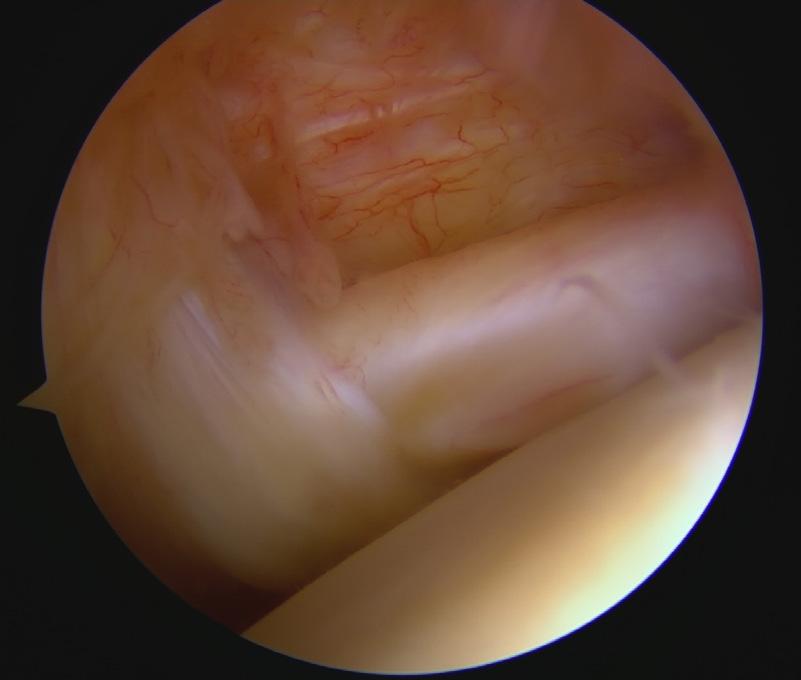
BILDE 1: Intakt subscapularisseneinnfestning. Caput humerus til høyre i bilde. Midtre glenohumeralligament krysser senen vertikalt til venstre i bildet. Pasienten har samtykket til publisering av bildet.
mel pasient med gradvis utviklede skuldersmerter over måneder vil derfor avvike fra tilnærmingen til en 45 år gammel pasient, som etter et fall under løping får akutt innsettende smerter og kraftsvikt i utadrotasjon. Morfologisk klassifiseres rupturene som partielle eller fulltykkelsesrupturer, avhengig av om deler av eller hele senens tykkelse er affisert. Se avsnittet om bildeutredning for mer informasjon om morfologi.
EN NATURLIG DEL AV ALDRINGSPROSESSEN?
Symptomatiske RCrupturer vil gi plager som smerter, redusert skulderbevegelse og manglende muskelstyrke. Det er godt dokumentert at rupturene ikke nødvendigvis er symptomatiske. Blant 211 personer med RCruptur, bosatt i en japansk landsby og i alder 3487 år, var 65 % asymptomatiske (2). Tilsvarende, i en studie av 464 kvinner i
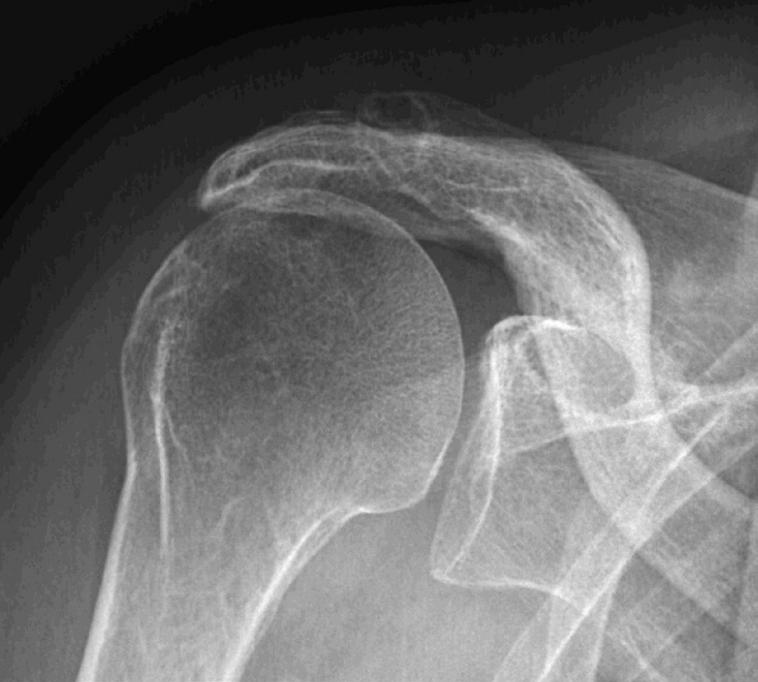
BILDE 2: Røntgen som viser høystand av caput humerus. Langvarig feilstilling har ført til at caput har slitt bort undersiden av acromion, «acetabularisering». Pasienten har samtykket til publisering av bildet.
alderen 6487 år bosatt i Storbitannia, var 48% asymptomatiske (3). Vi vet at ved delrupturer er prosentandelen av asymptomatiske pasienter enda høyere. Utfordringen er klinisk å vurdere hvem som har en symptomatisk RCruptur og følgelig hvem som vil ha nytte av kirurgisk behandling.
PROGNOSTISKE FAKTORER
Flere prognostiske faktorer som alder, diabetes mellitus type 2, røyking, hyperlipidemi, overvekt, og kjønnshormonmangel (østrogen eller testostosteronmangel) spiller en rolle i utvikling av RCskader. De har også en negativ innvirkning på tilheling. Har man en RCruptur vil størrelsen på rupturen fortsette å øke med tid, men selv i studier med lang oppfølgingstid ser vi at økningen er liten til moderat og det funksjonelle resultatet er adekvat. Hos
Klinisk parameter Supraspinatusruptur
Primær funksjon Initiering av abduksjon (0–15°)
Smerteområde Laterale overarm
Infraspinatusruptur Subscapularisruptur
Utadrotasjon
Innadrotasjon
Posterolateralt i skulderen Anteriort i skulderen
Aktiv bevegelighet Smertefull/svekket abduksjon Redusert utadrotasjon Redusert innadrotasjon
Passiv bevegelighet Ofte bevart
Ofte bevart Ofte bevart Kraftsvikt Abduksjonssvikt Utadrotasjonssvikt Innadrotasjonssvikt
Spesifikke kliniske tester Jobe (Empty can), painful arc test, drop arm test
Pseudoparalyse Kan forekomme ved større rupturer
Assosierte funn Subakromial smerte
Typisk etiologi
Degenerativ
External rotation lag sign, lillefingertest
Lift-off, belly press test
Sjeldent isolert Kan forekomme ved større rupturer
Ofte kombinert med supraspinatusruptur Bicepsaffeksjon (pulley-lesjon)
Degenerativ/kombinert Ofte traumatisk
TABELL 1: Sammenlikning av typiske funn ved skade til de forskjellige rotatorcuff-senene.
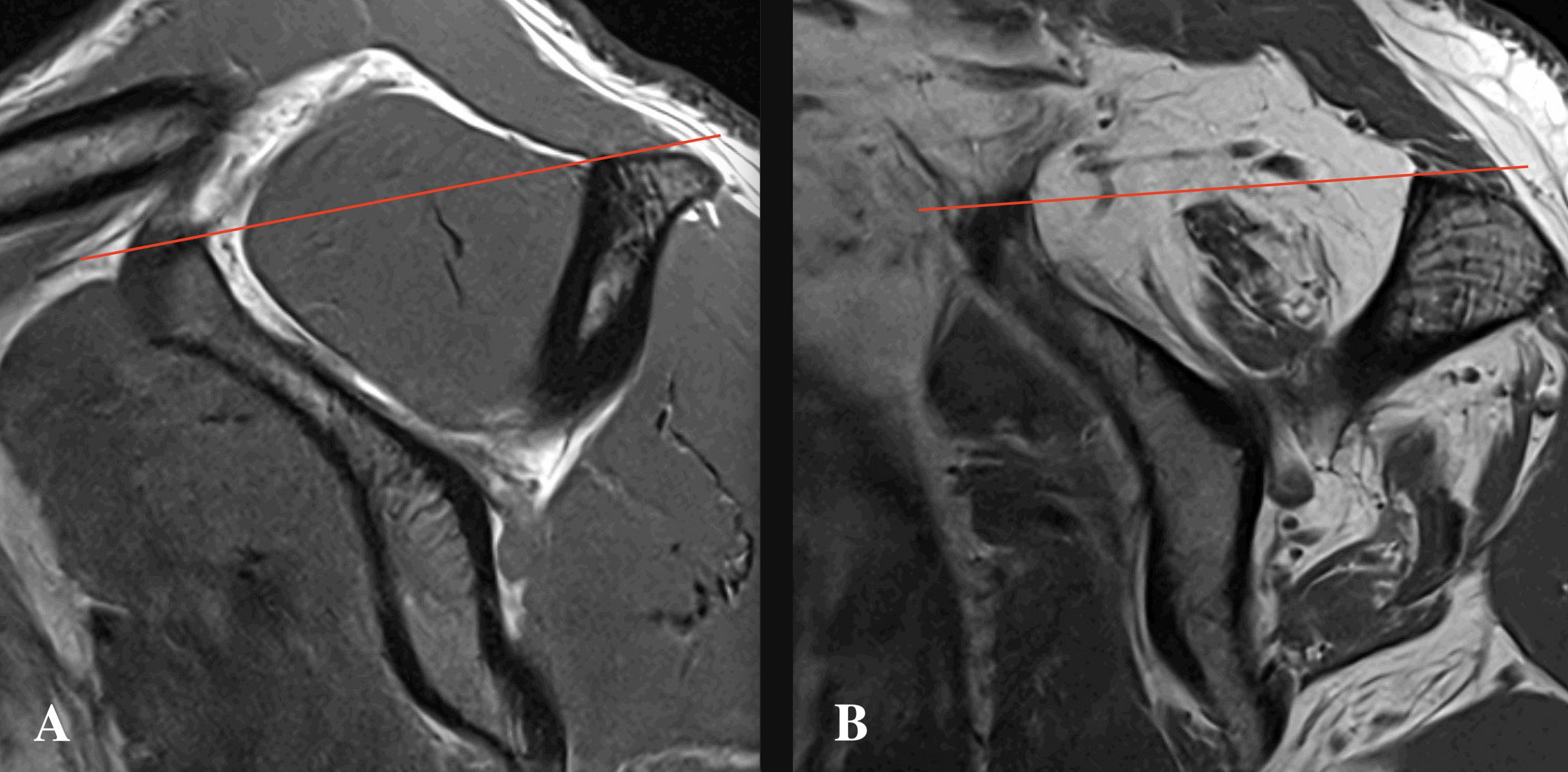
BILDE 3: A) Et negativt tangenttegn foreligger når supraspinatus-muskelen berører eller krysser en tenkt linje (rød linje) mellom spina scapulae og coracoid, som indikerer bevart muskelvolum. B) Et positivt tangenttegn foreligger når muskelen ikke når opp til denne linjen, noe som tyder på fettinfiltrasjon og muskelatrofi. Pasientene har samtykket til publisering av bildet.
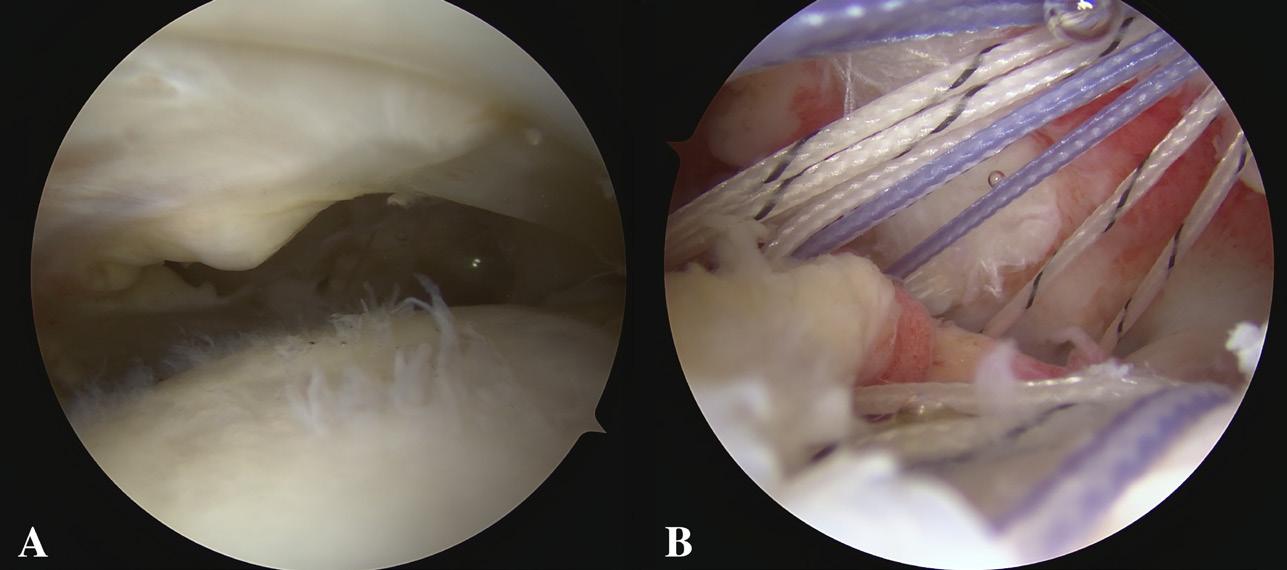
4: A) Supraspinatusruptur B) Sutur av supraspinatusruptur. Pasienten har samtykket til publisering av bildet.
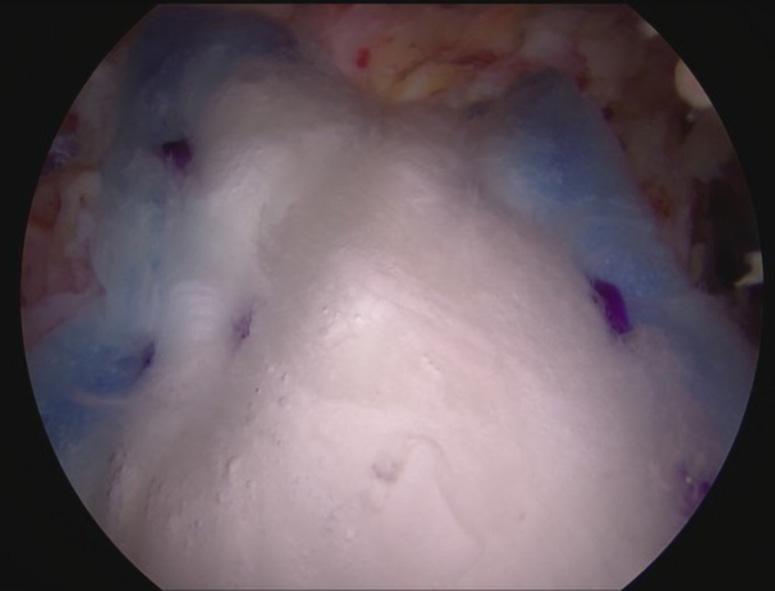
BILDE 5: Bruk av bioinduktivt collagenimplantat som forsterkning ved sutur av supraspinatus. Pasienten har samtykket til publisering av bildet.
noen få vil rupturen progrediere mer og de kan samtidig utvikle muskelatrofi og fettinfiltrasjon. Dette kan igjen gi et dårlig funksjonelt resultat (4).
KLINISK
Klinisk kan pasienter med RCrupturer grovt deles i to hovedgrupper: pasienter med akutte traumatiske rupturer og pasienter med kroniske degenerative rupturer. Akutte traumatiske rupturer presenteres typisk med plutselig innsettende smerter og kraftsvikt. Degenerative rupturer utvikler seg gradvis over tid, hvor smerter som regel er mer fremtredende enn funksjonstap. Den største pasientgruppen er imidlertid de med en akutt på kronisk ruptur, der et tilsynelatende beskjedent traume, for eksempel løft av en gjenstand fra en hylle, utløser symptomene og videre utredning med MR viser at muskelen allerede hadde kroniske forandringer som atrofi og fettinfiltrasjon.
Anamnesen bør derfor alltid inkludere spørsmål om skulderfunksjon og symptomer i tiden før den aktuelle hendelsen. Mange pasienter vil da beskrive langvarige, fluktuerende plager. Ettersom RC-patologi ofte er bilateral, bør funksjonen i kontralateral skulder også vurderes. Det finnes flere kliniske tester for vurdering av RC-muskulaturen (Tabell 1). Testenes sensitivitet og spesifisitet varierer (5). Funnene må derfor tolkes i sammenheng med anamnese og bildediagnostikk for å stille korrekt diagnose.
BILDEDIAGNOSTISK VURDERING
Konvensjonell røntgenundersøkelse bør alltid utføres initialt for å utelukke fraktur og vurdere benete forhold. Ultralyd (UL) og/eller magnetisk resonans (MR) benyttes deretter for diagnostikk av RCrupturer. En fordel med UL er muligheten for dynamisk undersøkelse ved aktiv og passiv bevegelse av skulderen. Metoden er kostnadseffektiv og ofte lett tilgjengelig, men undersøkelseskvaliteten er i stor grad operatøravhengig.
MR gir en mer detaljert fremstilling av senekvalitet og muskulatur og er avgjørende for vurdering av prognostiske faktorer. Det er særlig viktig å vurdere grad av fettinfiltrasjon og muskelatrofi, som begge er assosiert med dårligere prognose. Fettinfiltrasjon klassifiseres etter Goutallier, mens muskelatrofi i supraspinatus kan vurderes ved positivt tangenttegn i sagittalplanet (Bilde 3).
MR benyttes videre til å måle rupturens anteroposteriore utbredelse samt grad av seneretraksjon i mediolateral retning. Samlet gir disse faktorene, fettinfiltrasjon, muskelatrofi, rupturstørrelse og retraksjon, et grunnlag for klassifikasjon av skaden og vurdering av kirurgisk behandlingsmulighet.
Ved større, kroniske rupturer vil caput humeri over tid kunne migrere kranialt og føre til kontakt og slitasje mot undersiden av acromion (Bilde 2). Denne høystanden kalles cuff-artropati og skyldes endret glenohumeral biomekanikk som følge av sviktende RCfunksjon. Graden av kranial migrasjon korrelerer med rupturens størrelse. Fenomenet kan påvises på konvensjonell røntgen, men lar seg ikke adekvat vurdere på MR ettersom undersøkelsen utføres i liggende stilling.
INDIKASJONER FOR KONSERVATIV VERSUS KIRURGISK BEHANDLING.
Faktorer som taler for konservativ behandling inkluderer høy alder (≥ 70 år), beskjedne symptomer, lang sykehistorie, fravær av traume, uttalt fettinfiltrasjon i muskulaturen, røyking og betydelig komorbiditet. Faktorer som taler for kirurgisk behandling er yngre pasienter (< 60 år), kort symptomvarighet, forutgående traume samt kraftsvikt eller pseudoparalyse. (Bilde 4). Pasienter med liten seneretraksjon på MR, god skulderfunksjon, tilfredsstillende kraft og begrensede smerter kan i første omgang behandles konservativt. De behandles med strukturert trening i regi av fysioterapeut, følges poliklinisk og informeres om rekontakt ved symptomforverring. Pasienter over 65 år i god allmenntilstand med akutt skade og betydelig krafttap bør vurderes for og som hovedregel tilbys kirurgisk behandling (6). Det er samtidig viktig å informere pasienten om at kirurgisk behandling innebærer en langvarig rehabiliteringsperiode, noe som for mange vil ha betydning for behandlingsvalget.
POSTOPERATIV OPPFØLGING OG REHABILITERING
Etter kirurgi har pasienten armen i fatle i 36 uker. De starter bevegelighetstrening fra dag 1 etter operasjon, men med begrensninger i bevegelsesutslag de første ukene. Det er viktig å unngå vektbelastning i 3 måneder etter kirurgi da senene har lang tilhelingstid. Total rehabiliteringstid og opptrening tar ca. 1 år (6).
RESULTATER OG PROGNOSE
All kirurgisk behandling innebærer risiko for komplikasjoner. Ved artroskopisk sutur av RCrupturer rapporteres en forekomst av adhesiv kapsulitt på 3 %, samt 12 % risiko for nerveskade og 0,8% risiko for dyp infeksjon (7). Reruptur er en velkjent komplikasjon etter RCsutur, med rapporterte rater på 10–75 % ved sutur av supraspinatus med eller uten samtidig infraspinatusaffeksjon (8). Resultatene er noe bedre ved sutur av subscapularis, hvor rerupturraten er rapportert til 0–32 % (9). Variasjonen i rerupturfrekvens reflekterer blant annet pasientrelaterte faktorer som alder, grad av fettinfiltrasjon og komorbiditet.
Korttidsresultater etter kirurgi er gjennomgående gode, også hos pasienter som utvikler reruptur (10). Langtidsdata viser imidlertid at reruptur er assosiert med dårligere funksjonelle resultater over tid.
Ved små og mellomstore rotatorcuffrupturer viser sammenlignende studier at både kirurgisk behandling og strukturert fysioterapi gir gode resultater på kort sikt (11). Over tid har imidlertid opererte pasienter bedre utfall enn pasienter behandlet konservativt (11). Samtidig viser studiene at majoriteten av pasienter som initialt behandles med fysioterapi ikke har behov for senere kirurgi, og at de som eventuelt opereres etter mislykket konservativ behandling oppnår gode resultater (11). Dette understreker betydningen av grundig pasientinformasjon, nøye vurdering av prognostiske faktorer og individuell tilpasning av behandlingsstrategi, inkludert optimal timing for kirurgi.
NÅR BØR PASIENTEN HENVISES?
Pasienter med indikasjon for kirurgisk behandling bør henvises til ortopedisk vurdering. Hastighetsgrad ved vurdering avhenger av pasientrelaterte faktorer og skadetype. Enkelte pasientgrupper har særlig nytte av tidlig henvisning og bør derfor henvises akutt: Totalrupturer av infraspinatus bør opereres så raskt som mulig ettersom denne senen raskt utvikler fettinfiltrasjon og atrofi. Akutte subscapularisrupturer bør ideelt opereres innen 68 uker da arrdannelse og seneretraksjon vanskeliggjør sutur ved senere kirurgi. Akutte supraspinatusrupturer bør som hovedregel opereres innen 4 måneder fra skadetidspunkt. Pasienter med degenerative RCrupturer som har gjennomgått adekvat og strukturert treningsbehandling med fysioterapeut i minst 3 måneder uten tilfredsstillende klinisk bedring, bør også henvises for vurdering.
FREMSKRITT I BEHANDLINGEN
Til tross for utvikling av nye kirurgiske teknikker som for eksempel «doublerow repair», hvor man bruker to rader med suturankre, har rerupturraten ved RCsutur forblitt relativt uendret. Svikt kan oppstå både i senetilbentilhelingen og som progresjon av degenerative forandringer i selve senen. Dette har ført til økt interesse for tilleggsbehandlinger og alternative kirurgiske strategier med mål om å forbedre tilheling og redusere reruptur.
Flere tilnærminger er undersøkt, inkludert ortobiologiske tiltak som benmargsstimulering, platerikt plasma (PRP), stamcellebehandling og graftforsterkning med allo, xeno og autograft. I tillegg er alternative kirurgiske løsninger utviklet, særlig for pasienter med massive rotatorcuffrupturer, herunder øvre kapselrekonstruksjon og subakromiell ballongimplantasjon. Flere av disse meto
dene benyttes internasjonalt, spesielt i USA, men regnes per i dag som eksperimentelle i Norge og bør fortrinnsvis utføres innenfor rammen av kliniske studier. Dette skyldes begrenset dokumentasjon, hovedsakelig basert på små studier, og fravær av robuste langtidsdata som dokumenterer sikker klinisk effekt.
Det foreligger imidlertid nylig publiserte data fra en randomisert kontrollert studie fra Spania med 124 pasienter, der bruk av et bioinduktivt kollagenimplantat som forsterkning ved rotatorcuffsutur ble evaluert (Bilde 5). Studien har publisert både 1 og 2års oppfølgingsdata og viser en signifikant reduksjon i rerupturrate ved både 1 og 2 år. Ved 2årskontroll var rerupturraten 12,3 % i intervensjonsgruppen sammenlignet med 35,1 % i kontrollgruppen, vurdert med MR (p < 0,01) (8). Langtidsdata mangler fortsatt, men de foreløpige resultatene fremstår lovende.
IRREPARABLE MASSIVE
Ved rupturer som omfatter både supraspinatus, infraspinatus og subscapularis kan man forsøke å gjøre en delsutur og sy bakre (infraspinatus) og fremre (subscapularis) del av cuffrupturen og på den måten bedre balansen i skulderen. Hos de yngre med høye krav til skulderfunksjon kan det gjøres senetransfer hvor man flytter på senefester så en sene utenfor rotatorcuffen tar over jobben til senen med skade. Et eksempel på dette er latissimus dorsisenetransfer ved skade på supraspinatus og infraspinatus. For de eldre pasientene hvor skaden er for stor til dette vil gullstandard av behandling være revers skulderprotese.
OG KLINISKE ANBEFALINGER
Rotatorcuffen består av fire muskler med ulik klinisk presentasjon, undersøkelsesfunn og behandlingsrespons. Behandlingsvalg må baseres på en helhetsvurdering av pasientfaktorer som alder, skademekanisme, symptombyrde, komorbiditet og aktivitetsnivå, samt bildediagnostiske funn som rupturstørrelse, retraksjon, fettinfiltrasjon og muskelatrofi. Totalrupturer av infraspinatus bør opereres så tidlig som mulig etter skadetidspunkt. Subscapularisrupturer bør ideelt behandles kirurgisk innen 6–8 uker etter skade.
I arbeidet med manuskriptet er kunstig intelligens baserte språkverktøy benyttet til språklig forbedring og strukturering. Bruken har ikke påvirket de faglige vurderingene.
REFERANSER : Se bakerst i nettutgaven på kirurgen.no
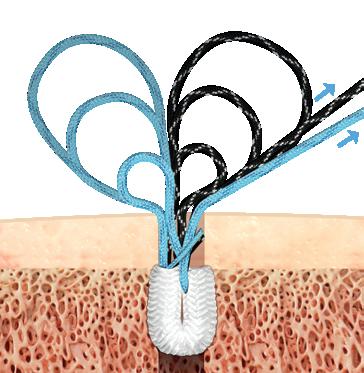
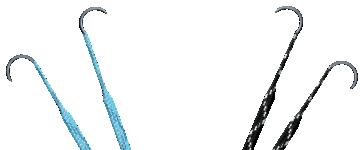
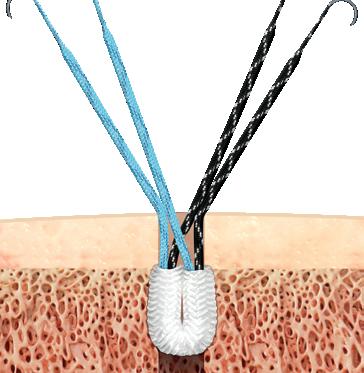

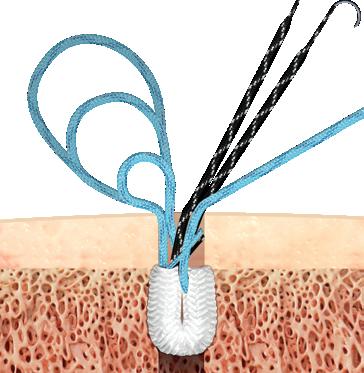

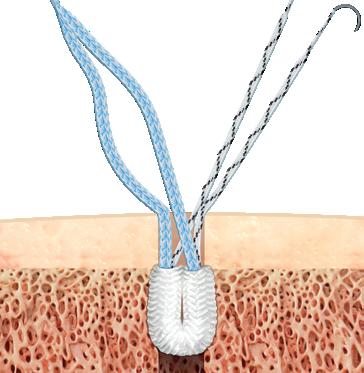
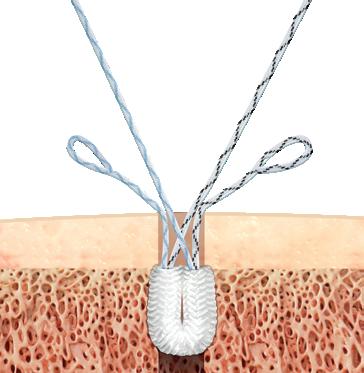
›
›
›
›
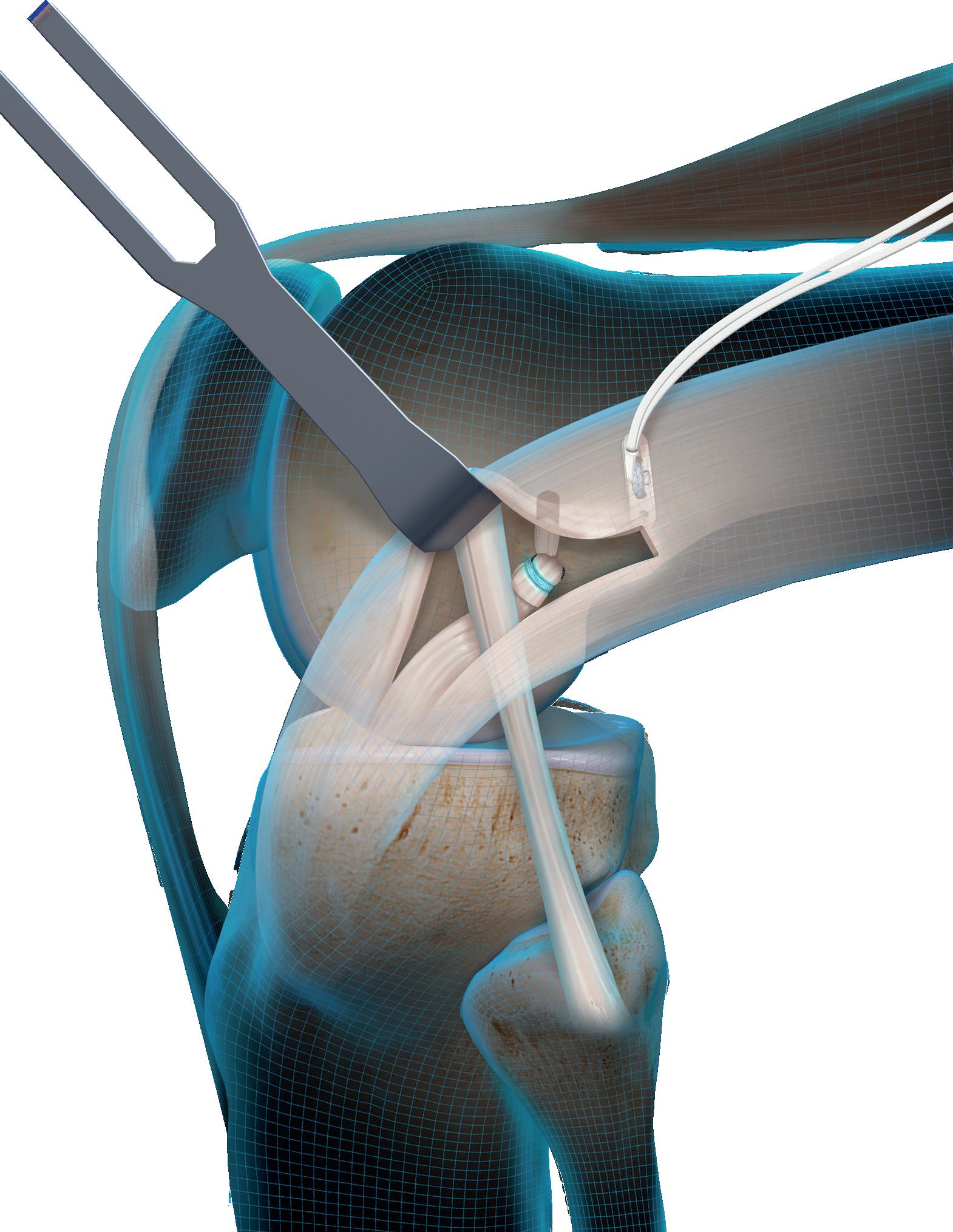
Artroskopi fikk sitt gjennombrudd i 1970- og 1980-årene, og i begynnelsen ble albueartroskopi nesten utelukkende benyttet til diagnostikk og fjerning av frie legemer. I løpet av de siste 30 årene har metoden imidlertid utviklet seg til et terapeutisk verktøy med et bredt spekter av anvendelser, både ved akutte og kroniske tilstander. I denne artikkelen oppsummerer vi indikasjoner og tekniske prinsipper, og belyser metodens plass og potensial i moderne albuekirurgi.
ASTRID ROSENBERG 1, ANNE - MARI ROSENLUND 1, HALLGEIR BRATBERG 1, ENDRE SØREIDE 1, OLE A. K. FOSSE 1, SONDRE HASSELLUND 1 1 SEKSJON FOR HÅND - OG ALBUEKIRURGI, OUS AKER
KORRESPONDANSE: ASTRID ROSENBERG - ASTRRO @ OUS - HF.NO
ANATOMI OG TEKNISKE FORHOLD
Relevant anatomi
God anatomisk kunnskap er grunnleggende for trygg og effektiv albueartroskopi. Albuen tillater fleksjon/ekstensjon i ulnohumeralleddet og rotasjon i det proksimale radioulnarleddet, og kjennskap til biomekanikk samt statiske og dynamiske stabilisatorer er nødvendig. Både fremre og bakre leddkammer undersøkes og behandles. Sentrale landemerker markeres alltid preoperativt: laterale og mediale epikondyl, caput radii, olecranon og ulnarisnervens forløp.
Nærheten til nevrovaskulære strukturer krever presis portalplassering og instrumenthåndtering. For å øke avstanden til kar og nerver settes vanligvis cirka 20 ml natriumklorid intraartikulært i “soft spot” før man introduserer trokar og skop.
Preoperativt bør ulnarisnerven palperes mens albuen beveges for å avdekke subluksasjon. Manglende oppmerksom for dette øker risikoen for nerveskade. Tidligere albuekirurgi, særlig ulnaristransposisjon, kan gjøre tilgangen vanskeligere og øke komplikasjonsrisikoen, og pasienten må informeres om dette før inngrepet.
Portalplassering
Riktig portalvalg er avgjørende for oversikt og sikkerhet. Nedenfor beskrives de vanligste portalene (13), se Figur 1.
Proksimale anterolaterale portal: Standard startportal, plassert cirka 2 cm proksimalt og anteriort for laterale epikondyl.
Anteromedial portal: Brukes ofte sammen med den laterale portalen ved skopi i fremre leddkammer. Den etableres stort sett med “insideout”teknikk, hvor en butt trokar føres fra lateralt gjennom albueleddet og gjennom kapsel ut anteromedialt for trochlea. Hudincisjonen legges der trokarspissen butter mot huden, typisk 1–2 cm distalt og 2 cm anteriort for mediale epikondyl.
Proksimal anteromedial portal: Plassert cirka 2 cm proksimalt og anteriort for epikondylen. Ved behandling av laterale albuesmerter kan denne være fordelaktig for å kunne vurdere laterale kapsel og radiocapitellærleddet før debridement. Det er viktig å palpere septum intermuskulare og identifisere mediale epikondyl tydelig før innføring.
Posterolaterale portaler (soft spot): Posterolateralt plasseres oftest to portaler, en i soft spot og en langs olecranonkanten 2 cm pr oksimalt. Gjennom disse portalene får man god oversikt over triangulærpunktet, bakre del av capitellum, caput radii samt ulnohumeralleddet.
Transtriceptal portal: Plasseres cirka 3 cm proksimalt for olecranon. Kombinert med den proksimale posterolaterale portalen får man god oversikt over fossa olecranii og mediale gutter.
I bakre deler av leddet må man ofte gjøre et debridement med shaver før man oppnår god oversikt. I fossa olecranii er det viktig å være varsom med shaver/benfres mot medialt for å unngå skade på ulnarisnerven. Man bør også være oppmerksom på at noen har en anatomisk åpning i fossa olecranii som gir kommunikasjon mellom fremre og bakre leddkammer.
Leiring og utstyr
Albueskopi kan utføres i rygg, side eller mageleie. Vi bruker sideleie med armen over en pøll, slik det er beskrevet av O’Driscoll og Morrey (1, 4). En blodtomhetsmansjett plasseres proksimalt, skulderen abduseres 90°, og pøllen støtter overarmen slik at albuen ligger i 90° fleksjon (Figur 2). Det er viktig at pasienten ikke siger bakover, da pøllen ellers havner for distalt og reduserer plassen i fremre leddkammer. Albuen må kunne flekteres, ekstenderes og roteres fritt.
Vi bruker rutinemessig 2.9 mm artroskop med hylse uten skyllehull, men skop og instrumenter med større kaliber (4.0, kneskop) kan være nyttig for eksempel i et degenerativt ledd med mye synovitt og påleiringer. Shaver brukes alltid for å etablere oversikt. Andre instrumenter det er nyttig å ha tilgjengelig er benfres, bor, fattetenger, skarp skje, meisler og retraktorer. Vi bruker ikke egne hylser i portalene, og det kan i starten være utfordrende å få instrumenter ut og inn. Et tips er å føre kameraet med kamerahylsen gjennom leddet og ut motsatt portal, slik at hylsen kan brukes til å føre et instrument inn i leddet.
Trykket i leddet holdes rundt 30–45 mmHg for å redusere ødem. I fremre leddkammer kan leddhulen kollapse ved aktivt sug og det kan være utfordrende å skaffe seg god oversikt. Bruk av retraktor kan være nyttig.
INDIKASJONER FOR ALBUEARTROSKOPI
Frie legemer
Frie legemer gir typisk mekaniske plager med smerte, låsning og opphakning. Fjerning av frie legemer har tradisjonelt vært den vanligste indikasjonen for albueartroskopi. Diagnosen stilles oftest med CT eller MR. Legemene
kan ligge nær sagt hvor som helst, men hyppigst i fossa coronoidea, fossa olecranii og ved triangulærpunktet posterolateralt. Små legemer kommer ofte til syne når shaveren brukes med lett sug. De fanges med fattetang straks de er synlig. Større legemer krever ofte utvidede portaler for å kunne fjernes uten fragmentering.
«Frie legemer» er ikke alltid helt frie. Mange sitter delvis fast i kapsel og må løsnes med shaver før fjerning. Artroskopisk teknikk gir samtidig utmerket oversikt over leddbrusken og synovialhinnen (Figur 3), slik at eventuelle bruskskader og synovitt kan vurderes og behandles.
Artrose
Artrose i albuen rammer særlig middelaldrende menn i fysisk krevende arbeid (5). Risikoen øker ved tidligere skader, både skader behandlet konservativt og operativt, men særlig etter mer omfattende skader som frakturluksasjoner (6).
I motsetning til artrose i vektbærende ledd er bruskhøyden i albuen ofte bedre bevart. Funnene domineres oftest av osteofytter (påleiringer) og frie legemer (7). Kapselkontraktur er særlig typisk ved posttraumatisk artrose. Osteofytter gir typisk impingementsmerter i ytterstilling for fleksjon og ekstensjon.
CT er nyttig for å kartlegge omfanget og planlegge behandling av albueartrosen (Figur 4). Før kirurgi forsøkes konservativ behandling med hvile og NSAIDs. Hovedmålet hos pasienter uten større bevegelsesbegrensning er smertelindring og færre mekaniske plager. Mange vil også oppleve bedret, men sjelden normal, bevegelighet etter operasjon. Oftest vil artroskopisk behandling av albueartrose innebære debridement, fjerning av frie legemer, reseksjon av osteofytter med meisel eller benfres og eventuelt fremre kapsulotomi (8, 9). Ved samtidig tegn til ulnarisnevropati anbefales åpen dekompresjon av nerven dersom dette er en vesentlig del av symptomene.
Etter inngrepet får pasienten bevege fritt, men skal avlaste (0,5 kg) til de har smertefri bevegelighet.
Posttraumatisk stiv albue
Albuen er mer disponert enn andre ledd for tilstivning, typisk etter skade eller kirurgi. Leddet kan i prinsippet stivne i alle retninger. Rotasjonstap gir oftest mindre symptomer, mens tap av ekstensjon er den vanligste plagen hos pasientene. Det er to hovedgrupper av intraartikulære årsaker til tilstivning; kapselfortykkelse og fibrose/adheranser i selve leddspalten, hvor kapselfortykkelse er vanligst.
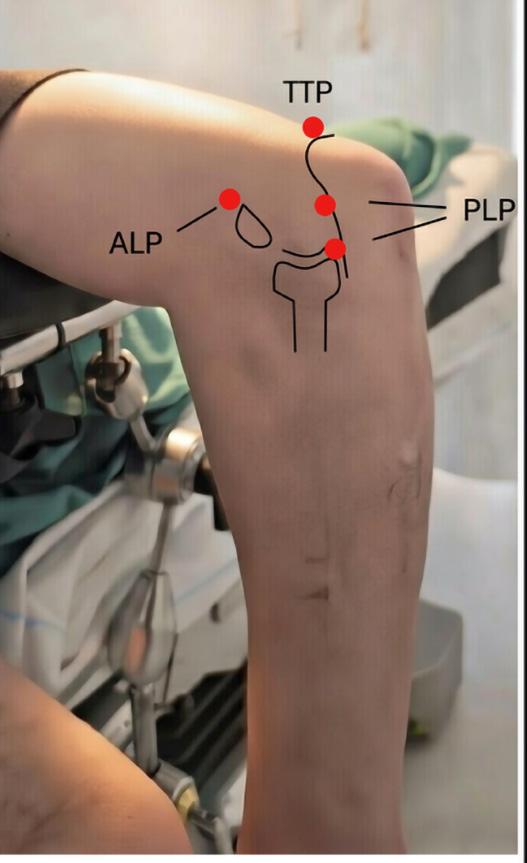
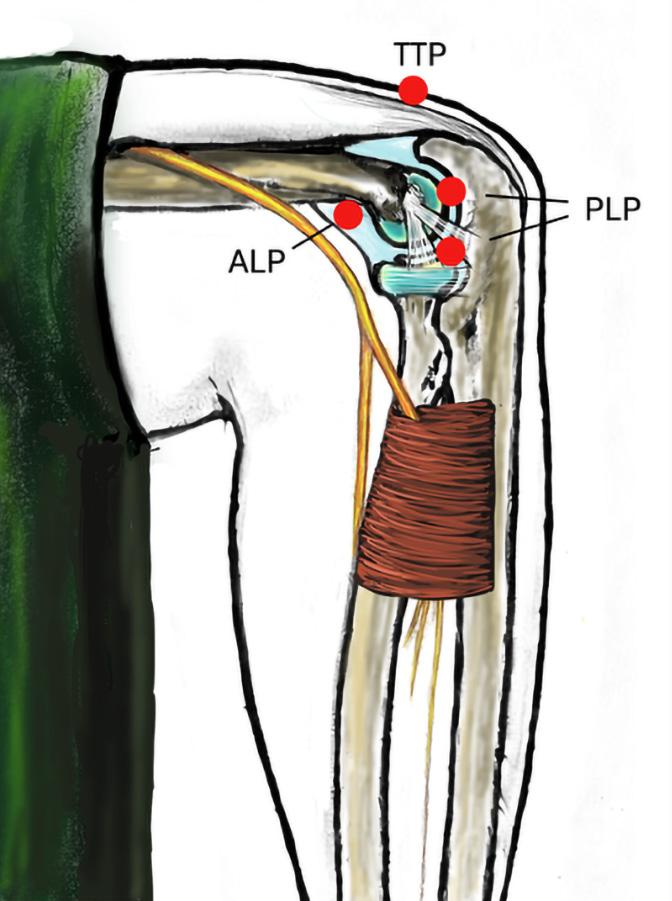
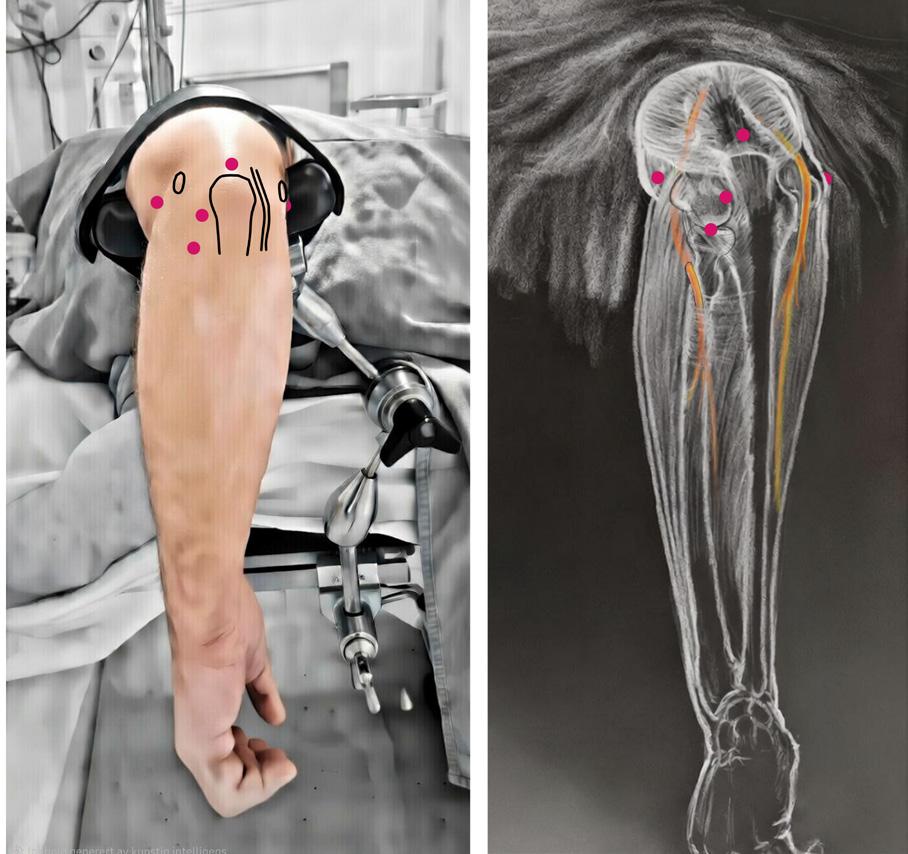
FIGUR 1: Portalplassering. A og B viser standardportaler avmerket i rødt sett fra lateralsiden, skissen til høyre viser relasjon av portaler i forhold til radialisnerven. TTP: Transtricipital portal, PLP: Posterolaterale portaler, PAL: Proksimal anterolateral portal. C og D viser portalene sett fra dorsalt med relasjon til ulnarisnerven. Illustrasjon O.A.K. Fosse.
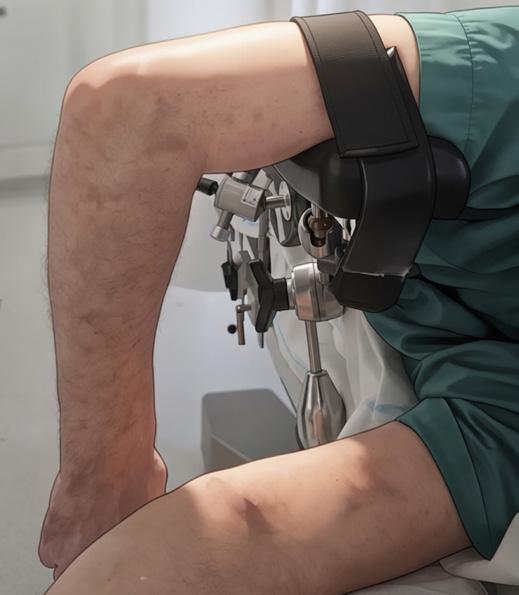
2: Leiring i sideleie. Bildet viser lateralsiden av albuen med 90 grader vinkel i skulder og albue, hvor albuen hviler i støtte mot overarmen.
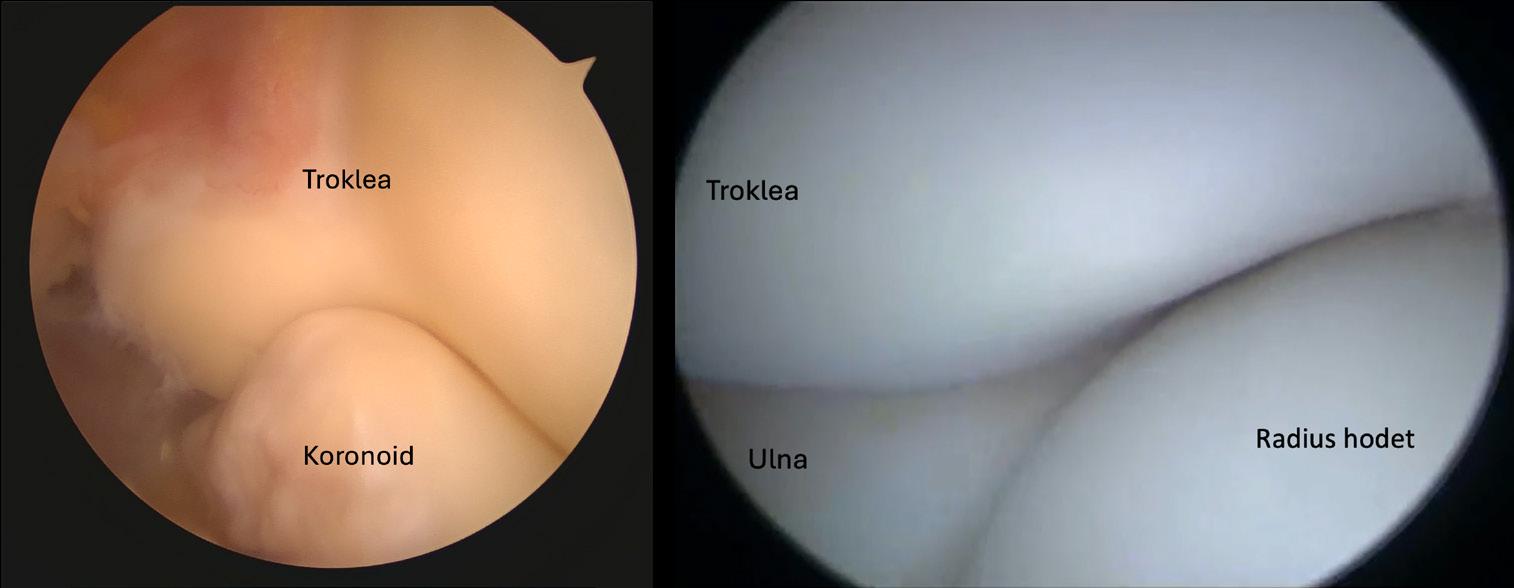
3: Venstre: Artroskopisk oversikt over leddet mellom koronoid og troklea sett fra anterolateralt. Høyre: Triangulærpunktet, der proksimale ulna, troklea og radiushodet møtes, sett fra direkte posterolateral portal.
Stram fremre kapsel og osteofytter baktil begrenser ekstensjon, mens stram bakre kapsel og osteofytter fortil hemmer fleksjon. Kirurgisk behandling vurderes når bevegelsesinnskrenkningen er funksjonelt plagsom. En fleksjon-ekstensjonsbue på omtrent 30–130 ° og 50 ° hver av pronasjon og supinasjon regnes som nødvendig for de fleste dagliglivsaktiviteter (10). Generelt har vi høyere toleranse for tap av ekstensjon. Ekstensjonsdeficit opp til 30 ° tolereres derfor som regel godt, mens dårligere fleksjon enn til 130 ° ofte gir praktiske problemer ved spising, hygiene og personlig stell. Noen pasienter med posttraumatisk stivhet har samtidig artrose, og det kan være indikasjon for operasjon ved mindre bevegelsesinnskrenkning dersom pasienten har vondt. Ulnarisnerven bidrar hos noen til utvikling av stivhet og dekompresjon eller transposisjon må vurderes.
Posttraumatisk stiv albue behandles skopisk med kapsulotomi ved kapselfortykkelse og fjerning av eventuelle påleiringer og adheranser. I enkelte tilfeller benyttes en kombinasjon av artroskopisk og åpen tilgang, for eksempel
ved platefjerning eller ulnarisdekompresjon. Noen ganger velges kun åpen tilgang, særlig ved uttalt ossifikasjon.
Postoperativ oppfølging er avgjørende. Pasientene bør følges opp av fysioterapeut med gradvis mobilisering i 36 måneder. Det er ofte behov for nattortose med armen i ekstensjon i 2–3 måneder. Man skal unngå kraftige tøyninger, da dette kan virke mot sin hensikt og trigge ny tilstivning. Det er viktig med motivert og samarbeidsvillig pasient for å oppnå godt resultat etter albueartrolyse. Informasjon både i forkant og underveis er viktig.
Osteochondritis dissecans (OCD)
Osteochondritis dissecans (OCD) i albuen ses hos ungdom fra 1112 års alder. Patogenesen er uklar, men mekaniske skjæringskrefter og repetitiv belastning antas å bidra til avaskulær nekrose i et subkondralt område, typisk fortil på capitellum. Dominant arm er hyppigst affisert, og cirka 20 % har bilateral affeksjon. Ungdom som driver med idrett med belastning i håndstående og over hodet, eksempelvis turn og håndball, er overrepresentert.
FIGUR 5: Instabilitet. Ved manipulering ser man avstand mellom koronoid og troklea som tegn på medial og lateral instabilitet.
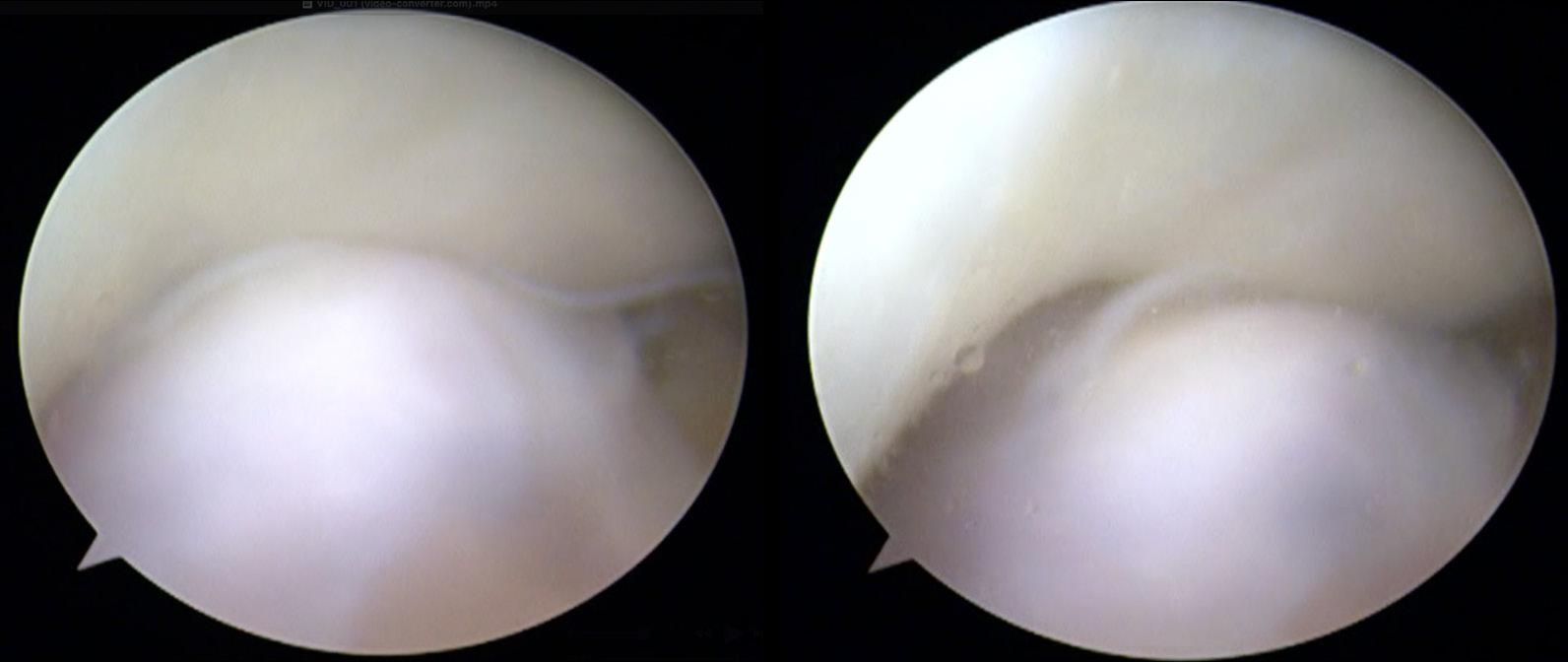
FIGUR 4: CT-bilde av typiske artroseforandringer i albueleddet. Det er et større legeme anteriort og påleiringer i fossa både anteriort og posteriort samt påleiringer på olecranonspissen. Disse forandringene gir typisk redusert bevegelighet og smerter i ytterpunkt for strekk og bøy.
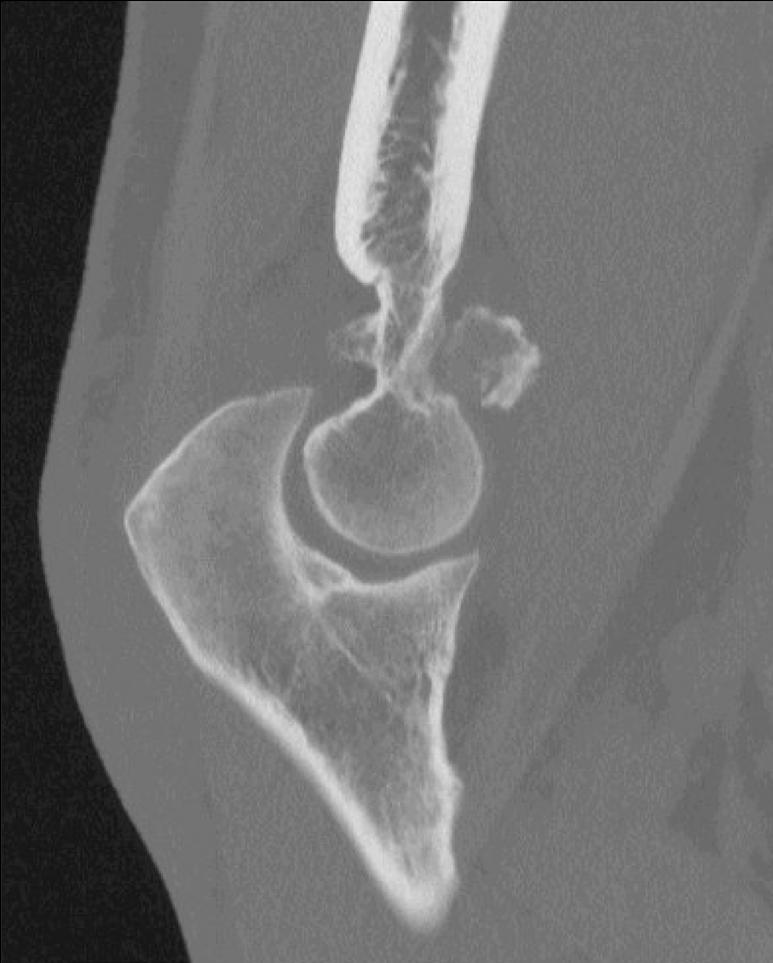
Symptomene er hovedsakelig smerter og låsning. Kliniske funn kan være sparsomme, men lett redusert bevegelighet, særlig ekstensjon, og moderat hydrops er vanlig. Diagnosen stilles best med MR eller CT. CT gir bedre informasjon om OCDlesjonens utbredelse, involvering av laterale vegg (av capitellum) og frie legemer. MR gir i tillegg informasjon om det er sprekk i brusken. Ved tidlig diagnose uten brusksprekk anbefales avlastning i tre måneder. Ved vedvarende smerter ved belastning eller ved mekaniske symptomer er artroskopisk behandling aktuelt.
Artroskopisk behandling innebærer fjerning av frie legemer og løse fragmenter, samt opprensing i det skadede osteokondrittområdet til stabile bruskkanter og blødende benflate er oppnådd. Større lesjoner kan hos yngre pasienter fikseres med skrue eller stift. Mikrofraktur har ikke vist effekt.
Postoperativt tillates fri bevegelighet, men albuen avlastes (0.5 kg) til full smertefri bevegelighet. De fleste gjen
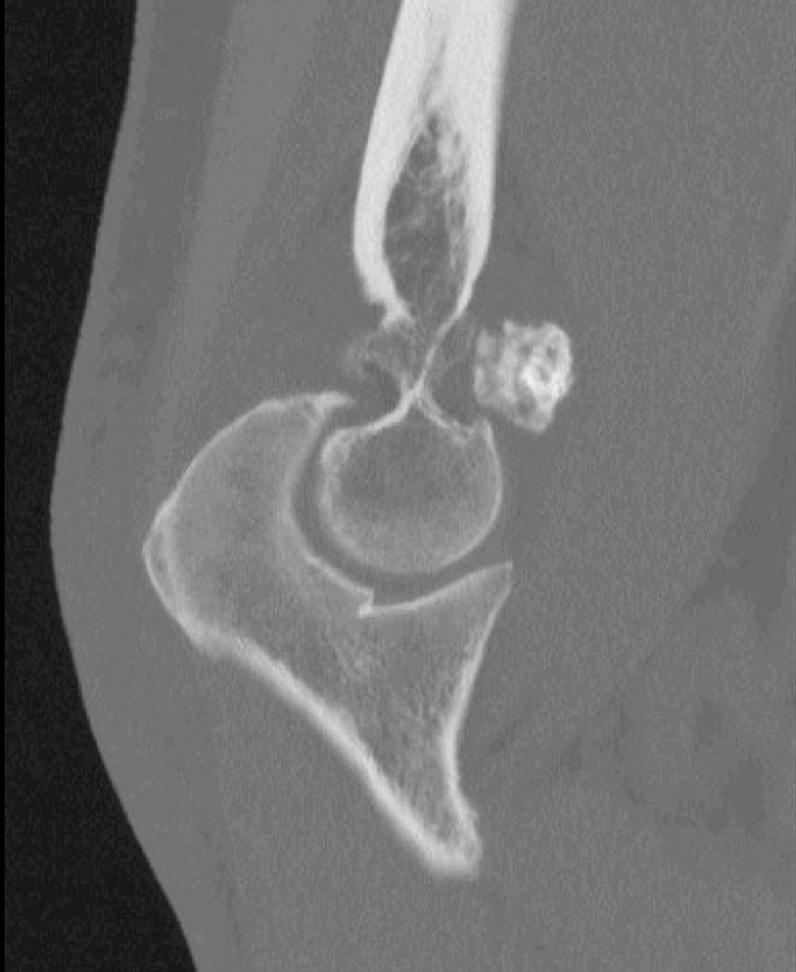
vinner nær full funksjon etter 6–8 uker. Aksial belastning bør unngås i minst 3 måneder. Residiv med nye frie legemer sees hos omtrent 10 %.
Albueleddet tåler slike defekter generelt godt. Retur til idrett varierer fra 4080 %, avhengig av idrettstype. Rundt halvparten får radiologisk lettgradig artrose på sikt, men få utvikler kliniske plager. Et unntak fra dette er store laterale lesjoner (> 15 mm). De kan påvirke artikulasjonen og osteokondralt graft må vurderes. Bedre prognose ses hos yngre pasienter med mindre lesjoner, åpne fyser og kort symptomvarighet. Involvering av laterale vegg eller lesjoner som omfatter > 50 % av capitellum gir dårligere prognose.
OCD må skilles fra Panners sykdom, som opptrer hos yngre barn (8–11 år) og som gir bringebærformet capitellum på røntgen. Panners er selvbegrensende, behandles med tilpasset aktivitet og skal ikke opereres.
Laterale albuesmerter
Laterale albuesmerter kan ha flere årsaker. Vanligste årsak er tennisalbue (ECRBlesjon). Dette er stort sett en selvbegrensende tilstand og man skal være tilbakeholden med operativ behandling. Pasienter med vedvarende symptomer, gjerne mer enn12 måneder, opereres med artroskopisk debridement av seneutspringet. Ved artroskopisk behandling får man samtidig god oversikt over leddet og annen patologi kan oppdages.
Plica syndrom er en annen årsak til laterale smerter. Det er en synovial fold som kan fanges i leddet og kan gi klikking og smerter. Pasientene rapporterer smerter i endeekstensjon, samt trykkømhet på baksiden av radiocapitellærleddet. Synovial plica er velegnet å fjerne artroskopisk. Posterolateral instabilitet bør også være med som en differensialdiagnose ved laterale smerter. Instabiliteten kan være vanskelig å avdekke klinisk, og skopi er nyttig for å stille diagnosen (Figur 5). Artroskopisk sutur for oppstramming av laterale kollateralligamentkompleks er godt egnet hos en del av disse pasientene, men ved uttalt instabilitet er det indikasjon for åpen leddbåndrekonstruksjon med fritt senegraft.
Akutte skader
Både akutte leddbåndsskader og enkelte brudd er egnet for artroskopisk eller artroskopisk assistert behandling. Forholdene intraartikulært er imidlertid ofte uoversiktlige, og prosedyrene bør derfor utføres av kirurger med mye erfaring i albueskopi. Intraartikulære brudd i radiushode, capitellum og coronoid kan behandles artroskopisk assistert. Etter luksasjon kan artroskopisk vurdering av ligament og bruskskader, samt eventuell sutur av leddbåndsskaden, være aktuelt.
Bakteriell artritt
Som i flere andre ledd, er artroskopi et nyttig verktøy ved bakteriell artritt i albuen. Artroskopisk biopsitaking og gjennomskylling gir god tilgang til alle leddkamre, også de som kan være vanskelige å nå ved åpen revisjon.
Ved bruk av pumpe koblet til sug kan leddet skylles raskt og effektivt. Teknikken muliggjør samtidig prøvetakning for bakteriologisk analyse og grundig synovektomi. Vevsprøver bør tas før gjennomskylling, gjerne ved å begynne med tørrskopi. I mange tilfeller kan artroskopisk skylling erstatte åpen prosedyre, med fordeler som bedre oversikt i over hele leddet, mindre bløtvevstraume og raskere rehabilitering.
KOMPLIKASJONER OG BEGRENSNINGER
Komplikasjoner etter albueartroskopi er generelt sjeldne. Alvorlige hendelser er rapportert hos rundt 0,5 % av pasientene (11). Noen studier angir komplikasjoner rundt 10 %, der de fleste er milde og forbigående (12, 13). Variasjonen skyldes ulike definisjoner, der enkelte inkluderer senere kirurgi relatert til grunnsykdom og forbigående stivhet som komplikasjon.
De fleste nerveskader gir forbigående parestesier, men permanente utfall er også beskrevet. Ulnarisnerven kan skades ved arbeid i bakre leddkammer, mens radialisnerven kan affiseres ved anterolaterale portaler eller ved fremre kapsulotomi. Risikoen reduseres gjennom presis portalplassering og lavt pumpetrykk. Postoperativ infeksjon er sjelden, men potensielt alvorlig og krever rask revisjon og skylling ved symptomer.
Albueartroskopi er teknisk krevende og har en relativt lang læringskurve. Strukturert opplæring under veiledning og gradvis progresjon fra enkle til mer komplekse prosedyrer anbefales, og et visst årlig volum er nødvendig for å opprettholde ferdighetene. Albueleddet har lavt volum (10–15 ml), og synovitt, fibrose, adheranser og osteofytter kan ytterligere begrense sikten. Dersom oversikten er dårlig, er systematisk debridement avgjørende før hovedinngrepet påbegynnes.
OPPSUMMERING OG FREMTIDSUTSIKTER
Albueartroskopi har på få tiår utviklet seg fra diagnostisk supplement til en etablert terapeutisk metode med høy presisjon og lav komplikasjonsrate. Metoden gir utmerket visualisering og mulighet for behandling av et bredt spekter av tilstander, forutsatt god anatomisk forståelse og tilstrekkelig erfaring. Risikoen for komplikasjoner reduseres med økende volum og strukturert opplæring.
Videre utvikling av instrumenter og optikk vil etter all sannsynlighet utvide indikasjonene ytterligere. Albueartroskopi står derfor som et verdifullt og veletablert verktøy i albuekirurgens arsenal. Et minimalt invasivt alternativ som kan gi rask rehabilitering, gode resultater og høy pasienttilfredshet.
REFERANSER : Se bakerst i nettutgaven på kirurgen.no
Learn more at smith-nephew.com
Smith & Nephew
Croxley Park, Building 5
Hatters Lane, Watford
Hertfordshire WD18 8YE
United Kingdom
T +44 (0)1923 477100
◊Trademark of Smith+Nephew ©2025 Smith+Nephew xxx-uk 05/25
For more information on the application, as well as indications for use, contraindications, and product safety information, please consult the instructions for Use (IFU) for the product.


Frakturer med større feilstilling bør generelt behandles med operasjon for å få best mulig resultat. Ved standard åpen frakturkirurgi i ankel og fot er det risiko for bløtdelskomplikasjoner, som sårinfeksjon og sårnekrose, grunnet stor hevelse og sårbare bløtdeler. I tillegg er det ofte utilstrekkelig oversikt over leddflatene for å oppnå nøyaktig reposisjon, som gir risiko for utvikling av artrose. De senere årene har det blitt forsøkt alternative operasjonsmetoder, hvor man fikserer frakturene under direkte visualisering med artroskop. Med denne teknikken kan man kontrollere leddreposisjonen og fiksasjonen, vurdere andre intraartikulære skader, og redusere forekomsten av bløtdelskomplikasjoner med mindre insisjoner. Vi vil her gå igjennom artroskopisk assistert kirurgi ved ankel-, talus, og calcaneusfrakturer (Figur 1).
INGRID KVELLO STAKE, MICHAEL PIHL, WOLFRAM GRÜN, ARE STØDLE ORTOPEDISK KLINIKK, AKER, OSLO UNIVERSITETSSYKEHUS
KORRESPONDANSE: INGRID KVELLO STAKE – INSTAK @ OUS - HF.NO
ANKELFRAKTURER
Bakgrunn
Ankelfraktur oppstår som regel ved at man får en kraftig vridning av foten i forhold til leggen. Disse frakturene kan være stabile eller ustabile avhengig av frakturmønster og assosierte leddbåndsskader. Standard behandling av stabile ankelfrakturer er ikkekirurgisk behandling med ankelskinne. Ustabile ankelfrakturer behandles med kirurgi med åpen reposisjon og intern fiksasjon (ORIF) med plate og/eller skruer. Noen pasienter har dårlige resultater etter ankelfraktur, og det er antatt at dette kan være relatert til samtidig skade på intraartikulære strukturer, inkludert brusk og ligamentskade.
Det er usikkert hvor mange pasienter som har slike assosierte skader, men en systematisk oversiktsartikkel fra 2022 rapporterte at 55 % (738/1355) av alle ankelfrakturer som ble artroskopert på samme tidspunkt som ORIF eller like etterpå, hadde en bruskskade (1). Forekomsten var høyest ved Weber C frakturer og ved uni og trimalleolære frakturer. De assosierte skadene kan overses på preoperative bilder og ved standard åpen kirurgi, og kan bidra til kroniske smerter, funksjonsnedsettelse og utvikling av artrose.
I litteraturen er det beskrevet at man kan gjøre artroskopisk vurdering av ankelleddet som en tilleggsprosedyre til standard åpen kirurgi. Potensielle fordeler med
dette er at man kan (2):
• Fjerne løse ben og bruskbiter i tillegg til hematom og inflammatoriske cytokiner.
• Vurdere og behandle assosierte intraartikulære skader, spesielt bruskskader og skade av syndesmoseeller ankelligamentene.
• Bedre vurdere reposisjonen av benfragmentene og syndesmosen, spesielt ved mer komplekse ankelfrakturer hvor bakre eller mediale malleol er involvert.
• Redusere behovet for store tilganger og dermed bevare sirkulasjonen bedre.
Vurderingen av ankelleddet med artroskopi kan gjøres før fikseringen av ankelfrakturen ettersom man har mer fleksibilitet med den ustabile ankelfrakturen, og dermed får bedre oversikt over ankelleddet (2) (Figur 2a). Standard portaler for fremre ankelskopi benyttes, og man renser opp og fjerner hematom og debris. Man gjør deretter en vurdering av syndesmoseligamentene, de laterale og mediale ankelligamentene (Figur 2b) og brusken (Figur 2c). Dersom nødvendig kan behandling av assosierte skader gjøres direkte. Etter at man har reponert frakturen via standard åpen tilgang kan man sette inn skopet igjen for å gjøre en vurdering av reposisjonen. Dersom frakturen ikke er optimalt reponert, kan man gjøre et nytt reponeringsforsøk før man endelig stabiliserer frakturen (Figur 2d).
FIGUR 1A, B og C: Oversikt over ankelleddet med knokler og ankelligamenter (a). Talus (b). Calcaneus (c). Image courtesy of Complete Anatomy.
FIGUR 2A, B, C og D: Seks uker gammel ankelfraktur som ble operert med fremre ankelskopi før stabilisering av frakturen for å vurdere assosierte intraartikulære skader (a). Peroperativt var det stor avstand medialt i ankelleddet som tegn på skade av mediale Ankelligamenter, her vist med en krok som kunne roteres medialt i ankelleddet (b). I tillegg fant man en liten bruskskade i talus (c). Syndesmosen var også skadet. Postoperativt røntgen viser at frakturen i fibula er fiksert med plate og skruer, syndesmosen er fiksert med én skrue og en sutur button, og mediale ankelligamenter er erstattet med senegraft og festet med anker/sutur button i talus, calcaneus og tibia (d). Samtykke er innhentet fra pasienten.
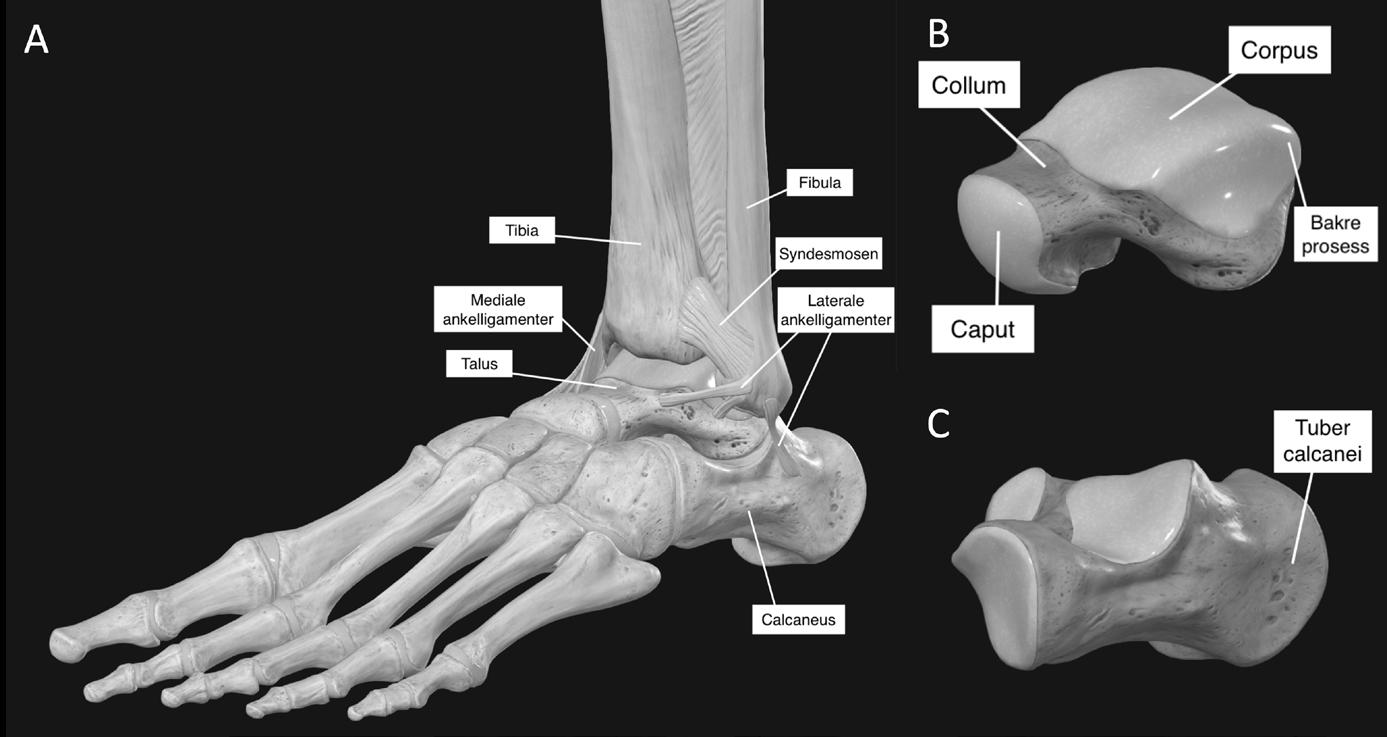
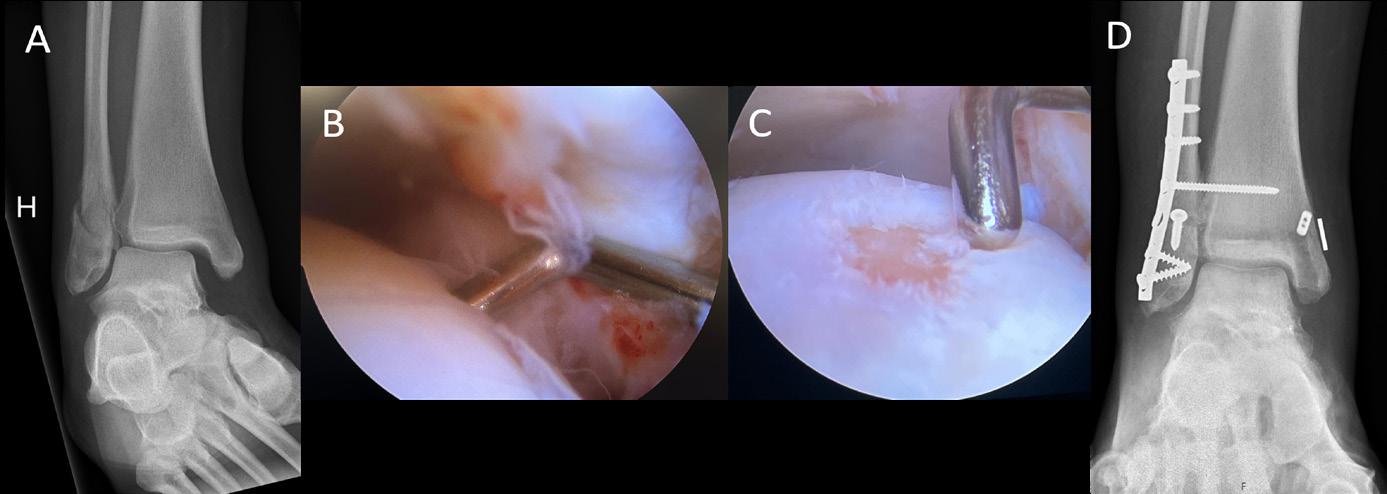
Resultater
En studie fra 2021 sammenliknet 25 pasienter operert med artroskopisk assistert ORIF (prospektivt inkludert) og 25 matchede pasienter operert med ORIF alene (retrospektivt inkludert) (3). Etter fire år fant de en bedre funksjonsscore og flere pasienter som kom tilbake til idrett etter artroskopisk assistert ORIF sammenliknet med ORIF alene. En systematisk oversiktsartikkel fra 2025 inkluderte seks artikler med unimalleolære ankelfrakturer og seks artikler med bi og/eller trimalleolære ankelfrakturer som sammenliknet artroskopisk assistert ORIF med standard ORIF (4). Av artiklene med unimalleolære ankelfrakturer rapporterte fire av seks artikler bedre funksjonsscore etter artroskopisk assistert ORIF. Kun to av seks artikler med bi og/eller trimalleolære ankelfrakturer rapporterte bedre funksjonsscore etter artroskopisk assistert ORIF. Mer alvorlig skade med bi og trimalleolære frakturer kan maskere fordelene av artroskopisk assistert kirurgi, men disse studiene var også heterogene og med dårlig kvalitet. Ingen av studiene fant noen forskjell i forekomst av komplikasjoner, men operasjonstiden økte med gjennomsnittlig 17 minutter med artroskopisk assistert ORIF.
Selv om det er flere tilhengere av artroskopisk assistert ORIF, har andre studier rapportert at den egentlige fordelen er usikker. I en studie med 32 307 ankelfrakturer var det ingen forskjell i reoperasjoner basert på om artro
skopiske prosedyrer var gjort eller ikke (5). Vel å merke var det kun 248 (0,77 %) ankler som ble artroskopert. En annen studie inkluderte 14 artikler og rapporterte sammenliknbare resultater etter kirurgi med og uten artroskopi (6). I denne studien ble det gjort artroskopiske tilleggsprosedyrer hos 79 % av pasientene. Det har også blitt rapportert sammenliknbare kliniske resultat etter ankelfrakturer med behandlet bruskskade som ved ankelfrakturer uten bruskskade (7).
Ulemper med artroskopisk assistert ORIF inkluderer lengre varighet av operasjon, økte kostnader og skopirelaterte komplikasjoner, inkludert nerveskade i forbindelse med etablering av artroskopiportalene. I tillegg er operasjonen mer krevende og bør gjøres av en kirurg med erfaring med ankelskopi.
Konklusjon
Forekomsten av bruskskader ved ankelfraktur er høy. Selv om det er usikkert hvordan det kliniske resultatet blir uten behandling av en bruskskade, er det manglende bevis i litteraturen på at det er en fordel å gjøre rutinemessig ankelskopi. Systematiske oversiktsartikler baserer konklusjonene sine på heterogene pasientmaterialer med ulike frakturtyper, kirurgisk teknikker og scoringsskjemaer. I tillegg er de fleste publiserte studiene ikkerandomiserte og retrospektive studier hvor behandling med artroskopi som tilleggsprosedyre til
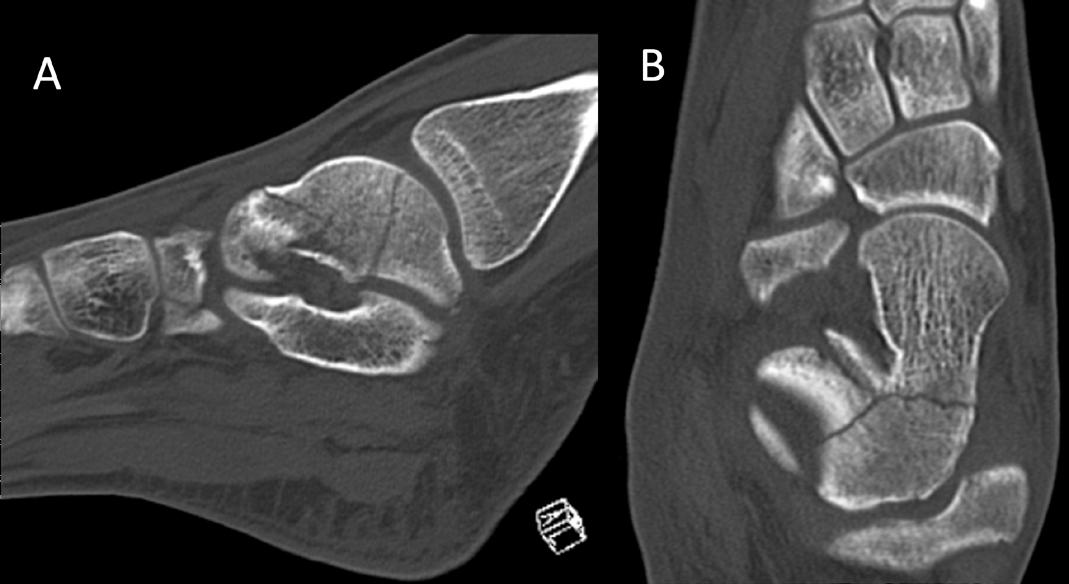
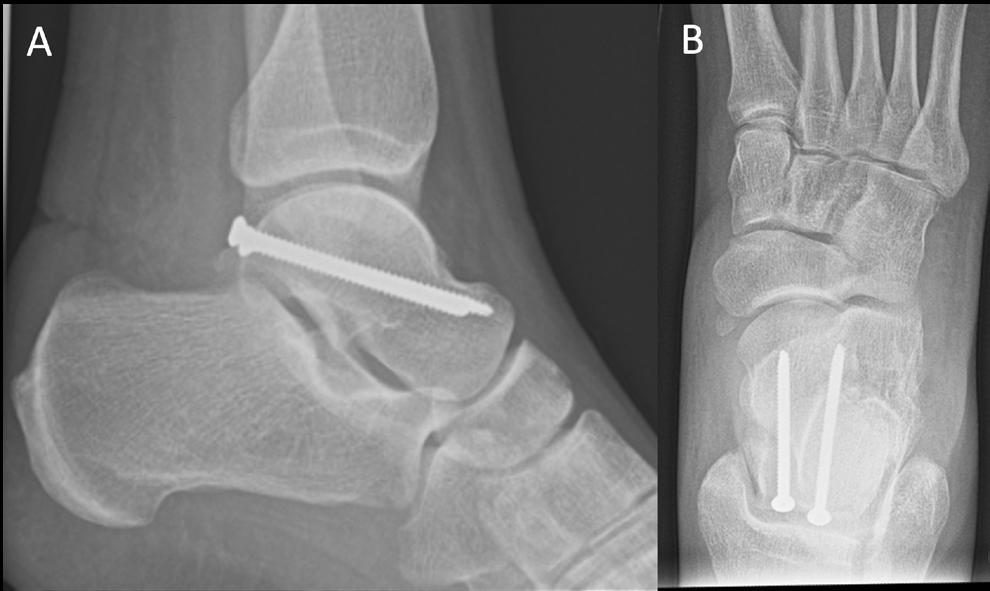
ORIF er basert på kirurgens beslutning uten konsensus om indikasjonen.
Det er ikke evidens for rutinemessig artroskopi som tilleggsprosedyre ved ankelfrakturer, og dette praktiseres heller ikke rutinemessig ved vår avdeling.
TALUSFRAKTURER
Bakgrunn
Talusfrakturer (vristbensbrudd) er relativt sjeldne frakturer og utgjør kun 3–5 % av alle fot- og ankelfrakturer (8). Blant disse utgjør corpusfrakturer ca. 20 %, og de oppstår vanligvis etter høyenergitraumer som bilulykker eller fall fra høyde (9). Talusfrakturer kan variere fra ikkedisloserte frakturer til komplekse frakturluksasjoner som involverer flere ledd, og behandlingen representerer en betydelig utfordring innen fot og ankeltraumatologi.
For enkelte udisloserte frakturer kan ikkeoperativ behandling være tilstrekkelig. Derimot krever disloserte eller ustabile frakturer kirurgi med anatomisk reposisjon og intern fiksasjon for å gjenopprette leddflatene og forebygge senkomplikasjoner (10). Resultatene korrelerer med skadens alvorlighetsgrad. Det er rapportert høye forekomster av posttraumatisk artrose i omkringliggende ledd (tibiotalarledd, subtalarledd og talonavikulærledd), avaskulær nekrose (AVN), vedvarende smerte og behov for sekundær kirurgi (11).
Talus har en sårbar blodforsyning som kan bli påvirket ved skade, og risikoen for AVN øker med skadens alvorlighetsgrad og graden av bløtdelsskade. Åpen kirurgi med omfattende bløtdelsdisseksjon kan også føre til AVN (12). Tradisjonelt har åpen reposisjon og intern fiksasjon (ORIF) via medial og lateral tilgang vært gullstandard, men ved corpusfrakturer kan disse tilgangene gi utilstrekkelig oversikt over leddflatene for å oppnå nøyaktig reposisjon.
Minimalt invasive alternativer, som perkutan artroskopisk assistert talusosteosyntese, heretter kalt PATO, har blitt utviklet for å løse disse utfordringene (13).
Indikasjoner
PATOteknikken er teknisk krevende og forutsetter erfaring med bakre ankelskopi. Ved større dislokasjoner er artroskopisk reposisjon vanskelig, og metoden egner seg best for minimalt til moderat disloserte corpus talifrakturer eller frakturer av bakre prosess (14). Dette vurderes ut fra preoperative røntgen og CTundersøkelser (Figur 3a og b).
Operasjonsteknikk
Pasienten plasseres i mageleie, og standard bakre ankelskopi utføres. Dette gir direkte visualisering av bakre del av subtalarleddet, ankelleddet og talus. Frakturen reponeres nøyaktig under synets veiledning og fikseres med skruer fra posteriort under artroskopisk og gjennomlysningskontroll (15) (Figur 4a og b).
Litteraturen indikerer at artroskopisk behandling av talusfrakturer kan gi gode til svært gode resultater med lav komplikasjonsrate (16). Kunnskapsgrunnlaget er imidlertid fortsatt begrenset, da de fleste studier omfatter få pasienter eller enkeltkasus, og det finnes foreløpig ingen store randomiserte kontrollerte studier.
Teknikken brukes derfor hovedsakelig i utvalgte tilfeller, avhengig av frakturtype og kirurgens erfaring.
Posterior skrueplassering har flere fordeler sammenlignet med anterior: skruene kan plasseres sentralt i talus’ lengdeakse, noe som gir optimal kompresjon og stabilitet (17). Imidlertid kan posterior plassering medføre risiko for skade på viktige strukturer som nervus tibialis, arte
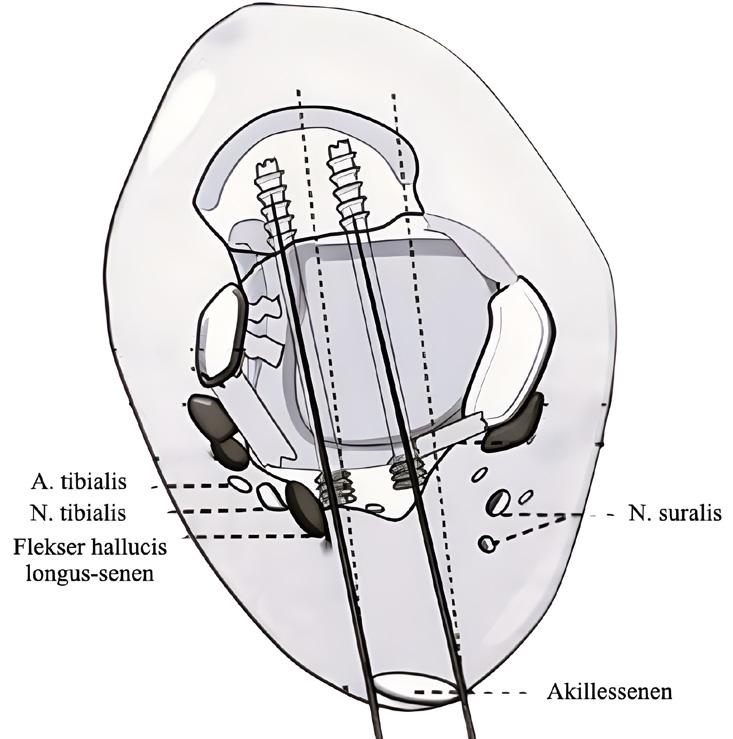
FIGUR 5: Illustrasjon av skrueplassering i aksialplanet. Utsatte strukturer medialt beskyttes under inngrepet.
FIGUR 6: Skrue visualisert peroperativt via artroskop. Samtykke er innhentet fra pasienten.
ria tibialis eller fleksor hallucis longus-senen (18) (Figur 5). Risikoen reduseres betraktelig ved at skruene plasseres under artroskopisk veiledning (Figur 6).
Retrospektive studier som sammenligner åpen kirurgi og PATO har vist kortere operasjonstid, bedre funksjonsscore, økt bevegelighet i ankelleddet og lavere komplikasjons og reoperasjonsrater i den artroskopisk assisterte gruppen (19).
Ved Oslo universitetssykehus har vi de senere årene behandlet flere pasienter med talusfrakturer ved bruk av posterior skruefiksasjon assistert av bakre ankelskopi. Ved vurdering av funksjon, egenopplevd helse og smerte, samt CT og røntgenbilder ser vi at denne metoden gir godt klinisk og røntgenologisk resultat hos selekterte pasienter.
Konklusjon
PATO er et lite invasivt behandlingsalternativ ved utvalgte corpus tali og bakre prosess frakturer. Våre egne undersøkelser og øvrig litteratur på emnet indikerer at det er en trygg metode med lav risiko for bløtdelskomplikasjoner. Det gir gode kliniske og røntgenologiske resultater, men krever kompetanse innen ankelartroskopi og at frakturene er nøye selektert.
CALCANEUSFRAKTURER
Bakgrunn
Calcaneusfrakturer (hælbensbrudd) oppstår også vanligvis ved fall fra større høyde eller i andre høyenergisenarioer, som for eksempel trafikkulykker. De er oftest intraartikulære, med frakturer og feilstilling inn i subtalarleddet, og oppstår gjerne etter et relativt forutsigbart mønster med noen frakturkomponenter som ofte er til stede (Figur 7a og b). Calcaneusfrakturer er ofte forbundet med betydelig bløtdelspåvirkning, noe som
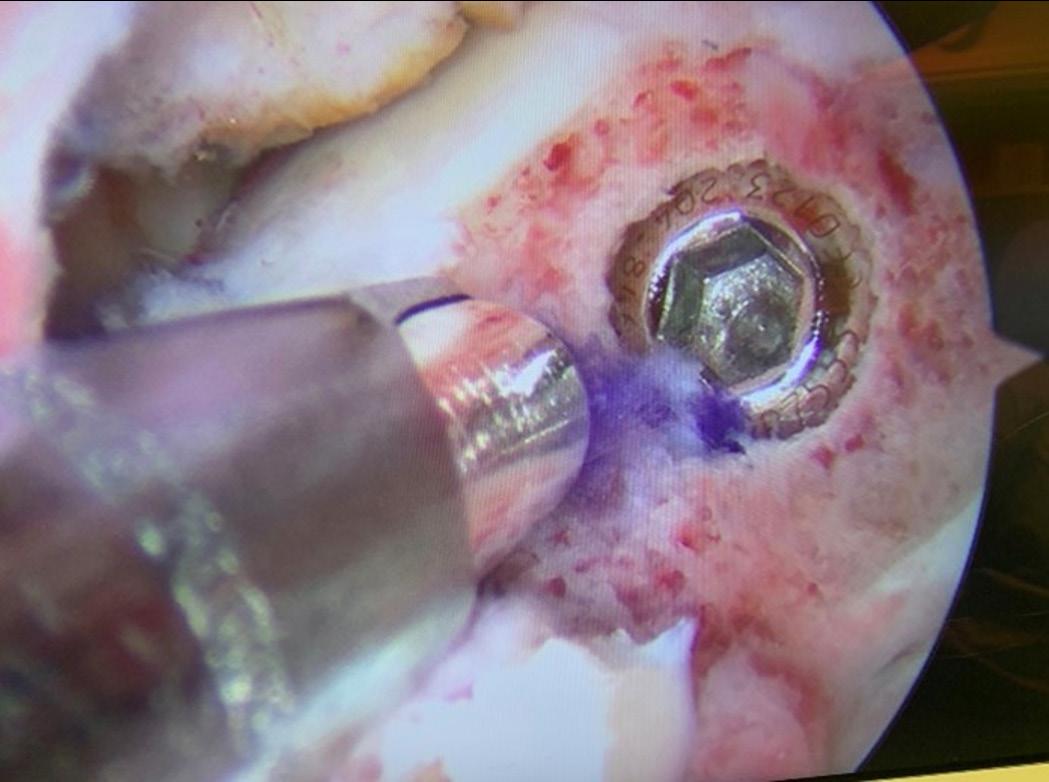
gjør de spesielt krevende å behandle. Tradisjonell åpen reposisjon og platefiksasjon kan gi god anatomisk rekonstruksjon, men innebærer også en ikke ubetydelig risiko for sårkomplikasjon, infeksjon og bløtdelsnekrose. Dette har ført til økende interesse for mindre invasive behandlingsmetoder. En av disse er perkutan artroskopisk assistert calcaneusosteosyntese (PACO).
Ved PACO utføres reposisjon og fiksasjon av frakturen perkutant, samtidig som man gjør bakre ankelskopi. Artroskopien muliggjør direkte visualisering av subtalarleddet og brukes til å kontrollere leddreposisjonen og fiksasjonen (20).
Indikasjoner
PACO er en teknisk krevende prosedyre som forutsetter erfaring både med artroskopi og behandling av calcaneusfrakturer. Metoden anbefales derfor primært ved enklere frakturtyper.
Frakturen vurderes grundig på preoperativ CT. Fragmentene må være tilstrekkelig store til å kunne reponeres og stabiliseres med skruer alene. Ved uttalt knusning i frakturen kan det være vanskelig å oppnå en stabil fiksasjon uten plate. Hos enkelte pasientgrupper kan PACO være den foretrukne operasjonsmetoden, spesielt hos pasienter med kompromitterte bløtdeler, diabetes eller perifer karsykdom, på grunn av lav risiko for infeksjon og bløtdelskomplikasjoner. En ytterligere fordel er at inngrepet kan utføres tidlig – helst innen syv dager etter skade – og at betydelig hevelse eller blemmer ikke nødvendigvis utgjør en kontraindikasjon, ettersom inngrepet kun krever små hudincisjoner.
Operasjonsteknikk
Pasienten plasseres i mageleie og det benyttes standard portaler for bakre ankelskopi, og ved behov kan en ekstra
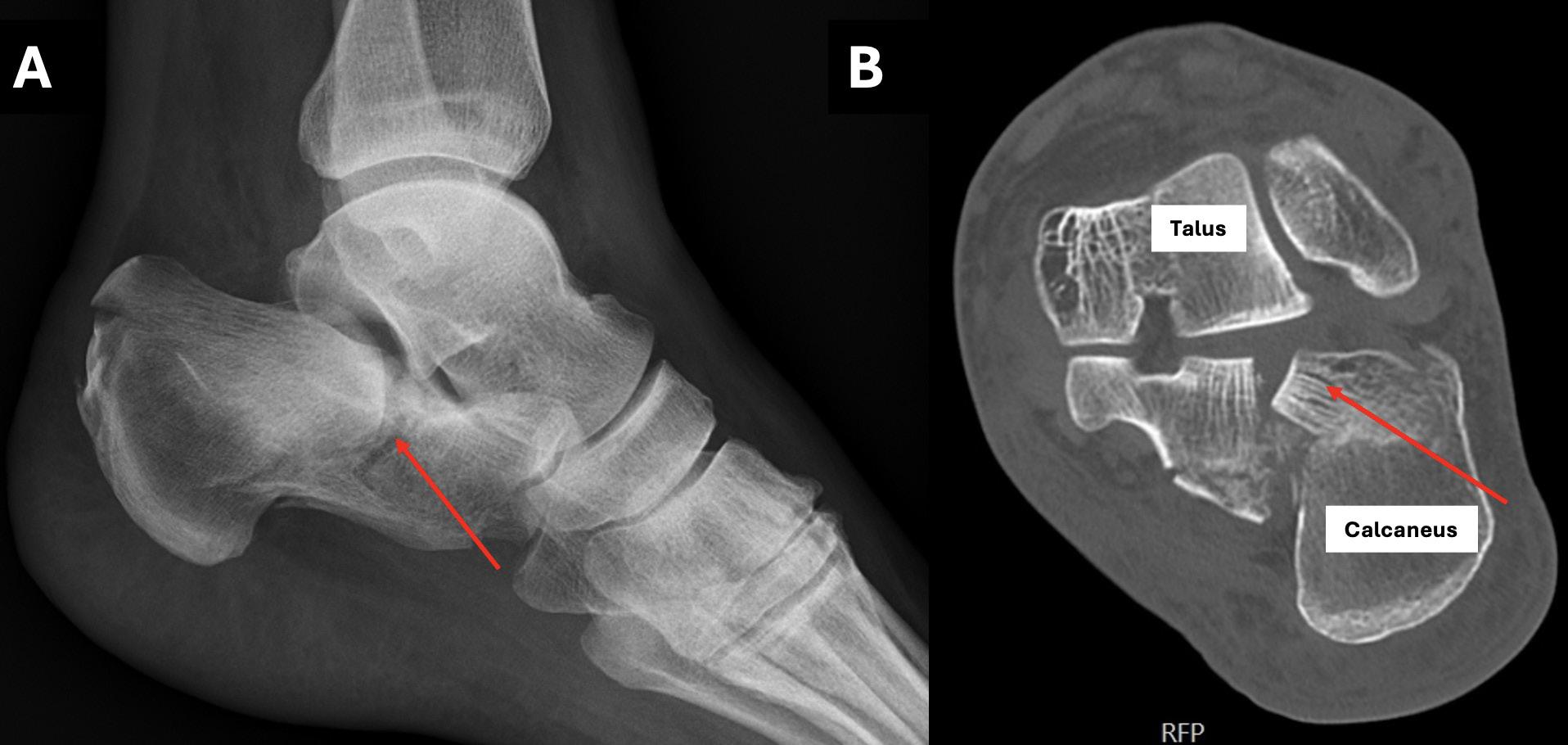
leddflaten mot talus (pil) (b). Samtykke er innhentet fra pasienten.
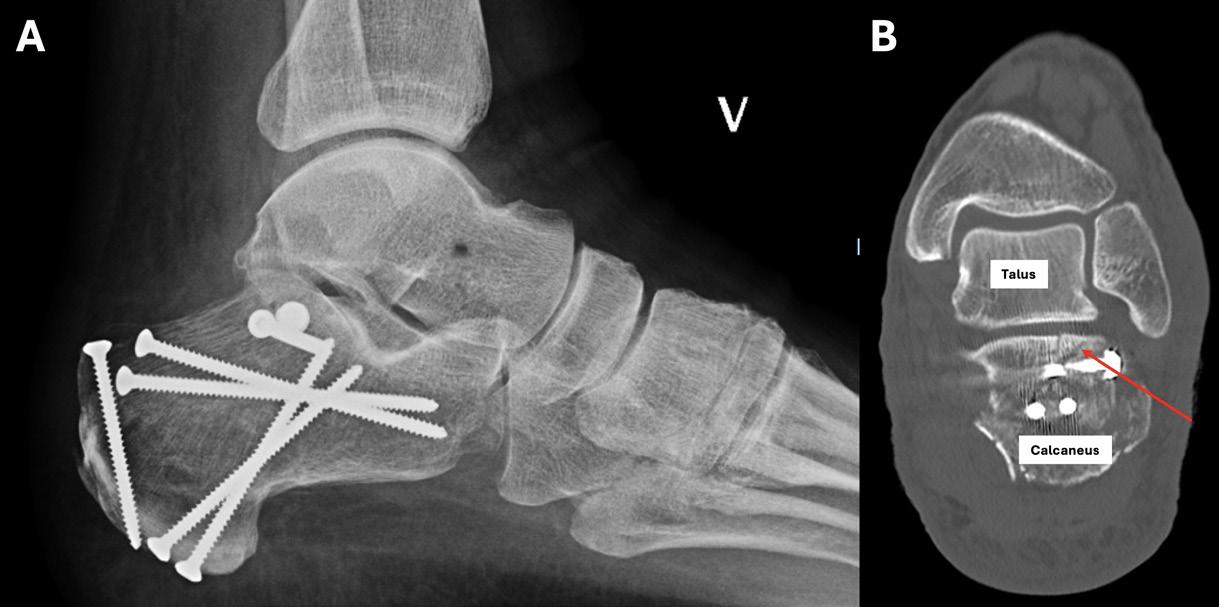
lateral portal anlegges for å visualisere fremre deler av subtalarleddet. Hematom fjernes før frakturfragmentene inspiseres (Figur 8).
Vanligvis reponeres først bakre del av hælbeinet (tuber calcanei) og fikseres midlertidig med kraftige pinner. Deretter reponeres subtalarleddet under artroskopisk kontroll som også fikseres midlertidig med pinner. Til slutt sikres frakturen med flere perkutane skruer som gir en stabil fiksasjon (Figur 9a og b).
Resultater
Flere pasientserier har rapportert gjennomgående gode kliniske resultater hos utvalgte pasienter (21,22). Publiserte pasientserier rapporterer en bløtdelskomplikasjonsrate på under 1 %, noe som er markant lavere enn ved åpen kirurgi, hvor komplikasjonsrater på opptil 25 % er rapportert (23). Vedvarende stivhet i bakfoten, der inversjon og eversjon skjer i subtalarleddet, samt smerter ved aktivitet kan forekomme. Flere pasienter oppnår ikke samme funksjonsnivå som før skaden, og for enkelte kan en calcaneusfraktur få yrkesmessige konsekvenser, til tross for et godt radiologisk resultat.
Kunnskapsgrunnlaget for PACO består i dag hovedsakelig av nivå III–IVstudier med relativt kort oppfølging, inkludert en norsk studie fra 2020 som rapporterer resultater
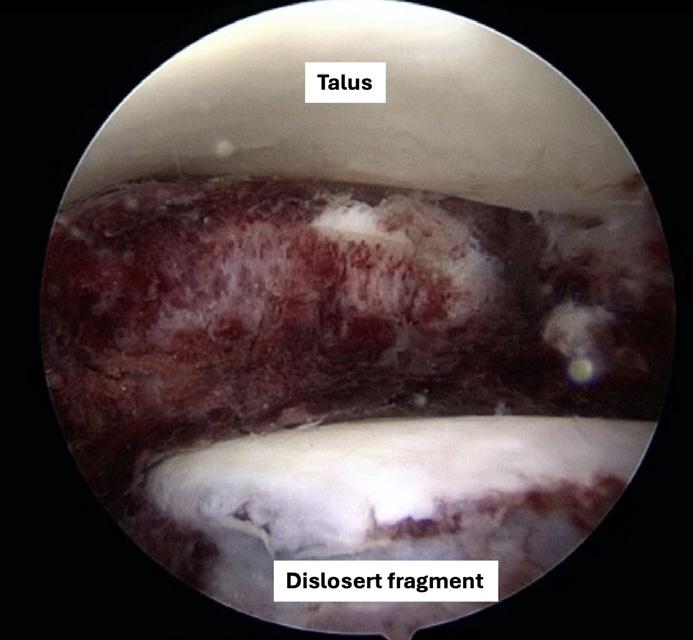
FIGUR 8: Artroskopisk bilde tatt under PACO. Nederst ses et dislosert intraartikulært bruskdekket fragment. Fragmentet reponeres og fikseres for å gjenopprette en kongruent leddflate mot talus. Samtykke er innhentet fra pasienten.
FIGUR 9A og B: Postoperativ bildediagnostikk av samme fot som illustrert i Figur 7. Lateralt postoperative røntgenbilde av foten som viser calcaneusfraktur som ble reponert og fiksert med skruer (a). Koronalt CT-snitt som demonstrerer anatomisk reposisjon av den intraartikulære leddflaten mot talus (pil) (b). Samtykke er innhentet fra pasienten.
fra 25 pasienter. Pasientmaterialene er heterogene, og seleksjonsbias er sannsynlig.
I Norge pågår det nå en randomisert, kontrollert multisenterstudie som sammenlikner PACO med miniinvasiv plateosteosyntese via den såkalte sinus tarsitilgangen. Toårsresultatene forventes mot slutten av 2026, og det er også planlagt langtidsoppfølging av pasientene.
Konklusjon
PACO er et minimalt invasivt behandlingsalternativ ved utvalgte intraartikulære calcaneusfrakturer. Metoden er forbundet med svært lav risiko for sår og bløtdelskomplikasjoner, men forutsetter tidlig kirurgi og betydelig kirurgisk erfaring. De rapporterte kort til mellomlangsiktige resultatene er lovende, men kunnskapsgrunnlaget er fortsatt begrenset, og langtidsresultater samt komparative studier mot åpne teknikker mangler. Artroskopisk assistert behandling representerer derfor et viktig supplement i behandlingsarsenalet, der riktig pasientseleksjon og erfaring er avgjørende for gode resultater.
REFERANSER : Se bakerst i nettutgaven på kirurgen.no
– The Journal of Arthoplasty, februar 2024
– sårlukking og bandasjering TKA og THA, 20 internasjonale ortopeder

TKA sårbehandlingsintervensjoner
• Bruk av knytefrie suturer fremfor standard suturer (lavere sårkomplikasjoner, bedre kosmetisk utseende, raskere lukketider og totale kostnadsbesparelser)
• Bruk av triklosanbelagte suturer fremfor ikke-antimikrobielle suturer (lavere risiko for infeksjon på operasjonsstedet)
• Bruk av mesh-lim fremfor andre hudlukkingsmetoder (lavere sårkomplikasjoner, høyere pasienttilfredshet, lavere reinnleggelsesfrekvens)
THA sårbehandlingsintervensjoner
• Bruk av knytefrie fremfor standard suturer (raskere lukketider og totale kostnadsbesparelser)
• Bruk av triklosanbelagte suturer fremfor ikke-antimikrobielle suturer (lavere risiko for infeksjon på operasjonsstedet)
• Bruk av subkutikulære/intrakutane suturer over hudstifter (lavere risiko for overfladiske infeksjoner og høyere pasienttilfredshet, men lengre lukketider)
Last ned studiene, ring oss på 67 51 86 00 eller besøk ortomedic.no.
Hjelp jeg må artroskopere på vakt! Hvor var det man plasserte portalene igjen? Hva gjør jeg hvis jeg ikke finner meg selv? Som fersk skopør av knær og skuldre må du først mestre en diagnostisk artroskopi. Dette er en grunnleggende prosedyre som også kommer deg til nytte når du på vakt må gjøre skyllinger av septiske artritter. I denne oversiktsartikkelen tar vi for oss hvordan man tar seg inn og rundt i knær og skuldre artroskopisk.
KORRESPONDANSE: GRY THERESE HEIR - GRHEIR @ OUS - HF.NO
ARTROSKOPI - RACKEN
Artroskopiracken inneholder skjerm, kameraboks, pumpe, shaver og ablatorenhet. Gjør deg kjent med lokalt utstyr og enkel feilsøking, særlig knyttet til væsketilførsel og trykk. Representanter fra industrien og/eller operasjonssykepleiere kan hjelpe deg med dette på dagtid.
GENERELL TEKNIKK
Orientering: Start med å finne horisonten. Bruk kameraet aktivt ved å rotere på hånden som holder det. I kneet kan du bruke tibias leddflate som horisontlinje, mens i skulder kan du orientere deg etter leddflaten på glenoid. Pilen på skjermen peker mot den retningen kameraet ser. Optikken er 30 grader vinklet i enden, så du ser aldri rett frem, og den vinklede enden av optikken peker alltid motsatt vei fra lysledningen.
Triangulering: Trianguleringen krever trening. Se utenfor leddet om de to instrumentene dine er i samme plan. Trekk kameraet litt tilbake for bedre oversikt, sikt tuppen av instrumentene mot hverandre i samme plan til du ser deg selv.
Væsketrykket: God sikt i leddet oppnås ved et lett overtrykk i forhold til pasientens blodtrykk. For lavt trykk gir blødning og dårlig oversikt, for høyt trykk gir økt ekstravasjon og hevelse. Godt samarbeid med anestesien, der de tilstreber et jevnt lavt blodtrykk, gir deg bedre arbeidsforhold.
ARTROSKOPI - INSTRUMENTER (Figur 1 og 2)
Skophylse med mandreng: En artroskopisk prosedyre starter når skophylsen med mandreng settes inn i leddet. Skophylsen har en diameter som er litt større enn optikken og tillater derfor gjennomskyll av sterilt vann.
Optikken: La skophylsen stå, ta ut den butte mandrengen, og erstatt den med optikken. Den vanligste optikken er 30 grader vinklet i enden, og fordi optikken er 30 grader vinklet må man huske på:
• Det er umulig å zoome inn på noe kun ved å gå rett frem og nærmere med skopet.
• Du kan se deg rundt fra et punkt i leddet ved å rotere lysledningen.
• Du endrer retningen av synsfeltet ditt ved å løfte eller senke hånden som holder kameraet.
Radiofrekvens-probe (RF-probe): RFproben har en koagulerende (typisk blå) og en kuttende (typisk gul) knapp. RFproben smelter vevet ved at den genererer varme, og har tre forskjellige grader (low, medium og high flow). Kommer i forskjellige vinkler, hvor 90° og 50° er vanligst i kne og skulder.
Bløtdelsshaver: Finnes i forskjellige varianter og størrelser. I vaktsetting kommer du langt med en 4,5 mm i både kne og skulder. Styres enten for hånd eller med fotpedal, og har tre knapper: forward, backward eller oscillering. Ved bløtdelsshaving skal bladet oscillere. Rett over knap

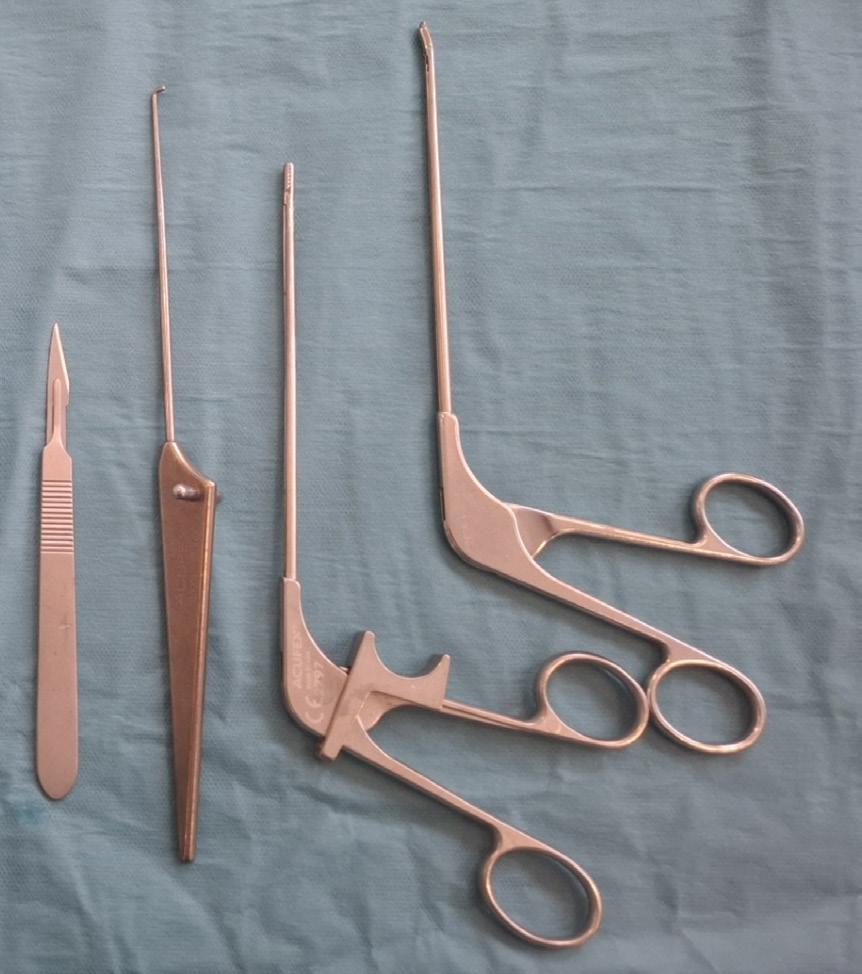
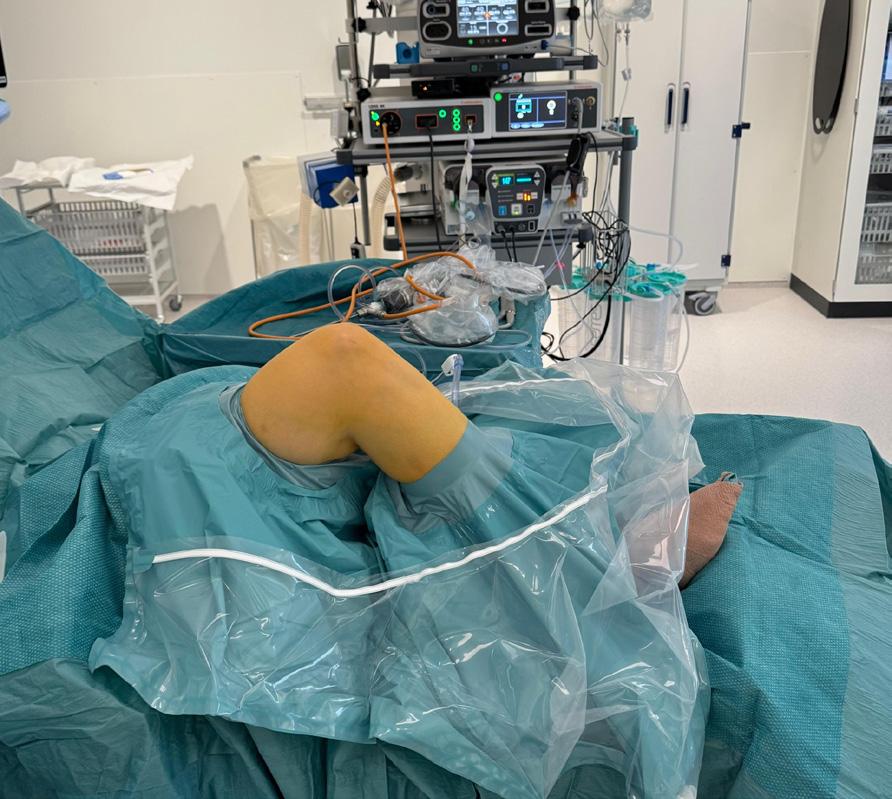
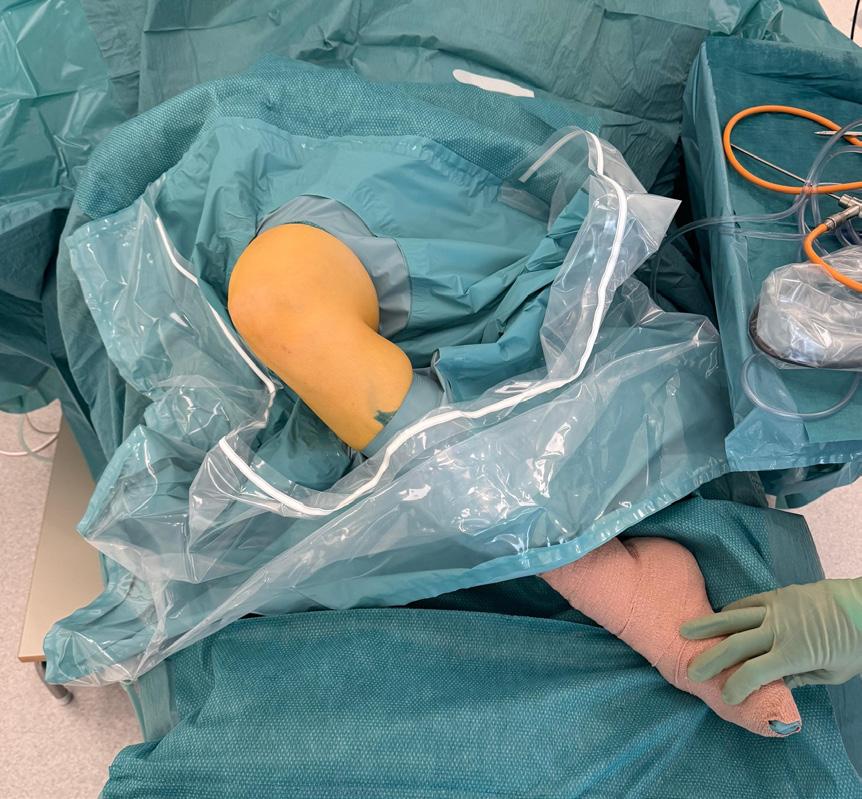
pene er det en pendel, denne regulerer graden av sug. Juster suget aktivt for å få gjennomskyll og bedre sikt.
Skopi-kniv: Et 11blad som brukes til å lage portalene.
Artroskopi-krok: Kan brukes til å «palpere» om det foreligger skade av meniskvev og labrum, eller for å sjekke om brusken er fast eller bløt.
Fattetang: Kan for eksempel brukes til å hente ut løse ben/bruskbiter fra leddet.
Stansetang: Kommer i flere varianter, og hvert sykehus har gjerne sine egne lokale navn for de ulike typene –«breiflabb», «dolokk», «optimist» også videre. Brukes typisk til å gjøre partielle meniskektomier i knær.
ARTROSKOPI AV KNELEDDET
Anestesi og leiring
Artroskopi av kneleddet gjøres oftest i narkose, eventuelt supplert med en blokade eller lokal bedøvelse. Pasienten leires på rygg med en sidestøtte lateralt for låret på aktuelle ben og en pøll under leggen (Figur 3). Blodtomhet brukes ikke regelmessig, men ha den i beredskap i tilfelle det blør mye og sikten hindres, i så fall 250 mmHg i maks to timer.
Sidestøtten og valgusstress av kneet med benet plassert på hoften din gir bedre innsyn i mediale leddkammer. Tilsvarende gir firetalls-posisjon av benet og varusstress mer innsyn i laterale leddkammer (Figur 4). Pøllen tillater at du kan sette ifra deg kneet i 90 grader når du jobber sentralt.
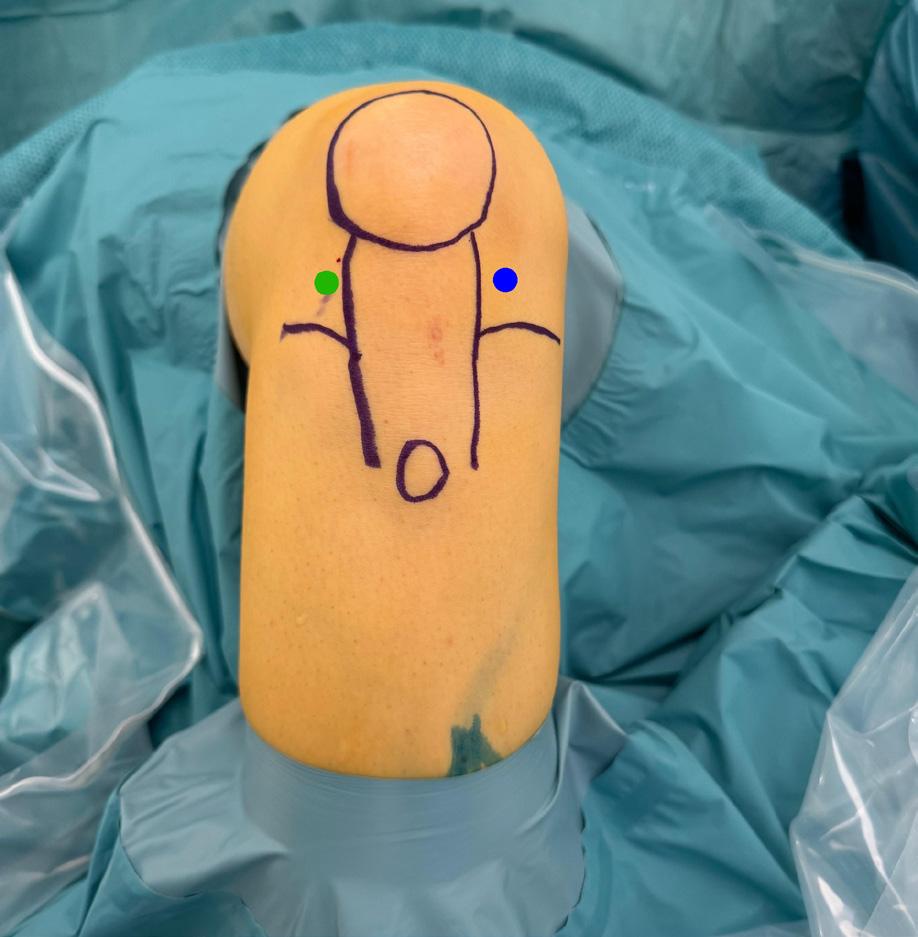
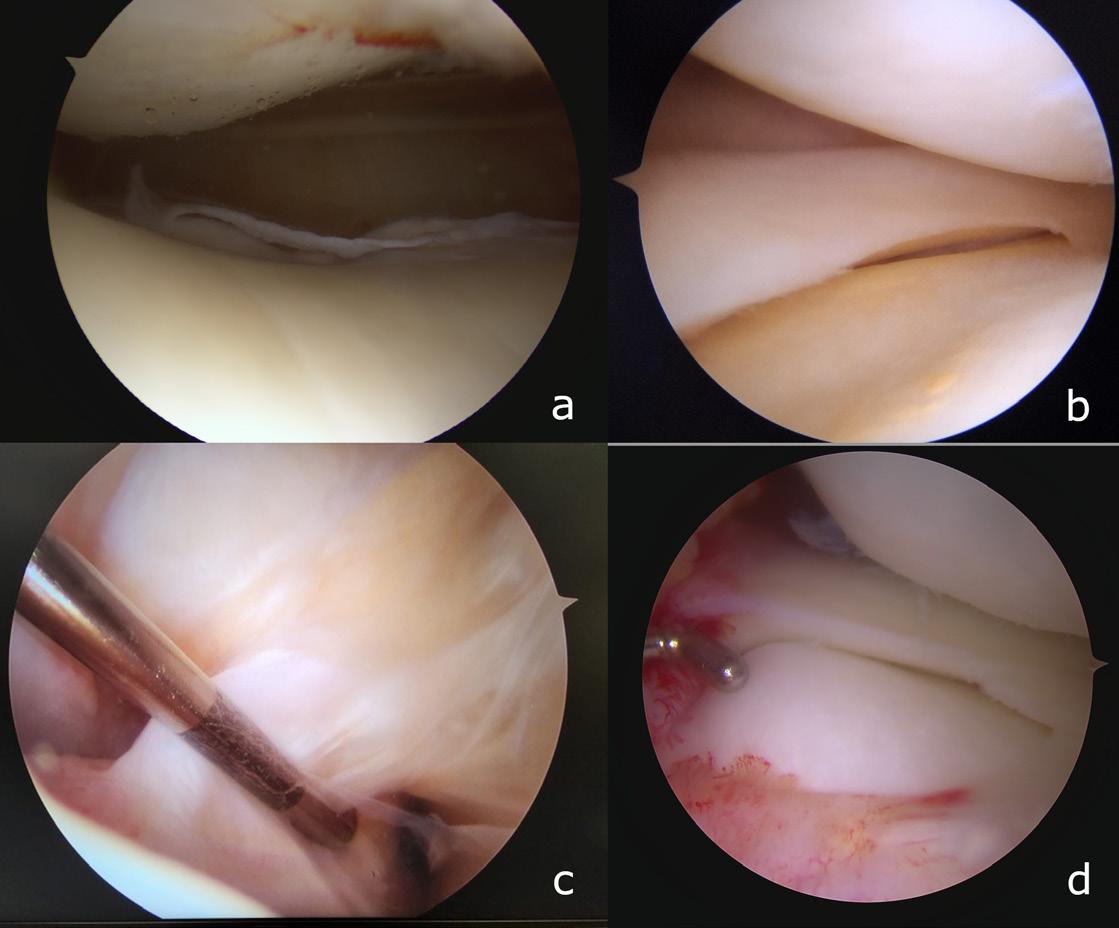
Stabilitetstesting
Test alltid kneleddet før du starter. Start gjerne prosedyrebeskrivelsen med å beskrive en standard stabilitetstesting, for eksempel: «Tester kneet i narkose: Full fleksjon og ekstensjon, ingen hyperekstensjon. Negativ fremre og bakre skuffe. Negativ Lachmann. Negativ pivot shift. Stabilt medialt og lateralt på både strakt kne og i 30° fleksjon.»
Portaler
For en diagnostisk artroskopi (eller en skylling) av kneleddet trenger du to portaler: anterolateral kameraportal og anteromedial arbeidsportal. Disse blir enklere å etablere om du kjenner din overflateanatomi. Palper ut og tegn på patellas omriss, mediale og laterale rand av patellarsenen, tuborositas tibiae og leddspalten medialt og lateralt (Figur 5). Kniveggen skal alltid peke opp ved etablering av disse portalene, for å unngå å skade menisken.
Anterolateral kameraportal
1. Sett foten mot pøllen for 90° fleksjon i kneet.
2. Palper ut nedre pol av patella og laterale rand av patellarsenen.
3. Finn softspot lateralt for patellarsenen, legg snittet ditt vertikalt inn, så nærme patellarsenen som mulig. Bruk et 11blad igjennom hud og kapsel.
4. Sett skophylsen med mandreng vannrett inn siktende mot midten av kneet, deretter opp og bak patella samtidig som du ekstenderer kneet.
5. Ta ut mandrengen, sett inn kameraet og skru på vannet. Du skal nå stå i suprapatellare recess.
Anteromedial arbeidsportal
1. Ha kneet i 90° fleksjon likt som lateralt (eller lett valgisert for etablering under visuell kontroll, se punkt 6).
2. Palper ut nedre pol av patella og mediale rand av patellarsenen.
3. Finn softspot medialt for patellarsenen, legg snittet ditt vertikalt inn med et 11blad igjennom hud og kapsel.
4. Ved behov kan kanalen utvides med en butt mandreng eller rett saks.
5. Før inn artroskopikroken for å palpere under en diagnostisk artroskopi.
6. Er du usikker, etablerer du denne portalen under visuell kontroll: Før kameraet inn i mediale leddkammer. Se mot anteromediale leddkapsel. Stikk en grønn nål inn i tenkt riktig posisjon, se at nålen legger seg rett over menisken og at den sikter i den retningen du ønsker. Følg nålens rute med skopikniv igjennom hud og kapsel.
Ved behov: Suprapatellar portal for skyllekanyle
1. Legg kneet i full ekstensjon.
2. Stå med kameraet suprapatellart og se mot lateralt.
3. Stikk en grønn nål lateralt for quadricepssenen, proksimalt for patella i retning femur, gå helt inn til du ser nålen suprapatellart.
4. Gjør en minimal langsgående insisjon gjennom hud og fett. Sett inn utløpskanylen med mandrengen i, sikre at alle hullene på skyllekanylen står inn i ledd.
5. Ta ut mandrengen og koble på outflow-slangen.
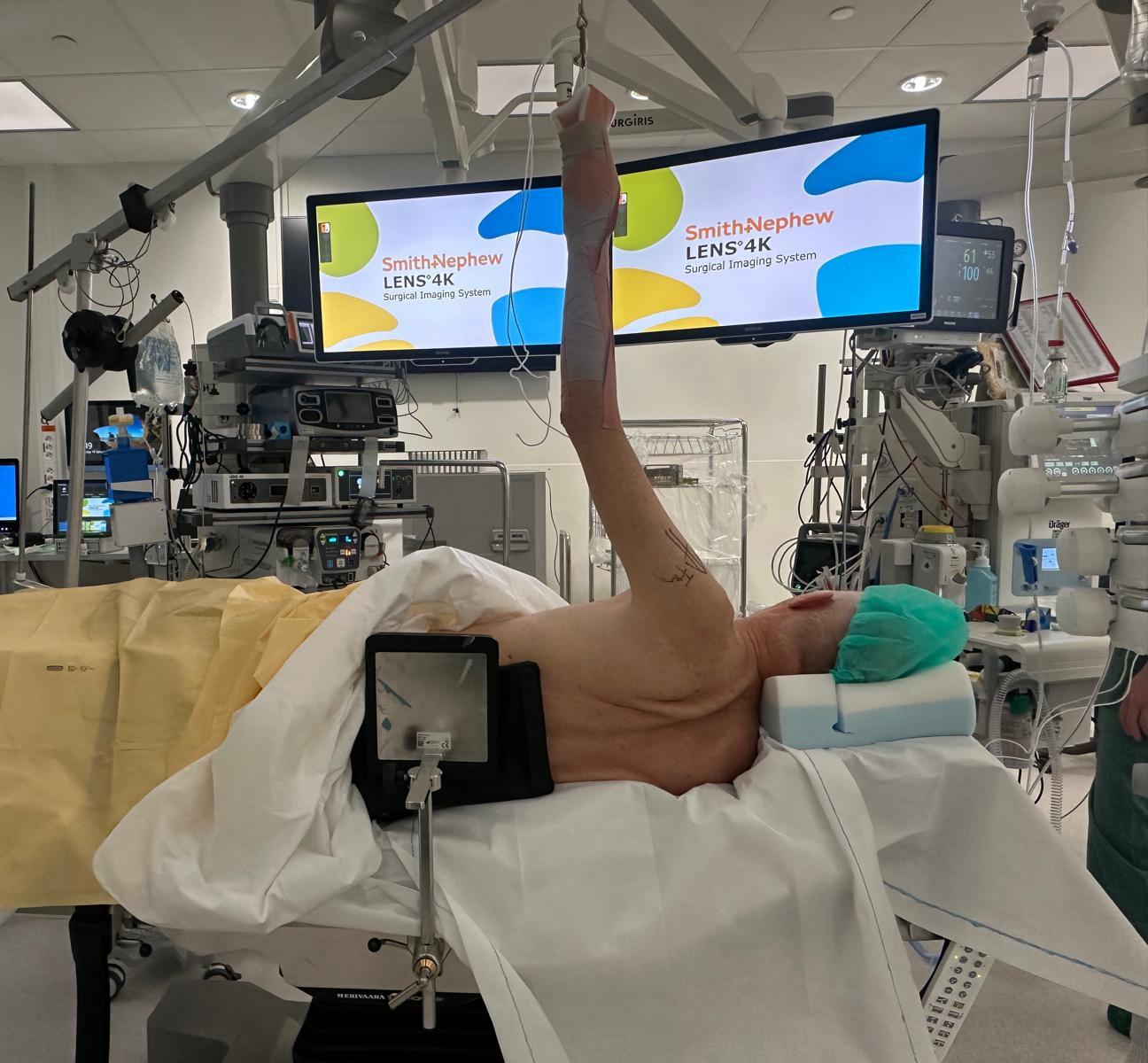
7: Leiring av pasienten i sideleie. Armen er hengt opp for å legge til rette for steril vask. Når loddene settes på og armen legges i strekk går den 45° ut fra kroppen. Bildet er tatt med tillatelse fra pasienten.
DIAGNOSTISK ARTROSKOPI AV KNELEDDET, STEG - FOR- STEG
Ha kameraet i anterolateral portal og kroken i anteromediale arbeidsportal. Lag deg en fast runde som du gjør hver gang, du skal innom disse punktene;
1. Suprapatellart: Vurder synovitt og fremmedlegemer.
2. Patellofemoralt: Vurder brusk på patella og i trochlea samt patellatracking ved fleksjon/ekstensjon (Figur 6a).
3. Mediale recess: Vurder synovitt, plica og fremmedlegemer.
4. Mediale leddkammer: Bruk kroken aktivt for å vurdere brusken og menisken (Figur 6b). Gå baktil ved hjelp av Gillquist manøver for å se på bakre rot og eventuelle rampelesjoner.
5. Sentralt: Vurder fremre og bakre korsbånd med kneet i 90° fleksjon (Figur 6c).
6. Laterale leddkammer: I firetallsposisjon vurderer du menisk, bakre rot og brusk; husk at økt bevegelighet av menisken er normalt nær popliteussenen (Figur 6d).
7. Laterale recess: Vurder synovitt, fremmedlegemer og popliteussenen.
8. Avslutning: Tøm leddet for væske og lukk portalene.
ARTROSKOPI AV SKULDERLEDDET
Anestesi og leiring
Artroskopi av skulderleddet gjøres som regel i narkose. Ved Oslo universitetssykehus, Aker sykehus, leires pasienten i sideleie med ryggen lutet 3045° bakover, og med den aktuelle armen i strekk. Strekket gjøres ved hjelp av lodd, som kan tilsvare maks 10 % av pasientens kroppsvekt (ofte cirka 4 kg lodd hos kvinner og cirka 5 kg lodd
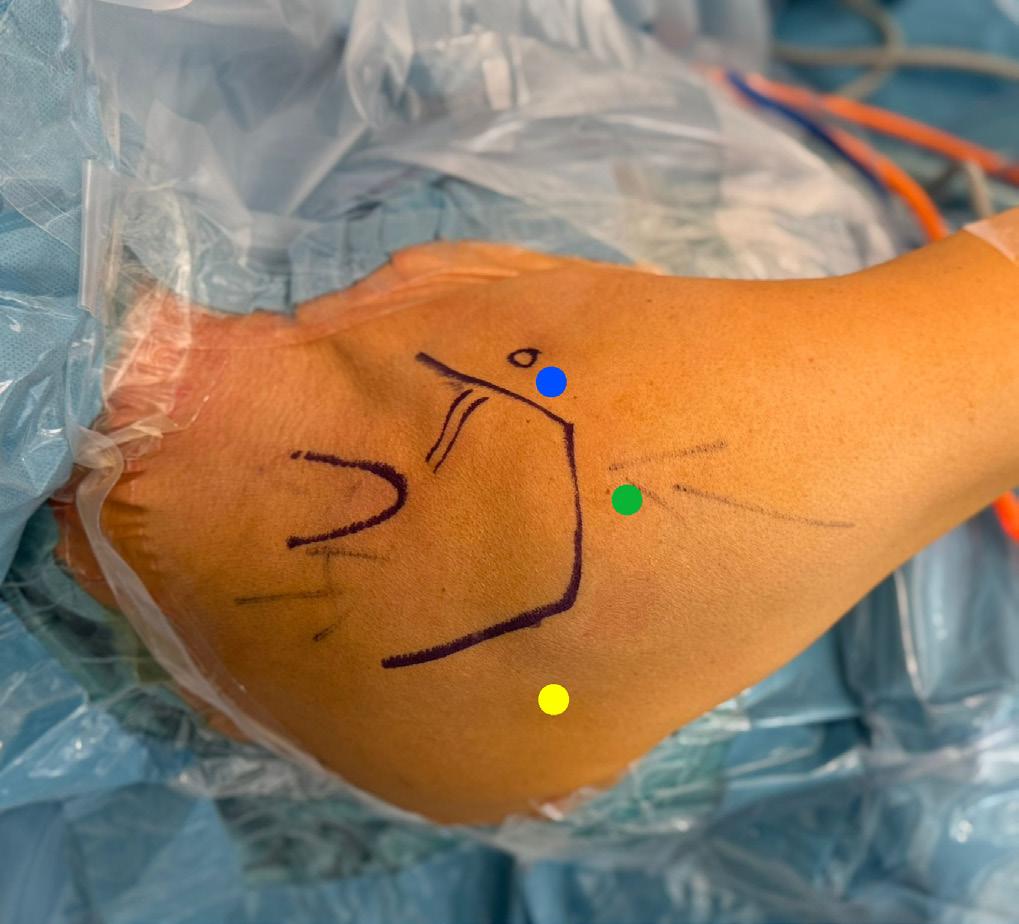
8: Høyre skulder i strekk med påtegnet overflateanatomi. Gul sirkel = bakre kameraportal, blå sirkel = fremre arbeidsportal, grønn sirkel = lateral portal. Bildet er tatt med tillatelse fra pasienten.
hos menn). Loddene festes i en snor, og ved hjelp av en trinse og plasterstrekk i aktuelle arm får man et drag i armen som øker avstanden mellom glenoid og caput humeri. Dette bedrer innsyn og arbeidsforhold i leddet (Figur 7).
Skulderleddet blåser seg raskt opp ved artroskopi og det kan bli vanskelig å orientere seg fra utsiden. Vi anbefaler derfor å strekke ut armen ved å henge på lodd, og tegne på overflateanatomien helt i starten av prosedyren. Det er alltid mulig å palpere bakre laterale hjørne av akromion før du begynner. I tillegg markerer vi spina scapula, akromioklavikulærleddet (ACleddet), krageben, fremre laterale hjørne av akromion, laterale kant og processus coracoid (Figur 8).
For å gjøre en diagnostisk artroskopi (eller en skylling) av skulderleddet trenger du to portaler: bakre kameraportal og en fremre arbeidsportal.
Bakre kameraportal
Den første portalen du etablerer:
1. Palper ut bakre laterale hjørne av akromion.
2. Gå 2 cm inferiort og 1 cm medialt, her palperer du softspot, åpne huden med skopikniv.
3. Palper ut coracoiden, sett skophylsen med mandreng inn i portalen, og sikt mot coracoiden.
4. Kjenn at du står mot bakre kapsel i sjiktet mellom caput og glenoid. Gå igjennom kapsel og videre inn i leddet, roter deg forsiktig inn hvis mye motstand.
5. Bytt ut mandrengen med kameraet og skru på vannet.
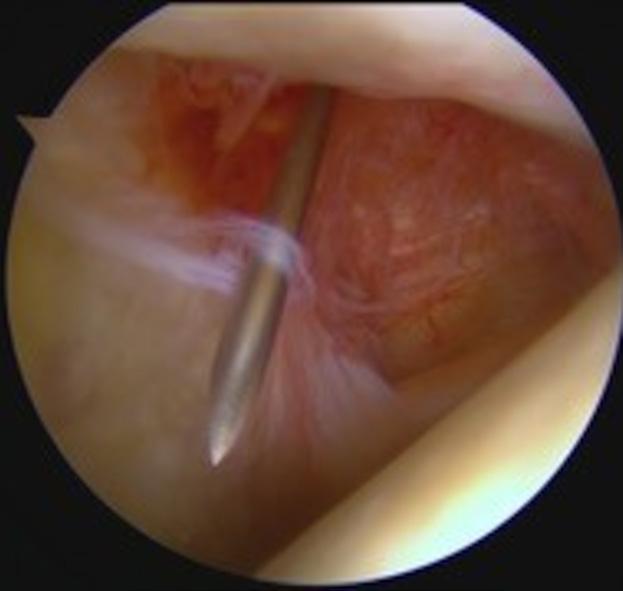
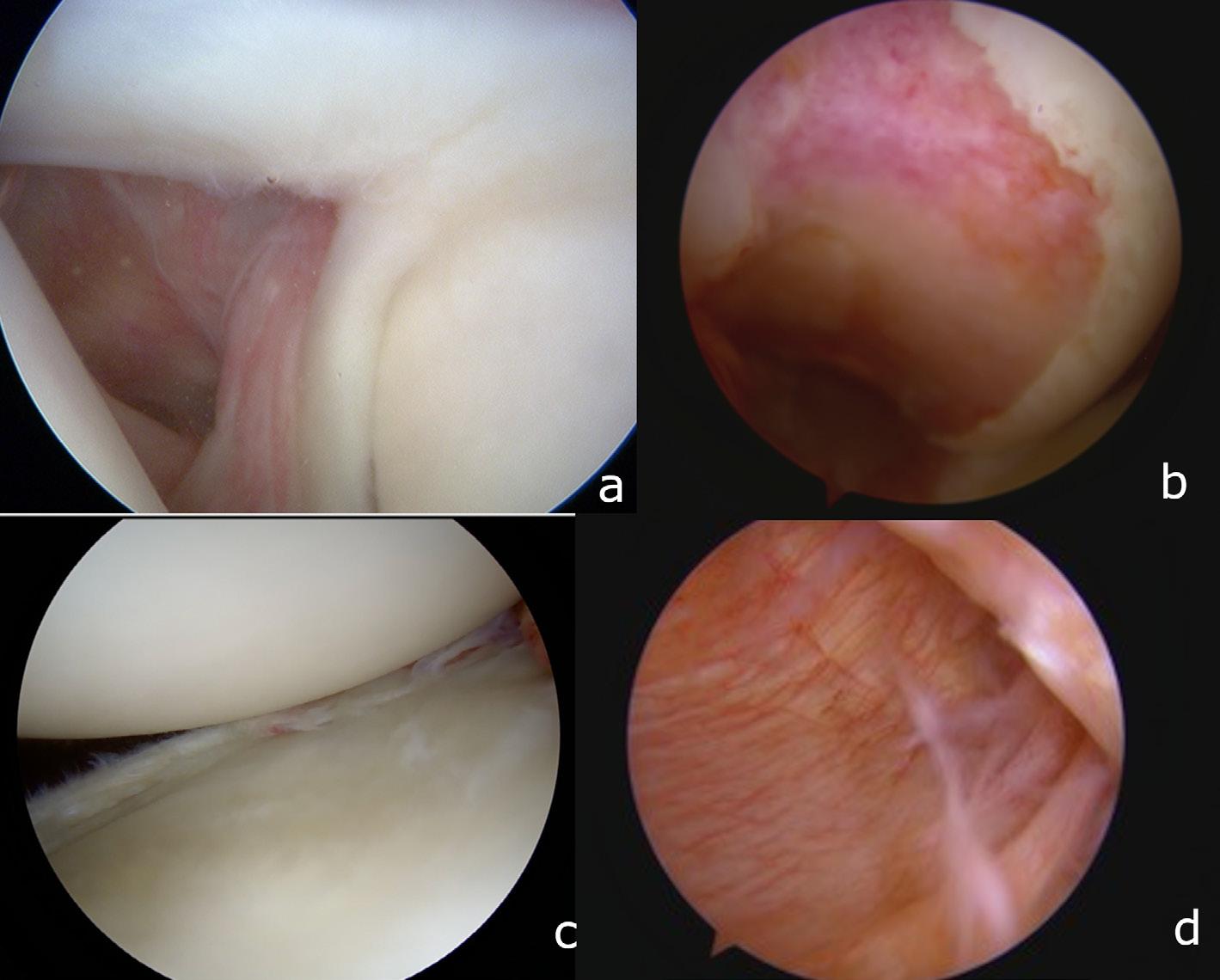
Fremre arbeidsportal
Den andre portalen du etablerer. Gjøres med outsidein teknikk (Figur 9):
1. Se forover og oppover med kameraet.
2. Bruk en grønn nål og sikt deg inn i området som er lateralt for coracoiden og anteriort for AC-leddet. Se at nålen kommer inn igjennom rotator intervallet og at du har en retning som tar deg inn under bicepssenen, men over subscapularissenen.
3. Åpne hud med kniv og bruk mandrengen for å sprenge ut en åpning i kapsel. Før inn krok, og start din diagnostiske artroskopi.
Ved behov: subakromiell kameraportal
Benytt den allerede etablerte bakre kameraportalen.
1. Ta ut optikken og sett den butte mandrengen inn i skophylsen. Gå helt ut til subkutant vev.
2. Sett mandrengspissen mot bakre akromion sin benkant og skli under den. Sikt rett medialt for fremre hjørne av akromion. Når du kjenner at du står under ben er det lov til å bevege skophylsen sideveis for å
lage et hulrom. Sett inn optikken. Du skal nå stå i et rom (omringet av spindelvevaktig bursavev) hvor undersiden av akromion er opp i bildet, og den bursasidige-cuffen er ned.
Ved behov: lateral portal for instrumentering subakromielt
1. Palper ut midten av laterale akromionkant og gå cirka 2 cm ned på armen fra benkanten.
2. Finn retningen ved hjelp av en grønn nål som settes inn under akromion og visualiseres med kameraet som står subakromielt. Se ut mot lateralt med kameraet.
3. Åpne huden med kniv og spreng ut portalen med for eksempel en mandreng.
DIAGNOSTISK ARTROSKOPI AV SKULDERLEDDET, STEG - FOR- STEG
Lag deg en fast runde du alltid gjør. Ha kameraet i bakre portal mens du har en krok i fremre portal. Her beskrives en metode hvor man deler inn i glenohumeralt og subakromielt, og videre deler inn leddet igjen i fire regioner (8)
Glenohumeralt
Superiort:
1. Finn det lange hodet av bicepssenen (Figur 10a). Se på senens innfestning til øvre labrum. Følg senen mot lateralt og ned i bicepssulcus. Bruk kroken for å trekke senen litt inn i leddet, da ser du eventuell patologi på den delen av senen som normalt ligger i sulcus.
2. Trekk skopet litt til deg, beveg kamera posteriort for biceps og bruk optikken for å se lateralt etter rupturer i supraspinatus sin innfestning mot tuberculum majus.
3. Gå videre bakover og finn «bare area» til caput som ligger inn under innfestningen til infraspinatus. Se etter rupturer i innfestningen til infraspinatus og teres minor
Anteriort:
4. Vurder brusken til caput og glenoid (Figur 10c).
5. Vurder stabiliteten til fremre labrum med krok. En normalvariant av anatomien i skulderleddet er at øvre, fremre labrum kan være løs (over klokka 3). I nedre del (klokka 3-6) er løs labrum patologisk.
6. Se etter rupturer i subscapularis, roter armen innover og trekk caput humeri bakover for å vurdere innfestningen. Mediale glenomhumerale ligament kommer fra medialt og ligger over subscapularis på leddsiden.
Inferiort:
7. Gå ned i nedre recess (Figur 10d) og vurder kapselen sin innfestning til caput. Avrivning av kapselen fra humerus kalles «humeral avulsion of the glenohumeral ligament» (HAGL-lesjon).
Posteriort:
8. Trekk skopet forsiktig bakover, pass på at du ikke faller ut. Undersøk baksiden til caput for Hill-Sachs lesjon (Figur 10b).
9. Vurder eventuell slitasje og rifter/løsning av bakre labrum. Ved tegn til skade testes stabiliteten av labrum med krok.
Subakromielt
10. Lokaliser fremre laterale hjørne av akromion ved hjelp av korakoakromialligamentet. Vurder fremre laterale hjørne av akromion for om det foreligger benete påleiringer som kan gi impingement.
11. Se etter rupturer i rotatorcuffen fra bursasiden
TIPS OG TRIKS, OG VANLIGE UTFORDRINGER VED ARTROSKOPI
Det er dårlig sikt fra starten av: Er pumpen koblet riktig? Forsøk å tømme leddet for væske og fyll på igjen. Eventuelt, bytt optikk og lyskilde.
Det ble plutselig dårlig sikt utover i inngrepet: Er vannet på? Ellers ofte på grunn av blødning. Tøm leddet for væske og fyll på igjen. Prøv å øke trykket på pumpa forbigående (lavage/rinse). Eventuelt skru på blodtomhet hvis du står med et kneledd.
Det er vanskelig å se noe i kneet: Da står du som oftest i Hoffas fettpute. Før inn shaver, og sikre at shaveren står i hoffas (du vil se tennene til shaveren) før du fjerner noe av hoffas ved å oscillere.
Jeg kommer meg ikke inn i kneet igjen: Portalene består av en hudinsisjon og en kapselinsisjon. Relasjonen mellom disse endres når du bytter posisjon på kneet. Kommer du ikke inn etter å ha forsøkt mandrengen et par ganger, går du tilbake til utgangsposisjonen med kneet i 90° og opp i suprapatellare recess.
Ved septisk artritt, for best mulige prøver av leddvæsken: Sett inn skophylsen med mandreng, koble vannslangen fra skophylsen og tapp leddet for væske med en sprøyte satt inn i inflow-kranen.
For å kjøre gjennom vannet raskere ved en skylling (uten å måtte være engstelig for å shave bort strukturer du egentlig vil beholde): Knepp ut innmaten til shaveren.
Tuppen på de fleste krokene er cirka 4-5 mm: Dette kan du bruke til å for eksempel måle størrelse på bruskdefekter.
For å beskrive funn på glenoid eller labrum bruker vi klokka: Klokka 12 er alltid innfestningen av bicepssenen. Klokka 3 er anteriort uansett om du er i høyre eller venstre skulder. Det vil si at venstre skulder refereres speilvendt.
Hvis du absolutt ikke klarer å komme inn i skulderen med skophylsa og mistenker infeksjon i leddet: Gjør en vanlig deltopectoral tilgang. Leddet må skylles!
Da er det bare å gå i gang med diagnostiske artroskopier (og skyllinger) av kne og skulder, dette klarer du! Lykke til!
REFERANSER :
Se bakerst i nettutgaven på kirurgen.no
Årlig fjernes omtrent 8000 galleblærer i Norge, og antallet er økende. Hos 2-12 % av kolecystektomerte foreligger koledokusstein (1). Ved koledokusstein og samtidig indikasjon for kolecystektomi finnes flere behandlingsstrategier. I Norge er den vanligste strategien å gjøre to-seanse-behandling med endoskopisk retrograd kolangiopankreatografi (ERCP) først, og deretter laparoskopisk kolecystektomi (2). Retningslinjer fra European Society of Gastrointestinal Endoscopy anbefaler i utgangspunktet en-seanse-behandling med enten intraoperativ rendezvous-ERCP eller laparoskopisk intraoperativ steinsanering (3).
MAGNUS HØLMO FASTING 1, HENRIK KROSSØY THOMASSEN 2, TOM GLOMSAKER 1
1 OSLO UNIVERSITETSSYKEHUS, ULLEVÅL
2 HARALDSPLASS SYKEHUS
KORRESPONDANSE: MAGNUS HØLMO FASTING – MAGFAS @ OUS - HF.NO
INTRAOPERATIV STRATEGI FOR SANERING AV GALLEGANGSSTEIN
1. Gi butylskopolamin 20 mg i.v. Vent på pulsstigning og prøv å skyll steinene ut.
2. Tre 150 cm 0,035 tommer ledevaier gjennom ureterkateter og få den ned i duodenum.
3. Tre ureterkateteret over ledevaier ned mot papillen og forsøk å stake steinene ut.
4. Tre blokkeballong over ledevaier og ned i koledokus. Denne kan skyves gjennom huden og mates ned i cysticus med laparoskopitenger. Blokk papillen til 6/7/8 mm avhengig av steinenes størrelse og diameter på choledochus.
5. Trekk blokkeballong opp i ductus cysticus og blås den litt opp. Gjør cholangiografi og skylling gjennom blokkeballongen.
6. Gjør antegrad «feiing» av steinene ned i duodenum med blokkeballongen noe blåst opp i choledochus og ledevaier ned i duodenum.
7. Blokk ductus cysticus for å fasilitere choledochoskopi.
8. Etabler en 5 mm port høyt oppunder høyre costalbue. Bruk stiv introducerhylse for skopet.
9. Gjør koledochoskopi.
10. Fisk steinene opp med kurv, evt. skyv dem ned i duodenum med skopet.
11. Hvis mislykket, evt. peroperativ ERCP (rendezvous) (4,5m 0,035 tommer ledevaier), evt. ERCP påfølgende dag.
RAMME
BAKGRUNN
Enseansebehandling med intraoperativ sanering av gallegangsstein har flere fordeler sammenlignet med pre eller postoperativ ERCP. For det første gjennomføres behandlingen med en enkelt prosedyre, med de fordeler det gir for pasienten med tanke på sykeleie og sykefravær (4). Videre er det i mange tilfeller slik at små gallegangssteiner avgår spontant, og derfor ikke trenger ERCP før kirurgi. Dessuten er det flere studier som tyder på at komplikasjonsrisikoen ved intraoperativ sanering av gallegangsstein er lavere enn ved pre eller postoperativ ERCP (58).
Ved Oslo Universitetssykehus Ullevål begynte vi med intraoperativ gallesteinssanering for fullt i 2019 (9).
I dag er dette en fullt integrert del av behandlingen av alle pasienter med gallegangsstein og samtidig indikasjon for kolecystektomi. De fleste overlegene ved øvreseksjonen behersker prosedyren, og interesserte LIS blir raskt selvstendige. Vi bruker en step-up-algoritme der spyling med saltvann, blokking av papillen og transcystisk koledokoskopi er noen av trinnene (Ramme 1).
I det følgende vil indikasjoner, nødvendig utstyr og praktisk gjennomføring av prosedyren presenteres.
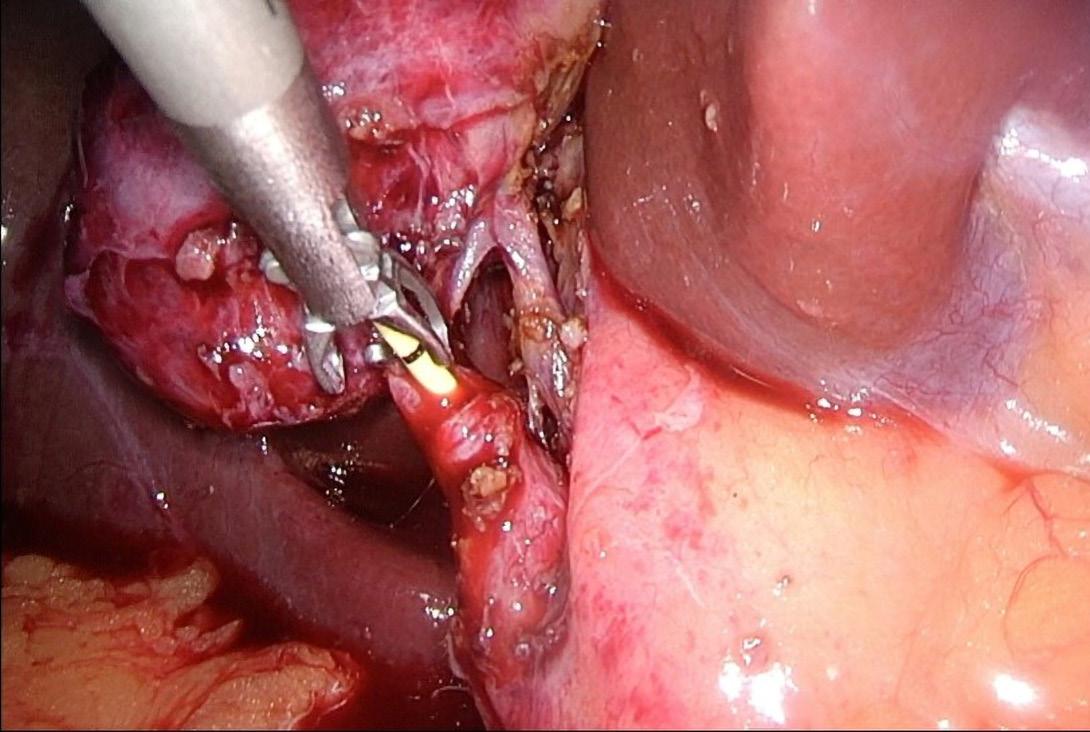
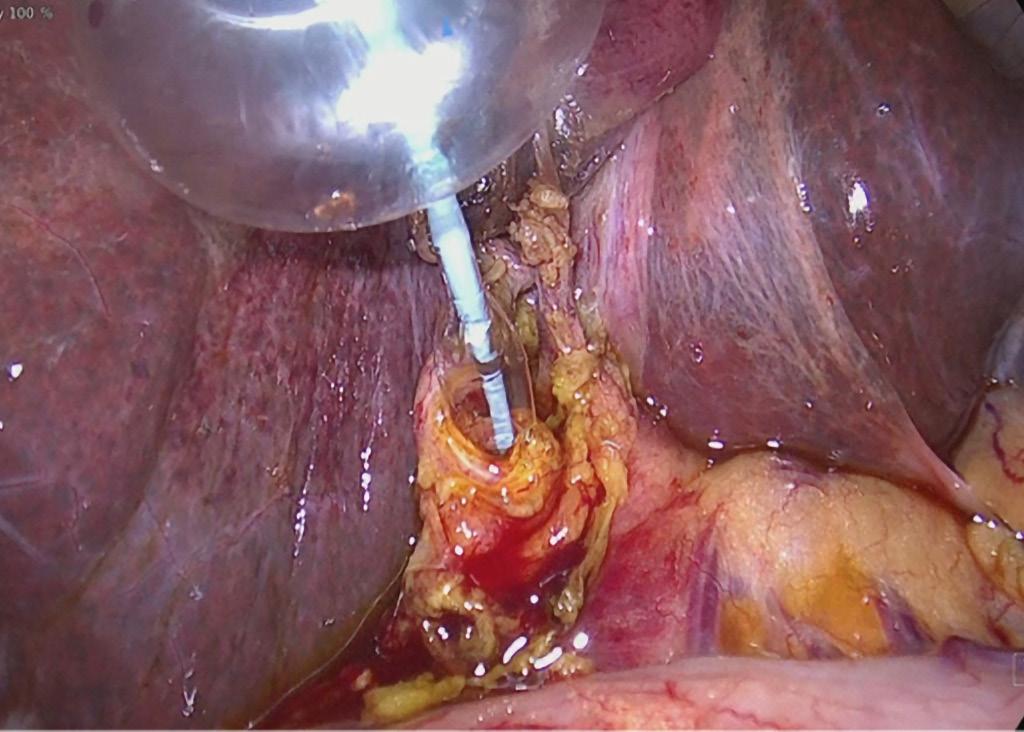
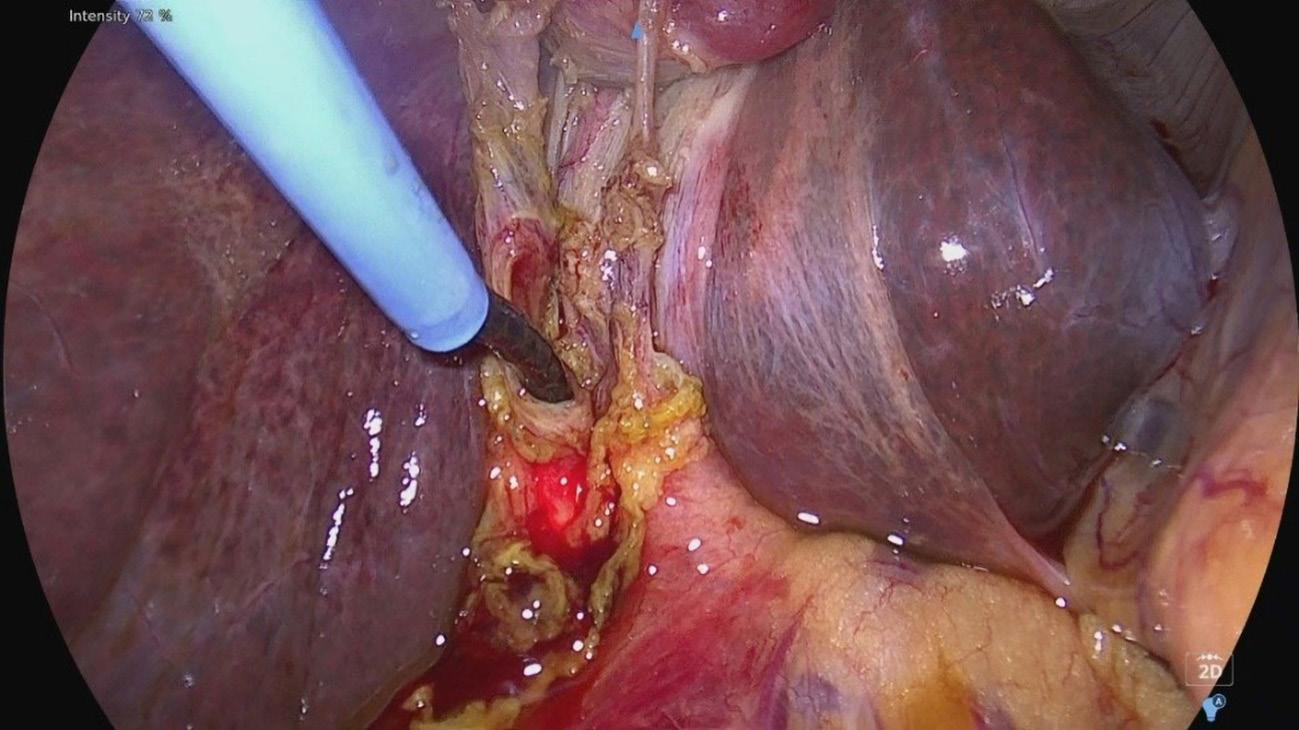
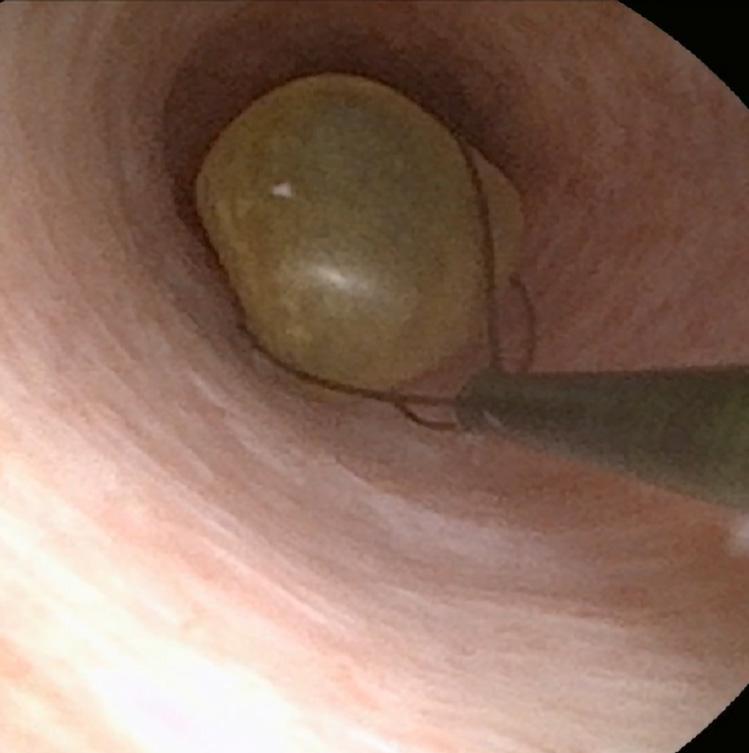
Koledokoskopi-assistert ekstraksjon av konkrement i ductus koledokus.
En lignende versjon av denne artikkelen ble publisert i NGFNytt i 2024 (10).
INDIKASJON FOR INTRAOPERATIV GALLESTEINSSANERING
De fleste pasientene som trenger behandling for koledokusstein blir innlagt som øyeblikkelig hjelp. Ved OUS Ullevål får de fleste pasienter med mistanke om gallegangsstein gjennomført en MRCP (MR undersøkelse av gallegangene). Dersom pasienten er medisinsk og teknisk operabel, og gallegangssteinene er små (< 68 mm), få (< 45 steiner) og ligger gunstig til anatomisk (i distale koledokus), er den foretrukne behandlingen laparoskopisk kolecystektomi med intraoperativ steinsanering. Dette er i prinsippet uavhengig av hvilken galleveisrelatert tilstand pasientene har: akutt pankreatitt, akutt kolecystitt, akutt kolangitt eller gallesteinssmerter.
Ved kirurgisk endret anatomi i øvre GItraktus er metoden spesielt velegnet. Dette gjelder først og fremst pasienter med RouxenYrekonstruksjon, med utilgjengelig papille for vanlig ERCPskop.
NØDVENDIG UTSTYR
For å gjennomføre intraoperativ gallesteinssanering er man avhengig av mulighet for gjennomlysning med en Cbue. Videre trengs et utvalg av ledevaiere og blokkeballonger. Dersom det skal gjøres koledokoskopi trengs videre et skop og stenekstraksjonsutstyr. Vi bruker engangs ureterorenoskop, noe som flere leverandører tilbyr. En oversikt over nødvendig utstyr er presentert i Ramme 2.
PRAKTISK GJENNOMFØRING
Laparoskopisk kolecystektomi planlegges og gjennomføres på vanlig måte. Antibiotikaprofylakse gis etter retningslinjer. Man kan vurdere pankreatittprofylakse med 100 mg diklofenak supp. Calots triangel dissekeres fram og ductus cysticus identifiseres. Det settes klips på ductus cysticus like under infundibulum og det føres inn et 4 Ch ureterkateter gjennom en knepunksjonskanyle eller en Olsens tang (Bilde 1A). Gjennom kateteret gjøres kolangiografi. Dersom det påvises koledokuskonkrementer eller det ikke er kontrastovergang til duodenum, startes en stepupalgoritme (Ramme 1). Stepupalgoritmen avsluttes i det man har steinfrie sentrale galleveier.
Ved små steiner i distale koledokus kommer man til målet i de aller fleste tilfeller med butylskopolamin, blokking av papillen og eventuelt antegrad feiing av koledokus. For å få gjennomført dette trengs kun Cbue, ledevaier, blokkeutstyr og vilje til å holde på med ledevaier. Man må rigge seg til på operasjonsstua slik at man kan gjennomlyse og håndtere laparoskopiinstrumenter samtidig. Vi senker operasjonsbordet helt ned mot Cbuen slik at vi får mest mulig plass. Man kan også fiksere tangen som holder i galleblærefundus med tøyklyper eller lignende mot operasjonsdekningen for å frigjøre en hånd. Direkte steinekstraksjon med steinfangerutstyr med gjennomlysning har vi ikke erfaring med hos oss, men det er beskrevet av andre.
Dersom steinene er over 56 mm må det ofte gjøres koledokoskopi med steinekstraksjon med kurv (Bilde 1D). Vi etablerer da en ekstra 5 mm port under høyre ribbebue og bruker en innføringshylse for koledokoskopet (Bilde 1C). Dersom det skal gjøres koledokoskopi er det ofte lurt å få med en tredje kirurg på inngrepet, da man må holde styr på laparoskopikamera, koledokoskop, laparoskopitenger og ledevaiere. Det er også nødvendig å plassere skjermer på en slik måte at man kan se bildene fra koledokoskopet, fra laparoskopien og fra gjennomlysningen samtidig. I oppstartsfasen er det lurt å holde prosedyren på få hender, da det er flere små tekniske grep som er avgjørende for at prosedyren lykkes.
Ved OUS Ullevål har vi valgt å kun gjøre transcystisk koledokoskopi. Dette for det første fordi det nødvendige volumet av koledokotomi er såpass lite slik at erfaringen med dette per kirurg blir svært begrenset. Videre har flere studier vist at forekomsten av postoperative komplikasjoner som gallelekkasje og påfølgende liggetid i sykehus er en del høyere ved direkte koledokoskopi sammenlignet med transcystisk koledokoskopi, slik at det etter vår vurdering ikke forsvarer metoden framfor ERCP (11).
Dersom vi ikke oppnår steinfrihet og det ikke er mulig å gjøre intraoperativ rendezvousERCP fullføres kolecystektomien som normalt og ductus cysticus lukkes med med klips eller Hemolok®. Pasienten henvises til ERCP i løpet av de neste par dagene. Vi har ikke opplevd lekkasje fra cysticusstumpen i denne ventetiden.
POSTOPERATIV OPPFØLGING
Det er en risiko for postprosedyre pankreatitt ved antegrad manipulasjon av papillen. Forekomsten av pankreatitt etter denne prosedyren er usikker, men har blitt rapportert som lav (< 5 %) i flere studier (9, 12-14). Det
FOR BLOKKING AV PAPILLE OG FEIING AV KOLEDOKUS
1. Cbue
2. Knepunksjonskanyle
3. 4 Ch ureterkateter
4. 150 cm ledevaier 0,035 tommer – med rett og bøyd tupp
5. 6/7/8 mm blokkeballong og tilhørende blokkepumpe
FOR KOLEDOKOSKOPI
1. Engangsskop – uretrorenoskop (flere leverandører)
2. Hylse til å føre skopet gjennom laparoskopiport
3. Kurver til å hente ut steiner
VED BEHOV FOR INTRAOPERATIV RENDEZVOUS ERCP
1. 450 cm ledevaier som kan hentes ut av ERCPskop
RAMME 2: Nødvendig utstyr for sanering av gallegangsstein
eksisterer imidlertid ingen gode diagnostiske kriterier for pankreatitt etter intraoperativ steinsanering (15, 16). Vi måler rutinemessig amylase på disse pasientene første postoperative dag.
Ved usikkerhet om pasienten er steinfri har bilirubinog leververdier i blodet de første postoperative dagene liten verdi. Erfaringsmessig vil mange pasienter få en forbigående økning av disse uten at det betyr at det foreligger restkonkrementer. MRCP de første dagene er også vanskelig å tolke, da små steiner og luftbobler kan være vanskelig å skille. Ved usikkerhet om pasientene er helt steinfrie, og dersom de ellers er i god allmenntilstand, kan de skrives ut og kontrollere levergalleprøver etter 57 dager. De må også få beskjed om å kontakte sykehus ved symptomer på gallekolikk.
KONKLUSJON
Laparoskopisk kolecystektomi med intraoperativ transcystisk sanering av gallegangsstein er en metode som kan implementeres i de fleste kirurgiske avdelinger uten store investeringer i hverken utstyr eller opplæring. Det er lite komplikasjoner, og pasienter kan sannsynligvis spares for flere prosedyrer og unødvendig liggetid på sykehus.
REFERANSER:
Se bakerst i nettutgaven på kirurgen.no


Pankreatisk duktalt adenokarsinom (PDAC) er blant de dødeligste kreftformene, og målet med denne avhandlingen var å undersøke hvordan presisjonsmedisin, tidlig diagnostikk og risikobaserte strategier samlet kan bidra til tidligere diagnose og mer effektiv behandling.
LINNEA MALGERUD BARNEKIRURGISK AVDELING, OSLO UNIVERSITETSSYKEHUS, RIKSHOSPITALET KORRESPONDANSE: LINNEA.MALGERUD @ GMAIL.COM
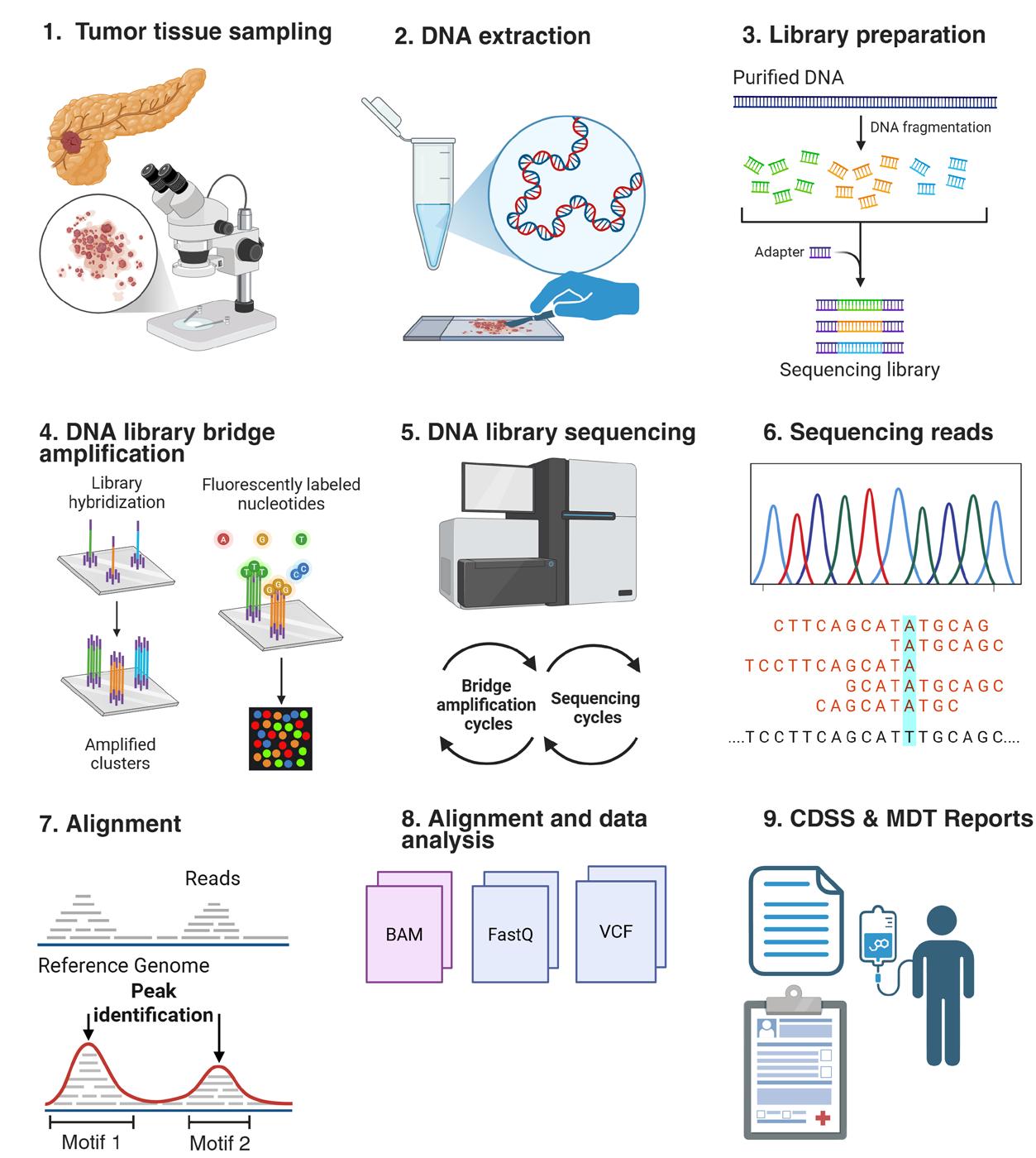
Studie 1 var retrospektiv og hadde som mål å evaluere innføringen av persontilpasset kreftbehandling som klinisk rutine. I studie 1 og 4 ble tumorprøver og tilhørende kontrollprøver fra henholdsvis 14 og 39 pasienter analysert ved Avdeling for klinisk patologi og cytologi ved Karolinska Universitetssjukhuset (KS), i henhold til SWEDAC-sertifiserte arbeidsmetoder. Vevsblokker ble vurdert av patolog, og kun prøver med ≥20 % tumorinnhold ble brukt til DNAekstraksjon. Sekvenseringen ble gjennomført, og dataene analysert ved hjelp av et klinisk beslutningsstøttesystem (CDSS).
CDSS genererte rapporter som predikerte legemiddeleffektivitet, resistens og toksisitet, vurderte onkogen relevans, og estimerte funksjonell betydning av genetiske varianter basert på evidensbaserte modeller. Rapportene ble vurdert ved en Molecular Tumor Board (MTB/ MDT) på KS. Ved bruk av CDSS ble positive responsbiomarkører identifisert hos alle unntatt én pasient (1–8 per pasient), biomarkører som predikerte manglende effekt hos alle pasienter (1–4 per pasient), og toksisitetsmarkører hos alle pasienter (1–5 per pasient), inkludert seks FDAgodkjente farmakogenomiske mar
kører. Pasientene i studie 1 fikk standardbehandling, og behandlingsvalg ble ikke endret basert på CDSSanbefalingene. I studie 4 ble det derimot gitt «off-label» anbefalinger basert på CDSS, som i enkelte tilfeller ble brukt som annenlinjebehandling. Selv om mange potensielle behandlingsalternativer ble identifisert, kreves mer data for å kunne vurdere effekten av sekvensering på pasientutfall. Studiene oppnådde likevel et delmål ved å vise at sekvensering kan integreres i klinisk drift innen en rimelig tidsramme.
Studie 2 undersøkte prediktorer for malign transformasjon av intraduktal papillær mucinøs tumor (IPMN), et kjent forstadium til PDAC. I en retrospektiv kohort som besto av 152 kirurgisk resekerte IPMNpasienter (samtlige ved Karolinska Universitetssjukhus, 2008–2015) var hovedpankreasgangdilatasjon (MPD) ≥6 mm, ikterus og forhøyet CA199 uavhengig assosiert med høygradig dysplasi eller invasiv kreft. Disse preoperative risikofaktorene kan bidra til tidligere kirurgisk intervensjon hos høyrisikopasienter.
Studie 3 analyserte sammenhengen mellom nyoppstått diabetes mellitus (NODM), antidiabetisk behandling og risiko for PDAC. Nyoppstått type 2diabetes og økende HbA1cnivåer var uavhengige risikofaktorer med høyest risiko blant insulinbrukere, etterfulgt av sulfonylurea, mens metformin viste svakere sammenheng. Risikoen var sterkest det første året etter diabetesdiagnose.
Samlet viser alle fire studier at presisjonsonkologiske metoder basert på sekvensering kan integreres i klinisk praksis innenfor korte tidsrammer, samtidig som kliniske og metabolske risikofaktorer kan bidra til tidligere intervensjon. Studiene viser både potensialet og behovet for kritisk evaluering av nye verktøy i persontilpasset behandling av PDAC.
Avhandlingen er tilgjengelig i sin helhet på https://doi.org/10.69622/29995699
REFERANSER :
Se bakerst i nettutgaven på kirurgen.no
1.-2.6.2026 –
Gastrokirurgisk avdeling ved Haukeland Universitetssjukehus inviterer alle interesserte til Nordic Early ColoRectal Cancer Meeting (NERC) 01.0602.06. NERC er et nordisk, tverrfaglig møte med hovedfokus på tidlig kolorektal kreft, arrangert på Solstrand Hotel & Bad utenfor Bergen. Møtet har sitt opphav i TEM Scandinavia (etablert i 2006), men er nå relansert med utvidet mandat som omfatter både tidlig kolon og rektumcancer og med tydelig vekt på organbevarende, individualisert og evidensbasert behandling.
Programmet er bygget rundt hele forløpet ved tidlig kolorektal kreft: fra endrede diagnostiske strategier til valg mellom endoskopisk lokalbehandling, onkologisk behandling og organreseksjoner. Det legges stor vekt på histopatologisk risikostratifisering, vurdering av når lokal eksisjon er tilstrekkelig, og når pasienten bør tilbys kompletterende kirurgi eller onkologisk behandling.
En rød tråd gjennom årets møte er hvordan nye teknikker og konsepter kan tas i bruk på en trygg måte: EMR/ESD/
EID og eFTR, laparoendoskopiske reseksjoner, samt bruk av radioterapi og organbevarende strategier ved utvalgte tidlige lesjoner. I tillegg adresseres verktøy som ctDNA, immunterapi ved tidlig kolorektal kreft og prospektive studier som TESAR og STARTREC, med tanke på å definere fremtidige behandlingsalgoritmer.
NERC er en konsentrert faglig møteplass for alle som ønsker å ligge i front i den pågående utviklingen mot mer skånsom, men onkologisk trygg behandling av tidlig kolon og rektumcancer.
Velkommen!



Vi presenterer et spennende, tverrfaglig program med nyheter, oppdateringer og aktuelle diskusjoner for diagnostikk og behandling på kreftområdet. Programmet spenner over hele gastrointestinal trakten og er tverrfaglig sammensatt.
Vi ser frem til sosial sammenkomst og hyggelig festmiddag på torsdags kveld.
Møtet har vært populært og vi satser også i år på fullt hus! Deltagelse følger etter ‘først til mølla’ prinsippet (begrenset med plasser). Lenke til påmelding, hotellbestilling og detaljert program vil legges ut på hjemmesiden; ngicg.no
På vegne av arrangørene ønskes velkommen til et spennende fagmøte!
Tom Mala Leder NGICG
• «Early onset» kolorektal cancer
• Arvelig GI cancer hvem skal henvises for genetisk utredning og hvorfor?
• Skrøpelighetsvurdering
• Samvalg, over og underbehandling
• Presisjonsmedisin hvor langt er vi kommet innen GI cancer
• Hvilken presisjonsdiagnostikk skal utføres på GI cancer i 2026
• Beslutningsforum/Nye metoder arbeidsprosess og prinsipper for prioritering
• MSIHigh behandlingsmuligheter ved kolorektal vs. annen GI cancer
• Immunterapi ved øvre GI cancer og analcancer
• Resultater fra kolorektal, øsofagus/ ventrikkel og pankreaskreft registrene
• Nytt fra ledere av NGICG faggruppene – kolorektal/HPB/øvre GI
• Nytt innen endoskopiske avlastningsprosedyrer ved øvre GI/HPB cancer
• Bridge to surgery ved stenoserende koloncancer – stent eller bøylestomi?
• Robotassistert kirurgi ved GI cancer i Norge – en revolusjon eller bare en ny tilgang?
• Fra min PhD: Presentasjon av doktorgrader innen GI cancer fra 2025
• Organbevarende behandling ved rektumcancer og kreft i spiserør/magesekk
• Resultater fra NORGAST 2025
Dr. Alexander Malthe (1845-1928) har vært banebrytende i norsk kirurgi. Han arbeidet ved Rikshospitalet, og startet privat kirurgisk praksis i Christiania. Malthe hadde flere studieopphold i utlandet, bla London, Paris og Tyskland. Han utførte den første operasjonen for appendisitt i Norge (1889), den første ventrikkelreseksjonen (1897) og den første elektive brokkplastikken.
VILLANGER LEDER MALTHES LEGAT
• Dr Alexander Malthes legat opprettet i 1920, drevet av Oslo kirurgiske forening og overført Norsk kirurgisk forening i 2014
• Formålet er å fremme norsk kirurgi i form av reisestipend, hospitering etc for dyktige yngre leger til videre utdannelse
• Stipend lyses ut i mange kanaler, blant annet i Kirurgen, sosiale medier, mail, og i samarbeid med Foreningen for unge norske kirurger (FUNK). Søknaden må inneholde en beskrivelse av formål med stipendet og et budsjettforslag.
• Stipendmottagerne må levere en kort reiserapport med beskrivelse av faglig utbytte, til publisering i Kirurgen
• Søknad vurderes av styret for Malthelegatet: Olaug Villanger (OUS, leder), ArneChristian Mohn (Helse Vest), Birgitte Brandt (Kalnes). I tillegg har legatet en fonds/legatbestyrer (advokat)
I 2025 har fondene har utviklet seg bra. I anledning 100års jubileum for Høstmøtet ble det besluttet å dele ut 4 store stipend á NOK 35 000 på Jubileumsmiddagen, samt dekke kostnad for denne.
STIPENDMOTTAGERNE :
1. Gina Dufseth Vangen, LIS i kirurgi Ringerike. Stipend til deltagelse på «DavosCourse GI Surgery», Davos april 2026.
2. Torbjørn Stubø, LIS i kirurgi Ringerike. Stipend til deltagelse på «DavosCourse GI Surgery», Davos april 2026.
3. Henriette Vaage Valen, LIS i generell kirurgi og transplantasjonskirurgi OUS RH. Stipend til hospitering på Universitetssykehuset i Groningen, Nederland for læring av ny teknikk; bruk av maskinperfusjon av lever ved transplantasjon. Tre uker hospitering i 2026.
4. Sondre Busund, klinisk stipendiat og LIS i gastrokirurgi OUS RH. Stipend til deltagelse i internasjonal kongress i lever/galle/pankreas med planer om innsending av abstrakt, IHPBA Singapore oktober 2026.

1. Burman MS. Arthroscopy or the direct visualization of joints: an experimental cadaver study. Clin Orthop Relat Res 1931;390:5–9.
2. Takagi K. The classic arthroscope. Clin Orthop Relat Res 1982;167:6-8. Translated and reprinted with permission from: Takagi K.:Arthroscope. J Jap Orthop. Assoc 1939;14:359.
3. van Dijk CN, Scholte D. Arthroscopy of the ankle joint. Arthroscopy 1997;13(1):90–96.
4. van Dijk CN, Scholten PE, Krips R. A 2-portal endoscopic approach for diagnosis and treatment of posterior ankle pathology. Arthroscopy. 2000;16:871–876.
5. van Dijk CN. Ankle Arthroscopy: Techniques Developed by the Amsterdam Foot and Ankle School. Berlin: Springer; 2014.
6. Shah R, Bandikalla VS. Role of arthroscopy in various ankle disorders. Indian J Orthop 2021;55(2):333–341.
7. Glazebrook MA, Ganapathy V, Bridge MA, Stone WS, Allard JP. Evidence-based indicators for ankle arthroscopy. Arthroscopy 2009;25(12):1478–1490.
8. Shimozono Y, Seow D, Kennedy JG, Stone JW. Ankle arthroscopic surgery. Sports Med Arthrosc Rev 2018;26(4):190–195.
9. Spennacchio P, Cucchi D, Randelli PS et al. Evidence-based indications for hindfoot endoscopy. Knee Surg Sports Traumatol Arthrosc 2016;24(4):1386–1395.
10. Chinnakkannu K, Barbachan Mansur NS, Glass N et al. Risks associated with posterior ankle hindfoot arthroscopy complications. Foot Ankle Int 2023;44(5):385–391.
11. Epstein DM, Black BS, Sherman SL. Anterior ankle arthroscopy: indications, pitfalls, and complications. Foot Ankle Clin 2015;20(1):41–57.
12. Rodríguez-Merchán EC. Encinas-Ullán CA, Ruiz-Pèrez JS et al. Complications of ankle arthroscopy: frequency, prevention, and treatment. EFORT Open Rev 2024;9(1):3-15.
13. Zengerink M, van Dijk CN. Complications in ankle arthroscopy. Knee Surg Sports Traumatol Arthrosc 2012;20:1420-1431
14. Zekry M, Shahban SA, El Gamal T et al. A literature review of complications following anterior and posterior ankle arthroscopy. Foot Ankle Surg 2019;25(5):553-558.
15. Arshad Z, Aslam A, Al Shdefat S et al. Complications following ankle arthroscopy a systematic review. Bone Joint J 2023;105-B(3):239–246.
1. Philippon MJ et al. Knee Surg Sports Traumatol Arthrosc. 2014;22(4):722–729.
2. Domb BG, Perets I, et al. Arthroscopy. 2020;36(2):477–489.
3. Kalisvaart MM, Safran MR. J Bone Joint Surg Am. 2022;104(3):261–270.
4. Palmer A, et al. Br J Sports Med. 2018;52(9):601–610.
5. Agricola R, et al. Am J Sports Med. 2012;40(5):1099–1106.
6. Heerey JJ, et al. Br J Sports Med. 2018;52(9):581–593.
7. Frank JM, et al. Am J Sports Med. 2021;49(2):304–314.
8. Krych AJ, et al. Arthroscopy. 2013;29(1):46–53.
9. Lodhia P, et al. Arthroscopy. 2020;36(5):1367–1377.
10. Domb BG, et al. Arthroscopy. 2015;31(3):520–529.
11. Nakano N, et al. Bone Joint J. 2017;99-B(12):1577–1583.
12. O’Connor M, et al. Am J Sports Med. 2023;51(1):59–69.
13. Griffin DR, et al. BMJ. 2018;361:k1121.
14. Palmer AJR, et al. Lancet. 2019;391(10136):2225–2235.
15. Khan M, et al. Arthroscopy. 2016;32(1):177–189.
16. Menge TJ, et al. Am J Sports Med. 2022;50(10):2790–2801.
17. FASHIoN Trial Investigators. Lancet. 2019;391(10136):2225–2235.
18. FAIT Trial Group. BMJ. 2018;361:k1121.
19. Risberg MA, et al. J Orthop Sports Phys Ther. 2018;48(4):325–335.
1. del Pinal F, Garcia-Bernal FJ, Pisani D, Regalado J, Ayala H, Studer A. Dry arthroscopy of the wrist: surgical technique. J Hand Surg Am. 2007;32(1):119–23.
2. Kakar S, Burnier M, Atzei A, Ho PC, Herzberg G, Del Pinal F. Dry Wrist Arthroscopy for Radial-Sided Wrist Disorders. J Hand Surg Am. 2020;45(4):341–53.
3. Geissler W. Wrist and elbow arthroscopy with selected open procedures : a practical surgical guide to techniques. Third edition. ed.
4. Kastenberger T, Kaiser P, Schmidle G, Schwendinger P, Gabl M, Arora R. Arthroscopic assisted treatment of distal radius fractures and concomitant injuries. Arch Orthop Trauma Surg. 2020;140(5):623–38.
5. Pinal Fd. Arthroscopic management of distal radius fractures. 1st ed. New York: Springer; 2010.
6. del Pinal F, Studer A, Thams C, Glasberg A. An all-inside technique for arthroscopic suturing of the volar scapholunate ligament. J Hand Surg Am. 2011;36(12):2044–6.
7. Mathoulin CL, Dauphin N, Wahegaonkar AL. Arthroscopic dorsal capsuloligamentous repair in chronic scapholunate ligament tears. Hand Clin. 2011;27(4):563–72, xi.
8. Geissler WB. Arthroscopic management of scapholunate instability. J Wrist Surg. 2013;2(2):129–35.
9. Ahsan ZS, Yao J. Complications of Wrist and Hand Arthroscopy. Hand Clin. 2017;33(4):831–8.
10. Shi H, Lu P, Yu D, Wang J, Wang Z, Zhuang B, et al. The training of wrist arthroscopy. Front Med (Lausanne). 2022;9:947459.
S24: KIRURGISK BEHANDLING AV ROTATORCUFFRUPTURER – INDIKASJONER, TIMING OG PROGNOSE
1. Bedi A, Bishop J, Keener J et.al. Rotator Cuff Tears. Nature Reviews Disease Primers. 2024;10(8):1-20
2. Yamamoto A, Takagishi K, Kobayashi T, et al. Factors involved in the presence of symptoms associated with rotator cuff tears: a comparison of asymptomatic and symptomatic rotator cuff tears in the general population. J Shoulder Elbow Surg 2011;20:1133–7.
3. Hinsley H, Ganderton C, Arden NK, et al. Prevalence of rotator cuff tendon tears and symptoms in a Chingford general population cohort, and the resultant impact on UK health services: a cross- sectional observational study. BMJ Open 2022;12:e059175. doi:10.1136/bmjopen-2021-059175
4. Moosmayer S, Gärtner AV, Tariq R. The natural course of nonoperatively treated rotator cuff tears: an 8.8-year follow-up of tear anatomy and clinical outcome in 49 patients. J Shoulder Elbow Surg 2017; 26; 627-634.
5. Enger M, Schmidt M, Nordsletten L et.al. Physical examination tests in the acute phase of shoulder injuries with negative radiographs: a diagnostic accuracy study. BMC Musculoskeletal Disorders. 2025;26(546):1-11.
6. Oslo universitetssykehus (OUS). Skulderen – rotatorcuffruptur. Metodebok. Sitert 14. jan 2026. Tilgjengelig fra: https://metodebok.no/emne/pcAUfG3a/skulderen--rotatorcuffruptur/ortopedi-(ous)
7. Desai V, Southam BR, Grawe B. Complications Following Arthroscopic Rotator Cuff Repair and Reconstruction. JBJS Reviews. 2018;6(1):e5,1-11.
8. Ibán MAR, Navlet MG, Marco SM et.al. Augmentation of a Posterosuperior Cuff Repair With a Bovine Bioinductive Collagen Implant Shows a Lower Retear Rate but Similar Outcomes Compared With No Augmentation: 2-Year Results of a Randomized Controlled Trial. The J of Arthroscopic and Related Surg. 2025;41(10):3869-3879.
9. Xiao M, Cohen SA, Cheung EV et. al. Arthroscopic Single and Double Row Repair of Isolated and Combined Subscapularis Tears Result in Similar Improvements in Outcomes: A Systematic Review. Arthroscopy: The J. of Arthroscopy and Related. Surg. 2022;38(1):159-173.
10. Holtedahl R, Bøe B, Brox JI. The Clinical Impact of Retears after Repair of Posterosuperior Rotator Cuff: A Systematic Review and Meta-analysis. J Shoulder Elbow Surg. 2023;32:1333–1346.
11. Moosmayer S, Lund G, Seljom S et.al. Fifteen-Year Results of a Comparative Analysis of Tendon Repair Versus Physiotherapy for Small-to-Medium-Sized Rotator Cuff Tears A Concise Follow-up of Previous Reports*. The J. of Bone and Joint Surg. 2024;106(1):1785-96.
S 30: ALBUEARTROSKOPISKOPI – INDIKASJONER, TEKNIKK OG PLASS I MODERNE ALBUEKIRURGI
1. Camp CL, Degen RM, Dines JS, Altchek DW, Sanchez-Sotelo J. Basics of Elbow Arthroscopy Part III: Positioning and Diagnostic Arthroscopy in the Lateral Decubitus Position. Arthroscopy techniques. 2016;5(6):e1351–e5.
2. Morrey BF, Sanchez-Sotelo J, Morrey ME. Morrey’s the elbow and its disorders. Philadelphia, Pa: Elsevier; 2018.
3. Adams JE, King GJW, Steinmann SP, Cohen MS. Elbow arthroscopy: indications, techniques, outcomes, and complications. Journal of the American Academy of Orthopaedic Surgeons. 2014;22(12):810–8.
4. O’Driscoll SW, Morrey BF. Arthroscopy of the elbow. Diagnostic and therapeutic benefits and hazards. Journal of bone and joint surgery. 1992;74(1):84–94.
5. Stanley D. Prevalence and etiology of symptomatic elbow osteoarthritis. J Shoulder Elbow Surg. 1994;3(6):386–9.
6. Antoni M, Mereb T, Ginot G, Meyer N, Clavert P. Prognostic factors for traumatic elbow osteoarthritis after terrible triad surgery, and functional impact. Orthop Traumatol Surg Res. 2021;107(2):102826.
7. Martinez-Catalan N, Sanchez-Sotelo J. Primary Elbow Osteoarthritis: Evaluation and Management. J Clin Orthop Trauma. 2021;19:67–74.
8. Gramstad GD, Galatz LM. Management of elbow osteoarthritis. J Bone Joint Surg Am. 2006;88(2):421–30.
9. Guerrero EM BG, Helmkamp JK, Madrid A, Ledbetter L, Richard MJ, Garrigues GE. The clinical impact of arthroscopic vs. open osteocapsular débridement for primary osteoarthritis of the elbow: a systematic review. J Shoulder Elbow Surg. 2020(Apr;29(4)):689–98.
10. Morrey BF, Askew LJ, Chao EY. A biomechanical study of normal functional elbow motion. J Bone Joint Surg Am. 1981;63(6):872–7.
11. Elfeddali R, Schreuder MHE, Eygendaal D. Arthroscopic elbow surgery, is it safe? Journal of shoulder and elbow surgery : JSES. 2013;22(5):647–52.
12. Ahmed AF, Alzobi OZ, Hantouly AT, Toubasi A, Farsakoury R, Alkhelaifi K, et al. Complications of Elbow Arthroscopic Surgery: A Systematic Review and Meta-analysis. Orthop J Sports Med. 2022;10(11):23259671221137863.
13. Kelly EW, Morrey BF, O’Driscoll SW. Complications of elbow arthroscopy. Journal of bone and joint surgery. 2001;83(1):25–34.
1. Williamson ERC, Shimozono Y, Toale J et al. Incidence of Chondral and Osteochondral Lesions in Ankle Fracture Patients Identified With Ankle Arthroscopy Following Rotational Ankle Fracture: A Systematic Review. J Foot Ankle Surg. 2022;61(3):668-73.
2. Aragoneses López P, López Hernández G, Malagelada F. The Role of Arthroscopy in Ankle Fracture Fixation. Foot Ankle Clin. 2025;30(4):723-36.
3. Baumbach SF, Urresti-Gundlach M, Braunstein M et al. Propensity score-matched analysis of arthroscopically assisted ankle facture treatment versus conventional treatment. Foot Ankle Int. 2021;42(4):400–8.
4. Miksch RC, Spindler FT, Böcker W et al. Arthroscopically assisted (AORIF) ankle fracture treatment seems to lead to superior results when compared to open reduction and internal fixation (ORIF) only: results of a systematic review. Arch Orthop Trauma Surg. 2025;145(1):451.
5. Yasui Y, Shimozono Y, Hung CW et al. Postoperative Reoperations and Complications in 32,307 Ankle Fractures With and Without Concurrent Ankle Arthroscopic Procedures in a 5-Year Period Based on a Large U.S. Healthcare Database. J Foot Ankle Surg. 2019;58(1):6-9.
6. Williams CE, Joo P, Oh I et al. Arthroscopically Assisted Internal Fixation of Foot and Ankle Fractures: A Systematic Review. Foot Ankle Orthop. 2021;6(1):1-10.
7. Darwich A, Adam J, Dally FJ et al. Incidence of concomitant chondral/osteochondral lesions in acute ankle fractures and their effect on clinical outcome: a systematic review and meta-analysis. Arch Orthop Trauma Surg. 2021;141(1):63-74.
8. Lindvall E, Haidukewych GJ, DiPasquale T et al. Open reduction and internal fixation of displaced talar neck fractures: results and complications. J Bone Joint Surg Am. 2004;86(1):2229–34.
9. Vallier HA, Nork SE, Barei DP et al. Talar neck fractures: results and outcomes. J Bone Joint Surg Am. 2004;86(8):1616–24.
10. Chalayon O, Müller J, Barg A et al. Talar body fractures: results and outcomes. Foot Ankle Int. 2013;34(6):766–77.
11. Vallier HA. Fractures of the talus: state of the art. J Orthop Trauma. 2015;29(9):385–92.
12. Ebraheim NA, Patil V, Frisch NC et al. Diagnosis of Talar Neck Fractures. Clin Orthop Relat Res. 2008;466(1):2060–6.
13. Bonasia DE, Rossi R, Saltzman CL et al. Posterior ankle and subtalar arthroscopy: indications, technique, and results. J Bone Joint Surg Am. 2011;93(23):2115–26.
14. Vega J, Malagelada F, Dalmau-Pastor M et al. Arthroscopic fixation of talar body fractures. Foot Ankle Clin. 2015;20(1):149–65.
15. Vega J et al. Arthroscopically assisted reduction and fixation of ankle and hindfoot fractures. J Orthop Trauma. 2013;27(2):e35–e39.
16. Malagelada F, Vega J, Dalmau-Pastor M. Arthroscopically assisted fixation of talar fractures. EFORT Open Rev. 2020;5(1):1–8.
17. Choi WJ, Lee JW. Posterior screw fixation for displaced talar body fractures. Foot Ankle Int. 2003;24(8):667–73.
18. Lui TH. Complications of posterior ankle and subtalar arthroscopy. Arthroscopy. 2006;22(8):869–74.
19. Tsai J, Chen CL, Lee WC et al. Comparing open versus arthroscopic-assisted reduction and fixation in talar body fractures: a retrospective cohort study. Foot Ankle Int. 2021;42(7):880–9.
20. Rammelt S, Gavlik JM, Barthel S et al. The value of subtalar arthroscopy in the management of intra-articular calcaneus fractures. Foot Ankle Int. 2002;23(10):906–16.
21. Grün W, Molund M, Nilsen F et al. Results After Percutaneous and Arthroscopically Assisted Osteosynthesis of Calcaneal Fractures. Foot Ankle Int. 2020;41(6):689-97.
22. Sivakumar BS, Wong P, Dick CG et al. Arthroscopic Reduction and Percutaneous Fixation of Selected Calcaneus Fractures: Surgical Technique and Early Results. 2014;28(10):569-76.
23. Nosewicz TL, Dingemans SA, Backes M et al. A systematic review and meta-analysis of the sinus tarsi and extended lateral approach in the operative treatment of displaced intra-articular calcaneal fractures. Foot Ankle Surg. 2019;25(5):580-8.
S 42: DIAGNOSTISK ARTROSKOPI
- TIPS OG TRIKS VED ARTROSKOPI AV KNE OG SKULDER
1. Lubowitz JH, Poehling GG. Arthroscopic evaluation of the knee: a systematic approach. Arthroscopy.2006;22(4):375–380.
2. Stäubli HU, Delcogliano A. The knee joint: diagnostic arthroscopy. In: Stäubli HU, Dejour D, editors. The unstable knee. Berlin: Springer; 2017. p. [sidenumre hvis ønskelig].
3. Balabaud L, Gaudias J, Boeri C, Jenny JY, Kehr P. Arthroscopic management of septic arthritis of the knee. Arthroscopy. 2007;23(9):934–940.
4. Johns BP, Loewenthal MR, Dewar DC. Arthroscopic versus open treatment of septic arthritis of the knee. J Bone Joint Surg Am. 2017;99(6):499–505.
5. Funk L, Snow M. Shoulder arthroscopy: principles and practice. London: Springer; 2012.
6. Snyder SJ, editor. Shoulder arthroscopy. 2nd ed. Philadelphia: Lippincott Williams & Wilkins; 2003.
7. Burkhart SS, Lo IKY, Brady PC. The Cowboy’s companion to shoulder arthroscopy. Philadelphia: Lippincott Williams & Wilkins; 2006.
8. Milano G, Grasso A, Brzóska R, Kovačič L, editors. Shoulder arthroscopy: principles and practice. 2nd ed. London: Springer; 2023.
1. Thompson M, Tranter S. All-comers policy for laparoscopic exploration of the common bile duct. Journal of British Surgery. 2002;89(12):1608–12.
2. Kazaryan AF, Magnus Hølmo; Glomsaker, Tom; Søvik, Torgeir; Mala, Tom; Fyhn, Thomas Johan. Behandling av gallesteinssykdom ved norske akuttkirurgiske sykehus: en nasjonal spørreundersøkelse. 2025;(Submitted).
3. Manes G, Paspatis G, Aabakken L, et al. Endoscopic management of common bile duct stones: European Society of Gastrointestinal Endoscopy (ESGE) guideline. Endoscopy. 2019;51(05):472–91.
4. Bansal VK, Misra MC, Rajan K, et al. Single-stage laparoscopic common bile duct exploration and cholecystectomy versus two-stage endoscopic stone extraction followed by laparoscopic cholecystectomy for patients with concomitant gallbladder stones and common bile duct stones: a randomized controlled trial. Surg Endosc. 2014;28(3):875–85.
5. Kochar B, Akshintala VS, Afghani E, et al. Incidence, severity, and mortality of postERCP pancreatitis: a systematic review by using randomized, controlled trials. Gastrointestinal endoscopy. 2015;81(1):143–9. e9.
6. Gloor S, Minder S, Schnell B, et al. Antegrade balloon dilatation of the duodenal papilla during laparoscopic cholecystectomy versus endoscopic retrograde cholangiography in patients with acute choledocholithiasis: a case control matched study. Surgical Endoscopy. 2024;38(7):3810–8.
7. Szulman C, Giménez M, Sierre S. Antegrade papillary balloon dilation for extrahepatic bile duct stone clearance: lessons learned from treating 300 patients. Journal of vascular and interventional radiology. 2011;22(3):346–53.
8. Liu S, Fang C, Tan J, et al. A Comparison of the Relative Safety and Efficacy of Laparoscopic Choledochotomy with Primary Closure and Endoscopic Treatment for Bile Duct Stones in Patients with Cholelithiasis. Journal of Laparoendoscopic & Advanced Surgical Techniques. 2020;30(7):742–8.
9. Thomassen HK, Kilander FS, Mala T, et al. Laparoskopisk transcystisk ekstraksjon av gallegangskonkrementer. Tidsskrift for Den norske legeforening. 2024.
10. Thomassen HKF, Magnus Hølmo; Glomsaker, Tom. Laparoskopisk transcystisk ekstraksjon av gallegangskonkrementer. NGF-Nytt. 2024.
11. Zheng B, Lu Y, Li E, et al. Comparison of the efficacy of LTCBDE and LCBDE for common bile duct stones: a systematic review and meta-analysis. Front Surg. 2024;11:1412334.
12. Seo YR, Moon JH, Choi HJ, et al. Papillary balloon dilation is not itself a cause of post-endoscopic retrograde cholangiopancreatography pancreatitis; results of anterograde and retrograde papillary balloon dilation. Journal of gastroenterology and hepatology. 2013;28(8):1416–21.
13. Lyu Y, Cheng Y, Li T, et al. Laparoscopic common bile duct exploration plus cholecystectomy versus endoscopic retrograde cholangiopancreatography plus laparoscopic cholecystectomy for cholecystocholedocholithiasis: a meta-analysis. Surgical Endoscopy. 2019;33(10):3275–86.
14. Lan WF, Li JH, Wang QB, et al. Comparison of laparoscopic common bile duct exploration and endoscopic retrograde cholangiopancreatography combined with laparoscopic cholecystectomy for patients with gallbladder and common bile duct stones a meta-analysis of randomized controlled trials. European review for medical and pharmacological sciences. 2023;27(10):4656–69.
15. Cotton P, Lehman G, Vennes J, et al. Endoscopic sphincterotomy complications and their management: an attempt at consensus. Gastrointestinal endoscopy. 1991;37(3):383–93.
16. Smeets XJ, Bouhouch N, Buxbaum J, et al. The revised Atlanta criteria more accurately reflect severity of post-ERCP pancreatitis compared to the consensus criteria. United European gastroenterology journal. 2019;7(4):557–64.
S 52: RISIKOSTRATIFISERING OG PERSONTILPASSET BEHANDLING AV PANKREATISK DUKTALT ADENOKARSINOM
1. Malgerud L, Lindberg J, Wirta V, Gustafsson-Liljefors M, Karimi M, Moro CF, Stecker K, Picker A, Huelsewig C, Stein M, Bohnert R, Del Chiaro M, Haas SL, Heuchel RL, Permert J, Maeurer MJ, Brock S, Verbeke CS, Engstrand L, Jackson DB, Grönberg H, Löhr JM. Bioinformatory-assisted analysis of next-generation sequencing data for precision medicine in pancreatic cancer. Mol Oncol. 2017;11(10):1413–29.
2. Ateeb Z, Valente R, PozziMucelli RM, Malgerud L, Schlieper Y, Rangelova E, FernandezMoro C, Löhr JM, Arnelo U, Del Chiaro M. Main pancreatic duct dilation greater than 6 mm and elevated preoperative CA199 levels are associated with an increased risk of highgrade dysplasia and cancer in IPMN patients. Langenbecks Arch Surg. 2019;404(1):3137.
3. Lu Y, García-Rodríguez LA, Malgerud L, González-Pérez A, Martín-Pérez M, Lagergren J, Bexelius TS. New-onset type 2 diabetes, elevated HbA1c, anti-diabetic medications, and risk of pancreatic cancer. Br J Cancer. 2015 Nov 17;113(11):1607–1614.
4. Malgerud L*, Kordes M*, Frödin JE, Yachnin J, Fernandez Moro C, Ghazi S, Pozzi Mucelli R, Kartalis N, Ghorbani P, Del Chiaro M, Wirta V, Björnstedt M, Liljefors MG, Löhr JM. Consistency of a clinical decision support system with molecular tumour board recommendations for tumour sequencingguided treatment of pancreatic cancer: a prospective observational study. ESMO Gastrointestinal Oncology. 2024;1(1):100070. *Equal contributions as first authors

Indication: this medicinal product is for diagnostic use only. Carmyne is indicated in adults for the intra-operative detection of suspected ureteral injuries during abdominal and pelvic surgery.
Carmyne 40 mg – Plikttekst for Carmyne 40 mg «Indigokarmin» injeksjonsvæske, oppløsning Reseptgruppe C. Indikasjoner: Kun til bruk ved diagnostiske formål. Indisert hos voksne til intraoperativ påvisning av mistenkte ureterskader under abdominal kirurgi og bekkenkirurgi. Dosering: Anbefalt startdose er 1 ampulle på 5 ml ved langsom i.v. injeksjon. En andre ampulle kan injiseres 20 til 30 minutter etter den første injeksjonen, om nødvendig. Se SPC for spesielle pasientgrupper og administrasjonsmåte. Kontraindikasjoner: Overfølsomhet for innholdsstoffene. Forsiktighetsregler: Kan forårsake en forbigående økning av blodtrykket og refleksbradykardi, spesielt hos pasienter under generell anestesi eller under spinalanestesi. Sjeldne idiosynkratiske reaksjoner med bradykardi og hypotensjon er også rapportert. Det er derfor nødvendig å overvåke hjertefrekvens og blodtrykk under og noen minutter etter injeksjonen. I.v. injeksjon bør stoppes ved følgende symptomer: bradykardi, takykardi, hypotensjon, hypertensjon, utslett eller erytem, luftveissymptomer som dyspné eller bronkospasme. Har ikke blitt studert hos pasienter med GFR <30 ml/min, og bør derfor ikke brukes hos disse. Kan forstyrre puls eller cerebrale oksymetrimålinger. Bør brukes med forsiktighet ved: høyt blodtrykk, lav hjertefrekvens, hjerte- og ledningsforstyrrelser, samtidig bruk av legemidler som induserer bradykardi eller påvirker blodtrykket eller produksjonen av nitrogenoksid, koronare lidelser på grunn av dets perifere vasokonstriktoreffekt. Bruk bør unngås hos pasienter med: hemodynamisk ustabilitet, ukontrollert hjertesvikt, allergiske reaksjoner i anamnesen. Graviditet, amming og fertilitet: Graviditet: Ingen data. Anbefales ikke under graviditet og hos fertile kvinner som ikke bruker prevensjon. Amming: Overgang i morsmelk er ukjent. Risiko for diende barn kan ikke utelukkes. Nytte-/risikovurdering må foretas. Bivirkninger: Svært vanlig: Bradykardi, hypertensjon (forbigående). Svært sjeldne: Anafylaktoide reaksjoner, AV-blokk, bronkial hyperreaktivitet, dyspné, hypotensjon, misfarging av hud, utslett og erytem, takykardi. Overdosering/ Forgiftning: En overdose kan indusere en hypertensiv krise og alvorlig bradykardi. Ved overdosering kan det vurderes behandling med en perifer vasodilator.
For mer informasjon, se Felleskatalogteksten eller preparatomtalen (SPC)Innehaver av markedsføringstillatelsen: SERB S.A., Belgia. Kontaktinformasjon: Telefon: 003227920500. E-post: safety@serb.eu. Basert på SPC godkjent av DMP/EMA: 19.06.2024. Pakninger og priser per 17.07.2024: Ampulle 10 × 5 ml. 4713,00 kr. (priser og ev. refusjon oppdateres hver 14. dag). Refusjon: Ingen refusjon. Utarbeidet 07/2024