Avances tecnológicos de bioanálisis.














By: Charlina Sánchez/ Marleny Morillo.
Abril 2025.


Editorial.
Vivimos en una era donde la tecnología avanza a pasos agigantados, transformando todos los aspectos de nuestra vida. Uno deloscamposdondeestosavances han generado un impacto profundo eslasalud,especialmenteenáreas como el bioanálisis, una disciplina clave para el diagnóstico, la prevención y el tratamiento de enfermedades.
Esta revista nace del interés por explorar cómo las innovaciones tecnológicas están revolucionando los métodos tradicionales de análisis clínico, desde la incorporación de inteligencia artificialhastadispositivosportátiles dediagnóstico.Comoestudiantede enfermería, considera esencial comprender estos cambios, ya que
marcarán el futuro de nuestra profesiónyelbienestardenuestros pacientes.
En esta edición encontrarás artículos que abordan tecnologías emergentes como los biosensores, la secuenciación genética y los laboratorios miniaturizados, entre otros.Tambiénincluimosunartículo de opinión sobre los retos éticos y sociales que surgen con estos avances.
Teinvitamosaleercadapáginacon curiosidad y mente abierta. Porque entender la tecnología que nos rodea no solo es una herramienta, sino también una responsabilidad que,comoprofesionalesdelasalud, nopodemosignorar.
¡Bienvenidos a esta edición dedicada al fascinante mundo del bioanálisis!

Historia de bioanálisis.
Elbioanálisistienesusraícesenla antigüedad, cuando los primeros médicosobservabancambiosenla orinayotrosfluidoscorporalespara diagnosticar enfermedades. Sin embargo,fueenelsigloXIXcuando se establecieron las bases del análisis clínico moderno, con el desarrollo de técnicas como la microscopíaylaespectroscopía.
Durante el siglo XX, el bioanálisis experimentó un rápido crecimiento gracias a los avances en bioquímica, inmunología y biología molecular. La automatización de procesos,eldesarrollodereactivos más precisos y la introducción de computadoras en los laboratorios permitieronunamejorasignificativa enlavelocidadyconfiabilidaddelos resultados.
En la actualidad, el bioanálisis combina tecnologías de punta con conocimientos multidisciplinarios, convirtiéndose en una herramienta esencialenlamedicinamoderna,la investigacióncientíficaylaindustria farmacéutica.
http://www.ula.ve/farmaciabioanalisis/historia-bioanalisis

Bioanálisis.
El bioanálisis es una disciplina científica que se enfoca en el análisisdelassustanciaspresentes en organismos vivos, como seres humanos, animales y plantas, a través de técnicas y pruebas de laboratorio. El objetivo principal del bioanálisis es medir, identificar y cuantificar las sustancias en el organismoparaobtenerinformación sobre el estado de salud del individuo, detectar enfermedades, monitorear tratamientos y evaluar los efectos de los fármacos en el organismo.
Bioanalista.
Esunprofesionalqueseespecializa enelanálisisdemuestrasbiológicas utilizando métodos y equipos científicos. Su trabajo es crucial en diversos campos, incluyendo la medicina,lainvestigacióncientífica, la industria farmacéutica y la biotecnología.
Este es el personal a cargo de analizar;
• muestrasbiológicas
• realizarlaspruebasdelaboratorio
• Participan en la creación y prueba de métodos para analizar las muestras.
• Análisiseinterpretacióndedatos
• Mantenimiento de registros y elaboracióndeinformes
• Mantenimiento y calibración de equiposdelaboratorio.

Opinión:
Elbioanálisisesunacienciafundamentalque,aunquemuchasvecestrabaja trasbastidores,tieneunimpactodirectoenlasaluddetodos.Losbioanalistas son los ojos clínicos que, desde el laboratorio, ayudan a detectar enfermedades, monitorear tratamientos y prevenir complicaciones. Son profesionalescomprometidosconlaprecisión,laéticayelbienestarhumano.
Avances tecnológicos de bioanálisis.
El campo del bioanálisis está experimentando una rápida transformación gracias a la integración de diversos avances tecnológicos. Estas innovaciones están mejorando la precisión, la eficiencia, la velocidad y la capacidad de análisis de muestras biológicas, lo que tiene un impacto significativo en el diagnóstico de enfermedades, la investigación
científica y el desarrollo de nuevas terapias.
Estos avances están impactando positivamente en el diagnóstico temprano y preciso de enfermedades, la medicina personalizada, el desarrollo de nuevas terapias, la investigación científicaeficienteylamejoradela salud pública. En resumen, la tecnología está transformando el bioanálisis hacia un futuro de análisismásrápidos,precisosycon mayorcapacidad.

Ventajas.
• Mayorprecisiónyexactitud
• Rapidezenlosresultados
• Detección temprana de enfermedades
• Procesamiento de grandes volúmenesdemuestras
• Mejora en la trazabilidad y control decalidad
• Acceso a tecnologías moleculares avanzadas
Desventajas
• Alto costo de adquisición y mantenimiento
• Dependenciadelatecnología
• Necesidad de capacitación permitenanálisismásespecíficos.
• Deshumanizacióndelproceso
• Obsolescenciarápida
• Problemaséticosydeprivacidad
Biosensores y nanotecnología: detección a nivel molecular.
Los biosensores y la nanotecnología se han unido para revolucionar la detección a nivel molecular, ofreciendo herramientas sin precedentes para el análisis de entidadesbiológicasyquímicascon una sensibilidad y especificidad extremadamentealtas.
Los nanobiosensores son dispositivos analíticos que integran un componente de reconocimiento biológico (enzimas, anticuerpos, ADN,etc.)conunnano-transductor. La interacción específica entre el componentebiológicoylamolécula objetivo genera una señal que el nano-transductor convierte en una señal medible (eléctrica, óptica, mecánica,etc.)

Seaplicanendiversoscampos:
Diagnóstico médico: Detección tempranadeenfermedades.
• Portabilidad y miniaturización: Facilidadde uso en diversos entornos e inclusoinvivo.
Detección de patógenos: Identificación rápida y sensible de bacterias,virus,hongos.
Monitoreo ambiental: Detección de contaminantes químicos y biológicos en el aire, el agua y el suelo.
Seguridadalimentaria: Control de calidadydeteccióndeadulterantes, alérgenosypatógenos.
Descubrimiento de fármacos: Cribado de alto rendimiento de posibles candidatos a fármacos y monitorizacióndesuinteraccióncon dianasmoleculares. Ventajas.
• Altasensibilidad: Capacidad paradetectarconcentraciones muybajasdeanalitos.
• Alta especificidad: Reconocimiento selectivo de la molécula objetivo, minimizando las interferencias.
• Detección rápida y en tiempo real: Permiten obtener resultados rápidamente,loqueescrucial enmuchasaplicaciones.
• Potencial para bajo costo: La producción a gran escala podría reducir los costos en comparación con métodos tradicionales.
• Menorconsumodemuestra yreactivos: Beneficiosopara el análisis de muestras limitadas y la reducción de residuos.
Desventajas:
• Costos iniciales de desarrolloyfabricación
• Escalabilidad: Laproducción agranescalamanteniendola uniformidad y el rendimiento puedeserundesafío.
• Toxicidad potencial de nanomateriales
• Interferencias no específicas
• Validaciónyregulación: La validación clínica y la regulación de los
Opinión.
nanobiosensores para aplicaciones médicas aún estánendesarrollo.
• Complejidad de la interfaz biológica-nano

La integración de biosensores con nanotecnología permite detectar sustancias a nivel molecular con gran precisión y rapidez. Gracias a materiales como nanopartículas o nanotubos, estos dispositivos pueden identificar virus, proteínas o toxinas en cantidades mínimas, incluso antes de que aparezcan síntomas. Esta tecnología está transformando el diagnóstico médico, haciéndolo más temprano, preciso y accesible.
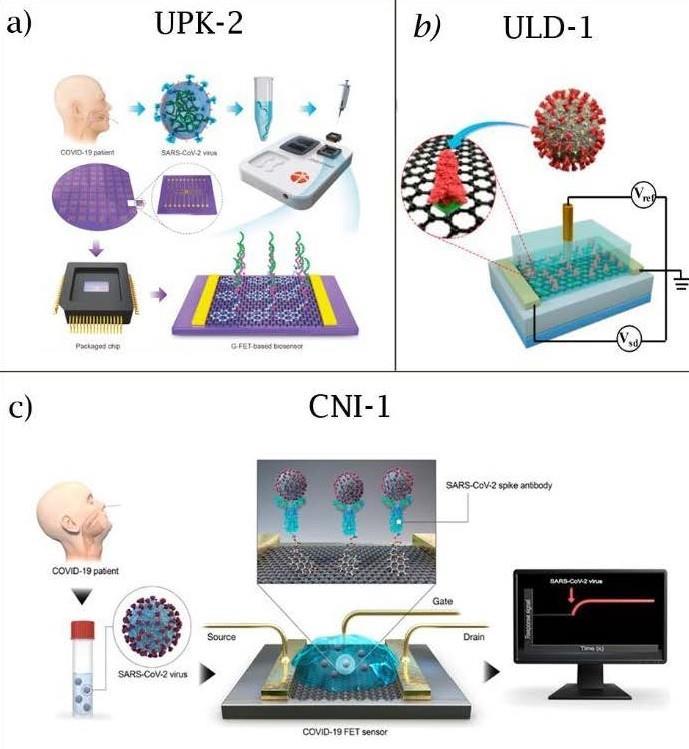
Espectrometría de masas: precisión en la identificación de compuestos Es una técnica analítica poderosa que se destaca por su precisión excepcional en la identificación y cuantificación de compuestos a nivel molecular. Su capacidad para determinar la masa exacta de las moléculasysusfragmentosiónicos la convierte en una herramienta indispensable en diversos campos científicos y aplicaciones industriales.
¿Cómologralaespectrometríade masasestaprecisión?
La EM funciona bajo el principio fundamental de ionizar las moléculas de una muestra y luego separarestosionesenfuncióndesu relaciónmasa-carga(m/z).Almedir con exactitud estas relaciones y la abundanciadecadaion,segenera un espectro de masas, que actúa comounahuelladactilarúnicapara cadacompuesto.
Aplicacionesdondelaprecisión delaespectrometríademasases crucial:
• Química analítica: Identificación y cuantificación de componentes en mezclas complejas, control de calidad deproductosquímicos.
• Farmacéutica: Descubrimiento y desarrollo de fármacos, análisis de pureza y metabolitos de medicamentos.
• Proteómica y metabolómica: Identificación ycuantificacióndeproteínasy metabolitos.
• Medicinaclínica: Diagnóstico de enfermedades metabólicas.

• Ciencia forense: Identificación de sustancias desconocidas en escenas del crimen,análisisdedrogas…
• Ciencias ambientales: Detección y cuantificación de contaminantesenagua,airey suelo.
• Seguridad alimentaria: Análisisdelacomposiciónde alimentos, detección de adulterantesycontaminantes.

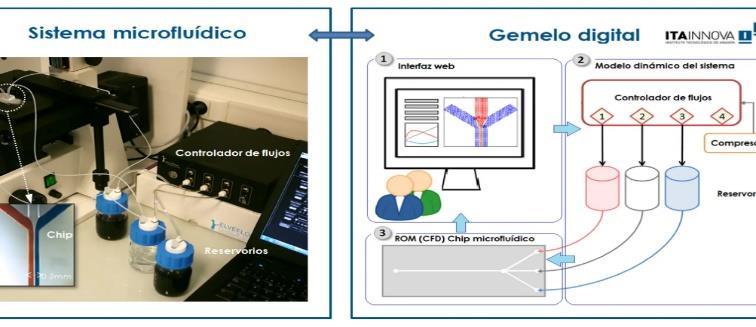
Microfluídica y dispositivos lab-on-a-chip: laboratorios en miniatura
La microfluídica es un campo multidisciplinario que se enfoca en el comportamiento preciso y la manipulación de fluidos que están geométricamente confinados a una escalapequeña.
Los dispositivos lab-on-a-chip (LOC) son la culminación de la microfluídica, representando la miniaturizacióneintegracióndeuna ovariasfuncionesdelaboratorioen un único chip, que a menudo tiene un tamaño de solo unos pocos milímetros o centímetros cuadrados.

¿Cómo funcionan los laboratoriosenminiatura?
Estos dispositivos utilizan redes intrincadas de micro canales, cámaras de reacción, sensores y actuadores para realizar tareas complejas de análisis y procesamiento de muestras. El controlprecisodelosfluidosaesta escala se logra mediante
fenómenos físicos que se vuelven dominantes a nivel micro, como la tensión superficial y la difusión laminar.
Ventajas.
• Reducción del consumo de muestrasyreactivos
• Tiempos de análisis más rápidos.
• Capacidad para la automatización y el alto rendimiento.
• Reducción de la contaminacióncruzada
• Potencial para la fabricación debajocosto.
¿Quénospermite?
Estos dispositivos permiten realizar análisis rápidos y eficientes con cantidades mínimas de muestra, lo cual esidealparaentornosclínicos conrecursoslimitadososituaciones de emergencia, como brotes epidémicos.
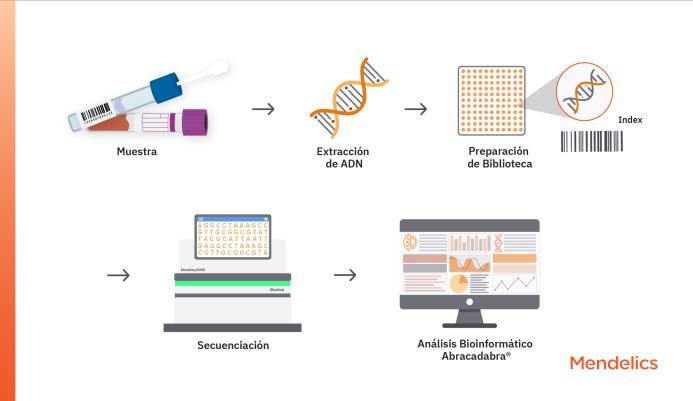
SECUENCIACION GENETICA (NGS)
Es un conjunto de tecnologías de secuenciación de ADN que han revolucionado la investigación genómica y el diagnóstico clínico. Estapermitesecuenciarmillonesde fragmentos deADN en paralelo, lo que resulta en un rendimiento mucho mayor y una reducción significativa en el tiempo y el costo porbasesecuenciada.
¿CómofuncionalaNGS?
• Preparacióndelabiblioteca deADN:ElADNdelamuestra se fragmenta en pequeños trozos. Se añaden adaptadores a los extremos deestosfragmentos.
• Amplificación: Los fragmentos de ADN unidos a la superficie se amplifican para generar múltiples copias idénticas
• Secuenciación: Se añaden nucleótidos marcados fluorescentemente a la cadena de ADN en crecimiento. Una cámara detecta la incorporación de cada nucleótido en cada clústerentiemporeal.
• Análisisdedatos: Elenorme volumen de datos generados se analiza bioinformáticamente para alinear las secuencias obtenidas con un genoma de referencia, identificar variantes genéticas y
cuantificar la abundancia de lassecuencias.
VentajasdelaNGS:
• Altorendimiento.
• Bajocosto.
• Altavelocidad.
• Altasensibilidad.
• Versatilidad.
DesventajasdelaNGS:
• Generaciónmasivadedatos
• Análisis bioinformático complejo
• Longituddelecturamáscorta (enalgunasplataformas.
• Posibilidad de artefactos y errores.
• Costoinicialdelosequipos.
Opinión.
Lasecuenciacióngenéticadenueva generación (NGS) es una tecnología poderosa que ha transformado la forma en que estudiamos y comprendemos el genoma.
Espectroscopía infrarroja.
Se basa en la absorción de radiación infrarroja por las moléculas.Cuandolafrecuenciade la luz IR coincide con la frecuencia vibracionaldeunenlacequímicoen la molécula, la energía es absorbida, causando un cambio en laamplituddelavibración.

Ventajas del análisis no invasivo con espectroscopíaIR:
• Preservación de la muestra: Permite el análisis de materiales valiosos, únicos o delicados sin causarlesdaño.
• Análisisinsituyentiemporeal: Lasmedicionessepuedenrealizar directamenteenelobjetoosistema bajo estudio sin necesidad de extracción o preparación de muestras, lo que permite el monitoreo en tiempo real de procesos.
• Reducción delacontaminación: Al evitar la manipulación y preparación de muestras, se minimiza el riesgo de introducir contaminantes.
• Análisis de muestras heterogéneas: Permiten obtener informacióndediferentesáreasde
una muestra sin necesidad de homogeneización.
• Aplicaciones versátiles: Pueden aplicarse a una amplia gama de materialesyendiversoscampos.
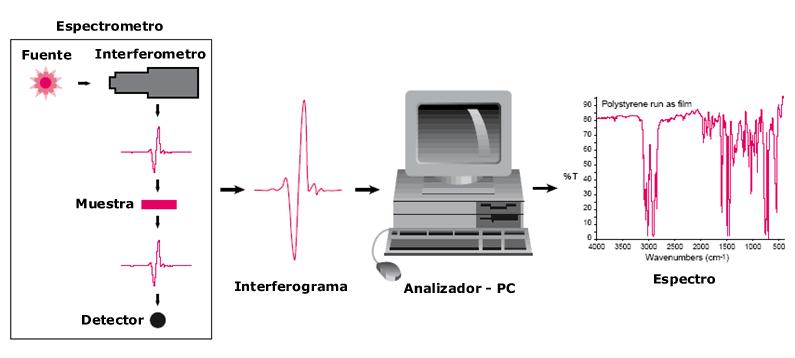
la espectroscopía infrarroja se ha consolidado como una herramienta poderosa para el análisis no invasivo gracias a su capacidad parainteractuarconlasvibraciones moleculares sin dañar la muestra. Suversatilidadyladisponibilidadde diferentes técnicas y accesorios permiten su aplicación en una amplia gama de campos, proporcionando información valiosa sobre la composición y las propiedades de los materiales de manerasegurayeficiente.


